JP4352849B2 - プラスチックの表面処理方法、プラスチック基板およびプラスチック製バイオチップ - Google Patents
プラスチックの表面処理方法、プラスチック基板およびプラスチック製バイオチップ Download PDFInfo
- Publication number
- JP4352849B2 JP4352849B2 JP2003355768A JP2003355768A JP4352849B2 JP 4352849 B2 JP4352849 B2 JP 4352849B2 JP 2003355768 A JP2003355768 A JP 2003355768A JP 2003355768 A JP2003355768 A JP 2003355768A JP 4352849 B2 JP4352849 B2 JP 4352849B2
- Authority
- JP
- Japan
- Prior art keywords
- plastic
- functional group
- group
- treatment method
- surface treatment
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 239000004033 plastic Substances 0.000 title claims description 100
- 229920003023 plastic Polymers 0.000 title claims description 100
- 239000000758 substrate Substances 0.000 title claims description 69
- 238000000034 method Methods 0.000 title claims description 50
- 238000000018 DNA microarray Methods 0.000 title claims description 38
- 238000004381 surface treatment Methods 0.000 title claims description 38
- 125000000524 functional group Chemical group 0.000 claims description 63
- 125000003277 amino group Chemical group 0.000 claims description 27
- 230000003647 oxidation Effects 0.000 claims description 24
- 238000007254 oxidation reaction Methods 0.000 claims description 24
- 239000013543 active substance Substances 0.000 claims description 20
- 125000003172 aldehyde group Chemical group 0.000 claims description 18
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 15
- 229910052760 oxygen Inorganic materials 0.000 claims description 15
- 239000001301 oxygen Substances 0.000 claims description 15
- 230000009467 reduction Effects 0.000 claims description 14
- 102000039446 nucleic acids Human genes 0.000 claims description 12
- 108020004707 nucleic acids Proteins 0.000 claims description 12
- 150000007523 nucleic acids Chemical class 0.000 claims description 12
- -1 lithium aluminum hydride Chemical compound 0.000 claims description 11
- 238000009832 plasma treatment Methods 0.000 claims description 10
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 claims description 9
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical group O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 claims description 8
- 150000001299 aldehydes Chemical class 0.000 claims description 8
- 102000004169 proteins and genes Human genes 0.000 claims description 7
- 108090000623 proteins and genes Proteins 0.000 claims description 7
- SJECZPVISLOESU-UHFFFAOYSA-N 3-trimethoxysilylpropan-1-amine Chemical compound CO[Si](OC)(OC)CCCN SJECZPVISLOESU-UHFFFAOYSA-N 0.000 claims description 5
- 229910052987 metal hydride Inorganic materials 0.000 claims description 5
- 150000004681 metal hydrides Chemical class 0.000 claims description 5
- 239000012279 sodium borohydride Substances 0.000 claims description 5
- 229910000033 sodium borohydride Inorganic materials 0.000 claims description 5
- 239000000126 substance Substances 0.000 claims description 5
- 102000003886 Glycoproteins Human genes 0.000 claims description 4
- 108090000288 Glycoproteins Proteins 0.000 claims description 4
- 239000012298 atmosphere Substances 0.000 claims description 4
- 238000003851 corona treatment Methods 0.000 claims description 4
- 150000001875 compounds Chemical class 0.000 claims description 3
- 125000000468 ketone group Chemical group 0.000 claims description 3
- 239000012280 lithium aluminium hydride Substances 0.000 claims description 3
- 108091093037 Peptide nucleic acid Proteins 0.000 claims description 2
- 230000001590 oxidative effect Effects 0.000 claims description 2
- 239000000243 solution Substances 0.000 description 16
- 150000001343 alkyl silanes Chemical class 0.000 description 12
- 238000006722 reduction reaction Methods 0.000 description 12
- 239000003638 chemical reducing agent Substances 0.000 description 11
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 10
- 239000007853 buffer solution Substances 0.000 description 9
- 239000012756 surface treatment agent Substances 0.000 description 9
- 238000006243 chemical reaction Methods 0.000 description 8
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 7
- 238000007654 immersion Methods 0.000 description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 7
- 238000001514 detection method Methods 0.000 description 6
- 238000005259 measurement Methods 0.000 description 6
- 239000002262 Schiff base Substances 0.000 description 5
- 150000004753 Schiff bases Chemical class 0.000 description 5
- 238000009396 hybridization Methods 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- 238000002493 microarray Methods 0.000 description 5
- 239000006087 Silane Coupling Agent Substances 0.000 description 4
- 230000000052 comparative effect Effects 0.000 description 4
- 125000004122 cyclic group Chemical group 0.000 description 4
- 229920000098 polyolefin Polymers 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 230000009257 reactivity Effects 0.000 description 4
- 239000002904 solvent Substances 0.000 description 4
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 3
- 125000003700 epoxy group Chemical group 0.000 description 3
- 238000011156 evaluation Methods 0.000 description 3
- 239000011521 glass Substances 0.000 description 3
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 3
- 102000007469 Actins Human genes 0.000 description 2
- 108010085238 Actins Proteins 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- 150000008065 acid anhydrides Chemical class 0.000 description 2
- 238000003491 array Methods 0.000 description 2
- 229940098773 bovine serum albumin Drugs 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 239000007850 fluorescent dye Substances 0.000 description 2
- 230000003100 immobilizing effect Effects 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 230000001766 physiological effect Effects 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 229920005992 thermoplastic resin Polymers 0.000 description 2
- 125000003396 thiol group Chemical group [H]S* 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- WYTZZXDRDKSJID-UHFFFAOYSA-N (3-aminopropyl)triethoxysilane Chemical compound CCO[Si](OCC)(OCC)CCCN WYTZZXDRDKSJID-UHFFFAOYSA-N 0.000 description 1
- 125000000022 2-aminoethyl group Chemical group [H]C([*])([H])C([H])([H])N([H])[H] 0.000 description 1
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 1
- 125000003158 alcohol group Chemical group 0.000 description 1
- 239000000427 antigen Substances 0.000 description 1
- 102000036639 antigens Human genes 0.000 description 1
- 108091007433 antigens Proteins 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000007385 chemical modification Methods 0.000 description 1
- 239000007979 citrate buffer Substances 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 239000006059 cover glass Substances 0.000 description 1
- 238000007876 drug discovery Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- 125000001033 ether group Chemical group 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000001746 injection moulding Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 239000012046 mixed solvent Substances 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- PHQOGHDTIVQXHL-UHFFFAOYSA-N n'-(3-trimethoxysilylpropyl)ethane-1,2-diamine Chemical compound CO[Si](OC)(OC)CCCNCCN PHQOGHDTIVQXHL-UHFFFAOYSA-N 0.000 description 1
- HZGIOLNCNORPKR-UHFFFAOYSA-N n,n'-bis(3-trimethoxysilylpropyl)ethane-1,2-diamine Chemical compound CO[Si](OC)(OC)CCCNCCNCCC[Si](OC)(OC)OC HZGIOLNCNORPKR-UHFFFAOYSA-N 0.000 description 1
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 125000002081 peroxide group Chemical group 0.000 description 1
- 239000008055 phosphate buffer solution Substances 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920005672 polyolefin resin Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 238000003498 protein array Methods 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 1
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 238000001291 vacuum drying Methods 0.000 description 1
- 239000004711 α-olefin Substances 0.000 description 1
Landscapes
- Investigating Or Analysing Materials By The Use Of Chemical Reactions (AREA)
Description
バイオチップ上のシグナル検出には、蛍光ラベル法を利用することが多い。たとえば核酸マイクロアレイの場合、検体の核酸を予め蛍光ラベルしておき、マイクロアレイ上に固定化された核酸とのハイブリダイゼーション量を蛍光スキャナーで読み取る。蛍光シグナル検出において、基板に由来する蛍光(バックグラウンド)が高いと、S/N比の低下により検出精度が低下する。ゆえに、バイオチップ基板の材料には低蛍光性のものを使用することが多い。また、基板表面には核酸を効率良く固定化するための化学的修飾が施されることが通常であり、アルデヒド基やアミノ基を導入したものが多用されている。これらの官能基導入に由来する蛍光を低減することは、バイオチップを用いたアッセイの精度向上の観点から重要となってくる。
通常、プラスチックの表面は不活性であり、そのままではシランカップリング剤との反応性が低く、十分に表面処理を行うことができない。そのため、プラスチック表面を酸化処理により活性化することが多い。すなわち、酸化処理により、水酸基、カルボニル基などの極性の強い含酸素官能基を導入することにより、表面を活性化したのちに、シランカップリング剤を接触させる。しかしながら、このような方法で表面処理を施したプラスチック表面は、比較的強い蛍光を発することから、バイオチップとしての検出精度を低下させる原因となっていた。
「細胞工学別冊 DNAマイクロアレイと最新PCR法」秀潤社、2000年
(1)プラスチック表面を酸化処理する工程、及び酸化処理によって生成した含酸素官能基を還元処理する工程を有し、プラスチック表面に第1の官能基を導入することを特徴とするプラスチックの表面処理方法であって、酸化処理が、プラズマ処理、コロナ放電処理、フレーム処理、及び紫外線照射処理から選ばれる少なくとも1つの処理を含むものであり、還元される含酸素官能基が、カルボニル基を含むものであり、還元処理する工程が、金属水素化物を含む溶液へ浸漬する工程を有するものであるプラスチックの表面処理方法。
(2)カルボニル基がアルデヒド基及び/又はケトン基を含むものである(1)記載のプラスチックの表面処理方法。
(3)酸化処理が、酸素雰囲気下でのプラズマ処理を含むものである(1)又は(2)記載のプラスチックの表面処理方法。
(4)金属水素化物が水素化ホウ素ナトリウム及び/又は水素化アルミニウムリチウムを含むものである(1)〜(3)いずれか記載のプラスチックの表面処理方法。
(5)還元処理する工程後、更にプラスチック表面に導入された第1の官能基を介して第2の官能基を導入する工程を有する(1)〜(4)いずれか記載のプラスチックの表面処理方法。
(6)第2の官能基の導入が、アルキルシラン化合物とプラスチック表面との結合によってなる(5)記載のプラスチックの表面処理方法。
(7)アルキルシラン化合物が、アミノ基を有するアミノアルキルシランを含み、第2の官能基がアミノ基である(6)記載のプラスチックの表面処理方法。
(8)アミノアルキルシラン化合物が、3-アミノプロピルトリメトキシシランを含むものである(7)記載のプラスチックの表面処理方法。
(9)(5)〜(8)いずれか記載のプラスチックの表面処理方法によってプラスチック基板表面に第2の官能基が導入されたプラスチック基板。
(10)第2の官能基を導入した後、更に該第2の官能基を介して第3の官能基を導入する工程を有する(5)〜(8)いずれか記載のプラスチックの表面処理方法。
(11)アミノ基を導入した後、更に該アミノ基を介して第3の官能基を導入する工程を有する(7)又は(8)記載のプラスチックの表面処理方法。
(12)第3の官能基を導入する工程が多官能性アルデヒドと反応させることにより、アミノ基を介してアルデヒド基を導入する工程を有する(11)記載のプラスチックの表面処理方法。
(13)多官能性アルデヒドがグルタルアルデヒドである(12)記載のプラスチックの表面処理方法。
(14)(10)〜(13)いずれか記載のプラスチックの表面処理方法によってプラスチック基板表面に第3の官能基を導入されたプラスチック基板。
(15)(9)記載のプラスチック基板の表面に、更に第2の官能基を介して生理活性物質が固定化されているプラスチック製バイオチップ。
(16)(14)記載のプラスチック基板の表面に、更に第3の官能基を介して生理活性物質が固定化されているプラスチック製バイオチップ。
(17)生理活性物質が,他の物質を特異的に捕捉する性質を有する(15)又は(16)記載のプラスチック製バイオチップ。
(18)生理活性物質が、核酸、タンパク質、抗体、糖鎖、糖タンパク、及びペプチド核酸から選ばれる少なくとも1つである(17)記載のプラスチック製バイオチップ。
(19)生理活性物質が蛍光によるシグナルによって検出されるものである(15)〜(18)いずれか記載のプラスチック製バイオチップ。
一般的にプラスチックの表面は不活性であるため、そのままの状態でアルキルシランなどの表面処理剤を結合することは難しい。そのため、前処理として酸化処理を施すことが普通である。本発明のプラスチックの表面処理は、酸化処理によって生成した含酸素官能基を還元することにより、表面の官能基に占める水酸基の割合を増加させることを特徴とする。酸化処理によって含酸素官能基を導入することにより、プラスチック表面の反応性が向上し、表面処理剤との親和性が高くなる効果がある。酸化処理によってアルデヒド基などの活性な官能基が導入されると、酸化処理の後に行う表面処理に支障をきたす場合がある。たとえば、表面処理剤としてアミノ基をもつアルキルシランを用いる場合を考える。酸化処理によってアルデヒド基が導入されていると、アルキルシランのアミノ基との間にシッフ塩基を形成してしまう。本発明者は、表面にシッフ塩基が存在すると、プラスチック表面の蛍光発生量が増大することを見出している。そこで、蛍光発生量を低減するためには、酸化処理によって生成したカルボニルおよびその他の化学的に活性な官能基をあらかじめより不活性な官能基に変換しておくことが有効となる。
本発明において酸化処理とは、プラスチック表面の少なくとも一部に含酸素官能基を導入する処理をいう。酸化処理として好適に用いられる手段は、プラズマ処理、コロナ放電処理、フレーム処理、紫外線照射処理などであり、好ましくはプラズマ処理およびコロナ放電処理であり、より好ましくはプラズマ処理であり、最も好ましくは酸素雰囲気下でのプラズマ処理である。含酸素官能基とは、カルボニル基(アルデヒド基、ケトン基などを含む)、カルボキシル基、水酸基、エーテル基、エステル基、パーオキサイド基、エポキシ基などに代表される、極性をもった官能基群であるがこれらに限定されない。酸化処理によって含酸素官能基を導入することにより、プラスチック表面の反応性が向上し、表面処理剤との親和性が高くなる効果がある。
活性な官能基のより不活性な官能基への変換工程は、還元反応を主な機構とすることが好ましい。該工程はプラスチック表面に還元剤を作用させる操作であることが好ましく、具体的には、たとえば還元剤溶液へのプラスチック基板の浸漬操作である。還元剤としては金属水素化物が好ましく、水素化ホウ素ナトリウム、シアノトリヒドロホウ酸ナトリウム、水素化アルミニウムリチウムなどを用いることができるが、取り扱いの安全性の観点から水素化ホウ素ナトリウムが好ましい。還元剤溶液は水、緩衝液、その他の溶媒に還元剤を溶解した溶液であり、最も好ましい溶媒はエタノールを含むpH6〜8の緩衝液である。緩衝液には好ましくは5〜50体積%、より好ましくは10〜30体積%のエタノールを添加することが好ましい。エタノールの添加により、還元剤を緩衝液に溶解する際の気泡の発生を抑えることができ、より均一な還元処理が可能となる。還元剤溶液中の還元剤濃度は、好ましくは0.001〜10重量%、より好ましくは0.01〜1重量%、さらに好ましくは0.1〜0.5重量%であり、最も好ましくは0.25重量%である。上記の還元剤処理により、たとえばアルデヒド基はより不活性な官能基であるアルコール基(水酸基)に変換される。
酸化処理および還元処理を経たプラスチック基板の表面には、水酸基を主とする第1の官能基が導入されている。これに表面処理剤を反応させることにより、種々の第2の官能基を導入することが可能である。表面処理剤として好適に用いられるのはアルキルシランである。アルキルシランによって導入可能な官能基は多岐にわたるが、バイオチップ基板として有用なものにはアミノ基、カルボキシル基、エポキシ基、水酸基、酸無水物、チオール基などが挙げられる。なかでもアミノ基(1級アミノ基等)を有するアミノアルキルシランは特に有用である。1級アミノ基を有するアミノアルキルシランとしては、3−アミノプロピルトリメトキシシラン、3−アミノプロピルトリエトキシシラン、N−2−(アミノエチル)−3−アミノプロピルトリメトキシシラン、N−2−(アミノエチル)−3−アミノプロピルトリエトキシシランなど、一般的なものを用いることができるが、3−アミノプロピルトリメトキシシランが最も好ましい。1級アミノ基を含まないアミノアルキルシランとしては、たとえば N、N'−ビス[3−(トリメトキシシリル)プロピル]エチレンジアミンなどを好適に用いることができる。
上述の還元処理がなされていない場合、プラスチック表面にはアルデヒド基などの活性なカルボニル基が存在する。ここにアミノアルキルシランを反応させると、アルデヒド基とアミノ基との間にシッフ塩基が形成される。シッフ塩基は蛍光を発しやすいため、基板の蛍光発生量(バックグラウンド)が上昇してしまう。一方、本発明に基づいて還元処理を施しておくと、プラスチック表面には活性なカルボニル基が実質的に存在しないため、シッフ塩基は形成されず、蛍光発生量も増大しない。
上述の手段によりアミノ基等を導入したプラスチック表面に、アミノ基等との反応性を有する物質を反応させることにより、第3の官能基を導入することができる。第3の官能基としては、アルデヒド基、カルボキシル基、エポキシ基、水酸基、酸無水物、チオール基などが挙げられるが、これらに限定されない。なかでも特に有用な官能基として、アルデヒド基を挙げることができる。アルデヒド基を導入するには、たとえば分子内に2個以上のアルデヒド基をもつ化合物(多官能性アルデヒド)を作用させることで達成される。すなわち、プラスチック表面に導入されているアミノ基と、多官能性アルデヒド分子内の少なくとも1つのアルデヒド基を反応させることで、表面にアルデヒド基を導入することができる。多官能性アルデヒドとしては、たとえばグルタルアルデヒドを好適に用いることができる。グルタルアルデヒドの基板表面への反応は、たとえばグルタルアルデヒド溶液に基板を浸漬することで達成される。その際のグルタルアルデヒドの濃度は、好ましくは0.1〜20重量%、より好ましくは0.1〜5重量%、さらに好ましくは0.5〜5重量%、最も好ましくは0.5〜2重量%である。溶媒としては水、緩衝液、その他の有機溶媒を用いることができるが、緩衝液が特に好ましい。緩衝液のpHは、6〜14が好ましく、6〜12がさらに好ましく、6〜11が最も好ましい。浸漬時のグルタルアルデヒド溶液の温度、浸漬時間を変化させることにより、グルタルアルデヒドの導入量を変化させることが可能である。
バイオチップ用基板の素材としては、ガラス、プラスチック、金属その他が一般的に用いられている。表面処理の容易性、量産性の観点から、プラスチックが特に好ましく、なかでも熱可塑性樹脂が好ましい。熱可塑性樹脂としては、蛍光発生量の少ないものが好ましく、たとえばポリエチレン、ポリプロピレン等の直鎖状ポリオレフィン、環状ポリオレフィン、含フッ素樹脂等を用いることが好ましく、耐熱性、耐薬品性、低蛍光性、成形性に特に優れる飽和環状ポリオレフィンを用いることがより好ましい。ここで飽和環状ポリオレフィンとは、環状オレフィン構造を有する重合体単独または環状オレフィンとα−オレフィンとの共重合体を水素添加した飽和重合体をさす。
上述の手段で表面に第2又は第3の官能基を導入したプラスチック基板上に、第2又は第3の官能基を介して生理活性物質を固定化することができる。生理活性物質としては、核酸、タンパク質、抗体、糖鎖、糖タンパク、およびこれらの類似物を用いることができるが、これらに限定されない。生理活性物質の固定化は、プラスチック基板表面の第2又は第3の官能基と、生理活性物質に含まれる官能基と間の化学結合によることが好ましいが、静電的結合や物理的吸着、水素結合などによるものであってもよい。固定化される生理活性物質は、本来の生理活性を実質的に保っていることが好ましい。ここで本来の生理活性とは、たとえば核酸の場合はハイブリダイゼーション現象、抗体の場合は抗原認識能といったものである。基板上に固定化された生理活性物質と、別途調製した生理活性物質(検体)を反応させ、その反応を定量化することにより検体の情報を得ることができる。定量化の手段として一般的に用いられている方法は、検体を蛍光標識しておき、その蛍光量を読み取る方法である。本発明のプラスチック基板は蛍光発生量が低く抑えられているため、定量に蛍光標識を利用するバイオチップの基板として好適に用いることができる。また、蛍光標識を用いないバイオチップの基板としても当然用いることができる。
(酸化処理,還元処理)
飽和環状ポリオレフィン樹脂を射出成形法で成形し,厚さ1mmの平板状の基板を作製した。酸素雰囲気下のプラズマ処理によって基板表面に酸化処理を施した。プラズマ処理直後の基板を還元剤溶液に15分間浸漬した。ここで還元剤溶液は,0.25重量%の水素化ホウ素ナトリウムを,リン酸緩衝溶液(pH7.4)/エタノール混合溶媒(体積比4:1)に溶解した溶液であった。浸漬後,基板を純水で洗浄し,乾燥した。
(アミノ基の導入)
3−アミノプロピルトリメトキシシランを2重量%の濃度で純水に溶解した。この溶液に上述の基板を浸漬した。浸漬は25℃で1時間行った。浸漬後,基板を純水で洗浄し,乾燥した。これを45℃に保った真空乾燥機を用いて真空乾燥した。
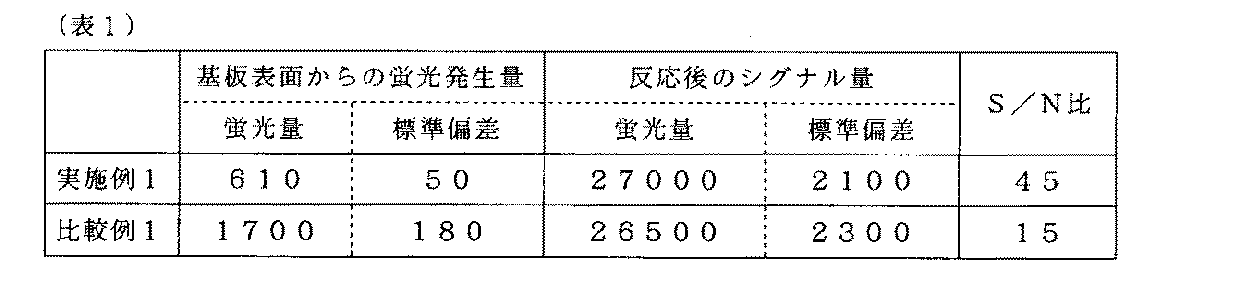
(基板の蛍光量の測定)
アミノ基導入後の基板表面の蛍光発生量を,マイクロアレイ用スキャナー(ScanArrayLITE, Packard BioChip Technologies社製)を用いて測定した。測定条件は,レーザー出力90%,PMT感度70%,スキャン解像度30μm,測定波長はCy3およびCy5チャンネルであった。結果を表1に示す。
(DNA固定化/ハイブリダイゼーション性能の評価)
PCR法で合成したDNA(β−アクチン部位,約600bp)を2×SSC(クエン酸緩衝液)に溶解した。この溶液を,アミノ基を導入した基板の表面に点着し,80℃のオーブン内で1時間静置した。基板表面を洗浄した後,0.1重量%のBSA(ウシ血清アルブミン)を含む緩衝液に1時間浸漬することで,残存するアミノ基をブロッキングした。PCR法で合成した蛍光標識化DNA(β−アクチン部位,約600bp,Cy5標識)を,0.5重量%のラウリル硫酸ナトリウムを含む5×SSCに溶解した。この溶液を,ブロッキング後の基板表面に滴下し,カバーグラスを被せた後に50℃のインキュベーター内で18時間反応させた。反応終了後,基板表面を洗浄し,乾燥した。基板表面に固定したDNAと蛍光標識化DNAとの結合量を,マイクロアレイ用スキャナーを用いて定量化した。測定条件は,レーザー出力90%,PMT感度45%,スキャン解像度30μm,測定波長はCy5チャンネルであった。結果を表1に示す。
(酸化処理)
実施例1と同様の方法で基板を成形し,表面を酸化処理した。酸化処理後に還元処理は行わなかった。
(アミノ基の導入)
実施例1と同様の方法で基板表面にアミノ基を導入した。
(基板の蛍光量の測定)
実施例1と同様の方法で基板表面の蛍光発生量を測定した。結果を表1に示す。
(DNA固定化/ハイブリダイゼーション性能の評価)
実施例1と同様の方法でDNAの固定化を行い,蛍光標識化DNAの結合量を測定した。結果を表1に示す。
Claims (19)
- プラスチック表面を酸化処理する工程、及び酸化処理によって生成した含酸素官能基を還元処理する工程を有し、プラスチック表面に第1の官能基を導入することを特徴とするプラスチックの表面処理方法であって、酸化処理が、プラズマ処理、コロナ放電処理、フレーム処理、及び紫外線照射処理から選ばれる少なくとも1つの処理を含むものであり、還元される含酸素官能基が、カルボニル基を含むものであり、還元処理する工程が、金属水素化物を含む溶液へ浸漬する工程を有するものであるプラスチックの表面処理方法。
- カルボニル基がアルデヒド基及び/又はケトン基を含むものである請求項1記載のプラスチックの表面処理方法。
- 酸化処理が、酸素雰囲気下でのプラズマ処理を含むものである請求項1又は2記載のプラスチックの表面処理方法。
- 金属水素化物が水素化ホウ素ナトリウム及び/又は水素化アルミニウムリチウムを含むものである請求項1〜3いずれか記載のプラスチックの表面処理方法。
- 還元処理する工程後、更にプラスチック表面に導入された第1の官能基を介して第2の官能基を導入する工程を有する請求項1〜4いずれか記載のプラスチックの表面処理方法。
- 第2の官能基の導入が、アルキルシラン化合物とプラスチック表面との結合によってなる請求項5記載のプラスチックの表面処理方法。
- アルキルシラン化合物が、アミノ基を有するアミノアルキルシランを含み、第2の官能基がアミノ基である請求項6記載のプラスチックの表面処理方法。
- アミノアルキルシラン化合物が、3-アミノプロピルトリメトキシシランを含むものである請求項7記載のプラスチックの表面処理方法。
- 請求項5〜8いずれか記載のプラスチックの表面処理方法によってプラスチック基板表面に第2の官能基が導入されたプラスチック基板。
- 第2の官能基を導入した後、更に該第2の官能基を介して第3の官能基を導入する工程を有する請求項5〜8いずれか記載のプラスチックの表面処理方法。
- アミノ基を導入した後、更に該アミノ基を介して第3の官能基を導入する工程を有する請求項7又は8記載のプラスチックの表面処理方法。
- 第3の官能基を導入する工程が多官能性アルデヒドと反応させることにより、アミノ基を介してアルデヒド基を導入する工程を有する請求項11記載のプラスチックの表面処理方法。
- 多官能性アルデヒドがグルタルアルデヒドである請求項12記載のプラスチックの表面処理方法。
- 請求項10〜13いずれか記載のプラスチックの表面処理方法によってプラスチック基板表面に第3の官能基を導入されたプラスチック基板。
- 請求項9記載のプラスチック基板の表面に、更に第2の官能基を介して生理活性物質が固定化されているプラスチック製バイオチップ。
- 請求項14記載のプラスチック基板の表面に、更に第3の官能基を介して生理活性物質が固定化されているプラスチック製バイオチップ。
- 生理活性物質が,他の物質を特異的に捕捉する性質を有する請求項15又は16記載のプラスチック製バイオチップ。
- 生理活性物質が、核酸、タンパク質、抗体、糖鎖、糖タンパク、及びペプチド核酸から選ばれる少なくとも1つである請求項17記載のプラスチック製バイオチップ。
- 生理活性物質が蛍光によるシグナルによって検出されるものである請求項15〜18いずれか記載のプラスチック製バイオチップ。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003355768A JP4352849B2 (ja) | 2003-10-16 | 2003-10-16 | プラスチックの表面処理方法、プラスチック基板およびプラスチック製バイオチップ |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003355768A JP4352849B2 (ja) | 2003-10-16 | 2003-10-16 | プラスチックの表面処理方法、プラスチック基板およびプラスチック製バイオチップ |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2005121443A JP2005121443A (ja) | 2005-05-12 |
| JP4352849B2 true JP4352849B2 (ja) | 2009-10-28 |
Family
ID=34613216
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003355768A Expired - Fee Related JP4352849B2 (ja) | 2003-10-16 | 2003-10-16 | プラスチックの表面処理方法、プラスチック基板およびプラスチック製バイオチップ |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4352849B2 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5364971B2 (ja) * | 2006-09-28 | 2013-12-11 | 住友ベークライト株式会社 | 生理活性物質の固定化方法 |
| JP5616309B2 (ja) | 2010-12-01 | 2014-10-29 | アークレイ株式会社 | デバイス及びその製造方法 |
| JP7700430B2 (ja) * | 2017-09-07 | 2025-07-01 | 三菱瓦斯化学株式会社 | バイオチップ用基体、バイオチップ、バイオチップの製造方法およびその保存方法 |
-
2003
- 2003-10-16 JP JP2003355768A patent/JP4352849B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2005121443A (ja) | 2005-05-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Palladino et al. | Polydopamine: surface coating, molecular imprinting, and electrochemistry—successful applications and future perspectives in (bio) analysis | |
| CN103147133B (zh) | 微阵列生物芯片的三维载体及其制备方法 | |
| WO2016079170A1 (en) | Porous membranes with a polymer grafting, methods and uses thereof | |
| CN101498719B (zh) | 酶功能化纳米免疫标记物的制备方法及其应用 | |
| Yoon et al. | Biocatalytic precipitation induced by an affinity reaction on dendrimer-activated surfaces for the electrochemical signaling from immunosensors | |
| Liu et al. | Photografted poly (methyl methacrylate)-based high performance protein microarray for hepatitis B virus biomarker detection in human serum | |
| Muguruma | Plasma-polymerized films for biosensors II | |
| JP4352849B2 (ja) | プラスチックの表面処理方法、プラスチック基板およびプラスチック製バイオチップ | |
| WO2016079171A1 (en) | Device comprising porous membranes with a polymer grafting, methods and uses thereof | |
| JP4419715B2 (ja) | バイオチップ用基板およびバイオチップ | |
| CN107255713B (zh) | 可用于诊断人肠道病毒感染的试剂盒 | |
| JP2008224327A (ja) | バイオチップ | |
| JP5344438B2 (ja) | 物質固定用基板、物質固定化基板および分析方法 | |
| JP4534817B2 (ja) | 蛋白質の検出方法及びペプチドの検出方法 | |
| TWI246593B (en) | Method and substrate for biochips by using single-step manufacturing process | |
| CA2487483C (fr) | Dispositif de presentation de peptides ou de proteines, son procede de preparation et ses utilisations | |
| Pei et al. | Covalently derivatized NTA microarrays on porous silicon for multi-mode detection of His-tagged proteins | |
| JP4347211B2 (ja) | バイオチップ用基板およびバイオチップ | |
| JP4112345B2 (ja) | マイクロアレイ用プラスチック基板の使用方法 | |
| CN100396791C (zh) | 寡聚核苷酸嵌入染料荧光共振能量传递分子检测方法 | |
| JP2005010004A (ja) | バイオチップ | |
| JP4370874B2 (ja) | マイクロアレイ用基板 | |
| CN1635378A (zh) | 胶体金-银增强方法检测蛋白质芯片 | |
| JP4353073B2 (ja) | バイオチップおよびその製造方法 | |
| JP4259343B2 (ja) | 選択結合性物質の固定化方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20060613 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20080428 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090303 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090423 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20090707 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20090720 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120807 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120807 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130807 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140807 Year of fee payment: 5 |
|
| LAPS | Cancellation because of no payment of annual fees |