JP3553085B2 - 新規の置換ナフトピラン類 - Google Patents
新規の置換ナフトピラン類 Download PDFInfo
- Publication number
- JP3553085B2 JP3553085B2 JP51646598A JP51646598A JP3553085B2 JP 3553085 B2 JP3553085 B2 JP 3553085B2 JP 51646598 A JP51646598 A JP 51646598A JP 51646598 A JP51646598 A JP 51646598A JP 3553085 B2 JP3553085 B2 JP 3553085B2
- Authority
- JP
- Japan
- Prior art keywords
- alkyl
- poly
- group
- monomers
- photochromic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- -1 hydroxy, benzoyloxy Chemical group 0.000 claims description 102
- 150000001875 compounds Chemical class 0.000 claims description 76
- 239000000463 material Substances 0.000 claims description 65
- 239000000178 monomer Substances 0.000 claims description 54
- 239000000203 mixture Substances 0.000 claims description 47
- 125000000217 alkyl group Chemical group 0.000 claims description 43
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 41
- 239000001257 hydrogen Substances 0.000 claims description 35
- 229910052739 hydrogen Inorganic materials 0.000 claims description 35
- 239000000126 substance Substances 0.000 claims description 30
- 125000001153 fluoro group Chemical group F* 0.000 claims description 27
- VCMLCMCXCRBSQO-UHFFFAOYSA-N 3h-benzo[f]chromene Chemical class C1=CC=CC2=C(C=CCO3)C3=CC=C21 VCMLCMCXCRBSQO-UHFFFAOYSA-N 0.000 claims description 24
- 229910052736 halogen Inorganic materials 0.000 claims description 24
- 150000002367 halogens Chemical class 0.000 claims description 22
- 229920000642 polymer Polymers 0.000 claims description 22
- 229920001577 copolymer Chemical compound 0.000 claims description 21
- 125000003545 alkoxy group Chemical group 0.000 claims description 20
- 125000003003 spiro group Chemical group 0.000 claims description 19
- 150000002431 hydrogen Chemical class 0.000 claims description 18
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 17
- 238000010521 absorption reaction Methods 0.000 claims description 16
- 229910052799 carbon Inorganic materials 0.000 claims description 16
- 125000001424 substituent group Chemical group 0.000 claims description 16
- XFCMNSHQOZQILR-UHFFFAOYSA-N 2-[2-(2-methylprop-2-enoyloxy)ethoxy]ethyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCOCCOC(=O)C(C)=C XFCMNSHQOZQILR-UHFFFAOYSA-N 0.000 claims description 14
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 13
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 11
- 229920006395 saturated elastomer Polymers 0.000 claims description 11
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 10
- 229910052760 oxygen Inorganic materials 0.000 claims description 10
- 239000001301 oxygen Substances 0.000 claims description 10
- 239000004814 polyurethane Substances 0.000 claims description 10
- 229920002635 polyurethane Polymers 0.000 claims description 10
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 claims description 9
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 9
- 125000005843 halogen group Chemical group 0.000 claims description 9
- 150000002430 hydrocarbons Chemical group 0.000 claims description 9
- 229920002037 poly(vinyl butyral) polymer Polymers 0.000 claims description 9
- 229920002689 polyvinyl acetate Polymers 0.000 claims description 9
- 239000011118 polyvinyl acetate Substances 0.000 claims description 9
- 229920001169 thermoplastic Polymers 0.000 claims description 9
- 239000004416 thermosoftening plastic Substances 0.000 claims description 9
- HIACAHMKXQESOV-UHFFFAOYSA-N 1,2-bis(prop-1-en-2-yl)benzene Chemical compound CC(=C)C1=CC=CC=C1C(C)=C HIACAHMKXQESOV-UHFFFAOYSA-N 0.000 claims description 8
- JKJWYKGYGWOAHT-UHFFFAOYSA-N bis(prop-2-enyl) carbonate Chemical compound C=CCOC(=O)OCC=C JKJWYKGYGWOAHT-UHFFFAOYSA-N 0.000 claims description 8
- 125000002541 furyl group Chemical group 0.000 claims description 8
- 229920000515 polycarbonate Polymers 0.000 claims description 8
- 239000004417 polycarbonate Substances 0.000 claims description 8
- JHQVCQDWGSXTFE-UHFFFAOYSA-N 2-(2-prop-2-enoxycarbonyloxyethoxy)ethyl prop-2-enyl carbonate Chemical compound C=CCOC(=O)OCCOCCOC(=O)OCC=C JHQVCQDWGSXTFE-UHFFFAOYSA-N 0.000 claims description 7
- 239000004926 polymethyl methacrylate Substances 0.000 claims description 7
- 229920005862 polyol Polymers 0.000 claims description 7
- 150000003077 polyols Chemical class 0.000 claims description 7
- GTELLNMUWNJXMQ-UHFFFAOYSA-N 2-ethyl-2-(hydroxymethyl)propane-1,3-diol;prop-2-enoic acid Chemical class OC(=O)C=C.OC(=O)C=C.OC(=O)C=C.CCC(CO)(CO)CO GTELLNMUWNJXMQ-UHFFFAOYSA-N 0.000 claims description 6
- CERQOIWHTDAKMF-UHFFFAOYSA-M Methacrylate Chemical compound CC(=C)C([O-])=O CERQOIWHTDAKMF-UHFFFAOYSA-M 0.000 claims description 6
- 125000004244 benzofuran-2-yl group Chemical group [H]C1=C(*)OC2=C([H])C([H])=C([H])C([H])=C12 0.000 claims description 6
- 125000004534 benzothien-2-yl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 claims description 6
- QUZSUMLPWDHKCJ-UHFFFAOYSA-N bisphenol A dimethacrylate Chemical class C1=CC(OC(=O)C(=C)C)=CC=C1C(C)(C)C1=CC=C(OC(=O)C(C)=C)C=C1 QUZSUMLPWDHKCJ-UHFFFAOYSA-N 0.000 claims description 6
- 125000004988 dibenzothienyl group Chemical group C1(=CC=CC=2SC3=C(C21)C=CC=C3)* 0.000 claims description 6
- 125000001624 naphthyl group Chemical group 0.000 claims description 6
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 claims description 6
- 229920003229 poly(methyl methacrylate) Polymers 0.000 claims description 6
- 229920001223 polyethylene glycol Polymers 0.000 claims description 6
- 125000004076 pyridyl group Chemical group 0.000 claims description 6
- 125000001544 thienyl group Chemical group 0.000 claims description 6
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 claims description 5
- 239000004793 Polystyrene Substances 0.000 claims description 5
- 125000006615 aromatic heterocyclic group Chemical class 0.000 claims description 5
- 125000003118 aryl group Chemical group 0.000 claims description 5
- 229920002301 cellulose acetate Polymers 0.000 claims description 5
- 229920006217 cellulose acetate butyrate Polymers 0.000 claims description 5
- STVZJERGLQHEKB-UHFFFAOYSA-N ethylene glycol dimethacrylate Chemical compound CC(=C)C(=O)OCCOC(=O)C(C)=C STVZJERGLQHEKB-UHFFFAOYSA-N 0.000 claims description 5
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 5
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 claims description 5
- IJGRMHOSHXDMSA-UHFFFAOYSA-N nitrogen Substances N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 5
- 229910052757 nitrogen Inorganic materials 0.000 claims description 5
- 229920000728 polyester Polymers 0.000 claims description 5
- 229920002223 polystyrene Polymers 0.000 claims description 5
- 239000007787 solid Substances 0.000 claims description 5
- MGADZUXDNSDTHW-UHFFFAOYSA-N 2H-pyran Chemical compound C1OC=CC=C1 MGADZUXDNSDTHW-UHFFFAOYSA-N 0.000 claims description 4
- 229920008347 Cellulose acetate propionate Polymers 0.000 claims description 4
- 229920002284 Cellulose triacetate Polymers 0.000 claims description 4
- 229920001328 Polyvinylidene chloride Polymers 0.000 claims description 4
- NNLVGZFZQQXQNW-ADJNRHBOSA-N [(2r,3r,4s,5r,6s)-4,5-diacetyloxy-3-[(2s,3r,4s,5r,6r)-3,4,5-triacetyloxy-6-(acetyloxymethyl)oxan-2-yl]oxy-6-[(2r,3r,4s,5r,6s)-4,5,6-triacetyloxy-2-(acetyloxymethyl)oxan-3-yl]oxyoxan-2-yl]methyl acetate Chemical compound O([C@@H]1O[C@@H]([C@H]([C@H](OC(C)=O)[C@H]1OC(C)=O)O[C@H]1[C@@H]([C@@H](OC(C)=O)[C@H](OC(C)=O)[C@@H](COC(C)=O)O1)OC(C)=O)COC(=O)C)[C@@H]1[C@@H](COC(C)=O)O[C@@H](OC(C)=O)[C@H](OC(C)=O)[C@H]1OC(C)=O NNLVGZFZQQXQNW-ADJNRHBOSA-N 0.000 claims description 4
- QWIONAAFTRAZMO-UHFFFAOYSA-N [2,2-bis(4-methoxyphenyl)-6-phenylbenzo[h]chromen-5-yl]methanol Chemical compound C1=CC(OC)=CC=C1C1(C=2C=CC(OC)=CC=2)C=CC(C(CO)=C(C=2C=CC=CC=2)C=2C3=CC=CC=2)=C3O1 QWIONAAFTRAZMO-UHFFFAOYSA-N 0.000 claims description 4
- 125000004532 benzofuran-3-yl group Chemical group O1C=C(C2=C1C=CC=C2)* 0.000 claims description 4
- 125000004197 benzothien-3-yl group Chemical group [H]C1=C(*)C2=C([H])C([H])=C([H])C([H])=C2S1 0.000 claims description 4
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 claims description 4
- 229920001519 homopolymer Polymers 0.000 claims description 4
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims description 4
- 150000002829 nitrogen Chemical class 0.000 claims description 4
- QIWKUEJZZCOPFV-UHFFFAOYSA-N phenyl 2-methylprop-2-enoate Chemical class CC(=C)C(=O)OC1=CC=CC=C1 QIWKUEJZZCOPFV-UHFFFAOYSA-N 0.000 claims description 4
- 229920003251 poly(α-methylstyrene) Polymers 0.000 claims description 4
- 229920000058 polyacrylate Polymers 0.000 claims description 4
- 229920000139 polyethylene terephthalate Polymers 0.000 claims description 4
- 239000005020 polyethylene terephthalate Substances 0.000 claims description 4
- 229920000193 polymethacrylate Polymers 0.000 claims description 4
- 229920002451 polyvinyl alcohol Polymers 0.000 claims description 4
- 239000004800 polyvinyl chloride Substances 0.000 claims description 4
- 229920000915 polyvinyl chloride Polymers 0.000 claims description 4
- 150000005846 sugar alcohols Polymers 0.000 claims description 4
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 claims description 3
- NDBUXOQDQMDJSK-UHFFFAOYSA-N [2,2-bis(4-methoxyphenyl)-6-phenylbenzo[h]chromen-5-yl]methyl acetate Chemical compound C1=CC(OC)=CC=C1C1(C=2C=CC(OC)=CC=2)C=CC(C(COC(C)=O)=C(C=2C=CC=CC=2)C=2C3=CC=CC=2)=C3O1 NDBUXOQDQMDJSK-UHFFFAOYSA-N 0.000 claims description 3
- VVPGTNYWULJEMV-UHFFFAOYSA-N [9-methoxy-2,2-bis(4-methoxyphenyl)-6-methylbenzo[h]chromen-5-yl]methanol Chemical compound C1=CC(OC)=CC=C1C1(C=2C=CC(OC)=CC=2)C=CC(C(CO)=C(C)C=2C3=CC(OC)=CC=2)=C3O1 VVPGTNYWULJEMV-UHFFFAOYSA-N 0.000 claims description 3
- DCBMHXCACVDWJZ-UHFFFAOYSA-N adamantylidene Chemical group C1C(C2)CC3[C]C1CC2C3 DCBMHXCACVDWJZ-UHFFFAOYSA-N 0.000 claims description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 3
- 125000004573 morpholin-4-yl group Chemical group N1(CCOCC1)* 0.000 claims description 3
- WCQAZRJBAWCCMZ-UHFFFAOYSA-N 2,3-dihydro-1h-indole;2h-pyran Chemical compound C1OC=CC=C1.C1=CC=C2NCCC2=C1 WCQAZRJBAWCCMZ-UHFFFAOYSA-N 0.000 claims description 2
- UJKRMSUGENCHEY-UHFFFAOYSA-N 2,3-dihydro-1h-indole;2h-pyrano[3,2-b]quinoline Chemical compound C1=CC=C2NCCC2=C1.C1=CC=C2N=C(C=CCO3)C3=CC2=C1 UJKRMSUGENCHEY-UHFFFAOYSA-N 0.000 claims description 2
- LGXJWAKEBMORMA-UHFFFAOYSA-N 2-tert-butyl-9-methoxy-5-(methoxymethyl)-2-(4-methoxyphenyl)-6-phenylbenzo[h]chromene Chemical compound COCC1=C2C=CC(C(C)(C)C)(C=3C=CC(OC)=CC=3)OC2=C2C=C(OC)C=CC2=C1C1=CC=CC=C1 LGXJWAKEBMORMA-UHFFFAOYSA-N 0.000 claims description 2
- VFUGUWZYXGNQHR-UHFFFAOYSA-N 2h-1,2-benzoxazine;2,3-dihydro-1h-indole Chemical compound C1=CC=C2NCCC2=C1.C1=CC=C2C=CNOC2=C1 VFUGUWZYXGNQHR-UHFFFAOYSA-N 0.000 claims description 2
- ZLLLODBXLDFWER-UHFFFAOYSA-N 2h-chromene;2,3-dihydro-1h-indole Chemical compound C1=CC=C2NCCC2=C1.C1=CC=C2C=CCOC2=C1 ZLLLODBXLDFWER-UHFFFAOYSA-N 0.000 claims description 2
- HEDFZCGDROAIPW-UHFFFAOYSA-N 3h-benzo[f]chromene;2,3-dihydro-1h-benzo[g]indole Chemical compound C1=CC=CC2=C(NCC3)C3=CC=C21.C1=CC=CC2=C(C=CCO3)C3=CC=C21 HEDFZCGDROAIPW-UHFFFAOYSA-N 0.000 claims description 2
- VQEXVGHCYCLGMW-UHFFFAOYSA-N 3h-benzo[f]chromene;2,3-dihydro-1h-indole Chemical compound C1=CC=C2NCCC2=C1.C1=CC=CC2=C(C=CCO3)C3=CC=C21 VQEXVGHCYCLGMW-UHFFFAOYSA-N 0.000 claims description 2
- YRLGJEWILPSJPJ-UHFFFAOYSA-N 6-methoxy-5-(methoxymethyl)-2,2-diphenylbenzo[h]chromene Chemical compound C1=CC=2C(COC)=C(OC)C3=CC=CC=C3C=2OC1(C=1C=CC=CC=1)C1=CC=CC=C1 YRLGJEWILPSJPJ-UHFFFAOYSA-N 0.000 claims description 2
- OAICMCPFPDINEH-UHFFFAOYSA-N C1=CNOC2=C1C1=CC=CC=C1C=C2.N2CCC1=CC=C3C(=C21)C=CC=C3 Chemical compound C1=CNOC2=C1C1=CC=CC=C1C=C2.N2CCC1=CC=C3C(=C21)C=CC=C3 OAICMCPFPDINEH-UHFFFAOYSA-N 0.000 claims description 2
- VQAHQJWVBJCWJC-UHFFFAOYSA-N [6-methoxy-2,2-bis(4-methoxyphenyl)benzo[h]chromen-5-yl]methanol Chemical compound C1=CC(OC)=CC=C1C1(C=2C=CC(OC)=CC=2)C=CC(C(CO)=C(OC)C=2C3=CC=CC=2)=C3O1 VQAHQJWVBJCWJC-UHFFFAOYSA-N 0.000 claims description 2
- WLHDYJMURDFFPT-UHFFFAOYSA-N [6-methoxy-2,2-bis(4-methoxyphenyl)benzo[h]chromen-5-yl]methoxy-trimethylsilane Chemical compound C1=CC(OC)=CC=C1C1(C=2C=CC(OC)=CC=2)C=CC(C(CO[Si](C)(C)C)=C(OC)C=2C3=CC=CC=2)=C3O1 WLHDYJMURDFFPT-UHFFFAOYSA-N 0.000 claims description 2
- 125000002252 acyl group Chemical group 0.000 claims description 2
- 125000002490 anilino group Chemical class [H]N(*)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 claims description 2
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 claims description 2
- 125000002755 pyrazolinyl group Chemical group 0.000 claims description 2
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 claims 12
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims 4
- 125000000171 (C1-C6) haloalkyl group Chemical group 0.000 claims 3
- 125000006619 (C1-C6) dialkylamino group Chemical group 0.000 claims 2
- 125000006662 (C2-C4) acyloxy group Chemical group 0.000 claims 2
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims 2
- UEOGLANRPZAEAC-UHFFFAOYSA-N indeno-naphthopyran Chemical compound O1C=CC=C2C3=C4C=C(C=CC=C5)C5=C4C=CC3=CC=C21 UEOGLANRPZAEAC-UHFFFAOYSA-N 0.000 claims 2
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 claims 1
- ITHGKFNFXCDUDC-UHFFFAOYSA-N 2,3-dihydro-1h-benzo[g]indole;2h-pyrido[2,3-h][1,2]benzoxazine Chemical compound C1=CC=CC2=C(NCC3)C3=CC=C21.C1=CC2=NC=CC=C2C2=C1C=CNO2 ITHGKFNFXCDUDC-UHFFFAOYSA-N 0.000 claims 1
- RFPBBTGDNJHSRB-UHFFFAOYSA-N 2,3-dihydro-1h-indole;2h-pyrido[2,3-h][1,2]benzoxazine Chemical compound C1=CC=C2NCCC2=C1.C1=CC2=NC=CC=C2C2=C1C=CNO2 RFPBBTGDNJHSRB-UHFFFAOYSA-N 0.000 claims 1
- PAPKWSZJNIYRIA-UHFFFAOYSA-N 3,10b-dihydro-2h-benzo[h]chromene Chemical compound C1=CC2=CC=CC=C2C2C1=CCCO2 PAPKWSZJNIYRIA-UHFFFAOYSA-N 0.000 claims 1
- ITPCCQOGYMDBHK-UHFFFAOYSA-N 3h-benzo[f][1,2]benzoxazine;2,3-dihydro-1h-indole Chemical compound C1=CC=C2NCCC2=C1.C1=CC=CC2=C(C=CNO3)C3=CC=C21 ITPCCQOGYMDBHK-UHFFFAOYSA-N 0.000 claims 1
- QXXOQHRPPIEPBG-UHFFFAOYSA-N 3h-naphtho[1,2-h]chromene Chemical compound C1=CC2=CC=CC=C2C(C=C2)=C1C1=C2C=CCO1 QXXOQHRPPIEPBG-UHFFFAOYSA-N 0.000 claims 1
- PAMAFKWZBHMXIG-UHFFFAOYSA-N 5-(chloromethyl)-2-(2,3-dihydro-1-benzofuran-5-yl)-9-methoxy-2-(4-methoxyphenyl)-6-methylbenzo[h]chromene Chemical compound C1=CC(OC)=CC=C1C1(C=2C=C3CCOC3=CC=2)C=CC(C(CCl)=C(C)C=2C3=CC(OC)=CC=2)=C3O1 PAMAFKWZBHMXIG-UHFFFAOYSA-N 0.000 claims 1
- 239000004215 Carbon black (E152) Substances 0.000 claims 1
- 229930195733 hydrocarbon Natural products 0.000 claims 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims 1
- 238000006243 chemical reaction Methods 0.000 description 41
- 239000000047 product Substances 0.000 description 31
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 30
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 27
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 27
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 21
- 239000002904 solvent Substances 0.000 description 20
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 18
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 15
- 238000005481 NMR spectroscopy Methods 0.000 description 12
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 12
- 230000003287 optical effect Effects 0.000 description 12
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 12
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 11
- 238000000034 method Methods 0.000 description 10
- 239000003086 colorant Substances 0.000 description 9
- 150000004880 oxines Chemical class 0.000 description 9
- 125000004309 pyranyl group Chemical group O1C(C=CC=C1)* 0.000 description 9
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 9
- 238000001228 spectrum Methods 0.000 description 8
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 8
- 230000008859 change Effects 0.000 description 7
- 239000013078 crystal Substances 0.000 description 7
- 239000003973 paint Substances 0.000 description 7
- 230000000153 supplemental effect Effects 0.000 description 7
- KJCVRFUGPWSIIH-UHFFFAOYSA-N 1-naphthol Chemical compound C1=CC=C2C(O)=CC=CC2=C1 KJCVRFUGPWSIIH-UHFFFAOYSA-N 0.000 description 6
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 6
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 6
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 6
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 6
- 239000002585 base Substances 0.000 description 6
- 239000010410 layer Substances 0.000 description 6
- 230000007935 neutral effect Effects 0.000 description 6
- 239000003921 oil Substances 0.000 description 6
- 238000000967 suction filtration Methods 0.000 description 6
- 0 C(CC1C2)C2C*11C=C1 Chemical compound C(CC1C2)C2C*11C=C1 0.000 description 5
- 239000002253 acid Substances 0.000 description 5
- 150000001721 carbon Chemical group 0.000 description 5
- 230000000052 comparative effect Effects 0.000 description 5
- 239000003480 eluent Substances 0.000 description 5
- 238000005562 fading Methods 0.000 description 5
- 239000012280 lithium aluminium hydride Substances 0.000 description 5
- UHOVQNZJYSORNB-UHFFFAOYSA-N monobenzene Natural products C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 5
- 239000012044 organic layer Substances 0.000 description 5
- TVDSBUOJIPERQY-UHFFFAOYSA-N prop-2-yn-1-ol Chemical compound OCC#C TVDSBUOJIPERQY-UHFFFAOYSA-N 0.000 description 5
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 4
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 4
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 4
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 4
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 4
- WETWJCDKMRHUPV-UHFFFAOYSA-N acetyl chloride Chemical compound CC(Cl)=O WETWJCDKMRHUPV-UHFFFAOYSA-N 0.000 description 4
- 239000012346 acetyl chloride Substances 0.000 description 4
- 230000004913 activation Effects 0.000 description 4
- 150000001350 alkyl halides Chemical class 0.000 description 4
- 239000012965 benzophenone Substances 0.000 description 4
- 150000001562 benzopyrans Chemical class 0.000 description 4
- 239000011248 coating agent Substances 0.000 description 4
- 238000000576 coating method Methods 0.000 description 4
- 239000000975 dye Substances 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 4
- 239000011159 matrix material Substances 0.000 description 4
- 238000002844 melting Methods 0.000 description 4
- 230000008018 melting Effects 0.000 description 4
- 229920003023 plastic Polymers 0.000 description 4
- 239000004033 plastic Substances 0.000 description 4
- WGYKZJWCGVVSQN-UHFFFAOYSA-N propylamine Chemical compound CCCN WGYKZJWCGVVSQN-UHFFFAOYSA-N 0.000 description 4
- 239000011541 reaction mixture Substances 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 239000000741 silica gel Substances 0.000 description 4
- 229910002027 silica gel Inorganic materials 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- RFNDMLXNYMQMGN-UHFFFAOYSA-N 1,1-bis(4-methoxyphenyl)prop-2-yn-1-ol Chemical compound C1=CC(OC)=CC=C1C(O)(C#C)C1=CC=C(OC)C=C1 RFNDMLXNYMQMGN-UHFFFAOYSA-N 0.000 description 3
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 description 3
- VCDAWCBLCCVSKE-UHFFFAOYSA-N 2h-benzo[h]chromene Chemical compound C1=CC2=CC=CC=C2C2=C1C=CCO2 VCDAWCBLCCVSKE-UHFFFAOYSA-N 0.000 description 3
- QGJOPFRUJISHPQ-UHFFFAOYSA-N Carbon disulfide Chemical compound S=C=S QGJOPFRUJISHPQ-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N Vilsmeier-Haack reagent Natural products CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical compound CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 description 3
- AGEZXYOZHKGVCM-UHFFFAOYSA-N benzyl bromide Chemical compound BrCC1=CC=CC=C1 AGEZXYOZHKGVCM-UHFFFAOYSA-N 0.000 description 3
- IISBACLAFKSPIT-UHFFFAOYSA-N bisphenol A Chemical compound C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 description 3
- 150000008371 chromenes Chemical class 0.000 description 3
- 238000004040 coloring Methods 0.000 description 3
- 125000000623 heterocyclic group Chemical group 0.000 description 3
- 150000002576 ketones Chemical class 0.000 description 3
- SFDZETWZUCDYMD-UHFFFAOYSA-N monosodium acetylide Chemical compound [Na+].[C-]#C SFDZETWZUCDYMD-UHFFFAOYSA-N 0.000 description 3
- 239000002985 plastic film Substances 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- 239000003381 stabilizer Substances 0.000 description 3
- 238000012546 transfer Methods 0.000 description 3
- 238000009281 ultraviolet germicidal irradiation Methods 0.000 description 3
- CTRANZVACSOARI-UHFFFAOYSA-N (3-carbonochloridoyl-7-methoxy-4-methylnaphthalen-1-yl) acetate Chemical compound CC1=C(C(Cl)=O)C=C(OC(C)=O)C2=CC(OC)=CC=C21 CTRANZVACSOARI-UHFFFAOYSA-N 0.000 description 2
- XSQLBFRCPJPRAR-UHFFFAOYSA-N (4-hydroxy-6-methoxy-1-methylnaphthalen-2-yl)-piperidin-1-ylmethanone Chemical compound C1=C(O)C2=CC(OC)=CC=C2C(C)=C1C(=O)N1CCCCC1 XSQLBFRCPJPRAR-UHFFFAOYSA-N 0.000 description 2
- LBUJPTNKIBCYBY-UHFFFAOYSA-N 1,2,3,4-tetrahydroquinoline Chemical compound C1=CC=C2CCCNC2=C1 LBUJPTNKIBCYBY-UHFFFAOYSA-N 0.000 description 2
- VOJUXHHACRXLTD-UHFFFAOYSA-N 1,4-dihydroxy-2-naphthoic acid Chemical compound C1=CC=CC2=C(O)C(C(=O)O)=CC(O)=C21 VOJUXHHACRXLTD-UHFFFAOYSA-N 0.000 description 2
- WBIQQQGBSDOWNP-UHFFFAOYSA-N 2-dodecylbenzenesulfonic acid Chemical compound CCCCCCCCCCCCC1=CC=CC=C1S(O)(=O)=O WBIQQQGBSDOWNP-UHFFFAOYSA-N 0.000 description 2
- MCSXGCZMEPXKIW-UHFFFAOYSA-N 3-hydroxy-4-[(4-methyl-2-nitrophenyl)diazenyl]-N-(3-nitrophenyl)naphthalene-2-carboxamide Chemical compound Cc1ccc(N=Nc2c(O)c(cc3ccccc23)C(=O)Nc2cccc(c2)[N+]([O-])=O)c(c1)[N+]([O-])=O MCSXGCZMEPXKIW-UHFFFAOYSA-N 0.000 description 2
- UBQBZILVAOYAAE-UHFFFAOYSA-N 4-acetyloxy-6-methoxy-1-methylnaphthalene-2-carboxylic acid Chemical compound CC1=C(C(O)=O)C=C(OC(C)=O)C2=CC(OC)=CC=C21 UBQBZILVAOYAAE-UHFFFAOYSA-N 0.000 description 2
- FKKBOVSMMAPNPM-UHFFFAOYSA-N 4-hydroxy-6-methoxy-1-methylnaphthalene-2-carboxylic acid Chemical compound CC1=C(C(O)=O)C=C(O)C2=CC(OC)=CC=C21 FKKBOVSMMAPNPM-UHFFFAOYSA-N 0.000 description 2
- 125000004172 4-methoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C([H])C([H])=C1* 0.000 description 2
- KYNSBQPICQTCGU-UHFFFAOYSA-N Benzopyrane Chemical compound C1=CC=C2C=CCOC2=C1 KYNSBQPICQTCGU-UHFFFAOYSA-N 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- MUXOBHXGJLMRAB-UHFFFAOYSA-N Dimethyl succinate Chemical compound COC(=O)CCC(=O)OC MUXOBHXGJLMRAB-UHFFFAOYSA-N 0.000 description 2
- 238000005727 Friedel-Crafts reaction Methods 0.000 description 2
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 2
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 2
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 2
- MQENKENHAOIGLI-UHFFFAOYSA-N [7-methoxy-4-methyl-3-(piperidine-1-carbonyl)naphthalen-1-yl] acetate Chemical compound C1=C(OC(C)=O)C2=CC(OC)=CC=C2C(C)=C1C(=O)N1CCCCC1 MQENKENHAOIGLI-UHFFFAOYSA-N 0.000 description 2
- 239000006096 absorbing agent Substances 0.000 description 2
- 125000003668 acetyloxy group Chemical group [H]C([H])([H])C(=O)O[*] 0.000 description 2
- 150000001266 acyl halides Chemical class 0.000 description 2
- VSCWAEJMTAWNJL-UHFFFAOYSA-K aluminium trichloride Chemical compound Cl[Al](Cl)Cl VSCWAEJMTAWNJL-UHFFFAOYSA-K 0.000 description 2
- 125000003368 amide group Chemical group 0.000 description 2
- HUMNYLRZRPPJDN-UHFFFAOYSA-N benzaldehyde Chemical compound O=CC1=CC=CC=C1 HUMNYLRZRPPJDN-UHFFFAOYSA-N 0.000 description 2
- RWCCWEUUXYIKHB-UHFFFAOYSA-N benzophenone Chemical compound C=1C=CC=CC=1C(=O)C1=CC=CC=C1 RWCCWEUUXYIKHB-UHFFFAOYSA-N 0.000 description 2
- 150000008366 benzophenones Chemical class 0.000 description 2
- PASDCCFISLVPSO-UHFFFAOYSA-N benzoyl chloride Chemical class ClC(=O)C1=CC=CC=C1 PASDCCFISLVPSO-UHFFFAOYSA-N 0.000 description 2
- 230000005540 biological transmission Effects 0.000 description 2
- 230000003197 catalytic effect Effects 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 238000004042 decolorization Methods 0.000 description 2
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 2
- 229940060296 dodecylbenzenesulfonic acid Drugs 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 125000004356 hydroxy functional group Chemical group O* 0.000 description 2
- 238000005213 imbibition Methods 0.000 description 2
- 239000012442 inert solvent Substances 0.000 description 2
- 230000001678 irradiating effect Effects 0.000 description 2
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 2
- 235000019341 magnesium sulphate Nutrition 0.000 description 2
- CRMAPJSLKLVFBT-UHFFFAOYSA-N methyl 1,4-dihydroxynaphthalene-2-carboxylate Chemical compound C1=CC=CC2=C(O)C(C(=O)OC)=CC(O)=C21 CRMAPJSLKLVFBT-UHFFFAOYSA-N 0.000 description 2
- SSRKOKIFWFDSJJ-UHFFFAOYSA-N methyl 2,2-bis(4-methoxyphenyl)-6-phenylbenzo[h]chromene-5-carboxylate Chemical compound COC(=O)C1=C2C=CC(C=3C=CC(OC)=CC=3)(C=3C=CC(OC)=CC=3)OC2=C2C=CC=CC2=C1C1=CC=CC=C1 SSRKOKIFWFDSJJ-UHFFFAOYSA-N 0.000 description 2
- LODJLIXTQXVWGZ-UHFFFAOYSA-N methyl 4-acetyloxy-1-phenylnaphthalene-2-carboxylate Chemical compound COC(=O)C1=CC(OC(C)=O)=C2C=CC=CC2=C1C1=CC=CC=C1 LODJLIXTQXVWGZ-UHFFFAOYSA-N 0.000 description 2
- JAFZJAZARVCZPS-UHFFFAOYSA-N methyl 4-hydroxy-1-phenylnaphthalene-2-carboxylate Chemical compound COC(=O)C1=CC(O)=C2C=CC=CC2=C1C1=CC=CC=C1 JAFZJAZARVCZPS-UHFFFAOYSA-N 0.000 description 2
- HMNABSBBBWHDPT-UHFFFAOYSA-N methyl 4-hydroxy-6-methoxy-1-methylnaphthalene-2-carboxylate Chemical compound C1=C(OC)C=CC2=C(C)C(C(=O)OC)=CC(O)=C21 HMNABSBBBWHDPT-UHFFFAOYSA-N 0.000 description 2
- UMHCZDCIHMPSNS-UHFFFAOYSA-N methyl 9-methoxy-2,2-bis(4-methoxyphenyl)-6-methylbenzo[h]chromene-5-carboxylate Chemical compound C1=CC=2C(C(=O)OC)=C(C)C3=CC=C(OC)C=C3C=2OC1(C=1C=CC(OC)=CC=1)C1=CC=C(OC)C=C1 UMHCZDCIHMPSNS-UHFFFAOYSA-N 0.000 description 2
- 239000012299 nitrogen atmosphere Substances 0.000 description 2
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 2
- 229920006254 polymer film Polymers 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 239000011347 resin Substances 0.000 description 2
- 229920005989 resin Polymers 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 230000002441 reversible effect Effects 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 239000001632 sodium acetate Substances 0.000 description 2
- 235000017281 sodium acetate Nutrition 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- 239000012258 stirred mixture Substances 0.000 description 2
- 229910052715 tantalum Inorganic materials 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- 238000002834 transmittance Methods 0.000 description 2
- 239000012780 transparent material Substances 0.000 description 2
- WFKWXMTUELFFGS-UHFFFAOYSA-N tungsten Chemical compound [W] WFKWXMTUELFFGS-UHFFFAOYSA-N 0.000 description 2
- 229910052721 tungsten Inorganic materials 0.000 description 2
- 239000010937 tungsten Substances 0.000 description 2
- 229910052724 xenon Inorganic materials 0.000 description 2
- FHNFHKCVQCLJFQ-UHFFFAOYSA-N xenon atom Chemical compound [Xe] FHNFHKCVQCLJFQ-UHFFFAOYSA-N 0.000 description 2
- FMCAFXHLMUOIGG-IWFBPKFRSA-N (2s)-2-[[(2s)-2-[[(2s)-2-[[(2r)-2-formamido-3-sulfanylpropanoyl]amino]-3-methylbutanoyl]amino]-3-(4-hydroxy-2,5-dimethylphenyl)propanoyl]amino]-4-methylsulfanylbutanoic acid Chemical compound O=CN[C@@H](CS)C(=O)N[C@@H](C(C)C)C(=O)N[C@H](C(=O)N[C@@H](CCSC)C(O)=O)CC1=CC(C)=C(O)C=C1C FMCAFXHLMUOIGG-IWFBPKFRSA-N 0.000 description 1
- NUKYZORHZFFSCL-UHFFFAOYSA-N 1-(2,3-dihydro-1-benzofuran-5-yl)-1-(4-methoxyphenyl)prop-2-yn-1-ol Chemical compound C1=CC(OC)=CC=C1C(O)(C#C)C1=CC=C(OCC2)C2=C1 NUKYZORHZFFSCL-UHFFFAOYSA-N 0.000 description 1
- CYNYIHKIEHGYOZ-UHFFFAOYSA-N 1-bromopropane Chemical compound CCCBr CYNYIHKIEHGYOZ-UHFFFAOYSA-N 0.000 description 1
- SJJCQDRGABAVBB-UHFFFAOYSA-N 1-hydroxy-2-naphthoic acid Chemical compound C1=CC=CC2=C(O)C(C(=O)O)=CC=C21 SJJCQDRGABAVBB-UHFFFAOYSA-N 0.000 description 1
- SDJHPPZKZZWAKF-UHFFFAOYSA-N 2,3-dimethylbuta-1,3-diene Chemical group CC(=C)C(C)=C SDJHPPZKZZWAKF-UHFFFAOYSA-N 0.000 description 1
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical compound N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 1
- VPEYJONLDLPGCG-UHFFFAOYSA-N 2-(9-bicyclo[3.3.1]nonanylidene)-3-(2-bicyclo[3.2.1]octanylidene)bicyclo[4.3.2]undecane Chemical compound C1CC2CC1CCC2=C(C1=C2C3CCCC2CCC3)CCC2CCCC1CC2 VPEYJONLDLPGCG-UHFFFAOYSA-N 0.000 description 1
- SDTMFDGELKWGFT-UHFFFAOYSA-N 2-methylpropan-2-olate Chemical compound CC(C)(C)[O-] SDTMFDGELKWGFT-UHFFFAOYSA-N 0.000 description 1
- DJQWQMZLUOHZAC-UHFFFAOYSA-N 3-methoxycarbonyl-4,4-diphenylbut-3-enoic acid Chemical compound C=1C=CC=CC=1C(=C(CC(O)=O)C(=O)OC)C1=CC=CC=C1 DJQWQMZLUOHZAC-UHFFFAOYSA-N 0.000 description 1
- QEQVCPKISCKMOQ-UHFFFAOYSA-N 3h-benzo[f][1,2]benzoxazine Chemical group C1=CC=CC2=C(C=CNO3)C3=CC=C21 QEQVCPKISCKMOQ-UHFFFAOYSA-N 0.000 description 1
- ZLUYNTSDRUGERY-UHFFFAOYSA-N 3h-benzo[f]chromen-6-ol Chemical compound C12=CC=CC=C2C(O)=CC2=C1C=CCO2 ZLUYNTSDRUGERY-UHFFFAOYSA-N 0.000 description 1
- KWOLFJPFCHCOCG-UHFFFAOYSA-N Acetophenone Natural products CC(=O)C1=CC=CC=C1 KWOLFJPFCHCOCG-UHFFFAOYSA-N 0.000 description 1
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 1
- 229920002799 BoPET Polymers 0.000 description 1
- DQEFEBPAPFSJLV-UHFFFAOYSA-N Cellulose propionate Chemical compound CCC(=O)OCC1OC(OC(=O)CC)C(OC(=O)CC)C(OC(=O)CC)C1OC1C(OC(=O)CC)C(OC(=O)CC)C(OC(=O)CC)C(COC(=O)CC)O1 DQEFEBPAPFSJLV-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 1
- 238000005863 Friedel-Crafts acylation reaction Methods 0.000 description 1
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 1
- 229920004142 LEXAN™ Polymers 0.000 description 1
- 239000002841 Lewis acid Substances 0.000 description 1
- 239000004418 Lexan Substances 0.000 description 1
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 1
- 239000005041 Mylar™ Substances 0.000 description 1
- OZAIFHULBGXAKX-QXMHVHEDSA-N N(=N/C(C#N)(C)C)/C(C#N)(C)C Chemical compound N(=N/C(C#N)(C)C)/C(C#N)(C)C OZAIFHULBGXAKX-QXMHVHEDSA-N 0.000 description 1
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 1
- VEQPNABPJHWNSG-UHFFFAOYSA-N Nickel(2+) Chemical compound [Ni+2] VEQPNABPJHWNSG-UHFFFAOYSA-N 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- YGYAWVDWMABLBF-UHFFFAOYSA-N Phosgene Chemical compound ClC(Cl)=O YGYAWVDWMABLBF-UHFFFAOYSA-N 0.000 description 1
- 229920005372 Plexiglas® Polymers 0.000 description 1
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 1
- 229920007962 Styrene Methyl Methacrylate Polymers 0.000 description 1
- 229910021627 Tin(IV) chloride Inorganic materials 0.000 description 1
- 238000005299 abrasion Methods 0.000 description 1
- 150000001242 acetic acid derivatives Chemical class 0.000 description 1
- 150000008062 acetophenones Chemical class 0.000 description 1
- 125000004423 acyloxy group Chemical group 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 125000004849 alkoxymethyl group Chemical group 0.000 description 1
- 125000003282 alkyl amino group Chemical group 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 150000008365 aromatic ketones Chemical class 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- RFVHVYKVRGKLNK-UHFFFAOYSA-N bis(4-methoxyphenyl)methanone Chemical compound C1=CC(OC)=CC=C1C(=O)C1=CC=C(OC)C=C1 RFVHVYKVRGKLNK-UHFFFAOYSA-N 0.000 description 1
- 238000004061 bleaching Methods 0.000 description 1
- 239000007844 bleaching agent Substances 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 229920001727 cellulose butyrate Polymers 0.000 description 1
- 229920006218 cellulose propionate Polymers 0.000 description 1
- 125000004218 chloromethyl group Chemical group [H]C([H])(Cl)* 0.000 description 1
- IJOOHPMOJXWVHK-UHFFFAOYSA-N chlorotrimethylsilane Chemical compound C[Si](C)(C)Cl IJOOHPMOJXWVHK-UHFFFAOYSA-N 0.000 description 1
- ARUVKPQLZAKDPS-UHFFFAOYSA-L copper(II) sulfate Chemical compound [Cu+2].[O-][S+2]([O-])([O-])[O-] ARUVKPQLZAKDPS-UHFFFAOYSA-L 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 125000004386 diacrylate group Chemical group 0.000 description 1
- 125000004663 dialkyl amino group Chemical group 0.000 description 1
- 229910003460 diamond Inorganic materials 0.000 description 1
- 239000010432 diamond Substances 0.000 description 1
- 238000002845 discoloration Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 125000005677 ethinylene group Chemical group [*:2]C#C[*:1] 0.000 description 1
- ZKQFHRVKCYFVCN-UHFFFAOYSA-N ethoxyethane;hexane Chemical compound CCOCC.CCCCCC ZKQFHRVKCYFVCN-UHFFFAOYSA-N 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 150000002390 heteroarenes Chemical class 0.000 description 1
- 125000001072 heteroaryl group Chemical group 0.000 description 1
- UQEAIHBTYFGYIE-UHFFFAOYSA-N hexamethyldisiloxane Chemical compound C[Si](C)(C)O[Si](C)(C)C UQEAIHBTYFGYIE-UHFFFAOYSA-N 0.000 description 1
- 238000005286 illumination Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- HVTICUPFWKNHNG-UHFFFAOYSA-N iodoethane Chemical compound CCI HVTICUPFWKNHNG-UHFFFAOYSA-N 0.000 description 1
- 150000007517 lewis acids Chemical class 0.000 description 1
- 239000004611 light stabiliser Substances 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- ADFPJHOAARPYLP-UHFFFAOYSA-N methyl 2-methylprop-2-enoate;styrene Chemical compound COC(=O)C(C)=C.C=CC1=CC=CC=C1 ADFPJHOAARPYLP-UHFFFAOYSA-N 0.000 description 1
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- PVWOIHVRPOBWPI-UHFFFAOYSA-N n-propyl iodide Chemical compound CCCI PVWOIHVRPOBWPI-UHFFFAOYSA-N 0.000 description 1
- 150000004780 naphthols Chemical class 0.000 description 1
- 229910001453 nickel ion Inorganic materials 0.000 description 1
- 239000013110 organic ligand Substances 0.000 description 1
- 238000006053 organic reaction Methods 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- QNGNSVIICDLXHT-UHFFFAOYSA-N para-ethylbenzaldehyde Natural products CCC1=CC=C(C=O)C=C1 QNGNSVIICDLXHT-UHFFFAOYSA-N 0.000 description 1
- 235000011837 pasties Nutrition 0.000 description 1
- 238000001782 photodegradation Methods 0.000 description 1
- 125000000587 piperidin-1-yl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 229920006255 plastic film Polymers 0.000 description 1
- 229920002285 poly(styrene-co-acrylonitrile) Polymers 0.000 description 1
- 229920005668 polycarbonate resin Polymers 0.000 description 1
- 239000004431 polycarbonate resin Substances 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 125000006239 protecting group Chemical group 0.000 description 1
- 239000011253 protective coating Substances 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 239000013557 residual solvent Substances 0.000 description 1
- 230000025600 response to UV Effects 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 239000012312 sodium hydride Substances 0.000 description 1
- 229910000104 sodium hydride Inorganic materials 0.000 description 1
- 239000012265 solid product Substances 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000004753 textile Substances 0.000 description 1
- HPGGPRDJHPYFRM-UHFFFAOYSA-J tin(iv) chloride Chemical compound Cl[Sn](Cl)(Cl)Cl HPGGPRDJHPYFRM-UHFFFAOYSA-J 0.000 description 1
- ILWRPSCZWQJDMK-UHFFFAOYSA-N triethylazanium;chloride Chemical compound Cl.CCN(CC)CC ILWRPSCZWQJDMK-UHFFFAOYSA-N 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
Classifications
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B5/00—Optical elements other than lenses
- G02B5/20—Filters
- G02B5/22—Absorbing filters
- G02B5/23—Photochromic filters
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/78—Ring systems having three or more relevant rings
- C07D311/92—Naphthopyrans; Hydrogenated naphthopyrans
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/04—Oxygen-containing compounds
- C08K5/15—Heterocyclic compounds having oxygen in the ring
- C08K5/151—Heterocyclic compounds having oxygen in the ring having one oxygen atom in the ring
- C08K5/1545—Six-membered rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Physics & Mathematics (AREA)
- Optics & Photonics (AREA)
- Pyrane Compounds (AREA)
- Eyeglasses (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Optical Filters (AREA)
Description
本発明は、ある種の新規ナフトピラン化合物に関する。より詳しくは、本発明は、新規フォトクロミックナフトピラン化合物、ならびにそのような新規ナフトピラン化合物を含有する組成物および物品に関する。日光のまたは水銀ランプの光での紫外線照射のような、紫外線を含む光照射に暴露されると、多くのフォトクロミック化合物は可逆的な色の変化を示す。紫外線照射が中止されると、そのようなフォトクロミック化合物は、その元の色または無色状態に戻る。
種々のフォトクロミック化合物が合成され、日光によって誘発される可逆的な色の変化または暗色化が所望される用途への使用が提案されている。米国特許第3567605号公報(Becker)には、ある種のベンゾピラン類およびナフトピラン類を包含する一連のピラン誘導体を開示している。これらの化合物は、クロメンの誘導体として記載され、約−30℃以下の温度における紫外線照射で、例えば無色から黄色−オレンジ色に、変色することが開示されている。その化合物を可視光で照射することによって、または温度を約0℃よりも高い温度に上げたときに、着色状態から無色状態に戻ることが記載されている。
米国特許第5066818号公報には、種々の3,3−ジアリール−3H−ナフト[2,1−b]ピランが、眼または他の用途に対して、望ましいフォトクロミック特性(即ち、高着色性および許容できる退色)を有すると記載されている。前記米国特許第5066818号公報には、活性化後の退色に許容できない長い期間を必要とする異性2,2−ジアリール−2H−ナフト[1,2−b]ピランも比較例として開示されている。
米国特許第3627690号公報は、塩基または弱〜中程度の強度の酸のいずれかを少量含有するフォトクロミック2,2−2置換−2H−ナフト[1,2−b]ピラン組成物を開示している。ナフトピラン組成物への酸または塩基のいずれかの添加は、着色ナフトピランの退色速度を高め、それによって、サングラスのような眼を保護する用途に有益なものとなると記載している。同特許公報は、前記添加剤を含まない2H−ナフト−[1,2−b]ピランの退色速度が、完全に元の色に戻るまでに数時間〜多日数であることを、さらに開示している。米国特許第4818096号公報は、オルトまたはパラ位に窒素含有置換基を有するフェニル基を、ピラン環の酸素に対してα位に有している青色着色フォトクロミックベンゾ−またはナフトピランを開示している。
本発明は、高活性強度および高着色率に加えて、許容できる退色速度を有することが意外にも見出された、新規の置換された2H−ナフト[1,2−b]ピラン化合物に関する。特に、ナフトピラン化合物のナフト部位の5位におけるある種の置換基の使用は、酸または塩基を添加することなく、退色速度を高める。さらに、これらの化合物は、ピラン環の2位にある種の置換基を有する。ある種の置換基は、ナフトピランのナフト部位の第6、第7、第8、第9または第10炭素に存在していてよい。
発明の詳細な説明
近年、フォトクロミックプラスチック材料、特に光学的用途のためのプラスチック材料が大きな関心を集めている。特に、フォトクロミック眼用プラスチックレンズは、ガラスレンズと比べて重量的な利点を付与することから、研究がなされている。さらに、車および飛行機のような乗り物のためのフォトクロミック透明材料が、そのような透明材料によって付与される潜在的安全性によって、関心を集めている。
本発明によれば、許容される退色速度、高活性強度および高着色率を有するある種の新規な2H−ナフト[1,2−b]ピラン化合物を製造し得ることが見い出された。これらの化合物は、ピラン環の2位に、およびナフトピラン環のナフト部位の第5炭素に、ある種の置換基を有するナフトピラン類として記載され得る。ある種の置換基は、ナフトピラン環のナフト部位の第6、第7、第8、第9または第10炭素に存在していてもよい。これらの化合物は、下記の式で表され得る。
式Iにおいて、R1は、−CH2X基または−C(O)Y基であってよい〔式中、Xは、ハロゲン、ヒドロキシ、ベンゾイロキシ、C1〜C6アルコキシ基、C2〜C6アシルキシ基、アミノ基、C1〜C6モノアルキルアミノ基、C1〜C6ジアルキルアミノ基(すなわち、ジ(C1〜C6)アルキルアミノ基)、モルホリノ基、ピペリジノ基、1−インドリニル基、ピロリジル基、トリメチルシリロキシ基または−OCH(R11)Z基であってよく;Yは、−OCH(R11)Z基、であってよく;Zは、−CN、−C(O)R12または−COOR12であり;R11及びR12それぞれは、水素またはC1〜C6アルキルであってよく;およびハロゲンはクロロまたはフルオロであってよい。〕。
好ましくは、R1は、−CH2X基または−C(O)Y基である〔式中、Xは、水素、C1〜C4アルコキシまたはC2〜C4アシロキシであり、Yは、−OCH(R11)Z基(ただし、Zは、−CN、−C(O)R12または−COOR12であり、R11及びR12それぞれは、水素またはC1〜C4アルキルである。)〕。
より好ましくは、R1は、−CH2X基〔式中、Xは、水素、C1〜C4アルコキシまたはC2〜C4アシロキシである。〕。最も好ましくは、R1は、ヒドロキシメチルまたはアセトキシメチルである。
上記式I中、R2およびR3はそれぞれ、水素、C1〜C6アルキル基、C3〜C7シクロアルキル基、未置換、モノ−、2−または3−置換フェニル基、−OR6基[式中、R6は、水素、(C1〜C6)アルキル、フェニル(C1〜C3)アルキル、モノ置換フェニル(C1〜C3)アルキル、(C1〜C6)アルコキシ(C2〜C4)アルキル、C3〜C7シクロアルキル、モノ(C1〜C4)アルキル置換されたC3〜C7シクロアルキル、C1〜C6ハロアルキル、アリル、−CH(R7)W基〔式中、Wは、−CN、−CF3、ハロゲン、−C(O)R7または−COOR7であってよい(ただし、R7は、水素、C1〜C6アルキルまたは(C1〜C6)アルコキシ(C2〜C4)アルキルであってよい。)。〕であってよく;または、R6は、−C(O)T基(式中、Tは、水素、C1〜C6アルキル、C1〜C6アルコキシ、置換または未置換のアリール基:フェニルまたはナフチル、フェノキシ、C1〜C6モノ−またはジ−アルキル置換されたフェノキシ、C1〜C6モノ−またはジ−アルコキシ置換されたフェノキシ、C1〜C6モノ−またはジ−アルコキシ置換されたフェニルアミノであってよく、前記フェニルまたはナフチルの置換基はそれぞれ、C1〜C6アルキル、C1〜C6アルコキシまたはハロゲンであり、ハロゲンまたはハロ置換基はそれぞれ、クロロまたはフルオロである。]であってよく、およびnは、0、1、2および3の整数から選ばれる。
好ましくは、R2およびR3はそれぞれ、水素、C1〜C4アルキル基、未置換、モノ−、2−または3−置換フェニル基、−OR6基であり[式中、R6は、C1〜C4アルキルまたは−CH(R7)W基である〔式中、Wは、−COOR7である(ただし、R7は、水素、C1〜C4アルキルである。)。〕。]、前記フェニルの置換基は、C1〜C4アルキル、C1〜C4アルコキシまたはフルオロであり、およびnは、0、1および2の整数から選ばれる。
より好ましくは、R2およびR3はそれぞれ、水素、C1〜C2アルキル基、未置換、モノ−、2−または3−置換フェニル基、−OR6基であり[式中、R6は、C1〜C2アルキルまたは−CH(R7)W基である〔ただし、Wは、−COOR7である(式中、R7は、水素、C1〜C4アルキルである。)。〕。]、前記フェニルの置換基は、C1〜C2アルキル、C1〜C2アルコキシまたはフルオロであり、およびnは、0、1および2の整数から選ばれる。最も好ましくは、R2およびR3はそれぞれ、水素、フェニル、メトキシ、メチルまたはフルオロである。
上記式I中、BおよびB'はそれぞれ、
(i)未置換、モノ−、2−および3−置換のアリール基フェニルおよびナフチル;
(ii)未置換、モノ−および2−置換の複素環系芳香族基:ピリジル、フラニル、ベンゾフラン−2−イル、ベンゾフラン−3−イル、チエニル、ベンゾチエン−2−イル、ベンゾチエン−3−イル、ジベンゾチエニル、ジベンゾフラニルおよびカルバゾリル[ただし、アリールおよび複素環の置換基は、ヒドロキシ、アミノ、C1〜C6モノアルキルアミノ、C1〜C6ジアルキルアミノ、モルホリノ、ピペリジノ、1−インドリニル、ピロリジル、1−イミダゾリジル、2−イミダゾリン−1−イル、2−ピラゾリジル、ピラゾリニル、1−ピペラジニル、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6アルコキシ、モノ(C1〜C6)アルコキシ(C1〜C4)アルキル、アクリロキシ、メタクリロキシおよびハロゲンからなる群より選ばれる(ただし、ハロゲンまたは(ハロ)基は、フルオロまたはクロロであってよい。)];
(iii)以下の式II AおよびII B:
[式中、Dは、炭素または酸素であってよく、およびEは、酸素または置換された窒素であってよく(ただし、Eが置換された窒素であるとき、Dは炭素である。)、前記窒素の置換基は、水素、C1〜C6アルキル、およびC2〜C6アシルからなる群より選ばれ、R8はそれぞれ、C1〜C6アルキル、C1〜C6アルコキシ、ヒドロキシまたはハロゲンからなる群より選ばれ(ただし、ハロゲンは、クロロまたはフルオロであってよい。)、R9およびR10はそれぞれ、水素またはC1〜C6アルキルであってよく、およびmは、0、1または2整数であってよい。]
で表される基;
(iv)C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6アルコキシ(C1〜C4)アルキル、C3〜C6シクロアルキル、モノ(C1〜C6)アルコキシ(C3〜C6)シクロアルキル、モノ(C1〜C6)アルキル(C3〜C6)シクロアルキルおよびハロ(C3〜C6)シクロアルキル(ただし、前記ハロ基は、フルオロまたはクロロである。)
;および
(v)下記式II C:
[式中、Uは、水素またはC1〜C4アルキルであってよく、Vは、ナフチル、フェニル、フラニルおよびチエニルからなる群の未置換、モノ−および2−置換基から選ばれてよい(ただし、前記基の各群における置換基は、C1〜C4アルキル、C1〜C4アルコキシ、フルオロまたはクロロである)。]
で表される基;あるいは
(vi)BおよびB'を合わせて、未置換、モノ−または2−置換のフルオレン−9−イリデンを形成するか、あるいは飽和C3〜C12スピロ−単環炭化水素環(例えば、シクロプロピリデン、シクロブチリデン、シクロペンチリデン、シクロヘキシリデン、シクロヘプチリデン、シクロオクチリデン、シクロノニリデン、シクロデシリデン、シクロウンデシリデン、シクロドデシリデン)、飽和C7〜C12スピロ−二環炭化水素環(例えば、ビシクロ[2.2.1]ヘプチリデン、すなわちノルボニリデン、1,7,7−トリメチルビシクロ[2.2.1]ヘプチリデン、すなわち、ボニリデン、ビシクロ[3.2.1]オクチリデン、ビシクロ[3.3.1]ノナン−9−イリデン、ビシクロ[4.3.2]ウンデカン)および飽和C7〜C12スピロ−三環炭化水素環(例えば、トリシクロ[2.2.1.02,6]ヘプチリデン、トリシクロ[5.3.1.12,6]ドデシリデンおよびトリシクロ[3.3.1.13,7]デシリデン、すなわち、アダマンチリデン)からなる群より選ばれる基を形成してもよく、前記フロオレン−9−イリデン置換基が、C1−C4アルキル、C1−C4アルコキシ、フルオロおよびクロロから成る群から選択され得るもの
からなる群より選ばれてよい。
好ましくは、BおよびB'はそれぞれ、
(i)未置換、モノ−、2−および3−置換のフェニル;
(ii)未置換、モノ−および2−置換の複素環系芳香族基:ピリジル、フラニル、ベンゾフラン−2−イル、ベンゾフラン−3−イル、チエニル、ベンゾチエン−2−イル、ベンゾチエン−3−イル、ジベンゾチエニル、ジベンゾフラニルおよびカルバゾリルであって、前記フェニルおよび複素環の置換基がそれぞれ、モルホリノ、ピペリジノ、C1〜C4アルキル、C1〜C4アルコキシおよびハロゲン
からなる群より選ばれ、前記ハロゲンまたは(ハロ)基が、フルオロまたはクロロであるもの;
(iii)上記式II A[式中、Dは、炭素であり、およびEは酸素であり;R8はそれぞれ、C1〜C4アルキル、C1〜C4アルコキシ、ヒドロキシまたはハロゲンであり、前記ハロゲンは、クロロまたはフルオロであり;R9およびR10はそれぞれ、水素またはC1〜C4アルキルであり;およびmは、0、1または2の整数である。]で表される基;
(iv)C1〜C4アルキル、C1〜C6アルコキシ(C1〜C4)アルキルおよびC3〜C6シクロアルキル;および
(v)上記式II C[式中、Uは、水素またはメチルであり、およびVはフェニルまたはモノ−置換フェニルであり、前記フェニルの置換基は、C1〜C4アルキル、C1〜C4アルコキシまたはフルオロである。]で表される基;または
(vi)BおよびB'を合わせて、未置換またはモノ−置換のフルオレン−9−イリデン、あるいは飽和C3〜C6スピロ−単環炭化水素環、飽和C7〜C10スピロ−二環炭化水素環および飽和C7〜C10スピロ−三環炭化水素環からなる群より選ばれる基を形成するもの
からなる群より選ばれる。
より好ましくは、BおよびB'はそれぞれ、(i)未置換、モノ−および2−置換のフェニル;(ii)未置換、モノ−および2−置換の複素環芳香族基ピリジル、ベンゾフラン−2−イル、ベンゾチエン−2−イル、ジベンゾチエニルおよびジベンゾフラニルであって、前記フェニルおよび複素環の置換基はそれぞれ、モルホリノ、ピペリジノ、C1〜C2アルキルおよびC1〜C2アルコキシからなる群より選ばれるもの;および(iii)上記式II A[式中、Dは、炭素であり、およびEは、酸素でありR8はそれぞれ、C1〜C2アルキル、C1〜C2アルコキシまたはフルオロであり;R9およびR10はそれぞれ、水素またはC1〜C2アルキルであり;およびmは、0、1または2の整数である。]で表される基;または
(iv)BおよびB'を合わせて、フルオレン−9−イリデン、ボニリデン、ノルボルニリデン、ビシクロ[3.3.1]ノナン−9−イリデンまたはアダマンチリデンを形成するもの
からなる群より選ばれる。最も好ましくは、BおよびB'はそれぞれ、フェニル、メトキシ置換されたフェニル、モルホリノ置換されたフェニル、ジベンゾフラン−2−イルまたは2,3−ジヒドロベンゾフラン−5−イルである。
上記式Iで表される化合物は、以下の工程により調製されてよい。式VおよびV Aで表されるベンゾフェノン類は、式IVで表される適切に置換されたまたは未置換の塩化ベンゾイル、および式IIIで表される市販の置換または未置換のベンゼン化合物を用いて、フリーデル−クラフツ法によって生成または調製される。出版物Friedel−Crafts and Related Reactions,George A.Olah著、Interscience Publishers、1964年第3巻第XXXI章(芳香族ケトンの合成)、およびIshihara、Yugiら著、J.Chem.Soc.、「Regioselective Friedel−Crafts Acylation of 1,2,3,4−Tetrahydroquinoline and Related Nitrogen Heterocycles:Effect on NH Protective Groups and Ring Size」、Perkin Trans.1、第3401〜3406頁、1992年を参照。
下記の式IIIおよびIVで表される化合物を、二硫化炭素または塩化メチレンのような溶媒に溶解し、塩化アルミニウムまたは四塩化スズのようなルイス酸の存在下において反応させて、式V(または反応B中のV A)で表される、対応する置換ベンゾフェノンを生成する。RおよびR'は、元々保有するフェニル置換基を表す。
反応Bでは、式V A(式中、BおよびB'は、置換または未置換のフェニル以外の基を表し得る。)で表される置換または未置換のケトンを、無水テトラヒドロフラン(THF)のような好適な溶媒中でナトリウムアセチリドと反応させて、式IVで表される、対応のプロパルギルアルコールを生成する。置換および未置換フェニル以外のBまたはB'基を有するプロパルギルアルコールは、市販のケトン類から生成されても、例えば、置換または未置換のベンゼン、ナフタレンまたはヘテロ芳香族化合物とハロゲン化アシルとの反応を介して調製されるケトン類から生成されてよい。上記II Cで表されるBまたはB'基を有するプロパルギルアルコールは、米国特許第5274231号公報、第2列、第40〜68行に記載の方法によって調製され得る。
構造式Iで表されるナフトピランの製造に用いる構造式VIIおよびXIIIで表されるナフトールは反応CまたはDに記載のようにして調製してもよい。反応Cにおいては、構造式VIIで表される1,4−ジヒドロキシ−2−ナフトエ酸を、無水ジメチルホルムアミド(DMF)のような適当な溶剤中において、エチルジイソプロピルアミンの存在下でヨウ化メチルのようなハロゲン化アルキルと反応させることによって構造式VIIIで表される対応するメチル−1,4−ジヒドロキシ−2−ナフトエートを生成させる。この反応は次の文献に記載されている:The Journal of Organic Chemistry,第46巻、第17号、第3477頁(1981年)。
反応Dにおいては、構造式IXで表される置換もしくは非置換のアセトフェノン、ベンゾフェノンまたはベンズアルデヒドを、トルエンやTHFのような適当な溶剤中において、水素化ナトリウムやカリウムt−ブトキシドのような塩基の存在下でジメチルスクシネート(構造式X)と反応させることによって構造式XIで表されるα−アリルデンコハク酸の適当に置換されたモノエステルを生成させる。化合物XIを無水酢酸と無水酢酸ナトリウムと共に加熱することによって構造式XIIで表される対応するアセテート誘導体が得られる。化合物XIIを塩酸と無水アルコール(例えば、無水メタノール)と反応させることによって構造式XIIIで表される対応するナフトールが得られる。反応Dは次のテキストに記載されている:Organic Reactions,第VI巻、第1章、第1頁〜第73頁[ジョン・ウィリー・アンド・サンズ社(ニューヨーク)発行]。
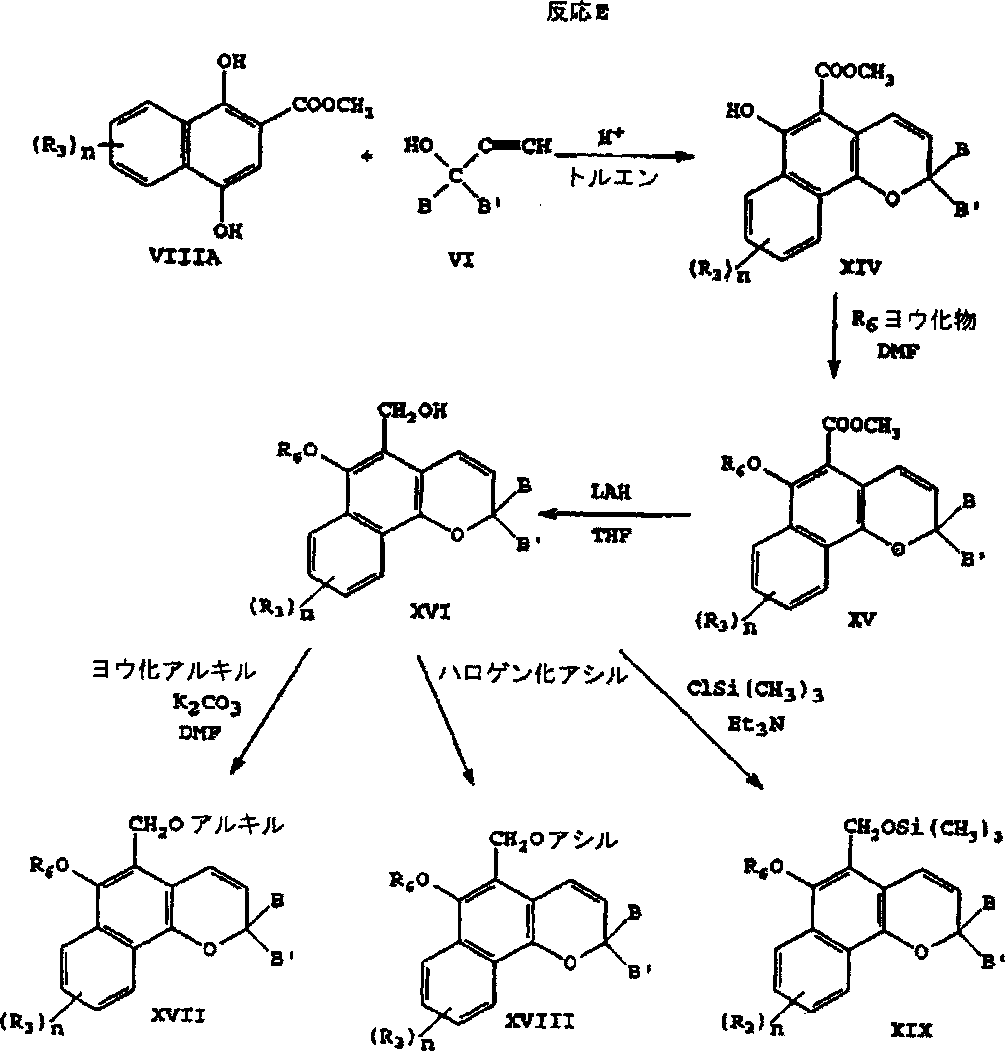
反応Eにおいては、構造式VIで表されるプロパルギルアルコールを構造式VIII Aで表されるナフトール[式VIIIで表される化合物が(R3)nによってさらに置換された化合物]とカップリングさせることによって構造式XIVで表される6−ヒドロキシナフトピランを生成させる。構造式XIVで表される化合物の6−ヒドロキシ置換基をハロゲン化アルキル(例えば、ヨウ化メチル、ヨウ化エチル、臭化ベンジル等)との反応によって、例えば、6−アルコキシ基に変換させることによって構造式XVで表される化合物を生成させてもよい。構造式XVで表される化合物はTHFのような不活性溶剤中において、例えば水素化アルミニウムリチウムを用いて還元させることによって構造式XVIで表される5−ヒドロキシメチル置換化合物を得てもよい。構造式XVIで表される化合物の5−ヒドロキシメチル置換基は種々の方法によって修飾してもよい。該置換基は、構造式XVIで表される化合物を炭酸カリウムのような塩基の存在下においてハロゲン化アルキル(例えばヨウ化メチル、臭化n−プロピル、臭化ベンジル等)と反応させてアルコキシメチルに変換することができ、これによって構造式XVIIで表される化合物が得られる。あるいは、該ヒドロキシメチル基をハロゲン化アシル(例えば、塩化アセチル、塩化ベンゾイル等)を用いてアシル化することによって構造式XVIIIで表される化合物を調製することができる。第3の例においては、該ヒドロキシメチル基を酸受容体(例えば、トリエチルアミン)の存在下においてトリメチルシリルクロリドと反応させることによって構造式XIXで表されるトリメチルシリルエーテルを調製してもよい。
反応Fにおいては、構造式VIで表されるプロパルギルアルコールを構造式XIIIで表されるナフトールとカップリングさせることによって6−位にアリール基、アルキル基または水素原子を有する構造式XXで表されるナフトピラン化合物を生成させる。構造式XXで表される化合物をTHFのような不活性溶剤中において例えば水素化アルミニウムリチウム(LAH)を用いて還元することによって構造式XXIで表される5−ヒドロキシメチル化合物を得てもよい。構造式XXIで表される化合物の5−ヒドロキシメチル置換基は種々の方法によって修飾してもよい。該置換基は構造式XXIで表される化合物と塩化チオニルとの反応によってクロロメチル基に変換させることができ、これによって構造式XXIIで表される化合物が得られる。構造式XXIIで表される化合物の5−クロロメチル基は当該分野において既知の反応、例えば第一アミン、第二アミンまたはヘテロ環状アミン(例えばプロピルアミン、ジエチルアミン、モルホリン等)との反応によってさらに修飾することができ、これによって構造式XXIIIで表される5−アミノメチル化合物が得られる。あるいは、構造式XXIで表される化合物のヒドロキシメチル基をハロゲン化アルキル(例えばヨウ化メチル、ヨウ化プロピル、臭化ベンジル等)と反応させることによって構造式XXIVで表される化合物を得ることができる。
5−位置に置換されたアミド基を有する化合物を反応Gに示した一連の反応により調製した。水およびアルコールの混合物中に溶解した水酸化カリウムを用いて、化学式XIIIにより表されるナフトールを式XXIにより表されるカルボキシナフトールに加水分解する。式XXIの化合物の遊離ヒドロキシ置換基は、塩化アセチルとの反応により保護されて、化学式XXVIのアセトキシ置換化合物を得る。式XXVIの化合物のカルボキシ置換基は、塩化チオニルとの反応により酸塩化物に変換されて、化学式XXVIIの化合物を得る。式XXVIIの化合物の酸塩化物は、第一、第二または複素環式アミン、例えばプロピルアミン、ジエチルアミン、モルホリン、ピペリジン等との反応によりアミド基に変換されて、化学式XXVIIIの化合物を得る。化学式XXVIIIの化合物のアセトキシ基はHCl存在下でメタノールとの反応により脱保護(deprotect)されて、化学式XXIXのナフトールを得る。化学式XXXにより表される5−アミド基を含有するピランは、化学式XXIXのナフトールを化学式VIのプロパギルアルコールと反応させることにより調製される。
化学式Iで示される化合物は、光学レンズ、例えば、視力修正眼用レンズおよび平面レンズ、フェースシールド(face shields)、ゴーグル、まびさし(visors)、カメラレンズ、窓、自動車のフロントガラス、航空機および自動車の透明物、例えば、Tルーフ、サイドライトおよびバックライト、プラスチックフィルムおよびシート、織物および塗料、例えば、ペイントのような塗料組成物、ならびに、真正の認証または証明が所望される銀行券、パスポートおよび自動車免許証のような保証書類上の証明マークのような、有機フォトクロミック物質が使用される用途に使用することができる。化学式Iで示されるナフトピランは、無色から黄色〜赤色/紫色の範囲の着色という色の変化を示す。
本発明の範囲に含まれるナフトピラン化合物の例は下記のものである:
(a)2,2−ビス−(4−メトキシフェニル)−5−ヒドロキシメチル−6−メチル−9−メトキシ−2H−ナフト[1,2−b]ピラン;
(b)2,2−ビス(4−メトキシフェニル)−5−ヒドロキシメチル−6−フェニル−2H−ナフト[1,2−b]ピラン;
(c)2,2−ビス(4−メトキシフェニル)−5−アセトキシメチル−6−フェニル−2H−ナフト[1,2−b]ピラン;
(D)2,2−ビス−(4−メトキシフェニル)−5−ヒドロキシメチル−6−メトキシ−2H−ナフト[1,2−b]ピラン;
(E)2,2−ジフェニル−5−メトキシメチル−6−メトキシ−2H−ナフト[1,2−b]ピラン;
(F)2,2−スピロアダマンチレン−5−アセトキシメチル−6−メトキシ−2H−ナフト[1,2−b]ピラン;
(G)2,2−ビス−(4−メトキシフェニル)−5−トリメチルシリルオキシメチル−6−メトキシ−2H−ナフト[1,2−b]ピラン;
(H)2−(4−メトキシフェニル)−2−t−ブチル−5−メトキシメチル−6−フェニル−9−メトキシ−2H−ナフト[1,2−b]ピラン;および
(I)2−(4−メトキシフェニル)−2−(2,3−ジヒドロベンゾフラン−5−イル)−5−クロロメチル−6−メチル−9−メトキシ−2H−ナフト[1,2−b]ピラン;
(2,3−ジヒドロベンゾフラン−5−イル)−5−ピペリジノカルボニル−6−メチル−9−メトキシ−2H−ナフト[1,2−b]ピラン。
本発明の化学式Iの有機フォトクロミックナフトピランは、適当な補足的有機フォトクロミック物質と組み合わせて使用することができ、そのようなフォトクロミック物質を含有するプラスチックレンズを紫外線に暴露した時に、それらは共に灰色中間色または褐色中間色に近いシェードを生じる。例えば、黄色に着色する化合物を適当な紫色に着色する化合物と混合して、褐色のシェードを生じさせてもよい。同様に、着色状態でオレンジ色である化合物は、適当な青色着色化合物と共に用いたときに灰色のシェードを生じる。前述のフォトクロミック物質の組合せを、眼用レンズ以外の用途に用いてもよい。
本発明の新規ナフトピラン化合物は、前述のように単独で使用することもでき、また補足的有機フォトクロミック物質、即ち、約400〜700nmの範囲内の少なくとも1つの活性吸収極大を有する有機フォトクロミック化合物、またはそれを含有する物質との組み合わせで使用することもでき、フォトクロミック物品を製造するのに使用され、活性化したときに適切な色に着色するポリマー有機ホスト材料中に、組み込む、例えば溶解または分散させることもできる。
本発明の有機フォトクロミックナフトピランに用いることのできる補足的有機フォトクロミック物質の第1グループは、570nmを超える可視領域内、例えば約570を超え700nmまでに活性吸収極大を有するものである。これらの物質は、適当な溶媒またはマトリックス中で紫外線に暴露した時に、通常、青色、青味をおびた緑色、または青味をおびた紫色を呈する。そのような化合物の多くは、刊行物に記載されている。例えば、スピロ(インドリン)ナフトオキサジンが特に米国特許第3,562,172号、同3,578,602号、同4,215,010号および、同3,342,668号に開示されており;分子中のナフトオキサジン部分の8'および9'の位置にある置換基を有するスピロ(インドリン)ナフトオキサジンが米国特許第5,405,958号開示されており;スピロ(インドリン)ピリドベンズオキサジンが米国特許第4,637,698号に開示されており;スピロ(ベンゼインドリン)ピリドベンズオキサジンおよびスピロ(ベンズインドリン)ナフトオキサジンが米国特許第4,931,219号に開示されており;スピロ(ベンズインドリン)ナフトピランが日本国特許公開第62/195383号に開示されており;スピロ(インドリン)ベンズオキサジンが米国特許第4,816,584号に開示されており;スピロ(インドリン)ベンゾピラン、スピロ(インドリン)ナフトピランおよびスピロ(インドリン)キノピランが例えば米国特許第4,880,667号に開示されており;ピラン環の2−位置に窒素含有置換基を有するベンゾピランおよびナフトピランが米国特許第4,818,096号に開示されている。スピロ(インドリン)ピランは、グレン(Glenn)H.ブラウン(Brown)のテクニクス・イン・ケミストリー(Techniques in Chemistry)、第III巻、「フォトクロミズム(Photochromism)」、第3章、1971年、ニューヨークのジョン・ウィレイ・アンド・サンズ社(John Wiley and Sons Inc.)発行にも開示されている。
本発明の有機フォトクロミックナフトピランに用いることのできる補足的有機フォトクロミック物質の第2グループは、約400から500nm未満の可視領域内に吸収極大を有するものである。これらの物質は、適当な溶媒またはマトリックス中で紫外線に暴露した時に、通常、橙黄色(yellow−orange)を呈する。そのような化合物には、いくつかのクロメン、即ち、ベンゾピランおよびナフトピランを含む。そのようなクロメンの多くは、刊行物、例えば米国特許第3,567,605号、同4,826,977号および同5,066,818号に記載されている。本発明の上記ナフトピランに用いることのできる補足的ベンゾピランおよびナフトピランの他の例には、米国特許第4,826,977号に開示のピラン環の酸素原子に対するα位置にスピロアダマンタン基を有するもの;1993年12月9日出願の同時係属米国特許出願第08/164,187号の主題である、ナフトピランのナフト部分の5および6位置の炭素原子に、およびピランの2位置に、ある置換基を有する2H−ナフト[2,1−b]ピラン化合物;米国特許第5,066,818号に開示のピラン環の3位置に少なくとも1つのオルソ−置換したフェニル置換基を有する3H−ナフト[2,1−b]ピラン;1993年6月21日出願の同時係属米国特許出願第08/080,246号の主題である、8位置の炭素原子にある置換基を、および7または9位置の炭素原子にある置換基を有し、全ての置換基がナフトピランのナフト部分にある3H−ナフト[2,1−b]ピラン化合物;米国特許第5,384,077号に開示のピラン環の3位置を(i)アリール置換基および(ii)フェニル置換基の3および4位置の炭素原子で縮合した5員または6員複素環を有するフェニル置換基で置換された3H−ナフト[2,1−b]ピラン;1994年4月8日出願の同時係属米国特許出願第08/225,022号の主題である、ナフトピランのg、i、またはl位置(side)に対して縮合された置換または非置換の5員または6員複素環を有するジアリル−3H−ナフト[2,1−b]ピラン化合物;米国特許第5,238,931号の主題である、ナフトピランのナフト部分の8位置の炭素原子において、例えばメトキシ基で置換したナフトピラン化合物;米国特許第5,274,132号に開示の、その例が3−アリール−3−アリールアルケニルナフトピランであるナフトピラン化合物;および、米国特許第5,244,602号の主題である5位置の炭素原子において、例えばアセトキシ基で置換されたナフト[2,1−b]ピラン;を含む。
本発明の有機フォトクロミックナフトピランに用いることのできる補足的有機フォトクロミック物質の第3グループは、約400から約500nmの可視領域内に吸収極大および約400から約700nmの可視領域内に別の吸収極大を有するものである。これらの物質は、適当な溶媒またはマトリックス中で紫外線に暴露した時に、通常、黄色から紫色および黄色/褐色から紫色/灰色の範囲の色を呈する。これらの化合物の例には、いくつかの置換2H−フェナントロ[4,3−b]ピラン;置換3H−フェナントロ[1,2−b]ピラン;およびベンゾピラン化合物、例えばピラン環の2−位置で置換されたもの、および置換または非置換複素環式環、例えばベンゾピランのベンズ部分に対して縮合したベンゾチエノまたはベンゾフラノ環が挙げられる。後者の化合物は、1994年8月4日出願の同時係属米国特許出願第08/286,039号および米国特許第5,411,679号の主題である。
本発明のフォトクロミック物品は、要すれば、1種のフォトクロミック化合物またはフォトクロミック化合物の混合物を含有してもよい。個々のフォトクロミック化合物またはフォトクロミック化合物の混合物は、いくつかの活性化した色、例えば中間灰色または褐色を達成するのに用いてもよい。
本発明の化合物(以下第2グループのフォトクロミック化合物と呼び、第2グループのフォトクロミック化合物として含まれる)は、本明細書中に記載されたフォトクロミック化合物の第1の補足的グループの有機フォトクロミック物質、例えば青色、青味をおびた緑色または青味をおびた紫色に着色するもの、または前述のフォトクロミック化合物の第2グループ中の他の有機フォトクロミック物質と組合せて用いてもよい。フォトクロミック化合物またはそれらの混合物の第1および第2グループのいずれの構成要素を、黄色から紫色および黄色/褐色から紫色/灰色の範囲の色を呈する本明細書中に記載の第3グループと組合せてもよく、共に用いてもよい。
本明細書中に記載されている各フォトクロミック物質は、フォトクロミック化合物または化合物の混合物が被覆または組み込まれている有機ホスト材料が、結果として生ずる所望の色、例えば、未フィルターの日光で活性化されたときに実質的中間色(neutral colour)を示す、即ち、活性化されたフォトクロミック化合物の色が可能な限り中間色に近い色を示すような量(または比率)で使用される。
中間灰色は、400〜700ナノメートルの可視範囲において、比較的等しい吸収を有するスペクトルを示す。中間褐色は、400〜550ナノメートルの範囲における吸収が、550〜700ナノメートルの範囲におけるよりも適度に大きいスペクトルを示す。色を記載する別の方法は色度座標によるものであり、これは、輝度要素に加えた色の質、即ち色度、を記載するものである。CIEシステムにおいては、三刺激値のそれらの合計に対する比、例えばx=X/(X+Y+Z)およびy=Y/(X+Y+Z)を求めることによって、色度座標が得られる。CIEシステムで記載される色を色度グラフにプロットすることができ、通常、色度座標xおよびyのプロットである。F.W.Billmeyer,Jr.,およびMax SaltzmanによるPrinciples of Color Technology,Second Edition,John Wiley and Sons,N.Y.(1981)のp.47−52を参照。本明細書で使用されている中間色に近い色とは、色の「x」および「y」の色度座標値が下記範囲内(D65発光体)である色を意味する:太陽輻射(気団1または2)への暴露により40%の視感透過に活性化後、x=0.260〜0.400、y=0.280〜0.400。
ホスト材料に被覆または組み込まれる、フォトクロミック物質またはそれを含有する組成物の量は、活性時に裸眼で識別できるフォトクロミック効果を生じるのに充分な量が使用されることを条件として、限定されない。一般に、そのような量を、フォトクロミック量として記載することができる。特定の使用量は、フォトクロミック物質の照射時に所望される色の強度、およびそのフォトクロミック物質を組み込む、または被覆するのに使用される方法に依存する場合が多い。一般に、より多くのフォトクロミック物質が適用または組み込まれるほど、ある限界までの色の強度がより高くなる。
使用される前記フォトクロミック化合物の相対量は、そのような化合物の活性種の色の相対強度、および所望される最終の色によって、部分的に変化および依存する。一般に、フォトクロミック光学ホスト材料に組み込みまたは被覆される全フォトクロミック物質の量は、フォトクロミック物質が組み込みまたは被覆される表面1平方センチメートルにつき約0.05〜約1.0、例えば、0.1〜約0.45ミリグラムである。前述の有機フォトクロミック補足的グループの混合物を用いる場合、そのような物質の重量比、即ち、(第1:第2)(第2:第3)および(本発明のナフトピラン:他の第2グループ化合物)は、約1:3〜約3:1、例えば約0.75:1〜約2:1で変化してもよい。第1、第2および第3の有機フォトクロミック補足的グループの組合せは、約1:3:1〜3:1:3で変化する重量比を有してもよい。
発明のフォトクロミック物質を、文献に記載されている種々の方法によって、ポリマー有機ホスト材料のようなホスト材料に、被覆ままは組み込むことができる。そのような方法は、ホスト材料中にフォトクロミック物質を溶解または分散させることを包含し、例えば、重合の前に、モノマーホスト材料にフォトクロミック物質を加えることによって、それを適所に注入すること;フォトクロミック物質の熱溶液にホスト材料を浸漬することによって、または熱移動によって、ホスト材料中にフォトクロミック物質を吸収させること(imbibition);隣接するホスト材料の層の間に、フォトクロミック物質を、分離層として、例えばポリマーフイルムの一部として、配置すること;およびホスト材料の表面上に配置される被膜の一部として、フォトクロミック物質を被覆すること;を包含する。「吸収(imbibition)」または「吸収する(imbibe)」という語は、フォトクロミック物質のみのホスト材料への透過、フォトクロミック物質の、多孔質ホリマーへの溶媒補助移動、蒸気層移動、および他のそのような移動メカニズムを意味し、包含する。
相溶性(化学的および色的に)の色材(tint)、即ち染料を、ホスト材料に被覆して、医学的理由またはファッション的理由に対して、より審美的な結果を生じさせることができる。選択される特定の染料は、前記の要求および達成すべき結果に依存して変化する。1つの態様においては、活性フォトクロミック物質から生じる色を補足するために、例えば、より中間色の色を得るために、または入射光の特定の波長を吸収するために、染料が選択される。別の態様においては、フォトクロミック物質が未活性状態にあるときに、主マトリックスに所望の色合いを与えるように、染料が選択される。
また補助剤類は、ホトクロミック物質の主物質中への適用または組み込みに先だって、またはそれと同時に、またはその後にホトクロミック物質とともに主物質に組み込んでもよい。例えば、紫外線吸収剤類は、主物質に適用する前にホロクロミック物質と混合してもよいし、またはこのような紫外線吸収剤は、ホトクロミック物質と入射光線との間に層として重ね合わせてもよい。更に、ホトクロミック物質の光劣化抵抗性を向上するために、安定剤類を、主物質へ適用前にこれをホトクロミック物質と混合してもよい。ヒンダードアミン光安定剤およびシングレット酸素クエンチャーのような安定剤、例えばニッケルイオンと有機リガンドの錯体が考えられる。これらは単独で用いてもよいし、組み合わせて用いてもよい。このような安定剤類は米国特許第4,720,356号明細書に記載されている。最後に適当な保護塗料を主物質の表面に塗布してもよい。塗料は磨耗抵抗性塗料および/または酸素バリアーとして働く塗料であってもよい。このような塗料は当業界で公知である。
主物質は通常透明であるが、半透明または不透明でさえあってもよい。主物質は、電磁波スペクトルの、ホトクロミック物質を活性化する部分、即ち、主物質の開いた形を生成する紫外線の波長領域および主物質の紫外線活性形、即ち開いた形の状態にある主物質の最大吸収波長を不む可視光線の部分、に対して透明でありさえすればよい。好ましくは、主物質の色はホトクロミック物質の活性形の色をわからなくするものであってはならず、即ち、そうすることによって色の変化が観察者に容易に分かる。主物質は完全透明であるかまたは光学的に透明であること、例えば平面および眼科用レンズ、窓、自動車の透明体、例えば風除け、航空機の透明体、プラスチックシート、重合体フィルム類等のような光学用途に適した物質であることが更に好ましい。
ホトクロミック物質または本明細書に記載されている組成物とともに用いてもよい有機重合体主物質の例としては、ポリマー類、即ちポリオール(アリルカーボネート)モノマー類、ジエチレングリコールジメタクリレートモノマー類、ジイソプロペニルベンゼンモノマー類、およびエトキシ化トリメチロールプロパントリアクリレートモノマー類のようなアルコキシル化多価アルコールアクリレートモノマー類のホモポリマー類およびコポリマー類;多官能、即ちモノ−、ジ−、トリ−、テトラ−または多官能のアクリレートおよび/またはメタクリレートモノマー類のポリマー、即ちホモポリマー類およびコポリマー類、ポリアクリレート類、ポリメタクリレート類、ポリ(メチルメタクリレート)類のポリ(C1−C12アルキルメタクリレート)類、ポリ(エチレングリコールビスメタクリレート)類等のポリオキシ(アルキレンメタクリレート)類、ポリ(エトキシ化ビスフェノールAジメタクリレート)等のポリ(アルコキシ化フェノールメタクリレート)類、セルロースアセテート、セルローストリアセテート、セルロースアセテートプロピオネート、セルロースアセテートブチレート、ポリ(ビニルアセテート)、ポリ(ビニルアルコール)、ポリ(ビニルクロライド)、ポリ(ビニリデンクロライド)、ポリウレタン類、熱可塑性ポリカーボネート類、ポリエステル類、ポリ(エチレンテレフタレート)、ポリスチレン、ポリ(α−メチルスチレン)、スチレン−メチルメタクリレート共重合体、スチレン−アクリロニトリル共重合体、ポリビニルブチラールおよびジアリリデンペンタエリスリトールのホモポリマーおよびコポリマー、特にポリオール(アリルカーボネート)モノマー類、例えばジエチレングリコールビス(アリルカーボネート)、およびアクリレートモノマー類とのコポリマー類が含まれる。
透明コポリマーおよび透明ポリマー類のブレンド物も主物質として好適である。主物質は、「レクサン(LEXAN)」という商品名で市販されているビスフェノールAとホスゲンからのカーボネート架橋樹脂のような熱可塑性ポリカーボネート樹脂;「マイラー(MYLAR)」という商品名で市販されているポリエステル;「プレキシグラス(PLEXIGLAS)」という商品名で市販されているポリ(メチルメタクリレート);ポリオール(アリルカーボネート)モノマー、特に「CR−39」という商品名で市販されているジエチレングリコールビス(アリルカーボネート)の重合体類、およびポリオール(アリルカーボネート)例えばジエチレングリコールビス(アリルカーボネート)の他の共重合性モノマー類との共重合体、例えば、酢酸ビニルとの共重合体、例えば、80〜90%のジエチレングリコールビス(アリルカーボネート)と10〜20%の酢酸ビニルからの共重合体、特に80〜85%のビス(アリルカーボネート)と15〜20%の酢酸ビニルからの共重合体、および米国特許第4,360,653号明細書および米国特許第4,994,208号明細書に記載されているような末端にジアクリレート基を有するポリウレタンとの共重合体、および米国特許第5,200,483号明細書に記載されているような末端部にアリルまたはアクリリル官能基を有する脂肪族ウレタン類とのコポリマー類;ポリ(ビニルアセテート)、ポリビニルブチラール、ポリウレタン、ジエチレングリコールジメタクリレートモノマー類、ジイソプロペニルベンゼンモノマー類、およびエトキシ化トリメチロールプロパントリアクリレートモノマー類からなる群のモノマーからのポリマー類;セルロースアセテート、セルロースプロピオネート、セルロースブチレート、セルロースアセテートブチレート、ポリスチレンおよびスチレンとメチルメタクリレート、ビニルアセテートおよびアクリロニトリルとの共重合体、から調製される光学的に透明な有機重合材料であることが好ましい。より好ましくは、本発明のホトクロミックナフトピラン類を、光学的に透明な重合体、例えば平面および眼科用レンズ、窓、および自動車用透明体のような光学用途に好適な材料を製造するために用いられる光学的有機樹脂のモノマー類とともに使用することが考えられる。このような光学的に透明な重合体は約1.48〜約1.75、例えば約1.495〜約1.66の範囲の屈折率を持っていてもよい。
本発明は、より詳しくは次の実施例に記載されている。実施例は単に例示として考えられるべきで、当業者には多数の応用や変形形態が考えられよう。
実施例1
工程1
アセチレンで飽和した無水テトラヒドロフラン200mlの入った反応フラスコ中に4,4'−ジメトキシベンゾフェノン(0.27モル)を溶解し、室温で撹拌した。キシレン/鉱物油中に分散した18重量%濃度のナトリウムアセチライド懸濁液(ナトリウムアセチライドとして0.3モル)を反応フラスコに添加し、混合物を撹拌した。窒素雰囲気下、室温で16時間撹拌後、反応フラスコの内容物を、5重量%の塩酸水溶液と氷の混合物中に加えた。得られた混合物をジエチルエーテルで抽出した。有機層を分離し、洗浄し、無水硫酸ナトリウム上で乾燥した。溶媒類、ジエチルエーテルおよびテトラヒドロフランを真空下で除去して、1,1−ビス(4−メトキシフェニル)−2−プロピン−1−オールを含む油状生成物を得た。この生成物はそれ以上精製せずに直接次工程で使用した。
工程2
工程1で得られた1,1−ビス(4−メトキシフェニル)−2−プロピン−1−オール(約0.025モル)とメチル−4−ヒドロキシ−6−メトキシ−1−メチル−2−ナフトエート(5g、0.022モル)をトルエン200mlを含む反応フラスコに加え、撹拌した。触媒量のp−トルエンスルホン酸(約100mg)を加え、混合物を4時間撹拌した。その後、反応混合物を10重量%濃度の水酸化ナトリウム溶液中に注いだ。有機層を分離し、水で洗浄して無水硫酸ナトリウム上で乾燥した。残留溶媒であるトルエンを真空下で除去した。得られた油状物をシリカゲルカラムおよび溶離剤としてクロロホルム:ヘキサンの1:3混合物を用いて精製した。ホトクロミック成分を一緒にして溶離剤を真空下で除去した。得られた生成物をヘキサンから結晶化させた。回収した生成物は融点が132〜133℃であった。核磁気共鳴スペクトルから生成物は2,2−ビス(4−メトキシフェニル)−5−メトキシカルボニル−6−メチル−9−メトキシ−2H−ナフト〔1,2−b〕ピランに一致する構造を有することが示された。
ステップ3
ステップ2由来の2,2−ビス(4−メトキシフェニル)−5−メトキシカルボニル−6−メチル−9−メトキシ−[2H]−ナフト[1,2−b]ピラン(1.7g、0.0034モル)を、テトラヒドロフラン200mlを含む反応フラスコ中、溶解し、撹拌した。水素化リチウムアルミニウム(0.13g、0.0034モル)を注意して添加し、混合物を室温で2時間撹拌した。2−プロパノールを添加し、5重量%塩酸水溶液を添加した。得られた混合物を、2つのメチレンクロライド100ml部で抽出した。有機抽出液を合わせ、硫酸マグネシウムで乾燥した。溶媒、メチレンクロライドを減圧下で除去した。生成物をジエチルエーテルから結晶化させ、結晶を吸引濾過により集めた。回収された生成物1.0gの融点は125−127℃であった。核磁気共鳴(NMR)スペクトルは、生成物が、2,2−ビス(4−メトキシフェニル)−5−ヒドロキシメチル−6−メチル−9−メトキシ−2H−ナフト[1,2−b]ピランと一致する構造を有することを示した。
実施例2
ステップ1
ポタジウムt−ブトキシド(75グラム(g)、0.75モル)を、トルエン200ミリリットル(ml)を含む反応フラスコに添加した。ベンゾフェノン(91g、0.5モル)、ジメチルスクシネート(90g、0.62モル)およびトルエン(100g)の混合物を30分間にわたって添加しながら、得られたスラリーを窒素雰囲気下で還流温度に加熱した。添加後、得られたペースト状混合物を還流温度で2時間維持し、その後室温まで冷却した。約400mlの水を添加し、混合物を30分間撹拌した。水性層を分離し、希塩酸で酸性化し、トルエン200mlで抽出した。溶媒を減圧下で除去して、生成物4,4−ジフェニル−3−メトキシカルボニル−3−ブテン酸を含み、後で凝固する粘性オイルを得た。この物質はさらに精製することなく、次のステップで直接用いた。
ステップ2
ステップ1の生成物を、トルエン200mlを含む反応フラスコに溶解した。無水酢酸(100g)および無水酢酸ナトリウム(15g)を反応フラスコに添加し、混合物を17時間還流した。得られた混合物を室温まで冷却し、溶媒を減圧下で除去した。得られた残査を含む反応フラスコにメチレンクロライド(200ml)を添加した。水(200ml)を反応フラスコに添加した後、固形炭酸ナトリウムを、二酸化炭素の発生がやむまで、ゆっくり添加した。メチレンクロライド層を分離し、水で洗浄し、溶媒を減圧下で除去して、1−アセトキシ−3−メトキシカルボニル−4−フェニルナフタレンを含む粘性オイルを得た。
ステップ3
メタノール(400ml)を、ステップ2由来の1−アセトキシ−3−メトキシカルボニル−4−フェニルナフタレンを含む反応フラスコに添加した。濃塩酸(2ml)を反応フラスコに添加し、得られた混合物を還流温度に加熱した。4時間後、混合物を室温まで冷却し、溶媒を減圧下で除去し、得られた結晶を吸引濾過により集めた。集められた結晶をメタノールで洗浄し、空気乾燥した。回収された生成物100gの融点は174−176℃であった。各磁気共鳴(NMR)スペクトルは、生成物が、4−フェニル−3−メトキシカルボニル−1−ナフトールと一致する構造を有することを示した。
ステップ4
ステップ3由来の4−フェニル−3−メトキシカルボニル−1−ナフトール(2g)および実施例1のステップ1由来の1,1−ビス(4−メトキシフェニル)−2−プロピン−1−オル(2g)を、トルエン100mlを含む反応フラスコに添加し、撹拌した。得られた混合物を40℃に加熱し、触媒量(2、3滴)、すなわち混合物中で深赤色を得るのに十分な量のドデシルベンゼンスルホン酸を添加した。40℃で3時間撹拌した後、混合物を冷却し、水で洗浄した。有機層を分離し、溶媒、トルエンを減圧下で除去した。得られたオイルを、シリカゲルカラムおよび溶離剤として2:1ヘキサン:酢酸エチル混合液を用いて、精製した。ホトクロミックフラクション(photochromic fractions)を集め、溶媒を減圧下で除去した。得られた生成物(2.0g)をヘキサン−エーテル混合液から結晶化し、吸引濾過によりオフ−ホワイト結晶として集めた。回収された生成物の融点は168−169℃であった。核磁気共鳴(NMR)スペクトルは、生成物が、2,2−ビス(4−メトキシフェニル)−5−メトキシカルボニル−6−フェニル−2H−ナフト[1,2−b]ピランと一致する構造を有することを示した。
ステップ5
ステップ4由来の2,2−ビス(4−メトキシフェニル)−5−メトキシカルボニル−6−フェニル−2H−ナフト[1,2−b]ピラン(10.0g、0.02モル)を、テトラヒドロフラン300mlを含む反応フラスコに溶解した。水素化リチウムアルミニウム(1.2g、0.032モル)を注意して、撹拌された溶液に添加し、混合物を2−1/2時間40℃に加熱した。室温まで冷却した後、2−プロパノールを添加し、5重量%塩酸水溶液を添加した。得られた混合物を、3つのジエチルエーテル100ml部で抽出した。有機抽出液を合わせ、硫酸マグネシウムで乾燥した。溶媒、ジエチルエーテルを減圧下で除去した。得られた残渣をジエチルエーテルから結晶化させ、結晶を吸引濾過により集めた。所望の生成物を3g回収した。核磁気共鳴(NMR)スペクトルは、生成物が、2,2−ビス(4−メトキシフェニル)−5−ヒドロキシメチル−6−フェニル−2H−ナフト[1,2−b]ピランと一致する構造を有することを示した。
実施例3
実施例2のステップ4由来の2,2−ビス(4−メトキシフェニル)−5−ヒドロキシメチル−6−フェニル−2H−ナフト[1,2−b]ピラン(2.0g、0.004モル)を、メチレンクロライド200mlおよびトリエチルアミン1.2当量を含む反応フラスコに溶解した。アセチルクロライド(0.37g、0.0048モル)を、撹拌された混合物に添加し、4時間還流温度に加熱した。室温まで冷却した後、ジエチルエーテルを添加し、トリエチルアミンヒドロクロライド、副生物を濾過で除去した。得られた生成物をシリカゲルカラムで溶離剤としてクロロホルムを用いて精製した。ホトクロミックフラクション(photochromic fractions)を集め、溶媒を減圧下で除去した。回収された生成物0.2gをジエチルエーテルから結晶化させた。核磁気共鳴(NMR)スペクトルは、生成物が、2,2−ビス(4−メトキシフェニル)−5−アセトキシメチル−6−フェニル−2H−ナフト[1,2−b]ピランと一致する構造を有することを示した。
比較例
ステップ1
3−メトキシカルボニル−4−メチル−7−メトキシ−1−ナフトール(12g)を、水酸化カリウム(25g)、水(250ml)およびエタノール(50ml)を含む反応フラスコに添加した。混合物を蒸気浴で6時間加熱し、室温まで冷却し、過剰量の冷希塩酸水溶液(約5重量%)に注いだ。得られた固形生成物を吸引濾過により取り出し、乾燥して、所望の生成物3−カルボキシ−4−メチル−7−メトキシ−1−ナフトールを11g得た。
ステップ2
ステップ1由来の3−カルボキシ−4−メチル−7−メトキシ−1−ナフトール(11g)を、メチレンクロライド100mlを含む反応フラスコに添加した。トリエチルアミン(10g、0.1モル)を撹拌しながら添加した。得られた発熱反応混合物を氷浴中で冷却した。アセチルクロライド(4g、0.05モル)を、温度を5℃に維持しながら滴下した。混合物をさらに5℃で15分間撹拌し、その後室温まで温め、そこでさらに15分間撹拌し、過剰量の冷希塩酸水溶液(約5重量%)に注いだ。沈殿した生成物を2相混合物から吸引濾過し、フレッシュメチレンクロライドで洗浄し、乾燥して、所望の生成物を11g得た。NMRスペクトルは、生成物が、1−アセトキシ−3−カルボキシ−4−メチル−7−メトキシナフタレンと一致する構造を有することを示した。
ステップ3
ステップ2で得た1−アセトキシ−3−カルボキシ−4−メチル−7−メトキシナフタレン(11g)を20mlのチオニルクロライドを含む反応フラスコへ添加し、混合物を蒸気浴上で加熱した。約30分後、HClの発生が終了時に、ロータリーエバポレーターにかけて過剰のチオニルクロライドを除き、酸クロライドを固形として得た。生成物、1−アセトキシ−3−クロロカルボニル−4−メチル−7−メトキシナフタレンは、精製せずに、次のステップに直接用いた。
ステップ4
ステップ3で得た1−アセトキシ−3−クロロカルボニル−4−メチル−7−メトキシナフタレンの半分を、メチレンクロライド(50ml)、ピペリジン(4.25g,0.05モル)およびトリエチルアミン(5g,0.05モル)の混合物を含む反応フラスコへ、少しずつ添加した。添加が終了した後、過剰量の冷希塩酸(およそ5重量%)を加え、得られた溶液を混合した。有機層を分離し、水、希炭酸ナトリウム水溶液、および水と続けて洗浄した。溶媒、メチレンクロライドを真空下で除き、所望の生成物を油状物質として得た。NMR分析により、生成物の構造が1−アセトキシ−3−ピペリジノカルボニル−4−メチル−7−メトキシナフタレンと一致することが示された。
ステップ5
メタノール(200ml)と濃塩酸(2ml)の混合物を、ステップ4で得た1−アセトキシ−3−ピペリジノカルボニル−4−メチル−7−メトキシナフタレンを含有する反応フラスコへ添加した。得られた反応混合物を、蒸気浴上で2時間、還流させた。その後、混合物を室温まで冷却し、希塩酸内へ注いだ。得られる沈殿を吸引濾過し、水で洗浄し、乾燥して4.8gの所望の生成物を褐色結晶として得た。NMR分光分析により、生成物の構造が3−ピペリジノカルボニル−4−メチル−7−メトキシ−1−ナフトールと一致することが示された。
ステップ6
ステップ5で得た3−ピペリジノカルボニル−4−メチル−7−メトキシ−1−ナフトール(2.5g)および1−(2,3−ジヒドロベンゾフル−5−イル)−1−(4−メトキシフェニル)−2−プロピン−1−オール(2.5g)を100mlのトルエンを含む反応フラスコに添加し、攪拌した。攪拌した混合物を50℃まで加熱し、ここへ数滴のドデシルベンゼンスルホン酸(深赤色を生成するのに充分な量)を添加した。2時間後、反応混合物を室温まで冷却し、水を添加した。有機層は水で洗浄し、溶媒をロータリーエバポレーターで除いた。得られた油状物質をシリカゲルカラムにて、溶離剤として1:1 ヘキサン:酢酸エチル混合物を用いて精製した。フォトクロミックフラクションを合わせ、濃縮して、少量のジエチルエーテル:ヘキサン混合物より結晶化を誘導した。所望の生成物を吸引濾過により回収し、乾燥して、融点が201〜203℃である結晶2.6gを得た。NMR分光分析により、生成物の構造が2−(4−メトキシフェニル)−2−(2,3−ジヒドロベンゾフラン−5−イル)−5−ピペリジノカルボニル−6−メチル−9−メトキシ−2H−ナフト[1,2−b]ピランと一致することが示された。
実施例4
パートA
実施例および比較例で得たフォトクロミックナフトピランを、重合性試料内に以下の方法にて取り込んで試験を行った。計算上溶液中のモル濃度が1.5×10-3となる量のナフトピランを、50gのモノマーブレンドを含むフラスコへ添加した。モノマーブレンドは、4部のエトキシル化ビスフェノールAジメタクリレート(BPA 2EODMA)、1部のポリ(エチレングリコール)600ジメタクリレート、および、0.033重量%の2,2'−z−アゾビス(2−メチルプロピオニトリル)(AIBN)からなる。攪拌および必要に応じて穏やかに加熱することによって、ナフトピランをモノマーブレンド内へ溶解させた。透明な溶液が得られた後、内法の寸法が2.2mm×6インチ(15.24cm)×6インチ(15.24cm)のフラットシート型へ流し込んだ。型を密封して、水平の空気流があり、5時間かけて40℃から95℃まで温度を上げ、温度を95℃に3時間保持し、次いで温度を60℃まで温度を下げて、硬化サイクルの終了の前少なくとも2時間保持するよう、セットしたプログラムオーブン内に置いた。型を開けた後、ポリマーシートをダイアモンド刃ののこぎりにて2インチ角(5.1cm)に切断して試験片を得た。
パートB
パートAで調製したフォトクロミック試験片のフォトクロミック応答速度をオプティカルベンチ上で試験した。オプティカルベンチ上で試験するのに先立ち、フォトクロミック試験片に365ナノメーターの紫外をおよそ15分間照射してフォトクロミック化合物を活性化させ、次いで76℃のオーブン内に15分間置き、フォトクロミック化合物を脱色または不活性化させた。次いで試験片を室温まで冷却し、蛍光室内灯による照射を少なくとも2時間行い、次いで被覆下に少なくとも2時間置いた後、75゜F(23.9℃)に保持したオプティカルベンチ上で試験した。このベンチには150ワットのキセノンアーク灯、リモートコントロールシャッター、このアーク灯のヒートシンクとして作用する硫酸銅槽、短波長の照射を除くショット(Schott)WG−320nmカット−オフフィルター;中性密度フィルターおよび試料片を挿入する試料ホルダーが備えられている。タングステンランプからの平行光線を、試験片に対して垂直に対して少し傾いた角度で試験片を通過させた。試験片を通過した後、タングステンランプからの光は検出器に取り付けられたフォトピックフィルターへを通過するよう導かれる。フォトピックフィルターは検出器がヒトの目の応答を模倣するよう、波長を通過させる。検出器から出力される信号は、ラジオメーターにて処理した。
光学密度の変化(△OD)は、脱色した状態の試験片を試料ホルダーに挿入し、このときの透過率のスケールを100%とし、キセノンランプのシャッターを開けて紫外線照射を行って試験片を脱色状態から活性化状態(黒くなる)とし、活性化状態における透過率を測定し、光学密度の変化を式△OD=log(100/%Ta)(式中、%Taは活性化状態における透過率であり、対数の底は10である)に基づいて計算して得た。
△OD/分は、フォトクロミック化合物のUV光に対する応答の感受性を表すが、この値は最初の5秒間のUV照射において測定されたものを、毎分あたりの数値として表したものである。表1の実施例の飽和光学密度(OD)は、紫外線照射を20分間続けて行った以外は、△OD/分の場合と同じ条件にて得た。表1のラムダマックスとは、ジエチレングリコールビス(アリルカーボネート)化合物内のフォトクロミック化合物の活性化(着色)体が、最大吸収を示す可視領域の波長である。脱色速度(T1/2)は、活性化光源を除いた後、室温(75゜F、23.9℃)において、試験片内のナフトピランの活性化体の吸収が最大の半分に達するまでの時間を秒で示したものである。実施例および比較例の化合物の結果を表1にまとめた。
表1の結果は、2H−ナフト[1,2−b]ピラン類の脱色速度が、5位置換基の性質により、劇的な影響を受けることを示す。例えば、化合物1から3は許容し得る脱色速度、即ち退色速度を有するが、比較例の退色はかなり遅い。4化合物全ては飽和時、すなわち、強く活性化された際には高いODを有し、高い着色速度、即ち感受性を有している。
本発明を特定の態様に基づいて上記に詳しく説明したが、以下の請求の範囲に含まれるものについては、かかる詳細な記載はこの発明の範囲を限定しようとするものではない。
Claims (20)
- 以下の式で示されるナフトピラン化合物:
式中、
(a)R1は−CH2X及び−C(O)Y[式中、Xはハロゲン、ヒドロキシ、ベンゾイルオキシ、C1〜C6アルコキシ、C2〜C6アシルオキシ、アミノ、C1〜C6モノアルキルアミノ、C1〜C6ジアルキルアミノ、モルホリノ、ピペリジノ、1−インドリニル、ピロリジル、トリメチルシリルオキシ、又は−OCH(R11)Zであり、Yは−OCH(R11)Z{式中、Zは−CN、−C(O)R12、又は−COOR12(式中、各R11及びR12は水素又はC1〜C6アルキルである。)である。}であり、該ハロゲンはクロロ又はフルオロである。]からなる群から選択される基である;
(b)R2及び各R3は水素、C1〜C6アルキル、C3〜C7シクロアルキル、無置換、モノ、ジ、又はトリ置換フェニル、−OR6[式中、R6は水素、(C1〜C6)アルキル、フェニル(C1〜C3)アルキル、モノ置換フェニル(C1〜C3)アルキル、(C1〜C6)アルコキシ(C2〜C4)アルキル、C3〜C7シクロアルキル、モノ(C1〜C4)アルキル、置換C3〜C7シクロアルキル、C1〜C6ハロアルキル、アリル、−CH(R7)W{式中、Wは−CN、−CF3、ハロゲン、−C(O)R7、又は−COOR7(式中、R7は水素、C1〜C6アルキル、又は(C1〜C6)アルコキシ(C2〜C4)アルキルである。)である}で示される基、又はR6は−C(O)T{式中、Tは水素、C1〜C6アルキル、C1〜C6アルコキシ、置換もしくは無置換アリール基(フェニル又はナフチル)、フェノキシ、C1〜C6モノもしくはジアルキル置換フェノキシ、C1〜C6モノもしくはジアルコキシ置換フェノキシ、C1〜C6モノもしくはジアルコキシ置換フェニルアミノ(該フェニル又はナフチル置換基のそれぞれはC1〜C6アルキル、C1〜C6アルコキシ又はハロゲンであり、該ハロゲン又はハロ置換基のそれぞれはクロロ又はフルオロである。)である。}で示される基であり、nは0、1、2、及び3からなる群から選択される整数である;
(c)B及びB'はそれぞれ以下の(i)〜(vi)からなる群から選択される:
(i)無置換、モノ、ジ及びトリ置換アリール基(フェニル及びナフチル);
(ii)無置換、モノ及びジ置換芳香族複素環基(ピリジル、フラニル、ベンゾフラン−2−イル、ベンゾフラン−3−イル、チエニル、ベンゾチエン−2−イル、ベンゾチエン−3−イル、ジベンゾチエニル、ジベンゾフラニル、カルバゾリル)、該アリール及び複素環置換基はヒドロキシ、アミノ、C1〜C6モノアルキルアミノ、C1〜C6ジアルキルアミノ、モルホリノ、ピペリジノ、1−インドリニル、ピロリジル、1−イミダゾリジル、1−イミダゾリジン−1−イル、2−ピラゾリジル、ピラゾリニル、1−ピペラジニル、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6アルコキシ、モノ(C1〜C6)アルコキシ(C1〜C4)アルキル、アクリルオキシ、メタクリルオキシ、及びハロゲン(該ハロゲン又は(ハロ)基はフルオロ又はクロロである)からなる群から選択される;
(iii)以下の式で示される基:
式中、Dは炭素、又は酸素であり、Eは酸素又は置換窒素であるが、ただし、Eが置換窒素であるときDは炭素であり、該窒素置換基は水素、C1〜C6アルキル及びC2〜C6アシルからなる群から選択され;各R8はC1〜C6アルキル、C1〜C6アルコキシ、ヒドロキシ、クロロ又はフルオロであり;R9及びR10はそれぞれ水素又はC1〜C6アルキルであり;そしてmは0、1又は2の整数である;
(iv)C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6アルコキシ(C1〜C4)アルキル、C3〜C6シクロアルキル、モノ(C1〜C6)アルコキシ(C3〜C6)シクロアルキル、モノ(C1〜C6)アルキル(C3〜C6)シクロアルキル、及びハロ(C3〜C6)シクロアルキル(該ハロ基はフルオロ又はクロロである。);及び
(v)以下の式で示される基:
式中、Uは水素又はC1〜C4アルキルであり、そしてVはナフチル、フェニル、フラニル及びチエニルからなる群の無置換、モノ及びジ置換成員から選択されるが、該置換基のそれぞれはC1〜C4アルキル、C1〜C4アルコキシ、フルオロ又はクロロである;
(vi)B及びB'は一緒になって無置換、モノもしくはジ置換フルオレン−9−イリデン、又は飽和C3〜C12スピロ単環式炭化水素環、飽和C7〜C12スピロ二環式炭化水素環、及び飽和C7〜C12スピロ三環式炭化水素環からなる群から選択される成員を形成するが、該フルオレン−9−インデン置換基のそれぞれはC2〜C4アルキル、C1〜C4アルコキシ、フルオロ及びクロロからなる群から選択される。 - 以下の条件を満足する請求項1記載のインデノナフトピラン:
(a)R1は−CH2X及び−C(O)Y[式中、Xはヒドロキシ、C1〜C4アルコキシ、C2〜C4アシルオキシであり、Yは−OCH(R11)Z{式中、Zは−CN、−C(O)R12、又は−COOR12(式中、各R11及びR12は水素又はC1〜C4アルキルである。)である。}である]からかる群から選択される基である;
(b)R2及び各R3は水素、C1〜C4アルキル、無置換、モノ、ジ、又はトリ置換フェニル、−OR6[式中、R6はC1〜C4アルキル、又は−CH(R7)W{式中、Wは−COOR7(式中、R7は水素、C1〜C4アルキルである。)である。}である。]で示される基であり、該フェニル置換基はC1〜C4アルキル、C1〜C4アルコキシ又はフルオロであり、nは0、1、及び2からなる群から選択される整数である;
(c)B及びB'はそれぞれ以下の(i)〜(vi)からなる群から選択される:
(i)無置換、モノ、ジ及びトリ置換フェニル;
(ii)無置換、モノ及びジ置換芳香族複素環基(ピリジル、フラニル、ベンゾフラン−2−イル、ベンゾフラン−3−イル、チエニル、ベンゾチエン−2−イル、ベンゾチエン−3−イル、ジベンゾチエニル、ジベンゾフラニル、カルバゾリル)、該フェニル及び複素環置換基のそれぞれはモルホリノ、ピペリジノ、C1〜C4アルキル、C1〜C4アルコキシ、及びハロゲン(該ハロゲン又は(ハロ)基はフルオロ又はクロロである。)である;
(iii)以下の式で示される基:
式中、Dは炭素であり、Eは酸素であり;各R8はC1〜C4アルキル、C1〜C4アルコキシ、ヒドロキシ、又はハロゲン(該ハロゲンはクロロ又はフルオロである。)であり;R9及びR10はそれぞれ水素又はC1〜C4アルキルであり;そしてmは0、1又は2の整数である;
(iv)C1〜C4アルキル、C1〜C6アルコキシ(C1〜C4)アルキル、及びC3〜C6シクロアルキル;及び
(v)以下の式で示される基:
式中、Uは水素又はメチルであり、そしてVはフェニル、又はモノ置換フェニル(該フェニル置換基はC1〜C4アルキル、C1〜C4アルコキシ、又はフルオロである;
(vi)B及びB'は一緒になって無置換又はモノ置換フルオレン−9−イリデン、又は飽和C3〜C8スピロ単環式炭化水素環、飽和C7〜C10スピロ二環式炭化水素環及び飽和C7〜C10スピロ三環式炭化水素環からなる群から選択される成員を形成する。 - 以下の条件を満足する請求項2に記載のインデノナフトピラン:
(a)R1は−CH2X[式中、Xはヒドロキシ、C1〜C4アルコキシ、又はC2〜C4アシルオキシである];
(b)R2及び各R3は水素、C1〜C2アルキル、無置換、モノ、ジ、又はトリ置換フェニル、−OR6[式中、R6はC1〜C2アルキル、又は−CH(R7)W{式中、Wは−COOR7(式中、R7はC1〜C2アルキルである。)である。}である。]で示される基であり、該フェニル置換基はC1〜C2アルキル、C1〜C2アルコキシ又はフルオロであり、nは0、1、及び2からなる群から選択される整数である;
(c)B及びB'は以下の(i)〜(iv)からなる群から選択される;
(i)無置換、モノ及びジ置換フェニル;
(ii)無置換、モノ及びジ置換芳香族複素環基(ピリジル、ベンゾフラン−2−イル、ベンゾチエン−2−イル、ジベンゾチエニル、及びジベンゾフラニル)、該フェニル及び複素環置換基のそれぞれはモルホリノ、ピペリジノ、C1〜C2アルキル、C1〜C2アルコキシである;
(iii)以下の式で示される基:
式中、Dは炭素であり、Eは酸素であり;各R8はC1〜C2アルキル、C1〜C2アルコキシ、又はフルオロであり;R9及びR10はそれぞれ水素又はC1〜C2アルキルであり;そしてmは0、1又は2の整数である;
(iv)B及びB'は一緒になってフルオレン−9−イリデン、ボルニリデン、ノルボルニリデン、ビシクロ[3.3.1]ノナン−9−イリデン、又はアダマンチリデンを形成する。 - R1がヒドロキシメチル又はアセトキシメチルであり;R2及び各R3が水素、フェニル、メトキシ又はメチルであり;そしてB及びB'がそれぞれフェニル、メトキシ置換フェニル、モルホリノ置換フェニル、ジベンゾフラン−2−イル、又は2,3−ジヒドロベンゾフラン−5−イルである、請求項3記載のナフトピラン。
- 以下の(a)〜(i)からなる群から選択されるナフトピラン化合物:
(a)2,2−ビス(4−メトキシフェニル)−5−ヒドロキシメチル−6−メチル−9−メトキシ−2H−ナフト[1,2−b]ピラン;
(b)2,2−ビス(4−メトキシフェニル)−5−ヒドロキシメチル−6−フェニル−2H−ナフト[1,2−b]ピラン;
(c)2,2−ビス(4−メトキシフェニル)−5−アセトキシメチル−6−フェニル−2H−ナフト[1,2−b]ピラン;
(d)2,2−ビス(4−メトキシフェニル)−5−ヒドロキシメチル−6−メトキシ−2H−ナフト[1,2−b]ピラン;
(e)2,2−ジフェニル−5−メトキシメチル−6−メトキシ−2H−ナフト[1,2−b]ピラン;
(f)2,2−スピロアダマンチレン−5−アセトキシメチル−6−メトキシ−2H−ナフト[1,2−b]ピラン;
(g)2,2−ビス(4−メトキシフェニル)−5−トリメチルシリルオキシメチル−6−メトキシ−2H−ナフト[1,2−b]ピラン;
(h)2−(4−メトキシフェニル)−2−t−ブチル−5−メトキシメチル−6−フェニル−9−メトキシ−2H−ナフト[1,2−b]ピラン;及び
(i)2−(4−メトキシフェニル)−2−(2,3−ジヒドロベンゾフラン−5−イル)−5−クロロメチル−6−メチル−9−メトキシ−2H−ナフト[1,2−b]ピラン。 - ポリマー有機ホスト材料とホトクロミック量の請求項1記載のナフトピラン化合物とを含有するホトクロミック物品。
- 前記ポリマー有機ホスト材料がポリアクリレート、ポリメタクリレート、ポリ(C1〜C12アルキルメタクリレート)、ポリオキシ(アルキレンメタクリレート)、ポリ(アルコキシル化フェノールメタクリレート)、セルロースアセテート、セルローストリアセテート、セルロースアセテートプロピオネート、セルロースアセテートブチレート、ポリ(酢酸ビニル)、ポリ(ビニルアルコール)、ポリ(ビニルクロリド)、ポリ(ビニリデンクロリド)、熱可塑性ポリカーボネート、ポリエステル、ポリウレタン、ポリ(エチレンテレフタレート)、ポリスチレン、ポリ(αメチルスチレン)、コポリ(スチレン−メチルメタクリレート)、コポリ(スチレン−アクリロニトリル)、ポリビニルブチラール、及びポリオール(アリルカーボネート)モノマー、多官能アクリレートモノマー、多官能メタクリレートモノマー、ジエチレングリコールジメタクリレートモノマー、ジイソプロペニルベンゼンモノマー、アルコキシル化多価アルコールアクリレートモノマー及びジアリリデンペンタエリスリトールモノマーからなる群の成員のポリマーからなる群から選択される請求項6記載のホトクロミック物品。
- ポリマー有機ホスト材料とホトクロミック量の請求項2記載のナフトピラン化合物とを含有するホトクロミック物品。
- 前記ポリマー有機ホスト材料がポリアクリレート、ポリメタクリレート、ポリ(C1〜C12アルキルメタクリレート)、ポリオキシ(アルキレンメタクリレート)、ポリ(アルコキシル化フェノールメタクリレート)、セルロースアセテート、セルローストリアセテート、セルロースアセテートプロピオネート、セルロースアセテートブチレート、ポリ(酢酸ビニル)、ポリ(ビニルアルコール)、ポリ(ビニルクロリド)、ポリ(ビニリデンクロリド)、熱可塑性ポリカーボネート、ポリエステル、ポリウレタン、ポリ(エチレンテレフタレート)、ポリスチレン、ポリ(αメチルスチレン)、コポリ(スチレン−メチルメタクリレート)、コポリ(スチレン−アクリロニトリル)、ポリビニルブチラール、及びポリオール(アリルカーボネート)モノマー、多官能アクリレートモノマー、多官能メタクリレートモノマー、ジエチレングリコールジメタクリレートモノマー、ジイソプロペニルベンゼンモノマー、アルコキシル化多価アルコールアクリレートモノマー及びジアリリデンペンタエリスリトールモノマーからなる群の成員のポリマーからなる群から選択される請求項8記載のホトクロミック物品。
- 前記ポリマー有機ホスト材料がポリ(メチルメタクリレート)、ポリ(エチレングリコールビスメタクリレート)、ポリ(エトキシル化ビスフェノールAジメタクリレート)、熱可塑性ポリカーボネート、ポリ(酢酸ビニル)、ポリビニルブチラール、ポリウレタン、及びジエチレングリコールビス(アリルカーボネートモノマー、ジエチレングリコールジメタクリレートモノマー、ジイソプロペニルベンゼンモノマー及びエトキシル化トリメチロールプロパントリアクリレートモノマーからなる群の成員のポリマーからなる群から選択される固体透明ポリマーである請求項9記載のホトクロミック物品。
- ホトクロミック物質が組み込まれるか塗布される有機ホスト材料表面の平方センチメートル当たり0.05〜1.0ミリグラムのホトクロミック化合物が存在する請求項10記載のホトクロミック物品。
- 前記物品がレンズである請求項11記載のホトクロミック物品。
- ポリ(メチルメタクリレート)、ポリ(エチレングリコールビスメタクリレート)、ポリ(エトキシル化ビスフェノールAジメタクリレート)、熱可塑性ポリカーボネート、ポリ(酢酸ビニル)、ポリビニルブチラール、ポリウレタン、及びジエチレングリコールビス(アリルカーボネート)モノマー、ジエチレングリコールジメタクリレートモノマー、ジイソプロペニルベンゼンモノマー及びエトキシル化トリメチロールプロパントリアクリレートモノマーからなる群の成員のポリマーからなる群から選択されるポリマー有機ホスト材料と、ホトクロミック量の請求項3記載のナフトピラン化合物とを、含有するホトクロミック物品。
- ポリ(メチルメタクリレート)、ポリ(エチレングリコールビスメタクリレート)、ポリ(エトキシル化ビスフェノールAジメタクリレート)、熱可塑性ポリカーボネート、ポリ(酢酸ビニル)、ポリビニルブチラール、ポリウレタン、及びジエチレングリコールビス(アリルカーボネート)モノマー、ジエチレングリコールジメタクリレートモノマー、ジイソプロペニルベンゼンモノマー及びエトキシル化トリメチロールプロパントリアクリレートモノマーからなる群の成員のポリマーからなる群から選択されるポリマー有機ホスト材料と、ホトクロミック量の請求項4記載のナフトピラン化合物とを、含有するホトクロミック物品。
- 固体透明ポリマー有機ホスト材料と、ホトクロミック量の(a)少なくとも一種の請求項1記載のナフトピラン化合物、及び(b)400〜700ナノメートルの間の範囲内に少なくとも一つの活性化吸収極大を有する少なくとも一種の他の有機ホトクロミック化合物のそれぞれとの、組み合わせを含有するホトクロミック物品。
- 前記ポリマー有機ホスト材料がポリアクリレート、ポリメタクリレート、ポリ(C1〜C12アルキルメタクリレート)、ポリオキシ(アルキレンメタクリレート)、ポリ(アルコキシル化フェノールメタクリレート)、セルロースアセテート、セルローストリアセテート、セルロースアセテートプロピオネート、セルロースアセテートブチレート、ポリ(酢酸ビニル)、ポリ(ビニルアルコール)、ポリ(ビニルクロリド)、ポリ(ビニリデンクロリド)、熱可塑性ポリカーボネート、ポリエステル、ポリウレタン、ポリ(エチレンテレフタレート)、ポリスチレン、ポリ(αメチルスチレン)、コポリ(スチレン−メチルメタクリレート)、コポリ(スチレン−アクリロニトリル)、ポリビニルブチラール、及びポリオール(アリルカーボネート)モノマー、多官能アクリレートモノマー、多官能メタクリレートモノマー、ジエチレングリコールジメタクリレートモノマー、ジイソプロペニルベンゼンモノマー、アルコキシル化多価アルコールアクリレートモノマー及びジアリリデンペンタエリスリトールモノマーからなる群の成員のポリマーからなる群から選択される請求項15記載のホトクロミック物品。
- 前記有機ホトクロミック化合物(b)が以下の(a)〜(d)からなる群から選択される請求項15記載のホトクロミック物品:
(a)400〜500nmの可視領域に少なくとも一つの吸収極大を有する有機ホトクロミック物質;
(b)400〜500nmの可視領域に吸収極大、及び500〜700nmの可視領域に吸収極大を有する有機ホトクロミック物質;
(c)570nmを上回る可視領域に活性化吸収極大を有する有機ホトクロミック物質;
(d)これら有機ホトクロミック物質の混合物。 - 前記有機ホトクロミック化合物(b)が570nmを上回る可視領域に活性化吸収極大を有する有機ホトクロミック物質である請求項17記載のホトクロミック物品。
- 前記ポリマー有機ホスト材料がポリ(メチルメタクリレート)、ポリ(エチレングリコールビスメタクリレート)、ポリ(エトキシル化ビスフェノールAジメタクリレート)、熱可塑性ポリカーボネート、ポリ(酢酸ビニル)、ポリビニルブチラール、ポリウレタン、及びジエチレングリコールビス(アリルカーボネートモノマー、ジエチレングリコールジメタクリレートモノマー、ジイソプロペニルベンゼンモノマー及びエトキシル化トリメチロールプロパントリアクリレートモノマーからなる群の成員のポリマーからなる群から選択される固体透明ホモポリマー又はコポリマーである請求項16記載のホトクロミック物品。
- 前記有機ホトクロミック化合物(b)がスピロ(インドリン)ナフトオキサジン、スピロ(インドリン)ピリドベンズオキサジン、スピロ(ベンズインドリン)ピリドベンズオキサジン、スピロ(ベンズインドリン)ナフトオキサジン、スピロ(ベンズインドリン)ナフトピラン、スピロ(インドリン)ベンズオキサジン、スピロ(インドリン)ベンゾピラン、スピロ(インドリン)ナフトピラン、スピロ(インドリン)キノピラン、スピロ(インドリン)ピラン、3H−ナフト[1,2−b]ピラン、2H−フェナントロ[4,3−b]ピラン、3H−フェンナントロ[1,2−b]ピラン、ベンゾピラン化合物、及びこのようなホトクロミック物質の混合物である請求項17記載のホトクロミック物品。
Applications Claiming Priority (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US08/490,190 US5656206A (en) | 1995-06-14 | 1995-06-14 | Substituted naphthopyrans |
| PCT/US1996/015843 WO1998014443A1 (en) | 1995-06-14 | 1996-10-02 | Novel substituted naphthopyrans |
| CA002187100A CA2187100C (en) | 1995-06-14 | 1996-10-03 | Novel substituted naphthopyrans |
| EP96116144A EP0835870B1 (en) | 1995-06-14 | 1996-10-09 | Photochromic substituted naphthopyrans |
| HU9602961A HUP9602961A3 (en) | 1995-06-14 | 1996-10-25 | Naphtopyran compounds and photocromic articles |
| BRPI9604649-0A BR9604649B1 (pt) | 1995-06-14 | 1996-12-03 | artigo fotocrÈmico. |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2000516254A JP2000516254A (ja) | 2000-12-05 |
| JP3553085B2 true JP3553085B2 (ja) | 2004-08-11 |
Family
ID=89994386
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP51646598A Expired - Fee Related JP3553085B2 (ja) | 1995-06-14 | 1996-10-02 | 新規の置換ナフトピラン類 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US5656206A (ja) |
| EP (1) | EP0835870B1 (ja) |
| JP (1) | JP3553085B2 (ja) |
| KR (1) | KR20000048885A (ja) |
| AU (1) | AU735837B2 (ja) |
| BR (1) | BR9604649B1 (ja) |
| CA (1) | CA2187100C (ja) |
| DE (1) | DE69631765T2 (ja) |
| ES (1) | ES2217295T3 (ja) |
| HU (1) | HUP9602961A3 (ja) |
| WO (1) | WO1998014443A1 (ja) |
Families Citing this family (37)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5973039A (en) * | 1994-12-12 | 1999-10-26 | Corning Incorporated | Temperature stable and sunlight protected photochromic articles |
| US6262155B1 (en) | 1994-12-12 | 2001-07-17 | Corning Incorporated | Temperature stable and sunlight protected photochromic articles |
| AU1866597A (en) * | 1995-10-28 | 1997-05-15 | Optische Werke G. Rodenstock | Photochrome diaryl-3H-naphthopyrane |
| ES2175443T3 (es) * | 1996-07-25 | 2002-11-16 | Corning Inc | Compuestos de naptopirano y articulos que los contienen. |
| DE69807864D1 (de) * | 1997-03-21 | 2002-10-17 | Corning Sa | Naphthopyranderivate, zubereitungen und dieselben enthaltende (co)polymermatrizen |
| US5891368A (en) * | 1997-10-01 | 1999-04-06 | Ppg Industries, Inc. | Fluoranthenopyrans |
| EP1005464B1 (de) * | 1998-06-19 | 2002-04-17 | Optische Werke G. Rodenstock | Photochrome naphthopyrane |
| GB9827596D0 (en) * | 1998-12-15 | 1999-02-10 | James Robinson Ltd | Photochromic 2H-naphtho[1,2-b]pyrans |
| FR2796077B1 (fr) * | 1999-07-08 | 2001-10-05 | Essilor Int | Composes photochromiques naphto (2,1-b) pyranes a substitutions bi ou terthienyle, leur procede de fabrication, materiaux et articles photochromiques obtenus |
| US6348604B1 (en) | 1999-09-17 | 2002-02-19 | Ppg Industries Ohio, Inc. | Photochromic naphthopyrans |
| US6296785B1 (en) | 1999-09-17 | 2001-10-02 | Ppg Industries Ohio, Inc. | Indeno-fused photochromic naphthopyrans |
| FR2800738B1 (fr) | 1999-11-04 | 2002-02-08 | Corning Sa | Naphtopyranes ayant un substituant perfluoroalkyle en position 5, preparation et compositions et matrices (co)polymeres les renfermant |
| US6353102B1 (en) | 1999-12-17 | 2002-03-05 | Ppg Industries Ohio, Inc. | Photochromic naphthopyrans |
| US6340766B1 (en) | 2000-01-12 | 2002-01-22 | Transition Optical, Inc. | Substituted napthopyrans |
| BR0109755B1 (pt) * | 2000-03-22 | 2013-09-17 | composto de naftopirano e artigo fotocromÁtico | |
| US6433043B1 (en) * | 2000-11-28 | 2002-08-13 | Transitions Optical, Inc. | Removable imbibition composition of photochromic compound and kinetic enhancing additive |
| FR2819258B1 (fr) | 2001-01-11 | 2003-04-11 | Essilor Int | Procede d'obtention d'un latex photochromique stabilise, latex obtenu et application a l'optique ophtalmique |
| JP4407225B2 (ja) * | 2003-10-07 | 2010-02-03 | セイコーエプソン株式会社 | 描画方法 |
| US20070159594A9 (en) * | 2004-05-13 | 2007-07-12 | Jani Dharmendra M | Photochromic blue light filtering materials and ophthalmic devices |
| JP4879030B2 (ja) * | 2007-01-10 | 2012-02-15 | 株式会社トクヤマ | ナフトピラン化合物の製造方法 |
| US8110127B2 (en) | 2008-06-19 | 2012-02-07 | Essilor International (Compagnie Generale D'optique) | Photochromic coating exhibiting improved performance |
| AU2009335824B2 (en) * | 2008-12-18 | 2013-07-04 | Wyeth Llc | Method for controlling Streptococcus pneumoniae polysaccharide molecular weight using carbon |
| KR101146986B1 (ko) | 2010-03-16 | 2012-05-22 | 삼성모바일디스플레이주식회사 | 광학 필터 및 이를 구비하는 유기 발광 장치 |
| CN115151549B (zh) * | 2020-02-18 | 2023-12-19 | 株式会社德山 | 光致变色环状化合物和包含该光致变色环状化合物的固化性组合物 |
| US20210284778A1 (en) | 2020-03-11 | 2021-09-16 | Alcon Inc. | Photochromic polydiorganosiloxane vinylic crosslinkers |
| TWI785630B (zh) | 2020-06-02 | 2022-12-01 | 瑞士商愛爾康公司 | 光致變色矽酮水凝膠接觸鏡片及可聚合組合物及製造彼等之方法 |
| EP4237232B1 (en) | 2020-10-28 | 2024-11-27 | Alcon Inc. | Method for making photochromic contact lenses |
| US11886045B2 (en) | 2020-11-04 | 2024-01-30 | Alcon Inc. | Method for making photochromic contact lenses |
| HUE069913T2 (hu) | 2020-11-04 | 2025-04-28 | Alcon Inc | Eljárás fotokróm kontaktlencsék elõállítására |
| WO2022168989A1 (ja) | 2021-02-08 | 2022-08-11 | ホヤ レンズ タイランド リミテッド | フォトクロミック化合物、フォトクロミック組成物、フォトクロミック物品及び眼鏡 |
| KR20230131494A (ko) | 2021-03-08 | 2023-09-13 | 알콘 인코포레이티드 | 광기능성 콘택트 렌즈의 제조 방법 |
| WO2022191334A1 (ja) | 2021-03-12 | 2022-09-15 | ホヤ レンズ タイランド リミテッド | フォトクロミック化合物、フォトクロミック組成物、フォトクロミック物品及び眼鏡 |
| EP4313567B1 (en) | 2021-04-01 | 2025-01-29 | Alcon Inc. | Method for making photochromic contact lenses |
| JP2023111569A (ja) | 2022-01-31 | 2023-08-10 | ホヤ レンズ タイランド リミテッド | フォトクロミック化合物、フォトクロミック組成物、フォトクロミック物品及び眼鏡 |
| JP2023111570A (ja) | 2022-01-31 | 2023-08-10 | ホヤ レンズ タイランド リミテッド | フォトクロミック化合物、フォトクロミック組成物、フォトクロミック物品及び眼鏡 |
| EP4515325A1 (en) | 2022-04-26 | 2025-03-05 | Essilor International | Photochromic optical article having a mirror coating |
| US20230364832A1 (en) | 2022-04-28 | 2023-11-16 | Alcon Inc. | Method for making uv and hevl-absorbing ophthalmic lenses |
Family Cites Families (36)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3567605A (en) * | 1966-03-30 | 1971-03-02 | Ralph S Becker | Photochemical process |
| GB1186987A (en) * | 1967-08-30 | 1970-04-08 | Fuji Photo Film Co Ltd | Photochromic Compounds |
| JPS4948631B1 (ja) * | 1968-10-28 | 1974-12-23 | ||
| US3627690A (en) * | 1969-10-01 | 1971-12-14 | Itek Corp | Photochromic naphthopyran compositions |
| US4215010A (en) * | 1978-09-08 | 1980-07-29 | American Optical Corporation | Photochromic compounds |
| US4342668A (en) * | 1978-09-08 | 1982-08-03 | American Optical Corporation | Photochromic compounds |
| US4637698A (en) * | 1983-11-04 | 1987-01-20 | Ppg Industries, Inc. | Photochromic compound and articles containing the same |
| US4880667A (en) * | 1985-09-24 | 1989-11-14 | Ppg Industries, Inc. | Photochromic plastic article and method for preparing same |
| GB8611837D0 (en) * | 1986-05-15 | 1986-06-25 | Plessey Co Plc | Photochromic spiropyran compounds |
| GB8614680D0 (en) * | 1986-06-17 | 1986-07-23 | Plessey Co Plc | Photoreactive lenses |
| US4816584A (en) * | 1986-11-12 | 1989-03-28 | Ppg Industries, Inc. | Photochromic spiro(indoline)benzoxazines |
| US4931219A (en) * | 1987-07-27 | 1990-06-05 | Ppg Industries, Inc. | Photochromic compound and articles containing the same |
| US4931221A (en) * | 1988-12-30 | 1990-06-05 | Ppg Industries, Inc. | Photochromic spiropyran compounds |
| US4994208A (en) * | 1989-04-18 | 1991-02-19 | Ppg Industries, Inc. | Photochromic polymeric article |
| DE69015886T2 (de) * | 1989-06-05 | 1995-08-03 | Tokuyama Corp | Fotochromische Verbindung, deren Zusammensetzung und Verwendung. |
| US4980089A (en) * | 1989-07-12 | 1990-12-25 | Ppg Industries, Inc. | Photochromic spiropyran compounds |
| US5066818A (en) * | 1990-03-07 | 1991-11-19 | Ppg Industries, Inc. | Photochromic naphthopyran compounds |
| US5200116A (en) * | 1990-07-23 | 1993-04-06 | Ppg Industries, Inc. | Photochromic chromene compounds |
| US5244602A (en) * | 1990-12-03 | 1993-09-14 | Ppg Industries, Inc. | Photochromic naphthopyrans |
| US5238981A (en) * | 1992-02-24 | 1993-08-24 | Transitions Optical, Inc. | Photochromic naphthopyrans |
| FR2688782A1 (fr) * | 1992-03-19 | 1993-09-24 | Essilor Int | Nouveaux chromenes heterocycliques et leur utilisation dans le domaine de l'optique ophtalmique. |
| US5274132A (en) * | 1992-09-30 | 1993-12-28 | Transitions Optical, Inc. | Photochromic naphthopyran compounds |
| US5405958A (en) * | 1992-12-21 | 1995-04-11 | Transitions Optical, Inc. | Photochromic spiro(indoline)naphthoxazine compounds |
| WO1994020869A1 (en) * | 1993-03-12 | 1994-09-15 | Ppg Industries, Inc. | Novel benzopyrans |
| IT1265072B1 (it) * | 1993-05-18 | 1996-10-30 | Mini Ricerca Scient Tecnolog | Composti spiro-piranici dotati di caratteristiche fotocromatiche |
| IT1264563B1 (it) * | 1993-06-09 | 1996-10-04 | Enichem Sintesi | Composti fotocromatici e metodo per la loro preparazione |
| US5384077A (en) * | 1993-06-21 | 1995-01-24 | Transitions Optical, Inc. | Photochromic naphthopyran compounds |
| JPH0741758A (ja) * | 1993-07-29 | 1995-02-10 | Toray Ind Inc | フォトクロミック材料 |
| JPH0748363A (ja) * | 1993-08-03 | 1995-02-21 | Toray Ind Inc | フォトクロミック材料 |
| JPH0748566A (ja) * | 1993-08-04 | 1995-02-21 | Toray Ind Inc | フォトクロミック材料 |
| JPH0748567A (ja) * | 1993-08-05 | 1995-02-21 | Toray Ind Inc | フォトクロミック材料 |
| GB9316857D0 (en) * | 1993-08-13 | 1993-09-29 | Pilkington Plc | Photochromic compounds |
| US5458814A (en) * | 1993-12-09 | 1995-10-17 | Transitions Optical, Inc. | Substituted naphthopyrans |
| US5451344A (en) * | 1994-04-08 | 1995-09-19 | Transitions Optical, Inc. | Photochromic naphthopyran compounds |
| US5514817A (en) * | 1994-08-04 | 1996-05-07 | Ppg Industries, Inc. | Substituted phenanthropyrans |
| FR2732019B1 (fr) * | 1995-03-24 | 1997-06-13 | Flamel Tech Sa | Spiropyrannes photochromiques, compositions et articles les contenant |
-
1995
- 1995-06-14 US US08/490,190 patent/US5656206A/en not_active Expired - Lifetime
-
1996
- 1996-10-02 WO PCT/US1996/015843 patent/WO1998014443A1/en not_active Ceased
- 1996-10-02 AU AU72537/96A patent/AU735837B2/en not_active Expired
- 1996-10-02 JP JP51646598A patent/JP3553085B2/ja not_active Expired - Fee Related
- 1996-10-02 KR KR1019990702903A patent/KR20000048885A/ko not_active Withdrawn
- 1996-10-03 CA CA002187100A patent/CA2187100C/en not_active Expired - Lifetime
- 1996-10-09 DE DE69631765T patent/DE69631765T2/de not_active Expired - Lifetime
- 1996-10-09 EP EP96116144A patent/EP0835870B1/en not_active Expired - Lifetime
- 1996-10-09 ES ES96116144T patent/ES2217295T3/es not_active Expired - Lifetime
- 1996-10-25 HU HU9602961A patent/HUP9602961A3/hu unknown
- 1996-12-03 BR BRPI9604649-0A patent/BR9604649B1/pt not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| JP2000516254A (ja) | 2000-12-05 |
| KR20000048885A (ko) | 2000-07-25 |
| AU735837B2 (en) | 2001-07-19 |
| EP0835870A1 (en) | 1998-04-15 |
| HUP9602961A3 (en) | 1999-09-28 |
| DE69631765T2 (de) | 2005-02-24 |
| CA2187100C (en) | 2001-02-27 |
| HUP9602961A2 (hu) | 1998-07-28 |
| BR9604649B1 (pt) | 2009-05-05 |
| WO1998014443A1 (en) | 1998-04-09 |
| ES2217295T3 (es) | 2004-11-01 |
| EP0835870B1 (en) | 2004-03-03 |
| DE69631765D1 (de) | 2004-04-08 |
| HU9602961D0 (en) | 1996-12-30 |
| AU7253796A (en) | 1998-04-24 |
| BR9604649A (pt) | 1998-09-29 |
| CA2187100A1 (en) | 1998-04-03 |
| US5656206A (en) | 1997-08-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP3553085B2 (ja) | 新規の置換ナフトピラン類 | |
| EP1642895B1 (en) | Novel substituted naphthopyrans | |
| CA2204179C (en) | Novel photochromic indeno-fused naphthopyrans | |
| US5955520A (en) | Photochromic indeno-fused naphthopyrans | |
| US6353102B1 (en) | Photochromic naphthopyrans | |
| US5658501A (en) | Substituted naphthopyrans | |
| JP4383544B2 (ja) | 新規ホトクロミック複素環縮合インデノナフトピラン | |
| US5645767A (en) | Photochromic indeno-fused naphthopyrans | |
| US5573712A (en) | Substituted naphthopyrans | |
| US5650098A (en) | Substituted naphthopyrans | |
| US5658500A (en) | Substituted naphthopyrans | |
| US5891368A (en) | Fluoranthenopyrans | |
| JP4216344B2 (ja) | 新規置換ナフトピラン | |
| CN1234796A (zh) | 新的取代萘并吡喃化合物 | |
| JP3029460B6 (ja) | 新規フォトクロミックインデノ縮合ナフトピラン |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20040330 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20040428 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20090514 Year of fee payment: 5 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20090514 Year of fee payment: 5 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100514 Year of fee payment: 6 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110514 Year of fee payment: 7 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110514 Year of fee payment: 7 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120514 Year of fee payment: 8 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120514 Year of fee payment: 8 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130514 Year of fee payment: 9 |
|
| LAPS | Cancellation because of no payment of annual fees |