JP2023522010A - α1-アンチトリプシンの欠損により媒介される呼吸器系疾患の処置のための好中球エラスターゼ阻害剤アルベレスタットに関連する方法 - Google Patents
α1-アンチトリプシンの欠損により媒介される呼吸器系疾患の処置のための好中球エラスターゼ阻害剤アルベレスタットに関連する方法 Download PDFInfo
- Publication number
- JP2023522010A JP2023522010A JP2022562608A JP2022562608A JP2023522010A JP 2023522010 A JP2023522010 A JP 2023522010A JP 2022562608 A JP2022562608 A JP 2022562608A JP 2022562608 A JP2022562608 A JP 2022562608A JP 2023522010 A JP2023522010 A JP 2023522010A
- Authority
- JP
- Japan
- Prior art keywords
- methyl
- salt
- dosage form
- alberestat
- oxo
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 238000000034 method Methods 0.000 title claims abstract description 54
- 230000001404 mediated effect Effects 0.000 title claims description 57
- 208000023504 respiratory system disease Diseases 0.000 title claims description 57
- 238000011282 treatment Methods 0.000 title claims description 39
- 108010050122 alpha 1-Antitrypsin Proteins 0.000 title description 9
- 229940024142 alpha 1-antitrypsin Drugs 0.000 title description 7
- 230000007812 deficiency Effects 0.000 title description 5
- 108010000303 Secretory Proteinase Inhibitory Proteins Proteins 0.000 title description 2
- 102000002255 Secretory Proteinase Inhibitory Proteins Human genes 0.000 title description 2
- 239000003591 leukocyte elastase inhibitor Substances 0.000 title description 2
- 102000015395 alpha 1-Antitrypsin Human genes 0.000 title 1
- 150000003839 salts Chemical class 0.000 claims abstract description 121
- 239000002552 dosage form Substances 0.000 claims abstract description 48
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims abstract description 47
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 claims abstract description 44
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims abstract description 44
- 208000006682 alpha 1-Antitrypsin Deficiency Diseases 0.000 claims description 65
- 239000007909 solid dosage form Substances 0.000 claims description 63
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 claims description 56
- QNQZWEGMKJBHEM-UHFFFAOYSA-N 6-methyl-5-(2-methylpyrazol-3-yl)-n-[(5-methylsulfonylpyridin-2-yl)methyl]-2-oxo-1-[3-(trifluoromethyl)phenyl]pyridine-3-carboxamide Chemical compound O=C1N(C=2C=C(C=CC=2)C(F)(F)F)C(C)=C(C=2N(N=CC=2)C)C=C1C(=O)NCC1=CC=C(S(C)(=O)=O)C=N1 QNQZWEGMKJBHEM-UHFFFAOYSA-N 0.000 claims description 49
- 230000036470 plasma concentration Effects 0.000 claims description 20
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 17
- 201000010099 disease Diseases 0.000 claims description 16
- 206010014561 Emphysema Diseases 0.000 claims description 15
- 230000001154 acute effect Effects 0.000 claims description 14
- 206010039083 rhinitis Diseases 0.000 claims description 13
- 206010001052 Acute respiratory distress syndrome Diseases 0.000 claims description 12
- 208000013616 Respiratory Distress Syndrome Diseases 0.000 claims description 12
- 208000011341 adult acute respiratory distress syndrome Diseases 0.000 claims description 12
- 201000000028 adult respiratory distress syndrome Diseases 0.000 claims description 12
- 238000002560 therapeutic procedure Methods 0.000 claims description 11
- 208000006673 asthma Diseases 0.000 claims description 10
- 239000007787 solid Substances 0.000 claims description 10
- 206010011224 Cough Diseases 0.000 claims description 7
- 201000009240 nasopharyngitis Diseases 0.000 claims description 7
- 201000009267 bronchiectasis Diseases 0.000 claims description 6
- 201000009151 chronic rhinitis Diseases 0.000 claims description 6
- 208000005069 pulmonary fibrosis Diseases 0.000 claims description 6
- 208000002815 pulmonary hypertension Diseases 0.000 claims description 6
- 208000035939 Alveolitis allergic Diseases 0.000 claims description 5
- 201000002909 Aspergillosis Diseases 0.000 claims description 5
- 208000036641 Aspergillus infections Diseases 0.000 claims description 5
- 241000711573 Coronaviridae Species 0.000 claims description 5
- 208000027445 Farmer Lung Diseases 0.000 claims description 5
- 208000036142 Viral infection Diseases 0.000 claims description 5
- 208000022195 farmer lung disease Diseases 0.000 claims description 5
- 230000000642 iatrogenic effect Effects 0.000 claims description 5
- 206010022000 influenza Diseases 0.000 claims description 5
- 206010033675 panniculitis Diseases 0.000 claims description 5
- 201000008827 tuberculosis Diseases 0.000 claims description 5
- 230000009385 viral infection Effects 0.000 claims description 5
- 201000003883 Cystic fibrosis Diseases 0.000 claims description 4
- 241000725643 Respiratory syncytial virus Species 0.000 claims description 4
- 230000000954 anitussive effect Effects 0.000 claims description 4
- 206010006451 bronchitis Diseases 0.000 claims description 4
- 239000002775 capsule Substances 0.000 claims description 4
- 201000000306 sarcoidosis Diseases 0.000 claims description 4
- 206010020751 Hypersensitivity Diseases 0.000 claims description 3
- 206010035664 Pneumonia Diseases 0.000 claims description 3
- 239000004480 active ingredient Substances 0.000 claims description 3
- 125000004216 fluoromethyl group Chemical group [H]C([H])(F)* 0.000 claims description 3
- 208000026935 allergic disease Diseases 0.000 claims description 2
- 230000009610 hypersensitivity Effects 0.000 claims description 2
- 230000001174 ascending effect Effects 0.000 claims 2
- 206010001258 Adenoviral infections Diseases 0.000 claims 1
- 125000005490 tosylate group Chemical class 0.000 claims 1
- 108010028275 Leukocyte Elastase Proteins 0.000 description 91
- 102100033174 Neutrophil elastase Human genes 0.000 description 91
- 230000000694 effects Effects 0.000 description 82
- 210000000440 neutrophil Anatomy 0.000 description 35
- 102000035195 Peptidases Human genes 0.000 description 34
- 108091005804 Peptidases Proteins 0.000 description 34
- 235000019833 protease Nutrition 0.000 description 33
- 102000016387 Pancreatic elastase Human genes 0.000 description 24
- 108010067372 Pancreatic elastase Proteins 0.000 description 24
- 239000003112 inhibitor Substances 0.000 description 24
- 230000001965 increasing effect Effects 0.000 description 23
- 150000001875 compounds Chemical class 0.000 description 21
- 229940012952 fibrinogen Drugs 0.000 description 20
- 108010049003 Fibrinogen Proteins 0.000 description 19
- 102000008946 Fibrinogen Human genes 0.000 description 19
- 230000005764 inhibitory process Effects 0.000 description 18
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 18
- 238000003776 cleavage reaction Methods 0.000 description 15
- 239000000047 product Substances 0.000 description 15
- 230000007017 scission Effects 0.000 description 15
- 210000004072 lung Anatomy 0.000 description 13
- 229920013636 polyphenyl ether polymer Polymers 0.000 description 13
- GVUGADOWXGKRAE-SRVKXCTJSA-N 4-[[(2s)-1-[[(2s)-1-[[(2s)-1-(4-nitroanilino)-1-oxopropan-2-yl]amino]-1-oxopropan-2-yl]amino]-1-oxopropan-2-yl]amino]-4-oxobutanoic acid Chemical compound OC(=O)CCC(=O)N[C@@H](C)C(=O)N[C@@H](C)C(=O)N[C@@H](C)C(=O)NC1=CC=C([N+]([O-])=O)C=C1 GVUGADOWXGKRAE-SRVKXCTJSA-N 0.000 description 12
- 239000003814 drug Substances 0.000 description 10
- 239000000203 mixture Substances 0.000 description 10
- 210000002381 plasma Anatomy 0.000 description 10
- 108010008211 N-Formylmethionine Leucyl-Phenylalanine Proteins 0.000 description 9
- PRQROPMIIGLWRP-BZSNNMDCSA-N chemotactic peptide Chemical compound CSCC[C@H](NC=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](C(O)=O)CC1=CC=CC=C1 PRQROPMIIGLWRP-BZSNNMDCSA-N 0.000 description 9
- 229940079593 drug Drugs 0.000 description 9
- 230000000638 stimulation Effects 0.000 description 9
- 239000000758 substrate Substances 0.000 description 9
- 102100022712 Alpha-1-antitrypsin Human genes 0.000 description 8
- 230000003416 augmentation Effects 0.000 description 7
- 230000002401 inhibitory effect Effects 0.000 description 7
- 210000001519 tissue Anatomy 0.000 description 7
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- 102000004190 Enzymes Human genes 0.000 description 6
- 108090000790 Enzymes Proteins 0.000 description 6
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 6
- 102000012479 Serine Proteases Human genes 0.000 description 6
- 108010022999 Serine Proteases Proteins 0.000 description 6
- 230000004913 activation Effects 0.000 description 6
- 229940088598 enzyme Drugs 0.000 description 6
- 208000015181 infectious disease Diseases 0.000 description 6
- 229940016286 microcrystalline cellulose Drugs 0.000 description 6
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 6
- 239000008108 microcrystalline cellulose Substances 0.000 description 6
- 230000003389 potentiating effect Effects 0.000 description 6
- 102000016942 Elastin Human genes 0.000 description 5
- 108010014258 Elastin Proteins 0.000 description 5
- 229920000392 Zymosan Polymers 0.000 description 5
- 210000004369 blood Anatomy 0.000 description 5
- 239000008280 blood Substances 0.000 description 5
- 210000004027 cell Anatomy 0.000 description 5
- 230000001066 destructive effect Effects 0.000 description 5
- 229920002549 elastin Polymers 0.000 description 5
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical class CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 5
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 5
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 4
- 150000003857 carboxamides Chemical class 0.000 description 4
- 230000008859 change Effects 0.000 description 4
- 238000011161 development Methods 0.000 description 4
- 230000018109 developmental process Effects 0.000 description 4
- 239000003085 diluting agent Substances 0.000 description 4
- 238000011156 evaluation Methods 0.000 description 4
- 238000009472 formulation Methods 0.000 description 4
- 239000012458 free base Substances 0.000 description 4
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 4
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 4
- 238000000338 in vitro Methods 0.000 description 4
- 108090000623 proteins and genes Proteins 0.000 description 4
- 102000004169 proteins and genes Human genes 0.000 description 4
- 230000001105 regulatory effect Effects 0.000 description 4
- 238000011160 research Methods 0.000 description 4
- 230000000241 respiratory effect Effects 0.000 description 4
- 241000701161 unidentified adenovirus Species 0.000 description 4
- 208000035285 Allergic Seasonal Rhinitis Diseases 0.000 description 3
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 3
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 3
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 3
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 3
- 229930195725 Mannitol Natural products 0.000 description 3
- 101150069374 Serpina1 gene Proteins 0.000 description 3
- 239000002671 adjuvant Substances 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 239000000872 buffer Substances 0.000 description 3
- XAAHAAMILDNBPS-UHFFFAOYSA-L calcium hydrogenphosphate dihydrate Chemical compound O.O.[Ca+2].OP([O-])([O-])=O XAAHAAMILDNBPS-UHFFFAOYSA-L 0.000 description 3
- 235000010980 cellulose Nutrition 0.000 description 3
- 229920002678 cellulose Polymers 0.000 description 3
- 239000001913 cellulose Substances 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 230000002950 deficient Effects 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 230000002255 enzymatic effect Effects 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 210000002744 extracellular matrix Anatomy 0.000 description 3
- 201000001155 extrinsic allergic alveolitis Diseases 0.000 description 3
- 238000000684 flow cytometry Methods 0.000 description 3
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 3
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 3
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 3
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 3
- 208000022098 hypersensitivity pneumonitis Diseases 0.000 description 3
- 238000011534 incubation Methods 0.000 description 3
- 230000003834 intracellular effect Effects 0.000 description 3
- 239000000594 mannitol Substances 0.000 description 3
- 235000010355 mannitol Nutrition 0.000 description 3
- 239000008194 pharmaceutical composition Substances 0.000 description 3
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 3
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 3
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 3
- 230000002685 pulmonary effect Effects 0.000 description 3
- 210000002966 serum Anatomy 0.000 description 3
- -1 sucrose fatty acid ester Chemical class 0.000 description 3
- GUBGYTABKSRVRQ-UHFFFAOYSA-N 2-(hydroxymethyl)-6-[4,5,6-trihydroxy-2-(hydroxymethyl)oxan-3-yl]oxyoxane-3,4,5-triol Chemical compound OCC1OC(OC2C(O)C(O)C(O)OC2CO)C(O)C(O)C1O GUBGYTABKSRVRQ-UHFFFAOYSA-N 0.000 description 2
- 102000008186 Collagen Human genes 0.000 description 2
- 108010035532 Collagen Proteins 0.000 description 2
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 2
- 206010017533 Fungal infection Diseases 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 101000851058 Homo sapiens Neutrophil elastase Proteins 0.000 description 2
- 208000026350 Inborn Genetic disease Diseases 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 208000004852 Lung Injury Diseases 0.000 description 2
- 208000019693 Lung disease Diseases 0.000 description 2
- 241000699670 Mus sp. Species 0.000 description 2
- 208000031888 Mycoses Diseases 0.000 description 2
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 2
- 208000000592 Nasal Polyps Diseases 0.000 description 2
- 208000037581 Persistent Infection Diseases 0.000 description 2
- 206010037394 Pulmonary haemorrhage Diseases 0.000 description 2
- 206010039094 Rhinitis perennial Diseases 0.000 description 2
- 239000006146 Roswell Park Memorial Institute medium Substances 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- 206010069363 Traumatic lung injury Diseases 0.000 description 2
- 206010069351 acute lung injury Diseases 0.000 description 2
- 230000032683 aging Effects 0.000 description 2
- 208000037883 airway inflammation Diseases 0.000 description 2
- 230000000172 allergic effect Effects 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 208000010668 atopic eczema Diseases 0.000 description 2
- 239000000090 biomarker Substances 0.000 description 2
- CJZGTCYPCWQAJB-UHFFFAOYSA-L calcium stearate Chemical compound [Ca+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CJZGTCYPCWQAJB-UHFFFAOYSA-L 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 208000013116 chronic cough Diseases 0.000 description 2
- 230000001684 chronic effect Effects 0.000 description 2
- 229920001436 collagen Polymers 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 235000019700 dicalcium phosphate Nutrition 0.000 description 2
- 229940095079 dicalcium phosphate anhydrous Drugs 0.000 description 2
- 239000007884 disintegrant Substances 0.000 description 2
- 239000000428 dust Substances 0.000 description 2
- 239000002158 endotoxin Substances 0.000 description 2
- 239000000945 filler Substances 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 208000016361 genetic disease Diseases 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- 102000052502 human ELANE Human genes 0.000 description 2
- 238000003018 immunoassay Methods 0.000 description 2
- 230000002458 infectious effect Effects 0.000 description 2
- 230000002427 irreversible effect Effects 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- 231100000515 lung injury Toxicity 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 230000035772 mutation Effects 0.000 description 2
- 230000001272 neurogenic effect Effects 0.000 description 2
- 239000000041 non-steroidal anti-inflammatory agent Substances 0.000 description 2
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 2
- 230000001991 pathophysiological effect Effects 0.000 description 2
- 230000002085 persistent effect Effects 0.000 description 2
- PHEDXBVPIONUQT-RGYGYFBISA-N phorbol 13-acetate 12-myristate Chemical compound C([C@]1(O)C(=O)C(C)=C[C@H]1[C@@]1(O)[C@H](C)[C@H]2OC(=O)CCCCCCCCCCCCC)C(CO)=C[C@H]1[C@H]1[C@]2(OC(C)=O)C1(C)C PHEDXBVPIONUQT-RGYGYFBISA-N 0.000 description 2
- 239000000902 placebo Substances 0.000 description 2
- 229940068196 placebo Drugs 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 102000004196 processed proteins & peptides Human genes 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- 230000029058 respiratory gaseous exchange Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 230000002441 reversible effect Effects 0.000 description 2
- 230000003248 secreting effect Effects 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 229960004793 sucrose Drugs 0.000 description 2
- 239000006228 supernatant Substances 0.000 description 2
- 230000009469 supplementation Effects 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 238000002054 transplantation Methods 0.000 description 2
- 238000010200 validation analysis Methods 0.000 description 2
- 208000001319 vasomotor rhinitis Diseases 0.000 description 2
- LQIAZOCLNBBZQK-UHFFFAOYSA-N 1-(1,2-Diphosphanylethyl)pyrrolidin-2-one Chemical compound PCC(P)N1CCCC1=O LQIAZOCLNBBZQK-UHFFFAOYSA-N 0.000 description 1
- KRSNUHUVJHIFPL-UHFFFAOYSA-N 1-[3-(trifluoromethyl)phenyl]-2h-pyridine-3-carboxamide Chemical compound C1C(C(=O)N)=CC=CN1C1=CC=CC(C(F)(F)F)=C1 KRSNUHUVJHIFPL-UHFFFAOYSA-N 0.000 description 1
- OACPRYMPBJXXEB-UHFFFAOYSA-N 2-oxo-1-[3-(trifluoromethyl)phenyl]pyridine-3-carboxamide Chemical compound O=C1C(C(=O)N)=CC=CN1C1=CC=CC(C(F)(F)F)=C1 OACPRYMPBJXXEB-UHFFFAOYSA-N 0.000 description 1
- XPYQFIISZQCINN-QVXDJYSKSA-N 4-amino-1-[(2r,3e,4s,5r)-3-(fluoromethylidene)-4-hydroxy-5-(hydroxymethyl)oxolan-2-yl]pyrimidin-2-one;hydrate Chemical compound O.O=C1N=C(N)C=CN1[C@H]1C(=C/F)/[C@H](O)[C@@H](CO)O1 XPYQFIISZQCINN-QVXDJYSKSA-N 0.000 description 1
- 206010067484 Adverse reaction Diseases 0.000 description 1
- 208000000884 Airway Obstruction Diseases 0.000 description 1
- 229920000945 Amylopectin Polymers 0.000 description 1
- BSYNRYMUTXBXSQ-UHFFFAOYSA-N Aspirin Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O BSYNRYMUTXBXSQ-UHFFFAOYSA-N 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 108090000317 Chymotrypsin Proteins 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- 229920002785 Croscarmellose sodium Polymers 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 206010065563 Eosinophilic bronchitis Diseases 0.000 description 1
- 235000014755 Eruca sativa Nutrition 0.000 description 1
- 244000024675 Eruca sativa Species 0.000 description 1
- 101710205374 Extracellular elastase Proteins 0.000 description 1
- 102000016359 Fibronectins Human genes 0.000 description 1
- 108010067306 Fibronectins Proteins 0.000 description 1
- 206010016654 Fibrosis Diseases 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 101000823116 Homo sapiens Alpha-1-antitrypsin Proteins 0.000 description 1
- 101000856199 Homo sapiens Chymotrypsin-like protease CTRL-1 Proteins 0.000 description 1
- 101001010513 Homo sapiens Leukocyte elastase inhibitor Proteins 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 208000029523 Interstitial Lung disease Diseases 0.000 description 1
- 229920003085 Kollidon® CL Polymers 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- 229930182816 L-glutamine Natural products 0.000 description 1
- 102000007547 Laminin Human genes 0.000 description 1
- 108010085895 Laminin Proteins 0.000 description 1
- 235000019759 Maize starch Nutrition 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 108090000973 Myeloblastin Proteins 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 229920003081 Povidone K 30 Polymers 0.000 description 1
- 229920003082 Povidone K 90 Polymers 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 229940124158 Protease/peptidase inhibitor Drugs 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 206010063837 Reperfusion injury Diseases 0.000 description 1
- 208000002200 Respiratory Hypersensitivity Diseases 0.000 description 1
- 208000036284 Rhinitis seasonal Diseases 0.000 description 1
- 102000003667 Serine Endopeptidases Human genes 0.000 description 1
- 108090000083 Serine Endopeptidases Proteins 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 1
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- VJHCJDRQFCCTHL-UHFFFAOYSA-N acetic acid 2,3,4,5,6-pentahydroxyhexanal Chemical compound CC(O)=O.OCC(O)C(O)C(O)C(O)C=O VJHCJDRQFCCTHL-UHFFFAOYSA-N 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 229960001138 acetylsalicylic acid Drugs 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 108010016828 adenylyl sulfate-ammonia adenylyltransferase Proteins 0.000 description 1
- 230000006838 adverse reaction Effects 0.000 description 1
- 230000036428 airway hyperreactivity Effects 0.000 description 1
- 230000010085 airway hyperresponsiveness Effects 0.000 description 1
- 201000010105 allergic rhinitis Diseases 0.000 description 1
- 229950005666 alvelestat Drugs 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000000118 anti-neoplastic effect Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 229920001222 biopolymer Polymers 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 230000036765 blood level Effects 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 235000013539 calcium stearate Nutrition 0.000 description 1
- 239000008116 calcium stearate Substances 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 125000002057 carboxymethyl group Chemical group [H]OC(=O)C([H])([H])[*] 0.000 description 1
- 229950008138 carmellose Drugs 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 239000003593 chromogenic compound Substances 0.000 description 1
- 229960002376 chymotrypsin Drugs 0.000 description 1
- 235000019504 cigarettes Nutrition 0.000 description 1
- 229940075614 colloidal silicon dioxide Drugs 0.000 description 1
- 210000002808 connective tissue Anatomy 0.000 description 1
- GLNDAGDHSLMOKX-UHFFFAOYSA-N coumarin 120 Chemical compound C1=C(N)C=CC2=C1OC(=O)C=C2C GLNDAGDHSLMOKX-UHFFFAOYSA-N 0.000 description 1
- 229960001681 croscarmellose sodium Drugs 0.000 description 1
- 229960000913 crospovidone Drugs 0.000 description 1
- 235000010947 crosslinked sodium carboxy methyl cellulose Nutrition 0.000 description 1
- 230000000254 damaging effect Effects 0.000 description 1
- 230000006735 deficit Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000000593 degrading effect Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 235000013681 dietary sucrose Nutrition 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 230000004064 dysfunction Effects 0.000 description 1
- 239000003602 elastase inhibitor Substances 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 230000002327 eosinophilic effect Effects 0.000 description 1
- MVPICKVDHDWCJQ-UHFFFAOYSA-N ethyl 3-pyrrolidin-1-ylpropanoate Chemical compound CCOC(=O)CCN1CCCC1 MVPICKVDHDWCJQ-UHFFFAOYSA-N 0.000 description 1
- 230000003090 exacerbative effect Effects 0.000 description 1
- 210000001808 exosome Anatomy 0.000 description 1
- 210000001723 extracellular space Anatomy 0.000 description 1
- 238000013213 extrapolation Methods 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 230000004761 fibrosis Effects 0.000 description 1
- 238000007421 fluorometric assay Methods 0.000 description 1
- 230000005714 functional activity Effects 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 102000054767 gene variant Human genes 0.000 description 1
- 230000009931 harmful effect Effects 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 238000010874 in vitro model Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 230000003960 inflammatory cascade Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 230000009878 intermolecular interaction Effects 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 208000012947 ischemia reperfusion injury Diseases 0.000 description 1
- 238000012933 kinetic analysis Methods 0.000 description 1
- 229960001375 lactose Drugs 0.000 description 1
- 238000012417 linear regression Methods 0.000 description 1
- 229920006008 lipopolysaccharide Polymers 0.000 description 1
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 1
- 230000004199 lung function Effects 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 229960001855 mannitol Drugs 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 230000003278 mimic effect Effects 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 230000000414 obstructive effect Effects 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 231100000915 pathological change Toxicity 0.000 description 1
- 230000036285 pathological change Effects 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000007310 pathophysiology Effects 0.000 description 1
- 208000022719 perennial allergic rhinitis Diseases 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 230000035479 physiological effects, processes and functions Effects 0.000 description 1
- 230000007180 physiological regulation Effects 0.000 description 1
- 238000007747 plating Methods 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 description 1
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229940068968 polysorbate 80 Drugs 0.000 description 1
- 229920000053 polysorbate 80 Polymers 0.000 description 1
- 235000013809 polyvinylpolypyrrolidone Nutrition 0.000 description 1
- 229920000523 polyvinylpolypyrrolidone Polymers 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 230000006920 protein precipitation Effects 0.000 description 1
- 230000007115 recruitment Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000000284 resting effect Effects 0.000 description 1
- 206010039073 rheumatoid arthritis Diseases 0.000 description 1
- 208000017022 seasonal allergic rhinitis Diseases 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 238000004088 simulation Methods 0.000 description 1
- 239000000779 smoke Substances 0.000 description 1
- 230000000391 smoking effect Effects 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 229940083542 sodium Drugs 0.000 description 1
- 235000015424 sodium Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 1
- 229940045902 sodium stearyl fumarate Drugs 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 229960002920 sorbitol Drugs 0.000 description 1
- 235000010356 sorbitol Nutrition 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 238000004885 tandem mass spectrometry Methods 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 210000000115 thoracic cavity Anatomy 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 238000000954 titration curve Methods 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 108700012359 toxins Proteins 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 238000011870 unpaired t-test Methods 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- 239000000304 virulence factor Substances 0.000 description 1
- 230000007923 virulence factor Effects 0.000 description 1
- 238000012800 visualization Methods 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 230000003442 weekly effect Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/444—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a six-membered ring with nitrogen as a ring heteroatom, e.g. amrinone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Chemical & Material Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Epidemiology (AREA)
- Pulmonology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Virology (AREA)
- Pain & Pain Management (AREA)
- Rheumatology (AREA)
- Molecular Biology (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Medicinal Preparation (AREA)
Abstract
本発明は、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミド(すなわち、アルベレスタット)またはその塩の剤形及び投与計画、ならびに当該剤形及び投与計画を用いる関連方法を開示するものである。【選択図】なし
Description
関連出願の相互参照
本出願は、2020年4月16日に出願された英国特許出願番号2005519.0、及び2020年4月16日に出願された英国特許出願番号2005520.8、ならびに2020年8月4日に出願された米国仮出願US62/706,195の優先権の利益を主張するものである。これらの出願の内容は、参照により本明細書に組み込まれる。
本出願は、2020年4月16日に出願された英国特許出願番号2005519.0、及び2020年4月16日に出願された英国特許出願番号2005520.8、ならびに2020年8月4日に出願された米国仮出願US62/706,195の優先権の利益を主張するものである。これらの出願の内容は、参照により本明細書に組み込まれる。
本発明は、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミド及びその塩の新規剤形及び投与計画を開示するものである。
エラスターゼは、おそらく体内で最も破壊的な酵素であり、実質的に全結合組織の構成要素を分解する能力を有する。
セリンプロテアーゼのキモトリプシンスーパーファミリーの一員である、ヒト好中球エラスターゼ(hNE)は、好中球のアズール顆粒に貯留されている33KDaの酵素である。好中球では、NE(好中球エラスターゼ)の濃度が5mMを超え、その細胞内総量は最大3pgと推定されている。活性化されると、NEは顆粒から細胞外間隙に速やかに放出される(Kawabat et al.2002,Eur.J.Pharmacol.451,1-10を参照)。NEの主な細胞内生理機能は、好中球によって貪食された外来有機分子の分解であるが、細胞外エラスターゼの主な標的はエラスチンである(Janoff and Scherer,1968,J.Exp.Med.128,1137-1155)。NEは、エラスチン、3型及び4型コラーゲン、ラミニン、フィブロネクチン、サイトカインなどを含む、ほとんど全ての細胞外マトリックス及び主要血漿タンパク質を分解する能力を有するという点で(Kawabat et al.,2002,Eur.J.Pharmacol.451,1-10を参照)、他のプロテアーゼ(例えば、プロテイナーゼ3)と比較して独特である(Ohbayashi,H.,2002,Expert Opin.Investig.Drugs,11,965-980)。NEは、慢性肺疾患に見られる多くの病理学的変化に共通する主要メディエーターである(Stockley,R.A.1994,Am.J.Resp.Crit.Care Med.150,109-113)。
NEの破壊的な役割は、約40年前にLaurell及びErikssonが、慢性気流閉塞及び肺気腫と、血清α1-アンチトリプシンの欠損との関連性を報告し(Laurell and Eriksson,1963,Scand.J.Clin.Invest.15,132-140)、血清α1-アンチトリプシンがNEの最も重要な内因性インヒビターであることが認められた際に固まった。NEと内因性アンチプロテアーゼとの間の不均衡により、肺組織に過剰なNEが生じると考えられており、それが慢性閉塞性肺疾患(COPD)の主要な病原性因子としてみなされている。NEが過剰になると正常な肺構造が破壊され、続いて主に肺気腫で見られるように、呼吸器気腔が不可逆的に拡張する。α1-プロテイナーゼインヒビター欠損マウスにおいては、肺でのエラスターゼ量の増加及び肺気腫に関連する、肺への好中球の動員が増加する(Cavarra et al.,1996,Lab.Invest.75,273-280)。気管支肺胞洗浄液中のNE-α1プロテアーゼインヒビター複合体レベルがより高い個体では、レベルがより低い個体と比較して、肺機能の低下が著しく促進されることが示されている(Betsuyaku et al.2000,Respiration,67,261-267)。ラットにおいて気管を介してNEを注入すると、肺出血、急性期での好中球蓄積及び慢性期での気腫性変化が生じる(Karaki et al.,2002,Am.J.Resp.Crit.Care Med.,166,496-500)。ハムスターにおいて、NEにより生じた急性期肺気腫及び肺出血は、NEインヒビターで前処置することによって抑制できることが研究で示されている(Fujie et al.,1999,Inflamm.Res.48,160-167)。
実験動物におけるエンドトキシンにより生じた急性肺損傷は、NEレベルの上昇に関連している(Kawabata,et al.,1999,Am.J.Resp.Crit.Care,161,2013-2018)。マウスにおいてリポ多糖を気管内注射することによって生じる急性肺炎症は、気管支肺胞洗浄液中のNE活性を上昇させるが、これはNEインヒビターによって著しく抑制されることが示されている(Fujie et al.,1999,Eur.J.Pharmacol.,374,117-125 ;Yasui,et al.,1995,Eur.Resp.J.,8,1293-1299)。NEはまた、単離されたウサギ灌流肺における、腫瘍壊死因子<x(TNFce)及びホルボールミリステートアセテート(PMA)によって生じる急性肺損傷モデルで観察される、好中球誘導性の肺微小血管透過性の亢進において重要な役割を果たす(Miyazaki et al.,1998,Am.J.Respir.Crit.Care Med.,157,89-94)。
NEは、肺気腫、肺線維症、成人呼吸窮迫症候群(ARDS)、虚血再灌流障害、関節リウマチ、及び肺高血圧症などの多くの疾患の促進や増悪に関係づけられている。
本発明は、NEならびにプロテイナーゼ3及び膵臓エラスターゼなどの相同セリンプロテアーゼのインヒビターであり、それによって治療に有用な、2-ピリジオン(pyridione)誘導体の剤形及び投与計画を開示するものである。
参照により全体が本明細書に組み込まれるWO2005/026123は、治療に有用なNEインヒビターのクラスを教示するものである。WO2005/026123はさらにその中で、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミド及びその塩として同定される、特定のNEインヒビター化合物を開示している(実施例94、85頁)。本明細書では、この化合物を化合物(I)と名付ける。化合物(I)は、アルベレスタット(alvelestat)、AZD9668、またはMPH966としても公知である。
同様に、参照により全体が本明細書に組み込まれるWO2010/094964は、WO2005/026123に関して上で示したように、化合物(I)の塩形態を教示するものである。この文献では、化合物(I)が1日あたり最大200mgの量で毎日投与されることが報告されている。
化合物(I)は、以下:気管支、アレルギー性、内因性、外因性、運動誘発性、薬物誘発性(アスピリン及びNSAID誘発性を含む)及び粉塵誘発性喘息、間欠性及び持続性の両方、ならびにあらゆる重症度の喘息、ならびに気道過敏性亢進の他の原因を含む喘息;慢性閉塞性肺疾患(COPD);感染性及び好酸球性気管支炎を含む気管支炎;肺気腫;気管支拡張症;嚢胞性線維症;サルコイドーシス;農夫肺及び関連疾患;過敏性肺炎;成人呼吸窮迫症候群(ARDS);原因不明の線維化性胞隔炎、特発性間質性肺炎、抗腫瘍性治療に合併する線維症、及び慢性感染症(結核ならびにアスペルギルス症及び他の真菌感染症を含む)を含む肺線維症;肺移植の合併症;気道の炎症及び分泌状態に関連する慢性の咳、及び医原性の咳の処置を含む鎮咳活性;薬物性鼻炎及び血管運動性鼻炎を含む急性及び慢性鼻炎;神経性鼻炎(枯草熱)を含む、通年性及び季節性アレルギー性鼻炎;鼻茸;感冒、肺高血圧症、ならびに呼吸器合胞体ウイルス、インフルエンザ、コロナウイルス(SARSを含む)及びアデノウイルスによる感染症を含む急性ウイルス感染症を含む、気道の閉塞性疾患などの呼吸器/系疾患の処置に有用であり得る。
NEの初期活性化を回避する必要性は甚だしい。一旦活性化が起こると、その後に続く炎症カスケードにより、不可逆的損傷が生じることがあり、それ自体を逆戻りさせることは困難である。したがって、本発明は、投与期間を通じてNEを阻害するのに必要な血中濃度以上を達成及び維持し、特にNEの初期活性化を防ぐ、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミド及びその塩の投与計画によって、高効率のNE阻害を提供することを目的とする。
第1の態様において、本発明は、120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む、固体剤形を提供する。
他の第1の態様において、本発明は、220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む、固体剤形を提供する。
本発明の第2の態様において、本発明は、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形(複数可)を提供するものであって、前記単一または複数の固体剤形(複数可)は、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む。
本発明の他の第2の態様において、本発明は、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形(複数可)を提供するものであって、前記単一または複数の固体剤形(複数可)は、投与あたり合計220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む。
本発明の第3の態様において、本発明は、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形(複数可)を提供するものであって、前記単一または複数の固体剤形(複数可)は、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含み、各用量の投与は、1日2回、少なくとも8時間の投与間隔で行われる。
本発明の他の第3の態様において、本発明は、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形(複数可)を提供するものであって、前記単一または複数の固体剤形(複数可)は、投与あたり合計220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含み、各用量の投与は、1日2回、少なくとも8時間の投与間隔で行われる。
本発明の第4の態様において、本発明は、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の複数の固体剤形を含むキットを提供するものであって、前記キットは、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を順次投与するための指示書を含有し、各用量の投与は、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けて、1日2回、少なくとも8時間の投与間隔で行われる。
本発明の他の第4の態様において、本発明は、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の複数の固体剤形を含むキットを提供するものであって、前記キットは、投与あたり合計220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を順次投与するための指示書を含有し、各用量の投与は、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けて、1日2回、少なくとも8時間の投与間隔で行われる。
本発明の第5の態様において、本発明は、経口投与用の複数の固体剤形を含むキットを提供するものであって、各剤形は、120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含み、前記キットは、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、順次、1日2回の各用量の投与に対する指示書を含有する。
本発明の他の第5の態様において、本発明は、経口投与用の複数の固体剤形を含むキットを提供するものであって、各剤形は、220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含み、前記キットは、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、順次、1日2回の各用量の投与に対する指示書を含有する。
本発明の第6の態様において、本発明は、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患を患うヒト患者に対する、単一または複数の固体剤形(複数可)の1日2回の経口投与を含む、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患を処置するための方法を提供するものであって、前記単一または複数の固体剤形(複数可)は、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む。
本発明の他の第6の態様において、本発明は、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患を患うヒト患者に対する、単一または複数の固体剤形(複数可)の1日2回の経口投与を含む、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患を処置するための方法を提供するものであって、前記単一または複数の固体剤形(複数可)は、投与あたり合計220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む。
本発明の第7の態様において、本発明は、COPD(慢性閉塞性肺疾患)の処置に向けた、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形(複数可)を提供するものであって、前記単一または複数の固体剤形(複数可)は、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む。
本発明の他の第7の態様において、本発明は、COPD(慢性閉塞性肺疾患)の処置に向けた、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形(複数可)を提供するものであって、前記単一または複数の固体剤形(複数可)は、投与あたり合計220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む。
本発明の第8の態様において、本発明は、COPD(慢性閉塞性肺疾患)の処置に向けた、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形(複数可)を提供するものであって、前記単一または複数の固体剤形(複数可)は、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含み、各用量の投与は、1日2回、少なくとも8時間の投与間隔で行われる。
本発明の他の第8の態様において、本発明は、COPD(慢性閉塞性肺疾患)の処置に向けた、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形(複数可)を提供するものであって、前記単一または複数の固体剤形(複数可)は、投与あたり合計220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含み、各用量の投与は、1日2回、少なくとも8時間の投与間隔で行われる。
本発明の第9の態様において、本発明は、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の複数の固体剤形を含むキットを提供するものであって、前記キットは、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を順次投与するための指示書を含有し、各用量の投与は、COPD(慢性閉塞性肺疾患)の処置に向けて、1日2回、少なくとも8時間の投与間隔で行われる。
本発明の他の第9の態様において、本発明は、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の複数の固体剤形を含むキットを提供するものであって、前記キットは、投与あたり合計220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を順次投与するための指示書を含有し、各用量の投与は、COPD(慢性閉塞性肺疾患)の処置に向けて、1日2回、少なくとも8時間の投与間隔で行われる。
本発明の第10の態様において、本発明は、経口投与用の複数の固体剤形を含むキットを提供するものであって、各剤形は、120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含み、前記キットは、COPD(慢性閉塞性肺疾患)の処置に向けた、順次、1日2回の各用量の投与に対する指示書を含有する。
本発明の他の第10の態様において、本発明は、経口投与用の複数の固体剤形を含むキットを提供するものであって、各剤形は、220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含み、前記キットは、COPD(慢性閉塞性肺疾患)の処置に向けた、順次、1日2回の各用量の投与に対する指示書を含有する。
本発明の第11の態様において、本発明は、COPD(慢性閉塞性肺疾患)を患うヒト患者に対する単一または複数の固体剤形(複数可)の1日2回の経口投与を含む、COPDを処置するための方法を提供するものであって、前記単一または複数の固体剤形(複数可)は、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む。
本発明の他の第11の態様において、本発明は、COPD(慢性閉塞性肺疾患)を患うヒト患者に対する、単一または複数の固体剤形(複数可)の1日2回の経口投与を含む、COPDを処置するための方法を提供するものであって、前記単一または複数の固体剤形(複数可)は、投与あたり合計220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む。
慢性閉塞性肺疾患(COPD)は、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の一例である。
α1-アンチトリプシンの欠損(AATD)が、COPDとして現れる肺障害の発生に関わる特異的危険因子であることから、呼吸器系疾患とNE、特にCOPDとNEに関しては、明確な病理学的関連がある。α1-アンチトリプシンの主な生理作用はNEを中和することである。NE活性に対抗するものがないことにより、AATDに関連するCOPD、特に肺気腫における肺組織の破壊が促進するとみなされている。肺が特に影響されやすい理由は2つある:(1)日常的に吸入される有害物質、特にタバコの煙は、NEの放出を引き起こす好中球の強力な活性化因子である;(2)エラスターゼの標的であるエラスチンは、肺組織の主要構成要素(他の組織よりも顕著)であり、NEインヒビターの保護がないと、肺の繊細構造を支えるエラスチンは分解され、肺組織は次第に破壊される。
したがって、本発明の全態様において、呼吸器系疾患、特にCOPDは、α1-アンチトリプシン欠損症(AATD)に関連するのが好ましい。同様に、本発明の全態様において、呼吸器系疾患(例えば、COPD)は、NE阻害により処置されるのが好ましい。
本発明は、α1-アンチトリプシン欠損症(AATD)に関連する呼吸器系疾患に限定されるものではない。実際、他の疾患(例えば、脂肪織炎)がα1-アンチトリプシン欠損症(AATD)に関連する可能性がある。したがって、本明細書に記載される本発明の各態様について、疾患がα1-アンチトリプシン欠損症(AATD)に関連する任意の疾患(例えば、脂肪織炎)であり得る、さらなる追加の態様もまた提供される。
COPDなどのα-1アンチトリプシン欠損症により媒介される呼吸器系疾患において、NE活性化を回避し、ひいてはNEに関連する障害を回避するために、阻害処置では、ヒトにおいてCmin(血漿中トラフ濃度)閾値300nM以上が達成及び維持されなければならないと判断されている。このことは図1に示されている。このようなCmin閾値を達成及び維持することは、かかる患者の生存確率の向上、及びより良いクオリティオブライフと相関する。
これにより、従来考えられていた用量よりも実質的に多い6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドの用量が必要とされる。例えば、先行技術では、1日の最大量として200mgが投与されるべきであることが開示されている。
本明細書で使用する場合、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、気管支、アレルギー性、内因性、外因性、運動誘発性、薬物誘発性(アスピリン及びNSAID誘発性を含む)及び粉塵誘発性喘息、間欠性及び持続性の両方、ならびにあらゆる重症度の喘息、ならびに気道過敏性亢進の他の原因を含む喘息;慢性閉塞性肺疾患(COPD);感染性及び好酸球性気管支炎を含む気管支炎;肺気腫;気管支拡張症;嚢胞性線維症;サルコイドーシス;農夫肺及び関連疾患;過敏性肺炎;成人呼吸窮迫症候群(ARDS);原因不明の線維化性胞隔炎、特発性間質性肺炎、抗腫瘍性治療に合併する線維症、及び慢性感染症(結核ならびにアスペルギルス症及び他の真菌感染症を含む)を含む肺線維症;肺移植の合併症;気道の炎症及び分泌状態に関連する慢性の咳、及び医原性の咳の処置を含む鎮咳活性;薬物性鼻炎及び血管運動性鼻炎を含む急性及び慢性鼻炎;神経性鼻炎(枯草熱)を含む、通年性及び季節性アレルギー性鼻炎;鼻茸;感冒、肺高血圧症、ならびに呼吸器合胞体ウイルス、インフルエンザ、コロナウイルス(SARSを含む)、及びアデノウイルスによる感染症を含む急性ウイルス感染症を含む。
好ましい実施形態において、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、慢性閉塞性肺疾患(COPD)である。別の好ましい実施形態において、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、肺気腫である。別の好ましい実施形態において、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、気管支拡張症である。別の好ましい実施形態において、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、喘息である。
本明細書で使用する場合、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、本明細書に記載の呼吸器系疾患(例えば、慢性閉塞性肺疾患(COPD)または肺気腫)を患うα-1アンチトリプシン欠損症患者を含む。
本明細書で使用する場合、α-1アンチトリプシン欠損症によって媒介される疾患は、疾患を患うα-1アンチトリプシン欠損症患者を含む。本明細書で使用する場合、α-1アンチトリプシン欠損症によって媒介される疾患は、脂肪織炎を含む。
α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患を患う患者に、120mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を1日2回投与すると、Cmin閾値が達成及び維持されることが示されている。好ましくは、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患(例えば、COPD)を患うヒト患者には、最低でも120mgが1日2回投与される。したがって、最低でも1日に合計240mg、好ましくは440mg、より好ましくは480mgの用量が投与される。
本発明のさらなる実施形態では、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患(例えば、COPD)を患うヒト患者には、最低でも180mgのアルベレスタットまたはその塩が1日2回投与される。したがって、最低でも1日に合計360mg、好ましくは540mgの用量が投与される。
さらに、α-1アンチトリプシン欠損症によって媒介される呼吸器疾患(例えば、COPD)を患う患者に、240mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を1日2回投与すると、かかるCmin閾値が達成及び維持されることが示されている。好ましくは、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患(例えば、COPD)を患うヒト患者には、最低でも240mgが1日2回投与される。したがって、最低でも1日に合計440mg、好ましくは480mgの用量が投与される。
Cminは、2回目の用量を投与する前に薬物が到達する最小血液血漿中濃度についての、薬物動態学で用いられる用語である。例えばCminは、図2で認められる血漿中トラフ濃度であり得る。Cminは、薬物が到達する最高濃度(例えば、血漿中ピーク濃度)であるCmaxの反対である。
本明細書に開示される本発明の全態様については、アルベレスタットまたはその塩を投与すると、患者における血漿中濃度Cminが少なくとも300nMになる。
本明細書に開示される本発明の全態様については、好ましくは、アルベレスタットまたはその塩を投与すると、患者における血漿中濃度Cmaxが少なくとも1000nMになる。
本明細書に開示される本発明の全態様については、好ましくは、アルベレスタットまたはその塩を投与すると、患者における血漿中濃度Cminが少なくとも300nMになり、血漿中濃度Cmaxが少なくとも1000nMになる。
本明細書に開示される本発明の全態様については、各剤形は単一の固体物であることが好ましい。しかしながら、各投与では、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩が300mg以下、好ましくは、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩が240~480mgであることを条件に、各投与が複数の固体剤形から構成されてもよい。
1日2回の投与とは、一定の間隔、好ましくは少なくとも8時間の間隔、より好ましくは少なくとも10時間の間隔、例えば約12時間の間隔±1時間で投与することを意味する。
本明細書に開示される本発明の全態様については、1日の最大用量が、好ましくは600mgを超えない、より好ましくは500mg以下である。
本明細書に開示される本発明の全態様については、好ましくは、各個別の用量は、120~250mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩、例えば120mg、180mgまたは240mgを含有する。
本明細書に開示される本発明の全態様については、好ましくは、各個別の用量は、160~250mg(例えば、180mg)の6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含有する。
本明細書に開示される本発明の全態様については、好ましくは、各個別の用量は、220~250mg(例えば、240mg)の6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含有する。
6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩は、長期にわたって投与するのが好ましい。したがって、本発明の第5及び第10の態様の好ましい実施形態では、キットは、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の剤形を、毎週、隔週または毎月供給するなど、規定して剤形を供給することを構成する。
本発明の一実施形態では、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドの塩は、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドのトシレート塩である。
6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩は、所望の一定期間または継続期間、例えば、少なくとも1週間、少なくとも約1ヶ月、少なくとも約2ヶ月、少なくとも約3ヶ月、少なくとも約6ヶ月、少なくとも約12ヶ月、少なくとも約24ヶ月、またはそれ以上の期間で、有効な投与計画に従って個人に投与され得る。例えば、当該化合物は、対象の生命が存続する期間、毎日または間欠的なスケジュールで投与され得る。
本発明の全方法において、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の用量は、投与量漸増計画に従って投与され得る。これにより、1日のアルベレスタット用量を、例えば1日2回(BID)120mgまで安全に設定することが可能になる。例えば、1日2回の本発明によるアルベレスタット用量120mgまでの投与量漸増計画は、アルベレスタットまたはその塩を、第1の一定期間、1日2回のアルベレスタット用量60mgで投与し、続いて、それ以降は1日2回120mgで投与することを構成する。第1の期間は5~20日間、好ましくはそれぞれ約1週間(7日間)であり得る。特に、アルベレスタットまたはその塩は、1日2回60mgで1週間投与され、続いて、それ以降は1日2回120mgで投与される。用量は、アルベレスタット遊離塩基の当量として言及される。
また、1日のアルベレスタット用量を、例えば1日2回(BID)240mgまで安全に設定可能にするために、用量漸増計画が用いられることがある。例えば、1日2回の本発明によるアルベレスタット用量240mgまでの投与量漸増計画は、アルベレスタットまたはその塩を、第1の一定期間、1日2回のアルベレスタット用量60mgで投与し、続いて、第2の一定期間、1日2回120mgで投与し、続いて、第3の一定期間、1日2回180mgで投与し、それ以降は1日2回240mgで投与することを構成する。第1、第2及び第3の期間は、それぞれ5~20日間、好ましくはそれぞれ約1週間(7日間)であり得る。特に、アルベレスタットまたはその塩は、1日2回60mgで1週間投与され、続いて、1日2回120mgで1週間投与され、続いて、1日2回180mgで1週間投与され、それ以降は1日2回240mgで投与される。用量は、アルベレスタット遊離塩基の当量として言及される。
本発明の一実施形態では、投与量、用量または固体剤形において言及されるアルベレスタットまたはその塩の量(例えば、mg)は、アルベレスタットまたはその塩におけるアルベレスタット遊離塩基の量に対応する。例えば、本発明の方法でアルベレスタットまたはその塩の240mg用量の投与が必要となる場合、使用されるアルベレスタット塩の量は、240mgのアルベレスタット遊離塩基に相当することになる。
実施例に示すように、記載の投与計画によって達成されたアルベレスタットCmax濃度では、好中球エラスターゼ(NE)活性が72.6%抑制された(図9参照)。対照的に、AAT補充での「増強」を用いるα-1欠損症の処置で治療上達成される濃度のAATでは、NE活性が56.7%しか抑制されなかった(図8参照)。したがって、アルベレスタットは、AAT増強療法よりも強力なNEインヒビターであり得る。したがって、アルベレスタットは、AAT増強療法では十分な応答が示されなかった患者の処置に有用であり得る、と信じられている。このような増強療法は、AATDにより媒介される呼吸器系疾患の進行を遅らせるために、AATを静脈内投与することに関与する。
したがって、本発明は、AAT療法では応答が示されなかった、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患(例えば、COPD)を処置するための方法を必要とする患者におけるその方法であって、本明細書に開示されたアルベレスタットまたはその塩を有効量(例えば120~300mg BID、特に220~300mg BID)で患者に投与することを含む、前記方法を提供する。一実施形態では、アルベレスタットまたはその塩は、AAT増強療法の代わりに、またはAAT増強療法と併用して投与される。非レスポンダーとは、AATではAATDによって媒介される呼吸器系疾患(例えば、COPD)が処置されないかまたはその進行が遅くならない患者であり得る。
したがって、本明細書に開示される本発明の全態様について、処置を必要とする患者は、AATの投与によって、α-1アンチトリプシン欠損症について以前に処置されている可能性があるか、または現在処置されている。化合物(I)またはその塩は、適切な場合には単独で、あるいは本発明の化合物を薬学的に許容される希釈剤、アジュバントまたは担体と組み合わせて含む適切な医薬組成物の形態で使用され得る。有害反応(例えば、アレルギー反応)を引き起こす可能性のある物質を含有しない組成物が特に好ましい。
本明細書で定義される固体剤形(複数可)は、好ましくは錠剤(複数可)形態、またはカプセル剤(複数可)形態、最も好ましくは錠剤形態である。
本発明によれば、薬学的に許容される希釈剤または担体と混合された化合物(I)またはその塩を含む、医薬組成物が提供される。化合物(I)またはその塩は、好ましくは微粉化または粉砕された形態で使用される。化合物(I)またはその塩は、本明細書に記載の組成物(経口組成物を含む)における組成物の全重量に対して、好ましくは50重量%未満、より好ましくは30重量%未満である。
本発明の各方法及び全方法について、本発明は、その方法においてその方法を必要とする患者にアルベレスタットまたはその塩を投与することを含む処置方法に関する、さらなる実施形態を提供する。本発明の各方法及び全方法について、本発明は、その方法において使用するためのアルベレスタットまたはその塩に関する、さらなる実施形態を提供する。本発明の各方法及び全方法について、本発明は、その方法に向けた医薬の製造におけるアルベレスタットまたはその塩に関する、さらなる実施形態を提供する。
本明細書に記載の方法の一実施形態では、アルベレスタットまたはその塩が、それを必要とするヒト患者に投与される。
経口投与のために、化合物(I)またはその塩は、例えば、アジュバント、希釈剤または充填剤、例えば、水和及び無水形態を含むラクトース、サッカロース、ソルビトール、マンニトール、二塩基性リン酸カルシウム(dicalcium phosphate);デンプン、例えば、ジャガイモデンプン、トウモロコシ(maize)デンプンまたはアミロペクチン;セルロース誘導体、例えば、結晶セルロース(MCC)またはケイ酸処理結晶セルロース(SMCC)などと混合されていてもよい。いくつかの実施形態では、これらの混合物が使用され得る。一実施形態では、化合物(I)トシレートは、マンニトールと混合されない。一実施形態では、完全製剤におけるMCCなどの親水性セルロースの量は、50%~98%の範囲にある。これらのアジュバント、希釈剤及び充填剤は合計で、固体製剤の重量100あたり、その60~98、好ましくは70~95の割合で使用される。結晶セルロースなどのセルロース誘導体の例としては、Avicel PHlOl、PH 102、PH 102 SCG、PH200、PH301、PH302、及びPH-F20、Avicel RC-A591NFが挙げられる。ケイ酸処理結晶セルロース製品の例は、MCCとコロイド状二酸化ケイ素の混合物である、ProSolv 90 HD(JRS Pharma製)である。二塩基性リン酸カルシウム二水和物製品の例は、Calipharm D(ThermoPhos)、ICL D(ICL Performance Products)、Calstar(FMC Biopolymer)、Di-Cafos(Chemische Fabrik Budenheim)、DI-TAB(Innophos)及びEmcompress(JRS Pharma LP)である。二塩基性リン酸カルシウム無水物の例は、ICL A(ICL Performance Products)、Fuji Calin(Fuji Chemicals)、A-TAB(Innophos)、Di-Cafos AN(Chemische Fabrik Budenheim)、及びEmcompress Anhydrous(JRS Pharma LP)である。マンニトール製品の例は、Pearlitol DC 300及びPearlitol SD200(Roquette製)である。ラクトース製品の例は、Pharmatose DCL 15(DMV製)である。
所望により結合剤、例えば、ヒドロキシプロピルセルロース(HPC)、ヒドロキシプロピルメチルセルロース(HPMC)、ポリビニルピロリドン(PVP)またはゼラチンを使用してもよく、固体医薬製剤の重量100あたり、その0.5~10、好ましくは1~4の割合で使用される。ヒドロキシプロピルセルロースの例としては、HPC LFが挙げられる。ヒドロキシプロピルメチルセルロースの例としては、PVP K30、及びPVP K90が挙げられる。
崩壊剤としては、例えば、カルメロースカルシウム、カルボキシメチルデンプンナトリウム、クロスカルメロースナトリウム、クロスポビドン(架橋ポリビニルピロリドン)などが挙げられ、固体医薬製剤の重量100あたり、その0.5~15、好ましくは2~10の割合で使用される。Kollidon CL(BASF製)が崩壊剤の例となる。
滑沢剤としては、ステアリン酸マグネシウム、ステアリン酸カルシウム、ショ糖脂肪酸エステル、フマル酸ステアリルナトリウム、ステアリン酸、ポリエチレングリコール、ワックス、パラフィンなどが挙げられる。滑沢剤の量は、0.05%~5%であり、好ましくは0.5%~3.5%であり、ここで、%は製剤の重量に対するものである。
界面活性剤としては、ラウリル硫酸ナトリウム、ポリソルベート80、硬化油、ポリオキシエチレン(160)ポリオキシプロピレン(30)グリコールなどが挙げられる。界面活性剤の量は、2%未満、好適には1.5%未満、例えば1.1%未満であり、ここで、%は製剤の重量に対するものである。
実施例1
全血中のex vivoザイモサン刺激好中球エラスターゼ(NE)活性に対するアルベレスタットの効果を評価した。アルベレスタット反復漸増投与(MAD)試験の健康なボランティアから、ベースライン(アルベレスタット処置前)にて、また、アルベレスタット処置またはプラセボの各種用量に基づいて血液を採取した。クエン酸処理した血液試料をザイモサンとインキュベートし、得られたNE活性を蛍光切断生成物である7-アミノ-4-メチルクマリンの生成に基づく蛍光アッセイで測定した。アルベレスタットまたはプラセボのNE抑制効果は、処置前(ベースライン)のザイモサン刺激NEに関する阻害率として表した。血漿中のアルベレスタット濃度は、タンパク質沈殿法で測定し、続いて、液体クロマトグラフィー及びタンデム質量分析法により、NE活性と同じ時点で測定した。血漿中濃度は、分析のために、<3nM;3-30nM;30-300nM及び>300nMとしてグループ化した。
図1は、アルベレスタットの漸増濃度における、血漿中のザイモサン刺激好中球エラスターゼ(NE)の阻害率を示しており、アルベレスタットの血漿中濃度が300nM以上で、約100%のNE阻害が達成可能であることを指し示している。
実施例2
図2は、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドのトシレート塩を、最大用量240mgでBID(1日2回)またはQD(1日1回)投与したことに関する、集団PKシミュレーション血漿中濃度中央値(濃いライン)を、95%CIを表しながら示している。中央値及び95%CI領域(グレー)は、240mg BIDでの予測PKレベルが、閾値300nM(点線)超を満たすことを示している。また、図2は、120mg BIDでの予測PKレベルが、閾値300nM(点線)を満たすことも示している。
表1は、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドのトシレート塩を、最大用量240mgでBID(1日2回)またはQD(1日1回)投与したことに関する、集団PKシミュレーション血漿中濃度中央値を、QD及びBID投与計画について、中央値、上下四分位範囲(lIQ及びuIQ)、上下95%CI(l95%CI及びu95%CI)を表しながら示している。これら全ては、240mg BIDでの予測PKレベルが、閾値300nM(点線)超を満たすことを示している。中央値は、120mg BIDでの予測PKレベルが、閾値300nM(点線)超を満たすことを示している。
ヒトにおいて、中央値が少なくとも300nMの閾値Cmin(血漿中トラフ濃度)に達し、規制ガイドライン(EU及び米国の規制当局を含む)によるもののような予測Cmin周囲の125%までの分散を許容するためには、最小120mgのBID投与が必要であることが理解できる。
好ましくは、ヒトにおいて、95%CI下限が少なくとも300nMの閾値Cmin(血漿中トラフ濃度)に達し、規制ガイドライン(EU及び米国の規制当局を含む)によるもののような予測Cmin周囲の125%までの分散を許容するためには、最小240mgのBID投与が好ましい。
実施例3:アルベレスタット(好中球エラスターゼインヒビター)によるプロテイナーゼ関連肺障害の保護
概要
アルファ-1アンチトリプシン欠損症(AATD)とは、保護性の抗プロテイナーゼであるα-1アンチトリプシン(AAT)の放出が、減少/消失し得る遺伝病である。この潜在的に破壊的なプロテイナーゼの主要インヒビターが欠損すると、プロテイナーゼ/抗プロテイナーゼの不均衡状態が持続する。プロテイナーゼ、特にエラスターゼの活性が阻害されないと、肺の構造変化が引き起こされ、肺気腫及び気道閉塞につながる。このin vitro不均衡モデルを用いることで、病態生理に関与する好中球セリンプロテイナーゼ(NSP)に対する、エラスターゼインヒビターの効果を、生理学的に評価することができる。
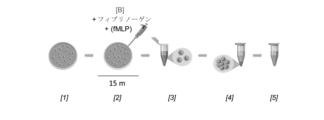
本実施例では、プロセスに関するエラスターゼ特異的マーカーの放出をモニタリングすることでエラスターゼ活性の変化を評価するために、刺激した好中球-フィブリノーゲン緩衝液モデルにアルベレスタットを添加することの効果について説明する。
プロテイナーゼ/抗プロテイナーゼ不均衡モデルを開発し、エラスターゼ活性フットプリントイムノアッセイにより、非阻害NSP活性に対する生理的インヒビターAATの効果を説明することで検証した。次いで、アルベレスタットを当該モデルに添加した。
アルベレスタットの添加により得られた結果から、本化合物は、in vitroでエラスターゼ活性を首尾よくかつ迅速に阻害することができ、生理的インヒビターAATよりも効果的であることが指し示された。
序論
アルファ-1アンチトリプシン欠損症(AATD)は、破壊的な好中球セリンプロテイナーゼの阻害に非常に重要な糖タンパク質アルファ-1アンチトリプシン(AAT)をコードする、SERPINA1遺伝子の変異から起こる遺伝病である[1]。SERPINA1遺伝子の変異により、血液及び組織内へほとんど分泌されない/全く分泌されないAATバリアントが産生され、それによって、潜在的に有害なプロテイナーゼの生理的制御が抑制される。
健康な組織では、破壊的プロテイナーゼは抗プロテイナーゼ(主にAAT)によって調節されているが、AATDでは、AATの欠損により、これらのプロテイナーゼが過剰に活性したままとなり、したがって、重大なプロテイナーゼ/抗プロテイナーゼの不均衡につながる[2][3][4]。
このプロテイナーゼ/抗プロテイナーゼの不均衡は、AATD COPD(慢性閉塞性肺疾患)を有する患者に関連する、病態生理学的な不可逆的気腫性変化の原因であると信じられている[4]。
プロテイナーゼが阻害されないと、エラスチン、コラーゲン及びフィブリノーゲンなどの主要な細胞外マトリックス(ECM)タンパク質が自由に切断され、肺の構造が損傷され、肺気腫につながる[5]。
実際、臨床的には、11μM未満のAAT血清中濃度は、気腫性変化の増進、ひいては臨床的肺疾患をもたらす非生理的相互作用の鍵とみなされ、推定上の「リスク閾値」と称されている[6]。
歴史的に、COPDにおけるプロテイナーゼ障害は、動物実験によって実証されているように、主として好中球エラスターゼ(NE)活性に起因するものとされてきた[7]。
最近、対象の血漿中における特異的フィブリノーゲン切断生成物の検出に基づく、NE用のin vivoプロテイナーゼ活性フットプリントイムノアッセイが開発されたことにより、AATDにおけるプロテイナーゼ/抗プロテイナーゼ不均衡の重大性に関する説が支持されてきている[8]。
NE活性について測定された全てのAAT欠損表現型では、健康な喫煙ボランティアと比較して、これらのフットプリントのエビデンスが増加することが実証され、AAT表現型間で異なるプロファイルが示された[8]。
当該モデルにアルベレスタットを添加することにより、臨床試験で使用される用量範囲を支持する曝露応答を含む、in vitroでの薬効に関するデータが得られ、医薬品の効果、ひいては臨床効果のバイオマーカーとして、このモデルの製品が支持されるであろうと仮定した。
本モデルの主な目的は、アルベレスタットNEインヒビターの適用に関するエラスターゼ活性の変化を説明することである。
材料及び方法:
酵素反応速度論
初期工程では、より生理的な実験に使用されるべき酵素及びインヒビターの生物学的活性の評価を必要とした。
工程1は、Lineweaver-Burk逆数プロット分析[9]を用いたブタ膵臓エラスターゼ活性の評価を伴うものであった。
工程2では、PPE活性を確認した後、精製AATバッチ(Athens Research & Technology,US)の本酵素に対する阻害機能を測定し、それを以降の全実験に使用した。
工程3は、純粋AATを用いて純粋NE調製物(Athens Research and Technology,US)の阻害を評価して、それらの活性機能を導出することを伴うものであった。次いで、当該酵素活性を用いて、アルベレスタットの活性を評価した。
アルベレスタット活性は、濃度及び活性が既知のエラスターゼに対して当該化合物を滴定した際に、N-スクシニル-Ala-Ala-Ala-p-ニトロアニリド(SlaaapN)切断を測定することによって算出した[2]。これらの方法を用いて、アルベレスタットのNEに対する活性が88%となることを結論付けた。結果は、Prismソフトウェアを用いて計算により決定した。
プロテイナーゼ/抗プロテイナーゼ不均衡モデル
健康な若いボランティアからの好中球を、Jepsen及びSkottunによって広範に説明された方法[10]を用いて単離した。
次いで、好中球を、ペニシリン-ストレプトマイシン(1% v/v;Sigma Aldrich)を添加したRoswell Park Memorial Institute培地1640(RPMI;Sigma-Aldrich;L-グルタミン及び重炭酸ナトリウムを含む)において、550nMのフィブリノーゲン(Calbiochem,San Diego,CA,US)、10μMのN-ホルミル-L-メチオニル-L-ロイシル-フェニルアラニン(fMLP;Sigma-Aldrich,St.Louis,MO,US)、ならびに0~11μMの濃度の活性AAT(Athens Research and Technology,Athens,GA,US)及び濃度漸増AZD9668と共に、37°Cにて15分間インキュベートした-図3。
遠心分離により上清を得、NE活性フットプリントを測定した。
特異的プロテイナーゼ活性アッセイ
従来Carter et al.及びNewby et al.によって説明されている逆蛍光免疫測定法(Inverse fluorescence immunoassay methods)[8]を、好中球エラスターゼ及びプロテイナーゼ3活性フットプリントを測定するために利用した。
研究対象
Institute of Inflammation and Ageing,University of Birminghamが開く「Investigations of the ageing immune system」(ERN_12-1184)に基づく倫理的承認を受けて、健康で若い(<35歳)非喫煙者の血液及び血漿を採取した。
結果
1.フィブリノーゲン含有緩衝液中の単離した好中球を用いた新規in vitroモデルの開発
アルベレスタットの評価に適したモデルを生成するため、フィブリノーゲン緩衝液好中球モデルの開発に関与するパラメータを個別に探索し、最適な条件を選定した。
i.休止時の好中球を用いたAα-Val
360
アッセイのバリデーション
最適なフィブリノーゲン濃度を選択するため、0~8797nMの範囲にある、未切断フィブリノーゲン滴定曲線に沿って好中球をインキュベートした。8797nMは、文献に記載されているヒト血中フィブリノーゲン濃度の平均値である。当該曲線は、好中球を有しない陰性対照と並行して測定した(図4参照)。
ii.刺激した好中球を用いたAα-Val
360
アッセイのバリデーション
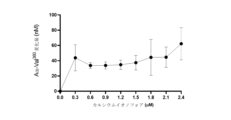
最大刺激を決定するために、好中球の強力な刺激因子であるCaI[11]を0~2.4μMで滴定し、特異的プロテイナーゼフィブリノーゲン切断生成物を測定した。
NE活性フットプリントは、0.3μMのCaIで好中球を刺激した後、43.8nM(+/-17.1)分急激に上昇し、次いで、また定常に達した(図5)。
フローサイトメトリーで好中球の脱顆粒を確認し、また、強い刺激にもかかわらず、好中球の生存率が高いままであることも確認した。フローサイトメトリー評価により、アルベレスタットを溶解するために使用したDMSOが、好中球に脱顆粒するように刺激しなかったことを確認した。
次いで、より生理的な刺激を評価するために、好中球をN-ホルミルメチオニン-ロイシル-フェニルアラニン(fMLP)と共にインキュベートした。
プロテイナーゼ活性の急激な増加が、0~1μMの刺激により観察された。
0.1μMにおいて、NE活性は11.4nM増加し、1μMにおいて、活性はさらに7.3nM増加した。活性は、10μMのfMLPにおける35.0まで増加し続けたが、増加率はより小さくなった(図6)。
フローサイトメトリー評価により、fMLPが細胞生存率に影響を与えずに脱顆粒を刺激し、DMSOが好中球に脱顆粒するように刺激しなかったことを再確認した。
2.酵素活性
i.ブタ膵臓エラスターゼ活性
インヒビターを適用する前に、1時間かけて基質の光学密度を測定することでPPE活性を測定し、次いで、反応速度及び基質切断率を算出した。Michaelis-Mentenプロットは放物線を示しており、そのため、反応は通常のMichaelis-Menten式で記述でき、協同性またはアロステリック性はない[12]。6種の濃度の基質SlaaapN(N-スクシニル-Ala-Ala-Ala-p-ニトロアニリド-CAS番号:52299-14-6)と共にインキュベートしたPPEの、15分間(450秒)にわたる吸光度(410nm)の変化。また、Lineweaver-Burkプロットも作成した。計算で得られた軸のクロスポイントを用いて、最大速度(Vmax)及びMichaelis定数(Km)の値を算出することができた。N-スクシニル-Ala-Ala-Ala-p-ニトロアニリドは、キモトリプシン様セリンプロテアーゼ、膵臓エラスターゼ及びセリンエンドペプチダーゼの発色基質であり得る。基質としてSlaaapNを使用してエラスターゼ生成物を測定する手順は公知である。
これらの値及び触媒効率に関する公知の公表値[13]を用いて、PPEの機能的活性を測定することができ、この値をその後の実験に使用した。PPE活性は81.5%であると結論付けた。
ii.アルファ-1アンチトリプシン活性
AAT活性は、既知の活性モル濃度のPPEをAATとインキュベートした後、既知のPPE活性によるSlaaapNの切断を測定することにより、速度論的に評価した。
経時的にSlaaapN切断量は増加した。AAT:[活性PPE]のモル比が増加するにつれて、インヒビターの濃度がより高くなった場合、切断率はより低くなった。AATが存在しないとPPE活性は100%であり、PPE活性を中和するには、1モルのPPEに対して1.208モルのAATというモル濃度が必要であった。
このことは、1モルの活性PPEを阻害するためには、1.208モルのAATが必要であったことを意味した。AATが完全に活性化している場合、PPEは1:1で阻害されるはずである。したがって、機能的AAT活性は結果として83%であると計算できる。
iii.好中球エラスターゼ活性
次いで、既知の活性モル濃度のAATで阻害した際のNEによるSlaaapN切断を測定することにより、NE活性を速度論的に評価した。経時的にSlaaapN切断量は増加した。[活性AAT]:NEのモル比が増加するにつれて、インヒビターの濃度がより高くなった場合、切断率はより低くなった。
このことは、純粋な活性AATが0.99:1のモル比でNEを阻害し、NEの完全な活性化が確認されたことを意味するものであった。
iv.アルベレスタット活性
アルベレスタット活性は、阻害曲線に沿ったインヒビターの存在下、既知のエラスターゼ活性による基質切断を測定することにより、速度論的に評価した。経時的にSlaaapN切断量は減少した。
速度論的解析により、アルベレスタットは、非常に強力であり、かつ急速な可逆的NEインヒビターであることが実証された[14]。NEを完全に阻害するために必要な化合物のモル比は、以下に概説するように、0.87:1である。
このことから本発明者らは、外挿により、1モルのNEを阻害するためには0.87モルのアルベレスタットが必要である、と結論付けることができる。したがって、実験誤差の範囲内にある活性は十分であると判断できる。
説明:アルベレスタット存在下において算出したSlaaapNに対するNE酵素活性に対して、アルベレスタット:NE比を比較することにより得られた軸切片及び傾きの最良適合値。
3.AAT用量を増加した状況でのセリンプロテイナーゼペプチドの生成
プロテイナーゼ/抗プロテイナーゼモデルに、AATを、機能的濃度を増加させながら、基質(フィブリノーゲン)及び刺激物(fMLP)と共に添加した。病態生理学的濃度は、American Thoracic and European Respiratory Societiesによって記述されている(0μMはPi「欠損」遺伝子型、2.6~6.5μMはPiZZ遺伝子型、及び10.4~14.3μMはPiSZ遺伝子型を表す[15])、各種疾患遺伝子型AAT濃度を模倣するように選択した。
AAT濃度が増加するにつれて、NEのプロテイナーゼ活性シグナルが減少し、11μM付近で定常に達した(図8)。特異的プロテイナーゼフィブリノーゲン切断生成物による活性の変化を調べることで(ベースラインは0μMにおいて100%活性として設定)、このことがNEに関して56.7%の減少率を表したことを見出した(図8)。
4.アルベレスタット用量を増加した状況でのセリンプロテイナーゼペプチドの生成
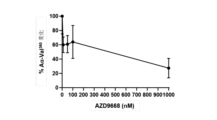
アルベレスタットは、従来の文献で報告されている薬理学的活性濃度を用いて、用量反応曲線に沿ってモデルに添加した。酵素活性を考慮して再評価した際、1000nM、100nM、50nM、10nM及び0nMでの活性アルベレスタット濃度が、プロテイナーゼ/抗プロテイナーゼ不均衡モデル内のNE活性に及ぼす効果を評価した(n=3)。
データによると、10nMの当該化合物をモデルに添加した場合、特異的好中球エラスターゼフィブリノーゲン切断生成物で定義される活性変化(ベースラインは0μMにおいて100%活性として設定)は、NEに関して60.1%まで減少したことが示された(図9)。より高濃度の1000nMで処理した場合、NE活性は未処理値の27.4%までさらに低下した。
考察
文献には、アルベレスタットがin vitroでエラスターゼの強力なインヒビターであるとして記載されている[14][16]。このことは、プロテイナーゼ/抗プロテイナーゼバイオマーカーモデルを用いた本報告のデータからも支持される。この抗エラスターゼ濃度が増加するにつれて、特異的エラスターゼ切断フィブリノーゲン生成物の量が急速に減少することが観察された。
しかし、エラスターゼ活性の阻害は、AATで観察されたよりも低いモル濃度で生じた。このことは、当該化合物が、より大きなAAT分子が近づけないエラスターゼを阻害できたことを意味するはずであり、おそらく細胞膜結合または細胞内阻害成分であることを指し示している。
アルベレスタットの分子間相互作用を説明する公表されたエビデンスは限られている。したがって、本発明者らは、当該化合物が、基質結合前の細胞プロテイナーゼの効果的なインヒビターにもなり得ることを提案する。
概要説明
本報告は、アルファ-1アンチトリプシン欠損症及びその処置に関連する、より生理的なプロテイナーゼ/抗プロテイナーゼ不均衡モデル内における、アルベレスタットのプロテイナーゼ活性に対する効果を実証するものである。
本実施例で収集したプロテイナーゼ/抗プロテイナーゼモデルデータは、エラスターゼ活性の強力なインヒビターとしてのアルベレスタットの役割を支持するものである。さらに、データは、アルベレスタットがAATD関連疾患に付随する機能障害を「正常化」することができ、生理的AATタンパク質よりもエラスターゼの抑制に効果的であることを支持するものである。また、データは、当該インヒビターの作用機序が予想を超えるものであることを示唆するものでもあり、NEに対する活性が、AATなどの生理的インヒビターとは異なるメカニズムを介したものであることを示唆している。アルベレスタットは、本出願において説明される投与計画によって達成される濃度において、AATDの増強療法によって達成されるタンパク質濃度でのAATよりも、NEをより強力に阻害することができる。このことは、増強療法が機能しなかった患者において、増強療法の代替とするか、または増強療法と組み合わせて、アルベレスタットをAATDの処置として使用することを支持するものである。
さらなる要点:
1.アルベレスタットまたはその塩は、120~300mg、あるいは220~300mgのBID投与で、好中球エラスターゼ(NE)を阻害する活性を示す。このことは、約300nMのアルベレスタット血漿中濃度で約100%のNE阻害が認められた図1から理解することができる。シミュレーションPKモデリング(図2)は、対象の血漿中アルベレスタット(またはその塩)濃度が約300nMを達成するには、120~300mgのBID投与が必要であることを示唆するものである。アルベレスタット(またはその塩)の血漿中濃度が約300nMを達成することをより確実にするためには、220~300mgのBID投与が必要である。最後に、実施例3は、アルベレスタットまたはその塩は、120~300mg、あるいは220~300mgのBID投与で、好中球エラスターゼ(NE)を阻害する活性(例えば、A-α-Val360によって測定される(図9))を示すことを明らかにするものである。図9は、A-α-Val360の変化率の測定を介して、濃度300nMのアルベレスタットによりNE阻害が達成されることを示すものである。また、実施例3は、A-α-Val360が好中球エラスターゼの特異的生成物であることを示すものでもある。A-α-Val360は、AATD患者において上昇することが示されている。A-α-Val360の濃度がより高くなることは、疾患(例えばAATD)の重症度の上昇と関連している。したがって、患者におけるA-α-Val360レベルの上昇は、アルベレスタットによる処置に対する潜在的なレスポンダーとして患者を特定し得る。
2.アルベレスタットのNE阻害効果を天然タンパク質であるAATのNE阻害効果と比較した。AATによるNE阻害では、56.7%の阻害(すなわち、ベースラインより43.3%上-図8)で定常に達したのに対し、アルベレスタットによる阻害では、1000nMのアルベレスタットでより大きな72.6%の阻害(すなわち、ベースラインより27.4%上-図9)を示した。ここで本発明者らは、シミュレーションPK Cmax濃度を介して、約1000nMのアルベレスタット濃度が、本発明の提案用量/投与計画(例えば、120~300mg、及び220~300mg、BID投与)での投与後に達成されるであろうことを示す(表3)。表3は、アルベレスタットトシレート塩を、アルベレスタット用量120mg及び240mgでBID(1日2回)投与したことに関する、選択した集団PKシミュレーション血漿中濃度Cmaxを、BID投与計画について、中央値、上下四分位範囲(lIQ及びuIQ)、上下95%CI(l95%CI及びu95%CI)を表しながら示している。見て分かるように、表3の値は1000nM以上であり、したがって、本発明の投与計画は、AAT補充での「増強」を用いるアルファ-1欠損症の処置で治療上達成される濃度のAATと比較して、治療目的のNE抑制が改善されるためのアルベレスタット濃度を提供する。
3.驚くべきことに、アルベレスタットは、天然インヒビター(AAT)と比較してより高い効力を示した。この効果は、(立体障害のためにAATが十分に阻害しない)細胞表面エラスターゼを阻害するアルベレスタットの能力に起因している可能性がある。AATは細胞に侵入できず、そのため細胞内で阻害することができないので、当該効果はまた、好中球の活性化により放出されるエラスターゼを含有するエクソソーム(AATに対しては抵抗性である)を阻害するアルベレスタットの能力に起因している可能性もある。
参考文献:
1.Zorzetto,M.,et al.,SERPINA1 Gene Variants in Individuals from the General Population with Reduced α1-Antitrypsin Concentrations.Clinical Chemistry,2008.54(8):p.1331.
2.Sinden,N.J.and R.A.Stockley,Proteinase 3 Activity in Sputum from Subjects with Alpha-1 Anti-trypsin Deficiency and COPD.European Respiratory Journal,2013.41:p.1042-1050.
3.Sinden,N.J.,et al.,Alpha-1-Antitrypsin Variants and the Proteinase/Anti-Proteinase Imbalance in Chronic Obstructive Pulmonary Disease.American Journal of Physiology,Lung Cellular and Molecular Physiology,2015.308:p.12.
4.Stockley,R.A.,Neutrophils and Protease/Antiprotease Imbalance.American Journal of Respiratory and Critical Care Medicine,1999.160:p.S49-S52.
5.Rao,N.V.,et al.,Characterisation of Proteinase 3 (PR-3),a Neutrophil Serine Proteinase:Structural and Functional Properties.The Journal of Biological Chemistry,1991.266(15):p.9540-9548.
6.Wewers,M.D.,et al.,Replacement therapy for alpha 1-antitrypsin deficiency associated with emphysema.N Engl J Med,1987.316(17):p.1055-62.
7.Lucey,E.C.,et al.,Effect of Combined Human Neutrophil Cathepsin G and Elastase on Induction of Secretory Cell Metaplasia and Emphysema in Hamsters,with in vitro Observations on Elastolysis by these Enzymes.American Review of Respiratory Disease,1985.132(2):p.362-366.
8.Carter,R.I.,et al.,The Fibrinogen Cleavage Product Aa-Val360,a Specific Marker of Neutrophil Elastase Activity in Vivo.Thorax,2015.66:p.7.
9.Lineweaver,H.and D.Burk,The Determination of Enzyme Dissociation Constants,in The Fertilizer Investigations Unit,Bureau of Chemistry and Soils,United States,Department of Agriculture.1934.p.658-66.
10.Jepsen,L.V.and T.Skottun,A Rapid One-step Method for the Isolation of Human Granulocytes from Whole Blood.Scandinavian Journal of Clinical and Laboratory Investigation,1982.42(3):p.235-238.
11.Lefrancais,E.,et al.,IL-33 is Processed Into Mature Biosactive Forms by Neutrophil Elastase and Cathepsin G.Proceedings of the National Academy of Sciences of the United States of America,2012.109(5):p.6.
12.Michaelis,L.and M.L.Menten,Die Kinetik der Invertinwirkung.Biochemische Zeitschrift,1913.26:p.333-69.
13.Nakajima,K.,et al.,Mapping the Extended Substrate Binding Site of Cathepsin G and Human Leukocyte Elastase.Studies with Peptide Substrates Related to the Alpha 1-protease Inhibitor Reactive Site.J Biol Chem,1979.254(10):p.4027-32.
14.Stevens,T.,et al.,AZD9668:Pharmacological Characterization of a Novel Oral Inhibitor of Neutrophil Elastase.Journal of Pharmacology and Experimental Therapeutics,2011.339(1):p.313.
15.American Thoracic Society/European Respiratory Society,American Thoracic Society/European Respiratory Society Statement.American Journal of Respiratory and Critical Care Medicine,2003.168(7):p.818-900.
16.Gunawardena,K.A.,H.Gullstrand,and J.Perrett,Pharmacokinetics and safety of AZD9668,an oral neutrophil elastase inhibitor,in healthy volunteers and patients with COPD.Int J Clin Pharmacol Ther,2013.51(4):p.288-304.
1.Zorzetto,M.,et al.,SERPINA1 Gene Variants in Individuals from the General Population with Reduced α1-Antitrypsin Concentrations.Clinical Chemistry,2008.54(8):p.1331.
2.Sinden,N.J.and R.A.Stockley,Proteinase 3 Activity in Sputum from Subjects with Alpha-1 Anti-trypsin Deficiency and COPD.European Respiratory Journal,2013.41:p.1042-1050.
3.Sinden,N.J.,et al.,Alpha-1-Antitrypsin Variants and the Proteinase/Anti-Proteinase Imbalance in Chronic Obstructive Pulmonary Disease.American Journal of Physiology,Lung Cellular and Molecular Physiology,2015.308:p.12.
4.Stockley,R.A.,Neutrophils and Protease/Antiprotease Imbalance.American Journal of Respiratory and Critical Care Medicine,1999.160:p.S49-S52.
5.Rao,N.V.,et al.,Characterisation of Proteinase 3 (PR-3),a Neutrophil Serine Proteinase:Structural and Functional Properties.The Journal of Biological Chemistry,1991.266(15):p.9540-9548.
6.Wewers,M.D.,et al.,Replacement therapy for alpha 1-antitrypsin deficiency associated with emphysema.N Engl J Med,1987.316(17):p.1055-62.
7.Lucey,E.C.,et al.,Effect of Combined Human Neutrophil Cathepsin G and Elastase on Induction of Secretory Cell Metaplasia and Emphysema in Hamsters,with in vitro Observations on Elastolysis by these Enzymes.American Review of Respiratory Disease,1985.132(2):p.362-366.
8.Carter,R.I.,et al.,The Fibrinogen Cleavage Product Aa-Val360,a Specific Marker of Neutrophil Elastase Activity in Vivo.Thorax,2015.66:p.7.
9.Lineweaver,H.and D.Burk,The Determination of Enzyme Dissociation Constants,in The Fertilizer Investigations Unit,Bureau of Chemistry and Soils,United States,Department of Agriculture.1934.p.658-66.
10.Jepsen,L.V.and T.Skottun,A Rapid One-step Method for the Isolation of Human Granulocytes from Whole Blood.Scandinavian Journal of Clinical and Laboratory Investigation,1982.42(3):p.235-238.
11.Lefrancais,E.,et al.,IL-33 is Processed Into Mature Biosactive Forms by Neutrophil Elastase and Cathepsin G.Proceedings of the National Academy of Sciences of the United States of America,2012.109(5):p.6.
12.Michaelis,L.and M.L.Menten,Die Kinetik der Invertinwirkung.Biochemische Zeitschrift,1913.26:p.333-69.
13.Nakajima,K.,et al.,Mapping the Extended Substrate Binding Site of Cathepsin G and Human Leukocyte Elastase.Studies with Peptide Substrates Related to the Alpha 1-protease Inhibitor Reactive Site.J Biol Chem,1979.254(10):p.4027-32.
14.Stevens,T.,et al.,AZD9668:Pharmacological Characterization of a Novel Oral Inhibitor of Neutrophil Elastase.Journal of Pharmacology and Experimental Therapeutics,2011.339(1):p.313.
15.American Thoracic Society/European Respiratory Society,American Thoracic Society/European Respiratory Society Statement.American Journal of Respiratory and Critical Care Medicine,2003.168(7):p.818-900.
16.Gunawardena,K.A.,H.Gullstrand,and J.Perrett,Pharmacokinetics and safety of AZD9668,an oral neutrophil elastase inhibitor,in healthy volunteers and patients with COPD.Int J Clin Pharmacol Ther,2013.51(4):p.288-304.
また、本発明は、以下の番号付けされた実施形態も提供する。
1.120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミド及びその塩を含む、固体剤形。
1.120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミド及びその塩を含む、固体剤形。
2.α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形(複数可)であって、前記単一または複数の固体剤形(複数可)は、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む、前記単一または複数の固体剤形(複数可)。
3.α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形(複数可)であって、前記単一または複数の固体剤形(複数可)は、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含み、各用量の投与は、1日2回、少なくとも8時間の投与間隔で行われる、前記単一または複数の固体剤形(複数可)。
4.6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形を含むキットであって、前記キットは、投与あたり合計120~300mgの前記6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を順次投与するための指示書を含有し、各用量の投与は、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けて、1日2回、少なくとも8時間の投与間隔で行われる、前記キット。
5.経口投与用の複数の固体剤形を含むキットであって、前記剤形は、120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含み、前記キットは、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、順次、1日2回の各用量の投与に対する指示書を含有する、前記キット。
6.COPDを患うヒト患者に対する、単一または複数の固体剤形(複数可)の1日2回の経口投与を含む、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患を処置するための方法であって、前記単一または複数の固体剤形(複数可)は、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む、前記方法。
7.有効成分が、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドのトシレート塩を含むかまたはそれからなる、先行実施形態のいずれか1項に記載の剤形、キットまたは方法。
8.6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドが、120~300mg、好ましくは240~280mg、最も好ましくは240mgの量で、剤形(複数可)中に存在する、先行実施形態のいずれか1項に記載の剤形、キットまたは方法。
9.錠剤(複数可)形態、またはカプセル剤(複数可)形態、好ましくは錠剤形態である、先行実施形態のいずれか1項で定義される固体剤形。
10.最小1日総用量が240mg、好ましくは480mgである、先行実施形態のいずれか1項に記載の剤形、キットまたは方法。
11.α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、喘息、慢性閉塞性肺疾患(COPD)、気管支炎、肺気腫、気管支拡張症、嚢胞性線維症、サルコイドーシス、農夫肺、過敏性肺炎、成人呼吸窮迫症候群(ARDS)、肺線維症、結核、アスペルギルス症、鎮咳活性、医原性の咳、急性及び慢性鼻炎、急性ウイルス感染症、肺高血圧症、ならびに呼吸器合胞体ウイルス、インフルエンザ、コロナウイルス及びアデノウイルスによる感染症からなる群より選択される、先行実施形態のいずれか1項に記載の剤形、キットまたは方法。
12.α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、COPD(慢性閉塞性肺疾患)である、先行実施形態のいずれか1項に記載の剤形、キットまたは方法。
また、本発明は、以下の他の実施形態も提供する。
1.220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミド及びその塩を含む、固体剤形。
1.220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミド及びその塩を含む、固体剤形。
2.α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形(複数可)であって、前記単一または複数の固体剤形(複数可)は、投与あたり合計220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む、前記単一または複数の固体剤形(複数可)。
3.α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形(複数可)であって、前記単一または複数の固体剤形(複数可)は、投与あたり合計220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含み、各用量の投与は、1日2回、少なくとも8時間の投与間隔で行われる、前記単一または複数の固体剤形(複数可)。
4.6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の複数の固体剤形を含むキットであって、前記キットは、投与あたり合計220~300mgの前記6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を順次投与するための指示書を含有し、各用量の投与は、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けて、1日2回、少なくとも8時間の投与間隔で行われる、前記キット。
5.経口投与用の複数の固体剤形を含むキットであって、前記剤形は、220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含み、前記キットは、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、順次、1日2回の各用量の投与に対する指示書を含有する、前記キット。
6.COPDを患うヒト患者に対する、単一または複数の固体剤形(複数可)の1日2回の経口投与を含む、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患を処置するための方法であって、前記単一または複数の固体剤形(複数可)は、投与あたり合計220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む、前記方法。
7.有効成分が、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドのトシレート塩を含むかまたはそれからなる、先行実施形態のいずれか1項に記載の剤形、キットまたは方法。
8.6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドが、240~300mg、好ましくは240~280mg、最も好ましくは240mgの量で、剤形(複数可)中に存在する、先行実施形態のいずれか1項に記載の剤形、キットまたは方法。
9.錠剤(複数可)形態、またはカプセル剤(複数可)形態、好ましくは錠剤形態である、先行実施形態のいずれか1項で定義される固体剤形。
10.最小1日総用量が440mg、好ましくは480mgである、先行実施形態のいずれか1項に記載の剤形、キットまたは方法。
11.α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、喘息、慢性閉塞性肺疾患(COPD)、気管支炎、肺気腫、気管支拡張症、嚢胞性線維症、サルコイドーシス、農夫肺、過敏性肺炎、成人呼吸窮迫症候群(ARDS)、肺線維症、結核、アスペルギルス症、鎮咳活性、医原性の咳、急性及び慢性鼻炎、急性ウイルス感染症、肺高血圧症、ならびに呼吸器合胞体ウイルス、インフルエンザ、コロナウイルス及びアデノウイルスによる感染症からなる群より選択される、先行実施形態のいずれか1項に記載の剤形、キットまたは方法。
12.α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、COPD(慢性閉塞性肺疾患)である、先行実施形態のいずれか1項に記載の剤形、キットまたは方法。
Claims (29)
- 単一または複数の固体剤形(複数可)の1日2回の経口投与を含む、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患を処置するための方法であって、前記単一または複数の固体剤形(複数可)は、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む、前記方法。
- 120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む、固体剤形。
- α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形(複数可)であって、前記単一または複数の固体剤形(複数可)は、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む、前記単一または複数の固体剤形(複数可)。
- α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の単一または複数の固体剤形(複数可)であって、前記単一または複数の固体剤形(複数可)は、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含み、各用量の前記投与は、1日2回、少なくとも8時間の投与間隔で行われる、前記単一または複数の固体剤形(複数可)。
- 6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩の経口投与用の複数の固体剤形を含むキットであって、前記キットは、投与あたり合計120~300mgの前記6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を順次投与するための指示書を含有し、各用量の前記投与は、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けて、1日2回、少なくとも8時間の投与間隔で行われる、前記キット。
- 経口投与用の複数の固体剤形を含むキットであって、前記剤形は、120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含み、前記キットは、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患の処置に向けた、順次、1日2回の各用量の投与に対する指示書を含有する、前記キット。
- COPDを患うヒト患者に対する、単一または複数の固体剤形(複数可)の1日2回の経口投与を含む、α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患を処置するための方法であって、前記単一または複数の固体剤形(複数可)は、投与あたり合計120~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む、前記方法。
- 有効成分が、6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドのトシレート塩を含むかまたはそれからなる、請求項1~7のいずれか1項に記載の剤形、キットまたは方法。
- 前記6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドが、120~300mg、好ましくは240~280mg、最も好ましくは240mgの量で、前記剤形(複数可)中に存在する、請求項1~8のいずれか1項に記載の剤形、キットまたは方法。
- 錠剤(複数可)形態、またはカプセル剤(複数可)形態、好ましくは錠剤形態である、請求項2~4のいずれか1項で定義される固体剤形。
- 最小1日総用量が240mg、好ましくは480mgである、請求項1~10のいずれか1項に記載の剤形、キットまたは方法。
- 前記α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、喘息、慢性閉塞性肺疾患(COPD)、気管支炎、肺気腫、気管支拡張症、嚢胞性線維症、サルコイドーシス、農夫肺、過敏性肺炎、成人呼吸窮迫症候群(ARDS)、肺線維症、結核、アスペルギルス症、鎮咳活性、医原性の咳、急性及び慢性鼻炎、急性ウイルス感染症、肺高血圧症、ならびに呼吸器合胞体ウイルス、インフルエンザ、コロナウイルス及びアデノウイルスによる感染症からなる群より選択される、請求項1~11のいずれか1項に記載の剤形、キット、または方法。
- 前記α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、COPD(慢性閉塞性肺疾患)である、請求項1~12のいずれか1項に記載の剤形、キットまたは方法。
- 前記α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、肺気腫である、請求項1~13のいずれか1項に記載の剤形、キットまたは方法。
- 前記α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、気管支拡張症である、請求項1~14のいずれか1項に記載の剤形、キットまたは方法。
- 前記α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患は、喘息である、請求項1~15のいずれか1項に記載の剤形、キットまたは方法。
- 前記単一または複数の固体剤形(複数可)は、合計220~300mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩を含む、請求項1~16のいずれか1項に記載の剤形、キットまたは方法。
- 最小1日総用量が440mg、好ましくは480mgである、請求項1~17のいずれか1項に記載の剤形、キットまたは方法。
- 最小1日総用量が360mg、好ましくは480mgである、請求項1~18のいずれか1項に記載の剤形、キットまたは方法。
- 請求項1~19のいずれか1項で言及されるようなα-1アンチトリプシン欠損症によって媒介される呼吸器系疾患を処置するための方法を必要とする患者におけるその方法であって、120mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩をBIDで前記患者に投与することを含む、前記方法。
- 請求項1~20のいずれか1項で言及されるようなα-1アンチトリプシン欠損症によって媒介される呼吸器系疾患を処置するための方法を必要とする患者におけるその方法であって、240mgの6-メチル-5-(1-メチル-1H-ピラゾール-5-イル)-N-{[5-(メチルスルホニル)ピリジン-2-イル]メチル}-2-オキソ-1-[3-(トリフルオロメチル)フェニル]-1,2-ジヒドロピリジン-3-カルボキサミドまたはその塩をBIDで前記患者に投与することを含む、前記方法。
- α-1アンチトリプシン欠損症によって媒介される呼吸器系疾患(例えば、COPD)を処置するための方法を必要とする、従来のAAT療法では応答が示されなかった患者におけるその方法であって、アルベレスタットまたはその塩を有効量で前記患者に投与することを含む、前記方法。
- α-1アンチトリプシン欠損症によって媒介される疾患(例えば、COPDまたは脂肪織炎)を処置するための方法を必要とする患者におけるその方法であって、アルベレスタットまたはその塩を以下:
-アルベレスタットまたはその塩を、第1の一定期間、用量60mgで1日2回投与すること、
-アルベレスタットまたはその塩を、それ以降、用量120mgで1日2回投与すること、
ここで、前記第1の期間は5~20日間、好ましくは約1週間(7日間)である、
を含む投与量漸増計画で投与することを含む、前記方法。 - α-1アンチトリプシン欠損症によって媒介される疾患(例えば、COPDまたは脂肪織炎)を処置するための方法を必要とする患者におけるその方法であって、アルベレスタットまたはその塩を以下:
-アルベレスタットまたはその塩を、第1の一定期間、用量60mgで1日2回投与すること、
-アルベレスタットまたはその塩を、第2の一定期間、用量120mgで1日2回投与すること、
-アルベレスタットまたはその塩を、第3の一定期間、用量180mgで1日2回投与すること、及び
-アルベレスタットまたはその塩を、それ以降、用量240mgで1日2回投与すること、
ここで、前記第1、第2及び第3の期間は5~20日間、好ましくは約1週間(7日間)である、
を含む投与量漸増計画で投与することを含む、前記方法。 - 前記アルベレスタットまたはその塩の投与により、前記患者における血漿中濃度Cminが少なくとも300nMになる、請求項1~24のいずれか1項に記載の剤形、キットまたは方法。
- 前記アルベレスタットまたはその塩の投与により、前記患者における血漿中濃度Cmaxが少なくとも1000nMになる、請求項1~25のいずれか1項に記載の剤形、キットまたは方法。
- 前記アルベレスタットまたはその塩の投与により、前記患者において、血漿中濃度Cminが少なくとも300nMになり、かつ、血漿中濃度Cmaxが少なくとも1000nMになる、請求項1~26のいずれか1項に記載の剤形、キットまたは方法。
- 投与あたり120mgのアルベレスタットまたはその塩が投与される、請求項1~27のいずれか1項に記載の剤形、キットまたは方法。
- 投与あたり240mgのアルベレスタットまたはその塩が投与される、請求項1~28のいずれか1項に記載の剤形、キットまたは方法。
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB2005520.8A GB202005520D0 (en) | 2020-04-16 | 2020-04-16 | Elastase inhibition |
| GB2005519.0 | 2020-04-16 | ||
| GBGB2005519.0A GB202005519D0 (en) | 2020-04-16 | 2020-04-16 | Elastase inhibition |
| GB2005520.8 | 2020-04-16 | ||
| US202062706195P | 2020-08-04 | 2020-08-04 | |
| US62/706,195 | 2020-08-04 | ||
| PCT/GB2021/050653 WO2021209739A1 (en) | 2020-04-16 | 2021-03-16 | Methods involving neutrophil elastase inhibitor alvelestat for treating respiratory disease mediated by alpha-1 antitrypsin deficiency |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2023522010A true JP2023522010A (ja) | 2023-05-26 |
| JPWO2021209739A5 JPWO2021209739A5 (ja) | 2024-03-19 |
Family
ID=78083570
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022562608A Pending JP2023522010A (ja) | 2020-04-16 | 2021-03-16 | α1-アンチトリプシンの欠損により媒介される呼吸器系疾患の処置のための好中球エラスターゼ阻害剤アルベレスタットに関連する方法 |
Country Status (16)
| Country | Link |
|---|---|
| US (2) | US20230190723A1 (ja) |
| EP (2) | EP4106757B1 (ja) |
| JP (1) | JP2023522010A (ja) |
| AU (1) | AU2021256835A1 (ja) |
| DK (1) | DK4106757T3 (ja) |
| ES (1) | ES2962498T3 (ja) |
| FI (1) | FI4106757T3 (ja) |
| HR (1) | HRP20231065T1 (ja) |
| HU (1) | HUE064089T2 (ja) |
| IL (1) | IL297211A (ja) |
| LT (1) | LT4106757T (ja) |
| MX (1) | MX2022012942A (ja) |
| PL (1) | PL4106757T3 (ja) |
| PT (1) | PT4106757T (ja) |
| SI (1) | SI4106757T1 (ja) |
| WO (2) | WO2021209740A1 (ja) |
Family Cites Families (85)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5674708A (en) | 1989-06-23 | 1997-10-07 | Trustees Of The University Of Pennsylvania | α-1-antichymotrypsin analogues having elastase inhibitory activity |
| CA2105304C (en) | 1991-03-01 | 2005-10-04 | Arthur C. Ley | Inhibitors of human neutrophil elastase and human cathepsin g |
| WO1992020357A1 (en) | 1991-05-23 | 1992-11-26 | Merrell Dow Pharmaceuticals Inc. | Inhibitors of cathepsin g and elastase for preventing connective tissue degradation |
| US5216022A (en) | 1991-12-19 | 1993-06-01 | Cortech, Inc. | Aromatic esters of phenylenedialkanoates as inhibitors of human neutrophil elastase |
| CA2133658A1 (en) | 1992-04-16 | 1993-10-28 | Peter R. Bernstein | Heterocyclic derivatives |
| WO1993021214A1 (en) | 1992-04-16 | 1993-10-28 | Zeneca Limited | Alpha-aminoboronic acid peptides and their use as elastase inhibitors |
| US5441960A (en) | 1992-04-16 | 1995-08-15 | Zeneca Limited | 1-pyrimidinylacetamide human leukocyte elastate inhibitors |
| US5486529A (en) | 1992-04-16 | 1996-01-23 | Zeneca Limited | Certain pyridyl ketones for treating diseases involving leukocyte elastase |
| GB9307555D0 (en) | 1992-04-16 | 1993-06-02 | Zeneca Ltd | Heterocyclic compounds |
| GB9211783D0 (en) | 1992-06-04 | 1992-07-15 | Ici Plc | Amide derivatives |
| GB9214053D0 (en) | 1992-07-02 | 1992-08-12 | Ici Plc | Heterocyclic amides |
| GB9402680D0 (en) | 1994-02-11 | 1994-04-06 | Zeneca Ltd | Pyrrolidine derivatives |
| EP0763055B1 (en) | 1994-06-02 | 1999-11-03 | Merrell Pharmaceuticals Inc. | Perfluoroalkyl ketone inhibitors of elastase and processes for making the same |
| ATE246708T1 (de) | 1994-06-02 | 2003-08-15 | Aventis Pharma Inc | Elatase-inhibitoren |
| US5618792A (en) | 1994-11-21 | 1997-04-08 | Cortech, Inc. | Substituted heterocyclic compounds useful as inhibitors of (serine proteases) human neutrophil elastase |
| GB9502152D0 (en) | 1995-02-03 | 1995-03-29 | Zeneca Ltd | Proline derivatives |
| AR006401A1 (es) | 1996-03-28 | 1999-08-25 | Glaxo Group Ltd | Compuestos de pirrolopirrolona, una composicion farmaceutica que los contiene, su uso en la fabricacion de un medicamento y en terapia, procesospara su preparación y compuestos intermediarios para dichos procesos. |
| ATE297466T1 (de) | 1996-04-12 | 2005-06-15 | American Nat Red Cross | Mutierter plasminogen-aktivator-inhibitor typ 1 und seine verwendungen |
| GB9719187D0 (en) | 1997-09-09 | 1997-11-12 | Glaxo Group Ltd | Compounds |
| PE107899A1 (es) | 1997-09-09 | 1999-11-17 | Glaxo Group Ltd | Derivados de pirrolopirrolona como inhibidores de elastasa leucocitaria |
| KR20010078724A (ko) | 1998-06-03 | 2001-08-21 | 존 더블류. 갈루치 2세 | 세린 프로테아제 저해제로서의 인돌 및테트라히드로이소퀴놀린을 함유하는 α-케토 옥사디아졸 |
| WO1999062538A1 (en) | 1998-06-03 | 1999-12-09 | Cortech Inc. | Alpha-keto oxadiazoles as serine protease inhibitors |
| US20030069187A1 (en) | 2001-10-05 | 2003-04-10 | Rao Srinivasa K. | Elastase inhibitors |
| US20030119073A1 (en) | 2001-12-21 | 2003-06-26 | Stephen Quirk | Sensors and methods of detection for proteinase enzymes |
| GB0219896D0 (en) | 2002-08-27 | 2002-10-02 | Bayer Ag | Dihydropyridine derivatives |
| TW200500341A (en) | 2002-11-12 | 2005-01-01 | Astrazeneca Ab | Novel compounds |
| SE0302324D0 (sv) | 2003-08-28 | 2003-08-28 | Astrazeneca Ab | Novel compounds |
| SE0302323D0 (sv) | 2003-08-28 | 2003-08-28 | Astrazeneca Ab | Novel compounds |
| SE0302486D0 (sv) | 2003-09-18 | 2003-09-18 | Astrazeneca Ab | Novel compounds |
| SE0302487D0 (sv) | 2003-09-18 | 2003-09-18 | Astrazeneca Ab | Novel compounds |
| JP4825194B2 (ja) | 2004-02-26 | 2011-11-30 | バイエル・シェーリング・ファルマ・アクチェンゲゼルシャフト | 1,4−ジアリール−ジヒドロピリミジン−2−オン化合物およびヒト好中球エラスターゼ阻害剤としてのそれらの使用 |
| WO2005082863A2 (en) | 2004-02-26 | 2005-09-09 | Bayer Healthcare Ag | 1,4 diaryl-dihydropyrimidin-2 ones and their use as a human neutrophil elastase inhibitors |
| WO2006070012A1 (en) | 2004-12-30 | 2006-07-06 | Ingenium Pharmaceuticals Ag | Agents useful in treating inflammatory bowel disease |
| GB0502258D0 (en) | 2005-02-03 | 2005-03-09 | Argenta Discovery Ltd | Compounds and their use |
| TW200700392A (en) | 2005-03-16 | 2007-01-01 | Astrazeneca Ab | Novel compounds |
| GB0512940D0 (en) | 2005-06-24 | 2005-08-03 | Argenta Discovery Ltd | Compounds and their use |
| GB0605469D0 (en) | 2006-03-17 | 2006-04-26 | Argenta Discovery Ltd | Multimers of heterocyclic compounds and their use |
| WO2009013444A1 (en) | 2007-07-25 | 2009-01-29 | Argenta Discovery Limited | Tetrahydropyrrolopyrimidinediones and their use as human neutrophil elastase inhibitors |
| AU2007246889B2 (en) | 2006-05-04 | 2011-03-10 | Chiesi Farmaceutici S.P.A. | Tetrahydropyrrolopyrimidinediones and their use as human neutrophil elastase inhibitors |
| TW200808763A (en) | 2006-05-08 | 2008-02-16 | Astrazeneca Ab | Novel compounds I |
| TW200808771A (en) | 2006-05-08 | 2008-02-16 | Astrazeneca Ab | Novel compounds II |
| RU2419625C2 (ru) | 2006-05-23 | 2011-05-27 | Айрм Ллк | Соединения и композиции в качестве ингибиторов протеазы, активирующей каналы |
| WO2007137080A2 (en) | 2006-05-23 | 2007-11-29 | Irm Llc | Compounds and compositions as channel activating protease inhibitors |
| ES2293832B1 (es) | 2006-07-17 | 2009-05-04 | Cargoflet S.A. | Sistema de transporte masivo de gas natural a alta presion por via maritima. |
| US20110003858A1 (en) | 2006-09-04 | 2011-01-06 | Bergstroem Lena | Multimeric heterocyclic compounds useful as neutrophil elastase inhibitors |
| BRPI0716897A2 (pt) | 2006-09-21 | 2013-10-22 | Activx Biosciences Inc | Composto ou um derivado farmaceuticamente aceitável do mesmo, composição farmacêutica, métodos para inibir uma ação de uma serina hidrolase e para tratamento de uma doença mediada por serina hidrolase, e, artigo de fabricação. |
| ATE493174T1 (de) | 2007-01-10 | 2011-01-15 | Irm Llc | Verbindungen und zusammensetzungen als kanal- aktivierende proteasehemmer |
| JP2010518099A (ja) | 2007-02-09 | 2010-05-27 | アイアールエム・リミテッド・ライアビリティ・カンパニー | チャネル活性化プロテアーゼ阻害剤としての化合物および組成物 |
| WO2008104752A1 (en) | 2007-02-26 | 2008-09-04 | Astrazeneca Ab | Dihydropyridones as elastase inhibitors |
| WO2009037413A1 (en) | 2007-09-19 | 2009-03-26 | Argenta Discovery Limited | Dimers of 5- [ (4-cyanophenyl) sulfinyl] -6-methyl-2-oxo-1- [3- (trifluoromethyl)phenyl] -1,2-dihydropyridine-3-carboxamide as inhibitors of human neutrophil elastase for treating respiratory diseases |
| WO2009058076A1 (en) | 2007-11-02 | 2009-05-07 | Astrazeneca Ab | 2-pyrazinone derivatives and their use as inhibitors of neutrophile elastase |
| TW200924770A (en) | 2007-11-06 | 2009-06-16 | Astrazeneca Ab | Novel compounds 089 |
| WO2009060206A1 (en) | 2007-11-07 | 2009-05-14 | Argenta Discovery Limited | 3,4,6,7-tetrahydro-1h-pyrrolo[3,4-d]pyrimidine-2,5-diones and their therapeutic use |
| WO2009060158A1 (en) | 2007-11-07 | 2009-05-14 | Argenta Discovery Limited | 4- (4-cyanophenyl) -1- (3-trifluoromethylphenyl) -3,4, 6, 7-tetrahydro-1h-pyrrolo [3, 4- d] pyrimidine-2, 5-dione derivatives and their use as human neutrophil elastase inhibitors |
| GB0817429D0 (en) | 2008-09-23 | 2008-10-29 | Argenta Discovery Ltd | Enzyme inhibitors |
| TW201036957A (en) | 2009-02-20 | 2010-10-16 | Astrazeneca Ab | Novel salt 628 |
| BR112012007322A2 (pt) | 2009-10-02 | 2017-06-06 | Astrazeneca Ab | composto de 2-piridona usados como inibidores de neutrófilo elastase |
| US20110212181A1 (en) | 2010-02-26 | 2011-09-01 | The University Of Hong Kong | Compositions and methods for treating chronic respiratory inflammation |
| WO2011110852A1 (en) | 2010-03-10 | 2011-09-15 | Astrazeneca Ab | Polymorphic forms of 6- [2- (4 -cyanophenyl) - 2h - pyrazol - 3 - yl] - 5 -methyl - 3 - oxo - 4 - (trifluoromethyl - phenyl) 3,4-dihydropyrazine-2-carboxylic acid ethylamide |
| GB201004178D0 (en) | 2010-03-12 | 2010-04-28 | Pulmagen Therapeutics Inflamma | Enzyme inhibitors |
| GB201004179D0 (en) | 2010-03-12 | 2010-04-28 | Pulmagen Therapeutics Inflamma | Enzyme inhibitors |
| KR20140060513A (ko) | 2011-09-14 | 2014-05-20 | 키에시 파르마슈티시 엣스. 피. 에이. | 인체 호중구 엘라스타제 억제제인 테트라히드로트리아졸로피리미딘 유도체 |
| WO2013084199A1 (en) | 2011-12-07 | 2013-06-13 | Universidade De Lisboa | Boron heterocycles as new inhibitors of human neutrophil elastase |
| CA2878792A1 (en) | 2012-07-12 | 2014-01-16 | Chiesi Farmaceutici S.P.A. | Inhibition of enzymes |
| US20140057926A1 (en) | 2012-08-23 | 2014-02-27 | Boehringer Ingelheim International Gmbh | Substituted 4-pyridones and their use as inhibitors of neutrophil elastase activity |
| US9102624B2 (en) | 2012-08-23 | 2015-08-11 | Boehringer Ingelheim International Gmbh | Substituted 4-pyridones and their use as inhibitors of neutrophil elastase activity |
| US20140057920A1 (en) | 2012-08-23 | 2014-02-27 | Boehringer Ingelheim International Gmbh | Substituted 4-pyridones and their use as inhibitors of neutrophil elastase activity |
| US20140221335A1 (en) | 2013-02-06 | 2014-08-07 | Boehringer Ingelheim International Gmbh | Substituted bicyclic dihydropyrimidinones and their use as inhibitors of neutrophil elastase activity |
| US9115093B2 (en) | 2013-03-04 | 2015-08-25 | Boehringer Ingelheim International Gmbh | Substituted bicyclic dihydropyrimidinones and their use as inhibitors of neutrophil elastase activity |
| EP3083626B1 (en) | 2013-12-16 | 2017-10-25 | CHIESI FARMACEUTICI S.p.A. | Tetrahydrotriazolopyrimidine derivatives as human neutrophil elastase inhibitors |
| EA034910B1 (ru) | 2013-12-27 | 2020-04-06 | Полифор Аг | Бета-шпилечные пептидомиметики в качестве селективных ингибиторов эластазы |
| SI3087094T1 (sl) | 2013-12-27 | 2022-11-30 | Spexis Ag | BETA-lasnični peptidomimetiki kot selektivni zaviralci elastaze |
| US9221807B2 (en) | 2014-02-21 | 2015-12-29 | Boehringer Ingelheim International Gmbh | Substituted pyridones and pyrazinones and their use as inhibitors of neutrophil elastase activity |
| WO2015200349A2 (en) * | 2014-06-24 | 2015-12-30 | The California Institute For Biomedical Research | Elastase inhibitors |
| US9475779B2 (en) | 2014-07-31 | 2016-10-25 | Boehringer Ingelheim International Gmbh | Substituted bicyclic dihydropyrimidinones and their use as inhibitors of neutrophil elastase activity |
| US9290457B2 (en) | 2014-07-31 | 2016-03-22 | Boehringer Ingelheim International Gmbh | Substituted dihydropyrimidinones and their use as inhibitors of neutrophil elastase activity |
| US9657015B2 (en) * | 2014-07-31 | 2017-05-23 | Boehringer Ingelheim International Gmbh | Substituted bicyclic dihydropyrimidinones and their use as inhibitors of neutrophil elastase activity |
| US9458113B2 (en) | 2014-07-31 | 2016-10-04 | Boehringer Ingelheim International Gmbh | Substituted bicyclic dihydropyrimidinones and their use as inhibitors of neutrophil elastase activity |
| US9440930B2 (en) | 2014-07-31 | 2016-09-13 | Boehringer Ingelheim International Gmbh | Substituted bicyclic dihydropyrimidinones and their use as inhibitors of neutrophil elastase activity |
| EP3193910A1 (en) | 2014-08-05 | 2017-07-26 | Réunion Therapeutics B.V. | Mutants of leech derived neutrophil elastase inhibitors and uses thereof |
| WO2016050835A2 (en) | 2014-10-02 | 2016-04-07 | Ruprecht-Karls-Universität Heidelberg | Selective inhibitors of neutrophil elastase for treating neuropathic pain and chronic pain states harbouring a neuropathic component |
| US9890169B2 (en) | 2015-12-14 | 2018-02-13 | Chiesi Farmaceutici S.P.A. | Triazolinone compounds as HNE inhibitors |
| UA123109C2 (uk) | 2016-05-31 | 2021-02-17 | К'Єзі Фармачеутічі С.П.А. | Сполуки імідазолону як інгібітори нейтрофіл-еластази людини |
| KR20220079527A (ko) * | 2019-09-17 | 2022-06-13 | 메레오 바이오파마 4 리미티드 | 이식편 거부반응, 폐쇄성 세기관지염 증후군 및 이식편 대 숙주병의 치료에 사용하기 위한 알베레스타트 |
| WO2021178448A1 (en) * | 2020-03-02 | 2021-09-10 | Motor Life Sciences, Llc | Compositions and methods for diagnosing, preventing, and treating amyotrophic lateral sclerosis in patients with hypofunctional anti-trypsin activity |
-
2021
- 2021-03-16 IL IL297211A patent/IL297211A/en unknown
- 2021-03-16 US US17/995,909 patent/US20230190723A1/en active Pending
- 2021-03-16 WO PCT/GB2021/050658 patent/WO2021209740A1/en active Application Filing
- 2021-03-16 HU HUE21714345A patent/HUE064089T2/hu unknown
- 2021-03-16 HR HRP20231065TT patent/HRP20231065T1/hr unknown
- 2021-03-16 US US17/995,908 patent/US20230218596A1/en active Pending
- 2021-03-16 JP JP2022562608A patent/JP2023522010A/ja active Pending
- 2021-03-16 EP EP21714345.2A patent/EP4106757B1/en active Active
- 2021-03-16 EP EP23187058.5A patent/EP4252850A3/en active Pending
- 2021-03-16 LT LTEPPCT/GB2021/050653T patent/LT4106757T/lt unknown
- 2021-03-16 MX MX2022012942A patent/MX2022012942A/es unknown
- 2021-03-16 PL PL21714345.2T patent/PL4106757T3/pl unknown
- 2021-03-16 DK DK21714345.2T patent/DK4106757T3/da active
- 2021-03-16 ES ES21714345T patent/ES2962498T3/es active Active
- 2021-03-16 FI FIEP21714345.2T patent/FI4106757T3/fi active
- 2021-03-16 PT PT217143452T patent/PT4106757T/pt unknown
- 2021-03-16 WO PCT/GB2021/050653 patent/WO2021209739A1/en unknown
- 2021-03-16 SI SI202130071T patent/SI4106757T1/sl unknown
- 2021-03-16 AU AU2021256835A patent/AU2021256835A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| HRP20231065T1 (hr) | 2023-12-22 |
| EP4106757B1 (en) | 2023-08-23 |
| EP4252850A2 (en) | 2023-10-04 |
| US20230190723A1 (en) | 2023-06-22 |
| DK4106757T3 (da) | 2023-10-23 |
| WO2021209740A1 (en) | 2021-10-21 |
| HUE064089T2 (hu) | 2024-02-28 |
| EP4106757A1 (en) | 2022-12-28 |
| AU2021256835A1 (en) | 2022-10-13 |
| MX2022012942A (es) | 2023-01-11 |
| EP4252850A3 (en) | 2023-11-15 |
| FI4106757T3 (fi) | 2023-10-23 |
| SI4106757T1 (sl) | 2023-11-30 |
| IL297211A (en) | 2022-12-01 |
| US20230218596A1 (en) | 2023-07-13 |
| ES2962498T3 (es) | 2024-03-19 |
| PT4106757T (pt) | 2023-11-17 |
| LT4106757T (lt) | 2023-11-10 |
| WO2021209739A1 (en) | 2021-10-21 |
| PL4106757T3 (pl) | 2024-01-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CA2869269C (en) | Use of ccr3-inhibitors | |
| US20190309021A1 (en) | Composition Comprising a Peptide and an Inhibitor of Viral Neuraminidase | |
| US10806735B2 (en) | Use of neutrophil elastase inhibitors in liver disease | |
| ES2887358T3 (es) | Inhibidor de Alfa1-Proteinasa para demorar el comienzo o progresión de exacerbaciones pulmonares | |
| JP2023520323A (ja) | 2型アンギオテンシンii受容体アゴニストの新規使用 | |
| WO2010103384A1 (en) | Compositions and methods for treatment and prevention of cardiovascular disease | |
| Wu et al. | Advances in understanding mechanisms underlying mitochondrial structure and function damage by ozone | |
| JP2023522010A (ja) | α1-アンチトリプシンの欠損により媒介される呼吸器系疾患の処置のための好中球エラスターゼ阻害剤アルベレスタットに関連する方法 | |
| CN107466236B (zh) | 胸腺素α1用于囊性纤维化治疗的用途 | |
| US11439631B2 (en) | Use of a glutarimide derivative to treat diseases related to the aberrant activity of cytokines | |
| JPWO2006137423A1 (ja) | 肺胞破壊によって生じる肺疾患の治療または予防のためのクラリスロマイシンまたはその塩 | |
| JP2021510369A (ja) | 肺気腫及びその他の形態のcopdの治療のための組成物及び方法 | |
| WO2022200339A1 (en) | Treatment of hidradenitis suppurativa with orismilast | |
| EP4291239A2 (en) | Compounds, compositions and methods for treating age-related diseases and conditions | |
| Matos et al. | Combination therapy in Phe508del CFTR: how many will be enough? | |
| Kazuhito et al. | Suppressive activity of fexofenadine hydrochloride on the production of eosinophil chemoattractants from human nasal fibroblasts in vitro | |
| EP4046639A1 (en) | Prevention of pulmonary vascular leak in covid-19 | |
| US11161881B2 (en) | Composition comprising a peptide and an inhibitor of viral neuraminidase | |
| TW202122086A (zh) | 嗜中性白血球彈性蛋白酶抑制劑在肺部疾病中之使用 | |
| CN101631538B (zh) | 用于治疗慢性阻塞性肺病的药物 | |
| JP2006525277A (ja) | 神経保護因子としてのグルタミン酸レセプターアンタゴニスト | |
| Chen et al. | Targeting Neutrophil Serine Proteinases in Alpha 1 Antitrypsin Deficiency | |
| WO2023192779A2 (en) | Combined prevention and treatment of patients with respiratory diseases caused by rna viral infections | |
| Rezk et al. | Histopathological Effects of Therapeutic Doses of Combined XO-Inhibitors and ACE-Inhibitors on the Expression of VEGF-A in the Myocardium and Renal Cortex in Chronic Hypertensive Albino Rats | |
| WO2023203022A1 (en) | Treatment of neutrophilic dermatoses |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240308 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20240308 |