JP2022534412A - プロカスパーゼ‐3の活性化及びがんの治療のための免疫療法 - Google Patents
プロカスパーゼ‐3の活性化及びがんの治療のための免疫療法 Download PDFInfo
- Publication number
- JP2022534412A JP2022534412A JP2021570464A JP2021570464A JP2022534412A JP 2022534412 A JP2022534412 A JP 2022534412A JP 2021570464 A JP2021570464 A JP 2021570464A JP 2021570464 A JP2021570464 A JP 2021570464A JP 2022534412 A JP2022534412 A JP 2022534412A
- Authority
- JP
- Japan
- Prior art keywords
- cancer
- pac
- active agent
- protein
- cell
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/337—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having four-membered rings, e.g. taxol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/24—Heavy metals; Compounds thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
- A61K39/0011—Cancer antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/39—Medicinal preparations containing antigens or antibodies characterised by the immunostimulating additives, e.g. chemical adjuvants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/02—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/12—Carboxylic acids; Salts or anhydrides thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/14—Esters of carboxylic acids, e.g. fatty acid monoglycerides, medium-chain triglycerides, parabens or PEG fatty acid esters
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/26—Carbohydrates, e.g. sugar alcohols, amino sugars, nucleic acids, mono-, di- or oligo-saccharides; Derivatives thereof, e.g. polysorbates, sorbitan fatty acid esters or glycyrrhizin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
- A61K47/38—Cellulose; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/44—Oils, fats or waxes according to two or more groups of A61K47/02-A61K47/42; Natural or modified natural oils, fats or waxes, e.g. castor oil, polyethoxylated castor oil, montan wax, lignite, shellac, rosin, beeswax or lanolin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0014—Skin, i.e. galenical aspects of topical compositions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
- A61K9/0073—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
- A61K9/0073—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy
- A61K9/0078—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy for inhalation via a nebulizer such as a jet nebulizer, ultrasonic nebulizer, e.g. in the form of aqueous drug solutions or dispersions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/06—Ointments; Bases therefor; Other semi-solid forms, e.g. creams, sticks, gels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
- A61K9/2018—Sugars, or sugar alcohols, e.g. lactose, mannitol; Derivatives thereof, e.g. polysorbates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/2027—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone, poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2054—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2059—Starch, including chemically or physically modified derivatives; Amylose; Amylopectin; Dextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/485—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4858—Organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4866—Organic macromolecular compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2818—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against CD28 or CD152
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/545—Medicinal preparations containing antigens or antibodies characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Mycology (AREA)
- Inorganic Chemistry (AREA)
- Microbiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Biophysics (AREA)
- Dermatology (AREA)
- Biochemistry (AREA)
- Oncology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Otolaryngology (AREA)
- Pulmonology (AREA)
- Genetics & Genomics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Dispersion Chemistry (AREA)
- Endocrinology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Enzymes And Modification Thereof (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
Description
本出願は、2019年5月30日に出願された米国仮特許出願第62/854,823号及び2019年12月6日に出願された第62/944,404号の35U.S.C.§119(e)に基づく優先権を主張するものであり、これらの出願は参照により本明細書に組み込まれる。
本発明は、米国国立衛生研究所(National Institutes of Health)から交付されたグラントNo.R01 CA120439の政府支援を受けて行われたものである。政府はこの発明について一定の権利を有する。
免疫療法の成功は、メラノーマ、肺がん、膀胱がんの治療を大きく変え、他のいくつかのタイプの腫瘍にも大きな期待が寄せられている。一部の患者に見られた劇的な結果(例えば、末期の病気であっても持続的な効果が得られた)は、他の難治性のがんにもこのような治療法が有効であるという期待を抱かせた。腫瘍内の変異負荷と免疫チェックポイント阻害剤の効果には明らかな相関関係がある。この見解は、DNAミスマッチ修復欠損やマイクロサテライト不安定性(MSI)を有する患者に対するペムブロリズマブ(PD‐1に対する抗体であるキイトルーダ(Keytruda))の承認に反映されている。残念ながら、変異負荷の少ない多くのがんについては、免疫療法の臨床試験はほとんど期待外れであり、MSIの表現型を持つがんが10%未満であるという事実は、免疫療法の成功を広く拡大する上での課題を示している。膠芽腫(GBM)に対する免疫療法の課題は、ネオアンチゲンの発現が少ないこと、腫瘍内へのT細胞の浸潤がないこと、ほとんどの薬剤が血液脳関門(BBB)を通過するのが難しいことを考えると、さらに重大である。
(a)プロカスパーゼ‐3活性化剤;
(b)少なくとも1つの第2の活性剤、ここで該第2の活性剤は、チェックポイント阻害剤、がんワクチン、代謝調節剤、マクロファージ阻害剤、又は免疫刺激剤若しくは調節剤である;及び
(c)任意に、薬学的に許容される希釈剤、賦形剤、又は担体。
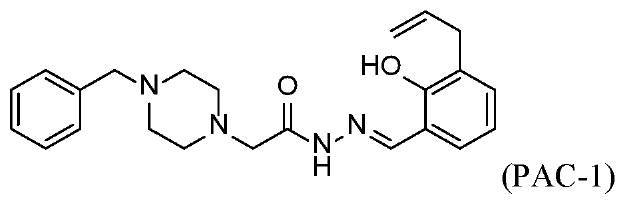
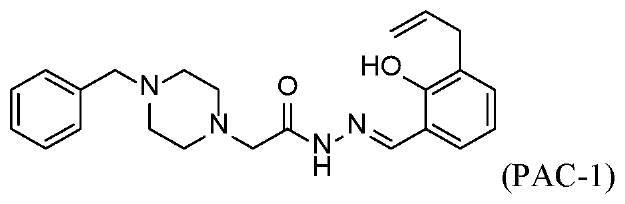
様々な実施形態において、プロカスパーゼ‐3活性化剤はPAC‐1である。
本明細書では、低変異負荷の腫瘍を高変異負荷の腫瘍に選択的に変換し、免疫療法の理想的な候補とする、メカニズムに基づく新しい戦略の開発を開示する。この戦略は、腫瘍抑制因子であるMLH1を標的として不活性化することを前提としている。本明細書で開示するように、MLH1のサイレンシングと抗PD‐1抗体への反応には強い相関関係があり、MLH1の遺伝子サイレンシングと腫瘍内の体細胞変異の数との関連性が説得力をもって示され、MLH1機能の喪失によるDNA損傷により高い免疫原性のストレス反応が誘導される。目標は、薬剤を介した腫瘍選択的なMLH1の不活性化により、免疫療法の力と可能性をGBMにもたらすことであった。MLH1はカスパーゼ‐3の主要な細胞基質であり、開示された方法では、PAC‐1と呼ばれる小分子を用いて、腫瘍細胞においてプロカスパーゼ‐3をカスパーゼ‐3に選択的に活性化させることで、MLH1の選択的切断をがん細胞において誘導することができる。
以下の定義は、本明細書及び特許請求の範囲の明確で一貫した理解を提供するために含まれている。本明細書では、記載されている用語は、以下の意味を持つ。本明細書で使用される他のすべての用語及び語句は、当業者が理解するであろう通常の意味を有する。このような通常の意味は、Hawley’s Condensed Chemical Dictionary 14thEdition,by R.J. Lewis,John Wiley & Sons,New York,N.Y.,2001などの技術辞書を参照して得ることができる。
本開示は、以下を含む組成物を提供する。
(a)プロカスパーゼ‐3活性化剤;
(b)少なくとも1つの第2の活性剤であって、該第2の活性剤が、チェックポイント阻害剤、がんワクチン、代謝調節剤、マクロファージ阻害剤、又は免疫刺激剤若しくは調節剤である;及び
(c)任意に、薬学的に許容される希釈剤、賦形剤、又は担体。
(a)化合物PAC‐1;
(b)少なくとも1つの第2の活性剤であって、該第2の活性剤が、チェックポイント阻害剤、がんワクチン、代謝調節剤、マクロファージ阻害剤、又は免疫刺激剤若しくは調節剤である;及び
(c)任意に、薬学的に許容される希釈剤、賦形剤、担体、又はそれらの組み合わせ;ここで、がんがそれによって治療される。
チェックポイント阻害剤を用いた免疫療法は、特定のがん(メラノーマ、NSCLC、尿路上皮など)に対して有効な治療法となっており、一部のがん患者に持続的な反応を誘発することができる。現在、免疫チェックポイント阻害剤と低分子薬剤を組み合わせた数十の臨床試験が進行中である。プロカスパーゼ‐3を直接活性化することで、DNAミスマッチ修復の鍵となるタンパク質MLH1の切断が促進され、その結果、T細胞が標的とする潜在的なネオアンチゲンが増加することで、免疫チェックポイント阻害剤の効果が劇的に高まるというメカニズム仮説が、ここに記載されているように検討されている。
本明細書に記載されている化合物及び組成物は、例えば、化合物を薬学的に許容される希釈剤、賦形剤、又はキャリアと組み合わせることによって、治療用の医薬組成物を調製するために使用することができる。化合物は、塩又は溶媒和物の形でキャリアに加えてもよい。例えば、化合物が十分に塩基性又は酸性であり、安定した無毒の酸又は塩基の塩を形成する場合、化合物を塩として投与することが適切であり得る。薬学的に許容される塩の例は、生理学的に許容されるアニオンを形成する酸で形成される有機酸付加塩であり、例えば、トシル酸塩、メタンスルホン酸塩、酢酸塩、クエン酸塩、マロン酸塩、酒石酸塩、コハク酸塩、安息香酸塩、アスコルビン酸塩、α‐ケトグルタル酸塩、及びβ‐グリセロリン酸塩である。また、塩酸塩、ハロゲン化物、硫酸塩、硝酸塩、重炭酸塩、炭酸塩などの適切な無機塩を形成することができる。
試薬。以下の抗体はBio X Cell社から購入した:抗マウスCTLA‐4モノクローナル抗体(9H10)、抗マウスPD‐1モノクローナル抗体(RMP1‐14)、ラットIgG2aアイソタイプ対照(2A3)、ポリクローナルSyrianハムスターIgG。
PAC‐1で処理したGL261腫瘍では、免疫細胞の浸潤が増加している。PAC‐1ががん細胞においてカスパーゼ‐3を介したMLH1の切断を誘導することを示すデータに加えて、PAC‐1と免疫療法戦略(チェックポイント阻害剤及びネオアンチゲンワクチンを含む)との相乗的な組み合わせを支持する他の多くの証拠がある:1)PAC‐1で処理したがん細胞の転写プロファイルでは、TNFα、自然免疫系のアゴニストであるIL‐1β、IL‐8などの主要な遺伝子が上昇しており、抗PD‐1療法への抵抗性に関連するマーカーの上昇は見られなかった(IPRES:例.CCL2,CCL7,CCL8,CCL13など)。2)別のグループの研究によると、PAC‐1は免疫サイトカインTRAILとの併用試験により、培養中の外因性細胞死を促進し得る。3)PAC‐1は、免疫システムが損なわれていないインビボ環境、例えば同系マウス(EL4、K7M2、GL261)(図7)及びラット(9L)モデル、及びイヌのがん患者に有効である。4)MDアンダーソンのGandhiグループ(Blood 2015,125,1126)は、PAC‐1及び誘導体がPMBCに対して最小限の毒性を有することを示している。5)PAC‐1は、INDを可能にするラット及びイヌの研究において非常に高用量で使用された場合でも、(マウス、ラット、イヌ、又はヒトにおいて)骨髄抑制を誘発することは観察されていない。6)PAC‐1はがん細胞に選択的にDNAダメージを与え、カスパーゼ‐3の活性化がゲノムの著しい不安定性をもたらし得るという研究結果をさらに検証する。PAC‐1が免疫反応を刺激する可能性を探る手始めとして、単剤のPAC‐1がTIL(CD3+細胞)の数を増加させることを示した同系のGL261マウスモデルを使った実験が行われた(図4)。
図8は、BALB/cマウスにおけるCT‐26 WT皮下疾患モデルの開発を示す。0日目に、BALB/cマウスに1x10個の6CT‐26_WT細胞を皮下注射した。様々な日間隔で、選択したマウスに、表1に示すように、空のビヒクル、PAC‐1(100mg/kg)、抗PD‐1抗体(10mg/kg;2回投与)、抗PD‐1抗体(10mg/kg;4回投与)、又はPAC‐1(100mg/kg)と抗PD‐1抗体(10mg/kg;)の組み合わせを注射(i.p.)した。
グループ1:3匹のマウス‐ビヒクル+ラットIgGアイソタイプmAb(10mg/kg)
グループ2:3匹のマウス‐PAC‐1(125mg/kg)+ラットIgGアイソタイプmAb(10mg/kg)
グループ3:3匹のマウス‐ビヒクル+抗PD1 mAb(10mg/kg)
グループ4:3匹のマウス‐PAC‐1(125mg/kg)+抗PD1 mAb(10mg/kg)
非腫瘍担持+ビヒクル
非腫瘍担持+PAC‐1(5回投与)
腫瘍担持+ビヒクル
腫瘍担持+PAC‐1(5回投与)
図16は、C57BL/6マウスにおけるMC‐38転移モデルの開発と、PAC‐1と抗PD‐1抗体の併用による治療を示している。MC‐38細胞を1x106細胞/マウスで尾静脈から注入した。PAC‐1は100mg/kg(i.p.)、抗PD‐1は10mg/kgをMC38注入後23日間にわたって注射した。PAC‐1/抗PD‐1を組み合わせて注射したマウスの体重は、約24日目から始まって32日目まで増加し、著しい体重回復を示した。
以下の製剤は、本明細書に記載されている式の組成物、本明細書に具体的に開示されている組成物、又はその薬学的に許容される塩(以下、「組成物X」と呼ぶ)の治療的又は予防的な投与に使用することができる代表的な医薬品剤形を例示している。
「組成物X」 100.0
ラクトース 77.5
ポビドン 15.0
クロスカルメロースナトリウム 12.0
微結晶セルロース 92.5
ステアリン酸マグネシウム 3.0
300.0
「組成物X」 20.0
微結晶セルロース 410.0
デンプン 50.0
デンプングリコール酸ナトリウム 15.0
ステアリン酸マグネシウム 5.0
500.0
「組成物X」 10.0
コロイド状二酸化ケイ素 1.5
ラクトース 465.5
プレジェル化デンプン 120.0
ステアリン酸マグネシウム 3.0
600.0
「組成物X」(遊離酸形) 1.0
二塩基性リン酸ナトリウム 12.0
一塩基性リン酸ナトリウム 0.7
塩化ナトリウム 4.5
1.0N 水酸化ナトリウム溶液 q.s.
(pHを7.0~7.5に調整)
注入用の水 q.s. ad 1mL
「組成物X」(遊離酸形) 10.0
一塩基性リン酸ナトリウム 0.3
二塩基性リン酸ナトリウム 1.1
ポリエチレングリコール400 200.0
0.1N水酸化ナトリウム溶液 q.s.
(pHを7.0~7.5に調整)
注入用の水 q.s. ad 1mL
「組成物X」 20
オレイン酸 10
トリクロロモノフルオロメタン 5,000
ジクロロジフルオロメタン 10,000
ジクロロテトラフルオロエタン 5,000
「組成物X」 5%
カルボマー934 1.25%
トリエタノールアミン q.s.
(pHを5~7に調整)
メチルパラベン 0.2%
精製水 q.s.100gまで
「組成物X」 5%
メチルセルロース 2%
メチルパラベン 0.2%
プロピルパラベン 0.02%
精製水 q.s.100gまで
「組成物X」 5%
プロピレングリコール 1%
無水軟膏ベース 40%
ポリソルベート80 2%
メチルパラベン 0.2%
精製水 q.s.100gまで
「組成物X」 5%
ホワイト蜜蝋 10%
流動パラフィン 30%
ベンジルアルコール 5%
精製水 q.s.100gまで
「組成物X」 5%
ステアリン酸 10%
モノステアリン酸グリセリル 3%
ポリオキシエチレンステアリルエーテル 3%
ソルビトール 5%
パルミチン酸イソプロピル 2%
メチルパラベン 0.2%
精製水 q.s.100gまで
Claims (26)
- (a)プロカスパーゼ‐3活性化剤;
(b)少なくとも1つの第2の活性剤、ここで該第2の活性剤は、チェックポイント阻害剤、がんワクチン、代謝調節剤、マクロファージ阻害剤、又は免疫刺激剤若しくは調節剤である;及び
(c)任意に、薬学的に許容される希釈剤、賦形剤、又は担体
を含む組成物。 - 第2の活性剤ががん細胞においてアポトーシスを誘導する効果を有し、PAC‐1が第2の活性剤の効果を相加効果よりも大きい量で増強し、PAC‐1が第2の活性剤に対するがん細胞の脆弱性をプライム化する、請求項1に記載の組成物。
- 第2の活性剤が、インドールアミン‐ピロール2,3‐ジオキシゲナーゼ(IDO)、アデノシンA2A受容体(A2AR)、トランスフォーミング成長因子β(TGF‐β)、C‐X‐Cケモカイン受容体タイプ4(CXCR‐4)、C‐Cケモカイン受容体タイプ4(CCR4)、腫瘍壊死因子受容体(CD27)、インターロイキン2受容体サブユニットβ(CD122)、デスレセプター5(DR5)、アポトーシスタンパク質の阻害剤(IAP)、グルタミナーゼ、コロニー刺激因子1受容体(CSF1R)、トール様受容体(TLR)、樹状細胞(DC)、又はそれらの組み合わせを調節する、請求項1に記載の組成物。
- 第2の活性剤が、ADXS11‐001、ADXS31‐142、AMP‐224、AMP‐514、アテゾリムマブ、アテゾリズマブ、アベルマブ、ベバシズマブ、セミプリマブ、BLZ945、BMS‐936559、BMS986016、BMS986156、BMS986205、CB839、CIMAvax、CMP001、CP870893、CPI‐444、CRS207、CV301、DCワクチン、DNX2401、DS‐8273a、デュルバルマブ、エパカドスタット、FAZ053、FPA008、GDC0919、GSK3174998、GVAX、GWN323、IMCgp100、IMP321、イムプリムPGG、インドキシミド、イピリムマブ、JTX‐2011、LAG525、LCL161、LK‐301、LY2157299、LY2510924、LY3022855、MBG453、MEDI0562、MEDI0680、MEDI6469、MEDI9447、MGN1703、モガムリズマブ、MOXR0916、ネオアンチゲンワクチン、NEO‐PV‐01、NIS793、ニボルマブ、NKTR‐214、PBF509、PDR001、ペムブロリズマブ、ペプチドワクチン、ペキシダルチニブ(PLX3397)。PF‐04518600、PF‐3512676、REGN2810、REGN3767、RO7009789、SD101、タリモゲン ラヘルパレプベク、TPIV200/huFR‐1、トレメリムマブ、TroVax、TSR022、ウロクプルマブ、ウレルマブ、ウトミルマブ、バルリルマブ、ビアゲンプマツセル‐L(HS‐110)、又はこれらの組み合わせである、請求項1に記載の組成物。
- 少なくとも1つの第2の活性剤が、プログラムされた細胞死タンパク質1(PD‐1)、プログラムされたデスリガンド1(PD‐L1)、細胞傷害性Tリンパ球関連タンパク質4(CTLA‐4)、T細胞免疫グロブリン及びムチンドメイン含有‐3(TIM‐3)、リンパ球活性化遺伝子3(LAG‐3)、腫瘍壊死因子受容体スーパーファミリーメンバー4(TNFRSF4又はOX40)、腫瘍壊死因子受容体スーパーファミリーメンバー9(TNFRSF9又は4‐1BB)、グルココルチコイド誘導性TNFR関連タンパク質(GITR)、誘導性T細胞コスティミュレーター(ICOS)、又はこれらの組み合わせを介して免疫応答を調節する少なくとも1つのチェックポイント阻害剤である、請求項1に記載の組成物。
- チェックポイント阻害剤が、抗PD‐1、抗CTLA‐4、又はそれらの組み合わせであり、抗PD‐1がニボルマブ又はペムブロリズマブであり、抗CTLA‐4がイピリムマブ又はトレメリムマブ、又はそれらの組み合わせである、請求項6に記載の組成物。
- PAC‐1の濃度が約0.1μM~約50μMであり、第2の活性剤の濃度が約1nM~約100μMである、請求項1に記載の組成物。
- 薬学的に許容される希釈剤、賦形剤、又は担体を含み、a)担体が、水、緩衝剤、糖類、セルロース、シクロデキストリン、ジメチルスルホキシド、ポリエチレングリコール、トコフェロール、リポソーム、ミセル、又はそれらの組み合わせを含むか、b)賦形剤が、結合剤、潤滑剤、吸着剤、ビヒクル、崩壊剤、保存剤、又はそれらの組み合わせを含む、請求項1に記載の組成物。
- 組成物ががん細胞を選択的に標的とし、がん細胞が、膀胱がん、乳がん、結腸がん、子宮内膜がん、膠芽腫、白血病、肝臓がん、肺がん、リンパ腫、メラノーマ、髄膜腫、多発性骨髄腫、卵巣がん、骨肉腫、膵臓がん、前立腺がん、腎がん、又は甲状腺がんの細胞であり、ここで、乳がんは任意にトリプルネガティブ乳がんであり、肺がんは任意に非小細胞肺がんであり、腎がんは任意に転移性腎細胞がんである、請求項1に記載の組成物。
- がん細胞を、請求項1~10のいずれか1項に記載の組成物の有効量と接触させ、それによってがん細胞の成長又は増殖を阻害することを含む、がん細胞の成長又は増殖を阻害する方法。
- ミスマッチ修復(MMR)タンパク質の抑制、又はカスパーゼ3活性化を媒介としたMutLホモログ1(MLH1)タンパク質の分解によって、がん細胞の成長又は増殖が抑制され、DNAのマイクロサテライト不安定性(MSI)が誘発される、請求項11に記載の方法。
- がん細胞に有効量の請求項1~10のいずれか1項に記載の組成物を接触させることを含む、がん細胞にアポトーシスを誘導する方法であって、がん細胞中のミスマッチ修復(MMR)タンパク質を抑制することによってアポトーシスを誘導する、上記方法。
- MMRタンパク質がMutLホモログ1(MLH1)タンパク質であり、プロカスパーゼ‐3活性化因子を介したカスパーゼ‐3活性化により媒介される、MLH1タンパク質の分解が、がん細胞のアポトーシスを誘導する、請求項13に記載の方法。
- 治療上有効な量のプロカスパーゼ‐3活性化剤と有効な量の第2の活性剤を、それを必要としている対象に同時又は順次投与することを含む、がんを治療する方法であって、第2の活性剤が免疫療法剤であり、免疫療法剤の効果がプロカスパーゼ‐3活性化剤の投与によって増強される、上記方法。
- PAC‐1の濃度が約0.1μM~約50μMであり、第2の活性剤の濃度が約1nM~約100μMである、請求項16に記載の方法。
- PAC‐1の濃度が約1μM~約10μMであり、第2の活性剤の濃度が約1nM~約1μMである;又は
PAC‐1の1日あたりの総投与量が約10mg/kg~約125mg/kgであり、第2の活性剤の1日あたりの総投与量が約1mg/kg~約100mg/kgである、請求項16に記載の方法。 - 第2の活性剤が、チェックポイント阻害剤、がんワクチン、代謝調節剤、マクロファージ阻害剤、免疫刺激剤、又は調節剤;又はそれらの組み合わせを含む、請求項15に記載の方法。
- 第2の活性剤が、アテゾリムマブ、アベルマブ、ベバシズマブ、BMS986016、BMS986156、CP870893、デュルバルマブ、FAZ053、GSK3174998、GWN323、IMP321、イピリムマブ、JTX‐2011、LAG525、MBG453、MEDI0562、MEDI0680、MEDI6469、MOXR0916、ニボルマブ、PDR001、ペムブロリズマブ、PF‐04518600、REGN2810、REGN3767、RO7009789、トレメリムマブ、TSR022、ウレルマブ、ウトミルマブ、又はこれらの組み合わせである、請求項15に記載の方法。
- 免疫療法剤がチェックポイント阻害剤であり、チェックポイント阻害剤が、プログラムされた細胞死タンパク質1(PD‐1)、プログラムされたデスリガンド1(PD‐L1)、細胞障害性Tリンパ球関連タンパク質4(CTLA‐4)、T細胞免疫グロブリン及びムチンドメイン含有3(TIM‐3)、リンパ球活性化遺伝子3(LAG‐3)、腫瘍壊死因子受容体スーパーファミリーメンバー4(TNFRSF4又はOX40)、腫瘍壊死因子受容体スーパーファミリーメンバー9(TNFRSF9又は4‐1BB)、グルココルチコイド誘導性TNFR関連タンパク質(GITR)、誘導性T細胞コスティミュレーター(ICOS)、又はそれらの組み合わせを介して免疫応答を調節する、請求項15に記載の方法。
- プロカスパーゼ‐3活性化剤がミスマッチ修復(MMR)タンパク質を抑制し、MMRタンパク質がMutLホモログ1(MLH1)タンパク質を含み、プロカスパーゼ‐3活性化剤を介したカスパーゼ‐3活性化により媒介される、MMRタンパク質の分解が、MMRタンパク質の欠損、DNAのマイクロサテライト不安定性(MSI)、ネオアンチゲンの発現、又はそれらの組み合わせを誘導し、それにより免疫治療薬の効果を高め、プロカスパーゼ‐3活性化剤ががんの腫瘍浸潤リンパ球を増加させる、請求項15に記載の方法
- がんが、膀胱がん、乳がん、結腸がん、子宮内膜がん、膠芽腫、白血病、肝臓がん、肺がん、リンパ腫、メラノーマ、髄膜腫、多発性骨髄腫、卵巣がん、骨肉腫、膵臓がん、前立腺がん、腎がん、又は甲状腺がんであり、乳がんは任意にトリプルネガティブ乳がんであり、肺がんは任意に非小細胞肺がんであり、腎がんは任意に転移性腎細胞がんである、請求項15に記載の方法。
- 化合物PAC‐1と第二の活性剤が対象に同時に投与される;又は
化合物PAC‐1及び第2の活性剤が対象に順次投与され、ここで、化合物PAC‐1が第2の活性剤の前に対象に投与されるか、又は化合物PAC‐1が第2の活性剤の後に対象に投与される、請求項15~23のいずれか1項に記載の方法。 - 化合物PAC‐1及び第2の活性剤が、対象に1日1回(q.d.)、1日2回(b.i.d.)、1日3回(t.i.d.)、又は1日4回(q.i.d.)投与され、PAC‐1の1日あたりの総投与量が約1mg/kg~約150mg/kgである;又は
PAC‐1の各投与量は、約70mg、約175mg、約250mg、約375mg、約450mg、約500mg、約625mg、約750mg、又は約1000mgである;
又はPAC‐1の各投与量は、約50mg/m2~約250mg/m2である、請求項15~23のいずれか1項に記載の方法。 - がんを治療する方法であって、それを必要とする対象に、PAC‐1及び抗PD‐1抗体を投与することを含み、PAC‐1は、PAC‐1の1日あたりの総投与量が約100mg/kg~約125mg/kgとなるように、21日以上連続して毎日投与され、抗PD‐1抗体は、21日以上連続して2回又は4回投与され、抗PD‐1抗体の投与量は約10mg/kgであり、抗PD‐1抗体の各投与量は別々の日に投与される、上記方法。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962854823P | 2019-05-30 | 2019-05-30 | |
| US62/854,823 | 2019-05-30 | ||
| US201962944404P | 2019-12-06 | 2019-12-06 | |
| US62/944,404 | 2019-12-06 | ||
| PCT/US2020/035578 WO2020243712A1 (en) | 2019-05-30 | 2020-06-01 | Procaspase-3 activation and immunotherapy for treatment of cancer |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2022534412A true JP2022534412A (ja) | 2022-07-29 |
| JP2022534412A5 JP2022534412A5 (ja) | 2023-05-31 |
| JP7648155B2 JP7648155B2 (ja) | 2025-03-18 |
Family
ID=73553321
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021570464A Active JP7648155B2 (ja) | 2019-05-30 | 2020-06-01 | プロカスパーゼ‐3の活性化及びがんの治療のための免疫療法 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US20220226311A1 (ja) |
| EP (1) | EP3976062A4 (ja) |
| JP (1) | JP7648155B2 (ja) |
| KR (1) | KR20220016104A (ja) |
| CN (1) | CN113905764B (ja) |
| AU (1) | AU2020283161A1 (ja) |
| CA (1) | CA3142157A1 (ja) |
| IL (1) | IL288433A (ja) |
| MX (1) | MX2021014758A (ja) |
| SG (1) | SG11202113213RA (ja) |
| WO (1) | WO2020243712A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN120289385A (zh) * | 2025-04-10 | 2025-07-11 | 沈阳药科大学 | 半胱天冬酶原活化物的类似物及其应用 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015509965A (ja) * | 2012-03-06 | 2015-04-02 | ザ ボード オブ トラスティーズ オブ ザ ユニヴァーシティー オブ イリノイ | 併用療法によるプロカスパーゼ3活性化 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2231147A2 (en) * | 2007-12-13 | 2010-09-29 | Novartis AG | Combinations of therapeutic agents for treating cancer |
| KR20120067715A (ko) * | 2010-12-16 | 2012-06-26 | 학교법인 동의학원 | 나린제닌 및 trail을 포함하는 폐암 치료 및 예방용 조성물 |
| AU2013230985B2 (en) * | 2012-03-06 | 2016-05-12 | The Board Of Trustees Of The University Of Illinois | Procaspase combination therapy for glioblastoma |
| IL256111B2 (en) * | 2015-06-05 | 2023-09-01 | Univ Illinois | Treatment of pac combinations |
| BR112017028269A2 (pt) * | 2015-07-13 | 2018-09-04 | Arvinas Inc | composto, composição farmacêutica, uso de uma quantidade efetiva de um composto, estado ou condição de doença, e, método para identificar um composto. |
| WO2017079746A2 (en) * | 2015-11-07 | 2017-05-11 | Multivir Inc. | Methods and compositions comprising tumor suppressor gene therapy and immune checkpoint blockade for the treatment of cancer |
| CA3063932A1 (en) * | 2017-05-18 | 2018-11-12 | The Regents Of The University Of California | Nano-enabled immunotherapy in cancer |
| AU2018368453B2 (en) * | 2017-11-17 | 2024-05-30 | The Board Of Trustees Of The University Of Illinois | Cancer therapy by degrading dual MEK signaling |
| CA3114385A1 (en) * | 2018-10-05 | 2020-04-09 | The Board Of Trustees Of The University Of Illinois | Combination therapy for the treatment of uveal melanoma |
-
2020
- 2020-06-01 EP EP20814836.1A patent/EP3976062A4/en active Pending
- 2020-06-01 MX MX2021014758A patent/MX2021014758A/es unknown
- 2020-06-01 WO PCT/US2020/035578 patent/WO2020243712A1/en not_active Ceased
- 2020-06-01 KR KR1020217041017A patent/KR20220016104A/ko not_active Ceased
- 2020-06-01 JP JP2021570464A patent/JP7648155B2/ja active Active
- 2020-06-01 SG SG11202113213RA patent/SG11202113213RA/en unknown
- 2020-06-01 CA CA3142157A patent/CA3142157A1/en active Pending
- 2020-06-01 US US17/615,402 patent/US20220226311A1/en active Pending
- 2020-06-01 CN CN202080040604.2A patent/CN113905764B/zh active Active
- 2020-06-01 AU AU2020283161A patent/AU2020283161A1/en not_active Abandoned
-
2021
- 2021-11-25 IL IL288433A patent/IL288433A/en unknown
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015509965A (ja) * | 2012-03-06 | 2015-04-02 | ザ ボード オブ トラスティーズ オブ ザ ユニヴァーシティー オブ イリノイ | 併用療法によるプロカスパーゼ3活性化 |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2020283161A1 (en) | 2022-01-06 |
| US20220226311A1 (en) | 2022-07-21 |
| KR20220016104A (ko) | 2022-02-08 |
| CN113905764A (zh) | 2022-01-07 |
| EP3976062A4 (en) | 2023-06-14 |
| EP3976062A1 (en) | 2022-04-06 |
| CN113905764B (zh) | 2024-06-11 |
| IL288433A (en) | 2022-01-01 |
| WO2020243712A1 (en) | 2020-12-03 |
| JP7648155B2 (ja) | 2025-03-18 |
| CA3142157A1 (en) | 2020-12-03 |
| MX2021014758A (es) | 2022-03-11 |
| SG11202113213RA (en) | 2021-12-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11622961B2 (en) | Combination therapies for treating cancer | |
| US12485174B2 (en) | HDAC6-activated macrophages, compositions, and uses thereof | |
| JP2024174949A (ja) | がんの処置のための組成物および方法 | |
| US20250161303A1 (en) | Combination therapies with cbl-b inhibitor compounds | |
| JP2022500496A (ja) | A2a阻害剤としてのチオカルバメート誘導体、その医薬組成物、及び抗がん剤との組み合わせ | |
| KR20190108144A (ko) | 질환 및 장애의 치료 및 방지를 위한 단쇄 지방산의 용도 | |
| US12083111B2 (en) | Use of hexokinase 2/mitochondria-detaching compounds for activating immune responses | |
| CN107921018A (zh) | 药物组合及其应用 | |
| JP2022534412A (ja) | プロカスパーゼ‐3の活性化及びがんの治療のための免疫療法 | |
| US20230405118A1 (en) | Stat-activated macrophages, compositions, and uses thereof | |
| JP2022551672A (ja) | 乳癌治療法 | |
| US20260055200A1 (en) | Combination therapies | |
| WO2023242100A1 (en) | Novel ras inhibitors | |
| JP2008540585A (ja) | 転移性メラノーマ及び他の癌を治療するための化合物、そのような化合物を含有する組成物、および治療方法 | |
| CN120939228A (zh) | 腺苷a2ar拮抗剂在制备用于增强pd-1抗体和/或pd-l1抗体免疫治疗肿瘤的药物中的应用 | |
| EP4536633A1 (en) | Novel ras inhibitors | |
| WO2023242107A1 (en) | Novel ras inhibitors | |
| JP2025524343A (ja) | 新規ras阻害剤 | |
| Amini-Vaughan | Harnessing Eosinophils as a Potential Tumoricidal Immunotherapy |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230523 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230523 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240529 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240827 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240918 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20241217 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241224 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250204 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250227 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7648155 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |