JP2019137675A - 薬剤を筋肉に送達するための方法 - Google Patents
薬剤を筋肉に送達するための方法 Download PDFInfo
- Publication number
- JP2019137675A JP2019137675A JP2019019212A JP2019019212A JP2019137675A JP 2019137675 A JP2019137675 A JP 2019137675A JP 2019019212 A JP2019019212 A JP 2019019212A JP 2019019212 A JP2019019212 A JP 2019019212A JP 2019137675 A JP2019137675 A JP 2019137675A
- Authority
- JP
- Japan
- Prior art keywords
- amino acid
- acid sequence
- antibody
- seq
- conjugate according
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 210000003205 muscle Anatomy 0.000 title claims abstract description 86
- 239000003814 drug Substances 0.000 title claims abstract description 84
- 238000000034 method Methods 0.000 title claims abstract description 55
- 229940079593 drug Drugs 0.000 title claims abstract description 50
- 102000004190 Enzymes Human genes 0.000 claims abstract description 54
- 108090000790 Enzymes Proteins 0.000 claims abstract description 54
- 230000002132 lysosomal effect Effects 0.000 claims abstract description 47
- 108010033576 Transferrin Receptors Proteins 0.000 claims abstract description 45
- 210000002027 skeletal muscle Anatomy 0.000 claims abstract description 16
- 230000001766 physiological effect Effects 0.000 claims abstract description 12
- 239000002253 acid Substances 0.000 claims abstract description 10
- 108010028144 alpha-Glucosidases Proteins 0.000 claims abstract description 10
- 102000005840 alpha-Galactosidase Human genes 0.000 claims abstract description 9
- 108010030291 alpha-Galactosidase Proteins 0.000 claims abstract description 9
- 210000004165 myocardium Anatomy 0.000 claims abstract description 8
- 102000007238 Transferrin Receptors Human genes 0.000 claims abstract 17
- 150000001413 amino acids Chemical group 0.000 claims description 191
- 108090000623 proteins and genes Proteins 0.000 claims description 184
- 102000004169 proteins and genes Human genes 0.000 claims description 87
- 210000004899 c-terminal region Anatomy 0.000 claims description 58
- 230000004064 dysfunction Effects 0.000 claims description 33
- 238000009739 binding Methods 0.000 claims description 28
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 claims description 27
- 101001018026 Homo sapiens Lysosomal alpha-glucosidase Proteins 0.000 claims description 24
- 102000045921 human GAA Human genes 0.000 claims description 24
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 23
- 208000032007 Glycogen storage disease due to acid maltase deficiency Diseases 0.000 claims description 22
- 201000004502 glycogen storage disease II Diseases 0.000 claims description 22
- 206010053185 Glycogen storage disease type II Diseases 0.000 claims description 21
- 239000008194 pharmaceutical composition Substances 0.000 claims description 21
- 208000024720 Fabry Disease Diseases 0.000 claims description 20
- 102100033448 Lysosomal alpha-glucosidase Human genes 0.000 claims description 20
- BCCRXDTUTZHDEU-VKHMYHEASA-N Gly-Ser Chemical compound NCC(=O)N[C@@H](CO)C(O)=O BCCRXDTUTZHDEU-VKHMYHEASA-N 0.000 claims description 17
- 230000005996 muscular dysfunction Effects 0.000 claims description 16
- 101000718525 Homo sapiens Alpha-galactosidase A Proteins 0.000 claims description 14
- 208000033868 Lysosomal disease Diseases 0.000 claims description 14
- 208000015439 Lysosomal storage disease Diseases 0.000 claims description 14
- 102000043404 human GLA Human genes 0.000 claims description 14
- 239000004471 Glycine Substances 0.000 claims description 11
- 125000000539 amino acid group Chemical group 0.000 claims description 10
- 239000003795 chemical substances by application Substances 0.000 claims description 9
- 238000004519 manufacturing process Methods 0.000 claims description 9
- XKUKSGPZAADMRA-UHFFFAOYSA-N glycyl-glycyl-glycine Chemical compound NCC(=O)NCC(=O)NCC(O)=O XKUKSGPZAADMRA-UHFFFAOYSA-N 0.000 claims description 8
- YWAQATDNEKZFFK-BYPYZUCNSA-N Gly-Gly-Ser Chemical compound NCC(=O)NCC(=O)N[C@@H](CO)C(O)=O YWAQATDNEKZFFK-BYPYZUCNSA-N 0.000 claims description 6
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 claims description 6
- 230000004220 muscle function Effects 0.000 claims description 6
- 108010067216 glycyl-glycyl-glycine Proteins 0.000 claims description 4
- 210000002460 smooth muscle Anatomy 0.000 claims description 3
- 210000001519 tissue Anatomy 0.000 abstract description 17
- 230000003387 muscular Effects 0.000 abstract 2
- 102100024295 Maltase-glucoamylase Human genes 0.000 abstract 1
- 125000003275 alpha amino acid group Chemical group 0.000 description 237
- 235000001014 amino acid Nutrition 0.000 description 131
- 241000282414 Homo sapiens Species 0.000 description 88
- 210000004027 cell Anatomy 0.000 description 87
- 241000699666 Mus <mouse, genus> Species 0.000 description 63
- 230000035772 mutation Effects 0.000 description 51
- 229940088598 enzyme Drugs 0.000 description 50
- 102100026144 Transferrin receptor protein 1 Human genes 0.000 description 46
- 235000018102 proteins Nutrition 0.000 description 44
- 102000037865 fusion proteins Human genes 0.000 description 39
- 108020001507 fusion proteins Proteins 0.000 description 39
- 238000006467 substitution reaction Methods 0.000 description 37
- 108010047041 Complementarity Determining Regions Proteins 0.000 description 33
- 239000000243 solution Substances 0.000 description 33
- 229940124597 therapeutic agent Drugs 0.000 description 31
- 241000699670 Mus sp. Species 0.000 description 28
- 238000012217 deletion Methods 0.000 description 28
- 230000037430 deletion Effects 0.000 description 28
- 229920002527 Glycogen Polymers 0.000 description 26
- 239000012634 fragment Substances 0.000 description 26
- 229940096919 glycogen Drugs 0.000 description 26
- 230000000694 effects Effects 0.000 description 24
- 239000013604 expression vector Substances 0.000 description 24
- 108020004414 DNA Proteins 0.000 description 23
- 239000012228 culture supernatant Substances 0.000 description 22
- 102000006496 Immunoglobulin Heavy Chains Human genes 0.000 description 21
- 108010019476 Immunoglobulin Heavy Chains Proteins 0.000 description 21
- 239000000427 antigen Substances 0.000 description 21
- 102000036639 antigens Human genes 0.000 description 21
- 108091007433 antigens Proteins 0.000 description 21
- 102000013463 Immunoglobulin Light Chains Human genes 0.000 description 19
- 108010065825 Immunoglobulin Light Chains Proteins 0.000 description 19
- 229920001223 polyethylene glycol Polymers 0.000 description 19
- 239000013598 vector Substances 0.000 description 19
- 210000004408 hybridoma Anatomy 0.000 description 18
- 241000282693 Cercopithecidae Species 0.000 description 17
- 241000124008 Mammalia Species 0.000 description 17
- 230000006870 function Effects 0.000 description 15
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 14
- 108050003222 Transferrin receptor protein 1 Proteins 0.000 description 14
- 239000002609 medium Substances 0.000 description 14
- 101000835093 Homo sapiens Transferrin receptor protein 1 Proteins 0.000 description 13
- 239000002299 complementary DNA Substances 0.000 description 13
- 230000000717 retained effect Effects 0.000 description 13
- 239000000872 buffer Substances 0.000 description 12
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 12
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 12
- 238000010494 dissociation reaction Methods 0.000 description 12
- 230000005593 dissociations Effects 0.000 description 12
- 238000005259 measurement Methods 0.000 description 12
- 238000007792 addition Methods 0.000 description 11
- 210000004962 mammalian cell Anatomy 0.000 description 11
- 201000010099 disease Diseases 0.000 description 10
- 230000003053 immunization Effects 0.000 description 10
- 238000002360 preparation method Methods 0.000 description 10
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 9
- NBSCHQHZLSJFNQ-QTVWNMPRSA-N D-Mannose-6-phosphate Chemical compound OC1O[C@H](COP(O)(O)=O)[C@@H](O)[C@H](O)[C@@H]1O NBSCHQHZLSJFNQ-QTVWNMPRSA-N 0.000 description 9
- 241001465754 Metazoa Species 0.000 description 9
- 241000700159 Rattus Species 0.000 description 9
- 238000002641 enzyme replacement therapy Methods 0.000 description 9
- 230000014509 gene expression Effects 0.000 description 9
- 239000007788 liquid Substances 0.000 description 9
- 239000012488 sample solution Substances 0.000 description 9
- 208000024891 symptom Diseases 0.000 description 9
- 241000588724 Escherichia coli Species 0.000 description 8
- 102000004547 Glucosylceramidase Human genes 0.000 description 8
- 108010017544 Glucosylceramidase Proteins 0.000 description 8
- 241000283973 Oryctolagus cuniculus Species 0.000 description 8
- 108010039203 Tripeptidyl-Peptidase 1 Proteins 0.000 description 8
- 102100034197 Tripeptidyl-peptidase 1 Human genes 0.000 description 8
- 230000006229 amino acid addition Effects 0.000 description 8
- -1 aspartyl Chemical group 0.000 description 8
- 108010030074 endodeoxyribonuclease MluI Proteins 0.000 description 8
- 239000000523 sample Substances 0.000 description 8
- 239000000126 substance Substances 0.000 description 8
- 102000016679 alpha-Glucosidases Human genes 0.000 description 7
- 238000011088 calibration curve Methods 0.000 description 7
- 238000012258 culturing Methods 0.000 description 7
- 238000002649 immunization Methods 0.000 description 7
- 238000001727 in vivo Methods 0.000 description 7
- 239000002245 particle Substances 0.000 description 7
- 102000004196 processed proteins & peptides Human genes 0.000 description 7
- 239000011780 sodium chloride Substances 0.000 description 7
- 238000012360 testing method Methods 0.000 description 7
- 238000005406 washing Methods 0.000 description 7
- 102000006772 Acid Ceramidase Human genes 0.000 description 6
- 108020005296 Acid Ceramidase Proteins 0.000 description 6
- 102100034561 Alpha-N-acetylglucosaminidase Human genes 0.000 description 6
- 102100028496 Galactocerebrosidase Human genes 0.000 description 6
- 108010042681 Galactosylceramidase Proteins 0.000 description 6
- 102000005327 Palmitoyl protein thioesterase Human genes 0.000 description 6
- 108020002591 Palmitoyl protein thioesterase Proteins 0.000 description 6
- 108010012864 alpha-Mannosidase Proteins 0.000 description 6
- 102000019199 alpha-Mannosidase Human genes 0.000 description 6
- 108010009380 alpha-N-acetyl-D-glucosaminidase Proteins 0.000 description 6
- 238000006243 chemical reaction Methods 0.000 description 6
- 238000005516 engineering process Methods 0.000 description 6
- 210000000987 immune system Anatomy 0.000 description 6
- 210000003712 lysosome Anatomy 0.000 description 6
- 102000005962 receptors Human genes 0.000 description 6
- 108020003175 receptors Proteins 0.000 description 6
- 239000000758 substrate Substances 0.000 description 6
- HKZAAJSTFUZYTO-LURJTMIESA-N (2s)-2-[[2-[[2-[[2-[(2-aminoacetyl)amino]acetyl]amino]acetyl]amino]acetyl]amino]-3-hydroxypropanoic acid Chemical compound NCC(=O)NCC(=O)NCC(=O)NCC(=O)N[C@@H](CO)C(O)=O HKZAAJSTFUZYTO-LURJTMIESA-N 0.000 description 5
- 108010023546 Aspartylglucosylaminase Proteins 0.000 description 5
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 5
- 241000282412 Homo Species 0.000 description 5
- 101000766306 Homo sapiens Serotransferrin Proteins 0.000 description 5
- 108060003951 Immunoglobulin Proteins 0.000 description 5
- 102100021003 N(4)-(beta-N-acetylglucosaminyl)-L-asparaginase Human genes 0.000 description 5
- 108010061312 Sphingomyelin Phosphodiesterase Proteins 0.000 description 5
- 239000007983 Tris buffer Substances 0.000 description 5
- 102000010126 acid sphingomyelin phosphodiesterase activity proteins Human genes 0.000 description 5
- 230000007812 deficiency Effects 0.000 description 5
- 102000018358 immunoglobulin Human genes 0.000 description 5
- 230000001965 increasing effect Effects 0.000 description 5
- 230000001868 lysosomic effect Effects 0.000 description 5
- 239000000203 mixture Substances 0.000 description 5
- XNSAINXGIQZQOO-SRVKXCTJSA-N protirelin Chemical compound NC(=O)[C@@H]1CCCN1C(=O)[C@@H](NC(=O)[C@H]1NC(=O)CC1)CC1=CN=CN1 XNSAINXGIQZQOO-SRVKXCTJSA-N 0.000 description 5
- 210000002363 skeletal muscle cell Anatomy 0.000 description 5
- 241000894007 species Species 0.000 description 5
- 238000011282 treatment Methods 0.000 description 5
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 5
- 238000002965 ELISA Methods 0.000 description 4
- 241000283086 Equidae Species 0.000 description 4
- 208000015872 Gaucher disease Diseases 0.000 description 4
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 4
- 208000010428 Muscle Weakness Diseases 0.000 description 4
- 206010028372 Muscular weakness Diseases 0.000 description 4
- 229930193140 Neomycin Natural products 0.000 description 4
- 102000005348 Neuraminidase Human genes 0.000 description 4
- 108010006232 Neuraminidase Proteins 0.000 description 4
- 208000002537 Neuronal Ceroid-Lipofuscinoses Diseases 0.000 description 4
- 102000010292 Peptide Elongation Factor 1 Human genes 0.000 description 4
- 108010077524 Peptide Elongation Factor 1 Proteins 0.000 description 4
- 206010035226 Plasma cell myeloma Diseases 0.000 description 4
- 229920001213 Polysorbate 20 Polymers 0.000 description 4
- 241000288906 Primates Species 0.000 description 4
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 4
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 4
- 230000002378 acidificating effect Effects 0.000 description 4
- 239000011324 bead Substances 0.000 description 4
- 230000000903 blocking effect Effects 0.000 description 4
- 210000004413 cardiac myocyte Anatomy 0.000 description 4
- 239000008103 glucose Substances 0.000 description 4
- 230000007062 hydrolysis Effects 0.000 description 4
- 238000006460 hydrolysis reaction Methods 0.000 description 4
- 238000000338 in vitro Methods 0.000 description 4
- 230000007721 medicinal effect Effects 0.000 description 4
- SXTAYKAGBXMACB-UHFFFAOYSA-N methionine sulfoximine Chemical compound CS(=N)(=O)CCC(N)C(O)=O SXTAYKAGBXMACB-UHFFFAOYSA-N 0.000 description 4
- 201000000050 myeloid neoplasm Diseases 0.000 description 4
- 229960004927 neomycin Drugs 0.000 description 4
- 201000007642 neuronal ceroid lipofuscinosis 1 Diseases 0.000 description 4
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 4
- COLNVLDHVKWLRT-QMMMGPOBSA-N phenylalanine group Chemical group N[C@@H](CC1=CC=CC=C1)C(=O)O COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 4
- 239000002504 physiological saline solution Substances 0.000 description 4
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 4
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 4
- 238000005215 recombination Methods 0.000 description 4
- 210000000952 spleen Anatomy 0.000 description 4
- 239000003381 stabilizer Substances 0.000 description 4
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 3
- 102100035028 Alpha-L-iduronidase Human genes 0.000 description 3
- 102100031317 Alpha-N-acetylgalactosaminidase Human genes 0.000 description 3
- 102100026189 Beta-galactosidase Human genes 0.000 description 3
- 102100026031 Beta-glucuronidase Human genes 0.000 description 3
- 101710124976 Beta-hexosaminidase A Proteins 0.000 description 3
- 101710124978 Beta-hexosaminidase B Proteins 0.000 description 3
- 102100032487 Beta-mannosidase Human genes 0.000 description 3
- 208000004652 Cardiovascular Abnormalities Diseases 0.000 description 3
- YQYJSBFKSSDGFO-UHFFFAOYSA-N Epihygromycin Natural products OC1C(O)C(C(=O)C)OC1OC(C(=C1)O)=CC=C1C=C(C)C(=O)NC1C(O)C(O)C2OCOC2C1O YQYJSBFKSSDGFO-UHFFFAOYSA-N 0.000 description 3
- 102000053187 Glucuronidase Human genes 0.000 description 3
- 108010060309 Glucuronidase Proteins 0.000 description 3
- 101001019502 Homo sapiens Alpha-L-iduronidase Proteins 0.000 description 3
- 101000933465 Homo sapiens Beta-glucuronidase Proteins 0.000 description 3
- 101000893741 Homo sapiens Tissue alpha-L-fucosidase Proteins 0.000 description 3
- 101710199679 Hyaluronidase-1 Proteins 0.000 description 3
- 102100039283 Hyaluronidase-1 Human genes 0.000 description 3
- 108010003381 Iduronidase Proteins 0.000 description 3
- 102000004627 Iduronidase Human genes 0.000 description 3
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 3
- 241000282567 Macaca fascicularis Species 0.000 description 3
- 108010023320 N-acetylglucosamine-6-sulfatase Proteins 0.000 description 3
- 108091028043 Nucleic acid sequence Proteins 0.000 description 3
- 102100025824 Palmitoyl-protein thioesterase 1 Human genes 0.000 description 3
- 102000003992 Peroxidases Human genes 0.000 description 3
- 239000002202 Polyethylene glycol Substances 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 108010076504 Protein Sorting Signals Proteins 0.000 description 3
- 102000017852 Saposin Human genes 0.000 description 3
- 108050007079 Saposin Proteins 0.000 description 3
- 102100040526 Tissue alpha-L-fucosidase Human genes 0.000 description 3
- 108010044965 UDP-N-acetylglucosamine-lysosomal-enzyme N-acetylglucosaminephosphotransferase Proteins 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 3
- 108010061314 alpha-L-Fucosidase Proteins 0.000 description 3
- 102000012086 alpha-L-Fucosidase Human genes 0.000 description 3
- 108010015684 alpha-N-Acetylgalactosaminidase Proteins 0.000 description 3
- 210000000628 antibody-producing cell Anatomy 0.000 description 3
- 108010005774 beta-Galactosidase Proteins 0.000 description 3
- 108010055059 beta-Mannosidase Proteins 0.000 description 3
- 238000012575 bio-layer interferometry Methods 0.000 description 3
- 238000004422 calculation algorithm Methods 0.000 description 3
- 230000000747 cardiac effect Effects 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 3
- 238000010276 construction Methods 0.000 description 3
- 230000004069 differentiation Effects 0.000 description 3
- 238000004520 electroporation Methods 0.000 description 3
- 125000000524 functional group Chemical group 0.000 description 3
- 230000002068 genetic effect Effects 0.000 description 3
- 108010054451 glucosamine acetyltransferase Proteins 0.000 description 3
- 108010089932 heparan sulfate sulfatase Proteins 0.000 description 3
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 3
- 239000007951 isotonicity adjuster Substances 0.000 description 3
- 238000012423 maintenance Methods 0.000 description 3
- 239000002736 nonionic surfactant Substances 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- 108040007629 peroxidase activity proteins Proteins 0.000 description 3
- 239000012264 purified product Substances 0.000 description 3
- 238000012207 quantitative assay Methods 0.000 description 3
- 238000012216 screening Methods 0.000 description 3
- 239000007790 solid phase Substances 0.000 description 3
- 210000004989 spleen cell Anatomy 0.000 description 3
- 230000008685 targeting Effects 0.000 description 3
- HFQKBOPMAOTAIR-TZSVBWBLSA-N α-d-galactosyl-(1->4)-β-d-galactosyl-(1->4)-β-d-glucosylceramide Chemical compound O[C@@H]1[C@@H](O)[C@H](OC[C@@H]([C@H](O)/C=C/CCCCCCCCCCCCC)NC(C)=O)O[C@H](CO)[C@H]1O[C@H]1[C@H](O)[C@@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO)O2)O)[C@@H](CO)O1 HFQKBOPMAOTAIR-TZSVBWBLSA-N 0.000 description 3
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 2
- GOJUJUVQIVIZAV-UHFFFAOYSA-N 2-amino-4,6-dichloropyrimidine-5-carbaldehyde Chemical group NC1=NC(Cl)=C(C=O)C(Cl)=N1 GOJUJUVQIVIZAV-UHFFFAOYSA-N 0.000 description 2
- 102100040894 Amylo-alpha-1,6-glucosidase Human genes 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- 241000282472 Canis lupus familiaris Species 0.000 description 2
- 241000283707 Capra Species 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 108020004705 Codon Proteins 0.000 description 2
- 241000699802 Cricetulus griseus Species 0.000 description 2
- WQZGKKKJIJFFOK-QTVWNMPRSA-N D-mannopyranose Chemical compound OC[C@H]1OC(O)[C@@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-QTVWNMPRSA-N 0.000 description 2
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 2
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 2
- 241000283073 Equus caballus Species 0.000 description 2
- 241000282326 Felis catus Species 0.000 description 2
- 102000004366 Glucosidases Human genes 0.000 description 2
- 108010056771 Glucosidases Proteins 0.000 description 2
- 101000574223 Homo sapiens Palmitoyl-protein thioesterase 1 Proteins 0.000 description 2
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 2
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 2
- 102000000853 LDL receptors Human genes 0.000 description 2
- 108010001831 LDL receptors Proteins 0.000 description 2
- 102000018697 Membrane Proteins Human genes 0.000 description 2
- 108010052285 Membrane Proteins Proteins 0.000 description 2
- 201000011442 Metachromatic leukodystrophy Diseases 0.000 description 2
- 101100236308 Mus musculus Gaa gene Proteins 0.000 description 2
- 239000012124 Opti-MEM Substances 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- RVGRUAULSDPKGF-UHFFFAOYSA-N Poloxamer Chemical compound C1CO1.CC1CO1 RVGRUAULSDPKGF-UHFFFAOYSA-N 0.000 description 2
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 2
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 2
- 208000021811 Sandhoff disease Diseases 0.000 description 2
- 206010047295 Ventricular hypertrophy Diseases 0.000 description 2
- 230000003213 activating effect Effects 0.000 description 2
- 150000001408 amides Chemical class 0.000 description 2
- 108010006759 amylo-1,6-glucosidase Proteins 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 210000004556 brain Anatomy 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 239000006285 cell suspension Substances 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 239000003638 chemical reducing agent Substances 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 208000035475 disorder Diseases 0.000 description 2
- 210000002257 embryonic structure Anatomy 0.000 description 2
- 210000003527 eukaryotic cell Anatomy 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 239000012894 fetal calf serum Substances 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- 125000005842 heteroatom Chemical group 0.000 description 2
- 230000006801 homologous recombination Effects 0.000 description 2
- 238000002744 homologous recombination Methods 0.000 description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 2
- 230000009545 invasion Effects 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 108020004999 messenger RNA Proteins 0.000 description 2
- 150000004712 monophosphates Chemical class 0.000 description 2
- 201000002273 mucopolysaccharidosis II Diseases 0.000 description 2
- 208000022018 mucopolysaccharidosis type 2 Diseases 0.000 description 2
- 210000000663 muscle cell Anatomy 0.000 description 2
- 210000000107 myocyte Anatomy 0.000 description 2
- 201000008051 neuronal ceroid lipofuscinosis Diseases 0.000 description 2
- 239000002773 nucleotide Substances 0.000 description 2
- 125000003729 nucleotide group Chemical group 0.000 description 2
- 230000002093 peripheral effect Effects 0.000 description 2
- 230000004962 physiological condition Effects 0.000 description 2
- 239000013612 plasmid Substances 0.000 description 2
- 229920001983 poloxamer Polymers 0.000 description 2
- 229960000502 poloxamer Drugs 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 229920001184 polypeptide Polymers 0.000 description 2
- 229920001451 polypropylene glycol Polymers 0.000 description 2
- 229920000136 polysorbate Polymers 0.000 description 2
- 229950008882 polysorbate Drugs 0.000 description 2
- 229940071643 prefilled syringe Drugs 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 210000001236 prokaryotic cell Anatomy 0.000 description 2
- RXWNCPJZOCPEPQ-NVWDDTSBSA-N puromycin Chemical compound C1=CC(OC)=CC=C1C[C@H](N)C(=O)N[C@H]1[C@@H](O)[C@H](N2C3=NC=NC(=C3N=C2)N(C)C)O[C@@H]1CO RXWNCPJZOCPEPQ-NVWDDTSBSA-N 0.000 description 2
- 210000003314 quadriceps muscle Anatomy 0.000 description 2
- 230000006798 recombination Effects 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- 239000012064 sodium phosphate buffer Substances 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 239000013589 supplement Substances 0.000 description 2
- 208000011580 syndromic disease Diseases 0.000 description 2
- 239000012581 transferrin Substances 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 1
- GEYOCULIXLDCMW-UHFFFAOYSA-N 1,2-phenylenediamine Chemical compound NC1=CC=CC=C1N GEYOCULIXLDCMW-UHFFFAOYSA-N 0.000 description 1
- IEJPPSMHUUQABK-UHFFFAOYSA-N 2,4-diphenyl-4h-1,3-oxazol-5-one Chemical compound O=C1OC(C=2C=CC=CC=2)=NC1C1=CC=CC=C1 IEJPPSMHUUQABK-UHFFFAOYSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- IVLXQGJVBGMLRR-UHFFFAOYSA-N 2-aminoacetic acid;hydron;chloride Chemical compound Cl.NCC(O)=O IVLXQGJVBGMLRR-UHFFFAOYSA-N 0.000 description 1
- 208000029602 Alpha-N-acetylgalactosaminidase deficiency Diseases 0.000 description 1
- 208000031277 Amaurotic familial idiocy Diseases 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 238000009020 BCA Protein Assay Kit Methods 0.000 description 1
- 102100022548 Beta-hexosaminidase subunit alpha Human genes 0.000 description 1
- 208000020446 Cardiac disease Diseases 0.000 description 1
- 206010007572 Cardiac hypertrophy Diseases 0.000 description 1
- 208000006029 Cardiomegaly Diseases 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- 229920002101 Chitin Polymers 0.000 description 1
- 241000701022 Cytomegalovirus Species 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- 206010059866 Drug resistance Diseases 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- CTKXFMQHOOWWEB-UHFFFAOYSA-N Ethylene oxide/propylene oxide copolymer Chemical compound CCCOC(C)COCCO CTKXFMQHOOWWEB-UHFFFAOYSA-N 0.000 description 1
- 208000001948 Farber Lipogranulomatosis Diseases 0.000 description 1
- 208000033149 Farber disease Diseases 0.000 description 1
- 238000009017 Fluorometric Assay Kit Methods 0.000 description 1
- 101150115151 GAA gene Proteins 0.000 description 1
- 201000008393 GM1 gangliosidosis type 1 Diseases 0.000 description 1
- 208000001905 GM2 Gangliosidoses Diseases 0.000 description 1
- 201000008905 GM2 gangliosidosis Diseases 0.000 description 1
- 208000010055 Globoid Cell Leukodystrophy Diseases 0.000 description 1
- 229930186217 Glycolipid Natural products 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 101001045440 Homo sapiens Beta-hexosaminidase subunit alpha Proteins 0.000 description 1
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 1
- 108700037017 Hyaluronidase Deficiency Proteins 0.000 description 1
- 208000005503 Hyaluronidase deficiency Diseases 0.000 description 1
- 208000011200 Kawasaki disease Diseases 0.000 description 1
- 208000028226 Krabbe disease Diseases 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 108010031099 Mannose Receptor Proteins 0.000 description 1
- 208000008955 Mucolipidoses Diseases 0.000 description 1
- 206010072928 Mucolipidosis type II Diseases 0.000 description 1
- 206010056893 Mucopolysaccharidosis VII Diseases 0.000 description 1
- 208000029578 Muscle disease Diseases 0.000 description 1
- 208000010316 Myotonia congenita Diseases 0.000 description 1
- 208000014060 Niemann-Pick disease Diseases 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 241000269908 Platichthys flesus Species 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 229940124158 Protease/peptidase inhibitor Drugs 0.000 description 1
- 101710130181 Protochlorophyllide reductase A, chloroplastic Proteins 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 208000001647 Renal Insufficiency Diseases 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 201000001828 Sly syndrome Diseases 0.000 description 1
- 238000002105 Southern blotting Methods 0.000 description 1
- 101710120037 Toxin CcdB Proteins 0.000 description 1
- 108700001567 Type I Schindler Disease Proteins 0.000 description 1
- 102000044159 Ubiquitin Human genes 0.000 description 1
- 108090000848 Ubiquitin Proteins 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 108010056760 agalsidase beta Proteins 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 125000003172 aldehyde group Chemical group 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- 201000008333 alpha-mannosidosis Diseases 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 201000006486 beta-mannosidosis Diseases 0.000 description 1
- 230000000975 bioactive effect Effects 0.000 description 1
- 229920002988 biodegradable polymer Polymers 0.000 description 1
- 239000004621 biodegradable polymer Substances 0.000 description 1
- 229960000074 biopharmaceutical Drugs 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 229960002685 biotin Drugs 0.000 description 1
- 235000020958 biotin Nutrition 0.000 description 1
- 239000011616 biotin Substances 0.000 description 1
- 125000005340 bisphosphate group Chemical group 0.000 description 1
- 230000008499 blood brain barrier function Effects 0.000 description 1
- 210000001218 blood-brain barrier Anatomy 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- 210000000234 capsid Anatomy 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 125000005587 carbonate group Chemical group 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical group 0.000 description 1
- 230000003683 cardiac damage Effects 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000007910 cell fusion Effects 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000010307 cell transformation Effects 0.000 description 1
- 210000001638 cerebellum Anatomy 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 238000007398 colorimetric assay Methods 0.000 description 1
- 238000004040 coloring Methods 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 201000011474 congenital myopathy Diseases 0.000 description 1
- 230000021615 conjugation Effects 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000000593 degrading effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 239000000539 dimer Substances 0.000 description 1
- 230000002526 effect on cardiovascular system Effects 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- CEIPQQODRKXDSB-UHFFFAOYSA-N ethyl 3-(6-hydroxynaphthalen-2-yl)-1H-indazole-5-carboximidate dihydrochloride Chemical compound Cl.Cl.C1=C(O)C=CC2=CC(C3=NNC4=CC=C(C=C43)C(=N)OCC)=CC=C21 CEIPQQODRKXDSB-UHFFFAOYSA-N 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 229940014516 fabrazyme Drugs 0.000 description 1
- 201000008049 fucosidosis Diseases 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 150000002402 hexoses Chemical group 0.000 description 1
- 230000000971 hippocampal effect Effects 0.000 description 1
- 229920002674 hyaluronan Polymers 0.000 description 1
- 229960003160 hyaluronic acid Drugs 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- LFKYBJLFJOOKAE-UHFFFAOYSA-N imidazol-2-ylidenemethanone Chemical group O=C=C1N=CC=N1 LFKYBJLFJOOKAE-UHFFFAOYSA-N 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 208000017482 infantile neuronal ceroid lipofuscinosis Diseases 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 238000012482 interaction analysis Methods 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 239000012948 isocyanate Substances 0.000 description 1
- 150000002513 isocyanates Chemical class 0.000 description 1
- 150000002540 isothiocyanates Chemical class 0.000 description 1
- 201000006370 kidney failure Diseases 0.000 description 1
- 238000012933 kinetic analysis Methods 0.000 description 1
- 208000025014 late infantile neuronal ceroid lipofuscinosis Diseases 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 210000001161 mammalian embryo Anatomy 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 230000013011 mating Effects 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 210000004115 mitral valve Anatomy 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 238000009126 molecular therapy Methods 0.000 description 1
- 210000000865 mononuclear phagocyte system Anatomy 0.000 description 1
- 230000008111 motor development Effects 0.000 description 1
- 208000001725 mucocutaneous lymph node syndrome Diseases 0.000 description 1
- 208000020460 mucolipidosis II alpha/beta Diseases 0.000 description 1
- 208000005340 mucopolysaccharidosis III Diseases 0.000 description 1
- 208000011045 mucopolysaccharidosis type 3 Diseases 0.000 description 1
- 208000025919 mucopolysaccharidosis type 7 Diseases 0.000 description 1
- 208000016334 muscle symptom Diseases 0.000 description 1
- 239000003471 mutagenic agent Substances 0.000 description 1
- 231100000707 mutagenic chemical Toxicity 0.000 description 1
- 230000003505 mutagenic effect Effects 0.000 description 1
- 229940103023 myozyme Drugs 0.000 description 1
- 210000002569 neuron Anatomy 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 1
- 210000005259 peripheral blood Anatomy 0.000 description 1
- 239000011886 peripheral blood Substances 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 239000007981 phosphate-citrate buffer Substances 0.000 description 1
- 229920001993 poloxamer 188 Polymers 0.000 description 1
- 229940044519 poloxamer 188 Drugs 0.000 description 1
- 229920001583 poly(oxyethylated polyols) Polymers 0.000 description 1
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 description 1
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 229940068977 polysorbate 20 Drugs 0.000 description 1
- 229920000053 polysorbate 80 Polymers 0.000 description 1
- 229940068968 polysorbate 80 Drugs 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 229920001289 polyvinyl ether Polymers 0.000 description 1
- 238000004393 prognosis Methods 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 230000000644 propagated effect Effects 0.000 description 1
- 210000000449 purkinje cell Anatomy 0.000 description 1
- 229950010131 puromycin Drugs 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 238000013207 serial dilution Methods 0.000 description 1
- 239000001488 sodium phosphate Substances 0.000 description 1
- 229910000162 sodium phosphate Inorganic materials 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 239000012089 stop solution Substances 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 210000003523 substantia nigra Anatomy 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 230000009469 supplementation Effects 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 229940126585 therapeutic drug Drugs 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 230000001131 transforming effect Effects 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 239000013638 trimer Substances 0.000 description 1
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 1
- 210000003462 vein Anatomy 0.000 description 1
- 239000008215 water for injection Substances 0.000 description 1
- 210000005253 yeast cell Anatomy 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/6811—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a protein or peptide, e.g. transferrin or bleomycin
- A61K47/6815—Enzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y302/00—Hydrolases acting on glycosyl compounds, i.e. glycosylases (3.2)
- C12Y302/01—Glycosidases, i.e. enzymes hydrolysing O- and S-glycosyl compounds (3.2.1)
- C12Y302/01022—Alpha-galactosidase (3.2.1.22)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/46—Hydrolases (3)
- A61K38/47—Hydrolases (3) acting on glycosyl compounds (3.2), e.g. cellulases, lactases
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/65—Peptidic linkers, binders or spacers, e.g. peptidic enzyme-labile linkers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6849—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a receptor, a cell surface antigen or a cell surface determinant
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2881—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against CD71
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K19/00—Hybrid peptides, i.e. peptides covalently bound to nucleic acids, or non-covalently bound protein-protein complexes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/62—DNA sequences coding for fusion proteins
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/24—Hydrolases (3) acting on glycosyl compounds (3.2)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/10—Immunoglobulins specific features characterized by their source of isolation or production
- C07K2317/14—Specific host cells or culture conditions, e.g. components, pH or temperature
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/33—Crossreactivity, e.g. for species or epitope, or lack of said crossreactivity
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/77—Internalization into the cell
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/33—Fusion polypeptide fusions for targeting to specific cell types, e.g. tissue specific targeting, targeting of a bacterial subspecies
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Genetics & Genomics (AREA)
- Epidemiology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Gastroenterology & Hepatology (AREA)
- General Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biomedical Technology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Microbiology (AREA)
- General Chemical & Material Sciences (AREA)
- Neurology (AREA)
- Biotechnology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Cell Biology (AREA)
- Mycology (AREA)
- Physics & Mathematics (AREA)
- Endocrinology (AREA)
- Plant Pathology (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
Abstract
Description
1.抗ヒトトランスフェリン受容体抗体と薬剤との結合体であって,該薬剤が筋肉において機能を発揮させるべき生理活性を有するものである,結合体。
2.該抗ヒトトランスフェリン受容体抗体が,Fab抗体,F(ab’)2抗体,又はF(ab’)抗体である,上記1に記載の結合体。
3.該抗ヒトトランスフェリン受容体抗体が,scFab,scF(ab’),scF(ab’)2及びscFvからなる群から選ばれる一本鎖抗体である,上記1に記載の結合体。
4.該一本鎖抗体が,該抗ヒトトランスフェリン受容体抗体の軽鎖と重鎖とをリンカー配列を介して結合させたものである,上記3に記載の結合体。
5.該抗ヒトトランスフェリン受容体抗体の軽鎖と重鎖とを,該軽鎖のC末端側において,該リンカー配列を介して結合させたものである,上記4に記載の結合体。
6.該抗ヒトトランスフェリン受容体抗体の軽鎖と重鎖とを,該重鎖のC末端側において,該リンカー配列を介して結合させたものである,上記4に記載の結合体。
7.該リンカー配列が,8〜50個のアミノ酸残基からなるものである,上記4〜6の何れかに記載の結合体。
8.該リンカー配列が,アミノ酸配列(Gly Ser),アミノ酸配列(Gly Gly Ser),アミノ酸配列(Gly Gly Gly),配列番号3,及び配列番号4で示されるものからなる群から選択されるアミノ酸配列を含んでなるものである,上記7に記載の結合体。
9.該リンカー配列が,配列番号4で示されるアミノ酸配列が3回連続する15個のアミノ酸残基からなるものである,上記8に記載の結合体。
10.該抗ヒトトランスフェリン受容体抗体が,軽鎖の可変領域に配列番号22で示されるアミノ酸配列を含むものであり,重鎖の可変領域に配列番号23で示されるアミノ酸配列を含むものである,上記1〜9の何れかに記載の結合体。
11.該軽鎖の可変領域のアミノ酸配列が,配列番号22で示されるアミノ酸配列と80%以上の相同性を有するものであり,該重鎖の可変領域のアミノ酸配列が,配列番号23で示されるアミノ酸配列と80%以上の相同性を有するものである,上記10に記載の結合体。
12.該軽鎖の可変領域のアミノ酸配列が,配列番号22で示されるアミノ酸配列と90%以上の相同性を有するものであり,該重鎖の可変領域のアミノ酸配列が,配列番号23で示されるアミノ酸配列と90%以上の相同性を有するものである,上記10に記載の結合体。
13.該軽鎖の可変領域のアミノ酸配列が,配列番号22で示されるアミノ酸配列を構成する1〜10個のアミノ酸が,他のアミノ酸に置換されたものである,上記10に記載の結合体。
14.該軽鎖の可変領域のアミノ酸配列が,配列番号22で示されるアミノ酸配列を構成する1〜3個のアミノ酸が,他のアミノ酸に置換されたものである,上記10に記載の結合体。
15.該重鎖の可変領域のアミノ酸配列が,配列番号23で示されるアミノ酸配列を構成する1〜10個のアミノ酸が,他のアミノ酸に置換されたものである,上記10に記載の結合体。
16.該重鎖の可変領域のアミノ酸配列が,配列番号23で示されるアミノ酸配列を構成する1〜3個のアミノ酸が,他のアミノ酸に置換されたものである,上記10に記載の結合体。
17.該軽鎖の可変領域のアミノ酸配列が,配列番号22で示されるアミノ酸配列を構成する1〜10個のアミノ酸が,他のアミノ酸に置換されたものであり,該重鎖の可変領域のアミノ酸配列が,配列番号23で示されるアミノ酸配列を構成する1〜10個のアミノ酸が,他のアミノ酸に置換されたものである,上記10に記載の結合体。
18.該軽鎖の可変領域のアミノ酸配列が,配列番号22で示されるアミノ酸配列を構成する1〜3個のアミノ酸が,他のアミノ酸に置換されたものであり,該重鎖の可変領域のアミノ酸配列が,配列番号23で示されるアミノ酸配列を構成する1〜3個のアミノ酸が,他のアミノ酸に置換されたものである,上記10に記載の結合体。
19.該抗ヒトトランスフェリン受容体抗体が,軽鎖に配列番号24で示されるアミノ酸配列を含むものであり,重鎖に配列番号25で示されるアミノ酸配列を含むものである,上記10に記載の結合体。
20.該軽鎖のアミノ酸配列が,配列番号24で示されるアミノ酸配列と80%以上の相同性を有するものであり,該重鎖のアミノ酸配列が,配列番号25で示されるアミノ酸配列と80%以上の相同性を有するものである,上記19に記載の結合体。
21.該軽鎖のアミノ酸配列が,配列番号24で示されるアミノ酸配列と90%以上の相同性を有するものであり,該重鎖のアミノ酸配列が,配列番号25で示されるアミノ酸配列と90%以上の相同性を有するものである,上記19に記載の結合体。
22.薬剤がペプチド又は蛋白質である,上記1〜21の何れかに記載の結合体。
23.上記22の結合体であって,以下の(1)〜(4)からなる群から選択されるもの,
(1)該蛋白質が,該抗ヒトトランスフェリン受容体抗体の軽鎖のC末端側にペプチド結合により結合したもの,
(2)該蛋白質が,該抗ヒトトランスフェリン受容体抗体の軽鎖のN末端側にペプチド結合により結合したもの,
(3)該蛋白質が,該抗ヒトトランスフェリン受容体抗体の重鎖のC末端側にペプチド結合により結合したもの,及び
(4)該蛋白質が,該抗ヒトトランスフェリン受容体抗体の重鎖のN末端側にペプチド結合により結合したもの。
24.該蛋白質が,該抗ヒトトランスフェリン受容体抗体に,リンカー配列を介して結合したものである,上記23に記載の結合体。
25.該リンカー配列が,1〜50個のアミノ酸残基からなるものである,上記24に記載の結合体。
26.該リンカー配列が,1個のグリシン,1個のセリン,アミノ酸配列(Gly Ser),アミノ酸配列(Gly Gly Ser),配列番号3のアミノ酸配列,配列番号4のアミノ酸配列,及びこれらのアミノ酸配列が1〜10個連続してなるアミノ酸配列からなる群より選ばれるアミノ酸配列を含んでなるものである,上記25に記載の結合体。
27.該抗ヒトトランスフェリン受容体抗体がヒト化抗ヒトトランスフェリン受容体抗体である,上記1〜28の何れかの結合体。
28.該蛋白質が,リソソーム酵素である,上記22〜27の何れかに記載の結合体。
29.該リソソーム酵素が,ヒトα−ガラクトシダーゼAである,上記28に記載の結合体。
30.該ヒト化抗hTfR抗体の軽鎖が配列番号24のアミノ酸配列を含むものであり,該ヒト化抗hTfR抗体の重鎖がそのC末端側で,リンカー配列(Gly Ser)を介して,該ヒトα−ガラクトシダーゼAと結合しており,全体として配列番号29で示されるアミノ酸配列を含むものである,上記29に記載の結合体。
31.該リソソーム酵素がヒト酸性α-グルコシダーゼ,である,上記28に記載の結合体。
32.該ヒト化抗hTfR抗体の軽鎖が配列番号24のアミノ酸配列を含むものであり,該ヒト化抗hTfR抗体の重鎖がそのC末端側で,リンカー配列(Gly Ser)を介して,該ヒト酸性α-グルコシダーゼと結合しており,全体として配列番号27で示されるアミノ酸配列を含むものである,上記31に記載の結合体。
33.上記1〜32の何れかに記載の結合体を含有してなる,筋肉の機能を改善するための医薬組成物。
34.上記28に記載の結合体を含有してなる,リソソーム病に伴う筋肉の機能障害を改善するための,医薬組成物。
35.上記29又は30に記載の結合体を含有してなる,ファブリー病に伴う筋肉の機能障害を改善するための,医薬組成物。
36.上記31又は32に記載の結合体を含有してなる,ポンペ病に伴う筋肉の機能障害を改善するための,医薬組成物。
37.該筋肉が,骨格筋,心筋,又は平滑筋の何れかである,上記33〜36の何れかに記載の医薬組成物。
38.リソソーム病に伴う筋肉の機能障害を改善するための医薬組成物の製造のための,上記28〜32の何れかに記載の結合体の使用。
39.ファブリー病に伴う筋肉の機能障害を改善するための医薬組成物の製造のための,上記29又は30に記載の結合体の使用。
40.ポンペ病に伴う筋肉の機能障害を改善するための医薬組成物の製造のための,上記31又は32に記載の結合体の使用。
41.上記1〜32の何れかに記載の結合体の,筋肉の機能を改善するための医薬組成物としての使用。
42. 薬剤を筋肉に送達するための方法であって,該薬剤を抗ヒトトランスフェリン受容体抗体と結合させた結合体として製造するステップ,及び該結合体を個体に投与するステップことを含む,方法。
43.該結合体が,上記1〜32の何れかに記載の結合体である,請求項42に記載の方法。
44.該結合体の投与により該個体の筋肉の機能が改善されるステップを更に含む,上記42又は43に記載の方法。
45.該個体が,筋肉の機能障害を有するものである,上記42〜44の何れかに記載の方法。
46.該個体が,リソソーム病に伴う筋肉の機能障害を有するものである,上記42〜44の何れかに記載の方法。
47.該リソソーム病が,ファブリー病又はポンペ病である,上記46に記載の方法。
(1)1本の免疫グロブリン軽鎖と1本の免疫グロブリン重鎖の計2本のポリペプチド鎖からなるものや,以下に詳述するように,
(2)免疫グロブリン軽鎖のC末端側にリンカー配列を,そして更にそのC末端側に免疫グロブリン重鎖を結合させてなるものである一本鎖抗体,及び
(3)免疫グロブリン重鎖のC末端側にリンカー配列を,そして更にそのC末端側に免疫グロブリン軽鎖を結合させてなるものである一本鎖抗体も含まれる。また,
(4)本来の意味での抗体の基本構造からFc領域が欠失したものであるFab領域からなるもの及びFab領域とヒンジ部の全部若しくは一部とからなるもの(Fab,F(ab’)及びF(ab’)2を含む)も,
本発明における「抗体」に含まれる。
(5)上記(4)で示したFab,F(ab’)又はF(ab’)2を構成する軽鎖と重鎖を,リンカー配列を介して結合させて,それぞれ一本鎖抗体としたscFab,scF(ab’),及びscF(ab’)2も含まれる。ここで,scFab,scF(ab’),及びscF(ab’)2にあっては,軽鎖のC末端側にリンカー配列を,そして更にそのC末端側に重鎖を結合させてなるものでもよく,また,重鎖のC末端側にリンカー配列を,そして更にそのC末端側に軽鎖を結合させてなるものでもよい。更には,軽鎖の可変領域と重鎖の可変領域をリンカー配列を介して結合させて一本鎖抗体としたscFvも,本発明における抗体に含まれる。scFvにあっては,軽鎖の可変領域のC末端側にリンカー配列を,そして更にそのC末端側に重鎖の可変領域を結合させてなるものでもよく,また,重鎖の可変領域のC末端側にリンカー配列を,そして更にそのC末端側に軽鎖の可変領域を結合させてなるものでもよい。
ヒト脾臓Quick Clone cDNA(Clontech社)を鋳型として,プライマーhTfR5’(配列番号7)及びプライマーhTfR3’(配列番号8)を用いて,PCRによりヒトトランスフェリン受容体(hTfR)をコードする遺伝子断片を増幅させた。増幅させたhTfRをコードする遺伝子断片を,MluIとNotIで消化し,pCI-neoベクター(Promega社)のMluIとNotI間に挿入した。得られたベクターを,pCI-neo(hTfR)と名付けた。次いで,このベクターを,MluIとNotIで消化して,hTfRをコードする遺伝子断片を切り出し,国際公開公報(WO2012/063799)に記載された発現ベクターであるpE-mIRES-GS-puroのMluIとNotIの間に組み込むことにより,hTfR発現用ベクターであるpE-mIRES-GS-puro(hTfR)を構築した。
エレクトロポレーション法により,CHO-K1細胞にpE-mIRES-GS-puro(hTfR)を導入した後,メチオニンスルホキシミン(MSX)及びピューロマイシンを含むCD OptiCHOTM培地(Invitrogen社)を用いて細胞の選択培養を行い,組換えhTfR発現細胞を得た。この組換えhTfR発現細胞を培養して,組換えhTfRを調製した。
実施例2で調製した組換えhTfRを抗原として用いてマウスを免疫した。免疫は,マウスに抗原を静脈内投与又は腹腔内投与して行った。
最後に抗原を投与した日の約1週間後にマウスの脾臓を摘出してホモジナイズし,脾細胞を分離した。得られた脾細胞をマウスミエローマ細胞株(P3.X63.Ag8.653)とポリエチレングリコール法を用いて細胞融合させた。細胞融合終了後,(1 X)HATサプリメント(Life Technologies社)及び10% Ultra low IgGウシ胎児血清(Life Technologies社)を含むRPMI1640培地に細胞を懸濁させ,細胞懸濁液を96ウェルプレート20枚に200 μL/ウェルずつ分注した。炭酸ガス培養器(37℃,5% CO2)で細胞を10日間培養した後,各ウェルを顕微鏡下で観察し,単一のコロニーが存在するウェルを選択した。各ウェルの細胞がほぼコンフルエントになった時点で培養上清を回収し,これをハイブリドーマの培養上清として,以下のスクリーニングに供した。
組換えhTfR溶液(Sino Biologics社)を50 mM炭酸ナトリウム緩衝液(pH 9.5〜9.6)で希釈して5 μg/mLの濃度に調整し,これを固相溶液とした。固相溶液を,Nunc MaxiSorpTM flat-bottom 96ウェルプレート(基材:ポリスチレン, Nunc社)の各ウェルに50 μLずつ添加した後,プレートを室温で1時間静置し,組換えhTfRをプレートに吸着させて固定した。固相溶液を捨て,各ウェルを250 μLの洗浄液(PBS-T: 0.05% Tween20を含有するPBS)で3回洗浄した後,各ウェルにブロッキング液(1% BSAを含有するPBS)を200 μLずつ添加し,プレートを室温で1時間静置した。
実施例5で選択したクローン1株〜クローン14株の中から更にクローン株3を選択した。クローン株3のcDNAを調製し,このcDNAを鋳型として抗体の軽鎖及び重鎖をコードする遺伝子を増幅させた。増幅させた遺伝子の塩基配列を翻訳し,この細胞株の産生する抗hTfR抗体番号3の軽鎖及び重鎖の可変領域のアミノ酸配列を決定した。
抗hTfR抗体とヒトTfR及びサルTfRへの親和性の測定は,バイオレイヤー干渉法(BioLayer Interferometry:BLI)を用いた生体分子相互作用解析システムであるOctetRED96(ForteBio社, a division of Pall Corporation)を用いて実施した。バイオレイヤー干渉法の基本原理について,簡単に説明する。センサーチップ表面に固定された生体分子の層(レイヤー)に特定波長の光を投射したとき,生体分子のレイヤーと内部の参照となるレイヤーの二つの表面から光が反射され,光の干渉波が生じる。測定試料中の分子がセンサーチップ表面の生体分子に結合することにより,センサー先端のレイヤーの厚みが増加し,干渉波に波長シフトが生じる。この波長シフトの変化を測定することにより,センサーチップ表面に固定された生体分子に結合する分子数の定量及び速度論的解析をリアルタイムで行うことができる。測定は,概ねOctetRED96に添付の操作マニュアルに従って実施した。ヒトTfRとしては,N末端にヒスチジンタグが付加した,配列番号1に示されるアミノ酸配列の中でN末端側から89番目のシステイン残基からC末端のフェニルアラニンまでの,hTfRの細胞外領域のアミノ酸配列を有する組換えヒトTfR(rヒトTfR:Sino Biological社)を用いた。サルTfRとしては,N末端にヒスチジンタグが付加した,配列番号2に示されるアミノ酸配列の中でN末端側から89番目のシステイン残基からC末端のフェニルアラニンまでの,カニクイザルのTfRの細胞外領域のアミノ酸配列を有する組換えサルTfR(rサルTfR:Sino Biological社)を用いた。
抗hTfR抗体番号3の軽鎖及び重鎖の可変領域に含まれるアミノ酸配列のヒト化を試みた。そして,配列番号22に示されるアミノ酸配列を有するヒト化された軽鎖の可変領域と,配列番号23に示されるアミノ酸配列を有するヒト化された重鎖の可変領域を得た。更に,軽鎖については,可変領域に配列番号22に示されるアミノ酸配列を有する,配列番号24で示されるアミノ酸配列の軽鎖を得た。また,重鎖については,可変領域に配列番号23に示されるアミノ酸配列を有する,配列番号25で示されるアミノ酸配列の重鎖を得た。なお,配列番号25で示されるアミノ酸配列の重鎖はIgG4タイプのものである。こうして得られたヒト化抗hTfR抗体のヒトTfRとの解離定数(KD)を実施例7に記載の方法で測定した。その結果,ヒト化抗hTfR抗体のヒトTfRとの解離定数(KD)は1X10−12M以下であり,サルTfRとの解離定数(KD)は約1X10−9Mであった。これらの結果は,得られた抗hTfR抗体番号3のヒト化抗体が,ヒトTfRのみならずサルTfRとも高い親和性を有する抗体であることを示すものである。
配列番号24で示されるアミノ酸配列の軽鎖をコードするDNA断片(配列番号26)を合成した。このDNA断片は,5’側には,5’端から順にMluI配列と,分泌シグナルとして機能するリーダーペプチドをコードする配列とを有し,3’側にはNotI配列を有する。
pEF/myc/nucベクター(インビトロジェン社)を,KpnIとNcoIで消化し,EF-1αプロモーター及びその第一イントロンを含む領域を切り出し,これをT4 DNAポリメラーゼで平滑末端化処理した。pCI-neo(インビトロジェン社)を,BglII及びEcoRIで消化して,CMVのエンハンサー/プロモーター及びイントロンを含む領域を切除した後に,T4 DNAポリメラーゼで平滑末端化処理した。これに,上記のEF-1αプロモーター及びその第一イントロンを含む領域を挿入して,pE-neoベクターを構築した。pE-neoベクターを,SfiI及びBstXIで消化し,ネオマイシン耐性遺伝子を含む約1 kbpの領域を切除した。pcDNA3.1/Hygro(+)(インビトロジェン社)を鋳型にしてプライマーHyg−Sfi5’(配列番号30)及びプライマーHyg−BstX3’(配列番号31)を用いて,PCR反応によりハイグロマイシン遺伝子を増幅した。増幅したハイグロマイシン遺伝子を,SfiI及びBstXIで消化し,上記のネオマイシン耐性遺伝子を切除したpE-neoベクターに挿入して,pE-hygrベクターを構築した。
CHO細胞(CHO-K1:American Type Culture Collectionから入手)を,下記の方法により,GenePulser(Bio-Rad社)を用いて,実施例10で構築したpE-hygr(LC)及びpE-neo(HC-hGAA)で形質転換した。細胞の形質転換は概ね以下の方法で行った。5 X 105個のCHO-K1細胞をCD OptiCHOTM培地(Life Technologies社)を添加した3.5 cm培養ディッシュに播種し,37℃, 5% CO2の条件下で一晩培養した。培地をOpti-MEMTM I培地(Life Technologies社)に交換し,細胞を5 X 106細胞/mLの密度となるように懸濁した。細胞懸濁液100 μLを採取し,これにOpti-MEMTM I培地で100 μg/mLに希釈したpE-hygr(LC1)及びpE-neo(HC1)プラスミドDNA溶液を5 μLずつ添加した。GenePulser(Bio-Rad社)を用いて,エレクトロポレーションを実施し,細胞にプラスミドを導入した。細胞を,37℃, 5% CO2の条件下で一晩培養した後,0.5 mg/mLのハイグロマイシン及び0.8 mg/mLのG418を添加したCD OptiCHOTM培地で選択培養した。
hGAA-抗hTfR抗体を,以下の方法で製造した。実施例11で得たhGAA-抗hTfR抗体高発現株を,細胞濃度が約2 X 105個/mLとなるように,CD OptiCHOTM培地で希釈し,1 Lの三角フラスコに200 mLの細胞懸濁液を加え,37℃で,5% CO2と95% 空気からなる湿潤環境で約70 rpmの撹拌速度で6〜7日間培養した。培養上清を遠心操作により回収し,0.22 μmフィルター(Millipore社)でろ過して,培養上清とした。回収した培養上清に,カラム体積の5倍容の150 mL NaClを含む20 mM Tris緩衝液(pH 8.0)を添加し,カラム体積の3倍容の150 mM NaClを含む20 mM Tris緩衝液(pH 8.0)で予め平衡化しておいたProtein Aカラム(カラム体積:1 mL,Bio-Rad社)に負荷した。次いで,カラム体積の5倍容の同緩衝液を供給してカラムを洗浄した後,150 mM NaClを含むカラム体積の4倍容の50 mM グリシン緩衝液(pH 2.8)で,吸着したhGAA−抗hTfR抗体を溶出させた。このhGAA−抗hTfR抗体を含む溶出液のpHを1 M Tris緩衝液(pH 8.0)を添加してpH 7.0に調整し,次いでアミコンウルトラ30kDa膜(Millipore社)を用いてPBSにバッファー交換した。これをhGAA-抗hTfR抗体の精製品とした。
ヒト骨格筋細胞(PromoCell社)をSkeletal Muscle Cell Growth Medium(Ready-to-use) (PromoCell社)にて8.0 X 104個/mLに希釈し,250μLずつCellnestTM(富士フイルム)でコートした96穴プレートの各ウェルに播種する。37℃, 5% CO2下で3日間培養後,培地を骨格筋細胞分化誘導用の培地Skeletal Muscle Cell Differentiation Medium (Ready-to-use) (PromoCell社)に交換する。そして,2日毎に分化誘導用培地で培地交換を行い,6日間分化誘導する。培地を除去した後,分化誘導用培地を用いて調製したhGAA-抗hTfR抗体ならびにhGAAの段階希釈液(0.005〜20.0 μg/mL)を,被検物質として,それぞれ100 μLずつ各ウェルに添加し,37℃,5% CO2下で更に20時間培養する。
酸性α-グルコシダーゼ遺伝子(GAA遺伝子)をノックアウトし,且つヒトトランスフェリン受容体遺伝子(CD71遺伝子)をノックインしたCD71-KI/GAA-KOマウスを,一般的な遺伝子工学的手法により作製した。作成方法は概ね以下のとおりである。マウスGAA遺伝子のエクソン6に存在するBamHI部位に終止コドンとネオマイシン耐性遺伝子を挿入することにより,マウスGAA遺伝子をノックアウトすることのできるターゲティングベクター(GAAノックアウトベクター)を構築した。このターゲティングベクターは,配列番号32で示される塩基配列を含む。ターゲティングベクターを線状化した後,C57BL/6系統のES細胞にエレクトロポレーション法により導入した。導入後,ネオマイシン薬剤耐性を指標とした選択培養を行い,薬剤耐性ESクローンを取得した。得られた薬剤耐性ESクローンをゲノムPCRおよびサザンブロットによってスクリーニングし,特異的な相同組換えが成立したクローン(相同組換えESクローン)を選別した。相同組換えESクローンとICR系統の8細胞期胚を用い,アグリゲーション法でキメラ胚を作製した。レシピエントマウスにキメラ胚を移植してキメラマウスを出産させた。
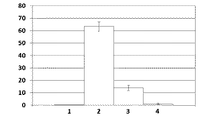
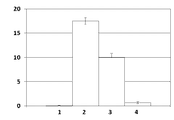
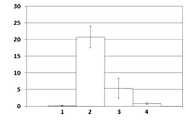
実施例12で作製したhGAA-抗hTfR抗体の精製品及び市販の医療用hGAAを,それぞれ生理食塩水を用いて4 mg/mLの溶液とした。これらの溶液を用いて,CD71-KI/GAA-KOマウスに,hGAA-抗hTfR抗体とhGAAをそれぞれ尾静脈より投与した。hGAA-抗hTfR抗体とhGAAの何れも1回当たりの投与量を20mgとして,隔週で計4回投与した。最後の投与の2週間後に,マウスを放血死させて,心臓,横隔膜,ヒラメ筋,前脛骨筋,及び大腿四頭筋を採取した。採取した組織は生理食塩水で洗浄した。これら筋組織に含まれるグリコーゲン濃度(mg/g湿組織重量)を実施例16に記載の方法で測定した。hGAA-抗hTfR抗体を投与した群をhGAA-抗hTfR抗体投与群,市販の医療用hGAAを投与した群をhGAA投与群とした。また,等量の生理食塩水を投与したCD71-KI/GAA-KOマウスをKOコントロール群とした。更に,等量の生理食塩水を投与した野生型マウスを野生型コントロール群とした。各群ともマウス5匹とした。
ビーズ破砕機(BEADS CRUSHER μT-12,タイテック社)にセットしたホルダーに,実施例15で得た組織と15個の直径0.5 mmのSUSビーズを入れ,更に注射用水を加えた。ビーズ破砕機を作動させて組織を破砕した。得られた組織破砕物を15,000 rpm,10分間,4℃で遠心し,上清を検体溶液として採取し,測定時まで凍結保存した。
配列番号4:リンカー例2のアミノ酸配列
配列番号7:プライマーhTfR5’,合成配列
配列番号8:プライマーhTfR3’,合成配列
配列番号9:マウス抗hTfR抗体番号3の軽鎖の可変領域のアミノ酸配列
配列番号10:マウス抗hTfR抗体番号3の重鎖の可変領域のアミノ酸配列
配列番号11:マウス抗hTfR抗体番号3の軽鎖CDR1のアミノ酸配列1
配列番号12:マウス抗hTfR抗体番号3の軽鎖CDR1のアミノ酸配列2
配列番号13:マウス抗hTfR抗体番号3の軽鎖CDR2のアミノ酸配列1
配列番号14:マウス抗hTfR抗体番号3の軽鎖CDR2のアミノ酸配列2
配列番号15:マウス抗hTfR抗体番号3の軽鎖CDR3のアミノ酸配列
配列番号16:マウス抗hTfR抗体番号3の重鎖CDR1のアミノ酸配列1
配列番号17:マウス抗hTfR抗体番号3の重鎖CDR1のアミノ酸配列2
配列番号18:マウス抗hTfR抗体番号3の重鎖CDR2のアミノ酸配列1
配列番号19:マウス抗hTfR抗体番号3の重鎖CDR2のアミノ酸配列2
配列番号20:マウス抗hTfR抗体番号3の重鎖CDR3のアミノ酸配列1
配列番号21:マウス抗hTfR抗体番号3の重鎖CDR3のアミノ酸配列2
配列番号22:ヒト化抗hTfR抗体番号3の軽鎖の可変領域のアミノ酸配列
配列番号23:ヒト化抗hTfR抗体番号3の重鎖の可変領域のアミノ酸配列
配列番号24:ヒト化抗hTfR抗体番号3の軽鎖のアミノ酸配列
配列番号25:ヒト化抗hTfR抗体番号3の重鎖のアミノ酸配列
配列番号26:ヒト化抗hTfR抗体番号3の軽鎖のアミノ酸配列をコードする塩基配列,合成配列
配列番号27:ヒト化抗hTfR抗体番号3の重鎖とhGAAの融合蛋白質のアミノ酸配列
配列番号28:ヒト化抗hTfR抗体番号3の重鎖とhGAAの融合蛋白質のアミノ酸配列をコードする塩基配列,合成配列
配列番号29:ヒト化抗hTfR抗体番号3の重鎖とhα-GalAの融合蛋白質のアミノ酸配列
配列番号30:プライマーHyg−Sfi5’,合成配列
配列番号31:プライマーHyg−BstX3’,合成配列
配列番号32:GAAノックアウトベクターの塩基配列,合成配列
Claims (47)
- 抗ヒトトランスフェリン受容体抗体と薬剤との結合体であって,該薬剤が筋肉において機能を発揮させるべき生理活性を有するものである,結合体。
- 該抗ヒトトランスフェリン受容体抗体が,Fab抗体,F(ab’)2抗体,又はF(ab’)抗体である,請求項1に記載の結合体。
- 該抗ヒトトランスフェリン受容体抗体が,scFab,scF(ab’),scF(ab’)2及びscFvからなる群から選ばれる一本鎖抗体である,請求項1に記載の結合体。
- 該一本鎖抗体が,該抗ヒトトランスフェリン受容体抗体の軽鎖と重鎖とをリンカー配列を介して結合させたものである,請求項3に記載の結合体。
- 該抗ヒトトランスフェリン受容体抗体の軽鎖と重鎖とを,該軽鎖のC末端側において,該リンカー配列を介して結合させたものである,請求項4に記載の結合体。
- 該抗ヒトトランスフェリン受容体抗体の軽鎖と重鎖とを,該重鎖のC末端側において,該リンカー配列を介して結合させたものである,請求項4に記載の結合体。
- 該リンカー配列が,8〜50個のアミノ酸残基からなるものである,請求項4〜6の何れかに記載の結合体。
- 該リンカー配列が,アミノ酸配列(Gly Ser),アミノ酸配列(Gly Gly Ser),アミノ酸配列(Gly Gly Gly),配列番号3,及び配列番号4で示されるものからなる群から選択されるアミノ酸配列を含んでなるものである,請求項7に記載の結合体。
- 該リンカー配列が,配列番号4で示されるアミノ酸配列が3回連続する15個のアミノ酸残基からなるものである,請求項8に記載の結合体。
- 該抗ヒトトランスフェリン受容体抗体が,軽鎖の可変領域に配列番号22で示されるアミノ酸配列を含むものであり,重鎖の可変領域に配列番号23で示されるアミノ酸配列を含むものである,請求項1〜9の何れかに記載の結合体。
- 該軽鎖の可変領域のアミノ酸配列が,配列番号22で示されるアミノ酸配列と80%以上の同一性を有するものであり,該重鎖の可変領域のアミノ酸配列が,配列番号23で示されるアミノ酸配列と80%以上の同一性を有するものである,請求項10に記載の結合体。
- 該軽鎖の可変領域のアミノ酸配列が,配列番号22で示されるアミノ酸配列と90%以上の同一性を有するものであり,該重鎖の可変領域のアミノ酸配列が,配列番号23で示されるアミノ酸配列と90%以上の同一性を有するものである,請求項10に記載の結合体。
- 該軽鎖の可変領域のアミノ酸配列が,配列番号22で示されるアミノ酸配列を構成する1〜10個のアミノ酸が,他のアミノ酸に置換されたものである,請求項10に記載の結合体。
- 該軽鎖の可変領域のアミノ酸配列が,配列番号22で示されるアミノ酸配列を構成する1〜3個のアミノ酸が,他のアミノ酸に置換されたものである,請求項10に記載の結合体。
- 該重鎖の可変領域のアミノ酸配列が,配列番号23で示されるアミノ酸配列を構成する1〜10個のアミノ酸が,他のアミノ酸に置換されたものである,請求項10に記載の結合体。
- 該重鎖の可変領域のアミノ酸配列が,配列番号23で示されるアミノ酸配列を構成する1〜3個のアミノ酸が,他のアミノ酸に置換されたものである,請求項10に記載の結合体。
- 該軽鎖の可変領域のアミノ酸配列が,配列番号22で示されるアミノ酸配列を構成する1〜10個のアミノ酸が,他のアミノ酸に置換されたものであり,該重鎖の可変領域のアミノ酸配列が,配列番号23で示されるアミノ酸配列を構成する1〜10個のアミノ酸が,他のアミノ酸に置換されたものである,請求項10に記載の結合体。
- 該軽鎖の可変領域のアミノ酸配列が,配列番号22で示されるアミノ酸配列を構成する1〜3個のアミノ酸が,他のアミノ酸に置換されたものであり,該重鎖の可変領域のアミノ酸配列が,配列番号23で示されるアミノ酸配列を構成する1〜3個のアミノ酸が,他のアミノ酸に置換されたものである,請求項10に記載の結合体。
- 該抗ヒトトランスフェリン受容体抗体が,軽鎖に配列番号24で示されるアミノ酸配列を含むものであり,重鎖に配列番号25で示されるアミノ酸配列を含むものである,請求項10に記載の結合体。
- 該軽鎖のアミノ酸配列が,配列番号24で示されるアミノ酸配列と80%以上の同一性を有するものであり,該重鎖のアミノ酸配列が,配列番号25で示されるアミノ酸配列と80%以上の同一性を有するものである,請求項19に記載の結合体。
- 該軽鎖のアミノ酸配列が,配列番号24で示されるアミノ酸配列と90%以上の同一性を有するものであり,該重鎖のアミノ酸配列が,配列番号25で示されるアミノ酸配列と90%以上の同一性を有するものである,請求項19に記載の結合体。
- 薬剤がペプチド又は蛋白質である,請求項1〜21の何れかに記載の結合体。
- 請求項22の結合体であって,以下の(1)〜(4)からなる群から選択されるもの,
(1)該蛋白質が,該抗ヒトトランスフェリン受容体抗体の軽鎖のC末端側にペプチド結合により結合したもの,
(2)該蛋白質が,該抗ヒトトランスフェリン受容体抗体の軽鎖のN末端側にペプチド結合により結合したもの,
(3)該蛋白質が,該抗ヒトトランスフェリン受容体抗体の重鎖のC末端側にペプチド結合により結合したもの,及び
(4)該蛋白質が,該抗ヒトトランスフェリン受容体抗体の重鎖のN末端側にペプチド結合により結合したもの。 - 該蛋白質が,該抗ヒトトランスフェリン受容体抗体に,リンカー配列を介して結合したものである,請求項23に記載の結合体。
- 該リンカー配列が,1〜50個のアミノ酸残基からなるものである,請求項24に記載の結合体。
- 該リンカー配列が,1個のグリシン,1個のセリン,アミノ酸配列(Gly Ser),アミノ酸配列(Gly Gly Ser),配列番号3のアミノ酸配列,配列番号4のアミノ酸配列,及びこれらのアミノ酸配列が1〜10個連続してなるアミノ酸配列からなる群より選ばれるアミノ酸配列を含んでなるものである,請求項25に記載の結合体。
- 該抗ヒトトランスフェリン受容体抗体がヒト化抗ヒトトランスフェリン受容体抗体である,上記1〜28の何れかの結合体。
- 該蛋白質が,リソソーム酵素である,請求項22〜27の何れかに記載の結合体。
- 該リソソーム酵素が,ヒトα−ガラクトシダーゼAである,請求項28に記載の結合体。
- 該ヒト化抗hTfR抗体の軽鎖が配列番号24のアミノ酸配列を含むものであり,該ヒト化抗hTfR抗体の重鎖がそのC末端側で,リンカー配列(Gly Ser)を介して,該ヒトα−ガラクトシダーゼAと結合しており,全体として配列番号29で示されるアミノ酸配列を含むものである,請求項29に記載の結合体。
- 該リソソーム酵素がヒト酸性α-グルコシダーゼ,である,請求項28に記載の結合体。
- 該ヒト化抗hTfR抗体の軽鎖が配列番号24のアミノ酸配列を含むものであり,該ヒト化抗hTfR抗体の重鎖がそのC末端側で,リンカー配列(Gly Ser)を介して,該ヒト酸性α-グルコシダーゼと結合しており,全体として配列番号27で示されるアミノ酸配列を含むものである,請求項31に記載の結合体。
- 請求項1〜32の何れかに記載の結合体を含有してなる,筋肉の機能を改善するための医薬組成物。
- 請求項28に記載の結合体を含有してなる,リソソーム病に伴う筋肉の機能障害を改善するための,医薬組成物。
- 請求項29又は30に記載の結合体を含有してなる,ファブリー病に伴う筋肉の機能障害を改善するための,医薬組成物。
- 請求項31又は32に記載の結合体を含有してなる,ポンペ病に伴う筋肉の機能障害を改善するための,医薬組成物。
- 該筋肉が,骨格筋,心筋,又は平滑筋の何れかである,請求項33〜36の何れかに記載の医薬組成物。
- リソソーム病に伴う筋肉の機能障害を改善するための医薬組成物の製造のための,請求項28〜32の何れかに記載の結合体の使用。
- ファブリー病に伴う筋肉の機能障害を改善するための医薬組成物の製造のための,請求項29又は30に記載の結合体の使用。
- ポンペ病に伴う筋肉の機能障害を改善するための医薬組成物の製造のための,請求項31又は32に記載の結合体の使用。
- 請求項1〜32の何れかに記載の結合体の,筋肉の機能を改善するための医薬組成物としての使用。
- 薬剤を筋肉に送達するための方法であって,該薬剤を抗ヒトトランスフェリン受容体抗体と結合させた結合体として製造するステップ,及び該結合体を個体に投与するステップことを含む,方法。
- 該結合体が,請求項1〜32の何れかに記載の結合体である,請求項41に記載の方法。
- 該結合体の投与により該個体の筋肉の機能が改善されるステップを更に含む,請求項42又は43に記載の方法。
- 該個体が,筋肉の機能障害を有するものである,請求項42〜44の何れかに記載の方法。
- 該個体が,リソソーム病に伴う筋肉の機能障害を有するものである,請求項42〜44の何れかに記載の方法。
- 該リソソーム病が,ファブリー病又はポンペ病である,請求項46に記載の方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2023150649A JP2023165038A (ja) | 2018-02-05 | 2023-09-19 | 薬剤を筋肉に送達するための方法 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018018652 | 2018-02-05 | ||
| JP2018018652 | 2018-02-05 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023150649A Division JP2023165038A (ja) | 2018-02-05 | 2023-09-19 | 薬剤を筋肉に送達するための方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2019137675A true JP2019137675A (ja) | 2019-08-22 |
| JP2019137675A5 JP2019137675A5 (ja) | 2022-01-18 |
Family
ID=67479985
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019019212A Pending JP2019137675A (ja) | 2018-02-05 | 2019-02-05 | 薬剤を筋肉に送達するための方法 |
| JP2023150649A Pending JP2023165038A (ja) | 2018-02-05 | 2023-09-19 | 薬剤を筋肉に送達するための方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023150649A Pending JP2023165038A (ja) | 2018-02-05 | 2023-09-19 | 薬剤を筋肉に送達するための方法 |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US20210038739A1 (ja) |
| EP (1) | EP3750921A4 (ja) |
| JP (2) | JP2019137675A (ja) |
| KR (1) | KR20200116952A (ja) |
| CN (1) | CN111683972A (ja) |
| AU (1) | AU2019215782A1 (ja) |
| BR (1) | BR112020013305A2 (ja) |
| CA (1) | CA3090373A1 (ja) |
| EA (1) | EA202091816A1 (ja) |
| IL (1) | IL276327B2 (ja) |
| MX (1) | MX2020008041A (ja) |
| SG (1) | SG11202006433PA (ja) |
| WO (1) | WO2019151539A1 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MA50546A (fr) | 2017-06-07 | 2020-09-16 | Regeneron Pharma | Compositions et méthodes pour l'internalisation d'enzymes |
| CN115335062A (zh) * | 2020-01-10 | 2022-11-11 | 达因疗法公司 | 肌肉靶向复合物及其用于调节与肌肉健康相关的基因的用途 |
| EP4096695A4 (en) * | 2020-01-31 | 2024-02-28 | Dyne Therapeutics Inc | ANTI-TRANSFERRIN RECEPTOR (TFR) ANTIBODIES AND RELATED USES |
| AU2021224412A1 (en) | 2020-02-22 | 2022-09-15 | Jcr Pharmaceuticals Co., Ltd. | Human transferrin receptor binding peptide |
| AU2022329794A1 (en) | 2021-08-19 | 2024-02-22 | Jcr Pharmaceuticals Co., Ltd. | Human transferrin receptor–binding peptide |
| WO2023027125A1 (ja) | 2021-08-24 | 2023-03-02 | ペプチドリーム株式会社 | ヒトトランスフェリンレセプター結合抗体-ペプチドコンジュゲート |
| PE20240895A1 (es) | 2021-09-01 | 2024-04-24 | Biogen Ma Inc | Anticuerpos del receptor antitransferrina y usos de los mismos |
| US20230338477A1 (en) * | 2022-02-02 | 2023-10-26 | Regeneron Pharmaceuticals, Inc. | Anti-tfr:gaa and anti-cd63:gaa insertion for treatment of pompe disease |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013118165A1 (en) * | 2012-02-07 | 2013-08-15 | Jcr Pharmaceuticals Co., Ltd. | Pharmaceutical agents fused with atf for improved bioavailability |
| WO2014130723A1 (en) * | 2013-02-20 | 2014-08-28 | Valerion Therapeutics, Llc | Methods and compositions for treatment of pompe disease |
| WO2016208695A1 (ja) * | 2015-06-24 | 2016-12-29 | Jcrファーマ株式会社 | 血液脳関門を通過する抗ヒトトランスフェリン受容体抗体 |
| WO2017100467A2 (en) * | 2015-12-08 | 2017-06-15 | Regeneron Pharmaceuticals, Inc. | Compositions and methods for internalizing enzymes |
| WO2018038243A1 (ja) * | 2016-08-25 | 2018-03-01 | Jcrファーマ株式会社 | 抗体融合蛋白質の製造方法 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6261558B1 (en) | 1993-10-19 | 2001-07-17 | The Scripps Research Institute | Synthetic human neutralizing monoclonal antibodies to human immunodeficiency virus |
| AUPN523995A0 (en) | 1995-09-05 | 1995-09-28 | Crc For Biopharmaceutical Research Pty Ltd | Method for producing phage display vectors |
| US7341720B2 (en) * | 2005-04-06 | 2008-03-11 | Genzyme Corporation | Targeting of glycoprotein therapeutics |
| WO2012063799A1 (ja) | 2010-11-08 | 2012-05-18 | 日本ケミカルリサーチ株式会社 | 新規発現ベクター |
| MA38632B1 (fr) * | 2013-05-20 | 2019-10-31 | Genentech Inc | Anticorps anti-récepteur de transferrine et procédés d'utilisation |
-
2019
- 2019-02-05 BR BR112020013305-1A patent/BR112020013305A2/pt unknown
- 2019-02-05 CA CA3090373A patent/CA3090373A1/en active Pending
- 2019-02-05 EA EA202091816A patent/EA202091816A1/ru unknown
- 2019-02-05 US US16/963,956 patent/US20210038739A1/en not_active Abandoned
- 2019-02-05 MX MX2020008041A patent/MX2020008041A/es unknown
- 2019-02-05 IL IL276327A patent/IL276327B2/en unknown
- 2019-02-05 SG SG11202006433PA patent/SG11202006433PA/en unknown
- 2019-02-05 JP JP2019019212A patent/JP2019137675A/ja active Pending
- 2019-02-05 CN CN201980011522.2A patent/CN111683972A/zh active Pending
- 2019-02-05 AU AU2019215782A patent/AU2019215782A1/en active Pending
- 2019-02-05 EP EP19747769.8A patent/EP3750921A4/en active Pending
- 2019-02-05 KR KR1020207024561A patent/KR20200116952A/ko not_active Application Discontinuation
- 2019-02-05 WO PCT/JP2019/004123 patent/WO2019151539A1/ja unknown
-
2023
- 2023-09-19 JP JP2023150649A patent/JP2023165038A/ja active Pending
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013118165A1 (en) * | 2012-02-07 | 2013-08-15 | Jcr Pharmaceuticals Co., Ltd. | Pharmaceutical agents fused with atf for improved bioavailability |
| WO2014130723A1 (en) * | 2013-02-20 | 2014-08-28 | Valerion Therapeutics, Llc | Methods and compositions for treatment of pompe disease |
| WO2016208695A1 (ja) * | 2015-06-24 | 2016-12-29 | Jcrファーマ株式会社 | 血液脳関門を通過する抗ヒトトランスフェリン受容体抗体 |
| WO2017100467A2 (en) * | 2015-12-08 | 2017-06-15 | Regeneron Pharmaceuticals, Inc. | Compositions and methods for internalizing enzymes |
| WO2018038243A1 (ja) * | 2016-08-25 | 2018-03-01 | Jcrファーマ株式会社 | 抗体融合蛋白質の製造方法 |
| JP2018033454A (ja) * | 2016-08-25 | 2018-03-08 | Jcrファーマ株式会社 | 抗体融合蛋白質の製造方法 |
Non-Patent Citations (3)
| Title |
|---|
| SCHNYDER, A., ET AL.: ""Targeting of skeletal muscle in vitro using biotinylated immunoliposomes."", BIOCHEM. J., vol. 377, JPN6019015124, 2004, pages 61 - 67, ISSN: 0004958387 * |
| SUGO, T., ET AL.: ""Development of antibody-siRNA conjugate targeted to cardiac and skeletal muscles."", JOURNAL OF CONTROLLED RELEASE, vol. 237, JPN6019015125, 29 June 2016 (2016-06-29), pages 1 - 13, ISSN: 0004958388 * |
| SUNG, C., ET AL.: ""Pharmacokinetic analysis of immunotoxin uptake in solid tumors: role of plasma kinetics, capillary", CANCER RESEARCH, vol. 50, JPN6019015126, 15 November 1990 (1990-11-15), pages 7382 - 7392, XP055629256, ISSN: 0004958389 * |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2023165038A (ja) | 2023-11-14 |
| IL276327B1 (en) | 2024-01-01 |
| EP3750921A4 (en) | 2021-11-10 |
| KR20200116952A (ko) | 2020-10-13 |
| CN111683972A (zh) | 2020-09-18 |
| BR112020013305A2 (pt) | 2021-02-02 |
| EA202091816A1 (ru) | 2020-10-26 |
| EP3750921A1 (en) | 2020-12-16 |
| US20210038739A1 (en) | 2021-02-11 |
| WO2019151539A1 (ja) | 2019-08-08 |
| CA3090373A1 (en) | 2019-08-08 |
| IL276327A (en) | 2020-09-30 |
| IL276327B2 (en) | 2024-05-01 |
| AU2019215782A1 (en) | 2020-07-16 |
| SG11202006433PA (en) | 2020-08-28 |
| MX2020008041A (es) | 2020-09-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7385723B2 (ja) | 血液脳関門を通過する新規な抗ヒトトランスフェリン受容体抗体 | |
| JP7411743B2 (ja) | 血液脳関門を通過する抗ヒトトランスフェリン受容体抗体 | |
| WO2019151539A1 (ja) | 薬剤を筋肉に送達するための方法 | |
| JP7042220B2 (ja) | 凍結乾燥製剤 | |
| JP7188944B2 (ja) | 水性医薬組成物 | |
| CN103687620A (zh) | 用于抑制masp-2依赖的补体活化的组合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220107 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220107 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20220502 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230110 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230509 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20230509 |
|
| A603 | Late request for extension of time limit during examination |
Free format text: JAPANESE INTERMEDIATE CODE: A603 Effective date: 20230510 Free format text: JAPANESE INTERMEDIATE CODE: A603 Effective date: 20230509 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20230704 |