JP2017128564A - 植物の耐塩性向上剤 - Google Patents
植物の耐塩性向上剤 Download PDFInfo
- Publication number
- JP2017128564A JP2017128564A JP2017003961A JP2017003961A JP2017128564A JP 2017128564 A JP2017128564 A JP 2017128564A JP 2017003961 A JP2017003961 A JP 2017003961A JP 2017003961 A JP2017003961 A JP 2017003961A JP 2017128564 A JP2017128564 A JP 2017128564A
- Authority
- JP
- Japan
- Prior art keywords
- substituted
- unsubstituted
- plant
- methyl
- adenosyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A40/00—Adaptation technologies in agriculture, forestry, livestock or agroalimentary production
- Y02A40/10—Adaptation technologies in agriculture, forestry, livestock or agroalimentary production in agriculture
- Y02A40/13—Abiotic stress
- Y02A40/135—Plants tolerant to salinity
Landscapes
- Breeding Of Plants And Reproduction By Means Of Culturing (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
Abstract
Description
(1) 式(I):
nは、1以上の整数であり、
R1は、置換若しくは非置換のアルキル、置換若しくは非置換のアルケニル、置換若しくは非置換のアルキニル、置換若しくは非置換のシクロアルキル、置換若しくは非置換のシクロアルケニル、置換若しくは非置換のシクロアルキニル、置換若しくは非置換のヘテロシクロアルキル、置換若しくは非置換のシクロアルキルアルキル、置換若しくは非置換のヘテロシクロアルキルアルキル、置換若しくは非置換のアリール、置換若しくは非置換のアリールアルキル、置換若しくは非置換のヘテロアリール、又は置換若しくは非置換のヘテロアリールアルキルである。]
で表される化合物若しくはその塩、又はそれらの溶媒和物を有効成分として含有する、植物の耐塩性向上剤。
(2) nが、1又は2である、前記(1)に記載の植物の耐塩性向上剤。
(3) R1が、置換若しくは非置換のC1〜C5アルキルである、前記(1)に記載の植物の耐塩性向上剤。
(4) ファルネソール酸メチル又はゲラニル酸メチルを有効成分として含有する、植物の耐塩性向上剤。
(5) 前記(1)〜(4)のいずれかに記載の植物の耐塩性向上剤を有効成分として含有する、植物の耐塩性を向上させるための農業化学製剤。
(6) 前記(1)〜(4)のいずれかに記載の植物の耐塩性向上剤と、1種以上の農業上許容される成分とを含有する、植物の耐塩性を向上させるための農業化学組成物。
(7) 農業上有効な量の前記(1)〜(4)のいずれかに記載の植物の耐塩性向上剤を、植物又はそこから該植物が生育する土壌、培地若しくは培養液に施用することを含む、該植物の耐塩性を向上する方法。
(8) 1個以上のS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼ遺伝子の発現が増加されている、耐塩性が向上した植物。
(9) 1個以上のS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼ遺伝子が、ファルネソール酸カルボキシル-O-メチルトランスフェラーゼ遺伝子である、前記(8)に記載の耐塩性が向上した植物。
(10) 1個以上のS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼ遺伝子が、以下の(a)〜(c):
(a)配列番号1又は2で示されるアミノ酸配列からなるポリペプチド、
(b)配列番号1又は2で示されるアミノ酸配列において1若しくは数個のアミノ酸が欠失、置換又は付加されたアミノ酸配列からなり、且つS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼ活性を有するポリペプチド、及び
(c)配列番号1で示されるアミノ酸配列の第34〜348位の領域に相当するポリペプチド断片に対して92%以上の同一性を有し、且つS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼ活性を有するポリペプチド
のいずれかのポリペプチドをコードする遺伝子である、前記(8)又は(9)に記載の耐塩性が向上した植物。
前記以外の、課題、構成及び効果は、以下の実施形態の説明により明らかにされる。
<1:環境ストレス耐性向上剤>
本発明において、「環境ストレス」は、対象となる植物の外部環境に起因して、植物が被るストレスを意味する。本発明において、環境ストレスは、1個以上のS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼの活性を向上させることにより、それに対する耐性が増強される任意の環境ストレスを包含する。本発明の対象となる環境ストレスとしては、限定するものではないが、例えば、塩ストレス、乾燥ストレス及び低温ストレスを挙げることができる。環境ストレスは、対象となる植物の好適な生育条件に依存して、様々な外部環境がその要因となる。当業者であれば、対象となる植物に基づき、環境ストレスの要因となる外部環境の具体的な条件を容易に決定することができる。
nが、1〜4の範囲であり、
R1が、置換若しくは非置換のC1〜C5アルキル、置換若しくは非置換のC2〜C5アルケニル、置換若しくは非置換のC2〜C5アルキニル、置換若しくは非置換のC3〜C6シクロアルキル、置換若しくは非置換のC3〜C6シクロアルケニル、置換若しくは非置換のC3〜C6シクロアルキニル、置換若しくは非置換の3〜6員のヘテロシクロアルキル、置換若しくは非置換のC7〜C11シクロアルキルアルキル、置換若しくは非置換の3〜6員のヘテロシクロアルキル-C1〜C5アルキル、置換若しくは非置換のC6〜C15アリール、置換若しくは非置換のC7〜C20アリールアルキル、置換若しくは非置換の5〜15員のヘテロアリール、又は置換若しくは非置換の5〜15員のヘテロアリール-C1〜C5アルキルであり、
前記基が置換されている場合、該置換基は、それぞれ独立して、ハロゲン(フッ素、塩素、臭素又はヨウ素)、カルボキシル、シアノ、ニトロ、ヒドロキシル、置換若しくは非置換のC1〜C5アルキル、置換若しくは非置換のC2〜C5アルケニル、置換若しくは非置換のC2〜C5アルキニル、置換若しくは非置換のC3〜C6シクロアルキル、置換若しくは非置換のC3〜C6シクロアルケニル、置換若しくは非置換のC3〜C6シクロアルキニル、置換若しくは非置換の3〜6員のヘテロシクロアルキル、置換若しくは非置換のC7〜C11シクロアルキルアルキル、置換若しくは非置換の3〜6員のヘテロシクロアルキル-C1〜C5アルキル、置換若しくは非置換のC6〜C15アリール、置換若しくは非置換のC7〜C20アリールアルキル、置換若しくは非置換の5〜15員のヘテロアリール、置換若しくは非置換の5〜15員のヘテロアリール-C1〜C5アルキル、置換若しくは非置換のC1〜C6アルコキシ、置換若しくは非置換のC3〜C6シクロアルコキシ、置換若しくは非置換の3〜6員ヘテロシクロアルコキシ、置換若しくは非置換のC6〜C15アリールオキシ、置換若しくは非置換のC7〜C20アリールアルキルオキシ、置換若しくは非置換の5〜15員のヘテロアリールオキシ、置換若しくは非置換の5〜15員のヘテロアリール-C1〜C5アルキルオキシ、置換若しくは非置換のC1〜C6アルコキシカルボニル、置換若しくは非置換のC3〜C6シクロアルコキシカルボニル、置換若しくは非置換のC1〜C20アシル、置換若しくは非置換のC1〜C20アシルオキシ、及び置換若しくは非置換のアミノからなる群より選択される少なくとも1個の1価基である。
nが、1〜4の範囲であり、
R1が、置換若しくは非置換のC1〜C5アルキルであり、
前記基が置換されている場合、該置換基は、それぞれ独立して、ハロゲン(フッ素、塩素、臭素又はヨウ素)、カルボキシル、シアノ、ニトロ、ヒドロキシル、置換若しくは非置換のC1〜C5アルキル、置換若しくは非置換のC2〜C5アルケニル、置換若しくは非置換のC2〜C5アルキニル、置換若しくは非置換のC3〜C6シクロアルキル、置換若しくは非置換のC3〜C6シクロアルケニル、置換若しくは非置換のC3〜C6シクロアルキニル、置換若しくは非置換の3〜6員のヘテロシクロアルキル、置換若しくは非置換のC7〜C11シクロアルキルアルキル、置換若しくは非置換の3〜6員のヘテロシクロアルキル-C1〜C5アルキル、置換若しくは非置換のC6〜C15アリール、置換若しくは非置換のC7〜C20アリールアルキル、置換若しくは非置換の5〜15員のヘテロアリール、置換若しくは非置換の5〜15員のヘテロアリール-C1〜C5アルキル、置換若しくは非置換のC1〜C6アルコキシ、置換若しくは非置換のC3〜C6シクロアルコキシ、置換若しくは非置換の3〜6員ヘテロシクロアルコキシ、置換若しくは非置換のC6〜C15アリールオキシ、置換若しくは非置換のC7〜C20アリールアルキルオキシ、置換若しくは非置換の5〜15員のヘテロアリールオキシ、置換若しくは非置換の5〜15員のヘテロアリール-C1〜C5アルキルオキシ、置換若しくは非置換のC1〜C6アルコキシカルボニル、置換若しくは非置換のC3〜C6シクロアルコキシカルボニル、置換若しくは非置換のC1〜C20アシル、置換若しくは非置換のC1〜C20アシルオキシ、及び置換若しくは非置換のアミノからなる群より選択される少なくとも1個の1価基である。
nが、1又は2であり、
R1が、置換若しくは非置換のC1〜C5アルキルであり、
前記基が置換されている場合、該置換基は、それぞれ独立して、ハロゲン(フッ素、塩素、臭素又はヨウ素)、カルボキシル、シアノ、ニトロ、ヒドロキシル、置換若しくは非置換のC1〜C5アルキル、置換若しくは非置換のC2〜C5アルケニル、置換若しくは非置換のC2〜C5アルキニル、置換若しくは非置換のC3〜C6シクロアルキル、置換若しくは非置換のC3〜C6シクロアルケニル、置換若しくは非置換のC3〜C6シクロアルキニル、置換若しくは非置換の3〜6員のヘテロシクロアルキル、置換若しくは非置換のC7〜C11シクロアルキルアルキル、置換若しくは非置換の3〜6員のヘテロシクロアルキル-C1〜C5アルキル、置換若しくは非置換のC6〜C15アリール、置換若しくは非置換のC7〜C20アリールアルキル、置換若しくは非置換の5〜15員のヘテロアリール、置換若しくは非置換の5〜15員のヘテロアリール-C1〜C5アルキル、置換若しくは非置換のC1〜C6アルコキシ、置換若しくは非置換のC3〜C6シクロアルコキシ、置換若しくは非置換の3〜6員ヘテロシクロアルコキシ、置換若しくは非置換のC6〜C15アリールオキシ、置換若しくは非置換のC7〜C20アリールアルキルオキシ、置換若しくは非置換の5〜15員のヘテロアリールオキシ、置換若しくは非置換の5〜15員のヘテロアリール-C1〜C5アルキルオキシ、置換若しくは非置換のC1〜C6アルコキシカルボニル、置換若しくは非置換のC3〜C6シクロアルコキシカルボニル、置換若しくは非置換のC1〜C20アシル、置換若しくは非置換のC1〜C20アシルオキシ、及び置換若しくは非置換のアミノからなる群より選択される少なくとも1個の1価基である。
nが、1又は2であり、
R1が、メチル、エチル、プロピル、ブチル又はペンチルである。
(1)nが、1であり、且つ
R1が、メチルである、或いは;
(2)nが、2であり、且つ
R1が、メチルである。
前記で説明したように、本発明の一態様の式(I)で表される化合物、特にファルネソール酸メチル又はゲラニル酸メチルを有効成分として含有する植物の環境ストレス耐性向上剤を植物に施用することにより、該植物の環境ストレス耐性を向上させることができる。それ故、本発明の別の一態様は、式(I)で表される化合物若しくはその塩、又はそれらの溶媒和物、特にファルネソール酸メチル又はゲラニル酸メチルを有効成分として含有する農業化学製剤又は農薬に関する。本態様の一実施形態は、本発明の環境ストレス耐性向上剤を有効成分として含有する農業化学製剤又は農薬である。本発明の別の一態様はまた、農業上有効な量の前記で説明した式(I)で表される化合物若しくはその塩、又はそれらの溶媒和物、特にファルネソール酸メチル又はゲラニル酸メチルを、植物又はそこから該植物が生育する土壌、培地若しくは培養液に施用することを含む、該植物の環境ストレス耐性を向上する方法に関する。本態様の一実施形態は、農業上有効な量の本発明の一態様の環境ストレス耐性向上剤を、植物又はそこから該植物が生育する土壌、培地若しくは培養液に施用することを含む、該植物の環境ストレス耐性を向上する方法である。
本発明の特定の一実施形態における環境ストレス耐性向上剤の有効成分であるファルネソール酸メチルは、特定のS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼによって、セスキテルペンの一種であるファルネソール酸から産生される化合物である。それ故、本発明の別の一態様は、1個以上のS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼ遺伝子の発現が増加されている、環境ストレス耐性が向上した植物に関する。前記環境ストレスは、塩ストレス、乾燥ストレス又は低温ストレスであることが好ましく、塩ストレスであることがより好ましい。本態様により、植物において産生されるファルネソール酸メチルを増加させることによって、耐塩性のような該植物の環境ストレス耐性が向上した植物を得ることができる。
(a)配列番号1又は2で示されるアミノ酸配列からなるポリペプチド、
(b)配列番号1又は2で示されるアミノ酸配列において1若しくは数個のアミノ酸が欠失、置換又は付加されたアミノ酸配列からなり、且つS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼ活性を有するポリペプチド、及び
(c)配列番号1で示されるアミノ酸配列の第34〜348位の領域に相当するポリペプチド断片に対して92%以上の同一性を有し、且つS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼ活性を有するポリペプチド
のいずれかのポリペプチドをコードする遺伝子である。
野生型のシロイヌナズナ(Col-0)の種子を滅菌した。滅菌処理されたシロイヌナズナ種子を、5 mlの1/2 MS液体培地(2.15 g/LのMS粉末、1質量%スクロース、1/1000濃度のB5ビタミン、0.5 g/L MES、及び0.1質量%寒天、1N KOHでpH5.7に調整)に浮かべるように播種した。播種後の種子を、4℃、暗所にて2日間低温処理した。低温処理した種子を22℃に設定されたインキュベーター内に移動し、シロイヌナズナを22℃で4日間生育させた。5 μLの1 μMの試験化合物(シクロ[-L-2-アミノ-7-(2-オキソプロピルチオ)ヘプタノイル-アミノイソブチリル-L-フェニルアラニル-D-プロリル-]、Ky-72)溶液又は5 μLのDMSOを培地に添加して、シロイヌナズナをさらに22℃で24時間生育させた。その後、100 μLの5 M NaCl水溶液(最終濃度100 mM)を培地に添加した。以下の5種類の植物体試料を得た:試料I-1 4日間生育させた植物体(試験化合物非処理);試料I-2 試験化合物存在下で24時間生育させた植物体;試料I-3 試験化合物存在下で24時間生育させた後、100 mM NaCl存在下で2時間生育させた植物体;試料I-4 DMSO存在下で24時間生育させた植物体;試料I-5 DMSO存在下で24時間生育させた後、100 mM NaCl存在下で2時間生育させた植物体。植物RNA試薬(Invitrogen)を用いて各植物体試料から全RNAを抽出し、クイックAmpラベリングキット(Agilent Technologies)を用いて標識した。標識したcRNAを、Arabidopsis custom 60KオリゴDNAマイクロアレイ(Agilent Technologies)を用いてハイブリダイズした。二元配置の分散分析(2-way ANOVA)法によって得られたデータを解析した。ratio≧0.4(log2値)及びfalse discovery rate (FDR)<0.05。
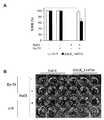
定量的RT-PCR解析により、マイクロアレイ解析の結果を確認した。前記Iと同様の手順により、試料I-1〜I-5の5種類の植物体試料を得た。表1に示す遺伝子のうち、ERF1、VQ29、bHLH、並びにFAMT1及び2遺伝子のNaCl処理前後における相対的発現量を定量的RT-PCR解析(3生物学的反復、N=30、平均±SD)によって得た。ERF1、VQ29、bHLH、並びにFAMT1及び2遺伝子のいずれも、試験化合物処理によってNaCl処理前後における相対的発現量が増加した。この結果から、マイクロアレイ解析の結果と同様に、ERF1、VQ29、bHLH、並びにFAMT1及び2遺伝子の発現が、100 mM NaCl存在下で植物体を2時間生育させた場合、DMSO処理植物体と比較して試験化合物処理植物体で誘導されたことが確認された。
野生型のシロイヌナズナ(Col-0)及び欠損変異体(ddf1(SALK_127759C及びSALK_137015)、cyp715(SALK_072265及びSALK_076001)、bhlh(GABI_461E05)、erf1(GABI_850A03)、vq29(SALK_061586)及びfamt2(SALK_144710)、これらの変異体は、Arabidopsis Biological Resource Center(ABRC)より入手した)の種子を滅菌した。滅菌処理された24穴マイクロプレートの各ウェルに、1 mlの1/2 MS液体培地を添加した。滅菌処理されたシロイヌナズナ種子を、1ウェルあたり3粒ずつ、ウェル中の1/2 MS液体培地に浮かべるように播種した。播種後の種子を、4℃、暗所にて2日間低温処理した。その後、マイクロプレートを、22℃に設定されたインキュベーター内に移動し、シロイヌナズナを22℃で4日間生育させた。所定のウェルに、1 μMの試験化合物(Ky-72)を添加して、シロイヌナズナをさらに22℃で24時間生育させた。その後、所定のウェルに、100 mM NaClを添加して、シロイヌナズナを22℃で4日間生育させた。肉眼又は実体顕微鏡で、生育させたシロイヌナズナの表現型を観察した。NaCl非添加区のシロイヌナズナ植物体と比較して、子葉若しくは本葉の黄化又は白化が観察された植物体を、塩ストレスによる影響を受けた植物体と判定した。各試験区において、植物体の総数(3×4ウェル=12植物体)に対する塩ストレスによる影響を受けた植物体の数の百分率を、塩ストレス条件下における生存率(%)として算出した。Col-0体及び各変異体における各試験区について、それぞれ2回反復試験を行い、その平均値及び標準誤差を算出した。その結果、試験した変異体のうちfamt2変異体のみが、生存率が低下することが明らかとなった。1 μMの試験化合物(Ky-72)処理後、NaCl存在下で4日間生育させたCol-0体及びfamt2変異体の表現型を図2に示す。
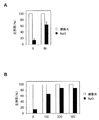
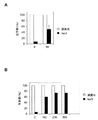
野生型のシロイヌナズナ(Col-0)の種子を滅菌した。滅菌処理された24穴マイクロプレートの各ウェルに、1 mlの1/2 MS液体培地を添加した。滅菌処理されたシロイヌナズナ種子を、1ウェルあたり3粒ずつ、ウェル中の1/2 MS液体培地に浮かべるように播種した。播種後の種子を、4℃、暗所にて2日間低温処理した。その後、マイクロプレートを、22℃に設定されたインキュベーター内に移動し、シロイヌナズナを22℃で4日間生育させた。所定のウェルに、所定量のファルネソール酸メチル(MeFA)を添加して、シロイヌナズナをさらに22℃で24時間生育させた。その後、所定のウェルに、100 mM NaClを添加して、シロイヌナズナを22℃で所定の期間生育させた。肉眼又は実体顕微鏡で、生育させたシロイヌナズナの表現型を観察した。前記IIIと同様の手順により、各試験区における塩ストレス条件下におけるシロイヌナズナ植物体の生存率(%)を算出した。各試験区について、それぞれ2回反復試験を行い、その平均値及び標準誤差を算出した。ファルネソール酸メチル濃度と生存率との関係を図3に示す。図中、Aは、NaCl存在下で3日間生育後の結果を、Bは、NaCl存在下で4日間生育後の結果を、Cは、NaCl存在下で5日間生育後の結果を、それぞれ示す。また、所定量のファルネソール酸メチル処理後、NaCl存在下で3〜5日間生育後のシロイヌナズナ植物体の表現型を図4〜9に示す。
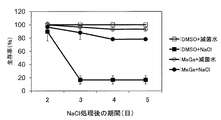
前記IVにおいて、添加する化合物を30 μg/mlのゲラニル酸メチル(MeGe)に変更した他は、前記と同様の手順により、塩ストレス条件下におけるシロイヌナズナ植物体の生存率(%)を算出した。ゲラニル酸メチル又は対照としてDMSOで処理したシロイヌナズナ植物体を塩ストレス条件下で生育させた期間と生存率との関係を図10に示す。図中、白抜き四角は、DMSOで処理したシロイヌナズナ植物体をNaCl非存在下で生育させた結果を、黒塗り四角は、DMSOで処理したシロイヌナズナ植物体をNaCl存在下で生育させた結果を、白抜き丸は、ゲラニル酸メチルで処理したシロイヌナズナ植物体をNaCl非存在下で生育させた結果を、黒塗り丸は、ゲラニル酸メチルで処理したシロイヌナズナ植物体をNaCl存在下で生育させた結果を、それぞれ示す。
Claims (10)
- 式(I):
nは、1以上の整数であり、
R1は、置換若しくは非置換のアルキル、置換若しくは非置換のアルケニル、置換若しくは非置換のアルキニル、置換若しくは非置換のシクロアルキル、置換若しくは非置換のシクロアルケニル、置換若しくは非置換のシクロアルキニル、置換若しくは非置換のヘテロシクロアルキル、置換若しくは非置換のシクロアルキルアルキル、置換若しくは非置換のヘテロシクロアルキルアルキル、置換若しくは非置換のアリール、置換若しくは非置換のアリールアルキル、置換若しくは非置換のヘテロアリール、又は置換若しくは非置換のヘテロアリールアルキルである。]
で表される化合物若しくはその塩、又はそれらの溶媒和物を有効成分として含有する、植物の耐塩性向上剤。 - nが、1又は2である、請求項1に記載の植物の耐塩性向上剤。
- R1が、置換若しくは非置換のC1〜C5アルキルである、請求項1又は2に記載の植物の耐塩性向上剤。
- ファルネソール酸メチル又はゲラニル酸メチルを有効成分として含有する、植物の耐塩性向上剤。
- 請求項1〜4のいずれか1項に記載の植物の耐塩性向上剤を有効成分として含有する、植物の耐塩性を向上させるための農業化学製剤。
- 請求項1〜4のいずれか1項に記載の植物の耐塩性向上剤と、1種以上の農業上許容される成分とを含有する、植物の耐塩性を向上させるための農業化学組成物。
- 農業上有効な量の請求項1〜4のいずれか1項に記載の植物の耐塩性向上剤を、植物又はそこから該植物が生育する土壌、培地若しくは培養液に施用することを含む、該植物の耐塩性を向上する方法。
- 1個以上のS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼ遺伝子の発現が増加されている、耐塩性が向上した植物。
- 1個以上のS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼ遺伝子が、ファルネソール酸カルボキシル-O-メチルトランスフェラーゼ遺伝子である、請求項8に記載の耐塩性が向上した植物。
- 1個以上のS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼ遺伝子が、以下の(a)〜(c):
(a)配列番号1又は2で示されるアミノ酸配列からなるポリペプチド、
(b)配列番号1又は2で示されるアミノ酸配列において1若しくは数個のアミノ酸が欠失、置換又は付加されたアミノ酸配列からなり、且つS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼ活性を有するポリペプチド、及び
(c)配列番号1で示されるアミノ酸配列の第34〜348位の領域に相当するポリペプチド断片に対して92%以上の同一性を有し、且つS-アデノシル-L-メチオニン依存性メチルトランスフェラーゼ活性を有するポリペプチド
のいずれかのポリペプチドをコードする遺伝子である、請求項8又は9に記載の耐塩性が向上した植物。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016007190 | 2016-01-18 | ||
| JP2016007190 | 2016-01-18 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2017128564A true JP2017128564A (ja) | 2017-07-27 |
| JP6917046B2 JP6917046B2 (ja) | 2021-08-11 |
Family
ID=59394387
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017003961A Active JP6917046B2 (ja) | 2016-01-18 | 2017-01-13 | 植物の耐塩性向上剤 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6917046B2 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2020054878A1 (ja) * | 2018-09-14 | 2020-03-19 | 積水化学工業株式会社 | 植物の耐塩性向上剤 |
| WO2020130145A1 (ja) * | 2018-12-21 | 2020-06-25 | アクプランタ株式会社 | 植物の耐熱性あるいは耐塩性向上剤 |
| CN116035006A (zh) * | 2023-02-10 | 2023-05-02 | 山东大学 | 甲硫氨酸在提高植物耐盐能力中的应用及方法 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08151304A (ja) * | 1994-11-28 | 1996-06-11 | Cosmo Sogo Kenkyusho:Kk | 植物の耐塩性向上剤 |
| JP2013075881A (ja) * | 2011-09-30 | 2013-04-25 | Fukui Prefectural Univ | 植物の生長促進及び耐塩性向上剤 |
| JP2013523795A (ja) * | 2010-04-06 | 2013-06-17 | バイエル・インテレクチユアル・プロパテイー・ゲー・エム・ベー・ハー | 植物のストレス耐性を増強させるための4−フェニル酪酸及び/又はその塩の使用 |
| JP2013237668A (ja) * | 2012-04-20 | 2013-11-28 | Shiseido Co Ltd | ケトール脂肪酸の包接化合物 |
-
2017
- 2017-01-13 JP JP2017003961A patent/JP6917046B2/ja active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08151304A (ja) * | 1994-11-28 | 1996-06-11 | Cosmo Sogo Kenkyusho:Kk | 植物の耐塩性向上剤 |
| JP2013523795A (ja) * | 2010-04-06 | 2013-06-17 | バイエル・インテレクチユアル・プロパテイー・ゲー・エム・ベー・ハー | 植物のストレス耐性を増強させるための4−フェニル酪酸及び/又はその塩の使用 |
| JP2013075881A (ja) * | 2011-09-30 | 2013-04-25 | Fukui Prefectural Univ | 植物の生長促進及び耐塩性向上剤 |
| JP2013237668A (ja) * | 2012-04-20 | 2013-11-28 | Shiseido Co Ltd | ケトール脂肪酸の包接化合物 |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2020054878A1 (ja) * | 2018-09-14 | 2020-03-19 | 積水化学工業株式会社 | 植物の耐塩性向上剤 |
| JPWO2020054878A1 (ja) * | 2018-09-14 | 2021-09-16 | 積水化学工業株式会社 | 植物の耐塩性向上剤 |
| JP7325429B2 (ja) | 2018-09-14 | 2023-08-14 | 積水化学工業株式会社 | 植物の耐塩性向上剤 |
| WO2020130145A1 (ja) * | 2018-12-21 | 2020-06-25 | アクプランタ株式会社 | 植物の耐熱性あるいは耐塩性向上剤 |
| JPWO2020130145A1 (ja) * | 2018-12-21 | 2021-11-04 | アクプランタ株式会社 | 植物の耐熱性あるいは耐塩性向上剤 |
| JP2024129096A (ja) * | 2018-12-21 | 2024-09-26 | アクプランタ株式会社 | 植物の耐熱性あるいは耐塩性向上剤 |
| JP7575777B2 (ja) | 2018-12-21 | 2024-10-30 | アクプランタ株式会社 | 植物の耐熱性あるいは耐塩性向上剤 |
| JP7804362B2 (ja) | 2018-12-21 | 2026-01-22 | アクプランタ株式会社 | 植物の耐熱性あるいは耐塩性向上剤 |
| CN116035006A (zh) * | 2023-02-10 | 2023-05-02 | 山东大学 | 甲硫氨酸在提高植物耐盐能力中的应用及方法 |
| CN116035006B (zh) * | 2023-02-10 | 2024-05-28 | 山东大学 | 甲硫氨酸在提高植物耐盐能力中的应用及方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP6917046B2 (ja) | 2021-08-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Hong et al. | Premature leaf senescence 3, encoding a methyltransferase, is required for melatonin biosynthesis in rice | |
| Dare et al. | Phenotypic changes associated with RNA interference silencing of chalcone synthase in apple (Malus× domestica) | |
| Kakkar et al. | Polyamine research in plants–a changing perspective | |
| Guan et al. | Diverse roles of strigolactone signaling in maize architecture and the uncoupling of a branching-specific subnetwork | |
| Lee et al. | Further characterization of a rice AGL12 group MADS-box gene, OsMADS26 | |
| Lange et al. | MTR4, a putative RNA helicase and exosome co‐factor, is required for proper rRNA biogenesis and development in Arabidopsis thaliana | |
| Guo et al. | MID1 plays an important role in response to drought stress during reproductive development | |
| EP1420630A2 (en) | Stress-related polynucleotides and polypeptides in plants | |
| Xu et al. | Sorbitol induces flower bud formation via the MADS‐box transcription factor EjCAL in loquat | |
| Li et al. | Overexpressing broccoli tryptophan biosynthetic genes BoTSB1 and BoTSB2 promotes biosynthesis of IAA and indole glucosinolates | |
| EP2820037B1 (en) | Modulation of seed vigor | |
| Imhof et al. | The small subunit 1 of the Arabidopsis isopropylmalate isomerase is required for normal growth and development and the early stages of glucosinolate formation | |
| JP6917046B2 (ja) | 植物の耐塩性向上剤 | |
| Zhou et al. | The cauliflower Orange gene enhances petiole elongation by suppressing expression of eukaryotic release factor 1 | |
| WO2025026473A1 (en) | A method for increasing plant resistance to stress, and stress resistant plants | |
| Meenu et al. | Genomic origin, expression differentiation and regulation of multiple genes encoding CYP83A1, a key enzyme for core glucosinolate biosynthesis, from the allotetraploid Brassica juncea | |
| JP2009540822A (ja) | 植物の構造及び成長を調節するための植物クロマチンリモデリング遺伝子の使用 | |
| Mei et al. | OsWRKY78 regulates panicle exsertion via gibberellin signaling pathway in rice | |
| WO2019201059A1 (zh) | 调控抗铝毒转录因子stop1蛋白的基因及其应用 | |
| Khodakovskaya et al. | Expression of ipt gene controlled by an ethylene and auxin responsive fragment of the LEACO1 promoter increases flower number in transgenic Nicotiana tabacum | |
| JPWO2018123651A1 (ja) | 植物の環境ストレス耐性向上剤 | |
| Hwang et al. | Over-expression of the IGI1 leading to altered shoot-branching development related to MAX pathway in Arabidopsis | |
| Forster et al. | Transgenic technologies for enhanced molecular breeding of white clover (Trifolium repens L.) | |
| US20250049032A1 (en) | Ethylene signaling activator modulates root system architecture | |
| Hua et al. | The Ethylene Response factor SmERF1 Improves Salinity Tolerance and Impacts Seed Size in Tobacco |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20191224 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210126 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210323 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210622 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210712 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6917046 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |