JP2017010842A - 非水系電解質二次電池用正極活物質とその製造方法、および該正極活物質を用いた非水系電解質二次電池 - Google Patents
非水系電解質二次電池用正極活物質とその製造方法、および該正極活物質を用いた非水系電解質二次電池 Download PDFInfo
- Publication number
- JP2017010842A JP2017010842A JP2015126718A JP2015126718A JP2017010842A JP 2017010842 A JP2017010842 A JP 2017010842A JP 2015126718 A JP2015126718 A JP 2015126718A JP 2015126718 A JP2015126718 A JP 2015126718A JP 2017010842 A JP2017010842 A JP 2017010842A
- Authority
- JP
- Japan
- Prior art keywords
- positive electrode
- active material
- electrode active
- lithium
- electrolyte secondary
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Abstract
【課題】ニッケル、コバルト、マンガンを含むリチウム過剰系金属複合酸化物を正極材に用いた場合に、高容量を維持するとともに、高い初期充放電効率、レート特性が得られる非水系電解質二次電池用正極活物質を提供する。【解決手段】ニッケルコバルトマンガン複合水酸化物あるいはニッケルコバルトマンガン複合酸化物にリチウム化合物を加え、混合・焼成を経て得られるリチウム過剰系金属複合酸化物の二次粒子を酸による洗浄を行いさらにある温度範囲で焙焼することで比表面積を高くした、高エネルギーを与えると酸素放出をするような容量に起因する酸素を出しやすい粉体を得ることを可能とする。【選択図】 なし
Description
本発明は、非水系電解質二次電池用正極活物質とその製造方法、および該正極活物質を用いた非水系電解質二次電池に関するものである。
近年、携帯電話やノート型パソコンなどの携帯電子機器の普及に伴い、高いエネルギー密度を有する小型で軽量な非水系電解質二次電池の開発、さらにはハイブリット自動車を始めとする電気自動車用の電池として高出力の二次電池が強く望まれている。
この要求を満たす二次電池として、リチウムイオン二次電池がある。このリチウムイオン二次電池は、負極および正極と電解液等で構成され、負極および正極の活物質は、リチウムを脱離および挿入することの可能な材料が用いられている。
この要求を満たす二次電池として、リチウムイオン二次電池がある。このリチウムイオン二次電池は、負極および正極と電解液等で構成され、負極および正極の活物質は、リチウムを脱離および挿入することの可能な材料が用いられている。
このリチウムイオン二次電池は、現在研究、開発が盛んに行われているところであるが、中でも、層状またはスピネル型のリチウム金属複合酸化物を正極材料に用いたリチウムイオン二次電池は、4V級の高い電圧が得られるため、高いエネルギー密度を有する電池として実用化が進んでいる。
これまで主に提案されている材料としては、合成が比較的容易なリチウムコバルト複合酸化物(LiCoO2)や、コバルトよりも安価なニッケルを用いたリチウムニッケル複合酸化物(LiNiO2)、リチウムニッケルコバルトマンガン複合酸化物(LiNi1/3Co1/3Mn1/3O2)、マンガンを用いたリチウムマンガン複合酸化物(LiMn2O4)などを挙げることができる。
これまで主に提案されている材料としては、合成が比較的容易なリチウムコバルト複合酸化物(LiCoO2)や、コバルトよりも安価なニッケルを用いたリチウムニッケル複合酸化物(LiNiO2)、リチウムニッケルコバルトマンガン複合酸化物(LiNi1/3Co1/3Mn1/3O2)、マンガンを用いたリチウムマンガン複合酸化物(LiMn2O4)などを挙げることができる。
このうちリチウムニッケル複合酸化物およびリチウムニッケルコバルトマンガン複合酸化物は、サイクル特性が良く、低抵抗で高出力が得られる材料として注目されており、近年では高出力化に必要な低抵抗化が重要視されている。
このリチウムニッケルコバルトマンガン複合酸化物の中でもさらに容量の高いリチウム過剰ニッケルコバルトマンガン複合酸化物には、抵抗が高いという課題以外に、初期の充放電効率が80%前後と他の正極活物質よりも10%以上低い問題があり、そのため余分な負極面積が必要となる課題があった。
このリチウムニッケルコバルトマンガン複合酸化物の中でもさらに容量の高いリチウム過剰ニッケルコバルトマンガン複合酸化物には、抵抗が高いという課題以外に、初期の充放電効率が80%前後と他の正極活物質よりも10%以上低い問題があり、そのため余分な負極面積が必要となる課題があった。
そこで、初期の充放電効率を改善したリチウム過剰ニッケルコバルトマンガン複合酸化物として、例えば、非特許文献1ではリチウム過剰系正極活物質を(NH4)2SO4水溶液中で攪拌後、水を除去することで表面に(NH4)2SO4をコートし、300℃で熱処理することで表面にLi2SO4を形成し、それを水洗・除去することで、表面にスピネルライク層を形成し、一次粒子サイズを減少させずにレート特性が向上することが記載されている。
しかしながら、出力特性としてのレート特性の向上に関して記載されているものの、初期の充放電効率に関して考慮したものとはなっていない。
しかしながら、出力特性としてのレート特性の向上に関して記載されているものの、初期の充放電効率に関して考慮したものとはなっていない。
また、非特許文献2では、リチウム過剰系正極活物質を0.1MのHNO3中で攪拌・ろ過・水洗後、100℃で乾燥することで、初回の不可逆容量が減少することが記載されている。一方、出力特性としてのレート特性は処理する前に比べて劣るとされ、高い出力と効率を両立したものとはなっていない。
一方、特許文献1では、リチウム過剰系正極活物質を水洗または0.1MのHNO3中で処理後、NH3ガス流通下、200℃で還元処理した正極活物質が開示されている。
この発明によれば、初回の不可逆容量が減少して充放電効率が増加するとされているが、レート特性については記載されておらず、出力特性に対する効果は不明である。
また、特許文献2では、リチウム過剰系正極活物質をpH5以上の溶液中で加熱処理した後、200℃以上900℃以下の温度で24時間以内熱処理することによって得られた一次粒子表面の二乗平均平方根粗さ(RMS)が1.5nm以下の正極活物質が開示されている。しかしながら、この発明においては、初回の充放電効率が高く、レート特性に優れるとされているが、更なる改善が期待されている。
この発明によれば、初回の不可逆容量が減少して充放電効率が増加するとされているが、レート特性については記載されておらず、出力特性に対する効果は不明である。
また、特許文献2では、リチウム過剰系正極活物質をpH5以上の溶液中で加熱処理した後、200℃以上900℃以下の温度で24時間以内熱処理することによって得られた一次粒子表面の二乗平均平方根粗さ(RMS)が1.5nm以下の正極活物質が開示されている。しかしながら、この発明においては、初回の充放電効率が高く、レート特性に優れるとされているが、更なる改善が期待されている。
Denis Y.W.Yu,Katsunori Yanagida,and Hiroshi Nakamura,Journal of The Electrochemical Society,157(2010)A1177−A1182
S.−H.Kang,C.S.Johnson,J.T.Vaughey,K.Amine,and M.M.Thackeray, Journal of The Electrochemical Society, 153(2006)A1186−A1192
本発明は、かかる問題点に鑑み、電池の正極活物質として用いられた場合に、高容量を維持するとともに、高い初期充放電効率と、優れたレート特性が得られる非水系電解質二次電池用正極活物質と、その正極活物質を用いた良好な電池特性を有する非水系電解質二次電池を提供する。
さらに、本発明では、上記非水系電解質二次電池用正極活物質の工業的な製造方法も提供する。
さらに、本発明では、上記非水系電解質二次電池用正極活物質の工業的な製造方法も提供する。
本発明者は、上記課題を解決するため、非水系電解質二次電池用正極活物質として用いられるリチウム過剰系のリチウム金属複合酸化物の粒子構造および粉体特性が、電池の初期充放電効率、サイクル特性に及ぼす影響について鋭意研究したところ、特定の粒子構造を有するとともに粒子構造が安定したリチウム過剰系金属複合酸化物は、電池の正極活物質として用いた際に高容量であり、初期充放電効率が高く、優れたレート特性を実現できるとの知見を得た。
さらに、リチウム過剰系金属複合酸化物粉末を、酸洗浄によって粒子構造を維持したままリチウム濃度を下げ、その後、熱処理することでスピネルライク層を形成させることで粒子構造の安定化が可能であるとの知見を得て、本発明を完成させるに至った。
さらに、リチウム過剰系金属複合酸化物粉末を、酸洗浄によって粒子構造を維持したままリチウム濃度を下げ、その後、熱処理することでスピネルライク層を形成させることで粒子構造の安定化が可能であるとの知見を得て、本発明を完成させるに至った。
すなわち、本発明の第1の発明は、一般式:Li1+uNixCoyMnzAtO2+α(0.1≦u<0.3、0.03≦x≦0.25、0.03≦y≦0.25、0.4≦z<0.6、0<x+y、x+y+z+u+t=1、0≦α<0.3、0≦t<0.1、Aは2価から6価までの価数のいずれかをとる金属元素のうち少なくとも1種以上とする)で表され、一次粒子および該一次粒子が凝集した二次粒子で構成されたリチウム過剰系金属複合酸化物粒子からなる非水系電解質二次電池用正極活物質であって、それぞれの元素の価数をLi=1、Ni=2、Co=3、Mn=4、O=2として算出したOの価数計(OV)に対するLi、Ni、Co、およびMnの価数計の合計(MV)の比として算出した価数比(MV/OV)が0.95〜1.05であり、Heガス雰囲気中でTG−MS測定を行った際の、600〜800℃の範囲における酸素由来の質量減少率が0.3〜2.0%であることを特徴とする非水系電解質二次電池用正極活物質である。
本発明の第2の発明は、第1の発明におけるリチウム過剰系金属複合酸化物粒子が、粉末X線回折測定において、M2を金属元素として表されるスピネル型酸化物LiM2 2O4由来の(400)面のピークを2θ=43〜45°の範囲に有し、M3を金属元素として表される層状化合物Li2M3O3由来の(020)、(110)面のピークを2θ=20〜22°の範囲に有することを特徴とする非水系電解質二次電池用正極活物質である。
本発明の第3の発明は、第2の発明におけるリチウム過剰系金属複合酸化物粒子が、M1、M2、M3をそれぞれ金属元素として一般式:pLiM1O2・qLiM2 2O4・(1−p−q)Li2M3O3で表され、粉末X線回折測定において得られる回折ピークから半定量分析して得られるpおよびqの値が、0.4≦p≦0.6、0.02≦q≦0.08であることを特徴とする非水系電解質二次電池用正極活物質である。
本発明の第4の発明は、第1から第3の発明におけるリチウム過剰系金属複合酸化物粒子の比表面積が3.0〜8.0m2/gであることを特徴とする非水系電解質二次電池用正極活物質である。
本発明の第5の発明は、第1から第4の発明におけるリチウム過剰系金属複合酸化物粒子の平均粒径D50が3〜10μm、最大径Dmaxが50μm未満、且つタップ密度が1.5〜2.4g/cm3であることを特徴とする非水系電解質二次電池用正極活物質である。
本発明の第6の発明は、一般式:Li1+uNixCoyMnzAtO2+α(0.1≦u<0.3、0.03≦x≦0.25、0.03≦y≦0.25、0.4≦z<0.6、0<x+y、x+y+z+u+t=1、0≦α<0.3、0≦t<0.1、Aは2価から6価までの価数のいずれかをとる金属元素のうち少なくとも1種以上とする)で表され、一次粒子および該一次粒子が凝集した二次粒子で構成されたリチウム過剰系金属複合酸化物粒子からなる非水系電解質二次電池用正極活物質の製造方法であって、少なくともニッケル、コバルト、マンガンを含む水酸化物、オキシ水酸化物、酸化物、及び炭酸塩の少なくとも1種からなる一次粒子が凝集した二次粒子とリチウム化合物を混合してリチウム混合物を得る混合工程と、前記リチウム混合物を、酸化性雰囲気中にて800〜1050℃の温度で焼成して焼成物を得る焼成工程と、その焼成物に酸を添加して形成したスラリーを用いて、酸洗前後での焼成物のリチウム含有量の差を酸洗前の焼成物のリチウム含有量で除したリチウム除去率が10〜30%となるように制御して酸洗を焼成物に施した後、水洗して酸洗ケーキを得る酸洗工程と、その酸洗ケーキを、酸化性雰囲気中にて200〜500℃の温度で熱処理する熱処理工程とを含むことを特徴とする非水系電解質二次電池用正極活物質の製造方法である。
本発明の第7の発明は、第6の発明における焼成工程において、得られる焼成物の二次粒子の平均粒径D50が、3〜10μm、最大径Dmaxが50μm未満、且つタップ密度が1.5〜2.4g/m3であることを特徴とする非水系電解質二次電池用正極活物質の製造方法である。
本発明の第8の発明は、第6及び第7の発明における酸洗工程において用いる酸が、0.5〜5Nの濃度である無機酸を用いることを特徴とする非水系電解質二次電池用正極活物質の製造方法である。
本発明の第9の発明は、第8の発明における無機酸が、塩酸または硫酸であることを特徴とする非水系電解質二次電池用正極活物質の製造方法である。
本発明の第10の発明は、第8及び第9の発明における酸洗工程において、前記焼成物をpH1〜4の無機酸に投入することを特徴とする非水系電解質二次電池用正極活物質の製造方法である。
本発明の第11の発明は、第6〜第10の発明における酸洗工程において、酸洗する際のスラリー濃度が、100〜1500g/Lであることを特徴とする非水系電解質二次電池用正極活物質の製造方法である。
本発明の第12の発明は、第1〜第5の発明における非水系電解質二次電池用正極活物質を含む正極を具備することを特徴とする非水系電解質二次電池である。
本発明によれば、電池の正極活物質に用いた場合に、高容量を維持するとともに初期充放電効率が高くかつ、レート特性に優れた非水系電解質二次電池用正極活物質が得られる。また、その正極活物質を用いた正極を有する非水系電解質二次電池は、優れた電池特性を有したものとなる。
さらに、その製造方法は、容易で工業的規模での生産に適したものであり、工業的価値が極めて大きい。
さらに、その製造方法は、容易で工業的規模での生産に適したものであり、工業的価値が極めて大きい。
以下、本発明について、まず本発明の正極活物質について説明した後、その製造方法と本発明による正極活物質を用いた非水系電解質二次電池について説明する。
(1)正極活物質
本発明の非水系電解質二次電池用正極活物質(以下、単に正極活物質という)は、一般式:Li1+uNixCoyMnzAtO2+α(0.1≦u<0.3、0.03≦x≦0.25、0.03≦y≦0.25、0.4≦z<0.6、0<x+y、x+y+z+u+t=1、0≦α<0.3、0≦t<0.1、Aは2価から6価までの価数のいずれかをとる金属元素のうち少なくとも1種以上とする)で表され、一次粒子および該一次粒子が凝集した二次粒子で構成されたリチウム過剰系金属複合酸化物粒子からなるものである。
本発明の非水系電解質二次電池用正極活物質(以下、単に正極活物質という)は、一般式:Li1+uNixCoyMnzAtO2+α(0.1≦u<0.3、0.03≦x≦0.25、0.03≦y≦0.25、0.4≦z<0.6、0<x+y、x+y+z+u+t=1、0≦α<0.3、0≦t<0.1、Aは2価から6価までの価数のいずれかをとる金属元素のうち少なくとも1種以上とする)で表され、一次粒子および該一次粒子が凝集した二次粒子で構成されたリチウム過剰系金属複合酸化物粒子からなるものである。
このリチウム過剰系金属複合酸化物粒子は、Li以外の金属元素をM1、M3とした一般式によって表されるLiM1O2とLi2M3O3とからなり、好ましくはLi2M3O3のM3をMnとしたLiM1O2とLi2MnO3とからなり、より好ましくはこれらの固溶体であり、正極活物質全体としてのリチウムの過剰量、すなわち、リチウム過剰系金属複合酸化物がLiM1O2からなるとして算出したリチウムの過剰量を低減したものである。
LiM1O2からなるとして算出したリチウムの過剰量を低減することにより、LiM1O2とLi2M3O3とからなるリチウム過剰系金属複合酸化物であっても、初期充電時にリチウム過剰系金属複合酸化物粒子から引き抜くことが必要なリチウム原子の量と放電時にリチウム過剰系金属複合酸化物粒子に挿入されるリチウム原子の量との差を抑制することが可能となり、高い初期充放電効率を得ることができる。
LiM1O2からなるとして算出したリチウムの過剰量を低減することにより、LiM1O2とLi2M3O3とからなるリチウム過剰系金属複合酸化物であっても、初期充電時にリチウム過剰系金属複合酸化物粒子から引き抜くことが必要なリチウム原子の量と放電時にリチウム過剰系金属複合酸化物粒子に挿入されるリチウム原子の量との差を抑制することが可能となり、高い初期充放電効率を得ることができる。
すなわち、LiM1O2からなるとして算出したリチウムの過剰量が多いと、初期充電時に引き抜くことが必要なリチウム原子の量が、本来LiM2O2のLi席からリチウムを引き抜いて充電するために必要な量より、過剰分だけ多くなり、充電量が多くなってしまう。一方、放電時はLi席にリチウムが挿入されるのみであるため、放電量が少なくなり、初期の充電量に対する放電量の効率である初期充放電効率が低下する。また、Li2M3O3は、結晶構造上、充電時に引き抜いたLiの量と同量のLiが放電時に挿入されないため、初期充放電効率が低下する。
したがって、リチウムの過剰量を低減することにより、充電時にLiM1O2から過剰なリチウムを引き抜くために用いられる充電量と、Li2M3O3において放電時に挿入されないLiを予め低減することで、Li席からリチウムを引く抜くことに充電量が効率的に用いられ、初期充放電効率を向上することが可能となる。
したがって、リチウムの過剰量を低減することにより、充電時にLiM1O2から過剰なリチウムを引き抜くために用いられる充電量と、Li2M3O3において放電時に挿入されないLiを予め低減することで、Li席からリチウムを引く抜くことに充電量が効率的に用いられ、初期充放電効率を向上することが可能となる。
そこで、正極活物質全体としてのリチウム(Li)の過剰量を示す上記一般式におけるuを0.1以上、0.3未満の範囲とすることで、LiM1O2とLi2M3O3とからなり、正極活物質全体としてのリチウムの過剰量を、高い初期充放電効率が得られるまでに低減することができる。
そのuが0.1未満になると、正極活物質を構成するリチウム過剰系金属複合酸化物粒子中の層状化合物(LiM1O2)のリチウム含有量が少なくなり過ぎて、高い放電容量が得られない。一方、uが0.3以上では、正極活物質全体としてのリチウムの過剰量が大きくなりすぎるため、初期充電時にリチウム過剰系金属複合酸化物粒子から過大に過剰量のリチウム原子を引き抜くことが必要となって、放電時にリチウム過剰系金属複合酸化物粒子に挿入されるリチウム原子の量との差が大きくなり、初期充放電効率が低下する。
そのuが0.1未満になると、正極活物質を構成するリチウム過剰系金属複合酸化物粒子中の層状化合物(LiM1O2)のリチウム含有量が少なくなり過ぎて、高い放電容量が得られない。一方、uが0.3以上では、正極活物質全体としてのリチウムの過剰量が大きくなりすぎるため、初期充電時にリチウム過剰系金属複合酸化物粒子から過大に過剰量のリチウム原子を引き抜くことが必要となって、放電時にリチウム過剰系金属複合酸化物粒子に挿入されるリチウム原子の量との差が大きくなり、初期充放電効率が低下する。
また、本発明の正極活物質は、それぞれの元素の価数をLi=1、Ni=2、Co=3、Mn=4、O=2として算出したOの価数計(OV)に対するLi、Ni、Co、およびMnの価数計の合計(MV)の比として算出した価数比(MV/OV)が0.95〜1.05である。価数をこの範囲に制御することにより、Li席からリチウムを引く抜くことに充電量が効率的に用いられ、初期充放電効率を向上することが可能となる。
すなわち、価数比が0.95未満になると、リチウムの過剰量が過度に少なくなった状態を示し、放電容量が低下する。一方、価数比が1.05を超えると、リチウムの過剰量が多く、放電時にリチウム過剰系金属複合酸化物粒子に挿入されるリチウム原子の量との差が大きくなり、初期充放電効率が低下する。
すなわち、価数比が0.95未満になると、リチウムの過剰量が過度に少なくなった状態を示し、放電容量が低下する。一方、価数比が1.05を超えると、リチウムの過剰量が多く、放電時にリチウム過剰系金属複合酸化物粒子に挿入されるリチウム原子の量との差が大きくなり、初期充放電効率が低下する。
価数比は、例えば以下のようにして算出することができる。正極活物質の上記一般式中の金属成分と不純物元素(S、Ca、Si、Mg等)の含有量をICP発光分光法により分析する。さらに、カール・フィッシャー滴定法により水分量、高周波燃焼−赤外吸収法により炭素含有量を測定し、正極活物質から金属成分と不純物元素、水分量および炭素含有量を差し引いた残りを酸素量とし、それぞれの元素の価数を上記数値として価数に組成比を乗じて価数比を算出する。
さらに、正極活物質のHeガス雰囲気中でTG−MS測定を行った際の、600〜800℃の範囲における酸素由来の質量減少率が0.3〜2.0%である。質量減少率が0.3%未満であると、結晶構造が安定してLi2M3O3の反応抵抗が上昇し高容量を発現し難くなる。
また、2.0%を超えると、初期の高容量には繋がるが、結晶構造が崩れて粒子表面がアモルファス化するため、抵抗が再び上昇してレート特性が悪化する。TG−MS測定における昇温速度は、例えば、20℃/分とすることが好ましい。これにより、600〜800℃の範囲における酸素由来の質量減少率を高い精度で測定することができる。
また、2.0%を超えると、初期の高容量には繋がるが、結晶構造が崩れて粒子表面がアモルファス化するため、抵抗が再び上昇してレート特性が悪化する。TG−MS測定における昇温速度は、例えば、20℃/分とすることが好ましい。これにより、600〜800℃の範囲における酸素由来の質量減少率を高い精度で測定することができる。
上記LiM1O2とLi2M3O3とからなるリチウム過剰系金属複合酸化物粒子で構成されたものであれば、高容量かつ高い初期充放電効率が得られるが、粉末X線回折測定において、M2を金属元素として表されるスピネル型酸化物LiM2 2O4由来の(400)面のピークを2θ=43〜45°の範囲に有し、M3を金属元素として表される層状化合物Li2M3O3由来の(020)、(110)面のピークを2θ=20〜22°の範囲に有することが好ましい。
そのスピネル相は、一次粒子表面に形成され、一次粒子間の粒界に存在する空隙を埋めて一次粒子間の結合力を強化し、充放電を繰り返した際に生じる粒子崩壊による孤立粒子発生および体積膨張収縮を抑え、サイクル特性を高めると考えられる。
また、2.5〜3.0Vの領域において放電量を増加させ、低電圧領域までの放電量を利用することにより、従来より高容量の電池が得られる。放電容量が増加するため、初期充放電効率もさらに向上させることが可能である。
粉末X線回折測定において、スピネル型酸化物LiM2 2O4由来のピークと、層状化合物Li2M3O3由来のピークを有する状態とすることで、十分な量のLiM2 2O4およびLi2M3O3とリチウムの過剰量が低減されたLiM1O2とからなるものとすることができ、より高い電池容量を得ることができる。
また、2.5〜3.0Vの領域において放電量を増加させ、低電圧領域までの放電量を利用することにより、従来より高容量の電池が得られる。放電容量が増加するため、初期充放電効率もさらに向上させることが可能である。
粉末X線回折測定において、スピネル型酸化物LiM2 2O4由来のピークと、層状化合物Li2M3O3由来のピークを有する状態とすることで、十分な量のLiM2 2O4およびLi2M3O3とリチウムの過剰量が低減されたLiM1O2とからなるものとすることができ、より高い電池容量を得ることができる。
さらに、そのリチウム過剰系金属複合酸化物粒子が、M1、M2、M3をそれぞれ金属元素とし、一般式:pLiM1O2・qLiM2 2O4・(1−p−q)Li2M3O3で表され、粉末X線回折測定において得られる回折ピークから半定量分析して得られるpおよびqの値が、0.4≦p≦0.6、0.02≦q≦0.08であることがより好ましい。
上記一般式におけるxは、正極活物質全体、すなわち、リチウム過剰系金属複合酸化物粒子全体としてのニッケル(Ni)の含有量を示すものである。
xを0.03以上、0.25以下の範囲とすることで、電池に用いた際に高容量と高出力が得られる。xが0.03未満になると、Li2M3O3が多くなり過ぎ、電池に用いた際に抵抗が増加するため高出力が得られない。一方、xが0.25を超えると、Li2M3O3が少なくなり過ぎ、電池に用いた際に高容量が得られない。
上記一般式におけるxは、正極活物質全体、すなわち、リチウム過剰系金属複合酸化物粒子全体としてのニッケル(Ni)の含有量を示すものである。
xを0.03以上、0.25以下の範囲とすることで、電池に用いた際に高容量と高出力が得られる。xが0.03未満になると、Li2M3O3が多くなり過ぎ、電池に用いた際に抵抗が増加するため高出力が得られない。一方、xが0.25を超えると、Li2M3O3が少なくなり過ぎ、電池に用いた際に高容量が得られない。
また、正極活物質全体としてのコバルト(Co)の含有量を示す上記一般式におけるyの範囲を0.03以上、0.25以下とすることで、電池に用いた際に優れたサイクル特性と高出力が得られる。
yが0.03未満になると、LiM1O2の結晶構造の安定に寄与するコバルトが少なくなり、サイクル特性が悪化する。一方、yが0.25を超えると、Li2M3O3が少なくなり過ぎ、電池に用いた際に高容量が得られない。
yが0.03未満になると、LiM1O2の結晶構造の安定に寄与するコバルトが少なくなり、サイクル特性が悪化する。一方、yが0.25を超えると、Li2M3O3が少なくなり過ぎ、電池に用いた際に高容量が得られない。
さらに、一般式におけるzは、正極活物質全体としてのマンガン(Mn)の含有量を示すもので、MnはLi2M3O3を構成する元素であり、zにより形成されるLi2M3O3量を制御することができる。zを0.4以上、0.6未満の範囲とすることで、電池に用いた際に高容量と高出力が得られる。
zが0.4未満になると、Li2M3O3が少なくなり過ぎ、電池に用いた際に高容量が得られない。一方、zが0.6以上では、Li2M3O3、特にLi2MnO3が多くなり過ぎ、電池に用いた際に抵抗が増加するため高出力が得られない。
zが0.4未満になると、Li2M3O3が少なくなり過ぎ、電池に用いた際に高容量が得られない。一方、zが0.6以上では、Li2M3O3、特にLi2MnO3が多くなり過ぎ、電池に用いた際に抵抗が増加するため高出力が得られない。
次に、上記一般式におけるtは、正極活物質全体としての添加元素Aの含有量を示すものである。
この添加元素Aは、電池特性を改善するために添加されるものであるが、tが0.1以上になると、Li2M3O3やLiM1O2が少なくなり過ぎ、電池に用いた際に高容量が得られない。
また添加元素Aは、2価から6価までの価数のいずれかをとる金属元素からなる群から選択される少なくとも1種であるが、電池特性を改善する効果が高いAl、Ti、Mg、W、Nb、Moからなる群から選択される少なくとも1種であることが好ましい。
この添加元素Aは、電池特性を改善するために添加されるものであるが、tが0.1以上になると、Li2M3O3やLiM1O2が少なくなり過ぎ、電池に用いた際に高容量が得られない。
また添加元素Aは、2価から6価までの価数のいずれかをとる金属元素からなる群から選択される少なくとも1種であるが、電池特性を改善する効果が高いAl、Ti、Mg、W、Nb、Moからなる群から選択される少なくとも1種であることが好ましい。
これまで説明してきた正極活物質は、十分な量のLi2M3O3とLiMO2とにより構成され、リチウム過剰系金属複合酸化物粒子全体としてリチウムの過剰量が低減されたことにより効果が得られるものであり、上記一般式に示される組成範囲であれば、添加元素による効果と上記効果が両立できることを確認している。
その正極活物質は、ほぼ全量を一次粒子が凝集した二次粒子で構成されるが、その二次粒子から剥がれた一次粒子の存在を含む一次粒子および該一次粒子が凝集した二次粒子で構成されたリチウム過剰系金属複合酸化物粒子からなる。一次粒子が凝集した二次粒子で構成されることで、比表面積が大きくなり一次粒子間に電解液が侵入可能な間隙が形成され、二次粒子内部まで電解液の浸透が可能であり、電解液とリチウム過剰系金属複合酸化物粒子の反応面積が増加するため、高い電池容量と出力特性が得られる。
その正極活物質は、ほぼ全量を一次粒子が凝集した二次粒子で構成されるが、その二次粒子から剥がれた一次粒子の存在を含む一次粒子および該一次粒子が凝集した二次粒子で構成されたリチウム過剰系金属複合酸化物粒子からなる。一次粒子が凝集した二次粒子で構成されることで、比表面積が大きくなり一次粒子間に電解液が侵入可能な間隙が形成され、二次粒子内部まで電解液の浸透が可能であり、電解液とリチウム過剰系金属複合酸化物粒子の反応面積が増加するため、高い電池容量と出力特性が得られる。
また、一次粒子が板状粒子であることが好ましく、板状粒子は、粒子径が大きくなっても粒子内部から電解液と反応する粒子表面までの距離が短く維持されるとともに粒子間の接触面積も高くすることが可能であるため、高い電池容量と出力特性を得るために有利である。
一方、通常の活物質の多くの構成に見られる球状若しくは略球状の一次粒子では、比表面積を大きくするとともに、粒子表面までの距離を短くするためには微細化する必要があり、微細化し、かつ電解液が侵入可能な間隙を形成させると、一次粒子間の接触面積が少なくなり、粒界抵抗の増加を招いたり、電極充填性を損ねるなど高出力、高容量を引き出せなくなる問題が生ずることがある。さらに、上記球状若しくは略球状などの一次粒子で構成された二次粒子の粒径を小さくしても、二次粒子間で同様に高出力、高容量を引き出せなくなる問題が生ずる。
本発明に係る正極活物質の比表面積は、3.0〜8.0m2/gであり、電解液とリチウム過剰系金属複合酸化物粒子の反応面積が大きく、界面抵抗が小さくなるため、高い電池容量と出力特性を得ることができる。
比表面積が3.0m2/g未満では、反応面積が不足して高い電池容量と出力特性を得ることができない。一方、比表面積が8.0m2/gを超えると、正極を得る際に電極に塗布するスラリーの製造における混練工程において、ゲル化を引き起こしやすくなる。また、NMPに代表される有機溶剤を多量に使うことになり、工業的に適さない。
比表面積が3.0m2/g未満では、反応面積が不足して高い電池容量と出力特性を得ることができない。一方、比表面積が8.0m2/gを超えると、正極を得る際に電極に塗布するスラリーの製造における混練工程において、ゲル化を引き起こしやすくなる。また、NMPに代表される有機溶剤を多量に使うことになり、工業的に適さない。
さらに、この正極活物質においては、二次粒子の平均粒径D50が3〜10μm、最大径Dmaxが50μm未満であり、タップ密度が1.5〜2.4g/cm3であることが好ましい。
この二次粒子の平均粒径D50、最大径Dmax、及びタップ密度を、上記範囲とすることで、充填性を高めて電池の容積当たりの充放電容量を高めるとともに、反応面積を確保して優れた出力特性を得ることができる。
二次粒子の平均粒径D50が3μm未満では、充填性が低下して電池の容積当たりの電池容量が低下することがある。また、二次粒子間の接触面積が少なくなる問題も生じる。一方、平均粒径D50が10μmを超えると、電解液と接触面積が少なくなって前記反応面積が不足することがある。
また、最大径Dmaxが50μm以上になると、電池を製造する際に均一な正極膜を得ることができず、電池特性が低下することがある。
さらに、タップ密度が1.5g/cm3未満になると、正極への充填性が十分に得られないことがある。一方、タップ密度が2.4g/cm3を超えると、一次粒子間の空隙が少なくなり、電解液とリチウム過剰系金属複合酸化物粒子の接触面積が十分に得られないことがある。
二次粒子の平均粒径D50が3μm未満では、充填性が低下して電池の容積当たりの電池容量が低下することがある。また、二次粒子間の接触面積が少なくなる問題も生じる。一方、平均粒径D50が10μmを超えると、電解液と接触面積が少なくなって前記反応面積が不足することがある。
また、最大径Dmaxが50μm以上になると、電池を製造する際に均一な正極膜を得ることができず、電池特性が低下することがある。
さらに、タップ密度が1.5g/cm3未満になると、正極への充填性が十分に得られないことがある。一方、タップ密度が2.4g/cm3を超えると、一次粒子間の空隙が少なくなり、電解液とリチウム過剰系金属複合酸化物粒子の接触面積が十分に得られないことがある。
(2)正極活物質の製造方法
本発明に係る製造方法は、一般式:Li1+uNixCoyMnzAtO2+α(0.1≦u<0.3、0.03≦x≦0.25、0.03≦y≦0.25、0.4≦z<0.6、0<x+y、x+y+z+u+t=1、0≦α<0.3、0≦t<0.1、Aは2価から6価までの価数のいずれかをとる金属元素のうち少なくとも1種以上とする)で表され、一次粒子が凝集した二次粒子で構成されたリチウム過剰系金属複合酸化物粒子からなる非水系電解質二次電池用正極活物質の製造方法で、少なくともニッケル、コバルト、マンガンを含む水酸化物、オキシ水酸化物、酸化物、及び炭酸塩の少なくとも1種からなる一次粒子が凝集した二次粒子とリチウム化合物を混合し焼成して得られた焼成物を、酸洗前後での焼成物のリチウム含有量の差を酸洗前の焼成物のリチウム含有量で除したリチウム除去率を、10〜30%に制御して酸洗した後、酸化性雰囲気中にて200〜500℃の温度で熱処理することに特徴を有するものである。
本発明に係る製造方法は、一般式:Li1+uNixCoyMnzAtO2+α(0.1≦u<0.3、0.03≦x≦0.25、0.03≦y≦0.25、0.4≦z<0.6、0<x+y、x+y+z+u+t=1、0≦α<0.3、0≦t<0.1、Aは2価から6価までの価数のいずれかをとる金属元素のうち少なくとも1種以上とする)で表され、一次粒子が凝集した二次粒子で構成されたリチウム過剰系金属複合酸化物粒子からなる非水系電解質二次電池用正極活物質の製造方法で、少なくともニッケル、コバルト、マンガンを含む水酸化物、オキシ水酸化物、酸化物、及び炭酸塩の少なくとも1種からなる一次粒子が凝集した二次粒子とリチウム化合物を混合し焼成して得られた焼成物を、酸洗前後での焼成物のリチウム含有量の差を酸洗前の焼成物のリチウム含有量で除したリチウム除去率を、10〜30%に制御して酸洗した後、酸化性雰囲気中にて200〜500℃の温度で熱処理することに特徴を有するものである。
特に、酸による洗浄で、活物質全体のリチウム濃度を酸洗前後で10〜30%下げ、リチウム過剰系金属複合酸化物粒子を得るために過剰に添加されたリチウムを粒子表面及び粒内から除去することで、充電時に過剰なリチウムを引き抜くために用いられる充電量を抑制することができ、初期充放電効率を向上させることが可能となる。
さらに、この酸洗により、一次粒子径を小さくすることなく、その比表面積を3.0〜8.0m2/gと高くすることもできる。
さらに、この酸洗により、一次粒子径を小さくすることなく、その比表面積を3.0〜8.0m2/gと高くすることもできる。
これらにより、リチウム過剰系金属複合酸化物を用いることにより得られる高い充放電容量と、比表面積増加による界面抵抗の低減だけでなく、過剰なリチウムの除去による初期充放電効率の向上を実現させるものである。
そのリチウム除去率が10%未満の場合、洗浄不足で充電容量はあまり改善されず、初期充放電効率は高くならない。また、30%を超えた洗浄をすると初期充放電効率は100%を超えるまでに達するが、過度の洗浄によってLiとのプロトン置換が激しく起こり始め、充電容量が抑制されるとともに放電容量まで大幅に低下してしまうため、本来有する高容量の優位性を失ってしまう。
そのリチウム除去率が10%未満の場合、洗浄不足で充電容量はあまり改善されず、初期充放電効率は高くならない。また、30%を超えた洗浄をすると初期充放電効率は100%を超えるまでに達するが、過度の洗浄によってLiとのプロトン置換が激しく起こり始め、充電容量が抑制されるとともに放電容量まで大幅に低下してしまうため、本来有する高容量の優位性を失ってしまう。
一般的に、比表面積を高める手法としては、焼成温度を下げるあるいは焼結防止剤を添加して一次粒子径を小さくする、二次粒子径を小さくするといったことが挙げられる。しかし、これらの方法では高出力、高容量を引き出せなくなる問題が生じてしまう。
そこで、本発明においては、リチウム過剰系金属複合酸化物粒子を強酸で酸洗することで二次粒子を形成する一次粒子の表面を溶解し、凹凸を形成させることで、抵抗に大きく影響する比表面積を飛躍的に上昇させ、電解液との接触面を増やすことで高出力に係わる界面抵抗を下げることを可能とするものである。また、二次粒子径を構成する要素である、一次粒子径や二次粒子径自体に変化を与えないため、出力特性や電池容量を阻害することはない。
さらに、このようなリチウム過剰系金属複合酸化物を酸洗浄することにより、初期充放電効率を向上させるだけでなく、その後200〜500℃で熱処理することにより、サイクル特性を高めるものである。
さらに、このようなリチウム過剰系金属複合酸化物を酸洗浄することにより、初期充放電効率を向上させるだけでなく、その後200〜500℃で熱処理することにより、サイクル特性を高めるものである。
即ち、酸洗によるリチウムの除去では、二次粒子を形成する一次粒子間の界面に存在していたLiリッチ層が溶解したことにより、その界面に空隙が生じるため、充放電サイクルを繰り返すと二次粒子が崩壊し、二次粒子を形成しない一次粒子や微細な二次粒子(これらをまとめて孤立粒子という)が発生して充放電容量が下がり、サイクル特性が低下する問題があり、サイクル特性を高めるためには、このような孤立粒子を生じないように、一次粒子間の結合を強固なものとしておく必要がある。200〜500℃で熱処理することにより、一次粒子間の結合を強固なものとすることができる。
さらに、酸洗後の熱処理の温度は、300〜500℃とすることが好ましい。これにより、一次粒子表面にスピネル相を形成させ、サイクル特性を高めるとともに放電容量を増加させ、放電初期充放電効率を向上させることができる。
本発明の酸洗工程では、過剰なリチウムのみでなく、層状化合物であるLiM1O2のLi層からもLiが幾分か引き抜かれる。その後、酸化性雰囲気中での熱処理により、Liに対するMの比がLiM1O2より少ないスピネル相(LiM2 2O4)を形成する反応が進行し、一次粒子表面にスピネル相が形成され、一次粒子間をさらに強固に結合して孤立粒子発生および体積膨張収縮を抑制することが可能となり、放電容量が増加するため、初期充放電効率もさらに向上させることができる。
本発明の酸洗工程では、過剰なリチウムのみでなく、層状化合物であるLiM1O2のLi層からもLiが幾分か引き抜かれる。その後、酸化性雰囲気中での熱処理により、Liに対するMの比がLiM1O2より少ないスピネル相(LiM2 2O4)を形成する反応が進行し、一次粒子表面にスピネル相が形成され、一次粒子間をさらに強固に結合して孤立粒子発生および体積膨張収縮を抑制することが可能となり、放電容量が増加するため、初期充放電効率もさらに向上させることができる。
以下、本発明の非水系電解質二次電池用正極活物質の製造方法を工程ごとに詳細に説明する。
[混合工程]
混合工程は、少なくともニッケル、コバルト、マンガンを含む水酸化物、オキシ水酸化物、酸化物、炭酸塩の少なくとも1種からなる一次粒子が凝集した二次粒子とリチウム化合物を混合してリチウム混合物を得る工程である。
混合工程は、少なくともニッケル、コバルト、マンガンを含む水酸化物、オキシ水酸化物、酸化物、炭酸塩の少なくとも1種からなる一次粒子が凝集した二次粒子とリチウム化合物を混合してリチウム混合物を得る工程である。
本発明の正極活物質は、板状の一次粒子が凝集した二次粒子で構成されたリチウム過剰系金属複合酸化物粒子からなるものである。このような正極活物質の粒子構造は、原料となる水酸化物、オキシ水酸化物、酸化物、炭酸塩(以下、これらを合わせて原料化合物という)の構造を継承するため、原料化合物の構造を板状の一次粒子が凝集した二次粒子とすることが必要である。原料化合物の中でも、上記構造を有するものが容易に得られる水酸化物、オキシ水酸化物、酸化物の少なくとも1種が好ましい。
さらに、これらの原料化合物の粒子構造を制御することにより、正極活物質としての好ましい態様を実現することができる。すなわち、二次粒子の平均粒径D50が3〜10μm、最大径Dmaxが50μm未満であることが好ましい。
さらに、これらの原料化合物の粒子構造を制御することにより、正極活物質としての好ましい態様を実現することができる。すなわち、二次粒子の平均粒径D50が3〜10μm、最大径Dmaxが50μm未満であることが好ましい。
上記正極活物質は、上記一般式にあるようにマンガンを含むため、例えば、晶析法により金属塩水溶液を中和して水酸化物粒子を得る際に、非酸化性にして一次粒子を発達させることで、上記構造を有する水酸化物粒子が得られ、その晶析条件を制御することにより上記特性を有する粒子とすることができ、板状粒子とすることも可能である。
さらに、この水酸化物粒子を酸化させることで、オキシ水酸化物粒子あるいは酸化物粒子を得る。
また、この正極活物質は、リチウム混合物中の金属元素の組成比も継承するため、リチウム混合物中の組成比を、一般式における金属元素の組成比と同様にする。したがって、原料化合物として一般式と同様の組成比を有するものを用いるとよい。また、添加元素などで被覆され、粒子全体として一般式と同様の組成比を有するものを用いることもでき、リチウム混合物中に添加元素の化合物を別途添加して組成を調整することも可能である。
さらに、この水酸化物粒子を酸化させることで、オキシ水酸化物粒子あるいは酸化物粒子を得る。
また、この正極活物質は、リチウム混合物中の金属元素の組成比も継承するため、リチウム混合物中の組成比を、一般式における金属元素の組成比と同様にする。したがって、原料化合物として一般式と同様の組成比を有するものを用いるとよい。また、添加元素などで被覆され、粒子全体として一般式と同様の組成比を有するものを用いることもでき、リチウム混合物中に添加元素の化合物を別途添加して組成を調整することも可能である。
本発明の製造方法においては、リチウム過剰系金属複合酸化物粒子から余剰のリチウムの酸洗による除去を特徴とするものであり、焼成物中にLi2M3O3が生成されればよいが、リチウム混合物中のリチウム以外の金属元素の合計(Me)に対するリチウム(Li)の比(Li/Me)が1.25〜1.85となるように混合することが好ましい。これにより、焼成物中にLi2M3O3を十分に生成させ、得られた正極活物質を電池に用いた際に高い放電容量が得られる。
このLi/Meが1.25未満であると、得られた正極活物質中のLi2M3O3が少なくなりすぎて、放電容量が低下してしまうことがある。また、Li/Meが1.85を超えると、不活性なLi2MO3が多くなって電気的特性が落ちて正極活物質の初期放電容量が低下するとともに、正極の反応抵抗も増加してしまうことがある。
このLi/Meが1.25未満であると、得られた正極活物質中のLi2M3O3が少なくなりすぎて、放電容量が低下してしまうことがある。また、Li/Meが1.85を超えると、不活性なLi2MO3が多くなって電気的特性が落ちて正極活物質の初期放電容量が低下するとともに、正極の反応抵抗も増加してしまうことがある。
混合機については、均一にする必要があるため、一般的な混合機を使用することも可能であるが、シェーカーミキサーやVブレンダーではなく、ジュリアミキサーやスパルタンリューザーやノビルタといった攪拌羽根を有し高速精密混合が可能な装置を用いることがより好ましい。
[焼成工程]
焼成工程は、混合工程で得られたリチウム混合物を、酸化性雰囲気中にて800〜1050℃の温度で焼成して焼成物を得る工程である。
この工程により、一次粒子が凝集した二次粒子で構成されたリチウム過剰系金属複合酸化物粒子が得られる。
焼成工程は、混合工程で得られたリチウム混合物を、酸化性雰囲気中にて800〜1050℃の温度で焼成して焼成物を得る工程である。
この工程により、一次粒子が凝集した二次粒子で構成されたリチウム過剰系金属複合酸化物粒子が得られる。
その焼成温度が800℃未満になると、結晶性が非常に低く、電池特性として放電容量の低い正極活物質となる。また、1050℃を超えると、焼結による粒成長が激しくなり、比表面積が大幅に低下し、放電容量が低い正極活物質となってしまう。
焼成時の雰囲気は、酸化性雰囲気であればよいが、安価で取扱いが容易な大気雰囲気とすることが好ましい。
焼成時に用いられる炉は、通常のリチウム過剰系金属複合酸化物が製造可能な炉であればよく、バッチ式の焼成炉やローラーハースキルンなどの連続炉を用いることができる。
焼成時の雰囲気は、酸化性雰囲気であればよいが、安価で取扱いが容易な大気雰囲気とすることが好ましい。
焼成時に用いられる炉は、通常のリチウム過剰系金属複合酸化物が製造可能な炉であればよく、バッチ式の焼成炉やローラーハースキルンなどの連続炉を用いることができる。
得られる正極活物質の粒子構造は、焼成工程によって得られる焼成物と同様となる。したがって、使用した原料化合物と上記焼成条件の制御により、好ましい態様を有する焼成物が得られる。得られる焼成物の好ましい態様としては、一次粒子が凝集した二次粒子で構成されたリチウム過剰系金属複合酸化物粒子であり、一次粒子が板状であることがより好ましい。
[酸洗工程]
酸洗工程は、焼成工程で得られた焼成物を、酸洗前後での焼成物のリチウム含有量の差を酸洗前の焼成物のリチウム含有量で除したリチウム除去率を10〜30%に制御して酸洗した後、水洗する工程で、得られた焼成物を酸により洗浄することで、充電容量を抑制し、90%以上という高い初期充放電効率に至らせる。また、二次粒子を形成する一次粒子の表面に凹凸を形成させることで、一次粒子を微細化することなく比表面積を高くすることを可能とし、反応抵抗(界面抵抗)の小さい活物質が得られるのである。
酸洗工程は、焼成工程で得られた焼成物を、酸洗前後での焼成物のリチウム含有量の差を酸洗前の焼成物のリチウム含有量で除したリチウム除去率を10〜30%に制御して酸洗した後、水洗する工程で、得られた焼成物を酸により洗浄することで、充電容量を抑制し、90%以上という高い初期充放電効率に至らせる。また、二次粒子を形成する一次粒子の表面に凹凸を形成させることで、一次粒子を微細化することなく比表面積を高くすることを可能とし、反応抵抗(界面抵抗)の小さい活物質が得られるのである。
ここで、リチウム除去率は、下記化学式(1)により算出した過剰なLiの溶解に用いられる酸の量を予備実験により補正して、酸洗における酸の必要量を求め、求めた酸の必要量を混合して酸洗することにより制御することができる。予備実験により決められれば、酸の種類や酸洗時間などの条件によって酸の必要量は安定しており、容易にリチウム除去率を制御することが可能である。
この酸洗に用いる酸は、リチウム除去率を10〜30%とするため、0.5〜5Nの濃度である無機酸を用いることが好ましい。
酸の濃度が0.5N未満では、リチウム除去率が10%未満になることがある。一方、酸の濃度が5Nを越えると、溶解力が高い酸を用いた場合、リチウム除去率が30%を超えることがある。
また、解離定数の高い強酸性を示す酸が好ましく、塩酸、硝酸、硫酸などの無機酸のいずれかとすることがより好ましく、塩酸、硫酸のいずれかとすることがさらに好ましい。
塩酸、硫酸は非酸化性の酸であり、酸化性の酸である硝酸より焼成物に対する溶解力が弱く、余剰リチウムを焼成物から引き抜いて除去するが、焼成物自体の溶解を抑える。一方、硝酸を用いると焼成物自体を溶解して十分な比表面積が得られないおそれがある。
酸の濃度が0.5N未満では、リチウム除去率が10%未満になることがある。一方、酸の濃度が5Nを越えると、溶解力が高い酸を用いた場合、リチウム除去率が30%を超えることがある。
また、解離定数の高い強酸性を示す酸が好ましく、塩酸、硝酸、硫酸などの無機酸のいずれかとすることがより好ましく、塩酸、硫酸のいずれかとすることがさらに好ましい。
塩酸、硫酸は非酸化性の酸であり、酸化性の酸である硝酸より焼成物に対する溶解力が弱く、余剰リチウムを焼成物から引き抜いて除去するが、焼成物自体の溶解を抑える。一方、硝酸を用いると焼成物自体を溶解して十分な比表面積が得られないおそれがある。
そこで、強酸を用いない場合、結晶構造からリチウムを引き抜くことが難しく、また一次粒子の表面に微細な凹凸を形成するだけの溶解を引き起こせないため、界面抵抗を下げることが出来ないことがある。さらに、酢酸以上に分子量の大きい有機酸を用いた場合は粒子表面にカーボン由来の不純物が付着・残留して抵抗成分となることがあり好ましくない。カーボン付着を防止するためには無機酸を用いることが好ましい。
酸洗工程においては、このような無機酸を用いた場合、焼成物を投入する際の酸の25℃基準におけるpH(以下、単にpHということがある)が1〜4となるように制御することが好ましい。これにより、酸の溶解力を適正にして、比表面積の制御とプロトン交換の抑制を容易にすることができる。
酸の溶解力が弱くなり過ぎる、具体的にはpHが4を超えると、3.0m2/g以上の比表面積が得られないことがある。また、リチウム除去率も10%未満になることがある。一方、酸の溶解力が強くなり過ぎる、具体的にはpHが1未満になると、焼成物自体が溶解し、一次粒子間の結合力が低下するとともに比表面積が大きくなり過ぎることがある。また、プロトン交換が起こりやすくなる。
酸の溶解力が弱くなり過ぎる、具体的にはpHが4を超えると、3.0m2/g以上の比表面積が得られないことがある。また、リチウム除去率も10%未満になることがある。一方、酸の溶解力が強くなり過ぎる、具体的にはpHが1未満になると、焼成物自体が溶解し、一次粒子間の結合力が低下するとともに比表面積が大きくなり過ぎることがある。また、プロトン交換が起こりやすくなる。
酸洗する際のスラリー濃度は、100〜1500g/Lとすることが好ましい。
スラリー濃度を薄くしすぎると、酸洗浄に長い時間がかかりプロトン交換が進んで放電容量の低下が起こることがある。一方、濃すぎると、酸の反応が局所的に激しく起こりやすく、全体が均一なリチウム濃度になるのを妨げる要因になるため好ましくない。
スラリー濃度を薄くしすぎると、酸洗浄に長い時間がかかりプロトン交換が進んで放電容量の低下が起こることがある。一方、濃すぎると、酸の反応が局所的に激しく起こりやすく、全体が均一なリチウム濃度になるのを妨げる要因になるため好ましくない。
酸洗後、さらに水洗、ろ過するが、後工程で熱処理するため、ろ過したままの状態でもよいが、乾燥させることが好ましい。
乾燥雰囲気は、大気雰囲気あるいは真空雰囲気とすることが好ましい。その乾燥温度は80〜200℃程度でよく、完全に乾燥させる必要はないが、80℃未満では、乾燥後においても水分率が高過ぎて後工程の熱処理時にリチウム過剰系金属複合酸化物粒子が凝集することがあり、好ましくない。200℃を超えても効果がない。
乾燥雰囲気は、大気雰囲気あるいは真空雰囲気とすることが好ましい。その乾燥温度は80〜200℃程度でよく、完全に乾燥させる必要はないが、80℃未満では、乾燥後においても水分率が高過ぎて後工程の熱処理時にリチウム過剰系金属複合酸化物粒子が凝集することがあり、好ましくない。200℃を超えても効果がない。
[熱処理工程]
熱処理工程は、酸洗工程後の焼成物を、酸化性雰囲気中にて200〜500℃の温度で熱処理する工程である。この熱処理工程により、一次粒子間の結合を強固なものとすることができる。
200℃未満では、一次粒子間の結合が弱く、サイクル特性を向上させることができない。一方、500℃を超えた場合は、二次粒子の焼結が進行するとともに一次粒子表面も結晶成長が進むため、比表面積が小さくなり過ぎて電池特性の低下を招いてしまう。
熱処理工程は、酸洗工程後の焼成物を、酸化性雰囲気中にて200〜500℃の温度で熱処理する工程である。この熱処理工程により、一次粒子間の結合を強固なものとすることができる。
200℃未満では、一次粒子間の結合が弱く、サイクル特性を向上させることができない。一方、500℃を超えた場合は、二次粒子の焼結が進行するとともに一次粒子表面も結晶成長が進むため、比表面積が小さくなり過ぎて電池特性の低下を招いてしまう。
そこで、さらに熱処理の温度は、300〜500℃とすることが好ましい。これにより、一次粒子表面にスピネル相を形成させ、一次粒子間の結合をさらに高めて、サイクル特性を高めるとともに放電容量を増加させ、放電初期充放電効率を向上させることができる。
(3)非水系電解質二次電池
本発明の非水系電解質二次電池は、正極、負極および非水系電解液などからなり、一般の非水系電解質二次電池と同様の構成要素により構成される。
なお、以下で説明する実施形態は例示に過ぎず、本発明の非水系電解質二次電池は、本明細書に記載されている実施形態を基に、当業者の知識に基づいて種々の変更、改良を施した形態で実施することができる。また、本発明の非水系電解質二次電池は、その用途を特に限定するものではない。
本発明の非水系電解質二次電池は、正極、負極および非水系電解液などからなり、一般の非水系電解質二次電池と同様の構成要素により構成される。
なお、以下で説明する実施形態は例示に過ぎず、本発明の非水系電解質二次電池は、本明細書に記載されている実施形態を基に、当業者の知識に基づいて種々の変更、改良を施した形態で実施することができる。また、本発明の非水系電解質二次電池は、その用途を特に限定するものではない。
(a)正極
先に述べた非水系電解質二次電池用正極活物質を用いて、例えば、以下のようにして、非水系電解質二次電池の正極を作製する。
まず、粉末状の正極活物質、導電材、結着剤を混合し、さらに必要に応じて活性炭、粘度調整等の目的の溶剤を添加し、これを混練して正極合材ペーストを作製する。
その正極合材ペースト中のそれぞれの混合比も、非水系電解質二次電池の性能を決定する重要な要素となる。溶剤を除いた正極合材の固形分の全質量を100質量部とした場合、一般の非水系電解質二次電池の正極と同様、正極活物質の含有量を60〜95質量部とし、導電材の含有量を1〜20質量部とし、結着剤の含有量を1〜20質量部とすることが望ましい。
先に述べた非水系電解質二次電池用正極活物質を用いて、例えば、以下のようにして、非水系電解質二次電池の正極を作製する。
まず、粉末状の正極活物質、導電材、結着剤を混合し、さらに必要に応じて活性炭、粘度調整等の目的の溶剤を添加し、これを混練して正極合材ペーストを作製する。
その正極合材ペースト中のそれぞれの混合比も、非水系電解質二次電池の性能を決定する重要な要素となる。溶剤を除いた正極合材の固形分の全質量を100質量部とした場合、一般の非水系電解質二次電池の正極と同様、正極活物質の含有量を60〜95質量部とし、導電材の含有量を1〜20質量部とし、結着剤の含有量を1〜20質量部とすることが望ましい。
得られた正極合材ペーストを、例えば、アルミニウム箔製の集電体の表面に塗布し、乾燥して、溶剤を飛散させる。必要に応じ、電極密度を高めるべく、ロールプレス等により加圧することもある。このようにして、シート状の正極を作製することができる。
このシート状の正極は、目的とする電池に応じて適当な大きさに裁断等をして、電池の作製に供することができる。ただし、正極の作製方法は、例示のものに限られることなく、他の方法によってもよい。
このシート状の正極は、目的とする電池に応じて適当な大きさに裁断等をして、電池の作製に供することができる。ただし、正極の作製方法は、例示のものに限られることなく、他の方法によってもよい。
正極の作製にあたって、導電材としては、例えば、黒鉛(天然黒鉛、人造黒鉛、膨張黒鉛など)や、アセチレンブラック、ケッチェンブラック(登録商標)などのカーボンブラック系材料などを用いることができる。
結着剤は、活物質粒子をつなぎ止める役割を果たすもので、例えば、ポリフッ化ビニリデン(PVDF)、ポリテトラフルオロエチレン(PTFE)、フッ素ゴム、エチレンプロピレンジエンゴム、スチレンブタジエン、セルロース系樹脂、ポリアクリル酸などを用いることができる。
なお、必要に応じ、正極活物質、導電材、活性炭を分散させ、結着剤を溶解する溶剤を正極合材に添加する。
結着剤は、活物質粒子をつなぎ止める役割を果たすもので、例えば、ポリフッ化ビニリデン(PVDF)、ポリテトラフルオロエチレン(PTFE)、フッ素ゴム、エチレンプロピレンジエンゴム、スチレンブタジエン、セルロース系樹脂、ポリアクリル酸などを用いることができる。
なお、必要に応じ、正極活物質、導電材、活性炭を分散させ、結着剤を溶解する溶剤を正極合材に添加する。
溶剤としては、具体的には、N−メチル−2−ピロリドン等の有機溶剤を用いることができる。
また、正極合材には、電気二重層容量を増加させるために、活性炭を添加することができる。
また、正極合材には、電気二重層容量を増加させるために、活性炭を添加することができる。
(b)負極
負極には、金属リチウムやリチウム合金等、あるいは、リチウムイオンを吸蔵および脱離できる負極活物質に、結着剤を混合し、適当な溶剤を加えてペースト状にした負極合材を、銅等の金属箔集電体の表面に塗布、乾燥して必要に応じて電極密度を高めるべく圧縮して形成したものを使用する。
負極には、金属リチウムやリチウム合金等、あるいは、リチウムイオンを吸蔵および脱離できる負極活物質に、結着剤を混合し、適当な溶剤を加えてペースト状にした負極合材を、銅等の金属箔集電体の表面に塗布、乾燥して必要に応じて電極密度を高めるべく圧縮して形成したものを使用する。
負極活物質としては、例えば、天然黒鉛、人造黒鉛、フェノール樹脂等の有機化合物焼成体、コークス等の炭素物質の粉状体を用いることができる。この場合、負極結着剤としては、正極同様、PVDF等の含フッ素樹脂等を用いることができ、これらの活物質および結着剤を分散させる溶剤としては、N−メチル−2−ピロリドン等の有機溶剤を用いることができる。
(c)セパレータ
正極と負極との間には、セパレータを挟み込んで配置する。
使用するセパレータは、正極と負極とを分離し、電解質を保持するものであり、ポリエチレン、ポリプロピレン等の薄い膜で、微少な孔を多数有する膜を用いることができる。
正極と負極との間には、セパレータを挟み込んで配置する。
使用するセパレータは、正極と負極とを分離し、電解質を保持するものであり、ポリエチレン、ポリプロピレン等の薄い膜で、微少な孔を多数有する膜を用いることができる。
(d)非水系電解液
非水系電解液は、支持塩としてのリチウム塩を有機溶媒に溶解したものである。
有機溶媒としては、エチレンカーボネート、プロピレンカーボネート、ブチレンカーボネート、トリフルオロプロピレンカーボネート等の環状カーボネート、また、ジエチルカーボネート、ジメチルカーボネート、エチルメチルカーボネート、ジプロピルカーボネート等の鎖状カーボネート、さらに、テトラヒドロフラン、2−メチルテトラヒドロフラン、ジメトキシエタン等のエーテル化合物、エチルメチルスルホン、ブタンスルトン等の硫黄化合物、リン酸トリエチル、リン酸トリオクチル等のリン化合物等から選ばれる1種を単独で、あるいは2種以上を混合して用いることができる。
支持塩としては、LiPF6、LiBF4、LiClO4、LiAsF6、LiN(CF3SO2)2等、およびそれらの複合塩を用いることができる。
さらに、非水系電解液は、ラジカル捕捉剤、界面活性剤および難燃剤等を含んでいてもよい。
非水系電解液は、支持塩としてのリチウム塩を有機溶媒に溶解したものである。
有機溶媒としては、エチレンカーボネート、プロピレンカーボネート、ブチレンカーボネート、トリフルオロプロピレンカーボネート等の環状カーボネート、また、ジエチルカーボネート、ジメチルカーボネート、エチルメチルカーボネート、ジプロピルカーボネート等の鎖状カーボネート、さらに、テトラヒドロフラン、2−メチルテトラヒドロフラン、ジメトキシエタン等のエーテル化合物、エチルメチルスルホン、ブタンスルトン等の硫黄化合物、リン酸トリエチル、リン酸トリオクチル等のリン化合物等から選ばれる1種を単独で、あるいは2種以上を混合して用いることができる。
支持塩としては、LiPF6、LiBF4、LiClO4、LiAsF6、LiN(CF3SO2)2等、およびそれらの複合塩を用いることができる。
さらに、非水系電解液は、ラジカル捕捉剤、界面活性剤および難燃剤等を含んでいてもよい。
(e)電池の形状、構成
以上のように説明してきた正極、負極、セパレータおよび非水系電解液で構成される本発明の非水系電解質二次電池の形状は、円筒型、積層型等、種々のものとすることができる。
いずれの形状を採る場合であっても、正極および負極を、セパレータを介して積層させて電極体とし、得られた電極体に、非水系電解液を含浸させ、正極集電体と外部に通ずる正極端子との間、および、負極集電体と外部に通ずる負極端子との間を、集電用リード等を用いて接続し、電池ケースに密閉して、非水系電解質二次電池を完成させる。
以上のように説明してきた正極、負極、セパレータおよび非水系電解液で構成される本発明の非水系電解質二次電池の形状は、円筒型、積層型等、種々のものとすることができる。
いずれの形状を採る場合であっても、正極および負極を、セパレータを介して積層させて電極体とし、得られた電極体に、非水系電解液を含浸させ、正極集電体と外部に通ずる正極端子との間、および、負極集電体と外部に通ずる負極端子との間を、集電用リード等を用いて接続し、電池ケースに密閉して、非水系電解質二次電池を完成させる。
(f)特性
本発明の正極活物質を用いた非水系電解質二次電池は、高容量で高出力となる。
特により好ましい形態で得られた本発明による正極活物質を用いた非水系電解質二次電池は、例えば、2032型コイン電池の正極に用いた場合、250mAh/g以上の高い初期放電容量と85%以上の高い初期充放電効率が得られ、さらにレート特性にも優れたものである。また、熱安定性が高く、安全性においても優れているといえる。
本発明の正極活物質を用いた非水系電解質二次電池は、高容量で高出力となる。
特により好ましい形態で得られた本発明による正極活物質を用いた非水系電解質二次電池は、例えば、2032型コイン電池の正極に用いた場合、250mAh/g以上の高い初期放電容量と85%以上の高い初期充放電効率が得られ、さらにレート特性にも優れたものである。また、熱安定性が高く、安全性においても優れているといえる。
本発明により得られた正極活物質を用いた正極を有する二次電池について、その性能(初期放電容量、初期充放電効率、レート特性)を測定した。
以下、本発明の実施例を用いて具体的に説明するが、本発明は、これらの実施例によって何ら限定されるものではない。
以下、本発明の実施例を用いて具体的に説明するが、本発明は、これらの実施例によって何ら限定されるものではない。
(電池の製造および評価)
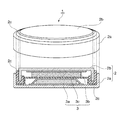
正極活物質の評価には、図1に示す2032型コイン電池1(以下、コイン型電池と称す)を使用した。
コイン型電池1は、ケース2と、このケース2内に収容された電極3とから構成されている。
ケース2は、中空かつ一端が開口された正極缶2aと、この正極缶2aの開口部に配置される負極缶2bとを有しており、負極缶2bを正極缶2aの開口部に配置すると、負極缶2bと正極缶2aとの間に電極3を収容する空間が形成されるように構成されている。
電極3は、正極3a、セパレータ3cおよび負極3bとからなり、この順で並ぶように積層されており、正極3aが正極缶2aの内面に接触し、負極3bが負極缶2bの内面に接触するようにケース2に収容されている。
なお、ケース2はガスケット2cを備えており、このガスケット2cによって、正極缶2aと負極缶2bとの間が非接触の状態を維持するように相対的な移動が固定されている。また、ガスケット2cは、正極缶2aと負極缶2bとの隙間を密封してケース2内と外部との間を気密液密に遮断する機能も有している。
正極活物質の評価には、図1に示す2032型コイン電池1(以下、コイン型電池と称す)を使用した。
コイン型電池1は、ケース2と、このケース2内に収容された電極3とから構成されている。
ケース2は、中空かつ一端が開口された正極缶2aと、この正極缶2aの開口部に配置される負極缶2bとを有しており、負極缶2bを正極缶2aの開口部に配置すると、負極缶2bと正極缶2aとの間に電極3を収容する空間が形成されるように構成されている。
電極3は、正極3a、セパレータ3cおよび負極3bとからなり、この順で並ぶように積層されており、正極3aが正極缶2aの内面に接触し、負極3bが負極缶2bの内面に接触するようにケース2に収容されている。
なお、ケース2はガスケット2cを備えており、このガスケット2cによって、正極缶2aと負極缶2bとの間が非接触の状態を維持するように相対的な移動が固定されている。また、ガスケット2cは、正極缶2aと負極缶2bとの隙間を密封してケース2内と外部との間を気密液密に遮断する機能も有している。
図1に示すコイン型電池1は、以下のようにして製作した。
まず、非水系電解質二次電池用正極活物質52.5mg、アセチレンブラック15mg、およびポリテトラフッ化エチレン樹脂(PTFE)7.5mgを混合し、直径10mmで10mg程度の重量になるまで薄膜化して、正極3aを作製した。作製した正極3aを真空乾燥機中120℃で12時間乾燥した。
この正極3aと、負極3b、セパレータ3cおよび電解液とを用いて、上述したコイン型電池1を、露点が−80℃に管理されたAr雰囲気のグローブボックス内で作製した。
なお、負極3bには、直径14mmの円盤状に打ち抜かれた平均粒径20μm程度の黒鉛粉末とポリフッ化ビニリデンが銅箔に塗布された負極シートを用いた。
セパレータ3cには膜厚25μmのポリエチレン多孔膜を用いた。電解液には、1MのLiPF6を支持電解質とするエチレンカーボネート(EC)とジエチルカーボネート(DEC)の3:7混合液(富山薬品工業株式会社製)を用いた。
まず、非水系電解質二次電池用正極活物質52.5mg、アセチレンブラック15mg、およびポリテトラフッ化エチレン樹脂(PTFE)7.5mgを混合し、直径10mmで10mg程度の重量になるまで薄膜化して、正極3aを作製した。作製した正極3aを真空乾燥機中120℃で12時間乾燥した。
この正極3aと、負極3b、セパレータ3cおよび電解液とを用いて、上述したコイン型電池1を、露点が−80℃に管理されたAr雰囲気のグローブボックス内で作製した。
なお、負極3bには、直径14mmの円盤状に打ち抜かれた平均粒径20μm程度の黒鉛粉末とポリフッ化ビニリデンが銅箔に塗布された負極シートを用いた。
セパレータ3cには膜厚25μmのポリエチレン多孔膜を用いた。電解液には、1MのLiPF6を支持電解質とするエチレンカーボネート(EC)とジエチルカーボネート(DEC)の3:7混合液(富山薬品工業株式会社製)を用いた。
作製したコイン型電池1の性能を示す初期放電容量、初期充放電効率、レート特性は、以下のように評価した。
初期放電容量は、コイン型電池1を製作してから24時間程度放置し、開回路電圧OCV(Open Circuit Voltage)が安定した後、正極の理論容量を270mAh/gとしたときの0.05Cに相当する電流を電流値としてカットオフ電圧4.8Vまで充電し、1時間の休止後、カットオフ電圧2.5Vまで放電したときの容量を初期放電容量とし、充電に対する放電の容量比(%)を初期充放電効率(初期効率)とした。
初期放電容量は、コイン型電池1を製作してから24時間程度放置し、開回路電圧OCV(Open Circuit Voltage)が安定した後、正極の理論容量を270mAh/gとしたときの0.05Cに相当する電流を電流値としてカットオフ電圧4.8Vまで充電し、1時間の休止後、カットオフ電圧2.5Vまで放電したときの容量を初期放電容量とし、充電に対する放電の容量比(%)を初期充放電効率(初期効率)とした。
レート特性は、負荷効率により評価した。電圧範囲2.0から4.55Vにおいて、正極の理論容量を270mAh/gとしたときの0.1Cで充放電した際の放電容量を分母に、充電0.1C放電2Cで行ったときの放電容量を分子としたときの割合(%)を負荷効率とした。
(価数比)
正極活物質の金属成分および不純物元素(Ni、Co、Mn、S、Ca、Si、Mg)の含有量をICP発光分光法、水分量を300℃カール・フィッシャー滴定法により、炭素含有量を高周波燃焼‐赤外吸収法によりを測定し、正極活物質から金属成分と不純物元素、水分量および炭素含有量を差し引いた残りを酸素量とし、組成比を求めた。
それぞれの元素の価数をLi=1、Ni=2、Co=3、Mn=4、O=2とし、得られた組成比を乗じて各元素の価数値を求め、価数比は、そのようにして求めたOの価数値(OV)に対するLi、Ni、Co、およびMnの価数値の合計(MV)の比として価数比(MV/OV)を算出した。
正極活物質の金属成分および不純物元素(Ni、Co、Mn、S、Ca、Si、Mg)の含有量をICP発光分光法、水分量を300℃カール・フィッシャー滴定法により、炭素含有量を高周波燃焼‐赤外吸収法によりを測定し、正極活物質から金属成分と不純物元素、水分量および炭素含有量を差し引いた残りを酸素量とし、組成比を求めた。
それぞれの元素の価数をLi=1、Ni=2、Co=3、Mn=4、O=2とし、得られた組成比を乗じて各元素の価数値を求め、価数比は、そのようにして求めたOの価数値(OV)に対するLi、Ni、Co、およびMnの価数値の合計(MV)の比として価数比(MV/OV)を算出した。
(酸素質量減少率)
Heガス雰囲気中でのTG−MS測定により求めた。測定温度範囲は600〜800℃とし、その間の昇温速度は20℃/分とした。
Heガス雰囲気中でのTG−MS測定により求めた。測定温度範囲は600〜800℃とし、その間の昇温速度は20℃/分とした。
(結晶構造)
粉末X線回折測定により、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、及び2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークの存在の有無を確認した。
また、得られた回折ピークから半定量分析し、正極活物質をpLiM1O2・qLiM2 2O4・(1−p−q)Li2M3O3として表した際のp及びqを求めた。
粉末X線回折測定により、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、及び2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークの存在の有無を確認した。
また、得られた回折ピークから半定量分析し、正極活物質をpLiM1O2・qLiM2 2O4・(1−p−q)Li2M3O3として表した際のp及びqを求めた。
(比表面積)
BET1点法により測定した。
BET1点法により測定した。
予め40℃に加温した純水の入った反応槽に硫酸ニッケルと硫酸コバルト、硫酸マンガンの水和物の結晶を純水に溶解した混合原液(金属元素モル比でNi:Co:Mn=2:1:7)、アンモニア水を規定の流量で滴下しつつpHを11.5に維持するよう水酸化ナトリウム水溶液を滴下することで反応晶析によって、まず前駆体であるニッケルコバルトマンガン複合水酸化物スラリーを生成させた。
生成した複合水酸化物を、ろ過、乾燥して粉末を得た。
次に、得られた粉末化した複合水酸化物中のニッケル、コバルト、マンガンの原子数の総量に対して150原子%の量になるように計算して秤量した炭酸リチウムを、スパルタンリューザーで複合水酸化物と混合し、リチウム混合物を作製した。
このときの複合水酸化物の平均粒子径は6.4μmであった。
次に、得られた粉末化した複合水酸化物中のニッケル、コバルト、マンガンの原子数の総量に対して150原子%の量になるように計算して秤量した炭酸リチウムを、スパルタンリューザーで複合水酸化物と混合し、リチウム混合物を作製した。
このときの複合水酸化物の平均粒子径は6.4μmであった。
次に、雰囲気を大気とし、950℃で10時間保持するように焼成を行い、リチウム過剰系金属複合酸化物を得た。このリチウム過剰系金属複合酸化物に対し、液温25℃基準のpHで2.3に調整した塩酸を用い、リチウムを17%除去するように塩酸の必要量を算出して混合、洗浄した。その後、水洗、ろ過後に、真空雰囲気中200℃で乾燥させた。
さらに、大気雰囲気中400℃で1時間保持することで熱処理し、リチウム過剰系金属複合酸化物粒子からなる正極活物質を得た。
さらに、大気雰囲気中400℃で1時間保持することで熱処理し、リチウム過剰系金属複合酸化物粒子からなる正極活物質を得た。
得られた正極活物質の結晶構造を、粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.05であった。
さらに比表面積測定、TG−MS測定、価数比測定、電池評価を行った。得られた特性結果を表1に示す。
塩酸のpHを3.8とした以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.04であった。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.04であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
酸洗浄後の熱処理温度を400℃から300℃に変更した以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.06であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.06であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
酸洗浄後の熱処理温度を400℃から500℃に変更した以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.4、q=0.07であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.4、q=0.07であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
塩酸のpHを1.9とし、さらにリチウム除去率が27%となるように溶液量を増やして酸洗浄したこと以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.4、q=0.07であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.4、q=0.07であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
複合水酸化物の組成がモル比 Ni:Co:Mn:Al=1.95:0.95:6.95:0.15となるように、反応晶析においてアルミン酸ナトリウム溶液を添加した以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.05であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.05であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
正極活物質のLi以外の金属元素のモル比がNi:Co:Mn:Mg=1.85:1:7:0.15となるように、混合工程において酸化マグネシウム(MgO)を混合してリチウム混合物を得た以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.05であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.05であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
正極活物質のLi以外の金属元素のモル比がNi:Co:Mn:Ti=2:1:6.85:0.15となるように、混合工程において酸化チタン(TiO2)を混合してリチウム混合物を得た以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.05であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.05であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
正極活物質のLi以外の金属元素のモル比がNi:Co:Mn:W=1.99:0.99:6.99:0.03となるように、混合工程において酸化タングステン(WO3)を混合してリチウム混合物を得た以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.05であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.05であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
(比較例1)
酸洗浄後の熱処理温度を400℃から150℃に変更した以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認されたが、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピークの存在は確認されなかった。また、得られた回折ピークから半定量分析して求めたpは、p=0.5であったが、スピネル型酸化物LiM2 2O4由来の(111)面のピークの存在が確認されなかったため、q=0.00とした。比表面積測定、TG−MS測定、価数比測定、特性評価で得られた特性結果を表1に示す。
酸洗浄後の熱処理温度を400℃から150℃に変更した以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認されたが、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピークの存在は確認されなかった。また、得られた回折ピークから半定量分析して求めたpは、p=0.5であったが、スピネル型酸化物LiM2 2O4由来の(111)面のピークの存在が確認されなかったため、q=0.00とした。比表面積測定、TG−MS測定、価数比測定、特性評価で得られた特性結果を表1に示す。
(比較例2)
酸洗浄後の熱処理温度を400℃から700℃に変更した以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.4、q=0.09であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
酸洗浄後の熱処理温度を400℃から700℃に変更した以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.4、q=0.09であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
(比較例3)
塩酸のpHを5.9とした以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.01であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
塩酸のpHを5.9とした以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.5、q=0.01であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
(比較例4)
塩酸のpHを2.2とし、さらにリチウム除去率が36%となるように溶液量を増やして酸洗浄したこと以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.6、q=0.09であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
塩酸のpHを2.2とし、さらにリチウム除去率が36%となるように溶液量を増やして酸洗浄したこと以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピーク、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認された。また、得られた回折ピークから半定量分析して求めたp及びqは、p=0.6、q=0.09であった。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
(比較例5)
塩酸による酸洗を実施しなかった以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認されたが、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピークの存在は確認されなかった。また、得られた回折ピークから半定量分析して求めたpは、p=0.5であったが、スピネル型酸化物LiM2 2O4由来の(111)面のピークの存在が確認されなかったため、q=0.00とした。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
塩酸による酸洗を実施しなかった以外は、実施例1と同様にして正極活物質を得て、特性評価した。
得られた正極活物質の結晶構造を粉末X線回折測定により確認したところ、2θ=20〜22°の範囲において層状化合物Li2M3O3由来の(020)、(110)面のピークが存在することが確認されたが、2θ=43〜45°の範囲においてスピネル型酸化物LiM2 2O4由来の(400)面のピークの存在は確認されなかった。また、得られた回折ピークから半定量分析して求めたpは、p=0.5であったが、スピネル型酸化物LiM2 2O4由来の(111)面のピークの存在が確認されなかったため、q=0.00とした。
比表面積測定、TG−MS測定、価数比測定、電池評価で得られた特性結果を表1に示す。
本発明の非水系二次電池は、高容量の優れた電気特性を有することから、最近の携帯電話やノート型パソコンなどの携帯電子機器などの高エネルギー密度が要求される小型電源装置として好適である。
また、本発明の非水系二次電池は、優れた安全性を有することから、純粋に電気エネルギーで駆動される電気自動車、ガソリンエンジンやディーゼルエンジンなどの燃焼機関と併用するハイブリッド自動車もしくはプラグインハイブリッド自動車などの大型電源装置としても好適に用いることができる。
また、本発明の非水系二次電池は、優れた安全性を有することから、純粋に電気エネルギーで駆動される電気自動車、ガソリンエンジンやディーゼルエンジンなどの燃焼機関と併用するハイブリッド自動車もしくはプラグインハイブリッド自動車などの大型電源装置としても好適に用いることができる。
1 コイン型電池
2 ケース
2a 正極缶
2b 負極缶
2c ガスケット
3 電極
3a 正極
3b 負極
3c セパレータ
2 ケース
2a 正極缶
2b 負極缶
2c ガスケット
3 電極
3a 正極
3b 負極
3c セパレータ
Claims (12)
- 一般式:Li1+uNixCoyMnzAtO2+α(0.1≦u<0.3、0.03≦x≦0.25、0.03≦y≦0.25、0.4≦z<0.6、0<x+y、x+y+z+u+t=1、0≦α<0.3、0≦t<0.1、Aは2価から6価までの価数のいずれかをとる金属元素のうち少なくとも1種以上とする)で表され、一次粒子および該一次粒子が凝集した二次粒子で構成されたリチウム過剰系金属複合酸化物粒子からなる非水系電解質二次電池用正極活物質であって、
それぞれの元素の価数をLi=1、Ni=2、Co=3、Mn=4、O=2として算出したOの価数値(OV)に対するLi、Ni、Co、およびMnの価数値の合計(MV)の比として算出した価数比(MV/OV)が0.95〜1.05であり、Heガス雰囲気中でTG−MS測定を行った際の、600〜800℃の範囲における酸素由来の質量減少率が0.3〜2.0%であることを特徴とする非水系電解質二次電池用正極活物質。 - 前記リチウム過剰系金属複合酸化物粒子が、粉末X線回折測定において、M2を金属元素として表されるスピネル型酸化物LiM2 2O4由来の(400)面のピークを2θ=43〜45°の範囲に有し、M3を金属元素として表される層状化合物Li2M3O3由来の(020)、(110)面のピークを2θ=20〜22°の範囲に有することを特徴とする請求項1に記載の非水系電解質二次電池用正極活物質。
- 前記リチウム過剰系金属複合酸化物粒子が、M1、M2、M3をそれぞれ金属元素として一般式:pLiM1O2・qLiM2 2O4・(1−p−q)Li2M3O3で表され、
粉末X線回折測定において得られる回折ピークから半定量分析して得られるpおよびqの値が、0.4≦p≦0.6、0.02≦q≦0.08であることを特徴とする請求項2に記載の非水系電解質二次電池用正極活物質。 - 前記リチウム過剰系金属複合酸化物粒子の比表面積が、3.0〜8.0m2/gであることを特徴とする請求項1〜3のいずれかに記載の非水系電解質二次電池用正極活物質。
- 前記リチウム過剰系金属複合酸化物粒子の平均粒径D50が3〜10μm、
最大径Dmaxが50μm未満、且つタップ密度が1.5〜2.4g/cm3であることを特徴とする請求項1〜4のいずれかに記載の非水系電解質二次電池用正極活物質。 - 一般式:Li1+uNixCoyMnzAtO2+α(0.1≦u<0.3、0.03≦x≦0.25、0.03≦y≦0.25、0.4≦z<0.6、0<x+y、x+y+z+u+t=1、0≦α<0.3、0≦t<0.1、Aは2価から6価までの価数のいずれかをとる金属元素のうち少なくとも1種以上とする)で表され、一次粒子および該一次粒子が凝集した二次粒子で構成されたリチウム過剰系金属複合酸化物粒子からなる非水系電解質二次電池用正極活物質の製造方法であって、
少なくともニッケル、コバルト、マンガンを含む水酸化物、オキシ水酸化物、酸化物、及び炭酸塩の少なくとも1種からなる一次粒子が凝集した二次粒子とリチウム化合物を混合してリチウム混合物を得る混合工程と、
前記リチウム混合物を、酸化性雰囲気中にて800〜1050℃の温度で焼成して焼成物を得る焼成工程と、
前記焼成物に酸を添加して形成したスラリーを用いて、酸洗前後での焼成物のリチウム含有量の差を酸洗前の焼成物のリチウム含有量で除したリチウム除去率が10〜30%となるように制御して酸洗を前記焼成物に施した後、水洗して酸洗ケーキを得る酸洗工程と、
前記酸洗ケーキを、酸化性雰囲気中にて200〜500℃の温度で熱処理する熱処理工程を含むことを特徴とする非水系電解質二次電池用正極活物質の製造方法。 - 前記焼成工程において、得られる焼成物の二次粒子の平均粒径D50が、3〜10μm、最大径Dmaxが50μm未満、且つタップ密度が1.5〜2.4g/m3であることを特徴とする請求項6に記載の非水系電解質二次電池用正極活物質の製造方法。
- 前記酸洗工程において用いる酸が、0.5〜5Nの濃度である無機酸を用いることを特徴とする請求項6又は7に記載の非水系電解質二次電池用正極活物質の製造方法。
- 前記無機酸が、塩酸又は硫酸であることを特徴とする請求項8に記載の非水系電解質二次電池用正極活物質の製造方法。
- 前記酸洗工程において、前記焼成物をpH1〜4の無機酸に投入することを特徴とする請求項8又は9に記載の非水系電解質二次電池用正極活物質の製造方法。
- 前記酸洗工程において、酸洗する際のスラリー濃度が、100〜1500g/Lであることを特徴とする請求項6〜10のいずれか1項に記載の非水系電解質二次電池用正極活物質の製造方法。
- 請求項1〜5に記載の非水系電解質二次電池用正極活物質を含む正極を具備することを特徴とする非水系電解質二次電池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015126718A JP2017010842A (ja) | 2015-06-24 | 2015-06-24 | 非水系電解質二次電池用正極活物質とその製造方法、および該正極活物質を用いた非水系電解質二次電池 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015126718A JP2017010842A (ja) | 2015-06-24 | 2015-06-24 | 非水系電解質二次電池用正極活物質とその製造方法、および該正極活物質を用いた非水系電解質二次電池 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2017010842A true JP2017010842A (ja) | 2017-01-12 |
Family
ID=57761754
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015126718A Pending JP2017010842A (ja) | 2015-06-24 | 2015-06-24 | 非水系電解質二次電池用正極活物質とその製造方法、および該正極活物質を用いた非水系電解質二次電池 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2017010842A (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018117813A (ja) * | 2017-01-25 | 2018-08-02 | 株式会社三共 | 遊技機 |
| CN109216651A (zh) * | 2017-06-30 | 2019-01-15 | 三星电子株式会社 | 复合正极活性材料、包括其的正极和锂电池、以及制备所述复合正极活性材料的方法 |
| CN110214389A (zh) * | 2017-05-29 | 2019-09-06 | 松下知识产权经营株式会社 | 正极活性物质以及电池 |
| CN111295785A (zh) * | 2017-10-31 | 2020-06-16 | 住友金属矿山株式会社 | 非水电解质二次电池正极活性物质及制造方法、及使用正极活性物质的非水电解质二次电池 |
-
2015
- 2015-06-24 JP JP2015126718A patent/JP2017010842A/ja active Pending
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018117813A (ja) * | 2017-01-25 | 2018-08-02 | 株式会社三共 | 遊技機 |
| CN110214389A (zh) * | 2017-05-29 | 2019-09-06 | 松下知识产权经营株式会社 | 正极活性物质以及电池 |
| CN110214389B (zh) * | 2017-05-29 | 2023-06-20 | 松下知识产权经营株式会社 | 正极活性物质以及电池 |
| CN109216651A (zh) * | 2017-06-30 | 2019-01-15 | 三星电子株式会社 | 复合正极活性材料、包括其的正极和锂电池、以及制备所述复合正极活性材料的方法 |
| CN109216651B (zh) * | 2017-06-30 | 2023-04-25 | 三星电子株式会社 | 复合正极活性材料、包括其的正极和锂电池、以及制备所述复合正极活性材料的方法 |
| US11799078B2 (en) | 2017-06-30 | 2023-10-24 | Samsung Electronics Co., Ltd. | Composite cathode active material, cathode and lithium battery including the same, and method of preparing the composite cathode active material |
| CN111295785A (zh) * | 2017-10-31 | 2020-06-16 | 住友金属矿山株式会社 | 非水电解质二次电池正极活性物质及制造方法、及使用正极活性物质的非水电解质二次电池 |
| CN111295785B (zh) * | 2017-10-31 | 2023-09-26 | 住友金属矿山株式会社 | 非水电解质二次电池正极活性物质及制造方法、及使用正极活性物质的非水电解质二次电池 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7001082B2 (ja) | 非水系電解質二次電池用正極活物質の製造方法、及び非水系電解質二次電池の製造方法 | |
| KR102603503B1 (ko) | 비수계 전해질 이차 전지용 정극 활물질과 그의 제조 방법 및 비수계 전해질 이차 전지 | |
| JP5614513B2 (ja) | 非水系電解質二次電池用正極活物質の製造方法、非水系電解質二次電池用正極活物質及びこれを用いた非水系電解質二次電池 | |
| JP4840545B1 (ja) | ニッケル複合水酸化物粒子および非水系電解質二次電池 | |
| JP6241349B2 (ja) | 非水電解質二次電池用正極活物質の前駆体とその製造方法、及び非水電解質二次電池用正極活物質とその製造方法 | |
| JP5730676B2 (ja) | 非水系電解質二次電池用正極活物質とその製造方法、ならびに、ニッケルコバルトマンガン複合水酸化物とその製造方法 | |
| JP4915488B1 (ja) | ニッケルマンガン複合水酸化物粒子とその製造方法、非水系電解質二次電池用正極活物質とその製造方法、および非水系電解質二次電池 | |
| JP4894969B1 (ja) | ニッケルマンガン複合水酸化物粒子とその製造方法、非水系電解質二次電池用正極活物質とその製造方法、ならびに、非水系電解質二次電池 | |
| JP6578634B2 (ja) | 非水系電解質二次電池用正極活物質の製造方法、非水系電解質二次電池用正極活物質及びこれを用いた非水系電解質二次電池 | |
| JP5590337B2 (ja) | マンガン複合水酸化物粒子、非水系電解質二次電池用正極活物質、および非水系電解質二次電池と、それらの製造方法 | |
| WO2016017783A1 (ja) | 非水系電解質二次電池用正極活物質とその製造方法 | |
| JP2015122234A (ja) | 非水系電解質二次電池用正極活物質とその製造方法 | |
| JP6340791B2 (ja) | 非水系電解質二次電池用正極活物質の製造方法 | |
| JP5392036B2 (ja) | 非水系電解質二次電池正極活物質用マンガン複合水酸化物粒子とその製造方法、非水系電解質二次電池用正極活物質とその製造方法、および非水系電解質二次電池 | |
| KR20130076860A (ko) | 비수계 전해질 이차전지용 양극 활물질과 그 제조 방법 및 비수계 전해질 이차전지 | |
| KR20170125074A (ko) | 비수계 전해질 이차 전지용 정극 활물질 및 그의 제조 방법 | |
| JP2011116580A (ja) | ニッケルコバルトマンガン複合水酸化物粒子とその製造方法、非水系電解質二次電池用正極活物質とその製造方法、および非水系電解質二次電池 | |
| JP2011116580A5 (ja) | ||
| KR20160113330A (ko) | 니켈 복합 수산화물과 그의 제조 방법, 비수계 전해질 이차 전지용 정극 활물질과 그의 제조 방법, 및 비수계 전해질 이차 전지 | |
| CN107078292B (zh) | 非水系电解质二次电池用的正极活性物质及其制造方法、以及非水系电解质二次电池 | |
| JP6061149B2 (ja) | 非水系電解質二次電池用正極活物質とその製造方法 | |
| WO2016104305A1 (ja) | 非水系電解質二次電池用正極活物質とその製造方法、及び該正極活物質を用いた非水系電解質二次電池 | |
| JP2017010841A (ja) | 非水系電解質二次電池用正極活物質とその製造方法、および該正極活物質を用いた非水系電解質二次電池 | |
| JP2017010842A (ja) | 非水系電解質二次電池用正極活物質とその製造方法、および該正極活物質を用いた非水系電解質二次電池 | |
| JP2018067549A (ja) | 非水系電解質二次電池用正極活物質、及びこれを用いた非水系電解質二次電池 |