JP2014503593A - 閉塞性睡眠時無呼吸を処置するための方法 - Google Patents
閉塞性睡眠時無呼吸を処置するための方法 Download PDFInfo
- Publication number
- JP2014503593A JP2014503593A JP2013551354A JP2013551354A JP2014503593A JP 2014503593 A JP2014503593 A JP 2014503593A JP 2013551354 A JP2013551354 A JP 2013551354A JP 2013551354 A JP2013551354 A JP 2013551354A JP 2014503593 A JP2014503593 A JP 2014503593A
- Authority
- JP
- Japan
- Prior art keywords
- sleep
- osa
- subject
- apnea
- pyridostigmine
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 208000001797 obstructive sleep apnea Diseases 0.000 title claims abstract description 106
- 238000000034 method Methods 0.000 title claims abstract description 59
- RVOLLAQWKVFTGE-UHFFFAOYSA-N Pyridostigmine Chemical compound CN(C)C(=O)OC1=CC=C[N+](C)=C1 RVOLLAQWKVFTGE-UHFFFAOYSA-N 0.000 claims abstract description 92
- 229960002290 pyridostigmine Drugs 0.000 claims abstract description 92
- 230000007958 sleep Effects 0.000 claims abstract description 79
- 206010041235 Snoring Diseases 0.000 claims abstract description 41
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 31
- 208000008784 apnea Diseases 0.000 claims description 45
- 206010021079 Hypopnoea Diseases 0.000 claims description 42
- 210000002966 serum Anatomy 0.000 claims description 26
- 206010021143 Hypoxia Diseases 0.000 claims description 15
- 230000007954 hypoxia Effects 0.000 claims description 13
- 239000003085 diluting agent Substances 0.000 claims description 12
- 239000003937 drug carrier Substances 0.000 claims description 11
- 238000010521 absorption reaction Methods 0.000 claims description 4
- 230000002496 gastric effect Effects 0.000 claims description 3
- 239000006186 oral dosage form Substances 0.000 claims description 3
- 239000003814 drug Substances 0.000 abstract description 53
- 208000024891 symptom Diseases 0.000 abstract description 16
- 229940079593 drug Drugs 0.000 description 25
- 206010041349 Somnolence Diseases 0.000 description 23
- 230000003860 sleep quality Effects 0.000 description 17
- 208000007590 Disorders of Excessive Somnolence Diseases 0.000 description 14
- 230000009467 reduction Effects 0.000 description 14
- 230000004622 sleep time Effects 0.000 description 13
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 12
- 206010062519 Poor quality sleep Diseases 0.000 description 10
- 230000029058 respiratory gaseous exchange Effects 0.000 description 10
- 230000007423 decrease Effects 0.000 description 9
- 239000000203 mixture Substances 0.000 description 9
- 239000000902 placebo Substances 0.000 description 9
- 229940068196 placebo Drugs 0.000 description 9
- 230000002829 reductive effect Effects 0.000 description 9
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 8
- 238000001356 surgical procedure Methods 0.000 description 8
- 210000004369 blood Anatomy 0.000 description 7
- 239000008280 blood Substances 0.000 description 7
- 208000035475 disorder Diseases 0.000 description 7
- 230000001225 therapeutic effect Effects 0.000 description 7
- 230000002618 waking effect Effects 0.000 description 7
- 230000037007 arousal Effects 0.000 description 6
- 230000000241 respiratory effect Effects 0.000 description 6
- 208000000044 Amnesia Diseases 0.000 description 5
- 208000024172 Cardiovascular disease Diseases 0.000 description 5
- 206010019280 Heart failures Diseases 0.000 description 5
- 208000008589 Obesity Diseases 0.000 description 5
- 238000013270 controlled release Methods 0.000 description 5
- 239000002552 dosage form Substances 0.000 description 5
- 238000009472 formulation Methods 0.000 description 5
- 231100000863 loss of memory Toxicity 0.000 description 5
- 208000030159 metabolic disease Diseases 0.000 description 5
- 235000020824 obesity Nutrition 0.000 description 5
- 150000002926 oxygen Chemical class 0.000 description 5
- 208000002815 pulmonary hypertension Diseases 0.000 description 5
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 5
- 230000003247 decreasing effect Effects 0.000 description 4
- 208000016097 disease of metabolism Diseases 0.000 description 4
- 230000001771 impaired effect Effects 0.000 description 4
- 206010022489 Insulin Resistance Diseases 0.000 description 3
- 208000032140 Sleepiness Diseases 0.000 description 3
- 206010003119 arrhythmia Diseases 0.000 description 3
- 230000006793 arrhythmia Effects 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 208000010877 cognitive disease Diseases 0.000 description 3
- 206010012601 diabetes mellitus Diseases 0.000 description 3
- 238000003745 diagnosis Methods 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 238000001802 infusion Methods 0.000 description 3
- 238000001990 intravenous administration Methods 0.000 description 3
- 210000001428 peripheral nervous system Anatomy 0.000 description 3
- 230000037321 sleepiness Effects 0.000 description 3
- 208000037905 systemic hypertension Diseases 0.000 description 3
- 102100033639 Acetylcholinesterase Human genes 0.000 description 2
- 108010022752 Acetylcholinesterase Proteins 0.000 description 2
- 206010067484 Adverse reaction Diseases 0.000 description 2
- 206010003497 Asphyxia Diseases 0.000 description 2
- 206010003658 Atrial Fibrillation Diseases 0.000 description 2
- 206010007559 Cardiac failure congestive Diseases 0.000 description 2
- 206010013975 Dyspnoeas Diseases 0.000 description 2
- 206010020772 Hypertension Diseases 0.000 description 2
- 208000006011 Stroke Diseases 0.000 description 2
- OIPILFWXSMYKGL-UHFFFAOYSA-N acetylcholine Chemical compound CC(=O)OCC[N+](C)(C)C OIPILFWXSMYKGL-UHFFFAOYSA-N 0.000 description 2
- 229960004373 acetylcholine Drugs 0.000 description 2
- 229940022698 acetylcholinesterase Drugs 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 230000006838 adverse reaction Effects 0.000 description 2
- 239000000935 antidepressant agent Substances 0.000 description 2
- 229940005513 antidepressants Drugs 0.000 description 2
- 239000000739 antihistaminic agent Substances 0.000 description 2
- 229940125715 antihistaminic agent Drugs 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 238000007681 bariatric surgery Methods 0.000 description 2
- 229940049706 benzodiazepine Drugs 0.000 description 2
- 150000001557 benzodiazepines Chemical class 0.000 description 2
- 210000003169 central nervous system Anatomy 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 239000000544 cholinesterase inhibitor Substances 0.000 description 2
- 230000003920 cognitive function Effects 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- -1 cyclopyrrolone Substances 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 230000001627 detrimental effect Effects 0.000 description 2
- ADEBPBSSDYVVLD-UHFFFAOYSA-N donepezil Chemical compound O=C1C=2C=C(OC)C(OC)=CC=2CC1CC(CC1)CCN1CC1=CC=CC=C1 ADEBPBSSDYVVLD-UHFFFAOYSA-N 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 239000007887 hard shell capsule Substances 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 239000012729 immediate-release (IR) formulation Substances 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 210000000663 muscle cell Anatomy 0.000 description 2
- 230000000422 nocturnal effect Effects 0.000 description 2
- 230000000414 obstructive effect Effects 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 210000002345 respiratory system Anatomy 0.000 description 2
- 230000033764 rhythmic process Effects 0.000 description 2
- 239000012896 selective serotonin reuptake inhibitor Substances 0.000 description 2
- 229940124834 selective serotonin reuptake inhibitor Drugs 0.000 description 2
- 210000002784 stomach Anatomy 0.000 description 2
- 229940100578 Acetylcholinesterase inhibitor Drugs 0.000 description 1
- 0 CNC=CCCCOC(*=O)N(C)CC* Chemical compound CNC=CCCCOC(*=O)N(C)CC* 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical group NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 1
- 108010009685 Cholinergic Receptors Proteins 0.000 description 1
- 229940122041 Cholinesterase inhibitor Drugs 0.000 description 1
- 102000003914 Cholinesterases Human genes 0.000 description 1
- 108090000322 Cholinesterases Proteins 0.000 description 1
- 208000017667 Chronic Disease Diseases 0.000 description 1
- 208000030453 Drug-Related Side Effects and Adverse reaction Diseases 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 208000007101 Muscle Cramp Diseases 0.000 description 1
- 208000010428 Muscle Weakness Diseases 0.000 description 1
- 206010028372 Muscular weakness Diseases 0.000 description 1
- PIJVFDBKTWXHHD-UHFFFAOYSA-N Physostigmine Natural products C12=CC(OC(=O)NC)=CC=C2N(C)C2C1(C)CCN2C PIJVFDBKTWXHHD-UHFFFAOYSA-N 0.000 description 1
- VNYBTNPBYXSMOO-UHFFFAOYSA-M Pyridostigmine bromide Chemical compound [Br-].CN(C)C(=O)OC1=CC=C[N+](C)=C1 VNYBTNPBYXSMOO-UHFFFAOYSA-M 0.000 description 1
- 206010039203 Road traffic accident Diseases 0.000 description 1
- 208000013738 Sleep Initiation and Maintenance disease Diseases 0.000 description 1
- 108010052164 Sodium Channels Proteins 0.000 description 1
- 102000018674 Sodium Channels Human genes 0.000 description 1
- 208000005392 Spasm Diseases 0.000 description 1
- 206010070863 Toxicity to various agents Diseases 0.000 description 1
- 206010000059 abdominal discomfort Diseases 0.000 description 1
- 102000034337 acetylcholine receptors Human genes 0.000 description 1
- 210000000577 adipose tissue Anatomy 0.000 description 1
- 230000036626 alertness Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 230000008499 blood brain barrier function Effects 0.000 description 1
- 210000001218 blood-brain barrier Anatomy 0.000 description 1
- 230000007211 cardiovascular event Effects 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229940048961 cholinesterase Drugs 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000000916 dilatatory effect Effects 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 229960003530 donepezil Drugs 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 238000001647 drug administration Methods 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000005802 health problem Effects 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 208000018875 hypoxemia Diseases 0.000 description 1
- 230000001146 hypoxic effect Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 206010022437 insomnia Diseases 0.000 description 1
- 238000001361 intraarterial administration Methods 0.000 description 1
- 238000007917 intracranial administration Methods 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000007919 intrasynovial administration Methods 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 1
- 210000004373 mandible Anatomy 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 230000004118 muscle contraction Effects 0.000 description 1
- 206010028417 myasthenia gravis Diseases 0.000 description 1
- 210000001087 myotubule Anatomy 0.000 description 1
- 239000002858 neurotransmitter agent Substances 0.000 description 1
- 238000002496 oximetry Methods 0.000 description 1
- 238000006213 oxygenation reaction Methods 0.000 description 1
- 230000001499 parasympathomimetic effect Effects 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 229960001697 physostigmine Drugs 0.000 description 1
- PIJVFDBKTWXHHD-HIFRSBDPSA-N physostigmine Chemical compound C12=CC(OC(=O)NC)=CC=C2N(C)[C@@H]2[C@@]1(C)CCN2C PIJVFDBKTWXHHD-HIFRSBDPSA-N 0.000 description 1
- 229960002516 physostigmine salicylate Drugs 0.000 description 1
- HZOTZTANVBDFOF-PBCQUBLHSA-N physostigmine salicylate Chemical compound OC(=O)C1=CC=CC=C1O.C12=CC(OC(=O)NC)=CC=C2N(C)[C@@H]2[C@@]1(C)CCN2C HZOTZTANVBDFOF-PBCQUBLHSA-N 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 230000005180 public health Effects 0.000 description 1
- 229960002151 pyridostigmine bromide Drugs 0.000 description 1
- 208000023504 respiratory system disease Diseases 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000004043 responsiveness Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 201000002859 sleep apnea Diseases 0.000 description 1
- 230000008667 sleep stage Effects 0.000 description 1
- 235000011888 snacks Nutrition 0.000 description 1
- 229910001415 sodium ion Inorganic materials 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 230000000946 synaptic effect Effects 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 230000004797 therapeutic response Effects 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 238000009423 ventilation Methods 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4412—Non condensed pyridines; Hydrogenated derivatives thereof having oxo groups directly attached to the heterocyclic ring
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F5/00—Orthopaedic methods or devices for non-surgical treatment of bones or joints; Nursing devices; Anti-rape devices
- A61F5/56—Devices for preventing snoring
- A61F5/566—Intra-oral devices
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4425—Pyridinium derivatives, e.g. pralidoxime, pyridostigmine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M16/00—Devices for influencing the respiratory system of patients by gas treatment, e.g. mouth-to-mouth respiration; Tracheal tubes
- A61M16/0057—Pumps therefor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/16—Central respiratory analeptics
Landscapes
- Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Pulmonology (AREA)
- Engineering & Computer Science (AREA)
- Heart & Thoracic Surgery (AREA)
- Biomedical Technology (AREA)
- Nursing (AREA)
- Otolaryngology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Vascular Medicine (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Emergency Medicine (AREA)
- Anesthesiology (AREA)
- Hematology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Description
本願は、2011年1月28日に出願された米国仮出願第61/437272号の利益を主張し、その内容は、参照により本明細書において、それらの全体において、及び、全ての目的のために組み入れられる。
本発明は、一般的に、それを必要とする被験者において閉塞性睡眠時無呼吸(OSA)又は他の関連症状を処置するための方法、関連する医薬、医薬組成物、及び医薬を調製するための方法に関する。
閉塞性睡眠時無呼吸(OSA)は、深刻な、潜在的に生命を脅かす、高度に流行性の慢性障害である。それは、心血管事象の発生におけるその役割、生活の質に対する負の影響のため、及び交通事故の原因として、重要な未解決の公衆衛生ケアの問題である。OSAの徴候、症状、及び結果は、上気道の反復的な虚脱に起因する気流停止(即ち、無呼吸)又は低下(即ち、低呼吸)の反復エピソードの直接的な結果である。睡眠の間での低下した換気が、低酸素血症の反復エピソード、動脈CO2の増加、及び動脈O2の減少を引き起こす。OSA患者は、しばしば、心血管疾患(例えば、全身性高血圧、肺高血圧、不整脈、及び心不全)、精神神経疾患(例えば、過度の日中の眠気により引き起こされる認知機能障害、いびきにより引き起こされる生活の質の低下、覚醒に起因する睡眠分断、及びうつ病)、及び代謝性疾患(例えば、肥満、糖尿病、及びインスリン抵抗性)を伴うという相関が明らかに確立されている。OSAは、成人人口の少なくとも2%から4%に発症し、世間にますます認識されている。より最近のレポートでは、OSAは、成人の約5%に発症すると推定されている。しかし、OSAの有病率は、最近の肥満傾向のため、増加しうる。
本発明は、閉塞性睡眠時無呼吸(OSA)又は他の関連する症状を処置におけるピリドスチグミン(PYD)の使用、ならびに、好ましくは、特定の投与形態及び投与量を使用した、PYDを含む医薬組成物又は医薬に関する。
本発明は、ピリドスチグミン(PYD)(アセチルコリンエステラーゼ阻害剤)が、閉塞性睡眠時無呼吸(OSA)の処置に有効であるという発見に基づく。特に、PYDは、無呼吸、低呼吸、いびき、及び低酸素飽和事象を低下させる、及びOSA患者の睡眠の質及び日中の生活の質を改善するのに有効である。
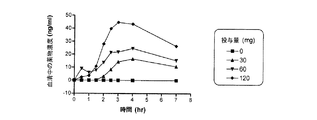
PYDを用いた無作為化、二重盲検、プラセボ対照、クロスオーバー試験を、中程度から重度のOSAを伴う12人の患者において行った。PYDは、Sunve Pharmaceutical Co., LTD.(Shanghai, China)により製造されたピリドスチグミンブロミドピルを粉砕することにより調製し、ハードシェルカプセル中に再カプセル化した。PYDブロミドを30mg、60mg、120mgで、又はプラセボを、患者に、睡眠前に、合計4夜連続で各晩に経口投与した。明かりは、投与後5分以内に消えた。血液を、投与後0、0.5、1、1.5、2、2.5、3、4、及び7時間に採取し、血清薬物濃度を、血液サンプルの適した前処理後にLC−MS方法により決定した。患者は、PSG又はPMのいずれかにより、夜を通してモニターされた。
二重盲検、無作為化、クロスオーバー、プラセボ対照試験を行い、6人の診断されたOSA患者においてPYDの効力及び安全性を評価した。試験は、1日の順化期間、その直後に続く、2日の二重盲検処置期間(患者は、軽食と共に、睡眠前に、ハードシェルカプセル中の90mgのPYDブロミド又はマッチングプラセボのいずれかを与えられた)からなる。全ての患者が、夜を通して仰臥位で維持されることが要求された。なぜなら、OSAは、患者が仰向けにある場合、最も深刻であるからである。そのような方法において、結果は、薬物の治療的効果を判断する際により慎重であることが予想される。光は、薬物の投与後5分以内に消された。患者は、PSGによりモニターされた。無呼吸、低呼吸、いびき、血液O2飽和は、モニターされ、記録され、スコア化された。睡眠アンケートを、睡眠後に毎日取り、睡眠の満足に対する影響を評価し、夕方に、日中の間での生活の質を評価した。薬物の安全性もモニターし、評価した。
AHIの統計的に有意な低下は、0〜2時間の睡眠期間の間に見出されなかった(図3)。2〜7時間の睡眠期間の間に、AHIの低下が、全ての患者において見出され、13.9%から61.6%の範囲(平均28.0%)であった。より大きな低下が、中程度の患者において、重度の患者と比較して、見出された。
AIの統計的に有意な低下は、0〜2時間の睡眠期間の間に見出されなかった(図4)。2〜7時間の睡眠期間の間に、AIの低下が、5人の患者において見出され、24.7%から68.8%の範囲(6人の患者における平均37.3%)であった。低下は、2.1のAIを示した1人の患者において見出されなかった。
総無呼吸/低呼吸時間は、無呼吸又は低呼吸が生じた総睡眠時間のパーセンテージとして表した。総無呼吸/低呼吸時間の統計的に有意な低下は、0〜2時間の睡眠期間の間に見出されなかった(図5)。2〜7時間の睡眠期間の間に、総無呼吸/低呼吸時間の低下が、全ての患者において見出され、11.3%から66.2%の範囲(平均36.4%)であった。
低O2飽和は、1時間当たりの低O2飽和事象の数として表した。低O2飽和事象は、4%より大きい動脈O2飽和の連続的な減少として特徴付けられる。低O2飽和の統計的に有意な低下は、0〜2時間の睡眠期間の間に見出されなかった(図6)。2〜7時間の睡眠期間の間に、低O2飽和の低下が、4人の患者において見出され、24.2%から39.4%の範囲であった。低下は1人の患者において見出されず、患者において事象の数が増加した。
いびきは、1時間当たりのいびきの数として算出した。いびきの統計的に有意な低下は、0〜2時間の睡眠期間の間に見出されなかった(図7)。2〜7時間の睡眠期間の間に、いびきの低下が、全ての患者において見出され、3.7%から36.9%の範囲(平均18.8%)であった。処置夜におけるいびきは、プラセボ夜と比較して、より静かであったが、薬物がいびきのノイズを低下させたことを示している。3.7%低下を示した患者においてでさえ、処置夜中でのいびきは短く、高調であったが、このように、総いびき時間は低下するが、いびきの数はそれほど変化しなかった。
各々の患者がアンケートを受け、起床後に自分たちの睡眠を自己評価した。自己評価におけるスコアを、プラセボ夜と処置夜の間で比較した(図8)。3人の患者が、処置夜において、より長い総睡眠時間(彼らの自然な起床までの総睡眠時間)を示した(平均33分より多く);2人の患者が、恐らくは長い睡眠時間(8時間にわたる)に起因して、本質的に睡眠時間における変化を示さなかった;そして、1人の患者が、軽度の胃のもたれのために睡眠に戻れなかったため、より少ない睡眠時間を示した。一般的に、患者は、より良い睡眠、より頭がさえており、よりエネルギッシュであり、より満足な睡眠を、処置夜中に報告したが、薬物が患者において睡眠の質を改善したことを示している。
患者は、薬物処置夜に続く日中の間に、より多くのエネルギーを有し、より集中しており、眠気がより少ないと報告した。これは、薬物処置が、日中の眠気を低下させ、損なわれた認知機能(損なわれた記憶)を回復させ、生活の質を改善させたことを示す。
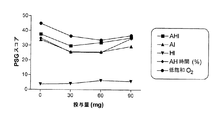
実施例1に記載される臨床試験から得られた結果は、PYDの治療的効果が、薬物の増加投与量と常に相関するわけではないことを示す。例えば、患者は、30〜60mgのPYDブロミドを用いて処置された場合、120mgのPYDブロミドを用いて処置された者と比較して、より低いAHI及びより低いO2飽和を記録した(図2)。この用量反応におけるこの知見は、予想外で、特有である。
Claims (15)
- 被験者に、ピリドスチグミンを含む医薬組成物の有効量を、睡眠前に投与することを含む、必要とする被験者において閉塞性睡眠時無呼吸(OSA)を処置するための方法。
- 被験者における無呼吸、低呼吸、いびき、又は低酸素飽和事象を低下させる、請求項1記載の方法。
- 被験者の睡眠の質又は日中の生活の質を改善する、請求項1記載の方法。
- 医薬組成物の有効量が、少なくとも1時間にわたり、2〜150ng/mlの範囲で、被験者にピリドスチグミンの標的血清濃度をもたらすように選択される、請求項1記載の方法。
- 標的血清濃度が3〜60ng/mlの範囲である、請求項4記載の方法。
- 標的血清濃度が3〜45ng/mlの範囲である、請求項4記載の方法。
- 標的血清濃度が3〜30ng/mlの範囲である、請求項4記載の方法。
- 標的血清濃度が3〜15ng/mlの範囲である、請求項4記載の方法。
- 標的血清濃度が少なくとも3時間維持される、請求項4記載の方法。
- 医薬組成物が、30〜360mgのピリドスチグミンを含む、請求項1記載の方法。
- 医薬組成物が、被験者に、睡眠前の2時間以内に投与される、請求項1記載の方法。
- 医薬組成物が、被験者に、単回投与で投与される、請求項1記載の方法。
- 医薬組成物が、さらに、医薬的に許容可能な担体又は希釈剤を含む、請求項1記載の方法。
- 医薬組成物が、被験者に、経口投与形態で投与される、請求項1記載の方法。
- 医薬組成物が、被験者に、胃腸吸収のために投与される、請求項14記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161437272P | 2011-01-28 | 2011-01-28 | |
| US61/437,272 | 2011-01-28 | ||
| PCT/US2012/022825 WO2012103398A2 (en) | 2011-01-28 | 2012-01-27 | Methods for treating obstructive sleep apnea |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017000145A Division JP6342525B2 (ja) | 2011-01-28 | 2017-01-04 | 閉塞性睡眠時無呼吸を処置するための方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2014503593A true JP2014503593A (ja) | 2014-02-13 |
| JP2014503593A5 JP2014503593A5 (ja) | 2015-03-19 |
Family
ID=46577943
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013551354A Pending JP2014503593A (ja) | 2011-01-28 | 2012-01-27 | 閉塞性睡眠時無呼吸を処置するための方法 |
| JP2017000145A Active JP6342525B2 (ja) | 2011-01-28 | 2017-01-04 | 閉塞性睡眠時無呼吸を処置するための方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017000145A Active JP6342525B2 (ja) | 2011-01-28 | 2017-01-04 | 閉塞性睡眠時無呼吸を処置するための方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US8753327B2 (ja) |
| EP (1) | EP2672972B1 (ja) |
| JP (2) | JP2014503593A (ja) |
| CN (2) | CN103458899A (ja) |
| CA (1) | CA2825309C (ja) |
| WO (1) | WO2012103398A2 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024143302A1 (ja) * | 2022-12-28 | 2024-07-04 | 西川株式会社 | 健康リスク判定システム、自律神経判定システム、生活改善システム、寝姿勢判定システム、寝姿勢判定プログラム、歯ぎしり検出システム、および歯ぎしり検出プログラム |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8753327B2 (en) * | 2011-01-28 | 2014-06-17 | Pfantastic Medical Research Institute, Llc | Methods for treating obstructive sleep apnea |
| JP2017506929A (ja) * | 2014-03-03 | 2017-03-16 | スリープ イノベイションズ プロプライアタリー リミティド | 睡眠時無呼吸治療の装置及び方法 |
| WO2016014229A1 (en) * | 2014-07-25 | 2016-01-28 | Mendelowitz David | Oxytocin improves treatment of obstructive sleep apnea |
| EP4186548A1 (en) | 2015-04-02 | 2023-05-31 | Hill-Rom Services PTE. LTD. | Mask leakage detection for a respiratory device |
| EP3558178B1 (en) * | 2016-12-23 | 2021-03-17 | Koninklijke Philips N.V. | System for treating snoring among at least two users |
| SG10202111623TA (en) * | 2017-04-28 | 2021-12-30 | Brigham & Womens Hospital Inc | Methods and compositions for treating sleep apnea |
| KR20200115598A (ko) | 2018-01-30 | 2020-10-07 | 애프니메드, 인코포레이티드 (델라웨어) | 수면 무호흡증을 치료하기 위한 방법 및 조성물 |
| EP3609472B1 (en) * | 2018-06-18 | 2020-12-30 | Kashiv Specialty Pharmaceuticals, LLC | Extended release compositions comprising pyridostigmine |
| CN112601568B (zh) * | 2018-08-24 | 2024-07-26 | 皇家飞利浦有限公司 | 利用压力治疗系统提供睡眠治疗 |
| US20200282215A1 (en) | 2019-03-06 | 2020-09-10 | Medtronic Xomed, LLC | Evaluating stimulation eficacy for treating sleep apnea and lingual muscle tone sensing system for improved osa therapy |
| CN114504643B (zh) * | 2021-12-24 | 2024-03-26 | 北京大学第一医院 | 抗IgE抗体在用于治疗OSAS中的应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000511873A (ja) * | 1995-12-19 | 2000-09-12 | エー プラス サイエンス インヴエスト アクチエボラグ | 睡眠時呼吸障害を治療および診断する方法、並びにこの方法を実施する手段 |
| JP2007502297A (ja) * | 2003-08-13 | 2007-02-08 | ジヤンセン・フアーマシユーチカ・ナームローゼ・フエンノートシヤツプ | コリンエステラーゼ阻害剤を用いる睡眠障害の処置 |
| WO2008042707A2 (en) * | 2006-09-29 | 2008-04-10 | Nellcor Puritan Bennett Llc | Device for managing obstructive sleep apnea and snoring |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2247662B (en) | 1990-08-31 | 1994-11-02 | Instance Ltd David J | Labels and manufacture thereof |
| AU2006291581A1 (en) * | 2005-09-16 | 2007-03-22 | Cereuscience Ab | Method and means of preventing and treating sleep disordered breathing |
| US20080066739A1 (en) * | 2006-09-20 | 2008-03-20 | Lemahieu Edward | Methods and systems of delivering medication via inhalation |
| US8753327B2 (en) * | 2011-01-28 | 2014-06-17 | Pfantastic Medical Research Institute, Llc | Methods for treating obstructive sleep apnea |
-
2012
- 2012-01-27 US US13/359,692 patent/US8753327B2/en active Active
- 2012-01-27 CN CN2012800065522A patent/CN103458899A/zh active Pending
- 2012-01-27 CN CN201610821591.8A patent/CN107007602A/zh active Pending
- 2012-01-27 CA CA2825309A patent/CA2825309C/en active Active
- 2012-01-27 WO PCT/US2012/022825 patent/WO2012103398A2/en active Application Filing
- 2012-01-27 JP JP2013551354A patent/JP2014503593A/ja active Pending
- 2012-01-27 EP EP12739245.4A patent/EP2672972B1/en active Active
-
2014
- 2014-05-05 US US14/269,326 patent/US9295670B2/en active Active
-
2017
- 2017-01-04 JP JP2017000145A patent/JP6342525B2/ja active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000511873A (ja) * | 1995-12-19 | 2000-09-12 | エー プラス サイエンス インヴエスト アクチエボラグ | 睡眠時呼吸障害を治療および診断する方法、並びにこの方法を実施する手段 |
| JP2007502297A (ja) * | 2003-08-13 | 2007-02-08 | ジヤンセン・フアーマシユーチカ・ナームローゼ・フエンノートシヤツプ | コリンエステラーゼ阻害剤を用いる睡眠障害の処置 |
| WO2008042707A2 (en) * | 2006-09-29 | 2008-04-10 | Nellcor Puritan Bennett Llc | Device for managing obstructive sleep apnea and snoring |
Non-Patent Citations (1)
| Title |
|---|
| JPN6016034591; NEW薬理学(改訂第3版) , 19970801, p.234-241 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024143302A1 (ja) * | 2022-12-28 | 2024-07-04 | 西川株式会社 | 健康リスク判定システム、自律神経判定システム、生活改善システム、寝姿勢判定システム、寝姿勢判定プログラム、歯ぎしり検出システム、および歯ぎしり検出プログラム |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2672972A4 (en) | 2014-09-10 |
| CA2825309A1 (en) | 2012-08-02 |
| WO2012103398A9 (en) | 2012-09-27 |
| US8753327B2 (en) | 2014-06-17 |
| CN103458899A (zh) | 2013-12-18 |
| US9295670B2 (en) | 2016-03-29 |
| EP2672972B1 (en) | 2020-11-04 |
| CN107007602A (zh) | 2017-08-04 |
| JP2017095485A (ja) | 2017-06-01 |
| US20120197235A1 (en) | 2012-08-02 |
| WO2012103398A2 (en) | 2012-08-02 |
| EP2672972A2 (en) | 2013-12-18 |
| US20140238412A1 (en) | 2014-08-28 |
| CA2825309C (en) | 2019-10-01 |
| JP6342525B2 (ja) | 2018-06-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6342525B2 (ja) | 閉塞性睡眠時無呼吸を処置するための方法 | |
| Robinson et al. | Sleep· 6: obstructive sleep apnoea/hypopnoea syndrome and hypertension | |
| Hla et al. | The effect of correction of sleep-disordered breathing on BP in untreated hypertension | |
| Hedner et al. | A randomized controlled clinical trial exploring safety and tolerability of sulthiame in sleep apnea | |
| US5612379A (en) | Modafinil for the treatment of sleep apneas and ventilatory disorders of central origin | |
| JP2020517719A (ja) | 睡眠時無呼吸を治療する方法及び組成物 | |
| JP5093967B2 (ja) | 睡眠時の自律的安定性に関するカンナビノイドの機能的役割 | |
| JP2022519721A (ja) | 睡眠時無呼吸を治療するための方法および組成物 | |
| Jyothi et al. | Obstructive sleep apnea: a pathophysiology and pharmacotherapy approach | |
| Guilleminault et al. | Obstructive sleep apnea syndrome | |
| JP2019511555A (ja) | 睡眠時無呼吸の処置のためのスルチアム | |
| Carswell et al. | Obstructive sleep apnea: Part I. Pathophysiology, diagnosis, and medical management | |
| CN101641090B (zh) | 莫达非尼在制备治疗多动腿综合征的药物中的应用 | |
| Qasrawi et al. | Sleep-Related Breathing Disorders in Adults | |
| Krieger et al. | Obstructive sleep apnea and cardiovascular disease: implications for clinical practice. | |
| Buchanan et al. | Continuous positive airway pressure | |
| Qamar et al. | Obstructive sleep Apnea | |
| King | The Effect of Mandibular Advancement Devices on Sympathetic Nerve Activity and Markers of Cardiovascular Health in Obstructive Sleep Apnea Patients: A Feasibility Trial | |
| Huang et al. | Anesthetic Management during Endovascular Ultrasound Renal Denervation for hypertensive patients with Obstructive Sleep Apnea: Two case reports. | |
| Dobbin et al. | Obstructive sleep apnea: recognition and management considerations for the aged patient | |
| Chopra et al. | NEUROPSYCHIATRY OF PRIMARY SLEEP DISORDERS | |
| Brozovic et al. | Anaphylactic reaction after rocuronium | |
| Dodds | Anaesthetic considerations in the elderly | |
| Colle et al. | Hypertension in obstructive sleep apnoea | |
| Casati et al. | A clinical comparison between bispectral index (BIS) and high frequency EEG signal detection (SNAP) |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150126 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20150126 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20150310 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20151110 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20160210 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20160310 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160411 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20160906 |