JP2014135941A - 熱サイクル装置及び熱サイクル方法 - Google Patents
熱サイクル装置及び熱サイクル方法 Download PDFInfo
- Publication number
- JP2014135941A JP2014135941A JP2013006997A JP2013006997A JP2014135941A JP 2014135941 A JP2014135941 A JP 2014135941A JP 2013006997 A JP2013006997 A JP 2013006997A JP 2013006997 A JP2013006997 A JP 2013006997A JP 2014135941 A JP2014135941 A JP 2014135941A
- Authority
- JP
- Japan
- Prior art keywords
- biochip
- region
- arrangement
- temperature
- heating unit
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Abstract
【解決手段】熱サイクル装置は、複数の液滴からなる反応液140を形成する液滴形成部9と、反応液140と、反応液140よりも比重が小さく、かつ反応液140とは相分離する液体130とが充填され、反応液140が移動する流路110を含むバイオチップ100を装着する装着部と、装着部にバイオチップ100を装着した場合に流路110の第1領域を加熱する加熱部と、装着部及び加熱部の配置を、第1の配置と第2の配置との間で切り換える駆動機構と、を含み、第1の配置は、第1領域が重力の作用する方向における流路110の最下部に位置する配置であり、第2の配置は、反応液140が移動する方向における位置が第1領域とは異なる流路110の第2領域が重力の作用する方向における流路110の最下部に位置する配置である。
【選択図】図4
Description
1.実施形態
1−1.実施形態における熱サイクル装置の構成
1−2.実施形態における熱サイクル装置を用いた熱サイクル処理
1−3.実施形態における熱サイクル装置及び熱サイクル処理の効果
2.変形例
1−1.実施形態における熱サイクル装置の構成
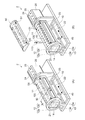
図1は、実施形態に係る熱サイクル装置1の斜視図である。(A)は熱サイクル装置1の蓋50を閉じた状態、(B)は熱サイクル装置1の蓋50を開けた状態であり、装着部11にバイオチップ100が装着された状態を表す。図2は、実施形態に係る熱サイクル装置1における本体10の分解斜視図である。図3は、実施形態に係る熱サイクル装置1における本体10の、図1(A)のA−A線における断面を模式的に示す断面図である。(A)は第1の配置、(B)は第2の配置を示す。
図4は、実施形態に係るバイオチップ100の断面図である。以下では、まず、実施形態に係るバイオチップ100について説明する。
流路110内を液体130で満たした状態で、流路110の両端を異なる温度の第1加熱部12及び第2加熱部13(図3参照)で加熱することにより、図5に示すように、流路110内の液体130に60℃と95℃との2水準の領域(温度帯)を設けておく。ここに検体からDNA若しくはRNAを抽出した溶液を含む反応液140を、流路110内で反応液140が複数(2個以上)の液滴になるよう液滴形成部9を用いて形成する(図4(A)参照)。
本実施形態に係る熱サイクル装置1で反応を行った結果、従来の反応液を単一の状態で流路110内に注入する方法に比べて、同体積の反応液140を複数の液滴に分割した場合は各反応温度で保持する時間を短縮することが可能であることを確認した。
PCRのターゲット及び反応液140には、図6に示す組成を使用し、PCR産物量の評価はアガロースゲル電気泳動法を用いて行った。
次に、複数液滴によって熱サイクル処理を行う際に有効な流路110の内径と液滴の直径の比を説明する。前述の通り、流路110の内壁と液滴表面間の隙間が増加することで液滴の移動に伴う液体130の移動が速くなり液滴の移動が円滑になる。したがって、「高速条件」に対応できる液滴サイズを規定するに当たって、適切な液滴サイズは流路110の内径に依存することになる。そこで、流路110の内径と液滴の直径の比率を考えることで液滴サイズを規定した。
図9は、本実施形態における熱サイクル装置1を用いた熱サイクル処理の手順を表すフローチャートである。
本実施形態に係る熱サイクル装置及び熱サイクル方法によれば、以下の効果を得ることができる。
本実施形態は、複数の液滴からなる反応液140を用いることにより、液滴移動による加熱冷却サイクルを高速化することにより熱サイクル処理に要する時間を短縮するための方法である。バイオチップ100を回転させることで加熱冷却サイクルを行うために流路110内の液体130に反応液140を注入するが、その際、複数の液滴からなる反応液140を形成させる。同体積の反応液を単一の状態で流路110内に注入する場合に比べ、液滴が流路110内壁に接触する面積が減少するため移動速度が速くなる。このことにより、2水準の各温度で液滴を保持する時間を短縮することができ、熱サイクル処理の高速化を可能にする。
以下、実施形態に基づいて変形例について説明する。
図10は、変形例に係る熱サイクル装置2の斜視図である。図10(A)は蓋50を閉じた状態、図10(B)は蓋50を開けた状態を示す。図11は、変形例5に係るバイオチップ100の断面図である。図12は、変形例に係る熱サイクル装置2の本体10aの、図10(A)のB−B線における断面を模式的に示す断面図である。以下の変形例は、相互に矛盾しない構成である限り任意の組合せが可能であり、図10(A)、図10(B)、並びに図12に示す熱サイクル装置2は、変形例2、5、17、18の構成を組み合わせた例である。該当する変形例については、図10ないし図12を参照して説明する。以下においては実施形態とは異なる構成について詳述し、実施形態と同様の構成については同一の符号を付して説明を省略する。
本実施形態において、複数の液滴からなる反応液140を形成させる方法として、ピエゾ素子を搭載した液滴吐出用ヘッドを挙げたが、さらに、単一の液滴に対してバイオチップ100の外から強い振動等の衝撃を加えてもよい。また、液滴を吐出するノズルの内径を小さくする、若しくは吐出速度を増加させる、若しくはこの両方を組み合わせてもよい。さらに、ノズルの先端を網目状にしてもよい。若しくはそれと同等の効果を示す網状の部品をノズル先端に取り付けることで液滴を吐出する口を分割してもよい。
実施形態においては、熱サイクル装置1が検出装置を含まない例を示したが、図10(A)及び図10(B)に示すように、本変形例に係る熱サイクル装置2は蛍光検出器40を含んでもよい。これにより、例えばリアルタイムPCRのような蛍光検出を伴う用途に熱サイクル装置2を使用できる。蛍光検出器40の数は検出が問題なく行える限り任意である。本変形例においては、1個の蛍光検出器40をスライド22に沿って移動させて蛍光検出を行う。蛍光検出を行う場合には、本体10aの第2加熱部13側に測定窓18(図12参照)を設けることが好ましい。これにより、蛍光検出器40と、反応液140との間に存在する部材を少なくすることができるので、より適切な蛍光測定ができる。
実施形態においては、第1の温度及び第2の温度は熱サイクル処理の開始から終了まで一定としたが、第1の温度及び第2の温度のうち少なくとも一方を処理の途中で変更してもよい。第1の温度及び第2の温度は、制御部の制御によって変更できる。第1加熱部12及び装着部11の配置を切り換えて反応液140を移動させることで、変更された温度に反応液140を加熱できる。したがって、加熱部の数を増やしたり、装置の構造を複雑にしたりすることなく、例えば逆転写PCRのような、2種類以上の温度の組合せを必要とする反応を行うことができる。
実施形態においては、装着部11がスロット構造である例を示したが、装着部11はバイオチップ100を保持できる構造であればよい。例えば、バイオチップ100の形状に合わせた窪みにバイオチップ100をはめ込む構造や、バイオチップ100を挟んで保持する構造を採用してもよい。
実施形態においては、バイオチップ100の位置を定める構造は底板17であったが、位置を定める構造は所望の位置にバイオチップ100を保持できるものであればよい。位置を定める構造は、熱サイクル装置1に設けられた構造であっても、バイオチップ100に設けられた構造であっても、両方の組合せであってもよい。例えば、螺子、差込式の棒、バイオチップ100に突出部を設けた構造、装着部11とバイオチップ100とが勘合する構造を採用できる。螺子や棒を用いる場合には、螺子の長さやねじ込む長さ、棒を差し込む位置を変更することで、熱サイクルの反応条件やバイオチップ100の大きさ等に合わせて保持する位置を調節できるようにしてもよい。
実施形態においては、第1加熱部12と第2加熱部13とがともにカートリッジヒーターである例を示したが、第1加熱部12は第1領域111を第1の温度に加熱できるものであればよい。第2加熱部13は第2領域112を第2の温度に加熱できるものであればよい。例えば、第1加熱部12及び第2加熱部13としては、カーボンヒーター、シートヒーター、IH(電磁誘導加熱)、ペルチェ素子、加熱液体、加熱気体を使用できる。また、第1加熱部12と第2加熱部13とで異なる加熱機構を採用してもよい。
実施形態においては、バイオチップ100を第1加熱部12と第2加熱部13によって加熱する例を示したが、第2加熱部13の代わりに第2領域112を冷却する冷却部を設けてもよい。冷却部としては、例えばペルチェ素子を使用できる。これにより、例えば、バイオチップ100の第1領域111からの熱によって第2領域112の温度が低下しにくい場合にも、流路110に所望の温度勾配を形成できる。また、例えば、加熱と冷却を繰り返す熱サイクルを反応液140に施すことができる。
実施形態においては、第1ヒートブロック12b及び第2ヒートブロック13bの材質がアルミニウムである例を示したが、ヒートブロックの材質は熱伝導率、保温性、加工しやすさ等の条件を考慮して選択できる。例えば銅合金を使用してもよく、複数の材質を組み合わせてもよい。また、第1ヒートブロック12bと第2ヒートブロック13bとが異なる材質であってもよい。
実施形態に例示したように、装着部11が第1加熱部12の一部として形成されている場合には、装着部11をバイオチップ100に密着させる機構を設けてもよい。密着させる機構は、バイオチップ100の少なくとも一部を装着部11に密着させることができればよい。例えば、本体10や蓋50に設けたバネによってバイオチップ100を装着部11の一方の壁面に押し付けてもよい。これにより、第1加熱部12の熱をバイオチップ100にさらに安定して伝えることができるので、バイオチップ100の温度をさらに安定させることができる。
実施形態においては、第1加熱部12及び第2加熱部13の温度が、バイオチップ100を加熱する温度と実質的に等しくなるよう制御される例を示したが、第1加熱部12及び第2加熱部13の温度制御は、実施形態に限定されない。第1加熱部12及び第2加熱部13の温度は、バイオチップ100の第1領域111及び第2領域112が所望の温度に加熱されるように制御されていればよい。例えば、バイオチップ100の材質や大きさを考慮することで、第1領域111及び第2領域112の温度をより正確に所望の温度に加熱できる。
実施形態においては、駆動機構20がモーターである例を示したが、駆動機構20は装着部11、第1加熱部12、並びに第2加熱部13を駆動できる機構であればよい。駆動機構20が装着部11、第1加熱部12、並びに第2加熱部13を回転させる機構である場合、駆動機構20は遠心力によって液体130の温度勾配が乱されない程度の回転速度に制御可能であることが好ましい。また、配線に生じた捩れを解消するために、回転の方向を反転させることができるものであることが好ましい。このような機構としては、例えばハンドル、ぜんまい等を採用できる。
実施形態においては、装着部11が第1加熱部12の一部である例を示したが、駆動機構20を動作させた場合に両者の位置関係が変化しない限り、装着部11と第1加熱部12とは別の部材であってもよい。装着部11と第1加熱部12とが別の部材である場合には、両者が直接又は他の部材を介して固定されていることが好ましい。また、装着部11と第1加熱部12とは同一の機構によって駆動されても、別個の機構によって駆動されてもよいが、両者の位置関係を一定に保つように動作することが好ましい。これにより、駆動機構20を動作させた場合に装着部11と第1加熱部12との位置関係を一定に維持できるので、バイオチップ100の所定の領域を所定の温度に加熱できる。なお、装着部11、第1加熱部12、並びに第2加熱部13を駆動する機構が別個の機構である場合には、両者を合わせて駆動機構20とする。
実施形態においては、温度センサーが熱電対である例を示したが、例えば測温抵抗体やサーミスターを使用してもよい。
実施形態においては、固定部51が磁石である例を示したが、固定部51は蓋50と本体10を固定できるものであればよい。例えば、蝶番やキャッチクリップを採用してもよい。
実施形態においては、駆動軸の方向は装着部11の長手方向に対して垂直であるとしたが、駆動軸の方向は、装着部11、第1加熱部12、並びに第2加熱部13の配置を第1の配置と第2の配置との間で切り換えることができる限り任意である。駆動機構20が装着部11、第1加熱部12、並びに第2加熱部13を回転駆動する機構である場合、装着部11の長手方向に対して非平行な直線を回転の軸とすることで、装着部11、第1加熱部12、並びに第2加熱部13の配置を切り換えることができる。
実施形態においては、制御部は電子制御である例を示したが、第1の時間又は第2の時間を制御する制御部(時間制御部)は、第1の時間又は第2の時間を制御できるものであればよい。すなわち、駆動機構20の動作又は停止のタイミングを制御できるものであればよい。また、熱サイクルのサイクル数を制御する制御部(サイクル数制御部)は、サイクル数を制御できるものであればよい。時間制御部及びサイクル数制御部としては、例えば、物理的な機構や電子制御機構、及びこれらの組合せを採用できる。
熱サイクル装置は、図10(A)及び図10(B)に例示するように、設定部25を含んでもよい。設定部25はUI(ユーザーインターフェイス)であり、熱サイクルの条件を設定する機器である。設定部25を操作することにより、第1の温度、第2の温度、第1の時間、第2の時間、及び熱サイクルのサイクル数のうち、少なくとも1つを設定できる。設定部25は制御部と機械的又は電子的に連動しており、設定部25での設定が制御部の制御に反映される。これにより、反応の条件を変更できるので、所望の熱サイクルを反応液140に施すことができる。設定部25は、上記のいずれかの項目を個別に設定できるものであっても、例えば事前に登録した複数の反応条件の中から1つを選択すると、必要な項目が自動的に設定されるものであってもよい。図10の例では設定部25はボタン式であり、項目別にボタンを押すことで反応条件を設定できる。
熱サイクル装置は、図10(A)及び図10(B)に例示するように表示部24を含んでもよい。表示部24は表示装置であり、熱サイクル装置に関する各種情報を表示する。表示部24は、設定部25で設定される条件や熱サイクル処理中の実際の時間や温度を表示してもよい。例えば、設定を行う場合には入力された条件を表示したり、熱サイクル処理中には温度センサーによって測定された温度、第1の配置又は第2の配置において経過した時間、熱サイクルを施したサイクル数を表示したりしてもよい。また、熱サイクル処理が終了した場合や、装置に何らかの異常が発生した場合にも、その旨を表示してもよい。さらに、音声による通知を行ってもよい。表示や音声による通知を行うことで、熱サイクル処理の進行や終了を装置の使用者が容易に把握できる。
実施形態においては、流路110の断面が円形のバイオチップ100を例示したが、流路110の形状は、対向する内壁に近接して反応液140が移動できる限り任意である。すなわち、反応液が第1領域111と第2領域112との間を移動する時間の変動が、両領域における反応液140の加熱時間に影響を与えない限り任意である。なお、バイオチップ100の流路110の断面が多角形の場合には、「対向する内壁」は、流路110に内接する断面が円形の流路を仮定した場合に、該流路の対向する内壁であるものとする。すなわち、流路110に内接する、断面が円形の仮想流路の対向する内壁に近接して反応液140が移動するように流路110が形成されていればよい。これにより、流路110の断面が多角形の場合にも、第1領域111と第2領域112との間を反応液140が移動する経路を、ある程度規定できる。したがって、反応液140が第1領域111と第2領域112との間を移動する所要時間を、ある程度の範囲に制限できる。
実施形態においては、液体130は反応液140よりも比重が小さい液体であるとしたが、液体130は、反応液140とは相分離し、かつ、反応液140と比重が異なる液体であればよい。例えば、反応液140とは相分離し、かつ、反応液140よりも比重が大きい液体を採用してもよい。液体130が反応液140よりも比重が大きい場合には、反応液140は重力方向における流路110の最上部に位置する。
実施形態においては、ステップS104における回転の方向と、ステップS107における回転の方向を反対方向としたが、同じ方向への回転を複数回行った後に、反対方向へ同じ回数回転させてもよい。これにより、配線に生じた捩れを解消できるので、反対方向への回転を行わない場合と比較して、配線の劣化を抑制できる。
実施形態における熱サイクル装置1は、第1加熱部12及び第2加熱部13を含んだが、第2加熱部13は無くてもよい。すなわち、加熱部は第1加熱部12のみであってもよい。これにより、使用する部材の数を減らすことができるので、製造コストを削減できる。
実施形態においては、熱サイクル装置1が蓋50を含む例を示したが、蓋50は無くてもよい。これにより、使用する部材の数を減らすことができるので、製造コストを削減できる。
実施形態においては、熱サイクル装置1がスペーサー14を含む例を示したが、スペーサー14は無くてもよい。これにより、使用する部材の数を減らすことができるので、製造コストを削減できる。
実施形態においては、熱サイクル装置1が底板17を含む例を示したが、図12に示すように、底板17は無くてもよい。これにより、使用する部材の数を減らすことができるので、製造コストを削減できる。
実施形態においては、熱サイクル装置1が固定板19を含む例を示したが、固定板19は無くてもよい。これにより、使用する部材の数を減らすことができるので、製造コストを削減できる。
実施形態においては、スペーサー14と固定板19とが別個の部材である例を示したが、図12に示すように、スペーサー14と固定板19と一体に形成されていてもよい。また、底板17とスペーサー14と、あるいは底板17と固定板19とが一体に形成されていてもよい。
スペーサー14及び固定板19は、透明であってもよい。これにより、透明なバイオチップ100を熱サイクル処理に使用した場合に、装置の外部から反応液140が移動する様子を観察できる。したがって、熱サイクル処理が適切に行われているか否かを、目視により確認できる。したがって、ここでの「透明」の程度は、これらの部材を熱サイクル装置1に採用して熱サイクル処理を行った場合に、反応液140の移動が視認できる程度であればよい。
熱サイクル装置1の内部を観察するためには、スペーサー14を透明にして固定板19を無くしても、固定板19を透明にしてスペーサー14を無くしても、スペーサー14と固定板19との両方を無くしてもよい。観察者と観察対象のバイオチップ100の間に存在する部材が少ないほど、物体による光の屈折の影響が少なくなるので、内部の観察が容易になる。また、部材が少なければ、製造コストを削減できる。
熱サイクル装置1の内部を観察するためには、図10及び図12に例示するように、本体10aに観察窓23を設けてもよい。観察窓23は、例えば、スペーサー14又は固定板19に形成された穴やスリットであってもよい。図12の例では、観察窓23は固定板19と一体に形成された透明なスペーサー14に設けられた凹部である。観察窓23を設けることで、観察者と観察対象のバイオチップ100の間に存在する部材の厚みを少なくできるので、内部の観察が容易になる。
実施形態においては、本体10の底板17側に第1加熱部12が、蓋50の側に第2加熱部13が配置されている例を示したが、図12に示すように、蓋50の側に第1加熱部12が配置されていてもよい。第1加熱部12が蓋50の側に配置されている場合には、実施形態のステップS101においてバイオチップ100を装着した場合の装着部11、第1加熱部12、並びに第2加熱部13の配置は第2の配置である。すなわち、第2領域112が重力の作用する方向における流路110の最下部に位置する配置である。したがって、本変形例の熱サイクル装置2を実施形態に係る熱サイクル処理に適用した場合には、バイオチップ100を装着部11に装着したら、第1の配置への切り換えが行われる。具体的には、ステップS101からステップS102及びステップS103へ移行する前に、ステップS107の処理が行われる。
実施形態においては、第1加熱部12及び第2加熱部13によってバイオチップ100を加熱する工程(ステップS102)と、第1の時間が経過したか否かの判定を行う工程(ステップS103)とが、バイオチップ100を装着部11に装着したら(ステップS101)開始される例を示したが、ステップS102を開始するタイミングは実施形態に限定されない。ステップS103において計時が開始される時点までに第1領域111が第1の温度に加熱される限り、ステップS102は任意のタイミングで開始してよい。ステップS102を行うタイミングは、使用するバイオチップ100の大きさや材料、第1ヒートブロック12bの加熱に必要な時間等を考慮して決定される。例えば、ステップS101より前、ステップS101と同時、及びステップS101より後でステップS103より前、のいずれかとしてもよい。
実施形態においては、第1の温度、第2の温度、第1の時間、第2の時間、及び熱サイクルのサイクル数、駆動機構20の動作を制御部によって制御する例を示したが、これらの項目のうち少なくとも1つを使用者が制御することも可能である。使用者が第1の温度又は第2の温度を制御する場合は、例えば温度センサーによって測定された温度を表示部24で表示し、使用者が設定部25を操作して温度を調節してもよい。使用者が熱サイクルのサイクル数を制御する場合、所定回数に達した場合に使用者が熱サイクル装置1を停止させる。サイクル数の計数は、使用者が行っても、熱サイクル装置1が計数を行ってサイクル数を表示部24に表示してもよい。
実施形態においては、駆動機構20の回転によって装着部11、第1加熱部12、並びに第2加熱部13の配置を切り換える場合の回転角度が180°である例を示したが、回転角度は、第1領域111と第2領域112との、重力方向における上下の位置関係が変化する角度であればよい。例えば、回転角度が180°未満であれば、反応液140の移動速度が遅くなる。したがって、回転角度を調節することで、反応液140が第1の温度と第2の温度との間を移動する時間を調節できる。すなわち、反応液140の温度が第1の温度と第2の温度との間で変化する時間を調節できる。
Claims (9)
- 複数の液滴からなる反応液を形成する液滴形成部と、
前記反応液と、該反応液よりも比重が小さく、かつ、該反応液とは相分離する液体とが充填され、該反応液が対向する内壁に近接して移動する流路を含むバイオチップを装着する装着部と、
前記装着部に前記バイオチップを装着した場合に、前記流路の第1領域を加熱する加熱部と、
前記装着部及び前記加熱部の配置を、第1の配置と、第2の配置との間で切り換える駆動機構と、
を含み、
前記第1の配置は、前記装着部に前記バイオチップを装着した場合に、前記第1領域が、重力の作用する方向における前記流路の最下部に位置する配置であり、
前記第2の配置は、前記装着部に前記バイオチップを装着した場合に、前記反応液が移動する方向における位置が前記第1領域とは異なる前記流路の第2領域が、重力の作用する方向における前記流路の最下部に位置する配置であることを特徴とする熱サイクル装置。 - 請求項1に記載の熱サイクル装置において、
前記バイオチップの流路の長手方向と交差する断面の内径に対する前記反応液の液滴の直径の比は、0.29〜0.86となるように、前記反応液の個々の液滴の体積が調整されることを特徴とする熱サイクル装置。 - 請求項1又は2に記載の熱サイクル装置において、
前記駆動機構は、
前記第1の配置から前記第2の配置へ切り換える場合と前記第2の配置から前記第1の配置へ切り換える場合とで、反対方向に前記装着部及び前記加熱部を回転させることを特徴とする熱サイクル装置。 - 請求項1〜3のいずれか一項に記載の熱サイクル装置において、
前記駆動機構は、
前記第1の配置において第1の時間が経過した場合に、前記配置を前記第2の配置へ切り換え、
前記第2の配置において第2の時間が経過した場合に、前記配置を前記第1の配置へ切り換えることを特徴とする熱サイクル装置。 - 請求項1〜4のいずれか一項に記載の熱サイクル装置において、
前記装着部は、
前記流路の長手方向に前記反応液が移動する前記バイオチップを装着し、
前記第1領域は、前記長手方向における一方の端部を含む領域であり、前記第2領域は、前記長手方向における他方の端部を含む領域であることを特徴とする熱サイクル装置。 - 請求項1〜5のいずれか一項に記載の熱サイクル装置において、
さらに、前記装着部に前記バイオチップを装着した場合に、前記第2領域を加熱する第2加熱部を含み、
前記加熱部は、第1の温度に前記第1領域を加熱し、
前記第2加熱部は、前記第1の温度とは異なる第2の温度に、前記第2領域を加熱することを特徴とする熱サイクル装置。 - 請求項6に記載の熱サイクル装置において、
前記第1の温度は、前記第2の温度よりも高い温度であることを特徴とする熱サイクル装置。 - 請求項7に記載の熱サイクル装置において、
前記第1の時間は、前記第2の時間よりも短いことを特徴とする熱サイクル装置。 - 複数の液滴からなる反応液を形成することと、
前記反応液と、該反応液よりも比重が小さく、かつ、該反応液とは相分離する液体とが充填され、該反応液が、対向する内壁に近接して移動する流路を含むバイオチップを装着部に装着することと、
前記流路の第1領域が、重力の作用する方向における前記流路の最下部に位置する第1の配置に前記バイオチップを保持することと、
前記第1領域を加熱することと、
前記反応液が移動する方向における位置が前記第1領域とは異なる前記流路の第2領域が、重力の作用する方向における前記流路の最下部に位置する第2の配置に前記バイオチップを保持することと、
を含むことを特徴とする熱サイクル方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013006997A JP2014135941A (ja) | 2013-01-18 | 2013-01-18 | 熱サイクル装置及び熱サイクル方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013006997A JP2014135941A (ja) | 2013-01-18 | 2013-01-18 | 熱サイクル装置及び熱サイクル方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2014135941A true JP2014135941A (ja) | 2014-07-28 |
| JP2014135941A5 JP2014135941A5 (ja) | 2016-02-18 |
Family
ID=51413818
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013006997A Withdrawn JP2014135941A (ja) | 2013-01-18 | 2013-01-18 | 熱サイクル装置及び熱サイクル方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2014135941A (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016192931A (ja) * | 2015-04-01 | 2016-11-17 | セイコーエプソン株式会社 | 核酸増幅反応用カートリッジおよび核酸増幅装置 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009118798A (ja) * | 2007-11-16 | 2009-06-04 | Tokyo Medical & Dental Univ | 核酸増幅装置、方法および細胞培養・核酸増幅方法 |
| JP2009136250A (ja) * | 2007-12-10 | 2009-06-25 | Seiko Epson Corp | 生体試料反応用チップ、生体試料反応装置、および生体試料反応方法 |
| JP2012115208A (ja) * | 2010-12-01 | 2012-06-21 | Seiko Epson Corp | 熱サイクル装置及び熱サイクル方法 |
| WO2012100198A2 (en) * | 2011-01-20 | 2012-07-26 | University Of Washington Through Its Center For Commercialization | Methods and systems for performing digital measurements |
-
2013
- 2013-01-18 JP JP2013006997A patent/JP2014135941A/ja not_active Withdrawn
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009118798A (ja) * | 2007-11-16 | 2009-06-04 | Tokyo Medical & Dental Univ | 核酸増幅装置、方法および細胞培養・核酸増幅方法 |
| JP2009136250A (ja) * | 2007-12-10 | 2009-06-25 | Seiko Epson Corp | 生体試料反応用チップ、生体試料反応装置、および生体試料反応方法 |
| JP2012115208A (ja) * | 2010-12-01 | 2012-06-21 | Seiko Epson Corp | 熱サイクル装置及び熱サイクル方法 |
| WO2012100198A2 (en) * | 2011-01-20 | 2012-07-26 | University Of Washington Through Its Center For Commercialization | Methods and systems for performing digital measurements |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016192931A (ja) * | 2015-04-01 | 2016-11-17 | セイコーエプソン株式会社 | 核酸増幅反応用カートリッジおよび核酸増幅装置 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5867668B2 (ja) | 熱サイクル装置及び熱サイクル方法 | |
| JP5896100B2 (ja) | 熱サイクル装置 | |
| US20150087026A1 (en) | Thermal cycler and control method of thermal cycler | |
| JP5967361B2 (ja) | 熱サイクル装置 | |
| US9789459B2 (en) | Nucleic acid amplification reaction vessel and nucleic acid amplification reaction apparatus | |
| US20150343448A1 (en) | Nucleic acid amplification reaction apparatus | |
| JP2014135941A (ja) | 熱サイクル装置及び熱サイクル方法 | |
| JP2014135942A (ja) | 熱サイクル装置及び熱サイクル方法 | |
| JP5971463B2 (ja) | 熱サイクル装置及び熱サイクル装置の制御方法 | |
| JP6120030B2 (ja) | 熱サイクル装置 | |
| JP5896110B2 (ja) | 熱サイクル装置及び熱サイクル装置の制御方法 | |
| JP2013252091A (ja) | 熱サイクル装置 | |
| US20150232922A1 (en) | Nucleic acid amplification reaction apparatus | |
| EP3135376A1 (en) | Nucleic acid amplification reaction container, nucleic acid amplification reaction device, and reaction method for amplifying nucleic acid | |
| JP6090554B2 (ja) | 熱サイクル装置 | |
| JP2013208066A (ja) | 熱サイクル装置及び熱サイクル装置の制御方法 | |
| JP5853494B2 (ja) | 熱サイクル装置及び異常判定方法 | |
| JP5935985B2 (ja) | 熱サイクル装置 | |
| JP5849443B2 (ja) | 熱サイクル装置 | |
| JP5910304B2 (ja) | 熱サイクル装置 | |
| JP5842391B2 (ja) | 熱サイクル装置 | |
| JP2018014931A (ja) | 熱サイクル装置 | |
| JP2018011566A (ja) | 熱サイクル装置、反応容器及び核酸増幅反応方法 | |
| JP2015223083A (ja) | 核酸増幅反応装置の制御方法 | |
| JP2017112842A (ja) | 熱サイクル装置および熱サイクル装置の制御方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20150109 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20151225 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20151225 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20160610 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20160624 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20160728 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160817 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20161007 |