JP2012507030A - 重症敗血症及び敗血症性ショック中の死亡の危険性が高い患者を迅速に決定するための方法及びキット - Google Patents
重症敗血症及び敗血症性ショック中の死亡の危険性が高い患者を迅速に決定するための方法及びキット Download PDFInfo
- Publication number
- JP2012507030A JP2012507030A JP2011533853A JP2011533853A JP2012507030A JP 2012507030 A JP2012507030 A JP 2012507030A JP 2011533853 A JP2011533853 A JP 2011533853A JP 2011533853 A JP2011533853 A JP 2011533853A JP 2012507030 A JP2012507030 A JP 2012507030A
- Authority
- JP
- Japan
- Prior art keywords
- level
- complex
- patient
- septic shock
- patients
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5091—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing the pathological state of an organism
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6893—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids related to diseases not provided for elsewhere
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/26—Infectious diseases, e.g. generalised sepsis
Abstract
【選択図】図1
Description
- 「敗血症」は、感染に応答する全身性の炎症である。
- 「重症敗血症」は、少なくとも1つの臓器機能不全を伴う敗血症と定義される。
- 重症敗血症症候群のうち、最も重症な事例は、2つ又はさらにより多くの臓器不全を示す。一般的ではないが、急性循環不全とは別の2つの臓器機能不全を伴ういくつかの重症敗血症が観察されている。このような事例は、「少なくとも2つの臓器不全を伴う重症敗血症」と定義され、敗血症性ショックとは区別される。
- 「急性循環不全」は、低血圧のその他の原因がない中での適切な輸血蘇生(volume resuscitation)にもかかわらない持続性の動脈性低血圧(収縮期動脈圧<90 mmHg、MAP<60 mmHg又はベースラインからの収縮期血圧の低減>40 mmHg)である。
- 「少なくとも2つの臓器不全を伴う敗血症性ショック」は、急性循環不全に加えて少なくとも1つの臓器不全(例えば腎臓、肝臓など)と伴う敗血症性ショックである。
-本明細書において、考慮される患者は、重症敗血症又は敗血症性ショックのいずれかの患者であるが、両方の場合において少なくとも2つの臓器不全を伴う。これらの患者について、「第0日」は、第2の臓器不全の発症後24時間の期間を指す。
1- 細菌:
グラム陽性桿菌:コリネバクテリウム(Corynebacterium)
クロストリジウム(Clostridium)
リステリア(Listeria)
バチルス(Bacillus)
グラム陰性球菌:ナイセリア(Neisseria)
グラム陰性桿菌:腸内細菌:大腸菌(E. coli)、シゲラ(Shigella)、クレブシエラ(Klebsiella)、サルモネラ(Salmonella)、セラチア(Serratia)、プロテウス(Proteus)、シュードモナス(Pseudomonas)、エルシニア(Yersinia)
リケッチア(Rickettsia)
ヘモフィラス(Haemophilus)
レジオネラ(Legionella)
プロビデンシア(Providencia)
バクテロイド(Bacteroides)
グラム陽性球菌:ストレプトコッカス(Streptococcus)
スタフィロコッカス(Staphylococcus)
インフルエンザウイルス
パラミクソウイルス
コロナウイルス
パラインフルエンザウイルス
呼吸器多核体ウイルス
アルボウイルス
3- 寄生体:プラスモディウム(Plasmodium)
トキソプラズマ(Toxoplasma)
(i) 前記対象者からの生体試料から、S100A8及び/又はS100A9及び/又はS100A8/A9複合体のレベルを測定するステップと、
(ii)前記レベルを、予め決定された閾値と比較するステップと
を含み、予め決定された前記閾値より高いS100A8及び/又はS100A9及び/又はS100A8/A9複合体のレベルが、悪い予後を示し、予め決定された前記閾値より低いS100A8及び/又はS100A9及び/又はS100A8/A9複合体のレベルが、良い予後を示す、前記方法である。
生体試料は、例えば、血漿、唾液、尿、脳脊髄液、胸膜液及び腹水から選択され得る。
また、イムノアッセイとは異なる技術を用いて本発明による方法を行うことができる。具体的には、質量分析を、その目的のために有利に用いることができる。
(i)請求項1に記載の方法により上記の患者の予後を確立するステップ(第2の臓器不全の発症後できる限りすぐに)と、
(ii)治療の数日後(例えば2週間)に得られた上記の患者からの生体試料中のS100A8/A9のレベルを測定するステップと
を含み、S100A8/A9のレベルの減少が観察されず、臨床状態が重症のままである場合に、治療中止を決定する、前記方法に関する。この方法を行う場合に、医師は、患者が2つ以上の臓器不全をまだ有する場合に、臨床状態が重症のままであると考慮する。治療中止は、具体的には、ステップ(i)において測定されるS100A8/A9のレベルが上記で規定される閾値より高く、治療の数日後にこの閾値より高いままである場合に決定される。
(i)少なくとも2つの臓器不全を伴う重症敗血症又は少なくとも2つの臓器不全を伴う敗血症性ショックの患者を選択し、上記の医薬的治療の開始前に上記の患者から得られる生体試料中のS100A8/A9のレベルを決定するステップと、
(ii)上記の患者から、上記の医薬的治療の開始後に得られた少なくとも別の試料から、S100A8/A9のレベルを決定するステップと、
(iii)上記の得られた値同士を比較するステップと
を含み、医薬的治療の開始の後のS100A8/A9レベルの減少が、上記の治療が患者にとって有益であり、少なくとも2つの臓器不全を伴う重症症候群の転帰を改善する可能性があることを示す、前記方法にも関する。
もちろん、本発明によるキットは、イムノアッセイを行うための試薬(バッファー、酵素、標識分子など)、品質管理、1つ以上の標準物質などから選択されるその他の成分も含むことができる。
材料及び方法
以下に報告する全ての実験は、以下の材料及び方法を用いて行った。
患者
この多施設での研究は、Cochin Hospital倫理委員会(# CCPPRB 2061)により承認され、集中治療室(2つの医療的、2つの外科的)からの患者を含めた。ACCP/SCCMコンセンサス会議(Boneら, 1992)に従って定義される敗血症性ショックの基準を満たす患者だけをスクリーニングした。参加基準により、敗血症性ショックの患者は、SOFA (経時的臓器不全評価;Sequential Organ Failure Assessment)スコア(Vincentら, 1998)により定義される少なくとも2つの臓器不全を有することが必要であった。最初の血液試料は、第2の臓器不全の発生の24時間以内に生じると定義される第0日(D0)に採取した。
倫理委員会の許可の後の試験コホートからの試料を、同じ期間に(2004年2月〜2005年11月)重症敗血症についての多施設での研究に参加した同じ参加基準を満たす患者から得た(Programme Hospitalier de Recherche Clinique第AOR 02006号)。このコホートを用いて、学習コホートから第0日に得た血漿S100A8/A9複合体レベルの予測能力を評価した。
全血を、蛍光色素(フルオレセインイソチオシアネート(FiTC)又はフィコエリスリン(PE))とコンジュゲートした適切な抗体とインキュベートした:抗CD14-FiTC (クローンRMO52、Beckman Coulter, Marseille, France)及びPEとコンジュゲートした無関係のアイソタイプ対照抗体(Simultestコントロール、BD Biosciences, San Jose, CA, USA)又は抗HLA-DR-PE (クローンL243、BD Biosciences)。平均蛍光強度を、細胞あたりに結合した抗体の数(AB/C)に、QFCM (定量フローサイトメトリー;Quantitative Flow CytoMetry)を用いて変換した。
血漿IL-10 (optEIA(商標)セット; PharMingen, San Diego, CA, USA)、IL-12p40及びMIF (R&D Systems, Abingdon, Oxon, UK)の濃度を、製造業者の指示に従う免疫酵素法(ELISA)により測定した。標準試料は、IL-10について7.8〜500 pg/ml、IL-12p40及びMIFについて31.2〜2000 pg/mlの範囲であった。検出閾値は、IL-10について2.7±3.1 pg/ml、IL-12p40について25.8±33.3 pg/ml、MIFについて25.7±34.6 pg/mlであった。
この技術は、以前の出版物(Ikemotoら, 2003)から、年齢及び性別により対にした34名の健常対象者から採取した血液を用いて改変した。レベルは、平均0.26μg/mlであり、0.052〜0.468μg/mlの範囲であった。簡単に、100μlの希釈溶液を、第1抗体(Mo2B9; 0.166 mg/L)で被覆した96ウェルポリカーボネートプレートの各ウェルに加えた。Block-Ace(商標) (Dainippon Pharmacology Co Ltd)希釈溶液で予め希釈した血漿試料又はMRP8/14複合体標準物質溶液を、次いで加えて、15秒間混合した。プレートを、次いで、1時間インキュベートして、免疫反応を進行させた。5回の洗浄後に、100μlのF(ab')2-ビオチンコンジュゲート(0.5 g/Lチメロサール含有Block-Ace(商標)希釈溶液中の第2抗体Mo3D2)を加え、プレートをさらに1時間インキュベートした。上記のような繰り返しの洗浄の後に、Block-Ace希釈溶液で1500倍に希釈した100μlのストレプトアビジン-HRPコンジュゲートを加え、プレートをさらに30分間インキュベートした。HRP活性を、比色法により決定した。測定内変動係数(CV)は3.9〜5.6%であり、日同士のCVは5.9〜7.6%であり、平均回収率(recovery)は98%(範囲85〜103%)であった。アッセイは、臨床転帰について隠した研究員により行われた。
RNA試料を、D0及びD1に、フィコール勾配遠心分離により成熟PMNを除去した後に得た。細胞分析は、光散乱による形態学的特徴決定と、未成熟細胞(顆粒球系統)の割合を評価するためのCD66b発現(FACScalibur)を含んだ(Payenら, 2008)。D0及びD1にて、末梢血単核細胞(PBMC)の割合は、およそ50%であった。トータルRNAを、Rneasyキット(Qiagen)を用いて抽出して、試料を、RnaseフリーDNAse Iで処理した。質及び量をAgilentバイオアナライザーで推定し、トータルRNAの量を、Nanodrop分光光度計で確認した。qRT-PCRを、S100A8 (Hs00374264_g1)及びS100A9 (Hs00610058_m1)について、製造業者の明記(Applied Biosystems, Foster City, CA, USA, 表1)に従って行い、内在性対照である真核18S rRNA (Hs99999901_s1)と比較した。結果は、デルタCt (濃度閾値): CtS100Ax-Ct18Sで表す。
定量結果を、中央値及び25百分位数〜75百分位数として表す。量的変数の比較は、マン-ホイットニー検定を用い、質的変数は、カイ二乗検定により行った。相関の研究は、スピアマンの相関検定により行った。p値<0.05を、統計的に有意とみなした。ヒト敗血症性ショックについて以前に発表されたデータ(Payenら, 2008)に基づいて、本発明者らは、敗血症性ショック患者における死亡率が40%(Annaneら, 2007; Sprungら, 2008)、及び標準誤差2.35 (Payenら, 2008)で、生存者と非生存者との間のS100A8/A9複合体の差が2μg/mlと仮定した。よって、47名の患者の標本サイズを、学習コホートのために採用して、I型誤差確率0.05及び検定力0.80に制御する必要があった。
統計解析は、SAS 9.1 (SAS Inc, Cary, NC)ソフトウェアパッケージ及びR 2.8.0 (http://www.R-project.org)ソフトウェアパッケージを用いて行った。
学習コホート
49名の患者が参加した。彼らの臨床的特徴を、以下の表2にまとめる。患者管理について、Surviving Sepsis Campaignのガイドラインに従った(Dellingerら, 2004)。9名の患者(18%)が、活性化プロテインCを受け、35名(71%)がヒドロコルチゾンで処置された。31名の患者が過去2日間に外科的手法を受けていた。15名の患者が28日間の研究期間中に死亡し、12名は最初の7日間に死亡した。D7より後(D24に1名及びD26に2名)に死亡した3名の患者は、処置不可能な呼吸不全及び重症低酸素症、遅延型多臓器不全、並びに治療の制限を要求する瀕死状態を原因として死亡した。D0に、SAPSII臨床重症度スコアは、生存者と非生存者とで異なっていたが、SOFAスコアは同様であった(表2)。
D0において、S100 A8/A9複合体の血漿レベルは、最終的な生存者と非生存者との間で著しく異なっていた(3.7μg/ml (3.2〜4.2)対13.3μg/ml (10.1〜15.6)、p<0.0001)。群の間に重複はなかった。同様の結果が、D1について得られた(図1)。結果として、100%の特異性及び感度と、8.1μg/mlの死亡危険性の閾値血漿レベルとが得られた。感度のLaplace推定値は94.1%(95%信頼区間: 84.7%〜100%)であり、特異性について97.2% (95%信頼区間: 92.6%〜100%)であった。重要なことに、これは、D0に測定された臓器不全の数には影響されなかった。類似の血漿レベルが、2つの臓器不全[3.5μg/ml IQ 1.4 (n=8)]又は2より多い臓器不全[3.7μg/ml IQ 0.9 (n=25)]の患者で見られた。
同じ参加基準を満たす62名の患者からの試料を研究した。転帰による臨床的特徴及び炎症の変数を、表4及び5に示す。臨床変数は、有意により高かった第28日までの死亡率(56.5%に対して30.6%;p=0.01)以外について学習コホートと同等であった(表6)。試験コホートにおいて、HLA-DR発現及び血漿MIFレベルは同様であったが、IL-10の値はより低かった(p<0.05)。最初のコホートと同様に、最終的な生存者[5.3μg/ml (4.43〜6.43)]と非生存者[12.5μg/ml (10.23〜14.08) p<0.0001]との間で、S100A8/A9複合体の血漿レベルに明確な差があった。AUCの値は0.99であり、学習コホートから得られた8.1μg/mlの閾値血漿の値が、それぞれ94.3%及び100% (Laplace推定値:96.55%)の感度及び特異性で生存者を非生存者から区別した。2名の患者のみが誤って分類された。彼らの血漿S100A8/A9の値は、良い予後を示唆したが、彼らは、肝硬変を背景にする非代償性肝不全により3週間後に死亡した。学習コホートでと同様に、臓器不全の数もaPC又はヒドロコルチゾンでの治療も、血漿S100A8/A9レベルにより提供される予後判定に影響しなかった(データは示さず)。
我々は、S100A8/A9複合体の血漿レベルが、第2の臓器不全の出現の最初の日ほど初期に考慮しても、敗血症性ショックの患者における転帰の優れた予測因子であることを見出した。これは、D0での臓器不全の数にも、活性化プロテインC又はコルチコステロイド類のその後の使用にも依存しなかった。これは、少なくとも最初の2日間は、8.1μg/mlの死亡についての予測閾値で安定したままであった。49名の患者の学習コホートで得られたこの閾値の有効性を、その後、62名の患者の試験コホートで確認した。血漿タンパク質レベルの差は、末梢白血球上のS100A8及びA9遺伝子発現と相関せず、このことは、少なくともこの初期段階における循環免疫細胞以外のこの複合体の起源を示唆する。
第0日及び第1日について実施例1で行ったのと同じ実験を、28日間にわたって完了した(D0、D1、D7、D14及びD28)。
111名の患者(実施例1の「学習コホート」の49名及び「試験コホート」の62名)についての結果は、生存者において血漿タンパク質レベルが経時的に減少したが、非生存者では減少しなかったことを示す(図5)。血漿S100A8/A9は、対照と比較して生存者においてD28においてまだ上昇していた(中央値2.65μg/ml (IQR 2.60))。
最終的に予後が良かった1名の患者だけが、驚異的に高いレベルのS100A8/A9複合体をD14にて示した。この患者において、S100A8/A9の値は、D0にて4.7μg/ml、D1にて4.0μg/ml、D7にて4.5μg/ml、D14にて20.1μg/mlであったが、彼の進展は良好であり、最終的に良好な予後であった(D28前に退院)。D14でのS100A8/A9レベルは、しかし、対照を用いておらず、この驚異的な結果は、測定アーチファクトであり得る。
D0〜D28、p<0.0001、n=34
D0〜D14、p<0.0001、n=41
D0〜D7、p=0.0005、n=57
で減少し、D28前に死亡した患者について、S100A8/A9血漿レベルは:
D0〜D14、有意でない
D0〜D7、p=0.0010、n=15
で増加した。
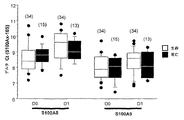
図6及び図7は、32名の患者におけるS100A8及びS100A9遺伝子発現を示す。これらのデータは、EP 2085486 A1に記載されるのと同じ方法を用いてAffymetrix HG-U133 Plus 2.0アレイで行ったマイクロアレイ解析から抽出した。
S100A8遺伝子発現は、第0日と第7日の間で、生存者においてわずかに減少したが、これでさえ28日間では有意でなかった。この傾向は、非生存者では観察されなかった。S100A8遺伝子発現の統計は、次のとおりである:
生存者におけるフリードマン検定 D0〜D28、n=11:NS
D0〜D7、n=18:p=0.0421
生存者におけるウィルコクソン検定 D0〜D1、n=17:NS
非生存者におけるウィルコクソン検定 D0〜D1、n=9:NS
生存者対非生存者のマンホイットニー検定:D1にて有意、p=0.035。
生存者におけるフリードマン検定 D0〜D28、n=11:p=0.0199
D0〜D7、n=18:p<0.0001
生存者におけるウィルコクソン検定 D0〜D1、n=17:p=0.0019
非生存者におけるウィルコクソン検定 D0〜D1、n=9:NS
生存者対非生存者のマンホイットニー検定:各時点において有意でない。
血漿S100A8/A9レベルを、D0にてショックがない16名の患者において測定した。これらの患者は、2つの臓器不全を伴う重症敗血症であった(以前のコホートと同じ臓器機能不全についての基準)。
8名がD28より前に死亡した。血漿S100A8/A9は、生存者と比較して、非生存者において有意により高かった(図8及び表7)。
Claims (21)
- (i) 対象者からの生体試料から、S100A8/A9複合体のレベルを測定するステップと、
(ii)前記レベルを、予め決定された閾値と比較するステップと
を含み、予め決定された前記閾値より高いS100A8/A9複合体のレベルが、悪い予後を示し、予め決定された前記閾値より低いS100A8/A9複合体のレベルが、良い予後を示す、少なくとも2つの臓器不全を伴う重症敗血症又は少なくとも2つの臓器不全を伴う敗血症性ショックの対象者についての予後をインビトロで確立する方法。 - 前記生体試料が、第2の臓器不全の発症の後の第0日、第1日又は第2日に回収される請求項1に記載の方法。
- 予め決定された前記閾値が、7〜9μg/mlの範囲にある請求項1に記載の方法。
- 予め決定された前記閾値が、7.8〜8.3μg/mlの範囲にある請求項1に記載の方法。
- 予め決定された前記閾値が、8.1μg/mlである請求項1に記載の方法。
- 前記生体試料が、血漿、唾液、尿、脳脊髄液、胸膜液及び腹水から選択される請求項1に記載の方法。
- ステップ(i)における前記測定が、イムノアッセイにより行われる請求項1に記載の方法。
- 前記イムノアッセイが、S100A8/A9複合体と特異的に結合する抗体を用いて行われる請求項7に記載の方法。
- 前記抗体が、蛍光標識されている請求項8に記載の方法。
- 前記イムノアッセイが、ELISAアッセイである請求項7に記載の方法。
- 前記生体試料中の少なくとも1つのその他の種のレベルを測定するステップであって、前記その他の種が、プロカルシトニン(PCT)、N末端プロ脳性ナトリウム利尿ペプチド(BNP)、骨髄系細胞上で発現される可溶性刺激受容体-1(sTREM)、IL-6及びsRAGEから選択されるステップと、前記レベルを、予め決定された閾値と比較するステップとをさらに含む請求項1に記載の方法。
- 患者におけるS100A8/A9複合体の血漿レベルの進展を測定することによる少なくとも2つの臓器不全を伴う重症敗血症又は少なくとも2つの臓器不全を伴う敗血症性ショックの患者のフォローアップを行う方法であって、前記レベルの減少が、前記患者が回復していることを示す、前記方法。
- 患者におけるS100A8及び/又はS100A9の発現レベルの進展を測定することによる少なくとも2つの臓器不全を伴う重症敗血症又は少なくとも2つの臓器不全を伴う敗血症性ショックの患者のフォローアップを行う方法であって、前記レベルの減少が、前記患者が回復していることを示す、前記方法。
- 前記発現レベルが、定量的増幅により測定される請求項13に記載の方法。
- 測定が、入院後のいくつかの時点にて前記患者から得られる生体試料に対して行われる請求項12又は13に記載の方法。
- (i)請求項1に記載の方法により患者の予後を確立するステップと、
(ii)治療の数日後に得られた前記患者からの生体試料中のS100A8/A9複合体のレベルを測定するステップと
を含み、S100A8/A9複合体のレベルの減少が観察されず、臨床状態が重症のままである場合に、治療中止を決定する、少なくとも2つの臓器不全を伴う重症敗血症又は少なくとも2つの臓器不全を伴う敗血症性ショックの患者の治療中止についての決定を補助する方法。 - 少なくとも2つの臓器不全を伴う重症敗血症又は少なくとも2つの臓器不全を伴う敗血症性ショックの対象者が、そのような患者の集中的な援助の必要性を短くするための医薬的治療の効力を評価するための臨床試験に参加するかどうかを決定するための方法であって、請求項1に記載の方法により前記対象者の予後を確立するステップを含み、S100A8/A9複合体の測定されたレベルが、予め決定された閾値より低い場合に、前記患者が参加する、前記方法。
- 少なくとも2つの臓器不全を伴う重症敗血症又は少なくとも2つの臓器不全を伴う敗血症性ショックの対象者が、そのような患者の転帰を改善するための医薬的治療の効力を評価するための臨床試験に参加するかどうかを決定するための方法であって、請求項1に記載の方法により前記対象者の予後を確立するステップを含み、S100A8/A9複合体の測定されたレベルが、予め決定された閾値より高い場合に、前記患者が参加する、前記方法。
- (i)少なくとも2つの臓器不全を伴う重症敗血症又は少なくとも2つの臓器不全を伴う敗血症性ショックの患者を選択し、医薬的治療の開始前に前記患者から得られる生体試料中のS100A8/A9複合体のレベルを決定するステップと、
(ii)前記患者から、前記医薬的治療の開始後に得られた少なくとも別の試料から、S100A8/A9複合体のレベルを決定するステップと、
(iii)前記得られた値同士を比較するステップと
を含み、医薬的治療の開始の後のS100A8/A9複合体レベルの減少が、前記治療が患者にとって有益であり、少なくとも2つの臓器不全を伴う重症症候群の転帰を改善する可能性があることを示す、少なくとも2つの臓器不全を伴う重症症候群の転帰を改善するための医薬的治療の効力を試験する方法。 - S100A8/A9複合体に特異的な抗体と、敗血症性ショックの転帰についてのS100A8/A9複合体の血漿レベルの予測値を示す使用説明とを含む、請求項1に記載の方法を行うためのキット。
- イムノアッセイを行うための試薬をさらに含む請求項20に記載のキット。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US12/259,596 US8283131B2 (en) | 2008-10-28 | 2008-10-28 | Methods and kits for the rapid determination of patients at high risk of death during severe sepsis and septic shock |
| US12/259,596 | 2008-10-28 | ||
| US15852009P | 2009-03-09 | 2009-03-09 | |
| US61/158,520 | 2009-03-09 | ||
| PCT/IB2009/007493 WO2010049818A1 (en) | 2008-10-28 | 2009-10-27 | Methods and kits for the rapid determination of patients at high risk of death during severe sepsis and septic shock |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2012507030A true JP2012507030A (ja) | 2012-03-22 |
| JP2012507030A5 JP2012507030A5 (ja) | 2012-11-29 |
| JP5619016B2 JP5619016B2 (ja) | 2014-11-05 |
Family
ID=41572522
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011533853A Expired - Fee Related JP5619016B2 (ja) | 2008-10-28 | 2009-10-27 | 重症敗血症及び敗血症性ショック中の死亡の危険性が高い患者を迅速に決定するための方法及びキット |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20110287433A1 (ja) |
| EP (1) | EP2350646B1 (ja) |
| JP (1) | JP5619016B2 (ja) |
| CN (1) | CN102257387A (ja) |
| WO (1) | WO2010049818A1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017514459A (ja) * | 2014-03-14 | 2017-06-08 | イー.ダブリュ. ハンコック,ロバート | 敗血症の診断 |
| KR101929772B1 (ko) * | 2016-11-02 | 2018-12-17 | 연세대학교 산학협력단 | 패혈증 진단을 위한 정보를 제공하는 방법 및 이를 이용한 키트 |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2556771T3 (es) * | 2009-01-19 | 2016-01-20 | bioMérieux S.A. | Procedimientos para determinar la susceptibilidad de contraer una infección nosocomial en un paciente y para establecer un pronóstico de evolución de un síndrome séptico |
| CA2826033A1 (en) * | 2011-01-21 | 2012-07-26 | (Inserm) Institut National De La Sante Et De La Recherche Medicale | Methods and kits for predicting the risk of respiratory failure, renal failure or thrombopenia in a septic patient by measuring endocan levels in blood |
| FR2970975B1 (fr) * | 2011-01-27 | 2016-11-04 | Biomerieux Sa | Procede et kit pour determiner in vitro le statut immunitaire d'un individu |
| CN102636645A (zh) * | 2012-04-24 | 2012-08-15 | 广州吉赛生物科技有限公司 | 一种sTERM-1酶联免疫检测试剂盒及其方法 |
| EP3074536B1 (en) * | 2013-11-25 | 2019-06-19 | Children's Hospital Medical Center | Temporal pediatric sepsis biomarker risk model |
| CN108982844B (zh) * | 2018-08-17 | 2021-09-24 | 北京市心肺血管疾病研究所 | 血清S100a8/9复合体水平在急性心肌梗死诊断及预后判断中的应用 |
| WO2021207365A1 (en) * | 2020-04-07 | 2021-10-14 | The Wistar Institute Of Anatomy And Biology | Reawakening of dormant tumor cells by modified lipids derived from stress activated neutrophils |
| CN114606308A (zh) * | 2022-01-26 | 2022-06-10 | 江门市中心医院 | 脓毒症ards的预后与治疗标志物 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007041623A2 (en) * | 2005-10-03 | 2007-04-12 | Biosite Incorporated | Methods and compositions for diagnosis and/or prognosis in systemic inflammatory response syndromes |
| WO2008097773A1 (en) * | 2007-02-02 | 2008-08-14 | Aspenbio Pharma, Inc. | Methods and devices for diagnosis of appendicitis |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1297922A (zh) * | 1999-11-26 | 2001-06-06 | 上海博道基因技术有限公司 | 一种多肽-人钙结合s100蛋白21和编码该多肽的多核苷酸 |
| DE50108027D1 (de) * | 2001-12-04 | 2005-12-15 | Brahms Ag | Verwendung der Glycin-N-Acyl-Transferase (GNAT) für die Diagnose von Entzündungserkrankungen und Sepsis |
| JP4656493B2 (ja) * | 2002-11-20 | 2011-03-23 | ベー・エル・アー・ハー・エム・エス・ゲーエムベーハー | 部分的proANPペプチドを同定するためのサンドイッチイムノアッセイ |
| BRPI0414887A (pt) * | 2003-09-29 | 2006-12-12 | Warren Pharmaceuticals Inc E T | métodos de tratamento, prevenção, retardo do inìcio ou redução dos efeitos de citocinas pró-inflamatórias em um mamìfero e de tratamento, prevenção, retardo do inìcio de uma condição associada com um efeito de citocinas pró-inflamatórias em um mamìfero, e, composição farmacêutica |
| SG150497A1 (en) * | 2004-07-23 | 2009-03-30 | Aspenbio Pharma Inc | Methods and devices for diagnosis of appendicitis |
| CN101193622A (zh) * | 2005-06-09 | 2008-06-04 | 比奥里波克斯公司 | 治疗炎性疾病的方法和组合物 |
| EP1950310A1 (en) * | 2007-01-23 | 2008-07-30 | Charite-Universitätsmedizin Berlin | Method for risk prediction of a postoperative sepsis in a human |
| DE102007009751A1 (de) * | 2007-02-28 | 2008-09-04 | B.R.A.H.M.S Aktiengesellschaft | Verfahren zur selektiven Bestimmung von Procalcitonin 1-116 für diagnostische Zwecke sowie Antikörper und Kits zur Durchführung eines solchen Verfahrens |
| EP2085486A1 (en) * | 2008-02-01 | 2009-08-05 | Assistance Publique - Hopitaux de Paris | Methods and kits for the rapid determination of patients at high risk of death during septic shock |
| US8283131B2 (en) * | 2008-10-28 | 2012-10-09 | Assistance Publique-Hopitaux De Paris | Methods and kits for the rapid determination of patients at high risk of death during severe sepsis and septic shock |
-
2009
- 2009-10-27 WO PCT/IB2009/007493 patent/WO2010049818A1/en active Application Filing
- 2009-10-27 US US13/126,575 patent/US20110287433A1/en not_active Abandoned
- 2009-10-27 EP EP09760590.1A patent/EP2350646B1/en not_active Not-in-force
- 2009-10-27 CN CN2009801518443A patent/CN102257387A/zh active Pending
- 2009-10-27 JP JP2011533853A patent/JP5619016B2/ja not_active Expired - Fee Related
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007041623A2 (en) * | 2005-10-03 | 2007-04-12 | Biosite Incorporated | Methods and compositions for diagnosis and/or prognosis in systemic inflammatory response syndromes |
| WO2008097773A1 (en) * | 2007-02-02 | 2008-08-14 | Aspenbio Pharma, Inc. | Methods and devices for diagnosis of appendicitis |
Non-Patent Citations (2)
| Title |
|---|
| JPN5012002449; DIDIER PAYEN: 'GENE PROFILING IN HUMAN BLOOD LEUCOCYTES DURING RECOVERY FROM SEPTIC SHOCK' INTENSIVE CARE MEDICINE V34 N8, 20080405, P1371-1376, SPRINGER * |
| JPN5012002451; IKEMOTO MASAKI: 'NEW ELISA SYSTEM FOR MYELOID-RELATED PROTEIN COMPLEX (MRP8/14) AND ITS CLINICAL SIGNIFICANCE AS A SE' CLINICAL CHEMISTRY V49 N4, 20030401, P594-600, AMERICAN ASSOCIATION FOR CLINICAL CHEMISTRY * |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017514459A (ja) * | 2014-03-14 | 2017-06-08 | イー.ダブリュ. ハンコック,ロバート | 敗血症の診断 |
| JP2020162615A (ja) * | 2014-03-14 | 2020-10-08 | イー.ダブリュ. ハンコック,ロバート | 敗血症の診断 |
| JP2022065095A (ja) * | 2014-03-14 | 2022-04-26 | イー.ダブリュ. ハンコック,ロバート | 敗血症の診断 |
| KR101929772B1 (ko) * | 2016-11-02 | 2018-12-17 | 연세대학교 산학협력단 | 패혈증 진단을 위한 정보를 제공하는 방법 및 이를 이용한 키트 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102257387A (zh) | 2011-11-23 |
| EP2350646A1 (en) | 2011-08-03 |
| WO2010049818A1 (en) | 2010-05-06 |
| EP2350646B1 (en) | 2016-01-13 |
| US20110287433A1 (en) | 2011-11-24 |
| JP5619016B2 (ja) | 2014-11-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5619016B2 (ja) | 重症敗血症及び敗血症性ショック中の死亡の危険性が高い患者を迅速に決定するための方法及びキット | |
| Lesur et al. | Proven infection-related sepsis induces a differential stress response early after ICU admission | |
| JP2017500562A (ja) | アルツハイマー病に関するバイオマーカー及び方法 | |
| WO2009114532A2 (en) | Markers for diagnosis of pulmonary inflammation and methods related thereto | |
| JP2018519499A (ja) | 慢性腎疾患の発症のリスクを予測するための方法 | |
| JP2023095851A (ja) | 抗生物質治療をモニタリングするためのマーカーとしてのpctおよびpro-adm | |
| US8283131B2 (en) | Methods and kits for the rapid determination of patients at high risk of death during severe sepsis and septic shock | |
| RU2672595C2 (ru) | Способ диагностики молекулярного фенотипа пациента, страдающего заболеванием, сопровождающимся хроническими воспалениями | |
| WO2019117132A1 (ja) | がん免疫療法の予後予測のためのバイオマーカー | |
| EP2034305B1 (en) | Method for determination of inflammatory bowel disease | |
| US20160244835A1 (en) | Urinary neuropilin-1 (nrp-1) as a prognostic marker for nephritis and lupus nephritis | |
| Matboli et al. | Evaluation of urinary autophagy transcripts expression in diabetic kidney disease | |
| JP2015521732A (ja) | 腎機能不全のバイオマーカー | |
| CN116547536A (zh) | 用于预测患有covid-19的患者的疾病严重度的gdf-15 | |
| JP7329503B2 (ja) | 重篤患者用の療法モニタリングマーカーとしてのpro-adm | |
| RU2788885C2 (ru) | Прокальцитонин и про-адм в качестве маркеров для мониторинга лечения антибиотиками | |
| RU2782305C2 (ru) | Про-адм в качестве маркера мониторинга терапии для критически больных пациентов | |
| KR20240031236A (ko) | 무증상 거부반응의 비-침습적 진단 | |
| US20090162868A1 (en) | Gene Markers and Utilization of the Same | |
| WO2019000029A1 (en) | METHODS OF DIAGNOSING INFLAMMATORY PHENOTYPES OF OBSTRUCTIVE CHRONIC BRONCHOPNEUMOPATHY | |
| Lesur et al. | Research Proven infection-related sepsis induces a differential stress response early after ICU admission | |
| Galluzzo et al. | Jacobs Journal of Emergency Medicine | |
| WO2017147492A1 (en) | Methods of detecting and treating airway inflammatory diseases | |
| DE102005057753A1 (de) | Verfahren zur Diagnose von Sepsis mit IgA |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121011 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20121011 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20131022 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20131023 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140120 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140127 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140418 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140819 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140916 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5619016 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |