JP2012504619A - 肥満および糖尿病の有望な治療薬としてのグレリンo−アシルトランスフェラーゼ阻害剤の合成方法および使用方法 - Google Patents
肥満および糖尿病の有望な治療薬としてのグレリンo−アシルトランスフェラーゼ阻害剤の合成方法および使用方法 Download PDFInfo
- Publication number
- JP2012504619A JP2012504619A JP2011530103A JP2011530103A JP2012504619A JP 2012504619 A JP2012504619 A JP 2012504619A JP 2011530103 A JP2011530103 A JP 2011530103A JP 2011530103 A JP2011530103 A JP 2011530103A JP 2012504619 A JP2012504619 A JP 2012504619A
- Authority
- JP
- Japan
- Prior art keywords
- ghrelin
- tat
- subject
- coa
- therapeutically effective
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 0 CCCCCCC(*)C(N**(*)**)=O Chemical compound CCCCCCC(*)C(N**(*)**)=O 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/575—Hormones
- C07K14/60—Growth-hormone releasing factors (GH-RF) (Somatoliberin)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
- A61K47/645—Polycationic or polyanionic oligopeptides, polypeptides or polyamino acids, e.g. polylysine, polyarginine, polyglutamic acid or peptide TAT
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/12—Antidiuretics, e.g. drugs for diabetes insipidus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Abstract
【解決手段】いくつかの実施形態では、本発明は、例えば、肥満および糖尿病の治療に有効であり得るグレリンO−アシルトランスフェラーゼの2基質類似体阻害剤を提供する。
【選択図】図14
Description
胃によって分泌される強力な食欲刺激ホルモン、グレリンは、動物およびヒトの体重増加を刺激する重要なペプチドホルモンであるとされてきた。その効果を発揮するために、グレリンは、アシル化、すなわち3位のセリン残基の通常ではない翻訳後オクタノイル化を必要とする。グレリンのオクタノイル化型は、通常アシル−グレリンと呼ばれる。
いくつかの実施形態では、本発明は式Iの化合物および薬学的に許容される賦形剤を含む組成物を提供する。本明細書では、「薬学的に許容される」は、健全な医学的判断の範囲内で、妥当な便益/リスク比に見合って、過剰な毒性、刺激、アレルギー応答またはその他の問題となる合併症がなくヒトおよび動物の組織との接触に適した化合物、物質、組成物および/または剤形を包含する。いくつかの実施形態では、用語「薬学的に許容される」は、連邦政府または合衆国政府の規制当局によって承認されているか、あるいは合衆国薬局方または動物、より特定すればヒトで使用するために一般的に認識されているその他の国際的薬局方に挙げられていることを意味する。本明細書では、「賦形剤」とは、医薬組成物の製剤で使用される物質を意味し、それ自体は治療価値の無いものであってもよい。参考として組み込んだRemington: The Science and Practice of Pharmacy, 21st Ed. (2006)において記載されたものを含む様々な賦形剤を本発明で使用することができる。賦形剤には、限定はしないが、抗酸化剤、(治療効果を示すものとは対照的に)製剤自体の崩壊を防ぐ抗菌剤、保存剤、キレート化剤、緩衝剤、毒性を調節するための薬剤、着色剤、芳香剤および希釈剤、乳化剤および懸濁剤ならびに薬学的に適用されるその他の物質が含まれる。
別の態様では、本発明は式Iの化合物の調製方法を提供する。いくつかの実施形態では、この方法は、3〜15個のN末端アミノ酸残基を含むグレリンペプチド配列を提供する工程であって、3位のセリン残基がアロック保護1,2−ジアミノプロピオン酸に置換されており、Tat配列がペプチド配列の一末端に結合している工程と、ブロモ−オクタノイル化中間体を得るために、1または複数個の反応容器中で、グレリンペプチド配列を、Pd(PPh3)4パラジウム試薬、n−ブロモオクタン酸無水物および試薬Kと一緒にする工程と、前記ブロモオクタノイル化中間体と補酵素Aを一緒にする工程とを含むことができる。
別の態様では、本発明は、治療有効量の式Iの化合物を含む組成物を使用して、様々な疾患、障害または症状を予防および/または治療する方法を提供する。
別の態様では、本発明はキットを提供する。いくつかの実施形態では、これらのキットは、式Iの化合物の治療有効量の少なくとも1用量を含む組成物を含む。
3種類の細胞系におけるアシル−グレリン産生に対するGO−CoA−Tatの効果
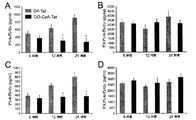
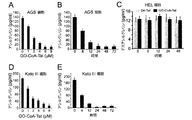
この研究に着手したとき、インビトロGOATアッセイはまだ開発されていなかったため、HELヒト赤白血病細胞(図1D〜E)、KatoIIIヒト胃細胞(図5)およびAGSヒト胃上皮細胞(図5)を含む3種類の細胞においてアシル−グレリン産生に対するGO−CoA−Tatの効果を調べた(3種類の細胞系は全てATCC、Manassas、VAから入手した)。D4-Tat(テトラ−アスパラギン酸は、負のCoA電荷を模倣し、同様にTatペプチドに結合する)を対照として使用した。細胞系それぞれにおいて、アシル−グレリンのレベルは、GO−CoA−Tatによって、IC50が1〜2μMの範囲でD4-Tat対照と比べて有意に減少したが、デスアシル−グレリンは減少しなかった。興味深いことに、最大阻害は、化合物に24時間曝露した後においてのみ実現し、遅い反応速度は非定型酵素特性または予め形成されたアシル−グレリン貯蔵のいずれかから生じているかもしれない。この遅延をさらに調べるために、放射活性アッセイを使用し、組換えミクロソームGOATを用いてインビトロでGO−CoA−Tatを試験した(14)(図1Fおよび6)。完全なGOAT阻害はGO−CoA−Tat 100nMで5分以内に実現し、細胞アシル−グレリンレベルのゆっくりした見かけ上の減少は大きな既存の細胞内貯蔵を反映している可能性があることが示唆された。
マウスにおけるアシル−グレリン産生に対するGO−CoA−Tat投与の効果
次に、正常マウスにおいてGO−CoA−Tatがアシル−グレリン産生を阻害するかどうかを調べた。化合物を投与する6時間前に絶食したマウスにおいて、2種類の腹腔内(IP)GO−CoA−Tat用量、15mg/kgおよび29mg/kgを試験した。分布容積が動物の体重と等しいと仮定すると、これらの用量はそれぞれ、約4μMおよび8μMの最大濃度を実現すると予測される。培養細胞で観察されたように、GO−CoA−Tatによる処理は血清アシル−グレリンの用量依存的阻害を引き起こし(図2)、29mg/kg用量で24時間後に最大の70%阻害が得られたが、D4-Tat対照では阻害は引き起こされなかった(図2)。また、デスアシルグレリンの血清レベルにあまり影響はなかったが、少し増加傾向があった。これらの結果は、GO−CoA−Tatがインビボにおいて選択的にアシル−グレリン産生を標的としていることを示している。
マウスにおける体重増加に対するGO−CoA−Tat投与の効果
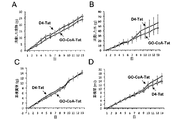
次に、正常マウスに12日間にわたって高脂肪食を与えることによって、体重増加に対するGO−CoA−Tatの効果を調べた。24時間毎にGO−CoA−Tat(29mg/kg IP)でこれらのマウスを処理し、代謝ケージに入れて、毎日摂取および排出ならびに体重のモニターを可能にした。さらに、動物の脂肪量および除脂肪量を評価するために、マウスに3日毎に定量的核磁気共鳴(QMR)分光法を実施した(15)。これらの実験によって、GO−CoA−Tatで処理したマウスは、D4-Tatで処理したマウスと比較して統計学的に有意な体重減少を表すことが示された(図3A)。さらに、QMR測定によって、対象と比較して、GO−CoA−Tat処理動物では脂肪量の約5%の相対的減少を表し、6日後も維持されたが、除脂肪量の減少は表れないことが示された(図3B〜D)。食事または水の摂取および糞尿排出には統計学的有意差はなかったが(図8)、中程度の試料数ではこれらの値には比較的大きな変動があり、そのため摂取減少の関与を除外することはできなった。以前の遺伝子研究では、グレリンの欠如は、食欲ならびに代謝率に影響を及ぼすことによって体重に影響を与え得ることが示唆されている(2〜8)。
グルコース曝露に対するインスリン応答へのGO−CoA−Tatの効果
グルコース曝露に対するインスリン応答へのGO−CoA−Tatの効果を調べるために、ヒト膵島細胞をGO−CoA−Tatで24時間まで予め処理して、これらの細胞が、24時間GO−CoA−Tatに曝露したとき、グルコース曝露に対するインスリン応答の統計学的有意な増加を示すことを示した(図10)。これらの結果は、アシル化グレリンはインスリン応答鈍化に直接的役割を担うことを示唆している。このことをインビボで調べるために、GO−CoA−Tatで予め処理した後、経口的にグルコース曝露したマウスを研究した。膵島細胞研究と矛盾することなく、経口的グルコース曝露(1mg/kg)の前に24時間GO−CoA−Tat 15mg/kgを与えられた動物は、インスリン応答の統計学的有意な増加を示した(図10)。これらの結果は、2.5g/kgの腹腔内グルコース曝露と共にGO−CoA−Tat 29mg/kgを投与されたマウスにおいてさらによりはっきりしていた(図4A)。このインスリン応答の増加には、グルコースの統計学的有意な減少が伴い、機能的に重要な効果が示唆された(図4B)。
化学合成(化合物1〜7、D4-Tat、グレリン−27−ビオチン)
化学合成用の試薬は全て、AldrichまたはAcros Organicsから購入した。市販の試薬は全て、購入時のままさらに精製することなく使用した。2基質類似体阻害剤、ペプチドおよび対照化合物の調製用HPLC単離は、逆相C−18カラム(25×2.14cm、Microsorbtm-100, Rainin)を使用して実施し、水(トリフルオロ酢酸(TFA)0.05%、移動相A)およびアセトニトリル(TFA0.05%、移動相B)の勾配で溶出した。グレリン−27−ビオチン(GSSFLSPEHQRVQQRKESKKPPAKLQPK(ビオチン)G)およびD4−Tatは、Fmoc法を使用して調製した。GO−CoA−Tatおよび関連誘導体の合成は、以前に記載された方法(33、34)と類似しており、グレリンから開始して、Fmoc法を使用した。様々な長さのグレリンペプチド(3から15個のC末端配列)を使用し、グレリンのSer3をAlloc(アリルオキシカルボニル)保護1,2−ジアミノプロピオン酸で置換した。遊離アミノ基を得るために、CHCl3:AcOH:N−メチルモルホリン(37:2:1)中においてテトラキス(トリフェニルホスフィン)パラジウム(0)を使用したAllocの直交脱保護を実施し、次いでラセミ化α−ブロモオクタン酸無水物(化合物5ではオクタン酸無水物および化合物6ではブロモ酢酸無水物)と反応させた(図1C参照)。補酵素Aとの結合は、α−ブロモ−アミドをCoASHと反応させることによって実施した。ブロモ−アミドペプチドの撹拌溶液(濃度2〜10mMのddH2O溶液)に室温で重炭酸トリエチルアンモニウムの水性緩衝液(pH8.0)1.0Mに溶かしたCoASHの溶液(2.0〜3.0当量)を滴下した。48〜72時間後、混合物を一晩凍結乾燥し、所望の生成物を単離するために残渣を調製用HPLCに添加した。HPLCカラムは水(TFA0.05%、移動相A)およびアセトニトリル(TFA0.05%、移動相B)(0分、5%B;5〜65分、60%Bまで直線的に増加;10mL/分)の勾配で溶出し、214nmでモニターした。収集した画分を減圧下で濃縮し、凍結乾燥して最終生成物を白色固形物として得た。マトリックス支援レーザー脱離イオン化(MALDI)およびエレクトロスプレー(ES)質量分析データは、計算値と矛盾せず、アッセイ用の水性溶液中の化合物最終濃度はアミノ酸分析によって測定した。
細胞培養、細胞溶解調製物およびEIA測定
HEL細胞およびAGS細胞(ATCC, Manassas VA)は、不活性化牛胎児血清10%、ストレプトマイシン−ペニシリン100IU/mlおよびグルタミン4mMを補給したRPMI1640培地(Sigma)で増殖させ、週に2回常法通り継代した。KatoIII細胞(ATCC, Manaasas VA)は、不活性化牛胎児血清10%、ストレプトマイシン−ペニシリン100IU/mlおよびグルタミン4mMを補給したDMEM培地(Sigma)で増殖させ、週に2回常法通り継代した。いくつかの実施形態では、アシル−グレリン産生の阻害を評価するために、HEL細胞は7種類の化合物の1種で処理した。3種類の細胞種全ての細胞溶解物を以下のようにRIPA緩衝液中で調製した。細胞(7.5×106細胞)は、卓上型遠心機で1000rpmで5分間遠心分離した。次に細胞ペレットを洗浄し、これに含有する氷冷した改変RIPA緩衝液0.25mlを添加し、激しくピペット操作し、ボルテックスして、その後完全に細胞が溶解するまで4℃で10分間静置させた。次に、溶解物を予め冷却した遠心機で2000rpmで15分間遠心した。遠心直後、上清を−80℃で保存した。細胞溶解物および血清中のアシル−およびデスアシル−グレリンのレベルならびに培養培地および血清試料中のインスリンレベルを評価するために、2抗体サンドイッチをベースにした市販の酵素免疫アッセイ法(Alpco Diagnostics)で分析した。
分子クローニング
GOATは、マウス胃から2段階ネステッドRT−PCR法によってクローニングした。全RNAは、組織ホモジェナイザーおよびRNeasy(登録商標)キット(Qiagen)を使用して、マウス胃の約半分から抽出した。cDNAは、Invitrogen SuperScript(商標)II RTで逆転写することによって調製した。cDNAの2μlをプライマー、TTTACAAGGGCACCGCTTAG/CAAGGCATCTTCTGGCATTTで増幅した。次いで、反応混合物1μlをネステッドプライマーGCCACCATGGATTGGCTCCAGCTC/GAGATGAAGGGCAGGGAAAでさらに増幅した。約1.3kBのバンドをゲルから切り出し、pCR(登録商標)2.1−TOPO(登録商標)(Invitrogen)に連結した。
GOATトランスフェクションおよびミクロソーム単離
GnTI欠損HEK293T細胞(Reeves et al., Proc Natl Acad Sci U S A. 2002 Oct 15 ;99(21): 13419-24)は、L−グルタミン2mMおよびFBS1%を補給したFreestyle293T培地(Invitrogen)中でCO28%を含有する雰囲気中で増殖させた。トランスフェクションの日に、細胞400mlを2×106/mlの濃度に設定した。細胞に、Aricescuらによって記載されたように(Acta Cryst. (2006). D62, 1243-1250)、ポリエチレンイミン「Max」強力直鎖状PEI(Polysciences)を使用してプラスミドをトランスフェクトした。簡単に説明すると、最終培養量の20分の1と等しい未補給ハイブリドーマSFM培地(Invitrogen)中で、DNA1μg/mlをトランスフェクション試薬3μg/mlと混合し、室温で20分間インキュベートし、細胞に添加した。4日後、細胞を実験毎に収集し、PBSで1回洗浄した。
GOATアシルトランスフェラーゼアッセイ
アッセイ方法は、Yangら(36)を改変した。アッセイ混合物は、HEPES 50mM、pH7.0、オクタノイル−CoA(33dpm/fMol、American Radiolabeled Chemicals)1μM、グレリン27−ビオチン 10μM、ミクロソームタンパク質50μgおよびパルミトイル−CoA(Avanti Polar Lipids)50μMを含有した。反応は、膜タンパク質を添加することによって開始し、37℃で5分間インキュベートした。指示がある場合、GO−CoA−Tatは膜タンパク質と共に5分間予めインキュベートした。ストレプトアビジンプラスウルトラリンク樹脂(Pierce)150μlを予め混合した反応停止緩衝液(TBS+SDS 2%(w/v))850μlを添加し、回転ミキサーで15分間インキュベートすることによって反応を停止した。この混合物をPoly−Prep(登録商標)クロマトグラフィーカラム(Bio-Rad)に移し、洗浄緩衝液(TBS+SDS 0.1%)30mlで洗浄した。混合物は反応停止緩衝液1mlを含有する1.5ml微量遠心管に移し、98℃で5分間煮沸し、シンチレーション測定を行った。
細胞生存率アッセイ
様々な濃度のGO−CoA−Tatで処置したHEL細胞系およびヒト不死化肝細胞系HepG2(ATCC, Manassas, VA)の生存率は、LIVE/DEAD生存率アッセイキット(Molecular Probes)を使用して測定した。ラット骨髄間質細胞(RBMSC)は、2種類のプローブ、細胞内エステラーゼ活性についてはカルセイン−AM(緑色)2μMで30分間、細胞膜強度についてはエチジウムホモダイマー−1(EtdD-1、淡赤色)4μMで10分間インキュベートした。カルセイン−AMは、500nmレーザー光線を使用して励起し、放出した蛍光は535nmロングパスフィルターによって検出した。EtdD−1は、514nmレーザー光線を使用して励起し、放出した蛍光は550nmロングパスフィルターによって検出した。赤色蛍光(EtdD-1)を放つ細胞は死細胞として計数し、緑色蛍光(カルセイン-AM)は生細胞として計数した。部分的に赤および緑で2重に染色している場合は、死細胞として計数した。
ヒト膵島の実験
新鮮なヒト死体膵島は、National Islet Cell Resource centerから提供された。平均純度は70%、生存率は85%であった。ヒト膵島実験用に、膵島をGO−CoA−Tat 5μMを含む無血清RPMI培地で24時間インキュベートし、その後グルコース50、150および300mg/dlを添加した無グルコースRPMI培地中で30分間静的インキュベーションアッセイを行い、培地中に分泌されたインスリンをELISA(Alpco Diagnostics)で評価した。
アセチルトランスフェラーゼアッセイ
GO−CoA−Tatのアセチルトランスフェラーゼp300、PCAFおよびAANATとの特異性は、α−ケトグルタル酸脱水素酵素(α-KGDH)関連分光測定法(37)を使用して測定した。組換えアセチルトランスフェラーゼドメインおよびヒストン尾部ペプチドは、以前に記載されたように調製した(38〜40)。アセチルトランスフェラーゼによるCoASHの産生は、NADHの形成と共役しており、Beckman DU−640分光光度計によって340nm(ε340=6230M−1cm−1)でモニターした。反応物は全て、チアミンピロリン酸200μM、MgCl2 5mM、DTT 1mM、BSA 50μg/mL、NAD 200μM、α−ケトグルタル酸2.4mM、GO−CoA−Tat 10μMおよびアセチル−CoA 50μMを含有する。p300との反応は、HEPES 100mM、pH7.9(α−KGDH 0.1単位およびH4〜15 200μM、ヒストンH4尾部の配列に基づく15マーペプチド基質を含有する)中で実施した。p300反応は、30℃でインキュベートした後、p300 100nMを添加して開始して30℃で行う。PCAFとの反応は、HEPES 100mM、pH7.9(α−KGDH 0.037単位およびH3〜20 100μM、ヒストンH3尾部の配列に基づく20マーペプチド基質を含有する)中で実施する。PCAF反応は、30℃で10分間インキュベートした後、PCAF 100nMを添加して開始して30℃で行う。AANATとの反応は、NH4OAc 100mM、pH6.8(α−KGDH 0.1単位およびトリプタミン200μMを含有する)中で実施する。AANAT反応は、25℃で10分間インキュベートした後、AANAT 10.83nMを添加して開始して25℃で行う。反応は全て反応進行曲線の直線部分にあり、直線回帰によって初速度が得られる。
マウスにおける実験
24時間の実験では全て、C57BL/6マウスはGO−CoA−TatまたはD4−TatをIP注射する前に6時間絶食させた。各時点で、経心的穿刺によって血液を採取した。血液試料は、EDTAおよびp−ヒドロキシメルクリ安息香酸(PHMB)1mMを含有する試験管に収集した。試料を+4℃で3500rpmで5分間遠心分離して、次に上清を別の試験管に移した。次いですぐに細胞溶解物1mL当たり1N HCl 100μlを添加し、試験管を+4℃で3500rpmで5分間遠心分離した。上清をクライオバイアルに移し、−80℃で保存した。デスアシル−およびアシル−グレリンの血清レベルは、ELISA(Alpco Diagnostics)によって測定した。糖尿病の成果については、経口的グルコース曝露(1g/kg)を血液試料採取の30分前に行うこと以外は前記の方法にしたがった。糖尿病の成果のために、化合物を絶食していないマウスに18時間の絶食の6時間前に投与し、その時点で2.5g/kg腹腔内グルコース負荷試験(IP-GTT)を意識のあるマウスに実施した。血液は、IP−GTT後0、15、30、60および120分に尾静脈から採取した。グルコースは、グルコメータ(LifeScan OneTouch)で測定し、インスリン値はELISA(Alpco Diagnostics)によって評価した。毎日のGO−CoA−TatのIP投与の体組成に対する効果を評価するために、同腹仔の8週齢C57BL6Jマウス(Jackson Laboratories, Bar Harbor, ME)の体重を2群23.2±1.2g(n=3)および22.6±2.2(n=3)に一致させ、処置前に7日間高脂肪食を与えた。8日目に、マウスには高脂肪食を継続させたが、GO−CoA−Tat 29mg/kg用量(n=3)または等モル用量のD4−Tatペプチド(n=3)の投与を開始した。マウスは、食物および水の摂取ならびに糞尿の生成を毎日測定する直接熱量計測ケージ(Nalgene)中で2週間モニターした。さらに、マウスの身体プロファイルを3日毎にQNMR(EchoMRI)で評価した。身体測定それぞれについて、3つの別個の測定の平均を得た。糞便分析では、糞便を3日間収集し、1.5mL超遠心管に保存した。糞便は再水和して、GO−CoA−Tat(n=4)およびD4−Tat(n=4)の全糞便を4つの別個の測定と比較した。
QRT−PCR
膵島は膵臓をコラゲナーゼおよびDNアーゼIで消化した後、Songら(41)で記載されたように単離した。全RNAは、トリゾールを使用して抽出した。RT−PCRは、one−tube RT−PCR Sybr greenミックス(BioRad)を使用して標準的方法にしたがって実施した。発現レベルの倍数変化は、DDCT法を使用して算出した。2連の結果をステューデントt検定を使用して分析した。RT−PCRで使用したプライマー:インスリンFw:CGAGGCTTCTTCTACACACC;インスリンRv:GAGGGAGCAGATGCTGGT;グルカゴンFw:CCACTCACAGGGCACATTCA;グルカゴンRv:GTCCCTGGTGGCAAGATTGT GHSR FW:ACCTGCTCTGCAAACTCTTCCAGT;GHSR RV:CAAACACCACCACAGCAAGCATCT グレリンFw:ACTCAGCATGCTCTGGATGGACA;グレリンRv:ATGCCAACATCGAAGGGAGCATTG UCP2−001 Fw:TGGTTGGTTTCAAGGCCACAGATG;UCP2−001 Rv:TCTCGTGCAATGGTCTTGTAGGCT 36B4 Fw:TGTTTGACAACGGCAGCATTT;36B4 Rv:CCGAGGCAACAGTTGGGTA
免疫組織化学
マウスの膵臓およびヒト膵島を10%緩衝ホルマリンまたはブアン固定液で固定し、パラフィンに包埋し、5μmの切片を作製した。脱脂し、再水和してクエン酸緩衝液中で抗原を回復した後、免疫染色をモルモット抗インスリン(Abcam)、ウサギ抗グレリン(Abcam)およびニワトリ抗GHSR(Chemicon)で実施した。適切な蛍光タグ第2抗体(ロバ抗モルモットCy3、ロバ抗ウサギFITC、Jackson Immunoresearch)を抗原分布のために使用した。核は、封入媒体に含めたDAPI(Vector Biolabs)を使用して対比染色した。画像作製のために擬似カラー化用CCDデジタルカメラを装着したZeiss Axioskopおよびデジタル画像処理装置を連結したApotome光学切片装置(optical sectioning device)を使用した。
MCT食でのグレリン欠損(グレリンKO)および野生型(WT)マウスの長期調査
グレリン欠損マウスは、前述されたように、ハイスループットVelociGene遺伝子標的化システムを使用して作製した(42)。全動物は、22℃で12:12時間の明暗サイクルで維持し、中鎖トリグリセリドの豊富な食餌(MCT)−(MCT10%、スクロース40%、Teklad TD 08622)を与え、食餌および水は自由に摂取させた。GO−CoA−Tat 40mg/kgはWTおよびKOマウスに投与し、ビヒクルはWTマウスに投与した。全体の体組成(脂肪および除脂肪)は3〜4日毎にNMR技術(EchoMRI, Houston, TX)を使用して測定し、体重測定は毎日行った。結果を図11に示す。
グレリンKOおよびWTマウスにおけるグルコース負荷試験
糖尿病の成果のために、GO−CoA−Tat 40mg/kg(図12の「inhib」)を絶食していないwtマウス(n=5)およびグレリン−koマウス(n=5)に投与し、ビヒクル(2回蒸留水、図12の「Vhc」)を月齢を一致させたwtマウス(n=5)およびグレリン−koマウス(n=5)に投与し、6時間経ってから18時間絶食させた。18時間絶食した後、2.5g/kg腹腔内グルコース負荷試験(IP-GTT)を意識のあるマウスに実施した。血液は、IP−GTT後0、15、30、60および120分に尾静脈から採取した。グルコースはグルコメータ(Lifescan OneTouch)で測定した。
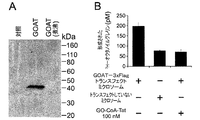
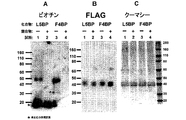
光活性化可能な(photoactivatable)GO−CoA−Tat類似体および可溶性GOATの架橋結合
FLAG−GOAT酵素を、SF9細胞で過剰産生し、界面活性剤で可溶化し、GO−CoA−Tatのベンゾイル−フェニルアラニン含有類似体およびビオチン含有類似体(5μM)の存在下でUV光で処理した。これらはビオチンブロットで示したように架橋結合を誘導し(図13A)、標準GO−CoA−Tat(100uM)で阻害することができた。FLAG(図13B)およびクーマシー(図13C)ゲルでは、これらのレーンへの負荷が等しいことを示している。
GOAT阻害剤はIGF−1に対して影響を及ぼす
血液は、EDTAコーティングMicrovette管を使用して経心的穿刺によって収集し、すぐに氷で冷却した。4℃で3000gで15分間遠心した後、血漿を−80℃で保存した。血漿IGF−1レベルを定量するために、市販のアッセイを使用した(R&D Systems, Minneapolis, MN)。このアッセイは、酸性化していない血漿試料におけるIGF−1の測定に有効で、タンパク質抽出を必要としない。このアッセイはアッセイ製造元の指示に従って実施した。結果を図14に示す。
Claims (26)
- Rが1〜12個のアミノ酸残基のペプチドである、請求項1に記載の化合物。
- Rがグレリン残基4から10までに対応する7個のアミノ酸残基のペプチドである、請求項1に記載の化合物。
- Rがグレリン残基4から15までに対応する12個のアミノ酸残基のペプチドである、請求項1に記載の化合物。
- Rがグレリン残基4から5までに対応する2個のアミノ酸残基のペプチドである、請求項1に記載の化合物。
- Rがグレリン残基4から28までに対応する25個のアミノ酸残基のペプチドである、請求項1に記載の化合物。
- 請求項1〜6のいずれか1項に記載の化合物および薬学的に許容される賦形剤または担体を含む組成物。
- 請求項1〜6のいずれか1項に記載の化合物を調製する方法であって、
3〜5個のN末端アミノ酸残基を含むグレリンペプチド配列を提供する工程であって、3位のセリン残基がアロック保護1,2−ジアミノプロピオン酸に置換されており、D4−Tatがペプチド配列の一末端に結合している、工程と、
ブロモオクタノイル化中間体を得るために、1または複数個の反応容器中で、グレリンペプチド配列を、Pd(PPh3)4パラジウム試薬、n−ブロモオクタン酸無水物および試薬Kと一緒にする工程と、
前記ブロモオクタノイル化中間体を補酵素Aと一緒にする工程と
を含む方法。 - 請求項1〜6のいずれか1項に記載の化合物の治療有効量を含む組成物を対象に投与することを含む、肥満の治療方法。
- 前記組成物の投与が、対象において除脂肪量よりも大きい脂肪量減少をもたらす、請求項9に記載の方法。
- 前記組成物の投与が、対象においてアシル−グレリンに対するグレリンの比の増加をもたらす、請求項9に記載の方法。
- 前記治療有効量が少なくとも約5mg/kg対象の体重である、請求項9に記載の方法。
- 前記治療有効量が少なくとも約15mg/kg対象の体重である、請求項9に記載の方法。
- 前記治療有効量が少なくとも約25mg/kg対象の体重である、請求項9に記載の方法。
- 請求項1に記載の化合物の治療有効量を含む組成物を対象に投与することを含む、II型糖尿病の治療方法。
- 前記組成物の投与が、対象においてインスリン産生増加をもたらす、請求項15に記載の方法。
- 前記組成物の投与が、対象においてグルコース曝露に対する応答性増加をもたらす、請求項15に記載の方法。
- 前記組成物の投与が対象において脱共役タンパク質2(UCP−2)mRNAレベルの減少をもたらす、請求項15に記載の方法。
- 前記治療有効量が少なくとも約5mg/kg対象の体重である、請求項15に記載の方法。
- 前記治療有効量が少なくとも約15mg/kg対象の体重である、請求項15に記載の方法。
- 前記治療有効量が少なくとも約25mg/kg対象の体重である、請求項15に記載の方法。
- 請求項1に記載の化合物の治療有効量を含む組成物を対象に投与することを含む、mBOAT関連疾患の治療方法。
- 請求項1に記載の化合物の治療有効量を含む組成物を対象に投与することを含む、過敏性腸症候群の治療方法。
- 請求項1に記載の化合物の治療有効量の少なくとも1用量を含む組成物を含むキット。
- さらなる体重減少治療薬の少なくとも1用量をさらに含む、請求項24に記載のキット。
- 前記対象がヒトである、請求項9〜23のいずれか1項に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10254908P | 2008-10-03 | 2008-10-03 | |
| US61/102,549 | 2008-10-03 | ||
| PCT/US2009/057512 WO2010039461A2 (en) | 2008-10-03 | 2009-09-18 | Methods for synthesis and uses of inhibitors of ghrelin o-acyltransferase as potential therapeutic agents for obesity and diabetes |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012504619A true JP2012504619A (ja) | 2012-02-23 |
| JP2012504619A5 JP2012504619A5 (ja) | 2012-11-15 |
Family
ID=42074096
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011530103A Withdrawn JP2012504619A (ja) | 2008-10-03 | 2009-09-18 | 肥満および糖尿病の有望な治療薬としてのグレリンo−アシルトランスフェラーゼ阻害剤の合成方法および使用方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US8772229B2 (ja) |
| EP (1) | EP2340258A4 (ja) |
| JP (1) | JP2012504619A (ja) |
| AU (1) | AU2009298892A1 (ja) |
| CA (1) | CA2739418A1 (ja) |
| WO (1) | WO2010039461A2 (ja) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9724381B2 (en) | 2009-05-12 | 2017-08-08 | The Administrators Of The Tulane Educational Fund | Methods of inhibiting the ghrelin/growth hormone secretatogue receptor pathway and uses thereof |
| CA2761901C (en) * | 2009-05-12 | 2019-08-13 | The Administrators Of The Tulane Educational Fund | Methods of inhibiting the ghrelin/growth hormone secretatogue receptor pathway and uses thereof |
| JP2013509434A (ja) | 2009-10-30 | 2013-03-14 | トランザイム・ファーマ,インコーポレイテッド | 大環状グレリン受容体アンタゴニストおよびインバースアゴニストならびにその使用方法 |
| US9315546B2 (en) | 2010-06-16 | 2016-04-19 | The Administrators Of The Tulane Educational Fund | Growth hormone secretatogue receptor antagonists and uses thereof |
| WO2013119800A1 (en) | 2012-02-07 | 2013-08-15 | Massachusetts Institute Of Technology | Use of antagonists of ghrelin or ghrelin receptor to prevent or treat stress-sensitive psychiatric illness |
| US9724396B2 (en) | 2013-03-15 | 2017-08-08 | Massachusetts Institute Of Technology | Use of antagonists of growth hormone or growth hormone receptor to prevent or treat stress-sensitive psychiatric illness |
| WO2015010210A1 (en) * | 2013-07-24 | 2015-01-29 | Bucio Alfonso Abizaid | Compounds for regulating acylated ghrelin |
| WO2016138099A1 (en) | 2015-02-24 | 2016-09-01 | Massachusetts Institute Of Technology | Use of ghrelin or functional ghrelin receptor agonists to prevent and treat stress-sensitive psychiatric illness |
| AU2017273857B2 (en) | 2016-06-01 | 2021-08-19 | Athira Pharma, Inc. | Compounds |
| CN108610337A (zh) * | 2018-05-30 | 2018-10-02 | 王丽萍 | 一种苯并[b]噻吩类化合物及其在肥胖和糖尿病中的应用 |
| KR102333926B1 (ko) * | 2020-03-11 | 2021-12-02 | 연세대학교 산학협력단 | Tat 펩타이드 변이체를 유효성분으로 포함하는 대사질환의 예방 또는 치료용 조성물 |
| CN112014340A (zh) * | 2020-09-01 | 2020-12-01 | 广西玮美生物科技有限公司 | 非人灵长类动物胃饥饿素的检测方法 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2420305C2 (ru) * | 2005-09-29 | 2011-06-10 | Ипсен Фарма С.А.С. | Композиции и способы стимуляции двигательной функции желудочно-кишечного тракта |
| US8013015B2 (en) * | 2008-10-02 | 2011-09-06 | Board Of Regents, The University Of Texas System | Small molecule inhibitors of ghrelin O-acyltransferase |
-
2009
- 2009-09-18 AU AU2009298892A patent/AU2009298892A1/en not_active Abandoned
- 2009-09-18 WO PCT/US2009/057512 patent/WO2010039461A2/en active Application Filing
- 2009-09-18 CA CA2739418A patent/CA2739418A1/en not_active Abandoned
- 2009-09-18 US US13/122,438 patent/US8772229B2/en not_active Expired - Fee Related
- 2009-09-18 JP JP2011530103A patent/JP2012504619A/ja not_active Withdrawn
- 2009-09-18 EP EP09818229A patent/EP2340258A4/en not_active Withdrawn
Also Published As
| Publication number | Publication date |
|---|---|
| US8772229B2 (en) | 2014-07-08 |
| AU2009298892A1 (en) | 2010-04-08 |
| US20110257086A1 (en) | 2011-10-20 |
| WO2010039461A3 (en) | 2010-07-01 |
| EP2340258A2 (en) | 2011-07-06 |
| EP2340258A4 (en) | 2013-02-20 |
| WO2010039461A2 (en) | 2010-04-08 |
| CA2739418A1 (en) | 2010-04-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2012504619A (ja) | 肥満および糖尿病の有望な治療薬としてのグレリンo−アシルトランスフェラーゼ阻害剤の合成方法および使用方法 | |
| KR102578890B1 (ko) | 세포 투과성 펩티드, 그를 포함한 컨쥬게이트 및 그를 포함한 조성물 | |
| JP5000663B2 (ja) | 神経ペプチド2受容体アゴニスト | |
| JP7209364B2 (ja) | 内在化ペプチド連結薬剤と抗炎症剤との共投与 | |
| JP5547719B2 (ja) | Jnkシグナル伝達経路の細胞透過性のペプチド性阻害剤の、慢性または非慢性の炎症性消化器疾患の治療のための、使用 | |
| JP2020172509A (ja) | 胆汁酸に関係した障害の治療方法 | |
| KR20170108936A (ko) | 신규한 α4β7 펩타이드 단량체 및 이량체 길항제 | |
| US20100016242A1 (en) | Myosin light chain kinase inhibitors and methods of use | |
| US11046739B2 (en) | BH4 stabilized peptides and uses thereof | |
| AU2022231763A1 (en) | Protein tyrosine-tyrosine analogs and methods of using the same | |
| PT2197900E (pt) | Péptidos receptores duplamente cíclicos mutados que inibem anticorpos anti-receptor adrenérgico β1 | |
| WO2020112565A1 (en) | Antagonists of mitofusion 1 and beta ii pkc association for treating heart failure | |
| AU2012272550A1 (en) | Prevention and treatment of acute inflammatory conditions | |
| WO2023028486A1 (en) | Leukocyte-specific cell penetrating molecules | |
| JP5844971B2 (ja) | コンジュゲートされた物質を組織に送達するためのアプロチニン様ポリペプチド | |
| CN101305099A (zh) | 具有提高的生物利用度的t3和t4的前药 | |
| US20220288156A1 (en) | Treatment | |
| US7879572B2 (en) | Regulation of F1-ATPase beta subunit cellular location | |
| JPWO2007105442A1 (ja) | 摂食障害または摂水障害の治療薬 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120907 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120912 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120912 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20131204 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20131204 |