JP2012242366A - バイオセンサとこれを用いた分析方法 - Google Patents
バイオセンサとこれを用いた分析方法 Download PDFInfo
- Publication number
- JP2012242366A JP2012242366A JP2011116211A JP2011116211A JP2012242366A JP 2012242366 A JP2012242366 A JP 2012242366A JP 2011116211 A JP2011116211 A JP 2011116211A JP 2011116211 A JP2011116211 A JP 2011116211A JP 2012242366 A JP2012242366 A JP 2012242366A
- Authority
- JP
- Japan
- Prior art keywords
- reaction
- working electrode
- biosensor
- electrode
- target substance
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54366—Apparatus specially adapted for solid-phase testing
- G01N33/54373—Apparatus specially adapted for solid-phase testing involving physiochemical end-point determination, e.g. wave-guides, FETS, gratings
- G01N33/5438—Electrodes
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/28—Electrolytic cell components
- G01N27/30—Electrodes, e.g. test electrodes; Half-cells
- G01N27/327—Biochemical electrodes, e.g. electrical or mechanical details for in vitro measurements
- G01N27/3271—Amperometric enzyme electrodes for analytes in body fluids, e.g. glucose in blood
- G01N27/3272—Test elements therefor, i.e. disposable laminated substrates with electrodes, reagent and channels
Abstract
【課題】短時間で正確な検出が可能なバイオセンサを提供することである。
【解決手段】ターゲット物質と反応し生成物を生成する反応物質、または、ターゲット物質と結合する結合物質が固定されている作用極と、対極と、該ターゲット物質を含む試料液を溜める反応部と、を備えており、該作用極および該対極は、該反応部の底面に配置されており、該反応部の底面において該作用極が占める割合が0.7以上であることを特徴とするバイオセンサである。
【選択図】図1
【解決手段】ターゲット物質と反応し生成物を生成する反応物質、または、ターゲット物質と結合する結合物質が固定されている作用極と、対極と、該ターゲット物質を含む試料液を溜める反応部と、を備えており、該作用極および該対極は、該反応部の底面に配置されており、該反応部の底面において該作用極が占める割合が0.7以上であることを特徴とするバイオセンサである。
【選択図】図1
Description
本発明は、生体、環境、医療、食品などの分析に用いるのに好適なバイオセンサとこれを用いた分析方法に関する。
溶液中の電気化学反応を利用した電気化学測定法は、生体、環境、医療、食品などの分析においてよく用いられている。たとえば、生体試料中の物質(糖、中性脂肪など)の測定には、酵素電極を用いた電気化学測定法がある。
また、生体試料中の微量物質(タンパク質、ホルモンなど)の分析には、電気化学検出型の免疫分析法がよく用いられている。これらの分析に用いられる電気化学測定用電極は、基板上に導電性材料である所定の電極(作用極、対極、参照極等)が形成された構成になっており、電極上に反応物質(酵素、抗体、ペプチドなど)が固定されている。電極上や電極近傍において、ELISA反応または酵素基質反応を用いて電気化学的にターゲット物質を検出する。
上記測定法を用いた発明については、下記の特許文献に記載されている。
特許文献1には、絶縁性基板上に形成された作用極(測定極)と対極と、これらの電極系に接触している酵素などとを含む反応層を備えたバイオセンサが記載されている。
特許文献2には、絶縁性基板上に形成された作用極と対極と、これらの電極系の上部または近傍に酵素などを含むポリマー層と、さらにその上部に、中性脂肪分解酵素が担持された濾紙層とを備えたバイオセンサが記載されている。
特許文献3には、絶縁性基板上に、導電性材料をパターニングすることにより、作用極、対極および参照極を形成した平板型の電極が記載されており、この平板型電極内に形成されている作用極上に酵素を固定化した電気化学検出センサーが例示されている。
特許文献4には、絶縁性基板上にある金属電極に抗体が共有結合により固定化されたイムノアッセイ用の電気化学センサーが記載されている。
より正確な検出が可能なバイオセンサを提供することは望ましい。特に、短時間でも正確な検出が可能なバイオセンサを提供することはより望ましい。
本発明は、上記課題に鑑みてなされたものであり、その目的は、短時間で正確な検出が可能なバイオセンサ、およびこれを用いた分析方法を提供することである。
本発明者らは、鋭意検討の結果、シミュレーションにより、電気化学測定時に液の触れる領域の底面積に対し、作用極の面積の比が、分析の精度に影響を及ぼすことを見出し、本発明を完成させた。
シミュレーションにより、電気化学測定時に液の触れる領域の底面積に対し、作用極の面積の比が大きくなるほど、理論から求める初速度と真の初速度との値の差が小さくなることが判明した。また上記作用極の面積の比が、0.7以上になった場合には理論から求める初速度と真の初速度がほぼ等しくなることもシミュレーションの結果から判明した。なお、シミュレーションの詳細については後述する。
本発明に係るバイオセンサは、ターゲット物質と反応し生成物を生成する反応物質、または、ターゲット物質と結合する結合物質が固定されている作用極と、対極と、該ターゲット物質を含む試料液を溜める反応部と、を備えており、該作用極および該対極は、該反応部の底面に配置されており、該反応部の底面において該作用極が占める割合が0.7以上であることを特徴としている。
上記の構成により、生成物を生成する反応の反応初期において、ある時間の生成物量と原点を結ぶ直線の傾きから求めた反応の初速度と真の初速度との差異を、従来技術に係るバイオセンサに比べて小さくすることが出来るので、反応が飽和するのを待つことなく、短時間の反応時間であってもより正確な検出を実現することができる。
これを詳細に説明すれば、まず、従来技術に係るバイオセンサ(特許文献1〜4)は、基板内において試料液および測定液の触れる領域に対して、作用極(測定極)の占める割合は小さい。これは作用極において発生した電流を流すための電極である対極は、通常、電流が流れにくくなるのを防ぐために、作用極と同程度の若しくは作用極以上の面積比率となるように形成されるからである。そのため、従来技術に係るバイオセンサにおいては、液の触れる面積に対して、作用極の占める割合を0.5以下としている。
ここで、通常、作用極上で生成した生成物は、拡散によって作用極上から徐々に移動する。そして、電気化学検出は、作用極近傍の生成物しか検出することができない。それゆえ、従来技術に係るバイオセンサのように、反応部の底面積に対する作用極の面積比が0.5であると、すなわち作用極以外の領域が多いということなので、拡散によって検出範囲外へ移動する生成物量も多くなる。それゆえに、反応初期で反応時間と生成物量(作用極上の生成物量)との間の線形性の程度が小さい。
これに対し、上記のように作用極の面積比を反応部の底面積に対して0.7以上と大きくしたバイオセンサでは、作用極以外の領域が少ないので、検出範囲外へ移動する生成物量も少なくなる。そのため、生成物の拡散が無視できるような状況を擬似的に作り出すことができ、反応初期でも反応時間と生成物量(作用極上の生成物量)との関係がより線形性の程度が大きくなる、つまり、直線に近くなると考えられる。これにより、上記の構成によれば、生成物を生成する反応の反応初期において、ある時間の生成物量と原点を結ぶ直線の傾きから求めた反応の初速度と真の初速度との差異を小さくして、短時間の反応時間であってもより正確な検出を実現することができる。
本発明に係るバイオセンサでは、上記作用極を複数備えていることが好ましい。
上記の構成により、個々の作用極の面積が小さくなるので、微小電極の効果により、電流値が大きくなり、高感度な測定が可能である。
本発明に係るバイオセンサでは、さらに参照極を備えていることが好ましい。
上記の構成により、作用極に所望の安定した電位を印加することができる。
本発明に係るバイオセンサでは、疎水性を有する疎水性部分を備えており、該疎水性部分が上記反応部を囲むように配置されていることが好ましい。
上記の構成により、疎水性部分によって、上記反応部を囲むことによって、上記反応部からの液の広がりを抑えることができる。これにより、例えば、液滴による測定が可能となる。
本発明に係るバイオセンサでは、上記反応部を囲む壁面を備えていることが好ましい。
上記の構成により、検出電極の周囲を囲む壁面によって液の広がりが抑えられる。これにより、微量の試料液を用いた場合も首尾よく測定することができる。
本発明に係るバイオセンサでは、上記反応部を格納する反応チャンバを備えており、該反応チャンバは、該反応チャンバ内に上記試料液を注入するための注入口と、上記反応チャンバ内の上記試料液を排出するための排出口とを備えていることが好ましい。
上記の構成により、反応チャンバにより反応部を格納することができ、試料液の微量化、測定時間の短縮化、分析操作の簡便化が可能となり、短時間で正確かつ効率的な測定を実現することができる。
本発明に係るバイオセンサでは、上記作用極の中心が、上記反応部の底面の中央部にあることが好ましい。
上記の構成により、反応部のうち、電気化学測定に関与する拡散層の濃度勾配が作用極を中心としておおよそ均等となるため、電気化学反応が均一に起こり、より短時間の反応時間での検出が可能となる。なお中央部は、反応部の中心を基準に反応部全体に対して三分の一程度の領域を指す。
本発明に係るバイオセンサでは、上記作用極の底面の形状が、上記反応部の底面の形状と相似形であることが好ましい。
上記の構成により、反応部のうち、電気化学測定に関与する拡散層の濃度勾配が作用極を中心として均等となるため、電気化学反応が均一に起こり、より短時間の反応時間での検出が可能となる。
本発明に係るバイオセンサでは、上記反応物質は、ターゲット物質と特異的に反応するものであることが好ましい。また、上記反応物質が、上記ターゲット物質の反応を触媒する酵素であることがより好ましい。
上記の構成により、酵素に反応する基質をターゲット物質として検出することができる。
本発明に係るバイオセンサでは、上記結合物質は、ターゲット物質と特異的に結合するものであることが好ましい。また、上記結合物質が、上記ターゲット物質に対する抗体、または、上記ターゲット物質に特異的に結合するペプチドがより好ましい。
上記の構成により、ターゲット物質と反応する第二の結合物質をさらに反応させることで、イムノアッセイが可能となる。第二の結合物質とは、ターゲット物質と結合し、基質と反応して、生成物を生成する物質のことである。たとえば、酵素標識抗体などが該当する。
本発明に係る分析方法は、上記バイオセンサを用いた分析方法であって、ターゲット物質を含む試料液を、上記反応部に導入する導入工程、および上記作用極と上記対極との間に電圧を印加することで、反応または結合した上記ターゲット物質に応じた電流を得る工程とを含むことを特徴とする。
上記の構成により、導入工程にて、ターゲット物質を含む試料液を上記反応部へ導入することにより、作用極上に固定した反応物質とターゲット物質とが反応、または作用極上に固定した結合物質とターゲット物質とが結合する。そして、作用極と対極の間に電圧を印加することによって、反応または結合したターゲット物質に応じた電流値を得ることができる。このとき、生成物を生成する反応の反応初期において、反応時間と生成物の生成量の間の線形性の程度が大きい(より直線に近くなる)ので、ある短時間の反応時間における電流値と原点とを結ぶ直線の傾きから求めた初速度が、真の初速度とほぼ等しい値となる。よって、短時間の反応時間でも正確な分析が可能となる。
本発明に係るバイオセンサは、ターゲット物質と反応し生成物を生成する反応物質、または、ターゲット物質と結合する結合物質が固定されている作用極と、対極と、該ターゲット物質を含む試料液が導入される反応部と、を備えており、該ターゲット物質が、該反応物質と反応し、または、該結合物質と結合することにより生成される液が触れる領域である反応部を有し、該反応部の底面積に対する該作用極の面積の比が0.7以上であるため、反応が飽和するのを待つことなく、短時間で正確な検出を実現できるという効果を有する。
本発明の分析方法は、上記バイオセンサを用いた分析方法であって、ターゲット物質を含む試料液を、上記反応部に導入する導入工程と、上記反応物質と上記ターゲット物質との反応によって生成物が生成する工程または上記結合物質が上記ターゲット物質と結合する工程と、作用極に電圧を印加することで、反応または結合したターゲット物質に応じた電流値を得る工程とを含んでいるので、反応が飽和するのを待つことなく、短時間で、正確な分析を行うことができるという効果を有する。
図12は、ELISA法または酵素法によって起こる酵素基質反応における時間に対しての生成物量を表すグラフである。ELISA法または酵素法によって起こる酵素基質反応は、通常、反応初期では時間と反応総量との間に線形性がある。その直線の傾きは、酵素基質反応の初速度であり、反応初期の区間を初期速度区間という。
酵素が基質に対して過剰に存在する場合、初速度は基質濃度に比例する。ターゲット物質が基質の場合(たとえば、グルコースをターゲット物質とするグルコースセンサーなど)、初速度と基質濃度が比例する現象を利用し、初速度を求めることによって、基質濃度、つまりターゲット濃度を求めることができる。
また、基質が酵素に対して過剰に存在する場合、初速度は酵素濃度に比例する。ターゲット物質と結合する物質(例えば抗体など)を用いてターゲット物質を検出する場合(抗体を用いる場合はイムノアッセイ)、初速度と酵素濃度とが比例する現象を利用して、初速度を求めることで、酵素濃度を求めることができる。酵素濃度は、ターゲット物質に結合している酵素標識抗体濃度であり、すなわち、結合しているターゲット物質濃度として求められる。
このように、酵素基質反応の初速度は、測定系の、基質濃度および酵素濃度を求めるのに、非常に重要な因子である。
特に、上記のようなバイオセンサにおいて、免疫反応および酵素基質反応等の検出を電気化学的に行う場合は、検出された電流値(電流値は生成物量に比例する)と時間との関係において、反応初期において線形性を持たせることが必要である。しかし、電気化学的な手法では、生成物の全量ではなく、作用極上の限られた範囲に存在する生成物しか検出することが出来ないため、必ずしも線形性を持たせて反応させることが容易ではない。これは、拡散による物質移動によって、作用極上で生成した生成物が、その範囲外へと移動してしまうので、電気化学的な手法では生成物の総量を測定することができないためである。
ここで、検出電流値は生成物量に比例するため、この後は検出電流値を生成物量として説明する。
生成物量と時間との間に線形性がある場合、その初速度は、ある反応時間における生成物量を、反応時間で割った数値、すなわち、原点との2点を結ぶ直線の傾きとして求めることができる。しかし、上記のような一般的な(従来の)バイオセンサおよび電気検出センサーの場合、生成物量と時間との間の線形性の程度が小さいために、同様にして求めた直線の傾きは、真の初速度とはずれがある。したがって、近似直線から得た初速度を基に算出した生成物量は、真の生成物量との誤差が大きくなってしまう。したがって、正確な検出を行うためには、反応が飽和し、安定するまで反応させてから電気化学測定を行う必要がある。つまり、正確な検出を行うためには、検出に時間を要し、また、短時間で検出を行うと、正確な検出を行うことができない。
図14は、電気化学測定時に液の触れる領域の底面積に対し、作用極の面積の比が0.5のバイオセンサ(従来のもの)において、時間と作用極上の検出可能な範囲における生成物量との関係を示した結果である。また、図13は、電気化学測定時に液の触れる領域の底面積に対し、作用極の面積の比が0.7のバイオセンサ(本発明のもの)において、時間と作用極上の検出可能な範囲における生成物量との関係を示した結果である。図13も図14も反応初期である数10秒程度までの結果を示した。
ここで、線形性の程度を一次近似直線の相関関数Rの二乗値のR2値によって評価する。R2値が1に近づくほど、時間と生成物量との間の線形性の程度が大きくなるということになる。従来型のバイオセンサでは、図13のグラフの0〜10秒における近似直線のR2値は、0.9928であった。一方、本発明のバイオセンサでは、図14のグラフの0〜10秒における近似直線のR2値は、0.9990であった。したがって、面積比0.5の電気化学検出用バイオセンサでは、時間と生成物量との間の線形性の程度が小さく、ある時間における点と原点とを結ぶ直線の傾きから求めた初速度と、真の初速度とにずれがある。一方、面積比率0.7のバイオセンサでは、時間と生成物量との間の線形性の程度が大きく、より直線に近くなる。
さらに、図15は、反応初期(0〜10秒)の一次近似直線の相関係数Rの二乗値R2を、電気化学測定時に液の触れる領域の底面積に対する作用極の面積比ごとにプロットしたグラフである。図15より、作用極の面積比が大きくなるほど、R2値が1に近づいており、作用極の面積比が0.7以上1未満では、R2値が0.999以上、つまりほぼ1となる。逆に、面積比が0.7より小さくなるにつれR2値は急激に小さくなり、面積比0.1ではR2値は0.96まで悪くなる。したがって、作用極の面積比が0.7以上のバイオセンサは、短時間の反応時間で検出を行ったときに、その直線の傾きから求めた速度と、真の初速度との誤差が小さく、ほぼ等しい値となると言える。つまり、作用極の面積比を大きくすることによって短時間の反応時間でも、ターゲット物質の濃度をより正確に検出することが可能となる。
〔第1実施形態〕
図1は、本発明の一実施形態(第1実施形態)に係るバイオセンサ100の概略構成を示す上面図である。図1に示すように、バイオセンサ100は、作用極1、対極2、絶縁膜4、接続パットA1およびA2、リード電極部B1およびB2、反応部5、ならびに、基板20を備えている。
図1は、本発明の一実施形態(第1実施形態)に係るバイオセンサ100の概略構成を示す上面図である。図1に示すように、バイオセンサ100は、作用極1、対極2、絶縁膜4、接続パットA1およびA2、リード電極部B1およびB2、反応部5、ならびに、基板20を備えている。
図1に示すように、バイオセンサ100では、基板20上の一方の端部に接続パットA1およびA2が形成され、反対側に、並列して作用極1および対極2が形成されている構造になっている。作用極1と接続パッドA1とを接続するようにリード電極部B1が形成され、対極2とA2とを接続するようにリード電極部B2が形成されている。さらに、リード電極部B1およびB2が試料液と接触しないように、リード電極部B1およびB2を覆うための絶縁膜4が形成された構造になっている。詳しい構造については下記にて記載する。
作用極1は、試料液中にて生成した電気化学的活性物質である生成物を電気化学反応(酸化または還元)により検出する電極である。作用極1の材料としては、例えば、金属、カーボン、グラファイトなどの導電性材料が用いられる。
対極2は、作用極1にて生じた電流を流すための電極である。対極2の材料としては、作用極1と同様の導電性材料を用いることができる。また、作用極1と異なる導電性材料を用いてもよい。
絶縁膜4は、リード電極部B1およびB2と、試料液が接触しないために形成されている絶縁性を有する膜である。絶縁膜4の材料としては、例えば、ポリイミドなどの絶縁性材料を用いることができる。
接続パットA1およびA2は、電気化学検出用バイオセンサを電気化学測定装置(例えばポテンショスタット等)に接続するときに用いられ、作用極1と対極2と電気化学測定装置とを接続するために設けられている。接続パッドA1およびA2の材料としては、作用極1または対極2と同様の導電性材料を用いることができる。また、作用極1または対極2と異なる導電性材料を用いてもよい。
リード電極部B1およびB2は、作用極1と対極2とを、それぞれ接続パッドA1およびA2とつなぐために形成されている。リード電極部B1およびB2の大きさ(寸法)についても、任意の大きさを設定することができる。リード電極部B1およびB2の材料としては、作用極1および対極2と同様の材料を用いることができる。
基板20は、電子部品等を表面に固定し、何らかの機能を実現するための板状またはフィルム上の部品をいう。例えば、ガラス、石英、セラミックス、プラスチックなどの絶縁性材料が用いられる。
反応部5は、電気化学測定の際に、試料液を溜める(試料液が触れる)領域のことをいい、作用極1および対極2を含む電極系を含むように形成される。反応部5では、作用極1上に固定化された反応物質または結合物質とターゲット物質が直接または段階的に反応して、電気化学活性のある生成物を生成する反応が生じる。バイオセンサ100は、上記電極系(作用極1および対極2)を用いて、反応部5における上記反応を電気化学的に検出する。なお、反応物質および結合物質については後述する。
バイオセンサ100は、例えば、以下のように製造することができる。まず、基板20上にパターニングすることにより、作用極1、対極2、接続パットA1およびA2ならびにリード電極部B1およびB2をそれぞれ形成する。基板20の表面に作用極1を形成する方法としては、例えば、スパッタ法、蒸着法または印刷法等を用いることができる。対極2、接続パットA1およびA2、ならびに、リード電極部B1およびB2を形成させる場合についても、作用極1と同様の方法を用いることができる。また、バイオセンサ100を大量生産する場合には、バイオセンサ100が備える部材を複数パターニングした基板を分割してもよい。
つぎに、絶縁膜4を、リード電極部B1およびB2を完全に覆うようにして形成させる。これは、リード電極部B1およびB2と試料液とが接触してバイオセンサ100が誤動作することを防止することが目的である。これにより、試料液を反応部5にのみに接触させることができる。基板20の表面に、リード電極部B1およびB2を覆うようにして絶縁膜4を形成する方法は、例えば、フォトリソグラフィー、スクリーン印刷などの方法を用いることができる。
絶縁膜4の形成により、試料液が接触する反応部5が規定される。絶縁膜4の大きさは、絶縁膜4によって規定される反応部5の大きさ(底面積)と、作用極1との面積比率が0.7以上となるように、絶縁膜4の大きさを調整して生成する。これにより、反応部5の大きさを、反応部5に対する作用極1の面積比率が0.7以上となるように設定することができる。
なお、本実施形態では、反応部5の外縁は絶縁膜4によって規定されているが、この方法に制限されるものではなく、後述するような様々な方法を用いて形成することができる。
対極2の大きさは、反応部5のうち、作用極が占める領域の残りの部分から、任意の大きさを選択できる。前述のように、対極2は作用極1から生じた電流を流すための電極であるので、対極2が作用極1に対して余りにも小さい場合、電流が流れにくくなり、正確な電気化学測定を行うことができなくなる。したがって、対極2は、作用極1から生じる電流を流すのに必要な大きさを選択することが望ましい。
接続パッドA1およびA2それぞれの位置は、電気化学測定装置との接続位置に応じて適宜設定可能であり、接続可能な位置であれば特に限定されない。また、接続パッドA1およびA2の大きさは、電気化学測定装置側の接続パッドと充分に接触する大きさであればよい。
作用極1上に、ターゲット物質と反応し生成物を生成する反応物質またはターゲット物質と結合する結合物質を固定化させる。
反応物質は、ターゲット物質と直接反応して生成物を生成する。結合物質は、ターゲット物質と反応後、さらなる反応によって生成物を生成する。
反応物質あるいは結合物質は、検出したいターゲット物質によって酵素、抗体、ペプチド、DNA、オリゴヌクレオチド、レクチン、レセプター、糖など任意の生体材料を選択する。例えば、試料液中の糖を検出する場合には、グルコースオキシダーゼなどの酵素が選択される。
試料液中のターゲット物質がイムノアッセイにより検出される場合は、ターゲットの物質を特異的に結合する抗体もしくはペプチドなどが選択される。反応物質あるいは結合物質は、作用極1の全面に固定化されていることが好ましい。
上記固定化に関しては、作用極1の全面に隙間無く行う必要はなく、離散的に固定化されていてもよい。ただし、その固定化された面積は反応部の面積に対して0.7以上であることが好ましい。
反応物質あるいは結合物質を作用極1に固定化する方法としては、例えば、物理吸着、作用極1の表面に形成した官能基と反応物質との共有結合、または3次元網目構造を有する高分子材料によるタンパク質の取り込み(包括)等を利用した、公知の方法を採用することができる。離散的に固定化する場合、スポッターなどを用いてもよい。
なお、本実施形態に係るバイオセンサ100は、基板20上に、作用極1および対極2が集約して形成されているので、検出に必要な試料液の量を少なくすることができるという利点も有している。
なお、作用極1、対極2、絶縁膜4、接続パットA1およびA2、リード電極部B1およびB2、反応部5ならびに基板20の形状は図1に示されたものである必要はなく、特に限定されるものではなく、矩形、円形、楕円形またはその他任意の形状とすることができる。
〔バイオセンサを用いた分析方法〕
この分析方法は、ターゲット物質を含む試料溶液を、上記反応部5に導入する導入工程と、上記反応物質と上記ターゲット物質との反応によって生成された電気化学活性物質を測定する測定工程からなる。
この分析方法は、ターゲット物質を含む試料溶液を、上記反応部5に導入する導入工程と、上記反応物質と上記ターゲット物質との反応によって生成された電気化学活性物質を測定する測定工程からなる。
上記バイオセンサ100の構成により、ターゲット物質を含む試料液を反応部5に導入すれば、作用極1上に固定した反応物質と反応し生成物を生成、または作用極1上に固定した結合物質と結合する。上記反応または結合をさせた後、電気化学測定を行うことにより、検出された電流値から試料液中のターゲット物質の濃度を求めることができる。
まず、電気化学検出用バイオセンサの接続パッドA1、A2およびA3を、電気化学測定装置(例えばポテンショスタット)に接続する。接続パッドA1、A2およびA3の接続方法としては、例えば両端にワニ口クリップが設けられたコードを用意し、一方のクリップにより接続パッドA1、A2およびA3を挟み、他方のクリップによりポテンショスタットの端子を挟む方法が挙げられるが、この方法に制限されるものではない。
以下、バイオセンサ100を用いた分析方法の一例として、試料液中の糖(グルコース)を測定する方法について説明するが、本実施形態はこれに限定されず、その他のターゲット物質の測定にも適用可能である。
試料液中の糖を測定する場合、バイオセンサ100の作用極1には、反応物質として、酵素(グルコースオキシダーゼ)を固定化する。前記反応物質を作用極1に固定化する方法としては、上述のように、物理吸着、作用極1の表面に形成した官能基と反応物質との共有結合、または3次元網目構造を有する高分子材料によるタンパク質の取り込み(包括)等を利用した、公知の方法を採用することができる。また、作用極1における反応物質の固定化箇所は、特に限定されないが、作用極1の全面に固定ることが好ましい。
次に、グルコースを含む試料液を反応部5に導入する。具体的には、バイオセンサ100の反応部5に試料液を滴下する。グルコースと作用極1に固定化された酵素とが反応して、生成物(過酸化水素)が生成する。作用極1と対極2との間にに電圧を印加することにより、グルコース量に応じた電流が得られ、その結果から試料液中のグルコースの濃度を測定することができる。
試料液には、電子移動を仲介するためのメディエーターを加えてもよい。メディエーターとしては、フェロシアン化カリウム/フェリシアン化カリウム、ベンゾキノン/ハイドロキノン、フェリシニウム/フェロセンなどの系を用いることができる。グルコースを測定する系の場合、酵素とグルコースとが反応し、メディエーターを介在した電子の移動にともなって生ずる電流をシグナルとして測定する。そうすることで、検出された電流値から試料液中のターゲット物質の濃度を求めることができる。
次に、バイオセンサ100を用いた分析方法の他の例として、試料液中の微量物質をイムノアッセイにて測定する方法について説明する。
試料液中の微量物質をイムノアッセイにて測定する場合、バイオセンサ100の作用極1には、結合物質としてターゲット物質を特異的に捕捉することのできる抗体またはペプチドを固定する(以下、抗体を固定した場合について説明するが、ペプチドを固定した場合も分析方法は同様である)。固定する方法としては、酵素を固定する場合と同様の方法を採用することができる。また、結合物質は、作用極1の全面に固定することが好ましい。また、試料液を滴下する前に、作用極1の表面をアルブミン水溶液により処理して、非特異吸着防止膜を形成した後、バッファー液を用いて洗浄しておいてもよい。これにより、作用極1の表面へのターゲット物質の非特異的な吸着を防ぐことができる。
ターゲット物質を含む試料液を反応部5に滴下することによって、抗原抗体反応が進行する。続いて、反応部5を、バッファー液を用いて洗浄した後、第二の結合物質である酵素標識抗体を含む液を滴下して反応させる。ここで、作用極1の表面には、抗体−ターゲット物質−酵素標識抗体のサンドイッチ複合体が形成される。続いて、反応部5を、バッファー液を用いて洗浄する。次いで、酵素に対する基質を含む試料液を反応部5に滴下する。作用極1の表面に形成されたサンドイッチ複合体の中において、酵素基質反応が進行し、電気化学活性のある生成物が生成する。作用極1に電圧を印加することによって、ターゲット物質量に応じた電流が得られる。その結果から試料液中のターゲット物質の濃度を求めることができる。
また、基質を含む試料液には、上述と同様に、電子移動を仲介するためのメディエーターを加えてもよい。
〔第2実施形態〕
図2は、本発明の一実施形態(第2実施形態)に係るバイオセンサ200の概略構成を示す上面図である。
図2は、本発明の一実施形態(第2実施形態)に係るバイオセンサ200の概略構成を示す上面図である。
なお、説明の便宜上、前記第1実施形態にて説明した図面と同じ機能を有する部材については、同じ符号を付記し、その説明を省略する。またバイオセンサを用いた分析方法に関しても上述した方法と同様のため、その説明も省略する。
図2に示すように、バイオセンサ200は、作用極1、対極2、参照極3、絶縁膜4、接続パットA1、A2およびA3、リード電極部B1、B2およびB3、反応部5ならびに基板20を備えている。
基板20における一方の端部に、接続パッドA1、A2およびA3が形成されている。また、作用極1、対極2および参照極3が、基板20上の、接続パッドA1、A2およびA3が形成されている側とは反対側に形成されている。また、作用極1と接続パッドA1とを、対極2と接続パッドA2とをおよび参照極3と接続パッドA3とを接続するように、リード電極部B1、B2およびB3がそれぞれ形成されている。さらに、リード電極部B1、B2およびB3が試料液と接触しないように、リード電極部を覆うように絶縁膜4が形成されている。それゆえに試料液は図2に示す反応部5にのみ接触するようになっている。
上記構造を有し、作用極1を反応部5に対して面積比率0.7以上で形成するという条件を満たしていれば、各部材の大きさおよび形状は限定されない。第2実施形態は、参照極3を含むという点が、第1実施形態とは異なる。
参照極3は、作用極1に所望の安定した電位を印加するための電極である。図2に示されるバイオセンサ200では、参照極3は、作用極1の中に埋め込まれるようにして形成されている。参照極3の位置はこの位置に制限されるものではないが、参照極3は、溶液抵抗によりIRドロップが生じることを考慮すると、できる限り作用極1の近傍に配置されていることが望ましい。また参照極3の大きさ(寸法)は、特に限定されないが、作用極1を反応部5に対して面積比率0.7以上で形成するため、参照極3は小さいことが好ましい。
参照極3の材料は、導電性材料であり、かつ、電流が流れた際にも電位が安定している材料が望ましい。例えば、銀塩化銀電極はよく用いられる参照極の一つである。
基板20の表面に参照極3を形成する方法としては、例えば、スパッタ法、蒸着法、印刷法等を用いることができる。
参照極3によって、作用極1に安定した電位を印加することができるので、より正確な検出が可能となるという特徴を有する。
また、作用極1の中心が、反応部5の底面の中央部にあることが望ましい。
上記の構成により、反応部5のうち、電気化学測定に関与する拡散層の濃度勾配が作用極5を中心としておおよそ均等となるため、電気化学反応が均一に起こり、より短時間の反応時間での検出が可能となるからである。なお中央部は、反応部の中心を基準に反応部全体に対して三分の一程度の領域を指すものとし、作用極の中心が反応部の底面の中央部にあればいいので、図2の形状には限定されない。
さらに、作用極1の底面の形状が、反応部5の底面の形状と相似形であることが望ましい。
上記の構成により、反応部5のうち、電気化学測定に関与する拡散層の濃度勾配が作用極を中心として均等となるため、電気化学反応が均一に起こり、より短時間の反応時間での検出が可能となるからである。作用極の底面の形状が、反応部の底面の形状と相似形であればいいので、図2の形状には限定されない。
〔第3実施形態〕
図3は、本発明の一実施形態(第3実施形態)に係るバイオセンサ300の概略構成を示す上面図である。
図3は、本発明の一実施形態(第3実施形態)に係るバイオセンサ300の概略構成を示す上面図である。
図3に示されるバイオセンサ300は、絶縁膜4の代替として、接続パッドA1、A2およびA3ならびに反応部5以外の部分を、疎水性膜(疎水性部分)6を用いて被覆させている点で図2のバイオセンサ200と異なる。したがって、反応部5は、疎水性膜6によって規定される。それ以外の点においては、第2実施形態と同様である。
疎水性膜6は、反応部5を規定し、それ以外の領域に試料液の液滴を広がらせないためのものである。バイオセンサ300では、反応部5以外の部分を覆うように形成されている。
疎水性膜6の材料は、その表面が疎水性を有し、かつ、絶縁性の材料が望ましい。疎水性膜6の形成方法は、例えば、疎水性ポリマーをコートしたり、オクタドデシルトリクロロシランのトルエン溶液によって化学修飾したりするなどの方法を採用することができる。
疎水性膜6によって、反応部5が首尾よく規定されるので、最小限の液量により測定することが可能であるという効果を有する。
〔第4実施形態〕
図4は、本発明の一実施形態(第4実施形態)に係るバイオセンサ400の概略構成を示す上面図である。
図4は、本発明の一実施形態(第4実施形態)に係るバイオセンサ400の概略構成を示す上面図である。
図4に示される電気化学検出用バイオセンサは、作用極1が複数個から成り、それぞれの作用極1において、接続パットA1と接続させるためにリード電極部B1が形成されている以外は、第3実施形態と同様である。
複数の作用極の総面積は、反応部5の底面積の0.7以上を占めるように形成されている。
作用極が複数になることより、個々の作用極の面積が小さくなるが、微小電極の効果により電流値が増幅され、高感度の検出が可能であるという効果を有する。
〔第5実施形態〕
図5は、本発明の一実施形態(第5実施形態)に係るバイオセンサ500の概略構成を示す上面図である。
図5は、本発明の一実施形態(第5実施形態)に係るバイオセンサ500の概略構成を示す上面図である。
図5に示されるバイオセンサ500は、作用極1の大きさが反応部5の大きさよりも大きいこと以外は、第3実施形態と同様である。疎水性膜6によって、反応部5内の作用極の有効面積が規定される。バイオセンサ500では、作用極の有効面積が、反応部5の0.7以上となっている。
図5に示されたバイオセンサ500のように、作用極1の全部分が反応部5からはみ出して形成されていてもよいし、図6に示されたバイオセンサ500´ように、作用極1の一部分が反応部5からはみ出して形成されてもよい。
〔第6実施形態〕
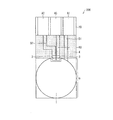
図7は、本発明の一実施形態(第6実施形態)に係るバイオセンサ600の概略構成を示す上面図である。図8は第6実施形態のバイオセンサ600の概略構造を示す斜視図である。図8においては、作用極1等の詳細な構造は省略してある。
図7は、本発明の一実施形態(第6実施形態)に係るバイオセンサ600の概略構成を示す上面図である。図8は第6実施形態のバイオセンサ600の概略構造を示す斜視図である。図8においては、作用極1等の詳細な構造は省略してある。
バイオセンサ600は、反応部5がその周囲を囲む壁面7によって規定されている点および疎水性膜6によって被覆されていない点以外は、第5実施形態と同様である。
壁面7は、反応部6を規定し、それ以外の領域に試料液の液滴を広がらせないためのものである。バイオセンサ600では、壁面7は、平面視において円形の反応部6を取り囲むように円周状に形成されている。しかしながら、この形状に制限されるものではなく、反応部6の形状に応じて任意に形成することができる。また壁面7は、液が広がっていかない高さがあればよい。壁面7の材料は、ガラス、石英、セラミックス、プラスチックなどを用いることができる。ポリジメチルシロキサン(PDMS)を材料として用いることによって、加工および量産が容易となる。
壁面7を形成する方法は、例えば、機械的に加工する方法、エッチングなどの化学処理により形成する方法などが挙げられ、特に限定されない。また各部パターンを形成した型に光硬化性樹脂または熱硬化性樹脂を流し込んで固めて作成する方法もある。またポリオレフィン系樹脂、ポリメタクリル酸系樹脂、またはポリカーボネイト樹脂からなる材料を、各部パターンを形成した型を用いて、ホットエンボス法により形成してもよい。
作成した壁面7を基板20と貼り合わせることによって、反応部6が規定される。
壁面7を導入することにより、反応部5以外に試料液が広がることを確実に抑制することができる。
〔第7実施形態〕
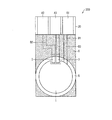
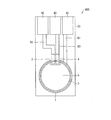
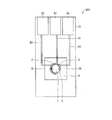
図9は、本発明の一実施形態(第7実施形態)に係るバイオセンサ700の概略構成を示す上面図およびX−Y断面図である。図10は第7実施形態のバイオセンサの概略構造を示す斜視図である。図10においては、作用極1等の詳細構造は省略してある。
図9は、本発明の一実施形態(第7実施形態)に係るバイオセンサ700の概略構成を示す上面図およびX−Y断面図である。図10は第7実施形態のバイオセンサの概略構造を示す斜視図である。図10においては、作用極1等の詳細構造は省略してある。
反応チャンバ8は、反応部5を囲む壁面および天井部分からなっており、反応部5を空間として規定している。さらに反応チャンバ8には、液を入れるための導入部9および液を排出するための排出部10が形成されている。
バイオセンサ700は、基板20上に導入部9および排出部10を有する反応チャンバ8が形成されている点ならびに絶縁膜4が被覆されていない点以外は、実施の形態2と同様である。
反応チャンバ8は、円柱状の空間として形成されているが、この形状に制限されるものではなく、反応部6の形状に応じて任意に形成することが可能である。反応チャンバ8の材料は、ガラス、石英、セラミックス、プラスチックなどを用いることができる。ポリジメチルシロキサン(PDMS)を材料として用いることよって、加工および量産が容易となる。
反応チャンバ8を形成する方法は、上記壁面7を形成する方法と同様のものを用いてもよく、特に限定されない。
反応チャンバ8により、空間として反応部5を規定することによって、反応部5以外へ試薬液が広がることを確実に抑制することができる。
反応チャンバ8は、反応部5を空間として規定するためのものである。
導入部9は、反応部5へ試料液などを導入するためのものである。
排出部10は、反応部5に導入された試料液を排出するためのものである。また、導入時には、空気穴としての役割も果たすことができる。
バイオセンサ700では、導入部9および排出部10は、反応部5から接続して開口した円形の穴として形成されているが、液を導入できる形状であれば他の形状でもよい。
また液の排出は、導入部9から行ってもよく、この場合は、排出部10は空気穴として使用する。
以下、第7実施形態に示された電気化学検出用バイオセンサを用いた分析方法について説明する。この分析方法は、実施の形態1〜6に示された電気化学検出用バイオセンサを用いた分析方法とは、試料液またはバッファー液等を反応部5へ滴下していた部分が、導入部9から液を導入し、排出部10から排出するという点で異なるが、後は同様である。
本発明は上述した各実施形態に限定されるものではなく、請求項に示した範囲において種々の変更が可能であり、異なる実施形態にそれぞれ開示された技術的手段を適宜組み合わせて得られる実施形態についても本発明の技術的範囲に含まれる。
〔実施例1〕
図11は実施例1に係るバイオセンサ800の概略構成を示す上面図である。図11を用いて実施例1を説明する。
図11は実施例1に係るバイオセンサ800の概略構成を示す上面図である。図11を用いて実施例1を説明する。
まず、10cm×10cm×厚さ0.5mmのガラスウェハ(コーニング社製 EagleXG)に作用極1、対極2、接続パッドA1、A2およびA3、リード電極部B1、B2およびB3を、フォトリソグラフィを用いて形成した。これらは全て金をスパッタすることによって形成した。作用極1は、直径2mmの円形とし、対極2は作用極1を囲むような円弧状の形状に形成した。
次に、同様にフォトリソグラフィを用いて、銀電極を形成した。そして極の一部を化学的に塩化銀に変化させ、銀および塩化銀からなる参照極3を形成した。
ガラスウェハには図11に示す電極基板(1cm×2cm)を複数枚形成し、ガラスカッターを用いて1枚1枚切断した。
続いて、反応チャンバを作製するための型を作製した。シリコンウェハに、底面の形状が直径2.3mmの円形であって、高さ40umの型を作製した。ここにポリジメチルシロキサン(PDMS)を流しこみ、焼き固めて反応チャンバを作製した。反応チャンバの両端に直径0.5mmの穴をあけて、導入部9および排出部10とした。
電極基板の作用極上に形成したチオール分子による自己組織化単分子膜(SAM)を介して、グルコースオキシダーゼを固定化した。
反応チャンバを、グルコースオキシダーゼを固定化した基板に貼り合わせ、実施例1のバイオセンサ800とした。
この実施例1における反応チャンバによって形成される反応部の底面積と、作用極との面積比率は、0.76となった。
〔比較例1〕
反応チャンバを作製するための型において、底面の形状が直径2.8mmの円形であって、高さ40umの型を作製した。ここにPDMSを流し込み、焼き固めて反応チャンバを作製した。
反応チャンバを作製するための型において、底面の形状が直径2.8mmの円形であって、高さ40umの型を作製した。ここにPDMSを流し込み、焼き固めて反応チャンバを作製した。
グルコースオキシダーゼを固定化した基板に、反応チャンバを貼り合わせ、比較例1のバイオセンサとした。
この比較例1における、反応チャンバによって形成される反応部の底面積と、作用極との面積比率は、0.51となった。
(グルコースの検出)
実施例1および比較例1のバイオセンサを用いて、グルコースの検出を行った。グルコース溶液は、50mg/dL、100mg/dL、250mg/dLのものを調製した。
実施例1および比較例1のバイオセンサを用いて、グルコースの検出を行った。グルコース溶液は、50mg/dL、100mg/dL、250mg/dLのものを調製した。
反応部にグルコース溶液を入れ、10秒後の電流値を測定した。バックグラウンド電流を補正後、時間に対して電流値をプロットし、原点との2点を結ぶ直線の傾きから初速度を求めた。
面積比率0.51の比較例1の場合、グルコース濃度と初速度とは比例しなかったが、面積比率0.76の実施例1の場合、グルコース濃度は初速度に比例した。直線の傾きから求めた初速度が、真の初速度とほぼ等しく求めることができた。
以上のことから、本発明に係るバイオセンサによれば、短時間の反応時間でも、未知濃度のグルコース測定の初速度を正確に求めることができ、ある既知濃度のグルコース測定の初速度と比較することによって、グルコースの濃度を求めることができる。
〔実施例2〕
実施例1と同様に作製した電極基板の作用極上に、チオール分子による自己組織化単分子膜(SAM)を介して、抗CRP抗体を固定化した。実施例1と同様の反応チャンバを貼り合わせて、実施例2のバイオセンサとした。
実施例1と同様に作製した電極基板の作用極上に、チオール分子による自己組織化単分子膜(SAM)を介して、抗CRP抗体を固定化した。実施例1と同様の反応チャンバを貼り合わせて、実施例2のバイオセンサとした。
〔比較例2〕
実施例1と同様に作製した電極基板の作用極上に、実施例2と同様に抗CRP抗体を固定化した。比較例1と同様の反応チャンバを貼り合わせて、比較例2のバイオセンサとした。
実施例1と同様に作製した電極基板の作用極上に、実施例2と同様に抗CRP抗体を固定化した。比較例1と同様の反応チャンバを貼り合わせて、比較例2のバイオセンサとした。
(CRPの検出)
実施例2および比較例2のバイオセンサを用いて、CRPの検出を行った。まず、実施例2および比較例2のバイオセンサの反応部に、カゼイン溶液を入れ、30分室温にて静置し、非特異吸着防止膜を形成した。カゼイン溶液を排出し、PBS溶液を用いて反応部内を洗浄した。次に、反応部にCRP溶液を入れ、3分室温にて静置し、作用極上に固定化された抗体とCRPとの複合体を形成した。CRP溶液は、0.2mg/dL、2mg/dL、10mg/dLのものを使用した。CRP溶液を排出し、反応部内を洗浄した。次に、反応部に第二の結合物質として、ALP標識抗CRP抗体溶液を入れ、3分室温にて静置し、固定化抗体−CRP−ALP標識抗体のサンドイッチ複合体を形成した。ALPとは、アルカリフォスファターゼという酵素のことである。ALP標識抗体を排出し、反応部内を洗浄した。反応部に、p−アミノフェニルリン酸塩(pAPP)溶液を入れ、10秒後の電流値を測定した。バックグラウンド電流を補正後、時間に対して電流値をプロットし、原点との2点を結ぶ直線の傾きから初速度を求めた。
実施例2および比較例2のバイオセンサを用いて、CRPの検出を行った。まず、実施例2および比較例2のバイオセンサの反応部に、カゼイン溶液を入れ、30分室温にて静置し、非特異吸着防止膜を形成した。カゼイン溶液を排出し、PBS溶液を用いて反応部内を洗浄した。次に、反応部にCRP溶液を入れ、3分室温にて静置し、作用極上に固定化された抗体とCRPとの複合体を形成した。CRP溶液は、0.2mg/dL、2mg/dL、10mg/dLのものを使用した。CRP溶液を排出し、反応部内を洗浄した。次に、反応部に第二の結合物質として、ALP標識抗CRP抗体溶液を入れ、3分室温にて静置し、固定化抗体−CRP−ALP標識抗体のサンドイッチ複合体を形成した。ALPとは、アルカリフォスファターゼという酵素のことである。ALP標識抗体を排出し、反応部内を洗浄した。反応部に、p−アミノフェニルリン酸塩(pAPP)溶液を入れ、10秒後の電流値を測定した。バックグラウンド電流を補正後、時間に対して電流値をプロットし、原点との2点を結ぶ直線の傾きから初速度を求めた。
面積比率0.51の比較例2の場合、CRP濃度と初速度とは比例しなかったが、面積比率0.76の実施例2の場合、CRP濃度は初速度に比例した。直線の傾きより求めた初速度を、真の初速度とほぼ等しく求めることができた。
以上のことから、本発明を用いると、短時間の反応時間によって、未知濃度のCRP測定の初速度を正確に求めることができ、ある既知濃度のCRP測定の初速度と比較することにより、グルコースの濃度を求めることができる。
なお、CRPに限ったものではなく、本発明はイムノアッセイ一般に用いることも可能である。
本発明にかかるバイオセンサは、電気化学測定を行うことにより、検出された電流値から試料液中のターゲット物質の濃度を求めることができるため、生体、環境、医療、食品などに関する試料の分析に利用することができる。
1 作用極
2 対極
3 参照極
A1〜A3 接続パッド
B1〜B3 リード電極部
4 絶縁膜
5 反応部
6 疎水性膜
7 壁面
8 反応チャンバ
9 導入部
10 排出部
20 基板
2 対極
3 参照極
A1〜A3 接続パッド
B1〜B3 リード電極部
4 絶縁膜
5 反応部
6 疎水性膜
7 壁面
8 反応チャンバ
9 導入部
10 排出部
20 基板
Claims (13)
- ターゲット物質と反応し生成物を生成する反応物質、または、ターゲット物質と結合する結合物質が固定されている作用極と、
対極と、
該ターゲット物質を含む試料液を溜める反応部と、を備えており、
該作用極および該対極は、該反応部の底面に配置されており、
該反応部の底面において該作用極が占める割合が0.7以上であることを特徴とするバイオセンサ。 - 上記作用極を複数備えていることを特徴とする請求項1に記載のバイオセンサ。
- 参照極をさらに備えていることを特徴とする請求項1または2に記載のバイオセンサ。
- 疎水性を有する疎水性部分を備えており、
該疎水性部分が上記反応部を囲むように配置されていることを特徴とする請求項1から3の何れか1項に記載のバイオセンサ。 - 上記反応部を囲む壁面を備えていることを特徴とする請求項1から3の何れか1項に記載のバイオセンサ。
- 上記反応部を格納する反応チャンバを備えており、
該反応チャンバは、該反応チャンバ内に上記試料液を注入するための注入口と、上記反応チャンバ内の上記試料液を排出するための排出口とを備えていることを特徴とする請求項1から3の何れか1項に記載のバイオセンサ。 - 上記作用極の中心が、上記反応部の底面の中央部にあることを特徴とする請求項1から6の何れか1項に記載のバイオセンサ。
- 上記作用極の底面の形状が、上記反応部の底面の形状と相似形であることを特徴とする請求項7に記載のバイオセンサ。
- 上記反応物質は、上記ターゲット物質と特異的に反応するものであることを特徴とする請求項1から8の何れか1項に記載のバイオセンサ。
- 上記反応物質が、上記ターゲット物質の反応を触媒する酵素であることを特徴とする請求項9に記載のバイオセンサ。
- 上記結合物質は、上記ターゲット物質と特異的に結合するものであることを特徴とする請求項1から8の何れか1項に記載のバイオセンサ。
- 上記結合物質が、上記ターゲット物質に対する抗体、または、上記ターゲット物質に特異的に結合するペプチドであることを特徴とする請求項11に記載のバイオセンサ。
- 請求項1から12のいずれか1項に記載のバイオセンサを用いた分析方法であって、
ターゲット物質を含む試料液を、上記反応部に導入する導入工程、および
上記作用極と上記対極との間に電圧を印加することで、反応または結合した上記ターゲット物質に応じた電流値を測定する工程、を含むことを特徴とする分析方法。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011116211A JP2012242366A (ja) | 2011-05-24 | 2011-05-24 | バイオセンサとこれを用いた分析方法 |
| US13/419,456 US20120298528A1 (en) | 2011-05-24 | 2012-03-14 | Biosensor and analysis method using same |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011116211A JP2012242366A (ja) | 2011-05-24 | 2011-05-24 | バイオセンサとこれを用いた分析方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2012242366A true JP2012242366A (ja) | 2012-12-10 |
Family
ID=47218493
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011116211A Pending JP2012242366A (ja) | 2011-05-24 | 2011-05-24 | バイオセンサとこれを用いた分析方法 |
Country Status (2)
| Country | Link |
|---|---|
| US (1) | US20120298528A1 (ja) |
| JP (1) | JP2012242366A (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2021009942A1 (ja) * | 2019-07-18 | 2021-01-21 | 株式会社ファーストスクリーニング | 電気化学センサユニット |
| JP2021018227A (ja) * | 2019-12-23 | 2021-02-15 | 株式会社ファーストスクリーニング | 電気化学センサユニット |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103412012B (zh) * | 2013-03-28 | 2015-09-09 | 利多(香港)有限公司 | 生物传感器 |
| CN103454321B (zh) * | 2013-03-28 | 2015-09-09 | 利多(香港)有限公司 | 生物传感器及其制造方法 |
| EP4031869A1 (en) * | 2019-09-20 | 2022-07-27 | Momm Diagnostics GmbH | Immunoassay analyzer, immunoassay kit and method for detecting analyte in liquid sample |
| IT202100021668A1 (it) * | 2021-08-10 | 2023-02-10 | Fondazione St Italiano Tecnologia | Biosensore elettrochimico e metodo per la rilevazione di contaminanti ambientali |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001215208A (ja) * | 2000-02-01 | 2001-08-10 | Nec Corp | 化学センサカートリッジ及びそれを備えた化学センサ並びにそれを用いた試料の測定方法 |
| JP2005114687A (ja) * | 2003-10-10 | 2005-04-28 | Seiko Epson Corp | 電気化学式センサおよびその製造方法 |
| JP2007278981A (ja) * | 2006-04-11 | 2007-10-25 | Japan Advanced Institute Of Science & Technology Hokuriku | プレナー型電極及びこれを用いた電気化学検出センサー |
| JP2009139114A (ja) * | 2007-12-04 | 2009-06-25 | Toyobo Co Ltd | 免疫測定用電気化学センサー |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4511659A (en) * | 1983-03-04 | 1985-04-16 | Esa, Inc. | Liquid chromatograph with electrochemical detector and method |
| US6511854B1 (en) * | 1997-07-31 | 2003-01-28 | The Uab Research Foundation | Regenerable biosensor using total internal reflection fluorescence with electrochemical control |
| US6670115B1 (en) * | 1999-11-24 | 2003-12-30 | Biotronic Technologies, Inc. | Devices and methods for detecting analytes using electrosensor having capture reagent |
| US7169273B2 (en) * | 2000-09-25 | 2007-01-30 | Asahi Kasei Kabushiki Kaisha | Enzyme electrode |
| US6863800B2 (en) * | 2002-02-01 | 2005-03-08 | Abbott Laboratories | Electrochemical biosensor strip for analysis of liquid samples |
| EP1548427B1 (en) * | 2002-08-13 | 2011-01-19 | Gunze Limited | Biosensor and method for manufacturing same |
| TW200510721A (en) * | 2003-08-29 | 2005-03-16 | Toshiba Kk | Color reagent, concentration measuring kit, concentration measuring method and sensor chip for use therein |
| JPWO2008044530A1 (ja) * | 2006-10-05 | 2010-02-12 | パナソニック株式会社 | 多項目成分分析センサおよび多項目成分の測定方法 |
-
2011
- 2011-05-24 JP JP2011116211A patent/JP2012242366A/ja active Pending
-
2012
- 2012-03-14 US US13/419,456 patent/US20120298528A1/en not_active Abandoned
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001215208A (ja) * | 2000-02-01 | 2001-08-10 | Nec Corp | 化学センサカートリッジ及びそれを備えた化学センサ並びにそれを用いた試料の測定方法 |
| JP2005114687A (ja) * | 2003-10-10 | 2005-04-28 | Seiko Epson Corp | 電気化学式センサおよびその製造方法 |
| JP2007278981A (ja) * | 2006-04-11 | 2007-10-25 | Japan Advanced Institute Of Science & Technology Hokuriku | プレナー型電極及びこれを用いた電気化学検出センサー |
| JP2009139114A (ja) * | 2007-12-04 | 2009-06-25 | Toyobo Co Ltd | 免疫測定用電気化学センサー |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2021009942A1 (ja) * | 2019-07-18 | 2021-01-21 | 株式会社ファーストスクリーニング | 電気化学センサユニット |
| JP2021018119A (ja) * | 2019-07-18 | 2021-02-15 | 株式会社ファーストスクリーニング | 電気化学センサユニット |
| JP2021018227A (ja) * | 2019-12-23 | 2021-02-15 | 株式会社ファーストスクリーニング | 電気化学センサユニット |
Also Published As
| Publication number | Publication date |
|---|---|
| US20120298528A1 (en) | 2012-11-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Li et al. | A microfluidic paper‐based origami nanobiosensor for label‐free, ultrasensitive immunoassays | |
| Kuo et al. | Improving sensitivity of a miniaturized label-free electrochemical biosensor using zigzag electrodes | |
| CN104203808B (zh) | 具有纳米结构电极的生物传感器 | |
| US9746441B2 (en) | Sensor, sensor kit and method for detecting an analyte | |
| JP2012242366A (ja) | バイオセンサとこれを用いた分析方法 | |
| Lakey et al. | Impedimetric array in polymer microfluidic cartridge for low cost point-of-care diagnostics | |
| US6878539B1 (en) | Affinity sensor for detecting specific molecular binding events and use thereof | |
| Lim et al. | Microfabricated on-chip-type electrochemical flow immunoassay system for the detection of histamine released in whole blood samples | |
| JP2001524673A (ja) | 検体検出のための装置およびプロセス | |
| Laschi et al. | Planar electrochemical sensors for biomedical applications | |
| Dutta et al. | Electrochemical biosensors for cytokine profiling: recent advancements and possibilities in the near future | |
| US20200072825A1 (en) | Electrochemical sensors and methods of use thereof | |
| Li et al. | Band electrodes in sensing applications: response characteristics and band fabrication methods | |
| CN112020645A (zh) | 基于多孔电极的生物传感器 | |
| KR100563834B1 (ko) | 미세유체 채널이 집적화된 3차원 전극시스템 | |
| WO2019134741A1 (en) | Single-channel multianalyte biosensor | |
| Laczka et al. | Electrochemical detection of testosterone by use of three-dimensional disc–ring microelectrode sensing platforms: application to doping monitoring | |
| Xue et al. | CMOS and MEMS based micro hemoglobin-A1c biosensors fabricated by various antibody immobilization methods | |
| Zhang et al. | Electrochemical Biosensors Based on Micro‐fabricated Devices for Point‐of‐Care Testing: A Review | |
| Xie et al. | A ten-minute, single step, label-free, sample-to-answer assay for qualitative detection of cytokines in serum at femtomolar levels | |
| KR20110126942A (ko) | 바이오칩 및 그 제조 방법, 이를 이용한 분석 대상 물질 검출 방법 | |
| Wu et al. | A microfluidic chip integrating electrochemical impedimetric immunosensors constructed by top-bottom opposite electrodes for rapid detection of peanut allergen-Ara h 1 | |
| Chuang et al. | Label-free impedance biosensors for Point-of-Care diagnostics | |
| KR102290258B1 (ko) | 플렉서블 바이오 센서 및 이의 제조 방법 | |
| Honda et al. | Toward a Practical Impedimetric Biosensor: A Micro-Gap Parallel Plate Electrode Structure That Suppresses Unexpected Device-to-Device Variations |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130319 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20130321 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130820 |