JP2011512323A - 幹細胞の成長を調節するための方法および組成物 - Google Patents
幹細胞の成長を調節するための方法および組成物 Download PDFInfo
- Publication number
- JP2011512323A JP2011512323A JP2010533155A JP2010533155A JP2011512323A JP 2011512323 A JP2011512323 A JP 2011512323A JP 2010533155 A JP2010533155 A JP 2010533155A JP 2010533155 A JP2010533155 A JP 2010533155A JP 2011512323 A JP2011512323 A JP 2011512323A
- Authority
- JP
- Japan
- Prior art keywords
- alkyl
- hydroxy
- cyclo
- halogen
- hydrogen
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 210000000130 stem cell Anatomy 0.000 title claims abstract description 69
- 239000000203 mixture Substances 0.000 title claims abstract description 37
- 238000000034 method Methods 0.000 title claims description 24
- 230000001105 regulatory effect Effects 0.000 title claims description 8
- 230000010261 cell growth Effects 0.000 title description 2
- -1 prostaglandin compound Chemical class 0.000 claims abstract description 73
- 230000004663 cell proliferation Effects 0.000 claims abstract description 15
- 230000024245 cell differentiation Effects 0.000 claims abstract description 14
- 125000000217 alkyl group Chemical group 0.000 claims description 95
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 70
- 125000003545 alkoxy group Chemical group 0.000 claims description 58
- 229910052736 halogen Inorganic materials 0.000 claims description 33
- 150000002367 halogens Chemical class 0.000 claims description 33
- 239000001257 hydrogen Substances 0.000 claims description 33
- 229910052739 hydrogen Inorganic materials 0.000 claims description 33
- 125000003118 aryl group Chemical group 0.000 claims description 32
- 125000000623 heterocyclic group Chemical group 0.000 claims description 32
- 125000004043 oxo group Chemical group O=* 0.000 claims description 29
- 125000004423 acyloxy group Chemical group 0.000 claims description 26
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical group N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 21
- 125000004104 aryloxy group Chemical group 0.000 claims description 20
- 230000004069 differentiation Effects 0.000 claims description 19
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 18
- 229920006395 saturated elastomer Polymers 0.000 claims description 18
- 125000001820 oxy group Chemical group [*:1]O[*:2] 0.000 claims description 17
- 125000005843 halogen group Chemical group 0.000 claims description 16
- 229910052799 carbon Inorganic materials 0.000 claims description 15
- 150000002431 hydrogen Chemical class 0.000 claims description 15
- 125000001931 aliphatic group Chemical group 0.000 claims description 13
- 230000035755 proliferation Effects 0.000 claims description 13
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 12
- 229910052760 oxygen Inorganic materials 0.000 claims description 12
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical group [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 11
- 229910052757 nitrogen Inorganic materials 0.000 claims description 11
- 239000001301 oxygen Substances 0.000 claims description 11
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 claims description 10
- 229910052717 sulfur Chemical group 0.000 claims description 10
- 239000011593 sulfur Chemical group 0.000 claims description 10
- 125000004356 hydroxy functional group Chemical group O* 0.000 claims description 9
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 7
- 239000008194 pharmaceutical composition Substances 0.000 claims description 6
- 238000004519 manufacturing process Methods 0.000 claims description 5
- 210000001671 embryonic stem cell Anatomy 0.000 claims description 4
- 238000000338 in vitro Methods 0.000 claims description 3
- 210000001988 somatic stem cell Anatomy 0.000 claims description 2
- 150000001721 carbon Chemical group 0.000 claims 6
- 150000001875 compounds Chemical class 0.000 description 44
- 210000004027 cell Anatomy 0.000 description 41
- 125000004432 carbon atom Chemical group C* 0.000 description 35
- 229940126062 Compound A Drugs 0.000 description 24
- NLDMNSXOCDLTTB-UHFFFAOYSA-N Heterophylliin A Natural products O1C2COC(=O)C3=CC(O)=C(O)C(O)=C3C3=C(O)C(O)=C(O)C=C3C(=O)OC2C(OC(=O)C=2C=C(O)C(O)=C(O)C=2)C(O)C1OC(=O)C1=CC(O)=C(O)C(O)=C1 NLDMNSXOCDLTTB-UHFFFAOYSA-N 0.000 description 24
- KOWJANGMTAZWDT-UHFFFAOYSA-N 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridin-1-ium;chloride Chemical compound Cl.C1N(C)CCC(C=2C=CC=CC=2)=C1 KOWJANGMTAZWDT-UHFFFAOYSA-N 0.000 description 17
- 108091000117 Tyrosine 3-Monooxygenase Proteins 0.000 description 13
- 102000048218 Tyrosine 3-monooxygenases Human genes 0.000 description 13
- 230000000694 effects Effects 0.000 description 13
- 125000001424 substituent group Chemical group 0.000 description 13
- 241000699670 Mus sp. Species 0.000 description 11
- 208000027418 Wounds and injury Diseases 0.000 description 11
- 210000001519 tissue Anatomy 0.000 description 11
- 206010052428 Wound Diseases 0.000 description 10
- 150000003839 salts Chemical class 0.000 description 10
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 9
- 238000012360 testing method Methods 0.000 description 9
- 239000000835 fiber Substances 0.000 description 8
- 210000002901 mesenchymal stem cell Anatomy 0.000 description 8
- 239000002674 ointment Substances 0.000 description 8
- 150000001338 aliphatic hydrocarbons Chemical group 0.000 description 7
- 239000000243 solution Substances 0.000 description 7
- 239000003981 vehicle Substances 0.000 description 7
- 239000000654 additive Substances 0.000 description 6
- 150000005215 alkyl ethers Chemical class 0.000 description 6
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 6
- 210000001577 neostriatum Anatomy 0.000 description 6
- 210000001778 pluripotent stem cell Anatomy 0.000 description 6
- 239000000725 suspension Substances 0.000 description 6
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 5
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 5
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 5
- 239000004698 Polyethylene Substances 0.000 description 5
- 239000004480 active ingredient Substances 0.000 description 5
- 239000003795 chemical substances by application Substances 0.000 description 5
- 239000001963 growth medium Substances 0.000 description 5
- 150000002430 hydrocarbons Chemical group 0.000 description 5
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 4
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 4
- 210000001185 bone marrow Anatomy 0.000 description 4
- 239000000460 chlorine Substances 0.000 description 4
- 229910052801 chlorine Inorganic materials 0.000 description 4
- 239000000839 emulsion Substances 0.000 description 4
- 150000002148 esters Chemical class 0.000 description 4
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 4
- 229910052731 fluorine Inorganic materials 0.000 description 4
- 239000011737 fluorine Substances 0.000 description 4
- 230000012010 growth Effects 0.000 description 4
- 230000035876 healing Effects 0.000 description 4
- 238000011534 incubation Methods 0.000 description 4
- 239000003701 inert diluent Substances 0.000 description 4
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 4
- 239000003883 ointment base Substances 0.000 description 4
- 210000000056 organ Anatomy 0.000 description 4
- 210000000963 osteoblast Anatomy 0.000 description 4
- 230000004072 osteoblast differentiation Effects 0.000 description 4
- 239000000843 powder Substances 0.000 description 4
- 230000002062 proliferating effect Effects 0.000 description 4
- 210000003523 substantia nigra Anatomy 0.000 description 4
- 239000000829 suppository Substances 0.000 description 4
- 208000032467 Aplastic anaemia Diseases 0.000 description 3
- 101000605172 Aspergillus niger (strain CBS 513.88 / FGSC A1513) Probable endopolygalacturonase E Proteins 0.000 description 3
- 101000605171 Aspergillus niger Endopolygalacturonase E Proteins 0.000 description 3
- 101000941281 Bos taurus Gastric triacylglycerol lipase Proteins 0.000 description 3
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- 101000595923 Homo sapiens Placenta growth factor Proteins 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- 102000004067 Osteocalcin Human genes 0.000 description 3
- 108090000573 Osteocalcin Proteins 0.000 description 3
- 208000001132 Osteoporosis Diseases 0.000 description 3
- 102100035194 Placenta growth factor Human genes 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 125000005907 alkyl ester group Chemical group 0.000 description 3
- 150000001408 amides Chemical class 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 125000002619 bicyclic group Chemical group 0.000 description 3
- 230000010478 bone regeneration Effects 0.000 description 3
- 210000004556 brain Anatomy 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 238000001514 detection method Methods 0.000 description 3
- 206010012601 diabetes mellitus Diseases 0.000 description 3
- 239000003085 diluting agent Substances 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 208000035475 disorder Diseases 0.000 description 3
- 210000005064 dopaminergic neuron Anatomy 0.000 description 3
- 235000019441 ethanol Nutrition 0.000 description 3
- 150000002170 ethers Chemical class 0.000 description 3
- 238000000684 flow cytometry Methods 0.000 description 3
- 230000006870 function Effects 0.000 description 3
- 230000001771 impaired effect Effects 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- 201000006938 muscular dystrophy Diseases 0.000 description 3
- 230000003287 optical effect Effects 0.000 description 3
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 3
- 239000003755 preservative agent Substances 0.000 description 3
- WGJJROVFWIXTPA-OALUTQOASA-N prostanoic acid Chemical compound CCCCCCCC[C@H]1CCC[C@@H]1CCCCCCC(O)=O WGJJROVFWIXTPA-OALUTQOASA-N 0.000 description 3
- 230000008439 repair process Effects 0.000 description 3
- 210000003491 skin Anatomy 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 2
- SZNYYWIUQFZLLT-UHFFFAOYSA-N 2-methyl-1-(2-methylpropoxy)propane Chemical compound CC(C)COCC(C)C SZNYYWIUQFZLLT-UHFFFAOYSA-N 0.000 description 2
- 0 C(*1)C1C(*1)C2C1CCCC2 Chemical compound C(*1)C1C(*1)C2C1CCCC2 0.000 description 2
- 229930194542 Keto Natural products 0.000 description 2
- 101150046735 LEPR gene Proteins 0.000 description 2
- 101150063827 LEPROT gene Proteins 0.000 description 2
- 108010004729 Phycoerythrin Proteins 0.000 description 2
- 239000002671 adjuvant Substances 0.000 description 2
- 239000000443 aerosol Substances 0.000 description 2
- 125000003342 alkenyl group Chemical group 0.000 description 2
- 125000002947 alkylene group Chemical group 0.000 description 2
- 125000000304 alkynyl group Chemical group 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 239000002585 base Substances 0.000 description 2
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 2
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 2
- 230000032823 cell division Effects 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 239000007884 disintegrant Substances 0.000 description 2
- 239000002270 dispersing agent Substances 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- 210000002514 epidermal stem cell Anatomy 0.000 description 2
- 210000002615 epidermis Anatomy 0.000 description 2
- 239000000796 flavoring agent Substances 0.000 description 2
- 125000001153 fluoro group Chemical group F* 0.000 description 2
- 235000013355 food flavoring agent Nutrition 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 239000003205 fragrance Substances 0.000 description 2
- 238000012744 immunostaining Methods 0.000 description 2
- 239000007972 injectable composition Substances 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 125000000468 ketone group Chemical group 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- 239000003550 marker Substances 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 125000002950 monocyclic group Chemical group 0.000 description 2
- 230000000877 morphologic effect Effects 0.000 description 2
- 210000003205 muscle Anatomy 0.000 description 2
- 210000001178 neural stem cell Anatomy 0.000 description 2
- 210000002569 neuron Anatomy 0.000 description 2
- 229940094443 oxytocics prostaglandins Drugs 0.000 description 2
- 230000001766 physiological effect Effects 0.000 description 2
- 239000006187 pill Substances 0.000 description 2
- 150000003180 prostaglandins Chemical class 0.000 description 2
- 239000001397 quillaja saponaria molina bark Substances 0.000 description 2
- 229930182490 saponin Natural products 0.000 description 2
- 150000007949 saponins Chemical class 0.000 description 2
- 229930195734 saturated hydrocarbon Natural products 0.000 description 2
- 239000008247 solid mixture Substances 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 230000004936 stimulating effect Effects 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 239000006190 sub-lingual tablet Substances 0.000 description 2
- 125000003107 substituted aryl group Chemical group 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 125000003944 tolyl group Chemical group 0.000 description 2
- 230000007704 transition Effects 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 239000000080 wetting agent Substances 0.000 description 2
- PNKZBZPLRKCVLI-UHFFFAOYSA-N (2-methylpropan-2-yl)oxybenzene Chemical compound CC(C)(C)OC1=CC=CC=C1 PNKZBZPLRKCVLI-UHFFFAOYSA-N 0.000 description 1
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 description 1
- FFJCNSLCJOQHKM-CLFAGFIQSA-N (z)-1-[(z)-octadec-9-enoxy]octadec-9-ene Chemical compound CCCCCCCC\C=C/CCCCCCCCOCCCCCCCC\C=C/CCCCCCCC FFJCNSLCJOQHKM-CLFAGFIQSA-N 0.000 description 1
- NKJOXAZJBOMXID-UHFFFAOYSA-N 1,1'-Oxybisoctane Chemical compound CCCCCCCCOCCCCCCCC NKJOXAZJBOMXID-UHFFFAOYSA-N 0.000 description 1
- PUBSWBHFVCUPOF-UHFFFAOYSA-N 1-(1-cyclopropylethoxy)ethylcyclopropane Chemical compound C1CC1C(C)OC(C)C1CC1 PUBSWBHFVCUPOF-UHFFFAOYSA-N 0.000 description 1
- HXKKHQJGJAFBHI-UHFFFAOYSA-N 1-aminopropan-2-ol Chemical class CC(O)CN HXKKHQJGJAFBHI-UHFFFAOYSA-N 0.000 description 1
- DURPTKYDGMDSBL-UHFFFAOYSA-N 1-butoxybutane Chemical compound CCCCOCCCC DURPTKYDGMDSBL-UHFFFAOYSA-N 0.000 description 1
- POEDHWVTLBLWDA-UHFFFAOYSA-N 1-butylindole-2,3-dione Chemical compound C1=CC=C2N(CCCC)C(=O)C(=O)C2=C1 POEDHWVTLBLWDA-UHFFFAOYSA-N 0.000 description 1
- CMCBDXRRFKYBDG-UHFFFAOYSA-N 1-dodecoxydodecane Chemical compound CCCCCCCCCCCCOCCCCCCCCCCCC CMCBDXRRFKYBDG-UHFFFAOYSA-N 0.000 description 1
- FDCJDKXCCYFOCV-UHFFFAOYSA-N 1-hexadecoxyhexadecane Chemical compound CCCCCCCCCCCCCCCCOCCCCCCCCCCCCCCCC FDCJDKXCCYFOCV-UHFFFAOYSA-N 0.000 description 1
- 125000004066 1-hydroxyethyl group Chemical group [H]OC([H])([*])C([H])([H])[H] 0.000 description 1
- PRHCBRXAHBBRKA-UHFFFAOYSA-N 2-(2-hydroxypropan-2-yloxy)propan-2-ol Chemical compound CC(C)(O)OC(C)(C)O PRHCBRXAHBBRKA-UHFFFAOYSA-N 0.000 description 1
- PLNNBRYFKARCEV-UHFFFAOYSA-N 2-[(2-hydroxyphenyl)methoxymethyl]phenol Chemical compound OC1=CC=CC=C1COCC1=CC=CC=C1O PLNNBRYFKARCEV-UHFFFAOYSA-N 0.000 description 1
- 125000000143 2-carboxyethyl group Chemical group [H]OC(=O)C([H])([H])C([H])([H])* 0.000 description 1
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- 125000003762 3,4-dimethoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C(OC([H])([H])[H])C([H])=C1* 0.000 description 1
- ATVJXMYDOSMEPO-UHFFFAOYSA-N 3-prop-2-enoxyprop-1-ene Chemical compound C=CCOCC=C ATVJXMYDOSMEPO-UHFFFAOYSA-N 0.000 description 1
- XHWSCQCJAPLELI-UHFFFAOYSA-N 4-(3,4-dimethoxyphenoxy)-1,2-dimethoxybenzene Chemical compound C1=C(OC)C(OC)=CC=C1OC1=CC=C(OC)C(OC)=C1 XHWSCQCJAPLELI-UHFFFAOYSA-N 0.000 description 1
- JLLYLQLDYORLBB-UHFFFAOYSA-N 5-bromo-n-methylthiophene-2-sulfonamide Chemical compound CNS(=O)(=O)C1=CC=C(Br)S1 JLLYLQLDYORLBB-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- PQZMNQPMCZVXDZ-UTCJRWHESA-N C(C1CC1)/C=C\C1CCCC1 Chemical compound C(C1CC1)/C=C\C1CCCC1 PQZMNQPMCZVXDZ-UTCJRWHESA-N 0.000 description 1
- CBTWSONLCCYHGW-UHFFFAOYSA-N CC(CCC1)C1C1=CC1 Chemical compound CC(CCC1)C1C1=CC1 CBTWSONLCCYHGW-UHFFFAOYSA-N 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 1
- LCGLNKUTAGEVQW-UHFFFAOYSA-N Dimethyl ether Chemical compound COC LCGLNKUTAGEVQW-UHFFFAOYSA-N 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical class NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- 239000004606 Fillers/Extenders Substances 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 102100031132 Glucose-6-phosphate isomerase Human genes 0.000 description 1
- 101150020741 Hpgds gene Proteins 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- VQTUBCCKSQIDNK-UHFFFAOYSA-N Isobutene Chemical group CC(C)=C VQTUBCCKSQIDNK-UHFFFAOYSA-N 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical class NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 208000029549 Muscle injury Diseases 0.000 description 1
- 101150080623 PGB gene Proteins 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 229920000954 Polyglycolide Polymers 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 101710191567 Probable endopolygalacturonase C Proteins 0.000 description 1
- QOSMNYMQXIVWKY-UHFFFAOYSA-N Propyl levulinate Chemical compound CCCOC(=O)CCC(C)=O QOSMNYMQXIVWKY-UHFFFAOYSA-N 0.000 description 1
- 208000028990 Skin injury Diseases 0.000 description 1
- 206010072170 Skin wound Diseases 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical class OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- QYKIQEUNHZKYBP-UHFFFAOYSA-N Vinyl ether Chemical compound C=COC=C QYKIQEUNHZKYBP-UHFFFAOYSA-N 0.000 description 1
- QUXMPZUVBXHUII-UHFFFAOYSA-N [1,1-bis(hydroxymethylamino)ethylamino]methanol Chemical class OCNC(C)(NCO)NCO QUXMPZUVBXHUII-UHFFFAOYSA-N 0.000 description 1
- PVQATPQSBYNMGE-UHFFFAOYSA-N [benzhydryloxy(phenyl)methyl]benzene Chemical compound C=1C=CC=CC=1C(C=1C=CC=CC=1)OC(C=1C=CC=CC=1)C1=CC=CC=C1 PVQATPQSBYNMGE-UHFFFAOYSA-N 0.000 description 1
- XXFXTBNFFMQVKJ-UHFFFAOYSA-N [diphenyl(trityloxy)methyl]benzene Chemical compound C=1C=CC=CC=1C(C=1C=CC=CC=1)(C=1C=CC=CC=1)OC(C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 XXFXTBNFFMQVKJ-UHFFFAOYSA-N 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 125000000641 acridinyl group Chemical group C1(=CC=CC2=NC3=CC=CC=C3C=C12)* 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 125000004183 alkoxy alkyl group Chemical group 0.000 description 1
- 230000000735 allogeneic effect Effects 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 150000003931 anilides Chemical class 0.000 description 1
- 230000000767 anti-ulcer Effects 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 239000007900 aqueous suspension Substances 0.000 description 1
- 125000000637 arginyl group Chemical class N[C@@H](CCCNC(N)=N)C(=O)* 0.000 description 1
- 125000002029 aromatic hydrocarbon group Chemical group 0.000 description 1
- 125000004391 aryl sulfonyl group Chemical group 0.000 description 1
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 1
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 150000003939 benzylamines Chemical class 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 229920002988 biodegradable polymer Polymers 0.000 description 1
- 239000004621 biodegradable polymer Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 230000036760 body temperature Effects 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 210000004271 bone marrow stromal cell Anatomy 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- RYYVLZVUVIJVGH-UHFFFAOYSA-N caffeine Chemical class CN1C(=O)N(C)C(=O)C2=C1N=CN2C RYYVLZVUVIJVGH-UHFFFAOYSA-N 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 1
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000011437 continuous method Methods 0.000 description 1
- 238000007428 craniotomy Methods 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000000000 cycloalkoxy group Chemical group 0.000 description 1
- 125000000753 cycloalkyl group Chemical group 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 229940097362 cyclodextrins Drugs 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 150000003946 cyclohexylamines Chemical class 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 230000007850 degeneration Effects 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- AQEFLFZSWDEAIP-UHFFFAOYSA-N di-tert-butyl ether Chemical compound CC(C)(C)OC(C)(C)C AQEFLFZSWDEAIP-UHFFFAOYSA-N 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical class OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- UZBQIPPOMKBLAS-UHFFFAOYSA-N diethylazanide Chemical compound CC[N-]CC UZBQIPPOMKBLAS-UHFFFAOYSA-N 0.000 description 1
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 150000004656 dimethylamines Chemical class 0.000 description 1
- QKIUAMUSENSFQQ-UHFFFAOYSA-N dimethylazanide Chemical compound C[N-]C QKIUAMUSENSFQQ-UHFFFAOYSA-N 0.000 description 1
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Chemical compound C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 1
- POLCUAVZOMRGSN-UHFFFAOYSA-N dipropyl ether Chemical compound CCCOCCC POLCUAVZOMRGSN-UHFFFAOYSA-N 0.000 description 1
- 208000037765 diseases and disorders Diseases 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 239000008393 encapsulating agent Substances 0.000 description 1
- ZCRZCMUDOWDGOB-UHFFFAOYSA-N ethanesulfonimidic acid Chemical compound CCS(N)(=O)=O ZCRZCMUDOWDGOB-UHFFFAOYSA-N 0.000 description 1
- 150000002169 ethanolamines Chemical class 0.000 description 1
- 125000004494 ethyl ester group Chemical group 0.000 description 1
- CQYBANOHCYKAEE-UHFFFAOYSA-N ethynoxyethyne Chemical compound C#COC#C CQYBANOHCYKAEE-UHFFFAOYSA-N 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 235000019197 fats Nutrition 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 125000003838 furazanyl group Chemical group 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 1
- 150000002373 hemiacetals Chemical class 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- 125000004836 hexamethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000010562 histological examination Methods 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 1
- 238000010191 image analysis Methods 0.000 description 1
- 125000002632 imidazolidinyl group Chemical group 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000005956 isoquinolyl group Chemical group 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- HNQIVZYLYMDVSB-UHFFFAOYSA-N methanesulfonimidic acid Chemical compound CS(N)(=O)=O HNQIVZYLYMDVSB-UHFFFAOYSA-N 0.000 description 1
- NSPJNIDYTSSIIY-UHFFFAOYSA-N methoxy(methoxymethoxy)methane Chemical compound COCOCOC NSPJNIDYTSSIIY-UHFFFAOYSA-N 0.000 description 1
- 125000004184 methoxymethyl group Chemical group [H]C([H])([H])OC([H])([H])* 0.000 description 1
- 150000004702 methyl esters Chemical class 0.000 description 1
- 150000003956 methylamines Chemical class 0.000 description 1
- MGJXBDMLVWIYOQ-UHFFFAOYSA-N methylazanide Chemical compound [NH-]C MGJXBDMLVWIYOQ-UHFFFAOYSA-N 0.000 description 1
- 125000002911 monocyclic heterocycle group Chemical group 0.000 description 1
- 210000004165 myocardium Anatomy 0.000 description 1
- 230000002632 myometrial effect Effects 0.000 description 1
- AIAKLPAJNLBVEA-UHFFFAOYSA-N n-[2-(2-benzamidophenoxy)phenyl]benzamide Chemical compound C=1C=CC=CC=1C(=O)NC1=CC=CC=C1OC1=CC=CC=C1NC(=O)C1=CC=CC=C1 AIAKLPAJNLBVEA-UHFFFAOYSA-N 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- 208000015122 neurodegenerative disease Diseases 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 230000033667 organ regeneration Effects 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 229920002866 paraformaldehyde Polymers 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 125000004817 pentamethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 230000010412 perfusion Effects 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 125000004934 phenanthridinyl group Chemical group C1(=CC=CC2=NC=C3C=CC=CC3=C12)* 0.000 description 1
- 125000001484 phenothiazinyl group Chemical group C1(=CC=CC=2SC3=CC=CC=C3NC12)* 0.000 description 1
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 150000003053 piperidines Chemical class 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 229940068965 polysorbates Drugs 0.000 description 1
- 230000018039 positive regulation of osteoblast differentiation Effects 0.000 description 1
- 159000000001 potassium salts Chemical class 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000003822 preparative gas chromatography Methods 0.000 description 1
- MFDFERRIHVXMIY-UHFFFAOYSA-N procaine Chemical class CCN(CC)CCOC(=O)C1=CC=C(N)C=C1 MFDFERRIHVXMIY-UHFFFAOYSA-N 0.000 description 1
- 235000010409 propane-1,2-diol alginate Nutrition 0.000 description 1
- 239000003380 propellant Substances 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 239000008213 purified water Substances 0.000 description 1
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 1
- 210000002637 putamen Anatomy 0.000 description 1
- 125000004309 pyranyl group Chemical group O1C(C=CC=C1)* 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000003072 pyrazolidinyl group Chemical group 0.000 description 1
- 125000002755 pyrazolinyl group Chemical group 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- 125000005493 quinolyl group Chemical group 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000001172 regenerating effect Effects 0.000 description 1
- 230000028344 regulation of stem cell differentiation Effects 0.000 description 1
- 230000020943 regulation of stem cell proliferation Effects 0.000 description 1
- 238000007363 ring formation reaction Methods 0.000 description 1
- JZWFDVDETGFGFC-UHFFFAOYSA-N salacetamide Chemical group CC(=O)NC(=O)C1=CC=CC=C1O JZWFDVDETGFGFC-UHFFFAOYSA-N 0.000 description 1
- DCKVNWZUADLDEH-UHFFFAOYSA-N sec-butyl acetate Chemical compound CCC(C)OC(C)=O DCKVNWZUADLDEH-UHFFFAOYSA-N 0.000 description 1
- 210000002027 skeletal muscle Anatomy 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000007901 soft capsule Substances 0.000 description 1
- 208000010110 spontaneous platelet aggregation Diseases 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 239000003206 sterilizing agent Substances 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 125000004434 sulfur atom Chemical group 0.000 description 1
- 239000002511 suppository base Substances 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 230000002195 synergetic effect Effects 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 238000007910 systemic administration Methods 0.000 description 1
- 150000005621 tetraalkylammonium salts Chemical class 0.000 description 1
- 125000000383 tetramethylene group Chemical group [H]C([H])([*:1])C([H])([H])C([H])([H])C([H])([H])[*:2] 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 210000001541 thymus gland Anatomy 0.000 description 1
- 230000017423 tissue regeneration Effects 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 150000003626 triacylglycerols Chemical class 0.000 description 1
- 125000002221 trityl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C([*])(C1=C(C(=C(C(=C1[H])[H])[H])[H])[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 230000005740 tumor formation Effects 0.000 description 1
- 230000024883 vasodilation Effects 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 229920001567 vinyl ester resin Polymers 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 125000005023 xylyl group Chemical group 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C53/00—Saturated compounds having only one carboxyl group bound to an acyclic carbon atom or hydrogen
- C07C53/132—Saturated compounds having only one carboxyl group bound to an acyclic carbon atom or hydrogen containing rings
- C07C53/134—Saturated compounds having only one carboxyl group bound to an acyclic carbon atom or hydrogen containing rings monocyclic
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/557—Eicosanoids, e.g. leukotrienes or prostaglandins
- A61K31/5575—Eicosanoids, e.g. leukotrienes or prostaglandins having a cyclopentane, e.g. prostaglandin E2, prostaglandin F2-alpha
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Physical Education & Sports Medicine (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Rheumatology (AREA)
- Epidemiology (AREA)
- Hematology (AREA)
- Diabetes (AREA)
- Neurology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
Description
下付1:13,14-不飽和-15-OH
下付2:5,6-および13,14-ジ不飽和-15-OH
下付3:5,6-、13,14-および17,18-トリ不飽和-15-OH。
本発明は、哺乳類対象における幹細胞の増殖および/または分化を調節するための方法に関するもので、該方法はその必要のある患者に、有効量のプロスタグランジン化合物を投与することを含む。
本明細書において用いるプロスタグランジンン化合物の命名は、上記式(A)に示したプロスタン酸の番号付け系に基づく。
Aは、-CH3、または-CH2OH、-COCH2OH、-COOHまたはそれらの官能性誘導体であり;
Bは、単結合、-CH2-CH2-、-CH=CH-、-C≡C-、-CH2-CH2-CH2-、-CH=CH-CH2-、-CH2-CH=CH-、-C≡C-CH2-または-CH2-C≡C-であり;
Zは、
ここで、R4およびR5は、水素、ヒドロキシ、ハロゲン、低級アルキル、低級アルコキシまたはヒドロキシ(低級)アルキルであり、R4およびR5が同時にヒドロキシおよび低級アルコキシであることはなく;
R1は、非置換、またはハロゲン、アルキル、ヒドロキシ、オキソ、アリールまたは複素環基により置換された、二価の飽和または不飽和の低〜中級の脂肪族炭化水素残基であり、脂肪族炭化水素中の少なくとも1つの炭素原子は所望により酸素、窒素または硫黄により置換されており;そして
Raは、非置換、またはハロゲン、オキソ、ヒドロキシ、低級アルキル、低級アルコキシ、低級アルカノイルオキシ、シクロ(低級)アルキル、シクロ(低級)アルキルオキシ、アリール、アリールオキシ、複素環基または複素環オキシ基によって置換された、飽和または不飽和の低〜中級の脂肪族炭化水素残基;低級アルコキシ;低級アルカノイルオキシ;シクロ(低級)アルキル;シクロ(低級)アルキルオキシ;アリール;アリールオキシ;複素環基;複素環オキシ基である]。
Aは、-CH3、または-CH2OH、-COCH2OH、-COOHまたはそれらの官能性誘導体であり;
Bは、単結合、-CH2-CH2-、-CH=CH-、-C≡C-、-CH2-CH2-CH2-、-CH=CH-CH2-、-CH2-CH=CH-、-C≡C-CH2-または-CH2-C≡C-であり;
Zは、
ここで、R4およびR5は、水素、ヒドロキシ、ハロゲン、低級アルキル、低級アルコキシまたはヒドロキシ(低級)アルキルであり、R4およびR5が同時にヒドロキシおよび低級アルコキシであることはなく;
X1およびX2は、水素、低級アルキル、またはハロゲンであり;
R1は、非置換、またはハロゲン、アルキル、ヒドロキシ、オキソ、アリールまたは複素環基により置換された、二価の飽和または不飽和の低〜中級の脂肪族炭化水素残基であり、脂肪族炭化水素中の少なくとも1つの炭素原子は所望により酸素、窒素または硫黄により置換されており;
R2は、単結合または低級アルキレンであり;そして
R3は、低級アルキル、低級アルコキシ、低級アルカノイルオキシ、シクロ(低級)アルキル、シクロ(低級)アルキルオキシ、アリール、アリールオキシ、複素環基または複素環オキシ基である]。
-CH2-CH2-CH2-CH2-CH2-CH2-、
-CH2-CH=CH-CH2-CH2-CH2-、
-CH2-CH2-CH2-CH2-CH=CH-、
-CH2-C≡C-CH2-CH2-CH2-、
-CH2-CH2-CH2-CH2-O-CH2-、
-CH2-CH=CH-CH2-O-CH2-、
-CH2-C≡C-CH2-O-CH2-、
-CH2-CH2-CH2-CH2-CH2-CH2-CH2-、
-CH2-CH=CH-CH2-CH2-CH2-CH2-、
-CH2-CH2-CH2-CH2-CH2-CH=CH-、
-CH2-C≡C-CH2-CH2-CH2-CH2-、
-CH2-CH2-CH2-CH2-CH2-CH(CH3)-CH2-、
-CH2-CH2-CH2-CH2-CH(CH3)-CH2-、
-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-、
-CH2-CH=CH-CH2-CH2-CH2-CH2-CH2-、
-CH2-CH2-CH2-CH2-CH2-CH2-CH=CH-、
-CH2-C≡C-CH2-CH2-CH2-CH2-CH2-、および
-CH2-CH2-CH2-CH2-CH2-CH2-CH(CH3)-CH2-。
X1'およびX2'は、水素、低級アルキル、またはハロゲンであり;
Yは、
ここで、R4'およびR5'は、水素、ヒドロキシ、ハロゲン、低級アルキル、低級アルコキシまたはヒドロキシ(低級)アルキルであり、R4'およびR5'が同時にヒドロキシおよび低級アルコキシであることはなく、
R1は、非置換、またはハロゲン、アルキル、ヒドロキシ、オキソ、アリールまたは複素環基により置換された、二価の飽和または不飽和の低〜中級の脂肪族炭化水素残基であり、脂肪族炭化水素中の少なくとも1つの炭素原子は所望により酸素、窒素または硫黄により置換されており;
R2'は、非置換、またはハロゲン、オキソ、ヒドロキシ、低級アルキル、低級アルコキシ、低級アルカノイルオキシ、シクロ(低級)アルキル、シクロ(低級)アルキルオキシ、アリール、アリールオキシ、複素環基または複素環オキシ基により置換された、飽和または不飽和の低〜中級の脂肪族炭化水素残基;低級アルコキシ;低級アルカノイルオキシ;シクロ(低級)アルキル;シクロ(低級)アルキルオキシ;アリール;アリールオキシ;複素環基;複素環オキシ基であり;
R3'は水素、低級アルキル、シクロ(低級)アルキル、アリールまたは複素環基である]。
障害のあるニューロンに対する化合物 A (11-デオキシ-13,14-ジヒドロ-15-ケト-16,16-ジフルオロ-PGE1)の効果を試験した。1-メチル-4-フェニル-1,2,3,6-テトラヒドロピリジンハイドロクロライド(MPTP)を、2日間の投薬期間中(実験1日目および2日目)、およそ3時間の間隔で1日に4回、15 mg/kg/投薬を10週齢のC57BL/6 雄マウスに腹腔内投与し、脳内のドーパミン作動性ニューロンを破壊した。最終のMPTP投与が終わった翌日(3日目)に、数匹のMPTP処置マウスを屠殺し、線条体においてチロシンヒドロキシラーゼ(TH)-陽性免疫染色された繊維面積を計測することにより、変性の重症度および黒質線条体ドーパミン作動性ニューロンの喪失を評価した。他のMPTP処置マウスは、最終のMPTP投与が終わった翌日から開始して5日間(3日から7日)、1日に2回、化合物 A (11-デオキシ-13,14-ジヒドロ-15-ケト-16,16-ジフルオロ-PGE1)またはビヒクルを経口投与した。該マウスを、化合物 A またはビヒクルの最終の投与が終わった翌日(8日目)に断頭し、その全脳を頭蓋骨の切断により取出し、ブアン液(pH3.5−4.0)に入れた。線条体(ブレグマの前方0.74 mm)および黒質(ブレグマの後方3.08 mm)の位置での該脳切片を切り取った。脱水後に、この薄い切片のパラフィン埋包を行った。切片(約6 μmの厚み)を、ブレグマ0.74 mmおよびブレグマ−3.08 mm部分の薄い切片の各々に調製し、該切片をTH免疫染色に使用した。ブレグマ−3.08 mm部分の右側の黒質緻密部(SNC)においてTH-陽性免疫染色された細胞数を、×20顕微鏡対物レンズを備えた光学顕微鏡OLYMPUS BH-2 (Olympus Corp.)を用いて目視観測により計測した。線条体においてTH-陽性免疫染色された繊維面積を測定するために、×40顕微鏡対物レンズを備えた光学顕微鏡OLYMPUS BH-2 (Olympus Corp.)により得たブレグマ 0.74 mm部分の右側の尾状核被殻(CPu)においてTH-陽性免疫染色された繊維の画像を、OLYMPUS MCD-350を介してコンピューターに取り込み、そして5 μm2よりも大きいこのTH-陽性の繊維面積を画像分析機器 Win ROOF (V5.6、Mitani Corp.)を用いて計測し、1 mm2の面積に換算して表した。
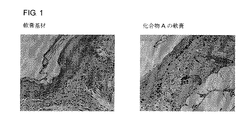
切除創の治癒に対する化合物 A (11-デオキシ-13,14-ジヒドロ-15-ケト-16,16-ジフルオロ-PGE1)の効果を試験した。12週齢の雌の糖尿病マウス(BKS.Cg-+Leprdb/+Leprdb/Jcl)の背中に全層厚切除創(1.5 x 1.5 cm)を作成した。切除創を有孔フィルムドレッシング剤にて被覆した。各試験用軟膏を、21G 皮下注射用の針を取付けた1mLの使い捨てポリプロピレンシリンジ内に入れて、この試験用軟膏(0.1 mL)を、切除創を被覆するフィルムドレッシング剤に皮下注射針を突き刺して該切除創に適用した。該適用は、該切除創を作成したその日から開始して21日間、1日に1回行った;該切除創を作成した日を1日目と規定した。組織学的試験のために、該切除創を含む皮膚を、各試験用軟膏で6日間処置した動物より得て、増殖細胞のマーカータンパク質としてKi67に対する抗体を用いる免疫染色に供した。適用前(1日目)ならびに投与6、8、11、13、15、18、20および22日に、各切除創の外郭をトレースした。トレースした切除創の面積を、面積-線計器にて計測した。各測定日の該創傷面積を、1日目を100%とした該創傷領域の比率として表し、該創傷面積(%)としての面積−時間曲線(AUC)を台形法により計算した。
化合物 A (11-デオキシ-13,14-ジヒドロ-15-ケト-16,16-ジフルオロ-PGE1)の間葉幹細胞の骨芽細胞分化に対する効果を試験した。
方法
ヒト骨髄ドナーサンプルを得て、該試験のために間葉幹細胞 (MSC)の産生を開始した。次いで、該MSCを、組織培養フラスコ中で増殖させた。使用するまでDMSO中で−20℃にて凍結保存した化合物 A を、終濃度が各ウェル中に5nM、10nM、および50nMとなるように培地に希釈した。骨芽細胞の分化に対する化合物 A の効果を決定するために、最初にMSC(1 x 106/ml)を24ウェルプレート内の培養培地中で48時間培養した。該細胞を成長表面(growth surface)に接着させた後、該培地をそっと取り除き、各化合物 A の希釈物(100 μl)を、4ウェル(4 replicate wells)に添加した。その後、骨芽細胞培養培地(0.9ml)を加え、該細胞をインキュベートした。
図2は、AP-PEおよびOC-PEの双方を用いて検出した場合の化合物 A の骨芽細胞の分化に対する効果を示す。図2は、平均蛍光強度を示す。AP-PE マーカーは、化合物 A の投薬量を増加させると、50mMまでAPが増加したことを示した。バックグラウンドまたはビヒクルコントロールに対して得られたこの増加は、上記のとおりである。そのため、化合物 A は、MSCに由来する骨芽細胞分化の刺激を示すアルカリフォスファタ−ゼの蛍光強度において相乗作用をもたらす。
Claims (24)
- 哺乳類対象の幹細胞の増殖および/または分化を調節するための医薬組成物を製造するための、下記一般式(I)により表されるプロスタグランジンン化合物の使用:
Aは、-CH3、または-CH2OH、-COCH2OH、-COOHまたはそれらの官能性誘導体であり;
Bは、単結合、-CH2-CH2-、-CH=CH-、-C≡C-、-CH2-CH2-CH2-、-CH=CH-CH2-、-CH2-CH=CH-、-C≡C-CH2-または-CH2-C≡C-であり;
Zは、
ここでR4およびR5は、水素、ヒドロキシ、ハロゲン、低級アルキル、低級アルコキシまたはヒドロキシ(低級)アルキルであり、R4およびR5が同時にヒドロキシおよび低級アルコキシであることはなく;
R1は、非置換、またはハロゲン、アルキル、ヒドロキシ、オキソ、アリールまたは複素環基により置換された、二価の飽和または不飽和の低〜中級の脂肪族炭化水素残基であり、脂肪族炭化水素中の少なくとも1つの炭素原子は所望により酸素、窒素または硫黄により置換されており;そして
Raは、非置換、またはハロゲン、オキソ、ヒドロキシ、低級アルキル、低級アルコキシ、低級アルカノイルオキシ、シクロ(低級)アルキル、シクロ(低級)アルキルオキシ、アリール、アリールオキシ、複素環基または複素環オキシ基により置換された、飽和または不飽和の低〜中級の脂肪族炭化水素残基;低級アルコキシ;低級アルカノイルオキシ;シクロ(低級)アルキル;シクロ(低級)アルキルオキシ;アリール;アリールオキシ;複素環基;複素環オキシ基である]。 - 哺乳類対象の幹細胞の増殖および/または分化を調節するための医薬組成物を製造するための、下記一般式(I)により表されるプロスタグランジンン化合物の使用:
Aは、-CH3、または-CH2OH、-COCH2OH、-COOHまたはそれらの官能性誘導体であり;
Bは、単結合、-CH2-CH2-、-CH=CH-、-C≡C-、-CH2-CH2-CH2-、-CH=CH-CH2-、-CH2-CH=CH-、-C≡C-CH2-または-CH2-C≡C-であり;
Zは、
ここでR4およびR5は、水素、ヒドロキシ、ハロゲン、低級アルキル、低級アルコキシまたはヒドロキシ(低級)アルキルであり、R4およびR5が同時にヒドロキシおよび低級アルコキシであることはなく;
R1は、非置換、またはハロゲン、アルキル、ヒドロキシ、オキソ、アリールまたは複素環基により置換された、二価の飽和または不飽和の低〜中級の脂肪族炭化水素残基であり、脂肪族炭化水素中の少なくとも1つの炭素原子は所望により酸素、窒素または硫黄により置換されており;そして
Raは、非置換、またはハロゲン、オキソ、ヒドロキシ、低級アルキル、低級アルコキシ、低級アルカノイルオキシ、シクロ(低級)アルキル、シクロ(低級)アルキルオキシ、アリール、アリールオキシ、複素環基または複素環オキシ基により置換された、飽和または不飽和の低〜中級の脂肪族炭化水素残基;低級アルコキシ;低級アルカノイルオキシ;シクロ(低級)アルキル;シクロ(低級)アルキルオキシ;アリール;アリールオキシ;複素環基;複素環オキシ基である]
ここで該調節は、該組成物を該幹細胞と接触させることにより行われる。 - 該組成物はイン・ビトロまたはエキソ・ビボにおいて幹細胞と接触される、請求項2記載の使用。
- 該幹細胞がヒト起源幹細胞の幹細胞である、請求項1-3いずれか一項記載の使用。
- 該幹細胞が前駆細胞である、請求項1-3いずれか一項記載の使用。
- 該幹細胞が、胚の幹細胞、体細胞の幹細胞またはその組合せ物である、請求項1-3いずれか一項記載の使用。
- 該プロスタグランジン化合物が、16-モノまたはジハロゲン-プロスタグランジン化合物である、請求項1-3いずれか一項記載の使用。
- 該プロスタグランジン化合物が、15-ケト-プロスタグランジン化合物である、請求項1-3いずれか一項記載の使用。
- 該プロスタグランジン化合物が、13,14-ジヒドロ-16-モノまたはジハロゲン-プロスタグランジン化合物である、請求項1-3いずれか一項記載の使用。
- 該プロスタグランジン化合物が、13,14-ジヒドロ-15-ケト-プロスタグランジン化合物である、請求項1-3いずれか一項記載の使用。
- 該プロスタグランジン化合物が、13,14-ジヒドロ-15-ケト-16-モノまたはジハロゲン-プロスタグランジン化合物である、請求項1-3いずれか一項記載の使用。
- 該プロスタグランジン化合物が、13,14-ジヒドロ-16-モノまたはジフルオロ-プロスタグランジン化合物である、請求項1-3いずれか一項記載の使用。
- 該プロスタグランジン化合物が、15-ケト-16-モノまたはジフルオロ-プロスタグランジン化合物である、請求項1-3いずれか一項記載の使用。
- 該プロスタグランジン化合物が、13,14-ジヒドロ-15-ケト-16-モノまたはジフルオロ-プロスタグランジン化合物である、請求項1-3いずれか一項記載の使用。
- 該プロスタグランジン化合物が、13,14-ジヒドロ-16-モノまたはジハロゲン-プロスタグランジンE化合物である、請求項1-3いずれか一項記載の使用。
- 該プロスタグランジン化合物が、15-ケト-16-モノまたはジハロゲン-プロスタグランジンE化合物である、請求項1-3いずれか一項記載の使用。
- 該プロスタグランジン化合物が、13,14-ジヒドロ-15-ケト-16-モノまたはジハロゲン-プロスタグランジンE化合物である、請求項1-3いずれか一項記載の使用。
- 該プロスタグランジン化合物が、13,14-ジヒドロ-16,16-ジフルオロ-プロスタグランジンE1化合物である、請求項1-3いずれか一項記載の使用。
- 該プロスタグランジン化合物が、13,14-ジヒドロ-15-ケト-プロスタグランジンE1化合物である、請求項1-3いずれか一項記載の使用。
- 該プロスタグランジン化合物が、11-デオキシ-13,14-ジヒドロ-15-ケト-16,16-ジフルオロ-プロスタグランジンE1化合物である、請求項1-3いずれか一項記載の使用。
- 下記一般式(I)により表されるプロスタグランジンン化合物を含む、哺乳類対象において幹細胞の増殖および/または分化を調節するための組成物:
Aは、-CH3、または-CH2OH、-COCH2OH、-COOHまたはそれらの官能性誘導体であり;
Bは、単結合、-CH2-CH2-、-CH=CH-、-C≡C-、-CH2-CH2-CH2-、-CH=CH-CH2-、-CH2-CH=CH-、-C≡C-CH2-または-CH2-C≡C-であり;
Zは、
ここでR4およびR5は、水素、ヒドロキシ、ハロゲン、低級アルキル、低級アルコキシまたはヒドロキシ(低級)アルキルであり、R4およびR5が同時にヒドロキシおよび低級アルコキシであることはなく;
R1は、非置換、またはハロゲン、アルキル、ヒドロキシ、オキソ、アリールまたは複素環基により置換された、二価の飽和または不飽和の低〜中級の脂肪族炭化水素残基であり、脂肪族炭化水素中の少なくとも1つの炭素原子は所望により酸素、窒素または硫黄により置換されており;そして
Raは、非置換、またはハロゲン、オキソ、ヒドロキシ、低級アルキル、低級アルコキシ、低級アルカノイルオキシ、シクロ(低級)アルキル、シクロ(低級)アルキルオキシ、アリール、アリールオキシ、複素環基または複素環オキシ基により置換された、飽和または不飽和の低〜中級の脂肪族炭化水素残基;低級アルコキシ;低級アルカノイルオキシ;シクロ(低級)アルキル;シクロ(低級)アルキルオキシ;アリール;アリールオキシ;複素環基;複素環オキシ基である] - 下記一般式(I)により表されるプロスタグランジンン化合物を含む、哺乳類対象の幹細胞の増殖および/または分化を調節するための組成物:
Aは、-CH3、または-CH2OH、-COCH2OH、-COOHまたはそれらの官能性誘導体であり;
Bは、単結合、-CH2-CH2-、-CH=CH-、-C≡C-、-CH2-CH2-CH2-、-CH=CH-CH2-、-CH2-CH=CH-、-C≡C-CH2-または-CH2-C≡C-であり;
Zは、
ここでR4およびR5は、水素、ヒドロキシ、ハロゲン、低級アルキル、低級アルコキシまたはヒドロキシ(低級)アルキルであり、R4およびR5が同時にヒドロキシおよび低級アルコキシであることはなく;
R1は、非置換、またはハロゲン、アルキル、ヒドロキシ、オキソ、アリールまたは複素環基により置換された、二価の飽和または不飽和の低〜中級の脂肪族炭化水素残基であり、脂肪族炭化水素中の少なくとも1つの炭素原子は所望により酸素、窒素または硫黄により置換されており;そして
Raは、非置換、またはハロゲン、オキソ、ヒドロキシ、低級アルキル、低級アルコキシ、低級アルカノイルオキシ、シクロ(低級)アルキル、シクロ(低級)アルキルオキシ、アリール、アリールオキシ、複素環基または複素環オキシ基により置換された、飽和または不飽和の低〜中級の脂肪族炭化水素残基;低級アルコキシ;低級アルカノイルオキシ;シクロ(低級)アルキル;シクロ(低級)アルキルオキシ;アリール;アリールオキシ;複素環基;複素環オキシ基である]
ここで、該調節は該組成物を該幹細胞と接触させることにより行われる。 - 哺乳類対象における幹細胞の増殖および/または分化を調節するための方法であって、下記一般式(I)により表される有効量のプロスタグランジン化合物をその必要のある患者に投与することを含む方法:
Aは、-CH3、または-CH2OH、-COCH2OH、-COOHまたはそれらの官能性誘導体であり;
Bは、単結合、-CH2-CH2-、-CH=CH-、-C≡C-、-CH2-CH2-CH2-、-CH=CH-CH2-、-CH2-CH=CH-、-C≡C-CH2-または-CH2-C≡C-であり;
Zは、
ここでR4およびR5は、水素、ヒドロキシ、ハロゲン、低級アルキル、低級アルコキシまたはヒドロキシ(低級)アルキルであり、R4およびR5が同時にヒドロキシおよび低級アルコキシであることはなく;
R1は、非置換、またはハロゲン、アルキル、ヒドロキシ、オキソ、アリールまたは複素環基により置換された、二価の飽和または不飽和の低〜中級の脂肪族炭化水素残基であり、脂肪族炭化水素中の少なくとも1つの炭素原子は所望により酸素、窒素または硫黄により置換されており;そして
Raは、非置換、またはハロゲン、オキソ、ヒドロキシ、低級アルキル、低級アルコキシ、低級アルカノイルオキシ、シクロ(低級)アルキル、シクロ(低級)アルキルオキシ、アリール、アリールオキシ、複素環基または複素環オキシ基により置換された、飽和または不飽和の低〜中級の脂肪族炭化水素残基;低級アルコキシ;低級アルカノイルオキシ;シクロ(低級)アルキル;シクロ(低級)アルキルオキシ;アリール;アリールオキシ;複素環基;複素環オキシ基である]。 - 哺乳類対象の幹細胞の増殖および/または分化を調節するための方法であって、下記一般式(I)により表される有効量のプロスタグランジン化合物を該幹細胞と接触させることを含む方法:
Aは、-CH3、または-CH2OH、-COCH2OH、-COOHまたはそれらの官能性誘導体であり;
Bは、単結合、-CH2-CH2-、-CH=CH-、-C≡C-、-CH2-CH2-CH2-、-CH=CH-CH2-、-CH2-CH=CH-、-C≡C-CH2-または-CH2-C≡C-であり;
Zは、
ここでR4およびR5は、水素、ヒドロキシ、ハロゲン、低級アルキル、低級アルコキシまたはヒドロキシ(低級)アルキルであり、R4およびR5が同時にヒドロキシおよび低級アルコキシであることはなく;
R1は、非置換、またはハロゲン、アルキル、ヒドロキシ、オキソ、アリールまたは複素環基により置換された、二価の飽和または不飽和の低〜中級の脂肪族炭化水素残基であり、脂肪族炭化水素中の少なくとも1つの炭素原子は所望により酸素、窒素または硫黄により置換されており;そして
Raは、非置換、またはハロゲン、オキソ、ヒドロキシ、低級アルキル、低級アルコキシ、低級アルカノイルオキシ、シクロ(低級)アルキル、シクロ(低級)アルキルオキシ、アリール、アリールオキシ、複素環基または複素環オキシ基により置換された、飽和または不飽和の低〜中級の脂肪族炭化水素残基;低級アルコキシ;低級アルカノイルオキシ;シクロ(低級)アルキル;シクロ(低級)アルキルオキシ;アリール;アリールオキシ;複素環基;複素環オキシ基である]。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US2971308P | 2008-02-19 | 2008-02-19 | |
| PCT/JP2009/053474 WO2009104807A1 (en) | 2008-02-19 | 2009-02-19 | Composition for modulating stem cell growth with prostaglandins |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2011512323A true JP2011512323A (ja) | 2011-04-21 |
| JP2011512323A5 JP2011512323A5 (ja) | 2015-03-05 |
Family
ID=40602552
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010533155A Ceased JP2011512323A (ja) | 2008-02-19 | 2009-02-19 | 幹細胞の成長を調節するための方法および組成物 |
Country Status (16)
| Country | Link |
|---|---|
| US (2) | US8871752B2 (ja) |
| EP (2) | EP2303278A1 (ja) |
| JP (1) | JP2011512323A (ja) |
| KR (1) | KR20100119803A (ja) |
| CN (2) | CN104248638A (ja) |
| AR (1) | AR073158A1 (ja) |
| AU (1) | AU2009216067B2 (ja) |
| BR (1) | BRPI0907831A2 (ja) |
| CA (1) | CA2715486A1 (ja) |
| IL (1) | IL207652A0 (ja) |
| MX (1) | MX2010009131A (ja) |
| NZ (1) | NZ587348A (ja) |
| RU (1) | RU2010138603A (ja) |
| TW (1) | TW200942614A (ja) |
| WO (1) | WO2009104807A1 (ja) |
| ZA (1) | ZA201006125B (ja) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010108028A2 (en) * | 2009-03-19 | 2010-09-23 | Fate Therapeutics, Inc. | Compositions comprising cyclic amp enhancers and/or ep ligands, and methods of preparing and using the same |
| US8569279B2 (en) | 2009-05-27 | 2013-10-29 | Sucampo Ag | Method for modulating claudin mediated functions |
| NZ596555A (en) * | 2009-05-27 | 2014-01-31 | Univ Osaka | Pharmaceutical composition comprising prostaglandin derivatives for use in modulating claudin mediated functions and in the treatment of dermatological disorders |
| KR101171912B1 (ko) | 2010-11-29 | 2012-08-07 | 기아자동차주식회사 | 밸브브릿지 일체형 가변 밸브 액츄에이터 |
| EP2785350B1 (en) | 2011-12-02 | 2018-05-02 | Fate Therapeutics, Inc. | Improved methods of treating ischemia |
| WO2013082243A1 (en) | 2011-12-02 | 2013-06-06 | Fate Therapeutics, Inc. | Enhanced stem cell composition |
| WO2014159679A1 (en) | 2013-03-12 | 2014-10-02 | The United States Of America, As Represented By The Secretary, Department Of Health & Human Services | Methods for using lubiprostone to absorb fluid from the subretinal space |
| WO2014150602A1 (en) | 2013-03-15 | 2014-09-25 | Fate Therapeutics, Inc. | Cell potency assay for therapeutic potential |
| US20140371304A1 (en) * | 2013-06-13 | 2014-12-18 | Sucampo Ag | Method for suppressing tumorigenicity of stem cells |
| AU2017225999B2 (en) * | 2016-03-04 | 2022-08-18 | The Board Of Trustees Of The Leland Stanford Junior University | Compositions and methods for muscle regeneration using prostaglandin E2 |
| US9918994B2 (en) | 2016-03-04 | 2018-03-20 | The Board Of Trustees Of The Leland Stanford Junior University | Compositions and methods for muscle regeneration using prostaglandin E2 |
| AU2018280264B2 (en) | 2017-06-09 | 2024-07-11 | Myoforte Therapeutics, Inc. | Compositions and methods for preventing or treating muscle conditions |
| RU2686718C1 (ru) * | 2018-03-12 | 2019-04-30 | Федеральное государственное бюджетное научное учреждение "Томский национальный исследовательский медицинский центр Российской академии наук" (Томский НИМЦ) | Средство, стимулирующее функции мезенхимальных клеток-предшественников in vitro |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006080549A2 (en) * | 2005-01-27 | 2006-08-03 | Sucampo Ag | Method and composition for treating central nervous system disorders |
| WO2007070964A1 (en) * | 2005-12-22 | 2007-06-28 | Es Cell International Pte Ltd | Direct differentiation of cardiomyocytes from human embryonic stem cells |
| WO2007112084A2 (en) * | 2006-03-24 | 2007-10-04 | Children's Medical Center Corporation | Method to modulate hematopoietic stem cell growth |
| JP2010519177A (ja) * | 2007-02-27 | 2010-06-03 | スキャンポ・アーゲー | ミトコンドリアを保護するための組成物および方法 |
| JP2010528642A (ja) * | 2007-06-05 | 2010-08-26 | クリスティーナ、ラジャラ | 胚幹細胞の培養処方および方法 |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5166174A (en) | 1987-01-28 | 1992-11-24 | K.K. Ueno Seiyaku Oyo Kenkyujo | Prostaglandins E and anti-ulcers containing same |
| CA1322749C (en) | 1987-01-28 | 1993-10-05 | Ryuzo Ueno | Prostaglandins of the d series, and tranquilizers and soporifics containing the same |
| US5221763A (en) | 1987-04-30 | 1993-06-22 | R-Tech Ueno, Ltd. | Prostaglandins of the F series |
| TW224942B (ja) | 1990-04-04 | 1994-06-11 | Adka Ueno Kk | |
| DE69213057T2 (de) * | 1991-03-14 | 1997-01-09 | Ueno Seiyaku Oyo Kenkyujo Kk | Stimulierung von Wundheilung mit 15-Keto-prostaglandinverbindungen |
| CA2150287C (en) | 1994-06-03 | 2004-08-10 | Ryuji Ueno | Agent for treating hepato-biliary diseases |
| US5703108A (en) * | 1996-02-28 | 1997-12-30 | Pfizer Inc. | Bone deposition by certain prostaglandin agonists |
| EP0857718B1 (en) | 1996-06-10 | 2002-08-14 | Sucampo AG | Endothelin antagonist |
| KR100788226B1 (ko) | 2000-03-24 | 2007-12-26 | 수캄포 아게 | 15-케토-프로스타글란딘 또는 이의 유도체를 포함하는세포자연사 억제 조성물 |
| JP4557288B2 (ja) * | 2005-01-28 | 2010-10-06 | アイシン・エィ・ダブリュ株式会社 | 画像認識装置及び画像認識方法、並びにそれを用いた位置特定装置、車両制御装置及びナビゲーション装置 |
| KR20140098857A (ko) | 2005-03-04 | 2014-08-08 | 수캄포 아게 | 말초 혈관 질환 치료를 위한 방법 및 조성물 |
| US20060281818A1 (en) | 2005-03-21 | 2006-12-14 | Sucampo Ag, North Carolina State University | Method for treating mucosal disorders |
| EP2094839B1 (en) | 2006-12-08 | 2020-02-05 | University of Rochester | Expansion of hematopoietic stem cells |
-
2009
- 2009-02-18 US US12/388,048 patent/US8871752B2/en not_active Expired - Fee Related
- 2009-02-19 RU RU2010138603/15A patent/RU2010138603A/ru not_active Application Discontinuation
- 2009-02-19 WO PCT/JP2009/053474 patent/WO2009104807A1/en active Application Filing
- 2009-02-19 CN CN201410464976.4A patent/CN104248638A/zh active Pending
- 2009-02-19 NZ NZ587348A patent/NZ587348A/en not_active IP Right Cessation
- 2009-02-19 AU AU2009216067A patent/AU2009216067B2/en not_active Ceased
- 2009-02-19 JP JP2010533155A patent/JP2011512323A/ja not_active Ceased
- 2009-02-19 TW TW098105222A patent/TW200942614A/zh unknown
- 2009-02-19 EP EP09712320A patent/EP2303278A1/en not_active Withdrawn
- 2009-02-19 MX MX2010009131A patent/MX2010009131A/es not_active Application Discontinuation
- 2009-02-19 AR ARP090100582A patent/AR073158A1/es unknown
- 2009-02-19 CN CN200980114702XA patent/CN102014921A/zh active Pending
- 2009-02-19 KR KR1020107021031A patent/KR20100119803A/ko not_active Application Discontinuation
- 2009-02-19 EP EP13178225.2A patent/EP2656845A1/en not_active Withdrawn
- 2009-02-19 CA CA2715486A patent/CA2715486A1/en not_active Abandoned
- 2009-02-19 BR BRPI0907831A patent/BRPI0907831A2/pt not_active IP Right Cessation
-
2010
- 2010-08-17 IL IL207652A patent/IL207652A0/en unknown
- 2010-08-27 ZA ZA2010/06125A patent/ZA201006125B/en unknown
-
2014
- 2014-09-16 US US14/487,153 patent/US20150005381A1/en not_active Abandoned
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006080549A2 (en) * | 2005-01-27 | 2006-08-03 | Sucampo Ag | Method and composition for treating central nervous system disorders |
| WO2007070964A1 (en) * | 2005-12-22 | 2007-06-28 | Es Cell International Pte Ltd | Direct differentiation of cardiomyocytes from human embryonic stem cells |
| WO2007112084A2 (en) * | 2006-03-24 | 2007-10-04 | Children's Medical Center Corporation | Method to modulate hematopoietic stem cell growth |
| JP2010519177A (ja) * | 2007-02-27 | 2010-06-03 | スキャンポ・アーゲー | ミトコンドリアを保護するための組成物および方法 |
| JP2010528642A (ja) * | 2007-06-05 | 2010-08-26 | クリスティーナ、ラジャラ | 胚幹細胞の培養処方および方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2656845A1 (en) | 2013-10-30 |
| NZ587348A (en) | 2012-04-27 |
| US8871752B2 (en) | 2014-10-28 |
| ZA201006125B (en) | 2011-05-25 |
| IL207652A0 (en) | 2010-12-30 |
| MX2010009131A (es) | 2010-12-06 |
| BRPI0907831A2 (pt) | 2017-04-11 |
| AR073158A1 (es) | 2010-10-20 |
| AU2009216067B2 (en) | 2014-02-13 |
| CN102014921A (zh) | 2011-04-13 |
| CA2715486A1 (en) | 2009-08-27 |
| WO2009104807A1 (en) | 2009-08-27 |
| AU2009216067A1 (en) | 2009-08-27 |
| RU2010138603A (ru) | 2012-03-27 |
| TW200942614A (en) | 2009-10-16 |
| KR20100119803A (ko) | 2010-11-10 |
| CN104248638A (zh) | 2014-12-31 |
| EP2303278A1 (en) | 2011-04-06 |
| US20150005381A1 (en) | 2015-01-01 |
| US20090209643A1 (en) | 2009-08-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8871752B2 (en) | Method for modulating stem cell growth | |
| JP2008291033A (ja) | 15−ケトプロスタグランジンを含む胆汁分泌促進剤組成物 | |
| JP2015205915A (ja) | 黄斑変性を処置するための方法および組成物 | |
| JP2017222708A (ja) | 統合失調症の処置方法 | |
| JP6641263B2 (ja) | 神経障害性疼痛の処置方法 | |
| JP2012528077A (ja) | クローディン媒介機能の調節および皮膚疾患の処置に使用するための、プロスタグランジン誘導体を含む医薬組成物 | |
| US20080207759A1 (en) | Method for protecting mitochondria | |
| JP2016521678A (ja) | 幹細胞の腫瘍形成能の抑制方法 | |
| US8569279B2 (en) | Method for modulating claudin mediated functions | |
| US20160120840A1 (en) | Method and composition for treating nonerosive reflux disease | |
| JP2014515004A (ja) | イオン輸送体の調節方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120217 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120217 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130730 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130919 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130927 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140130 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140916 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20141215 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20150115 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20150302 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150512 |
|
| A045 | Written measure of dismissal of application [lapsed due to lack of payment] |
Free format text: JAPANESE INTERMEDIATE CODE: A045 Effective date: 20150929 |