JP2010526857A - ジヨードチロニンを含んでなる新規な医薬組成物及びその治療的使用 - Google Patents
ジヨードチロニンを含んでなる新規な医薬組成物及びその治療的使用 Download PDFInfo
- Publication number
- JP2010526857A JP2010526857A JP2010507937A JP2010507937A JP2010526857A JP 2010526857 A JP2010526857 A JP 2010526857A JP 2010507937 A JP2010507937 A JP 2010507937A JP 2010507937 A JP2010507937 A JP 2010507937A JP 2010526857 A JP2010526857 A JP 2010526857A
- Authority
- JP
- Japan
- Prior art keywords
- day
- diiodothyronine
- iodothyronine
- active substance
- diabetes
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 239000008194 pharmaceutical composition Substances 0.000 title claims abstract description 27
- ZHSOTLOTTDYIIK-ZDUSSCGKSA-N (2S)-2-amino-3-[4-(4-hydroxyphenoxy)-3,5-diiodophenyl]propanoic acid Chemical compound IC1=CC(C[C@H](N)C(O)=O)=CC(I)=C1OC1=CC=C(O)C=C1 ZHSOTLOTTDYIIK-ZDUSSCGKSA-N 0.000 title description 4
- 230000001225 therapeutic effect Effects 0.000 title description 3
- ZHSOTLOTTDYIIK-UHFFFAOYSA-N 3,5-Diiodothyronine Chemical compound IC1=CC(CC(N)C(O)=O)=CC(I)=C1OC1=CC=C(O)C=C1 ZHSOTLOTTDYIIK-UHFFFAOYSA-N 0.000 claims abstract description 118
- CPCJBZABTUOGNM-UHFFFAOYSA-N 3',3-diiodothyronine Natural products IC1=CC(CC(N)C(O)=O)=CC=C1OC1=CC=C(O)C(I)=C1 CPCJBZABTUOGNM-UHFFFAOYSA-N 0.000 claims abstract description 51
- 239000013543 active substance Substances 0.000 claims abstract description 37
- CPCJBZABTUOGNM-LBPRGKRZSA-N 3,3'-diiodo-L-thyronine Chemical compound IC1=CC(C[C@H](N)C(O)=O)=CC=C1OC1=CC=C(O)C(I)=C1 CPCJBZABTUOGNM-LBPRGKRZSA-N 0.000 claims abstract description 26
- SXQVOFSDWXYIRP-ZDUSSCGKSA-N (2s)-2-azaniumyl-3-[4-(4-hydroxyphenoxy)-3-iodophenyl]propanoate Chemical compound IC1=CC(C[C@H](N)C(O)=O)=CC=C1OC1=CC=C(O)C=C1 SXQVOFSDWXYIRP-ZDUSSCGKSA-N 0.000 claims abstract description 24
- RUIUIJSMLKJUDC-ZDUSSCGKSA-N 3'-monoiodothyronine Chemical compound C1=CC(C[C@H](N)C(O)=O)=CC=C1OC1=CC=C(O)C(I)=C1 RUIUIJSMLKJUDC-ZDUSSCGKSA-N 0.000 claims abstract description 15
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 claims description 66
- 206010012601 diabetes mellitus Diseases 0.000 claims description 60
- 238000011282 treatment Methods 0.000 claims description 56
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 claims description 37
- 239000008103 glucose Substances 0.000 claims description 37
- 102000004877 Insulin Human genes 0.000 claims description 33
- 108090001061 Insulin Proteins 0.000 claims description 33
- 229940125396 insulin Drugs 0.000 claims description 33
- 229940088597 hormone Drugs 0.000 claims description 32
- 239000005556 hormone Substances 0.000 claims description 32
- 208000001072 type 2 diabetes mellitus Diseases 0.000 claims description 26
- 206010022489 Insulin Resistance Diseases 0.000 claims description 20
- 201000001421 hyperglycemia Diseases 0.000 claims description 20
- 208000008589 Obesity Diseases 0.000 claims description 19
- 239000003814 drug Substances 0.000 claims description 19
- 230000001476 alcoholic effect Effects 0.000 claims description 17
- 210000004003 subcutaneous fat Anatomy 0.000 claims description 13
- 208000032928 Dyslipidaemia Diseases 0.000 claims description 11
- 208000017170 Lipid metabolism disease Diseases 0.000 claims description 11
- 230000007812 deficiency Effects 0.000 claims description 11
- 230000007170 pathology Effects 0.000 claims description 11
- 238000007920 subcutaneous administration Methods 0.000 claims description 11
- 208000035484 Cellulite Diseases 0.000 claims description 10
- 206010033307 Overweight Diseases 0.000 claims description 10
- 206010049752 Peau d'orange Diseases 0.000 claims description 10
- 230000036232 cellulite Effects 0.000 claims description 10
- 208000030159 metabolic disease Diseases 0.000 claims description 10
- 201000001320 Atherosclerosis Diseases 0.000 claims description 9
- 208000035150 Hypercholesterolemia Diseases 0.000 claims description 9
- 230000002440 hepatic effect Effects 0.000 claims description 9
- 208000006575 hypertriglyceridemia Diseases 0.000 claims description 9
- 208000019423 liver disease Diseases 0.000 claims description 9
- 210000002374 sebum Anatomy 0.000 claims description 9
- 208000001319 vasomotor rhinitis Diseases 0.000 claims description 9
- 238000004519 manufacturing process Methods 0.000 claims description 8
- 239000000126 substance Substances 0.000 claims description 8
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 claims description 7
- 238000010521 absorption reaction Methods 0.000 claims description 6
- 230000008021 deposition Effects 0.000 claims description 6
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 4
- 230000001575 pathological effect Effects 0.000 claims description 4
- 208000020694 gallbladder disease Diseases 0.000 claims description 3
- 231100000245 skin permeability Toxicity 0.000 claims description 3
- VSWSDTLXDWESGZ-AWEZNQCLSA-N (2s)-3-[4-(4-hydroxyphenoxy)phenyl]-2-(iodoamino)propanoic acid Chemical compound C1=CC(C[C@@H](C(=O)O)NI)=CC=C1OC1=CC=C(O)C=C1 VSWSDTLXDWESGZ-AWEZNQCLSA-N 0.000 claims description 2
- 230000003178 anti-diabetic effect Effects 0.000 claims description 2
- 239000003472 antidiabetic agent Substances 0.000 claims description 2
- 230000029087 digestion Effects 0.000 claims description 2
- 230000002708 enhancing effect Effects 0.000 claims description 2
- 229940126701 oral medication Drugs 0.000 claims description 2
- 230000028327 secretion Effects 0.000 claims description 2
- 241000700159 Rattus Species 0.000 description 104
- 230000037396 body weight Effects 0.000 description 62
- 239000000902 placebo Substances 0.000 description 43
- 229940068196 placebo Drugs 0.000 description 43
- 230000000694 effects Effects 0.000 description 40
- 239000005495 thyroid hormone Substances 0.000 description 35
- 229940036555 thyroid hormone Drugs 0.000 description 35
- 241001465754 Metazoa Species 0.000 description 33
- AUYYCJSJGJYCDS-LBPRGKRZSA-N Thyrolar Chemical class IC1=CC(C[C@H](N)C(O)=O)=CC(I)=C1OC1=CC=C(O)C(I)=C1 AUYYCJSJGJYCDS-LBPRGKRZSA-N 0.000 description 31
- 239000008280 blood Substances 0.000 description 28
- 210000004369 blood Anatomy 0.000 description 28
- 239000000758 substrate Substances 0.000 description 24
- 241000700157 Rattus norvegicus Species 0.000 description 22
- 210000000577 adipose tissue Anatomy 0.000 description 21
- CZMRCDWAGMRECN-UHFFFAOYSA-N 2-{[3,4-dihydroxy-2,5-bis(hydroxymethyl)oxolan-2-yl]oxy}-6-(hydroxymethyl)oxane-3,4,5-triol Chemical compound OCC1OC(CO)(OC2OC(CO)C(O)C(O)C2O)C(O)C1O CZMRCDWAGMRECN-UHFFFAOYSA-N 0.000 description 20
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 20
- 210000003205 muscle Anatomy 0.000 description 19
- 238000005259 measurement Methods 0.000 description 17
- 235000012631 food intake Nutrition 0.000 description 16
- 230000001965 increasing effect Effects 0.000 description 16
- 210000004027 cell Anatomy 0.000 description 15
- 229940079593 drug Drugs 0.000 description 15
- 230000037406 food intake Effects 0.000 description 15
- 230000007423 decrease Effects 0.000 description 14
- 150000002632 lipids Chemical class 0.000 description 14
- 210000004185 liver Anatomy 0.000 description 14
- 238000000034 method Methods 0.000 description 14
- 230000003647 oxidation Effects 0.000 description 14
- 238000007254 oxidation reaction Methods 0.000 description 14
- 210000003486 adipose tissue brown Anatomy 0.000 description 12
- 210000003470 mitochondria Anatomy 0.000 description 12
- 239000000203 mixture Substances 0.000 description 12
- 230000036470 plasma concentration Effects 0.000 description 12
- 238000013293 zucker diabetic fatty rat Methods 0.000 description 12
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 11
- 238000005831 deiodination reaction Methods 0.000 description 11
- 229930195712 glutamate Natural products 0.000 description 11
- 229940049920 malate Drugs 0.000 description 11
- BJEPYKJPYRNKOW-UHFFFAOYSA-N malic acid Chemical compound OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 11
- 235000020824 obesity Nutrition 0.000 description 11
- 230000010412 perfusion Effects 0.000 description 11
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 11
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 10
- 150000001720 carbohydrates Chemical class 0.000 description 10
- 235000014633 carbohydrates Nutrition 0.000 description 10
- 235000012000 cholesterol Nutrition 0.000 description 10
- 229940080817 rotenone Drugs 0.000 description 10
- 150000003626 triacylglycerols Chemical class 0.000 description 10
- 210000000227 basophil cell of anterior lobe of hypophysis Anatomy 0.000 description 9
- 230000012010 growth Effects 0.000 description 9
- JUVIOZPCNVVQFO-UHFFFAOYSA-N rotenone Natural products O1C2=C3CC(C(C)=C)OC3=CC=C2C(=O)C2C1COC1=C2C=C(OC)C(OC)=C1 JUVIOZPCNVVQFO-UHFFFAOYSA-N 0.000 description 9
- 210000001519 tissue Anatomy 0.000 description 9
- 238000011680 zucker rat Methods 0.000 description 9
- 102000006404 Mitochondrial Proteins Human genes 0.000 description 8
- 108010058682 Mitochondrial Proteins Proteins 0.000 description 8
- 239000000872 buffer Substances 0.000 description 8
- 230000000241 respiratory effect Effects 0.000 description 8
- 210000002027 skeletal muscle Anatomy 0.000 description 8
- 108010052832 Cytochromes Proteins 0.000 description 7
- 102000018832 Cytochromes Human genes 0.000 description 7
- 238000007707 calorimetry Methods 0.000 description 7
- 201000010099 disease Diseases 0.000 description 7
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 7
- 235000021588 free fatty acids Nutrition 0.000 description 7
- 210000003494 hepatocyte Anatomy 0.000 description 7
- 238000011534 incubation Methods 0.000 description 7
- 230000003914 insulin secretion Effects 0.000 description 7
- 230000002438 mitochondrial effect Effects 0.000 description 7
- 230000006686 mitochondrial oxygen consumption Effects 0.000 description 7
- 230000036284 oxygen consumption Effects 0.000 description 7
- XTWYTFMLZFPYCI-KQYNXXCUSA-N 5'-adenylphosphoric acid Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](COP(O)(=O)OP(O)(O)=O)[C@@H](O)[C@H]1O XTWYTFMLZFPYCI-KQYNXXCUSA-N 0.000 description 6
- XTWYTFMLZFPYCI-UHFFFAOYSA-N Adenosine diphosphate Natural products C1=NC=2C(N)=NC=NC=2N1C1OC(COP(O)(=O)OP(O)(O)=O)C(O)C1O XTWYTFMLZFPYCI-UHFFFAOYSA-N 0.000 description 6
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 6
- CXTATJFJDMJMIY-UHFFFAOYSA-N O-octanoylcarnitine Chemical compound CCCCCCCC(=O)OC(CC([O-])=O)C[N+](C)(C)C CXTATJFJDMJMIY-UHFFFAOYSA-N 0.000 description 6
- 230000003247 decreasing effect Effects 0.000 description 6
- 239000010432 diamond Substances 0.000 description 6
- 201000010063 epididymitis Diseases 0.000 description 6
- 210000000232 gallbladder Anatomy 0.000 description 6
- 239000008188 pellet Substances 0.000 description 6
- 102000004169 proteins and genes Human genes 0.000 description 6
- 108090000623 proteins and genes Proteins 0.000 description 6
- 230000002829 reductive effect Effects 0.000 description 6
- 230000036387 respiratory rate Effects 0.000 description 6
- 239000000725 suspension Substances 0.000 description 6
- MNULEGDCPYONBU-WMBHJXFZSA-N (1r,4s,5e,5'r,6'r,7e,10s,11r,12s,14r,15s,16s,18r,19s,20r,21e,25s,26r,27s,29s)-4-ethyl-11,12,15,19-tetrahydroxy-6'-[(2s)-2-hydroxypropyl]-5',10,12,14,16,18,20,26,29-nonamethylspiro[24,28-dioxabicyclo[23.3.1]nonacosa-5,7,21-triene-27,2'-oxane]-13,17,23-trio Polymers O([C@@H]1CC[C@@H](/C=C/C=C/C[C@H](C)[C@@H](O)[C@](C)(O)C(=O)[C@H](C)[C@@H](O)[C@H](C)C(=O)[C@H](C)[C@@H](O)[C@H](C)/C=C/C(=O)O[C@H]([C@H]2C)[C@H]1C)CC)[C@]12CC[C@@H](C)[C@@H](C[C@H](C)O)O1 MNULEGDCPYONBU-WMBHJXFZSA-N 0.000 description 5
- MNULEGDCPYONBU-DJRUDOHVSA-N (1s,4r,5z,5'r,6'r,7e,10s,11r,12s,14r,15s,18r,19r,20s,21e,26r,27s)-4-ethyl-11,12,15,19-tetrahydroxy-6'-(2-hydroxypropyl)-5',10,12,14,16,18,20,26,29-nonamethylspiro[24,28-dioxabicyclo[23.3.1]nonacosa-5,7,21-triene-27,2'-oxane]-13,17,23-trione Polymers O([C@H]1CC[C@H](\C=C/C=C/C[C@H](C)[C@@H](O)[C@](C)(O)C(=O)[C@H](C)[C@@H](O)C(C)C(=O)[C@H](C)[C@H](O)[C@@H](C)/C=C/C(=O)OC([C@H]2C)C1C)CC)[C@]12CC[C@@H](C)[C@@H](CC(C)O)O1 MNULEGDCPYONBU-DJRUDOHVSA-N 0.000 description 5
- XOMRRQXKHMYMOC-NRFANRHFSA-N (3s)-3-hexadecanoyloxy-4-(trimethylazaniumyl)butanoate Chemical compound CCCCCCCCCCCCCCCC(=O)O[C@@H](CC([O-])=O)C[N+](C)(C)C XOMRRQXKHMYMOC-NRFANRHFSA-N 0.000 description 5
- MNULEGDCPYONBU-YNZHUHFTSA-N (4Z,18Z,20Z)-22-ethyl-7,11,14,15-tetrahydroxy-6'-(2-hydroxypropyl)-5',6,8,10,12,14,16,28,29-nonamethylspiro[2,26-dioxabicyclo[23.3.1]nonacosa-4,18,20-triene-27,2'-oxane]-3,9,13-trione Polymers CC1C(C2C)OC(=O)\C=C/C(C)C(O)C(C)C(=O)C(C)C(O)C(C)C(=O)C(C)(O)C(O)C(C)C\C=C/C=C\C(CC)CCC2OC21CCC(C)C(CC(C)O)O2 MNULEGDCPYONBU-YNZHUHFTSA-N 0.000 description 5
- MNULEGDCPYONBU-VVXVDZGXSA-N (5e,5'r,7e,10s,11r,12s,14s,15r,16r,18r,19s,20r,21e,26r,29s)-4-ethyl-11,12,15,19-tetrahydroxy-6'-[(2s)-2-hydroxypropyl]-5',10,12,14,16,18,20,26,29-nonamethylspiro[24,28-dioxabicyclo[23.3.1]nonacosa-5,7,21-triene-27,2'-oxane]-13,17,23-trione Polymers C([C@H](C)[C@@H](O)[C@](C)(O)C(=O)[C@@H](C)[C@H](O)[C@@H](C)C(=O)[C@H](C)[C@@H](O)[C@H](C)/C=C/C(=O)OC([C@H]1C)[C@H]2C)\C=C\C=C\C(CC)CCC2OC21CC[C@@H](C)C(C[C@H](C)O)O2 MNULEGDCPYONBU-VVXVDZGXSA-N 0.000 description 5
- MNULEGDCPYONBU-UHFFFAOYSA-N 4-ethyl-11,12,15,19-tetrahydroxy-6'-(2-hydroxypropyl)-5',10,12,14,16,18,20,26,29-nonamethylspiro[24,28-dioxabicyclo[23.3.1]nonacosa-5,7,21-triene-27,2'-oxane]-13,17,23-trione Polymers CC1C(C2C)OC(=O)C=CC(C)C(O)C(C)C(=O)C(C)C(O)C(C)C(=O)C(C)(O)C(O)C(C)CC=CC=CC(CC)CCC2OC21CCC(C)C(CC(C)O)O2 MNULEGDCPYONBU-UHFFFAOYSA-N 0.000 description 5
- 210000002237 B-cell of pancreatic islet Anatomy 0.000 description 5
- 102000015779 HDL Lipoproteins Human genes 0.000 description 5
- 108010010234 HDL Lipoproteins Proteins 0.000 description 5
- 108020005497 Nuclear hormone receptor Proteins 0.000 description 5
- 229940072107 ascorbate Drugs 0.000 description 5
- 235000010323 ascorbic acid Nutrition 0.000 description 5
- 239000011668 ascorbic acid Substances 0.000 description 5
- 230000036757 core body temperature Effects 0.000 description 5
- 238000005265 energy consumption Methods 0.000 description 5
- 235000013305 food Nutrition 0.000 description 5
- 238000009472 formulation Methods 0.000 description 5
- 108020004017 nuclear receptors Proteins 0.000 description 5
- 102000006255 nuclear receptors Human genes 0.000 description 5
- 229930191479 oligomycin Natural products 0.000 description 5
- MNULEGDCPYONBU-AWJDAWNUSA-N oligomycin A Polymers O([C@H]1CC[C@H](/C=C/C=C/C[C@@H](C)[C@H](O)[C@@](C)(O)C(=O)[C@@H](C)[C@H](O)[C@@H](C)C(=O)[C@@H](C)[C@H](O)[C@@H](C)/C=C/C(=O)O[C@@H]([C@@H]2C)[C@@H]1C)CC)[C@@]12CC[C@H](C)[C@H](C[C@@H](C)O)O1 MNULEGDCPYONBU-AWJDAWNUSA-N 0.000 description 5
- 229910052760 oxygen Inorganic materials 0.000 description 5
- 230000037361 pathway Effects 0.000 description 5
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 4
- 201000004624 Dermatitis Diseases 0.000 description 4
- 238000003556 assay Methods 0.000 description 4
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 239000002775 capsule Substances 0.000 description 4
- 235000005911 diet Nutrition 0.000 description 4
- 230000037213 diet Effects 0.000 description 4
- 235000014113 dietary fatty acids Nutrition 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 229930195729 fatty acid Natural products 0.000 description 4
- 239000000194 fatty acid Substances 0.000 description 4
- 150000004665 fatty acids Chemical class 0.000 description 4
- 238000002955 isolation Methods 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- -1 oxaloacetate dinitrothiobenzoate Chemical compound 0.000 description 4
- 238000003127 radioimmunoassay Methods 0.000 description 4
- 230000008929 regeneration Effects 0.000 description 4
- 238000011069 regeneration method Methods 0.000 description 4
- 230000035806 respiratory chain Effects 0.000 description 4
- 230000029058 respiratory gaseous exchange Effects 0.000 description 4
- 230000004584 weight gain Effects 0.000 description 4
- 235000019786 weight gain Nutrition 0.000 description 4
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 3
- WHBMMWSBFZVSSR-UHFFFAOYSA-N 3-hydroxybutyric acid Chemical compound CC(O)CC(O)=O WHBMMWSBFZVSSR-UHFFFAOYSA-N 0.000 description 3
- VMEGFMNVSYVVOM-UHFFFAOYSA-N 6-decylubiquinone Chemical compound CCCCCCCCCCC1=C(C)C(=O)C(OC)=C(OC)C1=O VMEGFMNVSYVVOM-UHFFFAOYSA-N 0.000 description 3
- 230000002407 ATP formation Effects 0.000 description 3
- 102100022900 Actin, cytoplasmic 1 Human genes 0.000 description 3
- 108010085238 Actins Proteins 0.000 description 3
- 108090000365 Cytochrome-c oxidases Proteins 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- 102000005548 Hexokinase Human genes 0.000 description 3
- 108700040460 Hexokinases Proteins 0.000 description 3
- FBWADIKARMIWNM-UHFFFAOYSA-N N-3,5-dichloro-4-hydroxyphenyl-1,4-benzoquinone imine Chemical compound C1=C(Cl)C(O)=C(Cl)C=C1N=C1C=CC(=O)C=C1 FBWADIKARMIWNM-UHFFFAOYSA-N 0.000 description 3
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 3
- 102000011923 Thyrotropin Human genes 0.000 description 3
- 108010061174 Thyrotropin Proteins 0.000 description 3
- 239000007983 Tris buffer Substances 0.000 description 3
- 238000010171 animal model Methods 0.000 description 3
- 230000000692 anti-sense effect Effects 0.000 description 3
- 208000010668 atopic eczema Diseases 0.000 description 3
- 239000006285 cell suspension Substances 0.000 description 3
- 238000006243 chemical reaction Methods 0.000 description 3
- 230000001684 chronic effect Effects 0.000 description 3
- 230000000875 corresponding effect Effects 0.000 description 3
- 229940088598 enzyme Drugs 0.000 description 3
- 230000003834 intracellular effect Effects 0.000 description 3
- 210000002311 liver mitochondria Anatomy 0.000 description 3
- 230000002503 metabolic effect Effects 0.000 description 3
- 210000001256 muscle mitochondria Anatomy 0.000 description 3
- 235000021590 normal diet Nutrition 0.000 description 3
- 230000010627 oxidative phosphorylation Effects 0.000 description 3
- 210000000496 pancreas Anatomy 0.000 description 3
- 230000026731 phosphorylation Effects 0.000 description 3
- 238000006366 phosphorylation reaction Methods 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 238000003757 reverse transcription PCR Methods 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 239000006228 supernatant Substances 0.000 description 3
- 238000013268 sustained release Methods 0.000 description 3
- 239000012730 sustained-release form Substances 0.000 description 3
- WHBMMWSBFZVSSR-UHFFFAOYSA-M 3-hydroxybutyrate Chemical compound CC(O)CC([O-])=O WHBMMWSBFZVSSR-UHFFFAOYSA-M 0.000 description 2
- 208000002874 Acne Vulgaris Diseases 0.000 description 2
- UIFFUZWRFRDZJC-UHFFFAOYSA-N Antimycin A1 Natural products CC1OC(=O)C(CCCCCC)C(OC(=O)CC(C)C)C(C)OC(=O)C1NC(=O)C1=CC=CC(NC=O)=C1O UIFFUZWRFRDZJC-UHFFFAOYSA-N 0.000 description 2
- NQWZLRAORXLWDN-UHFFFAOYSA-N Antimycin-A Natural products CCCCCCC(=O)OC1C(C)OC(=O)C(NC(=O)c2ccc(NC=O)cc2O)C(C)OC(=O)C1CCCC NQWZLRAORXLWDN-UHFFFAOYSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 208000017667 Chronic Disease Diseases 0.000 description 2
- 102000000634 Cytochrome c oxidase subunit IV Human genes 0.000 description 2
- XUIIKFGFIJCVMT-GFCCVEGCSA-N D-thyroxine Chemical compound IC1=CC(C[C@@H](N)C(O)=O)=CC(I)=C1OC1=CC(I)=C(O)C(I)=C1 XUIIKFGFIJCVMT-GFCCVEGCSA-N 0.000 description 2
- QRLVDLBMBULFAL-UHFFFAOYSA-N Digitonin Natural products CC1CCC2(OC1)OC3C(O)C4C5CCC6CC(OC7OC(CO)C(OC8OC(CO)C(O)C(OC9OCC(O)C(O)C9OC%10OC(CO)C(O)C(OC%11OC(CO)C(O)C(O)C%11O)C%10O)C8O)C(O)C7O)C(O)CC6(C)C5CCC4(C)C3C2C QRLVDLBMBULFAL-UHFFFAOYSA-N 0.000 description 2
- 102000011687 Electron Transport Complex II Human genes 0.000 description 2
- 108010076322 Electron Transport Complex II Proteins 0.000 description 2
- 230000005856 abnormality Effects 0.000 description 2
- ZSLZBFCDCINBPY-ZSJPKINUSA-N acetyl-CoA Chemical compound O[C@@H]1[C@H](OP(O)(O)=O)[C@@H](COP(O)(=O)OP(O)(=O)OCC(C)(C)[C@@H](O)C(=O)NCCC(=O)NCCSC(=O)C)O[C@H]1N1C2=NC=NC(N)=C2N=C1 ZSLZBFCDCINBPY-ZSJPKINUSA-N 0.000 description 2
- 206010000496 acne Diseases 0.000 description 2
- 238000005273 aeration Methods 0.000 description 2
- 239000000556 agonist Substances 0.000 description 2
- UIFFUZWRFRDZJC-SBOOETFBSA-N antimycin A Chemical compound C[C@H]1OC(=O)[C@H](CCCCCC)[C@@H](OC(=O)CC(C)C)[C@H](C)OC(=O)[C@H]1NC(=O)C1=CC=CC(NC=O)=C1O UIFFUZWRFRDZJC-SBOOETFBSA-N 0.000 description 2
- PVEVXUMVNWSNIG-UHFFFAOYSA-N antimycin A3 Natural products CC1OC(=O)C(CCCC)C(OC(=O)CC(C)C)C(C)OC(=O)C1NC(=O)C1=CC=CC(NC=O)=C1O PVEVXUMVNWSNIG-UHFFFAOYSA-N 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 230000002051 biphasic effect Effects 0.000 description 2
- 238000009534 blood test Methods 0.000 description 2
- 239000007853 buffer solution Substances 0.000 description 2
- 230000015556 catabolic process Effects 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 239000013066 combination product Substances 0.000 description 2
- 229940127555 combination product Drugs 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 238000006731 degradation reaction Methods 0.000 description 2
- 238000003745 diagnosis Methods 0.000 description 2
- 235000015872 dietary supplement Nutrition 0.000 description 2
- UVYVLBIGDKGWPX-KUAJCENISA-N digitonin Chemical compound O([C@@H]1[C@@H]([C@]2(CC[C@@H]3[C@@]4(C)C[C@@H](O)[C@H](O[C@H]5[C@@H]([C@@H](O)[C@@H](O[C@H]6[C@@H]([C@@H](O[C@H]7[C@@H]([C@@H](O)[C@H](O)CO7)O)[C@H](O)[C@@H](CO)O6)O[C@H]6[C@@H]([C@@H](O[C@H]7[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O7)O)[C@@H](O)[C@@H](CO)O6)O)[C@@H](CO)O5)O)C[C@@H]4CC[C@H]3[C@@H]2[C@@H]1O)C)[C@@H]1C)[C@]11CC[C@@H](C)CO1 UVYVLBIGDKGWPX-KUAJCENISA-N 0.000 description 2
- UVYVLBIGDKGWPX-UHFFFAOYSA-N digitonine Natural products CC1C(C2(CCC3C4(C)CC(O)C(OC5C(C(O)C(OC6C(C(OC7C(C(O)C(O)CO7)O)C(O)C(CO)O6)OC6C(C(OC7C(C(O)C(O)C(CO)O7)O)C(O)C(CO)O6)O)C(CO)O5)O)CC4CCC3C2C2O)C)C2OC11CCC(C)CO1 UVYVLBIGDKGWPX-UHFFFAOYSA-N 0.000 description 2
- GNGACRATGGDKBX-UHFFFAOYSA-N dihydroxyacetone phosphate Chemical compound OCC(=O)COP(O)(O)=O GNGACRATGGDKBX-UHFFFAOYSA-N 0.000 description 2
- 230000037149 energy metabolism Effects 0.000 description 2
- 230000007613 environmental effect Effects 0.000 description 2
- DEFVIWRASFVYLL-UHFFFAOYSA-N ethylene glycol bis(2-aminoethyl)tetraacetic acid Chemical compound OC(=O)CN(CC(O)=O)CCOCCOCCN(CC(O)=O)CC(O)=O DEFVIWRASFVYLL-UHFFFAOYSA-N 0.000 description 2
- 238000005194 fractionation Methods 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 244000144993 groups of animals Species 0.000 description 2
- 230000013632 homeostatic process Effects 0.000 description 2
- QWPPOHNGKGFGJK-UHFFFAOYSA-N hypochlorous acid Chemical compound ClO QWPPOHNGKGFGJK-UHFFFAOYSA-N 0.000 description 2
- 208000003532 hypothyroidism Diseases 0.000 description 2
- 230000002989 hypothyroidism Effects 0.000 description 2
- 238000002513 implantation Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- QWTDNUCVQCZILF-UHFFFAOYSA-N isopentane Chemical compound CCC(C)C QWTDNUCVQCZILF-UHFFFAOYSA-N 0.000 description 2
- 210000003734 kidney Anatomy 0.000 description 2
- 230000037356 lipid metabolism Effects 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 210000005229 liver cell Anatomy 0.000 description 2
- 210000004379 membrane Anatomy 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 108020004999 messenger RNA Proteins 0.000 description 2
- 230000004060 metabolic process Effects 0.000 description 2
- 239000002207 metabolite Substances 0.000 description 2
- 230000008811 mitochondrial respiratory chain Effects 0.000 description 2
- 229930027945 nicotinamide-adenine dinucleotide Natural products 0.000 description 2
- BOPGDPNILDQYTO-NNYOXOHSSA-N nicotinamide-adenine dinucleotide Chemical compound C1=CCC(C(=O)N)=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](COP(O)(=O)OP(O)(=O)OC[C@@H]2[C@H]([C@@H](O)[C@@H](O2)N2C3=NC=NC(N)=C3N=C2)O)O1 BOPGDPNILDQYTO-NNYOXOHSSA-N 0.000 description 2
- 150000005830 nonesterified fatty acids Chemical class 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- 230000001590 oxidative effect Effects 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 238000002264 polyacrylamide gel electrophoresis Methods 0.000 description 2
- 230000002265 prevention Effects 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 238000011002 quantification Methods 0.000 description 2
- 239000003642 reactive oxygen metabolite Substances 0.000 description 2
- 235000020989 red meat Nutrition 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 208000008742 seborrheic dermatitis Diseases 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 230000002588 toxic effect Effects 0.000 description 2
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 2
- 239000001226 triphosphate Substances 0.000 description 2
- 235000011178 triphosphate Nutrition 0.000 description 2
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 2
- SXQVOFSDWXYIRP-UHFFFAOYSA-N 2-azaniumyl-3-[4-(4-hydroxyphenoxy)-3-iodophenyl]propanoate Chemical compound IC1=CC(CC(N)C(O)=O)=CC=C1OC1=CC=C(O)C=C1 SXQVOFSDWXYIRP-UHFFFAOYSA-N 0.000 description 1
- 108010030844 2-methylcitrate synthase Proteins 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 201000004384 Alopecia Diseases 0.000 description 1
- 206010003645 Atopy Diseases 0.000 description 1
- 206010003694 Atrophy Diseases 0.000 description 1
- 101100283604 Caenorhabditis elegans pigk-1 gene Proteins 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 208000001348 Chloracne Diseases 0.000 description 1
- 108010071536 Citrate (Si)-synthase Proteins 0.000 description 1
- 102000006732 Citrate synthase Human genes 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- 102000029816 Collagenase Human genes 0.000 description 1
- 108060005980 Collagenase Proteins 0.000 description 1
- 102100030497 Cytochrome c Human genes 0.000 description 1
- 108010075031 Cytochromes c Proteins 0.000 description 1
- NBSCHQHZLSJFNQ-GASJEMHNSA-N D-Glucose 6-phosphate Chemical compound OC1O[C@H](COP(O)(O)=O)[C@@H](O)[C@H](O)[C@H]1O NBSCHQHZLSJFNQ-GASJEMHNSA-N 0.000 description 1
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 1
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 1
- 101000666228 Danio rerio Thyroid hormone receptor alpha-A Proteins 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 102000008013 Electron Transport Complex I Human genes 0.000 description 1
- 108010089760 Electron Transport Complex I Proteins 0.000 description 1
- 206010015150 Erythema Diseases 0.000 description 1
- 208000010201 Exanthema Diseases 0.000 description 1
- 208000034826 Genetic Predisposition to Disease Diseases 0.000 description 1
- VFRROHXSMXFLSN-UHFFFAOYSA-N Glc6P Natural products OP(=O)(O)OCC(O)C(O)C(O)C(O)C=O VFRROHXSMXFLSN-UHFFFAOYSA-N 0.000 description 1
- 108010015776 Glucose oxidase Proteins 0.000 description 1
- 239000004366 Glucose oxidase Substances 0.000 description 1
- 102000017011 Glycated Hemoglobin A Human genes 0.000 description 1
- 102000000587 Glycerolphosphate Dehydrogenase Human genes 0.000 description 1
- 108010041921 Glycerolphosphate Dehydrogenase Proteins 0.000 description 1
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 1
- 206010020649 Hyperkeratosis Diseases 0.000 description 1
- 206010020850 Hyperthyroidism Diseases 0.000 description 1
- 102100034343 Integrase Human genes 0.000 description 1
- 208000001126 Keratosis Diseases 0.000 description 1
- YQEZLKZALYSWHR-UHFFFAOYSA-N Ketamine Chemical compound C=1C=CC=C(Cl)C=1C1(NC)CCCCC1=O YQEZLKZALYSWHR-UHFFFAOYSA-N 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- 102000016267 Leptin Human genes 0.000 description 1
- 108010092277 Leptin Proteins 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 102100040200 Mitochondrial uncoupling protein 2 Human genes 0.000 description 1
- 102100040216 Mitochondrial uncoupling protein 3 Human genes 0.000 description 1
- 239000004677 Nylon Substances 0.000 description 1
- 239000002033 PVDF binder Substances 0.000 description 1
- 206010051246 Photodermatosis Diseases 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- LCTONWCANYUPML-UHFFFAOYSA-M Pyruvate Chemical compound CC(=O)C([O-])=O LCTONWCANYUPML-UHFFFAOYSA-M 0.000 description 1
- 239000012162 RNA isolation reagent Substances 0.000 description 1
- 108010092799 RNA-directed DNA polymerase Proteins 0.000 description 1
- 101710141795 Ribonuclease inhibitor Proteins 0.000 description 1
- 229940122208 Ribonuclease inhibitor Drugs 0.000 description 1
- 102100037968 Ribonuclease inhibitor Human genes 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 241001303601 Rosacea Species 0.000 description 1
- 206010039710 Scleroderma Diseases 0.000 description 1
- 206010039792 Seborrhoea Diseases 0.000 description 1
- 206010039793 Seborrhoeic dermatitis Diseases 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 108010021111 Uncoupling Protein 2 Proteins 0.000 description 1
- 108010021098 Uncoupling Protein 3 Proteins 0.000 description 1
- 206010048214 Xanthoma Diseases 0.000 description 1
- 206010048215 Xanthomatosis Diseases 0.000 description 1
- 210000001015 abdomen Anatomy 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- WDJHALXBUFZDSR-UHFFFAOYSA-M acetoacetate Chemical compound CC(=O)CC([O-])=O WDJHALXBUFZDSR-UHFFFAOYSA-M 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- GFFGJBXGBJISGV-UHFFFAOYSA-N adenyl group Chemical class N1=CN=C2N=CNC2=C1N GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 1
- 210000001789 adipocyte Anatomy 0.000 description 1
- 210000000593 adipose tissue white Anatomy 0.000 description 1
- 239000011543 agarose gel Substances 0.000 description 1
- 238000000246 agarose gel electrophoresis Methods 0.000 description 1
- 230000000172 allergic effect Effects 0.000 description 1
- 231100000360 alopecia Toxicity 0.000 description 1
- 210000000709 aorta Anatomy 0.000 description 1
- 230000037444 atrophy Effects 0.000 description 1
- 235000015278 beef Nutrition 0.000 description 1
- 230000003542 behavioural effect Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 235000021028 berry Nutrition 0.000 description 1
- AFYNADDZULBEJA-UHFFFAOYSA-N bicinchoninic acid Chemical compound C1=CC=CC2=NC(C=3C=C(C4=CC=CC=C4N=3)C(=O)O)=CC(C(O)=O)=C21 AFYNADDZULBEJA-UHFFFAOYSA-N 0.000 description 1
- 230000002715 bioenergetic effect Effects 0.000 description 1
- 230000036760 body temperature Effects 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 238000007816 calorimetric assay Methods 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 229960002424 collagenase Drugs 0.000 description 1
- 235000009508 confectionery Nutrition 0.000 description 1
- 238000013270 controlled release Methods 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 238000002316 cosmetic surgery Methods 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 238000006114 decarboxylation reaction Methods 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- AAOVKJBEBIDNHE-UHFFFAOYSA-N diazepam Chemical compound N=1CC(=O)N(C)C2=CC=C(Cl)C=C2C=1C1=CC=CC=C1 AAOVKJBEBIDNHE-UHFFFAOYSA-N 0.000 description 1
- 229960003529 diazepam Drugs 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- AFABGHUZZDYHJO-UHFFFAOYSA-N dimethyl butane Natural products CCCC(C)C AFABGHUZZDYHJO-UHFFFAOYSA-N 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 230000000667 effect on insulin Effects 0.000 description 1
- 238000001378 electrochemiluminescence detection Methods 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 239000008393 encapsulating agent Substances 0.000 description 1
- 230000002124 endocrine Effects 0.000 description 1
- 210000000918 epididymis Anatomy 0.000 description 1
- 210000000981 epithelium Anatomy 0.000 description 1
- 231100000321 erythema Toxicity 0.000 description 1
- ZMMJGEGLRURXTF-UHFFFAOYSA-N ethidium bromide Chemical compound [Br-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CC)=C1C1=CC=CC=C1 ZMMJGEGLRURXTF-UHFFFAOYSA-N 0.000 description 1
- 229960005542 ethidium bromide Drugs 0.000 description 1
- 230000001610 euglycemic effect Effects 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 201000005884 exanthem Diseases 0.000 description 1
- 238000013265 extended release Methods 0.000 description 1
- 235000013861 fat-free Nutrition 0.000 description 1
- 230000004634 feeding behavior Effects 0.000 description 1
- 230000001605 fetal effect Effects 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 238000002695 general anesthesia Methods 0.000 description 1
- 230000009395 genetic defect Effects 0.000 description 1
- 239000003862 glucocorticoid Substances 0.000 description 1
- 230000009229 glucose formation Effects 0.000 description 1
- 230000010030 glucose lowering effect Effects 0.000 description 1
- 230000004153 glucose metabolism Effects 0.000 description 1
- 229940116332 glucose oxidase Drugs 0.000 description 1
- 235000019420 glucose oxidase Nutrition 0.000 description 1
- 108091005995 glycated hemoglobin Proteins 0.000 description 1
- 230000020169 heat generation Effects 0.000 description 1
- 235000009200 high fat diet Nutrition 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 125000004435 hydrogen atom Chemical class [H]* 0.000 description 1
- 206010021198 ichthyosis Diseases 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 239000012729 immediate-release (IR) formulation Substances 0.000 description 1
- 238000003119 immunoblot Methods 0.000 description 1
- 229940027941 immunoglobulin g Drugs 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 210000002660 insulin-secreting cell Anatomy 0.000 description 1
- 210000001596 intra-abdominal fat Anatomy 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 230000003780 keratinization Effects 0.000 description 1
- 229960003299 ketamine Drugs 0.000 description 1
- 229940039781 leptin Drugs 0.000 description 1
- NRYBAZVQPHGZNS-ZSOCWYAHSA-N leptin Chemical compound O=C([C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](N)CC(C)C)CCSC)N1CCC[C@H]1C(=O)NCC(=O)N[C@@H](CS)C(O)=O NRYBAZVQPHGZNS-ZSOCWYAHSA-N 0.000 description 1
- 231100001231 less toxic Toxicity 0.000 description 1
- 201000011486 lichen planus Diseases 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 230000004130 lipolysis Effects 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 238000002483 medication Methods 0.000 description 1
- 210000000713 mesentery Anatomy 0.000 description 1
- 230000006677 mitochondrial metabolism Effects 0.000 description 1
- 230000006705 mitochondrial oxidative phosphorylation Effects 0.000 description 1
- 230000006540 mitochondrial respiration Effects 0.000 description 1
- 210000000663 muscle cell Anatomy 0.000 description 1
- 230000009707 neogenesis Effects 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 230000001019 normoglycemic effect Effects 0.000 description 1
- 235000016709 nutrition Nutrition 0.000 description 1
- 230000035764 nutrition Effects 0.000 description 1
- 229920001778 nylon Polymers 0.000 description 1
- WWZKQHOCKIZLMA-UHFFFAOYSA-M octanoate Chemical compound CCCCCCCC([O-])=O WWZKQHOCKIZLMA-UHFFFAOYSA-M 0.000 description 1
- KQMZYOXOBSXMII-CECATXLMSA-N octanoyl-CoA Chemical compound O[C@@H]1[C@H](OP(O)(O)=O)[C@@H](COP(O)(=O)OP(O)(=O)OCC(C)(C)[C@@H](O)C(=O)NCCC(=O)NCCSC(=O)CCCCCCC)O[C@H]1N1C2=NC=NC(N)=C2N=C1 KQMZYOXOBSXMII-CECATXLMSA-N 0.000 description 1
- KLAKIAVEMQMVBT-UHFFFAOYSA-N p-hydroxy-phenacyl alcohol Natural products OCC(=O)C1=CC=C(O)C=C1 KLAKIAVEMQMVBT-UHFFFAOYSA-N 0.000 description 1
- MNBKLUUYKPBKDU-BBECNAHFSA-N palmitoyl-CoA Chemical compound O[C@@H]1[C@H](OP(O)(O)=O)[C@@H](COP(O)(=O)OP(O)(=O)OCC(C)(C)[C@@H](O)C(=O)NCCC(=O)NCCSC(=O)CCCCCCCCCCCCCCC)O[C@H]1N1C2=NC=NC(N)=C2N=C1 MNBKLUUYKPBKDU-BBECNAHFSA-N 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 229960001412 pentobarbital Drugs 0.000 description 1
- WEXRUCMBJFQVBZ-UHFFFAOYSA-N pentobarbital Chemical compound CCCC(C)C1(CC)C(=O)NC(=O)NC1=O WEXRUCMBJFQVBZ-UHFFFAOYSA-N 0.000 description 1
- 230000021715 photosynthesis, light harvesting Effects 0.000 description 1
- 230000037081 physical activity Effects 0.000 description 1
- 230000001766 physiological effect Effects 0.000 description 1
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 1
- 235000015277 pork Nutrition 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 210000003240 portal vein Anatomy 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 230000006318 protein oxidation Effects 0.000 description 1
- 230000005180 public health Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 206010037844 rash Diseases 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 210000000664 rectum Anatomy 0.000 description 1
- 230000008439 repair process Effects 0.000 description 1
- 239000003161 ribonuclease inhibitor Substances 0.000 description 1
- 201000004700 rosacea Diseases 0.000 description 1
- KQMZYOXOBSXMII-FFJUWABQSA-N s-[2-[3-[[4-[[[(2r,3s,4r,5r)-5-(6-aminopurin-9-yl)-4-hydroxy-3-phosphonooxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-hydroxyphosphoryl]oxy-2-hydroxy-3,3-dimethylbutanoyl]amino]propanoylamino]ethyl] octanethioate Chemical compound O[C@@H]1[C@H](OP(O)(O)=O)[C@@H](COP(O)(=O)OP(O)(=O)OCC(C)(C)C(O)C(=O)NCCC(=O)NCCSC(=O)CCCCCCC)O[C@H]1N1C2=NC=NC(N)=C2N=C1 KQMZYOXOBSXMII-FFJUWABQSA-N 0.000 description 1
- 239000012266 salt solution Substances 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 231100000241 scar Toxicity 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 230000001568 sexual effect Effects 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 229920002545 silicone oil Polymers 0.000 description 1
- 230000037380 skin damage Effects 0.000 description 1
- 208000017520 skin disease Diseases 0.000 description 1
- JVBXVOWTABLYPX-UHFFFAOYSA-L sodium dithionite Chemical compound [Na+].[Na+].[O-]S(=O)S([O-])=O JVBXVOWTABLYPX-UHFFFAOYSA-L 0.000 description 1
- 238000002798 spectrophotometry method Methods 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 210000005070 sphincter Anatomy 0.000 description 1
- 210000000952 spleen Anatomy 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N succinic acid Chemical compound OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 239000008399 tap water Substances 0.000 description 1
- 235000020679 tap water Nutrition 0.000 description 1
- 210000001685 thyroid gland Anatomy 0.000 description 1
- 229940034208 thyroxine Drugs 0.000 description 1
- XUIIKFGFIJCVMT-UHFFFAOYSA-N thyroxine-binding globulin Natural products IC1=CC(CC([NH3+])C([O-])=O)=CC(I)=C1OC1=CC(I)=C(O)C(I)=C1 XUIIKFGFIJCVMT-UHFFFAOYSA-N 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002103 transcriptional effect Effects 0.000 description 1
- 230000004102 tricarboxylic acid cycle Effects 0.000 description 1
- 125000002264 triphosphate group Chemical class [H]OP(=O)(O[H])OP(=O)(O[H])OP(=O)(O[H])O* 0.000 description 1
- UNXRWKVEANCORM-UHFFFAOYSA-N triphosphoric acid Chemical compound OP(O)(=O)OP(O)(=O)OP(O)(O)=O UNXRWKVEANCORM-UHFFFAOYSA-N 0.000 description 1
- 210000003462 vein Anatomy 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 230000004580 weight loss Effects 0.000 description 1
- 238000001262 western blot Methods 0.000 description 1
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
- A61K9/0024—Solid, semi-solid or solidifying implants, which are implanted or injected in body tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/02—Nasal agents, e.g. decongestants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/16—Otologicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Diabetes (AREA)
- Obesity (AREA)
- Hematology (AREA)
- Dermatology (AREA)
- Biomedical Technology (AREA)
- Epidemiology (AREA)
- Neurosurgery (AREA)
- Child & Adolescent Psychology (AREA)
- Emergency Medicine (AREA)
- Endocrinology (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Urology & Nephrology (AREA)
- Vascular Medicine (AREA)
- Otolaryngology (AREA)
- Pulmonology (AREA)
- Gastroenterology & Hepatology (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
本発明は、活性物質として、3,5-ジヨードチロニン(3,5-T2)、3',3-ジヨードチロニン(3',3-T2)、3',5-ジヨードチロニン(3',5-T2)、3'-ヨードチロニン(3'-T)、3-ヨードチロニン(3-T)又は5-ヨードチロニン(5-T)の中から選択される少なくとも1つのホルモンを、医薬的に許容され得るビヒクルと組み合せて含んでなる医薬組成物に関する。
【選択図】なし
【選択図】なし
Description
本発明は、ジヨードチロニンを含んでなる新規な医薬組成物及びその治療的使用に関する。
甲状腺ホルモンは古くから知られている。甲状腺ホルモンファミリーはT4ホルモン及びT4の逐次モノ脱ヨード化から生じる誘導ヨードチロニンからなる。T4の脱ヨード化カスケードの経路は、Hulbert A.J.(Biol. Rev.,2000)により記載されている。T4は外環5'-脱ヨード化を経てT3を生じるか、又は内環5'-脱ヨード化を経てrT3を生じる。T3は外環5'-脱ヨード化を経て3,5-T2を生じるか、又は内環5'-脱ヨード化を経て3,3'-T2を生じる。rT3は外環5'-脱ヨード化を経て3,3'-T2を生じるか、又は内環5'-脱ヨード化を経て3',5'-T2を生じる。3-T1は、3,5-T2から内環5'-脱ヨード化を経て又は3,3'-T2から外環5'-脱ヨード化を経て得られる。3'-T1は、3,3'-T2から内環5'-脱ヨード化を経て又は3',5'-T2から外環5'-脱ヨード化を経て得られる。
甲状腺ホルモン、特にT3ホルモンの公知の効果は、主に、甲状腺ホルモンの2つの核レセプターTRα-1及びTRβ-1(異なる効果を有すると考えられている核レセプターTRα及びTRβのファミリーに属する)への結合に起因する。これらレセプターは、特にヨウ素の数及び空間的配置(spatial arrangement)に関して、T3に高度に特異的であると考えられている(Bolgerら,J. Biol. Chem.,1980;Koernerら,J. Biol. Chem.,1975;Dietrichら,J. Med Chem.,1977)。甲状腺核レセプターの発見以来、ほとんどの科学者は、甲状腺ホルモンの転写変化の効果に注目している。
T3ホルモンは核レセプターに非常に効率的に結合する一方、T4ホルモンの結合は効率がより低い。T4及びT3から誘導されるホルモンは核レセプターに結合しない(Koernerら,J. Biol. Chem.,1975;Lazar,Endocrine Rev.,1993;Hulbert,Bio. Rev.,2000;Oppenheimer,Biochimie,1999;Yen,Physiol. Rev.,2001)。
肥満を治療するためのT3ホルモンの使用は当業者に周知である。しかし、その使用は、T3ホルモンの重篤な副作用、特に心臓への副作用のために、高度に制限されている。甲状腺機能低下症の治療はT3による。T3は、直接使用され得るか、又は極僅かに活性な前駆体であるT4ホルモンの変換によりインビボで産生され得る(Yen,Physiol. Rev.,2001)。T3は真の活性甲状腺ホルモンとして知られている。
甲状腺ホルモン、例えばT3により核レセプター経路を経て誘導される効果は、非常に低濃度で観察される生理学的に重要な効果である。これら効果は、T3を甲状腺機能低下症を患っていない被検体に投与したときには、しばしば有害である。これら効果は、核レセプター経路に関係する「甲状腺機能亢進効果」と考えることができる。
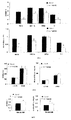
国際出願WO2005/009433及び対応する科学論文(Lanniら,The FASEB Journal,2005)は、エネルギー代謝に対する3,5-T2の効果を開示している。より詳細には、高脂肪食餌を与え、3,5-T2の腹膜注射で毎日処置した正常ラットは、未処置ラットより、体重増加が少なく、脂肪沈着も少なかった。このため、3,5-T2ホルモンは肥満及び関連する病状の治療用に提案された。
肥満は、先進国及び発展途上国における公衆衛生上の主要な関心事の1つである。肥満に関与する機序はあまり理解されていない。肥満に関与する要因は、特に栄養(alimentation)(脂肪食及び甘味食)及び環境条件(身体的活動、社会環境、食物の入手容易性)である。
先行技術には、甲状腺ホルモンがインスリン及び血糖に対する効果を有し得ることは決して開示されていない。
糖尿病は高血糖により特徴付けられる慢性疾患である。
1型糖尿病は、インスリンを分泌する膵臓β細胞の破壊により生じる。1型糖尿病の治療は、特には、インスリンの投与である。
2型糖尿病は、集団内で1型糖尿病より頻度が高く、一般には肥満に伴う。2型糖尿病は、独立した2つの異常により特徴付けられる:インスリン抵抗性及び血糖に応答したインスリン産生の減少。
1型糖尿病は、インスリンを分泌する膵臓β細胞の破壊により生じる。1型糖尿病の治療は、特には、インスリンの投与である。
2型糖尿病は、集団内で1型糖尿病より頻度が高く、一般には肥満に伴う。2型糖尿病は、独立した2つの異常により特徴付けられる:インスリン抵抗性及び血糖に応答したインスリン産生の減少。
2型糖尿病の治療は、特には、インスリンのアゴニスト薬剤又はβ細胞によるインスリン分泌のアゴニストを用いることであり、糖尿病患者の血糖及び体重を減少させることである。
加えて、糖尿病、肥満及び関連する病状の治療に古典的に使用される投与態様は、活性物質(特には甲状腺ホルモン)の肝臓によって起こり得る分解が関与し得るガレヌス製剤に頼っている。
加えて、糖尿病、肥満及び関連する病状の治療に古典的に使用される投与態様は、活性物質(特には甲状腺ホルモン)の肝臓によって起こり得る分解が関与し得るガレヌス製剤に頼っている。
(特に、副作用、患者の快適性(例えば使用頻度及び投与経路)に関して)より効率的でより適切な治療が、慢性疾患、例えば糖尿病、肥満及び異脂肪血症に対して必要である。
本発明の1つの目的は、新たな治療クラスの糖尿病治療用薬剤を提供することである。
本発明の別の目的は、糖尿病の治療用を意図した、同時、別々又は逐次の使用のための組合せ製品を提供することである。
本発明の別の目的は、糖尿病の治療用を意図した、同時、別々又は逐次の使用のための組合せ製品を提供することである。
本発明の別の目的は、活性物質として甲状腺ホルモンを含んでなる新たな医薬組成物を提供することである。このガレヌス製剤は、先行技術で一般に使用されているものと比較して減少した量で活性物質を使用することができるものである。
本発明の別の目的は、糖尿病、肥満及び関連する病状の治療用の、活性物質として甲状腺ホルモンを含んでなる新たな医薬組成物を提供することである。
本発明は、3,5-ジヨードチロニン、3',3-ジヨードチロニン、3',5-ジヨードチロニン、3'-ヨードチロニン、3-ヨードチロニン又は5-ヨードチロニンの中から選択される少なくとも1つのホルモンの、高血糖、インスリン抵抗性、β膵臓細胞不全又は関連する病状の中から選択される病状の治療用を意図した薬剤の製造のための使用に関する。
本発明によれば、用語「3,5-ジヨードチロニン、3',3-ジヨードチロニン、3',5-ジヨードチロニン、3'-ヨードチロニン、3-ヨードチロニン及び5-ヨードチロニン」は、それぞれ、3,5-T2、3',3-T2、3',5-T2、3'-T、3-T及び5-Tという。
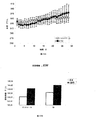
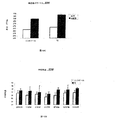
本発明者らは、3,5-T2、3',3-T2、3',5-T2、3'-T、3-T及び5-Tが血糖及びインスリンの血漿濃度を減少させることができることを最初に示した。したがって、これら甲状腺ホルモンは、高血糖、インスリン抵抗性、β膵臓細胞不全又は関連する病状の中から選択される病状の治療に使用することができる。
更に、本発明者らは、3,5-T2が糖尿病被験体の血糖に対してのみ有益な効果を有し、非糖尿病被験体の血糖に対しては有意な効果を有しないことを提案する(実施例の章を参照)。
更に、本発明者らは、3,5-T2が糖尿病被験体の血糖に対してのみ有益な効果を有し、非糖尿病被験体の血糖に対しては有意な効果を有しないことを提案する(実施例の章を参照)。
高血糖は、1g/l(又は100mg/dl若しくは5.5mmol/l)より高い、特に1.2g/lより高い空腹時グルコース濃度により特徴付けられる。3,5-T2、3',3-T2、3',5-T2、3'-T、3-T及び5-Tの使用により血糖を正常濃度まで減少させることが可能になる。
表現「グルコースの正常濃度」とは、4.4mmol/l〜5.5mmol/lのグルコース血漿濃度を意味し、「異常」血中グルコースは空腹時血漿グルコース>5.55mmol/lで定義され、糖尿病は空腹時血漿グルコース>6.1mmol/lで定義される(Meggsら,Diabetes,2003)。
表現「グルコースの正常濃度」とは、4.4mmol/l〜5.5mmol/lのグルコース血漿濃度を意味し、「異常」血中グルコースは空腹時血漿グルコース>5.55mmol/lで定義され、糖尿病は空腹時血漿グルコース>6.1mmol/lで定義される(Meggsら,Diabetes,2003)。
血糖は、参照としてグルコースオキシダーゼ法を使用する古典的な血液検査により評価される(Yeni-Komshianら,Diabetes Care,2000,p171-175;Chewら,MJA,2006,p445-449;Wallaceら,Diabetes Care,2004,p1487-1495)。
インスリン抵抗性は、8mU/l又は60pmol/lより高いインスリン血漿濃度により特徴付けられる(Wallaceら,Diabetes Care,2004,p1487-1495)。
インスリン抵抗性は、正常量のインスリンが脂肪、筋肉及び肝臓細胞からの正常応答を生じるには不十分である状態、すわわちインスリンの生理学的作用に対して抵抗性である状態である。
インスリン抵抗性は、正常量のインスリンが脂肪、筋肉及び肝臓細胞からの正常応答を生じるには不十分である状態、すわわちインスリンの生理学的作用に対して抵抗性である状態である。
それは、調べた集団中、インスリン感受性の尺度(例えば、オイグリセミッククランプの間のインスリン刺激グルコース摂取)の最も低い四分位数又は空腹時インスリン又は恒常性モデル評価(HOMA)インスリン抵抗性指標の最も高い四分位数として規定される(Albertiら,「Definition,diagnosis and classification of diabetes mellitus and its complications. Part 1: Diagnosis and classification of diabetes mellitus,provisional report of a WHO consultation」,Diabetic Med,1998,p539-553;Wallaceら,Diabetes Care,2004,p1487-1495)。
上記の活性物質の使用により、インスリン血漿濃度を正常濃度に減少させること、インスリンに対する感受性を増大させること及びグルコース及び脂質の代謝を改善させることが可能になる。
表現「インスリンの正常濃度」とは、5〜8mU/l(36〜60pmol/l)のインスリン血漿濃度を意味する。
表現「インスリンの正常濃度」とは、5〜8mU/l(36〜60pmol/l)のインスリン血漿濃度を意味する。
インスリン濃度は古典的な血液検査により評価される(ヒト抗体を用いるRIAアッセイ;Yeni-Komshianら,Diabetes Care,2000,p171-175;Chewら,MJA,2006,p445-449;Wallaceら,Diabetes Care,2004,p1487-1495)。
インスリンに対する感受性はHOMA(恒常性モデル評価)法により評価することができる(Wallaceら,Diabetes Care,2004,p1487-1495、1489頁の図2を参照)。
インスリンに対する感受性はHOMA(恒常性モデル評価)法により評価することができる(Wallaceら,Diabetes Care,2004,p1487-1495、1489頁の図2を参照)。
驚くべきことに、上記の活性物質の使用は、膵臓β細胞の生存を改善し、よってインスリン分泌細胞の再生を改善するようである。
前記細胞の再生は、インスリン濃度の測定(ヒト抗体を用いるRIAアッセイ;Yeni-Komshianら,Diabetes Care,2000,p171-175;Chewら,MJA,2006,p445-449;Wallaceら,Diabetes Care,2004,p1487-1495)により評価する。
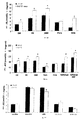
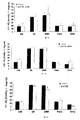
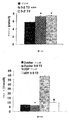
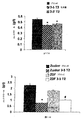
ZDFラットで得られた結果は、3,5-T2での処置がグルコース濃度の減少及び血漿インスリン濃度の増加を誘導したことを示している。
前記細胞の再生は、インスリン濃度の測定(ヒト抗体を用いるRIAアッセイ;Yeni-Komshianら,Diabetes Care,2000,p171-175;Chewら,MJA,2006,p445-449;Wallaceら,Diabetes Care,2004,p1487-1495)により評価する。
ZDFラットで得られた結果は、3,5-T2での処置がグルコース濃度の減少及び血漿インスリン濃度の増加を誘導したことを示している。
2型糖尿病の遺伝モデルであるGoto-Kakizaki(GK)ラットには、胎齢の早期にβ細胞量(cell mass)の制限が存在し、これは成体動物で維持される。β細胞量の制限は、このモデルで明白な糖尿病を導くシーケンスにおける重大な事象と考えられている。GKモデルでは、β細胞の再生は、非糖尿病Wistarラットと比較して、より低い効率で起こる。GKラットにおけるこの欠損は、変化したβ細胞新生能力に寄与する遺伝的素因及び成体動物に特異的な減少したβ細胞増殖能を導く環境因子(例えば慢性高血糖)の両方の結果である。これら結果は、Movassatら,Diabetologia,1997,p916-925及びPlachotら,Histochem Cell Biol.,2001,p131-139に記載されている(共に、その内容の全体が参照により本明細書中に組み込まれる)。
慢性高血糖が膵臓β細胞の破壊、したがってインスリン分泌の減少を誘導したと仮定すれば、回復された正常インスリン濃度はβ細胞が再生されることを意味し得る。
β細胞の機能的な量は、HOMA法によるインスリン分泌レベルに相関付けることができる。動物モデルでは、当業者は膵臓量(pancreas mass)の直接評価を考えることができる。
β細胞の機能的な量は、HOMA法によるインスリン分泌レベルに相関付けることができる。動物モデルでは、当業者は膵臓量(pancreas mass)の直接評価を考えることができる。
本発明は、特に、前記ホルモンが3,5-ジヨードチロニン、3',3-ジヨードチロニン又は3',5-ジヨードチロニンの中から選択される上記の使用に関する。
本発明は、更に、糖尿病の治療、特に1型又は2型糖尿病の治療のための上記の使用に関する。
本発明は、更に、糖尿病の治療、特に1型又は2型糖尿病の治療のための上記の使用に関する。
上記のホルモンが古典的な投薬及び先行技術で古典的に使用されるガレヌス製剤で投与される場合、治療される病状としては、
− 過体重に関連する前病的及び病的状態、肥満、アルコール及び非アルコール肝炎性皮脂欠乏症、異脂肪血症(高コレステロール血症及び高トリグリセリド血症を含む)、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、糖尿病被験体における変化した脂質代謝、胆嚢疾患、皮下脂肪の沈着(セリュライトを含む)、血管運動神経性鼻炎(アレルギー性のものを含む)
− 過体重に関連する前病的及び病的状態、肥満、アルコール及び非アルコール肝炎性皮脂欠乏症、異脂肪血症(高コレステロール血症及び高トリグリセリド血症を含む)、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、糖尿病被験体における変化した脂質代謝、胆嚢疾患、皮下脂肪の沈着(セリュライトを含む)、血管運動神経性鼻炎(アレルギー性のものを含む)
− 皮膚疾患(線条、セリュライト、粗い皮膚、光線性皮膚損傷、本来的に老化した皮膚、光損傷皮膚、扁平苔癬、魚鱗癬、アクネ、乾癬、皺の多い皮膚、Dernier病、湿疹、アトピー性皮膚炎、脂漏性皮膚炎強皮症、コラーゲン欠損皮膚、グルココルチコイド誘導萎縮症、塩素ざ瘡、粃糠疹、皮脂性上皮目詰まり(clogging of sebaceous epithelium)、角質化の乱れ、しゅさ性ざ瘡、キサントーマ、乾燥落屑性皮膚炎、脱毛症、紅斑、老人性湿疹、毛孔角化症、急性脂漏症、皮膚瘢痕、美容外科手術前の保護的処置
が含まれない。
が含まれない。
本発明はまた、活性物質として、3,5-ジヨードチロニン、3',3-ジヨードチロニン、3',5-ジヨードチロニン、3'-ヨードチロニン、3-ヨードチロニン又は5-ヨードチロニンの中から選択される少なくとも1つのホルモンを、皮下又は経皮経路を介する投与に適切である医薬的に許容され得るビヒクルと組み合せて含んでなる医薬組成物に関する。
表現「医薬的に許容され得るビヒクル」とは、医薬組成物を製造するために製薬産業で通常用いられている、医薬的に許容され得る固体又は液体の、希釈剤又はカプセル化剤、充填剤又はキャリア剤を意味する。
皮下経路では、薬剤は、皮膚直下の脂肪組織中に直接注射することができるか、又は薬剤は、皮膚の下に挿入されるカプセル中に含ませることができる。
経皮経路では、薬剤は注射することなく血流まで皮膚を通過する。詳細には、薬剤は、皮膚に適用されるパッチ中に含まれる。パッチ製剤に関しては、薬剤は、皮膚透過性を亢進させる化学物質(例えばアルコール)と混合させることができる。
剤形としては、即時放出、延長放出、パルス放出、可変放出、制御放出、時限放出、持続放出、遅延放出、長期作用及びそれらの組合せが挙げられる。
経皮経路では、薬剤は注射することなく血流まで皮膚を通過する。詳細には、薬剤は、皮膚に適用されるパッチ中に含まれる。パッチ製剤に関しては、薬剤は、皮膚透過性を亢進させる化学物質(例えばアルコール)と混合させることができる。
剤形としては、即時放出、延長放出、パルス放出、可変放出、制御放出、時限放出、持続放出、遅延放出、長期作用及びそれらの組合せが挙げられる。
本発明の有利な実施形態において、本医薬組成物は(特にパッチによる)経皮用に適切である。
有利な実施形態において、本医薬組成物の投与は、薬剤が(このホルモンの重要な分解をもたらす)肝臓を通過することを部分的に回避する。
本発明の別の有利な実施形態において、本医薬組成物は(特に皮膚の直下に注入されるカプセルによる)皮下投与用に適切である。
有利な実施形態において、本医薬組成物の投与は、薬剤が(このホルモンの重要な分解をもたらす)肝臓を通過することを部分的に回避する。
本発明の別の有利な実施形態において、本医薬組成物は(特に皮膚の直下に注入されるカプセルによる)皮下投与用に適切である。
本発明の別の有利な実施形態において、本医薬組成物は、全ての病状、特に
− 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎
の中から選択される病状の治療に適切である。
− 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎
の中から選択される病状の治療に適切である。
本発明は、更に、前記医薬的に許容され得るビヒクルが前記活性物質の連続放出、好ましくは定常放出を可能にする上記の医薬組成物に関する。
活性物質の連続放出、好ましくは定常放出により、
− 代謝障害に対する、別の投与態様を介して得られる結果と比較して増加した効果、又は、
− 以前にはポジティブな結果がみられなかった動物モデルの代謝障害に対して新たに観察される効果
を得ることが可能になる。
− 代謝障害に対する、別の投与態様を介して得られる結果と比較して増加した効果、又は、
− 以前にはポジティブな結果がみられなかった動物モデルの代謝障害に対して新たに観察される効果
を得ることが可能になる。
表現「連続放出」とは、少なくとも24時間、好ましくは少なくとも1ヶ月、最も好ましくは少なくとも2ヶ月、特に3ヶ月にわたる薬剤の連続放出を意味する。
表現「定常放出」とは、放出される薬剤の量/時間単位が本質的に一定であり、少なくとも24時間、好ましくは少なくとも1ヶ月、最も好ましくは少なくとも2ヶ月、特に3ヶ月にわたる薬剤の連続放出を意味する。
連続及び定常放出は、例えば、パッチ又は皮膚の下に注入されるカプセルを用いることによって達成される。
表現「定常放出」とは、放出される薬剤の量/時間単位が本質的に一定であり、少なくとも24時間、好ましくは少なくとも1ヶ月、最も好ましくは少なくとも2ヶ月、特に3ヶ月にわたる薬剤の連続放出を意味する。
連続及び定常放出は、例えば、パッチ又は皮膚の下に注入されるカプセルを用いることによって達成される。
本発明の有利な実施形態において、本医薬組成物は、全ての病状、特に
− 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎
の中から選択される病状の治療に適切である。
− 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎
の中から選択される病状の治療に適切である。
本発明は、特に、約0.01μg/kg/日〜約250μg/kg/日、特に約0.01μg/kg/日〜約25μg/kg/日、特に約0.1μg/kg/日〜約15μg/kg/日の活性物質、更に特には約0.1μg/kg/日〜約5μg/kg/日の活性物質、最も特には約0.1μg/kg/日〜1μg/kg/日の活性物質の放出に適切な形態である上記の医薬組成物に関する。
活性物質の投薬量は投与経路に特に依存し、これは、当業者によって容易に決定される。
活性物質の投薬量は投与経路に特に依存し、これは、当業者によって容易に決定される。
本発明の有利な実施形態において、本医薬組成物は、全ての病状、特に
− 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎
の中から選択される病状の治療に適切である。
− 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎
の中から選択される病状の治療に適切である。
本発明は、更に、期間の満了時に放出されるべき活性物質を、投薬単位基準で、(70kgのヒトについて上記値の範囲(μg/kg/日又はmg/kg/日)に対応する)約5μg〜約1.5g、特に約75mg〜約750mg含んでなる上記の医薬組成物に関する。
例として、70kgのヒトの治療には、投薬量は
− 8日の処置を達成するためには、約5μg〜約150mg、特に約5μg〜約15mg、特に約50μg〜約10mg、特に約50μg〜約3mg、最も特には約50μg〜約500μgの活性物質、
− 30日の処置を達成するためには、約20μg〜約500mg、特に約20μg〜約50mg、特に約200μg〜約30mg、特に約200μg〜約10mg、最も特には約200μg〜約2mgの活性物質、
− 90日の処置を達成するためには、約60μg〜約1.5g、特に約60μg〜約150mg、特に約600μg〜約100mg、特に約600μg〜約30mg、最も特には約600μg〜約6mgの活性物質
である。
− 8日の処置を達成するためには、約5μg〜約150mg、特に約5μg〜約15mg、特に約50μg〜約10mg、特に約50μg〜約3mg、最も特には約50μg〜約500μgの活性物質、
− 30日の処置を達成するためには、約20μg〜約500mg、特に約20μg〜約50mg、特に約200μg〜約30mg、特に約200μg〜約10mg、最も特には約200μg〜約2mgの活性物質、
− 90日の処置を達成するためには、約60μg〜約1.5g、特に約60μg〜約150mg、特に約600μg〜約100mg、特に約600μg〜約30mg、最も特には約600μg〜約6mgの活性物質
である。
表現「投薬単位」とは、1薬剤単位中に含まれる活性物質の量を意味する。
本医薬組成物の投与経路及び製剤に依存して、投薬単位中に含まれる活性物質は、迅速に又は或る期間にわたって連続的に放出され得る。本医薬組成物はまた徐放薬剤であり得る。
本医薬組成物の投与経路及び製剤に依存して、投薬単位中に含まれる活性物質は、迅速に又は或る期間にわたって連続的に放出され得る。本医薬組成物はまた徐放薬剤であり得る。
本発明の医薬組成物は、部分用量(partial dose)又は1用量で24時間の間に1回又はそれより多い回数投与され得る。分割投薬、2回又はその他の複数回投薬は、同時に又は24時間の間で異なる時間に行い得る。
有利な実施形態において、本発明の医薬組成物は、少なくとも24時間、好ましくは少なくとも1週間、より好ましくは少なくとも1ヶ月間、最も好ましくは少なくとも2ヶ月間、特に少なくとも3ヶ月間の間の連続放出を可能にする独特な用量で投与される。
有利な実施形態において、本発明の医薬組成物は、少なくとも24時間、好ましくは少なくとも1週間、より好ましくは少なくとも1ヶ月間、最も好ましくは少なくとも2ヶ月間、特に少なくとも3ヶ月間の間の連続放出を可能にする独特な用量で投与される。
本発明の別の有利な実施形態において、本医薬組成物は、全ての病状、特に
− 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎
の中から選択される病状の治療に適切である。
− 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎
の中から選択される病状の治療に適切である。
本発明は、更に、前記医薬的に許容され得るビヒクルが皮膚透過性の亢進に使用される化学物質(例えばアルコール)である上記の医薬組成物に関する。
活性物質の連続及び/又は定常放出を可能にする手段は、パッチ又は皮膚の下に注入されるカプセルの中から選択される。
活性物質の連続及び/又は定常放出を可能にする手段は、パッチ又は皮膚の下に注入されるカプセルの中から選択される。
本発明はまた、3,5-ジヨードチロニン、3',3-ジヨードチロニン、3',5-ジヨードチロニン、3'-ヨードチロニン、5'-ヨードチロニン、3-ヨードチロニン又は5-ヨードチロニンの中から選択される少なくとも1つのホルモンの、
− 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎
の中から選択される病状の治療用を意図した薬剤の製造のための使用であって、
− 前記ホルモン及び前記医薬的に許容され得るビヒクルは皮下又は経皮経路を介する投与に適切な形態にある、使用に関する。
− 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎
の中から選択される病状の治療用を意図した薬剤の製造のための使用であって、
− 前記ホルモン及び前記医薬的に許容され得るビヒクルは皮下又は経皮経路を介する投与に適切な形態にある、使用に関する。
本発明は、更に特には、高血糖、インスリン抵抗性、β膵臓細胞不全又は関連する病状の治療のための上記の使用に関し、前記ホルモン及び前記医薬的に許容され得るビヒクルは皮下又は経皮経路を介する投与に適切な形態にある。
有利な実施形態において、本発明は、糖尿病の治療、特に1型又は2型糖尿病の治療のための上記の使用に関し、前記ホルモン及び前記医薬的に許容され得るビヒクルは皮下又は経皮経路を介する投与に適切な形態にある。
有利な実施形態において、本発明は、糖尿病の治療、特に1型又は2型糖尿病の治療のための上記の使用に関し、前記ホルモン及び前記医薬的に許容され得るビヒクルは皮下又は経皮経路を介する投与に適切な形態にある。
本発明は、更に特には、
− 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎
の中から選択される病状の治療のための上記の使用に関し、
ここで、前記医薬的に許容され得るビヒクルは前記活性物質の連続放出、好ましくは定常放出を可能にする。
− 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎
の中から選択される病状の治療のための上記の使用に関し、
ここで、前記医薬的に許容され得るビヒクルは前記活性物質の連続放出、好ましくは定常放出を可能にする。
本発明はまた、更に特には、
− 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎、
の中から選択される病状の治療のための上記使用に関し、
ここで、前記ホルモン及び前記医薬的に許容され得るビヒクルは、約0.01μg/kg/日〜約250μg/kg/日、特に約0.01μg/kg/日〜約25μg/kg/日、特に約0.1μg/kg/日〜約15μg/kg/日の活性物質、更に特には約0.1μg/kg/日〜約5μg/kg/日の活性物質、最も特には約0.1μg/kg/日〜1μg/kg/日の活性物質の放出に適切な形態である。
− 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に関連するヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎、
の中から選択される病状の治療のための上記使用に関し、
ここで、前記ホルモン及び前記医薬的に許容され得るビヒクルは、約0.01μg/kg/日〜約250μg/kg/日、特に約0.01μg/kg/日〜約25μg/kg/日、特に約0.1μg/kg/日〜約15μg/kg/日の活性物質、更に特には約0.1μg/kg/日〜約5μg/kg/日の活性物質、最も特には約0.1μg/kg/日〜1μg/kg/日の活性物質の放出に適切な形態である。
本発明はまた、糖尿病の治療用を意図した同時、別々又は逐次の使用のための組合せ製品として、
− 3,5-ジヨードチロニン、3',3-ジヨードチロニン、3',5-ジヨードチロニン、3'-ヨードチロニン、3-ヨードチロニン又は5-ヨードチロニンの中から選択される少なくとも1つのホルモンと、
− (特に抗糖尿病性経口薬剤の中から選択される)インスリンの膵臓分泌を活性化する少なくとも1つの活性物質、又はグルコースの消化吸収の緩徐化を可能にする少なくとも1つの活性物質と
を含んでなる製品に関する。
− 3,5-ジヨードチロニン、3',3-ジヨードチロニン、3',5-ジヨードチロニン、3'-ヨードチロニン、3-ヨードチロニン又は5-ヨードチロニンの中から選択される少なくとも1つのホルモンと、
− (特に抗糖尿病性経口薬剤の中から選択される)インスリンの膵臓分泌を活性化する少なくとも1つの活性物質、又はグルコースの消化吸収の緩徐化を可能にする少なくとも1つの活性物質と
を含んでなる製品に関する。
本発明はまた、3,5-ジヨードチロニン、3',3-ジヨードチロニン、3',5-ジヨードチロニン、3'-ヨードチロニン、3-ヨードチロニン又は5-ヨードチロニンの中から選択される少なくとも1つのホルモンを含んでなる栄養補助物質又は食品組成物に関する。
本発明はまた、特に:
3,5-ジヨードチロニン、3',3-ジヨードチロニン、3',5-ジヨードチロニン、3'-ヨードチロニン、3-ヨードチロニン又は5-ヨードチロニンの中から選択される少なくとも1つのホルモンを含んでなる栄養補助物質又は食品組成物の投与により、
− 通常の食餌で飼育した動物の脂肪組織の重量と比較して、動物の脂肪組織の重量を低下させ、
− 通常の食餌で飼育した動物の赤身(lean tissue)の重量と比較して、赤身の重量を維持又は増加させることによって、
脂肪組織の重量と赤身の重量との比を制御することにより哺乳動物及び鳥類の肉質、特に豚肉及び牛肉の質を改善する方法に関する。
3,5-ジヨードチロニン、3',3-ジヨードチロニン、3',5-ジヨードチロニン、3'-ヨードチロニン、3-ヨードチロニン又は5-ヨードチロニンの中から選択される少なくとも1つのホルモンを含んでなる栄養補助物質又は食品組成物の投与により、
− 通常の食餌で飼育した動物の脂肪組織の重量と比較して、動物の脂肪組織の重量を低下させ、
− 通常の食餌で飼育した動物の赤身(lean tissue)の重量と比較して、赤身の重量を維持又は増加させることによって、
脂肪組織の重量と赤身の重量との比を制御することにより哺乳動物及び鳥類の肉質、特に豚肉及び牛肉の質を改善する方法に関する。
実施例
実施例1:肥満及び異脂肪血症の治療のための3,5-T2ホルモンの使用
1.材料及び方法
動物の取り扱い
Laboratory of Fundamental and Applied Bioenergeticsの動物室施設で飼育した成体雄性ラット(Wistar系統)又はCharles-River Laboratories,Domaine des oncins,L'ARBRESLE Franceから購入した成体雄性ラット[(遺伝的に肥満の正常血糖(Zucker又はFa/Fa)又は糖尿病(ZDF)]を個々にステンレススチール製吊り下げケージに入れ、22℃、50±10%相対湿度にて12時間:12時間の明:暗環境で維持した。全ての動物を、標準ラット固形飼料(Safe A04,Villemoisson,France)及び水道水を自由摂取させて飼育した。ボディマス(body mass)及び食物摂取を1週間に2/3回記録し、動物の摂食行動の妨害を最小限にするために、同時に新鮮な食物を提供した。
実施例1:肥満及び異脂肪血症の治療のための3,5-T2ホルモンの使用
1.材料及び方法
動物の取り扱い
Laboratory of Fundamental and Applied Bioenergeticsの動物室施設で飼育した成体雄性ラット(Wistar系統)又はCharles-River Laboratories,Domaine des oncins,L'ARBRESLE Franceから購入した成体雄性ラット[(遺伝的に肥満の正常血糖(Zucker又はFa/Fa)又は糖尿病(ZDF)]を個々にステンレススチール製吊り下げケージに入れ、22℃、50±10%相対湿度にて12時間:12時間の明:暗環境で維持した。全ての動物を、標準ラット固形飼料(Safe A04,Villemoisson,France)及び水道水を自由摂取させて飼育した。ボディマス(body mass)及び食物摂取を1週間に2/3回記録し、動物の摂食行動の妨害を最小限にするために、同時に新鮮な食物を提供した。
ペレット埋め込み
ジアゼパム4mg/kg及びケタミン100mg/kgの同時腹腔内注射により8週齢ラット(300g±10g)を麻酔した。外科手術(10分間)の間体温を維持するため、動物を暖かい毛布の上に置いた。肩甲骨間の剃毛後、0.5cmの小さな皮膚切開により、10ゲージの精密トロカールでの(rT3又は3',3-T2を含有する)小ペレットの皮下移植を可能にする。ペレット(Innovative Research of America(Sarasota,Florida,USA)製)は、動物に活性製品を効果的で連続的に放出する生分解性マトリクスから構成される。
ジアゼパム4mg/kg及びケタミン100mg/kgの同時腹腔内注射により8週齢ラット(300g±10g)を麻酔した。外科手術(10分間)の間体温を維持するため、動物を暖かい毛布の上に置いた。肩甲骨間の剃毛後、0.5cmの小さな皮膚切開により、10ゲージの精密トロカールでの(rT3又は3',3-T2を含有する)小ペレットの皮下移植を可能にする。ペレット(Innovative Research of America(Sarasota,Florida,USA)製)は、動物に活性製品を効果的で連続的に放出する生分解性マトリクスから構成される。
60日間にわたって連続的で定常的な薬物送達を提供するために、3-5ジヨードチロニン(3-5T2)又は3-3'ジヨードチロニン(3-3'T2)を異なる用量(5、0.5又は0.1mg/ペレット)で使用して埋め込んだ(これは25μg、2.5μg又は0.5μg/日/100g BWを表す)。
間接熱量測定
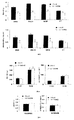
エネルギー消費及び酸化される基質(炭水化物又は脂質)の性質を間接熱量測定により調べた。この原理は、各動物によるCO2放出(VCO2)及びO2消費(VO2)の決定に基づく。O2は呼吸鎖における基質の酸化(水生成を導く)に全体的に関与する一方、CO2放出は(クレブス回路における)基質の脱カルボキシル化に関係すると考えられる。これら測定により、エネルギー消費(EE)及び呼吸商(VO2/VCO2、RQ)を評価することが可能になる。EEは、安静時及び活動時の絶対エネルギー散逸を表す。RQは、酸化的経路に関与する炭水化物 対 脂質の比を示す相対的測定値である。比1.0は独占的な炭水化物酸化を示す一方、比0.7は独占的な脂質酸化を示す。これら2つの極値の間の各値は、各基質の相対的比率を示す(注記:タンパク質酸化は評価しなかった)。例として、RQは、絶食の間に脂質酸化を示す0.7に接近し、絶食後は逆に、食物摂取及び血漿インスリンの上昇に起因して、RQは増加して炭水化物酸化を示す1に近づく。同様に、高炭水化物食餌で飼育した動物は、高脂質食餌で飼育した動物より高いRQを有する。
エネルギー消費及び酸化される基質(炭水化物又は脂質)の性質を間接熱量測定により調べた。この原理は、各動物によるCO2放出(VCO2)及びO2消費(VO2)の決定に基づく。O2は呼吸鎖における基質の酸化(水生成を導く)に全体的に関与する一方、CO2放出は(クレブス回路における)基質の脱カルボキシル化に関係すると考えられる。これら測定により、エネルギー消費(EE)及び呼吸商(VO2/VCO2、RQ)を評価することが可能になる。EEは、安静時及び活動時の絶対エネルギー散逸を表す。RQは、酸化的経路に関与する炭水化物 対 脂質の比を示す相対的測定値である。比1.0は独占的な炭水化物酸化を示す一方、比0.7は独占的な脂質酸化を示す。これら2つの極値の間の各値は、各基質の相対的比率を示す(注記:タンパク質酸化は評価しなかった)。例として、RQは、絶食の間に脂質酸化を示す0.7に接近し、絶食後は逆に、食物摂取及び血漿インスリンの上昇に起因して、RQは増加して炭水化物酸化を示す1に近づく。同様に、高炭水化物食餌で飼育した動物は、高脂質食餌で飼育した動物より高いRQを有する。
間接熱量測定システム(Panlab,Barcelona,Spain)は、ケージ、ポンプ、フローコントローラ、バルブ及びアナライザーからなる。これは、4つの別々のケージ中のO2及びCO2濃度並びにエアフローをシーケンシャルに測定するためにコンピュータ制御される。このことにより、4つ同時の決定が可能になる。4つの代謝チャンバーの1つにラットを隔離し、周囲O2及びCO2濃度を周期的にモニターするための参照として室中の空気を使用する。
所定の間隔で、コンピュータが信号を送り、データ獲得ハードウェア(Metabolism,Panlab,Barcelona,Spain)で差分のCO2及びO2濃度、流量を記憶して、VCO2、VO2、RQ及びEEの算出を可能にする(Weirの式)。
身体組成、血液及び組織サンプリング
実験期間の終時に、ミトコンドリアの代謝に対する全身麻酔の周知の効果を回避するために、動物を断頭により犠牲にした。後の血清代謝物及びホルモンの決定のために、血液サンプルを即時に収集し、血漿を凍結させた。肝臓、筋肉及び脂肪沈着を素早く切り取り、秤量した。肝臓中葉を迅速に凍結クランプした。筋肉(足底筋、ヒラメ筋及び腓腹筋)を、液体窒素中で予め冷却したイソペンタン中で凍結させた。腸間膜脂肪は、胃食道括約筋から直腸の末端までの胃腸管の周囲の脂肪組織からなった。膵臓を区別して除くように特に注意を払った。腰部筋肉に沿った各腎臓の背後の別の沈着として腹膜後脂肪体を採取した。精巣上体脂肪は、精巣上体の上部の脂肪組織からなった。皮下沈着測定のために、各動物の右側で、腹部正中線から脊柱まで、右腰部と第1肋骨との間で皮膚の方片を採取した。肩甲骨間の褐色脂肪組織を取り出し、隣接する筋肉及び白色脂肪組織を切り取った。心室、右腎臓及び脾臓も摘出し、秤量し、凍結させた。
実験期間の終時に、ミトコンドリアの代謝に対する全身麻酔の周知の効果を回避するために、動物を断頭により犠牲にした。後の血清代謝物及びホルモンの決定のために、血液サンプルを即時に収集し、血漿を凍結させた。肝臓、筋肉及び脂肪沈着を素早く切り取り、秤量した。肝臓中葉を迅速に凍結クランプした。筋肉(足底筋、ヒラメ筋及び腓腹筋)を、液体窒素中で予め冷却したイソペンタン中で凍結させた。腸間膜脂肪は、胃食道括約筋から直腸の末端までの胃腸管の周囲の脂肪組織からなった。膵臓を区別して除くように特に注意を払った。腰部筋肉に沿った各腎臓の背後の別の沈着として腹膜後脂肪体を採取した。精巣上体脂肪は、精巣上体の上部の脂肪組織からなった。皮下沈着測定のために、各動物の右側で、腹部正中線から脊柱まで、右腰部と第1肋骨との間で皮膚の方片を採取した。肩甲骨間の褐色脂肪組織を取り出し、隣接する筋肉及び白色脂肪組織を切り取った。心室、右腎臓及び脾臓も摘出し、秤量し、凍結させた。
ミトコンドリアの単離
肝臓の主要部及び各四頭筋の赤色部分をリンスし、単離培地(250mMスクロース、20mM Tris-HCl及び1mM EGTA-Tris、pH7.4)中に切り刻んで入れた。800gで10分間の遠心分離により核及び細胞片を除去した。次いで、8,000gにて10分間の遠心によりミトコンドリアを上清から単離した。ミトコンドリアのペレットを0.5mlの単離緩衝剤中に再懸濁し、氷上に維持した。ミトコンドリアタンパク質はビシンコニン酸法(Pierce,Rockford,Illinois)により測定した。最終のミトコンドリア懸濁物を氷上に維持し、酸素消費速度及び反応性酸素種(ROS)産生の測定に使用した。
肝臓の主要部及び各四頭筋の赤色部分をリンスし、単離培地(250mMスクロース、20mM Tris-HCl及び1mM EGTA-Tris、pH7.4)中に切り刻んで入れた。800gで10分間の遠心分離により核及び細胞片を除去した。次いで、8,000gにて10分間の遠心によりミトコンドリアを上清から単離した。ミトコンドリアのペレットを0.5mlの単離緩衝剤中に再懸濁し、氷上に維持した。ミトコンドリアタンパク質はビシンコニン酸法(Pierce,Rockford,Illinois)により測定した。最終のミトコンドリア懸濁物を氷上に維持し、酸素消費速度及び反応性酸素種(ROS)産生の測定に使用した。
ミトコンドリア酸素消費
インキュベーションチャンバー中2mlのインキュベーション培地(125mM KCl、10mM Pi-Tris、20mM Tris-HCl、0.1mM EGTA、pH7.2)を充填したClarkタイプO2電極を用いて、ミトコンドリア酸素消費(JO2)の速度を30℃で測定した。全ての測定は、種々の基質:グルタメート/マレート(5mM/2.5mM)単独又はスクシネート(5mM)との組合せ、パルミトイルカルニチン(55μM)及びオクタノイルカルニチン(100μM)のいずれかとインキュベートしたミトコンドリア(肝臓及び骨格筋について、1.0又は0.2mgミトコンドリアタンパク質/ml)を用いて実施した。各基質について、JO2を基質の存在下、単独(状態2)で及び1mM ADPの添加後(状態3)に記録した。オリゴマイシン(1.25μg/mgタンパク質)をミトコンドリア懸濁物に加えて非リン酸化呼吸数を決定した(状態4)。インキュベーション培地は組み込まれた電磁式スターラー及び撹拌棒で定常的に撹拌した。ミトコンドリアの酸化的リン酸化の効率は、リン酸化による酸化に課せられる制御の程度を測定する状態3/状態4比により評価した(呼吸制御比、RCR)。
インキュベーションチャンバー中2mlのインキュベーション培地(125mM KCl、10mM Pi-Tris、20mM Tris-HCl、0.1mM EGTA、pH7.2)を充填したClarkタイプO2電極を用いて、ミトコンドリア酸素消費(JO2)の速度を30℃で測定した。全ての測定は、種々の基質:グルタメート/マレート(5mM/2.5mM)単独又はスクシネート(5mM)との組合せ、パルミトイルカルニチン(55μM)及びオクタノイルカルニチン(100μM)のいずれかとインキュベートしたミトコンドリア(肝臓及び骨格筋について、1.0又は0.2mgミトコンドリアタンパク質/ml)を用いて実施した。各基質について、JO2を基質の存在下、単独(状態2)で及び1mM ADPの添加後(状態3)に記録した。オリゴマイシン(1.25μg/mgタンパク質)をミトコンドリア懸濁物に加えて非リン酸化呼吸数を決定した(状態4)。インキュベーション培地は組み込まれた電磁式スターラー及び撹拌棒で定常的に撹拌した。ミトコンドリアの酸化的リン酸化の効率は、リン酸化による酸化に課せられる制御の程度を測定する状態3/状態4比により評価した(呼吸制御比、RCR)。
酸化的リン酸化効率
呼吸基質として5mMグルタメート/2.5mMマレート/5mMスクシネート又はオクタノイル-カルニチン(100μM)を用いたATP/O比を、ヘキソキナーゼ(EC 2.7.1.1)+グルコースに基づくADP再生系を用いるATP合成速度(JATP) 対 呼吸数JO2から決定した。JATP及びJO2は、125mM KCl、1mM EGTA、5mM Tris-Pi、20mM Tris-HCl、0.1%脂肪フリーBSA(pH7.2)を含有する培地中で上記のように測定した。JATPは、20mMグルコース、1mM MgCl2及び125μM ATPの存在下でのグルコース6-ホスフェートの形成から決定した。JO2及びJATPは漸増濃度のヘキソキナーゼの添加により調整した(Nogueiraら,J Bioenerg Biomemb.,34:55-66,2002)。
呼吸基質として5mMグルタメート/2.5mMマレート/5mMスクシネート又はオクタノイル-カルニチン(100μM)を用いたATP/O比を、ヘキソキナーゼ(EC 2.7.1.1)+グルコースに基づくADP再生系を用いるATP合成速度(JATP) 対 呼吸数JO2から決定した。JATP及びJO2は、125mM KCl、1mM EGTA、5mM Tris-Pi、20mM Tris-HCl、0.1%脂肪フリーBSA(pH7.2)を含有する培地中で上記のように測定した。JATPは、20mMグルコース、1mM MgCl2及び125μM ATPの存在下でのグルコース6-ホスフェートの形成から決定した。JO2及びJATPは漸増濃度のヘキソキナーゼの添加により調整した(Nogueiraら,J Bioenerg Biomemb.,34:55-66,2002)。
酵素活性
呼吸鎖複合体I、II及びIVの比活性の測定は、分光光度学的に実施した。複合体I及びIIの活性を決定するために合計8〜10μgのミトコンドリアタンパク質が必要であり、4μgを複合体IV用に使用した。酵素活性は、還元又は酸化された基質のnmole/分/mgミトコンドリアタンパク質として表した。
呼吸鎖複合体I、II及びIVの比活性の測定は、分光光度学的に実施した。複合体I及びIIの活性を決定するために合計8〜10μgのミトコンドリアタンパク質が必要であり、4μgを複合体IV用に使用した。酵素活性は、還元又は酸化された基質のnmole/分/mgミトコンドリアタンパク質として表した。
複合体I(ロテノン感受性NADH-ユビキノンオキシドレダクターゼ、EC 1.6.99.3)の測定:アッセイは、BSA(3.75mg/ml)を含有する10mM KH2PO4/K2HPO4緩衝剤(pH7.5)中、KCN(2mM)及びアンチマイシンA(7.5μM)の存在下にて、電子受容体としてのデシルユビキノン(100μM)及び供給体としてのNADH(200μM)を用いて実施した。次いで、ロテノン(4μM)の添加前及び後に、NADHの酸化を340nmで測定した。このことにより、複合体Iのロテノン感受性比活性の算出が可能となった。
複合体II(スクシネート-ユビキノンレダクターゼ、EC 1.3.99.1)の測定:スクシネート-ユビキノンオキシドレダクターゼ活性は、600nmにてDCPIP(100μM)の還元に起因するUV吸収の減少を測定することにより定量化した。測定は、50mM KH2PO4/K2HPO4(pH7.5)を含有する培地中、デシルユビキノン(100μM)、ロテノン(2μM)及びKCN(2mM)の存在下で行った。
複合体IV(シトクロムcオキシダーゼ、EC 1.9.3.1)の測定:アッセイは、50mM KH2PO4/K2HPO4緩衝剤(pH7.0)中、550nmにてシトクロムc(100μM)の酸化を測定することにより行った。
複合体IV(シトクロムcオキシダーゼ、EC 1.9.3.1)の測定:アッセイは、50mM KH2PO4/K2HPO4緩衝剤(pH7.0)中、550nmにてシトクロムc(100μM)の酸化を測定することにより行った。
クエン酸シンターゼ活性は、150mM Tris緩衝剤(pH8)中、オキサロアセテートジニトロチオ安息香酸及びアセチル-CoAの存在下で、イオンメルカプチドの生成に起因する412nmのUV吸収を測定することにより決定した(Garaitら,Free Rad Biol Med,2005)。
ミトコンドリアのグリセロール3-ホスフェートデヒドロゲナーゼ(mGPdH)活性は、単離したミトコンドリアの3サイクルの凍結-解凍サイクル後の上清について測定した。40μgのミトコンドリアを、9.3μMのアンチマイシンA、5μMのロテノン及びデシルユビキノン(50μM)を含有するKH2PO4/K2HPO4緩衝剤(50mM、pH7.5)中でインキュベートした。mGPDHによる50μMジクロロ-インドフェノール(DCIP)の還元は37℃にて600nmで分光光学的に測定し、酵素活性はμmol.min-1.mg prot-1として表した。
ミトコンドリアのグリセロール3-ホスフェートデヒドロゲナーゼ(mGPdH)活性は、単離したミトコンドリアの3サイクルの凍結-解凍サイクル後の上清について測定した。40μgのミトコンドリアを、9.3μMのアンチマイシンA、5μMのロテノン及びデシルユビキノン(50μM)を含有するKH2PO4/K2HPO4緩衝剤(50mM、pH7.5)中でインキュベートした。mGPDHによる50μMジクロロ-インドフェノール(DCIP)の還元は37℃にて600nmで分光光学的に測定し、酵素活性はμmol.min-1.mg prot-1として表した。
シトクロム
ミトコンドリア呼吸鎖のシトクロム含量は、並行実験において、完全に酸化されたシトクロム(フェリシアン化カリウム) 対 完全に還元されたシトクロム(亜ジチオン酸ナトリウムの少数の結晶)のスペクトルを比較することによって測定した。各シトクロムの吸収における他方のシトクロムの主要な最大吸収及び最小吸収に対する寄与が分かれば、4つの未知数を有する4つの連立方程式のセットを導くことができ、各シトクロムの濃度を算出することができる(Williams,Arch Biochem Biophys.;107:537-43,1964)。
ミトコンドリア呼吸鎖のシトクロム含量は、並行実験において、完全に酸化されたシトクロム(フェリシアン化カリウム) 対 完全に還元されたシトクロム(亜ジチオン酸ナトリウムの少数の結晶)のスペクトルを比較することによって測定した。各シトクロムの吸収における他方のシトクロムの主要な最大吸収及び最小吸収に対する寄与が分かれば、4つの未知数を有する4つの連立方程式のセットを導くことができ、各シトクロムの濃度を算出することができる(Williams,Arch Biochem Biophys.;107:537-43,1964)。
肝細胞の単離
20〜24時間絶食したWistarラットをペントバルビタールナトリウム(10mg/100g体重i.p.)で麻酔し、肝細胞を、Groenら(Eur. J. Biochem. 122:87-93,1982)により改変されたBerry及びFriend(J. Cell. Biol. 43:506-520,1969)の方法に従って単離した。簡潔には、門脈にカニューレを挿入し、Ca2+フリーのKrebs-Ringer炭酸水素塩緩衝剤(25ml/分;37℃、pH=7.4、95% O2-5% CO2で連続的に曝気)での2分間の順行性灌流を行い、肝臓から血液を除去した。同じ灌流媒体を用いて背側大動脈を通じての10分間の逆行性灌流(25ml/分)を開始した。その後、0.25mg/mlのコラゲナーゼ(タイプIV、Sigma、St. Louis、MO)を補充した100mlのKrebs-Ringer媒体で再循環灌流を行った(40ml/分で20分間)。次いで、肝臓を切除し、定常曝気(95% O2-5% CO2)下で2分間灌流媒体中で振盪させた。最後に、ナイロンガーゼ(孔サイズ120μm)を通過させて細胞懸濁液を濾過し、1.6mMのCa2+を含有するKrebs-Ringer炭酸水素塩緩衝剤で2回洗浄し、次いで1%のBSAを補充した同じ緩衝剤で3回目の洗浄を行った。
20〜24時間絶食したWistarラットをペントバルビタールナトリウム(10mg/100g体重i.p.)で麻酔し、肝細胞を、Groenら(Eur. J. Biochem. 122:87-93,1982)により改変されたBerry及びFriend(J. Cell. Biol. 43:506-520,1969)の方法に従って単離した。簡潔には、門脈にカニューレを挿入し、Ca2+フリーのKrebs-Ringer炭酸水素塩緩衝剤(25ml/分;37℃、pH=7.4、95% O2-5% CO2で連続的に曝気)での2分間の順行性灌流を行い、肝臓から血液を除去した。同じ灌流媒体を用いて背側大動脈を通じての10分間の逆行性灌流(25ml/分)を開始した。その後、0.25mg/mlのコラゲナーゼ(タイプIV、Sigma、St. Louis、MO)を補充した100mlのKrebs-Ringer媒体で再循環灌流を行った(40ml/分で20分間)。次いで、肝臓を切除し、定常曝気(95% O2-5% CO2)下で2分間灌流媒体中で振盪させた。最後に、ナイロンガーゼ(孔サイズ120μm)を通過させて細胞懸濁液を濾過し、1.6mMのCa2+を含有するKrebs-Ringer炭酸水素塩緩衝剤で2回洗浄し、次いで1%のBSAを補充した同じ緩衝剤で3回目の洗浄を行った。
肝細胞のペリフュージョン
Groenら(Eur. J. Biochem. 122:87-93,1982)により改変されたvan der Meer及びTager(FEBS Lett. 67:36-40,1976)の方法に従って、肝臓細胞のペリフュージョン(perifusion)を行った。肝細胞(225〜250mg乾燥質量)を37℃の15mlペリフュージョンチャンバー中に配置し、連続的に曝気した(95% O2-5% CO2)、0.2%のBSAを含有するKrebs-Ringer炭酸水素塩溶液(pH=7.4)でペリフュージョンした(5ml/分)。実験は、並列に配置した2つのペリフュージョンチャンバー中で二連で行った。チャンバー出口で、ペリフュージョン液のO2含量をClark電極(Yellow Springs Instruments、Yellow Springs、OH)でモニターして、肝細胞懸濁物のO2取り込みを評価した。40分後、O2取込みが定常状態に到達したら、肝細胞を、0.4mMオクタノエートの存在下又は不在下で、漸増量のグリセロール(0.15、0.30、0.60、1.2、2.4、4.8及び9.6mM)でペリフュージョンした。20分間の各定常状態の終時に、その後のグルコース、ラクテート、ピルベート、アセトアセテート及びβ-ヒドロキシブチレート濃度の測定のために、ペリフュージョン液及び細胞サンプルを2分間隔で収集した。サンプルは4℃で貯蔵し、実験の終了後12時間以内に分析した。加えて、細胞内及び細胞外分画のために、300μlの細胞懸濁液をチャンバーからサンプリングした。この目的には、Zuurendonk及びTager(Biochim. Biophys. Acta 333:393-399,1974)により記載されたジギトニン分画法でミトコンドリア及び細胞質ゾル空間を分離した。簡潔には、細胞懸濁液を、2.2ml Eppendorfチューブにおいて、2mMのジギトニン(Merck,Lyon,France)を含有する等張培地(4℃)中に置いた。15秒後、チューブを10,000gにて15秒間遠心分離して、ミトコンドリアを、その下の800μlのシリコンオイル(Rhodorsil 640 V 100,Rhone-Poulenc)層を通過させ250μl HClO4(10%質量/vol)+25mM EDTA中に沈降させた。上清(700μl)を直ぐに取り出し、HClO4(5%質量/vol)で除タンパク質処理し、中和した。次いで、細胞内代謝物(DHAP及びG3P、分光光度法)及びアデニンヌクレオチド含量(HPLC)の決定のために、細胞内含有物を中和して−20℃で維持した。
Groenら(Eur. J. Biochem. 122:87-93,1982)により改変されたvan der Meer及びTager(FEBS Lett. 67:36-40,1976)の方法に従って、肝臓細胞のペリフュージョン(perifusion)を行った。肝細胞(225〜250mg乾燥質量)を37℃の15mlペリフュージョンチャンバー中に配置し、連続的に曝気した(95% O2-5% CO2)、0.2%のBSAを含有するKrebs-Ringer炭酸水素塩溶液(pH=7.4)でペリフュージョンした(5ml/分)。実験は、並列に配置した2つのペリフュージョンチャンバー中で二連で行った。チャンバー出口で、ペリフュージョン液のO2含量をClark電極(Yellow Springs Instruments、Yellow Springs、OH)でモニターして、肝細胞懸濁物のO2取り込みを評価した。40分後、O2取込みが定常状態に到達したら、肝細胞を、0.4mMオクタノエートの存在下又は不在下で、漸増量のグリセロール(0.15、0.30、0.60、1.2、2.4、4.8及び9.6mM)でペリフュージョンした。20分間の各定常状態の終時に、その後のグルコース、ラクテート、ピルベート、アセトアセテート及びβ-ヒドロキシブチレート濃度の測定のために、ペリフュージョン液及び細胞サンプルを2分間隔で収集した。サンプルは4℃で貯蔵し、実験の終了後12時間以内に分析した。加えて、細胞内及び細胞外分画のために、300μlの細胞懸濁液をチャンバーからサンプリングした。この目的には、Zuurendonk及びTager(Biochim. Biophys. Acta 333:393-399,1974)により記載されたジギトニン分画法でミトコンドリア及び細胞質ゾル空間を分離した。簡潔には、細胞懸濁液を、2.2ml Eppendorfチューブにおいて、2mMのジギトニン(Merck,Lyon,France)を含有する等張培地(4℃)中に置いた。15秒後、チューブを10,000gにて15秒間遠心分離して、ミトコンドリアを、その下の800μlのシリコンオイル(Rhodorsil 640 V 100,Rhone-Poulenc)層を通過させ250μl HClO4(10%質量/vol)+25mM EDTA中に沈降させた。上清(700μl)を直ぐに取り出し、HClO4(5%質量/vol)で除タンパク質処理し、中和した。次いで、細胞内代謝物(DHAP及びG3P、分光光度法)及びアデニンヌクレオチド含量(HPLC)の決定のために、細胞内含有物を中和して−20℃で維持した。
ウェスタンブロット分析
mGPdH定量化のために、以前(23)に記載されたようにポリアクリルアミドゲル電気泳動及びイムノブロッティングを行った。簡潔には、溶解させた肝細胞を、40mMのTris(ヒドロキシメチル)アミノメタン(pH6.8)、1%のSDS、6%のグリセロール及び1%のβ-メルカプトエタノールを含有する200μlの緩衝剤と混合した。次いで、この混合物を100℃に10分間加熱し、5%の濃縮用ゲル及び12.5%の分離用ゲルを用いて一次元のドデシル硫酸ナトリウム(SDS)-PAGEに12時間供した。電気泳動による分離後、定電圧でPVDFメンブレンにタンパク質を移した。タンパク質を移した後、メンブレンを2時間ブロッキングし、次いでmGPDHに特異的なモノクローナル抗体(J. Weitzel博士の厚意による)と2時間インキュベートし、次いで二次抗体(西洋ワサビペルオキシダーゼにコンジュゲートしたヤギ抗マウス免疫グロブリンG(Bio-Rad)、1:10000希釈)に曝露させた。mGPDHは増強化学発光検出法により可視化した(RPN 2106,Amersham)。濃度計でのスキャニングを行い、ブロットのバンドを定量化し、データは、積分光学密度の任意単位として数値的に表した。
mGPdH定量化のために、以前(23)に記載されたようにポリアクリルアミドゲル電気泳動及びイムノブロッティングを行った。簡潔には、溶解させた肝細胞を、40mMのTris(ヒドロキシメチル)アミノメタン(pH6.8)、1%のSDS、6%のグリセロール及び1%のβ-メルカプトエタノールを含有する200μlの緩衝剤と混合した。次いで、この混合物を100℃に10分間加熱し、5%の濃縮用ゲル及び12.5%の分離用ゲルを用いて一次元のドデシル硫酸ナトリウム(SDS)-PAGEに12時間供した。電気泳動による分離後、定電圧でPVDFメンブレンにタンパク質を移した。タンパク質を移した後、メンブレンを2時間ブロッキングし、次いでmGPDHに特異的なモノクローナル抗体(J. Weitzel博士の厚意による)と2時間インキュベートし、次いで二次抗体(西洋ワサビペルオキシダーゼにコンジュゲートしたヤギ抗マウス免疫グロブリンG(Bio-Rad)、1:10000希釈)に曝露させた。mGPDHは増強化学発光検出法により可視化した(RPN 2106,Amersham)。濃度計でのスキャニングを行い、ブロットのバンドを定量化し、データは、積分光学密度の任意単位として数値的に表した。
RNA精製及び逆転写PCR
Tripure RNA単離試薬(Roche Diagnostics)を用いて、組織からトータルRNAを抽出した。260及び280nmでの光学密度を測定することにより濃度及び純度を確かめた。1%アガロースゲル電気泳動(Eurobio)により完全性を検証した。β-アクチンを参照として使用する半定量逆転写ポリメラーゼ連鎖反応(RT-PCR)によりmRNA濃度を測定した。プライマー配列を表1に示す。各標的mRNAについて、最終容量25μL中の100UのM-MLV Reverse Transcriptase(Promega)、5μLのM-MLV RT 5×緩衝剤、20UのRNasinリボヌクレアーゼインヒビター、12ピコモルのデオキシヌクレオシド三リン酸及び15ピコモルの特異的アンチセンスプライマーを用い、0.1μgのトータルRNAからRTを実施した。反応は、70℃にて5分間(RNA及びアンチセンスプライマー)、次いで42℃にて60分間(全ミックス)、続いて70℃にて15分間からなった。冷却後、5μLをPCR反応に使用した。5μLのRT媒体を、6ピコモルのMgCl2、8ピコモルのデオキシヌクレオシド三リン酸、2.5UのREDTad DNAポリメラーゼ(Sigma)、15ピコモルの対応するアンチセンスプライマー及び22.5ピコモルのセンスプライマーを含有する45μLのPCRミックス(5μL 10×REDTaq PCR緩衝剤)に添加した。PCR条件は、94℃にて2分間、続いてUCP3、UCP2及びβ-アクチンについてそれぞれ28サイクル、35サイクル又は18サイクル(1サイクル=94℃にて1分間、60℃にて1分間、72℃にて1分間)であった。PCRを72℃にて10分間で終了した。生成物を、臭化エチジウムで予め染色した2%アガロースゲル上で分析した。相対的バンド強度の定量のために、Camera DC120(Kodak)で写真を撮影し、Kodak Digital Science 1D 2.0(Kodak Scientific Imaging System)を用いて、各サンプルについてβ-アクチンに対する各標的の比を決定した。
Tripure RNA単離試薬(Roche Diagnostics)を用いて、組織からトータルRNAを抽出した。260及び280nmでの光学密度を測定することにより濃度及び純度を確かめた。1%アガロースゲル電気泳動(Eurobio)により完全性を検証した。β-アクチンを参照として使用する半定量逆転写ポリメラーゼ連鎖反応(RT-PCR)によりmRNA濃度を測定した。プライマー配列を表1に示す。各標的mRNAについて、最終容量25μL中の100UのM-MLV Reverse Transcriptase(Promega)、5μLのM-MLV RT 5×緩衝剤、20UのRNasinリボヌクレアーゼインヒビター、12ピコモルのデオキシヌクレオシド三リン酸及び15ピコモルの特異的アンチセンスプライマーを用い、0.1μgのトータルRNAからRTを実施した。反応は、70℃にて5分間(RNA及びアンチセンスプライマー)、次いで42℃にて60分間(全ミックス)、続いて70℃にて15分間からなった。冷却後、5μLをPCR反応に使用した。5μLのRT媒体を、6ピコモルのMgCl2、8ピコモルのデオキシヌクレオシド三リン酸、2.5UのREDTad DNAポリメラーゼ(Sigma)、15ピコモルの対応するアンチセンスプライマー及び22.5ピコモルのセンスプライマーを含有する45μLのPCRミックス(5μL 10×REDTaq PCR緩衝剤)に添加した。PCR条件は、94℃にて2分間、続いてUCP3、UCP2及びβ-アクチンについてそれぞれ28サイクル、35サイクル又は18サイクル(1サイクル=94℃にて1分間、60℃にて1分間、72℃にて1分間)であった。PCRを72℃にて10分間で終了した。生成物を、臭化エチジウムで予め染色した2%アガロースゲル上で分析した。相対的バンド強度の定量のために、Camera DC120(Kodak)で写真を撮影し、Kodak Digital Science 1D 2.0(Kodak Scientific Imaging System)を用いて、各サンプルについてβ-アクチンに対する各標的の比を決定した。
2.結果
図1(A、B及びC)に示されるように、コントロール(プラシーボ処置)Wistarラットの身体は、34日間で150g(1A)及び21日間で約60g(1B)の正常な成長速度を示している。高用量の3,5-T2(図1A)又は3,3'-T2(図1C)のいずれかで処置した動物は、類似の体重増加を示さなかった。3,5-T2で処置した群では、二相性曲線が観察され、10日目と15日目の間に体重増加を有し、その後ボディマスは、低3,5-T2(図1B)又は高3,3-T2投薬量(1C)のいずれでの処置での場合のように、変化しなかった。
このことは、これら若齢成体動物における正常体重増加の非常に強力な防止を示している。
図1(A、B及びC)に示されるように、コントロール(プラシーボ処置)Wistarラットの身体は、34日間で150g(1A)及び21日間で約60g(1B)の正常な成長速度を示している。高用量の3,5-T2(図1A)又は3,3'-T2(図1C)のいずれかで処置した動物は、類似の体重増加を示さなかった。3,5-T2で処置した群では、二相性曲線が観察され、10日目と15日目の間に体重増加を有し、その後ボディマスは、低3,5-T2(図1B)又は高3,3-T2投薬量(1C)のいずれでの処置での場合のように、変化しなかった。
このことは、これら若齢成体動物における正常体重増加の非常に強力な防止を示している。
図2(A、B及びC)に示されるように、プラシーボ群の食物摂取は、実験期間にわたって約30gの食物/日で安定であった。食物摂取は低用量3,5-T2処置ではほとんど影響されななかった(又は僅かに減少、図2B)が、高投薬量3,5-T2群(図2A)では明らかな増加が観察され、3,3'-T2で二相性効果が観察された:初期の減少に続いて、10日目より後の増加。
それ故、両処置動物群の体重減少は、食物摂取の変化無しか又は増加と関連していた。
それ故、両処置動物群の体重減少は、食物摂取の変化無しか又は増加と関連していた。
ラットのエネルギー消費(EE)は間接熱量測定(材料及び方法の章を参照)により評価し、値は24時間(=1440分間)にわたって分析した。プラシーボ(図3A及び3B)、低用量3,5-T2(図3A)又は3,3'-T2(図3B)で処置した2群の動物は、これらげっ歯類の当然の古典的な夜行性の活動及び摂食行動並びに対照的な昼間の不活発という昼夜変化を示した。両処置ラット群は、コントロール値の25〜30に達するエネルギー消費の劇的な増加を示した。この差は、2.5μg/100g bwが与えられた3,5-T2と比較して、より高量のホルモン(25μg/100g bw)を与えられた3,3'-T2群でより顕著に現れた。
この非常に重要な結果は、代謝消費が2つの処置によって夜間及び昼間の両方で大いに増加することを示している。
呼吸商(RQ)は、放出二酸化炭素と消費酸素との間の比VCO2/VO2と定義される。この比が酸化される基質の起源(炭水化物 対 脂質)を示すことは概して受け容れられている。この値は炭水化物が専らエネルギー源であるとき1に等しくなり、脂質が唯一のエネルギー基質であると0.7に等しくなる。
呼吸商(RQ)は、放出二酸化炭素と消費酸素との間の比VCO2/VO2と定義される。この比が酸化される基質の起源(炭水化物 対 脂質)を示すことは概して受け容れられている。この値は炭水化物が専らエネルギー源であるとき1に等しくなり、脂質が唯一のエネルギー基質であると0.7に等しくなる。
EEについて既に示したように、RQもまた昼夜で変化する(図4A及び4B)。RQは、夜間、動物が摂食し、したがってより多くの炭水化物を酸化しているときにはより高くなる。逆に、昼間は、RQはより低くなり、脂質が優勢な基質である絶食状態を示す。3,5-T2低用量(図4A)に関して、RQは、昼間及び夜間の最初の部分では、プラシーボ処置でのRQより低く、夜間の終時にはほとんど同じであるように見える。一般に、そして昼夜の変化を考慮すれば、RQは、高3,3'-T2と比較して、低3,5-T2の群でより低い。このことは、より高い割合の炭水化物又は(より可能性が高いのは)炭水化物からの正味の脂質合成のいずれかを示し得る(1より高いRQ値に至る)。これら動物により示される値は、給餌状態の間の基質酸化及び基質(脂質合成)の合計である。
高用量3,5-T2(図5A)又はプラシーボで処置したラットの身体組成の変化は、絶対値(g)又はトータルボディマスのパーセンテージの両方として提示する。なぜならば、この2つの動物群は3週間後に同じ質量を示さなかったからである(図1Aを参照)。
全ての部位の脂肪質量は、プラシーボ(図5A)と比較して、3,5-T2群で有意に低かった(p<0.01)。この差は、データを絶対値で表わそうが相対値で表わそうが非常に実質的であった(腸間膜相対質量を除く)。興味深いことに、筋肉質量は全く影響を受けなかった(図5B)一方で、褐色脂肪組織(代謝効率及び熱生成に関与することが知られている組織)は、3,5-T2処置動物で有意に増加した(図5C)。
これら結果は、3,5-T2処置後のボディマスの減少が脂肪質量の損失に純粋に起因し、除脂肪ボディマスは影響されないことを明確に示している。
これら結果は、3,5-T2処置後のボディマスの減少が脂肪質量の損失に純粋に起因し、除脂肪ボディマスは影響されないことを明確に示している。
類似の結果が3,5-T2低用量(図6A、6B及び6C)又は3,3'-T2(図7A、7B及び7C)で得られ、脂肪質量(有意に減少)及び除脂肪ボディマス(影響なし)に対するそれらの効果に関して同じ結論への到達を導いた。興味深いことに、褐色脂肪組織は3,3'-T2処置(高用量)によって有意に増加したが、低用量の3,5-T2では増加しなかった。
非常に興味深いことに、遺伝的肥満ラット(すわわち、レプチンシグナル伝達経路に遺伝的欠損を有する、Fa/Fa)では、動物成長の強い阻止も観察された。プラシーボでは30日間で+170g、これに対し、低3,5-T2群(図8A)では有意な成長はなかった一方で、食物摂取はプラシーボと比較して有意に低かった(図8B)。両動物の容貌の差は著しい(図8C)。
Wistarラットでの観察と同様に、全ての部位で脂肪沈着の絶対値は、3,5-T2処置動物で有意に低かった。減少は皮下部位に関して特に劇的であった(図9A)。筋肉質量は影響されず(図9B)、褐色脂肪組織は有意に増加した(図9C)。
Wistarラットでの観察と同様に、全ての部位で脂肪沈着の絶対値は、3,5-T2処置動物で有意に低かった。減少は皮下部位に関して特に劇的であった(図9A)。筋肉質量は影響されず(図9B)、褐色脂肪組織は有意に増加した(図9C)。
対照的に、ZDFラットを調べると、動物成長に対する3,5-T2高用量の有意な効果は見出せなかった(図10A)一方で、プラシーボと比較して、脂肪質量増加はより少なく(図10B)、除脂肪ボディマス増加はより高かった(図10C)。更に、処置動物の中核体温は、プラシーボと比較して、より高かった(図10D)。この糖尿病動物モデルにおいて、インスリン分泌は、恐らく膵臓β細胞に対する高血漿グルコースの進行性の「糖毒性(gluco-toxicity)」のために、徐々に損なわれる(下記参照)ことに留意することが重要である。よって、これら糖尿病動物の成長速度は、肥満非糖尿病同腹仔の成長速度より遥かに小さい(図8A(+170g)及び10A(ほとんど変化無し)のプラシーボ群の成長速度と比較)。興味深いことに、3,5-T2群では中程度ではあるが明白な成長が存在する。このことは毒性効果がより小さいことを示唆している。
図11Dに示されるように、処置の終時では、コレステロールは、3,5-T2で処置したZDFラットの群では有意に低かった一方で、トリグリセリドレベルは2群間で異ならなかった。
肝臓ミトコンドリア呼吸鎖のレベルで、酸化とリン酸化との間の共役の効力に対する両処置(3,5-T2、高用量及び低用量、又は3,3'-T2)の効果を評価した(図12)。異なる条件グルタメート/マレート、スクシネート-ロテノン、グルタメート/マレート/スクシネート、パルミトイルCoA、オクタノイルCoAは、呼吸鎖に提供される異なる基質を示している。図12A(3,5-T2高投薬量)、12C(3,5-T2低投薬量)及び12E(3,3'-T2)は、種々の基質供給でリン酸化条件(すわわち、ADPの存在下)にて達成される肝臓ミトコンドリアの最大呼吸数を表す:TMPDアスコルベートは、DNPによる非共役状態でないか又は非共役状態である複合体4(シトクロムcオキシダーゼ)を調べる。概略的に、全ての条件で、処置は非常に有意な呼吸数増加に関与した。このことは、処置が全ての基質(脂肪酸を含む)について最大呼吸容量を増加させたことを示している。
非リン酸化性(すわわち、オリゴマイシンの存在下)のミトコンドリアの呼吸数を、異なる処置動物群(3,5-T2 高用量及び低用量、又は3,3'-T2:それぞれ図12B、12D及び12F)対プラシーボで測定した。プラシーボと比較して、低3,5-T2群のみで、呼吸は実質的に高かった。
非常に興味深いことに、筋肉ミトコンドリアで完全に異なる結果が得られた。事実、3,5-T2低及び高投薬量並びに3,3'-T2は、リン酸化状態(状態3、図14A、14B及び14C)及び非リン酸化状態(状態4、図15A、15B及び15C)の両方に実質的に影響しなかった。
非常に興味深いことに、筋肉ミトコンドリアで完全に異なる結果が得られた。事実、3,5-T2低及び高投薬量並びに3,3'-T2は、リン酸化状態(状態3、図14A、14B及び14C)及び非リン酸化状態(状態4、図15A、15B及び15C)の両方に実質的に影響しなかった。
よって、このことは、低及び高投薬量の3,5-T2並びに3,3'-T2の両方が肝臓ミトコンドリアに対して強力な効果を示すが、薬剤が全ての組織に対して投与された(ペレットからの皮下徐放)という事実にもかかわらず、筋肉ミトコンドリアに対しては効果はほとんど見出せなかったことを示した。
図15は、Wistarラット(図15A)及びZuckerラット(図15B)における、処置の終時でのグルコースに対する3,5-T2及び3,3'-T2の効果を示す。これら非糖尿病動物では、処置は、Wistarで増加するか、又はZuckerで減少するかのいずれかの僅かな変化に関与するのみであった。
トリグリセリド(図16A及び16B)及びコレステロール(図17A及び17B)は、Wistar、Zucker及びZDFラットにおいて全ての処置で減少した一方で、遊離脂肪酸(図18A及び18B)は増加した。このことは、間接熱量測定で得られたデータによって既に示唆されているように、高率の脂肪分解及び脂肪酸酸化を示している。HDL(図19A及び19B)はZucker又はZDFラットでのみ減少した。血漿脂肪酸は、動物で観察されたように、より高かった。
最後に、図20(A及びB)に示した、酸化的リン酸化(ATP/酸素比)の効率を直接調べたデータは、3,5-T2が、脂肪酸(パルミトイル-及びオクタノイル-CoAの両方)及びスクシネート(図20B、20C及び20D)でのATP合成の収率を低下させることを示している。
最後に、図20(A及びB)に示した、酸化的リン酸化(ATP/酸素比)の効率を直接調べたデータは、3,5-T2が、脂肪酸(パルミトイル-及びオクタノイル-CoAの両方)及びスクシネート(図20B、20C及び20D)でのATP合成の収率を低下させることを示している。
結論として、ボディマスで観察された劇的効果は脂肪質量の減少により完全に説明される一方で、除脂肪ボディマス(筋肉質量)は影響されないようである。食物消費の増加にもかかわらず観察されるこの効果は、間接熱量測定により証明されたエネルギー消費の増加に起因する。これら動物の正常食餌は脂質含量(4〜5%)がむしろ乏しいので、脂肪酸化の増加は、脂肪質量の強力な減少によって示されるように脂肪貯蔵の消費によって達成され、恐らくは消費性経路であるデノボ脂質生成(食餌期間に観察されたより高いRQを説明するかもしれない)によっても達成される。エネルギー代謝(間接熱量測定)の全体的増加に関するデータは、肝臓単離ミトコンドリアで得られたデータと非常に良好に一致し、このことは、呼吸鎖及びATP合成のレベルで、有意により高い最大呼吸容量に関連するエネルギー浪費プロセスが恐らく存在していることを示している。最も驚くべきことには、これら効果のいずれもが筋肉ミトコンドリアでは観察されないことである。このことは、浪費プロセスが筋肉質量より肝臓に大きく影響し、脂質酸化に関わることを示している。
よって、全体として、高及び低投薬量の3,5-T2並びに3,3'-T2の両方が脂質酸化及びエネルギー消費を亢進して、脂肪組織のみで質量の顕著な減少を導く。
実施例2:糖尿病の治療のための3,5-T2ホルモンの使用
1.材料及び方法
材料及び方法は実施例1に記載したものである。
動物
ラットは、遺伝的肥満の正常血糖ラット(Zucker又はFa/Fa)、10〜11週齢糖尿病ラット(ZDF)又は遺伝的非過体重糖尿病(2型糖尿病)ラット(Goto-Kakizaki(GK)モデル)であった。
1.材料及び方法
材料及び方法は実施例1に記載したものである。
動物
ラットは、遺伝的肥満の正常血糖ラット(Zucker又はFa/Fa)、10〜11週齢糖尿病ラット(ZDF)又は遺伝的非過体重糖尿病(2型糖尿病)ラット(Goto-Kakizaki(GK)モデル)であった。
血液採取
一晩(18時間)の絶食期間の後、この研究の当日に、覚醒ラットにおいて尾静脈から血液採取を行う。
一晩(18時間)の絶食期間の後、この研究の当日に、覚醒ラットにおいて尾静脈から血液採取を行う。
血液パラメータ
以下の生化学的パラメータを分析した:血糖、インスリン血、HbA1c、TG及びコレステロール。
甲状腺刺激ホルモン(TSH)及びチロキシン(T4)を、ラット標準(TSH及びT4についてそれぞれ、RPA 554 Amersham bioscience,RIA FT4-immunotech)を用いるラジオイムノアッセイにより測定した。
インスリンレベルは市販キット(Linco Research)で決定した。
グルコース及び3-ヒドロキシブチレート(3-HB)は酵素的に測定し、非エステル化脂肪酸(NEFA)は熱量測定アッセイ(Wako Chemicals)により測定した。
トリグリセリド及びコレステロールは、古典的なルーチン自動装置により測定した。
以下の生化学的パラメータを分析した:血糖、インスリン血、HbA1c、TG及びコレステロール。
甲状腺刺激ホルモン(TSH)及びチロキシン(T4)を、ラット標準(TSH及びT4についてそれぞれ、RPA 554 Amersham bioscience,RIA FT4-immunotech)を用いるラジオイムノアッセイにより測定した。
インスリンレベルは市販キット(Linco Research)で決定した。
グルコース及び3-ヒドロキシブチレート(3-HB)は酵素的に測定し、非エステル化脂肪酸(NEFA)は熱量測定アッセイ(Wako Chemicals)により測定した。
トリグリセリド及びコレステロールは、古典的なルーチン自動装置により測定した。
2.結果
図11A及び15Bに示されるように、高投薬量の3,5-T2は、1週間後に既に、ZDFラットの血漿グルコース濃度の劇的な減少を生じ、この効果は、4週間の実験期間にわたって存在する。この血中グルコース低下効果は、慢性高血糖の良好なマーカーである糖化ヘモグロビン(HbA1c)の有意な減少によって確証される(図11B)。この効果は、処置群においては、インスリン濃度の高レベルでの維持を伴い、対照的にプラシーボ群ではインスリンレベルは時間に伴って徐々に減少する(図11C)。コントロールZDFラットにおけるインスリンレベルの減少は、膵臓β細胞に対する高グルコースの毒性効果に関連するインスリン分泌の減少によって説明される。よって、実験期間全体を通じての高インスリンレベルの維持は、β細胞の保護を示し、この保護は血中グルコースの低下、細胞死の予防又は再生プロセスのいずれかに起因し得る。いずれにせよ、この結果は、処置群における膵臓によるより高いインスリン分泌を示している。
図11A及び15Bに示されるように、高投薬量の3,5-T2は、1週間後に既に、ZDFラットの血漿グルコース濃度の劇的な減少を生じ、この効果は、4週間の実験期間にわたって存在する。この血中グルコース低下効果は、慢性高血糖の良好なマーカーである糖化ヘモグロビン(HbA1c)の有意な減少によって確証される(図11B)。この効果は、処置群においては、インスリン濃度の高レベルでの維持を伴い、対照的にプラシーボ群ではインスリンレベルは時間に伴って徐々に減少する(図11C)。コントロールZDFラットにおけるインスリンレベルの減少は、膵臓β細胞に対する高グルコースの毒性効果に関連するインスリン分泌の減少によって説明される。よって、実験期間全体を通じての高インスリンレベルの維持は、β細胞の保護を示し、この保護は血中グルコースの低下、細胞死の予防又は再生プロセスのいずれかに起因し得る。いずれにせよ、この結果は、処置群における膵臓によるより高いインスリン分泌を示している。
更に、10日間の間に低投薬量3,5-T2(2.5μg/100g BW)で処置したGKラットは、コントロール動物(血中グルコース濃度2.64±0.21g/l(n=22))と比較して、血中グルコース濃度の有意な減少を示す(−24±6%(n=5、p<0.01))。10日間の処置後に既に生じた血中グルコースのこの減少は、高血糖がインスリン欠損及びインスリン抵抗性の両方に起因すると考えられているこのモデルにおける高血糖(糖尿病)状態の改善を示している。
結論として、3,5-T2は、重篤な「2型」糖尿病のモデル(ZDFラット)において、インスリンの増加に伴う特徴である血中グルコースの劇的な減少に関与する。このことはインスリン感受性及びインスリン分泌の増加を示している。従来、治療は、このような動物において、糖尿病の発症を遅延させるのみであり、糖尿病を矯正しないと考えられていたので、この重要な特徴は新規である。
結論として、3,5-T2は、重篤な「2型」糖尿病のモデル(ZDFラット)において、インスリンの増加に伴う特徴である血中グルコースの劇的な減少に関与する。このことはインスリン感受性及びインスリン分泌の増加を示している。従来、治療は、このような動物において、糖尿病の発症を遅延させるのみであり、糖尿病を矯正しないと考えられていたので、この重要な特徴は新規である。
Claims (14)
- 高血糖、インスリン抵抗性、β膵臓細胞不全又は関連する病状の中から選択される病状の治療用を意図した薬剤の製造のための、3,5-ジヨードチロニン、3',3-ジヨードチロニン、3',5-ジヨードチロニン、3'-ヨードチロニン、3-ヨードチロニン又は5-ヨードチロニンの中から選択される少なくとも1つのホルモンの使用。
- 前記ホルモンが3,5-ジヨードチロニン、3',3-ジヨードチロニン又は3',5-ジヨードチロニンの中から選択される請求項1に記載の使用。
- 糖尿病、特に1型又は2型糖尿病の治療用である請求項1又は2に記載の使用。
- 活性物質として、3,5-ジヨードチロニン、3',3-ジヨードチロニン、3',5-ジヨードチロニン、3'-ヨードチロニン、3-ヨードチロニン又は5-ヨードチロニンの中から選択される少なくとも1つのホルモンを、皮下又は経皮経路を介する投与に適切である医薬的に許容され得るビヒクルと組み合せて含んでなる医薬組成物。
- 前記医薬的に許容され得るビヒクルが前記活性物質の連続放出、好ましくは定常放出を可能にする請求項4に記載の医薬組成物。
- 約0.01μg/kg/日〜約250μg/kg/日、特に約0.01μg/kg/日〜約25μg/kg/日、特に約0.1μg/kg/日〜約15μg/kg/日の活性物質、更に特には約0.1μg/kg/日〜約5μg/kg/日の活性物質、最も特には約0.1μg/kg/日〜1μg/kg/日の活性物質の放出に適切な形態である請求項4又は5に記載の医薬組成物。
- 投薬単位基準で、約5μg〜約1.5gの活性物質、特に約75mg〜約750mgの活性物質を含んでなる請求項4〜6のいずれか1項に記載の医薬組成物。
- 前記医薬的に許容され得るビヒクルが皮膚透過性の亢進に使用される化学物質、例えばアルコールである請求項4〜7のいずれか1項に記載の医薬組成物。
- − 高血糖、インスリン抵抗性、β膵臓細胞不全、糖尿病又は関連する病状、
− 肥満、過体重又は関連する病状、高コレステロール血症、高トリグリセリド血症、異脂肪血症、アルコール肝炎性及び非アルコール肝炎性皮脂欠乏症、アテローム性動脈硬化症、代謝異常に伴うヘパトパシー、胆嚢疾患、皮下脂肪の沈着、特にセリュライト、又は血管運動神経性鼻炎
の中から選択される病状の治療用を意図した薬剤の製造のための、3,5-ジヨードチロニン、3',3-ジヨードチロニン、3',5-ジヨードチロニン、3'-ヨードチロニン、5'-ヨードチロニン、3-ヨードチロニン又は5-ヨードチロニンの中から選択される少なくとも1つのホルモンの使用であって、前記ホルモン及び前記医薬的に許容され得るビヒクルが皮下又は経皮経路を介する投与に適切な形態にある使用。 - 高血糖、インスリン抵抗性、β膵臓細胞不全又は関連する病状の治療用である請求項9に記載の使用。
- 糖尿病、特に1型又は2型糖尿病の治療用である請求項9又は10に記載の使用。
- 前記医薬的に許容され得るビヒクルが前記活性物質の連続放出、好ましくは定常放出を可能にする請求項9〜11のいずれか1項に記載の使用。
- 前記ホルモン及び前記医薬的に許容され得るビヒクルが、約0.01μg/kg/日〜約250μg/kg/日、特に約0.01μg/kg/日〜約25μg/kg/日、特に約0.1μg/kg/日〜約15μg/kg/日の活性物質、更に特には約0.1μg/kg/日〜約5μg/kg/日の活性物質、最も特には約0.1μg/kg/日〜1μg/kg/日の活性物質の放出に適切な形態にある請求項9〜12のいずれか1項に記載の使用。
- 糖尿病の治療用を意図した同時、別々又は逐次使用のための組合せ品として
− 3,5-ジヨードチロニン、3',3-ジヨードチロニン、3',5-ジヨードチロニン、3'-ヨードチロニン、3-ヨードチロニン又は5-ヨードチロニンの中から選択される少なくとも1つのホルモンと、
− 特に抗糖尿病経口薬剤から選択されるインスリンの膵臓分泌を活性化する少なくとも1つの活性物質、又はグルコースの消化吸収の緩徐化を可能にする少なくとも1つの活性物質とを
含んでなる製品。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP07290634 | 2007-05-16 | ||
| PCT/EP2008/056074 WO2008138993A1 (en) | 2007-05-16 | 2008-05-16 | New pharmaceutical compositions comprising diiodothyronine and their therapeutic use |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010526857A true JP2010526857A (ja) | 2010-08-05 |
| JP2010526857A5 JP2010526857A5 (ja) | 2011-06-23 |
Family
ID=38521888
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010507937A Withdrawn JP2010526857A (ja) | 2007-05-16 | 2008-05-16 | ジヨードチロニンを含んでなる新規な医薬組成物及びその治療的使用 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20110028554A1 (ja) |
| EP (1) | EP2068858A1 (ja) |
| JP (1) | JP2010526857A (ja) |
| CA (1) | CA2687380A1 (ja) |
| WO (1) | WO2008138993A1 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1992341A1 (en) * | 2007-05-16 | 2008-11-19 | Université Joseph Fourier | New pharmaceutical compositions comprising a thyroid hormon and their therapeutic use |
| US20120065267A1 (en) * | 2010-09-09 | 2012-03-15 | T*Amine, Llc | Compositions including 3,5-l-t2 and methods of use thereof |
| CN104737016B (zh) | 2012-08-20 | 2017-09-29 | 大塚制药株式会社 | 测定糖代谢能力的方法及用于该方法的组合物 |
| CN105051533B (zh) | 2013-03-15 | 2019-03-26 | 大塚制药株式会社 | 基于脂肪酸燃烧的测定胰岛素抵抗性的方法及用于该方法的组合物 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3067247A (en) * | 1958-08-19 | 1962-12-04 | Hoechst Ag | Process for preparing l(+)-3, 5-diiodothyronine |
| US4426453A (en) * | 1980-09-18 | 1984-01-17 | Amersham International Limited | Derivatives of iodothyronine compounds and their use in an assay for the free iodothyronine compounds |
| US5767227A (en) * | 1989-11-03 | 1998-06-16 | Lotus Biochemical Corp. | Iodothyronine polymers |
| US6221911B1 (en) * | 1995-06-07 | 2001-04-24 | Karo Bio Ab | Uses for thyroid hormone compounds or thyroid hormone-like compounds |
| US5635209A (en) * | 1995-10-31 | 1997-06-03 | Vintage Pharmaceuticals, Inc. | Stabilized composition of levothyroxine sodium medication and method for its production |
| US7163918B2 (en) * | 2000-08-22 | 2007-01-16 | New River Pharmaceuticals Inc. | Iodothyronine compositions |
| ITRM20030363A1 (it) * | 2003-07-24 | 2005-01-25 | Fernando Goglia | Composizioni comprendenti la 3, 5diiodotironina e uso farmaceutico di esse. |
-
2008
- 2008-05-16 CA CA002687380A patent/CA2687380A1/en not_active Abandoned
- 2008-05-16 JP JP2010507937A patent/JP2010526857A/ja not_active Withdrawn
- 2008-05-16 WO PCT/EP2008/056074 patent/WO2008138993A1/en active Application Filing
- 2008-05-16 US US12/600,109 patent/US20110028554A1/en not_active Abandoned
- 2008-05-16 EP EP08759706A patent/EP2068858A1/en not_active Withdrawn
Also Published As
| Publication number | Publication date |
|---|---|
| US20110028554A1 (en) | 2011-02-03 |
| WO2008138993A1 (en) | 2008-11-20 |
| EP2068858A1 (en) | 2009-06-17 |
| CA2687380A1 (en) | 2008-11-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Wessels et al. | Metformin impairs mitochondrial function in skeletal muscle of both lean and diabetic rats in a dose-dependent manner | |
| Abdul-Ghani et al. | Deleterious action of FA metabolites on ATP synthesis: possible link between lipotoxicity, mitochondrial dysfunction, and insulin resistance | |
| Casirola et al. | α-Glucosidase inhibitors prevent diet-induced increases in intestinal sugar transport in diabetic mice | |
| Hwang et al. | Fructose-induced insulin resistance and hypertension in rats. | |
| US5834032A (en) | Compositions and methods for treating diabetes | |
| Stevens et al. | Nicotinamide reverses neurological and neurovascular deficits in streptozotocin diabetic rats | |
| Watała et al. | Anti-diabetic effects of 1-methylnicotinamide (MNA) in streptozocin-induced diabetes in rats | |
| Tessari | Changes in protein, carbohydrate, and fat metabolism with aging: possible role of insulin | |
| JP2010526858A (ja) | 甲状腺ホルモンを含んでなる新たな医薬組成物及びその治療的使用 | |
| JP2010526857A (ja) | ジヨードチロニンを含んでなる新規な医薬組成物及びその治療的使用 | |
| Larner | D-chiro-inositol in insulin action and insulin resistance-old-fashioned biochemistry still at work. | |
| JPS61500496A (ja) | 膵臓のランゲルハンス島のインシュリン分泌を高めるためのシステイン誘導体またはその塩類の使用 | |
| Zhao et al. | HYPOGLYCAEMIC AND HYPOLIPIDAEMIC EFFECTS OF EMODIN AND ITS EFFECT ON L‐TYPE CALCIUM CHANNELS IN DYSLIPIDAEMIC–DIABETIC RATS | |
| Shimotoyodome et al. | Coingestion of acylglycerols differentially affects glucose-induced insulin secretion via glucose-dependent insulinotropic polypeptide in C57BL/6J mice | |
| FR3125409A1 (fr) | Complément alimentaire permettant de lutter contre l’infertilité féminine et masculine | |
| WO2014066830A1 (en) | Composition and methods for the prevention and treatment of diet-induced obesity | |
| Srivastava et al. | Polyherbal preparation for anti-diabetic activity: a screening study | |
| Srivastava et al. | Neutraceutical approaches to control diabetes: A natural requisite approach | |
| A Rendon | The bioenergetics of isolated mitochondria from different animal models for diabetes | |
| Weissman et al. | Starvation | |
| JP2005517716A (ja) | ヒトにおける老化および老化障害の治療法および予防的治療 | |
| JP2004215562A (ja) | 飲食物用添加剤、医薬組成物、glut4トランスロケート剤及びトランスロケート方法 | |
| RU2153878C1 (ru) | Способ получения лекарственных форм изониазида, обладающих пониженной гепатотоксичностью | |
| Becker | Rapid effects of estradiol on motivated behaviors | |
| Breuillé et al. | Assessment of tissue glutathione status during experimental sepsis |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110502 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110502 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20121002 |