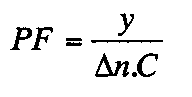JP2010526041A - 活性成分を制御放出するための自己沈澱製剤 - Google Patents
活性成分を制御放出するための自己沈澱製剤 Download PDFInfo
- Publication number
- JP2010526041A JP2010526041A JP2010504756A JP2010504756A JP2010526041A JP 2010526041 A JP2010526041 A JP 2010526041A JP 2010504756 A JP2010504756 A JP 2010504756A JP 2010504756 A JP2010504756 A JP 2010504756A JP 2010526041 A JP2010526041 A JP 2010526041A
- Authority
- JP
- Japan
- Prior art keywords
- formulation
- group
- polymer
- active ingredient
- cationic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 136
- 238000009472 formulation Methods 0.000 title claims abstract description 124
- 239000004480 active ingredient Substances 0.000 title claims abstract description 63
- 238000013270 controlled release Methods 0.000 title 1
- 229920000642 polymer Polymers 0.000 claims abstract description 207
- 239000000243 solution Substances 0.000 claims abstract description 97
- 125000002091 cationic group Chemical group 0.000 claims abstract description 76
- 125000000291 glutamic acid group Chemical group N[C@@H](CCC(O)=O)C(=O)* 0.000 claims abstract description 32
- 125000001165 hydrophobic group Chemical group 0.000 claims abstract description 30
- 238000012360 testing method Methods 0.000 claims abstract description 30
- 239000002245 particle Substances 0.000 claims abstract description 28
- 238000002360 preparation method Methods 0.000 claims abstract description 28
- 238000000034 method Methods 0.000 claims abstract description 26
- 239000007853 buffer solution Substances 0.000 claims abstract description 16
- 239000002253 acid Substances 0.000 claims abstract description 15
- 238000002156 mixing Methods 0.000 claims abstract description 8
- 239000007788 liquid Substances 0.000 claims abstract description 5
- 235000018102 proteins Nutrition 0.000 claims description 43
- 102000004169 proteins and genes Human genes 0.000 claims description 43
- 108090000623 proteins and genes Proteins 0.000 claims description 43
- -1 hetero atom cyclic compound Chemical class 0.000 claims description 36
- 230000002209 hydrophobic effect Effects 0.000 claims description 25
- 230000007935 neutral effect Effects 0.000 claims description 25
- 238000001556 precipitation Methods 0.000 claims description 21
- 239000012730 sustained-release form Substances 0.000 claims description 20
- 238000013268 sustained release Methods 0.000 claims description 19
- 102000006992 Interferon-alpha Human genes 0.000 claims description 15
- 108010047761 Interferon-alpha Proteins 0.000 claims description 15
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 13
- 150000001768 cations Chemical class 0.000 claims description 12
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 claims description 10
- 125000000217 alkyl group Chemical group 0.000 claims description 10
- 125000005842 heteroatom Chemical group 0.000 claims description 10
- 239000012669 liquid formulation Substances 0.000 claims description 10
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 claims description 8
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 claims description 8
- 150000003839 salts Chemical class 0.000 claims description 8
- ODHCTXKNWHHXJC-VKHMYHEASA-N 5-oxo-L-proline Chemical compound OC(=O)[C@@H]1CCC(=O)N1 ODHCTXKNWHHXJC-VKHMYHEASA-N 0.000 claims description 7
- 150000001413 amino acids Chemical class 0.000 claims description 7
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims description 7
- WHUUTDBJXJRKMK-VKHMYHEASA-L glutamate group Chemical group N[C@@H](CCC(=O)[O-])C(=O)[O-] WHUUTDBJXJRKMK-VKHMYHEASA-L 0.000 claims description 7
- 229920001223 polyethylene glycol Polymers 0.000 claims description 7
- 108700012941 GNRH1 Proteins 0.000 claims description 6
- 239000000579 Gonadotropin-Releasing Hormone Substances 0.000 claims description 6
- 150000003862 amino acid derivatives Chemical class 0.000 claims description 6
- 239000000122 growth hormone Substances 0.000 claims description 6
- 125000001453 quaternary ammonium group Chemical group 0.000 claims description 6
- 102000004127 Cytokines Human genes 0.000 claims description 5
- 108090000695 Cytokines Proteins 0.000 claims description 5
- 239000002202 Polyethylene glycol Substances 0.000 claims description 5
- 235000001014 amino acid Nutrition 0.000 claims description 5
- 239000000427 antigen Substances 0.000 claims description 5
- 102000036639 antigens Human genes 0.000 claims description 5
- 108091007433 antigens Proteins 0.000 claims description 5
- 125000004432 carbon atom Chemical group C* 0.000 claims description 5
- 229930195712 glutamate Natural products 0.000 claims description 5
- 230000014759 maintenance of location Effects 0.000 claims description 5
- 239000000843 powder Substances 0.000 claims description 5
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 claims description 4
- 102000007350 Bone Morphogenetic Proteins Human genes 0.000 claims description 4
- 108010007726 Bone Morphogenetic Proteins Proteins 0.000 claims description 4
- 102100023804 Coagulation factor VII Human genes 0.000 claims description 4
- 102400001368 Epidermal growth factor Human genes 0.000 claims description 4
- 101800003838 Epidermal growth factor Proteins 0.000 claims description 4
- 108010023321 Factor VII Proteins 0.000 claims description 4
- 102400000921 Gastrin Human genes 0.000 claims description 4
- 108010052343 Gastrins Proteins 0.000 claims description 4
- 108010088406 Glucagon-Like Peptides Proteins 0.000 claims description 4
- 102000004269 Granulocyte Colony-Stimulating Factor Human genes 0.000 claims description 4
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 claims description 4
- 102000004457 Granulocyte-Macrophage Colony-Stimulating Factor Human genes 0.000 claims description 4
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 claims description 4
- 108090001061 Insulin Proteins 0.000 claims description 4
- 102000004877 Insulin Human genes 0.000 claims description 4
- 102000007651 Macrophage Colony-Stimulating Factor Human genes 0.000 claims description 4
- 108010046938 Macrophage Colony-Stimulating Factor Proteins 0.000 claims description 4
- 108010025020 Nerve Growth Factor Proteins 0.000 claims description 4
- 102000015336 Nerve Growth Factor Human genes 0.000 claims description 4
- 229910019142 PO4 Inorganic materials 0.000 claims description 4
- 108010038512 Platelet-Derived Growth Factor Proteins 0.000 claims description 4
- 102000010780 Platelet-Derived Growth Factor Human genes 0.000 claims description 4
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 claims description 4
- 108060008682 Tumor Necrosis Factor Proteins 0.000 claims description 4
- 125000002877 alkyl aryl group Chemical group 0.000 claims description 4
- 125000000539 amino acid group Chemical group 0.000 claims description 4
- 150000001450 anions Chemical class 0.000 claims description 4
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 4
- 229940112869 bone morphogenetic protein Drugs 0.000 claims description 4
- AOXOCDRNSPFDPE-UKEONUMOSA-N chembl413654 Chemical compound C([C@H](C(=O)NCC(=O)N[C@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@H](CCSC)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC=1C=CC=CC=1)C(N)=O)NC(=O)[C@@H](C)NC(=O)[C@@H](CCC(O)=O)NC(=O)[C@@H](CCC(O)=O)NC(=O)[C@@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H]1N(CCC1)C(=O)CNC(=O)[C@@H](N)CCC(O)=O)C1=CC=C(O)C=C1 AOXOCDRNSPFDPE-UKEONUMOSA-N 0.000 claims description 4
- 229940012413 factor vii Drugs 0.000 claims description 4
- 229940125396 insulin Drugs 0.000 claims description 4
- 229940053128 nerve growth factor Drugs 0.000 claims description 4
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 claims description 4
- 239000010452 phosphate Substances 0.000 claims description 4
- 238000006116 polymerization reaction Methods 0.000 claims description 4
- 239000003488 releasing hormone Substances 0.000 claims description 4
- 239000007787 solid Substances 0.000 claims description 4
- 102000003390 tumor necrosis factor Human genes 0.000 claims description 4
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 claims description 4
- 108010088751 Albumins Proteins 0.000 claims description 3
- 102000009027 Albumins Human genes 0.000 claims description 3
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 claims description 3
- 108010036949 Cyclosporine Proteins 0.000 claims description 3
- 108090000790 Enzymes Proteins 0.000 claims description 3
- 102000004190 Enzymes Human genes 0.000 claims description 3
- 108010000817 Leuprolide Proteins 0.000 claims description 3
- 108091034117 Oligonucleotide Proteins 0.000 claims description 3
- 125000003545 alkoxy group Chemical group 0.000 claims description 3
- 125000003282 alkyl amino group Chemical group 0.000 claims description 3
- 150000001414 amino alcohols Chemical group 0.000 claims description 3
- 229960001265 ciclosporin Drugs 0.000 claims description 3
- 229930182912 cyclosporin Natural products 0.000 claims description 3
- 150000002009 diols Chemical group 0.000 claims description 3
- 229940088598 enzyme Drugs 0.000 claims description 3
- 150000001261 hydroxy acids Chemical group 0.000 claims description 3
- GFIJNRVAKGFPGQ-LIJARHBVSA-N leuprolide Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CC=C(O)C=C1 GFIJNRVAKGFPGQ-LIJARHBVSA-N 0.000 claims description 3
- 229960004338 leuprorelin Drugs 0.000 claims description 3
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims description 3
- 229920001515 polyalkylene glycol Polymers 0.000 claims description 3
- 108091033319 polynucleotide Proteins 0.000 claims description 3
- 239000002157 polynucleotide Substances 0.000 claims description 3
- 102000040430 polynucleotide Human genes 0.000 claims description 3
- 108010064733 Angiotensins Proteins 0.000 claims description 2
- 102000015427 Angiotensins Human genes 0.000 claims description 2
- 108010001478 Bacitracin Proteins 0.000 claims description 2
- 241000283690 Bos taurus Species 0.000 claims description 2
- 101800004538 Bradykinin Proteins 0.000 claims description 2
- 102400000967 Bradykinin Human genes 0.000 claims description 2
- 108010037003 Buserelin Proteins 0.000 claims description 2
- 108060001064 Calcitonin Proteins 0.000 claims description 2
- 102400000113 Calcitonin Human genes 0.000 claims description 2
- 108010078777 Colistin Proteins 0.000 claims description 2
- 102400000739 Corticotropin Human genes 0.000 claims description 2
- 101800000414 Corticotropin Proteins 0.000 claims description 2
- 102000018832 Cytochromes Human genes 0.000 claims description 2
- 108010052832 Cytochromes Proteins 0.000 claims description 2
- 108010092674 Enkephalins Proteins 0.000 claims description 2
- 108010074604 Epoetin Alfa Proteins 0.000 claims description 2
- 108090000394 Erythropoietin Proteins 0.000 claims description 2
- 102000003951 Erythropoietin Human genes 0.000 claims description 2
- 108010008165 Etanercept Proteins 0.000 claims description 2
- 102000003972 Fibroblast growth factor 7 Human genes 0.000 claims description 2
- 108090000385 Fibroblast growth factor 7 Proteins 0.000 claims description 2
- 102400000321 Glucagon Human genes 0.000 claims description 2
- 108060003199 Glucagon Proteins 0.000 claims description 2
- 102000003886 Glycoproteins Human genes 0.000 claims description 2
- 108090000288 Glycoproteins Proteins 0.000 claims description 2
- BLCLNMBMMGCOAS-URPVMXJPSA-N Goserelin Chemical compound C([C@@H](C(=O)N[C@H](COC(C)(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N1[C@@H](CCC1)C(=O)NNC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 BLCLNMBMMGCOAS-URPVMXJPSA-N 0.000 claims description 2
- 108010069236 Goserelin Proteins 0.000 claims description 2
- 108010026389 Gramicidin Proteins 0.000 claims description 2
- 102000018997 Growth Hormone Human genes 0.000 claims description 2
- 108010051696 Growth Hormone Proteins 0.000 claims description 2
- QXZGBUJJYSLZLT-UHFFFAOYSA-N H-Arg-Pro-Pro-Gly-Phe-Ser-Pro-Phe-Arg-OH Natural products NC(N)=NCCCC(N)C(=O)N1CCCC1C(=O)N1C(C(=O)NCC(=O)NC(CC=2C=CC=CC=2)C(=O)NC(CO)C(=O)N2C(CCC2)C(=O)NC(CC=2C=CC=CC=2)C(=O)NC(CCCN=C(N)N)C(O)=O)CCC1 QXZGBUJJYSLZLT-UHFFFAOYSA-N 0.000 claims description 2
- 108010054147 Hemoglobins Proteins 0.000 claims description 2
- 102000001554 Hemoglobins Human genes 0.000 claims description 2
- 108010022901 Heparin Lyase Proteins 0.000 claims description 2
- 102000014150 Interferons Human genes 0.000 claims description 2
- 108010050904 Interferons Proteins 0.000 claims description 2
- 108010002350 Interleukin-2 Proteins 0.000 claims description 2
- 102000015696 Interleukins Human genes 0.000 claims description 2
- 108010063738 Interleukins Proteins 0.000 claims description 2
- URLZCHNOLZSCCA-VABKMULXSA-N Leu-enkephalin Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(O)=O)NC(=O)CNC(=O)CNC(=O)[C@@H](N)CC=1C=CC(O)=CC=1)C1=CC=CC=C1 URLZCHNOLZSCCA-VABKMULXSA-N 0.000 claims description 2
- 229940124041 Luteinizing hormone releasing hormone (LHRH) antagonist Drugs 0.000 claims description 2
- 102100033342 Lysosomal acid glucosylceramidase Human genes 0.000 claims description 2
- 108010021717 Nafarelin Proteins 0.000 claims description 2
- 108010013106 O-raffinose cross-linked human hemoglobin Proteins 0.000 claims description 2
- 101800000989 Oxytocin Proteins 0.000 claims description 2
- 102400000050 Oxytocin Human genes 0.000 claims description 2
- XNOPRXBHLZRZKH-UHFFFAOYSA-N Oxytocin Natural products N1C(=O)C(N)CSSCC(C(=O)N2C(CCC2)C(=O)NC(CC(C)C)C(=O)NCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(CCC(N)=O)NC(=O)C(C(C)CC)NC(=O)C1CC1=CC=C(O)C=C1 XNOPRXBHLZRZKH-UHFFFAOYSA-N 0.000 claims description 2
- 108091006006 PEGylated Proteins Proteins 0.000 claims description 2
- 108010079943 Pentagastrin Proteins 0.000 claims description 2
- 108010040201 Polymyxins Proteins 0.000 claims description 2
- 102000003946 Prolactin Human genes 0.000 claims description 2
- 108010057464 Prolactin Proteins 0.000 claims description 2
- 102100028255 Renin Human genes 0.000 claims description 2
- 108090000783 Renin Proteins 0.000 claims description 2
- 102100037505 Secretin Human genes 0.000 claims description 2
- 108010086019 Secretin Proteins 0.000 claims description 2
- 102000005157 Somatostatin Human genes 0.000 claims description 2
- 108010056088 Somatostatin Proteins 0.000 claims description 2
- 108010039185 Tenecteplase Proteins 0.000 claims description 2
- 108010061174 Thyrotropin Proteins 0.000 claims description 2
- 102000011923 Thyrotropin Human genes 0.000 claims description 2
- 108090000373 Tissue Plasminogen Activator Proteins 0.000 claims description 2
- 102000003978 Tissue Plasminogen Activator Human genes 0.000 claims description 2
- 108010050144 Triptorelin Pamoate Proteins 0.000 claims description 2
- GXBMIBRIOWHPDT-UHFFFAOYSA-N Vasopressin Natural products N1C(=O)C(CC=2C=C(O)C=CC=2)NC(=O)C(N)CSSCC(C(=O)N2C(CCC2)C(=O)NC(CCCN=C(N)N)C(=O)NCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(CCC(N)=O)NC(=O)C1CC1=CC=CC=C1 GXBMIBRIOWHPDT-UHFFFAOYSA-N 0.000 claims description 2
- 102000002852 Vasopressins Human genes 0.000 claims description 2
- 108010004977 Vasopressins Proteins 0.000 claims description 2
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 claims description 2
- 125000002252 acyl group Chemical group 0.000 claims description 2
- 229960002964 adalimumab Drugs 0.000 claims description 2
- 125000005907 alkyl ester group Chemical group 0.000 claims description 2
- 229960003318 alteplase Drugs 0.000 claims description 2
- 229960002616 ancestim Drugs 0.000 claims description 2
- 108700024685 ancestim Proteins 0.000 claims description 2
- KBZOIRJILGZLEJ-LGYYRGKSSA-N argipressin Chemical compound C([C@H]1C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CSSC[C@@H](C(N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N1)=O)N)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCN=C(N)N)C(=O)NCC(N)=O)C1=CC=CC=C1 KBZOIRJILGZLEJ-LGYYRGKSSA-N 0.000 claims description 2
- 229960003071 bacitracin Drugs 0.000 claims description 2
- 229930184125 bacitracin Natural products 0.000 claims description 2
- CLKOFPXJLQSYAH-ABRJDSQDSA-N bacitracin A Chemical compound C1SC([C@@H](N)[C@@H](C)CC)=N[C@@H]1C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]1C(=O)N[C@H](CCCN)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2N=CNC=2)C(=O)N[C@H](CC(O)=O)C(=O)N[C@@H](CC(N)=O)C(=O)NCCCC1 CLKOFPXJLQSYAH-ABRJDSQDSA-N 0.000 claims description 2
- 229960000182 blood factors Drugs 0.000 claims description 2
- QXZGBUJJYSLZLT-FDISYFBBSA-N bradykinin Chemical compound NC(=N)NCCC[C@H](N)C(=O)N1CCC[C@H]1C(=O)N1[C@H](C(=O)NCC(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CO)C(=O)N2[C@@H](CCC2)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)CCC1 QXZGBUJJYSLZLT-FDISYFBBSA-N 0.000 claims description 2
- CUWODFFVMXJOKD-UVLQAERKSA-N buserelin Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](COC(C)(C)C)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CC=C(O)C=C1 CUWODFFVMXJOKD-UVLQAERKSA-N 0.000 claims description 2
- 229960002719 buserelin Drugs 0.000 claims description 2
- BBBFJLBPOGFECG-VJVYQDLKSA-N calcitonin Chemical compound N([C@H](C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(N)=O)C(C)C)C(=O)[C@@H]1CSSC[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1 BBBFJLBPOGFECG-VJVYQDLKSA-N 0.000 claims description 2
- 229960004015 calcitonin Drugs 0.000 claims description 2
- 229960005395 cetuximab Drugs 0.000 claims description 2
- 229960003346 colistin Drugs 0.000 claims description 2
- 229920001577 copolymer Polymers 0.000 claims description 2
- IDLFZVILOHSSID-OVLDLUHVSA-N corticotropin Chemical compound C([C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CC(N)=O)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(O)=O)NC(=O)[C@@H](N)CO)C1=CC=C(O)C=C1 IDLFZVILOHSSID-OVLDLUHVSA-N 0.000 claims description 2
- 229960000258 corticotropin Drugs 0.000 claims description 2
- 150000001923 cyclic compounds Chemical class 0.000 claims description 2
- 125000004427 diamine group Chemical group 0.000 claims description 2
- 229940056176 drotrecogin alfa Drugs 0.000 claims description 2
- 229940116977 epidermal growth factor Drugs 0.000 claims description 2
- 229960003388 epoetin alfa Drugs 0.000 claims description 2
- 108010002601 epoetin beta Proteins 0.000 claims description 2
- 229960004579 epoetin beta Drugs 0.000 claims description 2
- 229940105423 erythropoietin Drugs 0.000 claims description 2
- 229960000403 etanercept Drugs 0.000 claims description 2
- 125000003754 ethoxycarbonyl group Chemical group C(=O)(OCC)* 0.000 claims description 2
- 239000012634 fragment Substances 0.000 claims description 2
- MASNOZXLGMXCHN-ZLPAWPGGSA-N glucagon Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 MASNOZXLGMXCHN-ZLPAWPGGSA-N 0.000 claims description 2
- 229960004666 glucagon Drugs 0.000 claims description 2
- 150000004676 glycans Chemical class 0.000 claims description 2
- 125000003827 glycol group Chemical group 0.000 claims description 2
- 229960002913 goserelin Drugs 0.000 claims description 2
- 229960004905 gramicidin Drugs 0.000 claims description 2
- ZWCXYZRRTRDGQE-SORVKSEFSA-N gramicidina Chemical compound C1=CC=C2C(C[C@H](NC(=O)[C@@H](CC(C)C)NC(=O)[C@H](CC=3C4=CC=CC=C4NC=3)NC(=O)[C@@H](CC(C)C)NC(=O)[C@H](CC=3C4=CC=CC=C4NC=3)NC(=O)[C@@H](CC(C)C)NC(=O)[C@H](CC=3C4=CC=CC=C4NC=3)NC(=O)[C@H](C(C)C)NC(=O)[C@H](C(C)C)NC(=O)[C@@H](C(C)C)NC(=O)[C@H](C)NC(=O)[C@H](NC(=O)[C@H](C)NC(=O)CNC(=O)[C@@H](NC=O)C(C)C)CC(C)C)C(=O)NCCO)=CNC2=C1 ZWCXYZRRTRDGQE-SORVKSEFSA-N 0.000 claims description 2
- 239000003102 growth factor Substances 0.000 claims description 2
- 229960004732 hemoglobin raffimer Drugs 0.000 claims description 2
- 230000011132 hemopoiesis Effects 0.000 claims description 2
- 208000002672 hepatitis B Diseases 0.000 claims description 2
- 229960002127 imiglucerase Drugs 0.000 claims description 2
- 108010039650 imiglucerase Proteins 0.000 claims description 2
- 229960000598 infliximab Drugs 0.000 claims description 2
- 229940079322 interferon Drugs 0.000 claims description 2
- 125000005647 linker group Chemical group 0.000 claims description 2
- 125000001160 methoxycarbonyl group Chemical group [H]C([H])([H])OC(*)=O 0.000 claims description 2
- 238000012986 modification Methods 0.000 claims description 2
- 230000004048 modification Effects 0.000 claims description 2
- JORAUNFTUVJTNG-BSTBCYLQSA-N n-[(2s)-4-amino-1-[[(2s,3r)-1-[[(2s)-4-amino-1-oxo-1-[[(3s,6s,9s,12s,15r,18s,21s)-6,9,18-tris(2-aminoethyl)-3-[(1r)-1-hydroxyethyl]-12,15-bis(2-methylpropyl)-2,5,8,11,14,17,20-heptaoxo-1,4,7,10,13,16,19-heptazacyclotricos-21-yl]amino]butan-2-yl]amino]-3-h Chemical compound CC(C)CCCCC(=O)N[C@@H](CCN)C(=O)N[C@H]([C@@H](C)O)CN[C@@H](CCN)C(=O)N[C@H]1CCNC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCN)NC(=O)[C@H](CCN)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@H](CCN)NC1=O.CCC(C)CCCCC(=O)N[C@@H](CCN)C(=O)N[C@H]([C@@H](C)O)CN[C@@H](CCN)C(=O)N[C@H]1CCNC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCN)NC(=O)[C@H](CCN)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@H](CCN)NC1=O JORAUNFTUVJTNG-BSTBCYLQSA-N 0.000 claims description 2
- RWHUEXWOYVBUCI-ITQXDASVSA-N nafarelin Chemical compound C([C@@H](C(=O)N[C@H](CC=1C=C2C=CC=CC2=CC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N1[C@@H](CCC1)C(=O)NCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 RWHUEXWOYVBUCI-ITQXDASVSA-N 0.000 claims description 2
- 229960002333 nafarelin Drugs 0.000 claims description 2
- 229960000470 omalizumab Drugs 0.000 claims description 2
- XNOPRXBHLZRZKH-DSZYJQQASA-N oxytocin Chemical compound C([C@H]1C(=O)N[C@H](C(N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CSSC[C@H](N)C(=O)N1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CC(C)C)C(=O)NCC(N)=O)=O)[C@@H](C)CC)C1=CC=C(O)C=C1 XNOPRXBHLZRZKH-DSZYJQQASA-N 0.000 claims description 2
- 229960001723 oxytocin Drugs 0.000 claims description 2
- 229960000444 pentagastrin Drugs 0.000 claims description 2
- ANRIQLNBZQLTFV-DZUOILHNSA-N pentagastrin Chemical compound C([C@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1[C]2C=CC=CC2=NC=1)NC(=O)CCNC(=O)OC(C)(C)C)CCSC)C(N)=O)C1=CC=CC=C1 ANRIQLNBZQLTFV-DZUOILHNSA-N 0.000 claims description 2
- 229920001281 polyalkylene Polymers 0.000 claims description 2
- XDJYMJULXQKGMM-UHFFFAOYSA-N polymyxin E1 Natural products CCC(C)CCCCC(=O)NC(CCN)C(=O)NC(C(C)O)C(=O)NC(CCN)C(=O)NC1CCNC(=O)C(C(C)O)NC(=O)C(CCN)NC(=O)C(CCN)NC(=O)C(CC(C)C)NC(=O)C(CC(C)C)NC(=O)C(CCN)NC1=O XDJYMJULXQKGMM-UHFFFAOYSA-N 0.000 claims description 2
- KNIWPHSUTGNZST-UHFFFAOYSA-N polymyxin E2 Natural products CC(C)CCCCC(=O)NC(CCN)C(=O)NC(C(C)O)C(=O)NC(CCN)C(=O)NC1CCNC(=O)C(C(C)O)NC(=O)C(CCN)NC(=O)C(CCN)NC(=O)C(CC(C)C)NC(=O)C(CC(C)C)NC(=O)C(CCN)NC1=O KNIWPHSUTGNZST-UHFFFAOYSA-N 0.000 claims description 2
- 229920001282 polysaccharide Polymers 0.000 claims description 2
- 239000005017 polysaccharide Substances 0.000 claims description 2
- OXCMYAYHXIHQOA-UHFFFAOYSA-N potassium;[2-butyl-5-chloro-3-[[4-[2-(1,2,4-triaza-3-azanidacyclopenta-1,4-dien-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol Chemical compound [K+].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C2=N[N-]N=N2)C=C1 OXCMYAYHXIHQOA-UHFFFAOYSA-N 0.000 claims description 2
- 230000001376 precipitating effect Effects 0.000 claims description 2
- 229940097325 prolactin Drugs 0.000 claims description 2
- 229940043131 pyroglutamate Drugs 0.000 claims description 2
- 150000003254 radicals Chemical class 0.000 claims description 2
- 229960004641 rituximab Drugs 0.000 claims description 2
- 229960002101 secretin Drugs 0.000 claims description 2
- OWMZNFCDEHGFEP-NFBCVYDUSA-N secretin human Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(N)=O)[C@@H](C)O)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)C1=CC=CC=C1 OWMZNFCDEHGFEP-NFBCVYDUSA-N 0.000 claims description 2
- NHXLMOGPVYXJNR-ATOGVRKGSA-N somatostatin Chemical compound C([C@H]1C(=O)N[C@H](C(N[C@@H](CO)C(=O)N[C@@H](CSSC[C@@H](C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2C3=CC=CC=C3NC=2)C(=O)N[C@@H](CCCCN)C(=O)N[C@H](C(=O)N1)[C@@H](C)O)NC(=O)CNC(=O)[C@H](C)N)C(O)=O)=O)[C@H](O)C)C1=CC=CC=C1 NHXLMOGPVYXJNR-ATOGVRKGSA-N 0.000 claims description 2
- 229960000553 somatostatin Drugs 0.000 claims description 2
- 229960000216 tenecteplase Drugs 0.000 claims description 2
- 229960005267 tositumomab Drugs 0.000 claims description 2
- 108010078749 trafermin Proteins 0.000 claims description 2
- 229950009227 trafermin Drugs 0.000 claims description 2
- 229960000575 trastuzumab Drugs 0.000 claims description 2
- 150000004072 triols Chemical group 0.000 claims description 2
- VXKHXGOKWPXYNA-PGBVPBMZSA-N triptorelin Chemical compound C([C@@H](C(=O)N[C@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)NCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 VXKHXGOKWPXYNA-PGBVPBMZSA-N 0.000 claims description 2
- 229960004824 triptorelin Drugs 0.000 claims description 2
- 229960005486 vaccine Drugs 0.000 claims description 2
- 229960003726 vasopressin Drugs 0.000 claims description 2
- 229960000284 efalizumab Drugs 0.000 claims 1
- 239000003814 drug Substances 0.000 abstract description 15
- 239000007900 aqueous suspension Substances 0.000 abstract description 5
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 48
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 41
- 108010020346 Polyglutamic Acid Proteins 0.000 description 26
- 229920000370 gamma-poly(glutamate) polymer Polymers 0.000 description 26
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 24
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 22
- GVJHHUAWPYXKBD-IEOSBIPESA-N α-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-IEOSBIPESA-N 0.000 description 21
- 230000001225 therapeutic effect Effects 0.000 description 20
- 230000015572 biosynthetic process Effects 0.000 description 18
- 239000011780 sodium chloride Substances 0.000 description 18
- 238000003786 synthesis reaction Methods 0.000 description 16
- 239000002105 nanoparticle Substances 0.000 description 12
- 239000002244 precipitate Substances 0.000 description 12
- UMMQVDUMUMBTAV-YFKPBYRVSA-N (2s)-2-amino-3-(1h-imidazol-5-yl)propanamide Chemical compound NC(=O)[C@@H](N)CC1=CN=CN1 UMMQVDUMUMBTAV-YFKPBYRVSA-N 0.000 description 11
- 239000000725 suspension Substances 0.000 description 11
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 10
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 10
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 9
- SJRJJKPEHAURKC-UHFFFAOYSA-N N-Methylmorpholine Chemical compound CN1CCOCC1 SJRJJKPEHAURKC-UHFFFAOYSA-N 0.000 description 9
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 9
- 229940087168 alpha tocopherol Drugs 0.000 description 9
- 229940079593 drug Drugs 0.000 description 9
- 229960000984 tocofersolan Drugs 0.000 description 9
- 235000004835 α-tocopherol Nutrition 0.000 description 9
- 239000002076 α-tocopherol Substances 0.000 description 9
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 8
- OHDXDNUPVVYWOV-UHFFFAOYSA-N n-methyl-1-(2-naphthalen-1-ylsulfanylphenyl)methanamine Chemical compound CNCC1=CC=CC=C1SC1=CC=CC2=CC=CC=C12 OHDXDNUPVVYWOV-UHFFFAOYSA-N 0.000 description 8
- 230000036470 plasma concentration Effects 0.000 description 8
- 229920000867 polyelectrolyte Polymers 0.000 description 8
- GVJHHUAWPYXKBD-UHFFFAOYSA-N d-alpha-tocopherol Natural products OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 7
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- NTYJJOPFIAHURM-UHFFFAOYSA-N Histamine Chemical compound NCCC1=CN=CN1 NTYJJOPFIAHURM-UHFFFAOYSA-N 0.000 description 6
- 230000002378 acidificating effect Effects 0.000 description 6
- 125000000524 functional group Chemical group 0.000 description 6
- 229920001308 poly(aminoacid) Polymers 0.000 description 6
- 229920002643 polyglutamic acid Polymers 0.000 description 6
- 239000007864 aqueous solution Substances 0.000 description 5
- 230000000052 comparative effect Effects 0.000 description 5
- 150000002410 histidine derivatives Chemical class 0.000 description 5
- 102000004196 processed proteins & peptides Human genes 0.000 description 5
- 239000012429 reaction media Substances 0.000 description 5
- KBPLFHHGFOOTCA-UHFFFAOYSA-N 1-Octanol Chemical compound CCCCCCCCO KBPLFHHGFOOTCA-UHFFFAOYSA-N 0.000 description 4
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 4
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 4
- 150000001408 amides Chemical class 0.000 description 4
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 4
- 238000010382 chemical cross-linking Methods 0.000 description 4
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 4
- 238000007865 diluting Methods 0.000 description 4
- LQZZUXJYWNFBMV-UHFFFAOYSA-N dodecan-1-ol Chemical compound CCCCCCCCCCCCO LQZZUXJYWNFBMV-UHFFFAOYSA-N 0.000 description 4
- 239000013020 final formulation Substances 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- 229940049906 glutamate Drugs 0.000 description 4
- 238000001727 in vivo Methods 0.000 description 4
- 239000000178 monomer Substances 0.000 description 4
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 4
- 239000002243 precursor Substances 0.000 description 4
- HLZKNKRTKFSKGZ-UHFFFAOYSA-N tetradecan-1-ol Chemical compound CCCCCCCCCCCCCCO HLZKNKRTKFSKGZ-UHFFFAOYSA-N 0.000 description 4
- YOETUEMZNOLGDB-UHFFFAOYSA-N 2-methylpropyl carbonochloridate Chemical compound CC(C)COC(Cl)=O YOETUEMZNOLGDB-UHFFFAOYSA-N 0.000 description 3
- 238000002965 ELISA Methods 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- ULEBESPCVWBNIF-BYPYZUCNSA-N L-arginine amide Chemical compound NC(=O)[C@@H](N)CCCNC(N)=N ULEBESPCVWBNIF-BYPYZUCNSA-N 0.000 description 3
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- 241000700159 Rattus Species 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 3
- 229940024606 amino acid Drugs 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 230000008878 coupling Effects 0.000 description 3
- 238000010168 coupling process Methods 0.000 description 3
- 238000005859 coupling reaction Methods 0.000 description 3
- 150000004985 diamines Chemical class 0.000 description 3
- 238000002296 dynamic light scattering Methods 0.000 description 3
- 125000004494 ethyl ester group Chemical group 0.000 description 3
- 238000004108 freeze drying Methods 0.000 description 3
- 229960002989 glutamic acid Drugs 0.000 description 3
- 238000010438 heat treatment Methods 0.000 description 3
- 229960001340 histamine Drugs 0.000 description 3
- 238000000338 in vitro Methods 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 150000004702 methyl esters Chemical class 0.000 description 3
- 229910052760 oxygen Inorganic materials 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 125000006850 spacer group Chemical group 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 238000007920 subcutaneous administration Methods 0.000 description 3
- 229930003799 tocopherol Natural products 0.000 description 3
- 239000011732 tocopherol Substances 0.000 description 3
- 229960001295 tocopherol Drugs 0.000 description 3
- 235000010384 tocopherol Nutrition 0.000 description 3
- ALSTYHKOOCGGFT-KTKRTIGZSA-N (9Z)-octadecen-1-ol Chemical compound CCCCCCCC\C=C/CCCCCCCCO ALSTYHKOOCGGFT-KTKRTIGZSA-N 0.000 description 2
- BDNKZNFMNDZQMI-UHFFFAOYSA-N 1,3-diisopropylcarbodiimide Chemical compound CC(C)N=C=NC(C)C BDNKZNFMNDZQMI-UHFFFAOYSA-N 0.000 description 2
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 2
- 239000005695 Ammonium acetate Substances 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 2
- ZQISRDCJNBUVMM-UHFFFAOYSA-N L-Histidinol Natural products OCC(N)CC1=CN=CN1 ZQISRDCJNBUVMM-UHFFFAOYSA-N 0.000 description 2
- ZQISRDCJNBUVMM-YFKPBYRVSA-N L-histidinol Chemical compound OC[C@@H](N)CC1=CNC=N1 ZQISRDCJNBUVMM-YFKPBYRVSA-N 0.000 description 2
- 238000005481 NMR spectroscopy Methods 0.000 description 2
- 206010028980 Neoplasm Diseases 0.000 description 2
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 125000002947 alkylene group Chemical group 0.000 description 2
- 150000001412 amines Chemical group 0.000 description 2
- 125000003277 amino group Chemical group 0.000 description 2
- 229940043376 ammonium acetate Drugs 0.000 description 2
- 235000019257 ammonium acetate Nutrition 0.000 description 2
- 239000001961 anticonvulsive agent Substances 0.000 description 2
- 239000012736 aqueous medium Substances 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 229920001400 block copolymer Polymers 0.000 description 2
- 150000001718 carbodiimides Chemical class 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 229940107161 cholesterol Drugs 0.000 description 2
- 235000012000 cholesterol Nutrition 0.000 description 2
- 239000000084 colloidal system Substances 0.000 description 2
- 238000009833 condensation Methods 0.000 description 2
- 230000005494 condensation Effects 0.000 description 2
- 239000007822 coupling agent Substances 0.000 description 2
- BGRWYRAHAFMIBJ-UHFFFAOYSA-N diisopropylcarbodiimide Natural products CC(C)NC(=O)NC(C)C BGRWYRAHAFMIBJ-UHFFFAOYSA-N 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 235000019441 ethanol Nutrition 0.000 description 2
- 235000013922 glutamic acid Nutrition 0.000 description 2
- 239000004220 glutamic acid Substances 0.000 description 2
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 2
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 2
- 230000000147 hypnotic effect Effects 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 238000007912 intraperitoneal administration Methods 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- QYSGYZVSCZSLHT-UHFFFAOYSA-N octafluoropropane Chemical compound FC(F)(F)C(F)(F)C(F)(F)F QYSGYZVSCZSLHT-UHFFFAOYSA-N 0.000 description 2
- 229940055577 oleyl alcohol Drugs 0.000 description 2
- XMLQWXUVTXCDDL-UHFFFAOYSA-N oleyl alcohol Natural products CCCCCCC=CCCCCCCCCCCO XMLQWXUVTXCDDL-UHFFFAOYSA-N 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 239000008363 phosphate buffer Substances 0.000 description 2
- 229920000768 polyamine Polymers 0.000 description 2
- 150000003077 polyols Chemical class 0.000 description 2
- 239000001103 potassium chloride Substances 0.000 description 2
- 235000011164 potassium chloride Nutrition 0.000 description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 2
- 239000003368 psychostimulant agent Substances 0.000 description 2
- 230000002685 pulmonary effect Effects 0.000 description 2
- KIDHWZJUCRJVML-UHFFFAOYSA-N putrescine Chemical compound NCCCCN KIDHWZJUCRJVML-UHFFFAOYSA-N 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 150000003384 small molecules Chemical class 0.000 description 2
- 238000010254 subcutaneous injection Methods 0.000 description 2
- 239000007929 subcutaneous injection Substances 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- BGRJTUBHPOOWDU-NSHDSACASA-N (S)-(-)-sulpiride Chemical compound CCN1CCC[C@H]1CNC(=O)C1=CC(S(N)(=O)=O)=CC=C1OC BGRJTUBHPOOWDU-NSHDSACASA-N 0.000 description 1
- KWTSXDURSIMDCE-QMMMGPOBSA-N (S)-amphetamine Chemical compound C[C@H](N)CC1=CC=CC=C1 KWTSXDURSIMDCE-QMMMGPOBSA-N 0.000 description 1
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 1
- 238000005160 1H NMR spectroscopy Methods 0.000 description 1
- 206010000599 Acromegaly Diseases 0.000 description 1
- QYPPJABKJHAVHS-UHFFFAOYSA-N Agmatine Natural products NCCCCNC(N)=N QYPPJABKJHAVHS-UHFFFAOYSA-N 0.000 description 1
- 208000007848 Alcoholism Diseases 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 0 CC(C)NC(CCC(*)=O)C(C(C)(C)NC(CCC(NC(Cc1c[n]cn1)C(N)=O)=O)C(*(C)C(C)(C)NC(CCC(*)O)C(N)=O)=O)=O Chemical compound CC(C)NC(CCC(*)=O)C(C(C)(C)NC(CCC(NC(Cc1c[n]cn1)C(N)=O)=O)C(*(C)C(C)(C)NC(CCC(*)O)C(N)=O)=O)=O 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 206010011224 Cough Diseases 0.000 description 1
- 201000003883 Cystic fibrosis Diseases 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- QOSSAOTZNIDXMA-UHFFFAOYSA-N Dicylcohexylcarbodiimide Chemical compound C1CCCCC1N=C=NC1CCCCC1 QOSSAOTZNIDXMA-UHFFFAOYSA-N 0.000 description 1
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 1
- 201000009273 Endometriosis Diseases 0.000 description 1
- 208000010228 Erectile Dysfunction Diseases 0.000 description 1
- PLDUPXSUYLZYBN-UHFFFAOYSA-N Fluphenazine Chemical compound C1CN(CCO)CCN1CCCN1C2=CC(C(F)(F)F)=CC=C2SC2=CC=CC=C21 PLDUPXSUYLZYBN-UHFFFAOYSA-N 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- 102000002265 Human Growth Hormone Human genes 0.000 description 1
- 108010000521 Human Growth Hormone Proteins 0.000 description 1
- 239000000854 Human Growth Hormone Substances 0.000 description 1
- 102000003839 Human Proteins Human genes 0.000 description 1
- 108090000144 Human Proteins Proteins 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- AHLPHDHHMVZTML-BYPYZUCNSA-N L-Ornithine Chemical compound NCCC[C@H](N)C(O)=O AHLPHDHHMVZTML-BYPYZUCNSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- 229930195714 L-glutamate Natural products 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 208000026139 Memory disease Diseases 0.000 description 1
- 101001026869 Mus musculus F-box/LRR-repeat protein 3 Proteins 0.000 description 1
- 108010038807 Oligopeptides Proteins 0.000 description 1
- 102000015636 Oligopeptides Human genes 0.000 description 1
- AHLPHDHHMVZTML-UHFFFAOYSA-N Orn-delta-NH2 Natural products NCCCC(N)C(O)=O AHLPHDHHMVZTML-UHFFFAOYSA-N 0.000 description 1
- UTJLXEIPEHZYQJ-UHFFFAOYSA-N Ornithine Natural products OC(=O)C(C)CCCN UTJLXEIPEHZYQJ-UHFFFAOYSA-N 0.000 description 1
- 208000001132 Osteoporosis Diseases 0.000 description 1
- RGCVKNLCSQQDEP-UHFFFAOYSA-N Perphenazine Chemical compound C1CN(CCO)CCN1CCCN1C2=CC(Cl)=CC=C2SC2=CC=CC=C21 RGCVKNLCSQQDEP-UHFFFAOYSA-N 0.000 description 1
- 229920002873 Polyethylenimine Polymers 0.000 description 1
- 239000004721 Polyphenylene oxide Substances 0.000 description 1
- 239000005700 Putrescine Substances 0.000 description 1
- GUGOEEXESWIERI-UHFFFAOYSA-N Terfenadine Chemical compound C1=CC(C(C)(C)C)=CC=C1C(O)CCCN1CCC(C(O)(C=2C=CC=CC=2)C=2C=CC=CC=2)CC1 GUGOEEXESWIERI-UHFFFAOYSA-N 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- 238000002479 acid--base titration Methods 0.000 description 1
- 150000007513 acids Chemical group 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- QYPPJABKJHAVHS-UHFFFAOYSA-P agmatinium(2+) Chemical compound NC(=[NH2+])NCCCC[NH3+] QYPPJABKJHAVHS-UHFFFAOYSA-P 0.000 description 1
- 239000000556 agonist Substances 0.000 description 1
- 201000007930 alcohol dependence Diseases 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- 150000001370 alpha-amino acid derivatives Chemical class 0.000 description 1
- 235000008206 alpha-amino acids Nutrition 0.000 description 1
- 229960003036 amisulpride Drugs 0.000 description 1
- NTJOBXMMWNYJFB-UHFFFAOYSA-N amisulpride Chemical compound CCN1CCCC1CNC(=O)C1=CC(S(=O)(=O)CC)=C(N)C=C1OC NTJOBXMMWNYJFB-UHFFFAOYSA-N 0.000 description 1
- 229940025084 amphetamine Drugs 0.000 description 1
- 230000003444 anaesthetic effect Effects 0.000 description 1
- 230000000202 analgesic effect Effects 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 229920001448 anionic polyelectrolyte Polymers 0.000 description 1
- 229940045799 anthracyclines and related substance Drugs 0.000 description 1
- 239000004004 anti-anginal agent Substances 0.000 description 1
- 230000001088 anti-asthma Effects 0.000 description 1
- 230000001093 anti-cancer Effects 0.000 description 1
- 230000001078 anti-cholinergic effect Effects 0.000 description 1
- 230000001773 anti-convulsant effect Effects 0.000 description 1
- 230000001430 anti-depressive effect Effects 0.000 description 1
- 230000003178 anti-diabetic effect Effects 0.000 description 1
- 230000003474 anti-emetic effect Effects 0.000 description 1
- 230000003556 anti-epileptic effect Effects 0.000 description 1
- 230000000843 anti-fungal effect Effects 0.000 description 1
- 230000001384 anti-glaucoma Effects 0.000 description 1
- 230000001387 anti-histamine Effects 0.000 description 1
- 230000002924 anti-infective effect Effects 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 230000000648 anti-parkinson Effects 0.000 description 1
- 230000000840 anti-viral effect Effects 0.000 description 1
- 229940124345 antianginal agent Drugs 0.000 description 1
- 239000003416 antiarrhythmic agent Substances 0.000 description 1
- 239000000924 antiasthmatic agent Substances 0.000 description 1
- 239000003146 anticoagulant agent Substances 0.000 description 1
- 229940127219 anticoagulant drug Drugs 0.000 description 1
- 239000000935 antidepressant agent Substances 0.000 description 1
- 229940005513 antidepressants Drugs 0.000 description 1
- 239000003472 antidiabetic agent Substances 0.000 description 1
- 239000002111 antiemetic agent Substances 0.000 description 1
- 229960003965 antiepileptics Drugs 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 229940006133 antiglaucoma drug and miotics carbonic anhydrase inhibitors Drugs 0.000 description 1
- 239000000739 antihistaminic agent Substances 0.000 description 1
- 239000002220 antihypertensive agent Substances 0.000 description 1
- 229940030600 antihypertensive agent Drugs 0.000 description 1
- 229940124433 antimigraine drug Drugs 0.000 description 1
- 239000000939 antiparkinson agent Substances 0.000 description 1
- 239000004019 antithrombin Substances 0.000 description 1
- 239000002249 anxiolytic agent Substances 0.000 description 1
- 230000000949 anxiolytic effect Effects 0.000 description 1
- 239000002830 appetite depressant Substances 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000013011 aqueous formulation Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N aspartic acid group Chemical group N[C@@H](CC(=O)O)C(=O)O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- 238000005311 autocorrelation function Methods 0.000 description 1
- HNYOPLTXPVRDBG-UHFFFAOYSA-N barbituric acid Chemical compound O=C1CC(=O)NC(=O)N1 HNYOPLTXPVRDBG-UHFFFAOYSA-N 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 229940049706 benzodiazepine Drugs 0.000 description 1
- 150000001557 benzodiazepines Chemical class 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 229920002988 biodegradable polymer Polymers 0.000 description 1
- 239000004621 biodegradable polymer Substances 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 229920001222 biopolymer Polymers 0.000 description 1
- 210000005252 bulbus oculi Anatomy 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 239000003489 carbonate dehydratase inhibitor Substances 0.000 description 1
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 1
- 229920006317 cationic polymer Polymers 0.000 description 1
- 210000004027 cell Anatomy 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 239000003576 central nervous system agent Substances 0.000 description 1
- 229940125693 central nervous system agent Drugs 0.000 description 1
- 208000015114 central nervous system disease Diseases 0.000 description 1
- 238000002144 chemical decomposition reaction Methods 0.000 description 1
- FZFAMSAMCHXGEF-UHFFFAOYSA-N chloro formate Chemical compound ClOC=O FZFAMSAMCHXGEF-UHFFFAOYSA-N 0.000 description 1
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 1
- 229960001231 choline Drugs 0.000 description 1
- 239000000544 cholinesterase inhibitor Substances 0.000 description 1
- NJMYODHXAKYRHW-DVZOWYKESA-N cis-flupenthixol Chemical compound C1CN(CCO)CCN1CC\C=C\1C2=CC(C(F)(F)F)=CC=C2SC2=CC=CC=C2/1 NJMYODHXAKYRHW-DVZOWYKESA-N 0.000 description 1
- 229960004170 clozapine Drugs 0.000 description 1
- QZUDBNBUXVUHMW-UHFFFAOYSA-N clozapine Chemical compound C1CN(C)CCN1C1=NC2=CC(Cl)=CC=C2NC2=CC=CC=C12 QZUDBNBUXVUHMW-UHFFFAOYSA-N 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 239000003433 contraceptive agent Substances 0.000 description 1
- 229940124558 contraceptive agent Drugs 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- 150000001985 dialkylglycerols Chemical class 0.000 description 1
- 239000010432 diamond Substances 0.000 description 1
- 230000001079 digestive effect Effects 0.000 description 1
- 125000000118 dimethyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- PXEDJBXQKAGXNJ-QTNFYWBSSA-L disodium L-glutamate Chemical class [Na+].[Na+].[O-]C(=O)[C@@H](N)CCC([O-])=O PXEDJBXQKAGXNJ-QTNFYWBSSA-L 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 239000003136 dopamine receptor stimulating agent Substances 0.000 description 1
- 230000002526 effect on cardiovascular system Effects 0.000 description 1
- 230000005684 electric field Effects 0.000 description 1
- 230000009881 electrostatic interaction Effects 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- DQYBDCGIPTYXML-UHFFFAOYSA-N ethoxyethane;hydrate Chemical compound O.CCOCC DQYBDCGIPTYXML-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 238000002270 exclusion chromatography Methods 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 230000035558 fertility Effects 0.000 description 1
- 239000002871 fertility agent Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 238000007667 floating Methods 0.000 description 1
- 229960002419 flupentixol Drugs 0.000 description 1
- 229960002690 fluphenazine Drugs 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 229960003878 haloperidol Drugs 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- 231100000086 high toxicity Toxicity 0.000 description 1
- 239000012456 homogeneous solution Substances 0.000 description 1
- 229920001519 homopolymer Polymers 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 239000003326 hypnotic agent Substances 0.000 description 1
- 239000012729 immediate-release (IR) formulation Substances 0.000 description 1
- 229960003444 immunosuppressant agent Drugs 0.000 description 1
- 239000003018 immunosuppressive agent Substances 0.000 description 1
- 201000001881 impotence Diseases 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 239000000411 inducer Substances 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 239000007972 injectable composition Substances 0.000 description 1
- 239000008141 laxative Substances 0.000 description 1
- 229940125722 laxative agent Drugs 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 239000006194 liquid suspension Substances 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 239000003607 modifier Substances 0.000 description 1
- 229940035363 muscle relaxants Drugs 0.000 description 1
- 239000003158 myorelaxant agent Substances 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- 239000002777 nucleoside Substances 0.000 description 1
- 150000003833 nucleoside derivatives Chemical class 0.000 description 1
- 150000002892 organic cations Chemical class 0.000 description 1
- 229960003104 ornithine Drugs 0.000 description 1
- 229940094443 oxytocics prostaglandins Drugs 0.000 description 1
- 239000000734 parasympathomimetic agent Substances 0.000 description 1
- 230000001499 parasympathomimetic effect Effects 0.000 description 1
- 229940005542 parasympathomimetics Drugs 0.000 description 1
- 238000005897 peptide coupling reaction Methods 0.000 description 1
- 229960000762 perphenazine Drugs 0.000 description 1
- 108010064470 polyaspartate Proteins 0.000 description 1
- 229920000570 polyether Polymers 0.000 description 1
- 239000004626 polylactic acid Substances 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 150000003180 prostaglandins Chemical class 0.000 description 1
- 125000006239 protecting group Chemical group 0.000 description 1
- 239000003223 protective agent Substances 0.000 description 1
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 1
- 229940001470 psychoactive drug Drugs 0.000 description 1
- 239000004089 psychotropic agent Substances 0.000 description 1
- 229960004431 quetiapine Drugs 0.000 description 1
- URKOMYMAXPYINW-UHFFFAOYSA-N quetiapine Chemical compound C1CN(CCOCCO)CCN1C1=NC2=CC=CC=C2SC2=CC=CC=C12 URKOMYMAXPYINW-UHFFFAOYSA-N 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 229960001534 risperidone Drugs 0.000 description 1
- RAPZEAPATHNIPO-UHFFFAOYSA-N risperidone Chemical compound FC1=CC=C2C(C3CCN(CC3)CCC=3C(=O)N4CCCCC4=NC=3C)=NOC2=C1 RAPZEAPATHNIPO-UHFFFAOYSA-N 0.000 description 1
- 239000000932 sedative agent Substances 0.000 description 1
- 229940125723 sedative agent Drugs 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 239000000021 stimulant Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- 229960004940 sulpiride Drugs 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 229940125725 tranquilizer Drugs 0.000 description 1
- 239000003204 tranquilizing agent Substances 0.000 description 1
- 230000002936 tranquilizing effect Effects 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 210000001215 vagina Anatomy 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 229940124549 vasodilator Drugs 0.000 description 1
- 239000003071 vasodilator agent Substances 0.000 description 1
- 229960000607 ziprasidone Drugs 0.000 description 1
- MVWVFYHBGMAFLY-UHFFFAOYSA-N ziprasidone Chemical compound C1=CC=C2C(N3CCN(CC3)CCC3=CC=4CC(=O)NC=4C=C3Cl)=NSC2=C1 MVWVFYHBGMAFLY-UHFFFAOYSA-N 0.000 description 1
- WFPIAZLQTJBIFN-DVZOWYKESA-N zuclopenthixol Chemical compound C1CN(CCO)CCN1CC\C=C\1C2=CC(Cl)=CC=C2SC2=CC=CC=C2/1 WFPIAZLQTJBIFN-DVZOWYKESA-N 0.000 description 1
- 125000001020 α-tocopherol group Chemical group 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/02—Peptides of undefined number of amino acids; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/42—Proteins; Polypeptides; Degradation products thereof; Derivatives thereof, e.g. albumin, gelatin or zein
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
- A61K47/645—Polycationic or polyanionic oligopeptides, polypeptides or polyamino acids, e.g. polylysine, polyarginine, polyglutamic acid or peptide TAT
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1641—Organic macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyethylene glycol, poloxamers
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Immunology (AREA)
- Dispersion Chemistry (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Dermatology (AREA)
- Gastroenterology & Hepatology (AREA)
- Zoology (AREA)
- Endocrinology (AREA)
- Inorganic Chemistry (AREA)
- Medicinal Preparation (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
本発明は、第1態様において、少なくとも一つの活性成分(AP)とポリマー(PO)のコロイド粒子を基にした水性懸濁液とを備える液体製剤に関するものであり、前記製剤は、以下の4つの条件:
(a)ポリマー(PO)が、グルタミン酸残基を含むポリアミノ酸であり、ここで、
一部のグルタミン酸残基は、それぞれがペンダントの陽イオン基(CG)を有し、前記陽イオン基は、互いに同一でも異なっていてもよく、
他のグルタミン酸残基は、それぞれがペンダントの疎水基(GH)を有し、前記疎水基(GH)は、互いに同一でも異なっていてもよいこと、
(b)前記製剤のpHのpHf値が、3.0〜6.5の間であること;
(c)前記pHf値にて、ポリマー(PO)が、活性成分(AP)と自発的に非共有で会合しているコロイド溶液を形成すること;
(d)1mlの前記製剤が、体積1mlのテスト緩衝溶液Tpと混合する間に沈殿すること、
を満たす。
本発明はまた、かかる製剤を調製する方法と、かかる製剤を含む薬剤を調製する方法とに関するものである。
Description
1.活性および非変性治療用プロテイン、例えば、ヒトタンパク質または合成タンパク質を持続放出し、血漿濃度を治療用の濃度に維持すること
2.容易に注入可能とするのに十分に低い注射での粘度
3.優れた毒性・耐性プロファイルを示す生体適合性および生分解性
(a)ポリマー(PO)が、グルタミン酸残基を含むポリアミノ酸であり、ここで、
一部のグルタミン酸残基は、それぞれがペンダントの陽イオン基(CG)を有し、前記陽イオン基は、互いに同一でも異なっていてもよく、
他のグルタミン酸残基は、それぞれがペンダントの疎水基(GH)を有し、前記疎水基(GH)は、互いに同一でも異なっていてもよく、
任意には、更に他のグルタミン酸残基が、それぞれペンダントの中性基(NG)を有し、前記中性基(NG)は、互いに同一でも異なっていてもよく、
任意には、更に他のグルタミン酸残基が、未変性であること;
(b)前記製剤のpH値(pHf)が、3.0〜6.5の間であること;
(c)pHfにて、ポリマー(PO)が、活性成分(AP)と自発的に非共有で会合しているコロイド溶液を形成すること;
(d)1mlの前記製剤が、体積1mlのテスト緩衝溶液Tpとの混合中に沈殿すること;
を満たす。
(a)ポリマー(PO)が、グルタミン酸残基を含むポリアミノ酸であり、ここで、
一部のグルタミン酸残基は、それぞれがペンダントの陽イオン基(CG)を有し、前記陽イオン基は、互いに同一でも異なっていてもよく、
他のグルタミン酸残基は、それぞれがペンダントの疎水基(GH)を有し、前記疎水基(GH)は、互いに同一でも異なっていてもよく、
任意には、更に他のグルタミン酸残基が、それぞれペンダントの中性基(NG)を有し、該中性基(NG)は、互いに同一でも異なっていてもよく、
任意には、更に他のグルタミン酸残基が、未変性であること;
(b)前記製剤のpH値(pHf)が、3.0〜6.5の間であること;
(c)pHfにて、ポリマー(PO)が、活性成分(AP)と自発的に非共有で会合しているコロイド溶液を形成すること;
(d)前記製剤が、200より大きい、好ましくは400より大きい、好ましくは800より大きい、さらに好ましくは1500より大きい沈殿因子PFを示すこと;
を満たす。
1)3〜6.5の間のpH値で、グルタミン酸残基を含むポリアミノ酸ポリマー(PO)の水性コロイド溶液を準備する工程であって、ここで、
一部のグルタミン酸残基は、それぞれがペンダントの陽イオン基(CG)を有し、前記陽イオン基は、互いに同一でも異なっていてもよく、
他のグルタミン酸残基は、それぞれがペンダントの疎水基(GH)を有し、前記疎水基(GH)は、互いに同一でも異なっていてもよく、
任意には、更に他のグルタミン酸残基が、それぞれペンダントの中性基(NG)を有し、該中性基(NG)は、互いに同一でも異なっていてもよく、
任意には、更に他のグルタミン酸残基が、未変性であり;
陽イオン基(CG)、疎水基(GH)、任意の中性基(NG)および任意のグルタミン酸塩の各モル分率は、1mlの前記製剤が体積1mlのテスト緩衝溶液Tpとの混合中に沈殿するほどである工程と;
2)少なくとも一つの活性成分(AP)を工程1において得られたポリマー(PO)に加える工程であって、前記活性成分が前記ポリマーのコロイド溶液の粒子と非共有で会合している工程と、
を備えてなり、前記製剤の最終的な治療上での使用の直前(例えば30分前)に前記活性成分を加える工程を行うことができる。
本明細書において、「陽イオン基」という用語は、一つもしくはそれ以上のアミノ基又は一つもしくはそれ以上の第4級アンモニウムを備えるグルタミン酸基に共有結合している基を意味すると理解される。アミノ官能基の場合、該基は、主にそのpKa以下のどんなpHでもイオン化し、第4級アンモニウムの場合には、該基がどんなpHでもイオン化している。他に特に規定がなければ、アルキルラジカルは、1〜10の炭素原子を示す。
0.15Mの塩化ナトリウムを含む1又は2mg/mlのポリマーPO濃縮液を、酢酸又は1Mの水酸化ナトリウム溶液を加えることによってpH4にし、24時間攪拌しながら置いておく。その後、この溶液を0.8〜0.2μmフィルタに通して濾過する。次いで、この溶液を0.1Mの水酸化ナトリウム溶液で滴定し、ポリマーPO溶液の500nmでの吸光度の変化を、Perkin−Elmer Lambda 35UV Spectrometerタイプの装置を用いて、前記溶液のpHの関数として記録する。沈澱のpH(pH*)は、吸光度が急激に増加して1より大きな値に到達するときのpHの値に相当する。
本発明に従う体積Vの製剤は、すぐに投与できる状態にあり、25℃にて200μlのラット血清プールに加えられる。そのナノ粒子が沈殿した後、浮遊物中の遊離タンパク質濃度をELISAテストによって測定する。
体積Vの値を増大させるために同じテストを繰り返すことによって、製剤の体積のV*値を決定でき、該V*値では、浮遊物中の遊離タンパク質のモル分率が10%より大きくなることが認められている
保持因子RQは、200μlラット血清に対する体積V*の比によって与えられる。
例えば、V*=1mlに対して、RQ=5である。
本発明に従うポリマーの粒子の平均流体力学的直径は、以下に規定される手法Mdに従って測定される。
0.15MのNaCl媒体中、ポリマー溶液を1または2mg/mlの濃度で準備し、24時間攪拌して置いておく。その次に、これらの溶液を0.8〜0.2μmのフィルタに通して濾過した後、波長632.8nmの垂直に偏光したHe−Neレーザービームで動作するMalvern Compact Goniometer System型の装置を用いた動的光散乱において分析する。ポリマーナノ粒子の流体力学的直径は、「Surfactant Science Series」,第22巻,Surfactant Solutions,編集R.Zana,第3章,M.Dekker,1984の研究に説明されるように、キュムラント法による電界の自己相関関数から算出される。
30mg/gのウシアルブミン画分V(Aldrich)、0.01Mのリン酸緩衝液、0.0027Mの塩化カリウム、0.137Mの塩化ナトリウム(AldrichのPBS)および0.015Mの酢酸アンモニウム(Aldrich)を備えた流量2.83ml/hの水性媒体によって水浴したポリウレタン/ポリエーテル(PU−PE)発泡体からなる辺長1.5cmの立方体中に、50μlの製剤を注入する。サンプルは、連続相から定期的に回収され、そのサンプルのタンパク質含有量をELISAによって分析する。
2〜6の炭素原子を有する直鎖ジアミン、好ましくはプトレッシン
アグマチン
酸素を介して結合したエタノールアミン
酸素を介して結合したコリン
側鎖が中性のpHにて正に帯電しているアミノ酸のエステル又はアミド誘導体、すなわち、α位のアミン官能基を介して結合したリシン、アルギニン又はオルニチン
xが、10〜55%の間であり、
yが、2〜30%の間であり、
zが、10%より大きいか又は等しく、(x−10)%と(x+15)%の間であり、
中性基の数が、100%に到達するための追加のパーセンテージに相当しており、任意には0に等しく
なるようにすることができる。
xが、20〜55%の間であり、
yが、2〜7.5%の間であり、
zが、20%より大きいか又は等しく、(x−10)%と(x+15)%の間であり、
中性基の数が、100%に到達するための追加のパーセンテージに相当しており、任意には0に等しく
なるようにすることもできる。
・ヒスチジンエステル、好ましくはそのメチルエステル及びそのエチルエステル、ヒスチジノール、ヒスタミン、ヒスチジンアミド、ヒスチジンアミドのN−モノメチル誘導体及びヒスチジンアミドのN,N'−ジメチル誘導体からなる群から選択されるヒスチジン誘導体と一致するか、又は
・下記一般式:
X=O又はNH
Y=独立してH又はCH3
L=カルボキシル官能基又はその誘導体で任意に置換される直鎖(C2〜C6)アルキレン)を有する。
−NH−(CH2)w−NH3 +,Z−(ここで、wは2〜6の間であり、好ましくはwが4である)、
−NH−(CH2)4−NH−C(=NH)−NH3 +,Z−、
−O−(CH2)2−NH3 +,Z−、
−O−(CH2)2−N+(CH3)3,Z−、
下記式:
の内の一つを有することができ、ここで、Z−は、塩化物、硫酸塩、リン酸塩又は酢酸塩であり、好ましくは塩化物である。
・任意には少なくとも一つの不飽和結合及び/又は少なくとも一つのヘテロ原子を有することができる直鎖又は分岐C8〜C30アルキル、
・任意には少なくとも一つの不飽和結合及び/又は少なくとも一つのヘテロ原子を有することができるC8〜C30アルキルアリール又はアリールアルキル、並びに
・任意には少なくとも一つの不飽和結合及び/又は少なくとも一つのヘテロ原子を有することができるC8〜C30(多)環式化合物、
からなる群から慎重に選択される。
・Aは、独立して、
NHR基(ここで、RはH、直鎖C2〜C10もしくは分岐C3〜C10アルキル又はベンジルを示す)、
次式:
R7は、OH、OR9又はNHR10であり、
R8、R9及びR10は、独立して、H、直鎖C2〜C10もしくは分岐C3〜C10アルキル又はベンジルである)の末端アミノ酸残基又は末端アミノ酸誘導体、
であり;
・Bは、直接結合、又は二価、三価もしくは四価の結合基であり、好ましくは−O−、−NH−、−N(C1〜C5アルキル)−、アミノ酸(好ましくは天然アミノ酸)残基、ジオール残基、トリオール残基、ジアミン残基、トリアミン残基、アミノアルコール残基又は1〜6の炭素原子を有するヒドロキシ酸残基から選択され;
・Dは、H、直鎖C2〜C10もしくは分岐C3〜C10アシル基又はピログルタミン酸塩であり;
・疎水基(GH)は、それぞれが互いに独立して、
・任意には少なくとも一つの不飽和結合及び/又は少なくとも一つのヘテロ原子(好ましくはO及び/又はN及び/又はS)を有することができる直鎖または分岐C8〜C30アルキル、又は
・任意には少なくとも一つの不飽和結合及び/又は少なくとも一つのヘテロ原子(好ましくはO及び/又はN及び/又はS)を有することができるC8〜C30アルキルアリール又はアリールアルキル、又は
・任意には少なくとも一つの不飽和結合及び/又は少なくとも一つのヘテロ原子(好ましくはO及び/又はN及び/又はS)を有することができるC8〜C30(多)環式化合物、
から選択される基であり;
好ましくは、疎水基(GH)の少なくとも一つが、グラフトによって、オクタノール、ドデカノール、テトラデカノール、ヘキサデカノール、オクタデカノール、オレイルアルコール、トコフェロール及びコレステロールからなる群から選択される前駆体から得られ、Bが直接結合を表し;
・R70は、
−NH−(CH2)w−NH3 +(ここで、wは2〜6の間であり、好ましくはwが4である)、
−NH−(CH2)4−NH−C(=NH)−NH3 +、
−O−(CH2)2−NH3 +、
−O−(CH2)2−N+(CH3)3、
下記式:
次式:
から選択される基であり、
R70基の対アニオンが、便宜の基であり、特に塩化物、硫酸塩、リン酸塩又は酢酸塩から選択され、好ましくは塩化物であり;
・R90は、ヒドロキシエチルアミノ−、ヒドロキシアルキルオキシ−、又はポリオキシアルキレンであり;
・p,q,r及びsは、正の整数であり;
・(p)/(p+q+r+s)は、疎水基GHのモルグラフト度として定義され、2〜30モル%の範囲であり、但し、各コポリマー鎖は、平均して、少なくとも三つの疎水性グラフト部を有しており;
・(q)/(p+q+r+s)は、陽イオン基のモルグラフト度として定義され、10〜98モル%の範囲であり;
・(p+q+r+s)は、50〜300の範囲であり、好ましくは100〜250の間であり;
・(r)/(p+q+r+s)は、0〜78モル%の範囲であり;
・(s)/(p+q+r+s)は、0〜55モル%の範囲である)を有し、また、その製剤可能な塩を包含する。
更に、ヒスチジンに由来するもの以外の式(I)のポリアミノ酸の調製及び合成に関する詳細に関しては、仏国特許出願FR 07 03185を参照されたい。
a)pH*として記録される沈殿pHの測定
酸性pHf3〜6.5にて、APを持つコロイド溶液は、ナノ粒子を備える透明の液体として存在し、該ナノ粒子の平均流体力学的直径は、T'テストに従い動的光散乱によって測定したところ、0.5μm未満か又はそれに等しく、好ましくは5〜500nmの間であり、更に好ましくは10〜80nmの間である。pHを高めると、本発明に従う溶液は、生理学的pHより低いか又はそれに等しいpHに対して沈殿する必要がある。該溶液が沈殿するpH*値は、Pテストに従って測定される。
b)PFの測定
TM法に従って、ポリマーPO1mgを備えるコロイド溶液0.5mlをpHfからpH*にするのに必要な水酸化ナトリウムのモル数,Δnの測定である。
Cを製剤中のポリマーPOの濃度とし(mg/gで表す)、yを疎水性サイドグラフト部を有するポリマーPOの単量体のモル分率とすることによって、製剤の沈殿因子PFは、下記式:
更に好ましくは、エポエチンアルファ、エポエチンベータ、ダーベポエチン等のエリスロポエチン、ヘモグロビンラフィマー、それらの類似体又はそれらの誘導体;オキシトシン、バソプレシン、副腎皮質刺激ホルモン、上皮細胞増殖因子、血小板由来増殖因子(PDGF)、造血を刺激する因子及びそれらの混合物の他、アルテプラーゼ、テネクテプラーゼ、第VII(a)因子又は第VII因子等の血液因子;ヘモグロビン、シトクロム、アルブミン、プロラクチン、ルリベリンの他、ロイプロリド、ゴセレリン、トリプトレリン、ブセレリン又はナファレリン等の黄体形成ホルモン放出ホルモン(LHRH)及び類似体;LHRHアンタゴニスト、LHRH競合体、ヒト、ブタ又はウシの成長ホルモン(GHs)、成長ホルモン放出因子、インスリン、ソマトスタチン、グルカゴン、インターロイキン又はその混合体(IL−2,IL−11,IL−12)の他、インターフェロンアルファ、アルファ−2b、ベータ、ベータ−1a又はガンマ等のインターフェロン;ガストリン、テトラガストリン、ペンタガストリン、ウロガストロン、セクレチン、カルシトニン、エンケファリン、エンドモルフィン、アンジオテンシン、甲状腺刺激ホルモン放出ホルモン(TRH)、腫瘍壊死因子(TNF)、神経成長因子(NGF)の他、ベクラペルミン、トラフェルミン、アンセスチム又はケラチノサイト成長因子等の成長因子、顆粒球コロニー刺激因子(G−CSF)、顆粒球マクロファージコロニー刺激因子(GM−CSF)、マクロファージコロニー刺激因子(M−CSF)、ヘパリナーゼ、骨形成タンパク質(BMP)、hANP、グルカゴン様ペプチド(GLP−1)、VEG−F、組換えB型肝炎表面抗原(rHBsAg)、レニン、サイトカイン、ブラジキニン、バシトラシン、ポリミキシン、コリスチン、チロシジン、グラミシジン、エタネルセプト、イミグルセラーゼ、ドロトレコギンアルファ、シクロスポリン及び合成類似体、並びに酵素、サイトカイン、抗体、抗原及びワクチンの製剤可能な修飾体及び断片、リツキシマブ、インフリキシマブ、トラスツズマブ、アダリムマブ、オマリズマブ、トシツモマブ、エファリズマブ及びセツキシマブ等の抗体の下位群から選択される。
1)3〜6.5の間のpH値で、ポリアミノ酸ポリマー(PO)の水性コロイド溶液を準備する工程であって、陽イオン基(CG)、疎水基(GH)、任意の中性基(NG)及び任意のグルタミン酸塩の各モル分率が、1mlの前記製剤が体積1mlのテスト緩衝溶液Tpとの混合中に沈殿するほどである工程と;
2)少なくとも一つの活性成分(AP)を工程1において得られたポリマー(PO)に加える工程であって、前記活性成分が前記ポリマーのコロイド溶液の粒子と非共有で会合している工程と、
を備える。
a)比較:疎水基を有する陰イオン高分子電解質ポリマーPOの合成(合成起源のα−トコフェロールでグラフトしたポリグルタミン酸塩)
ポリオキシエチレン基準に対して約16900Daに相当する重量のα−L−ポリグルタミン酸15gを80℃で加熱しながらジメチルホルムアミド(DMF)288ml中に溶解させ、ポリマーを溶解させた。その溶液を15℃に冷却し、あらかじめ8mlのDMF中に溶解させた2.5gのD,L-α−トコフェロール(>98%、Fluka(登録商標)から得られる)と、あらかじめ1mlのDMF中に溶解させた280mgの4−ジメチルアミノピリジンと、あらかじめ6mlのDMF中に溶解させた1.6gのジイソプロピルカルボジイミドとを続けて加える。3時間攪拌した後、反応媒体を、15%の塩化ナトリウムと塩酸を含む水1200ml(pH2)に注ぎ込む。その後、沈澱したポリマーを濾過によって回収し、0.1Nの塩酸、水、及びジイソプロピルエーテルで洗浄する。その後、ポリマーを真空下40℃のオーブン中で乾燥させる。およそ90%の収率を得る。モル質量を立体排除クロマトグラフィーによって測定したところ、ポリオキシエチレン基準に対して15500である。グラフトしたトコフェロールのレベルをプロトンNMR分光法によって測定したところ、5.1モル%である。
合成a)に従って得られたポリマーPOを用いる。
PO溶液12.64gを水2.19gで希釈することで、ポリマーPOのコロイド溶液24mg/gを得る。その次に、必要量のNaCl水溶液とNaOH溶液とをそれぞれ導入することによって、コロイドPO溶液のオスモル濃度及びそのpHを290mOsm及びpH6.95に調整する。
以下、得られた製剤の特性を表に示す。
粒径をT'テストに従って測定する。
3.1)例2.1:PO−A1の濃度が10mg/gと等しく、IFN-αを備える
a)PO−A1のコロイド溶液の調製
上述の合成b)に従って得られたポリマーPO−A1を用いる。
PO−A1を水で希釈し、pHを(適切なNaOH溶液で)調整し、オスモル濃度を(適切なNaCl溶液で)調整する。
2.4mg/gのタンパク質IFN−α2.18gをPO−A1のコロイド溶液8gに加え、適切なNaCl溶液(0.18g)で希釈することによって、最終濃度を調整する。
上述の合成b)に従って得られたポリマーPO−A1を用いる。
PO−A1を水で希釈し、pHを(適切なNaOH溶液で)調整し、オスモル濃度を(適切なNaCl溶液で)調整する。
a)0.5eq.のZn++を備えるPO−A1のコロイド溶液の調製
上述の合成b)に従って得られたポリマーPO−A1を用いる。
PO−A1を水で希釈し、pHを(適切なNaOH溶液で)調整し、オスモル濃度を(適切なNaCl溶液で)調整する。
2.4mg/gのタンパク質IFN−α2.17gを段階a)で調製したPO−A1のコロイド溶液7.96gに加え、適切なNaCl溶液(0.18g)で希釈することによって、最終濃度を調整する。
溶液中に存在する陽イオン誘導体当たり0.5モル当量の陽イオンZn++を達成するため、濃縮された204mg/gのZnCl2溶液の必要量を先の製剤に加える。
以下、最終製剤の特徴を表に示す。
粒径をT'テストに従って測定する。
a)PO−A2のコロイド溶液の調製
上述の合成c)に従って得られたポリマーPO−A2を用いる。
PO−A2を水で希釈し、pHを(適切なNaOH溶液で)調整し、オスモル濃度を(適切なNaCl溶液で)調整する。
2.4mg/gのタンパク質IFN−α2.18gをPO−A2のコロイド溶液8gに加え、適切なNaCl溶液(0.18g)で希釈することによって、最終濃度を調整する。
5.1)例4.1:PO−Bの濃度が10mg/gに等しく、IFN-αを備える
a)PO−Bのコロイド溶液の調製
上述の合成d)に従って得られたポリマーPO−Bを用いる。
PO−Bを水で希釈し、pHを(適切なNaOH溶液で)調整し、オスモル濃度を(適切なNaCl溶液で)調整する。
2.7mg/gのタンパク質IFN−α1.8gをPO−Bのコロイド溶液8gに加え、適切なNaCl溶液で希釈することによって、最終濃度を調整する。
粒径をT'テストに従って測定する。
以下、最終製剤の特徴を表に示す。
上述の合成d)に従って得られたポリマーPO−Bを用いる。
PO−Bを水で希釈し、pHを(適切なNaOH溶液で)調整し、オスモル濃度を(適切なNaCl溶液で)調整する。
上述の合成a)に従って得られたポリマーPOを用いる。
ポリマーPOを水中に溶解することで、ポリマーPOのコロイド溶液を得、NaOH溶液を加えることでpHを7.52に調整する。必要量のNaCl水溶液を導入することで溶液のオスモル濃度を108mOsmに調整する。ポリマーPOの濃度を29.05mg/gに調整する。
濃縮された2.4mg/gのタンパク質IFN−αを先のポリマーPOコロイド溶液に加える。25℃で一晩、会合を形成する。
以下、得られた粒子の特徴を表に示す。
粒径をT'テストに従って測定する。
このために、本発明に従う製剤からの活性成分の放出をLテストによって測定する。
Lテストにおける放出を時間と共に放出されるタンパク質の割合の形式で図1に示す。
比較の例5の製剤は、POの粒子を23mg/gで含んでおり、10時間で放出されたタンパク質が93%であることを特徴とする放出プロファイルを示す。
例2.1及び3の製剤は、48時間でそれぞれ67%及び65%の注入されたタンパク質を放出するという遅延放出プロファイルを示す。
例2.3の粒子の場合、実験の終わりでゼロにならない放出流量の形成が観察され、48時間で注入されたタンパク質の59%が放出される。
44匹のラットを8又は12匹の5グループに分け、並行して即時放出IR製剤もしくは比較の例5に対応する持続放出製剤、又は本発明の例2及び3の製剤の一つを300μg/kgの投与量で受けた。
以下、薬物動態の結果を表に示す。
Tmax中央値は、血漿中濃度が最大となる時間の中央値を示す。
AUCは、時間の関数として血漿中濃度の曲線下平均面積を示す。
T50%AUCは、曲線下面積がその合計値の50%に到する平均時間を示す。
RBAは、検討中の製剤の曲線下面積のIFN IR製剤の曲線下面積に対する比を示す。
比較例5との比較すると、本発明に従う全ての製剤の終わりの傾きがより小さく、持続した残留吸着を示唆する。
例2.1及び例3の製剤(10mg/g PO−A1および30mg/g PO−A2)に関しては、それぞれのRBA値が57%及び約100%を示す5日以上かけての持続放出に(比較例5の製剤の約3日と比較して)注目すべきである。
Claims (20)
- 少なくとも一つの活性成分(AP)を持続放出する液体製剤であって、前記製剤は、少なくとも一つの活性成分(AP)と、ポリマー(PO)又はその製剤可能な塩のコロイド粒子を基にした水性懸濁液とを備えてなり、以下の4つの条件:
(a)ポリマー(PO)が、グルタミン酸残基を含むポリアミノ酸であり、ここで、
一部のグルタミン酸残基は、それぞれがペンダントの陽イオン基(CG)を有し、前記陽イオン基は、互いに同一でも異なっていてもよく、
他のグルタミン酸残基は、それぞれがペンダントの疎水基(GH)を有し、前記疎水基(GH)は、互いに同一でも異なっていてもよく、
任意には、更に他のグルタミン酸残基が、それぞれペンダントの中性基(NG)を有し、前記中性基(NG)は、互いに同一でも異なっていてもよく、
任意には、更に他のグルタミン酸残基が、未変性であること;
(b)前記製剤のpHのpHf値が、3.0〜6.5の間であること;
(c)前記pHf値にて、ポリマー(PO)が、活性成分(AP)と自発的に非共有で会合しているコロイド溶液を形成すること;及び
(d)1mlの前記製剤が、体積1mlのテスト緩衝溶液Tpとの混合中に沈殿すること、
を満たすことを特徴とする製剤。 - 前記製剤が、200より大きい、好ましくは400より大きい、好ましくは800より大きい、更に好ましくは1500より大きい沈殿因子PFを有することを特徴とする請求項1に記載の製剤。
- 前記製剤が、5より大きい、好ましくは10より大きい、好ましくは15より大きい、更に好ましくは20より大きい保持因子RQを有することを特徴とする請求項2に記載の製剤。
- ポリマー(PO)は、pGlu(x)GH(y)CG(z)NG(1−x−y−z)の構造で、合計の重合度(DP)が50〜300の間、好ましくは100〜250の間である構造を有し、ここで、(x)は0〜0.45の間で、(y)は0.02〜0.3の間で、(z)は0.4〜0.98の間で、(1−x−y−z)は0〜0.5の間であることを特徴とする請求項1〜3のいずれかに記載の製剤。
- 前記陽イオン基(CG)は、半中和pHが7.0未満の弱塩基から選択されることを特徴とする請求項1に記載の製剤。
- 前記陽イオン基(CG)は、少なくとも一つの第4級アンモニウム又は少なくとも一つの強塩基を含む陽イオン基から選択され、半中和pHが8.0より大きいことを特徴とする請求項1に記載の製剤。
- 前記陽イオン基(CG)が、以下の基:
−NH−(CH2)w−NH3 +,Z−(ここで、wは2〜6の間であり、好ましくはwが4である)、
−NH−(CH2)4−NH−C(=NH)−NH3 +,Z−、
−O−(CH2)2−NH3 +,Z−、
−O−(CH2)2−N+(CH3)3,Z−、及び
下記式:
から選択され、Z−が、塩化物、硫酸塩もしくはリン酸塩又は酢酸塩であり、好ましくは塩化物であることを特徴とする請求項6に記載の製剤。 - xが10〜55%の間であり、
yが2〜30%の間であり、
zが10%より大きいか又は10%と等しく、(x−10)%から(x+15)%の間であり、
中性基の数は100%に到達するための追加のパーセンテージに相当しており、任意には0と等しくすることができることを特徴とする請求項3、6及び7のいずれかに記載の製剤。 - xが20〜55%の間であり、
yが2〜7.5%の間であり、
zが20%より大きいか又は20%と等しく、(x−10)%から(x+15)%の間であり、
中性基の数は100%に到達するための追加のパーセンテージに相当しており、任意には0と等しくすることができることを特徴とする請求項3、6及び7のいずれかに記載の製剤。 - 前記疎水基(GH)が、
・任意には少なくとも一つの不飽和結合及び/又は少なくとも一つのヘテロ原子を有することができる直鎖又は分岐C8〜C30アルキル、
・任意には少なくとも一つの不飽和結合及び/又は少なくとも一つのヘテロ原子を有することができるC8〜C30アルキルアリール又はアリールアルキル、並びに
・任意には少なくとも一つの不飽和結合及び/又は少なくとも一つのヘテロ原子を有することができるC8〜C30(多)環式化合物、
からなる群から選択されることを特徴とする請求項1〜4のいずれかに記載の製剤。 - 前記中性基(NG)が、ヒドロキシエチルアミノ−ラジカル、ヒドロアルキルオキシ−ラジカル及びポリオキシアルキレンからなる群から選択されることを特徴とする請求項1に記載の製剤。
- 前記ポリマー(PO)が、グルタミン酸塩残基に結合したポリアルキレン(好ましくはポリエチレン)グリコールタイプのグラフト部を少なくとも一つ有することを特徴とする請求項1に記載の製剤。
- 前記ポリアミノ酸(PO)が、下記式(I):
・Aは、独立して、
−NHR基(ここで、RはH、直鎖C2〜C10もしくは分岐C3〜C10アルキル又はベンジルを示す)、
次式:
R7は、OH、OR9又はNHR10であり、
R8、R9及びR10は、独立して、H、直鎖C2〜C10もしくは分岐C3〜C10アルキル又はベンジルである)の末端アミノ酸残基又は末端アミノ酸誘導体、
であり;
・Bは、直接結合、又は二価、三価もしくは四価の結合基であり、好ましくは−O−、−NH−、−N(C1〜C5アルキル)−、アミノ酸(好ましくは天然アミノ酸)残基、ジオール残基、トリオール残基、ジアミン残基、トリアミン残基、アミノアルコール残基又は1〜6の炭素原子を有するヒドロキシ酸残基のラジカルから選択され;
・Dは、H、直鎖C2〜C10もしくは分岐C3〜C10アシル基又はピログルタミン酸塩であり;
・疎水基GHは、それぞれが互いに独立して、
・任意には少なくとも一つの不飽和結合及び/又は少なくとも一つのヘテロ原子(好ましくはO及び/又はN及び/又はS)を有することができる直鎖又は分岐C8〜C30アルキル、又は
・任意には少なくとも一つの不飽和結合及び/又は少なくとも一つのヘテロ原子(好ましくはO及び/又はN及び/又はS)を有することができるC8〜C30アルキルアリール又はアリールアルキル、又は
・任意には少なくとも一つの不飽和結合及び/又は少なくとも一つのヘテロ原子(好ましくはO及び/又はN及び/又はS)を有することができるC8〜C30(多)環式化合物、
から選択される基であり;
・R70は、
−NH−(CH2)w−NH3 +(ここで、wは2〜6の間であり、好ましくはwが4である)、
−NH−(CH2)4−NH−C(=NH)−NH3 +、
−O−(CH2)2−NH3 +、
−O−(CH2)2−N+(CH3)3、
下記式:
次式:
から選択される基であり、
前記R70の対アニオンが、便宜の基であり、好ましくは塩化物であり;
・R90は、ヒドロキシエチルアミノ−、ヒドロキシアルキルオキシ−、又はポリオキシアルキレンであり;
・p,q,r及びsは、正の整数であり;
・(p)/(p+q+r+s)は、疎水基GHのモルグラフト度として定義され、2〜30モル%の範囲であり、但し、各コポリマー鎖は、平均して、少なくとも三つの疎水性グラフト部を有しており;
・(q)/(p+q+r+s)は、陽イオン基のモルグラフト度として定義され、10〜98モル%の範囲であり;
・(p+q+r+s)は、50〜300の範囲であり、好ましくは100〜250の間であり;
・(r)/(p+q+r+s)は、0〜78モル%の範囲であり;
・(s)/(p+q+r+s)は、0〜55モル%の範囲である)を有することを特徴とする請求項1に記載の製剤。 - ポリマー(PO)又はその製剤可能な塩の濃度が、前記製剤中4〜50mg/mlの間であることを特徴とする請求項1に記載の製剤。
- 活性成分(AP)濃度のポリマー(PO)又はその製剤可能な塩の濃度に対する比Rが、0.0001〜1.5の間であることを特徴とする請求項1に記載の製剤。
- 二価の陽イオンZn++を、陽イオン基(CG)のモル濃度に対して0.05〜2モル当量の割合で備えることを特徴とする請求項1に記載の製剤。
- 前記製剤が、追加される二価の陽イオンを備えていないことを特徴とする請求項1に記載の製剤。
- 前記活性成分(AP)が、タンパク質、糖タンパク質、一つ又はそれ以上のポリアルキレングルコール鎖と結合したタンパク質[好ましくは、ポリエチレングリコール(PEG):「PEG化タンパク質」]、ペプチド、多糖類、リポ糖類、オリゴヌクレオチド、ポリヌクレオチド、及びそれらの混合物からなる群から選択され、
更に好ましくは、エポエチンアルファ、エポエチンベータ、ダーベポエチン等のエリスロポエチン、ヘモグロビンラフィマー、それらの類似体又はそれらの誘導体;オキシトシン、バソプレシン、副腎皮質刺激ホルモン、上皮細胞増殖因子、血小板由来増殖因子(PDGF)、造血を刺激する因子及びそれらの混合物の他、アルテプラーゼ、テネクテプラーゼ、第VII(a)因子又は第VII因子等の血液因子;ヘモグロビン、シトクロム、アルブミン、プロラクチン、ルリベリンの他、ロイプロリド、ゴセレリン、トリプトレリン、ブセレリン又はナファレリン等の黄体形成ホルモン放出ホルモン(LHRH)及び類似体;LHRHアンタゴニスト、LHRH競合体、ヒト、ブタ又はウシの成長ホルモン(GHs)、成長ホルモン放出因子、インスリン、ソマトスタチン、グルカゴン、インターロイキン又はそれらの混合物(IL−2,IL−11,IL−12)の他、インターフェロンアルファ、アルファ−2b、ベータ、ベータ−1a又はガンマ等のインターフェロン;ガストリン、テトラガストリン、ペンタガストリン、ウロガストロン、セクレチン、カルシトニン、エンケファリン、エンドモルフィン、アンジオテンシン、甲状腺刺激ホルモン放出ホルモン(TRH)、腫瘍壊死因子(TNF)、神経成長因子(NGF)の他、ベクラペルミン、トラフェルミン、アンセスチム又はケラチノサイト成長因子等の成長因子、顆粒球コロニー刺激因子(G−CSF)、顆粒球マクロファージコロニー刺激因子(GM−CSF)、マクロファージコロニー刺激因子(M−CSF)、ヘパリナーゼ、骨形成タンパク質(BMP)、hANP、グルカゴン様ペプチド(GLP−1)、VEG−F、組換えB型肝炎表面抗原(rHBsAg)、レニン、サイトカイン、ブラジキニン、バシトラシン、ポリミキシン、コリスチン、チロシジン、グラミシジン、エタネルセプト、イミグルセラーゼ、ドロトレコギンアルファ、シクロスポリン及び合成類似体、並びに酵素、サイトカイン、抗体、抗原及びワクチンの製剤可能な活性修飾体及び断片、リツキシマブ、インフリキシマブ、トラスツズマブ、アダリムマブ、オマリズマブ、トシツモマブ、エファリズマブ及びセツキシマブ等の抗体の下位群から選択されることを特徴とする請求項1に記載の製剤。 - 請求項1〜18のいずれかに記載の液体製剤から得られた乾燥粉末の形態を備えることを特徴とする少なくとも一つの活性成分(AP)を持続放出する固体の製剤。
- 請求項1〜18のいずれかに記載の少なくとも一つの活性成分(AP)を持続放出する製剤を調製する方法であって、
1)3〜6.5の間のpH値で、ポリアミノ酸ポリマー(PO)の水性コロイド溶液を準備する工程であって、前記ポリアミノ酸ポリマー(PO)がグルタミン酸残基を含み、ここで、
一部のグルタミン酸残基は、それぞれがペンダントの陽イオン基(CG)を有し、前記陽イオン基は、互いに同一でも異なっていてもよく、
他のグルタミン酸残基は、それぞれがペンダントの疎水基(GH)を有し、前記疎水基(GH)は、互いに同一でも異なっていてもよく、
任意には、更に他のグルタミン酸残基が、それぞれペンダントの中性基(NG)を有し、前記中性基(NG)は、互いに同一でも異なっていてもよく、
任意には、更に他のグルタミン酸残基が、未変性であり;
陽イオン基(CG)、疎水基(GH)、任意の中性基(NG)及び任意のグルタミン酸塩の各モル分率は、1mlの前記製剤が体積1mlのテスト緩衝溶液Tpとの混合中に沈殿するほどである工程と;
2)少なくとも一つの活性成分(AP)を工程1において得られたポリマー(PO)に加える工程であって、前記活性成分が前記ポリマーのコロイド溶液の粒子と非共有で会合している工程と、
を備えることを特徴とする方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0703186A FR2915683B1 (fr) | 2007-05-03 | 2007-05-03 | Formulations pharmaceutiques auto-precipitantes pour la liberation modifiee de principe actif |
| PCT/EP2008/055506 WO2008135562A1 (fr) | 2007-05-03 | 2008-05-05 | Formulations pharmaceutiques auto-precipitantes pour la liberation modifiee de principe actif |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2010526041A true JP2010526041A (ja) | 2010-07-29 |
Family
ID=39027559
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010504756A Pending JP2010526041A (ja) | 2007-05-03 | 2008-05-05 | 活性成分を制御放出するための自己沈澱製剤 |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US8236353B2 (ja) |
| EP (1) | EP2155164A1 (ja) |
| JP (1) | JP2010526041A (ja) |
| KR (1) | KR20100016513A (ja) |
| CN (1) | CN101674809A (ja) |
| AU (1) | AU2008248603A1 (ja) |
| BR (1) | BRPI0809288A2 (ja) |
| CA (1) | CA2685873A1 (ja) |
| FR (1) | FR2915683B1 (ja) |
| IL (1) | IL201465A0 (ja) |
| MX (1) | MX2009011814A (ja) |
| WO (1) | WO2008135562A1 (ja) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2563737T3 (es) * | 2011-05-20 | 2016-03-16 | Ares Trading S.A. | Composiciones de IFN-beta, métodos de preparación y usos de las mismas |
| DK2741765T3 (en) | 2011-08-10 | 2016-06-13 | Adocia | Injectable solution of at least one type of basal insulin |
| US9198971B2 (en) * | 2012-01-09 | 2015-12-01 | Adocia | Injectable solution at pH 7 comprising at least one basal insulin the pI of which is between 5.8 and 8.5 and a substituted co-polyamino acid |
| US20150314003A2 (en) | 2012-08-09 | 2015-11-05 | Adocia | Injectable solution at ph 7 comprising at least one basal insulin the isoelectric point of which is between 5.8 and 8.5 and a hydrophobized anionic polymer |
| EP3079668A1 (en) | 2013-12-09 | 2016-10-19 | Durect Corporation | Pharmaceutically active agent complexes, polymer complexes, and compositions and methods involving the same |
| US9849125B1 (en) | 2015-11-03 | 2017-12-26 | Banner Lifie Sciences LLC | Anti-overingestion dosage forms |
| BR112018075250A2 (pt) * | 2016-06-07 | 2019-03-12 | Adocia | composição na forma de uma solução aquosa injetável, cujo ph é de 6,0 a 8,0 |
| FR3052072A1 (fr) * | 2016-06-07 | 2017-12-08 | Adocia | Solution injectable a ph 7 comprenant au moins une insuline basale dont le pi est compris entre 5,8 et 8,5 et un co-polyaminoacide porteur de charges carboxylates et de radicaux hydrophobes |
| US10335375B2 (en) | 2017-05-30 | 2019-07-02 | Patheon Softgels, Inc. | Anti-overingestion abuse deterrent compositions |
| CN111698999A (zh) * | 2017-12-06 | 2020-09-22 | 阿道恰公司 | 包含至少一种pi在5.8与8.5之间的基础胰岛素和带有羧酸根电荷及疏水基的共聚氨基酸的ph为7的可注射溶液 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006079614A2 (fr) * | 2005-01-27 | 2006-08-03 | Flamel Technologies | Copolyhydroxyalkylglutamines fonctionnalises par des groupements hydrophobes et leurs applications notamment therapeutiques |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6201072B1 (en) * | 1997-10-03 | 2001-03-13 | Macromed, Inc. | Biodegradable low molecular weight triblock poly(lactide-co- glycolide) polyethylene glycol copolymers having reverse thermal gelation properties |
| EP1034207B1 (en) | 1997-10-03 | 2005-03-02 | Macromed Inc. | BIODEGRADABLE LOW MOLECULAR WEIGHT TRIBLOCK POLY(LACTIDE-co-GLYCOLIDE) POLYETHYLENE GLYCOL COPOLYMERS HAVING REVERSE THERMAL GELATION PROPERTIES |
| EP0963758A3 (en) * | 1998-05-07 | 2000-03-22 | Universiteit Gent | Synthetic polyaminoacid complexes for delivery of nucleic acids to target cells |
| US6143314A (en) * | 1998-10-28 | 2000-11-07 | Atrix Laboratories, Inc. | Controlled release liquid delivery compositions with low initial drug burst |
| FR2786098B1 (fr) * | 1998-11-20 | 2003-05-30 | Flamel Tech Sa | Particules a base de polyaminoacide(s) et susceptibles d'etre utilisees comme vecteurs de principe(s) actif(s), suspension colloidale les comprenant et leurs procedes de fabrication |
| FR2801226B1 (fr) | 1999-11-23 | 2002-01-25 | Flamel Tech Sa | Suspension colloidale de particules submicroniques de vectorisation de principes actifs et son mode de preparation |
| FR2840614B1 (fr) * | 2002-06-07 | 2004-08-27 | Flamel Tech Sa | Polyaminoacides fonctionnalises par de l'alpha-tocopherol et leurs applications notamment therapeutiques |
| FR2855521B1 (fr) * | 2003-05-28 | 2005-08-05 | Flamel Tech Sa | Polyaminoacides fonctionnalises par au moins un groupement h ydrophobe et leurs applications notamment therapeutiques. |
| FR2862536B1 (fr) | 2003-11-21 | 2007-11-23 | Flamel Tech Sa | Formulations pharmaceutiques pour la liberation prolongee de principe(s) actif(s), ainsi que leurs applications notamment therapeutiques |
| FR2892725B1 (fr) | 2005-10-31 | 2011-03-04 | Flamel Tech Sa | Acides polyglutamiques fonctionnalises par des derives de l'histidine et des groupements hydrophobes et leurs applications notamment therapeutiques |
| FR2915748B1 (fr) * | 2007-05-03 | 2012-10-19 | Flamel Tech Sa | Acides polyglutamiques fonctionnalises par des groupes cationiques et des groupements hydrophobes et leurs applications, notamment therapeutiques |
-
2007
- 2007-05-03 FR FR0703186A patent/FR2915683B1/fr not_active Expired - Fee Related
-
2008
- 2008-05-05 CN CN200880014417A patent/CN101674809A/zh active Pending
- 2008-05-05 US US12/149,541 patent/US8236353B2/en not_active Expired - Fee Related
- 2008-05-05 EP EP08750063A patent/EP2155164A1/fr not_active Withdrawn
- 2008-05-05 JP JP2010504756A patent/JP2010526041A/ja active Pending
- 2008-05-05 MX MX2009011814A patent/MX2009011814A/es unknown
- 2008-05-05 WO PCT/EP2008/055506 patent/WO2008135562A1/fr not_active Ceased
- 2008-05-05 KR KR1020097023698A patent/KR20100016513A/ko not_active Ceased
- 2008-05-05 BR BRPI0809288-5A2A patent/BRPI0809288A2/pt not_active IP Right Cessation
- 2008-05-05 CA CA002685873A patent/CA2685873A1/fr not_active Withdrawn
- 2008-05-05 AU AU2008248603A patent/AU2008248603A1/en not_active Abandoned
-
2009
- 2009-10-12 IL IL201465A patent/IL201465A0/en unknown
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006079614A2 (fr) * | 2005-01-27 | 2006-08-03 | Flamel Technologies | Copolyhydroxyalkylglutamines fonctionnalises par des groupements hydrophobes et leurs applications notamment therapeutiques |
Non-Patent Citations (1)
| Title |
|---|
| JPN6012031350; Wei-Chiang Shen: Biochimica et Biophysica Acta 1034(1), 1990, p.122-124 * |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2008248603A1 (en) | 2008-11-13 |
| BRPI0809288A2 (pt) | 2014-10-14 |
| US8236353B2 (en) | 2012-08-07 |
| FR2915683B1 (fr) | 2009-08-07 |
| EP2155164A1 (fr) | 2010-02-24 |
| WO2008135562A1 (fr) | 2008-11-13 |
| CA2685873A1 (fr) | 2008-11-13 |
| FR2915683A1 (fr) | 2008-11-07 |
| KR20100016513A (ko) | 2010-02-12 |
| US20090011028A1 (en) | 2009-01-08 |
| IL201465A0 (en) | 2010-05-31 |
| CN101674809A (zh) | 2010-03-17 |
| MX2009011814A (es) | 2009-11-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2010526041A (ja) | 活性成分を制御放出するための自己沈澱製剤 | |
| US8716217B2 (en) | Polyglutamic acids functionalized by cationic groups and hydrophobic groups and applications thereof, in particular therapeutic applications thereof | |
| KR101463952B1 (ko) | 활성 성분의 지연 방출용 약학 제제와, 이들의 용도, 특히 치료 용도 | |
| US20080152675A1 (en) | Dispersion of polyamino acids in a continuous lipid phase | |
| JP5302197B2 (ja) | 両親媒性コポリマーおよび調節放出の有効成分を基にした微小粒子、ならびにこれらを含む医薬製剤 | |
| EP2042184B1 (en) | Physiologically active polypeptide, polymer micelle having protein enclosed therein, and process for production of the polymer micelle | |
| ZA200603950B (en) | Pharmaceutical formulations for the sustained release of one or more active principles and applications thereof, such as therapeutic applications | |
| US20140105993A1 (en) | Modified-release microparticles based on amphiphilic copolymer and on active principle(s) and pharmaceutical formulations comprising them | |
| US8481019B2 (en) | Modified-release particles of polyelectrolytes and pharmaceutical formulations thereof | |
| US20120156256A1 (en) | Nanoparticles having at least one active ingredient and at least two polyelectrolytes | |
| HK1126408A (en) | Physiologically active polypeptide, polymer micelle having protein enclosed therein, and process for production of the polymer micelle |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110218 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20130131 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130205 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130418 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130425 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20131119 |