JP2010096506A - 癌が疑われる患者または癌患者由来の組織の癌部と非癌部との判別方法およびそれに用いる判別試薬 - Google Patents
癌が疑われる患者または癌患者由来の組織の癌部と非癌部との判別方法およびそれに用いる判別試薬 Download PDFInfo
- Publication number
- JP2010096506A JP2010096506A JP2008264794A JP2008264794A JP2010096506A JP 2010096506 A JP2010096506 A JP 2010096506A JP 2008264794 A JP2008264794 A JP 2008264794A JP 2008264794 A JP2008264794 A JP 2008264794A JP 2010096506 A JP2010096506 A JP 2010096506A
- Authority
- JP
- Japan
- Prior art keywords
- cancer
- cancerous
- patient
- tissue
- antibody
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Landscapes
- Investigating Or Analysing Biological Materials (AREA)
Abstract
【解決手段】癌が疑われる患者または癌患者由来の組織検体中のクラスリンヘビーチェインおよびホルムイミノトランスフェラーゼシクロデアミナーゼの少なくとも一つの発現レベルを測定することにより、癌部と非癌部とを、感度良くかつ特異的に、判別することができる。
【選択図】なし
Description
通常、HCCの検出には血清マーカーおよび画像診断に分かれる。血清マーカーにはAFP−L3、PIVKA−IIがあり、広く利用されているが早期発見は困難である(非特許文献1および非特許文献2)。画像診断には超音波検査が用いられ、2cm以下の結節を検出することが可能であるが、HCCとの確定診断は困難である。2cm以下の結節においては、生検組織の病理学的診断が推奨されている。病理医はこれを小さな切片内の情報のみで診断しなければならないが、この様な小さな結節の良・悪性の診断は、経験豊かな病理医でさえ困難であることが多い。
近年肝硬変における初期原発性肝細胞性癌(eHCC)と良性結節を鑑別する検討として、Grypican−3等をマーカーとして用いた病理診断が有用と報告された(非特許文献3および非特許文献4)。しかし、本発明者らの検討によると、これらの診断では、癌を癌と高い確率で判定できるとは言えず、また、非癌を非癌と高い確率で判定できるとも言えず、新たなマーカーの開発が望まれている。
ところで、近年、ヒトゲノムプロジェクトによりゲノム・データベースが発表され、さらにMS/MS技術の開発によって蛋白の高効率な同定が可能になった。これらの分析・解析技術の発展は、蛋白質の網羅的な発現解析、すなわちプロテオーム解析を可能にした。
HCCにおいても、病態と正常時の発現を比較することにより、2次元電気泳動や多重蛍光標識2次元電気泳動法、2次元高速液体クロマトグラフィー法を用いたプロテオーム解析が報告された。これらの結果、多くの蛋白がeHCCマーカー候補として同定された。しかしながら、いずれも臨床応用された例はほとんど無い。
Lancet 2003; 362:1907-1917 Am J Gastroenterol 1999;94:650-654 Gastroenterology 2003;125:89-97 HEPATOLOGY 2007;45:725-734
更に、本発明は、抗クラスリンヘビーチェイン抗体および抗ホルムイミノトランスフェラーゼシクロデアミナーゼ抗体を含む、癌が疑われる患者または癌患者由来の組織の癌部と非癌部とを判別するための判別試薬に関する。
本発明において、クラスリンヘビーチェイン(Clathrin heavy chain)とはCHCと標記され、Swiss−Prot entry No, Q00610でコードされる分子量192kDa、1675アミノ酸で構成される蛋白質であり、Hc; CHC; CHC17; CLH−17; CLTCL2; KIAA0034; CLTC等の略称を持つ、細胞膜および細胞内小器官の表面で細胞内輸送の受容体や様々な高分子物質の貪食に関与する蛋白を云う。
本発明において、ホルムイミノトランスフェラーゼシクロデアミナーゼ(formiminotransferase cyclodeaminase)とは、FTCDと標記され、Swiss−Prot entry O95954でコードされる分子量59kDa,541アミノ酸で構成される蛋白質であり、FTCD, LCHC1等の略称を持つ、葉酸代謝(formiminotransferase)およびグルタミン酸代謝(cyclodeaminase)の2種類の機能を持つ肝臓特異的に発現する酵素を云う。
ここで、感度とは、癌を癌と判定できた確率を言い、特異性とは、非癌を非癌と判定できた確率を言う。感度並びに特異性を上昇させることがより正確な判別にとって必要である。
従って、CHCとFTCDの両者の発現レベルを測定して、両者の発現レベルに基づき判別することにより、より感度良く特異的に、癌部と非癌部とを判別することができる。すなわち、CHCの発現レベルが、通常レベルより高く、またはFTCDの発現レベルが、通常レベルより低い場合には、より感度良く、癌部と判定でき、他方、CHCの発現レベルが、通常レベルより低く、かつFTCDの発現レベルが、通常レベルより高い場合には、より特異的に、非癌部と判定できる。
また、本発明では、癌が疑われる患者あるいは癌患者の結節の組織について、CHCおよびFTCDの少なくとも一つの発現レベルを測定することにより、良性結節と悪性結節とを、感度良くかつ特異的に判別することができる。更には、癌の分化度を判別することも可能である。
ここで、発現レベルとは、CHCおよびFTCD遺伝子の転写産物のmRNAの量でもよく、翻訳産物の蛋白質量でもよく、さらにFTCDの場合はその酵素活性値にても表示することが可能である。例えば、蛋白質量であればそれを認識する抗体で通常の方法で測定される蛋白質量にて表示することも可能である。また、例えば、以下に詳細に説明する、標識化抗体を用いた組織免疫染色法では、発現レベルを染色強度として検出することも可能である。
本発明において組織免疫染色法とは、標識化抗体を用いる免疫反応により組織・細胞等を顕微鏡等で観察することができるように染色する方法をいう。組織免疫染色法によるCHCおよびFTCDの蛋白質の発現レベルを検出するときは、例えば、以下のようにする。癌等が疑われている患者の組織を一部とり、常法によりホルマリン固定をした後、パラフィンに抱埋をしてミクロトームにて薄切し、組織検体として使用する。組織切片はキシレンの処理で完全にパラフィンを除き、アルコール溶液をくぐらせた後、水洗する。続いてクエン酸緩衝液中で、80℃〜還流にて2〜10分間のマイクロウェーブ処理を2〜5回行い、抗原を賦活化する。自然冷却した後、流水で水洗し、その後、過酸化水素溶液で内因性ペルオキシダーゼを失活させる。精製水ですすいだ後、1%ウシアルブミン溶液を10分間のせる。標本上の1%ウシアルブミン溶液を落してそのまま1次抗体をのせる。1次抗体とは抗CHC抗体または抗FTCD抗体を希釈したものを用いる。この状態のまま4℃で一晩反応させた後、PBSで2〜10分ずつ、1〜5回洗浄する。ここに酵素標識抗体(CHC:mouse抗体, FTCD:rabbit抗体)を乗せ、1〜30℃で0.5〜10時間反応させる。PBSで5分×3回洗浄後、DAB等の発色試薬で1〜30分反応させ、PBSで洗浄後精製水中に2分浸透させる。対比染色としてヘマトキシリン核染色を行い、水洗する。アルコール溶液およびキシレンをくぐらせた後に封入剤を滴下し、カバーガラスを被せる。こうして染色された組織標本を顕微鏡で観察することにより、組織中のCHCまたはFTCDの各蛋白質発現レベルを染色強度として検出できる。
本発明では、これらの抗CHC抗体および抗FTCD抗体の少なくとも一つを含む、癌が疑われる患者または癌患者由来の組織の癌部と非癌部を判別するための判別試薬が提供される。この判別試薬においては、必要に応じて、組織免疫染色法あるいはイムノブロット法で通常使用される2次抗体などの他の試薬を含んでいてもよい。
実施例1
組織免疫染色法による癌部と非癌部の判別
本発明の判別方法により、原発性肝細胞癌から採取した組織検体について、CHCおよびFTCDの発現レベルを測定した。
原発性肝細胞癌(HCC)組織は、外科手術の前に、すべての患者から書面によるインフォームドコンセントを得た後に、切除例から得た。切除試料は癌部・非癌部組織とも手術後1時間以内に得られた。全ての切除組織は直ちに液体窒素で冷凍し、分析に使用するまで−80℃で保存した。
組織免疫染色法によるCHCおよびFTCD蛋白質の発現レベルの検出は以下のようにして行った。すなわち、患者から得たHCC組織を検体とし、その検体を常法によりホルマリン固定をした後、パラフィンに抱埋をしてミクロトームにて薄切し、組織検体として使用した。組織切片はキシレンの処理で完全にパラフィンを除き、アルコール溶液をくぐらせた後、水洗した。続いてクエン酸緩衝役中で100℃5分間のマイクロウェーブ処理を3回行い、抗原を賦活化した。20分の自然冷却後、流水で水洗し、その後過酸化水素溶液で内因性ペルオキシダーゼを失活させた。精製水ですすいだ後、1%ウシアルブミン溶液を10分間乗せた。標本上の1%ウシアルブミン溶液を落してそのまま1次抗体を載せた。1次抗体として、抗CHCモノクローナル抗体(BDバイオサイエンス社製)または抗FTCDモノクローナル抗体(Abcam社製)を抗体希釈液(DAKO社製)で200倍に希釈したものを用いた。この状態のまま4℃で一晩反応させた後、PBSで5分×3回洗浄した。ここにENVISIONポリマー試薬(DAKO社製CHC:mouse抗体,FTCD:rabbit抗体)を乗せ、室温2時間または4℃5−6時間反応させた。PBSで5分×3回洗浄後、発色試薬(DAB)で10分反応させ、PBSで洗浄後精製水中に2分浸透させた。対比染色としてヘマトキシリン核染色を行い、水洗した。アルコール溶液およびキシレンをくぐらせた後に封入剤を滴下し、カバーガラスを被せた。こうして染色された組織標本を顕微鏡で観察することにより、組織検体中のCHCまたはFTCDの各蛋白質発現レベルを染色強度として検出した。
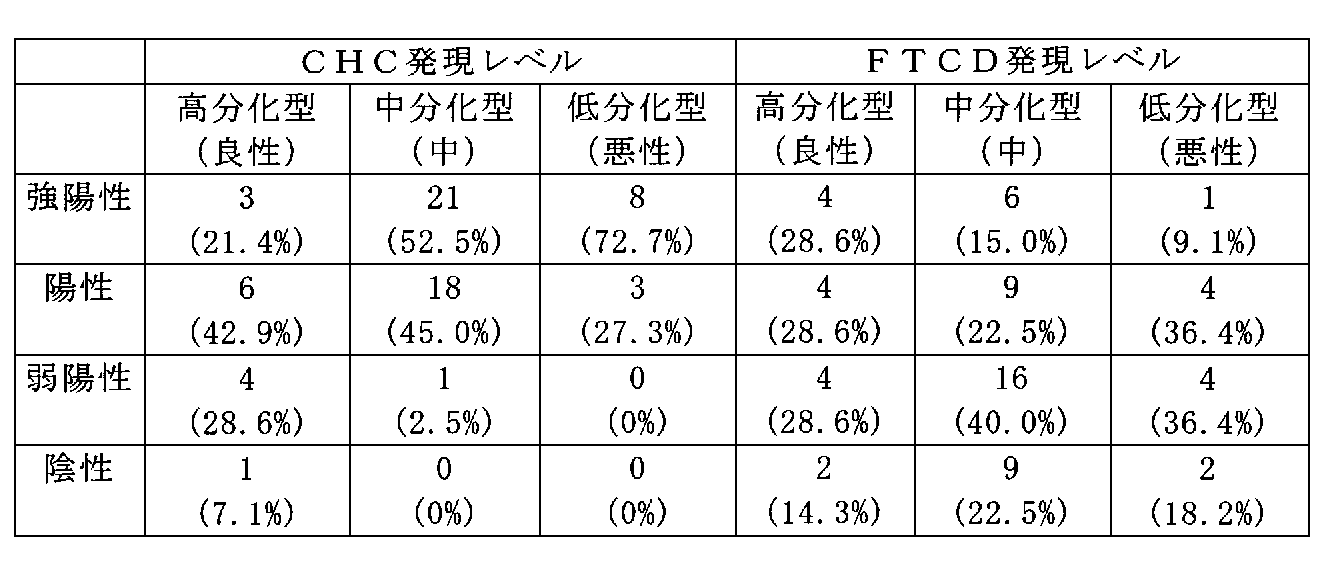
1)実施対象は原発性肝細胞癌83例および非癌部68例である。各部の組織を一部取り出し、上記の方法により、染色性後、顕微鏡で染色性を観察し、染色強度を、陰性、弱陽性、陽性、強陽性の4段階に分類した。結果を表1に示した。
CHCの染色性が強陽性であれば原発性肝細胞癌であるとした場合、感度(癌を癌と判定できた確率)51.8%(43例/83例)、特異度(非癌を非癌と判定できた確率)は95.6%(65例/68例)であった。またFTCDの染色性が弱陽性以下であれば原発性肝細胞癌であるとした場合、感度は61.4%(51例/83例)、特異度は98.5%(67例/68例)であった。いずれの蛋白も感度50%以上でかつ特異度が95%以上と高い判定精度を示したことから、CHCおよびFTCDの蛋白発現レベルは原発性肝細胞癌の診断に有用であることが確認された。CHCおよびFTCDの染色により癌部と非癌部の境目がこの方法により判定できることがわかった。
組織免疫染色法による悪性結節と良性結節の判別
原発性肝細胞癌は数cm程度の結節から発生する場合が多いが、肝臓においては良性の結節も多く発生し、これらを正しく鑑別・診断することは非常に重要である。特に原発性肝細胞癌の初期段階である早期肝細胞癌を、細胞の形だけから診断することは病理医にとっても困難である。
経験を積んだ病理医によって細胞の浸潤や被膜の状態などの総合的な判断によって診断された、早期肝細胞癌17または18例、良性結節8例および良性腫瘍2例の結節辺縁部分を、実施例1の(1)の方法と同様にして染色した。CHCの染色性が非癌部(または非結節部)に比較して強く発現していれば早期肝細胞癌であるとすると、感度(癌を癌と判定できた確率)は41.2%(7例/17例)、特異度(非癌を非癌と判定できた確率)は77.8%(7例/9例)であった。またFTCDの染色性が非癌部(または非結節部)に比較して弱く発現していれば早期肝細胞癌であるとすると、感度は44.4%(8例/18例)、特異度は80.0%(8例/10例)であった。また両蛋白を組み合わせることで、感度が72.2%と上昇した。従って肝臓の結節辺縁部のCHCおよびFTCDの蛋白発現レベル、すなわち染色強度は、結節が早期肝細胞癌か、あるいは良性結節であるかの判定に有用であった。
CHC発現レベルによる各種癌での判別
CHCは、ほかの癌においても発現が増大するため、肝癌以外の組織診断の有用性を確認した。対象は膀胱癌20例および膀胱非癌部5例、乳癌34例および乳房非癌部5例、肺癌30例および肺非癌部5例、卵巣癌34例および卵巣非癌部5例、前立腺癌20例および前立腺非癌部5例、皮膚癌20例および皮膚非癌部5例、甲状腺癌20例および甲状腺非癌部5例である。
膀胱において強陽性は膀胱癌であると仮定した場合、感度(癌を癌と判定できた確率)75.0%,特異度(非癌を非癌と判定できた確率)100%であった。同様に乳房において陽性あるいは強陽性は乳癌であると仮定した場合、感度76.4%,特異度100%、肺において強陽性は肺癌であると仮定した場合、感度86.6%,特異度100%、卵巣において強陽性は卵巣癌であると仮定した場合、感度58.8%,特異度80.0%、前立腺において強陽性は前立腺癌であると仮定した場合、感度36.8%,特異度100%、皮膚において強陽性は皮膚癌であると仮定した場合、感度55.2%,特異度70.0%、甲状腺において陽性あるいは強陽性は膀胱癌であると仮定した場合、感度100%,特異度100%であった。
従ってCHCは少なくとも膀胱癌、乳癌、肺癌、卵巣癌、前立腺癌、皮膚癌、甲状腺癌の組織診断に有用であった。またあらゆる悪性腫瘍の組織診断に有用である可能性が示された。
Claims (9)
- 癌が疑われる患者または癌患者由来の組織検体中における、クラスリンヘビーチェインおよび/またはホルムイミノトランスフェラーゼシクロデアミナーゼの発現レベルを測定して、癌部と非癌部とを判別することを特徴とする、癌が疑われる患者または癌患者由来の組織の癌部と非癌部の判別方法。
- 癌が原発性肝細胞癌である、請求項1に記載の判別方法。
- 組織検体中のクラスリンヘビーチェインおよびホルムイミノトランスフェラーゼシクロデアミナーゼの発現レベルを測定する、請求項1または2に記載の判別方法。
- 抗クラスリンヘビーチェイン抗体および/または抗ホルムイミノトランスフェラーゼシクロデアミナーゼ抗体を用いて、組織免疫染色法により組織検体中のクラスリンヘビーチェインおよび/またはホルムイミノトランスフェラーゼシクロデアミナーゼを測定する、請求項1から3のいずれか1項に記載の判別方法。
- 癌が疑われる患者または癌患者の結節由来の組織検体中における、クラスリンヘビーチェインおよび/またはホルムイミノトランスフェラーゼシクロデアミナーゼの発現レベルを測定して、悪性結節と良性結節を判別する、請求項1から4のいずれか1項に記載の判別方法。
- 組織検体中のクラスリンヘビーチェインおよびホルムイミノトランスフェラーゼシクロデアミナーゼの少なくとも一つの発現レベルを測定して、癌の分化度を判別する、請求項1から5のいずれか1項に記載の判別方法。
- 抗クラスリンヘビーチェイン抗体および抗ホルムイミノトランスフェラーゼシクロデアミナーゼ抗体を含む、癌が疑われる患者または癌患者由来の組織の癌部と非癌部とを判別するための判別試薬。
- 抗クラスリンヘビーチェイン抗体および抗ホルムイミノトランスフェラーゼシクロデアミナーゼ抗体を含む、請求項7に記載の判別試薬。
- 組織免疫染色法により判別するための、請求項7または8に記載の判別試薬。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008264794A JP5133842B2 (ja) | 2008-10-14 | 2008-10-14 | 癌が疑われる患者または癌患者由来の組織の癌部と非癌部との判別方法およびそれに用いる判別試薬 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008264794A JP5133842B2 (ja) | 2008-10-14 | 2008-10-14 | 癌が疑われる患者または癌患者由来の組織の癌部と非癌部との判別方法およびそれに用いる判別試薬 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2010096506A true JP2010096506A (ja) | 2010-04-30 |
| JP2010096506A5 JP2010096506A5 (ja) | 2011-12-01 |
| JP5133842B2 JP5133842B2 (ja) | 2013-01-30 |
Family
ID=42258307
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008264794A Expired - Fee Related JP5133842B2 (ja) | 2008-10-14 | 2008-10-14 | 癌が疑われる患者または癌患者由来の組織の癌部と非癌部との判別方法およびそれに用いる判別試薬 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5133842B2 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011117781A (ja) * | 2009-12-02 | 2011-06-16 | Nitto Boseki Co Ltd | クラスリン重鎖とその自己抗体との複合体の免疫測定方法、それに用いるキット及びそれを用いた癌判定方法 |
| TWI485158B (zh) * | 2011-10-04 | 2015-05-21 | Academia Sinica | 供抑制腫瘤血管生成及生長之新穎的抗網格蛋白重鏈之單株抗體及其應用 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3208839B2 (ja) | 1992-04-20 | 2001-09-17 | 大同特殊鋼株式会社 | 被処理材の熱処理方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009034092A (ja) * | 2007-08-01 | 2009-02-19 | National Yang Ming Univ | グリシンメチルトランスフェラーゼ(gnmt)動物モデル及びその使用 |
| JP2009531332A (ja) * | 2006-03-23 | 2009-09-03 | ライフ テクノロジーズ コーポレーション | 癌細胞株のインビボイメージングのための方法及び試薬 |
| JP2009541741A (ja) * | 2006-06-20 | 2009-11-26 | ジェネンテック・インコーポレーテッド | アポトーシスを観察するための方法と材料 |
-
2008
- 2008-10-14 JP JP2008264794A patent/JP5133842B2/ja not_active Expired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009531332A (ja) * | 2006-03-23 | 2009-09-03 | ライフ テクノロジーズ コーポレーション | 癌細胞株のインビボイメージングのための方法及び試薬 |
| JP2009541741A (ja) * | 2006-06-20 | 2009-11-26 | ジェネンテック・インコーポレーテッド | アポトーシスを観察するための方法と材料 |
| JP2009034092A (ja) * | 2007-08-01 | 2009-02-19 | National Yang Ming Univ | グリシンメチルトランスフェラーゼ(gnmt)動物モデル及びその使用 |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011117781A (ja) * | 2009-12-02 | 2011-06-16 | Nitto Boseki Co Ltd | クラスリン重鎖とその自己抗体との複合体の免疫測定方法、それに用いるキット及びそれを用いた癌判定方法 |
| TWI485158B (zh) * | 2011-10-04 | 2015-05-21 | Academia Sinica | 供抑制腫瘤血管生成及生長之新穎的抗網格蛋白重鏈之單株抗體及其應用 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5133842B2 (ja) | 2013-01-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Lopez | Recent developments in the first detection of hepatocellular carcinoma | |
| CN103547923B (zh) | 乳腺癌的生物标记 | |
| CN112345755A (zh) | 乳腺癌的生物标志物及其应用 | |
| Malov et al. | Search for effective serum tumor markers for early diagnosis of hepatocellular carcinoma associated with hepatitis C | |
| JP2017133831A (ja) | 大腸がんの転移検出方法 | |
| Ciregia et al. | Proteomic analysis of fine-needle aspiration in differential diagnosis of thyroid nodules | |
| EP3493819A1 (en) | Keratin 17 as a biomarker for bladder cancer | |
| CN109187979B (zh) | 蛋白芯片、蛋白质芯片诊断试剂盒制备及使用方法 | |
| Dong et al. | Serum Golgi protein 73 is a prognostic rather than diagnostic marker in hepatocellular carcinoma | |
| JP5133842B2 (ja) | 癌が疑われる患者または癌患者由来の組織の癌部と非癌部との判別方法およびそれに用いる判別試薬 | |
| JP2011209101A (ja) | CapGをマーカーとする悪性腫瘍の予後予測検査方法 | |
| Hu et al. | Correlation between serum ESPL1 and hepatitis B virus-related hepatocellular carcinoma histological grade: a Chinese single-center case-control study | |
| Jin et al. | 2‐D DIGE and MALDI‐TOF‐MS analysis of the serum proteome in human osteosarcoma | |
| JPWO2008096767A1 (ja) | 肝細胞がんタンパク質マーカーとそれを用いた肝細胞がん検出方法及び装置 | |
| Subwongcharoen et al. | Serum AFP and AFP-L3 in clinically distinguished hepatocellular carcinoma from patients with liver masses | |
| CN119630966A (zh) | 用于对膀胱癌进行风险分层和管理的方法和系统 | |
| Kalfert et al. | Pretreatment Serum Levels of Soluble Cytokeratin Fragments (Cyfra 21-1, TPS, MonoTotal) in Relation to Clinical and Pathobiological Aspects of Head and Neck Squamous Cell Carcinomas | |
| CN114660289A (zh) | 肝癌标志物及其应用 | |
| JP2006308576A (ja) | 膵液による膵管内乳頭粘液性腺癌および膵臓癌の検出法及び検出キット | |
| CN113721021A (zh) | Prkcz自身抗体在食管鳞癌辅助诊断中的应用 | |
| CN113671180A (zh) | Paip1自身抗体在食管鳞癌辅助诊断中的应用 | |
| CN108362884B (zh) | 一种肿瘤危险度和治疗效果评估的血清及组织分子指标 | |
| US20120225441A1 (en) | Protein markers for detecting liver cancer and method for identifying the markers thereof | |
| JP5130465B2 (ja) | 肝細胞癌マーカー及び肝細胞癌の検査方法 | |
| CN113588951B (zh) | Eca作为分子标志物在制备用于诊断和/或预后评价肝癌的试剂盒中的应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111014 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20111014 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120821 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20120822 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121005 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20121102 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20121108 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20151116 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 Ref document number: 5133842 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20151116 Year of fee payment: 3 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313117 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |