JP2008526322A - 多層を含む生分解性コーティング組成物 - Google Patents
多層を含む生分解性コーティング組成物 Download PDFInfo
- Publication number
- JP2008526322A JP2008526322A JP2007549730A JP2007549730A JP2008526322A JP 2008526322 A JP2008526322 A JP 2008526322A JP 2007549730 A JP2007549730 A JP 2007549730A JP 2007549730 A JP2007549730 A JP 2007549730A JP 2008526322 A JP2008526322 A JP 2008526322A
- Authority
- JP
- Japan
- Prior art keywords
- bioactive agent
- article
- coating
- polymer
- coat layer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 0 C*C(c(cc1)ccc1C(**C(c1ccc(C=O)cc1)=O)=O)=O Chemical compound C*C(c(cc1)ccc1C(**C(c1ccc(C=O)cc1)=O)=O)=O 0.000 description 2
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/14—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L31/148—Materials at least partially resorbable by the body
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/08—Materials for coatings
- A61L31/10—Macromolecular materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/14—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L31/16—Biologically active materials, e.g. therapeutic substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/60—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a special physical form
- A61L2300/606—Coatings
- A61L2300/608—Coatings having two or more layers
- A61L2300/61—Coatings having two or more layers containing two or more active agents in different layers
Abstract
本発明は、用具の少なくとも1部分が、生分解性材料の多層コート層からなる生分解性コーティングを供える、患者の治療用具を提供する。本発明は、当該用具を利用する治療方法を更に提供する。
Description
発明の分野
本発明は、患者の体内の治療部位を効果的に治療するために、例えば、血管構造及び体内の他の部位の治療に有用である、生分解性成分を有する医療用具に関する。より具体的には、本発明は、移植可能医療物品と関連する薬物送達のための生分解性コーティング組成物に関する。
本発明は、患者の体内の治療部位を効果的に治療するために、例えば、血管構造及び体内の他の部位の治療に有用である、生分解性成分を有する医療用具に関する。より具体的には、本発明は、移植可能医療物品と関連する薬物送達のための生分解性コーティング組成物に関する。
関連出願の相互参照
本通常の出願は、2005年1月5日に出願され、「多層を含む生分解性コーティング組成物」のタイトルを有する、シリアル番号60/641,557を有する共同仮出願の利益を請求する。
本通常の出願は、2005年1月5日に出願され、「多層を含む生分解性コーティング組成物」のタイトルを有する、シリアル番号60/641,557を有する共同仮出願の利益を請求する。
発明の背景
管状臓器及び構造、例えば、血管は、管腔の狭窄又は閉塞を受けやすい。かかる狭窄又は閉塞は、様々な外傷性疾患又は器官疾患により引き起こされ、症状は、低度の炎症及び不快感から、麻痺及び死までの範囲であり得る。治療は、典型的には、部位-特異的であり、閉塞の性質及び程度と共に変動する。
管状臓器及び構造、例えば、血管は、管腔の狭窄又は閉塞を受けやすい。かかる狭窄又は閉塞は、様々な外傷性疾患又は器官疾患により引き起こされ、症状は、低度の炎症及び不快感から、麻痺及び死までの範囲であり得る。治療は、典型的には、部位-特異的であり、閉塞の性質及び程度と共に変動する。
命を脅かす狭窄は、心臓血管系に最も一般的に関連し、通常、経皮的冠動脈血栓溶解術(PTCA)を用いて治療される。この方法は、バルーンカテーテルを用いて閉塞部位での血管径を拡げることにより、管腔の狭くなった部分を改善する。しかしながら、PTCA後3〜6ケ月には、約30%〜40%の患者が、再狭窄を経験する。再狭窄は、PTCA中の、動脈壁に対する損傷により開始されると考えられている。再狭窄は、主に、損傷部位での、血管平滑筋細胞増殖及び細胞外マトリックス分泌から起こる。再狭窄は、頸動脈、大腿動脈、腸骨動脈及び腎動脈を含む非-冠動脈系疾患での主な問題でもある。
非-血管管状構造の再狭窄は、通常、炎症、新生物及び/又は良性内膜肥厚化により引き起こされる。食道及び腸構造の場合には、閉塞は、外科的に除くことができ、管腔は、接合により修復することができる。管及び導管に関連するより小さな経管腔も、この方法により修復することができる;しかしながら、内膜肥厚化により生じる再狭窄が一般的である。更に、披裂も、一般的には、更なる外科手術を必要とする接合に関連し、組織損傷の増加、炎症、及び再狭窄につながる組織傷跡を生じ得る。
ほとんどの最近の関心は、生物活性剤をその周囲(例えば、管腔壁又は冠動脈)に提供し又は放出する薬物溶出ステント(DES)に向けられている。一般的には、生物活性剤は、医療物品表面に表面修飾により結合し、ポリマー材料(マトリックス-型)内に埋め込み、そこから放出し、又は担体(リザーバ-型)により囲み、担体を通して放出することができる。かかる適用でのポリマー材料は、好ましくは、生物的に不活性なバリアとして働き、体内に更なる炎症を誘導しない。しかしながら、ポリマーの分子量、多孔性、及びポリマーコーティングの厚さは、医療用具に対して逆反応の原因となり得る。
用具、例えばステントに適用される、この薬物溶出コーティングによる現在の技術的挑戦は、望ましくない全身性の副作用を生じることなく、体内で一定期間、標的部位において局所的に生物活性剤の治療的濃度を達成することである。血管ステントの移植は、望ましくない全身性の副作用も生じ得る生物活性剤を利用する局所療法が必要とされる状況の主な例である。ステントは、配置の間及び移植の際には、血流内に置かれるので、可能性のある望ましくない全身性効果は、血流に入る治療物質の望ましくない量(例えば、望ましくないことに、高量)から起こることがある。更に、治療物質の量が、「バースト」効果の一部として血流に放出される場合には、ステントが一旦据え付けられると、潜在的に不十分な局所投薬を招き、試料物質のほとんどは、現実の局所治療には利用することができない。
ステント及びDESに関連する分解性材料を利用するいくつかの最近の研究がなされている。分解性用具及び用具上に提供される分解性コーティングは、典型的には、ポリマー内に物理的に固定される生物活性剤を有する。生物活性剤は、ポリマー材料の至るところに溶解し及び/又は分散することができる。分解性ポリマー材料は、一般的には、不安定な結合の加水分解により長期間、加水分解的に分解され、ポリマーを体液中に侵食させ、生物活性剤を体液中に放出する。一般的には、親水性ポリマーは、典型的には、疎水性ポリマーに比べて侵食の速度が速い。疎水性ポリマーは、ほとんど純水な水の表面拡散を有し、その結果、表面から内部への侵食を起こすと考えられている。親水性ポリマーは、水を、ポリマー表面に浸透させ、表面下の不安定な結合を加水分解し、ポリマーとの均一性又はポリマーの大量侵食を招き得ると考えられている。
徐放システムの目標は、治療範囲内で生物活性剤濃度、理想的には一定かつ予測可能な濃度を維持することである。比較的一定の濃度を達成するためには、生物活性剤は、時間の経過と共に変化しない速度で送達システムから放出されなければならない(いわゆる、ゼロ-オーダー放出)。好ましくは、生物活性剤の最初の用量は、送達システムにより維持される治療的用量である。しかしながら、多くのシステムでは、生物活性剤放出は、時間に比例するか(ゼロ-オーダー放出)又は時間の平方根である(Fickian放出)。
生物活性剤送達のための非分解性ポリマーマトリックス系では、生物活性剤は、マトリックスの至るところに分散し、マトリックスの至るところを溶解し、至るところに拡散するように放出される。生物活性剤は、マトリックスの外面から先ず放出され、この層は、消耗され、次いで、用具のコア内から更に放出される生物活性剤は、この消耗されたマトリックスを通して分散されなければならない。最終的な結果は、放出速度が長期に渡って遅くなることである。
ポリマーマトリックス系が分解性であるときには、生物活性剤の放出は、(非分解性ポリマーマトリックス系について考察したように)拡散により起こり、ポリマーの分解によっても起こり得る。生分解性ポリマーのin vivoでの寿命は、その分子量、結晶性、生物安定性及び架橋度に依拠することができる。一般的に、分子量が大きくなればなる程、結晶性の程度は高くなり、生物安定性は高くなり、生分解性は遅くなるだろう。従って、分解時間は、例えば、1日未満〜数ケ月まで広く変動し得る。従って、生分解性ポリマーマトリックス系からの放出反応速度論は、より複雑になる。生分解性ポリマーマトリックスからの生物活性剤の放出の複数のメカニズムの結果として、これらの種類の系からのゼロ-オーダー放出は、達成するのが非常に困難である。
発明の概要
一般的に、本発明は、移植可能医療物品の表面上へのコーティングとしての、生分解性組成物を含む移植可能医療物品を提供する。いくつかの局面では、本発明のポリマー製剤は、所望の用途に許容される期間内に生分解する。ある局面では、例えばin vivo療法では、かかる分解は、約25℃〜約37℃の範囲の温度を有する6〜8のpHを有する生理的溶液への曝露の際に、通常、約1年未満、又は約6ケ月未満、3ケ月未満、1ケ月未満、15日未満、5日未満、3日未満の期間内にもしくは1日未満の期間内にさえ起こる。ある実施態様では、ポリマー製剤は、所望の用途によって、約1時間〜数週間の範囲の期間に分解する。
一般的に、本発明は、移植可能医療物品の表面上へのコーティングとしての、生分解性組成物を含む移植可能医療物品を提供する。いくつかの局面では、本発明のポリマー製剤は、所望の用途に許容される期間内に生分解する。ある局面では、例えばin vivo療法では、かかる分解は、約25℃〜約37℃の範囲の温度を有する6〜8のpHを有する生理的溶液への曝露の際に、通常、約1年未満、又は約6ケ月未満、3ケ月未満、1ケ月未満、15日未満、5日未満、3日未満の期間内にもしくは1日未満の期間内にさえ起こる。ある実施態様では、ポリマー製剤は、所望の用途によって、約1時間〜数週間の範囲の期間に分解する。
その物品の局面では、本発明は、表面及び表面上に処置されたコーティングを有する用具であって、当該コーティングが、生物活性剤、及び第一生分解性ポリマーと第二生分解性ポリマーとのブレンドを含む、前記用具を提供する。ここで、第一生分解性ポリマーは、好ましくは、ポリエーテルエステルコポリマー、例えばポリ(エチレングリコール)テレフタレート/ポリブチレンテレフタレート(PEGT/PBT)である。ある実施態様において、用具はステントであり、特に血管ステントである。
生分解性組成物は、生分解性ポリマーの多層からなる。場合により、2超コート層は、コーティングを含むことができる。第一生分解性ポリマー及び第二生分解性ポリマーは、異なった生物活性剤放出速度を有する。ある実施態様において、第二生分解性ポリマーは、第一生分解性ポリマーよりも遅い生物活性剤放出速度を有する。生物活性剤は、コート層の少なくとも1つに存在する。
ある物品局面において、本発明は、表面に生物活性放出コーティングを有する移植可能な医療物品であって、当該コーティングが、(a) 生物活性剤及び第一生分解性ポリマーを含む第一コート層、ここで、第一生分解性ポリマーは、ポリアルキレングリコールテレフタレートと芳香族ポリエステルとのコポリマーであり:及び (b) 第一コート層の少なくとも1部分を覆いかつ第二生分解性ポリマーを含む第二コート層、を含み、ここで、第一生分解性ポリマー及び第二生分解性ポリマーは異なり、そして、第二生分解性ポリマーは、第一生分解性ポリマーに比べてより遅い生物活性剤放出剤速度を有するように選択される、前記物品を提供する。
他の物品局面において、本発明は、表面に生物活性放出コーティングを有する移植可能な医療物品であって、当該コーティングが、(a) 生物活性剤及び第二生分解性ポリマーを含む第一コート層、及び (b) ポリアルキレングリコールテレフタレートと芳香族ポリエステルとのコポリマーであるポリエーテルエステルコポリマーを含む外コート層を含み、、ここで、ポリエーテルエステルコポリマー及び第二生分解性ポリマーは異なり、そして、第二生分解性ポリマーは、ポリエーテルエステルコポリマーに比べてより遅い生物活性剤放出剤速度を有するように選択される、前記物品を提供する。
ポリマーエーテルエステルコポリマーに加えて、好適な第一生分解性ポリマーであるエステル結合を有する他のポリマーは、リン-含有結合を有するテレフタレート、及び異なったエステル結合を有するセグメント化コポリマーを含む。他の好適な第一生分解性ポリマーは、ポリカーボネート-含有ランダムポリマーを含む。第二生分解性ポリマーは、生分解性組成物からの生物活性剤放出速度を変更して、制御された放出速度を達成するように選択される。
ある局面では、生分解性組成物は、表面、例えば移植可能用具表面、上のコーティングを含む。本明細書に記載の「コーティング」は、1以上の「コート層」を含むことができる。各コート層は、1以上のコーティング成分を含む。場合によっては、コーティングは、第一生分解性ポリマーからなる第一コート層及び第二生分解性ポリマーからなる第二コート層を含む。生物活性剤は、1以上のコート層中に存在することができる。1超のコート層が用具表面に適用されるとき、それは、典型的に、連続して適用される。例えば、コート層は、典型的には、用具上のコーティング材料を浸漬し、当該コーティング材料に噴霧し又はブラシをかけて層を形成し、次いでコート層を乾燥することにより、形成される。この方法は、多層コート層を有するコーティングであって、少なくとも1層は生物活性剤を含む、前記コーティングを提供するために反復することができる。典型的には(常にとは限らないが)、用具表面に最も近く位置する少なくともコート層は、生物活性剤を含む。例えば、ある局面では、第一コート層は、第一生分解性ポリマー及び生物活性剤を含むことができ、第二コート層は、(生物活性剤なしで)第二生分解性ポリマーのみを含むことができる。
考察の目的のために、コーティングは、「第一」コート層、「第二」コート層等を含むと記載する。この態様でのコート層の意味は、コート層の化学組成を区別することを意味し、用具表面及び/又は他のコート層に関連してコート層の特定の位置に必ずしも起因するものではない。典型的には、必ずしもそうでないが、第一コート層は、用具表面の最も近傍に位置する。第二コート層は、典型的には、必ずしもそうでないが、第一コート層上に適用され、よって、2-層コーティング等のための用具の最外表面に位置する。連続的な方法でのコート層の記載は、本発明の概念のみを説明する目的のために利用され、このような考察は、コート層の組成を任意の特定のオーダーに限定する意図ではない。例えば、コート層の適用のオーダーは、第一生分解性層が最外コート層で利用され、一方、第二生分解性層が用具表面のコート層で利用されるように、変更することができる。
ある局面では、2超コート層が存在し得る。かかる他の層は、第一コート層及び/又は第二コート層と同一でも又は異なってもよい。特定の医療物品への使用のためのコーティングの好適性、及び適用技術の好適性は、当業者により評価することができ、本明細書の説明に記載されている。
その方法の局面では、本発明は、生物活性剤の制御された放出のための用具の製造法であって、以下のステップ:表面を有する用具を提供し;表面に、第一コート層、第二コート層及び生物活性剤からなる、多層の生分解性コーティング組成物を提供すること、を含む、前記方法を提供する。第一コート層は、第一生分解性ポリマーを含み、第二コート層は、第二生分解性ポリマーを含む。生物活性剤は、コート層の少なくとも1つに存在する。2超のコート層は、必要ならば、コーティングを含むことができる。好ましくは、処置ステップ(例えば、加熱、圧力の適用等)は、個々のコート層の適用の間に必要とされない。
更なる局面では、本発明は、制御された方法での患者への生物活性剤の送達のための方法であって、以下のステップ:患者に用具を提供すること、ここで用具は、表面、及び表面上に処置される生分解性コーティング組成物を有し、生分解性コーティング組成物は、第一コート層、第二コート層及び生物活性剤を含む、前記方法を提供する。ある局面では、当該方法は、選択された時間である、生物活性剤が制御されかつ予測可能な方法でコーティング組成物から放出される時間、患者に用具を提供するステップを含む。
より特定の局面では、本発明は、(例えば、血管構造の)治療を提供するための、生分解性である少なくとも1つの成分を含む用具、及び方法を提供する。好ましい局面では、体内に残る(分解されない及び/又は吸収されない)用具の任意の部分は、重大な逆の異質身体反応を起こさない。
本発明に従う好ましい組成物及び方法は、長期間、用具表面からの生物活性剤の放出速度を制御する能力を提供する。ある局面では、かかる制御は、生物活性剤の所望の放出プロファイルを達成するために、第二ポリマーを選択し、及び/又は第一ポリマー及び第二ポリマーの相対量を調整することにより提供される。第一ポリマー及び第二ポリマーからの生物活性剤放出速度は、相違する。同様に、コーティングが、2超のコート層を含むときには、生物活性剤の制御された放出は、第二、第三、及び(場合により)次のポリマーの選択により達成することができる。かかる次のポリマーの相対量、及びコーティング内の各コートポリマー層の相対的位置も、制御することができる。コーティングを含む個々のポリマーの放出速度は、好ましくは相違する。
好ましい局面では、本発明の生分解性組成物は、生分解性コーティングからの生物活性剤の制御された放出プロファイルを提供するように選択される。放出プロファイルは、放出された生物活性剤の累積量対時間である。中程度の放出及び徐放を含む、生物活性剤の放出の時間プロファイルは、本発明の組成物及び方法を利用して予測的に制御することができる。本発明のある局面では、生物活性剤の初期放出は、制御され、それによって、より多くの生物活性剤を、より長い放出期間、より後の時間に、なお利用させることができる。初期放出後の放出プロファイルの形状は、コーティングのコート層とコーティング中の生物活性剤(複数)との組成により、直線的、対数状、又はいくつかのより複雑な形状であるように制御することができる。ある実施態様では、更に放出速度を制御するために、生分解性組成物中に添加物を含めることができる。好ましい局面では、本発明の生分解性組成物は、治療的範囲内の生物活性剤濃度、理想的には相対的に一定の濃度を維持する。
驚くべきことに、本発明のある実施態様は、長期間に渡って、直線的に、生物活性剤を再現的に放出する用具及び方法を提供する。本明細書に記載のように、本発明の好ましい実施態様のin vitro溶出アッセイは、驚くべきことに、長期間の、生物活性剤の制御可能な放出を示す。好ましい実施態様では、(ポリマー比の点で)多様な製剤を有するコーティング組成物は、生物活性剤の実質的に直線的放出を提供することができる。本明細書で提供されるin vitroデータに基づいて、in vivo放出速度は、長期間に渡って、直線での再現可能な放出速度を提供するだろう。従って、本発明は、所望の治療期間及び投薬量を提供するように調整することができる、移植可能な部位への生物活性剤の制御された放出を供することができる。本発明は、移植可能部位への1以上の生物活性剤の局所的送達を提供することができるので、本発明はまた、好ましいことに、全身性治療中に必要とされ得る生物活性剤の毒性濃度を避ける。
生物活性剤が比較的低分子を含むときには、本発明の生分解性組成物は、特定の用途を見出すことができる。好ましい局面では、本発明のテーマは、低分子の制御された放出を、移植可能な用具表面上に提供された生分解性コーティングからの治療上有効な方式で達成させる方法を提供する。低分子は、典型的には、2つの経路、すなわち、ポリマー材料を介する拡散及びポリマー材料の分解、により生分解性ポリマー組成物から放出される。従って、かかる分子の放出を制御するのは、特に、用具の移植後の初期期間中に比較的速い「バースト」放出を抑制するか又は最小限に抑えたい場合には、特に困難である。本発明の生分解性組成物は、例えば、生分解性組成物からの生物活性剤の初期放出を調節することによって、かかる低分子の放出に改善した制御を提供することができる。典型的には、低分子の生物活性剤は、一般的に約1500未満の分子量を有する。
いくつかの例証的な生物活性剤は、抗-増殖剤 (例えば、アクチノマイシンD、パクリタキセル、タキサン等)、抗-炎症剤 (例えば、デキサメタゾン、プレドニソロン、トラニラスト等)、免疫抑制剤 (例えば、シクロスポリン、CD-34抗体、エベロリムス、マイコフェノール酸、シロリムス、タクロリムス等)を有するより低分子、より低分子の抗生物質などを含む。好適な生物活性剤を記載してきた、例えば、生物活性剤及び治療的化合物の包括的リストは、The Merck Index, 第13版, Merck & Co. (2001) に見出される。当業者は、本明細書の説明の案内を用いて、本発明のポリマーマトリックスから溶出するために好適な生物活性剤を容易に選択することができる。
使用においては、移植可能医療用具は、生分解性コーティング当業者と共に提供され、体内の治療部位に配置される。1つのかかる適用においては、ステントは、処置、例えば血管形成術の後に体内の管に配置される。ステントは所定の位置に留置され、生分解性コーティングが分解する。ステントの配置、及び生分解性コーティングの生理的体液への曝露の際に、生物活性剤がステントから放出される。典型的には、生物活性剤の初期放出が観察され、生物活性剤の徐放が長期間観察される。生分解性コーティングが分解すると、生物活性剤は、制御された方法で放出され続け、それにより、治療コースに渡って、生物活性剤の治療上有効量を治療部位に提供する。
これらの局面と他の局面、及び利点をより詳細に記載する。
本明細書に組み込まれている、及び本明細書の一部を構成する添付の図面は、本発明のいくつかの局面及び好ましい実施態様の説明を説明し、本発明の趣旨を説明するために役立つ。
発明の詳細な説明
以下に記載の本発明の実施態様は、本発明を、以下の詳細な説明に開示されたまさにその形態に網羅されている又は限定されることを意図してない。むしろ、実施態様は、他の当業者が本発明の趣旨及び実施を評価しそして理解できるように、選択されかつ記載される。
以下に記載の本発明の実施態様は、本発明を、以下の詳細な説明に開示されたまさにその形態に網羅されている又は限定されることを意図してない。むしろ、実施態様は、他の当業者が本発明の趣旨及び実施を評価しそして理解できるように、選択されかつ記載される。
本発明は、コーティング形態中に、生分解性材料を供えた、コーティング形態の医療用具に関する。用具の少なくとも1部分は、生分解性材料でコートされ、この部分は、移植後に体内で徐々に分解される。ある実施態様では、生分解性組成物は、生分解性であることに加えて生体吸収性であり得る。これらの実施態様によれば、生分解性組成物は、体内に吸収される。成分が体内に吸収されることは必要とはされない;ある実施態様では、生分解性組成物は、体内に完全に吸収されない多数の部分に分解される。
本発明は、患者の体内の治療部位、特に、血管部位、を効果的に治療する方法及び器具に関する。本発明の好ましい実施態様によれば、ステントの少なくとも1部分(例えば、コーティング)が分解した後の所望の期間、体内の部位に治療を提供することができるステントが提供される。本発明の方法及び器具は、制御された方法で治療部位に生物活性剤を送達するために利用することができる。本発明に従うかかる方法及び器具は、治療期間及び治療部位に送達される生物活性剤の種類においてフレキシビリティーを提供するために使用することができる。特に、本発明は、所望の治療コースにおいて体内の治療部位に1以上の生物活性剤を制御可能に提供するために開発された。
本明細書で用いる「制御された放出」は、(投薬速度及び総投薬量を含む)所望の投薬量及び治療期間で、患者の体内への化合物(例えば、生物活性剤)の放出を称する。
用語「移植部位」は、移植可能用具が本発明に従って位置される患者の体内の部位を称する。次に、「治療部位」は、移植部位、及び用具成分から直接的又は間接的に治療を受けることになる体内の部位を含む。例えば、生物活性剤は、移植部位から用具自体の周辺部位に移動することができ、それによって、単に移植部位よりもより広い部位を治療することができる。
生物活性剤は、長期間、本発明のコーティングから放出され、この関係は、放出プロファイル(放出された生物活性剤の累積的量対時間)を確立するためにプロットすることができる。典型的には、生物活性剤は、生物活性剤の初期放出、及び長期間の生物活性剤の放出を含むと考えることができ、これらの2つの違いは、通常、単に、時間量であり得る。初期放出は、用具が移植された直後に放出された生物活性剤の量であり、長期間の生物活性剤の放出は、より長期間(例えば、生分解性組成物の寿命)を含む。
場合によっては、初期放出は、「バースト」放出として特徴付けられる。生物活性剤の「バースト放出」を提供するコーティングに関して、大量の生物活性剤の初期放出は、移植可能用具が患者内に提供された後の比較的短い期間内に観察される。典型的なバースト放出は、比較的短い時間での、より高い放出(例えば、移植後の最初の24時間内にコーティングに含まれる生物活性剤の量の30%超)である。対照的に、コーティングは、生物活性剤の実質的な直線的放出を提供することができる。そこでは、生物活性剤の初期放出が放出プロファイル全体と比べて著しく異なった傾き又は形状を含まない。別の方法では、バースト放出は、長期間の生物活性剤の放出と比較して、放出された生物活性剤が大量である点で相違する、初期放出として特徴付けられる(すなわち、最初の期間中に著しい量が放出される)。
バースト放出の意義はまた、生物活性剤を含む特定のポリマー材料に関連して考慮され得る。例えば、4週間の重量半減分解時間(half-weight degradation time)を有する生分解性ポリマーに関しては、かなりのバースト放出は、最初の24時間の期間内に放出されるコーティング中に含まれる生物活性剤の約30%超であると考えられる。4週間超の重量半減分解時間を有する生分解性ポリマーに関しては、より長いバースト期間が、同一の量の生物活性剤について著しいと考えられる。例えば、ポリ(D,L-ラクチド) (PLA) の重量半減分解時間は、約155日である(ポリマーの分子量に依拠する)、これに対して、ポリ(D,L-ラクチド-グリコリドコポリマー) (PLGA)では30日である。従って、PLGAに比べてPLAからのバースト放出には、より長期間が治療上関連すると考えられる。
本発明のある局面に従って、生物活性剤放出曲線の形状は、コーティングの1以上の特徴、例えば、コーティングをつくるコート層の化学組成、コーティングを含むコート層の相対的位置、及び/又はコーティングを含む個々のポリマーの相対的量(例えば、個々のコート層のコート重量)を制御することにより調節することができる。本発明に従って、生物活性剤の放出の時間プロファイルは、(階段関数のように)薬物が直ちに溶出する速放から、薬物が数ケ月又は数年をかけて均一に放出される、極度に遅く、直線的(すなわち、ゼロ-オーダー)放出までを含む、任意の所望の形状を提供するように調節することができる。薬物及び治療されるべき症状によって、様々な放出プロファイルを達成することができる。ポリマーの多層コート層を有するコーティングをつくる目的は、階段関数と低-傾斜のゼロ-オーダー放出との間にある放出プロファイルの広い範囲が得られることである。好ましくは、生分解性組成物の各層の相対的位置は、所望の放出プロファイルを提供するように選択される。加えて、又は代替的に、第二ポリマーの組成物(及び含まれるならば、追加の層(複数))は、所望の放出プロファイルを提供するように選択される。本明細書に記載の放出プロファイルを制御することにより、生物活性剤による治療の効率に著しい改善がなされる。
生物活性剤の所望の放出プロファイルは、選択された特定の生物活性剤、移植部位に提供されることになる個々の生物活性剤の数、達成されるべき治療効果、体内のインプラントの持続期間のような因子、及び当業者に公知の他の因子に依拠し得る。
驚くべきことに、多層の生分解性コーティングの層組成物は、溶出速度プロファイルにおける顕著な相違を提供するように扱うことができる、ことを発見した。例えば、トップコート(用具表面から最も遠く、生物環境に接する層)中のポリエーテルエステルコポリマーの含有は、このようなトップコートを含まない類似のコート組成物と比べて、初期放出速度を増加させることができる、ことを発見した。場合によっては、PEGT/PBTのトップコートの含有は、PEGT/PBTのトップコートを含まないがその他の点では組成的に等価であるコート組成物に比べて、初期放出相を増加させることができる。他の局面では、様々なポリマー及びコポリマーが放出プロファイルに高い制御を提供するために多層形式で提供することができる、ことを発見した。
本明細書に記載の本発明の多層コーティングは、生物活性剤のコーティングからの初期バーストを制御するように(例えば、限定することにより、又は更に限定することより)設計される。バースト放出がより長期間に渡り、作用部位に放出された後に、コーティング中には生物活性剤が依然として残る。初期放出相の後の放出プロファイルの形状(放出された生物活性剤対時間の割合)は、コーティング中のポリマー層及び生物活性剤の組成により、直線的もしくは対数状又は更に複雑な形状に制御することができる。
本明細書で使用する、治療コースは、生物活性剤が患者に送達される期間である。治療コースの期間は、典型的には、治療される症状、患者の年齢及び症状、ステント移植を必要とする処置(例えば、血管形成術)に対する体の通常の反応時間等に基づいて、医師により決定される。典型的には、治療コースは、数時間から数日まで、数時間から数週間まで、又は数時間から更に数ケ月までの範囲であろう。例えば、ステントの移植の際の再狭窄の危険性を最小限に抑える典型的な治療コースは、約4週間以上である。
生物活性剤のin vivo放出は、生物活性剤のin vitro放出を観察することによって概算することができる。例えば、移植可能用具は、生物活性剤を含む生分解性コーティングを含むように構成することができる。次いで、コートされた移植可能用具は、一定期間、好適な溶液中に置くことができる(例えば、緩衝液、例えばリン酸緩衝生理食塩水又は酢酸ツィーン緩衝液)。用具のインキュベーション中、溶液は、溶液への、生物活性剤のin vitro放出速度を決定するために、定期的に監視することができる。ステントは、溶液から除き、定期的なサンプリング時間に新しいバイアル内の新鮮な緩衝液中に入れる。各サンプリングでの生物活性剤の濃度は、各生物活性剤の特徴的な波長を用いて、分光法により使用した緩衝液中で測定することができる。濃度は、モル吸収率を用いて、コーティングから放出された生物活性剤の量に変換することができる。放出された生物活性剤の累積的量は、各々除いた後に各試料量を添加することにより計算することができる。放出プロファイルは、放出された生物活性剤の累積的量を時間関数としてプロットすることにより得られる。この測定されたin vitro放出速度から、in vivo放出速度は、公知の技術を用いて概算することができる。
本発明によれば、移植可能用具は、第一ポリマー層及び第二ポリマー層を含む多層からなる生分解性組成物を含む。生分解性組成物は、治療部位の治療のための生物活性剤を更に含む。生物活性剤は、1以上のコート層に含まれ得る。好ましい局面では、本発明は、治療部位に生物活性剤の制御された放出を提供する用具及び方法を提供する。
ある局面では、本発明の生分解性組成物は、生物活性剤の実質的な量が1度に生物的に利用できる、(生物活性剤の初期バースト放出を含む)ボーラス型の投与とは対照的に、制御された放出特性を示すことができる。例えば、ある実施態様では、体を、血液、脊髄液、リンパ液等を含む体液と接触させる際に、(本明細書で提供するように製剤化される)生分解性組成物は、所望の量の生物活性剤の初期放出を可能にし、次いで、長期間の、持続的で予測可能な生物活性剤の送達を提供する。この放出は、任意の組み込まれた生物活性剤の治療上有効量の長期間送達をもたらすことができる。徐放は、本明細書により詳細に記載したある実施態様では変動するだろう。
語句「治療上有効量」は、当該分野で理解されている用語である。ある局面では、当該用語は、本発明の生分解性組成物に組み込まれるときに、任意の医療的処置に適用可能な合理的な利点/リスク比で所望の効果を生じる生物活性剤の量を称する。ある局面では、当該用語は、再狭窄の危険性をなくし又は減少させるために必要又は十分なその量を称する。治療上有効量は、治療される症状、投与される特定の生物活性剤(複数)、患者の体重、症状の重度等の因子によって、変動することができる。このましい局面では、治療上有効量は、任意の選択された期間に、特に、移植中の期間、及び用具を配置した直後(初期放出)の期間に、生分解性組成物から放出される生物活性剤の量を考慮する。従って、治療上有効量は、生分解性組成物からの生物活性剤の初期放出にも当てはまる。生分解性組成物からの初期放出を制御することによって、好ましい実施態様は、移植後の早い段階で、望ましくない高量の薬物放出を潜在的に減少させるか又はなくすことができる。当業者は、過度な実験をすることなく、特定の生物活性剤の有効量を経験的に決定することができる。
従って、本発明の好ましい局面は、治療的ウィンドウ内の生物活性剤濃度を長期間維持し、そして生物活性剤の効力を改善することができる持続的生物活性剤送達を提供する能力を含む、1以上の利点を提供することができる。局所送達は、薬物投薬量、毒性効果、及び治療薬の投薬量に典型的に関連する他の副作用を減少させることができる。
本発明によれば、使用中に(少なくとも一部)分解するコーティングを有する用具を提供することが望ましい体内の任意の移植部位を治療するために使用することができる用具を開発した。ある実施態様では、用具は、好ましくは、移植部位の開存性を元に戻し及び維持し、同時に移植部位の機能を可能にすることが望ましい体内の移植部位を治療するために使用される。例えば、血管適用では、用具は、用具で処置された血管部位の開存性を元に戻し及び維持することができ、そのため、治療部位を通る持続的血流を可能にする。本発明の用具は、1以上の生物活性剤の制御された放出を更に提供する。本発明のこの局面によれば、用具は、生物活性剤の、体内の治療部位への制御された放出を提供することができる。本明細書に記載のように、治療部位での制御された放出は、投薬速度及び総投薬量の双方においての制御を意味する。
本発明の考察を補助するために、血管部位を治療するための本発明の使用に取り組むだろう。本発明の特徴、特に制御可能な薬物送達可能性に関連する特徴は、明らかに提供することができるため、血管治療が選択される。更に、患者に対する危険性を減らすと同時に優れた品質を提供することができる、生物活性剤の制御された及び予測可能な送達を提供する能力は、当該分野で著しい進歩を遂げ得る。ステント内の血管部位の治療は重要である;しかしながら、他の用具、例えば血管フィルター(例えば、閉鎖フィルター)も、本発明の概念を利用することができる。
開示された用具及び方法は、任意の治療要求、例えば、眼科用用具、整形外科用適用、又は骨もしくは結合組織の損傷を修復するための骨セメント(例えば、骨スクリュー、及び、限定されないが、結合用具、例えば、ヒモ、テーザー等を含む、治療中に骨の相対的位置及び安定性を維持するために使用することができる他の固定力のある用具)、分解性もしくは非分解性織物又は紙素材、組織設計用のスカフォールド等に適用できる、ことが理解される。
ある実施態様では、生分解性組成物は、追加の層を、例えば、第一層及び第二層との間に、及び/又はコート用具の最外層(従って、組織-接触表面)に含むことができ、一方、他の実施態様では、生分解性組成物は、本明細書に詳細に記載の層からなる。
ある局面では、本発明の生分解性組成物は、第一生分解性ポリマー、第二生分解性ポリマー及び生物活性剤のブレンドからなるコーティングを提供するために利用される。第一生分解性ポリマーは、好ましくは、ポリエーテルエステルコポリマー、例えば、PEGT/PBT、である。好適な第一生分解性ポリマーである、エステル結合を含む他のポリマーは、リン-含有結合を有するテレフタレートエステル及び異なったエステル結合を有するセグメント化コポリマーを含む。更なる局面では、第一生分解性ポリマーは、ポリカーボネート-含有ランダムコポリマーを含むことができる。これらの局面をより詳細に記載する。
本明細書で用いる用語「脂肪族」は、直鎖、分枝、及び/又は環状のアルカン、アルケン又はアルキンを称する。リン酸エステル結合を含むポリマー材料中の好ましい脂肪族基は、1〜10の炭素原子を有する直鎖もしくは分枝のアルカン、又は1〜7の炭素原子を有する直鎖アルカンである。
本明細書で用いる用語「芳香族」は、4n+2 π電子を有する不飽和環状炭素原子-含有化合物を称する。
本明細書で用いる用語「ヘテロサイクリック」は、環中に炭素原子以外の1以上の原子、例えば窒素原子、酸素原子又はイオウ原子を有する、飽和又は不飽和環化合物を称する。
一般的に言えば、ポリエーテルエステルコポリマーは、親水性ブロック(例えば、ポリアルキレングリコール、例えばポリエチレングリコール)及び疎水性ブロック(例えば、ポリエチレンテレフタレート)を含む、両親媒性ブロックコポリマーである。
1つの実施態様では、ポリエーテルエステルコポリマーは、ポリアルキレングリコールである第一成分、及び2〜の8炭素原子を有するアルキレングリコールとジカルボン酸との反応混合物として形成される、ポリエステルである第二成分を含む。ポリアルキレングリコールは、1つの実施態様では、ポリエチレングリコール、ポリプロピレングリコール、及びポリブチレングリコールからなる群より選ばれる。1つの実施態様では、ポリアルキレングリコールは、ポリエチレングリコールである。
別の実施態様では、ポリエステルは、ポリエチレンテレフタレート、ポリプロピレンテレフタレート、及びポリブチレンテレフタレートからなる群より選ばれる。好ましい実施態様では、ポリエステルは、ポリブチレンテレフタレートである。
1つの好ましい実施態様では、コポリマーは、ポリエチレングリコール/ポリブチレンテレフタレートブロックコポリマー(本明細書では、交換的にPEGTVPBT又はPEG/PBTコポリマーと称される)である。
別の実施態様では、ポリエステルは、以下の繰り返し記載する構造式I:
[式中、nは2〜8であり;そして、R1、R2、R3及びR4の各々は、水素、ハロゲン(例えば、塩素、ヨウ素、臭素)、ニトロ-又はアルコキシであり、R1、R2、R3及びR4の各々は、同一又は異なる。]
を有する。好ましくは、R1、R2、R3及びR4の各々は、水素である。代替的に、ポリエステルは、下記構造式II:
を有する。好ましくは、R1、R2、R3及びR4の各々は、水素である。代替的に、ポリエステルは、下記構造式II:
[式中、Xは、−O−、−SO2−又は−CH2−である。]
を有する二核芳香族二価酸から得られる。
を有する二核芳香族二価酸から得られる。
好ましい実施態様では、コポリマーは、多数の第一成分の繰り返し単位及び第二成分の単位を含む、セグメント化された熱可塑性生分解性ポリマーである。第一成分は、式III:
[式中、Oは酸素であり;Cは炭素であり;Lは、ポリ(オキシアルキレン)グリコールからの末端水酸基の除去後に残る、二価の有機ラジカルであり;そして、Rは、ジカルボン酸からカルボキル基の除去後に残る、置換又は非置換の二価ラジカルである。]
の単位の(コポリマーの重量基準で)約30重量パーセント〜約99重量パーセントを含む。
の単位の(コポリマーの重量基準で)約30重量パーセント〜約99重量パーセントを含む。
第二成分は、(コポリマーの重量基準で)約1重量パーセント〜約7重量パーセントの量で存在し、式IV:
[式中、Eは、2〜8の炭素原子を有する置換又は非置換アルキレンラジカル、及び置換又は非置換エーテル部分からなる群より選ばれる有機ラジカルである。]
の単位からなる。Rは式IIIに記載したとおりである。
の単位からなる。Rは式IIIに記載したとおりである。
ポリ(オキシアルキレン)グリコールは、1つの実施態様では、ポリ (オキシエチレン)グリコール、ポリ(オキシプロピレン) グリコール、ポリ (オキシブチレン) グリコール、及びそれらの組み合わせからなる群より選ばれる。好ましくは、ポリ(オキシアルキレン)グリコールは、ポリ(オキシエチレン)グリコールである。
ポリ(オキシエチレン)グリコールは、約200〜約20,000、又は約200〜約10,000の範囲の分子量を有することができる。ポリ(オキシエチレン)グリコールの正確な分子量は、生分解性粗生物に組み込まれる生物活性剤の種類を含む、様々な因子による。
1つの実施態様において、Eは、2〜8の炭素原子を有する、好ましくは、2〜4の炭素原子を有する置換又は非置換のアルキレンラジカルからなる群より選ばれる。好ましくは、第二成分は、ポリエチレンテレフタレート、ポリプロピレンテレフタレート及びポリブチレンテレフタレートからなる群より選ばれる。1つの実施態様において、第二成分は、ポリブチレンテレフタレートである。
好ましい実施態様では、コポリマーは、ポリエチレングリコール/ポリブチレンテレフタレートコポリマーである。
1つの実施態様において、ポリエチレングリコール/ポリブチレンテレフタレートコポリマーは、ジメチルテレフタレート、ブタンジオール(過剰)、ポリエチレングリコール、抗酸化剤及び触媒の混合物から合成することができる。混合物を、反応容器に入れ、約180℃まで加熱し、エステル交換が起こるようにメタノールを蒸留する。エステル交換中に、メチルとのエステル結合は、ブチレン及び/又はポリエチレングリコールとのエステル結合と交換する。エステル交換後に、温度を約245℃までゆっくりと昇温し、真空(最終的には、0.1 mbar未満)を得る。過剰のブタンジオールを蒸留し、ブタンジオールテレフタレートのプレポリマーをポリエチレングリコールと縮合して、ポリエチレングリコール/ポリブチレンテレフタレートコポリマーを形成する。テレフタレート部分をポリエチレングリコール単位と結合して、コポリマーのポリブチレンテレフタレート単位を形成し、このコポリマーは、本明細書では、ポリエチレングリコールテレフタレート/ポリブチレンテレフタレートコポリマー(PEGT/PBT又はPEG/PBTコポリマーとも称される)と称することがある。代替的には、ポリエチレングリコールは、PEGT/PBTコポリマーと混合される遊離のポリエチレングリコールとして存在する。更に代替的には、ポリアルキレングリコール/ポリエステルコポリマーは、米国特許第3,908,201号明細書に記載のようにして調製することができる。
好ましいコポリマーの上記の考察は、本発明を、考察した特定のコポリマー又はその任意の特定の手段に限定するものではない。
生分解性組成物は、所望の分解性速度を提供するように製剤化することができる。生分解性組成物の分解は、エステル結合の加水分解及び/又はエーテル基の酸化により起こる。更に、生分解性組成物は、生物活性剤を含むとき、生分解性組成物の製剤化は、生物活性剤のポリマーからの拡散速度を制御するように調整することができる。
ある実施態様では、PEGT/PBTコポリマーの分解は、2つの一般的方法で制御することができる。例えば、分解速度は、ポリマー材料中に疎水性抗酸化剤を含むことにより増加させることができる。加えて又は代替的に、分解速度は、芳香族基を脂肪族基で部分的に置換することにより増加させることができる。例えば、より疎水性の芳香族基、例えば、テレフタレート基は、より疎水性の脂肪族基、例えば、二価酸基(例えば、コハク酸)と置換することができる。別の実施例では、より疎水性のブチレン基は、より疎水性基、例えばジオキシエチレンと少なくとも部分的に置換することができる。置換度は、分解速度に選択された効果を与えるように決定することができる。
本発明に従って、ポリエーテルエステルコポリマーの増加した分解は、酸形成における顕著な悪影響の増加を伴わない。コポリマーの分解は、ある量の酸を生じ得る、エステル結合の分解及びエーテル基の酸化により起こる。しかしながら、分解中に生じる酸のレベルは、1つの局面では、他の公知の分解性ポリマー(例えば、PLA)により生じるレベルよりも低く、別の局面では、組織及び/又は生物活性剤への悪影響がない。分解環境の酸性度は、当該環境における生物活性剤の安定性に影響を与えることができる。場合により、親水性抗酸化剤は、ポリマー材料中に含むことができる。かかる親水性抗酸化剤を、本明細書の至るところでより詳細に説明し、生分解性組成物がペプチド又はタンパク質分子を含むときには、かかる親水性抗酸化剤は特に好ましい。本発明のこの局面によれば、タンパク質又はペプチド分子がその分解の際に生分解性組成物から放出されるときには、タンパク質は、酸分解生成物により変性されない。分解がポリマー環境の酸性度を増加させる場合には、このことは、PLA又はPLGAを含む分解性ポリマーを超える顕著な利点を提供することができる。本発明のこれら局面を、生物活性剤が生分解性組成物から放出される、本発明の実施態様に関してより詳細に記載する。
本発明のある実施態様では、ポリマー材料は、リン原子-含有結合を含む生分解性テレフタレートコポリマーを含む。リン酸エステル結合を有するポリマー、いわゆるポリ(リン酸エステル)、ポリ(ホスホン酸エステル)及びポリ(亜リン酸エステル)は、公知である。例えば、Penczek et al., Handbook of Polymer Synthesis, Chapter 17: "Phosphorus-Containing Polymers," 1077-1132 (Hans R. Kricheldorf ed., 1992)、及び米国特許第6,153,212号明細書、同6,485,737号明細書、同6,322,797号明細書、同6,600,010号明細書、同6,419,709号明細書を参照。これらの3種の化合物の各々の構造は、以下のとおりである。各々は、リン原子に結合した、異なった側鎖を有する。
これらのポリマーの汎用性は、反応の多様性が知られている、リン原子の汎用性に関連する。その結合は、3p軌道又は様々な3s-3p混成を含むことができ; spd混成もまた、利用できるd軌道のため、可能である。従って、ポリ(リン酸エステル)の物理化学的性質は、R又はR’基のいずれかを変化させることにより容易に変えることができる。これらの実施態様に従うポリマー材料の生分解性は、ポリマー骨格中の生理的に不安定なリン酸エステル結合に関連する。骨格又は側鎖を操作することにより、様々な生分解速度が得られる。
ポリ(リン酸エステル)の追加の特徴は、機能性側鎖の有用性である。リン原子は五価であるので、生物活性剤(例えば、薬物)は、ポリマーに化学的に結合することができる。例えば、カルボキシ基を有する生物活性剤は、加水分解性可能である、エステル結合を介してリン原子に結合することができる。骨格中のP-O-C基も、ポリマーのガラス転移温度(Tg)を下げ、重要なことには、通常の有機溶媒中での溶解性を与える。これは、ポリマーの特徴及び加工に望ましい。
1つの実施態様では、テレフタレートポリエステルは、亜リン酸エステルであるリン酸エステル結合を含む。例えば、米国特許第6,419,709号明細書 (Mao et al., ”Biodegradable Terephthalate Polyester-Poly(Phosphite) Compositions, Articles, and Methods of Using the Same”)には、好適なテレフタレートポリエステル-ポリ亜リン酸エステルコポリマーが記載されている。この実施態様によれば、ポリマー材料は、下記式V:
[式中、Rは二価の有機部分である。]
の繰り返しモノマー単位を含む。Rは、重合化、共重合化、又はコポリマーの生分解性反応を妨害しない限り、任意の二価の有機部分でよい。特に、Rは、脂肪族基、例えば、アルケン、例えばエチレン、1,2-ジメチルエチレン、n-プロピレン、イソプロピレン、2-メチルプロピレン、2,2-ジメチルプロピレン又はtert-ブチレン、tert-ペンチレン、n-ヘキシレン、n-ヘプチレン等; アルケニレン、例え、エテニレン、プロペニレン、ドデセニレン等;アルキニレン、例えば、プロピニレン、ヘキシニレン、オクタデシニレン等;非-妨害置換基で置換された脂肪族基、例えば、ヒドロキシ-、ハロゲン-又は窒素-置換脂肪族基;又は、環状脂肪族基、例えば、シクロペンチレン、2-メチルシクロペンチレン、シクロヘキシレン等でよい。
の繰り返しモノマー単位を含む。Rは、重合化、共重合化、又はコポリマーの生分解性反応を妨害しない限り、任意の二価の有機部分でよい。特に、Rは、脂肪族基、例えば、アルケン、例えばエチレン、1,2-ジメチルエチレン、n-プロピレン、イソプロピレン、2-メチルプロピレン、2,2-ジメチルプロピレン又はtert-ブチレン、tert-ペンチレン、n-ヘキシレン、n-ヘプチレン等; アルケニレン、例え、エテニレン、プロペニレン、ドデセニレン等;アルキニレン、例えば、プロピニレン、ヘキシニレン、オクタデシニレン等;非-妨害置換基で置換された脂肪族基、例えば、ヒドロキシ-、ハロゲン-又は窒素-置換脂肪族基;又は、環状脂肪族基、例えば、シクロペンチレン、2-メチルシクロペンチレン、シクロヘキシレン等でよい。
Rはまた、二価の芳香族基、例えば、フェニレン、ベンジレン、ナフタレン、フェナンスレニレン等、又は非-妨害置換基で置換された二価の芳香族基でよい。更に、Rはまた、二価のへテロサイクリック基、例えば、ピロリレン、フラニレン、チオフェニレン、アルキレン-ピロリレン-アルキレン、ピリジレン、ピリジニレン、ピリミジニレン等でよく;又は、非-妨害置換基で置換されたこれらの任意でよい。
しかしながら、好ましくは、Rは、アルキレン基、環状脂肪族基、フェニレン基、又式はVI:
[式中、Yは、酸素、置換窒素又はイオウであり;mは1〜3である。]
の二価の基である。ある好ましい実施態様では、Rは、1〜7の炭素原子を有するアルキレン基であり、好ましくは、Rはエチレン基である。
の二価の基である。ある好ましい実施態様では、Rは、1〜7の炭素原子を有するアルキレン基であり、好ましくは、Rはエチレン基である。
xの値は、ポリマーの所望の溶解性、所望のTg、ポリマーの所望の安定性、最終ポリマーの所望の剛性、及び生分解性及びポリマーの所望の放出特徴により、変動し得る。一般的に、xは1以上であり、典型的には、xは1〜40の間で変動する。ある好ましい実施態様では、xは1〜30の範囲、好ましくは、1〜20の範囲、又は2〜20の範囲にある。
nの数は、生分解性及びポリマーの所望の放出特徴により大幅に変動し得るが、典型的には、約3〜約7,500、好ましくは5〜5,000で変動する。ある好ましい実施態様では、nは、約5〜約300の範囲にあり、又は約5〜約200の範囲にある。
xの値を制御する最も一般的な方法は、モノマーに対する「x」部分のフィード率を変化させることである。例えば、モノマーVII:
を製造する場合には、ジアルキル亜リン酸エステル「x」反応物の様々なフィード率は、ジオール反応物を用いて使用することができる。反応物のフィード率は、容易に、99:1〜1:99、例えば 95:5、90:10、85:15、80:20、75:25、70:30、65:35、60:40、55:45、50:50、45:55、20:80、15:85等で変化し得る。好ましくは、ジアルキル亜リン酸エステル反応物とジオール反応物とのフィード率は、約90:10〜約50:50、又は約85:15〜約50:50、又は約80:20〜約50:50で変化する。
ポリ(亜リン酸エステル)の製造における最も一般的な反応は、次式に従う、ジオールと、ジアルキル又はジアリール亜リン酸エステルとの縮合である。
ポリ(亜リン酸エステル)は、次式に従って、縮合剤として、リン酸のテトラアルキルジアミドを用いることにより得ることもできる。
上記の重合反応は、バルク又は溶液重合のいずれかでよい。バルク重縮合の利点は、溶媒及び過剰の他の添加剤の使用を避けることであり、そのため、精製をより簡単にすることができる。それは、かなりの高分子量のポリマーを提供することもできる。
溶液重縮合用の典型的な溶媒は、ハロゲン系有機溶媒、例えば、クロロホルム、ジクロロメタン又はジクロロエタンを含む。溶液重合は、好ましくは、反応物の等モル量及び酸受容体、通常、四級アミン、例えば、ピリジン又はトリエチルアミン、の化学量論量の存在下に行う。次いで、生成物を、典型的には、非溶媒による沈殿によって溶液から単離し、当業者に公知の慣用的技術、例えば、水性酸性溶液、例えば希塩酸、による洗浄、により塩酸塩を除くために精製する。
高分子量ポリアーが高反応率で望まれる場合に、界面重縮合は用いられる。温和な条件は、副反応を最小限に抑える。また、溶液法に固有のジオールと亜リン酸エステルとの化学量論的当量に対する高分子量の依拠は、除かれる。しかしながら、酸クロリドの加水分解は、アルカリ水性相で起こることがある。相間移動触媒、例えば、クランエーテル又は四級アンモニウムクロリドは、界面にイオン化ジオールを移動させて、重縮合反応を促進するために使用することができる。界面重縮合後の得られたポリマーの収率及び分子量は、反応時間、モノマーのモル比、非混和性溶媒の体積比、酸受容体の種類、及び相間移動触媒の種類と濃度により、影響を受け得る。
好ましい実施態様では、下記式Vの生分解性テレフタレートポリマーの製造法であって、下記式VIII:
[式中、Rは、式VIで定義したとおりである。]
を有するジオール化合物のpモルを、式IX:
を有するジオール化合物のpモルを、式IX:
[式中、p>qである。]
のqモルのジアルキル又はジアリールと重合して、式X:
のqモルのジアルキル又はジアリールと重合して、式X:
[式中、R及びxは、ポリマーV及びVIIIで定義したとりである。]
で表されるqモルのホモポリマーを生成するステップを含む。そのように生成したホモポリマーは、単離、精製し、及びそのようなものとして使用することができる。代替的には、単離又は非単離されたホモポリマーは、以下のステップ:(a) 上記のように重合し;そして、(b) 式Xのホモポリマーと、(p-q) モルの式XI:
で表されるqモルのホモポリマーを生成するステップを含む。そのように生成したホモポリマーは、単離、精製し、及びそのようなものとして使用することができる。代替的には、単離又は非単離されたホモポリマーは、以下のステップ:(a) 上記のように重合し;そして、(b) 式Xのホモポリマーと、(p-q) モルの式XI:
を有するテレフタロイルクロリドとを更に反応させて、式Vのコポリマーを形成させることにより、本発明のブロックコポリマー組成物を製造するために、使用することができる。
重合ステップ (a) は、使用される溶媒、所望の溶解性、所望の分子量、及び反応物の、副反応の生じ易さにより、様々な温度で起こり得る。しかしながら、好ましくは、重合ステップ (a) は、約-40℃〜約160℃の範囲の温度で起こり;溶液重合では、約0℃〜約65℃の範囲の温度で起こり;バルク重合では、約150℃の温度で起こる。
重合ステップ(a)に必要な時間も、使用される重合の種類及び所望の分子量により、幅広く変化し得る。しかしながら、好ましくは、重合ステップ(a)は、約30分〜約24時間内に起こる。
重合ステップ(a)が、バルク、溶液、界面重縮合、又は任意の他の簡便な重合法でよいが、好ましくは、重合ステップ(a)は、溶液重合反応である。特に、溶液重合反応が使用される場合には、酸受容体は、重合ステップ(a)の間、有利に存在する。特に好適な酸受容体の種類は、四級アミン、例えばピリジン、トリメチルアミン、トリエチルアミン、置換アニリン及び置換アミノピリジンを含む。最も好ましい酸受容体は、置換アミノピリジン 4-ジメチル-アミノピリジン(「DMAP」)である。
ステップ(b)の共重合の目的は、(i) 重合ステップ (a) の結果として、製造されるリン酸化ホモポリマー鎖、及び (ii) 相互に結合しているポリエステル単位を含む、ブロックコポリマーを形成することである。結果は、特に制御された放出生分解性組成物として使用するために好適な微結晶性構造を有するブックコポリマーである。
本発明の共重合ステップ (b) は、通常、重合ステップ (a) の温度よりも少し高い温度で起こるが、使用される共重合反応の種類、1以上の触媒の存在、所望の分子量、所望の溶解性、及び反応物の、望ましくない副反応の生じ易さにより、広く変動もし得る。しかしながら、共重合ステップ (b) が溶液重合反応として実行されるときには、典型的には、約-40℃〜約100℃の範囲の温度で起こる。典型的な溶媒は、メチレンクロリド、クロロホルム、又は任意の様々な不活性の有機溶媒を含む。
重合ステップ (b) に必要な時間も、所望の原料の分子量、及び一般的には、所望の完了度に反応を進行させるための多少の厳密な条件を使用する必要性により、幅広く変化し得る。しかしながら、典型的には、共重合ステップ (b) は、約30分〜約24時間内に起こる。
ホモポリマー又はブロックポリマーのいずれかの、製造されるテレフタレート-ポリ(亜リン酸エステル)ポリマーは、慣用的技術、例えば沈殿、非混和性溶媒での抽出、蒸発、濾過、結晶化等により、反応混合物から単離される。しかしながら、典型的には、式Vのポリマーは、非-溶媒又は部分的溶媒、例えばジエチルエーテル又は石油エーテルを用いて、当該ポリマーの溶液をクエンチすることにより、単離されかつ精製される。
別の実施態様では、テレフタレートポリエステルは、ホスホン酸エステルであるリン酸エステル結合を含む。好適なテレフタレートポリエステル-ポリ(リン酸エステル)コポリマーが、例えば、米国特許第6,485,737号明細書及び同第6,153,212号明細書 (Mao et al., ”Biodegradable Terephthalate Polyester-Poly(Phosphonate) Compositions, Articles and Methods of Using the Same”)に記載されている。この実施態様によれば、ポリマー材料は、式XII:
[式中、Rは、式Vのテレフタレートポリ(亜リン酸エステル)について上で定義した二価の有機部分であり;そして、この実施態様のポリマー材料中のR'は、脂肪族、芳香族、又はヘテロサイクリック残基である。]
で表される繰り返しモノマー単位を含む。R'が脂肪族であるとき、それは、好ましくは、アルキル、例えば、メチル、エチル、n-プロピル、イソプロピル、n-ブチル、tert-ブチル、−C8H17等であり;又は、非-妨害置換基、例えば、ハロゲン、アルコキシ又はニトロで置換されたアルキルである。
で表される繰り返しモノマー単位を含む。R'が脂肪族であるとき、それは、好ましくは、アルキル、例えば、メチル、エチル、n-プロピル、イソプロピル、n-ブチル、tert-ブチル、−C8H17等であり;又は、非-妨害置換基、例えば、ハロゲン、アルコキシ又はニトロで置換されたアルキルである。
R'が芳香族であるときには、それは、典型的には、約5〜約14の炭素原子、又は約5〜約12の炭素原子を含む。場合により、互いに縮合する1以上の環を含むことができる。特に好適な芳香族基の例は、フェニル、ナフチル、アンスラセニル、フェナンスラニル等を含む。
R'がヘテロサイクリックであるときには、それは、典型的には、約5〜約14の環原子、好ましくは約5〜12の環原子及び1以上のヘテロ原子を含む。1つの好ましい実施態様では、R'は、アルキル基又はフェニル基であり、より好ましくは1〜7の炭素原子を有するアルキル基である、好ましくは、R'はエチル基である。
xの値は、亜リン酸エステル結合を含むポリマー材料について上記のように変化し得る。同様に、xの値を制御する1つの方法は、モノマーに対して、「x」部分のフィード率を変化させることである。この特定の実施態様において、エチルホスホン酸クロリド「x」反応物(「EP」)のフィード率は、式XIII:
のポリマーを製造するために、テレフタロイルクロリド反応物(「TC」)を用いて使用することができる。
ポリ(ホスホン酸エステル)の製造における最も一般的な反応は、次式に従う、ホスホン酸ジクロリド及びジオールとの間の脱ヒドロハロゲン化反応である。
バルク重縮合、溶液重縮合、又は界面重縮合は、ポリマーを合成するために使用することができる。フリーデル-クラフツ反応も、ポリ(ホスホン酸エステル)を合成するために使用することができる。重合は、典型的には、ビス(クロロメチル)化合物を芳香族炭化水素と反応させる、又はクロロメチル化ジフェニルエーテルをトリアリールホスホン酸エステルと反応させるかのいずれかにより、行うことができる。ポリ(ホスホン酸エステル)も、通常、窒素又は他の不活性ガス下で、ジイミダゾリドリン及び芳香族ジオール、例えば、レゾルシノール及びキノリン、との間のバルク縮合により得られる。
1つの好ましい実施態様では、式XIIIの生分解性テレフタレートポリマーの製造法は、上記式VIIIを有するジオール化合物のpモルを、式XIV:
[式中、R'は、上記定義のとおりであり、p>qである。]
のホスホン酸ジクロリドのqモルと重合させて、式XV:
のホスホン酸ジクロリドのqモルと重合させて、式XV:
[式中、R、R'及びxは、前記定義のとおりである。]
のホモポリマーのqモルを生成するステップを含む。このように形成されたホモポリマーは、単離し、生成し及びそのようなものとして使用することができる。代替的には、単離又は非単離のホモポリマーは、以下のステップ:(a) 上記のように重合し;そして、(b) 式XVのホモポリマーと、式VIIIの過剰のジオールとを、式XVI:
のホモポリマーのqモルを生成するステップを含む。このように形成されたホモポリマーは、単離し、生成し及びそのようなものとして使用することができる。代替的には、単離又は非単離のホモポリマーは、以下のステップ:(a) 上記のように重合し;そして、(b) 式XVのホモポリマーと、式VIIIの過剰のジオールとを、式XVI:
を有するテレフタロイルクロリドの(p-q)モルと更に反応させて、式XIIのコポリマーを形成させることにより、本発明のブロックコポリマー組成物を製造するために、使用することができる。
ステップ (a) の重合反応の機能は、ジエステル出発物質をリン酸化し、次いで、それを重合してホモポリマーを形成することである。亜リン酸エステル結合を含むポリマー材料について上記したように、重合ステップ (a) は、様々な温度及び時間で起こり得る。
重合ステップ (a) の追加の手順は、式VIIIのジオールの相対的反応性、式XIVのホスホン酸ジクロリド、及び式XVのホモポリマー;これらの反応物の純度;重合反応が行われる温度;重合反応に使用される攪拌度等により顕著に変動し得る。しかしながら、好ましくは、式VIIIのジオールは、溶媒及び酸受容体と混合され、ホスホン酸クロリドは、ゆっくりと添加される、例えば、ホスホン酸クロリドの溶媒溶液は、ジオール、溶媒及び酸受容体の冷却された反応混合物に一滴ずつ垂らすか又は一滴ずつ添加することができ、重合反応の速度を制御することができる。
ステップ (b) の共重合の目的及び条件は、亜リン酸エステル結合を含むポリマー材料について上記したとおりである。
式XIIのポリマーは、ホモポリマーであるか又はブロックポリマーであるかにかかわらず、慣用的な方法、例えば、沈殿、非混和性溶媒での抽出、蒸発、濾過、結晶化等、により反応混合物から単離される。しかしながら、典型的には、式XIIのポリマーは、非-溶媒又は部分的溶媒、例えば、ジエチルエーテル又は石油エーテルで、ポリマー溶液をクエンチすることにより単離及び精製される。
式XIIのポリマーは、通常、ホスホエステル結合又は生分解中のポリマーの加水分解の機能として少なくとも一部分が制御される、in vivoでの生物活性剤の放出速度により特徴付けられる。
更に、側鎖の構造は、ポリマーの放出挙動に影響を与えることができる。例えば、より脂肪親和性、より疎水性又は嵩高い基への、リン原子を含む側鎖の変換は、分解過程を遅くするだろう。従って、例えば、放出は、通常、嵩高い芳香族側鎖を有するコポリマー組成物からよりも、低分子の脂肪族基の側鎖を有するコポリマー組成物からの方がより速い。
別の実施態様では、テレフタレートポリエステルは、リン酸エステルであるホスホエステル結合を含む。好適なテレフタレートポリエステル-ポリ(リン酸エステル)コポリマーは、例えば、米国特許第6,322,797号明細書及び同6,600,010号明細書 (Mao et al., ”Biodegradable Terephthalate Polyester-Poly(Phosphate) Polymers, Compositions, Articles, and Methods for Making and Using the Same”)に記載されている。この実施態様によれば、ポリマー材料は、式XVII:
[式中、Rは、式Vのテレフタレートポリ(亜リン酸エステル)及び式VIIのテレフタレートポリ(ホスホン酸エステル)について上記した二価の有機部分である。]
で示される繰り返しモノマー単位を含む。好ましくは、Rは、アルキレン基、環状脂肪族基、フェニレン基又は式XVIII:
で示される繰り返しモノマー単位を含む。好ましくは、Rは、アルキレン基、環状脂肪族基、フェニレン基又は式XVIII:
[式中、Xは、酸素原子、置換窒素原子、又はイオウ原子であり;そして、nは1〜3である。]
の二価基である。好ましくは、Rは1〜7の炭素原子を有するアルキレン基であり、好ましくは、Rはエチレン基、2-メチル-プロピレン基、又は2,2'-ジメチルプロピレン基である。R'は、式Vのテレフタレートポリ(亜リン酸エステル)及び式XIIのテレフタレートポリ(ホスホン酸エステル)について上記したとおりである。但し、R'はまた、ペンダント生物活性剤送達システムを形成するために、生物的に活性な物質に結合したアルキルを含む。値xは1以上であり、式Vのテレフタレートポリ(亜リン酸エステル)及び式XIIのテレフタレートポリ(ホスホン酸エステル)について記載したように変動し得る。同様に、xの値を制御する1つの方法は、他のモノマーに対する「x」部分のフィード率を変化させることである(例えば、テレフタロイルクロリド反応物(「TC」)に対する、エチルホスホロジクロリデート「x」反応物(「EOP」)のフィード率を変化させる)。上記の式Vのテレフタレートポリ(亜リン酸エステル)及び式XIIのテレフタレートポリ(ホスホン酸エステル)のnの値は、1〜5,000である。
の二価基である。好ましくは、Rは1〜7の炭素原子を有するアルキレン基であり、好ましくは、Rはエチレン基、2-メチル-プロピレン基、又は2,2'-ジメチルプロピレン基である。R'は、式Vのテレフタレートポリ(亜リン酸エステル)及び式XIIのテレフタレートポリ(ホスホン酸エステル)について上記したとおりである。但し、R'はまた、ペンダント生物活性剤送達システムを形成するために、生物的に活性な物質に結合したアルキルを含む。値xは1以上であり、式Vのテレフタレートポリ(亜リン酸エステル)及び式XIIのテレフタレートポリ(ホスホン酸エステル)について記載したように変動し得る。同様に、xの値を制御する1つの方法は、他のモノマーに対する「x」部分のフィード率を変化させることである(例えば、テレフタロイルクロリド反応物(「TC」)に対する、エチルホスホロジクロリデート「x」反応物(「EOP」)のフィード率を変化させる)。上記の式Vのテレフタレートポリ(亜リン酸エステル)及び式XIIのテレフタレートポリ(ホスホン酸エステル)のnの値は、1〜5,000である。
ポリ(リン酸エステル)を調製する際の最も一般的な反応は、次式に従う、ホスホジクロリネートとジオールとの脱ヒドロクロル化反応である。
フリーデル・クラフツ反応も、ポリ(リン酸エステル)を合成するために使用することができる。ポリ(ホスホン酸エステル)について述べた原則は、ポリ(リン酸エステル)の合成にも利用することができる。ポリ(リン酸エステル)は、本明細書に記載したように、バルク重縮合、溶液重縮合及び界面重縮合により合成することができる。
好ましい実施態様では、式XVIIの生分解性テレフタレートホモポリマーの製造法は、式XIX:
[式中、Rは、前記定義のとおりである。]
を有するジオールのpモルを、式XX:
を有するジオールのpモルを、式XX:
[式中、R'は、前記定義のとおりであり、p>qである。]
のホスホロジクロリデートのqモルと重合させて、下記式XXI:
のホスホロジクロリデートのqモルと重合させて、下記式XXI:
[式中、R、R'及びxは、前記定義のとおりである。]
で示されるホモポリマーのqモルを得るステップを含む。このように形成されたホモポリマーは、単離、精製し、そのようなものとして使用することができる。代替的には、ホモポリマーは、単離されても又はされなくても、以下のステップ:(a) 上記のように重合し;そして、(b) 式XXIのホモポリマー及び式XIXの過剰のジオールと、(p-q) モルの式XVIを有するテレフタロイルクロリドとを更に反応させて、式XVIIのコポリマーを形成させることにより、本発明のブロックコポリマー組成物を製造するために、使用することができる。
で示されるホモポリマーのqモルを得るステップを含む。このように形成されたホモポリマーは、単離、精製し、そのようなものとして使用することができる。代替的には、ホモポリマーは、単離されても又はされなくても、以下のステップ:(a) 上記のように重合し;そして、(b) 式XXIのホモポリマー及び式XIXの過剰のジオールと、(p-q) モルの式XVIを有するテレフタロイルクロリドとを更に反応させて、式XVIIのコポリマーを形成させることにより、本発明のブロックコポリマー組成物を製造するために、使用することができる。
ステップ (a) 及び (b) の重合の機能、並びにそのための条件は、ポリ(ホスホン酸エステル)について上記したとおりである。共重合ステップ (b) の追加の手順は、式XXIのホモポリマー及び式XVIのテレフタロイルクロリドの相対的反応性;これらの反応物の純度;共重合反応が行われる温度;共重合反応に使用される攪拌度等により、顕著に変動し得る。しかしながら、好ましくは、式XVIのテレフタロイルクロリドは、反応混合物に、その反対の場合よりも、ゆっくりと添加される。例えば、テレフタロイルクロリドの溶媒溶液は、冷却又は室温の反応に一滴ずつ垂らすか又は一滴ずつ添加して、共重合反応の速度を制御することができる。
リン原子-含有結合 (ポリ(リン酸エステル)、ポリ(ホスホン酸エステル)及びポリ(亜リン酸エステル))を含む生分解性テレフタレートコポリマーを含むポリマー材料は、追加の生体適合性モノマー単位がポリマー材料の生分解性を妨害しない限り、かかるモノマー単位を含むことができる。かかる追加のモノマー単位は、ある実施態様では、標的とする生物活性剤送達に好ましい正確な放出プロファイル、又は生分解性の正確な速度を設計する点でより大きなフレキシビリティーを提供することができる。かかる追加の生体適合性モノマーの例は、限定されないが、ポリカーボネート、ポリオルトエステル、ポリアミド、ポリ(イミノカーボネート)及びポリ無水物に見られる繰り返し単位を含む。
これらの実施態様のポリマー材料は、好ましくは、製造及び処理の各々のための、1以上の一般的な有機溶媒に溶解性である。一般的な有機溶媒は、クロロホルム、ジクロロメタン、アセトン、酢酸エチル、DMAC、N-メチルピロリジン、ジメチルホルムアミド及びジメチルスルホキシドを含むことができる。ポリマー材料は、好ましくは、これらの溶媒の少なくとも1つに溶解性である。
これらの実施態様に従うポリマー材料のTgは、ポリマーを調製するために使用されるジオールの分枝、ポリマーを製造するために使用されるリン原子-含有モノマーの相対比などによって様々に変動し得る。しかしながら、好ましくは、Tgは、約-10℃〜約100℃の範囲、又は約0℃〜約50℃の範囲内である。
ポリ(リン酸エステル)及びポリ(ホスホン酸エステル)を取り扱うときには、側鎖の構造は、ポリマーの放出挙動に影響を与えることができる。例えば、一般的に、本明細書に記載のポリ(ホスホエステル)の種類を用いて、より脂肪親水性、より疎水性又は嵩高い基へのリン酸原子含有側鎖の変換は、分解過程を遅くするだろう。例えば、放出は、通常、嵩高い芳香族側鎖を有するコポリマー組成物からよりも、低分子の脂肪族基の側鎖を有するコポリマー組成物の方からより速いだろう。
式Vのテレフタレートポリ(亜リン酸エステル)は、通常、生分解中のポリマーのホスホエステル結合の加水分解の1機能として少なくとも一部を制御する、in vivoでの生物活性剤の放出速度により特徴付けられる。しかしながら、ポリ(亜リン酸エステル)は、生分解速度に影響を与えるように操作することができる側鎖を有さない。
本発明の更なる実施態様では、第一ポリマーは、少なくとも2つの異なったエステル結合を含む、生分解性の、セグメント化された分子構造を含むコポリマーを含む。これらの特定の実施態様によれば、第一ポリマーは、(AB又はABA型の)ブロックコポリマー、又は(マルチブロック又はランダム-ブロックとしても知られている)(AB)nのセグメント化コポリマーを含むことができる。これらのコポリマーは、エステル交換反応に対して全く異なった感受性を有するコポリマー中に結合を形成する2(又はそれ以上の)環状エステルモノマーを用いて、2(又はそれ以上の)段階の開環共重合において形成される。これらの実施態様は、例えば米国特許第5,252,701号明細書 (Jarrett et al., "Segmented Absorbable Copolymer")に記載され、本明細書で、更に詳細に説明する。
1つの局面では、第一ポリマーは、少なくとも2つの異なったエステル結合を含む生分解性の、セグメント化された分子構造を含むコポリマーを含む。一般的に、セグメント化された分子構造は、多数の速いエステル交換結合及び多数の遅いエステル交換結合を含む。速いエステル交換結合は、1.3超のセグメント長分布を有する。環状エステルモノマーの逐次付加共重合は、選択的なエステル交換現象と関連して利用されて、特定の構造を有する生分解性コポリマー分子をつくる。
本発明によれば、コポリマーは、少なくとも2つの段階で、少なくとも2つの異なった環状エステルモノマーの逐次付加により製造することができる。第一の環状エステルモノマーは、カーボネート及びラクトン、並びにそれらの混合物から選ばれる。第二の環状エステルモノマーは、ラクチド及びその混合物から選ばれる。逐次付加は、以下のステップを含む:
(1) 約160℃〜約220℃の範囲の温度で、触媒の存在下に、少なくとも第一環状エステルモノマーを、第一段階で先ず重合して、第一ポリマー融解物を得;
(2) 第一ポリマー融解物に、少なくとも第二環状エステルモノマーを加え;及び
(3) 第二段階で、第一ポリマー融解物を、少なくとも第二環状エステルモノマーと共重合して、第二コポリマー融解物を得ること。
(1) 約160℃〜約220℃の範囲の温度で、触媒の存在下に、少なくとも第一環状エステルモノマーを、第一段階で先ず重合して、第一ポリマー融解物を得;
(2) 第一ポリマー融解物に、少なくとも第二環状エステルモノマーを加え;及び
(3) 第二段階で、第一ポリマー融解物を、少なくとも第二環状エステルモノマーと共重合して、第二コポリマー融解物を得ること。
工程はまた、約180℃超の温度で約5時間まで、第二コポリマー融解物をエステル交換することを含む。
生分解性の、セグメント化された分子構造を有するコポリマーの別の製造法は、3段階で、少なくとも2つの異なった環状エステルモノマーの逐次付加を含む。第一環状エステルモノマーは、カーボネート、ラクトン及びそれらの混合物から選ばれる。第二環状エステルモノマーは、ラクチド及びその混合物から選ばれる。逐次付加は、以下のステップを含む:
(1) 約160℃〜約220℃の範囲の温度で、触媒の存在下に、少なくとも第一環状エステルモノマーを、第一段階で先ず重合して、第一ポリマー融解物を得;
(2) 第一ポリマー融解物に、少なくとも第二環状エステルモノマーを加え;
(3) 第二段階で、第一ポリマー融解物を、少なくとも第二環状エステルモノマーと第二共重合して、第二コポリマー融解物を得;
(4) 少なくとも第二環状エステルモノマーを、第二コポリマー融解物に第二添加し;及び
(5) 第三段階で、第二コポリマー融解物を、少なくとも第二環状エステルモノマーを共重合させて、第三コポリマー融解物を得ること。
(1) 約160℃〜約220℃の範囲の温度で、触媒の存在下に、少なくとも第一環状エステルモノマーを、第一段階で先ず重合して、第一ポリマー融解物を得;
(2) 第一ポリマー融解物に、少なくとも第二環状エステルモノマーを加え;
(3) 第二段階で、第一ポリマー融解物を、少なくとも第二環状エステルモノマーと第二共重合して、第二コポリマー融解物を得;
(4) 少なくとも第二環状エステルモノマーを、第二コポリマー融解物に第二添加し;及び
(5) 第三段階で、第二コポリマー融解物を、少なくとも第二環状エステルモノマーを共重合させて、第三コポリマー融解物を得ること。
工程はまた、約180℃超の温度で約5時間まで、第三コポリマー融解物をエステル交換することを含む。
場合により、工程は、金属配位触媒及び/又は開始剤の存在下での重合を含むことができる。ある実施態様では、開始剤は、一機能性及び多機能性アルコールから選ばれる。一般的に、モノマーを連続的に加えることにより、単一反応容器中で逐次重合を行うのが好ましい。しかしながら、必要ならば、段階の1以上は、別々の反応容器中で重合し、最後に、単一反応容器中でエステル交換の段階を併せることができる。かかる工程は、環状ポリエステルを使用して、1以上の段階のためのモノマーを形成させるだろう。
環状モノマー由来の脂肪族ポリエステルのエステル交換は、当該分野で知られている。例えば、Gnanou and Rempp, Macromol. Chem., 188: 2267-2275 (1987) は、同時交換(simultaneous reshuffling)を伴うリビング重合として、リチウムアルコキシドの存在下でε-カプロラクトンのアニオン重合を記載している。この文献によれば、交換が2つの異なった分子間で起こる場合、「スクランブリング」と称される。交換が、分子内で起こり(back-bitingと呼ばれるが)そしてサイクルを形成する場合には、残りの直鎖高分子は、より低分子量であるが、鎖末端で活性部位をなお有する。
更なる実施態様では、第一ポリマーは、少なくとも1つのカーボネート単位を主な成分として含むランダムコポリマーを含む。カーボネートは少なくとも1つの第二モノマー成分と共重合している。これらの実施態様によれば、ある脂肪族カーボネートは、好適なカーボネートが主な成分として存在する限り、他のモノマー成分との高結晶性ランダムコポリマーを形成することができる。これらのコポリマーは、1以上の利点、例えば、比較的高い係数及び引っ張り強度、制御可能な生分解速度、血液適合性、及び生組織との生体適合性、を有することができる。好ましい局面では、加水分解性脱重合によるカーボネートポリマーの生分解性が生理的に中性のpHを有する分解物質を生じるので、これらのコポリマーはまた、最小の炎症性組織を誘導する。例示的なランダムコポリマーは、例えば、米国特許第. 4,891,263号明細書 (Kotliar et al.)、同第5,120,802号明細書 (Mares et al.)、同第4,916,193号明細書 (Tang et al.)、同第5,066,772号明細書 (Tang et al.)、及び同第5,185,408号明細書 (Tang et al.) に記載されている。
これらの実施態様によれば、コポリマーは、少量の成分として1以上の繰り返しモノマー単位を含み、主な成分として下記の一般構造(XXII):
[式中、
Zは、隣接へテロ原子が存在しないように選ばれ;
n及びmは、同一又は異なる、約1〜約8の整数であり;及び
R1、R2、R3及びR4は、同一又は異なる、水素原子、アルコキシアリール、アリールオキシアリール、アリールアルキル、アルキルアリールアルキル、アリールアルキルアリール、アルキルアリール、アリールカルボニルアルキル、アリールオキシアルキル、アルキル、アリール、アルキルカルボニルアルキル、シクロアルキル、アリールカルボニルアリール、アルキルカルボニルアリール、アルコキシアルキル、又は1以上の生物的適合性置換基で置換されたアリールもしくはアルキル、例えば、アルキル、アリール、アルコキシ、アリールオキシ、ジアルキルアミノ、ジアリールアミノ、アルキルアリールアミノ置換基であり;
R5及びR6は同一又は異なり、R1、R2、R3、R4、ジアルキルアミノ、ジアリールアミノ、アルキルアリールアミノ、アルコキシ、アリールオキシ、アルカノイル、又はアリールカルボニルであるか;又は、R1〜R6の内の任意の2つは、一緒になって、3、4、5、6、7、8又は9員の単環式、脂環式、スピロ式、二環式及び/又は三環式系を有するアルキレン鎖を形成することができ、当該系は、場合により、1以上の非-隣接カルボニル、オキサ、アルキルアザ又はアリールアザ基を含むことができる。但し、R1〜R6の少なくとも1つは、水素原子以外である。]
の繰り返しカーボネートモノマー単位又はその組み合わせを含む、ランダムコポリマーである。
Zは、隣接へテロ原子が存在しないように選ばれ;
n及びmは、同一又は異なる、約1〜約8の整数であり;及び
R1、R2、R3及びR4は、同一又は異なる、水素原子、アルコキシアリール、アリールオキシアリール、アリールアルキル、アルキルアリールアルキル、アリールアルキルアリール、アルキルアリール、アリールカルボニルアルキル、アリールオキシアルキル、アルキル、アリール、アルキルカルボニルアルキル、シクロアルキル、アリールカルボニルアリール、アルキルカルボニルアリール、アルコキシアルキル、又は1以上の生物的適合性置換基で置換されたアリールもしくはアルキル、例えば、アルキル、アリール、アルコキシ、アリールオキシ、ジアルキルアミノ、ジアリールアミノ、アルキルアリールアミノ置換基であり;
R5及びR6は同一又は異なり、R1、R2、R3、R4、ジアルキルアミノ、ジアリールアミノ、アルキルアリールアミノ、アルコキシ、アリールオキシ、アルカノイル、又はアリールカルボニルであるか;又は、R1〜R6の内の任意の2つは、一緒になって、3、4、5、6、7、8又は9員の単環式、脂環式、スピロ式、二環式及び/又は三環式系を有するアルキレン鎖を形成することができ、当該系は、場合により、1以上の非-隣接カルボニル、オキサ、アルキルアザ又はアリールアザ基を含むことができる。但し、R1〜R6の少なくとも1つは、水素原子以外である。]
の繰り返しカーボネートモノマー単位又はその組み合わせを含む、ランダムコポリマーである。
有用なR1、R2、R3及びR4基の例は、水素原子;アルキル、例えば、メチル、エチル、プロピル、ブチル、ペンチル、オクチル、ノニル、tert-ブチル、ネオペンチル、イソプロピル、sec-ブチル、ドデシル等;シクロアルキル、例えば、シクロへキシル、シクロペンシル、シクロオクチル、シクロヘプチル等;アルコキシアルキレン、例えば、メトキシメチレン、エトキシメチレン、ブトキシメシレン、プロポキシエチレン、ペントキシブチレン等;アリールオキシアルキレン及びアリールオキシアリーレン、例えば、フェノキシフェニレン、フェノキシメチレン等;及び、様々な置換アルキル及びアリール基、例えば。4-ジメチルアミノブチル等を含む。
他のR1〜R4基の例は、二価の脂肪族鎖である。これは、場合により、1以上の酸素原子、三置換アミノ又はカルボニル基、例えば、−(CH2)2−、-CH2(O)CH2-、−(CH2)3−、-CH2-CH(CH3)−、−(CH2)4−、−(CH2)5−、−CH2OCH2-、−(CH2)2−N(CH3)CH2-、-CH2C(O)CH2-、−(CH2)2−N(CH3)−(CH2)2−等、及び縮合、スピロ、二環性又は三環性環系、例えば、−CH(CH2CH2)2CH−、−CH(CH2CH2CH2)2CH−、-CH(CH2)(CH2CH2)CH-、-CH(CH2)(CH2-CH2CH2)CH-、-CH(C(CHS)2)(CH2CH2)CH-等を形成するための、二価鎖を含むことができる。
R5及びR6基の例は、-OCH2C(O)CH2-、−(CH2)2−NCH3-、-OCH2C(O)CH2-、−O−(CH2)2−O−、アルコキシ、例えば、プロポキシ、ブトキシ、メトキシ、イソプロポキシ、ペントキシ、ノニルオキシ、エトキシ、オクチルオキシ等;ジアルキルアミノ、例えば、ジメチルアミノ、メチルエチルアミノ、ジエチルアミノ、ジブチルアミノ等;アルカノイル、例えば、プロパノイル、アセチル、ヘキサノイル等;アリールカルボニル、例えば、フェニルカルボニル、p-メチルフェニルカルボニル等;及びジアリールアミノ及びアリールアルキルアミノ、例えば、ジフェニルアミノ、メチルフェニルアミノ、エチルフェニルアミノ等を含む、上記の代表的なR1〜R4基である。
これらの実施態様に従う使用には、主成分として式XXIIA(式中、Zは、−(R5−C−R6)−又はその組み合わせであり;nは、1、2又は3であり; 及びR1〜R6は、前記定義のとおりであり、好ましくは、R1〜R6に含まれる脂肪族部分は、約10炭素原子を含み、アリール部分は、最高約16炭素原子を含む。)のカーボネート繰り返し単位を含むランダムコポリマーが好ましい。
これらの好ましいコポリマーの例は、主成分として、nが1であり、Zが式XXIII:
[式中、
-C-は、Zが−C(R5)(R6)−のとき、Zの中心炭素原子であり;
R7は、同一又は異なって、縮合、スピロ、二環性及び/又は三環性構造等を含む、3〜16員環構造を有するアリール、アルキル又はアルキレン鎖であり;
R8及びR9は、同一又は異なって、R7又は水素原子であり、sは、同一又は異なって、0〜3であり、開環価数は水素原子で置換される。]
のコポリマーである。
-C-は、Zが−C(R5)(R6)−のとき、Zの中心炭素原子であり;
R7は、同一又は異なって、縮合、スピロ、二環性及び/又は三環性構造等を含む、3〜16員環構造を有するアリール、アルキル又はアルキレン鎖であり;
R8及びR9は、同一又は異なって、R7又は水素原子であり、sは、同一又は異なって、0〜3であり、開環価数は水素原子で置換される。]
のコポリマーである。
また、これらの好ましい主成分の例は、式XXIV:
[式中、
R1、R2、R3及びR4は、同一又は異なって、エチル、n-プロピル、イソプロピル、n-ブチル、sec-ブチル、t-ブチル、ネオペンチル等;フェニル;アニシル;フェニルアルキル、例えば、べンジル、フェネチル等;1以上のアルキル又はアルコキシ基で置換されたフェニル、例えば、トルイル、キシリル、p-メトキシフェニル、m-エトキシフェニル、p-プロポキシフェニル等;及びアルコキシアルキル、例えば、メトキシメチル、エトキシメチル等であり;
R5及びR6は、同一又は異なって、R1〜R4;アルコキシ、アルカノイル、アリールカルボニル、ジアルキルアミノであるか;又はR1〜R4の内の任意の2つが一緒になって、4、5、6、7、8又は9員の単環性、スピロ式、二環性及び/又は三環性環構造を有するアルキレン鎖を形成することができ、当該構造は、場合により、1以上の非-隣接カルボニル、オキサ、アルキルアザ又はアリールアザ基を含むことができる。但し、R1〜R6の少なくとも1つは、水素原子以外である;そして、
n及びmは、同一又は異なって、1、2又は3である。]
の繰り返し単位を含む成分である。
R1、R2、R3及びR4は、同一又は異なって、エチル、n-プロピル、イソプロピル、n-ブチル、sec-ブチル、t-ブチル、ネオペンチル等;フェニル;アニシル;フェニルアルキル、例えば、べンジル、フェネチル等;1以上のアルキル又はアルコキシ基で置換されたフェニル、例えば、トルイル、キシリル、p-メトキシフェニル、m-エトキシフェニル、p-プロポキシフェニル等;及びアルコキシアルキル、例えば、メトキシメチル、エトキシメチル等であり;
R5及びR6は、同一又は異なって、R1〜R4;アルコキシ、アルカノイル、アリールカルボニル、ジアルキルアミノであるか;又はR1〜R4の内の任意の2つが一緒になって、4、5、6、7、8又は9員の単環性、スピロ式、二環性及び/又は三環性環構造を有するアルキレン鎖を形成することができ、当該構造は、場合により、1以上の非-隣接カルボニル、オキサ、アルキルアザ又はアリールアザ基を含むことができる。但し、R1〜R6の少なくとも1つは、水素原子以外である;そして、
n及びmは、同一又は異なって、1、2又は3である。]
の繰り返し単位を含む成分である。
これらの実施態様における使用には、主成分として式XXV:
[式中、
R1〜R4は、同一又は異なって、アルキル、水素原子、アルコキシアルキル、フェニルアルキル、アルコキシフェニル又はアルキルフェニル、ここで、脂肪族部分は、1〜9の炭素原子を含み;そして、
R5及びR6は、同一又は異なって、R1〜R4置換基、アリールオキシ及びアルコキシからなる群より選ばれるか、又はR5及びR6は、一緒になって、3〜1員のスピロ式、二環性及び/又は三環性環構造を有する脂肪族鎖を形成することができ、当該構造は、1又は2の非-隣接オキサ、アルキルアザ又はアリールアザ基を含むことができる。但し、R1〜R4の少なくとも1つは、水素原子以外である。]
の繰り返し単位を含む、ランダムコポリマーが特に好ましい。
R1〜R4は、同一又は異なって、アルキル、水素原子、アルコキシアルキル、フェニルアルキル、アルコキシフェニル又はアルキルフェニル、ここで、脂肪族部分は、1〜9の炭素原子を含み;そして、
R5及びR6は、同一又は異なって、R1〜R4置換基、アリールオキシ及びアルコキシからなる群より選ばれるか、又はR5及びR6は、一緒になって、3〜1員のスピロ式、二環性及び/又は三環性環構造を有する脂肪族鎖を形成することができ、当該構造は、1又は2の非-隣接オキサ、アルキルアザ又はアリールアザ基を含むことができる。但し、R1〜R4の少なくとも1つは、水素原子以外である。]
の繰り返し単位を含む、ランダムコポリマーが特に好ましい。
好ましくは、ランダムコポリマーは、主成分として、式XXVI:
[式中、
nは1であり;
R5及びR6は、同一又は異なって、水素原子、フェニル、フェニルアルキル、又は1以上のアルキルもしくはアルコキシ基で置換されたフェニル又はフェニルアルキルであるか;又は、アルキル又はR5及びR6は、一緒になって、二価の鎖に、1又は2の非-隣接カルボニル、オキサ、アルキルアザ又はアリールアザ基を含むことができる、3〜6員環のスピロ、二環性及び/又は三環性の環構造を形成させる。但し、R5及びR6の少なくとも1つは、水素原子以外である。]
の繰り返しモノマー単位を含む。
nは1であり;
R5及びR6は、同一又は異なって、水素原子、フェニル、フェニルアルキル、又は1以上のアルキルもしくはアルコキシ基で置換されたフェニル又はフェニルアルキルであるか;又は、アルキル又はR5及びR6は、一緒になって、二価の鎖に、1又は2の非-隣接カルボニル、オキサ、アルキルアザ又はアリールアザ基を含むことができる、3〜6員環のスピロ、二環性及び/又は三環性の環構造を形成させる。但し、R5及びR6の少なくとも1つは、水素原子以外である。]
の繰り返しモノマー単位を含む。
ランダムコポリマーは、主成分として、式XXVI、特に、R5及びR6は、同一又は異なって、アルキル、フェニル、フェニルアルキル、フェニル、又は1以上のアルキル又はアルコキシ基で置換されたフェニルアルキルであるか;又は3〜10員、好ましくは5〜7員の、スピロ又は二環性環構造を形成する二価鎖であり、場合により、当該鎖は、1以上の非-隣接オキサ、カルボニル又は二置換アミノ基を含むことができる、の繰り返しモノマー単位を含むことが好ましい。R5及びR6は、同一又は異なって、フェニル、アルキルフェニル又はフェニルアルキル、例えば、トリルベネイル、フェネチル又はフェニル、又は1〜7の炭素原子の低級アルキル、例えば、メチル、エチル、プロピル、イソプロピル、n-ブチル、tert-ブチル、ペンチル、ネオペンチル、ヘキシル及びsec-ブチルであることが特に好ましい。
式XXVIを利用する最も好ましい実施態様において、R5及びR6は、同一又は異なって、約1〜約4の炭素原子を有する低級アルキル基であり、約3超の炭素原子、好ましくは約2超の炭素原子が互いに異ならない。R5及びR6は、同一であり、約1〜2の炭素原子のアルキル、好ましくはR5及びR6の内の1つはメチル、を含む、ことが好ましい。
これらの実施態様によれば、コポリマーは、1以上の他の繰り返しモノマー単位を含む少量の成分を含む。本発明のランダムコポリマーの少量成分は、様々に変化し得る。少量成分も生分解性かつ生体吸収性であることが好ましい。
第二の繰り返し単位成分の例は、式XXIIA(ここで、nは、(Z)nにおいて1〜8である)、及び式XXIIB及び式XXVI(ここで、nは1である)の範囲内に含まれるあるモノマー単位に限定されないカーボネートから得られるもの、特に主成分として好ましくないもの、並びに置換又は非置換のエチレンカーボネート、テトラメチレンカーボネート、トリメチレンカーボネート、ペンタメチレンカーボネート等から得られるものである。また、第二の繰り返し単位成分の例は、開環重合により重合されるモノマーから得られるもの、例えば、置換又は非置換ベータ、ガンマ、デルタ、オメガ、及び他のラクトン、例えば式XXVII:
[式中、R10は、アルコキシ、アルキル又はアリールであり、qは0〜3であり、ここで、開放原子価(open valencies)は水素原子で置換される。]
のものである。かかるラクトンは、カプロラクトン、バレロラクトン、ブチロラクトン、プロピオラクトン、及びヒドロキシカルボン酸、例えば、3-ヒドロキシ-2-フェニルプロパン酸、3-ヒドロキシブタン酸、3-ヒドロキシ-3-メチルブタン酸、3-ヒドロキシペンタン酸、5-ヒドロキシペンタン酸、3-ヒドロキシ-4-メチルヘプタン酸、4-ヒドロキシオクタン酸等のラクトン;及びラクチド、例えば、L-ラクチド、D-ラクチド、D,L-ラクチド; グリコリド; 及びジラクトン、例えば、式XXVIII:
のものである。かかるラクトンは、カプロラクトン、バレロラクトン、ブチロラクトン、プロピオラクトン、及びヒドロキシカルボン酸、例えば、3-ヒドロキシ-2-フェニルプロパン酸、3-ヒドロキシブタン酸、3-ヒドロキシ-3-メチルブタン酸、3-ヒドロキシペンタン酸、5-ヒドロキシペンタン酸、3-ヒドロキシ-4-メチルヘプタン酸、4-ヒドロキシオクタン酸等のラクトン;及びラクチド、例えば、L-ラクチド、D-ラクチド、D,L-ラクチド; グリコリド; 及びジラクトン、例えば、式XXVIII:
[式中、R10及びqは、式XXVIIで定義したとおりであり、開放原子価が水素原子で置換されている。]
で表されるものである。かかるジラクトンは、2-ヒドロキシ酪酸、2-ヒドロキシ-2-フェニルプロパン酸、2-ヒドロキシル-3-メチルブタン酸、2-ヒドロキシペンタン酸、2-ヒドロキシ-4-メチルペンタン酸、2-ヒドロキシへキサン酸、2-ヒドロキシオクタン酸等のジラクトン、を含む。
で表されるものである。かかるジラクトンは、2-ヒドロキシ酪酸、2-ヒドロキシ-2-フェニルプロパン酸、2-ヒドロキシル-3-メチルブタン酸、2-ヒドロキシペンタン酸、2-ヒドロキシ-4-メチルペンタン酸、2-ヒドロキシへキサン酸、2-ヒドロキシオクタン酸等のジラクトン、を含む。
更なる有用な少数成分の例は、ジオキセパノンから得られる単位、例えば、米国特許第4,052,988号明細書及び英国特許第1,273,733号明細書に記載の単位である。かかるジオキセパノンは、式XXIX:
のアルキル及びアリール置換、及び非置換のジオキセパノン、並びにジオキサノンから得られるモノマー単位、例えば、米国特許第3,952,016号明細書、同第4,052,988号明細書、同第4,070,375号明細書及び同第3,959,185号明細書に記載のモノマー単位を含む。例えば、式XXX:
[式中、qは前記定義のとおりであり; R10は、同一又は異なって、ヒドロキシカルボニル基、例えばアルキル及び置換アルキル、及びアリール又は置換アリールであり、開放原子価が水素原子で置換されている。]
のアルキル及びアリール置換、及び非置換のジオキサノンである。好ましくは、R10は、同一又は異なって、1〜6の炭素原子、好ましくは1又は2の炭素原子を含むアルキル基であり;そして、qは0又は1である。
のアルキル及びアリール置換、及び非置換のジオキサノンである。好ましくは、R10は、同一又は異なって、1〜6の炭素原子、好ましくは1又は2の炭素原子を含むアルキル基であり;そして、qは0又は1である。
好適な少数成分はまた、エーテルから得られるモノマー単位、例えば、2,4-ジメチル-1,3-ジオキサン、1,3-ジオキサン、1,4-ジオキサン、2-メチル-5-メトキシ-1,3-ジオキサン、4-メチル-1,3-ジオキサン、4-メチル-4-フェニル-1,3-ジオキサン、オキセタン、テトラヒドロフラン、テトラヒドロピラン、ヘキサメチレンオキシド、ヘプタメチレンオキシド、オクタメチレンオキシド、ノナメチレンオキシド等、を含む。
更なる少数成分は、エポキシドから得られるモノマー単位、例えば、エチレンオキシド、プロピレンオキシド、アルキル置換エチレンオキシド、例えばエチル、プロピル及びブチル置換エチレンオキシド、様々な内部オレフィンのオキシド、例えば、2-ブテン、2-ペンテン、2-へキセン、3-へキセンのオキシド、エポキシド類縁体を含み;並びに、二酸化炭素と共にエポキシドから得られる単位も含み;並びに、オルトエステル又はオルトカーボネートから得られるモノマー単位、例えば、アルキル又はアリール置換又は非置換オルトエステル、オルトカーボネート、及び場合により1以上のオキサ、アルキルアザ、アリールアザ及び式XXXI:
[式中、q及びR10は、上記のとおりであり;rは、0〜約10であり;R13は同一又は異なって、アルキル又はアリールであり;R11及びR12は同一又は異なって、水素原子、アルキル又はアリールである。]
のカルボニル基を含むことがある、環状無水物を含む。
のカルボニル基を含むことがある、環状無水物を含む。
これらの実施態様のコポリマーを形成する繰り返しモノマー単位の各々の相対的パーセンテージは、広く変動し得る。唯一の要件は、式XXIIAの範囲内の繰り返しモノマー単位の少なくとも1種が主要量であり、繰り返しモノマー単位の他の種が少ない量であることである。本明細書に記載の「主要量」は、コポリマー中の全ての繰り返しモノマー単位の総重量基準で、約50重量%超であり、「少ない量」は、コポリマー中の全ての繰り返しモノマー単位の総重量基準で、約20重量%未満である。
加えて、ある適用のためには、これらのバイオポリマーの末端保護が好ましい。末端保護は、例えば、アシル化、アルキル化、シリル化剤等により達成することができる。
従って、本発明は、第一生分解性ポリマーを含む第一コート層及び第二ポリマーを含む第二コート層を含むコーティング組成物を含む、移植可能用具(例えば、ステント)を提供する。第一生分解性ポリマーは、好ましくは、ポリエーテルエステルコポリマー、例えば、PEGT/PBTである。他の好適な第一ポリマーは、本明細書に記載されている。第二ポリマーは、生物活性剤の制御された放出を提供するように選択される、生分解性ポリマーを含む。本発明のこれらの局面を記載する。
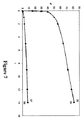
「実施例」に例証されているように、PEGT/PBTのみを含む単一層のコーティングが低分子生物活性剤(例えば、デキサメタゾン)により製剤化されるときには、生物活性剤は、コーティングから迅速に放出される。実施例1に示すように、例えば、90%超のデキサメタゾンが、非ブレンドPEGT/PBTからなるコーティングから24時間内に放出される。しかしながら、本発明によれば、第二(又は第三、第四等でも)コート層がPEGT/PBTコート層と関連して一旦提供されると、生物活性剤の初期バーストが制御され、より長期間、生物活性剤のより持続的放出を可能にする。選択された第二ポリマー、及び用具表面及び/又は生物活性剤に比べた第一ポリマー及び第二ポリマーの相対的位置により、低分子量の生物活性剤の放出は、最初の24時間以内に顕著に減少し得る。初期放出期間の後に、生物活性剤の実質的な直線的放出を達成することができ、それによって、生物活性剤の制御された放出を提供する(長期間の直線的放出に加えて、他の放出プロファイルも企画される)。
本発明に従って、ポリエーテルエステルコポリマー(又は他の第一ポリマー)は、多層配置中に第二生分解性ポリマーを提供されて、生物的条件に曝露されたときに、制御的に生物活性剤を放出することができる生分解性コーティングを形成する。様々な第二ポリマーは、本発明の趣旨に従って利用することができる。典型的には、第二ポリマーは、第一ポリマーに比べてより遅い生物活性剤放出速度を有する。第二ポリマーは、分解されたときに、生理的に許容される分解生成物を生じる、有機エステル又はエーテルを含むことができる。加えて、無水物、アミド、オルトエステル等も使用できる。第二ポリマーは、架橋又は非-架橋された、付加又は縮合ポリマーからなることができる。主として、炭素原子及び水素原子に加えて、ポリマーは、酸素原子及び窒素原子、特に酸素原子を含むだろう。酸素原子は、オキシ(例えば、ヒドロキシ、エーテル、カルボニル等)、カルボン酸エステル等として存在し得る。窒素原子は、アミド、シアノ又はアミノとして存在し得る。表1は、本発明に従う第二ポリマーとして使用することができる、公知の生分解性ポリマーを掲載する。
ポリ(ラクチド)は、天然異性体である、ポリ(L-ラクチド)(PLLA)及びポリ (D,L-ラクチド) (PLA) を含むと理解される。更に、ポリ無水物は、ポリ[ビス (p-カルボキシフェノキシ) プロパン] 無水物 (PCPP) 及びポリ (テレフタル酸ム無水物 (PTA)) を含む。
ある局面では、脂肪族ポリエステルは、有用な第二ポリマーであり得る。ある実施態様においては、乳酸、グリコール酸、カプロラクトン、エチレングリコール、エチルオキシリン酸エステル及び類似のモノマー単位から選ばれるモノマーから得られる脂肪族ポリエステルは、有用であり得る。これらのポリマーは、ホモポリマー又はコポリマーでよい。この性質の脂肪族ポリエステルの例は、ポリ (1,4-ブチレン アジピン酸エステル-ポリカプロラクタム共重合体); ポリカプロラクトン; ポリカプロラクトン ジオール; ポリグリコリド; ポリ (DL-ラクチド); ポリ-L-ラクチド; ポリ (DL-ラクチド-カプロラクトン共重合体) (様々なmole%のDL-ラクチド); ポリ (L-ラクチド-カプロラクトン-グリコリド共重合体) (様々なMW及び様々なmole%のDL-ラクチド); 及びポリ (DL-ラクチド-グリコリド共重合体) (様々なMW及び様々なmole%のDL-ラクチド)を含むが、これらに限定されない。
ある局面では、ポリホスホエステルは、生物活性剤送達に重要な多くの性質を示すことができるため、第二ポリマーとして有用であり得る。ポリホスホエステルは、加水分解及びおそらく酵素消化により生分解し、これらのポリマー及びコポリマーの多くは、有機溶媒、例えば、THF、クロロホルム、アセトニトリル及び酢酸エチル、の範囲内で溶解性である。ある実施態様では、ラクチド及び/又はエチレングリコールのモノマー単位を含むポリホスホエステルは、有用であり得る。本発明の趣旨に従う有用なリホスホエステルは、第一ポリマー(ポリエーテルエステルコポリマー)よりも遅い生物活性剤溶出速度を有して、本明細書で企画される生物活性剤の制御された放出を提供する。ある局面では、有用なポリホスホエステルは、第一ポリマー及び生物活性剤に一般的な溶媒中で溶解性である。それにより、第一ポリマー、第二ポリマー及び生物活性剤の組み合わせに、当該溶媒での真の溶液を形成させることができる。
更なる局面では、第二ポリマー自体は、ポリマーの混合物を含むことができる。例えば、2以上のポリ(エステル-アミド)ポリマー(PEA)のブレンド、米国特許第6,703,040号明細書 (Katsarava et al.)に記載されているもの、を利用することができる。かかるポリマーは、ジオール(D)、ジカルボン酸(C)及びα-アミノ酸 (A) の重合により、形態(DACA)n中のエステル及びアミド結合を介して製造することができる。アミノ酸の例は、任意の天然又は合成α-アミノ酸、特に中性アミノ酸、を含む。
これらの局面によれば、好適なジオールは、任意の脂肪族ジオール、例えば、アルキレンジオール、例えばHO−(CH2)k−OH (すなわち、非-分枝)、分枝ジオール (例えば、プロピレングリコール)、環状ジオール (例えば、ジアンヒドロヘキシトール及びシクロヘキサンジオール)、又はエチレンジオールに基づくオリゴマージオール(例えば、ジエチレングリコール、トリエチレングリコール、テトラエチレングリコール、又はポリ(エチレングリコール))を含む。ジカルボン酸は、任意の脂肪族ジカルボン酸、例えば、α,ω-ジカルボン酸(すなわち、非-分枝)、分枝ジカルボン酸、環状ジカルボン酸(例えば、シクロへキサンジカルボン酸)でよい。
ある局面では、PEAポリマーは、下記式XXXII:
[式中、
k=2〜12、特に、2、3、4又は6であり;
m=2〜12、特に4又は8であり;そして
R=CH(CH3)2、CH2CH(CHa)2、CH(CH3)CH2CH3、(CH2)3CH3、CH2C6H5、又は(CH2)3SCH3である。]
を有する。
k=2〜12、特に、2、3、4又は6であり;
m=2〜12、特に4又は8であり;そして
R=CH(CH3)2、CH2CH(CHa)2、CH(CH3)CH2CH3、(CH2)3CH3、CH2C6H5、又は(CH2)3SCH3である。]
を有する。
ある実施態様では、第二ポリマーは、AがL-フェニルアラニン (Phe-PEA) である第一のPEAポリマーと、AがL-ロイシン (Leu-PEA) である第二のPEAポリマーとの混合物を含む。Phe-PEAのLeu-PEAに対する比は、10:1〜1:1、又は5:1〜2.5:1の範囲である。
場合により、PEAポリマー混合物は、PEAポリマーを加水分解的に開裂することができる酵素、例えば、α-キモトリプシンを含む。酵素は、生分解性コート組成物の表面に吸着することができ、又は酵素作用により放出されるバクテリオファージ中に含むことができる。
本発明によれば、第二ポリマーは、第一ポリマーの性質、例えば、迅速な生物活性剤の放出、比較的弱い機械特性及び溶媒溶解性を賛辞するように選択することができる。ある局面では、許容される第二ポリマーは、低拡散率を示す、遅い生物活性剤の放出を有することができる。これは、より高いガラス転移温度、結晶性、又は生物活性剤との特定の化学的相互作用の1機能であり得る。
機械的特性の例は、柔軟性及び接着を含む。例えば、本発明のコーティングでコートされることになる医療用具が拡張可能な用具(例えば、ステント)であるときには、第二ポリマーは、用具拡張に頑強であるように選択することができる。例えば、頑強であると考えられるポリマーは、より低いガラス転移温度及びより低い結晶性が望ましいことを示す、用具拡張に適応するように十分な柔軟性を有することができる。第二ポリマーは、用具表面へのポリマーコーティングの高い接着を提供するように選択することができる。これらの局面では、第一ポリマーの非ブレンドコーティングは、用具表面に十分には接着することができない。例えば、PEGT/PBTは、典型的には、金属基板にはうまく接着しない。しかしながら、本発明の趣旨に従って異なったポリマーからなる追加のコート層の添加の場合には、用具表面へのかかる接着が増大され得る。
ある局面では、第二ポリマーは、典型的に、第一ポリマー(例えば、PEGT/PBT)と同一の溶媒(例えば、クロロホルム、THF、ジクロロメタン及びトリクロロメタン)に溶解する。
ある局面では、本発明の生分解性コーティングの1以上のコート層は、2以上のポリマーのブレンドからなることができる。かかるブレンドは、例えば、異なった生物活性剤放出速度を有する2以上のポリマーからなることができる。ある実施態様では、ブレンドは、(本明細書に第一ポリマーとして記載されているものから選ばれる)第一ポリマー及び(本明細書に第二ポリマーとして記載されているものから選ばれる)第二ポリマーを含む。他の実施態様では、ブレンドは、第二ポリマーとしての使用に好適であると記載されているものから選ばれる2以上のポリマーを含む(例えば、PLAとPLGAとのブレンド、又はコラーゲンとヒアルロン酸とのブレンド等)。特定のブレンドの個々のポリマーは、所望の生物活性剤の放出速度を提供するように選択され得る。例えば、より速放性ポリマー(例えば、ポリアクティブ(商標)ポリマー)は、比較的遅い放出のポリマー(例えば、PLLA)とブレンドして、いずれかのポリマー(ポリアクティブ(商標)ポリマー又はPLLA)のみの放出速度の中間である放出速度を証明するブレンドされたポリマーを提供することができる。
ある局面では、ブレンドの個々のポリマーは、ポリマーの他の特徴、例えば、各ポリマーの分解生成物の化学的特徴に基づいて選択することができる。例えば、相対的に酸性の分解生成物(例えば、PLLA)を有するポリマーは、非-酸性分解生成物を有する他のポリマーとブレンドすることができる。例えば、コーティングに含まれる特定の生物活性剤が酸性環境に敏感であるときには、かかるブレンドは有利であり得る。分解生成物の酸性度を減少させるように選択されるポリマーをブレンドすることにより、治療部位の酸性度は、減じられ、それによって、治療部位における生物活性剤の有効性を高める。
第一生分解性ポリマー及び第二生分解性ポリマーは、多層形式で提供され、それによって、生物活性剤放出コーティングを形成する。生物活性剤は、第一ポリマー、第二ポリマー又は両方に存在し得る(言い換えれば、生物活性剤は、1以上のコーティングの個々のコート層に存在し得る)。ある局面では、コート組成物は、使用条件(典型的には、使用条件は、保存条件から用具の使用温度にまで及ぶ)下で著しい相分離を起こさない。典型的な保存温度は、周囲温度(又は約18℃〜約30℃)であるが、典型的な使用温度は、体温(又は約36℃〜約38℃)である。一旦、医療物品表面に提供されると、個々のコート層は、相間の成分をほとんど又は全く混合されることなく、依然として区別可能であり得る。本明細書の[実施例」で示すように、本発明は、個々のコート層が完全に用具表面上に保持され、生物活性剤が、生物活性剤を含むように選択された特定のコート層(複数)内でうまく混合される、多層形式を提供することができる。
第二ポリマーの選択は、1以上の考慮すべき事項、例えば、特定の適用のために望ましい生物活性剤の放出速度、第二ポリマーとして検討中の個々のポリマーの生物活性剤の放出速度、個々のポリマーの疎水性及び溶媒適合性によって影響を受け得る。開始ステップとして、生物活性剤は、治療のために選択される。次に、患者に生物活性剤の治療的投薬量を提供することになる放出速度は、例えば、本明細書に記載の考慮すべき事項の多くに基づいて決定することができる。一旦、生分解性組成物の放出速度が決定されると、その速度は、第二ポリマーの選択用のパラメーターを確立するために利用することができる。第一ポリマーの生物活性剤放出速度は、本明細書で考察されるように、決定することができる。第二ポリマーの生物活性剤放出速度は、例えば、ポリマーの供給者により提供される情報を用いて別個に決定することができる。典型的には、生分解性組成物放出速度は、第一ポリマーのみ及び第二ポリマーのみの放出速度の中間の速度である。
長期間送達される生物活性剤の相対的量及び投薬速度は、以下の任意の1以上を調整することにより制御することができる:第二生分解性ポリマーの選択;生分解性組成物内の、より遅い放出ポリマーに対する速放性ポリマーの量を調整すること;層としての生分解性ポリマーの生分解性組成物内の配置(例えば、コーティングの外表面対用具表面に近いより内部の位置での配置、又は内側と外側の間の中間の位置での配置)。より高い初期放出速度について、より速放性ポリマーの割合は、より遅い放出ポリマーに比べて増加することができる。投薬量のほとんどが長期間に渡り放出されるのが望ましい場合には、より遅い放出ポリマーの割合は、より遅い放出ポリマーに比べて増加することができる。
第二ポリマーの相対的疎水性は、生物活性剤の放出速度に影響を与えることができる。例えば、PEGT/PBT (比較的親水性のコポリマーである)の1以上のコート層、より疎水性の第二ポリマーの1以上の層からなる組成物は、長時間、生物活性剤の放出プロファイルを調節するように選択することができる。
第二ポリマー用の別の選択パラメーターは、溶媒適合性である。ある好ましい局面では、第一ポリマー及び第二ポリマー用の溶媒系は適合性である。更なる局面では、第一ポリマー、第二ポリマー及び生物活性剤用の溶媒系は、適合性である。更に、第一ポリマー及び第二ポリマーは、用具表面に簡単に適用されるコーティング溶液を提供するように製剤化することができる。例えば、スプレイ法を用いて、コーティング溶液を用具表面に適用することが望ましいときには、適用工程中に相分離を経ずに、かかる適用のために良好な噴霧を提供するコーティング溶液を形成することは、有用であり得る。
多くの生分解性ポリマー(及び特にラクチド及びグリコリドポリマー、及びコポリマー)の分解の主な形式は、加水分解である。分解は、先ず、原料への水の拡散、次いで原料のランダム加水分解、断片化、最後に、食作用、拡散及び代謝を伴う、より強力な加水分解、により進行する。加水分解は、特にポリマー原料のサイズ及び親水性、ポリマーの結晶性、環境のpH及び温度により影響を受け得る。
ポリマーが一旦加水分解されると、加水分解生成物は、代謝されるか又は分泌されるかのいずれかである。PLAの加水分解的分解によって生じる乳酸は、トリカルボン酸サイクルに入り、二酸化炭素及び水として分泌される。ポリグリコール酸(PGA)はまた、他の代謝種に分泌されるか又は酵素的に変換されるかのいずれかであるグリコール酸への非特異的酵素的加水分解を伴うランダム加水分解により、分解される。
ある局面では、PLA、PGA等の分解は、用具に近接した酸性環境を生じることができる。かかる酸性条件は、生物活性剤、生分解性ポリマー、又はこれら双方に不利に影響を与え得る。好ましい局面では、酸性分解生成物(例えば、PLLA又はPLGAの分解の際に生じるもの)の量が、生分解性組成物中に提供される生物活性剤に対するダメージのリスクを減少させ又は最小限に抑えるように制御されるように、本発明の生分解性組成物は製剤化される。多くの生物活性剤は酸性-に敏感であるので、分解時に酸性環境をつくることができる生分解性ポリマーの量を減らすことができる生分解性組成物を提供し、及び/又はかかる生物活性剤の保護環境を提供することは有益であり得る。
ある局面では、分解性組成物は、PEGT/PBTポリマー(ポリアクティブ(商標)の名称の下で、Octoplus BVから商業的に入手可能)からなる第一コート層及びPLLAからなる第二コート層を含む。これらの実施態様は、ポリアクティブ(商標)からなる単一コート層を有する実施態様に比べて、より長期間に渡り、より低い初期バーストにより生物活性剤を送達する。生物活性剤放出は、ポリアクティブ(商標)ポリマーのみの放出速度とPLLAのみの放出速度との中間である。第一コート層及び第二コート層の相対的厚さは、初期投薬速度と、次の一定かつより長い持続的投薬速度との所望の組み合わせを達成するように調整することができる。
コート層の位置及び化学組成は、生物活性剤の制御された放出を提供するように選択することができる。本明細書で説明したように、「第一」コート層、「第二」コート層等の名称は、本発明の組成物及び方法を、表面上の特定の順序のコート層に限定することを意味しない。しかしながら、本発明を説明する目的で、コーティングを含むコート層は、コート層の区別可能な化学組成を示すように表される。
多層コーティングは、第一コート層(典型的には、移植可能用具表面と直接接触して配置されるコート層)、第二コート層(典型的には、第一コート層と直接接触して配置されるコート層)等を含む。次いで、2-層構成の場合には、第二コート層は、最外コート層であると考えられる。3-層構成では、第三コート層は、最外コート層であると考えられる。用具の移植の際に体液と最初に接触するのは最外コート層である。特定の理論に拘束されるものではないが、用具上の最外コート層の選択は、生体適合性及び生分解性組成物放出速度に影響を与え得ると考えられる。ある好ましい局面では、親水性ポリマーは、最外コート層として選択され、よって体内での用具の配置の際に体液と接触する層である。
例えば、最外コート層は、コーティング生物適合性を改善するように選択することができる。1つのかかる好ましい実施態様では、ポリアクティブ(商標)の最外コート層は、疎水性生分解性ポリマーよりも分解中に、PLLA、PDLLA、PLGA等に比べてほとんど酸を発生しない表面を提供することにより、コーティング生物適合性を改善することができる。結果として、少なくとも移植部位(及びおそらく移植可能用具の周りの大きな部位)は、生分解性組成物の分解中にほとんど酸性とならないだろう。
更に、より親水性最外コート層(例えば、ポリアクティブ(商標)ポリマー)の配置もまた、好ましくは、コーティング中へのより大きな水の浸透率を可能にすることにより、コーティングの分解速度を増加させることができる。
代替的には、酸性の分解生成物の発生は問題とならないときには、PLLA(又は類似のポリマー)の最外コート層を提供することができる。実施態様によれば、最外層は、第一コート層よりも遅い生物活性剤放出速度を有するだろう。従って、最外層は、生分解性組成物からの生物活性剤の放出を遅くするように働くことができる。更に、これらの種類のポリマー(例えば、PLLA)の比較的疎水性は、生分解性組成物の水透過性を減少させることができ、それによって、生分解性組成物からの生物活性剤の拡散を減少させる。このことは、生物活性剤の初期放出に影響を与え得る。
生分解性組成物を製剤化するために使用することができる好適な溶媒は、クロロホルム、水、アルコール(例えば、メチル、エチル、イソプロピル等を含む)、アセトン、アセトニトリル、エーテル、メチルエチルケトン(MEK)、酢酸エチル、テトラヒドロフラン(THF)、ジオキサン、塩化メチレン、キシレン、トルエン、N,N-ジメチルホルムアミド(DMF)、ジメチルスルホキシド(DMSO)、N,N-ジメチルアセトアミド (DMAC)、N-メチルピロリドン (NMP)、ジクロロメタン、ヘキサン、これらの組み合わせなどを含むが、これらに限定されない。
生物活性剤により生分解性組成物を形成するために、選択された生分解性ポリマーは、生物活性剤と混合される。生物活性剤は、液体、細粉砕固体又は任意の他の好適な物理的形状として存在し得る。本発明のポリマーと関連して用いることができる異なった生物活性剤の種類は広い。本発明の生分解性組成物は、本明細書に記載の低分子量の生物活性剤の送達のために特定の有用性を見出すことができる。場合により、生分解性組成物は、1以上の添加剤、例えば、希釈剤、担体、賦形剤、安定剤等を含むことができる。
体液と接触すると、生分解性組成物は、徐々に分解(主に、加水分解による)を受け、持続的期間又は長期間、生物活性剤の放出を伴う。このことは、生物活性剤の治療上有効量の長期間送達(例えば、数週間の期間)を生じ得る。治療上有効量は、治療されるべき患者、症状の重度、処方する医師の判断等の要素に基づいて、決定することができる。本明細書の教示の点から、当業者は、様々な製剤を調製することができるだろう。
様々な図は、コーティング材料及び生分解性ポリマーの相対的位置を変化させながら、可能性のある溶出速度の変化を説明するだろう。本明細書の様々な実施例は、様々な組成、コーティング中の様々な相対的位置、様々なコーティング厚等のコート層について可能性のある異なった溶出速度を例証する。
各コーティング系は、ポリマー組成物及びコーティング中の個々のポリマー層の相対的位置により調整することができる、自己の放出速度プロファイルを有する。各生分解性コーティングは、異なったポリマーからなり、異なった分子(生物活性剤及び他の添加剤)を有することができる。このことは、各コート層での放出速度を制御する能力を提供し、次いで、生分解性組成物からの1以上の生物活性剤の投薬量を操作する能力を提供する。
本発明の生分解性組成物は、1以上の生物活性剤を含み、それによって薬物-送達用具を提供する。これらの薬物-送達局面をより詳細に記載する。
本明細書で用いる「生物活性剤」は、生物組織の生理機能に影響を与える薬剤を称する。本発明に従う有用な生物活性剤は、移植部位への適用用の所望の治療的特徴を有する任意の物質を実質的に含む。
考察の容易のために、繰り返し、「生物活性剤」に言及されるだろう。「生物活性剤」に言及される間は、本発明は、治療部位に任意の数の生物活性剤を提供することができる、ことが理解されるだろう。従って、「生物活性剤」という単数形の言及は、同様に複数形を包含する意図である。更に、考察の目的のために、生物活性剤と、PEGT/PBTと第二ポリマー、例えばPLAとのブレンドからなる生分解性組成物との関連に言及されるだろう。しかしながら、生物活性剤が本明細書に記載の生分解性組成物の任意と関連し得ることは、本開示の検討の上では、明らかであろう。更に、本明細書に記載の添加剤は、同様に、開示されている全てのポリマー系に適用可能である。
生物活性剤の例は、トロンビンインヒビター、抗血栓剤、血栓溶解剤、線維素溶解薬、抗凝結薬、抗血小板剤、血管痙攣インヒビター、カルシウムチャンネル遮断薬、ステロイド、血管拡張剤、血圧降下剤、抗菌薬、抗生物質、抗菌剤、駆虫薬及び/又は抗原虫薬、ッ殺菌剤、抗真菌剤、血管形成剤、血管形成阻害剤、表面糖タンパク質受容体のインヒビター、細胞分裂抑制薬、微小管インヒビター、抗分泌薬、アクチンインヒビター、リモデリングインヒビター、アンチセンスヌクレオチド、代謝拮抗剤、縮瞳薬、抗-増殖剤、抗癌性化学療法剤、抗-新生物剤、抗ポリメラーゼ、抗ウイルス剤、抗-AIDS物質、抗-炎症性ステロイド又は非-ステロイド性抗-炎症剤、鎮痛剤、解熱剤、免疫抑制剤、免疫調節因子、成長ホルモンアンタゴニスト、成長因子、放射線療法剤、ペプチド、タンパク質、酵素、細胞外マトリックス成分、ACEインヒビター、フリーラジカルスキャベンジャー、キレーター、抗-酸化剤、光線力学療法剤、遺伝子療法剤、麻酔薬、抗毒素、神経毒、オピオイド、ドーパミンアゴニスト、睡眠薬、抗ヒスタミン薬、トランキライザー、抗痙攣薬、筋弛緩剤及び抗-パーキンソン物質、鎮痙薬及び筋肉収縮剤、抗コリン作用薬、眼科薬、抗緑内障薬、プリスタグランジン、抗鬱薬、抗精神病薬、神経伝達物質、制吐剤、造影剤、特異的標的剤、及び細胞反応調節因子を含むが、これらに限定されない。
より具体的には、実施態様では、活性剤は、ヘパリン、共有結合型ヘパリン、合成ヘパリン塩、又は別のトロンビン抑制物質;ヒルジン、ヒルログ、アルガトロバン、D-フェニルアラニル-L-ポリ-L-アルギニル クロロメチルケトン、又は別の抗血栓剤; ウロキナーゼ、ストレプトキナーゼ、組織プラスミノーゲン活性化因子、又は別の血栓溶解剤;線維素溶解薬; 血管痙攣抑制剤; カルシウムチャンネル遮断薬、硝酸塩、一酸化窒素、一酸化窒素プロモーター、一酸化窒素ドナー、ジピリダモール、又は別の血管拡張神経; HYTRIN(登録商標)又は他の降圧剤; 糖タンパク質IIb/IIIaインヒビター (アブシキマブ) 又は表面糖タンパク質受容体の別のインヒビター;アスピリン、チクロピデン、クロピドゲル又ア別の抗血小板物質;コルヒチン又は別の抗有糸分裂性又は別の微小管インヒビター;ジメチルスルホキシド(DMSO)、レチノイド又は別の抗分泌剤;サイトカラシン又は別のアクチンインヒビター;細胞サイクルインヒビター;リモデリングインヒビター;デオキシリボ核酸、アンチセンスヌクレオチド又は分子遺伝的インターベンション用の別の薬剤;メトトレキサート、又は別の代謝拮抗剤もしくは抗増殖剤;タモキシフェンクエン酸塩、TAXOL(登録商標)、パクリタキセル又はその誘導体、ラパマイシン(又は他のラパローグ、例えば、ABT-578又はシロリムス)、ビンブラスチン、ビンクリスチン、ビノレルビン、エトポシド、テノピシド、ダクシノマイシン(アクチノマイシンD)、ダウノルビシン、ドコソルビシン、イダルビシン、アンスラサイクリン、マイトキサントロン、ブレオマイシン、プリカマイシン(ミスラマイシン)、マイトマイシン、メクロレタミン、シクロホスファミド及びそのアナログ、クロラムブシル、エチレンイミン、メチルメラミン、アルキルスルホネート(例えば、ブスルファン)、ニトロソウレア(カルムスチン等)、ストレプトゾシン、(多くの処方に使用される)メトトレキサート、フルオロウラシル、フロクスウリジン、シタラビン、メルカプトプリン、チオグアニン、ペントスタチン、2-クロロデオキシアデノシン、シスプラチン、カーボプラチン、プロカルバジン、ヒドロキシウレア、モルホリノ ホスホロジアミデートオリゴマー又は他の抗癌性化学療法剤;シクロスポリン、タクロリムス (FK-506)、ピメクロリムス、アザチオプリン、マイコフェノレート モフェティル、mTORインヒビター又は別の免疫抑制剤; コルチソール、コルチゾン、デキサメタゾン、デキサメタゾンリン酸ナトリウム、酢酸デキサメタゾン、デキサメタゾン誘導体、ベータメタゾン、フルドロコルチソン、プレドニソン、プレドニソロン、6U-メチルプレドニソロン、トリアムシノロン(例えば、トリアムシノロン アセトニド)、又は別のステロイド剤;トラピジル (PDGFアンタゴニスト)、アンギオペプチン (成長ホルモンアンタゴニスト)、アンギオジェニン、成長因子(例えば、血管内皮細胞成長因子 (VEGF))、又は抗-成長因子抗体 (例えば、LUCENTIS(商標)で市販されているラニビズマブ)、又は別の成長因子アンタゴニストもしくはアゴニスト; ドーパミン、ブロモクリプチン メシレート、ペルゴリド メシレート、又は別のドーパミンアゴニスト; 60Co (5.3年半減期)、192Ir (73.8日)、32P (14.3日)、111In (68時間)、90Y (64時間)、99Tc (6時間)、又は別の放射線治療剤;ヨウ素-含有化合物、バリウム-含有化合物、金、タンタル、白金、タングステン又は放射線不糖化性剤として機能する別の重金属; ペプチド、タンパク質、細胞外マトリックス成分、細胞成分又は別の生物剤;カプトプリル、エナラプリル又は別のアンジオテンシン変換酵素(ACE)インヒビター;アンジオテンシン受容体遮断薬;酵素インヒビター(成長因子情報伝達キナーゼインイビター);アスコルビン酸、アルファトコフェロール、スーパーオキシド ジスマターゼ、デフェロキサミン、21-アミノステロイド (ラサロイド) 又は別のフリーラジカルスキャベンジャー、鉄キレーター又は抗酸化剤; 14C-、3H-、131I-、32P-又は36 S-放射性同位体形態又は先の任意の他の放射性同位体形態; エストロゲン (例えば、エストラジオール、エストリコール、エストロン等) 又は別の性ホルモン; AZT又は他の抗ポリメラーゼ; アシクロビル、ファムシクロビル、リマンタジン塩酸塩、ガンシクロビルナトリウム、ノルビル、クリキシバン、又は他の抗ウイルス剤;5-アミノレブリン酸、メタ-テトラヒドロキシフェニルクロリン、ヘキサデカフルオロジンク フタロシアニン、テトラメチル へマトポルフィリン、ローダミン123又は他の光線力学療法;緑膿菌(Pseudomonas aeruginosa)外毒素Aに対するIgG2 カッパ抗体であって、A431類表皮癌細胞と反応する当該抗体、サポリンに結合する、ノルアドレナリン作用性酵素ドーパミンベータ-ヒドロキシラーゼに対するモノクローナル抗体、又は治療剤を標的とする他の抗体;遺伝子療法剤;エナラプリル及び他のプロドラッグ;PROSCAR(登録商標)、HYTRIN(登録商標)又は良性前立腺過形成(BHP)を治療するための他の薬剤、マイトタン、アミノグルテチミド、ブレベルジン、アセトアミノフェン、エトダラク、トルメチン、ケトロラク、イブプロフェン及び誘導体、メフェナム酸、メクロフェナム産、ピロキシカム、テノキシカム、フェニルブタゾン、オキシフェンブタゾン、ナブメトン、オーラノフィン、オーラノチオグルコース、金ナトリウムチオマレート、これらの任意の混合物、又はこれらの任意の誘導体を含むことができる。
またコーティング材料に含まれ得る他の生物的に有用な化合物は、ホルモン、β-遮断薬、抗-アンギナ性剤、強心剤、コルチステロイド、鎮痛剤、抗炎症剤、抗不整脈剤、免疫抑制剤、抗菌剤、抗高血圧性剤、抗マラリア剤、抗新生物剤、抗原生動物剤、抗甲状腺剤、鎮痛薬、催眠薬及び神経安定薬、利尿薬、抗パーキンソン剤、胃腸薬、抗ウイルス剤、抗糖尿病剤、抗癲癇剤、抗真菌剤、ヒスタミンH-受容体アンタゴニスト、脂質調節剤、筋弛緩剤、栄養剤、例えばビタミン及びミネラル、刺激剤、核酸、ポリペプチド及びワクチンを含むが、これらに限定されない。
抗生物質は、微生物の増殖を阻害し又は死滅させる物質である。抗生物質は、合成的に又は微生物により製造することができる。抗生物質の例は、ペニシリン、テトラサイクリン、クロラムフェニコール、ミノサイクリン、ドキシサイクリン、バンコマイシン、バシトラシン、カナマイシン、ネオマイシン、ゲンタイマイシン、エリスロマイシン、ゲルダナマイシン、ゲルダナマイシンアナログ、セファロスポリン等を含む。セファロスポリンの例は、セファロチン、セファピリン、セファゾリン、セファレキシン、セフラジン、セファドロキシル、セファマンドール、セフォキシチン、セファクロール、セフロキシム、セフォニシド、セフォラニド、セフォタキシム、モキラクタム、セフチゾキシム、セフトリアゾン、及びセフォペラゾンを含む。
殺菌剤は、一般的に、非特異的形式で、例えば、その活性を阻害するか又はそれを破壊することのいずれかによって、微生物の増殖もしくは作用を抑制又は止める物質として理解される。殺菌剤の例は、銀スルファジアジン、クロルヘキシジン、グルタルアルデヒド、過酢酸、次亜塩素酸ナトリウム、フェノール、フェノール性化合物、ヨードフォア化合物、四級アンモニウム化合物及び塩素化合物を含む。
抗ウイルス剤は、ウイルスの複製を崩壊又は抑制することができる物質である。抗ウイルス剤の例は、α-メチル-1-アダマンタンメチルアミン、ヒドロキシ-エトキシメチルグアニン、アダマンタンアミン、5-ヨード-2'-デオキシウリジン、トリフルオロチミジン、インターフェロン、及びアデニンアラビノシドを含む。
酵素インヒビターは、酵素反応を阻害する物質である。酵素インヒビターの例は、塩化エドロホニウム、N-メチルフィゾスチグミン、臭化ネオスチグミン、フィゾスチグミン 硫酸塩、タクリンHCL、タクリン、1-ヒドロキシマレイン酸塩、ヨードツベルシジン、p-ブロモテトラミゾール、10-(α-ジエチルアミノプロピオニル)-フェノチアジン 塩酸塩、塩化カルミダゾリウム、ヘミコリニウム-3,3,5-ジニトロカテコール、ジアシルグリセロール キナーゼ インヒビターI、ジアシルグリセロール キナーゼ インヒビターII、3-フェニルプロパルギルアミン、N-モノメチル-L-アルギニン 酢酸塩、カルビドーパ、3-ヒドロキシベンジルヒドラジン HCl、ヒドラジン HCl、クロルグリシン HCl、デプレニル HCl L(-)、デプレニル HCl D(+)、ヒドロキシアミン HCl、イプロニアジドリン酸塩、6- MeO-テトラヒドロ-9H-ピリド-インドール、ニアラミド、パーギリン HCl、キナクリン HCl、セミカルバジド HCl、トラニルシプロミン HCl、N,N-ジエチルアミノエチル-2,2-ジ-フェニル吉草酸エステル 塩酸塩、3-イソブチル-1-メチルキサンチン、パパベリン HCl、インドメタシン、2-シクロオクチル-2-ヒドロキシエチルアミン 塩酸塩、2,3-ジクロロ-α-メチルベンジルアミン (DCMB)、8,9-ジクロロ-2,3,4,5-テトラヒドロ-1H-2-ベンザゼピン 塩酸塩、p-アミノグルテチミド、p-アミノグルテチミド 酒石酸塩 R(+)、p-アミノグルテチミド酒石酸塩 S(-)、3-ヨードチロシン、アルファ-メチルチロシン L(-)、アルファ-メチルチロシン D(-)、セタゾラミド、ジクロルフェナミド、6-ヒドロキシ-2-ベンゾチアゾールスルホンアミド及びアロプリノールを含む。
解熱剤は、熱を取り除き又は軽減することができる物質である。抗炎症剤は、炎症を弱め又は抑制することができる物質である。かかる薬剤の定は、アスピリン(サリチル酸)、インドメタシン、インドメタシンナトリウム 三水和物、サリチルアミド、ナプロキセン、コルヒチン、フェノプロフェン、スリンダク、ジフルニサル、ジクロフェナク、インドプロフェン、及びサリチルアミドナトリウムを含む。
局所麻酔薬は、局所に麻酔効果を有する物質である。かかる麻酔薬の例は、プロカイン、リドカイン、テトラカイン及びジブカインを含む。
造影剤は、所望の位置、例えば、腫瘍、in vivoで画像化することができる薬剤である。造影剤の例は、in vivoで検出可能な標識を有する物質、例えば、蛍光標識に結合した抗体、を含む。用語抗体は、完全抗体又はその断片を含む。
細胞応答調整剤は、化学走化性因子、例えば血小板-由来成長因子(PDGF)である。他の化学走化性因子は、好中球-活性化タンパク質、単球化学誘引タンパク質、マクロファージ-炎症タンパク質、SIS(低誘導性分泌(small inducible secreted))、血小板因子、血小板塩基性タンパク質、黒色腫成長刺激活性、上皮成長因子、形質転換成長因子アルファ、線維芽細胞増殖因子、血小板-由来内皮細胞成長因子、インシュリン-様成長因子、神経成長因子、骨成長/軟骨-誘導因子(アルファ及びベータ)、マトリックスメタロプロテイナーゼインヒビターを含む。他の細胞応答調整剤は、インターロイキン、インターロイキン受容体、インターロイキンインヒビター、アルファ、ベータ及びガンマを含むインターフェロン;エリスロポイエチン、顆粒球コロニー刺激因子、マクロファージコロニー刺激因子及び顆粒球-マクロファージコロニー刺激因子を含む、造血因子;アルファ及びベータを含む腫瘍壊死因子;ベータ-1、ベータ-2、ベータ-3、インヒビン、アクチビンを含む形質転換成長因子(ベータ)、これらのタンパク質の任意の産生をコードするDNA、アンチセンス分子、アンドロゲン受容体遮断薬及びスタチン剤である。
1つの実施態様では、活性剤は、微粒子中に存在し得る。1つの実施態様では、微粒子は、基材の表面上に分散することができる。
活性剤に起因するコーティングの重量は、所与の適用において所定の活性剤について望ましい任意の範囲でよい。ある実施態様では、活性剤に起因するコーティングの重量は、約1ミリグラム〜約10ミリグラムの活性剤/用具の有効表面積 cm2の範囲にある。「有効表面積」とは、組成物それ自体でコートされることになる表面を意味する。平らな、非多孔性の表面については、例えば、これは、一般的に、巨視的表面積そのものであろうが、一方、相当に多孔性又は回旋状の表面(例えば、波形、ひだ状、又は繊維状)では、有効表面積は、対応する巨視的表面積よりも著しく大きいことがある。1つの実施態様では、活性剤に起因するコーティングの重量は、約0.01 mg〜約0.5 mgの活性剤/用具の全表面積 cm2の範囲にある。1つの実施態様では、活性剤に起因するコーティングの重量は、約0.01 mg超である。
ある実施態様では、1超の活性剤は、コーティング中で使用することができる。具体的には、共-薬剤又は共-薬物が使用できる。共-薬剤又は共-薬物は、第一の薬剤又は薬物とは異なって作用することができる。共-薬剤又は共-薬物は、第一の薬剤又は薬物とは異なった溶出プロファイルを有することができる。
ある実施態様では、活性剤は、親水性でよい。1つの実施態様では、活性剤は、1500ダルトン未満の分子量を有することができ、25℃で10 mg/ml超の水溶性を有することができる。ある実施態様では、活性剤は、疎水性でよい。1つの実施態様では、活性剤は、25℃で10 mg/ml未満の水溶性を有することができる。
生分解性組成物は、1以上の活性剤とポリマーとを混合することにより、製剤化することができる。生物活性剤は、液体、細粉砕された固体、又は任意の他の好適な物理的形状として存在し得る。典型的には、しかし、場合により、生分解性組成物は、1以上の添加剤、例えば、希釈剤、担体、賦形剤、安定剤等を含むだろう。
特定の生物活性剤又は生物活性剤の組み合わせは、1以上の以下の因子によって選択することができる:用具(例えば、冠状ステント、整形外科用用具、固定要素)の適用、ポリマー原料からなる用具の量(例えば、ポリマー原料の用具全体を構成する量に対して、コーティングとしてのポリマー原料を用具基材上に提供する量)、治療されるべき病状、治療の予想期間、移植部位の特徴、利用される生物活性剤の数及び種類等。
生分解性組成物中の生物活性剤の濃度は、最終生分解性組成物の重量基準で、約0.01重量%〜約75重量%、又は約0.01重量%〜約50重量%、又は約1重量%〜約35重量%、又は約1重量%〜約20重量%、又は約1重量%〜約10重量%の範囲でよい。ある局面では、生物活性剤は、生分解性組成物中に、約75重量%未満、又は約50重量%未満、又は約35重量%未満、又は約25重量%未満、又は約10重量%未満の範囲の量で存在する。生分解性組成物中の生物活性剤の量は、約1 μg〜約10 mg、又は約100 μg〜約1000 μg、又は約300 μg〜約600 μgの範囲でよい。
ある局面では、生物活性剤は、コーティング組成物用の選択された溶媒中で安定でなければならない。例えば、ある有機溶媒は、特に、生物活性剤が長期間、溶媒中に存在するときには、生物活性剤の安定性に逆に影響する可能性がある。ある実施態様では、生物活性剤、例えばラパマイシンは、水溶液中に存在するときには、長期間に渡って、逆に影響する(例えば、分解する)可能性がある。従って、コーティング組成物用の溶媒系の選択は、医療用具から送達されるべき生物活性剤をある程度考慮して、決定することができる。
1つの例示的実施態様では、比較的低分子の生物活性剤(例えば、多くの抗菌剤、抗ウイルス剤等)がPEGT/PBTポリマー原料中に含まれるときには、コポリマーのポリエチレングリコール成分は、好ましくは、約200〜約10,000、又は約300〜約4,000の範囲の分子量を有する。また、ポリエチレングリコールテレフタレートは、好ましくは、コポリマー中に、コポリマーの重量の約30重量%〜約80重量%の範囲、又は、コポリマーの重量の約50重量%〜約60重量%の範囲の量で存在する。これらの特定の実施態様では、ポリブチレンテレフタレートは、コポリマー約20重量%〜約70重量%の範囲、又は、コポリマーの約40重量%〜約50重量%の範囲の量で存在する。
ある局面では、1以上の生分解性組成物のポリマーに1以上の添加剤を提供することが望ましいことがある。かかる添加剤は、生物活性剤が生分解性組成物を含むポリマー中に含まれるときに特に望ましい。添加剤は、用具からの生物活性剤の放出に影響を与えるように含むことができる。これらの局面に従う好適な添加剤は、疎水性抗酸化剤、疎水性分子、及び親水性抗酸化剤及び賦形剤を含むが、これらに限定されない。代替的に、添加剤は、用具が一旦移植されると、用具の画像化に影響を与えるように含むことができる。添加剤の例を、より詳細に説明する。しかしながら、かかる添加剤は任意であると理解される;ある局面では、第一ポリマー及び第二ポリマーの選択、及び用具表面上でのコート層の相対的配置は、添加剤を使用することなく、様々な生物活性剤放出速度を達成することができるので、本発明のコーティング組成物は、生物活性剤の放出に影響を与える任意の添加剤を必要としない。従って、ある実施態様では、利用される任意の添加剤は、生物活性剤放出速度に加えて、コーティングの他の特徴に有用である。
ある実施態様では、生分解性組成物を含む1以上のポリマーは、場合により、少なくとも1つの疎水性抗酸化剤を含むことができる。例えば、ポリエーテルエステル原料(例えば、PEGT/PBT)が疎水性の低分子薬物(例えば、ステロイドホルモン)を含むとき、ポリマー原料は少なくとも1つの疎水性抗酸化剤を含むことができる。使用することができる疎水性抗酸化剤の例は、ブチル化ヒドロキシトルエン (BHT) トコフェロール (例えば、α-トコフェロール、β-トコフェロール、γ-トコフェロール、δ-トコフェロール、ε-トコフェロール、ゼータ1-トコフェロール、ゼータ2-トコフェロール、及びエタ-トコフェロール)、及びアスコルビン酸 6-パルミチン酸塩を含むが、これらに限定されない。かかる疎水性抗酸化剤は、ポリエーテルエステルコポリマー原料の分解を遅らせることができ、ポリマーに含まれる生物活性剤の放出を遅らせることができる。従って、疎水性又は脂肪親和性の抗酸化剤の使用は、ポリマーから速く放出される傾向にある薬物、例えば、1500未満の分子量を有する低分子薬物分子を含む生分解性組成物の形成に特に望ましいことがある(言いかえれば、疎水性又は脂肪親和性の抗酸化剤の使用は、必要ならば、生分解性組成物からの薬物の放出を遅らせることができる)。ある実施態様では、抗酸化剤は、薬物安定性も同様に改善することができる。例えば、ラパマイシンが期待よりも不安定であり得るので、薬物溶出ステント(「DES」)中のラパマイシンの含有は、問題となることがある。従って、疎水性抗酸化剤の含有は、ある実施態様では、生物活性剤の送達用具におけるラパマイシンの安定性を改善する。
疎水性抗酸化剤(複数)は、ポリマー中に、ポリマーの総重量の約0.01重量%〜約10重量%の範囲、又はポリマーの総重量の約0.5重量%〜約2重量%の範囲の量で存在し得る。
ある実施態様では、生分解性組成物を含む1以上のポリマーは、場合により、1以上の疎水性分子を含むことができる。例えば、ポリエーテルエステル原料が親水性の低分子薬物(例えば、アミノグリコシド、例えばゲンタマイシン)を含むときには、生分解性組成物はまた、本明細書に記載の疎水性抗酸化剤に加えて又はその代りに、少なくとも1つの疎水性分子、例えば、コレステロール、エルゴステロール、リトコール酸、コリン酸、ジノステロール、べツリン、及び/又はオレアノール酸を含むことができる。1以上の疎水性分子は、ポリエーテルエステルコポリマーからの生物活性剤の放出速度を遅らせるように働くことができる。かかる疎水性分子は、生分解性組成物への水の浸透を抑制することができるが、生分解性組成物の分解性を解決しない。加えて、かかる分子は、150℃〜200℃以上の範囲の融点を有する。そのため、これらの分子の低パーセンテージは、ポリマーのTgを上げる。これは、放出される生物活性剤のマトリックス拡散係数を減少させる。従って、かかる疎水性分子は、生分解性組成物からの生物活性剤のより持続的放出を提供することができる。
疎水性分子(複数)は、ポリマーの総重量基準で、ポリマー中に、約0.1重量%〜約20重量%、又は約1重量%〜約5重量%の範囲で存在し得る。
ポリエーテルエステルコポリマーがタンパク質を含むとき、コポリマーも、場合により親水性抗酸化剤を含むことができる。親水性抗酸化剤の例は、下記構造式XXXIII:
[式中、
Y及びZの各々は、0又は1であり、Y及びZの少なくとも1つは1であり;
X1及びX2の各々は、下記式XXXIV:
Y及びZの各々は、0又は1であり、Y及びZの少なくとも1つは1であり;
X1及びX2の各々は、下記式XXXIV:
(式中、各R1は、水素原子又は1〜4の炭素原子を有するアルキル基、好ましくはメチルであり、各R1は、同一又は異なる;R2は、水素原子又は1〜4の炭素原子を有するアルキル基、好ましくはメチルであり;Qは、NH又は酸素原子である。)
の化合物からなる群より独立に選ばれ;
X1及びX2の各々は、同一又は異なることがあり;
Aは、
の化合物からなる群より独立に選ばれ;
X1及びX2の各々は、同一又は異なることがあり;
Aは、
(式中、R3は、1又は2の炭素原子を有するアルキル、好ましくは2の炭素原子を有するアルキルであり;nは1〜100、好ましくは4〜22であり; R4は、1〜4の炭素原子を有するアルキル、好ましくは1又は2の炭素原子を有するアルキルである。)である。]
を有するものを含むが、これらに限定されない。
を有するものを含むが、これらに限定されない。
1つの実施態様において、Y及びZの1つは、1であり、Y及びZの他の1つは、0である。他の実施態様において、Y及びZの各々は、1である。
更に別の実施態様では、R3はエチルである。
更なる実施態様では、R4はメチル又はエチルである。
更に別の実施態様では、R1はメチルであり、R2はメチルであり、R3はエチルであり、R4はメチルであり、Y及びZの1つは1であり、Y及びZの他の1つは0であり、QはNHであり、nは21又は22であり、抗酸化剤は、下記構造式XXXVI:
を有する。
別の実施態様において、親水性抗酸化剤は、下記構造式:
[式中、
Y及びZの各々は、0又は1であり、Y及びZの少なくとも1つは1であり;
X3及びX4の各々は、
Y及びZの各々は、0又は1であり、Y及びZの少なくとも1つは1であり;
X3及びX4の各々は、
(式中、各R1は、水素原子又は1〜4の炭素原子を有するアルキル基であり;R2は、1〜4の炭素原子を有するアルキル基であり;xは0又は1であり;Qは、NH又は酸素原子であり;各R1は同一又は異なる。)
であり;
X1及びX2の各々は、同一又は異なり;
Aは、
であり;
X1及びX2の各々は、同一又は異なり;
Aは、
(式中、R3は、1又は2の炭素原子を有するアルキル、好ましくは2の炭素原子を有するアルキルであり;nは1〜100、好ましくは4〜22であり; R4は、1〜4の炭素原子を有するアルキル、好ましくは1又は2の炭素原子を有するアルキルである。)である。]
を有する。
を有する。
1つの実施態様では、R1部分の少なくとも1つ、好ましくは、2つは、tert-ブチル部分である。R1部分の2つがtert-ブチル部分であるとき、各tert-ブチル部分は、好ましくは、-OH基に隣接する。
親水性抗酸化剤(複数)は、ポリマー中に、ポリマーの総重量基準で、約0.1重量%〜約10重量%の範囲、又は約1重量%〜約5重量%の範囲の量で存在し得る。
本明細書で考察したように、生分解性組成物を含む1以上のポリマーは、疎水性抗酸化剤、疎水性分子及び/又は親水性抗酸化剤を、本明細書に記載の量で含むことができる。使用される抗酸化剤又は疎水性分子の種類及び正確な量は、生物活性剤(タンパク質)の分子量、及びポリマー自体の性質に依拠し得る。ポリマーが大きなポリペプチド又はタンパク質(例えば、インシュリン)を含む場合には、マトリックスはまた、場合により、親水性抗酸化剤、例えば本明細書に記載のものを本明細書に記載の量で含むことができ、約1,000〜約4,000の範囲の分子量を有するポリエチレングリコールをコポリマーの総重量基準で約1重量%〜約10重量%の範囲の量で含むことができる。
ある実施態様では、生分解性組成物を含む1以上のポリマーは、画像化材料を更に含むことができる。例えば、材料は、用具を一旦移植した後は用具の医療画像を補助するように、生分解性組成物中に含むことができる。医療画像材料はよく知られている。画像化材料の例は、常磁性体、例えば、超微粒子酸化鉄、Gd又はMn、放射性同位元素、及び非-毒性の放射性-不透明マーカー(例えば、ケージ状硫酸バリウム及び三酸化ビスマス)を含む。これは、体内に移植される(治療部位に据え付けられる)か、又は体の一部を介して移動する(すなわち、用具の移植中に)医療用具の検出に有用であり得る。常磁性共鳴画像化、超音波画像化、又は他の好適な検出法は、かかるコート医療用具を検出することができる。別の実施態様では、気相化学物質を含む微粒子は、超音波画像化のために使用することができる。有用な気相化学物質は、米国特許第5,558,854号明細書 (1996年9月24日に発行)に記載されているパーフルオロハイドロカーボン、例えば、パーフルオロペンタン及びパーフルオロへキサンを含む;超音波画像化のために有用な他の気相化学物質は、米国特許第6,261,537号明細書 (2001年7月17日に発行) に見出される。
ある局面では、生分解性組成物を含む1以上のポリマーは、賦形剤を含むことができる。具体的な賦形剤は、その融点、選択された溶媒(例えば、ポリマー及び/又は生物活性剤を溶解する溶媒)中での溶解性、及び得られた組成物の特徴に基づいて選択することができる。賦形剤は、含まれる特定のポリマーの、数パーセント、約5%、10%、15%、20%、25%、30%、40%、50%、又はより高いパーセンテージを含むことができる。
緩衝剤、酸、及び塩基は、pHを調整するために、ポリマー又はポリマー類(複数)に組み込むことができる。ポリマーマトリックスから放出される生物活性剤の拡散距離を延ばすための薬剤も含めることができる。賦形剤の例は、塩、PEG、又は親水性ポリマー、及び酸性化合物を含む。従って、生物活性剤の放出を制御し、生分解性組成物の分解に影響を与え、及び/又は既に移植された用具の画像化に影響を与えるのに役立つ添加剤は、生分解性組成物を含む1以上のポリマー中に含むことができる。
生物活性剤の放出は、生分解性組成物を含むポリマーの修飾によって影響を受け得る。生物活性剤の放出に影響を与える別の方法は、用具の配置を変更することを含むことができる。
場合により、コポリマー自体は、生物活性剤の分解速度及び放出速度に影響を与えるように修飾することができる。これらの局面は、PEGT/PBTを含む実施態様において特に有用である。例えば、コポリマーは、特定の疎水性を有する成分(モノマー単位)を、異なった疎水性を有する成分(モノマー単位)と置換することにより、修飾することができる。
ある実施態様では、用具の配置は、生物活性剤の放出を制御するように動かすことができる。例えば、用具の表面及び/又はサイズは、移植部位に提供される生物活性剤(複数)の投薬量を制御するように動かすことができる。
コポリマーの組成及び/又は用具の配置は、添加剤がコポリマー中に含まれるか否かに関わらず、変更することができる。
好ましくは、生分解性組成物は、選択された医療用具、例えばステントの表面に適用される。ステント自体は、異なった材料から構成される。生分解性組成物コーティングは、好ましくはポリエーテルエステルコポリマー、例えばPEGT/PBTである第一ポリマー、及び本明細書に記載されているように選択される第二ポリマーを含むことができる。好適な第一生分解性ポリマーである、エステル結合を含む他のポリマーは、本明細書に記載されている。
好ましい局面では、本発明は、生物活性剤を含む生分解性コーティングを医療用具に提供するための組成物及び方法を提供する。本発明は、様々な生体材料表面を有する医療用具と関連して利用することができる。生体材料の例は、金属及びセラミックを含む。金属は、チタン、ニチノール、ステンレス鋼、タンタル、及びコバルトクロムを含むが、これらに限定されない。第二のクラスの金属は、貴金属、例えば、金、銀、銅及びプラチナイリジウムを含む。金属合金も、生体材料に好適である。セラミックは、窒化ケイ素、炭化ケイ素、ジルコニア及びアルミナ、及びガラス、シリカ及びサファイアを含むが、これらに限定されない。
他の生体材料の例は、付加又は縮合重合のいずれかから得られる、オリゴマー、ホモポリマー、及びコポリマーを含む、合成ポリマーから形成されるものを含む。好適な付加重合体の例は、アクリル、例えば、メチルアクリル酸、メチルメタクリル酸、ヒドロキシエチルメタクリル酸、ヒドロキシエチルアクリル酸、アクリル酸、メタクリル酸、グリセリルアクリル酸、グリセリルメタクリル酸、メタクリルアミド及びアクリルアミドから重合されるもの;ビニル、例えば、エチレン、プロピレン、塩化ビニル、酢酸ビニル、ビニルピロリドン及びビニリデンジフルオリドを含むが、これらに限定されない。縮合重合体の例は、ナイロン、例えば、ポリカプロラクタム、ポリラウリルラクタム、ポリヘキサメチレン アジパミド、及びポリヘキサメチレン ドデカンジアミド、並びにポリウレタン、ポリカーボネート、ポリアミド、ポリスルホン、ポリ(エチレン テレフタレート)、ポリ乳酸、ポリグリコール酸、ポリジメチルシロキサン及びポリエーテルケトンを含むが、これらに限定されない。
ヒト組織、例えば、骨、軟骨、皮膚及び歯;及び他の有機材料、例えば、木材、セルロース、圧縮炭素及びゴムを含む、ある天然材料もまた、好適な生体材料である。
セラミック及び金属の組み合わせは、生体材料の別のクラスである。生体材料の別のクラスは、本来、繊維状又は多孔質である。かかる生体材料の表面は、必要ならば、生体材料の表面特性を変更するために、(例えば、パリレンコーティング組成物により)予備処理することができる。
本発明のコーティングは、表面上に好適な耐久性かつ接着性コーティングを提供するために十分な方法で、表面に適用される。典型的には、コーティングは、表面に化学的に結合しないような方法で提供される。むしろ、コーティングは、用具表面をカプセル化するものと考えることができる。コーティングと表面との関係の性質を考えると、コーティングが、任意の表面材料に実質的に適用して、好適な耐久性かつ接着性コーティングを提供することができる、ことは容易に明らかであろう。更に、ある実施態様では、好適な表面予備処理を利用して、コーティングと用具表との関係を強化することができる。例えば、用具基材表面は、粗くしてもよく、又は当該分野でよく知られている方法(例えば、磨耗又は微-磨耗)を利用することにより表面テクスチャとしてもよい。
ある実施態様では、生分解性組成物は、本明細書の「実施例」に記載されている、移植可能用具の表面上にスプレイコートする。他の実施態様では、ステントは、生分解性組成物溶液中に浸漬することができる。代替的には、生分解性組成物は、チューブの形態で押し出され、後でステンレス鋼又はニチノールのチューブ上に同時に引き込む。金属チューブ上に生分解性組成物の2つのチューブの同時に引き込むことにより、1つは、金属チューブの外側辺りに配置され、もう1つは、金属チューブ内に配置され、多-層壁を有するチューブを形成することができる。スピン及び支柱の所定のパターンを特定するための、その後のチューブ壁の穿孔は、ステントをつくるために、チューブに所望の柔軟性及び拡張性を与えることができる。
本発明の生分解性組成物は、用具表面の任意の所望の部分に適用することができる。例えば、ある実施態様では、生分解性組成物は、用具表面全体に提供することができる。他の実施態様では、用具の一部分のみが、生分解性組成物コーティングを含むことができる。生分解性組成物コーティングを有する用具の当該部分は、用具の適用、治療部位に適用されるべき生物活性剤の量、送達されるべき活性剤の数及び種類の因子、並びに類似の因子に基づいて、選択することができる。
更に、生分解性組成物の各コート層は、任意の数の適用において用具表面上に適用することができる。適用の数は、各々の好適な厚さのコート層、及び、必要ならば、生分解性組成物の多数のコート層の所望の総数を提供するように選択することができる。かかる実施態様では、コーティグの各々の層の組成は、必要に応じて、同一でも又は異なってもよい。典型的には、最外コート層の厚さは、約1 μm〜約50 μmの範囲、又は約1 μm〜約100 μmの範囲である。最外コート層の厚さは、最外コート層の化学組成等の因子(選択されたポリマー、生物活性剤の含有等)に基づいて選択することができる。ある実施態様では、適用の数は、ポリマーコーティングに所望の全体的厚さを提供するように制御することができる。一般的に、コーティングの厚さは、移植用の用具のプロファイル及び患者内の使用を顕著に増加させないように選択される。典型的には、生分解性組成物コーティングの全体的厚さは、約1 μm〜約100 μmのオーダーである。
生分解性組成物は、病状の予防又は治療のために哺乳動物に一次的又は永久に導入される任意の用具上に多層コーティングとして適用することができる。これらの用具は、臓器、組織、又は臓器の管腔、例えば、動脈、静脈、脳室又は心臓上半部内に置くように、皮下的に、経皮的に又は外科的に導入される任意のものを含む。
本発明の生分解性組成物は、様々な移植可能な用具の表面をコートするために使用することができる。例えば:薬物-送達血管ステント(例えば、典型的にはニチノール製の自己-拡張型ステント、典型的にはステンレス鋼製のバルーン-拡張型ステント);他の血管用具(例えば、グラフト、カテーテル、バルブ、人工心臓、心臓補助用具);移植可能な除細動器;血液酸素付加装置(例えば、チューブ、膜);外科用具(例えば、縫合糸、留め金、接合用具、脊椎板、骨ピン、縫合アンカー、止血バリア、クランプ、スクリュー、プレート、クリップ、血管インプラント、組織接着剤及びシーラント、組織スキャフォールド);膜;細胞培養用具;クロマトグラフィー支持材料;バイオセンサー;水頭用シャント;損傷管理用具;内視鏡具;感染制御用具;整形外科用具(例えば、ジョイントプラント、骨折修復器);歯科用具(例えば、歯科インプラント、破砕修復用具)、泌尿器用具(例えば、ぺニス、括約筋、尿道口、膀胱及び腎臓用具、及びカテーテル);結腸瘻バッグ付着用具;眼科用具;緑内障排液シャント;人工器官(例えば、乳房);眼内レンズ;呼吸器、末梢心血管、脊髄、神経、歯、耳/鼻/喉(例えば、耳排液チューブ);腎臓用具;及び透析(例えば、チューブ、膜、グラフト)。
有用な用具の例は、泌尿カテーテル(例えば、抗菌剤例えばバンコマイシン又はノルフロキサチンで表面-コート)、静脈カテーテル(例えば、抗血栓剤(例えば、ヘパリン、ヒルジン、クーマディン)で処理)、小サイズのグラフト、血管グラフト、人工肺カテーテル、心房中隔欠損閉塞症、心律動管理のための電気-刺激リード(例えば、ペーサーリード)、グルコースセンサー(長期及び短期)、分解性冠状ステント(例えば、分解性、非分解性、末梢性)、血圧及びステントグラフトカテーテル、バースコントロール用具、良性前立腺及び前立腺癌インプラント、骨修復/拡張用具、乳房インプラント、軟骨修復用具、歯科用インプラント、インプラントされた薬物注入チューブ、眼内薬物送達用具、神経再生導管、癌研究用インプラント、電気刺激リード、疼痛管理インプラント、脊髄/整形外科用修復用具、損傷包帯、塞栓症保護フィルター、腹部大動脈瘤グラフト、心臓弁(例えば、機械性、ポリマー性、組織性、経皮的、カーボン性、ソーイングカフ性)、弁環状形成用具、僧帽弁修復用具、血管インターベンション用具、左心室補助具、神経動脈瘤処理コイル、神経のカテーテル、左心房附属器フィルター、血液透析用具、カテーテルカフ、吻合封鎖、血管アクセスカテーテル、心臓センサー、子宮出血パッチ、泌尿カテーテル/ステント/インプラント、in vitro診断薬、動脈瘤排除用具、及び神経パッチを含む。
他の好適な用具の例は、大静脈フィルター、尿透析器、内視鏡外科組織抽出器、アテローム切除カテーテル、血栓抽出カテーテル、経皮経管的血管形成カテーテル、PTCAカテーテル、針金(血管及び非血管)、冠状ガイドワイヤー、薬物注入カテーテル、食道ステント、循環支持系、血管造影カテーテル、移行性鞘及び透析器、冠状及び末梢ガイドワイヤー、血液透析カテーテル、神経血管バルーンカテーテル、中耳腔換気用口チューブ、脳脊髄液シャント、除細動器リード、経皮的封鎖用具、導尿用チューブ、胸腔吸引排液カテーテル、電気生理学カテーテル、卒中治療カテーテル、膿瘍排液カテーテル、胆管排液、透析カテーテル、中心動脈アクセスカテーテル、及び親からの供給カテーテルを含むが、これらに限定されない。
本発明に好適な医療用具の例は、カテーテル、移植可能な血管アクセスポート、血液保存バッグ、血管ステント、血液チューブ、動脈カテーテル、血管グラフト、大動脈内バルーンパンピング、心血管縫合糸、総人口心臓及び心室補助ポンプ、体外用具、例えば、血液酸素付加装置、血液フィルター、血液透析ユニット、血液潅流ユニット、血漿交換ユニット、ハイブリッド人工臓器、例えば、膵臓又は肝臓、及び人工肺、並びに塞栓症を捕らえるための血管中での配置用のフィルター(「末端保護用具」としても知られている)を含むが、これらに限定されない。
ある局面では、ポリマー組成物は、眼科用具に関連して用いることができる。これらの局面に従う好適な眼科用具は、眼の任意の所望の部位に生物活性剤を提供することができる。ある局面では、用具は、眼の前部(レンズの前)及び/又は眼の後部(レンズの後ろ)に生物活性剤を送達するために利用することができる。好適な眼科用具はまた、必要ならば、眼の近傍の組織に生物活性剤を提供するために利用することができる。
ある局面では、ポリマー組成物は、眼の内部又は外部に配置するために構成される眼科用具と関連して利用することができる。好適な外部用具は、生物活性剤の局所投与のために構成することができる。かかる外部用具は、眼の外面、例えば、角膜(例えば、コンタクトレンズ)又は眼球結膜上に配置することができる。ある実施態様では、好適な外部用具は、眼の外面近傍に配置することができる。
眼の内部での配置のために構成される用具は、眼の所望の任意の位置内に置くことができる。ある実施態様では、眼科用具は、眼部、例えばガラス質での配置のために構成することができる。眼内用具の例は、米国特許第6,719,750 B2号明細書 ("Devices for Intraocular Drug Delivery," Varner et al.) 及び同第5,466,233号明細書 ("Tack for Intraocular Drug Delivery and Method for Inserting and Removing Same," Weiner et al.); 米国出願公開第2005/0019371 A1号("Controlled Release Bioactive Agent Delivery Device," Anderson et al.)、同第2004/0133155 A1号 ("Devices for Intraocular Drug Delivery," Varner et al.)、同第2005/0059956 A1号 ("Devices for Intraocular Drug Delivery," Varner et al.)、及び同第2003/0014036 A1号 ("Reservoir Device for Intraocular Drug Delivery," Varner et al.); 及び米国出願第11/204,195号 (2005年8月15日出願, Anderson et al.)、同第11/204,271号 (2005年8月15日出願, Anderson et al.)、同第11/203,981号 (2005年8月15日出願, Anderson et al.)、同第11/203,879号 (2005年8月15日出願, Anderson et al.)、同第11/203,931号 (2005年8月15日出願, Anderson et al.)、同第11/225,301号 (2005年9月12日出願, Anderson et al.); 並びに関連出願に記載されているものを含むが、これらに限定されない。
ある実施態様では、眼科用具は、眼内の網膜下部位に配置するために構成することができる。網膜下適用のための眼科用具の例は、米国特許公開第2005/0143363号("Method for Subretinal Administration of Therapeutics Including Steroids; Method for Localizing Pharmacodynamic Action at the Choroid and the Retina; and Related Methods for Treatment and/or Prevention of Retinal Diseases," de Juan et al.); 米国出願第11/175,850号 ("Methods and Devices for the Treatment of Ocular Conditions," de Juan et al.);及び関連出願に記載されているものを含むが、これらに限定されない。
好適な眼科用具は、眼の任意の所望の組織内に配置のために構成することができる。例えば、眼科用具、例えば、強膜外的であるが結膜下に配置される用具、例えば、緑内障ドレイン用具等は、眼の結膜下部位での配置のために構成することができる。
組成物は、特に、水性系、例えば体液に接触することになる用具に特に有用である。かかる用具は、長期かつ制御された方法で生物活性剤を放出するように適合されるコーティング組成物でコートされる。当該コーティングは、一般的に、用具表面とその水性環境との最初の接触で開始する。生物活性剤の組み合わせの局所的送達は、任意の数の医療用具を利用する様々な条件を処理し、又は用具の機能及び/又は寿命を高めるために利用することができる、ことに注目するのは重要である。本質的に、任意の種類の医療用具は、用具又は生物活性剤の単一使用の使用を超える処理を高める1以上の生物活性剤で、ある様式でコートすることができる。
1つの好ましい実施態様では、コーティング組成物はまた、ステント、例えば、ニチノールから典型的に調製される自己-拡張ステント、又はステンレス鋼から典型的に調製されるバルーン-拡張可能なステントのいずれかをコートするために使用することができる。他のステント材料、例えば、コバルトクロム合金も同様に、コーティング組成物によりコートすることができる。
血管ステント、例えば、自己-拡張ステント及びバルーン拡張可能なステントを含む用具は、特に好適である。本発明で有用な自己-拡張ステントの例は、Wallstenに発行されている米国特許第4,655,771号明細書及び同第4,954,126号明細書、及びWallsten et al.に発行されている米国特許第5,061,275号明細書に説明されている。好適なバルーン-拡張可能なステントの例は、Palmazに発行されている米国特許第4,733,665号明細書、Gianturcoに発行されている米国特許第4,800,882号明細書、及びWiktorに発行されている米国特許第4,886,062号明細書に見られる。
場合により、生体材料の表面は、生体材料の表面特性を変えるために、(例えば、パリレン(商標)コーティング組成物で)予備処理することができる。パリレン(商標)は、パラ-クロロ-キシレンの低分子量ダイマーのポリマー体である。Specialty Coating Systems (Indianapolis) により供給されるパリレン(商標)コーティングは、様々な医療用具の部分上に連続コーティングとして蒸着して、均等に分散された透明コーティングを提供することができる。この蒸着は、蒸着重合と称される方法により達成される。そこでは、ダイマーパリレン(商標)組成物は、150℃で減圧下で蒸発し、680℃で熱分解して、反応性モノマーを形成し、次いで、25℃でコートされる成分を含むチェンバー内にポンプで送られる。低チェンバー温度では、モノマー性キシレンは、フリー-ラジカル方法により直ちに重合する場合には、当該部分上に蒸着される。
キシレンモンマーの蒸着は、中程度の真空(0.1 torr) のみで起こり、視野方向ではない。すなわち、モノマーは、コートされる部分の全ての側を囲む機会を有し、クレビス又は管の中を通り、鋭角な点及び縁をコーティングし、いわゆる「絶縁保護」コーティングをつくる。他の例示的な処理材料は、シラン、シロキサン、ポリウレタン、ポリブタジエン及びポリカルボジイミドを含む。
好ましい局面では、生分解性コーティングを含む多層は、連続的に、そして中間的な養生又は積層ステップなしに適用される。典型的には、個々のポリマー層は、適用の間に乾燥されるにすぎない。好ましくは、コート層は、任意の加熱、加圧、又は生物活性剤及び/又はコーティングのポリマー成分の安定性に影響を与えることができた他の処理を必要とすることなく、用具表面に及び互いに接着する。驚くべきことに、コート層は、かかる処理を必要とすることなく、用具表面上に実質的に耐久性のあるコーティングを提供する。
使用において、移植可能な用具は、患者の所望の移植部位に置かれる。体液と接触する際に、体液は、生分解性組成物の少なくとも1部分において最初に透過し、生分解性組成物からの生物活性剤の溶解及び分散を可能にする。生分解性組成物は、徐々に分解し(通常、主に加水分解による)、持続的期間又は長期間、分散された生物活性剤の放出を伴う。このことは、生物活性剤の治療上有効量の長期送達をもたらすことができる。
好ましい局面では、生分解性組成物は、表面腐食性及びバルク腐食性生分解性材料であるポリマーを含む。表面腐食性材料は、生理的環境、例えば体液と直接接触する材料の表面で主にバルク質量が喪失する材料である。バルク腐食性材料は、材料の大部分に渡ってバルク質量が喪失する材料である;言いかえれば、バルク質量の喪失は、生理的環境と直接接触する材料の表面において主に起こる質量喪失に限定されない。好ましい局面では、生分解性組成物は、生分解性ポリマーのみからなる。言いかえれば、生分解性組成物の成分は、長期間に渡って体内で破壊されるように選択される。
典型的には、現在の薬物-ステントは、4週間以上の期間に渡って、抗-再狭窄剤を放出する。好ましい局面では、本発明の生分解性組成物は、生物活性剤の制御された放出を提供することができ、それによって、意図した利益を提供するために十分な時間、生物活性剤の治療上有効量を提供する。制御された放出は、生物活性剤の初期放出及び次の徐放を含む。
好ましい局面では、本発明の生分解性組成物は、優れた均一性及び使用中の耐久性を証明するコーティングを提供する。コーティング均一性及び耐久性は、以下のように観察し、評価することができる。
コーティング均一性の1つの局面は、コーティングの表面性に関する。本発明のコーティングは、表面性の詳細な画像化を可能にする低ビーム電圧 (1 kV) で、電界放出走査電子顕微鏡 (SEM) を用いて、均一性及び欠陥について試験した。表面欠陥の例は、コーティングの層割れ又はクラッキングの部位、1以上の層を欠く表面積等を含むことができる。コーティング品質の全体的調査は、低倍率で行われ、対象の特性が特定されるときにより高い倍率の画像がとれる。全体的調査から、コーティング中の欠陥の相対的な量及び種類の定量的ランキングをつくることができる。
コーティング均一性の別の局面は、生分解性組成物に生物活性剤を混合するという均一性に関する。コーティングのこの局面は、共焦点走査ラマン顕微鏡を用いて画像化することができる。レーザー光(532 nm波長)を、100x顕微鏡対物レンズ(開口数0.95)によりコーティング上に焦点を合わせ、圧電変換器従動プラターを用いて、コーティングを3方向にスキャンする。コーティングからの拡散光を顕微鏡により集め、フィルターを通し、スペクトログラフを用いてそのスペクトルに分割し、CCD検出器で検出した。従って、画像中の各位置(ピクセル)について、ラマンスペクトルを測定する。純粋な生物活性剤及び純粋なポリマーの対照スペクトルは、拡張された制約付き最小二乗法分析に取り込んで、生物活性剤のみ及びポリマーのみの別個の画像をつくる。これらの画像は、ポリマー内の生物活性剤の分布の合成カラーコード画像(composite color coded image)をつくるように重複する。
コーティング内の活性化剤分布の均一性は、生物活性剤の放出プロファイルに影響を与えることができる。生物活性剤のほとんどの割合がコーティングの特定の部分に濃縮される場合には、生物活性剤の放出は、制御された放出速度論を示す可能性はほとんどない。例えば、生物活性剤のほとんどの割合がコーティング層表面に濃縮される場合には、生物活性剤が表面から大きな拡散距離を有さないので、生物活性剤は、コート層から速く放出される可能性がより高い。対照的に、用具表面に濃縮される生物活性剤は、移動するより大きな拡散距離を有することがあり、よって、生物活性剤の放出は、模範的なコーティングの前に比べて遅れることがある。更に、ポリマー分解が生物活性剤濃度の領域に近づくにつれて、コーティング内の生物活性剤の濃度は、放出において1以上の急激な増加を含む放出プロファイルをもたらすことができる。
本明細書で用いる用語「耐久性」は、典型的に使用中に出くわす力を受けるときに、用具表面に接着するコーティングの能力(例えば、通常の力、剪断力等)を称する。より耐久性のコーティングは、磨耗又は圧縮により基材から容易に離れにくい。コーティングの耐久性は、使用条件をまねる条件に用具を供することにより評価することができる。コートされたステントの使用をまねるために、コートされたステントは、試料血管形成バルーン上に配置される。次いで、ステントを、実験室試験捲縮機Machine Solutions, Brooklyn, NYから入手可能)を用いてバルーン上に捲縮する。ステント及びバルーンを次いで、37℃の温度を有する水浴中に置く。5分間浸漬した後、バルーンを、5大気圧(3800 torr)で空気を用いて拡張する。次いで、バルーンの空気を抜き、ステントを除く。ステントは、次いで、光学及び走査電子顕微鏡を用いて検査して、クラッキング及び/又は層割れによって起こるコーティング損傷の量を決定する。本明細書では、この耐久性試験は、「機械的試験」と称される。広範囲の損傷を有するコーティングは、商業的な医療用具用には許容されないと考えられる。試験は、接触角試験、トルイジンブルー (Aldrich, Milwaukee, Wis.) 溶液中の染色、及び/又は基材へのコーティングの接着を視覚化するためのSEM分析により追跡することができる。
本明細書の本発明の趣旨を説明する目的のため、本考察は、コーティング形態で生分解性組成物を用具表面上に提供することに焦点を当ててきた。しかしながら、本説明を考えると、当業者は、生分解性組成物が用具自体の構造的成分を形成するために利用することができることを容易に理解するだろう。これらの局面では、用具構造の任意の選択された成分は、必要ならば、本発明の生分解性組成物から構成することができる。
以下の非-限定的例を参考に本発明を説明する。
以下の手法及び材料を実施例に使用した。
実施例のために、ポリ(エチレングリコール)テレフタレート/ポリ(1,4-ブチレン)テレフタレート(PEGT/PBT)の3種のマルチブロックコポリマーをOctoPlus, B.V. Leiden, The Netherlandsから入手した。これらのポリマーは、ポリアクティブ(商標)と呼ばれ、以下の性質を有する。
重量平均分子量100,000〜150,000及びインへレント粘度0.90〜1.20 dL/gを有するポリ(L-ラクチド)を、更に精製することなく使用した。重量平均分子量75,000〜120,000及びインへレント粘度0.55〜0.75 dL/gを有するポリ(DL-ラクチド)を、更に精製することなく使用した。重量平均分子量50,000〜75,000を有するポリ(DL-ラクチド-co-グリコリド)及び各モノマーの50 moleパーセントの組成物を、更に精製することなく使用した。これらのポリマーは、各々、PLLA、PDLLA及びPLGAと称する。3つのポリマー全ては、Sigma-Aldrich (St. Louis, USA) から購入した。
ポリ(L-ラクチド-co-カプロラクトン-co-グリコリド)[P(LLA-CL-GLA)]をSigma-Aldrich (St. Louis, USA; 製品番号568562、GPCによる平均Mw 約100,000, L-ラクチド 70%)から得た。
ポリ[(ラクチド-co-エチレングリコール)-co-エチルオキシホスホネート]をSigma-Aldrich (St. Louis, USA; 製品番号659606) から得た。
デキサメタゾン(「デキサ」)をSigma Aldrich (St. Louis, USA) から購入した、純度は98%であった。パクリタキセル(「PTX」)をC Laboratories (Division of PKC Pharmaceuticals, Inc., Woburn, MA) から購入した、純度は99%超であった。
パリレンC(商標)コーティングの適用による表面予備処理
実施例の全てについて、ステントは、パリレンC(商標)の処理コート層したものをまず提供した。パリレンC(商標)コーティングは、蒸着重合と称される方法により達成した。その方法では、ダイマーのパリレンC(商標)組成物は、150℃で真空下蒸発させ、680℃で熱分解して反応性モノマーを形成させ、次いで25℃でコートされる成分を含むチェンバー内にポンプで入れた。低チェンバー温度では、モノマー性キシリレンを、フリーラジカルプロセスを介して直ちに重合される部分上に蒸着させた。ポリマーコーティングは、約500キロダルトンの分子量に近づいた。
実施例の全てについて、ステントは、パリレンC(商標)の処理コート層したものをまず提供した。パリレンC(商標)コーティングは、蒸着重合と称される方法により達成した。その方法では、ダイマーのパリレンC(商標)組成物は、150℃で真空下蒸発させ、680℃で熱分解して反応性モノマーを形成させ、次いで25℃でコートされる成分を含むチェンバー内にポンプで入れた。低チェンバー温度では、モノマー性キシリレンを、フリーラジカルプロセスを介して直ちに重合される部分上に蒸着させた。ポリマーコーティングは、約500キロダルトンの分子量に近づいた。
キシリレンモノマーの蒸着は、中程度の真空 (0.1 torr) のみで行い、視野方向ではなかった。すなわち、モノマーは、コートされる部分の全ての側を囲む機会を有し、クレビス又は管内を通り、鋭角な点及び縁をコーティングし、いわゆる「絶縁保護」コーティングをつくる。
ポリアクティブ(商標)ポリマーを含むコート層の調製
デキサメタゾンを含むポリマーコーティング組成物の調製に関しては、デキサメタゾンをTHFに先ず溶解し、次いでポリマー/クロロホルム溶液に加えた。各ポリアクティブ(商標)ポリマーをデキサメタゾン又はパクリタキセルと共にクロロホルムに溶解した。ポリアクティブ(商標)ポリマーの濃度は、27ミリグラム/ミリリットルであったが、デキサメタゾン又はパクリタキセルの濃度は3ミリグラム/ミリリットルであった。目視によって不溶性材料の形跡がなくなるまで、得られた溶液を25℃で攪拌した。
デキサメタゾンを含むポリマーコーティング組成物の調製に関しては、デキサメタゾンをTHFに先ず溶解し、次いでポリマー/クロロホルム溶液に加えた。各ポリアクティブ(商標)ポリマーをデキサメタゾン又はパクリタキセルと共にクロロホルムに溶解した。ポリアクティブ(商標)ポリマーの濃度は、27ミリグラム/ミリリットルであったが、デキサメタゾン又はパクリタキセルの濃度は3ミリグラム/ミリリットルであった。目視によって不溶性材料の形跡がなくなるまで、得られた溶液を25℃で攪拌した。
PLLA、PDLLA又はPLGAコーティングの調製
デキサメタゾンを含むポリマーコーティング組成物の調製に関しては、デキサメタゾンをTHFに先ず溶解し、次いでポリマー/クロロホルム溶液に加えた。各PLLA、PDLLA及びPLAGAポリマーをデキサメタゾン又はパクリタキセルと共にクロロホルムに溶解した。ポリマーの濃度は、27ミリグラム/ミリリットルであったが、デキサメタゾン又はパクリタキセルの濃度は3ミリグラム/ミリリットルであった。目視によって不溶性材料の形跡がなくなるまで、得られた溶液を25℃で攪拌した。
デキサメタゾンを含むポリマーコーティング組成物の調製に関しては、デキサメタゾンをTHFに先ず溶解し、次いでポリマー/クロロホルム溶液に加えた。各PLLA、PDLLA及びPLAGAポリマーをデキサメタゾン又はパクリタキセルと共にクロロホルムに溶解した。ポリマーの濃度は、27ミリグラム/ミリリットルであったが、デキサメタゾン又はパクリタキセルの濃度は3ミリグラム/ミリリットルであった。目視によって不溶性材料の形跡がなくなるまで、得られた溶液を25℃で攪拌した。
コーティング手法
シリンジポンプに結合した超音波スプレイヘッドを用いて、商業的に入手可能なステンレス鋼ステント(例えば、Laserage Technology Corporation, IL)に各コーティング溶液を適用した。米国特許出願公開第US 2004/0062875 A1号 (Chappa et al., "Advance Coating Apparatus and Method," April 1, 2004) を参照。コーティング後に、ステントを真空下に置いて、溶媒を除いた。各ステント上の典型的なコーティング重量は、特に反対のことを言わない限り、乾燥後に、約500マイクログラムであった。
シリンジポンプに結合した超音波スプレイヘッドを用いて、商業的に入手可能なステンレス鋼ステント(例えば、Laserage Technology Corporation, IL)に各コーティング溶液を適用した。米国特許出願公開第US 2004/0062875 A1号 (Chappa et al., "Advance Coating Apparatus and Method," April 1, 2004) を参照。コーティング後に、ステントを真空下に置いて、溶媒を除いた。各ステント上の典型的なコーティング重量は、特に反対のことを言わない限り、乾燥後に、約500マイクログラムであった。
生物活性剤溶出実験
以下の溶出実験を、デキサメタゾンを含むコーティングに利用した。ステントコーティングの前後に、ステント上のコーティング量を測定するために各ステントを計量した。リン酸緩衝生理食塩水(PBS, pH 7.4)又は0.45% 酢酸Tween緩衝液 (蒸留水中のTAB) 中で、生物活性剤放出を測定した。典型的な方法では、各ステントを5-ミリリットル褐色シンチレーションバイアル中に入れた。電磁攪拌バー及び4ミリリットルのPBS緩衝液(1リットルの水、9グラムの塩化ナトリウム、0.27グラムの一塩基性リン酸カリウム (KH2PO4)、及び1.4グラムの二塩基性リン酸カリウム (K2HPO4) を各バイアルに加えた。バイアルを37℃の水浴中に置いた。各サンプリング時(通常、初日に4又は5回、次いで日に1回)に、ステントを除き、新しいバイアル中の新鮮な緩衝液中に入れた。各サンプリング時に、各生物活性剤の特徴的波長を用いて、生物活性剤(デキサメタゾン)の濃度をUV分光法により消費した緩衝液中で測定した。この濃度は、モル吸収率を用いてコーティングから放出される生物活性剤の質量に変換した。
以下の溶出実験を、デキサメタゾンを含むコーティングに利用した。ステントコーティングの前後に、ステント上のコーティング量を測定するために各ステントを計量した。リン酸緩衝生理食塩水(PBS, pH 7.4)又は0.45% 酢酸Tween緩衝液 (蒸留水中のTAB) 中で、生物活性剤放出を測定した。典型的な方法では、各ステントを5-ミリリットル褐色シンチレーションバイアル中に入れた。電磁攪拌バー及び4ミリリットルのPBS緩衝液(1リットルの水、9グラムの塩化ナトリウム、0.27グラムの一塩基性リン酸カリウム (KH2PO4)、及び1.4グラムの二塩基性リン酸カリウム (K2HPO4) を各バイアルに加えた。バイアルを37℃の水浴中に置いた。各サンプリング時(通常、初日に4又は5回、次いで日に1回)に、ステントを除き、新しいバイアル中の新鮮な緩衝液中に入れた。各サンプリング時に、各生物活性剤の特徴的波長を用いて、生物活性剤(デキサメタゾン)の濃度をUV分光法により消費した緩衝液中で測定した。この濃度は、モル吸収率を用いてコーティングから放出される生物活性剤の質量に変換した。
TABを利用するアッセイに関しては、4ミリリットルのTAB緩衝液(1リットルの水、0.704 g 酢酸ナトリウム、1.6 ml 1M 酢酸、及び4.05 ml Tween 80) を各バイアルに加えた。バイアルを37℃の水浴中に置いた。PBS溶出アッセイについて記載したように、各サンプリング時に、ステントを除き、新しいバイアル中の新鮮な緩衝液中に入れた。消費した緩衝液中で、HPLCにより各サンプリング時の生物活性剤の濃度を測定した。
各々除去後の各試料質量を添加することにより、放出された生物活性剤の累積的量を計算した。時間関数として放出された生物活性剤の量をプロットすることにより放出プロフィルを得た。
溶出実験が完了したら直ちに、室温(25〜27℃)にて真空オーブン中で、終夜、ステントを乾燥し、UV分光の結果の正確性を確かにするために計量した。
パクリタキセルを含むコーティングについては、以下の方法に従い、生物活性剤溶液を観察した。パクリタキセルでコートされたステントを、コバルトクロムステント表面からパクリタキセルを含むコート材料を溶解する2.5〜4 ml 0.1%酢酸のメタノール溶液で満たしたガラス試験管に漬けることにより、コートされたステント試料からのパクリタキセル含有量及び量を分析した。試験管に栓をし、アルミニウムホイルで覆い、機械振盪器を用いて3時間振盪した。振盪後に、(抽出されたパクリタキセルを有する)0.45ミクロンNylon Acrodiscシリンジフィルターで溶液を濾過し、以下のパラメーターを用いてHPLCにより分析した:
HPLCカラム = ODS Hypersil C18, 150 x 4.6 mm, 5 μ粒径
カラム温度 = 35 deg C
移動相 = 50:50 アセトニトリル/水
流速 = 1.2 ml/分
注入体積 = 10 μl
濯ぎ溶液 = 80:20 アセトニトリル/水
UV検出波長 = 227 nm
実行時間 = 10分。
HPLCカラム = ODS Hypersil C18, 150 x 4.6 mm, 5 μ粒径
カラム温度 = 35 deg C
移動相 = 50:50 アセトニトリル/水
流速 = 1.2 ml/分
注入体積 = 10 μl
濯ぎ溶液 = 80:20 アセトニトリル/水
UV検出波長 = 227 nm
実行時間 = 10分。
HPLCカラムを移動相溶液(50:50 アセトニトリル/水)で平衡化し、227 nmにパクリタキセルのピークを生じるパクリタキセル標品を用いて試験した。ステントコーティング中のパクリタキセル(μg)含有量を決定するために、3種のパクリタキセル標品溶液を2点で実行した。キャリブレーション曲線(ピーク面積対濃度(μg /ml))を作るために、各標品の平均ピーク面積を使用した。次ぎに、試験試料(コートされたステントから抽出されたパクリタキセルを含む0.1% AA/MeOH)をHPLCで実行した。PTX濃度(μg/ml)を、標準曲線から決定し、0.1 % AA/MeOHの体積を乗じて、コートされたステントから抽出されたパクリタキセルの量(μg)を決定した。
実施例1−2つのコート層を含む代表的な多層コーティングからの生物活性剤の溶出
代表的な低分子量の生物活性剤を含むように様々な生分解性コーティングを調製し、得られた溶出プロファイルを観察した。
代表的な低分子量の生物活性剤を含むように様々な生分解性コーティングを調製し、得られた溶出プロファイルを観察した。
ベースライン比較のために、2つのグループのステントに生物活性剤を含む単一コート層を提供した。ステントの第一グループには、PLLA及びデキサメタゾンの単一コート層(コーティングA)を提供した。コーティング組成物は、上記のように調製した。ステントの第二グループには、ポリアクティブ(商標)ポリマー及びデキサメタゾンの単一コート層(コーティングB)を提供した。コーティング組成物は、上記のように調製した。
加えて、ステントのグループには、ポリアクティブ(商標)ポリマーからなる第二コート層(生物活性剤の添加なし)(コーティングC)を提供した。ポリアクティブ(商標)ポリマーを含むこれらのコート層に関して、ポリアクティブ(商標)ポリマーをクロロホルムに溶解し、20ミリグラム/ミリリットルの濃度にし、得られたコーティング溶液を先に記載した超音波スプレイにより第一コート層上に適用した。
様々なコート層を先に記載したステンレス鋼ステントに適用した。次いで、室温で3時間、真空オーブン内でステントを乾燥した。表2に、コーティング及び生物活性剤の重量を記載する。表1のコーティングから得られたデキサメタゾン溶出結果を図1に示す。
結果は、(非ブレンドされた)個々のポリマーが規定の放出速度を表したことを示した。ポリアクティブ(商標)ポリマーの単一コート層を含むステントコーティングは、水透過性及び迅速な生物活性剤拡散を可能にするポリマーの親水性部分に因り、デキサメタゾンを速く放出した(コーティングB)。PLLAの単一コート層を含むステントコーティングは、PLLAの疎水性に因り、デキサメタゾンを非常にゆっくりと放出した(コーティングA)。多層コーティング組成物、コーティングCを作製することにより、放出速度は、これらの両極端の間に至った。コーティングB及びCは、生分解性組成物によるデキサメタゾンの溶解により、急激な初期放出を示した。コーティングCについては、急激な初期放出の後に、生分解性組成物の多層構造により制御される徐放があった。コーティングCの徐放は、16日間、観察された。
図1で示される観察された放出プロファイルは、以下のように説明することができる。デキサメタゾンは、相対的に低分子量(MW = 392)を有し、よって、より大きな分子量の生物活性剤よりも、より容易にポリマーマトリックスを通して拡散する。ポリアクティブ(商標)ポリマー(コーティングB)からなる単一コート層からのデキサメタゾンの放出は、初日に、生物活性剤の実質的なバーストを示した(薬物の90%超)。対照的に、PLLAからなる単一コート層からなるコーティングは、PLLAの疎水性に起因してデキサメタゾンを非常によりゆっくりと放出した(コーティングA)。PLLAの単一コート層では、バースト放出は観察されなかった。多層コーティングについて、初日に、デキサメタゾンの約30%の初期放出が観察され、次いで初期放出に続く生物活性剤の実質的に制御された放出が観察された。従って、これらの実験は、生分解性コーティング組成物からの、比較的低分子量の生物活性剤の初期バーストを制御する能力を証明した。
図1はまた、3つの異なった生分解性コーティングについての長時間放出されたデキサメタゾンの累積パーセンテージを示す。デキサメタゾンを用いるポリアクティブ(商標)ポリマーの単一コート層を含むコーティングと比べて、多層コーティングは、徐放速度を明確に証明した。例えば、50%デキサメタゾン(t1/2)の放出時間は、多層コーティングでは8日間であった。対照的に、単一層ポリアクティブ(商標)ポリマー製剤からデキサメタゾンの90%超が初日に放出した。更に、16日目には、単一層PLLAコーティングが、デキサメタゾンの10%未満を放出した。
実験の期間(約16日)を考慮すると、デキサメタゾンの放出は、ポリマーマトリックスによる生物活性剤の拡散に主に起因し、ポリマーマトリックスの分解に因らない。
実施例2−3つのコート層を含む代表的な多層コーティング及びポリアクティブ(商標)ポリマー外側コーティングからの生物活性剤の溶出
第一コート層がモデルとなる低分子量生物活性剤、デキサメタゾンを含む、3つのコート層からなるコーティングをステンレス鋼ステントに提供した。以下のように生物活性剤放出についてコーティングを評価した。
第一コート層がモデルとなる低分子量生物活性剤、デキサメタゾンを含む、3つのコート層からなるコーティングをステンレス鋼ステントに提供した。以下のように生物活性剤放出についてコーティングを評価した。
PLLA及びデキサメタゾンからなる第一コート層を調製し、先に記載のステントに適用した。PLLAからなる第二コート層(生物活性剤なし)を調製し、先に記載のステントに適用した。ポリアクティブ(商標)ポリマーからなる第三コート層(生物活性剤なし)を調製し、先に記載のステントに適用した。ステントに対する第三コート層の平均重量は、130ミリグラムであった。表3には、コーティング重量及び最初の2つのコート層の組成を示す。
図2では、これら多層コーティングが、生物活性剤なしの第三コート層を含まないコーティングよりも、非常に低い初期放出を表した、ことを結果は示した。デキサメタゾンの溶出を、適用される生物活性剤なしの第二コート層の量で制御した。放出制御は、生物活性剤の初期放出、及び続く放出(すなわち、0.25日で始まり、その後、相対的に一定の放出速度で続く)で観察された。第二コート層が厚くなれば厚くなるほど、生物活性剤はコーティングから遅く溶出した。全てのコーティングD〜Fは、生分解性組成物を介するデキサメタゾンの分解に因る急激な初期放出を含む2相放出、次ぐ生分解性組成物の多層構造により制御される徐放を証明した。コーティングは、異なったバースト用量を証明したが、類似の徐放速度を明らかにしなかった。コーティングは同一の多層構造を有したが、第一コート層及び第二コート層のコート層の厚さは異なった。
生物活性剤の溶出を制御することに加えて、第三コート層(ポリアクティブ(商標)ポリマー)は、疎水性生分解性ポリマーよりも、分解中に、PLLA、PDLLA、PLGA等に比べて、ほとんど酸を生じない表面を提示することにより、コーティング生体適合性を好適に改善することができる。親水性の第三コート層はまた、コーティングへのより高い水透過性率を可能にすることにより、コーティングの分解速度を増加させることができる。これらの結果は、図2に説明されている。
図2で説明される観察された放出プロファイルは、以下のように説明することができる。コーティング組成物の各々について、第一ポリマー層及び第二ポリマー層の重量を調整した。全てのコーティングは、130 μgの平均コート層重量を有するポリアクティブ(商標)ポリマーからなる、第三の、最外コート層を含んだ。コーティングDは、最も少ない量の第二コート層を含んだ。コーティングDからのデキサメタゾンの放出は、最初のおおよそ6時間内に、(コーティング組成物内に含まれる生物活性剤の10%未満であるが)最も高い初期放出を示した。対照的に、コーティングFは、第一コート層の最も少ない量及び第二コート層の最大量を含んだ。得られた初期放出速度及び続く徐放速度は、コーティングDよりも顕著に低かった。最も厚い第一コート層及び中間の第二コート層を含むコーティングEは、初期放出速度、及び他のコーティングの中間である次の放出速度を示した。
中間のPLLA層(第二コート層)の修飾は、生分解性コーティング組成物からの比較的低分子量の生物活性剤の初期放出速度及び次の放出速度を制御することができる。従って、初期放出速度及び次の徐放速度は、第一及び第二コート層の相対的コーティング重量を調整することにより正確に制御することができる。
図2は、3つの異なった生分解性コーティングについて長期間放出されたデキサメタゾンの累積パーセンテージを示す。全てのコーティングは、生物活性剤の制御された初期放出及び徐放速度を証明する。
放出速度は、第一コート層中での生物活性剤の異なった装填、生物活性剤なしのPLLA型ポリマー及び/又はポリアクティブ(商標)ポリマーの異なった層厚を用いて変えることができる。
実施例3−PLLA外層を含む代表的な多層コーティングからの生物活性剤の溶出
生物活性剤放出プロファイルに対する多層コート層の効果を説明するため実験を行った。
生物活性剤放出プロファイルに対する多層コート層の効果を説明するため実験を行った。
ポリアクティブ(商標)ポリマー又はPLLAのいずれかを含む第一コート層、及びモデルとなる生物活性剤としてパクリタキセルをステントに提供した。これらのコーティングを調製し、先に記載のようにステンレス鋼ステントに適用した。ステントの1群(ステントK)について、生物活性剤なしのPLLAの第二コート層を適用して、生物活性剤放出速度を調整した。これらコート層について、PLLAをテトラヒドロフランに溶解し、20ミリグラム/ミリリットルの濃度にし、次いで、コーティングを含む既存の生物活性剤上に超音波スプレイにより第二層として適用した。次いで、室温に設定した真空オーブン中でステントを乾燥した。
表4に、コーティング組成物及び生物活性剤の重量を示す。図3は、パクリタキセル溶出結果を示す。PLLAの外側コート層は、ポリアクティブ(商標)ポリマーにより示されるよりも低い生物活性剤バーストを含むポリマーの両極端(polymer extremes)と、生物活性剤を含み層のみとの間の速度に、溶出を遅くした。
図3に示すように、初期生物活性剤放出及び次の放出速度は、PLLAを含む第二コート層を提供することにより制御することができる。コーティングJは、パクリタキセルを含むポリアクティブ(商標)ポリマーの単一層を含み、コーティングLは、パクリタキセルを含むPLLAの単一層を含んだ。これらの2つの単一層コーティングは、PLLAの第二ポリマーコーティングを欠いた。コーティングKについて、PLLAの第二コート層の存在は、パクリタキセルの初期放出を減少させ、生物活性剤の徐放速度を提供した。
図3はまた、長期間の、放出されたパクリタキセルの累積パーセンテージ又は3つの異なった生分解性コーティング組成物を示す。ポリアクティブ(商標)及びパクリタキセルからなる単一層コーティングについて、生物活性剤の約85%を第一日目に放出した。対照的に、PLLAからなる単一層コーティングから放出されるパクリタキセルの総量は、8日目で、10%未満であった。ポリアクティブ(商標)及びパクリタキセルを含む第一コート層、及びPLLAの第二コート層(生物活性剤なし)からなる多層コーティングは、ゼロ-オーダー速度に近似する、中間の制御された放出プロファイルを示した。(第一日目の)パクリタキセルの初期放出は、10%未満であり、7日目では、生物活性剤の20%を少し超える総量を放出した。
PLLAからなる第二コート層の含有は、初期の生物活性剤の放出速度、及びその後の生分解性コーティング組成物からの比較的低分子量の生物活性剤の放出速度を制御することができることを、結果は示す。従って、初期バースト放出及び次の徐放速度(おおよそゼロ-オーダー放出)は、第一及び第二コート層の相対的コーティング重量を調整することにより正確に制御することができる。
実施例4−変化する重量のPLLA外層を含む代表的な多層コーティングからの生物活性剤の溶出
これらの実験のために、多層コーティングを調製し、ステントに適用した。(生物活性剤を含まない)PLLAコート層の量は、生物活性剤放出速度に対する層厚の効果を示すように変えた。
これらの実験のために、多層コーティングを調製し、ステントに適用した。(生物活性剤を含まない)PLLAコート層の量は、生物活性剤放出速度に対する層厚の効果を示すように変えた。
ポリアクティブ(商標)ポリマー及びデキサメタゾンを含む第一コート層を先に記載のようにして調製し、先に記載のステントに適用した。PLLAからなる第二コート層(生物活性剤なし)を先に記載のようにして調製し、先に記載の第一コート層に適用した。表5に、本試験のコーティング組成物及び重量を示す。これらのコーティングの溶出結果を図4に示す。
図4に示すように、PLLAコート層厚が増えると、バースト放出及び次の放出速度が低下した、ことを結果は示した。第二コート層の最少量を含むコーティングからのデキサメタゾンの放出は、最高の初期バースト放出を示した。PLLAの第二コート層の重量が増えると、初期バースト及び次の放出速度はいずれも顕著に減少した。従って、これらの実験は、生分解性コーティング組成物からの、比較的低分子量の生物活性剤の初期バースト及び徐放を制御する能力を示す。結果は、コーティング重量が特定の投薬要件を満たすように溶出速度を調整するために使用することができる、ことを示す。
図4はまた、3つの異なった生分解性コーティングのための、長時間放出されたデキサメタゾンの累積パーセンテージを示す。PLLA第二コート層の最少量を含むコーティングの時間t1/2は、6時間のオーダーであった。相対的に、PLLA第二層の量が増えると、t1/2は、顕著に延びた。中間のPLLAコーティング厚について、t1/2は、1日超まで延びた。210 μgの重量でPLLA第二コーティングを含むコーティング組成物について、デキサメタゾンの約20%が3日目に放出した。
実施例5−PLGA外層を含む代表的な多層コーティングからの生物活性剤の溶出
生物活性剤不出プロファイルに対する多層コート層の効果を説明するために実験を行った。
生物活性剤不出プロファイルに対する多層コート層の効果を説明するために実験を行った。
ポリアクティブ(商標)ポリマー又はPLGAのいずれか、及びモデルとなる生物活性剤としてデキサメタゾンを含む第一コート層をステントに提供した。これらのコーティングを調製し、先に記載のようにステンレス鋼ステントに適用した。ステントの1群について、生物活性剤なしのPLGAの第二コート層を適用して、生物活性剤放出速度を調整した。これらのコート層について、PLGAをテトラヒドロフランに溶解して、20ミリグラム/ミリリットルの濃度にし、次いで、超音波スプレイによりコーティングを含む既存の生物活性剤上に第二層として適用した。次いで、室温に設定された真空オーブン中でステントを乾燥した。
表6に、コーティング組成物及び生物活性剤の重量を示す。図5は、デキサメタゾン溶出結果を示す。
図5に示すように、生物活性剤の放出速度は、PLGAからなる第二コート層を提供することにより制御することができる。「PLGAのみ」と称されるステントは、デキサメタゾンを含むPLGAの単一コート層を含み、「PLGA TC」と称されるステントは、デキサメタゾンを有するポリアクティブ(商標)の第一コート層、及びPLGAの第二コート層(生物活性剤なし)を含んだ。ポリアクティブ(商標)ポリマーの第一コート層上での第二コート層としてのPLGAの含有は、生物活性剤の制御された放出を提供した。
先に実施例1に示したように、生物活性剤を有するポリアクティブ(商標)ポリマーの単一コート層の含有は、ポリマーコーティングを介するデキサメタゾンの迅速な拡散に因る、生物活性剤の非常に速い放出を提供する。図5は、生物活性剤を含むPLGAの単一コート層により提供される比較的遅い放出速度を説明する。PLGAが、デキサメタゾンを有するポリアクティブ(商標)ポリマーの第一コート層上に第二コート層として提供されるとき、得られたコーティングは、デキサメタゾンの制御された放出を提供する。初期放出は、最初の3〜4日に観察され、次いで徐放が観察された。初期放出は、デキサメタゾンを含むポリアクティブ(商標)ポリマーコーティングについての実施例1で観察されたバースト放出よりも低いが、デキサメタゾンを有するPLGAの放出速度よりも高い、デキサメタゾンの制御された放出を示す。
図5はまた、2つの異なった生分解性コーティング組成物について、長時間、放出されたデキサメタゾンの累積パーセンテージを示す。PLGA及びデキサメタゾンからなる単一層コーティングについては、生物活性剤の約20%が16日目に放出された。対照的に、ポリアクティブ(商標)ポリマー及びPLGAからなる多層コーティングから放出されるデキサメタゾンの総量は、14日目でおおよそ100%であった。ポリアクティブ(商標)ポリマー及デキサメタゾンを含む第一コート層、及びPLGAの第二コート層(生物活性剤なし)からなる多層コーティングは、初期放出、次いでゼロ-オーダー速度に近似する徐放を含む、制御された放出プロファイルを示した。
結果は、PLGAからなる第二コート層の含有が、生分解性コーティング組成物からの比較的低分子量の生物活性剤の初期バースト放出及びこれに続く放出速度を制御することができる、ことを示す。従って、初期バースト放出及び次の放出速度(ゼロ-オーダー放出に近似する)は、第一及び第二コート層の相対的コーティング重量を調整することにより、正確に制御することができる。
実施例6-PDLLA外層を含む代表的な多層コーティングからの生物活性剤の溶出
生物活性剤不出プロファイルに対する多層コート層の効果を説明するために実験を行った。
生物活性剤不出プロファイルに対する多層コート層の効果を説明するために実験を行った。
ポリアクティブ(商標)ポリマー又はPDLLAのいずれか、及びモデルとなる生物活性剤としてデキサメタゾンを含む第一コート層をステントに提供した。これらのコーティングを調製し、先に記載のようにステンレス鋼ステントに適用した。生物活性剤放出速度を調整するために、ステントの1群について、生物活性剤なしのPDLLAの第二コート層を適用した。これらのコート層について、PDLLAをテトラヒドロフランに溶解して、20ミリグラム/ミリリットルの濃度にし、次いで、超音波スプレイによりコーティングを含む既存の生物活性剤上に第二層として適用した。次いで、室温に設定された真空オーブン中でステントを乾燥した。
表7に、コーティング組成物及び生物活性剤の重量を示す。図6は、デキサメタゾン溶出結果を示す。
図6に示すように、生物活性剤の放出速度は、PDLLAからなる第二コート層を提供することにより制御することができる。「PDLLAのみ」と称されるステントは、デキサメタゾンを含むPDLLAの単一コート層を含み、「PDLLA TC」と称されるステントは、デキサメタゾンを有するポリアクティブ(商標)の第一コート層、及びPDLLAの第二コート層(生物活性剤なし)を含んだ。ポリアクティブ(商標)ポリマーの第一コート層上での第二コート層としてのPDLLAの含有は、生物活性剤の制御された放出を提供した。
先に実施例1に示したように、生物活性剤を有するポリアクティブ(商標)ポリマーの単一コート層の含有は、ポリマーコーティングを介するデキサメタゾンの迅速な拡散に因る、生物活性剤の非常に速い放出を提供する。図6は、生物活性剤を含むPDLLAの単一コート層により提供される比較的遅い放出速度を説明する。PDLLAが、デキサメタゾンを有するポリアクティブ(商標)ポリマーの第一コート層上に第二コート層として提供されるとき、得られたコーティングは、デキサメタゾンの制御された放出を提供する。初期放出は、最初の3日に観察され、次いで徐放が観察された。初期放出は、デキサメタゾンを含むポリアクティブ(商標)ポリマーコーティングについての実施例1で観察されたバースト放出よりも低いが、デキサメタゾンを有するPDLLAの放出速度よりも高い、デキサメタゾンの制御された放出を示す。
図6はまた、2つの異なった生分解性コーティング組成物について、長時間、放出されたデキサメタゾンの累積パーセンテージを示す。PDLLA及びデキサメタゾンからなる単一層コーティングについては、生物活性剤の約10%が16日目に放出された。対照的に、ポリアクティブ(商標)ポリマー及びPDLLAからなる多層コーティングから放出されるデキサメタゾンの総量は、同一の時点でおおよそ90%であった。ポリアクティブ(商標)ポリマー及デキサメタゾンを含む第一コート層、及びPDLLAの第二コート層(生物活性剤なし)からなる多層コーティングは、初期放出、次いでゼロ-オーダー速度に近似する徐放を含む、制御された放出プロファイルを示した。
結果は、PDLLAからなる第二コート層の含が、生分解性コーティング組成物からの比較的低分子量の生物活性剤の初期バースト放出及びこれに続く放出速度を制御することができ、ことを示す。従って、初期バースト放出及び次の放出速度(ゼロ-オーダー放出に近似する)は、第一及び第二コート層の相対的コーティング重量を調整することにより、正確に制御することができる。
実施例7−ポリアクティブ(商標)/生物活性剤ベースコートを含む代表的な多層コーティングからの生物活性剤の溶出
モデルとなる生物活性剤としてのパクリタキセルと共にポリアクティブ(商標)ポリマーを含む第一コート層をステントに提供した。これらのコーティングを調製し、先に記載のようにステンレス鋼ステントに適用した。生物活性剤放出速度を調整するために、生物活性剤なしの P(LLA-CL-GLA) の第二コート層をベースコート上に適用した。ステントの1群について、生物活性剤なしのポリアクティブ(商標)の第三コート層を第二コート層上に適用した。
モデルとなる生物活性剤としてのパクリタキセルと共にポリアクティブ(商標)ポリマーを含む第一コート層をステントに提供した。これらのコーティングを調製し、先に記載のようにステンレス鋼ステントに適用した。生物活性剤放出速度を調整するために、生物活性剤なしの P(LLA-CL-GLA) の第二コート層をベースコート上に適用した。ステントの1群について、生物活性剤なしのポリアクティブ(商標)の第三コート層を第二コート層上に適用した。
ベースコート用には、先に記載によう、ポリアクティブ(商標)ポリマーをパクリタキセルと共にクロロホルムに溶解した。ポリアクティブ(商標)ポリマーの濃度は、40ミリグラム/ミリリットルであった。生物活性剤を含まないコート層については、先に記載のように、P(LLA-CL-GLA) 又はポリアクティブ(商標)ポリマーをクロロホルムに溶解し、20ミリグラム/ミリリットルの濃度にした。
コーティング組成物を超音波スプレイにより適用した。次いで、室温に設定した真空オーブン中で、コートされたステントを乾燥した。
表8に、コーティング組成物及び生物活性剤の重量を示す。図7は、パクリタキセル溶出結果を示す。
ステントの各群について、2つの試料を溶出試験に供した。1つの試料は、表面特性(光学、ラマン及びSEM)に供し、他の1つの試料は機械的試験に供した。
溶出試験
図7に示すように、生物活性剤の放出速度は、P(LLA-CL-GLA) からなる第二コート層を提供することにより制御することができる。ポリアクティブ(商標)ポリマーの第一コート層上の第二コート層としての P(LLA-CL-GLA) の含有は、生物活性剤の制御された放出を提供した。ポリアクティブ(商標)からなる第三コート層の付加は、コーティングからのパクリタキセルの溶出速度を更に減少させなかった。試料34及び35については、パクリタキセルの約50%が最初の24時間以内に放出した。14日目に、パクリタキセルの81%超が放出した。対照的に、(2つのコート層のみを含む)試料37及び38は、最初の24時間以内に、パクリタキセルの約2%、14日目に、パクリタキセルの8.5%以下を、これらの試料から放出した。従って、2-層試料は、より低い初期放出相を有するだけでなく、初期放出相の後に、長時間、より遅い放出速度を有した(ゼロ-オーダー放出速度に近似する)。従って、アッセイの結果では、2-層コーティングには、次により長い治療的処置期間を提供することができる、より多くのパクリタキセルが残った。
図7に示すように、生物活性剤の放出速度は、P(LLA-CL-GLA) からなる第二コート層を提供することにより制御することができる。ポリアクティブ(商標)ポリマーの第一コート層上の第二コート層としての P(LLA-CL-GLA) の含有は、生物活性剤の制御された放出を提供した。ポリアクティブ(商標)からなる第三コート層の付加は、コーティングからのパクリタキセルの溶出速度を更に減少させなかった。試料34及び35については、パクリタキセルの約50%が最初の24時間以内に放出した。14日目に、パクリタキセルの81%超が放出した。対照的に、(2つのコート層のみを含む)試料37及び38は、最初の24時間以内に、パクリタキセルの約2%、14日目に、パクリタキセルの8.5%以下を、これらの試料から放出した。従って、2-層試料は、より低い初期放出相を有するだけでなく、初期放出相の後に、長時間、より遅い放出速度を有した(ゼロ-オーダー放出速度に近似する)。従って、アッセイの結果では、2-層コーティングには、次により長い治療的処置期間を提供することができる、より多くのパクリタキセルが残った。
結果は、P(LLA-CL-GLA) からなる第二コート層の含有が、生分解性コーティング組成物からの比較的低分子量の生物活性剤の初期バースト放出及び次の放出速度を制御することができる、ことを示す。従って、初期バースト放出及び次の徐放速度(ゼロ-オーダー放出に近似する)は、第一及び第二コート層の相対的コーティング重量を調整することにより、正確に制御することができる。結果はまた、このより遅い放出速度が、2つのコート層上への第三コート層(外層、又はトップコート)、ここで、第三コーティング組成物はポリアクティブ(商標)からなる、の含有により、中間速度に加速することができる、ことを示す。この後者の特徴は、用具の最終的な適用により、選択された生物活性剤の放出プロファイルを微調整するために利用することができる。
表面特性
ステント上のポリマーコーティングを特徴付け、コーティング品質、均一性を観察し、及び成分を混合するために、試料の表面分析を行った。
ステント上のポリマーコーティングを特徴付け、コーティング品質、均一性を観察し、及び成分を混合するために、試料の表面分析を行った。
光学画像及びSEM像は、金属ステント上のコーティングが網目、クラッキング又はコーティング層割れがないことを示した。光学画像及びSEM像では、パクリタキセルの結晶は、見られなかった。結局、コーティングは、各ステントに均一であるようであった。図8及び9は、コーティング36及び39(100Xの拡大率)の各々の光学画像を示す。図10及び11は、コーティング36及39のSEM画像を示す。SEM画像は、ポリアクティブ(商標)トップコートを含むコーティングが表面に凹凸パターンを有したが;P(LLA-CL-GLA)のトップコートを含むステント表面上には凹凸パターンがなかった、ことを示した。従って、表面(外側コート層)のポリアクティブ(商標)ポリマーの存在は、用具上の凹凸表面特性を示すことができる、ようである。
共焦点ラマン画像は、各ステント上のコーティング成分の分布を示した。(金属ステント支柱に垂直である)横断面のラマン画像は、幅50 μm、深さ10又は15 μmの領域に得られた。横断面画像では、コーティング上の空気は、ラマンシグナルを有さず、コーティングは強いラマンシグナルを有し、コーティング下の金属はラマンシグナルを有さなかった。
画像中の各画素では、ラマンスペクトル全体が得られた。P(LLA-CL-GLA)、1000PEGT55PBT45、1000PETT80PBT20、パクリタキセル及びパリレン(商標)の参照スペクトルを用いて、個々の成分の画像にデータ群を逆重畳する(deconvolute)するために、拡張された制約付き最小二乗法(CLS)アルゴリズムを適用した。
試験したステント全てにおいて、生分解性ポリマー及びパクリタキセルは、完全に混合されているように見え、コーティング内で形成された大きな分離又は薬物結晶はなかった。パクリタキセルが生分解性ポリマーに均一に混合し、コーティング中に形成された大きな相分離又は結晶がない、ことを画像は示した。更に、ラマン画像では、コーティングの中間コート及びトップコートは明確に見え、互いに又はパクリタキセルと混合したようには見えなかった。従って、コーティング層は完全な状態で、これらの試料中に保持されているようである。
機械的試験
選択されたステントの慣用的なバルーン拡張後に、6.3x拡大率下で、ステントコーティングの目視を行い、ステント上のコーティング品質を決定した。第二ポリマーは許容されるコーティングを提供するので、目視により、多層コート層を有するステントコーティングが、パクリタキセル、ポリアクティブ(商標)及びP (LLA-CL-GLA) からなることが明となった。許容されるステントコーティングは、外観、例えば、最小の表面クラッキング、ステント支柱間の最小の網目、コーティング表面の平滑なテクスチャ、及びステント基材へのコーティング粘着により特徴付けられた。
選択されたステントの慣用的なバルーン拡張後に、6.3x拡大率下で、ステントコーティングの目視を行い、ステント上のコーティング品質を決定した。第二ポリマーは許容されるコーティングを提供するので、目視により、多層コート層を有するステントコーティングが、パクリタキセル、ポリアクティブ(商標)及びP (LLA-CL-GLA) からなることが明となった。許容されるステントコーティングは、外観、例えば、最小の表面クラッキング、ステント支柱間の最小の網目、コーティング表面の平滑なテクスチャ、及びステント基材へのコーティング粘着により特徴付けられた。
実施例8−ポリアクティブ(商標)/生物活性剤ベースコートを含む代表的な多層コーティングからの生物活性剤の溶出
ステントに、モデルとなる生物活性剤としてのパクリタキセルを有するポリアクティブ(商標)ポリマーを含む第一コート層を提供した。これらのコーティングを調製し、先に記載のようにステンレス鋼ステントに適用した。生物活性剤なしの P(LLA-EG-EOP) の第二コート層をベースコート上に適用して、生物活性剤放出速度を調整した。ステントの1群のために、生物活性剤なしのポリアクティブ(商標)の第三コート層を第二コート層上に適用した。
ステントに、モデルとなる生物活性剤としてのパクリタキセルを有するポリアクティブ(商標)ポリマーを含む第一コート層を提供した。これらのコーティングを調製し、先に記載のようにステンレス鋼ステントに適用した。生物活性剤なしの P(LLA-EG-EOP) の第二コート層をベースコート上に適用して、生物活性剤放出速度を調整した。ステントの1群のために、生物活性剤なしのポリアクティブ(商標)の第三コート層を第二コート層上に適用した。
ベースコート用には、先に記載によう、ポリアクティブ(商標)ポリマーをパクリタキセルと共にクロロホルムに溶解した。ポリアクティブ(商標)ポリマーの濃度は、40ミリグラム/ミリリットルであった。生物活性剤を含まないコート層については、先に記載のように、P(LLA-CL-GLA) 又はポリアクティブ(商標)ポリマーをクロロホルムに溶解し、20ミリグラム/ミリリットルの濃度にした。
コーティング組成物を超音波スプレイにより適用した。次いで、室温に設定した真空オーブン中で、コートされたステントを乾燥した。
表9に、コーティング組成物及び生物活性剤の重量を示す。図12は、パクリタキセル溶出結果を示す。
ステントの各群について、2つの試料を溶出試験に供した。1つの試料は、表面特性(光学、ラマン及びSEM)に供し、他の1つの試料は機械的試験に供した。
溶出試験
図12に示すように、生物活性剤の放出速度は、P(LLA-EG-EOP) からなる第二コート層を提供することにより制御することができる。ポリアクティブ(商標)トープコートの含有は、初期放出相(初期バースト)を増加させた。しかしながら、初期バーストの後に、溶出速度は同様に見えた。試料52及び53(ポリアクティブ(商標)トップコート)では、パクリタキセルの約83〜84%が、最初の24時間以内に放出した。試料56及び57(2つのコート層のみ、P(LLA-EG-EOP) のトップコーを含む)では、パクリタキセルの約69%及び73%が、最初の24時間以内に放出した。14日目では、ポリアクティブ(商標)トップコート試料は、パクリタキセルの約88%を放出したが、P(LLA-EG-EOP) トップコート試料は、パクリタキセルの約85%を放出した。
図12に示すように、生物活性剤の放出速度は、P(LLA-EG-EOP) からなる第二コート層を提供することにより制御することができる。ポリアクティブ(商標)トープコートの含有は、初期放出相(初期バースト)を増加させた。しかしながら、初期バーストの後に、溶出速度は同様に見えた。試料52及び53(ポリアクティブ(商標)トップコート)では、パクリタキセルの約83〜84%が、最初の24時間以内に放出した。試料56及び57(2つのコート層のみ、P(LLA-EG-EOP) のトップコーを含む)では、パクリタキセルの約69%及び73%が、最初の24時間以内に放出した。14日目では、ポリアクティブ(商標)トップコート試料は、パクリタキセルの約88%を放出したが、P(LLA-EG-EOP) トップコート試料は、パクリタキセルの約85%を放出した。
図12を図7と比較すると、コート組成物において P(LLA-CL-GLA) ポリマーから劇的な効果が認められた。トップコートとしての P(LLA-CL-GLA) の含有は、生物活性剤の初期放出の顕著な減少、及び生物活性剤の徐放を与えた。P(LLA-EG-EOP) がより親水性であり、よってポリアクティブ(商標)により類似するため、ポリアクティブ(商標)又は P(LLA-EG-EOP) のいずれかからなるトップコートは、顕著に高い初期放出、更に、試験の過程に渡って、生物活性剤の総放出を有した。
表面特性
ステント上のポリマーコーティングを特徴付け、コーティング品質、均一性を観察し、及び成分を混合するために、試料の表面分析を行った。
ステント上のポリマーコーティングを特徴付け、コーティング品質、均一性を観察し、及び成分を混合するために、試料の表面分析を行った。
光学画像及びSEM像は、金属ステント上のコーティングが網目、クラッキング又はコーティング層割れがないことを示した。光学画像及びSEM像では、パクリタキセルの結晶は、見られなかった。結局、コーティングは、各ステントに均一であるようであった。コーティングのうねりが観察された。図13及び14は、各々、コーティング54及び58の光学画像を示す(100X 拡大率)。図15及び16は、コーティング54及び58のSEM画像を示す。SEM画像は、ポリアクティブ(商標)トップコートを含むコーティングが表面上に凹凸パターンを有することを示した;しかしながら、P(LLA-EG-EOP) のトップコートを含むステント表面上には凹凸パターンはなかった。従って、表面(外側コート層)のポリアクティブ(商標)ポリマーの存在は、用具上の凹凸表面特性を示すことができるようである。
共焦点ラマン画像は、各ステント上のコーティング成分の分布を示した。(金属ステント支柱に垂直である)横断面のラマン画像は、幅50 μm、深さ10又は15 μmの領域に得られた。横断面画像では、コーティング上の空気は、ラマンシグナルを有さず、コーティングは強いラマンシグナルを有し、コーティング下の金属はラマンシグナルを有さなかった。
画像中の各画素では、ラマンスペクトル全体が得られた。P(LLA-EG-EOP)、1000PEGT55PBT45、1000PETT80PBT20、パクリタキセル及びパリレン(商標)の参照スペクトルを用いて、個々の成分の画像にデータ群を逆重畳する(deconvolute)するために、拡張された制約付き最小二乗法(CLS)アルゴリズムを適用した。
試験したステント全てにおいて、生分解性ポリマー及びパクリタキセルは、完全に混合されているように見え、コーティング内で形成された分離又は薬物結晶はなかった。パクリタキセルが生分解性ポリマーに均一に混合し、コーティング中に形成された大きな相分離又は結晶がない、ことを画像は示した。加えて、コーティングの中間コート及びトップコート層は、ラマン画像で明確に見え、互いに又はパクリタキセルと混合されたようには見えなかった。従って、コーティング層の完全な状態は、これらの試料中で、保持されているようであった。
機械的試験
選択されたステントの慣用的なバルーン拡張後に、6.3x拡大率下で、ステントコーティングの目視を行い、ステント上のコーティング品質を決定した。第二ポリマーは許容されるコーティングを提供するので、目視により、多層コート層を有するステントコーティングが、パクリタキセル、ポリアクティブ(商標)及び P(LLA-EG-EOP) からなることが明らかとなった。許容されるステントコーティングは、外観、例えば、最小の表面クラッキング、ステント支柱間の最小の網目、コーティング表面の平滑なテクスチャ、及びステント基材へのコーティング粘着により特徴付けられた。
選択されたステントの慣用的なバルーン拡張後に、6.3x拡大率下で、ステントコーティングの目視を行い、ステント上のコーティング品質を決定した。第二ポリマーは許容されるコーティングを提供するので、目視により、多層コート層を有するステントコーティングが、パクリタキセル、ポリアクティブ(商標)及び P(LLA-EG-EOP) からなることが明らかとなった。許容されるステントコーティングは、外観、例えば、最小の表面クラッキング、ステント支柱間の最小の網目、コーティング表面の平滑なテクスチャ、及びステント基材へのコーティング粘着により特徴付けられた。
実施例9−P(LLA-CL-GLA) /生物活性剤ベースコートを含む代表的な多層コーティングからの生物活性剤の溶出
ステントに、モデルとなる生物活性剤としてのパクリタキセルを有する P(LLA-CL-GLA) コポリマーを含む第一コート層を提供した。これらのコーティングを調製し、先に記載のようにステンレス鋼ステントに適用した。ベースコートとして、先に記載のように、P(LLA-CL-GLA) コポリマーをクロロホルムにパクリタキセルと共に溶解した。P(LLA-CL-GLA) コポリマーの濃度は、40ミリグラム/ミリリットルであった。
ステントに、モデルとなる生物活性剤としてのパクリタキセルを有する P(LLA-CL-GLA) コポリマーを含む第一コート層を提供した。これらのコーティングを調製し、先に記載のようにステンレス鋼ステントに適用した。ベースコートとして、先に記載のように、P(LLA-CL-GLA) コポリマーをクロロホルムにパクリタキセルと共に溶解した。P(LLA-CL-GLA) コポリマーの濃度は、40ミリグラム/ミリリットルであった。
ステントの2つ群を調製した。第一群では、ポリアクティブ(商標)を含む第二コート層を適用した。第二群では、3つのコート層の合計をステントに適用した;すなわち、P(LLA-CL-GLA) からなる第二コート層をベースコート上に適用し、ポリアクティブ(商標)からなる第三コート層を第二コート層上に適用した。従って、両群について、トープコートは、ポリアクティブ(商標)からなり、P(LLA-CL-GLA) の中間-コート層の存在は、試料のいくつかに含まれた。
生物活性剤を含まないコート層について、先に記載のように、P(LLA-CL-GLA) 又はポリアクティブ(商標)ポリマーをクロロホルムに溶解して、20ミリグラム/ミリリットルの濃度にした。
コーティング組成物を超音波スプレイにより適用した。次いで、室温に設定された真空オーブン中でコートされたステントを乾燥した。
表10に、コーティング組成物及び生物活性剤の重量を示す。図17は、パクリタキセル溶出結果を示す。
ステントの各群について、2つの試料を溶出試験に供した。1つの試料は、表面特性(光学、ラマン及びSEM)に供し、他の1つの試料は機械的試験に供した。
溶出試験
図17に示すように、中間コート層(ベースコートとトップコートとの間の第二コート層としての P(LLA-CL-GLA) の利用は、パクリタキセルの溶出速度を減少させた。ポリアクティブ(商標)トップコートの含有は、初期放出相(初期バースト)を増加させた。初期放出相の相違は、ポリアクティブ(商標)トップコートの結果であるように考えられる。しかしながら、初期バーストの後に、溶出速度は同様に見えた。試料31及び32(P(LLA-CL-GLA) の第二コート層を含む)では、パクリタキセルの約14%が、最初の24時間以内に放出した。試料28及び29(中間コート層を含まない)では、パクリタキセルの約17%及び18%が、最初の24時間以内に放出した。14日目では、3-層試料は、パクリタキセルの約20%を放出したが、2-層試料は、パクリタキセルの約24%〜25%を放出した。
図17に示すように、中間コート層(ベースコートとトップコートとの間の第二コート層としての P(LLA-CL-GLA) の利用は、パクリタキセルの溶出速度を減少させた。ポリアクティブ(商標)トップコートの含有は、初期放出相(初期バースト)を増加させた。初期放出相の相違は、ポリアクティブ(商標)トップコートの結果であるように考えられる。しかしながら、初期バーストの後に、溶出速度は同様に見えた。試料31及び32(P(LLA-CL-GLA) の第二コート層を含む)では、パクリタキセルの約14%が、最初の24時間以内に放出した。試料28及び29(中間コート層を含まない)では、パクリタキセルの約17%及び18%が、最初の24時間以内に放出した。14日目では、3-層試料は、パクリタキセルの約20%を放出したが、2-層試料は、パクリタキセルの約24%〜25%を放出した。
表面特性
ステント上のポリマーコーティングを特徴付け、コーティング品質、均一性を観察し、及び成分を混合するために、試料の表面分析を行った。
ステント上のポリマーコーティングを特徴付け、コーティング品質、均一性を観察し、及び成分を混合するために、試料の表面分析を行った。
光学画像及びSEM像は、金属ステント上のコーティングが網目、クラッキング又はコーティング層割れがないことを示した。光学画像及びSEM像では、パクリタキセルの結晶は、見られなかった。結局、コーティングは、各ステントに均一であるようであった。コーティングのうねりが観察された。図18及び19は、各々、コーティング30及び33の光学画像を示す(100X 拡大率)。図20及び21は、コーティング30及び33のSEM画像を示す。SEM画像は、コートされたステント表面上に凹凸パターン表面を明らかにした。
共焦点ラマン画像は、各ステント上のコーティング成分の分布を示した。(金属ステント支柱に垂直である)横断面のラマン画像は、幅50 μm、深さ10又は15 μmの領域に得られた。横断面画像では、コーティング上の空気は、ラマンシグナルを有さず、コーティングは強いラマンシグナルを有し、コーティング下の金属はラマンシグナルを有さなかった。
画像中の各画素では、ラマンスペクトル全体が得られた。P(LLA-CL-GLA)、1000PEGT55PBT45、1000PETT80PBT20、パクリタキセル及びパリレン(商標)の参照スペクトルを用いて、個々の成分の画像にデータ群を逆重畳する(deconvolute)するために、拡張された制約付き最小二乗法(CLS)アルゴリズムを適用した。
試験したステント全てにおいて、生分解性ポリマー及びパクリタキセルは、完全に混合されているように見え、コーティング内で形成された分離又は薬物結晶はなかった。パクリタキセルが生分解性ポリマーに均一に混合し、コーティング中に形成された大きな相分離又は結晶がない、ことを画像は示した。加えて、コーティングの中間コート及びトップコート層は、ラマン画像で明確に見え、互いに又はパクリタキセルと混合されたようには見えなかった。従って、コーティング層の完全な状態は、これらの試料中で、保持されているようであった。
機械的試験
選択されたステントの慣用的なバルーン拡張後に、6.3x拡大率下で、ステントコーティングの目視を行い、ステント上のコーティング品質を決定した。第二ポリマーは許容されるコーティングを提供するので、目視により、多層コート層を有するステントコーティングが、パクリタキセル、ポリアクティブ(商標)及び P(LLA-CL-GLA) からなることが明らかとなった。許容されるステントコーティングは、外観、例えば、最小の表面クラッキング、ステント支柱間の最小の網目、コーティング表面の平滑なテクスチャ、及びステント基材へのコーティング粘着により特徴付けられた。
選択されたステントの慣用的なバルーン拡張後に、6.3x拡大率下で、ステントコーティングの目視を行い、ステント上のコーティング品質を決定した。第二ポリマーは許容されるコーティングを提供するので、目視により、多層コート層を有するステントコーティングが、パクリタキセル、ポリアクティブ(商標)及び P(LLA-CL-GLA) からなることが明らかとなった。許容されるステントコーティングは、外観、例えば、最小の表面クラッキング、ステント支柱間の最小の網目、コーティング表面の平滑なテクスチャ、及びステント基材へのコーティング粘着により特徴付けられた。
実施例10−P(LLA-EG-EOP) /生物活性剤ベースコートを含む代表的な多層コーティングからの生物活性剤の溶出
ステントに、モデルとなる生物活性剤としてのパクリタキセルと共に P(LLA-EG-EOP) コポリマーを含む第一コート層を提供した。これらのコーティングを調製し、先に記載したように、ステンレス鋼ステントに適用した。先に記載したように、ベースコートとして、P(LLA-EG-EOP) をパクリタキセルと共にクロロホルムに溶解した。P(LLA-EG-EOP) コポリマーの濃度は、40ミリグラム/ミリリットルであった。
ステントに、モデルとなる生物活性剤としてのパクリタキセルと共に P(LLA-EG-EOP) コポリマーを含む第一コート層を提供した。これらのコーティングを調製し、先に記載したように、ステンレス鋼ステントに適用した。先に記載したように、ベースコートとして、P(LLA-EG-EOP) をパクリタキセルと共にクロロホルムに溶解した。P(LLA-EG-EOP) コポリマーの濃度は、40ミリグラム/ミリリットルであった。
ステントの2つ群を調製した。第一群では、ポリアクティブ(商標)を含む第二コート層を適用した。第二群では、3つのコート層の合計をステントに適用した;すなわち、P(LLA-EG-EOP) からなる第二コート層をベースコート上に適用し、ポリアクティブ(商標)からなる第三コート層を第二コート層上に適用した。従って、両群について、トープコートは、ポリアクティブ(商標)からなり、P(LLA-EG-EOP) の中間-コート層の存在は、試料のいくつかに含まれた。
生物活性剤を含まないコート層について、先に記載のように、P(LLA-EG-EOP) 又はポリアクティブ(商標)ポリマーをクロロホルムに溶解して、20ミリグラム/ミリリットルの濃度にした。
コーティング組成物を超音波スプレイにより適用した。次いで、室温に設定された真空オーブン中でコートされたステントを乾燥した。
表11に、コーティング組成物及び生物活性剤の重量を示す。図22は、パクリタキセルの溶出結果を示す。
ステントの各群について、2つの試料を溶出試験に供した。1つの試料は、表面特性(光学、ラマン及びSEM)に供し、他の1つの試料は機械的試験に供した。
溶出試験
図22に示すように、中間コート層(ベースコートとトップコートとの間の第二コート層としての P(LLA-EG-EOP) の利用は、パクリタキセルの溶出速度を減少させた。ポリアクティブ(商標)トップコートの含有は、初期放出相(初期バースト)を増加させた。初期放出相の相違は、ポリアクティブ(商標)トップコートの結果であるように考えられる。
図22に示すように、中間コート層(ベースコートとトップコートとの間の第二コート層としての P(LLA-EG-EOP) の利用は、パクリタキセルの溶出速度を減少させた。ポリアクティブ(商標)トップコートの含有は、初期放出相(初期バースト)を増加させた。初期放出相の相違は、ポリアクティブ(商標)トップコートの結果であるように考えられる。
しかしながら、初期バーストの後に、溶出速度は同様に見えた。試料44及び45(P(LLA-EG-EOP) の第二コート層を含む)では、パクリタキセルの約26〜約28%が、最初の24時間以に放出した。試料48及び49(中間コート層を含まない)では、パクリタキセルの約44%〜46%が、最初の24時間以内に放出した。14日目では、3-層試料は、パクリタキセルの約73%〜75%を放出したが、2-層試料は、パクリタキセルの約80%〜84%を放出した。
実施例9及び10の結果は、P(LLA-CL-GLA) コポリマーが、P(LLA-EG-EOP) コポリマーよりも、低分子(パクリタキセル)の放出を遅らせるようである、ことを示唆する。
表面特性
ステント上のポリマーコーティングを特徴付け、コーティング品質、均一性を観察し、及び成分を混合するために、試料の表面分析を行った。
ステント上のポリマーコーティングを特徴付け、コーティング品質、均一性を観察し、及び成分を混合するために、試料の表面分析を行った。
光学画像及びSEM像は、金属ステント上のコーティングが網目、クラッキング又はコーティング層割れがないことを示した。光学画像及びSEM像では、パクリタキセルの結晶は、見られなかった。結局、コーティングは、各ステントに均一であるようであった。コーティングのうねりが観察された。図23及び24は、各々、コーティング50及び46の光学画像を示す(100X 拡大率)。図25及び26は、コーティング50及び46のSEM画像を示す。SEM画像は、コートされたステント表面上に凹凸パターン表面を明らかにした。
共焦点ラマン画像は、各ステント上のコーティング成分の分布を示した。(金属ステント支柱に垂直である)横断面のラマン画像は、幅50 μm、深さ10又は15 μmの領域に得られた。横断面画像では、コーティング上の空気は、ラマンシグナルを有さず、コーティングは強いラマンシグナルを有し、コーティング下の金属はラマンシグナルを有さなかった。
画像中の各画素では、ラマンスペクトル全体が得られた。P(LLA-CL-GLA)、1000PEGT55PBT45、1000PETT80PBT20、パクリタキセル及びパリレン(商標)の参照スペクトルを用いて、個々の成分の画像にデータ群を逆重畳する(deconvolute)するために、拡張された制約付き最小二乗法(CLS)アルゴリズムを適用した。
試験したステント全てにおいて、生分解性ポリマー及びパクリタキセルは、完全に混合されているように見え、コーティング内で形成された分離又は薬物結晶はなかった。パクリタキセルが生分解性ポリマーに均一に混合し、コーティング中に形成された大きな相分離又は結晶がない、ことを画像は示した。加えて、コーティングの中間コート及びトップコート層は、ラマン画像で明確に見え、互いに又はパクリタキセルと混合されたようには見えなかった。従って、コーティング層の完全な状態は、これらの試料中で、保持されているようであった。
機械的試験
選択されたステントの慣用的なバルーン拡張後に、6.3x拡大率下で、ステントコーティングの目視を行い、ステント上のコーティング品質を決定した。第二ポリマーは許容されるコーティングを提供するので、目視により、多層コート層を有するステントコーティングが、パクリタキセル、ポリアクティブ(商標)及び P(LLA-EG-EOP) からなることが明らかとなった。許容されるステントコーティングは、外観、例えば、最小の表面クラッキング、ステント支柱間の最小の網目、コーティング表面の平滑なテクスチャ、及びステント基材へのコーティング粘着により特徴付けられた。
選択されたステントの慣用的なバルーン拡張後に、6.3x拡大率下で、ステントコーティングの目視を行い、ステント上のコーティング品質を決定した。第二ポリマーは許容されるコーティングを提供するので、目視により、多層コート層を有するステントコーティングが、パクリタキセル、ポリアクティブ(商標)及び P(LLA-EG-EOP) からなることが明らかとなった。許容されるステントコーティングは、外観、例えば、最小の表面クラッキング、ステント支柱間の最小の網目、コーティング表面の平滑なテクスチャ、及びステント基材へのコーティング粘着により特徴付けられた。
生物活性剤の制御された放出を提供することができるコーティングの設計においては、放出曲線の形状を調整する可能性を有することが望ましい。生物活性剤の放出の時間プロファイルは、(まるで階段関数のように)薬物が直ちに全てを溶出する速放から、薬物が何ケ月又は何年にも渡って最終的に放出される、非常に遅い、直線的(ゼロオーダー)放出までの範囲にわたることができる。薬物及び治療される症状によって、所定の様々な放出プロファイルが存在する。生分解性ポリマーのブレンドを含むコーティングをつくる目的は、段階関数と、低-傾斜の、ゼロ-オーダー放出との間にある放出プロファイルの広範な範囲を得ることができることである。
生物活性剤の放出を制御する主な戦略の1つは、生物活性剤の初期放出(又は「バースト」)を制限することである。このことが達成することができれば、より多くの生物活性剤が、より長期の放出期間、より後の時期に利用することができる。本明細書に記載のポリマーのブレンドからなる生分解性コーティングの含有は、コーティングからの生物活性剤のバーストを制限する又はなくすさえするために設計される。生物活性剤は、初期バーストがより長期間に渡って作用部位に放出された後に、コーティング中に依然として残っている。バースト後の放出プロファイルの形状(放出された薬物のパーセンテージ対時間)は、同様に、ブレンド系を含むポリマーとコーティング中の生物活性剤との組成によって、直線的もしくは対数的、又はより複雑な形状に制御することができる。
治療的範囲が、(例えば、医師により)一旦決定されると、本発明のコーティングは、治療的範囲内ある投薬量で生物活性剤を提供するように調整することができる。本発明の組成物は、生物活性剤の放出を制御するための改良された手段を提供するものであり、よって、所望の速度及び量で生物活性剤を送達する高い能力を提供する。
先の実施例で議論した結果は、本発明のブレンド生分解性コーティング組成物が、生物活性剤の初期放出を制限し、放出プロファイル曲線の形状の制御を提供することができる、ことを示す。
本発明の他の実施態様は、本明細書を考慮して又は本明細書に開示された発明の実施から、当業者に明らかであろう。本明細書に記載の本質及び実施態様についての様々な省略、修正、及び変更は、クレームによって示される発明の真の範囲及び趣旨から逸脱することなく当業者によって行うことができる。これによって、本明細書に引用された全ての特許、特許文献、及び刊行物は、あたかも各々が引用されるように、参照として本明細書に引用される。
Claims (46)
- 表面に、生物活性剤を放出するコーティングを有する移植可能医療物品であって、当該コーティングが以下:
(a) 生物活性剤及び第一生分解性ポリマーを含む第一コート層、ここで、当該第一生分解性ポリマーは、ポリアルキレングリコールテレフタレートと芳香族ポリエステルとのコポリマーである;及び
(b) 第一コート層の少なくとも1部分を覆い、かつ第二生分解性ポリマーを含む、第二コート層
を含み、
ここで、第一生分解性ポリマーと第二生分解性ポリマーとは相違し、そして、第二生分解性ポリマーは、第一生分解性ポリマーに比べてより遅い生物活性剤放出速度を有するように選択される、前記物品。 - 前記ポリアルキレングリコールテレフタレートが、ポリエチレングリコールテレフタレート、ポリプロピレングリコールテレフタレート、ポリブチレングリコールテレフタレート及びそれらの組み合わせから選ばれる、請求項1記載の物品。
- 前記ポリアルキレングリコールが、ポリエチレングリコールである、請求項2記載の物品。
- 前記ポリエステルが、ポリエチレンテレフタレート、ポリプロピレンテレフタレート、ポリブチレンテレフタレート及びそれらの組み合わせから選ばれる、請求項1記載の物品。
- 前記ポリエステルが、ポリブチレンテレフタレートである、請求項4記載の物品。
- 前記第二生分解性ポリマーが、第一生分解性ポリマーに比べてより疎水性である、請求項1記載の物品。
- 前記第二生分解性ポリマーが、乳酸、グリコール酸、カプロラクトン、エチレングリコール及びエチルオキシリン酸エステルから選ばれるモノマーから得られるポリマーを含む、請求項1記載の物品。
- 前記生物活性剤が、疎水性の低分子生物活性剤である、請求項1記載の物品。
- 前記生物活性剤が、1500以下の分子量を有する、請求項8記載の物品。
- 前記生物活性剤が、抗-増殖剤、抗-炎症剤、免疫抑制剤、低分子の抗生物質、エストロゲン及びそれらの任意の組み合わせから選ばれる、請求項9記載の物品。
- 前記生物活性剤が、アクチノマイシンD、パクリタキセル、タキサン、デキサメタゾン、プレドニソロン、トラニラスト、シクロスポリン、エベロリムス、マイコフェノール酸、シロリムス、タクロリムス、エストラジオール及びそれらの任意の組み合わせから選ばれる、請求項10記載の物品。
- 前記第一コート層内の総生物活性剤の含量が、50%以下である、請求項1記載の物品。
- 2以上の生物活性剤が、コーティング中に含まれる、請求項1記載の物品。
- 生物的環境中における物品の配置により前記生物活性剤が放出され、そして、その放出は、生物的環境における物品の配置後24時間以内で10%未満である、請求項9記載の物品。
- 前記生物活性剤放出が、生物的環境における物品の配置後24時間以内で2%未満である、請求項14記載の物品。
- 前記生物活性剤放出が、生物的環境における物品の配置後7日以内で20%未満である、請求項14記載の物品。
- 物品が患者内に移植されるとき、前記生物活性剤が、少なくとも1週間、治療上有効濃度で放出される、請求項9記載の物品。
- 物品が患者内に移植されるとき、前記生物活性剤が、少なくとも4週間、治療上有効濃度で放出される、請求項9記載の物品。
- 前記コーティングが、総物品表面積の100%未満を含む物品の表面に提供される、請求項1記載の物品。
- 前記生物活性剤放出コーティングが、パリレン、シラン、シロキサン、ポリウレタン、ポリブタジエン、ポリカルボジイミド又はそれらの任意の混合物を含むコーティング層を更に含む、請求項1記載の物品。
- 前記表面が、表面テクスチャを備える、請求項1記載の物品。
- ステント、グラフト、カテーテル、弁、心臓用具、眼科用具又は創傷包帯である、請求項1記載の物品。
- 表面に、生物活性剤放出コーティングを有する移植可能医療物品であって、当該コーティングが以下:
(a) 生物活性剤及び第二生分解性ポリマーを含む第一コート層;並びに
(b) ポリアルキレングリコールテレフタレートと芳香族ポリエステルとのコポリマーであるポリエーテルエステルコポリマーを含む、外側コート層、
を含み、
ここで、ポリエーテルエステルコポリマーと第二生分解性ポリマーとは相違し、そして、第二生分解性ポリマーは、ポリエーテルエステルコポリマーに比べてより遅い生物活性剤放出速度を有するように選択される、前記物品。 - 前記コーティングが、第一コート層と外側コート層との間に配置される1以上の中間コート層を更に含む、請求項23記載の物品。
- 前記の1以上の中間コート層が、ポリエーテルエステルコポリマー以外のポリマーを含む、請求項23記載の物品。
- 前記ポリアルキレングリコールテレフタレートが、ポリエチレングリコールテレフタレート、ポリプロピレングリコールテレフタレート、ポリブチレングリコールテレフタレート及びそれらの組み合わせから選ばれる、請求項23記載の物品。
- 前記ポリエステルが、ポリエチレンテレフタレート、ポリプロピレンテレフタレート、ポリブチレンテレフタレート及びそれらの組み合わせから選ばれる、請求項23記載の物品。
- 前記ポリアルキレングリコールテレフタレートが、ポリエチレングルコールテレフタレートであり、かつ、前記ポリエステルが、ポリブチレンテレフタレートである、請求項23記載の物品。
- 前記第二生分解性ポリマーが、ポリエーテルエステルコポリマーに比べてより疎水性である、請求項23記載の物品。
- 前記第二生分解性ポリマーが、乳酸、グリコール酸、カプロラクトン、エチレングリコール及びエチルオキシリン酸エステルから選ばれるモノマーから得られるポリマーを含む、請求項24記載の物品。
- 前記生物活性剤が、1500以下の分子量を有する、請求項23記載の物品。
- 前記生物活性剤が、抗-増殖剤、抗-炎症剤、免疫抑制剤、低分子の抗生物質、エストロゲン及びそれらの任意の組み合わせから選ばれる、請求項31記載の物品。
- 前記生物活性剤が、アクチノマイシンD、パクリタキセル、タキサン、デキサメタゾン、プレドニソロン、トラニラスト、シクロスポリン、エベロリムス、マイコフェノール酸、シロリムス、タクロリムス、エストラジオール及びそれらの任意の組み合わせから選ばれる、請求項32記載の物品。
- 前記第一コート層内の総生物活性剤の含量が、50%以下である、請求項23記載の物品。
- 生物的環境中における物品の配置により前記生物活性剤が放出され、そして、その放出は、生物的環境における物品の配置後24時間以内で35%未満である、請求項31記載の物品。
- 前記生物活性剤放出が、生物的環境における物品の配置後7日以内で20%未満である、請求項31記載の物品。
- 物品が患者内に移植されるとき、前記生物活性剤が、少なくとも1週間、治療上有効濃度で放出される、請求項31記載の物品。
- 前記コーティングが、総物品表面積の100%未満を含む物品の表面上に提供される、請求項23記載の物品。
- 前記生物活性剤放出コーティングが、パリレン、シラン、シロキサン、ポリウレタン、ポリブタジエン、ポリカルボジイミド又はそれらの任意の混合物を更に含む、請求項23記載の物品。
- 前記表面が、表面テクスチャを備える、請求項23記載の物品。
- ステント、グラフト、カテーテル、弁、心臓用具、眼科用具又は創傷包帯である、請求項23記載の物品。
- 表面に、生物活性剤放出コーティングを有する移植可能医療物品であって、当該コーティングが以下:
(a) 生物活性剤及び第一生分解性ポリマーを含む第一コート層、ここで、当該第一生分解性ポリマーは、ポリアルキレングリコールテレフタレートと芳香族ポリエステルとのコポリマーであり;
(b) 第一コート層の少なくとも1部分を覆い、かつ第二生分解性ポリマーを含む、第二コート層;及び
(c) ポリアルキレングリコールテレフタレートと芳香族ポリエステルとのコポリマーを含む第三コート層、
を含み、
ここで、第一生分解性ポリマーと第二生分解性ポリマーとは相違し、そして、第二生分解性ポリマーは、第一生分解性ポリマーに比べてより遅い生物活性剤放出速度を有するように選択される、前記物品。 - 前記の第三コートポリマーのコポリマーが、第一コート層の第一生分解性ポリマーと同一である、請求項42記載の物品。
- 移植可能医療物品の製造法であって、以下のステップ:
(a) 医療物品を提供し;
(b) 医療物品上に第一コート層を提供するために、医療物品の表面に第一コーティング組成物を処置し、ここで、当該第一コーティング組成物は、生物活性剤及び第一生分解性ポリマーを含み、当該第一生分解性ポリマーは、ポリアルキレングリコールテレフタレートと芳香族ポリエステルとのコポリマーであり;並びに
(c) 第一コート層上に第二コーティング組成物を処置すること、当該第二コーティング組成物は、第一生分解性ポリマーとは異なる第二生分解性ポリマーを含む、
を含み、
ここで、第二生分解性ポリマーは、第一生分解性ポリマーに比べてより遅い生物活性剤放出速度を有するように選択される、前記方法。 - 移植可能医療物品の製造法であって、以下のステップ:
(a) 医療物品を提供し;
(b) 医療物品上に第一コート層を提供するために、医療物品の表面に第一コーティング組成物を処置し、ここで、当該第一コーティング組成物は、生物活性剤及び第二生分解性ポリマーを含み;並びに
(c) 第一コート層上に外側コーティング組成物を処置すること、当該外側コーティング組成物は、ポリアルキレングリコールテレフタレートと芳香族ポリエステルとのコポリマーであるポリエーテルエステルコポリマーを含む、
を含み、
ここで、ポリエーテルエステルコポリマーと第二生分解性ポリマーは相違し、そして、第二生分解性ポリマーは、ポリエーテルエステルコポリマーに比べてより遅い生物活性剤放出速度を有するように選択される、前記方法。 - 制御された方式での患者への生物活性剤の送達法であって、以下のステップ:
(a) 請求項1に記載の物品を患者に提供し;及び
(b) 生物活性剤が制御された方式でコーティング組成物から放出される期間である、選択された期間中、患者内に当該物品を維持すること、
を含む、前記方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US64155705P | 2005-01-05 | 2005-01-05 | |
| US11/316,787 US20060147491A1 (en) | 2005-01-05 | 2005-12-22 | Biodegradable coating compositions including multiple layers |
| PCT/US2006/000528 WO2006074406A2 (en) | 2005-01-05 | 2006-01-05 | Biodegradable coating compositions including multiple layers |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2008526322A true JP2008526322A (ja) | 2008-07-24 |
Family
ID=36580579
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007549730A Pending JP2008526322A (ja) | 2005-01-05 | 2006-01-05 | 多層を含む生分解性コーティング組成物 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20060147491A1 (ja) |
| EP (1) | EP1841472A2 (ja) |
| JP (1) | JP2008526322A (ja) |
| CA (1) | CA2594030A1 (ja) |
| WO (1) | WO2006074406A2 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013524903A (ja) * | 2010-04-19 | 2013-06-20 | インノラ・ゲー・エム・ベー・ハー | リムス被覆医療デバイス |
| JP2018507765A (ja) * | 2015-02-27 | 2018-03-22 | ポリガニクス アイピー ベーフェー | 薬物溶出発泡体及びその製造 |
Families Citing this family (51)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7846202B2 (en) * | 1995-06-07 | 2010-12-07 | Cook Incorporated | Coated implantable medical device |
| CA2178541C (en) * | 1995-06-07 | 2009-11-24 | Neal E. Fearnot | Implantable medical device |
| US7611533B2 (en) | 1995-06-07 | 2009-11-03 | Cook Incorporated | Coated implantable medical device |
| PT1509256E (pt) | 2002-05-24 | 2009-10-15 | Angiotech Int Ag | Composições e métodos de revestimento de implantes médicos |
| US8313760B2 (en) | 2002-05-24 | 2012-11-20 | Angiotech International Ag | Compositions and methods for coating medical implants |
| EP1781264B1 (en) | 2004-08-04 | 2013-07-24 | Evonik Corporation | Methods for manufacturing delivery devices and devices thereof |
| US20060147491A1 (en) * | 2005-01-05 | 2006-07-06 | Dewitt David M | Biodegradable coating compositions including multiple layers |
| US20060198868A1 (en) * | 2005-01-05 | 2006-09-07 | Dewitt David M | Biodegradable coating compositions comprising blends |
| KR100511618B1 (ko) * | 2005-01-17 | 2005-08-31 | 이경범 | 약물방출 조절형 다층 코팅 스텐트 및 이의 제조방법 |
| WO2007079209A2 (en) * | 2005-12-30 | 2007-07-12 | C. R. Bard, Inc. | Catheter including a catheter valve, method of at least partially coating a catheter valve surface, and an apparatus for at least partially opening a catheter valve |
| WO2007140320A2 (en) * | 2006-05-26 | 2007-12-06 | Nanyang Technological University | Implantable article, method of forming same and method for reducing thrombogenicity |
| EP2044140B1 (en) | 2006-07-20 | 2017-05-17 | OrbusNeich Medical, Inc. | Bioabsorbable polymeric composition for a medical device |
| US8900619B2 (en) * | 2006-08-24 | 2014-12-02 | Boston Scientific Scimed, Inc. | Medical devices for the release of therapeutic agents |
| WO2008070304A2 (en) | 2006-10-20 | 2008-06-12 | Orbusneich Medical, Inc. | Bioabsorbable polymeric composition and medical device background |
| US7959942B2 (en) | 2006-10-20 | 2011-06-14 | Orbusneich Medical, Inc. | Bioabsorbable medical device with coating |
| ES2409759T3 (es) | 2007-01-21 | 2013-06-27 | Hemoteq Ag | Producto médico para el tratamiento de la estenosis de los canales del cuerpo y para la prevención de la estenosis amenazante |
| US20080208315A1 (en) * | 2007-02-27 | 2008-08-28 | National Taiwan University Of Science & Technology | Coronary stent having a surface of multi-layer immobilized structures |
| EP2134380A2 (en) * | 2007-03-28 | 2009-12-23 | Boston Scientific Scimed, Inc. | Medical devices having bioerodable layers for the release of therapeutic agents |
| US9056155B1 (en) * | 2007-05-29 | 2015-06-16 | Abbott Cardiovascular Systems Inc. | Coatings having an elastic primer layer |
| US9192697B2 (en) | 2007-07-03 | 2015-11-24 | Hemoteq Ag | Balloon catheter for treating stenosis of body passages and for preventing threatening restenosis |
| WO2009064442A1 (en) * | 2007-11-13 | 2009-05-22 | Brookwood Pharmaceuticals, Inc. | Viscous terpolymers as drug delivery platform |
| EP2222281B1 (en) | 2007-12-20 | 2018-12-05 | Evonik Corporation | Process for preparing microparticles having a low residual solvent volume |
| US8206636B2 (en) | 2008-06-20 | 2012-06-26 | Amaranth Medical Pte. | Stent fabrication via tubular casting processes |
| US10898620B2 (en) | 2008-06-20 | 2021-01-26 | Razmodics Llc | Composite stent having multi-axial flexibility and method of manufacture thereof |
| US8206635B2 (en) | 2008-06-20 | 2012-06-26 | Amaranth Medical Pte. | Stent fabrication via tubular casting processes |
| US8974808B2 (en) * | 2008-12-23 | 2015-03-10 | Surmodics, Inc. | Elastic implantable composites and implants comprising same |
| US9415197B2 (en) * | 2008-12-23 | 2016-08-16 | Surmodics, Inc. | Implantable suction cup composites and implants comprising same |
| US9480643B2 (en) * | 2008-12-23 | 2016-11-01 | Surmodics Pharmaceuticals, Inc. | Implantable composites and implants comprising same |
| US20100168807A1 (en) * | 2008-12-23 | 2010-07-01 | Burton Kevin W | Bioactive terpolymer compositions and methods of making and using same |
| US8951546B2 (en) * | 2008-12-23 | 2015-02-10 | Surmodics Pharmaceuticals, Inc. | Flexible implantable composites and implants comprising same |
| US9265633B2 (en) | 2009-05-20 | 2016-02-23 | 480 Biomedical, Inc. | Drug-eluting medical implants |
| US8888840B2 (en) * | 2009-05-20 | 2014-11-18 | Boston Scientific Scimed, Inc. | Drug eluting medical implant |
| EP2451496B1 (en) | 2009-07-10 | 2015-07-22 | Boston Scientific Scimed, Inc. | Use of nanocrystals for a drug delivery balloon |
| EP2962707B1 (en) | 2009-07-17 | 2019-07-24 | Boston Scientific Scimed, Inc. | Drug delivery balloons with improved crystal size and density |
| WO2011035190A1 (en) * | 2009-09-18 | 2011-03-24 | Nano Terra Inc. | Polyolefin fibers for use as battery separators and methods of making and using the same |
| WO2012030823A1 (en) | 2010-08-30 | 2012-03-08 | Surmodics Pharmaceuticals, Inc. | Biodegradable terpolymers and terpolymer blends as pressure-sensitive adhesives |
| EP2611476B1 (en) | 2010-09-02 | 2016-08-10 | Boston Scientific Scimed, Inc. | Coating process for drug delivery balloons using heat-induced rewrap memory |
| US8669360B2 (en) | 2011-08-05 | 2014-03-11 | Boston Scientific Scimed, Inc. | Methods of converting amorphous drug substance into crystalline form |
| US9056152B2 (en) | 2011-08-25 | 2015-06-16 | Boston Scientific Scimed, Inc. | Medical device with crystalline drug coating |
| EP2758183B1 (en) | 2011-09-18 | 2022-02-09 | Bio Plasmar Ltd | Bio-degradable plant pot or foodware |
| US10842802B2 (en) | 2013-03-15 | 2020-11-24 | Medicis Pharmaceutical Corporation | Controlled release pharmaceutical dosage forms |
| US10293044B2 (en) | 2014-04-18 | 2019-05-21 | Auburn University | Particulate formulations for improving feed conversion rate in a subject |
| ES2782428T3 (es) | 2014-04-18 | 2020-09-15 | Univ Auburn | Formulaciones vacunales de partículas para la inducción de inmunidad innata y adaptativa |
| US20150328373A1 (en) * | 2014-05-19 | 2015-11-19 | Abbott Cardiovascular Systems Inc. | Additives To Increase Degradation Rate Of A Biodegradable Scaffolding And Methods Of Forming Same |
| US9238090B1 (en) | 2014-12-24 | 2016-01-19 | Fettech, Llc | Tissue-based compositions |
| US10583199B2 (en) | 2016-04-26 | 2020-03-10 | Northwestern University | Nanocarriers having surface conjugated peptides and uses thereof for sustained local release of drugs |
| CN108883211B (zh) * | 2016-05-04 | 2021-09-24 | 北京阿迈特医疗器械有限公司 | 改性的可生物降解的医用聚合物装置及其制备方法 |
| CN105903092A (zh) * | 2016-06-23 | 2016-08-31 | 刘芸 | 子宫置入物及子宫置入物的置入系统 |
| US10941270B2 (en) | 2018-03-09 | 2021-03-09 | John Nguyen Ta | Biodegradation of polymer using surface chemistry |
| US10960110B2 (en) * | 2018-08-21 | 2021-03-30 | Jian Xie | Iron-based biodegradable metals for implantable medical devices |
| CN114940747A (zh) * | 2022-05-05 | 2022-08-26 | 红色未来科技(北京)有限公司 | 一种具有形状记忆功能的面部填充剂及其应用 |
Family Cites Families (62)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US254638A (en) * | 1882-03-07 | John geayes | ||
| US287184A (en) * | 1883-10-23 | Isbael e | ||
| GB1425577A (en) * | 1972-06-30 | 1976-02-18 | Ici Ltd | Prosthetics comprising plastics materials |
| US3952016A (en) * | 1974-03-18 | 1976-04-20 | Lever Brothers Company | 2-Keto-6-substituted dioxane-(1,4) compounds |
| US3959185A (en) * | 1974-03-18 | 1976-05-25 | Lever Brothers Company | Perfume blend including 2-keto-6-substituted-dioxanes-(1,4) |
| US4052988A (en) * | 1976-01-12 | 1977-10-11 | Ethicon, Inc. | Synthetic absorbable surgical devices of poly-dioxanone |
| US4070375A (en) * | 1976-08-05 | 1978-01-24 | Chevron Research Company | Process for preparing 1,4-dioxan-2-ones |
| US4286064A (en) * | 1979-11-05 | 1981-08-25 | Riker Laboratories, Inc. | Process for isolating active debriding agent from bromelain |
| NZ203337A (en) * | 1982-02-26 | 1986-02-21 | M S M Lefebvre | Immobilised inorganic counter diffusion barriers and their applications |
| SE445884B (sv) * | 1982-04-30 | 1986-07-28 | Medinvent Sa | Anordning for implantation av en rorformig protes |
| US4733665C2 (en) * | 1985-11-07 | 2002-01-29 | Expandable Grafts Partnership | Expandable intraluminal graft and method and apparatus for implanting an expandable intraluminal graft |
| SE453258B (sv) * | 1986-04-21 | 1988-01-25 | Medinvent Sa | Elastisk, sjelvexpanderande protes samt forfarande for dess framstellning |
| US4800882A (en) * | 1987-03-13 | 1989-01-31 | Cook Incorporated | Endovascular stent and delivery system |
| US4894231A (en) * | 1987-07-28 | 1990-01-16 | Biomeasure, Inc. | Therapeutic agent delivery system |
| EP0310361A3 (en) * | 1987-09-30 | 1989-05-24 | Beckman Instruments, Inc. | Tridentate conjugate and method of use thereof |
| US4886062A (en) * | 1987-10-19 | 1989-12-12 | Medtronic, Inc. | Intravascular radially expandable stent and method of implant |
| US5120802A (en) * | 1987-12-17 | 1992-06-09 | Allied-Signal Inc. | Polycarbonate-based block copolymers and devices |
| US4891263A (en) * | 1987-12-17 | 1990-01-02 | Allied-Signal Inc. | Polycarbonate random copolymer-based fiber compositions and method of melt-spinning same and device |
| US4916193A (en) * | 1987-12-17 | 1990-04-10 | Allied-Signal Inc. | Medical devices fabricated totally or in part from copolymers of recurring units derived from cyclic carbonates and lactides |
| US5252701A (en) * | 1990-07-06 | 1993-10-12 | American Cyanamid Company | Segmented absorbable copolymer |
| MX9205298A (es) * | 1991-09-17 | 1993-05-01 | Steven Carl Quay | Medios gaseosos de contraste de ultrasonido y metodo para seleccionar gases para usarse como medios de contraste de ultrasonido |
| US5811447A (en) * | 1993-01-28 | 1998-09-22 | Neorx Corporation | Therapeutic inhibitor of vascular smooth muscle cells |
| US5464450A (en) * | 1991-10-04 | 1995-11-07 | Scimed Lifesystems Inc. | Biodegradable drug delivery vascular stent |
| JPH07505813A (ja) * | 1992-04-24 | 1995-06-29 | オステオテク,インコーポレイテッド | 組織癒着予防装置 |
| US5443458A (en) * | 1992-12-22 | 1995-08-22 | Advanced Cardiovascular Systems, Inc. | Multilayered biodegradable stent and method of manufacture |
| US5464650A (en) * | 1993-04-26 | 1995-11-07 | Medtronic, Inc. | Intravascular stent and method |
| US5448035A (en) * | 1993-04-28 | 1995-09-05 | Advanced Surfaces And Processes, Inc. | Method and apparatus for pulse fusion surfacing |
| US5994341A (en) * | 1993-07-19 | 1999-11-30 | Angiogenesis Technologies, Inc. | Anti-angiogenic Compositions and methods for the treatment of arthritis |
| US5466233A (en) * | 1994-04-25 | 1995-11-14 | Escalon Ophthalmics, Inc. | Tack for intraocular drug delivery and method for inserting and removing same |
| US5641501A (en) * | 1994-10-11 | 1997-06-24 | Ethicon, Inc. | Absorbable polymer blends |
| US5980948A (en) * | 1996-08-16 | 1999-11-09 | Osteotech, Inc. | Polyetherester copolymers as drug delivery matrices |
| US6261537B1 (en) * | 1996-10-28 | 2001-07-17 | Nycomed Imaging As | Diagnostic/therapeutic agents having microbubbles coupled to one or more vectors |
| EP0973818B1 (en) * | 1997-04-03 | 2004-10-13 | Guilford Pharmaceuticals Inc. | Biodegradable terephthalate polyester-poly(phosphate) polymers, compositions, articles, and methods for making and using the same |
| US6077916A (en) * | 1997-06-04 | 2000-06-20 | The Penn State Research Foundation | Biodegradable mixtures of polyphoshazene and other polymers |
| US6153252A (en) * | 1998-06-30 | 2000-11-28 | Ethicon, Inc. | Process for coating stents |
| US6419709B1 (en) * | 1998-10-02 | 2002-07-16 | Guilford Pharmaceuticals, Inc. | Biodegradable terephthalate polyester-poly(Phosphite) compositions, articles, and methods of using the same |
| US6153212A (en) * | 1998-10-02 | 2000-11-28 | Guilford Pharmaceuticals Inc. | Biodegradable terephthalate polyester-poly (phosphonate) compositions, articles, and methods of using the same |
| US6419692B1 (en) * | 1999-02-03 | 2002-07-16 | Scimed Life Systems, Inc. | Surface protection method for stents and balloon catheters for drug delivery |
| US6258121B1 (en) * | 1999-07-02 | 2001-07-10 | Scimed Life Systems, Inc. | Stent coating |
| CA2379909C (en) * | 1999-08-06 | 2011-01-04 | Board Of Regents, The University Of Texas System | Drug releasing biodegradable fiber implant |
| US6579533B1 (en) * | 1999-11-30 | 2003-06-17 | Bioasborbable Concepts, Ltd. | Bioabsorbable drug delivery system for local treatment and prevention of infections |
| US6338739B1 (en) * | 1999-12-22 | 2002-01-15 | Ethicon, Inc. | Biodegradable stent |
| US6703040B2 (en) * | 2000-01-11 | 2004-03-09 | Intralytix, Inc. | Polymer blends as biodegradable matrices for preparing biocomposites |
| ES2312456T3 (es) * | 2000-08-30 | 2009-03-01 | Johns Hopkins University | Dispositivos para suministro intraocular de farmacos. |
| EP1247537A1 (en) * | 2001-04-04 | 2002-10-09 | Isotis B.V. | Coating for medical devices |
| EP2316394B1 (en) * | 2001-06-12 | 2016-11-23 | The Johns Hopkins University | Reservoir device for intraocular drug delivery |
| AU2002341959A1 (en) * | 2001-10-04 | 2003-04-14 | Case Western Reserve University | Drug delivery devices and methods |
| US20030153971A1 (en) * | 2002-02-14 | 2003-08-14 | Chandru Chandrasekaran | Metal reinforced biodegradable intraluminal stents |
| AU2003241515A1 (en) * | 2002-05-20 | 2003-12-12 | Orbus Medical Technologies Inc. | Drug eluting implantable medical device |
| US20040002755A1 (en) * | 2002-06-28 | 2004-01-01 | Fischell David R. | Method and apparatus for treating vulnerable coronary plaques using drug-eluting stents |
| US7192484B2 (en) * | 2002-09-27 | 2007-03-20 | Surmodics, Inc. | Advanced coating apparatus and method |
| AU2003279055A1 (en) * | 2002-09-29 | 2004-04-19 | Surmodics, Inc. | Methods for treatment and/or prevention of retinal disease |
| US6702850B1 (en) * | 2002-09-30 | 2004-03-09 | Mediplex Corporation Korea | Multi-coated drug-eluting stent for antithrombosis and antirestenosis |
| US7323289B2 (en) * | 2002-10-08 | 2008-01-29 | Brewer Science Inc. | Bottom anti-reflective coatings derived from small core molecules with multiple epoxy moieties |
| US6852122B2 (en) * | 2003-01-23 | 2005-02-08 | Cordis Corporation | Coated endovascular AAA device |
| US20040215313A1 (en) * | 2003-04-22 | 2004-10-28 | Peiwen Cheng | Stent with sandwich type coating |
| DE602004028638D1 (de) * | 2003-05-02 | 2010-09-23 | Surmodics Inc | System zur kontrollierten Freisetzung eines bioaktiven Wirkstoffs im hinteren Bereich des Auges |
| US7435788B2 (en) * | 2003-12-19 | 2008-10-14 | Advanced Cardiovascular Systems, Inc. | Biobeneficial polyamide/polyethylene glycol polymers for use with drug eluting stents |
| US20050214339A1 (en) * | 2004-03-29 | 2005-09-29 | Yiwen Tang | Biologically degradable compositions for medical applications |
| US20050287184A1 (en) * | 2004-06-29 | 2005-12-29 | Hossainy Syed F A | Drug-delivery stent formulations for restenosis and vulnerable plaque |
| WO2006014484A2 (en) * | 2004-07-02 | 2006-02-09 | Surmodics, Inc. | Methods and devices for the treatment of ocular conditions |
| US20060147491A1 (en) * | 2005-01-05 | 2006-07-06 | Dewitt David M | Biodegradable coating compositions including multiple layers |
-
2005
- 2005-12-22 US US11/316,787 patent/US20060147491A1/en not_active Abandoned
-
2006
- 2006-01-05 WO PCT/US2006/000528 patent/WO2006074406A2/en active Application Filing
- 2006-01-05 JP JP2007549730A patent/JP2008526322A/ja active Pending
- 2006-01-05 EP EP06717696A patent/EP1841472A2/en not_active Withdrawn
- 2006-01-05 CA CA002594030A patent/CA2594030A1/en not_active Abandoned
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013524903A (ja) * | 2010-04-19 | 2013-06-20 | インノラ・ゲー・エム・ベー・ハー | リムス被覆医療デバイス |
| JP2018507765A (ja) * | 2015-02-27 | 2018-03-22 | ポリガニクス アイピー ベーフェー | 薬物溶出発泡体及びその製造 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20060147491A1 (en) | 2006-07-06 |
| WO2006074406A2 (en) | 2006-07-13 |
| WO2006074406A3 (en) | 2006-12-21 |
| EP1841472A2 (en) | 2007-10-10 |
| CA2594030A1 (en) | 2006-07-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2008526322A (ja) | 多層を含む生分解性コーティング組成物 | |
| JP2008526371A (ja) | ブレンドを含む生分解性コーティング組成物 | |
| US9468707B2 (en) | Biodegradable triblock copolymers for implantable devices | |
| EP1808167B1 (en) | Drug-eluting articles with improved drug release profiles | |
| JP5026956B2 (ja) | 医療用具のための天然生分解性多糖コーティング | |
| JP5463003B2 (ja) | 医療用生体分解性組成物 | |
| EP1986711B1 (en) | Implantable medical device with surface-eroding polyester drug delivery coating | |
| CN102596278B (zh) | 包含含有双-(α-氨基-二醇-二酯)的聚酯酰胺的涂层 | |
| US7442721B2 (en) | Durable biocompatible controlled drug release polymeric coatings for medical devices | |
| US8257729B2 (en) | Implants with membrane diffusion-controlled release of active ingredient | |
| EP2442841B1 (en) | Implantable medical devices and coatings therefor comprising block copolymers of poly (ethylene glycol) and a poly (lactide-glycolide) | |
| US8952123B1 (en) | Dioxanone-based copolymers for implantable devices | |
| JP2007530169A (ja) | 生物適合性表面を調製するための組成物及び方法 | |
| WO2006002399A2 (en) | Biodegradable implantable medical devices, methods and systems | |
| JP2007512094A (ja) | 乳酸のポリマーを含む埋め込み型用具用コーティングおよびこのコーティングの製造方法 | |
| JP2007530173A (ja) | 生体適合性表面のための方法およびシステム | |
| US20070020312A1 (en) | Method of fabricating a bioactive agent-releasing implantable medical device |