JP2006517032A - ある種の癌治療の有効性を評価するための方法 - Google Patents
ある種の癌治療の有効性を評価するための方法 Download PDFInfo
- Publication number
- JP2006517032A JP2006517032A JP2006503077A JP2006503077A JP2006517032A JP 2006517032 A JP2006517032 A JP 2006517032A JP 2006503077 A JP2006503077 A JP 2006503077A JP 2006503077 A JP2006503077 A JP 2006503077A JP 2006517032 A JP2006517032 A JP 2006517032A
- Authority
- JP
- Japan
- Prior art keywords
- sample
- kda
- therapeutic agent
- caspase
- fragment
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/573—Immunoassay; Biospecific binding assay; Materials therefor for enzymes or isoenzymes
Abstract
Description
腫瘍細胞が見られる身体組織、または該治療薬で処置する哺乳類からの体液のサンプルを得ること、ここで、該組織または体液はカスパーゼ3の17kDa断片を含み得、この断片はin vivoにおけるカスパーゼ3の特異的切断によって得られたものである;
該カスパーゼ3の17kDa断片の存在量を測定すべく該サンプルをアッセイすること;
該治療薬を該哺乳類に投与すること;
該哺乳類から、該身体組織または体液の第二のサンプルを得ること;および
該切断カスパーゼ3の17kDa断片の存在量を測定すべく該第二のサンプルをアッセイすること
を含み、該第一のサンプルで測定された量に対する、該第二のサンプルで測定された該17kDa断片の量の増加が、該治療薬によるアポトーシス刺激および該治療薬の有効性に相関する。
図1はP30およびP6カラムで精製したマウス血漿由来の17kDa切断カスパーゼ3サブユニットを示す。
図2はTfRscFv−LipA−p53の静注後のPanc−1異種移植片における外因性wtp53の発現および17kDaカスパーゼ3サブユニットの発現を示す。
図3はPanc−1異種移植片における、葉酸−LipA−p53複合体静注後の経時的な17kDaカスパーゼ3サブユニットの発現を示す。図中、UT=対照として用いた非処置動物;Fpp53=葉酸−リポソームA−p53複合体;およびFpVec=エンプティーベクターを有する葉酸−リポソームA複合体。
図4はトランスフェリン−リポソームA−p53複合体およびシスプラチン(CDDP)で処置した後のDU145担癌マウスから抽出した血液細胞ペレットにおける17kDaタンパク質の存在を示す。
図5はトランスフェリン−リポソームA−p53を含む複合体とシスプラチンの組合せで処置した後の、PANC−1異種移植片腫瘍を持つ、または持たないマウス由来の血清における、カスパーゼ3の17kDaサブユニットの存在を示す。
図6はTfRscFv−リポソームA−アンチセンスHER−2の複合体で処置した後のPANC−1細胞におけるカスパーゼ3の17kDaサブユニットの存在を、TfRscFv−リポソームA−スクランブルHER−2の複合体で処置した、かかる細胞と比較して示す。
図7はTfRscFv−リポソームA−アンチセンスHER−2複合体とジェムザール(Gemzar)(登録商標)の組合せで処置した後の、PANC−1細胞におけるカスパーゼ3の17kDaサブユニットの存在を、非処置細胞と、また、ジェムザール(登録商標)単独、TfRscFv−リポソームA−ASHER−2複合体単独、またはTfRscFv−リポソームA−スクランブルHER−2複合体とジェムザール(登録商標)の組合せのいずれかで処置したものと比較して示す。
図8はTfRscFv−リポソームA−アンチセンスHER−2の複合体とジェムザール(登録商標)の組合せの静脈投与後のPANC−1異種移植片腫瘍担持マウス由来の血漿におけるカスパーゼ3の17kDaサブユニットの存在を、非処置動物と、また、ジェムザール(登録商標)単独、TfRscFv−リポソームA−AS HER−2複合体単独またはTfRscFv−リポソームA−スクランブルHER−2の複合体とジェムザール(登録商標)の組合せのいずれかで処置したものと比較して示す。
図9Aおよび9Bは、各々、PANC−1およびCOLO357細胞のトランスフェクション8時間後の、TfRscFv−リポソームA−アンチセンスHER−2単独による、またはジェムザール(登録商標)との組合せによるアポトーシス経路におけるタンパク質発現のin vitro抑制的調節を示す。両細胞種ともカスパーゼ3の17kDaサブユニットの存在の明瞭な結果を示した。これらの結果は、非処置細胞の結果およびジェムザール(登録商標)単独またはジェムザール(登録商標)とTFRsvFv−リポソームA−スクランブルHER−2の組合せで処置した細胞の結果と対照的である。
図10はTfRscFv−リポソームA−アンチセンスHER−2単独による、またはPANC−1細胞のジェムザール(登録商標)6時間後トランスフェクションの組合せによるアポトーシス経路におけるタンパク質発現のin vitro抑制的調節を示す。対照は図9Aおよび9Bと同じである。
図11は皮下PANC−1異種移植片腫瘍を担持するヌードマウスへの、TfRscFv−LipA−アンチセンスHER−2複合体単独またはジェムザール(登録商標)と組み合わせた静脈送達後の腫瘍細胞におけるアンチセンスHER−2作用の局在を示す。17kDaサブユニットの存在を示す矢印は、肝細胞または肺細胞サンプルのいずれにも存在しない腫瘍における中央のバンドを指している。
図12はPANC−1異種移植片腫瘍におけるTfRscFv−リポソームA−アンチセンスHER−2とジェムザール(登録商標)の組合せ処置のin vivo作用を、非処置腫瘍、またはジェムザール(登録商標)単独、複合体単独もしくはジェムザール(登録商標)とTfRscFv−リポソーム A−スクランブルHER−2a複合体の組合せで処置した腫瘍と比較して示すグラフである。
図13はRB94腫瘍抑制遺伝子で全身処置した後のマウス血漿におけるカスパーゼ3の17kDaサブユニットの存在を示す。
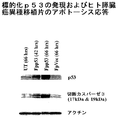
図14は化学療法後のヒト乳癌患者の血清におけるカスパーゼ3の17kDaサブユニットの存在を示す。
アポトーシスのメカニズムは進化を通じて顕著に保存され、システインプロテアーゼファミリーによって制御されている。これらの酵素はそれらの特異的基質であるアスパラギン酸残基の後ろで切断することで、アポトーシス細胞を特徴付ける多くの典型的な生化学的・形態学的変化を媒介する。当業者ならば、アポトーシスの指標または生化学的マーカーとして活性化カスパーゼの同定が使用できることを知っているが、それらの使用はこれまでのところ、in vitro細胞培養物もしくは細胞溶解物、または無傷の生細胞の場合に限られていた。
細胞培養物およびからタンパク質を単離する方法
A.細胞培養物において17kDa活性型カスパーゼ3断片の存在を検出するため、次の実施例で下記の手順を用いて、生細胞および浮遊している死細胞の双方から全タンパク質を単離した。細胞培養容器からの培地を除去し、保存した。
冷PBS 10mlの入った容器(例えば、75cm2フラスコ)で細胞を洗浄する。このPBSと保存していた培地を合わせる。各フラスコにPBS 5mlを加え、ラバーポリスマンで細胞を掻き取る。この細胞を培地/PBS溶液に加える。各フラスコにPBS5mlを加え、洗浄する。顕微鏡下で確認して、残存している細胞の量を調べる。必要に応じて、再びPBS 5mlを加え、掻き取る。前記の溶液に加える。
a)イソプロパノール中10mg/mlのPMSF(10μl/mlで使用)
b)アプロチニン(Sigmaカタログ番号A6279、30μl/mlで使用)
c)冷凍アリコートとして100mMのオルトバナジウム酸ナトリウム(10μl/mlで使用)
ドライアイス上に組織を置き、使用前、数分間、無菌Bessman組織粉砕器を液体窒素中に入れる。
血中のカスパーゼ3 17kDa断片の分析のための血漿の調製
以下の実施例で示される手順では、2つの方法のいずれかを用いてカスパーゼ3 17kDa断片の評価のために用いる血漿の調製のための血液を採取した。
カスパーゼ3 17kDaの発現に関するタンパク質のウエスタン分析
血液または組織からのタンパク質のウエスタン分析は次のように行った。
全タンパク質細胞溶解物(全タンパク質20〜60μg)を4℃の同量のRIPAバッファーで希釈する。よく混合する。
10μlのヒト血清(P−30またはP−6精製後のもの)を4×サンプルバッファー(Invitrogen)および同溶液で1×サンプルバッファーとなるように希釈し、このカラム後サンプルを全量24μl(1mmコームの場合)および36μl(1.5mmコームの場合)とする。NuPAGE(登録商標)還元剤(安定化した液体形態中で0.5M DTT)を加えて最終サンプル量の10%ととした後すぐにこの溶液を65〜75℃(好ましくは、70℃)で加熱し、このサンプルをNuPAGE(登録商標)ゲル上に載せる。MES SDS泳動バッファーを用い、ゲル当たり100〜200の一定のボルト数および70〜125mAでゲルの泳動を行う。
サンプルバッファー
NuPAGE(登録商標)LDSサンプルバッファー
(4×)10ml
グリセロール 4.00g
Tris塩基 0.682g
TrisHCl 0.666g
LDS 0.800g
EDTA 0.006g
Serva Blue G250 0.75ml(1%溶液)
フェノールレッド 0.25ml(1%溶液)
超純水 10mlまで
1×バッファーはpH8.5としなければならない。
pH調整には酸も塩基も用いてはならない。
LDS=ドデシル硫酸リチウム
還元条件:
以下のように、20×NuPAGE(登録商標)SDS泳動バッファー(MES)を希釈し、1×NuPAGE(登録商標)SDS泳動バッファーを調製する。
十分混合する。
NuPAGE(登録商標)SDS泳動バッファー(MES)(20×) 50ml
超純水 950ml
下層(外部)バッファーチャンバーで用いるための1×NuPAGE(登録商標)SDS泳動バッファー800mlをとっておく。約600mlの1×泳動バッファー下層に満たす。泳動直前に、200mlの1×NuPAGE(登録商標)SDS泳動バッファー当たり500μlのNuPAGE(登録商標)酸化防止剤を加えることで、上層(内部)バッファーチャンバー用の残りの200mlを調製する。十分混合する。
MES SDS泳動バッファー:
(20×)500ml
MES 97.6g(1.00M)
2−(N−モルホリノ)エタンスルホン酸Tris塩基 60.6g(1.00M)
SDS 10.0g(69.3mM)
EDTA 3.0g(20.5mM)
超純水 500mlまで
1×バッファーはpH7.3でなければならない。pH調整には酸も塩基も用いてはならない。
血液または組織からのカスパーゼ3 17kDaタンパク質の検出のための免疫ブロット法
免疫ブロット法
膜をBlotto A[Blotto A(一般用):5%(w/v)粉乳、TBS、0.05%Tween−20]中に1時間浸漬することにより、非特異的タンパク質結合を遮断する。全ウエスタンが1日で完了できない場合には、膜を4℃にてTBS(Tween−20を含まない)で覆い、一晩浸漬しなければならない。
膵臓腫瘍および肝臓における切断カスパーゼ3 17kDaタンパク質の検出
1つの治療薬として、出典明示により本明細書の一部とする米国特許出願出願番号09/914,046に詳細に記載されているTfRscFv−LipA−p53複合体を用いた。ヒト膵臓癌(PANC−1)皮下異種移植片腫瘍を担持する無胸腺ヌードマウスにTfRscFv−LipA−p53を24時間で3回静注した。各注射で複合体は全量800μl/マウス注に40μgのp53プラスミドDNAを含んだ。最後の注射から6時間後、動物を安楽死させ、腫瘍および肝臓を摘出し、実施例1、3および4と同様にウエスタン分析用にタンパク質を単離した。非処置動物の腫瘍および肝臓からのタンパク質も対照として含めた。次に、この膜を負荷量が等しいかどうかを調べるため、アクチンに特異的な市販の抗体でプローブした。
血液細胞における切断カスパーゼ3の17kDa断片の検出
血中で17kDa断片が検出できれば、wtp53遺伝子療法の有効性を確認する非侵襲的手段として使用できるものと考えられる。このことを評価するため、標的化リガンドとしてTfを有するTf−LipA−p53を全身処置したマウスから血液を採取した。100mm3を超えるDul45異種移植片腫瘍を担持する無胸腺ヌードマウスにTf−LipA−p53(100μg p53)を1回静脈投与した。また、このマウスには化学療法薬シスプラチン(CDDP)5mg/kgの1回注射(腹腔内)も施した。60時間後、マウスを安楽死させ、約1mlの血液をヘパリン処理試験管に採取した。遠心分離により細胞を分離し、実施例1のように細胞ペレットからタンパク質を単離し、実施例3のように13%ポリアクリルアミドゲル上で泳動させた。カスパーゼ3の17kDaの切断型活性サブユニットを、実施例4に記載したように抗17kDa特異的抗体(Cell Signaling)を用いてウエスタン分析により同定した。
切断カスパーゼ3の7kDa断片の発現が治療に対する腫瘍応答に関連していることの証明
実施例6の結果は、Tf−LipA−p53およびCDDPでの全身処置から60時間後のDU145腫瘍担持マウスから抽出した血液細胞ペレットにおける17kDaタンパク質の存在を示す。正常なリンパ球はp53により誘導されるアポトーシスに感受性がある。従って、血中における17kDa断片の出現が本当に腫瘍と関連しているかどうかを調べるために評価を行った。実施例6で記載したDU145腫瘍担持マウスに施したものと同じ処置を、PANC−1皮下異種移植片腫瘍存在を有する、または有さないマウスに繰り返した。さらに、この試験では、血液細胞の存在による複雑化を避けるために血清の使用を試してみた。血清を用いるので、負荷量が等しいかどうかを評価するためにハウスキーピング遺伝子を用いることはできないが、各レーンに等量を負荷した。実施例2に記載したようにヘパリンを用いずに全血1mlから血清を単離し、実施例3および4に記載したようにウエスタン分析を行った。図5に示すように、17kDa断片は担癌動物で、さらには担癌動物のみに強く発現した。よって、このバンドの存在はwtp53/CDDP治療に対する腫瘍応答と明らかに関連している。
アポトーシス指標としてのカスパーゼ3の17kDa断片の検出:in vitroでのAS−HER−2 ODN処置後
本発明のさらなる特定の実施形態では、切断17kDaサブユニットがアンチセンス(AS)HER−2による治療の有効性を証明する手段として腫瘍および/または血液で検出できること、すなわち、アポトーシス経路がASHER−2処置によって誘導されることが証明された。(用いたアンチセンスHER−2オリゴヌクレオチドは、出典明示によりその全開示内容を本明細書の一部とする米国特許第6,027,89号および米国出願出願番号09,716,320に記載されているものである)。そのP13K/Akt経路HER−2との相互作用によりアポトーシスに影響を及ぼし得ることが示されている。従って、TfRscFv−LipA−ASHER−2複合体を介したHER−2の抑制的調節はカスパーゼ3の切断を誘導するものと思われた。17kDa断片に対する市販(Cell Signaling Technology)の抗体を用い、実施例3および4のようにウエスタン分析によりその発現を検出した。タンパク質溶解物は実施例で記載した手順を用いて得た。トランスフェクション24時間後、ASHER−2またはスクランブル(SC)HER−2 ODNのいずれかを有するTfRscFv−lipA複合体で処置した細胞からのタンパク質は実施例1で記載したように単離した。スクランブルHER−2 ODNは、順序は無作為であるが、アンチセンス分子と同様のヌクレオチド組成を有する。ある実施形態では、AS−HER−2 ODNは、ヒトHER−2遺伝子をコードする遺伝子センス鎖と開始コドンが相同な、ヌクレオチド15個のDNA片である。T75フラスコに1.2×106のPANC−1細胞を播種し、24時間後、0.5μMのAS HER−2またはスクランブル(SC)ODNを含有するTfRscFv−LipA複合体でトランスフェクトした。実施例1で記載したようにウエスタン分析用にタンパク質を単離した。4〜20%勾配ポリアクリルアミド/SDSゲルの各レーン当たりの負荷量は40μgであった。ニトロセルロース膜に転写した後、ブロットを、実施例3および4のように、カスパーゼ3の17kDa断片に特異的な市販のAbおよび負荷量が等しいかどうかを調べるためのアクチンでプローブした。17kDaより上のバンドは17kDaサブユニットの19kDa前駆体を示す。図6に示すように、カスパーゼ3 17kDa断片の誘導は明白であり、TfRscFv−LipA−AS HER−2処置後にアポトーシス経路が刺激されることを示している。非処置またはSC HER−2 ODN処置細胞ではいずれもこのバンドは明でなく、このことは明らかなAS HER−2特異的作用であることを示している。
AS HER−2で処置した後のin vivoにおける切断カスパーゼ3の17kDa断片の検出:in vivo薬力学マーカー
この17kDaタンパク質はまた、AS HER−2治療の有効性を確認するための非侵襲的in vivo薬力学マーカーとしても使用できる。AS HER−2またはSC ODN(9mg/kg)のいずれかを有するTfRscFv−LipAの多回静脈処置(全部で19回)および11回のジェムザール(登録商標)(60mg/kg)の腹腔内注射を施したPANC−1異種移植片腫瘍担持マウスにおける17kDa断片の誘導に対する組合せ処置(TfRscFv−LipA−AS HER−2およびジェムザール(登録商標))の作用を調べた。ジェムザール(登録商標)またはTfRscFv−LipA AS HER−2複合体いずれか単独を施す動物を対照として用いた。
シグナル変換経路のin vitro抑制的調節におけるAS HER−2に関する切断カスパーゼ3の17kDa断片の発現
腫瘍を標的とするTfRscFv−LipA−AS HER−2複合体での膵臓癌(PanCa)の処置はHER−2の発現(過剰発現でない場合でも)をダウンレギュレーションすることができ、従って、細胞の増殖/生存に負の作用をし、腫瘍細胞の死滅の増強に導くアポトーシス経路を積極的に促進する。TfRscFv−リポソーム複合体を介したHER−2のダウンレギュレーションが下流のシグナル伝達経路に影響を及ぼし得ることを証明するため、PanCa細胞系統PANC−1およびCOLO357においてこの複合体の、PI3K/AKT経路およびアポトーシスの成分に作用する能力をウエスタン分析により評価した。これら2つの細胞系統はHER−2発現のレベルが異なり、COLO357はPANC−1より有意に高いHER−2レベルを発現することから選択した。開始コドン領域(5’−TCC ATG GTG CTC ACT−3’)に相補的なホスホロチオエート配列特異的AS HER−2と、対照としての非配列特異的SC(5’−CTA GCC ATG CTT GTC−3’)ODNを合成し、Ransom Hill Biosciences (Ramona, CA)による逆相HPLCにより精製した。GenBankデータベースに対してASおよびSC配列をスクリーニングしたところ、AS ODNはHER−2に対してのみ相同性を有していたが、SC ODNとデータベース中の配列には相同性はなかったことが示された。PANC−1またはCOLO 357細胞を6穴プレートに播種し、24時間後に、1μM(PANC−1の場合)または0.5μM(COLO 357の場合)のAS HER−2またはSCHER−2ODN(陰性対照)を有するTfRscFv−LipA複合体でトランスフェクトした。オリゴ単独、または相乗作用を見出すためにはするゲムシタビン(ジェムザール(登録商標))との組合せで細胞をトランスフェクトした。示された時間に細胞を回収し、RIPAバッファー中で溶解させ、タンパク質を測定し、4〜20%勾配ポリアクリルアミド/SDSゲル上で泳動させ(全タンパク質60μg/レーン)、実施例1、3および4で記載したようにウエスタン分析のためにするニトロセルロースに転写した。HER−タンパク質の発現を検出するため、膜を抗ヒトHER−2/Neu(C−18)ウサギポリクローナルAb(Santa Cruz Biotechnolog)でプローブし、ECL(Amersham)によりシグナルを検出した。非処置細胞に比べた場合のタンパク質発現の変化を、全および/またはリン酸化Akt(Ser 473)、PI3K経路における中枢的成分(抗ヒトポリクローナルAb, Cell Signaling Technologyを使用)、リン酸化BAD(Ser 136)、アポトーシスの調節に重要な因子(抗ヒトウサギポリクローナル抗体,Cell Signaling Technologyを使用)、ならびに切断カスパーゼ3(Asp 175)(17kDaサブユニットに特異的なウサギポリクローナル抗体,Cell Signaling Technologyを使用)およびPARP/切断PARP(ポリADPリボポリメラーゼ、アポトーシスのもう1つのマーカー)(抗ヒトウサギポリクローナル抗体,Cell Signaling Technology使用)(両者ともアポトーシスの下流指標)に関しても確認した。
AS HER−2によるPanCa腫瘍の全身処置後のin vivoにおける切断カスパーゼ3の17kDa断片の腫瘍特異的局在の検出
そのPI3K/Akt経路との相互作用により、HER−2がアポトーシスを阻害し得ることが示された。従って、TfRscFv−LipA−AS HER−2複合体を介したHER−2の抑制的調節はカスパーゼ3の切断を誘導するはずである。
TfRscFv−LipA−AS−HER−2によるPanCa異種移植片腫瘍のin vivo化学増感
上記のin vitro研究では、PanCa細胞のTfRscFv−LipA−AS HER−2複合体での処置はそれらのジェムザール(登録商標)応答を高めることが示されている。この遺伝子療法送達系がヒト癌、例えばPanCaにとって臨床上信頼できるものとなるためには、in vitroで見られた増感の上昇をn vivoモデルへと翻訳しなければならない。in vivoPanCaの処置におけるTfRscFv−LipA−AS HER−2の有効性は、皮下PANC−1異種移植片マウスモデルを用いて評価した。約50mm3の皮下異種移植片腫瘍を担持する無胸腺ヌードマウス(5〜9個体/1個体当たり2つの腫瘍を有する群)を、ODNを含有するTfRscFv−LipA−AS HER−2複合体9mg/kg/注射で1週間に3回処置した。対照としてある動物群には、ジェムザール(登録商標)単独、TfRscFv−LipA−AS HER−2単独、またはジェムザール(登録商標)と、SC ODNを有する複合体との組合せを施した。ジェムザール(登録商標)は、60mg/kgを1週間に2回腹腔内投与した。動物には全部で、複合体の静注18回とジェムザール(登録商標)12回を施した。図12に示されるように、ジェムザール(登録商標)単独は腫瘍の増殖に最小の作用だけを示したが、AS HER−2単独では効果はなかった。ジェムザール(登録商標)単独または対照SC ODNおよびジェムザール(登録商標)を施した群は統計学的に差がなく、このことはTfRscFv−LipA−SC ODNおよびジェムザール(登録商標)による増殖阻害が厳密に薬物の作用であることを示している。しかしながら、TfRscFv−LipA−AS HER−2とジェムザール(登録商標)の組合せを施したマウスにおいて腫瘍増殖は実質的に阻害された。併用療法およびジェムザール(登録商標)単独またはTfRscFv−LipA−AS HER−2単独を施した群の間の差は統計学的に極めて有意である(スチューデントのt検定によりp<0.001)。よって、AS HER−2を有する複合体の、ジェムザール(登録商標)と組み合わせた静脈投与はPanCaに対して有効である。
マウス血漿における腫瘍抑制RB94検出による17kDa切断カスパーゼ3断片の誘導
異なる腫瘍抑制遺伝子RB94でのin vivo処置も、アポトーシスの指標である切断カスパーゼ3の17kDa断片の発現を誘導することが示されている。網膜芽細胞腫遺伝子RBは、928のアミノ酸の核リンタンパク質をコードする腫瘍抑制因子である。この110kDaのタンパク質の通常の機能は、DNAの転写を抑制し、細胞分裂を妨げ、従って、細胞増殖を阻害することである。(Li et.al., Cancer Research 62:4637-44, 2002; Xu et.al., PNAS 91:9837-41, 1994.)
治療後のヒト乳癌患者からの血清における17kDa切断カスパーゼ3断片の検出
動物モデルで得られた結果がヒトに適用できること、および17kDa切断カスパーゼ3断片の発現が治療効果を非侵襲的に評価するために使用できることを確認するため、通常の化学療法を用いて乳癌の処置を受けた2名の患者から相当する血清サンプルセットを得た。これらの血清サンプルは処置前と処置後に得た。血清はP6(Tris)Micro−Bio−Spin(登録商標)クロマトグラフィーカラム(Bio-Rad Laboratories, Hercules, CA)を用いて精製した(実施例2)。カラム透過物を血清:RIPAバッファーが0.1:1〜10:1、好ましくは1:1の比率で希釈した。等量(1〜100μl)を、実施例3および4に記載のように、4〜20%ポリアクリルアミド/SDSゲル上で泳動させ、転写し、17kDa切断カスパーゼ3断片の発現に関してプローブした。図14に示されているように、17kDa切断カスパーゼ3断片は対照(非担癌)ヒト被験者または処置前の患者のいずれからの血清においても明らかでない。しかしながら、このバンドは標準的化学療法後では明らかに存在している。よって、動物モデルで示されたように、アポトーシスの指標である17kDa切断カスパーゼ3断片の発現はヒト患者における癌治療(遺伝子、アンチセンス、および化学療法)とも相関がある。従って、放射線療法をはじめ、アポトーシスを誘導するいずれの治療についても、本願に含まれている実施例に記載されているような、17kDa切断カスパーゼ3断片に関する血液(血清または血漿)の分析が、治療の有効性を監視するための比較的非侵襲的な方法となり得る。ヒト癌患者では、血液(1ml〜3ml)をヘパリン処理試験管に採り、4〜27℃で3〜10分間、300〜1000xgで遠心分離を行って血漿を得ればよいと考えられる。この血漿は(実施例3および4で記載したように)そのまま泳動させることもできるし、あるいは、サンプルの一部20〜75μlを、4〜27℃(好ましくは18〜24℃、最も好ましくは20℃)で1〜10分間(好ましくは4分間)、P6またはP30 Micro Bio−Spin(登録商標)クロマトグラフィーカラム(好ましくはP6)により300〜2000xg(好ましくは1000xg)での遠心分離によってさらに精製してもよい。透過物を血漿:RIPAが0.1:1〜10:1、好ましくは1:1の比率で希釈した後、4〜20%ポリアクリルアミド/SDSゲル上で電気泳動を行い、孔径0.1か0.45μm、好ましくは0.22μmのいずれかのナイロンまたはニトロセルロース固相支持体膜、好ましくはProtran(登録商標)(S+S)に転写する。検出は、17kDa断片を、好ましくは17kDa断片のみを検出するポリクローナルまたはモノクローナル抗カスパーゼ3抗体を用い、放射性または非放射性手段、好ましくは非放射性、好ましくは非比色定量的、好ましくは化学発光を介する、好ましくはECLウエスタンブロット検出試薬および分析システム(Amersham Biosciences, Piscataway, NJ)(30秒〜24時間、好ましくは1分〜18時間の範囲の時間、限定されるものではないが、Hyperfilm ECLをはじめとするオートラジオグラフィーフィルムに露光する)で見られるような増強された化学発光によって行う。
Claims (18)
- 哺乳類の身体において治療薬の有効性を評価するための方法であって、該薬剤はアポトーシスを刺激する働きをし、
該治療薬で処置する哺乳類から、腫瘍細胞が存在する身体組織または体液のサンプルを得ること、ここで、該組織または体液はカスパーゼ3の17kDa断片を含み得、この断片はin vivoにおけるカスパーゼ3の特異的切断によって生じたものである;
該切断カスパーゼ3の17kDa断片の存在量を測定すべく該サンプルをアッセイすること;
該治療薬を該哺乳類に投与すること;
該哺乳類から、該身体組織または該体液の第二のサンプルを得ること;および
該切断カスパーゼ3の17kDa断片の存在量を測定すべく該第二のサンプルをアッセイすること
を含み、該第一のサンプルで測定された量に対する、該第二のサンプルで測定された該17kDa断片の量の増加が、アポトーシス刺激および該治療薬の有効性に相関する、方法。 - 前記体液が血液または血液成分である、請求項1に記載の方法。
- 前記血液成分が血漿、血清または血液細胞を含む、請求項2に記載の方法。
- 前記体液が唾液である、請求項1に記載の方法。
- 前記治療薬が化学療法薬、放射性治療薬、腫瘍抑制核酸、オリゴヌクレオチドまたはそれらの組合せを含む、請求項1に記載の方法。
- 前記治療薬が核酸を含む、請求項1に記載の方法。
- 前記核酸が、野生型p53分子、RB分子、RB94分子、アポプチン分子またはアンチセンスHER−2をコードするDNA分子を含む、請求項6に記載の方法。
- 前記治療薬がリガンド−カチオンリポソームとの複合体として投与される、請求項1に記載の方法。
- 前記リガンドがトランスフェリン、葉酸または抗トランスフェリン受容体単鎖抗体フラグメントを含む、請求項8に記載の方法。
- 前記リガンドが抗体または抗体フラグメントを含む、請求項8に記載の方法。
- 前記抗体または抗体フラグメントがトランスフェリン受容体またはHER−2と結合する、請求項10に記載の方法。
- 前記抗体フラグメントがscFvフラグメントである、請求項10に記載の方法。
- 前記リポソームがジオレオイルトリメチルアンモニウムホスフェート(DOTAP)とジオレオイルホスファチジルエタノールアミン(DOPE)もしくはコレステロールまたはそれらの組合せとの混合物、あるいはジメチルジオクタデシルアンモニウムブロミド(DDAB)とDOPEもしくはコレステロールまたはそれらの組合せとの混合物を含む、請求項8に記載の方法。
- 前記治療薬が化学療法薬または放射性治療薬をさらに含む、請求項8に記載の方法。
- 前記第二のサンプル中の切断17kDaサブユニットの量が、前記第一のサンプル中の切断サブユニットの量の少なくとも1.5〜約2倍である、請求項1に記載の方法。
- 哺乳類の身体において治療薬の有効性を評価するための方法であって、該薬剤はアポトーシスを刺激する働きをし、
該治療薬で処置する哺乳類から、血液または血液成分のサンプルを得ること;
該サンプル中に存在するカスパーゼ3の17kDa断片の量を測定すべく該サンプルをアッセイすること、ここで、該フラグメントはin vivoにおけるカスパーゼ3の特異的切断によって生じたものである;
該治療薬を該哺乳類に投与すること;
該哺乳類から、血液または血液成分の第二のサンプルを得ること;および
該サンプル中に存在する切断カスパーゼ3の17kDa断片の量を測定すべく該第二のサンプルをアッセイすること
を含み、該第一のサンプルで測定された量に対する、該第二のサンプルで測定された該17kDa断片の量の増加が、アポトーシス刺激および該治療薬の有効性に相関する、方法。 - 前記血液成分が血漿、血清または血液細胞を含む、請求項16に記載の方法。
- 前記治療薬が化学療法薬、放射性治療薬、腫瘍抑制核酸、オリゴヌクレオチドまたはそれらの組合せを含む、請求項16に記載の方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US44290203P | 2003-01-28 | 2003-01-28 | |
| PCT/US2004/002261 WO2004066946A2 (en) | 2003-01-28 | 2004-01-28 | Method for evaluating the efficacy of certain cancer treatments |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2006517032A true JP2006517032A (ja) | 2006-07-13 |
| JP2006517032A5 JP2006517032A5 (ja) | 2007-03-15 |
Family
ID=32825276
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006503077A Pending JP2006517032A (ja) | 2003-01-28 | 2004-01-28 | ある種の癌治療の有効性を評価するための方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20040241088A1 (ja) |
| EP (1) | EP1595142A4 (ja) |
| JP (1) | JP2006517032A (ja) |
| CA (1) | CA2513769A1 (ja) |
| WO (1) | WO2004066946A2 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2022075439A1 (ja) * | 2020-10-08 | 2022-04-14 | 国立大学法人東海国立大学機構 | 抗トランスフェリンレセプター抗体の薬効又は感受性の判定方法 |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8617514B2 (en) | 1999-02-22 | 2013-12-31 | Georgetown University | Tumor-targeted nanodelivery systems to improve early MRI detection of cancer |
| CA2638899C (en) * | 2005-10-20 | 2016-01-05 | Georgetown University | Tumor-targeted nanodelivery systems to improve early mri detection of cancer |
| US9908772B2 (en) | 2008-12-30 | 2018-03-06 | 3M Innovative Properties Company | Nanostructured articles and methods of making nanostructured articles |
| US20140120157A1 (en) | 2012-09-19 | 2014-05-01 | Georgetown University | Targeted liposomes |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001522871A (ja) * | 1997-11-19 | 2001-11-20 | ジョージタウン・ユニバーシティ | 標的化リポゾーム遺伝子送達 |
| JP2002537318A (ja) * | 1999-02-22 | 2002-11-05 | ジョージタウン・ユニバーシティ | 全身性遺伝子送達のための抗体標的化フラグメントイムノリポソーム |
| JP2002537818A (ja) * | 1999-03-05 | 2002-11-12 | アイドゥン ファーマシューティカルズ, インコーポレイテッド | 膜由来カスパーゼ活性およびそのモジュレーターを検出する方法 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6462175B1 (en) * | 1995-11-13 | 2002-10-08 | Thomas Jefferson University | Mch3, a novel apoptotic protease, nucleic acids encoding and methods of use |
| US6887851B2 (en) * | 2001-09-18 | 2005-05-03 | Bioexpertise, Llc | IGF-binding protein-derived peptide |
-
2004
- 2004-01-28 JP JP2006503077A patent/JP2006517032A/ja active Pending
- 2004-01-28 EP EP04705988A patent/EP1595142A4/en not_active Withdrawn
- 2004-01-28 US US10/765,568 patent/US20040241088A1/en not_active Abandoned
- 2004-01-28 CA CA002513769A patent/CA2513769A1/en not_active Abandoned
- 2004-01-28 WO PCT/US2004/002261 patent/WO2004066946A2/en active Application Filing
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001522871A (ja) * | 1997-11-19 | 2001-11-20 | ジョージタウン・ユニバーシティ | 標的化リポゾーム遺伝子送達 |
| JP2002537318A (ja) * | 1999-02-22 | 2002-11-05 | ジョージタウン・ユニバーシティ | 全身性遺伝子送達のための抗体標的化フラグメントイムノリポソーム |
| JP2002537818A (ja) * | 1999-03-05 | 2002-11-12 | アイドゥン ファーマシューティカルズ, インコーポレイテッド | 膜由来カスパーゼ活性およびそのモジュレーターを検出する方法 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2022075439A1 (ja) * | 2020-10-08 | 2022-04-14 | 国立大学法人東海国立大学機構 | 抗トランスフェリンレセプター抗体の薬効又は感受性の判定方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA2513769A1 (en) | 2004-08-12 |
| WO2004066946A3 (en) | 2005-08-18 |
| EP1595142A2 (en) | 2005-11-16 |
| EP1595142A4 (en) | 2006-08-23 |
| WO2004066946A2 (en) | 2004-08-12 |
| US20040241088A1 (en) | 2004-12-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7386711B2 (ja) | 腫瘍を治療するための方法 | |
| JP2014169293A (ja) | Sparc及びその使用方法 | |
| CN113164589A (zh) | 用于调节单核细胞和巨噬细胞发炎表型的组合物和方法以及其免疫疗法用途 | |
| JP2010046086A (ja) | 悪性新生物の診断および処置 | |
| US20070122414A1 (en) | Surface marker-directed cancer therapeutics | |
| CN101932604A (zh) | EphB4作为诊断标记和作为卵巢癌的治疗靶标的用途 | |
| US20070077583A1 (en) | Alpha enolase-directed diagnostics and therapeutics for cancer and chemotherapeutic drug resistance | |
| US20070243548A1 (en) | Calumenin-directed diagnostics and therapeutics for cancer and chemotherapeutic drug resistance | |
| US20210069330A1 (en) | Methods and compositions for tumor radiosensitization | |
| JP6941565B2 (ja) | がん転移を処置または防止するのに有用な化合物および組成物、ならびにこれらの使用法 | |
| WO2004113497A2 (en) | Gene delivery to tumors | |
| Jones et al. | Survivin is a key factor in the differential susceptibility of gastric endothelial and epithelial cells to alcohol-induced injury | |
| JP2006517032A (ja) | ある種の癌治療の有効性を評価するための方法 | |
| US6982252B2 (en) | Inhibition of vacuolar proton ATPase activity and/or the modulation of acidic organelle function sensitizes cells to radiation, chemotherapy and biological agents | |
| JP2009519351A (ja) | 多発性骨髄腫細胞を死滅させるためのeIF−5Aの使用 | |
| US20110165173A1 (en) | Therapeutic agent and detection reagent for arteriosclerotic disease which targets for salusin | |
| US20070122830A1 (en) | Prohibitin-directed diagnostics and therapeutics for cancer and chemotherapeutic drug resistance | |
| US6235729B1 (en) | Uses of phospholipase C inhibitors | |
| US20030144236A1 (en) | Novel specific inhibitor of the cyclin kinase inhibitor p21 (wafl/cip1) | |
| US20110039789A1 (en) | Use of Huntingtin Protein for the Diagnosis and the Treatment of Cancer | |
| US9644019B2 (en) | Compounds for treating cardiac damage after ischaemia/reperfusion | |
| US9078856B2 (en) | Improving efficacy of cancer therapy | |
| JP2006517032A5 (ja) | ||
| JP4684512B2 (ja) | p21Cip1リウマチ治療剤 | |
| JP2002095476A (ja) | トランスフェリン受容体を介した遺伝子導入法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070123 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070123 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20091105 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20091110 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20100406 |