JP2005298522A - 消化器系疾患の予防、治療用組成物 - Google Patents
消化器系疾患の予防、治療用組成物 Download PDFInfo
- Publication number
- JP2005298522A JP2005298522A JP2005188527A JP2005188527A JP2005298522A JP 2005298522 A JP2005298522 A JP 2005298522A JP 2005188527 A JP2005188527 A JP 2005188527A JP 2005188527 A JP2005188527 A JP 2005188527A JP 2005298522 A JP2005298522 A JP 2005298522A
- Authority
- JP
- Japan
- Prior art keywords
- par
- component
- composition
- substance
- gastric
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 64
- 208000010643 digestive system disease Diseases 0.000 title claims abstract description 13
- 230000001225 therapeutic effect Effects 0.000 title abstract description 7
- 230000003449 preventive effect Effects 0.000 title abstract description 5
- 230000028327 secretion Effects 0.000 claims abstract description 17
- 210000003097 mucus Anatomy 0.000 claims abstract description 11
- 208000007882 Gastritis Diseases 0.000 claims abstract description 8
- 208000007107 Stomach Ulcer Diseases 0.000 claims abstract description 8
- 208000000718 duodenal ulcer Diseases 0.000 claims abstract description 8
- 210000001035 gastrointestinal tract Anatomy 0.000 claims abstract description 8
- 206010012735 Diarrhoea Diseases 0.000 claims abstract description 7
- 201000005917 gastric ulcer Diseases 0.000 claims abstract description 7
- 208000004232 Enteritis Diseases 0.000 claims abstract description 6
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 56
- NTQVODZUQIATFS-WAUHAFJUSA-N (2s)-2-[[(2s)-6-amino-2-[[2-[[(2s,3s)-2-[[(2s)-2-[[(2s)-2-amino-3-hydroxypropanoyl]amino]-4-methylpentanoyl]amino]-3-methylpentanoyl]amino]acetyl]amino]hexanoyl]amino]-3-methylbutanoic acid Chemical compound OC[C@H](N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C(C)C)C(O)=O NTQVODZUQIATFS-WAUHAFJUSA-N 0.000 claims description 55
- 101710121435 Proteinase-activated receptor 2 Proteins 0.000 claims description 55
- 102100037132 Proteinase-activated receptor 2 Human genes 0.000 claims description 55
- 238000002360 preparation method Methods 0.000 claims description 30
- 239000003814 drug Substances 0.000 claims description 29
- 239000000126 substance Substances 0.000 claims description 29
- 229940079593 drug Drugs 0.000 claims description 25
- 230000027119 gastric acid secretion Effects 0.000 claims description 19
- 230000002496 gastric effect Effects 0.000 claims description 17
- 102000004169 proteins and genes Human genes 0.000 claims description 12
- 108090000623 proteins and genes Proteins 0.000 claims description 12
- 230000002401 inhibitory effect Effects 0.000 claims description 10
- 230000001737 promoting effect Effects 0.000 claims description 7
- 210000004877 mucosa Anatomy 0.000 claims description 6
- 239000003405 delayed action preparation Substances 0.000 claims description 4
- 229940122344 Peptidase inhibitor Drugs 0.000 claims description 3
- 230000000699 topical effect Effects 0.000 claims description 3
- 201000010099 disease Diseases 0.000 claims description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 2
- 230000000694 effects Effects 0.000 abstract description 18
- 230000009471 action Effects 0.000 abstract description 11
- 102000002020 Protease-activated receptors Human genes 0.000 abstract description 6
- 108050009310 Protease-activated receptors Proteins 0.000 abstract description 6
- 238000011282 treatment Methods 0.000 abstract description 6
- 230000002265 prevention Effects 0.000 abstract description 4
- 210000001519 tissue Anatomy 0.000 abstract description 4
- 230000007246 mechanism Effects 0.000 abstract description 3
- 238000002560 therapeutic procedure Methods 0.000 abstract description 2
- 102100021022 Gastrin Human genes 0.000 abstract 1
- 108010052343 Gastrins Proteins 0.000 abstract 1
- AOXOCDRNSPFDPE-UKEONUMOSA-N chembl413654 Chemical compound C([C@H](C(=O)NCC(=O)N[C@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@H](CCSC)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC=1C=CC=CC=1)C(N)=O)NC(=O)[C@@H](C)NC(=O)[C@@H](CCC(O)=O)NC(=O)[C@@H](CCC(O)=O)NC(=O)[C@@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H]1N(CCC1)C(=O)CNC(=O)[C@@H](N)CCC(O)=O)C1=CC=C(O)C=C1 AOXOCDRNSPFDPE-UKEONUMOSA-N 0.000 abstract 1
- 210000004400 mucous membrane Anatomy 0.000 abstract 1
- 230000001629 suppression Effects 0.000 abstract 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 40
- 238000000034 method Methods 0.000 description 17
- 239000004698 Polyethylene Substances 0.000 description 15
- 239000000556 agonist Substances 0.000 description 14
- 235000019441 ethanol Nutrition 0.000 description 14
- 102000004196 processed proteins & peptides Human genes 0.000 description 14
- 150000001413 amino acids Chemical group 0.000 description 12
- 239000011347 resin Substances 0.000 description 12
- 229920005989 resin Polymers 0.000 description 12
- 210000004027 cell Anatomy 0.000 description 11
- 235000018102 proteins Nutrition 0.000 description 11
- 239000003795 chemical substances by application Substances 0.000 description 10
- 230000001681 protective effect Effects 0.000 description 10
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 9
- 238000009472 formulation Methods 0.000 description 9
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 8
- QFAADIRHLBXJJS-ZAZJUGBXSA-N amastatin Chemical compound CC(C)C[C@@H](N)[C@H](O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@H](C(O)=O)CC(O)=O QFAADIRHLBXJJS-ZAZJUGBXSA-N 0.000 description 8
- 108010052590 amastatin Proteins 0.000 description 8
- 235000001014 amino acid Nutrition 0.000 description 8
- 229940024606 amino acid Drugs 0.000 description 8
- -1 etc.) Chemical compound 0.000 description 8
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 8
- 235000002639 sodium chloride Nutrition 0.000 description 8
- CBPJQFCAFFNICX-IBGZPJMESA-N (2s)-2-(9h-fluoren-9-ylmethoxycarbonylamino)-4-methylpentanoic acid Chemical compound C1=CC=C2C(COC(=O)N[C@@H](CC(C)C)C(O)=O)C3=CC=CC=C3C2=C1 CBPJQFCAFFNICX-IBGZPJMESA-N 0.000 description 7
- 241000700159 Rattus Species 0.000 description 7
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 7
- 208000027418 Wounds and injury Diseases 0.000 description 7
- 230000006378 damage Effects 0.000 description 7
- 239000002552 dosage form Substances 0.000 description 7
- 208000014674 injury Diseases 0.000 description 7
- 229920000642 polymer Polymers 0.000 description 7
- 150000003839 salts Chemical class 0.000 description 7
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 6
- 102000015728 Mucins Human genes 0.000 description 6
- 108010063954 Mucins Proteins 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- 229920002678 cellulose Polymers 0.000 description 6
- 239000001913 cellulose Substances 0.000 description 6
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 6
- 229920001577 copolymer Polymers 0.000 description 6
- 210000001156 gastric mucosa Anatomy 0.000 description 6
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 6
- 238000001727 in vivo Methods 0.000 description 6
- 239000000047 product Substances 0.000 description 6
- 238000003786 synthesis reaction Methods 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- SGPMJRPYYIJZPC-JYAZKYGWSA-N (2s,3s)-2-[[(2s)-2-[[(2s)-2-amino-3-hydroxypropanoyl]amino]-4-methylpentanoyl]amino]-n-[2-[[(2s)-1-[[(2s)-1-amino-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-2-oxoethyl]-3-methylpentanamide Chemical compound OC[C@H](N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CCCN=C(N)N)C(=O)N[C@@H](CC(C)C)C(N)=O SGPMJRPYYIJZPC-JYAZKYGWSA-N 0.000 description 5
- 125000001433 C-terminal amino-acid group Chemical group 0.000 description 5
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 5
- 101710121440 Proteinase-activated receptor 1 Proteins 0.000 description 5
- 102100037136 Proteinase-activated receptor 1 Human genes 0.000 description 5
- 229930006000 Sucrose Natural products 0.000 description 5
- 238000010162 Tukey test Methods 0.000 description 5
- 239000002253 acid Substances 0.000 description 5
- 125000000539 amino acid group Chemical group 0.000 description 5
- 239000002585 base Substances 0.000 description 5
- 239000002775 capsule Substances 0.000 description 5
- AIXAANGOTKPUOY-UHFFFAOYSA-N carbachol Chemical compound [Cl-].C[N+](C)(C)CCOC(N)=O AIXAANGOTKPUOY-UHFFFAOYSA-N 0.000 description 5
- 229960004484 carbachol Drugs 0.000 description 5
- 238000007796 conventional method Methods 0.000 description 5
- 210000004051 gastric juice Anatomy 0.000 description 5
- 239000008101 lactose Substances 0.000 description 5
- 229940031703 low substituted hydroxypropyl cellulose Drugs 0.000 description 5
- 239000005720 sucrose Substances 0.000 description 5
- 239000003826 tablet Substances 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- REITVGIIZHFVGU-IBGZPJMESA-N (2s)-2-(9h-fluoren-9-ylmethoxycarbonylamino)-3-[(2-methylpropan-2-yl)oxy]propanoic acid Chemical compound C1=CC=C2C(COC(=O)N[C@@H](COC(C)(C)C)C(O)=O)C3=CC=CC=C3C2=C1 REITVGIIZHFVGU-IBGZPJMESA-N 0.000 description 4
- HNICLNKVURBTKV-NDEPHWFRSA-N (2s)-5-[[amino-[(2,2,4,6,7-pentamethyl-3h-1-benzofuran-5-yl)sulfonylamino]methylidene]amino]-2-(9h-fluoren-9-ylmethoxycarbonylamino)pentanoic acid Chemical compound C12=CC=CC=C2C2=CC=CC=C2C1COC(=O)N[C@H](C(O)=O)CCCN=C(N)NS(=O)(=O)C1=C(C)C(C)=C2OC(C)(C)CC2=C1C HNICLNKVURBTKV-NDEPHWFRSA-N 0.000 description 4
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 4
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 4
- 241000416162 Astragalus gummifer Species 0.000 description 4
- 108010010803 Gelatin Proteins 0.000 description 4
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 4
- 239000007821 HATU Substances 0.000 description 4
- 108091005804 Peptidases Proteins 0.000 description 4
- 102000035195 Peptidases Human genes 0.000 description 4
- 101710121439 Proteinase-activated receptor 4 Proteins 0.000 description 4
- 102100023710 Proteinase-activated receptor 4 Human genes 0.000 description 4
- 229920002472 Starch Polymers 0.000 description 4
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 4
- 229920001615 Tragacanth Polymers 0.000 description 4
- 235000010489 acacia gum Nutrition 0.000 description 4
- 230000003213 activating effect Effects 0.000 description 4
- 230000004913 activation Effects 0.000 description 4
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 4
- 239000008280 blood Substances 0.000 description 4
- 210000004369 blood Anatomy 0.000 description 4
- 210000004899 c-terminal region Anatomy 0.000 description 4
- 150000001875 compounds Chemical class 0.000 description 4
- 239000008273 gelatin Substances 0.000 description 4
- 229920000159 gelatin Polymers 0.000 description 4
- 229940014259 gelatin Drugs 0.000 description 4
- 235000019322 gelatine Nutrition 0.000 description 4
- 235000011852 gelatine desserts Nutrition 0.000 description 4
- 238000004128 high performance liquid chromatography Methods 0.000 description 4
- 229940077716 histamine h2 receptor antagonists for peptic ulcer and gord Drugs 0.000 description 4
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 4
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 4
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 4
- 239000003112 inhibitor Substances 0.000 description 4
- 239000007924 injection Substances 0.000 description 4
- 238000002347 injection Methods 0.000 description 4
- 235000019359 magnesium stearate Nutrition 0.000 description 4
- 229940126409 proton pump inhibitor Drugs 0.000 description 4
- 239000000612 proton pump inhibitor Substances 0.000 description 4
- 102000005962 receptors Human genes 0.000 description 4
- 108020003175 receptors Proteins 0.000 description 4
- 235000010413 sodium alginate Nutrition 0.000 description 4
- 239000000661 sodium alginate Substances 0.000 description 4
- 229940005550 sodium alginate Drugs 0.000 description 4
- 239000002904 solvent Substances 0.000 description 4
- 210000002784 stomach Anatomy 0.000 description 4
- 235000010487 tragacanth Nutrition 0.000 description 4
- 239000000196 tragacanth Substances 0.000 description 4
- 229940116362 tragacanth Drugs 0.000 description 4
- CDBPTZOOUNAWQA-LSBAASHUSA-N (2s)-n-[(2s)-1-[[(2s)-1-amino-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]-2-[[(2s)-2-[[(2s)-2-amino-3-hydroxypropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanamide Chemical compound NC(N)=NCCC[C@@H](C(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@@H](N)CO)CC1=CC=CC=C1 CDBPTZOOUNAWQA-LSBAASHUSA-N 0.000 description 3
- QXVFEIPAZSXRGM-DJJJIMSYSA-N (2s,3s)-2-(9h-fluoren-9-ylmethoxycarbonylamino)-3-methylpentanoic acid Chemical compound C1=CC=C2C(COC(=O)N[C@@H]([C@@H](C)CC)C(O)=O)C3=CC=CC=C3C2=C1 QXVFEIPAZSXRGM-DJJJIMSYSA-N 0.000 description 3
- 244000215068 Acacia senegal Species 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 3
- 239000001856 Ethyl cellulose Substances 0.000 description 3
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 3
- 239000005977 Ethylene Substances 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 3
- 229920000084 Gum arabic Polymers 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 101710186509 Partitioning defective 3 homolog Proteins 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 102100037133 Proteinase-activated receptor 3 Human genes 0.000 description 3
- 101710121425 Proteinase-activated receptor 3 Proteins 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 239000000205 acacia gum Substances 0.000 description 3
- 239000000654 additive Substances 0.000 description 3
- 230000001270 agonistic effect Effects 0.000 description 3
- 239000011248 coating agent Substances 0.000 description 3
- 239000003623 enhancer Substances 0.000 description 3
- 150000002148 esters Chemical class 0.000 description 3
- DZGCGKFAPXFTNM-UHFFFAOYSA-N ethanol;hydron;chloride Chemical compound Cl.CCO DZGCGKFAPXFTNM-UHFFFAOYSA-N 0.000 description 3
- 235000019325 ethyl cellulose Nutrition 0.000 description 3
- 229920001249 ethyl cellulose Polymers 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 239000000796 flavoring agent Substances 0.000 description 3
- 239000008103 glucose Substances 0.000 description 3
- 229960003511 macrogol Drugs 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 229920000609 methyl cellulose Polymers 0.000 description 3
- 239000001923 methylcellulose Substances 0.000 description 3
- 235000010981 methylcellulose Nutrition 0.000 description 3
- 150000007524 organic acids Chemical class 0.000 description 3
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 3
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 3
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 3
- 239000008107 starch Substances 0.000 description 3
- 235000019698 starch Nutrition 0.000 description 3
- 229940124597 therapeutic agent Drugs 0.000 description 3
- 239000003981 vehicle Substances 0.000 description 3
- DJAHKBBSJCDSOZ-AJLBTXRUSA-N (5z,9e,13e)-6,10,14,18-tetramethylnonadeca-5,9,13,17-tetraen-2-one;(5e,9e,13e)-6,10,14,18-tetramethylnonadeca-5,9,13,17-tetraen-2-one Chemical compound CC(C)=CCC\C(C)=C\CC\C(C)=C\CC\C(C)=C/CCC(C)=O.CC(C)=CCC\C(C)=C\CC\C(C)=C\CC\C(C)=C\CCC(C)=O DJAHKBBSJCDSOZ-AJLBTXRUSA-N 0.000 description 2
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- SUBDBMMJDZJVOS-UHFFFAOYSA-N 5-methoxy-2-{[(4-methoxy-3,5-dimethylpyridin-2-yl)methyl]sulfinyl}-1H-benzimidazole Chemical compound N=1C2=CC(OC)=CC=C2NC=1S(=O)CC1=NC=C(C)C(OC)=C1C SUBDBMMJDZJVOS-UHFFFAOYSA-N 0.000 description 2
- 102000004400 Aminopeptidases Human genes 0.000 description 2
- 108090000915 Aminopeptidases Proteins 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 239000005711 Benzoic acid Substances 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 2
- 229920002785 Croscarmellose sodium Polymers 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 208000018522 Gastrointestinal disease Diseases 0.000 description 2
- 101001098529 Homo sapiens Proteinase-activated receptor 1 Proteins 0.000 description 2
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 2
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- 239000004372 Polyvinyl alcohol Substances 0.000 description 2
- 239000004365 Protease Substances 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- 108010086019 Secretin Proteins 0.000 description 2
- 102100037505 Secretin Human genes 0.000 description 2
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 108090000631 Trypsin Proteins 0.000 description 2
- 102000004142 Trypsin Human genes 0.000 description 2
- 108060005989 Tryptase Proteins 0.000 description 2
- 102000001400 Tryptase Human genes 0.000 description 2
- 208000025865 Ulcer Diseases 0.000 description 2
- TVXBFESIOXBWNM-UHFFFAOYSA-N Xylitol Natural products OCCC(O)C(O)C(O)CCO TVXBFESIOXBWNM-UHFFFAOYSA-N 0.000 description 2
- MMWCIQZXVOZEGG-HOZKJCLWSA-N [(1S,2R,3S,4S,5R,6S)-2,3,5-trihydroxy-4,6-diphosphonooxycyclohexyl] dihydrogen phosphate Chemical compound O[C@H]1[C@@H](O)[C@H](OP(O)(O)=O)[C@@H](OP(O)(O)=O)[C@H](O)[C@H]1OP(O)(O)=O MMWCIQZXVOZEGG-HOZKJCLWSA-N 0.000 description 2
- AMZWNNKNOQSBOP-UHFFFAOYSA-M [n'-(2,5-dioxoimidazolidin-4-yl)carbamimidoyl]oxyaluminum;dihydrate Chemical compound O.O.NC(=O)NC1N=C(O[Al])NC1=O AMZWNNKNOQSBOP-UHFFFAOYSA-M 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 229940015825 aldioxa Drugs 0.000 description 2
- 235000010233 benzoic acid Nutrition 0.000 description 2
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- OSGAYBCDTDRGGQ-UHFFFAOYSA-L calcium sulfate Chemical compound [Ca+2].[O-]S([O-])(=O)=O OSGAYBCDTDRGGQ-UHFFFAOYSA-L 0.000 description 2
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 2
- 229920002301 cellulose acetate Polymers 0.000 description 2
- OSASVXMJTNOKOY-UHFFFAOYSA-N chlorobutanol Chemical compound CC(C)(O)C(Cl)(Cl)Cl OSASVXMJTNOKOY-UHFFFAOYSA-N 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- 235000015165 citric acid Nutrition 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 239000003086 colorant Substances 0.000 description 2
- 235000010947 crosslinked sodium carboxy methyl cellulose Nutrition 0.000 description 2
- 239000001767 crosslinked sodium carboxy methyl cellulose Substances 0.000 description 2
- 210000002249 digestive system Anatomy 0.000 description 2
- 231100000673 dose–response relationship Toxicity 0.000 description 2
- 210000001198 duodenum Anatomy 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- 235000013355 food flavoring agent Nutrition 0.000 description 2
- 238000004108 freeze drying Methods 0.000 description 2
- 229930182830 galactose Natural products 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- 229940093915 gynecological organic acid Drugs 0.000 description 2
- 239000001341 hydroxy propyl starch Substances 0.000 description 2
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 2
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 2
- 235000013828 hydroxypropyl starch Nutrition 0.000 description 2
- 150000007529 inorganic bases Chemical class 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 238000002350 laparotomy Methods 0.000 description 2
- 235000010445 lecithin Nutrition 0.000 description 2
- 239000000787 lecithin Substances 0.000 description 2
- 229940067606 lecithin Drugs 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- 230000010534 mechanism of action Effects 0.000 description 2
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- XJRBAMWJDBPFIM-UHFFFAOYSA-N methyl vinyl ether Chemical compound COC=C XJRBAMWJDBPFIM-UHFFFAOYSA-N 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 239000011259 mixed solution Substances 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 229960000381 omeprazole Drugs 0.000 description 2
- 235000005985 organic acids Nutrition 0.000 description 2
- 150000007530 organic bases Chemical class 0.000 description 2
- 230000036961 partial effect Effects 0.000 description 2
- 238000010647 peptide synthesis reaction Methods 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 229920001184 polypeptide Polymers 0.000 description 2
- 229920001296 polysiloxane Polymers 0.000 description 2
- 229920002451 polyvinyl alcohol Polymers 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 229960003857 proglumide Drugs 0.000 description 2
- 230000000069 prophylactic effect Effects 0.000 description 2
- 150000003180 prostaglandins Chemical class 0.000 description 2
- 235000019833 protease Nutrition 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 239000008213 purified water Substances 0.000 description 2
- 210000001187 pylorus Anatomy 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical class O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 238000012216 screening Methods 0.000 description 2
- 229960002101 secretin Drugs 0.000 description 2
- OWMZNFCDEHGFEP-NFBCVYDUSA-N secretin human Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(N)=O)[C@@H](C)O)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)C1=CC=CC=C1 OWMZNFCDEHGFEP-NFBCVYDUSA-N 0.000 description 2
- 230000006641 stabilisation Effects 0.000 description 2
- 238000011105 stabilization Methods 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 229960004291 sucralfate Drugs 0.000 description 2
- MNQYNQBOVCBZIQ-JQOFMKNESA-A sucralfate Chemical compound O[Al](O)OS(=O)(=O)O[C@@H]1[C@@H](OS(=O)(=O)O[Al](O)O)[C@H](OS(=O)(=O)O[Al](O)O)[C@@H](COS(=O)(=O)O[Al](O)O)O[C@H]1O[C@@]1(COS(=O)(=O)O[Al](O)O)[C@@H](OS(=O)(=O)O[Al](O)O)[C@H](OS(=O)(=O)O[Al](O)O)[C@@H](OS(=O)(=O)O[Al](O)O)O1 MNQYNQBOVCBZIQ-JQOFMKNESA-A 0.000 description 2
- 239000006228 supernatant Substances 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 239000000375 suspending agent Substances 0.000 description 2
- 230000002459 sustained effect Effects 0.000 description 2
- 238000013268 sustained release Methods 0.000 description 2
- 239000012730 sustained-release form Substances 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- 229950006156 teprenone Drugs 0.000 description 2
- 239000002562 thickening agent Substances 0.000 description 2
- 230000017423 tissue regeneration Effects 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- 239000012588 trypsin Substances 0.000 description 2
- 231100000397 ulcer Toxicity 0.000 description 2
- 239000000811 xylitol Substances 0.000 description 2
- 235000010447 xylitol Nutrition 0.000 description 2
- HEBKCHPVOIAQTA-SCDXWVJYSA-N xylitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)CO HEBKCHPVOIAQTA-SCDXWVJYSA-N 0.000 description 2
- 229960002675 xylitol Drugs 0.000 description 2
- HDTRYLNUVZCQOY-UHFFFAOYSA-N α-D-glucopyranosyl-α-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(O)C(O)C(CO)O1 HDTRYLNUVZCQOY-UHFFFAOYSA-N 0.000 description 1
- BGRJTUBHPOOWDU-NSHDSACASA-N (S)-(-)-sulpiride Chemical compound CCN1CCC[C@H]1CNC(=O)C1=CC(S(N)(=O)=O)=CC=C1OC BGRJTUBHPOOWDU-NSHDSACASA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 1
- JKNCOURZONDCGV-UHFFFAOYSA-N 2-(dimethylamino)ethyl 2-methylprop-2-enoate Chemical compound CN(C)CCOC(=O)C(C)=C JKNCOURZONDCGV-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- BSKHPKMHTQYZBB-UHFFFAOYSA-N 2-methylpyridine Chemical compound CC1=CC=CC=N1 BSKHPKMHTQYZBB-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- ZGDLVKWIZHHWIR-UHFFFAOYSA-N 4-[5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)pyridin-2-yl]morpholine Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=C(N2CCOCC2)N=C1 ZGDLVKWIZHHWIR-UHFFFAOYSA-N 0.000 description 1
- IVVHAAOJLULJLK-YDXSIYMFSA-E Aceglutamide aluminum Chemical compound [OH-].[OH-].[OH-].[OH-].[Al+3].[Al+3].[Al+3].CC(=O)N[C@H](C([O-])=O)CCC(N)=O.CC(=O)N[C@H](C([O-])=O)CCC(N)=O.CC(=O)N[C@H](C([O-])=O)CCC(N)=O.CC(=O)N[C@H](C([O-])=O)CCC(N)=O.CC(=O)N[C@H](C([O-])=O)CCC(N)=O IVVHAAOJLULJLK-YDXSIYMFSA-E 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 229940097396 Aminopeptidase inhibitor Drugs 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- VGGGPCQERPFHOB-MCIONIFRSA-N Bestatin Chemical compound CC(C)C[C@H](C(O)=O)NC(=O)[C@@H](O)[C@H](N)CC1=CC=CC=C1 VGGGPCQERPFHOB-MCIONIFRSA-N 0.000 description 1
- VGGGPCQERPFHOB-UHFFFAOYSA-N Bestatin Natural products CC(C)CC(C(O)=O)NC(=O)C(O)C(N)CC1=CC=CC=C1 VGGGPCQERPFHOB-UHFFFAOYSA-N 0.000 description 1
- 206010007281 Carcinoid tumour of the stomach Diseases 0.000 description 1
- 229920000623 Cellulose acetate phthalate Polymers 0.000 description 1
- 229940123150 Chelating agent Drugs 0.000 description 1
- 229920002101 Chitin Polymers 0.000 description 1
- 229920001661 Chitosan Polymers 0.000 description 1
- 206010009900 Colitis ulcerative Diseases 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- 208000011231 Crohn disease Diseases 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- XBPCUCUWBYBCDP-UHFFFAOYSA-N Dicyclohexylamine Chemical compound C1CCCCC1NC1CCCCC1 XBPCUCUWBYBCDP-UHFFFAOYSA-N 0.000 description 1
- 229920000219 Ethylene vinyl alcohol Polymers 0.000 description 1
- 102000009123 Fibrin Human genes 0.000 description 1
- 108010073385 Fibrin Proteins 0.000 description 1
- BWGVNKXGVNDBDI-UHFFFAOYSA-N Fibrin monomer Chemical compound CNC(=O)CNC(=O)CN BWGVNKXGVNDBDI-UHFFFAOYSA-N 0.000 description 1
- 206010016654 Fibrosis Diseases 0.000 description 1
- 206010016717 Fistula Diseases 0.000 description 1
- 102000003688 G-Protein-Coupled Receptors Human genes 0.000 description 1
- 108090000045 G-Protein-Coupled Receptors Proteins 0.000 description 1
- 108010015133 Galactose oxidase Proteins 0.000 description 1
- 206010061164 Gastric mucosal lesion Diseases 0.000 description 1
- 206010061459 Gastrointestinal ulcer Diseases 0.000 description 1
- ZPACYDRSPFRDHO-ROBAGEODSA-N Gefarnate Chemical compound CC(C)=CCC\C(C)=C\CC\C(C)=C\CCC(=O)OC\C=C(/C)CCC=C(C)C ZPACYDRSPFRDHO-ROBAGEODSA-N 0.000 description 1
- 229920001386 Gefarnate Polymers 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- FWKQNCXZGNBPFD-UHFFFAOYSA-N Guaiazulene Chemical compound CC(C)C1=CC=C(C)C2=CC=C(C)C2=C1 FWKQNCXZGNBPFD-UHFFFAOYSA-N 0.000 description 1
- 241000590002 Helicobacter pylori Species 0.000 description 1
- 206010060377 Hypergastrinaemia Diseases 0.000 description 1
- 206010021033 Hypomenorrhoea Diseases 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- AHLPHDHHMVZTML-BYPYZUCNSA-N L-Ornithine Chemical compound NCCC[C@H](N)C(O)=O AHLPHDHHMVZTML-BYPYZUCNSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- XGDCYUQSFDQISZ-BQBZGAKWSA-N Leu-Ser Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](CO)C(O)=O XGDCYUQSFDQISZ-BQBZGAKWSA-N 0.000 description 1
- NNJVILVZKWQKPM-UHFFFAOYSA-N Lidocaine Chemical compound CCN(CC)CC(=O)NC1=C(C)C=CC=C1C NNJVILVZKWQKPM-UHFFFAOYSA-N 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-M Methacrylate Chemical compound CC(=C)C([O-])=O CERQOIWHTDAKMF-UHFFFAOYSA-M 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 108010038807 Oligopeptides Proteins 0.000 description 1
- 102000015636 Oligopeptides Human genes 0.000 description 1
- AHLPHDHHMVZTML-UHFFFAOYSA-N Orn-delta-NH2 Natural products NCCCC(N)C(O)=O AHLPHDHHMVZTML-UHFFFAOYSA-N 0.000 description 1
- UTJLXEIPEHZYQJ-UHFFFAOYSA-N Ornithine Natural products OC(=O)C(C)CCCN UTJLXEIPEHZYQJ-UHFFFAOYSA-N 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- 208000008469 Peptic Ulcer Diseases 0.000 description 1
- 102000003992 Peroxidases Human genes 0.000 description 1
- 241000218657 Picea Species 0.000 description 1
- RVGRUAULSDPKGF-UHFFFAOYSA-N Poloxamer Chemical compound C1CO1.CC1CO1 RVGRUAULSDPKGF-UHFFFAOYSA-N 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 229920000954 Polyglycolide Polymers 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- HCBIBCJNVBAKAB-UHFFFAOYSA-N Procaine hydrochloride Chemical compound Cl.CCN(CC)CCOC(=O)C1=CC=C(N)C=C1 HCBIBCJNVBAKAB-UHFFFAOYSA-N 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 102000003923 Protein Kinase C Human genes 0.000 description 1
- 108090000315 Protein Kinase C Proteins 0.000 description 1
- 241000700157 Rattus norvegicus Species 0.000 description 1
- 101001098558 Rattus norvegicus Proteinase-activated receptor 2 Proteins 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- SMTZFNFIKUPEJC-UHFFFAOYSA-N Roxane Chemical compound CC(=O)OCC(=O)NCCCOC1=CC=CC(CN2CCCCC2)=C1 SMTZFNFIKUPEJC-UHFFFAOYSA-N 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- DWAQJAXMDSEUJJ-UHFFFAOYSA-M Sodium bisulfite Chemical compound [Na+].OS([O-])=O DWAQJAXMDSEUJJ-UHFFFAOYSA-M 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- 108090000190 Thrombin Proteins 0.000 description 1
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 1
- HDTRYLNUVZCQOY-WSWWMNSNSA-N Trehalose Natural products O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-WSWWMNSNSA-N 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- FSRLGULMGJGKGI-BTJKTKAUSA-N Trimebutine maleate Chemical compound OC(=O)\C=C/C(O)=O.C=1C=CC=CC=1C(CC)(N(C)C)COC(=O)C1=CC(OC)=C(OC)C(OC)=C1 FSRLGULMGJGKGI-BTJKTKAUSA-N 0.000 description 1
- 201000006704 Ulcerative Colitis Diseases 0.000 description 1
- JPKKQJKQTPNWTR-BRYCGAMXSA-N [(1r,5s)-8-methyl-8-azabicyclo[3.2.1]octan-3-yl] 3-hydroxy-2-phenylpropanoate;sulfuric acid;hydrate Chemical compound O.OS(O)(=O)=O.C([C@H]1CC[C@@H](C2)N1C)C2OC(=O)C(CO)C1=CC=CC=C1.C([C@H]1CC[C@@H](C2)N1C)C2OC(=O)C(CO)C1=CC=CC=C1 JPKKQJKQTPNWTR-BRYCGAMXSA-N 0.000 description 1
- 239000001785 acacia senegal l. willd gum Substances 0.000 description 1
- 229960002627 aceglutamide aluminum Drugs 0.000 description 1
- 235000011054 acetic acid Nutrition 0.000 description 1
- VJHCJDRQFCCTHL-UHFFFAOYSA-N acetic acid 2,3,4,5,6-pentahydroxyhexanal Chemical compound CC(O)=O.OCC(O)C(O)C(O)C(O)C=O VJHCJDRQFCCTHL-UHFFFAOYSA-N 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 239000002386 air freshener Substances 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 229940024546 aluminum hydroxide gel Drugs 0.000 description 1
- SMYKVLBUSSNXMV-UHFFFAOYSA-K aluminum;trihydroxide;hydrate Chemical compound O.[OH-].[OH-].[OH-].[Al+3] SMYKVLBUSSNXMV-UHFFFAOYSA-K 0.000 description 1
- LSQZJLSUYDQPKJ-NJBDSQKTSA-N amoxicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=C(O)C=C1 LSQZJLSUYDQPKJ-NJBDSQKTSA-N 0.000 description 1
- 229960003022 amoxicillin Drugs 0.000 description 1
- 229940069428 antacid Drugs 0.000 description 1
- 239000003159 antacid agent Substances 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000001078 anti-cholinergic effect Effects 0.000 description 1
- 230000002467 anti-pepsin effect Effects 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 229960003121 arginine Drugs 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 229960002028 atropine sulfate Drugs 0.000 description 1
- LFYJSSARVMHQJB-QIXNEVBVSA-N bakuchiol Chemical compound CC(C)=CCC[C@@](C)(C=C)\C=C\C1=CC=C(O)C=C1 LFYJSSARVMHQJB-QIXNEVBVSA-N 0.000 description 1
- 229950005162 benexate Drugs 0.000 description 1
- JUHORIMYRDESRB-UHFFFAOYSA-N benzathine Chemical compound C=1C=CC=CC=1CNCCNCC1=CC=CC=C1 JUHORIMYRDESRB-UHFFFAOYSA-N 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- NZUPCNDJBJXXRF-UHFFFAOYSA-O bethanechol Chemical compound C[N+](C)(C)CC(C)OC(N)=O NZUPCNDJBJXXRF-UHFFFAOYSA-O 0.000 description 1
- 229960000910 bethanechol Drugs 0.000 description 1
- 229920002988 biodegradable polymer Polymers 0.000 description 1
- 239000004621 biodegradable polymer Substances 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- KGBXLFKZBHKPEV-UHFFFAOYSA-N boric acid Chemical compound OB(O)O KGBXLFKZBHKPEV-UHFFFAOYSA-N 0.000 description 1
- 239000004327 boric acid Substances 0.000 description 1
- 235000010338 boric acid Nutrition 0.000 description 1
- 238000009395 breeding Methods 0.000 description 1
- 230000001488 breeding effect Effects 0.000 description 1
- 239000006189 buccal tablet Substances 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 235000001465 calcium Nutrition 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 229950008138 carmellose Drugs 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 229940081734 cellulose acetate phthalate Drugs 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- FHRSHSOEWXUORL-HDJSIYSDSA-N cetraxate Chemical compound C1C[C@@H](C[NH3+])CC[C@@H]1C(=O)OC1=CC=C(CCC([O-])=O)C=C1 FHRSHSOEWXUORL-HDJSIYSDSA-N 0.000 description 1
- 229950009533 cetraxate Drugs 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- IAXUQWSLRKIRFR-SAABIXHNSA-N chembl2104696 Chemical compound C1C[C@@H](CNC(=N)N)CC[C@@H]1C(=O)OC1=CC=CC=C1C(=O)OCC1=CC=CC=C1 IAXUQWSLRKIRFR-SAABIXHNSA-N 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 230000001055 chewing effect Effects 0.000 description 1
- 229960004926 chlorobutanol Drugs 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- 208000023652 chronic gastritis Diseases 0.000 description 1
- 229960001380 cimetidine Drugs 0.000 description 1
- CCGSUNCLSOWKJO-UHFFFAOYSA-N cimetidine Chemical compound N#CNC(=N/C)\NCCSCC1=NC=N[C]1C CCGSUNCLSOWKJO-UHFFFAOYSA-N 0.000 description 1
- 230000007882 cirrhosis Effects 0.000 description 1
- 208000019425 cirrhosis of liver Diseases 0.000 description 1
- DCSUBABJRXZOMT-IRLDBZIGSA-N cisapride Chemical compound C([C@@H]([C@@H](CC1)NC(=O)C=2C(=CC(N)=C(Cl)C=2)OC)OC)N1CCCOC1=CC=C(F)C=C1 DCSUBABJRXZOMT-IRLDBZIGSA-N 0.000 description 1
- 229960005132 cisapride Drugs 0.000 description 1
- DCSUBABJRXZOMT-UHFFFAOYSA-N cisapride Natural products C1CC(NC(=O)C=2C(=CC(N)=C(Cl)C=2)OC)C(OC)CN1CCCOC1=CC=C(F)C=C1 DCSUBABJRXZOMT-UHFFFAOYSA-N 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 230000008602 contraction Effects 0.000 description 1
- 239000003246 corticosteroid Substances 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- GVJHHUAWPYXKBD-UHFFFAOYSA-N d-alpha-tocopherol Natural products OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 230000007123 defense Effects 0.000 description 1
- 230000002074 deregulated effect Effects 0.000 description 1
- 238000009795 derivation Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- UGMCXQCYOVCMTB-UHFFFAOYSA-K dihydroxy(stearato)aluminium Chemical compound CCCCCCCCCCCCCCCCCC(=O)O[Al](O)O UGMCXQCYOVCMTB-UHFFFAOYSA-K 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 1
- 229910000397 disodium phosphate Inorganic materials 0.000 description 1
- 235000019800 disodium phosphate Nutrition 0.000 description 1
- FGXWKSZFVQUSTL-UHFFFAOYSA-N domperidone Chemical compound C12=CC=CC=C2NC(=O)N1CCCN(CC1)CCC1N1C2=CC=C(Cl)C=C2NC1=O FGXWKSZFVQUSTL-UHFFFAOYSA-N 0.000 description 1
- 229960001253 domperidone Drugs 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 229960003559 enprostil Drugs 0.000 description 1
- 208000010227 enterocolitis Diseases 0.000 description 1
- 230000008029 eradication Effects 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 229960001596 famotidine Drugs 0.000 description 1
- XUFQPHANEAPEMJ-UHFFFAOYSA-N famotidine Chemical compound NC(N)=NC1=NC(CSCCC(N)=NS(N)(=O)=O)=CS1 XUFQPHANEAPEMJ-UHFFFAOYSA-N 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 229950003499 fibrin Drugs 0.000 description 1
- 230000003890 fistula Effects 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 235000002864 food coloring agent Nutrition 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 239000003205 fragrance Substances 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 235000011087 fumaric acid Nutrition 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 230000005176 gastrointestinal motility Effects 0.000 description 1
- 229960003779 gefarnate Drugs 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- 229960005150 glycerol Drugs 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 229960002350 guaiazulen Drugs 0.000 description 1
- 229940037467 helicobacter pylori Drugs 0.000 description 1
- 229920006130 high-performance polyamide Polymers 0.000 description 1
- 239000008172 hydrogenated vegetable oil Substances 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 229940031704 hydroxypropyl methylcellulose phthalate Drugs 0.000 description 1
- 229920000639 hydroxypropylmethylcellulose acetate succinate Polymers 0.000 description 1
- 206010020718 hyperplasia Diseases 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 230000028709 inflammatory response Effects 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 229960003174 lansoprazole Drugs 0.000 description 1
- MJIHNNLFOKEZEW-UHFFFAOYSA-N lansoprazole Chemical compound CC1=C(OCC(F)(F)F)C=CN=C1CS(=O)C1=NC2=CC=CC=C2N1 MJIHNNLFOKEZEW-UHFFFAOYSA-N 0.000 description 1
- 231100000518 lethal Toxicity 0.000 description 1
- 230000001665 lethal effect Effects 0.000 description 1
- 229940069445 licorice extract Drugs 0.000 description 1
- 229960004194 lidocaine Drugs 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 229960003646 lysine Drugs 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 239000000395 magnesium oxide Substances 0.000 description 1
- CPLXHLVBOLITMK-UHFFFAOYSA-N magnesium oxide Inorganic materials [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 1
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- FPYJFEHAWHCUMM-UHFFFAOYSA-N maleic anhydride Chemical compound O=C1OC(=O)C=C1 FPYJFEHAWHCUMM-UHFFFAOYSA-N 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- WSFSSNUMVMOOMR-NJFSPNSNSA-N methanone Chemical compound O=[14CH2] WSFSSNUMVMOOMR-NJFSPNSNSA-N 0.000 description 1
- OJLOPKGSLYJEMD-URPKTTJQSA-N methyl 7-[(1r,2r,3r)-3-hydroxy-2-[(1e)-4-hydroxy-4-methyloct-1-en-1-yl]-5-oxocyclopentyl]heptanoate Chemical compound CCCCC(C)(O)C\C=C\[C@H]1[C@H](O)CC(=O)[C@@H]1CCCCCCC(=O)OC OJLOPKGSLYJEMD-URPKTTJQSA-N 0.000 description 1
- PTOJVMZPWPAXER-VFJVYMGBSA-N methyl 7-[(1r,2r,3r)-3-hydroxy-2-[(e,3r)-3-hydroxy-4-phenoxybut-1-enyl]-5-oxocyclopentyl]hepta-4,5-dienoate Chemical compound O[C@@H]1CC(=O)[C@H](CC=C=CCCC(=O)OC)[C@H]1\C=C\[C@@H](O)COC1=CC=CC=C1 PTOJVMZPWPAXER-VFJVYMGBSA-N 0.000 description 1
- TTWJBBZEZQICBI-UHFFFAOYSA-N metoclopramide Chemical compound CCN(CC)CCNC(=O)C1=CC(Cl)=C(N)C=C1OC TTWJBBZEZQICBI-UHFFFAOYSA-N 0.000 description 1
- 229960004503 metoclopramide Drugs 0.000 description 1
- 229960005249 misoprostol Drugs 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 210000002200 mouth mucosa Anatomy 0.000 description 1
- 230000003843 mucus production Effects 0.000 description 1
- 229920005615 natural polymer Polymers 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- SGXXNSQHWDMGGP-IZZDOVSWSA-N nizatidine Chemical compound [O-][N+](=O)\C=C(/NC)NCCSCC1=CSC(CN(C)C)=N1 SGXXNSQHWDMGGP-IZZDOVSWSA-N 0.000 description 1
- 229960004872 nizatidine Drugs 0.000 description 1
- 239000000041 non-steroidal anti-inflammatory agent Substances 0.000 description 1
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 1
- 239000007764 o/w emulsion Substances 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 239000003538 oral antidiabetic agent Substances 0.000 description 1
- 229940127209 oral hypoglycaemic agent Drugs 0.000 description 1
- 229960003104 ornithine Drugs 0.000 description 1
- 230000003204 osmotic effect Effects 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- LSQZJLSUYDQPKJ-UHFFFAOYSA-N p-Hydroxyampicillin Natural products O=C1N2C(C(O)=O)C(C)(C)SC2C1NC(=O)C(N)C1=CC=C(O)C=C1 LSQZJLSUYDQPKJ-UHFFFAOYSA-N 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 229940127557 pharmaceutical product Drugs 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- FFNMBRCFFADNAO-UHFFFAOYSA-N pirenzepine hydrochloride Chemical compound [H+].[H+].[Cl-].[Cl-].C1CN(C)CCN1CC(=O)N1C2=NC=CC=C2NC(=O)C2=CC=CC=C21 FFNMBRCFFADNAO-UHFFFAOYSA-N 0.000 description 1
- 229960000293 pirenzepine hydrochloride Drugs 0.000 description 1
- 229960000502 poloxamer Drugs 0.000 description 1
- 229920001983 poloxamer Polymers 0.000 description 1
- 229920000747 poly(lactic acid) Polymers 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920001610 polycaprolactone Polymers 0.000 description 1
- 239000004632 polycaprolactone Substances 0.000 description 1
- 229920002721 polycyanoacrylate Polymers 0.000 description 1
- 239000004633 polyglycolic acid Substances 0.000 description 1
- 239000004626 polylactic acid Substances 0.000 description 1
- 235000019422 polyvinyl alcohol Nutrition 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 150000003141 primary amines Chemical class 0.000 description 1
- 229960001309 procaine hydrochloride Drugs 0.000 description 1
- 210000002307 prostate Anatomy 0.000 description 1
- 235000019419 proteases Nutrition 0.000 description 1
- 239000003223 protective agent Substances 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 229960001778 rabeprazole sodium Drugs 0.000 description 1
- VMXUWOKSQNHOCA-LCYFTJDESA-N ranitidine Chemical compound [O-][N+](=O)/C=C(/NC)NCCSCC1=CC=C(CN(C)C)O1 VMXUWOKSQNHOCA-LCYFTJDESA-N 0.000 description 1
- 229960000620 ranitidine Drugs 0.000 description 1
- 230000000384 rearing effect Effects 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 235000019719 rose oil Nutrition 0.000 description 1
- 239000010666 rose oil Substances 0.000 description 1
- 229960003320 roxatidine Drugs 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- 150000003335 secondary amines Chemical class 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 210000000813 small intestine Anatomy 0.000 description 1
- 239000000344 soap Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 229940001607 sodium bisulfite Drugs 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 235000010267 sodium hydrogen sulphite Nutrition 0.000 description 1
- GFWRVVCDTLRWPK-KPKJPENVSA-N sofalcone Chemical compound C1=CC(OCC=C(C)C)=CC=C1\C=C\C(=O)C1=CC=C(OCC=C(C)C)C=C1OCC(O)=O GFWRVVCDTLRWPK-KPKJPENVSA-N 0.000 description 1
- 229950004782 sofalcone Drugs 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 229960002920 sorbitol Drugs 0.000 description 1
- 235000010356 sorbitol Nutrition 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 239000006190 sub-lingual tablet Substances 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 229960004793 sucrose Drugs 0.000 description 1
- 229960004940 sulpiride Drugs 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 238000002198 surface plasmon resonance spectroscopy Methods 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 229920001059 synthetic polymer Polymers 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 238000007910 systemic administration Methods 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- RTKIYNMVFMVABJ-UHFFFAOYSA-L thimerosal Chemical compound [Na+].CC[Hg]SC1=CC=CC=C1C([O-])=O RTKIYNMVFMVABJ-UHFFFAOYSA-L 0.000 description 1
- 229940033663 thimerosal Drugs 0.000 description 1
- 210000000115 thoracic cavity Anatomy 0.000 description 1
- 229960004072 thrombin Drugs 0.000 description 1
- 229940098465 tincture Drugs 0.000 description 1
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 235000010384 tocopherol Nutrition 0.000 description 1
- 239000011732 tocopherol Substances 0.000 description 1
- 229960001295 tocopherol Drugs 0.000 description 1
- 229930003799 tocopherol Natural products 0.000 description 1
- 210000003437 trachea Anatomy 0.000 description 1
- 229960005345 trimebutine Drugs 0.000 description 1
- 229950009811 ubenimex Drugs 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 description 1
- 229940099259 vaseline Drugs 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 239000007762 w/o emulsion Substances 0.000 description 1
- 239000008215 water for injection Substances 0.000 description 1
- 229920003169 water-soluble polymer Polymers 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 229940100445 wheat starch Drugs 0.000 description 1
- GVJHHUAWPYXKBD-IEOSBIPESA-N α-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-IEOSBIPESA-N 0.000 description 1
Images
Landscapes
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
Abstract
【課題】 安全で効果的な消化器系疾患の予防、治療用組成物、特に胃潰瘍、十二指腸潰瘍、胃炎、下痢、腸炎等を治療、予防するための組成物を提供する。また、これまでの公知の作用機序では困難であった副作用の問題を解決すべく、新規な作用機序を有する組成物を提供する。
【解決手段】 PAR−2を活性化させる成分を必須成分とする胃酸分泌抑制用、消化管粘液分泌促進用、消化管粘膜保護用、消化管組織修復用、消化器系疾患の予防、治療用として有用な医薬組成物。
【選択図】 なし
【解決手段】 PAR−2を活性化させる成分を必須成分とする胃酸分泌抑制用、消化管粘液分泌促進用、消化管粘膜保護用、消化管組織修復用、消化器系疾患の予防、治療用として有用な医薬組成物。
【選択図】 なし
Description
本発明は、消化器系疾患予防、治療用組成物、特に、胃潰瘍、十二指腸潰瘍、胃炎、下痢、腸炎等を予防および/または治療するための組成物に関する。
胃潰瘍、十二指腸潰瘍等の消化器系潰瘍の原因は、攻撃因子と防御因子とのバランスの破綻により生じる。破綻を惹起する因子としては、薬物(例えば、非ステロイド系消炎剤、副腎皮質ホルモン剤、抗生物質、抗ガン剤、経口血糖降下剤)、ストレス、アルコール、腐食性薬物、肝硬変、アニキサス、食生活等が挙げられる。現在、臨床においては、攻撃因子抑制薬、防御因子増強薬およびこれらの組み合わせが使用されている。
攻撃因子抑制薬としては、制酸薬(例えば、重曹、水酸化アルミニウムゲル、酸化マグネシウム等)、抗コリン薬(例えば、硫酸アトロピン、塩酸ピレンゼピン等)、H2受容体拮抗薬(例えば、シメチジン、ラニチジン、ファモチジン、ニザチジン、ロキサチジン等)、プロトンポンプ阻害薬(例えば、オメプラゾール、ランソプラゾール、ラベプラゾールナトリウム等)、抗ガストリン薬(例えば、プログルミド、セクレチン、ウロガストロン)および抗ペプシン薬(ショ糖硫酸エステル、スクラルファート等)等が臨床において使用されている。
防御因子増強薬としては、粘膜保護薬(例えば、スクラルファート、レパミピド、テプレノン等)、粘膜被覆薬(例えば、アルギン酸ナトリウム、アズノール製剤等)、組織修復促進薬(例えば、アセグルタミドアルミニウム、アルジオキサ、ゲファルナート等)、粘液産生促進薬(例えば、プログルミド、テプレノン、セクレチン、アルジオキサ等)、粘膜微小循環改善薬(例えば、塩酸セトラキサート、ベネキサート、スルピリド等)、プロスタグランジン合成促進薬(例えば、ソファルコン)およびプロスタグランジン製剤(例えば、オルソプロスチル、ミソプロストール、エンプロスチル等)等が臨床において使用されている。また、慢性胃炎には、消化管運動機能改善薬(例えば、シサプリド、ナパジシル酸アクラトニウム、ベタネコール、ドンペリドン、メトクロプラミド、マレイン酸トリメブチン)も使用されている。
攻撃因子抑制薬であるH2受容体拮抗薬およびプロトンポンプ阻害薬等は強力な胃酸分泌抑制作用を有し、かつ顕著な治療効果を有しているため広く使用されている。しかしながら、一旦完治した後であっても薬物の服用を中止すると、胃酸分泌のリバウンド、潰瘍の再発や悪化が高頻度で認められることが明らかとなっている。また、H2受容体拮抗薬では完治しない潰瘍が存在すること、およびプロトンポンプ阻害薬の使用によってはエンテロクロマフィン様細胞の過形成、高ガストリン血症、胃カルチノイドの出現等が報告され、その投薬量が制限されている等の問題があった。また、防御因子増強薬は上記攻撃因子抑制薬に比較して作用が穏やかであるが、治療効果は補助的なものであった。そのため、消化器系疾患を有する患者および内科医からは、H2受容体拮抗薬およびプロトンポンプ阻害薬ではなく、他の作用機序を介して安全で効果的に用いることのできる攻撃因子抑制薬または防御因子増強薬の開発が望まれていた。
攻撃因子抑制薬としては、制酸薬(例えば、重曹、水酸化アルミニウムゲル、酸化マグネシウム等)、抗コリン薬(例えば、硫酸アトロピン、塩酸ピレンゼピン等)、H2受容体拮抗薬(例えば、シメチジン、ラニチジン、ファモチジン、ニザチジン、ロキサチジン等)、プロトンポンプ阻害薬(例えば、オメプラゾール、ランソプラゾール、ラベプラゾールナトリウム等)、抗ガストリン薬(例えば、プログルミド、セクレチン、ウロガストロン)および抗ペプシン薬(ショ糖硫酸エステル、スクラルファート等)等が臨床において使用されている。
防御因子増強薬としては、粘膜保護薬(例えば、スクラルファート、レパミピド、テプレノン等)、粘膜被覆薬(例えば、アルギン酸ナトリウム、アズノール製剤等)、組織修復促進薬(例えば、アセグルタミドアルミニウム、アルジオキサ、ゲファルナート等)、粘液産生促進薬(例えば、プログルミド、テプレノン、セクレチン、アルジオキサ等)、粘膜微小循環改善薬(例えば、塩酸セトラキサート、ベネキサート、スルピリド等)、プロスタグランジン合成促進薬(例えば、ソファルコン)およびプロスタグランジン製剤(例えば、オルソプロスチル、ミソプロストール、エンプロスチル等)等が臨床において使用されている。また、慢性胃炎には、消化管運動機能改善薬(例えば、シサプリド、ナパジシル酸アクラトニウム、ベタネコール、ドンペリドン、メトクロプラミド、マレイン酸トリメブチン)も使用されている。
攻撃因子抑制薬であるH2受容体拮抗薬およびプロトンポンプ阻害薬等は強力な胃酸分泌抑制作用を有し、かつ顕著な治療効果を有しているため広く使用されている。しかしながら、一旦完治した後であっても薬物の服用を中止すると、胃酸分泌のリバウンド、潰瘍の再発や悪化が高頻度で認められることが明らかとなっている。また、H2受容体拮抗薬では完治しない潰瘍が存在すること、およびプロトンポンプ阻害薬の使用によってはエンテロクロマフィン様細胞の過形成、高ガストリン血症、胃カルチノイドの出現等が報告され、その投薬量が制限されている等の問題があった。また、防御因子増強薬は上記攻撃因子抑制薬に比較して作用が穏やかであるが、治療効果は補助的なものであった。そのため、消化器系疾患を有する患者および内科医からは、H2受容体拮抗薬およびプロトンポンプ阻害薬ではなく、他の作用機序を介して安全で効果的に用いることのできる攻撃因子抑制薬または防御因子増強薬の開発が望まれていた。
一方、PAR(protease-activated receptor)は7回膜貫通型のG蛋白共役受容体に属し、プロテアーゼによって活性化される受容体であることが知られている(Hollenberg, M.D., Trends Pharmacol. Sci., 17, 3-6, 1996;Hollenberg, M.D., Trends Pharmacol. Sci., 20, 271-273, 1999)。PARはプロテアーゼにより細胞外ドメインのある特定のN末端部位で切断され、新しいN末端を露出させる。新たに露出したN末端が鎖状リガンドとなって自身の活性部位に結合することにより、受容体の活性化が起こるものと考えられている(Hollenberg, M.D., Trends Pharmacol. Sci., 17, 3-6, 1996;Hollenberg, M.D., Trends Pharmacol. Sci., 20, 271-273, 1999;Vu, T.K. et al., Cell, 64, 1057-68, 1991)。
PARにはPAR−1、PAR−2、PAR−3およびPAR−4のサブタイプが存在し、それぞれ機能が異なることが報告されている。PAR−1、PAR−3およびPAR−4はトロンビンによって活性化され(Vu, T. K. et al., Cell, 64, 1057-1063, 1991;Hollenberg, M.D., Trends Pharmacol. Sci., 17, 3-6, 1996;Ishihara, H. et al., Nature, 386, 502-6, 1997;Kahn, M. L. et al., Nature, 394, 690-4, 1998;Xu, W. F. et al., Proc. Natl. Acad. Sci. USA, 95, 6642-6, 1998)、PAR−2はトリプシン(Nystedt, S. et al., Proc. Natl. Acad. Sci. USA, 91, 9208-12, 1994;Molino, M. et al., J. Biol. Chem., 272, 6011-7, 1997)およびトリプターゼ(Molino, M. et al., J. Biol. Chem., 272, 6011-7, 1997;Fox, M. T. et al., FEBS Lett, 417, 267-9, 1997)によって活性化されることが判明している。
また、PAR−1(Vu, T. K. et al., Cell, 64, 1057-1063, 1991)、PAR−2(Nystedt, S. et al., Proc. Natl. Acad. Sci. USA, 91, 9208-12, 1994)、PAR−3(Ishihara, H. et al., Nature, 386, 502-6, 1997)およびPAR−4(Kahn, M. L. et al., Nature, 394, 690-4, 1998;Xu, W. F. et al., Proc. Natl. Acad. Sci. USA, 95, 6642-6, 1998)のアミノ酸配列上での切断部位が知られており、PAR−1、PAR−2およびPAR−4に関しては、切断部位の活性アミノ酸配列に基づいて合成した5〜6個のアミノ酸から成る合成ペプチドを外来性に与えることにより、該受容体が活性化されることも知られている(Vu, T.K. et al., Cell, 64, 1057-68, 1991;Nystedt, S. et al., Proc. Natl. Acad. Sci. USA, 91, 9208-12, 1994;Ishihara, H. et al., Nature, 386, 502-6, 1997;Kahn, M. L. et al., Nature, 394, 690-4, 1998;Xu, W. F. et al., Proc. Natl. Acad. Sci. USA, 95, 6642-6, 1998;Dery, O. et al., Am. J. Physiol., 274, C1429-52, 1998)。
PAR−2を介する細胞内シグナルの1つとしては、イノシトール1,4,5−トリリン酸(IP3)およびプロテインキナーゼC系の活性化が知られている(Hollenberg, M.D., Trends Pharmacol. Sci., 20, 271-273, 1999;Dery, O. et al., Am. J. Physiol., 274, C1429-52, 1998;Zheng, X. L. et al., J Pharmacol Exp Ther, 285, 325-34, 1998)。
PAR−2に関しては、炎症反応(Cirono, G. et al., J. Exp. Med., 183, 821-827, 1996;Kawabata, A et al., Br. J. Pharmacol., 125, 419-422, 1998)、気管の収縮および弛緩作用(Saifeddine, M. et al., Br. J. Pharmacol., 118, 521-531, 1996;Moffatt, J. D. et al., Br. J. Pharmacol., 125, 591-594, 1998;Cocks, T. M. et al., Nature, 398, 156-160, 1999;Hollenberg, M. D. et al., Can. J. Physiol. Pharmacol., 75, 832-884, 1997)の作用が報告されており、また、PAR−2は前立腺、小腸、結腸、肝臓、腎臓および膵臓での発現が報告されている(Stephan, K. B. et al., Biochem. J., 341, 1009-1016, 1996)。
しかし、PAR−2の胃酸分泌抑制作用、粘液分泌促進作用、粘膜保護作用等の消化器系に関する報告は現在まで存在しない。
Nystedt, S. et al., Proc. Natl. Acad. Sci. USA, 91, 9208-12, 1994 Hollenberg, M.D., Trends Pharmacol. Sci., 20, 271-273, 1999
PARにはPAR−1、PAR−2、PAR−3およびPAR−4のサブタイプが存在し、それぞれ機能が異なることが報告されている。PAR−1、PAR−3およびPAR−4はトロンビンによって活性化され(Vu, T. K. et al., Cell, 64, 1057-1063, 1991;Hollenberg, M.D., Trends Pharmacol. Sci., 17, 3-6, 1996;Ishihara, H. et al., Nature, 386, 502-6, 1997;Kahn, M. L. et al., Nature, 394, 690-4, 1998;Xu, W. F. et al., Proc. Natl. Acad. Sci. USA, 95, 6642-6, 1998)、PAR−2はトリプシン(Nystedt, S. et al., Proc. Natl. Acad. Sci. USA, 91, 9208-12, 1994;Molino, M. et al., J. Biol. Chem., 272, 6011-7, 1997)およびトリプターゼ(Molino, M. et al., J. Biol. Chem., 272, 6011-7, 1997;Fox, M. T. et al., FEBS Lett, 417, 267-9, 1997)によって活性化されることが判明している。
また、PAR−1(Vu, T. K. et al., Cell, 64, 1057-1063, 1991)、PAR−2(Nystedt, S. et al., Proc. Natl. Acad. Sci. USA, 91, 9208-12, 1994)、PAR−3(Ishihara, H. et al., Nature, 386, 502-6, 1997)およびPAR−4(Kahn, M. L. et al., Nature, 394, 690-4, 1998;Xu, W. F. et al., Proc. Natl. Acad. Sci. USA, 95, 6642-6, 1998)のアミノ酸配列上での切断部位が知られており、PAR−1、PAR−2およびPAR−4に関しては、切断部位の活性アミノ酸配列に基づいて合成した5〜6個のアミノ酸から成る合成ペプチドを外来性に与えることにより、該受容体が活性化されることも知られている(Vu, T.K. et al., Cell, 64, 1057-68, 1991;Nystedt, S. et al., Proc. Natl. Acad. Sci. USA, 91, 9208-12, 1994;Ishihara, H. et al., Nature, 386, 502-6, 1997;Kahn, M. L. et al., Nature, 394, 690-4, 1998;Xu, W. F. et al., Proc. Natl. Acad. Sci. USA, 95, 6642-6, 1998;Dery, O. et al., Am. J. Physiol., 274, C1429-52, 1998)。
PAR−2を介する細胞内シグナルの1つとしては、イノシトール1,4,5−トリリン酸(IP3)およびプロテインキナーゼC系の活性化が知られている(Hollenberg, M.D., Trends Pharmacol. Sci., 20, 271-273, 1999;Dery, O. et al., Am. J. Physiol., 274, C1429-52, 1998;Zheng, X. L. et al., J Pharmacol Exp Ther, 285, 325-34, 1998)。
PAR−2に関しては、炎症反応(Cirono, G. et al., J. Exp. Med., 183, 821-827, 1996;Kawabata, A et al., Br. J. Pharmacol., 125, 419-422, 1998)、気管の収縮および弛緩作用(Saifeddine, M. et al., Br. J. Pharmacol., 118, 521-531, 1996;Moffatt, J. D. et al., Br. J. Pharmacol., 125, 591-594, 1998;Cocks, T. M. et al., Nature, 398, 156-160, 1999;Hollenberg, M. D. et al., Can. J. Physiol. Pharmacol., 75, 832-884, 1997)の作用が報告されており、また、PAR−2は前立腺、小腸、結腸、肝臓、腎臓および膵臓での発現が報告されている(Stephan, K. B. et al., Biochem. J., 341, 1009-1016, 1996)。
しかし、PAR−2の胃酸分泌抑制作用、粘液分泌促進作用、粘膜保護作用等の消化器系に関する報告は現在まで存在しない。
Nystedt, S. et al., Proc. Natl. Acad. Sci. USA, 91, 9208-12, 1994 Hollenberg, M.D., Trends Pharmacol. Sci., 20, 271-273, 1999
本発明は上記従来技術に鑑みて行われたものであり、本発明の目的は、安全で効果的な消化器系疾患の予防、治療用組成物、特に胃潰瘍、十二指腸潰瘍、胃炎、下痢、腸炎等を治療および/または予防するための組成物を提供することである。また、これまでの公知の作用機序では困難であった副作用の問題を解決すべく、新規な作用機序を有する上記組成物を提供することである。
本発明者らは、消化器系疾患、特に胃潰瘍、十二指腸潰瘍、胃炎、下痢、腸炎等を治療および/または予防するための組成物として好ましい薬剤を開発すべく研究を行い、新たな作用機序を見出すために誠意研究した結果、PAR−2を活性化させる成分(アゴニスト)が消化器系に対する作用を有すること、すなわち、胃酸分泌を抑制し、消化管粘液分泌を促進し、さらに粘膜保護作用を有することを初めて見出し、本発明を完成した。
すなわち、本発明は、
すなわち、本発明は、
(1)PAR−2を活性化させる成分を含むことを特徴とする胃酸分泌抑制用組成物。
(2)PAR−2を活性化させる成分を含むことを特徴とする消化管粘液分泌促進用組成物、
(3) PAR−2を活性化させる成分を含むことを特徴とする消化管粘膜保護用組成物、
(4)PAR−2を活性化させる成分を含むことを特徴とする、消化器系疾患の予防、治療用組成物、
(5)消化器系疾患が、胃潰瘍、十二指腸潰瘍、胃炎、下痢および腸炎から選択される疾患である請求項4記載の組成物、
(6)成分がペプチドである上記(1)〜(5)いずれか1項の組成物、
(7)成分がタンパク質である上記(1)〜(5)いずれか1項の組成物、
(8)成分を失活化または分解する物質を阻害する物質を組み合わせる請求項上記(1)〜(7)いずれか1項の組成物、
(9)成分を失活化または分解する物質を阻害する物質を併用する上記(8)の組成物、
(10)成分を失活化または分解する物質を阻害する物質を配合する上記(8)の組成物、
(11)阻害する物質がペプチダーゼインヒビターである上記(8)〜(10)いずれか1項記載の組成物、および
(12)徐放化製剤、局所適用製剤、薬物放出制御製剤、腸溶性製剤および胃溶性製剤よりなる群から選択されるDDS製剤とされる上記(1)〜(11)いずれか1項の組成物
を提供するものである。
(2)PAR−2を活性化させる成分を含むことを特徴とする消化管粘液分泌促進用組成物、
(3) PAR−2を活性化させる成分を含むことを特徴とする消化管粘膜保護用組成物、
(4)PAR−2を活性化させる成分を含むことを特徴とする、消化器系疾患の予防、治療用組成物、
(5)消化器系疾患が、胃潰瘍、十二指腸潰瘍、胃炎、下痢および腸炎から選択される疾患である請求項4記載の組成物、
(6)成分がペプチドである上記(1)〜(5)いずれか1項の組成物、
(7)成分がタンパク質である上記(1)〜(5)いずれか1項の組成物、
(8)成分を失活化または分解する物質を阻害する物質を組み合わせる請求項上記(1)〜(7)いずれか1項の組成物、
(9)成分を失活化または分解する物質を阻害する物質を併用する上記(8)の組成物、
(10)成分を失活化または分解する物質を阻害する物質を配合する上記(8)の組成物、
(11)阻害する物質がペプチダーゼインヒビターである上記(8)〜(10)いずれか1項記載の組成物、および
(12)徐放化製剤、局所適用製剤、薬物放出制御製剤、腸溶性製剤および胃溶性製剤よりなる群から選択されるDDS製剤とされる上記(1)〜(11)いずれか1項の組成物
を提供するものである。
本発明の組成物は優れた胃酸分泌抑制作用、粘液分泌促進作用、粘膜保護作用、消化管組織修復作用等を有する優れた予防、治療薬となる。
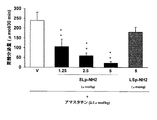
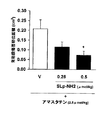
したがって、PAR−2を活性化させる成分であるSer-Leu-Ile-Gly-Arg-Leu-NH2および/またはtrans-シンナモイル-Leu-Ile-Gly-Arg-Leu-オルニチン-NH2等のペプチドを使用することにより、効果的に消化器系疾患を予防および/または治療することができる。また、上記ペプチドは生体に存在するペプチダーゼにより分解されることから、ペプチダーゼインヒビターであるアマスタチン等の薬物と併用あるいは配合することにより、上記ペプチドの作用の持続性を高めることができる。
したがって、PAR−2を活性化させる成分であるSer-Leu-Ile-Gly-Arg-Leu-NH2および/またはtrans-シンナモイル-Leu-Ile-Gly-Arg-Leu-オルニチン-NH2等のペプチドを使用することにより、効果的に消化器系疾患を予防および/または治療することができる。また、上記ペプチドは生体に存在するペプチダーゼにより分解されることから、ペプチダーゼインヒビターであるアマスタチン等の薬物と併用あるいは配合することにより、上記ペプチドの作用の持続性を高めることができる。
「PAR−2を活性化させる成分」は、PAR−2を活性化する能力を有する、天然に存在するか、または人工的に合成されたいずれもの物質をいい、例えば、ペプチド、タンパク質、他の化合物などを包含する。さらに詳しくは、PAR−2を活性化させる成分としては、例えば、天然のPAR−2活性化タンパク質であるトリプシンおよびトリプターゼ、既に報告されているヒトPAR−1アミノ酸配列(Vu, T. K. et al., Cell, 64(6), 1057-1068, 1991)に基づいて合成され、ヒトPAR−1に対しアゴニスト作用を有し(Hollenberg, M.D., Molec. Pharmacol., 43, 921-930, 1993;Hollenberg, M. D., Trends Pharmacol. Sci., 17, 3-6, 1996)、かつPAR−2に対し弱いアゴニスト作用を有することが知られているSer-Phe-Leu-Leu-Arg-NH2ペプチド(配列番号3)(以下、「SFp-NH2」という。) (Kawabata, A. et al., J. Pharmacol. Exp. Ther., 288, 358-70, 1999)、ラットPAR−2のアミノ酸配列(Saifeddine, M. et al., Br. J. Pharmacol., 118(3), 521-530, 1996)より、ラットPAR−2に対しアゴニスト作用を有するSer-Leu-Ile-Gly-Arg-Leu-NH2ペプチド(配列番号1)(以下、「SLp-NH2」という。)(Hollenberg, M.D., Trends Pharmacol. Sci., 17, 3-6, 1996;Nystedt, S. et al., Proc. Natl. Acad. Sci. USA, 91, 9208-12, 1994)、SLp-NH2のC末端がアミド化されていないSer-Leu-Ile-Gly-Arg-Leu-OHペプチド(配列番号4)(以下、「SLp-OH」という。)およびPAR−2を特異的に活性化することが報告されているtrans-シンナモイル-Leu-Ile-Gly-Arg-Leu-オルニチン-NH2ペプチド(配列番号2)(以下、「tcLp-NH2」という。)(Hollenberg, M. D. et al., Can J Physiol Pharmacol, 75, 832-41, 1997)等が挙げられる。さらに、PAR−2に対する抗体またはそのフラグメントも、PAR−2を特異的に活性化するタンパク質またはペプチドとなる可能性がある。
種々の物質を、いずれかの公知の方法にしたがって、PAR−2を活性化する能力についてスクリーニングすることによって、PAR−2を活性化する成分を得てもよい。例えば、PAR−2と試験物質との相互作用を、放射性同位元素での標識または表面プラズモン共鳴などを使用して直接的に検出することによって、PAR−2と結合する物質をスクリーニングすることができる。PAR−2を発現する細胞または組織におけるPAR−2の活性化によって引き起こされる生物学的活性を指標として、PAR−2を介するシグナル伝達を誘導する物質をスクリーニングしてもよい。さらに、実施例に示す胃酸分泌量、粘液分泌量または粘膜保護作用の測定方法を使用して、胃酸分泌抑制作用、粘液分泌促進作用または粘膜保護作用を示す物質をスクリーニングすることができる。PAR−2の活性化についてのアッセイは、例えば、Hollenberg, M. D., Can. J. Physiol. Pharmacol., 75, 832-841, 1997およびKawabata, A., J. Pharmacol. Exp. Ther., 288, 358-370, 1999に記載されている。受容体に結合してこれに作用する物質(すなわち、アゴニスト)についてのスクリーニング方法は当該分野において周知である(例えば、Hollenberg, M. D., Trends Pharmacol. Sci., 20, 271-273, 1999;Dery, O., Am. J. Physiol., 274, C1429-C1452, 1998;Kawabata, A., J. Pharmacol. Exp. Ther., 288, 358-370, 1990を参照のこと)。
本明細書で用いる「ペプチド」なる用語は、オリゴペプチドおよび比較的短いポリペプチドをいう。ペプチドは、例えば、2〜40のアミノ酸残基、好ましくは3〜20アミノ酸残基、より好ましくは5〜15アミノ酸残基を含む。ペプチドは天然に存在するものであってもよく、または化学的に合成されたものであってもよい。ペプチドは、例えば、Carpino, L. A. et al., J. Org. Chem., 37, 3404-3409, 1972に記載されるような公知の方法にしたがって、合成することができる。ペプチドを組換えDNA技術を使用して製造することも可能である。さらに、ペプチドは修飾または非天然アミノ酸残基を含んでいてもよい。
本明細書で用いる「タンパク質」なる用語は、ペプチドに比較してより長いポリペプチドをいう。タンパク質は天然供給源から精製されたものであってもよく、またはこのタンパク質をコードするDNAを含む組換え宿主細胞を培養することによって製造してもよい。ペプチドと同様に、タンパク質を化学的に合成することも可能である。タンパク質は修飾または非天然アミノ酸残基を含んでいてもよい。
本明細書で用いる「タンパク質」なる用語は、ペプチドに比較してより長いポリペプチドをいう。タンパク質は天然供給源から精製されたものであってもよく、またはこのタンパク質をコードするDNAを含む組換え宿主細胞を培養することによって製造してもよい。ペプチドと同様に、タンパク質を化学的に合成することも可能である。タンパク質は修飾または非天然アミノ酸残基を含んでいてもよい。
かくして、PAR−2を活性化させる成分は、胃酸分泌を抑制し、消化管粘液分泌を促進し、さらに粘膜保護作用を有するので、本発明のPAR−2を活性化させる成分を含む組成物は、胃酸分泌抑制用組成物、消化管粘液分泌促進用組成物、消化管組織修復用組成物および消化管粘膜保護用組成物として有用であり、消化器系疾患の予防、治療用組成物、特に胃潰瘍、十二指腸潰瘍、胃炎、下痢、腸炎等を予防および/または治療するのに有用である。
予防剤または治療剤として用いる場合、本発明の組成物を、そのままあるいは水に希釈する等の各種処理を施して使用することができ、医薬品、医薬部外品等に配合して使用することができる。この場合、PAR−2を活性化させる成分の配合量は製品に応じて適宜選択されるところではあるが、通常全身投与製剤の場合には、0.001〜50重量%、特に0.01〜10重量%とすることができ、0.001%より少ないと満足する予防または治療作用が認められない可能性があり、また、50%を越えると製品そのものの安定性や香味等の特性が損なわれる可能性がある。
予防剤または治療剤として用いる場合、本発明の組成物を、そのままあるいは水に希釈する等の各種処理を施して使用することができ、医薬品、医薬部外品等に配合して使用することができる。この場合、PAR−2を活性化させる成分の配合量は製品に応じて適宜選択されるところではあるが、通常全身投与製剤の場合には、0.001〜50重量%、特に0.01〜10重量%とすることができ、0.001%より少ないと満足する予防または治療作用が認められない可能性があり、また、50%を越えると製品そのものの安定性や香味等の特性が損なわれる可能性がある。
本発明の組成物に含まれるPAR−2を活性化する成分は、製剤学的に許容される塩として製剤中に含有されていてもよい。薬剤学的に許容される塩としては、例えば、無機塩基、有機塩基等の塩基との塩、無機酸、有機酸、塩基性または酸性アミノ酸などの酸付加塩等が挙げられる。無機塩基としては、例えば、ナトリウム、カリウム等のアルカリ金属、カルシウム、マグネシウム等のアルカリ土類金属、アルミニウム、アンモニウム等が挙げられる。有機塩基としては、例えば、エタノールアミン等の第一級アミン、ジエチルアミン、ジエタノールアミン、ジシクロヘキシルアミン、N,N'-ジベンジルエチレンジアミン等の第二級アミン、トリメチルアミン、トリエチルアミン、ピリジン、ピコリン、トリエタノールアミン等の第三級アミン等が挙げられる。無機酸としては、例えば、塩酸、臭化水素酸、硝酸、硫酸、リン酸等が挙げられる。有機酸としては、例えば、ギ酸、酢酸、乳酸、トリフルオロ酢酸、フマール酸、シュウ酸、酒石酸、マレイン酸、安息香酸、クエン酸、コハク酸、リンゴ酸、メタンスルホン酸、エタンスルホン酸、ベンゼンスルホン酸、p-トルエンスルホン酸等が挙げられる。塩基性アミノ酸としては、例えば、アルギニン、リジン、オルニチン等が挙げられる。酸性アミノ酸としては、例えば、アスパラギン酸、グルタミン酸等が挙げられる。
また、ペプチドおよびタンパク質は生体に存在するペプチダーゼにより分解されることから、PAR−2を活性化させる成分としてペプチドまたはタンパク質を用いる場合、ペプチダーゼインヒビターであるアマスタチン等の薬物と併用あるいは配合して組み合わせることにより、PAR−2を活性化する作用の持続性を高めることができる。上記成分がペプチドでない場合、当業者は適切に、この成分を失活化または分解する物質を同定し、これを阻害する物質を選択し、これを併用あるいは配合できる。
また、ペプチドおよびタンパク質は生体に存在するペプチダーゼにより分解されることから、PAR−2を活性化させる成分としてペプチドまたはタンパク質を用いる場合、ペプチダーゼインヒビターであるアマスタチン等の薬物と併用あるいは配合して組み合わせることにより、PAR−2を活性化する作用の持続性を高めることができる。上記成分がペプチドでない場合、当業者は適切に、この成分を失活化または分解する物質を同定し、これを阻害する物質を選択し、これを併用あるいは配合できる。
本発明の組成物の投与方法としては、経口投与、静脈内投与以外に、経粘膜投与、経皮投与、筋肉内投与、皮下投与、直腸内投与等が適宜選択でき、その投与方法に応じて、種々の製剤として用いることができる。
以下に、各製剤について記載するが、本発明において用いられる剤型はこれらに限定されるものではなく、医薬製剤分野において通常用いられる各種製剤として用いることができる。
以下に、各製剤について記載するが、本発明において用いられる剤型はこれらに限定されるものではなく、医薬製剤分野において通常用いられる各種製剤として用いることができる。
消化器系疾患の予防薬または治療薬として用いる場合には、PAR−2を活性化させる成分の経口投与量は、3mg/kg〜300mg/kgの範囲が好ましく、より好ましくは10mg/kg〜100mg/kgである。全身投与を行う場合、特に静脈内投与の場合には老若男女または体型等により変動があるが、有効血中濃度が2μg/mL〜200μg/mL、より好ましくは5μg/mL〜100μg/mLの範囲となるように投与すべきである。
経口投与を行う場合の剤型として、散剤、顆粒剤、カプセル剤、丸剤、錠剤、エリキシル剤、懸濁剤、乳剤およびシロップ剤等があり、適宜選択することができる。また、それら製剤について徐放化、安定化、易崩壊化、難崩壊化、腸溶性化、易吸収化等の修飾を施すことができる。また、口腔内局所投与を行う場合の剤型として、咀嚼剤、舌下剤、バッカル剤、トローチ剤、軟膏剤、貼布剤、液剤等があり、適宜選択することができる。また、それら製剤について徐放化、安定化、易崩壊化、難崩壊化、腸溶性化、易吸収化等の修飾を施すことができる。
上記の各剤型について、公知のドラッグデリバリーシステム(DDS)の技術を採用することができる。本明細書でいうDDS製剤とは、徐放化製剤、局所適用製剤(トローチ、バッカル錠、舌下錠等)、薬物放出制御製剤、腸溶性製剤および胃溶性製剤等、投与経路、バイオアベイラビリティー、副作用等を勘案した上で、最適の製剤形態にした製剤をいう。
DDSの構成要素には基本的に薬物、薬物放出モジュール、被膜および治療プログラムから成り、各々の構成要素について、特に放出を停止させた時に速やかに血中濃度が低下する半減期の短い薬物が好ましく、投与部位の生体組織と反応しないおおいが好ましく、さらに、設定された期間において最良の薬物濃度を維持する治療プログラムを有するのが好ましい。薬物放出モジュールは基本的に薬物貯蔵庫、放出制御部、エネルギー源および放出孔または放出表面を有している。これら基本的構成要素は全て揃っている必要はなく、適宜追加あるいは削除等を行い、最良の形態を選択することができる。
DDSに使用できる材料としては、高分子、シクロデキストリン誘導体、レシチン等がある。高分子には不溶性高分子(シリコーン、エチレン・酢酸ビニル共重合体、エチレン・ビニルアルコール共重合体、エチルセルロース、セルロースアセテート等)、水溶性高分子およびヒドロキシルゲル形成高分子(ポリアクリルアミド、ポリヒドロキシエチルメタクリレート架橋体、ポリアクリル架橋体、ポリビニルアルコール、ポリエチレンオキシド、水溶性セルロース誘導体、架橋ポロキサマー、キチン、キトサン等)、徐溶解性高分子(エチルセルロース、メチルビニルエーテル・無水マレイン酸共重合体の部分エステル等)、胃溶性高分子(ヒドロキシプロピルメチルセルロース、ヒドロキシプロピルセルロース、カルメロースナトリウム、マクロゴール、ポリビニルピロリドン、メタアクリル酸ジメチルアミノエチル・メタアクリル酸メチルコポリマー等)、腸溶性高分子(ヒドロキシプロピルメチルセルロースフタレート、酢酸フタルセルロース、ヒドロキシプロピルメチルセルロースアセテートサクシネート、カルボキシメチルエチルセルロース、アクリル酸系ポリマー等)、生分解性高分子(熱凝固または架橋アルブミン、架橋ゼラチン、コラーゲン、フィブリン、ポリシアノアクリレート、ポリグリコール酸、ポリ乳酸、ポリβヒドロキシ酢酸、ポリカプロラクトン等)があり、剤型によって適宜選択することができる。
特に、シリコーン、エチレン・酢酸ビニル共重合体、エチレン−ビニルアルコール共重合体、メチルビニルエーテル・無水マレインサン共重合体の部分エステルは薬物の放出制御に使用でき、セルロースアセテートは浸透圧ポンプの材料として使用でき、エチルセルロース、ヒドロキシプロピルメチルセルロース、ヒドロキシプロピルセルロース、メチルセルロースは徐放性製剤の膜素材として使用でき、ポリアクリル架橋体は口腔粘膜あるいは眼粘膜付着剤として使用できる。
また、製剤中にはその剤形(経口投与剤、注射剤、座剤等の公知の剤形)に応じて、溶剤、賦形剤、コーティング剤、基剤、結合剤、滑沢剤、崩壊剤、溶解補助剤、懸濁化剤、粘稠剤、乳化剤、安定剤、緩衝剤、等張化剤、無痛化剤、保存剤、矯味剤、芳香剤、着色剤等の添加剤を加えて製造することができる。
これら各添加剤について、それぞれ具体例を挙げて例示するが、これらに特に限定されるものではない。
経口投与を行う場合の剤型として、散剤、顆粒剤、カプセル剤、丸剤、錠剤、エリキシル剤、懸濁剤、乳剤およびシロップ剤等があり、適宜選択することができる。また、それら製剤について徐放化、安定化、易崩壊化、難崩壊化、腸溶性化、易吸収化等の修飾を施すことができる。また、口腔内局所投与を行う場合の剤型として、咀嚼剤、舌下剤、バッカル剤、トローチ剤、軟膏剤、貼布剤、液剤等があり、適宜選択することができる。また、それら製剤について徐放化、安定化、易崩壊化、難崩壊化、腸溶性化、易吸収化等の修飾を施すことができる。
上記の各剤型について、公知のドラッグデリバリーシステム(DDS)の技術を採用することができる。本明細書でいうDDS製剤とは、徐放化製剤、局所適用製剤(トローチ、バッカル錠、舌下錠等)、薬物放出制御製剤、腸溶性製剤および胃溶性製剤等、投与経路、バイオアベイラビリティー、副作用等を勘案した上で、最適の製剤形態にした製剤をいう。
DDSの構成要素には基本的に薬物、薬物放出モジュール、被膜および治療プログラムから成り、各々の構成要素について、特に放出を停止させた時に速やかに血中濃度が低下する半減期の短い薬物が好ましく、投与部位の生体組織と反応しないおおいが好ましく、さらに、設定された期間において最良の薬物濃度を維持する治療プログラムを有するのが好ましい。薬物放出モジュールは基本的に薬物貯蔵庫、放出制御部、エネルギー源および放出孔または放出表面を有している。これら基本的構成要素は全て揃っている必要はなく、適宜追加あるいは削除等を行い、最良の形態を選択することができる。
DDSに使用できる材料としては、高分子、シクロデキストリン誘導体、レシチン等がある。高分子には不溶性高分子(シリコーン、エチレン・酢酸ビニル共重合体、エチレン・ビニルアルコール共重合体、エチルセルロース、セルロースアセテート等)、水溶性高分子およびヒドロキシルゲル形成高分子(ポリアクリルアミド、ポリヒドロキシエチルメタクリレート架橋体、ポリアクリル架橋体、ポリビニルアルコール、ポリエチレンオキシド、水溶性セルロース誘導体、架橋ポロキサマー、キチン、キトサン等)、徐溶解性高分子(エチルセルロース、メチルビニルエーテル・無水マレイン酸共重合体の部分エステル等)、胃溶性高分子(ヒドロキシプロピルメチルセルロース、ヒドロキシプロピルセルロース、カルメロースナトリウム、マクロゴール、ポリビニルピロリドン、メタアクリル酸ジメチルアミノエチル・メタアクリル酸メチルコポリマー等)、腸溶性高分子(ヒドロキシプロピルメチルセルロースフタレート、酢酸フタルセルロース、ヒドロキシプロピルメチルセルロースアセテートサクシネート、カルボキシメチルエチルセルロース、アクリル酸系ポリマー等)、生分解性高分子(熱凝固または架橋アルブミン、架橋ゼラチン、コラーゲン、フィブリン、ポリシアノアクリレート、ポリグリコール酸、ポリ乳酸、ポリβヒドロキシ酢酸、ポリカプロラクトン等)があり、剤型によって適宜選択することができる。
特に、シリコーン、エチレン・酢酸ビニル共重合体、エチレン−ビニルアルコール共重合体、メチルビニルエーテル・無水マレインサン共重合体の部分エステルは薬物の放出制御に使用でき、セルロースアセテートは浸透圧ポンプの材料として使用でき、エチルセルロース、ヒドロキシプロピルメチルセルロース、ヒドロキシプロピルセルロース、メチルセルロースは徐放性製剤の膜素材として使用でき、ポリアクリル架橋体は口腔粘膜あるいは眼粘膜付着剤として使用できる。
また、製剤中にはその剤形(経口投与剤、注射剤、座剤等の公知の剤形)に応じて、溶剤、賦形剤、コーティング剤、基剤、結合剤、滑沢剤、崩壊剤、溶解補助剤、懸濁化剤、粘稠剤、乳化剤、安定剤、緩衝剤、等張化剤、無痛化剤、保存剤、矯味剤、芳香剤、着色剤等の添加剤を加えて製造することができる。
これら各添加剤について、それぞれ具体例を挙げて例示するが、これらに特に限定されるものではない。
溶剤:精製水、注射用水、生理食塩水、ラッカセイ油、エタノール、グリセリン、
賦形剤:デンプン類、乳糖、ブドウ糖、白糖、結晶セルロース、硫酸カルシウム、炭酸カルシウム、タルク、酸化チタン、トレハロース、キシリトール、
コーティング剤:白糖、ゼラチン、酢酸フタル酸セルロースおよび上記記載した高分子、
基剤:ワセリン、植物油、マクロゴール、水中油型乳剤性基剤、油中水型乳剤性基剤、
結合剤:デンプンおよびその誘導体、セルロースおよびその誘導体、ゼラチン、アルギン酸ナトリウム、トラガント、アラビアゴム等の天然高分子化合物、ポリビニルピロリドン等の合成高分子化合物、デキストリン、ヒドロキシプロピルスターチ、
滑沢剤:ステアリン酸およびその塩類、タルク、ワックス類、コムギデンプン、マクロゴール、水素添加植物油、ショ糖脂肪酸エステル、ポリエチレングリコール、
崩壊剤:デンプンおよびその誘導体、寒天、ゼラチン末、炭酸水素ナトリウム、セルロースおよびその誘導体、カルメロースカルシウム、ヒドロキシプロピルスターチ、カルボキシメチルセルロースおよびその塩類ならびにその架橋体、低置換型ヒドロキシプロピルセルロース、
溶解補助剤:シクロデキストリン、エタノール、プロピレングリコール、ポリエチレングリコール、
懸濁化剤:アラビアゴム、トラガント、アルギン酸ナトリウム、モノステアリン酸アルミニウム、クエン酸、各種界面活性剤、
粘稠剤:カルメロースナトリウム、ポリビニルピロリドン、メチルセルロース、ホドロキシプロピルメチルセルロース、ポリビニルアルコール、トラガント、アラビアゴム、アルギン酸ナトリウム、
乳化剤:アラビアゴム、コレステロール、トラガント、メチルセルロース、各種界面活性剤、レシチン、
安定剤:亜硫酸水素ナトリウム、アスコルビン酸、トコフェロール、キレート剤、不活性ガス、還元性物質、
緩衝剤:リン酸水素ナトリウム、酢酸ナトリウム、ホウ酸、
等張化剤:塩化ナトリウム、ブドウ糖、
無痛化剤:塩酸プロカイン、リドカイン、ベンジルアルコール、
保存剤:安息香酸およびその塩類、パラオキシ安息香酸エステル類、クロロブタノール、逆性石けん、ベンジルアルコール、フェノール、チロメサール、
矯味剤:白糖、サッカリン、カンゾウエキス、ソルビトール、キシリトール、グリセリン、
芳香剤:トウヒチンキ、ローズ油、
着色剤:水溶性食用色素、レーキ色素。
賦形剤:デンプン類、乳糖、ブドウ糖、白糖、結晶セルロース、硫酸カルシウム、炭酸カルシウム、タルク、酸化チタン、トレハロース、キシリトール、
コーティング剤:白糖、ゼラチン、酢酸フタル酸セルロースおよび上記記載した高分子、
基剤:ワセリン、植物油、マクロゴール、水中油型乳剤性基剤、油中水型乳剤性基剤、
結合剤:デンプンおよびその誘導体、セルロースおよびその誘導体、ゼラチン、アルギン酸ナトリウム、トラガント、アラビアゴム等の天然高分子化合物、ポリビニルピロリドン等の合成高分子化合物、デキストリン、ヒドロキシプロピルスターチ、
滑沢剤:ステアリン酸およびその塩類、タルク、ワックス類、コムギデンプン、マクロゴール、水素添加植物油、ショ糖脂肪酸エステル、ポリエチレングリコール、
崩壊剤:デンプンおよびその誘導体、寒天、ゼラチン末、炭酸水素ナトリウム、セルロースおよびその誘導体、カルメロースカルシウム、ヒドロキシプロピルスターチ、カルボキシメチルセルロースおよびその塩類ならびにその架橋体、低置換型ヒドロキシプロピルセルロース、
溶解補助剤:シクロデキストリン、エタノール、プロピレングリコール、ポリエチレングリコール、
懸濁化剤:アラビアゴム、トラガント、アルギン酸ナトリウム、モノステアリン酸アルミニウム、クエン酸、各種界面活性剤、
粘稠剤:カルメロースナトリウム、ポリビニルピロリドン、メチルセルロース、ホドロキシプロピルメチルセルロース、ポリビニルアルコール、トラガント、アラビアゴム、アルギン酸ナトリウム、
乳化剤:アラビアゴム、コレステロール、トラガント、メチルセルロース、各種界面活性剤、レシチン、
安定剤:亜硫酸水素ナトリウム、アスコルビン酸、トコフェロール、キレート剤、不活性ガス、還元性物質、
緩衝剤:リン酸水素ナトリウム、酢酸ナトリウム、ホウ酸、
等張化剤:塩化ナトリウム、ブドウ糖、
無痛化剤:塩酸プロカイン、リドカイン、ベンジルアルコール、
保存剤:安息香酸およびその塩類、パラオキシ安息香酸エステル類、クロロブタノール、逆性石けん、ベンジルアルコール、フェノール、チロメサール、
矯味剤:白糖、サッカリン、カンゾウエキス、ソルビトール、キシリトール、グリセリン、
芳香剤:トウヒチンキ、ローズ油、
着色剤:水溶性食用色素、レーキ色素。
上記したように、医薬品を除法化製剤、腸溶性製剤または薬物放出制御製剤等のDDS製剤化することにより、薬物の有効血中濃度の持続化、バイオアベイラビリティーの向上等の効果が期待できる。しかし、PAR−2を活性化させる成分は生体内で失活化または分解され、その結果、所望の効果が低下または消失する可能性がある。例えば、PAR−2を活性化させる成分がペプチドである場合、そのようなペプチドの多くは生体内において、アミノペプチダーゼにより分解されることが知られている(Godin, D. et al., Eur. J. Pharmacol., 253, 225-30, 1994)。したがって、、PAR−2を活性化させる成分を失活化または分解する物質を阻害する物質(例えば、アミノペプチダーゼを阻害する物質)を本発明の組成物と併用することにより、成分の効果をさらに持続化させ得る。
アミノペプチダーゼ阻害薬としては、アマスタチン、アファメニンA、アファメニンBおよびベスタチン等が知られている。これらの化合物を製剤中に配合してもよく、または別々に投与してもよい。上記成分がペプチドでない場合、当業者は適切に、この成分を失活化または分解する物質を同定し、これを阻害する物質を選択し、配合あるいは併用することができる。
製剤中には、上記以外の添加物として通常の組成物に使用されている成分を用いることができ、これらの成分の添加量は、本発明の効果を妨げない範囲で通常量とすることができる。
アミノペプチダーゼ阻害薬としては、アマスタチン、アファメニンA、アファメニンBおよびベスタチン等が知られている。これらの化合物を製剤中に配合してもよく、または別々に投与してもよい。上記成分がペプチドでない場合、当業者は適切に、この成分を失活化または分解する物質を同定し、これを阻害する物質を選択し、配合あるいは併用することができる。
製剤中には、上記以外の添加物として通常の組成物に使用されている成分を用いることができ、これらの成分の添加量は、本発明の効果を妨げない範囲で通常量とすることができる。
本発明の組成物は、ヘリコバクター・ピロリ菌の除菌療法にも併用できる。例えば、オメプラゾール40mg(1日2回)とアモキシシリン1,500mg(1日3回)に加えて、本発明の組成物300mg(1日3回)を併用できる。
慢性消化性潰瘍、若年者に多い潰瘍性大腸炎、クローン病等の難治性消化管障害の治療にも有用である。
慢性消化性潰瘍、若年者に多い潰瘍性大腸炎、クローン病等の難治性消化管障害の治療にも有用である。
つぎに、実施例を挙げて本発明をさらに詳しく説明するが、本発明は、これらに限定されるものではない。
各種ペプチドの合成方法
実施例で使用したアゴニストペプチド(Ser-Leu-Ile-Gly-Arg-Leu-NH2(SLp-NH2))およびコントロールペプチド(Leu-Ser-Ile-Gly-Arg-Leu-NH2(LSp-NH2))を、既知の方法(Carpino, L. A. et al., J. Org. Chem., 37, 3404-3409, 1972)に準じて合成した。
Ser-Leu-Ile-Gly-Arg-Leu-NH2(配列番号1、SLp-NH2)の合成
Fmoc-PAL-PEG-PS-樹脂(PEバイオシステムズ)を1.33g(0.17meq/g)秤取し、これにジメチルホルムアミド10mLを加えて2〜3時間放置し、樹脂を膨張させた後、ペプチド合成用のカラムに充填した。
Fmoc-L-Leu-OH 283mg(WAKO)、Fmoc-L-Arg(Pbf)-OH 519mg(PEバイオシステムズ)、Fmoc-L-Gly-OH 238mg(BACHEM)、Fmoc-L-Ile-OH 283mg(WAKO)、Fmoc-L-Leu-OH 283mg(WAKO)、Fmoc-L-Ser(tBu)-OH 307mg(PEバイオシステムズ)を試験管に秤量し、これにHATU(0-(7-アザベンゾトリアゾール-1-イル)-1,1,3,3-テトラメチルウロニウムヘキサフルオロホスフェート)(PEバイオシステムズ)を各380mg加えた。上記のアミノ酸をC末端から順に並べ、ペプチド合成機PIONEER(PEバイオシステムズ)を用いて合成を行った。合成したペプチド−樹脂をTFA-H20-フェノール-トリイソプロピルシラン(8.8:0.5:0.5:0.2)の混合溶液で3時間処理した後、樹脂を濾過し、濾液をエーテルで再結晶し、粗ペプチドを得た。次に、この粗ペプチドをHPLC(A:0.02%TFA含H2O、B:0.02%TFA含50%CH3CN)に供し精製した。得られたフラクションを凍結乾燥し、Ser-Leu-Ile-Gly-Arg-Leu-NH2を得た。
Leu-Ser-Ile-Gly-Arg-Leu-NH2(配列番号5、LSp-NH2)
LSp-NH2はSLp-NH2のSerとLeuを入れ替えることにより不活性体となる(Hollenberg, M.D., Trends Pharmacol. Sci., 17, 3-6, 1996、Nystedt, S. et al., Proc. Natl. Acad. Sci. USA, 91, 9208-12, 1994)。
上記方法に準じてペプチド合成用カラムを作製し、Fmoc-L-Leu-OH 283mg(WAKO)、Fmoc-L-Arg(Pbf)-OH 519mg(PEバイオシステムズ)、Fmoc-L-Gly-OH 238mg(BACHEM)、Fmoc-L-Ile-OH 283mg(WAKO) 、Fmoc-L-Ser(tBu)-OH 307mg(PEバイオシステムズ)、Fmoc-L-Leu-OH 283mg(WAKO)を試験管に秤量し、これにHATU各380mg加えた。上記のアミノ酸をC末端から順に並べ、ペプチド合成機PIONEERを用いて合成を行った。合成したペプチド−樹脂を上記した方法により粗ペプチドを得、その後HPLCに供し精製した。得られたフラクションを凍結乾燥してLeu-Ser--Ile-Gly-Arg-Leu-NH2を得た。
また、同じく実施例で使用したアゴニストペプチドであるtrans-シンナモイル-Leu-Ile-Gly-Arg-Leu-オルニチン-NH2(配列番号2、tcLp-NH2)は、米国カルガリー大学医学部のHollenberg, M. D. 教授より御供与いただいた。
実施例で使用したアゴニストペプチド(Ser-Leu-Ile-Gly-Arg-Leu-NH2(SLp-NH2))およびコントロールペプチド(Leu-Ser-Ile-Gly-Arg-Leu-NH2(LSp-NH2))を、既知の方法(Carpino, L. A. et al., J. Org. Chem., 37, 3404-3409, 1972)に準じて合成した。
Ser-Leu-Ile-Gly-Arg-Leu-NH2(配列番号1、SLp-NH2)の合成
Fmoc-PAL-PEG-PS-樹脂(PEバイオシステムズ)を1.33g(0.17meq/g)秤取し、これにジメチルホルムアミド10mLを加えて2〜3時間放置し、樹脂を膨張させた後、ペプチド合成用のカラムに充填した。
Fmoc-L-Leu-OH 283mg(WAKO)、Fmoc-L-Arg(Pbf)-OH 519mg(PEバイオシステムズ)、Fmoc-L-Gly-OH 238mg(BACHEM)、Fmoc-L-Ile-OH 283mg(WAKO)、Fmoc-L-Leu-OH 283mg(WAKO)、Fmoc-L-Ser(tBu)-OH 307mg(PEバイオシステムズ)を試験管に秤量し、これにHATU(0-(7-アザベンゾトリアゾール-1-イル)-1,1,3,3-テトラメチルウロニウムヘキサフルオロホスフェート)(PEバイオシステムズ)を各380mg加えた。上記のアミノ酸をC末端から順に並べ、ペプチド合成機PIONEER(PEバイオシステムズ)を用いて合成を行った。合成したペプチド−樹脂をTFA-H20-フェノール-トリイソプロピルシラン(8.8:0.5:0.5:0.2)の混合溶液で3時間処理した後、樹脂を濾過し、濾液をエーテルで再結晶し、粗ペプチドを得た。次に、この粗ペプチドをHPLC(A:0.02%TFA含H2O、B:0.02%TFA含50%CH3CN)に供し精製した。得られたフラクションを凍結乾燥し、Ser-Leu-Ile-Gly-Arg-Leu-NH2を得た。
Leu-Ser-Ile-Gly-Arg-Leu-NH2(配列番号5、LSp-NH2)
LSp-NH2はSLp-NH2のSerとLeuを入れ替えることにより不活性体となる(Hollenberg, M.D., Trends Pharmacol. Sci., 17, 3-6, 1996、Nystedt, S. et al., Proc. Natl. Acad. Sci. USA, 91, 9208-12, 1994)。
上記方法に準じてペプチド合成用カラムを作製し、Fmoc-L-Leu-OH 283mg(WAKO)、Fmoc-L-Arg(Pbf)-OH 519mg(PEバイオシステムズ)、Fmoc-L-Gly-OH 238mg(BACHEM)、Fmoc-L-Ile-OH 283mg(WAKO) 、Fmoc-L-Ser(tBu)-OH 307mg(PEバイオシステムズ)、Fmoc-L-Leu-OH 283mg(WAKO)を試験管に秤量し、これにHATU各380mg加えた。上記のアミノ酸をC末端から順に並べ、ペプチド合成機PIONEERを用いて合成を行った。合成したペプチド−樹脂を上記した方法により粗ペプチドを得、その後HPLCに供し精製した。得られたフラクションを凍結乾燥してLeu-Ser--Ile-Gly-Arg-Leu-NH2を得た。
また、同じく実施例で使用したアゴニストペプチドであるtrans-シンナモイル-Leu-Ile-Gly-Arg-Leu-オルニチン-NH2(配列番号2、tcLp-NH2)は、米国カルガリー大学医学部のHollenberg, M. D. 教授より御供与いただいた。
PAR−2を活性化させる成分である他の各種ペプチドは、例えば、以下のようにして合成できる。
Ser-Phe-Leu-Leu-Arg-NH2(配列番号3、SFp-NH2)の合成
Fmoc-PAL-PEG-PS-樹脂(PEバイオシステムズ)を1.33g(0.17meq/g)秤取し、これにジメチルホルムアミド10mLを加えて2〜3時間放置し、樹脂を膨張させた後、ペプチド合成用のカラムに充填する。
Fmoc-L-Arg(Pbf)-OH 519mg(PEバイオシステムズ)、Fmoc-L-Leu-OH 283mg(WAKO)、Fmoc-L-Leu-OH 283mg(WAKO)、Fmoc-L-Phe-OH 305mg(WAKO)、Fmoc-L-Ser(tBu)-OH 307mg(PEバイオシステムズ)を試験管に秤量し、これにHATU (PEバイオシステムズ)を各380mg加える。上記のアミノ酸をC末端から順に並べ、ペプチド合成機PIONEER(PEバイオシステムズ)を用いて合成を行う。合成したペプチド−樹脂をTFA-H20-フェノール-トリイソプロピルシラン(8.8:0.5:0.5:0.2)の混合溶液で3時間処理した後、樹脂を濾過し、濾液をエーテルで再結晶し、粗ペプチドを得る。次に、この粗ペプチドをHPLC(A:0.02%TFA含H2O、B:0.02%TFA含50%CH3CN)に供し精製する。得られたフラクションを凍結乾燥することにより、Ser-Phe-Leu-Leu-Arg-NH2を得ることができる。
Ser-Leu-Ile-Gly-Arg-Leu-OH(配列番号4、SLp-OH)の合成
Fmoc-L-Leu-PEG-PS-樹脂(PEバイオシステムズ)を1.00g(0.21meq/g)秤取し、これにジメチルホルムアミド10mLを加えて2〜3時間放置し、樹脂を膨張させた後、ペプチド合成用のカラムに充填する。
Fmoc-L-Arg(Pbf)-OH 519mg(PEバイオシステムズ)、Fmoc-L-Gly-OH 238mg(BACHEM)、Fmoc-L-Ile-OH 283mg(WAKO)、Fmoc-L-Leu-OH 283mg(WAKO)、Fmoc-L-Ser(tBu)-OH 307mg(PEバイオシステムズ)を試験管に秤量し、これにHATU各380mg加える。上記のアミノ酸をC末端から順に並べ、ペプチド合成機PIONEERを用いて合成を行う。合成したペプチド−樹脂を上記した方法により粗ペプチドを得、その後、HPLCに供し精製する。得られたフラクションを凍結乾燥することにより、Ser-Leu-Ile-Gly-Arg-Leu-OH を得ることができる。
Ser-Phe-Leu-Leu-Arg-NH2(配列番号3、SFp-NH2)の合成
Fmoc-PAL-PEG-PS-樹脂(PEバイオシステムズ)を1.33g(0.17meq/g)秤取し、これにジメチルホルムアミド10mLを加えて2〜3時間放置し、樹脂を膨張させた後、ペプチド合成用のカラムに充填する。
Fmoc-L-Arg(Pbf)-OH 519mg(PEバイオシステムズ)、Fmoc-L-Leu-OH 283mg(WAKO)、Fmoc-L-Leu-OH 283mg(WAKO)、Fmoc-L-Phe-OH 305mg(WAKO)、Fmoc-L-Ser(tBu)-OH 307mg(PEバイオシステムズ)を試験管に秤量し、これにHATU (PEバイオシステムズ)を各380mg加える。上記のアミノ酸をC末端から順に並べ、ペプチド合成機PIONEER(PEバイオシステムズ)を用いて合成を行う。合成したペプチド−樹脂をTFA-H20-フェノール-トリイソプロピルシラン(8.8:0.5:0.5:0.2)の混合溶液で3時間処理した後、樹脂を濾過し、濾液をエーテルで再結晶し、粗ペプチドを得る。次に、この粗ペプチドをHPLC(A:0.02%TFA含H2O、B:0.02%TFA含50%CH3CN)に供し精製する。得られたフラクションを凍結乾燥することにより、Ser-Phe-Leu-Leu-Arg-NH2を得ることができる。
Ser-Leu-Ile-Gly-Arg-Leu-OH(配列番号4、SLp-OH)の合成
Fmoc-L-Leu-PEG-PS-樹脂(PEバイオシステムズ)を1.00g(0.21meq/g)秤取し、これにジメチルホルムアミド10mLを加えて2〜3時間放置し、樹脂を膨張させた後、ペプチド合成用のカラムに充填する。
Fmoc-L-Arg(Pbf)-OH 519mg(PEバイオシステムズ)、Fmoc-L-Gly-OH 238mg(BACHEM)、Fmoc-L-Ile-OH 283mg(WAKO)、Fmoc-L-Leu-OH 283mg(WAKO)、Fmoc-L-Ser(tBu)-OH 307mg(PEバイオシステムズ)を試験管に秤量し、これにHATU各380mg加える。上記のアミノ酸をC末端から順に並べ、ペプチド合成機PIONEERを用いて合成を行う。合成したペプチド−樹脂を上記した方法により粗ペプチドを得、その後、HPLCに供し精製する。得られたフラクションを凍結乾燥することにより、Ser-Leu-Ile-Gly-Arg-Leu-OH を得ることができる。
カルバコール誘発胃酸分泌亢進に及ぼす影響
使用動物
実験には5週齢のWistar系雄性ラットを使用した。各動物は室温23±2℃、湿度50±5%および12時間の明暗サイクル(明期:07:00から19:00)の環境下で1週間の予備飼育の後、実験に供した。予備飼育期間および実験期間中は水および固型飼料を自由に摂取させた。
また、実験に用いた例数は全て4〜14匹であり、結果を平均値±標準誤差で示した。有意差検定はTukeyの多重比較検定で行った。
方法
18〜24時間の絶食後、ラットをエーテルで麻酔し、胸部剣状骨下端下方を、約1 cm開腹した。開腹孔より十二指腸をはさみだし、幽門と十二指腸の接合部を結紮し、開腹部を縫合した。その30分後にラットを放血致死させ、胃を取り出し、胃液を採取した。採取した胃液を濾過した後、胃液中の酸度を滴定法により測定した。カルバコール (60μg/kg) は幽門結紮直後に皮下投与し、その1分後にアマスタチン (2.5μmol/kg) を、また、その1分後にSLp-NH2およびLSp-NH2を静脈内投与し、カルバコールの投与によって亢進した胃酸分泌に対する作用を調べた。
結果
結果を図1に示す。
図1において、縦軸は胃酸分泌量(μmol/30min)を、横軸は投与薬物および投与量(Vは、ビヒクルの投与)を示す。図1に示すごとく、PAR−2アゴニストペプチドであるSLp-NH2は1.25から5μmol/kgの用量においてカルバコールの投与によって亢進した胃酸分泌を用量依存的に抑制した。これに対して、SLp-NH2のコントロールペプチドであるLSp-NH2は5μmol/kgの用量においてもカルバコールによって亢進した胃酸分泌に対して何ら影響を与えなかった。
使用動物
実験には5週齢のWistar系雄性ラットを使用した。各動物は室温23±2℃、湿度50±5%および12時間の明暗サイクル(明期:07:00から19:00)の環境下で1週間の予備飼育の後、実験に供した。予備飼育期間および実験期間中は水および固型飼料を自由に摂取させた。
また、実験に用いた例数は全て4〜14匹であり、結果を平均値±標準誤差で示した。有意差検定はTukeyの多重比較検定で行った。
方法
18〜24時間の絶食後、ラットをエーテルで麻酔し、胸部剣状骨下端下方を、約1 cm開腹した。開腹孔より十二指腸をはさみだし、幽門と十二指腸の接合部を結紮し、開腹部を縫合した。その30分後にラットを放血致死させ、胃を取り出し、胃液を採取した。採取した胃液を濾過した後、胃液中の酸度を滴定法により測定した。カルバコール (60μg/kg) は幽門結紮直後に皮下投与し、その1分後にアマスタチン (2.5μmol/kg) を、また、その1分後にSLp-NH2およびLSp-NH2を静脈内投与し、カルバコールの投与によって亢進した胃酸分泌に対する作用を調べた。
結果
結果を図1に示す。
図1において、縦軸は胃酸分泌量(μmol/30min)を、横軸は投与薬物および投与量(Vは、ビヒクルの投与)を示す。図1に示すごとく、PAR−2アゴニストペプチドであるSLp-NH2は1.25から5μmol/kgの用量においてカルバコールの投与によって亢進した胃酸分泌を用量依存的に抑制した。これに対して、SLp-NH2のコントロールペプチドであるLSp-NH2は5μmol/kgの用量においてもカルバコールによって亢進した胃酸分泌に対して何ら影響を与えなかった。
ラット胃粘膜細胞からのムチン分泌に及ぼす影響
方法
上記と同様の方法で胃幽門を結紮した。結紮直後にアマスタチン (2.5μmol/kg)を、また、アマスタチン投与1分後にSLp-NH2、LSp-NH2およびtcLp-NH2を静脈内投与した。結紮30分後にラットを放血致死させ、胃を取り出し、胃液を採取した。得られた胃液サンプルを10000gで30分間遠心分離し、上清をMillipore MC FREE (MW10000)で限外濾過した後凍結乾燥した。この凍結乾燥サンプルに2MのTFAを加え100℃の条件下で4時間加水分解を行った。その後遠心分離を行い、上清を蒸発乾固した。この蒸発乾固したサンプルに0.1 M Tris-HCl 200μLを加え溶解した。このサンプル50μLにガラクトースオキシダーゼ (1 U)、パーオキシダーゼ(0.5 mU)およびHPPA (0.25 μmol)を含む反応溶液を150μL加え37℃で30分間インキュベートした後、励起波長320nmおよび蛍光波長405nmでガラクトース量を測定した。
結果
結果を図2に示す。
図2において、縦軸はムチン分泌量(ng ガラクトース)を、横軸は投与薬物および投与量(Vは、ビヒクルの投与)を示す。図2に示すごとく、SLp-NH2は0.02から5μmol/kgの用量においてラット胃粘膜細胞からのムチン分泌を用量依存的に亢進させた。また、SLp-NH2よりもPAR−2特異的であるアゴニストペプチドのtcLp-NH2もSLp-NH2と同様にムチン分泌を亢進させた。これに対して、SLp-NH2のコントロールペプチドであるLSp-NH2はムチン分泌に影響を与えなかった。
方法
上記と同様の方法で胃幽門を結紮した。結紮直後にアマスタチン (2.5μmol/kg)を、また、アマスタチン投与1分後にSLp-NH2、LSp-NH2およびtcLp-NH2を静脈内投与した。結紮30分後にラットを放血致死させ、胃を取り出し、胃液を採取した。得られた胃液サンプルを10000gで30分間遠心分離し、上清をMillipore MC FREE (MW10000)で限外濾過した後凍結乾燥した。この凍結乾燥サンプルに2MのTFAを加え100℃の条件下で4時間加水分解を行った。その後遠心分離を行い、上清を蒸発乾固した。この蒸発乾固したサンプルに0.1 M Tris-HCl 200μLを加え溶解した。このサンプル50μLにガラクトースオキシダーゼ (1 U)、パーオキシダーゼ(0.5 mU)およびHPPA (0.25 μmol)を含む反応溶液を150μL加え37℃で30分間インキュベートした後、励起波長320nmおよび蛍光波長405nmでガラクトース量を測定した。
結果
結果を図2に示す。
図2において、縦軸はムチン分泌量(ng ガラクトース)を、横軸は投与薬物および投与量(Vは、ビヒクルの投与)を示す。図2に示すごとく、SLp-NH2は0.02から5μmol/kgの用量においてラット胃粘膜細胞からのムチン分泌を用量依存的に亢進させた。また、SLp-NH2よりもPAR−2特異的であるアゴニストペプチドのtcLp-NH2もSLp-NH2と同様にムチン分泌を亢進させた。これに対して、SLp-NH2のコントロールペプチドであるLSp-NH2はムチン分泌に影響を与えなかった。
エタノールおよび塩酸−エタノール誘発胃粘膜傷害に及ぼす影響
方法
エタノールおよび塩酸−エタノール誘発胃粘膜傷害の作製は、Robert (Robert, A. et al., Gastroenteral, 77, 433-443, 1979)らの方法に準じて行った。すなわち、ラットを18-24時間絶食した後、75%エタノールまたは150 mM塩酸を含む60%エタノール1mLを経口投与し、60分後に放血致死させ胃を摘出した。摘出した胃を大彎に沿って切開し、洗浄したのち10%ホルムアルデヒドにて固定し、胃粘膜傷害部位の面積を画像解析ソフト Mac acpect(三谷商事株式会社、千葉県)を用いて測定した。SLp-NH2は75%エタノールあるいは150mM塩酸含有60%エタノール投与の5分前に静脈内投与した。また、アマスタチン (2.5μmol/kg) はSLp-NH2投与1分前に投与した。
結果
75%エタノール投与の結果を図3に、また、150mM塩酸含有60%エタノール投与の結果を図4に示す。
図3および図4において、縦軸は胃粘膜障害部位の面積(cm2)を、横軸は投与薬物および投与量(Vは、ビヒクルの投与)を示す。
図3に示すごとく、エタノールによる胃粘膜傷害に対してSLp-NH2は0.25および0.5μmol/kgの用量において保護作用を示した。また、図4に示すごとく、塩酸−エタノールによる胃粘膜傷害に対してもエタノールによる胃粘膜傷害と同様に0.25および0.5μmol/kgの用量において保護作用を示した。
方法
エタノールおよび塩酸−エタノール誘発胃粘膜傷害の作製は、Robert (Robert, A. et al., Gastroenteral, 77, 433-443, 1979)らの方法に準じて行った。すなわち、ラットを18-24時間絶食した後、75%エタノールまたは150 mM塩酸を含む60%エタノール1mLを経口投与し、60分後に放血致死させ胃を摘出した。摘出した胃を大彎に沿って切開し、洗浄したのち10%ホルムアルデヒドにて固定し、胃粘膜傷害部位の面積を画像解析ソフト Mac acpect(三谷商事株式会社、千葉県)を用いて測定した。SLp-NH2は75%エタノールあるいは150mM塩酸含有60%エタノール投与の5分前に静脈内投与した。また、アマスタチン (2.5μmol/kg) はSLp-NH2投与1分前に投与した。
結果
75%エタノール投与の結果を図3に、また、150mM塩酸含有60%エタノール投与の結果を図4に示す。
図3および図4において、縦軸は胃粘膜障害部位の面積(cm2)を、横軸は投与薬物および投与量(Vは、ビヒクルの投与)を示す。
図3に示すごとく、エタノールによる胃粘膜傷害に対してSLp-NH2は0.25および0.5μmol/kgの用量において保護作用を示した。また、図4に示すごとく、塩酸−エタノールによる胃粘膜傷害に対してもエタノールによる胃粘膜傷害と同様に0.25および0.5μmol/kgの用量において保護作用を示した。
錠剤
以下の処方に従い、常法により錠剤を調製した。
結晶セルロース 18mg
SLp-NH2 15mg
低置換度ヒドロキシプロピルセルロース 12mg
ヒドロキシプロピルメチルセルロース 10mg
ステアリン酸マグネシウム 1mg
乳糖 適量
合計 100mg
以下の処方に従い、常法により錠剤を調製した。
結晶セルロース 18mg
SLp-NH2 15mg
低置換度ヒドロキシプロピルセルロース 12mg
ヒドロキシプロピルメチルセルロース 10mg
ステアリン酸マグネシウム 1mg
乳糖 適量
合計 100mg
錠剤
以下の処方に従い、常法により錠剤を調製した。
アマスタチン 20mg
結晶セルロース 18mg
SLp-NH2 15mg
低置換度ヒドロキシプロピルセルロース 12mg
ヒドロキシプロピルメチルセルロース 10mg
ステアリン酸マグネシウム 1mg
乳糖 適量
合計 100mg
以下の処方に従い、常法により錠剤を調製した。
アマスタチン 20mg
結晶セルロース 18mg
SLp-NH2 15mg
低置換度ヒドロキシプロピルセルロース 12mg
ヒドロキシプロピルメチルセルロース 10mg
ステアリン酸マグネシウム 1mg
乳糖 適量
合計 100mg
カプセル剤
以下の処方に従い、常法によりカプセル剤を調製した。
SLp-NH2 15mg
低置換度ヒドロキシプロピルセルロース 15mg
架橋型カルボキシメチルセルロースナトリウム 5mg
ステアリン酸マグネシウム 2mg
乳糖 63mg
合計 100mg
以下の処方に従い、常法によりカプセル剤を調製した。
SLp-NH2 15mg
低置換度ヒドロキシプロピルセルロース 15mg
架橋型カルボキシメチルセルロースナトリウム 5mg
ステアリン酸マグネシウム 2mg
乳糖 63mg
合計 100mg
カプセル剤
以下の処方に従い、常法によりカプセル剤を調製した。
SLp-NH2 15mg
低置換度ヒドロキシプロピルセルロース 15mg
アマスタチン 5mg
架橋型カルボキシメチルセルロースナトリウム 5mg
ステアリン酸マグネシウム 2mg
乳糖 63mg
合計 100mg
以下の処方に従い、常法によりカプセル剤を調製した。
SLp-NH2 15mg
低置換度ヒドロキシプロピルセルロース 15mg
アマスタチン 5mg
架橋型カルボキシメチルセルロースナトリウム 5mg
ステアリン酸マグネシウム 2mg
乳糖 63mg
合計 100mg
注射剤
以下の処方に従い、常法により注射剤を調製した。
ブドウ糖 10mg
SLp-NH2 1mg
アマスタチン 1mg
注射用精製水 適量
合計 200mL
これらの実施例5〜9で得られた製剤は、いずれも本発明の胃酸分泌抑制用組成物、消化管粘液分泌促進用組成物、消化管粘膜保護用組成物、消化器系疾患の予防、治療用組成物として使用できる。
以下の処方に従い、常法により注射剤を調製した。
ブドウ糖 10mg
SLp-NH2 1mg
アマスタチン 1mg
注射用精製水 適量
合計 200mL
これらの実施例5〜9で得られた製剤は、いずれも本発明の胃酸分泌抑制用組成物、消化管粘液分泌促進用組成物、消化管粘膜保護用組成物、消化器系疾患の予防、治療用組成物として使用できる。
SEQ ID NO: 1
Designed peptide having PAR-2 agonist activity. The C-terminal amino acid residue is amidated.
SEQ ID NO: 2
Designed peptide having PAR-2 agonist activity. Xaa at 1 is trans-cynnamoyl-Leu. Xaa at 6 is Orn. The C-terminal amino acid residue is amidated.
SEQ ID NO: 3
Designed peptide having PAR-1 and PAR-2 agonist activity. The C-terminal amino acid residue is amidated.
SEQ ID NO: 4
Designed peptide having PAR-2 agonist activity. The C-terminal amino acid residue is hydroxylated.
SEQ ID NO: 5
Designed control peptide. The C-terminal amino acid residue is amidated.
Designed peptide having PAR-2 agonist activity. The C-terminal amino acid residue is amidated.
SEQ ID NO: 2
Designed peptide having PAR-2 agonist activity. Xaa at 1 is trans-cynnamoyl-Leu. Xaa at 6 is Orn. The C-terminal amino acid residue is amidated.
SEQ ID NO: 3
Designed peptide having PAR-1 and PAR-2 agonist activity. The C-terminal amino acid residue is amidated.
SEQ ID NO: 4
Designed peptide having PAR-2 agonist activity. The C-terminal amino acid residue is hydroxylated.
SEQ ID NO: 5
Designed control peptide. The C-terminal amino acid residue is amidated.
Claims (12)
- PAR−2を活性化させる成分を含むことを特徴とする胃酸分泌抑制用組成物。
- PAR−2を活性化させる成分を含むことを特徴とする消化管粘液分泌促進用組成物。
- PAR−2を活性化させる成分を含むことを特徴とする消化管粘膜保護用組成物。
- PAR−2を活性化させる成分を含むことを特徴とする、消化器系疾患の予防、治療用組成物。
- 消化器系疾患が、胃潰瘍、十二指腸潰瘍、胃炎、下痢および腸炎から選択される疾患である請求項4記載の組成物。
- 成分がペプチドである請求項1〜5いずれか1項記載の組成物。
- 成分がタンパク質である請求項1〜5いずれか1項記載の組成物。
- 成分を失活化または分解する物質を阻害する物質を組み合わせる請求項1〜7いずれか1項記載の組成物。
- 成分を失活化または分解する物質を阻害する物質を併用する請求項8記載の組成物。
- 成分を失活化または分解する物質を阻害する物質を配合する請求項8記載の組成物。
- 阻害する物質がペプチダーゼインヒビターである請求項8〜10いずれか1項記載の組成物。
- 徐放化製剤、局所適用製剤、薬物放出制御製剤、腸溶性製剤および胃溶性製剤よりなる群から選択されるDDS製剤とされる請求項1〜11いずれか1項記載の組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005188527A JP2005298522A (ja) | 2005-06-28 | 2005-06-28 | 消化器系疾患の予防、治療用組成物 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005188527A JP2005298522A (ja) | 2005-06-28 | 2005-06-28 | 消化器系疾患の予防、治療用組成物 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2000047515A Division JP4065642B2 (ja) | 2000-02-24 | 2000-02-24 | 消化器系疾患の予防、治療用組成物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2005298522A true JP2005298522A (ja) | 2005-10-27 |
| JP2005298522A5 JP2005298522A5 (ja) | 2007-03-01 |
Family
ID=35330480
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2005188527A Pending JP2005298522A (ja) | 2005-06-28 | 2005-06-28 | 消化器系疾患の予防、治療用組成物 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2005298522A (ja) |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10503522A (ja) * | 1994-08-04 | 1998-03-31 | ロヨラ ユニバーシティ オブ シカゴ | 化学療法剤とともに使用するための防御性プロスタグランジン |
-
2005
- 2005-06-28 JP JP2005188527A patent/JP2005298522A/ja active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10503522A (ja) * | 1994-08-04 | 1998-03-31 | ロヨラ ユニバーシティ オブ シカゴ | 化学療法剤とともに使用するための防御性プロスタグランジン |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2565536C2 (ru) | Производное аналога glp-1 или его фармацевтически приемлемые соли и их применение | |
| JP4148994B2 (ja) | グルカゴン様ペプチド―2アナログ | |
| KR101200227B1 (ko) | 글루카곤 유사 펩티드-2(glp-2) 유사체 | |
| US10968264B2 (en) | Cyclic peptide tyrosine tyrosine compounds as modulators of neuropeptide Y receptors | |
| KR101794781B1 (ko) | 펩타이드계 glp-2 작용제 | |
| JP3677421B2 (ja) | 涙液分泌促進組成物 | |
| JP5926279B2 (ja) | Dpp−4阻害剤 | |
| EP0692971A1 (en) | Analogs of peptide yy and uses thereof | |
| JP4065642B2 (ja) | 消化器系疾患の予防、治療用組成物 | |
| US20120196798A1 (en) | Glp-1 analogues and their pharmaceutical salts and uses | |
| KR20160016872A (ko) | 마르팡 증후군 및 관련 장애의 치료에서의 안지오텐신 펩티드 | |
| JP4249970B2 (ja) | Par−1を介する消化器系疾患の予防および/または治療用組成物 | |
| JP2005298522A (ja) | 消化器系疾患の予防、治療用組成物 | |
| JP2024509829A (ja) | Glp-1受容体作動薬を経口投与するための医薬組成物 | |
| CN1738606A (zh) | 肽经口输递的改进 | |
| HK1033324B (en) | Glucagon-like peptide-2 analogs |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070112 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070112 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100216 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20100720 |