FR2813018A1 - COSMETIC COMPOSITIONS CONTAINING AT LEAST ONE COMPOUND STIMULATING LAMININ NEOSYNTHESIS, AND/OR INTEGRINE ALPHA-2 BETA-1 AND/OR COLLAGEN IV OF THE DERMO-EPIDERMAL JUNCTION - Google Patents
COSMETIC COMPOSITIONS CONTAINING AT LEAST ONE COMPOUND STIMULATING LAMININ NEOSYNTHESIS, AND/OR INTEGRINE ALPHA-2 BETA-1 AND/OR COLLAGEN IV OF THE DERMO-EPIDERMAL JUNCTION Download PDFInfo
- Publication number
- FR2813018A1 FR2813018A1 FR0010773A FR0010773A FR2813018A1 FR 2813018 A1 FR2813018 A1 FR 2813018A1 FR 0010773 A FR0010773 A FR 0010773A FR 0010773 A FR0010773 A FR 0010773A FR 2813018 A1 FR2813018 A1 FR 2813018A1
- Authority
- FR
- France
- Prior art keywords
- sep
- collagen
- lys
- thr
- cosmetic composition
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/63—Steroids; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/64—Proteins; Peptides; Derivatives or degradation products thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/64—Proteins; Peptides; Derivatives or degradation products thereof
- A61K8/645—Proteins of vegetable origin; Derivatives or degradation products thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/64—Proteins; Peptides; Derivatives or degradation products thereof
- A61K8/65—Collagen; Gelatin; Keratin; Derivatives or degradation products thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
- A61Q19/08—Anti-ageing preparations
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
- A61Q19/007—Preparations for dry skin
Abstract
Description
<Desc/Clms Page number 1> <Desc / Clms Page number 1>
La présente invention concerne de nouvelles compositions cosmétiques renfermant au moins un composé stimulant la néosynthèse des laminines, et/ou de l'intégrine [alpha]2ss1 et/ou du collagène IV de la jonction dermo- épidermique
La peau humaine est constituée de trois tissus superposés : l'hypoderme (le plus profond), le derme et enfin l'épiderme (le plus externe). The present invention relates to new cosmetic compositions containing at least one compound stimulating the neosynthesis of laminins, and / or the integrin [alpha] 2ss1 and / or collagen IV of the dermoepidermal junction.
Human skin consists of three superimposed tissues: the hypodermis (the deepest), the dermis and finally the epidermis (the outermost).
Pour assurer son rôle de première protection contre les agressions (mécaniques, chimiques, microbiologiques), l'épiderme a une structure hautement différenciée : depuis la couche basale, les cellules appelées kératinocytes subissent un processus métabolique de kératinisation qui les fait se transformer au fur et à mesure qu'elles migrent vers les couches supérieures pour finalement devenir des cornéocytes extrêmement résistants et peu perméables, formant avec les lipides épidermiques sécrétés par les kératinocytes de la couche granuleuse, le Stratum Corneum, la couche la plus externe de l'épiderme, en contact avec le milieu extérieur. To ensure its role as a first protection against aggression (mechanical, chemical, microbiological), the epidermis has a highly differentiated structure: from the basal layer, the cells called keratinocytes undergo a metabolic process of keratinization that causes them to transform as they develop. as they migrate to the upper layers to finally become extremely resistant and low permeability corneocytes, forming with the epidermal lipids secreted by the keratinocytes of the granular layer, the Stratum Corneum, the outermost layer of the epidermis, in contact with the external environment.
Par ailleurs l'épiderme contient d'autres types cellulaires ayant des fonctions importantes et à forte capacité de communication : mélanocytes, cellules de Langherans, cellules de Merckel
Ce processus de forte différentiation et ces nombreuses communications intercellulaires nécessitent de nombreux éléments nutritifs. Or l'épiderme n'est pas irrigué par des vaisseaux sanguins ou lymphatiques. Ces éléments nutritifs doivent donc lui parvenir depuis le derme qui, lui, est irrigué. Il faut donc une diffusion correcte de ces éléments à travers la Jonction DermoEpidermique (JDE) qui fait le lien entre ces deux tissus. In addition, the epidermis contains other cell types with important functions and high communication capacity: melanocytes, Langherans cells, Merckel cells
This process of strong differentiation and many intercellular communications require many nutrients. The epidermis is not irrigated by blood or lymphatic vessels. These nutrients must therefore reach him from the dermis which is irrigated. It is therefore necessary a correct diffusion of these elements through the DermoEpidermic Junction (JDE) which is the link between these two tissues.
Cette Jonction Dermo-Epidermique, doit en outre gérer la diffusion de messagers biochimiques entres les deux tissus. Il a été montré que de nombreuses substances émises par chacun de ces tissus interfèrent sur l'activité de l'autre (travaux du Pr R E.Burgeson, Smola H., Exp.Cell.Res. 1998 Mar 15 ;239(2) :399-410)
Enfin la JDE doit assurer le contact entre ces deux tissus qui sont de nature très différente. This Dermo-Epidermal Junction must also manage the diffusion of biochemical messengers between the two tissues. It has been shown that many substances emitted by each of these tissues interfere with the activity of the other (work of Prof. R. E. Burgeson, Smola H., Exp.Cell.Res, 1998 Mar 15, 239 (2) : 399-410)
Finally the JDE must ensure the contact between these two tissues which are very different in nature.
<Desc/Clms Page number 2> <Desc / Clms Page number 2>
Le derme est un tissu constitué d'une substance fondamentale dans laquelle baignent peu de cellules (les fibroblastes) et de très nombreuses fibres (collagènes et élastine), ce qui donne au derme une structure amorphe et compacte, cependant capable de s'étirer sous une contrainte mécanique puis de revenir à sa dimension initiale quand la contrainte est relâchée. The dermis is a tissue consisting of a fundamental substance in which few cells (fibroblasts) and a large number of fibers (collagen and elastin) bathe, which gives the dermis an amorphous and compact structure, yet able to stretch under a mechanical stress and then return to its original dimension when the stress is released.
L'épiderme est de type stratifié à forte densité de cellules jointives et empilées. The epidermis is of stratified type with a high density of contiguous and stacked cells.
La JDE doit donc être capable d'assurer la cohésion entre ces deux tissus aux propriétés mécaniques peu compatibles quand la peau est mécaniquement déformée. Pour assurer cette fonction, la JDE a une forme en vagues fortement marquées. JDE must therefore be able to ensure cohesion between these two tissues with little mechanical properties when the skin is mechanically deformed. To ensure this function, the JDE has a shape in strongly marked waves.
Toutes ces raisons font que la JDE a un rôle très important d'un point de vue métabolique et mécanique pour la bonne santé de la peau. All these reasons make the JDE has a very important role from a metabolic and mechanical point of view for the good health of the skin.
Or il est établi que, au cours du processus du vieillissement, la qualité de la JDE tend à diminuer : elle s'aplatit et assure beaucoup moins bien son rôle de ressort (B. Le Varlet et AI. Journal of Investigative Dermatology Symposium Proceedings 3:172-179,1998). However, it is established that, during the process of aging, the quality of the DED tends to decrease: it flattens and ensures much less well its spring role (Le Varlet and AI Journal of Investigative Dermatology Symposium Proceedings 3 : 172-179.1998).
Le rôle important de la JDE est également attesté par la possibilité de maladies métaboliques quand un des éléments de la JDE est absent ou de mauvaise qualité. On peut citer le cas de la pemphigoïde bulleuse dans laquelle l'absence d'un élément important (laminine-5) entraîne la formation de bulles : l'épiderme se détache du derme et forme des bulles qui évoluent en plaies difficiles à cicatriser. The important role of JDE is also evidenced by the possibility of metabolic diseases when one of the elements of JDE is absent or of poor quality. We can mention the case of bullous pemphigoid in which the absence of an important element (laminin-5) causes the formation of bubbles: the epidermis is detached from the dermis and forms bubbles that evolve into wounds difficult to heal.
La structure de la JDE est de mieux en mieux connue : on distingue quatre couches qui ont chacune des composants spécifiques et un rôle bien précis (Allen J., Br.J.Dermatol. 1997 DEc;137(6) :907-15),(M.Aumailley, Kidney Internat.,Vol 47, Suppl.49(1995),pp S-4-S-7). The structure of the JDE is better and better known: there are four layers that each have specific components and a specific role (Allen J., Br.J.Dermatol 1997 DEc 137 (6): 907-15) , (M.Aumailley, Kidney Internat., Vol 47, Suppl.49 (1995), pp. S-4-S-7).
On peut citer dans ces éléments importants des laminines, des intégrines et surtout des collagènes parmi lesquels principalement le collagène IV. These important elements include laminins, integrins and especially collagens, of which mainly collagen IV.
Pour lutter contre le relâchement, la perte de souplesse et de tonicité, l'aspect terne et/ou flétri de la peau, des produits cosmétiques se sont attachés à revitaliser les éléments du derme et/ou de l'épiderme To fight against slackening, loss of suppleness and tonicity, dullness and / or withering of the skin, cosmetic products have tried to revitalize the elements of the dermis and / or the epidermis
<Desc/Clms Page number 3> <Desc / Clms Page number 3>
Une tendance nouvelle consiste à stimuler la synthèse des éléments importants de la JDE. A new trend is to stimulate the synthesis of important elements of the JDE.
C'est en sélectionnant par deux tests spécifiques (décrits ci-après dans la partie expérimentale), des ingrédients actifs pour cette fonction, que la demanderesse a découvert que l'acide ursolique et l'acide oléanolique, non décrits dans la littérature pour ce type de propriétés, sont en fait capables de stimuler la néosynthèse de collagène IV; et que, de plus, l'association à un palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser spécifique pour cette activité, augmentait leur pouvoir stimulant d'une façon synergique inattendue. It is by selecting by two specific tests (described hereinafter in the experimental part), active ingredients for this function, that the Applicant has discovered that ursolic acid and oleanolic acid, not described in the literature for this purpose. type of properties, are in fact able to stimulate the neosynthesis of collagen IV; and that, additionally, the association with palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser specific for this activity, increased their stimulating potency in an unexpectedly synergistic manner.
Par ailleurs ce palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser est capable de stimuler la synthèse de l'intégrine [alpha]2ss1 et de laminine. Moreover, this palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser is capable of stimulating the synthesis of integrin [alpha] 2ssl and laminin.
Enfin, la demanderesse a découvert qu'un autre principe actif, un extrait peptidique de lupin blanc, connu pour ses propriétés anti-élastases et anti-collagénases (anti-métallo protéinases) est également capable de stimuler significativement la synthèse du collagène IV. Finally, the Applicant has discovered that another active ingredient, a peptide extract of white lupine, known for its anti-elastase and anti-collagenase (anti-metalloproteinase) properties, is also capable of significantly stimulating the synthesis of collagen IV.
Ces principes actifs seuls ou associés sont donc parfaitement aptes à stimuler toute une série de fonctions de la peau, en particulier la néosynthèse d'éléments importants de la JDE, comme les laminines, l'intégrine [alpha]2ss1 et de façon synergique le collagène IV. These active ingredients alone or in combination are therefore perfectly capable of stimulating a whole series of skin functions, in particular the neosynthesis of important elements of JDE, such as laminins, integrin [alpha] 2ss1 and synergistically collagen. IV.
C'est pourquoi la présente demande a pour objet une composition cosmétique renfermant au moins un composé stimulant la néosynthèse d'au moins un et de préférence deux, particulièrement trois éléments importants de la jonction dermo-épidermique et plus particulièrement des laminines, et/ou de l'intégrine [alpha]2ss1 et/ou du collagène IV
Parmi les composés stimulant la néosynthèse d'éléments importants de la jonction dermo-épidermique, on peut citer de préférence l'acide ursolique, l'acide oléanolique, le palmitoyl pentapeptide dans lequel le pentapeptide a la formule : -Lys-Thr-Thr-Lys-Ser et les extraits peptidiques de Lupin blanc. This is why the present application relates to a cosmetic composition containing at least one compound stimulating the neosynthesis of at least one and preferably two, especially three important elements of the dermal-epidermal junction and more particularly of laminins, and / or integrin [alpha] 2ss1 and / or collagen IV
Among the compounds stimulating the neosynthesis of important elements of the dermal-epidermal junction, there may be mentioned preferably ursolic acid, oleanolic acid, palmitoyl pentapeptide in which the pentapeptide has the formula: -Lys-Thr-Thr- Lys-Ser and Peptide Extracts of White Lupine.
L'acide ursolique est un triterpène pentacyclique : l'acide 3sshydroxyurs-12-en-28-oique. On le trouve dans un grand nombre de plantes notamment le romarin Il est généralement associé dans ces plantes, et dans les extraits commercialement disponibles, à son isomère l'acide oléanolique (acide 3-hydoxyoléan-12-en-oique). Ces 2 produits ont beaucoup de propriétés Ursolic acid is a pentacyclic triterpene: 3-hydroxy-12-en-28-oic acid. It is found in a large number of plants including rosemary It is generally associated in these plants, and in commercially available extracts, its isomer is oleanolic acid (3-hydoxyolean-12-en-oic acid). These 2 products have a lot of properties
<Desc/Clms Page number 4><Desc / Clms Page number 4>
biologiques communes comme décrit par Jie Liu dans le Journal of Ethnopharmacology 49 (1995) 57-68) : effets hépatoprotecteurs, antiinflammatoires, anti-tumoral, hypolipémiant, anti-athérosclérosant, antiulcéreux, antimicrobien, hypoglycémiant, protecteur contre la toxicité induite par la cyclophosphamide, anti-cariogène, et anti-fertilité. D'autre publications détaillent certaines propriétés comme l'inhibition de l'élastase leucocytaire humaine (Ying, Biochem. J (1991) 277,521-526), l'effet protecteur contre la lipoperoxydation lipidique (Balanehru, Biochemistry Internat. Vol 24, N 5, July 1991,981-990), l'inhibition de la lipoxygénase et de la prolifération des cellules leucémiques HL60 (Simon, Biochimica et Biophysica Acta, 1125 (1992) 68-72), et enfin l'activité anti-virale (Serra, Pharmacological Reseach, Vol.29, N 4, 1994, 359-366). common biologics as described by Jie Liu in the Journal of Ethnopharmacology 49 (1995) 57-68): hepatoprotective, anti-inflammatory, anti-tumor, lipid-lowering, anti-atherosclerotic, antiulcer, antimicrobial, hypoglycemic, protective effects against cyclophosphamide-induced toxicity , anti-cariogenic, and anti-fertility. Other publications detail certain properties such as the inhibition of human leukocyte elastase (Ying, Biochem J (1991) 277, 521-526), the protective effect against lipid lipoperoxidation (Balanehru, Biochemistry Internat., Vol 24, N 5). , July 1991, 931-990), inhibition of lipoxygenase and proliferation of leukemic HL60 cells (Simon, Biochimica and Biophysica Acta, 1125 (1992) 68-72), and finally anti-viral activity (Serra , Pharmacological Reseach, Vol.29, No. 4, 1994, 359-366).
Les mélanges d'acide ursolique/acide oléanolique se présentent généralement sous la forme de sel de sodium, les proportions respectives des deux variant de 80-20 à 70-30 suivant la plante dont sont extraits les dits mélanges, le pureté du mélange des deux pouvant aller de 60 à 98%. De ce fait les compositions selon l'invention pourront contenir l'un l'autre ou les deux acides. The mixtures of ursolic acid / oleanolic acid are generally in the form of sodium salt, the respective proportions of the two varying from 80-20 to 70-30 depending on the plant from which said mixtures are extracted, the purity of the mixture of the two ranging from 60 to 98%. As a result, the compositions according to the invention may contain one or both of the acids.
L'extrait peptidique de lupin blanc (variété L. albus) contient des peptides purs de faible poids moléculaire, obtenus à partir de graines délipidées selon un procédé biotechnologique éliminant des polysaccharides. Ce procédé, qui comprend les étapes unitaires de solubilisation des protéines végétales, d'hydrolyse enzymatique et d'ultrafiltrations, permet d'obtenir des peptides comprenant 5 à 6 motifs d'acides aminés en moyenne. Ce type de produit est commercialisé notamment par la Société Expanchimie sous le nom commercial de Actimp 1.9.3# et il est connu pour ses propriétés inhibitrices des matrice métallo protéinases (MMP). Le produit est une solution aqueuse qui contient environ 10% de matières sèches , son pH est de 6,5 à 7,5. The peptide extract of white lupine (variety L. albus) contains pure peptides of low molecular weight, obtained from delipidated seeds according to a biotechnological process eliminating polysaccharides. This method, which comprises the unitary steps of solubilization of plant proteins, enzymatic hydrolysis and ultrafiltration, makes it possible to obtain peptides comprising 5 to 6 average amino acid units. This type of product is sold in particular by the company Expanchimie under the trade name Actimp 1.9.3 # and is known for its inhibiting properties of the matrix metallo proteinases (MMP). The product is an aqueous solution that contains about 10% solids, its pH is 6.5 to 7.5.
Le palmitoyl pentapeptide -Lys-Thr-Thr-Lys-Ser est mimétique d'un fragment de procollagène de type # Il est obtenu par synthèse peptidique et ensuite lié à une chaîne palmitique pour lui conférer une meilleure lipophilie et donc une meilleure pénétration cutanée. Le palmitoyl pentapeptide-Lys-ThrThr-Lys-Ser est commercialisé par la Société Sederma sous le nom commercial The palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser is mimetic of a # type procollagen fragment It is obtained by peptide synthesis and then linked to a palmitic chain to confer a better lipophilicity and thus a better skin penetration. Palmitoyl pentapeptide-Lys-ThrThr-Lys-Ser is marketed by Sederma under the trade name
<Desc/Clms Page number 5><Desc / Clms Page number 5>
Matrixyl, inclus dans un gel à la dose de 100 ppm, le gel contenant 25% environ d'eau, 20% environ de butylène glycol, 1% environ de carbomer, et 0,5% environ de polysorbate 20. Le produit commercial se présente sous forme d'un gel opalescent blanchâtre, de pH 4 à 6, de densité à 20 C de 1,140 à 1,160, ayant un indice de réfraction à 25 C compris entre 1,425 et 1,445. Matrixyl, included in a gel at a dose of 100 ppm, the gel containing about 25% of water, about 20% of butylene glycol, about 1% of carbomer, and about 0.5% of polysorbate 20. The commercial product is present in the form of a whitish opalescent gel, pH 4 to 6, with a density at 20 ° C. of 1,140 to 1,160, having a refractive index at 25 ° C. of between 1.425 and 1.445.
Dans des conditions préférentielles de mise en oeuvre de l'invention, une composition ci-dessus renferme de l'acide ursolique et/'Ou de l'acide oléanolique et en outre le palmitoyl pentapeptide dans lequel le pentapeptide a la formule : -Lys-Thr-Thr-Lys-Ser. Under preferred conditions of implementation of the invention, a composition above contains ursolic acid and / or oleanolic acid and in addition the palmitoyl pentapeptide in which the pentapeptide has the formula: -Lys- Thr-Thr-Lys-Ser.
Dans les compositions selon l'invention, l'acide ursolique pourra représenter par exemple de 0,001 % à 10 %, notamment de 0,01 % à 5%, de préférence de 0,05 % à 2 % et tout particulièrement de 0,07 % à 1 % de la composition terminée. In the compositions according to the invention, the ursolic acid may represent, for example, from 0.001% to 10%, especially from 0.01% to 5%, preferably from 0.05% to 2% and most preferably from 0.07% to % to 1% of the finished composition.
L'acide oléanolique pourra représenter par exemple de 0,00025 % à 2,5 %, notamment de 0,0025 % à 1,3 %, de préférence de 0,0125 % à 0,5 % et tout particulièrement de 0,0175 % à 0,25 % de la composition terminée. Oleanolic acid may represent, for example, from 0.00025% to 2.5%, in particular from 0.0025% to 1.3%, preferably from 0.0125% to 0.5% and most particularly from 0.0175%. % to 0.25% of the finished composition.
Le palmitoyl pentapeptide pourra représenter par exemple de 0,1 à 30 ppm, notamment de 0,5 à 20 ppm, de préférence de 1 à 15 ppm, et tout particulièrement de 2 à 10 ppm de la composition terminée. The palmitoyl pentapeptide may for example represent from 0.1 to 30 ppm, especially from 0.5 to 20 ppm, preferably from 1 to 15 ppm, and most preferably from 2 to 10 ppm of the finished composition.
L'extrait peptidique de Lupin blanc pourra représenter par exemple de 0,2 % à 10 %, notamment de 0,5 % à 5%, de préférence de 0,7 % à 4 % et tout particulièrement de 1 % à 3 % de la composition terminée. The peptide extract of white Lupine may represent, for example, from 0.2% to 10%, in particular from 0.5% to 5%, preferably from 0.7% to 4% and most particularly from 1% to 3% of the finished composition.
On peut citer tout particulièrement les compositions contenant de 0,01% à 5% d'acide ursolique/acide oléanolique associé à 0,1 à 30 ppm de palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser et celles contenant de 0,2% à 2% d'acide ursolique/acide oléanolique associé à 1 à 10 ppm de palmitoyl pentapeptide -Lys-Thr-Thr-Lys-Ser
Des associations particulièrement préférées de principes actifs sont des associations dans la même composition - d'acide ursolique et d'acide oléanolique, - d'acide ursolique et/ou d'acide oléanolique et de palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser, Particularly exemplary compositions containing from 0.01% to 5% ursolic acid / oleanolic acid associated with 0.1 to 30 ppm palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser and those containing 0, 2% to 2% ursolic acid / oleanolic acid combined with 1 to 10 ppm palmitoyl pentapeptide -Lys-Thr-Thr-Lys-Ser
Particularly preferred combinations of active ingredients are combinations in the same composition - ursolic acid and oleanolic acid, - ursolic acid and / or oleanolic acid and palmitoyl pentapeptide-Lys-Thr-Thr-Lys- Ser,
<Desc/Clms Page number 6><Desc / Clms Page number 6>
- d'acide ursolique et/ou d'acide oléanolique et d'extrait peptidique de Lupin blanc, - d'acide ursolique et/ou d'acide oléanolique, de palmitoyl pentapeptide -Lys-Thr-Thr-Lys-Ser et d'extrait peptidique de Lupin blanc. ursolic acid and / or oleanolic acid and peptide extract of white Lupine, ursolic acid and / or oleanolic acid, palmitoyl pentapeptide -Lys-Thr-Thr-Lys-Ser and Peptide extract of white Lupine.
Les compositions selon l'invention sont essentiellement destinées à être appliquées sur la peau. Elles prendront avantageusement la forme de gels hydro-alcooliques ou hydro-glycoliques, d'émulsions eau/huile 'ou huile/eau, avec ou sans émulsionnants, avec ou sans phases lamellaires, d'émulsions triples eau/huile/eau ou huile/eau/huile, de micro émulsions, de mini-émulsions. The compositions according to the invention are essentially intended to be applied to the skin. They will advantageously take the form of hydro-alcoholic or hydro-glycolic gels, water / oil or oil / water emulsions, with or without emulsifiers, with or without lamellar phases, triple emulsions water / oil / water or oil / water / oil, micro emulsions, mini-emulsions.
Les compositions objet de la présente invention possèdent de très intéressantes propriétés. Elles sont doués notamment de remarquables propriétés dans la lutte contre les effets du vieillissement cutané. The compositions which are the subject of the present invention possess very interesting properties. They are endowed notably with remarkable properties in the fight against the effects of skin aging.
Ces propriétés sont illustrées ci-après dans la partie expérimentale. These properties are illustrated below in the experimental part.
Elles justifient l'utilisation des compositions ci-dessus décrites à titre de compositions cosmétiques. They justify the use of the compositions described above as cosmetic compositions.
Les compositions selon la présente invention trouvent leur emploi par exemple dans la lutte tant curative que préventive contre les effets du vieillissement cutané. The compositions according to the present invention find their use for example in the fight both curative and preventive against the effects of skin aging.
Elles trouvent aussi leur emploi dans les soins du visage et du corps pour lutter contre le relâchement cutané, dans les soins d'amincissement, tant pour les peaux sensibles que matures que grasses
Les compositions selon la présente invention sont préparées selon les méthodes usuelles. Le ou les composés actifs peuvent y être incorporés à des excipients habituellement employés dans les compositions cosmétiques destinées à la voie topique, tels que la glycérine, le sorbitol, les stéarates, les PEG, les silicones, le beurre de cacao, les véhicules aqueux ou non, les corps gras d'origine animale ou végétale, les dérivés paraffiniques, les glycols, les alcools ou acides gras, divers agents mouillants, dispersants ou émulsifiants, les conservateurs, les parfums. They also find their use in face and body care to fight against sagging skin, in slimming care, both for sensitive skin that mature and fat
The compositions according to the present invention are prepared according to the usual methods. The active compound (s) may be incorporated therein in excipients usually employed in cosmetic compositions intended for the topical route, such as glycerin, sorbitol, stearates, PEGs, silicones, cocoa butter, aqueous vehicles or no, fatty substances of animal or vegetable origin, paraffinic derivatives, glycols, alcohols or fatty acids, various wetting agents, dispersants or emulsifiers, preservatives, perfumes.
La présente invention a encore pour objet un procédé de préparation d'une composition ci-dessus décrite, caractérisé en ce que l'on mélange, selon des méthodes connues en elles mêmes, le ou les principes actifs avec des excipients acceptables, notamment cosmétiquement acceptables. En général, on The subject of the present invention is also a process for the preparation of a composition described above, characterized in that, by methods known per se, the active ingredient (s) are mixed with acceptable excipients, in particular cosmetically acceptable excipients. . In general, we
<Desc/Clms Page number 7><Desc / Clms Page number 7>
préparera séparément une phase aqueuse et une phase grasse, puis on les mélangera à chaud sous agitation
La présente demande a encore pour objet l'utilisation d'un composé stimulant la néosynthèse d'au moins un et de préférence deux, particulièrement trois éléments importants de la jonction dermo-épidermique et plus particulièrement des laminines, et/ou de l'intégrine [alpha]2ss1 et/ou du collagène IV pour le traitement de la peau et notamment dans la lutte tarit curative que préventive contre les effets du vieillissement cutané, ainsi qu'un procédé de lutte tant curative que préventive contre les effets du vieillissement cutané dans lequel on applique par voie topique une quantité efficace d'une composition telle que décrite ci-dessus. will separately prepare an aqueous phase and a fatty phase, then they will be stirred while stirring
The present application also relates to the use of a compound stimulating the neosynthesis of at least one and preferably two, particularly three important elements of the dermal-epidermal junction and more particularly of laminins, and / or integrin. [alpha] 2ss1 and / or collagen IV for the treatment of the skin and in particular in the fight against healing curative than the effects of skin aging, and a method of both curative and preventive control against the effects of skin aging in which is applied topically an effective amount of a composition as described above.
Les conditions préférentielles de mise en oeuvre des compositions cidessus décrites s'appliquent également aux autres objets de l'invention visés cidessus. The preferred conditions of implementation of the compositions described above also apply to the other objects of the invention referred to above.
Les exemples qui suivent illustrent la présente invention. The following examples illustrate the present invention.
Exemple 1. :Crème anti-rides
On a préparé une crème anti-rides pour les peaux normales et les peaux mixtes comme suit :
On prépare la phase grasse suivante : Alcool cétylique et stéarate de glycéryle et stéarate de PEG-7S et ceteth-20 et stéareth-20 4g Huile de jojoba 3g Triglycérides capryliques/capriques 3g Esters de jojoba 1g Polyisobutène hydrogéné 2g Cyclométhicone 5g
Ce mélange est porté à 70 C et bien homogénéisé. Example 1: Anti-wrinkle cream
An anti-wrinkle cream has been prepared for normal and combination skin as follows:
The following fatty phase is prepared: cetyl alcohol and glyceryl stearate and stearate of PEG-7S and ceteth-20 and steareth-20 4g jojoba oil 3g caprylic / capric triglycerides 3g Jojoba esters 1g Hydrogenated polyisobutene 2g Cyclomethicone 5g
This mixture is brought to 70 C and well homogenized.
Par ailleurs, on prépare la phase aqueuse suivante : Eau purifiée quantité suffisante pour (QSP) 100g EDTA tétrasodique 0,05g Sorbitol 2g Moreover, the following aqueous phase is prepared: Purified water quantity sufficient for (QSP) 100g tetrasodium EDTA 0.05g Sorbitol 2g
<Desc/Clms Page number 8><Desc / Clms Page number 8>
Cellulose 1g Billes de silice enrobées d'oxyde de titane et d'oxyde de fer 1 g Copolymère sodium acryloydiméthyltaurate et isohexadecane et Polysorbate 80 2g
Tous les ingrédients de la phase aqueuse sont dissous dans l'eau et l'ensemble est porté à 70 C
La phase grasse, homogène et chauffée à 70 C, est versée lentement sur la phase aqueuse portée à la même température, sous agitation assez vive. L'agitation est maintenue pendant 10 minutes après la fin de l'introduction de la phase grasse. L'émulsion huile dans eau se forme. Cellulose 1g Silica beads coated with titanium oxide and iron oxide 1 g Copolymer sodium acryloydimethyltaurate and isohexadecane and Polysorbate 80 2g
All the ingredients of the aqueous phase are dissolved in water and the whole is brought to 70 C
The fatty phase, homogeneous and heated to 70 C, is poured slowly on the aqueous phase brought to the same temperature, with vigorous stirring. Stirring is maintained for 10 minutes after the end of the introduction of the fat phase. The oil-in-water emulsion is formed.
Ensuite, l'émulsion est refroidie sous agitation modérée. Then, the emulsion is cooled with moderate stirring.
Quand la température atteint 40 C, on ajoute successivement sous agitation modérée: Gel de palmitoyl pentapeptide -Lys-Thr-Thr-Lys-Ser 3g Extrait de Lupin blanc 1g Acide ursolique/acide oléanolique, sel de sodium Polyéthylène glycol 400 (PEG400) (10/90) 2g Hyaluronate de sodium 0,5g Conservateurs 0,15g Parfum 0,35g
Après homogénéisation, l'émulsion est refroidie jusqu'à 30 C sous agitation lente. When the temperature reaches 40 ° C., the following are added successively with moderate agitation: Palmitoyl pentapeptide gel -Lys-Thr-Thr-Lys-Ser 3g White Lupine extract 1g Ursolic acid / oleanolic acid, sodium salt Polyethylene glycol 400 (PEG400) ( 10/90) 2g Sodium Hyaluronate 0.5g Preservatives 0.15g Perfume 0.35g
After homogenization, the emulsion is cooled to 30 ° C. with slow stirring.
On obtient ainsi une émulsion de couleur rosée, de consistance agréable, adaptée pour les peaux normales et mixtes. This gives a pinkish emulsion, pleasant consistency, suitable for normal and mixed skin.
Exemple 2. ' Emulsion cosmétique
On prépare la phase grasse suivante Alcool cétylique et stéarate de glycéryle et stéarate de PEG-7S et ceteth-20 et stéareth-20 4g Huile de jojoba 4g Triglycérides capryliques/capriques 4g Esters de Jojoba 1 g Polyisobutène hydrogéné 4g Example 2 Cosmetic Emulsion
The following fat phase is prepared Cetyl alcohol and glyceryl stearate and PEG-7S stearate and ceteth-20 and steareth-20 4g Jojoba oil 4g Caprylic / capric triglycerides 4g Jojoba esters 1g Hydrogenated polyisobutene 4g
<Desc/Clms Page number 9><Desc / Clms Page number 9>
Stéarate d'isocétyle 4g Ricinoléate de cétyle 4g Beurre de karité 1g Huile de silicone (phényl triméthicone) 5g Huile de silicone (diméthicone) 2g Dipentaérythrityl hexacaprylate/hexacaprate 3g
Ce mélange est porté à 70 C et bien homogénéisé. Isocetyl stearate 4g Cetyl cetinolate 4g Shea butter 1g Silicone oil (phenyl trimethicone) 5g Silicone oil (dimethicone) 2g Dipentaerythrityl hexacaprylate / hexacaprate 3g
This mixture is brought to 70 C and well homogenized.
Par ailleurs, on prépare la phase aqueuse suivante : Eau purifiée quantité suffisante pour (QSP) 100g EDTA tétrasodique 0,05g Sorbitol 3g Glycérine 4g Polyméthacrylate de glycéryle /propylène glycol 5g Cellulose 2g Billes de silice enrobées d'oxyde de titane et d'oxyde de fer 1g Copolymère acryloyldiméthyltaurate de sodium et isohexadécane et polysorbate 80 1,25g
Tous les ingrédients de la phase aqueuse sont dissous dans l'eau et l'ensemble est porté à 70 C. In addition, the following aqueous phase is prepared: Purified water quantity sufficient for (QSP) 100g tetrasodium EDTA 0.05g Sorbitol 3g Glycerin 4g Polymethacrylate glyceryl / propylene glycol 5g Cellulose 2g Silica beads coated with titanium oxide and oxide 1g Copolymer acryloyldimethyltaurate sodium and isohexadecane and polysorbate 80 1.25g
All the ingredients of the aqueous phase are dissolved in water and the whole is heated to 70 C.
La phase grasse, homogène et chauffée à 70 C, est versée lentement sur la phase aqueuse portée à la même température, sous agitation assez vive. L'agitation est maintenue pendant 10 minutes après la fin de l'introduction de la phase grasse. L'émulsion huile dans eau se forme. The fatty phase, homogeneous and heated to 70 C, is poured slowly on the aqueous phase brought to the same temperature, with vigorous stirring. Stirring is maintained for 10 minutes after the end of the introduction of the fat phase. The oil-in-water emulsion is formed.
Ensuite, l'émulsion est refroidie sous agitation modérée. Then, the emulsion is cooled with moderate stirring.
Quand la température atteint 40 C, on ajoute successivement sous agitation modérée: Gel de palmitoyl pentapeptide - Lys-Thr-Thr-Lys-Ser 3g Extrait de lupin blanc 1g Acide ursolique/acide oléanolique, sel de sodium Polyéthylène glycol 400 (10/90) 2g Hyaluronate de sodium 0,1g Conservateurs 0,15g When the temperature reaches 40 ° C., it is added successively with moderate agitation: Palmitoyl pentapeptide gel - Lys-Thr-Thr-Lys-Ser 3g White lupine extract 1g Ursolic acid / oleanolic acid, sodium salt Polyethylene glycol 400 (10/90 ) 2g Sodium Hyaluronate 0.1g Preservatives 0.15g
<Desc/Clms Page number 10><Desc / Clms Page number 10>
Parfum 0,45g
Après homogénéisation, l'émulsion est refroidie jusqu'à 30 C sous agitation lente. Perfume 0.45g
After homogenization, the emulsion is cooled to 30 ° C. with slow stirring.
On obtient ainsi une émulsion de couleur rosée, de consistance agréable, adaptée pour les peaux sèches et très sèches. This gives an emulsion of pink color, pleasant consistency, suitable for dry and very dry skin.
Exemple 3. : Crème de type huile/eau
On prépare la crème de type huile/eau suivante :
La phase grasse est constituée de :
Example 3. Cream of oil / water type
The following oil / water type cream is prepared:
The fatty phase consists of:
<tb>
<tb> Diméthicone <SEP> copolyol <SEP> et <SEP> triglycérides <SEP> capryliques/capriques <SEP> 3g
<tb> Néopentanoate <SEP> d'isodécyle <SEP> 5g
<tb> Polyisobutène <SEP> hydrogéné <SEP> 5g
<tb> triglycérides <SEP> capryliques/capriques <SEP> 5g
<tb> Huile <SEP> de <SEP> jojoba <SEP> 5g
<tb> Alcool <SEP> cétylique <SEP> 1g
<tb> Acide <SEP> stéarique <SEP> 1 <SEP> g
<tb> Cire <SEP> d'abeilles <SEP> 1g
<tb> Stéarate <SEP> de <SEP> glycérol <SEP> 0,5g
<tb> Huile <SEP> de <SEP> silicone <SEP> (Diméthicone) <SEP> 2g
<tb>
Cette phase grasse est chauffée à 70 C et bien homogénéisée. Par ailleurs on prépare la phase aqueuse suivante
<Tb>
<tb> Dimethicone <SEP> copolyol <SEP> and <SEP> triglycerides <SEP> caprylic / capric <SEP> 3g
<tb> Neopentanoate <SEP> Isodecyl <SEP> 5g
<tb> Polyisobutene <SEP> hydrogenated <SEP> 5g
<tb> triglycerides <SEP> caprylic / capric <SEP> 5g
<tb> Oil <SEP> of <SEP> jojoba <SEP> 5g
<tb> Alcohol <SEP> cetyl <SEP> 1g
<tb> Stearic acid <SEP><SEP> 1 <SEP> g
<tb> Wax <SEP> of bees <SEP> 1g
<tb> Stearate <SEP> of <SEP> glycerol <SEP> 0.5g
<tb> Oil <SEP> of <SEP> silicone <SEP> (Dimethicone) <SEP> 2g
<Tb>
This fatty phase is heated to 70 ° C. and well homogenized. In addition, the following aqueous phase is prepared
<tb>
<tb> Eau <SEP> purifiée <SEP> quantité <SEP> suffisante <SEP> pour <SEP> (QSP) <SEP> 100g
<tb> EDTA <SEP> tétrasodique <SEP> 0,05g
<tb> Glycérine <SEP> 3g
<tb> Sorbitol <SEP> 2g
<tb> Carbomer <SEP> 0,25g
<tb> Gomme <SEP> xanthane <SEP> 0,2g
<tb> Biosaccharide <SEP> Gum-1 <SEP> 5g
<tb> Polyéthylène <SEP> glycol <SEP> 400 <SEP> 2g
<tb> Méthyle <SEP> paraben <SEP> 0,25g
<tb> Propyle <SEP> paraben <SEP> 0,15g
<tb> Soude <SEP> à <SEP> 10% <SEP> 0,5g
<tb> <Tb>
<tb> Water <SEP> purified <SEP> quantity <SEP> sufficient <SEP> for <SEP> (QSP) <SEP> 100g
<tb> EDTA <SEP> tetrasodium <SEP> 0.05g
<tb> Glycerine <SEP> 3g
<tb> Sorbitol <SEP> 2g
<tb> Carbomer <SEP> 0.25g
<tb> Gum <SEP> xanthan <SEP> 0.2g
<tb> Biosaccharide <SEP> Gum-1 <SEP> 5g
<tb> Polyethylene <SEP> Glycol <SEP> 400 <SEP> 2g
<tb> Methyl <SEP> Paraben <SEP> 0.25g
<tb> Propyl <SEP> paraben <SEP> 0.15g
<tb> Soda <SEP> to <SEP> 10% <SEP> 0.5g
<Tb>
<Desc/Clms Page number 11> <Desc / Clms Page number 11>
Tous les ingrédients de la phase aqueuse sont dissous dans l'eau et l'ensemble est porté à 70 C
La phase grasse, homogène et chauffée à 70 C, est versée lentement sur la phase aqueuse portée à la même température, sous agitation assez vive. L'agitation est maintenue pendant 10 minutes après la fin de l'introduction de la phase grasse. L'émulsion huile dans eau se forme. All the ingredients of the aqueous phase are dissolved in water and the whole is brought to 70 C
The fatty phase, homogeneous and heated to 70 C, is poured slowly on the aqueous phase brought to the same temperature, with vigorous stirring. Stirring is maintained for 10 minutes after the end of the introduction of the fat phase. The oil-in-water emulsion is formed.
Ensuite, l'émulsion est refroidie sous agitation modérée. Then, the emulsion is cooled with moderate stirring.
Quand la température atteint 40 C, on ajoute successivement sous agitation modérée: Gel de palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser 10g Extrait de lupin blanc 0,5g Acide ursolique/acide oléanolique, éthoxydiglycol (10/90) 0,2g Parfum 0,35g
Après homogénéisation, l'émulsion est refroidie jusqu'à 30 C sous agitation lente
On obtient une crème blanche onctueuse, au toucher très frais. When the temperature reaches 40 ° C., the following are added successively with moderate stirring: Palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser gel 10g White lupine extract 0.5g Ursolic acid / oleanolic acid, ethoxydiglycol (10/90) 0, 2g Perfume 0.35g
After homogenization, the emulsion is cooled to 30 ° C. with slow stirring
We obtain a creamy white cream with a very fresh touch.
Exemple 4. : Composition cosmétique
On a préparé la crème eau/huile suivante :
La phase grasse est constituée de : Copolyol cétyl diméthicone 3g Néopentanoate d'isodécyle 5g Polyisobutène hydrogéné 1,5g Triglycérides capryliques/capriques 1,5g Huile de jojoba 1,5g Béhénate de diméthiconol 1,5g Copolymère de cyclométhicone et diméthicone 10g
Cette phase grasse est chauffée à 60 C et bien homogénéisée. Example 4: Cosmetic composition
The following water / oil cream was prepared:
The fatty phase consists of: Copolyol cetyl dimethicone 3g Isodecyl neopentanoate 5g Hydrogenated polyisobutene 1.5g Caprylic / capric triglycerides 1.5g Jojoba oil 1.5g Dimethiconol behenate 1.5g Copolymer cyclomethicone and dimethicone 10g
This fatty phase is heated to 60 C and well homogenized.
Par ailleurs on prépare la phase aqueuse suivante : Eau purifiée quantité suffisante pour (QSP) 100g Chlorure de sodium 0,5g Glycérine 2g In addition, the following aqueous phase is prepared: Purified water quantity sufficient for (QSP) 100g Sodium chloride 0.5g Glycerin 2g
<Desc/Clms Page number 12><Desc / Clms Page number 12>
Sorbitol 2g Polyéthylène Glycol 400 2g Méthyle paraben 0,25g Propyle paraben 0,15g
Tous les ingrédients de la phase aqueuse sont dissous dans l'eau et l'ensemble est porté à 60 C. Sorbitol 2g Polyethylene Glycol 400 2g Paraben Methyl 0.25g Propyl Paraben 0.15g
All the ingredients of the aqueous phase are dissolved in water and the whole is brought to 60 C.
La phase grasse, homogène et chauffée à 60 C, est versée lentement sur la phase aqueuse portée à la même température, sous agitation assez vive. L'agitation est maintenue pendant 10 minutes après la fin de l'introduction de la phase grasse. L'émulsion eau dans huile se forme. The fatty phase, homogeneous and heated to 60 C, is poured slowly on the aqueous phase brought to the same temperature, with vigorous stirring. Stirring is maintained for 10 minutes after the end of the introduction of the fat phase. The water-in-oil emulsion is formed.
Ensuite, l'émulsion est refroidie sous agitation modérée. Then, the emulsion is cooled with moderate stirring.
Quand la température atteint 40 C, on ajoute successivement sous agitation modérée: Gel de palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser 1g Extrait de lupin blanc 2g Acide ursolique/acide oléanolique, éthoxydiglycol (10/90) 10% Parfum : 0,35%
Après homogénéisation, l'émulsion est refroidie jusqu'à 30 C sous agitation lente. When the temperature reaches 40 ° C., it is added successively with moderate agitation: Palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser gel 1g White lupine extract 2g Ursolic acid / oleanolic acid, ethoxydiglycol (10/90) 10% Perfume: 0.35%
After homogenization, the emulsion is cooled to 30 ° C. with slow stirring.
On obtient une crème blanche très onctueuse, pouvant être appliquée la nuit. A very creamy white cream is obtained which can be applied at night.
Exemple 5. : Crème huile/eau à phases lamellaires
On a préparé la crème huile/eau à phases lamellaires suivante :
La phase grasse est constituée de Alcool cétéarylique et Glucoside cétéarylique 6 g Stéarate d'octyle 2g Cire d'abeilles 1,5g Propylène glycol dicaprylate/dicaprate 2,5g Huile de jojoba 4g Beurre de karité 4g Huile de silicone (Diméthicone) 2g Example 5: Oil / water cream with lamellar phases
The following lamellar phase oil / water cream was prepared:
The fatty phase consists of Cetearyl alcohol and cetearyl glucoside 6 g Octyl stearate 2g Beeswax 1.5g Propylene glycol dicaprylate / dicaprate 2.5g Jojoba oil 4g Shea butter 4g Silicone oil (Dimethicone) 2g
<Desc/Clms Page number 13> <Desc / Clms Page number 13>
Cette phase grasse est chauffée à 80 C et bien homogénéisée. This fatty phase is heated to 80 C and well homogenized.
Par ailleurs on prépare la phase aqueuse suivante : Eau purifiée quantité suffisante pour (QSP) 100g EDTA tétrasodique 0,05g Polyméthacrylate de glycéryle et propylène glycol 10g Polyéthylène glycol 400 2g Méthyl paraben 0,25g Propyl paraben 0,15g O-Cymen-5-ol 0,1 g
Tous les ingrédients de la phase aqueuse sont dissous dans l'eau et l'ensemble est porté à 80 C. In addition, the following aqueous phase is prepared: Purified water quantity sufficient for (QSP) 100 g tetrasodium EDTA 0.05 g glyceryl polymethacrylate and propylene glycol 10 g polyethylene glycol 400 2 g methyl paraben 0.25 g propyl paraben 0.15 g O-Cymen-5- ol 0.1 g
All the ingredients of the aqueous phase are dissolved in water and the whole is heated to 80 C.
La phase grasse, homogène et chauffée à 80 C, est versée lentement sur la phase aqueuse portée à la même température, sous agitation assez vive. L'agitation est maintenue pendant 10 minutes après la fin de l'introduction de la phase grasse. L'émulsion huile dans eau se forme. The fatty phase, homogeneous and heated to 80 C, is poured slowly on the aqueous phase brought to the same temperature, with vigorous stirring. Stirring is maintained for 10 minutes after the end of the introduction of the fat phase. The oil-in-water emulsion is formed.
Ensuite, l'émulsion est refroidie sous agitation modérée. Then, the emulsion is cooled with moderate stirring.
Quand la température atteint 40 C, on ajoute successivement sous agitation modérée Gel de palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser 5g Extrait de lupin blanc 5g Acide ursolique/acide oléanolique, sel de sodium/ Polyéthylène glycol 400 (20/80) 10% Parfum 0,35%
Après homogénéisation, l'émulsion est refroidie jusqu'à 30 C sous agitation lente. When the temperature reaches 40 ° C., it is added successively with moderate agitation. Palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser gel 5g White lupine extract 5g Ursolic acid / oleanolic acid, sodium salt / Polyethylene glycol 400 (20/80 ) 10% Perfume 0.35%
After homogenization, the emulsion is cooled to 30 ° C. with slow stirring.
On obtient une crème blanche très onctueuse, à phases lamellaires, qui peuvent faciliter la pénétration des principes actifs et en prolonger l'hydratation
Etude pharmacologique
Cytotoxicité A very creamy white cream with lamellar phases is obtained which can facilitate the penetration of the active ingredients and prolong their hydration.
Pharmacological study
cytotoxicity
<Desc/Clms Page number 14> <Desc / Clms Page number 14>
L'ensemble de ces produits et mélanges ci-après se sont avérés ne pas être cytotoxiques aux concentrations utiles, dans les conditions décrites dans l'expérimentation 1 . All of these products and mixtures below have been found not to be cytotoxic at useful concentrations under the conditions described in Experiment 1.
Expérimentation 1 : des produits testés sur la production de collagène IV, de laminine et d'intégrine a2(31 par des fibroblastes humains (méthode immuno enzymatique de type immunoempreinte)
On a testé les produits et mélanges suivants : - P1 : Gel de palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser à 1 ou 2% - P2 : Extrait de Malt à 1 ou 2% - P3 Extrait de Levure 2 ou 3% - P4 : Acide ursolique/acide oléanolique, sel de sodium à 0,0037 ou 0,0075% - M1 : Mélanges P1 (2%) +P2 (2%) ou P1 (1 %) +P2(1 %) - M2 : Mélanges P1 (2%)+ P3 (3%) ou P1 (1 %)+P3(2%) - M3 : Mélanges P1 (2%)+ P4 (0,0075%) ou P1 (1 %)+ P4 (0,0037%) - M4 : Mélanges P2 (2%)+ P3 (3%) ou P2(1 %)+ P3 (2%) - M5 : Mélanges P2 (2%)+ ou P2(1 %)+ P4 (0,0037%) - M6 : Mélanges P3 (3%)+ ou P3 (2%)+ -TGFss (transforming growth factor ss) humain (TGFp, Sigma T7039) 10 ng/ml (final) - Acide rétinoïque (AR, all-trans retinoic acid , Sigma R2625)10-8 M, connu pour son effet antivieillissement
On procède comme suit :
On ensemence des fibroblastes dermiques humains normaux (NHDF, R8PF2, utilisés au 8e passage) dans un milieux MEM/M199 (Gibco) sans sérum. On les cultive jusqu'à confluence à 37 C et sous 5% de C02. Puis on traite en triplicata respectivement avec les 12 préparations ou mélanges en continu pendant 72H . Experiment 1: Products Tested on the Production of Collagen IV, Laminin and Integrin A2 (31 by Human Fibroblasts (Enzyme Immunoassay Method)
The following products and mixtures were tested: P1: Palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser gel 1% or 2% -P2: Malt extract 1% or 2% -P3 Yeast extract 2 or 3 % - P4: Ursolic acid / oleanolic acid, sodium salt at 0.0037 or 0.0075% - M1: Mixtures P1 (2%) + P2 (2%) or P1 (1%) + P2 (1%) - M2: Blends P1 (2%) + P3 (3%) or P1 (1%) + P3 (2%) - M3: Blends P1 (2%) + P4 (0.0075%) or P1 (1%) + P4 (0.0037%) - M4: Mixtures P2 (2%) + P3 (3%) or P2 (1%) + P3 (2%) - M5: Mixtures P2 (2%) + or P2 (1%) + P4 (0.0037%) - M6: Human P3 (3%) + or P3 (2%) + -TGFss (transforming growth factor ss) mixtures (TGFp, Sigma T7039) 10 ng / ml (final) - Retinoic acid (AR, all-trans retinoic acid, Sigma R2625) 10-8 M, known for its anti-aging effect
We proceed as follows:
Normal human dermal fibroblasts (NHDF, R8PF2, used at the 8th pass) were seeded into serum-free MEM / M199 (Gibco) media. They are cultured to confluence at 37 ° C. and 5% CO 2. Then treated in triplicate with the 12 preparations or mixtures continuously for 72 hours.
Les tapis cellulaires sont observés à la fin des traitements et les échantillons sont congelés à -80 C. A la fin des traitements, les milieux de culture sont complémentés par du dodécyl sulfate de sodium (SDS) (1 % final), The cell mats are observed at the end of the treatments and the samples are frozen at -80 ° C. At the end of the treatments, the culture media are supplemented with sodium dodecyl sulfate (SDS) (1% final),
<Desc/Clms Page number 15><Desc / Clms Page number 15>
les protéines cellulaires et extracellulaires sont extraites pendant 30 min sous agitation, l'extraction est complétée par une sonication douce de tous les échantillons
On procède alors à une Immunoempreinte# Les fractions protéiques sont transférées sur nitrocellulose (Hybond, ECL, Amersham), à l'aide d'un module MilliBlot (Millipore, transfert sous vide). Deux nitrocelluloses sont utilisées pour chaque anticorps utilisé (8 membranes en tout; #45 spots par membrane). Pour chaque série, des puits contrôles (sans cellule) avec du milieu de culture contenant les produits à l'essai à la plus forte concentration sont réalisés (ceci afin de détecter une éventuelle reconnaissance du produit à l'essai par l'un ou l'autre des anticorps). D'autre part, des contrôles sans anticorps primaires ont été réalisés (cellules non traitées). the cellular and extracellular proteins are extracted for 30 min with stirring, the extraction is completed by a gentle sonication of all the samples
The protein fractions are then transferred to nitrocellulose (Hybond, ECL, Amersham), using a MilliBlot module (Millipore, transfer under vacuum). Two nitrocelluloses are used for each antibody used (8 membranes in all, # 45 spots per membrane). For each series, control wells (without cell) with culture medium containing the test products at the highest concentration are performed (this in order to detect possible recognition of the test product by one or the other). other antibodies). On the other hand, controls without primary antibodies were performed (untreated cells).
Les membranes ont été saturées par incubation 16 heures (4 C) dans un tampon phosphate PBS/0,05 % Tween 20/5 % lait écrémé (PBSTL). Les bandes de puits contrôles sans anticorps primaire ont été découpées pour traitement à part (incubation avec le conjugué-peroxydase seulement). Après lavages, les sites antigéniques spécifiques ont été marqués par les anticorps primaires (voir tableau ci-dessous) aux dilutions indiquées (dans du PBSTL, voir tableau ci-dessous), pendant 1 h, à 37 C. Les anticorps primaires fixés ont été révélés par un conjugué anti-immunoglobulines-peroxydase. Après lavages extensifs en PBS/0,05 % Tween 20 (PBST), l'activité peroxydase a été révélée par la méthode ECL (Enhanced ChimiLuminescence, Amersham), sur film Kodak MP. La saisie des images a été réalisée sur GelPrint 2000i (BioPhotonics Corp ), les analyses densitométriques ont été obtenues à l'aide du logiciel One-D-Scan (Scanalytics) Le paramètre d'évaluation est l' hydrolyse MTT
Les différents anticorps utilisés sont les suivants . The membranes were saturated by incubation for 16 hours (4 C) in phosphate buffer PBS / 0.05% Tween 20/5% Skimmed Milk (PBSTL). Control well strips without primary antibodies were cut for separate treatment (incubation with peroxidase conjugate only). After washes, the specific antigenic sites were labeled with the primary antibodies (see table below) at the indicated dilutions (in PBSTL, see table below), for 1 hour, at 37 C. The primary antibodies fixed were revealed by an anti-immunoglobulin-peroxidase conjugate. After extensive washes in PBS / 0.05% Tween 20 (PBST), peroxidase activity was revealed by the ECL method (Enhanced ChimiLuminescence, Amersham), on Kodak MP film. Image capture was performed on GelPrint 2000i (BioPhotonics Corp), densitometric analyzes were obtained using One-D-Scan software (Scanalytics) The evaluation parameter is MTT hydrolysis
The different antibodies used are as follows.
<Desc/Clms Page number 16> <Desc / Clms Page number 16>
<tb>
<tb> marqueur <SEP> anticorps <SEP> primaire <SEP> référence <SEP> dilution
<tb> P-actine <SEP> monoclonal <SEP> Sigma <SEP> A4700 <SEP> 1/500e
<tb> intégrine <SEP> [alpha]2ss1 <SEP> mélange <SEP> polyclonal <SEP> anti-a2 <SEP> Chemicon <SEP> AB1944 <SEP> 1/500e
<tb> + <SEP> polyclonal <SEP> anti-ss1 <SEP> Chemicon <SEP> AB1952 <SEP> 1/500e
<tb> laminine <SEP> polyclonal <SEP> Chemicon <SEP> AB19012 <SEP> 1/500e
<tb> collagène <SEP> IV <SEP> polyclonal <SEP> Rockland <SEP> 600-401-106-0.1 <SEP> 1/1000e
<tb> marqueur <SEP> anticorps <SEP> secondaire <SEP> référence
<tb> P-actine <SEP> RAM-peroxydase <SEP> (Blot) <SEP> Sigma <SEP> A9044
<tb> ou <SEP> GAM-FITC <SEP> (immunofluo.) <SEP> Tebu <SEP> M30801
<tb> intégrine <SEP> [alpha]2ss1 <SEP> GAR-peroxydase <SEP> (Blot) <SEP> Sigma <SEP> A9169
<tb> ou <SEP> GAR <SEP> -FITC <SEP> (immunofluo.) <SEP> Tebu <SEP> L42001
<tb> laminine <SEP> GAR-peroxydase <SEP> (Blot) <SEP> Sigma <SEP> A9169
<tb> ou <SEP> GAR <SEP> -FITC <SEP> (immunofluo <SEP> ) <SEP> Tebu <SEP> L42001
<tb> collagène <SEP> IV <SEP> GAR-peroxydase <SEP> (Blot) <SEP> Sigma <SEP> A9169
<tb> ou <SEP> GAR <SEP> -FITC <SEP> (immunofluo.) <SEP> Tebu <SEP> L42001
<tb> <Tb>
<tb> marker <SEP> antibody <SEP> primary <SEP> reference <SEP> dilution
<tb> P-actin <SEP> monoclonal <SEP> Sigma <SEP> A4700 <SEP> 1 / 500th
<tb> integrin <SEP> [alpha] 2ss1 <SEP> mixture <SEP> polyclonal <SEP> anti-α2 <SEP> Chemicon <SEP> AB1944 <SEP> 1 / 500th
<tb> + <SEP> polyclonal <SEP> anti-ss1 <SEP> Chemicon <SEP> AB1952 <SEP> 1 / 500th
<tb> laminin <SEP> polyclonal <SEP> Chemicon <SEP> AB19012 <SEP> 1 / 500th
<tb> collagen <SEP> IV <SEP> polyclonal <SEP> Rockland <SEP> 600-401-106-0.1 <SEP> 1 / 1000th
<tb> marker <SEP> antibody <SEP> secondary <SEP> reference
<tb> P-actin <SEP> RAM-peroxidase <SEP> (Blot) <SEP> Sigma <SEP> A9044
<tb> or <SEP> GAM-FITC <SEP> (immunofluo.) <SEP> Tebu <SEP> M30801
<tb> integrin <SEP> [alpha] 2ss1 <SEP> GAR-peroxidase <SEP> (Blot) <SEP> Sigma <SEP> A9169
<tb> or <SEP> GAR <SEP> -FITC <SEP> (immunofluo.) <SEP> Tebu <SEP> L42001
<tb> Laminin <SEP> GAR-Peroxidase <SEP> (Blot) <SEP> Sigma <SEP> A9169
<tb> or <SEP> GAR <SEP> -FITC <SEP> (immunofluo <SEP>) <SEP> Tebu <SEP> L42001
<tb> Collagen <SEP> IV <SEP> GAR-Peroxidase <SEP> (Blot) <SEP> Sigma <SEP> A9169
<tb> or <SEP> GAR <SEP> -FITC <SEP> (immunofluo.) <SEP> Tebu <SEP> L42001
<Tb>
Les données brutes sont transférées et traitées sous le logiciel PRISM# (Graph Pad Software) Les comparaisons intergroupes ont été réalisées par analyse de variance (ANOVA), à l'aide du test de comparaison multiple de DUNNETT. The raw data is transferred and processed using the PRISM # software (Graph Pad Software) The intergroup comparisons were performed by analysis of variance (ANOVA), using the DUNNETT multiple comparison test.
Immunofluorescence
Les contrôles en immunofluorescence ont été réalisés sur des tapis cellulaires non traités (témoins), fixés au méthanol à -20 C et séchés. Le principe, les réactifs et les temps ont été les mêmes que pour l'immunoempreinte. Les anticorps secondaires étaient des conjugués - Nisothiocyanate de fluorescéine (FITC) (voir tableau ci-dessus) au lieu de conjugués peroxydase. Les noyaux cellulaires ont été colorés par incubation dans une solution de colorant de Hoechst 1 g/ml (bis-benzimide, Sigma B1155). immunofluorescence
The immunofluorescence controls were carried out on untreated cellular mats (controls), fixed with methanol at -20 ° C. and dried. The principle, the reagents and the times were the same as for immunoblotting. Secondary antibodies were fluorescein Nisothiocyanate (FITC) conjugates (see table above) instead of peroxidase conjugates. The cell nuclei were stained by incubation in a solution of Hoechst dye 1 g / ml (bis-benzimide, Sigma B1155).
Les coupes ont été observées au microscope en épifluorescence (NIKON, Diaphot 300). Sections were observed under an epifluorescence microscope (NIKON, Diaphot 300).
<Desc/Clms Page number 17> <Desc / Clms Page number 17>
Les saisies d'images ont été réalisées à l'aide d'une caméra COHU pilotée par un logiciel Visiolab 200. The images were captured using a COHU camera controlled by Visiolab 200 software.
Les résultats obtenus sont les suivants :
Globalement, l'acide rétinoïque (10-8 M) et le TGF (3 (10 ng/ml) n'ont pas (ou peu) stimulé la production des marqueurs sélectionnés, alors qu'une efficacité relative du TGF ss vis à vis de la production de collagène IV et de laminine pouvait être attendue. The results obtained are as follows:
Overall, retinoic acid (10-8 M) and TGF (3 (10 ng / ml) did not (or did not) stimulate the production of selected markers, whereas a relative efficacy of TGF ss Collagen IV and laminin production could be expected.
Effet sur l'actine
L'actine a été prise comme marqueur de référence pour montrer que le modèle de cellules utilisé était valide. Une relative fluctuation des résultats a été observée avec l'anticorps monoclonal anti-actine. En règle générale, aucun des produits ou mélanges n'a montré de stimulation notable de l'expression d'actine (pas de prolifération cellulaire accrue de façon significative; l'expérience a été réalisée à confluence). D'autre part, les produits et mélanges n'ont pas réduit de façon significative la production d'actine, bien que l'Extrait de Malt (2 % et 1 %) et l'acide ursolique/acide oléanolique, sel de sodium (0,0075 %) aient eu apparemment tendance à diminuer le signal mesuré. Effect on actin
Actin was taken as a reference marker to show that the cell model used was valid. A relative fluctuation of the results was observed with the anti-actin monoclonal antibody. In general, none of the products or mixtures showed significant stimulation of actin expression (no significantly increased cell proliferation, the experiment was performed at confluence). On the other hand, the products and mixtures did not significantly reduce actin production, although malt extract (2% and 1%) and ursolic acid / oleanolic acid, sodium salt ( 0.0075%) have apparently tended to decrease the measured signal.
A noter une interférence avec l'extrait de levure : le produit seul (sans cellule) produit un signal visible suggérant qu'une composante du produit est reconnue par l'anticorps monoclonal anti-actine. Note interference with yeast extract: the product alone (without cell) produces a visible signal suggesting that a component of the product is recognized by the monoclonal anti-actin antibody.
Effet sur l'intégrine [alpha]2ss1
Le gel de palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser testé seul aux deux concentrations sélectionnées a conduit à une augmentation du signal intégrine [alpha]2ss1. Effect on integrin [alpha] 2ss1
The palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser gel tested alone at the two selected concentrations led to an increase in the [alpha] 2ss1 integrin signal.
Les autres produits testés n'ont pas montré d'augmentation significative (reproductible) d'intégrine [alpha]2ss1. The other products tested did not show a significant (reproducible) increase in integrin [alpha] 2ss1.
A noter un très fort signal obtenu avec l'extrait de levure ; produit contient des composants ayant des épitopes reconnus par l'un ou l'autre des anticorps anti-intégrine du mélange utilisé Il semble donc hautement probable que ce produit contienne des composants protéiques d'origine cellulaire, et cela To note a very strong signal obtained with the yeast extract; product contains components with epitopes recognized by any of the anti-integrin antibodies of the mixture used. It therefore seems highly probable that this product contains protein components of cellular origin, and this
<Desc/Clms Page number 18><Desc / Clms Page number 18>
en quantité non négligeable L'activité de ce produit sur la production d'intégrine [alpha]2ss1 ne peut donc être mesurée en utilisant les conditions expérimentales de cet essai. in significant amount The activity of this product on the production of [alpha] 2ss1 integrin can not be measured using the experimental conditions of this test.
Les mélanges contenant l'extrait de malt, l'extrait de levure et l'acide ursolique/acide oléanolique, sel de sodium n'ont pas montré d'activité significative. Mixtures containing malt extract, yeast extract and ursolic acid / oleanolic acid, sodium salt did not show significant activity.
Effet sur la laminine
Le gel de palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser testé seul à 2 % et 1 % a stimulé de façon significative la production de laminine par les NHDF. Effect on laminin
Palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser gel tested alone at 2% and 1% significantly stimulated laminin production by NHDFs.
L'extrait de malt, l'extrait de levure et l'acide ursolique/acide oléanolique, sel de sodium n'ont pas montré de stimulation significative dans ces conditions expérimentales
Les mélanges ont montré des activités variables. Malt extract, yeast extract and ursolic acid / oleanolic acid, sodium salt did not show significant stimulation under these experimental conditions
The mixtures showed variable activities.
Effet sur le collagène IV
Les mesures de production relative de collagène IV ont montré des résultats homogènes. Effect on collagen IV
Measurements of relative production of collagen IV showed consistent results.
Le gel de palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser a fortement stimulé la production de collagène IV ; d'autre part, tous les mélanges contenant le gel de palmitoyl pentapeptide -Lys-Thr-Thr-Lys-Ser ont stimulé d'un facteur supérieur à 2 fois la production de collagène IV. Palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser gel strongly stimulated the production of IV collagen; on the other hand, all the mixtures containing palmitoyl pentapeptide -Lys-Thr-Thr-Lys-Ser gel stimulated by a factor greater than 2 times the production of collagen IV.
L'extrait de malt et l'extrait de levure n'ont pas montré de stimulation significative. A noter que, comme pour la laminine, l'extrait de levure n'est pas reconnu par l'anti-collagène IV (pas de signal significatif dans le contrôle de l'extrait de levure sans cellules). Malt extract and yeast extract did not show significant stimulation. Note that, as for laminin, yeast extract is not recognized by anti-collagen IV (no significant signal in the control of yeast extract without cells).
L'acide ursolique/acide oléanolique, sel de sodium à 0,0075 % a montré une intensification significative du signal (facteur 1,5) ; une stimulation plus faible (non significative) a été observée à 0,0037 %. Les mélanges contenant l'acide ursolique/acide oléanolique, sel de sodium à 0,0075 % ont une activité du même ordre que le produit seul Ursolic acid / oleanolic acid, 0.0075% sodium salt showed significant signal intensification (factor 1.5); a lower (not significant) stimulation was observed at 0.0037%. The mixtures containing ursolic acid / oleanolic acid, 0.0075% sodium salt have an activity of the same order as the product alone
<Desc/Clms Page number 19> <Desc / Clms Page number 19>
Les résultats obtenus avec les produits isolés sont reportés dans le tableau ci-dessous (analyse densitométrique, résultats en % par rapport au témoin non traité)
The results obtained with the isolated products are shown in the table below (densitometric analysis, results in% relative to the untreated control)
<tb>
<tb> Traitements <SEP> Intégrine <SEP> Laminine <SEP> Collagène <SEP> IV <SEP> p <SEP> Actine <SEP>
<tb> [alpha]2ss1
<tb> P1 <SEP> à <SEP> 2% <SEP> (P11) <SEP> + <SEP> 104% <SEP> + <SEP> 55% <SEP> + <SEP> 160% <SEP> . <SEP> -12%
<tb> P1à1%(P12) <SEP> +125% <SEP> +27% <SEP> +122% <SEP> -13%
<tb> <Tb>
<tb> Treatments <SEP> Integrin <SEP> Laminin <SEP> Collagen <SEP> IV <SEP> p <SEP> Actinase <SEP>
<tb> [alpha] 2ss1
<tb> P1 <SEP> to <SEP> 2% <SEP> (P11) <SEP> + <SEP> 104% <SEP> + <SEP> 55% <SEP> + <SEP> 160% <SEP>. <SEP> -12%
<tb> P1 to 1% (P12) <SEP> + 125% <SEP> + 27% <SEP> + 122% <SEP> -13%
<Tb>
P2 à 2% (P21 ) + 20% - 4% - 6% - 28%
P2 at 2% (P21) + 20% - 4% - 6% - 28%
<tb>
<tb> P2 <SEP> à <SEP> 1 <SEP> % <SEP> (P22) <SEP> - <SEP> 10% <SEP> - <SEP> 3% <SEP> - <SEP> 6% <SEP> - <SEP> 30% <SEP>
<tb> P3 <SEP> à <SEP> 3% <SEP> (P31) <SEP> + <SEP> 516% <SEP> -10% <SEP> + <SEP> 21% <SEP> -10%
<tb> P3à <SEP> 2% <SEP> (P32) <SEP> +429% <SEP> -20% <SEP> + <SEP> 9% <SEP> - <SEP> 5% <SEP>
<tb> P4 <SEP> à <SEP> 0,0075% <SEP> (P41) <SEP> + <SEP> 44% <SEP> - <SEP> 23% <SEP> + <SEP> 59% <SEP> -25%
<tb> P4 <SEP> à <SEP> 0,0037% <SEP> (P42) <SEP> + <SEP> 31 <SEP> % <SEP> - <SEP> 21 <SEP> % <SEP> + <SEP> 24% <SEP> -19%
<tb> TGF <SEP> ss <SEP> +4% <SEP> 0% <SEP> - <SEP> 19% <SEP> -14%
<tb> Acide <SEP> rétinoique <SEP> -3% <SEP> - <SEP> 18% <SEP> - <SEP> 13% <SEP> -8%
<tb> Témoin <SEP> 0% <SEP> 0% <SEP> 0% <SEP> 0%
<tb> <Tb>
<tb> P2 <SEP> to <SEP> 1 <SEP>% <SEP> (P22) <SEP> - <SEP> 10% <SEP> - <SEP> 3% <SEP> - <SEP> 6% <SEP> - <SEP> 30% <SEP>
<tb> P3 <SEP> to <SEP> 3% <SEP> (P31) <SEP> + <SEP> 516% <SEP> -10% <SEP> + <SEP> 21% <SEP> -10%
<tb> P3 to <SEP> 2% <SEP> (P32) <SEP> + 429% <SEP> -20% <SEP> + <SEP> 9% <SEP> - <SEP> 5% <SEP>
<tb> P4 <SEP> to <SEP> 0.0075% <SEP> (P41) <SEP> + <SEP> 44% <SEP> - <SEP> 23% <SEP> + <SEP> 59% <SEP > -25%
<tb> P4 <SEP> to <SEP> 0.0037% <SEP> (P42) <SEP> + <SEP> 31 <SEP>% <SEP> - <SEP> 21 <SEP>% <SEP> + <SEP> 24% <SEP> -19%
<tb> TGF <SEP> ss <SEP> + 4% <SEP> 0% <SEP> - <SEP> 19% <SEP> -14%
<tb><SEP> Retinoic acid <SEP> -3% <SEP> - <SEP> 18% <SEP> - <SEP> 13% <SEP> -8%
<tb> Control <SEP> 0% <SEP> 0% <SEP> 0% <SEP> 0%
<Tb>
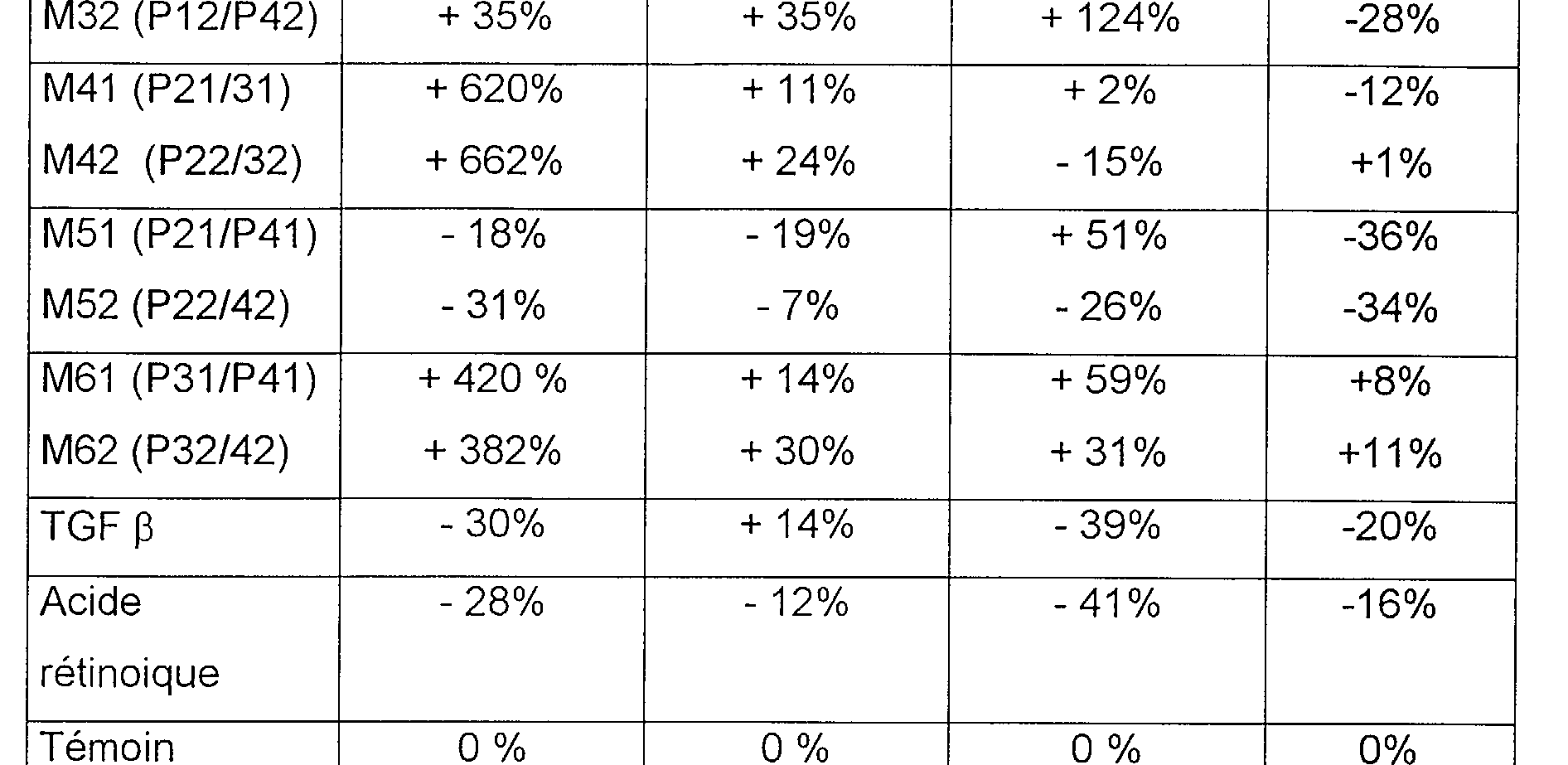
Les résultats obtenus avec les mélanges sont reportés dans le tableau ci-dessous. The results obtained with the mixtures are reported in the table below.
<Desc/Clms Page number 20> <Desc / Clms Page number 20>
<tb>
<tb> Intégrine <SEP> [alpha]2ss1 <SEP> Laminine <SEP> Collagène <SEP> IV <SEP> (3 <SEP> Actine <SEP>
<tb> <Tb>
<tb> Integrin <SEP> [alpha] 2ss1 <SEP> Laminin <SEP> Collagen <SEP> IV <SEP> (3 <SEP> Actinase <SEP>
<Tb>
M11(P11/P21) +13% +14% +198% -12%
M11 (P11 / P21) + 13% + 14% + 198% -12%
<tb>
<tb> M12 <SEP> (P12/P22) <SEP> + <SEP> 3% <SEP> +20% <SEP> +147% <SEP> -14%
<tb> M21 <SEP> (P11/P31) <SEP> + <SEP> 528% <SEP> + <SEP> 5% <SEP> + <SEP> 152% <SEP> -7%
<tb> M22 <SEP> (P12/P32) <SEP> +481% <SEP> +16% <SEP> +139% <SEP> +2%
<tb> <Tb>
<tb> M12 <SEP> (P12 / P22) <SEP> + <SEP> 3% <SEP> + 20% <SEP> + 147% <SEP> -14%
<tb> M21 <SEP> (P11 / P31) <SEP> + <SEP> 528% <SEP> + <SEP> 5% <SEP> + <SEP> 152% <SEP> -7%
<tb> M22 <SEP> (P12 / P32) <SEP> + 481% <SEP> + 16% <SEP> + 139% <SEP> + 2%
<Tb>
M31 (P11/P41 ) - 3% + 7% + 102% -46%
M31 (P11 / P41) - 3% + 7% + 102% -46%
<tb>
<tb> M32 <SEP> (P12/P42) <SEP> +35% <SEP> +35% <SEP> +124% <SEP> -28%
<tb> M41 <SEP> (P21/31) <SEP> + <SEP> 620% <SEP> + <SEP> 11 <SEP> % <SEP> +2% <SEP> -12%
<tb> M42 <SEP> (P22/32) <SEP> +662% <SEP> +24% <SEP> -15% <SEP> +1%
<tb> M51 <SEP> (P21/P41) <SEP> -18% <SEP> -19% <SEP> +51% <SEP> -36%
<tb> M52 <SEP> (P22/42) <SEP> - <SEP> 31 <SEP> % <SEP> - <SEP> 7% <SEP> -26% <SEP> -34%
<tb> M61 <SEP> (P31/P41) <SEP> + <SEP> 420 <SEP> % <SEP> + <SEP> 14% <SEP> + <SEP> 59% <SEP> +8%
<tb> M62 <SEP> (P32/42) <SEP> +382% <SEP> +30% <SEP> +31% <SEP> +11%
<tb> TGF <SEP> ss <SEP> - <SEP> 30% <SEP> + <SEP> 14% <SEP> - <SEP> 39% <SEP> -20%
<tb> Acide <SEP> - <SEP> 28% <SEP> -12% <SEP> -41% <SEP> -16%
<tb> rétinoique
<tb> Témoin <SEP> 0 <SEP> % <SEP> 0 <SEP> % <SEP> 0 <SEP> % <SEP> 0% <SEP>
<tb> <Tb>
<tb> M32 <SEP> (P12 / P42) <SEP> + 35% <SEP> + 35% <SEP> + 124% <SEP> -28%
<tb> M41 <SEP> (P21 / 31) <SEP> + <SEP> 620% <SEP> + <SEP> 11 <SEP>% <SEP> + 2% <SEP> -12%
<tb> M42 <SEP> (P22 / 32) <SEP> + 662% <SEP> + 24% <SEP> -15% <SEP> + 1%
<tb> M51 <SEP> (P21 / P41) <SEP> -18% <SEP> -19% <SEP> + 51% <SEP> -36%
<tb> M52 <SEP> (P22 / 42) <SEP> - <SEP> 31 <SEP>% <SEP> - <SEP> 7% <SEP> -26% <SEP> -34%
<tb> M61 <SEP> (P31 / P41) <SEP> + <SEP> 420 <SEP>% <SEP> + <SEP> 14% <SEP> + <SEP> 59% <SEP> + 8%
<tb> M62 <SEP> (P32 / 42) <SEP> + 382% <SEP> + 30% <SEP> + 31% <SEP> + 11%
<tb> TGF <SEP> ss <SEP> - <SEP> 30% <SEP> + <SEP> 14% <SEP> - <SEP> 39% <SEP> -20%
<tb> Acid <SEP> - <SEP> 28% <SEP> -12% <SEP> -41% <SEP> -16%
<tb> retinoic
<tb> Control <SEP> 0 <SEP>% <SEP> 0 <SEP>% <SEP> 0 <SEP>% <SEP> 0% <SEP>
<Tb>
Conclusions :
Le gel de palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser (P1) stimule la production des trois marqueurs de la jonction dermo-épidermique sélectionnés. Conclusions:
Palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser gel (P1) stimulates the production of the three markers of the selected dermal-epidermal junction.
L'activité du produit est particulièrement nette sur le collagène IV. The activity of the product is particularly clear on collagen IV.
L'extrait de malt (P2), seul ou en mélange n'a pas montré d'activité particulière. Malt extract (P2), alone or in mixture did not show any particular activity.
L'Extrait de levure (P3) a produit des artefacts avec l'anticorps antiactine et surtout avec l'anticorps anti-intégrine. Le produit seul ou en mélange n'a pas montré d'activité particulière en ce qui concerne la laminine et le collagène IV. Yeast extract (P3) produced artifacts with the antiactin antibody and especially with the anti-integrin antibody. The product alone or in mixture did not show any particular activity with regard to laminin and collagen IV.
L'acide ursolique/acide oléanolique, sel de sodium (P4) a stimulé la production de collagène IV. L'effet observé est moins net qu'avec le gel de palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser ; cet effet est cependant apparemment reproductible (reproduit avec les mélanges contenant acide ursolique/acide oléanolique, sel de sodium). Ursolic acid / oleanolic acid, sodium salt (P4) stimulated the production of IV collagen. The effect observed is less clear than with palmitoyl Pentapeptide-Lys-Thr-Thr-Lys-Ser gel; this effect is however apparently reproducible (reproduced with mixtures containing ursolic acid / oleanolic acid, sodium salt).
<Desc/Clms Page number 21> <Desc / Clms Page number 21>
Expérimentation 2 : Evaluation de l'activation de la néosynthèse de collagène IV dans le modèle d'épiderme reconstruit SkinEthic. Experiment 2: Evaluation of the activation of collagen IV neosynthesis in the SkinEthic reconstructed epidermis model.
On a testé les produits suivants - Placebo : PEG400/eau purifiée(10/90) ; appelée Po - Formulation 1 : Acide ursolique/acide oléanolique, sel de sodium à 0,1%, appelé F1 - Formulation2 Gel de palmitoyl pentapeptide -Lys-Thr-Thr-Lys-Ser à 3%, appelé F2 - Formulation 3 : mélange d'acide ursolique/acide oléanolique, sel de sodium à 0,1% et de Gel de palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser à 3%, appelé F3 - Formulation 4 : Extrait de lupin blanc à 1 %, appelé F4, (F1, F2, F3, et F4 sont utilisés en solution aqueuse dans 10 % final de PEG 400), comme suit :
On utilise des épidermes reconstruits de type Skinethic de 13 jours (4 cm2), cultivés dans du milieu Skinethic. On vénfie l'expression des messagers intégnne a2, ss1 et collagène IV dans les épidermes reconstruits par méthode RT-polymerase chain reaction (RT-PCR). The following products were tested - Placebo: PEG400 / purified water (10/90); called Po - Formulation 1: Ursolic acid / oleanolic acid, 0.1% sodium salt, called F1 - Formulation2 Palmitoyl pentapeptide gel -Lys-Thr-Thr-Lys-Ser 3%, called F2 - Formulation 3: mixture of ursolic acid / oleanolic acid, 0.1% sodium salt and 3% palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser gel, called F3 - Formulation 4: 1% white lupine extract, called F4, (F1, F2, F3, and F4 are used in aqueous solution in 10% PEG 400 final), as follows:
13-day Skinethic reconstructed epidermis (4 cm 2) cultured in Skinethic medium is used. The expression of the integrated messengers a2, ss1 and collagen IV is deferred in the reconstructed epidermis by RT-polymerase chain reaction (RT-PCR) method.
20 épidermes ont été traités par les formulations ou le placebo, en application topique, à raison de 5 mg/cm2 par épiderme (20 NI). Quatre épidermes ont été traités avec 20 l pour chaque produit ; pour chaque traitement, deux épidermes ont été cultivés pendant 18 h et extraits pour analyse ; les deux autres épidermes de chaque lot ont été à nouveau traités et re-cultivés pendant 48 h supplémentaires avant extraction (72 h de traitement en tout)
On analyse alors les ARN par northern blot et les protéines par southern blot
Analyse des ARN par northern blot 20 epidermals were treated with the formulations or placebo, topically applied at a rate of 5 mg / cm 2 per epidermis (20 NI). Four skins were treated with 20 l for each product; for each treatment, two epidermals were cultured for 18 h and extracted for analysis; the other two epidermis from each lot were again treated and re-cultured for an additional 48 h before extraction (72 h total treatment)
RNAs are then analyzed by northern blot and proteins by southern blot
RNA analysis by northern blot
<Desc/Clms Page number 22> <Desc / Clms Page number 22>
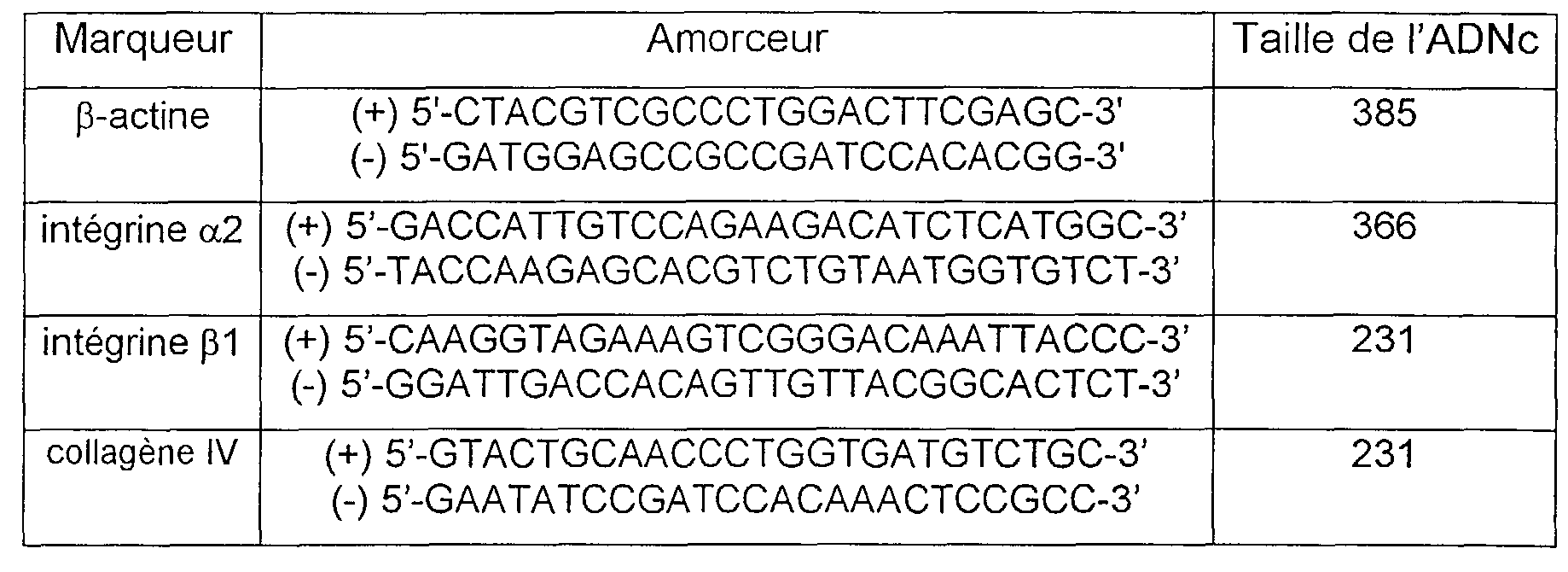
On a préparé les sondes ADN ci-après à partir des fragments d'ADNc réalisés lors des étapes préliminaires, après réamplification et purification.
The following DNA probes were prepared from the cDNA fragments made during the preliminary steps, after reamplification and purification.
<tb>
<tb> <Tb>
<Tb>
Marqueur <SEP> Amorceur <SEP> Taille <SEP> de <SEP> l'ADNc
<tb> ss-actine <SEP> (+) <SEP> 5'-CTACGTCGCCCTGGACTTCGAGC-3' <SEP> 385
<tb> (-)5'-GATGGAGCCGCCGATCCACACGG-3'
<tb> intégrine <SEP> a2 <SEP> (+) <SEP> 5'-GACCATTGTCCAGAAGACATCTCATGGC-3' <SEP> 366
<tb> (-) <SEP> 5'-TACCAAGAGCACGTCTGTAATGGTGTCT-3'
<tb> intégrine <SEP> ss1 <SEP> (+) <SEP> 5'-CAAGGTAGAAAGTCGGGACAAATTACCC-3' <SEP> 231
<tb> (-) <SEP> 5'-GGATTGACCACAGTTGTTACGGCACTCT-3' <SEP>
<tb> collagène <SEP> IV <SEP> (+) <SEP> 5'-GTACTGCAACCCTGGTGATGTCTGC-3' <SEP> 231
<tb> (-) <SEP> 5'-GAATATCCGATCCACAAACTCCGCC-3' <SEP>
<tb> Marker <SEP> Primer <SEP> Size <SEP> of <SEP> cDNA
<tb> ss-actin <SEP> (+) <SEP>5'-CTACGTCGCCCTGGACTTCGAGC-3'<SEP> 385
<tb> (-) 5'-GATGGAGCCGCCGATCCACACGG-3 '
<tb> integrin <SEP> a2 <SEP> (+) <SEP>5'-GACCATTGTCCAGAAGACATCTCATGGC-3'<SEP> 366
<tb> (-) <SEP>5'-TACCAAGAGCACGTCTGTAATGGTGTCT-3'
<tb> integrin <SEP> ss1 <SEP> (+) <SEP>5'-CAAGGTAGAAAGTCGGGACAAATTACCC-3'<SEP> 231
<tb> (-) <SEP>5'-GGATTGACCACAGTTGTTACGGCACTCT-3'<SEP>
<tb> Collagen <SEP> IV <SEP> (+) <SEP>5'-GTACTGCAACCCTGGTGATGTCTGC-3'<SEP> 231
<tb> (-) <SEP>5'-GAATATCCGATCCACAAACTCCGCC-3'<SEP>
<Tb>
Schématiquement, on a procédé à l'amplification du brin antisens de chaque ADNc en utilisant le mélange réactionnel suivant (25 l; concentrations finales): 25 U/ml RedTaq (Sigma D4309); 2. 5 l tampon RedTaq 10x ; 20 M dTTP; 20 M dCTP; 20 M dGTP; 2 M [[alpha]-32P]-dATP (15 l, 150 Ci, 3000 Ci/mmol, Amersham PB10204); 1 ng/ l ADNc purifié ; 1 M Amorceur antisens (-). Conditions de PCR: 94 C 2 min ; 30 fois la séquence (95 C 1 min, 55 C 1 min, 72 C 2 min), puis 1 cycle d'élongation de 7 min, à 72 C puis procédé à la purification des 3 sondes sur 3 colonnes Chroma Spin-200 (Clontech S0269), selon les directives du fournisseur ; de la purification par comptage en scintillation liquide , rassemblement des fractions relatives à chaque sonde. Schematically, amplification of the antisense strand of each cDNA was carried out using the following reaction mixture (25 l, final concentrations): 25 U / ml RedTaq (Sigma D4309); 2. 5 l RedTaq buffer 10x; 20M dTTP; 20 m dCTP; 20 M dGTP; 2 M [[alpha] -32 P] -dATP (15 l, 150 Ci, 3000 Ci / mmol, Amersham PB10204); 1 ng / l purified cDNA; 1 M Antisense primer (-). PCR conditions: 94 C 2 min; 30 times the sequence (95 C 1 min, 55 C 1 min, 72 C 2 min), then 1 cycle of elongation of 7 min at 72 C then proceeded to the purification of the 3 probes on 3 columns Chroma Spin-200 ( Clontech S0269), as directed by the supplier; of the liquid scintillation counting purification, collecting the fractions relative to each probe.
Extraction d'ARN total, électrophorèses et transfert
A la fin du traitement, les épidermes ont été dissociés de leur nacelle et congelés immédiatement ( -80 C) dans 1,25 ml de Tri-Reagent (TR, Sigma T9424), en tube Eppendorf sans RNAse. Total RNA extraction, electrophoresis and transfer
At the end of the treatment, the epidermis were dissociated from their nacelle and immediately frozen (-80 ° C.) in 1.25 ml of Tri-Reagent (TR, Sigma T9424), in Eppendorf tube without RNAse.
Le northern blot a été réalisé comme suit - décongélation des échantillons, broyage extensif et élimination des particules solides (membrane-support...) - extraction de l'ARN total de chaque épiderme selon la méthodologie préconisée par le fournisseur de Tri-Reagent (Sigma) ; la fraction renfermant les protéines a été gardée pour analyse à part. The northern blot was carried out as follows: - thawing of the samples, extensive grinding and removal of the solid particles (membrane-support ...) - extraction of the total RNA from each epidermis according to the methodology recommended by the supplier of Tri-Reagent ( Sigma); the fraction containing the proteins was kept for separate analysis.
<Desc/Clms Page number 23> <Desc / Clms Page number 23>
- solubilisation de l'ARN extrait dans 50 l d'eau sans RNAse (eauDiEthylPyroCarbonate (DEPC) (Maniatis et al , 2nd éd.). solubilization of the extracted RNA in 50 l of water without RNAse (water of EthylPyroCarbonate (DEPC) (Maniatis et al, 2nd ed.).
- vérification de la qualité et de l'homogénéité des échantillons d'ARN après séparation d'un aliquote (2 l) par électrophorèse en gel d'agarose/formaldéhyde en présence de bromure d'éthydium (Maniatis et al., 2nd éd. ). Observation sous UV et saisie des images sur GelPrint 2000i (BioPhotonics Corp.) ; - quantification de l'ARN par mesure de l'absorption à 260 nm ; ajustement des solutions d'ARN à 1 pg/pl ; - séparation de chacun des échantillons d'ARN sur 4 gels d'agarose/formaldéhyde (2 g d'ARN/puits pour l'actine et les intégrines ; 5 pg/puits pour le collagène IV) - transfert par capillarité (Maniatis et al.) sur membranes de nylon Hybond-N (Amersham RPN1510N), 16 heures (une membrane par sonde) ; couplage covalent des ARN au nylon par chauffage des membranes sèches 90 min, à 80 C. - Verification of the quality and homogeneity of the RNA samples after separation of an aliquot (2 l) by agarose gel electrophoresis / formaldehyde in the presence of ethidium bromide (Maniatis et al., 2nd ed. ). UV observation and image capture on GelPrint 2000i (BioPhotonics Corp.); - quantification of the RNA by measuring the absorption at 260 nm; adjustment of the RNA solutions to 1 μg / μl; separation of each of the RNA samples on 4 agarose / formaldehyde gels (2 g of RNA / well for actin and integrins, 5 μg / well for collagen IV) - capillary transfer (Maniatis et al. .) on Hybond-N nylon membranes (Amersham RPN1510N), 16 hours (one membrane per probe); covalent coupling of the RNAs to the nylon by heating the dry membranes for 90 min at 80 C.
Hybridations et analyses - préhybridation des membranes individuelles dans 8 ml d'ExpressHyb (Clontech S1135)/0,1 mg/ml salmon testes DNA, Sigma D7656 dénaturé ; préhybridation à 68 C, 20 min (3 bouteilles à hybridation ; four Stuart) ; - hybridation 16 heures à 68 C, après addition de sonde marquée ; - 4 lavages en 2x saline sodium citrate (SSC) (Maniatis et a/.)/1 % SDS, à 68 C, pendant 30 min ; lavage en 0,1x SSC/0,5 % SDS, à 68 C; 1 lavage en 2x SSC ; - autoradiographie des membranes enveloppées dans du Saran wrap , à - 80 C, sur film Kodak Biomax MS. Saisie des images ; - comptage direct de la radioactivité des spots à l'aide d'un Instantlmager (Packard Instruments)
Analyse des protéines southern blot
Les protéines ont été repurifiées à partir des interfaces eau/solvant issues du protocole de purification des ARN La fraction protéique totale a été Hybridations and assays - prehybridization of individual membranes in 8 ml of ExpressHyb (Clontech S1135) / 0.1 mg / ml salmon testes DNA, denatured Sigma D7656; prehybridization at 68 ° C, 20 min (3 hybridization bottles, Stuart oven); hybridization for 16 hours at 68 ° C., after addition of labeled probe; 4 washes in 2x saline sodium citrate (SSC) (Maniatis et al.) / 1% SDS, at 68 ° C., for 30 minutes; washing in 0.1x SSC / 0.5% SDS, at 68 ° C; 1 wash in 2x SSC; autoradiography of membranes wrapped in Saran wrap, at -80 C, on Kodak Biomax MS film. Entering images - direct counting of spot radioactivity using an Instantlmager (Packard Instruments)
Southern blot protein analysis
The proteins were repurified from the water / solvent interfaces resulting from the RNA purification protocol. The total protein fraction was
<Desc/Clms Page number 24><Desc / Clms Page number 24>
préparée comme spécifié dans le protocole d'utilisation du Tri-reagent. Les protéines ont été finalement dissociées en tampon de dépôt d'électrophorèse SDS (SDS-PAGE) ; les concentrations finales de SDS et de 2-mercaptoéthanol étaient de 2 %. prepared as specified in the Tri-reagent usage protocol. The proteins were finally dissociated in SDS electrophoresis deposition buffer (SDS-PAGE); the final concentrations of SDS and 2-mercaptoethanol were 2%.
Les protéines ont été séparées par SDS-PAGE (gels d'acrylamide 8 %) et transférées (transfert électrique en milieu liquide) sur nitrocellulose (Hybond, ECL, Amersham). Dans chaque série, des contrôles sans anticorps primaires ont été réalisés. Les membranes ont été saturées par incubation 16 heures (4 C) dans un tampon PBS/0,05 % Tween 20/5 % lait écrémé (PBSTL). Les bandes de puits contrôles sans anticorps primaire ont été découpées pour traitement à part (incubation avec le conjugué peroxydase seulement). Après lavages, les sites antigéniques spécifiques ont été marqués par les anticorps primaires aux dilutions indiquées dans du PBSTL (voir tableau ci-dessous), pendant 1 h, à 37 C. Les anticorps primaires fixés ont été révélés par un conjugué anti-immunoglobulines - peroxydase. Après lavages extensifs en PBST, l'activité peroxydase a été révélée par la méthode ECL (enhanced chimiluminescence, Amersham), sur film Kodak MP. La saisie des images a été réalisée sur GelPrint 2000i (BioPhotonics Corp.); les analyses densitométriques ont été obtenues à l'aide du logiciel One-D-Scan (Scanalytics). The proteins were separated by SDS-PAGE (8% acrylamide gels) and transferred (liquid electric transfer) onto nitrocellulose (Hybond, ECL, Amersham). In each series, controls without primary antibodies were performed. The membranes were saturated by incubation for 16 hours (4 C) in PBS buffer / 0.05% Tween 20/5% skim milk (PBSTL). Control well strips without primary antibodies were cut for separate treatment (incubation with peroxidase conjugate only). After washes, the specific antigenic sites were labeled with the primary antibodies at the indicated dilutions in PBSTL (see table below), for 1 h at 37 C. The fixed primary antibodies were revealed by an anti-immunoglobulin conjugate - peroxidase. After extensive PBST washes, the peroxidase activity was revealed by ECL (enhanced chemiluminescence, Amersham) method on Kodak MP film. Image capture was performed on GelPrint 2000i (BioPhotonics Corp.); the densitometric analyzes were obtained using the One-D-Scan software (Scanalytics).
Le tableau ci-dessous liste les différents anticorps utilisés.
The table below lists the different antibodies used.
<tb>
<tb> marqueur <SEP> anticorps <SEP> primaire <SEP> référence <SEP> dilution
<tb> p-actine <SEP> monoclonal <SEP> Sigma <SEP> A4700 <SEP> 1/500e
<tb> intégrine <SEP> a2pl <SEP> mélange <SEP> polyclonal <SEP> anti-a2 <SEP> Chemicon <SEP> AB1944 <SEP> 1/500e
<tb> + <SEP> polyclonal <SEP> anti-p1 <SEP> Chemicon <SEP> AB1952 <SEP> 1/500e
<tb> collagène <SEP> IV <SEP> polyclonal <SEP> Rockland <SEP> 600-401-106-0.1 <SEP> 1/1000e
<tb> <Tb>
<tb> marker <SEP> antibody <SEP> primary <SEP> reference <SEP> dilution
<tb> p-actin <SEP> monoclonal <SEP> Sigma <SEP> A4700 <SEP> 1 / 500th
<tb> integrin <SEP> a2pl <SEP> mixture <SEP> polyclonal <SEP> anti-α2 <SEP> Chemicon <SEP> AB1944 <SEP> 1 / 500th
<tb> + <SEP> polyclonal <SEP> anti-p1 <SEP> Chemicon <SEP> AB1952 <SEP> 1 / 500th
<tb> collagen <SEP> IV <SEP> polyclonal <SEP> Rockland <SEP> 600-401-106-0.1 <SEP> 1 / 1000th
<Tb>
<Desc/Clms Page number 25> <Desc / Clms Page number 25>
<tb>
<tb> marqueur <SEP> anticorps <SEP> secondaire <SEP> référence
<tb> P-actine <SEP> RAM-peroxydase <SEP> (Blot) <SEP> Sigma <SEP> A9044
<tb> ou <SEP> GAM-FITC <SEP> (immunofluo.) <SEP> Tebu <SEP> M30801
<tb> intégrine <SEP> a2p1 <SEP> GAR-peroxydase <SEP> (Blot) <SEP> Sigma <SEP> A9169
<tb> ou <SEP> GAR <SEP> -FITC <SEP> (immunofluo.) <SEP> Tebu <SEP> L42001
<tb> collagène <SEP> IV <SEP> GAR-peroxydase <SEP> (Blot) <SEP> Sigma <SEP> A9169
<tb> ou <SEP> GAR <SEP> -FITC <SEP> (immunofluo.) <SEP> Tebu <SEP> L42001
<tb> <Tb>
<tb> marker <SEP> antibody <SEP> secondary <SEP> reference
<tb> P-actin <SEP> RAM-peroxidase <SEP> (Blot) <SEP> Sigma <SEP> A9044
<tb> or <SEP> GAM-FITC <SEP> (immunofluo.) <SEP> Tebu <SEP> M30801
<tb> integrin <SEP> a2p1 <SEP> GAR-peroxidase <SEP> (Blot) <SEP> Sigma <SEP> A9169
<tb> or <SEP> GAR <SEP> -FITC <SEP> (immunofluo.) <SEP> Tebu <SEP> L42001
<tb> Collagen <SEP> IV <SEP> GAR-Peroxidase <SEP> (Blot) <SEP> Sigma <SEP> A9169
<tb> or <SEP> GAR <SEP> -FITC <SEP> (immunofluo.) <SEP> Tebu <SEP> L42001
<Tb>
Les résultats obtenus sont les suivants :
Effets sur la transcription, northern blot
Les effets observés par Phosphorlmager sont quantifiés en % versus placebo.
The results obtained are as follows:
Effects on transcription, northern blot
The effects observed by Phosphorlmager are quantified in% versus placebo.
<tb>
<tb> <Tb>
<Tb>
Traitement <SEP> Intégrine <SEP> a2 <SEP> Intégrine <SEP> ss1 <SEP> Collagène <SEP> IV
<tb> PO <SEP> 0 <SEP> 0 <SEP> 0 <SEP>
<tb> F1 <SEP> -17% <SEP> +16% <SEP> +21%
<tb> F2-34% <SEP> -2% <SEP> -6%
<tb> F3-30% <SEP> -24% <SEP> -12%
<tb> F4 <SEP> -16% <SEP> -39% <SEP> +20% <SEP>
<tb> P0 <SEP> à <SEP> 72H <SEP> 0 <SEP> 0 <SEP> 0
<tb> F1 <SEP> à <SEP> 72H <SEP> +17% <SEP> +12%-53%
<tb> F2 <SEP> à <SEP> 72H <SEP> -37% <SEP> +12% <SEP> -41 <SEP> % <SEP>
<tb> F3 <SEP> à <SEP> 72H-58% <SEP> -18%-80%
<tb> F4 <SEP> à <SEP> 72H <SEP> -8% <SEP> +6% <SEP> -30%
<tb> Treatment <SEP> Integrin <SEP> a2 <SEP> Integrin <SEP> ss1 <SEP> Collagen <SEP> IV
<tb> PO <SEP> 0 <SEP> 0 <SEP> 0 <SEP>
<tb> F1 <SEP> -17% <SEP> + 16% <SEP> + 21%
<tb> F2-34% <SEP> -2% <SEP> -6%
<tb> F3-30% <SEP> -24% <SEP> -12%
<tb> F4 <SEP> -16% <SEP> -39% <SEP> + 20% <SEP>
<tb> P0 <SEP> to <SEP> 72H <SEP> 0 <SEP> 0 <SEP> 0
<tb> F1 <SEP> to <SEP> 72H <SEP> + 17% <SEP> + 12% -53%
<tb> F2 <SEP> to <SEP> 72H <SEP> -37% <SEP> + 12% <SEP> -41 <SEP>% <SEP>
<tb> F3 <SEP> to <SEP> 72H-58% <SEP> -18% -80%
<tb> F4 <SEP> to <SEP> 72H <SEP> -8% <SEP> + 6% <SEP> -30%
<Tb>
Actine (référence)
L'ARN de tous les échantillons a été quantifié ; la même quantité d'ARN a été déposée pour tous les échantillons traités. Ainsi, dans la mesure où le nombre de copies de messager actine est considéré comme stable et importante dans une cellule normale, la quantité de messagers actine doit être stable en l'absence de modifications profondes du profil d'expression des gènes cellulaires (hyperprolifération, cytotoxicité... ). Mises à part quelques fluctuations expérimentales, la quantité de messager actine mesurée était relativement Actin (reference)
RNA from all samples was quantified; the same amount of RNA was deposited for all treated samples. Thus, since the actin messenger copy number is considered stable and important in a normal cell, the amount of actin messengers must be stable in the absence of profound changes in the expression pattern of the cellular genes (hyperproliferation, cytotoxicity ...). Apart from some experimental fluctuations, the amount of actin messenger measured was relatively
<Desc/Clms Page number 26><Desc / Clms Page number 26>
stable après 18 h de traitement, des fluctuations plus importantes ont été observées au temps 72 h
La mesure de l'expression des différents marqueurs dans chaque échantillon a été rapportée à l'expression relative d'actine dans le même échantillon. stable after 18 h of treatment, larger fluctuations were observed at 72 h
The measurement of the expression of the different markers in each sample was related to the relative expression of actin in the same sample.
Intégrine a2
Les traitements n'ont pas montré d'effet stimulant très net sur l'expression de messager intégrine a2. Seule la formulation F1 a montré une légère tendance, au temps 72 h seulement (+17 % par rapport au témoin). Integrate a2
The treatments did not show a strong stimulating effect on the expression of integrin messenger a2. Only the F1 formulation showed a slight trend, at 72 h only (+ 17% compared to the control).
Intégrine ss1
Les traitements n'ont pas montré d'effet stimulant très net sur l'expression du messager intégrine (31. Integrin ss1
The treatments did not show a very stimulating effect on the expression of the integrin messenger (31.
La formulation F1 a eu tendance à stimuler l'expression à 18 h (+16 % par rapport au témoin) et à 72 h (+12 %). F2 a aussi eu tendance à stimuler l'expression, au temps 72 h seulement (+12 % par rapport au témoin). Formulation F1 tended to stimulate expression at 18 h (+ 16% vs. control) and 72 h (+ 12%). F2 also tended to stimulate expression at 72 h only (+ 12% compared to control).
Collagène IV (chaîne a2)
Les formulations F1 et F4 ont eu tendance à stimuler l'expression au temps 18 h (de l'ordre de +20 % du témoin). Tous les traitements ont inhibé l'expression de collagène IV au temps 72 h ; cet effet est apparemment relié à une forte intensité de marquage du collagène IV dans le placebo, à 72 h. Collagen IV (a2 chain)
Formulations F1 and F4 tended to stimulate the expression at the time of 18 h (of the order of + 20% of the control). All treatments inhibited IV collagen expression at 72 h; this effect is apparently related to a high intensity of labeling of collagen IV in the placebo at 72 h.
Effets sur la quantité de marqueurs protéiques, western blot
Les résultats sont donnés en chiffres relatifs par rapport à l'actine versus placebo, après analyse densitométrique des bandes immunodétectées. Effects on the amount of protein markers, western blot
The results are given in relative figures compared with actin versus placebo, after densitometric analysis of the immunodetected bands.
<Desc/Clms Page number 27> <Desc / Clms Page number 27>
<tb>
<tb> Traitement <SEP> Intégrine <SEP> [alpha]2ss1 <SEP> Collagène <SEP> IV
<tb> PO <SEP> à <SEP> 18H <SEP> 0 <SEP> 0 <SEP>
<tb> F1 <SEP> à <SEP> 18H <SEP> +90% <SEP> +53% <SEP>
<tb> F2 <SEP> à <SEP> 18H <SEP> +87% <SEP> +5% <SEP>
<tb> F3 <SEP> à <SEP> 18H <SEP> +34% <SEP> -8% <SEP>
<tb> F4 <SEP> à <SEP> 18H <SEP> -3% <SEP> -8%
<tb> PO <SEP> à <SEP> 72H <SEP> 0 <SEP> 0 <SEP>
<tb> F1 <SEP> à <SEP> 72H <SEP> +33% <SEP> +10% <SEP>
<tb> F2 <SEP> à <SEP> 72H <SEP> +47% <SEP> +6% <SEP>
<tb> F3 <SEP> à <SEP> 72H <SEP> +48% <SEP> +44% <SEP>
<tb> F4 <SEP> à <SEP> 72H <SEP> -34% <SEP> +31 <SEP> % <SEP>
<tb> <Tb>
<tb> Treatment <SEP> Integrin <SEP> [alpha] 2ss1 <SEP> Collagen <SEP> IV
<tb> PO <SEP> to <SEP> 18H <SEP> 0 <SEP> 0 <SEP>
<tb> F1 <SEP> to <SEP> 18H <SEP> + 90% <SEP> + 53% <SEP>
<tb> F2 <SEP> to <SEP> 18H <SEP> + 87% <SEP> + 5% <SEP>
<tb> F3 <SEP> to <SEP> 18H <SEP> + 34% <SEP> -8% <SEP>
<tb> F4 <SEP> to <SEP> 18H <SEP> -3% <SEP> -8%
<tb> PO <SEP> to <SEP> 72H <SEP> 0 <SEP> 0 <SEP>
<tb> F1 <SEP> to <SEP> 72H <SEP> + 33% <SEP> + 10% <SEP>
<tb> F2 <SEP> to <SEP> 72H <SEP> + 47% <SEP> + 6% <SEP>
<tb> F3 <SEP> to <SEP> 72H <SEP> + 48% <SEP> + 44% <SEP>
<tb> F4 <SEP> to <SEP> 72H <SEP> -34% <SEP> +31 <SEP>% <SEP>
<Tb>
Pour mémoire F3=F1+F2
L'analyse immunoenzymatique a été effectuée sur des fractions protéiques repurifiées et après séparation par SDS-PAGE. For memory F3 = F1 + F2
Enzyme immunoassay was performed on repurified protein fractions and after separation by SDS-PAGE.
Actine (référence)
La bande d'actine était parfaitement nette et relativement homogène à l'intérieur de chaque groupe d'échantillons (18 h et 72 h ; ungel par temps de traitement). Actin (reference)
The actin band was perfectly clear and relatively homogeneous within each group of samples (18 h and 72 h, ungel per treatment time).
Intégrine [alpha]2ss1
Contrairement au cas des autres anticorps utilisés, le mélange d'anticorps anti-intégrines a généré un important bruit de fond rendant difficile l'interprétation des résultats
Il apparaît cependant que les formulations F1, F2, F3 ont eu tendance à augmenter l'intensité du signal [alpha]2ss1. Integral [alpha] 2ss1
Unlike the other antibodies used, the mixture of anti-integrin antibodies generated a large background noise making it difficult to interpret the results.
It appears however that the formulations F1, F2, F3 have tended to increase the intensity of the signal [alpha] 2ss1.
Collagène IV
Les extraits d'épidermes traité par F1 pendant 18 h présentent une intensité du marquage du collagène IV supérieure à celle des témoins (+53 % par rapport au témoin). L'effet était moins net au temps 72 h. Ces résultats confirment ceux obtenus par northern blot. Collagen IV
Epidermal extracts treated with F1 for 18 h show an intensity of labeling of collagen IV greater than that of the controls (+53% relative to the control). The effect was less clear at 72 h. These results confirm those obtained by northern blot.
<Desc/Clms Page number 28> <Desc / Clms Page number 28>
Les traitements par F3 et F4 ont au contraire eu tendance à stimuler la production de collagène IV après le double traitement de 72 h. On the contrary, the F3 and F4 treatments tended to stimulate the production of IV collagen after the 72 h double treatment.
Conclusions :
Dans le test western blot, l'acide ursolique et le palmitoyl pentapeptide augmentent tous les deux la néosynthèse d'intégrine [alpha]2ss1, sans avoir d'effet synergique entre eux. Dans ce modèle, ces deux composés ont une faible action chacun sur la néosynthèse de collagène IV ; par contre, à 72 heures, ils ont une forte action synergique quand on les utilise ensemble. Conclusions:
In the western blot test, ursolic acid and palmitoyl pentapeptide both increase the [alpha] 2ss1 integrin neosynthesis, without having a synergistic effect between them. In this model, these two compounds have a weak action each on the neosynthesis of collagen IV; on the other hand, at 72 hours, they have a strong synergetic action when used together.
Quand à l'extrait peptidique de lupin blanc, s'il a une action négligeable sur la néosynthèse d'intégrine [alpha]2ss1, par contre il a à 72 heures une très bonne activité sur la néosynthèse du Collagène IV. As for the peptide extract of white lupine, if it has a negligible action on the neogenesis of integrin [alpha] 2ss1, on the other hand it has at 72 hours a very good activity on the neosynthesis of Collagen IV.
Expérimentation 3: essai avec 3 composés en mélange en comparaison avec les composés séparés, selon le même protocole que cidessus et en procédant uniquement à l'analyse de l'expression du collagène IV. Experiment 3: test with 3 compounds in mixture in comparison with the separated compounds, according to the same protocol as above and carrying out only the analysis of the expression of collagen IV.
On a testé les produits suivants - Placebo : appelé Po - Formulation 1 : Acide ursolique/acide oléanolique, sel de sodium à 0,1% appelé F1 - Formulation2: Gel de palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser à 3% appelé F2 - Formulation 3 : mélange d'acide ursolique/acide oléanolique, sel de sodium à 0,1 % et de Gel de palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser à 3% appelé F3 - Formulation 4 Extrait de lupin blanc à 1 % appelé F4 - Formulation 5 = F1 +F4 appelé F5 - Formulation 6 = F2+F4 appelé F6 - Formulation 7 = F1+ F2+ F4 appelé F7 en solution aqueuse dans 10 % final de PEG 400
Résultats (analyse par Western blot versus placebo) : The following products were tested - Placebo: called Po - Formulation 1: Ursolic acid / oleanolic acid, 0.1% sodium salt called F1 - Formulation2: Palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser gel at 3 % called F2 - Formulation 3: mixture of ursolic acid / oleanolic acid, 0.1% sodium salt and 3% palmitoyl pentapeptide-Lys-Thr-Thr-Lys-Ser gel called F3 - Formulation 4 Extract 1% white lupine called F4 - Formulation 5 = F1 + F4 called F5 - Formulation 6 = F2 + F4 called F6 - Formulation 7 = F1 + F2 + F4 called F7 in aqueous solution in 10% final of PEG 400
Results (Western blot versus placebo analysis):
<Desc/Clms Page number 29> <Desc / Clms Page number 29>
<tb>
<tb> Traitement <SEP> Collagène <SEP> IV
<tb> PO <SEP> 0% <SEP>
<tb> F1 <SEP> +32% <SEP>
<tb> F2 <SEP> -1 <SEP> % <SEP>
<tb> F3 <SEP> +25% <SEP>
<tb> F4 <SEP> +3% <SEP>
<tb> F5 <SEP> +61% <SEP>
<tb> F6 <SEP> +60% <SEP>
<tb> F7 <SEP> +101% <SEP>
<tb> <Tb>
<tb> Treatment <SEP> Collagen <SEP> IV
<tb> PO <SEP> 0% <SEP>
<tb> F1 <SEP> + 32% <SEP>
<tb> F2 <SEP> -1 <SEP>% <SEP>
<tb> F3 <SEP> + 25% <SEP>
<tb> F4 <SEP> + 3% <SEP>
<tb> F5 <SEP> + 61% <SEP>
<tb> F6 <SEP> + 60% <SEP>
<tb> F7 <SEP> + 101% <SEP>
<Tb>
Conclusions
Parmi les 3 composés, l'acide ursolique/oléanolique montre une augmentation de la néosynthèse de collagène IV par rapport au placebo, tandis que le mélange des trois composés montre une augmentation de la néosynthèse de collagène IV significativement plus importante avec un effet synergique évident. conclusions
Among the 3 compounds, ursolic / oleanolic acid showed an increase in collagen IV neosynthesis compared with placebo, while the mixture of the three compounds showed a significantly higher increase in IV collagen neosynthesis with an obvious synergistic effect.
Expérimentation 4 . Experimentation 4.
On a étudié les effets de la composition de l'exemple 1 sur une population de 40 femmes caucasiennes d'âge moyen 46 ans, dont 3 de phototype Il, 18 de phototype III et 19 de phototype IV et concernant le type de peau :36 à peau mixte et 4 à peau mixte à tendance grasse. The effects of the composition of Example 1 on a population of 40 Caucasian women of mean age 46 years were studied, of which 3 of phototype II, 18 of phototype III and 19 of phototype IV and concerning the type of skin: 36 with mixed skin and 4 with combination skin with a fatty tendency.
Les expérimentatrices ont procédé à une application biquotidienne de la composition de l'exemple 1 pendant 8 semaines, en quantité usuelle, au niveau du visage dans son ensemble, contour des yeux et cou. The experimenters proceeded to a twice-daily application of the composition of Example 1 for 8 weeks, in the usual amount, in the face as a whole, around the eyes and neck.
On a procédé à un contrôle de la tolérance et à une évaluation de l'efficacité par l'investigateur, - des empreintes cutanées, - des mesures cutométriques, - des macrophotographies à titre illustratif, - un questionnaire d'auto-évaluation complété par les volontaires. A tolerance check and an evaluation of the investigator's effectiveness were carried out, - skin prints, - cutometric measurements, - macrophotographies for illustrative purposes, - a self-assessment questionnaire supplemented by the volunteers.
<Desc/Clms Page number 30> <Desc / Clms Page number 30>
Le déroulement de l'essai était le suivant :
Etat initiai, SO - examen médical d'inclusion, - vérification des critères d'inclusion et de non-inclusion, - cotation clinique initiale des signes fonctionnels et physiques de tolérance locale et de l'état cutané avant traitement, - empreintes cutanées au niveau de la patte-d'oie, - mesures cutométriques au niveau de la pommette, - macrophotographies de la patte-d'oie chez 15 volontaires. The course of the test was as follows:
State initiai, SO - inclusion medical examination, - verification of inclusion and non-inclusion criteria, - initial clinical score of functional and physical signs of local tolerance and skin condition before treatment, - cutaneous impressions at the level of of the crow's feet, - cutometric measurements at the cheekbone, - macrophotographies of crow's feet in 15 volunteers.
Après 4 semaines de traitement (28 jours), S4 : - cotation clinique intermédiaire des signes fonctionnels et physiques de tolérance locale et d'efficacité, - empreintes cutanées au niveau de la patte-d'oie, - mesures cutométriques au niveau de la pommette, - auto-évaluation intermédiaire par les volontaires. After 4 weeks of treatment (28 days), S4: - Intermediate clinical score for functional and physical signs of local tolerance and efficacy, - Skin prints at the crow's feet, - Cutometric measurements at the cheekbone , - intermediate self-evaluation by volunteers.
Après 8 semaines de traitement (56 jours), S8 : - cotation clinique finale des signes fonctionnels et physiques de tolérance locale et d'efficacité, - empreintes cutanées au niveau de la patte-d'oie, - mesures cutométriques au niveau de la pommette, - macrophotographies de la patte-d'oie chez 15 volontaires, - auto-évaluation finale par les volontaires. After 8 weeks of treatment (56 days), S8: - final clinical score of the functional and physical signs of local tolerance and efficacy, - skin prints at the crow's feet, - cutometric measurements at the cheekbone - macrophotographies of crow's feet in 15 volunteers, - final self-evaluation by volunteers.
Les résultats obtenus sont les suivants :
L'examen d'efficacité montre à l'issue de 8 semaines d'applications biquotidiennes de la composition de l'exemple 1 . The results obtained are as follows:
The efficacy test shows at the end of 8 weeks of twice-daily applications of the composition of Example 1.
- une diminution significative de la laxité cutanée, dès le premier mois de traitement, - une diminution du nombre de ridules, significative à partir du deuxième mois de traitement, - a significant decrease in cutaneous laxity, from the first month of treatment, - a decrease in the number of fine lines, significant from the second month of treatment,
<Desc/Clms Page number 31><Desc / Clms Page number 31>
- une diminution significative de la profondeur de ces ridules dès le premier mois, - une diminution de leur longueur, significative au cours du deuxième mois. - a significant decrease in the depth of these wrinkles in the first month, - a decrease in their length, significant in the second month.
L'ensemble des paramètres analysés sur les empreintes cutanées de la patte-d'oie montre une évolution favorable au cours des 8 semaines de traitement, avec en particulier une diminution statistiquement significative de la rugosité moyenne, une diminution notable de l'écart maximum, et une diminution significative de la proportion de sillons de profondeur moyenne (Classe 2). All the parameters analyzed on the skin prints of the crow's foot show a favorable evolution during the 8 weeks of treatment, with in particular a statistically significant decrease in the mean roughness, a significant decrease in the maximum difference, and a significant decrease in the proportion of medium depth furrows (Class 2).
Les mesures cutométriques permettent d'objectiver de manière statistiquement significative une peau plus tendue, moins fatigable et plus tonique ; ces effets, caractérisant une amélioration de la fermeté de la peau, sont significatifs dès le premier mois de traitement. Cutometric measurements make it possible to statistically signify a more tense, less fatiguing and more toned skin; these effects, which characterize an improvement of the firmness of the skin, are significant from the first month of treatment.
Enfin, les questionnaires d'auto-évaluation reflètent une perception très favorable de la composition de l'exemple 1 par une très forte majorité des volontaires, aussi bien en ce qui concerne ses qualités cosmétiques que son efficacité ; elle est jugée efficace ou très efficace en tant qu'anti-rides et raffermissant par 91 % des sujets, et 87. 5% des volontaires achèteraient ce produit qu'elles ont noté 8/10 en moyenne. Finally, the self-assessment questionnaires reflect a very favorable perception of the composition of Example 1 by a very large majority of volunteers, both as regards its cosmetic qualities and its effectiveness; it is considered effective or very effective as anti-wrinkle and firming by 91% of the subjects, and 87. 5% of the volunteers would buy this product which they noted 8/10 on average.
Expérimentation 5
On a étudié les effets de la composition de l'exemple 2 sur une population de 34 femmes caucasiennes d'âge moyen 52 ans, dont 17 de phototype III et 17 de phototype IV et concernant le type de peau : 15 à peau légèrement sèche et 19 à peau modérément sèche. Experiment 5
The effects of the composition of Example 2 were studied on a population of 34 Caucasian women of 52 years of age, of whom 17 were of type III and 17 were of type IV and the skin type was: 15 with slightly dry skin and 19 with moderately dry skin.
Les expérimentatrices ont procédé à une application biquotidienne de la composition de l'exemple 2 pendant 8 semaines, en quantité usuelle, au niveau du visage dans son ensemble, contour des yeux et cou, ainsi qu'au niveau d'un avant-bras. The experimenters proceeded to twice daily application of the composition of Example 2 for 8 weeks, in the usual amount, at the level of the face as a whole, around the eyes and neck, as well as at the level of a forearm.
On a procédé à un contrôle clinique de la tolérance et à une évaluation de l'efficacité par, Clinical control of the safety and efficacy evaluation was performed by
<Desc/Clms Page number 32><Desc / Clms Page number 32>
- des empreintes cutanées, - des mesures cutométriques, - des macrophotographies à titre illustratif, - un questionnaire d'auto-évaluation complété par les volontaires. - skin prints, - cutometric measurements, - macrophotographies for illustrative purposes, - a self-assessment questionnaire supplemented by volunteers.
Le déroulement de l'essai était le suivant :
Etat initial, SO : - examen d'inclusion, - vérification des critères d'inclusion et de non-inclusion, - cotation clinique initiale des signes fonctionnels et physiques de tolérance locale et de l'état cutané avant traitement, - empreintes cutanées au niveau de la patte d'oie, - mesures cutométriques au niveau de la pommette, - macrophotographies de la patte d'oie chez 15 volontaires,
Après 4 semaines de traitement (28 jours), S4 : - cotation intermédiaire des signes fonctionnels et physiques de tolérance locale et d'efficacité, - empreintes cutanées au niveau de la patte d'oie, - mesures cutométriques au niveau de la pommette, - auto-évaluation intermédiaire par les volontaires. The course of the test was as follows:
Initial state, N / A: - inclusion test, - verification of inclusion and non-inclusion criteria, - initial clinical score of functional and physical signs of local tolerance and skin condition before treatment, - skin impressions at the level of crow's feet, - cutometric measurements at the cheekbone, - macrophotographies of crow's feet in 15 volunteers,
After 4 weeks of treatment (28 days), S4: - intermediate score of the functional and physical signs of local tolerance and efficacy, - cutaneous impressions on the crow's feet, - cutometric measurements on the cheekbone, - intermediate self-evaluation by volunteers.
Après 8 semaines de traitement (56 jours), S8 : - cotation clinique finale des signes fonctionnels et physiques de tolérance locale et d'efficacité, - empreintes cutanées au niveau de la patte d'oie, - mesures cutométriques au niveau de la pommette, - auto-évaluation finale par les volontaires. After 8 weeks of treatment (56 days), S8: - final clinical score of the functional and physical signs of local tolerance and efficacy, - cutaneous impressions on the crow's feet, - cutometric measurements on the cheekbone, - final self-evaluation by the volunteers.
Les résultats obtenus sont les suivants :
L'efficacité anti-rides est cliniquement caractérisée par une diminution significative de la laxité cutanée, de la quantité de ridules et de leur profondeur ; ces améliorations sont statistiquement significatives dès le premier The results obtained are as follows:
Anti-wrinkle efficacy is clinically characterized by a significant decrease in cutaneous laxity, the amount of fine lines and their depth; these improvements are statistically significant from the first
<Desc/Clms Page number 33><Desc / Clms Page number 33>
mois de traitement. Une diminution de la longueur des sillons s'amorce également de façon significative au cours du deuxième mois de traitement. month of treatment. A decrease in groove length also begins significantly during the second month of treatment.
L'ensemble des paramètres analysés sur les empreintes cutanées de la patte-d'oie évolue favorablement au cours des 8 semaines de traitement, avec en particulier une diminution significative de la longueur développée, du nombre total de sillons et de la proportion de sillons de profondeur moyenne, ces évolutions intervenant au cours des 4 premières semaines de traitement. All the parameters analyzed on the skin prints of the crow's foot evolve favorably during the 8 weeks of treatment, with in particular a significant decrease in the length developed, the total number of furrows and the proportion of furrows in the average depth, these changes occurring during the first 4 weeks of treatment.
Les mesures cutométriques permettent d'objectiver de manière statistiquement significative une peau plus tonique, moins fatigable et plus tendue ; l'amélioration de la tonicité et les effets tenseur et anti-stress se manifestent dès la 4ème semaine d'applications de façon statistiquement significative. Cutometric measurements make it possible to statistically signify a more toned, less tiring and more tense skin; the improvement of the tone and the tensor and anti-stress effects appear in the 4th week of applications in a statistically significant way.
Enfin, les questionnaires d'auto-évaluation reflètent une perception très favorable du produit testé par une très forte majorité des volontaires, aussi bien en ce qui concerne ses qualités cosmétiques que son efficacité ; il est jugé efficace ou très efficace en tant qu'hydratant, anti-rides et raffermissant par 91 % des sujets. 82% des volontaires achèteraient ce produit qu'elles ont noté 8/10 en moyenne. Finally, the self-assessment questionnaires reflect a very favorable perception of the product tested by a very large majority of volunteers, as regards both its cosmetic qualities and its effectiveness; it is considered effective or very effective as a moisturizer, anti-wrinkle and firming by 91% of subjects. 82% of volunteers would buy this product that they rated 8/10 on average.
Claims (4)
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0010773A FR2813018B1 (en) | 2000-08-21 | 2000-08-21 | COSMETIC COMPOSITIONS CONTAINING AT LEAST ONE COMPONENT STIMULATING THE NEOSYNTHESIS OF LAMININS, AND / OR INTEGRIN ALPHA-2 BETA-1 AND / OR COLLAGEN IV OF THE DERMO-EPIDERMAL JUNCTION |
| EP01969626A EP1408925A1 (en) | 2000-08-21 | 2001-08-20 | Cosmetic compositions |
| PCT/EP2001/009652 WO2002015869A1 (en) | 2000-08-21 | 2001-08-20 | Cosmetic compositions containing compounds stimulating the neosynthesis of components of the dermo-epidermal junction |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0010773A FR2813018B1 (en) | 2000-08-21 | 2000-08-21 | COSMETIC COMPOSITIONS CONTAINING AT LEAST ONE COMPONENT STIMULATING THE NEOSYNTHESIS OF LAMININS, AND / OR INTEGRIN ALPHA-2 BETA-1 AND / OR COLLAGEN IV OF THE DERMO-EPIDERMAL JUNCTION |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| FR2813018A1 true FR2813018A1 (en) | 2002-02-22 |
| FR2813018B1 FR2813018B1 (en) | 2004-02-06 |
Family
ID=8853622
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| FR0010773A Expired - Fee Related FR2813018B1 (en) | 2000-08-21 | 2000-08-21 | COSMETIC COMPOSITIONS CONTAINING AT LEAST ONE COMPONENT STIMULATING THE NEOSYNTHESIS OF LAMININS, AND / OR INTEGRIN ALPHA-2 BETA-1 AND / OR COLLAGEN IV OF THE DERMO-EPIDERMAL JUNCTION |
Country Status (3)
| Country | Link |
|---|---|
| EP (1) | EP1408925A1 (en) |
| FR (1) | FR2813018B1 (en) |
| WO (1) | WO2002015869A1 (en) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1327438A1 (en) * | 2002-01-12 | 2003-07-16 | Dr. Scheller Cosmetics AG | Cosmetic composition and use of same |
| FR2848116A1 (en) * | 2002-12-10 | 2004-06-11 | Nuxe Lab | Cosmetic and/or dermatological compositions, especially for combating skin aging symptoms, containing lipopeptide and metalloproteinase inhibitor, preferably Siegesbeckia extract |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102004009155A1 (en) * | 2004-02-20 | 2005-09-01 | Beiersdorf Ag | Skin care product containing ursolic acid and ginkgo extract |
| US8987212B2 (en) * | 2007-08-07 | 2015-03-24 | Muhammed Majeed | Oleanoyl peptide composition and method of treating skin aging |
| BE1020210A3 (en) * | 2011-09-06 | 2013-06-04 | Auriga Internat | DERMATOLOGICAL COMPOSITION BASED ON FRAGMENTS OF HYALURONATE OR HYALURONIC ACID. |
| KR101459070B1 (en) * | 2013-12-09 | 2014-11-17 | (주) 뉴메딕 | Long lasting crosslinked polysaccharide gel formulation |
| FR3023164B1 (en) * | 2014-07-03 | 2017-10-20 | Expanscience Lab | PEPTIDE EXTRACTS FROM LUPINE AND CLOSURE OF THE SKIN |
| WO2018081779A1 (en) | 2016-10-31 | 2018-05-03 | Sytheon Limited | Skin enhancing compositions and methods |
| FR3060307B1 (en) | 2016-12-16 | 2019-01-25 | L'oreal | COSMETIC COMPOSITION COMPRISING SOLID FATTY BODIES AND A GELIFYING POLYMER |
| KR101990097B1 (en) * | 2017-06-21 | 2019-06-18 | 코오롱인더스트리 주식회사 | Eco-friendly cosmetic composition for moisturizing and improving skin elasticity |
| WO2018236069A1 (en) * | 2017-06-21 | 2018-12-27 | 코오롱인더스트리 주식회사 | Eco-friendly cosmetic composition for skin moisturizing and elasticity enhancement |
| WO2020192865A1 (en) * | 2019-03-22 | 2020-10-01 | Symrise Ag | Plant peptides and their applications |
Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2152365A1 (en) * | 1971-09-08 | 1973-04-27 | Serdex | Triterpenic acid compsns - for modification of protein synthesis esp in collagen diseases |
| WO1996025143A1 (en) * | 1995-02-17 | 1996-08-22 | Lvmh Recherche | Cosmetic or pharmaceutical, particularly dermatological, composition containing a bertholletia extract |
| WO1998013019A1 (en) * | 1996-09-27 | 1998-04-02 | Unilever Plc | Skin care compositions containing an acid and a retinoid |
| JPH1112122A (en) * | 1997-06-20 | 1999-01-19 | Pola Chem Ind Inc | Skin-improving cosmetic |
| FR2778565A1 (en) * | 1998-05-14 | 1999-11-19 | Silab Sa | Extraction of plant components useful in composition for increasing thickness of stratum corneum |
| FR2779058A1 (en) * | 1998-05-29 | 1999-12-03 | Dior Christian Parfums | USE OF AT LEAST ONE COSMETICALLY ACCEPTABLE SAPONIN OR SAPOGENOL AS A COSMETIC AGENT FOR INCREASING THE QUANTITY OF COLLAGEN IV IN THE DERMO-EPIDERMAL JUNCTION |
| FR2779059A1 (en) * | 1998-05-29 | 1999-12-03 | Guerlain | Use of an agent for promoting adhesion of epidermal basal layer keratinocytes for prevention of, e.g. skin aging |
| FR2783169A1 (en) * | 1998-09-15 | 2000-03-17 | Sederma Sa | Use of pentapeptides in cosmetic or dermatological compositions for improving skin appearance and tone and aiding wound healing |
| FR2792202A1 (en) * | 1999-04-19 | 2000-10-20 | Pharmascience Lab | Lupin peptide extract having a metalloprotease inhibiting activity, for treatment of disorders due to excessive destruction of collagen or supporting macroproteins |
| WO2000062743A2 (en) * | 1999-04-19 | 2000-10-26 | The Procter & Gamble Company | Skin care compositions containing combination of skin care actives |
| FR2797186A1 (en) * | 1999-08-02 | 2001-02-09 | Silab Sa | New yeast extract active at the dermo-epidermal junction, useful as anti-aging treatment for the skin |
-
2000
- 2000-08-21 FR FR0010773A patent/FR2813018B1/en not_active Expired - Fee Related
-
2001
- 2001-08-20 EP EP01969626A patent/EP1408925A1/en not_active Withdrawn
- 2001-08-20 WO PCT/EP2001/009652 patent/WO2002015869A1/en not_active Application Discontinuation
Patent Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2152365A1 (en) * | 1971-09-08 | 1973-04-27 | Serdex | Triterpenic acid compsns - for modification of protein synthesis esp in collagen diseases |
| WO1996025143A1 (en) * | 1995-02-17 | 1996-08-22 | Lvmh Recherche | Cosmetic or pharmaceutical, particularly dermatological, composition containing a bertholletia extract |
| WO1998013019A1 (en) * | 1996-09-27 | 1998-04-02 | Unilever Plc | Skin care compositions containing an acid and a retinoid |
| JPH1112122A (en) * | 1997-06-20 | 1999-01-19 | Pola Chem Ind Inc | Skin-improving cosmetic |
| FR2778565A1 (en) * | 1998-05-14 | 1999-11-19 | Silab Sa | Extraction of plant components useful in composition for increasing thickness of stratum corneum |
| FR2779058A1 (en) * | 1998-05-29 | 1999-12-03 | Dior Christian Parfums | USE OF AT LEAST ONE COSMETICALLY ACCEPTABLE SAPONIN OR SAPOGENOL AS A COSMETIC AGENT FOR INCREASING THE QUANTITY OF COLLAGEN IV IN THE DERMO-EPIDERMAL JUNCTION |
| FR2779059A1 (en) * | 1998-05-29 | 1999-12-03 | Guerlain | Use of an agent for promoting adhesion of epidermal basal layer keratinocytes for prevention of, e.g. skin aging |
| FR2783169A1 (en) * | 1998-09-15 | 2000-03-17 | Sederma Sa | Use of pentapeptides in cosmetic or dermatological compositions for improving skin appearance and tone and aiding wound healing |
| FR2792202A1 (en) * | 1999-04-19 | 2000-10-20 | Pharmascience Lab | Lupin peptide extract having a metalloprotease inhibiting activity, for treatment of disorders due to excessive destruction of collagen or supporting macroproteins |
| WO2000062743A2 (en) * | 1999-04-19 | 2000-10-26 | The Procter & Gamble Company | Skin care compositions containing combination of skin care actives |
| FR2797186A1 (en) * | 1999-08-02 | 2001-02-09 | Silab Sa | New yeast extract active at the dermo-epidermal junction, useful as anti-aging treatment for the skin |
Non-Patent Citations (3)
| Title |
|---|
| DATABASE BIOSIS [online] BIOSCIENCES INFORMATION SERVICE, PHILADELPHIA, PA, US; LEE HO-YOUNG ET AL.: "Induction of differentiation in the cultured F9 teracarcinoma stem cells by triterpene acids.", XP002169196, Database accession no. PREV199497465087 * |
| DATABASE CAPLUS [online] CHEMICAL ABSTRACTS SERVICE, COLUMBUS, OHIO, US; XP002169195, retrieved from STN Database accession no. 1999:49152 * |
| JOURNAL OF CANCER RESEARCH AND CLINICAL ONCOLOGY, vol. 120, no. 9, 1994, pages 513 - 518 * |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1327438A1 (en) * | 2002-01-12 | 2003-07-16 | Dr. Scheller Cosmetics AG | Cosmetic composition and use of same |
| FR2848116A1 (en) * | 2002-12-10 | 2004-06-11 | Nuxe Lab | Cosmetic and/or dermatological compositions, especially for combating skin aging symptoms, containing lipopeptide and metalloproteinase inhibitor, preferably Siegesbeckia extract |
| WO2004062637A1 (en) * | 2002-12-10 | 2004-07-29 | Laboratoire Nuxe | Cosmetic composition comprising a metalloproteinase inhibitor and a lipopeptide |
Also Published As
| Publication number | Publication date |
|---|---|
| FR2813018B1 (en) | 2004-02-06 |
| EP1408925A1 (en) | 2004-04-21 |
| WO2002015869A9 (en) | 2002-06-13 |
| WO2002015869A1 (en) | 2002-02-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP1555999B1 (en) | Cosmetical use of kombucha for treating skin aging | |
| EP1638991B1 (en) | Cosmetic or dermopharmaceutical composition for reducing the signs of cutaneous ageing | |
| EP1021161B1 (en) | Use of ellagic acid and its derivatives in cosmetics and dermatology | |
| FR3057462A1 (en) | ANIGOZANTHOS FLAVIDUS EXTRACT FOR ITS COSMETIC USE | |
| FR2885522A1 (en) | COSMETIC OR DERMOPHARMACEUTICAL COMPOSITION CONTAINING TEPRENONE | |
| FR2929511A1 (en) | NEW ACTIVE PRINCIPLE STIMULATING THE PROLIFERATION AND / OR THE ACTIVITY OF FIBROBLASTS. | |
| FR2791684A1 (en) | COSMETIC OR DERMOPHARMACEUTICAL COMPOSITION CONTAINING TRIPEPTIDE N-N-BIOTINYL-GLY-HIS-LYS TO PREVENT, REDUCE OR ELIMINATE HAIR LOSS AS WELL AS TO PROMOTE HAIR REGROWTH | |
| KR20130108805A (en) | Cosmetic composition comprising golden silkworm(bombyx moril) derived materials as active ingredient | |
| EP0946138B1 (en) | Use of a potentilla erecta extract in the cosmetic and pharmaceutical field | |
| FR2813018A1 (en) | COSMETIC COMPOSITIONS CONTAINING AT LEAST ONE COMPOUND STIMULATING LAMININ NEOSYNTHESIS, AND/OR INTEGRINE ALPHA-2 BETA-1 AND/OR COLLAGEN IV OF THE DERMO-EPIDERMAL JUNCTION | |
| FR2997299A1 (en) | ASSOCIATION OF PLANT EXTRACTS, COSMETIC ACTIVE INGREDIENT AND COMPOSITION CONTAINING THE SAME, AND COSMETIC TOPICAL USE | |
| EP2240505B1 (en) | Peptide for activating aquaporin synthesis | |
| FR3018449A1 (en) | COSMETIC USE OF A MIRABILIS JALAPA EXTRACT, ACTIVE INGREDIENT AND CORRESPONDING COSMETIC COMPOSITION | |
| KR101426415B1 (en) | The cosmetic composition for the prevention and improvement of striae distensae | |
| FR2827171A1 (en) | Use of an enzymatic hydrolysate of salmon eggs for preventing or treating the effects of aging caused by physiology or sunlight | |
| WO2015036704A1 (en) | Cosmetic or dermatological use of an extract of tapirira guianensis | |
| FR3011742A1 (en) | NOVEL ACTIVE TO HOMOGENIZE LIP VERMILLON AND COSMETIC COMPOSITIONS COMPRISING SAME | |
| FR3008890B1 (en) | OAK EXTRACT, COMPOSITION COMPRISING SAID EXTRACT AND USES IN PARTICULAR COSMETICS | |
| KR102432887B1 (en) | Skin health improvement set including skin cosmetics and edible film and skin care method using the same | |
| FR3139467A1 (en) | Use of a Sichuan pepper extract for skin treatment and a composition adapted to this use. | |
| FR2889948A1 (en) | Cosmetic composition, useful in the (dermo)cosmetic product to correct, maintain and improve the moisture level of the skin, comprises an association of apple seed extract and vitamin-B3 | |
| WO2022269176A1 (en) | Cosmetic use of a phacelia extract, in particular for the care of skin appendages | |
| JP2001354518A (en) | Skin care preparation | |
| FR3123807A1 (en) | ACTIVATING COSMETIC SERUM AND USE IN A COSMETIC TREATMENT PROCESS | |
| FR3116728A1 (en) | Vegetable water from Camargue rice and uses in particular in cosmetics |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ST | Notification of lapse |