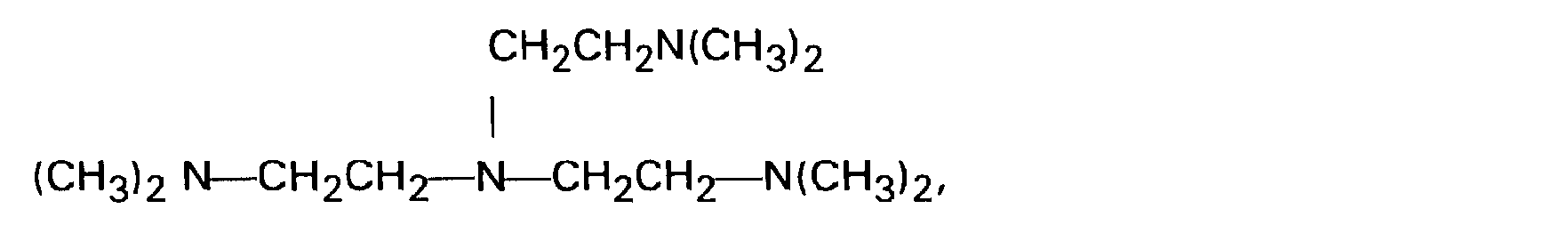FR2812639A1 - Procede de preparation d'alcoxyamines a partir de nitroxydes - Google Patents
Procede de preparation d'alcoxyamines a partir de nitroxydes Download PDFInfo
- Publication number
- FR2812639A1 FR2812639A1 FR0010344A FR0010344A FR2812639A1 FR 2812639 A1 FR2812639 A1 FR 2812639A1 FR 0010344 A FR0010344 A FR 0010344A FR 0010344 A FR0010344 A FR 0010344A FR 2812639 A1 FR2812639 A1 FR 2812639A1
- Authority
- FR
- France
- Prior art keywords
- sep
- radical
- ranging
- metal
- atom
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 238000000034 method Methods 0.000 title claims abstract description 46
- 230000008569 process Effects 0.000 title claims description 19
- 238000002360 preparation method Methods 0.000 title claims description 14
- 239000002608 ionic liquid Substances 0.000 claims abstract description 31
- 239000002184 metal Substances 0.000 claims abstract description 30
- 229910052751 metal Inorganic materials 0.000 claims abstract description 30
- 125000005262 alkoxyamine group Chemical group 0.000 claims abstract description 22
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical class ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 claims abstract description 18
- 239000003446 ligand Substances 0.000 claims abstract description 16
- 239000012074 organic phase Substances 0.000 claims abstract description 14
- 239000003960 organic solvent Substances 0.000 claims abstract description 14
- 150000003839 salts Chemical class 0.000 claims abstract description 14
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 10
- 150000001875 compounds Chemical class 0.000 claims abstract description 9
- 230000002051 biphasic effect Effects 0.000 claims abstract description 4
- 238000001704 evaporation Methods 0.000 claims abstract description 4
- 239000012429 reaction media Substances 0.000 claims abstract description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 claims description 77
- -1 alkyl radical Chemical class 0.000 claims description 48
- 239000012071 phase Substances 0.000 claims description 17
- 125000004432 carbon atom Chemical group C* 0.000 claims description 16
- UKODFQOELJFMII-UHFFFAOYSA-N pentamethyldiethylenetriamine Chemical compound CN(C)CCN(C)CCN(C)C UKODFQOELJFMII-UHFFFAOYSA-N 0.000 claims description 15
- 229910021589 Copper(I) bromide Inorganic materials 0.000 claims description 14
- 238000003756 stirring Methods 0.000 claims description 14
- 229910052757 nitrogen Inorganic materials 0.000 claims description 13
- 125000002524 organometallic group Chemical group 0.000 claims description 12
- 230000008929 regeneration Effects 0.000 claims description 11
- 238000011069 regeneration method Methods 0.000 claims description 11
- 230000003647 oxidation Effects 0.000 claims description 10
- 238000007254 oxidation reaction Methods 0.000 claims description 10
- 125000000217 alkyl group Chemical group 0.000 claims description 8
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Chemical group BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 claims description 8
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 8
- 125000004429 atom Chemical group 0.000 claims description 7
- 229910052801 chlorine Inorganic materials 0.000 claims description 7
- 150000003254 radicals Chemical class 0.000 claims description 7
- AJRFBXAXVLBZMP-UHFFFAOYSA-M 1-methyl-3-propylimidazol-1-ium;bromide Chemical compound [Br-].CCCN1C=C[N+](C)=C1 AJRFBXAXVLBZMP-UHFFFAOYSA-M 0.000 claims description 6
- FHDQNOXQSTVAIC-UHFFFAOYSA-M 1-butyl-3-methylimidazol-3-ium;chloride Chemical compound [Cl-].CCCCN1C=C[N+](C)=C1 FHDQNOXQSTVAIC-UHFFFAOYSA-M 0.000 claims description 5
- 229910052794 bromium Inorganic materials 0.000 claims description 5
- 229910052799 carbon Inorganic materials 0.000 claims description 5
- 239000000460 chlorine Substances 0.000 claims description 5
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 5
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 claims description 4
- CIUQDSCDWFSTQR-UHFFFAOYSA-N [C]1=CC=CC=C1 Chemical compound [C]1=CC=CC=C1 CIUQDSCDWFSTQR-UHFFFAOYSA-N 0.000 claims description 4
- 150000007942 carboxylates Chemical group 0.000 claims description 4
- JEVCWSUVFOYBFI-UHFFFAOYSA-N cyanyl Chemical compound N#[C] JEVCWSUVFOYBFI-UHFFFAOYSA-N 0.000 claims description 4
- 125000005843 halogen group Chemical group 0.000 claims description 4
- 229910052740 iodine Chemical group 0.000 claims description 4
- 229910001507 metal halide Inorganic materials 0.000 claims description 4
- 150000005309 metal halides Chemical class 0.000 claims description 4
- OMKZWUPRGQMQJC-UHFFFAOYSA-N n'-[3-(dimethylamino)propyl]propane-1,3-diamine Chemical compound CN(C)CCCNCCCN OMKZWUPRGQMQJC-UHFFFAOYSA-N 0.000 claims description 4
- 125000002827 triflate group Chemical group FC(S(=O)(=O)O*)(F)F 0.000 claims description 4
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 3
- 125000004122 cyclic group Chemical group 0.000 claims description 3
- 230000008020 evaporation Effects 0.000 claims description 3
- 229910052760 oxygen Inorganic materials 0.000 claims description 3
- 238000006479 redox reaction Methods 0.000 claims description 3
- 229910052723 transition metal Inorganic materials 0.000 claims description 3
- 150000003624 transition metals Chemical class 0.000 claims description 3
- JOLFMOZUQSZTML-UHFFFAOYSA-M 1-methyl-3-propylimidazol-1-ium;chloride Chemical compound [Cl-].CCCN1C=C[N+](C)=C1 JOLFMOZUQSZTML-UHFFFAOYSA-M 0.000 claims description 2
- SLRMQYXOBQWXCR-UHFFFAOYSA-N 2154-56-5 Chemical compound [CH2]C1=CC=CC=C1 SLRMQYXOBQWXCR-UHFFFAOYSA-N 0.000 claims description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 2
- 125000005078 alkoxycarbonylalkyl group Chemical group 0.000 claims description 2
- 150000004945 aromatic hydrocarbons Chemical class 0.000 claims description 2
- 150000001721 carbon Chemical group 0.000 claims description 2
- 229910052736 halogen Inorganic materials 0.000 claims description 2
- 125000005842 heteroatom Chemical group 0.000 claims description 2
- 125000002029 aromatic hydrocarbon group Chemical group 0.000 claims 1
- 238000002156 mixing Methods 0.000 abstract description 2
- 238000005406 washing Methods 0.000 abstract description 2
- 238000013019 agitation Methods 0.000 abstract 1
- 239000010949 copper Substances 0.000 description 22
- 238000004064 recycling Methods 0.000 description 17
- CRRUGYDDEMGVDY-UHFFFAOYSA-N 1-bromoethylbenzene Chemical compound CC(Br)C1=CC=CC=C1 CRRUGYDDEMGVDY-UHFFFAOYSA-N 0.000 description 16
- 238000006243 chemical reaction Methods 0.000 description 15
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 14
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 10
- 238000011068 loading method Methods 0.000 description 9
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 9
- 239000002904 solvent Substances 0.000 description 8
- 229910052786 argon Inorganic materials 0.000 description 7
- 239000000178 monomer Substances 0.000 description 7
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- 238000005481 NMR spectroscopy Methods 0.000 description 6
- 239000000203 mixture Substances 0.000 description 6
- 239000011541 reaction mixture Substances 0.000 description 6
- ROFVEXUMMXZLPA-UHFFFAOYSA-N Bipyridyl Chemical compound N1=CC=CC=C1C1=CC=CC=N1 ROFVEXUMMXZLPA-UHFFFAOYSA-N 0.000 description 5
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 5
- FMJIREFIIGRAAJ-UHFFFAOYSA-N o-(1-phenylethyl)hydroxylamine Chemical compound NOC(C)C1=CC=CC=C1 FMJIREFIIGRAAJ-UHFFFAOYSA-N 0.000 description 5
- WVDDUSFOSWWJJH-UHFFFAOYSA-N 1-methyl-3-propylimidazol-1-ium Chemical compound CCCN1C=C[N+](C)=C1 WVDDUSFOSWWJJH-UHFFFAOYSA-N 0.000 description 4
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 4
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 description 4
- 229920002521 macromolecule Polymers 0.000 description 4
- 238000006116 polymerization reaction Methods 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 239000012230 colorless oil Substances 0.000 description 3
- 229910052802 copper Inorganic materials 0.000 description 3
- 150000004820 halides Chemical class 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- 238000010526 radical polymerization reaction Methods 0.000 description 3
- 230000035484 reaction time Effects 0.000 description 3
- IQQRAVYLUAZUGX-UHFFFAOYSA-N 1-butyl-3-methylimidazolium Chemical compound CCCCN1C=C[N+](C)=C1 IQQRAVYLUAZUGX-UHFFFAOYSA-N 0.000 description 2
- MCTWTZJPVLRJOU-UHFFFAOYSA-N 1-methyl-1H-imidazole Chemical compound CN1C=CN=C1 MCTWTZJPVLRJOU-UHFFFAOYSA-N 0.000 description 2
- UXBLSWOMIHTQPH-UHFFFAOYSA-N 4-acetamido-TEMPO Chemical group CC(=O)NC1CC(C)(C)N([O])C(C)(C)C1 UXBLSWOMIHTQPH-UHFFFAOYSA-N 0.000 description 2
- XUXUHDYTLNCYQQ-UHFFFAOYSA-N 4-amino-TEMPO Chemical group CC1(C)CC(N)CC(C)(C)N1[O] XUXUHDYTLNCYQQ-UHFFFAOYSA-N 0.000 description 2
- UZFMOKQJFYMBGY-UHFFFAOYSA-N 4-hydroxy-TEMPO Chemical group CC1(C)CC(O)CC(C)(C)N1[O] UZFMOKQJFYMBGY-UHFFFAOYSA-N 0.000 description 2
- SFXHWRCRQNGVLJ-UHFFFAOYSA-N 4-methoxy-TEMPO Chemical group COC1CC(C)(C)N([O])C(C)(C)C1 SFXHWRCRQNGVLJ-UHFFFAOYSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 2
- RPDUDBYMNGAHEM-UHFFFAOYSA-N PROXYL Chemical group CC1(C)CCC(C)(C)N1[O] RPDUDBYMNGAHEM-UHFFFAOYSA-N 0.000 description 2
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 2
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 2
- 150000001450 anions Chemical class 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 150000001723 carbon free-radicals Chemical class 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- 238000007334 copolymerization reaction Methods 0.000 description 2
- 230000008034 disappearance Effects 0.000 description 2
- 238000000921 elemental analysis Methods 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 238000011065 in-situ storage Methods 0.000 description 2
- 238000001095 inductively coupled plasma mass spectrometry Methods 0.000 description 2
- 239000011261 inert gas Substances 0.000 description 2
- 239000003999 initiator Substances 0.000 description 2
- 238000004452 microanalysis Methods 0.000 description 2
- DWFKOMDBEKIATP-UHFFFAOYSA-N n'-[2-[2-(dimethylamino)ethyl-methylamino]ethyl]-n,n,n'-trimethylethane-1,2-diamine Chemical compound CN(C)CCN(C)CCN(C)CCN(C)C DWFKOMDBEKIATP-UHFFFAOYSA-N 0.000 description 2
- 229920000768 polyamine Polymers 0.000 description 2
- 238000011403 purification operation Methods 0.000 description 2
- 239000000377 silicon dioxide Substances 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- BULLJMKUVKYZDJ-UHFFFAOYSA-N 1,1,1,2,2,3,3,4,4,5,5,6,6-tridecafluoro-6-iodohexane Chemical compound FC(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)I BULLJMKUVKYZDJ-UHFFFAOYSA-N 0.000 description 1
- BQCIDUSAKPWEOX-UHFFFAOYSA-N 1,1-Difluoroethene Chemical compound FC(F)=C BQCIDUSAKPWEOX-UHFFFAOYSA-N 0.000 description 1
- WLDGDTPNAKWAIR-UHFFFAOYSA-N 1,4,7-trimethyl-1,4,7-triazonane Chemical compound CN1CCN(C)CCN(C)CC1 WLDGDTPNAKWAIR-UHFFFAOYSA-N 0.000 description 1
- HRFJEOWVAGSJNW-UHFFFAOYSA-N 1,4,8,11-tetramethyl-1,4,8,11-tetrazacyclotetradecane Chemical compound CN1CCCN(C)CCN(C)CCCN(C)CC1 HRFJEOWVAGSJNW-UHFFFAOYSA-N 0.000 description 1
- LRPVVAOGGZFVFO-UHFFFAOYSA-N 1,5,9-trimethyl-1,5,9-triazacyclododecane Chemical compound CN1CCCN(C)CCCN(C)CCC1 LRPVVAOGGZFVFO-UHFFFAOYSA-N 0.000 description 1
- CYNYIHKIEHGYOZ-UHFFFAOYSA-N 1-bromopropane Chemical compound CCCBr CYNYIHKIEHGYOZ-UHFFFAOYSA-N 0.000 description 1
- BYLAWYTWAYOBDP-UHFFFAOYSA-N 1-chlorobutane Chemical compound [CH2]CCCCl BYLAWYTWAYOBDP-UHFFFAOYSA-N 0.000 description 1
- UUFQTNFCRMXOAE-UHFFFAOYSA-N 1-methylmethylene Chemical compound C[CH] UUFQTNFCRMXOAE-UHFFFAOYSA-N 0.000 description 1
- 238000005160 1H NMR spectroscopy Methods 0.000 description 1
- WURBRXPDUPECQX-UHFFFAOYSA-N 2,2,6,6-tetramethyl-1-(1-phenylethoxy)piperidine Chemical compound C=1C=CC=CC=1C(C)ON1C(C)(C)CCCC1(C)C WURBRXPDUPECQX-UHFFFAOYSA-N 0.000 description 1
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical compound N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 1
- GEPIUTWNBHBHIO-UHFFFAOYSA-N 3-carboxy-PROXYL Chemical compound CC1(C)CC(C(O)=O)C(C)(C)N1[O] GEPIUTWNBHBHIO-UHFFFAOYSA-N 0.000 description 1
- 238000004679 31P NMR spectroscopy Methods 0.000 description 1
- BLDQUHPMDSICNF-UHFFFAOYSA-N 4-nonan-5-yl-2-(4-nonan-5-ylpyridin-2-yl)pyridine Chemical compound CCCCC(CCCC)C1=CC=NC(C=2N=CC=C(C=2)C(CCCC)CCCC)=C1 BLDQUHPMDSICNF-UHFFFAOYSA-N 0.000 description 1
- WSGDRFHJFJRSFY-UHFFFAOYSA-N 4-oxo-TEMPO Chemical compound CC1(C)CC(=O)CC(C)(C)N1[O] WSGDRFHJFJRSFY-UHFFFAOYSA-N 0.000 description 1
- OZAIFHULBGXAKX-VAWYXSNFSA-N AIBN Substances N#CC(C)(C)\N=N\C(C)(C)C#N OZAIFHULBGXAKX-VAWYXSNFSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- 239000004342 Benzoyl peroxide Substances 0.000 description 1
- OMPJBNCRMGITSC-UHFFFAOYSA-N Benzoylperoxide Chemical compound C=1C=CC=CC=1C(=O)OOC(=O)C1=CC=CC=C1 OMPJBNCRMGITSC-UHFFFAOYSA-N 0.000 description 1
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical compound [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 1
- KZBUYRJDOAKODT-UHFFFAOYSA-N Chlorine Chemical compound ClCl KZBUYRJDOAKODT-UHFFFAOYSA-N 0.000 description 1
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical class S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- RAXXELZNTBOGNW-UHFFFAOYSA-O Imidazolium Chemical compound C1=C[NH+]=CN1 RAXXELZNTBOGNW-UHFFFAOYSA-O 0.000 description 1
- KWYHDKDOAIKMQN-UHFFFAOYSA-N N,N,N',N'-tetramethylethylenediamine Chemical compound CN(C)CCN(C)C KWYHDKDOAIKMQN-UHFFFAOYSA-N 0.000 description 1
- 238000004639 Schlenk technique Methods 0.000 description 1
- QYTDEUPAUMOIOP-UHFFFAOYSA-N TEMPO Chemical group CC1(C)CCCC(C)(C)N1[O] QYTDEUPAUMOIOP-UHFFFAOYSA-N 0.000 description 1
- BZHJMEDXRYGGRV-UHFFFAOYSA-N Vinyl chloride Chemical compound ClC=C BZHJMEDXRYGGRV-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 150000001336 alkenes Chemical class 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 229910052787 antimony Inorganic materials 0.000 description 1
- WATWJIUSRGPENY-UHFFFAOYSA-N antimony atom Chemical compound [Sb] WATWJIUSRGPENY-UHFFFAOYSA-N 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000002635 aromatic organic solvent Substances 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 235000019400 benzoyl peroxide Nutrition 0.000 description 1
- 229910052796 boron Inorganic materials 0.000 description 1
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 239000007810 chemical reaction solvent Substances 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- ARUVKPQLZAKDPS-UHFFFAOYSA-L copper(II) sulfate Chemical compound [Cu+2].[O-][S+2]([O-])([O-])[O-] ARUVKPQLZAKDPS-UHFFFAOYSA-L 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 150000001993 dienes Chemical class 0.000 description 1
- VVRKSAMWBNJDTH-UHFFFAOYSA-N difluorophosphane Chemical compound FPF VVRKSAMWBNJDTH-UHFFFAOYSA-N 0.000 description 1
- AASUFOVSZUIILF-UHFFFAOYSA-N diphenylmethanone;sodium Chemical compound [Na].C=1C=CC=CC=1C(=O)C1=CC=CC=C1 AASUFOVSZUIILF-UHFFFAOYSA-N 0.000 description 1
- 239000003480 eluent Substances 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 229910052733 gallium Inorganic materials 0.000 description 1
- 229910052732 germanium Inorganic materials 0.000 description 1
- ZRALSGWEFCBTJO-UHFFFAOYSA-O guanidinium Chemical compound NC(N)=[NH2+] ZRALSGWEFCBTJO-UHFFFAOYSA-O 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 150000002443 hydroxylamines Chemical class 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 1
- 235000019341 magnesium sulphate Nutrition 0.000 description 1
- 125000005395 methacrylic acid group Chemical group 0.000 description 1
- VMGSQCIDWAUGLQ-UHFFFAOYSA-N n',n'-bis[2-(dimethylamino)ethyl]-n,n-dimethylethane-1,2-diamine Chemical compound CN(C)CCN(CCN(C)C)CCN(C)C VMGSQCIDWAUGLQ-UHFFFAOYSA-N 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 1
- 238000006053 organic reaction Methods 0.000 description 1
- 125000002734 organomagnesium group Chemical group 0.000 description 1
- 150000002902 organometallic compounds Chemical class 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- XYFCBTPGUUZFHI-UHFFFAOYSA-O phosphonium Chemical compound [PH4+] XYFCBTPGUUZFHI-UHFFFAOYSA-O 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 238000001637 plasma atomic emission spectroscopy Methods 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 230000000135 prohibitive effect Effects 0.000 description 1
- JUJWROOIHBZHMG-UHFFFAOYSA-O pyridinium Chemical compound C1=CC=[NH+]C=C1 JUJWROOIHBZHMG-UHFFFAOYSA-O 0.000 description 1
- 238000007342 radical addition reaction Methods 0.000 description 1
- 239000007870 radical polymerization initiator Substances 0.000 description 1
- 239000011833 salt mixture Substances 0.000 description 1
- 229940116351 sebacate Drugs 0.000 description 1
- CXMXRPHRNRROMY-UHFFFAOYSA-L sebacate(2-) Chemical compound [O-]C(=O)CCCCCCCCC([O-])=O CXMXRPHRNRROMY-UHFFFAOYSA-L 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 150000003440 styrenes Chemical class 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 1
- 125000004434 sulfur atom Chemical group 0.000 description 1
- 238000011282 treatment Methods 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D295/00—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms
- C07D295/22—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with hetero atoms directly attached to ring nitrogen atoms
- C07D295/24—Oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C239/00—Compounds containing nitrogen-to-halogen bonds; Hydroxylamino compounds or ethers or esters thereof
- C07C239/08—Hydroxylamino compounds or their ethers or esters
- C07C239/20—Hydroxylamino compounds or their ethers or esters having oxygen atoms of hydroxylamino groups etherified
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/38—Phosphonic acids [RP(=O)(OH)2]; Thiophosphonic acids ; [RP(=X1)(X2H)2(X1, X2 are each independently O, S or Se)]
- C07F9/40—Esters thereof
- C07F9/4003—Esters thereof the acid moiety containing a substituent or a structure which is considered as characteristic
- C07F9/4006—Esters of acyclic acids which can have further substituents on alkyl
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/54—Improvements relating to the production of bulk chemicals using solvents, e.g. supercritical solvents or ionic liquids
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
L'invention concerne un procédé de préparation d'alcoxyamines en milieu biphasique. Ce procédé consiste à mélanger un liquide ionique, un solvant organique, un sel métallique, un ligand du métal, un composé halogéno-carboné ZX et un nitroxyde, à maintenir le milieu réactionnel sous agitation à une température comprise entre 20degreC et 90degreC, jusqu'à disparition du nitroxyde, à décanter, à récupérer la phase organique, à la laver éventuellement avec de l'eau puis à isoler l'alcoxyamine par évaporation du solvant organique sous pression réduite.
Description
<Desc/Clms Page number 1>
PROCEDE DE PREPARATION
D'ALCOXYAMINES A PARTIR DE NITROXYDES La présente invention a pour objet un procédé de préparation
d'hydroxylamines oc,(3,j3-trisubstituées, ci-après désignées par alcoxyamines, obtenues à partir de nitroxydes, utilisables notamment comme amorceurs des polymérisations radicalaires. L'utilisation des alcoxyamines telles que celles dérivées du (2,2,6,6-tétraméthylpipéridinyl)-N-oxyde (TEMPO) dans la préparation des macromolécules a donné lieu à de nombreuses publications.
D'ALCOXYAMINES A PARTIR DE NITROXYDES La présente invention a pour objet un procédé de préparation
d'hydroxylamines oc,(3,j3-trisubstituées, ci-après désignées par alcoxyamines, obtenues à partir de nitroxydes, utilisables notamment comme amorceurs des polymérisations radicalaires. L'utilisation des alcoxyamines telles que celles dérivées du (2,2,6,6-tétraméthylpipéridinyl)-N-oxyde (TEMPO) dans la préparation des macromolécules a donné lieu à de nombreuses publications.
Ainsi, Hawker C. J. et coll. (Macromolécules 1996,29, pages 5245-5254) ont montré que l'utilisation d'alcoxyamines dérivées du
TEMPO telles que le (2',2',6',6'-tétraméthyl-1'-pipéridinyloxy)méthyl- benzène comme amorceurs de polymérisation radicalaire du styrène permettait de contrôler la polymérisation et d'accéder à des polymères bien définis avec de bas indices de polydispersité et ils ont constaté que les vitesses de polymérisation étaient sensiblement équivalentes aux vitesses obtenues lorsqu'ils utilisaient des amorceurs classiques tels que l'AIBN ou le peroxyde de benzoyle en présence de TEMPO.
TEMPO telles que le (2',2',6',6'-tétraméthyl-1'-pipéridinyloxy)méthyl- benzène comme amorceurs de polymérisation radicalaire du styrène permettait de contrôler la polymérisation et d'accéder à des polymères bien définis avec de bas indices de polydispersité et ils ont constaté que les vitesses de polymérisation étaient sensiblement équivalentes aux vitesses obtenues lorsqu'ils utilisaient des amorceurs classiques tels que l'AIBN ou le peroxyde de benzoyle en présence de TEMPO.
Les alcoxyamines peuvent être préparées selon des méthodes connues dans la littérature. La méthode la plus courante implique le couplage d'un radical carboné avec un radical nitroxyde.
une alcoxyamine, Y1, y2@ y3, Y4, y5@ y6@ Z étant définis plus loin, le radical carboné Z@ peut être généré par différentes méthodes décrites dans la littérature : décomposition d'un composé azoïque, abstraction d'un atome d'hydrogène sur un substrat approprié, addition d'un radical sur une oléfine. Le radical Z@ peut également être généré à partir d'un composé organométallique comme un organomagnésien Z-MgX tel que décrit par Hawker C. J. et coll. dans Macromolécules 1996,29, 5245- 5254 ou à partir d'un dérivé halogéné Z-X en présence d'un système organométallique comme CuX/bipyridine (X = Cl ou Br) selon une réaction
<Desc/Clms Page number 2>
de type ATRA (Atom Transfer Radical Addition) telle que décrit par Dorota Greszta et coll. dans Macromolecules 1996,29, 7661-7670.
Une des méthodes les plus utilisées pour la préparation des alcoxyamines (I) est la méthode mettant en jeu la réaction ATRA.
Cette méthode consiste à transférer un atome ou un groupe d'atomes sur une autre molécule en présence d'un système organométallique CuX/bipyridine, en milieu solvant selon le schéma :
De préférence, X dans le système organométallique représente un atome de brome, de chlore ou d'iode.
Le mode opératoire généralement utilisé consiste à mettre en solution le système organométallique tel que CuBr/bipyridine dans un solvant organique de préférence aromatique tel que le benzène ou le toluène, puis à introduire dans la solution le composé ZX et le nitroxyde (II).
Cette façon d'opérer présente l'inconvénient majeur de nécessiter des durées de réactions longues, rédhibitoires pour une préparation industrielle d'alcoxyamines ou d'utiliser un large excès d'un des réactifs.
En outre, l'élimination du métal résiduel des produits obtenus est difficile, nécessitant des opérations coûteuses de purification telles que le passage des produits sur colonne de silice.
Ainsi, par exemple Matyjaszewski K. et coll. dans la demande de brevet internationale WO 98/40415 obtiennent le 1-(2,2,6,6tétraméthylpipéridinyloxy)-1-phényléthane avec un rendement de 69 %
<Desc/Clms Page number 3>
après purification par chromatographie sur colonne en faisant réagir pendant 2 heures à 90 C le TEMPO et le (1-bromoéthyl)benzène selon un rapport molaire TEMPO/(1-bromoéthyl)benzène égal à 2 (soit un excès molaire de TEMPO égal à 100 %), en présence d'un système organométallique [4,4'-di(5-nonyl)2,2'-bipyridine/ Cu (OTf)2/Cu ].
On a maintenant trouvé un procédé de préparation d'alcoxyamines de formule :
à partir de nitroxydes :
ledit procédé consistant à faire réagir ledit nitroxyde (II) avec un composé halogénocarboné ZX dans lequel X représente un atome de chlore, de brome ou d'iode, en présence d'un système organométallique MAn (L)y (III) dans lequel :
M représente un métal de transition à un degré d'oxydation n tel qu'il puisse participer à une réaction rédox avec l'atome ou le groupe transférable,
A représente un atome d'halogène, un groupement carboxylate ou un groupement triflate,
L représente un ligand du métal M, y est égal à 1, 2 ou 3, n est égal à 1 ou 2, selon le schéma :
ledit procédé étant caractérisé en ce que l'on opère dans un milieu
à partir de nitroxydes :
ledit procédé consistant à faire réagir ledit nitroxyde (II) avec un composé halogénocarboné ZX dans lequel X représente un atome de chlore, de brome ou d'iode, en présence d'un système organométallique MAn (L)y (III) dans lequel :
M représente un métal de transition à un degré d'oxydation n tel qu'il puisse participer à une réaction rédox avec l'atome ou le groupe transférable,
A représente un atome d'halogène, un groupement carboxylate ou un groupement triflate,
L représente un ligand du métal M, y est égal à 1, 2 ou 3, n est égal à 1 ou 2, selon le schéma :
ledit procédé étant caractérisé en ce que l'on opère dans un milieu
<Desc/Clms Page number 4>
biphasique comprenant au moins un liquide ionique et un solvant organique non miscible avec ledit liquide ionique.
Le procédé selon l'invention consiste à effectuer les étapes suivantes : a) on mélange sous agitation un sel métallique MAn, éventuellement un métal M au degré d'oxydation zéro, un ligand L, au moins un liquide ionique, un solvant organique, le composé halogénocarboné ZX et le nitroxyde (II) selon un rapport molaire ZX/nitroxyde (II) allant de 1 à
1,5 et, de préférence voisin de 1 ; b) on maintient le milieu réactionnel sous agitation à une température comprise entre 20 C et 90 C et, de préférence, à une température allant de 20 C à 35 C jusqu'à disparition complète du nitroxyde (II) ; puis c) on arrête l'agitation, on décante, on récupère la phase organique qui est éventuellement lavée à l'eau puis, d) on isole l'alcoxyamine (1) de la phase organique par évaporation du solvant organique sous pression réduite, et e) éventuellement, la phase liquide ionique est recyclée au moins une fois avec régénération de l'espèce active du métal M(Mn).
1,5 et, de préférence voisin de 1 ; b) on maintient le milieu réactionnel sous agitation à une température comprise entre 20 C et 90 C et, de préférence, à une température allant de 20 C à 35 C jusqu'à disparition complète du nitroxyde (II) ; puis c) on arrête l'agitation, on décante, on récupère la phase organique qui est éventuellement lavée à l'eau puis, d) on isole l'alcoxyamine (1) de la phase organique par évaporation du solvant organique sous pression réduite, et e) éventuellement, la phase liquide ionique est recyclée au moins une fois avec régénération de l'espèce active du métal M(Mn).
Selon la présente invention, le nombre de recyclages de la phase liquide ionique n'est pas limitatif. De préférence, on recyclera la phase liquide ionique un nombre de fois allant de 1 à 10.
Selon la présente invention, on désigne par liquides ioniques des sels organiques liquides aux températures de réaction.
A titre d'illustration de sels organiques utilisables selon la présente invention, on citera les sels d'ammonium, de pyridinium, d'imidazolium, de triazolium, de guanidinium, de phosphonium ou de sulfonium. L'anion peut être entre autres un halogénure comme Ci, Br-, I- un halogénure d'étain comme SnCl3-, un halogénure de germanium comme GeCl3-, un halogénure de gallium comme GaCl3-, un halogénure
d'aluminium comme AIC14-, AI2CI7", A13CIlo-, un halogénure de métal de transition comme CuCl2-, un fluorure de bore, d'antimoine ou de phosphore comme BF4, SbF6ou PF6-, un carboxylate comme CF3CO2-, un
sulfonate comme CF3S03 ou FS03-, un amidure comme (CF 3S02)2N-, un tétralkyl- ou tétraarylborure comme B(C6F5)4. Le cation et l'anion du sel ou du mélange de sels seront choisi de façon appropriée pour avoir un liquide à température de réaction. Eventuellement, le liquide ionique pourra contenir de l'eau. Selon la présente invention, on utilisera de
d'aluminium comme AIC14-, AI2CI7", A13CIlo-, un halogénure de métal de transition comme CuCl2-, un fluorure de bore, d'antimoine ou de phosphore comme BF4, SbF6ou PF6-, un carboxylate comme CF3CO2-, un
sulfonate comme CF3S03 ou FS03-, un amidure comme (CF 3S02)2N-, un tétralkyl- ou tétraarylborure comme B(C6F5)4. Le cation et l'anion du sel ou du mélange de sels seront choisi de façon appropriée pour avoir un liquide à température de réaction. Eventuellement, le liquide ionique pourra contenir de l'eau. Selon la présente invention, on utilisera de
<Desc/Clms Page number 5>
préférence les sels de N,N'-dialkylimidazolium. Comme exemple de tels sels, on citera : - le chlorure de 1-butyl-3-méthylimidazolium, le chlorure de 1-propyl-3-méthylimidazolium, - le bromure de 1-propyl-3-méthylimidazolium.
Le solvant organique est choisi de façon à avoir un système biphasique avec le (ou les) liquide(s) ionique (s). De préférence, le solvant organique sera choisi parmi les hydrocarbures aliphatiques ou aromatiques, ou bien parmi les éthers. On utilisera tout particulièrement le toluène.
Selon la présente invention, M représente de préférence Cu(l), Fe(II), Ni%'11) et, tout particulièrement Cu(l).
L'espèce active du métal M, ci-après Mn, est générée à partir d'un sel métallique, de préférence un halogénure métallique MnXn. Elle peut également être générée in situ selon une réaction redox de type :
dans laquelle l'exposant du métal M représente le degré d'oxydation dudit métal, M représente le métal M au degré d'oxydation zéro et n = 1 ou 2.
dans laquelle l'exposant du métal M représente le degré d'oxydation dudit métal, M représente le métal M au degré d'oxydation zéro et n = 1 ou 2.
Globalement, le ratio Mn/RX doit être au moins égal à 1.
L'halogénure métallique préféré est CuBr.
De préférence, A représente un halogène tel que CI ou Br, un groupement carboxylate tel qu'acétate ou un groupement triflate et X représente un atome de chlore ou un atome de brome.
Selon la présente invention, le ligand L qui coordine le métal M peut contenir un ou plusieurs atomes d'azote, de phosphore, d'oxygène ou de soufre. Les ligands préférés sont les polyamines linéaires représentés par la formule générale (IV) :
dans laquelle R1, R2, R3 et R4, identiques ou différents, représentent un atome d'hydrogène, un groupe alkyle, linéaire ou ramifié ayant un
dans laquelle R1, R2, R3 et R4, identiques ou différents, représentent un atome d'hydrogène, un groupe alkyle, linéaire ou ramifié ayant un
<Desc/Clms Page number 6>
nombre d'atomes de carbone allant de 1 à 10 et, de préférence allant de 1 à 4, R5 représente un atome d'hydrogène, un groupe alkyle, linéaire ou ramifié, ayant un nombre d'atome de carbone allant de 1 à 10 et, de préférence, allant de 1 à 4, un reste
dans lequel R6 et R7 ont les mêmes significations que R5, ou bien encore au moins deux des radicaux R1, R2, R3, R4 et R5 peuvent être liés entre eux pour former un cycle ; m, p et q, identiques ou différents, représentent des nombres entiers allant de 1 à 4 et, de préférence, égaux à 2, x allant de 0 à 4.
dans lequel R6 et R7 ont les mêmes significations que R5, ou bien encore au moins deux des radicaux R1, R2, R3, R4 et R5 peuvent être liés entre eux pour former un cycle ; m, p et q, identiques ou différents, représentent des nombres entiers allant de 1 à 4 et, de préférence, égaux à 2, x allant de 0 à 4.
A titre d'illustration de ligands L représentés par la formule (IV), on citera : - la tris[2-(diméthylamino)éthyl]amine :
- la N, N, N', N', N" - pentaméthyldiéthylènetriamine (PMDETA) :
- la N,N,N',N'-tétraméthyléthylènediamine :
- la 1,1, 4,7, 10, 10-hexaméthyltriéthylènetétramine (HMTETA) :
- la N, N, N', N', N" - pentaméthyldiéthylènetriamine (PMDETA) :
- la N,N,N',N'-tétraméthyléthylènediamine :
- la 1,1, 4,7, 10, 10-hexaméthyltriéthylènetétramine (HMTETA) :
<Desc/Clms Page number 7>
- la N,N-diméthyldipropylènetriamine (DMAPAPA) :
les polyamines cycliques telles que : - le 1,4,7-triméthyl-1,4,7-triazacyclononane, - le 1,5,9-triméthyl-1,5,9-triazacyclododécane,
- le 1,4,8,11-tétraméthyl-1,4,8,11-tétraazacyclotétradécane.
les polyamines cycliques telles que : - le 1,4,7-triméthyl-1,4,7-triazacyclononane, - le 1,5,9-triméthyl-1,5,9-triazacyclododécane,
- le 1,4,8,11-tétraméthyl-1,4,8,11-tétraazacyclotétradécane.
On utilisera de préférence la PMDETA et la DMAPAPA.
Le ligand L tel que défini précédemment est utilisé selon un rapport (molaire) L/Mn allant de 0,2 à 4 et, de préférence allant de 0,4 à 2.
Le procédé selon l'invention consiste donc à mélanger sous forte agitation au moins un liquide ionique avec un sel métallique, un ligand L, le composé à atomes ou groupes transférables RX, le nitroxyde Il et éventuellement le métal M au degré d'oxydation zéro et un solvant organique.
La réaction est conduite à une température comprise entre 20 C et 90 C, et de préférence voisine de la température ambiante. On opère sous atmosphère de gaz inerte tel que l'azote ou l'argon et de préférence à pression atmosphérique.
La fin de réaction peut être contrôlée par disparition des réactifs par des méthodes chromatographiques (CPG, HPLC, CCM). La réaction terminée, le mélange réactionnel est décanté. La phase organique est récupérée. La phase liquide ionique peut être éventuellement extraite avec le solvant organique de réaction. Les alcoxyamines (I) sont récupérées par des traitements classiques de la phase organique comme des lavages à l'eau suivis d'une évaporation du solvant. Les alcoxyamines (I) peuvent être caractérisées par analyse élémentaire, HPLC, IR et RMN.
Selon la présente invention, la phase liquide ionique peut être réutilisée pour une nouvelle réaction d'ATRA. La régénération du système organométallique peut être effectuée selon deux variantes.
Selon une première variante, la phase liquide ionique contenant le système organométallique peut être traitée avec le métal concerné au degré d'oxydation 0. La quantité de M rajoutée est comprise entre 0,5
<Desc/Clms Page number 8>
et 2 équivalents par rapport au composé RX engagé initialement, de préférence voisine de 1 équivalent. La régénération de l'espèce active de métal Mn peut être effectuée à une température comprise entre 20 C et 90 C, de préférence entre 20 C et 60 C, sur une durée comprise entre 0,5 et 3 heures. La phase liquide ionique peut ensuite être ainsi réutilisée pour une nouvelle réaction d'ATRA en rajoutant simplement le composé RX, le nitroxyde et le solvant organique et en procédant comme décrit précédemment. Ces cycles réaction/régénération du système organométallique peuvent être effectués plusieurs fois.
Selon une seconde variante, la régénération du système organométallique consiste à rajouter simultanément à la phase liquide ionique le composé RX, le nitroxyde, le solvant organique et le métal au degré d'oxydation 0 dans les proportions adéquates. La régénération s'effectue ainsi in situ et la réaction (d'ATRA) peut se produire comme décrit précédemment. Cette procédure peut également être répétée plusieurs fois.
Ainsi, un des avantages de la présente invention est que le système organométallique peut être régénéré sur plusieurs cycles sans rajout de sel métallique et de ligand. Ceci permet de réduire le coût du procédé en augmentant la productivité en alcoxyamine par rapport aux quantités de sel métallique et de ligand utilisées en système homogène.
En outre, le procédé selon l'invention présente l'avantage d'être réalisé avec des ligands disponibles dans le commerce. La réaction entre le nitroxyde (II) et le composé halogénocarboné ZX est rapide.
Le procédé selon l'invention permet d'obtenir des alcoxyamines exemptes quasiment de métal M. Les alcoxyamines obtenues selon le procédé de l'invention, présente une teneur en métal M inférieure à 10 ppm.
Les alcoxyamines sont ainsi obtenues avec des rendements élevés par un procédé facile à mettre en #uvre et ne nécessitant pas d'opération coûteuse de purification.
Le procédé selon l'invention s'applique tout particulièrement à la préparation des alcoxyamines de formule :
<Desc/Clms Page number 9>
à partir de nitroxydes de formule :
dans les formules desquelles les groupes Y1 à Y6, identiques ou différents, représentent un atome d'hydrogène, un radical alkyle, linéaire ou ramifié, ayant un nombre d'atomes de carbone allant de 1 à 10, un radical cycloalkyle ayant un nombre d'atomes de carbone allant de 3 à 20, un atome d'halogène, un radical cyano, un radical phényle, un radical hydroxyalkyle ayant un nombre d'atomes de carbone allant de 1 à 4, un radical dialcoxyphosphonyle, diphénoxyphosphonyle, un radical alcoxycarbonyle, alcoxycarbonylalkyle, ou bien 2 ou plus des groupes Y1 à Y6 peuvent être liés avec l'atome de carbone qui les porte pour former des structures cycliques, lesquelles peuvent comprendre une ou plusieurs fonctions extracycliques, choisis parmi : HO-, CH3C(O)-, alkyl -C(O)O - ou le radical alkyle, linéaire ou ramifié, à un nombre d'atomes de carbone allant de 1 à 30, CH30-, H2N-CH3C(O)NH-, (CH3)2N- ; ou bien encore peuvent comprendre 1 ou plusieurs hétéroatomes extra- ou intracyliques tels que 0, N ;
Z est un reste de formule
dans laquelle W1, W2 et W3, identiques ou différents, représentent un atome d'hydrogène, un radical alkyle, linéaire ou ramifié, ayant un nombre d'atomes de carbone allant de 1 à 10 , un radical phényle, un radical benzyle, un radical cyano, un radical cycloalkyle ayant un nombre d'atomes de carbone allant de 3 à 12 ; unradical -(CH2)r C(O)OW4 dans lequel W4 représente un alkyle, linéaire ou ramifié, ayant un nombre d'atomes de carbone allant de 1 à 6 , r=0 à 6 ;
X représente un atome de chlore, de brome ou d'iode,
dans les formules desquelles les groupes Y1 à Y6, identiques ou différents, représentent un atome d'hydrogène, un radical alkyle, linéaire ou ramifié, ayant un nombre d'atomes de carbone allant de 1 à 10, un radical cycloalkyle ayant un nombre d'atomes de carbone allant de 3 à 20, un atome d'halogène, un radical cyano, un radical phényle, un radical hydroxyalkyle ayant un nombre d'atomes de carbone allant de 1 à 4, un radical dialcoxyphosphonyle, diphénoxyphosphonyle, un radical alcoxycarbonyle, alcoxycarbonylalkyle, ou bien 2 ou plus des groupes Y1 à Y6 peuvent être liés avec l'atome de carbone qui les porte pour former des structures cycliques, lesquelles peuvent comprendre une ou plusieurs fonctions extracycliques, choisis parmi : HO-, CH3C(O)-, alkyl -C(O)O - ou le radical alkyle, linéaire ou ramifié, à un nombre d'atomes de carbone allant de 1 à 30, CH30-, H2N-CH3C(O)NH-, (CH3)2N- ; ou bien encore peuvent comprendre 1 ou plusieurs hétéroatomes extra- ou intracyliques tels que 0, N ;
Z est un reste de formule
dans laquelle W1, W2 et W3, identiques ou différents, représentent un atome d'hydrogène, un radical alkyle, linéaire ou ramifié, ayant un nombre d'atomes de carbone allant de 1 à 10 , un radical phényle, un radical benzyle, un radical cyano, un radical cycloalkyle ayant un nombre d'atomes de carbone allant de 3 à 12 ; unradical -(CH2)r C(O)OW4 dans lequel W4 représente un alkyle, linéaire ou ramifié, ayant un nombre d'atomes de carbone allant de 1 à 6 , r=0 à 6 ;
X représente un atome de chlore, de brome ou d'iode,
<Desc/Clms Page number 10>
A titre d'illustration de nitroxydes (II) utilisables selon la présente invention, on citera : - le 2,2,5,5 tétraméthyl-1-pyrrolidinyloxy (généralement commercialisé sous la marque PROXYL) ; - le 3-carboxy-2,2,5,5-tétraméthyl-pyrrolidinyloxy (communément appelé 3-carboxy PROXYL) ; - le 2,2,6,6-tétraméthyl-1-pipéridinyloxy (communément appelé TEMPO) ; - le 4-hydroxy-2,2,6,6-tétraméthyl-1-pipéridinyloxy (communément appelé le 4-hydroxy-TEMPO) ; - le 4-méthoxy-2,2,6,6-tétraméthyl-1-pipéridinyloxy (communément appelé le 4-méthoxy-TEMPO) ; - le 4-oxo-2,2,6,6-tétraméthyl-1-pipéridinyloxy (communément appelé le 4-oxo-TEMPO) ; - le 4-amino-2,2,6,6-tétraméthyl-1-pipéridinyloxy (communément appelé le 4-amino-TEMPO) ; - le 4-acétamido-2,2,6,6-tétraméthyl-1-pipéridinyloxy (communément appelé le 4-acétamido-TEMPO) ; - le 4-stéaryloxy-2,2,6,6-tétraméthyl-1-pipéridinyloxy (communément appelé le 4-stéaryloxy-TEMPO) ; - le N-tertiobutyl-1-phényl-2-méthylpropyl nitroxyde, - le N-(2-hydroxyméthylpropyl)-1-phényl-2-méthylpropylnitroxyde),
- le N-fiertiobutyl-1-diéthylphosphono-2,2-diméthyl-propylnitroxyde, - le N-tertiobutyl-1-dibenzylphosphono-2,2diméthylpropylnitroxyde, - le N-tertiobutyl-1-di(2,2,2-trifluoroéthyl)phosphono-2,2diméthylpropylnitroxyde, - le N-tertiobutyl-[(1-diéthylphosphono)-2-méthylpropyl]nitroxyde, - le N-( 1-méthyléthyl)-1-cyclohexyl-1-(diéthyl-phosphono)nitroxyde,
- le N-( 1 -phényl benzyl)-[ ( 1-diéthyl phosphono )-1 -méthyléthyl] nitroxyde : - le N-phényl-1-diéthylphosphono-2,2-diméthylpropylnitroxyde, - le N-phényl-1-diéthylphosphono-1-rriéthyléthylnitroxyde, - le N-(1 -phényl2-méthylpropyl)-1 -diéthylphosphonméthyléthylnitroxyde, - le bis-1-oxyl-2,2,6,6-tétraméthylpipéridine-4-yl)sébaçate commercialisé sous la marque "CXA 5415" par la Société CIBA SPEC. CHEM.
- le N-fiertiobutyl-1-diéthylphosphono-2,2-diméthyl-propylnitroxyde, - le N-tertiobutyl-1-dibenzylphosphono-2,2diméthylpropylnitroxyde, - le N-tertiobutyl-1-di(2,2,2-trifluoroéthyl)phosphono-2,2diméthylpropylnitroxyde, - le N-tertiobutyl-[(1-diéthylphosphono)-2-méthylpropyl]nitroxyde, - le N-( 1-méthyléthyl)-1-cyclohexyl-1-(diéthyl-phosphono)nitroxyde,
- le N-( 1 -phényl benzyl)-[ ( 1-diéthyl phosphono )-1 -méthyléthyl] nitroxyde : - le N-phényl-1-diéthylphosphono-2,2-diméthylpropylnitroxyde, - le N-phényl-1-diéthylphosphono-1-rriéthyléthylnitroxyde, - le N-(1 -phényl2-méthylpropyl)-1 -diéthylphosphonméthyléthylnitroxyde, - le bis-1-oxyl-2,2,6,6-tétraméthylpipéridine-4-yl)sébaçate commercialisé sous la marque "CXA 5415" par la Société CIBA SPEC. CHEM.
A titre d'illustration de composés ZX utilisables, on citera les composés de formule : C6H5CH(CH3)Br, C6H5CH2Br, (CH3) 2C(CN)Br, CH30C(O)C(CH3)2Br, CH30C(O)CH(CH3)Br, C6F13I.
Les alcoxyamines de formule (I) obtenues selon le procédé de la présente invention peuvent être utilisées pour la polymérisation et la
<Desc/Clms Page number 11>
copolymérisation de tout monomère présentant une double liaison carbone-carbone susceptible de polymériser par voie radicalaire. La polymérisation ou la copolymérisation est réalisée dans les conditions habituelles connues de l'homme du métier compte tenu du ou des monomères considérés. Les monomères considérés peuvent être un monomère vinylaromatique (styrène, styrènes substitués), un diène, un monomère acrylique ou méthacrylique. Le monomère peut également être le chlorure de vinyle, le difluorure de vinylidène ou l'acrylonitrile.
Les exemples suivants illustrent l'invention.
EXEMPLES :
REMARQUES GENERALES
Les essais ont été réalisés sous atmosphère de gaz inerte (argon ou azote) en employant des techniques de Schlenk (standard).
REMARQUES GENERALES
Les essais ont été réalisés sous atmosphère de gaz inerte (argon ou azote) en employant des techniques de Schlenk (standard).
Le 1-bromoéthylbenzène et le N-tertobutyl-1-diéthylphosphono- 2,2-diméthylpropylnitroxyde (DEPN) sont préalablement dégazés.
Le solvant utilisé est le toluène qui est préalablement distillé sous argon sur sodium-benzophénone.
Les ligands utilisés sont : - la N,N,N',N',N"-pentaméthyldiéthyldiéthylènetriamine désignée ci- après par PMDETA, - la bipyridine désignée ci-après par BIPY.
- Les alcoxyamines obtenues ont été caractérisées par RMN du 1H,
13C et 31P, et par analyse élémentaire.
13C et 31P, et par analyse élémentaire.
Les teneurs en cuivre résiduel ont été déterminées par la technique de spectroscopie d'émission atomique à plasma avec détection par spectrométrie de masse désignée ci-après ICP-MS (Inductively Coupled Plasma - Mass Spectrometry).
Préparation des liquides ioniques utilisés 1/ Synthèse du bromure de 1-propyl-3-méthylimidazolium
Dans un réacteur en verre de 1 I, on charge 450 g de 1bromopropane (3,66 mol). On chauffe à 70 C, puis sous agitation on coule goutte à goutte 200 g de 1-méthylimidazole (2,44 mol). On laisse réagir 1 h à 70 C. Après retour à température ambiante, on décante. La phase inférieure liquide ionique est récupérée, lavée au toluène (1x100 ml), puis évaporée sous vide. On obtient 475 g de bromure de 1-méthyl- 3-propylimidazolium sous forme de liquide jaune. Le produit est utilisé tel quel sans purification supplémentaire.
Dans un réacteur en verre de 1 I, on charge 450 g de 1bromopropane (3,66 mol). On chauffe à 70 C, puis sous agitation on coule goutte à goutte 200 g de 1-méthylimidazole (2,44 mol). On laisse réagir 1 h à 70 C. Après retour à température ambiante, on décante. La phase inférieure liquide ionique est récupérée, lavée au toluène (1x100 ml), puis évaporée sous vide. On obtient 475 g de bromure de 1-méthyl- 3-propylimidazolium sous forme de liquide jaune. Le produit est utilisé tel quel sans purification supplémentaire.
<Desc/Clms Page number 12>
2/ Synthèse du chlorure de 1-butyl-3-méthylïmidazolium
Dans un réacteur en verre de 1 I, on charge 251,4 g de 1chlorobutane (2,7 mol). On chauffe à 60 C, puis sous agitation on coule goutte à goutte 148,6 g de 1-méthylimidazole (1,8 mol). On laisse réagir 24 h à 80 C. Le mélange réactionnel est évaporé sous vide. On obtient 309 g de chlorure de 1-butyl-3-méthylimidazolium sous forme de solide jaunâtre (rendement = 98%). Le produit est utilisé tel quel sans purification supplémentaire.
Dans un réacteur en verre de 1 I, on charge 251,4 g de 1chlorobutane (2,7 mol). On chauffe à 60 C, puis sous agitation on coule goutte à goutte 148,6 g de 1-méthylimidazole (1,8 mol). On laisse réagir 24 h à 80 C. Le mélange réactionnel est évaporé sous vide. On obtient 309 g de chlorure de 1-butyl-3-méthylimidazolium sous forme de solide jaunâtre (rendement = 98%). Le produit est utilisé tel quel sans purification supplémentaire.
EXEMPLE 1 (non conforme à l'invention) PREPARATION DU N-TERTIOBUTYL, N-1-DIETHYLPHOSPHONO-2,2-DIMETHYLPROPYL, O-1-PHENYLETHYLHYDROXYLAMINE :
Dans un tube de Schlenk de 100 ml purgé à l'argon, on introduit 0,57 g de CuBr (4 mmol) et 1,25 g de BIPY (8 mmol) (rapport molaire BIPY/CuBr=2). On ajoute 0,74 g de (1-bromoéthyl)benzène (4 mmol) et 0,68 g de DEPN 86 % (2 mmol) dissous dans 9 ml de toluène anhydre.
Sous agitation, on laisse réagir pendant 48 heures à température ambiante. Le mélange réactionnel est filtré sur célite. Le filtrat est lavé avec une solution aqueuse à 5 % de sulfate de cuivre, puis à l'eau. La phase organique est séchée sur sulfate de magnésium, puis le solvant est évaporé. On obtient une huile verdâtre contenant du cuivre qui est purifiée par chromatographie sur colonne de silice en utilisant un éluant pentane/éther 6/4. On obtient 0,75 g de N-tertiobutyl, N-1diéthylphosphono-2, 2-diméthylpropyl-O-1-phényléthylhydroxylamine (rendement = 95 %) sous la forme de deux diastéréoisomères dans des proportions 64/36 déterminées sur le spectre 31P du mélange brut par intégration des signaux à 23,14 et 24,36 ppm (1/11 = 64/36).
Les résultats analytiques sont donnés ci-après :
Isomère 1
RMN 31P(CDCl3) : # 23,14
RMN 1 H(CDCI3) : Ô 0,88 (t,JH.H = 7,2Hz,3H) :
1,27 (m,21H) ; 1,55 (d, JH-H=6,6Hz,3H) (s, 9H) ; 3,40 (d,JH-p=26Hz, 1 H) ; 3,18-3,40 et 3,70-4,05 (m, 4H) ; (q, JH- H=6,6Hz, 1H) ; 7,24-7,47 (m,5H).
Isomère 1
RMN 31P(CDCl3) : # 23,14
RMN 1 H(CDCI3) : Ô 0,88 (t,JH.H = 7,2Hz,3H) :
1,27 (m,21H) ; 1,55 (d, JH-H=6,6Hz,3H) (s, 9H) ; 3,40 (d,JH-p=26Hz, 1 H) ; 3,18-3,40 et 3,70-4,05 (m, 4H) ; (q, JH- H=6,6Hz, 1H) ; 7,24-7,47 (m,5H).
<Desc/Clms Page number 13>
RMN 13C (CDCI3) : # 16,23 (2d,JC-P = 7Hz, CH3CH2), 21,18 (s,CH3CH), 28,19 (s,CH3-C-CH), 30,63 (d,Jc-p=7Hz, CH3-CN), 35,33
(d,J~p = 6Hz, C-CH-P), 58,58 (d, J~p = 7,5Hz, C-CH3), 61,4 (d,JC- p=7Hz, CH2-0), 70,06 (d, JC-P = 138,5 Hz, CH-P), 78,36 (s, CH-O), 127,33 (s,CH ar), 127,81 (s,CH ar), 127,88 (s,CH ar), 143,31 (s, Car).
(d,J~p = 6Hz, C-CH-P), 58,58 (d, J~p = 7,5Hz, C-CH3), 61,4 (d,JC- p=7Hz, CH2-0), 70,06 (d, JC-P = 138,5 Hz, CH-P), 78,36 (s, CH-O), 127,33 (s,CH ar), 127,81 (s,CH ar), 127,88 (s,CH ar), 143,31 (s, Car).
Microanalyse (C21H37NO4P) : % calculé C 63,12 ; 9,59 ; 3,51. % trouvé C 63,01 ; 9,60 ; N3,42.
Isomère Il :
RMN 31P (CDCI3) : # 24,36. RMN 1H (CDC13) : # 0,82 (s, 9H) ; 1,22 (s, 9H) ; 1,29 (t, JH-H 7,OHz , 3H) ; 1,32 (t, JH-H=7,OHz, 3H) ; 1,58 (d, JH-H = 6,7Hz, 3H) ; 3,32 (d, JH-P = 26,2Hz, 1H) ; 3,9-4,2 et 4,3- 4,4 (m, 4H) ; 4,97 (q,JH-H=6,8Hz, 1 H) ; 7,17-7,3 (m, 5H).
RMN 31P (CDCI3) : # 24,36. RMN 1H (CDC13) : # 0,82 (s, 9H) ; 1,22 (s, 9H) ; 1,29 (t, JH-H 7,OHz , 3H) ; 1,32 (t, JH-H=7,OHz, 3H) ; 1,58 (d, JH-H = 6,7Hz, 3H) ; 3,32 (d, JH-P = 26,2Hz, 1H) ; 3,9-4,2 et 4,3- 4,4 (m, 4H) ; 4,97 (q,JH-H=6,8Hz, 1 H) ; 7,17-7,3 (m, 5H).
RMN 13C (CDC13) : # 16,24 (d,Jc-p=7,1Hz, CH3CH2), 16,71 (d, JC-P = 5,2Hz, CH3CH2), 24,00 (s, CH3CH), 28,50 (s, CH3-C-CH), 30,12
(d, J~p=5,7Hz, CH3-C-N), 35,37 (d, J~p=5,8Hz, C-CH-p), 58,80 (d, J-p = 7,4Hz, CH2-0), 61,10 (s, C-N), 61,56 (d, J~p = 6Hz, CH2-0), 69,84 (d, JC-P = 138,4Hz, CH-P), 85,23 (s, CH-O), 126,96 (s, CH ar), 127,08 (s, CH ar), 127,95 (s, CH ar), 145,36 (s, C ar).
(d, J~p=5,7Hz, CH3-C-N), 35,37 (d, J~p=5,8Hz, C-CH-p), 58,80 (d, J-p = 7,4Hz, CH2-0), 61,10 (s, C-N), 61,56 (d, J~p = 6Hz, CH2-0), 69,84 (d, JC-P = 138,4Hz, CH-P), 85,23 (s, CH-O), 126,96 (s, CH ar), 127,08 (s, CH ar), 127,95 (s, CH ar), 145,36 (s, C ar).
Microanalyse (C21H37NO4P) : % calculé C 63,12 ; 9,59 ; N3,51. % trouvé C 63,05 ; 9,51 ; 3,50.
EXEMPLE 2 (conforme à l'invention) PREPARATION DU N-TERTIOBUTYL, N-1-DIETHYLPHOSPHONO-2,2-DIMETHYLPROPYL, 0-1-PHENYLETHYLHYDROXYLAMINE EN PRESENCE DE BROMURE DE 1-METHYL-3- PROPYLIMIDAZOLIUM :
Dans un réacteur de 250 ml muni d'une agitation à turbine tournant à 500 tr/min purgé à l'argon, on charge 3,3 g de CuBr (23 mmol), 1,6 g de PMDETA (9 mmol), 1,46 g de Cu(0) (23 mmol) et 32 g de 1-méthyl-3-propylimidazolium. On rajoute 4,3 g de (1- bromoéthyl)benzène (23 mmol) et 5,56 g de DEPN 90% (17 mmol) dissous dans 60 g de toluène dégazé. On laisse réagir sous agitation à température ambiante. La disparition du DEPN est suivie par CCM. Après 24 heures, le mélange réactionnel est décanté. La phase organique est récupérée et la phase liquide ionique est extraite avec 60 g de toluène. Les phases organiques rassemblées sont lavées à l'eau (2x60 g). Le solvant est évaporé pour donner 6,6 g de N-tertiobutyl, N-1- diéthylphosphono-2,2-diméthylpropyl, 0-1-phényléthylhydroxylamine sous forme d'huile incolore (rendement = 97%, pureté = 97%).
Dans un réacteur de 250 ml muni d'une agitation à turbine tournant à 500 tr/min purgé à l'argon, on charge 3,3 g de CuBr (23 mmol), 1,6 g de PMDETA (9 mmol), 1,46 g de Cu(0) (23 mmol) et 32 g de 1-méthyl-3-propylimidazolium. On rajoute 4,3 g de (1- bromoéthyl)benzène (23 mmol) et 5,56 g de DEPN 90% (17 mmol) dissous dans 60 g de toluène dégazé. On laisse réagir sous agitation à température ambiante. La disparition du DEPN est suivie par CCM. Après 24 heures, le mélange réactionnel est décanté. La phase organique est récupérée et la phase liquide ionique est extraite avec 60 g de toluène. Les phases organiques rassemblées sont lavées à l'eau (2x60 g). Le solvant est évaporé pour donner 6,6 g de N-tertiobutyl, N-1- diéthylphosphono-2,2-diméthylpropyl, 0-1-phényléthylhydroxylamine sous forme d'huile incolore (rendement = 97%, pureté = 97%).
La teneur en cuivre résiduel est inférieure à 10 ppm.
<Desc/Clms Page number 14>
La phase liquide ionique extraite est recyclée une première fois en lui ajoutant 1,46 g de Cu (23 mmol), 4,3 g de (1bromoéthyl)benzène (23 mmol), 5,56 g de DEPN 90% (17 mmol) dissous dans 60 g de toluène dégazé et on opère comme décrit comme précédemment. La phase liquide ionique extraite de ce premier recyclage est recyclée en lui ajoutant comme précédemment les mêmes réactifs et solvant en des quantités identiques. On effectue au total 4 recyclages.
<tb>
<tb> Rendement
<tb> Essai <SEP> Chargement <SEP> T <SEP> ( C) <SEP> t <SEP> (h) <SEP> (%)
<tb> 1 <SEP> a <SEP> 20 <SEP> 24 <SEP> 97
<tb> recyclage <SEP> 1 <SEP> b <SEP> 20 <SEP> 24 <SEP> 95
<tb> recyclage <SEP> 2 <SEP> b <SEP> 20 <SEP> 24 <SEP> 95
<tb> recyclage <SEP> 3 <SEP> b <SEP> 20 <SEP> 24 <SEP> 97
<tb> recyclage <SEP> 4 <SEP> b <SEP> 20 <SEP> 24 <SEP> 93
<tb>
<tb> Rendement
<tb> Essai <SEP> Chargement <SEP> T <SEP> ( C) <SEP> t <SEP> (h) <SEP> (%)
<tb> 1 <SEP> a <SEP> 20 <SEP> 24 <SEP> 97
<tb> recyclage <SEP> 1 <SEP> b <SEP> 20 <SEP> 24 <SEP> 95
<tb> recyclage <SEP> 2 <SEP> b <SEP> 20 <SEP> 24 <SEP> 95
<tb> recyclage <SEP> 3 <SEP> b <SEP> 20 <SEP> 24 <SEP> 97
<tb> recyclage <SEP> 4 <SEP> b <SEP> 20 <SEP> 24 <SEP> 93
<tb>
TABLEAU 1 chargement a : CuBr = 3,3 g ; PMDETA =1,6 g ; Cu = 1,46g ; (1bromoéthyl)benzène=4,3 g; DEPN 90%=5,6 g ; toluène=60 g; 1méthyl-3-propylimidazolium=32 g chargement b : Cu =1,46g ; (1-bromoéthyl)benzène=4,3 g; DEPN 90% = 5,6 g ; toluène = 60 g
Globalement, nous avons produit 32,4 g de N-tertiobutyl, N-1diéthylphosphono-2,2-diméthylpropyl, O-1-phényléthylhydroxylamine (81 mmol) pour 3,3 g de CuBr (23 mmol), 1,6 g de PMDETA (9 mmol) et 7,3 g de Cu (115 mmol).
Globalement, nous avons produit 32,4 g de N-tertiobutyl, N-1diéthylphosphono-2,2-diméthylpropyl, O-1-phényléthylhydroxylamine (81 mmol) pour 3,3 g de CuBr (23 mmol), 1,6 g de PMDETA (9 mmol) et 7,3 g de Cu (115 mmol).
PREPARATION DU N-TERTIOBUTYL, N-1-DIETHYLPHOSPHONO-2,2-DIMETHYLPROPYL, O-1-PHENYLETHYLHYDROXYLAMINE EN PRESENCE DE BROMURE DE 1-PROPYL-3METHYLIMIDAZOLIUM :
Dans cet exemple, la régénération de l'espèce active est effectuée préalablement à la réaction.
Dans cet exemple, la régénération de l'espèce active est effectuée préalablement à la réaction.
Dans un réacteur de 250 ml purgé à l'argon, on charge 3,3 g de CuBr (23 mmol), 4,0 g de PMDETA (23 mmol), 1,46 g de Cu (23 mmol) et 32 g de 1-méthyl-3-propylimidazolium. On rajoute 4,3 g de (1bromoéthyl)benzène (23 mmol) et 6,4 g de DEPN 92% (20 mmol) dissous dans 40 g de toluène dégazé. On laisse réagir 6 h sous agitation à 20 C. Le mélange réactionnel est décanté. La phase organique est
<Desc/Clms Page number 15>
récupérée, et la phase liquide ionique est extraite avec 20 g de toluène.
Les phases organiques rassemblées sont lavées à l'eau (2x40 g). Le solvant est évaporé pour donner 7,6 g de N-tertiobutyl, N-1diéthylphosphono-2,2-diméthylpropyl, O-1-phényléthylhydroxylamine sous forme d'huile incolore (rendement = 95%).
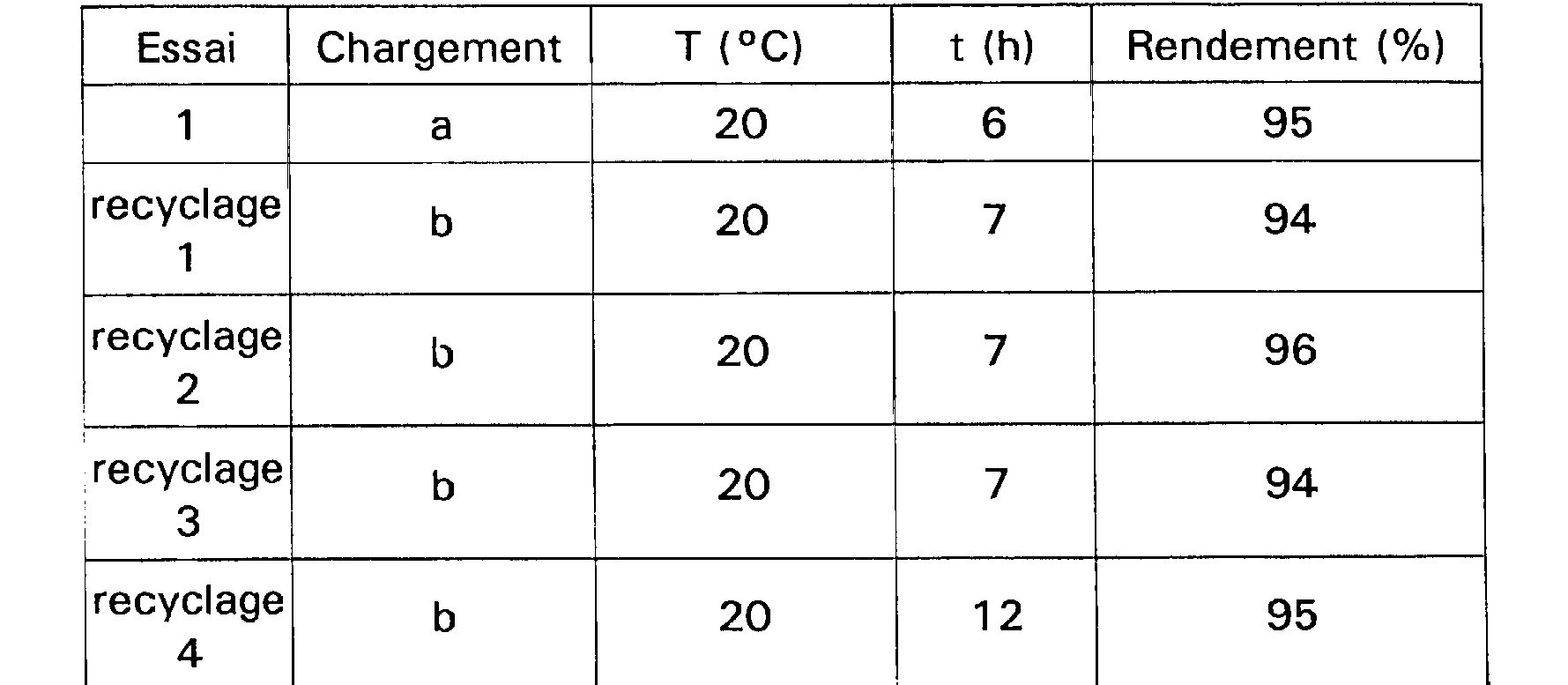
On rajoute ensuite à la phase liquide ionique extraite 1,46 g de Cu et 20 g de toluène, puis on chauffe 3 h à 60 C. Une nouvelle réaction peut alors être effectuée en rajoutant 4,3 g de (1bromoéthyl)benzène (23 mmol), 6,4 g de DEPN 92% (20 mmol) dissous dans 20 g de toluène. Selon cette procédure, 4 recyclages ont été effectués avec des durées réactionnelles telles qu'indiquées dans le tableau 2. Les résultats sont résumés dans le tableau 2 suivant :
<tb>
<tb> Essai <SEP> Chargement <SEP> T <SEP> ( C) <SEP> t <SEP> (h) <SEP> Rendement <SEP> (%)
<tb> 1 <SEP> a <SEP> 20 <SEP> 6 <SEP> 95
<tb> recyclage <SEP> b <SEP> 20 <SEP> 7 <SEP> 94
<tb> 1
<tb> recyclage <SEP> b <SEP> 20 <SEP> 7 <SEP> 96
<tb> 2
<tb> recyclage <SEP> b <SEP> 20 <SEP> 7 <SEP> 94
<tb> 3
<tb> recyclage <SEP> b <SEP> 20 <SEP> 12 <SEP> 95
<tb> 4
<tb>
<tb> Essai <SEP> Chargement <SEP> T <SEP> ( C) <SEP> t <SEP> (h) <SEP> Rendement <SEP> (%)
<tb> 1 <SEP> a <SEP> 20 <SEP> 6 <SEP> 95
<tb> recyclage <SEP> b <SEP> 20 <SEP> 7 <SEP> 94
<tb> 1
<tb> recyclage <SEP> b <SEP> 20 <SEP> 7 <SEP> 96
<tb> 2
<tb> recyclage <SEP> b <SEP> 20 <SEP> 7 <SEP> 94
<tb> 3
<tb> recyclage <SEP> b <SEP> 20 <SEP> 12 <SEP> 95
<tb> 4
<tb>
TABLEAU 2 chargement a : CuBr=3,3 g ; PMDETA = 4,0 g ; Cu =1,46g ; (1bromoéthyl)benzène=4,3 g; DEPN 92% = 6,4 g ; toluène=40 g ; 1- méthyl-3-propylimidazolium = 32 g chargement b : Cu =1,46g ; toluène = 20g (régénération 3 h à 60 C) ; puis (1-bromoéthyl)benzène=4,3 g ; DEPN 92%=6,4 g; toluène = 20 g
Globalement, nous avons produit 37,9 g de N-tertiobutyl, N-1diéthylphosphono-2,2-diméthylpropyl, 0-1-phényléthylhydroxylamine (95 mmol) pour 3,3 g de CuBr (23 mmol), 4 g de PMDETA (23 mmol) et 7,3 g de Cu 0 (115 mmol).
Globalement, nous avons produit 37,9 g de N-tertiobutyl, N-1diéthylphosphono-2,2-diméthylpropyl, 0-1-phényléthylhydroxylamine (95 mmol) pour 3,3 g de CuBr (23 mmol), 4 g de PMDETA (23 mmol) et 7,3 g de Cu 0 (115 mmol).
<Desc/Clms Page number 16>
Exemple 4 : Préparation du N-tertiobutyl, N-1-diéthylphosphono-2,2- diméthylpropyl, 0-1-phényléthylhydroxylamine en présence de chlorure de 1-butyl-3-méthylimidazolium
Dans un réacteur de 250 ml purgé à l'argon, on charge 3,3 g de CuBr (23 mmol), 4,0 g de PMDETA (23 mmol), 1,46 g de Cu(0) (23 mmol), 32 g de 1-butyl-3-méthylimidazolium et 5 g d'eau. On rajoute 4,3 g de (1-bromoéthyl)benzène (23 mmol) et 5,4 g de DEPN 92% (17 mmol) dissous dans 40 g de toluène dégazé. On laisse réagir 3 h sous agitation à 35 C. Le mélange réactionnel est décanté. La phase organique est récupérée, et la phase liquide ionique est extraite avec 20 g de toluène. Les phases organiques rassemblées sont lavées à l'eau (2x40 g). Le solvant est évaporé pour donner 6,45 g de N-tertiobutyl, N- 1-diéthylphosphono-2,2-diméthylpropyl, 0-1 -phényléthylhydroxylamine sous forme d'huile incolore (rendement = 95%).
Dans un réacteur de 250 ml purgé à l'argon, on charge 3,3 g de CuBr (23 mmol), 4,0 g de PMDETA (23 mmol), 1,46 g de Cu(0) (23 mmol), 32 g de 1-butyl-3-méthylimidazolium et 5 g d'eau. On rajoute 4,3 g de (1-bromoéthyl)benzène (23 mmol) et 5,4 g de DEPN 92% (17 mmol) dissous dans 40 g de toluène dégazé. On laisse réagir 3 h sous agitation à 35 C. Le mélange réactionnel est décanté. La phase organique est récupérée, et la phase liquide ionique est extraite avec 20 g de toluène. Les phases organiques rassemblées sont lavées à l'eau (2x40 g). Le solvant est évaporé pour donner 6,45 g de N-tertiobutyl, N- 1-diéthylphosphono-2,2-diméthylpropyl, 0-1 -phényléthylhydroxylamine sous forme d'huile incolore (rendement = 95%).
La régénération de l'espèce active est effectuée préalablement à la réaction selon les conditions ci-après.
On rajoute à la phase liquide ionique extraite 1,46 g de Cu et 20 g de toluène, puis on chauffe 2 h à 35 C. Une nouvelle réaction peut alors être effectuée en rajoutant 4,3 g de (1-bromoéthyl)benzène (23 mmol), 5,4 g de DEPN 92% (17 mmol) dissous dans 20 g de toluène. Selon cette procédure, 9 recyclages ont été effectués avec des durées réactionnelles telles qu'indiquées dans le tableau 3. Les résultats sont résumés dans le tableau 3 suivant :
<tb>
<tb> Essai <SEP> Chargement <SEP> T <SEP> ( C) <SEP> t <SEP> (h) <SEP> Rendement <SEP> (%)
<tb> 1 <SEP> a <SEP> 35 <SEP> 3 <SEP> 95
<tb> recyclage <SEP> 1 <SEP> b <SEP> 35 <SEP> 3 <SEP> 94
<tb> recyclage <SEP> 2 <SEP> b <SEP> 35 <SEP> 3 <SEP> 97
<tb> recyclage <SEP> 3 <SEP> b <SEP> 35 <SEP> 3 <SEP> 95
<tb> recyclage <SEP> 4 <SEP> b <SEP> 35 <SEP> 3 <SEP> 93
<tb> recyclage <SEP> 5 <SEP> b <SEP> 35 <SEP> 1,5 <SEP> 92
<tb> recyclage <SEP> 6 <SEP> b <SEP> 35 <SEP> 3 <SEP> 96
<tb> recyclage <SEP> 7 <SEP> b <SEP> 35 <SEP> 3 <SEP> 97
<tb> recyclage <SEP> 8 <SEP> b <SEP> 35 <SEP> 3 <SEP> 95
<tb> recyclage <SEP> 9 <SEP> b <SEP> 35 <SEP> 3 <SEP> 95
<tb>
TABLEAU 3
<tb> Essai <SEP> Chargement <SEP> T <SEP> ( C) <SEP> t <SEP> (h) <SEP> Rendement <SEP> (%)
<tb> 1 <SEP> a <SEP> 35 <SEP> 3 <SEP> 95
<tb> recyclage <SEP> 1 <SEP> b <SEP> 35 <SEP> 3 <SEP> 94
<tb> recyclage <SEP> 2 <SEP> b <SEP> 35 <SEP> 3 <SEP> 97
<tb> recyclage <SEP> 3 <SEP> b <SEP> 35 <SEP> 3 <SEP> 95
<tb> recyclage <SEP> 4 <SEP> b <SEP> 35 <SEP> 3 <SEP> 93
<tb> recyclage <SEP> 5 <SEP> b <SEP> 35 <SEP> 1,5 <SEP> 92
<tb> recyclage <SEP> 6 <SEP> b <SEP> 35 <SEP> 3 <SEP> 96
<tb> recyclage <SEP> 7 <SEP> b <SEP> 35 <SEP> 3 <SEP> 97
<tb> recyclage <SEP> 8 <SEP> b <SEP> 35 <SEP> 3 <SEP> 95
<tb> recyclage <SEP> 9 <SEP> b <SEP> 35 <SEP> 3 <SEP> 95
<tb>
TABLEAU 3
<Desc/Clms Page number 17>
chargement a : CuBr=3,3 g ; PMDETA=4,0 g ; Cu = 1,46g ; (1bromoéthyl)benzène=4,3 g ; DEPN 92%=5,4 g ; toluène=40 g ; 1butyl-3-méthylimidazolium=32 g ; H20 = 5 g chargement b : Cu = 1,46g ; toluène = 20g (régénération 2 h à 35 C) ; puis (1-bromoéthyl)benzène=4,3 g ; DEPN 92%=5,4 g; toluène = 20 g
Globalement, nous avons produit 64,5 g de N-tertiobutyl, N-1diéthylphosphono-2,2-diméthylpropyl, O-1-phényléthylhydroxylamine (0,161 mol) pour 3,3 g de CuBr (0,023 mol), 4 g de PMDETA (0,023 mol) et 14,6 g de Cu (0,230 mol).
Globalement, nous avons produit 64,5 g de N-tertiobutyl, N-1diéthylphosphono-2,2-diméthylpropyl, O-1-phényléthylhydroxylamine (0,161 mol) pour 3,3 g de CuBr (0,023 mol), 4 g de PMDETA (0,023 mol) et 14,6 g de Cu (0,230 mol).
Claims (15)
- dans laquelle W1, W2 et W3, identiques ou différents, représentent unZ est un reste de formuledans les formules desquelles les groupes Y1 à Y6, identiques ou différents, représentent un atome d'hydrogène, un radical alkyle, linéaire ou ramifié, ayant un nombre d'atomes de carbone allant de 1 à 10, un radical cycloalkyle ayant un nombre d'atomes de carbone allant de 3 à 20, un atome d'halogène, un radical cyano, un radical phényle, un radical hydroxyalkyle ayant un nombre d'atomes de carbone allant de 1 à 4, un radical dialcoxyphosphonyle, diphénoxyphosphonyle, un radical alcoxycarbonyle, alcoxycarbonylalkyle, ou bien 2 ou plus des groupes Y1 à Y6 peuvent être liés avec l'atome de carbone qui les porte pour former des structures cycliques, lesquelles peuvent comprendre une ou plusieurs fonctions extracycliques, choisis parmi : HO-, CH3C(O)-, alkyl -C(O)O - ou le radical alkyle, linéaire ou ramifié, à un nombre d'atomes de carbone allant de 1 à 30, CH30-, H2N-CH3C(O)NH-, (CH3)2N- ; ou bien encore peuvent comprendre 1 ou plusieurs hétéroatomes extra- ou intracyliques tels que 0, N ;à partir de nitroxydes de formule :Revendications 1. Procédé de préparation d'alcoxyamines de formule :<Desc/Clms Page number 19>ledit procédé étant caractérisé en ce que l'on opère dans un milieu biphasique comprenant au moins un liquide ionique et un solvant organique non miscible avec ledit liquide ionique.L représente un ligand du métal M, y est égal à 1,2 ou 3, n est égal à 1, ou 2, selon le schéma :A représente un atome d'halogène, un groupement carboxylate ou un groupement triflate,M représente un métal de transition à un degré d'oxydation n tel qu'il puisse participer à une réaction redox avec l'atome ou le groupe transferrable,X représente un atome de chlore, de brome ou d'iode, ledit procédé consistant à faire réagir ledit nitroxyde (II) avec un composé halogénocarboné ZX, en présence d'un système organométallique MA(L)y (III) dans lequel:atome d'hydrogène, un radical alkyle, linéaire ou ramifié, ayant un nombre d'atomes de carbone allant de 1 à 10 , un radical phényle, un radical benzyle, un radical cyano, un radical cycloalkyle ayant un nombre d'atomes de carbone allant de 3 à 12 ; unradical -(CH2)rC(O)OW4 dans lequel W4 représente un alkyle, linéaire ou ramifié, ayant un nombre d'atomes de carbone allant de 1 à 6 , r = 0 à 6 ;
- 2. Procédé selon la revendication 1, caractérisé en ce qu'il consiste à effectuer les étapes suivantes : a) on mélange sous agitation un sel métallique MAn, éventuellement un métal M au degré d'oxydation zéro, un ligand L, au moins un liquide ionique, un solvant organique, le composé halogéno carboné ZX et le nitroxyde (II) selon un rapport molaireZX/nitroxyde (II) allant de 1 à 1,5 et, de préférence voisin de 1 ;<Desc/Clms Page number 20>b) on maintient le milieu réactionnel sous agitation à une température comprise entre 20 C et 90 C et, de préférence, à une température allant de 20 C à 35 C jusqu'à disparition complète du nitroxyde (II) ; puis c) on arrête l'agitation, on décante, on récupère la phase organique qui est éventuellement lavée à l'eau puis, d) on isole l'alcoxyamine (I) de la phase organique par évaporation du solvant organique sous pression réduite, et e) éventuellement la phase liquide ionique est recyclée au moins une fois et, de préférence un nombre de fois allant de 1 à 10, avec régénération de l'espèce active du métal M (Mn).
- 3. Procédé selon l'une des revendications 1 ou 2, caractérisé en ce que le liquide ionique est choisi parmi les sels deN,N'dialkylimidazolium.
- 4. Procédé selon la revendication 3, caractérisé en ce que le liquide ionique est le chlorure de 1-butyl-3-méthylimidazolium, le chlorure de 1-propyl-3-méthylimidazolium ou le bromure de 1-propyl-3- méthylimidazolium.
- 5. Procédé selon la revendication 1, caractérisé en ce que le ligand L du métal M du système organométallique (III) est choisi parmi les composés représentés par la formule générale (IV) :dans laquelle R1, R2, R3 et R4, identiques ou différents, représentent un atome d'hydrogène, un groupe alkyle, linéaire ou ramifié ayant un nombre d'atomes de carbone allant de 1 à 10 et, de préférence allant de 1 à 4, R5 représente un atome d'hydrogène, un groupe alkyle, linéaire ou ramifié, ayant un nombre d'atome de carbone allant de 1 à 10 et, de préférence, allant de 1 à 4, un reste<Desc/Clms Page number 21>dans lequel R6 et R7 ont les mêmes significations que R5, ou bien encore au moins deux des radicaux R1, R2, R3, R4 et R5 peuvent être liés entre eux pour former un cycle ; m, p et q, identiques ou différents, représentent des nombres entiers allant de 1 à 4 et, de préférence, égaux à 2, x allant de 0 à 4.
- 6. Procédé selon la revendication 1 ou 2, caractérisé par le fait que M représente Cu(l), Fe(II), Ni())) et, de préférence M représente Cu(l).
- 7. Procédé selon l'une des revendications 1 ou 2, caractérisé par le fait que A représente un atome de brome et X représente un atome de chlore ou un atome de brome.
- 8. Procédé selon l'une des revendications 1 à 4 caractérisé en ce que le rapport molaire ZX/ nitroxyde (II) est voisin de 1.
- 9. Procédé selon l'une des revendications 1,2, 6 ou 7, caractérisé en ce que le sel métallique MAn est un halogénure métallique MnXn dans la formule duquel l'exposant n du métal M représente le degré d'oxydation dudit métal et est égal à 1 ou 2.
- 10. Procédé selon la revendication 9, caractérisé en ce que l'halogénure métallique MnXn est CuBr.
- 11. Procédé selon l'une des revendications 1à 7, caractérisé en ce que le rapport molaire L/ espèce active Mn va de 0,2 à 4.
- 12. Procédé selon la revendication 8, caractérisé en ce que le rapport molaire L/ Mn va de 0,4 à 2.
- 13. Procédé selon l'une des revendications 1 ou 2, caractérisé en ce que le solvant organique est un hydrocarbure aromatique.<Desc/Clms Page number 22>
- 14. Procédé selon la revendication 13, caractérisé en ce que l'hydrocarbure aromatique est le toluène.
- 15. Procédé selon l'une des revendications 1 à 14, caractérisé en ce que le ligand L est la N, N, N', N', N"-pentaméthyldiéthylènetria- mine (PMDETA) ou la N,N-diméthyldipropylènetrimaine (DMAPAPA).
Priority Applications (10)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0010344A FR2812639B1 (fr) | 2000-08-04 | 2000-08-04 | Procede de preparation d'alcoxyamines a partir de nitroxydes |
| US10/089,720 US6700007B2 (en) | 2000-08-04 | 2001-08-02 | Method for preparing alkoxyamines from nitroxides |
| MXPA02003380A MXPA02003380A (es) | 2000-08-04 | 2001-08-02 | Metodo de preparacion de alcoxiaminas a partir de nitroxidos. |
| ES01963050T ES2231539T3 (es) | 2000-08-04 | 2001-08-02 | Procedimiento de preparacion de alcoxiaminas a partir de nitroxidos. |
| JP2002517452A JP2004505934A (ja) | 2000-08-04 | 2001-08-02 | ニトロオキシドからアルコキシアミンを製造する方法 |
| EP01963050A EP1311472B1 (fr) | 2000-08-04 | 2001-08-02 | Procede de preparation d'alcoxyamines a partir de nitroxydes |
| DE60106633T DE60106633T2 (de) | 2000-08-04 | 2001-08-02 | Verfahren zur herstellung von alkoxyaminen aus nitroxyle |
| AU2001284100A AU2001284100A1 (en) | 2000-08-04 | 2001-08-02 | Method for preparing alkoxyamines from nitroxides |
| AT01963050T ATE280149T1 (de) | 2000-08-04 | 2001-08-02 | Verfahren zur herstellung von alkoxyaminen aus nitroxyle |
| PCT/FR2001/002526 WO2002012149A2 (fr) | 2000-08-04 | 2001-08-02 | Procede de preparation d'alcoxyamines a partir de nitroxydes |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0010344A FR2812639B1 (fr) | 2000-08-04 | 2000-08-04 | Procede de preparation d'alcoxyamines a partir de nitroxydes |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| FR2812639A1 true FR2812639A1 (fr) | 2002-02-08 |
| FR2812639B1 FR2812639B1 (fr) | 2002-09-27 |
Family
ID=8853329
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| FR0010344A Expired - Fee Related FR2812639B1 (fr) | 2000-08-04 | 2000-08-04 | Procede de preparation d'alcoxyamines a partir de nitroxydes |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US6700007B2 (fr) |
| EP (1) | EP1311472B1 (fr) |
| JP (1) | JP2004505934A (fr) |
| AT (1) | ATE280149T1 (fr) |
| AU (1) | AU2001284100A1 (fr) |
| DE (1) | DE60106633T2 (fr) |
| ES (1) | ES2231539T3 (fr) |
| FR (1) | FR2812639B1 (fr) |
| MX (1) | MXPA02003380A (fr) |
| WO (1) | WO2002012149A2 (fr) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2864455B1 (fr) * | 2003-12-24 | 2006-03-17 | Coatex Sas | Utilisation de polymeres hydrosolubles structures obtenus par polymerisation radicalaire controlee comme dispersant et agent d'aide au broyage de matieres minerales |
| US7816483B2 (en) * | 2005-08-11 | 2010-10-19 | Bridgestone Corporation | Amine functionalized polymer |
| CA2633263A1 (fr) * | 2005-12-16 | 2007-07-12 | Arkema Inc. | Procedes de fabrication d'un copolymere sequence a faible energie de surface et applications |
| US7498398B2 (en) * | 2006-03-21 | 2009-03-03 | Sabic Innovative Plastics Ip B.V. | Thermoplastic composition, method of making, and articles formed therefrom |
| CN119972172B (zh) * | 2024-12-25 | 2025-10-28 | 武汉光化学技术研究院 | 非均相有机聚合物催化剂及制备方法、合成醛或内酯类化合物的方法 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1998040415A1 (fr) * | 1997-03-11 | 1998-09-17 | Carnegie Mellon University | Perfectionnements applicable a la polymerisation par transfert d'atomes ou de groupes |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3046308A (en) * | 1958-10-16 | 1962-07-24 | Union Carbide Corp | O-allyl-n, n-diallylhydroxylamine and method of preparation |
| US3163677A (en) * | 1961-08-07 | 1964-12-29 | American Cyanamid Co | Process for preparing n, n, o-trisubstituted hydroxyl amines and n, n-disubstituted nitroxides and products |
| FR2791979B1 (fr) * | 1999-04-08 | 2003-05-16 | Atochem Elf Sa | Procede de preparation d'alcoxyamines a partir de nitroxydes |
-
2000
- 2000-08-04 FR FR0010344A patent/FR2812639B1/fr not_active Expired - Fee Related
-
2001
- 2001-08-02 DE DE60106633T patent/DE60106633T2/de not_active Expired - Fee Related
- 2001-08-02 AU AU2001284100A patent/AU2001284100A1/en not_active Abandoned
- 2001-08-02 AT AT01963050T patent/ATE280149T1/de not_active IP Right Cessation
- 2001-08-02 MX MXPA02003380A patent/MXPA02003380A/es active IP Right Grant
- 2001-08-02 JP JP2002517452A patent/JP2004505934A/ja not_active Withdrawn
- 2001-08-02 WO PCT/FR2001/002526 patent/WO2002012149A2/fr not_active Ceased
- 2001-08-02 ES ES01963050T patent/ES2231539T3/es not_active Expired - Lifetime
- 2001-08-02 EP EP01963050A patent/EP1311472B1/fr not_active Expired - Lifetime
- 2001-08-02 US US10/089,720 patent/US6700007B2/en not_active Expired - Fee Related
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1998040415A1 (fr) * | 1997-03-11 | 1998-09-17 | Carnegie Mellon University | Perfectionnements applicable a la polymerisation par transfert d'atomes ou de groupes |
Also Published As
| Publication number | Publication date |
|---|---|
| ATE280149T1 (de) | 2004-11-15 |
| MXPA02003380A (es) | 2002-10-11 |
| WO2002012149A2 (fr) | 2002-02-14 |
| WO2002012149A8 (fr) | 2002-07-04 |
| US6700007B2 (en) | 2004-03-02 |
| EP1311472B1 (fr) | 2004-10-20 |
| US20030050507A1 (en) | 2003-03-13 |
| EP1311472A2 (fr) | 2003-05-21 |
| DE60106633T2 (de) | 2006-02-09 |
| JP2004505934A (ja) | 2004-02-26 |
| DE60106633D1 (de) | 2004-11-25 |
| AU2001284100A1 (en) | 2002-02-18 |
| WO2002012149A3 (fr) | 2003-02-27 |
| FR2812639B1 (fr) | 2002-09-27 |
| ES2231539T3 (es) | 2005-05-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP1086073B1 (fr) | Procede de preparation d'alcoxyamines a partir de nitroxydes | |
| FR2794459A1 (fr) | Polyalcoxyamines issues de nitroxydes beta-substitues | |
| FR2843394A1 (fr) | Alcoxyamines issues de nitroxydes b-phosphore, leur utilisation en polymerisation radicalaire | |
| JP4405089B2 (ja) | β亜燐酸ニトロキシドラジカルの製造方法 | |
| EP1140807B1 (fr) | Procede de preparation de nitroxydes | |
| EP1464648A1 (fr) | Alcoxyamines beta-phosporees et leur utilisation pour la preparation de polymères alpha-omega fonctionnels | |
| EP1311472B1 (fr) | Procede de preparation d'alcoxyamines a partir de nitroxydes | |
| EP1349862B1 (fr) | PROCEDE DE PREPARATION DE RADICAUX NITROXYDE Beta-PHOSPHORES | |
| JP7718088B2 (ja) | 3-(メタ)アクリロイルスルホランの製造方法 | |
| EP2167514B1 (fr) | Procede ameliore de preparation d'alcoxyamines issues de nitroxydes beta-phosphores | |
| FR2843393A1 (fr) | Alcoxyamines issues de nitroxydes b-phosphore, leur utilisation en polymerisation radicalaire | |
| JP2002145861A (ja) | 立体障害n−オキシル化合物の製造方法 | |
| FR2585700A1 (fr) | Nouveaux propanediamides et leurs procedes de preparation |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ST | Notification of lapse |
Effective date: 20070430 |