FR2676364A1 - Composition pharmaceutique a base de derives d'aminobutanone. - Google Patents
Composition pharmaceutique a base de derives d'aminobutanone. Download PDFInfo
- Publication number
- FR2676364A1 FR2676364A1 FR9106048A FR9106048A FR2676364A1 FR 2676364 A1 FR2676364 A1 FR 2676364A1 FR 9106048 A FR9106048 A FR 9106048A FR 9106048 A FR9106048 A FR 9106048A FR 2676364 A1 FR2676364 A1 FR 2676364A1
- Authority
- FR
- France
- Prior art keywords
- resin
- buflomedil
- composition according
- formula
- hydrochloride
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 239000008194 pharmaceutical composition Substances 0.000 title claims abstract description 5
- QCWWEZIJUCPALZ-UHFFFAOYSA-N 1-aminobutan-2-one Chemical class CCC(=O)CN QCWWEZIJUCPALZ-UHFFFAOYSA-N 0.000 title abstract description 3
- 239000002245 particle Substances 0.000 claims abstract description 11
- NWUYHJFMYQTDRP-UHFFFAOYSA-N 1,2-bis(ethenyl)benzene;1-ethenyl-2-ethylbenzene;styrene Chemical group C=CC1=CC=CC=C1.CCC1=CC=CC=C1C=C.C=CC1=CC=CC=C1C=C NWUYHJFMYQTDRP-UHFFFAOYSA-N 0.000 claims abstract description 5
- 239000003456 ion exchange resin Substances 0.000 claims abstract description 4
- 229920003303 ion-exchange polymer Polymers 0.000 claims abstract description 4
- 239000011347 resin Substances 0.000 claims description 44
- 229920005989 resin Polymers 0.000 claims description 44
- OWYLAEYXIQKAOL-UHFFFAOYSA-N 4-(1-pyrrolidinyl)-1-(2,4,6-trimethoxyphenyl)-1-butanone Chemical compound COC1=CC(OC)=CC(OC)=C1C(=O)CCCN1CCCC1 OWYLAEYXIQKAOL-UHFFFAOYSA-N 0.000 claims description 29
- 229960001415 buflomedil Drugs 0.000 claims description 28
- 239000000203 mixture Substances 0.000 claims description 23
- 150000001875 compounds Chemical class 0.000 claims description 17
- 230000002378 acidificating effect Effects 0.000 claims description 13
- 239000002253 acid Substances 0.000 claims description 5
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 4
- 239000003729 cation exchange resin Substances 0.000 claims description 4
- 229910052757 nitrogen Inorganic materials 0.000 claims description 4
- 150000003839 salts Chemical class 0.000 claims description 4
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 claims description 3
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 claims description 2
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 claims description 2
- 150000007513 acids Chemical class 0.000 claims description 2
- 125000005842 heteroatom Chemical group 0.000 claims description 2
- 125000002768 hydroxyalkyl group Chemical group 0.000 claims description 2
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 2
- 125000004430 oxygen atom Chemical group O* 0.000 claims description 2
- 125000001424 substituent group Chemical group 0.000 claims description 2
- 239000011593 sulfur Substances 0.000 claims description 2
- 229910052717 sulfur Inorganic materials 0.000 claims description 2
- 125000000623 heterocyclic group Chemical group 0.000 claims 1
- ZDPACSAHMZADFZ-UHFFFAOYSA-N 1-[3-(2,4,6-Trimethoxybenzoyl)propyl]pyrrolidinium chloride Chemical compound [Cl-].COC1=CC(OC)=CC(OC)=C1C(=O)CCC[NH+]1CCCC1 ZDPACSAHMZADFZ-UHFFFAOYSA-N 0.000 description 22
- 229960002113 buflomedil hydrochloride Drugs 0.000 description 20
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 17
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 12
- 235000019658 bitter taste Nutrition 0.000 description 9
- MYRTYDVEIRVNKP-UHFFFAOYSA-N 1,2-Divinylbenzene Chemical compound C=CC1=CC=CC=C1C=C MYRTYDVEIRVNKP-UHFFFAOYSA-N 0.000 description 8
- 230000007935 neutral effect Effects 0.000 description 8
- 239000000839 emulsion Substances 0.000 description 7
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical group Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 6
- 125000002091 cationic group Chemical group 0.000 description 6
- 239000002552 dosage form Substances 0.000 description 5
- 230000008030 elimination Effects 0.000 description 5
- 238000003379 elimination reaction Methods 0.000 description 5
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 4
- 238000005341 cation exchange Methods 0.000 description 4
- 239000013256 coordination polymer Substances 0.000 description 4
- 229920001577 copolymer Polymers 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 241000282472 Canis lupus familiaris Species 0.000 description 3
- 229920002125 Sokalan® Polymers 0.000 description 3
- 229920001429 chelating resin Polymers 0.000 description 3
- 229920003145 methacrylic acid copolymer Polymers 0.000 description 3
- 238000000034 method Methods 0.000 description 3
- 239000012071 phase Substances 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 235000019640 taste Nutrition 0.000 description 3
- 238000011282 treatment Methods 0.000 description 3
- 239000004925 Acrylic resin Substances 0.000 description 2
- 229920000178 Acrylic resin Polymers 0.000 description 2
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 2
- 229920002307 Dextran Polymers 0.000 description 2
- 229920003136 Eudragit® L polymer Polymers 0.000 description 2
- 229920003137 Eudragit® S polymer Polymers 0.000 description 2
- 229930195725 Mannitol Natural products 0.000 description 2
- 229920001214 Polysorbate 60 Polymers 0.000 description 2
- 238000000540 analysis of variance Methods 0.000 description 2
- 235000019636 bitter flavor Nutrition 0.000 description 2
- 229940023913 cation exchange resins Drugs 0.000 description 2
- 150000001768 cations Chemical class 0.000 description 2
- 239000001913 cellulose Substances 0.000 description 2
- 229920002678 cellulose Polymers 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 235000003599 food sweetener Nutrition 0.000 description 2
- 230000002496 gastric effect Effects 0.000 description 2
- 125000005456 glyceride group Chemical group 0.000 description 2
- 238000005342 ion exchange Methods 0.000 description 2
- 239000000594 mannitol Substances 0.000 description 2
- 235000010355 mannitol Nutrition 0.000 description 2
- 230000000873 masking effect Effects 0.000 description 2
- 230000004962 physiological condition Effects 0.000 description 2
- 230000036470 plasma concentration Effects 0.000 description 2
- 239000001818 polyoxyethylene sorbitan monostearate Substances 0.000 description 2
- 235000010989 polyoxyethylene sorbitan monostearate Nutrition 0.000 description 2
- 229940113124 polysorbate 60 Drugs 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 230000002035 prolonged effect Effects 0.000 description 2
- 238000001179 sorption measurement Methods 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 239000003765 sweetening agent Substances 0.000 description 2
- JKNCOURZONDCGV-UHFFFAOYSA-N 2-(dimethylamino)ethyl 2-methylprop-2-enoate Chemical compound CN(C)CCOC(=O)C(C)=C JKNCOURZONDCGV-UHFFFAOYSA-N 0.000 description 1
- 125000003341 7 membered heterocyclic group Chemical group 0.000 description 1
- 239000004923 Acrylic lacquer Substances 0.000 description 1
- 229910002016 Aerosil® 200 Inorganic materials 0.000 description 1
- 206010062542 Arterial insufficiency Diseases 0.000 description 1
- 229920003148 Eudragit® E polymer Polymers 0.000 description 1
- 238000010155 Games-Howell test Methods 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 208000018262 Peripheral vascular disease Diseases 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 239000004809 Teflon Substances 0.000 description 1
- 229920006362 Teflon® Polymers 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 230000007059 acute toxicity Effects 0.000 description 1
- 231100000403 acute toxicity Toxicity 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 230000002238 attenuated effect Effects 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- NEDGUIRITORSKL-UHFFFAOYSA-N butyl 2-methylprop-2-enoate;2-(dimethylamino)ethyl 2-methylprop-2-enoate;methyl 2-methylprop-2-enoate Chemical compound COC(=O)C(C)=C.CCCCOC(=O)C(C)=C.CN(C)CCOC(=O)C(C)=C NEDGUIRITORSKL-UHFFFAOYSA-N 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- WCHFOOKTKZYYAE-UHFFFAOYSA-N ethoxyperoxyethane Chemical compound CCOOOCC WCHFOOKTKZYYAE-UHFFFAOYSA-N 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 238000000227 grinding Methods 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000013178 mathematical model Methods 0.000 description 1
- 125000005397 methacrylic acid ester group Chemical group 0.000 description 1
- 239000011325 microbead Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000005325 percolation Methods 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 210000003296 saliva Anatomy 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 230000009919 sequestration Effects 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000002798 spectrophotometry method Methods 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 230000000304 vasodilatating effect Effects 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0087—Galenical forms not covered by A61K9/02 - A61K9/7023
- A61K9/0095—Drinks; Beverages; Syrups; Compositions for reconstitution thereof, e.g. powders or tablets to be dispersed in a glass of water; Veterinary drenches
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/12—Ketones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/38—Heterocyclic compounds having sulfur as a ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/58—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. poly[meth]acrylate, polyacrylamide, polystyrene, polyvinylpyrrolidone, polyvinylalcohol or polystyrene sulfonic acid resin
- A61K47/585—Ion exchange resins, e.g. polystyrene sulfonic acid resin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2095—Tabletting processes; Dosage units made by direct compression of powders or specially processed granules, by eliminating solvents, by melt-extrusion, by injection molding, by 3D printing
Abstract
La présente invention a pour objet une composition pharmaceutique comprenant un dérivé d'aminobutanone fixé sur une résine échangeuse d'ions, ayant une taille de particules inférieure à 200 micromètres.
Description
La présente invention concerne de nouvelles compositions pharmaceutiques à base de dérivés d'aminobutanone pour la voie orale, permettant notamment de masquer l'amertume de ces dérivés et/ou de prolonger la libération de ces dérivés.
Le buflomédil ou 4-(l-pyrrolidinyl)-l-(2,4,6- triméthoxyphényl)-l-butanone (décrit notamment dans FR-A2 134 218) répond à la formule
Le buflomédil sous forme de chlorhydrate est utilisé chez l'homme pour le traitement des maladies vasculaires périphériques et notamment pour le traitement des insuffisances artérielles périphériques.
Le buflomédil sous forme de chlorhydrate se présente sous la forme d'une poudre cristalline blanche, de saveur amère, facilement soluble dans l'eau et d'une grande stabilité chimique et thermique.
Chez l'homme, sa demie-vie d'élimination se situe entre 1,9 et 3,6 heures. La cinétique est linéaire entre 150 et 450 mg par voie orale et entre 50 mg et 200 mpg par voie intraveineuse.
Sa toxicité aigüe (DL 50) per os est relativement faible, elle se situe 9 :
620 + 4 mg/kg chez le rat mâle,
407 + 30 mg/kg chez la souris.
620 + 4 mg/kg chez le rat mâle,
407 + 30 mg/kg chez la souris.
La toxicité zéro, absence de mort chez le chien, est constatée jusqu'a la dose de 350 mg/kg.
Les études de tolérance clinique montrent une très bonne marge thérapeutique.
Le buflomédil sous forme de chlorhydrate est commercialisé en France sous la marque Fonzylane, sous forme de comprimés enrobés a 150 mg. Les comprimés sont pelliculés, le film d'enrobage étant destiné à masquer l'amertume du principe actif.
Du fait de ses propriétés physico-chimiques et organoleptiques (sa solubilité dans l'eau, sa stabilité chimique et thermique, son amertume très prononcée, difficile à corriger par les méthodes usuelles) et de ses propriétés pharmacocinétiques (sa demie-vie d' élimination courte), il a été recherché des compositions permettant de masquer l'amertume du buflomédil et/ou de prolonger sa libération.
On a par ailleurs décrit dans FR-A-2 134 218 ainsi que dans la demande de brevet français 90 15 591 d'autres composés voisins à activité vasodilatatrice qui présentent le même problème d'amertume et/ou de biodisponibilité.
Il a donc été recherché également des compositions qui permettent de masquer l'amertume de ces composés et/ou de prolonger leur libération.
I1 a été découvert que de telles compositions peuvent être obtenues par fixation d'un composé de ce type sur des résines échangeuses d'ions.
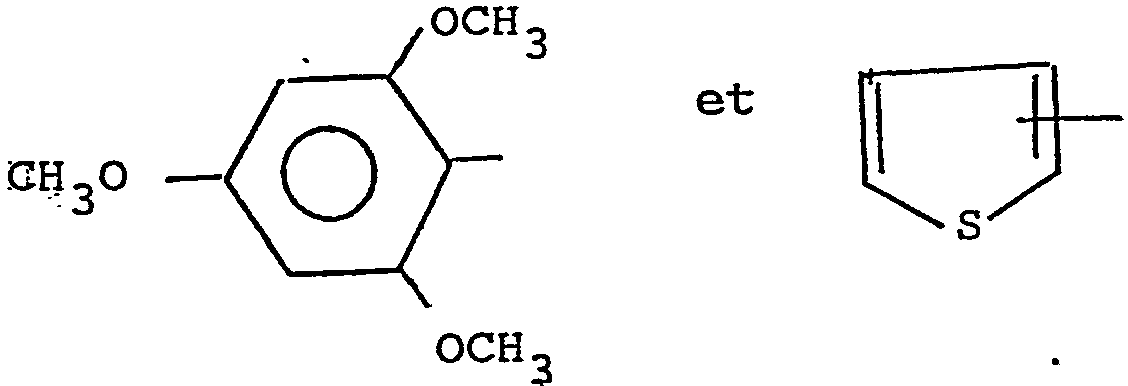
La présente invention a ainsi pour objet une composition pharmaceutique constituée par un composé de formule
dans laquelle A est choisi parmi les groupes de formule
dans laquelle R1 et R2 identiques ou différents représentent chacun un groupe alkyle en C1-C4, ou R1 et R2 forment ensemble avec l'atome d'azote auquel ils sont lies un groupe hétéro-cyclique de 5 à 7 chaînons pouvant contenir un second hetéroatome choisi parmi les atomes de soufre, d'azote et d'oxygène, et pouvant présenter des substituants choisis parmi les groupes alkyle en C1-C3 et hydroxyalkyle (C1-C3) ou un de ses sels d'addition avec des acides pharmaceutiquement acceptables, fixé sur une résine échangeuse d'ions, ayant une taille de particules inférieure à 200 micromètres.
dans laquelle A est choisi parmi les groupes de formule
dans laquelle R1 et R2 identiques ou différents représentent chacun un groupe alkyle en C1-C4, ou R1 et R2 forment ensemble avec l'atome d'azote auquel ils sont lies un groupe hétéro-cyclique de 5 à 7 chaînons pouvant contenir un second hetéroatome choisi parmi les atomes de soufre, d'azote et d'oxygène, et pouvant présenter des substituants choisis parmi les groupes alkyle en C1-C3 et hydroxyalkyle (C1-C3) ou un de ses sels d'addition avec des acides pharmaceutiquement acceptables, fixé sur une résine échangeuse d'ions, ayant une taille de particules inférieure à 200 micromètres.
Les résines que l'on peut utiliser dans la presente invention peuvent être de plusieurs types
1 - des résines échangeuses de cations fortement acides.
1 - des résines échangeuses de cations fortement acides.
Ces résines sont généralement constituées de copolymères de styrène et de divinylbenzène présentant des cations sulfoniques. Leur capacité d'échange d'ions est indépendante du pH.
Ces résines forment avec le composé de formule
I des composés insolubles qui présentent une amertume très fortement atténuée.
I des composés insolubles qui présentent une amertume très fortement atténuée.
2 - Des résines échangeuses de cations faiblement acides.
Ces résines sont généralement des copolymères d'acide méthacrylique (ou acrylique) et de divinylbenzène. En milieu acide ces résines sont essentiellement sous forme non ionique. Elles peuvent être utilisées sous forme ionique à un pH égal ou supérieur à 6, le cation étant H+, le sodium ou le potassium.
Ces résines forment avec les composés de formule I des compositions insolubles qui présentent une amertume fortement masquée et qui peuvent avoir une libération prolongée.
3 - Des résines acryliques anioniques.
Ces resines peuvent être des copolymères d'acide méthacrylique et de méthacrylate de méthyle tels que ceux commercialises sous les marques Eudragit L et
S.
S.
Ces résines sont insolubles en milieu acide (pH < 5) et solubles en milieu intestinal (à un pH compris entre 6 et 7 pour Eudragit L et à un pH supérieur à 7 pour Eudragit S).
Les composés de formule I, sous forme de base ou sous forme de sel, se fixent sur ces copolymères suivant une réaction d'échange d'ions. Les produits formés sont insolubles dans l'eau et la saveur amère est fortement atténuée.
4. Des résines acryliques cationiques.
Ces résines peuvent être des copolymères de méthacrylate de diméthylaminoéthyle et d'esters neutres d'acide méthacrylique tels que ceux commercialisés sous la marque Eudragit E. Ces résines sont insolubles dans la salive (ce qui est intéressant pour le masquage du goût) et solubles en milieu gastrique. La libération des composés de formule I a lieu en milieu gastrique.
Les résines du commerce qui sont utilisées dans l'invention ont généralement une taille de particules trop élevée et l'on doit procéder à une réduction de la taille des particules. A cet effet, on peut effectuer
- un broyage soit en phase humide (broyeur à microbilles), soit en phase sèche (broyeur à boulets par exemple) permettant de réduire la taille des particules a une valeur de 30 à 100 micromètres
- une micronisation par jet d'air pour obtenir une taille de particules de 5 à 50 micromètres et éventuellement une double micronisation pour obtenir une taille de particules de 5 à 30 micromètres.
- un broyage soit en phase humide (broyeur à microbilles), soit en phase sèche (broyeur à boulets par exemple) permettant de réduire la taille des particules a une valeur de 30 à 100 micromètres
- une micronisation par jet d'air pour obtenir une taille de particules de 5 à 50 micromètres et éventuellement une double micronisation pour obtenir une taille de particules de 5 à 30 micromètres.
La fixation des composés de formule I sur les résines peut être effectuée de manière classique par mélange de la résine avec une solution du composé, éventuellement sous forme de sel, dans un solvant approprié.
On peut ainsi fixer les composés de formule I généralement dans une proportion de 10 à 50 * par rapport à la composition.
Les compositions selon 1' invention peuvent être présentées sous des formes galéniques classiques telles que poudres en sachet, gélules, comprimés, granulés, en mélange avec les véhicules classiques pour ces formes.
Les comprimés peuvent être protégés éventuellement par un agent d'enrobage de type dérivé cellulosique, laque acrylique, gélatine, gomme.
En outre, les particules de résine contenant les composés de formule I peuvent être enrobées d'une pellicule de type cellulosique ou acrylique permettant d'améliorer le masquage du goût amer et la libération prolongée.
Les compositions selon l'invention peuvent en outre être présentées sous forme de lyophilisat oral qui peut être préparé comme décrit dans les brevets FR-A-2 081 586 et FR-A-2 562 327.
Les exemples suivants illustrent la présente invention.
Les exemples ci-après sont donnés à titre indicatif et ne sont pas limitatifs.
Dans ces exemples, les dosages des compositions sont faits par élution de la résine à l'acide chlorhydrique 2N, suivie du dosage du composé sous forme chlorhydrate dans la solution d'élution.
EXEMPLE 1
On utilise une résine Amberlite IRP-64 de type échangeuse de cations faiblement acide ayant une granulométrie de 35-150p. Cette résine est un copolymère d'acide méthacrylique et de divinylbenzène.
On utilise une résine Amberlite IRP-64 de type échangeuse de cations faiblement acide ayant une granulométrie de 35-150p. Cette résine est un copolymère d'acide méthacrylique et de divinylbenzène.
Sur une colonne renfermant 10 g de résine
Amberlite IRP-64, sous forme H+, on passe par percolation lente 10,8 g de buflomédil base en solution dans 25 ml d'isopropanol. La résine est ensuite lavée à l'isopropanol jusqu'à neutralité, puis séchée en étuve à vide à 40 C, jusqu'à un poids constant.
Amberlite IRP-64, sous forme H+, on passe par percolation lente 10,8 g de buflomédil base en solution dans 25 ml d'isopropanol. La résine est ensuite lavée à l'isopropanol jusqu'à neutralité, puis séchée en étuve à vide à 40 C, jusqu'à un poids constant.
Poids de produit recueilli : 14,35 g.
Dosage : 1 g de produit renferme 0,987 meq de buflomédil chlorhydrate, soit 30,3 % p/p exprimé en buflomédil base, ou 33,9 % p/p exprimé en buflomédil chlorhydrate.
EXEMPLE 2
Dans un récipient approprié on agite trois heures à l'aide d'un barreau aimanté 10 g de résine IRP64 (la même qu'à l'exemple 1), sous forme H+, et une solution de 8,95 g de buflomédil base dans 50 ml d'éthanol 96". On laisse reposer une nuit et la résine est filtrée, lavee à l'éthanol jusqu'à neutralité puis séchée en étuve à vide à 40 C jusqu'à un poids constant.
Dans un récipient approprié on agite trois heures à l'aide d'un barreau aimanté 10 g de résine IRP64 (la même qu'à l'exemple 1), sous forme H+, et une solution de 8,95 g de buflomédil base dans 50 ml d'éthanol 96". On laisse reposer une nuit et la résine est filtrée, lavee à l'éthanol jusqu'à neutralité puis séchée en étuve à vide à 40 C jusqu'à un poids constant.
Poids de produit recueilli : 15,6 g.
Dosage : 1 g de produit renferme 1,13 meq de buflomédil chlorhydrate, soit 34,7 * p/p exprimé en buflomédil base ou 38,8 % p/p exprimé en buflomedil chlorhydrate.
EXEMPLE 3
Dans un récipient approprié on agite trois heures à l'aide d'un barreau aimanté 10 g de resine IRP64 (la même qu'à l'exemple 1), sous forme H+, et une solution de 8,95 g de buflomédil base dans un mélange de 50 ml d'éthanol et 25 ml d'eau. On laisse reposer une nuit. La résine est filtrée, lavée à l'éthanol jusqu'à neutralité, puis séchée en étuve à vide à 40 C, jusqu'à un poids constant.
Dans un récipient approprié on agite trois heures à l'aide d'un barreau aimanté 10 g de resine IRP64 (la même qu'à l'exemple 1), sous forme H+, et une solution de 8,95 g de buflomédil base dans un mélange de 50 ml d'éthanol et 25 ml d'eau. On laisse reposer une nuit. La résine est filtrée, lavée à l'éthanol jusqu'à neutralité, puis séchée en étuve à vide à 40 C, jusqu'à un poids constant.
Poids de produit recueilli : 17,8 g.
Dosage : 1 g de produit renferme 1,43 meq de buflomédil chlorhydrate soit 43,9 % p/p exprimé en buflomédil base ou 49,1 * p/p exprime en buflomédil chlorhydrate.
EXEMPLE 4
Dans un récipient approprié an agite cinq heures à l'aide d'un barreau aimanté 50 g de résine IRP64 micronisée à 5-40 micromètres, sous forme H+, et une solution de 44,4 g de buflomédil base dans un mélange de 200 ml d'éthanol et de 40 ml d'eau. On laisse reposer une nuit et la resine est filtrée, lavée à l'éthanol jusqu'à neutralité, puis séchée en étuve à vide à 40 C jusqu'à un poids constant.
Dans un récipient approprié an agite cinq heures à l'aide d'un barreau aimanté 50 g de résine IRP64 micronisée à 5-40 micromètres, sous forme H+, et une solution de 44,4 g de buflomédil base dans un mélange de 200 ml d'éthanol et de 40 ml d'eau. On laisse reposer une nuit et la resine est filtrée, lavée à l'éthanol jusqu'à neutralité, puis séchée en étuve à vide à 40 C jusqu'à un poids constant.
Poids de produit recueilli : 88,6 g.
Dosage : 1 g de produit renferme 1,41 meq de buflomédil chlorhydrate soit 43,3 % p/p exprimé en buflomédil base ou 48,4 * p/p exprimé en buflomédil chlorhydrate.
EXEMPLE 5
On utilise une résine Amberlite IRP-69 du type échangeuse de cations fortement acide et micronisée à 534 micromètres. Cette résine est un copolymère sulfoné de styrène et de divinylbenzène.
On utilise une résine Amberlite IRP-69 du type échangeuse de cations fortement acide et micronisée à 534 micromètres. Cette résine est un copolymère sulfoné de styrène et de divinylbenzène.
Dans un ballon de 6 litres on dissout 750 g de buflomédil chlorhydrate dans 3 litres d'eau déminéralisée. On ajoute 750 g de résine IRP-69 micronisée, sous forme H+, et 1,5 litre d'eau déminéralisée. On agite avec un agitateur en téflon, à ancre, à bonne vitesse, pendant 11 heures. On filtre et lave le produit à l'eau déminéralisée jusqu'à neutralité. On sèche le produit à l'étuve sous vide à 40 C jusqu'à un poids constant.
Poids de produit recueilli : 1149 g.
Dosage : 1 g de produit renferme 1,13 meq de buflomédil chlorhydrate, soit 34,7 % p/p exprimé en buflomédil base ou 38,8 * p/p exprimé en buflomédil chlorhydrate.
EXEMPLE 6
On utilise une résine Duolite CP 2000 du type échangeuse de cations fortement acide.
On utilise une résine Duolite CP 2000 du type échangeuse de cations fortement acide.
Dans un récipient approprié on agite dix heures à l'aide d'un barreau aimanté 50 g de résine Duolite CP 2000 micronisée, sous forme H+, et une solution de 48,5 g de buflomédil chlorhydrate dans 270 ml d'eau déminéralisée. Le produit est filtré et lavé à l'eau déminéralisée jusqu'à neutralité, puis séché en étuve à vide à 40 C jusqu'à un poids constant.
Poids de produit recueilli : 76,3 g (il y a de fortes pertes dues aux filtrations difficiles).
Dosage : 1 g de produit renferme 1,60 meq de buflomédil chlorhydrate, soit 49,1 % p/p exprimé en buflomédil base ou 55 % p/p exprimé en buflomédil chlorhydrate.
EXEMPLE 7
On utilise une résine Duolite CP 2110 du type échangeuse de cations fortement acide.
On utilise une résine Duolite CP 2110 du type échangeuse de cations fortement acide.
Dans un ballon de 1 litre on dissout 130 g de buflomédil chlorhydrate dans 500 ml d'eau déminéralisée.
On ajoute 130 g de résine CP 2100 micronisée, sous forme
H+. On agite à l'aide d'un barreau aimanté pendant 24 heures. On filtre et lave le produit à l'eau déminéralisée jusqu'à neutralité et le sèche en étuve à vide à 40 C, jusqu'à un poids constant.
H+. On agite à l'aide d'un barreau aimanté pendant 24 heures. On filtre et lave le produit à l'eau déminéralisée jusqu'à neutralité et le sèche en étuve à vide à 40 C, jusqu'à un poids constant.
Poids de produit recueilli : 220 g (il y a de fortes pertes dues aux filtrations difficiles).
Dosage : 1 g de produit renferme 1,51 meq de buflomédil chlorhydrate, soit 46,4 % p/p exprimé en buflomédil base ou 51,9 * p/p exprimé en buflomédil chlorhydrate.
EXEMPLE 8
Préparation d'un lyophilisat oral de buflomédil fixé sur résine cationique fortement acide obtenu selon l'exemple 6 ou 7.
Préparation d'un lyophilisat oral de buflomédil fixé sur résine cationique fortement acide obtenu selon l'exemple 6 ou 7.
Composition
Chlorhydrate de buflomédil) 320 mg contenant 150 mg de fixé sur résine cationique) chlorhydrate de buflomédil fortement acide
Edulcorant 35 mg
Aromatisant 26 mg
Dextran 70 000 20 mg
Aérosil 200 8 mg
Mannitol 606 mg
Eau comme solvant intermédiaire 700 mg.
Chlorhydrate de buflomédil) 320 mg contenant 150 mg de fixé sur résine cationique) chlorhydrate de buflomédil fortement acide
Edulcorant 35 mg
Aromatisant 26 mg
Dextran 70 000 20 mg
Aérosil 200 8 mg
Mannitol 606 mg
Eau comme solvant intermédiaire 700 mg.
Les différents composants sont mélangés pour former une suspension fluide que l'on répartit dans des alvéoles ronds en PVC. Le produit est introduit sur les plateaux d'un lyophilisateur, il est congelé à -40" C et lyophilisé.
En fin de lyophilisation les plaquettes sont fermées par une feuille d'aluminium enduit pour thermocollage.
Le produit fini a un goût tout-à-fait acceptable. On peut le prendre tel quel sans eau; on peut aussi le disperser dans un liquide.
EXEMPLE 9
Préparation d'un lyophilisat oral, sous forme émulsion, de buflomédil fixé sur résine cationique fortement acide obtenu selon l'exemple 6 ou 7.
Préparation d'un lyophilisat oral, sous forme émulsion, de buflomédil fixé sur résine cationique fortement acide obtenu selon l'exemple 6 ou 7.
Composition
Chlorhydrate de buflomédil) 320 mg (contenant 150 mg fixé sur résine fortement ) de buflomédil HCl) acide
Edulcorant 35 mg
Aromatisant 26 mg
Dextran 70 000 40 mg
Miglyol 812 50 mg
Poly éthoxy éther de glycérides gras 5 mg
Polysorbate 60 5 mg
Mannitol 526 mg
Solvant intermédiaire (eau) 700 mg
A. Préparation de la phase huileuse à 60 C
Miglyol 812 + Polyéthoxyéther de glycérides gras +
Polysorbate 60.
Chlorhydrate de buflomédil) 320 mg (contenant 150 mg fixé sur résine fortement ) de buflomédil HCl) acide
Edulcorant 35 mg
Aromatisant 26 mg
Dextran 70 000 40 mg
Miglyol 812 50 mg
Poly éthoxy éther de glycérides gras 5 mg
Polysorbate 60 5 mg
Mannitol 526 mg
Solvant intermédiaire (eau) 700 mg
A. Préparation de la phase huileuse à 60 C
Miglyol 812 + Polyéthoxyéther de glycérides gras +
Polysorbate 60.
B. Préparation de la phase aqueuse à 60 C : on mélange les autres éléments dans l'eau et porte à 60 C.
On mélange A et B et homogénéise.
On répartit l'émulsion obtenue dans des alvéoles ronds en PVC; on congèle et lyophilise.
Le produit obtenu est un solide poreux de goût acceptable.
Introduit dans l'eau, le produit se disperse rapidement et l'on obtient une suspension d'aspect laiteux.
On donnera ci-après les résultats d'une étude de la cinétique de libération du buflomédil administré sous forme
1) libre (comprimé de 150 mg)
2) fixé à une résine cationique fortement acide dans un lyophilisat oral simple (lyoc pâte)
3) fixé à une résine cationique fortement acide dans un lyophilisat oral émulsion (lyoc émulsion).
1) libre (comprimé de 150 mg)
2) fixé à une résine cationique fortement acide dans un lyophilisat oral simple (lyoc pâte)
3) fixé à une résine cationique fortement acide dans un lyophilisat oral émulsion (lyoc émulsion).
Le but de l'étude est
- de vérifier que l'adsorption du buflomédil sur résine ne provoquait pas sa séquestration dans des conditions physiologiques
- de comparer les cinétiques du buflomédil administré sous forme de comprimé (Fonzylane), de lyoc pâte, ou de lyoc émulsion.
- de vérifier que l'adsorption du buflomédil sur résine ne provoquait pas sa séquestration dans des conditions physiologiques
- de comparer les cinétiques du buflomédil administré sous forme de comprimé (Fonzylane), de lyoc pâte, ou de lyoc émulsion.
METHODE
Neuf chiens ont reçu les trois formes galéniques à une semaine d'intervalle suivant un plan expérimental en carrés latins. Chaque forme galénique était dosée à 150 mg de buflomédil. Les administrations étaient faites sur des chiens à jeun depuis 16 heures au moins.
Neuf chiens ont reçu les trois formes galéniques à une semaine d'intervalle suivant un plan expérimental en carrés latins. Chaque forme galénique était dosée à 150 mg de buflomédil. Les administrations étaient faites sur des chiens à jeun depuis 16 heures au moins.
A intervalle régulier, des prélèvements de sang étaient effectués sur héparine sèche. Après extraction puis séparation en chromatographie liquide haute performance, le buflomédil était dosé par spectrophotométrie dans 1 'ultra-violet.
L'ajustement des concentrations plasmatiques expérimentales sur un modèle mathématique ouvert à 1 compartiment avec cinétique de résorption et d'élimination d'ordre 1 a été effectué à l'aide de programme développé sur micro-ordinateur.
Pour le calcul de la clairance et du volume de distribution un facteur de biodisponibilité de 0,6 a été appliqué.
Les comparaisons statistiques des principaux paramètres pharmacocinétiques ont été réalisées en utilisant l'analyse de variance appliquée au carré latin; les comparaisons de traitements 2 à 2 ont été faites par le test de Games-Howell en cas de variances homogènes ou par la T-méthode en cas de variances inhomogènes. Enfin, un test non paramétrique a été utilisé. Toutes les comparaisons statistiques ont été faites sur microordinateur.
RESULTATS
Les concentrations plasmatiques moyennes pour les trois formes galéniques sont illustrées sur la figure unique.
Les concentrations plasmatiques moyennes pour les trois formes galéniques sont illustrées sur la figure unique.
L'étude de la figure unique montre que la résine ne séquestre pas le buflomédil. Toutefois cette libération n'est pas immédiate
- l'aspect général des courbes montre que la mise à disposition du buflomédil est plus lente avec les lyophilisats qu'avec le comprimé
- les valeurs de temps de latence à la résorption, des constantes de résorption et des temps de la concentration maximale expérimentale sont dans l'ordre croissant suivant : comprimé < lyoc pâte < lyoc émulsion ;
- les constantes et les demi-vies d'élimination biologique ne sont pas modifiées par la forme galénique ;
- les concentrations maximales expérimentales sont statistiquement très différentes ; l'analyse de variance révélant un facteur période important pour ce paramètre, une analyse effectuée uniquement sur les premiers passages montre également une différence entre les formes galéniques. Cette différence est significative entre la forme comprimé (la meilleure des formes pour ce paramètre) et la forme lyoc pâte (la moins bonne des formes) ; il n'y a aucune différence statistiquement significative avec la forme lyoc émulsion. Comme il n'y a pas de différence au niveau des demi-vies d'élimination biologique, cette différence ne peut être due qu'à une différence de mise à disposition ;
- les aires sous la courbe concentrations plasmatiques-temps ne sont pas différentes.
- l'aspect général des courbes montre que la mise à disposition du buflomédil est plus lente avec les lyophilisats qu'avec le comprimé
- les valeurs de temps de latence à la résorption, des constantes de résorption et des temps de la concentration maximale expérimentale sont dans l'ordre croissant suivant : comprimé < lyoc pâte < lyoc émulsion ;
- les constantes et les demi-vies d'élimination biologique ne sont pas modifiées par la forme galénique ;
- les concentrations maximales expérimentales sont statistiquement très différentes ; l'analyse de variance révélant un facteur période important pour ce paramètre, une analyse effectuée uniquement sur les premiers passages montre également une différence entre les formes galéniques. Cette différence est significative entre la forme comprimé (la meilleure des formes pour ce paramètre) et la forme lyoc pâte (la moins bonne des formes) ; il n'y a aucune différence statistiquement significative avec la forme lyoc émulsion. Comme il n'y a pas de différence au niveau des demi-vies d'élimination biologique, cette différence ne peut être due qu'à une différence de mise à disposition ;
- les aires sous la courbe concentrations plasmatiques-temps ne sont pas différentes.
L'adsorption de buflomédil sur une résine n'empêche pas sa libération en conditions physiologiques.
Cette mise à disposition est toutefois plus lente pour la forme lyoc pâte comparée à celle obtenue avec un comprimé.
Claims (8)
1. Composition pharmaceutique constituée par un composé de formule
dans laquelle A est choisi parmi les groupes de formule
dans laquelle R1 et R2 identiques ou différents représentent chacun un groupe alkyle en C1-C4, ou R1 et R2 forment ensemble avec l'atome d'azote auquel ils sont liés un groupe hétérocyclique de 5 à 7 chaînons pouvant contenir un second hétéroatome choisi parmi les atomes de soufre, d'azote et d'oxygène, et pouvant présenter des substituants choisis parmi les groupes alkyle en C1-C3 et hydroxyalkyle (C1-C3), ou un de ses sels d'addition avec des acides pharmaceutiquement acceptables, fixé sur une résine échangeuse d'ions, ayant une taille de particules inférieure à 200 micromètres.
2. Composition selon la revendication 1, dans laquelle la résine est une résine échangeuse de cations fortement acide.
3. Composition selon la revendication 1, dans laquelle la résine est une résine échangeuse de cations faiblement acide.
4. Composition selon l'une quelconque des revendications 1 à 3, dans laquelle la résine a une taille de 5 à 50 micromètres.
5. Composition selon l'une quelconque des revendications 1 à 3, dans laquelle le composé de formule
I représente de 10 à 50 i du poids de la composition.
6. Composition selon l'une quelconque des revendications 1 à 5 sous forme de particules enrobées d'une pellicule de type cellulosique ou acrylique.
7. Composition selon l'une quelconque des revendications 1 à 6, caractérisée en ce que le composé de formule I est le buflomédil.
8. Lyophilisat oral contenant une composition selon l'une quelconque des revendication 1 à 7.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR9106048A FR2676364B1 (fr) | 1991-05-17 | 1991-05-17 | Composition pharmaceutique a base de derives d'aminobutanone. |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR9106048A FR2676364B1 (fr) | 1991-05-17 | 1991-05-17 | Composition pharmaceutique a base de derives d'aminobutanone. |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| FR2676364A1 true FR2676364A1 (fr) | 1992-11-20 |
| FR2676364B1 FR2676364B1 (fr) | 1993-09-10 |
Family
ID=9412915
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| FR9106048A Expired - Fee Related FR2676364B1 (fr) | 1991-05-17 | 1991-05-17 | Composition pharmaceutique a base de derives d'aminobutanone. |
Country Status (1)
| Country | Link |
|---|---|
| FR (1) | FR2676364B1 (fr) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0622083A1 (fr) * | 1993-04-28 | 1994-11-02 | Takeda Chemical Industries, Ltd. | Préparation solide masquant le mauvais goût et sa production |
| WO1996005864A1 (fr) * | 1994-08-24 | 1996-02-29 | Hi Pharmtech | Forme pharmaceutique solide pour l'administration d'une substance active liquide liposoluble |
| WO1999004779A1 (fr) * | 1997-07-24 | 1999-02-04 | Astra Pharmaceuticals Ltd. | Formulation pharmaceutique comprenant un derive de 2-aminoacetamide et une resine echangeuse d'ions |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0188040A1 (fr) * | 1985-01-11 | 1986-07-23 | Abbott Laboratories Limited | Préparation solide à libération lente |
| JPS63183529A (ja) * | 1986-10-22 | 1988-07-28 | ビオメディカ・フォスカマ・インデュストリア・キミコ−ファルマチエウティカ・エッセ・ピ・ア | 放出がコントロールされた錠剤形の、ブフロメジル塩酸塩に基づく医薬調製物およびその製造方法 |
| EP0298864A1 (fr) * | 1987-07-08 | 1989-01-11 | Laboratoire L. Lafon | Filtre comprenant un matériau obtenu par cryodessiccation, procédé de préparation et utilisation notamment en galénique |
-
1991
- 1991-05-17 FR FR9106048A patent/FR2676364B1/fr not_active Expired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0188040A1 (fr) * | 1985-01-11 | 1986-07-23 | Abbott Laboratories Limited | Préparation solide à libération lente |
| JPS63183529A (ja) * | 1986-10-22 | 1988-07-28 | ビオメディカ・フォスカマ・インデュストリア・キミコ−ファルマチエウティカ・エッセ・ピ・ア | 放出がコントロールされた錠剤形の、ブフロメジル塩酸塩に基づく医薬調製物およびその製造方法 |
| EP0298864A1 (fr) * | 1987-07-08 | 1989-01-11 | Laboratoire L. Lafon | Filtre comprenant un matériau obtenu par cryodessiccation, procédé de préparation et utilisation notamment en galénique |
Non-Patent Citations (1)
| Title |
|---|
| BASE DE DONNEES: WPIL, numéro d'accèss 88-302441, Derwent Publications Ltd, Londres, GB; & JP-A-63 183 529 (BIOMEDICA FOSCAMA) 28-07-1988 * |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0622083A1 (fr) * | 1993-04-28 | 1994-11-02 | Takeda Chemical Industries, Ltd. | Préparation solide masquant le mauvais goût et sa production |
| US5464612A (en) * | 1993-04-28 | 1995-11-07 | Takeda Chemical Industries, Ltd. | Solid preparation comprising ion exchanger and active agent |
| WO1996005864A1 (fr) * | 1994-08-24 | 1996-02-29 | Hi Pharmtech | Forme pharmaceutique solide pour l'administration d'une substance active liquide liposoluble |
| FR2723846A1 (fr) * | 1994-08-24 | 1996-03-01 | Hi Pharmtech | Forme pharmaceutique solide pour l'administration d'une substance active liquide liposoluble |
| WO1999004779A1 (fr) * | 1997-07-24 | 1999-02-04 | Astra Pharmaceuticals Ltd. | Formulation pharmaceutique comprenant un derive de 2-aminoacetamide et une resine echangeuse d'ions |
| US6193962B1 (en) | 1997-07-24 | 2001-02-27 | Astrazeneca Uk Limited | Pharmaceutical formulation comprising a 2-aminoacetamide derivative and an ion exchange resin |
Also Published As
| Publication number | Publication date |
|---|---|
| FR2676364B1 (fr) | 1993-09-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20230165837A1 (en) | Novel clonidine formulation | |
| CA2952223C (fr) | Formulations de treprostinil | |
| EP0330532B1 (fr) | Nouvelle forme galénique du fénofibrate | |
| EP2605757B1 (fr) | Formulations a base de nalbuphine et leurs utilisations | |
| EP0256933A1 (fr) | Procédé de préparation d'un médicament à base de fénofibrate, médicament obtenu par ce procédé | |
| EP2349217A1 (fr) | Nouvelle composition à base d'acide gamma-hydroxybutyrique | |
| JPH09508619A (ja) | ポリ不飽和脂肪酸の塩とこれらを含む医薬製剤 | |
| EP0757911A1 (fr) | Nouvelles formulations galéniques du fénofibrate et leurs applications | |
| BE1015217A5 (fr) | ||
| EP0078785A1 (fr) | Sels d'acide valproîque, leur préparation et leur utilisation | |
| FR2541287A1 (fr) | Preparation stable administrable par voie orale de macrolides antibiotiques et procede pour les stabiliser | |
| PL194847B1 (pl) | Sposób wytwarzania nowych fenofibratowych preparatów galenowych, otrzymane preparaty galenowe i zastosowanie ciekłego medium | |
| EP1372617B1 (fr) | Sels de cetoacides et d'acides amines gastroresistants et leur utilisation pour la preparation de medicaments | |
| FR2676364A1 (fr) | Composition pharmaceutique a base de derives d'aminobutanone. | |
| LU83363A1 (fr) | Compositions antitumeurs | |
| HU229409B1 (en) | Compositions comprising modafinil compounds | |
| CA2354574C (fr) | Troxerutine a forte teneur en trihydroxy-ethyl-rutoside et procede de preparation | |
| JPH11286440A (ja) | 口粘膜経路用の、特に鼻腔経路用の新規な調合剤 | |
| US11918689B1 (en) | Liquid clonidine extended release composition | |
| EP0412877A1 (fr) | Nouvelle forme galénique orale améliorant la biodisponibilité | |
| BE1000087A3 (fr) | Compositions pharmaceutiques contenant de la vinburnine et leur procede de preparation. | |
| EP0406743A2 (fr) | Compositions parmaceutiques gastroprotectrices contenant des sels de N-benzyl-N-((1S,5S)-6,6-diméthylbicyclo[3.1.1]hept-2-yl-éthoxy-éthyl)-morpholinium | |
| JPS5813511A (ja) | 光不安定性医薬の被包用軟カプセル | |
| BRPI0607372B1 (pt) | Medicamento destinado à administração oral, compreendendo um inibidor da ciclooxigenase-2, e método de preparação do mesmo | |
| FR2816944A1 (fr) | Nouveaux sels de lithium, les compositions pharmaceutiques a base de ces sels de lithium et leurs applications comme medicament |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ST | Notification of lapse |
Effective date: 20080131 |