ES2899639T3 - Betaína para la prevención de la obesidad - Google Patents
Betaína para la prevención de la obesidad Download PDFInfo
- Publication number
- ES2899639T3 ES2899639T3 ES18722567T ES18722567T ES2899639T3 ES 2899639 T3 ES2899639 T3 ES 2899639T3 ES 18722567 T ES18722567 T ES 18722567T ES 18722567 T ES18722567 T ES 18722567T ES 2899639 T3 ES2899639 T3 ES 2899639T3
- Authority
- ES
- Spain
- Prior art keywords
- betaine
- betaine compound
- subject
- obesity
- use according
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- KWIUHFFTVRNATP-UHFFFAOYSA-N Betaine Natural products C[N+](C)(C)CC([O-])=O KWIUHFFTVRNATP-UHFFFAOYSA-N 0.000 title claims abstract description 252
- 229960003237 betaine Drugs 0.000 title claims abstract description 170
- 208000008589 Obesity Diseases 0.000 title claims abstract description 60
- 235000020824 obesity Nutrition 0.000 title claims abstract description 60
- 230000002265 prevention Effects 0.000 title claims abstract description 43
- KWIUHFFTVRNATP-UHFFFAOYSA-O N,N,N-trimethylglycinium Chemical compound C[N+](C)(C)CC(O)=O KWIUHFFTVRNATP-UHFFFAOYSA-O 0.000 title 1
- -1 betaine compound Chemical class 0.000 claims abstract description 81
- 238000009825 accumulation Methods 0.000 claims abstract description 26
- 208000030159 metabolic disease Diseases 0.000 claims abstract description 18
- 239000000203 mixture Substances 0.000 claims description 51
- 230000006651 lactation Effects 0.000 claims description 27
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 24
- 238000011282 treatment Methods 0.000 claims description 22
- 239000000969 carrier Substances 0.000 claims description 18
- 235000015872 dietary supplement Nutrition 0.000 claims description 15
- 235000013350 formula milk Nutrition 0.000 claims description 15
- 239000008194 pharmaceutical composition Substances 0.000 claims description 9
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims description 4
- 125000004429 atom Chemical group 0.000 claims description 4
- 229910052736 halogen Inorganic materials 0.000 claims description 4
- 150000002367 halogens Chemical class 0.000 claims description 4
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 claims description 2
- 125000005843 halogen group Chemical group 0.000 claims description 2
- 125000001424 substituent group Chemical group 0.000 claims description 2
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 28
- 235000013336 milk Nutrition 0.000 description 28
- 239000008267 milk Substances 0.000 description 28
- 210000004080 milk Anatomy 0.000 description 28
- 241000699670 Mus sp. Species 0.000 description 27
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 22
- 230000035508 accumulation Effects 0.000 description 21
- 235000005911 diet Nutrition 0.000 description 21
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 19
- 239000008103 glucose Substances 0.000 description 19
- 230000037213 diet Effects 0.000 description 18
- 244000005709 gut microbiome Species 0.000 description 18
- 230000009469 supplementation Effects 0.000 description 18
- 230000001965 increasing effect Effects 0.000 description 17
- 230000008774 maternal effect Effects 0.000 description 17
- 241000282414 Homo sapiens Species 0.000 description 16
- 230000012010 growth Effects 0.000 description 16
- 230000037396 body weight Effects 0.000 description 15
- 102000004877 Insulin Human genes 0.000 description 14
- 108090001061 Insulin Proteins 0.000 description 14
- 208000035475 disorder Diseases 0.000 description 14
- 208000015181 infectious disease Diseases 0.000 description 14
- 229940125396 insulin Drugs 0.000 description 14
- 206010033307 Overweight Diseases 0.000 description 12
- 238000004458 analytical method Methods 0.000 description 12
- 230000003247 decreasing effect Effects 0.000 description 12
- 230000007358 intestinal barrier function Effects 0.000 description 12
- 230000002503 metabolic effect Effects 0.000 description 12
- 150000001875 compounds Chemical class 0.000 description 11
- 230000000694 effects Effects 0.000 description 11
- 238000000034 method Methods 0.000 description 11
- ZJUKTBDSGOFHSH-WFMPWKQPSA-N S-Adenosylhomocysteine Chemical compound O[C@@H]1[C@H](O)[C@@H](CSCC[C@H](N)C(O)=O)O[C@H]1N1C2=NC=NC(N)=C2N=C1 ZJUKTBDSGOFHSH-WFMPWKQPSA-N 0.000 description 10
- 208000015380 nutritional deficiency disease Diseases 0.000 description 10
- 230000009286 beneficial effect Effects 0.000 description 9
- 230000036541 health Effects 0.000 description 9
- 235000009200 high fat diet Nutrition 0.000 description 9
- 210000004185 liver Anatomy 0.000 description 9
- 235000019786 weight gain Nutrition 0.000 description 9
- YPWSLBHSMIKTPR-UHFFFAOYSA-N Cystathionine Natural products OC(=O)C(N)CCSSCC(N)C(O)=O YPWSLBHSMIKTPR-UHFFFAOYSA-N 0.000 description 8
- ILRYLPWNYFXEMH-UHFFFAOYSA-N D-cystathionine Natural products OC(=O)C(N)CCSCC(N)C(O)=O ILRYLPWNYFXEMH-UHFFFAOYSA-N 0.000 description 8
- 208000027244 Dysbiosis Diseases 0.000 description 8
- ILRYLPWNYFXEMH-WHFBIAKZSA-N L-cystathionine Chemical compound [O-]C(=O)[C@@H]([NH3+])CCSC[C@H]([NH3+])C([O-])=O ILRYLPWNYFXEMH-WHFBIAKZSA-N 0.000 description 8
- 241001465754 Metazoa Species 0.000 description 8
- MEFKEPWMEQBLKI-AIRLBKTGSA-N S-adenosyl-L-methioninate Chemical compound O[C@@H]1[C@H](O)[C@@H](C[S+](CC[C@H](N)C([O-])=O)C)O[C@H]1N1C2=NC=NC(N)=C2N=C1 MEFKEPWMEQBLKI-AIRLBKTGSA-N 0.000 description 8
- 229960001570 ademetionine Drugs 0.000 description 8
- 230000008901 benefit Effects 0.000 description 8
- 201000010099 disease Diseases 0.000 description 8
- 230000007140 dysbiosis Effects 0.000 description 8
- ZNOVTXRBGFNYRX-ABLWVSNPSA-N levomefolic acid Chemical compound C1NC=2NC(N)=NC(=O)C=2N(C)C1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 ZNOVTXRBGFNYRX-ABLWVSNPSA-N 0.000 description 8
- 235000007635 levomefolic acid Nutrition 0.000 description 8
- 239000011578 levomefolic acid Substances 0.000 description 8
- 241000282412 Homo Species 0.000 description 7
- 208000002720 Malnutrition Diseases 0.000 description 7
- 208000007683 Pediatric Obesity Diseases 0.000 description 7
- 238000000692 Student's t-test Methods 0.000 description 7
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 7
- 229960001231 choline Drugs 0.000 description 7
- 235000020256 human milk Nutrition 0.000 description 7
- 210000004251 human milk Anatomy 0.000 description 7
- 230000000968 intestinal effect Effects 0.000 description 7
- 235000000824 malnutrition Nutrition 0.000 description 7
- 230000001071 malnutrition Effects 0.000 description 7
- 238000012353 t test Methods 0.000 description 7
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 7
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 6
- 208000025972 Maternal Obesity Diseases 0.000 description 6
- 235000013305 food Nutrition 0.000 description 6
- 230000006872 improvement Effects 0.000 description 6
- 230000010034 metabolic health Effects 0.000 description 6
- 239000002207 metabolite Substances 0.000 description 6
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 6
- 230000009885 systemic effect Effects 0.000 description 6
- 230000004584 weight gain Effects 0.000 description 6
- 206010020772 Hypertension Diseases 0.000 description 5
- 102000004889 Interleukin-6 Human genes 0.000 description 5
- 108090001005 Interleukin-6 Proteins 0.000 description 5
- FFFHZYDWPBMWHY-VKHMYHEASA-N L-homocysteine Chemical compound OC(=O)[C@@H](N)CCS FFFHZYDWPBMWHY-VKHMYHEASA-N 0.000 description 5
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 5
- CMUNUTVVOOHQPW-LURJTMIESA-N L-proline betaine Chemical compound C[N+]1(C)CCC[C@H]1C([O-])=O CMUNUTVVOOHQPW-LURJTMIESA-N 0.000 description 5
- 230000001580 bacterial effect Effects 0.000 description 5
- 229910052799 carbon Inorganic materials 0.000 description 5
- 230000014509 gene expression Effects 0.000 description 5
- 210000002175 goblet cell Anatomy 0.000 description 5
- 230000002757 inflammatory effect Effects 0.000 description 5
- 239000004615 ingredient Substances 0.000 description 5
- 230000007774 longterm Effects 0.000 description 5
- 108020004999 messenger RNA Proteins 0.000 description 5
- 230000004060 metabolic process Effects 0.000 description 5
- 229930182817 methionine Natural products 0.000 description 5
- 235000015097 nutrients Nutrition 0.000 description 5
- 235000016709 nutrition Nutrition 0.000 description 5
- 230000035764 nutrition Effects 0.000 description 5
- 239000000843 powder Substances 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 230000002441 reversible effect Effects 0.000 description 5
- 210000001519 tissue Anatomy 0.000 description 5
- 241000702460 Akkermansia Species 0.000 description 4
- SPTHHTGLGVZZRH-UHFFFAOYSA-N Arsenobetaine Chemical compound C[As+](C)(C)CC([O-])=O SPTHHTGLGVZZRH-UHFFFAOYSA-N 0.000 description 4
- 102100021943 C-C motif chemokine 2 Human genes 0.000 description 4
- 101710155857 C-C motif chemokine 2 Proteins 0.000 description 4
- 208000032928 Dyslipidaemia Diseases 0.000 description 4
- 208000017170 Lipid metabolism disease Diseases 0.000 description 4
- 101150058357 Muc2 gene Proteins 0.000 description 4
- 101150082427 Tlr4 gene Proteins 0.000 description 4
- 230000007423 decrease Effects 0.000 description 4
- 230000037406 food intake Effects 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- 238000012423 maintenance Methods 0.000 description 4
- WEXRUCMBJFQVBZ-UHFFFAOYSA-N pentobarbital Chemical compound CCCC(C)C1(CC)C(=O)NC(=O)NC1=O WEXRUCMBJFQVBZ-UHFFFAOYSA-N 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 108090000623 proteins and genes Proteins 0.000 description 4
- 201000002859 sleep apnea Diseases 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- MUNWAHDYFVYIKH-RITPCOANSA-N trans-4-hydroxy-L-proline betaine Chemical compound C[N+]1(C)C[C@H](O)C[C@H]1C([O-])=O MUNWAHDYFVYIKH-RITPCOANSA-N 0.000 description 4
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 3
- 241000702462 Akkermansia muciniphila Species 0.000 description 3
- 208000024172 Cardiovascular disease Diseases 0.000 description 3
- 101150003028 Hprt1 gene Proteins 0.000 description 3
- 206010061218 Inflammation Diseases 0.000 description 3
- 206010022489 Insulin Resistance Diseases 0.000 description 3
- 206010028980 Neoplasm Diseases 0.000 description 3
- 108010022233 Plasminogen Activator Inhibitor 1 Proteins 0.000 description 3
- 102100039418 Plasminogen activator inhibitor 1 Human genes 0.000 description 3
- 206010042576 Suppressed lactation Diseases 0.000 description 3
- 208000026935 allergic disease Diseases 0.000 description 3
- 150000001413 amino acids Chemical class 0.000 description 3
- 239000003242 anti bacterial agent Substances 0.000 description 3
- 229940088710 antibiotic agent Drugs 0.000 description 3
- 230000003115 biocidal effect Effects 0.000 description 3
- 210000000481 breast Anatomy 0.000 description 3
- 208000029078 coronary artery disease Diseases 0.000 description 3
- 230000002596 correlated effect Effects 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 230000000378 dietary effect Effects 0.000 description 3
- 239000004744 fabric Substances 0.000 description 3
- 235000012631 food intake Nutrition 0.000 description 3
- 235000019253 formic acid Nutrition 0.000 description 3
- 230000002496 gastric effect Effects 0.000 description 3
- 239000008187 granular material Substances 0.000 description 3
- 230000004054 inflammatory process Effects 0.000 description 3
- 238000001294 liquid chromatography-tandem mass spectrometry Methods 0.000 description 3
- 230000003050 macronutrient Effects 0.000 description 3
- 235000021073 macronutrients Nutrition 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 230000000813 microbial effect Effects 0.000 description 3
- 230000035935 pregnancy Effects 0.000 description 3
- 102000004169 proteins and genes Human genes 0.000 description 3
- 230000000241 respiratory effect Effects 0.000 description 3
- 235000021391 short chain fatty acids Nutrition 0.000 description 3
- 150000004666 short chain fatty acids Chemical class 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 3
- 230000004580 weight loss Effects 0.000 description 3
- FFFHZYDWPBMWHY-ZDDHPQOTSA-N (2S)-2,3-dideuterio-2-(dideuterioamino)-4-sulfanylbutanoic acid Chemical compound N([C@@](C(CS)[2H])(C(=O)O)[2H])([2H])[2H] FFFHZYDWPBMWHY-ZDDHPQOTSA-N 0.000 description 2
- 208000037487 Endotoxemia Diseases 0.000 description 2
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- WZUVPPKBWHMQCE-UHFFFAOYSA-N Haematoxylin Chemical compound C12=CC(O)=C(O)C=C2CC2(O)C1C1=CC=C(O)C(O)=C1OC2 WZUVPPKBWHMQCE-UHFFFAOYSA-N 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 238000000585 Mann–Whitney U test Methods 0.000 description 2
- 241000736262 Microbiota Species 0.000 description 2
- 241000906086 Miris Species 0.000 description 2
- 241000699666 Mus <mouse, genus> Species 0.000 description 2
- 229930193140 Neomycin Natural products 0.000 description 2
- 241000605947 Roseburia Species 0.000 description 2
- 238000010162 Tukey test Methods 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 210000001789 adipocyte Anatomy 0.000 description 2
- 210000000577 adipose tissue Anatomy 0.000 description 2
- 230000004075 alteration Effects 0.000 description 2
- 229960000723 ampicillin Drugs 0.000 description 2
- AVKUERGKIZMTKX-NJBDSQKTSA-N ampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 AVKUERGKIZMTKX-NJBDSQKTSA-N 0.000 description 2
- 235000008452 baby food Nutrition 0.000 description 2
- 238000007622 bioinformatic analysis Methods 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 201000011510 cancer Diseases 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 150000001720 carbohydrates Chemical class 0.000 description 2
- 235000014633 carbohydrates Nutrition 0.000 description 2
- 210000004027 cell Anatomy 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 239000002299 complementary DNA Substances 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 230000002550 fecal effect Effects 0.000 description 2
- OVBPIULPVIDEAO-LBPRGKRZSA-N folic acid Chemical compound C=1N=C2NC(N)=NC(=O)C2=NC=1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 OVBPIULPVIDEAO-LBPRGKRZSA-N 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 230000007773 growth pattern Effects 0.000 description 2
- 210000003128 head Anatomy 0.000 description 2
- 230000002440 hepatic effect Effects 0.000 description 2
- AOHCBEAZXHZMOR-ZDUSSCGKSA-N hypaphorine Chemical compound C1=CC=C2C(C[C@H]([N+](C)(C)C)C([O-])=O)=CNC2=C1 AOHCBEAZXHZMOR-ZDUSSCGKSA-N 0.000 description 2
- 210000003405 ileum Anatomy 0.000 description 2
- 230000005847 immunogenicity Effects 0.000 description 2
- 230000001771 impaired effect Effects 0.000 description 2
- 210000005027 intestinal barrier Anatomy 0.000 description 2
- 238000007912 intraperitoneal administration Methods 0.000 description 2
- 208000002551 irritable bowel syndrome Diseases 0.000 description 2
- 230000007794 irritation Effects 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 239000007937 lozenge Substances 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 238000004949 mass spectrometry Methods 0.000 description 2
- 230000013011 mating Effects 0.000 description 2
- 230000035800 maturation Effects 0.000 description 2
- 244000005700 microbiome Species 0.000 description 2
- 238000010172 mouse model Methods 0.000 description 2
- 229960004927 neomycin Drugs 0.000 description 2
- 239000002417 nutraceutical Substances 0.000 description 2
- 235000021436 nutraceutical agent Nutrition 0.000 description 2
- 229920001542 oligosaccharide Polymers 0.000 description 2
- 150000002482 oligosaccharides Chemical class 0.000 description 2
- 238000001543 one-way ANOVA Methods 0.000 description 2
- 244000052769 pathogen Species 0.000 description 2
- 229960001412 pentobarbital Drugs 0.000 description 2
- YPJUNDFVDDCYIH-UHFFFAOYSA-N perfluorobutyric acid Chemical compound OC(=O)C(F)(F)C(F)(F)C(F)(F)F YPJUNDFVDDCYIH-UHFFFAOYSA-N 0.000 description 2
- 230000005180 public health Effects 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 239000013589 supplement Substances 0.000 description 2
- 238000011477 surgical intervention Methods 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 239000006188 syrup Substances 0.000 description 2
- 235000020357 syrup Nutrition 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- 231100000419 toxicity Toxicity 0.000 description 2
- 230000001988 toxicity Effects 0.000 description 2
- 150000003626 triacylglycerols Chemical class 0.000 description 2
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 1
- 108020004465 16S ribosomal RNA Proteins 0.000 description 1
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- 241001156739 Actinobacteria <phylum> Species 0.000 description 1
- 239000004956 Amodel Substances 0.000 description 1
- 206010002091 Anaesthesia Diseases 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 108020000946 Bacterial DNA Proteins 0.000 description 1
- FERIUCNNQQJTOY-UHFFFAOYSA-M Butyrate Chemical compound CCCC([O-])=O FERIUCNNQQJTOY-UHFFFAOYSA-M 0.000 description 1
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Natural products CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 1
- 102000000018 Chemokine CCL2 Human genes 0.000 description 1
- 208000017667 Chronic Disease Diseases 0.000 description 1
- 208000015943 Coeliac disease Diseases 0.000 description 1
- 238000007399 DNA isolation Methods 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- 206010014733 Endometrial cancer Diseases 0.000 description 1
- 206010014759 Endometrial neoplasm Diseases 0.000 description 1
- 108700039887 Essential Genes Proteins 0.000 description 1
- 208000001362 Fetal Growth Retardation Diseases 0.000 description 1
- 208000030271 Fetal Nutrition disease Diseases 0.000 description 1
- 206010070531 Foetal growth restriction Diseases 0.000 description 1
- 206010016862 Foetal malnutrition Diseases 0.000 description 1
- 208000005577 Gastroenteritis Diseases 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 208000034826 Genetic Predisposition to Disease Diseases 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 206010053759 Growth retardation Diseases 0.000 description 1
- PMMYEEVYMWASQN-DMTCNVIQSA-N Hydroxyproline Chemical compound O[C@H]1CN[C@H](C(O)=O)C1 PMMYEEVYMWASQN-DMTCNVIQSA-N 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 206010022678 Intestinal infections Diseases 0.000 description 1
- 108010092277 Leptin Proteins 0.000 description 1
- 102000016267 Leptin Human genes 0.000 description 1
- 101710091439 Major capsid protein 1 Proteins 0.000 description 1
- OVBPIULPVIDEAO-UHFFFAOYSA-N N-Pteroyl-L-glutaminsaeure Natural products C=1N=C2NC(N)=NC(=O)C2=NC=1CNC1=CC=C(C(=O)NC(CCC(O)=O)C(O)=O)C=C1 OVBPIULPVIDEAO-UHFFFAOYSA-N 0.000 description 1
- 241000785902 Odoribacter Species 0.000 description 1
- 241001607451 Oscillospiraceae Species 0.000 description 1
- 238000001358 Pearson's chi-squared test Methods 0.000 description 1
- 241000589516 Pseudomonas Species 0.000 description 1
- 238000011529 RT qPCR Methods 0.000 description 1
- 229920000294 Resistant starch Polymers 0.000 description 1
- 208000006011 Stroke Diseases 0.000 description 1
- 239000012163 TRI reagent Substances 0.000 description 1
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 1
- 102100040247 Tumor necrosis factor Human genes 0.000 description 1
- 229930003779 Vitamin B12 Natural products 0.000 description 1
- 229930003448 Vitamin K Natural products 0.000 description 1
- 210000000579 abdominal fat Anatomy 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 210000003486 adipose tissue brown Anatomy 0.000 description 1
- 210000000593 adipose tissue white Anatomy 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- 230000037005 anaesthesia Effects 0.000 description 1
- 238000000540 analysis of variance Methods 0.000 description 1
- 230000000845 anti-microbial effect Effects 0.000 description 1
- 238000003149 assay kit Methods 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 239000000090 biomarker Substances 0.000 description 1
- 238000007707 calorimetry Methods 0.000 description 1
- 150000001721 carbon Chemical class 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 239000007910 chewable tablet Substances 0.000 description 1
- 229940068682 chewable tablet Drugs 0.000 description 1
- 229940112822 chewing gum Drugs 0.000 description 1
- 235000015218 chewing gum Nutrition 0.000 description 1
- 235000015111 chews Nutrition 0.000 description 1
- WORJEOGGNQDSOE-UHFFFAOYSA-N chloroform;methanol Chemical compound OC.ClC(Cl)Cl WORJEOGGNQDSOE-UHFFFAOYSA-N 0.000 description 1
- 238000011260 co-administration Methods 0.000 description 1
- FDJOLVPMNUYSCM-WZHZPDAFSA-L cobalt(3+);[(2r,3s,4r,5s)-5-(5,6-dimethylbenzimidazol-1-yl)-4-hydroxy-2-(hydroxymethyl)oxolan-3-yl] [(2r)-1-[3-[(1r,2r,3r,4z,7s,9z,12s,13s,14z,17s,18s,19r)-2,13,18-tris(2-amino-2-oxoethyl)-7,12,17-tris(3-amino-3-oxopropyl)-3,5,8,8,13,15,18,19-octamethyl-2 Chemical compound [Co+3].N#[C-].N([C@@H]([C@]1(C)[N-]\C([C@H]([C@@]1(CC(N)=O)C)CCC(N)=O)=C(\C)/C1=N/C([C@H]([C@@]1(CC(N)=O)C)CCC(N)=O)=C\C1=N\C([C@H](C1(C)C)CCC(N)=O)=C/1C)[C@@H]2CC(N)=O)=C\1[C@]2(C)CCC(=O)NC[C@@H](C)OP([O-])(=O)O[C@H]1[C@@H](O)[C@@H](N2C3=CC(C)=C(C)C=C3N=C2)O[C@@H]1CO FDJOLVPMNUYSCM-WZHZPDAFSA-L 0.000 description 1
- 230000008133 cognitive development Effects 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 235000008504 concentrate Nutrition 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 235000009508 confectionery Nutrition 0.000 description 1
- 230000001186 cumulative effect Effects 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 230000007123 defense Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 235000013325 dietary fiber Nutrition 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- VHJLVAABSRFDPM-QWWZWVQMSA-N dithiothreitol Chemical compound SC[C@@H](O)[C@H](O)CS VHJLVAABSRFDPM-QWWZWVQMSA-N 0.000 description 1
- PMMYEEVYMWASQN-UHFFFAOYSA-N dl-hydroxyproline Natural products OC1C[NH2+]C(C([O-])=O)C1 PMMYEEVYMWASQN-UHFFFAOYSA-N 0.000 description 1
- 239000006196 drop Substances 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 235000006694 eating habits Nutrition 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- YQGOJNYOYNNSMM-UHFFFAOYSA-N eosin Chemical compound [Na+].OC(=O)C1=CC=CC=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C(O)=C(Br)C=C21 YQGOJNYOYNNSMM-UHFFFAOYSA-N 0.000 description 1
- 201000010063 epididymitis Diseases 0.000 description 1
- 238000010195 expression analysis Methods 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 210000003608 fece Anatomy 0.000 description 1
- ZXKXJHAOUFHNAS-UHFFFAOYSA-N fenfluramine hydrochloride Chemical compound [Cl-].CC[NH2+]C(C)CC1=CC=CC(C(F)(F)F)=C1 ZXKXJHAOUFHNAS-UHFFFAOYSA-N 0.000 description 1
- 208000030941 fetal growth restriction Diseases 0.000 description 1
- 239000010408 film Substances 0.000 description 1
- 235000019152 folic acid Nutrition 0.000 description 1
- 239000011724 folic acid Substances 0.000 description 1
- 229960000304 folic acid Drugs 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- ZZUFCTLCJUWOSV-UHFFFAOYSA-N furosemide Chemical compound C1=C(Cl)C(S(=O)(=O)N)=CC(C(O)=O)=C1NCC1=CC=CO1 ZZUFCTLCJUWOSV-UHFFFAOYSA-N 0.000 description 1
- 208000020694 gallbladder disease Diseases 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 231100000001 growth retardation Toxicity 0.000 description 1
- 230000009554 growth spurt Effects 0.000 description 1
- 230000005802 health problem Effects 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 125000001183 hydrocarbyl group Chemical group 0.000 description 1
- 238000002013 hydrophilic interaction chromatography Methods 0.000 description 1
- 229960002591 hydroxyproline Drugs 0.000 description 1
- 238000007654 immersion Methods 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 208000027866 inflammatory disease Diseases 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 235000001705 insufficient nutrition Nutrition 0.000 description 1
- 229940100601 interleukin-6 Drugs 0.000 description 1
- 230000009545 invasion Effects 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 235000015110 jellies Nutrition 0.000 description 1
- 239000008274 jelly Substances 0.000 description 1
- 229940039781 leptin Drugs 0.000 description 1
- NRYBAZVQPHGZNS-ZSOCWYAHSA-N leptin Chemical compound O=C([C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](N)CC(C)C)CCSC)N1CCC[C@H]1C(=O)NCC(=O)N[C@@H](CS)C(O)=O NRYBAZVQPHGZNS-ZSOCWYAHSA-N 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 230000006372 lipid accumulation Effects 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- 208000019423 liver disease Diseases 0.000 description 1
- 244000144972 livestock Species 0.000 description 1
- 230000006742 locomotor activity Effects 0.000 description 1
- 230000005923 long-lasting effect Effects 0.000 description 1
- 208000018773 low birth weight Diseases 0.000 description 1
- 231100000533 low birth weight Toxicity 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 230000009985 maternal smoking Effects 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 230000003818 metabolic dysfunction Effects 0.000 description 1
- 238000002705 metabolomic analysis Methods 0.000 description 1
- 230000001431 metabolomic effect Effects 0.000 description 1
- 239000000401 methanolic extract Substances 0.000 description 1
- 229960004452 methionine Drugs 0.000 description 1
- 238000004476 mid-IR spectroscopy Methods 0.000 description 1
- 208000001022 morbid obesity Diseases 0.000 description 1
- 230000007659 motor function Effects 0.000 description 1
- 230000000474 nursing effect Effects 0.000 description 1
- 235000003715 nutritional status Nutrition 0.000 description 1
- 238000013116 obese mouse model Methods 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 235000019198 oils Nutrition 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 239000006072 paste Substances 0.000 description 1
- 230000008506 pathogenesis Effects 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 206010034674 peritonitis Diseases 0.000 description 1
- SHUZOJHMOBOZST-UHFFFAOYSA-N phylloquinone Natural products CC(C)CCCCC(C)CCC(C)CCCC(=CCC1=C(C)C(=O)c2ccccc2C1=O)C SHUZOJHMOBOZST-UHFFFAOYSA-N 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 235000017924 poor diet Nutrition 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 230000000770 proinflammatory effect Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 235000021254 resistant starch Nutrition 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 230000037152 sensory function Effects 0.000 description 1
- 230000014639 sexual reproduction Effects 0.000 description 1
- 210000002027 skeletal muscle Anatomy 0.000 description 1
- 238000007682 sleeve gastrectomy Methods 0.000 description 1
- 235000021055 solid food Nutrition 0.000 description 1
- 239000012086 standard solution Substances 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 238000004885 tandem mass spectrometry Methods 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 108700012359 toxins Proteins 0.000 description 1
- 230000005945 translocation Effects 0.000 description 1
- 238000009966 trimming Methods 0.000 description 1
- 238000004704 ultra performance liquid chromatography Methods 0.000 description 1
- 235000000112 undernutrition Nutrition 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 235000019163 vitamin B12 Nutrition 0.000 description 1
- 239000011715 vitamin B12 Substances 0.000 description 1
- 235000019168 vitamin K Nutrition 0.000 description 1
- 239000011712 vitamin K Substances 0.000 description 1
- 150000003721 vitamin K derivatives Chemical class 0.000 description 1
- 229940046010 vitamin k Drugs 0.000 description 1
- 239000003643 water by type Substances 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/205—Amine addition salts of organic acids; Inner quaternary ammonium salts, e.g. betaine, carnitine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/28—Compounds containing heavy metals
- A61K31/285—Arsenic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/401—Proline; Derivatives thereof, e.g. captopril
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
- A61K31/405—Indole-alkanecarboxylic acids; Derivatives thereof, e.g. tryptophan, indomethacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/24—Heavy metals; Compounds thereof
- A61K33/36—Arsenic; Compounds thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/20—Milk; Whey; Colostrum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Hematology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Diabetes (AREA)
- Child & Adolescent Psychology (AREA)
- Obesity (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Cell Biology (AREA)
- Developmental Biology & Embryology (AREA)
- Immunology (AREA)
- Virology (AREA)
- Zoology (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Dairy Products (AREA)
- Coloring Foods And Improving Nutritive Qualities (AREA)
Abstract
Un compuesto de betaína para su uso en la prevención de la obesidad, la acumulación excesiva de grasa y/o los trastornos metabólicos asociados a cualquiera de los anteriores en un sujeto, en el que la prevención comprende administrar el compuesto de betaína directamente al sujeto durante la infancia o, alternativamente, a la madre del sujeto durante la lactancia.
Description
DESCRIPCIÓN
Betaína para la prevención de la obesidad
Esta solicitud reivindica el beneficio de la solicitud de patente europea EP17382270.1 presentada el 12.05.2017.
Campo de la técnica
La presente invención se refiere al campo de la nutrición y la enfermedad, más particularmente con la prevención y el tratamiento de la obesidad y las enfermedades relacionadas.
Estado de la técnica
La obesidad está ampliamente reconocida como una enfermedad crónica asociada a muchos problemas de salud graves, como la diabetes de tipo 2, las enfermedades cardiovasculares, la hipertensión y al menos una docena de tipos de cáncer. En las últimas tres décadas, la prevalencia de la obesidad y el sobrepeso ha aumentado considerablemente y afecta a más de 600 millones de personas en todo el mundo. Las autoridades de todo el mundo la consideran uno de los problemas de salud pública más graves del siglo XXI.
El aumento excesivo de peso está influido por un amplio abanico de factores, como la predisposición genética, la alimentación inadecuada, el comportamiento individual y los factores ambientales y sociales. El papel de los nutrientes de la dieta en la obesidad se ha debatido durante mucho tiempo y se han realizado numerosos estudios para encontrar compuestos útiles en la prevención y el tratamiento de la obesidad, con un éxito limitado. A pesar de la intensa investigación sobre terapias y suplementos dietéticos, el estándar de oro para la prevención y el tratamiento de la obesidad es la dieta y el ejercicio físico. Sin embargo, los programas de dietas suelen producir una pérdida de peso a corto plazo, pero el mantenimiento de esta pérdida de peso es difícil, ya que a menudo requiere un ejercicio continuo y una dieta permanente de menor energía alimentaria. El incumplimiento de este régimen y el consiguiente aumento de peso es especialmente elevado en la población obesa y con sobrepeso.
Las intervenciones quirúrgicas son eficaces para el tratamiento de la obesidad y se realizan de forma rutinaria en algunos países en pacientes con obesidad grave. Los tipos de procedimientos incluyen la banda gástrica ajustable por laparoscopia, el bypass gástrico en Y de Roux, la gastrectomía de manga vertical y la derivación biliopancreática. La cirugía para la obesidad grave se asocia con la pérdida de peso a largo plazo, la mejora de las enfermedades relacionadas con la obesidad y la disminución de la mortalidad general. Sin embargo, los costes asociados para la sanidad pública son elevados y se producen complicaciones en aproximadamente el 17% de los casos (la re-operación es necesaria en el 7% de los casos). Debido a su coste y sus riesgos, los investigadores están buscando otros tratamientos eficaces y menos invasivos para esta enfermedad.
La obesidad infantil no ha dejado de aumentar en los países desarrollados y se ha convertido en una de las principales preocupaciones de la población. Los gobiernos de todo el mundo diseñan planes estratégicos y lanzan programas de publicidad oficial para concienciar sobre este problema. Pero la obesidad infantil no es fácil de tratar, ya que las dietas constantes son difíciles de observar por los niños y las intervenciones quirúrgicas no están indicadas. Se están haciendo grandes esfuerzos en las estrategias de prevención, pero a menudo fracasan ante el estilo de vida y los hábitos alimentarios.
Existe un consenso generalizado sobre la necesidad de hacer especial hincapié en las estrategias de prevención para la población con riesgo de desarrollar obesidad infantil. Entre los factores de riesgo, el sobrepeso materno provoca un crecimiento acelerado y es un importante factor de predicción de la obesidad infantil. Esto tiene consecuencias críticas para la epidemia de obesidad, ya que el sobrepeso en la infancia a menudo se traslada a la vida adulta, dando lugar a un ciclo obesogénico que perpetúa la obesidad y el riesgo metabólico en las siguientes generaciones. También se ha descrito que la nutrición postnatal desempeña un papel importante en la determinación del crecimiento y el riesgo de obesidad. En comparación con la lactancia materna, el uso de leche artificial se ha asociado sistemáticamente con el sobrepeso infantil, y su composición influye en el riesgo de obesidad. La duración de la lactancia materna se asocia inversamente con el riesgo de obesidad, y las diferencias en la composición de la leche, incluida la diversidad de oligosacáridos y los niveles hormonales, se correlacionan con el crecimiento infantil, la adiposidad y la composición de la microbiota. Sin embargo, aunque algunos informes han identificado alteraciones en la composición de la leche inducidas por la obesidad materna (mayor cantidad de leptina, insulina, IL-6, TNF-a), éstas no están relacionadas con el aumento de peso acelerado del lactante, e incluso se ha sugerido que son factores de protección. Por lo tanto, no se sabe muy bien cómo contribuyen los componentes específicos de la leche a la transmisión del riesgo de obesidad de la madre al niño.
El documento EP2143341 describe una composición para ser administrada a un bebé para prevenir la obesidad futura, dicha composición comprende oligosacáridos. CN101322698 describe que la betaína es eficaz en el
tratamiento para prevenir o tratar la obesidad. FR2710245 y US2014/050810 describen composiciones para tratar la obesidad que comprenden betaína. Linde van Lee, et al (The American Journal of Clinical Nutrition, volumen 104, número 5, noviembre de 2016, páginas 1327-1333) divulgan que un estado materno alto en betaína se asocia generalmente con un tamaño menor del bebé al nacer y una menor masa grasa abdominal.
Debido a la elevada prevalencia de la obesidad y sus consecuencias para la salud, se necesitan estrategias eficaces para reducir la incidencia de la obesidad y, en particular, para poner fin al ciclo obesogénico que perpetúa esta condición poco saludable a lo largo de las generaciones en los individuos de riesgo.
Resumen de la invención
Los inventores han descubierto sorprendentemente que la administración de betaína a los bebés reduce la incidencia de la obesidad y trastornos asociados no sólo mientras se realiza la suplementación, sino también más adelante en la vida de dichos bebés, mucho después de que se haya interrumpido la suplementación con betaína. Este sorprendente efecto se demuestra en los ejemplos que siguen. Como se muestra en los ejemplos, los inventores han encontrado una fuerte asociación entre un menor contenido de betaína en la leche y un crecimiento temprano acelerado en los bebés con riesgo de obesidad. Además, los experimentos de suplementación materna en ratones han demostrado que el aumento de la ingesta de betaína durante la lactancia disminuía la adiposidad y mejoraba el metabolismo sistémico durante la edad adulta.
Así, un primer aspecto de la invención proporciona un compuesto de betaína para su uso en la prevención de la obesidad, la acumulación excesiva de grasa y/o trastornos metabólicos asociados a cualquiera de los anteriores en un sujeto, en el que la prevención comprende la administración del compuesto de betaína directamente al sujeto durante la infancia o, alternativamente, a la madre del sujeto durante la lactancia.
El aspecto anterior puede reformularse como el uso de un compuesto de betaína para la preparación de una composición para la prevención de la obesidad, la acumulación excesiva de grasa y/o trastornos metabólicos asociados con cualquiera de los anteriores en un sujeto, donde la prevención comprende la administración del compuesto de betaína directamente al sujeto durante la infancia o, alternativamente, a la madre del sujeto durante la lactancia. La invención también se refiere a un método para la prevención de la obesidad, la acumulación excesiva de grasa y/o trastornos metabólicos asociados con cualquiera de los anteriores en un sujeto que comprende la administración de una cantidad eficaz del compuesto de betaína junto con excipientes y/o vehículos farmacéutica o comestiblemente aceptables directamente al sujeto durante la infancia o, alternativamente, a la madre del sujeto durante la lactancia.
En un segundo aspecto, la invención proporciona una composición que comprende una cantidad eficaz de un compuesto de betaína junto con uno o más excipientes y/o vehículos farmacéuticamente o comestiblemente aceptables para su uso como se ha definido anteriormente. La composición puede ser una composición farmacéutica (es decir, un medicamento) o una composición no farmacéutica, como una composición comestible, por ejemplo un producto alimenticio o un suplemento dietético.
Breve descripción de los dibujos
FIG. 1: A) Niveles relativos de betaína en unidades arbitrarias. B) Composición de macronutrientes de la leche en g/100 mL (n=5/grupo); Ch, carbohidratos; Prot, proteínas. C) Contenido energético de la leche en Kcal/mL (n=5/grupo). D) Niveles de betaína en plasma en unidades arbitrarias en machos de 2 semanas (n=6/grupo). E) Peso corporal de las crías durante la lactancia (el gráfico de la izquierda representa a los machos, n=18; el gráfico de la derecha representa a las hembras, n=12); el eje Y representa el peso corporal en g; el eje X representa las semanas de vida. F) Ingesta de leche a la semana de edad expresada en % de peso corporal (n=4 camadas/grupo). Los datos son media±sem. *, test-t p<0,05; **, p<0,0001. Para todas las figuras de barras: las barras blancas representan la leche de las madres control (n=8), y las barras negras representan la leche de las madres tratadas con betaína (n=8).
FIG. 2: A) Masa grasa expresada en g (derecha) y % (izquierda) en ratones macho de 6 semanas de edad procedentes de madres control (barras blancas, n=7) o tratadas con betaína (negras, n=9). B) Peso corporal de las crías macho de madres obesas de control (MO-C, n=19) o tratadas con betaína (MO-B, n=21); el eje Y representa el peso corporal (g); el eje X representa las semanas de edad. C) Ingesta de leche a la semana de edad (n=3 camadas/grupo) expresada en % del peso corporal. D) Masa grasa expresada en g en ratones macho de 6 semanas de edad (n=8/grupo). Los datos son media±sem. *, prueba t p<0,05; **, p<0,0001.
FIG. 3. Abundancia relativa (%) de géneros diferencialmente enriquecidos identificados por LEfSe en crías macho de madres tratadas con betaína (B, n=10) o de control (C, n=10) a las 2 semanas de edad (A) y a las 6 semanas de
edad (B).
FIG: 4: A) Número de células caliciformes expresado como células caliciformes/100 |jm en secciones del íleon a las 6 semanas de vida (n=16/grupo). B) Expresión relativa del ARNm de los marcadores inflamatorios Ccl2m Tlr4 y Cd11c en el eWAT de ratones macho de 6 semanas de edad (n=8-10/grupo). C) Niveles circulantes de los marcadores inflamatorios MCP1, IL-6 y Pai-1 expresados en pg/mL en ratones macho de 6 semanas (n=10/grupo). D) Niveles relativos de ARNm ileal de Muc2 a las 6 semanas de vida (n=8/grupo). Los datos son media±sem. *, test-t p<0,05; #, test U de Mann-Whitney p<0,05. Para todas las figuras: las barras blancas representan los ratones de control (C, n=10) y las barras negras representan los ratones tratados con betaína (B, n=10).
FIG. 5: A) Las crías macho del control (barras blancas/círculos, n=16) o de las madres tratadas con betaína (barras negras/círculos, n=16) fueron alimentadas con una dieta chow después del destete y el peso corporal (expresado en g; eje Y) fue monitorizado hasta las 24 semanas de edad (semanas de edad en el eje X). B) Peso del hígado (L) y del eWAT expresado en g tras el sacrificio; el eje Y representa el peso del tejido en g. C) Tolerancia a la glucosa en la semana 20; el eje Y representa la concentración de glucosa en mg/dL; el eje X representa el tiempo en minutos. D) Niveles de insulina a los tiempos 0 y 15 minutos después de la carga de glucosa; el eje Y representa la concentración de insulina en pmol/L. E) Las crías macho de las madres obesas de control (MO-C, n=11) y de las tratadas con betaína (MO-B, n=13) se mantuvieron con una dieta de chow después del destete y se controló el peso corporal (expresado en g; eje Y) hasta las 24 semanas de edad (semanas de edad en el eje X). F) Peso del hígado (L) y del eWAT tras el sacrificio; el eje Y representa el peso del tejido en g. G) Tolerancia a la glucosa en la semana 20; el eje Y representa la concentración de glucosa en mg/dL; el eje X representa el tiempo en minutos. H) Niveles de insulina a los 0 y 15 minutos después de la carga de glucosa; el eje Y representa la concentración de insulina en pmol/L. Los datos son media±sem. *, test-t p<0,05; **, p<0,01; ***, p<0,001.
FIG. 6: A) Ratones de seis semanas de edad nacidos de madres de control (barras blancas/círculos) y tratadas con betaína (barras negras/círculos) fueron alimentados con una dieta alta en calorías (HFD) durante 4 meses (machos (M) : n=14 y n=20 para HF-C y HF-B; hembras (F): n=14/grupo); se calculó el aumento de peso corporal (expresado en g; eje Y) durante la alimentación con alto contenido en grasa. B) Tolerancia a la glucosa en ratones macho a las 18 semanas de vida; el eje Y representa la concentración de glucosa en mg/dL; el eje X representa el tiempo en minutos. C) Niveles de insulina en ratones macho a las 18 semanas de vida a los tiempos 0 y 15 minutos después de la carga de glucosa; el eje Y representa la concentración de insulina en pmol/L. D) Niveles de triglicéridos hepáticos en ratones macho (n=8/grupo); el eje Y representa jg de TAG/mg de proteína. Los datos son media±sem. *, test-t p<0,05; **, p<0,01; ***, p<0,001.
FIG. 7: Se analizaron las crías macho de las madres tratadas con betaína (grupo B, círculos/barras negras), antibióticos (grupo AB, triángulos blancos/barras punteadas), antibióticos y betaína (grupo AB-B, triángulo negro/barras punteadas), o sin suplemento (grupo C, círculos/barras blancas) (n=12 de 3 camadas/grupo). A) El peso corporal se controló hasta las 24 semanas de edad; el eje Y representa el peso corporal en g; el eje X representa la edad en semanas. B) Peso del hígado (L) y del depósito de eWAT tras el sacrificio; el eje Y representa el peso del tejido en g. C) Tolerancia a la glucosa a las 22 semanas de edad; el eje Y representa la concentración de glucosa en mg/dL; el eje X representa el tiempo en minutos. D) Expresión relativa del ARNm de los marcadores inflamatorios Ccl2m y Cd11c en eWAT (n=8-12/grupo). Los datos son media±sem. *, ANOVA unidireccional con prueba post-hoc de Tukey p<0,05 en comparación con los controles.
Descripción detallada de la invención
La presente invención está relacionada con la prevención de la obesidad, la acumulación excesiva de grasa y trastornos asociados mediante la administración de un compuesto de betaína a los bebés.
"La obesidad" es una condición en la que la reserva natural de energía, almacenada en el tejido graso de los animales, en particular de los humanos y otros mamíferos, aumenta hasta un punto en el que se asocia con ciertas condiciones de salud o con un aumento de la mortalidad. La expresión "acumulación excesiva de grasa" se entiende como tener más grasa corporal de la que es óptima para la salud. La "acumulación excesiva de grasa" también puede denominarse "sobrepeso". La obesidad y la acumulación excesiva de grasa suelen definirse por el índice de masa corporal de un individuo. "Índice de masa corporal" o "IMC" significa la relación entre el peso en kg dividido por la altura en metros, al cuadrado. "Obesidad" se define generalmente para un adulto humano como tener un IMC superior a 30. "Sobrepeso" se considera generalmente para los adultos humanos como un IMC de 25 a 30. En el caso de los niños de más de 2 años, el IMC se representa en un gráfico de crecimiento del IMC en función de la edad (tanto para las niñas como para los niños) para obtener una clasificación percentil. En el caso de los niños menores de 2 años (bebés), lo que se representa es el peso por la longitud en lugar del IMC. Los percentiles y las puntuaciones z son los indicadores más utilizados para evaluar el tamaño y los patrones de crecimiento de cada niño. El percentil indica la posición relativa del IMC o del peso para la talla del niño en una población de individuos del mismo sexo y edad. La puntuación z indica el número de desviaciones estándar (SDS) que un individuo se
desvía de la media de una población con el mismo sexo y edad. Los niños humanos se consideran con sobrepeso si su IMC o percentil de peso por talla se sitúa entre el percentil 85 y el 95, o la puntuación z entre 1 y 2 SDS. Los niños humanos se consideran obesos si su IMC o percentil de peso por longitud se sitúa en el percentil 95 o por encima de él, o la puntuación z es igual o superior a 2 SDS.
El término "desnutrición", también denominado "subalimentación", se entiende como la falta de nutrición adecuada resultante de una alimentación insuficiente, una dieta desequilibrada o una asimilación defectuosa. La desnutrición también puede producirse como resultado de ciertas enfermedades o condiciones genéticas. Los bebés humanos suelen denominarse desnutridos si su IMC o peso por talla se sitúa en el percentil 10 o por debajo de él. La desnutrición grave en los bebés humanos suele considerarse si el IMC o el peso por talla se sitúan en el percentil 3 o por debajo de él.
Los trastornos metabólicos asociados al sobrepeso, la obesidad y/o la acumulación excesiva de grasa son bien conocidos por los expertos. Por ejemplo, estos trastornos incluyen enfermedades cardiovasculares como la cardiopatía coronaria, la resistencia a la insulina, la diabetes de tipo 2, la hipertensión, la apnea del sueño, los problemas respiratorios y/o la dislipidemia, pero también algunos cánceres como el de endometrio, de mama y/o de colon, los accidentes cerebrovasculares, las enfermedades del hígado y de la vesícula biliar, la artrosis y/o los problemas ginecológicos. En particular, en las realizaciones de la invención, los trastornos metabólicos que se asocian a la obesidad y/o a la acumulación excesiva de grasa se seleccionan entre la cardiopatía coronaria, la resistencia a la insulina, la diabetes de tipo 2, la hipertensión, la dislipidemia y la apnea del sueño, más particularmente con la cardiopatía coronaria, la hipertensión, la dislipidemia y la apnea del sueño.
En el sentido de la presente invención, el término "infancia" se entiende como el periodo de tiempo en el que un sujeto tiene una edad para la que se recomienda la lactancia materna, ya sea como único medio de alimentación o combinada con fórmulas infantiles y/o alimentos sólidos. En los seres humanos, la infancia suele considerarse desde los 0 hasta los 2 años de edad aproximadamente, es decir, desde el nacimiento hasta los 2 años de edad aproximadamente. Sin embargo, el experto entenderá que el término "infancia", al igual que los términos "niñez", "adolescencia" y "edad adulta", no es un término absoluto, ya que depende de la maduración de cada individuo. Así, cada uno de estos términos se asocia a una franja de edad media, más que a una franja de edad exacta.
Por "niñez" se entiende, en el sentido de la presente invención, el período comprendido entre la infancia y el comienzo de la pubertad. "Pubertad" se define generalmente como el proceso de cambios físicos a través del cual el cuerpo de un niño madura hasta convertirse en un cuerpo adulto capaz de reproducirse sexualmente. Los términos "pubertad" y "adolescencia" se utilizan indistintamente. Por término medio, las niñas comienzan la pubertad alrededor de los 10-11 años y los niños alrededor de los 11-12 años. Por lo tanto, para los humanos, la "infancia" se expande en promedio desde los 3 hasta los 12 años de edad. La "pubertad" se extiende en los seres humanos, por término medio, desde los 13 hasta los 18 años.
"La edad adulta" se define generalmente como el periodo que comienza a partir del final de la pubertad, cuando el individuo está en pleno crecimiento y madurez sexual. En el contexto humano, el término adulto tiene además significados asociados a conceptos sociales y legales. En el sentido de la presente invención, el término "edad adulta" se refiere preferentemente a la edad adulta biológica, que en los seres humanos comienza alrededor de los 18 años hasta la muerte del individuo.
"Prevención" se entiende en el sentido de evitar el desarrollo de la obesidad, la acumulación excesiva de grasa y/o los trastornos metabólicos asociados a cualquiera de los anteriores, así como de reducir la probabilidad de desarrollar la obesidad, la acumulación excesiva de grasa y/o los trastornos metabólicos asociados a cualquiera de los anteriores.
En el sentido de la presente invención, "madre" es la mujer que amamanta al sujeto cuando es un bebé. La madre suele ser, aunque no necesariamente, la progenitora del sujeto.
Por "infección" se entiende la invasión de los tejidos corporales de un organismo por agentes causantes de enfermedades (a menudo llamados patógenos), su multiplicación y la reacción de los tejidos del huésped a estos organismos y a las toxinas que producen. Las infecciones son la causa de un gran número de enfermedades.
La expresión "cantidad eficaz", tal como se utiliza en el presente documento, se refiere a la cantidad de un compuesto que, cuando se administra, es suficiente para prevenir el desarrollo de, o aliviar en cierta medida, uno o más de los síntomas de la condición que se aborda. La dosis particular del compuesto administrado de acuerdo con esta invención se determinará, por supuesto, por las circunstancias particulares que rodean el caso, incluyendo el compuesto administrado, la vía de administración, la condición particular que se está tratando, y consideraciones similares. Cuando la composición de la invención es una composición farmacéutica, la "cantidad efectiva" es una "cantidad terapéuticamente efectiva".
La expresión "excipientes y/o vehículos farmacéuticamente aceptables" se refiere a materiales, composiciones o vehículos farmacéuticamente aceptables. Cada componente debe ser farmacéuticamente aceptable en el sentido de ser compatible con los demás ingredientes de la composición farmacéutica. También debe ser adecuado para su uso en contacto con el tejido u órgano de los seres humanos y los animales sin una toxicidad excesiva, irritación, respuesta alérgica, inmunogenicidad u otros problemas o complicaciones acordes con una relación beneficio/riesgo razonable. Del mismo modo, la expresión "excipientes y/o vehículos comestibles aceptables" se refiere a los ingredientes, materiales, composiciones o vehículos que son aceptables para las composiciones comestibles, como los productos alimentarios, nutracéuticos o suplementos dietéticos. Los "excipientes y/o vehículos comestibles aceptables" deben ser ingredientes de grado alimentario. Cada componente debe ser comestiblemente aceptable en el sentido de ser compatible con los demás ingredientes de la composición comestible. También debe ser adecuado para su uso cuando se ingiere sin excesiva toxicidad, irritación, respuesta alérgica, inmunogenicidad u otros problemas o complicaciones acordes con una relación beneficio/riesgo razonable.
Los términos "suplemento dietético", "suplemento alimenticio" o "suplemento nutricional" o "nutracéutico", tal y como se utilizan en este documento, se refieren indistintamente a un preparado destinado a complementar la dieta y a proporcionar nutrientes que pueden faltar o que no se consumen en cantidad suficiente en la dieta de una persona. Por "fórmula infantil" se entiende, en general, un alimento manufacturado diseñado y comercializado para alimentar a los bebés y, por lo general, preparado para la alimentación con biberón o taza a partir de polvo (mezclado con agua) o líquido (con o sin agua adicional).
"Compuesto de betaína" en el sentido de la presente invención se entiende como compuestos zwitteriónicos como la glicina betaína (también llamada N,N,N-trimetilamonioacetato o N,N,N-trimetilglicina) y compuestos similares a la glicina betaína derivados de otros aminoácidos.
En una realización, el compuesto de betaína tiene la fórmula (I):
en la que:
X es N o As;
R1 y R2 son independientemente (C1-C6)alquilo opcionalmente sustituido con uno o más átomos de halógeno; y R3 y R4 forman un anillo de 5 a 6 miembros junto con los átomos a los que están unidos que está opcionalmente sustituido con uno o más sustituyentes seleccionados entre OH, halógeno y (C1-C3)alquilo opcionalmente sustituido con uno o más átomos de halógeno; o alternativamente
R3 es (C1-C6)alquilo; y
R4 es H o (1H-indol-3-il)metilo.
El término "(C1-Cn)-alquilo", tal y como se utiliza aquí, se refiere a una cadena lateral de hidrocarburo saturada, ramificada o lineal, con 1 a n átomos de carbono.
En particular, el compuesto de betaína se selecciona entre la glicina betaína, la arsenobetaína, la prolina betaína, la 4-hidroxiprolina betaína y el triptófano betaína, representados, respectivamente, por las fórmulas II a VI:
Fórmula II (glicina betaína)
Fórmula IV (prolina betaína)
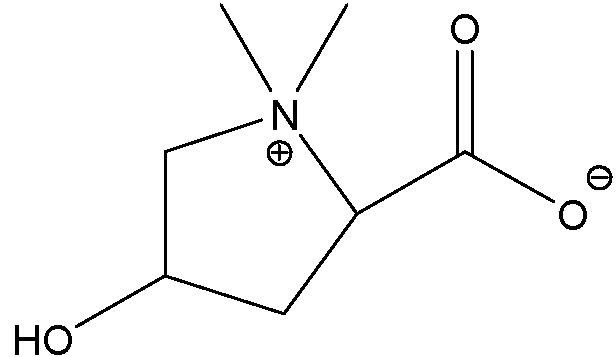
Fórmula V (betaína 4-hidroxiprolina)
En otra realización particular, el compuesto de betaína se selecciona entre la glicina betaína, la arsenobetaína y la prolina betaína. En otra realización, el compuesto de betaína es glicina betaína.
La presente invención tiene aplicación en mamíferos, en el ámbito veterinario o medicinal. La invención es útil en particular en los campos de la salud de los animales domésticos, la salud del ganado y la salud humana. Preferentemente, la presente invención encuentra aplicación en la salud humana. Así, en una realización preferida del primer aspecto de la invención, el compuesto de betaína es para su administración a los seres humanos.
En realizaciones preferidas del primer aspecto de la invención, el compuesto de betaína es para la prevención de la obesidad.
Curiosamente, los inventores han encontrado consecuencias metabólicas beneficiosas duraderas, incluida la reducción de la acumulación de grasa, cuando se administra el compuesto de betaína sólo durante la infancia. Los datos experimentales indican claramente que una mayor exposición al compuesto de betaína durante los primeros años de vida (la infancia) podría ser suficiente para reducir la adiposidad y mejorar la salud metabólica más adelante. Este hallazgo es ventajoso para proporcionar finalmente una estrategia largamente buscada para la prevención de la obesidad y los trastornos asociados, en particular para la prevención de la obesidad infantil. Por lo tanto, en una realización de la presente invención la prevención de la obesidad, la acumulación excesiva de grasa y/o los trastornos metabólicos asociados a cualquiera de los anteriores comprende la prevención después de la infancia, es decir, en la niñez del sujeto, en la adolescencia del sujeto y/o en la edad adulta del sujeto. En otra
realización, la prevención de la obesidad, la acumulación excesiva de grasa y/o los trastornos metabólicos asociados con cualquiera de los anteriores comprende la prevención a partir de los 3 años de edad, a partir de los 13 años de edad y/o a partir de los 18 años de edad.
Algunos sujetos tienen un mayor riesgo de desarrollar obesidad, acumulación excesiva de grasa y/o trastornos metabólicos asociados a cualquiera de los anteriores. Las intervenciones para reducir la probabilidad de desarrollar estas condiciones en dicha población de riesgo son particularmente beneficiosas. Así, en una realización particular del primer aspecto de la invención, los sujetos están en riesgo de padecer obesidad, acumulación excesiva de grasa y/o trastornos metabólicos asociados a cualquiera de los anteriores.
Algunos factores de las primeras etapas de la vida se han asociado claramente con el sobrepeso, la obesidad y los trastornos asociados más adelante, es decir, durante la infancia, la adolescencia y/o la edad adulta. Entre ellos, son especialmente representativos la obesidad y la diabetes maternas, la desnutrición del feto, el aumento excesivo de peso durante la gestación, la falta de lactancia materna, el tabaquismo de la madre y el rápido crecimiento del bebé. Estos factores de riesgo pueden deberse al estilo de vida o a razones genéticas. Aunque la asociación puede ser modesta para cada uno de los factores de riesgo, se puede conseguir un gran efecto cuando se actúa sobre un riesgo atribuible pequeño si el factor de riesgo es muy prevalente en una población. Además, algunos posibles determinantes pueden ser más importantes que otros porque son más fáciles de abordar mediante la aplicación de una intervención eficaz. En una realización particular del primer aspecto de la invención, los sujetos tienen una condición seleccionada entre haber nacido de madres obesas, haber sufrido un retraso en el crecimiento intrauterino, tener bajo peso al nacer (en particular un peso para la talla situado en el percentil 3 o por debajo de él), tener un rápido aumento de peso después del nacimiento, y combinaciones de las mismas.
Según los hallazgos de los inventores, el aumento de la ingesta de betaína durante la lactancia disminuyó la adiposidad y mejoró el metabolismo sistémico durante la edad adulta. Por lo tanto, una estrategia eficaz para prevenir la obesidad, la acumulación excesiva de grasa y/o los trastornos asociados puede ser alimentar a las madres lactantes con un compuesto de betaína. En una realización particular del primer aspecto de la invención, el compuesto de betaína se administra a la madre del sujeto durante la lactancia. Sin embargo, esta estrategia no siempre es posible, ya que algunos bebés son alimentados principalmente o únicamente con fórmulas infantiles. Además, los bebés alimentados con fórmula tienen un mayor riesgo de crecimiento acelerado y obesidad. La prevención de la obesidad mediante la administración del compuesto de betaína a estos bebés es deseable. Así, en otra realización del primer aspecto de la invención, el compuesto de betaína se administra directamente al sujeto durante la infancia. La administración directa al sujeto durante la infancia puede lograrse, por ejemplo, mediante la inclusión del compuesto de betaína en la fórmula infantil, la comida para bebés o los suplementos dietéticos para bebés. La administración directa a los sujetos durante la infancia también puede ser en forma de una solución que contenga el compuesto de betaína y excipientes y/o vehículos apropiados para la administración oral, por ejemplo, con una jeringa o con un gotero. En otra realización del primer aspecto de la invención, el compuesto de betaína se administra a un sujeto humano masculino durante la infancia. En otra realización del primer aspecto de la invención, el compuesto de betaína se administra a un sujeto humano femenino durante la infancia.
Los inventores han encontrado que la cantidad de compuesto de betaína que se necesita para obtener el efecto de prevenir la obesidad, la acumulación excesiva de grasa y/o los trastornos metabólicos asociados a cualquiera de los anteriores está muy por encima de lo que se puede obtener con la dieta natural, y también está muy por encima de lo que se podría obtener aumentando la ingestión de fuentes naturales de betaína. En general, los inventores han encontrado que la cantidad de compuesto de betaína que necesita ser administrada directamente al sujeto durante la infancia para lograr el efecto buscado puede ser de 2 a 500 mg/Kg/día, en particular de 4 a 100 mg/Kg/día, más particularmente de 4 a 50 mg/Kg/día. Así, otra realización de la invención se refiere a un compuesto de betaína para su uso como se ha definido anteriormente, en el que la prevención y/o el tratamiento comprende la administración directa al sujeto durante la infancia de 4 a 100 mg de compuesto de betaína/Kg/día. Esto también se denomina generalmente "dosis diaria". Cuando el compuesto de betaína se administra a la madre del sujeto durante la lactancia, la dosis diaria a administrar a la madre puede ser de 500 mg a 20 g por día, en particular de 1 a 10 g/día, más particularmente de 2 a 6 g/día. Así, otra realización de la invención se refiere a un compuesto de betaína para su uso como se ha definido anteriormente, en el que la prevención y/o el tratamiento comprende la administración de 1 a 10 g de compuesto de betaína/día a la madre del sujeto durante la lactancia.
La presente invención contempla la administración del compuesto de betaína como un compuesto de betaína puro, por ejemplo, en forma de polvo para ser ingerido directamente o disuelto en líquidos. La invención, sin embargo, contempla adicionalmente la formulación del compuesto de betaína como composición que comprende una cantidad efectiva de compuesto de betaína junto con otros ingredientes, tales como excipientes y/o vehículos.
Un segundo aspecto de la invención proporciona, por tanto, una composición que comprende una cantidad efectiva de compuesto de betaína junto con uno o más excipientes y/o vehículos farmacéuticamente o comestibles aceptables para su uso, tal como se ha definido anteriormente. La cantidad efectiva en la composición puede ser
determinada por el experto teniendo en cuenta el compuesto administrado, la dosis diaria, la vía de administración, la edad del sujeto, el peso del sujeto y otras consideraciones. La composición de la invención puede administrarse una vez al día, una vez a la semana, varios días a la semana o varias veces al día.
En una realización del segundo aspecto de la invención, la composición para su uso como se ha definido anteriormente es una composición farmacéutica y los excipientes son excipientes farmacéuticamente aceptables. En otra realización, la composición para el uso definido anteriormente es un suplemento dietético y los excipientes son excipientes comestibles. En particular, la composición es un suplemento dietético para mujeres en periodo de lactancia. En otra realización particular, la composición es un suplemento dietético para bebés.
Las composiciones farmacéuticas y los suplementos dietéticos de la invención pueden formularse en varias formas que incluyen, pero no se limitan a, soluciones, comprimidos, cápsulas, gránulos, suspensiones, dispersiones, polvos, pastillas, caramelos masticables, barras de caramelo, concentrados, gotas, elixir, emulsión, película, gel, gránulo, goma de mascar, jalea, aceite, pasta, pastilla, gránulo, jarabe, forma de gelatina masticable o comprimido masticable. La selección de los excipientes y los métodos más apropiados para la formulación en vista del propósito particular de la composición está dentro del alcance de las personas expertas en la materia. Por ejemplo, las gotas, las soluciones, los jarabes y las suspensiones pueden ser más apropiados para la administración del compuesto de betaína directamente a los bebés, mientras que el polvo, los comprimidos y las cápsulas pueden ser más apropiados para la administración del compuesto de betaína a la madre lactante. En general, se prefieren las composiciones farmacéuticas y los suplementos dietéticos de administración oral.
Otras realizaciones del segundo aspecto de la invención proporcionan la composición que comprende una cantidad efectiva de compuesto de betaína junto con excipientes y/o vehículos comestibles aceptables para su uso como se ha definido anteriormente, donde la composición es un producto comestible. En una realización particular, la composición es un producto infantil comestible. En otra realización, la composición comestible es una fórmula infantil.
Los ejemplos que se presentan a continuación demuestran que una mayor ingesta de betaína durante la lactancia disminuyó la adiposidad y mejoró el metabolismo sistémico más adelante en la vida. Sin querer ceñirse a la teoría, los inventores piensan que las mejoras inducidas por la betaína en la salud metabólica de la descendencia pueden estar mediadas por la modulación de la microbiota intestinal del lactante. Esta teoría está respaldada por las pruebas obtenidas en relación con la capacidad de la betaína para promover el crecimiento de ciertas comunidades bacterianas intestinales beneficiosas y por la disrupción de los efectos de la betaína a consecuencia del tratamiento continuado con antibióticos.
La microbiota intestinal desempeña un papel importante en la salud y la enfermedad. Ejerce importantes actividades metabólicas extrayendo energía de polisacáridos dietéticos que de otro modo serían indigeribles, como el almidón resistente y las fibras dietéticas. Estas actividades metabólicas también conducen a la producción de nutrientes importantes, como los ácidos grasos de cadena corta (AGCC), las vitaminas (por ejemplo, la vitamina K, la vitamina B12 y el ácido fólico) y los aminoácidos, que los seres humanos no pueden producir por sí mismos. Además, la microbiota intestinal participa en la defensa contra los patógenos mediante mecanismos como la resistencia a la colonización y la producción de compuestos antimicrobianos. Además, la microbiota intestinal participa en el desarrollo, la maduración y el mantenimiento de las funciones sensoriales y motoras gastrointestinales, la barrera intestinal y el sistema inmunitario de la mucosa. Cada vez hay más pruebas de que la disbiosis de la microbiota intestinal está asociada a la patogénesis de trastornos tanto intestinales como extraintestinales. "Disbiosis" es un término que designa el desequilibrio o la mala adaptación de la microbiota intestinal.
La modulación beneficiosa de la microbiota intestinal proporcionada por la suplementación con betaína puede, por tanto, dar lugar a beneficios adicionales. La presente divulgación también se refiere a un compuesto de betaína para su uso en la modulación beneficiosa de la microbiota intestinal. Por modulación beneficiosa se entiende el aumento del crecimiento de las comunidades microbianas intestinales beneficiosas. La presente descripción también se refiere a un compuesto de betaína para su uso en la prevención y/o el tratamiento de trastornos asociados a la disbiosis de la microbiota intestinal en un sujeto, donde la prevención y/o el tratamiento comprenden la administración del compuesto de betaína directamente al sujeto durante la infancia o, alternativamente, a la madre del sujeto durante la lactancia. Esto puede reformularse como el uso de un compuesto de betaína para la preparación de una composición para la prevención y/o el tratamiento de trastornos asociados a la disbiosis de la microbiota intestinal en un sujeto, donde la composición se administra directamente al sujeto durante la infancia o, alternativamente, a la madre del sujeto durante la lactancia. La divulgación también se refiere a un método para la prevención y/o el tratamiento de trastornos asociados a la disbiosis de la microbiota intestinal que comprende la administración directa a un sujeto durante la infancia o, alternativamente, a la madre del sujeto durante la lactancia, de una cantidad eficaz de un compuesto de betaína, junto con excipientes y/o vehículos farmacéutica o comestiblemente aceptables. Dichos trastornos incluyen la desnutrición, las infecciones, la enfermedad inflamatoria
intestinal, el síndrome del intestino irritable (SII), la enfermedad celíaca, la alergia, el asma, así como la obesidad y los trastornos asociados, como las enfermedades cardiovasculares, la resistencia a la insulina, la diabetes de tipo 2; la hipertensión, la apnea del sueño, los problemas respiratorios, la dislipidemia y el cáncer.
En el contexto de los beneficios proporcionados por la suplementación con betaína, los inventores también han descubierto que la betaína promueve la integridad de la barrera intestinal (véase el ejemplo 2.4 y la figura 4). La presente divulgación también se refiere a un compuesto de betaína para su uso en el mantenimiento o mejora de la función de barrera intestinal en un sujeto, en el que el mantenimiento o mejora de la función de barrera intestinal comprende la administración del compuesto de betaína directamente al sujeto durante la infancia o, alternativamente, a la madre del sujeto durante la lactancia. Esto puede reformularse como el uso de un compuesto de betaína para la preparación de una composición para mantener o mejorar la función de barrera intestinal en un sujeto, en la que la composición se administra directamente al sujeto durante la infancia o, alternativamente, a la madre del sujeto durante la lactancia. La divulgación también se refiere a un método para mantener o mejorar la función de barrera intestinal en un sujeto que comprende la administración directa al sujeto durante la infancia o, alternativamente, a la madre del sujeto durante la lactancia, de una cantidad eficaz de un compuesto de betaína, junto con excipientes y/o vehículos farmacéuticos o comestibles aceptables. En una realización particular, el sujeto es un ser humano. En otra realización particular, el sujeto es un animal.
La desnutrición infantil provoca una disbiosis intestinal y un deterioro de la función de la barrera intestinal, lo que tiene múltiples consecuencias para el niño, como la mala absorción de nutrientes, el deterioro del crecimiento y el desarrollo cognitivo, la translocación de bacterias (endotoxemia) y la inflamación sistémica. Esto puede tener consecuencias críticas, desde el retraso en el crecimiento hasta la peritonitis. Por lo tanto, mejorar o mantener la función de la barrera intestinal en los bebés desnutridos podría afectar potencialmente a la absorción y el metabolismo de aminoácidos, proteínas, lípidos, carbohidratos y otros nutrientes.
El mantenimiento o la mejora de la función de barrera intestinal no sólo contribuye a mejorar la salud metabólica de la descendencia, sino que tiene otros beneficios, en particular, en la prevención de la endotoxemia y las infecciones. Esto es especialmente relevante para los bebés con riesgo de sufrir infecciones frecuentes, como los bebés desnutridos.
La presente divulgación se refiere además a un compuesto de betaína para su uso en la prevención de infecciones en un sujeto, donde la prevención comprende la administración del compuesto de betaína directamente al sujeto durante la infancia o, alternativamente, a la madre del sujeto durante la lactancia. Esto puede reformularse como el uso de un compuesto de betaína para la preparación de una composición para la prevención de infecciones en un sujeto, en la que la composición se administra directamente al sujeto durante la infancia o, alternativamente, a la madre del sujeto durante la lactancia. La divulgación también se refiere a un método de prevención de infecciones en un sujeto que comprende la administración directa al sujeto durante la infancia o, alternativamente, a la madre del sujeto durante la lactancia, de una cantidad eficaz de un compuesto de betaína, junto con excipientes y/o vehículos farmacéutica o comestiblemente aceptables. En una realización particular, el sujeto es un ser humano. En otra realización particular, el sujeto es un animal.
Todas las realizaciones descritas anteriormente para la prevención de la obesidad, la acumulación excesiva de grasa y/o los trastornos metabólicos asociados a cualquiera de los anteriores también se aplican a la prevención y/o el tratamiento de los trastornos asociados a la disbiosis de la microbiota intestinal, al mantenimiento o la mejora de la función de barrera intestinal y a la prevención de las infecciones. El compuesto de betaína, como se ha definido anteriormente, se selecciona preferentemente de entre la glicina betaína, la arsenobetaína, la prolina betaína, la 4-hidroxiprolina betaína y el triptófano betaína, más preferentemente de entre la glicina betaína, la arsenobetaína y la prolina betaína, y aún más preferentemente es la glicina betaína.
Como se ha descrito anteriormente, el compuesto de betaína puede administrarse al lactante a través de la leche materna, es decir, alimentando con el compuesto de betaína a la madre del sujeto durante la lactancia, o, alternativamente, puede administrarse directamente al sujeto durante la infancia, por ejemplo, como suplemento dietético o incluido en la fórmula o la comida para lactantes. La dosis diaria del compuesto de betaína que debe administrarse directamente al lactante para obtener los beneficios mencionados puede ser de 2 a 500 mg/Kg/día, en particular de 4 a 100 mg/Kg/día, más particularmente de 4 a 50 mg/Kg/día. Cuando el compuesto de betaína se administra a la madre del sujeto, la dosis diaria puede ser de 500 mg a 20 g por día, en particular de 1 a 10 g/día, más particularmente de 2 a 6 g/día
La dosis diaria eficaz del compuesto de betaína según la presente divulgación puede administrarse mediante la ingestión directa del compuesto de betaína puro, por ejemplo en forma de polvo para ser ingerido directamente o disuelto en líquidos. Sin embargo, la presente divulgación también está relacionada con una composición que comprende una cantidad eficaz de compuesto de betaína junto con uno o más excipientes y/o vehículos farmacéutica o comestiblemente aceptables para su uso en la prevención y/o tratamiento de trastornos asociados a
la disbiosis de la microbiota intestinal, para mantener o mejorar la función de barrera intestinal y para prevenir infecciones, como se ha definido anteriormente. La composición puede ser una composición farmacéutica con excipientes y/o vehículos farmacéuticamente aceptables o, alternativamente, un suplemento dietético con excipientes y/o vehículos comestibles aceptables o, alternativamente, un producto comestible con excipientes y/o vehículos comestibles. Cuando la composición es un producto comestible puede ser, por ejemplo, una fórmula infantil.
Al considerar la prevención de las infecciones, éstas son, en particular, infecciones intestinales, por ejemplo, infecciones que causan gastroenteritis, como los enteropatógenos. Además, la prevención de infecciones, preferentemente intestinales, puede comprender la prevención durante la infancia y/o la niñez. La presente divulgación también contempla que los sujetos pueden ser sujetos con riesgo de padecer infecciones, en particular por padecer desnutrición y/o por ser objeto de tratamientos antibióticos.
A lo largo de la descripción y las reivindicaciones, la palabra "comprende" y sus variaciones no pretenden excluir otras características técnicas, aditivos, componentes o pasos. Además, la palabra "comprende" abarca el caso de "consistente en". Los objetos, ventajas y características adicionales de la invención se harán evidentes para los expertos en la materia tras el examen de la descripción o podrán aprenderse mediante la práctica de la invención. Los siguientes ejemplos y dibujos se proporcionan a modo de ilustración, y no pretenden ser limitativos de la presente invención. Además, la presente invención abarca todas las combinaciones posibles de las realizaciones particulares y preferidas descritas en el presente documento.
Ejemplos
La betaína en todos los ejemplos es glicina betaína.
1. Materiales y métodos
1.1. Diseño del estudio en humanos
Brevemente, las madres con lactancia materna exclusiva y los bebés llegaron entre las 8:00 y las 10:00 de la mañana al campus de la Universidad de Ciencias de la Salud de Oklahoma (Oklahoma City, Ok, EE.UU.). Se animó a la madre a vaciar todo el pecho utilizando un sacaleches de uso hospitalario. Nuestra principal variable de resultado para el presente estudio fue la puntuación z de peso por longitud (WLZ) al mes de edad, ajustada por el WLZ de nacimiento (y otras covariables). Esto es algebraicamente idéntico a la diferencia de WLZ entre el nacimiento y el primer mes de vida ajustado por el WLZ del nacimiento, y por lo tanto refleja el cambio en el WLZ durante el primer mes de vida.
1.2. Análisis de la metabolómica de la leche
Los metabolitos de un carbono s-adenosilmetionina (SAM), s-adenosilhomocisteína (SAH), metionina, cistationina, colina y betaína, se determinaron por LC-MS/MS como se describió anteriormente (M. Inoue-Choi, et al, One-carbon metabolism nutrient status and plasma s-adenosylmethionine concentrations in middle-aged and older Chinese in Singapore. Int J Mol Epidemiol Genet 3, 160-173 (2012)). El 5-metiltetrahidrofolato se midió por LC-MS/MS como se describió previamente (E. Arning, et al, Quantitation of 5-methyltetrahydrofolate in cerebrospinal fluid using liquid chromatography-electrospray tandem mass spectrometry. Methods Mol Biol 1378, 175-182 (2016)). La homocisteína total se midió por LC-MS/MS.
Para este análisis, las muestras se prepararon añadiendo 10 pl de leche materna o estándares a 120 pl de solución de estándar interno (que contenía d4-homocisteína en 4 mM de ditiotreitol disuelto en agua destilada). Tras la incubación a temperatura ambiente durante 30 minutos, las muestras se desproteinizaron con 200 pl de acetonitrilo y ácido fórmico al 0,1%, y se centrifugaron a 1.400 rpm durante
5 minutos. Las muestras se analizaron tras la inyección de 10 pL de extracto en un Synergi Hydro 4p 150x3mm (Phenomenex), mantenido a 30 °C, y eluyendo en un gradiente con tampón A (100% agua, 0,5% ácido fórmico y 0,25% ácido heptafluorobutírico) y tampón B (100% acetonitrilo, 0,5% ácido fórmico 0,25% ácido heptafluorobutírico). La velocidad de flujo fue de 0,5 mL/min, con un gradiente por pasos durante un tiempo total de ejecución de 10 minutos. La espectrometría de masas se realizó en un 4000 QTrap (Sciex, Framingham, MA) y los valores observados (m/z) de los iones de fragmento fueron homocisteína (m/z 136^ 90) y d4-homocisteína (m/z 140^ 94). Todos los datos se recogieron y procesaron con el software Analyst v1.4.2 (Sciex, Framingham, MA).
1.3. Cuidados y tratamientos de los animales
Todos los protocolos de los animales fueron aprobados por el Comité Institucional de Cuidado y Uso de Animales de la Universidad de Barcelona (España). Los ratones se alojaron en un ciclo de luz y oscuridad de 12 horas con libre acceso a comida y agua. Se aparearon ratones ICR-CD1 (Envigo) machos y hembras para obtener la progenie. Para minimizar la variabilidad del crecimiento, las camadas se ajustaron a 8 crías por madre al nacer, eliminando los ratones más pesados y los más ligeros. Se
administró glicina betaína (1% p/vol), ampicilina (1 g/L) y neomicina (0,5 g/L) (Sigma-Aldrich) en el agua durante la lactancia. Tras el destete, los ratones se alojaron en 4 por jaula y fueron alimentados con la dieta Teklad 2014 (Envigo). Para la obesidad inducida por la dieta, se suministró una dieta alta en grasas (HFD, 45% kcal de grasa) (D12451, Research Diets). Para los estudios de obesidad materna, se alimentó a las hembras de 6 semanas de edad con una HFD durante 8 semanas antes del apareamiento; esta misma dieta se mantuvo durante la gestación y la lactancia. Para evaluar la ingesta de leche, se separó a las crías de las madres durante 2 horas y se las devolvió a sus jaulas durante 1 hora; la diferencia de peso corporal antes y después de la alimentación se expresó como gramos por peso corporal inicial por hora. Para la recogida de leche, se tomaron muestras manualmente bajo anestesia (pentobarbital, 40 mg/kg) el día 14 después del nacimiento; las madres y las crías fueron sacrificadas después de la recogida de leche, y se obtuvo el contenido cecal para los estudios del microbioma. La composición corporal se determinó mediante un sistema de resonancia magnética Bruker Biospect de 7,0 T (Bruker Medical Gmbh, Alemania). Se midió la calorimetría indirecta en jaulas metabólicas (PhenoMaster/LabMaster, TSE Systems GmbH, Alemania); se monitorizaron el O2 , el CO2 , la ingesta de alimentos y la actividad locomotora durante 48 horas, y los datos se analizaron mediante ANOVA de 2 vías para medidas repetidas. Se realizaron pruebas de tolerancia a la glucosa intraperitoneal (1,5 g/kg) y a la insulina (0,6 U/kg) tras un ayuno de 16 o 4 horas, respectivamente. Los ratones fueron anestesiados (pentobarbital intraperitoneal, 50 mg/kg) y sacrificados entre las 9 y las 11 horas.
1.4. Análisis bioquímicos
Las muestras de leche de ratón se diluyeron 1:3 antes del análisis de macronutrientes mediante espectroscopia de infrarrojo medio en un analizador Miris (Miris AB). Las concentraciones relativas de betaína se determinaron por cromatografía líquida (columna Acquity UPLC BEH HILIC, Waters) acoplada a espectrometría de masas (QqQ/MS 6490, Agilent). La insulina plasmática se determinó mediante ELISA (Millipore). La MCP-1, IL-6 y PAI-1 plasmáticas se midieron mediante Milliplex Map (EMD Millipore, Merck). Los triglicéridos hepáticos y fecales se cuantificaron en extractos de cloroformo-metanol de hígado o heces (50 mg) utilizando el kit de ensayo de triglicéridos (Sigma-Aldrich).
1.5. Análisis de la expresión génica
El ARN total de los tejidos se aisló con el reactivo TRI (Sigma-Aldrich) y el ADNc se obtuvo con el kit de ADNc de alta capacidad (Applied Biosystems). La qPCR se realizó con SybrGreen (Takara Bio), utilizando Hprt como gen de mantenimiento. Las secuencias de los cebadores son las siguientes
Ccl2 forward: 5'-CAAGATGATCCCAATGAGTAG-3' (SEQ ID NO: 1)
Ccl2 reverso: 5'-TTGGTGACAAAAACTACAGC-3' (SEQ ID NO: 2)
Tlr4 forward: 5'-GCCTCCCTGGCTCCTGGCTA-3' (SEQ ID NO: 3)
Tlr4 reverso: 5'-CAGGGACTTTGCTGAGTTTCTGATCCA-3' (SEQ ID NO: 4)
Cd11c forward: 5'-AGTCTGTTGGTTCTGTAAG-3' (SEQ ID NO: 5)
Cd11c reverso: 5'-ACAGTTCTGTTATGACATGC-3' (SEQ ID NO: 6)
Hprt forward: 5'-GCCCCAAAATGGTTAAGGTTG-3' (SEQ ID NO: 7)
Hprt reverso: 5'-GTCAAGGGCATATCCAACAAC-3' (SEQ ID NO: 8)
Muc2 forward: 5'-CTGACCAAGAGCGAACACAA-3' (SEQ ID NO: 9)
Muc2 reverso: 5'-CATGACTGGAAGCAACTGGA-3' (SEQ ID NO: 10)
1.6. Análisis histológico
Los tejidos se fijaron por inmersión en formol, se incluyeron en parafina y se tiñeron las secciones con hematoxilina/eosina. Para el WAT, se midió el área de adipocitos en 30 campos microscópicos aleatorios por animal (10-20 células/campo). Para el íleon, los cortes transversales se tiñeron con el método de ácido periódico-Schiff (PAS). Se analizaron diez vellosidades por ratón de 5-6 secciones. Se determinó el número de células caliciformes por vellosidad y se expresó como número de células por 100 pm. Los análisis se realizaron con ImageJ por un investigador que no conocía la identificación de la muestra.
1.7. Análisis del microbioma intestinal
Se recogió el contenido cecal de ratones machos de 2 y 6 semanas de edad procedentes de madres magras de control y tratadas con betaína y se almacenó a -80°C hasta que se aisló el ADN bacteriano utilizando el kit de aislamiento de ADN PowerSoil® (MOBIO Laboratories). La composición microbiana se analizó utilizando el sistema Illumina MiSeq para secuenciar la región V3-V4 del gen 16S rRNA. Las lecturas pareadas se procesaron con QIIME v1.9 y se asignaron a los niveles de filo, clase, orden, familia, género y especie. La diversidad dentro de la muestra se estimó con una profundidad de rarefacción de 4827 lecturas por muestra, y la diversidad filogenética se expresó en función de la profundidad de la secuencia. Se utilizaron distancias UniFrac no ponderadas para realizar el análisis de coordenadas principales (PCoA). Las diferencias en la abundancia relativa se determinaron
utilizando LEfSe (N. Segata, et al, Metagenomic biomarker discovery and explanation. Genome Biol 12, R60 (2011)).
1.8. Análisis estadístico
A menos que se indique lo contrario, los datos se presentan como media ± sem. Los datos de los metabolitos de la leche humana se transformaron en logaritmos y se aplicó una regresión multivariante en
SPSS 19.0 (Armonk, NY: IBM Corp.). Para determinar la significación estadística se aplicó la prueba t de
dos colas, la prueba U de Mann-Whitney para datos con distribución no normal, o el ANOVA de una vía
con la prueba post-hoc de Tukey para más de dos grupos. P<0,05 se consideró significativo para todos
los análisis.
2. Resultados
2.1. Los niveles de betaína en la leche materna están inversamente relacionados con el crecimiento temprano del bebé en los seres humanos
Para determinar si los metabolitos del carbono de la leche estaban asociados con el sobrepeso materno y el crecimiento del lactante, se estudiaron 34 díadas madre-lactante en un rango de IMC materno (18,5-47,2 kg/m2), que fueron alimentadas exclusivamente con leche materna (Tabla 1). El sobrepeso u obesidad materna (OWO) dio lugar a una mayor puntuación z de peso para la longitud (WLZ), masa grasa y masa magra del lactante al mes en comparación con las madres de peso normal (NW) (Tabla 1).
Tabla 1. Características demográficas y metabólicas de los participantes.
Todo NW OWO
n=34 n=15 n=19 Valor p MADRE
Edad (años) 29,1 (5,1) 27,7 (5,5) 30,1 (4,7) 0,182 IMC antes del embarazo (kg/m2) 27,3 (7,1) 21,6 (1,8) 31,8 (6,4) <0,001 INFANTE
Nacimiento
Sexo (femenino/masculino) 19/15 9 / 6 10/9 0,668 Edad gestacional (semanas) 39,6 (1,2) 39,4 (1,1) 39,8 (1,2) 0,295 Peso (kg) 3,53 (0,48) 3,39 (0,51) 3,64 (0,45) 0,148 Longitud (cm) 51,6 (2,3) 51,6 (2,3) 51,6 (2,3) 0,989 WLZ -0,59 (1,20) -1,07 (1,30) -0,21 (1,00) 0,035 1 mes
Peso (kg) 4,67 (0,71) 4,45 (0,63) 4,84 (0,73) 0,115 Longitud (cm) 55,8 (2,1) 55,8 (2,1) 55,8 (2,2) 0,955 WLZ -0,36 (1,04) -0,87 (0,91) 0,05 (0,98) 0,008 Perímetro cefálico (cm) 38,3 (1,3) 38,4 (1,4) 38,2 (1,3) 0,676 Masa de grasa DXA (%) 24,1 (2,8) 22,9 (3,0) 25,0 (2,4) 0,027 Masa de grasa DXA (kg) 1,19 (0,29) 1,06 (0,27) 1,30 (0,26) 0,013 Masa magra DXA (kg) 3,64 (0,50) 3,45 (0,46) 3,78 (0,48) 0,050 LECHE MATERNA
Colina (pmol/L) 96,8 (49,0) 96,3 (61,4) 97,1 (38,2) 0,541 Betaína (pmol/L) 3,12 (2,65) 3,34 (3,30) 2,95 (2,09) 0,951
Todo NW OWO
n=34 n=15 n=19 Valor p Metionina (pmol/L) 4,39 (2,69) 4,70 (3,51) 4,15 (1,89) 0,732 SAM (nmol/L) 1469 (436) 1427 (483) 1503 (406) 0,542 SAH (nmol/L) 216 (81) 201 (83) 227 (80) 0,279 Cistationina (nmol/L) 44,9 (34,3) 44,0 (35,4) 45,7 (34,3) 0,896 5-metiltetrahidrofolato (nmol/L) 29,5 (15,9) 27,0 (16,5) 31,5 (15,6) 0,420 Homocisteína (nmol/L) 207 (68) 215 (55) 201 (77) 0,529 Los valores representan la media (DE). La letra negrita indica p<0,05. a Prueba t de dos colas entre los grupos NW y OWO para las variables continuas; prueba chi-cuadrado de Pearson para las variables categóricas (género). NW: peso normal; OWO: sobrepeso u obesidad; WLZ: puntuación z de peso por longitud.
Se analizaron muestras de leche al mes del nacimiento para cuantificar colina, betaína, metionina, SAM, SAH, cistationina, 5-metiltetrahidrofolato (5-MTHF) y homocisteína total (tHcy), y se encontraron correlaciones significativas entre los metabolitos. Una comparación categórica entre las madres NW y OWO no reveló diferencias en los niveles de metabolitos de la leche (Tabla 1). A continuación, examinamos las posibles asociaciones entre los analitos de la leche y la ZLT del lactante. Entre todos los metabolitos, la betaína fue la única variable significativamente correlacionada con el WLZ al mes de vida (r=-0,40, p=0,018), y sólo se observó una tendencia para la SAH y la cistationina (Tabla 2).
Tabla 2. Correlaciones multivariadas entre los metabolitos de la leche y la ZLT del lactante al mes de vida.
Todos los sujetos Peso normal
Sin ajustar Ajustada Sin ajustar Ajustada
r p val Ustd p val r p val Ustd p val
CHO -0,09 0,593 -0,07 0,666 0,01 0,981 0,05 0,890
BET -0,40 0,018 -0,37 0,041 -0,09 0,759 0,07 0,904
MET 0,08 0,649 0,15 0,441 0,16 0,557 0,11 0,760
SAM 0,04 0,822 -0,06 0,755 -0,10 0,716 0,16 0,720
SAH -0,29 0,094 -0,31 0,068 -0,14 0,609 0,07 0,854
CYSTA -0,34 0,050 -0,33 0,062 -0,34 0,216 -0,15 0,693
5-MTHF 0,13 0,449 0,10 0,568 0,32 0,248 0,17 0,614
tHCY -0,00 0,996 0,09 0,629 0,13 0,643 0,15 0,650
Sobrepeso y obesidad
Sin ajustar Ajustada
CHO -0,35 0,142 -0,38 0,200
BET -0,78 <0,001 -0,80 <0,001
MET 0,09 0,718 0,18 0,664
SAM 0,07 0,772 0,09 0,776
SAH -0,66 0,002 -0,83 0,001
CYSTA -0,43 0,070 -0,64 0,042
Los niveles de los metabolitos se transformaron en logaritmos y se evaluó la correlación con la WLZ de 1 mes. La letra negrita indica p<0,05. IJstd: coeficiente beta estandarizado del modelo de regresión; CHO: colina; BET: betaína; MET: metionina; SAM: s-adenosilmetionina; SAH: s-adenosilhomocisteína; CYSTA: cistationina; 5-MTHF: 5-metiltetrahidrofolato; tHCY: homocisteína total. aModelo ajustado por la edad materna, el IMC pregestacional, la edad gestacional y el WLZ al nacer.
El ajuste por edad materna, IMC pregestacional, edad gestacional y WLZ al nacer no modificó sustancialmente las estimaciones no ajustadas (Gstd=-0,37, p=0,041, Tabla 2). La correlación entre betaína y WLZ fue particularmente fuerte en los bebés de madres OWO (Gstd=-0,80, p<0,001), mientras que no se observó ninguna asociación en las madres NW (I3std=0,07, p=0,904; Tabla 2). Se observó un efecto similar dependiente de la obesidad para la HSA (Tabla 2). El contenido de betaína en la leche también se correlacionó con otros parámetros de crecimiento, incluido el índice ponderal, y no se observó ninguna correlación con el perímetro cefálico o las medidas de composición corporal (datos no mostrados).
En conjunto, estos resultados indican que los bebés nacidos de madres con obesidad pero expuestos a un mayor contenido de betaína en la leche mostraron un menor crecimiento al mes, en comparación con los bebés con una menor exposición a la betaína.
2.2. La betaína dietética se transfiere a la leche materna y disminuye la adiposidad de las crías en ratones Para estudiar si la betaína de la leche modula el crecimiento y el riesgo de obesidad, realizamos experimentos de suplementación materna en ratones exclusivamente durante la lactancia. Las madres fueron asignadas aleatoriamente a grupos de control (C) o de tratamiento (B, 1% de betaína en agua) el primer día después del parto. Se recogieron muestras de leche en el día 14 después del parto de un subconjunto de madres para determinar los niveles de betaína. La suplementación aumentó el contenido de betaína en la leche en 5 veces (p<0,0001, Figura 1A) sin alterar la composición de macronutrientes o el contenido energético (Figuras 1B-2C). Las crías de catorce días mostraron un aumento de la betaína en plasma (1,8 veces, p<0,05, Figura 1D). La suplementación no moduló los patrones de crecimiento de las crías durante la lactancia (Figura 1E) ni el consumo de leche (Figura 1F). Sin embargo, el análisis de la composición corporal a las 6 semanas de edad reveló una disminución de la masa grasa en los ratones macho tratados con betaína en comparación con los de control (p<0,05, Figura 2A). Otros parámetros metabólicos, como la tolerancia a la glucosa, la ingesta de alimentos, el gasto energético, el índice de intercambio respiratorio y los niveles de actividad, no difirieron entre los grupos de ratones jóvenes (datos no mostrados).
Para comprobar si la betaína interactúa con la obesidad materna, se administró un suplemento de betaína durante la lactancia en un modelo de ratón de obesidad materna. Las madres fueron alimentadas con una dieta alta en grasas (HFD) durante 8 semanas antes del apareamiento, y asignadas aleatoriamente a los grupos de control (MO-C) o de tratamiento con betaína (MO-B) en el momento del parto. La suplementación se realizó como se ha descrito anteriormente. La obesidad materna dio lugar a un aumento de peso de las crías durante la lactancia, en comparación con las crías de madres delgadas (compárense las figuras 1E y 2B). En este contexto, la suplementación con betaína moderó el crecimiento de las crías en comparación con los controles (Figura 2B), sin diferencias en la ingesta de leche (Figura 2C), e indujo una tendencia hacia una menor masa grasa a las 6 semanas de edad (Figura 2D).
Los cambios inducidos por la betaína materna en los ratones jóvenes se tradujeron en efectos metabólicos a largo plazo en las crías macho, y también protegieron contra la obesidad inducida por la dieta tanto en los ratones machos como en las hembras. Estos datos indican que una mayor exposición a la betaína durante los primeros años de vida podría ser suficiente para reducir la adiposidad. El tratamiento también protegió contra la acumulación de lípidos en el hígado tras una alimentación rica en grasas.
2.3. La suplementación materna con betaína modula la microbiota intestinal de los hijos en los primeros años de vida
Dado que el microbioma intestinal está influenciado por la nutrición postnatal, se consideró si las alteraciones del microbioma pueden mediar los efectos de la betaína. Se analizó el contenido cecal de ratones machos de 2 y 6 semanas de edad procedentes de madres magras de control y tratadas con betaína. Para tener en cuenta la variabilidad entre camadas, se analizaron 8 y 6 camadas por grupo a las 2 y 6 semanas de vida, respectivamente. El análisis de coordenadas principales de las distancias UniFrac no ponderadas mostró que la betaína materna modulaba la composición de la comunidad microbiana a las 2 semanas de edad, sin que se observaran diferencias a las 6 semanas. La diversidad filogenética no difirió entre los grupos. El análisis del tamaño del efecto del análisis lineal discriminante (LEfSe) identificó varios grupos bacterianos que diferían significativamente entre los grupos,
incluyendo Actinobacteria spp., Akkermansia spp. y Pseudomonas spp. a las 2 semanas, y Akkermansia spp., Odoribacter spp., Oscillospiraceae spp. y Roseburia spp. a las 6 semanas (Figura 3A-3B). Entre estos grupos bacterianos, sólo las diferencias en los niveles de Akkermansia spp. soportaron un análisis bioinformático más estricto recortando las lecturas de secuencia de muy baja abundancia antes de la LEfSe.
Roseburia spp. son conocidos productores de butirato, que pueden inducir efectos metabólicos beneficiosos en el huésped. En particular, Akkermansia muciniphila fue la única especie alterada tanto a las 2 como a las 6 semanas de edad, y el único grupo bacteriano que soportó un análisis bioinformático más estricto. Varios estudios han informado de una asociación entre Akkermansia muciniphila y una mejor salud metabólica. Curiosamente, el aumento de la población de Akkermansia spp. se ha asociado recientemente con un aumento de peso más lento en un modelo de ratón de desnutrición postnatal. Además, estudios anteriores de Akkermansia muciniphila demuestran que la administración a ratones adultos aumenta el número de células caliciformes ileales y mejora la función de barrera intestinal, lo que conduce a una disminución de la inflamación sistémica y a una mejora de la salud metabólica.
No se encontraron diferencias en los ácidos grasos de cadena corta cecales a las 6 semanas de edad. Además, la suplementación con betaína no modificó el microbioma intestinal materno.
2.4. La suplementación materna con betaína mejora la función del epitelio intestinal, la inflamación sistémica de bajo grado y la disfunción metabólica.
Las crías de seis semanas de edad de las madres tratadas con betaína no mostraron diferencias en la longitud de las vellosidades ileales, pero tenían un mayor número de células caliciformes (1,3 veces, p<0,05, figura 4A) y expresión de ARNm de Muc2 (figura 4D). Estos cambios iban acompañados de una disminución de los niveles de ARNm de los marcadores inflamatorios (Ccl2, Tlr4, Cd11c) en el tejido adiposo blanco epididimario (eWAT, figura 4B). La expresión de Ccl2 (o de la proteína quimioatrayente de monocitos 1, MCP-1) también disminuyó en el tejido adiposo marrón, el hígado y el músculo esquelético. Además, la suplementación disminuyó los niveles circulantes del marcador proinflamatorio interleucina-6 (IL-6, p<0,05), mientras que la MCP-1 y el inhibidor del activador del plasminógeno-1 (PAI-1) sólo mostraron una disminución numérica (p=0,08 y p=0,25, respectivamente, Figura 4C).
2.5. La suplementación materna con betaína mejora la salud metabólica de la descendencia durante la edad adulta.
También se investigó si los cambios mencionados durante los primeros años de vida se traducían en mejoras metabólicas a largo plazo. Se mantuvo a las crías con una dieta de comida después del destete y se las controló hasta las 24 semanas de edad. Los ratones machos nacidos de madres tratadas con betaína mostraron una menor ganancia de peso corporal durante la edad adulta y una disminución del peso eWAT (Figuras 5A-B), pero no se observó ningún efecto en las hembras. En consonancia con una menor adiposidad, el tamaño de los adipocitos y los marcadores inflamatorios disminuyeron en las crías macho de las madres tratadas con betaína. Los ratones machos mostraron una notable mejora en la tolerancia a la glucosa (Figura 5C), sin efecto en las crías hembras. Además, los niveles de insulina basal disminuyeron en un 40% en el grupo tratado en comparación con el grupo de control (p<0,05, Figura 5D). Las pruebas de tolerancia a la insulina revelaron una glucosa en sangre significativamente menor en cada punto temporal en los machos del grupo de tratamiento, pero ninguna diferencia en la respuesta a la administración de insulina. La suplementación no tuvo un efecto significativo sobre la acumulación de triglicéridos en el hígado. Se observó un fenotipo similar en el modelo de ratón con obesidad materna, en el que las crías macho adultas mostraron un menor peso corporal y adiposidad (Figuras 5E-4F), una mejor tolerancia a la glucosa (Figura 5G) y una disminución de los niveles de insulina basal (Figura 5H) en el grupo tratado con betaína en comparación con el grupo de control.
A continuación se comprobó si esta intervención en las primeras etapas de la vida protegía contra la obesidad inducida por la dieta. Para ello, las crías de 6 semanas de edad de las madres magras de control o tratadas con betaína fueron alimentadas con una HFD durante 16 semanas (grupos HF-C y HF-B, respectivamente). Cuando se les administró una HFD, tanto las crías macho como las hembras del grupo tratado con betaína mostraron un menor aumento de peso corporal en comparación con el grupo de control (Figura 6A). Se observó una modesta disminución numérica en la ingesta acumulada de alimentos, que no alcanzó significación estadística, y no hubo diferencias en el contenido de lípidos fecales. La suplementación mejoró la tolerancia a la glucosa (Figura 6B), y disminuyó la glucosa en ayunas (Tiempo 0, Figura 6B) y los niveles de insulina (Figura 6C). La acumulación hepática de triglicéridos se redujo en un 30% en el grupo h F-B (p<0,05, Figura 6D).
2.6. La coadministración de antibióticos durante la lactancia reduce los efectos metabólicos a largo plazo de la betaína
La administración materna de antibióticos durante los primeros años de vida altera la composición de la microbiota intestinal de las crías. Anteriormente se había observado que la administración materna de ampicilina y neomicina aumenta el peso del ciego y disminuye el contenido bacteriano cecal en las crías de dos semanas. Para comprobar si el microbioma intestinal en las primeras etapas de la vida contribuye a los efectos metabólicos beneficiosos a largo
Claims (15)
1. Un compuesto de betaína para su uso en la prevención de la obesidad, la acumulación excesiva de grasa y/o los trastornos metabólicos asociados a cualquiera de los anteriores en un sujeto, en el que la prevención comprende administrar el compuesto de betaína directamente al sujeto durante la infancia o, alternativamente, a la madre del sujeto durante la lactancia.
2. El compuesto de betaína para su uso según la reivindicación 1, en el que el compuesto de betaína
tiene la fórmula (I):
en la que:
X es N o As;
R1 y R2 son independientemente (C1-C6)alquilo opcionalmente sustituido con uno o más átomos de halógeno; y R3 y R4 forman un anillo de 5 a 6 miembros junto con los átomos a los que están unidos que está opcionalmente sustituido por uno o más sustituyentes seleccionados entre OH, halógeno y (C1-C3)alquilo opcionalmente sustituido con uno o más átomos de halógeno; o alternativamente
R3 es (C1-C6)alquilo; y
R4 es H o (1H-indol-3-il)metilo.
3. El compuesto de betaína para su uso según la reivindicación 2, en el que el compuesto de betaína es glicina betaína.
4. El compuesto de betaína para su uso según cualquiera de las reivindicaciones 1 a 3, que es para la prevención de la obesidad.
5. El compuesto de betaína para su uso según cualquiera de las reivindicaciones 1-4, en el que la prevención de la obesidad, la acumulación excesiva de grasa y/o los trastornos metabólicos asociados a cualquiera de los anteriores comprende la prevención en la infancia del sujeto, en la adolescencia del sujeto y/o en la edad adulta del sujeto.
6. El compuesto de betaína para su uso según cualquiera de las reivindicaciones 1-5, en el que los sujetos están en riesgo de padecer obesidad, acumulación excesiva de grasa y/o trastornos metabólicos asociados a cualquiera de los anteriores.
7. El compuesto de betaína para su uso según la reivindicación 6, en el que los sujetos tienen madres obesas.
8. El compuesto de betaína para su uso según cualquiera de las reivindicaciones 1-7, en el que el compuesto de betaína se administra a la madre del sujeto durante la lactancia.
9. El compuesto de betaína para su uso según la reivindicación 8, en el que la cantidad de compuesto de betaína administrado a la madre es de 1 a 10 g/día.
10. El compuesto de betaína para su uso según cualquiera de las reivindicaciones 1-7, en el que el compuesto de betaína se administra directamente al sujeto durante la lactancia.
11. El compuesto de betaína para su uso según la reivindicación 10, en el que la cantidad de compuesto de betaína administrado directamente al sujeto durante la infancia es de 4 a 100 mg/Kg/día.
12. Una composición que comprende una cantidad eficaz de compuesto de betaína junto con uno o más excipientes y/o vehículos farmacéutica o comestiblemente aceptables para su uso en la prevención y/o tratamiento de la obesidad, la acumulación excesiva de grasa y/o los trastornos metabólicos asociados a cualquiera de los anteriores, tal como se define en cualquiera de las reivindicaciones 1-11.
13. La composición para el uso según la reivindicación 12, que es una composición farmacéutica y en la que los excipientes son excipientes farmacéuticamente aceptables.
14. La composición para el uso según la reivindicación 12, que es un suplemento dietético y en la que los excipientes son excipientes comestibles aceptables.
15. La composición para el uso según la reivindicación 12, que es una fórmula infantil.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP17382270.1A EP3400935A1 (en) | 2017-05-12 | 2017-05-12 | Betaine for the prevention of obesity |
| PCT/EP2018/062203 WO2018206763A1 (en) | 2017-05-12 | 2018-05-11 | Betaine for the prevention of obesity |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2899639T3 true ES2899639T3 (es) | 2022-03-14 |
Family
ID=58765789
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES18722567T Active ES2899639T3 (es) | 2017-05-12 | 2018-05-11 | Betaína para la prevención de la obesidad |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US11464754B2 (es) |
| EP (2) | EP3400935A1 (es) |
| JP (1) | JP7184805B2 (es) |
| CN (2) | CN110831587A (es) |
| ES (1) | ES2899639T3 (es) |
| PL (1) | PL3621605T3 (es) |
| WO (1) | WO2018206763A1 (es) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115868628B (zh) * | 2022-10-11 | 2024-01-26 | 泓博元生命科技(深圳)有限公司 | 减肥组合物 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| LU88373A1 (fr) * | 1993-07-12 | 1994-04-01 | Michel Urso Prof Medecin Et Ch | Produit pour maigrir |
| ATE228779T1 (de) * | 1999-01-20 | 2002-12-15 | Nutricia Nv | Säuglingsnährpräparat |
| EP1643865A1 (en) * | 2003-06-04 | 2006-04-12 | Willem Jacob Serfontein | Nutritional compositions and use thereof |
| WO2006086856A1 (en) | 2005-02-15 | 2006-08-24 | Messadek, Jallal | Combination therapeutic compositions and method of use |
| WO2007107319A1 (en) | 2006-03-17 | 2007-09-27 | Biotecmarin Gmbh | Isolation, structure determination, synthesis and bioactivity of damipipecolin and damituricin |
| CN101322698A (zh) * | 2007-06-15 | 2008-12-17 | 复旦大学 | 甜菜碱在制备预防和治疗饮食性肥胖药物中的应用 |
| EP2143341A1 (en) * | 2008-07-08 | 2010-01-13 | Nestec S.A. | Nutritional Composition Containing Oligosaccharide Mixture |
| KR101412221B1 (ko) * | 2012-08-14 | 2014-06-27 | (주)바이오뉴트리젠 | 구기자잎 추출 분말과 베타인을 유효성분으로 함유하는 항비만 조성물 |
-
2017
- 2017-05-12 EP EP17382270.1A patent/EP3400935A1/en not_active Withdrawn
-
2018
- 2018-05-11 ES ES18722567T patent/ES2899639T3/es active Active
- 2018-05-11 WO PCT/EP2018/062203 patent/WO2018206763A1/en active Application Filing
- 2018-05-11 CN CN201880030180.4A patent/CN110831587A/zh active Pending
- 2018-05-11 EP EP18722567.7A patent/EP3621605B1/en active Active
- 2018-05-11 PL PL18722567T patent/PL3621605T3/pl unknown
- 2018-05-11 US US16/612,806 patent/US11464754B2/en active Active
- 2018-05-11 JP JP2019562641A patent/JP7184805B2/ja active Active
- 2018-05-11 CN CN202311207964.9A patent/CN117243938A/zh active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| JP2020519650A (ja) | 2020-07-02 |
| WO2018206763A1 (en) | 2018-11-15 |
| US20200147027A1 (en) | 2020-05-14 |
| EP3621605B1 (en) | 2021-07-07 |
| EP3400935A1 (en) | 2018-11-14 |
| EP3621605A1 (en) | 2020-03-18 |
| CN117243938A (zh) | 2023-12-19 |
| US11464754B2 (en) | 2022-10-11 |
| JP7184805B2 (ja) | 2022-12-06 |
| PL3621605T3 (pl) | 2022-01-03 |
| CN110831587A (zh) | 2020-02-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CA2559755C (en) | Dietary supplement and method for treating digestive system-related disorders | |
| ES2431142T3 (es) | Inhibidor de acumulación de grasa para el tratamiento de síndrome metabólico | |
| ES2712740T3 (es) | Tratamiento de afecciones asociadas con eotaxina incrementada con 25-hidroxivitamina D3 | |
| IL178049A (en) | Dietary supplement for the treatment and prevention of digestive system and digestive system-related disorders comprising a lipid supplement, a soluble fiber and at least one amino acid | |
| AU2017298212A1 (en) | Compositions and methods for managing digestive disorders and a healthy microbiome | |
| ES2899639T3 (es) | Betaína para la prevención de la obesidad | |
| ES2743955T3 (es) | Composiciones que comprenden cinamaldehído y zinc y métodos para utilizar tales composiciones | |
| US20170368026A1 (en) | Promotion of healing of intestinal mucosa using proline, serine and threonine | |
| ES2261383T3 (es) | Un metodo para mantener o mejorar la sintesis de mucinas. | |
| JP6368368B2 (ja) | p−アニスアルデヒドを使用する組成物及び方法 | |
| Namratha Pai et al. | Nutritional implications in head and neck cancer-a review | |
| Laake et al. | The ADHD and autism nutritional supplement handbook: the cutting-edge biomedical approach to treating the underlying deficiencies and symptoms of ADHD and autism | |
| ES2958918T3 (es) | Suplemento dietético para tratar la disbiosis | |
| US11826338B2 (en) | Methods for treating obesity | |
| Hsu et al. | EFFECT OF FOLIC ACID DEFICIENCY ON ABSORPTION OF Co 60-LABELED VITAMIN B 12 BY RATS | |
| Beer | ACNEM fellowship certification level 1: A case study of PMDD | |
| CN116546981A (zh) | 使用至少一种甘氨酸或其衍生物和/或至少一种n-乙酰半胱氨酸或其衍生物以及至少一种百里酚和/或香芹酚的组合物和方法 | |
| CN117715634A (zh) | 包含化合物的混合物的组合物及其用途 | |
| Phiske et al. | Scurvy in a boy with thalassemia major. | |
| BR102014022457A2 (pt) | composição farmacêutica contendo sais de iodo; suplemento e medicamento contendo a mesma e seu uso |