ES2857815T3 - Métodos de uso de preparado fermentado para lactantes - Google Patents
Métodos de uso de preparado fermentado para lactantes Download PDFInfo
- Publication number
- ES2857815T3 ES2857815T3 ES17728777T ES17728777T ES2857815T3 ES 2857815 T3 ES2857815 T3 ES 2857815T3 ES 17728777 T ES17728777 T ES 17728777T ES 17728777 T ES17728777 T ES 17728777T ES 2857815 T3 ES2857815 T3 ES 2857815T3
- Authority
- ES
- Spain
- Prior art keywords
- weight
- nutritional composition
- lactic acid
- infant
- kcal
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000000034 method Methods 0.000 title claims abstract description 21
- 239000000203 mixture Substances 0.000 claims abstract description 136
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 claims abstract description 112
- 235000016709 nutrition Nutrition 0.000 claims abstract description 95
- 235000013350 formula milk Nutrition 0.000 claims abstract description 81
- 229920001542 oligosaccharide Polymers 0.000 claims abstract description 76
- 150000002482 oligosaccharides Chemical class 0.000 claims abstract description 60
- 235000014655 lactic acid Nutrition 0.000 claims abstract description 55
- 239000004310 lactic acid Substances 0.000 claims abstract description 55
- 239000004615 ingredient Substances 0.000 claims abstract description 51
- 102000004169 proteins and genes Human genes 0.000 claims abstract description 48
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 48
- 241000894006 Bacteria Species 0.000 claims abstract description 46
- 230000001976 improved effect Effects 0.000 claims abstract description 24
- 150000002632 lipids Chemical class 0.000 claims abstract description 20
- 150000001720 carbohydrates Chemical class 0.000 claims abstract description 19
- 235000019577 caloric intake Nutrition 0.000 claims abstract description 18
- 238000002560 therapeutic procedure Methods 0.000 claims abstract description 14
- 238000002360 preparation method Methods 0.000 claims description 41
- 235000013305 food Nutrition 0.000 claims description 24
- 241000186012 Bifidobacterium breve Species 0.000 claims description 18
- 235000019789 appetite Nutrition 0.000 claims description 17
- 230000036528 appetite Effects 0.000 claims description 17
- 230000004634 feeding behavior Effects 0.000 claims description 17
- 230000036186 satiety Effects 0.000 claims description 15
- 235000019627 satiety Nutrition 0.000 claims description 15
- 235000014113 dietary fatty acids Nutrition 0.000 claims description 14
- 229930195729 fatty acid Natural products 0.000 claims description 14
- 239000000194 fatty acid Substances 0.000 claims description 14
- 150000004665 fatty acids Chemical class 0.000 claims description 14
- 230000003247 decreasing effect Effects 0.000 claims description 13
- 230000004043 responsiveness Effects 0.000 claims description 13
- 241000194020 Streptococcus thermophilus Species 0.000 claims description 10
- 235000021255 galacto-oligosaccharides Nutrition 0.000 claims description 9
- 150000003271 galactooligosaccharides Chemical class 0.000 claims description 9
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 claims description 6
- 230000003979 response to food Effects 0.000 claims description 6
- 235000005686 eating Nutrition 0.000 claims description 5
- 235000005911 diet Nutrition 0.000 claims description 3
- 230000037213 diet Effects 0.000 claims description 3
- RFSUNEUAIZKAJO-ARQDHWQXSA-N Fructose Chemical class OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-ARQDHWQXSA-N 0.000 claims description 2
- 235000020660 omega-3 fatty acid Nutrition 0.000 claims description 2
- 239000002253 acid Substances 0.000 abstract description 7
- 235000018102 proteins Nutrition 0.000 description 42
- 230000012010 growth Effects 0.000 description 37
- 235000013336 milk Nutrition 0.000 description 30
- 239000008267 milk Substances 0.000 description 30
- 210000004080 milk Anatomy 0.000 description 30
- 239000000758 substrate Substances 0.000 description 28
- 235000019786 weight gain Nutrition 0.000 description 26
- 230000004584 weight gain Effects 0.000 description 26
- 238000000855 fermentation Methods 0.000 description 25
- 230000004151 fermentation Effects 0.000 description 25
- FTSSQIKWUOOEGC-RULYVFMPSA-N fructooligosaccharide Chemical compound OC[C@H]1O[C@@](CO)(OC[C@@]2(OC[C@@]3(OC[C@@]4(OC[C@@]5(OC[C@@]6(OC[C@@]7(OC[C@@]8(OC[C@@]9(OC[C@@]%10(OC[C@@]%11(O[C@H]%12O[C@H](CO)[C@@H](O)[C@H](O)[C@H]%12O)O[C@H](CO)[C@@H](O)[C@@H]%11O)O[C@H](CO)[C@@H](O)[C@@H]%10O)O[C@H](CO)[C@@H](O)[C@@H]9O)O[C@H](CO)[C@@H](O)[C@@H]8O)O[C@H](CO)[C@@H](O)[C@@H]7O)O[C@H](CO)[C@@H](O)[C@@H]6O)O[C@H](CO)[C@@H](O)[C@@H]5O)O[C@H](CO)[C@@H](O)[C@@H]4O)O[C@H](CO)[C@@H](O)[C@@H]3O)O[C@H](CO)[C@@H](O)[C@@H]2O)[C@@H](O)[C@@H]1O FTSSQIKWUOOEGC-RULYVFMPSA-N 0.000 description 19
- 229940107187 fructooligosaccharide Drugs 0.000 description 19
- 108010046377 Whey Proteins Proteins 0.000 description 18
- 102000007544 Whey Proteins Human genes 0.000 description 17
- 230000000694 effects Effects 0.000 description 17
- 235000014633 carbohydrates Nutrition 0.000 description 15
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 14
- 208000008589 Obesity Diseases 0.000 description 13
- YZXBAPSDXZZRGB-DOFZRALJSA-N arachidonic acid Chemical compound CCCCC\C=C/C\C=C/C\C=C/C\C=C/CCCC(O)=O YZXBAPSDXZZRGB-DOFZRALJSA-N 0.000 description 13
- 239000008101 lactose Substances 0.000 description 13
- 235000020824 obesity Nutrition 0.000 description 13
- 239000012736 aqueous medium Substances 0.000 description 12
- 230000020595 eating behavior Effects 0.000 description 12
- 239000003925 fat Substances 0.000 description 12
- 235000019197 fats Nutrition 0.000 description 12
- 238000012360 testing method Methods 0.000 description 12
- 206010033307 Overweight Diseases 0.000 description 11
- 230000018109 developmental process Effects 0.000 description 11
- JVTAAEKCZFNVCJ-REOHCLBHSA-N L-lactic acid Chemical compound C[C@H](O)C(O)=O JVTAAEKCZFNVCJ-REOHCLBHSA-N 0.000 description 10
- 125000002252 acyl group Chemical group 0.000 description 10
- 239000005018 casein Substances 0.000 description 10
- BECPQYXYKAMYBN-UHFFFAOYSA-N casein, tech. Chemical compound NCCCCC(C(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(CC(C)C)N=C(O)C(CCC(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(C(C)O)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(COP(O)(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(N)CC1=CC=CC=C1 BECPQYXYKAMYBN-UHFFFAOYSA-N 0.000 description 10
- 235000021240 caseins Nutrition 0.000 description 10
- 235000020978 long-chain polyunsaturated fatty acids Nutrition 0.000 description 10
- 239000005862 Whey Substances 0.000 description 9
- 235000021119 whey protein Nutrition 0.000 description 9
- 241000186000 Bifidobacterium Species 0.000 description 8
- MBMBGCFOFBJSGT-KUBAVDMBSA-N docosahexaenoic acid Natural products CC\C=C/C\C=C/C\C=C/C\C=C/C\C=C/C\C=C/CCC(O)=O MBMBGCFOFBJSGT-KUBAVDMBSA-N 0.000 description 8
- 239000000047 product Substances 0.000 description 8
- 230000004044 response Effects 0.000 description 8
- 229920001202 Inulin Polymers 0.000 description 7
- 235000020669 docosahexaenoic acid Nutrition 0.000 description 7
- JYJIGFIDKWBXDU-MNNPPOADSA-N inulin Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)OC[C@]1(OC[C@]2(OC[C@]3(OC[C@]4(OC[C@]5(OC[C@]6(OC[C@]7(OC[C@]8(OC[C@]9(OC[C@]%10(OC[C@]%11(OC[C@]%12(OC[C@]%13(OC[C@]%14(OC[C@]%15(OC[C@]%16(OC[C@]%17(OC[C@]%18(OC[C@]%19(OC[C@]%20(OC[C@]%21(OC[C@]%22(OC[C@]%23(OC[C@]%24(OC[C@]%25(OC[C@]%26(OC[C@]%27(OC[C@]%28(OC[C@]%29(OC[C@]%30(OC[C@]%31(OC[C@]%32(OC[C@]%33(OC[C@]%34(OC[C@]%35(OC[C@]%36(O[C@@H]%37[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O%37)O)[C@H]([C@H](O)[C@@H](CO)O%36)O)[C@H]([C@H](O)[C@@H](CO)O%35)O)[C@H]([C@H](O)[C@@H](CO)O%34)O)[C@H]([C@H](O)[C@@H](CO)O%33)O)[C@H]([C@H](O)[C@@H](CO)O%32)O)[C@H]([C@H](O)[C@@H](CO)O%31)O)[C@H]([C@H](O)[C@@H](CO)O%30)O)[C@H]([C@H](O)[C@@H](CO)O%29)O)[C@H]([C@H](O)[C@@H](CO)O%28)O)[C@H]([C@H](O)[C@@H](CO)O%27)O)[C@H]([C@H](O)[C@@H](CO)O%26)O)[C@H]([C@H](O)[C@@H](CO)O%25)O)[C@H]([C@H](O)[C@@H](CO)O%24)O)[C@H]([C@H](O)[C@@H](CO)O%23)O)[C@H]([C@H](O)[C@@H](CO)O%22)O)[C@H]([C@H](O)[C@@H](CO)O%21)O)[C@H]([C@H](O)[C@@H](CO)O%20)O)[C@H]([C@H](O)[C@@H](CO)O%19)O)[C@H]([C@H](O)[C@@H](CO)O%18)O)[C@H]([C@H](O)[C@@H](CO)O%17)O)[C@H]([C@H](O)[C@@H](CO)O%16)O)[C@H]([C@H](O)[C@@H](CO)O%15)O)[C@H]([C@H](O)[C@@H](CO)O%14)O)[C@H]([C@H](O)[C@@H](CO)O%13)O)[C@H]([C@H](O)[C@@H](CO)O%12)O)[C@H]([C@H](O)[C@@H](CO)O%11)O)[C@H]([C@H](O)[C@@H](CO)O%10)O)[C@H]([C@H](O)[C@@H](CO)O9)O)[C@H]([C@H](O)[C@@H](CO)O8)O)[C@H]([C@H](O)[C@@H](CO)O7)O)[C@H]([C@H](O)[C@@H](CO)O6)O)[C@H]([C@H](O)[C@@H](CO)O5)O)[C@H]([C@H](O)[C@@H](CO)O4)O)[C@H]([C@H](O)[C@@H](CO)O3)O)[C@H]([C@H](O)[C@@H](CO)O2)O)[C@@H](O)[C@H](O)[C@@H](CO)O1 JYJIGFIDKWBXDU-MNNPPOADSA-N 0.000 description 7
- 229940029339 inulin Drugs 0.000 description 7
- 235000020777 polyunsaturated fatty acids Nutrition 0.000 description 7
- 235000021068 Western diet Nutrition 0.000 description 6
- 238000004458 analytical method Methods 0.000 description 6
- 235000021342 arachidonic acid Nutrition 0.000 description 6
- 229940114079 arachidonic acid Drugs 0.000 description 6
- 235000020256 human milk Nutrition 0.000 description 6
- 210000004251 human milk Anatomy 0.000 description 6
- 230000002779 inactivation Effects 0.000 description 6
- 235000020218 follow-on milk formula Nutrition 0.000 description 5
- 239000012634 fragment Substances 0.000 description 5
- 244000005709 gut microbiome Species 0.000 description 5
- 238000010438 heat treatment Methods 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- YUFFSWGQGVEMMI-JLNKQSITSA-N (7Z,10Z,13Z,16Z,19Z)-docosapentaenoic acid Chemical compound CC\C=C/C\C=C/C\C=C/C\C=C/C\C=C/CCCCCC(O)=O YUFFSWGQGVEMMI-JLNKQSITSA-N 0.000 description 4
- 102000004190 Enzymes Human genes 0.000 description 4
- 108090000790 Enzymes Proteins 0.000 description 4
- 241000194017 Streptococcus Species 0.000 description 4
- 230000001580 bacterial effect Effects 0.000 description 4
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 4
- 235000020673 eicosapentaenoic acid Nutrition 0.000 description 4
- 229910052500 inorganic mineral Inorganic materials 0.000 description 4
- 235000010755 mineral Nutrition 0.000 description 4
- 239000011707 mineral Substances 0.000 description 4
- 230000002265 prevention Effects 0.000 description 4
- 235000013343 vitamin Nutrition 0.000 description 4
- 239000011782 vitamin Substances 0.000 description 4
- 229940088594 vitamin Drugs 0.000 description 4
- 229930003231 vitamin Natural products 0.000 description 4
- 241001608472 Bifidobacterium longum Species 0.000 description 3
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 3
- 241000186660 Lactobacillus Species 0.000 description 3
- 229920002774 Maltodextrin Polymers 0.000 description 3
- 208000007683 Pediatric Obesity Diseases 0.000 description 3
- 230000009286 beneficial effect Effects 0.000 description 3
- 230000000975 bioactive effect Effects 0.000 description 3
- 235000015155 buttermilk Nutrition 0.000 description 3
- 229940041514 candida albicans extract Drugs 0.000 description 3
- 235000009508 confectionery Nutrition 0.000 description 3
- 230000001079 digestive effect Effects 0.000 description 3
- 239000012467 final product Substances 0.000 description 3
- 239000008103 glucose Substances 0.000 description 3
- 238000011534 incubation Methods 0.000 description 3
- 235000021073 macronutrients Nutrition 0.000 description 3
- 108090000765 processed proteins & peptides Proteins 0.000 description 3
- 102000004196 processed proteins & peptides Human genes 0.000 description 3
- 230000001737 promoting effect Effects 0.000 description 3
- 239000003531 protein hydrolysate Substances 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 235000019871 vegetable fat Nutrition 0.000 description 3
- 239000012138 yeast extract Substances 0.000 description 3
- JVTAAEKCZFNVCJ-REOHCLBHSA-M (S)-lactate Chemical compound C[C@H](O)C([O-])=O JVTAAEKCZFNVCJ-REOHCLBHSA-M 0.000 description 2
- OWEGMIWEEQEYGQ-UHFFFAOYSA-N 100676-05-9 Natural products OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(OC2C(OC(O)C(O)C2O)CO)O1 OWEGMIWEEQEYGQ-UHFFFAOYSA-N 0.000 description 2
- SNFSYLYCDAVZGP-OLAZETNGSA-N 2'-fucosyllactose Chemical compound O[C@H]1[C@H](O)[C@H](O)[C@H](C)O[C@H]1O[C@H]1[C@H](O[C@@H]2[C@H](OC(O)[C@H](O)[C@H]2O)CO)O[C@H](CO)[C@H](O)[C@@H]1O SNFSYLYCDAVZGP-OLAZETNGSA-N 0.000 description 2
- OZZQHCBFUVFZGT-UHFFFAOYSA-N 2-(2-hydroxypropanoyloxy)propanoic acid Chemical compound CC(O)C(=O)OC(C)C(O)=O OZZQHCBFUVFZGT-UHFFFAOYSA-N 0.000 description 2
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 2
- 241000186016 Bifidobacterium bifidum Species 0.000 description 2
- 241000186011 Bifidobacterium catenulatum Species 0.000 description 2
- 241000186015 Bifidobacterium longum subsp. infantis Species 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 2
- 206010011469 Crying Diseases 0.000 description 2
- 101710088194 Dehydrogenase Proteins 0.000 description 2
- 244000199885 Lactobacillus bulgaricus Species 0.000 description 2
- 239000005913 Maltodextrin Substances 0.000 description 2
- GUBGYTABKSRVRQ-PICCSMPSSA-N Maltose Natural products O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@@H](CO)OC(O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-PICCSMPSSA-N 0.000 description 2
- 102000014171 Milk Proteins Human genes 0.000 description 2
- 108010011756 Milk Proteins Proteins 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- SNFSYLYCDAVZGP-UHFFFAOYSA-N UNPD26986 Natural products OC1C(O)C(O)C(C)OC1OC1C(OC2C(OC(O)C(O)C2O)CO)OC(CO)C(O)C1O SNFSYLYCDAVZGP-UHFFFAOYSA-N 0.000 description 2
- DTOSIQBPPRVQHS-PDBXOOCHSA-N alpha-linolenic acid Chemical compound CC\C=C/C\C=C/C\C=C/CCCCCCCC(O)=O DTOSIQBPPRVQHS-PDBXOOCHSA-N 0.000 description 2
- 235000008452 baby food Nutrition 0.000 description 2
- GUBGYTABKSRVRQ-QUYVBRFLSA-N beta-maltose Chemical compound OC[C@H]1O[C@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@@H]1O GUBGYTABKSRVRQ-QUYVBRFLSA-N 0.000 description 2
- 239000000337 buffer salt Substances 0.000 description 2
- 125000004432 carbon atom Chemical group C* 0.000 description 2
- 235000012000 cholesterol Nutrition 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 235000014048 cultured milk product Nutrition 0.000 description 2
- 235000018417 cysteine Nutrition 0.000 description 2
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 2
- 235000021051 daily weight gain Nutrition 0.000 description 2
- 235000013367 dietary fats Nutrition 0.000 description 2
- 150000002190 fatty acyls Chemical group 0.000 description 2
- BJHIKXHVCXFQLS-UYFOZJQFSA-N fructose group Chemical group OCC(=O)[C@@H](O)[C@H](O)[C@H](O)CO BJHIKXHVCXFQLS-UYFOZJQFSA-N 0.000 description 2
- 210000001035 gastrointestinal tract Anatomy 0.000 description 2
- 125000002791 glucosyl group Chemical group C1([C@H](O)[C@@H](O)[C@H](O)[C@H](O1)CO)* 0.000 description 2
- 150000004676 glycans Chemical class 0.000 description 2
- -1 inulin Chemical compound 0.000 description 2
- 229940116871 l-lactate Drugs 0.000 description 2
- 230000003050 macronutrient Effects 0.000 description 2
- 229940035034 maltodextrin Drugs 0.000 description 2
- 150000004667 medium chain fatty acids Chemical class 0.000 description 2
- 244000005700 microbiome Species 0.000 description 2
- 239000011785 micronutrient Substances 0.000 description 2
- 235000013369 micronutrients Nutrition 0.000 description 2
- 230000021332 multicellular organism growth Effects 0.000 description 2
- 235000015097 nutrients Nutrition 0.000 description 2
- 230000035764 nutrition Effects 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 235000005985 organic acids Nutrition 0.000 description 2
- 229920001282 polysaccharide Polymers 0.000 description 2
- 239000005017 polysaccharide Substances 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 230000013777 protein digestion Effects 0.000 description 2
- 235000021003 saturated fats Nutrition 0.000 description 2
- 235000020183 skimmed milk Nutrition 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 239000011573 trace mineral Substances 0.000 description 2
- 235000013619 trace mineral Nutrition 0.000 description 2
- KVZLHPXEUGJPAH-BXRBKJIMSA-N (2s)-2-oxidanylpropanoic acid Chemical compound C[C@H](O)C(O)=O.C[C@H](O)C(O)=O KVZLHPXEUGJPAH-BXRBKJIMSA-N 0.000 description 1
- JVTAAEKCZFNVCJ-UWTATZPHSA-M (R)-lactate Chemical compound C[C@@H](O)C([O-])=O JVTAAEKCZFNVCJ-UWTATZPHSA-M 0.000 description 1
- 229940062827 2'-fucosyllactose Drugs 0.000 description 1
- OVSKIKFHRZPJSS-UHFFFAOYSA-N 2,4-D Chemical compound OC(=O)COC1=CC=C(Cl)C=C1Cl OVSKIKFHRZPJSS-UHFFFAOYSA-N 0.000 description 1
- HWHQUWQCBPAQQH-UHFFFAOYSA-N 2-O-alpha-L-Fucosyl-lactose Natural products OC1C(O)C(O)C(C)OC1OC1C(O)C(O)C(CO)OC1OC(C(O)CO)C(O)C(O)C=O HWHQUWQCBPAQQH-UHFFFAOYSA-N 0.000 description 1
- WJPIUUDKRHCAEL-UHFFFAOYSA-N 3FL Natural products OC1C(O)C(O)C(C)OC1OC1C(OC2C(C(O)C(O)C(CO)O2)O)C(CO)OC(O)C1O WJPIUUDKRHCAEL-UHFFFAOYSA-N 0.000 description 1
- 208000004998 Abdominal Pain Diseases 0.000 description 1
- 206010000060 Abdominal distension Diseases 0.000 description 1
- 235000021411 American diet Nutrition 0.000 description 1
- 241000186018 Bifidobacterium adolescentis Species 0.000 description 1
- 241000186014 Bifidobacterium angulatum Species 0.000 description 1
- 241001134770 Bifidobacterium animalis Species 0.000 description 1
- 241001312346 Bifidobacterium gallicum Species 0.000 description 1
- 241001134772 Bifidobacterium pseudocatenulatum Species 0.000 description 1
- 241001034431 Bifidobacterium thermacidophilum Species 0.000 description 1
- 241001468229 Bifidobacterium thermophilum Species 0.000 description 1
- 241000206594 Carnobacterium Species 0.000 description 1
- 208000002881 Colic Diseases 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- 235000021294 Docosapentaenoic acid Nutrition 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 241000194033 Enterococcus Species 0.000 description 1
- 241000192125 Firmicutes Species 0.000 description 1
- 229920002670 Fructan Polymers 0.000 description 1
- 229930091371 Fructose Natural products 0.000 description 1
- 239000005715 Fructose Substances 0.000 description 1
- 229920000855 Fucoidan Polymers 0.000 description 1
- 229930186217 Glycolipid Natural products 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 102000004407 Lactalbumin Human genes 0.000 description 1
- 108090000942 Lactalbumin Proteins 0.000 description 1
- 235000013960 Lactobacillus bulgaricus Nutrition 0.000 description 1
- 241000194036 Lactococcus Species 0.000 description 1
- LKOHREGGXUJGKC-UHFFFAOYSA-N Lactodifucotetraose Natural products OC1C(O)C(O)C(C)OC1OC1C(OC2C(C(O)C(O)OC2CO)OC2C(C(O)C(O)C(C)O2)O)OC(CO)C(O)C1O LKOHREGGXUJGKC-UHFFFAOYSA-N 0.000 description 1
- 241000192132 Leuconostoc Species 0.000 description 1
- OYHQOLUKZRVURQ-HZJYTTRNSA-N Linoleic acid Chemical compound CCCCC\C=C/C\C=C/CCCCCCCC(O)=O OYHQOLUKZRVURQ-HZJYTTRNSA-N 0.000 description 1
- 102000004895 Lipoproteins Human genes 0.000 description 1
- 108090001030 Lipoproteins Proteins 0.000 description 1
- 238000000585 Mann–Whitney U test Methods 0.000 description 1
- 241000736262 Microbiota Species 0.000 description 1
- MSFSPUZXLOGKHJ-UHFFFAOYSA-N Muraminsaeure Natural products OC(=O)C(C)OC1C(N)C(O)OC(CO)C1O MSFSPUZXLOGKHJ-UHFFFAOYSA-N 0.000 description 1
- 241000202223 Oenococcus Species 0.000 description 1
- 229920006576 PP-G Polymers 0.000 description 1
- 241000192001 Pediococcus Species 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 108010013639 Peptidoglycan Proteins 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- LCTONWCANYUPML-UHFFFAOYSA-M Pyruvate Chemical compound CC(=O)C([O-])=O LCTONWCANYUPML-UHFFFAOYSA-M 0.000 description 1
- 235000019904 Raftiline® Nutrition 0.000 description 1
- 244000061456 Solanum tuberosum Species 0.000 description 1
- 235000002595 Solanum tuberosum Nutrition 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 241000500334 Tetragenococcus Species 0.000 description 1
- 241000207194 Vagococcus Species 0.000 description 1
- 241000202221 Weissella Species 0.000 description 1
- 206010000059 abdominal discomfort Diseases 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- JAZBEHYOTPTENJ-JLNKQSITSA-N all-cis-5,8,11,14,17-icosapentaenoic acid Chemical compound CC\C=C/C\C=C/C\C=C/C\C=C/C\C=C/CCCC(O)=O JAZBEHYOTPTENJ-JLNKQSITSA-N 0.000 description 1
- WQZGKKKJIJFFOK-PHYPRBDBSA-N alpha-D-galactose Chemical compound OC[C@H]1O[C@H](O)[C@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-PHYPRBDBSA-N 0.000 description 1
- LKOHREGGXUJGKC-GXSKDVPZSA-N alpha-L-Fucp-(1->3)-[alpha-L-Fucp-(1->2)-beta-D-Galp-(1->4)]-beta-D-Glcp Chemical compound C[C@@H]1O[C@@H](O[C@@H]2[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]2O[C@@H]2[C@@H](CO)O[C@@H](O)[C@H](O)[C@H]2O[C@@H]2O[C@@H](C)[C@@H](O)[C@@H](O)[C@@H]2O)[C@@H](O)[C@H](O)[C@@H]1O LKOHREGGXUJGKC-GXSKDVPZSA-N 0.000 description 1
- 235000020661 alpha-linolenic acid Nutrition 0.000 description 1
- 235000001014 amino acid Nutrition 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 102000005936 beta-Galactosidase Human genes 0.000 description 1
- 108010005774 beta-Galactosidase Proteins 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 208000024330 bloating Diseases 0.000 description 1
- 210000000481 breast Anatomy 0.000 description 1
- 235000014121 butter Nutrition 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 230000008131 children development Effects 0.000 description 1
- 230000001332 colony forming effect Effects 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 235000020247 cow milk Nutrition 0.000 description 1
- 235000015140 cultured milk Nutrition 0.000 description 1
- 235000013365 dairy product Nutrition 0.000 description 1
- 238000007405 data analysis Methods 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- AJNVQOSZGJRYEI-UHFFFAOYSA-N digallium;oxygen(2-) Chemical compound [O-2].[O-2].[O-2].[Ga+3].[Ga+3] AJNVQOSZGJRYEI-UHFFFAOYSA-N 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- 229940090949 docosahexaenoic acid Drugs 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 239000003797 essential amino acid Substances 0.000 description 1
- 235000020776 essential amino acid Nutrition 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 230000037406 food intake Effects 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 229930182830 galactose Natural products 0.000 description 1
- 230000002641 glycemic effect Effects 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 235000020981 healthy eating habits Nutrition 0.000 description 1
- 238000000265 homogenisation Methods 0.000 description 1
- 208000003532 hypothyroidism Diseases 0.000 description 1
- 230000002989 hypothyroidism Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 235000021125 infant nutrition Nutrition 0.000 description 1
- 238000011081 inoculation Methods 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- DLRVVLDZNNYCBX-RTPHMHGBSA-N isomaltose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1OC[C@@H]1[C@@H](O)[C@H](O)[C@@H](O)C(O)O1 DLRVVLDZNNYCBX-RTPHMHGBSA-N 0.000 description 1
- 229940039696 lactobacillus Drugs 0.000 description 1
- 229940004208 lactobacillus bulgaricus Drugs 0.000 description 1
- AIHDCSAXVMAMJH-GFBKWZILSA-N levan Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)OC[C@@H]1[C@@H](O)[C@H](O)[C@](CO)(CO[C@@H]2[C@H]([C@H](O)[C@@](O)(CO)O2)O)O1 AIHDCSAXVMAMJH-GFBKWZILSA-N 0.000 description 1
- 235000020778 linoleic acid Nutrition 0.000 description 1
- OYHQOLUKZRVURQ-IXWMQOLASA-N linoleic acid Natural products CCCCC\C=C/C\C=C\CCCCCCCC(O)=O OYHQOLUKZRVURQ-IXWMQOLASA-N 0.000 description 1
- 229960004488 linolenic acid Drugs 0.000 description 1
- 230000008376 long-term health Effects 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 150000003272 mannan oligosaccharides Chemical class 0.000 description 1
- 235000012054 meals Nutrition 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 235000021239 milk protein Nutrition 0.000 description 1
- 230000003278 mimic effect Effects 0.000 description 1
- 238000009343 monoculture Methods 0.000 description 1
- 229910000402 monopotassium phosphate Inorganic materials 0.000 description 1
- 235000019796 monopotassium phosphate Nutrition 0.000 description 1
- 150000002772 monosaccharides Chemical group 0.000 description 1
- 229910000403 monosodium phosphate Inorganic materials 0.000 description 1
- 235000019799 monosodium phosphate Nutrition 0.000 description 1
- 235000021281 monounsaturated fatty acids Nutrition 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- 235000006180 nutrition needs Nutrition 0.000 description 1
- 235000008935 nutritious Nutrition 0.000 description 1
- 235000021131 obesogenic diet Nutrition 0.000 description 1
- 235000020665 omega-6 fatty acid Nutrition 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 230000020477 pH reduction Effects 0.000 description 1
- IPCSVZSSVZVIGE-UHFFFAOYSA-N palmitic acid group Chemical group C(CCCCCCCCCCCCCCC)(=O)O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 1
- 238000009928 pasteurization Methods 0.000 description 1
- PJNZPQUBCPKICU-UHFFFAOYSA-N phosphoric acid;potassium Chemical compound [K].OP(O)(O)=O PJNZPQUBCPKICU-UHFFFAOYSA-N 0.000 description 1
- 230000037081 physical activity Effects 0.000 description 1
- 229920000157 polyfructose Polymers 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- 235000020991 processed meat Nutrition 0.000 description 1
- 235000021075 protein intake Nutrition 0.000 description 1
- 230000006920 protein precipitation Effects 0.000 description 1
- 235000020989 red meat Nutrition 0.000 description 1
- 230000003362 replicative effect Effects 0.000 description 1
- 235000020161 semi-skimmed milk Nutrition 0.000 description 1
- 210000000813 small intestine Anatomy 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 238000001694 spray drying Methods 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 235000008939 whole milk Nutrition 0.000 description 1
- 235000020138 yakult Nutrition 0.000 description 1
- 235000021241 α-lactalbumin Nutrition 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/40—Complete food formulations for specific consumer groups or specific purposes, e.g. infant formula
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/125—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives containing carbohydrate syrups; containing sugars; containing sugar alcohols; containing starch hydrolysates
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/135—Bacteria or derivatives thereof, e.g. probiotics
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/17—Amino acids, peptides or proteins
- A23L33/19—Dairy proteins
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/20—Reducing nutritive value; Dietetic products with reduced nutritive value
- A23L33/21—Addition of substantially indigestible substances, e.g. dietary fibres
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2400/00—Lactic or propionic acid bacteria
- A23V2400/21—Streptococcus, lactococcus
- A23V2400/249—Thermophilus
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2400/00—Lactic or propionic acid bacteria
- A23V2400/51—Bifidobacterium
- A23V2400/519—Breve
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2236/00—Isolation or extraction methods of medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicine
- A61K2236/10—Preparation or pretreatment of starting material
- A61K2236/19—Preparation or pretreatment of starting material involving fermentation using yeast, bacteria or both; enzymatic treatment
Abstract
Método no terapéutico para promover una autorregulación mejorada de la ingesta de energía en un lactante, donde dicho método comprende administrar una composición nutricional que es un preparado para lactantes que comprende de 3 a 7 g de lípidos/100 kcal, de 1,25 a 5 g de proteína/100 kcal y de 6 a 16 g de carbohidrato digerible/100 kcal y donde la composición nutricional comprende un ingrediente fermentado por bacterias productoras de ácido láctico, y de un 0,05 a un 1,5 % en peso de ácido láctico basado en el peso seco y donde la composición nutricional comprende de un 0,25 % en peso a un 20 % en peso de oligosacáridos no digeribles basado en el peso seco de la composición nutricional, donde la composición nutricional se administra a un lactante con una edad por debajo de los 6 meses, más preferiblemente por debajo de los 4 meses de edad y la autorregulación mejorada de la ingesta de energía se compara con la autorregulación de la ingesta de energía de lactantes alimentados con preparado infantil que no comprende un ingrediente fermentado por bacterias productoras de ácido láctico, y de un 0,05 a 1,5% en peso de ácido láctico basado en el peso en seco.
Description
DESCRIPCIÓN
Métodos de uso de preparado fermentado para lactantes
CAMPO DE LA INVENCIÓN
[0001] La invención se refiere a un alimento para lactantes, en particular un preparado para lactantes.
ANTECEDENTES DE LA INVENCIÓN
[0002] La leche humana es el patrón oro indiscutible de la nutrición infantil. Sin embargo, en algunos casos la lactancia es inadecuada o no tiene éxito por razones médicas o debido a la elección de no amamantar. Para tales situaciones se han desarrollado preparados para lactantes o de seguimiento. En la actualidad se usan comúnmente preparados para lactantes comerciales para proporcionar una fuente de alimento complementaria o única en los primeros años de vida. Estos preparados comprenden un rango de nutrientes para satisfacer las necesidades nutricionales del lactante en crecimiento e incluyen típicamente grasa, carbohidratos, proteínas, vitaminas, minerales y otros nutrientes útiles para un crecimiento y desarrollo infantil óptimo. Los preparados para lactantes comerciales están diseñados para imitar, tan fielmente como sea posible, la composición y la función de la leche humana.
[0003] Se ha observado desde hace tiempo que los lactantes amamantados tienen un patrón o trayectoria de aumento de peso diferente en comparación con los lactantes alimentados con preparados. Numerosos estudios realizados en varias regiones de todo el mundo han informado de que los lactantes amamantados tienen un aumento de peso más lento. El aumento de longitud tiende a diferir menos entre los lactantes amamantados y los alimentados con preparados y, como resultado, los lactantes amamantados están más magros. Así, en la técnica se ha indicado que la curva de crecimiento de los lactantes alimentados con preparados para lactantes comerciales difiere de la curva de crecimiento de los lactantes amamantados. Típicamente, un preparado para lactantes tiene un efecto de aceleración del crecimiento (peso) en el primer año de vida. Además, esta diferencia en las trayectorias de crecimiento se correlaciona con un mayor índice de masa corporal en las primeras etapas de la vida y un mayor riesgo de desarrollar obesidad en el futuro. Li et al, 2010, Pediatrics 125: e1386-e1393 revelan que los niños que se alimentan con biberón en la primera infancia tienen más probabilidades de acabarse el biberón o el vaso al final de la infancia que los que se alimentan directamente del pecho. La alimentación con biberón, independientemente del tipo de leche, difiere de la alimentación directamente del pecho en su efecto sobre la autorregulación de la ingesta de leche de los niños.
[0004] En el estado de la técnica en el campo de los preparados para lactantes para mejorar la trayectoria de crecimiento para que sea más similar a la trayectoria de crecimiento de los lactantes amamantados, el foco está en un preparado para lactantes con menos proteína y/o menor densidad calórica. La WO 2008/071667 divulga una composición nutricional para lactantes en riesgo de desarrollar obesidad más adelante en la vida que comprende una fuente de proteínas, una fuente de lípidos y una fuente de carbohidratos. El contenido de proteína es inferior a 1,8 g/100 kcal y la densidad energética es inferior a 650 kcal/litro. En la WO 2010/070613 se revela que se observó un aumento de peso inferior en la primera semana de vida cuando se usa un preparado con un contenido calórico muy bajo y un bajo contenido de proteína basado en volumen. Koletzko et al, 2009, Am J Clin Nutr 89: 1836-1845 revelan que el uso de un preparado isocalórico para lactantes y de continuación con un contenido de proteína de 1,77 y 2,1 g/100 kcal dio lugar a un menor aumento de peso que en el grupo de lactantes que consumieron un preparado para lactantes o de continuación con una alta concentración de proteína de 2,9 y 4,4 g/100 kcal. A los 24 meses, la puntuación z del peso por longitud de los lactantes en el grupo de preparado con menos proteína fue inferior que la del grupo con un alto contenido de proteína y no difirió de la del grupo de referencia de amamantados. En la WO 2015/078505 se observa un aumento de peso inferior en el período de 3 a 6 meses cuando se administra un preparado que comprende un contenido de proteína inferior que en el control. La WO 2015/091789 se centra en mezclas de oligosacáridos que comprenden oligosacárido N-acetilado, galactooligosacárido y/u oligosacárido sialilado que promueve una velocidad de crecimiento que se aproxima a la velocidad de crecimiento de los lactantes amamantados. La WO 2012/1078039 se refiere a unos preparados fermentados para lactantes para disminuir el esfuerzo digestivo de las proteínas mediante la disminución de la cantidad de proteasas formadas endógenamente, concomitante con un aumento de la digestión de las proteínas. La digestión mejorada permite reducir los niveles de proteína. La WO 2012/1078039 también se refiere a preparados fermentados para lactantes con poca proteína. La US 2014/0162223 proporciona métodos para prevenir y/o reducir la obesidad infantil temprana que pueden ayudar a inculcar hábitos de alimentación sana tempranos y preferencias por alimentos nutritivos en lactantes y niños pequeños, promover una trayectoria de crecimiento temprano apropiada y un estado de peso a largo plazo que sea consistente con las recomendaciones de las políticas públicas y esté asociado a la salud a largo plazo. La WO 2013/187764 divulga preparados fermentados para lactantes que comprenden oligosacáridos no digeribles para mejorar la salud del tracto intestinal mediante la disminución del esfuerzo digestivo de las proteínas. La WO 2015/065194 divulga un preparado fermentado para lactantes o de continuación que comprende oligosacáridos no digeribles para disminuir la duración de los llantos, reducir los episodios de llanto y la incidencia de cólicos en los lactantes.
RESUMEN DE LA INVENCIÓN
[0005] Un estudio de eficacia sobre el crecimiento y la seguridad de un preparado para lactantes parcialmente fermentado durante una intervención de 3-4 meses se investigó en lactantes sanos nacidos a término en comparación con un preparado estándar y una referencia de amamantados. En un ensayo clínico prospectivo aleatorizado controlado doble ciego multicéntrico, fueron inscritos lactantes antes de los 28 días de edad y se asignaron para recibir uno de dos preparados hasta las 17 semanas de edad: 1) un preparado para lactantes que comprende un preparado fermentado o 2) un preparado para lactantes no fermentado. La composición de los preparados fue similar en energía y composición de macronutrientes. Como referencia, se incluyó un grupo de lactantes que fue exclusivamente amamantado hasta las 17 semanas de edad. El crecimiento se evaluó por análisis de equivalencia de aumento de peso al día y el aumento del IMC al día durante el período de intervención usando márgenes de equivalencia de ± 0,5 DE, entre los grupos de preparado al igual que en comparación con el grupo de referencia de amamantados. También se monitoreó la longitud mensualmente.
[0006] A las 17 semanas se observó un aumento de peso y un aumento del IMC mayores estadísticamente significativos para el grupo de control, en comparación con el grupo de referencia de amamantados. No hubo ninguna diferencia estadísticamente significativa en el aumento de peso o el aumento del IMC en los lactantes alimentados con el preparado fermentado en comparación con el grupo de referencia de amamantados, ni en comparación con los lactantes alimentados con el preparado de control.
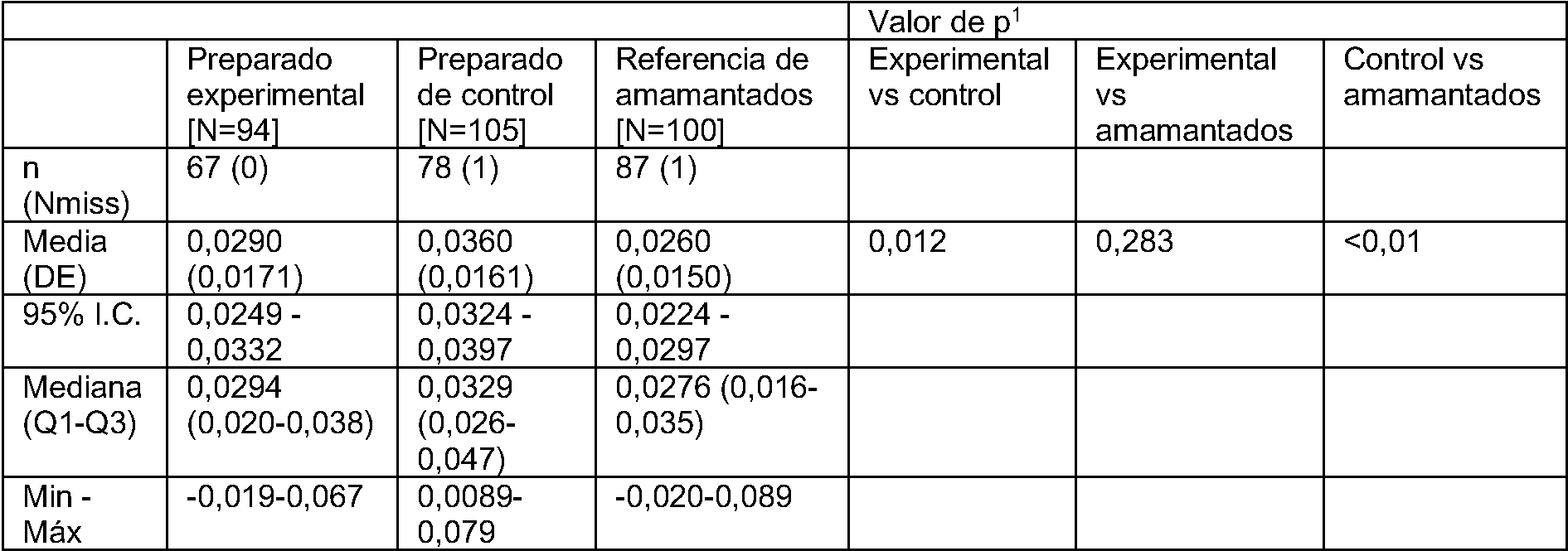
[0007] A las 17 semanas de edad se observaron diferencias significativas en los comportamientos alimentarios, en particular se observó una respuesta a la saciedad aumentada, una respuesta a los alimentos disminuida y un apetito general disminuido en el grupo que recibió el preparado fermentado. Esto es indicativo de la mejora de la autorregulación de la ingesta de energía del lactante hacia la autorregulación de la ingesta de energía observada en los lactantes amamantados.
[0008] Tanto el efecto observado en las trayectorias de crecimiento temprano en la vida, que son más similares al grupo de referencia de amamantados, como el observado en el comportamiento alimentario son indicativos de un menor riesgo de tener sobrepeso u obesidad más adelante en la vida en lactantes que consumen un preparado fermentado.
[0009] Mientras que en la técnica se considera normalmente que una ingesta de proteína demasiado alta durante la infancia es un factor de riesgo del sobrepeso y/o la obesidad y, por lo tanto, se considera beneficioso reducir el nivel de proteína en un preparado para lactantes, sorprendentemente los presentes inventores descubrieron que la inclusión de un ingrediente fermentado en el alimento infantil bajo en proteína mejoraba independientemente los efectos sobre el comportamiento alimentario y la trayectoria de crecimiento y así mejora el efecto sobre la prevención del sobrepeso y/o la obesidad.
DESCRIPCIÓN DETALLADA DE LA INVENCIÓN
[0010] La presente invención, por lo tanto, concierne a un método no terapéutico para promover una autorregulación mejorada de la ingesta de energía en un lactante, donde dicho método comprende administrar una composición que es un preparado para lactantes que comprende de 3 a 7 g de lípidos/100 kcal, de 1,25 a 5 g de proteína/100 kcal y de 6 a 16 g de carbohidrato digerible/100 kcal y donde la composición nutricional comprende un ingrediente fermentado por bacterias productoras de ácido láctico, y de un 0,05 a un 1,5 % en peso de ácido láctico basado en el peso seco y donde la composición nutricional comprende de un 0,25 % en peso a un 20 % en peso de oligosacáridos no digeribles basado en el peso seco de la composición nutricional, donde la composición nutricional se administra a un lactante con una edad menor de 6 meses, más preferiblemente menor de 4 meses de edad, y la autorregulación mejorada de la ingesta de energía se compara con la autorregulación de la ingesta de energía en lactantes alimentados con preparado para lactantes que no comprende un ingrediente fermentado por bacterias productoras de ácido láctico y de 0,05 a 1,5% en peso de ácido láctico basado en el peso en seco.
[0011] En otra forma de realización, la presente invención se refiere a un método no terapéutico para promover un comportamiento alimentario mejorado en un niño, en el que el comportamiento alimentario mejorado se selecciona del grupo que consiste en una mayor lentitud al comer, una mayor capacidad de respuesta a la saciedad, una disminución de la respuesta a los alimentos, un disfrute óptimo de los alimentos y un apetito óptimo, más preferiblemente una mayor capacidad de respuesta a la saciedad, una disminución de la capacidad de respuesta a los alimentos y una disminución del apetito general, donde dicho método comprende administrar una composición nutricional que es un preparado para lactantes que comprende de 3 a 7 g de lípidos/100 kcal, de 1,25 a 5 g de proteína/100 kcal y de 6 a 16 g de carbohidrato digerible/100 kcal y donde la composición nutricional comprende un ingrediente fermentado por bacterias productoras de ácido láctico, y de un 0,05 a un 1,5 % en peso de ácido láctico basado en el peso seco, y donde la composición nutricional comprende de un 0,25 % en peso a un 20 % en peso de oligosacáridos no digeribles basado en el peso seco de la composición nutricional, en el que la composición nutricional se administra a un lactante con una edad menor de 6 meses, más preferiblemente menor de 4 meses de edad y el comportamiento alimentario mejorado se compara con la velocidad de ingesta, la respuesta a la saciedad; capacidad de respuesta a los alimentos y/o nivel de apetito en lactantes alimentados con
preparado para lactantes que no comprende un ingrediente fermentado por bacterias productoras de ácido láctico, y de 0,05 a 1,5 % en peso de ácido láctico basado en el peso seco y el comportamiento alimentario mejorado se determina utilizando el Cuestionario de comportamiento alimentario infantil (BEBQ).
[0012] Por definición, las palabras "no terapéutico" excluyen cualquier efecto terapéutico.
[0013] En el contexto de la presente invención, la composición nutricional no es leche humana.
Ingrediente fermentado
[0014] La composición nutricional en los métodos o usos según la presente invención, denominada de aquí en adelante también como la presente composición nutricional, comprende un ingrediente fermentado. La presencia del ingrediente fermentado en la composición nutricional mejora en lactantes el comportamiento alimentario y/o la autorregulación de la ingesta de energía. Por lo tanto, la presencia del ingrediente fermentado en la composición nutricional reduce el riesgo del desarrollo de sobrepeso u obesidad.
[0015] El ingrediente fermentado es una composición que está fermentado por bacterias productoras de ácido láctico. La fermentación preferiblemente tiene lugar durante el proceso de producción de la composición nutricional. Preferiblemente, la composición nutricional no contiene cantidades significativas de bacterias viables en el producto final debido a la inactivación térmica después de la fermentación o la inactivación por otros medios. Preferiblemente el ingrediente fermentado es un producto derivado de la leche, que es un sustrato de leche que está fermentado por bacterias productoras de ácido láctico, y dicho sustrato de leche comprende al menos uno seleccionado del grupo consistente en leche, suero de leche, proteína de suero de leche, hidrolizado de proteína de suero de leche, caseína, hidrolizado de caseína y lactosa o mezclas derivadas. Adecuadamente, se describen composiciones nutricionales que comprenden un ingrediente fermentado y oligosacáridos no digeribles y su modo de producción en la WO 2009/151330, la WO 2009/151331 y la WO 2013/187764.
[0016] El ingrediente fermentado comprende preferiblemente fragmentos de células bacterianas como glicoproteínas, glicolípidos, peptidoglicano, ácido lipoteicoico (LTA), lipoproteínas, nucleótidos y/o polisacáridos capsulares. Además, tras la fermentación y/o otras interacciones de las bacterias productoras de ácido láctico con el sustrato de leche, se forman compuestos bioactivos adicionales, tales como péptidos bioactivos y/u oligosacáridos y ácidos orgánicos. Además, el preparado fermentado mejora la eficacia de la digestión de las proteínas. Por lo tanto, el ingrediente fermentado, en particular el producto derivado de la leche fermentado, se cree que tiene un efecto mejorado en comparación con el ingrediente no fermentado, en particular el producto derivado de la leche no fermentado.
[0017] Preferiblemente, la composición nutricional comprende de un 5 a un 97,5 % en peso del ingrediente fermentado basado en el peso seco, más preferiblemente de un 10 a un 95 % en peso, más preferiblemente de un 20 a un 90 % en peso, aún más preferiblemente de un 25 a un 60 % en peso. Como una manera de especificar la extensión de la fermentación, se puede tomar el nivel de la suma de ácido láctico y lactato en la composición nutricional, ya que este es el producto final metabólico producido por las bacterias productoras de ácido láctico tras la fermentación. La presente composición nutricional comprende de un 0,05 a un 1,5 % en peso de la suma de ácido láctico y lactato basado en el peso seco de la composición, más preferiblemente de un 0,05 a un 1,0 % en peso, aún más preferiblemente de un 0,1 a un 0,75 % en peso, aún más preferiblemente de un 0,1 a un 0,6 % en peso, aún más preferiblemente de un 0,1 a un 0,5 % en peso. Preferiblemente al menos un 50 % en peso, aún más preferiblemente al menos un 90 % en peso, de la suma de ácido láctico y lactato está en forma del isómero L(+). Así, en una forma de realización, la suma de ácido L(+)-láctico y L(+)-lactato es más de un 50 % en peso, más preferiblemente más de un 90 % en peso, basado en la suma de ácido láctico total y lactato. En la presente, L(+)-lactato y ácido L(+)-láctico también se denominan L-lactato y ácido L-láctico.
Bacterias productoras de ácido láctico usadas para producir el ingrediente fermentado
[0018] Las bacterias productoras de ácido láctico usadas para preparar el ingrediente fermentado, en particular para la fermentación del sustrato de leche se proporcionan preferiblemente como un monocultivo o un cultivo mixto. Las bacterias productoras de ácido láctico consisten en los géneros Bifidobacterium, Lactobacillus, Carnobacterium, Enterococcus, Lactococcus, Leuconostoc, Oenococcus, Pediococcus, Streptococcus, Tetragenococcus, Vagococcus y Weissella. Preferiblemente, las bacterias productoras de ácido láctico usadas para la fermentación comprenden las bacterias del género Bifidobacterium y/o Streptococcus.
[0019] Preferiblemente el Streptococcus es una cepa de S. thermophilus. Preferiblemente el Streptococcus desarrolla actividad de beta-galactosidasa en el curso de la fermentación del sustrato. La selección de una cepa adecuada de S. thermophilus se describe en el ejemplo 2 de la EP 778885 y en el ejemplo 1 de la FR 2723960. En otra forma de realización preferida según la presente invención, la composición nutricional comprende 103-106 ufc de bacterias vivas de S. thermophilus, por g de peso seco de la composición nutricional, preferiblemente la composición nutricional comprende 103-105 de bacterias vivas de S. thermophilus por g de peso seco.
[0020] Las cepas preferidas de S. thermophilus para preparar el ingrediente fermentado con el fin de la presente invención han sido depositadas por la Compagnie Gervais Danone en la Collection Nationale de Cultures de Microorganismes (CNCM) dirigida por el Instituto Pasteur, 25 rue du Docteur Roux, París, Francia, el 23 de agosto de 1995 bajo el número de registro I-1620 y el 25 de agosto de 1994 bajo el número de registro I-1470.
[0021] Las bifidobacterias son bacterias grampositivas anaeróbicas en forma de bastoncillo. Preferiblemente las bacterias productoras de ácido láctico usadas para la fermentación comprenden o son al menos una bifidobacteria seleccionada del grupo que consiste en B. breve, B. infantis, B. bifidum, B. catenulatum, B. adolescentis, B. thermophilum, B. gallicum, B. animalis o lactis, B. angulatum, B. pseudocatenulatum, B. thermacidophilum y B. longum, más preferiblemente B. breve, B. infantis, B. bifidum, B. catenulatum, B. longum, más preferiblemente B. longum y B. breve, aún más preferiblemente B. breve, más preferiblemente B. breve seleccionada del grupo que consiste en B. breve Bb-03 (Rhodia/Danisco), B. breve M-16V (Morinaga), B. breve R0070 (Instituto Rosell, Lallemand), B. breve BR03 (Probiotical), B. breve BR92 (Cell Biotech) DSM 20091, LMG 11613 y B. breve I-2219 depositadas en el CNCM, París, Francia. Más preferiblemente, la B. breve es B. breve M-16V (Morinaga) o B. breve I-2219, aún más preferiblemente B. breve I-2219.
[0022] Más preferiblemente, la composición nutricional comprende un ingrediente fermentado que está fermentado por las bacterias de ácido láctico que comprenden tanto B. breve como S. thermophilus. En una forma de realización, la fermentación por bacterias de ácido láctico, es una fermentación por Streptococcus thermophilus y Bifidobacterium breve. En una forma de realización, la composición nutricional comprende un ingrediente fermentado donde las bacterias de ácido láctico se inactivan después de la fermentación.
[0023] Preferiblemente, el ingrediente fermentado no está fermentado por Lactobacillus bulgaricus. Los productos fermentados por L. bulgaricus se consideran no adecuados para los lactantes, ya que, en los lactantes pequeños, la deshidrogenasa específica que convierte el D-lactato en piruvato es mucho menos activa que la deshidrogenasa que convierte el L-lactato.
[0024] Preferiblemente, la presente composición nutricional comprende bacterias productoras de ácido láctico inactivadas y/o fragmentos bacterianos derivados de bacterias productoras de ácido láctico obtenidos de más de 1x104 ufc de bacterias productoras de ácido láctico por g basado en el peso seco de la composición final, más preferiblemente más de 1x105 ufc, aún más preferiblemente más de 1x106 ufc. Preferiblemente, las bacterias inactivadas o los fragmentos bacterianos se obtienen de menos de 1x1014 ufc de bacterias productoras de ácido láctico por g basado en el peso seco de la composición final, más preferiblemente menos de 1x1013 ufc, aún más preferiblemente menos de 1x1012 ufc.
Proceso de fermentación
[0025] El sustrato de leche que se va a fermentar está adecuadamente presente en un medio acuoso. El sustrato de leche que se va a fermentar se selecciona preferiblemente del grupo que consiste en leche, suero de leche, proteína de suero de leche, hidrolizado de proteína de suero de leche, caseína, hidrolizado de caseína y lactosa, y sus mezclas derivadas. La leche puede ser leche entera, leche semidesnatada y/o leche desnatada. Preferiblemente, el sustrato de leche que se va a fermentar comprende leche desnatada. El suero de leche puede ser suero de leche dulce y/o suero de leche ácido. Preferiblemente, el suero de leche está presente en una concentración de 3 a 80 g de peso seco por l de medio acuoso que contiene sustrato de leche, más preferiblemente de 40 a 60 g por l. Preferiblemente, el hidrolizado de proteína de suero de leche está presente en de 2 a 80 g de peso seco por l de medio acuoso que contiene sustrato de leche, más preferiblemente de 5 a 15 g/l. Preferiblemente, la lactosa está presente en de 5 a 50 g de peso seco por l de sustrato acuoso, más preferiblemente de 1 a 30 g/l. Preferiblemente, el medio acuoso que contiene sustrato de leche comprende sales amortiguadoras para mantener el pH dentro de un rango deseado. Preferiblemente, el dihidrógeno fosfato de sodio o potasio se usa como sal amortiguadora, preferiblemente en de 0,5 a 5 g/l, más preferiblemente de 1,5 a 3 g por l. Preferiblemente, el medio acuoso que contiene sustrato de leche comprende cisteína en una cantidad de 0,1 a 0,5 g por l de sustrato acuoso, más preferiblemente de 0,2 a 0,4 g/l. La presencia de cisteína da lugar a un bajo potencial redox del sustrato, que es ventajoso para la actividad de las bacterias productoras de ácido láctico, particularmente las bifidobacterias. Preferiblemente, el medio acuoso que contiene sustrato de leche comprende extracto de levadura en una cantidad de 0,5 a 5 g/l de medio acuoso que contiene sustrato de leche, más preferiblemente de 1,5 a 3 g/l. El extracto de levadura es una fuente rica de cofactores enzimáticos y factores de crecimiento para las bacterias productoras de ácido láctico. La presencia de extracto de levadura aumentará la fermentación por bacterias productoras de ácido láctico.
[0026] Adecuadamente, el sustrato de leche, en particular el medio acuoso que contiene el sustrato de leche, se pasteuriza antes del paso de fermentación para eliminar la presencia de bacterias vivas no deseadas. Adecuadamente, el producto se pasteuriza después de la fermentación, para inactivar enzimas. Adecuadamente, la inactivación enzimática tiene lugar a 75 °C durante 3 min. Adecuadamente, el medio acuoso que contiene sustrato de leche se homogeneiza antes y/o el producto derivado de la leche se homogeneiza después de la fermentación. La homogeneización da lugar a un sustrato y/o un producto fermentado más estables, especialmente en presencia de grasa.
[0027] La densidad de inoculación está preferiblemente entre 1x102 y 5x1010, preferiblemente entre 1x104 y 5x109 ufc de bacterias productoras de ácido láctico/ml de medio acuoso que contiene sustrato de leche, más preferiblemente entre 1x107 y 1x109 ufc de bacterias productoras de ácido láctico/ml de medio acuoso que contiene sustrato de leche. La densidad bacteriana final después de la fermentación está preferiblemente entre 1x103 y 1x1010, más preferiblemente entre 1x104 y 1x109 UFC/ml de medio acuoso que contiene sustrato de leche.
[0028] La fermentación se realiza preferiblemente a una temperatura de aproximadamente 20 °C a 50 °C, más preferiblemente de 30 °C a 45 °C, aún más preferiblemente aproximadamente de 37 °C a 42 °C. La temperatura óptima para el crecimiento y/o la actividad de las bacterias productoras de ácido láctico, más particularmente lactobacilos y/o bifidobacterias, está entre 37 °C y 42 °C.
[0029] La incubación se realiza preferiblemente a un pH de 4 a 8, más preferiblemente de 6 a 7,5. Este pH no induce la precipitación de proteínas y/o un gusto adverso, mientras que, al mismo tiempo, las bacterias productoras de ácido láctico tales como lactobacilos y/o bifidobacterias son capaces de fermentar el sustrato de leche.
[0030] El período de incubación varía preferiblemente de 10 minutos a 48 h, preferiblemente de 2 h a 24 h, más preferiblemente de 4 h a 12 h. Un período de tiempo suficientemente largo permite que la fermentación y la producción concomitante de fragmentos celulares, compuestos bioactivos y ácidos orgánicos tengan lugar en gran medida, a la vez que el período de incubación no tiene que ser innecesariamente largo por razones económicas.
[0031] Los procedimientos para preparar ingredientes fermentados adecuados con el fin de la presente invención se conocen per se. La EP 778885 divulga en particular en el ejemplo 7 un proceso adecuado para preparar un ingrediente fermentado. La FR 2723960 divulga en particular en el ejemplo 6 un proceso adecuado para preparar un ingrediente fermentado. Brevemente, un sustrato de leche, preferiblemente pasteurizado, que contiene lactosa y macronutrientes opcionalmente adicionales tales como grasas, preferiblemente grasas vegetales, caseína, proteína de suero de leche, vitaminas y/o minerales, etc. se concentra, por ejemplo a entre un 15 y un 50% de materia seca y luego se inocula con S. thermophilus, por ejemplo con un 5% de un cultivo que contiene 106 a 1010 bacterias por ml. Preferiblemente, este sustrato de leche comprende péptidos de proteína de la leche. La temperatura y la duración de la fermentación son como se ha mencionado anteriormente. Adecuadamente después de la fermentación, el ingrediente fermentado se puede pasteurizar o esterilizar y, por ejemplo, secar por atomización o liofilizar para proporcionar una forma adecuada para formularse en el producto final.
[0032] Un método preferido para preparar el ingrediente fermentado de la presente invención se divulga en la WO 01/01785, más particularmente en los ejemplos 1 y 2. Un método preferido para preparar el producto fermentado de la presente invención se describe en la WO 2004/093899, más particularmente en el ejemplo 1.
Métodos de inactivación y/o eliminación física de células vivas
[0033] Preferiblemente, las células vivas de bacterias productoras de ácido láctico en el ingrediente fermentado se eliminan después de la fermentación, por ejemplo por inactivación y/o eliminación física. Preferiblemente las células se inactivan. Preferiblemente las células se tratan para que se vuelvan no replicativas. Preferiblemente las bacterias productoras de ácido láctico se matan por calor después de la fermentación del sustrato de leche. Maneras preferibles de matar por calor son la pasteurización (rápida), la esterilización, el tratamiento de temperatura ultra alta, el tratamiento térmico de temperatura alta/tiempo corto y/o el secado por atomización a temperaturas a las que las bacterias no sobreviven o ya no son capaces de replicarse. Los fragmentos celulares se obtienen preferiblemente por tratamiento térmico. Con este tratamiento térmico se inactivan preferiblemente al menos un 90 % de los microorganismos vivos, más preferiblemente al menos un 95%, aún más preferiblemente al menos un 99 %. Preferiblemente, la composición nutricional fermentada comprende menos de 1x105 unidades formadoras de colonias (ufc) de bacterias de ácido láctico vivas por g de peso seco, más preferiblemente menos de 1x104, aún más preferiblemente menos de 1x103 ufc de bacterias de ácido láctico vivas por g de peso seco. El tratamiento térmico se realiza preferiblemente a una temperatura que varía de 70 a 180 °C, preferiblemente de 80 a 150 °C, preferiblemente durante aproximadamente 3 minutos a 2 horas, preferiblemente en el rango de 80 a 140 °C durante 5 minutos a 40 minutos. La inactivación de las bacterias de ácido láctico da lugar ventajosamente a una menor acidificación posterior y un producto más seguro. Esto es especialmente ventajoso cuando la composición nutricional se va a administrar a lactantes o niños pequeños. Adecuadamente después de la fermentación, el ingrediente fermentado se puede pasteurizar o esterilizar y, por ejemplo, secar por atomización o liofilizar para proporcionar una forma adecuada para formularse en el producto final.
Oligosacárido no digerible
[0034] La presente composición nutricional comprende un oligosacárido no digerible y comprende preferiblemente al menos dos oligosacáridos no digeribles diferentes, en particular dos fuentes diferentes de oligosacáridos no digeribles. La presencia de un oligosacárido no digerible ayuda a promover un comportamiento alimentario o una autorregulación de la ingesta de energía mejorados. La presencia de oligosacáridos no digeribles afecta beneficiosamente a la microbiota intestinal y la hace más similar a la microbiota intestinal de los lactantes
amamantados. Dicha microbiota está asocida con un menor riesgo de obesidad. La combinación de un ingrediente fermentado y oligosacáridos no digeribles mejorará adicionalmente los beneficios reivindicados de la invención.
[0035] El término "oligosacárido" como se utiliza en la presente se refiere a sacáridos con un grado de polimerización (GP) de 2 a 250, preferiblemente un GP de 2 a 100, más preferiblemente de 2 a 60, aún más preferiblemente de 2 a 10. Si se incluye un oligosacárido con un GP de 2 a 100 en la presente composición nutricional, esto da lugar a composiciones que pueden contener oligosacáridos con un GP de 2 a 5, un GP de 50 a 70 y un GP de 7 a 60. El término "oligosacárido no digerible" como se usa en la presente invención se refiere a oligosacáridos que no son digeridos en el intestino por la acción de ácidos o enzimas digestivas presentes en el tracto digestivo superior humano, por ejemplo el intestino delgado y el estómago, sino que son fermentados preferiblemente por la microbiota intestinal humana. Por ejemplo, la sacarosa, la lactosa, la maltosa y las maltodextrinas se consideran digeribles.
[0036] Preferiblemente el presente oligosacárido no digerible es soluble. El término "soluble" como se utiliza en la presente, cuando hace referencia a un polisacárido, una fibra o un oligosacárido, significa que la sustancia es al menos soluble según el método descrito por L. Prosky et al., J. Assoc. Off. Anal. Chem. 71, 1017-1023 (1988).
[0037] El oligosacárido no digerible incluido en las presentes composiciones nutricionales en los métodos o usos según la presente invención incluyen preferiblemente una mezcla de oligosacáridos no digeribles. El oligosacárido no digerible se selecciona preferiblemente del grupo que consiste en fructo-oligosacárido, tal como la inulina, dextrinas no digeribles, galacto-oligosacárido, tal como transgalacto-oligosacárido, xilo-oligosacárido, arabinooligosacárido, arabinogalacto-oligosacárido, gluco-oligosacárido, gentio-oligosacárido, glucomananooligosacárido, galactomanano-oligosacárido, manano-oligosacárido, isomalto-oligosacárido, nigero-oligosacárido, glucomanano-oligosacárido, quito-oligosacárido, oligosacárido de soja, oligosacárido de ácido urónico, sialiloligosacárido, tal como 3-sialil-lactosa (3-SL), 6-sialil-lactosa (6-SL), lactosialiltetrasacárido a, b, c (LST), disialil-lacto-N-tetrosa (DSLNT), sialil-lacto-N-hexosa (S-LNH), DS-LNH, y fuco-oligosacárido, tal como oligosacárido de fucoidano (no) sulfatado, 2'-fucosil-lactosa (2'-FL), 3-fucosil-lactosa (3-FL), difucosil-lactosa, lacto-N-fucopentosa (LNFP) I, II, III, V, lacto-N-neofucopentosa (LNnFP), lacto-N-difucosil-hexosa (LNDH), y sus mezclas derivadas, aún más preferiblemente se selecciona del grupo que consiste en fructo-oligosacárido, tal como la inulina, galacto-oligosacárido, tal como un transgalacto-oligosacárido, y fuco-oligosacárido y sus mezclas derivadas, aún más preferiblemente transgalacto-oligosacárido y/o inulina, más preferiblemente transgalactooligosacárido. En una forma de realización en la composición o los métodos según la presente invención, el oligosacárido no digerible se selecciona del grupo que consiste en transgalacto-oligosacárido, fructo-oligosacárido y mezclas derivadas.
[0038] El oligosacárido no digerible se selecciona preferiblemente del grupo que consiste en p-galactooligosacárido, a-galacto-oligosacárido y galactano. Según una forma de realización más preferida, el oligosacárido no digerible es p-galacto-oligosacárido. Preferiblemente, el oligosacárido no digerible comprende galactooligosacárido con enlaces glicosídicos P(1,4), P(1,3) y/o p(1,6) y una glucosa terminal. Un transgalactooligosacárido está disponible, por ejemplo, bajo el nombre comercial Vivinal®GOS (Domo FrieslandCampina Ingredients), Bi2muno (Clasado), Cup-oligo (Nissin Sugar) y Oligomate55 (Yakult).
[0039] El oligosacárido no digerible comprende preferiblemente un fructo-oligosacárido. Un fructo-oligosacárido puede, en otro contexto, tener nombres como fructopolisacárido, oligofructosa, polifructosa, polifructano, inulina, levano y fructano y pueden referirse a oligosacáridos que comprenden unidades de fructosa con enlaces p, que se enlazan preferiblemente mediante enlaces glicosídicos P(2,1) y/o P(2,6), y un GP preferible entre 2 y 200. Preferiblemente, el fructo-oligosacárido contiene una glucosa terminal con enlace glicosídico P(2,1). Preferiblemente, el fructo-oligosacárido contiene al menos 7 unidades de fructosa con enlaces p. En otra forma de realización preferida se usa la inulina. La inulina es un tipo de fructo-oligosacárido donde al menos un 75% de los enlaces glicosídicos son enlaces P(2,1). Típicamente, la inulina tiene una longitud de cadena media entre 8 y 60 unidades de monosacárido. Un fructo-oligosacárido adecuado para usar en las composiciones de la presente invención está comercialmente disponible bajo el nombre comercial Raftiline®HP (Orafti). Otras fuentes adecuadas son Raftilose (Orafti), Fibrulose y Fibruline (Cosucra) y Frutafit y Frutalose (Sensus).
[0040] Preferiblemente, la presente composición nutricional comprende una mezcla de galacto-oligosacárido y fructo-oligosacárido. Preferiblemente, la mezcla de galacto-oligosacárido y fructo-oligosacárido está presente en una proporción en peso de 1/99 a 99/1, más preferiblemente de 1/19 a 19/1, más preferiblemente de 1/1 a 19/1, más preferiblemente de 2/1 a 15/1, más preferiblemente de 5/1 a 12/1, aún más preferiblemente de 8/1 a 10/1, aún más preferiblemente en una proporción de aproximadamente 9/1. Esta proporción en peso es particularmente ventajosa cuando el galacto-oligosacárido tiene un GP medio bajo y el fructo-oligosacárido tiene un GP relativamente alto. Más preferida es una mezcla de galacto-oligosacárido con un GP medio por debajo de 10, preferiblemente por debajo de 6, y un fructo-oligosacárido con un GP medio por encima de 7, preferiblemente por encima de 11, aún más preferiblemente por encima de 20. Tal mezcla mejora sinérgicamente la microbiota intestinal.
[0041] Preferiblemente, la presente composición nutricional comprende una mezcla de fructo-oligosacárido de cadena corta y fructo-oligosacárido de cadena larga. Preferiblemente, la mezcla de fructo-oligosacárido de cadena corta y fructo-oligosacárido de cadena larga está presente en una proporción en peso de 1/99 a 99/1, más preferiblemente de 1/19 a 19/1, aún más preferiblemente de 1/10 a 19/1, más preferiblemente de 1/5 a 15/1, más preferiblemente de 1/1 a 10/1. Se prefiere una mezcla de fructo-oligosacárido de cadena corta con un GP medio por debajo de 10, preferiblemente por debajo de 6, y un fructo-oligosacárido con un GP medio por encima de 7, preferiblemente por encima de 11, aún más preferiblemente por encima de 20.
[0042] La presente composición nutricional comprende de un 0,25 a un 20 % en peso de oligosacárido no digerible total, preferiblemente de un 2,5 a un 20 % en peso, más preferiblemente de un 2,5 a un 15 % en peso, aún más preferiblemente de un 3,0 a un 10 % en peso, más preferiblemente de un 5,0 a un 7,5 % en peso, basado en el peso seco de la composición nutricional. Basado en 100 ml, la presente composición nutricional comprende preferiblemente de un 0,35 a un 2,5 % en peso de oligosacárido no digerible total, más preferiblemente de un 0,35 a un 2,0 % en peso, aún más preferiblemente de un 0,4 a un 1,5 % en peso, basado en 100 ml de la composición nutricional. Una cantidad inferior de oligosacárido no digerible será menos eficaz en la promoción un comportamiento alimentario mejorado o en la mejora de la microbiota intestinal, mientras que una cantidad demasiado alta dará lugar a efectos secundarios de hinchamiento e incomodidad abdominal.
Preparado para lactantes y preparado de continuación
[0043] La composición nutricional que se va a administrar en el método según la presente invención se selecciona de un preparado para lactantes. Esto significa que la presente composición nutricional no es leche humana. Alternativamente, el término "preparado" significa que se refiere a una composición que se prepara artificialmente o, en otras palabras, que es sintética. Por lo tanto, en una forma de realización, la composición nutricional se selecciona de un preparado para lactantes artificial y un preparado de continuación artificial o un preparado para lactantes sintético y un preparado de continuación sintético. En el presente contexto, el preparado para lactantes se refiere a composiciones nutricionales, artificialmente preparadas, destinadas a lactantes de 0 a aproximadamente 4 a 6 meses de edad y destinadas a ser un sustituto de la leche humana. Típicamente, los preparados para lactantes son adecuados para usarse como única fuente de alimento. Tales preparados se conocen también como preparado de iniciación. Los preparados para lactantes partiendo de los 4 a 6 meses de vida hasta los 12 meses de vida están destinados a ser alimentos suplementarios para los lactantes que empiezan a destetarse con otros alimentos. Tales preparados se conocen también como fórmulas de continuación. Los preparados para lactantes y de continuación están sujetos a regulaciones estrictas, por ejemplo a la directiva de la comisión de la UE 2006/141/EC.
[0044] La composición nutricional comprende de 3 a 7 g de lípidos/100 kcal, preferiblemente de 4 a 6 g de lípidos/100 kcal, más preferiblemente de 4,5 a 5,5 g de lípidos/100 kcal, de 1,25 a 5 g de proteína/100 kcal, preferiblemente de 1,25 a 4 g de proteína/100 kcal, más preferiblemente de 1,25 a 3 g de proteína/100 kcal, más preferiblemente de 1,25 a 2,5 g de proteína/100 kcal, más preferiblemente de 1,25 a 2,25 g/100 kcal, aún más preferiblemente de 1,25 a 2,1 g de proteína/100 kcal, aún más preferiblemente de 1,6 a 2,0 g de proteína/100 kcal, aún más preferiblemente de 1,7 a 2,0 g de proteína/100 kcal, aún más preferiblemente de 1,75 a 1,95 g de proteína/100 kcal y de 6 a 16 g de carbohidrato digerible/100 kcal, preferiblemente de 8 a 16 g de carbohidrato digerible/100 kcal, más preferiblemente de 10 a 15 g de carbohidrato digerible/100 kcal.
Lípido
[0045] En la presente, LA se refiere a cadena de acilo y/o ácido linoleico (18:2 n6); ALA se refiere a cadena de acilo y/o ácido a-linolénico (18:3 n3); PUFA se refiere a cadenas de acilo y/o ácidos grasos poliinsaturados; MUFA se refiere a cadenas de acilo y/o ácidos grasos monoinsaturados; LC-PUFA se refiere a cadenas de acilo y/o ácidos grasos poliinsaturados de cadena larga que comprenden al menos 20 átomos de carbono en la cadena de acilo graso y con 2 o más enlaces insaturados; DHA se refiere a cadena de acilo y/o ácido docosahexaenoico (22:6, n3); EPA se refiere a cadena de acilo y/o ácido eicosapentaenoico (20:5 n3); ARA se refiere a cadena de acilo y/o ácido araquidónico (20:4 n6); DPA se refiere a cadena de acilo y/o ácido docosapentaenoico (22:5 n3). PA se refiere a cadenas de acilo y/o ácido palmítico (C16:0). Los ácidos grasos de cadena media (MCFA) se refieren a cadenas de acilo y/o ácidos grasos con una longitud de cadena de 6, 8 o 10 átomos de carbono.
[0046] El lípido en la composición nutricional que se va a administrar en el método o el uso según la presente invención comprende preferiblemente lípidos vegetales. El lípido que está presente en la composición nutricional en el método o el uso según la invención comprende preferiblemente PUFA, más preferiblemente LC-PUFA, ya que los LC-PUFA mejoran adicionalmente el desarrollo del lactante. La composición nutricional comprende preferiblemente de un 5 a un 35 % en peso de PUFA, más preferiblemente de un 10 a un 30 % en peso de PUFA, más preferiblemente de un 15 a un 20 % en peso de PUFA, basado en lípido total. En una forma de realización, el lípido en la composición nutricional para el método o el uso según la invención comprende al menos un 10 % en peso de ácido graso poliinsaturado basado en los ácidos grasos totales. También se prefiere que la composición nutricional comprenda MUFA, preferiblemente de un 10 a un 80 % en peso de MUFA, más preferiblemente de un
20 a un 70 % en peso de MUFA, más preferiblemente de un 35 a un 55 % en peso de MUFA, basado en lípido total.
[0047] El LA está presente preferiblemente en una cantidad suficiente para promover un crecimiento y desarrollo sanos, pero en una cantidad tan baja como sea posible para evitar la aparición de desequilibrios en el crecimiento o el desarrollo corporal. Por lo tanto, la composición nutricional comprende preferiblemente menos de un 20 % en peso de LA basado en lípido total, preferiblemente de un 5 a un 16 % en peso, más preferiblemente de un 10 a un 14,5 % en peso. Preferiblemente, la composición nutricional comprende al menos un 5 % en peso de LA basado en lípido total. Por 100 kcal, la composición nutricional comprende preferiblemente 350-1400 mg de LA. Preferiblemente, el ALA está presente en una cantidad suficiente para promover un crecimiento y desarrollo sanos del lactante. Por lo tanto, la composición nutricional comprende preferiblemente al menos un 1,0 % en peso de ALA basado en lípido total. Preferiblemente la composición nutricional comprende al menos un 1,5 % en peso de ALA basado en lípido total, más preferiblemente al menos un 2,0 % en peso. Preferiblemente, la composición nutricional comprende menos de un 12,5 % en peso de ALA, más preferiblemente menos de un 10,0 % en peso, más preferiblemente menos de un 5,0 % en peso. Preferiblemente, la composición nutricional comprende una proporción en peso de LA/ALA de 2 a 20, más preferiblemente de 3 a 16, más preferiblemente de 4 a 14, más preferiblemente de 5 a 12.
[0048] Según la presente invención, la composición nutricional comprende preferiblemente un LC-PUFA, más preferiblemente un LC-PUFA n-3, ya que un LC-PUFA n-3 promueve un crecimiento ventajoso. Más preferiblemente, la composición nutricional comprende EPA, DPA y/o DHA, aún más preferiblemente d Ha . Ya que una baja concentración de DHA, DPA y/o EPA es ya eficaz y el crecimiento y el desarrollo normales son importantes, el contenido de un LC-PUFA n-3 en la composición nutricional preferiblemente no excede de un 15 % en peso del contenido de ácidos grasos total, preferiblemente no excede de un 10 % en peso, aún más preferiblemente no excede de un 5 % en peso. Preferiblemente, la composición nutricional comprende al menos un 0,15 % en peso, preferiblemente al menos un 0,35 % en peso, más preferiblemente al menos un 0,75 % en peso, de un LC-PUFA n-3, basado en el contenido de ácidos grasos. El contenido de DHA en la composición nutricional preferiblemente no excede de un 10 % en peso del contenido de ácidos grasos total, preferiblemente no excede de un 5 % en peso. Preferiblemente, la composición nutricional comprende al menos un 0,15 % en peso, preferiblemente al menos un 0,35 % en peso, % en peso de DHA basado en los ácidos grasos totales.
[0049] Como el grupo de ácidos grasos n-6, especialmente el ácido araquidónico (ARA) y el LA como su precursor, contrarresta al grupo de ácidos grasos n-3, especialmente el DHA y el EPA y el a La como su precursor, la composición nutricional comprende cantidades relativamente bajas de ARA. El contenido de LC-PUFA n-6, más preferiblemente ARA, preferiblemente no excede de un 5 % en peso, más preferiblemente no excede de un 2,0 % en peso, más preferiblemente no excede de un 0,75 % en peso, aún más preferiblemente no excede de un 0,5 % en peso, basado en los ácidos grasos totales. El ARA también puede estar ausente.
Proteína
[0050] La composición nutricional comprende proteínas en las cantidades de 1,25 a 5 g de proteína/100 kcal, preferiblemente de 1,25 a 4 g de proteína/100 kcal, más preferiblemente de 1,25 a 3 g de proteína/100 kcal, más preferiblemente de 1,25 a 2,5 g de proteína/100 kcal, más preferiblemente de 1,25 a 2,25 g/100 kcal, aún más preferiblemente de 1,25 a 2,1 g de proteína/100 kcal, aún más preferiblemente de 1,6 a 2,1 g de proteína/100 kcal, aún más preferiblemente de 1,6 a 2,0 g de proteína/100 kcal, aún más preferiblemente de 1,7 a 2,0 g de proteína/100 kcal, aún más preferiblemente de 1,75 a 1,95 g de proteína/100 kcal. Una cantidad óptima de proteína afectará beneficiosamente al comportamiento alimentario. La combinación de un ingrediente fermentado y la cantidad óptima de proteína tiene un efecto mejorado adicionalmente sobre el comportamiento alimentario y/o la autorregulación de la ingesta de energía. La fuente de la proteína debería seleccionarse de manera que se satisfagan los requisitos mínimos para el contenido de aminoácido esenciales y se asegure un crecimiento satisfactorio. Por lo tanto, se prefieren fuentes de proteína basadas en proteínas de la leche de las vacas tales como suero de leche, caseína y sus mezclas derivadas y proteínas basadas en soja, patata o guisante. En el caso de que se usen proteínas de suero de leche, la fuente de proteínas se basa preferiblemente en suero de leche ácido o suero de leche dulce, aislado de proteína de suero o mezclas derivadas y puede incluir a-lactoalbúmina y P-lactoglobulina. Más preferiblemente, la fuente de proteínas se basa en suero de leche ácido o suero de leche dulce del que se ha eliminado el caseino-gluco-macropéptido (CGMP). Preferiblemente, la composición comprende al menos un 3 % en peso de caseína basado en el peso seco. Preferiblemente la caseína está intacta y/o no hidrolizada. Para la presente invención, la proteína incluye péptidos y aminoácidos libres.
Carbohidratos digeribles
[0051] La composición nutricional comprende carbohidrato digerible en las cantidades especificadas anteriormente. Fuentes de carbohidratos digeribles preferidas son la lactosa, la glucosa, la sacarosa, la fructosa, la galactosa, la maltosa, el almidón y la maltodextrina. La lactosa es el carbohidrato digerible principal presente en la leche humana. La lactosa tiene ventajosamente un índice glucémico bajo. La composición nutricional comprende preferiblemente lactosa. La composición nutricional comprende preferiblemente carbohidrato digerible, donde al
menos un 35 % en peso, más preferiblemente al menos un 50 % en peso, más preferiblemente al menos un 75 % en peso, aún más preferiblemente al menos un 90 % en peso, más preferiblemente al menos un 95 % en peso del carbohidrato digerible es lactosa. Basado en el peso seco, la presente composición comprende preferiblemente al menos un 25 % en peso de lactosa, preferiblemente al menos un 40 % en peso.
Aplicación
[0052] En el método o el uso según la presente invención, una composición nutricional se administra a un lactante o se usa en un lactante. En el contexto de la presente invención, un lactante tiene una edad de hasta 12 meses. Preferiblemente, la composición nutricional se administra a o se usa en un lactante nacido a término. Un lactante nacido a término significa un lactante nacido con una edad gestacional de >37 a <42 semanas. Preferiblemente, la composición nutricional se administra a o se usa en un lactante sano. Preferiblemente, la composición nutricional se usa al menos durante los primeros 2 meses de vida, preferiblemente al menos durante los primeros 3 meses de vida del lactante, más preferiblemente al menos durante los primeros 4 meses de vida del lactante. La composición nutricional se administra a un lactante con una edad por debajo de los 6 meses, más preferiblemente por debajo de los 4 meses de edad.
[0053] En una forma de realización la presente invención es adecuada particularmente más adelante en la vida para los lactantes criados en un entorno obesogénico, o que siguen la dieta occidental
[0054] Un entorno obesogénico, o dieta obesogénica, o dieta de tipo occidental es alta en calorías, alta en grasa y alta en azúcar. La grasa es alta en grasa saturada, tiene una alta proporción de ácidos grasos n6/n3 y es alta en colesterol. La dieta se caracteriza generalmente por una alta ingesta de carne procesada, carne roja, mantequilla, muchos productos lácteos grasos, azúcar y granos refinados. La OMS/FAO tiene pautas para la dieta recomendada y la dieta de tipo occidental se está desviando de estas pautas, Food and Nutrition Paper 91: Fats and fatty acids in human nutrition - Report of an expert consultation de la FAO (Organización de las Naciones Unidas para la Alimentación y la Agricultura), que tuvo lugar los días 10-14 de noviembre de 2008 en Ginebra, disponible de forma impresa en noviembre de 2010, ISBN 978-92-5-106733-8. La dieta de tipo occidental se denomina a veces también dieta americana estándar. A efectos de la presente invención, los alimentos occidentales o, en otras palabras, una dieta de tipo occidental se caracteriza preferiblemente por el hecho de que 1) más de un 30% de las calorías totales está proporcionado por grasa, 2) comprende al menos un 10 % en peso de grasa saturada basado en la cantidad total de grasa, 3) comprende al menos un 0,5 % en peso de colesterol basado en la grasa total, 4) la proporción n6/n3 de los ácidos grasos en la grasa dietética está por encima de 4 y, en una definición mejorada, la proporción n6/n3 de los ácidos grasos en la grasa dietética está por encima de 10.
[0055] Así, según una forma de realización de la presente invención, la composición nutricional se va a usar en un lactante que está expuesto a un entorno obesogénico y/o a una dieta de tipo occidental más adelante en la vida, preferiblemente cuando el lactante tenga una edad por encima de los 36 meses. Por lo tanto, la presente invención está destinada en particular a niños con riesgo de ser obesos más adelante en la vida. Por tanto, la presente invención está destinada en particular a niños criados en un entorno obesogénico. Un entorno obesogénico es un entorno donde los seres humanos están rodeados de comida barata, rápida, nutricionalmente inferior y un entorno construido que disuade de la actividad física.
[0056] La presente invención también se refiere a la mejora de la autorregulación de la ingesta de energía del lactante hacia la autorregulación de la ingesta de energía observada en lactantes amamantados, preferiblemente en comparación con la autorregulación de la ingesta de energía en lactantes alimentados con fórmula infantil que no comprende ingrediente fermentado como se define aquí, o en otras palabras que no comprende ácido láctico en el rango que se define aquí. En una forma de realización preferida, la conducta alimentaria mejorada se selecciona del grupo que consiste en una mayor lentitud en la alimentación, una mayor capacidad de respuesta a la saciedad, una disminución de la respuesta a los alimentos, un disfrute óptimo de la comida y un apetito óptimo, más preferiblemente, una mayor capacidad de respuesta a la saciedad, una disminución de la capacidad de respuesta a los alimentos y una disminución del apetito general, preferiblemente en comparación con la tasa de ingesta, la capacidad de respuesta a la saciedad, la capacidad de respuesta a los alimentos, el nivel de disfrute de la comida y/o el nivel de apetito en los lactantes alimentados con fórmula infantil que no comprende un ingrediente fermentado como se define en este aquí, o en otras palabras, que no comprende ácido láctico en el rango que se define aquí
[0057] Se promueve la reducción del riesgo de desarrollar sobrepeso y/o obesidad y/o la prevención de sobrepeso y/u obesidad en un lactante. Más preferiblemente, se promueve una reducción del riesgo de desarrollar sobrepeso y/u obesidad más adelante en la vida y/o la prevención de sobrepeso y/u obesidad en un lactante más adelante en la vida. Más preferiblemente, se promueve una reducción del riesgo de obesidad infantil y/o la prevención de la obesidad infantil en un lactante.
EJEMPLOS
Ejemplo 1: trayectorias de crecimiento y desarrollo de la composición corporal en los primeros años de vida en lactantes que consumen un preparado para lactantes parcialmente fermentado o un preparado de control en comparación con un grupo de referencia de amamantados
[0058] Se investigó el crecimiento y la seguridad de un preparado experimental (preparado 1) frente a un preparado de control (preparado 2) en un estudio clínico exploratorio, usando una intervención de 3-4 meses en lactantes nacidos a término sanos. En un ensayo clínico prospectivo aleatorizado controlado doble ciego multicéntrico, fueron inscritos lactantes antes de los 28 días de edad y se asignaron para recibir uno de dos preparados hasta las 17 semanas de edad.
[0059] El preparado para lactantes experimental 1 es un preparado para lactantes que contiene 0,8 g/100 ml de oligosacáridos no digeribles de scGOS (fuente Vivinal® GOS) y lcFOS (fuente RaftilinHP®) en una proporción en peso de 9:1. De este preparado para lactantes, un 30% basado en el peso seco derivaba de Lactofidus™, un preparado para lactantes disponible comercialmente comercializado bajo la marca Gallia. Lactofidus™ es una composición derivada de leche fermentada y se produce fermentando con S. thermophilus y comprende B. breve. Se emplea un tratamiento térmico suave. El preparado para lactantes 1 comprendía aproximadamente un 0,33 % en peso de ácido láctico lactato basado en el peso seco, del cual al menos un 95% es ácido L-láctico L-lactato. El preparado para lactantes de control 2 es un preparado para lactantes no fermentado sin scGOS/lcFOS. La composición de los dos preparados fue similar en energía y composición de macronutrientes (por 100 ml: 66 kcal, 1,2 g de proteína (proteína de suero de leche bovino/caseína en proporción de 1/1 en peso), 7,7 g de carbohidrato digerible (de los que 7,6 g son lactosa), 3,4 g de grasa (principalmente grasa vegetal). La composición comprendía además vitaminas, minerales, oligoelementos y otros micronutrientes según la directiva internacional 2006/141/EC para un preparado para lactantes.
[0060] Como referencia, se incluyó un grupo de lactantes que fue exclusivamente amamantado hasta las 17 semanas de edad. La población por intención de tratar (ITT) consistió en todos los sujetos asignados al azar al preparado para lactantes (n = 199), además se incluyeron 100 sujetos en el grupo de referencia de amamantados. La población ITT consistió en 94 sujetos en el grupo experimental, 105 sujetos en el grupo de control. La población por protocolo (PP) consistió en todos los sujetos del grupo ITT sin desviaciones del protocolo predeterminado. Para el análisis de datos de crecimiento, el análisis PP fue considerado el análisis primario (principal), esta población consistió en 145 sujetos asignados al azar (71 en el grupo experimental y 74 en el grupo de control) y 86 sujetos amamantados. Un total de 75 sujetos terminaron el estudio prematuramente, n = 22 para el grupo experimental, n = 25 para el grupo de control (sin diferencia significativa entre los grupos) y n = 28 en el grupo de referencia de amamantados. Las razones de la terminación temprana fueron sujetos con un evento adverso (n = 5 para el experimental, n = 9 para el control, n = 0 para los amamantados), retirada del consentimiento (n = 2 para el experimental, n = 3 para el control, n = 17 para los amamantados), perdidos para el seguimiento (n = 4 para el experimental, n = 1 para el control, n = 7 para los amamantados) y otros (n = 11 para el experimental, n = 11 para el control, n = 4 para los amamantados). No hubo ninguna diferencia entre el grupo experimental y el de control con respecto a las características de la línea base, excepto que había más gemelos en el grupo de control. No hubo ninguna diferencia entre el grupo experimental y el de control con respecto a las características parentales.
[0061] El crecimiento se evaluó por análisis de equivalencia de aumento de peso al día durante el período de intervención usando márgenes de equivalencia de ± 0,5 DE, entre los grupos de preparado (por protocolo) al igual que en comparación con el grupo de referencia de amamantados. Además, el aumento de longitud también se monitoreó mensualmente. Se usó un modelo de curva de crecimiento paramétrico (PGC) para probar la equivalencia de aumento de peso en los diferentes brazos de tratamiento. Además del modelo PGC (curva de crecimiento paramétrico), se usaron modelos GLM (modelo lineal generalizado (ANCOVA)) y AMN (modelo de medias arbitrarias) para controlar la corrección del modelo. ANCOVA y AMN generaron resultados similares al PGC, lo que indica la validez del modelo PGC.
Resultados
[0062] El aumento de peso al día (gramos/día) se calculó como la "diferencia en peso" dividida entre la "diferencia en tiempo transcurrido" para probar la superioridad. La tabla 1 muestra el aumento de peso (g/día) durante todo el período de estudio (desde la línea base hasta la semana 17). Las comparaciones con el grupo de referencia de amamantados llevaron a diferencias estadísticamente significativas para el grupo de control 2, como resultado del mayor aumento de peso en el grupo de control, (valor de p del control vs. amamantados 0,028). No hubo ninguna diferencia estadísticamente significativa a lo largo del tiempo para los lactantes alimentados con el preparado experimental 1 en comparación con los lactantes alimentados con el preparado de control 2, o con el grupo de referencia de amamantados. Los resultados de la población ITT estaban en línea con los resultados de la población PP.
[0063] En la tabla 2 se presentan los resultados del modelo PGC con estimaciones de contraste para la diferencia en el aumento de peso (gramos/día) entre los grupos de estudio para la población PP. Se confirmó la equivalencia en el aumento de peso entre el grupo experimental 1 y el grupo de referencia de amamantados (IC: -0,5161 a 3,0293 y estimación 1,2566) (p = 0,2432), pero, para el grupo de control 2, no se demostró ninguna equivalencia con los amamantados (IC: 0,7619 a 4,0966 y estimación 2,4292) (p = 0,0168), con un mayor aumento de peso en el grupo de control 1. Cuando se comparan los 2 grupos de preparados, los intervalos de confianza al 90% de la diferencia estimada (IC: -2,9260 a 0,6442 y estimación -1,1409) estaban completamente entre -0,5*DE y 0,5*DE (margen de equivalencia), lo que significa que todas las comparaciones confirmaron la equivalencia en el aumento de peso (g/día) entre el grupo experimental 1 y grupo de control 2 (p = 0,2926). Los resultados de la población ITT estaban en línea con los resultados de la población PP.
Tabla 2: estimaciones de contraste para la diferencia en el aumento de peso (gramos/día) entre los grupos de estudio PP e ITT
[0064] No se observó ninguna diferencia estadísticamente significativa en el aumento de longitud entre grupo de preparado experimental 1, el grupo de preparado de control 2 y el grupo de referencia de amamantados, para el grupo PP, al igual que para el grupo ITT.
[0065] Cuando se analizó el aumento del índice de masa corporal (IMC) al día (kg/m2/día) se calculó como la "diferencia en IMC" dividida entre la "diferencia en tiempo transcurrido" para probar la superioridad. La tabla 3 muestra el aumento del IMC (kg/m2/día) a lo largo de todo el período de estudio (desde la línea base hasta la semana 17). Las comparaciones con el grupo de referencia de amamantados llevaron a diferencias estadísticamente significativas para el grupo de control 2, como resultado del mayor aumento del IMC en el grupo de control, (valor de p del control vs. amamantados 0,007). No hubo ninguna diferencia estadísticamente significativa a lo largo del tiempo para los lactantes alimentados con el preparado experimental 1 en comparación con los lactantes alimentados con el preparado de control 2, o con el grupo de referencia de amamantados. Los resultados de la población ITT estaban en línea con los resultados de la población PP, pero adicionalmente en el grupo experimental 1 el aumento del IMC reducido, en comparación con el grupo de preparado de control 2, fue estadísticamente significativo (p = 0,012).
Tabla 3a: aumento del IMC de los lactantes (kg/m2/día) desde la línea base hasta la semana 17, (PP)
Tabla 3b: aumento del IMC de los lactantes (kg/m2/día) desde la línea base hasta la semana 17, (ITT)
[0066] En la tabla 4 se presentan los resultados del modelo PGC con estimaciones de contraste para la diferencia en el aumento del IMC (kg/m2/día) entre los grupos de estudio para la población PP-G. Se confirmó la equivalencia en el aumento del IMC entre el grupo experimental 1 y el grupo de referencia de amamantados (IC: -0,0007 a 0,0086 y estimación 0,0039) (p = 0,1639). Para el grupo de control 2 no se demostró ninguna equivalencia con los amamantados (IC: 0,0012 a 0,0097 y estimación 0,0054) (p = 0,0334). Cuando se compararon los dos grupos de preparado, los intervalos de confianza al 90% de la diferencia estimada (IC: -0,0062 a 0,0028 y estimación -0,0017) estaban completamente entre -0,5*DE y 0,5*DE (margen de equivalencia), lo que significa que todas las comparaciones confirmaron la equivalencia en el aumento del IMC entre el grupo experimental 1 y el grupo de control 2 (p = 0,5292). Los resultados de la población ITT estaban en línea con los resultados de la población PP.
Tabla 4: estimaciones de contraste para la diferencia en el aumento del IMC (kg/m2/día) entre los grupos de estudio, PP e ITT
[0067] El preparado sin ingrediente fermentado, con un contenido de proteína de 1,8 g/100 kcal, que se considera bajo en la técnica, no muestra una trayectoria de crecimiento mejorada comparable al grupo de referencia de amamantados como tal, pero en presencia de ingrediente fermentado se mejora la trayectoria de crecimiento. Estos resultados son indicativos de una trayectoria de crecimiento y un desarrollo de la composición corporal en lactantes que consumen un preparado para lactantes que está parcialmente fermentado que es más similar a la trayectoria de crecimiento y desarrollo de la composición corporal en lactantes amamantados. Estos resultados son indicativos de un riesgo reducido de desarrollar sobrepeso u obesidad en los lactantes que consumen fórmula infantil fermentada al menos en parte.
Ejemplo 2: el comportamiento alimentario difiere en los lactantes que reciben el preparado experimental en comparación con el preparado de control en la semana 17
[0068] En el estudio clínico del ejemplo 1, los progenitores rellenaron cuestionarios del comportamiento alimentario de los bebés (Llewellyn et al. Appetite 2011, 57: 388-96). El cuestionario de comportamiento alimentario de los bebés (BEBQ) es una herramienta extensamente validada que ha demostrado ser capaz de valorar el comportamiento alimentario en los lactantes. El BEBQ genera puntuaciones en las escalas siguientes: respuesta a los alimentos, disfrute de los alimentos, respuesta a la saciedad, lentitud para comer y apetito general. El cuestionario de comportamiento alimentario de los bebés (BEBQ) tiene 18 preguntas con respuestas en una escala de 5 puntos (nunca, raramente, a veces, a menudo, siempre). Los elementos se utilizan para calcular puntuaciones en las escalas siguientes: respuesta a los alimentos (6 elementos), disfrute de los alimentos (4 elementos), respuesta a la saciedad (3 elementos), lentitud para comer (4 elementos) y apetito general (1 elemento).
[0069] En la primera visita (visita de inclusión), como se esperaba, no se observó ninguna diferencia significativa entre el grupo de control y el experimental. Sin embargo, cuando los lactantes tenían 17 semanas de edad se observaron diferencias significativas, véase la tabla 5, y también los cambios cuando se compara con la línea base, véase la tabla 6. La respuesta a la saciedad aumentó y el apetito general disminuyó en el grupo que recibió el preparado experimental en comparación con el grupo de control, mientras que la lentitud para comer aumentó, la respuesta a los alimentos disminuyó y el disfrute de los alimentos disminuyó, pero no mostraron diferencias significativas (pruebas de Wilcoxon-Mann-Whitney).
Cuando los lactantes tenían 17 semanas de edad se observaron diferencias significativas en el comportamiento alimentario cuando se compara con la línea base. La respuesta a la saciedad aumentó y la respuesta a los alimentos y el apetito general disminuyeron en el grupo que recibió el preparado experimental. La lentitud para comer aumentó y el disfrute de los alimentos fue inferior también, pero no estadísticamente significativos.
Tabla 5: Resultados del BEBQ de los lactantes que recibieron el preparado experimental en comparación con los lactantes que recibieron el preparado de control en la semana 17, ITT
Tabla 6: Resultados del BEBQ de los lactantes que recibieron el preparado experimental en comparación con los lactantes que recibieron el preparado de control en la semana 17, cambio desde la línea base, grupo ITT
[0070] Como se muestra en Llewellyn et al. (Appetite 2011, 57: 388-96), Mallan et al. (Apetite, 2014; 82: 43-49) y Jaarsveld et al. (JAMA Pediatr 2014, 168 (4): 345-350) todos los cambios observados en la conducta alimentaria en el grupo experimental, incluso si no llegan a tener importancia, son indicativos de un menor riesgo de desarrollar sobrepeso u obesidad más adelante en la vida.
[0071] Los datos sobre la ingesta de preparado también sugieren una correlación entre el comportamiento alimentario, en particular la respuesta a la saciedad y el apetito general, y la ingesta de preparado. Sin desear estar quedar limitados por la teoría, las trayectorias de crecimiento con un aumento de peso y un aumento del IMC inferiores observadas en el grupo experimental, que son más cercanas a las trayectorias de crecimiento del grupo de referencia de amamantados, podrían explicarse por una mejor autorregulación de la ingesta de energía debido a un comportamiento alimentario mejorado.
[0072] Tanto el efecto observado en la conducta alimentaria como las trayectorias de crecimiento, que son más similares al grupo de referencia amamantado, indican un menor riesgo de desarrollar sobrepeso u obesidad más adelante en la vida para los lactantes que consumen un preparado infantil (parcialmente) fermentado.
Ejemplo 3: trayectorias de crecimiento y desarrollo de la composición corporal en los primeros años de vida en lactantes que consumen un preparado para lactantes que comprende un preparado parcialmente fermentado, que comprende oligosacáridos no digeribles o que comprende ambos
[0073] Los datos siguientes se muestran par demostrar que el efecto sobre la trayectoria de crecimiento se debe principalmente a la presencia de un preparado parcialmente fermentado y que la presencia de oligosacáridos no digeribles tiene menos efecto.
Se realizó un ensayo clínico similar al descrito en el ejemplo 1. En un ensayo clínico prospectivo aleatorizado doble ciego multicéntrico, los lactantes fueron inscritos antes de los 28 días de edad y se asignaron a 3 grupos de prueba para recibir uno de tres preparados:
Grupo de prueba 1, preparado para lactantes 1 fermentado parcialmente con oligosacáridos no digeribles (50F+): donde el preparado para lactantes 1 comprende por 100 ml 66 kcal, 1,35 g de proteína (proteína de suero de leche bovino/caseína en proporción en peso 1/1), 8,2 g de carbohidrato digerible (de los que 5,6 g son lactosa y 2,1 g, maltodextrina), 3,0 g de grasa (principalmente grasa vegetal), 0,8 g de oligosacáridos no digeribles que comprenden scGOS (fuente Vivinal® GOS) y lcFOS (fuente RaftilinHP®) en una proporción en peso de 9:1. De este preparado para lactantes, aproximadamente un 50 % en peso basado en el peso seco deriva de Lactofidus™. El preparado para lactantes comprende aproximadamente un 0,55 % en peso de ácido láctico lactato basado en el peso seco, del cual al menos un 95% es ácido L(+)-láctico/lactato. La composición comprende además vitaminas, minerales, oligoelementos y otros micronutrientes según la directiva internacional 2006/141/EC para un preparado para lactantes.
Grupo de prueba 2: preparado para lactantes 2 parcialmente fermentado sin oligosacáridos no digeribles, (50F-) similar al preparado para lactantes 1 pero sin los oligosacáridos no digeribles scGOS y lcFOS. Grupo de prueba 3: preparado para lactantes 3 (0F+), un preparado para lactantes no fermentado con 0,8 g de oligosacáridos no digeribles que comprenden scGOS (fuente Vivinal® GOS) y lcFOS (fuente RaftilinHP®) en una proporción en peso de 9:1, y para el resto similar en composición al preparado para lactantes 1.
[0074] En los análisis estadísticos, se investigaron las comparaciones de interés. El efecto del preparado fermentado se evaluó por comparación de los grupos de prueba 3 (0F+) y 1 (50F+). El efecto de la adición de oligosacárido no digerible se evaluó por comparación de los grupos de prueba 3 (50F+) y 2 (50F).
[0075] Del total de 432 sujetos asignados al azar, 16 sujetos fueron excluidos de la población de todos los sujetos tratados (AST), ya que no consumieron ningún producto del estudio. Un sujeto fue diagnosticado con hipotiroidismo y se consideró no sano, se asignó al azar erróneamente y se excluyó del análisis ITT. Un total de 276 sujetos completaron el estudio hasta las 17 semanas de edad, mientras que 155 (36%) de los sujetos abandonaron el estudio prematuramente. Aparentemente, el número de sujetos que completaron el estudio no era diferente entre los grupos. No hubo ninguna diferencia en las razones para abandonar entre los grupos. La población por protocolo fue 79, 65 y 74 sujetos para los grupos 1,2 y 3, respectivamente. En la línea base, no se observó ninguna diferencia en las características de los sujetos, incluida la proporción de sexos, de los grupos de intervención PP, salvo un mayor número de lactantes primogénitos en el grupo 1 frente al grupo 2, que se considera estadísticamente significativo, diferente por casualidad y sin relevancia clínica. Las medidas antropométricas en la línea base no eran diferentes estadísticamente entre los grupos de tratamiento.
Resultados
[0076] El aumento de peso medio (gramo/día) en la población PP en la semana 17 fue máximo en el grupo de prueba 3 con oligosacáridos no digeribles pero sin ingrediente fermentado y mínimo en el grupo de prueba 2 con ingrediente fermentado pero sin oligosacáridos no digeribles. La mediana del aumento de peso mostró un patrón similar. El aumento de longitud medio (mm/día), por otro lado, fue bastante similar en los grupos 2 y 3, pero mayor en el grupo 1, véase la tabla 7.
Tabla 7: el aumento en el peso (gramo/día) y en la longitud (mm/día) por preparado desde la entrada al estudio hasta las 17 semanas de edad para el grupo por protocolo.
[0077] Usando el análisis de PGC (curva de crecimiento paramétrico) similar al ejemplo 1, la diferencia estimada en el aumento de peso en el grupo 3 (0F+) frente al grupo 1 (50F+) fue 0,15 y el aumento de longitud fue -0,05. En otras palabras, en el grupo que consumía el preparado con el ingrediente fermentado, el aumento de peso fue inferior que en el grupo que consumía un preparado sin ingrediente fermentado, mientras que el aumento de longitud en ambos grupos fue similar. En ambos preparados estaban presentes oligosacáridos no digeribles.
[0078] Asimismo, la diferencia estimada en el aumento de peso en el grupo 2 (50F vs. 50F+) frente al grupo 1 fue -0,31 y el aumento de longitud fue -0,03. En otras palabras, en el grupo que consumía el preparado con el ingrediente fermentado, pero sin oligosacáridos no digeribles, el aumento de peso fue inferior que en el grupo que consumía un preparado con ingrediente fermentado con oligosacáridos no digeribles y el aumento de longitud en ambos grupos fue similar.
En el mismo estudio, un grupo recibió el mismo preparado que el grupo de prueba 1 con la única diferencia de que en vez de un 50 % en peso contenía un 15 % en peso de Lactofidus™ basado en el peso seco de la composición. Los resultados sobre la trayectoria de crecimiento para el 15 % en peso de ingrediente fermentado fueron incluso más ventajosos que el 50 % en peso que mostró el efecto beneficioso en un amplio rango.
[0079] Estos efectos sobre el aumento de peso y de longitud son indicativos de un menor aumento de peso por longitud y un menor aumento del IMC principalmente debido al consumo de un preparado parcialmente fermentado y no, o en una menor medida, debido al consumo de un preparado con oligosacáridos no digeribles. Estos resultados muestran que el efecto beneficioso sobre la trayectoria de crecimiento y desarrollo corporal están causados principalmente por la presencia de un preparado para lactantes parcialmente fermentado, y no por la presencia de oligosacáridos no digeribles. En este estudio clínico no se incluyó ningún grupo de referencia de amamantados o grupo de control sin ingrediente fermentado y sin oligosacáridos no digeribles, de modo que solo se pueden extraer conclusiones sobre el efecto de un ingrediente fermentado que reduce el aumento de peso y reduce el aumento del IMC, mientras que la presencia de oligosacáridos no digeribles no tiene o tiene un menor efecto.
Claims (11)
1. Método no terapéutico para promover una autorregulación mejorada de la ingesta de energía en un lactante, donde dicho método comprende administrar una composición nutricional que es un preparado para lactantes que comprende de 3 a 7 g de lípidos/100 kcal, de 1,25 a 5 g de proteína/100 kcal y de 6 a 16 g de carbohidrato digerible/100 kcal y donde la composición nutricional comprende un ingrediente fermentado por bacterias productoras de ácido láctico, y de un 0,05 a un 1,5 % en peso de ácido láctico basado en el peso seco y donde la composición nutricional comprende de un 0,25 % en peso a un 20 % en peso de oligosacáridos no digeribles basado en el peso seco de la composición nutricional, donde la composición nutricional se administra a un lactante con una edad por debajo de los 6 meses, más preferiblemente por debajo de los 4 meses de edad y la autorregulación mejorada de la ingesta de energía se compara con la autorregulación de la ingesta de energía de lactantes alimentados con preparado infantil que no comprende un ingrediente fermentado por bacterias productoras de ácido láctico, y de un 0,05 a 1,5% en peso de ácido láctico basado en el peso en seco.
2. Método no terapéutico para promover un comportamiento alimentario mejorado en un lactante, donde el comportamiento alimentario mejorado se selecciona del grupo que consiste en una mayor lentitud para comer, una mayor capacidad de respuesta a la saciedad, una menor capacidad de respuesta a los alimentos, un disfrute óptimo de los alimentos y un apetito óptimo, más preferiblemente un aumento de la capacidad de respuesta a la saciedad, una disminución de la respuesta a los alimentos y una disminución del apetito general, donde dicho método comprende administrar una composición nutricional que es un preparado infantil que comprende de 3 a 7 g de lípidos/100 kcal, de 1,25 a 5 g de proteína/100 kcal y de 6 a 16 g de carbohidrato digerible/100 kcal y donde la composición nutricional comprende un ingrediente fermentado por bacterias productoras de ácido láctico, y de un 0,05 a un 1,5 % en peso de ácido láctico basado en el peso seco y donde la composición nutricional comprende de un 0,25 % en peso a un 20 % en peso de oligosacáridxos no digeribles basado en el peso seco de la composición nutricional, donde la composición nutricional se administra a un lactante con una edad por debajo de los 6 meses, más preferiblemente por debajo de los 4 meses de edad, y el comportamiento alimentario mejorado se compara con la tasa de alimentación, la capacidad de respuesta a la saciedad, la capacidad de respuesta a los alimentos y / o el nivel de apetito en lactantes alimentados con un preparado que no comprende un ingrediente fermentado por bacterias productoras de ácido láctico, y de 0,05 a 1,5% en peso de láctico ácido basado en el peso seco y el comportamiento alimentario mejorado se determina utilizando el cuestionario de comportamiento alimentario de los bebés (BEBQ).
3. Método no terapéutico según la reivindicación 1 o 2, donde la composición nutricional comprende de 1,6 a 2,1 g de proteína/100 kcal
4. Método no terapéutico según cualquiera de las reivindicaciones precedentes, donde los oligosacáridos no digeribles se seleccionan del grupo consistente en fructo-oligosacáridos y galacto-oligosacáridos.
5. Método no terapéutico según cualquiera de las reivindicaciones precedentes, donde las bacterias productoras de ácido láctico son Bifidobacterium breve y/o Streptococcus thermophilus.
6. Método no terapéutico según cualquiera de las reivindicaciones precedentes, donde la composición nutricional comprende bacterias productoras de ácido láctico inactivadas.
7. Método no terapéutico según cualquiera de las reivindicaciones precedentes, donde la composición nutricional comprende de 1,7 a 2,0 g de proteína/100 kcal.
8. Método no terapéutico según cualquiera de las reivindicaciones precedentes, donde la composición nutricional comprende de 1,75 a 1,95 g de proteína/100 kcal.
9. Método no terapéutico según cualquiera de las reivindicaciones precedentes, donde la composición nutricional comprende ácido láctico y lactato en una cantidad de un 0,1 a un 0,75 % en peso basado en el peso seco de la composición.
10. Método no terapéutico según cualquiera de las reivindicaciones precedentes, donde la composición nutricional comprende ácidos grasos poliinsaturados de cadena larga n-3 (LC-PUFA) en una cantidad que no excede del 15% en peso del contenido total de ácidos grasos, y que es al menos 0,15% en peso basado en el contenido de ácidos grasos.
11. Método no terapéutico según cualquiera de las reivindicaciones precedentes, donde el lactante se expone a un ambiente obesogénico y/o tipo de dieta occidental más tarde en la vida.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP16169015 | 2016-05-10 | ||
| PCT/EP2017/061193 WO2017194607A1 (en) | 2016-05-10 | 2017-05-10 | Fermented infant formula |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2857815T3 true ES2857815T3 (es) | 2021-09-29 |
Family
ID=55963221
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES17728777T Active ES2857815T3 (es) | 2016-05-10 | 2017-05-10 | Métodos de uso de preparado fermentado para lactantes |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20190142052A1 (es) |
| EP (2) | EP3454674B1 (es) |
| CN (1) | CN109688839A (es) |
| ES (1) | ES2857815T3 (es) |
| PL (1) | PL3454674T3 (es) |
| PT (1) | PT3454674T (es) |
| WO (1) | WO2017194607A1 (es) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7266580B2 (ja) * | 2018-03-23 | 2023-04-28 | 森永乳業株式会社 | 学童期以降の高血糖に起因する疾患の予防のための乳幼児用組成物 |
| US20210352925A1 (en) | 2019-02-04 | 2021-11-18 | N.V. Nutricia | Fermented formula with non digestible oligosaccharides for sleep improvement |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2723960B1 (fr) | 1994-08-31 | 1996-10-11 | Gervais Danone Co | Cultures de streptococcus thermophilus a activite beta-galactosidase elevee, leur procede d'obtention, et leurs utilisations |
| FR2723963B1 (fr) | 1994-08-31 | 1997-01-17 | Gervais Danone Co | Preparation de produits fermentes par streptococcus thermophilus, enrichis en galacto-oligosaccharides et en beta-galactosidase |
| FR2795917B1 (fr) | 1999-07-06 | 2001-08-31 | Gervais Danone Sa | Procede de preparation d'un produit lacte immunostimulant et ses applications |
| FR2853908B1 (fr) | 2003-04-16 | 2005-06-03 | Gervais Danone Sa | Produit immunomodulateur obtenu a partir d'une culture de bifidobacterium et compositions le contenant |
| ES2350907T3 (es) * | 2005-07-01 | 2011-01-28 | N.V. Nutricia | Nutrición para bebés con proteínas hidrolizadas. |
| WO2008054192A1 (en) * | 2006-11-02 | 2008-05-08 | N.V. Nutricia | Use of nutritional compositions for preventing disorders |
| EP1932437A1 (en) * | 2006-12-15 | 2008-06-18 | Nestec S.A. | Infant formula |
| DK2285387T3 (en) | 2008-06-13 | 2016-01-25 | Nutricia Nv | Nutrition for preventing infections |
| WO2010070613A2 (en) | 2008-12-18 | 2010-06-24 | University College London | Baby feeding formula and system |
| EP2910132A1 (en) | 2010-12-06 | 2015-08-26 | N.V. Nutricia | Fermented infant formula |
| EP2734992A4 (en) | 2011-07-22 | 2014-10-15 | Nestec Sa | METHOD FOR REDUCING CHILD OBESITY |
| WO2013036104A1 (en) * | 2011-09-08 | 2013-03-14 | N.V. Nutricia | Infant nutrition for regulating food intake later in life |
| WO2013187755A1 (en) | 2012-06-14 | 2013-12-19 | N.V. Nutricia | Fermented infant formula with non digestible oligosaccharides |
| RU2663065C2 (ru) * | 2013-11-04 | 2018-08-01 | Н.В. Нютрисиа | Ферментированное детское питание с неперевариваемыми олигосахаридами |
| RU2638323C1 (ru) | 2013-11-29 | 2017-12-13 | Нестек С.А. | Применение питательных композиций с низким количеством белка |
| MX2016007715A (es) | 2013-12-19 | 2016-09-07 | Nestec Sa | Composicion nutricional para reducir el estres metabolico en infantes. |
-
2017
- 2017-05-10 EP EP17728777.8A patent/EP3454674B1/en active Active
- 2017-05-10 WO PCT/EP2017/061193 patent/WO2017194607A1/en active Search and Examination
- 2017-05-10 EP EP20210984.9A patent/EP3841892A1/en active Pending
- 2017-05-10 CN CN201780042808.8A patent/CN109688839A/zh active Pending
- 2017-05-10 ES ES17728777T patent/ES2857815T3/es active Active
- 2017-05-10 PT PT177287778T patent/PT3454674T/pt unknown
- 2017-05-10 PL PL17728777T patent/PL3454674T3/pl unknown
- 2017-05-10 US US16/300,400 patent/US20190142052A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| CN109688839A (zh) | 2019-04-26 |
| EP3454674A1 (en) | 2019-03-20 |
| EP3841892A1 (en) | 2021-06-30 |
| EP3454674B1 (en) | 2020-12-02 |
| PT3454674T (pt) | 2021-03-09 |
| WO2017194607A1 (en) | 2017-11-16 |
| PL3454674T3 (pl) | 2021-06-14 |
| US20190142052A1 (en) | 2019-05-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2725464T3 (es) | Sistema de fórmula infantil con niveles adaptativos de oligosacáridos de leche humana (OLH) | |
| DK2285387T3 (en) | Nutrition for preventing infections | |
| ES2928210T3 (es) | Producto alimentario que comprende una mezcla de oligosacáridos y proteínas hidrolizadas que se utiliza para reducir las alergias alimentarias | |
| ES2706606T3 (es) | Composición nutricional con bifidobacteria no viable y oligosacárido no digerible | |
| ES2451020T3 (es) | Método para estimular la flora intestinal en bebés alumbrados por cesárea | |
| ES2882219T3 (es) | Fórmula infantil fermentada con oligosacáridos no digeribles | |
| CN111227045B (zh) | 乳制品在促进哺乳动物身长增长中的应用 | |
| CN101594789A (zh) | 益生菌(婴儿)食品 | |
| RU2650569C2 (ru) | Ферментированное питание с неусвояемыми олигосахаридами с повышенной биодоступностью железа | |
| CN103889241A (zh) | 用于促进健康的骨生长和/或用于预防和/或治疗骨疾病的组合物 | |
| CN109890222A (zh) | 包含人乳低聚糖的个性化儿科营养产品 | |
| RU2677924C2 (ru) | Высоколактозное ферментированное питание с повышенной биодоступностью железа | |
| CN116998729A (zh) | 含有不可消化寡糖的发酵配方物 | |
| WO2017043962A1 (en) | Method for stimulating microbiota health after non-natural birth | |
| BR112018013501B1 (pt) | Uso de um ingrediente fermentado e oligossacarídeo não digerível | |
| US20200315235A1 (en) | Normalization of the Intestinal Microbiota Composition in Infants or Toddlers Fed with an Amino Acid-Based Nutritional Composition | |
| ES2857815T3 (es) | Métodos de uso de preparado fermentado para lactantes | |
| ES2821914T3 (es) | Usos de un preparado fermentado para lactantes | |
| CN104837368A (zh) | 用于促进饱腹感的营养组合物 | |
| US20160206658A1 (en) | Nutrition for prevention of infections | |
| RU2716214C2 (ru) | Композиция для улучшения умственных способностей | |
| Falcão et al. | Infant Formulas: A Long Story | |
| EP3920723A1 (en) | Fermented formula with non digestible oligosaccharides for sleep improvement | |
| ES2966026T3 (es) | Composición nutricional que comprende urea y oligosacáridos no digeribles | |
| EP3968787A1 (en) | Fermented formula for improving intestinal development |