EP0275906A2 - Thermotrope Polymere enthaltende ungesättigte Polyesterharze, Verfahren zu ihrer Herstellung und ihre Verwendung zur Herstellung von Formkörpern - Google Patents
Thermotrope Polymere enthaltende ungesättigte Polyesterharze, Verfahren zu ihrer Herstellung und ihre Verwendung zur Herstellung von Formkörpern Download PDFInfo
- Publication number
- EP0275906A2 EP0275906A2 EP88100368A EP88100368A EP0275906A2 EP 0275906 A2 EP0275906 A2 EP 0275906A2 EP 88100368 A EP88100368 A EP 88100368A EP 88100368 A EP88100368 A EP 88100368A EP 0275906 A2 EP0275906 A2 EP 0275906A2
- Authority
- EP
- European Patent Office
- Prior art keywords
- acid
- bis
- fabrication
- unsaturated polyester
- polyester
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 229920000642 polymer Polymers 0.000 title claims abstract description 24
- 229920006337 unsaturated polyester resin Polymers 0.000 title claims abstract description 11
- 238000004519 manufacturing process Methods 0.000 title claims description 8
- 238000000034 method Methods 0.000 title claims description 8
- 239000000178 monomer Substances 0.000 claims abstract description 10
- 229920006305 unsaturated polyester Polymers 0.000 claims abstract description 9
- 229920000728 polyester Polymers 0.000 claims description 28
- 239000000203 mixture Substances 0.000 claims description 24
- 238000000465 moulding Methods 0.000 claims description 11
- 125000003118 aryl group Chemical group 0.000 claims description 9
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 claims description 5
- 229920001225 polyester resin Polymers 0.000 claims description 5
- 239000004645 polyester resin Substances 0.000 claims description 5
- 238000002360 preparation method Methods 0.000 claims description 2
- -1 aromatic dicarboxylic acids Chemical class 0.000 description 21
- 150000001875 compounds Chemical class 0.000 description 16
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 15
- 125000004432 carbon atom Chemical group C* 0.000 description 14
- 239000002253 acid Substances 0.000 description 10
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Natural products C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 9
- KKEYFWRCBNTPAC-UHFFFAOYSA-N Terephthalic acid Chemical compound OC(=O)C1=CC=C(C(O)=O)C=C1 KKEYFWRCBNTPAC-UHFFFAOYSA-N 0.000 description 9
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 9
- FJKROLUGYXJWQN-UHFFFAOYSA-N 4-hydroxybenzoic acid Chemical compound OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 8
- QIGBRXMKCJKVMJ-UHFFFAOYSA-N Hydroquinone Chemical compound OC1=CC=C(O)C=C1 QIGBRXMKCJKVMJ-UHFFFAOYSA-N 0.000 description 8
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 8
- XKZQKPRCPNGNFR-UHFFFAOYSA-N 2-(3-hydroxyphenyl)phenol Chemical compound OC1=CC=CC(C=2C(=CC=CC=2)O)=C1 XKZQKPRCPNGNFR-UHFFFAOYSA-N 0.000 description 6
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- WNLRTRBMVRJNCN-UHFFFAOYSA-N adipic acid Chemical compound OC(=O)CCCCC(O)=O WNLRTRBMVRJNCN-UHFFFAOYSA-N 0.000 description 6
- QQVIHTHCMHWDBS-UHFFFAOYSA-N isophthalic acid Chemical compound OC(=O)C1=CC=CC(C(O)=O)=C1 QQVIHTHCMHWDBS-UHFFFAOYSA-N 0.000 description 6
- DNIAPMSPPWPWGF-UHFFFAOYSA-N monopropylene glycol Natural products CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 6
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 5
- 150000008064 anhydrides Chemical class 0.000 description 5
- IISBACLAFKSPIT-UHFFFAOYSA-N bisphenol A Chemical class C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 description 5
- 238000009833 condensation Methods 0.000 description 5
- 230000005494 condensation Effects 0.000 description 5
- FPYJFEHAWHCUMM-UHFFFAOYSA-N maleic anhydride Chemical compound O=C1OC(=O)C=C1 FPYJFEHAWHCUMM-UHFFFAOYSA-N 0.000 description 5
- 239000000155 melt Substances 0.000 description 5
- 229940090248 4-hydroxybenzoic acid Drugs 0.000 description 4
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 4
- 150000002148 esters Chemical class 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 229920005989 resin Polymers 0.000 description 4
- 239000011347 resin Substances 0.000 description 4
- GHMLBKRAJCXXBS-UHFFFAOYSA-N resorcinol Chemical compound OC1=CC=CC(O)=C1 GHMLBKRAJCXXBS-UHFFFAOYSA-N 0.000 description 4
- CXMXRPHRNRROMY-UHFFFAOYSA-N sebacic acid Chemical compound OC(=O)CCCCCCCCC(O)=O CXMXRPHRNRROMY-UHFFFAOYSA-N 0.000 description 4
- 125000003903 2-propenyl group Chemical class [H]C([*])([H])C([H])=C([H])[H] 0.000 description 3
- 150000005168 4-hydroxybenzoic acids Chemical class 0.000 description 3
- OMPJBNCRMGITSC-UHFFFAOYSA-N Benzoylperoxide Chemical compound C=1C=CC=CC=1C(=O)OOC(=O)C1=CC=CC=C1 OMPJBNCRMGITSC-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- LGRFSURHDFAFJT-UHFFFAOYSA-N Phthalic anhydride Natural products C1=CC=C2C(=O)OC(=O)C2=C1 LGRFSURHDFAFJT-UHFFFAOYSA-N 0.000 description 3
- 239000001361 adipic acid Substances 0.000 description 3
- 235000011037 adipic acid Nutrition 0.000 description 3
- 235000019400 benzoyl peroxide Nutrition 0.000 description 3
- JQRRFDWXQOQICD-UHFFFAOYSA-N biphenylen-1-ylboronic acid Chemical compound C12=CC=CC=C2C2=C1C=CC=C2B(O)O JQRRFDWXQOQICD-UHFFFAOYSA-N 0.000 description 3
- JHIWVOJDXOSYLW-UHFFFAOYSA-N butyl 2,2-difluorocyclopropane-1-carboxylate Chemical compound CCCCOC(=O)C1CC1(F)F JHIWVOJDXOSYLW-UHFFFAOYSA-N 0.000 description 3
- 125000005587 carbonate group Chemical group 0.000 description 3
- SZXQTJUDPRGNJN-UHFFFAOYSA-N dipropylene glycol Chemical compound OCCCOCCCO SZXQTJUDPRGNJN-UHFFFAOYSA-N 0.000 description 3
- 239000000945 filler Substances 0.000 description 3
- 238000006068 polycondensation reaction Methods 0.000 description 3
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 3
- 125000000391 vinyl group Chemical class [H]C([*])=C([H])[H] 0.000 description 3
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 description 2
- DNIAPMSPPWPWGF-GSVOUGTGSA-N (R)-(-)-Propylene glycol Chemical compound C[C@@H](O)CO DNIAPMSPPWPWGF-GSVOUGTGSA-N 0.000 description 2
- MYRTYDVEIRVNKP-UHFFFAOYSA-N 1,2-Divinylbenzene Chemical compound C=CC1=CC=CC=C1C=C MYRTYDVEIRVNKP-UHFFFAOYSA-N 0.000 description 2
- HECLRDQVFMWTQS-RGOKHQFPSA-N 1755-01-7 Chemical compound C1[C@H]2[C@@H]3CC=C[C@@H]3[C@@H]1C=C2 HECLRDQVFMWTQS-RGOKHQFPSA-N 0.000 description 2
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 2
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 2
- VJIDDJAKLVOBSE-UHFFFAOYSA-N 2-ethylbenzene-1,4-diol Chemical compound CCC1=CC(O)=CC=C1O VJIDDJAKLVOBSE-UHFFFAOYSA-N 0.000 description 2
- QGNLHMKIGMZKJX-UHFFFAOYSA-N 3-chloro-4-hydroxybenzoic acid Chemical compound OC(=O)C1=CC=C(O)C(Cl)=C1 QGNLHMKIGMZKJX-UHFFFAOYSA-N 0.000 description 2
- XSAVLGOTFYRGCX-UHFFFAOYSA-N 3-ethyl-4-hydroxybenzoic acid Chemical compound CCC1=CC(C(O)=O)=CC=C1O XSAVLGOTFYRGCX-UHFFFAOYSA-N 0.000 description 2
- URFNSYWAGGETFK-UHFFFAOYSA-N 4,4'-Dihydroxybibenzyl Chemical compound C1=CC(O)=CC=C1CCC1=CC=C(O)C=C1 URFNSYWAGGETFK-UHFFFAOYSA-N 0.000 description 2
- VPWNQTHUCYMVMZ-UHFFFAOYSA-N 4,4'-sulfonyldiphenol Chemical class C1=CC(O)=CC=C1S(=O)(=O)C1=CC=C(O)C=C1 VPWNQTHUCYMVMZ-UHFFFAOYSA-N 0.000 description 2
- LTFHNKUKQYVHDX-UHFFFAOYSA-N 4-hydroxy-3-methylbenzoic acid Chemical compound CC1=CC(C(O)=O)=CC=C1O LTFHNKUKQYVHDX-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- 239000004342 Benzoyl peroxide Substances 0.000 description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 229920000106 Liquid crystal polymer Polymers 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N Propane Chemical compound CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- XXROGKLTLUQVRX-UHFFFAOYSA-N allyl alcohol Chemical compound OCC=C XXROGKLTLUQVRX-UHFFFAOYSA-N 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- VCCBEIPGXKNHFW-UHFFFAOYSA-N biphenyl-4,4'-diol Chemical group C1=CC(O)=CC=C1C1=CC=C(O)C=C1 VCCBEIPGXKNHFW-UHFFFAOYSA-N 0.000 description 2
- PXKLMJQFEQBVLD-UHFFFAOYSA-N bisphenol F Chemical compound C1=CC(O)=CC=C1CC1=CC=C(O)C=C1 PXKLMJQFEQBVLD-UHFFFAOYSA-N 0.000 description 2
- 229940106691 bisphenol a Drugs 0.000 description 2
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 2
- 229910052794 bromium Inorganic materials 0.000 description 2
- WERYXYBDKMZEQL-UHFFFAOYSA-N butane-1,4-diol Chemical compound OCCCCO WERYXYBDKMZEQL-UHFFFAOYSA-N 0.000 description 2
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical compound OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 2
- 150000001735 carboxylic acids Chemical class 0.000 description 2
- 238000005266 casting Methods 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- 239000000460 chlorine Substances 0.000 description 2
- 230000000052 comparative effect Effects 0.000 description 2
- ZQMIGQNCOMNODD-UHFFFAOYSA-N diacetyl peroxide Chemical compound CC(=O)OOC(C)=O ZQMIGQNCOMNODD-UHFFFAOYSA-N 0.000 description 2
- ROORDVPLFPIABK-UHFFFAOYSA-N diphenyl carbonate Chemical compound C=1C=CC=CC=1OC(=O)OC1=CC=CC=C1 ROORDVPLFPIABK-UHFFFAOYSA-N 0.000 description 2
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Chemical compound C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 2
- 238000004821 distillation Methods 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 230000032050 esterification Effects 0.000 description 2
- 238000005886 esterification reaction Methods 0.000 description 2
- 229910052736 halogen Inorganic materials 0.000 description 2
- 150000002367 halogens Chemical group 0.000 description 2
- XXMIOPMDWAUFGU-UHFFFAOYSA-N hexane-1,6-diol Chemical compound OCCCCCCO XXMIOPMDWAUFGU-UHFFFAOYSA-N 0.000 description 2
- 125000004464 hydroxyphenyl group Chemical group 0.000 description 2
- 238000011835 investigation Methods 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 2
- 239000011976 maleic acid Substances 0.000 description 2
- FZZQNEVOYIYFPF-UHFFFAOYSA-N naphthalene-1,6-diol Chemical compound OC1=CC=CC2=CC(O)=CC=C21 FZZQNEVOYIYFPF-UHFFFAOYSA-N 0.000 description 2
- 150000002978 peroxides Chemical class 0.000 description 2
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 2
- XNGIFLGASWRNHJ-UHFFFAOYSA-N phthalic acid Chemical compound OC(=O)C1=CC=CC=C1C(O)=O XNGIFLGASWRNHJ-UHFFFAOYSA-N 0.000 description 2
- 239000000049 pigment Substances 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- HJWLCRVIBGQPNF-UHFFFAOYSA-N prop-2-enylbenzene Chemical compound C=CCC1=CC=CC=C1 HJWLCRVIBGQPNF-UHFFFAOYSA-N 0.000 description 2
- 235000013772 propylene glycol Nutrition 0.000 description 2
- 150000003254 radicals Chemical class 0.000 description 2
- 239000012744 reinforcing agent Substances 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- CNHDIAIOKMXOLK-UHFFFAOYSA-N toluquinol Chemical compound CC1=CC(O)=CC=C1O CNHDIAIOKMXOLK-UHFFFAOYSA-N 0.000 description 2
- 229920002554 vinyl polymer Polymers 0.000 description 2
- ZGSHFDSKHTZINF-UHFFFAOYSA-N (2-methyl-6-phenylphenyl) hydrogen carbonate Chemical compound CC1=CC=CC(C=2C=CC=CC=2)=C1OC(O)=O ZGSHFDSKHTZINF-UHFFFAOYSA-N 0.000 description 1
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 1
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 description 1
- ZQHJVIHCDHJVII-OWOJBTEDSA-N (e)-2-chlorobut-2-enedioic acid Chemical compound OC(=O)\C=C(\Cl)C(O)=O ZQHJVIHCDHJVII-OWOJBTEDSA-N 0.000 description 1
- HCNHNBLSNVSJTJ-UHFFFAOYSA-N 1,1-Bis(4-hydroxyphenyl)ethane Chemical compound C=1C=C(O)C=CC=1C(C)C1=CC=C(O)C=C1 HCNHNBLSNVSJTJ-UHFFFAOYSA-N 0.000 description 1
- ROLAGNYPWIVYTG-UHFFFAOYSA-N 1,2-bis(4-methoxyphenyl)ethanamine;hydrochloride Chemical compound Cl.C1=CC(OC)=CC=C1CC(N)C1=CC=C(OC)C=C1 ROLAGNYPWIVYTG-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- 150000005208 1,4-dihydroxybenzenes Chemical group 0.000 description 1
- FRASJONUBLZVQX-UHFFFAOYSA-N 1,4-dioxonaphthalene Natural products C1=CC=C2C(=O)C=CC(=O)C2=C1 FRASJONUBLZVQX-UHFFFAOYSA-N 0.000 description 1
- BOKGTLAJQHTOKE-UHFFFAOYSA-N 1,5-dihydroxynaphthalene Chemical compound C1=CC=C2C(O)=CC=CC2=C1O BOKGTLAJQHTOKE-UHFFFAOYSA-N 0.000 description 1
- JFZVSHAMRZPOPA-UHFFFAOYSA-N 1-[n-(2-hydroxypropyl)-4-methylanilino]propan-2-ol Chemical compound CC(O)CN(CC(C)O)C1=CC=C(C)C=C1 JFZVSHAMRZPOPA-UHFFFAOYSA-N 0.000 description 1
- BQTPKSBXMONSJI-UHFFFAOYSA-N 1-cyclohexylpyrrole-2,5-dione Chemical compound O=C1C=CC(=O)N1C1CCCCC1 BQTPKSBXMONSJI-UHFFFAOYSA-N 0.000 description 1
- LGJCFVYMIJLQJO-UHFFFAOYSA-N 1-dodecylperoxydodecane Chemical compound CCCCCCCCCCCCOOCCCCCCCCCCCC LGJCFVYMIJLQJO-UHFFFAOYSA-N 0.000 description 1
- IGGDKDTUCAWDAN-UHFFFAOYSA-N 1-vinylnaphthalene Chemical compound C1=CC=C2C(C=C)=CC=CC2=C1 IGGDKDTUCAWDAN-UHFFFAOYSA-N 0.000 description 1
- YIYBRXKMQFDHSM-UHFFFAOYSA-N 2,2'-Dihydroxybenzophenone Chemical class OC1=CC=CC=C1C(=O)C1=CC=CC=C1O YIYBRXKMQFDHSM-UHFFFAOYSA-N 0.000 description 1
- RNFJDJUURJAICM-UHFFFAOYSA-N 2,2,4,4,6,6-hexaphenoxy-1,3,5-triaza-2$l^{5},4$l^{5},6$l^{5}-triphosphacyclohexa-1,3,5-triene Chemical compound N=1P(OC=2C=CC=CC=2)(OC=2C=CC=CC=2)=NP(OC=2C=CC=CC=2)(OC=2C=CC=CC=2)=NP=1(OC=1C=CC=CC=1)OC1=CC=CC=C1 RNFJDJUURJAICM-UHFFFAOYSA-N 0.000 description 1
- WMKGMCCZGTXXQU-UHFFFAOYSA-N 2,3-benzodioxine-1,4-dione Chemical compound C1=CC=C2C(=O)OOC(=O)C2=C1 WMKGMCCZGTXXQU-UHFFFAOYSA-N 0.000 description 1
- BJELTSYBAHKXRW-UHFFFAOYSA-N 2,4,6-triallyloxy-1,3,5-triazine Chemical compound C=CCOC1=NC(OCC=C)=NC(OCC=C)=N1 BJELTSYBAHKXRW-UHFFFAOYSA-N 0.000 description 1
- VXHYVVAUHMGCEX-UHFFFAOYSA-N 2-(2-hydroxyphenoxy)phenol Chemical compound OC1=CC=CC=C1OC1=CC=CC=C1O VXHYVVAUHMGCEX-UHFFFAOYSA-N 0.000 description 1
- BLDLRWQLBOJPEB-UHFFFAOYSA-N 2-(2-hydroxyphenyl)sulfanylphenol Chemical class OC1=CC=CC=C1SC1=CC=CC=C1O BLDLRWQLBOJPEB-UHFFFAOYSA-N 0.000 description 1
- XSVZEASGNTZBRQ-UHFFFAOYSA-N 2-(2-hydroxyphenyl)sulfinylphenol Chemical class OC1=CC=CC=C1S(=O)C1=CC=CC=C1O XSVZEASGNTZBRQ-UHFFFAOYSA-N 0.000 description 1
- QUWAJPZDCZDTJS-UHFFFAOYSA-N 2-(2-hydroxyphenyl)sulfonylphenol Chemical class OC1=CC=CC=C1S(=O)(=O)C1=CC=CC=C1O QUWAJPZDCZDTJS-UHFFFAOYSA-N 0.000 description 1
- JAHNSTQSQJOJLO-UHFFFAOYSA-N 2-(3-fluorophenyl)-1h-imidazole Chemical compound FC1=CC=CC(C=2NC=CN=2)=C1 JAHNSTQSQJOJLO-UHFFFAOYSA-N 0.000 description 1
- KYGLCUAXJICESS-UHFFFAOYSA-N 2-[2,3-di(propan-2-yl)phenyl]phenol Chemical class CC(C)C1=CC=CC(C=2C(=CC=CC=2)O)=C1C(C)C KYGLCUAXJICESS-UHFFFAOYSA-N 0.000 description 1
- DNUYOWCKBJFOGS-UHFFFAOYSA-N 2-[[10-(2,2-dicarboxyethyl)anthracen-9-yl]methyl]propanedioic acid Chemical compound C1=CC=C2C(CC(C(=O)O)C(O)=O)=C(C=CC=C3)C3=C(CC(C(O)=O)C(O)=O)C2=C1 DNUYOWCKBJFOGS-UHFFFAOYSA-N 0.000 description 1
- WIPYZRZPNMUSER-UHFFFAOYSA-N 2-chloro-4-hydroxybenzoic acid Chemical compound OC(=O)C1=CC=C(O)C=C1Cl WIPYZRZPNMUSER-UHFFFAOYSA-N 0.000 description 1
- SBYMUDUGTIKLCR-UHFFFAOYSA-N 2-chloroethenylbenzene Chemical class ClC=CC1=CC=CC=C1 SBYMUDUGTIKLCR-UHFFFAOYSA-N 0.000 description 1
- DTQQMULENZFWGF-UHFFFAOYSA-N 2-ethyl-4-hydroxybenzoic acid Chemical compound CCC1=CC(O)=CC=C1C(O)=O DTQQMULENZFWGF-UHFFFAOYSA-N 0.000 description 1
- UPHOPMSGKZNELG-UHFFFAOYSA-N 2-hydroxynaphthalene-1-carboxylic acid Chemical class C1=CC=C2C(C(=O)O)=C(O)C=CC2=C1 UPHOPMSGKZNELG-UHFFFAOYSA-N 0.000 description 1
- KGIGUEBEKRSTEW-UHFFFAOYSA-N 2-vinylpyridine Chemical compound C=CC1=CC=CC=N1 KGIGUEBEKRSTEW-UHFFFAOYSA-N 0.000 description 1
- DXIJHCSGLOHNES-UHFFFAOYSA-N 3,3-dimethylbut-1-enylbenzene Chemical compound CC(C)(C)C=CC1=CC=CC=C1 DXIJHCSGLOHNES-UHFFFAOYSA-N 0.000 description 1
- XIRDTMSOGDWMOX-UHFFFAOYSA-N 3,4,5,6-tetrabromophthalic acid Chemical compound OC(=O)C1=C(Br)C(Br)=C(Br)C(Br)=C1C(O)=O XIRDTMSOGDWMOX-UHFFFAOYSA-N 0.000 description 1
- WZHHYIOUKQNLQM-UHFFFAOYSA-N 3,4,5,6-tetrachlorophthalic acid Chemical compound OC(=O)C1=C(Cl)C(Cl)=C(Cl)C(Cl)=C1C(O)=O WZHHYIOUKQNLQM-UHFFFAOYSA-N 0.000 description 1
- MKTOIPPVFPJEQO-UHFFFAOYSA-N 4-(3-carboxypropanoylperoxy)-4-oxobutanoic acid Chemical compound OC(=O)CCC(=O)OOC(=O)CCC(O)=O MKTOIPPVFPJEQO-UHFFFAOYSA-N 0.000 description 1
- WVDRSXGPQWNUBN-UHFFFAOYSA-N 4-(4-carboxyphenoxy)benzoic acid Chemical compound C1=CC(C(=O)O)=CC=C1OC1=CC=C(C(O)=O)C=C1 WVDRSXGPQWNUBN-UHFFFAOYSA-N 0.000 description 1
- VAXBLYWAVAIJJJ-UHFFFAOYSA-N 4-[2-(4-carboxyphenoxy)ethoxy]benzoic acid Chemical compound C1=CC(C(=O)O)=CC=C1OCCOC1=CC=C(C(O)=O)C=C1 VAXBLYWAVAIJJJ-UHFFFAOYSA-N 0.000 description 1
- CDBAMNGURPMUTG-UHFFFAOYSA-N 4-[2-(4-hydroxycyclohexyl)propan-2-yl]cyclohexan-1-ol Chemical compound C1CC(O)CCC1C(C)(C)C1CCC(O)CC1 CDBAMNGURPMUTG-UHFFFAOYSA-N 0.000 description 1
- BBMFSGOFUHEVNP-UHFFFAOYSA-N 4-hydroxy-2-methylbenzoic acid Chemical compound CC1=CC(O)=CC=C1C(O)=O BBMFSGOFUHEVNP-UHFFFAOYSA-N 0.000 description 1
- IPXDGHZTUBSPSG-UHFFFAOYSA-N 4-hydroxy-2-phenylbenzoic acid Chemical compound OC(=O)C1=CC=C(O)C=C1C1=CC=CC=C1 IPXDGHZTUBSPSG-UHFFFAOYSA-N 0.000 description 1
- LPADJMFUBXMZNL-UHFFFAOYSA-N 4-hydroxy-3-phenylbenzoic acid Chemical compound OC(=O)C1=CC=C(O)C(C=2C=CC=CC=2)=C1 LPADJMFUBXMZNL-UHFFFAOYSA-N 0.000 description 1
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 1
- 229910002012 Aerosil® Inorganic materials 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- 229930185605 Bisphenol Natural products 0.000 description 1
- SDDLEVPIDBLVHC-UHFFFAOYSA-N Bisphenol Z Chemical compound C1=CC(O)=CC=C1C1(C=2C=CC(O)=CC=2)CCCCC1 SDDLEVPIDBLVHC-UHFFFAOYSA-N 0.000 description 1
- 125000000041 C6-C10 aryl group Chemical group 0.000 description 1
- 239000004641 Diallyl-phthalate Substances 0.000 description 1
- 238000005698 Diels-Alder reaction Methods 0.000 description 1
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 description 1
- GZDFHIJNHHMENY-UHFFFAOYSA-N Dimethyl dicarbonate Chemical compound COC(=O)OC(=O)OC GZDFHIJNHHMENY-UHFFFAOYSA-N 0.000 description 1
- 239000005264 High molar mass liquid crystal Substances 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- 239000004977 Liquid-crystal polymers (LCPs) Substances 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 1
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- YGYAWVDWMABLBF-UHFFFAOYSA-N Phosgene Chemical compound ClC(Cl)=O YGYAWVDWMABLBF-UHFFFAOYSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- UCKMPCXJQFINFW-UHFFFAOYSA-N Sulphide Chemical compound [S-2] UCKMPCXJQFINFW-UHFFFAOYSA-N 0.000 description 1
- ZJCCRDAZUWHFQH-UHFFFAOYSA-N Trimethylolpropane Chemical compound CCC(CO)(CO)CO ZJCCRDAZUWHFQH-UHFFFAOYSA-N 0.000 description 1
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical compound CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 description 1
- 239000001089 [(2R)-oxolan-2-yl]methanol Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 150000001335 aliphatic alkanes Chemical class 0.000 description 1
- 125000002877 alkyl aryl group Chemical group 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- XYLMUPLGERFSHI-UHFFFAOYSA-N alpha-Methylstyrene Chemical compound CC(=C)C1=CC=CC=C1 XYLMUPLGERFSHI-UHFFFAOYSA-N 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- DMLAVOWQYNRWNQ-UHFFFAOYSA-N azobenzene Chemical compound C1=CC=CC=C1N=NC1=CC=CC=C1 DMLAVOWQYNRWNQ-UHFFFAOYSA-N 0.000 description 1
- TZCXTZWJZNENPQ-UHFFFAOYSA-L barium sulfate Chemical compound [Ba+2].[O-]S([O-])(=O)=O TZCXTZWJZNENPQ-UHFFFAOYSA-L 0.000 description 1
- 239000010428 baryte Substances 0.000 description 1
- 229910052601 baryte Inorganic materials 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- 125000006267 biphenyl group Chemical group 0.000 description 1
- ZPOLOEWJWXZUSP-AATRIKPKSA-N bis(prop-2-enyl) (e)-but-2-enedioate Chemical compound C=CCOC(=O)\C=C\C(=O)OCC=C ZPOLOEWJWXZUSP-AATRIKPKSA-N 0.000 description 1
- QUDWYFHPNIMBFC-UHFFFAOYSA-N bis(prop-2-enyl) benzene-1,2-dicarboxylate Chemical compound C=CCOC(=O)C1=CC=CC=C1C(=O)OCC=C QUDWYFHPNIMBFC-UHFFFAOYSA-N 0.000 description 1
- 238000005282 brightening Methods 0.000 description 1
- CQEYYJKEWSMYFG-UHFFFAOYSA-N butyl acrylate Chemical compound CCCCOC(=O)C=C CQEYYJKEWSMYFG-UHFFFAOYSA-N 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000012320 chlorinating reagent Substances 0.000 description 1
- 150000001805 chlorine compounds Chemical class 0.000 description 1
- FZFAMSAMCHXGEF-UHFFFAOYSA-N chloro formate Chemical compound ClOC=O FZFAMSAMCHXGEF-UHFFFAOYSA-N 0.000 description 1
- HNEGQIOMVPPMNR-IHWYPQMZSA-N citraconic acid Chemical compound OC(=O)C(/C)=C\C(O)=O HNEGQIOMVPPMNR-IHWYPQMZSA-N 0.000 description 1
- 229940018557 citraconic acid Drugs 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 238000007906 compression Methods 0.000 description 1
- 230000006835 compression Effects 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 239000004035 construction material Substances 0.000 description 1
- 150000001924 cycloalkanes Chemical class 0.000 description 1
- 125000002993 cycloalkylene group Chemical group 0.000 description 1
- IFDVQVHZEKPUSC-UHFFFAOYSA-N cyclohex-3-ene-1,2-dicarboxylic acid Chemical compound OC(=O)C1CCC=CC1C(O)=O IFDVQVHZEKPUSC-UHFFFAOYSA-N 0.000 description 1
- HPXRVTGHNJAIIH-UHFFFAOYSA-N cyclohexanol Chemical compound OC1CCCCC1 HPXRVTGHNJAIIH-UHFFFAOYSA-N 0.000 description 1
- BSVQJWUUZCXSOL-UHFFFAOYSA-N cyclohexylsulfonyl ethaneperoxoate Chemical compound CC(=O)OOS(=O)(=O)C1CCCCC1 BSVQJWUUZCXSOL-UHFFFAOYSA-N 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 239000012933 diacyl peroxide Substances 0.000 description 1
- 150000001470 diamides Chemical class 0.000 description 1
- MHDVGSVTJDSBDK-UHFFFAOYSA-N dibenzyl ether Chemical class C=1C=CC=CC=1COCC1=CC=CC=C1 MHDVGSVTJDSBDK-UHFFFAOYSA-N 0.000 description 1
- 150000001990 dicarboxylic acid derivatives Chemical class 0.000 description 1
- 150000001991 dicarboxylic acids Chemical class 0.000 description 1
- 150000001993 dienes Chemical class 0.000 description 1
- 150000005690 diesters Chemical class 0.000 description 1
- FFYPMLJYZAEMQB-UHFFFAOYSA-N diethyl pyrocarbonate Chemical compound CCOC(=O)OC(=O)OCC FFYPMLJYZAEMQB-UHFFFAOYSA-N 0.000 description 1
- 150000004341 dihydroxyanthraquinones Chemical class 0.000 description 1
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 description 1
- 239000004316 dimethyl dicarbonate Substances 0.000 description 1
- 235000010300 dimethyl dicarbonate Nutrition 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- UIWXSTHGICQLQT-UHFFFAOYSA-N ethenyl propanoate Chemical compound CCC(=O)OC=C UIWXSTHGICQLQT-UHFFFAOYSA-N 0.000 description 1
- LDLDYFCCDKENPD-UHFFFAOYSA-N ethenylcyclohexane Chemical compound C=CC1CCCCC1 LDLDYFCCDKENPD-UHFFFAOYSA-N 0.000 description 1
- 125000002573 ethenylidene group Chemical class [*]=C=C([H])[H] 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 239000003063 flame retardant Substances 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 239000003365 glass fiber Substances 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- NWVVVBRKAWDGAB-UHFFFAOYSA-N hydroquinone methyl ether Natural products COC1=CC=C(O)C=C1 NWVVVBRKAWDGAB-UHFFFAOYSA-N 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 239000003999 initiator Substances 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- HNEGQIOMVPPMNR-NSCUHMNNSA-N mesaconic acid Chemical compound OC(=O)C(/C)=C/C(O)=O HNEGQIOMVPPMNR-NSCUHMNNSA-N 0.000 description 1
- IJFXRHURBJZNAO-UHFFFAOYSA-N meta--hydroxybenzoic acid Natural products OC(=O)C1=CC=CC(O)=C1 IJFXRHURBJZNAO-UHFFFAOYSA-N 0.000 description 1
- LVHBHZANLOWSRM-UHFFFAOYSA-N methylenebutanedioic acid Natural products OC(=O)CC(=C)C(O)=O LVHBHZANLOWSRM-UHFFFAOYSA-N 0.000 description 1
- HNEGQIOMVPPMNR-UHFFFAOYSA-N methylfumaric acid Natural products OC(=O)C(C)=CC(O)=O HNEGQIOMVPPMNR-UHFFFAOYSA-N 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- SEEYREPSKCQBBF-UHFFFAOYSA-N n-methylmaleimide Chemical compound CN1C(=O)C=CC1=O SEEYREPSKCQBBF-UHFFFAOYSA-N 0.000 description 1
- KYTZHLUVELPASH-UHFFFAOYSA-N naphthalene-1,2-dicarboxylic acid Chemical compound C1=CC=CC2=C(C(O)=O)C(C(=O)O)=CC=C21 KYTZHLUVELPASH-UHFFFAOYSA-N 0.000 description 1
- ABMFBCRYHDZLRD-UHFFFAOYSA-N naphthalene-1,4-dicarboxylic acid Chemical compound C1=CC=C2C(C(=O)O)=CC=C(C(O)=O)C2=C1 ABMFBCRYHDZLRD-UHFFFAOYSA-N 0.000 description 1
- PCILLCXFKWDRMK-UHFFFAOYSA-N naphthalene-1,4-diol Chemical compound C1=CC=C2C(O)=CC=C(O)C2=C1 PCILLCXFKWDRMK-UHFFFAOYSA-N 0.000 description 1
- RXOHFPCZGPKIRD-UHFFFAOYSA-N naphthalene-2,6-dicarboxylic acid Chemical compound C1=C(C(O)=O)C=CC2=CC(C(=O)O)=CC=C21 RXOHFPCZGPKIRD-UHFFFAOYSA-N 0.000 description 1
- MNZMMCVIXORAQL-UHFFFAOYSA-N naphthalene-2,6-diol Chemical compound C1=C(O)C=CC2=CC(O)=CC=C21 MNZMMCVIXORAQL-UHFFFAOYSA-N 0.000 description 1
- DFQICHCWIIJABH-UHFFFAOYSA-N naphthalene-2,7-diol Chemical compound C1=CC(O)=CC2=CC(O)=CC=C21 DFQICHCWIIJABH-UHFFFAOYSA-N 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- SLCVBVWXLSEKPL-UHFFFAOYSA-N neopentyl glycol Chemical compound OCC(C)(C)CO SLCVBVWXLSEKPL-UHFFFAOYSA-N 0.000 description 1
- 150000002825 nitriles Chemical class 0.000 description 1
- HVAMZGADVCBITI-UHFFFAOYSA-M pent-4-enoate Chemical compound [O-]C(=O)CCC=C HVAMZGADVCBITI-UHFFFAOYSA-M 0.000 description 1
- WXZMFSXDPGVJKK-UHFFFAOYSA-N pentaerythritol Chemical compound OCC(CO)(CO)CO WXZMFSXDPGVJKK-UHFFFAOYSA-N 0.000 description 1
- 150000002989 phenols Chemical class 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N phenylbenzene Natural products C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 1
- 229930015698 phenylpropene Natural products 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 229920003055 poly(ester-imide) Chemical class 0.000 description 1
- 229920000343 polyazomethine Polymers 0.000 description 1
- 229920000515 polycarbonate Polymers 0.000 description 1
- 239000004417 polycarbonate Substances 0.000 description 1
- 229920006149 polyester-amide block copolymer Chemical class 0.000 description 1
- 239000003505 polymerization initiator Substances 0.000 description 1
- 229920006295 polythiol Chemical class 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- BWJUFXUULUEGMA-UHFFFAOYSA-N propan-2-yl propan-2-yloxycarbonyloxy carbonate Chemical compound CC(C)OC(=O)OOC(=O)OC(C)C BWJUFXUULUEGMA-UHFFFAOYSA-N 0.000 description 1
- 239000001294 propane Substances 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 238000000235 small-angle X-ray scattering Methods 0.000 description 1
- MWNQXXOSWHCCOZ-UHFFFAOYSA-L sodium;oxido carbonate Chemical compound [Na+].[O-]OC([O-])=O MWNQXXOSWHCCOZ-UHFFFAOYSA-L 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 150000003440 styrenes Chemical class 0.000 description 1
- 125000003011 styrenyl group Chemical group [H]\C(*)=C(/[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 150000003900 succinic acid esters Chemical class 0.000 description 1
- 150000005846 sugar alcohols Polymers 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- BSYVTEYKTMYBMK-UHFFFAOYSA-N tetrahydrofurfuryl alcohol Chemical compound OCC1CCCO1 BSYVTEYKTMYBMK-UHFFFAOYSA-N 0.000 description 1
- UFDHBDMSHIXOKF-UHFFFAOYSA-N tetrahydrophthalic acid Natural products OC(=O)C1=C(C(O)=O)CCCC1 UFDHBDMSHIXOKF-UHFFFAOYSA-N 0.000 description 1
- 239000013008 thixotropic agent Substances 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- XHGIFBQQEGRTPB-UHFFFAOYSA-N tris(prop-2-enyl) phosphate Chemical compound C=CCOP(=O)(OCC=C)OCC=C XHGIFBQQEGRTPB-UHFFFAOYSA-N 0.000 description 1
- 238000000214 vapour pressure osmometry Methods 0.000 description 1
- KOZCZZVUFDCZGG-UHFFFAOYSA-N vinyl benzoate Chemical compound C=COC(=O)C1=CC=CC=C1 KOZCZZVUFDCZGG-UHFFFAOYSA-N 0.000 description 1
- 229920001567 vinyl ester resin Polymers 0.000 description 1
- DJWUNCQRNNEAKC-UHFFFAOYSA-L zinc acetate Chemical compound [Zn+2].CC([O-])=O.CC([O-])=O DJWUNCQRNNEAKC-UHFFFAOYSA-L 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L67/00—Compositions of polyesters obtained by reactions forming a carboxylic ester link in the main chain; Compositions of derivatives of such polymers
- C08L67/06—Unsaturated polyesters
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L67/00—Compositions of polyesters obtained by reactions forming a carboxylic ester link in the main chain; Compositions of derivatives of such polymers
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L69/00—Compositions of polycarbonates; Compositions of derivatives of polycarbonates
- C08L69/005—Polyester-carbonates
Definitions
- the invention relates to mixtures of unsaturated polyester resins and thermotropic polymers, a process for their preparation and their use for the production of moldings.
- the mixtures according to the invention are outstandingly suitable as casting resins and as a resin component of molding compounds and leveling compounds.
- Unsaturated polyester resins ie mixtures of ⁇ , ⁇ -ethylenically unsaturated polyester resins and thus copolymerizable monomers, are widely used as a valuable resin base for construction materials (molding compounds) and coatings (coating agents).
- the most common copolymerizable monomer in practice is styrene. Although it is built into the polymer network during the curing process, there is a risk before the curing process that it will escape into the atmosphere due to its high vapor pressure and be harmful because of its toxicity. A reduction in the content of copolymerizable monomers would therefore be desirable.
- thermotropic polymer makes it possible to manage with a considerably smaller amount of copolymerizable monomer.
- Preferred ⁇ , ⁇ -unsaturated polyesters A are the usual polycondensation products of at least one ⁇ , ⁇ -ethylenically unsaturated dicarboxylic acid with generally 4 or 5 C atoms or their ester-forming derivatives, for example their anhydrides, optionally in a mixture with up to 200 mol%, based on the unsaturated acid components, of at least one aliphatic dicarboxylic acid with 4 to 10 C atoms or a saturated or unsaturated cycloaliphatic, araliphatic or aromatic dicarboxylic acid with 8 to 10 C atoms or their ester-forming derivatives with at least one polyhydroxy compound, in particular dihydroxy compound with 2 to 8 C atoms - that is, polyester, as described in J. Björksten et al., "Polyesters and their Applications", Reinhold Publishing Corp., New York 1956 .
- Examples of preferred unsaturated dicarboxylic acids or their derivatives are maleic acid or maleic anhydride and fumaric acid.
- mesaconic acid, citraconic acid, itaconic acid or chloromaleic acid can also be used, for example.
- Examples of the aliphatic, saturated or unsaturated cycloaliphatic, araliphatic or aromatic dicarboxylic acids to be used, or of their derivatives, are phthalic acid and phthalic anhydride, isophthalic acid, terephthalic acid, hexa- and tetrahydrophthalic acid or their anhydrides, endomethylenedetane anhydride and their anhydrides, bernearic acid and tetrahydrofluoric anhydride and bernearic acid, respectively and succinic acid esters and chlorides, adipic acid, sebacic acid.
- flame-retardant resins e.g. B.
- hexachlorodomethylene-tetrahydrophthalic acid, tetrachlorophthalic acid or tetrabromophthalic acid can be used.
- Ethylene glycol, 1,2-propanediol, propane can be used as dihydric alcohols diol-1,3, diethylene glycol, dipropylene glycol, 1,3-butanediol, 1,4-butanediol, neopentyl glycol, 1,6-hexanediol, 2,2-bis (4-hydroxycyclohexyl) propany, bis-oxyalkylated bisphenol A, Perhydrobisphenol and others are used.
- Ethylene glycol, 1,2-propanediol, diethylene glycol and dipropylene glycol are preferably used.
- mono-, tri- or tetravalent alcohols with 1 to 6 carbon atoms such as methanol, ethanol, butanol, allyl alcohol, benzyl alcohol, cyclohexanol and tetrahydrofurfuryl alcohol, trimethylolpropane, glycerol and pentaerythritol, of mono-, di- and triallyl ethers and benzyl ethers of trihydric and polyhydric alcohols with 3 to 6 carbon atoms according to DE-AS 1 024 654, for example Trimethylolpropane diallyl ether, and by incorporating monobasic acids such as benzoic acid or acrylic acid.
- monobasic acids such as benzoic acid or acrylic acid.
- the unsaturated polyesters A can also be reaction products of polyester precondensates and dienes, e.g. Dicyclopentadiene, according to Diels-Alder.
- polyester precondensates and dienes e.g. Dicyclopentadiene
- Diels-Alder e.g. Diels-Alder.
- Such polyesters are e.g. at I.R. Lawrence “Polyester Resins", Reinhold Publ. Corp., New York 1960, pp. 18 f. and in the plastic handbook vol. VIII ("polyester”), Carl Hanser Verlag, Kunststoff 1973, pp. 247-312.
- the acid numbers of the polyester A are usually between 10 and 100, preferably between 20 and 70, the OH numbers between 10 and 150, preferably between 20 and 100, and the number average molecular weights n between approx. 500 and 5000, preferably between approx. 1000 and 3000 (measured by vapor pressure osmometry in dioxane and acetone; if the values differ, the lower one is considered the correct one).
- Unsaturated monomers B which are copolymerizable with the unsaturated polyesters A and are suitable in polyester technology are unsaturated compounds which preferably carry ⁇ -substituted vinyl or vinylidene groups or ⁇ -substituted allyl groups, preferably styrene; but also, for example, nuclear chlorinated and alkylated or alkenylated styrenes, where the alkyl groups contain 1 to 4 carbon atoms, for example vinyltoluene, divinylbenzene, ⁇ -methylstyrene, tert-butylstyrene, chlorostyrenes; Vinyl esters of carboxylic acids with 2 to 6 carbon atoms, preferably vinyl acetate, vinyl propionate, vinyl benzoate, vinyl pyridine, vinyl naphthalene, vinyl cyclohexane, acrylic acid and methacrylic acid and / or their esters (preferably vinyl, allyl and methallyl esters) with 1 to 4
- thermotropic Substances which form liquid-crystalline melts are termed "thermotropic".
- Thermotropic polymers are well known, cf. e.g. FE Mc Farlane et al., Liquid Crystal Polymers II, Contemporary Topics in Polymer Science, Vol. 2, Plenum Publishing Corporation, 1977; WJ Jackson and HF Kuhfuss, J. Polymer Science Polymer Chem. Ed. 14: 2042 (1976); WC Wooten et al. in A. Ciferri "Ultra-high Modulus Polymers", Applied Science Publ., London 1979, pp. 362 f .; A. Blumstein et al., "Liquid Crystalline Order in Polymers", Academic Press 1978; J. Preston, Angew.
- the liquid-crystalline state of polymer melts can be examined with the aid of a polarizing microscope:
- the eyepiece was equipped with an attachment which contained a photodiode arranged in the focal point of the eyepiece lens.
- the measured value was set to 100 divisions on a switched-on microscope with Nicol prisms arranged in parallel in the absence of a material sample. In the case of crossed Nichols prisms, this resulted in a value of 0.01 scale divisions.
- the layer thickness of the polymer melts examined was 100 ⁇ m.
- the polymers are examined after the samples have been melted at temperatures between 200 and 400 ° C. Provided that a brightening of the between the crossed in this entire area or in a part thereof Nicol's prisms observed melt, the polymer was classified as thermotropic liquid crystalline.
- liquid-crystalline polymers show values over 1 scale division, mostly values from 3 to 90 scale divisions in the measuring arrangement.
- amorphous melts e.g. aromatic polycarbonates, values of less than 0.1 scale were found.
- the method described above is particularly suitable for a quick determination in the laboratory and delivers unambiguous results in almost all cases. In cases of doubt, on the other hand, it can make sense to detect the presence of liquid-crystalline components in the melt using small-angle X-ray scattering, as is the case, for example, G.W. Gray and P.A. Windsor, "Plastic Crystals, Physico-Chemical Properties and Methods of Investigation", in particular Chapter 3, John Wiley & Sons, New York, Sydney, Toronto 1974.
- thermotropic polymers which are suitable in the form of fibers or powder for use in the mixtures according to the invention include thermotropic polyesters, polyester carbonates, polyester amides, polyester imides, polythiol esters, polyazomethines and thermotropic cellulose derivatives such as, for example, hydroxypropyl cellulose.
- Thermotropic polycondensates II can be produced, for example, from the following compounds: o-, m- or p-hydroxy-benzoic acid, Hydroquinone, hydroquinones substituted by halogen, C1 to C3 alkyl or phenyl, Hydroxy-naphthalene-carboxylic acids, Isophthalic acid, Terephthalic acid, Naphthalenedicarboxylic acid, 4,4 ⁇ -dihydroxydiphenyl, 4,4 ⁇ -dihydroxy stilbene, 1,2-bis (p-carboxy-phenoxy) ethane, 4,4 ⁇ -dihydroxyphenyl ether, 4,4'-diphenyl ether dicarboxylic acid, Resorcinol, 4,4 ⁇ -benzophenone dicarboxylic acid, 4,4 ⁇ -dihydroxy-diphenyl sulfide, 4,4 ⁇ -dihydroxy-diphenylsulfone, 2.5-furandicarboxylic acid, 4,4 ⁇ -bis (
- thermotropic polycondensates Not all combinations of the starting materials listed above result in thermotropic polycondensates. The person skilled in the art will make his selection on the basis of the literature cited above or, on the basis of his experience, proceed empirically. Since the thermotropic polycondensates II are known per se, a longer version at this point can be omitted.
- thermotropic polyester carbonates II can be up to 40 mol%, preferably 25 to 35 mol%, based on the sum of ester and carbonate groups.
- Preferred (a) p-hydroxybenzoic acids are p-hydroxybenzoic acids which are nucleus-substituted by C1-C4-alkyl, C1-C4-alkoxy, C6-C10-aryl or alkylaryl (such as phenyl, tolyl, naphthyl), halogen (preferably chlorine and bromine), such as 4-hydroxy-2-methylbenzoic acid, 4-hydroxy-3-methylbenzoic acid, 2-ethyl-4-hydroxybenzoic acid, 3-ethyl-4- hydroxybenzoic acid, 2- or 3-chloro-4-hydroxybenzoic acid, 4-hydroxy-2-phenylbenzoic acid or 4-hydroxy-3-phenylbenzoic acid, but preferably unsubstituted p-hydroxybenzoic acid itself.
- Preferred (b) diphenols are compounds of the formula HO - Z-OH (I) where Z is a divalent mononuclear or polynuclear aromatic radical having 6 to 30 carbon atoms, where Z is constructed such that the two OH groups are bonded directly to one carbon atom of an aromatic system, such as, for example (1) hydroquinone, methyl hydroquinone, ethyl hydroquinone, 1,4-dihydroxynaphthalene, 1,5-dihydroxynaphthalene, 2,6-dihydroxynaphthalene, which do not lead to any significant angulation of the polycondensate chain, and (2) Compounds which contribute to a substantial angulation of the polycondensate chain, such as resorcinol, 1,6-dihydroxynaphthalene, 2,5-dihydroxynaphthalene, 2,7-dihydroxynaphthalene and bisphenols of the formula in the Y is an alkylene or alkylidene radical with 1 to 7 C
- diphenol residues from group (2) it is advisable to select the diphenols such that a maximum of 30 mol%, based on the total amount of diphenol residues, are diphenol residues from group (2).
- a high proportion of diphenol residues of group (2) is particularly justifiable if it is replaced by additional linear residues, e.g. Terephthalic acid residues, "compensated".
- Preferred derivatives for incorporating the (c) carbonate groups are phosgene, diaryl carbonates, such as e.g. Diphenyl carbonate, ditolyl carbonate, phenyl-tolyl carbonate, dinaphthyl carbonate, dialkyl carbonate such as e.g. Diethyl carbonate, dimethyl carbonate, dimethyl dicarbonate, diethyl dicarbonate, gycol carbonate and chloroformate.
- diaryl carbonates such as e.g. Diphenyl carbonate, ditolyl carbonate, phenyl-tolyl carbonate, dinaphthyl carbonate, dialkyl carbonate such as e.g. Diethyl carbonate, dimethyl carbonate, dimethyl dicarbonate, diethyl dicarbonate, gycol carbonate and chloroformate.
- Preferred (d) aromatic dicarboxylic acids have 8 to 24, preferably 8 to 14, carbon atoms and can be substituted per aromatic ring by up to 4 C1-C4-alkyl radicals, C1-C4-alkoxy radicals or halogen atoms (preferably chlorine and bromine) , such as Naphthalene-1,4-dicarboxylic acid, diphenyl-2,2 ⁇ -dicarboxylic acid, diphenyl-4,4 ⁇ -dicarboxylic acid, diphenylmethane-4,4 ⁇ -dicarboxylic acid, diphenyl ether-4,4 ⁇ -dicarboxylic acid, diphenylsulfone-4,4 ⁇ -dicarboxylic acid, preferably terephthalic acid , isophthalic acid and naphthalene-2,6-dicarboxylic acid and their core-substituted derivatives.
- C1-C4-alkyl radicals preferably 8 to 14
- thermotropic polyesters or polyester carbonates II -H, -OH, -OC6H5 or residues originating from chain terminators can contain as end groups.
- thermotropic polyesters or polyester carbonates II can contain the radicals of the compounds (a) to (e) in statistical distribution or in blocks.
- thermotropic polyesters or polyester carbonates can be produced by various processes, e.g. by condensation of the carboxylic acid chlorides or by esterification of the carboxylic acid aryl esters with the phenolic compounds and subsequent polycondensation, the carboxylic acid chlorides also being able to be produced in situ from the corresponding carboxylic acids and chlorinating agents.
- esterification and subsequent polycondensation phenol is distilled off from the reaction mixture until the desired degree of condensation is reached.
- the mixtures according to the invention can also contain conventional additives, such as fillers, reinforcing agents, pigments, accelerators, brighteners, thixotropic agents and stabilizers, such as e.g. Hydroquinone or its derivatives can be added.
- conventional additives such as fillers, reinforcing agents, pigments, accelerators, brighteners, thixotropic agents and stabilizers, such as e.g. Hydroquinone or its derivatives can be added.
- fillers and / or reinforcing agents such as chalk, talc, barite, aerosil, glass fibers
- Dyes or pigments can of course also be added.
- the various components of the mixtures according to the invention are advantageously mixed in kneaders, dissolvers or on roller mills.
- polymerization initiators preferably diacyl peroxides or percarbonates
- diacyl peroxides or percarbonates can be added to the mixtures according to the invention in amounts of 1 to 10% by weight, based on polyester resin A + B.
- Preferred initiators are e.g. Peroxides and percarbonates such as diacetyl peroxide, dibenzoyl peroxide, di-p-chlorobenzoyl peroxide, phthaloyl peroxide, succinyl peroxide, dilauryl peroxide, acetylcyclohexanesulfonyl peroxide, isopropyl percarbonate, cyclohexyl percarbonate and bis (4-tert-butylcyclohexyl) percarbonate.
- Peroxides and percarbonates such as diacetyl peroxide, dibenzoyl peroxide, di-p-chlorobenzoyl peroxide, phthaloyl peroxide
- the mixtures according to the invention or the compositions prepared therefrom can be cured at temperatures from -15 ° C. to + 120 ° C., preferably from 0 ° C. to 90 ° C. or - if they are pre-accelerated - at room temperature.
- Compression and casting compounds produced from the mixtures according to the invention are particularly suitable for the production of moldings and leveling compounds which can be used in the most diverse areas of the construction industry, the electrical industry, boat building, medical technology and the motor vehicle industry.
- an unsaturated polyester is obtained in the usual melt condensation with addition of 1545 g of dicyclopentadiene, which has the following characteristics after mixing with styrene: Fixed salary: 62% Acid number: 12 mg KOH / g Viscosity: 500 mPa.s
- an unsaturated seed is obtained by conventional melt condensation polyester, which, when mixed with styrene, has the following characteristics: Fixed salary: 75% Acid number: 19 mg KOH / g Viscosity: 1600 mPa.s
- thermotropic polyester Production of the thermotropic polyester:
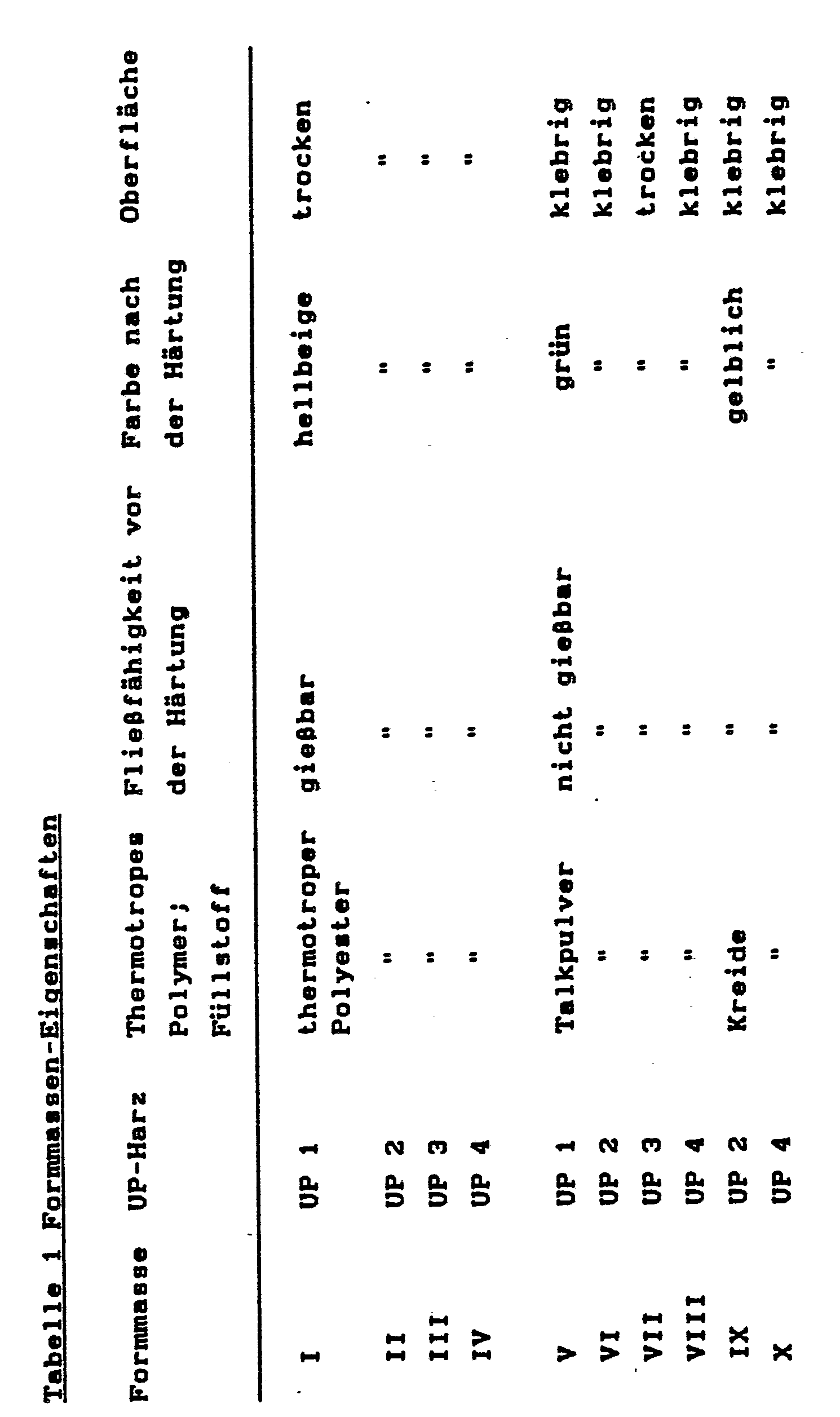
- Molding compositions were prepared from 50 g of unsaturated polyester resin, 1 g of amine accelerator from dipropoxy-p-toluidine and adipic acid, 1.15 g of benzoyl peroxide paste (50%) and 63.5 g of thermotropic polyester or filler, the properties of which are summarized in Table 1 .
- the properties of the molding compositions according to the invention differ significantly from those of the comparative tests.
- Molding compositions IX and X cure spontaneously after the addition of benzoyl peroxide, so that the pourability cannot be assessed. Both molding compounds are still pourable before the peroxide is added.
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Macromonomer-Based Addition Polymer (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Polyesters Or Polycarbonates (AREA)
Abstract
Description
- Die Erfindung betrifft Mischungen aus ungesättigten Polyesterharzen und thermotropen Polymeren, ein Verfahren zu ihrer Herstellung und ihre Verwendung zur Herstellung von Formkörpern. Die erfindungsgemäßen Mischungen eignen sich hervorragend als Gießharze und als Harzkomponente von Preßmassen und Spachtelmassen.
- Ungesättigte Polyesterharze, d.h. Mischungen α, β-ethylenisch ungesättigter Polyesterharze und damit copolymerisierbarer Monomerer, sind als wertvolle Harzgrundlage von Konstruktionswerkstoffen (Formmassen) und Beschichtungen (Überzugsmittel) weit verbreitet. Das in der Praxis gebräuchlichste copolymerisierbare Monomer ist Styrol. Zwar wird es bei der Härtung in das polymere Netzwerk eingebaut, aber vor der Härtung besteht die Gefahr, daß es aufgrund seines hohen Dampfdrucks in die Atmosphäre gelangt und wegen seiner Toxizität schadet. Eine Reduzierung des Gehalts copolymerisierbarer Monomerer wäre deshalb wünschenswert.
- Überraschenderweise wurde gefunden, daß es bei gegebener Viskosität des ungesättigten Polyesters durch Zusatz von thermotropem Polymer gelingt, mit einer beträchtlich geringeren Menge an copolymerisierbarem Monomer auszukommen.
- Gegenstand der Erfindung sind also Mischungen aus
- I) 10 bis 90, vorzugsweise 30 bis 70 Gew.-% ungesättigtem Polyesterharz und
- II) 90 bis 10, vorzugsweise 70 bis 30 Gew.-% thermotropem Polymer,
- Ungesättigte Polyesterharze I) im Sinne der Erfindung bestehen aus
- A) 30 bis 95, vorzugsweise 50 bis 90, Gew.-Teilen ungesättigtem Polyester und
- B) 70 bis 5, vorzugsweise 40 bis 10, Gew.-Teilen mit A) copolymerisierbarem Monomer.
- Bevorzugte α,β-ungesättigte Polyester A sind die üblichen Polykondensationsprodukte mindestens einer α,β-ethylenisch ungesättigten Dicarbonsäure mit in der Regel 4 oder 5 C-Atomen oder deren esterbildenden Derivate, z.B. ihren Anhydriden, gegebenenfalls in Abmischung mit bis zu 200 Mol-%, bezogen auf die ungesättigten Säurekomponenten, mindestens einer aliphatischen Dicarbonsäure mit 4 bis 10 C-Atomen oder einer gesättigten oder ungesättigten cycloaliphatischen, araliphatischen oder aromatischen Dicarbonsäure mit 8 bis 10 C-Atomen oder deren esterbildenden Derivate mit mindestens einer Polyhydroxyverbindung, insbesondere Dihydroxyverbindung mit 2 bis 8 C-Atomen - also Polyester, wie sie bei J. Björksten et al., "Polyesters and their Applications", Reinhold Publishing Corp., New York 1956, beschrieben sind.
- Beispiele für bevorzugt zu verwendende ungesättigte Dicarbonsäuren oder ihre Derivate sind Maleinsäure oder Maleinsäureanhydrid und Fumarsäure. Verwendet werden können z.B. jedoch auch Mesaconsäure, Citraconsäure, Itaconsäure oder Chlormaleinsäure. Beispiele für die gegebenenfalls zu verwendenden aliphatischen, gesättigten oder ungesättigten cyclo-aliphatischen, araliphatischen oder aromatischen Dicarbonsäuren oder für ihre Derivate sind Phthalsäure und Phthalsäureanhydrid, Isophthalsäure, Terephthalsäure, Hexa- und Tetrahydrophthalsäure bzw. deren Anhydride, Endomethylentetrahydrophthalsäuren und deren Anhydrid, Bernsteinsäure bzw. Bernsteinsäureanhydrid und Bernsteinsäureester und -chloride, Adipinsäure, Sebacinsäure. Um schwerentflammbare Harze herzustellen, können z. B. Hexachlorendomethylen-tetrahydrophthalsäure, Tetrachlorphthalsäure oder Tetrabromphthalsäure verwendet werden. Als zweiwertige Alkohole können Ethylenglykol, Propandiol-1,2, Propan diol-1,3, Diethylenglykol, Dipropylenglykol, Butandiol-1,3, Butandiol-1,4, Neopentylglykol, Hexandiol-1,6, 2,2-Bis-(4-hydroxycyclohexyl)-propany, bis-oxalkyliertes Bisphenol A, Perhydrobisphenol und andere eingesetzt werden. Bevorzugt verwendet werden Ethylenglykol, Propandiol-1,2, Diethylenglykol und Dipropylenglykol.
- Weitere Modifikationen sind möglich durch Einsatz ein-, drei- oder vierwertiger Alkohole mit 1 bis 6 C-Atomen wie Methanol, Ethanol, Butanol, Allylalkohol, Benzylalkohol, Cyclohexanol und Tetrahydrofurfurylalkohol, Trimethylolpropan, Glycerin und Pentaerythrit, von Mono-, Di- und Triallylethern und Benzylethern drei- und mehrwertiger Alkohole mit 3 bis 6 C-Atomen gemäß DE-AS 1 024 654, z.B. Trimethylolpropandiallylether, sowie durch Einbau einbasischer Säuren wie Benzoesäure oder Acrylsäure.
- Die ungesättigten Polyester A können auch Umsetzungsprodukte von Polyesterpräkondensaten und Dienen, z.B. Dicyclopentadien, nach Diels-Alder sein. Solche Polyester sind z.B. bei I.R. Lawrence "Polyester Resins", Reinhold Publ. Corp., New York 1960, S. 18 f. und im Kunststoff-Handbuch Bd. VIII ("Polyester"), Carl Hanser Verlag, München 1973, S. 247-312, beschrieben.
- Die Säurezahlen der Polyester A liegen gewöhnlich zwischen 10 und 100, vorzugsweise zwischen 20 und 70, die OH-Zahlen zwischen 10 und 150, vorzugsweise zwischen 20 und 100, und die als Zahlenmittel bestimmten Molekulargewichte n zwischen ca. 500 und 5000, vorzugsweise zwischen ca. 1000 und 3000 (dampfdruckosmometrisch gemessen in Dioxan und Aceton; bei differierenden Werten wird der niedrigere als der korrekte angesehen).
- Als mit den ungesättigten Polyestern A copolymerisierbare ungesättigte Monomere B eignen sich in der Polyestertechnologie gebräuchliche ungesättigte Verbindungen, die bevorzugt α-substituierte Vinyl- oder Vinylidengruppen oder β-substituierte Allylgruppen tragen, bevorzugt Styrol; aber auch beispielsweise kernchlorierte und -alkylierte bzw. -alkenylierte Styrole, wobei die Alkylgruppen 1 bis 4 Kohlenstoffatome enthlaten, können, z.B. Vinyltoluol, Divinylbenzol, α-Methylstyrol, tert.-Butylstyrol, Chlorstyrole; Vinylester von Carbonsäuren mit 2 bis 6 Kohlenstoffatomen, bevorzugt Vinylacetat, Vinylpropionat, Vinylbenzoat, Vinylpyridin, Vinylnaphthalin, Vinylcyclohexan, Acrylsäure und Methacrylsäure und/oder ihre Ester (vorzugsweise Vinyl-, Allyl- und Methallylester) mit 1 bis 4 Kohlenstoffatomen in der Alkoholkomponente, ihre Amide und Nitrile, Maleinsäureanhydrid, -halb- und -diester mit 1 bis 4 Kohlenstoffatomen in der Alkoholkomponente, -halb- und -diamide oder cyclische Imide wie Butylacrylat, Methylmethacrylat, Acrylnitril, N-Methylmaleinimid oder N-Cyclohexylmaleinimid; Allyverbindungen wie Allylbenzol und Allylester wie Allylacetat, Phthalsäurediallylester, Isophthalsäurediallylester, Fumarsäurediallylester, Allylcarbonate, Diallylcarbonate, Triallylphosphat und Triallylcyanurat.
- Als "thermotrop" bezeichnet man solche Substanzen, die flüssig-kristalline Schmelzen bilden. Thermotrope Polymere sind hinreichend bekannt, vgl. z.B. F.E. Mc Farlane et al., Liquid Crystal Polymers II, Contemporary Topics in Polymer Science, Vol. 2, Plenum Publishing Corporation, 1977;
W. J. Jackson und H. F. Kuhfuss, J. Polymer Science Polymer Chem. Ed. 14, 2042 (1976);
W. C. Wooten et al. in A. Ciferri "Ultra-high Modulus Polymers", Applied Science Publ., London 1979, S. 362 f.;
A. Blumstein et al., "Liquid Crystalline Order in Polymers", Academic Press 1978;
J. Preston, Angew. Makromol. Chem. 109/110, S. 1-19 (1982);
A. Ciferri, W. R. Krigbaum, R. B. Meyer "Polymer Liquid Crystals", Academic Press, New York, 1982;
P. J. Flory, I. Uematsu, S. P. Papkov, CH. Ober und R. W. Lenz, Advances in Polymer Science 59 (1984);
B. Wunderlich, J. Grebowicz, M. G. Dobb, J. Mc Intyre, H. Finkelmann, G. Rehage, V. P. Shibaev und N. Plate, Advances in Polymer Science 60/61 (1984);
EP 1185, 1340, 8855, 11 640, 15 856, 17 310, 18 145, 18 709. 22 344, 44 205, 49 615;
US 3 991 013, 3 991 014, 4 066 620, 4 067 852, 4 083 829, 4 107 143;
US-PS 3 991 013, 3 991 014, 4 066 620, 4 067 852, 4 083 829, 4 107 143;
WO 79/797, 79/1034, 79/1040. - Der flüssig-kristalline Zustand von Polymerschmelzen läßt sich mit Hilfe eines Polarisationsmikroskops untersuchen: Für die Untersuchungen war das Okular mit einem Aufsatz ausgerüstet, der eine Fotodiode im Brennpunkt der Okularlinse angeordnet enthielt. Anhand eines nachgeschalteten Meßverstärkers mit Regeleinrichtung wurde der Meßwert am eingeschalteten Mikroskop bei parallel angeordneten Nicolschen Prismen in Abwesenheit einer Materialprobe auf 100 Skalenteile eingestellt. Bei gekreuzten Nicholschen Prismen ergab sich dann ein Wert von 0,01 Skalenteilen.
- Die Schichtdicke der untersuchten Polymerschmelzen betrug 100 µm.
- Die Untersuchung der Polymeren erfolgt nach dem Aufschmelzen der Proben bei Temperaturen zwischen 200 und 400° C. Sofern in diesem gesamten Bereich oder in einem Teil davon eine Aufhellung der zwischen den gekreuzten Nicolschen Prismen beobachteten Schmelze auftrat, wurde das Polymere als thermotrop flüssigkristallin eingestuft.
- Die flüssig-kristallinen Polymeren zeigen in der Meßanordnung Werte über 1 Skalenteil, meist Werte von 3 bis 90 Skalenteilen. Für amorphe Schmelzen, z.B. aromatische Polycarbonate, wurden dagegen Werte von weniger als 0,1 Skalenteil gefunden.
- Die oben beschriebene Methode ist für eine Schnellbestimmung im Laboratorium besonders geeignet und liefert in nahezu allen Fällen zweifelsfreie Ergebnisse. In Zweifelsfällen kann es dagegen sinnvoll sein, das Vorhandensein flüssig-kristalliner Komponenten mittels Röntgenkleinwinkelstreuung in der Schmelze nachzuweisen, wie es z.B. G.W. Gray und P.A. Windsor, "Plastic Crystals, Physico-Chemical Properties and Methods of Investigation", insbesondere Chapter 3, John Wiley & Sons, New York, Sydney, Toronto 1974 beschrieben ist.
- Geeignete thermotrope Polymere, die in Form von Fasern oder Pulver zur Verwendung in den erfindungsgemäßen Mischungen geeignet sind, umfassen thermotrope Polyester, Polyestercarbonate, Polyesteramide, Polyesterimide, Polythiolester, Polyazomethine und thermotrope Cellulosederivate wie beispielsweise Hydroxypropylcellulose.
- Thermotrope Polykondensate II könnwn z.B. aus den folgenden Verbindungen hergestellt werden:
o-, m- oder p-Hydroxy-benzoesäure,
Hydrochinon,
durch Halogen, C₁- bis C₃-Alkyl oder Phenyl substituierte Hydrochinone,
Hydroxy-naphthalin-carbonsäuren,
Isophthalsäure,
Terephthalsäure,
Naphthalindicarbonsäure,
4,4ʹ -Dihydroxydiphenyl,
4,4ʹ -Dihydroxy-stilben,
1,2-Bis(p-carboxy-phenoxy)ethan,
4,4ʹ -Dihydroxyphenylether,
4,4ʹ -Diphenylether-dicarbonsäure,
Resorcin,
4,4ʹ -Benzophenondicarbonsäure,
4,4ʹ -Dihydroxy-diphenylsulfid,
4,4ʹ -Dihydroxy-diphenylsulfon,
2.5-Furandicarbonsäure,
4,4ʹ -Bis(p-hydroxy-phenoxy)diphenylether,
1,2-Bis(p-hydroxyphenyl)ethan,
Dihydroxyanthrachinone,
4,4ʹ -Hydroxy-diphenylether-carbonsäure,
Azobenzoldicarbonsäure,
Bisphenol-A,
Ethylenglykol, Hexandiol-1,6, Adipin-, Sebacinsäure,
Kohlensäure. - Nicht sämtliche Kombinationen der oben aufgezählten Ausgangsmaterialien ergeben thermotrope Polykondensate. Der Fachmann wird seine Auswahl jeweils anhand der oben zitierten Literatur treffen oder aber aufgrund seiner Erfahrung empirisch vorgehen. Da die thermotropen Polykondensate II an sich bekannt sind, kann eine längere Ausführung an dieser Stelle entfallen.
- Bevorzugte thermotrope Polymere II sind voll-aromatische Polyester und voll-aromatische Polyestercarbonate. Derartige Polyester und Polyestercarbonate sind bekannt;
vgl. DE-OS 33 25 704 = US-PS 45 79 934,
DE-OS 33 25 705 = US-PS 45 64 669,
DE-OS 33 25 703 = US-PS 46 03 190,
DE-OS 33 25 787 = US-PS 45 36 561,
DE-OS 34 15 530 = US-PS 46 00 764,
DE-OS 34 19 794, 34 27 886, 35 02 378, 35 17 270 und 35 17 948. - Der Carbonatgruppengehalt thermotroper Polyestercarbonate II kann bis zu 40 Mol-%, vorzugsweise 25 bis 35 Mol-%, bezogen auf die Summe von Ester- und Carbonatgruppen betragen.
- Bevorzugte thermotrope Polyestercarbonate II umfassen solche auf Basis von
- a) (gegebenenfalls substituierter) p-Hydroxybenzoesäure,
- b) Diphenol,
- c) Kohlensäure und gegebenenfalls
- d) aromatischer Dicarbonsäure,
- Bevorzugte (a) p-Hydroxybenzoesäuren sind durch C₁-C₄-Alkyl, C₁-C₄-Alkoxy, C₆-C₁₀-Aryl oder -Alkylaryl (wie Phenyl, Tolyl, Naphthyl), Halogen (vorzugsweise Chlor und Brom) kernsubstituierte p-Hydroxybenzoesäuren, wie z.B. 4-Hydroxy-2-methylbenzoesäure, 4-Hydroxy-3-methylbenzoesäure, 2-Ethyl-4-hydroxybenzoesäure, 3-Ethyl-4- hydroxybenzoesäure, 2- oder 3-Chlor-4-hydroxybenzoesäure, 4-Hydroxy-2-phenylbenzoesäure oder 4-Hydroxy-3-phenyl-benzoesäure, vorzugsweise jedoch unsubstituierte p-Hydroxybenzoesäure selbst.
- Bevorzugte (b) Diphenole sind Verbindungen der Formel
HO - Z-OH (I)
worin Z einen zweiwertigen ein- oder mehrkernigen aromatischen Rest mit 6 bis 30 C-Atomen bedeutetm wobei Z derart gebaut ist, daß die beiden OH-Gruppen direkt an je ein C-Atom eines aromatischen Systems gebunden sind, wie z.B.
(1) Hydrochinon, Methylhydrochinon, Ethylhydrochinon, 1,4-Dihydroxynaphthalin, 1,5-Dihydroxynaphthalin, 2,6-Dihydroxynaphthalin, die zu keiner wesentlichen Winkelung der Polykondensatkette führen, und
(2) Verbindungen, die zu einer wesentlichen Winkelung der Polykondensatkette beitragen wie z.B. Resorcin, 1,6-Dihydroxynaphthalin, 2,5-Dihydroxynaphthalin, 2,7-Dihydroxynaphthalin und Bisphenole der Formel
Y einen Alkylen- oder Alkylidenrest mit 1 bis 7 C-Atomen, einen Cycloalkylen- oder Cycloalkylidenrest mit 5 bis 12 C-Atomen, -O-, -S-, --, -SO₂- oder -- bedeutet,
sowie deren kernalkylierte und kernhalogenierte Derivate, z.B.
Bis-(hydroxyphenyl)-alkane,
Bis-(hydroxyphenyl)-cycloalkane,
Bis-(hydroxyphenyl)-sulfide,
Bis-(hydroxyphenyl)-ether,
Bis-(hydroxyphenyl)-ketone,
Bis-(hydroxyphenyl)-sulfoxide,
Bis-(hydroxyphenyl)-sulfone und
4,4ʹ -Bis-(hydroxyphenyl)-diisopropylbenzole
sowie deren kernalkylierte und kernhalogenierte Verbindungen, also z.B.
Bis-(4-hydroxyphenyl)-methan,
1,1-Bis-(4-hydroxyphenyl)-ethan,
Bisphenol A,
1,1-Bis-(4-hydroxyphenyl)-cyclohexan,
Bis-(4-hydroxyphenyl)-sulfon,
4,4ʹ -Dihydroxydiphenylether und
4,4ʹ -Dihydroxydiphenylsulfid. - Es empfiehlt sich, die Diphenole derart auszuwählen, daß maximal 30 Mol-%, bezogen auf die Gesamtmenge an Diphenolresten, Diphenolreste der Gruppe (2) sind. Dabei ist ein hoher Anteil an Diphenolresten der Gruppe (2) insbesondere dann vertretbar, wenn er durch zusätzliche lineare Reste, wie z.B. Terephthalsäurereste, "kompensiert" wird.
- Bevorzugte Derivate zum Einbau der (c) Carbonatgruppen sind Phosgen, Diarylcarbonate, wie z.B. Diphenylcarbonat, Ditolylcarbonat, Phenyl-tolylcarbonat, Dinaphthylcarbonat, Dialkylcarbonat wie z.B. Diethylcarbonat, Dimethylcarbonat, Dimethyldicarbonat, Diethyldicarbonat, Gykolcarbonat und Chlorameisensäureester.
- Bevorzugte (d) aromatische Dicarbonsäuren besitzen 8 bis 24, vorzugsweise 8 bis 14, C-Atome und können pro aromatischen Ring durch bis zu 4 C₁-C₄-Alkylreste, C₁-C₄-Alkoxyreste oder Halogenatome (vorzugsweise Chlor und Brom) substituiert s ein, wie z.B. Naphthalin-1,4-dicarbonsäure, Diphenyl-2,2ʹ -dicarbonsäure, Diphenyl-4,4ʹ -dicarbonsäure, Diphenylmethan-4,4ʹ -dicarbonsäure, Diphenylether-4,4ʹ -dicarbonsäure, Diphenylsulfon-4,4ʹ -dicarbonsäure, vorzugsweise Terephthalsäure, isophthalsäure und Naphthalin-2,6-dicarbonsäure sowie deren kernsubstituierte Derivate.
- Als Endgruppen können die thermotropen Polyester bzw. Polyestercarbonate II -H, -OH, -OC₆H₅ oder von Kettenabbrechern herrührende Reste enthalten.
- Die thermotropen Polyester bzw. Polyestercarbonate II können die Reste der Verbindungen (a) bis (e) in statistischer Verteilung oder in Blöcken enthalten.
- Die thermotropen Polyester bzw. Polyestercarbonate können nach verschiedenen Verfahren hergestellt werden, z.B. durch Kondensation der Carbonsäurechloride oder durch Veresterung der Carbonsäurearylester mit den phenolischen Verbindungen und anschließenden Polykondensation, wobei die Carbonsäurechloride auch aus den entsprechenden Carbonsäuren und Chlorierungsmitteln in situ erzeugt werden können. Im Falle der Veresterung und anschließender Polykondensation wird so lange Phenol aus der Reaktionsmischung abdestilliert, bis der gewünschte Kondensationsgrad erreicht ist.
- Den erfindungsgemäßen Mischungen können auch übliche Zusatzstoffe, wie Füllstoffe, Verstärkungsmittel, Pigmente, Beschleuniger, Aufheller, Thixotropiermittel und Stabilisatoren, wie z.B. Hydrochinon oder dessen Derivate, zugesetzt werden.
- Zur Herstellung von Formmassen können den erfindungsgemäßen Mischungen 50 bis 350 Gew.-%, bezogen auf Polyesterharz A + B, Füllstoffe und/oder Verstärkungsmittel, wie Kreide, Talkum, Baryt, Aerosil, Glasfasern, zugesetzt werden. Farbstoffe oder Pigmente können natürlich ebenfalls zugegeben werden. Das Mischen der verschiedenen Komponenten der erfindungsgemäßen Mischungen erfolgt zweckmäßig in Knetern, Dissolvern oder auf Walzenstühlen.
- Vor der Härtung können den erfindungsgemäßen Mischungen Polymerisationsinitiatoren, vorzugsweise Diacylperoxide oder Percarbonate, in Mengen von 1 bis 10 Gew.-%, bezogen auf Polyesterharz A + B, zugesetzt werden. Bevorzugte Initiatoren sind z.B. Peroxide und Percarbonate wie Diacetylperoxid, Dibenzoylperoxid, Di-p-chlorbenzoylperoxid, Phthaloylperoxid, Succinylperoxid, Dilaurylperoxid, Acetylcyclohexansulfonylperoxid, Isopropylpercarbonat, Cyclohexylpercarbonat und Bis-(4-tert.-butylcyclohexyl)-percarbonat.
- Die erfindungsgemäßen Mischungen bzw. die daraus hergestellten Massen können bei Temperaturen von -15° C bis +120° V, vorzugsweise von 0° C bis 90° C oder - falls sie vorbeschleunigt sind - bei Raumtemperatur gehärtet werden.
- Aus den erfindungsgemäßen Mischungen hergestellte Preß- und Gießmassen eignen sich insbesondere zur Herstellung von Formteilen und Spachtelmassen, die in den verschiedensten Gebieten der Bauindustrie, der Elektroindustrie, des Bootsbaus, der medizinischen Technik und der Kraftfahrzeugindustrie eingesetzt werden können.
- Aus 3265 g Diethylenglykol, 478 g Ethylenglykol und 3596 g Maleinsäureanhydrid wird in der üblichen Schmelzkondensation unter Addition von 1545 g Dicyclopentadien ein ungesättigter Polyester erhalten, der nach Abmischung mit Styrol folgende Kennzahlen aufweist:
Festgehalt: 62 %
Säurezahl: 12 mg KOH/g
Viskosität: 500 mPa.s - Aus 1458 g Ethylenglykol, 798 g 1,2-Propylenglykol, 3012 g Trimethylolpropan-diallylether, 3102 g Maleinsäureanhydrid, 521 g Phthalsäureanhydrid, 55 g Methanol und 550 g eines Esters aus Maleinsäure und Trimethylolpropan-diallylether erhält man in der üblichen Schmelzkondensation einen ungesättigten Polyester, der in Styrol gelöst wird.
Festgehalt: 75 %
Säurezahl: 20 mg KOH/g
Visosität: 2600 mPa.s - Aus 3028 g 1,2-Propylenglykol, 1620, Dipropylenglykol, 3838 g Maleinsäureanhydrid und 1175 g Phthalsäureanhydrid wird durch übliche Schmelzkondensation ein ungesät tigter Polyester hergestellt, der, mit Styrol gemischt, folgende Kennzahlen besitzt:
Festgehalt: 75 %
Säurezahl: 19 mg KOH/g
Viskosität: 1600 mPa.s - Fahrweise wie UP 2, aber mit anderen Kennzahlen:
Festgehalt: 85 %
Säurezahl: 20 mg KOH/g
Viskosität: 14 000 mPa.s - In einem Reaktionsgefäß mit Rührer und Destillierbrücke wurden 194 g p-Hydroxybenzoesäure, 48,6 g Hydrochinon, 40,7 g 4,4ʹ -Dihydroxybiphenyl, 17,1 g Terephthalsäure, 0,55 g Zink(II)acetat und 487,6 g Diphenylcarbonat auf 250° C erhitzt.
- Nach Erhöhung der Temperatur auf 295° C und nachlassender Destillationsgeschwindigkeit wurde bei dieser Temperatur langsam innerhalb 1 Stunde ein Vakuum von 0,5 x 10⁻³ bar angelegt und 1 Stunde nachkondensiert.
-
- Versuche I bis IV sind erfindungsgemäße Versuche, V bis X stellen Vergleichsversuche dar.
- Die Eigenschaften der erfindungsgemäßen Formmassen unterscheiden sich deutlich von denen der Vergleichsversuche.
- Formmassen IX und X härten nach Zugabe von Benzoylperoxid spontan aus, so daß die Gießfähigkeit nicht beurteilt werden kann. Vor der Peroxid-Zugabe sind beide Formmassen noch gießbar.
b - e = 0,02 bis 0,53, vorzugsweise 0,06 bis 0,36, insbesondere 0,1 bis 0,35,
c = 0,12 bis 0,6, vorzugsweise 0,175 bis 0,4,
d = 0 bis 0,24, vorzugsweise 0 bis 0/12, und e =0,02 bis 0,53, vorzugsweise 0,0275 bis 0,28, insbesondere 0,03 bis 0,16.
Claims (7)
I) 10 bis 90 Gew.-% ungesättigtem Polyesterharz und
II) 90 bis 10 Gew.-% thermotropem Polymer,
wobei sich die Prozentangaben jeweils auf die Summe I + II beziehen.
I) 30 bis 70 Gew.-% ungesättigtem Polyesterharz und
II) 70 bis 30 Gew.-% thermotropem Polymer.
A) 30 bis 95 Gew.-Teilen ungesättigtem Polyester und
B) 70 bis 5 Gew.-Teilen mit A copolymerisierbarem Monomer besteht.
A) 50 bis 90 Gew.-Teilen Polyester und
B) 50 bis 10 Gew.-Teilen Monomer besteht.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE3701740 | 1987-01-22 | ||
| DE19873701740 DE3701740A1 (de) | 1987-01-22 | 1987-01-22 | Thermotrope polymere enthaltende ungesaettigte polyesterharze, verfahren zu ihrer herstellung und ihre verwendung zur herstellung von formkoerpern |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| EP0275906A2 true EP0275906A2 (de) | 1988-07-27 |
| EP0275906A3 EP0275906A3 (de) | 1989-10-11 |
Family
ID=6319281
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP88100368A Ceased EP0275906A3 (de) | 1987-01-22 | 1988-01-13 | Thermotrope Polymere enthaltende ungesättigte Polyesterharze, Verfahren zu ihrer Herstellung und ihre Verwendung zur Herstellung von Formkörpern |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US5015689A (de) |
| EP (1) | EP0275906A3 (de) |
| JP (1) | JPS63189464A (de) |
| DE (1) | DE3701740A1 (de) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0572225A1 (de) * | 1992-05-29 | 1993-12-01 | Ge Plastics Japan Limited | Niedrig-schrumpfende hitzhärtbare Zusammensetzungen, die Polycarbonat enthalten |
| US5489655A (en) * | 1993-07-26 | 1996-02-06 | General Electric Company | Thermosetting resin compositions with low shrinkage |
| EP0816432A3 (de) * | 1996-07-02 | 1998-07-08 | Dsm Resins B.V. | Härtbare Polyesterharz-Formmassen |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE19825984C1 (de) | 1998-06-10 | 2000-03-16 | Fraunhofer Ges Forschung | Verfahren zur Herstellung thermotroper Gießharzsysteme und seine Verwendung |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS49110788A (de) * | 1973-02-23 | 1974-10-22 | ||
| DE2354716A1 (de) * | 1973-11-02 | 1975-05-07 | Bayer Ag | Rieselfaehige, schwundarm aushaertende ungesaettigte polyesterformmassen |
| JPS6055545B2 (ja) * | 1976-03-11 | 1985-12-05 | 帝人株式会社 | 樹脂組成物 |
| EP0030417B2 (de) * | 1979-11-30 | 1994-03-30 | Imperial Chemical Industries Plc | Zusammensetzungen in geschmolzenem Zustand verarbeitbarer Polymere mit verbesserter Verarbeitbarkeit und Verarbeitungsverfahren |
| US4251641A (en) * | 1979-12-04 | 1981-02-17 | Hitachi Chemical Company, Ltd. | Low shrinkage polyester resin compositions |
| US4489190A (en) * | 1980-06-11 | 1984-12-18 | Celanese Corporation | Blend of polyalkylene terephthalate and wholly aromatic polyester |
| JPS57164114A (en) * | 1981-04-01 | 1982-10-08 | Nippon Oil & Fats Co Ltd | Low-shrinkage unsaturated polyester resin composition |
| US4451611A (en) * | 1981-12-15 | 1984-05-29 | Celanese Corporation | Process for forming blend of polyalkylene terephthalate and wholly aromatic polyester which exhibits an anisotropic melt phase |
| US4563508A (en) * | 1984-05-18 | 1986-01-07 | Dart Industries, Inc. | Injection moldable aromatic polyesters compositions and method of preparation |
| DE3477799D1 (en) * | 1984-07-05 | 1989-05-24 | Celanese Corp | Melt blend of non-thermotropic and thermotropic wholly aromatic polyesters |
-
1987
- 1987-01-22 DE DE19873701740 patent/DE3701740A1/de not_active Withdrawn
-
1988
- 1988-01-13 EP EP88100368A patent/EP0275906A3/de not_active Ceased
- 1988-01-14 JP JP63004993A patent/JPS63189464A/ja active Pending
-
1989
- 1989-10-13 US US07/423,516 patent/US5015689A/en not_active Expired - Fee Related
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0572225A1 (de) * | 1992-05-29 | 1993-12-01 | Ge Plastics Japan Limited | Niedrig-schrumpfende hitzhärtbare Zusammensetzungen, die Polycarbonat enthalten |
| US5489655A (en) * | 1993-07-26 | 1996-02-06 | General Electric Company | Thermosetting resin compositions with low shrinkage |
| EP0816432A3 (de) * | 1996-07-02 | 1998-07-08 | Dsm Resins B.V. | Härtbare Polyesterharz-Formmassen |
Also Published As
| Publication number | Publication date |
|---|---|
| JPS63189464A (ja) | 1988-08-05 |
| US5015689A (en) | 1991-05-14 |
| DE3701740A1 (de) | 1988-08-04 |
| EP0275906A3 (de) | 1989-10-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0064648B2 (de) | Thermoplastische Formmassen aus Polycarbonat, Polyalkylenterephthalat und Pfropfpolymerisat | |
| DE3586645T2 (de) | Polyester-zusammensetzung und formlinge daraus. | |
| DE69633807T2 (de) | Doppelbrechungsarme Polycarbonatformmassen | |
| DE3750485T2 (de) | Harzzusammensetzung mit anisotropischen Schmelzeigenschaften. | |
| EP0315868A2 (de) | Verwendung von Redoxpfropfpolymerisaten zur Verbesserung der Benzinbeständigkeit von thermoplastischen, aromatischen Polycarbonat- und/oder Polyestercarbonat-Formmassen | |
| EP0673973A1 (de) | Mischungen auf der Basis von Polyarylenethern und Polyarylensulfiden | |
| EP0106027A1 (de) | Schlagzähe thermoplastische Formmassen mit hoher Wärmeformbeständigkeit | |
| EP0392357B1 (de) | Glasfaserverstärkte thermoplastische Formmassen auf der Basis von Polyestern und Pfropfpolymerisaten | |
| DE3783890T2 (de) | Harzmischungen mit schlagzaehigkeitseigenschaften. | |
| DE69922713T2 (de) | Polyesterformmasse | |
| US4758626A (en) | Melt of an amorphous aromatic polyester with a melt of a carboxy terminated polyacrylate oligomer | |
| DE3808839A1 (de) | Thermoplastische formmassen enthaltend spezielle copolymere | |
| DE3521956A1 (de) | Kaelteschlagzaehe thermoplastische formmassen aus polyester und polycarbonat | |
| DE69517926T2 (de) | Gammastrahlungsstabiler Blend von Polycarbonat mit Polyester | |
| DE69122433T2 (de) | Polybromstyrol enthaltende flammhemmende thermotrope Polyestermischung und Formteile daraus | |
| EP0310976A2 (de) | Glasfaserverstärkte thermoplastische Formmassen auf der Basis von Polyestern und Pfropfpolymerisaten | |
| EP0275906A2 (de) | Thermotrope Polymere enthaltende ungesättigte Polyesterharze, Verfahren zu ihrer Herstellung und ihre Verwendung zur Herstellung von Formkörpern | |
| EP0297353A2 (de) | Formmassen aus Polycarbonat, thermotropem Polymer, Pfropfpolymerisat und fluoriertem Polyolefin | |
| DE60118394T2 (de) | Transparente Zusammensetzung enthaltend ein Polycarbonat und ein Methylmethacrylat-Copolymer | |
| EP0695785B1 (de) | Mischungen aus Polycarbonat, phenolisch hydroxyfunktionellen verzweigten Dimerfettsäurepolyestern und gegebenenfalls Pfropfpolymerisat | |
| EP0142675A1 (de) | Formmassen aus thermoplastischem Polyester und Pfropfkautschuk, Verfahren zu ihrer Herstellung und ihre Verwendung zur Herstellung von Formkörpern | |
| EP0595082A2 (de) | Thermoplastisch verarbeitbare thermotrope Massen | |
| EP0456030A2 (de) | Polycarbonat-ABS-Formmassen | |
| EP0236837A2 (de) | Mischungen aus Polycarbonatpolysiloxan-Blockcokondensaten und thermotropen Polymeren, Verfahren zu ihrer Herstellung und ihre Verwendung zur Herstellung von Formkörpern, Filamenten, Fasern und Folien | |
| EP0332998B1 (de) | Mischungen aus aromatischen Polycarbonaten und/oder aromatischen Polyestern mit speziellen Copolymeren |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| 17P | Request for examination filed |
Effective date: 19880113 |
|
| AK | Designated contracting states |
Kind code of ref document: A2 Designated state(s): AT DE ES FR GB IT |
|
| PUAL | Search report despatched |
Free format text: ORIGINAL CODE: 0009013 |
|
| AK | Designated contracting states |
Kind code of ref document: A3 Designated state(s): AT DE ES FR GB IT |
|
| 17Q | First examination report despatched |
Effective date: 19920504 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: THE APPLICATION HAS BEEN REFUSED |
|
| 18R | Application refused |
Effective date: 19930425 |