EP0261567A2 - Wärmeentwicklungsverfahren und hierfür geeignetes farbfotografisches Aufzeichnungsmaterial - Google Patents
Wärmeentwicklungsverfahren und hierfür geeignetes farbfotografisches Aufzeichnungsmaterial Download PDFInfo
- Publication number
- EP0261567A2 EP0261567A2 EP87113515A EP87113515A EP0261567A2 EP 0261567 A2 EP0261567 A2 EP 0261567A2 EP 87113515 A EP87113515 A EP 87113515A EP 87113515 A EP87113515 A EP 87113515A EP 0261567 A2 EP0261567 A2 EP 0261567A2
- Authority
- EP
- European Patent Office
- Prior art keywords
- color
- recording material
- development
- silver
- light
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 238000011161 development Methods 0.000 title claims abstract description 55
- 238000000034 method Methods 0.000 title claims abstract description 29
- 230000008569 process Effects 0.000 title claims abstract description 17
- 239000000463 material Substances 0.000 title claims description 57
- 150000001875 compounds Chemical class 0.000 claims abstract description 52
- 238000009792 diffusion process Methods 0.000 claims abstract description 24
- 239000003795 chemical substances by application Substances 0.000 claims abstract description 23
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 15
- 125000003118 aryl group Chemical group 0.000 claims abstract description 10
- 125000000623 heterocyclic group Chemical group 0.000 claims abstract description 8
- 125000004433 nitrogen atom Chemical group N* 0.000 claims abstract description 6
- 125000003710 aryl alkyl group Chemical group 0.000 claims abstract description 5
- 125000000753 cycloalkyl group Chemical group 0.000 claims abstract description 5
- 229910052757 nitrogen Inorganic materials 0.000 claims abstract description 5
- 239000000975 dye Substances 0.000 claims description 65
- -1 silver halide Chemical class 0.000 claims description 61
- 229910052709 silver Inorganic materials 0.000 claims description 57
- 239000004332 silver Substances 0.000 claims description 57
- 239000011230 binding agent Substances 0.000 claims description 31
- GGCZERPQGJTIQP-UHFFFAOYSA-N sodium;9,10-dioxoanthracene-2-sulfonic acid Chemical compound [Na+].C1=CC=C2C(=O)C3=CC(S(=O)(=O)O)=CC=C3C(=O)C2=C1 GGCZERPQGJTIQP-UHFFFAOYSA-N 0.000 claims description 26
- 238000010438 heat treatment Methods 0.000 claims description 17
- 230000001737 promoting effect Effects 0.000 claims description 9
- 238000004040 coloring Methods 0.000 claims description 8
- 125000001424 substituent group Chemical group 0.000 claims description 7
- 125000004432 carbon atom Chemical group C* 0.000 claims description 5
- 125000002252 acyl group Chemical group 0.000 claims description 4
- 238000004519 manufacturing process Methods 0.000 claims description 4
- 238000012546 transfer Methods 0.000 abstract description 9
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 27
- 150000003378 silver Chemical class 0.000 description 16
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 13
- 239000000243 solution Substances 0.000 description 11
- 108010010803 Gelatin Proteins 0.000 description 10
- 239000000839 emulsion Substances 0.000 description 10
- 229920000159 gelatin Polymers 0.000 description 10
- 239000008273 gelatin Substances 0.000 description 10
- 235000019322 gelatine Nutrition 0.000 description 10
- 235000011852 gelatine desserts Nutrition 0.000 description 10
- 239000000126 substance Substances 0.000 description 10
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 8
- 239000003638 chemical reducing agent Substances 0.000 description 8
- 239000002245 particle Substances 0.000 description 8
- 239000002243 precursor Substances 0.000 description 8
- 239000002904 solvent Substances 0.000 description 8
- 230000003595 spectral effect Effects 0.000 description 8
- 238000006243 chemical reaction Methods 0.000 description 7
- 239000000470 constituent Substances 0.000 description 7
- 239000000203 mixture Substances 0.000 description 7
- 239000007787 solid Substances 0.000 description 7
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 6
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 6
- 239000012992 electron transfer agent Substances 0.000 description 6
- 230000003197 catalytic effect Effects 0.000 description 5
- 239000000084 colloidal system Substances 0.000 description 5
- 239000006185 dispersion Substances 0.000 description 5
- 150000003254 radicals Chemical class 0.000 description 5
- 230000035945 sensitivity Effects 0.000 description 5
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 4
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 4
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 238000005354 coacervation Methods 0.000 description 4
- 125000000524 functional group Chemical group 0.000 description 4
- 239000003973 paint Substances 0.000 description 4
- 238000012545 processing Methods 0.000 description 4
- 150000003839 salts Chemical class 0.000 description 4
- SQGYOTSLMSWVJD-UHFFFAOYSA-N silver(1+) nitrate Chemical compound [Ag+].[O-]N(=O)=O SQGYOTSLMSWVJD-UHFFFAOYSA-N 0.000 description 4
- KYVBNYUBXIEUFW-UHFFFAOYSA-N 1,1,3,3-tetramethylguanidine Chemical compound CN(C)C(=N)N(C)C KYVBNYUBXIEUFW-UHFFFAOYSA-N 0.000 description 3
- 229940126062 Compound A Drugs 0.000 description 3
- NLDMNSXOCDLTTB-UHFFFAOYSA-N Heterophylliin A Natural products O1C2COC(=O)C3=CC(O)=C(O)C(O)=C3C3=C(O)C(O)=C(O)C=C3C(=O)OC2C(OC(=O)C=2C=C(O)C(O)=C(O)C=2)C(O)C1OC(=O)C1=CC(O)=C(O)C(O)=C1 NLDMNSXOCDLTTB-UHFFFAOYSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- 206010070834 Sensitisation Diseases 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 125000001931 aliphatic group Chemical group 0.000 description 3
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 3
- 238000003776 cleavage reaction Methods 0.000 description 3
- 238000001816 cooling Methods 0.000 description 3
- 238000009826 distribution Methods 0.000 description 3
- 230000006870 function Effects 0.000 description 3
- 239000001257 hydrogen Substances 0.000 description 3
- 229910052739 hydrogen Inorganic materials 0.000 description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 238000002156 mixing Methods 0.000 description 3
- 230000003647 oxidation Effects 0.000 description 3
- 238000007254 oxidation reaction Methods 0.000 description 3
- 229920000642 polymer Polymers 0.000 description 3
- 230000008313 sensitization Effects 0.000 description 3
- 125000000020 sulfo group Chemical group O=S(=O)([*])O[H] 0.000 description 3
- YXIWHUQXZSMYRE-UHFFFAOYSA-N 1,3-benzothiazole-2-thiol Chemical compound C1=CC=C2SC(S)=NC2=C1 YXIWHUQXZSMYRE-UHFFFAOYSA-N 0.000 description 2
- PLIKAWJENQZMHA-UHFFFAOYSA-N 4-aminophenol Chemical compound NC1=CC=C(O)C=C1 PLIKAWJENQZMHA-UHFFFAOYSA-N 0.000 description 2
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical class C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 2
- ZRALSGWEFCBTJO-UHFFFAOYSA-N Guanidine Chemical compound NC(N)=N ZRALSGWEFCBTJO-UHFFFAOYSA-N 0.000 description 2
- QIGBRXMKCJKVMJ-UHFFFAOYSA-N Hydroquinone Chemical compound OC1=CC=C(O)C=C1 QIGBRXMKCJKVMJ-UHFFFAOYSA-N 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 150000007933 aliphatic carboxylic acids Chemical class 0.000 description 2
- 125000000129 anionic group Chemical group 0.000 description 2
- 235000010323 ascorbic acid Nutrition 0.000 description 2
- 229960005070 ascorbic acid Drugs 0.000 description 2
- 239000011668 ascorbic acid Substances 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 238000005266 casting Methods 0.000 description 2
- YCIMNLLNPGFGHC-UHFFFAOYSA-N catechol Chemical compound OC1=CC=CC=C1O YCIMNLLNPGFGHC-UHFFFAOYSA-N 0.000 description 2
- 230000009918 complex formation Effects 0.000 description 2
- JQVDAXLFBXTEQA-UHFFFAOYSA-N dibutylamine Chemical compound CCCCNCCCC JQVDAXLFBXTEQA-UHFFFAOYSA-N 0.000 description 2
- CZLCEPVHPYKDPJ-UHFFFAOYSA-N guanidine;2,2,2-trichloroacetic acid Chemical compound NC(N)=N.OC(=O)C(Cl)(Cl)Cl CZLCEPVHPYKDPJ-UHFFFAOYSA-N 0.000 description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 2
- 230000002209 hydrophobic effect Effects 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 238000002844 melting Methods 0.000 description 2
- 230000008018 melting Effects 0.000 description 2
- 229910021645 metal ion Inorganic materials 0.000 description 2
- MXWHMTNPTTVWDM-NXOFHUPFSA-N mitoguazone Chemical class NC(N)=N\N=C(/C)\C=N\N=C(N)N MXWHMTNPTTVWDM-NXOFHUPFSA-N 0.000 description 2
- 230000007935 neutral effect Effects 0.000 description 2
- 238000005554 pickling Methods 0.000 description 2
- 229920002635 polyurethane Polymers 0.000 description 2
- 239000004814 polyurethane Substances 0.000 description 2
- WQGWDDDVZFFDIG-UHFFFAOYSA-N pyrogallol Chemical compound OC1=CC=CC(O)=C1O WQGWDDDVZFFDIG-UHFFFAOYSA-N 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 229910001961 silver nitrate Inorganic materials 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- 229910052938 sodium sulfate Inorganic materials 0.000 description 2
- GEHJYWRUCIMESM-UHFFFAOYSA-L sodium sulfite Chemical compound [Na+].[Na+].[O-]S([O-])=O GEHJYWRUCIMESM-UHFFFAOYSA-L 0.000 description 2
- 235000011152 sodium sulphate Nutrition 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- CWERGRDVMFNCDR-UHFFFAOYSA-N thioglycolic acid Chemical compound OC(=O)CS CWERGRDVMFNCDR-UHFFFAOYSA-N 0.000 description 2
- 239000000080 wetting agent Substances 0.000 description 2
- QLDQYRDCPNBPII-UHFFFAOYSA-N 1,2-benzoxazol-3-one Chemical compound C1=CC=C2C(O)=NOC2=C1 QLDQYRDCPNBPII-UHFFFAOYSA-N 0.000 description 1
- DKYBVKMIZODYKL-UHFFFAOYSA-N 1,3-diazinane Chemical compound C1CNCNC1 DKYBVKMIZODYKL-UHFFFAOYSA-N 0.000 description 1
- YHMYGUUIMTVXNW-UHFFFAOYSA-N 1,3-dihydrobenzimidazole-2-thione Chemical compound C1=CC=C2NC(S)=NC2=C1 YHMYGUUIMTVXNW-UHFFFAOYSA-N 0.000 description 1
- 150000005208 1,4-dihydroxybenzenes Chemical class 0.000 description 1
- OSSNTDFYBPYIEC-UHFFFAOYSA-N 1-ethenylimidazole Chemical compound C=CN1C=CN=C1 OSSNTDFYBPYIEC-UHFFFAOYSA-N 0.000 description 1
- KJUGUADJHNHALS-UHFFFAOYSA-N 1H-tetrazole Chemical class C=1N=NNN=1 KJUGUADJHNHALS-UHFFFAOYSA-N 0.000 description 1
- HAZJTCQWIDBCCE-UHFFFAOYSA-N 1h-triazine-6-thione Chemical compound SC1=CC=NN=N1 HAZJTCQWIDBCCE-UHFFFAOYSA-N 0.000 description 1
- FVQQWSSTYVBNST-UHFFFAOYSA-N 2-(4-methyl-2-sulfanylidene-1,3-thiazol-3-yl)acetic acid Chemical class CC1=CSC(=S)N1CC(O)=O FVQQWSSTYVBNST-UHFFFAOYSA-N 0.000 description 1
- JKFYKCYQEWQPTM-UHFFFAOYSA-N 2-azaniumyl-2-(4-fluorophenyl)acetate Chemical compound OC(=O)C(N)C1=CC=C(F)C=C1 JKFYKCYQEWQPTM-UHFFFAOYSA-N 0.000 description 1
- FLFWJIBUZQARMD-UHFFFAOYSA-N 2-mercapto-1,3-benzoxazole Chemical compound C1=CC=C2OC(S)=NC2=C1 FLFWJIBUZQARMD-UHFFFAOYSA-N 0.000 description 1
- UIQPERPLCCTBGX-UHFFFAOYSA-N 2-phenylacetic acid;silver Chemical compound [Ag].OC(=O)CC1=CC=CC=C1 UIQPERPLCCTBGX-UHFFFAOYSA-N 0.000 description 1
- FLWVAHBGRKYNEE-UHFFFAOYSA-N 2-sulfanyl-3h-oxadiazole Chemical compound SN1NC=CO1 FLWVAHBGRKYNEE-UHFFFAOYSA-N 0.000 description 1
- IBWXIFXUDGADCV-UHFFFAOYSA-N 2h-benzotriazole;silver Chemical compound [Ag].C1=CC=C2NN=NC2=C1 IBWXIFXUDGADCV-UHFFFAOYSA-N 0.000 description 1
- UPMLOUAZCHDJJD-UHFFFAOYSA-N 4,4'-Diphenylmethane Diisocyanate Chemical compound C1=CC(N=C=O)=CC=C1CC1=CC=C(N=C=O)C=C1 UPMLOUAZCHDJJD-UHFFFAOYSA-N 0.000 description 1
- YLBAGJYQBOPFCD-UHFFFAOYSA-N 4-ethenyl-1-methyl-2h-pyridine Chemical compound CN1CC=C(C=C)C=C1 YLBAGJYQBOPFCD-UHFFFAOYSA-N 0.000 description 1
- KFDVPJUYSDEJTH-UHFFFAOYSA-N 4-ethenylpyridine Chemical compound C=CC1=CC=NC=C1 KFDVPJUYSDEJTH-UHFFFAOYSA-N 0.000 description 1
- CMGDVUCDZOBDNL-UHFFFAOYSA-N 4-methyl-2h-benzotriazole Chemical compound CC1=CC=CC2=NNN=C12 CMGDVUCDZOBDNL-UHFFFAOYSA-N 0.000 description 1
- NSPMIYGKQJPBQR-UHFFFAOYSA-N 4H-1,2,4-triazole Chemical class C=1N=CNN=1 NSPMIYGKQJPBQR-UHFFFAOYSA-N 0.000 description 1
- PZBQVZFITSVHAW-UHFFFAOYSA-N 5-chloro-2h-benzotriazole Chemical compound C1=C(Cl)C=CC2=NNN=C21 PZBQVZFITSVHAW-UHFFFAOYSA-N 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- SOPOWMHJZSPMBC-UHFFFAOYSA-L C(C1=CC=C(C(=O)[O-])C=C1)(=O)[O-].[Ag+2] Chemical compound C(C1=CC=C(C(=O)[O-])C=C1)(=O)[O-].[Ag+2] SOPOWMHJZSPMBC-UHFFFAOYSA-L 0.000 description 1
- AXVCDCGTJGNMKM-UHFFFAOYSA-L C(C=1C(C(=O)[O-])=CC=CC1)(=O)[O-].[Ag+2] Chemical compound C(C=1C(C(=O)[O-])=CC=CC1)(=O)[O-].[Ag+2] AXVCDCGTJGNMKM-UHFFFAOYSA-L 0.000 description 1
- DYYHUAGAPAAERQ-UHFFFAOYSA-L C(CCCCC(=O)[O-])(=O)[O-].[Ag+2] Chemical compound C(CCCCC(=O)[O-])(=O)[O-].[Ag+2] DYYHUAGAPAAERQ-UHFFFAOYSA-L 0.000 description 1
- IVNAZOGVWDHYGU-UHFFFAOYSA-L C(CCCCCCCCC(=O)[O-])(=O)[O-].[Ag+2] Chemical compound C(CCCCCCCCC(=O)[O-])(=O)[O-].[Ag+2] IVNAZOGVWDHYGU-UHFFFAOYSA-L 0.000 description 1
- GAWIXWVDTYZWAW-UHFFFAOYSA-N C[CH]O Chemical group C[CH]O GAWIXWVDTYZWAW-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical class S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 description 1
- BRLQWZUYTZBJKN-UHFFFAOYSA-N Epichlorohydrin Chemical compound ClCC1CO1 BRLQWZUYTZBJKN-UHFFFAOYSA-N 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 description 1
- WRYCSMQKUKOKBP-UHFFFAOYSA-N Imidazolidine Chemical compound C1CNCN1 WRYCSMQKUKOKBP-UHFFFAOYSA-N 0.000 description 1
- QAQJMLQRFWZOBN-LAUBAEHRSA-N L-ascorbyl-6-palmitate Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](O)[C@H]1OC(=O)C(O)=C1O QAQJMLQRFWZOBN-LAUBAEHRSA-N 0.000 description 1
- 239000011786 L-ascorbyl-6-palmitate Substances 0.000 description 1
- OYHQOLUKZRVURQ-HZJYTTRNSA-N Linoleic acid Chemical compound CCCCC\C=C/C\C=C/CCCCCCCC(O)=O OYHQOLUKZRVURQ-HZJYTTRNSA-N 0.000 description 1
- CWNSVVHTTQBGQB-UHFFFAOYSA-N N,N-Diethyldodecanamide Chemical compound CCCCCCCCCCCC(=O)N(CC)CC CWNSVVHTTQBGQB-UHFFFAOYSA-N 0.000 description 1
- AKNUHUCEWALCOI-UHFFFAOYSA-N N-ethyldiethanolamine Chemical compound OCCN(CC)CCO AKNUHUCEWALCOI-UHFFFAOYSA-N 0.000 description 1
- CHJJGSNFBQVOTG-UHFFFAOYSA-N N-methyl-guanidine Natural products CNC(N)=N CHJJGSNFBQVOTG-UHFFFAOYSA-N 0.000 description 1
- SJEYSFABYSGQBG-UHFFFAOYSA-M Patent blue Chemical compound [Na+].C1=CC(N(CC)CC)=CC=C1C(C=1C(=CC(=CC=1)S([O-])(=O)=O)S([O-])(=O)=O)=C1C=CC(=[N+](CC)CC)C=C1 SJEYSFABYSGQBG-UHFFFAOYSA-M 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 229910021607 Silver chloride Inorganic materials 0.000 description 1
- 229910021612 Silver iodide Inorganic materials 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- 229920002253 Tannate Polymers 0.000 description 1
- RZESOXIJGKVAAX-UHFFFAOYSA-L [Ag++].[O-]C(=O)CCC([O-])=O Chemical compound [Ag++].[O-]C(=O)CCC([O-])=O RZESOXIJGKVAAX-UHFFFAOYSA-L 0.000 description 1
- JXFDPVZHNNCRKT-TYYBGVCCSA-L [Ag+2].[O-]C(=O)\C=C\C([O-])=O Chemical compound [Ag+2].[O-]C(=O)\C=C\C([O-])=O JXFDPVZHNNCRKT-TYYBGVCCSA-L 0.000 description 1
- 230000004308 accommodation Effects 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 239000000980 acid dye Substances 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 125000004442 acylamino group Chemical group 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 150000003973 alkyl amines Chemical class 0.000 description 1
- 125000003282 alkyl amino group Chemical group 0.000 description 1
- 125000004414 alkyl thio group Chemical group 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- 150000001409 amidines Chemical class 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 239000001000 anthraquinone dye Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 125000000732 arylene group Chemical group 0.000 description 1
- 235000010385 ascorbyl palmitate Nutrition 0.000 description 1
- 239000000987 azo dye Substances 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- QRUDEWIWKLJBPS-UHFFFAOYSA-N benzotriazole Chemical class C1=CC=C2N[N][N]C2=C1 QRUDEWIWKLJBPS-UHFFFAOYSA-N 0.000 description 1
- 239000012964 benzotriazole Substances 0.000 description 1
- 150000001565 benzotriazoles Chemical class 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 238000004061 bleaching Methods 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- AXCZMVOFGPJBDE-UHFFFAOYSA-L calcium dihydroxide Chemical compound [OH-].[OH-].[Ca+2] AXCZMVOFGPJBDE-UHFFFAOYSA-L 0.000 description 1
- 239000000920 calcium hydroxide Substances 0.000 description 1
- 229910001861 calcium hydroxide Inorganic materials 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-N carbamic acid group Chemical group C(N)(O)=O KXDHJXZQYSOELW-UHFFFAOYSA-N 0.000 description 1
- 125000002837 carbocyclic group Chemical group 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000004210 cyclohexylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 125000004663 dialkyl amino group Chemical group 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- SWSQBOPZIKWTGO-UHFFFAOYSA-N dimethylaminoamidine Natural products CN(C)C(N)=N SWSQBOPZIKWTGO-UHFFFAOYSA-N 0.000 description 1
- ZUVOYUDQAUHLLG-OLXYHTOASA-L disilver;(2r,3r)-2,3-dihydroxybutanedioate Chemical compound [Ag+].[Ag+].[O-]C(=O)[C@H](O)[C@@H](O)C([O-])=O ZUVOYUDQAUHLLG-OLXYHTOASA-L 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 150000002023 dithiocarboxylic acids Chemical class 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 230000002996 emotional effect Effects 0.000 description 1
- ZEUUVJSRINKECZ-UHFFFAOYSA-N ethanedithioic acid Chemical compound CC(S)=S ZEUUVJSRINKECZ-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- LNTHITQWFMADLM-UHFFFAOYSA-N gallic acid Chemical compound OC(=O)C1=CC(O)=C(O)C(O)=C1 LNTHITQWFMADLM-UHFFFAOYSA-N 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- 150000002391 heterocyclic compounds Chemical class 0.000 description 1
- 150000003840 hydrochlorides Chemical class 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 150000004679 hydroxides Chemical class 0.000 description 1
- 238000005286 illumination Methods 0.000 description 1
- 125000001841 imino group Chemical group [H]N=* 0.000 description 1
- 238000007654 immersion Methods 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- GPSDUZXPYCFOSQ-UHFFFAOYSA-M m-toluate Chemical compound CC1=CC=CC(C([O-])=O)=C1 GPSDUZXPYCFOSQ-UHFFFAOYSA-M 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 125000004184 methoxymethyl group Chemical group [H]C([H])([H])OC([H])([H])* 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 125000004170 methylsulfonyl group Chemical group [H]C([H])([H])S(*)(=O)=O 0.000 description 1
- 239000012452 mother liquor Substances 0.000 description 1
- SFDYIYJEECZQQX-UHFFFAOYSA-N n,n-di(propan-2-yl)sulfamoyl chloride Chemical compound CC(C)N(C(C)C)S(Cl)(=O)=O SFDYIYJEECZQQX-UHFFFAOYSA-N 0.000 description 1
- VMJGICXHKZERPD-UHFFFAOYSA-N n,n-dibutylsulfamoyl chloride Chemical compound CCCCN(S(Cl)(=O)=O)CCCC VMJGICXHKZERPD-UHFFFAOYSA-N 0.000 description 1
- JFCHSQDLLFJHOA-UHFFFAOYSA-N n,n-dimethylsulfamoyl chloride Chemical compound CN(C)S(Cl)(=O)=O JFCHSQDLLFJHOA-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 230000000269 nucleophilic effect Effects 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- UCUUFSAXZMGPGH-UHFFFAOYSA-N penta-1,4-dien-3-one Chemical compound C=CC(=O)C=C UCUUFSAXZMGPGH-UHFFFAOYSA-N 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- CMCWWLVWPDLCRM-UHFFFAOYSA-N phenidone Chemical compound N1C(=O)CCN1C1=CC=CC=C1 CMCWWLVWPDLCRM-UHFFFAOYSA-N 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- 125000003170 phenylsulfonyl group Chemical group C1(=CC=CC=C1)S(=O)(=O)* 0.000 description 1
- 150000004714 phosphonium salts Chemical class 0.000 description 1
- 239000001007 phthalocyanine dye Substances 0.000 description 1
- 235000021110 pickles Nutrition 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920000139 polyethylene terephthalate Polymers 0.000 description 1
- 239000005020 polyethylene terephthalate Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000006239 protecting group Chemical group 0.000 description 1
- 229940079877 pyrogallol Drugs 0.000 description 1
- 125000001453 quaternary ammonium group Chemical group 0.000 description 1
- 238000006479 redox reaction Methods 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000027756 respiratory electron transport chain Effects 0.000 description 1
- 238000009666 routine test Methods 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical class C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Chemical class 0.000 description 1
- 238000007127 saponification reaction Methods 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- IZXSLAZMYLIILP-ODZAUARKSA-M silver (Z)-4-hydroxy-4-oxobut-2-enoate Chemical compound [Ag+].OC(=O)\C=C/C([O-])=O IZXSLAZMYLIILP-ODZAUARKSA-M 0.000 description 1
- NBYLLBXLDOPANK-UHFFFAOYSA-M silver 2-carboxyphenolate hydrate Chemical compound C1=CC=C(C(=C1)C(=O)O)[O-].O.[Ag+] NBYLLBXLDOPANK-UHFFFAOYSA-M 0.000 description 1
- CQLFBEKRDQMJLZ-UHFFFAOYSA-M silver acetate Chemical compound [Ag+].CC([O-])=O CQLFBEKRDQMJLZ-UHFFFAOYSA-M 0.000 description 1
- 229940071536 silver acetate Drugs 0.000 description 1
- AQRYNYUOKMNDDV-UHFFFAOYSA-M silver behenate Chemical compound [Ag+].CCCCCCCCCCCCCCCCCCCCCC([O-])=O AQRYNYUOKMNDDV-UHFFFAOYSA-M 0.000 description 1
- ADZWSOLPGZMUMY-UHFFFAOYSA-M silver bromide Chemical compound [Ag]Br ADZWSOLPGZMUMY-UHFFFAOYSA-M 0.000 description 1
- 229940045105 silver iodide Drugs 0.000 description 1
- HKZLPVFGJNLROG-UHFFFAOYSA-M silver monochloride Chemical compound [Cl-].[Ag+] HKZLPVFGJNLROG-UHFFFAOYSA-M 0.000 description 1
- YRSQDSCQMOUOKO-KVVVOXFISA-M silver;(z)-octadec-9-enoate Chemical compound [Ag+].CCCCCCCC\C=C/CCCCCCCC([O-])=O YRSQDSCQMOUOKO-KVVVOXFISA-M 0.000 description 1
- RUVFQTANUKYORF-UHFFFAOYSA-M silver;2,4-dichlorobenzoate Chemical compound [Ag+].[O-]C(=O)C1=CC=C(Cl)C=C1Cl RUVFQTANUKYORF-UHFFFAOYSA-M 0.000 description 1
- OEVSPXPUUSCCIH-UHFFFAOYSA-M silver;2-acetamidobenzoate Chemical compound [Ag+].CC(=O)NC1=CC=CC=C1C([O-])=O OEVSPXPUUSCCIH-UHFFFAOYSA-M 0.000 description 1
- JRTHUBNDKBQVKY-UHFFFAOYSA-M silver;2-methylbenzoate Chemical compound [Ag+].CC1=CC=CC=C1C([O-])=O JRTHUBNDKBQVKY-UHFFFAOYSA-M 0.000 description 1
- MCKXPYWOIGMEIZ-UHFFFAOYSA-M silver;2h-benzotriazole-4-carboxylate Chemical compound [Ag+].[O-]C(=O)C1=CC=CC2=NNN=C12 MCKXPYWOIGMEIZ-UHFFFAOYSA-M 0.000 description 1
- OXOZKDHFGLELEO-UHFFFAOYSA-M silver;3-carboxy-5-hydroxyphenolate Chemical compound [Ag+].OC1=CC(O)=CC(C([O-])=O)=C1 OXOZKDHFGLELEO-UHFFFAOYSA-M 0.000 description 1
- UCLXRBMHJWLGSO-UHFFFAOYSA-M silver;4-methylbenzoate Chemical compound [Ag+].CC1=CC=C(C([O-])=O)C=C1 UCLXRBMHJWLGSO-UHFFFAOYSA-M 0.000 description 1
- CLDWGXZGFUNWKB-UHFFFAOYSA-M silver;benzoate Chemical group [Ag+].[O-]C(=O)C1=CC=CC=C1 CLDWGXZGFUNWKB-UHFFFAOYSA-M 0.000 description 1
- JKOCEVIXVMBKJA-UHFFFAOYSA-M silver;butanoate Chemical compound [Ag+].CCCC([O-])=O JKOCEVIXVMBKJA-UHFFFAOYSA-M 0.000 description 1
- OIZSSBDNMBMYFL-UHFFFAOYSA-M silver;decanoate Chemical compound [Ag+].CCCCCCCCCC([O-])=O OIZSSBDNMBMYFL-UHFFFAOYSA-M 0.000 description 1
- MNMYRUHURLPFQW-UHFFFAOYSA-M silver;dodecanoate Chemical compound [Ag+].CCCCCCCCCCCC([O-])=O MNMYRUHURLPFQW-UHFFFAOYSA-M 0.000 description 1
- GXBIBRDOPVAJRX-UHFFFAOYSA-M silver;furan-2-carboxylate Chemical compound [Ag+].[O-]C(=O)C1=CC=CO1 GXBIBRDOPVAJRX-UHFFFAOYSA-M 0.000 description 1
- ORYURPRSXLUCSS-UHFFFAOYSA-M silver;octadecanoate Chemical compound [Ag+].CCCCCCCCCCCCCCCCCC([O-])=O ORYURPRSXLUCSS-UHFFFAOYSA-M 0.000 description 1
- OHGHHPYRRURLHR-UHFFFAOYSA-M silver;tetradecanoate Chemical compound [Ag+].CCCCCCCCCCCCCC([O-])=O OHGHHPYRRURLHR-UHFFFAOYSA-M 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 235000010265 sodium sulphite Nutrition 0.000 description 1
- MWASJOFAOJVIGL-UHFFFAOYSA-M sodium;2h-benzotriazole-4-carboxylate Chemical compound [Na+].[O-]C(=O)C1=CC=CC2=C1N=NN2 MWASJOFAOJVIGL-UHFFFAOYSA-M 0.000 description 1
- 230000003381 solubilizing effect Effects 0.000 description 1
- IIACRCGMVDHOTQ-UHFFFAOYSA-N sulfamic acid group Chemical class S(N)(O)(=O)=O IIACRCGMVDHOTQ-UHFFFAOYSA-N 0.000 description 1
- NVBFHJWHLNUMCV-UHFFFAOYSA-N sulfamide Chemical class NS(N)(=O)=O NVBFHJWHLNUMCV-UHFFFAOYSA-N 0.000 description 1
- 125000000565 sulfonamide group Chemical group 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- YBBRCQOCSYXUOC-UHFFFAOYSA-N sulfuryl dichloride Chemical compound ClS(Cl)(=O)=O YBBRCQOCSYXUOC-UHFFFAOYSA-N 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 125000000101 thioether group Chemical group 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- AAAQKTZKLRYKHR-UHFFFAOYSA-N triphenylmethane Chemical compound C1=CC=CC=C1C(C=1C=CC=CC=1)C1=CC=CC=C1 AAAQKTZKLRYKHR-UHFFFAOYSA-N 0.000 description 1
- 239000003021 water soluble solvent Substances 0.000 description 1
Classifications
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03C—PHOTOSENSITIVE MATERIALS FOR PHOTOGRAPHIC PURPOSES; PHOTOGRAPHIC PROCESSES, e.g. CINE, X-RAY, COLOUR, STEREO-PHOTOGRAPHIC PROCESSES; AUXILIARY PROCESSES IN PHOTOGRAPHY
- G03C8/00—Diffusion transfer processes or agents therefor; Photosensitive materials for such processes
- G03C8/40—Development by heat ; Photo-thermographic processes
- G03C8/4013—Development by heat ; Photo-thermographic processes using photothermographic silver salt systems, e.g. dry silver
- G03C8/408—Additives or processing agents not provided for in groups G03C8/402 - G03C8/4046
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03C—PHOTOSENSITIVE MATERIALS FOR PHOTOGRAPHIC PURPOSES; PHOTOGRAPHIC PROCESSES, e.g. CINE, X-RAY, COLOUR, STEREO-PHOTOGRAPHIC PROCESSES; AUXILIARY PROCESSES IN PHOTOGRAPHY
- G03C8/00—Diffusion transfer processes or agents therefor; Photosensitive materials for such processes
- G03C8/24—Photosensitive materials characterised by the image-receiving section
- G03C8/246—Non-macromolecular agents inhibiting image regression or formation of ghost images
Definitions
- the invention relates to a heat development process in which an imagewise exposed color photographic recording material which contains a binder layer with silver halide and at least one coloring compound on a common layer support in contact with an image receiving layer which is an integral part of the recording material or can be arranged on a separate layer support is subjected to the development of a heat treatment, at least one so-called thermal development and diffusion promoting agent being present.
- color-imparting compounds are those which can be embedded in the layer of a photographic recording material in a non-diffusing form and which, as a result of the development, can release a diffusible dye (color releaser).
- a recording material having a layer containing a combination of silver halide, silver benzotriazole, a color releasing agent and guanidine trichloroacetate is exposed imagewise and then subjected to a heat treatment in contact with an image-receiving sheet, whereby the image-released dye is transferred to the image-receiving sheet .
- the silver halide in each of these combinations being sensitive to a different spectral range of the light and, according to its spectral sensitivity, containing a color releaser which releases a dye of a different color, usually a color that is complementary is the color of the light for which the silver halide in question has a predominant sensitivity.
- Such assignments can be arranged one above the other in different layers.
- melt-formers so-called melt-formers or "thermal solvents", as described, for example, in RESEARCH DISCLOSURE publications 15027 (October 1976), 15,108 (November. 1976), 17 029 (June 1978) or in DE-A-33 39 810, EP-AO 119 615 and EP-AO 112 512.
- the compounds mentioned are generally solid under normal conditions, but are in molten form at the higher temperature of the heat treatment and, owing to their dipolar character, form a medium which promotes the development processes.
- Most of the thermal solvents mentioned are compounds with a protic character.
- the heat treatment is dry, i.e. can be carried out without moistening the recording materials or the image-receiving sheets, and in this case considerable results are achieved, it is desirable to further improve the process and in this way to shorten the required treatment time and / or to achieve higher color transfer densities.
- the invention relates to a heat development process for producing colored images, in which an imagewise exposed color photographic recording material with at least one on a layer support arranged binder layer, which contains light-sensitive silver halide, optionally in combination with a substantially non-light-sensitive silver salt, and at least one non-diffusing coloring compound which, as a result of the development, is able to release a diffusible dye, is developed by heat treatment in the presence of a thermal development and diffusion promoting agent , wherein the dye released imagewise from the non-diffusing coloring compound is transferred into an image-receiving layer which can be colored by diffusible dyes, characterized in that the thermal development and diffusion promoting agent corresponds to the following formula I: in what mean X -SO2- or -CO-; R1 - R4 alkyl, cycloalkyl, aralkyl or aryl; R5, R6 acyl or a radical as indicated for R1 - R4; wherein R1 together with R5, R2 together with R6,
- Another object of the invention is a color photographic recording material which is suitable for the heat development process and contains at least one thermal development and diffusion promoting agent of the type specified in at least one of its layers.
- R1 to R6 can be the same or different. They are preferably identical in pairs (R1, R2; R3, R4; R5, R6).
- An alkyl group represented by R1 to R6 can be unbranched or branched and optionally substituted and preferably contain 1 to 4 carbon atoms. Examples include methyl, ethyl, propyl, isopropyl, n-butyl, s-butyl, methoxymethyl, cyclohexylmethyl, hydroxyethyl.
- the alkyl groups, in particular those represented by R3 and R, can also individually contain up to 18 carbon atoms.
- a cycloalkyl group represented by R1 to R6 is, for example, cyclohexyl.
- An aralkyl group represented by R1 to R6 is, for example, benzyl.
- An aryl group represented by R1 to R6 is, for example, phenyl, tolyl, methoxyphenyl, N-methyl-N-acetylamino-phenyl.
- An acyl group represented by R5 or R6 can be derived from aliphatic or aromatic carboxylic or sulfonic acids or also from carbamic or sulfamic acids. Acetyl, methylsulfonyl, phenylsulfonyl, p-methoxyphenylsulfonyl and p-nitrophenylsulfonyl are examples of this.
- Heterocyclic rings which are formed by R1 and R5, R2 and R6, R3 and R4 and / or R1 and R2 are preferably 5- or 6-membered and have at least one nitrogen atom and optionally further heteroatoms.
- a heterocyclic ring formed by R1 together with R2 has at least 2 nitrogen atoms. Examples of such heterocyclic rings are pyrrolidine, piperidine, morpholine, imidazolidine and hexahydropyrimidine.
- the thermal development and diffusion promoting agents according to the invention apparently act under the conditions of heat development as a solvating medium for the reactions taking place such as development of the silver halide or the organic silver salt under the influence of a reducing agent, release of the diffusible Dyes from the coloring compounds and diffusion of the dyes into an image-receiving layer.
- TEDM thermal development and diffusion promoting agents
- Appropriate variation of the substituents R1 to R6, in particular the substituents R1 and R2 allows the solvent properties of the TEDM according to the invention to be influenced in a targeted manner in the direction of a more hydrophilic or hydrophobic character.
- thermal development and diffusion promoting agents (TEDM-) according to the invention are listed below:
- N, N-di-n-butyl sulfamic acid chloride (compound A) 129 g (1.0 mol) of di-n-butylamine were slowly added dropwise to 135 g (1.0 mol) of sulfuryl chloride with ice cooling and vigorous stirring within 5 h. The mixture was then stirred for a further 5 h at 90 ° C., mixed with ether after cooling and stirring, and the precipitate obtained was filtered off with suction. The ether phase was washed once with water, once with concentrated sodium hydrogen carbonate solution and again with water, dried over sodium sulfate and concentrated on a rotary evaporator. The oil obtained was distilled in vacuo and gave 60 g of compound A (bp 1mm 110-112 ° C).
- Thermal solvents which are solid at normal temperature
- Water-insoluble TEDM can be introduced in dispersed form.
- the amount used can be varied within a wide range; This depends, among other things, on whether the compounds are introduced distributed over several or all layers of the recording material according to the invention, or whether they are used in a concentrated manner only in a specific layer.
- the amount to be used per square meter also depends, of course, on the amount of binder used. The skilled worker can easily determine the appropriate concentration using simple routine tests.
- the concentration used can be between 2 and 100% by weight, based on the binder, but preferably in the range between 20 and 50% by weight. However, overdosing on TEDM usually leads to high color fog (Dmin).
- a color photographic recording material suitable for carrying out the heat development process according to the invention contains, on a dimensionally stable support, at least one binder layer in which a light-sensitive silver halide, optionally in combination with an essentially non-light-sensitive silver salt and a non-diffusing coloring compound, which contains a diffusible dye due to heat development can deliver, and the color photographic recording material further contains in one of its layers one or more of the thermal development and diffusion promoting agents (TEDM) according to the invention.
- TDM thermal development and diffusion promoting agents
- An essential component of the heat-developable recording material of the present invention is the silver halide, which consists of silver chloride, silver bromide, silver iodide or mixtures thereof and can have a particle size between 0.01 and 2.0 ⁇ m, preferably between 0.1 and 1.0 ⁇ m. It can be in the form of an unsensitized silver halide or it can also be chemically and / or spectrally sensitized by suitable additives.
- the amount of light-sensitive silver halide in the respective layer can be between 0.01 and 2.0 g per m 2, the actual amount of silver halide used due to its catalytic function (as exposed silver halide) in some embodiments mainly in the lower part of the range given emotional.
- the essentially non-light-sensitive silver salt can be, for example, a silver salt which is comparatively stable to light, e.g. trade an organic silver salt.
- Suitable examples include the silver salts of aliphatic or aromatic carboxylic acids and the silver salts of nitrogen-containing heterocycles; also silver salts of organic mercapto compounds.
- Preferred examples of silver salts of aliphatic carboxylic acids are silver behenate, silver stearate, silver oleate, silver laurate, silver caprate, silver myristate, Sil berpalmitate, silver maleate, silver fumarate, silver tartrate, silver furoate, silver linolate, silver adipate, silver sebacate, silver succinate, silver acetate or silver butyrate.
- the carboxylic acids on which these silver salts are based can be substituted, for example, by halogen atoms, hydroxyl groups or thioether groups.
- silver salts of aromatic carboxylic acids and other compounds containing carboxyl groups include silver benzoate, silver 3,5-dihydroxybenzoate, silver o-methylbenzoate, silver m-methylbenzoate, silver p-methylbenzoate, silver 2,4-dichlorobenzoate, silver acetamidobenzoate, silver gallate , Silver tannate, silver phthalate, silver terephthalate, silver salicylate, silver phenylacetate, silver pyromellitate, silver salts of 3-carboxymethyl-4-methyl-4-thiazolin-2-thione or similar heterocyclic compounds.
- Silver salts of organic mercaptans e.g.
- the silver salts of 3-mercapto-4-phenyl-1,2,4-trizole, 2-mercaptobenzimidazole, 2-mercaptobenzothiazole, 2-mercaptobenzoxazole, 2-mercaptooxadiazole, mercaptotriazine, thioglycolic acid furthermore the silver salts of dithiocarboxylic acids, e.g. the silver salt of dithioacetic acid.
- the silver salts of compounds having an imino group are also suitable.
- Preferred examples include the silver salts of benzotriazole and its derivatives, for example silver salts of alkyl and / or halogen-substituted benzotriazoles, such as the silver salts of methylbenzotriazole, 5-chlorobenzotriazole, as well as the silver salts of 1,2,4-triazole, 1-H-tetrazole, carbazole, saccharin and silver salts of imidazole and its derivatives.
- the application amount of essentially non-photosensitive silver salt according to the present invention in the respective layer is between 0.05 and 5 g per m2.
- the substantially non-light-sensitive silver salt and the light-sensitive silver halide can be present side by side as separate particles or in a combined form, which can be produced, for example, by treating a substantially non-light-sensitive silver salt in the presence of halide ions, the surface of which Particles of the essentially non-photosensitive silver salt are formed by double conversion (conversion) of photosensitive centers from photosensitive silver halide.
- halide ions the surface of which Particles of the essentially non-photosensitive silver salt are formed by double conversion (conversion) of photosensitive centers from photosensitive silver halide.
- the essentially non-light-sensitive silver salt serves as a reservoir for metal ions, which are reduced to elemental silver when heat is developed in the presence of a reducing agent under the catalytic influence of the imagewise exposed silver halide and thereby serve as an oxidizing agent (for the reducing agent present).
- Another essential constituent of the recording material according to the invention is a non-diffusing coloring compound which, as a result of a redox reaction taking place during development, is able to release a diffusible dye and which is referred to below as a color releasing agent.
- the dye releasers used according to the invention can be a variety of connection types, all of which are distinguished by a link which is redox-dependent in terms of their bond strength and which links a dye residue to a carrier residue containing a ballast residue.
- Redox-active color releasers of the formula have proven to be particularly advantageous BALLAST - REDOX - DYE, in what mean BALLAST a ballast remnant REDOX is a redox-active group, i.e. a group that can be oxidized or reduced under the conditions of alkaline development and, depending on whether it is in the oxidized or in the reduced state, is subject to different degrees to an elimination reaction, a nucleophilic displacement reaction, a hydrolysis or another cleavage reaction with the result that the rest of DYE is split off, and DYE the rest of a diffusible dye, for example a yellow, purple or cyan dye, or the rest of a dye precursor.
- a ballast remnant REDOX is a redox-active group, i.e. a group that can be oxidized or reduced under the conditions of alkaline development and, depending on whether it is in the oxidized or in the reduced state, is subject to different degrees to an elimination reaction, a nucleophilic
- Such residues are to be regarded as ballast residues which make it possible to store the color releasers according to the invention in a diffusion-resistant manner in the hydrophilic colloids usually used in photographic materials.
- Organic radicals which generally contain straight-chain or branched aliphatic groups with generally 8 to 20 C atoms and optionally also carbocyclic or heterocyclic optionally aromatic groups are preferably suitable for this purpose. With the rest of the molecule, these radicals are either directly or indirectly, for example connected via one of the following groups: -NHCO-, -NHSO2-, -NR-, where R is hydrogen or alkyl, -O- or -S-.
- ballast residue also contain water-solubilizing groups, such as sulfo groups or carboxyl groups, which may also be in anionic form. Since the diffusion properties depend on the molecular size of the total compound used, it is sufficient in certain cases, for example if the total molecule used is large enough, to use shorter-chain residues as ballast residues.
- Redox-active carrier residues of the BALLAST-REDOX structure and corresponding color releasers are known in a wide variety of embodiments. A detailed description can be omitted here with regard to the overview article in the app. Chem. Int. Ed. Engl. 22 (1983) 191-209.
- the groups enclosed in brackets are functional groups of the dye residue and are separated together with this from the remaining part of the carrier residue.
- the functional group can are a substituent which can have a direct influence on the absorption and, if appropriate, complex formation properties of the released dye.
- the functional group can also be separated from the chromophore of the dye by an intermediate link or a link.
- the functional group together with the intermediate member may also be of importance for the diffusion and pickling behavior of the released dye.
- Suitable intermediate members are, for example, alkylene or arylene groups.
- the residues of dyes of all classes of dyes are suitable as dye residues insofar as they are sufficiently diffusible to diffuse from the light-sensitive layer of the light-sensitive material into an image-receiving layer.
- the dye residues can be provided with one or more alkali-solubilizing groups.
- Suitable alkali-solubilizing groups include carboxyl groups, sulfo groups, sulfonamide groups and aromatic hydroxyl groups.
- Such alkali-solubilizing groups can already be pre-formed in the dye releasers or can only result from the cleavage of the dye residue from the carrier residue containing ballast groups.
- Suitable dyes include: azo dyes, azomethine dyes, anthraquinone dyes, phthalocyanine dyes, indigoid dyes, triphenylmethane dyes, including those dyes that are complexed or complexable with metal ions.
- the residues of dye precursors are to be understood as the residues of those compounds which, in the course of photographic processing, in particular under the conditions of heat development, either by oxidation, by coupling, by complex formation or by exposure of an auxochromic group in a chromophoric system, for example by saponification, can be converted into dyes.
- Dye precursors in this sense can be leuco dyes, couplers or dyes that are converted into other dyes during processing. Unless a distinction is made between dye residues and the residues of dye precursors, the latter should also be understood below as dye residues.
- Suitable color releasing agents are described, for example, in: US-A-3,227,550, US-A-3,443,939, USA-A-3,443,940, DE-A-19 30 215, DE-A-22 42 762, DE-A- 24 02 900, DE- A- 24 06 664, DE-A- 25 05 248, DE-A- 25 43 902, DE-A- 26 13 005, DE-A- 26 45 656, DE-A- 28 09 716, DE-A- 28 23 159, BE-A- 861 241, EP-A- 0 004 399, EP-A- 0 004 400, DE-A- 30 08 588, DE-A- 30 14 669, GB-A- 80 12 242 .
- the color releasers can be used as oxidizable or couplable color releasers, in other than reducible color releasers.
- the dye is released from the oxidized or from the reduced form of the color releasing agent, negative or positive illumination is obtained from the original when conventional negative-working silver halide emulsions are used. You can therefore create positive or negative images by selecting suitable color releasing systems.
- Oxidizable color releasers which are particularly suitable for the heat-developable recording materials according to the invention are, for example, in DE-A-22 42 762, DE-A-25 05 248, DE-A-26 13 005, DE-A-26 45 656 and GB-A-80 12 242.
- the paint releaser can be oxidized, then it is itself a reducing agent which, directly or indirectly, with the participation of electron transfer agents (electron transfer agent, ETA) through the imagewise exposed silver halide or through the essentially non-photosensitive silver salt under the catalytic action of the imagewise exposed Silver halide is oxidized.
- electron transfer agent electro transfer agent
- the paint releaser is reducible, then it is expediently used in combination with a reducing agent present in a limited amount, a so-called ten electron donor compound or an electron donor precursor compound, which in this case is contained in the same binder layer in addition to the color releaser, the light-sensitive silver halide and optionally the substantially non-light-sensitive silver salt.
- a reducing agent present in a limited amount
- a so-called ten electron donor compound or an electron donor precursor compound which in this case is contained in the same binder layer in addition to the color releaser, the light-sensitive silver halide and optionally the substantially non-light-sensitive silver salt.
- electron transfer agents can also prove to be advantageous in the case of the use of reducible color releasers in combination with electron donor compounds.
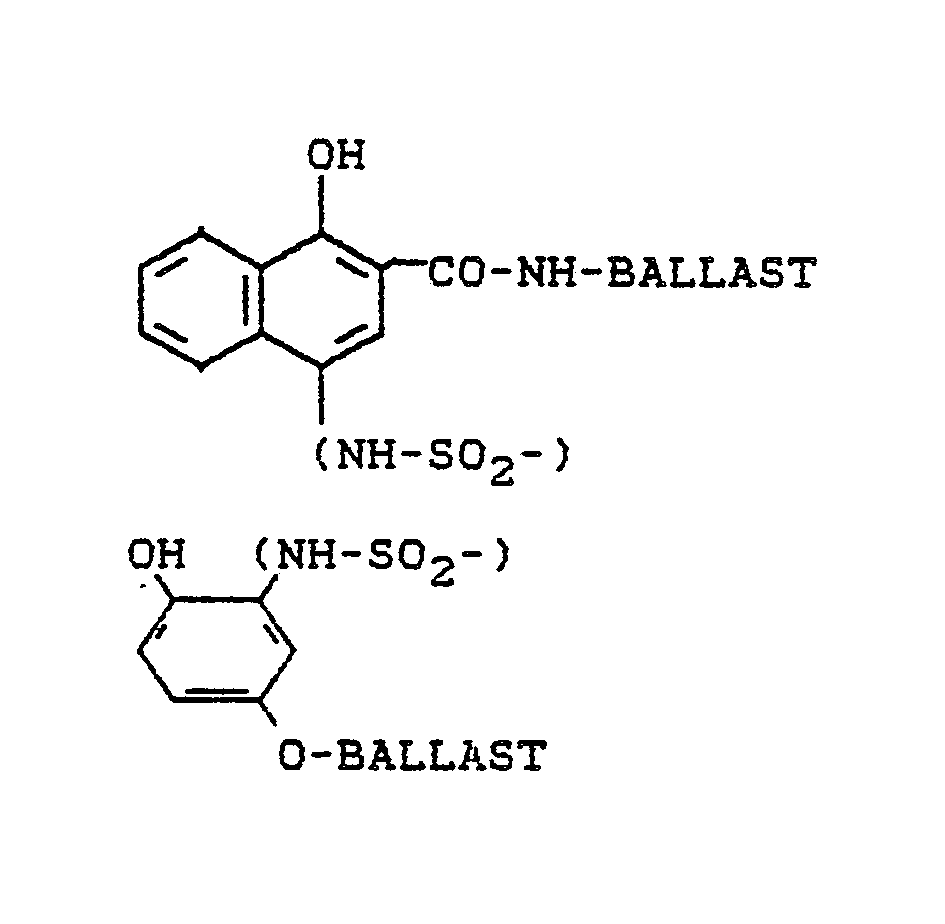
- a recording material according to the invention which contains reducible color releasers with a carrier residue of the following formula is suitable, for example, for producing positive color images of positive originals (original) when using negative working silver halide emulsions: in what mean R1 ⁇ alkyl or aryl; R2 ⁇ is alkyl, aryl or a group which together with R3 ⁇ completes a fused ring; R3 ⁇ hydrogen, alkyl, aryl, hydroxyl, halogen such as chlorine or bromine, amino, alkylamino, dialkylamino including cyclic amino groups (such as piperidino, morpholino), acylamino, alkylthio, alkoxy, aroxy, sulfo, or a group which together with R2 ⁇ fused one Ring completed; R4 ⁇ alkyl; R5 ⁇ alkyl or preferably hydrogen; and wherein at least one of the radicals R1 ⁇ to R4 ⁇ contains a ballast radical.
- reducible dye releasers and others which are also suitable in the context of the present invention are described, for example, in DE-A-28 09 716, EP-A-O 004 399, DE-A-30 08 588, DE-A-30 14 669.
- the electron donor compound used in combination with a reducible color releasing agent also serves as a reducing agent for the silver halide, the essentially non-photosensitive silver salt and the color releasing agent. Because the essentially non-light-sensitive silver salt and the color releaser compete with each other to a certain extent in the oxidation of the electron donor compound, but the latter is in any case superior to the latter in the presence of exposed silver halide, the silver halide present becomes determinant for that in accordance with a previous imagewise exposure Image areas, within which the color releaser is converted into its reduced form by the electron donor compound.
- the electron donor compound which is present in a limited amount, under the conditions of development, in the present case when the imagewise exposed color photographic material is heated in accordance with the extent of the exposure under the catalytic effect of the latent image nuclei produced by exposure in the silver halide by the essentially non-light-sensitive silver salt and that photosensitive silver halide oxidizes and is therefore no longer available for reaction with the color releaser. This creates an image-like distribution of unused electron donor compound.
- electron donor compounds are known from DE-A-29 47 425, DE-A-30 06 268, DE-A-31 30 842, DE-A-31 44 037, DE-A-32 17 877, EP-A- 0 124 915 and Research Disclosure 24 305 (July 1984). It has been shown that the electron donor compounds mentioned also meet the requirements placed on them under the conditions of heat development and are therefore also suitable as electron donor compounds in the context of the present invention.
- Electron donor compounds which are formed from the corresponding electron donor precursor compounds only under the conditions of heat development in the layer, i.e. Electron donor compounds that are only in a masked form in the recording material before development, in which they are practically ineffective. Under the conditions of heat development, the electron donor compounds, which are initially ineffective, are then converted into their effective form, for example by hydrolytically cleaving off certain protective groups.
- the electron donor precursor compounds mentioned are also understood as electron donor compounds.
- the above-mentioned essential constituents of the recording material used in the process according to the invention namely the light-sensitive silver halide, the possibly non-light-sensitive reducible silver salt and the color releaser, optionally in combination with an electron donor compound, are dispersed next to one another in a binder.
- a binder can be hydrophobic as well as hydrophilic binders, but the latter are preferred and gelatin is preferably used, but it can also be replaced in whole or in part by other natural or synthetic binders.
- polyurethanes optionally in a mixture with gelatin, have proven to be suitable binders, as described, for example, in DE-A-35 30 156.
- the light-sensitive binder layer contains one or more color releasers associated with the light-sensitive silver halide and optionally the non-light-sensitive silver salt, from which dyes of a specific color are released.
- the overall resulting color can be obtained by mixing several dyes.
- the color photographic recording material used in the method according to the invention contains several, ie generally three, assignments of color releasers and in each case differently spectrally sensitized silver halide, preferably the absorption range of the dye released from the color releaser with the range of the spectral sensitivity of the assigned Silver halide essentially coincides.
- the different assignments of color releaser and assigned silver halide can be accommodated in different binder layers of the color photographic recording material, preferably between these different binder layers there are separating layers made of a water-permeable binder, for example gelatin, which essentially have the function of separating the different assignments from one another and to counteract color distortion in this way.
- separating layers made of a water-permeable binder, for example gelatin, which essentially have the function of separating the different assignments from one another and to counteract color distortion in this way.
- the color photographic recording material includes, for example, a light-sensitive binder layer in which the silver halide contained therein is predominantly red-sensitive due to spectral sensitization, a further light-sensitive binder layer in which the silver halide contained therein is predominantly green-sensitive due to spectral sensitization, and a third light-sensitive binder layer in which the contained therein Silver halide is predominantly blue-sensitive due to its inherent sensitivity or due to spectral sensitization.
- the electron donor compounds optionally contained in the three light-sensitive layers can be the same or different.
- a complex coacervate is understood to mean a form of dispersion in which a mixture of the essential constituents is enclosed in a common covering made of a hardened binder. Such dispersions are also called packet emulsions. They are obtained through complex coacervation.
- complex coacervation means the occurrence of two phases when mixing an aqueous solution of a polycationic colloid and a polyanionic colloid, a concentrated colloid phase (hereinafter referred to as a complex coacervate) and a dilute colloid phase (hereinafter referred to as an equilibrium solution) ) are formed due to an electrical interaction.
- the complex coacervate is separated from the equilibrium solution in the form of droplets and appears as a white turbidity.
- a solid such as silver halide or fine oil droplets
- a dispersion of coacervate particles in which the solid (in the present case the light-sensitive silver halide and optionally the essentially non-light-sensitive silver salt) and oily droplets of a solution of the organic constituents (in the present case the color releasing agent and optionally further auxiliaries) are included are. It is then hardened with a hardening agent so that the original shape of the particles is not destroyed in the following steps for producing the photographic recording material, such as producing the casting solution and coating.
- the dispersion is expediently cooled to a temperature of 25 ° C. or below, preferably 10 ° C. or below, before curing, whereby a good quality packet emulsion is obtained.
- packet emulsions makes it possible to combine several emulsion components of different spectral sensitivity, including the relevant color releasers, in a single binder layer, without losing the spectral assignment and thereby causing color falsification. This is possible because the degree of exposure of a particular silver halide particle becomes almost exclusively the determining factor for the degree of dye release from the color releaser which is in the same coacervate particle (package) as the silver halide.
- packet emulsions thus enables the accommodation of a blue-sensitive, a green-sensitive and a red-sensitive silver halide emulsion with any additional, essentially non-light-sensitive silver salt and spectrally assigned color separators in the same binder layer, without fear of serious color falsification.
- the color photographic recording material used in the method according to the invention can contain further constituents and auxiliary substances which are used, for example, for carrying out the heat treatment and the process taking place here Color transfer are beneficial.
- These further constituents or auxiliary substances can be contained in a light-sensitive layer or in a non-sensitive layer.
- auxiliary substances are, for example, auxiliary developers.
- suitable auxiliary developers include hydroquinone, pyrocatechol, pyrogallol, hydroxylamine, ascorbic acid, 1-phenyl-3-pyrazolidone and their derivatives.
- auxiliary developers have a catalytic function, it is not necessary for them to be present in stoichiometric amounts. In general, it is sufficient if they are present in the layer in amounts of up to 1/2 mol per mol of color releaser. Familiarization with the The layer can be made, for example, from solutions in water-soluble solvents or in the form of aqueous dispersions obtained using oil formers.
- auxiliaries are, for example, basic substances or compounds which are able to provide basic substances under the influence of the heat treatment.
- Sodium hydroxide, potassium hydroxide, calcium hydroxide, sodium carbonate, sodium acetate and organic bases, in particular amines such as alkylamines, pyrrolidine, piperidine, amidine, guanidine and their salts, in particular salts with aliphatic carboxylic acids, are to be mentioned here, for example.
- a suitable medium is created during the heat treatment in the light-sensitive layer and the adjacent layers in order to ensure the release of the diffusible dyes from the dye releasers and their transfer to the image-receiving sheet.
- auxiliaries are, for example, compounds which are able to release water under the action of heat.
- inorganic salts containing water of crystallization are suitable, for example Na2SO4.1OH2O, NH4Fe (SO4) 2.12H2O, and also compounds of the sodium benzotriazolate type which crystallize as a complex with various amounts of water (up to 24 mol H2O) and which are described in US Pat. A-4 418 139.
- the water released during heating favors the development and diffusion processes required for image formation.
- TEDM further essential auxiliary substances
- these compounds do not necessarily have to be present in the same layer which also contains the light-sensitive silver halide and the color splitter. Rather, it is sufficient if any binder layer which is in contact with the light-sensitive layers during the heat treatment contains the TEDM mentioned in the required amount.
- the TEDM forms a suitable solubilizing medium that is conducive to the development and color diffusion processes in the layers that are involved in the development and color diffusion processes.
- the TEDM according to the invention can thus be contained in a light-sensitive layer which contains silver halide and a coloring compound, or in a non-light-sensitive binder layer or in several of the layers mentioned.
- the TEDM can also be contained in an image-receiving layer of a separate image-receiving material, provided contact is only made with the light-sensitive layers of the heat-developable photographic recording material during the heat treatment.
- the TEDM according to the invention can also be contained in dispersed form in an auxiliary sheet which is brought into contact with the light-sensitive recording material and is subjected to a heat treatment together with it.
- a corresponding method is described for example in DE-A-35 23 361.
- the TEDM according to the invention can also be used in combination with one or more of the so-called thermal solvents of the prior art, such as those described in DE-A-33 39 810, EP-A-0 119, without going beyond the scope of the invention 615 and EP-A-0 122 512.
- the development of the imagewise exposed color photographic recording material comprises the partial steps of silver halide development, generation of an imagewise distribution of diffusible dyes and diffusion transfer of this imagewise distribution into the image receiving layer. It is initiated by subjecting the exposed recording material to a heat treatment in which the photosensitive binder layer is brought to an elevated temperature, for example in the range from 80 to 250 ° C., for a period of about 0.5 to 300 s.
- a heat treatment in which the photosensitive binder layer is brought to an elevated temperature, for example in the range from 80 to 250 ° C., for a period of about 0.5 to 300 s.
- the Color-releasing, imagewise diffusible dyes are released and transferred to an image-receiving layer, which is either an integral part of the color photographic recording material according to the invention or is in contact with it at least during the development time.
- Image-wise silver development, dye release and color transfer take place synchronously in a one-step development process.
- the color image formation with the color photographic recording material according to the invention can also be carried out in a two-step development process, silver halide development and dye release taking place in a first step, followed in a second step by color image transfer from the light-sensitive part to an image receiving part brought into contact with it, e.g. by heating to a temperature between 50 and 150 ° C., preferably to 70 to 90 ° C., in which case diffusion aids (solvents) can still be applied externally before the photosensitive part and the image receiving part are laminated.
- diffusion aids solvents
- the image-receiving layer can accordingly be arranged on the same layer support as the light-sensitive element (single sheet material) or on a separate layer support (two-sheet material). It consists essentially of a binding agent, the mordant for the determination of the non-diffusing color cleavage released diffusible dyes contains. Long-chain quaternary ammonium or phosphonium compounds are preferably used as mordants for anionic dyes, for example those as described in US Pat. Nos. 3,271,147 and 3,271,148.
- certain metal salts and their hydroxides which form poorly soluble compounds with the acid dyes, can also be used.
- Polymeric mordants should also be mentioned here, such as those described in DE-A-23 15 304, DE-A-26 31 521 or DE-A-29 41 818.
- the dye mordants are dispersed in the mordant layer in one of the usual hydrophilic binders, e.g. in gelatin, polyvinylpyrrolidone, completely or partially hydrolyzed cellulose esters.
- some binders can also act as mordants, e.g.
- polymers of nitrogen-containing, optionally quaternary bases such as, for example, of N-methyl-4-vinylpyridine, 4-vinylpyridine, 1-vinylimidazole, as described, for example, in US Pat. No. 2,484,430.
- Further usable binding agents are, for example, guanylhydrazone derivatives of alkyl vinyl ketone polymers, such as described, for example, in US Pat. No. 2,882,156, or guanylhydrazone derivatives of acylstyrene polymers, as described, for example, in DE-A-20 09 498.
- other binders eg Add gelatin.
- the image-receiving layer also after completion Development remains in layer contact with the light-sensitive element, there is usually an alkali-permeable pigment-containing light-reflecting binder layer between them, which serves for the optical separation between negative and positive and as an aesthetically pleasing background for the positive color image.
- an alkali-permeable pigment-containing light-reflecting binder layer between them, which serves for the optical separation between negative and positive and as an aesthetically pleasing background for the positive color image.
- the image-receiving layer is arranged between the support and the photosensitive element and is separated from the latter by a pre-formed light-reflecting layer, either the support must be transparent so that the color transfer image produced can be viewed through it, or the photosensitive element together with the light-reflecting layer of the image-receiving layer are removed to expose the latter.
- the image-receiving layer can also be present as the uppermost layer in an integral color photographic recording material, in which case the exposure is expediently carried out through the transparent layer support.
- a light-sensitive element of a thermally developable photographic recording material according to the invention was produced in that the following layers were applied in succession to a transparent support made of polyethylene terephthalate 175 ⁇ m thick. The quantities given relate to 1m2.
- a layer consisting of 1 g guanidinium trichloroacetate, 0.03 g of wetting agent B, 0.24 g 4-methyl-4-hydroxymethylphenidone, 0.06 g sodium sulfite; 1.5 g of gelatin and 0.25 g or 0.5 g or 1.0 g of the compound TEDM-1 according to the invention.
- a hardening layer consisting of 0.5 g gelatin and 0.15 g hardening agent CAS Reg.-Nr. 65 411-60-1.
- the photosensitive element thus produced is referred to as material 1.
- Further materials 2 and 3 were produced, which differed from material 1 in that the compound TEDM-1 according to the invention was used in layer 2 in modified amounts, specifically Material 2 - 0.5 g Material 3 - 1.0 g
- Another material 4 was produced as a comparative material, which had the specified layers, but contained no TEDM in layer 2.
- An image-receiving element was produced in that the following layers were applied to a layer support made of paper laminated with polyethylene.
- the quantities given here also refer to 1 m2.
- a pickling layer consisting of 2 g of polyurethane pickle of 4,4'-diphenylmethane diisocyanate and N-ethyldiethanolamine, quaternized with epichlorohydrin (according to DE-A-26 31 521, preparation example 1), 0.035 g of wetting agent B and 2 g of gelatin.
- a hardening layer consisting of 0.8 g gelatin and 0.5 g of the hardening agent already mentioned.
- the photosensitive element materials 1-4
- processing was carried out in two steps.
- the photosensitive element was treated at 115 ° C. for 60 s. This was done with the help of a heating plate, the material being covered with another plate.
- the image-receiving element was laminated onto the already heat-treated, light-sensitive element after immersion in water, and the set thus formed was then treated under pressure analogously to the first process step for 2 min at 70 ° C. During this time the color transfer from the photosensitive element to the image receiving element took place. The two layer elements were then separated from one another. The image-receiving element showed a purple-colored negative image from the exposure original.
- Table 1 shows, when the compound TEDM-1 according to the invention is added, a clear increase in density can be observed in comparison to the layer structure without addition, without the minimum densities increasing in the same ratio.
Landscapes
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Non-Silver Salt Photosensitive Materials And Non-Silver Salt Photography (AREA)
- Thermal Transfer Or Thermal Recording In General (AREA)
- Plural Heterocyclic Compounds (AREA)
- Heat Sensitive Colour Forming Recording (AREA)
Abstract
Description
- Die Erfindung betrifft ein Wärmeentwicklungsverfahren, bei dem ein bildmäßig belichtetes farbfotografisches Aufzeichnungsmaterial, das auf einem gemeinsamen Schichtträger eine Bindemittelschicht mit Silberhalogenid und mindestens eine farbgebende Verbindung enthält, in Kontakt mit einer Bildempfangsschicht, die integraler Bestandteil des Aufzeichnungsmaterials ist oder auf einen separaten Schichtträger angeordnet sein kann, zur Entwicklung einer Wärmebehandlung unterworfen wird, wobei mindestens ein sogenanntes thermisches Entwicklungs- und Diffusionsförderungsmittel anwesend ist.
- Es ist bekannt, mittels geeigneter farbfotografischer Aufzeichnungsmaterialien farbige Bilder durch Wärmebehandlung herzustellen. Als farbgebende Verbindungen eignen sich hierbei in besonderem Maße solche, die in nicht-diffundierender Form in die Schicht eines fotografischen Aufzeichnungsmaterials eingelagert werden können und als Folge der Entwicklung einen diffusionsfähigen Farbstoff freizusetzen vermögen (Farbabspalter).
- Die besondere Eignung solcher Farbabspalter beruht auf dem Umstand, daß die bildmäßig freigesetzten Farbstoffe auf besondere Bildempfangsschichten übertragen werden können unter Bildung eines brillanten Farbbildes, das nicht von störendem Bildsilber oder Silberhalogenid überlagert ist und dementsprechend keiner Nachbehandlung bedarf. Durch Kombination des Wärmeentwicklungsverfahrens mit dem Farbdiffusionsverfahren ergibt sich somit ein vorteilhaftes Schnellverfahren zur Herstellung farbiger Bilder. Ein hierfür geeignetes Aufzeichnungsmaterial ist beispielsweise beschrieben in DE-A-32 15 485.
- Nach dieser Veröffentlichung wird ein Aufzeichnungsmaterial mit einer Schicht, die eine Kombination aus Silberhalogenid, Silberbenzotriazol, einem Farbabspalter und Guanidintrichloracetat (Basenspender) enthält, bildmäßig belichtet und anschließend in Kontakt mit einem Bildempfangsblatt einer Wärmebehandlung unterworfen, wobei der bildmäßig freigesetzte Farbstoff auf das Bildempfangsblatt übertragen wird. Für die Herstellung mehrfarbiger Bilder müssen mehrere solcher Kombinationen vorhanden sein, wobei das Silberhalogenid in jeder dieser Kombinationen für einen anderen Spektralbereich des Lichtes empfindlich ist und entsprechend seiner Spetralempfindlichkeit einen Farbabspalter zugeordnet enthält, der einen Farbstoff einer anderen Farbe freisetzt, meist einer Farbe, die komplementär ist zu der Farbe des Lichtes, für die das betreffende Silberhalogenid eine überwiegende Empfindlichkeit aufweist. Solche Zuordnungen können in verschiedenen Schichten übereinander angeordnet sein.
- Es ist bekannt das Wärmeentwicklungsverfahren in Gegenwart geeigneter Verbindungen, sogenannter Schmelzbildner ("melt-former") oder thermischer Lösungsmittel ("thermal solvent") durchzuführen, wie dies beispielsweise in den RESEARCH DISCLOSURE-Publikationen 15027 (Oktober 1976), 15 108 (November.1976), 17 029 (Juni 1978) oder in DE-A-33 39 810, EP-A-O 119 615 und EP-A-O 112 512 beschrieben ist. Die genannten Verbindungen sind im allgemeinen unter Normalbedingungen fest, liegen aber bei der höheren Temperatur der Wärmebehandlung in geschmolzener Form vor und bilden aufgrund ihres dipolaren Charakters ein die Entwicklungsvorgänge förderndes Medium. Überwiegend handelt es sich bei den genannten thermischen Lösungsmitteln um Verbindungen mit protischem Charakter. Obwohl bei Verwendung der genannten thermischen Lösungsmittel die Wärmebehandlung trocken, d.h. ohne Befeuchtung der Aufzeichnungsmaterialien oder der Bildempfangsblätter, durchgeführt werden kann und hierbei beachtliche Ergebnisse erzielt werden, ist es erwünscht das Verfahren weiter zu verbessern und auf diese Weise die erforderliche Behandlungszeit zu verkürzen und/oder zu höheren Farbübertragsdichten zu gelangen.
- Gegenstand der Erfindung ist ein Wärmeentwicklungsverfahren zur Herstellung farbiger Bilder, bei dem ein bildmäßig belichtetes farbfotografisches Aufzeichnungsmaterial mit mindestens einer auf einem Schichtträger angeordneten Bindemittelschicht, die lichtempfindliches Silberhalogenid, gegebenenfalls in Kombination mit einem im wesentlichen nicht lichtempfindlichen Silbersalz, und mindestens eine nicht diffundierende farbgebende Verbindung enthält, die als Folge der Entwicklung einen diffusionsfähigen Farbstoff freizusetzen vermag, durch Wärmebehandlung in Gegenwart eines thermischen Entwicklungs- und Diffusionsförderungsmittels entwickelt wird, wobei der aus der nicht diffundierenden farbgebenden Verbindung bildmäßig freigesetzte Farbstoff in eine durch diffusionsfähige Farbstoffe anfärbbare Bildempfangsschicht übertragen wird, dadurch gekennzeichnet, daß das thermische Entwicklungs- und Diffusionsförderungsmittel der folgenden Formel I entspricht:
X -SO₂- oder -CO-;
R¹ - R⁴ Alkyl, Cycloalkyl, Aralkyl oder Aryl;
R⁵, R⁶ Acyl oder einen Rest wie angegeben für R¹ - R⁴;
wobei R¹ zusammen mit R⁵, R² zusammen mit R⁶, R³ zusammen mit R⁴ und/oder R¹ zusammen mit R² jeweils einen mindestens ein Stickstoffatom enthaltenden heterocyclischen Ring bilden können. - Ein weiterer Gegenstand der Erfindung ist ein farbfotografisches Aufzeichnungsmaterial, das für das Wärmeentwicklungsverfahren geeignet ist und mindestens ein thermisches Entwicklungs- und Diffusionsförderungsmittel der angegebenen Art in mindestens einer seiner Schichten enthält.
- R¹ bis R⁶ können gleich oder verschieden sein. Vorzugsweise sind sie jeweils paarweise gleich (R¹, R²; R³, R⁴; R⁵, R⁶).
- Eine durch R¹ bis R⁶ dargestellte Alkylgruppe kann unverzweigt oder verzweigt, sowie gegebenenfalls substituiert sein und vorzugsweise 1 bis 4 C-Atome enthalten. Beispiele hierfür sind Methyl, Ethyl, Propyl, Isopropyl, n-Butyl, s-Butyl, Methoxymethyl, Cyclohexylmethyl, Hydroxyethyl. Die Alkylgruppen, insbesondere die durch R³ und R⁴ dargestellten, können aber auch einzeln bis zu 18 C-Atomen enthalten. Eine durch R¹ bis R⁶ dargestellte Cycloalkylgruppe ist beispielsweise Cyclohexyl. Eine durch R¹ bis R⁶ dargestellte Aralkylgruppe ist beispielsweise Benzyl. Eine durch R¹ bis R⁶ dargestellte Arylgruppe ist beispielsweise Phenyl, Tolyl, Methoxyphenyl, N-Methyl-N-acetylamino-phenyl.
- Eine durch R⁵ oder R⁶ dargestellte Acylgruppe kann sich von aliphatischen oder aromatischen Carbon- oder Sulfonsäuren oder auch von Carbamin- oder Sulfaminsäuren ableiten. Acetyl, Methylsulfonyl, Phenylsulfonyl, p-Methoxyphenylsulfonyl und p-Nitrophenylsulfonyl sind Beispiele hierfür.
- Heterocyclische Ringe, die durch R¹ und R⁵, R² und R⁶, R³ und R⁴ und/oder R¹ und R² gebildet werden, sind vorzugsweise 5- oder 6-gliedrig und weisen mindestens ein Stickstoffatom und gegebenenfalls weitere Heteroatome auf. Ein durch R¹ zusammen mit R² gebildeter heterocyclischer Ring weist mindestens 2 Stickstoffatome auf. Beispiele für solche heterocyclischen Ringe sind Pyrrolidin, Piperidin, Morpholin, Imidazolidin und Hexahydropyrimidin.
- Die erfindungsgemäßen thermischen Entwicklungs- und Diffusionsförderungsmittel (hierfür soll im folgenden das Acronym TEDM verwendet werden) wirken unter den Bedingungen der Wärmeentwicklung offenbar als solvatisierendes Medium für die ablaufenden Reaktionen wie Entwicklung des Silberhalogenids bzw. des organischen Silbersalzes unter dem Einfluß eines Reduktionsmittels, Freisetzung der diffusionsfähigen Farbstoffe aus den farbgebenden Verbindungen und Diffusion der Farbstoffe in eine Bildempfangsschicht. Durch geeignete Variation der Substituenten R¹ bis R⁶, insbesondere der Substituenten R¹ und R², lassen sich die Solvenseigenschaften der erfindungsgemäßen TEDM in Richtung auf hydrophileren oder hydrophoberen Charakter in gezielter Weise beeinflussen.
-
- Die Zugänglichkeit der Guanidylsulfamide bzw. ihrer Vorstufen ist bekannt.
-
- Beispielhaft seien hier die Synthese der Verbindungen TEDM-4 und TEDM-1 beschrieben.
- 1) N,N-Di-n-Butyl-Sulfamidsäurechlorid (Verbindung A)
Zu 135 g (1,0 mol)Sulfurylchlorid wuden unter Eiskühlung und kräftigem Rühren langsam 129 g (1,0 mol) Di-n-Butylamin innerhalb 5 h zugetropft. Dann wurde noch 5 h bei 90°C nachgerührt, nach Abkühlen unter Rühren mit Ether versetzt und vom angefallenen Niederschlag abgenutscht. Die Etherphase wurde einmal mit Wasser, einmal mit konzentrierter Natriumhydrogencarbonat-Lösung und nochmals mit Wasser gewaschen, über Natriumsulfat getrocknet und am Rotationsverdampfer eingeengt. Das erhaltene Öl wurde im Vakuum destilliert und lieferte 60 g Verbindung A (Kp1mm 110-112°C). - 2) 64,6 g (0,56 mol) Tetramethylguanidin wurden in 500 ml trockenem Methylenchlorid gelöst. Hierzu wurden innerhalb 3 h bei Raumtemperatur 50 g (0,23 mol) Verbindung A, gelöst in 120 ml trockenem Methylenchlorid, zugetropft. Dann wurde 3 h bei Raumtemperatur gerührt, mehrmals mit Wasser (bis neutral) gewaschen, mit 10 g Bleicherde geklärt, mit Natriumsulfat getrocknet, abgesaugt und die Mutterlauge eingeengt. Es wurden 55 g praktisch DC-reine Verbindung TEDM-4 als Öl erhalten.
- 11,5 g (0,1 mol) Tetramethylguanidin wurden in 100 ml Methylenchlorid gelöst und unter Kühlung wurden bei Raumtemperatur 14,4 g (0,1 mol) Dimethylsulfamidsäurechlorid, gelöst in 50 ml Methylenchlorid zugetropft. Dann wurde 1 h nachgerührt und eingeengt. Als Rückstand blieb ein gelber Brei, der mit 50 ml Petrolether verrührt und abgesaugt, festes HCl-Salz mit einem Schmelzpunkt von 205°C liefert. Dieses wurde in Wasser gelöst, mit Natriumhydrogencarbonatlösung auf pH = 7 gestellt, mit Methylenchlorid extrahiert; die Methylenchloridphase wurde getrocknet und eingeengt. 6 g weiße Festsubstanz mit einem Schmelzpunkt von 97°C.
- 6,9 g (0,06 mol) Tetramethylguanidin wurden in 50 ml Methylenchlorid gelöst. Bei Raumtemperatur wurde eine Lösung von 6,4 g (0,03 mol) N,N-Diisopropylsulfamidsäurechlorid in 25 ml Methylenchlorid zugetropft und 1 h nachgerührt. Dann wird mit Wasser neutral gewaschen. Die Methylenchloridphase wurde getrocknet (Na₂So₄) und eingeengt.
- Ausbeute: 9,0 g
- Die erfindungsgemäß verwendeten TEDM vom aprotischen Typ sind unter Normalbedingungen vorzugsweise flüssig (insoweit unterscheiden sie sich von den bisher bekannten thermischen Lösungsmitteln (= "thermal solvents"), die bei Normaltemperatur fest sind) und können meistens auf Grund ihrer guten Wasserlöslichkeit direkt unverdünnt oder als wäßrige Lösungen den Gießlösungen für die lichtempfindlichen oder nicht lichtempfindlichen Schichten zugesetzt werden. Wasserunlösliche TEDM können in dispergierter Form eingebracht werden. Solche Dispergate können Dispergate der Reinsubstanzen sein oder auch Dispergate von Lösungen der Reinsubstanzen in einem hochsiedenden organischen Lösungsmittel (= Ölbildner).
- Die eingesetzte Menge kann in einem weiten Bereich variiert werden; dies richtet sich unter anderem danach, ob die Verbindungen über mehrere oder alle Schichten des erfindungsgemäßen Aufzeichnungsmaterials verteilt eingebracht werden, oder ob sie konzentriert nur in einer bestimmten Schicht eingesetzt werden. Die einzusetzende Menge pro Quadratmeter hängt darüber hinaus selbstverständlich auch noch von der Menge des verwendeten Bindemittels ab. Die geeignete Konzentration kann vom Fachmann anhand einfacher routinemäßiger Versuche leicht ermittelt werden. Die Einsatzkonzentration kann bezogen auf das Bindemittel zwischen 2 und 100 Gew.-%, vorzugsweise jedoch im Bereich zwischen 20 und 50 Gew.-% liegen. Überdosierung an TEDM führt jedoch in der Regel zu hohem Farbschleier (Dmin).
- Ein für die Durchführung des erfindungsgemäßen Wärmeentwicklungsverfahren geeignetes farbfotografisches Aufzeichnungsmaterial enthält auf einem dimensionsstabilen Schichtträger mindestens eine Bindemittelschicht, in der ein lichtempfindliches Silberhalogenid, gegebenenfalls in Kombination mit einem im wesentlichen nicht lichtempfindlichen Silbersalz und eine nicht diffundierende farbgebende Verbindung enthalten ist, die durch Wärmeentwicklung einen diffusionsfähigen Farbstoff liefern kann, und das farbfotografische Aufzeichnungsmaterial enthält weiterhin in einer seiner Schichten eines oder mehrere der erfindungsgemäßen thermischen Entwicklungs- und Diffusionsförderungsmittel (TEDM).
- Ein wesentlicher Bestandteil des wärmeentwickelbaren Aufzeichnungsmaterials der vorliegenden Erfindung ist das Silberhalogenid, das aus Silberchlorid, Silberbromid, Silberiodid oder deren Gemischen bestehen und eine Teilchengröße zwischen 0,01 und 2,0 µm, vorzugsweise zwischen 0,1 und 1,0 µm aufweisen kann. Es kann als unsensibilisiertes Silberhalogenid vorliegen oder aber auch durch geeignete Zusätze chemisch und/oder spektral sensibilisiert sein.
- Die Menge des lichtempfindlichen Silberhalogenids kann in der jeweiligen Schicht zwischen 0,01 und 2,0 g pro m² betragen, wobei sich die tatsächliche Menge des eingesetzten Silberhalogenids wegen seiner katalytischen Funktion (als belichtetes Silberhalogenid) in manchen Ausführungsformen hauptsächlich im unteren Teil des angegebenen Bereiches bewegt.
- Bei dem im wesentlichen nicht lichtempfindlichen Silbersalz kann es sich beispielsweise um ein gegenüber Licht vergleichsweise stabiles Silbersalz, z.B. ein organisches Silbersalz handeln. Zu geeigneten Beispielen hierfür zählen die Silbersalze aliphatischer oder aromatischer Carbonsäuren sowie die Silbersalze von stickstoffhaltigen Heterocyclen; ferner auch Silbersalze organischer Mercaptoverbindungen.
- Bevorzugte Beispiele für Silbersalze aliphatischer Carbonsäuren sind Silberbehenat, Silberstearat, Silberoleat, Silberlaurat, Silbercaprat, Silbermyristat, Sil berpalmitat, Silbermaleat, Silberfumarat, Silbertartrat, Silberfuroat, Silberlinolat, Silberadipat, Silbersebacat, Silbersuccinat, Silberacetat oder Silberbutyrat. Die diesen Silbersalzen zugrunde liegenden Carbonsäuren können beispielsweise durch Halogenatome, Hydroxylgruppen oder Thioethergruppen substituiert sein.
- Zu Beispielen für Silbersalze aromatischer Carbonsäuren und anderer carboxylgruppenhaltiger Verbindungen gehören Silberbenzoat, Silber-3,5-dihydroxybenzoat, Silber-o-methylbenzoat, Silber-m-methylbenzoat, Silber-p-methylbenzoat, Silber-2,4-dichlorbenzoat, Silberacetamidobenzoat, Silbergallat, Silbertannat, Silberphthalat, Silberterephthalat, Silbersalicylat, Silberphenylacetat, Silberpyromellitat, Silbersalze von 3-Carboxymethyl-4-methyl-4-thiazolin-2-thion oder ähnlichen heterocyclischen Verbindungen. Geeignet sind ferner Silbersalze von organischen Mercaptanen, z.B. die Silbersalze von 3-Mercapto-4-phenyl-1,2,4-trizol, 2-Mercaptobenzimidazol, 2- Mercaptobenzothiazol, 2-Mercaptobenzoxazol, 2-Mercaptooxadiazol, Mercaptotriazin, Thioglykolsäure, ferner die Silbersalze von Dithiocarbonsäuren, wie z.B. das Silbersalz der Dithioessigsäure.
- Außerdem geeignet sind die Silbersalze von Verbindungen mit einer Iminogruppe. Zu bevorzugten Beispielen hierfür gehören die Silbersalze von Benzotriazol und dessen Derivaten, z.B. Silbersalze von alkyl- und/oder halogensubstituierten Benzotriazolen, wie z.B. die Silbersalze von Methylbenzotriazol, 5-Chlorbenzotriazol, sowie auch die Silbersalze von 1,2,4-Triazol, 1-H-Tetrazol, Carbazol, Saccharin und Silbersalze von Imidazol und dessen Derivaten.
- Die Auftragsmenge an im wesentlichen nicht lichtempfindlichem Silbersalz gemäß der vorliegenden Erfindung liegt in der jeweiligen Schicht zwischen 0,05 und 5 g pro m². Das im wesentlichen nicht lichtempfindliche Silbersalz und das lichtempfindliche Silberhalogenid können nebeneinander als getrennte Partikel vorliegen oder auch in einer kombinierten Form, die beispielsweise dadurch erzeugt werden kann, daß ein im wesentlichen nicht lichtempfindliches Silbersalz in Gegenwart von Halogenidionen behandelt wird, wobei sich auf der Oberfläche der Teilchen aus dem im wesentlichen nicht lichtempfindlichen Silbersalz durch doppelte Umsetzung (Konvertierung) lichtempfindliche Zentren aus lichtempfindlichem Silberhalogenid bilden. Hierzu ist zu verweisen auf US-A-3 457 075.
- Das im wesentlichen nicht lichtempfindliche Silbersalz dient als Reservoir für Metallionen, die bei der Wärmeentwicklung in Gegenwart eines Reduktionsmittels unter dem katalytischen Einfluß des bildmäßig belichteten Silberhalogenids zu elementarem Silber reduziert werden und dabei selbst als Oxidationsmittel (für das vorhandene Reduktionsmittel) dienen.
- Ein weiterer wesentlicher Bestandteil des erfindungsgemäßen Aufzeichnungsmaterials ist eine nicht diffundierende farbgebende Verbindung, die als Folge einer bei der Entwicklung stattfindenden Redoxreaktion einen diffusionsfähigen Farbstoff freizusetzen vermag und die im folgenden als Farbabspalter bezeichnet wird.
- Bei den erfindungsgemäß verwendeten Farbabspaltern kann es sich um eine Vielfalt von Verbindungstypen handeln, die sich sämtlich durch ein in seiner Bindungsfestigkeit redoxabhängiges Bindeglied auszeichnen, welches einen Farbstoffrest mit einem einen Ballastrest enthaltenden Trägerrest verknüpft.
- In diesem Zusammenhang ist auf eine zusammenfassende Darstellung des Sachgebiets in Angew. Chem. Int. Ed. Engl. 22 (1983), 191 - 209 zu verweisen, in der die wichtigsten der bekannten Systeme beschrieben sind.
- Als besonders vorteilhaft erweisen sich hierbei redoxaktive Farbabspalter der Formel
BALLAST - REDOX - FARBSTOFF,
worin bedeuten
BALLAST einen Ballastrest
REDOX eine redoxaktive Gruppe, d.h. eine Gruppe die unter den Bedingungen der alkalischen Entwicklung oxidierbar oder reduzierbar ist und je nachdem, ob sie im oxidierten oder im reduzierten Zustand vorliegt, in unterschiedlichem Ausmaß einer Eliminierungsreaktion, einer nukleophilen Verdrängungsreaktion, einer Hydrolyse oder einer sonstigen Spaltungsreaktion unterliegt mit der Folge, daß der Rest FARBSTOFF abgespalten wird, und
FARBSTOFF den Rest eines diffusionsfähigen Farbstoffes, z.B. eines Gelb-, Purpur- oder Blaugrünfarbstoffes, oder den Rest eines Farbstoffvorläufers. - Als Ballastreste sind solche Reste anzusehen, die es ermöglichen, die erfindungsgemäßen Farbabspalter in den üblicherweise bei fotografischen Materialien verwendeten hydrophilen Kolloiden diffusionsfest einzulagern. Hierzu sind vorzugsweise organische Reste geeignet, die im allgemeinen geradkettige oder verzweigte aliphatische Gruppen mit im allgemeinen 8 bis 20 C-Atomen und gegebenenfalls auch carbocyclische oder heterocyclische gegebenenfalls aromatische Gruppen enthalten. Mit dem übrigen Molekülteil sind diese Reste entweder direkt oder indirekt, z.B. über eine der folgenden Gruppen verbunden: -NHCO-, -NHSO₂-, -NR-, wobei R Wasserstoff oder Alkyl bedeutet, -O- oder -S-. Zusätzlich kann der Ballastrest auch wasserlöslichmachende Gruppen enthalten, wie z.B. Sulfogruppen oder Carboxylgruppen, die auch in anionischer Form vorliegen können. Da die Diffusionseigenschaften von der Molekülgröße der verwendeten Gesamtverbindung abhängen, genügt es in bestimmten Fällen, z.B. wenn das verwendete Gesamtmolekül groß genug ist, als Ballastreste auch kürzerkettige Reste zu verwenden.
- Redoxaktive Trägerreste der Struktur BALLAST-REDOX- und entsprechende Farbabspalter sind in den verschiedensten Ausführungsformen bekannt. Auf eine detaillierte Darstellung kann an dieser Stelle verzichtet werden im Hinblick auf den genannten Übersichtartikel im Angew. Chem. Int. Ed. Engl. 22 (1983) 191-209.
-
- Die in Klammern eingeschlossenen Gruppen sind funktionelle Gruppen des Farbstoffrestes und werden zusammen mit diesem vom zurückbleibenden Teil des Trägerrestes abgetrennt. Bei der funktionellen Gruppe kann es sich um einen Substituenten handeln, der einen unmittelbaren Einfluß auf die Absorptions- und gegebenenfalls Komplexbildungseigenschaften des freigesetzten Farbstoffes ausüben kann. Die funktionelle Gruppe kann andererseits aber auch von dem Chromophor des Farbstoffes durch ein Zwischenglied oder Verknüpfungsglied getrennt sein. Die funktionelle Gruppe kann schließlich auch gegebenenfalls zusammen mit dem Zwischenglied von Bedeutung sein für das Diffusions- und Beizverhalten des freigesetzten Farbstoffes. Geeignete Zwischenglieder sind beispielsweise Alkylen- oder Arylengruppen.
- Als Farbstoffreste sind grundsätzlich die Reste von Farbstoffen aller Farbstoffklassen geeignet, soweit sie genügend diffusionsfähig sind, um aus der lichtempfindlichen Schicht des lichtempfindlichen Materials in eine Bildempfangsschicht diffundieren zu können. Zu diesem Zweck können die Farbstoffreste mit einer oder mehreren alkalilöslichmachenden Gruppen versehen sein. Als alkalilöslichmachende Gruppen sind unter anderem geeignet Carboxylgruppen, Sulfogruppen, Sulfonamidgruppen sowie aromatische Hydroxylgruppen. Solche alkalilöslichmachende Gruppen können in den Farbabspaltern bereits vorgebildet sein oder erst aus der Abspaltung des Farbstoffrestes von dem mit Ballastgruppen behafteten Trägerrest resultieren. An geeigneten Farbstoffen sind zu erwähnen: Azofarbstoffe, Azomethinfarbstoffe, Anthrachinonfarbstoffe, Phthalocyaninfarbstoffe, indigoide Farbstoffe, Triphenylmethanfarbstoffe, einschließlich solcher Farbstoffe, die mit Metallionen komplexiert oder komplexierbar sind.
- Unter den Resten von Farbstoffvorläufern sind die Reste solcher Verbindungen zu verstehen, die im Laufe der fotografischen Verarbeitung, insbesondere unter den Bedingungen der Wärmeentwicklung, sei es durch Oxidation, sei es durch Kupplung, durch Komplexbildung oder durch Freilegung einer auxochromen Gruppe in einem chromophoren System, beispielsweise durch Verseifung, in Farbstoffe übergeführt werden. Farbstoffvorläufer in diesem Sinn können sein Leukofarbstoffe, Kuppler oder auch Farbstoffe, die im Laufe der Verarbeitung in andere Farbstoffe umgewandelt werden. Sofern nicht eine Unterscheidung zwischen Farbstoffresten und den Resten von Farbstoffvorläufern von wesentlicher Bedeutung ist, sollen letztere im folgenden auch unter der Bezeichnung Farbstoffreste verstanden werden.
- Geeignete Farbabspalter sind beispielsweise beschrieben in:
US-A- 3 227 550, US-A- 3 443 939, USA-A- 3 443 940, DE-A- 19 30 215, DE-A- 22 42 762, DE-A- 24 02 900, DE-A- 24 06 664, DE-A- 25 05 248, DE-A- 25 43 902, DE-A- 26 13 005, DE-A- 26 45 656, DE-A- 28 09 716, DE-A- 28 23 159, BE-A- 861 241, EP-A- 0 004 399, EP-A- 0 004 400, DE-A- 30 08 588, DE-A- 30 14 669, GB-A- 80 12 242. - Die Farbabspalter können in manchen Ausführungsformen des erfindungsgemäßen Wärmeentwicklungsverfahrens als oxidierbare oder kupplungsfähige Farbabspalter, in anderen als reduzierbare Farbabspalter vorliegen. Je nach dem, ob der Farbstoff aus der oxidierten oder aus der reduzierten Form der Farbabspalter freigesetzt wird, erhält man bei Verwendung üblicher negativ arbeitender Silberhalogenidemulsionen von der Vorlage eine negative oder positive Ablichtung. Man kann daher nach Wunsch durch Auswahl geeigneter Farbabspaltersysteme positive oder negative Bilder herstellen.
- Für die erfindungsgemäßen wärmeentwickelbaren Aufzeichnungsmaterialien besonders geeignete oxidierbare Farbabspalter sind beispielsweise in DE-A-22 42 762, DE-A-25 05 248, DE-A-26 13 005, DE-A-26 45 656 und GB-A-80 12 242 beschrieben.
- Wenn der Farbabspalter oxidierbar ist, dann stellt er selbst ein Reduktionsmittel dar, das unmittelbar oder mittelbar unter Mitwirkung von Elektronenübertragungsmitteln (elektron transfer agent, ETA) durch das bildmäßig belichtete Silberhalogenid bzw. durch das im wesentlichen nicht lichtempfindliche Silbersalz unter der katalytischen Einwirkung des bildmäßig belichteten Silberhalogenids oxidiert wird. Hierbei entsteht eine bildmäßige Differenzierung hinsichtlich der Fähigkeit, den diffusionsfähigen Farbstoff freizusetzen. Wenn andererseits der Farbabspalter reduzierbar ist, dann verwendet man ihn zweckmäßig in Kombination mit einem in begrenzter Menge vorliegenden Reduktionsmittel, einer sogenann ten Elektronendonorverbindung oder einer Elektronendonorvorläuferverbindung, die in diesem Fall neben dem Farbabspalter, dem lichtempfindlichen Silberhalogenid und gegebenenfalls dem in wesentlichen nicht lichtempfindlichen Silbersalz in der gleichen Bindemittelschicht enthalten ist. Auch im Fall der Verwendung von reduzierbaren Farbabspaltern in Kombination mit Elektronendonorverbindungen kann sich die Mitwirkung von Elektronenübertragungsmitteln als günstig erweisen.
- Für die Erzeugung positiver Farbbilder von positiven Vorlagen (Original) bei Verwendung negativ arbeitender Silberhalogenidemulsionen eignet sich beispielsweise ein erfindungsgemäßes Aufzeichnungsmaterial, das reduzierbare Farbabspalter mit einem Trägerrest der folgenden Formel enthält:
R¹ʹ Alkyl oder Aryl;
R²ʹ Alkyl, Aryl oder eine Gruppierung, die zusammen mit R³ʹ einen ankondensierten Ring vervollständigt;
R³ʹ Wasserstoff, Alkyl, Aryl, Hydroxyl, Halogen wie Chlor oder Brom, Amino, Alkylamino, Dialkylamino einschließlich cyclischer Aminogruppen (wie Piperidino, Morpholino), Acylamino, Alkylthio, Alkoxy, Aroxy, Sulfo, oder eine Gruppierung, die zusammen mit R²ʹ einen ankondensierten Ring vervollständigt;
R⁴ʹ Alkyl;
R⁵ʹ Alkyl oder vorzugsweise Wasserstoff;
und wobei mindestens einer der Reste R¹ʹ bis R⁴ʹ einen Ballastrest enthält. - Solche reduzierbare Farbstoffabspalter und andere, die ebenfalls im Rahmen der vorliegenden Erfindung geeignet sind, sind beispielsweise beschrieben in DE-A-28 09 716, EP-A-O 004 399, DE-A-30 08 588, DE-A-30 14 669.
- Die in Kombination mit einem reduzierbaren Farbabspalter verwendete Elektronendonorverbindung dient gleichermaßen als Reduktionsmittel für das Silberhalogenid, das im wesentlichen nicht lichtempfindliche Silbersalz und den Farbabspalter. Dadurch, daß das im wesentlichen nicht lichtempfindliche Silbersalz und der Farbabspalter bei der Oxidation der Elektronendonorverbindung gewissermaßen miteinander in Konkurrenz treten, ersteres dem letzteren aber jedenfalls in Gegenwart von belichtetem Silberhalogenid hierbei überlegen ist, wird das vorhandene Silberhalogenid nach Maßgabe einer vorausgegangenen bildmäßigen Belichtung bestimmend für die Bildbereiche, innerhalb derer der Farbabspalter durch die Elektronendonorverbindung in seine reduzierte Form überführt wird.
- Die in begrenzter Menge vorliegende Elektronendonorverbindung wird unter den Bedingungen der Entwicklung, im vorliegenden Fall beim Erwärmen des bildmäßig belichteten farbfotografischen Aufzeichnungsmaterials nach Maßgabe des Ausmaßes der Belichtung unter der katalytischen Wirkung der durch Belichtung in dem Silberhalogenid erzeugten Latentbildkeime durch das im wesentlichen nicht lichtempfindliche Silbersalz und das lichtempfindliche Silberhalogenid oxidiert und steht folglich nicht mehr für eine Reaktion mit dem Farbabspalter zur Verfügung. Hierbei entsteht gleichsam eine bildmäßige Verteilung an nicht verbrauchter Elektronendonorverbindung.
- Als Elektronendonorverbindung sind beispielsweise nicht oder nur wenig diffundierende Derivate des Hydrochinons, des Benzisoxazolons, des p-Aminophenols oder der Ascorbinsäure (z.B. Ascorbylpalmitat) beschrieben worden (DE-A-28 09 716).
- Weitere Beispiele für Elektronendonorverbindungen sind aus DE-A-29 47 425, DE-A-30 06 268, DE-A-31 30 842, DE-A-31 44 037, DE-A-32 17 877, EP-A-0 124 915 und Research Disclosure 24 305 (Juli 1984) bekannt. Es hat sich gezeigt, daß die genannten Elektronendonorverbindungen auch unter den Bedingungen der Wärmeentwicklung den an sie gerichteten Anforderungen genügen und daher auch als Elektronendonorverbindungen im Rahmen der vorliegenden Erfindung geeignet sind.
- Besonders geeignet sind solche Elektronendonorverbindungen, die erst unter den Bedingungen der Wärmeentwicklung in der Schicht aus entsprechenden Elektronendonorvorläuferverbindungen gebildet werden, d.h. Elektronendonorverbindungen, die in dem Aufzeichnungsmaterial vor der Entwicklung nur in einer verkappten Form vorliegen, in der sie praktisch unwirksam sind. Unter den Bedingungen der Wärmeentwicklung werden dann die zunächst unwirksamen Elektronendonorverbindungen in ihre wirksame Form überführt, indem beispielsweise bestimmte Schutzgruppen hydrolytisch abgespalten werden. Im vorliegenden Fall werden auch die erwähnten Elektronendonorvorläuferverbindungen als Elektronendonorverbindung verstanden.
- Die genannten wesentlichen Bestandteile des bei dem erfindungsgemäßen Verfahren verwendeten Aufzeichnungsmaterials, nämlich das lichtempfindliche Silberhalogenid, das gegebenenfalls vorhandene im wesentlichen nicht lichtempfindliche reduzierbare Silbersalz und der Farbabspalter, gegebenenfalls in Kombination mit einer Elektronendonorverbindung liegen nebeneinander in einem Bindemittel dispergiert vor. Hierbei kann es sich gleichermaßen um hydrophobe wie hydrophile Bindemittel handeln, letztere sind jedoch bevorzugt und vorzugsweise wird Gelatine verwendet, die aber auch ganz oder teilweise durch andere natürliche oder synthetische Bindemittel ersetzt werden kann. Als geeignete Bindemittel haben sich beispielsweise Polyurethane, gegebenenfalls in Abmischung mit Gelatine, erwiesen wie dies beispielsweise in DE-A-35 30 156 beschrieben ist.
- Die lichtempfindliche Bindemittelschicht enthält für die Erzeugung monochromer Farbbilder zugeordnet zu dem lichtempfindlichen Silberhalogenid und gegebenenfalls dem nicht lichtempfindlichen Silbersalz einen oder auch mehrere Farbabspalter, aus denen Farbstoffe einer bestimmten Farbe freigesetzt werden. Die insgesamt resultierende Farbe kann sich durch Mischung mehrerer Farbstoffe ergeben. Auf diese Weise ist es auch möglich, durch genau abgestimmte Abmischung mehrerer Farbabspalter unterschiedlicher Farbe schwarzweiße Bilder zu erzeugen. Zur Herstellung mehrfarbiger Farbbilder enthält das bei dem erfindungsgemäßen Verfahren verwendete farbfotografische Aufzeichnungsmaterial mehrere, d.h. in der Regel drei, Zuordnungen von Farbabspalter und jeweils unterschiedlich spektral sensibilisiertem Silberhalogenid, wobei bevorzugt jeweils der Absorptionsbereich des aus dem Farbabspalter freigeetzen Farbstoffes mit dem Bereich der spektralen Empfindlichkeit des zugeordneten Silberhalogenids im wesentlichen übereinstimmt. Die verschiedenen Zuordnungen aus Farbabspalter und zugeordneten Silberhalogenid können in verschiedenen Bindemittelschichten des farbfotografischen Aufzeichnungsmaterials untergebracht sein, wobei sich bevorzugt zwischen diesen verschiedenen Bindemittelschichten Trennschichten aus einem wasserdurchlässigen Bindemittel, z.B. Gelatine, befinden, die im wesentlichen die Funktion haben, die verschiedenen Zuordnungen voneinander zu trennen und auf diese Weise einer Farbverfälschung entgegenzuwirken. In einem solchen Fall enthält das bei dem erfindungsgemäßen Verfahren verwen dete farbfotografische Aufzeichnungsmaterial beispielsweise eine lichtempfindliche Bindemittelschicht, in der das darin enthaltene Silberhalogenid durch spektrale Sensibilisierung überwiegend rotempfindlich ist, eine weitere lichtempfindliche Bindemittelschicht, in der das darin enthaltene Silberhalogenid durch spektrale Sensibilisierung überwiegend grünempfindlich ist, und eine dritte lichtempfindliche Bindemittelschicht, in der das darin enthaltene Silberhalogenid aufgrund der Eigenempfindlichkeit oder durch spektrale Sensibilisierung überwiegend blauempfindlich ist. Die in den drei lichtempfindlichen Schichten gegebenenfalls enthaltenen Elektronendonorverbindungen können gleich oder verschieden sein.
- Jede der genannten Zuordnungen aus lichtempfindlichem Silberhalogenid, im wesentlichen nicht lichtempfindlichem Silbersalz (sofern vorhanden) und Farbabspalter kann auch in Form eines sogenannten komplexen Coazervates eingesetzt werden.
- Unter einem komplexen Coazervat wird eine Dispersionsform verstanden, bei der eine Mischung der wesentlichen Bestandteile in eine gemeinsame Umhüllung aus einem gehärteten Bindmittel eingeschlossen ist. Solche Dispersionen werden auch als Paketemulsion bezeichnet. Sie werden durch komplexe Coazervation erhalten.
- Unter der Bezeichnung "komplexe Coazervation" versteht man das Auftreten zweier Phasen bei der Vermischung je einer wäßrigen Lösung eines polykationischen Kolloids und eines polyanionischen Kolloids, wobei eine konzentrierte Kolloidphase (im folgenden als komplexes Coazervat bezeichnet) und eine verdünnte Kolloidphase (im folgenden als Gleichgewichtslösung bezeichnet) aufgrund einer elektrischen Wechselwirkung gebildet werden. Das komplexe Coazervat wird aus der Gleichgewichtslösung in der Form von Tröpfchen abgeschieden und erscheint als weiße Trübung. Wenn die komplexe Coazervation in Anwesenheit eines Feststoffes wie Silberhalogenid oder feiner Öltröpfchen durchgeführt wird, nimmt man allgemein an, daß das komplexe Coazervat den Feststoff oder die Tröpfchen im Innern von Kolloidteilchen einschließt. Als Ergebnis hiervon wird eine Dispersion von Coazervatteilchen erhalten, in denen der Feststoff (im vorliegenden Fall das lichtempfindliche Silberhalogenid sowie gegebenenfalls das im wesentlichen nicht lichtempfindliche Silbersalz) und ölige Tröpfchen einer Lösung der organischen Bestandteile (im vorliegenden Fall des Farbabspalters und gegebenenfalls weiterer Hilfsstoffe) eingeschlossen sind. Anschließend wird mit einem Härtungsmittel gehärtet, so daß die ursprüngliche Form der Teilchen in den folgenden Stufen zur Herstellung des fotografischen Aufzeichnungsmaterials, wie Herstellung der Gießlösung und Beschichtung, nicht zerstört wird. Zweckmäßigerweise wird die Dispersion vor der Härtung auf eine Temperatur von 25°C oder darunter, vorzugsweise 10°C oder darunter gekühlt, wodurch eine Paketemulsion guter Qualität erhalten wird.
- Methoden zur Herstellung einer Paketemulsion, in der eine farbbildende Substanz durch komplexe Coazervation eingearbeitet ist, sind beispielsweise beschrieben in US-A-3 276 869 und US-A-3 396 026.
- Die Verwendung von Paketemulsionen ermöglicht die Zusammenfassung mehrerer Emulsionsanteile unterschiedlicher spektraler Empfindlichkeit einschließlich der betreffenden Farbabspalter in einer einzigen Bindemittelschicht, ohne daß die spektrale Zuordnung verloren geht und hierdurch eine Farbverfälschung auftritt. Dies ist deswegen möglich, weil das Ausmaß der Belichtung eines bestimmten Silberhalogenidteilchens nahezu ausschließlich bestimmend wird für das Ausmaß der Farbstofffreisetzung aus demjenigen Farbabspalter, der sich in dem gleichen Coazervatteilchen (Paket) befindet wie das Silberhalogenid. Die Verwendung von Paketemulsionen ermöglicht somit die Unterbringung je einer blauempfindlichen, einer grünempfindlichen und einer rotempfindlichen Silberhalogenidemulsion mit gegebenenfalls zusätzlich vorhandenem im wesentlichen nicht lichtempfindlichen Silbersalz und jeweils spektral zugeordneten Farbabspaltern in der gleichen Bindemittelschicht, ohne daß eine schwerwiegende Farbverfälschung befürchtet werden muß.
- Über die bereits genannten Bestandteile hinaus kann das bei dem erfindungsgemäßen Verfahren verwendete farbfotografische Aufzeichnungsmaterial weitere Bestandteile und Hilfsstoffe enthalten, die beispielsweise für die Durchführung der Wärmebehandlung und des hierbei erfolgenden Farbübertrages förderlich sind. Diese weiteren Bestandteile bzw. Hilfsstoffe können in einer lichtempfindlichen Schicht oder in einer nicht empfindlichen Schicht enthalten sein.
- Solche Hilfstoffe sind beispielsweise Hilfsentwickler. Diese Hilfsentwickler haben im allgemeinen entwickelnde Eigenschaften für belichtetes Silberhalogenid; im vorliegenden Fall wirken sie sich in erster Linie förderlich auf die zwischen dem belichteten Silbersalz (= Silbersalz in Gegenwart von belichtetem Silberhalogenid) und dem Reduktionsmittel ablaufenden Reaktionen aus, wobei das Reduktionsmittel im Falle der Verwendung oxidierbarer Farbabspalter mit letzteren identisch ist, bzw. im Fall der Verwendung reduzierbarer Farbabspalter seinerseits mit dem Farbabspalter reagiert. Da diese Reaktionen hauptsächlich in einem Übertrag von Elektronen bestehen, werden die Hilfsentwickler auch als Elektronenübertragungsmittel (electron transfer agent; ETA) bezeichnet. Beispiele für geeignete Hilfsentwickler sind etwa Hydrochinon, Brenzkatechin, Pyrogallol, Hydroxylamin, Ascorbinsäure, 1-Phenyl-3-pyrazolidon und deren Derivate. Da die Hilfsentwickler gleichsam eine katalytische Funktion ausüben, ist es nicht erforderlich, daß sie in stöchiometrischen Mengen anwesend sind. Im allgemeinen reicht es aus, wenn sie in Mengen bis zu 1/2 mol pro mol Farbabspalter in der Schicht vorhanden sind. Die Einarbeitung in die Schicht kann beispielsweise aus Lösungen in wasserlöslichen Lösungsmitteln oder in Form von wäßrigen Dispersionen, die unter Verwendung von Ölbildnern gewonnen wurden, erfolgen.
- Weitere Hilfsstoffe sind beispielsweise basische Stoffe oder Verbindungen, die unter dem Einfluß der Wärmebehandlung basische Stoffe zur Verfügung zu stellen vermögen. Hier sind beispielsweise zu erwähnen Natriumhydroxid, Kaliumhydroxid, Calziumhydroxid, Natriumcarbonat, Natriumacetat und organische Basen, insbesondere Amine wie Alkylamine, Pyrrolidin, Piperidin, Amidin, Guanidin und deren Salze, insbesondere Salze mit aliphatischen Carbonsäuren. Durch Zurverfügungsstellung der basischen Stoffe wird bei der Wärmebehandlung in der lichtempfindlichen Schicht und den angrenzenden Schichten ein geeignetes Medium geschaffen, um die Freisetzung der diffusionsfähigen Farbstoffe aus den Farbabspaltern und ihre Übertragung auf das Bildempfangsblatt zu gewährleisten.
- Weitere Hilfsstoffe sind beispielsweise Verbindungen, die unter der Einwirkung von Wärme Wasser freizusetzen vermögen. Hierfür kommen insbesondere Kristallwasser enthaltende anorganische Salze in Frage, z.B. Na₂SO₄.1OH₂O, NH₄Fe(SO₄)₂.12H₂O, sowie auch Verbindungen vom Typ des Natriumbenztriazolats, die als Komplex mit verschiedenen Mengen Wasser (bis 24 mol H₂O) kristallisieren und die in US-A-4 418 139 beschrieben sind.
- Das bei der Erwärmung freigesetzte Wasser begünstigt die für die Bilderzeugung erforderlichen Entwicklungs- und Diffusionsvorgänge.
- Weitere wesentliche Hilfsstoffe sind gemäß vorliegender Erfindung die zuvor beschriebenen TEDM. Diese Verbindungen brauchen aber nicht notwendigerweise in der gleichen Schicht vorzuliegen, die auch das lichtempfindliche Silberhalogenid und den Farbspalter enthält. Es reicht vielmehr aus, wenn irgendeine Bindermittelschicht, die während der Wärmebehandlung mit den lichtempfindlichen Schichten in Kontakt steht, die genannten TEDM in der erforderlichen Menge enthält. Beim Erwärmen bildet das TEDM jedenfalls in den Schichten, die in die Entwicklungs- und Farbdiffusionsvorgänge einbezogen sind, ein geeignetes für die Entwicklungs- und Farbdiffusionsvorgänge förderliches solubilisierendes Medium. Das erfindungsgmäße TEDM kann somit in einer lichtempfindlichen Schicht, die Silberhalogenid und eine farbgebende Verbindung enthält, oder in einer nicht lichtempfindlichen Bindemittelschicht oder auch in mehreren der genannten Schichten enthalten sein. Es kann auch in einer Bildempfangsschicht enthalten sein, die sich auf dem gleichen Schichtträger befindet wie die lichtempfindlichen Schichten und mit jenen zusammen Bestandteil eines integralen Aufzeichnungsmaterials bildet. Desweiteren kann das TEDM auch in einer Bildempfangsschicht eines separaten Bildempfangsmaterials enthalten sein, sofern nur während der Wärmebehandlung ein Kontakt mit den lichtempfindlichen Schichten des wärmeentwickelbaren fotografischen Aufzeichnungsmaterials hergestellt wird.
- Schließlich kann das erfindungsgemäße TEDM auch in dispergierter Form in einem Hilfsblatt enthalten sein, das mit dem lichtempfindlichen Aufzeichnungsmaterial in Kontakt gebracht und mit ihm zusammen einer Wärmebehandlung unterworfen wird. Ein entsprechendes Verfahren ist beispielsweise DE-A-35 23 361 beschrieben.
- Das erfindungsgemäße TEDM kann auch, ohne daß dies den Rahmen der Erfindung sprengt, in Kombination mit einem oder mehreren der sogenannten thermischen Lösungsmittel des Standes der Technik verwendet werden, wie sie beispielsweise in DE-A-33 39 810, EP-A-0 119 615 und EP-A-0 122 512 beschrieben sind.
- Die Entwicklung des bildmäßig belichteten erfindungsgemäßen farbfotografischen Aufzeichnungsmaterials umfaßt die Teilschritte Silberhalogenidentwicklung, Erzeugung einer bildmäßigen Verteilung diffusionsfähiger Farbstoffe und Diffusionsübertragung dieser bildmäßigen Verteilung in die Bildempfangsschicht. Sie wird dadurch eingeleitet, daß man das belichtete Aufzeichnungsmaterial einer Wärmebehandlung unterzieht, bei der die lichtempfindliche Bindemittelschicht für eine Zeit von etwa 0,5 bis 300 s auf eine erhöhte Temperatur, z.B. im Bereich von 80 bis 250°C, gebracht wird. Hierdurch werden in dem Aufzeichnungsmaterial geeignete Bedingungen für die Entwicklungsvorgänge einschließlich der Farbstoffdiffusion geschaffen, ohne daß es der Zufuhr eines flüssigen Mediums, z.B. in Form eines Entwicklerbades bedarf. Bei der Entwicklung werden aus den Farbabspaltern bildmäßig diffusionsfähige Farbstoffe freigesetzt und auf eine Bildempfangsschicht übertragen, die entweder integraler Bestandteil des erfindungsgemäßen farbfotografischen Aufzeichnungsmaterials ist oder sich mit jenem zumindest während der Entwicklungszeit in Kontakt befindet. Hierbei finden in einem Einschritt-Entwicklungsprozeß bildmäßige Silberentwicklung, Farbstofffreisetzung und Farbtransfer synchron statt.
- Darüber hinaus kann die Farbbilderzeugung mit dem erfindungsgemäßen farbfotografischen Aufzeichnungsmaterial auch in einem Zweischritt-Entwicklungsprozeß erfolgen, wobei in einem ersten Schritt die Silberhalogenidentwicklung und Farbstofffreisetzung stattfindet, worauf in einem zweiten Schritt die Farbbildübertragung aus dem lichtempfindlichen Teil auf einen damit in Kontakt gebrachten Bildempfangsteil erfolgt, z.B. durch Erhitzen auf eine Temperatur zwischen 50 und 150°C, vorzugsweise auf 70 bis 90°C, wobei in diesem Fall vor dem Laminieren von lichtempfindlichem Teil und Bildempfangsteil noch Diffusionshilfsmittel (Lösungsmittel) extern angetragen werden können.
- Die Bildempfangsschicht kann demnach auf dem gleichen Schichtträger angeordnet sein wie das lichtempfindliche Element (Einzelblatt-Material) oder auf einem separaten Schichtträger (Zweiblatt-Material). Sie besteht im wesentlichen aus einem Bindemittel, das Beizmittel für die Festlegung der aus den nichtdiffundierenden Farb abspaltern freigesetzten diffusionsfähigen Farbstoffe enthält. Als Beizmittel für anionische Farbstoffe dienen vorzugsweise langkettige quaternäre Ammonium- oder Phosphoniumverbindungen, z.B. solche, wie sie beschrieben sind in US-A-3 271 147 und US-A-3 271 148.
- Ferner können auch bestimmte Metallsalze und deren Hydroxide, die mit den sauren Farbstoffen schwerlösliche Verbindungen bilden, verwandt werden. Weiterhin sind hier auch polymere Beizmittel zu erwähnen, wie etwa solche, die in DE-A-23 15 304, DE-A-26 31 521 oder DE-A-29 41 818 beschrieben sind. Die Farbstoffbeizmittel sind in der Beizmittelschicht in einem der üblichen hyrophilen Bindemittel dispergiert, z.B. in Gelatine, Polyvinylpyrrolidon, ganz oder partiell hydrolysierten Celluloseestern. Selbstverständlich können auch manche Bindemittel als Beizmittel fungieren, z.B. Polymerisate von stickstoffhaltigen, gegebenenfalls quaternären Basen, wie etwa von N-Methyl-4-vinylpyridin, 4-Vinylpyridin, 1-Vinylimidazol, wie beispielsweise beschrieben in US-A-2 484 430. Weitere brauchbare beizende Bindemittel sind beispielsweise Guanylhydrazonderivate von Alkylvinylketonpolymerisaten, wie beispielsweise beschrieben in der US-A-2 882 156, oder Guanylhydrazonderivate von Acylstyrolpolymerisaten, wie beispielsweise beschrieben in DE-A-20 09 498. Im allgemeinen wird man jedoch den zuletzt genannten beizenden Bindemitteln andere Bindemittel, z.B. Gelatine, zusetzen.
- Sofern die Bildempfangsschicht auch nach vollendeter Entwicklung in Schichtkontakt mit dem lichtempfindlichen Element verbleibt, befindet sich zwischen ihnen in der Regel eine alkalidurchlässige pigmenthaltige lichtreflektierende Bindemittelschicht, die der optischen Trennung zwischen Negativ und Positiv und als ästhetisch ansprechender Bildhintergrund für das übertragende positive Farbbild dient. Falls die Bildempfangsschicht zwischen Schichtträger und lichtempfindlichem Element angeordnet ist und von letzterem durch eine vorgebildete lichtreflektierende Schicht getrennt ist, muß entweder der Schichtträger transparent sein, so daß das erzeugte Farbübertragsbild durch ihn hindurch betrachtet werden kann, oder das lichtempfindliche Element muß mitsamt der lichtreflektierenden Schicht von der Bildempfangsschicht entfernt werden, um letztere freizulegen. Die Bildempfangsschicht kann aber auch als oberste Schicht in einem integralen farbfotografischen Aufzeichnungsmaterial vorhanden sein, in welch letzterem Fall die Belichtung zweckmäßigerweise durch den transparenten Schichtträger vorgenommen wird.
- Ein lichtempfindliches Element eines thermisch entwickelbaren fotographischen Aufzeichnungsmaterials gemäß der Erfindung wurde dadurch hergestellt, daß auf einen transparenten Träger aus Polyethylenterephthalat von 175 µm Dicke folgende Schichten nacheinander aufgetragen wurden. Die Mengenangaben beziehen sich dabei jeweils auf 1m².
- Eine Schicht mit einer grünsensibilisierten Silberhalogenidemulsion aus 0,5 g Silbernitrat mit einem Anteil von 4 mol-% Chlorid, 88,7 mol-% Bromid und 7,3 mol-% Iodid und einem Korndurchmesser von 0,3 µm, Silberbenzotriazolat aus 0,5 g Silbernitrat, 0,3 g Farbabspalter A, emulgiert in 0,15 g Diethyllauramid, und 1,5 g Gelatine.
- Eine Schicht bestehend aus 1 g Guanidiniumtrichloracetat, 0,03 g des Netzmittels B, 0,24 g 4-Methyl-4-hydroxy-methylphenidon, 0,06 g Natriumsulfit; 1,5 g Gelatine und 0,25 g bzw. 0,5 g bzw. 1,0 g der erfindungsgemäßen Verbindung TEDM-1.
- Eine Härtungsschicht bestehend aus 0,5 g Gelatine und 0,15 g Härtungsmittel CAS Reg.-Nr. 65 411-60-1.
- Das so hergestellte lichtempfindliche Element wird als Material 1 bezeichnet. Weitere Materialien 2 und 3 wurden hergestellt, die sich von Material 1 dadurch unterschieden, daß die erfindungsgemäße Verbindung TEDM-1 in Schicht 2 in veränderten Mengen verwendet wurde und zwar
Material 2 - 0,5 g
Material 3 - 1,0 g - Ein weiteres Material 4 wurde als Vergleichsmaterial hergestellt, das die angegebenen Schichten aufwies, jedoch in Schicht 2 kein TEDM enthielt.
- Ein Bildempfangselement wurde dadurch hergestellt, daß auf einen Schichtträger aus mit Polyethylen kaschiertem Papier folgende Schichten aufgetragen wurden. Die Mengenangaben beziehen sich auch hier jeweils auf 1 m².
- Eine Beizschicht bestehend aus 2 g Polyurethanbeize aus 4,4ʹ-Diphenylmethandiisocyanat und N-Ethyldiethanolamin, quaterniert mit Epichlorhydrin (gemäß DE-A-26 31 521, Herstellungsbeispiel 1), 0,035 g Netzmittel B und 2 g Gelatine.
- Eine Härtungsschicht bestehend aus 0,8 g Gelatine und 0,5 g des bereits erwähnten Härtungsmittels.
- Nach der Belichtung des lichtempfindlichen Elements (Materialien 1-4) durch einen Stufenkeil erfolgte die Verarbeitung in zwei Schritten. Im ersten Prozeßschritt wurde das lichtempfindliche Element 60 s bei 115°C behandelt. Dies erfolgte mit Hilfe einer Heizplatte, wobei das Material mit einer weiteren Platte abgedeckt wurde. Im zweiten Prozeßschritt wurde das Bildempfangselement nach Eintauchen in Wasser auf das bereits wärmebehandelte, lichtempfindliche Element auflaminiert, und der so gebildete Set wurde dann unter Andruck analog dem ersten Prozeßschritt für 2 min bei 70°C behandelt. Während dieser Zeit erfolgte der Farbübertrag aus dem lichtempfindlichen Element in das Bildempfangselement. Danach wurden beide Schichtelemente voneinander getrennt. Das Bildempfangselement zeigte ein purpurfarbenes Negativbild von der Belichtungsvorlage.
-
- Wie Tabelle 1 zeigt, ist bei Zusatz der erfindungsgemäßen Verbindung TEDM-1 im Vergleich zum Schichtaufbau ohne Zusatz ein deutlicher Dichteanstieg zu beobachten, ohne daß sich im gleichen Verhältnis die Minimaldichten erhöhten.
Claims (7)
X -SO₂- oder -CO-;
R¹ - R⁴ Alkyl, Cycloalkyl, Aralkyl oder Aryl;
R⁵, R⁶ Acyl oder einen Rest wie angegeben für R¹ -R⁴;
wobei R¹ zusammen mit R⁵, R² zusammen mit R⁶, R³ zusammen mit R⁴ und/oder R¹ zusammen mit R² jeweils einen mindestens ein Stickstoffatom enthaltenden heterocyclischen Ring bilden können.
l und m jeweils 0,1 oder 2 stehen, wobei jedoch l und m nicht gleichzeitig 0 sein können.
X -SO₂- oder -CO-;
R¹ - R⁴ Alkyl, Cycloalkyl, Aralkyl oder Aryl;
R⁵, R⁶ Acyl oder einen Rest wie angegeben für R¹ -R⁴;
wobei R¹ zusammen mit R⁵, R² zusammen mit R⁶, R³ zusammen mit R⁴ und/oder R¹ zusammen mit R² jeweils einen mindestens ein Stickstoffatom enthaltenden heterocyclischen Ring bilden können.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE19863632737 DE3632737A1 (de) | 1986-09-26 | 1986-09-26 | Waermeentwicklungsverfahren und hierfuer geeignetes farbfotografisches aufzeichnungsmaterial |
| DE3632737 | 1986-09-26 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| EP0261567A2 true EP0261567A2 (de) | 1988-03-30 |
| EP0261567A3 EP0261567A3 (de) | 1989-09-06 |
Family
ID=6310418
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP87113515A Withdrawn EP0261567A3 (de) | 1986-09-26 | 1987-09-16 | Wärmeentwicklungsverfahren und hierfür geeignetes farbfotografisches Aufzeichnungsmaterial |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US4816372A (de) |
| EP (1) | EP0261567A3 (de) |
| JP (1) | JPS6389849A (de) |
| DE (1) | DE3632737A1 (de) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6114080A (en) * | 1993-12-21 | 2000-09-05 | Eastman Kodak Company | Chromogenic black and white imaging for heat image separation |
| CA2215849A1 (en) * | 1997-09-11 | 1999-03-11 | Christophe Michot | New solvent and electrolytic composition with high conductivity and wide stability range |
| US7694887B2 (en) | 2001-12-24 | 2010-04-13 | L-1 Secure Credentialing, Inc. | Optically variable personalized indicia for identification documents |
| CA2470547C (en) | 2001-12-24 | 2008-05-20 | Digimarc Id Systems, Llc | Laser etched security features for identification documents and methods of making same |
| CA2470600C (en) | 2001-12-24 | 2009-12-22 | Digimarc Id Systems, Llc | Systems, compositions, and methods for full color laser engraving of id documents |
| US7728048B2 (en) | 2002-12-20 | 2010-06-01 | L-1 Secure Credentialing, Inc. | Increasing thermal conductivity of host polymer used with laser engraving methods and compositions |
| ATE552120T1 (de) | 2001-12-24 | 2012-04-15 | L 1 Secure Credentialing Inc | Verdeckte variableninformationen auf id- dokumenten und verfahren zu ihrer herstellung |
| CA2671998A1 (en) * | 2001-12-24 | 2003-07-10 | Digimarc Id Systems, Llc | Laser engraving methods and compositions, and articles having laser engraving thereon |
| WO2003088144A2 (en) | 2002-04-09 | 2003-10-23 | Digimarc Id Systems, Llc | Image processing techniques for printing identification cards and documents |
| US7824029B2 (en) | 2002-05-10 | 2010-11-02 | L-1 Secure Credentialing, Inc. | Identification card printer-assembler for over the counter card issuing |
| AU2003298731A1 (en) | 2002-11-26 | 2004-06-18 | Digimarc Id Systems | Systems and methods for managing and detecting fraud in image databases used with identification documents |
| US7763179B2 (en) * | 2003-03-21 | 2010-07-27 | Digimarc Corporation | Color laser engraving and digital watermarking |
| DE602004030434D1 (de) | 2003-04-16 | 2011-01-20 | L 1 Secure Credentialing Inc | Dreidimensionale datenspeicherung |
| PL440023A1 (pl) | 2021-12-29 | 2023-07-03 | Polska Wytwórnia Papierów Wartościowych Spółka Akcyjna | Sposób wytwarzania podłoża polimerowego ulegającego karbonizacji opatrzonego wyczuwalnym w dotyku oznakowaniem w postaci reliefu z efektem płaskorzeźby, oraz wytworzone tym sposobem zabezpieczone podłoże polimerowe |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS588690A (ja) * | 1981-07-10 | 1983-01-18 | Mitsubishi Paper Mills Ltd | 定着可能な多色発色感熱記録体 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3667959A (en) * | 1970-05-01 | 1972-06-06 | Eastman Kodak Co | Photosensitive and thermosensitive element,compositions and process |
| JPS5456423A (en) * | 1977-10-14 | 1979-05-07 | Asahi Chemical Ind | Thermal silver picture forming material |
| JPS59182446A (ja) * | 1983-04-01 | 1984-10-17 | Fuji Photo Film Co Ltd | 熱現像カラー感光材料およびそれを用いた画像形成方法 |
| JPS61132952A (ja) * | 1984-11-30 | 1986-06-20 | Fuji Photo Film Co Ltd | 色素転写方法 |
-
1986
- 1986-09-26 DE DE19863632737 patent/DE3632737A1/de not_active Withdrawn
-
1987
- 1987-09-14 US US07/095,904 patent/US4816372A/en not_active Expired - Fee Related
- 1987-09-16 EP EP87113515A patent/EP0261567A3/de not_active Withdrawn
- 1987-09-25 JP JP62240577A patent/JPS6389849A/ja active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS588690A (ja) * | 1981-07-10 | 1983-01-18 | Mitsubishi Paper Mills Ltd | 定着可能な多色発色感熱記録体 |
Non-Patent Citations (1)
| Title |
|---|
| PATENT ABSTRACTS OF JAPAN, Band 7, Nr. 81 (M-205)[1226], 5. April 1983, Seite 123 M 205; & JP-A-58 008 690 (MITSUBISHI SEISHI K.K.) 18-01-1983 * |
Also Published As
| Publication number | Publication date |
|---|---|
| US4816372A (en) | 1989-03-28 |
| DE3632737A1 (de) | 1988-03-31 |
| JPS6389849A (ja) | 1988-04-20 |
| EP0261567A3 (de) | 1989-09-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0261567A2 (de) | Wärmeentwicklungsverfahren und hierfür geeignetes farbfotografisches Aufzeichnungsmaterial | |
| DE2228361A1 (de) | Farbphotographisches diffusionsuebertragungsverfahren und zugehoeriges photographisches material | |
| EP0207401A2 (de) | Wärmeentwicklungsverfahren und hierfür geeignetes Hilfsblatt | |
| DE3345023C2 (de) | ||
| EP0222271A2 (de) | Wärmeentwicklungsverfahren und hierfür geeignetes farbfotografisches Aufzeichnungsmaterial | |
| EP0295507A2 (de) | Farbfotografisches Wärmeentwicklungsverfahren | |
| EP0250954B1 (de) | Farbfotografisches Aufzeichnungsmaterial mit einem Farbabspalter für blaugrüne Farbstoffe und ein mit diesen Farbstoffen erzeugtes Farbbild | |
| EP0247474B1 (de) | Durch Wärmebehandlung entwickelbares farbfotografisches Aufzeichnungsmaterial | |
| EP0212534B1 (de) | Durch Wärmebehandlung entwickelbares farbfotografisches Aufzeichnungsmaterial | |
| DE3514186A1 (de) | Durch waermebehandlung entwickelbares farbfotografisches aufzeichnungsmaterial | |
| EP0215356B1 (de) | Wärmeentwicklungsverfahren und hierfür geeignetes Bildempfangsblatt | |
| EP0226953A2 (de) | Farbfotografisches Aufzeichnungsmaterial | |
| EP0035685B1 (de) | Photographisches Aufzeichnungsmaterial für Diffusionsverfahren und hierfür geeignete neue nichtdiffundierende Sulfiliminverbindungen | |
| EP0267522B1 (de) | Fotografisches Aufzeichnungsmaterial | |
| EP0195979A2 (de) | Durch Wärmebehandlung entwickelbares farbfotografisches Aufzeichnungsmaterial | |
| EP0265808A2 (de) | Fotografisches Farbdiffusionsübertragungsverfahren und hierfür geeignetes farbfotografisches Aufzeichnungsmaterial | |
| EP0295492B1 (de) | Farbdiffusionsverfahren | |
| EP0247478B1 (de) | Durch Wärmebehandlung entwickelbares farbfotografisches Aufzeichnungsmaterial | |
| DE2630999A1 (de) | Lichtempfindliches diffusionsuebertragungselement | |
| DE3613621A1 (de) | Farbfotografisches aufzeichnungsmaterial mit einem farbabspalter fuer blaugruene farbstoffe, ein mit diesen fabstoffen erzeugtes farbbild und die farbstoffe selbst | |
| EP0056940B1 (de) | Neue Phthalocyaninverbindungen, ein farbfotografisches Aufzeichnungsmaterial, das die neuen Phthalocyaninverbindungen enthält sowie ein farbfotografisches Bild, das aus den Phthalocyaninverbindungen freigesetzte Phthalocyaninfarbstoffe als Bildfarbstoffe enthält | |
| EP0247473A2 (de) | Durch Wärmebehandlung entwickelbares farbfotografisches Aufzeichnungsmaterial | |
| EP0078959A1 (de) | Farbfotografisches Aufzeichnungsmaterial mit nicht diffundierenden Elektronendonor-Vorläuferverbindungen | |
| DE3704686A1 (de) | Farbdiffusionsverfahren | |
| DE3530238A1 (de) | In der waerme entwickelbares lichtempfindliches material |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| 17P | Request for examination filed |
Effective date: 19870916 |
|
| AK | Designated contracting states |
Kind code of ref document: A2 Designated state(s): BE DE FR GB NL |
|
| PUAL | Search report despatched |
Free format text: ORIGINAL CODE: 0009013 |
|
| AK | Designated contracting states |
Kind code of ref document: A3 Designated state(s): BE DE FR GB NL |
|
| 17Q | First examination report despatched |
Effective date: 19910408 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: THE APPLICATION HAS BEEN WITHDRAWN |
|
| 18W | Application withdrawn |
Withdrawal date: 19910423 |
|
| R18W | Application withdrawn (corrected) |
Effective date: 19910423 |
|
| RIN1 | Information on inventor provided before grant (corrected) |
Inventor name: SCHENK, GUENTHER, DR. Inventor name: PETERS, MANFRED, DR. |