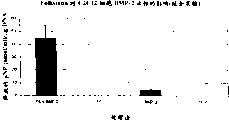CN1538850A - 用于骨或软骨再生的bmp结合蛋白 - Google Patents
用于骨或软骨再生的bmp结合蛋白 Download PDFInfo
- Publication number
- CN1538850A CN1538850A CNA028153421A CN02815342A CN1538850A CN 1538850 A CN1538850 A CN 1538850A CN A028153421 A CNA028153421 A CN A028153421A CN 02815342 A CN02815342 A CN 02815342A CN 1538850 A CN1538850 A CN 1538850A
- Authority
- CN
- China
- Prior art keywords
- bmp
- protein
- follistatin
- collagen protein
- collagen
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/04—Macromolecular materials
- A61L31/043—Proteins; Polypeptides; Degradation products thereof
- A61L31/044—Collagen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/02—Prostheses implantable into the body
- A61F2/28—Bones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/02—Prostheses implantable into the body
- A61F2/30—Joints
- A61F2/30756—Cartilage endoprostheses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/177—Receptors; Cell surface antigens; Cell surface determinants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/04—Macromolecular materials
- A61L31/043—Proteins; Polypeptides; Degradation products thereof
- A61L31/047—Other specific proteins or polypeptides not covered by A61L31/044 - A61L31/046
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
- C07K14/4701—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals not used
- C07K14/4702—Regulators; Modulating activity
- C07K14/4703—Inhibitors; Suppressors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/78—Connective tissue peptides, e.g. collagen, elastin, laminin, fibronectin, vitronectin, cold insoluble globulin [CIG]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/02—Prostheses implantable into the body
- A61F2/28—Bones
- A61F2002/2817—Bone stimulation by chemical reactions or by osteogenic or biological products for enhancing ossification, e.g. by bone morphogenetic or morphogenic proteins [BMP] or by transforming growth factors [TGF]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2310/00—Prostheses classified in A61F2/28 or A61F2/30 - A61F2/44 being constructed from or coated with a particular material
- A61F2310/00005—The prosthesis being constructed from a particular material
- A61F2310/00365—Proteins; Polypeptides; Degradation products thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Heart & Thoracic Surgery (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Vascular Medicine (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Pharmacology & Pharmacy (AREA)
- Rheumatology (AREA)
- Gastroenterology & Hepatology (AREA)
- Zoology (AREA)
- Epidemiology (AREA)
- Physical Education & Sports Medicine (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Molecular Biology (AREA)
- Transplantation (AREA)
- Toxicology (AREA)
- Cardiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Biomedical Technology (AREA)
- General Chemical & Material Sciences (AREA)
- Surgery (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Immunology (AREA)
- Cell Biology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Materials For Medical Uses (AREA)
Abstract
本发明涉及一种用于组织再生(如骨和/或软骨组织)的药物或装置,其中该药物或装置包含BMP结合蛋白。
Description
本发明主要涉及骨和软骨的生物学领域,并涉及提供促进组织(例如:骨和/或软骨)形成的方法、药用组合物/药物和装置以及制造包含这类组合物的诸如修复术性的装置。
骨
脊椎动物的骨作为一种对肌体提供机械性支持的组织,通过骨的形成和再吸收(目前广泛认为分别通过成骨细胞和破骨细胞的活性介导)经历持续性的再建。骨再建包含着细胞和细胞外基质间(ECM)间复杂和高度组织性的相互作用。然而,这种再建过程根据对生长或日常性活动的需要而调整。在一个正常健康成人的骨骼中,在称为骨再建的过程中,骨形成的速率与骨再吸收的速率大致相同。尽管骨的再吸收或形成不是整个骨骼同时发生的一个综合特征,但是却出现在可被静态骨区域包围的不同位置中。当出现过度再吸收时,或者在骨骼的特定区域或者在骨骼的更广泛的区域,可出现多种临床问题。
例如:骨质疏松症是一种以骨组织的数量和结构排列出现异常为特征的疾病。骨质疏松症是一种主要临床症状,其可导致只有极小外伤的骨折。骨质疏松症是由于骨的再吸收和形成之间的平衡向再吸收偏离而使纯骨量减少所引起。除患者的痛苦外,据估计直接用于骨质疏松症的医院费用仅在美国就将近130亿美元,在英国就将近7.5亿英镑。术语“骨质疏松症”实际上指的是与骨组织丢失并伴随着出现在松质骨空间中的结构异常相关的一组症状。当绝经期后妇女出现该症状时,其被称为绝经后骨质疏松症。骨折通常发生在臀、脊骨和桡骨末梢处,在许多国家被认为是主要的公众健康问题(Lindsay R(1993),Clinical Rheumatology Osteoporisis;V.7,No.3)。虽然遗传、饮食和生活方式似乎是该病发病的要素,但至少对于绝经后骨质疏松症,卵巢功能的丧失是一个重要的决定性因素。
骨质疏松症中骨形成水平低下的一个原因是活性成骨细胞数量的减少。因此,可将能够增加这些细胞数量的药物用在以低骨质为特征的症状中。
与骨质疏松相关的其它病症包括类固醇诱发的骨质疏松症,先天性幼年骨质疏松症和移植术后骨质疏松症,其中骨再吸收是疾病的一种继发病症。
在称为变形性骨炎的疾病中,存在骨的破骨细胞过度再吸收,从而引起过多的成骨细胞的骨形成,导致骨结构的紊乱。
长期卧床休息或各种原因的残疾与骨疾没有必然的直接联系,但在再运动或恢复活动能力上会导致骨丢失和骨折的危险。
在癌症中,原发和继发肿瘤的形成常引起再吸收和/或形成,从而增大骨折或功能损坏的倾向。
肿瘤诱导的骨质疏松症也会导致病态性血清钙水平的上升,目前认为这一点能明显增加癌症患者的病态。
目前已采用多种方法来治疗低骨质症,这些方法以使用可减少或抑制骨丢失的抗再吸收药物(例如二膦酸盐)为基础,但由于骨形成继发性增加出现缓慢,这些方法无一能十分满足要求。
使用二膦酸盐抑制骨再吸收仍不理想,原因是由于某些患者认为该类药物副作用程度过高,不可接受,很大比例的人群不能完全忍受使用该类药物。
雌激素和其它激素替代品单独或联合其它治疗剂用于绝经期后骨质疏松症已有一段历史。但是,由于子宫内膜癌和乳癌风险的增加以及持续性经血,这在占骨质疏松症大多数受害者的老年妇女人群中通常是不受欢迎的,因此需要提供另一种治疗方法。
目前已采用使用影响破骨细胞功能的药物(如降钙素或甲状旁腺激素)的其它疗法治疗骨质疏松症,但鲜有成功。
除对骨再生率具有影响的疾病和症状外,物理性碰撞和意外也会导致骨折。
仅在美国,估计每年的骨折率约为6百万例。
目前骨修复最好的方法为机械方法,该方法一般包含硬植入物和金属元件,例如钢板、针和螺钉。硬植入物的种类中包括塑料、有机合成粘合剂和金属修补物。在使用机械性金属元件和植入时,有两个主要的需要考虑和关心的事项。首先涉及的是金属进入机体系统的生理学综合效力,其次是被植入的非生物性材料的长期耐用性问题。尽管存在这些问题,机械植入仍很受欢迎,虽然植入物不包含活骨组织,但对帮助骨的重建有重大贡献。
当骨完全折断时,除简单固定(上石膏)外,折断的重要部分需要医治。这种情况下主要的问题是两骨末端不够接近。这样导致不适于修复且修复过程延长,从而妨碍痊愈。机体修复骨折至能适度承载的平均时间为25-100天,完全恢复则需一年。因而,单纯性骨折和医学上的复杂型骨折都受益于能加速和/或完成恢复过程的新的治疗手段。对于那些骨疾(指的是如骨质疏松症或骨质减少)同样如此,导致骨变薄,其原发症状为常见的衰老性骨折。
一直以来在进行某些研究,采用外源性生长因子(例如骨形态发生蛋白(BMP))帮助骨的再生。采用该方法将极大量的生长因子(例如BMP)给予到损伤的骨的部位。然而这种方法有其缺点,即高浓度的生长因子能引起生物学平衡的偏移,从而可能使该生长因子的效用降低。
使用生长因子(例如BMP)的另一个问题是90%的外源性生长因子在用后头二十四小时可被排出,这表明大多数的生长因子未达到其靶细胞。
在先前有关BMP和BMP结合蛋白(例如Follistatin)的研究中,认为Follistatin通过BMP结合而抑制BMP作用(Follistatin,KetanPatel,The International Journal of Biochemistry & Cell Biology 30(1998)1087-1093;Direct binding of Follistatin to a complex of bone-morphogenic protein and its receptor inhibits ventral and epidermal cellfates in early xenopus embryo,Shar-Lchiro lemura etal,Proc.Natl.Acs.Sci.USA.Vol.95 pp 9337-9342 August 1998Developmental Biology.)。这种BMP结合蛋白(如Follistatin)与BMP结合,产生失活的BMP,因而这一点是可信的。因此,认为BMP结合蛋白(例如Follistatin)通过抑制BMP活性抑制骨形成。
然而我们惊讶地发现与这些已确立的定理相反的是,当通过直接给予BMP结合蛋白(例如Follistatin)治疗缺陷性特征的疾病时,可促进细胞的分化和/或增殖。
我们发现BMP结合蛋白(例如Follistatin)增大基质干细胞、成肌细胞和未分化的基质干细胞至成骨细胞的分化。
软骨
软骨的自身恢复能力有限。
物理碰撞会损伤机体的软骨。受损软骨易于进一步恶化,即骨关节炎。
以关节软骨坏损为特征的骨关节炎症(OA)也会在无任何极小损伤的情况下发生。该病影响至少有1600万的美国人,75岁以上老人中80%患有该病。随着人口老龄化,其相关问题增加,并使健康服务的负担变得越来越大。
软骨的主要组成是胶原蛋白。
胶原蛋白是自然界最丰富的动物蛋白质之一。它存在于所有类型的多细胞动物(包括人类)中,现估计它约占整个人体蛋白质的30%。胶原蛋白构成软的结缔组织的纤维组分(如皮肤,韧带和腱),并且是钙化组织(如骨、牙质)的有机基质的主要成分。除了它结构上的意义外,胶原蛋白在生长和伤口愈合中起着重要的作用,并且还与衰老和一些疾病过程有关。
有几种遗传性不同类型的胶原蛋白,被称为I型、II型、III型等等。II型胶原蛋白是软骨的主要胶原蛋白。它由软骨细胞合成为原胶原分子,该原胶原分子具有非胶原蛋白性氨基前肽和羧基肽突出端。通过特定的肽酶除去这两种突出端,然后将II型胶原蛋白与原纤维结合。
术语软骨指动物或人体的任何软骨,包括但不限于:关节软骨、透明软骨、半月板软骨和黄弹性软骨。
因此,目前需要一种方法来增强软骨的生长、恢复和再生。
本发明另一方面的目标是提供一种新的组织再生的方法。
本发明再一方面的目标是提供一种帮助组织再生的组合物。
本发明一个目标是提供一种促进骨形成的组合物,其可作为目前推荐疗法(如二膦酸盐、甲状旁腺素(PTH)及其衍生物)的替代方法,用于治疗骨缺陷和骨异常。
本发明一个目标是提供一种结合骨形态发生蛋白(BMP)的支架结构,用以控制BMP释放。
本发明另一个目标是提供一种控制释放所结合的BMP的方法。
本发明再一个目标是提供一种帮助组织再生的支架结构。
本发明一个目标是提供一种新的软骨再生方法。
本发明一个目标是提供一种帮助软骨再生的支架。
本发明一个目标是提供一种帮助内源性或外源性BMP到达其靶细胞的支架。
本发明一个目标是提供一种供软骨形成的支架,它是目前的推荐疗法(如镶嵌塑料、自体软骨细胞移植法和组织工程学方法)的一种替代疗法。
本发明提供一种含有BMP结合蛋白的药物。
本发明还提供一种含有帮助组织再生的BMP结合蛋白的药物。
在本申请中,术语“药物”和“药用组合物”具有相同的含义。
术语BMP结合蛋白指能与BMP家族蛋白质结合的任何蛋白质。所述BMP结合蛋白优选结合BMP以提高BMP的活性,例如:增强组织的再生。术语BMP结合蛋白包括(但绝不限于)以下蛋白质:Follistatin、Follistatin相关的蛋白质(FSRP)、FLIK、α-2-HS糖蛋白、胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Chordin、Sog、Crim、Nell、结缔组织生长因子(CTGF)、Dan、Gremlin、Cerberus、Endoglin、Twisted Gastulation基因、ZFSTA2及其以上提到的蛋白质的衍生物、片段和/或类似物。
一组典型的BMP结合蛋白包括“Follistatin”组,其包括Follistatin、Follistatin相关的蛋白质(FSRP)、ZFSTA2、FLIK以及以上提到的BMP蛋白的衍生物、片段和/或类似物。
另一组典型的BMP结合蛋白包括“富含半胱氨酸”的BMP结合蛋白,其包括胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Chordin、Sog、Crim、Nell、结缔组织生长因子(CTGF)及以上提到的BMP蛋白的衍生物、片段和/或类似物。
另一组典型的BMP结合蛋白包括“Cerberus”BMP结合蛋白,其包括Cerberus、Gremlin、Dan及以上提到的BMP蛋白的衍生物、片段和类似物。
此外一组适合的BMP结合蛋白包括Follistatin、胶原蛋白IIa、胶原蛋白IV、Chordin、Nell、Crim及以上提到的蛋白质的衍生物、片段和类似物。
适宜的BMP结合蛋白包括Follistatin、FLIK、胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Endoglin、Dan、Gremlin、Cerberus、Chordin、Sog、Crim、Nell或以上提到的蛋白质的衍生物、片段和/或类似物。
所述BMP结合蛋白一般可以是Follistatin或胶原蛋白IIa或Follistatin或胶原蛋白IIa的衍生物、片段和/或类似物。
所述BMP结合蛋白最适合是Follistatin。或者在本发明的某些方面,BMP结合蛋白可以是胶原蛋白IIa。在本发明的其它方面,BMP结合蛋白可以是Endoglin。
本发明提供一种包含选自以下的蛋白质的药用组合物:Follistatin、FSRP、FLIK、ZFSTA2、α-2-HS糖蛋白、胶原蛋白Iia、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Chordin、Sog、Crim、Nell、结缔组织生长因子(CTGF)、Dan、Gremlin、Cerberus、Endoglin、Noggin、Twisted Gastulation基因、ZFSTA2或以上提到的BMP蛋白质的衍生物、片段和/或类似物。
本发明还提供一种包含选自以下的蛋白质的药用组合物:Follistatin、FSRP、FLIK、α-2-HS糖蛋白、胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Chordin、Sog、Crim、Nell、结缔组织生长因子(CTGF)、Dan、Gremlin、Cerberus、Endoglin、Noggin、Twisted Gastulation基因、ZFSTA2或以上提到的BMP蛋白质的衍生物、片段和/或类似物。
本发明适宜的BMP结合蛋白质包括:Follistatin、FSRP、ZFSTA2、FLIK、α-2-HS糖蛋白、胶原蛋白Iia、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Chordin、Sog、Crim、Nell、结缔组织生长因子(CTGF)、Dan、Gremlin、Cerberus、Endoglin、Twisted Gastulation基因或以上提到的BMP结合蛋白质的衍生物、片段和/或类似物。
本发明的BMP结合蛋白质一般包括:Follistatin、FLIK、α-2-HS糖蛋白、Nell、Crim、Endoglin及以上提到的BMP结合蛋白质的衍生物、片段和/或类似物。
例如本发明一组适宜的BMP结合蛋白质包括胶原蛋白型蛋白质,即胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1和胶原蛋白Vα2或以上提到的BMP结合蛋白质的衍生物、片段和/或类似物。
本发明另一组适宜的BMP结合蛋白例如为Endoglin、Dan、Sog、Crim、Nell和Chordin或以上提到的BMP结合蛋白的衍生物、片段和/或类似物。
本发明再一组适宜的BMP结合蛋白例如为Sog、Crim、Nell及以上提到的BMP结合蛋白的衍生物、片段和/或类似物。
本发明再一组适宜的BMP结合蛋白为Cerberus、Chordin、FLIK及其衍生物、片段和/或类似物。
所述BMP结合蛋白一般是Follistatin。
所述BMP结合蛋白一般是胶原蛋白IIa或其衍生物、片段和/或类似物。
在本发明的某些方面,BMP结合蛋白是Crim或其衍生物、片段或类似物。在本发明的其它方面,BMP结合蛋白是Dan或其衍生物、片段和/或类似物。在本发明的特定实施方案中,BMP结合蛋白是ZFSTA2或其衍生物、片段或类似物。在本发明的其它实施方案中,BMP结合蛋白是Endoglin或其衍生物、片段或类似物。同样地,本发明的BMP结合蛋白可以是Nell或其衍生物、片段或类似物。本发明的其它实施方案可包含作为BMP结合蛋白的BMP结合蛋白Nell或其衍生物、片段或类似物
术语BMP指BMP超家族的骨形成蛋白,它包括但不限于:
BMP-2、
BMP-3、
BMP-3B/GDF-10、
BMP-4、
BMP-5、
BMP-6、
BMP-7/OP-1、
BMP-8/OP-2、
BMP-8B、
BMP-9、
BMP-10、
BMP-11、
BMP-12、
BMP-13、
BMP-14、
CDMP-1、
CDMP-2、
CDMP-3、
GDF-1、
GDF-2、
GDF-3、
GDF-4、
GDF-5/CDMP-1/BMP-14、
GDF-6/CDMP-2/BMP-13、
GDF-7/CDMP-3/BMP-12、
GDF-8、
GDF-9。
在本发明的某些方面,BMP可以是例如已发现的天然存在于体内的内源性BMP,或者可以是加入到治疗部位的天然BMP。在本发明的其它方面,例如:BMP可以是或可以包括BMP重组体。
适合的BMP包括BMP-2、BMP-5、BMP-4、BMP-6和BMP-7。
一组典型的BMP包括BMP-5、BMP-6、BMP-7、BMP-8/OP-2和BMP-8B。另一组典型的BMP包括BMP-2和BMP-4。另一组典型的BMP还包括BMP3和BMP3B/GDF-10。此外,再一组典型的BMP包括GDF-5/CDMP-1/BMP-14、GDF-6/CDMP-2/BMP-13、GDF-7/CDMP-3/BMP-12。BMP一般可以是GDF-9。在本发明的其它实施方案中,BMP也可以是GDF3。本发明的适当的BMP可以包括BMP-2、BMP-4、BMP-6和BMP-7。
在本发明的具体实施方案中,BMP可以是在治疗部位发现的内源性BMP的混合物。在本发明的其它方面,可将重组BMP加入到治疗部位,或者加入构成本发明的装置中以确保BMP的存在。在本发明的某些实施方案中,BMP可以包括BMP-2。或者在本发明的某些实施方案中可包括BMP-4。另外,在本发明的其它实施方案中,BMP可以是BMP-7。同样地,再其它实施方案中,BMP可以是BMP-6。
本发明的实施方案还提供一种包含BMP结合蛋白的药物。
本发明进一步提供一种包含选自下列BMP结合蛋白的药物:Follistatin、FSRP、FLIK、ZFSTA2、α-2-HS-糖蛋白、胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Chordin、Sog、Crim、Nell、结缔组织生长因子(CTGF)、Dan、Gremlin、Cerberus、Endoglin、Twisted Gastulation基因或本文上以上提到的BMP结合蛋白质的衍生物、片段和/或类似物。
本发明再进一步提供一种包含选自下列BMP结合蛋白的药物:Follistatin、FSRP、ZFSTA2、FLIK、胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Endoglin、Dan、Gremlin、Cerberus、Chordin、Sog、Crim、Nell或以上提到的BMP结合蛋白质的衍生物、片段和/或类似物。
这类药物可用于治疗组织再生,例如骨和/或软骨组织的再生。
本发明提供一种包含选自以下的蛋白质的药用组合物:促卵胞抑制素(一种氨基酸序列(1)描述的蛋白质)或其衍生物、片段和/或类似物。
本发明还提供一种促进组织生成的药用组合物,其中该药用组合物包含选自促卵胞抑制素(一种以下氨基酸序列(1)描述的蛋白质)或其衍生物、片段和/或类似物的蛋白质。
所述氨基酸序列(I)是:
(I)
1 mvrarhqpgg lcllllllcq fmedrsaqa-g ncwlrqakng rcqvlyktel skeeccstgr
61 lstswteedv ndntlfkwmi fnggapncip cketcenvdc gpgkkcrmnkknkprcvcap
121 dcsnitwkgp vcgldgktyr necallkarc keqpelevqy qgrckktcrdvfcpgsstcv
181 vdqtnnaycv tcnricpepa sseqylcgnd gvtyssachl rkatcllgrs iglayegkci
241 kakscediqc tggkkclwdf kvgrgrcslc delcpdsksd epvcasdnatyasecamkea
301 acssgvllev khsgscneee eededqdysf pissilew
所述组织最好可是骨组织,因此本发明可以用于促进骨的生长。所述组织也可以是中枢神经系统组织,因此本发明可以用于促进中枢神经系统的生长和/或恢复,例如帮助中风病人的复原。
所述组织也可以是软骨细胞/软骨组织,因此本发明可以用于促进软骨生长和/或修复。
本发明还提供一种药物,其含有选自促卵胞抑制素(一种氨基酸序列(1)描述的蛋白质)或其片段和/或类似物的蛋白质。
本发明还提供一种用于治疗以骨缺陷为特征的疾病或临床症状的药物,其包含选自促卵胞抑制素(一种氨基酸序列(1)描述的蛋白质)或其片段的蛋白质。
本发明还提供BMP结合蛋白在制备一种药物中的用途,该药物用于治疗可通过促进组织再生(例如软骨和/或骨组织再生)而缓解的疾病或临床症状。
本发明进一步提供BMP结合蛋白在制备一种药物中的用途,该药物用于治疗可通过促进组织再生(例如软骨和/或骨组织再生)而缓解的疾病或临床症状,其中所述蛋白选自:Follistatin、FSRP、ZFSTA2、FLIK、α-2-HS-糖蛋白、胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Chordin、Sog、Crim、Nell、结缔组织生长因子(CTGF)、Dan、Gremlin、Cerberus、Endoglin、Twisted Gastulation基因或以上提到的BMP结合蛋白质的衍生物、片段和/或类似物。
本发明再进一步提供BMP结合蛋白在制备一种药物中的用途,该药物用于治疗可通过促进组织再生(例如软骨和/或骨组织再生)而缓解的疾病或临床症状,其中所述蛋白选自:Follistatin、FSRP、ZFSTA2、FLIK、α-2-HS-糖蛋白、胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Endoglin、Dan、Gremlin、Cerberus、Chordin、Sog、Crim、Nell或以上提到的BMP结合蛋白质的衍生物、片段和/或类似物。
因此,本发明提供一种能结合BMP的蛋白质在制备一种药物中的用途,该药物用于治疗可通过促进骨的形成而缓解的疾病或临床症状,其中所述蛋白质选自促卵胞抑制素(一种本文列出的氨基酸序列(1)描述的蛋白质)或其片段和/或类似物。
因此,本发明提供一种能结合BMP的蛋白质在制备一种药物中的用途,该药物用于治疗可通过促进组织生成(例如骨形成、软骨形成或中枢神经系统的组织形成)而缓解的疾病或临床症状,其中所述蛋白质选自促卵胞抑制素(一种以下列出的氨基酸序列(1)描述的蛋白质)或其片段和/或类似物。
本发明另一方面提供一种治疗可通过促进骨形成而缓解的疾病或临床症状的方法,该方法包括给予治疗有效量的能结合BMP的蛋白质这一步骤,其中所述蛋白质选自促卵胞抑制素(一种本文列出的氨基酸序列(1)描述的蛋白质)或其片段和/或类似物。
本发明再一方面提供一种预防可通过促进骨形成而缓解的疾病或临床症状的方法,该方法包括给予治疗有效量的能结合BMP的蛋白质这一步骤,其中所述蛋白质选自促卵胞抑制素(一种本文列出的氨基酸序列(1)描述的蛋白质)或其片段和/或类似物。
本发明另一方面提供一种促进骨形成的方法,该方法包括给予治疗有效量的能结合BMP的蛋白质这一步骤,其中所述蛋白质选自促卵胞抑制素(一种下文所列的氨基酸序列(1)描述的蛋白质)或其片段和/或类似物。
本发明另一方面提供一种预防或治疗可通过促进组织形成(例如骨、软骨或中枢神经系统的组织)而缓解的疾病或临床症状的方法,该方法包括给予治疗有效量的能结合BMP的蛋白质这一步骤,其中所述蛋白质选自促卵胞抑制素(一种以下列出的氨基酸序列(1)描述的蛋白质)或其片段和/或类似物。
本发明另一方面提供一种预防或治疗可通过促进组织形成(例如骨、软骨或中枢神经系统的组织)而缓解的疾病或临床症状的方法,该方法包括给予治疗有效量的BMP结合蛋白这一步骤。
在本发明其它方面提供诊断方法和诊断试剂盒。提供测定体内样本(如血液、尿、骨活检组织、骨髓细胞活检样品)中本发明蛋白质或其衍生物或分解物为基础的诊断方法和诊断试剂盒。
另外,本发明提供本发明蛋白质在应用用以鉴别个体基因型的基因多态性、突变、缺失或其它变异的DNA为基础的筛选技术中的用途,该用途用以鉴定骨疾(例如骨丢失)风险个体。
虽然设想本发明有助于骨折的恢复,但它也可用于治疗其它临床症状或疾病。
受益于本发明的骨丢失性临床症状或疾病包括但不限于:骨质疏松症(包括不用性骨质疏松症、Schuller氏病、绝经后骨质疏松症、创伤后骨质疏松症、老年性骨质疏松症),佩吉特氏病,癌症和肾病中特征性的不良骨再吸收以及类风湿性关节炎。
设想在不需高浓度BMP结合生长因子下,本发明可以用于治疗骨修复或诱发骨生长。目前使用高浓度BMP结合生长因子一直存在一个问题,即高浓度生长因子(如上所提)可引起生物平衡的偏离,从而可能导致该生长因子效能降低这一缺点。
本发明把能更好地使BMP到达其靶细胞。
使用生长因子(如BMP)的另一个问题是90%的外源性生长因子可在用药后头二十四小时里排泄,这表明大多数的生长因子未达到靶细胞。
适用于本发明的蛋白质包括促卵胞抑制素及其衍生物。具体地讲,本发明的蛋白质包括以下列出的氨基酸序列(1)描述的氨基酸和/或其片段或类似物。
(I)
1 mvrarhqpgg lcllllllcq fmedrsaqa-g ncwlrqakng rcqvlyktel skeeccstgr
61 lstswteedv ndntlfkwmi fnggapncip cketcenvdc gpgkkcrmnkknkprcvcap
121 dcsnitwkgp vcgldgktyr necallkarc keqpelevqy qgrckktcrdvfcpgsstcv
181 vdqtnnaycv tcnricpepa sseqylcgnd gvtyssachl rkatcllgrs iglayegkci
241 kakscediqc tggkkclwdf kvgrgrcslc delcpdsksd epvcasdnatyasecamkea
301 acssgvllev khsgscneee eededqdysf pissilew
本发明还提供一种促进组织产生的药用组合物,其中该药用组合物包含选自胶原蛋白IIa(一种以下所列的氨基酸序列(II)描述的蛋白质)或其衍生物、片段和/或类似物。
适用于本发明的蛋白质包括胶原蛋白IIa及其衍生物。具体地讲,本发明的蛋白质包括以下所列的氨基酸序列(II)描述的氨基酸和/或其片段或类似物。
所述氨基酸序列(II)是:
1 mirlgapqsl vlltllvaav lrcqgqdvqe agscvqdgqryndkdvwkpe pcricvcdtg
61 tvlcddiice dvkdclspei pfgeccpicp tdlatasgqpgpkgqkgepg dikdivgpkg
121 ppgpqgpage qgprgdrgdk gekgapgprg rdgepgtpgnpgppgppgpp gppglggnfa
181 aqmaggfdek aggaqlgvmq gpmgpmgprg ppgpagapgpqgfqgnpgep gepgvsgpmg
241 prgppgppgk pgddgeagkp gkagergppg pqgargfpgtpglpgvkghr gypgldgakg
301 eagapgvkge sgspgengsp gpmgprglpg ergrtgpagaagargndgqp gpagppgpvg
361 paggpgfpga pgakgeagpt gargpegaqg prgepgtpgspgpagasgnp gtdgipgakg
421 sagapgiaga pgfpgprgpp gpqgatgplg pkgqtgepgiagfkgeqgpk gepgpagpqg
481 apgpageegk rgargepggv gpigppgerg apgnrgfpgqdglagpkgap gergpsglag
541 pkgangdpgr pgepglpgar gltgrpgdag pqgkvgpsgapgedgrpgpp gpqgargqpg
601 vmgfpgpkga ngepgkagek glpgapglrg lpgkdgetgaagppgpagpa gergeqgapg
661 psgfqglpgp pgppgeggkp gdqgvpgeag apglvgprgergfpgergsp gaqglqgprg
721 lpgtpgtdgp kgasgpagpp gaqgppglqg mpgergaagiagpkgdrgdv gekgpegapg
781 kdggrgltgp igppgpagan gekgevgppg pagsagargapgergetgpp gpagfagppg
841 adgqpgakge qgeagqkgda gapgpqgpsg apgpqgptgvtgpkgargaq gppgatgfpg
901 aagrvgppgs ngnpgppgpp gpsgkdgpkg argdsgppgragepglqgpa gppgekgepg
961 ddgpsgaegp pgpqglagqr givglpgqrg ergfpglpgpsgepgkqgap gasgdrgppg
1021 pvgppgltgp agepgregsp gadgppgrdg aagvkgdrgetgavgapgap gppgspgpag
1081 ptgkqgdrge agaqgpmgps gpagargiqg pqgprgdkgeagepgerglk ghrgftglqg
1141 lpgppgpsgd qgasgpagps gprgppgpvg psgkdgangipgpigppgpr grsgetgpag
1201 ppgnpgppgp pgppgpgidm safaglgpre kgpdplqymradqaagglrq hdaevdatlk
1261 slnnqiesir spegsrknpa rtcrdlklch pewksgdywidpnqgctlda mkvfcnmetg
1321 etcvypnpan vpkknwwssk skekkhiwfg etinggfhfsygddnlapnt anvqmtflrl
1381 lstegsqnit yhcknsiayl deaagnlkka lliqgsndve iraegnsrffytalkdgctk
1441 htgkwgktvi eyrsqktsrl piidiapmdi ggpeqefgvd igpvcfl
本发明的典型蛋白质是有着上述氨基酸序列(I)的氨基酸序列的物质,优选该物质是本身肽或蛋白质;其功能性活性片段或其类似物;具有高度守恒性的同系物,特别是具有保持半胱氨酸区域的同系物以及编码包含氨基酸序列(I)描述的氨基酸序列的肽和蛋白质的载体例如DNA载体(质粒或病毒)。
功能性活性片段或类似物可通过添加、插入、修饰、取代或缺失以上所列的氨基酸序列(I)描述氨基酸序列中的一或多个氨基酸残基而形成。
术语“类似物”也包括嵌合蛋白质、融合蛋白、抗独特型抗体、上述化合物的前体和其它功能等效物或模拟物。也包括模拟BMP结合蛋白活性的合成体。
本发明也提供以上所列的氨基酸序列(I)或其功能性活性片段或类似物在制备用于促进骨形成的药物中的用途。
本发明还提供促进组织再生(例如骨和/或软骨组织再生)的方法,该方法包括给予BMP结合蛋白的步骤。
本发明还提供促进组织再生(例如骨和/或软骨组织再生)的方法,该方法包括给予BMP结合蛋白的步骤,其中BMP结合蛋白选自:Follistatin、FSRP、ZFSTA2、FLIK、α-2-HS糖蛋白、胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Chordin、Sog、Crim、Nell、结缔组织生长因子(CTGF)、Dan、Gremlin、Cerberus、Endoglin、Twisted Gastulation基因或以上提到的BMP结合蛋白质的衍生物、片段和/或类似物
本发明还提供促进哺乳动物患者(优选)骨形成的方法,该方法包括给予有效量的以上所列的氨基酸序列(I)或其功能性活性片段或类似物。
本发明一方面还包括表达本发明蛋白质及其片段的cDNA的DNA载体以及由表达该cDNA构建物转染的细胞在促进骨形成中的用途。上述cDNA和转染细胞可通过本领域技术人员已知的标准技术制备。
本发明还涵盖促进临床需要的哺乳动物患者(优选)骨形成的基因疗法。
可使本发明蛋白质与“寻找骨”物质(例如四环素或二膦酸盐)偶合以改善根据本领域技术人员熟知的靶向专一性。
可根据选择的适当方法制备本发明的功能改善药物。这些方法包括合成或重组的方法或从天然资源(如果存在)纯化的方法。
本发明的药用组合物可根据熟知的及公认的制药生产要求的方法制备。药用组合物适宜包含本发明的蛋白质以及药学上可接受的载体,并适宜为单位剂量形式。本发明的药用组合物可包含前药形式的本发明的蛋白质,该前药可在接受者宿主体内代谢转化成本发明物的活性形式。
本发明的药用组合物还可与其它疗法(例如二膦酸盐)联合应用,如同时、序贯或分别应用。本发明的药用组合物可包含有其它活性作用物,例如二膦酸盐、PTH、维生素D、BMP和雌激素。
另一方面,我们还提供一种包含本发明蛋白质的医用装置,例如:骨螺旋钉、体内假器官(例如髋假器官)或外伤钉(例如具有骨接触表面的髓内钉)。
本发明蛋白质适宜以层面的形式存在,例如覆盖在骨连接装置的表面的层面形式。本发明的医用装置适于通过将本发明的蛋白质吸附于如氧化钛或其它金属表面或多聚物表面的表面(如骨螺钉)上,通过将本发明蛋白质与载体物质结合,然后将载体包附于该医疗装置表面来制备。
在本发明该方面的一实施方案中,所述骨接触表面已经过“衍生的”或修饰,因此可将本发明蛋白质直接与表面结合(适于通过共价键结合)。
在本发明的另一个方面中,我们提供一种用于促进骨形成的人造支架材料,该支架能与本发明的蛋白质有效地结合。
本发明的支架可以是三维基质或层面(例如连续的薄膜或凝胶)的形式。该基质结构可由纤维或适宜的材料制造,然后通过纺织处理(例如编织、针织、交织或非交织、熔融吹制、粘结、水缠),并进一步制成所要求的三维形状。该基质结构也可以为其它形式,例如海绵状或泡沫状形式。
适宜的支架材料优选是生物可降分解的,而且不会抑制细胞生长或增殖。该材料优选不应该引起患者身体的不良反应,并且应能通过例如环氧乙烷处理灭菌。该材料一般具有骨传导性。
因此,适宜的材料包括生物可降解的聚酯,例如聚乳酸(PLA)、聚乙二醇酸(PGA)、聚二噁酮、多羟基链烷酸酯(例如多羟基丁酸酯(ICI))和透明质酸衍生物(如HYAFF(Fidia))。更适合的材料包括在结合到本文中作为参考的我们专利申请WO 91/13638和WO 97/06835中公开的那些,例如亲水性聚氨基甲酸酯、聚醚聚酯、聚环氧乙烷、聚醚聚酰胺、羧甲基纤维素、乙烯—醋酸乙烯酯共聚物、聚丁二烯、苯乙烯—丁二烯—苯乙烯嵌段共聚物等。
其它支架材料是以胶原蛋白为基础的物质,例如交联胶原蛋白/弹性蛋白材料、由酸溶性I型牛胶原蛋白原料制备的交联胶原蛋白、胶原蛋白凝胶(如那些商品名为COLLASTAT和COLETICA的物质)。天然或重组来源的胶原蛋白(如胶原蛋白IIa)均可使用。
本发明还提供了改良或嵌合重组性纤维状胶原蛋白(在此称为“改性胶原蛋白”),其与本发明蛋白质结合,并具有能增强其装配性、稳定性和作为生物材料的用途的特征。该改性胶原蛋白可以用作上述的支架材料。方法包括使用I型胶原蛋白的C-末端球状区域以促进三螺旋的形成;移出或改造该胶原酶裂解位点以抑制退化;掺杂其它的赖氨酸以促进交联,并改造N-末端球状区域的裂解位点以促进成熟纤维的N-末端区域的保留。例如,可将胶原蛋白IIa的chordin/SOG序列用蛋白质/多肽功能操控剂代替。可采用类似结构域改组方法使本发明的蛋白质结合入其它细胞外的基质组分中(例如纤连蛋白连接蛋白或胶原蛋白IV)或ECM结合分子或序列(例如肝素结合结构域)。参见例如WO 97/08311,其整个内容结合到本发明中作为参考。
在其它具体实施方案中,我们提供了一种含有一种合成材料的骨替代材料,该合成材料包含任意一种上述的支架材料和与本发明蛋白质结合的晶体相态(例如一种磷灰石,如羟磷灰石)。
在本发明的适当方面中,本发明的蛋白质作为支架以凝胶形式提供。该凝胶一般包括凝血酶、纤维蛋白原和因子XIII或其它与凝胶交联的转谷氨酰胺酶。
本发明还包括用于组织(如骨)疾病研究中的动物模型的研制。可采用非人类哺乳动物(例如小鼠)研究本发明的蛋白质在骨骼系统中的作用。
将适宜的蛋白质结合于一固体基质上,然后植入到要求的整形外科的部位。该手术的创伤(即植入结合蛋白的基质)能导致BMP的产生,由于BMP和本发明蛋白质的相互作用,所产生的BMP将结合在所述基质上。
本发明的蛋白质(优选结合固体基质)较先前技术具有优势,即不会浪费体内天然产生的过多的BMP。过量的BMP通常能迅速地从体内排出。本发明能浓集BMP,所述BMP可在体内自然生成,并通常能迅速地排出。
本发明提供一种含有胶原蛋白IIa的支架。
本发明还提供一种促进组织生成的支架,其中该支架包含BMP结合蛋白。
本发明还提供一种促进组织生成的支架,其中该支架包含胶原蛋白IIa。
所述支架装置适于完全或主要由胶原蛋白IIa制成,或者主要用胶原蛋白IIa包覆。
本发明提供一种包含胶原蛋白IIa的支架,该支架能够释放性结合BMP,并能控制BMP的释放。
因此,BMP的靶向性得到改善。
在具体实施方案中,所结合的BMP(一经结合)可通过正常细胞活动和/或通过一种可以释放该结合BMP的操控装置或药物释放。该BMP可通过所述支架的降解释放。
本发明适宜能使可溶性BMP与靶细胞(例如在缺损愈合部位)相互作用,在靶细胞能形成软骨的实施方案中,诱发这些靶细胞表达和合成软骨成分,从而使缺损部位复原。
然而BMP不一定释放方才具有本发明特定实施方案中所述的活性,结合型的BMP也有活性。
BMP和正规软骨型细胞的连续相互作用可以导致骨的形成。
骨可通过内部软骨的骨化过程形成,该过程中首先形成软骨,接着矿化软骨。在该过程中,骨通过软骨的形成而形成,因此发现能愈合骨的任何治疗都可被认定为能刺激软骨的形成,并认为该可逆过程也是正确的。
本发明另一方面提供一种治疗可通过促进软骨形成而缓解的疾病或临床症状的方法,该方法包括给予一种支架这一步骤,该支架包含治疗有效量的能结合BMP的胶原蛋白IIa。
本发明再一方面提供一种预防可通过促进软骨形成而缓解的疾病或临床症状的方法,该方法包括给予一种支架这一步骤,该支架包含治疗有效量的能结合BMP的胶原蛋白IIa。
本发明再一方面提供一种促进软骨形成的方法,该方法包括给予一种支架这一步骤,该支架包含治疗有效量的能结合BMP的胶原蛋白IIa。
尽管设想本发明有利于软骨修复,但还可以用来治疗其它临床症状和疾病。
可得益于本发明的软骨丢失的临床症状和疾病包括:骨关节炎、branchypodism、Hunter-Thompson软骨发育异常。也用于治疗关节的软骨病变,包括那些限于软骨和那些穿透软骨下骨的软骨病变,也可以用于治疗OA。
设想在不需高浓度生长因子下,本发明可以用于治疗软骨修复或诱发软骨生长。目前使用高浓度生长因子一直存在一个问题,即高浓度生长因子(如上所提)可引起生物平衡的偏离,从而可能导致该生长因子效能降低这一缺点。
本发明能更好地使BMP集中作用于其靶细胞。
使用生长因子(例如BMP)的另一个问题是90%的外源性生长因子在用药后头二十四小时可被排出,这表明大多数的生长因子未达到其靶细胞。
本发明胶原蛋白IIa或支架适宜以层面的形式存在,例如覆盖在软骨接触的装置表面上的层面形式。本发明的医用装置适于通过将本发明的胶原蛋白IIa或支架吸附于如软骨固定凹销的表面上,通过将本发明的胶原蛋白IIa或支架与载体物质结合,然后将载体包覆于该医疗装置表面来制备。
类似地,本发明的特定方面的胶原蛋白IIa或支架可以用于促进骨的再生。
本发明还提供一种制备促进组织工程化的支架的方法,该方法包括将支架用BMP结合蛋白包覆盖这一步骤。
在本发明该方面的一实施方案中,已将与软骨接触的表面衍生化或修饰,这样易于通过共价键直接将本发明的胶原蛋白IIa或支架结合于所述表面上。
本发明的支架可以是三维基质或层面(例如连续的薄膜或凝胶)的形式。该基质结构可由纤维或适宜的材料制造,然后通过纺织处理(例如编织、针织、交织或非交织、熔融吹制、粘结、水缠),并进一步制成所要求的三维形状。该支架构造也可以为其它形式(例如海绵状或泡沫状),其中可将该胶原蛋白IIa包覆或结合在该支架的表面上。
适宜的支架材料优选是生物可降解的,而且不会抑制细胞生长或增殖。该材料优选不应该引起患者身体的不良反应,并且应能通过例如环氧乙烷处理灭菌。该材料优选为具有骨传导性。
其它支架材料是以胶原蛋白为基础的物质,例如交联胶原蛋白/弹性蛋白材料,由酸溶性I型牛胶原蛋白原料制备的交联胶原蛋白、胶原蛋白凝胶(如那些商品名为COLLASTAT和COLETICA的物质)。天然或重组来源的胶原蛋白(如胶原蛋白IIa)均可使用。
本发明还提供了改良或嵌合重组性的纤维状胶原蛋白(本发明称为“改性胶原蛋白”),其与胶原蛋白IIa结合,并具有能增强其装配性、稳定性和作为生物材料的用途的特征。该改性胶原蛋白可以用作上述的支架材料。方法包括使用I型胶原蛋白的C-末端球状区域以促进三重螺旋的形成;移出或改造该胶原酶切割位点以抑制降解;掺入其它的赖氨酸以促进交联,并改造N-末端球状区域的切割位点以促进成熟纤维的N-末端区域的保留。例如,可将该胶原蛋白IIa的chordin/SOG序列用蛋白质/多肽功能操控剂代替。可采用类似重排区域的方法使本发明的蛋白质结合入其它细胞外的基质组分中(例如纤连蛋白连接蛋白或胶原蛋白IV)或ECM结合分子或序列(例如肝素结合结构域)。参见例如WO 97/08311,其整个内容结合到本发明中作为参考。
在其它具体实施方案中,我们提供了一种含有一种复合材料的软骨替代材料,该复合材料包含任意一种上述的支架材料和与BMP结合蛋白(例如胶原蛋白IIa)结合的陶瓷骨传导性或骨感应性相态物质(例如一种磷灰石,如羟磷灰石)。
在其它具体实施方案中,我们提供了一种含有一种复合材料的骨替代材料,该复合材料包含任意一种上述的支架材料和与BMP结合蛋白(胶原蛋白IIa)结合的陶瓷骨传导性或骨感应性相态物质(例如一种磷灰石,如羟磷灰石)。
在本发明的适当方面中,本发明的支架结构为凝胶形式。该凝胶一般包括凝血酶、纤维蛋白原和因子XIII或其它与凝胶交联的转谷氨酰胺酶。
本发明还包括用于软骨疾病研究中动物模型的研制。可采用非人类哺乳动物(例如小鼠)研究本发明的蛋白质在骨骼系统中的作用。
将适宜的BMP结合蛋白(例如胶原蛋白IIa)结合于一固体基质上,形成本发明的支架,然后植入到要求的整形外科的部位。据认为该手术的创伤(即植入BMP结合胶原蛋白IIa结合包覆的本发明支架)能导致BMP的产生,由于BMP和本发明支架上的BMP结合蛋白胶原蛋白IIa的相互作用,所产生的BMP会结合在所述支架上。所述BMP将通过正常细胞活动释放,而使该可溶性BMP与靶细胞相互作用刺激增殖和基质的生成。
本发明的支架较先前技术具有优势,即不会浪费体内天然产生的过多的BMP。组织创伤时产生的BMP不是局部性的,但是准确地提供给所述细胞。目前通过将BMP注射于损伤部位而给予BMP的方法不能克服这个问题,原因是该BMP还是不能准确地提供给所述细胞。过量的BMP通常能迅速地从体内排出。本发明浓集BMP(它们可在体内自然生成,并通常能迅速地排出),然后在所要求的区域缓慢逐步释放这些BMP。在本发明的某些实施方案中,可将所结合的BMP缓慢逐步释放到本发明的支架上,其中优选将胶原蛋白IIa本身结合或覆盖于固体基质上,然后这种情况可现在体内自然出现。结合BMP似乎并不含失活BMP或引起对BMP功能的任何永久性破坏。
现在仅以下列实施例、表格和图示的实例方式说明本发明,:
图1.1显示与各种对照组对比,含有Follistatin和BMP-2的细胞样本其每个细胞所释放的碱性磷酸酶的条棒图。
图1,2a-显示Follistatin对C2C12细胞BMP-2活性的影响(溶液实验)
图1,2b-也显示Follistatin对C2C12细胞BMP-2活性的影响(溶液实验)
图1,2c-显示Follistatin对C2C12细胞对BMP-5活性的影响(溶液实验)
图1,2d-显示Follistatin对C2C12细胞BMP-6活性的影响(溶液实验)
图1,2e-显示Follistatin对C2C12细胞BMP-7活性的影响(溶液实验)
图1,3a-显示Follistatin对C2C12细胞BMP-2活性的影响(结合实验)
图1,3b-显示Follistatin对C2C12细胞BMP-6活性的影响(结合实验)
图1,3c-也显示Follistatin对C2C12细胞BMP-6活性的影响(结合实验)
图1,3d-显示Follistatin对C2C12细胞BMP-7活性的影响(结合实验)
图1,4-显示Follistatin对C2C12细胞BMP-4活性的影响(溶液实验)
图1,5-显示Follistatin对C2C12细胞BMP-4活性的影响(结合实验)
图1,7-显示Follistatin对MC3T3E1细胞BMP-2活性的影响(结合实验)
图1,8-显示Follistatin288对C2C12细胞BMP-2活性的影响(溶液实验)
图1,9-显示Follistatin288对C2C12细胞BMP-2活性的影响(结合实验)
图1.10a显示只用BMP-2处理的大鼠腓肠肌中的钙化组织的放射显影图。
图1.10b显示大鼠腓肠肌中的钙化组织的放射显影图,其中与图1.10a对照,当存在Follistatin和BMP-2时,可发现骨形成增加。
图1.10c显示了在×50放大倍率下,用von Kossa和van Gieson复染剂染色的被植入了Follistatin和BMP-2的组织的组织切片的显微照相片。
图1.10d显示了在×100放大倍率下,用von Kossa和van Gieson复染剂染色的被植入了Follistatin和BMP-2的组织的组织切片的显微照相片。
图2.2a显示Follistatin和BMP-2对软骨细胞产生GAG的影响。
图2.2b显示Follistatin和BMP-2对软骨细胞产生胶原蛋白的影响。
图2.2c显示Follistatin和BMP-2对软骨细胞增殖的影响。
图2.3a显示Follistatin和BMP-2对体外软骨细胞产生GAG的影响(没进行抗坏血酸盐处理)。
图2.3b显示Follistatin对细胞形态的影响。
图2.4显示Follistatin和OP-1对软骨细胞产生GAG的影响。
实验所用的重组蛋白的来源
| Follistatin 300 | a)R&D Systems EuropeAbingdonOXONb)Produced on site at Smith&NephewGRC,York Science Park,YORK |
| Follistatin 288 | R&D Systems EuropeAbingdonOXON |
| BMP-2 | a)R&D Systems EuropeAbingdonOXONb)NIBSCPotters BarHertfordshire |
| BMP-4BMP-5BMP-6BMP-7 | a)R&D Systems EuropeAbingdonOXON |
溶液实验和结合实验的通法
溶解细胞的冷冻融溶法:从细胞中去除培养基,然后将细胞层用0.2M碳酸盐缓冲液洗涤。应用Rago等采用的冷冻融溶的方法(通过在蒸馏水中冷冻溶解细胞,然后采用Hoechst 33258在96孔组织培养板中进行DNA荧光法测试。Anal Biochem.191:p31-34,1990),将细胞融溶。向各孔中加入100μl 0.1%triton X-100在0.2M碳酸盐缓冲液的溶液。然后采用液氮,将培养板冷冻,在37℃下融溶,共进行3次。在光学显微镜下检查培养板以确保所有细胞均溶解。
对硝基苯基磷酸酯碱性磷酸酶试验:采用Leboy所述的测试方法(大鼠骨髓基质细胞培养物中地塞米松诱导的成骨细胞mRNA。1991,J Cell Physiol.146:p370-378)测定碱性磷酸酶活性。该反应包括通过碱性磷酸酶从对硝基苯基磷酸酯(pNPP)中酶促断裂磷酸酯基,得到有色产物对硝基苯酚(pNP)。采用微板读数器,在405nm处测定该产物的吸光度。从标准pNP溶液(0-250nM ml-1pNP的范围)的剂量反应曲线中,通过内插法计算碱性磷酸酶的活性。
PicoGreen试验:采用PicoGreen试验测定细胞数。该方法为荧光光度法,依据PicoGreen对双链DNA的高敏感性。由于每个细胞包含7.7pgDNA,所以可通过存在的DNA的量计算细胞数。制备(0-8μg ml-1范围的DNA标准液。在微板读数器上,在发射波长485nm和激发波长538nm处测定吸光度。采用回归模式处理微量滴定板的数据,以建立源于该标准DNA溶液的标准曲线,由其可测定DNA的浓度。
实施例1 Follistatin和BMP-2对C2C12细胞的影响
所用的BMP-2的浓度大约为1μg/ml。所用的Follistatin的浓度大约为25μg/ml。发现该Follistatin粘附于该组织培养塑料板的孔表面。在4℃下孵育过夜,约16小时。孵育后,将各孔用磷酸盐缓冲盐水(PBS)洗涤3次以除去未结合的Follistatin。然后将BMP-2与结合的Follistatin一起孵育。于37℃孵育1小时后,移去混合物,将各孔用PBS洗涤3次以除去未结合的BMP-2。将C2C12小鼠成肌细胞与该蛋白质混合物一起孵育。测试这些培养物的碱性磷酸酶的活性,发现与不含Follistatin的培养物相比,碱性磷酸酶的活性水平明显增加,表明该Follistatin能增加BMP-2的活性。
用以下试剂一式三份测定细胞样本(1.06×104细胞cm-2)的碱性磷酸酶的活性:
1.Follistatin
2.Follistatin和BMP-2
3.组织培养塑料(TCP)
4.BMP-2
5.牛血清白蛋白(BSA)
6.BSA和BMP-2
还测定了这些样本的总DNA的量,以每pg/ml的DNA表示。由于各细胞每ml含有7.7pg的DNA,所以将DNA的量除以7.7得到细胞的平均数。然后计算每个细胞中碱性磷酸酶的量pmol/ml。
附表(表1.1)和图(图1.1)清晰表明用Follistatin和BMP-2处理的细胞样本的碱性磷酸酶活性明显增加,因此说明骨细胞形成增加。
实施例1.2:Follistatin和BMP-2、5、6和7对C2C12细胞的
影响-溶液法
BMP-2和BMP-7可通过将一安瓿的内容物用1ml无血清(SF)的Dulbeccos氏改良Eagle培养基(DMEM)稀释得到10μgml-1的浓度制备。再将其用SFDMEM稀释至5μg ml-1。
BMP-6可通过将一安瓿的内容物用1ml无血清SFDMEM稀释得到20μgml-1的浓度制备。再将其用SFDMEM稀释至5μg ml-1。
BMP-5可通过将一安瓿的内容物用1ml无血清SFDMEM稀释得到50μgml-1的浓度制备。再将其用SFDMEM稀释至5μg ml-1。
Follistatin可通过将一安瓿的内容物用3ml无血清SFDMEM稀释得到8.3μgml-1的终浓度制备。
用胰蛋白酶/EDTA从组织培养瓶中移出C2C12细胞(ECACC批号91031101)。采用锥虫蓝和Neubauer血细胞计数器测定细胞数和细胞的成活力。以3.4×104细胞/ml的密度培养细胞(96孔板每孔100μl,因此1.06×104细胞/cm2),在潮湿空气中,在37℃/5%CO2下孵育2小时。
然后将下列溶液加入到96孔组织培养板的各孔中(每孔最少重复四份):
BMP-2和Follistatin
条件1-40μlFollistatin+60μl SFDMEM
条件2-40μlFollistatin+20μl BMP-2+40μl SFDMEM
条件3-20μl BMP-2+80μl SFDMEM
条件4-100μl SFDMEM
BMP-5和Follistatin
条件1-40μlFollistatin+60μl SFDMEM
条件2-40μlFollistatin+20μl BMP-5+40μl SFDMEM
条件3-20μl BMP-5+80μl SFDMEM
条件4-100μl SFDMEM
对于BMP-6和Follistatin
条件1-40μlFollistatin+60μl SFDMEM
条件2-40μlFollistatin+22.6μl BMP-6+37.4μl SFDMEM
条件3-22.6μl BMP-6+77.4μl SFDMEM
条件4-100μl SFDMEM
对于BMP-7和Follistatin
条件1-40μlFollistatin+60μl SFDMEM
条件2-40μlFollistatin+19.4μl BMP-7+40.6μl SFDMEM
条件3-19.4μl BMP-7+80.6μl SFDMEM
条件4-100μl SFDMEM
在37℃/5%CO2下,将培养板孵育4日。4日后,用冷冻融溶法溶解细胞。用pNPP试验测定碱性磷酸酶的活性,然后采用通法中所列的PicoGreen试验法测定细胞数。
结果见表(1.2a-1.2e)和图(1.2a-1.2e)中所示。
从这些结果可以看出,与单独在BMP中生长的培养物所表达的碱性磷酸酶相比,在Follistatin和BMP的条件中生长的培养物所表达的碱性磷酸酶增加,这表明这些细胞已被刺激沿成骨细胞系进一步分化。
因此该结果说明细胞响应于Follistatin和BMP,从而导致高水平的成骨组织再生。
实施例1.3:Follistatin和BMP-2、6和7对C2C12细胞的影响
-结合法
BMP-2和BMP-7可通过将一安瓿的内容物用1ml无血清SFDMEM稀释得到10μgml-1的浓度制备。再将其用SFDMEM稀释至1μgml-1。
BMP-6可通过将一安瓿的内容物用1ml无血清SFDMEM稀释得到20μgml-1的浓度制备。再将其用SFDMEM稀释至1μg ml-1。
Follistatin可通过将一安瓿的内容物用3ml无血清SFDMEM稀释得到8.3μgml-1的终浓度制备。
在96孔培养板的各孔中开始建立四种条件(每个条件最少重复四份):
条件1)50μlFollistatin
条件2)50μlFollistatin
条件3)组织培养塑料(TCP)
条件4)TCP
将以上溶液加入到96孔组织培养板的各孔中,然后在4℃下孵育过夜。孵育后,移出该蛋白质溶液,将各孔用PBS洗涤3次。
向条件2和3(如上)的各孔中加入125.5μl/孔的BMP-2(1μgml-1)或142.5μl/孔的BMP-6(1μg ml-1)或121.5μl/孔的BMP-7(1μgml-1)。向条件1和4(如上)的各孔中加入100μl/孔的SFDMEM。将这些溶液在37℃/5%CO2下孵育1小时,然后移去溶液,将各孔用PBS洗涤3次。以3.4×104细胞ml-1的密度(96孔板每孔100μl,因此为1.06×104细胞/cm2),在各孔中加入100μl的C2C12细胞(ECACC批号91031101),然后在潮湿空气中,在37℃/5%CO2下孵育大约4日。
4日后,用冷冻融溶法溶解细胞,用pNPP试验测定碱性磷酸酶的活性,然后采用通法中所列的PicoGreen试验法归一化为DNA水平。
结果见表(1.3a-1.3d)和图(1.3a-1.3d)中所示。
从这些结果可以看出,与单独在BMP中生长的培养物所表达的碱性磷酸酶相比,在Follistatin和BMP的条件中生长的培养物所表达的碱性磷酸酶增加,这表明这些细胞已被刺激沿成骨细胞系进一步分化。
因此该结果说明细胞响应于Follistatin和BMP,从而导致高水平的成骨组织再生。
实施例1.4:Follistatin和BMP-4对C2C12细胞的影响-溶液法
BMP-4可通过将一安瓿的内容物用1ml SFDMEM稀释得到10μgml-1的浓度制备。再将其用SFDMEM稀释至2.5μg ml-1。Follistatin可通过将一安瓿的内容物用1ml SFDMEM稀释得到25μgml-1的终浓度制备。
在96孔培养板的各孔中开始建立四种条件(每个条件最少重复四份):
条件1-20μlFollistatin+80μl PBS
条件2-20μlFollistatin+10μl BMP-4+70μl PBS
条件3-10μl BMP-4+90μl PBS
条件4-100μl PBS
在潮湿空气中,在37℃/5%CO2下,将以上溶液孵育45分钟。温育后,在不移出试剂下,以3.4×104细胞/ml的密度(96孔板每孔100μl,因此1.06×104细胞/cm2),加入100μl的C2C12细胞(ECACC批号91031101)。在37℃/5%CO2下,将该培养板孵育大约4日。
用冷冻融溶法溶解细胞,用pNPP试验测定该培养物的碱性磷酸酶的活性,然后采用通法中所列的PicoGreen试验法归一化DNA水平。
结果见表(1.4)和图(1.4)中所示。
从这些结果可以看出,与单独在BMP中生长的培养物所表达的碱性磷酸酶相比,在Follistatin和BMP的条件中生长的培养物所表达的碱性磷酸酶增加,这表明这些细胞已被刺激沿成骨细胞系进一步分化。
因此该结果说明细胞响应于Follistatin和BMP,从而导致高水平的成骨组织再生。
实施例1.5:Follistatin和BMP-4对C2C12细胞的影响-结合法
BMP-4可通过将一安瓿的内容物用1ml SFDMEM稀释得到10μgml-1的浓度制备。再将其用SFDMEM稀释至2.5μg ml-1。Follistatin可通过将一安瓿的内容物用1ml SFDMEM稀释得到25μgml-1的终浓度制备。
在96孔培养板的各孔中开始建立四种条件(每个条件最少重复四份):
条件1-20μlFollistatin+80μl PBS
条件2-20μlFollistatin+80μl PBS
条件3-TCP
条件4-TCP
将以上溶液加入到96孔组织培养板的各孔中,然后在4℃下孵育过夜。孵育后,移出该蛋白质溶液,将各孔用PBS洗涤3次。将各孔用200μl/孔的BSA(2mg ml-1)封闭1小时,然后移去封闭液,将各孔用PBS洗涤3次。
向条件2和3(见上所列)的各孔中加入100μl/孔的BMP-2(2.5μg ml-1)或向条件1和4(如上)的各孔中加入100μl/孔的SFDMEM。将这些溶液在37℃/5%CO2下孵育1小时,然后移去溶液,将各孔用PBS洗涤3次。
以3.4×104细胞/ml的密度(96孔板每孔100μl,因此1.06×104细胞/cm2)加入C2C12成肌细胞。然后在潮湿空气中,在37℃/5%CO2下,将培养板孵育大约4日。4日后,用冷冻融溶法溶解细胞,用pNPP试验测定该培养物的碱性磷酸酶的活性,然后采用通法中所列的PicoGreen试验法归一化DNA水平。
结果见表(1.5)和图(1.5)中所示。
从这些结果可以看出,与单独在BMP中生长的培养物所表达的碱性磷酸酶相比,在Follistatin和BMP的条件中生长的培养物所表达的碱性磷酸酶增加,这表明这些细胞已被刺激沿成骨细胞系进一步分化。
因此该结果说明细胞响应于Follistatin和BMP,从而导致高水平的成骨组织再生。
实施例1.6:Follistatin和BMP-2对MC3T3E1细胞的影响-溶
液法
BMP-2可通过将一安瓿的内容物用1ml SFDMEM稀释得到10μgml-1的浓度制备。当需要时,再将其用SFDMEM稀释至1μg ml-1。Follistatin可通过将一安瓿的内容物用1ml SFDMEM稀释得到25μgml-1的终浓度制备。
在96孔培养板的各孔中建立四种条件(每个条件最少重复四份):
条件1-20μlFollistatin+80μl PBS
条件2-10μl BMP-2+20μlFollistatin+70μl PBS
条件3-10μl BMP-2+90μl PBS
条件4-100μl PBS
将这些蛋白质混合物室温孵育45分钟,然后在不移出试剂下,加入MC3T3E1(DSMZ,批号ACC210/3)。以6.4×104细胞ml-1的密度(每孔100μl,即在96孔板中每孔6.4×103细胞,因此2.0×104细胞cm-2)培养细胞。在潮湿空气中,在37℃/5%CO2下,将该培养板孵育大约4日。
用冷冻融溶法溶解细胞,用pNPP试验测定该培养物的碱性磷酸酶的活性,然后采用通法中所列的PicoGreen试验法归一化DNA的水平。
结果见表(1.6)中所示。
从这些结果可以看出,与单独在BMP中生长的培养物所表达的碱性磷酸酶相比,在Follistatin和BMP的条件中生长的培养物所表达的碱性磷酸酶增加,这表明这些细胞已被刺激沿成骨细胞系进一步分化。
因此该结果说明细胞响应于Follistatin和BMP,从而导致高水平的成骨组织再生。
实施例1.7:Follistatin和BMP-2对MC3T3E1细胞的影响-结
合法
BMP-2可通过将一安瓿的内容物用1ml无血清SFDMEM稀释得到10μgml-1的浓度制备。当需要时,再将其用SFDMEM稀释至1μg/ml。Follistatin可通过将一安瓿的内容物用1ml SFDMEM稀释得到25μgml-1的终浓度制备。在PBS中稀释BSA,得到的终浓度为2mgml-1。
在96孔培养板的各孔中开始建立五种条件(每个条件最少重复四份):
条件1)50μlFollistatin
条件2)50μlFollistatin
条件3)50μl BMP-2
条件4)50μl BSA
条件5)50μl BSA
将以上溶液加入到96孔组织培养板的各孔中,然后在4℃下孵育过夜。孵育后,移出该蛋白质溶液,将各孔用PBS洗涤3次。将各孔用200μl/孔的BSA(2mg ml-1)封闭1小时,然后移去封闭液,将各孔用PBS洗涤3次。
向条件2和5(见上所列)的各孔中加入100μl/孔的BMP-2(1μgml-1)或向条件1、3和4(如上)的各孔中加入100μl/孔的SFDMEM。将这些溶液在37℃/5%CO2下孵育1小时,然后移去溶液,将各孔用PBS洗涤3次。以6.4×104细胞ml-1的密度(每孔100μl,即在96孔板中每孔6.4×103细胞,因此2.0×104细胞cm-2)培养MC3T3E1细胞。然后在潮湿空气中,在37℃/5%CO2下,将培养板孵育4日。
用冷冻融溶法溶解细胞,用pNPP试验测定该培养物的碱性磷酸酶的活性,然后采用通法中所列的PicoGreen试验法归一化DNA的水平。
结果见表(1.7)和图(1.7)中所示。
从这些结果可以看出,与单独在BMP中生长的培养物所表达的碱性磷酸酶相比,在Follistatin和BMP的条件中生长的培养物所表达的碱性磷酸酶增加,这表明这些细胞已被刺激沿成骨细胞系进一步分化。
因此该结果说明细胞响应于Follistatin和BMP,从而导致高水平的成骨组织再生。
实施例1.8:Follistatin-288和BMP-2对C2C12细胞的影响-溶
液法
BMP-2可通过将一安瓿的内容物用1ml无血清SFDMEM稀释得到10μgml-1的终浓度制备。Follistatin-288可通过将一安瓿的内容物用1ml SFDMEM稀释得到25μgml-1的终浓度制备。
在96孔培养板的各孔中开始建立四种条件(每个条件最少重复四份):
条件1-20μlFollistatin-288+80μl PBS
条件2-20μlFollistatin-288+10μl BMP-2+70μl PBS
条件3-10μl BMP-2+90μl PBS
条件4-100μl PBS+70μl PBS
将以上溶液加入到96孔组织培养板的各孔中,然后在37℃下孵育45分钟。孵育后,在不移出试剂下,以3.4×104细胞/ml的密度加入100μl C2C12成肌细胞(96孔板中每孔100μl,因此1.0×104细胞/cm2)。在37℃/5%CO2下,将该培养板孵育大约3日。
用冷冻融溶法溶解细胞,用pNPP试验测定该培养物的碱性磷酸酶的活性,然后采用通法中所列的PicoGreen试验法归一化DNA的水平。
结果见表(1.8)和图(1.8)中所示。
从这些结果可以看出,与单独在BMP中生长的培养物所表达的碱性磷酸酶相比,在Follistatin和BMP的条件中生长的培养物所表达的碱性磷酸酶增加,这表明这些细胞已被刺激沿成骨细胞系进一步分化。
因此该结果说明细胞响应于Follistatin和BMP,从而导致高水平的成骨组织再生。
实施例1.9:Follistatin-288和BMP-2对C2C12细胞的影响-结
合法
BMP-2可通过将一安瓿的内容物用1ml无血清SFDMEM稀释得到10μgml-1的浓度制备。当需要时,再将其用SFDMEM稀释至1μg/ml。Follistatin-288可通过将一安瓿的内容物用1ml SFDMEM稀释得到25μgml-1的终浓度制备。在PBS中稀释BSA,得到的终浓度为2mgml-1。
在96孔培养板的各孔中建立四种条件(每个条件最少重复四份):
条件1-20μlFollistatin288+80μl PBS
条件2-20μlFollistatin-288+70μl PBS
条件3-TCP
条件4-TCP
将以上溶液在4℃下孵育过夜。孵育后,移出该蛋白质溶液,将各孔用PBS洗涤3次。室温下,将各孔用200μl/孔的BSA(2mg ml-1)的PBS溶液封闭1小时,然后移去封闭液,将各孔用PBS洗涤3次。
向条件2和3中加入100μl/孔的BMP-2(1μg ml-1)。向条件1孔中加入100μl/孔的SFDMEM,条件4的各孔空置。将这些溶液在37℃/5%CO2下孵育1小时,然后移去溶液,将各孔用PBS洗涤3次。
以3.4×104细胞/ml的浓度(在96孔板中每孔100μl,因此1.06×104细胞/cm2)加入C2C12细胞。然后在37℃/5%CO2下,将培养板孵育4日。
用冷冻融溶法溶解细胞,用pNPP试验测定该培养物的碱性磷酸酶的活性,然后采用通法中所列的PicoGreen试验法归一化DNA的水平。
结果见表1.9和图1.9中所示。
从这些结果可以看出,与单独在BMP中生长的培养物所表达的碱性磷酸酶相比,在Follistatin和BMP的条件中生长的培养物所表达的碱性磷酸酶增加,这表明这些细胞已被刺激沿成骨细胞系进一步分化。
因此该结果说明细胞响应于Follistatin和BMP,从而导致高水平的成骨组织再生。
实施例1.10:体内的肌内研究
将约285-365g的刚成年Sprague Dawley大鼠麻醉,将后肢剃光毛。将蛋白溶液(BMP-2和Follistatin300)和对照液装载于胶原蛋白海绵(10mm×3mm×3mm,Duragen,Life Sciences)中,然后植入腓肠肌中。植入八组(如下所列):
组1 载体
组2 载体+BMP(A)
组3 载体+BMP(B)
组4 载体+FS300(A)
组5 载体+FS300(B)
组6 载体+FS300(A)+BMP(A)
组7 载体+FS300(B)+BMP(B)
组8 载体+FS300(A)+BMP(B)
(A=20μg蛋白质 &B=5μg蛋白质)
处理日:第一日
动物 左后肢 右后肢
1 载体+FS300(B) 载体
2 载体+BMP2(A) 载体
3 载体+FS300(B)+BMP2(B) 载体+BMP2(B)
4 载体 载体+BMP2(B)
5 载体+FS300(A) 载体+FS300(A)+BMP2(A)
6 载体+FS300(A)+BMP2(B) 载体+FS300(B)+BMP2(B)
7 载体+BMP2(A) 载体+BMP2(B)
处理日:第二日
动物 左后肢 右后肢
8 载体+FS300(B)+BMP2(B) 载体+FS300(B)
9 载体+FS300(A)+BMP2(A) 载体+FS300(B)+BMP2(B)
10 载体+FS300(A)+BMP2(B) 载体+FS300(A)
11 载体+FS300(A) 载体+BMP2(A)
12 载体+FS300(B) 载体+FS300(A)+BMP2(B)
13 载体+BMP2(A) 载体+FS300(A)+BMP2(B)
14 载体+FS300(A)+BMP2(A) 载体+BMP2(A)
处理日:第三日
动物 左后肢 右后肢
15 载体 载体+FS300(A)
16 载体 载体+FS300(A)+BMP2(A)
17 载体+FS300(A)+BMP2(A) 载体+BMP2(B)
18 载体 载体+FS300(A)+BMP2(B)
19 载体+FS300(B) 载体+FS300(A)+BMP2(A)
20 载体+BMP2(B) 载体+FS300(B)
21 载体+FS300(A)+BMP2(A) 载体+FS300(A)+BMP2(B)
处理日:第四日
动物 左后肢 右后肢
22 载体+FS300(A) 载体+FS300(B)
23 载体 载体+FS300(B)+BMP2(B)
24 载体+FS300(B)+BMP2(B) 载体+FS300(A)
25 载体+BMP2(A) 载体+FS300(B)+BMP2(B)
26 载体+BMP2(A) 载体+FS300(B)
27 载体+BMP2(B) 载体+FS300(A)
28 载体+BMP2(B) 载体+FS300(A)+BMP2(B)
放射显影图分析
在植入后第17-18日之间进行放射性试验(见图1.10a和1.10b)。当在等倍放大量下扫描和测定时,用5μg的Follistatin和BMP-2处理的大鼠的钙化组织的面积为7.77mm2(图1.10b),单独用5μg的BMP-2处理的大鼠的钙化组织的面积为3.0mm2(图1.10a),单独用作对照的20μg的BMP-2处理的大鼠的钙化组织的面积为4.62mm2,因此,即用Follistatin和BMP-2处理形成更多的骨(未显示数据)。在阴性对照组(仅用载体处理)中未观测到骨。
组织学
移植4星期后,将动物处死。从腓肠肌上取出移植部位周围的皮肤,切去该腓肠肌。将样本在10%福尔马林缓冲液中固定过夜,用石蜡包埋处理,以5μm切片,用苏木精和曙红(H&E)染色,然后用van Gieson复染。从显微照片(图1.10c和1.10d,其中B是被染成暗红色的骨,O是被染成粉红色的类骨质,M是被染成黄色的肌肉)中可以清晰地看到在BMP-2和Follistatin组别中生成的物质是骨。
其它测试(包括碱性磷酸酶活性和钙含量)表明在Follistatin和BMP标本中骨再生水平增高。
实施例1.11
我们发现从R+D Systems UK购买的Follistatin对固体基质载体具有粘附性。所用的Follistatin的浓度约为25μg/ml。
将载体包覆的Follistatin皮下移植给28-35日龄的雄性大鼠。将不含Follistatin的移植作为空白对照。
移植21天后处死动物,然后定量测定移植部位的骨形成活性。将对BMP-2存在下所述载体上Follistatin进行的试验与1/载体+BMP和2/载体+Follistatin进行的试验相比较。
与对照组相比,移植有BMP-2存在下固体基质载体包覆的Follistatin的动物在移植部位显示出更好的骨形成活性。
实施例1.12
骨传导腔的移植包括将具有圆筒形内部空间的刻有螺纹状的钛腔移植入大鼠骨。该腔内径为2mm,长7mm。外径3.5mm,全长13mm。
该腔的一端留有供组织向内生长的许多孔。为在骨内移植该腔,可将该腔旋入骨内。
实验选用雄性Sprague-Dawley大鼠(每鼠移植一腔)。
移植钛腔后,将大鼠随机分组。第一组移植适宜的附有Follistatin的基质,第二组只移植基质,第三组不向腔内移植任何物质。
移植试验物质6星期后处死大鼠。用腔里的组织切片,评估骨的内生长。与对照组相比,用Follistatin处理的骨组织显示出更好的骨再生性。
实施例1.13
我们发现从R+D Systems UK购买的Follistatin对固体基质载体具有粘附性。所用的Follistatin的浓度约为25μg/ml。
将载体包覆的Follistatin肌内移植给28-35日龄的雄性大鼠。将不含Follistatin的移植作为空白对照。
移植21天后处死动物,然后定量测定移植部位的骨形成活性。将对BMP-2存在下所述载体上Follistatin进行的试验与1)载体+BMP和2)载体+Follistatin进行的试验相比较。
与对照组相比,移植有BMP-2存在下固体基质载体包覆的Follistatin的动物在移植部位显示出更好的骨形成活性。
实施例1.14
我们发现从R+D Systems UK购买的Follistatin对固体基质载体具有粘附性。所用的Follistatin的浓度约为25μg/ml。
将载体包覆的Follistatin移植入绵羊的部分楔形切开的腓骨内。移植30日后处死动物,然后定量测定移植部位的骨形成活性。
与单独移植载体的对照组相比,移植有固体基质载体包覆的Follistatin的动物在移植部位显示出更好的骨形成活性。
实施例1.15
节段损伤性体内模型
节段损伤桡骨/尺骨模型已在公开的文献中详细说明,并一直用于研究诸如去矿质骨基质和骨形成蛋白的化合物。最常使用以下动物进行桡骨/尺骨模型试验:大鼠、兔和狗。已报道狗的天性比兔或大鼠更好动,这样会导致加剧长骨的断裂损伤。因此,选用新西兰白兔类兔(骨骼成熟,即生长板融合)作为最适合的动物。
在兽医外科医师监督下进行外科手术前,先拍X-光照片,以确认骺板融合,即骨骼成熟。如果生长板融合,即可维持麻醉,然后进行外科手术。
手术方法
通过将手术部位的毛刮去,用适宜的手术用洗涤剂(如:Hibitane、Pevidine)洗净皮肤,准备出供无菌手术的手术区域。
1.直接在尺骨上方切口,然后切开周围的肌肉露出尺骨。
2.从尺骨的最末端测量3cm的距离,沿着尺骨的中轴放置一个定位装置。用解剖刀在该装置的两端标记尺骨。
3.使用摇摆式锯在各标记内进行该尺骨的完全截骨术。
4.使用解剖刀切断桡骨和尺骨间的韧带,以释放出该尺骨部分。
5.使用解剖刀刮去紧邻桡骨部分的骨膜。
6.用盐水冲洗缺损部位以去除碎片。
7.在缺损处移植入骨移植材料或让缺损部位保持空位。
8.缝合手术部位。
样本准备
各次移植含有重组BMP-2、Follistatin或它们的组合物。
分析
在肱尺/肱挠关节和桡腕关节处分离尺骨和桡骨结构,同时小心避免对桡骨和尺骨施加过度的弯曲力。除去皮肤后,将标本置于福尔马林中。
通过放射显影照片和组织学分析评价该节段损伤的骨愈合情况。结果表明Follistatin和BMP组比对照组能增强骨的生长。
实施例2.1:
通过制备适宜体积的支架,消毒后然后用胶原蛋白IIa(或者是完整的蛋白质或者是含有BMP结合位点的胶原蛋白IIa前肽)包覆制造试验装置。
在新西兰白兔的膝盖骨凹槽处制造直径为3mm深度为3mm的骨软骨缺损。将该缺损处或者让其空置、或者只用所述支架填充或者用上描述的装置填充。在第1、3、6月处死兔子,对损伤部位进行组织学检查。
采用O′Driscoll记录系统,由富有经验的组织学家用盲法对软骨修复进行分类。在所有时间点上,用包覆有胶原蛋白IIa的支架处理的缺损比任一对照组的缺损,软骨愈合明显改善。
该数据表明胶原蛋白IIa对骨软骨缺损的愈合有效,我们相信它是通过结合并提供自体BMP而起效。
Follistatin对软骨形成影响的体外测定方法
实施例2.2:对单层软骨细胞的影响
从新鲜的绵羊膝关节中分离出初级软骨细胞。从膝盖骨的凹槽和膝盖骨后解剖出关节软骨,剁碎该组织(约1-4mm3),然后用0.25%庆大霉素溶液洗涤。弃去该庆大霉素溶液,在37℃下,将软骨碎块在胶原酶溶液(0.2%)中轻轻振摇过夜。使用Worthington氏II型胶原酶,将该酶用培养基稀释,然后无菌过滤。培养基是包含有10%牛胎血清、1%青霉素/链霉素、1%非必需氨基酸和1%L-谷氨酰胺的标准DMEM(4.5g/L葡萄糖)。除另有说明,在整个细胞培养实验中都使用该培养基。
胶原酶过夜处理后,将得到的消化液倾倒通过70μm尼龙细胞渗滤器,将滤液转移至离心管中,用等体积的PBS和培养基洗涤。以1000rpm转速离心10分钟。弃去培养基,将沉淀用培养基洗涤,然后以1000rpm速度离心5分钟。将该细胞沉淀再悬浮于适量体积(最少5mL)的培养基中,取一小等份试样进行细胞计数。
以1×105/孔的密度,将该软骨细胞接种于24孔培养板的孔中。所用BMP-2(由R&D systems提供)的浓度在50ng/mL-1000ng/mL之间。尽管两种因子的比率不同,Follistatin(同样由R&D systems提供)的应用浓度相似。将浓度为50ng/mL的抗坏血酸加入到培养基中。设定适当的对照组,即单用BMP、单用Follistatin或不用生长因子处理。在37℃、5%CO2下,将细胞培养4天至一个月。每2-3天补充适量培养基供给细胞。培养结束时,通过生化分析法分析该样本:
生化分析:在供给细胞或培养结束时,保留培养基用于GAG分析。将该细胞单层进行木瓜蛋白酶消化。将1.42g磷酸氢二钠、0.0788g盐酸半胱氨酸和0.1861g乙二胺四乙酸(EDTA)混合,制备木瓜蛋白酶缓冲液。加入90mL UHQ水,搅拌至溶解,调节pH至6.5。将0.0264g木瓜蛋白酶溶解于25ml木瓜蛋白酶缓冲液中,制得木瓜蛋白酶溶液。向每个孔中加入0.5mL该溶液,将滴定板盖子置于每个培养板上。在杂交烘箱中于60℃,将培养板孵育过夜。
GAG试验:然后对细胞消化液进行GAG测定。将16mg 1,9-二甲基亚甲基蓝、2g甲酸钠、5mL 100%乙醇和2mL甲酸混合,溶解于UHQ水中,然后调至终体积为1000mL,制得1,9-二甲基亚甲基蓝(DMB)溶液。
制备1mg/ml软骨素-4-硫酸酯(硫酸软骨素A,牛气管)的UHQ水的溶液的储备液,用空白木瓜蛋白酶溶液1∶10稀释至100μg/ml。制备浓度范围在0-75μg/ml之间的一套标准液。
将20μL标准液或样品液置于96孔培养板的各孔中。加入200μl DMB溶液,立即在平板读数仪上,在双波长540nm(测量波长)和595nm(参比波长)下,读取该培养板。
同样对培养基样本进行GAG测定,但用10%DMEM而不是用空白木瓜蛋白酶制备标准液。
DNA试验:还对细胞消化液进行Hoechst DNA测试。将1.211gTris、3.802g EDTA和5.844g NaCl加入到800ml UHQ级水中,然后搅拌至溶解,制得Hoechst稀释缓冲液。调节pH至7.0,加入UHQ级水至终体积1000ml。将1mg/mL Hoechst储备液用稀释缓冲液按1∶2000稀释。用1mg/mL鲑睾丸DNA储备液制备DNA标准液,将其稀释至标准物浓度为0-100μg/ml的范围。
将75μl标准液或细胞消化液置于比色杯(4面清晰)中。加入1.5mlHoechst溶液,然后再加1mL稀释缓冲液。将样品混合,培养约5分钟,然后用荧光光度计在355nm激发波长和460nm发射波长下测定。
胶原蛋白试验:采用羟脯氨酸试验测定样品中胶原蛋白的总量。胶原蛋白由14.3%的羟脯氨酸组成,因此可通过计算存在的羟脯氨酸的量而计算出胶原蛋白的总量。这些实验的目的就是在样品间进行直接的比较,因而不必要将羟脯氨酸的量转变成总胶原蛋白的量。将50g柠檬酸和120g乙酸钠混合,然后溶于650ml UHQ水中,制得羟脯氨酸试验用储备液。将34g氢氧化钠溶于250ml UHQ水中,制得第二种溶液,然后将该溶液加入初始溶液中。加入12ml冰醋酸,用UHQ水补充至终体积1000ml。加入10滴甲苯。将150ml异丙醇加入到500ml羟脯氨酸储备液中,制得羟脯氨酸试验用工作溶液。将该溶液混匀,用盐酸调至pH6.0,然后用UHQ水补充至终体积750ml。
将20ml羟脯氨酸工作溶液加入到2.5ml异丙醇和0.3525g氯胺T中,制得氯胺T溶液。将该混合液搅拌至全部固体溶入溶液,室温下保存于玻璃容器内。将3.75g p-DAB加入到15ml异丙醇和6.5ml高氯酸中,制得对二甲氨基苯甲醛(p-DAB)溶液。
如下进行本试验。将250μl木瓜蛋白酶消化液加入到装有250μl浓盐酸的Pyrex(Corning)带磨口盖的玻璃管中,置加热板上在120℃下温育过夜。次日,将内容物转移至小玻璃瓶中,在90℃下开盖温育至干燥。将样品冷却至室温,将残留物溶解于1mL 0.25M磷酸钠缓冲液中。水解的木瓜蛋白酶溶液(HPS)提供代表性的空白对照,并为样本和标准液提供稀释剂。
用1mg/ml羟脯氨酸储备液制备0-30μg/mL浓度范围的标准液。将50μl标准液或样品液加入到96孔培养板的各孔中。加入50μl氯胺T溶液,将培养板在室温下培养20分钟。加入50μl p-DAB溶液,60℃下培养30分钟。将板冷却,然后用平板计数仪在单波长540nm下读数。
结果:表2.2给出这些结果的原始数据。
图2.2a、2.2b和2.2c分别表示GAG产生、胶原蛋白产生和增殖。
这些结果表明Follistatin与BMP-2联合能刺激增殖作用。细胞数量的增加与GAG和胶原蛋白产物(两者都是软骨产生的标志)的增长一致。在这些实验中,在Follistatin存在下,每μg DNA表达的细胞外基质组分没有增加。这表明在某些情况下胶原蛋白和GAG的增长是由于产生这些分子的细胞数量的增加。这些结果特别有意义,原因是增殖的增长通常与分化的减少相关联,即GAG和胶原蛋白的产生。Follistatin-刺激增殖不会导致分化的减少,这表明Follistatin是刺激软骨修复的适宜分子。
实施例2.3:抗坏血酸不存在时对单层软骨细胞的影响
第二实验重复上述工作,但研究的是无抗坏血酸下的影响。在该实验中每个细胞的GAG产物增加。在Follistatin存在下,并没增强增殖作用,这表明在抗坏血酸不存在时,Follistatin只刺激分化作用。本实验中也包括单一使用Follistatin。由图Fig.2.3a中可以看出Follistatin本身的刺激作用不在对照水平之上,因此它是BMP-2和Follistatin联合造成的影响。与BMP本身相比,BMP+Follistatin样品中每μgDNA的GAG产物在统计学上明显增加(P=0.02)。很显然无抗坏血酸盐就不会产生胶原蛋白,因此没有可测量的数据。这些实验的数据都包含在表2.3中,图为图2.3a。
图2.3b显示了Follistatin对细胞形态学的影响。用Follistatin+BMP-2处理这些细胞具有很明显的圆形形态,表明它们保留了软骨细胞的表型,这种表型在其它细胞中未见到。因此用Follistatin+BMP-2处理的细胞保留了软骨型细胞的特征。
实施例2.4:Follistatin和BMP-7(OP-1)的影响
重复实施例2.2,但用生长因子BMP-7或生骨蛋白-1代替BMP-2。所述生长因子由R&D systems提供,所用浓度同BMP-2。实验结果包含在表2.4中。结果以图示方式表达在图2.4中。与BMP一样,在Follistatin存在下,OP-1对软骨细胞产生的GAG具有增强作用。此效果显著(p=0.093)。
实施例2.5:Follistatin对骨髓基质细胞的影响
使用骨髓基质细胞(BMSCs)重复实施例2.2。从新处死的绵羊胫骨中分离出这些细胞。剥离去骨上的肉,用无菌钢锯锯开骨头。将骨髓用无菌刮刀从骨腔中挖出,转移至falcon管中。将培养基加入到该管中,以1000rpm转速离心10分钟。弃去堆积在基质表面的所有脂肪层。将细胞再悬浮,再离心。再次弃去脂肪,将细胞再悬浮。进行细胞计数,然后以每175cm2 2×106的密度,将细胞转移至组织培养瓶中。使BMSCs粘附2日。血细胞也存在于骨髓中,但不粘附在组织培养塑料上,因此可以从BMSCs中分离出来。待细胞一融合,立即将培养瓶表面的细胞胰蛋白酶化,计数,然后以5×104的密度置于24孔培养板的孔中。按软骨细胞所述处理,然后以同样的方式进行分析。
无BMP存在时,BMSCs不表达任何胶原蛋白或GAG。BMP存在时,生成的水平相对较低。带有Follistatin时,能增加所述表达,再次表明Follistatin可以提高BMP活性,并能刺激软骨形成。
实施例2.6:单层细胞的免疫组织化学
为确定软骨细胞在培养过程中是否保留其分化表型,通过免疫组织化学法测定II型胶原蛋白、聚集蛋白聚糖和胶原蛋白I的存在。
按实施例1所述分离软骨细胞,然后将其培养于12孔玻璃多玻片上。按已述的相同方法处理生长因子。一周培养期过后,将玻片在1∶1的甲醇∶丙酮混合液中固定,空气干燥。
采用间接链霉抗生物素ABC免疫过氧化物酶方法(Dako,Ely,UK)进行免疫组织化学。整个实验都使用Tris缓冲盐水(TBS)作为稀释剂和洗涤缓冲液(0.15M NaCl,0.05M Tris-(羟甲基)氨基甲烷,pH7.6,在DDW中),所有培养均在室温下进行。
通过用10%兔血清阻断中断非特异性背景的染色,然后通过用抗生物素蛋白/生物素封闭试剂盒(Vector Labs)处理切片,封闭内源性抗生物素蛋白结合部位。接着将切片在第一抗体中培养1小时,生物素化的兔抗-lg抗体(F(ab’)2片段)培养30分钟,再在链霉抗生物素/HRP ABC复合物(Vectastain elite ABC试剂盒,Vector Labs)中培养30分钟,同时在每个步骤之间都进行冲洗。通过经H2O2催化3,3’-二氨基联苯胺底物(DAB)反应,显现结合的抗体。用苏木素将切片反染色,然后脱水,清理,封固。从该标记流程中省略第一抗体,将此作为阴性对照。在BMP-2和Follistatin处理的样本中,对细胞II和聚集蛋白聚糖的染色增加。
实施例2.7:沉淀培养物
采用软骨细胞和BMSCs,在包含下列组分的培养基中制备沉淀培养物:DMEM(4.5g/l葡萄糖)+丙酮酸盐、ITS+预混合液(1ml/100ml培养基)、抗坏血酸盐-2-磷酸盐(100μM)、地塞米松(10-7M)、HEPES(20μl/ml)。还将浓度范围为50-1000ng/ml的BMP-2和相同浓度范围的Follistatin也补充到该培养基中。还建立单独含有BMP-2、单独含有Follistatin和不含任何生长因子的对照组。将0.5ml培养基中含500,000个细胞(软骨细胞和BMSCs)的各等分试样地加入2ml无菌圆底微量离心管中,以2500rpm的速度离心10分钟。使细胞在管底形成沉淀。在37℃下、5%CO2中,将该沉淀培养物培养两周。在此期间,每3-4日更换一次培养基。
两周培养期结束后,收集所述沉淀培养物,分析。通过全部生物化学分析或免疫组织化学和组织学染色进行分析。
生物化学分析:按实施例所述对这些样本进行生物化学分析。在用木瓜蛋白酶消化前,先将样本进行冷冻干燥。将冻结的样本置于排气管中,冷冻干燥过夜。然后在密封的eppendorf管中进行消化过夜。随后对消化液进行生物化学分析。
免疫组织化学:将沉淀培养物在10%中性福尔马林缓冲液中固定,然后用石蜡包封。在进行免疫标记前,将组织切片(5μm)脱蜡,然后通过不同分级乙醇至水再水化。按实施例1所述进行免疫组织学染色。
组织学分析:按用于免疫组织化学分析处理的切片还进行传统的组织学染色。使用爱茜蓝染色法进行粘多糖(GAG)组织化学染色。将切片在3%乙酸中漂洗,然后置于60℃下的爱茜蓝溶液(1%爱茜蓝(w/v)的3%冰醋酸溶液)中10分钟。将玻片用0.5%中性红水溶液复染色,用无水乙醇漂洗,在二甲苯中清理,然后固封。用该技术将GAGs染成蓝色。同样进行H&E染色,以检查组织的结构。用Safarin O染色法识别样本中的软骨。
结果表明:在Follistatin+BMP-2处理的样本中,软骨产生增加。
实施例2.8:三维毡圈培养物
为了测定在三维基质中Follistatin对细胞的影响,建立在多羟基乙酸(PGA)毡圈上的培养物。PGA毡圈由S&N制造。用环氧乙烷处理灭菌。将细胞(软骨细胞和BMSCs)接种于已用FCS预湿润的24孔培养板中的毡圈上。向每个支架上接种100μL标准10%FCS DMEM和抗坏血酸盐中的一百万个细胞。一小时后,将支架浸入含有上述生长因子混合物的培养基中。在37℃下、5%CO2中,在旋转震荡器上,将所述支架培养两周,每3-4天补充更换一次培养基。
培养期结束后,收集样本,然后按已述的方法进行生物化学、免疫组织化学和组织学分析。
结果表明:在Follistatin+BMP处理的样本中,软骨产生增加。
实施例2.9:体外测试GDF-5
用GDF-5(CDMP-1)重复所有已述的试验。该生长因子由R&Dsystems提供,所用浓度同BMP-2中所述。在所有的试验中,用GDF-5重复用BMP-2检测的趋向。
结果表明:在Follistatin+BMP处理的样本中,软骨产生增加。
实施例2.10:兔体内研究
对30只新西兰白兔进行动物研究。所有的兔子均为雄性,约8个月大小,即它们骨骼已发育成熟。
在双后关节处大腿骨的滑车形凹槽上钻直径为3mm深3mm的双侧全厚度缺损孔。缺损处于与关节成90o处,然后置于凹槽中心处。
将动物分为4个治疗组:
·缺损处空置
·仅用支架
·30μgFollistatin
·30μgFollistatin+10μg BMP-2
所述支架由直径为3.5mm深3mm的PGA毡圈组成,因而能被挤压入所制造的缺损孔洞内。将BMP-2和Follistatin的溶液或Follistatin本身的PBS溶液注射在毡圈上。每毡圈注射总量为30μl。对于仅放置了支架的缺损孔洞内,注射30μl的PBS。
依照下表分配总共三十只动物的缺损孔洞,然后在第3和6个月两个时间点进行评估。
| 缺损孔洞1 | 缺损孔洞2 | 三个月 | 六个月 |
| 空支架 | 未经处理的缺损 | N=2 | N=3 |
| 空支架 | 活性支架1 | N=2 | N=3 |
| 空支架 | 活性支架2 | N=2 | N=3 |
| 活性支架1 | 未经处理的缺损 | N=2 | N=3 |
| 活性支架1 | 活性支架2 | N=2 | N=3 |
| 活性支架2 | 未经处理的缺损 | N=2 | N=3 |
分析
在研究过程的结束时,将动物麻醉,然后使用致死量麻醉剂处死动物。切除动物的后肢,识别该经处理区域。对缺损孔洞部位进行宏观检查,记录观察值并拍下照片。完整地除去缺损孔洞周围的软骨,立即转移进行组织固定。按体外样本中所述方法,对样本进行组织学和免疫组织化学分析。
用结构紊乱的纤维组织填充未经处理的缺损孔洞。免疫组织化学表明该修复组织主要由I型胶原蛋白组成。仅包含支架的缺损孔洞显示出较好的组织结构,但仍含较高的I型胶原蛋白,并且在植入组织和天然的组织之间整合性较差。用Follistatin和Follistatin+BMP-2处理的缺陷孔洞在所有的时间点上都具有高水平的II型胶原蛋白和GAGs。在缺陷孔洞边缘和软骨下骨存在组织整合的迹象,并且该组织在本质上是高度有序结构。因此可以得出结论:将Follistatin加入到愈合关节中,可通过增强BMP活性致使软骨修复。
表1.1
| ALPnmol/ml(a) | DNA浓度pg/ml(b) | 细胞数(b/7.7)(c) | ALP nmol/ml(a/c)(d) | 每个细胞平均ALPpmol/ml(平均d) | |
| Follistatin | -38.5093 | 128940 | 16745.45 | -0.0023 | |
| -31.677 | 147080 | 19101.3 | -0.00166 | ||
| -29.8137 | 188780 | 24516.88 | -0.00122 | 0 | |
| Follistatin+BMP-2 | 241.6149 | 127620 | 16574.03 | 0.014578 | |
| 270.4969 | 115135 | 14952.6 | 0.01809 | ||
| 245.9327 | 223330 | 29003.9 | 0.00848 | 13.7 | |
| TCP | -44.0994 | 116910 | 15183.12 | -0.0029 | |
| -40.9938 | 167840 | 21797.4 | -0.00188 | ||
| -40.6832 | 205720 | 26716.88 | -0.00152 | 0 | |
| BMP-2 | 19.87578 | 87170 | 11320.78 | 0.001756 | |
| 29.19255 | 103860 | 13488.31 | 0.002164 | ||
| 37.57764 | 193300 | 25103.9 | 0.001497 | 1.8 | |
| BSA | -38.5093 | 102430 | 13302.6 | -0.00289 | |
| -36.9565 | 139390 | 18102.6 | -0.00204 | ||
| -33.2298 | 171140 | 22225.97 | -0.0015 | 0 | |
| BSA+BMP-2 | 83.22981 | 120740 | 15680.52 | 0.005308 | |
| 77.63975 | 102650 | 13331.17 | 0.005824 | ||
| 59.93789 | 220560 | 28644.16 | 0.002092 | 4.4 |
表1,2a-Follistatin对C2C12细胞BMP-2的影响(溶液实验)
| 处理 | 释放的pNP(nmol/ml) | DNA浓度μg/ml | pNP/DNA | 每μg DNA的平均pNP(nmol/ml) | SD |
| FS+BMP-2s | 209 | 3.250307038 | 64.30161752 | ||
| 214.6666667 | 3.422720831 | 62.71813485 | |||
| 215.5 | 3.338504622 | 64.54985821 | |||
| 215.6666667 | 3.148748229 | 68.49282668 | 65.01560931 | 2.456022384 | |
| FSs | 0 | 1.977414131 | 0 | ||
| 0 | 2.25907956 | 0 | |||
| 0 | 2.196929617 | 0 | |||
| 0 | 2.049281328 | 0 | 0 | 0 | |
| BMP-2s | 28.5 | 1.10534449 | 25.78381695 | ||
| 35 | 1.107011269 | 31.61666098 | |||
| 16.16666667 | 1.301140428 | 12.42499758 | |||
| 19.83333333 | 1.170558067 | 16.94348524 | 21.69224019 | 8.634573673 | |
| TCPs | 0 | 1.497624671 | 0 | ||
| 0 | 1.599183481 | 0 | |||
| 0 | 1.455853971 | 0 | |||
| 0 | 1.473601458 | 0 | 0 | 0 |
表1,2b-Follistatin对C2C12细胞BMP-2的影响(溶液实验)
| 处理 | 释放的pNP(nmol/ml) | DNA浓度μg/ml | pNP/DNA | 每μg DNA的平均pNP(nmol/ml) | SD |
| FS+BMP | 179.5 | 2.307530873 | 77.78877507 | ||
| 217.6666667 | 2.633666239 | 82.64777952 | |||
| 212.5 | 2.663425332 | 79.78447806 | |||
| 190.6666667 | 2.66113098 | 71.64873434 | 77.967 | 4.6607 | |
| FS | 0 | 1.697165801 | 0 | ||
| 0 | 1.664909913 | 0 | |||
| 0 | 1.364187867 | 0 | |||
| 0 | 1.565645455 | 0 | 0 | 0 | |
| BMP-2 | 14.33333333 | 0.966630677 | 14.82813827 | ||
| 21.16666667 | 1.109825224 | 19.07207207 | |||
| 28.16666667 | 1.100674809 | 25.59036186 | |||
| 20.83333333 | 1.08431743 | 19.21331591 | 19.676 | 4.4370 | |
| TCP | 0 | 0.974829611 | 0 | ||
| 0 | 1.076584115 | 0 | |||
| 0 | 1.141311829 | 0 | |||
| 0 | 1.060233484 | 0 | 0 | 0 |
表1,2c-Follistatin对C2C12细胞BMP-5的影响(溶液实验)
| 处理 | 释放的pNP(ALP)(nmol/ml) | DNA浓度μg/ml | pNP/DNA | 每μg DNA的平均pNP(nmol/ml) | SD |
| FS+BMP-5s | 43.297 | 7.18 | 6.03022284 | ||
| 49.122 | 7.6 | 6.46342105 | |||
| 53.261 | 7.35 | 7.24639456 | |||
| 37.719 | 7.24 | 5.20980663 | 6.237 | 0.8501 | |
| FSs | 0 | 5.91 | 0 | ||
| 0 | 5.38 | 0 | |||
| 0 | 4.42 | 0 | |||
| 0 | 4.89 | 0 | 0 | 0 | |
| BMP-5s | 19.494 | 6.21 | 3.13913043 | ||
| 19.478 | 5.6 | 3.47821429 | |||
| 19.772 | 6.24 | 3.16858974 | |||
| 19.052 | 6.11 | 3.11816694 | 3.226 | 0.1694 | |
| TCPs | 0 | 6.27 | 0 | ||
| 0 | 5.84 | 0 | |||
| 0 | 4.9 | 0 | |||
| 0 | 5.03 | 0 | 0 | 0 |
表1,2d-Follistatin对C2C12细胞BMP-6活性的影响(溶液实验)
| 处理 | 释放的pNP(ALP)(nmol/ml) | DNA浓度μg/ml | pNP/DNA | 每μg DNA的平均pNP(nmol/ml) | SD |
| FS+BMP-6s | 250.45 | 4.306332046 | 58.15854358 | ||
| 211.34 | 5.282303732 | 40.00905868 | |||
| 203.03 | 5.533758044 | 36.68935259 | |||
| 202.11 | 4.820900901 | 41.92369936 | 44.195 | 9.5568 | |
| FSs | 0.12 | 5.817696268 | 0.020626721 | ||
| 0.34 | 6.096396396 | 0.055770652 | |||
| 0.33 | 6.327631918 | 0.052152212 | |||
| 0.68 | 5.053539254 | 0.134559161 | 0.066 | 0.0485 | |
| BMP-6s | 155.24 | 5.475662806 | 28.35090573 | ||
| 159.03 | 6.15951094 | 25.81860826 | |||
| 157.95 | 5.658893179 | 27.91181862 | |||
| 163.04 | 5.022934363 | 32.45911418 | 28.635 | 2.7785 | |
| TCPs | 0.12 | 5.849433719 | 0 | ||
| -0.07 | 6.708764479 | 0 | |||
| -0.29 | 6.599227799 | 0 | |||
| -0.15 | 4.672754183 | 0 | 0 | 0 |
表1,2e-Follistatin对C2C12细胞BMP-7活性的影响(溶液实验)
| 处理 | 释放的pNP(nmol/ml) | DNA浓度μg/ml | pNP/DNA | 每μg DNA的平均pNP(nmol/ml) | SD |
| FS+BMP-7s | 85.05 | 4.284749035 | 19.8494706 | ||
| 95.65 | 3.777631918 | 25.32009526 | |||
| 81.74 | 4.613166023 | 17.7188507 | |||
| 80.96 | 6.076229086 | 13.32405327 | 19.053 | 4.9837 | |
| FSs | 4.55 | 5.817696268 | 0.782096519 | ||
| 5.19 | 6.096396396 | 0.851322595 | |||
| 5.08 | 6.327631918 | 0.802827988 | |||
| 5.94 | 5.053539254 | 1.175413844 | 0.903 | 0.1840 | |
| BMP-7s | 30.27 | 5.66978121 | 5.33883035 | ||
| 37.04 | 5.07099099 | 7.304292211 | |||
| 41.95 | 4.164388674 | 10.07350737 | |||
| 52.14 | 3.362458172 | 15.50651259 | 7.572 | 2.3787 | |
| TCPs | 4.7 | 5.849433719 | 0.803496582 | ||
| 4.52 | 6.708764479 | 0.673745518 | |||
| 3.46 | 6.599227799 | 0.524303768 | |||
| 4.11 | 4.672754183 | 0.879566919 | 0.720 | 0.1559 |
表1,3a-Follistatin对C2C12细胞BMP-2的影响(结合实验)
| 处理 | 释放的pNP(ALP)(nmol/ml) | DNA浓度μg/ml | pNP/DNA | 每μg DNA的平均pNP(nmol/ml) | SD |
| FS+BMP-2 | 251.84 | 6.52 | 38.62576687 | ||
| 284.41 | 6.37 | 44.64835165 | |||
| 236.17 | 6.39 | 36.95931142 | |||
| 335.16 | 5.68 | 59.00704225 | 44.810 | 10.0243 | |
| FS | 0 | 5.88 | 0 | ||
| 0 | 5.56 | 0 | |||
| 0 | 5.68 | 0 | |||
| 0 | 5.93 | 0 | 0 | 0 | |
| BMP-2 | 36.42 | 8.65 | 4.210404624 | ||
| 31.4 | 8.28 | 3.792270531 | |||
| 30.5 | 8.3 | 3.674698795 | |||
| 40.5 | 7.98 | 5.07518797 | 4.188 | 0.6345 | |
| TCP | 0 | 6.83 | 0 | ||
| 0 | 6.9 | 0 | |||
| 0 | 6.58 | 0 | |||
| 0 | 5.55 | 0 | 0 | 0 |
表1,3b-Follistatin对C2C12细胞BMP-6活性的影响(结合实验)
| 处理 | 释放的pNP(ALP)(nmol/ml) | DNA浓度μg/ml | pNP/DNA | 每μg DNA的平均pNP(nmol/ml) | SD |
| FS+BMP-6b | 101.64 | 4.377477477 | 23.21885162 | ||
| 87.31 | 5.005045045 | 17.44439844 | |||
| 94.68 | 5.020913771 | 18.85712528 | |||
| 108.71 | 5.012277992 | 21.68874116 | 20.302 | 2.6258 | |
| FSb | 25.81 | 4.895032175 | 5.272692615 | ||
| 21.82 | 4.735508366 | 4.607741834 | |||
| 19.18 | 5.078288288 | 3.776863169 | |||
| 19.69 | 5.66047619 | 3.478505931 | 4.284 | 0.8141 | |
| BMP-6b | 34.37 | 5.290888031 | 6.496073967 | ||
| 36.06 | 6.051544402 | 5.958809455 | |||
| 34.12 | 5.628095238 | 6.062441831 | |||
| 34.34 | 5.429009009 | 6.325279612 | 6.211 | 0.2449 | |
| TCPb | 15.76 | 5.573204633 | 2.827816496 | ||
| 15.28 | 5.063153153 | 3.017882244 | |||
| 11.66 | 5.625855856 | 2.072573542 | |||
| 13.14 | 5.944761905 | 2.210349247 | 2.532 | 0.4612 |
表1,3c-Follistatin对C2C12细胞BMP-6活性的影响(结合实验)
| 处理 | 释放的pNP(nmol/ml) | DNA浓度μg/ml | pNP/DNA | 每μg DNA的平均pNP(nmol/ml) | SD |
| FS+BMP-6b | 25.76 | 2.37 | 10.8692 | ||
| 33.16 | 1.28 | 25.90625 | |||
| 39.73 | 1.82 | 21.82967 | |||
| 48.9 | 1.63 | 30 | 22.151 | 8.2278 | |
| FSb | 0 | 1.9 | 0 | ||
| 0 | 1.81 | 0 | |||
| 0 | 1.82 | 0 | |||
| 0 | 1.27 | 0 | 0 | 0 | |
| BMP-6b | 0.37 | 1.66 | 0.222892 | ||
| -0.28 | 1.11 | -0.25225 | |||
| 0 | 1.01 | 0 | |||
| 0.05 | 0.92 | 0.054348 | 0.006 | 0.1967 | |
| TCPb | 0 | 1.6 | 0 | ||
| 0 | 1.88 | 0 | |||
| 0 | 1.85 | 0 | |||
| 0 | 1.66 | 0 | 0 | 0 |
表1,3d-Follistatin对C2C12细胞BMP-7活性的影响(结合实验)
| 处理 | 释放的pNP(nmol/ml) | DNA浓度μg/ml | pNP/DNA | 每μg DNA的平均pNP(nmol/ml) | SD |
| FS+BMP-7b | 34.17 | 4.313101673 | 7.922372944 | ||
| 39.15 | 4.124388674 | 9.492315854 | |||
| 30.07 | 5.063552124 | 5.938518903 | |||
| 32.08 | 4.12018018 | 7.786067258 | 7.785 | 1.4541 | |
| FSb | 25.81 | 4.895032175 | 5.272692615 | ||
| 21.82 | 4.735508366 | 4.607741834 | |||
| 19.18 | 5.078288288 | 3.776863169 | |||
| 19.69 | 5.66047619 | 3.478505931 | 4.284 | 0.8141 | |
| BMP-7b | 16.7 | 4.28993585 | 3.892832285 | ||
| 18.44 | 3.36957529 | 5.472499771 | |||
| 15.67 | 4.889485199 | 3.20483637 | |||
| 18.25 | 3.569189189 | 5.113206118 | 4.421 | 1.0556 | |
| TCPb | 15.76 | 5.573204633 | 2.827816496 | ||
| 15.28 | 5.063153153 | 3.017882244 | |||
| 11.66 | 5.825855856 | 2.072573542 | |||
| 13.14 | 5.944761905 | 2.210349247 | 2.532 | 0.4612 |
表1,4-Follistatin对C2C12细胞BMP-4的影响(溶液实验)
| 处理 | 释放的pNP(ALP)nmol/ml | DNA浓度μg/ml | pNP/DNA | 每μg DNA的平均pNP(nmol/ml) | SD |
| FS+BMP-4s | 82 | 4.7613 | 17.22219 | ||
| 102.1666667 | 4.8615 | 21.01546 | |||
| 85.16666677 | 4.2813 | 19.89271 | |||
| 89.83333333 | 5.0527 | 17.77927 | 18.977 | 1.7802 | |
| FSs | -2.666666667 | 6.3443 | -0.42032 | ||
| 0.666666667 | 8.0583 | 0.08273 | |||
| -4.833333333 | 7.0452 | -0.88605 | |||
| -4.833333333 | 6.8855 | -0.72513 | 0 | 0 | |
| BMP-4s | 24.66666667 | 4.6547 | 5.299303 | ||
| 25.33333333 | 5.0515 | 5.015012 | |||
| 41.16666667 | 4.6542 | 8.845058 | |||
| 20.33333333 | 4.669 | 4.354965 | 5.879 | 2.0168 | |
| TCPs | -2.166666667 | 5.4711 | -0.39602 | ||
| -4.666666667 | 5.6445 | -0.82676 | |||
| -5.166666667 | 5.7691 | -0.89558 | |||
| -4 | 5.5138 | -0.72545 | 0 | 0 |
表1,5-Follistatin对C2C12细胞BMP-4的影响(结合实验)
| 处理 | 释放的pNP(ALP)nmol/ml | DNA浓度μg/ml | pMP/DNA | 每μg DNA的平均pNP(nmol/ml) | SD |
| FS+BMP-4b | 184.1666667 | 3.79 | 48.59279 | ||
| 178.1666667 | 3.5472 | 50.22741 | |||
| 196.8333333 | 3.4499 | 57.05479 | |||
| 105.5 | 3.5566 | 29.66316 | 46.385 | 11.7346 | |
| FSb | -2.666666667 | 5.5329 | -0.48197 | ||
| -3.833333333 | 6.0595 | -0.63262 | |||
| 0.333333333 | 5.6301 | 0.059206 | |||
| -4.333333333 | 5.6836 | -0.76243 | 0 | 0 | |
| BMP-4b | 53.16666667 | 3.8842 | 13.68793 | ||
| 71.16666667 | 4.1643 | 17.08971 | |||
| 69 | 3.7796 | 18.2559 | |||
| 37.33333333 | 4.2224 | 8.841733 | 14.469 | 4.2224 | |
| TCPb | -4.5 | 4.791 | -0.93926 | ||
| -4.666666667 | 5.7638 | -0.80965 | |||
| -4.5 | 4.5645 | -0.98587 | |||
| -4.5 | 4.6975 | -0.95796 | 0 | 0 |
表1,6-Follistatin对MC3T3E1细胞BMP-2活性的影响(溶液实验)
| 处理 | 释放的pNP(nmol/ml) | DNA浓度μg/ml | pNP/DNA | 每μg DNA的平均pNP(nmol/ml) | SD |
| FS+BMP-2s | 130.521 | 4.0698 | 32.07062 | ||
| 131.678 | 3.8437 | 34.25814 | |||
| 148.667 | 3.8895 | 38.22265 | |||
| 130.455 | 4.0879 | 31.91247 | 34.116 | 2.9396 | |
| FSs | 0 | 3.2027 | 0 | ||
| 0 | 2.6139 | 0 | |||
| 0 | 2.5035 | 0 | |||
| 0 | 2.8822 | 0 | 0 | 0 | |
| BMP-2s | 0 | 1.2724 | 0 | ||
| 0 | 0.5672 | 0 | |||
| 55.556 | 1.7679 | 31.42485 | |||
| 63.264 | 1.592 | 39.73869 | 17.791 | 20.8218 | |
| TCPs | 0 | 3.6327 | 0 | ||
| 0 | 3.2233 | 0 | |||
| 0 | 3.2787 | 0 | |||
| 0 | 3.6762 | 0 | 0 | 0 |
表1,7-Follistatin对MC3T3E1细胞BMP-2活性的影响(结合实验)
| 处理 | 释放的pNP(nmol/ml) | DNA浓度μg/ml | pNP/DNA | 每μg DNA的平均pNP(nmol/ml) | SD |
| FS+BMP-2b | 66.97 | 4.503258487 | 14.87146 | ||
| 63.09 | 3.035459527 | 20.78433 | |||
| 54.45 | 4.914297529 | 11.07992 | 15.579 | 4.8907 | |
| FSb | 0 | 2.939935904 | 0 | ||
| 0 | 2.541300527 | 0 | |||
| 0 | 3.800268789 | 0 | 0 | 0 | |
| BMP-2b | 36.15 | 4.178573969 | 8.65542 | ||
| 33.32 | 3.93156208 | 8.475003 | |||
| 32.47 | 5.230641993 | 6.207651 | 7.779 | 1.3641 | |
| TCPb | 0 | 3.482083476 | 0 | ||
| 0 | 3.448588179 | 0 | |||
| 0 | 4.643233743 | 0 | 0 | 0 | |
表1.8-Follistatin288对C2C12细胞BMP-2活性的影响(溶液实验)
| 处理 | 释放的pNP(nmol/ml) | 平均pNP(nmol/ml)/孔 | SD |
| FS288+BMP-2s | 83 | ||
| 148.8333333 | |||
| 199.3333333 | |||
| 162.8333333 | 148.5 | 48.5793 | |
| FS288s | -3.5 | ||
| -3 | |||
| -3.5 | |||
| -3.333333333 | 0 | 0 | |
| BMP-2s | 5.666666667 | ||
| 13.5 | |||
| 13.33333333 | |||
| 0.5 | 8.25 | 6.3282 | |
| TCPs | -3.833333333 | ||
| -3.66666667 | |||
| -3.666666667 | |||
| -3.333333333 | 0 | 0 |
表1,9-Follistatin288对C2C12细胞BMP-2活性的影响(结合实验)
| 处理 | 释放的pNP(nmol/ml) | DNA浓度μg/ml | pNP/DNA | 每μg DNA的平均pNP(nmol/ml) | SD |
| FS288+BMP-2b | 31.25 | 4.232 | 7.384216 | ||
| 15.5 | 3.8651 | 4.010246 | |||
| 21.75 | 4.2676 | 5.096541 | |||
| 26.5 | 3.9742 | 6.668009 | 5.790 | 1.5232 | |
| FS288b | 1 | 4.2372 | 0.236005 | ||
| 1 | 4.8237 | 0.20731 | |||
| 1.75 | 4.5518 | 0.384463 | |||
| 1.75 | 4.3356 | 0.403835 | 0.308 | 0.1005 | |
| BMP-2b | 5.5 | 5.0876 | 1.08106 | ||
| 6.75 | 5.443 | 1.240125 | |||
| 4.25 | 5.1542 | 0.82457 | |||
| 5.75 | 4.6221 | 1.244023 | 1.097 | 0.1971 | |
| TCPb | 0.75 | 5.1705 | 0.145054 | ||
| 1 | 5.817 | 0.17191 | |||
| 0.75 | 5.5955 | 0.134036 | |||
| 0.5 | 5.416 | 0.092319 | 0.136 | 0.03311 |
| Young | 孔数 | 消化液体积 | DNA/ml | 总DNA | GAG med 1/m | GAG/ml med 2/ | GAG med 1 | GAG med 2 | 培养基总GAG | GAG/ml(消化液) | 消化液总GAG | 总GAG | 胶原蛋白/ml | 总胶原蛋白 |
| 对照 | 1 | 0.5 | 12.899 | 6.4495 | 54.9 | 52.75 | 9.62 | 26.375 | 35.995 | 19.24 | 9.62 | 45.615 | 2.55 | 1.275 |
| 2 | 0.5 | 11.938 | 5.969 | 44.2 | 41.31 | 9.225 | 20.655 | 29.88 | 18.45 | 9.225 | 39.105 | 2.34 | 1.17 | |
| 3 | 0.5 | 12.768 | 6.384 | 45.6 | 41.82 | 9.465 | 20.91 | 30.375 | 18.93 | 9.465 | 39.84 | 2.55 | 1.275 | |
| 4 | 0.5 | 12.784 | 6.392 | 42.32 | 39.82 | 9.45 | 19.91 | 29.36 | 18.9 | 9.45 | 36.81 | 2.65 | 1.325 | |
| 5 | 0.5 | 12.735 | 6.3675 | 43.62 | 47.57 | 9.73 | 23.785 | 33.515 | 19.46 | 9.73 | 43.245 | 2.51 | 1.255 | |
| 6.310.19 | 41.322.98 | 1.260.06 | ||||||||||||
| BMP-2 500mg | 6 | 0.5 | 22.527 | 11.2635 | 62.7 | 95.43 | 41.35 | 47.715 | 89.065 | 64.59 | 32.295 | 121.36 | 6.49 | 3.245 |
| 7 | 0.5 | 22.328 | 11.164 | 71.47 | 71.63 | 35.735 | 35.815 | 71.55 | 56.34 | 28.17 | 99.72 | 6.93 | 2.965 | |
| 8 | 0.5 | 23.807 | 11.9035 | 83.74 | 85.56 | 41.87 | 42.78 | 84.65 | 66.79 | 33.396 | 118.045 | 6.91 | 3.455 | |
| 9 | 0.5 | 21.575 | 10.7675 | 72.23 | 73.7 | 36.115 | 36.65 | 72.965 | 56.37 | 28.185 | 101.15 | 5.88 | 2.94 | |
| 10 | 0.5 | 22.589 | 11.2945 | 71.77 | 72.01 | 35.885 | 38.005 | 71.89 | 61.42 | 30.71 | 102.6 | 6.14 | 3.07 | |
| 11.28 | 108.56 | 3.14 | ||||||||||||
| 0.40 | 10.28 | 0.22 | ||||||||||||
| BMP∶FS 100∶300 | 11 | 0.5 | 15.331 | 7.6655 | 64.64 | 65.08 | 32.32 | 32.54 | 64.86 | 23.7 | 11.65 | 76.71 | 2.95 | 1.475 |
| 12 | 0.5 | 14.929 | 7.4645 | 57.69 | 51.64 | 28.845 | 25.82 | 54.665 | 24.16 | 12.08 | 66.745 | 3.24 | 1.62 | |
| 13 | 0.5 | 15.675 | 7.8375 | 66.81 | 58.47 | 33.405 | 29.235 | 62.64 | 22.55 | 11.275 | 73.915 | 2.97 | 1.485 | |
| 14 | 0.5 | 17.164 | 8.852 | 61.93 | 46.85 | 30.965 | 23.425 | 54.39 | 25.2 | 12.6 | 66.99 | 3.1 | 1.55 | |
| 15 | 0.5 | 14.273 | 7.1365 | 58.67 | 46.05 | 29.335 | 24.025 | 53.36 | 21.61 | 10.805 | 64.165 | 3 | 1.5 | |
| 7.74 | 69.71 | 1.53 | ||||||||||||
| 0.54 | 5.93 | 0.08 | ||||||||||||
| BMP∶FS 500∶1500 | 16 | 0.5 | 26.996 | 13.498 | 95.38 | 117.95 | 47.69 | 58.975 | 106.665 | 62.39 | 31.195 | 137.66 | 7.34 | 3.67 |
| 17 | 0.5 | 26.609 | 13.3045 | 92.79 | 107.45 | 46.395 | 53.725 | 100.12 | 61.04 | 31.345 | 131.465 | 6.82 | 3.41 | |
| 18 | 0.5 | 28.309 | 14.1545 | 93.86 | 105.63 | 46.93 | 52.815 | 99.745 | 62.69 | 30.875 | 130.62 | 7.43 | 3.715 | |
| 19 | 0.5 | 29.078 | 14.539 | 93.53 | 100.9 | 46.795 | 50.45 | 97.245 | 61.75 | 26.365 | 123.61 | 7.61 | 3.805 | |
| 20 | 0.5 | 26.682 | 13.341 | 88.79 | 92.92 | 44.395 | 46.46 | 90.855 | 52.73 | 26.365 | 117.22 | 6.97 | 3.465 | |
| 13.77 | 128.16 | 3.62 | ||||||||||||
| 0.55 | 7.93 | 0.15 |
表2.2
| 孔数 | 消化液体积 | DNA/ml | 总DNA | GAG/ml(培养基) | 培养基体积 | 培养基总GAG | GAG/ml(消化液) | 消化液总GAG | 总GAG | GAG/ug DNA | |
| 对照 | 1 | 0.5 | 8.19 | 4.095 | 17.1 | 0.5 | 8.55 | 8.65 | 4.325 | 12.875 | 3.14 |
| 2 | 0.5 | 9.27 | 4.635 | 20.1 | 0.5 | 10.05 | 9.12 | 4.56 | 14.61 | 3.15 | |
| 3 | 0.5 | 9.27 | 4.635 | 17.68 | 0.5 | 8.84 | 7.24 | 3.82 | 12.46 | 2.69 | |
| 4 | 0.5 | 9.2 | 4.6 | 16.8 | 0.5 | 8.4 | 7.88 | 3.94 | 12.34 | 2.68 | |
| 4.49 | 8.9 | 8.22 | 4.11 | 13.07 | 2.02 | ||||||
| 0.26 | 0.75 | 0.83 | 0.42 | 1.05 | 0.27 | ||||||
| BMP-2 | 5 | 0.5 | 9.28 | 4.64 | 28.79 | 0.5 | 14.395 | 13.36 | 6.68 | 21.075 | 4.54 |
| 6 | 0.5 | 9.05 | 4.525 | 28.93 | 0.5 | 14.465 | 12.41 | 6.205 | 20.67 | 4.57 | |
| 7 | 0.5 | 10.15 | 5.075 | 29.91 | 0.5 | 14.955 | 13.58 | 6.79 | 21.745 | 4.28 | |
| 8 | 0.5 | 9.78 | 4.89 | 26.44 | 0.5 | 13.22 | 12.71 | 6.355 | 19.575 | 4.00 | |
| 4.78 | 14.25 | 13.02 | 6.51 | 20.77 | 4.35 | ||||||
| 0.25 | 0.74 | 0.55 | 0.27 | 0.91 | 0.26 | ||||||
| FS | 9 | 0.5 | 8.8 | 4.4 | 17.55 | 0.5 | 8.775 | 7.21 | 3.605 | 12.38 | 2.81 |
| 10 | 0.5 | 8.82 | 4.41 | 18.25 | 0.5 | 9.125 | 6.93 | 3.465 | 12.59 | 2.85 | |
| 1112 | 0.50.5 | 8.958.81 | 4.4754.405 | 17.5217.95 | 0.50.5 | 8.768.975 | 6.657.7 | 3.3253.85 | 12.08512.825 | 2.702.91 | |
| 4.42 | 8.91 | 7.12 | 3.56 | 12.47 | 2.82 | ||||||
| 0.04 | 0.17 | 0.45 | 0.22 | 0.31 | 0.09 | ||||||
| BMP-2+FS | 13 | 0.5 | 6.93 | 3.465 | 25.06 | 0.5 | 12.53 | 10.56 | 5.28 | 17.81 | 5.14 |
| 14 | 0.5 | 8.8 | 4.4 | 25.98 | 0.5 | 12.99 | 13.94 | 6.97 | 19.96 | 4.54 | |
| 15 | 0.5 | 7.69 | 3.845 | 26.1 | 0.5 | 13.05 | 12.63 | 6.315 | 19.365 | 5.04 | |
| 16 | 0.5 | 7.53 | 3.765 | 23.4 | 0.5 | 11.7 | 14.18 | 7.09 | 18.79 | 4.99 | |
| 3.87 | 12.57 | 12.83 | 6.41 | 19.98 | 4.93 | ||||||
| 0.39 | 0.62 | 1.66 | 0.83 | 0.92 | 0.27 |
表2.3
| 孔数 | 消化液体积 | DNA/ml | 总DNA | GAG/ml(培养基) | 培养基体积 | 培养基总GAG | GAG/ml(消化液) | 消化液总GAG | 总GAG | GAG/ug DNA | |
| 对照 | 1 | 0.5 | 0.88 | 0.44 | 35.23 | 1 | 35.23 | 16.57 | 8.285 | 43.515 | 98.90 |
| 2 | 0.5 | 0.99 | 0.495 | 36.98 | 1 | 36.98 | 16.75 | 8.375 | 45.355 | 91.63 | |
| 3 | 0.5 | 1.07 | 0.535 | 35.85 | 1 | 35.85 | 15.87 | 7.935 | 43.785 | 81.84 | |
| 4 | 0.5 | 0.99 | 0.495 | 40.63 | 1 | 40.63 | 17.12 | 8.56 | 49.19 | 99.37 | |
| 92.93 | |||||||||||
| 8.20 | |||||||||||
| OP-1 | 13 | 0.5 | 1.31 | 0.655 | 66.24 | 1 | 66.24 | 36.85 | 19.425 | 85.665 | 130.79 |
| 14 | 0.5 | 1.19 | 0.595 | 66.48 | 1 | 66.48 | 39.35 | 19.675 | 86.155 | 144.80 | |
| 15 | 0.5 | 1.15 | 0.575 | 64.75 | 1 | 64.75 | 38.56 | 19.28 | 84.03 | 146.14 | |
| 16 | 0.6 | 1.29 | 0.645 | 54.1 | 1 | 54.1 | 28.35 | 14.175 | 68.275 | 105.85 | |
| 131.89 | |||||||||||
| 18.70 | |||||||||||
| OP-1+FS | 17 | 0.5 | 1.07 | 0.535 | 66.93 | 1 | 66.93 | 36.09 | 18.04 | 84.97 | 158.82 |
| 18 | 0.5 | 1.06 | 0.53 | 61.74 | 1 | 61.74 | 34.56 | 17.28 | 79.02 | 149.09 | |
| 19 | 0.5 | 1.05 | 0.525 | 61.61 | 1 | 61.61 | 33 | 16.5 | 78.11 | 148.78 | |
| 20 | 0.5 | 1.14 | 0.57 | 63.36 | 1 | 63.36 | 31.24 | 15.62 | 78.98 | 138.56 | |
| 148.31 | |||||||||||
| 8.27 |
表2.4
Claims (24)
1.一种包含BMP结合蛋白的药用组合物。
2.一种包含有助于组织再生的BMP结合蛋白的药用组合物。
3.权利要求1或2要求保护的药用组合物,其中所述BMP结合蛋白选自:Follistatin、ZFSTA2、FSRP、FLIK、α-2-HS糖蛋白、胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Chordin、Sog、Crim、Nell、结缔组织生长因子(CTGF)、Dan、Gremlin、Cerberus、Endoglin、Twisted Gastulation基因或以上提到的BMP结合蛋白的衍生物、片段和/或类似物。
4.权利要求1、2或3任一项要求保护的药用组合物,其中所述BMP结合蛋白选自:Follistatin、ZFSTA2、FSRP、FLIK、胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Endoglin、Dan、Gremlin、Cerberus、Chordin、Sog、Crim、Nell或以上提到的BMP结合蛋白的衍生物、片段和/或类似物。
5.任一项前述权利要求要求保护的药用组合物,其中所述BMP结合蛋白选自Follistatin或其衍生物、片段和/或类似物,所述Follistatin为所列出的氨基酸序列(1)描述的蛋白质。
6.权利要求1-4任一项要求保护的药用组合物,其中所述BMP结合蛋白为胶原蛋白IIa或其衍生物、片段和/或类似物。
7.权利要求2要求保护的药用组合物,其中所述组织为骨。
8.权利要求2要求保护的药周组合物,其中所述组织为软骨。
9.BMP结合蛋白在制备用于治疗可通过促进组织再生例如软骨和/或骨组织再生而缓解的疾病或临床症状的药物中的用途。
10.权利要求9要求保护的BMP结合蛋白的用途,其中所述BMP结合蛋白选自:Follistatin、ZFSTA2、FLIK、FSRP、α-2-HS糖蛋白、胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Chordin、Sog、Crim、Nell、结缔组织生长因子(CTGF)、Dan、Gremlin、Cerberus、Endoglin、Twisted Gastulation基因或以上提到的BMP结合蛋白的衍生物、片段和/或类似物。
11.权利要求9要求保护的BMP结合蛋白的用途,其中所述BMP结合蛋白选自:Follistatin、ZFSTA2、FLIK、FSRP、胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Endoglin、Dan、Gremlin、Cerberus、Chordin、Sog、Crim、Nell或以上提到的BMP结合蛋白的衍生物、片段和/或类似物。
12.权利要求9、10或11任一项要求保护的BMP结合蛋白在制备药物中的用途,其中所述组织为骨。
13.权利要求9、10或11任一项要求保护的BMP结合蛋白在制备药物中的用途,其中所述组织为软骨。
14.一种促进组织增殖的支架结构,其中该支架结构包含BMP结合蛋白。
15.权利要求15要求保护的促进组织增殖的支架结构,其中所述BMP结合蛋白为胶原蛋白IIa。
16.权利要求15要求保护的促进组织增殖的支架结构,其中所述BMP结合蛋白为Follistatin。
17.权利要求15要求保护的促进组织增殖的支架结构,其中所述BMP结合蛋白为胶原蛋白IIa。
18.权利要求15要求保护的促进组织增殖的支架结构,其中所述BMP结合蛋白选自:Follistatin、ZFSTA2、FLIK、FSRP、α-2-HS糖蛋白、胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Chordin、Sog、Crim、Nell、结缔组织生长因子(CTGF)、Dan、Gremlin、Cerberus、Endoglin、Twisted Gastulation基因或以上提到的BMP结合蛋白的衍生物、片段和/或类似物。
19.权利要求15要求保护的促进组织增殖的支架结构,其中所述BMP结合蛋白选自:Follistatin、FLIK、FSRP、胶原蛋白IIa、胶原蛋白IV、胶原蛋白Vα1、胶原蛋白Vα2、Endoglin、Dan、Gremlin、Cerberus、Chordin、Sog、Crim、Nell或以上提到的BMP结合蛋白的衍生物、片段和/或类似物。
20.权利要求15要求保护的促进组织增殖的支架结构,其中所述BMP结合蛋白为Endoglin。
21.权利要求15-21任一项要求保护的支架结构,其中所述组织为骨。
22.权利要求15-21任一项要求保护的支架结构,其中所述组织为软骨。
23.一种促进组织再生的装置,其中该仪器包含根据权利要求1-9任一项的药物。
24.一种制备用于促进组织增殖的支架结构的方法,该方法包括用BMP结合蛋白包覆支架结构的步骤。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB0113606A GB0113606D0 (en) | 2001-06-08 | 2001-06-08 | Composition |
| GB0113606.8 | 2001-06-08 | ||
| GB0200437.2 | 2002-01-10 | ||
| GB0200437A GB0200437D0 (en) | 2002-01-10 | 2002-01-10 | Composition |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN1538850A true CN1538850A (zh) | 2004-10-20 |
Family
ID=26246153
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNA028153421A Pending CN1538850A (zh) | 2001-06-08 | 2002-06-10 | 用于骨或软骨再生的bmp结合蛋白 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US20040176287A1 (zh) |
| EP (1) | EP1399177A1 (zh) |
| JP (1) | JP2004536818A (zh) |
| CN (1) | CN1538850A (zh) |
| CA (1) | CA2449573A1 (zh) |
| IL (1) | IL159240A0 (zh) |
| MX (1) | MXPA03011386A (zh) |
| NO (1) | NO20035453D0 (zh) |
| WO (1) | WO2002100426A1 (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN110072566A (zh) * | 2016-10-09 | 2019-07-30 | 刘英芹 | 骨与软组织同步再生诱导剂及其制备方法和用途 |
Families Citing this family (36)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7687462B2 (en) * | 1999-10-05 | 2010-03-30 | The Regents Of The University Of California | Composition for promoting cartilage formation or repair comprising a nell gene product and method of treating cartilage-related conditions using such composition |
| GB2385052A (en) | 2002-02-05 | 2003-08-13 | Leuven K U Res & Dev | Treatment of spondyloarthropathies |
| EP2255832A3 (en) * | 2004-06-16 | 2011-02-09 | Affinergy, Inc. | IFBM's to promote attachment of target analytes |
| US20180228621A1 (en) | 2004-08-09 | 2018-08-16 | Mark A. Reiley | Apparatus, systems, and methods for the fixation or fusion of bone |
| US8388667B2 (en) | 2004-08-09 | 2013-03-05 | Si-Bone, Inc. | Systems and methods for the fixation or fusion of bone using compressive implants |
| US20070156241A1 (en) | 2004-08-09 | 2007-07-05 | Reiley Mark A | Systems and methods for the fixation or fusion of bone |
| US9949843B2 (en) | 2004-08-09 | 2018-04-24 | Si-Bone Inc. | Apparatus, systems, and methods for the fixation or fusion of bone |
| US8425570B2 (en) | 2004-08-09 | 2013-04-23 | Si-Bone Inc. | Apparatus, systems, and methods for achieving anterior lumbar interbody fusion |
| US8414648B2 (en) | 2004-08-09 | 2013-04-09 | Si-Bone Inc. | Apparatus, systems, and methods for achieving trans-iliac lumbar fusion |
| US9662158B2 (en) | 2004-08-09 | 2017-05-30 | Si-Bone Inc. | Systems and methods for the fixation or fusion of bone at or near a sacroiliac joint |
| US20060036251A1 (en) | 2004-08-09 | 2006-02-16 | Reiley Mark A | Systems and methods for the fixation or fusion of bone |
| US7351423B2 (en) | 2004-09-01 | 2008-04-01 | Depuy Spine, Inc. | Musculo-skeletal implant having a bioactive gradient |
| US20090155332A1 (en) * | 2005-02-25 | 2009-06-18 | Eugene Sherry | Replacement bone tissue |
| GB0515477D0 (en) * | 2005-07-28 | 2005-08-31 | Smith & Nephew | Composition |
| AU2007230604A1 (en) | 2006-03-28 | 2007-10-04 | Wyeth | GDF-9/BMP-15 modulators for the treatment of bone disorders |
| WO2008060139A1 (en) * | 2006-11-17 | 2008-05-22 | Erasmus University Medical Center Rotterdam | Methods for controlling mineralization of extracellular matrix, therapeutic methods based thereon and medicaments for use therein |
| JP5593226B2 (ja) | 2007-09-28 | 2014-09-17 | ユーティー−バッテル・エルエルシー | 細胞分化シグナル伝達タンパク質nell1を用いた心臓血管障害の治療 |
| CA2699614C (en) | 2007-09-28 | 2020-03-24 | Ut-Battelle, Llc | Methods for promoting wound healing and muscle regeneration with the cell signaling protein nell1 |
| US20090183503A1 (en) * | 2008-01-18 | 2009-07-23 | Alberto Verdesi | Exhaust apparatus |
| CN101601858B (zh) * | 2009-05-27 | 2012-09-19 | 上海交通大学 | 中期因子蛋白的用途及含该蛋白的医用装置 |
| EP2822490A4 (en) | 2012-03-09 | 2016-03-02 | Si Bone Inc | INTEGRATED IMPLANT |
| US10363140B2 (en) | 2012-03-09 | 2019-07-30 | Si-Bone Inc. | Systems, device, and methods for joint fusion |
| IN2014DN08676A (zh) * | 2012-05-04 | 2015-05-22 | Si Bone Inc | |
| EP2902413B1 (en) * | 2012-09-26 | 2019-07-17 | FUJIFILM Corporation | Polypeptide, scaffold composition, composition for cartilage tissue restoration, composition for cartilage cell culture, and composition for promoting glycosaminoglycan production |
| WO2014145902A1 (en) | 2013-03-15 | 2014-09-18 | Si-Bone Inc. | Implants for spinal fixation or fusion |
| WO2015057866A1 (en) | 2013-10-15 | 2015-04-23 | Si-Bone Inc. | Implant placement |
| US11147688B2 (en) | 2013-10-15 | 2021-10-19 | Si-Bone Inc. | Implant placement |
| EP3782586A1 (en) | 2014-09-18 | 2021-02-24 | SI-Bone, Inc. | Matrix implant |
| WO2016044731A1 (en) | 2014-09-18 | 2016-03-24 | Si-Bone Inc. | Implants for bone fixation or fusion |
| US10376206B2 (en) | 2015-04-01 | 2019-08-13 | Si-Bone Inc. | Neuromonitoring systems and methods for bone fixation or fusion procedures |
| US10752663B2 (en) | 2016-08-29 | 2020-08-25 | NellOne Therapeutics, Inc. | Methods and compositions for regenerating tissues |
| WO2019067584A1 (en) | 2017-09-26 | 2019-04-04 | Si-Bone Inc. | SYSTEMS AND METHODS FOR DECORTICATING SACROILITIC JOINT |
| WO2020168269A1 (en) | 2019-02-14 | 2020-08-20 | Si-Bone Inc. | Implants for spinal fixation and or fusion |
| US11369419B2 (en) | 2019-02-14 | 2022-06-28 | Si-Bone Inc. | Implants for spinal fixation and or fusion |
| JP2023505055A (ja) | 2019-11-27 | 2023-02-08 | エスアイ-ボーン・インコーポレイテッド | 骨安定インプラント及び仙腸関節を横切る配置方法 |
| WO2022125619A1 (en) | 2020-12-09 | 2022-06-16 | Si-Bone Inc. | Sacro-iliac joint stabilizing implants and methods of implantation |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4816437A (en) * | 1987-06-01 | 1989-03-28 | Trustees Of Boston University | Methods for inducing general and localized bone apposition in-vivo |
| US5041538A (en) * | 1987-08-28 | 1991-08-20 | The Salk Institute For Biological Studies | Mammalian follistatin |
| US5837258A (en) * | 1991-08-30 | 1998-11-17 | University Of South Florida | Induction of tissue, bone or cartilage formation using connective tissue growth factor |
| US5846770A (en) * | 1994-11-22 | 1998-12-08 | Genetics Institute, Inc. | DNA molecules encoding human chordin |
| EP0975752A1 (en) * | 1997-04-29 | 2000-02-02 | Regeneron Pharmaceuticals, Inc. | Human cerberus protein |
| EP0950415A1 (en) * | 1998-04-08 | 1999-10-20 | Roche Diagnostics GmbH | Use of a combination of an osteoinductive protein and a dorsalizing factor for cartilage induction |
| US6355788B1 (en) * | 1998-10-15 | 2002-03-12 | Zymogenetics, Inc. | Follistatin-related protein zfsta2 |
| US7052856B2 (en) * | 1999-10-05 | 2006-05-30 | The Regents Of The University Of California | NELL-1 enhanced bone mineralization |
-
2002
- 2002-06-10 IL IL15924002A patent/IL159240A0/xx unknown
- 2002-06-10 CN CNA028153421A patent/CN1538850A/zh active Pending
- 2002-06-10 US US10/479,747 patent/US20040176287A1/en not_active Abandoned
- 2002-06-10 EP EP02730447A patent/EP1399177A1/en not_active Withdrawn
- 2002-06-10 WO PCT/GB2002/002427 patent/WO2002100426A1/en not_active Application Discontinuation
- 2002-06-10 MX MXPA03011386A patent/MXPA03011386A/es unknown
- 2002-06-10 CA CA002449573A patent/CA2449573A1/en not_active Abandoned
- 2002-06-10 JP JP2003503246A patent/JP2004536818A/ja not_active Withdrawn
-
2003
- 2003-12-08 NO NO20035453A patent/NO20035453D0/no not_active Application Discontinuation
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN110072566A (zh) * | 2016-10-09 | 2019-07-30 | 刘英芹 | 骨与软组织同步再生诱导剂及其制备方法和用途 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP1399177A1 (en) | 2004-03-24 |
| CA2449573A1 (en) | 2002-12-19 |
| MXPA03011386A (es) | 2004-05-27 |
| IL159240A0 (en) | 2004-06-01 |
| JP2004536818A (ja) | 2004-12-09 |
| NO20035453D0 (no) | 2003-12-08 |
| WO2002100426A1 (en) | 2002-12-19 |
| US20040176287A1 (en) | 2004-09-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1538850A (zh) | 用于骨或软骨再生的bmp结合蛋白 | |
| CN100339477C (zh) | 用于组织修复的方法和器件 | |
| Ramshaw | Biomedical applications of collagens | |
| Diekman et al. | Stem cell-based therapies for osteoarthritis: challenges and opportunities | |
| Miron et al. | Osteogenic potential of autogenous bone grafts harvested with four different surgical techniques | |
| CN1127568C (zh) | 成纤维细胞生长因子同系物 | |
| von Heimburg et al. | Comparison of viable cell yield from excised versus aspirated adipose tissue | |
| Isogai et al. | Experimental use of fibrin glue to induce site-directed osteogenesis from cultured periosteal cells | |
| CN1309428C (zh) | 关节软骨再生材料及其制造方法、关节软骨的再生方法及培养方法以及移植用人造关节软骨 | |
| Lee et al. | Synovium-derived mesenchymal stem cells encapsulated in a novel injectable gel can repair osteochondral defects in a rabbit model | |
| CN1649899A (zh) | 结缔组织刺激肽 | |
| Bigham-Sadegh et al. | Effects of adipose tissue stem cell concurrent with greater omentum on experimental long-bone healing in dog | |
| CN1823087A (zh) | 结合红细胞生成素受体的新肽 | |
| CN1541107A (zh) | 生长因子复合物 | |
| CN1960757A (zh) | 身高增加用组合物 | |
| Pilgrim et al. | A review of fetal bovine serum in the culture of mesenchymal stromal cells and potential alternatives for veterinary medicine | |
| CN1960758A (zh) | 关节炎的治疗剂或预防剂 | |
| CN1592781A (zh) | 脂肪衍生的干细胞和网格体 | |
| CN1307999C (zh) | 混合细胞组合物 | |
| Srouji et al. | Lentiviral-mediated integrin α5 expression in human adult mesenchymal stromal cells promotes bone repair in mouse cranial and long-bone defects | |
| CZ2002341A3 (cs) | Chrupavková membrána a její použití | |
| Knuth et al. | Mesenchymal stem cell-mediated endochondral ossification utilising micropellets and brief chondrogenic priming | |
| Murata et al. | Carrier-dependency of cellular differentiation induced by bone morphogenetic protein in ectopic sites | |
| CN1561235A (zh) | 具有骨诱导和骨传导特性的装置 | |
| CN1599749A (zh) | 促进细胞粘附、生长和分泌的肽 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |