CN116390910A - 药物化合物的晶型 - Google Patents
药物化合物的晶型 Download PDFInfo
- Publication number
- CN116390910A CN116390910A CN202180067242.0A CN202180067242A CN116390910A CN 116390910 A CN116390910 A CN 116390910A CN 202180067242 A CN202180067242 A CN 202180067242A CN 116390910 A CN116390910 A CN 116390910A
- Authority
- CN
- China
- Prior art keywords
- compound
- crystalline form
- disease
- pharmaceutical composition
- ray powder
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 265
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 59
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 45
- 201000010099 disease Diseases 0.000 claims abstract description 44
- 150000002305 glucosylceramides Chemical class 0.000 claims abstract description 37
- 150000002339 glycosphingolipids Chemical class 0.000 claims abstract description 27
- 230000002159 abnormal effect Effects 0.000 claims abstract description 22
- 238000004519 manufacturing process Methods 0.000 claims abstract description 13
- 239000003814 drug Substances 0.000 claims abstract description 9
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical group CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 claims description 96
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 claims description 72
- 238000000634 powder X-ray diffraction Methods 0.000 claims description 52
- 238000000034 method Methods 0.000 claims description 45
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 42
- 239000002904 solvent Substances 0.000 claims description 33
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 claims description 30
- 238000002844 melting Methods 0.000 claims description 28
- 230000008018 melting Effects 0.000 claims description 28
- 239000012458 free base Substances 0.000 claims description 20
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 claims description 18
- 239000000843 powder Substances 0.000 claims description 16
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 claims description 12
- 239000004615 ingredient Substances 0.000 claims description 12
- 208000007930 Type C Niemann-Pick Disease Diseases 0.000 claims description 11
- 239000002775 capsule Substances 0.000 claims description 11
- 238000002360 preparation method Methods 0.000 claims description 11
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 claims description 9
- 208000024891 symptom Diseases 0.000 claims description 9
- 208000010577 Niemann-Pick disease type C Diseases 0.000 claims description 8
- 208000015439 Lysosomal storage disease Diseases 0.000 claims description 7
- 208000021811 Sandhoff disease Diseases 0.000 claims description 7
- 208000001072 type 2 diabetes mellitus Diseases 0.000 claims description 7
- 239000003937 drug carrier Substances 0.000 claims description 6
- 102100022548 Beta-hexosaminidase subunit alpha Human genes 0.000 claims description 5
- 201000008892 GM1 Gangliosidosis Diseases 0.000 claims description 5
- 208000001905 GM2 Gangliosidoses Diseases 0.000 claims description 5
- 201000008905 GM2 gangliosidosis Diseases 0.000 claims description 5
- 101001045440 Homo sapiens Beta-hexosaminidase subunit alpha Proteins 0.000 claims description 5
- DQYBDCGIPTYXML-UHFFFAOYSA-N ethoxyethane;hydrate Chemical compound O.CCOCC DQYBDCGIPTYXML-UHFFFAOYSA-N 0.000 claims description 5
- 230000008569 process Effects 0.000 claims description 5
- 208000015872 Gaucher disease Diseases 0.000 claims description 4
- 238000004587 chromatography analysis Methods 0.000 claims description 4
- 208000015122 neurodegenerative disease Diseases 0.000 claims description 4
- 238000002560 therapeutic procedure Methods 0.000 claims description 4
- 201000001320 Atherosclerosis Diseases 0.000 claims description 3
- 206010067889 Dementia with Lewy bodies Diseases 0.000 claims description 3
- 208000024720 Fabry Disease Diseases 0.000 claims description 3
- 208000035150 Hypercholesterolemia Diseases 0.000 claims description 3
- 208000031226 Hyperlipidaemia Diseases 0.000 claims description 3
- 206010022489 Insulin Resistance Diseases 0.000 claims description 3
- 201000002832 Lewy body dementia Diseases 0.000 claims description 3
- 208000001145 Metabolic Syndrome Diseases 0.000 claims description 3
- 208000008955 Mucolipidoses Diseases 0.000 claims description 3
- 206010072927 Mucolipidosis type I Diseases 0.000 claims description 3
- 208000002033 Myoclonus Diseases 0.000 claims description 3
- 208000008589 Obesity Diseases 0.000 claims description 3
- 208000018737 Parkinson disease Diseases 0.000 claims description 3
- 201000000690 abdominal obesity-metabolic syndrome Diseases 0.000 claims description 3
- 208000037976 chronic inflammation Diseases 0.000 claims description 3
- 230000006020 chronic inflammation Effects 0.000 claims description 3
- 230000001747 exhibiting effect Effects 0.000 claims description 3
- 201000008977 glycoproteinosis Diseases 0.000 claims description 3
- 201000006370 kidney failure Diseases 0.000 claims description 3
- 235000020824 obesity Nutrition 0.000 claims description 3
- 208000030761 polycystic kidney disease Diseases 0.000 claims description 3
- 208000011985 sialidosis Diseases 0.000 claims description 3
- 241000699670 Mus sp. Species 0.000 description 55
- 241001465754 Metazoa Species 0.000 description 47
- 239000000523 sample Substances 0.000 description 37
- 210000004556 brain Anatomy 0.000 description 32
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 30
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 26
- 238000011067 equilibration Methods 0.000 description 25
- 206010044565 Tremor Diseases 0.000 description 24
- 239000003981 vehicle Substances 0.000 description 20
- 239000013078 crystal Substances 0.000 description 18
- 239000000203 mixture Substances 0.000 description 18
- 150000003839 salts Chemical class 0.000 description 17
- 238000002474 experimental method Methods 0.000 description 15
- 239000000243 solution Substances 0.000 description 15
- 210000001519 tissue Anatomy 0.000 description 14
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 13
- 238000000113 differential scanning calorimetry Methods 0.000 description 13
- 235000019253 formic acid Nutrition 0.000 description 13
- 238000005259 measurement Methods 0.000 description 13
- 239000000725 suspension Substances 0.000 description 13
- 230000001225 therapeutic effect Effects 0.000 description 13
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 12
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 12
- 238000012360 testing method Methods 0.000 description 12
- 229910021642 ultra pure water Inorganic materials 0.000 description 12
- 239000012498 ultrapure water Substances 0.000 description 12
- 238000001914 filtration Methods 0.000 description 11
- 210000000449 purkinje cell Anatomy 0.000 description 11
- 102000044956 Ceramide glucosyltransferases Human genes 0.000 description 10
- 201000000788 Niemann-Pick disease type C1 Diseases 0.000 description 10
- 108091000114 ceramide glucosyltransferase Proteins 0.000 description 10
- 230000000694 effects Effects 0.000 description 10
- 239000002953 phosphate buffered saline Substances 0.000 description 10
- 108010028310 Calbindin 1 Proteins 0.000 description 9
- 102000016838 Calbindin 1 Human genes 0.000 description 9
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 9
- 102100033342 Lysosomal acid glucosylceramidase Human genes 0.000 description 9
- 239000000047 product Substances 0.000 description 9
- 108090000623 proteins and genes Proteins 0.000 description 9
- 238000003756 stirring Methods 0.000 description 9
- 101001124388 Homo sapiens NPC intracellular cholesterol transporter 1 Proteins 0.000 description 8
- 241000699666 Mus <mouse, genus> Species 0.000 description 8
- 102100029565 NPC intracellular cholesterol transporter 1 Human genes 0.000 description 8
- 239000006228 supernatant Substances 0.000 description 8
- 108010017544 Glucosylceramidase Proteins 0.000 description 7
- 230000037396 body weight Effects 0.000 description 7
- 230000002490 cerebral effect Effects 0.000 description 7
- 230000002132 lysosomal effect Effects 0.000 description 7
- 238000001179 sorption measurement Methods 0.000 description 7
- 210000004369 blood Anatomy 0.000 description 6
- 239000008280 blood Substances 0.000 description 6
- 230000008859 change Effects 0.000 description 6
- 235000012000 cholesterol Nutrition 0.000 description 6
- -1 compound (I) Chemical class 0.000 description 6
- 238000009472 formulation Methods 0.000 description 6
- 230000036541 health Effects 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- 238000000386 microscopy Methods 0.000 description 6
- WEXRUCMBJFQVBZ-UHFFFAOYSA-N pentobarbital Chemical compound CCCC(C)C1(CC)C(=O)NC(=O)NC1=O WEXRUCMBJFQVBZ-UHFFFAOYSA-N 0.000 description 6
- 230000006920 protein precipitation Effects 0.000 description 6
- 102000004169 proteins and genes Human genes 0.000 description 6
- 238000005070 sampling Methods 0.000 description 6
- 239000003826 tablet Substances 0.000 description 6
- 238000001757 thermogravimetry curve Methods 0.000 description 6
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 5
- 230000015572 biosynthetic process Effects 0.000 description 5
- 210000005013 brain tissue Anatomy 0.000 description 5
- 235000011089 carbon dioxide Nutrition 0.000 description 5
- 210000001638 cerebellum Anatomy 0.000 description 5
- 238000011534 incubation Methods 0.000 description 5
- 239000007924 injection Substances 0.000 description 5
- 238000002347 injection Methods 0.000 description 5
- 230000035772 mutation Effects 0.000 description 5
- 238000001144 powder X-ray diffraction data Methods 0.000 description 5
- 206010003591 Ataxia Diseases 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- 101100282794 Caenorhabditis elegans gba-2 gene Proteins 0.000 description 4
- 241000283074 Equus asinus Species 0.000 description 4
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 4
- 102100027814 Non-lysosomal glucosylceramidase Human genes 0.000 description 4
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 4
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 4
- 238000010521 absorption reaction Methods 0.000 description 4
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 4
- 229910052782 aluminium Inorganic materials 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 4
- 238000012512 characterization method Methods 0.000 description 4
- 210000000172 cytosol Anatomy 0.000 description 4
- 238000010166 immunofluorescence Methods 0.000 description 4
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 4
- 239000000546 pharmaceutical excipient Substances 0.000 description 4
- 238000012216 screening Methods 0.000 description 4
- 238000003860 storage Methods 0.000 description 4
- 108700028369 Alleles Proteins 0.000 description 3
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 3
- 208000024806 Brain atrophy Diseases 0.000 description 3
- IBAQFPQHRJAVAV-ULAWRXDQSA-N Miglitol Chemical compound OCCN1C[C@H](O)[C@@H](O)[C@H](O)[C@H]1CO IBAQFPQHRJAVAV-ULAWRXDQSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 239000003570 air Substances 0.000 description 3
- 150000001298 alcohols Chemical class 0.000 description 3
- 230000009286 beneficial effect Effects 0.000 description 3
- 150000001642 boronic acid derivatives Chemical class 0.000 description 3
- 210000004027 cell Anatomy 0.000 description 3
- 230000006727 cell loss Effects 0.000 description 3
- 230000001413 cellular effect Effects 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 238000002425 crystallisation Methods 0.000 description 3
- 230000008025 crystallization Effects 0.000 description 3
- 238000001938 differential scanning calorimetry curve Methods 0.000 description 3
- 238000009826 distribution Methods 0.000 description 3
- 230000005021 gait Effects 0.000 description 3
- 230000003862 health status Effects 0.000 description 3
- 210000001320 hippocampus Anatomy 0.000 description 3
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 3
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 3
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 3
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 3
- 230000000977 initiatory effect Effects 0.000 description 3
- 150000002500 ions Chemical class 0.000 description 3
- 150000002632 lipids Chemical class 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 239000003550 marker Substances 0.000 description 3
- 229960001110 miglitol Drugs 0.000 description 3
- 238000002156 mixing Methods 0.000 description 3
- 230000007171 neuropathology Effects 0.000 description 3
- 238000003305 oral gavage Methods 0.000 description 3
- 239000002245 particle Substances 0.000 description 3
- 229960001412 pentobarbital Drugs 0.000 description 3
- 230000010412 perfusion Effects 0.000 description 3
- 239000006187 pill Substances 0.000 description 3
- 239000012521 purified sample Substances 0.000 description 3
- 230000005855 radiation Effects 0.000 description 3
- 230000002441 reversible effect Effects 0.000 description 3
- 210000002966 serum Anatomy 0.000 description 3
- 239000000741 silica gel Substances 0.000 description 3
- 229910002027 silica gel Inorganic materials 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 238000000527 sonication Methods 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 230000004580 weight loss Effects 0.000 description 3
- WXTMDXOMEHJXQO-UHFFFAOYSA-N 2,5-dihydroxybenzoic acid Chemical class OC(=O)C1=CC(O)=CC=C1O WXTMDXOMEHJXQO-UHFFFAOYSA-N 0.000 description 2
- 241000700199 Cavia porcellus Species 0.000 description 2
- 229910017488 Cu K Inorganic materials 0.000 description 2
- 229910017541 Cu-K Inorganic materials 0.000 description 2
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- 101150071246 Hexb gene Proteins 0.000 description 2
- 101000997662 Homo sapiens Lysosomal acid glucosylceramidase Proteins 0.000 description 2
- 101000859679 Homo sapiens Non-lysosomal glucosylceramidase Proteins 0.000 description 2
- JVTAAEKCZFNVCJ-REOHCLBHSA-N L-lactic acid Chemical class C[C@H](O)C(O)=O JVTAAEKCZFNVCJ-REOHCLBHSA-N 0.000 description 2
- 101710083785 Non-lysosomal glucosylceramidase Proteins 0.000 description 2
- 229930040373 Paraformaldehyde Natural products 0.000 description 2
- 241000283984 Rodentia Species 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 102000011971 Sphingomyelin Phosphodiesterase Human genes 0.000 description 2
- 108010061312 Sphingomyelin Phosphodiesterase Proteins 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 238000009825 accumulation Methods 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- 239000008186 active pharmaceutical agent Substances 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 2
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 2
- 229940092714 benzenesulfonic acid Drugs 0.000 description 2
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 2
- 230000017531 blood circulation Effects 0.000 description 2
- 238000012754 cardiac puncture Methods 0.000 description 2
- 210000000170 cell membrane Anatomy 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 210000000877 corpus callosum Anatomy 0.000 description 2
- 210000001653 corpus striatum Anatomy 0.000 description 2
- 230000007812 deficiency Effects 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 238000004821 distillation Methods 0.000 description 2
- 230000009977 dual effect Effects 0.000 description 2
- LXBIFEVIBLOUGU-JGWLITMVSA-N duvoglustat Chemical class OC[C@H]1NC[C@H](O)[C@@H](O)[C@@H]1O LXBIFEVIBLOUGU-JGWLITMVSA-N 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 238000000589 high-performance liquid chromatography-mass spectrometry Methods 0.000 description 2
- 238000010191 image analysis Methods 0.000 description 2
- 238000003364 immunohistochemistry Methods 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 238000001802 infusion Methods 0.000 description 2
- 239000003112 inhibitor Substances 0.000 description 2
- 239000007928 intraperitoneal injection Substances 0.000 description 2
- 230000001788 irregular Effects 0.000 description 2
- QWTDNUCVQCZILF-UHFFFAOYSA-N isopentane Chemical compound CCC(C)C QWTDNUCVQCZILF-UHFFFAOYSA-N 0.000 description 2
- 210000004185 liver Anatomy 0.000 description 2
- 210000003712 lysosome Anatomy 0.000 description 2
- 230000001868 lysosomic effect Effects 0.000 description 2
- 238000007726 management method Methods 0.000 description 2
- UQRORFVVSGFNRO-UTINFBMNSA-N miglustat Chemical compound CCCCN1C[C@H](O)[C@@H](O)[C@H](O)[C@H]1CO UQRORFVVSGFNRO-UTINFBMNSA-N 0.000 description 2
- 229960001512 miglustat Drugs 0.000 description 2
- 238000010172 mouse model Methods 0.000 description 2
- 210000002569 neuron Anatomy 0.000 description 2
- 230000016273 neuron death Effects 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 101150049361 npc-1 gene Proteins 0.000 description 2
- 101150107867 npc-2 gene Proteins 0.000 description 2
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 2
- 238000001543 one-way ANOVA Methods 0.000 description 2
- 238000000399 optical microscopy Methods 0.000 description 2
- 229920002866 paraformaldehyde Polymers 0.000 description 2
- 230000035515 penetration Effects 0.000 description 2
- 239000002504 physiological saline solution Substances 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 238000013105 post hoc analysis Methods 0.000 description 2
- 230000003389 potentiating effect Effects 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 238000011002 quantification Methods 0.000 description 2
- 210000005241 right ventricle Anatomy 0.000 description 2
- 238000010898 silica gel chromatography Methods 0.000 description 2
- 210000003625 skull Anatomy 0.000 description 2
- 239000011343 solid material Substances 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 238000001228 spectrum Methods 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 238000007619 statistical method Methods 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 238000005979 thermal decomposition reaction Methods 0.000 description 2
- 238000002411 thermogravimetry Methods 0.000 description 2
- 230000009261 transgenic effect Effects 0.000 description 2
- 230000003442 weekly effect Effects 0.000 description 2
- 230000004584 weight gain Effects 0.000 description 2
- 235000019786 weight gain Nutrition 0.000 description 2
- IWYDHOAUDWTVEP-SSDOTTSWSA-N (R)-mandelic acid Chemical class OC(=O)[C@H](O)C1=CC=CC=C1 IWYDHOAUDWTVEP-SSDOTTSWSA-N 0.000 description 1
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 1
- LBLYYCQCTBFVLH-UHFFFAOYSA-N 2-Methylbenzenesulfonic acid Chemical class CC1=CC=CC=C1S(O)(=O)=O LBLYYCQCTBFVLH-UHFFFAOYSA-N 0.000 description 1
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 1
- 239000005695 Ammonium acetate Substances 0.000 description 1
- 102100026189 Beta-galactosidase Human genes 0.000 description 1
- 101150061009 C1 gene Proteins 0.000 description 1
- GAWIXWVDTYZWAW-UHFFFAOYSA-N C[CH]O Chemical group C[CH]O GAWIXWVDTYZWAW-UHFFFAOYSA-N 0.000 description 1
- 101100289995 Caenorhabditis elegans mac-1 gene Proteins 0.000 description 1
- 101100080277 Caenorhabditis elegans ncr-1 gene Proteins 0.000 description 1
- 102100021851 Calbindin Human genes 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 206010053567 Coagulopathies Diseases 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 239000012591 Dulbecco’s Phosphate Buffered Saline Substances 0.000 description 1
- 238000011199 Dunnett post hoc test Methods 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 239000001856 Ethyl cellulose Substances 0.000 description 1
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 1
- 238000005033 Fourier transform infrared spectroscopy Methods 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 102100039289 Glial fibrillary acidic protein Human genes 0.000 description 1
- 101710193519 Glial fibrillary acidic protein Proteins 0.000 description 1
- 108010031186 Glycoside Hydrolases Proteins 0.000 description 1
- 102000005744 Glycoside Hydrolases Human genes 0.000 description 1
- 101001109579 Homo sapiens NPC intracellular cholesterol transporter 2 Proteins 0.000 description 1
- 238000004566 IR spectroscopy Methods 0.000 description 1
- 108010059881 Lactase Proteins 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 240000007472 Leucaena leucocephala Species 0.000 description 1
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- 101100459404 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) npc-1 gene Proteins 0.000 description 1
- 108700018419 Niemann-Pick C1 Proteins 0.000 description 1
- 240000007594 Oryza sativa Species 0.000 description 1
- 235000007164 Oryza sativa Nutrition 0.000 description 1
- 239000005662 Paraffin oil Substances 0.000 description 1
- 241000139306 Platt Species 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 238000001069 Raman spectroscopy Methods 0.000 description 1
- 208000035977 Rare disease Diseases 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 241000209140 Triticum Species 0.000 description 1
- 235000021307 Triticum Nutrition 0.000 description 1
- 229920004890 Triton X-100 Polymers 0.000 description 1
- 239000013504 Triton X-100 Substances 0.000 description 1
- 238000002441 X-ray diffraction Methods 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 1
- 210000001015 abdomen Anatomy 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000006978 adaptation Effects 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 102000016679 alpha-Glucosidases Human genes 0.000 description 1
- 108010028144 alpha-Glucosidases Proteins 0.000 description 1
- VREFGVBLTWBCJP-UHFFFAOYSA-N alprazolam Chemical compound C12=CC(Cl)=CC=C2N2C(C)=NN=C2CN=C1C1=CC=CC=C1 VREFGVBLTWBCJP-UHFFFAOYSA-N 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 239000012080 ambient air Substances 0.000 description 1
- 229940043376 ammonium acetate Drugs 0.000 description 1
- 235000019257 ammonium acetate Nutrition 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 239000003472 antidiabetic agent Substances 0.000 description 1
- 229940125708 antidiabetic agent Drugs 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 210000002376 aorta thoracic Anatomy 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- 210000001130 astrocyte Anatomy 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 230000003376 axonal effect Effects 0.000 description 1
- 238000003705 background correction Methods 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 235000019445 benzyl alcohol Nutrition 0.000 description 1
- 108010005774 beta-Galactosidase Proteins 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 238000001574 biopsy Methods 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- 108060001061 calbindin Proteins 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 238000001460 carbon-13 nuclear magnetic resonance spectrum Methods 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 210000005056 cell body Anatomy 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 230000031154 cholesterol homeostasis Effects 0.000 description 1
- 230000035602 clotting Effects 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 238000010668 complexation reaction Methods 0.000 description 1
- 230000021615 conjugation Effects 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 239000002178 crystalline material Substances 0.000 description 1
- 230000001186 cumulative effect Effects 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 238000007416 differential thermogravimetric analysis Methods 0.000 description 1
- AFABGHUZZDYHJO-UHFFFAOYSA-N dimethyl butane Natural products CCCC(C)C AFABGHUZZDYHJO-UHFFFAOYSA-N 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 238000007876 drug discovery Methods 0.000 description 1
- 229940125436 dual inhibitor Drugs 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 210000001163 endosome Anatomy 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 229940088598 enzyme Drugs 0.000 description 1
- 229920001249 ethyl cellulose Polymers 0.000 description 1
- 235000019325 ethyl cellulose Nutrition 0.000 description 1
- 230000005496 eutectics Effects 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 239000003885 eye ointment Substances 0.000 description 1
- 239000003925 fat Substances 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000005429 filling process Methods 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 230000008014 freezing Effects 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 125000002210 galactosylceramide group Chemical class 0.000 description 1
- 150000002270 gangliosides Chemical class 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 239000003349 gelling agent Substances 0.000 description 1
- 229960005219 gentisic acid Drugs 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 210000005046 glial fibrillary acidic protein Anatomy 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 230000005484 gravity Effects 0.000 description 1
- 230000002440 hepatic effect Effects 0.000 description 1
- 230000000971 hippocampal effect Effects 0.000 description 1
- 238000010562 histological examination Methods 0.000 description 1
- 230000036571 hydration Effects 0.000 description 1
- 238000006703 hydration reaction Methods 0.000 description 1
- 229960000443 hydrochloric acid Drugs 0.000 description 1
- 238000002013 hydrophilic interaction chromatography Methods 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 238000003125 immunofluorescent labeling Methods 0.000 description 1
- 238000002991 immunohistochemical analysis Methods 0.000 description 1
- 230000002055 immunohistochemical effect Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 239000003978 infusion fluid Substances 0.000 description 1
- 238000013383 initial experiment Methods 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 229940116108 lactase Drugs 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 210000005240 left ventricle Anatomy 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- IWYDHOAUDWTVEP-UHFFFAOYSA-N mandelic acid Chemical compound OC(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-N 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 230000006724 microglial activation Effects 0.000 description 1
- 230000002025 microglial effect Effects 0.000 description 1
- 230000000877 morphologic effect Effects 0.000 description 1
- 238000002552 multiple reaction monitoring Methods 0.000 description 1
- GOQYKNQRPGWPLP-UHFFFAOYSA-N n-heptadecyl alcohol Natural products CCCCCCCCCCCCCCCCCO GOQYKNQRPGWPLP-UHFFFAOYSA-N 0.000 description 1
- 230000001537 neural effect Effects 0.000 description 1
- 210000002241 neurite Anatomy 0.000 description 1
- 230000002981 neuropathic effect Effects 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 230000009871 nonspecific binding Effects 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 239000002997 ophthalmic solution Substances 0.000 description 1
- 230000003204 osmotic effect Effects 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- 239000012466 permeate Substances 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 238000001907 polarising light microscopy Methods 0.000 description 1
- 229920001515 polyalkylene glycol Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- XTUSEBKMEQERQV-UHFFFAOYSA-N propan-2-ol;hydrate Chemical compound O.CC(C)O XTUSEBKMEQERQV-UHFFFAOYSA-N 0.000 description 1
- 210000002637 putamen Anatomy 0.000 description 1
- 238000004445 quantitative analysis Methods 0.000 description 1
- 238000013139 quantization Methods 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 235000009566 rice Nutrition 0.000 description 1
- 238000013341 scale-up Methods 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 238000002791 soaking Methods 0.000 description 1
- 239000007909 solid dosage form Substances 0.000 description 1
- 238000007614 solvation Methods 0.000 description 1
- 238000002336 sorption--desorption measurement Methods 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 238000004611 spectroscopical analysis Methods 0.000 description 1
- 210000000952 spleen Anatomy 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 239000011550 stock solution Substances 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 229920001059 synthetic polymer Polymers 0.000 description 1
- 230000009897 systematic effect Effects 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 238000004885 tandem mass spectrometry Methods 0.000 description 1
- 239000008399 tap water Substances 0.000 description 1
- 235000020679 tap water Nutrition 0.000 description 1
- JZBRFIUYUGTUGG-UHFFFAOYSA-J tetrapotassium;2-[2-[bis(carboxylatomethyl)amino]ethyl-(carboxylatomethyl)amino]acetate Chemical compound [K+].[K+].[K+].[K+].[O-]C(=O)CN(CC([O-])=O)CCN(CC([O-])=O)CC([O-])=O JZBRFIUYUGTUGG-UHFFFAOYSA-J 0.000 description 1
- 238000002076 thermal analysis method Methods 0.000 description 1
- 210000000115 thoracic cavity Anatomy 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 238000007492 two-way ANOVA Methods 0.000 description 1
- 238000010200 validation analysis Methods 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000003643 water by type Substances 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 239000012224 working solution Substances 0.000 description 1
- 230000037303 wrinkles Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D211/00—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings
- C07D211/04—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D211/06—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D211/36—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D211/40—Oxygen atoms
- C07D211/44—Oxygen atoms attached in position 4
- C07D211/46—Oxygen atoms attached in position 4 having a hydrogen atom as the second substituent in position 4
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/13—Crystalline forms, e.g. polymorphs
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Heart & Thoracic Surgery (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Urology & Nephrology (AREA)
- Vascular Medicine (AREA)
- Cardiology (AREA)
- Psychology (AREA)
- Epidemiology (AREA)
- Psychiatry (AREA)
- Hospice & Palliative Care (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Medicinal Preparation (AREA)
- Saccharide Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
本发明涉及化合物(I)的晶型和制备化合物(I)的晶型的方法。本发明还提供了包含化合物(I)的晶型的药物组合物。此外,本发明涉及将化合物(I)的该晶型用作药物以及用于治疗涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病的方法。
Description
技术领域
本发明涉及化合物(I)的晶型,
本发明还涉及制备化合物(I)的晶型的方法以及包含化合物(I)的晶型的药物组合物。此外,本发明涉及将化合物(I)的该晶型用作药物以及用于治疗涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病的方法。
背景技术
当将化合物用于药物用途时,该化合物的晶体状态可能很重要。这是因为化合物的晶体状态的形态学、颗粒尺寸、多晶型、溶剂化或水合可能影响药剂的过滤、流动、压片、溶解和生物利用度。
脱氧野尻霉素衍生物是药物化学和药物发现中的重要的一类分子。N-(羟乙基)-脱氧野尻霉素作为用于2型糖尿病的抗糖尿病剂以米格列醇销售。米格列醇还充当多种肠糖苷酶(麦芽糖酶、蔗糖和乳糖酶)的广谱抑制剂(Hillebrand等,Diabetes,1986,第35卷,A93-A93)(Scott和Spencer,Drugs,2000,第59卷,521-549)。
N-丁基-脱氧野尻霉素(miglustat,)被开发为葡糖神经酰胺合酶(也称为神经酰胺葡糖基转移酶,EC 2.4.1.80,UniProt代码:Q16739)的抑制剂,并且在临床上用于治疗患有溶酶体贮积症、戈谢病(Platt等,J.Biol.Chem.,1994,第269卷,8362-8365)(Cox等,Lancet,2000,第355卷,1481-1485)和尼曼-皮克C型病(Pineda等Orphanet J.RareDis.,2018,第13卷,140)的患者。
WO2015/147639A1描述了脱氧野尻霉素的新衍生物,包括化合物(I),
其在治疗与异常水平的细胞溶质或溶酶体葡糖神经酰胺和/或较高水平的鞘糖脂相关的疾病方面是有效的。化合物(I)是葡糖神经酰胺合酶和非溶酶体葡糖神经酰胺酶(non-lysosomal glucosylcerebrosidase,GBA2,UniProt代码:Q9HCG7)的有效双重抑制剂。
可用于治疗异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的治疗性化合物通常以片剂形式施用。当制备用于以这样的片剂使用的药物组合物和制剂时,非常期望具有具备低水平吸湿性和/或低水平潮解性的治疗性化合物的晶型,从而允许化合物被压制成期望的形状或尺寸。
此外,治疗性化合物的相对高的熔点(通常大于约80℃)有利于抗分解,从而促进治疗性化合物的储存并延长保质期,这对于任何药剂都是期望的。
在考虑药剂的处理、制造和储存时,治疗性化合物不吸湿或基本上不吸湿也是特别有益的。如果药剂示出吸湿特性,则可能出现许多问题,例如:
·难以通过粉碎将材料减小成小颗粒或粉末;
·不需要的水分阻碍适当的反应并形成不需要的最终产品,这导致品质最低且保质期缩短;
·制造期间产生软的片剂,或者水分渗入到包装内;
·粉末粘附至传送带,这可能影响灌装过程。
因此,期望具有不吸湿或基本上不吸湿的治疗性化合物的晶型。
先前未报道过化合物(I)的晶型。因此,存在对稳定和/或不潮解的化合物(I)的晶型的需要,其优选基本上不吸湿和/或具有相对高的熔点。
发明内容
在第一方面中,本发明提供了化合物(I)的晶型,
除非有明确的相反指示,否则如本文中限定的每个方面或实施方案都可以与任何其他方面或实施方案组合。特别地,被指示为优选或有利的任何特征可以与被指示为优选或有利的任何其他一个或更多个特征组合。
在另一个方面中,本发明提供了包含如本文所述的化合物(I)的晶型的药物组合物。
在另一个方面中,本发明提供了如本文所述的化合物(I)的晶型或如本文所述的药物组合物,用于在治疗中的用途。
在另一个方面中,本发明提供了如本文所述的化合物(I)的晶型或如本文所述的药物组合物,用于作为药物的用途。
本发明的另一个方面涉及如本文所述的化合物(I)的晶型或如本文所述的药物组合物,用于在治疗涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病中的用途。
在另一个方面中,本发明提供了如本文所述的化合物(I)的晶型或如本文所述的药物组合物,用于在治疗尼曼-皮克C型病中的用途。
在另一个方面中,本发明提供了治疗人或动物患者涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病的方法,包括向有此需要的患者施用治疗有效量的如本文所述的化合物(I)的晶型或如本文所述的药物组合物。
在另一个方面中,本发明提供了治疗人或动物患者的尼曼-皮克C型病的方法,包括向有此需要的患者施用治疗有效量的如本文所述的化合物(I)的晶型或如本文所述的药物组合物。
在另一个方面中,本发明提供了制备如本文所述的化合物(I)的晶型的方法,包括使化合物(I)的样品与溶剂接触。
在另一个方面中,本发明提供了通过进行如本文所述的方法获得的化合物(I)的晶型。
在另一个方面中,本发明提供了化合物(I)的游离碱制备化合物(I)的晶型的用途。
在另一个方面中,本发明提供了制备化合物(I)的晶型的方法,包括使化合物(I)的游离碱结晶。
在另一个方面中,本发明提供了通过包括使化合物(I)的游离碱结晶的制备化合物(I)的晶型的方法获得的化合物(I)的晶型。
根据本发明的化合物的其他优选实施方案出现在整个说明书中并且特别是实施例中。
本发明人出乎意料地发现了稳定且不潮解的化合物(I)的晶型。本发明具有另外的有利特性,例如相对高的熔点和基本上没有吸湿性。
出乎预料地,本发明人另外发现了在水中示出良好的溶解性的化合物(I)的晶型。这些特性使得本发明的晶型特别适用于在药物组合物中使用。
治疗性化合物的结晶通常涉及使用不同的盐。通常,盐容易进行结晶,并且所得物质促进治疗性化合物的后续结晶。出于该原因,使用盐通常是用于使治疗性化合物结晶的优选方法。因此,出乎意料的是,本发明人发现了化合物(I)的结晶游离碱形式。
由于任何治疗性化合物的结晶游离碱形式不需要存在抗衡离子,因此游离碱晶型粉末中治疗化合物的浓度通常高于相应的盐形式,这是非常有益的,因为其降低了制造治疗性化合物的成本。
不希望受理论的束缚,认为本发明的晶型由于其晶体结构而倾向于示出以上讨论的有利效果。
附图说明
现在将参照附图描述本发明的这些和其他方面,其中:
图1示出了通过用乙腈平衡获得的化合物(I)的晶型(称为2型)的使用偏光显微镜检查获得的示例性图像;左边:以干粉形式,右边:分散在石蜡油中。
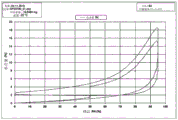
图2示出了通过用乙腈平衡获得的2型的X射线粉末衍射图。
图3A示出了通过用乙腈平衡获得的2型的TG-FTIR热谱图。
图3B示出了通过用乙腈平衡获得的2型的差示扫描量热法(DSC)热谱图。
图4A示出了通过用乙腈平衡获得的2型的动态蒸汽吸附(dynamic vapoursorption,DVS)等温线:水含量(红色曲线)和相对湿度(蓝色曲线)作为时间的函数的变化。
图4B示出了通过用乙腈平衡获得的2型的DVS等温线:水含量作为相对湿度的函数的变化。
图5示出了通过分别用乙腈、苯甲醚或乙酸乙酯平衡获得的化合物(I)的晶型(称为3型)的使用偏光显微镜检查获得的示例性图像。
图6A示出了通过用乙腈平衡获得的3型的X射线粉末衍射图。
图6B示出了通过分别用TBME、水、异丙醇、乙酸乙酯、乙腈或苯甲醚平衡获得的3型的X射线粉末衍射图的叠加。
图7示出了通过用乙腈平衡获得的化合物(I)的两种晶型的X射线粉末衍射图的叠加:
1)3型(实施例3),和
2)2型(实施例2)。
图8A示出了通过用乙酸乙酯平衡获得的3型的TG-FTIR热谱图。
图8B示出了通过用异丙醇平衡获得的3型的TG-FTIR热谱图。
图8C示出了通过用乙酸乙酯平衡获得的3型的DSC热谱图。
图9A示出了通过用乙酸乙酯平衡获得的3型的DVS等温线:水含量(红色曲线)和相对湿度(蓝色曲线)作为时间的函数的变化。
图9B示出了通过用乙酸乙酯平衡获得的3型的DVS等温线:水含量作为相对湿度的函数的变化。
图10示出了按照基于示出立体定位坐标的Paxinos&Franklin“The Mouse BrainAtlas,第2版”的切片方案获得的近似中矢状层面。
图11示出了在出生后(PND)第11天至第9周之间小鼠体量的百分比变化。
图12示出了自PND 11至PND 70在重复经口施用后的葡糖神经酰胺C16:0和C18:0水平。
图13示出了NPC(-/-)载剂和AZ-3102处理的小鼠自PND 56至PND 70的临床体征评分。
图14示出了NPC(-/-)载剂和AZ-3102处理的小鼠自PND 56至PND 70的震颤评分。
图15示出了目的区域(ROI)的限定。图像示出了小脑、海马结构、胼胝体和纹状体(尾状壳核)的ROI轮廓。
图16示出了脑免疫组织化学:NCP(-/-)和NPC(+/-)载剂处理的小鼠与NPC(+/+,野生型小鼠)和NPC(-/-)处理的小鼠相比的钙结合蛋白-D28k标记。
图17总结了化合物(I)的晶型(AZ-3102)的作用方式。
具体实施方式
除非本文另有定义,否则与本发明结合使用的科学和技术术语应当具有本领域普通技术人员通常理解的含义。术语的含义和范围应是明确的,然而,在有任何潜在歧义的情况下,本文提供的定义优先于任何词典或外在定义。
应理解,单数介词例如一个/一种通常为了方便而使用,然而,除非另有明确说明或根据上下文另有说明,否则单数的所有实例均旨在涵盖复数。术语“包含”、“包括”和“具有”旨在是包括性的,并且意指除了所列出的要素之外还可以存在另外的要素。此外,应理解,本公开内容中提及的所有参考文献(包括期刊文章、书、专利、技术文献等)均出于所有目的并通过引用整体并入本文。
如本文中所使用的用于数值数据的术语“约”是指在基础参数的10%内(即,加或减10%)的值,并且在一系列值的开始处使用术语“约”修饰每个值(即,“约1、2和3”是指约1、约2和约3)。例如,“约85℃”的温度可以包括75℃至95℃的温度。
本领域中的术语“熔点”。如本文中所使用的术语“相对高的熔点”旨在涵盖足够稳定而被配制为药物组合物的晶型。优选地,术语“相对高的熔点”描述大于约65℃的熔点。还更优选地熔点大于约80℃。
如本文中所使用的术语“组合物”旨在涵盖以指定量包含指定成分的产品,以及由指定量的指定成分的组合直接或间接产生的任何产品。与药物组合物相关的这样的术语旨在涵盖包含化合物(I)的晶型和任选地构成载体的另外成分的产品,以及由任何两种或更多种成分的组合、络合或聚集直接或间接产生的任何产品,或者由一种或更多种成分的解离直接或间接产生的任何产品,或者由一种或更多种成分的其他类型的反应或相互作用直接或间接产生的任何产品。因此,本发明的药物组合物涵盖包含本发明的晶型和任选地可药用载体的任何组合物。就“可药用”而言,其意指载体、稀释剂或赋形剂必须与制剂的其他成分相容并且对其接受者无害。
术语“治疗有效量”意指晶型或药物组合物的在施用于患者以治疗疾病时足以实现对疾病的这样的治疗的量。“治疗有效量”将根据疾病及其严重程度以及待治疗的患者的年龄和体重而变化。术语“患者”(或“对象”)包括但不限于动物,例如哺乳动物。优选地,患者为人。
本发明提供了化合物(I)的晶型,
化合物(I)的晶型可以处于任何晶体状态。化合物(I)的晶型可以为结晶盐或结晶游离碱(非离子形式)。优选地,化合物(I)的晶型为结晶游离碱。此外,化合物(I)可以形成共晶。
如果化合物(I)的晶型为结晶盐,则以上化合物(I)的分子结构包含质子化的氮原子。
本发明不限于化合物(I)的单一晶型。固体物质可以以多于一种晶型存在。这些可选的晶型被称为多晶型物。每种多晶型物在晶格中具有不同的分子取向和/或构象。由于晶体结构的不同,每种晶体状态或“多晶型物”都表现出独特的一组物理化学特性。
多晶型形式可以具有不同的机械特性,例如流动性和压缩性,这影响化合物的技术特性。化合物的稳定性和储存持续时间也可以取决于多晶型物。
多晶型物可以以不同的方式彼此区分。多晶型物清楚地表现出光谱特性,并且它们可以使用例如红外光谱、拉曼光谱和13C-NMR谱来确定。鉴于每种晶型以不同的方式折射X射线的事实,X射线粉末衍射(X-ray powder diffraction,XPD)也可以用于表征多晶型物。此外,诸如差示扫描量热法(DSC)和热重分析(TTA)的热方法可以提供关于特定多晶型物的独特信息。
正如粉末X射线衍射领域中公知的,粉末X射线衍射谱的相对峰高可以用于描述不同的晶型。因此,在“3型”方面中,本发明提供了在X射线粉末衍射图中显示以2θ值表示的在17.8±0.2°处的反射的化合物(I)的晶型,其中在17.8±0.2°处的反射为X射线粉末衍射图中的四个最强反射之一。优选地,在17.8±0.2°处的反射为X射线粉末衍射图中的三个最强反射之一,或者其中在17.8±0.2°处的反射为X射线粉末衍射图中的两个最强反射之一。更优选地,在17.8±0.2°处的反射为X射线粉末衍射图中的最强反射。还更优选地,在“3型”方面中,化合物(I)的晶型在X射线粉末衍射图中显示以2θ值表示的在17.8±0.1°处的反射,其中在17.8±0.1°处的反射为X射线粉末衍射图中的四个最强反射之一。优选地,在17.8±0.1°处的反射为X射线粉末衍射图中的三个最强反射之一,或者其中在17.8±0.1°处的反射为X射线粉末衍射图中的两个最强反射之一。更优选地,在17.8±0.1°处的反射为X射线粉末衍射图中的最强反射。
术语“最强反射”描述X射线粉末衍射图的最高峰。粉末X射线衍射图的峰高基于X射线强度(以计数或计数/秒为单位)确定。因此,最强反射是在X射线粉末衍射图中示出最高X射线强度的反射。例如,图6A中示出的X射线衍射图的最强反射是以2θ值表示的在17.8±0.2°处的反射。
除非明确相反的说明,否则所有X射线粉末衍射图是在约25℃下使用铜K-α辐射确定。
优选地,在“3型”方面中,化合物(I)的晶型在X射线粉末衍射图中还显示以2θ值表示的在4.1±0.2°、8.3±0.2°、12.4±0.2°、13.6±0.2°、14.5±0.2°、14.9±0.2°、15.2±0.2°、17.2±0.2°、19.3±0.2°、21.2±0.2°、22.4±0.2°、22.9±0.2°和23.3±0.2°中的一者或更多者处的一个或更多个反射。还更优选地,在“3型”方面中,化合物(I)的晶型在X射线粉末衍射图中还显示以2θ值表示的在4.1±0.1°、8.3±0.1°、12.4±0.1°、13.6±0.1°、14.5±0.1°、14.9±0.1°、15.2±0.1°、17.2±0.1°、19.3±0.1°、21.2±0.1°、22.4±0.1°、22.9±0.1°和23.3±0.1°中的一者或更多者处的一个或更多个反射。
粉末X射线衍射谱的峰的位置对实验细节相对不敏感。因此,本发明的结晶化合物可以通过具有某些峰位置的粉末X射线衍射图来表征。因此,在“3型”方面中,化合物(I)的晶型优选通过在X射线粉末衍射图中以2θ值表示的在17.2±0.2°、17.8±0.2°、21.2±0.2°和22.4±0.2°处的反射来表征。更优选地,在“3型”方面中,化合物(I)的晶型通过在X射线粉末衍射图中以2θ值表示的在4.1±0.2°、8.3±0.2°、12.4±0.2°、13.6±0.2°、14.5±0.2°、14.9±0.1°、15.2±0.2°、17.2±0.2°、17.8±0.2°、19.3±0.2°、21.2±0.2°、22.4±0.2°、22.9±0.2°和23.3±0.2°处的反射来表征。还更优选地,在“3型”方面中,化合物(I)的晶型通过在X射线粉末衍射图中以2θ值表示的在17.2±0.1°、17.8±0.1°、21.2±0.1°和22.4±0.1°处的反射来表征。最优选地,在“3型”方面中,化合物(I)的晶型通过在X射线粉末衍射图中以2θ值表示的在4.1±0.1°、8.3±0.1°、12.4±0.1°、13.6±0.1°、14.5±0.1°、14.9±0.1°、15.2±0.1°、17.2±0.1°、17.8±0.1°、19.3±0.1°、21.2±0.1°、22.4±0.1°、22.9±0.1°和23.3±0.1°处的反射来表征。
化合物的晶型可以通过差示扫描量热法(DSC)热谱图来表征。因此,在“3型”方面中,化合物(I)的晶型优选通过如图8C中看到的示出在约87℃下开始吸热热流和/或约92.4℃的熔点的DSC热谱图来表征。因此,优选地,在“3型”方面中,化合物(I)的晶型具有通过DSC确定的89℃至96℃的熔点。优选地,在“3型”方面中,晶型具有通过DSC确定的90℃至95℃的熔点。还更优选地,在“3型”方面中,化合物(I)的晶型具有通过DSC确定的91℃至94℃的熔点。最优选地,在“3型”方面中,化合物(I)的晶型具有通过DSC确定的92℃至93℃的熔点。
化合物的晶型可以通过其吸湿性来表征。产品的吸湿性表示在特定温度下其水含量作为相对湿度的函数的增加或减少。由于相对湿度的变化,基本上不吸湿的产品在其水含量方面不表现出变化或仅表现出轻微变化。在强吸湿性产品中,水含量可能变化较大。因此,优选地,化合物(I)的晶型基本上不吸湿。
化合物的晶型可以通过其热重迹线表征。因此,优选地,化合物(I)的晶型可以通过其热重迹线来表征。在一个实施方案中,化合物(I)的结晶通过图8A或图8B中描绘的热重迹线来表征。
化合物的晶型也可以通过其动态蒸汽吸附(DVS)曲线来表征。因此,化合物(I)的晶型可以优选通过如图9A和9B中看到的其DVS曲线来表征。优选地,化合物(I)的晶型具有可逆的吸附/解吸曲线。优选地,DVS曲线示出晶型的基本上不吸湿的性质。
基本上不吸湿的物质示出在约25℃的温度下测量的在约95%的相对湿度下小于约2%的吸水率。优选地,在约25℃的温度测量的在约95%的相对湿度下,吸水率小于约1%。吸水率的值通过测量测试晶型在约95%的相对湿度和约25℃的温度下相对于初始质量的质量增加来获得。
因此,化合物(I)的晶型优选在约95%的相对湿度、约25℃的温度下吸收0%至2%的水。还更优选地,化合物(I)的晶型在约95%的相对湿度、约25℃的温度下吸收0%至1.5%的水。最优选地,化合物(I)的晶型在约95%的相对湿度、约25℃的温度下吸收0%至1%的水。
另外地,本发明的晶型优选是稳定的。例如,在约25℃下在乙酸乙酯中延长培养(1周)产生良好品质的化合物(I)的晶型,如图5所示。
在“2型”方面中,本发明提供了化合物(I)的另外晶型,该晶型(2型)在X射线粉末衍射图中显示以2θ值表示的在16.9±0.2°处的反射,其中在16.9±0.2°处的反射为X射线粉末衍射图中的四个最强反射之一。优选地,在16.9±0.2°处的反射为X射线粉末衍射图中的三个最强反射之一,或者其中在16.9±0.2°处的反射为X射线粉末衍射图中的两个最强反射之一。更优选地,在16.9±0.2°处的反射为X射线粉末衍射图中的最强反射。还更优选地,在“2型”方面中,晶型在X射线粉末衍射图中显示以2θ值表示的在16.9±0.1°处的反射,其中在16.9±0.1°处的反射为X射线粉末衍射图中的四个最强反射之一。优选地,在16.9±0.1°处的反射为X射线粉末衍射图中的三个最强反射之一,或者其中在16.9±0.1°处的反射为X射线粉末衍射图中的两个最强反射之一。更优选地,在16.9±0.1°处的反射为X射线粉末衍射图中的最强反射。
优选地,在“2型”方面中,化合物(I)的晶型在X射线粉末衍射图中显示以2θ值表示的在15.2±0.2°、16.1±0.2°、16.5±0.2°、18.9±0.2°、23.1±0.2°、25.5±0.2°、27.7±0.2°和28.5±0.2°中的一者或更多者处的一个或更多个反射。还更优选地,在“2型”方面中,化合物(I)的晶型显示以2θ值表示的在15.2±0.1°、16.1±0.1°、16.5±0.1°、18.9±0.1°、23.1±0.1°、25.5±0.1°、27.7±0.1°和28.5±0.1°中的一者或更多者处的一个或更多个反射。
在“2型”方面中,化合物(I)的该晶型也可以通过在X射线粉末衍射图中以2θ值表示的在16.1±0.2°、16.5±0.2°、16.9±0.2°、18.9±0.2°和23.1±0.2°处的反射来表征。优选地,在“2型”方面中,化合物(I)的晶型也可以通过在X射线粉末衍射图中以20值表示的在16.1±0.1°、16.5±0.1°、16.9±0.1°、18.9±0.1°和23.1±0.1°处的反射来表征。
在“2型”方面中,化合物(I)的晶型可以通过如图3B中看到的示出在约58℃下开始吸热热流和约70℃的熔点的DSC热谱图来表征。因此,在“2型”方面中,化合物(I)的晶型具有67℃至74℃的熔点。优选地,在“2型”方面中,化合物(I)的晶型具有68℃至73℃的熔点。还更优选地,在“2型”方面中,化合物(I)的晶型具有69℃至72℃的熔点。最优选地,在“2型”方面中,化合物(I)的晶型具有69℃至71℃的熔点。
本申请的发明人出乎意料地发现:在“2型”方面中,化合物(I)的晶型特别易溶于水。因此,优选地,在“2型”方面中,化合物(I)的晶型的在约25℃下测量的水溶性为约75mg/mL至约85mg/mL。更优选地,在“2型”方面中,晶型的在约25℃下测量的的水溶性为约78mg/mL至约82mg/mL。最优选地,在“2型”方面中,化合物(I)的晶型的在约25℃下测量的水溶性为约80mg/mL。
用于测量溶解度的方法在本领域是已知的;例如,烧瓶振荡法、声处理、柱洗脱法以及紫外或可见光谱法。除非相反地明确说明,否则水溶性使用烧瓶振荡法和/或声处理来确定。
本发明还提供了包含如本文所述的化合物(I)的晶型的药物组合物。
通常,化合物(I)的晶型以药物组合物或制剂的形式施用于患者。这样的药物组合物可以通过任何可接受的施用途径施用于患者,包括但不限于经口、局部(包括经皮)和肠胃外施用方式。
本发明的药物组合物通常由可药用载体和一种或更多种任选的成分来制备。如果需要或期望,然后可以使用常规程序和设备将所得均匀共混的混合物成型或装入片剂、胶囊、丸剂、罐、药筒、分配器等中。
当打算以固体剂型(即,以胶囊剂、片剂、丸剂等)经口施用时,本发明的药物组合物将通常包含化合物(I)的晶型作为活性成分。优选地,本发明的药物组合物包含化合物(I)的晶型且不含其他成分。优选地,本发明的药物组合物包含在胶囊中。优选地,本发明的药物组合物包含在没有任何其他成分的胶囊中。胶囊可以为明胶胶囊或羟丙基甲基纤维素(HPMC)胶囊。或者,本发明的药物组合物可以包含化合物(I)的晶型作为活性成分和一种或更多种可药用载体。本领域技术人员将知晓合适的可药用载体,例如,脂肪、水、生理盐水、醇(例如,乙醇)、甘油、多元醇、葡萄糖水溶液、填充剂、崩解剂、结合剂、润滑剂、润湿剂、稳定剂、乳化剂、分散剂、防腐剂、甜味剂、着色剂、调味剂或芳香剂、浓缩剂、稀释剂、缓冲物质、溶剂或增溶剂、用于实现储存效果的化学品、用于改变渗透压的盐、包衣剂或抗氧化剂;糖类,例如乳糖或葡萄糖;玉米、小麦或稻的淀粉;脂肪酸,例如硬脂酸;无机盐,例如偏硅酸铝酸镁或无水磷酸钙;合成聚合物,例如聚乙烯吡咯烷酮或聚亚烷基二醇;醇,例如硬脂醇或苄醇;合成纤维素衍生物,例如甲基纤维素、羧甲基纤维素、乙基纤维素或羟丙基甲基纤维素;以及其他常规使用的添加剂,例如明胶、滑石、植物油和阿拉伯胶。
包含化合物(I)的晶型的药物组合物也可以使用已知的递送系统和赋形剂经皮或经黏膜施用。例如,药物组合物可以与渗透增强剂例如丙二醇、聚乙二醇单月桂酸酯、氮杂环烷-2-酮(azacycloalkan-2-ones)等混合,并且并入到贴剂或类似的递送系统中。还可以使用另外的赋形剂,包括胶凝剂、乳化剂和缓冲剂。
用于肠胃外施用的注射剂包括无菌水性或非水性溶液、混悬剂和乳剂。水性溶剂包括例如注射用蒸馏水和/或生理盐水。非水性溶剂的实例包括醇例如乙醇。
优选地,药物组合物包含一种或更多种另外的药物活性剂。该组合疗法涉及使用与一种或更多种另外的药物活性剂组合的化合物(I)的晶型,要么一起配制(例如,一起包装在单一制剂中),要么单独配制(例如,作为单独的单元剂型包装)。
在健康的个体中,核心鞘糖脂、葡糖神经酰胺在溶酶体中被酸性葡糖神经酰胺酶(也称为葡糖脑苷脂酶或GBA1,EC 3.2.1.45,UniProt代码:P04062)水解。此外,存在于细胞质中的非溶酶体葡糖神经酰胺酶(GBA2,UniProt代码:Q9HCG7)也能够处理葡糖神经酰胺。因此,GBA1和GBA2二者均参与了观察到几种溶酶体贮积症的神经病理学效应。
在患有溶酶体贮积症的患者中,发生鞘糖脂生物合成或降解的缺陷,导致异常水平的葡糖神经酰胺和/或其他鞘糖脂。
先前示出(在WO2015/147639 A1中)化合物(I)在治疗与不规律水平的细胞溶质或溶酶体葡糖神经酰胺和/或较高水平的鞘糖脂相关的疾病方面是有效的。由于化合物(I)的晶型的生物利用度与非晶化合物(I)的生物利用度相当,因此化合物(I)的晶型在治疗与异常水平的细胞葡糖神经酰胺和/或较高水平的鞘糖脂相关的疾病方面也是有效的。特别地,化合物(I)的晶型在治疗与异常水平的细胞溶质或溶酶体葡糖神经酰胺和/或较高水平的鞘糖脂相关的疾病方面是有效的。
如实施例4所示,化合物(I)的晶型(3型)在治疗与不规律水平的细胞溶质或溶酶体葡糖神经酰胺和/或较高水平的鞘糖脂相关的疾病方面是有效的。具体地,3型示出改善尼曼-皮克病C型小鼠的临床体征。
因此,本发明提供了如本文所述的化合物(I)的晶型或如本文所述的药物组合物,用于在治疗中的用途。
本发明还提供了如本文所述的晶型或如本文所述的药物组合物,用于作为药物的用途。
优选地,本发明提供了如本文所述的化合物(I)的晶型或如本文所述的药物组合物,用于在治疗涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病中的用途。优选地,涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病为溶酶体贮积病,例如戈谢病(1型、2型和3型)、法布里病、GM1神经节苷脂贮积症、GM2神经节苷脂贮积症(例如,泰-萨克斯病、桑德霍夫病和AB变异型)、唾液酸贮积症、尼曼-皮克病C型和动作性肌阵挛肾功能衰竭综合征;或者统称为代谢综合征的疾病中的一种的症状,例如肥胖、胰岛素抵抗、高脂血症、高胆固醇血症、多囊肾病、II型糖尿病和慢性炎症;或者神经退行性病症,例如帕金森病或路易体痴呆;或者动脉粥样硬化。还更优选地,化合物(I)的晶型或包含化合物(I)的晶型的药物组合物可用于治疗GM1神经节苷脂贮积症和/或GM2神经节苷脂贮积症(例如泰-萨克斯病、桑德霍夫病和AB变异型)。
还更优选地,本发明提供了如本文所述的化合物(I)的晶型或如本文所述的药物组合物,用于在治疗尼曼-皮克病C型中的用途。
本发明提供了如本文所述的化合物(I)的晶型或如本文所述的药物组合物,用于在治疗桑德霍夫病中的用途。
本发明提供了治疗人或动物患者涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病的方法,包括向有此需要的患者施用治疗有效量的如本文所述的化合物(I)的晶型或如本文所述的药物组合物。
本发明提供了如本文所述的化合物(I)的晶型或如本文所述的药物组合物,用于在减轻涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病的症状中的用途。
还更优选地,本发明提供了如本文所述的化合物(I)的晶型或如本文所述的药物组合物,用于在减轻尼曼-匹克病C型的症状中的用途。
本发明提供了如本文所述的化合物(I)的晶型或如本文所述的药物组合物,用于在减轻桑德霍夫病的症状中的用途。
本发明提供了减轻人或动物患者涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病的症状的方法,包括向有此需要的患者施用治疗有效量的如本文所述的化合物(I)的晶型或如本文所述的药物组合物。
化合物(I)的晶型(例如,3型)可以用于改善不同的临床体征,例如:
1)疾病相关的体重减轻;
2)震颤;和/或
3)共济失调步态。
如实施例4所示,化合物(I)的晶型(例如,3型)有效地渗透至脑。因此,化合物(I)的晶型(例如,3型)可以用于治疗或减轻源自脑中的疾病或疾病症状。例如,化合物(I)的晶型(例如,3型)可以用于预防或减少小脑浦肯野细胞(Purkinje cell)损失。化合物(I)的晶型(例如,3型)可以用于预防或减少神经元死亡。化合物(I)的晶型(例如,3型)可以用于预防或减少大脑萎缩。
化合物(I)的晶型在治疗涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病方面的高效性被理解为由于化合物(I)的晶型对葡糖神经酰胺合酶(glucosylceramide synthase,GCS)和非溶酶体葡糖脑苷脂酶(GBA2)的高效力。
本文所述的方法可以为体外方法或体内方法。
施用可以通过以下完成:经由片剂、丸剂、胶囊剂、颗粒剂、散剂、溶液剂等的经口施用;或者肠胃外施用,例如诸如关节内、静脉内和肌肉内注射的注射剂,栓剂,眼用溶液剂,眼用软膏剂或外用剂(例如经皮液体制剂、软膏剂、经皮贴剂、经黏膜液体制剂、经黏膜贴剂、吸入剂)等。
在经口施用中,日剂量通常为每体重约0.0001mg/kg至10mg/kg,优选地0.001mg/kg至1mg/kg、或0.005mg/kg至5mg/kg,并且更优选地0.01mg/kg至0.5mg/kg,以一份或以2至4个单独的份施用。例如,对于70kg的人患者,经口施用的最佳日剂量为约0.01mg/天至30mg/天。在静脉内施用的情况下,日剂量合适地以每体重约0.00001mg/kg至10mg/kg施用,一天一次或者一天两次或更多次。此外,经黏膜剂以每体重约0.0001mg/kg至10mg/kg的剂量施用,每天一次或者一天两次或更多次。剂量通过考虑症状、年龄和性别等根据个体情况适当地决定。
由于化合物(I)的晶型在治疗涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病(例如,尼曼-皮克病C型)方面的效力非常高,并且需要相对低的剂量,因此化合物(I)的晶型比用于治疗这样的疾病的已知化合物例如米格列醇(剂量1200mg/kg/天)产生更少的副作用。
本发明还提供了制备如本文所述的晶型的方法,包括使化合物(I)的样品与溶剂接触。优选地,溶剂选自乙腈、乙酸乙酯、异丙醇、苯甲醚、水和叔丁基甲基醚(TBME)。还更优选地,溶剂为乙酸乙酯、乙腈或异丙醇。优选地,在使化合物(I)的样品与溶剂接触之前,将化合物(I)的样品纯化以除去硼酸酯。优选地,使用色谱法纯化化合物(I)的样品。还更优选地,使用硅胶色谱柱纯化化合物(I)的样品。另外地,和/或替代地,通过用甲醇蒸馏来纯化化合物(I)的样品。
化合物(I)的3型晶型可以通过以下示例性方法中的任一者获得:
1)将约74mg化合物(I)和2.0ml乙腈的混合物在20℃至30℃范围内,例如约25℃的温度下搅拌三天,然后过滤以获得化合物(I)的晶型;
2)将约74mg化合物(I)和2.0ml苯甲醚的混合物在20℃至30℃范围内,例如约25℃的温度下搅拌三天,然后过滤以获得化合物(I)的晶型;
3)将约82mg化合物(I)和1.0ml乙酸乙酯的混合物在20℃至30℃范围内,例如约25℃的温度下搅拌三天,然后过滤以获得化合物(I)的晶型;
4)将约82mg化合物(I)和1.0ml异丙醇的混合物在20℃至30℃范围内,例如约25℃的温度下搅拌三天,然后过滤以获得化合物(I)的晶型;
5)将约45mg化合物(I)和1.0ml水的混合物在20℃至30℃范围内,例如约25℃的温度下搅拌三天,然后过滤以获得化合物(I)的晶型;
6)将约100mg化合物(I)和3.0ml TBME的混合物在20℃至30℃范围内,例如约25℃的温度下搅拌三天,然后过滤以获得化合物(I)的晶型。
优选地,在将化合物(I)与溶剂混合之前,将化合物(I)的样品纯化以除去硼酸酯。优选地,使用色谱法将化合物(I)的样品纯化。还更优选地,使用硅胶色谱柱将化合物(I)的样品纯化。另外地和/或替代地,通过用甲醇蒸馏来将化合物(I)的样品纯化。
过滤方法是本领域技术人员己知的,并且包括但不限于纸过滤和烧结玻璃过滤。
本文所述的化合物(I)的3型的生产方法可以在保持所使用的试剂的相似比率的更大规模上进行。例如,化合物(I)的3型晶型可以通过以下获得:将化合物(I)与乙酸乙酯在0.05g至1g比1mL[化合物(I)比乙酸乙酯]的比率下的混合物在20℃至30℃范围内,例如约25℃的温度下搅拌三天,然后过滤以获得化合物(I)的晶型。
本文所述的用于获得化合物(I)的3型的方法非常有效。本文所述的方法的产率通常大于70%(作为所获得的3型的量与最初使用的化合物(I)的量的重量比)。优选地,本文所述的方法的产率大于75%。
优选地,在形成3型晶型之前,2型晶型作为中间体形成。
优选地,在形成通过在X射线粉末衍射图中以2θ值表示的在17.2±0.2°、17.8±0.2°、21.2±0.2°和22.4±0.2°处的反射表征的3型晶型之前,通过在X射线粉末衍射图中以2θ值表示的在16.1±0.2°、16.5±0.2°、16.9±0.2°、18.9±0.2°和23.1±0.2°处的反射表征的2型晶型作为中间体形成。
本发明还提供了通过进行本文所述的方法获得的化合物(I)的晶型。
本发明还提供了化合物(I)的游离碱制备化合物(I)的晶型的用途。
本发明还提供了制备化合物(I)的晶型的方法,包括使化合物(I)的游离碱结晶。
本发明还提供了通过包括使化合物(I)的游离碱结晶的制备化合物(I)的晶型的方法而获得的化合物(I)的晶型。
在其他优点中,认为形成化合物(I)的晶型可用于纯化化合物(I)。例如,通过本文所述的方法获得的化合物(I)的晶型具有大于90%且通常大于95%的纯度。
前述详细描述已通过说明和举例的方式提供,并且不旨在限制所附权利要求的范围。在本文所示的目前优选的实施方案中的许多变化对于本领域普通技术人员而言将是明显的,并且仍在所附权利要求及其等同方案的范围内。
在以下条款中进一步公开了本发明。
1.一种化合物(I)的晶型,
2.根据条款1所述的晶型,其中所述晶型为结晶游离碱。
3.根据条款1或条款2所述的晶型,其中所述晶型在X射线粉末衍射图中显示以2θ值表示的在17.8±0.2°处的反射,其中在17.8±0.2°处的反射为X射线粉末衍射图中的四个最强反射之一。
4.根据条款3所述的晶型,在X射线粉末衍射图中还显示以2θ值表示的在4.1±0.2°、8.3±0.2°、12.4±0.2°、13.6±0.2°、14.5±0.2°、14.9±0.2°、15.2±0.2°、17.2±0.2°、19.3±0.2°、21.2±0.2°、22.4±0.2°、22.9±0.2°和23.3±0.2°中的一者或更多者处的一个或更多个反射。
5.根据条款1至4中任一者所述的晶型,通过在X射线粉末衍射图中以2θ值表示的在17.2±0.2°、17.8±0.2°、21.2±0.2°和22.4±0.2°处的反射来表征。
6.根据条款1至5中任一者所述的晶型,具有89℃至96℃的熔点。
7.根据条款1至6中任一者所述的晶型,具有92℃至93℃的熔点。
8.根据条款1至7中任一者所述的晶型,其中所述晶型基本上不吸湿。
9.根据条款1或条款2所述的晶型,其中所述晶型在X射线粉末衍射图中显示以2θ值表示的在16.9±0.2°处的反射,其中在16.9±0.2°处的反射为X射线粉末衍射图中的四个最强反射之一。
10.根据条款9所述的晶型,在X射线粉末衍射图中还显示以2θ值表示的在15.2±0.2°、16.1±0.2°、16.5±0.2°、18.9±0.2°、23.1±0.2°、25.5±0.2°、27.7±0.2°和28.5±0.2°中的一者或更多者处的一个或更多个反射。
11.根据条款1、2、9或10中任一者所述的晶型,通过在X射线粉末衍射图中以2θ值表示的在16.1±0.2°、16.5±0.2°、16.9±0.2°、18.9±0.2°和23.1±0.2°处的反射来表征。
12.根据条款9至11中任一者所述的晶型,具有67℃至74℃的熔点。
13.根据条款9至12中任一者所述的晶型,具有69℃至71℃的熔点。
14.根据条款9至13中任一者所述的晶型,具有75mg/mL至85mg/mL的水溶性。
15.一种药物组合物,包含根据条款1至14中任一者所述的晶型。
16.根据条款15所述的药物组合物,其中所述药物组合物包含在胶囊中。
17.根据条款16所述的药物组合物,其中所述药物组合物包含在没有任何其他成分的胶囊中。
18.根据条款15或条款16所述的药物组合物,包含至少一种可药用载体。
19.根据条款1至14中任一者所述的晶型或者根据条款15至18中任一者所述的药物组合物,用于在治疗中的用途。
20.根据条款1至14中任一者所述的晶型或者根据条款15至18中任一者所述的药物组合物,用于作为药物的用途。
21.根据条款1至14中任一者所述的晶型或者根据条款15至18中任一者所述的药物组合物,用于在治疗涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病中的用途。
22.根据条款21所述用于用途的晶型或药物组合物,其中涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病为溶酶体贮积病,例如戈谢病、法布里病、GM1神经节苷脂贮积症、GM2神经节苷脂贮积症(例如,泰-萨克斯病、桑德霍夫病和AB变异型)、唾液酸贮积症、尼曼-皮克病C型和动作性肌阵挛肾功能衰竭综合征;或者统称为代谢综合征的疾病中的一种的症状,例如肥胖、胰岛素抵抗、高脂血症、高胆固醇血症、多囊肾病、II型糖尿病和慢性炎症;或者神经退行性病症,例如帕金森病或路易体痴呆;或者动脉粥样硬化。
23.根据条款21或条款22所述用于用途的晶型或药物组合物,其中疾病为GM1神经节苷脂贮积症或GM2神经节苷脂贮积症(例如泰-萨克斯病、桑德霍夫病或AB变异型)。
24.一种治疗人或动物患者涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病的方法,包括向有此需要的患者施用治疗有效量的根据条款1至14中任一者所述的晶型、或者根据条款15至18中任一者所述的药物组合物。
25.一种制备根据条款1至8中任一者所述的晶型的方法,包括使化合物(I)的样品与溶剂接触。
26.根据条款25所述的方法,其中溶剂选自乙腈、乙酸乙酯、异丙醇、苯甲醚、水和叔丁基甲基醚(TBME)。
27.根据条款25或条款26所述的方法,其中在使化合物(I)的样品与溶剂接触之前,对化合物(J)的样品进行纯化。
28.根据条款27所述的方法,其中使用色谱法将化合物(I)的样品纯化。
29.根据条款28所述的方法,其中使用硅胶柱色谱法将化合物(I)的样品纯化。
30.根据条款27至29中任一项所述的方法,其中在纯化之后,化合物(I)的样品不含硼酸酯。
31.根据条款25至30中任一者所述的方法,其中在形成根据条款1至8中任一者所述的晶型之前,根据条款9至14中任一者所述的晶型作为中间体形成。
32.一种化合物(I)的晶型,通过进行根据条款25至31中任一者所述的方法获得。
33.化合物(I)的游离碱制备晶型的用途。
34.一种制备化合物(I)的晶型的方法,包括使化合物(I)的游离碱结晶。
35.一种通过根据条款34所述的方法获得的化合物(I)的晶型。
36.一种制备化合物(I)的晶型的方法,包括以下步骤:
i.将化合物(I)添加至纯化柱以产生经纯化的化合物(I)的样品;
ii.向经纯化的化合物(I)的样品中添加溶剂以产生化合物(I)在溶剂中的悬浮体;
iii.将化合物(I)在溶剂中的悬浮体搅拌以产生化合物(I)的晶型;以及
iv.将化合物(I)的晶型分离以产生化合物(I)的晶型的纯样品。
37.根据条款36所述的方法,其中经纯化的化合物(I)的样品不含硼酸酯。
38.根据条款36或37所述的方法,其中溶剂选自乙腈、乙酸乙酯、异丙醇、苯甲醚、水和叔丁基甲基醚(TBME)。
39.根据条款36至38中任一者所述的方法,其中步骤ii在25℃至35℃的温度下进行。
40.根据条款36至39中任一者所述的方法,其中步骤(iii)中的搅拌在20℃至35℃的温度下进行。
41.根据条款36至40中任一者所述的方法,其中步骤(iii)中的搅拌进行至少1小时。
42.根据条款41所述的方法,其中步骤(iii)中的搅拌进行至少16小时。
实验部分
用TA Instruments Q2000仪器(封闭的铝样品盘或盖子中具有针孔的铝样品盘,加热速率为20K/分钟)进行差示扫描量热法(DSC)。熔点被理解为峰最大值。
用来自ProUmid(先前的“Projekt Messtechnik”),August-Nagel-Str.23,89079乌尔姆市(德国)的SPS11-100n“Sorptions Prüfsystem”进行动态蒸汽吸附(Dynamicvapour sorption,DVS)测量。将约5mg至20mg样品放入铝样品盘中。使用每小时5%的湿度变化率。所应用的测量程序可以描述如下:
将样品放置在微量天平上的铝或铂夹具上,并使其在50%的相对湿度(RH)下平衡,然后开始预定义的湿度程序:
(1)在50%RH下2小时
(2)50%至0%RH(5%/小时);在0%RH下5小时
(3)0%至95%RH(5%/小时);在95%RH下5小时
(4)95%至0%RH(5%/小时);在0%RH下5小时
(5)0%至95%RH(5%/小时);在95%RH下5小时
(6)95%至50%RH(5%/小时);在50%RH下2小时
用配备有用Cu-Kα1辐射操作的Mythen1K检测器的Stoe Stadi P衍射仪进行粉末X射线衍射。用该仪器在40kV的管电压和40mA管功率下以传输方式进行测量。弯曲的Ge单色器允许用Cu-Kα1辐射进行测试。设定以下参数:0.02°2θ步长、12秒步进时间、1.5°至50.5°2θ扫描范围和1°2θ检测器步进(步进扫描中的检测器模式)。对于典型的样品制备,将约10mg样品放置在两个乙酸酯箔之间并安装在Stoe透射样品夹具中。将样品在测量期间旋转。所有样品制备和测量均在环境空气气氛(约25℃)中进行。
通过向约10mg化合物中逐渐添加溶剂,随后短时间振荡和/或声处理来确定近似溶解度。如果通过添加总计至少10ml溶剂不能溶解该物质,则溶解度表示为<1mg/ml。实验在约25℃下进行。
用与Bruker FTIR Spectrometer Vector 22(具有针孔的样品盘,N2气氛,加热速率10℃/分钟)耦接的Netzsch Thermo-Microbalance TG 209来进行热重测量(TG-FTIR)。
实施例
以下非限制性实施例进一步举例说明本发明。
实施例1-结晶盐形成
用表1中确定的16种不同的盐形成剂在六种不同条件下进行化合物(I)的高通量盐筛选程序,以尝试获得化合物(I)的晶型。
通过将化合物(I)在丙酮中的0.05M溶液添加到石英96-微量滴定板的每个孔中,然后添加浓度为0.1M的盐形成剂储备溶液,来进行初始筛选实验。在室温下在氮气流下从每个孔中蒸发溶剂。通过偏光显微镜检查研究孔中的固体残余物。
表1.针对盐筛选程序选择的酸
尽管该初始实验的目的是获得1:1比率的化合物(I)与盐形成剂,但光学显微镜检查研究揭示了一些适合于晶型形成的实验条件。例如,将化合物(I)与苯磺酸、盐酸、DL-扁桃酸、L-酒石酸、磷酸和硫酸混合形成结晶残余物。
在进一步的筛选实验中,选择六种溶剂体系,即丙酮、乙腈、乙酸乙酯、乙醇、异丙醇-水(3∶1)混合物和丙酮/水(9∶1)混合物。将200μL溶剂添加至每个孔中的残余物中用于浆料平衡。将如此准备的微量滴定板在室温(约25℃)下以400rpm搅拌一天。然后,在氮气流下蒸发溶剂,并通过偏光显微镜检查研究所获得的固体残余物。
基于光学显微镜检查研究,发现了苯磺酸、龙胆酸、盐酸、L-乳酸、D-扁桃酸、磷酸、L-酒石酸和甲苯磺酸的可能盐的线索。最有前景的线索中的一些被选择用于规模为50mg至200mg(放大实验)的后续实验。
所有测试条件的放大实验导致形成化合物(I)的非晶形式或化合物(I)的液体结晶盐。虽然显微镜检查经常显示双折射,但不能过滤所获得的混合物,并且在任何实验中都无法回收固体材料。
总而言之,用盐形成剂的所有实验都未能产生化合物(I)的晶型。
实施例2-2型晶型
由于实施例1中的实验未产生有用的结晶材料,因此研究了化合物(I)的游离碱形式。
使用硅胶柱对化合物(I)进行纯化以除去硼酸酯,然后在乙腈中短暂平衡(约1分钟至5分钟)。经纯化的化合物(I)在乙腈中的溶解度被确定为5mg/mL至8mg/mL。还检测了经纯化的化合物(I)在其他溶剂中的溶解度,并呈现在表2中。这些值通过将溶剂的少量的等分试样添加至约10mg固体化合物(I)中并在室温(约25℃)下短时间振荡/声处理来确定。
表2.经纯化的化合物(I)的近似溶解度值。
通过偏光显微镜检查、粉末X射线衍射(PXRD)实验、TG-FTIR、差示扫描量热法(DSC)和动态蒸汽吸附(DVS)来检测由在乙腈中短暂(约1分钟至5分钟)平衡产生的化合物(I)的2型晶型。
偏光显微镜检查研究的结果呈现在图1中,而PXRD图描绘在图2中。化合物(I)的该2型晶型在2θ值为16.1±0.2°、16.5±0.2°、16.9±0.2°、18.9±0.2°和23.1±0.2°处表现出最强反射。
在图3A中显现出由在乙腈中的短暂平衡而获得的化合物(I)的2型晶型的热分析表征结果(TG-FTIR热谱图),而DSC结果示于图3B中。结果表明样品含有约0.5%的水,在加热至约120℃时释放水。在较高的温度下,观察到热分解。DSC揭示了两个重要的吸热事件。具有在约70℃下的峰值温度和约54J/g的焓的第一个强吸热之后是在81℃的较弱信号和约3J/g的焓。
此外,在可变水蒸气压力下研究了结晶游离碱样品的行为。在高的相对湿度下,样品吸收约18%的水;然而,当相对湿度恢复至50%RH时,大部分吸收的水被释放。来自DVS测量的结果呈现在图4A和图4B中。
在表3中提供了作为实施例2的部分获得的化合物(I)的晶型的特性总结。
| 特性 | 值/描述 |
| 熔点 | 约70℃ |
| 吸湿性 | 在95%RH下为18%;吸湿的 |
| 水中的溶解度 | 约80mg/mL |
表3.化合物(I)的2型晶型的特性总结。
所获得的化合物(I)的2型晶型具有低稳定性,并且在暴露于升高的温度(高于约30℃)约1分钟至5分钟时转变为化合物(I)的另一种3型晶型。或者,在约25℃下在溶剂(例如,丙酮)中平衡多于5分钟时,2型转变为3型。化合物(I)的该另一种游离碱3型晶型具有更好的稳定性和一组独特的物理化学特性。
实施例3-3型
独立地,化合物(I)的稳定晶型由经纯化的化合物(I)在各种不同的溶剂中,例如,分别在乙腈、乙酸乙酯、异丙醇、苯甲醚、水或TBME中在室温(约25℃)下的悬浮体平衡实验而获得。
特别地,化合物(I)的3型晶型通过以下实验方法获得:
1)将约74mg化合物(I)添加至2.0ml乙腈中,并将悬浮体在室温(约25℃)下搅拌三天,然后过滤;
2)将约74mg化合物(I)添加至2.0ml苯甲醚中,并将悬浮体在室温(约25℃)下搅拌三天,然后过滤;
3)将约82mg化合物(I)添加至1.0ml乙酸乙酯中,并将悬浮体在室温(约25℃)下搅拌三天,然后过滤;
4)将约82mg化合物(I)添加至1.0ml异丙醇中,并将悬浮体在室温(约25℃)下搅拌三天,然后过滤;
5)将约45mg化合物(I)添加至1.0ml水中,并将悬浮体在室温(约25℃)下搅拌三天,然后过滤;
6)将约100mg化合物(I)添加至3.0ml TBME中,并将悬浮体在室温(约25℃)下搅拌三天,然后过滤。
在添加溶剂之前使用硅胶柱对化合物(I)进行纯化以除去硼酸酯。
所获得的化合物(I)的晶型通过偏光显微镜检查、粉末X射线衍射、TG-FTIR、DSC和DVS来表征。
对于所选择的溶剂的偏光显微镜检查研究结果呈现在图5中。
由用乙腈的悬浮体平衡实验获得的化合物(I)的3型晶型的PXRD图示于图6A中。由用其他溶剂的悬浮体平衡实验获得的化合物(I)的3型晶型的PXRD图的叠加示于图6B中。化合物(I)的该晶型在2θ值为17.2±0.2°、17.8±0.2°、21.2±0.2°和22.4±0.2°处示出最强反射。这是一致的,尽管使用不同的溶剂来获得化合物(I)的晶型。
为了比较,图7示出了在实施例2(2型)和本发明实施例(3型)中获得的晶型的PXRD图的叠加。两种晶型具有不同的PXRD图。
化合物(I)的3型晶型的示例性TG-FTIR表征实验的结果示于图8A(乙酸乙酯)和图8B(异丙醇)中。
图8A表明,尽管在40℃下在真空中干燥数天,但通过用乙酸乙酯平衡而获得的化合物(I)的3型晶型的样品包含约0.7%的乙酸乙酯。乙酸乙酯在约100℃至200℃释放。在较高的温度下观察到热分解。
由化合物(I)在异丙醇中的悬浮体产生的3型样品(并在室温下在空气中干燥)出乎意料地示出初始异丙醇含量低于0.5%(参见图8B)。
通过用乙酸乙酯平衡获得的化合物(I)的3型晶型样品的示例性DSC测量描绘在图8C中,并示出在约92℃下与约103J/g的焓相关的尖锐吸热熔化峰。因此,作为该实施例的部分获得的化合物(I)的3型晶型具有比来自实施例2的晶型(2型)更高的熔点。
此外,在可变水蒸汽压力下研究了通过用乙酸乙酯平衡获得的化合物(I)的3型晶型样品的行为。在95%的最高相对湿度下,样品吸收了约1.2%的水,当相对湿度恢复至50%RH时释放水。来自DVS测量的结果示于图9A和图9B中。吸收的水的量少,并且水吸收是可逆的。因此,化合物(I)的该3型晶型是不吸湿或基本上不吸湿的。
表4中提供了作为实施例3的部分获得的化合物(I)的3型晶型的特性总结。
| 特性 | 值/描述 |
| 熔点 | 约92.5℃ |
| 吸湿性 | 在95%RH下为约1%;基本上不吸湿的 |
| 水中的溶解度 | 未测量 |
表4.化合物(I)的3型晶型的特性总结。
实施例4-向患有尼曼-匹克C型(NPC)病的小鼠施用化合物(I)的晶型的效果
在实施例中,AZ-3102-00为3型化合物(I)的名称。
研究的目的
该研究的目的是使用经口管饲评估具有预测药理学活性剂量的AZ-3102-00对幼小NPC1(NPC(-/-)小鼠(P11至P70))的处理,并评估PK和组织学标记物以表征可能发生的神经病理学。
研究设计
在包含于本研究中的38只小鼠中,存在30只NPC(-/-)敲除(KO)小鼠、4只NPC(+/-)杂合小鼠和4只NPC(+/+)野生型(WT,Balb/c)小鼠。NPC1(-/-)小鼠过早截断蛋白质,删除13个跨膜域中的11个,使前两个跨膜域保持完好无损。NPC1(-/-)小鼠纯合的隐性NIH等位基因的尼曼匹克病C1型基因(Npc1mlN)示出鞘磷脂酶和葡糖脑苷脂酶活性的双重缺陷(JAX#003092)。动物在BALB/c OlaHsd背景下饲养。
将24只NPC1(-/-)小鼠自出生后第11天(P11)到出生后第70天(P70)每次经口管饲AZ-3102-00进行处理。年龄匹配的对照小鼠包括用载剂处理的6只NPC(-/-)和4只NPC(+/-)小鼠,以及接受AZ-3102-00的4只NPC(+/+)小鼠。在P70进行最后处理之后,将NPC(-/-)小鼠(每个时间点n=4)在以下时间点通过IP注射600mg/kg戊巴比妥实施安乐死:30分钟、1小时、2小时、4小时、8小时和24小时。在最后处理之后也处死了对照小鼠(时间不严格)。通过心脏穿刺在EDTA涂层管中收集终末血液。通过离心(在室温下3000x g 10分钟)收集血浆,并将50μL血浆等分试样转移至1.5mL管中,在干冰上冷冻并储存在-80℃下。
在经心灌注之后,移出脑并切半。右半脑被后固定并嵌入到低温模具中以进行进一步的免疫组织化学分析。将左半脑在干冰上冷冻用于进一步分析。
对脑进行冷冻切片(12个层面,各具有5个切片)。然后将每只动物的5个切片用于两个脑区域中的小胶质细胞(MAC1)和星形胶质细胞(GFAP)的定量免疫荧光标记。
测试系统和测试系统的论证
尼曼-匹克C型(NPC)病是常染色体隐性神经退行性病症,其与NPC1和NPC2基因中的突变相关并且通过未酯化胆固醇和鞘糖脂(GSL)的积累来表征。约95%的尼曼-匹克C型病例由NPC1基因中的基因突变引起,称为C1型;5%由NPC2基因中的突变引起,称为C2型。尼曼-匹克C1型和尼曼-匹克C2型的临床表现相似,因为各自的基因都参与脂质(特别是胆固醇)从晚期核内体或溶酶体的排出。NPC1基因编码位于细胞内的细胞膜中的蛋白质,并参与细胞内胆固醇和脂质的运动。缺乏该蛋白质导致细胞膜内脂质和胆固醇的异常积聚。NPC2基因编码结合和转运胆固醇的蛋白质。尼曼匹克C1型基因的隐性NIH等位基因的纯合小鼠示出鞘磷脂酶和葡糖脑苷脂酶活性的双重缺陷。突变小鼠在约7周龄时开始减轻重量并示出震颤和共济失调步态。重量减轻继续,并且震颤和共济失调变得更加严重,直至在约12周至14周龄时死亡。肝脏和脾脏也肿大,并且小脑中的浦肯野细胞严重耗竭。小鼠中的这些体征中的一些与人尼曼-匹克C型病患者的体征相似。
测试品项
表5.测试品项信息。
化合物制备:
在需要时将剂量制剂分成等分试样以允许在每次给药情况下分配。
表6.制剂信息。
称取所需量的测试品项并溶解在Elix水(重量/重量)中,并将pH调节至酸性pH。不添加另外的赋形剂。
未对测试品项的比重或测试品项的纯度/组成进行校正。
在每次剂量制备之后,将保留的溶液冷冻用于在研究结束时的分析。
预先结合方法开发和验证研究进行的稳定性分析表明,当在相同条件下制备和储存浓度与本研究中使用的浓度相符的测试品项时,其在与本研究中使用的浓度相符的浓度(0.01mg/mL至2mg/mL)下,在载剂中,在室温下避光至少24小时,至少8天冷藏(2℃至8℃)和在冰箱中(≤-15℃)至少3周是稳定的。
动物管理
动物的适应
将动物安置在于由Rettenmaier供应的标准化啮齿动物床品的单独通风的笼中。每个笼容纳最多五只小鼠。将保持室中的温度保持在20℃至24℃,以及相对湿度保持在45%至65%。将动物在恒定光照周期(12小时光照/黑暗)下安置。动物可随意获得干燥的丸粒状标准啮齿动物食物(Altromin)以及普通自来水。在主治兽医的指导下向动物供应湿食物。
辨别
通过经典的打耳标(earmark)对动物进行连续编号。
每个笼都用彩色卡片标识,表明动物的研究编号、性别、个体登记编号(IRN)、出生日期以及处理组分配。通过对转基因构建体特异的PCR来确定每只动物的基因型(转基因或野生型)。在研究开始之前使用从耳朵活检中分离的DNA对每只小鼠进行基因分型。
组分配
仅健康状况明显良好的动物被包括在研究中。每个笼进行随机化的组分配。动物被分配到不同的起始组(组群),包括所有处理组的动物。限制起始组中动物的数量以确保相同年龄和统一处理。
健康状况和笼侧观察结果
在参加研究之前,评估每只单独的动物的健康状况。在研究期间,每天进行观察,并且记录任何显著的笼侧观察结果并立即报告至研究负责人和主治兽医,由他们决定进一步行动(例如,安乐死)。
第一周每天记录体重和健康状况,之后每周记录一次。
提早终止和人道终点
没有动物必须过早安乐死。
材料和方法
动物
小鼠品系:NPC(-/-)
饲养员:QPS Austria GmbH,Grambach,澳大利亚
开始年龄:出生后第11天(P11)至出生后第70天(P70)
性别:混合的
动物的数量:30NPC(-/-)、4NPC(+/-)、4NPC(+/+)
处理
将24只NPC1(-/-)小鼠(D组至I组)自出生后第11天(P11)到出生后第70天(P70)每次经经口管饲(10mL/mg)AZ-3102-00进行处理。剂量自P11到P25以1.5mg/kg开始,然后剂量自P26到P70以3mg/kg。对照小鼠包括经载剂处理的6只NPC1(-/-)和4只NPC(+/-)小鼠以及接受AZ-3102-00的4只NPC(+/+)小鼠(A组至C组)。
在P70进行最后处理之后,NPC(-/-)小鼠(每个时间点n=4;D组至I组)在以下时间点通过IP注射600mg/kg戊巴比妥实施安乐死:30分钟、1小时、2小时、4小时、8小时和24小时。对照小鼠(A组、B组和C组)在最后处理之后也被处死(时间不严格)。
表7:处理组概述。
组织取样
在P70进行最后处理之后,在30分钟(D组)、1小时(+/-5分钟,E组)、2小时(+/-5分钟,F组)、4小时(+/-5分钟,G组)、8小时(+/-5分钟,H组)和24小时(+/-5分钟,I组)(所有的时间都很关键),通过ip注射对小鼠实施安乐死。
A组的6只NPC1(-/-)、经处理的B组的4只NPC(+/-)和C组的4只NPC(+/+)小鼠作为对照,并且也在P70实施安乐死(最后处理之后约2小时)。
通过i.p注射戊巴比妥(600mg/kg,剂量为10μL/克体重)对小鼠进行终末麻醉。
采血
打开胸腔,并通过用23号针进行心脏穿刺收集血液。取出针,并将血液转移至样品管(K2EDTA(乙二胺四乙酸钾)中。将管彻底倒置以促进EDTA的均匀分布并防止凝结。将血液样品在室温(22℃)下以3000xg离心10分钟。将50μL血浆等分试样转移至预先标记的1.5ml LoBind Eppendorf管中,在干冰上冷冻并储存在-80℃下。
灌注
然后用0.9%盐水对动物进行心脏灌注。为此,将与含有0.9%盐水的瓶连接的23号针插入到左心室中。用止血钳夹住肺与肝脏之间的胸主动脉,以阻止血液从心脏流向腹部,但允许血液流向脑。用剪刀打开右心室。通过将溶液瓶连接至压力计控制的空气压缩机,使灌注溶液保持100mmHg至120mmHg的恒定压力。继续进行灌注直至颅骨表面变白并且仅灌注溶液而不是血液流出右心室。
脑采样
在灌注之后打开颅骨,小心地移除脑并在冷却表面上切成对半。将左半球称重,在干冰上快速冷冻并储存在-80℃下。通过在室温下将右半球浸泡在4%多聚甲醛的磷酸盐缓冲液(pH 7.4)中2小时来固定。
组织学
组织制备
通过在室温下将小鼠右半脑浸泡到新鲜制备的4%多聚甲醛的PB(pH 7.4)中两小时来固定。之后,将半球转移至15%蔗糖/PBS中并储存在4℃下直至沉没以确保冷冻保护。然后根据需要对组织块进行修整,转移至冷冻模具中,嵌入OCT培养基中,在干冰冷却的异戊烷中冷冻,并储存在超低温冰箱(设定在-80℃的目标温度)中。
切片
将五个连续的冷冻切片在Leica冷冻切片机上以10μm厚度矢状切割。将每个层面接下来的25个切片丢弃。该收集方案针对12个层面重复,并且可以被修改以从正确的层面中收集,例如,如果由于年龄小或基因型而脑较小。总计收集了12x 5=60个切片。根据Paxinos和Franklin的脑图谱(“The Mouse Brain in Stereotaxic Coordinates”,第2版,2001)选择切片层面。切片的收集在距中线侧约0.2mm层面处开始,并延伸穿过半球,以确保通过目标区域进行系统随机取样(图10和图15)。将切片储存在-20℃下。将几乎整个脑切片,因此在收集所有切片时将残留的组织块丢弃。
免疫荧光Exp3531(钙结合蛋白-D28k)
对于每次孵育,选择每只小鼠的统一系统随机组的五个切片(来自层面2、4、6、8、10各自一个切片);关于系统随机抽样的信息请点击此链接:http:// www.stereology.info/sampling/
除非另有说明,否则所有步骤均在室温下在Dulbecco的磷酸盐缓冲盐水pH 7.2至7.8(PBS)中执行。
1.将冷冻切片风干45分钟并在PBS中洗涤10分钟
2.在潮湿室中用0.1%TritonX-100/PBS中的10%正常驴血清(Jackson ImmunoResearch)封闭非特异性结合位点60分钟
3.将切片各自在PBS中洗涤3x 5分钟
4.将切片与1%正常驴血清/PBS中的一抗在4℃下在潮湿室中培养过夜
·豚鼠钙多克隆抗体与钙结合蛋白-D28k(Synaptic Systems,214005)1∶1000
5.将切片各自在PBS中洗涤3x 5分钟
6.将切片与1%正常驴血清/PBS中的二抗在潮湿室(避光)中培养60分钟
·驴抗豚鼠(H+L),Cy3缀合(Jackson ImmunoResearch,706-165-148),1∶500
7.将切片各自在PBS中洗涤3x 5分钟(避光)
8.将切片与DAPI工作溶液培养15分钟(避光)
9.将切片在PBS中洗涤2x 5分钟(避光)
10.将切片在ddH2O中洗涤5分钟(避光)
11.将切片用Mowiol和盖玻片覆盖(避光)
成像
在配备有Zeiss Axiocam 506单声道和日立3CCD HV-F202SCL相机以及Zeiss ZEN2.3软件的具有高光圈透镜的Zeiss自动显微镜AxioScan Z1上记录染色切片的全切片扫描。
量化
用Image Pro 10(Media Cybernetics)进行图像分析。在开始时,通过在图像上绘制目的区域(ROI)来确定目标区域(小脑和海马体,或胼胝体和纹状体)。另外的ROI排除了皱褶、气泡或任何其他干扰测量的人工因素。之后,在确定的区域内对免疫荧光进行定量评估。
对于量化,如有必要则使用背景校正,并通过适当的阈值和形态学过滤(尺寸、形状)来检测免疫反应对象。然后将不同的对象特征量化;其中,基于ROI尺寸的累积对象区域的百分比(免疫反应区域;这是指示免疫反应性中是否存在差异的最综合参数)、归一化为ROI尺寸的对象数量(对象密度)、确定对象的平均信号强度(平均强度;这表明目标蛋白的细胞表达水平是否存在差异)以及以上阈值对象的尺寸。在测试运行中定义了目标对象的参数后,定量图像分析自动运行,使得结果是独立于操作员的且完全可重现的。
原始数据在Excel中进行整理和排序,然后传输至GraphPad Prism用于统计分析和图表制备。棱柱图是研究报告的部分,并且在执行质量检查之后,将具有分类原始数据的表附在最终报告中。
小鼠血浆和脑组织中AZ-3102和葡糖神经酰胺的测量
首先,用包含500nM内标葡糖神经酰胺C17:0(GlcCer C17:0)和0.1%甲酸的乙腈/超纯水/甲醇(90∶5∶5)的溶液对血浆样品进行蛋白质沉淀。在室温下混合5分钟之后,将样品离心5分钟(13,000rpm,20℃),并将50μL上清液转移至硅化的MTP 96-孔板中。
使用FastPrep24TM Microtube均质器,将脑组织在具有0.1%甲酸的超纯水∶甲醇(1∶1)的溶液(每克组织4mL)中均质化。然后将组织匀浆与包含500nM GlcCer C17:0和0.1%甲酸的乙腈∶超纯水∶甲醇(90∶5∶5)的溶液混合以进行蛋白质沉淀。在室温下培养5分钟之后,将样品离心5分钟(13000rpm,20℃),并将50μL上清液转移到硅化的MTP 96-孔板中。
AZ-3102的测量
首先将血浆样品与包含50ng/mL AZ-3101(内标)的乙腈溶液混合用于蛋白质沉淀。在室温下培养5分钟之后,将样品离心5分钟(13000rpm,4℃),并将上清液在具有0.1%甲酸的超纯水中稀释10倍。
使用FastPrep 24TM Microtube均质器(MP Biomedicals,美国)将脑组织在具有0.1%甲酸的超纯水∶甲醇(1∶1)的溶液(每克组织4mL)中均质化。将脑匀浆与包含10ng/mLAZ-3101(内标)的乙腈溶液混合用于蛋白质沉淀。在室温下培养5分钟之后,将样品离心5分钟(13000rpm,4℃),并将上清液在具有0.1%甲酸的超纯水中稀释10倍。
通过自动进样器(SIL-30,Shimadzu,美国)将稀释的血浆和脑组织上清液注入到Agilent LC系统(Agilent,美国)中。在保持在40℃温度下的反相XBridge BEH C8柱(2.1*50mm,2.5μm颗粒尺寸;Waters,美国)上,使用流动相B的线性梯度以0.800mL/分钟的流量通过液相色谱法将分析物分离。流动相A由具有0.1%甲酸的超纯水组成。流动相B是具有0.1%甲酸的乙腈。
使用配备涡轮离子喷雾接口的API 5500三重四极杆质谱仪(AB Sciex,美国)以正电离模式实现采集。使用AnalystTM数据系统(AB Sciex,版本1.6.3)对数据进行校正和量化。对于AZ-3102,LLOQ分别在血浆样品中为0.2ng/mL,在脑中为2ng/g组织。
葡糖神经酰胺的测量
首先,用包含500nM内标葡糖神经酰胺C17:0(GlcCer C17:0)和0.1%甲酸的乙腈/超纯水/甲醇(90∶5∶5)的溶液对血浆样品进行蛋白质沉淀。在室温下混合5分钟之后,将样品离心5分钟(13,000rpm,20℃),并将50μL上清液转移到硅化的MTP 96-孔板中。
使用FastPrep 24TM Microtube均质器将脑组织在具有0.1%甲酸的超纯水∶甲醇(1∶1)的溶液(每克组织4mL)中均质化。然后将组织匀浆与包含500nM GlcCer C17:0和0.1%甲酸的乙腈∶超纯水∶甲醇(90∶5∶5)的溶液混合以进行蛋白质沉淀。在室温下培养5分钟之后,将样品离心5分钟(13000rpm,20℃),并将50μL上清液转移到硅化的MTP 96-孔板中。
通过HPLC-MS/MS检测在多个-反应监测模式(MRM)中对样品脑的葡糖神经酰胺C16:0(GlcCer C16:0)、葡糖神经酰胺C18:0(GlcCerC18:0)和葡糖神经酰胺C24:1(GlcCerC24:1)浓度进行量化。通过HPLC-MS/MS分析上清液,同时使用来自Advanced MaterialsTechnology的HALO HILIC柱(150*4.6mm,2.7μm)区分半乳糖基-与葡糖基-神经酰胺异构体。使用配备涡轮离子喷雾接口的API 4000三重四极杆(Applied Biosystems,美国)以正电离模式实现MS/MS采集。GlcCer C16:0和GlcCer C18:0的分析使用具有流动相A(94.5%乙腈、2.5%甲醇、2.5%超纯水和0.5%甲酸中的5mM乙酸铵)和流动相B(超纯水和0.1%甲酸)的梯度来进行。在脑样品中对于GlcCer 16:0、GlcCer 18:0和GlcCer 24:1,LLOQ分别为25pmol/g组织、1pmol/g组织、250pmol/g组织和381.5pmol/g组织。
统计学
在GraphPad Prism 9中进行统计分析。数据表示为平均值±平均标准误差(SEM)或平均值+平均标准误差。
体内:对于重复测量值,用双向ANOVA测试组之间的差异,然后进行Bonferroni或Dunnett的事后分析。
组织学:由于n低,不能测试数据分布,因此假定正态分布。用单向ANOVA测试组之间的差异,然后进行Dunnett的事后分析。A组(NPC-/-,经载剂处理)用作参考组用于成对比较。
结果
体重
图11示出了PND 11与第9周之间的体重的百分比变化。图表示在第一个处理周和此后每周期间每天测量的每组体重[g]的进展。
结果示出,动物的一般健康(如通过平均百分比体重增加表示的)未受AZ-3102的影响,并且用AZ-3102处理的两种性别的NPC(-/-)小鼠比未处理的NPC(-/-)动物增重更多。
药代动力学
表8.自PND 11至PND 70重复经口施用之后AZ-3102的脑:血浆暴露比率。
葡糖神经酰胺水平
图12示出了自PND 11至PND 70重复经口施用之后的葡糖神经酰胺C16:0和C18:0水平。
用AZ-3102处理的小鼠示出在脑中葡糖神经酰胺C16:0和C18:0水平增加。
临床体征
临床评分和人道终点的定义
自P45开始直至研究结束每天监测临床体征(根据下表9中的模板)。记录参数“重量减轻”、“一般健康”、“临床发现”和“直线特异性发现”并根据评分量表进行评级。该评分的总和用于评估。
表9.临床体征评分表
震颤评分
表10.震颤评分。
图13示出了跨所有域以及按处理组针对每个NPC(-/-)经载剂和AZ-3102处理的小鼠的自PND 56至PND 70的总临床体征评分的总结。左侧:如用梯度可视化的按动物和处理组的总评分,其中较低评分为绿色,较高评分为红色,右侧:达到数值阈值的评分汇总。大于7的阈值评分在处理组中很少发生;然而,未处理的组在研究过程期间具有较高数值的总评分。
结果表明,与NPC(-/-)AZ-3102处理的动物相比,NPC(-/,)载剂处理的小鼠在总体临床体征方面恶化(更高的评分)。这在图13中进一步显示:右侧,其中与NPC(-/-)AZ-3102处理的动物相比,在NPC(-/-)载剂处理的组中更频繁观察到例如大于8的评分。研究这些评分,我们发现震颤的引发、持续时间以及强度也因用AZ-3102处理而减少(图14)。在所有(除了一只)NPC(-/-)载剂处理的动物中均观察到高程度震颤;而AZ-3102在除所测试的24只动物中的一只之外的所有动物中基本上消除了该高程度震颤。
图14示出了NPC(-/-)载剂和AZ-3102处理的小鼠中自出生后第56天至70天的震颤评分。粉色(=浅灰色)条表示高程度震颤的出现和持续时间(评分为5);而绿色(=深灰色)条表示轻微或中度震颤的出现和持续时间。除了未处理的组中的一只小鼠之外,所有其他小鼠均表现出高程度震颤(5只小鼠中的4只)。相比之下,AZ-3102处理的组中仅一只小鼠具有高程度震颤(24只中的1只)。可能的震颤评分:0:无震颤1:轻微不协调,轻微-中度震颤;5:高程度震颤,不协调的移动;10:减少的翻正反射(没有动物达到该评分)。
组织学结果
目标区域的定义
通过限定目的区域(ROI)来手动勾勒出目标区域,用于随后的荧光标记定量分析。
定量分析的读数
以下呈现的表显示了四个标准读数。
·区域大小[mm2]:这些数据显示了被目标区域覆盖的每个脑切片的平均面积。该信息对于验证正确的采样是重要的。其也有助于识别脑萎缩,脑萎缩是一些动物模型的表现型的一部分。
·免疫活性面积[%]。被高于阈值的免疫反应对象(例如:细胞体、神经突、斑块)覆盖的ROI的百分比;这是表明免疫反应性中是否存在整体差异的最综合的参数。
·对象密度[对象数目/mm2]:归一化为目标区域的大小的高于阈值的免疫反应对象的数量;这尤其可用于检测神经元密度的变化。
·对象强度[a.u.]:高于阈值的免疫反应对象的像素的平均亮度;这表明目标蛋白的细胞表达程度是否存在差异。
·对象大小[μm2]:高于阈值的免疫反应对象的大小;这可用于检测小胶质细胞活化或斑块生长的差异。
钙结合蛋白-D28k
用豚鼠多克隆抗体检测钙结合蛋白-D28k的免疫荧光,并在小脑和海马体形成中定量该信号。与NCP(+/-)和NPC(+/+)小鼠相比,NCP(-/-)小鼠示出明显减少的钙结合蛋白-D28k标记。在所有读数中,用测试品项处理显著增加了小脑中的钙结合蛋白-D28k。所有影响均是区域特异性的,因为在海马体中未检测到显著的组差异。
图16示出了脑免疫组织化学的结果:与NPC(+/+,野生型小鼠)和NPC(-/-)处理的小鼠相比,NCP(-/-)和NPC(+/-)载剂处理的小鼠中的钙结合蛋白-D28k标记。图呈现了在每只鼠的5个脑切片的ROI内测量的免疫荧光信号的平均值(每组n=2至4)。通过单因素ANOVA和Dunnett事后检验来分析数据。条形图表示组平均值+SEM。条形图表示组平均值+SEM,*Adj.P值:<0.001。
采用使用针对浦肯野细胞的钙结合蛋白-D28k标志物的免疫组织学技术,发现与载剂处理的NPC(-/-)小鼠相比,AZ-3102处理显著限制了小脑浦肯野细胞损失(图16)。
结论
AZ-3102是正在开发用于多种溶酶体贮积症的新的经口小分子。AZ-3102的独特作用方式在于其对葡糖神经酰胺合酶(GCS)、非溶酶体葡糖脑苷脂酶(GbA2)的高效力以及其脑渗透特性。在尼曼-皮克C型病的小鼠模型中研究了AZ-3102[1,2],其中NPC基因的隐性NIH等位基因纯合小鼠在约7周龄时重量开始减轻并且示出震颤和共济失调步态[3]。疾病严重程度与显著的小脑浦肯野细胞损失有关,并且临床体征恶化直至达到人道终点(通常在12至14周龄)[3]。在该研究中,研究了自出生后天数(PND)第11天到第70天向NPC(-/-)、NPC(-/+)和WT(NPC(+/+);Balb/c)小鼠每天经口给药AZ-3102以评估其药代动力学(PK)特性、调节葡糖神经酰胺(GlcCer C16:0、GlcCer C18:0)和改善临床体征的能力。此外,还检测了对于浦肯野细胞的免疫组织化学标志物的治疗效果,这与神经病理学一致。自PND 11至PND 70重复每天经口给药AZ-3102之后。AZ-3102未影响动物的一般健康,如通过平均百分比体重增加所表示的,并且用AZ-3102处理的两种性别的NPC(-/-)小鼠均比未处理的NPC(-/-)动物增重更多(图11)。AZ-3102证实了高的脑:血浆暴露(表8)并与AZ-3102目标管理一致,与载剂处理的动物相比,由全脑匀浆测量的GlcCer物质增加,对于GlcCer 16:0增加大于2倍,以及对于GlcCer 18:0增加约9倍。这些两种GlcCer物质可能代表也将对AZ-3102有反应的其他GlcCer物质。为了评估AZ-3102是否达到影响一般健康和神经病理学的更具体的体征的足够的脑浓度,测量了多种临床体征(表9)。当在观察期内相加时,这些评分提供了自PND 56至PND 70的健康图。图13是每个观察组群的每只动物随时间的图形视图。在该图中,与NPC(-/-)AZ-3102处理的动物相比,NPC(-/-)载剂处理的小鼠在总体临床体征方面恶化(更高的评分)。这在(图13:右侧)中进一步量化,其中与NPC(-/-)AZ-3102处理的动物相比,在NPC(-/-)载剂处理的组中更频繁观察到例如大于8的评分。研究这些评分,发现震颤的引发、持续时间以及强度也因用AZ-3102处理而减少(图14)。在所有(除了一只)NPC(-/-)载剂处理的动物中均观察到高程度震颤;然而,在除所测试的24只动物中的一只之外的所有动物中,AZ-3102基本上消除了该高程度震颤。采用使用针对浦肯野细胞的钙结合蛋白-D28k标志物的免疫组织学技术,发现与载剂处理的NP-C(-/-)小鼠相比,AZ-3102处理显著限制了小脑浦肯野细胞损失(图16)。该发现与人的尼曼-匹克C型相关,由于神经元死亡,特别是浦肯野细胞以及脑萎缩是该疾病的标志[4]。由于小脑功能对运动很重要,因此改善的临床体征和高程度震颤的显著减少可能是小脑浦肯野细胞存活的结果。
总之,AZ-3102(GCS和GbA2二者的经口可用的、高度强效(nM)抑制剂)能够渗入NPC(-/-)和野生型动物的脑中。此外,AZ-3102抑制了脑中的这些酶,如通过与载剂处理的动物相比,调节GlcCer物质,改善了临床体征,显著减少了高程度震颤,并且限制了小脑浦肯野细胞的损失所清楚地显示。
1.Loftus,S.K.,et al.,Murine model of Niemann-Pick C disease:mutationin a cholesterol homeostasis gene.Science,1997.277(5323):p.232-5.
2.Zervas,M.,K.Dobrenis,and S.U.Walkley,Neurons in Niemann-Pickdisease type C accumulate gangliosides as well as unesterified cholesteroland undergo dendritic and axonal alterations.J Neuropathol Exp Neurol,2001.60(1):p.49-64.
3.Santiago-Mujica,E.,et al.,Hepatic and neuronal phenotype of NPC1-/-mice.Heliyon,2019.5(3).
4.Vanier,M.T.,Niemann-Pick disease type C.Orphanet Journal of RareDiseases,2010.5(1):p.16.
实施例5-对患有桑德霍夫病(通过突变破坏鼠Hexb基因[Hexb(-/-)])的小鼠施用
化合物(I)的晶型的效果
对患有桑德霍夫病的小鼠施用治疗有效量的AZ-3102。初步数据表明,与治疗尼曼-匹克C型类似,患病动物的临床体征得到了改善。
Claims (15)
2.根据权利要求1所述的晶型,其中所述晶型为结晶游离碱。
3.根据权利要求1或权利要求2所述的晶型,其中所述晶型在X射线粉末衍射图中显示以2θ值表示的在17.8±0.2°处的反射,其中所述在17.8±0.2°处的反射为所述X射线粉末衍射图中的四个最强反射之一。
4.根据权利要求3所述的晶型,在X射线粉末衍射图中还显示以2θ值表示的在4.1±0.2°、8.3±0.2°、12.4±0.2°、13.6±0.2°、14.5±0.2°、14.9±0.2°、15.2±0.2°、17.2±0.2°、19.3±0.2°、21.2±0.2°、22.4±0.2°、22.9±0.2°和23.3±0.2°中的一者或更多者处的一个或更多个反射。
5.根据权利要求1至4中任一项所述的晶型:
(a)具有89℃至96℃的熔点;和/或
(b)其中所述晶型基本上不吸湿。
6.根据权利要求1或权利要求2所述的晶型,其中所述晶型在X射线粉末衍射图中显示以2θ值表示的在16.9±0.2°处的反射,其中所述在16.9±0.2°处的反射为所述X射线粉末衍射图中的四个最强反射之一,任选地其中所述晶型在X射线粉末衍射图中还显示以2θ值表示的在15.2±0.2°、16.1±0.2°、16.5±0.2°、18.9±0.2°、23.1±0.2°、25.5±0.2°、27.7±0.2°和28.5±0.2°中的一者或更多者处的一个或更多个反射。
7.一种药物组合物,包含根据权利要求1至6中任一项所述的晶型。
8.根据权利要求7所述的药物组合物,其中所述药物组合物包含在胶囊中,任选地其中所述药物组合物包含在(a)没有任何其他成分;或(b)具有至少一种可药用载体的胶囊中。
9.根据权利要求1至6中任一项所述的晶型或者根据权利要求7或权利要求8所述的药物组合物,用于在治疗中的用途。
10.根据权利要求1至6中任一项所述的晶型或者根据权利要求7或权利要求8所述的药物组合物,用于作为药物的用途。
11.根据权利要求1至6中任一项所述的晶型或者根据权利要求7或权利要求8所述的药物组合物,用于在治疗涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病中的用途,任选地其中所述涉及异常水平的葡糖神经酰胺和/或较高水平的鞘糖脂的疾病为溶酶体贮积病,例如戈谢病、法布里病、GM1神经节苷脂贮积症、GM2神经节苷脂贮积症(例如,泰-萨克斯病、桑德霍夫病或AB变异型)、唾液酸贮积症、尼曼-皮克病C型和动作性肌阵挛肾功能衰竭综合征;或者统称为代谢综合征的疾病中的一种的症状,例如肥胖、胰岛素抵抗、高脂血症、高胆固醇血症、多囊肾病、II型糖尿病和慢性炎症;或者神经退行性病症,例如帕金森病或路易体痴呆;或者动脉粥样硬化。
12.一种制备根据权利要求1至6中任一项所述的晶型的方法,包括使化合物(I)的样品与溶剂接触,任选地其中:
(a)所述溶剂选自乙腈、乙酸乙酯、异丙醇、苯甲醚、水和叔丁基甲基醚(TBME);和/或
(b)在使所述化合物(I)的样品与所述溶剂接触之前,对所述化合物(I)的样品进行纯化,任选地其中使用色谱法对所述化合物(I)的样品进行纯化。
13.一种通过进行根据权利要求12所述的方法获得的化合物(I)的晶型。
14.化合物(I)的游离碱制备晶型的用途。
15.一种制备化合物(I)的晶型的方法,包括使化合物(I)的游离碱结晶。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP20199934.9 | 2020-10-02 | ||
| EP20199934.9A EP3978474A1 (en) | 2020-10-02 | 2020-10-02 | Crystalline forms of a pharmaceutical compound |
| PCT/EP2021/077100 WO2022069709A1 (en) | 2020-10-02 | 2021-10-01 | Crystalline forms of a pharmaceutical compound |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN116390910A true CN116390910A (zh) | 2023-07-04 |
Family
ID=72744696
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202180067242.0A Pending CN116390910A (zh) | 2020-10-02 | 2021-10-01 | 药物化合物的晶型 |
Country Status (19)
| Country | Link |
|---|---|
| US (1) | US20240287001A9 (zh) |
| EP (3) | EP3978474A1 (zh) |
| JP (2) | JP2023524169A (zh) |
| KR (2) | KR102659466B1 (zh) |
| CN (1) | CN116390910A (zh) |
| AU (2) | AU2021353055B2 (zh) |
| BR (2) | BR122022018214A2 (zh) |
| CA (1) | CA3193939C (zh) |
| CL (1) | CL2023000943A1 (zh) |
| DK (1) | DK4114826T3 (zh) |
| ES (1) | ES2964105T3 (zh) |
| FI (1) | FI4114826T3 (zh) |
| IL (1) | IL301882A (zh) |
| MA (1) | MA58885B1 (zh) |
| MX (1) | MX2023003618A (zh) |
| PE (1) | PE20240138A1 (zh) |
| TW (1) | TW202229236A (zh) |
| WO (1) | WO2022069709A1 (zh) |
| ZA (1) | ZA202310184B (zh) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP4209215A1 (en) * | 2022-01-10 | 2023-07-12 | Azafaros B.V. | Treatment of gm2 gangliosidosis |
| IL314212A (en) * | 2022-01-10 | 2024-09-01 | Azafaros B V | Treatment of GM2 gangliosidosis |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015147639A1 (en) * | 2014-03-27 | 2015-10-01 | Academisch Medisch Centrum | N-(5-((aryl or heteroaryl)methyloxy)pentyl)-substituted iminosugars as inhibitors of glucosylceramide synthase |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20190195897A1 (en) * | 2015-06-24 | 2019-06-27 | Universiteit Leiden | Glycosylated metabolites |
-
2020
- 2020-10-02 EP EP20199934.9A patent/EP3978474A1/en not_active Withdrawn
-
2021
- 2021-10-01 WO PCT/EP2021/077100 patent/WO2022069709A1/en active Application Filing
- 2021-10-01 DK DK21798287.5T patent/DK4114826T3/da active
- 2021-10-01 TW TW110136766A patent/TW202229236A/zh unknown
- 2021-10-01 FI FIEP21798287.5T patent/FI4114826T3/fi active
- 2021-10-01 US US18/029,842 patent/US20240287001A9/en active Pending
- 2021-10-01 AU AU2021353055A patent/AU2021353055B2/en active Active
- 2021-10-01 MA MA58885A patent/MA58885B1/fr unknown
- 2021-10-01 EP EP21798287.5A patent/EP4114826B1/en active Active
- 2021-10-01 IL IL301882A patent/IL301882A/en unknown
- 2021-10-01 BR BR122022018214-3A patent/BR122022018214A2/pt not_active Application Discontinuation
- 2021-10-01 CA CA3193939A patent/CA3193939C/en active Active
- 2021-10-01 KR KR1020237014953A patent/KR102659466B1/ko active IP Right Grant
- 2021-10-01 EP EP23191550.5A patent/EP4295847A3/en active Pending
- 2021-10-01 BR BR112022018020-9A patent/BR112022018020B1/pt active IP Right Grant
- 2021-10-01 PE PE2023001212A patent/PE20240138A1/es unknown
- 2021-10-01 KR KR1020247012671A patent/KR20240056628A/ko active Application Filing
- 2021-10-01 JP JP2022577645A patent/JP2023524169A/ja active Pending
- 2021-10-01 CN CN202180067242.0A patent/CN116390910A/zh active Pending
- 2021-10-01 MX MX2023003618A patent/MX2023003618A/es unknown
- 2021-10-01 ES ES21798287T patent/ES2964105T3/es active Active
-
2022
- 2022-12-20 AU AU2022291486A patent/AU2022291486B2/en active Active
-
2023
- 2023-03-30 CL CL2023000943A patent/CL2023000943A1/es unknown
- 2023-10-30 ZA ZA2023/10184A patent/ZA202310184B/en unknown
-
2024
- 2024-02-02 JP JP2024015037A patent/JP2024054192A/ja active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015147639A1 (en) * | 2014-03-27 | 2015-10-01 | Academisch Medisch Centrum | N-(5-((aryl or heteroaryl)methyloxy)pentyl)-substituted iminosugars as inhibitors of glucosylceramide synthase |
Non-Patent Citations (2)
| Title |
|---|
| AMAR T. GHISAIDOOBE 等: "Identification and Development of Biphenyl Substituted Iminosugars as Improved Dual Glucosylceramide Synthase/Neutral Glucosylceramidase Inhibitors", JOURNAL OF MEDICINAL CHEMISTRY, vol. 57, no. 21, pages 9096 - 9104, XP055192380, DOI: 10.1021/jm501181z * |
| LAHAV DANIEL 等: "upporting Information A Fluorescence Polarization Activity-Based Protein Profiling Assay in the Discovery of Potent,Selective Inhibitors for Human Non-lysosomal Glucosylceramidase", JOURNAL OF THE AMERICAN CHEMICAL SOCIETY, pages 1 * |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2020189873A (ja) | グルコシルセラミドシンターゼの阻害剤としての非晶質及び結晶型のgenz112638ヘミ酒石酸塩 | |
| AU2022291486B2 (en) | Crystalline forms of a pharmaceutical compound | |
| US9662317B2 (en) | Methods of administering tolperisone for therapeutic purposes | |
| US20100021547A1 (en) | Pharmaceutical composition for piperidinoalkanol compounds | |
| US7423040B2 (en) | Stable crystalline form of bifeprunox mesylate, dosage forms thereof and methods for using same | |
| EA019819B1 (ru) | Кристаллическая полиморфная форма с ингибитора белка, активирующего 5-липоксигеназу, фармацевтическая композиция на ее основе и применение в лечении | |
| EP3505515B1 (en) | Crystals of cyclic amine derivative and pharmaceutical use thereof | |
| US7964604B2 (en) | Bifeprunox mesylate maintenance dose compositions and methods for using the same | |
| NZ798892B2 (en) | Crystalline forms of a pharmaceutical compound | |
| US10519157B2 (en) | Deuterated compounds for treating Fabry, Gaucher, Parkinson's and related diseases and conditions, and compositions and methods thereof | |
| EA045552B1 (ru) | Кристаллические формы фармацевтического соединения | |
| Lahiri et al. | Differential effects of two hexahydropyrroloindole carbamate-based anticholinesterase drugs on the amyloid beta protein pathway involved in Alzheimer disease | |
| US20230010368A1 (en) | Crystalline form of acetylcholinesterase inhibitor and preparation method therefor and application thereof | |
| TW202342414A (zh) | 環己烯酮化合物之結晶形 | |
| TW202337456A (zh) | Gm2神經節苷脂症之治療 | |
| CN118632693A (zh) | Gm2神经节苷脂贮积症的治疗 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |