CN115551509A - 包含craf抑制剂的治疗组合 - Google Patents
包含craf抑制剂的治疗组合 Download PDFInfo
- Publication number
- CN115551509A CN115551509A CN202180034241.6A CN202180034241A CN115551509A CN 115551509 A CN115551509 A CN 115551509A CN 202180034241 A CN202180034241 A CN 202180034241A CN 115551509 A CN115551509 A CN 115551509A
- Authority
- CN
- China
- Prior art keywords
- melanoma
- compound
- administered
- pharmaceutically acceptable
- acceptable salt
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000003112 inhibitor Substances 0.000 title claims abstract description 21
- 102100033479 RAF proto-oncogene serine/threonine-protein kinase Human genes 0.000 title claims abstract description 14
- 101100523539 Mus musculus Raf1 gene Proteins 0.000 title abstract description 6
- 230000001225 therapeutic effect Effects 0.000 title description 14
- 201000001441 melanoma Diseases 0.000 claims abstract description 272
- 238000011282 treatment Methods 0.000 claims abstract description 147
- 150000003839 salts Chemical class 0.000 claims abstract description 89
- 101000984753 Homo sapiens Serine/threonine-protein kinase B-raf Proteins 0.000 claims abstract description 81
- 102100027103 Serine/threonine-protein kinase B-raf Human genes 0.000 claims abstract description 81
- 206010027480 Metastatic malignant melanoma Diseases 0.000 claims abstract description 27
- 208000021039 metastatic melanoma Diseases 0.000 claims abstract description 27
- 239000002829 mitogen activated protein kinase inhibitor Substances 0.000 claims abstract description 10
- 229940124647 MEK inhibitor Drugs 0.000 claims abstract description 9
- 229940124297 CDK 4/6 inhibitor Drugs 0.000 claims abstract description 5
- 102100039788 GTPase NRas Human genes 0.000 claims abstract 20
- 101000744505 Homo sapiens GTPase NRas Proteins 0.000 claims abstract 20
- 150000001875 compounds Chemical class 0.000 claims description 267
- LIRYPHYGHXZJBZ-UHFFFAOYSA-N trametinib Chemical compound CC(=O)NC1=CC=CC(N2C(N(C3CC3)C(=O)C3=C(NC=4C(=CC(I)=CC=4)F)N(C)C(=O)C(C)=C32)=O)=C1 LIRYPHYGHXZJBZ-UHFFFAOYSA-N 0.000 claims description 97
- 229960004066 trametinib Drugs 0.000 claims description 95
- 239000003814 drug Substances 0.000 claims description 87
- 230000004044 response Effects 0.000 claims description 76
- 238000000034 method Methods 0.000 claims description 69
- 229940124597 therapeutic agent Drugs 0.000 claims description 64
- RHXHGRAEPCAFML-UHFFFAOYSA-N 7-cyclopentyl-n,n-dimethyl-2-[(5-piperazin-1-ylpyridin-2-yl)amino]pyrrolo[2,3-d]pyrimidine-6-carboxamide Chemical compound N1=C2N(C3CCCC3)C(C(=O)N(C)C)=CC2=CN=C1NC(N=C1)=CC=C1N1CCNCC1 RHXHGRAEPCAFML-UHFFFAOYSA-N 0.000 claims description 59
- 229950003687 ribociclib Drugs 0.000 claims description 55
- 239000003795 chemical substances by application Substances 0.000 claims description 54
- 230000004083 survival effect Effects 0.000 claims description 46
- 238000002560 therapeutic procedure Methods 0.000 claims description 43
- 239000012453 solvate Substances 0.000 claims description 35
- 230000000694 effects Effects 0.000 claims description 34
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 claims description 30
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 30
- 230000002411 adverse Effects 0.000 claims description 25
- 230000035772 mutation Effects 0.000 claims description 24
- 201000010099 disease Diseases 0.000 claims description 23
- 230000001394 metastastic effect Effects 0.000 claims description 23
- 206010061289 metastatic neoplasm Diseases 0.000 claims description 23
- 208000030381 cutaneous melanoma Diseases 0.000 claims description 22
- 201000003708 skin melanoma Diseases 0.000 claims description 22
- FDKXTQMXEQVLRF-ZHACJKMWSA-N (E)-dacarbazine Chemical compound CN(C)\N=N\c1[nH]cnc1C(N)=O FDKXTQMXEQVLRF-ZHACJKMWSA-N 0.000 claims description 16
- 229960003901 dacarbazine Drugs 0.000 claims description 16
- 238000002648 combination therapy Methods 0.000 claims description 14
- 229940076838 Immune checkpoint inhibitor Drugs 0.000 claims description 11
- 239000012274 immune-checkpoint protein inhibitor Substances 0.000 claims description 11
- 238000009169 immunotherapy Methods 0.000 claims description 11
- 229960005386 ipilimumab Drugs 0.000 claims description 11
- 229960003301 nivolumab Drugs 0.000 claims description 10
- 229960002621 pembrolizumab Drugs 0.000 claims description 10
- 238000002626 targeted therapy Methods 0.000 claims description 10
- YFCIFWOJYYFDQP-PTWZRHHISA-N 4-[3-amino-6-[(1S,3S,4S)-3-fluoro-4-hydroxycyclohexyl]pyrazin-2-yl]-N-[(1S)-1-(3-bromo-5-fluorophenyl)-2-(methylamino)ethyl]-2-fluorobenzamide Chemical compound CNC[C@@H](NC(=O)c1ccc(cc1F)-c1nc(cnc1N)[C@H]1CC[C@H](O)[C@@H](F)C1)c1cc(F)cc(Br)c1 YFCIFWOJYYFDQP-PTWZRHHISA-N 0.000 claims description 9
- BFSMGDJOXZAERB-UHFFFAOYSA-N dabrafenib Chemical compound S1C(C(C)(C)C)=NC(C=2C(=C(NS(=O)(=O)C=3C(=CC=CC=3F)F)C=CC=2)F)=C1C1=CC=NC(N)=N1 BFSMGDJOXZAERB-UHFFFAOYSA-N 0.000 claims description 9
- 229960002465 dabrafenib Drugs 0.000 claims description 9
- 230000009467 reduction Effects 0.000 claims description 9
- 150000003890 succinate salts Chemical class 0.000 claims description 9
- QCQCHGYLTSGIGX-GHXANHINSA-N 4-[[(3ar,5ar,5br,7ar,9s,11ar,11br,13as)-5a,5b,8,8,11a-pentamethyl-3a-[(5-methylpyridine-3-carbonyl)amino]-2-oxo-1-propan-2-yl-4,5,6,7,7a,9,10,11,11b,12,13,13a-dodecahydro-3h-cyclopenta[a]chrysen-9-yl]oxy]-2,2-dimethyl-4-oxobutanoic acid Chemical compound N([C@@]12CC[C@@]3(C)[C@]4(C)CC[C@H]5C(C)(C)[C@@H](OC(=O)CC(C)(C)C(O)=O)CC[C@]5(C)[C@H]4CC[C@@H]3C1=C(C(C2)=O)C(C)C)C(=O)C1=CN=CC(C)=C1 QCQCHGYLTSGIGX-GHXANHINSA-N 0.000 claims description 8
- 230000000747 cardiac effect Effects 0.000 claims description 8
- CBQGYUDMJHNJBX-RTBURBONSA-N reboxetine Chemical compound CCOC1=CC=CC=C1O[C@H](C=1C=CC=CC=1)[C@@H]1OCCNC1 CBQGYUDMJHNJBX-RTBURBONSA-N 0.000 claims description 8
- 229960003770 reboxetine Drugs 0.000 claims description 8
- 238000002512 chemotherapy Methods 0.000 claims description 7
- 238000011260 co-administration Methods 0.000 claims description 7
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 claims description 6
- 231100000419 toxicity Toxicity 0.000 claims description 5
- 230000001988 toxicity Effects 0.000 claims description 5
- 102000008096 B7-H1 Antigen Human genes 0.000 claims description 4
- 108010074708 B7-H1 Antigen Proteins 0.000 claims description 4
- 229940045513 CTLA4 antagonist Drugs 0.000 claims description 4
- 102100031480 Dual specificity mitogen-activated protein kinase kinase 1 Human genes 0.000 claims description 4
- 101710146526 Dual specificity mitogen-activated protein kinase kinase 1 Proteins 0.000 claims description 4
- 102000004232 Mitogen-Activated Protein Kinase Kinases Human genes 0.000 claims description 3
- 108090000744 Mitogen-Activated Protein Kinase Kinases Proteins 0.000 claims description 3
- 206010059516 Skin toxicity Diseases 0.000 claims description 3
- 229940127089 cytotoxic agent Drugs 0.000 claims description 3
- 239000002254 cytotoxic agent Substances 0.000 claims description 3
- 231100000599 cytotoxic agent Toxicity 0.000 claims description 3
- 229960004857 mitomycin Drugs 0.000 claims description 3
- OSTGTTZJOCZWJG-UHFFFAOYSA-N nitrosourea Chemical compound NC(=O)N=NO OSTGTTZJOCZWJG-UHFFFAOYSA-N 0.000 claims description 3
- 230000002829 reductive effect Effects 0.000 claims description 3
- 231100000438 skin toxicity Toxicity 0.000 claims description 3
- 206010012735 Diarrhoea Diseases 0.000 claims description 2
- 206010059024 Gastrointestinal toxicity Diseases 0.000 claims description 2
- 229950009791 durvalumab Drugs 0.000 claims description 2
- 231100000414 gastrointestinal toxicity Toxicity 0.000 claims description 2
- 229950010773 pidilizumab Drugs 0.000 claims description 2
- 102220198027 rs121434595 Human genes 0.000 claims 1
- 102200124916 rs121434596 Human genes 0.000 claims 1
- 102200124918 rs121913250 Human genes 0.000 claims 1
- 102220195076 rs121913255 Human genes 0.000 claims 1
- 239000012824 ERK inhibitor Substances 0.000 abstract 1
- 206010028980 Neoplasm Diseases 0.000 description 125
- 241000699670 Mus sp. Species 0.000 description 39
- 229940126062 Compound A Drugs 0.000 description 26
- NLDMNSXOCDLTTB-UHFFFAOYSA-N Heterophylliin A Natural products O1C2COC(=O)C3=CC(O)=C(O)C(O)=C3C3=C(O)C(O)=C(O)C=C3C(=O)OC2C(OC(=O)C=2C=C(O)C(O)=C(O)C=2)C(O)C1OC(=O)C1=CC(O)=C(O)C(O)=C1 NLDMNSXOCDLTTB-UHFFFAOYSA-N 0.000 description 26
- 230000008859 change Effects 0.000 description 26
- LVTJOONKWUXEFR-FZRMHRINSA-N protoneodioscin Natural products O(C[C@@H](CC[C@]1(O)[C@H](C)[C@@H]2[C@]3(C)[C@H]([C@H]4[C@@H]([C@]5(C)C(=CC4)C[C@@H](O[C@@H]4[C@H](O[C@H]6[C@@H](O)[C@@H](O)[C@@H](O)[C@H](C)O6)[C@@H](O)[C@H](O[C@H]6[C@@H](O)[C@@H](O)[C@@H](O)[C@H](C)O6)[C@H](CO)O4)CC5)CC3)C[C@@H]2O1)C)[C@H]1[C@H](O)[C@H](O)[C@H](O)[C@@H](CO)O1 LVTJOONKWUXEFR-FZRMHRINSA-N 0.000 description 25
- 239000000203 mixture Substances 0.000 description 22
- 229940079593 drug Drugs 0.000 description 19
- UEPXBTCUIIGYCY-UHFFFAOYSA-N n-[3-[2-(2-hydroxyethoxy)-6-morpholin-4-ylpyridin-4-yl]-4-methylphenyl]-2-(trifluoromethyl)pyridine-4-carboxamide Chemical compound C1=C(C=2C=C(N=C(OCCO)C=2)N2CCOCC2)C(C)=CC=C1NC(=O)C1=CC=NC(C(F)(F)F)=C1 UEPXBTCUIIGYCY-UHFFFAOYSA-N 0.000 description 18
- 102200006525 rs121913240 Human genes 0.000 description 18
- 239000003981 vehicle Substances 0.000 description 18
- 230000000259 anti-tumor effect Effects 0.000 description 17
- 241001465754 Metazoa Species 0.000 description 16
- 239000004480 active ingredient Substances 0.000 description 15
- 230000037396 body weight Effects 0.000 description 15
- 210000004027 cell Anatomy 0.000 description 14
- 102200006648 rs28933406 Human genes 0.000 description 14
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 12
- 108020004705 Codon Proteins 0.000 description 11
- 238000012360 testing method Methods 0.000 description 11
- 239000008194 pharmaceutical composition Substances 0.000 description 10
- 230000009286 beneficial effect Effects 0.000 description 9
- 230000037361 pathway Effects 0.000 description 9
- 239000002552 dosage form Substances 0.000 description 8
- 238000011156 evaluation Methods 0.000 description 8
- 238000009472 formulation Methods 0.000 description 8
- 230000004614 tumor growth Effects 0.000 description 8
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 8
- 102000043136 MAP kinase family Human genes 0.000 description 7
- 108091054455 MAP kinase family Proteins 0.000 description 7
- 238000004458 analytical method Methods 0.000 description 7
- 208000035475 disorder Diseases 0.000 description 7
- 208000024891 symptom Diseases 0.000 description 7
- 238000013413 tumor xenograft mouse model Methods 0.000 description 7
- 206010061818 Disease progression Diseases 0.000 description 6
- 230000006023 anti-tumor response Effects 0.000 description 6
- 230000008901 benefit Effects 0.000 description 6
- 201000011510 cancer Diseases 0.000 description 6
- 230000005750 disease progression Effects 0.000 description 6
- 239000000546 pharmaceutical excipient Substances 0.000 description 6
- 238000002360 preparation method Methods 0.000 description 6
- 208000037821 progressive disease Diseases 0.000 description 6
- 239000003826 tablet Substances 0.000 description 6
- 102000007665 Extracellular Signal-Regulated MAP Kinases Human genes 0.000 description 5
- 108010007457 Extracellular Signal-Regulated MAP Kinases Proteins 0.000 description 5
- 102000003855 L-lactate dehydrogenase Human genes 0.000 description 5
- 108700023483 L-lactate dehydrogenases Proteins 0.000 description 5
- 241000699660 Mus musculus Species 0.000 description 5
- 239000002775 capsule Substances 0.000 description 5
- 238000007405 data analysis Methods 0.000 description 5
- 230000002401 inhibitory effect Effects 0.000 description 5
- 230000000977 initiatory effect Effects 0.000 description 5
- 238000011580 nude mouse model Methods 0.000 description 5
- 239000006186 oral dosage form Substances 0.000 description 5
- 230000004580 weight loss Effects 0.000 description 5
- 238000013298 xenograft nude mouse model Methods 0.000 description 5
- 108700024394 Exon Proteins 0.000 description 4
- 229920002565 Polyethylene Glycol 400 Polymers 0.000 description 4
- 229920002690 Polyoxyl 40 HydrogenatedCastorOil Polymers 0.000 description 4
- 230000033228 biological regulation Effects 0.000 description 4
- 238000011284 combination treatment Methods 0.000 description 4
- 239000012050 conventional carrier Substances 0.000 description 4
- 239000003937 drug carrier Substances 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 235000013305 food Nutrition 0.000 description 4
- 230000003902 lesion Effects 0.000 description 4
- 230000036961 partial effect Effects 0.000 description 4
- 102000016914 ras Proteins Human genes 0.000 description 4
- 102200055464 rs113488022 Human genes 0.000 description 4
- 238000009097 single-agent therapy Methods 0.000 description 4
- 230000002195 synergetic effect Effects 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- 230000003442 weekly effect Effects 0.000 description 4
- 101100005789 Caenorhabditis elegans cdk-4 gene Proteins 0.000 description 3
- 102100030708 GTPase KRas Human genes 0.000 description 3
- 206010027476 Metastases Diseases 0.000 description 3
- 241000699666 Mus <mouse, genus> Species 0.000 description 3
- 102000007530 Neurofibromin 1 Human genes 0.000 description 3
- 108010085793 Neurofibromin 1 Proteins 0.000 description 3
- 102100040678 Programmed cell death protein 1 Human genes 0.000 description 3
- 101710089372 Programmed cell death protein 1 Proteins 0.000 description 3
- 230000003213 activating effect Effects 0.000 description 3
- 238000001574 biopsy Methods 0.000 description 3
- 210000003169 central nervous system Anatomy 0.000 description 3
- 239000002285 corn oil Substances 0.000 description 3
- 235000005687 corn oil Nutrition 0.000 description 3
- 230000034994 death Effects 0.000 description 3
- 231100000517 death Toxicity 0.000 description 3
- 239000012153 distilled water Substances 0.000 description 3
- 125000005456 glyceride group Chemical group 0.000 description 3
- 238000009396 hybridization Methods 0.000 description 3
- 230000006872 improvement Effects 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 238000002826 magnetic-activated cell sorting Methods 0.000 description 3
- 230000002062 proliferating effect Effects 0.000 description 3
- 230000000644 propagated effect Effects 0.000 description 3
- 108090000623 proteins and genes Proteins 0.000 description 3
- 208000004644 retinal vein occlusion Diseases 0.000 description 3
- 102200007373 rs17851045 Human genes 0.000 description 3
- 238000012216 screening Methods 0.000 description 3
- 210000004911 serous fluid Anatomy 0.000 description 3
- 230000000087 stabilizing effect Effects 0.000 description 3
- 238000007619 statistical method Methods 0.000 description 3
- 238000006467 substitution reaction Methods 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 230000002459 sustained effect Effects 0.000 description 3
- 230000009885 systemic effect Effects 0.000 description 3
- 238000009121 systemic therapy Methods 0.000 description 3
- 229940083114 trametinib 0.5 mg Drugs 0.000 description 3
- 229940083093 trametinib 1 mg Drugs 0.000 description 3
- WZFUQSJFWNHZHM-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)CC(=O)N1CC2=C(CC1)NN=N2 WZFUQSJFWNHZHM-UHFFFAOYSA-N 0.000 description 2
- ZKHQWZAMYRWXGA-KQYNXXCUSA-J ATP(4-) Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](COP([O-])(=O)OP([O-])(=O)OP([O-])([O-])=O)[C@@H](O)[C@H]1O ZKHQWZAMYRWXGA-KQYNXXCUSA-J 0.000 description 2
- ZKHQWZAMYRWXGA-UHFFFAOYSA-N Adenosine triphosphate Natural products C1=NC=2C(N)=NC=NC=2N1C1OC(COP(O)(=O)OP(O)(=O)OP(O)(O)=O)C(O)C1O ZKHQWZAMYRWXGA-UHFFFAOYSA-N 0.000 description 2
- 229940125431 BRAF inhibitor Drugs 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 108010058546 Cyclin D1 Proteins 0.000 description 2
- 208000010201 Exanthema Diseases 0.000 description 2
- 102100024165 G1/S-specific cyclin-D1 Human genes 0.000 description 2
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 108091000080 Phosphotransferase Proteins 0.000 description 2
- 229940124639 Selective inhibitor Drugs 0.000 description 2
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 2
- 230000005856 abnormality Effects 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- -1 coatings Substances 0.000 description 2
- 230000006552 constitutive activation Effects 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 230000009977 dual effect Effects 0.000 description 2
- 201000005884 exanthem Diseases 0.000 description 2
- 230000007717 exclusion Effects 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 235000013922 glutamic acid Nutrition 0.000 description 2
- 239000004220 glutamic acid Substances 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 230000001024 immunotherapeutic effect Effects 0.000 description 2
- 238000002513 implantation Methods 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 238000012002 interactive response technology Methods 0.000 description 2
- 210000004185 liver Anatomy 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 108010082117 matrigel Proteins 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 230000009401 metastasis Effects 0.000 description 2
- 238000010172 mouse model Methods 0.000 description 2
- 239000002105 nanoparticle Substances 0.000 description 2
- 102000020233 phosphotransferase Human genes 0.000 description 2
- 239000006187 pill Substances 0.000 description 2
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 2
- 229920000053 polysorbate 80 Polymers 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 235000018102 proteins Nutrition 0.000 description 2
- 102000004169 proteins and genes Human genes 0.000 description 2
- 150000003254 radicals Chemical class 0.000 description 2
- 108010014186 ras Proteins Proteins 0.000 description 2
- 206010037844 rash Diseases 0.000 description 2
- 102200006532 rs112445441 Human genes 0.000 description 2
- 102200006533 rs121913535 Human genes 0.000 description 2
- 230000011664 signaling Effects 0.000 description 2
- 150000003384 small molecules Chemical class 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical class CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 2
- 238000012384 transportation and delivery Methods 0.000 description 2
- 210000004881 tumor cell Anatomy 0.000 description 2
- 229960005486 vaccine Drugs 0.000 description 2
- 239000004474 valine Substances 0.000 description 2
- 229930024421 Adenine Natural products 0.000 description 1
- GFFGJBXGBJISGV-UHFFFAOYSA-N Adenine Chemical compound NC1=NC=NC2=C1N=CN2 GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 1
- 206010001488 Aggression Diseases 0.000 description 1
- 201000004384 Alopecia Diseases 0.000 description 1
- 208000031648 Body Weight Changes Diseases 0.000 description 1
- 208000020446 Cardiac disease Diseases 0.000 description 1
- 108010058545 Cyclin D3 Proteins 0.000 description 1
- 108010025468 Cyclin-Dependent Kinase 6 Proteins 0.000 description 1
- 102100026804 Cyclin-dependent kinase 6 Human genes 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 241001069765 Fridericia <angiosperm> Species 0.000 description 1
- 102100037859 G1/S-specific cyclin-D3 Human genes 0.000 description 1
- 102100029974 GTPase HRas Human genes 0.000 description 1
- 208000010412 Glaucoma Diseases 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 239000012981 Hank's balanced salt solution Substances 0.000 description 1
- 101000584633 Homo sapiens GTPase HRas Proteins 0.000 description 1
- 102000037984 Inhibitory immune checkpoint proteins Human genes 0.000 description 1
- 108091008026 Inhibitory immune checkpoint proteins Proteins 0.000 description 1
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 1
- 230000005723 MEK inhibition Effects 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- 241000204031 Mycoplasma Species 0.000 description 1
- 241000202944 Mycoplasma sp. Species 0.000 description 1
- 206010030043 Ocular hypertension Diseases 0.000 description 1
- 108700020796 Oncogene Proteins 0.000 description 1
- 206010033109 Ototoxicity Diseases 0.000 description 1
- 238000002944 PCR assay Methods 0.000 description 1
- 102000009516 Protein Serine-Threonine Kinases Human genes 0.000 description 1
- 108010009341 Protein Serine-Threonine Kinases Proteins 0.000 description 1
- 108010091528 Proto-Oncogene Proteins B-raf Proteins 0.000 description 1
- 102000018471 Proto-Oncogene Proteins B-raf Human genes 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 206010040914 Skin reaction Diseases 0.000 description 1
- 206010049418 Sudden Cardiac Death Diseases 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- 206010047700 Vomiting Diseases 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 239000003070 absorption delaying agent Substances 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 238000011374 additional therapy Methods 0.000 description 1
- 229960000643 adenine Drugs 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 238000009098 adjuvant therapy Methods 0.000 description 1
- 230000016571 aggressive behavior Effects 0.000 description 1
- 208000012761 aggressive behavior Diseases 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 231100000360 alopecia Toxicity 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 239000005557 antagonist Substances 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000003127 anti-melanomic effect Effects 0.000 description 1
- 230000001028 anti-proliverative effect Effects 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 238000011717 athymic nude mouse Methods 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 229950003054 binimetinib Drugs 0.000 description 1
- ACWZRVQXLIRSDF-UHFFFAOYSA-N binimetinib Chemical compound OCCONC(=O)C=1C=C2N(C)C=NC2=C(F)C=1NC1=CC=C(Br)C=C1F ACWZRVQXLIRSDF-UHFFFAOYSA-N 0.000 description 1
- 229960000074 biopharmaceutical Drugs 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 230000036765 blood level Effects 0.000 description 1
- 230000004579 body weight change Effects 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- 101150048834 braF gene Proteins 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 230000001364 causal effect Effects 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- BSMCAPRUBJMWDF-KRWDZBQOSA-N cobimetinib Chemical compound C1C(O)([C@H]2NCCCC2)CN1C(=O)C1=CC=C(F)C(F)=C1NC1=CC=C(I)C=C1F BSMCAPRUBJMWDF-KRWDZBQOSA-N 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 230000002860 competitive effect Effects 0.000 description 1
- 238000002591 computed tomography Methods 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 235000021438 curry Nutrition 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 239000000539 dimer Substances 0.000 description 1
- 230000008034 disappearance Effects 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 239000002612 dispersion medium Substances 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 125000000291 glutamic acid group Chemical group N[C@@H](CCC(O)=O)C(=O)* 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 238000005469 granulation Methods 0.000 description 1
- 230000003179 granulation Effects 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 238000013415 human tumor xenograft model Methods 0.000 description 1
- 150000003840 hydrochlorides Chemical class 0.000 description 1
- 229940091204 imlygic Drugs 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000000099 in vitro assay Methods 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 239000007951 isotonicity adjuster Substances 0.000 description 1
- 230000000366 juvenile effect Effects 0.000 description 1
- 230000003907 kidney function Effects 0.000 description 1
- 229940043355 kinase inhibitor Drugs 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 230000003908 liver function Effects 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 210000001165 lymph node Anatomy 0.000 description 1
- 238000007403 mPCR Methods 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 238000007726 management method Methods 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 229940083118 mekinist Drugs 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 229940125374 mitogen-activated extracellular signal-regulated kinase inhibitor Drugs 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 229940073213 naporafenib Drugs 0.000 description 1
- 230000000926 neurological effect Effects 0.000 description 1
- 238000007481 next generation sequencing Methods 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 238000012316 non-parametric ANOVA Methods 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- 201000002575 ocular melanoma Diseases 0.000 description 1
- 230000005853 oncogenic activation Effects 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 231100000262 ototoxicity Toxicity 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- JLFNLZLINWHATN-UHFFFAOYSA-N pentaethylene glycol Chemical compound OCCOCCOCCOCCOCCO JLFNLZLINWHATN-UHFFFAOYSA-N 0.000 description 1
- 229940124531 pharmaceutical excipient Drugs 0.000 description 1
- 230000003285 pharmacodynamic effect Effects 0.000 description 1
- 230000009038 pharmacological inhibition Effects 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 1
- 230000036470 plasma concentration Effects 0.000 description 1
- 229920001992 poloxamer 407 Polymers 0.000 description 1
- 238000010149 post-hoc-test Methods 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 238000004393 prognosis Methods 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 230000009993 protective function Effects 0.000 description 1
- GHBFNMLVSPCDGN-UHFFFAOYSA-N rac-1-monooctanoylglycerol Chemical compound CCCCCCCC(=O)OCC(O)CO GHBFNMLVSPCDGN-UHFFFAOYSA-N 0.000 description 1
- 230000000306 recurrent effect Effects 0.000 description 1
- 230000002336 repolarization Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 238000002271 resection Methods 0.000 description 1
- 229960004641 rituximab Drugs 0.000 description 1
- 102220014333 rs112445441 Human genes 0.000 description 1
- 102220198096 rs121913238 Human genes 0.000 description 1
- 102200006531 rs121913529 Human genes 0.000 description 1
- 102200006537 rs121913529 Human genes 0.000 description 1
- 102200006539 rs121913529 Human genes 0.000 description 1
- 102200006538 rs121913530 Human genes 0.000 description 1
- 102200006541 rs121913530 Human genes 0.000 description 1
- 102220197834 rs121913535 Human genes 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 238000004904 shortening Methods 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 231100000161 signs of toxicity Toxicity 0.000 description 1
- 231100000430 skin reaction Toxicity 0.000 description 1
- 230000035483 skin reaction Effects 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000011272 standard treatment Methods 0.000 description 1
- 238000010972 statistical evaluation Methods 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- 239000007940 sugar coated tablet Substances 0.000 description 1
- 238000009495 sugar coating Methods 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 201000005665 thrombophilia Diseases 0.000 description 1
- 229940113082 thymine Drugs 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- 239000000107 tumor biomarker Substances 0.000 description 1
- 150000003680 valines Chemical class 0.000 description 1
- 230000002861 ventricular Effects 0.000 description 1
- 238000011179 visual inspection Methods 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 150000003722 vitamin derivatives Chemical class 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
Abstract
本发明提供了药物组合,其包含CRAF抑制剂与以下的组合:(i)ERK抑制剂或(ii)MEK抑制剂或(iii)CDK4/6抑制剂,每种如本文所定义,或独立地在每种情况下,其药学上可接受的盐,用于在治疗NRAS突变型黑素瘤和在治疗BRAF突变型黑素瘤中使用,其中该黑素瘤可以是不可切除的和/或转移性的黑素瘤。
Description
技术领域
本发明提供了药物组合,其包含如本文所定义的纳波拉非尼布(naporafenib)(具有式(I)的化合物或化合物A)、或其药学上可接受的盐,以及选自由以下组成的组的第二治疗剂:(i)4-(3-氨基-6-((1S,3S,4S)-3-氟-4-羟基环己基)吡嗪-2-基)-N-((S)-1-(3-溴-5-氟苯基)-2-(甲氨基)乙基)-2-氟苯甲酰胺(里内特基布(rineterkib)或化合物B)、或其药学上可接受的盐,(ii)曲美替尼(化合物C)、或其药学上可接受的盐或溶剂化物(特别是其DMSO溶剂化物),以及(iii)瑞博西尼(化合物D)、或其药学上可接受的盐(特别是其琥珀酸盐),用于在治疗以下疾病中使用:NRAS突变型黑素瘤和/或BRAF突变型黑素瘤,尤其是不可切除的或转移性的NRAS突变型黑素瘤、和/或不可切除的或转移性的BRAF突变型黑素瘤,如下文进一步描述。
本发明还提供了药物组合,其包含(i)纳波拉非尼布和里内特基布;(ii)纳波拉非尼布和曲美替尼;或(iii)纳波拉非尼布和瑞博西尼;其中制备和/或使用两种化合物(或用于用途)(其中该用途是如上文或下文所定义),用于同时、分开或顺序施用来治疗相应的黑素瘤,以及用于包含这样的组合的药物组合物;治疗患有所述黑素瘤的患者的方法,该方法包括向有需要的患者施用治疗有效量的该组合或组合物;这样的组合或组合物用于治疗所述黑素瘤的用途;以及包含这样的组合的商业包装物,尤其是用于如上文或下文所定义的用途,并且优选地包括此类用途的说明书。
本发明还提供了纳波拉非尼布、里内特基布、曲美替尼或瑞博西尼,用于在治疗如本文所述的黑素瘤中使用,其中该治疗进一步包括施用本发明的药物组合中的其他组合配伍物。
背景技术
黑素瘤是所有皮肤黑素瘤中最具有攻击性的形式。黑素瘤的全球发病率是大约160,000个新病例/年,其中48,000例死亡(Ciurea A.(2016)Epidemiology and ClinicalCharacteristics of Melanoma[黑素瘤的流行病学和临床特征].在以下文献中:Torres-Cabala C.,Curry J.(编辑)Genetics of Melanoma.[黑素瘤的遗传学]MelanomaGenetics.[黑素瘤遗传学],施普林格出版公司(Springer),纽约,纽约州)。
RAS/RAF/MEK/ERK或MAPK途径是驱动细胞增殖、分化和存活的关键信号传导级联。RAS蛋白是GTP酶的超家族,其包括KRAS连同NRAS和HRAS。
在黑素瘤中,MAPK途径的激活是至关重要的。可以将黑素瘤基于它们的主要遗传驱动基因分组为分子亚型。
黑素瘤中MAPK途径的致癌激活的最常见机制是经由突变,BRAF激酶的t组成性激活,这发生在约40%-60%的病例中。BRAF编码细胞质丝氨酸苏氨酸激酶。在黑素瘤中超过97%的BRAF突变位于BRAF基因的密码子600中。V600E突变编码缬氨酸到谷氨酸的取代,从而暴露出BRAF的活性位点,从而使其能够独立于RAS地作为单体或二聚体进行组成型激活。在表达野生型BRAF的黑素瘤细胞中,或在BRAFV600驱动的黑素瘤患者的正常细胞中,抑制剂(例如维莫非尼)反常激活RAF信号传导。
BRAF(尤其是BRAFV600)突变阳性不可切除的或转移性的黑素瘤是具有差的总生存期的侵袭性恶性肿瘤。根据不可切除的和/或转移性的黑素瘤的当前管理,一线治疗选项包括抗PD-1单一疗法(派姆单抗或纳武单抗)或其组合,例如派姆单抗和伊匹单抗或纳武单抗和伊匹单抗。对于具有BRAFV600激活突变的患者,将组合的BRAF和MEK抑制剂,例如达拉菲尼和曲美替尼、维莫非尼和考美替尼、以及恩拉非尼和比美替尼用作一线或二线治疗。然而,患者通常关于这些疗法有进展,并且当前在进展后,不存在标准治疗方案。
在黑素瘤中第二最常见的MAPK途径异常是突变的NRAS,发生在约15%-20%的病例中。在黑色素瘤中,NRAS中的大多数激活性变异都发生在密码子61上,而密码子12和13上的变异发生频率较低(Gao等人,Sci Signal[科学信号],2013;van Elsas,Recent ResultsMelanoma Res[黑素瘤研究最新结果],1995)。NRAS突变型黑素瘤表现出侵袭性行为,在初次诊断时已经存在高肝和脑转移率(Bergamasco等人,2016)并且因此预后较差。
NRAS的选择性药理抑制仍然存在技术上的挑战性,因为迄今为止,针对其GTP酶活性一直未能成功设计出特异性小分子拮抗剂。此外,不存在特异性针对NRAS突变型黑素瘤的确定疗法,并且对标准护理化学疗法(例如达卡巴嗪(dacarbazine))的应答是非常有限的。一项3期研究表明,与使用达卡巴嗪的标准护理化学疗法相比,MEK抑制剂比美替尼有一些益处,例如总体应答率从7%改善至15%。然而,怀疑与研究药物相关的由不良事件引起的中止率很高(20%对比5%),并且无进展生存期(PFS)方面的益处并不转化为总生存期方面的改善(Dummer等人,Binimetinib versus dacarbazine in patients with advancedNRAS-mutant melanoma(NEMO):a multicentre,open-label,randomised,phase 3 trial[患有晚期NRAS突变型黑素瘤的患者中的比美替尼对比达卡巴嗪(NEMO)一项多中心、开放标签、随机3期试验];Dummer R.等人;Lancet Oncology[柳叶刀肿瘤学]卷18:4;435-445;2017)。
发明内容
因此,对于患有NRAS突变型黑素瘤和BRAF突变型黑素瘤的患者,特别是对于NRAS突变型黑素瘤,存在高度未满足的医学需求。对于已经接受先前的黑素瘤疗法并且对此已经失败或有进展的患者而言,这是特别真实的。先前疗法可以包括标准护理化学疗法(例如达卡巴嗪治疗)、免疫疗法(例如用派姆单抗、伊匹单抗、或纳武单抗及其组合进行治疗)、靶向疗法(例如用达拉菲尼和曲美替尼;维莫非尼和考美替尼;以及恩拉非尼和比美替尼进行治疗)。可能受益于本发明的组合的患者包括患有NRAS突变型黑素瘤、BRAF突变型黑素瘤的患者,尤其在黑素瘤是不可切除的和/或转移性的皮肤黑素瘤的情况下。
因此还需要安全和/或良好耐受的靶向疗法。对于这些患者而言,在临床环境中产生持久和持续应答的疗法是有益的。
本发明提供了本发明的组合,用于如本文所述使用,从而治疗这样的患者中的黑素瘤。
发现以下的组合治疗:纳波拉非尼布(化合物A)和选自由以下组成的组的第二治疗剂:(i)里内特基布(化合物B)、(ii)曲美替尼(化合物C)和(iii)瑞博西尼(化合物D)是良好耐受的,并且与NRAS突变型患者来源的黑素瘤异种移植物中的单一药剂相比,增加了抗肿瘤应答。这些数据表明,预期纳波拉非尼布和第二治疗剂(例如(i)里内特基布、(ii)曲美替尼和(iii)瑞博西尼)的组合活性导致按临床可耐受剂量,黑素瘤的治疗是有效并且可达到的。预期在NRAS突变型黑素瘤患者中,组合疗法达到了更大并且更持久的应答。
因为发现化合物A和选自由以下组成的组的第二治疗剂组合施用:(i)化合物B、(ii)曲美替尼(化合物C)和(iii)瑞博西尼(化合物D)以这样一种有益方式抑制MAPK途径中的癌基因信号传导,还可能给BRAF突变型黑素瘤患者带来临床益处,这是由于BRAF是Ras/Raf/MAPK途径中的关键组分。
因此,本发明提供了药物组合,其包含具有式(I)的化合物(化合物A,也称为纳波拉非尼布),
或其药学上可接受的盐、以及选自由以下组成的组的第二治疗剂:
(i)是化合物B的ERK(尤其是ERK1/2)抑制剂(也称为里内特基布),
或其药学上可接受的盐,尤其是HCl盐;
(ii)是化合物C的MEK(MEK1/2)抑制剂,
(也称为曲美替尼)、或其药学上可接受的盐或溶剂化物,尤其是其二甲亚砜(DMSO)溶剂化物;和
(iii)是化合物D的CDK4/6抑制剂,
(也称为瑞博西尼)、或其药学上可接受的盐,尤其是其琥珀酸盐,用于在治疗如本文所述的黑素瘤中使用,并且特别是NRAS突变型黑素瘤或BRAF突变型黑素瘤,尤其是其中黑素瘤是不可切除的皮肤黑素瘤和/或转移性皮肤黑素瘤。
这三种双重组合在本文中也称为“本发明的组合”。
本发明还提供了具有式(I)的化合物、或其药学上可接受的盐,如本文所述,通过与选自由以下组成的组的第二治疗剂共同施用,用于在治疗NRAS突变型黑素瘤和/或BRAF突变型黑素瘤中使用:
(i)4-(3-氨基-6-((1S,3S,4S)-3-氟-4-羟基环己基)吡嗪-2-基)-N-((S)-1-(3-溴-5-氟苯基)-2-(甲基氨基)乙基)-2-氟苯甲酰胺(化合物B)、或其药学上可接受的盐(特别是其盐酸盐);
(ii)曲美替尼(化合物C)、或其药学上可接受的盐或溶剂化物(特别是其DMSO溶剂化物),以及
(iii)瑞博西尼(化合物D)、或其药学上可接受的盐(特别是其琥珀酸盐)。
本发明提供了选自由以下组成的组的治疗剂:
(i)4-(3-氨基-6-((1S,3S,4S)-3-氟-4-羟基环己基)吡嗪-2-基)-N-((S)-1-(3-溴-5-氟苯基)-2-(甲基氨基)乙基)-2-氟苯甲酰胺(化合物B)、或其药学上可接受的盐(特别是其盐酸盐);
(ii)曲美替尼(化合物C)、或其药学上可接受的盐或溶剂化物(特别是其DMSO溶剂化物),以及
(iii)瑞博西尼(化合物D)、或其药学上可接受的盐(特别是其琥珀酸盐),并且如本文所述,通过与具有式(I)的化合物、或其药学上可接受的盐共同施用,用于在治疗NRAS突变型黑素瘤和/或BRAF突变型黑素瘤中使用。
本发明提供了如上文所述的本发明的药物组合或治疗剂,用于在治疗NRAS突变型黑素瘤或BRAF突变型黑素瘤中使用,其中向患者施用该组合或该治疗剂,并且该治疗伴随以下特征中的一个或多个:
-在施用本发明的组合后,患者经历至少3个月的无进展生存期(PFS);
-在施用本发明的组合后,患者经历至少7个月的应答持续时间(DOS);
-治疗伴随以下的增加:改善总体应答率(ORR)、疾病控制率(DCR)、应答持续时间(DOR)、无进展生存期(PFS)、或中位总生存期(mOS),特别是与标准护理或其他疗法进行比较时,例如对比比美替尼或对比达卡巴嗪施用;和
-伴随不良作用减少,任选地其中该不良作用选自QTc延长;不良心脏事件和皮肤毒性。
在另一方面,并且如本文所述,本发明提供了本发明的药物组合用于制备药物的用途,该药物用于治疗NRAS突变型黑素瘤和/或BRAF突变型黑素瘤,尤其是其中该黑素瘤是不可切除的皮肤的和/或转移性的黑素瘤。
在另一方面,并且如本文所述,本发明提供了用于治疗患有NRAS突变型黑素瘤和/或BRAF突变型黑素瘤的患者的方法,该方法包括向有需要的受试者施用治疗有效量的本发明的药物组合,尤其是其中该黑素瘤是不可切除的皮肤黑素瘤和/或转移性皮肤黑素瘤。
本发明还提供了如本文所述的治疗NRAS突变型黑素瘤和/或BRAF突变型黑素瘤的方法,该方法包括以一个量向有需要的受试者同时、分开或顺序施用本发明的组合,该量针对所述黑素瘤具有联合治疗有效性。
并且如本文所述,本发明还提供了药物组合物或组合制剂,其包含一定量的本发明组合(该量对癌症具有联合治疗有效性),以及任选地至少一种药学上可接受的载体,用于在治疗NRAS突变型黑素瘤和/或BRAF突变型黑素瘤中使用。
并且如本文所述,本发明还提供了组合制剂,其包含(a)一个或多个剂量单位的具有式(I)的化合物、或其药学上可接受的盐,以及(b)一个或多个剂量单位的其第二治疗剂,用于在治疗NRAS突变型黑素瘤或BRAF突变型黑素瘤中使用。
本发明还提供了商业包装物,其包含作为活性成分的本发明的组合和用于向有需要的患者同时、分开或顺序施用本发明的组合的说明书,用于在治疗NRAS突变型黑素瘤或BRAF突变型黑素瘤中使用。
本发明还提供了:
-纳波拉非尼布,用于在与曲美替尼一起的组合疗法中使用,用于治疗NRAS突变型黑素瘤,其中向有需要的患者施用纳波拉非尼布和曲美替尼,任选地其中该治疗伴随以下的增加:改善总体应答率(ORR)、疾病控制率(DCR)、应答持续时间(DOR)、无进展生存期(PFS)、或中位总生存期(mOS),例如对比标准护理或其他疗法,例如对比比美替尼或对比达卡巴嗪;和/或伴随不良作用减少,任选地其中该不良作用选自QTc延长;不良心脏事件和皮肤毒性。
-在NRAS突变型黑素瘤或BRAF突变型黑素瘤中,改善总体应答率(ORR)、疾病控制率(DCR)、应答持续时间(DOR)、无进展生存期(PFS)、或中位总生存期(mOS)的方法,其中向有需要的患者施用纳波拉非尼布与曲美替尼、或其药学上可接受的盐或溶剂化物的组合。
-在NRAS突变型黑素瘤或BRAF突变型黑素瘤中,改善总体应答率(ORR)、疾病控制率(DCR)、应答持续时间(DOR)、无进展生存期(PFS)、或中位总生存期(mOS)的方法,其中向有需要的患者施用纳波拉非尼布与里内特基布、或其药学上可接受的盐的组合。
-降低QTc延长的风险、并且治疗患有NRAS突变型黑素瘤或BRAF突变型黑素瘤的患者的方法,该方法包括向有需要的患者施用治疗有效量的纳波拉非尼布、或其药学上可接受的盐,以及治疗有效量的曲美替尼、或其药学上可接受的溶剂化物。
-降低QTc延长的风险、并且治疗患有NRAS突变型黑素瘤或BRAF突变型黑素瘤的患者的方法,该方法包括向有需要的患者施用治疗有效量的纳波拉非尼布、或其药学上可接受的盐,以及治疗有效量的里内特基布、或其药学上可接受的溶剂化物。
下面进一步详细描述了本发明的各个方面。另外的定义在整个申请书中陈述。
附图说明
图1是跨十个患者来源的NRAS突变型黑素瘤肿瘤异种移植小鼠模型,对化合物A(LXH254)和曲美替尼的应答的瀑布图。
图2是在单一药剂化合物A(LXH254)、曲美替尼或两种药剂的组合的每日治疗期间肿瘤达到700mm3大小的卡普兰-梅尔(Kaplan-Meier)时间图。
图3是跨十个患者来源的NRAS突变型黑素瘤肿瘤异种移植小鼠模型,对化合物A(LXH254)和化合物B的应答的瀑布图。
图4是在单一药剂化合物A(LXH254)、化合物B或两种药剂的组合的每日治疗期间肿瘤达到700mm3大小的卡普兰-梅尔时间图。
图5是跨九个患者来源的NRAS突变型黑素瘤肿瘤异种移植小鼠模型,对化合物A(LXH254)和瑞博西尼(LEE011)的应答的瀑布图。
图6是在单一药剂化合物A(LXH254)、瑞博西尼(LEE011)或两种药剂的组合的每日治疗期间肿瘤达到700mm3大小的卡普兰-梅尔时间图。
具体实施方式
本发明提供了如上文所述的本发明的组合,用于在治疗NRAS突变型黑素瘤或BRAF突变型黑素瘤中使用,尤其是其中所述黑素瘤是不可切除的皮肤黑素瘤和/或转移性皮肤黑素瘤。在本发明中,预期本发明的组合的施用会产生更有益的作用,例如协同的或改善的抗增殖作用,例如关于延缓进展或抑制癌症或其症状,并且还可能提供另外有益的作用,如以下任何一种或多种:如与标准护理疗法、使用组合配伍物中任一个的免疫疗法至靶向单一疗法、使用BRAF和MEK抑制剂的组合的疗法或针对黑素瘤的任何其他先前疗法相比,更低的心脏不良事件的风险((例如更低的QTc倾向)、更少的副作用(例如皮肤相关毒性(例如皮疹)和胃肠道毒性(例如腹泻))、改善的耐受性、更高的生活质量和降低的发病率。
因此,提供了本发明的组合,用于在治疗NRAS突变型黑素瘤或BRAF突变型黑素瘤中使用,其中根据RECIST v1.1当地研究人员评估,例如,如通过更高的证实的客观应答率(ORR)测量,与先前治疗相比,该治疗具有更高的临床功效。还可以通过根据RECIST版本1.1和总生存期(OS)测量总体应答率(ORR)、疾病控制率(DCR)、应答持续时间(DOR)、无进展生存期(PFS),测量更高的临床功效。
例如,可以通过用先前的或其他的疗法获得的改善的总体应答率,测量更有益的作用。
本发明的组合的治疗剂可以单独地、同时地或顺序地施用有需要的受试者。优选地,将这些治疗剂按治疗有效的剂量施用,当组合时其提供有益的作用。因此,在本发明的一个实施例中,本发明的组合用于在治疗NRAS突变型黑素瘤或BRAF突变型黑素瘤、特别是如本文所述的黑素瘤中使用。本发明的双重组合的各个组分还用于同时、分开或顺序施用,用于治疗NRAS突变型(优选地是不可切除的和/或转移性的)皮肤黑素瘤和/或BRAF突变型(优选地是皮肤的不可切除的和/或转移性的)皮肤黑素瘤,尤其是如在上文和下文的其他本发明实施例中所定义。
化合物A是公开的PCT申请WO 2014/151616中的实例1156。
化合物A是N-(3-(2-(2-羟基乙氧基)-6-吗啉代吡啶-4-基)-4-甲基苯基)-2-(三氟甲基)异烟酰胺,并且是具有以下结构的化合物:
化合物A、化合物A的药学上可接受的盐和包含化合物A的药物组合物的制备也在该PCT申请中公开,例如参见第739-741页。化合物A是BRAF和CRAF的选择性抑制剂。化合物A是BRAF和CRAF蛋白激酶的三磷酸腺苷(ATP)竞争性抑制剂。还已知化合物A是代号“LXH254”或为“纳波拉非尼布”。贯穿本披露,化合物A也称为CRAF抑制剂或CRAF激酶抑制剂。
化合物B是4-(3-氨基-6-((1S,3S,4S)-3-氟-4-羟基环己基)吡嗪-2-基)-N-((S)-1-(3-溴-5-氟苯基)-2-(甲基氨基)乙基)-2-氟苯甲酰胺,并且是具有以下结构的化合物。
披露了化合物B,并且其制备描述于公开的PCT专利申请WO 2015/066188中。化合物B是细胞外信号调节激酶1和2(ERK 1/2)的抑制剂。还已知化合物B是代号“LTT462”或为“里内特基布”。还出于本发明实施例的目的,里内特基布的特别有用的盐是其盐酸盐。
披露了化合物C(也称为曲美替尼),并且其制备描述于例如WO 2005/121142中,例如在实例4-1中或在“实例4-1(替代性方法)”中,并将其作为Mekinist销售。曲美替尼是批准的MEK1/2激酶的抑制剂。
化合物C是有效的并且选择性的MEK 1/2抑制剂。它是N-(3-{3-环丙基-5-[(2-氟-4-碘苯基)氨基]-6,8-二甲基-2,4,7-三氧代-3,4,6,7-四氢吡啶并[4,3-d]嘧啶-1(2H)-基}苯基)乙酰胺或曲美替尼并且是具有以下结构的化合物:
还出于本发明实施例的目的,曲美替尼的特别有用的溶剂化物是其二甲亚砜(DMSO)溶剂化物。
披露了化合物D(也称为瑞博西尼)并且例如其制备描述于WO 2010/020675中,例如描述于实例74中;琥珀酸盐的合成披露于US 2013/0217698中。瑞博西尼是批准的细胞周期蛋白D1(CDK4)和CDK6激酶的选择性抑制剂(CDK4/6抑制剂)。
瑞博西尼的化学名称是7-环戊基-2-(5-哌嗪-1-基-吡啶-2-基氨基)-7H-吡咯并[2,3-d]嘧啶-6-甲酸二甲酰胺,并且它是具有以下结构式的化合物:
瑞博西尼(在商标下使用)是一种口服生物利用的且高选择性的小分子抑制剂,对CDK4/细胞周期蛋白-D1和CDK6/细胞周期蛋白-D3酶复合体具有高度特异性的抑制活性。还出于本发明实施例的目的,瑞博西尼的特别有用的盐是其琥珀酸盐。
除非本文另外指示或与上下文明显矛盾,在提及化合物A、化合物B、化合物C或化合物D的情况下,技术人员将理解,提及将包括游离化合物和/或其药学上可接受的盐,或在化合物C的情况下,包括药学上的溶剂化物,例如其二甲亚砜(DMSO)溶剂化物。
本说明书中对“本发明”的提及旨在反映本说明书中披露的数项发明的实施例,并且不应被视为对所要求保护的主题的不必要限制。
本发明更通用的术语或特征的以下定义可用于代替每个发明实施例的一个、超过一个或所有术语特征,因此导致了更特定的发明实施例(其全部构成本发明的一部分)。
除非本文另外指示或与上下文明显矛盾,否则在描述本发明的上下文中,如本文所使用的术语“一个/种(a/an)”和“该(the)”以及类似提及应解释为包括单数和复数两者。当将复数形式用于化合物、盐等时,这也意指单一化合物、盐等。
除非上下文另有明确说明,否则术语“或”在本文中用于表示术语“和/或”并且可与术语“和/或”互换使用。术语“和/或”意指与之结合提到的特征中的任何单一项、其两个或三个或所有特征中的任何组合旨在包括在包括“和/或”的定义中。
“约”和“大约”通常意指在给定测量的性质或精度的情况下测量的量的可接受的误差度。示例性误差度在给定值或值范围的20%内,典型地在10%内,并且更典型地,在5%内。当将本文的剂量(dosage或dose)描述为指定量(即在指定量之前没有术语“约”,例如200mg),或描述为“约”指定量(例如约200mg)时,实际剂量(dosage或dose)可以从所述量变化达10%:这种使用承认,给定剂型中的精确量可能由于各种原因而与预期量略有不同,但不会实质上影响所施用化合物的体内作用。
技术人员将理解,当本文引用治疗化合物的剂量(dose或dosage)时,该量是指游离形式的治疗化合物的量。例如,当提及200mg(或约200mg)化合物B的剂量,并且化合物B以其盐酸盐使用时,所用治疗剂的量相当于200mg(或约200mg)游离形式的化合物B。
除非另外指明,否则术语“包含(comprising)”和“包括(including)”在本文中以其开放式和非限制性的含义使用。
“组合”或“与……组合”或“共同施用”或“与……共同施用”并不旨在暗示必须物理混合或同时施用疗法或治疗剂和/或配制这些治疗剂用于一起递送,尽管这些递送方法在本文所述的范围内。这些组合中的治疗剂可以与一种或多种其他另外的疗法或治疗剂同时、在其之前或之后施用。可以按任何顺序施用治疗剂。通常,每种药剂将以针对该药剂确定的剂量和/或时间表施用。还应理解,该组合中使用的另外的治疗剂可以按单一组合物一起施用或按不同组合物单独施用。通常,预期组合中使用的其他治疗剂以不超过它们单独使用时的水平使用。在一些实施例中,组合中使用的水平将低于单剂疗法中使用的水平。
本发明的组合具有治疗或保护功能或两者。
如本文使用的,术语“组合”、“治疗性组合”或“药物组合”是指在一个剂量单位形式中的固定组合、或非固定组合、或用于组合施用(共同施用)的成套试剂盒(kit ofparts),其中两种或更多种治疗剂可以一起、在同一时间独立地或在时间间隔内单独地施用,尤其在这些时间间隔允许组合配伍物显示合作(例如协同)效应的情况下。
治疗本文所述的黑素瘤的组合疗法或方法是指施用两种或更多种治疗剂以治疗如在本披露中所述的黑素瘤。这种施用涵盖以基本上同时的方式共同施用这些治疗剂,如以具有固定比率的活性成分的单个配制品施用或以每种活性成分的单独配制品(例如,胶囊和/或静脉内配制品)施用。此外,这种施用和共同施用也涵盖在大致相同的时间或在不同的时间以顺序或单独的方式使用每种类型的治疗剂。无论活性成分是作为单一配制品施用还是以分开的配制品施用,将药物作为同一疗程的一部分施用同一患者。在任何情况下,治疗方案将在治疗本文所述的病症或障碍方面提供有益作用。
在本发明的含义内,同时的治疗性使用是指通过相同途径并同时或基本上同时施用至少两种活性成分。
在本发明的含义内,单独使用特别是指通过不同途径同时或基本上同时施用至少两种活性成分。
顺序的治疗性使用是指在不同的时间施用至少两种活性成分,施用途径相同或不同。更特别地,施用方法意指根据该方法,在一种或多种其他活性成分开始施用之前进行一种活性成分的全部施用。
如本文使用的,术语“固定组合”、“固定剂量”和“单一配制品”是指配制的单一载体或媒介物或剂型,以向患者递送一定量的两种治疗剂,该量对于癌症的治疗具有联合治疗有效性。单一媒介物被设计为递送一定量的每种药剂连同任何药学上可接受的载体或赋形剂。在一些实施例中,媒介物是片剂、胶囊剂、丸剂或贴剂。在其他实施例中,媒介物是溶液或悬浮液。
术语“非固定组合”或“成套试剂盒”意指本发明组合的治疗剂作为分开的实体同时地、并行地或顺序地施用至患者(没有特定的时间限制),其中这种施用在有需要的受试者体内提供治疗有效水平的两种化合物。后者也适用于混合物疗法,例如三种或更多种活性成分的施用。
如本文使用的,术语“药学上可接受的”是指在合理医学判断的范围内适合用于与受试者(例如,哺乳动物或人)的组织相接触而无过度毒性、刺激、过敏反应和其他问题或并发症,并且与合理的益处/风险比相称的那些化合物、材料、组合物和/或剂型。
如本文使用的,术语“药学上可接受的赋形剂”或“药学上可接受的载体”包括如本领域技术人员应已知的任何和所有溶剂、分散介质、包衣、表面活性剂、抗氧化剂、防腐剂(例如,抗细菌剂、抗真菌剂)、等渗剂、吸收延迟剂、盐、防腐剂、药物、药物稳定剂、粘合剂、赋形剂、崩解剂、润滑剂、甜味剂、调味剂、染料、类似材料及其组合。除了任何常规载体与活性成分均不相容的情况外,考虑其在治疗或药物组合物中的用途。
本文将术语“药物组合物”定义为指含有至少一种待施用至患者以便治疗影响受试者的特定疾病或病症的治疗剂的混合物或溶液。本发明的药物组合可以配制成适合的药物组合物用于肠内或肠胃外施用,例如糖衣片剂、片剂、胶囊或栓剂或安瓿剂。如果未另外指明,那么这些以本身已知的方式进行制备,例如借助各种常规的混合、粉碎、直接压片、制粒、包糖衣、溶解、冻干方法或对本领域技术人员来说显而易见的制造技术。应当理解,包含在每种剂型的单独剂量中的组合配伍物的单位含量本身不必构成有效量,因为必需的有效量可以通过施用多个剂量单位达到。药物组合物可以含有从约0.1%至约99.9%,优选地从约1%至约60%的一种或多种治疗剂。本领域普通技术人员可以通过常规实验且无需任何不当负担关于剂型的特定所需特性来选择前述载体中的一种或多种。所使用的每种载体的量可以在本领域的常规范围内变化。以下参考文献披露了用于配制口服剂型的技术和赋形剂:The Handbook of Pharmaceutical Excipients[药物赋形剂手册],Rowe等人,编辑,American Pharmaceuticals Association[美国医药协会];和Remington:the Scienceand Practice of Pharmacy[雷明顿:药物科学与实践],Gennaro,编辑,LippincottWilliams和Wilkins。这些任选的附加的常规载体可以掺入到口服剂型中,方式为在制粒之前或期间将一种或多种常规载体掺入到初始混合物中,或将一种或多种常规载体与包含该药剂组合的颗粒或呈口服剂型的该药剂组合的单独药剂组合。在后一个实施例中,可以将组合的混合物例如通过V型共混器进一步共混,然后压制或模塑成片剂(例如单块式片剂),用胶囊包封,或填充到小袋中。
药物组合物可以按每单位剂量包含预定量的活性成分的单位剂型呈现。在某些实施例中,单位剂量包括一种或多种媒介物,使得每种媒介物包括有效量的至少一种治疗剂连同药学上可接受的载体和赋形剂。在一些实施例中,单位剂量是在相同时间施用患者的一种或多种片剂、胶囊、丸剂、注射剂、输注剂、贴剂等。如本领域技术人员已知的,活性成分/剂量的量将取决于所治疗的病症;施用途径;以及患者的年龄、体重和健康状况。优选的单位剂量组合物是含有活性成分的每日剂量或亚剂量、或其适当部分的那些。此外,此类药物组合物可以通过药学领域熟知的任何方法制备。
本发明的药物组合物可以包括“治疗有效量”或“有效量”的本发明化合物。治疗剂组合的术语“药学有效量”、“治疗有效量”或“临床有效量”是以必要的剂量和在必要的时间段内足以提供超过用该组合治疗的障碍的临床可观察的体征和症状的基线的、可观察的或临床上显著改善的量。治疗有效量将根据以下因素而变化:如个体的疾病状态、年龄、性别、和体重。治疗有效量也是治疗有益效果超过治疗剂的任何毒性或有害作用的量。“治疗有效剂量”优选地以所需方式调节可测量的参数,例如肿瘤生长速率或疾病进展。可以在预测人肿瘤中的功效的动物模型系统中评估化合物调节可测量参数的能力,以帮助建立适合的给药水平和时间表。可替代地,组合物的此性质可以通过使用本领域技术人员已知的体外测定检查化合物调节不希望的参数的能力来评估。
如本文使用的,术语“联合治疗活性”或“联合治疗作用”意指可以将治疗剂在其优选的时间间隔内联合地、单独地或顺序地给予,使得待治疗的受试者(尤其是人)仍显示出(优选地协同性)相互作用(联合治疗作用)。情况是否如此尤其可以通过以下方式确定:跟踪化合物的血液水平,证实两种化合物至少在某些时间间隔期间皆存在于待治疗的人的血液中。
“口服剂型”包括开处方或意欲用于口服施用的单位剂型。
可以按口服剂型施用化合物A、化合物B、化合物C和化合物D中的每一种。
如本文使用的,术语“治疗(treat、treatment和treating)”是指由施用一种或多种疗法导致的障碍(例如增殖性障碍)的进展、严重性和/或持续时间的减少或缓解,或者障碍的一种或多种症状(适当地,一种或多种可辨别的症状)的缓解。在具体的实施例中,术语“治疗(treat、treatment和treating)”是指改善增殖性障碍的至少一种可测量的物理参数,如肿瘤的生长,这不一定是患者可辨别的。在其他实施例中,术语“治疗(treat、treatment和treating)”是指通过例如稳定可辨别的症状来物理地,或通过例如稳定物理参数来生理地,或通过两者,抑制增殖性障碍的进展。在其他实施例中,术语“治疗(treat、treatment和treating)”是指减少或稳定肿瘤大小或癌细胞计数。
术语“治疗(treat、treatment和treating)”包括降低患者或患者群体中的不良事件(AE)和严重AE(SAE)的发生率和严重性,包括实验室值、生命体征和心电图(ECG)的变化。
术语“治疗(treat、treatment和treating)”包括改善患者或患者群体中的总体应答率(ORR)、疾病控制率(DCR)、应答持续时间(DOR)、无进展生存期(PFS),例如,根据实体瘤应答评估标准(RECIST)版本1.1。
在本披露的含义范围内,术语“治疗”还表示阻止、延迟发作(即在疾病的临床表现之前的时间段)和/或降低疾病发展或疾病恶化的风险。术语“保护”在本文中用于表示阻止、延迟或治疗,或者视情况而定既阻止、延迟又治疗受试者(例如哺乳动物或人)体内疾病的发展、持续或恶化。
因此,本发明提供了本发明的组合,用于在治疗患者中的NRAS突变型黑素瘤和/或BRAF突变型黑素瘤中使用,其中该治疗伴随以下的增加:改善总体应答率(ORR)、疾病控制率(DCR)、应答持续时间(DOR)、无进展生存期(PFS)、或中位总生存期(mOS),例如对比标准护理或其他疗法,例如对比比美替尼或对比达卡巴嗪。
如本文使用的,术语“患者”旨在包括动物,但是优选地是人类患者。患者尤其是需要黑素瘤治疗的人类患者。例如,患者是患有晚期黑素瘤、或转移性黑素瘤、或不可切除的黑素瘤的患者。在一些情况下,人类患者已经接受了使用另一种药剂的先前疗法并且对此有进展。如本文所述,黑素瘤可以是NRAS突变型、或BRAF突变型或NRAS突变型黑素瘤。
术语“抑制”或“抑制剂”包括给定分子或途径的某些参数(例如活性)的降低。例如,此术语包括将靶激酶(Raf或CDK4/6)的活性抑制5%、10%、20%、30%、40%或更多。因此,抑制可以是但不必是100%。
如本文使用的,“盐”(其由“或其多种盐”或“或其一种盐”表示)可以单独存在或以与本发明组合的游离化合物(例如Raf抑制剂即具有式(I)的化合物或CDK4/6抑制剂(优选瑞博西尼))的混合物存在,并且优选地是药学上可接受的盐。优选由具有碱性氮原子的本发明组合的化合物与有机酸或无机酸形成此类盐,例如作为酸加成盐,尤其是药学上可接受的盐。术语“药学上可接受的盐”是指保留化合物的生物有效性和特性并且典型地在生物学或其他方面并非不合意的盐。
适合的盐的列表可以见于“Remington’s Pharmaceutical Sciences[雷明顿药物科学]”、以及“Remington:the science and practice of pharmacy[雷明顿:药学科学与实践]”中。
如本文使用的,术语“协同作用”是指两种药剂的作用,这两种药剂例如像,Raf抑制剂即具有式(I)的化合物或其药学上可接受的盐、和选自化合物B、化合物C和化合物D的第二治疗剂、或其药学上可接受的盐(或在化合物C的情况下,其药学上可接受的溶剂化物),以产生如下效果,例如减缓癌症或其症状的症状进展,这比自身施用的每种药物的效果的简单加和要大。
在提及总体应答率(ORR)的情况下,根据实体瘤应答评估标准(RECIST v1.1),这(如果并未在本说明书的具体位置另外定义)是指部分应答和完全应答之和(定义为PR+CR(部分应答加完全应答))。可以基于RECIST标准(Therasse等人,2000)、New Guidelines toEvaluate the Response to Treatment in Solid Tumors[评估实体瘤对治疗响应的新指南],Journal of National Melanoma Institute[国家黑素瘤研究所杂志],卷92;205-16进行肿瘤评价和肿瘤负荷评估,并且根据修订的RECIST指南(版本1.1)(Eisenhauer等人,2009,New response evaluation criteria in solid tumours[实体瘤中的新应答评估标准]:revised RECIST guideline[修订的RECIST指南](版本1.1).Eur J Melanoma[欧洲黑素瘤杂志],45(2):228-47.),在本发明内进行肿瘤评价和肿瘤负荷评估。为了避免清晰度的问题,在本文将ORR定义为至少15%或定义为至少30%的情况下,ORR的上限可以是100%。在具体实施例中,ORR是30%、35%、40%、45%、50%、55%、60%、65%、70%、75%或80%(值越高,越是优选的)或更高中的任一项。
完全应答被定义为所有非结节靶病灶消失。此外,指定为靶病灶的任何病理性淋巴结在短轴中必须具有至<10mm1的缩减。
部分应答被定义为以基线的直径总和为参考,所有靶病灶的直径总和至少减少30%。
可以从下表推导出其他应答标准(根据RECIST v1.1):
可以通过本领域技术人员熟知的方法监测黑素瘤的进展、肿瘤负荷的增加或减少、以及对用根据本发明的抑制剂组合进行治疗的应答。因此,可通过目视检查来监测对黑素瘤的治疗的进展和应答,例如通过X射线、CT扫描或MRI或通过肿瘤生物标志物检测。
QT间隔是心动周期中Q波开始与T波结束之间的时间间隔。术语“QTc”是指这样的QT间隔:针对心率对其进行校正并且考虑了随着心率增加而发生的QT间隔的生理缩短。这种校正允许跨一系列心率,比较QT间隔。延长的QTc与心脏性猝死的增加风险相关。因此,治疗任何疾病状态应寻求将QTc延长的风险最小化并且降低建议治疗的QTc倾向。
术语QTcF是指通过Fridericia公式校正的QT间隔。
可以通过进行心电图(ECG)测量QTc和QTcF中的改变和增加。
已经发现,使用本文披露的给药方案,可能实现治疗功效和不良副作用的减小(例如QTc延长的减小)之间的平衡。
因此,提供了降低患者中的QTc延长的风险、并且治疗患有NRAS突变型黑素瘤或BRAF突变型黑素瘤的患者的方法,该方法包括向有需要的患者施用治疗有效量的纳波拉非尼布、或其药学上可接受的盐,以及治疗有效量的曲美替尼、或其药学上可接受的溶剂化物。
本文还提供了降低QTc延长的风险、并且治疗患有NRAS突变型黑素瘤或BRAF突变型黑素瘤的患者的方法,该方法包括向有需要的患者施用治疗有效量的纳波拉非尼布、或其药学上可接受的盐,以及治疗有效量的里内特基布、或其药学上可接受的溶剂化物。
在此上下文中,治疗有效量的纳波拉非尼布特别是小于800mg日总剂量,例如小于或等于400mg日总剂量。优选地,日总剂量是一天两次施用。
下文和在实例中描述了其他治疗有效量的纳波拉非尼布、曲美替尼和里内特基布。
本发明的组合尤其可以用于治疗NRAS突变型黑素瘤,特别是其中所述黑素瘤是先前治疗过的不可切除的或转移性的NRAS突变型皮肤黑素瘤。
15%-20%的皮肤转移性黑素瘤中发现NRAS突变,位于外显子2(密码子12或13)或外显子3(密码子61)中。因此,要用本发明的组合治疗的NRAS突变型黑素瘤包括具有在NRAS中的密码子61、密码子12或密码子13处(尤其是在密码子61处)的突变的黑素瘤。
感兴趣的NRAS突变可以选自G12C、G12R、G12D、G12V、G12S、G12A、G13R、G13D、G13C、G13A、G13、G13S、G13V、Q61R、Q61L、Q61K、Q61H、Q61P、Q61E及其组合。感兴趣的突变包括G12D或G13D。术语“NRAS突变型黑素瘤”包括展现突变的NRAS蛋白(特别是功能获得性NRAS突变)的任何黑素瘤肿瘤;尤其是任何G13R、Q61K、Q61L、或Q61R NRAS突变型肿瘤。因此,NRAS突变型黑素瘤包括具有至少一个NRAS突变的黑素瘤,该突变对应于Q61R、Q61L、Q61K、Q61H、Q61P或Q61E,更优选地对应于Q61K、Q61L或Q61R。要治疗的黑素瘤可以是NRAS QG13R突变型黑素瘤。NRAS突变型皮肤黑素瘤可以处于早期、中期或晚期阶段。NRAS突变型皮肤黑素瘤可以是局部晚期的或转移性的。NRAS突变型皮肤黑素瘤可以是不可切除的。
本发明的组合还可以用于治疗BRAF突变型黑素瘤,特别是其中所述黑素瘤是先前治疗过的不可切除的或转移性的BRAF突变型黑素瘤。
本发明的组合尤其可以用于治疗具有在BRAF中的密码子600处的突变的黑素瘤。
大多数BRAF突变聚集在两个区域:N叶的富含甘氨酸的P环以及激活区段和侧接区域。在多种癌症中已经检测到V600E突变,并且该突变归因于在核苷酸1799处用腺嘌呤取代胸腺嘧啶。这导致在密码子600处缬氨酸(V)被谷氨酸(E)取代(现在称为V600E)。
例如,BRAF突变型黑素瘤是展现出BRAFV600突变的黑素瘤。在黑素瘤中的BRAF突变可以选自BRAF V600E、V600K、V600R、V600R、V600M、V600D、V600G及其组合。BRAF突变尤其是V600D、V600E,V600R、V600K、或BRAFD287H突变。优选地,术语“BRAF突变型黑素瘤”是指BRAFV600E突变型、BRAFV600K突变型、BRAFV600R突变型和BRAFV600D突变型黑素瘤,更优选地是指BRAFV600E突变型和BRAFV600D突变型黑素瘤,最优选地是指BRAFV600E突变型黑素瘤。BRAF突变型黑素瘤可以处于早期、中期或晚期阶段。BRAF突变型黑素瘤可以是局部晚期的或转移性的。BRAF突变型黑素瘤可以是不可切除的。
在提到“NRAS突变型黑素瘤”“或BRAF突变型黑素瘤”的情况下,这尤其涉及眼或皮肤黑素瘤,除非上下文另外明确指出。优选地,此术语是指皮肤黑素瘤,特别是不可切除的和/或转移性的皮肤黑素瘤。
本发明提供了药物组合,用于在治疗患者中的黑素瘤中使用,其中先前已经治疗过黑素瘤,例如通过手术切除,或其他疗法,并且在此疗法后有进展。
要通过组合治疗的黑素瘤可以是对先前用另一种疗法进行治疗是难治或抗性的黑素瘤。因此,本发明的组合可以用作黑素瘤的二线、三线或四线治疗。
用于黑素瘤患者的先前治疗包括:
-用拉-他利莫近(talimogene laherparepvec)(也称为商品名T-Vec、Imlygic或Oncovex)进行治疗,其是生物药剂学药物,用来治疗不可切除的黑素瘤,并且将其直接注射到转移性病灶的子集中;
-标准护理化学疗法(例如达卡巴嗪);
-用细胞毒性剂,例如亚硝基脲和/或丝裂霉素C进行治疗;
-免疫疗法(例如派姆单抗、伊匹单抗、或纳武单抗及其组合);
-靶向疗法(例如达拉菲尼和曲美替尼;维莫非尼和考美替尼;以及恩拉非尼和比美替尼)。
因此,要治疗的患者包括患有NRAS突变型黑素瘤和/或BRAF突变型黑素瘤的患者,尤其是已经接受先前疗法(包括标准护理化学疗法(例如达卡巴嗪)、免疫疗法(例如派姆单抗、伊匹单抗、或纳武单抗及其组合)、靶向疗法(例如达拉菲尼和曲美替尼;维莫非尼和考美替尼;以及恩拉非尼和比美替尼))并且对先前疗法有进展的患者。患者可以是患有NRAS突变型黑素瘤和/或BRAF突变型黑素瘤的患者,尤其在黑素瘤是不可切除的和/或转移性的皮肤黑素瘤的情况下。
在另一个实施例中,NRAS突变型黑素瘤或BRAF突变型黑素瘤对标准护理具有抗性或难治性。
在另一个实施例中,NRAS突变型黑素瘤或BRAF突变型黑素瘤对使用达卡巴嗪的标准护理具有抗性或难治性,优选地是当黑素瘤是NRAS突变型黑素瘤时。
在另一个实施例中,黑素瘤对用BRAF抑制剂和/或MEK抑制剂进行治疗(即用“RAF+/-MEK”抑制剂进行治疗)具有抗性或难治性,优选地是当黑素瘤是BRAF突变型黑素瘤时。BRAF抑制剂可以选自达拉菲尼、维莫非尼和恩拉非尼。MEK抑制剂选自曲美替尼、考美替尼和比美替尼。
例如,可能受益于如本文所述的组合疗法的患者包括患有先前已经用以下中的一项或多项进行治疗的BRAFV600突变型黑素瘤的患者:(i)达拉菲尼和曲美替尼,(ii)维莫非尼和考美替尼,以及(iii)恩拉非尼和比美替尼。
在另一个实施例中,黑素瘤对用细胞毒性剂(例如亚硝基脲和/或丝裂霉素C)进行治疗具有抗性或难治性。
在另一个实施例中,黑素瘤对用免疫疗法治疗(包括使用一种或多种免疫检查点抑制剂的疗法)进行治疗具有抗性或难治性。
因此,在一个实施例中,要用本发明的组合治疗的黑素瘤是BRAF突变型黑素瘤或NRAS突变型黑素瘤,其对单独的或与抗CTLA4(细胞毒性T淋巴细胞相关蛋白)抗体(例如伊匹单抗)组合的免疫治疗性PD-1(程序性细胞死亡1受体)或PD-L1(PD-1的配体)治疗具有抗性。参见例如Tsai等人,Human Vaccines&Immunotherapeutics[人类疫苗&免疫治疗]10:11,3111--3116;2014年11月。
因此,在一个实施例中,要治疗的黑素瘤对用选自以下的一种或多种治疗剂进行治疗具有抗性或难治性:伊匹单抗、斯巴达珠单抗、纳武单抗、派姆单抗、匹地利珠单抗(pidizilumab)、BMS-9365559、MEDI4736、和MSB0010718C。
因此,要用本发明的组合治疗的黑素瘤包括BRAF突变型黑素瘤或NRAS突变型黑素瘤,其对抗PD-1单一疗法(例如派姆单抗或纳武单抗)或抗PD-1药剂与伊匹单抗的组合具有抗性。
如先前所述的,根据本领域已知的方法,例如可以使用SNaPshot或DFCIOncopanel进行患者中的BRAF、NRAS和NF1突变的遗传评估(Sholl LM等人JCI Insight[JCI见解]2016;1:e87062;Zheng Z等人,Nat Med[自然医学]2014;20:1479-84)。这两种测定的当前迭代均利用下一代测序,而SNaPshot的早期版本依赖于多重PCR。SNaPshot的当前版本询问BRAF的外显子11和15、KRAS和NRAS的外显子2-5、以及NF1的外显子1-58。Oncopanel检测涉及BRAF、KRAS、NRAS和NF1的所有外显子的改变。
可以在黑素瘤细胞系,例如SKMEL-30细胞(带有BRAFD287H)中通过实验证明本发明的组合针对黑素瘤的体外活性。
可替代地,例如,如在实例中或与实例类似地描述,可以使用人类肿瘤异种移植模型,其中使用突变型黑素瘤细胞。
在一个实施例中,本发明提供了治疗(例如抑制、减小、改善、或预防)患者中的BRAF突变型或NRAS突变型黑素瘤的方法,该方法包括在如以上本文所述的治疗中,向有需要的患者施用一个(或优选地治疗有效的)量的本发明的组合。本文描述了用于在此类方法中使用这些化合物的适合的剂量和施用时间表。具体地,根据本发明,要使用的治疗有效量的纳波拉非尼布、里内特基布、曲美替尼和瑞博西尼和给药方案见于以下段落和实例中。
口服施用或优选地口服施用化合物A、化合物B、化合物C或化合物D、或其相应的药学上可接受的盐。
可以连续施用化合物A、或其药学上可接受的盐。可以连续施用化合物B、或其药学上可接受的盐。可以连续或间歇地施用化合物C、或其药学上可接受的盐或溶剂化物。可以连续或间歇地施用瑞博西尼、或其药学上可接受的盐,例如施用三周并且停止一周。
可以每天一次施用化合物A、或其药学上可接受的盐的日总剂量,或可以将该日总剂量分为两份,并且化合物A的每个剂量以每天两次施用。优选地,每天一次施用具有式(I)的化合物的日总剂量。在另一个优选的实施例中,每天两次施用具有式(I)的化合物的日总剂量。
在本发明的实施例中,可以按从约50至约1200mg的日总剂量(TTD)施用化合物A。因此,组合疗法典型地使用50mg、100mg、200mg、250mg、300mg、350mg、400mg、600mg或1200mg日总剂量(TTD)的化合物A。可以QD(“qd”或每天一次)或BID(“bid”或每天两次)施用TTD。适合地,在本发明的组合和方法中,每天一次施用50mg、100mg、200mg、250mg、300或350mg的剂量的化合物A,或者BID施用100mg、200mg、300mg、400mg或600mg的剂量。优选地,本发明的组合中的化合物A的TTD剂量是从约100mg至400mg,例如100mg、200mg或400mg,其可以按每天一次或每天两次的基础施用。
在一个实施例中,按800mg的TTD施用化合物A。例如,可以按一天两次的400mg、或一天一次的800mg的剂量施用化合物A。
在优选的实施例中,按小于800mg(例如小于或等于400mg)的TTD施用化合物A。
在特别优选的实施例中,按400mg的TTD施用化合物A,一天两次(即200mg BID)进行施用。预期化合物A的此剂量和给药方案提供了功效和安全性的最佳平衡(例如不良副作用的风险更低,例如QTcF延长的风险更低,同时维持最佳抗肿瘤应答)。
按治疗有效量,向有需要的受试者施用作为在根据本发明的组合中的另外的治疗剂的化合物B。
在优选的实施例中,化合物B、或其药学上可接受的盐的日总剂量是选自约50mg/天至约300mg/天的量;适合地,该量选自约100mg/天至约200mg/天。在优选的实施例中,按约100mg或约200mg的日总剂量施用化合物B、或其药学上可接受的盐。可替代地,日总剂量可以分成两份剂量,将其每天两次进行施用。
作为本发明的组合疗法的一部分,优选地,连续施用化合物B。具体地,可以如下设想以下每日剂量:
@:可以每天一次或每天两次施用化合物A的日总剂量,优选地分成每天两次施用的两个相等剂量。因此,可以按每天一次的200mg的一个剂量或每天两次的100mg的剂量施用200mg的日总剂量
b:可以每天一次或每天两次、优选地每天一次施用化合物B的日总剂量
在一个实施例中,按800mg的日总剂量施用化合物A,并且按200mg的日总剂量施用化合物B。
在一个实施例中,按800mg的日总剂量施用化合物A,并且按100mg的日总剂量施用化合物B。
在一个实施例中,按400mg的日总剂量施用化合物A,并且按100mg或200mg的日总剂量施用化合物B。
在一个实施例中,按200mg的剂量一天两次施用化合物A,并且按100mg或200mg的剂量一天一次施用化合物B。
按治疗有效量,向有需要的受试者施用作为在根据本发明的组合中的另外的治疗剂的曲美替尼。
在优选的实施例中,曲美替尼、或其药学上可接受的盐或溶剂化物的日总剂量是选自约0.5mg/天至约2mg/天的量;适合地,该量选自约0.5mg/天、约1mg/天和约2mg/天的曲美替尼。在优选的实施例中,按0.5mg或1mg的日总剂量施用曲美替尼、或其药学上可接受的盐或溶剂化物。可替代地,日总剂量可以分成两份剂量,将其每天两次进行施用。
优选地可以每天两次施用日总剂量的化合物A,同时可以每天一次施用日总剂量的曲美替尼。还可以施用例如下表中的其他剂量。
更优选地,可以如下设想日总剂量:
@:可以每天一次或每天两次施用化合物A的日总剂量,优选地分成每天两次施用的两个相等剂量。因此,可以按每天一次的200mg的一个剂量或每天两次的100mg的剂量施用化合物A的200mg的日总剂量b:可以每天一次或每天两次、优选地每天一次施用曲美替尼的日总剂量
在优选的实施例中,按400mg的日总剂量施用化合物A,并且按1mg的日总剂量施用曲美替尼,特别以提供功效和安全性的最佳平衡(例如不良副作用的风险更低,例如QTcF延长的风险更低,同时维持最佳抗肿瘤应答)。
在优选的实施例中,按200mg的剂量每天两次施用化合物A,并且按1mg的剂量每天一次施用曲美替尼,特别以提供功效和安全性的最佳平衡(例如不良副作用的风险更低,例如QTcF延长的风险更低,同时维持最佳抗肿瘤应答)。
按治疗有效量,向有需要的受试者施用作为在根据本发明的组合中的另外的治疗剂的瑞博西尼。
在优选的实施例中,瑞博西尼、或其药学上可接受的盐的日总剂量是选自约100mg/天至约600mg/天的量;适合地,该量选自约200mg/天至约600mg/天。在优选的实施例中,按选自约100mg、约200mg、约400mg和约600mg的日总剂量施用瑞博西尼、或其药学上可接受的盐。可替代地,总剂量可以分为两份剂量,将其每日两次施用。
作为本发明的组合疗法的一部分,连续地或具有药物假期地施用瑞博西尼。因此,可以将瑞博西尼施用三周并且停止一周。典型地,瑞博西尼的日总剂量,(例如400mg或600mg(例如按两个或三个200mg片剂服用))可以服用(例如每天一次)持续连续的前21天,随后是连续7天的瑞博西尼药物假期。然后重复28天周期。
具体地,可以如下设想以下每日剂量:
更优选地,可以如下设想日总剂量:
@:可以每天一次或每天两次施用化合物A的日总剂量,优选地分成每天两次施用的两个相等剂量。因此,可以按每天一次的200mg的一个剂量或每天两次的100mg的剂量施用每天200mg的日总剂量
b:可以每天一次或每天两次、优选地每天一次施用瑞博西尼的日总剂量
#:优选地,将瑞博西尼施用三周并且停止一周
在一个实施例中,按800mg的日总剂量施用化合物A,并且按200mg的日总剂量施用瑞博西尼,任选地其中连续施用化合物A,并且将瑞博西尼施用三周并且停止一周。
在一个实施例中,按800mg的日总剂量施用化合物A,并且按400mg的日总剂量施用瑞博西尼,任选地其中连续施用化合物A,并且将瑞博西尼施用三周并且停止一周。
在一个实施例中,按400mg的剂量一天两次施用化合物A,并且按200mg的剂量一天一次施用瑞博西尼,任选地其中连续施用化合物A,并且将瑞博西尼施用三周并且停止一周。
在一个实施例中,按400mg的剂量一天两次施用化合物A,并且按400mg的剂量一天一次施用瑞博西尼,任选地其中连续施用化合物A,并且将瑞博西尼施用三周并且停止一周。
在一个优选的实施例中,按400mg的日总剂量施用化合物A,并且按400mg的日总剂量施用瑞博西尼,任选地其中连续施用化合物A,并且将瑞博西尼施用三周并且停止一周,特别以提供功效和安全性的最佳平衡(例如不良副作用的风险更低,例如QTcF延长的风险更低,同时维持最佳抗肿瘤应答)。
在一个优选的实施例中,按200mg的剂量一天两次施用化合物A,并且按400mg的剂量一天一次施用瑞博西尼,任选地其中连续施用化合物A,并且将瑞博西尼施用三周并且停止一周,特别以提供功效和安全性的最佳平衡(例如不良副作用的风险更低,例如QTcF延长的风险更低,同时维持最佳抗肿瘤应答)。
在给予剂量的情况下,可以按以下提供它们:一个单位剂型,例如片剂或胶囊,单独地针对活性成分中的每一个(化合物A、化合物B、化合物C、或化合物D),或其中它们中的两个处于组合中,和/或分成2、3、4或更多个,例如2或3个剂量单位。
特别地,使用根据本发明的组合的治疗适用于此类黑素瘤的治疗,此类黑素瘤对单独的化合物A或单独的化合物B或单独的化合物C或单独的化合物D的治疗没有应答或没有足够的应答。
典型地,根据本发明的组合疗法中使用的所有化合物都口服施用。
如本文所述的组合可以全身(例如,口服(优选的)、肠胃外、皮下、静脉内、直肠、肌肉内、腹膜内、鼻内、透皮)、或局部施用于患者。双重组合中的组合配伍物可以口服施用,并且可以遵循由治疗医师确定的给药方案一起(同时)或以任何顺序分开施用;适合的剂量和给药时间表在下文披露。
实例
以下实例用于帮助理解本发明(尽管其也是特定的发明实施例),但并不旨在且也不应解释为以任何方式限制其范围。
实例1:化合物A(也称为LXH254)和化合物C(曲美替尼)在SKMEL-30人肿瘤异种移
植小鼠中的组合功效。
方法:
a)动物和维持条件:
在操作前至少3天,允许远系杂交无胸腺的(Crl:NU(NCr)-Foxn1nu)雌性小鼠(查尔斯河实验室(Charles River Lab))(体重19-24g,年龄8周)在随意获取食物和水的诺华NIBRI动物设施中适应新环境。根据诺华ACUC条例和指南处理动物。
b)药物配制:
化合物A在蒸馏水中呈悬浮液的形式进行p.o.(口服)给药,该悬浮液在每次给药前通过在具有搅拌棒的琥珀色小瓶中将50mg/ml配制原液在MEPC4中稀释至2.5mg/ml来新鲜制备。MEPC4组合物=45%克列莫佛(Cremophor)RH40、27%PEG400、18%玉米油甘油酯+10%乙醇。
化合物C在pH 8的蒸馏水中的0.5%HPC和0.2%吐温80的媒介物中呈悬浮液形式进行p.o.给药;按0.03mg/mL和0.0015mg/mL配制曲美替尼。
c)细胞培养:
SKMEL-30人黑素瘤肿瘤细胞系购自ATCC,并已包括在诺华公司细胞系百科全书(Cell Line Encyclopedia(CLE))细胞系保藏中。在IMPACT-VIII PCR测定板(IDEXX生物研究公司(BioResearch),哥伦比亚,密苏里州)中,细胞系已经显示不含支原体属物种(Mycoplasma sp.)和鼠类病毒。
将SKMEL-30细胞维持在RPMI 1640(11875-093)中;所有培养基补充有10%FBS(Gibco#26140-079)(56℃持续30min,灭活的),在含有5%二氧化碳的湿润气氛中于37℃下。将细胞在80%-95%汇合时收获,用PBS洗涤并且用0.25%胰蛋白酶-EDTA(Gibco#25200-056)分离,在1200rpm离心5分钟后,用生长培养基中和,随后将细胞沉淀重悬于冷HBSS(Gibco#14175-095)中并且然后用等体积的MatrigelTM基质(康宁公司(Corning)#354234)混合以制备SKMEL-30的50x106个细胞/ml的终浓度。然后将100μl(5x106个细胞)皮下植入雌性裸小鼠的右胁。通过用卡尺测量并且用改进的椭圆体公式计算肿瘤体积,其中肿瘤体积(TV)(mm3)=[((l x w2)x 3.14159))/6],其中l是肿瘤的最长轴并且w垂直于l。每周两次监测小鼠的肿瘤生长、体重和健康状况。
SKMEL-30异种移植模型中的功效研究设计:
如表1-1所示,在SKMEL-30人黑素瘤小鼠模型中,进行用来确定化合物A与化合物C(曲美替尼)的组合的抗肿瘤功效的研究。按剂量体积为10mL/kg施用治疗。在肿瘤移植后第12天将小鼠随机分入治疗组,此时平均肿瘤体积为约190mm3。在肿瘤细胞植入后第34天,即治疗开始后22天确定抗肿瘤活性。
表1-1
媒介物=未经治疗的;p.o.(口服);口服(口服填喂法);qd(或QD):一天一次;bid(或BID):一天两次。
数据分析:
体重:体重变化百分比计算为(BW当前-W初始)/(BW初始)×100%。数据表示为相比治疗开始日的体重变化平均百分比±SEM。体重变化百分比计算为(BW当前-BW初始)/(BW初始)×100%。数据表示为相比治疗开始日的体重变化平均百分比±SEM。
肿瘤体积:使用以下公式计算治疗/对照(%T/C)值百分比:
%T/C=100xΔT/ΔC,如果ΔT≥0
回归%=100xΔT/T初始,如果ΔT<0
其中:
T=研究最后一天的药物治疗组的平均肿瘤体积;
ΔT=研究最后一天的药物治疗组的平均肿瘤体积-初始给药日的药物治疗组的平均肿瘤体积;
T初始=初始给药日的药物治疗组的平均肿瘤体积;
C=研究最后一天的对照组的平均肿瘤体积;和
VC=研究最后一天的对照组的平均肿瘤体积-初始给药日的对照组的平均肿瘤体积。
所有数据均表示为平均值±平均值标准误差(SEM)。在各组之间,使用克-瓦二氏(Kruskal-Wallis)非参数ANOVA用邓恩(Dunn)事后检验进行比较。对于所有统计评估,显著性水平设定为p<0.05。
除非另外说明,否则报告相比于媒介物对照组的显著性。通过记录每个组中的小鼠达到大约700mm3的肿瘤负荷的日期,产生存活分析。使用对数秩(曼特尔考克斯(Mantelcox))检验进行若干曲线的组间比较。
结果:
在NRAS/BRAF双突变型(NRASQ61K/BRAFD287H)SKMEL-30人黑素瘤异种移植无胸腺裸小鼠模型中,评估化合物A当与曲美替尼组合时的抗肿瘤功效。用媒介物、单一药剂化合物A(按25mg/kg口服(p.o.)每天两次(bid))、单一药剂曲美替尼(化合物C)(按0.3mg/kg口服每天一次(qd))、以及化合物A(按25mg/kg p.o.bid)与曲美替尼(按0.15mg/kg p.o.qd)的组合治疗小鼠。在表1-2中报道了在植入后34天(治疗开始后23天)的抗肿瘤活性、平均肿瘤体积变化、平均百分比体重变化和存活率。在第34天,研究中的媒介物治疗组的最后一天,化合物A治疗导致5%肿瘤消退,同时0.3mg/kg qd的曲美替尼导致8%T/C。当与媒介物治疗组比较时,以0.15mg/kg qd的化合物A与曲美替尼的组合导致抗肿瘤活性的进一步增加,48%肿瘤消退(表1-2)。3A).当与每个单一药剂比较时,化合物A+曲美替尼组合的抗肿瘤活性也显著改善(表1-2)。在研究期间,所有治疗组耐受性良好,体重减轻最小。在研究期间,将单剂组连续给药;在化合物A和曲美替尼组合的组中,仅提供了曲美替尼的短暂的给药假期(dosing holiday)(第28天至第31天),之后重新开始完整的组合至研究结束。
表1-2
上述研究表明,在NRAS/BRAF突变型黑素瘤异种移植SKMEL-30小鼠中,通过化合物A与曲美替尼的组合治疗,抗肿瘤功效大大改善。尽管使用曲美替尼作为单一药剂的治疗伴随肿瘤生长,但是使用化合物A和曲美替尼的组合治疗导致显著的肿瘤消退,即,使用化合物A作为单一药剂的治疗,发现肿瘤消退的10倍增加。在研究期间,如通过缺乏体重减轻的判断,所有治疗,包括用组合进行治疗,都是耐受的。
这些数据表明,在其黑素瘤具有MAPK途径激活的患者中,化合物A和曲美替尼的组合活性可以实现更大并且更持久的应答。
实例2:化合物A(也称为LXH254)和化合物C(曲美替尼)在NRAS突变型黑素瘤患者
来源的异种移植物中的组合功效
使用十个NRAS突变型患者来源的黑素瘤异种移植裸小鼠模型,如下确定当与曲美替尼组合时,化合物A的抗肿瘤功效:HMEX5727(NRASQ61K)、HMEX3486(NRASQ61K)、HMEX20667(NRASQ61R)、HMEX2921(NRASQ61R)、HMEX21684(NRASQ61K)、HMEX20585(NRASQ61R)、HMEX20864(NRASQ61R)、HMEX21124(NRASQ61H)、HMEX20744(NRASQ61K)、和HMEX4339(NRASQ61R)。将这些模型中的八个中的小鼠治疗90天或直到每组中的肿瘤大小达到>/=700mm3。在撰写时,仅治疗了来自两个模型的小鼠(HMEX4339、和HMEX20744),直到实现最佳应答,并且因此并不包括在存活分析中。
方法
在操作前至少3天,允许远系杂交无胸腺的(nu/nu)雌性小鼠(“HSD:AthymicNude-nu”)(查尔斯河,印第安纳波利斯)在随意获取食物和水的诺华公司NIBR动物设施中适应新环境。根据诺华NIBR ACUC条例和指南处理动物。
化合物A在MEPC4媒介物(45%克列莫佛RH40+27%PEG400+18%Capmul MCM C8+10%乙醇)中p.o.给药并且按5mg/mL配制。
化合物C(曲美替尼)在pH 8的蒸馏水中的0.5%HPC和0.2%吐温80的媒介物中进行p.o.给药;按0.03mg/mL、0.0075mg/mL、和0.000375mg/mL配制曲美替尼。
将患者来源的肿瘤异种移植物(PDX)HMEX5727、HMEX3486、HMEX20667、HMEX2921、HMEX21684、HMEX20864、HMEX20585、HMEX4339、HMEX20744、和HMEX21124通过肿瘤浆液的连续传代在裸小鼠中繁殖。简而言之,使用温和的MACS分离器(MACS美天旎生物技术公司(MACS Miltenyi Biotec)、#120-005-331)将先前传代的新鲜肿瘤片段匀浆,通过组织研磨机(Chemglass生命科学公司(Chemglass lifeSciences)#CLS-5020-085),在PBS中稀释,并与等体积的MatrigelTM基质(康宁#354234)混合。然后将200ul肿瘤浆液皮下植入雌性裸小鼠的右侧。通过用卡尺测量并使用公式计算肿瘤体积,其中肿瘤体积(Vt)(mm3)=(l x w2)/2,其中l是肿瘤的最长轴并且w垂直于l。监测小鼠的肿瘤生长、体重和身体状况,两次/周。
表2-1描述了所有模型的功效研究设计。以根据体重调整的10mL/kg的剂量体积给药测试剂。在随机分组时收集肿瘤尺寸和体重,之后在研究持续时间内每周收集两次。在8/10个模型中,当平均肿瘤体积为大约350mm3时,将小鼠随机分为治疗组(n=3-5/组),并实施治疗直至肿瘤长大(肿瘤体积>/=700mm3)或90天。通过将时间t处的肿瘤体积变化与其基线进行比较,确定所有模型的肿瘤体积变化百分比。最佳应答是t≥10天的肿瘤体积变化百分比的最小值。在处死未经治疗的对照小鼠时,也处死来自每组的2只小鼠,并收集肿瘤用于将来的PD分析。对超过这一点的3只小鼠/组进行功效研究。
表2-1功效研究的治疗组
p.o.:口服(口服填喂法)
qd:一天一次
bid:一天两次
数据分析
体重变化百分比计算为(BW当前-BW初始)/(BW初始)×100%。数据表示为相比治疗开始日的体重变化平均百分比±SEM。
通过将时间t处的肿瘤体积变化与其基线使用以下公式进行比较,确定肿瘤体积变化百分比:%肿瘤体积变化=ΔVt=100%×((Vt-V初始)/V初始)。最佳应答是t≥10d的ΔVt的最小值。
其中:
ΔVt=肿瘤体积变化
Vt=研究给定日药物治疗(或未经治疗)组的肿瘤体积;
V初始=给药初始日药物治疗(或未经治疗)组的肿瘤体积。最佳应答>/=-30%被认为肿瘤消退。
使用GraphPad Prism软件为达到肿瘤大小>/=700mm3的终点的个体小鼠生成卡普兰-梅尔存活图。使用对数秩(曼特尔-考克斯)检验对组之间的显著性进行统计学分析。p<0.05被认为是显著的。
结果
表2-2报告了肿瘤体积变化百分比(最佳应答)、体重变化百分比和存活率。
在60%的测试的模型中,按50mg/kg bid(化合物A)+0.075mg/kg qd(曲美替尼)或50mg/kg bid(化合物A)+0.0375mg/kg qd(曲美替尼)给药的化合物A和曲美替尼的组合活性导致肿瘤消退。相比之下,在任何测试的模型中,按50mg/kg bid给药的单一药剂化合物A或按0.3mg/kg qd给药的单一药剂曲美替尼(即按与组合治疗中相比更高剂量的曲美替尼单一药剂)都不能实现肿瘤消退(表2.2)。此外,与每种单一药剂(化合物A=12天;曲美替尼=7天)或未经治疗的对照(7天)相比,化合物A和曲美替尼的组合导致中位生存期显著增加(49天)。
除了几个小鼠以外,跨多个模型,全部两种单一药剂和组合治疗总体上是良好耐受的。由于体重减轻,在更早的时间点将一个用化合物A治疗的小鼠和四个用组合治疗的小鼠(在不同研究中铺展开)处死。
表2.2化合物A和曲美替尼在十个患者来源的NRAS突变型黑素瘤肿瘤异种移植小
鼠模型中的抗肿瘤功效和耐受性
*表示治疗的最后一天(肿瘤大小>/=700mm3)
#组在单独的实验中运行
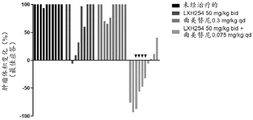
图1中示出了跨患者来源的NRAS突变型黑素瘤肿瘤异种移植小鼠模型,对化合物A(LXH254)和曲美替尼的应答的瀑布图。在图1中,每个柱代表在个体PDX中,每种治疗所获得的最佳应答(绘制为3-5只小鼠/治疗的平均值)。箭头指示用化合物A 50mg/kg bid+曲美替尼0.0375mg/kg qd治疗的模型。每种治疗的模型按以下顺序从左到右绘制:HMEX20667、HMEX5727、HMEX20744、HMEX4339、HMEX21124、HMEX20864、HMEX20585、HMEX3486、HMEX2921、和HMEX21684。
图2是在单一药剂化合物A、曲美替尼或两者组合的每日治疗期间肿瘤达到700mm3大小的卡普兰-梅尔(Kaplan-Meier)时间图。当每个模型的平均肿瘤大小为350mm3左右时开始治疗,并且在研究持续期间所有动物都接受连续的每日药物治疗。当对动物治疗90天或肿瘤大小达到>/=700mm3时,终止研究。与每种单一药剂或未经治疗的对照相比,组合组的存活曲线具有统计学意义[*p<0.05对数秩(曼特尔-考克斯(Mantel-Cox)检验)]。
在60%的测试的模型中,按50mg/kg bid(化合物A)+0.075mg/kg qd(曲美替尼)或50mg/kg bid(化合物A)+0.0375mg/kg qd(曲美替尼)给药的化合物A和曲美替尼的组合活性导致肿瘤消退。相比之下,在任何测试的模型中,按50mg/kg bid给药的单一药剂化合物A或按0.3mg/kg qd给药的单一药剂曲美替尼都不能实现肿瘤消退。此外,与每种单一药剂或未经治疗的对照相比,化合物A和曲美替尼的组合导致中位百分比生存期显著增加。总之,这些数据表明,在NRAS突变型黑素瘤患者中,化合物A和曲美替尼的组合可以实现更大并且更持久的应答。
实例3:化合物A(也称为LXH254)和化合物B在NRAS突变型黑素瘤患者来源的异种
移植物中的组合功效
使用NRAS突变型患者来源的黑素瘤异种移植裸小鼠模型,如下确定化合物A当与化合物B组合时的抗肿瘤功效。使用十个NRAS突变型患者来源的黑素瘤异种移植裸小鼠模型,确定化合物A当与化合物B组合时的抗肿瘤功效:HMEX5727(NRASQ61K)、HMEX3486(NRASQ61K)、HMEX20667(NRASQ61R)、HMEX2921(NRASQ61R)、HMEX21684(NRASQ61K)、HMEX20585(NRASQ61R)、HMEX20864(NRASQ61R)、HMEX21086(NRASQ61H)、HMEX20744(NRASQ61K)、和HMEX4339(NRASQ61R)。将小鼠治疗大约90-100天或直到每组中的肿瘤大小达到>/=700mm3。
方法
在操作前至少3天,允许远系杂交无胸腺的(nu/nu)雌性小鼠(“HSD:AthymicNude-nu”)(查尔斯河,印第安纳波利斯)在随意获取食物和水的诺华公司NIBR动物设施中适应新环境。根据诺华NIBR ACUC条例和指南处理动物。
将化合物A在MEPC4媒介物(45%克列莫佛RH40+27%PEG400+18%玉米油甘油酯(Maisine CC)+10%乙醇)中p.o.给药。在给药前5x(用DI水1:4)稀释MEPC 4原液。按2.5mg/mL和5mg/mL配制化合物A。
将化合物B在磷酸盐缓冲液中的0.5%HPC+0.5%普朗尼克(Pluronic)F-127的媒介物(pH 5)中p.o.给药。将最终pH调整至4-4.5。按1.5mg/mL和7.5mg/mL配制化合物B。
如实例2中所述,将所有患者来源的肿瘤异种移植物(PDX)通过肿瘤浆液的连续传代在裸小鼠中繁殖。如实例2中确定肿瘤体积。监测小鼠的肿瘤生长、体重和身体状况,两次/周。
以根据体重调整的10mL/kg的剂量体积给药测试剂。在随机分组时收集肿瘤尺寸和体重,之后在研究持续时间内每周收集两次。在9个模型中,当平均肿瘤体积为大约350mm3时,将小鼠随机分为治疗组(n=3-5/组),并实施治疗直至肿瘤长大(大约肿瘤体积700mm3)。在21天后中止对模型HMEX5727的治疗,并且来自此模型的数据并不包括在卡普兰-梅尔分析中。通过将时间t处的肿瘤体积变化与其基线进行比较,确定所有模型的肿瘤体积变化百分比。最佳应答是t≥10天的肿瘤体积变化百分比的最小值。在处死未经治疗的对照小鼠时,也处死来自每组的2只小鼠,并收集肿瘤用于将来的药效学分析。对超过这一点的2-3只小鼠/组进行功效研究。
表3-1功效研究的治疗组
p.o.:口服(口服填喂法)
qd:一天一次
bid:一天两次
数据分析
如实例2中所述进行数据分析。
使用GraphPad Prism软件为达到肿瘤大小大约700mm3的终点的个体小鼠生成卡普兰-梅尔存活图。使用对数秩(曼特尔-考克斯)检验对组之间的显著性进行统计学分析。p<0.05被认为是显著的。
结果
表3-2、图3和图4报告了肿瘤体积变化百分比(最佳应答)、体重变化百分比和存活率。
在30%的测试的模型中,按50mg/kg bid(化合物A)+15mg/kg qd(化合物B)或25mg/kg bid(化合物A)+75mg/kg qd(化合物B)给药的化合物A和化合物B的组合活性导致肿瘤消退。应当注意,即使在组合治疗中,按单一药剂实验中使用的量的一半或三分之一给药化合物A或化物B,按50mg/kg bid给药的单一药剂化合物A或按75mg/kg qd给药的化合物B都未实现测试的模型中的肿瘤消退(表3-2和图3)。
此外,与每种单一药剂(化合物A=14天;化合物B=9天)或未经治疗的对照(7天)相比,化合物A和化合物B的组合导致中位生存期显著增加(44天)(图4)。
跨多个模型,两种单一药剂和组合治疗均耐受性良好。
表3-2化合物A和化合物B在十个患者来源的NRAS突变型黑素瘤肿瘤异种移植小鼠模型中的抗肿瘤功效和耐受性
*表示治疗的最后一天(肿瘤大小>/=700mm3)
#组在单独的实验中运行
图3是跨十个患者来源的NRAS突变型黑素瘤肿瘤异种移植小鼠模型,对化合物A和化合物B的应答的瀑布图。每个柱代表在个体患者来源的异种移植物(PDX)中,每种治疗所获得的最佳应答(绘制为2-5只小鼠/治疗的平均值)。箭头指示用化合物A 25mg/kg bid+化合物B75mg/kg qd治疗的模型。图4是在单一药剂化合物A、化合物B或两者的组合的每日治疗期间肿瘤达到700mm3大小的卡普兰-梅尔时间图。当每个模型的平均肿瘤大小为350mm3左右时开始治疗,并且在研究持续期间所有动物都接受连续的每日药物治疗。当动物达到大约700mm3的肿瘤大小时,终止研究。与每种单一药剂或未经治疗的对照相比,组合组的存活曲线具有统计学意义[*p<0.05对数秩(曼特尔-考克斯(Mantel-Cox)检验)]。
在30%的测试的模型中,按50mg/kg bid(化合物A)+15mg/kg qd(化合物B)或25mg/kg bid(化合物A)+75mg/kg qd(化合物B)给药的化合物A和化合物B的组合活性导致肿瘤消退。相比之下,在测试的模型中,按50mg/kg bid给药的单一药剂化合物A或按75mg/kg qd给药的单一药剂化合物B都不能实现肿瘤消退。此外,与每种单一药剂或未经治疗的对照相比,化合物A和化合物B的组合导致中位百分比生存期显著增加。总之,这些数据表明,在NRAS突变型黑素瘤患者中,化合物A和化合物B的组合可以实现更大并且更持久的应答。
实例4:化合物A(也称为LXH254)和瑞博西尼(化合物D或LEE011)在NRAS突变型黑
素瘤患者来源的异种移植物中的组合功效
使用NRAS突变型患者来源的黑素瘤异种移植裸小鼠模型,如下确定化合物A当与化合物C组合时的抗肿瘤功效。使用九个NRAS突变型患者来源的黑素瘤异种移植裸小鼠模型,确定化合物A当与化合物B组合时的抗肿瘤功效:HMEX5727(NRASQ61K)、HMEX3486(NRASQ61K)、HMEX20667(NRASQ61R)、HMEX2921(NRASQ61R)、HMEX21684(NRASQ61K)、HMEX20585(NRASQ61R)、HMEX20864(NRASQ61R)、HMEX21086(NRASQ61H)、HMEX20744(NRASQ61K)、和HMEX4339(NRASQ61R)。将小鼠治疗大约90-100天或直到每组中的肿瘤大小达到>/=700mm3。
方法
在操作前至少3天,允许远系杂交无胸腺的(nu/nu)雌性小鼠(“HSD:AthymicNude-nu”)(查尔斯河,印第安纳波利斯)在随意获取食物和水的诺华公司NIBR动物设施中适应新环境。根据诺华NIBR ACUC条例和指南处理动物。
化合物A在MEPC4媒介物(45%克列莫佛RH40+27%PEG400+18%玉米油甘油酯+10%乙醇)中p.o.给药。按5mg/mL配制化合物A。
将瑞博西尼在0.5%甲基纤维素的媒介物中p.o.给药;按7.5mg/mL配制瑞博西尼。
如实例2中所述,将所有患者来源的肿瘤异种移植物(PDX)通过肿瘤浆液的连续传代在裸小鼠中繁殖。如实例2中确定肿瘤体积。监测小鼠的肿瘤生长、体重和身体状况,两次/周。
以根据体重调整的10mL/kg的剂量体积给药测试剂。在随机分组时收集肿瘤尺寸和体重,之后在研究持续时间内每周收集两次。当平均肿瘤体积为大约350mm3时,将小鼠随机分为治疗组(n=3-5/组),并实施治疗直至肿瘤长大(肿瘤体积>/=700mm3)或大约90天。通过将时间t处的肿瘤体积变化与其基线进行比较,确定所有模型的肿瘤体积变化百分比。最佳应答是t≥10天的肿瘤体积变化百分比的最小值。在处死未经治疗的对照小鼠时,也处死来自每组的2只小鼠,并收集肿瘤用于将来的PD分析。对超过这一点的3只小鼠/组进行功效研究。
表4-1功效研究的治疗组
| 组 | 小鼠的数量 | 化合物 | 剂量(mg/kg) | 途径 | 时间表 |
| 1 | 3-5 | 未经治疗的 | - | p.o. | - |
| 2 | 3-5 | 化合物A | 50 | p.o. | bid |
| 3 | 3-5 | 瑞博西尼 | 75 | p.o. | qd |
| 4 | 3-5 | 化合物A和瑞博西尼 | 50+75 | p.o. | bid+qd |
p.o.:口服(口服填喂法)
qd:一天一次
bid:一天两次
如实例2中所述进行数据分析。
使用GraphPad Prism软件为达到肿瘤大小>/=700mm3的终点的个体小鼠生成卡普兰-梅尔存活图。使用对数秩(曼特尔-考克斯)检验对组之间的显著性进行统计学分析。p<0.05被认为是显著的。
结果
表4-2和图5以及图6报告了肿瘤体积变化百分比(最佳应答)、体重变化百分比和存活率。
在44%的测试的模型中,按50mg/kg bid(化合物A)+75mg/kg qd(瑞博西尼)给药的化合物A和瑞博西尼的组合活性导致肿瘤消退。相比之下,在任何测试的模型中,按50mg/kg bid给药的单一药剂化合物A或按75mg/kg qd给药的单一药剂瑞博西尼都不能实现肿瘤消退(表3-2和图5)。此外,与每种单一药剂或未经治疗的对照相比,化合物A和瑞博西尼的组合导致中位生存期显著增加(图6)。
根据各模型缺乏体重减轻的判断,单一药剂和组合治疗均耐受性良好。由于体重减轻,在更早的时间点将一个用化合物A治疗的小鼠处死。
表4-2化合物A和瑞博西尼在九个患者来源的NRAS突变型黑素瘤肿瘤异种移植小鼠模型中的抗肿瘤功效和耐受性
*表示治疗的最后一天(肿瘤大小>/=700mm3)
#组在单独的实验中运行
图5示出了化合物A(LXH254)和瑞博西尼(LEE011)跨九个患者来源的NRAS突变型黑素瘤肿瘤异种移植小鼠模型的抗肿瘤活性。每个柱代表在个体PDX中,每种治疗所获得的最佳应答(绘制为3-5只小鼠/治疗的平均值)。每种治疗的模型按以下顺序从左到右绘制:HMEX20864、HMEX20744、HMEX4339、HMEX5727、HMEX21124、HMEX3486、HMEX20667、HMEX20585、和HMEX2921。
图6是在单一药剂化合物A、瑞博西尼或两者的组合的每日治疗期间肿瘤达到700mm3大小的卡普兰-梅尔时间图。当每个模型的平均肿瘤大小为350mm3左右时开始治疗,并且在研究持续期间所有动物都接受连续的每日药物治疗。当对动物治疗>/=90天或肿瘤大小达到>/=700mm3时,终止研究。与每种单一药剂或未经治疗的对照相比,组合组的存活曲线具有统计学意义[*p<0.05对数秩(曼特尔-考克斯(Mantel-Cox)检验)]。
在一组九个NRAS突变型患者来源的黑色素瘤异种移植物中,描述了化合物A和瑞博西尼组合在NRAS突变型黑素瘤中的体内活性。在44%的测试的模型中,按50mg/kg bid(化合物A)+75mg/kg qd(瑞博西尼)给药的化合物A和瑞博西尼的组合活性导致肿瘤消退。相比之下,在任何测试的模型中,按50mg/kg bid给药的单一药剂化合物A或按75mg/kg qd给药的单一药剂瑞博西尼都不能实现肿瘤消退。此外,与每种单一药剂或未经治疗的对照相比,化合物A和瑞博西尼的组合是良好耐受的并且导致中位百分比生存期显著增加。总之,这些数据表明,在NRAS突变型黑素瘤患者中,化合物A和瑞博西尼的组合可以实现更大并且更持久的应答。
实例5:在患有先前治疗的不可切除的或转移性的黑素瘤的患者中,化合物A与选
自由以下组成的组的第二治疗剂组合的功效和安全性的研究:(i)化合物B,(ii)化合物C
(曲美替尼)和(iii)化合物D(瑞博西尼)
可以如下测试本发明的组合。
在患有先前治疗的不可切除的或转移性的BRAFV600或NRAS突变型黑素瘤的患者中,进行用来评估多个化合物A组合的功效和安全性的一项随机、开放标签、多臂、两部分、II期研究。
预期测试的每个双重组合帮助克服对BRAF靶向疗法的内源性和获得性抗性,以及为NRAS突变型黑素瘤患者提供新的治疗选择。
此研究由两个部分组成:
第1部分:筛选部分
基于分子测试(当地的或中心的),将参与者分配到以下两个组中的一个:BRAFV600突变型或NRAS突变型。
第1组:患有BRAFV600突变型不可切除的或转移性的黑素瘤的参与者
第2组:患有NRAS突变型不可切除的或转移性的黑素瘤的参与者
在筛选程序完成后,可以使用交互式应答技术(IRT)系统将有资格的参与者随机化到每个相应的组的组合臂内。对于每个患者群体,可以通过基线乳酸脱氢酶(LDH)水平将随机化分层:LDH≤ULN(正常的上限),和LDH>ULN。
例如,正常LDH水平的范围可以是从140个单位/升(U/L)至280U/L或2.34mkat/L至4.68mkat/L。
在第1部分,基于BRAFV600或NRAS黑素瘤的突变状态,可以按相等概率将参与者随机化到两个组中的三个初始组合臂中:
第1组:患有BRAFV600突变型不可切除的或转移性的黑素瘤的参与者:
·臂1:化合物A 400mg BID(一天两次)和化合物B 200mg QD(一天一次)或化合物A 200mg BID(一天两次)和化合物B 200mg QD(一天一次)
·臂2:化合物A 400mg BID和曲美替尼0.5mg QD或化合物A 200mg BID和曲美替尼1mg QD
·臂3:化合物A 400mg BID和瑞博西尼400mg QD或化合物A 200mg BID和瑞博西尼400mg QD
第2组:患有NRAS突变型不可切除的或转移性的黑素瘤的参与者:
·臂4:化合物A 400mg BID和化合物B 200mg QD或化合物A 200mg BID(一天两次)和化合物B 200mg QD(一天一次)
·臂5:化合物A 400mg BID和曲美替尼0.5mg QD或化合物A 200mg BID和曲美替尼1mg QD
·臂6:化合物A 400mg BID和瑞博西尼400mg QD或化合物A 200mg BID和瑞博西尼400mg QD
每个周期是28天,并且将所有药物口服施用并且连续给予,除了瑞博西尼以外,将瑞博西尼给予3周/停止1周。
第2部分:扩展
第2部分进一步表征如第1部分中确定的认为是安全并且潜在有效的LXH254组合的功效。可以招募另外的参与者,用来进一步评估第1部分中测试的组合的功效。在第2部分中可以使用如在第1部分中所述的剂量和给药方案。
研究治疗:
每个周期是28天。可以将所有研究药物口服并且连续施用,除了瑞博西尼以外,可以每天施用瑞博西尼持续21天,随后停止一周。
给药方案的实例如下:
化合物A 400mg BID与化合物B 200mg QD组合;
化合物A 200mg BID与化合物B 200mg QD组合;
化合物A 400mg BID与曲美替尼0.5mg QD组合;
化合物A 200mg BID与曲美替尼1mg QD组合;
化合物A 400mg BID与瑞博西尼400mg QD组合;
化合物A 200mg BID与瑞博西尼400mg QD组合;
典型的剂量和方案如下
其他典型的剂量和方案包括:
例如由于毒性,可能剂量减小,同时维持临床功效
尤其是手足皮肤反应、恶心和呕吐、左室射血分数的降低、皮疹是毒性的迹象。
根据不良事件通用术语标准(CTCAE)5.0版,对不良事件进行评估并且分级。
为了确保参与者的安全性,在参与者已经提供知情同意书后并且直至30天发生每个严重不良事件(SAE)(无论因果关系),必须在获知其出现的24小时内,将其报告至诺华公司(Novartis)安全部门。
功效评估:
通过当地RECIST v1.1进行放射学肿瘤评估:
·筛选时
·在治疗期间:在随机化的日期后每8周(±7天),之后直至根据RECIST v1.1的疾病进展(如由研究者评估)、死亡、失访或撤回同意
·治疗的结束(EOT):仅要在研究治疗的结束之前30天内未进行扫描的情况下这样做
·功效随访:如果出于除了根据RECIST v1.1的疾病进展之外的理由,参与者中止研究治疗,则必须按照与治疗期间相同的时间表继续功效随访,直至根据RECIST v1.1的疾病进展,即使已经开始另外的抗肿瘤疗法。
可以根据本领域已知的方法确定ORR,例如使用下表中使用的方法中的任何一个或多个:
必须通过第二评估证实所有完全应答(CR)和部分应答(PR)。如果在正常扫描窗口外进行此第二评估,则不应早于第一次符合应答标准的情况下的扫描后4周进行此第二评估。
在证实的应答类别(排除“未知”和“未评估”)中,最佳总体应答是在给定参与者中观察到的基线后证实的最佳总体应答。将BOR定义为:从随机化开始直至疾病进展/复发死亡、新疗法的开始、撤回同意或研究的结束所记录的最佳应答,只要按照中心评估并且根据RECIST v1.1第一次出现。
此研究的主要目标是评估每个组合臂的功效,如根据RECIST v1.1,通过当地研究者的评估而证实的客观应答率(ORR)进行测量(也如上文所定义)。
次要目标是:
通过不良事件(AE)的发生率和严重性来表征每个组合臂的安全性和耐受性,这些不良事件包括实验室参数、生命体征、心脏评估的变化,剂量中断、减小,和研究治疗的永久中止;
根据当地评估,使用RECIST v1.1,通过应答持续时间(DOR)、无进展生存期(PFS)和疾病控制率(DCR)进一步评估每个组合臂的功效。另外,对于扩展的一个或多个治疗组合臂,根据中心评估,使用RECIST v1.1评估DOR、PFS、DCR和ORR;
评估每个组合臂的总生存期(OS),以及;
通过每个组合方案的血清/血浆浓度和药代动力学参数来表征每个组合方案的药代动力学。
群体:
成年(≥18岁)和青少年(12-17岁)参与者,患有先前用选自以下的疗法治疗的BRAFV600或NRAS突变型不可切除的或转移性的黑素瘤:用拉-他利莫近(T-vec)、免疫疗法(CPI)、和靶向疗法(例如RAF+/-MEK抑制剂)、及其组合进行治疗。例如,先前疗法可以是用检查点抑制剂(CPI)和RAF+/-MEK抑制剂或仅用CPI进行治疗。
关键入选标准包括:
·男性或女性,必须≥12岁
·仅对于青少年参与者(12-17岁):体重>40kg
·组织学证实的不可切除的或转移性的皮肤黑素瘤
·如通过诺华公司(Novartis)同意的当地测定确定,或如通过在诺华公司(Novartis)指定的实验室进行的中心预筛选评估确定,在研究治疗之前,肿瘤组织中BRAFV600或NRAS突变的记录。
先前对不可切除的或转移性的黑素瘤的治疗:
具有NRAS突变的参与者包括:
·参与者必须已经接受针对不可切除的或转移性的黑素瘤的先前全身性疗法,其中用抗PD-1/PD-L1检查点抑制剂作为单一药剂或与抗CTLA-4组合。针对不可切除的或转移性的黑素瘤,不允许另外的全身性治疗
·针对不可切除的或转移性的黑素瘤,允许最多两个先前全身性免疫疗法线
·必须在随机化之前超过4周已接受最后剂量的先前疗法(抗PD-1、抗PD-L1或抗CTLA-4)
·在使用检查点抑制剂疗法进行治疗时/之后,参与者必须具有根据RECIST v1.1的记录的证实的进展性疾病。必须在研究中的随机化之前12周内发生最后进展
患有BRAFV600突变型疾病的参与者包括:
·参与者必须已经接受针对不可切除的或转移性的黑素瘤的先前全身性疗法,其中用抗PD-1或PD-L1作为单一药剂或与抗CTLA-4组合。另外,参与者必须已经接受使用RAFi作为单一药剂或与MEKi组合的靶向疗法作为最后的先前疗法。针对晚期的或转移性的黑素瘤,不允许另外的全身性治疗
·针对不可切除的或转移性的黑素瘤,允许最多三个先前全身性疗法线
·必须在随机化之前超过2周已接受最后剂量的靶向疗法(最后的先前疗法)
·在使用靶向疗法进行治疗时/之后,参与者必须具有根据RECIST v1.1的记录的进展性疾病。必须在研究中的随机化之前12周内发生最后进展
·参与者必须具有适合重复活检的疾病部位,并且必须愿意根据治疗机构自己的指导方针和此类程序的要求在基线和治疗期间接受新的肿瘤活检。作为用于活检的部位,骨转移是不可接受的。
关键排除标准包括:
·所有原发性中枢神经系统(CNS)肿瘤或神经学不稳定的有症状的CNS转移
·在筛选就诊时,不足的骨髓、肝或肾功能
·如借助一式三份ECG确定的并经当地评估的异常心电图(ECG)
·心脏疾病或心脏复极异常
·由于先前抗黑素瘤疗法,存在≥CTCAE 2级毒性(除了脱发和耳毒性以外,如果≥CTCAE 3级,则将其排除)
·有视网膜静脉阻塞(RVO)的病史或当前证据,或有当前RVO危险因素(例如不受控制的青光眼或高眼压症,高粘血症或血凝过快综合征的病史)
还可以修改入选和或排除标准。例如,具有其他先前疗法的所有臂和组中的患者(例如接受了拉-他利莫近(T-vec)以及与CPI一起施用的研究药剂)也可以包括在临床试验中。此外,在6个月的辅助CPI疗法时或期间已经进展的患者中,在转移环境中的使用免疫疗法(CPI)的先前疗法可以不是强制的。
以下详细描述了来自根据本文所述的方法和用途进行的临床试验的初步数据。
在18名用化合物A和瑞博西尼的组合治疗的患者中,将来自至今已经接受6个周期的组合治疗并对其耐受的四名患者的应答分类为“稳定疾病(SD)”。将来自另外8名患者的应答分类为未证实的“稳定疾病”状态,并且6名患者患有进展性疾病(PD)。
下表示出了化合物A和曲美替尼的组合对于治疗NRAS突变型黑素瘤会是尤其有益的,尤其是当按200mg BID的剂量施用化合物A并且按1mg QD的剂量施用曲美替尼时。此组合和此给药施用引起功效改善(当与400mg BID的剂量的纳波拉非尼布和0.5mg QD的剂量的曲美替尼相比时,ORR增加20倍),并且可能伴随不良副作用的风险更低。
下表示出了纳波拉非尼布和曲美替尼的组合在NRAS突变型黑素瘤中的功效。
表5:基于研究者通过群组的方式(化合物A(LXH254)+曲美替尼(TMT)NRAS黑素瘤患者)进行确认的评估,根据RECIST 1.1的最佳总体应答
完整分析集
N:治疗组中受试者的总数量。它是百分比(%)计算的分母。
n:在相应类中的患者数量。
使用克洛珀-皮尔森(Clopper-Pearson)计算每个变量的频率分布的95%CI。
Claims (36)
1.纳波拉非尼布(具有式(I)的化合物),
或其药学上可接受的盐,通过与选自由以下组成的组的治疗剂共同施用,用于在治疗NRAS突变型黑素瘤和/或BRAF突变型黑素瘤中使用:
(i)4-(3-氨基-6-((1S,3S,4S)-3-氟-4-羟基环己基)吡嗪-2-基)-N-((S)-1-(3-溴-5-氟苯基)-2-(甲基氨基)乙基)-2-氟苯甲酰胺(里内特基布)、或其药学上可接受的盐(特别是其盐酸盐),
(ii)曲美替尼、或其药学上可接受的盐或溶剂化物(特别是其DMSO溶剂化物),以及
(iii)瑞博西尼、或其药学上可接受的盐(特别是其琥珀酸盐),
任选地其中所述黑素瘤是不可切除的和/或转移性的皮肤黑素瘤。
2.一种治疗剂,其选自由以下组成的组:
(i)4-(3-氨基-6-((1S,3S,4S)-3-氟-4-羟基环己基)吡嗪-2-基)-N-((S)-1-(3-溴-5-氟苯基)-2-(甲基氨基)乙基)-2-氟苯甲酰胺(里内特基布)、或其药学上可接受的盐(特别是其盐酸盐),
(ii)曲美替尼、或其药学上可接受的盐或溶剂化物(特别是其DMSO溶剂化物),以及
(iii)瑞博西尼、或其药学上可接受的盐(特别是其琥珀酸盐),通过与纳波拉非尼布(具有式(I)的化合物)、或其药学上可接受的盐共同施用,用于在治疗NRAS突变型黑素瘤和/或BRAF突变型黑素瘤中使用,任选地其中所述黑素瘤是不可切除的和/或转移性的皮肤黑素瘤。
3.一种药物组合,其包含纳波拉非尼布(具有式(I)的化合物),
或其药学上可接受的盐,
以及选自由以下组成的组的第二治疗剂:
(i)4-(3-氨基-6-((1S,3S,4S)-3-氟-4-羟基环己基)吡嗪-2-基)-N-((S)-1-(3-溴-5-氟苯基)-2-(甲基氨基)乙基)-2-氟苯甲酰胺(里内特基布)、或其药学上可接受的盐(特别是其盐酸盐),
(ii)曲美替尼、或其药学上可接受的盐或溶剂化物(特别是其DMSO溶剂化物),以及
(iii)瑞博西尼、或其药学上可接受的盐(特别是其琥珀酸盐);
用于在治疗NRAS突变型黑素瘤和/或BRAF突变型黑素瘤中使用,任选地其中所述黑素瘤是不可切除的和/或转移性的黑素瘤。
4.一种药物组合,其包含纳波拉非尼布或其药学上可接受的盐、以及选自由以下组成的组的第二治疗剂:
(i)ERK(ERK 1/2)抑制剂,尤其是里内特基布、或其药学上可接受的盐,
(ii)MEK(MEK1/2)抑制剂,尤其是曲美替尼、或其药学上可接受的盐或溶剂化物,或
(iii)CDK4/6抑制剂,尤其是瑞博西尼、或其药学上可接受的盐,
用于同时、分开或顺序施用,用于在以下的治疗中使用
(a)BRAF突变型黑素瘤(优选地是不可切除的和/或转移性的皮肤BRAF突变型黑素瘤);或
(b)NRAS突变型黑素瘤(优选地是不可切除的和/或转移性的皮肤NRAS突变型黑素瘤)。
5.一种治疗患有NRAS突变型黑素瘤和/或BRAF突变型黑素瘤的患者中的所述疾病的方法,该方法包括向该有需要的患者施用治疗有效量的药物组合,该药物组合包含具有式(I)的化合物(纳波拉非尼布),
或其药学上可接受的盐,
以及选自由以下组成的组的第二治疗剂:
(i)4-(3-氨基-6-((1S,3S,4S)-3-氟-4-羟基环己基)吡嗪-2-基)-N-((S)-1-(3-溴-5-氟苯基)-2-(甲基氨基)乙基)-2-氟苯甲酰胺(里内特基布)、或其药学上可接受的盐(特别是其盐酸盐),
(ii)曲美替尼、或其药学上可接受的盐或溶剂化物(特别是其DMSO溶剂化物),以及
(iii)瑞博西尼、或其药学上可接受的盐(特别是其琥珀酸盐);
其中该黑素瘤是不可切除的和/或转移性的皮肤黑素瘤。
6.根据权利要求1所述使用的化合物、根据权利要求2所述使用的治疗剂、根据权利要求3或权利要求4所述使用的药物组合、或根据权利要求5所述的方法,其中该黑素瘤是NRAS突变型黑素瘤。
7.根据权利要求6所述使用的化合物、使用的治疗剂、使用的药物组合、或根据权利要求6所述的方法,其中该NRAS突变型黑素瘤是选自由以下组成的组的突变:G12C、G12R、G12D、G12V、G12S、G12A、G13R、G13D、G13C、G13A、G13、G13S、G13V、Q61R、Q61L、Q61K、Q61H、Q61P、Q61E及其组合。
8.根据权利要求1所述使用的化合物、根据权利要求2所述使用的治疗剂、根据权利要求3或权利要求4所述使用的药物组合、或根据权利要求5所述的方法,其中该黑素瘤是BRAF突变型黑素瘤。
9.根据权利要求8所述使用的化合物、使用的治疗剂、使用的药物组合、或根据权利要求8所述的方法,其中该黑素瘤是BRAFD287H突变型黑素瘤或BRAFV600突变型黑素瘤。
10.根据权利要求8所述使用的化合物、使用的治疗剂、使用的药物组合、或根据权利要求8所述的方法,其中该黑素瘤是BRAFV600E突变型、BRAFV600K突变型黑素瘤、BRAFV600R突变型或BRAFV600D突变型,优选地其中该黑素瘤是BRAFV600E突变型、BRAFV600D突变型或BRAFV600K突变型黑素瘤。
11.根据前述权利要求中任一项所述使用的化合物、使用的治疗剂、使用的药物组合、或根据前述权利要求中任一项所述的方法,其中该黑素瘤对化学疗法,例如达卡巴嗪具有难治性或抗性。
12.根据前述权利要求中任一项所述使用的化合物、使用的治疗剂、使用的药物组合、或根据前述权利要求中任一项所述的方法,其中患有要治疗的黑素瘤的患者已经接受先前疗法,任选地其中该先前疗法选自由以下组成的组:
-用拉-他利莫近进行治疗;
-标准护理化学疗法(例如达卡巴嗪);
-用细胞毒性剂,例如亚硝基脲和/或丝裂霉素C进行治疗;
-免疫疗法(例如派姆单抗、伊匹单抗、或纳武单抗及其组合);
-用抗PD-1/PD-L1检查点抑制剂作为单一药剂(例如派姆单抗或纳武单抗)、或与抗CTLA-4(伊匹单抗)组合进行治疗;
-靶向疗法(例如达拉菲尼和曲美替尼;维莫非尼和考美替尼;以及恩拉非尼和比美替尼);
及其组合。
13.根据前述权利要求中任一项所述使用的化合物、使用的治疗剂、使用的药物组合、或根据前述权利要求中任一项所述的方法,其中要治疗的黑素瘤对用免疫疗法(例如选自以下的一种或多种治疗剂:伊匹单抗、斯巴达珠单抗、纳武单抗、派姆单抗、匹地利珠单抗、BMS-9365559、MEDI4736、和MSB0010718C、及其组合)进行治疗具有抗性或难治性。
14.根据前述权利要求中任一项所述使用的化合物、使用的治疗剂、使用的药物组合、或根据前述权利要求中任一项所述的方法,其中患有要治疗的黑素瘤的患者已经接受使用RAF抑制剂作为单一药剂或与MEK抑制剂组合的先前疗法。
15.根据权利要求14所述使用的化合物、使用的治疗剂、使用的药物组合、或根据权利要求14所述的方法,其中该RAF抑制剂选自来自由以下组成组中的多项中的一项:达拉菲尼、维莫非尼和恩拉非尼。
16.根据权利要求14或15所述使用的化合物、使用的治疗剂、使用的药物组合、或根据权利要求14或15所述的方法,其中该MEK抑制剂选自来自由以下组成组中的多项中的一项:曲美替尼、考美替尼和比美替尼。
17.根据权利要求14所述使用的化合物、使用的治疗剂、使用的药物组合、或根据权利要求14所述的方法,其中患有要治疗的黑素瘤的患者已经接受使用选自以下的组合的先前疗法:(i)达拉菲尼和曲美替尼,(ii)维莫非尼和考美替尼,以及(iii)恩拉非尼和比美替尼。
18.根据前述权利要求中任一项所述使用的化合物、使用的治疗剂、使用的药物组合、或根据前述权利要求中任一项所述的方法,其中QD(每天一次)或BID(每天两次)施用纳波拉非尼布、里内特基布、曲美替尼或瑞博西尼的日总剂量。
19.根据前述权利要求中任一项所述使用的化合物、使用的治疗剂、使用的药物组合、或根据前述权利要求中任一项所述的方法,其中连续施用纳波拉非尼布、里内特基布、曲美替尼或瑞博西尼。
20.根据权利要求1至18中任一项所述使用的化合物、使用的治疗剂、使用的药物组合、或根据权利要求1至18中任一项所述的方法,其中间歇地施用曲美替尼或瑞博西尼。
21.根据权利要求1至18中任一项所述使用的化合物、使用的治疗剂、使用的药物组合、或根据权利要求1至18中任一项所述的方法,其中将瑞博西尼每天施用持续连续的21天,随后连续7天停止施用。
22.根据前述权利要求中任一项所述使用的化合物、使用的治疗剂、使用的药物组合、或根据前述权利要求中任一项所述的方法,其中纳波拉非尼布的日总剂量是从约200mg至约800mg(例如约200mg、约400mg或约800mg),优选地每天两次施用。
23.根据前述权利要求中任一项所述使用的化合物、使用的治疗剂、使用的药物组合、或根据前述权利要求中任一项所述的方法,其中
(i)里内特基布的日总剂量是从约100mg至约400mg,优选地每天一次施用(例如约100mg、约200mg或约400mg);
(ii)曲美替尼的日总剂量是从约0.5mg至约1mg,优选地每天一次施用(例如约0.5mg或约1mg);或
(iii)瑞博西尼的日总剂量是从约100mg至约900mg,优选地每天一次施用(例如约100mg、约200mg、约400mg或约600mg)。
24.纳波拉非尼布、或其药学上可接受的盐,用于在治疗NRAS突变型黑素瘤或BRAF突变型黑素瘤中使用,其中按约800mg的日总剂量施用纳波拉非尼布(优选地每天两次施用),以及按约100mg或约200mg的日总剂量进一步施用里内特基布、或其药学上可接受的盐(优选地每天一次施用),任选地其中该黑素瘤是不可切除的和/或转移性的黑素瘤。
25.纳波拉非尼布、或其药学上可接受的盐,用于在治疗NRAS突变型黑素瘤或BRAF突变型黑素瘤中使用,其中按约400mg的日总剂量施用纳波拉非尼布(优选地每天两次施用),以及按约100mg或约200mg的日总剂量进一步施用里内特基布、或其药学上可接受的盐(优选地每天一次施用),任选地其中该黑素瘤是不可切除的和/或转移性的黑素瘤。
26.纳波拉非尼布、或其药学上可接受的盐,用于在治疗NRAS突变型黑素瘤或BRAF突变型黑素瘤中使用,其中按约800mg的日总剂量施用纳波拉非尼布(优选地每天两次施用),以及按约0.5mg或约1.0mg的日总剂量进一步施用曲美替尼、或其药学上可接受的溶剂化物(优选地每天一次施用),任选地其中该黑素瘤是不可切除的和/或转移性的黑素瘤。
27.纳波拉非尼布、或其药学上可接受的盐,用于在治疗NRAS突变型黑素瘤或BRAF突变型黑素瘤中使用,其中按约400mg的日总剂量施用纳波拉非尼布(优选地每天两次施用),以及按约0.5mg或约1.0mg的日总剂量进一步施用曲美替尼、或其药学上可接受的溶剂化物(优选地每天一次施用),任选地其中该黑素瘤是不可切除的和/或转移性的黑素瘤。
28.纳波拉非尼布、或其药学上可接受的盐,用于在治疗NRAS突变型黑素瘤或BRAF突变型黑素瘤中使用,其中按约800mg的日总剂量施用纳波拉非尼布(优选地每天两次施用),以及按约100mg、约200mg、约400mg或约600mg的日总剂量施用瑞博西尼、或其药学上可接受的盐(优选地每天一次施用),施用三周并且停止一周,任选地其中该黑素瘤是不可切除的和/或转移性的黑素瘤。
29.纳波拉非尼布、或其药学上可接受的盐,用于在治疗NRAS突变型黑素瘤或BRAF突变型黑素瘤中使用,其中按约400mg的日总剂量施用纳波拉非尼布(优选地每天两次施用),以及按约100mg、约200mg、约400mg或约600mg的日总剂量施用瑞博西尼、或其药学上可接受的盐(优选地每天一次施用),施用三周并且停止一周,任选地其中该黑素瘤是不可切除的和/或转移性的黑素瘤。
30.根据前述权利要求中任一项所述使用的化合物、使用的治疗剂、使用的药物组合、或根据前述权利要求中任一项所述的方法,其中向有需要的或患有黑素瘤的患者施用该化合物、治疗剂或药物组合,并且该治疗伴随选自以下的特征中的一个或多个:
-用该治疗,该患者经历至少3个月的无进展生存期(PFS);
-用该治疗,该患者经历至少7个月的应答持续时间(DOS);
-该治疗伴随以下的增加:改善总体应答率(ORR)、疾病控制率(DCR)、应答持续时间(DOR)、无进展生存期(PFS)、或中位总生存期(mOS),例如对比标准护理或其他疗法,例如对比比美替尼或对比达卡巴嗪;和
-伴随不良作用减少,任选地其中该不良作用选自QTc延长;不良心脏事件、胃肠道毒性(例如腹泻)和皮肤相关毒性。
31.纳波拉非尼布,用于在与曲美替尼一起的组合疗法中使用,用于治疗NRAS突变型黑素瘤,其中向有需要的患者施用纳波拉非尼布和曲美替尼,任选地其中该治疗伴随以下的增加:改善总体应答率(ORR)、疾病控制率(DCR)、应答持续时间(DOR)、无进展生存期(PFS)、或中位总生存期(mOS),例如对比标准护理或其他疗法,例如对比比美替尼或对比达卡巴嗪;和/或伴随不良作用减少,任选地其中该不良作用选自QTc延长;不良心脏事件和皮肤毒性。
32.根据权利要求31所述使用的化合物,其中按200mg的剂量一天两次施用纳波拉非尼布,并且按1mg/天的剂量施用曲美替尼。
33.一种在NRAS突变型黑素瘤或BRAF突变型黑素瘤中改善总体应答率(ORR)、疾病控制率(DCR)、应答持续时间(DOR)、无进展生存期(PFS)、或中位总生存期(mOS)的方法,其中向有需要的患者施用纳波拉非尼布与曲美替尼、或其药学上可接受的盐或溶剂化物的组合。
34.一种在NRAS突变型黑素瘤或BRAF突变型黑素瘤中改善总体应答率(ORR)、疾病控制率(DCR)、应答持续时间(DOR)、无进展生存期(PFS)、或中位总生存期(mOS)的方法,其中向有需要的患者施用纳波拉非尼布与里内特基布、或其药学上可接受的盐的组合。
35.一种减小QTc延长的风险以及治疗患有NRAS突变型黑素瘤或BRAF突变型黑素瘤的患者的方法,该方法包括向有需要的患者施用治疗有效量的纳波拉非尼布、或其药学上可接受的盐,以及治疗有效量的曲美替尼、或其药学上可接受的溶剂化物。
36.一种减小QTc延长的风险以及治疗患有NRAS突变型黑素瘤或BRAF突变型黑素瘤的患者的方法,该方法包括向有需要的患者施用治疗有效量的纳波拉非尼布、或其药学上可接受的盐,以及治疗有效量的里内特基布、或其药学上可接受的溶剂化物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202063023470P | 2020-05-12 | 2020-05-12 | |
| US63/023,470 | 2020-05-12 | ||
| PCT/IB2021/054013 WO2021229439A1 (en) | 2020-05-12 | 2021-05-11 | Therapeutic combinations comprising a craf inhibitor |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN115551509A true CN115551509A (zh) | 2022-12-30 |
Family
ID=75954158
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202180034241.6A Pending CN115551509A (zh) | 2020-05-12 | 2021-05-11 | 包含craf抑制剂的治疗组合 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20240000789A1 (zh) |
| EP (1) | EP4149472A1 (zh) |
| JP (1) | JP2023525100A (zh) |
| CN (1) | CN115551509A (zh) |
| TW (1) | TW202207942A (zh) |
| WO (1) | WO2021229439A1 (zh) |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2211849A2 (en) * | 2007-10-10 | 2010-08-04 | E-Therapeutics plc | Dexanabinol with inhibitors of braf or mek for the treatment of melanoma |
| CN104640545A (zh) * | 2012-08-17 | 2015-05-20 | 霍夫曼-拉罗奇有限公司 | 包括给药cobimetinib和威罗菲尼的黑色素瘤的组合疗法 |
| CN105530931A (zh) * | 2013-07-12 | 2016-04-27 | 皮拉马尔企业有限公司 | 用于治疗黑素瘤的药物组合 |
| CN108368171A (zh) * | 2015-07-10 | 2018-08-03 | 根马布股份公司 | 用于癌症治疗的axl特异性抗体-药物缀合物 |
| CN110494166A (zh) * | 2017-05-02 | 2019-11-22 | 诺华股份有限公司 | 组合疗法 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RS52670B (en) | 2004-06-11 | 2013-06-28 | Japan Tobacco Inc. | 5-AMINO-2,4,7-TRIOXO-3,4,7,8-TETRAHYDRO-2H-PIRIDO (2,3-D) PYRIMIDINE DERIVATIVES AND SIMILAR COMPOUNDS FOR CANCER TREATMENT |
| EP2331547B1 (en) | 2008-08-22 | 2014-07-30 | Novartis AG | Pyrrolopyrimidine compounds as cdk inhibitors |
| US20120115878A1 (en) | 2010-11-10 | 2012-05-10 | John Vincent Calienni | Salt(s) of 7-cyclopentyl-2-(5-piperazin-1-yl-pyridin-2-ylamino)-7h-pyrrolo[2,3-d]pyrimidine-6-carboxylic acid dimethylamide and processes of making thereof |
| AR091876A1 (es) * | 2012-07-26 | 2015-03-04 | Novartis Ag | Combinaciones farmaceuticas para el tratamiento de enfermedades proliferativas |
| US9242969B2 (en) | 2013-03-14 | 2016-01-26 | Novartis Ag | Biaryl amide compounds as kinase inhibitors |
| PE20161073A1 (es) | 2013-11-01 | 2016-10-30 | Novartis Ag | Amino-heteroaril-benzamidas como inhibidores de cinasa |
| US20180250302A1 (en) * | 2015-08-28 | 2018-09-06 | Giordano Caponigro | Combination of ribociclib and dabrafenib for treating or preventing cancer |
| CA3037456A1 (en) * | 2016-09-19 | 2018-03-22 | Novartis Ag | Therapeutic combinations comprising a raf inhibitor and a erk inhibitor |
| WO2020046966A1 (en) * | 2018-08-27 | 2020-03-05 | Kura Oncology, Inc. | Treatment of adenocarcinomas with mapk pathway inhibitors |
| KR20210105388A (ko) * | 2018-12-20 | 2021-08-26 | 노파르티스 아게 | 암 치료에서 사용하기 위한 raf 저해제와 cdk4/6 저해제를 이용하는 병용요법 |
| WO2021165849A1 (en) * | 2020-02-18 | 2021-08-26 | Novartis Ag | Therapeutic combinations comprising a raf inhibitor for use in treating braf mutant nsclc |
-
2021
- 2021-05-11 EP EP21726201.3A patent/EP4149472A1/en active Pending
- 2021-05-11 WO PCT/IB2021/054013 patent/WO2021229439A1/en unknown
- 2021-05-11 CN CN202180034241.6A patent/CN115551509A/zh active Pending
- 2021-05-11 JP JP2022568601A patent/JP2023525100A/ja active Pending
- 2021-05-11 US US17/998,391 patent/US20240000789A1/en active Pending
- 2021-05-12 TW TW110117160A patent/TW202207942A/zh unknown
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2211849A2 (en) * | 2007-10-10 | 2010-08-04 | E-Therapeutics plc | Dexanabinol with inhibitors of braf or mek for the treatment of melanoma |
| CN104640545A (zh) * | 2012-08-17 | 2015-05-20 | 霍夫曼-拉罗奇有限公司 | 包括给药cobimetinib和威罗菲尼的黑色素瘤的组合疗法 |
| CN105530931A (zh) * | 2013-07-12 | 2016-04-27 | 皮拉马尔企业有限公司 | 用于治疗黑素瘤的药物组合 |
| CN108368171A (zh) * | 2015-07-10 | 2018-08-03 | 根马布股份公司 | 用于癌症治疗的axl特异性抗体-药物缀合物 |
| CN110494166A (zh) * | 2017-05-02 | 2019-11-22 | 诺华股份有限公司 | 组合疗法 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP4149472A1 (en) | 2023-03-22 |
| US20240000789A1 (en) | 2024-01-04 |
| JP2023525100A (ja) | 2023-06-14 |
| TW202207942A (zh) | 2022-03-01 |
| WO2021229439A1 (en) | 2021-11-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN110494166B (zh) | 组合疗法 | |
| US10973829B2 (en) | Therapeutic uses of a C-RAF inhibitor | |
| CN114945369A (zh) | 图卡替尼与抗her2抗体-药物缀合物联合治疗her2阳性乳腺癌的方法 | |
| CN114746094A (zh) | 图卡替尼联合卡培他滨和曲妥珠单抗治疗her2阳性乳腺癌的方法 | |
| CN116171159A (zh) | 使用突变idh1抑制剂、脱氧腺苷类似物和铂药物的组合治疗 | |
| CN113329749A (zh) | 用于治疗葡萄膜黑色素瘤的联合疗法 | |
| US20230226030A1 (en) | Therapeutic combinations comprising a raf inhibitor for use in treating braf mutant nsclc | |
| CN115551509A (zh) | 包含craf抑制剂的治疗组合 | |
| US11419862B2 (en) | Quinoline derivative for treatment of nasopharyngeal carcinoma | |
| CN113453671A (zh) | 用于治疗癌症的Raf抑制剂和CDK4/6抑制剂的组合疗法 | |
| TW202146025A (zh) | 治療癌症之方法 | |
| CN115776889A (zh) | 用于治疗非小细胞肺癌的egfr tki | |
| KR20150003786A (ko) | Pi3k 저해제 및 mek 저해제를 이용한 암 치료 방법 | |
| US20230321110A1 (en) | Combination therapy of a raf inhibitor and a mek inhibitor for the treatment of sarcoma | |
| EP4110326B1 (en) | Combination comprising alpelisib and 6-(2,4-dichlorophenyl)-5-[4-[(3s)-1-(3-fluoropropyl)pyrrolidin-3-yl]oxyphenyl]-8,9-dihydro-7h-benzo[7]annulene-2-carboxylic acid | |
| JP2022547311A (ja) | 骨髄線維症の治療のためのmdm2阻害剤の使用 | |
| CN117580572A (zh) | 用安森司坦和帕博西尼治疗乳腺癌 | |
| TW202308641A (zh) | 用於治療癌症之方法及包含cdk抑制劑之給藥方案 | |
| EP4301356A1 (en) | Treatment of breast cancer with amcenestrant and palbociclib | |
| CN112533600A (zh) | 用于治疗小细胞肺癌的喹啉衍生物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| REG | Reference to a national code |
Ref country code: HK Ref legal event code: DE Ref document number: 40086978 Country of ref document: HK |