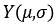CN114220480B - 一种药物成分分析方法及系统 - Google Patents
一种药物成分分析方法及系统 Download PDFInfo
- Publication number
- CN114220480B CN114220480B CN202210146868.7A CN202210146868A CN114220480B CN 114220480 B CN114220480 B CN 114220480B CN 202210146868 A CN202210146868 A CN 202210146868A CN 114220480 B CN114220480 B CN 114220480B
- Authority
- CN
- China
- Prior art keywords
- contour
- point
- drug
- points
- pixel
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000000034 method Methods 0.000 title claims abstract description 34
- 239000004615 ingredient Substances 0.000 title abstract description 4
- 239000003814 drug Substances 0.000 claims abstract description 152
- 229940079593 drug Drugs 0.000 claims abstract description 140
- 210000000056 organ Anatomy 0.000 claims abstract description 70
- 102000004169 proteins and genes Human genes 0.000 claims abstract description 46
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 46
- 125000000524 functional group Chemical group 0.000 claims abstract description 41
- 238000012545 processing Methods 0.000 claims abstract description 4
- 238000004458 analytical method Methods 0.000 claims description 27
- 238000004364 calculation method Methods 0.000 claims description 22
- 238000009499 grossing Methods 0.000 claims description 16
- 239000008194 pharmaceutical composition Substances 0.000 claims description 16
- 230000008569 process Effects 0.000 claims description 15
- 238000012549 training Methods 0.000 claims description 14
- 238000001328 terahertz time-domain spectroscopy Methods 0.000 claims description 9
- 238000010606 normalization Methods 0.000 claims description 7
- 238000000605 extraction Methods 0.000 claims description 6
- 238000001514 detection method Methods 0.000 claims description 5
- 238000005516 engineering process Methods 0.000 claims description 5
- 239000000126 substance Substances 0.000 claims description 4
- 238000009825 accumulation Methods 0.000 claims description 3
- 238000002372 labelling Methods 0.000 claims 1
- 230000009286 beneficial effect Effects 0.000 abstract description 3
- 150000001413 amino acids Chemical class 0.000 description 5
- 238000004590 computer program Methods 0.000 description 4
- 239000000203 mixture Substances 0.000 description 4
- 230000000694 effects Effects 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 230000003993 interaction Effects 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000008685 targeting Effects 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 230000008094 contradictory effect Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 238000007876 drug discovery Methods 0.000 description 1
- 238000012912 drug discovery process Methods 0.000 description 1
- 239000003596 drug target Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 230000014509 gene expression Effects 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000003062 neural network model Methods 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 230000004797 therapeutic response Effects 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B15/00—ICT specially adapted for analysing two-dimensional or three-dimensional molecular structures, e.g. structural or functional relations or structure alignment
- G16B15/30—Drug targeting using structural data; Docking or binding prediction
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/86—Signal analysis
- G01N30/8696—Details of Software
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/15—Medicinal preparations ; Physical properties thereof, e.g. dissolubility
-
- G06T5/70—
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T7/00—Image analysis
- G06T7/10—Segmentation; Edge detection
- G06T7/13—Edge detection
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T7/00—Image analysis
- G06T7/60—Analysis of geometric attributes
- G06T7/62—Analysis of geometric attributes of area, perimeter, diameter or volume
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T7/00—Image analysis
- G06T7/60—Analysis of geometric attributes
- G06T7/64—Analysis of geometric attributes of convexity or concavity
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B40/00—ICT specially adapted for biostatistics; ICT specially adapted for bioinformatics-related machine learning or data mining, e.g. knowledge discovery or pattern finding
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16C—COMPUTATIONAL CHEMISTRY; CHEMOINFORMATICS; COMPUTATIONAL MATERIALS SCIENCE
- G16C20/00—Chemoinformatics, i.e. ICT specially adapted for the handling of physicochemical or structural data of chemical particles, elements, compounds or mixtures
- G16C20/20—Identification of molecular entities, parts thereof or of chemical compositions
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16C—COMPUTATIONAL CHEMISTRY; CHEMOINFORMATICS; COMPUTATIONAL MATERIALS SCIENCE
- G16C20/00—Chemoinformatics, i.e. ICT specially adapted for the handling of physicochemical or structural data of chemical particles, elements, compounds or mixtures
- G16C20/50—Molecular design, e.g. of drugs
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16C—COMPUTATIONAL CHEMISTRY; CHEMOINFORMATICS; COMPUTATIONAL MATERIALS SCIENCE
- G16C20/00—Chemoinformatics, i.e. ICT specially adapted for the handling of physicochemical or structural data of chemical particles, elements, compounds or mixtures
- G16C20/70—Machine learning, data mining or chemometrics
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T2207/00—Indexing scheme for image analysis or image enhancement
- G06T2207/10—Image acquisition modality
- G06T2207/10056—Microscopic image
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T2207/00—Indexing scheme for image analysis or image enhancement
- G06T2207/20—Special algorithmic details
- G06T2207/20081—Training; Learning
Abstract
本发明提供了一种药物成分分析方法及系统,其中,方法包括:获取靶向蛋白、待检测的靶向药物以及具有所述靶向蛋白的器官轮廓图,对器官轮廓图进行处理得到对靶向药物的空间结构的预测图,再基于靶向药物的官能团实现对靶向药物的分子结构的预测。本发明的有益效果:通过获取靶向蛋白以及靶向药物以及对应的器官轮廓图,实现了将获取到器官轮廓图中靶蛋白的空间结构,再基于靶蛋白的空间结构和靶向药物的色谱图对靶向药物的分子结构进行预测,实现了对药物成分的空间结构进行预测分析,使得到的药物分子结构更精确。
Description
技术领域
本发明涉及数字医疗领域,特别涉及一种药物成分分析方法及系统。
背景技术
药物发现是确定具有潜在治疗作用的新候选化合物的过程,而药物分子和靶向蛋白质的相互作用(drug-target interactions, DTI)的预测,是药物发现过程中必不可少的一步。然药物分子的疗效取决于它们对靶蛋白或受体的亲和力。对靶蛋白没有任何相互作用或亲和力的药物分子将不能提供治疗反应。对于一些确定有疗效的药物分子的药物成分分析方法主要是通过简单的色谱图以及氢谱图进行分析,然而这种分析方法很难对药物成分的空间结构进行分析,从而导致无法对药物成分进行精确的认定。
发明内容
本发明的主要目的为提供一种药物成分分析方法及系统,旨在解决现有药物成分分析方法对药物成分分析精度差的问题。
本发明提供了一种药物成分分析方法,包括:
获取靶向蛋白、待检测的靶向药物以及具有所述靶向蛋白的器官轮廓图;
将所述器官轮廓图中轮廓上的任意一个像素点记为初始轮廓点,并将所述器官轮廓图中轮廓上的像素点用坐标进行表示,根据各轮廓点的坐标求得所述器官轮廓图中轮廓的轮廓周长;
,其中为当前坐标点至所述初始轮廓点的弧长为的轮廓点,和分别表示当前坐标点的横坐标和纵坐标,为与归一化处理相关的参数,分别代表平滑后当前坐标点的横坐标和纵坐标,表示弧长偏移距离为的横坐标,为一个距离变量,表示弧长,且0≤≤,L为所述轮廓周长;
截取所述突起处的微观图,并将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个形状预测结构;其中,所述空间结构预测模型通过不同形状的靶向蛋白以及其对应的目标靶向药物空间结构训练而成;
通过太赫兹时域光谱技术获取所述靶向药物的官能团,并将所述官能团作为所述靶向药物的子结构;
将所述子结构和所述多个形状预测结构输入至预设的分子结构预测模型中进行预测,得到所述靶向药物的分子结构,从而得到所述靶向药物的药物成分;其中,所述分子结构预测模型通过多种不同的药物分子的官能团,以及其预测结构作为输入,以对应的药物分子的分子结构作为输出训练而成。
进一步地,所述根据所述曲率识别所述形状的突起的步骤,包括:
根据每个所述轮廓点的曲率,将曲率为过零点的轮廓点提取出来作为第一轮廓点,其中,第一轮廓点的相邻点的曲率的乘积为负数;
提取所述第一轮廓点的a邻域两侧的离散点,所述离散点分别为Pi-a,Pi-a+1,…Pi-1和Pi+1,…Pi+a;其中Pi表示所述第一轮廓点;
将所述第一轮廓点Pi与离散点Pi-a的连线记为第一线段,将所述第一轮廓点Pi与离散点Pi+a的连线记为第二线段,然后将所述第一线段的中垂线与所述第二线段的中垂线的交点作为所述第一轮廓点的内切圆圆心;
计算所述第一轮廓点以及各离散点至所述内切圆圆心的距离,并取各计算得到的距离的平均值作为所述内切圆的半径;
判断所述内切圆的半径是否小于预设值;
若是,则判定所述第一轮廓点为所述形状的突起。
进一步地,所述将所述根据各轮廓点的坐标求得所述器官轮廓图中轮廓的轮廓周长的步骤,包括:
获取所述器官轮廓图中的所有像素点;
获取所述所有像素点对应的像素值;
检测每个所述像素点的像素值是否与相邻像素点的像素值都相同;
将与相邻像素点的像素值都相同的所述像素点的像素值进行累加作为第一累加值;
将所述器官轮廓图中所有像素点的像素值进行累加得到第二累加值,将所述第二累加值减去所述第一累加值得到所述轮廓周长。
进一步地,所述将所述子结构和所述多个形状预测结构输入至预设的分子结构预测模型中进行预测,得到所述靶向药物的分子结构的步骤之前,还包括:
将所述官能团输入至预设的药物组分分析模型中,得到多个目标药物组分;其中,所述药物组分分析模型根据各种药物组分以及对应的官能团训练而成;
将各所述目标药物组分输入至所述分子结构预测模型中,分别作为所述分子结构预测模型的输出通道。
进一步地,所述截取所述突起处的微观图,并将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个形状预测结构的步骤,包括:
截取所述突起处的微观图;
将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个所述预测结构以及所述预测结构的置信分值;其中,所述形状预测结构包括所述预测结构以及对应所述预测结构的置信分值。
本发明还提供了一种药物成分分析系统,包括:
第一获取模块,用于获取靶向蛋白、待检测的靶向药物以及具有所述靶向蛋白的器官轮廓图;
标记模块,用于将所述器官轮廓图中轮廓上的任意一个像素点记为初始轮廓点,并将所述器官轮廓图中轮廓上的像素点用坐标进行表示,根据各轮廓点的坐标求得所述器官轮廓图中轮廓的轮廓周长;
,其中为当前坐标点至所述初始轮廓点的弧长为的轮廓点,和分别表示当前坐标点的横坐标和纵坐标,为与归一化处理相关的参数,分别代表平滑后当前坐标点的横坐标和纵坐标,表示弧长偏移距离为的横坐标,为一个距离变量,表示弧长,且0≤≤,L为所述轮廓周长;
截取模块,用于截取所述突起处的微观图,并将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个形状预测结构;其中,所述空间结构预测模型通过不同形状的靶向蛋白以及其对应的目标靶向药物空间结构训练而成;
第二获取模块,用于通过太赫兹时域光谱技术获取所述靶向药物的官能团,并将所述官能团作为所述靶向药物的子结构;
预测模块,用于将所述子结构和所述多个形状预测结构输入至预设的分子结构预测模型中进行预测,得到所述靶向药物的分子结构,从而得到所述靶向药物的药物成分;其中,所述分子结构预测模型通过多种不同的药物分子的官能团,以及其预测结构作为输入,以对应的药物分子的分子结构作为输出训练而成。
进一步地,所述计算模块,包括:
轮廓点提取子模块,用于根据每个所述轮廓点的曲率,将曲率为过零点的轮廓点提取出来作为第一轮廓点,其中,第一轮廓点的相邻点的曲率的乘积为负数;
离散点提取子模块,用于提取所述第一轮廓点的a邻域两侧的离散点,所述离散点分别为Pi-a,Pi-a+1,…Pi-1和Pi+1,…Pi+a;其中Pi表示所述第一轮廓点;
记为子模块,用于将所述第一轮廓点Pi与离散点Pi-a的连线记为第一线段,将所述第一轮廓点Pi与离散点Pi+a的连线记为第二线段,然后将所述第一线段的中垂线与所述第二线段的中垂线的交点作为所述第一轮廓点的内切圆圆心;
计算子模块,用于计算所述第一轮廓点以及各离散点至所述内切圆圆心的距离,并取各计算得到的距离的平均值作为所述内切圆的半径;
判断子模块,用于判断所述内切圆的半径是否小于预设值;
判定子模块,用于若是,则判定所述第一轮廓点为所述形状的突起。
进一步地,所述标记模块,包括:
像素点获取子模块,用于获取所述器官轮廓图中的所有像素点;
像素值获取子模块,用于获取所述所有像素点对应的像素值;
像素值检测子模块,用于检测每个所述像素点的像素值是否与相邻像素点的像素值都相同;
累加子模块,用于将与相邻像素点的像素值都相同的所述像素点的像素值进行累加作为第一累加值;
轮廓周长计算子模块,用于将所述器官轮廓图中所有像素点的像素值进行累加得到第二累加值,将所述第二累加值减去所述第一累加值得到所述轮廓周长。
进一步地,所述药物成分分析系统,还包括:
第一输入模块,用于将所述官能团输入至预设的药物组分分析模型中,得到多个目标药物组分;其中,所述药物组分分析模型根据各种药物组分以及对应的官能团训练而成;
第二输入模块,用于将各所述目标药物组分输入至所述分子结构预测模型中,分别作为所述分子结构预测模型的输出通道。
进一步地,所述预测模块,包括:
截取子模块,用于截取所述突起处的微观图;
输入子模块,用于将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个所述预测结构以及所述预测结构的置信分值;其中,所述形状预测结构包括所述预测结构以及对应所述预测结构的置信分值。
本发明还提供了一种计算机设备,包括存储器和处理器,所述存储器存储有计算机程序,所述处理器执行所述计算机程序时实现上述任一项所述方法的步骤。
本发明还提供了一种计算机可读存储介质,其上存储有计算机程序,所述计算机程序被处理器执行时实现上述任一项所述的方法的步骤。
本发明的有益效果:通过获取靶向蛋白以及靶向药物以及对应的器官轮廓图,实现了将获取到器官轮廓图中靶蛋白的空间结构,再基于靶蛋白的空间结构和靶向药物的色谱图对靶向药物的分子结构进行预测,实现了对药物成分的空间结构进行预测分析,使得到的药物分子结构更精确。
附图说明
图1 是本发明一实施例的一种药物成分分析方法的流程示意图;
图2 是本发明一实施例的一种药物成分分析系统的结构示意框图。
本发明目的的实现、功能特点及优点将结合实施例,参照附图做进一步说明。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
需要说明,本发明实施例中所有方向性指示(诸如上、下、左、右、前、后等)仅用于解释在某一特定姿态(如附图所示)下各部件之间的相对位置关系、运动情况等,如果该特定姿态发生改变时,则该方向性指示也相应地随之改变,所述的连接可以是直接连接,也可以是间接连接。
本文中术语“和/或”,仅仅是一种描述关联对象的关联关系,表示可以存在三种关系,例如,A和B,可以表示:单独存在A,同时存在A和B,单独存在B这三种情况。
另外,在本发明中如涉及“第一”、“第二”等的描述仅用于描述目的,而不能理解为指示或暗示其相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括至少一个该特征。另外,各个实施例之间的技术方案可以相互结合,但是必须是以本领域普通技术人员能够实现为基础,当技术方案的结合出现相互矛盾或无法实现时应当认为这种技术方案的结合不存在,也不在本发明要求的保护范围之内。
参照图1,本发明提出一种药物成分分析方法,包括:
S1:获取靶向蛋白、待检测的靶向药物以及具有所述靶向蛋白的器官轮廓图;
S2:将所述器官轮廓图中轮廓上的任意一个像素点记为初始轮廓点,并将所述器官轮廓图中轮廓上的像素点用坐标进行表示,根据各轮廓点的坐标求得所述器官轮廓图中轮廓的轮廓周长;
,其中为当前坐标点至所述初始轮廓点的弧长为的轮廓点,和分别表示当前坐标点的横坐标和纵坐标,为与归一化处理相关的参数,分别代表平滑后当前坐标点的横坐标和纵坐标,表示弧长偏移距离为的横坐标,为一个距离变量,表示弧长,且0≤≤,L为所述轮廓周长;
S5:截取所述突起处的微观图,并将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个形状预测结构;其中,所述空间结构预测模型通过不同形状的靶向蛋白以及其对应的目标靶向药物空间结构训练而成;
S6:通过太赫兹时域光谱技术获取所述靶向药物的官能团,并将所述官能团作为所述靶向药物的子结构;
S7:将所述子结构和所述多个形状预测结构输入至预设的分子结构预测模型中进行预测,得到所述靶向药物的分子结构,从而得到所述靶向药物的药物成分;其中,所述分子结构预测模型通过多种不同的药物分子的官能团,以及其预测结构作为输入,以对应的药物分子的分子结构作为输出训练而成。
如上述步骤S1所述,获取靶向蛋白、待检测的靶向药物以及具有所述靶向蛋白的器官轮廓图。其中,获取的方式为接收人为输入或者从其他设备传输的靶向蛋白氨基酸组成结构,在检测该药物分子时,研究人员会分析出对应靶向蛋白的的氨基酸组成结构,因此,可以获取到该靶向蛋白的氨基酸组成结构,其组成结构还可以包括分子的空间结构,即氨基酸的空间结构,获取氨基酸的空间结构则可以便于后续检测空间结构是否可以与靶向药物相结合。对于靶向药物的靶向作用,不仅要与靶向蛋白上的靶点进行结合,还需要其空间结构相适配,才可以起到靶向作用,因此,还需要获取到靶向蛋白的器官轮廓图,需要说明的是,该器官轮廓图可以从拍摄仪器中进行获取,直接接收测试得到的图片,也可以是人为上传的图片,另外,需要说明的是,由于拍摄图片中一般具有多个靶向蛋白结构,也包含有正常的器官结构,其上的结节可以认定是否为靶向蛋白,并且机器拍摄的角度不同,其靶向蛋白的拍摄结构也具有一定的差异,即相同的靶向蛋白的轮廓可能完全不同。
如上述步骤S2所述,将所述器官轮廓图中轮廓上的任意一个像素点记为初始轮廓点,并将所述器官轮廓图中轮廓上的像素点用坐标进行表示,根据各轮廓点的坐标求得所述器官轮廓图中轮廓的轮廓周长。其中,计算轮廓周长的方式,可以是通过坐标进行累加得到,也可以是通过其他方式进行获取,本申请中具体的获取方式后续有详细说明,此处不再赘述。初始轮廓点的位置不作限定,可以是任意取轮廓上的点,此处只是为了便于后续进行计算,坐标点的确定也不作限定,例如,可以直接以该初始轮廓点作为坐标原点,也可以另外确定坐标原点。
如上述步骤S3所述,将所述器官轮廓图进行平滑处理。由于器官轮廓图原本就或多或少的具有一些图像噪声,因此需要对器官轮廓图进行平滑处理,使平滑的噪声不失真,先将每个轮廓点写成参数形式,然后对横坐标和纵坐标分别进行卷积,平滑处理的公式为,
,,消除归一化和图片本身携带的一些伪凸起,从而减少误差。需要注意的是,平滑后可能会将一些点移动,使闭合的轮廓曲线没有闭合,因此需要通过八邻域的检测方式再次得到闭合的曲线,当然在结节的判断过程中,也不需要用到闭合的曲线,因此也可以不用进行此项操作。
如上述步骤S4所述,通过公式计算每个轮廓点的曲率,如果一个轮廓点的相邻点曲率正好经历了正负值的变换,则说明此点为轮廓上由凹变凸(或由凸变凹)的转折点,这种点在数学上称作过零点。可以将该过零点视为一个形状的突起,当然,有一些过零点对应的轮廓点两端的曲线是很平滑的,这种不能算作形状的突起,因此也可以进行进一步地判断,将这部分的过零点过滤掉。
如上述步骤S5所述,截取所述突起处的微观图,并将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个形状预测结构。其中,微观图的截取可以将突起作为中心点进行截取,截取的大小不宜过小,否则无法进行顺利的预测,也不宜过大否则会包含有多个靶向蛋白,从而造成误差,由于靶向蛋白一般是内凹的形状,因此,可以根据过零点,选取三个突起作为一个靶向蛋白,微观图中含有该三个突起即可,将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个形状预测结构,具体地,该空间结构预测是二维的形状,由于前述已经说明该器官轮廓图含有靶向蛋白的各种表示,因此,该二维形状的多个形状预测结构均为靶向蛋白的二维结构,此外,空间结构预测模型是一种神经网络模型,其经过不同形状的靶向蛋白以及其对应的目标靶向药物空间结构训练而成。
如上述步骤S6所述,通过太赫兹时域光谱技术获取所述靶向药物的官能团,并将所述官能团作为所述靶向药物的子结构,太赫兹时域光谱技术可以探测材料在太赫兹波段的物理和化学信息,因此得到的色谱图相对于一般的色谱图而言具有更精确的信息,色谱图中含有各种化学键的信号,根据信号的强弱可以判断该化学键的含量,其中,宽谱太赫兹时域光谱技术具体可以是太赫兹时域光谱仪THz-TDS。
如上述步骤S7所述,将所述子结构和所述多个形状预测结构输入至预设的分子结构预测模型中进行预测,得到所述靶向药物的分子结构,从而得到所述靶向药物的药物成分,其中,分子结构预测模型的原理是基于各个分子结构进行拼装,以组成药物分子结构的模型,由于具有多个二维形状的形状预测结构,因此可以根据其获取到预测的药物分子结构,其中,分子结构预测模型通过多种不同的药物分子的官能团,以及其预测结构作为输入,以对应的药物分子的分子结构作为输出训练而成。从而实现了对药物成分的空间结构进行预测分析,使得到的药物分子结构更精确。
在一个实施例中,所述根据所述曲率识别所述形状的突起的步骤S4,包括:
S401:根据每个所述轮廓点的曲率,将曲率为过零点的轮廓点提取出来作为第一轮廓点,其中,第一轮廓点的相邻点的曲率的乘积为负数;
S402:提取所述第一轮廓点的a邻域两侧的离散点,所述离散点分别为Pi-a,Pi-a+1,…Pi-1和Pi+1,…Pi+a;其中Pi表示所述第一轮廓点;
S403:将所述第一轮廓点Pi与离散点Pi-a的连线记为第一线段,将所述第一轮廓点Pi与离散点Pi+a的连线记为第二线段,然后将所述第一线段的中垂线与所述第二线段的中垂线的交点作为所述第一轮廓点的内切圆圆心;
S404:计算所述第一轮廓点以及各离散点至所述内切圆圆心的距离,并取各计算得到的距离的平均值作为所述内切圆的半径;
S405:判断所述内切圆的半径是否小于预设值;
S406:若是,则判定所述第一轮廓点为所述形状的突起。
如上述步骤S401-S406所述,如果一个轮廓点的相邻点曲率正好经历了正负值的变换,则说明此点为轮廓上由凹变凸(/由凸变凹)的转折点,这种点在数学上称作过零点。可以将该过零点视为一个形状的突起,当然,有一些过零点对应的轮廓点两端的曲线是很平滑的,这种不能算作形状的突起,因此也可以进行进一步地判断,将这部分的过零点过滤掉。过滤的方法可以是通过计算每个过零点对应的内切圆半径,计算的方式为通过周围的离散点,该离散点也是形状的轮廓点,然后将第一线段和第二线段的中垂线交点作为圆心,然后以每个离散点到该圆心的距离的平均值作为内切圆的半径,从而求得内切圆的半径。再根据内切圆的半径筛选出符合要求的过零点作为形状的突起,然后统计个数,得到最终的形状的突起数目。
在一个实施例中,所述将所述根据各轮廓点的坐标求得所述器官轮廓图中轮廓的轮廓周长的步骤S2,包括:
S201:获取所述器官轮廓图中的所有像素点;
S202:获取所述所有像素点对应的像素值;
S203:检测每个所述像素点的像素值是否与相邻像素点的像素值都相同;
S204:将与相邻像素点的像素值都相同的所述像素点的像素值进行累加作为第一累加值;
S205:将所述器官轮廓图中所有像素点的像素值进行累加得到第二累加值,将所述第二累加值减去所述第一累加值得到所述轮廓周长。
如上述步骤S201-S205所述,计算轮廓周长的一种计算方式可以是,先获取到器官轮廓图中所有的像素点,然后获取对应的像素值,由于不是轮廓边缘的点,其相邻像素点的像素值都是相同的,故而可以相邻像素值都相同的像素点对应的像素值进行累加得到第一累加值,再将器官轮廓图中所有的像素值进行累加得到第二累加值,将第二累加值减去第一累加值得到轮廓周长,从而实现了对轮廓周长的计算,需要说明的是,本申请中获取到的器官轮廓图其轮廓周长无法直接得出,获取到的轮廓周长仅仅是器官轮廓图上的周长,其不一定为器官的轮廓周长。
在一个实施例中,所述将所述子结构和所述多个形状预测结构输入至预设的分子结构预测模型中进行预测,得到所述靶向药物的分子结构的步骤S7之前,还包括:
S601:将所述官能团输入至预设的药物组分分析模型中,得到多个目标药物组分;其中,所述药物组分分析模型根据各种药物组分以及对应的官能团训练而成;
S602:将各所述目标药物组分输入至所述分子结构预测模型中,分别作为所述分子结构预测模型的输出通道。
如上述步骤S601-S602所述,实现了对分子结构预测模型的输出通道的设定,即根据官能团数据可以获取到一些可能包含的药物组分,但是需要进一步的确定,而对于一些完全不可能包含的药物组分则可以省去,从而可以降低分子结构预测模型的计算量,避免计算各个输出通道的输出概率,只需要计算该设定的输出通道的概率即可,从而提高了分子结构预测模型的效率,减少了其运算量。
在一个实施例中,所述截取所述突起处的微观图,并将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个形状预测结构的步骤S5,包括:
S501:截取所述突起处的微观图;
S502:将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个所述预测结构以及所述预测结构的置信分值;其中,所述形状预测结构包括所述预测结构以及对应所述预测结构的置信分值。
如上述步骤S501-S502所述,将微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测时,可以从空间预测模型的输出层获取到对于的置信分值,此处将获取到的置信分值和预测结构直接输入至分子结构预测模型中进行预测,从而将置信分值作为一个因子,对最终的分子结构进行预测,从而使预测的结果更佳,提高了预测的精度,使预测效果更好。
参照图2,本发明还提供了一种药物成分分析系统,包括:
第一获取模块10,用于获取靶向蛋白、待检测的靶向药物以及具有所述靶向蛋白的器官轮廓图;
标记模块20,用于将所述器官轮廓图中轮廓上的任意一个像素点记为初始轮廓点,并将所述器官轮廓图中轮廓上的像素点用坐标进行表示,根据各轮廓点的坐标求得所述器官轮廓图中轮廓的轮廓周长;
,其中为当前坐标点至所述初始轮廓点的弧长为的轮廓点,和分别表示当前坐标点的横坐标和纵坐标,为与归一化处理相关的参数,分别代表平滑后当前坐标点的横坐标和纵坐标,表示弧长偏移距离为的横坐标,为一个距离变量,表示弧长,且0≤≤,L为所述轮廓周长;
截取模块50,用于截取所述突起处的微观图,并将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个形状预测结构;其中,所述空间结构预测模型通过不同形状的靶向蛋白以及其对应的目标靶向药物空间结构训练而成;
第二获取模块60,用于通过太赫兹时域光谱技术获取所述靶向药物的官能团,并将所述官能团作为所述靶向药物的子结构;
预测模块70,用于将所述子结构和所述多个形状预测结构输入至预设的分子结构预测模型中进行预测,得到所述靶向药物的分子结构,从而得到所述靶向药物的药物成分;其中,所述分子结构预测模型通过多种不同的药物分子的官能团,以及其预测结构作为输入,以对应的药物分子的分子结构作为输出训练而成。
在一个实施例中,所述计算模块40,包括:
轮廓点提取子模块,用于根据每个所述轮廓点的曲率,将曲率为过零点的轮廓点提取出来作为第一轮廓点,其中,第一轮廓点的相邻点的曲率的乘积为负数;
离散点提取子模块,用于提取所述第一轮廓点的a邻域两侧的离散点,所述离散点分别为Pi-a,Pi-a+1,…Pi-1和Pi+1,…Pi+a;其中Pi表示所述第一轮廓点;
记为子模块,用于将所述第一轮廓点Pi与离散点Pi-a的连线记为第一线段,将所述第一轮廓点Pi与离散点Pi+a的连线记为第二线段,然后将所述第一线段的中垂线与所述第二线段的中垂线的交点作为所述第一轮廓点的内切圆圆心;
计算子模块,用于计算所述第一轮廓点以及各离散点至所述内切圆圆心的距离,并取各计算得到的距离的平均值作为所述内切圆的半径;
判断子模块,用于判断所述内切圆的半径是否小于预设值;
判定子模块,用于若是,则判定所述第一轮廓点为所述形状的突起。
在一个实施例中,所述标记模块20,包括:
像素点获取子模块,用于获取所述器官轮廓图中的所有像素点;
像素值获取子模块,用于获取所述所有像素点对应的像素值;
像素值检测子模块,用于检测每个所述像素点的像素值是否与相邻像素点的像素值都相同;
累加子模块,用于将与相邻像素点的像素值都相同的所述像素点的像素值进行累加作为第一累加值;
轮廓周长计算子模块,用于将所述器官轮廓图中所有像素点的像素值进行累加得到第二累加值,将所述第二累加值减去所述第一累加值得到所述轮廓周长。
在一个实施例中,所述药物成分分析系统,还包括:
第一输入模块,用于将所述官能团输入至预设的药物组分分析模型中,得到多个目标药物组分;其中,所述药物组分分析模型根据各种药物组分以及对应的官能团训练而成;
第二输入模块,用于将各所述目标药物组分输入至所述分子结构预测模型中,分别作为所述分子结构预测模型的输出通道。
在一个实施例中,所述预测模块70,包括:
截取子模块,用于截取所述突起处的微观图;
输入子模块,用于将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个所述预测结构以及所述预测结构的置信分值;其中,所述形状预测结构包括所述预测结构以及对应所述预测结构的置信分值。
本发明的有益效果:通过获取靶向蛋白以及靶向药物以及对应的器官轮廓图,实现了将获取到器官轮廓图中靶蛋白的空间结构,再基于靶蛋白的空间结构和靶向药物的色谱图对靶向药物的分子结构进行预测,实现了对药物成分的空间结构进行预测分析,使得到的药物分子结构更精确。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的权利要求范围之内。
Claims (10)
1.一种药物成分分析方法,其特征在于,包括:
获取靶向蛋白、待检测的靶向药物以及具有所述靶向蛋白的器官轮廓图;
将所述器官轮廓图中轮廓上的任意一个像素点记为初始轮廓点,并将所述器官轮廓图中轮廓上的像素点用坐标进行表示,根据各轮廓点的坐标求得所述器官轮廓图中轮廓的轮廓周长;
,其中为当前坐标点至所述初始轮廓点的弧长为的轮廓点,和分别表示当前坐标点的横坐标和纵坐标,为与归一化处理相关的参数,分别代表平滑后当前坐标点的横坐标和纵坐标,表示弧长偏移距离为的横坐标,为一个距离变量,表示弧长,且0≤≤,L为所述轮廓周长;
截取所述突起处的微观图,并将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个形状预测结构;其中,所述空间结构预测模型通过不同形状的靶向蛋白以及其对应的目标靶向药物空间结构训练而成;
通过太赫兹时域光谱技术获取所述靶向药物的官能团,并将所述官能团作为所述靶向药物的子结构;
将所述子结构和所述多个形状预测结构输入至预设的分子结构预测模型中进行预测,得到所述靶向药物的分子结构,从而得到所述靶向药物的药物成分;其中,所述分子结构预测模型通过多种不同的药物分子的官能团,以及其预测结构作为输入,以对应的药物分子的分子结构作为输出训练而成。
2.如权利要求1所述的药物成分分析方法,其特征在于,所述根据所述曲率识别所述形状的突起的步骤,包括:
根据每个所述轮廓点的曲率,将曲率为过零点的轮廓点提取出来作为第一轮廓点,其中,第一轮廓点的相邻点的曲率的乘积为负数;
提取所述第一轮廓点的a邻域两侧的离散点,所述离散点分别为Pi-a,Pi-a+1,…Pi-1和Pi+1,…Pi+a;其中Pi表示所述第一轮廓点;
将所述第一轮廓点Pi与离散点Pi-a的连线记为第一线段,将所述第一轮廓点Pi与离散点Pi+a的连线记为第二线段,然后将所述第一线段的中垂线与所述第二线段的中垂线的交点作为所述第一轮廓点的内切圆圆心;
计算所述第一轮廓点以及各离散点至所述内切圆圆心的距离,并取各计算得到的距离的平均值作为所述内切圆的半径;
判断所述内切圆的半径是否小于预设值;
若是,则判定所述第一轮廓点为所述形状的突起。
3.如权利要求1所述的药物成分分析方法,其特征在于,所述将所述根据各轮廓点的坐标求得所述器官轮廓图中轮廓的轮廓周长的步骤,包括:
获取所述器官轮廓图中的所有像素点;
获取所述所有像素点对应的像素值;
检测每个所述像素点的像素值是否与相邻像素点的像素值都相同;
将与相邻像素点的像素值都相同的所述像素点的像素值进行累加作为第一累加值;
将所述器官轮廓图中所有像素点的像素值进行累加得到第二累加值,将所述第二累加值减去所述第一累加值得到所述轮廓周长。
4.如权利要求1所述的药物成分分析方法,其特征在于,所述将所述子结构和所述多个形状预测结构输入至预设的分子结构预测模型中进行预测,得到所述靶向药物的分子结构的步骤之前,还包括:
将所述官能团输入至预设的药物组分分析模型中,得到多个目标药物组分;其中,所述药物组分分析模型根据各种药物组分以及对应的官能团训练而成;
将各所述目标药物组分输入至所述分子结构预测模型中,分别作为所述分子结构预测模型的输出通道。
5.如权利要求1所述的药物成分分析方法,其特征在于,所述截取所述突起处的微观图,并将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个形状预测结构的步骤,包括:
截取所述突起处的微观图;
将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个所述预测结构以及所述预测结构的置信分值;其中,所述形状预测结构包括所述预测结构以及对应所述预测结构的置信分值。
6.一种药物成分分析系统,其特征在于,包括:
第一获取模块,用于获取靶向蛋白、待检测的靶向药物以及具有所述靶向蛋白的器官轮廓图;
标记模块,用于将所述器官轮廓图中轮廓上的任意一个像素点记为初始轮廓点,并将所述器官轮廓图中轮廓上的像素点用坐标进行表示,根据各轮廓点的坐标求得所述器官轮廓图中轮廓的轮廓周长;
,其中为当前坐标点至所述初始轮廓点的弧长为的轮廓点,和分别表示当前坐标点的横坐标和纵坐标,为与归一化处理相关的参数,分别代表平滑后当前坐标点的横坐标和纵坐标,表示弧长偏移距离为的横坐标,为一个距离变量,表示弧长,且0≤≤,L为所述轮廓周长;
截取模块,用于截取所述突起处的微观图,并将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个形状预测结构;其中,所述空间结构预测模型通过不同形状的靶向蛋白以及其对应的目标靶向药物空间结构训练而成;
第二获取模块,用于通过太赫兹时域光谱技术获取所述靶向药物的官能团,并将所述官能团作为所述靶向药物的子结构;
预测模块,用于将所述子结构和所述多个形状预测结构输入至预设的分子结构预测模型中进行预测,得到所述靶向药物的分子结构,从而得到所述靶向药物的药物成分;其中,所述分子结构预测模型通过多种不同的药物分子的官能团,以及其预测结构作为输入,以对应的药物分子的分子结构作为输出训练而成。
7.如权利要求6所述的药物成分分析系统,其特征在于,所述计算模块,包括:
轮廓点提取子模块,用于根据每个所述轮廓点的曲率,将曲率为过零点的轮廓点提取出来作为第一轮廓点,其中,第一轮廓点的相邻点的曲率的乘积为负数;
离散点提取子模块,用于提取所述第一轮廓点的a邻域两侧的离散点,所述离散点分别为Pi-a,Pi-a+1,…Pi-1和Pi+1,…Pi+a;其中Pi表示所述第一轮廓点;
记为子模块,用于将所述第一轮廓点Pi与离散点Pi-a的连线记为第一线段,将所述第一轮廓点Pi与离散点Pi+a的连线记为第二线段,然后将所述第一线段的中垂线与所述第二线段的中垂线的交点作为所述第一轮廓点的内切圆圆心;
计算子模块,用于计算所述第一轮廓点以及各离散点至所述内切圆圆心的距离,并取各计算得到的距离的平均值作为所述内切圆的半径;
判断子模块,用于判断所述内切圆的半径是否小于预设值;
判定子模块,用于若是,则判定所述第一轮廓点为所述形状的突起。
8.如权利要求6所述的药物成分分析系统,其特征在于,所述标记模块,包括:
像素点获取子模块,用于获取所述器官轮廓图中的所有像素点;
像素值获取子模块,用于获取所述所有像素点对应的像素值;
像素值检测子模块,用于检测每个所述像素点的像素值是否与相邻像素点的像素值都相同;
累加子模块,用于将与相邻像素点的像素值都相同的所述像素点的像素值进行累加作为第一累加值;
轮廓周长计算子模块,用于将所述器官轮廓图中所有像素点的像素值进行累加得到第二累加值,将所述第二累加值减去所述第一累加值得到所述轮廓周长。
9.如权利要求6所述的药物成分分析系统,其特征在于,所述药物成分分析系统,还包括:
第一输入模块,用于将所述官能团输入至预设的药物组分分析模型中,得到多个目标药物组分;其中,所述药物组分分析模型根据各种药物组分以及对应的官能团训练而成;
第二输入模块,用于将各所述目标药物组分输入至所述分子结构预测模型中,分别作为所述分子结构预测模型的输出通道。
10.如权利要求6所述的药物成分分析系统,其特征在于,所述预测模块,包括:
截取子模块,用于截取所述突起处的微观图;
输入子模块,用于将所述微观图输入至预设的空间结构预测模型对所述待检测的靶向药物进行空间结构进行预测,得到多个所述预测结构以及所述预测结构的置信分值;其中,所述形状预测结构包括所述预测结构以及对应所述预测结构的置信分值。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202210146868.7A CN114220480B (zh) | 2022-02-17 | 2022-02-17 | 一种药物成分分析方法及系统 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202210146868.7A CN114220480B (zh) | 2022-02-17 | 2022-02-17 | 一种药物成分分析方法及系统 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN114220480A CN114220480A (zh) | 2022-03-22 |
| CN114220480B true CN114220480B (zh) | 2022-05-10 |
Family
ID=80709130
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202210146868.7A Active CN114220480B (zh) | 2022-02-17 | 2022-02-17 | 一种药物成分分析方法及系统 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN114220480B (zh) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN117116384B (zh) * | 2023-10-20 | 2024-01-09 | 聊城高新生物技术有限公司 | 一种靶向诱导的医药分子结构生成方法 |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005053835A2 (en) * | 2003-12-02 | 2005-06-16 | Receptors Llc | Artificial receptors including gradients |
| CN107567312A (zh) * | 2015-05-06 | 2018-01-09 | 卡尔蒂希尔(2009)公司 | 优化的固体基质、与其一起使用的工具及其用于促进细胞和组织生长的用途 |
| CN110006863A (zh) * | 2019-04-08 | 2019-07-12 | 中南大学湘雅三医院 | 基于人血清蛋白功能化纳米二氧化硅的临床药物分析方法 |
| CN111742059A (zh) * | 2017-11-28 | 2020-10-02 | 格瑞尔公司 | 用于靶向测序的模型 |
| EP3745404A1 (en) * | 2019-05-29 | 2020-12-02 | Inoue, Asuka | Method and system for predicting coupling probabilities of g-protein coupled receptors with g-proteins |
| CN112382411A (zh) * | 2020-11-13 | 2021-02-19 | 大连理工大学 | 一种基于异质图的药物-蛋白质靶向作用预测方法 |
| WO2021152538A1 (en) * | 2020-01-29 | 2021-08-05 | Waters Technologies Ireland Limited | Techniques for sample analysis using product ion collision-cross section information |
| CN113255769A (zh) * | 2021-05-26 | 2021-08-13 | 北京百度网讯科技有限公司 | 化合物属性预测模型训练方法和化合物属性预测方法 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20150051090A1 (en) * | 2013-08-19 | 2015-02-19 | D.E. Shaw Research, Llc | Methods for in silico screening |
-
2022
- 2022-02-17 CN CN202210146868.7A patent/CN114220480B/zh active Active
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005053835A2 (en) * | 2003-12-02 | 2005-06-16 | Receptors Llc | Artificial receptors including gradients |
| CN107567312A (zh) * | 2015-05-06 | 2018-01-09 | 卡尔蒂希尔(2009)公司 | 优化的固体基质、与其一起使用的工具及其用于促进细胞和组织生长的用途 |
| CN111742059A (zh) * | 2017-11-28 | 2020-10-02 | 格瑞尔公司 | 用于靶向测序的模型 |
| CN110006863A (zh) * | 2019-04-08 | 2019-07-12 | 中南大学湘雅三医院 | 基于人血清蛋白功能化纳米二氧化硅的临床药物分析方法 |
| EP3745404A1 (en) * | 2019-05-29 | 2020-12-02 | Inoue, Asuka | Method and system for predicting coupling probabilities of g-protein coupled receptors with g-proteins |
| WO2021152538A1 (en) * | 2020-01-29 | 2021-08-05 | Waters Technologies Ireland Limited | Techniques for sample analysis using product ion collision-cross section information |
| CN112382411A (zh) * | 2020-11-13 | 2021-02-19 | 大连理工大学 | 一种基于异质图的药物-蛋白质靶向作用预测方法 |
| CN113255769A (zh) * | 2021-05-26 | 2021-08-13 | 北京百度网讯科技有限公司 | 化合物属性预测模型训练方法和化合物属性预测方法 |
Non-Patent Citations (1)
| Title |
|---|
| A deep learning-based method for drug-target interaction prediction based on long short-term memory neural network;Yan-Bin Wang 等;《BMC Medical Informatics and Decision Making》;20200318;第20卷;1-9 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN114220480A (zh) | 2022-03-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20200279125A1 (en) | Systems and methods for finding regions of interest in hematoxylin and eosin (h&e) stained tissue images and quantifying intratumor cellular spatial heterogeneity in multiplexed/hyperplexed fluorescence tissue images | |
| EP3091479B1 (en) | Method and apparatus for fingerprint identification | |
| CN111476827B (zh) | 目标跟踪方法、系统、电子装置及存储介质 | |
| KR101157073B1 (ko) | 근전도 센서와 자이로 센서를 이용한 지화 인식 방법 및 장치 | |
| US20220189579A1 (en) | Protein complex structure prediction from cryo-electron microscopy (cryo-em) density maps | |
| CN114220480B (zh) | 一种药物成分分析方法及系统 | |
| CN109840524A (zh) | 文字的类型识别方法、装置、设备及存储介质 | |
| Chen et al. | Deep learning for the detection and recognition of rail defects in ultrasound B-scan images | |
| CN104392455A (zh) | 基于方向检测的在线掌纹有效区域快速分割方法 | |
| CN111968160A (zh) | 图像匹配方法和存储介质 | |
| US11915823B1 (en) | Systems and methods for frame-based validation | |
| CN115691793A (zh) | 一种舌象数据处理方法、装置及相关设备 | |
| CN113469019B (zh) | 一种景观图像特征值计算方法、装置、设备及存储介质 | |
| CN109726679A (zh) | 一种遥感分类误差空间分布制图方法 | |
| CN115424000A (zh) | 一种指针式仪表识别方法、系统、设备及存储介质 | |
| CN109829440B (zh) | 一种检测道路差异的方法、装置、电子设备及存储介质 | |
| CN113506266A (zh) | 舌头腻苔的检测方法、装置、设备及存储介质 | |
| EP3803686A1 (en) | Predicting cancer recurrence from spatial multi-parameter cellular and subcellular imaging data | |
| CN116630867B (zh) | 一种基于Mask R-CNN的白带滴虫检测与跟踪方法 | |
| CN113192622B (zh) | 基于云边缘的ar巡检校验医疗数据的方法、装置及设备 | |
| KR102548863B1 (ko) | 나선그리기 오차거리 계산을 통한 이상운동증 진단 방법 및 시스템 | |
| CN109726646B (zh) | 一种手势识别方法和系统、显示方法和系统 | |
| US20230401691A1 (en) | Image defect detection method, electronic device and readable storage medium | |
| CN107368780B (zh) | 一种基于中心奇异点的指纹配准点提取方法 | |
| Heuschkel et al. | Reconsideration of Bertillonage in the age of digitalisation: Digital anthropometric patterns as a promising method for establishing identity |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |