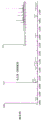CN112512564A - 铁蛋白蛋白 - Google Patents
铁蛋白蛋白 Download PDFInfo
- Publication number
- CN112512564A CN112512564A CN201980036305.9A CN201980036305A CN112512564A CN 112512564 A CN112512564 A CN 112512564A CN 201980036305 A CN201980036305 A CN 201980036305A CN 112512564 A CN112512564 A CN 112512564A
- Authority
- CN
- China
- Prior art keywords
- ferritin
- polypeptide
- seq
- cysteine
- amino acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 108050000784 Ferritin Proteins 0.000 title claims abstract description 758
- 102000008857 Ferritin Human genes 0.000 title claims abstract description 757
- 238000008416 Ferritin Methods 0.000 claims abstract description 735
- 108090000765 processed proteins & peptides Proteins 0.000 claims abstract description 442
- 229920001184 polypeptide Polymers 0.000 claims abstract description 420
- 102000004196 processed proteins & peptides Human genes 0.000 claims abstract description 420
- 230000035772 mutation Effects 0.000 claims abstract description 178
- 235000018417 cysteine Nutrition 0.000 claims abstract description 160
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 claims abstract description 149
- 235000001014 amino acid Nutrition 0.000 claims abstract description 135
- 230000003308 immunostimulating effect Effects 0.000 claims abstract description 112
- 150000001413 amino acids Chemical class 0.000 claims abstract description 109
- 230000000890 antigenic effect Effects 0.000 claims abstract description 102
- 210000004899 c-terminal region Anatomy 0.000 claims abstract description 10
- 229910052757 nitrogen Inorganic materials 0.000 claims abstract description 10
- 229940024606 amino acid Drugs 0.000 claims description 130
- 241000725643 Respiratory syncytial virus Species 0.000 claims description 103
- 239000002671 adjuvant Substances 0.000 claims description 93
- 241000701044 Human gammaherpesvirus 4 Species 0.000 claims description 92
- 239000000203 mixture Substances 0.000 claims description 88
- 206010022000 influenza Diseases 0.000 claims description 79
- 239000002245 particle Substances 0.000 claims description 65
- 241000590002 Helicobacter pylori Species 0.000 claims description 49
- 229940037467 helicobacter pylori Drugs 0.000 claims description 49
- 241000282414 Homo sapiens Species 0.000 claims description 37
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 claims description 36
- 239000000556 agonist Substances 0.000 claims description 34
- 241000589968 Borrelia Species 0.000 claims description 30
- 208000016604 Lyme disease Diseases 0.000 claims description 29
- 238000000034 method Methods 0.000 claims description 23
- -1 asparagine amino acid Chemical class 0.000 claims description 22
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 claims description 21
- 235000009582 asparagine Nutrition 0.000 claims description 21
- 229960001230 asparagine Drugs 0.000 claims description 21
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 claims description 15
- 150000007523 nucleic acids Chemical class 0.000 claims description 15
- 102100039390 Toll-like receptor 7 Human genes 0.000 claims description 14
- 101000669402 Homo sapiens Toll-like receptor 7 Proteins 0.000 claims description 12
- 102220623777 Pentraxin-4_S72C_mutation Human genes 0.000 claims description 11
- 102220635826 Probable C-mannosyltransferase DPY19L1_S26C_mutation Human genes 0.000 claims description 10
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 claims description 9
- 101000831567 Homo sapiens Toll-like receptor 2 Proteins 0.000 claims description 8
- 102100024333 Toll-like receptor 2 Human genes 0.000 claims description 8
- 108010002084 Apoferritins Proteins 0.000 claims description 7
- 102000000546 Apoferritins Human genes 0.000 claims description 7
- 108020004707 nucleic acids Proteins 0.000 claims description 7
- 102000039446 nucleic acids Human genes 0.000 claims description 7
- 108010060818 Toll-Like Receptor 9 Proteins 0.000 claims description 6
- 102100033117 Toll-like receptor 9 Human genes 0.000 claims description 6
- 229910052739 hydrogen Inorganic materials 0.000 claims description 6
- 239000001257 hydrogen Substances 0.000 claims description 6
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 3
- 239000003937 drug carrier Substances 0.000 claims description 3
- 108020004999 messenger RNA Proteins 0.000 claims description 3
- 102220272160 rs768754175 Human genes 0.000 claims description 2
- 239000002105 nanoparticle Substances 0.000 description 158
- 125000005647 linker group Chemical group 0.000 description 113
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 102
- 101710154606 Hemagglutinin Proteins 0.000 description 76
- 101710093908 Outer capsid protein VP4 Proteins 0.000 description 76
- 101710135467 Outer capsid protein sigma-1 Proteins 0.000 description 76
- 101710176177 Protein A56 Proteins 0.000 description 76
- 239000000185 hemagglutinin Substances 0.000 description 75
- 101710105714 Outer surface protein A Proteins 0.000 description 70
- 230000021615 conjugation Effects 0.000 description 65
- 230000000875 corresponding effect Effects 0.000 description 64
- 230000005875 antibody response Effects 0.000 description 62
- 241000699670 Mus sp. Species 0.000 description 53
- 125000003275 alpha amino acid group Chemical group 0.000 description 53
- 230000003053 immunization Effects 0.000 description 52
- 238000002649 immunization Methods 0.000 description 51
- 101710170470 Glycoprotein 42 Proteins 0.000 description 48
- 229940046168 CpG oligodeoxynucleotide Drugs 0.000 description 44
- 230000013595 glycosylation Effects 0.000 description 42
- 238000006206 glycosylation reaction Methods 0.000 description 42
- 108090000623 proteins and genes Proteins 0.000 description 42
- 238000002965 ELISA Methods 0.000 description 41
- 239000000427 antigen Substances 0.000 description 41
- 102000036639 antigens Human genes 0.000 description 41
- 108091007433 antigens Proteins 0.000 description 41
- 238000009739 binding Methods 0.000 description 41
- 239000013638 trimer Substances 0.000 description 39
- 235000018102 proteins Nutrition 0.000 description 37
- 102000004169 proteins and genes Human genes 0.000 description 37
- 230000004927 fusion Effects 0.000 description 33
- 239000000178 monomer Substances 0.000 description 33
- 229920001223 polyethylene glycol Polymers 0.000 description 32
- 238000006386 neutralization reaction Methods 0.000 description 28
- 230000003472 neutralizing effect Effects 0.000 description 28
- 238000006243 chemical reaction Methods 0.000 description 26
- 230000004044 response Effects 0.000 description 26
- 239000000499 gel Substances 0.000 description 23
- 230000028993 immune response Effects 0.000 description 23
- 238000003556 assay Methods 0.000 description 22
- 210000004027 cell Anatomy 0.000 description 22
- 238000002296 dynamic light scattering Methods 0.000 description 21
- 241000700605 Viruses Species 0.000 description 20
- 239000003795 chemical substances by application Substances 0.000 description 20
- 239000002202 Polyethylene glycol Substances 0.000 description 19
- 102000002689 Toll-like receptor Human genes 0.000 description 19
- 108020000411 Toll-like receptor Proteins 0.000 description 19
- 230000002829 reductive effect Effects 0.000 description 19
- 238000001542 size-exclusion chromatography Methods 0.000 description 19
- 238000011282 treatment Methods 0.000 description 19
- 241000270934 Rana catesbeiana Species 0.000 description 15
- 238000004458 analytical method Methods 0.000 description 15
- 230000009467 reduction Effects 0.000 description 14
- 206010069767 H1N1 influenza Diseases 0.000 description 13
- 241001465754 Metazoa Species 0.000 description 13
- 108010006232 Neuraminidase Proteins 0.000 description 13
- 102000005348 Neuraminidase Human genes 0.000 description 13
- 150000004676 glycans Chemical class 0.000 description 13
- 238000004949 mass spectrometry Methods 0.000 description 13
- 244000052769 pathogen Species 0.000 description 13
- 201000010740 swine influenza Diseases 0.000 description 13
- 229960005486 vaccine Drugs 0.000 description 13
- DPGCCPXHQRGEBE-UHFFFAOYSA-N 4a,5,6,7-tetrahydro-1H-pteridine-2,4-dione Chemical compound N1C(NC(C2NCCN=C12)=O)=O DPGCCPXHQRGEBE-UHFFFAOYSA-N 0.000 description 12
- 238000007792 addition Methods 0.000 description 12
- 230000015572 biosynthetic process Effects 0.000 description 12
- 238000010186 staining Methods 0.000 description 12
- 241000712461 unidentified influenza virus Species 0.000 description 12
- BWGNESOTFCXPMA-UHFFFAOYSA-N Dihydrogen disulfide Chemical compound SS BWGNESOTFCXPMA-UHFFFAOYSA-N 0.000 description 11
- PEEHTFAAVSWFBL-UHFFFAOYSA-N Maleimide Chemical compound O=C1NC(=O)C=C1 PEEHTFAAVSWFBL-UHFFFAOYSA-N 0.000 description 11
- 241000699666 Mus <mouse, genus> Species 0.000 description 11
- 238000012512 characterization method Methods 0.000 description 11
- 125000003636 chemical group Chemical group 0.000 description 11
- 102000037865 fusion proteins Human genes 0.000 description 11
- 108020001507 fusion proteins Proteins 0.000 description 11
- 125000003396 thiol group Chemical group [H]S* 0.000 description 11
- 238000001262 western blot Methods 0.000 description 11
- 238000000635 electron micrograph Methods 0.000 description 10
- 230000001717 pathogenic effect Effects 0.000 description 10
- 238000000746 purification Methods 0.000 description 10
- 241000894006 Bacteria Species 0.000 description 9
- ZUHQCDZJPTXVCU-UHFFFAOYSA-N C1#CCCC2=CC=CC=C2C2=CC=CC=C21 Chemical compound C1#CCCC2=CC=CC=C2C2=CC=CC=C21 ZUHQCDZJPTXVCU-UHFFFAOYSA-N 0.000 description 9
- 241000124008 Mammalia Species 0.000 description 9
- 241000255993 Trichoplusia ni Species 0.000 description 9
- 229940037003 alum Drugs 0.000 description 9
- 238000010790 dilution Methods 0.000 description 9
- 239000012895 dilution Substances 0.000 description 9
- 239000012634 fragment Substances 0.000 description 9
- 238000002347 injection Methods 0.000 description 9
- 239000007924 injection Substances 0.000 description 9
- 230000011664 signaling Effects 0.000 description 9
- 150000003384 small molecules Chemical class 0.000 description 9
- 238000006467 substitution reaction Methods 0.000 description 9
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 8
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 8
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 8
- 125000000539 amino acid group Chemical group 0.000 description 8
- 210000003719 b-lymphocyte Anatomy 0.000 description 8
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 8
- 239000003636 conditioned culture medium Substances 0.000 description 8
- 210000002966 serum Anatomy 0.000 description 8
- 229940044655 toll-like receptor 9 agonist Drugs 0.000 description 8
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 7
- 241000589969 Borreliella burgdorferi Species 0.000 description 7
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 7
- 108091028043 Nucleic acid sequence Proteins 0.000 description 7
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 7
- 101710196623 Stimulator of interferon genes protein Proteins 0.000 description 7
- 102220417854 c.293A>T Human genes 0.000 description 7
- 238000004422 calculation algorithm Methods 0.000 description 7
- 239000003153 chemical reaction reagent Substances 0.000 description 7
- 238000003776 cleavage reaction Methods 0.000 description 7
- 238000011260 co-administration Methods 0.000 description 7
- 238000004519 manufacturing process Methods 0.000 description 7
- 230000007017 scission Effects 0.000 description 7
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 7
- 210000003501 vero cell Anatomy 0.000 description 7
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 6
- 238000011735 C3H mouse Methods 0.000 description 6
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 6
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 6
- 241000282339 Mustela Species 0.000 description 6
- 229940124613 TLR 7/8 agonist Drugs 0.000 description 6
- 229940124614 TLR 8 agonist Drugs 0.000 description 6
- 150000001540 azides Chemical class 0.000 description 6
- 230000008901 benefit Effects 0.000 description 6
- 238000012650 click reaction Methods 0.000 description 6
- 230000006240 deamidation Effects 0.000 description 6
- 238000001514 detection method Methods 0.000 description 6
- 239000013642 negative control Substances 0.000 description 6
- 239000002773 nucleotide Substances 0.000 description 6
- 125000003729 nucleotide group Chemical group 0.000 description 6
- 229940046166 oligodeoxynucleotide Drugs 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 229940044616 toll-like receptor 7 agonist Drugs 0.000 description 6
- 238000002255 vaccination Methods 0.000 description 6
- 108010068327 4-hydroxyphenylpyruvate dioxygenase Proteins 0.000 description 5
- 239000004472 Lysine Substances 0.000 description 5
- 241001112090 Pseudovirus Species 0.000 description 5
- 108010073443 Ribi adjuvant Proteins 0.000 description 5
- 210000001744 T-lymphocyte Anatomy 0.000 description 5
- 230000001580 bacterial effect Effects 0.000 description 5
- 229910052799 carbon Inorganic materials 0.000 description 5
- 230000001268 conjugating effect Effects 0.000 description 5
- 238000013461 design Methods 0.000 description 5
- 238000002474 experimental method Methods 0.000 description 5
- 230000005847 immunogenicity Effects 0.000 description 5
- 208000015181 infectious disease Diseases 0.000 description 5
- 235000018977 lysine Nutrition 0.000 description 5
- 230000003647 oxidation Effects 0.000 description 5
- 238000007254 oxidation reaction Methods 0.000 description 5
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 5
- 230000037452 priming Effects 0.000 description 5
- 230000028327 secretion Effects 0.000 description 5
- RYYWUUFWQRZTIU-UHFFFAOYSA-K thiophosphate Chemical compound [O-]P([O-])([O-])=S RYYWUUFWQRZTIU-UHFFFAOYSA-K 0.000 description 5
- 238000005829 trimerization reaction Methods 0.000 description 5
- 230000003612 virological effect Effects 0.000 description 5
- FBFJOZZTIXSPPR-UHFFFAOYSA-N 1-(4-aminobutyl)-2-(ethoxymethyl)imidazo[4,5-c]quinolin-4-amine Chemical compound C1=CC=CC2=C(N(C(COCC)=N3)CCCCN)C3=C(N)N=C21 FBFJOZZTIXSPPR-UHFFFAOYSA-N 0.000 description 4
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- 241000282693 Cercopithecidae Species 0.000 description 4
- 108091006027 G proteins Proteins 0.000 description 4
- 102000030782 GTP binding Human genes 0.000 description 4
- 108091000058 GTP-Binding Proteins 0.000 description 4
- 239000004471 Glycine Substances 0.000 description 4
- 102000003886 Glycoproteins Human genes 0.000 description 4
- 108090000288 Glycoproteins Proteins 0.000 description 4
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 4
- 241000282560 Macaca mulatta Species 0.000 description 4
- 241000288906 Primates Species 0.000 description 4
- 108010076504 Protein Sorting Signals Proteins 0.000 description 4
- 102000002067 Protein Subunits Human genes 0.000 description 4
- 108010001267 Protein Subunits Proteins 0.000 description 4
- 229940123384 Toll-like receptor (TLR) agonist Drugs 0.000 description 4
- 108090000631 Trypsin Proteins 0.000 description 4
- 102000004142 Trypsin Human genes 0.000 description 4
- 239000002253 acid Substances 0.000 description 4
- IVRMZWNICZWHMI-UHFFFAOYSA-N azide group Chemical group [N-]=[N+]=[N-] IVRMZWNICZWHMI-UHFFFAOYSA-N 0.000 description 4
- 239000003814 drug Substances 0.000 description 4
- 238000001493 electron microscopy Methods 0.000 description 4
- 239000012678 infectious agent Substances 0.000 description 4
- 230000003993 interaction Effects 0.000 description 4
- 239000003446 ligand Substances 0.000 description 4
- 238000002156 mixing Methods 0.000 description 4
- 230000036961 partial effect Effects 0.000 description 4
- 229920001282 polysaccharide Polymers 0.000 description 4
- 239000005017 polysaccharide Substances 0.000 description 4
- 230000017854 proteolysis Effects 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- 239000002904 solvent Substances 0.000 description 4
- 230000000087 stabilizing effect Effects 0.000 description 4
- KZNICNPSHKQLFF-UHFFFAOYSA-N succinimide Chemical compound O=C1CCC(=O)N1 KZNICNPSHKQLFF-UHFFFAOYSA-N 0.000 description 4
- 239000012588 trypsin Substances 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- AUDYZXNUHIIGRB-UHFFFAOYSA-N 3-thiophen-2-ylpyrrole-2,5-dione Chemical group O=C1NC(=O)C(C=2SC=CC=2)=C1 AUDYZXNUHIIGRB-UHFFFAOYSA-N 0.000 description 3
- 241000238876 Acari Species 0.000 description 3
- 101001086191 Borrelia burgdorferi Outer surface protein A Proteins 0.000 description 3
- 241001148605 Borreliella garinii Species 0.000 description 3
- 102000004127 Cytokines Human genes 0.000 description 3
- 108090000695 Cytokines Proteins 0.000 description 3
- 241000238631 Hexapoda Species 0.000 description 3
- 241000712431 Influenza A virus Species 0.000 description 3
- 108010050904 Interferons Proteins 0.000 description 3
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 3
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 3
- 241000713666 Lentivirus Species 0.000 description 3
- 108010064548 Lymphocyte Function-Associated Antigen-1 Proteins 0.000 description 3
- 241000282567 Macaca fascicularis Species 0.000 description 3
- 241001406858 Monema Species 0.000 description 3
- 241000283973 Oryctolagus cuniculus Species 0.000 description 3
- 102000000447 Peptide-N4-(N-acetyl-beta-glucosaminyl) Asparagine Amidase Human genes 0.000 description 3
- 108010055817 Peptide-N4-(N-acetyl-beta-glucosaminyl) Asparagine Amidase Proteins 0.000 description 3
- 241000205156 Pyrococcus furiosus Species 0.000 description 3
- 229940044665 STING agonist Drugs 0.000 description 3
- 108091008874 T cell receptors Proteins 0.000 description 3
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 3
- 235000004279 alanine Nutrition 0.000 description 3
- SQVRNKJHWKZAKO-UHFFFAOYSA-N beta-N-Acetyl-D-neuraminic acid Natural products CC(=O)NC1C(O)CC(O)(C(O)=O)OC1C(O)C(O)CO SQVRNKJHWKZAKO-UHFFFAOYSA-N 0.000 description 3
- SBTXYHVTBXDKLE-UHFFFAOYSA-N bicyclo[6.1.0]non-6-yne Chemical compound C1CCCC#CC2CC21 SBTXYHVTBXDKLE-UHFFFAOYSA-N 0.000 description 3
- 230000001588 bifunctional effect Effects 0.000 description 3
- 238000011097 chromatography purification Methods 0.000 description 3
- 238000012217 deletion Methods 0.000 description 3
- 230000037430 deletion Effects 0.000 description 3
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 3
- 125000002228 disulfide group Chemical group 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 210000002919 epithelial cell Anatomy 0.000 description 3
- 238000011156 evaluation Methods 0.000 description 3
- 230000007717 exclusion Effects 0.000 description 3
- 238000011049 filling Methods 0.000 description 3
- 235000013922 glutamic acid Nutrition 0.000 description 3
- 239000004220 glutamic acid Substances 0.000 description 3
- 230000035931 haemagglutination Effects 0.000 description 3
- 229940124669 imidazoquinoline Drugs 0.000 description 3
- 210000000987 immune system Anatomy 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 210000004962 mammalian cell Anatomy 0.000 description 3
- 230000003278 mimic effect Effects 0.000 description 3
- 239000002953 phosphate buffered saline Substances 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 102000005962 receptors Human genes 0.000 description 3
- 108020003175 receptors Proteins 0.000 description 3
- 238000002864 sequence alignment Methods 0.000 description 3
- SQVRNKJHWKZAKO-OQPLDHBCSA-N sialic acid Chemical compound CC(=O)N[C@@H]1[C@@H](O)C[C@@](O)(C(O)=O)OC1[C@H](O)[C@H](O)CO SQVRNKJHWKZAKO-OQPLDHBCSA-N 0.000 description 3
- 241000894007 species Species 0.000 description 3
- 150000003573 thiols Chemical group 0.000 description 3
- 210000001519 tissue Anatomy 0.000 description 3
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 3
- YYGNTYWPHWGJRM-UHFFFAOYSA-N (6E,10E,14E,18E)-2,6,10,15,19,23-hexamethyltetracosa-2,6,10,14,18,22-hexaene Chemical compound CC(C)=CCCC(C)=CCCC(C)=CCCC=C(C)CCC=C(C)CCC=C(C)C YYGNTYWPHWGJRM-UHFFFAOYSA-N 0.000 description 2
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 2
- 241001148604 Borreliella afzelii Species 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 2
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 2
- 241000233756 Fabriciana elisa Species 0.000 description 2
- 241000282326 Felis catus Species 0.000 description 2
- 102000004961 Furin Human genes 0.000 description 2
- 108090001126 Furin Proteins 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 101000669447 Homo sapiens Toll-like receptor 4 Proteins 0.000 description 2
- 101000800483 Homo sapiens Toll-like receptor 8 Proteins 0.000 description 2
- 102000014150 Interferons Human genes 0.000 description 2
- 241000238681 Ixodes Species 0.000 description 2
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 2
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 2
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 2
- 230000004988 N-glycosylation Effects 0.000 description 2
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 2
- 108700038250 PAM2-CSK4 Proteins 0.000 description 2
- 241000702437 Parvovirus H3 Species 0.000 description 2
- 241001494479 Pecora Species 0.000 description 2
- 241000255969 Pieris brassicae Species 0.000 description 2
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 2
- LJUIOEFZFQRWJG-KKIBDXJDSA-N S-[2,3-bis(palmitoyloxy)propyl]-Cys-Ser-Lys-Lys-Lys-Lys Chemical group CCCCCCCCCCCCCCCC(=O)OCC(OC(=O)CCCCCCCCCCCCCCC)CSC[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(O)=O LJUIOEFZFQRWJG-KKIBDXJDSA-N 0.000 description 2
- 229920002125 Sokalan® Polymers 0.000 description 2
- BHEOSNUKNHRBNM-UHFFFAOYSA-N Tetramethylsqualene Natural products CC(=C)C(C)CCC(=C)C(C)CCC(C)=CCCC=C(C)CCC(C)C(=C)CCC(C)C(C)=C BHEOSNUKNHRBNM-UHFFFAOYSA-N 0.000 description 2
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 2
- 239000004473 Threonine Substances 0.000 description 2
- 241000723792 Tobacco etch virus Species 0.000 description 2
- 108010060825 Toll-Like Receptor 7 Proteins 0.000 description 2
- 102100039360 Toll-like receptor 4 Human genes 0.000 description 2
- 102100033110 Toll-like receptor 8 Human genes 0.000 description 2
- 241000607626 Vibrio cholerae Species 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 230000033289 adaptive immune response Effects 0.000 description 2
- 150000001408 amides Chemical class 0.000 description 2
- 125000000129 anionic group Chemical group 0.000 description 2
- 125000000613 asparagine group Chemical group N[C@@H](CC(N)=O)C(=O)* 0.000 description 2
- 235000003704 aspartic acid Nutrition 0.000 description 2
- 230000006472 autoimmune response Effects 0.000 description 2
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 2
- 238000012742 biochemical analysis Methods 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- RFCBNSCSPXMEBK-INFSMZHSSA-N c-GMP-AMP Chemical compound C([C@H]1O2)OP(O)(=O)O[C@H]3[C@@H](O)[C@H](N4C5=NC=NC(N)=C5N=C4)O[C@@H]3COP(O)(=O)O[C@H]1[C@@H](O)[C@@H]2N1C(N=C(NC2=O)N)=C2N=C1 RFCBNSCSPXMEBK-INFSMZHSSA-N 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 125000002091 cationic group Chemical group 0.000 description 2
- 210000000170 cell membrane Anatomy 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- SQQXRXKYTKFFSM-UHFFFAOYSA-N chembl1992147 Chemical compound OC1=C(OC)C(OC)=CC=C1C1=C(C)C(C(O)=O)=NC(C=2N=C3C4=NC(C)(C)N=C4C(OC)=C(O)C3=CC=2)=C1N SQQXRXKYTKFFSM-UHFFFAOYSA-N 0.000 description 2
- 230000000052 comparative effect Effects 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- 125000004122 cyclic group Chemical group 0.000 description 2
- DTPCFIHYWYONMD-UHFFFAOYSA-N decaethylene glycol Chemical compound OCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO DTPCFIHYWYONMD-UHFFFAOYSA-N 0.000 description 2
- 239000002274 desiccant Substances 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- PRAKJMSDJKAYCZ-UHFFFAOYSA-N dodecahydrosqualene Natural products CC(C)CCCC(C)CCCC(C)CCCCC(C)CCCC(C)CCCC(C)C PRAKJMSDJKAYCZ-UHFFFAOYSA-N 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 229930195712 glutamate Natural products 0.000 description 2
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 2
- 102000035122 glycosylated proteins Human genes 0.000 description 2
- 108091005608 glycosylated proteins Proteins 0.000 description 2
- 230000002209 hydrophobic effect Effects 0.000 description 2
- 230000002163 immunogen Effects 0.000 description 2
- 238000010348 incorporation Methods 0.000 description 2
- 229960003971 influenza vaccine Drugs 0.000 description 2
- 238000003780 insertion Methods 0.000 description 2
- 230000037431 insertion Effects 0.000 description 2
- PGLTVOMIXTUURA-UHFFFAOYSA-N iodoacetamide Chemical class NC(=O)CI PGLTVOMIXTUURA-UHFFFAOYSA-N 0.000 description 2
- 238000005342 ion exchange Methods 0.000 description 2
- 229910052742 iron Inorganic materials 0.000 description 2
- 238000012417 linear regression Methods 0.000 description 2
- UYEUUXMDVNYCAM-UHFFFAOYSA-N lumazine Chemical compound N1=CC=NC2=NC(O)=NC(O)=C21 UYEUUXMDVNYCAM-UHFFFAOYSA-N 0.000 description 2
- 125000005439 maleimidyl group Chemical group C1(C=CC(N1*)=O)=O 0.000 description 2
- 238000001819 mass spectrum Methods 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 230000034217 membrane fusion Effects 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 229960000402 palivizumab Drugs 0.000 description 2
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 2
- 150000004713 phosphodiesters Chemical class 0.000 description 2
- 239000004584 polyacrylic acid Substances 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 230000003389 potentiating effect Effects 0.000 description 2
- 238000011809 primate model Methods 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 230000001681 protective effect Effects 0.000 description 2
- 230000009257 reactivity Effects 0.000 description 2
- 238000001228 spectrum Methods 0.000 description 2
- 229940031439 squalene Drugs 0.000 description 2
- TUHBEKDERLKLEC-UHFFFAOYSA-N squalene Natural products CC(=CCCC(=CCCC(=CCCC=C(/C)CCC=C(/C)CC=C(C)C)C)C)C TUHBEKDERLKLEC-UHFFFAOYSA-N 0.000 description 2
- 238000007619 statistical method Methods 0.000 description 2
- 229940031626 subunit vaccine Drugs 0.000 description 2
- 229960002317 succinimide Drugs 0.000 description 2
- 229910052717 sulfur Inorganic materials 0.000 description 2
- 239000011593 sulfur Substances 0.000 description 2
- 229940095064 tartrate Drugs 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- ILLKMACMBHTSHP-UHFFFAOYSA-N tetradecaethylene glycol Chemical compound OCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO ILLKMACMBHTSHP-UHFFFAOYSA-N 0.000 description 2
- 150000007970 thio esters Chemical class 0.000 description 2
- 238000004627 transmission electron microscopy Methods 0.000 description 2
- XGOYIMQSIKSOBS-UHFFFAOYSA-N vadimezan Chemical compound C1=CC=C2C(=O)C3=CC=C(C)C(C)=C3OC2=C1CC(O)=O XGOYIMQSIKSOBS-UHFFFAOYSA-N 0.000 description 2
- 229950008737 vadimezan Drugs 0.000 description 2
- 239000013598 vector Substances 0.000 description 2
- 239000003981 vehicle Substances 0.000 description 2
- 229940118696 vibrio cholerae Drugs 0.000 description 2
- 230000007502 viral entry Effects 0.000 description 2
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 1
- 150000003923 2,5-pyrrolediones Chemical class 0.000 description 1
- VYMHBQQZUYHXSS-UHFFFAOYSA-N 2-(3h-dithiol-3-yl)pyridine Chemical compound C1=CSSC1C1=CC=CC=N1 VYMHBQQZUYHXSS-UHFFFAOYSA-N 0.000 description 1
- OWTQQPNDSWCHOV-UHFFFAOYSA-N 2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-(2-hydroxyethoxy)ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethanol Chemical compound OCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO OWTQQPNDSWCHOV-UHFFFAOYSA-N 0.000 description 1
- DHORSBRLGKJPFC-UHFFFAOYSA-N 2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-(2-hydroxyethoxy)ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethanol Chemical compound OCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO DHORSBRLGKJPFC-UHFFFAOYSA-N 0.000 description 1
- 125000000979 2-amino-2-oxoethyl group Chemical group [H]C([*])([H])C(=O)N([H])[H] 0.000 description 1
- 241000251468 Actinopterygii Species 0.000 description 1
- 235000006576 Althaea officinalis Nutrition 0.000 description 1
- 241000272813 Anser indicus Species 0.000 description 1
- 241000205042 Archaeoglobus fulgidus Species 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 238000012935 Averaging Methods 0.000 description 1
- 241000271566 Aves Species 0.000 description 1
- NOWKCMXCCJGMRR-UHFFFAOYSA-N Aziridine Chemical compound C1CN1 NOWKCMXCCJGMRR-UHFFFAOYSA-N 0.000 description 1
- 241001034576 Borrelia burgdorferi N40 Species 0.000 description 1
- 241000690120 Borrelia mayonii Species 0.000 description 1
- 241000568336 Borreliella bavariensis Species 0.000 description 1
- 108090000835 CX3C Chemokine Receptor 1 Proteins 0.000 description 1
- 102100039196 CX3C chemokine receptor 1 Human genes 0.000 description 1
- 241000282836 Camelus dromedarius Species 0.000 description 1
- 241000589875 Campylobacter jejuni Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 102000019034 Chemokines Human genes 0.000 description 1
- 108010012236 Chemokines Proteins 0.000 description 1
- 102000047200 Collagen Type XVIII Human genes 0.000 description 1
- 108010001463 Collagen Type XVIII Proteins 0.000 description 1
- 208000035473 Communicable disease Diseases 0.000 description 1
- 108091035707 Consensus sequence Proteins 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 206010015108 Epstein-Barr virus infection Diseases 0.000 description 1
- 241000283074 Equus asinus Species 0.000 description 1
- 241000283073 Equus caballus Species 0.000 description 1
- 102100020760 Ferritin heavy chain Human genes 0.000 description 1
- 102000009123 Fibrin Human genes 0.000 description 1
- 108010073385 Fibrin Proteins 0.000 description 1
- BWGVNKXGVNDBDI-UHFFFAOYSA-N Fibrin monomer Chemical compound CNC(=O)CNC(=O)CN BWGVNKXGVNDBDI-UHFFFAOYSA-N 0.000 description 1
- 101710189104 Fibritin Proteins 0.000 description 1
- 101710128254 Gene 42 protein Proteins 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- 241000702620 H-1 parvovirus Species 0.000 description 1
- 101001002987 Homo sapiens Ferritin heavy chain Proteins 0.000 description 1
- 101000940887 Homo sapiens LINE-1 retrotransposable element ORF1 protein Proteins 0.000 description 1
- 101000604197 Homo sapiens Neuronatin Proteins 0.000 description 1
- 101000999322 Homo sapiens Putative insulin-like growth factor 2 antisense gene protein Proteins 0.000 description 1
- 101001073409 Homo sapiens Retrotransposon-derived protein PEG10 Proteins 0.000 description 1
- 101001094545 Homo sapiens Retrotransposon-like protein 1 Proteins 0.000 description 1
- 101000643024 Homo sapiens Stimulator of interferon genes protein Proteins 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 241000713196 Influenza B virus Species 0.000 description 1
- 102100022339 Integrin alpha-L Human genes 0.000 description 1
- 102100027612 Kallikrein-11 Human genes 0.000 description 1
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 1
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- 102100031764 LINE-1 retrotransposable element ORF1 protein Human genes 0.000 description 1
- 241000270322 Lepidosauria Species 0.000 description 1
- 241000186781 Listeria Species 0.000 description 1
- 241000282553 Macaca Species 0.000 description 1
- 102000018697 Membrane Proteins Human genes 0.000 description 1
- 108010052285 Membrane Proteins Proteins 0.000 description 1
- GODBLDDYHFTUAH-CIUDSAMLSA-N Met-Asp-Glu Chemical compound CSCC[C@H](N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@H](C(O)=O)CCC(O)=O GODBLDDYHFTUAH-CIUDSAMLSA-N 0.000 description 1
- 102100029083 Minor histocompatibility antigen H13 Human genes 0.000 description 1
- 241000228347 Monascus <ascomycete fungus> Species 0.000 description 1
- XNPOFXIBHOVFFH-UHFFFAOYSA-N N-cyclohexyl-N'-(2-(4-morpholinyl)ethyl)carbodiimide Chemical compound C1CCCCC1N=C=NCCN1CCOCC1 XNPOFXIBHOVFFH-UHFFFAOYSA-N 0.000 description 1
- 102100038816 Neuronatin Human genes 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 108700026244 Open Reading Frames Proteins 0.000 description 1
- 102400001093 PAK-2p27 Human genes 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 241000009328 Perro Species 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 102100036485 Putative insulin-like growth factor 2 antisense gene protein Human genes 0.000 description 1
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 1
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 1
- 102100035844 Retrotransposon-derived protein PEG10 Human genes 0.000 description 1
- 102100035123 Retrotransposon-like protein 1 Human genes 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 238000012300 Sequence Analysis Methods 0.000 description 1
- 102100035533 Stimulator of interferon genes protein Human genes 0.000 description 1
- 238000000692 Student's t-test Methods 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 244000186561 Swietenia macrophylla Species 0.000 description 1
- 230000005867 T cell response Effects 0.000 description 1
- 238000003917 TEM image Methods 0.000 description 1
- 108010076818 TEV protease Proteins 0.000 description 1
- 241000204652 Thermotoga Species 0.000 description 1
- 101710152431 Trypsin-like protease Proteins 0.000 description 1
- 241000196259 Ulva pertusa Species 0.000 description 1
- 108010003533 Viral Envelope Proteins Proteins 0.000 description 1
- 230000010530 Virus Neutralization Effects 0.000 description 1
- 101710136524 X polypeptide Proteins 0.000 description 1
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 1
- 125000003647 acryloyl group Chemical group O=C([*])C([H])=C([H])[H] 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 238000001042 affinity chromatography Methods 0.000 description 1
- 210000001552 airway epithelial cell Anatomy 0.000 description 1
- HAXFWIACAGNFHA-UHFFFAOYSA-N aldrithiol Chemical compound C=1C=CC=NC=1SSC1=CC=CC=N1 HAXFWIACAGNFHA-UHFFFAOYSA-N 0.000 description 1
- 230000029936 alkylation Effects 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- 210000003423 ankle Anatomy 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 230000010056 antibody-dependent cellular cytotoxicity Effects 0.000 description 1
- 230000030741 antigen processing and presentation Effects 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 125000000637 arginyl group Chemical group N[C@@H](CCCNC(N)=N)C(=O)* 0.000 description 1
- 230000002238 attenuated effect Effects 0.000 description 1
- 230000005784 autoimmunity Effects 0.000 description 1
- 229940125717 barbiturate Drugs 0.000 description 1
- HNYOPLTXPVRDBG-UHFFFAOYSA-N barbituric acid Chemical compound O=C1CC(=O)NC(=O)N1 HNYOPLTXPVRDBG-UHFFFAOYSA-N 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 238000010364 biochemical engineering Methods 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 239000007434 bsk-medium Substances 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 150000001718 carbodiimides Chemical class 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 230000007969 cellular immunity Effects 0.000 description 1
- 230000036755 cellular response Effects 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 238000004590 computer program Methods 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000004665 defense response Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 210000004443 dendritic cell Anatomy 0.000 description 1
- 239000010432 diamond Substances 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- AFOSIXZFDONLBT-UHFFFAOYSA-N divinyl sulfone Chemical compound C=CS(=O)(=O)C=C AFOSIXZFDONLBT-UHFFFAOYSA-N 0.000 description 1
- WRZXKWFJEFFURH-UHFFFAOYSA-N dodecaethylene glycol Chemical compound OCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO WRZXKWFJEFFURH-UHFFFAOYSA-N 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 238000007876 drug discovery Methods 0.000 description 1
- 229940126534 drug product Drugs 0.000 description 1
- 235000013601 eggs Nutrition 0.000 description 1
- 239000012039 electrophile Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000013604 expression vector Substances 0.000 description 1
- 229950003499 fibrin Drugs 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 238000000684 flow cytometry Methods 0.000 description 1
- 230000002538 fungal effect Effects 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 102000034238 globular proteins Human genes 0.000 description 1
- 108091005896 globular proteins Proteins 0.000 description 1
- 150000002306 glutamic acid derivatives Chemical class 0.000 description 1
- 125000000404 glutamine group Chemical class N[C@@H](CCC(N)=O)C(=O)* 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 125000005179 haloacetyl group Chemical group 0.000 description 1
- XPJRQAIZZQMSCM-UHFFFAOYSA-N heptaethylene glycol Chemical compound OCCOCCOCCOCCOCCOCCOCCO XPJRQAIZZQMSCM-UHFFFAOYSA-N 0.000 description 1
- 239000000833 heterodimer Substances 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 230000004727 humoral immunity Effects 0.000 description 1
- 230000008348 humoral response Effects 0.000 description 1
- 230000000521 hyperimmunizing effect Effects 0.000 description 1
- 230000009610 hypersensitivity Effects 0.000 description 1
- 210000002865 immune cell Anatomy 0.000 description 1
- 229940127121 immunoconjugate Drugs 0.000 description 1
- 230000016784 immunoglobulin production Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 230000015788 innate immune response Effects 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 229940079322 interferon Drugs 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 230000006338 isoaspartate formation Effects 0.000 description 1
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 1
- 229960000310 isoleucine Drugs 0.000 description 1
- 239000006194 liquid suspension Substances 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 210000004779 membrane envelope Anatomy 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 102000035118 modified proteins Human genes 0.000 description 1
- 108091005573 modified proteins Proteins 0.000 description 1
- 108010050062 mutacin GS-5 Proteins 0.000 description 1
- 239000007908 nanoemulsion Substances 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- YZUUTMGDONTGTN-UHFFFAOYSA-N nonaethylene glycol Chemical compound OCCOCCOCCOCCOCCOCCOCCOCCOCCO YZUUTMGDONTGTN-UHFFFAOYSA-N 0.000 description 1
- 239000012038 nucleophile Substances 0.000 description 1
- 239000002777 nucleoside Substances 0.000 description 1
- 229940127073 nucleoside analogue Drugs 0.000 description 1
- 125000003835 nucleoside group Chemical class 0.000 description 1
- GLZWNFNQMJAZGY-UHFFFAOYSA-N octaethylene glycol Chemical compound OCCOCCOCCOCCOCCOCCOCCOCCO GLZWNFNQMJAZGY-UHFFFAOYSA-N 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 238000001543 one-way ANOVA Methods 0.000 description 1
- 101800002712 p27 Proteins 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 230000006461 physiological response Effects 0.000 description 1
- 210000004896 polypeptide structure Anatomy 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 230000004481 post-translational protein modification Effects 0.000 description 1
- AYXYPKUFHZROOJ-ZETCQYMHSA-N pregabalin Chemical group CC(C)C[C@H](CN)CC(O)=O AYXYPKUFHZROOJ-ZETCQYMHSA-N 0.000 description 1
- 229960001233 pregabalin Drugs 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 239000012264 purified product Substances 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 238000009877 rendering Methods 0.000 description 1
- 238000010845 search algorithm Methods 0.000 description 1
- 125000003607 serino group Chemical group [H]N([H])[C@]([H])(C(=O)[*])C(O[H])([H])[H] 0.000 description 1
- 125000005629 sialic acid group Chemical group 0.000 description 1
- 108010061514 sialic acid receptor Proteins 0.000 description 1
- YYGNTYWPHWGJRM-AAJYLUCBSA-N squalene Chemical compound CC(C)=CCC\C(C)=C\CC\C(C)=C\CC\C=C(/C)CC\C=C(/C)CCC=C(C)C YYGNTYWPHWGJRM-AAJYLUCBSA-N 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000012916 structural analysis Methods 0.000 description 1
- 150000003463 sulfur Chemical class 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 231100000057 systemic toxicity Toxicity 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 238000011287 therapeutic dose Methods 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 230000008719 thickening Effects 0.000 description 1
- 230000034005 thiol-disulfide exchange Effects 0.000 description 1
- 150000007944 thiolates Chemical class 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 150000003852 triazoles Chemical class 0.000 description 1
- 230000001960 triggered effect Effects 0.000 description 1
- 230000001810 trypsinlike Effects 0.000 description 1
- 230000006433 tumor necrosis factor production Effects 0.000 description 1
- PSVXZQVXSXSQRO-UHFFFAOYSA-N undecaethylene glycol Chemical compound OCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO PSVXZQVXSXSQRO-UHFFFAOYSA-N 0.000 description 1
- 241001515965 unidentified phage Species 0.000 description 1
- 238000011870 unpaired t-test Methods 0.000 description 1
- 238000012800 visualization Methods 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/105—Delta proteobacteriales, e.g. Lawsonia; Epsilon proteobacteriales, e.g. campylobacter, helicobacter
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/0225—Spirochetes, e.g. Treponema, Leptospira, Borrelia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
- A61K39/145—Orthomyxoviridae, e.g. influenza virus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/16—Antivirals for RNA viruses for influenza or rhinoviruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/005—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from viruses
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55555—Liposomes; Vesicles, e.g. nanoparticles; Spheres, e.g. nanospheres; Polymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55577—Saponins; Quil A; QS21; ISCOMS
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/60—Medicinal preparations containing antigens or antibodies characteristics by the carrier linked to the antigen
- A61K2039/6031—Proteins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/16011—Herpesviridae
- C12N2710/16211—Lymphocryptovirus, e.g. human herpesvirus 4, Epstein-Barr Virus
- C12N2710/16222—New viral proteins or individual genes, new structural or functional aspects of known viral proteins or genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/16011—Herpesviridae
- C12N2710/16211—Lymphocryptovirus, e.g. human herpesvirus 4, Epstein-Barr Virus
- C12N2710/16234—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/16011—Orthomyxoviridae
- C12N2760/16111—Influenzavirus A, i.e. influenza A virus
- C12N2760/16122—New viral proteins or individual genes, new structural or functional aspects of known viral proteins or genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/16011—Orthomyxoviridae
- C12N2760/16111—Influenzavirus A, i.e. influenza A virus
- C12N2760/16134—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/18011—Paramyxoviridae
- C12N2760/18511—Pneumovirus, e.g. human respiratory syncytial virus
- C12N2760/18522—New viral proteins or individual genes, new structural or functional aspects of known viral proteins or genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/18011—Paramyxoviridae
- C12N2760/18511—Pneumovirus, e.g. human respiratory syncytial virus
- C12N2760/18534—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Abstract
公开了铁蛋白蛋白,所述铁蛋白蛋白包含用半胱氨酸置换表面暴露的氨基酸的突变、含有半胱氨酸的N或C末端接头、和/或一个或多个经由表面暴露的氨基酸连接至所述铁蛋白蛋白的免疫刺激部分。所述铁蛋白蛋白可以进一步包含非铁蛋白多肽并且是抗原性的,例如以用于在引发针对所述非铁蛋白多肽的抗体中使用。
Description
本申请要求以下的权益:2018年4月3日提交的美国临时专利申请号62/652,217;2018年4月3日提交的美国临时专利申请号62/652,199;2018年4月3日提交的美国临时专利申请号62/652,201;2018年4月3日提交的美国临时专利申请号62/652,210;以及2018年4月3日提交的美国临时专利申请号62/652,204,将所述临时专利申请的全部内容通过引用并入本文。
本申请含有已经以ASCII格式电子提交并且通过引用以其整体特此并入的序列表。2019年3月27日创建的所述ASCII副本被命名为2019-03-27_01121-0035-00PCT_SL_ST25.txt,并且大小为1,115,992字节。
即使在疫苗学领域取得了许多成功,仍需要新的突破来保护人类免受许多威胁生命的传染性疾病的影响。当前许多已获许可的疫苗都依赖十年前的技术来产生活的减毒病原体或灭活的杀死病原体,所述病原体具有固有的安全性问题,并且在许多情况下,仅刺激短暂的弱免疫应答,从而需要给予多个剂量。虽然遗传学和生物化学工程学的进步使得开发针对具有挑战性的疾病靶标的治疗剂成为可能,但在疫苗学领域的这些应用尚未完全实现。
重组蛋白技术现在允许设计改善的抗原性多肽。另外,纳米颗粒已越来越多地展示出用于有效的抗原呈递和靶向药物递送的潜力。已经显示铁蛋白颗粒具有增加的结合亲合力,所述增加的结合亲合力凭借其分子货物的多价展示和由于其纳米尺寸而更有效地跨过生物屏障的能力而提供。与流感病毒血凝素(HA)蛋白融合的幽门螺杆菌(Helicobacterpylori(H.pylori))铁蛋白颗粒可以改善抗原稳定性并增加在小鼠流感模型中的免疫原性(参见Kanekiyo等人,Nature 499:102-106(2013))。此融合蛋白自组装成八面体对称性纳米颗粒并呈递8个三聚体HA刺突,从而在与佐剂一起使用时在各种临床前模型中产生稳健的免疫应答。然而,这些颗粒不是自佐剂化的,并且不清楚铁蛋白颗粒是否可以用作除HA流感以外的免疫原性可能低于HA的多肽的合适平台。
在此,提出了一组涉及铁蛋白的新多肽、纳米颗粒、组合物、方法和用途。本文描述了自佐剂化平台,其中免疫刺激部分(如佐剂)经由表面暴露的氨基酸或在铁蛋白与非铁蛋白多肽之间的接头缀合至铁蛋白。通过将非铁蛋白多肽与铁蛋白组合产生抗原性铁蛋白多肽。将免疫刺激部分缀合至与非铁蛋白多肽组合的铁蛋白允许在单一大分子实体中靶向共递送免疫刺激部分和非铁蛋白多肽,这可以大大降低全身性毒性的可能性,所述全身性毒性是在包含作为独立分子的抗原和免疫刺激分子(如佐剂)的更传统的疫苗的情况下所担忧的。免疫刺激部分与非铁蛋白多肽在大分子实体中的共递送以及它们在铁蛋白颗粒上的多价呈递也可以减少所需疫苗的总剂量,从而减少生产负担和成本。本文还公开了用于在免疫对抗呼吸道合胞病毒(RSV)、爱泼斯坦-巴尔病毒(Epstein Barr virus)(EBV)、流感和莱姆病的感染中使用的抗原性铁蛋白多肽、纳米颗粒和组合物。
此外,本文公开的多肽、纳米颗粒、组合物、方法和用途使得能够共递送来自病原体的非铁蛋白多肽和定制的免疫信号,所述定制的免疫信号可以引发特定类型的免疫应答以匹配针对特定病原体的所需免疫结果。一个例子是通过缀合至与血凝素(HA)融合的铁蛋白的TLR7/8激动剂对Th1型应答的诱导,这导致产生IgG2a转换抗体,已知所述转换抗体更有效地与FcγR接合以通过ADCC机制清除病毒感染的细胞(参见DiLillo等人,NatureMedicine 20:143-151(2014))。此外,将缀合至铁蛋白的免疫刺激部分与非铁蛋白多肽在单一分子实体中共递送可以确保免疫细胞的刺激在非铁蛋白多肽的存在下发生。相比之下,相同免疫刺激分子在没有缀合的情况下的掺合导致全身性分布,这通常需要更高的剂量,并且还存在因未被抗原接触的细胞中不加选择的免疫刺激所致的不希望影响的风险。
本文还描述了一种平台,其中例如通过提供包含第一和第二非铁蛋白多肽的重和轻铁蛋白链,将多种多肽掺入铁蛋白颗粒中。该平台可以提供二价的单一大分子实体,并且具有与铁蛋白治疗剂相关的其他优点,例如像如本文所述的免疫刺激部分的缀合。
发明内容
本公开文本的目的是提供可以提供以上讨论的一个或多个优点,或者至少为公众提供有用选择的组合物、试剂盒、方法和用途。因此,本文公开了以下实施方案。
实施方案1是一种铁蛋白蛋白,所述铁蛋白蛋白包含用半胱氨酸置换表面暴露的氨基酸的突变。
实施方案2是一种铁蛋白蛋白,所述铁蛋白蛋白包含含有半胱氨酸的N或C末端接头。
实施方案3是一种铁蛋白蛋白,所述铁蛋白蛋白包含一个或多个经由表面暴露的氨基酸连接至所述铁蛋白蛋白的免疫刺激部分。
实施方案4是前述实施方案所述的任一种,其为进一步包含非铁蛋白多肽的抗原性铁蛋白蛋白。
实施方案5是一种抗原性铁蛋白蛋白,所述抗原性铁蛋白蛋白包含(i)用半胱氨酸置换表面暴露的氨基酸的突变和连接至所述半胱氨酸的免疫刺激部分;和(ii)非铁蛋白多肽。
实施方案6是一种抗原性铁蛋白蛋白,所述抗原性铁蛋白蛋白包含(i)表面暴露的半胱氨酸,(ii)在所述铁蛋白蛋白N末端的肽接头,和(iii)在所述肽接头N末端的非铁蛋白多肽。
实施方案7是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白进一步包含用非天冬酰胺氨基酸置换表面暴露的天冬酰胺的突变。
实施方案8是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白进一步包含用非半胱氨酸氨基酸置换内部半胱氨酸的突变。
实施方案9是根据实施方案8所述的铁蛋白蛋白,其中所述内部半胱氨酸在幽门螺杆菌铁蛋白的位置31处,或如通过成对或结构比对确定的对应于幽门螺杆菌铁蛋白的位置31的位置处。
实施方案10是一种抗原性铁蛋白蛋白,所述抗原性铁蛋白蛋白包含:
a.用半胱氨酸置换表面暴露的氨基酸的突变和连接至所述半胱氨酸的免疫刺激部分;
b.用非半胱氨酸置换在幽门螺杆菌铁蛋白的位置31处的内部半胱氨酸的突变,或用非半胱氨酸置换如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中与位置31类似的位置处的内部半胱氨酸的突变;
c.用非天冬酰胺氨基酸置换表面暴露的天冬酰胺的突变;以及
d.非铁蛋白多肽。
实施方案11是根据实施方案8-10中任一项所述的铁蛋白蛋白,其中所述非半胱氨酸氨基酸是丝氨酸。
实施方案12是根据实施方案7-11所述的铁蛋白蛋白,其中所述天冬酰胺在幽门螺杆菌铁蛋白的位置19处,或如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中的类似位置处。
实施方案13是根据前述实施方案中任一项所述的铁蛋白蛋白,其中所述铁蛋白包含幽门螺杆菌铁蛋白的E12C、S26C、S72C、A75C、K79C、S100C和S111C突变中的一种或多种或如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中的一种或多种相应突变。
实施方案13a是根据实施方案13所述的铁蛋白蛋白,其中所述铁蛋白包含幽门螺杆菌铁蛋白的E12C突变,或如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中的相应突变。
实施方案13b是根据实施方案13所述的铁蛋白蛋白,其中所述铁蛋白包含幽门螺杆菌铁蛋白的S26C突变,或如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中的相应突变。
实施方案13c是根据实施方案13所述的铁蛋白蛋白,其中所述铁蛋白包含幽门螺杆菌铁蛋白的S72C突变,或如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中的相应突变。
实施方案13d是根据实施方案13所述的铁蛋白蛋白,其中所述铁蛋白包含幽门螺杆菌铁蛋白的A75C突变,或如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中的相应突变。
实施方案13e是根据实施方案13所述的铁蛋白蛋白,其中所述铁蛋白包含幽门螺杆菌铁蛋白的K79C突变,或如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中的相应突变。
实施方案13f是根据实施方案13所述的铁蛋白蛋白,其中所述铁蛋白包含幽门螺杆菌铁蛋白的S100C突变,或如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中的相应突变。
实施方案13g是根据实施方案13所述的铁蛋白蛋白,其中所述铁蛋白包含幽门螺杆菌铁蛋白的S111C突变,或如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中的相应突变。
实施方案14是根据实施方案4-13g中任一项所述的铁蛋白蛋白,其中所述非铁蛋白多肽是来自流感、爱泼斯坦-巴尔病毒、呼吸道合胞病毒(RSV)或疏螺旋体属(Borrelia)的多肽。
实施方案14a是根据实施方案4-13g中任一项所述的铁蛋白蛋白,其中所述非铁蛋白多肽包括来自流感的多肽,任选地其中所述多肽包括血凝素多肽。
实施方案14b是根据实施方案4-13g中任一项所述的铁蛋白蛋白,其中所述非铁蛋白多肽包括来自爱泼斯坦-巴尔病毒的多肽,任选地其中所述多肽包括gL、gH、gL/gH、gp220或gp42多肽。
实施方案14c是根据实施方案4-13g中任一项所述的铁蛋白蛋白,其中所述非铁蛋白多肽包括来自呼吸道合胞病毒的多肽,任选地其中所述多肽包括RSV F或RSV G多肽。
实施方案14d是根据实施方案4-13g中任一项所述的铁蛋白蛋白,其中所述非铁蛋白多肽包括来自疏螺旋体属的多肽,任选地其中所述多肽包括OspA多肽。
实施方案15是根据实施方案14或14c所述的铁蛋白蛋白,其中所述非铁蛋白多肽包括RSV G多肽,任选地其中所述RSV G多肽包含G多肽中心保守区。
实施方案15a是根据实施方案15所述的铁蛋白蛋白,其中所述RSV G多肽是未糖基化的。
实施方案15b是根据实施方案15或15a所述的铁蛋白蛋白,其中所述RSV G多肽化学缀合至所述铁蛋白蛋白。
实施方案16是根据实施方案4-5或7-15b中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白进一步包含在所述铁蛋白与所述非铁蛋白多肽之间的肽接头。
实施方案17是根据前述权利要求中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含免疫刺激部分,所述免疫刺激部分连接至所述半胱氨酸并且包含能够进行氢键结合或离子键结合的部分。
实施方案18是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含作为TLR2、TLR7/8、TLR9或STING的激动剂的免疫刺激部分。
实施方案18a是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含为TLR2的激动剂的免疫刺激部分,任选地其中所述激动剂是PAM2CSK4、FSL-1或PAM3CSK4。
实施方案18b是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含为TLR7/8的激动剂的免疫刺激部分,任选地其中所述激动剂是单链RNA、咪唑并喹啉、核苷类似物、3M-012或SM 7/8a。
实施方案18c是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含为TLR9的激动剂的免疫刺激部分,任选地其中所述激动剂是CpH寡脱氧核苷酸(ODN)、包含一个或多个含有5'嘌呤(Pu)-嘧啶(Py)-C-G-Py-Pu 3'的6聚体CpG基序的ODN、包含序列SEQ ID NO:210的ODN、或ISS-1018。
实施方案18d是根据实施方案18c所述的铁蛋白蛋白,其中所述TLR9的激动剂包含含有硫代磷酸酯连接的主链。
实施方案18e是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含为STING的激动剂的免疫刺激部分,任选地其中所述激动剂是环状二核苷酸(CDN)、cdA、cdG、cAMP-cGMP和2’-5’,3’-5’cGAMP或DMXAA。
实施方案19是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ ID NO:201-207或211-215中的任一个具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
实施方案19a是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ ID NO:201具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
实施方案19b是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ ID NO:202具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
实施方案19c是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ ID NO:203具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
实施方案19d是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ ID NO:201-207或211-215具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
实施方案19e是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ ID NO:204具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
实施方案19f是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ ID NO:205具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
实施方案19g是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ ID NO:206具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
实施方案19h是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ ID NO:207具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
实施方案19i是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ ID NO:211具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
实施方案19j是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ ID NO:212具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
实施方案19k是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ ID NO:213具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
实施方案19l是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ ID NO:214具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
实施方案19m是根据前述实施方案中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ ID NO:215具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
实施方案20是一种铁蛋白颗粒,所述铁蛋白颗粒包含根据前述实施方案中任一项所述的铁蛋白蛋白。
实施方案21是一种组合物,所述组合物包含根据前述实施方案中任一项所述的铁蛋白蛋白或铁蛋白颗粒和药学上可接受的载体。
实施方案22是一种组合物,所述组合物包含第一铁蛋白蛋白和第二铁蛋白蛋白,其中所述第一铁蛋白蛋白包含铁蛋白重链和第一非铁蛋白多肽,所述第二铁蛋白蛋白包含铁蛋白轻链和第二非铁蛋白多肽,并且所述第一非铁蛋白多肽和所述第二非铁蛋白多肽是不同的,任选地其中铁蛋白颗粒包含所述第一铁蛋白蛋白和所述第二铁蛋白蛋白。
实施方案23是根据实施方案21或22所述的组合物,所述组合物进一步包含佐剂。
实施方案24是根据实施方案4-23中任一项所述的铁蛋白蛋白、铁蛋白颗粒或组合物,用于在对受试者进行疫苗接种中使用。
实施方案25是一种对受试者进行疫苗接种的方法,所述方法包括向受试者给予根据实施方案4-23中任一项所述的铁蛋白蛋白、铁蛋白颗粒或组合物。
实施方案26是根据实施方案24所述的铁蛋白蛋白、铁蛋白颗粒或组合物或根据实施方案25所述的方法,其中所述受试者是人。
实施方案26a是根据实施方案24所述的铁蛋白蛋白、铁蛋白颗粒或组合物或根据实施方案25所述的方法,其中所述受试者是哺乳动物,任选地其中所述哺乳动物是灵长类动物或驯养哺乳动物,进一步任选地其中所述灵长类动物是非人灵长类动物、猴子、猕猴、恒河猴或食蟹猴或猿,或者所述驯养哺乳动物是犬、兔、猫、马、绵羊、牛、山羊、骆驼或驴。
实施方案27是一种核酸,所述核酸编码根据实施方案1-26a中任一项所述的铁蛋白蛋白,任选地其中所述核酸是mRNA。
实施方案F1是一种抗原性流感-铁蛋白多肽,所述抗原性流感-铁蛋白多肽包含(i)含有用半胱氨酸置换表面暴露的氨基酸的突变的铁蛋白蛋白,和(ii)流感多肽。
实施方案F2是一种抗原性流感-铁蛋白多肽,所述抗原性流感-铁蛋白多肽包含(i)铁蛋白蛋白,所述铁蛋白蛋白含有用半胱氨酸置换表面暴露的氨基酸的突变和与所述半胱氨酸缀合的免疫刺激部分,和(ii)流感多肽。
实施方案F3是根据实施方案F1所述的抗原性流感-铁蛋白多肽,所述抗原性流感-铁蛋白多肽进一步包含经由半胱氨酸缀合至所述铁蛋白蛋白的免疫刺激部分。
实施方案F4是根据实施方案F1-F3中任一项所述的抗原性流感-铁蛋白多肽,其中所述流感多肽包括血凝素(HA)或神经氨酸酶(NA)多肽。
实施方案F5是根据实施方案F4所述的抗原性流感-铁蛋白多肽,其中所述HA多肽包含保守区。
实施方案F6是根据实施方案F5所述的抗原性流感-铁蛋白多肽,其中所述保守区包含HA的全部或部分茎区。
实施方案F7是根据实施方案F1-F6中任一项所述的抗原性流感-铁蛋白多肽,其中所述流感抗原包括含有Y98F突变的HA抗原。
实施方案F8是根据实施方案F1-F7中任一项所述的抗原性流感-铁蛋白多肽,所述抗原性流感-铁蛋白多肽进一步包含用非半胱氨酸氨基酸置换内部半胱氨酸的突变。
实施方案F9是根据实施方案F8所述的抗原性流感-铁蛋白多肽,其中所述内部半胱氨酸在幽门螺杆菌铁蛋白的位置31处,或如通过成对或结构比对确定的对应于幽门螺杆菌铁蛋白的位置31的位置处,任选地其中所述内部半胱氨酸突变成丝氨酸。
实施方案F10是根据实施方案F1-F9中任一项所述的抗原性流感-铁蛋白多肽,所述抗原性流感-铁蛋白多肽进一步包含用非天冬酰胺氨基酸置换表面暴露的天冬酰胺的突变,任选地其中所述非天冬酰胺氨基酸是谷氨酰胺。
实施方案F11是根据实施方案F1-F10中任一项所述的抗原性流感-铁蛋白多肽,其中所述表面暴露的氨基酸是幽门螺杆菌铁蛋白的E12、S26、S72、A75、K79、S100或S111或如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中的类似氨基酸的突变。
实施方案F12是根据实施方案F11所述的抗原性流感-铁蛋白多肽,其中所述表面暴露的氨基酸处的所述突变是幽门螺杆菌铁蛋白的E12C、S26C、S72C、A75C、K79C、S100C或S111C或如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中的类似氨基酸。
实施方案F13是根据实施方案F1-F12中任一项所述的抗原性流感-铁蛋白多肽,其中所述免疫刺激部分是TLR7或TLR8的激动剂。
实施方案F14是根据实施方案F1-F13中任一项所述的抗原性流感-铁蛋白多肽,其中所述免疫刺激部分是TLR9的激动剂。
实施方案F15是根据实施方案F1或F3-F14中任一项所述的抗原性流感-铁蛋白多肽,所述抗原性流感-铁蛋白多肽进一步包含在所述免疫刺激部分与所述铁蛋白蛋白之间的接头。
实施方案F16是根据实施方案F15所述的抗原性流感-铁蛋白多肽,其中所述接头包括马来酰亚胺部分、聚乙二醇(PEG)部分和二苯并环辛炔(DBCO)部分中的一种、两种或三种。
实施方案F17是根据实施方案F1-F16中任一项所述的抗原性流感-铁蛋白多肽,所述抗原性流感-铁蛋白多肽进一步包含在所述铁蛋白蛋白与所述流感多肽之间的肽接头。
实施方案F18是一种铁蛋白颗粒,所述铁蛋白颗粒包含根据实施方案F1-F17中任一项所述的抗原性流感-铁蛋白多肽。
实施方案F19是一种组合物,所述组合物包含根据实施方案F1-F18中任一项所述的抗原性流感-铁蛋白多肽或铁蛋白颗粒和药学上可接受的载体。
实施方案F20是根据实施方案F19所述的组合物,所述组合物进一步包含含有铁蛋白蛋白和不同的流感多肽的第二抗原性流感-铁蛋白多肽。
实施方案F21是根据实施方案F20所述的组合物,其中所述流感多肽来自甲型流感并且所述第二抗原性流感-铁蛋白多肽的流感多肽来自乙型流感,或其中所述流感多肽和所述第二流感-铁蛋白多肽的流感多肽来自亚型H1、H2、H3、H4、H5、H6、H7、H8、H9、H10、H11、H12、H13、H14、H15、H16、H17或H18,或其中所述流感多肽中的一种或两种包括来自亚型H1、H3、H7或H10的工程化的稳定化茎抗原。
实施方案F22是根据实施方案F1-F21中任一项所述的抗原性流感-铁蛋白多肽、铁蛋白颗粒或组合物,用于在引发对流感的免疫应答或保护受试者免受流感感染的方法中使用。
实施方案F23是一种引发对流感的免疫应答或保护受试者免受流感感染的方法,所述方法包括向受试者给予根据实施方案F1-F22中任一项所述的任何一种或多种抗原性流感-铁蛋白多肽、铁蛋白颗粒或组合物。
实施方案F24是根据实施方案F1-F23中任一项所述的抗原性流感-铁蛋白多肽、铁蛋白颗粒、组合物或方法,其中所述受试者是人。
实施方案F25是一种核酸,所述核酸编码根据实施方案F1-F17中任一项所述的抗原性流感-铁蛋白多肽,任选地其中所述核酸是mRNA。
其他目的和优点将部分阐述于随后的描述中,并且部分将从所述描述中明显看出,或者可以通过实践获知。所述目的和优点将借助所附权利要求中特别指出的要素和组合来实现和获得。
应了解,上文的一般说明与下文的详细说明均仅是示例性和解释性的,并且对权利要求无限制性。
并入本说明书并且构成本说明书的一部分的附图展示了若干实施方案,并且附图连同本说明一起用于解释本文所述的原理。
附图说明
图1A至图1D示出了OspA-铁蛋白纳米颗粒的示例性设计。图1A.OspA与铁蛋白在基因上融合形成融合蛋白。OspA和铁蛋白序列由甘氨酸-丝氨酸接头(-GS-)隔开。图1B.描绘了OspA的胞外结构域的结构。其中OspA附接至铁蛋白的C末端用星号指示。图1C.由幽门螺杆菌铁蛋白的24个单体构成的示例性铁蛋白纳米颗粒。图1D.示例性OspA-铁蛋白融合蛋白纳米颗粒。描绘了铁蛋白(浅灰色)、甘氨酸-丝氨酸接头(GS)的位置和OspA(深灰色和黑色)(n:亚基数)。
图2A至图2D示出了示例性OspA-铁蛋白的表达和纯化。图2A.在Superose 6柱上纯化的示例性OspA-铁蛋白纳米颗粒的尺寸排阻色谱(SEC)图。图2B.来自Expi293细胞的纯化的示例性OspA-铁蛋白的SDS-PAGE凝胶。图2C.示例性OspA-铁蛋白纳米颗粒的动态光散射(DLS)图。半径为13nm,Pd%(归一化多分散性的量度)为7.4,并且质量为100%。图2D.由在67,000x放大倍率下对318个颗粒的透射电子显微照片的类别平均化构建而成的示例性OspA-铁蛋白的复合图像。铁蛋白纳米颗粒在透射电子显微镜上显现为具有空心中心的强圆形密度。每个纳米颗粒都被许多对应于OspA的短形状包围,所述短形状显现为圆形或微椭圆形。
图3A至图3B示出了在大肠杆菌中替代性血清型OspA纳米颗粒的产生。图3A.通过尺寸排阻色谱纯化的OspA-铁蛋白血清型1-5和7的SDS-PAGE生化分析。图3B.OspA-铁蛋白血清型1-5和7的透射电子显微镜(98,000x)。
图4示出了示例性血清型1OspA-铁蛋白纳米颗粒与莱姆(Lyme)(博氏疏螺旋体(Borrelia burgdorferi)的纯化的外表面蛋白A(OspA)的液体悬浮液)的免疫原性和持续时间的比较。在第0周和第4周,用1μg OspA-铁蛋白+Ribi佐剂(Sigmaadjuvant system目录号S6322-1vl)或莱姆(Lyme)肌内免疫C3H小鼠(n=5)。在每种组合物的情况下,通过在第2次免疫后2周(第6周)和在第2次免疫后21周(第25周)经由ELISA测量终点效价来评估抗体应答。
图5A至图5C呈现了关于示例性OspA-铁蛋白的信息,其中OspA多肽在OspA血清型1的与人白细胞功能相关抗原-1(hLFA-1)的序列片段具有同源性的表位处被修饰。图5A.示出了LFA-1同源位点(SEQ ID NO:83的氨基酸165-173)在OspA胞外结构域内的位置的结构。图5B.示出了SEQ ID NO:83(博氏疏螺旋体血清型1OspA)的OspA氨基酸165-173与hLFA-1和其他疏螺旋体物种和血清型中的相应序列的关系的系统树图。图5C.将SEQ ID NO:83的氨基酸165-173处的九个氨基酸的区段(九肽)(标记为“OspA”)与来自血清型2和血清型3OspA的相应九肽(分别为“S2”(SEQ ID NO:79)和“S3”(SEQ ID NO:80))、合理设计的取代九肽(“RD2”;SEQ ID NO:81)和来自hLFA-1的相应九肽(SEQ ID NO:78)进行比较。图5C按出现顺序分别公开了SEQ ID NO 77、79-81和78。
图5D.在第0周和第4周用1μg剂量的OspA血清型1-铁蛋白纳米颗粒与AddaVaxTM佐剂(基于角鲨烯的水包油纳米乳剂;可从InvivoGen获得,目录号vac-adx-10)肌内(IM)免疫C3H小鼠(n=5)。OspA序列包括野生型hLFA-1同源位点(即,SEQ ID NO:83的氨基酸165-173;“血清型1”)或如下的取代序列:SEQ ID NO:81(“RD”);SEQ ID NO:80(“血清型3置换物”);SEQ ID NO:79(“血清型2置换物”)。经由在所指示构建体的第2次免疫后2周通过ELISA测量的终点效价来评估抗体应答。
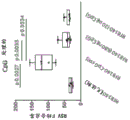
图6A至图6B呈现了关于与示例性免疫刺激部分TLR 7/8激动剂(3M-012)缀合的示例性OspA-铁蛋白纳米颗粒的信息。图6A.使用2步式点击化学策略将3M-012附接至铁蛋白。首先将DBCO-PEG4-马来酰亚胺接头附接至铁蛋白上的表面暴露的半胱氨酸。除去过量的接头后,添加叠氮化物-3M-012。图6B.在第0周和第4周用1μg所指示组合物肌内免疫C3H小鼠(n=5),并且在2周后进行分析。“缀合物”指示OspA-铁蛋白-3M-012缀合的纳米颗粒。“掺合物(Admix)”指示与29ng或20μg 3M-012或明矾一起给予的相同OspA-铁蛋白的非缀合混合物。OspA-铁蛋白和3M-012的29ng“掺和”混合物表示缀合的纳米颗粒上3M-012的摩尔当量。
图7A至图7C呈现了关于与示例性免疫刺激部分ISS-1018CpG(SEQ ID NO:210)缀合的示例性OspA-铁蛋白纳米颗粒的信息。图7A.使用2步式点击化学策略将CPG附接至铁蛋白。首先将DBCO-PEG4-马来酰亚胺接头附接至铁蛋白上的表面暴露的半胱氨酸。除去过量的接头后,添加叠氮化物-CpG。图7A公开了SEQ ID NO:534。图7B.通过SDS-PAGE凝胶对CpG-缀合进行的生化分析揭示出在与CpG缀合后分子量的移位,其中92%的OspA-铁蛋白与CpG缀合。图7C.在第0周和第4周用1μg所指示组合物肌内免疫C3H小鼠(n=5),并且在2周后进行分析。“缀合物”指示OspA-铁蛋白-CPG缀合的纳米颗粒。“掺合物”指示与339ng或50μgCpG或明矾一起给予的相同OspA-铁蛋白的非缀合混合物。OspA-铁蛋白和CPG的339ng“掺和”混合物表示缀合的纳米颗粒上CpG的摩尔当量。
图8A至图8F比较了在给予以下项之后对血清型1(图8A)、血清型2(图8B)、血清型3(图8C)、血清型4(图8D)、血清型5(图8E)和血清型7(图8F)的抗体应答:伴有明矾佐剂的单价血清型匹配的OspA-铁蛋白(1μg/剂量)(“单价的”)或伴有明矾佐剂的包含血清型1OspA-铁蛋白、血清型2OspA-铁蛋白、血清型3OspA-铁蛋白、血清型4OspA-铁蛋白、血清型5OspA-铁蛋白和血清型7OspA-铁蛋白中的每一种(各自为1μg/剂量)的六价组合物(“六价的”)。在第0周和第4周肌内免疫C3H小鼠(n=5),并且2周后经由通过ELISA测量的终点效价来评估抗体应答。将ELISA板用指定的OspA血清型包被。
图9A至图9G示出了在给予缀合的和非缀合的六价OspA-铁蛋白纳米颗粒组合物后,在小鼠中观察到的小鼠中对血清型1(图9A)、血清型2(图9B)、血清型3(图9C)、血清型4(图9D)、血清型5(图9E)、血清型6(图9F)和血清型7(图9G)的抗体应答。六价组合物包含血清型1OspA-铁蛋白、血清型2OspA-铁蛋白、血清型3OspA-铁蛋白、血清型4OspA-铁蛋白、血清型5OspA-铁蛋白和血清型7OspA-铁蛋白中的每一种,如对于图8A至F所述的,不同之处在于“六价-CPG”和“六价-3M-012”指示将纳米颗粒与CPG和3M-012化学缀合(参见图7A和6A和随附描述)。2周后经由通过ELISA测量的终点效价来评估抗体应答。将ELISA板用指定的OspA血清型包被。
图10A至图10G示出了对于六价OspA-铁蛋白纳米颗粒组合物,恒河猴(n=3/组)中的分别对血清型1-7的抗体应答,所述六价OspA-铁蛋白纳米颗粒组合物如图9A-G所述,不同之处在于剂量共为60μg(每种血清型10μg)并且含有非缀合的AF03佐剂。在第0周和第6周肌内对猴进行免疫。免疫后2周经由通过ELISA测量的终点效价来分析抗体应答。莱姆以10μg剂量用作比较参考。对于所有实验,将ELISA板用每个图片中指示的OspA血清型包被。
图10H至图10N示出了对于六价OspA-铁蛋白纳米颗粒组合物,恒河猴(n=3/组)中的分别对血清型1-7的抗体应答,所述六价OspA-铁蛋白纳米颗粒组合物如对于图10A-G所述,不同之处在于未使用AF03佐剂,而将纳米颗粒与3M-012或CpG缀合(参见图6A和图7A和随附描述)。剂量共使用60μg(每种血清型10μg)。在第0周和第6周肌内对猴进行免疫。免疫后2周经由通过ELISA测量的终点效价来分析抗体应答。对于所有实验,将ELISA板用每个图片中指示的OspA血清型包被。
图11示出了3M-012缀合的OspA-铁蛋白组合物的蜱虫攻击测试的结果。在第0周和第4周用1μg剂量的所指示组合物对小鼠进行免疫。单价组合物含有1μg与3M-012缀合的OspA-铁蛋白血清型1。“六价-3M-012”组合物如对于图9A-G所述的。对照颗粒缺少OspA多肽。在第二次免疫后两周,用感染博氏疏螺旋体N40菌株(血清型1)的5-6只蜱虫攻击小鼠5天,并且两周后将所述小鼠处死。将来自心脏、踝部和耳部的组织样品在BSK培养基中与针对博氏疏螺旋体的抗生素一起培养6周。通过PCR测试阴性样品中博氏疏螺旋体的存在。阳性样品是通过培养或PCR呈阳性的。
图12示出了通过质谱确认OspA-铁蛋白纳米颗粒与TLR 7/8激动剂3M-012的缀合。顶部图片示出了未缀合的,并且底部图片示出了缀合的构建体。数据显示出586.69道尔顿的质量移位,这与3M-012的添加一致。
图13示出了在如图所示的稀释系列上,通过ELISA测量的小鼠中与糖基化对应物(RD)相比对非糖基化突变体OspA-铁蛋白(NG-RD)的抗体应答。RD=SEQ ID NO:52。NG-RD=SEQ ID NO:53。在第0周和第4周以1μg剂量对小鼠进行疫苗接种。
图14示出了在如图所示的稀释系列上,通过ELISA测量的小鼠中与莱姆和阴性(免疫前)对照相比对OspA-铁蛋白(SEQ ID NO:52)、OspA-铁蛋白糖基化突变体N>Q(SEQ ID NO:53)和糖基化突变体S/T>A(SEQ ID NO:63)的抗体应答。
图15A至图15E示出了对包含不同接头(GS,Gly-Ser接头;GS1,Gly-Gly-Gly-Ser接头(SEQ ID NO:443);GS2,SEQ ID NO:91接头;GS5,SEQ ID NO:92接头;构建体序列分别为SEQ ID NO:53和60-62)的OspA构建体的纯化和表征。图15A.对纯化的包含如所指示接头的OspA构建体的考马斯染色。图15A按出现顺序分别公开了SEQ ID NO 443-445。图15B.包含GS1的OspA-铁蛋白纳米颗粒(SEQ ID NO:60)的动态光散射(DLS)。图15C.包含GS2的OspA-铁蛋白纳米颗粒(SEQ ID NO:61)的DLS。图15D.包含GS5的OspA-铁蛋白纳米颗粒(SEQ IDNO:62)的电子显微照片(EM)。图15E.包含GS5的OspA-铁蛋白纳米颗粒(SEQ ID NO:62)的DLS。
图16示出了在如图所示的稀释系列上,通过ELISA测量的小鼠中与莱姆和阴性(免疫前)对照相比对以下OspA-铁蛋白构建体的抗体应答,所述OspA-铁蛋白构建体包含不同的接头(接头1X GGGS构建体,SEQ ID NO:60(“1X GGGS”公开为SEQ ID NO:443);接头2x GGGS构建体,SEQ ID NO:61(“2x GGGS”公开为SEQ ID NO:444);接头5X GGGS构建体,SEQ ID NO:62(“5X GGGS”公开为SEQ ID NO:445))。
图17A至图17C示出了对2,4-二氧四氢喋啶合酶(lumazine synthase)OspA血清型4构建体(SEQ ID NO:18)的表征。图17A.DLS数据。图17B.尺寸排阻色谱(SEC)迹线的所指示级分22-64的考马斯凝胶。图17C.EM数据。
图18示出了小鼠中对伴有或不伴有明矾的OspA血清型4-铁蛋白构建体(SEQ IDNO:4)和OspA血清型4-2,4-二氧四氢喋啶合酶构建体(SEQ ID NO:18)的抗体应答。
图19A至图19C示出了对OspA血清型1-2,4-二氧四氢喋啶合酶构建体(SEQ ID NO:12)的表征。图19A.EM数据。图19B.SEC迹线的所指示级分20-40的考马斯凝胶。图19C.DLS数据。
图20A至图20C示出了对OspA血清型2-2,4-二氧四氢喋啶合酶构建体(SEQ ID NO:16)的表征。图20A.EM数据。图20B.SEC迹线的所指示级分27-56的考马斯凝胶。图20C.DLS数据。
图21A至图21B示出了对OspA血清型3-2,4-二氧四氢喋啶合酶构建体(SEQ ID NO:17)的表征。图21A.SEC迹线的所指示级分23-39的考马斯凝胶。图21B.DLS数据。
图22A至图22C示出了对OspA血清型5-2,4-二氧四氢喋啶合酶构建体(SEQ ID NO:19)的表征。图22A.EM数据。图22B.SEC迹线的所指示级分22-38的考马斯凝胶。图22C.DLS数据。
图23A至图23C示出了对OspA血清型7-2,4-二氧四氢喋啶合酶构建体(SEQ ID NO:21)的表征。图23A.EM数据。图23B.SEC迹线的所指示级分20-38的考马斯凝胶。图23C.DLS数据。
图24A至图24G示出了对于用明矾或AF03佐剂化的含有1ug对应于OspA血清型1-7的每种OspA-铁蛋白纳米颗粒的七价OspA-铁蛋白纳米颗粒组合物(共7ug)或对于莱姆,C3H小鼠(n=5/组)中分别对血清型1-7的抗体应答。对于所有实验,将ELISA板用每个图片中指示为“S X”的OspA血清型包被,其中X是血清型编号。
图25示出了恒河猴中终点抗体效价的时间历程。在第0周和第6周用伴有AF03佐剂的六价OspA-铁蛋白疫苗(在单独的纳米颗粒中含有血清型1、2、3、4、5和7的OspA)或肌内对猴进行免疫。将ELISA板用OspA血清型1包被。
图26A至图26B.代表性H1N1流感病毒株系的序列比较和同源性。(图26A)使用载体NTI AlignX软件对候选抗原性HA多肽的序列比对。白底黑字:源自给定位置处的完全保守残基的共有残基。黑底白字:源自给定位置处发生率大于50%的单一残基的共有残基。白底黑字加下划线和粗体:与给定位置处的共有残基弱相似的残基。白底黑字带有双下划线和斜体:源自给定位置处的相似残基块的共有残基。白底黑字加粗:非相似残基。示出的序列是以下序列的HA部分加上C末端处的接头丝氨酸:CA09 HA-Np=SEQ ID NO:315的残基1-519。COBRA P1 HA-Np=SEQ ID NO:327的残基1-519。COBRA X6 HA-Np=SEQ ID NO:329的残基1-518。NC99 HA-Np=SEQ ID NO:301的残基1-518。HK77 HA-Np=SEQ ID NO:318的残基1-519。FM47 HA-Np=SEQ ID NO:317的残基1-519。DV57 HA-Np=SEQ ID NO:321的残基1-518。MAL54 HA-Np=SEQ ID NO:316的残基1-519。(图26B)用邻接法(Vector NTI)针对来自所列出流感株系的HA蛋白序列生成的系统树图。箭头指示通过从这些序列产生HA-铁蛋白纳米颗粒并在小鼠中测试其免疫原性而被选择作为用于评价的候选物的株系。
图27.铁蛋白上的工程化的表面暴露的半胱氨酸(Cys)。在铁蛋白纳米颗粒的情境下示出了由置换表面暴露的氨基酸的突变产生的半胱氨酸的位置。
图28A至图28B.Toll样受体(TLR)激动剂与铁蛋白的缀合。(图28A)在铁蛋白纳米颗粒的情境下说明了将SM7/8a小分子经由含有马来酰亚胺反应性基团的PEG4接头与由置换铁蛋白中表面暴露的氨基酸的突变产生的半胱氨酸缀合的结果。(图28B)在铁蛋白纳米颗粒的情境下说明了通过马来酰亚胺-DBCO双官能接头和叠氮化物官能化的CpG试剂,使用2步式点击化学将CpG(SEQ ID NO:535)与由置换铁蛋白中表面暴露的氨基酸的突变产生的半胱氨酸缀合的结果。
图29A至图29B.Toll样受体(TLR)激动剂与铁蛋白的缀合。(图29A)包含HA多肽和3M-012的铁蛋白纳米颗粒的模型,所述3M-012经由马来酰亚胺-DBCO双官能接头和叠氮化物官能化的3M-012试剂,使用2步式点击化学反应而与铁蛋白的表面暴露的半胱氨酸缀合。(图29B)包含HA多肽和CpG的铁蛋白纳米颗粒的模型,所述CpG用马来酰亚胺-DBCO双官能接头和叠氮化物官能化的CpG试剂,使用2步式点击化学反应而与铁蛋白的表面暴露的半胱氨酸缀合。图29B公开了SEQ ID NO:534。
图30.某些铁蛋白纳米颗粒构建体的铁蛋白部分内的胰蛋白酶切割位点。一些铁蛋白纳米颗粒除了用于缀合佐剂的未配对表面暴露的半胱氨酸外还包含胰蛋白酶切割位点。图30中所呈现的氨基酸序列是“通用”序列,其示出了多个构建体共有的序列。例如,SEQID NO:314的残基519-694包含图30中所示的“通用”序列。“XXX”序列表示流感多肽。还指出了该序列中存在的铁蛋白S111C突变的位置。
图31A和图31B.在伴有或不伴有缀合的情况下的凝胶移位和质谱(MS)结果。(图31A)H1/茎-Np(SEQ ID NO:343)在存在(+)或不存在(-)与马来酰亚胺-PEG4-SM7/8a的缀合的情况下的凝胶移位和质谱结果。(图31B)H5/hCobra2-Np(SEQ ID NO:332)在存在(+)或不存在(-)与马来酰亚胺-PEG4-SM7/8a的缀合的情况下的凝胶移位和质谱结果。
图32A和图32B.在伴有或不伴有缀合的情况下的进一步凝胶移位结果。(图32A)在伴有或不伴有与马来酰亚胺-PEG4-SM7/8a或通过2步式点击化学与马来酰亚胺-PEG4-DBCO和叠氮化物-CpG的缀合的情况下,肽N-糖苷酶(PNGase)处理后的H1/茎-Np的凝胶移位结果。(图32B)在伴有或不伴有与马来酰亚胺-PEG4-SM7/8a或通过2步式点击化学与马来酰亚胺-PEG4-DBCO和叠氮化物-CpG的缀合的情况下,胰蛋白酶处理后的H1/茎-Np的凝胶移位结果。
图33A和图33B.在伴有或不伴有马来酰亚胺-PEG4-SM7/8a与H1/茎-Np的缀合的情况下的质谱。(图33A)PNGase处理后的MS数据显示出与马来酰亚胺-PEG4-SM7/8a缀合之前和之后的H1/茎-Np的质量。(图33B)用胰蛋白酶处理H1/茎-Np后的MS数据显示出与马来酰亚胺-PEG4-SM7/8a缀合之前和之后经切割铁蛋白的质量。
图34.在伴有或不伴有马来酰亚胺-PEG4-DBCO接头与H1/茎-Np的缀合的情况下的质谱。通过在添加接头后由MS测量的质量变化来确认至H1/茎-Np的马来酰亚胺-PEG4-DBCO接头添加。
图35.通过2步式点击化学缀合CpG之前和不同阶段的H1/茎-Np的SDS-PAGE。“叠氮化物-CpG之后”是指2步式点击反应的最终产物。
图36.对包含3M-012的接头与NC99 HA-TEV-Np构建体的缀合的表征。WT和+TEV泳道中的构建体具有序列SEQ ID NO:313;S26C是指SEQ ID NO:310;S72C是指SEQ ID NO:311;A75C是指SEQ ID No:312;并且S111C是指SEQ ID NO:309。除WT外,所有样品均用烟草蚀纹病毒蛋白酶(TEV)处理。
图37A至图37E.在伴有或不伴有还原或缀合的情况下各种构建体的质谱。(图37A)还原之前的包含S111C的H1/茎-Np。(图37B)还原之后的包含S111C的H1/茎-Np。还原之后观察到的质量下降(115Da)与去除抑制半胱氨酸反应性的翻译后修饰一致。(图37C)在伴有或不伴有与3M012的缀合的情况下NC99 HA-TEV-Np-S26C纳米颗粒(SEQ ID NO:310)的质谱。(图37D)在伴有或不伴有与3M012的缀合的情况下NC99 HA-TEV-Np-A75C纳米颗粒(SEQ IDNO:312)的质谱。(图37E)在伴有或不伴有与3M012的缀合的情况下NC99 HA-TEV-Np-S111C纳米颗粒(SEQ ID NO:309)的质谱。
图38A至图38F.在伴有或不伴有与SM7/8a、3M012或CpG的缀合的情况下H1/茎-Np或NC99 HA-Np的纳米颗粒的负染色电子显微镜(EM)图像。(图38A)未缀合的H1/茎-Np。(图38B)H1/茎-Np-SM7/8a缀合物。(图38C)H1/茎-Np-CpG缀合物。(图38D)NC99 HA-Np(SEQ IDNO:309)]。(图38E)NC99 HA-Np-3M012缀合物。(图38F).NC99 HA-Np-CpG缀合物。
图39A至图39C.H1/茎-Np-SM7/8a缀合物(图39A)、H1/茎-Np-CpG缀合物(图39B)或未缀合的H1/茎-Np(图39C)的动态光散射(DLS)分析。
图40A-B.对与掺合的如所指示佐剂一起配制或如图28A-B所示经由PEG4接头与TLR激动剂(如SM7/8a或CpG)缀合的H1/茎-Np的抗体应答。在免疫(第0周和第3周)后5周时从小鼠(n=5)收集血清,并且通过酶联免疫吸附测定(ELISA)测量抗体效价。该数据证明了H1/茎-Np-TLR-激动剂缀合物的自佐剂化特性。图40A示出了针对H1/新喀里多尼亚/20/1999HA三聚体的ELISA。PAA=聚丙烯酸;混合等摩尔=83.3ng SM7/8a(相当于用SM7/8缀合的铁蛋白纳米颗粒给予的剂量);高剂量=21.84μg(高于用SM7/8缀合的铁蛋白纳米颗粒给予的剂量)。图40B示出了针对H1/茎三聚体的ELISA。混合等摩尔=850ng CpG(相当于用CpG缀合的铁蛋白纳米颗粒给予的剂量);高剂量=20μg CpG。
图41A至图41C.用伴有或不伴有缀合或分开的3M-012的NC99HA-Np(SEQ ID NO:309)获得的效价的比较。在小鼠中测试了对NC99HA-Np-3M012缀合的纳米颗粒(0.22μg/剂量)的抗体应答。掺合物对照包括HA-Np(0.22μg/剂量)和10μg 3M012(典型的文献剂量)的混合物以及HA-Np(0.22μg/剂量)和1.7ng 3M012(缀合物的等摩尔匹配物)的混合物。另外的对照包括以匹配的HA含量(0.17μg HA/剂量)投配的未缀合HA-Np和IIV。基于ELISA终点效价(图41A)、假病毒(PsV)中和IC50效价(图41B)和血凝抑制(HAI)效价(图41C),HA-Np-3M012缀合物诱导了比等摩尔掺合物对照显著更强的抗体应答。与未缀合的纳米颗粒和IIV护理标准相比,缀合的纳米颗粒还诱导了更强的应答(ELISA)和更强的中和抗体应答(PsV),但是该结果在HAI分析中没有统计学显著性。测定是对于加强免疫后2周的血清的。一式三份地运行所有样品。对中值+/-SEM进行作图。****p<0.0001;***p<0.001;**p<0.01;*p<0.05。
图42A至图42C.用伴有或不伴有缀合或分开的CpG的NC99HA-Np(SEQ ID NO:309)获得的效价的比较。在小鼠中测试了对HA-Np-CpG缀合的纳米颗粒(0.22μg/剂量)的抗体应答。掺合物对照包括HA-Np(0.22μg/剂量)和20μg CpG(典型的治疗性剂量)的混合物以及HA-Np(0.22μg/剂量)和21ng CpG(缀合物的等摩尔匹配物)的混合物。另外的对照包括以匹配的HA含量(0.17μg HA/剂量)投配的未缀合HA-Np和IIV。基于ELISA终点效价(图42A)和假病毒中和IC50效价(图42B),与匹配的掺合物、未缀合的颗粒或IIV相比,缀合物诱导更强的结合和中和抗体应答。HA-Np-CpG缀合物还诱导了比等摩尔掺合物对照显著更强的HAI效价(图42C)。另外,HAI效价比未缀合的HA-Ferr和IIV高2.6和3.0倍,但是这些结果并不显著。ELISA和PsV测定是对于加强免疫后2周的血清的,并且在加强免疫后5周对血清进行HAI分析。一式三份地运行所有样品,并且对中值+/-SEM进行作图。****p<0.0001;***p<0.001;**p<0.01;*p<0.05。
图43A至图43C.对源自六个进化上相异的H1血凝素(HA)抗原和两个计算生成的(COBRA)抗原的自组装HA-铁蛋白纳米颗粒的表征。(图43A)通过动态光散射(DLS)测量纳米颗粒大小和多分散性(“分散性”)。(图43B)通过SDS-PAGE考马斯染色评估HA纳米颗粒的纯度。(图43C)通过负染色电子显微镜在80,000x放大倍率下使纳米颗粒完整性可视化。FM47=A/蒙茅斯堡/1-JY2/1947;MAL54=A/马来西亚/302/1954;DV57=A/丹佛/1957(DV57);HK77=A/香港/117/1977;NC99=A/新喀里多尼亚/20/99;CA09=A/加利福尼亚/4/2009。COBRA P1和COBRA X6是从多个序列计算生成的共有序列,最近由Carter DM等人,J Virol90:4720-4734(2016)所述。对于SEQ ID NO参见图26A-B的图例。
图44A至图44H.由各种HA-铁蛋白纳米颗粒(对于SEQ ID NO参见图26A-B的图例)引发的免疫应答的效力和广度。用所指示HA-Np疫苗免疫后6周,针对一组相异的H1N1流感病毒,对来自小鼠的血清的血凝抑制(HAI)效价(log2)进行测定。在第0周和第3周,用血凝素纳米颗粒(HA-Np)对小鼠(n=5)进行免疫。虚线指示测定检测极限。(图44A至图44E)伴有Ribi佐剂的数据。(图44F至图44H)伴有AF03佐剂的数据。x轴线指示从1934年到2013年按参考年份测试的H1N1流感株系组。表2给出了对应于每年的完整株系名称。星号指示匹配的株系。
图45A至图45F.由HA-铁蛋白纳米颗粒诱导的HA抗体应答。(图45A)用使用SigmaAdjuvant System(目录号S6322)的指定纳米颗粒或纳米颗粒组合对小鼠[n=5]进行免疫。IIV是指流感灭活疫苗。(图45B-F)通过确定对来自以下项的HA三聚体的ELISA效价来测量抗体应答:A/蒙茅斯堡/1/1947(图45B);A/马来西亚/302/1954(图45C);A/香港/117/1977(图45D);A/新喀里多尼亚/20/99(图45E);或A/加利福尼亚/4/2009(图45F)。第一次免疫后5周测量ELISA效价。测试的最低血清稀释度设定了测定检测极限,如通过虚线所指示的。空心圆圈指示给予至小鼠的纳米颗粒的起源株系与通过ELISA测定的株系之间的匹配。
图46A至图46H.如通过HAI效价的测定所测量的,对给予至小鼠的多种铁蛋白纳米颗粒的HA混合物的抗体应答。(图46A至图46B)双价组合。(图46C至图46E)三价组合。(图46F至图46H)四价组合。测定了一组相异的H1N1流感病毒的HAI效价(log2)。在伴有佐剂的情况下,在第0周和第3周用所指示HA-纳米颗粒组合对小鼠(n=5)进行免疫。在伴有AF03佐剂的情况下测试二价组合COBRA X6+COBRA P1 HA-Np,以与单价COBRA HA-Np的评价相一致。同样,单独株系HA-铁蛋白纳米颗粒的组合使用Ribi佐剂,以与单价单独株系HA-Np的评价相一致。星号指示给予至小鼠的纳米颗粒的起源株系与通过ELISA测定的株系之间的匹配。x轴线指示从1934年到2013年按参考年份测试的H1N1流感株系组。表2给出了针对每年的完整株系名称。虚线指示测定检测极限。
图47A至图47F.如通过HAI效价的测定所测量的,对伴有Ribi或AF03佐剂的组合物的抗体应答。对于NC99和CA09 HA-Np的二价组合(图47A至图47B),NC99、CA09和HK77 HA-Np的三价组合(图47C至图47D)和NC99、CA09和FM47 HA-Np的三价组合(图47E-47F),用Ribi佐剂获得的结果(图47A、图47C和图47E)相比于用AF03佐剂获得的结果(图47B、图47D和图47F)是相似的。初免剂量后6周,在小鼠血清中测定HAI效价,其中在第3周进行加强免疫。在伴有Ribi或AF03佐剂的情况下,用如所指示的HA-Np组合对小鼠[n=5]进行免疫。星号指示给予至小鼠的纳米颗粒的起源株系与通过ELISA测定的株系之间的匹配。x轴线指示从1934年到2013年按参考年份测试的H1N1流感株系组。表2给出了针对每年的完整株系名称。虚线指示测定检测极限。
图48A至图48C.如通过HAI效价的测定所测量的,由蛋中产生的NC99和CA09灭活流感疫苗(IIV)引发的比较性抗体应答。(图48A)NC99IIV。(图48B)CA09 IIV。(图48C)NC99+CA09 IIV。用所指示IIV疫苗(作为单一组分或共同给予的)免疫后6周,针对一组相异的H1N1流感病毒的来自小鼠的血清的血凝抑制(HAI)效价(log2)。在伴有Ribi佐剂的情况下,在第0周和第3周用170ng(HA含量)的每种疫苗对小鼠(n=5)进行免疫。x轴线指示从1934年到2013年按参考年份测试的H1N1流感株系组(也参见表2)。x轴线指示从1934年到2013年按参考年份测试的H1N1流感株系组。表2给出了针对每年的完整株系名称。虚线指示测定检测极限。
图49A至图49D.如通过HAI效价的测定所测量的,使用HA-铁蛋白纳米颗粒组合物或IIV对雪貂进行免疫后,针对各种流感病毒的抗体应答。在使用掺合有AF03佐剂的以下项进行两次免疫后来自雪貂(n=12/组)的血清的HAI效价(log2):图49A:单独的PBS;图49B:A/加利福尼亚/2009IIV;图49C:NC99+CA09+HK77 HA-Np;图49D:COBRA-X6+P1+HK77 HA-Np。
图49E.对用HA-铁蛋白纳米颗粒组合物、IIV或PBS免疫的雪貂的异源攻击。如对于图49A-D所述那样对雪貂进行免疫,并且在最后一次免疫后4周通过以下方式来用1947蒙茅斯堡病毒攻击:用1mL的A/蒙茅斯堡/1/1947病毒以50%组织培养物感染剂量(TCID50)的104.65倍进行鼻腔接种。在攻击后的七天时间历程中,在鼻洗液中定量病毒效价。虚线指示测定检测极限。根据单尾不配对t检验和单向方差分析[F(3,44)=5.18,p=0.00375],与媒介物(PBS)对照相比,在用HA-Np组合但未用CA09 IIV免疫的雪貂中,病毒效价在攻击后第5天显著降低。***=p≤0.001,根据学生t检验。
图50A-C.用以下项免疫后的食蟹猴(长尾猕猴(Macaca fascicularis))的抗体应答:50μg与掺合的AF03佐剂一起配制的H1/茎-Np、或200μg H1/茎-Np(无佐剂对照)、或200μg H1/茎-Np-SM7/8a缀合物(图28A中所示的)或200μg H1/茎-Np-CpG缀合物(图28B中所示的)。图50A示出了在所指示时间点(其中免疫在第0、4和10周进行)通过酶联免疫吸附测定(ELISA)在用H1/新喀里多尼亚/20/1999HA三聚体包被的板上测量的HA抗体效价。图50B示出了用H1/新喀里多尼亚/20/1999HA和NA假型化的慢病毒的中和IC50。图50C示出了用H5/越南/1203/2004HA和NA假型化的慢病毒的中和IC50。该数据证明了H1/茎-Np-TLR-激动剂缀合物在灵长类动物模型中的自佐剂化特性。
图51A至图51B.用伴有或不伴有缀合或分开的3M-012的NC99HA-Np(SEQ ID NO:309)获得的效价的比较。对以下四种剂量的与NC99HA-Np-3M012缀合的纳米颗粒的抗体应答:0.1μg、0.5μg、2.5μg和12.5μg。包括了掺合物对照和未缀合的纳米颗粒用于比较。计算用于“等摩尔”掺合物对照和“高剂量”掺合物对照的TLR激动剂的量,以维持最初的缀合研究中使用的抗原与佐剂的比率(0.22μg HA-NP,对于“等摩尔”伴有1.7ng 3M012或对于“高剂量”伴有10μg)。在NC99慢病毒报告物测定(左,图51A)和NC99HAI测定(右,图51B)中测量血清中和。箭头突出显示了2.5μg剂量,其中HA-NP-3M012缀合物尽管含有低超过5000倍的3M012佐剂,但诱导了与HA-NP+3M012相似的抗体效价。对平均值±SEM进行作图。
图52A至图52B通过考马斯和蛋白质印迹分析示出了去除或未去除His标签的纯化的单链gL和gH单体(图52A)(SEQ ID NO:406)和三聚体(图52B)(SEQ ID NO:411)。图52B还呈现了来自尺寸排阻柱(6)纯化的级分的UV吸收迹线。
图53A至图53E示出了对单链gL/gH-铁蛋白纳米颗粒(SEQ ID NO:414)的纯化和表征。示出了6纯化级分的UV吸收迹线(图53A),以及对从纯化中选择的级分的考马斯(图53B)和蛋白质印迹(图53C)分析(L指示分子量梯状标志;150和250kDa条带在如右图53B处所指示的150kDa和250kDa条带位置中被标记出)。还呈现了单链纳米颗粒的动态光散射(图53D)和电子显微镜(图53E)分析。
图54示出了不同的代表性单链gL/gH-铁蛋白构建体。
图55示出了用掺合有AF03佐剂(其是基于角鲨烯乳剂的佐剂)的单链gL/gH三聚体或纳米颗粒(NP)对小鼠进行免疫后的抗体效价。当将NP构建体与其对应的三聚体构建体进行比较时,*p-值=<0.05。从左至右,构建体是SEQ ID NO:416、410、411、413、412和414。
图56A至图56B示出了与单链gL/gH纳米颗粒和阴性对照裸铁蛋白(即,未与任何非铁蛋白多肽或免疫刺激部分缀合的铁蛋白)相比,小鼠中对包含gp220纳米颗粒(SEQ IDNO:401)和单链gL/gH纳米颗粒(“gL_gH_C5 NP”,SEQ ID NO:419)二者的二价组合物的抗gL/gH抗体应答。结果表明,相对于在单链gL/gH与阴性对照裸铁蛋白的情况下的结果,使用二价组合物不会导致对抗gL/gH抗体应答的干扰。两种组合物均包含AF03佐剂。示出了在各个稀释度(图56A)和结合效价(图56B)下的ELISA结果。
图57A至图57B示出了对如对于图57A-B所述的包含gp220纳米颗粒和单链gL/gH纳米颗粒的二价组合物的抗gp220抗体应答。结果表明,相对于在gp220纳米颗粒与阴性对照裸铁蛋白的情况下的结果,使用二价组合物不会导致对抗gp220抗体应答的干扰。两种组合物均包含AF03佐剂。示出了在各个稀释度(图57A)和结合效价(图57B)下的ELISA结果。
图58A示出了包含EBV多肽和铁蛋白的纳米颗粒的设计,所述铁蛋白包含用半胱氨酸置换表面暴露的氨基酸以用于与免疫刺激部分(如toll样受体(TLR)激动剂)缀合的突变。对于对应于该设计的示例性序列,参见SEQ ID NO:414,其中单链gL/gH抗原通过柔性的46个氨基酸接头与铁蛋白连接。图58B示出了适合于与根据图58A的构建体缀合的代表性toll样受体(TLR)激动剂(具有PEG4-马来酰亚胺接头的SM7/8a)。图58C示出了具有SM7/8a的gL/gH纳米颗粒的电子显微照片(EM)图像,所述SM7/8a经由铁蛋白表面上的半胱氨酸和PEG4-马来酰亚胺接头与所述gL/gH纳米颗粒缀合。
图59A示出了包含用半胱氨酸置换表面暴露的氨基酸的突变的铁蛋白的部分结构,其中指出了半胱氨酸的位置。图59B说明了通过并置铁蛋白、接头和CpG佐剂来将CpG佐剂(SEQ ID NO:535)缀合至铁蛋白,所述缀合被取向成显示每个部分的彼此邻近地附接的部分。
图60A至图60B示出了gL/gH-铁蛋白的未缀合形式(图60A)和SM7/8a缀合形式(图60B)的质谱(MS)光谱。主峰质量的差异为711Da,这大约相当于来自将SM7/8a与接头缀合的预测差异。
图61A至图61B示出了gp220-铁蛋白的未缀合形式(图61A)和SM7/8a缀合形式(图61B)的质谱(MS)光谱。主峰质量的差异为714.7Da,这大约相当于来自将SM7/8a与接头缀合的预测差异。
图62A至图62D示出了未缀合的(图62A、C)和缀合的(图62B、D)单链gL/gH(图62A、B)和gp220(图62C、D)铁蛋白纳米颗粒的电子显微镜(EM)图像,其表明SM7/8a与这些纳米颗粒的缀合没有破坏纳米颗粒结构。
图63A至图63B示出了用包含不伴有缀合的SM7/8a或其他佐剂、伴有作为单独分子的AF03佐剂或伴有缀合的SM7/8a的单链gL/gH的铁蛋白纳米颗粒治疗后小鼠中的抗体应答。ELISA结果显示为各个稀释度(图63A)和结合效价(图63B)。
图64A至图64B示出了用包含单独的、伴有作为单独分子的AF03佐剂或伴有缀合的SM7/8a的gp220的纳米颗粒治疗后小鼠中的抗体应答。ELISA结果显示为各个稀释度(图64A)和结合效价(图64B)。
图65A至图65B示出了如通过ELISA所测量的,与用与SM7/8a缀合的单链gL/gH铁蛋白纳米颗粒和裸铁蛋白的治疗相比,用与SM7/8a缀合的gp220纳米颗粒和与SM7/8a缀合的单链gL/gH铁蛋白纳米颗粒治疗后小鼠中的抗gL/gH抗体应答。示出了对于不伴有(图65A)或伴有(图65B)掺合的AF03的实验的结果。
图66A至图66B示出了如通过ELISA所测量的,与用与SM7/8a缀合的gp220纳米颗粒和裸铁蛋白的治疗相比,用与SM7/8a缀合的gp220纳米颗粒和与SM7/8a缀合的单链gL/gH纳米颗粒治疗后小鼠中的抗gp220抗体应答。示出了对于不伴有(图66A)或伴有(图66B)掺合的AF03的实验的结果。
图67示出了如通过ELISA终点效价所测量的,在伴有或不伴有掺合的AF03佐剂和/或与单链gL/gH纳米颗粒缀合的SM7/8a中的任一种或二者的情况下,用单链gL/gH纳米颗粒(gL/gH_C5;SEQ ID NO:419)和裸铁蛋白治疗后小鼠中的抗gL/gH抗体应答。
图68示出了在伴有或不伴有掺合的AF03佐剂和/或与gp220纳米颗粒缀合的SM7/8a中的任一种或二者的情况下,用gp220纳米颗粒和裸铁蛋白治疗后小鼠中的抗gp220抗体应答。
图69示出了用包含gp220纳米颗粒和单链gL/gH纳米颗粒的二价组合物治疗后小鼠中的抗gL/gH抗体应答。如图例中所指示,一些纳米颗粒与SM7/8a缀合,并且一些纳米颗粒与AF03掺合。图例中从上到下的符号顺序与图中从左到右的符号顺序匹配。
图70示出了用包含单链gL/gH纳米颗粒和gp220纳米颗粒和/或裸铁蛋白的二价组合物治疗后小鼠中的抗gp220抗体应答。如图例中所指示,一些纳米颗粒与SM7/8a缀合,并且一些纳米颗粒与AF03掺合。图例中从上到下的符号顺序与图中从左到右的符号顺序匹配。
图71A至图71D示出了在伴有或不伴有掺合的AF03佐剂和/或与SM7/8a(图71A、图71C或图71D)或CpG寡脱氧核苷酸(图71B)的缀合的情况下,用gL_gH_C7纳米颗粒(SEQ IDNO:420)治疗后小鼠中的抗体应答。示出了通过ELISA测量的来自初免取血的终点效价(图71A)、来自加强免疫取血的单独稀释度下的ELISA结果(图71B),以及通过ELISA测量的来自加强免疫取血(图71C)和终末期取血(图71D)的终点效价。
图72以通过ELISA测量的来自初免、加强免疫和终末期取血的终点效价示出了在伴有或不伴有掺合的AF03佐剂和/或与SM7/8a的缀合的情况下,用gL_gH_C5纳米颗粒(SEQID NO:419)治疗后小鼠中的抗体应答。
图73以通过ELISA测量的来自初免、加强免疫和终末期取血的终点效价示出了在伴有或不伴有掺合的AF03佐剂和/或与SM7/8a的缀合的情况下,用gp220纳米颗粒治疗后小鼠中的抗体应答。
图74A示出了通过考马斯染色可视化的粉纹夜蛾(T.ni)铁蛋白的伴有或不伴有与gp220或gL/gH的融合的轻链和重链。标记了图74A最右边泳道中的20、25、75、100和150kDa标记。图74B提供了包含粉纹夜蛾铁蛋白的伴有或不伴有与gp220或gL/gH的融合的轻链和重链的构建体的说明。
图75A至图75D展示了gp220-粉纹夜蛾铁蛋白的离子交换(Q柱)色谱纯化和尺寸排阻色谱(SEC)纯化。示出了来自在pH 7下的Q柱(图75A)和SEC6,16/600(图75B)的吸光度迹线;来自pH 7下的Q柱的级分的考马斯染色(图75C)(从左边开始的泳道是输入(“In”)、流通液(“FT”)、分子量梯状标志(大小以kD标记在左侧)和选择的级分);并且来自SEC6,16/600的级分的考马斯染色(图75D)(从左边开始的泳道是分子量梯状标志(大小以kD标记在左侧)和选择的级分)。图75E示出了构建体的说明。
图76A至图76D展示了gL/gH(轻)/gp220(重)-粉纹夜蛾铁蛋白的离子交换(Q柱)色谱纯化和尺寸排阻色谱(SEC)纯化。示出了来自在pH 7下的Q柱(图76A)和SEC6,16/600(图76B)的吸光度迹线;来自pH 7下的Q柱的级分的考马斯染色(图76C)(从左边开始的泳道是输入(“In”)、流通液(“FT”)、分子量梯状标志(大小以kD标记在左侧)和选择的级分);并且来自SEC6,16/600的级分的考马斯染色(图76D)(从左边开始的泳道是分子量梯状标志(大小以kD标记在左侧)和选择的级分)。图76E示出了构建体的说明。
图77A至图77H示出了通过考马斯染色考马斯可视化的(图77A和图77E)、示意性地说明的(图77B和图77F)、通过动态光散射(DLS)表征的(图77D和图77H)和在电子显微照片中可视化的(图77C和图77G)gp220-粉纹夜蛾铁蛋白或gL/gH(轻链)/gp220(重链)-粉纹夜蛾铁蛋白构建体。图77A至图77D呈现出在与轻链和重链融合的gp220(图77B中的图)的情况下的数据。图77E至图77H呈现出在与重链融合的gp220和与轻链融合的gL/gH(图77F中的图)的情况下的数据。
图78A至图78C示出了通过考马斯染色可视化的(图78A)、在电子显微照片中可视化的(图78B)和通过DLS表征的(图78C)裸粉纹夜蛾铁蛋白颗粒(即,未与非铁蛋白多肽融合)。
图79A示出了在纯化的gH/gL/gp42 NP构建体(SEQ ID NO:227)(其在293expi细胞中表达)的情况下的SDS变性考马斯染色凝胶(在左侧),和(在右侧)gH/gL/gp42 NP的尺寸排阻色谱(SEC)峰。SEC色谱图的水平轴线的单位是mL。图79B示出了从CHO池中纯化的gH/gL/gp42 NP,其具有约26.2nm的动态光散射半径。
图80A-B示出了由单价gH/gL/gp42纳米颗粒组合物与裸铁蛋白纳米颗粒的组合或二价组合物(gH/gL/gp42纳米颗粒与gp220的组合)引发的免疫应答的评估。图80A示出了B细胞中和。图80B示出了上皮细胞中和。
图81A-E示出了针对所指示抗原的终点结合效价。
图81F-G示出了来自如所指示那样进行疫苗接种的雪貂的血清的(分别在B细胞和上皮细胞中)EBV病毒中和测定。初免=Inj.1并且加强免疫=Inj.2。
图82A-B:图82A示出了使用Superose 6尺寸排阻色谱对gH/gL/gp42_NP_C12(SEQID NO:228)的纯化。箭头描绘了通过变性考马斯凝胶分析和使用抗铁蛋白抗体的蛋白质印迹分析从峰中收集的级分。图82B是图31A中样品的动态光散射分析,其显示出20.6nm的颗粒大小半径。
图83A-B:图83A示出了使用Superose 6尺寸排阻色谱对gH/gL/gp42_NP_C13(SEQID NO:229)的纯化。箭头描绘了通过变性考马斯凝胶分析和使用抗铁蛋白抗体的蛋白质印迹分析从峰中收集的级分。图83B是图32A中样品的动态光散射分析,其显示出17.1nm的颗粒大小半径。
图84A-B:图84A示出了使用Superose 6尺寸排阻色谱对gH/gL/gp42_NP_C14(SEQID NO:230)的纯化。箭头描绘了通过变性考马斯凝胶分析和使用抗铁蛋白抗体的蛋白质印迹分析从峰中收集的级分。图84B是图84A中样品的动态光散射分析,其显示出16.9nm的颗粒大小半径。
图85:左侧的SDS还原考马斯凝胶示出了纯化的单链gH/gL/gp42-His产物(SEQ IDNO:226)。使用镍亲和色谱纯化蛋白质。右侧是单链gH/gL/gp42-His产物(SEQ ID NO:226)的2.9埃晶体结构。Gp42(为深灰色并用箭头指示)与gH/gL异二聚体相互作用。
图86A-E:在图86A中示出了与铁蛋白融合的gH/gL/gp42的单链构建体(如在SEQID NO:227-231中的每一种中)的图片。每种蛋白质之间的融合是经由上文指定的柔性氨基酸接头或刚性氨基酸接头进行的。单链gH/gL/gp42分子将确保纳米颗粒上1:1:1比率的异三聚体形成。已解析出此异三聚体的晶体结构显示单链gH/gL/gp42可采用类似于自然界中发现的野生型gH、gL和gp42蛋白的异三聚体形态(图86B;也参见图85)。图86C是此单链gH/gL/gp42异三聚体如何通过与铁蛋白融合而在纳米颗粒上展示的模型。在单一纳米颗粒上展示二十四个拷贝的单链gH/gL/gp42。图86D示出了在293Expi细胞中表达SEQ ID NO:227后的纯化。变性SDS考马斯凝胶显示,与铁蛋白融合的gH/gL/gp42在糖基化的情况下高于150kD。图35E示出了纯化产物的负染色电子显微镜分析,其表明与铁蛋白融合的单链gH/gL/gp42可以成功地形成在表面上展示gH/gL/gp42抗原的纳米颗粒。
图87A至图87D示出了示例性RSV Pre-F-NP多肽结构。(图87A)列出了对应于每个区段的N末端的残基数的线性图。编号是根据SEQ ID NO:526的。结构域1-3分别用DI、DII和DIII指示,并且还标记了七肽重复区A(HRA)和七肽重复区B(HRB)。C末端铁蛋白被标记(铁蛋白纳米颗粒)。RSV F部分的F1和F2片段标记在图片下方。F1与F2片段之间的区域被描绘为一条线并在图片上方标记,在所述区域中,肽27片段(p27)融合肽(FP)和弗林蛋白酶切割位点(弗林蛋白酶位点)缺失并被柔性接头置换以形成单链F构建体。图上方的星号指示工程化糖基化位点E328N、S348N和R507N的大致位置。(图87B)融合前RSV F部分的结构模型,其指示出D25、AM14、101F和帕利珠单抗抗体的关键中和(Nab)表位。共享的融合前和融合后结构表位的大致区域用白色三角形指示。示例性的工程化糖基化位点E328N、S348N和R507N的位置被标记。将工程化糖基化位点映射到融合前构象与融合后构象之间结构上共享的区域,并且远离被抗体(如D25、AM14、101F和帕利珠单抗)识别的关键中和表位。这样,含有这些工程化聚糖位点的构建体仍然结合以上的中和抗体(数据未显示)。(图87C)RSV融合前F蛋白纳米颗粒(Pre-F-NP)的结构模型,其中HRA和HRB区域阴影更深。所得的折叠的Pre-F-NP构建体可以形成24聚体,其展示了图87B中列出的关键表位。(图87D)RSV Pre-F-NP构建体RF8085(SEQ ID NO:501)的电子显微照片的2D类别平均值,其显示出RSV F三聚体部分在24聚体铁蛋白纳米颗粒上的对称性。
图88示出了如通过D25抗体蛋白质印迹所测量的,在293细胞条件培养基中表达的若干种Pre-F-NP构建体的小规模表达。RF8090是SEQ ID NO:502,其是在CHO表达中使用的克隆变体,具有与RF8085即SEQ ID NO:501相同的序列。RF8085和RF8090是含有DS-CAV的二硫化物和空腔填充突变的Pre-F-NP构建体,具有图87A中所述的缺失和单链接头,融合至铁蛋白的N末端。RF8100-RF8105和RF8108-RF8112分别具有序列SEQ ID NO:503-508和511-514。scF-pFerr=RSV F多肽和铁蛋白的融合蛋白。将显现相对于RF8090基准改善构建体表达的突变指出在蛋白质印迹下方。值得注意的突变包括经由E328N、S348N和R507N突变添加聚糖位点以及中心螺旋加帽突变I327P,如通过蛋白质印记所测量的,所述突变增加RSV F纳米颗粒在条件培养基中的表达和分泌。
图89示出了如通过293表达的条件培养基的蛋白质印迹分析所测量的,RF8085(SEQ ID NO:501;对照构建体)和RF8106(SEQ ID NO:509;包含如RF8108中的I217P突变并且缺乏DS-CAV1的二硫化物(DS)突变)的表达。用中心螺旋加帽突变I217P置换DS显著增加表达。用中心螺旋加帽突变置换DS不影响构建体与融合前特异性抗体D25和AM14的结合。
图90示出了RF8106构建体(SEQ ID NO:509)的尺寸排阻色谱纯化的结果。在Superose 6制备性SEC柱上RF8106纳米颗粒的大约65ml的保留体积与折叠的24聚体纳米颗粒一致,这表明RF8106中的突变并不妨碍纳米颗粒形成。
图91A至图91B示出了未还原的(79A)和还原的(79B)RF8106的动态光散射(DLS)分析。与SEC分析一样,DLS证明RSV Pre-F-NP形成了预期的折叠纳米颗粒。还原的数据进一步显示,颗粒没有被还原破坏,所述还原是在通过突变将佐剂与铁蛋白上引入的表面暴露的半胱氨酸进行缀合之前进行的(参见图92)。
图92示出了伴有和不伴有与TLR9激动剂CpG的缀合的RF8106的考马斯染色的SDS-PAGE凝胶分析。CpG处理的纳米颗粒的增加的凝胶移位证明CpG佐剂可以添加至RSV F纳米颗粒上至大约40%-50%完成率。CpG或其他免疫刺激部分(如TLR7/8激动剂SM7/8)的缀合不会抑制颗粒结合融合前特异性抗体D25和AM14的能力。
图93示出了包含具有(RF8117,SEQ ID NO:517)和不具有附加聚糖(RF8085,SEQID NO:501;和RF8113,SEQ ID NO:516)的RSV F的纳米颗粒的蛋白质印迹。RF8113与RF8106相似,但是来自RF8106的S111C表面暴露的半胱氨酸(使用铁蛋白残基编号,即对应于SEQID NO:208的铁蛋白序列中的位置)已被K79C表面暴露的半胱氨酸(也使用铁蛋白残基编号)置换以使缀合位点远离Pre-F部分。与RF8106一样,RF8113与基准分子RF8085相比保留了改善的表达。RF8117与RF8113类似,但进一步包含图88中鉴定的三个糖基化突变,即E328N、S348N和R507N,以进一步改善表达并阻断如图87B中所述的融合前F构象与融合后F构象之间共享的非中和表位。
图94示出了在潜在的胰蛋白酶样蛋白酶切割位点具有不同取代的RSV F构建体的表达。在RF8090(与RF8085相同的蛋白质序列,具有适于CHO表达载体的不同DNA序列)的CHO细胞系表达中观察到,在F部分与铁蛋白部分之间的多肽被剪切,导致表达降低。通过F部分的所得质量,估计蛋白水解可能在Pre-F-NP构建体的HRB、牛蛙接头区域附近发生。研究了该区域(残基约450-550)内的赖氨酸和精氨酸残基的突变,以消除构建体的潜在的胰蛋白酶样蛋白水解。相对于RF8117的RF8122(SEQ ID NO:518)中的突变(K498L和K508Q)在293细胞中提供了改善的表达,并可减少或消除在CHO细胞中的蛋白水解。替代性突变限制了表达。
图95A-B.RF8090、RF8117和RF8140在稳定转染的CHO细胞中的表达。观察到RF8090(SEQ ID NO:501)的表达产量在低水平下。如上所述,向克隆到稳定表达的CHO细胞中的构建体RF8117(SEQ ID NO:517)和RF8140(SEQ ID NO:523)中引入置换DS-CAV1的二硫化物的突变以及对F部分与铁蛋白部分之间的接头的突变(以消除潜在胰蛋白酶切割位点)。(图95A)通过D25-蛋白质印迹分析,将分别来自三个和四个CHO细胞池的RF8117和RF8140在CHO条件培养基中的表达与RF8090在CHO条件培养基中的产量进行比较。RF8117的所有三个CHO池和RF8140的所有四个CHO池比RF8090具有更高的产量。(图95B)如通过Octet通过D25融合前F特异性抗体所测量的,RF8117在CHO条件培养基中的表达。左图片示出了相对于与蛋白A尖端上D25的结合的反应绘制的从已知浓度的293培养基中纯化的RF8140反应,从而提供标准曲线。单独的点表示针对来自RF8117 CHO条件培养基的D25结合的反应。右图片示出了基于D25结合反应,CHO池条件培养基中RF8117或RF8140的计算产量。如通过D25和AM14结合所测量的,RF8117和RF8140均在培养基中表达,这证明与293细胞一样,CHO细胞能够以折叠的方式表达Pre-F-NP,其保留融合前F三聚体结构。
图96A-B.对Pre-F-NP RF8117的中和抗体应答。(图96A)如通过VERO细胞测定所测量的由以下项的高剂量(1μg)和低剂量(0.1μg)免疫引发的RSV中和效价的比较:DS-CAV1(Pre-F三聚体,SEQ ID NO:525)、融合后F三聚体(Post-F三聚体;SEQ ID NO:524)或伴有工程化糖基化的Pre-F-NP(Pre-F-NP;RF8117,SEQ ID NO:517)。将所有RSV多肽与如本文所述的佐剂AF03一起给予。自始至终,除非另有说明,否则将AF03与RSV多肽或纳米颗粒一起给予,但不与之缀合。RSV多肽和剂量标记在x轴线下方。指示了相对于Pre-F-NP免疫的高剂量应答的统计分析。(图96B)如通过VERO细胞测定所测量的由用以下项的高剂量(1μg)和低剂量(0.1μg)免疫引发的RSV中和效价的比较:DS-CAV1(Pre-F三聚体)、不伴有工程化糖基化的Pre-F-NP(RF8113,SEQ ID NO:516)或伴有工程化糖基化的Pre-F-NP(RF8117,SEQ IDNO:517)。将所有RSV多肽与如本文所述的佐剂AF03(不与任何多肽或纳米颗粒缀合)一起给予。RSV多肽和剂量标记在x轴线下方。
图97A-D.在小鼠或非人灵长类动物模型中由用融合后F三聚体(SEQ ID NO:524)或Pre-F-NP(RF8140 SEQ ID NO:523)免疫引发的RSV融合前F三聚体(DS-CAV1)结合抗体和RSV中和抗体的比较。(图97A)比较了在小鼠中由融合后F与Pre-F-NP(RF8140,SEQ ID NO:523)之间的免疫引发的融合前F三聚体结合抗体应答。(图97B)示出了在小鼠中由用融合后F和Pre-F-NP(RF8140,SEQ ID NO:523)免疫引发的中和抗体应答。(图97C)比较了在伴有或不伴有佐剂(AF03,在下面的括号中指示)的情况下由Pre-F-NP在非人灵长类动物中引发的融合前F三聚体结合抗体应答。(图97D)比较了在伴有和不伴有AF03佐剂的情况下,由用Pre-F-NP(RF8140,SEQ ID NO:523)免疫引发的RSV中和效价。在小鼠中,与融合后三聚体相比,Pre-F-NP引发更高的融合前F结合应答和RSV中和应答。在非人灵长类动物中,Pre-F-NP引发强效的中和应答。
图98A至图98B显示工程化糖基化位点阻断融合后表位。(图98A)示出了如通过Octet所测量的,由用高(1μg)和低(0.1μg)剂量下的不伴有工程化糖基化的Pre-F-NP(RF8113)或伴有工程化糖基化的Pre-F-NP(工程化Gly颗粒)免疫引发的对融合前F(DS-CAV1)的抗体应答。(图98B)示出了如通过Octet所测量的,由用高(1μg)和低(0.1μg)剂量下的不伴有工程化糖基化的Pre-F-NP(RF8113)或伴有工程化糖基化的Pre-F-NP(RF8117)免疫引发的对融合后三聚体的抗体应答。如上,在免疫期间将所有RSV多肽与AF03混合。虽然RF8113和RF8117均引发对融合前F的稳健抗体应答,但由RF8117引发的融合后F抗体应答大大降低。这是由于映射到共享的融合前和融合后表位的工程化聚糖(图88B)。
图99A-C示出了工程化糖基化位点对非中和性表位的阻断。(图99A)如通过VERO细胞测定所测量的,在小鼠研究中,由用0.1μg剂量下的具有野生型糖基化位点的Pre-F NP(“Wt聚糖颗粒”;RF8113,SEQ ID NO:516)与具有另外的工程化糖基化位点的Pre-F NP(“+聚糖颗粒”;RF8117,SEQ ID NO:517)免疫引发的RSV中和效价的比较。(图99B)在小鼠研究中由用0.1μg剂量下的Wt聚糖颗粒(RF8113,SEQ ID NO:516)与+聚糖颗粒(RF8117,SEQ IDNO:517)免疫引发的RSV融合后F三聚体结合抗体应答的比较。(图99C)所测量的中和效价与图片A和B中的结合效价的比率,其证明工程化聚糖没有降低功能性中和抗体应答,但确实降低了针对共享的融合前/融合后表位(图87B)引发的非中和抗体,由此提高了中和/结合抗体比率。
图100A-D.对与铁蛋白纳米颗粒缀合的RSV G中心结构域肽(Gcc)的表征。(图100A)考马斯染色的SDS-PAGE凝胶,其显示出RSV G中心结构域(SEQ ID NO.529)与铁蛋白纳米颗粒的点击缀合,从而形成Gcc-NP抗原。(图100B)Gcc-NP的结构模型。(图100C)在小鼠研究中由用单独的Gcc肽(Gcc肽,SEQ ID NO.529)与缀合至纳米颗粒的Gcc肽(Gcc-NP)进行免疫引发的Gcc结合抗体的对比。将来自幼稚态血清( serum)的代表性应答示出在白色框中,而将来自第二次免疫后的应答示出在浅灰色框中,并且将来自第三次免疫后的应答示出在深灰色框中。(图100D)如通过HAE细胞测定所测量的,在第三次注射后的小鼠研究中,由用Gcc肽(SEQ ID NO.529)与Gcc-NP进行免疫引发的RSV中和效价的比较。合并来自幼稚态动物的血清和来自用Gcc肽免疫的动物的血清,并且将效价示出为条。
图101A-C.RSV Pre-F-NP(RF8140)和Gcc-NP的共同给予引发中和应答。用单独的Pre-F-NP(RF8140)、单独的Gcc-NP或组合的Pre-F-NP和Gcc-NP以1μg剂量/抗原对小鼠进行免疫。如上将所有免疫用AF03佐剂化。(图101A)用单独的RF8140(Pre-F-NP)或RF8140和Gcc-NP(Pre-F-NP+Gcc-NP)对小鼠进行免疫引发结合融合前F三聚体的抗体。(图101B)用单独的Gcc-NP(Gcc-NP)或RF8140和Gcc-NP(Pre-F-NO+Gcc-NP)对小鼠进行免疫引发结合Gcc肽的抗体。(图101C)用单独的Pre-F-NP、单独的Gcc-NP或Pre-F-NP和Gcc-NP的共同给予免疫的动物在第二次免疫后和第三次免疫后引发中和应答,如通过HAE中和测定所测量的。Pre-F-NP+Gcc-NP的共同给予引发的中和应答优于由仅用Pre-F-NP免疫引发的中和应答。
图102A-B.Pre-F-NP和Gcc-NP的共同给予不干扰结合融合前F三聚体或Gcc-纳米颗粒的抗体的引发。通过F-敏感性VERO细胞测定所测量的中和效价在图102A的左侧,而通过F-和G-敏感性HAE测定所测量的中和效价示于图102B的右侧。动物免疫如图101中。免疫中使用的RSV多肽在水平轴线下方。黑条表示从图101中所述的免疫组合并的血清,并且被类似地标记。幼稚态动物的血清也示出为黑色条并进行标记以便比较。用融合前F三聚体耗尽的血清为白色,正好位于相应黑色条的右侧。用G胞外结构域耗尽的血清呈对角条纹条,正好位于相应黑条的右侧。用融合前F三聚体耗尽之后用G胞外结构域耗尽的血清呈竖直条纹条。(图102A)在VERO细胞测定中对于来自RF8140免疫和RF8140+Gcc-NP共同给予的血清观察到中和效价,但对于幼稚态血清或来自单独的Gcc-NP免疫的血清没有观察到。用融合前F三聚体耗尽来自RF8140或RF8140+Gcc-NP组的血清降低了可测量中和效价。(图102B)在HAE细胞测定中对于来自用RF8140、Gcc-NP或与Gcc-NP共同给予的RF8140免疫的动物的血清观察到中和效价。来自幼稚态动物的血清没有中和应答。来自用RF8140免疫的动物的、用融合前F三聚体耗尽的血清具有可测量中和效价的降低。来自用Gcc-NP免疫的动物的、用G胞外结构域耗尽的血清具有可测量中和效价的降低。来自用RF8140和Gcc-NP的共同给予免疫的动物的血清在用单独的融合前F三聚体耗尽时没有降低的可测量中和效价,但是在用融合前F三聚体和G胞外结构域两者耗尽时具有降低的可测量中和效价。总之,这些数据表明用Pre-F-NP和Gcc-NP的共同给予不会干扰抗原各自引发对融合前F或G的中和抗体的能力。
图103A-B.相对于未佐剂化RF8117,用AF03、SPA09或明矾佐剂化RF8117或RF8140在小鼠中引发优越的中和应答。(图103A)示出了如通过VERO细胞测定所测量的,来自用以下情况下的RF8117免疫的小鼠的血清的中和效价:未佐剂化(无佐剂)、用明矾佐剂化、或用AF03佐剂化。(图103B)示出了如通过VERO细胞测定所测量的,来自用以下项免疫的小鼠的血清的中和效价:未佐剂化(无佐剂)的RF8117、用SPA09佐剂化的RF8117、或用AF03佐剂化的RF8140。在RF8117或RF8140的所有情况下,在幼稚态小鼠中,佐剂化组比未佐剂化组引发更高的中和效价。
图104A-B.相对于未佐剂化RF8140免疫,用AF03或SPA09佐剂化RF8140在非人灵长类动物(NHP)中引发优越的中和应答。(图104A)如通过ELISA所测量的,在用以下情况下的RF8140免疫之后,在NHP血清中测量的融合前F三聚体结合应答:未佐剂化(无佐剂)、用AF03佐剂化、或用SPA09(使用两种剂量的SPA09,如在下方所指示的)佐剂化。在所有时间点,用AF03或SPA09佐剂化引发优越的中和应答。(图104B)如通过VERO细胞测定所测量的,来自用以下情况下的RF8140免疫的NHP的血清的中和效价:未佐剂化(无佐剂)、用AF03佐剂化或用SPA09(使用两种剂量的SPA09,如在下方所指示的)佐剂化。在所有情况下,用伴有佐剂的RF8140进行的免疫在所有时间点均比未佐剂化组引发更高的中和效价。
图105A-B.相比于单独的未佐剂化RF8140,RF8140与TLR7/8激动剂SM7/8或TLR9激动剂CpG的缀合引发优越的融合前F结合效价。(图105A)示出了在来自以下项的血清中测量的融合前F三聚体结合应答:幼稚态小鼠,用未佐剂化RF8140免疫的小鼠,用与SM7/8佐剂缀合的RF8140、用130ng SM7/8佐剂化的RF8140或用20μg SM7/8佐剂化的RF8140免疫的小鼠。与未佐剂化或SM7/8佐剂化组相比,与SM7/8缀合的RF8140引发更高的融合前F三聚体结合效价。(图105B)示出了在来自以下项的血清中测量的融合前F三聚体结合应答:幼稚态小鼠,用未佐剂化RF8140免疫的小鼠,用与CpG佐剂缀合的RF8140、用680ng CpG佐剂化的RF8140或用20μg SM7/8佐剂化的RF8140免疫的小鼠。与未佐剂化或SM7/8佐剂化组相比,与SM7/8缀合的RF8140引发更高的融合前F三聚体结合效价。
图106A-G.在MIMIC系统中F亚单位疫苗候选物引发pre-F定向的中和抗体和Th1CD4+T细胞应答。(图106A)在以关于10ng/ml pre-F NP的F的摩尔当量浓度用每种Ag初免之后,通过AF测量MIMIC系统中的抗pre-F效价(n=48-49个供体/组)。(图106B)测量微中和效价,并以国际单位/ml(IU/ml)表示。(图106C)抗pre-F与post-F之间的比率>1表示pre-F结合抗体相对于post-F结合抗体的水平更高,而比率值<1表示对post-F的Ab应答更大。(图106D)使用流式细胞术测量用载有F蛋白的靶细胞再刺激的激活CD154+/CD4+T细胞中TNFα的产生(n=48)。经由Tukey-Kramer-HSD多重比较确定统计显著性(图106E)人受试者中先前存在的抗体效价(血清状态)与MIMIC系统中RSV免疫应答的强度高度相关。通过软件或算法生成显示来自每个供体的血清中的抗pre-F IgG与总抗pre-F IgG应答的关系的线性回归图,并且通过统计方法分析了共同斜率的p值(n=50)。Y轴线表示在用RSV初免后获得的抗pre-F IgG水平。(图106F)如在图106E中,显示在用F亚单位疫苗候选物(post-F呈正方形,pre-F-NP呈圆圈并且DC-Cav1呈菱形)初免后来自每个供体的血清中的抗-pre-F IgG与总抗-pre-F IgG的关系的线性回归图。抗pre-F IgG的先前存在的循环效价的范围为199,800至3,037,600,000。每个点代表每个单独供体的IgG值。(图106G)在人B细胞中由用单独的Gcc肽(Gcc肽)与缀合至纳米颗粒的Gcc肽(Gcc-NP)处理引发的Gcc结合抗体应答的比较。对于如上的比较,示出了未处理组。
图107A-C.由低剂量(0.5μg)的RSV Gcc-铁蛋白纳米颗粒(“Gcc-NP”)引发的中和抗体效价。示出了在第二次免疫后两周(2wp2)(图107A)或第三次免疫后两周(2wp3)(图107B)获取的血清中,由用含RSV A2 Gcc序列的RSV Gcc-NP(与AF03一起配制)免疫引发的RSV A株系HAE中和效价,其中幼稚态血清和超免疫血清作为阴性对照和阳性对照。还示出了在第三次免疫后两周(2wp3)获取的血清中,由用含RSV A2 Gcc序列的RSV Gcc-NP(与AF03一起配制)免疫引发的RSV B株系HAE中和效价(图107C)。
图108A-B.由RSV Gcc-NP引发的RSV A2株系抗原结合抗体应答。(图108A)由高剂量(5μg)的RSV Gcc-NP引发,在第二次注射后两周(浅灰色框)和第三次注射后两周(深灰色框)测量的针对Gcc A2株系引发的Gcc结合抗体应答。幼稚态小鼠血清应答作为阴性对照示出。(图108B)由低剂量(0.5μg)的RSV Gcc-NP引发,在第二次注射后两周(浅灰色框)和第三次注射后两周(深灰色框)测量的针对Gcc A2株系引发的Gcc结合抗体应答。
图109A-B.由RSV Gcc-NP引发的RSV B1株系抗原结合抗体应答。(图109A)由高剂量(5μg)的RSV Gcc-NP引发,在第二次注射后两周(浅灰色框)和第三次注射后两周(深灰色框)测量的针对Gcc B1株系引发的Gcc结合抗体应答。幼稚态小鼠血清应答作为阴性对照示出。(图109B)由低剂量(0.5μg)的RSV Gcc-NP引发,在第二次注射后两周(浅灰色框)和第三次注射后两周(深灰色框)测量的针对Gcc B1株系引发的Gcc结合抗体应答。
具体实施方式
本文提供了用于免疫的新型铁蛋白平台多肽和纳米颗粒。铁蛋白可以包含在表面暴露的氨基酸处的突变,以将非半胱氨酸氨基酸改变为半胱氨酸,由此使得免疫刺激部分可以直接缀合至工程化的表面暴露的半胱氨酸。本文提供的铁蛋白多肽可以进一步包含非铁蛋白多肽组分,并且在单独给予时可以是抗原性的,其中佐剂作为单独分子,和/或作为可以自佐剂化的纳米颗粒的一部分。铁蛋白平台蛋白和纳米颗粒的设计可以增加免疫原性和/或消除或减少对单独给予的佐剂的需要,并且还可能减少引发对与铁蛋白缔合(例如融合)的非铁蛋白多肽的免疫应答所需的佐剂/免疫刺激部分的量。还提供了编码本文所述多肽的核酸。
I.定义
如本文所用,“铁蛋白”或“铁蛋白蛋白”是指与幽门螺杆菌铁蛋白(SEQ ID NO:208或209)或本文所讨论的另一种铁蛋白(如激烈火球菌(P.furiosus)铁蛋白、粉纹夜蛾(Trichoplusia ni)铁蛋白或人铁蛋白)具有可检测的序列同一性的蛋白质,其用于例如在细胞内或组织中存储铁或在血流中携带铁。在下文详细讨论了此类示例性铁蛋白,包括以两条多肽链(称为重链和轻链)出现的那些(例如,粉纹夜蛾和人铁蛋白)。在一些实施方案中,铁蛋白包含与本文例如在表1(序列表)中公开的铁蛋白序列具有至少15%、20%、30%、40%、50%、60%、70%、75%、80%、85%、90%、95%、97%、98%、99%或99.5%同一性的序列。铁蛋白可以是全长天然存在的序列的片段。如本文所用,“野生型铁蛋白”是指其序列由天然存在的序列组成的铁蛋白。铁蛋白还包括其氨基酸序列与野生型铁蛋白有一个或多个差异的全长铁蛋白或铁蛋白片段。
如本文所用,“铁蛋白单体”是指未与其他铁蛋白分子组装的单一铁蛋白分子(或,在适用时,单一铁蛋白重链或轻链)。“铁蛋白多聚体”包含多个缔合的铁蛋白单体。“铁蛋白蛋白”包括单体铁蛋白和多聚体铁蛋白。
如本文所用,“铁蛋白颗粒”是指已经自组装成球状形式的铁蛋白。铁蛋白颗粒有时被称为“铁蛋白纳米颗粒”或简称为“纳米颗粒”。在一些实施方案中,铁蛋白颗粒包含24个铁蛋白单体(或,在适用时,总共24个重链和轻链)。
如本文所用,“杂合铁蛋白”是指包含幽门螺杆菌铁蛋白与牛蛙铁蛋白的氨基末端延伸区的铁蛋白。用作牛蛙铁蛋白的氨基末端延伸区的示例性序列呈现为SEQ ID NO:217。在杂合铁蛋白中,可以将牛蛙铁蛋白的氨基末端延伸区与幽门螺杆菌铁蛋白融合,由此使得使免疫刺激部分附接位点均匀分布在铁蛋白颗粒表面。如本文所用,“牛蛙接头”是包含序列SEQ ID NO:217的接头。杂合铁蛋白有时也称为“bfpFerr”或“bfp铁蛋白”。可以在没有牛蛙序列的情况下,例如像在没有接头或在具有替代性接头的情况下提供包含牛蛙序列的任何构建体。示例性牛蛙接头序列提供于表1中。在表1示出牛蛙接头的情况下,可以在没有接头或具有替代性接头的情况下制造相同的构建体。
如本文所用,“N-聚糖”是指在蛋白质的N(天冬酰胺)残基的酰胺氮处附接至蛋白质的糖链。这样,通过N-糖基化过程形成N-聚糖。此聚糖可以是多糖。
如本文所用,“糖基化”是指将糖单元添加至蛋白质。
如本文所用,“免疫应答”是指免疫系统的细胞(如B细胞、T细胞、树突细胞、巨噬细胞或多形核细胞)对刺激物(如抗原或疫苗)的应答。免疫应答可以包括参与宿主防御应答的身体的任何细胞,例如包括分泌干扰素或细胞因子的上皮细胞。免疫应答包括但不限于先天性和/或适应性免疫应答。如本文所用,“保护性免疫应答”是指保护受试者免受感染(例如,预防感染或预防与感染相关的疾病的发生)的免疫应答。测量免疫应答的方法在本领域中是熟知的,并且包括例如通过测量淋巴细胞(如B或T细胞)的增殖和/或活性、细胞因子或趋化因子的分泌、炎症、抗体产生等。“抗体应答”是其中产生抗体的免疫应答。
如本文所用,“抗原”是指引发免疫应答的因子;和/或当暴露或给予至生物体时由T细胞受体结合的因子(例如,当由MHC分子呈递时)或与抗体(例如,由B细胞产生)结合的因子。在一些实施方案中,抗原在生物体中引发体液应答(例如,包括产生抗原特异性抗体)。可替代地或另外,在一些实施方案中,抗原在生物体中引发细胞应答(例如,涉及其受体与抗原特异性相互作用的T细胞)。特定抗原可以在靶标生物体(例如,小鼠、兔、灵长类动物、人)的一个或若干成员中引发免疫应答,但不能在靶标生物体物种的所有成员中引发免疫应答。在一些实施方案中,抗原在靶标生物体物种的至少约25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%的成员中引发免疫应答。在一些实施方案中,抗原结合抗体和/或T细胞受体,并且在生物体中可能诱导或可能不诱导特定生理应答。在一些实施方案中,例如,抗原可以在体外结合抗体和/或T细胞受体,无论在体内是否发生这种相互作用。在一些实施方案中,抗原与特定体液或细胞免疫的产物(包括由异源免疫原诱导的那些)反应。抗原包括如本文所述的抗原性铁蛋白蛋白,其包含铁蛋白(例如,包含一个或多个突变)和非铁蛋白多肽。
如本文所用,“免疫刺激部分”是指共价附接至铁蛋白或抗原性铁蛋白多肽并可以激活免疫系统的组分(单独或当附接至铁蛋白或抗原性铁蛋白多肽时)的部分。示例性免疫刺激部分包括toll样受体(TLR)例如TLR4、7、8或9的激动剂。在一些实施方案中,免疫刺激部分是佐剂。
如本文所用,“佐剂”是指非特异性增强对抗原的免疫应答的物质或媒介物。佐剂可以包括而不限于其上吸附有抗原的矿物质(明矾、氢氧化铝或磷酸盐)的悬浮液;其中抗原溶液乳化在矿物油中或水中的油包水或水包油乳剂(例如,弗氏不完全佐剂)。有时包括杀死的分枝杆菌(例如,弗氏完全佐剂)以进一步增强抗原性。免疫刺激寡核苷酸(例如,CpG基序)也可用作佐剂(例如,参见美国专利号6,194,388;6,207,646;6,214,806;6,218,371;6,239,116;6,339,068;6,406,705;和6,429,199)。佐剂还可以包括生物分子,如Toll样受体(TLR)激动剂和共刺激分子。佐剂可以作为单独分子在组合物中给予或与铁蛋白或抗原性铁蛋白多肽共价结合(缀合)。
“抗原性铁蛋白多肽”和“抗原性铁蛋白蛋白”在本文中可互换用于指包含铁蛋白和非铁蛋白多肽的多肽,所述非铁蛋白多肽的长度足以使所述分子具有关于非铁蛋白多肽的抗原性。抗原性铁蛋白多肽可以进一步包含免疫刺激部分。抗原性可以是作为较大构建体的一部分的非铁蛋白序列的特征。即,所述构建体可以充当针对非铁蛋白多肽的抗原就足够了,而不管不伴有铁蛋白(如果适用,和免疫刺激部分)的非铁蛋白多肽是否可以如此。非铁蛋白多肽可以是从病原体的多肽获得、由病原体的多肽衍生或与病原体的多肽相似的分子(例如来自病原体的完整分子或分子片段),所述分子可以在抗原性铁蛋白多肽的情境下在其宿主中产生针对病原体的保护性免疫应答。非铁蛋白多肽可以包含天然存在的序列,或者可以经人工设计或修饰,由此使得其结构与天然存在的分子不同。例如,多肽可以不同于其天然存在的形式,由此使得其具有更大的免疫原性或降低的在受试者中介导不适当应答(例如自身免疫应答)的风险。在一些实施方案中,非铁蛋白多肽是RSV、流感、EBV或OspA多肽,在这种情况下,抗原性铁蛋白多肽也是“抗原性X多肽”,其中X是RSV、流感、EBV或OspA。然而,要清楚的是,抗原性RSV、流感、EBV或OspA多肽不需要包含铁蛋白。“抗原性多肽”在本文中用于指为抗原性铁蛋白多肽和抗原性RSV、EBV或OspA多肽中的任一者或两者的多肽。
“抗原性EBV多肽”在本文中用于指包含全部或部分EBV氨基酸序列的多肽,所述EBV氨基酸序列的长度足以使所述分子具有关于EBV的抗原性。抗原性可以是作为进一步包含异源序列(如铁蛋白或2,4-二氧四氢喋啶合酶蛋白和/或免疫刺激部分)的构建体的一部分的EBV序列的特征。即,如果EBV序列是进一步包含异源序列的构建体的一部分,则所述构建体可以充当产生抗EBV抗体的抗原就足够了,而不管不伴有异源序列的EBV序列是否可以如此。
“抗原性RSV多肽”在本文中用于指包含全部或部分RSV氨基酸序列的多肽,所述RSV氨基酸序列的长度足以使所述分子具有关于RSV的抗原性。抗原性可以是作为进一步包含异源序列(如铁蛋白和/或免疫刺激部分)的构建体的一部分的RSV序列的特征。即,如果RSV序列是进一步包含异源序列的构建体的一部分,则所述构建体可以充当产生抗RSV抗体的抗原就足够了,而不管不伴有异源序列的RSV序列是否可以如此。
“抗原性流感-铁蛋白多肽”在本文中用于指包含铁蛋白和流感多肽的分子,其中所述分子具有关于流感多肽的抗原性。抗原性可以是作为较大构建体的一部分的流感多肽的特征。即,所述构建体可以充当产生针对流感多肽的抗体的抗原就足够了,而不管不伴有铁蛋白的流感多肽是否可以如此。在一些实施方案中,将流感多肽和铁蛋白在基因上融合为融合蛋白。在一些实施方案中,流感多肽和铁蛋白是非基因连接的,例如通过化学缀合。
“抗原性OspA多肽”在本文中用于指包含全部或部分OspA的多肽,所述OspA的长度足以使所述多肽具有关于OspA的抗原性。全长OspA包含下文定义的跨膜结构域和胞外结构域。抗原性可以是作为进一步包含异源序列(如铁蛋白或2,4-二氧四氢喋啶合酶蛋白)的构建体的一部分的OspA序列的特征。即,如果OspA是进一步包含异源序列的构建体的一部分,则所述构建体可以充当产生抗OspA抗体的抗原就足够了,而不管不伴有异源序列的OspA序列是否可以如此。
如本文所用,“自佐剂化”是指组合物或多肽包含铁蛋白和直接缀合至铁蛋白的免疫刺激部分,使得铁蛋白和免疫刺激部分在同一分子实体中。可以将包含非铁蛋白多肽的抗原性铁蛋白多肽与免疫刺激部分缀合以产生自佐剂化多肽。
如本文所用,“表面暴露的”氨基酸是指蛋白质(例如,铁蛋白)中具有侧链的氨基酸残基,当所述蛋白质在多聚化后(如果适用)处于其天然的三维构象时,所述侧链可以被溶剂分子接触。因此,例如,在形成24聚体的铁蛋白的情况下,当铁蛋白组装为24聚体,例如组装为铁蛋白多聚体或铁蛋白颗粒时,表面暴露的氨基酸残基是其侧链可以被溶剂接触的氨基酸残基。
如本文所用,“受试者”是指动物界的任何成员。在一些实施方案中,“受试者”是指人。在一些实施方案中,“受试者”是指非人动物。在一些实施方案中,受试者包括但不限于哺乳动物、鸟、爬行动物、两栖动物、鱼、昆虫和/或蠕虫。在某些实施方案中,非人受试者是哺乳动物(例如,啮齿动物、小鼠、大鼠、兔、猴、犬、猫、绵羊、牛、灵长类动物和/猪)。在一些实施方案中,受试者可以是转基因动物、基因工程化动物和/或克隆。在本发明的某些实施方案中,受试者是成人、青少年或婴儿。在一些实施方案中,术语“个体”或“患者”被使用并且旨在与“受试者”可互换。
如本文所用,术语“疫苗接种(vaccination或vaccinate)”是指给予旨在例如对致病因子产生免疫应答的组合物。疫苗接种可以在暴露于致病因子和/或发生一种或多种症状之前、期间和/或之后给予,并且在一些实施方案中,在暴露于所述因子之前、期间和/或之后不久给予。在一些实施方案中,疫苗接种包括间隔适当时间的疫苗接种组合物的多次给予。
如本文所用,“EBV多肽”是指包含由EBV编码的全部或部分氨基酸序列的多肽。类似地,gL、gH、gp42和gp220多肽是指分别包含由EBV编码的全部或部分gL、gH、gp42或gp220氨基酸序列的多肽。与EBV编码的多肽具有例如至少80%同一性的多肽将必定包含EBV编码的多肽的一部分。术语“gL多肽”、“gH多肽”、“gp42多肽”和“gp220多肽”可分别与“EBV gL多肽”、“EBV gH多肽”、“EBV gp42多肽”和“EBV gp220多肽”互换使用。用作为抗原性多肽的一部分或全部的EBV多肽进行免疫可以赋予保护以免受EBV感染。除非上下文另有指示,否则本文公开的包含EBV多肽的任何多肽均可以包含由EBV编码的多种序列的全部或一部分(例如,EBV的gL和gH的全部或一部分,或EBV的gL、gH和gp42的全部或一部分)。
如本文所用,在EBV多肽的情境下,“单体”或“单体构建体”是指表达为单链蛋白质的构建体。单体可以包含以单链表达的EBV的gL和gH,或以单链表达的EBV的gL、gH和gp42。
如本文所用,在EBV多肽的情境下,“三聚体”或“三聚体构建体”是指包含EBV的gL和/或gH以及三聚化结构域(如源自T4噬菌体次要纤维蛋白(fibritin)的折叠子三聚化结构域)的构建体。其他三聚化结构域,如人胶原蛋白XVIII三聚化结构域(参见,例如Alvarez-Cienfuegos等人,Scientific Reports 2016;6:28643)和L1ORF1p三聚化结构域(参见,例如Khazina等人,Proc Natl Acad Sci U S A 2009年1月12日;106(3):731-36)也是本领域已知的,并且可以用于三聚体构建体中。
如本文所用,“抗原位点0”或“位点0表位”是指位于融合前RSV F三聚体顶点的位点,其包含野生型RSV F(SEQ ID NO:526)的氨基酸残基62-69和196-209。位点0表位是对融合前RSV F具有特异性的抗体(如D25和AM14)的结合位点,并且抗体与位点0表位的结合阻断了RSV的细胞表面附接(参见McLellan等人,Science 340(6136):1113-1117(2013))。
如本文所用,“抗原稳定性”是指抗原随时间或在溶液中的稳定性。
如本文所用,“空腔填充取代”是指用于填充存在于融合前RSV F三聚体中的空腔的工程化疏水性取代。
“F蛋白”或“RSV F蛋白”是指在病毒进入过程中负责驱动病毒包膜与宿主细胞膜融合的RSV蛋白。
“RSV F多肽”或“F多肽”是指包含F蛋白的至少一个表位的多肽。
如本文所用,“聚糖添加”是指引入野生型序列(例如,野生型RSV F)中不存在的糖基化位点的突变的添加,其可以被工程化以增加构建体表达、增加构建体稳定性或阻断融合前构象与融合后构象之间共享的表位。包含聚糖添加的修饰蛋白质将具有更多的糖基化,因此具有更高的分子量。聚糖添加可以降低RSV F多肽引发针对RSV F的融合后构象的抗体的程度。
如本文所用,“G蛋白”或“RSV G蛋白”是指负责使RSV与人气道上皮细胞缔合的附着蛋白。示例性的野生型RSV G氨基酸序列提供为SEQ ID NO:527。RSV G蛋白包含位于细胞外的胞外结构域(大致为RSV G(SEQ ID NO:527)的氨基酸66-297)。在RSV G的胞外结构域内是中心保守区(Gcc或CCR,大致为SEQ ID NO:527的氨基酸151-193)。RSV G的CCR包含CX3C基序。CX3C基序介导G蛋白与CX3CR1受体的结合。
如本文所用,“螺旋PRO加帽”或“螺旋脯氨酸加帽”是指螺旋帽包含可稳定化螺旋形成的脯氨酸的情况。
如本文所用,“原体内稳定化取代”描述了RSV F中的氨基酸取代,所述氨基酸取代通过稳定化RSV F三聚体的原体内的相互作用来稳定化融合前构象。
如本文所用,“原体间稳定化取代”描述了RSV F中的氨基酸取代,所述氨基酸取代通过稳定化RSV F三聚体的原体彼此的相互作用来稳定化融合前构象。
如本文所用,“蛋白酶切割”是指多肽序列中易感残基(例如,赖氨酸或精氨酸)的蛋白水解(在本领域中有时也称为“剪切”)。
如本文关于RSV F所用的,“融合后”是指RSV F的在病毒和细胞膜融合之后发生的稳定构象。
如本文关于RSV F所用的,“融合前”是指RSV F的在病毒-细胞相互作用之前所采用的构象。
如本文所用,“原体”是指寡聚蛋白质的结构单元。在RSV F的情况下,RSV F三聚体的单独单元是原体。
如本文所用,“血凝素”或“HA”是指任何流感病毒的负责结合宿主细胞膜上的唾液酸的糖蛋白(示例性血凝素是UniProt登录号:P03451)。HA涵盖被抗HA抗体识别或可以引发抗HA抗体的合成多肽,如下文所述的COBRA P1、COBRA X6和COBRA X3。
如本文所用,“HA茎”是指从缺乏完整HA头部的HA胞外结构域内的HA保守区设计的工程化流感多肽。关于保守的,其意指与作为整体的HA的序列同一性相比,所述区域在来自具有不同HA亚型的不同流感株系的HA之间保持显著更高的序列同一性。HA茎抗原例如详细讨论于以下文献中:Impagliazzo等人,Science 2015年9月18日,349(6254):1301-6;Valkenburg等人,Sci Rep.2016年3月7日,6:22666;Mallajosyula等人,FrontImmunol.2015,6:329。
如本文所用,“神经氨酸酶”或“NA”是指任何流感病毒的负责催化从病毒和细胞糖缀合物中去除末端唾液酸残基的糖蛋白(示例性神经氨酸酶为UniProt登录号:P03472)。
如本文在血凝素的情境下所用的,“Y98F突变”是指用苯丙氨酸置换野生型HA序列中的与唾液酸直接接触的酪氨酸。由该突变产生的苯丙氨酸的位置显示在图26A中。尽管在一些HA亚型中确切的位置可能有所不同,但可以通过序列比对或结构分析来鉴定。HA序列中存在Y98F突变意味着相应的野生型HA是包含与唾液酸直接接触的酪氨酸的亚型。
如本文所用,“免疫刺激部分”是指共价附接至铁蛋白或抗原性铁蛋白多肽并可以激活免疫系统的组分(单独或当附接至铁蛋白或抗原性铁蛋白多肽时)的部分。示例性免疫刺激部分包括toll样受体(TLR)例如TLR4、7、8或9的激动剂。在一些实施方案中,免疫刺激部分是佐剂。
如本文所用,术语“试剂盒”是指一组经包装的相关组分,如一种或多种化合物或组合物和一种或多种相关材料,如溶剂、溶液、缓冲液、说明书或干燥剂。
如本文所用,“N-聚糖”是指在蛋白质的N(天冬酰胺)残基的酰胺氮处附接至蛋白质的糖链。这样,通过N-糖基化过程形成N-聚糖。此聚糖可以是多糖。
如本文所用,“OspA胞外结构域”是指博氏疏螺旋体OspA的大约氨基酸残基27-273(UniProt登录号P0CL66)或如通过成对或结构比对鉴定的其同源物的相应位置。OspA胞外结构域的另外例子包括SEQ ID NO:83-89中任一个的位置27-X,其中X是相关序列的C末端位置,任选地其中C末端Lys被省略。在一些实施方案中,胞外结构域在其N-末端进一步包含相应的全长野生型序列的第26残基或第25和第26残基;在SEQ ID NO:83-89中,第25和26残基是Asp和Glu。OspA胞外结构域的再另外的例子包括SEQ ID NO:94-102中的任一个,任选地其中N末端1、2或3个残基(Met-Asp-Glu)被省略,进一步任选地其中C末端Lys被省略。
如本文所用,“OspA跨膜结构域”是指博氏疏螺旋体OspA的大约氨基酸残基2-24(UniProt登录号P0CL66)或如通过成对或结构比对鉴定的其同源物的相应位置。
本公开文本描述了分别与给定核酸序列或氨基酸序列(参考序列)具有一定同一性程度的核酸序列和氨基酸序列。
两个核酸序列之间的“序列同一性”指示序列之间相同的核苷酸的百分比。两个氨基酸序列之间的“序列同一性”指示序列之间相同的氨基酸的百分比。
术语“相同%”、“同一性%”或类似术语旨在具体是指在待比较的序列之间的最佳比对中相同的核苷酸或氨基酸的百分比。所述百分比是纯粹统计学的,并且两个序列之间的差异可以但不一定随机分布在待比较的序列的整个长度上。两个序列的比较通常通过以下方式进行:在最佳比对之后,关于区段或“比较窗口”比较所述序列,以鉴定相应序列的局部区域。用于比较的最佳比对可以手动地进行或借助于Smith和Waterman,1981,AdsApp.Math.2,482的局部同源性算法、借助于Needleman和Wunsch,1970,J.Mol.Biol.48,443的局部同源性算法、借助于Pearson和Lipman,1988,Proc.Natl Acad.Sci.USA 88,2444的相似性搜索算法、或借助于使用所述算法的计算机程序(在Wisconsin序列分析包(Genetics Computer Group,575Science Drive,威斯康星州麦迪逊)中的GAP、BESTFIT、FASTA、BLAST P、BLASTN和TFASTA)进行。
百分比同一性通过以下方式获得:确定待比较的序列对应的相同位置的数目,用此数目除以比较的位置的数目(例如,参考序列中的位置的数目),并且然后将此结果乘以100。
在一些实施方案中,同一性程度是针对区域给出的,所述区域是参考序列的整个长度的至少约50%、至少约60%、至少约70%、至少约80%、至少约90%或约100%。例如,如果参考核酸序列由200个核苷酸组成,则针对至少约100、至少约120、至少约140、至少约160、至少约180或约200个核苷酸(在一些实施方案中为连续核苷酸)给出同一性程度。在一些实施方案中,针对参考序列的整个长度给出同一性程度。
分别与给定核酸序列或氨基酸序列具有特定同一性程度的核酸序列或氨基酸序列可具有所述给定序列的至少一种功能特性,例如并且在一些情况下,在功能上等同于所述给定序列。一个重要的特性包括充当细胞因子的能力,特别是当给予受试者时。在一些实施方案中,与给定核酸序列或氨基酸序列具有一定同一性程度的核酸序列和氨基酸序列在功能上等同于所述给定序列。
如本文所用,术语“试剂盒”是指一组经包装的相关组分,如一种或多种化合物或组合物和一种或多种相关材料,如溶剂、溶液、缓冲液、说明书或干燥剂。
II.示例性铁蛋白、抗原铁蛋白多肽、缀合物、组合物、方法和用途
铁蛋白蛋白自组装成包含多个单独单体的球状蛋白复合物。自组装的铁蛋白复合物可以称为铁蛋白颗粒或纳米颗粒。
铁蛋白基因存在于许多物种中,并且尽管有序列变异,但通常显示出高度保守的α-螺旋结构。这样,任何铁蛋白都可以用于本发明,包括细菌、昆虫和人铁蛋白,但是其与任何特别描述的铁蛋白具有序列同一性。
在一些实施方案中,铁蛋白是细菌、昆虫、真菌、鸟类或哺乳动物的。在一些实施方案中,铁蛋白是人的。在一些实施方案中,铁蛋白是细菌的。在一些实施方案中,铁蛋白是幽门螺杆菌铁蛋白。
在一些实施方案中,铁蛋白是轻链和/或重链铁蛋白。在一些实施方案中,铁蛋白是任选地具有本文所述的一种或多种修饰的人重链铁蛋白(FTH1,GENE ID No:2495)或人轻链铁蛋白(FTL,GENE ID No:2512)。在一些实施方案中,铁蛋白是任选地具有本文所述的一个或多个突变的粉纹夜蛾重链铁蛋白(GenBank:AY970291.1)或粉纹夜蛾轻链铁蛋白(AY970292.1)。在一些实施方案中,铁蛋白纳米颗粒包含重链铁蛋白和轻链铁蛋白的24个总亚基,例如12个重链亚基和12个轻链亚基。在一些实施方案中,铁蛋白包含用半胱氨酸置换表面暴露的氨基酸的突变。
在一些实施方案中,提供了包含铁蛋白和非铁蛋白多肽的抗原性铁蛋白多肽,所述非铁蛋白多肽的长度足以使所述分子具有关于非铁蛋白多肽的抗原性。
在一些实施方案中,抗原性铁蛋白多肽包含重链铁蛋白或非铁蛋白多肽以及轻链铁蛋白和非铁蛋白多肽。可以组合此类多肽以允许在单一铁蛋白多聚体或颗粒上表达两种相同或不同的非铁蛋白多肽。在一些实施方案中,两种不同的非铁蛋白多肽由单一感染原编码。在一些实施方案中,两种不同的非铁蛋白多肽由两种不同的感染原编码。在一些实施方案中,感染原是病毒或细菌。在一些实施方案中,两种不同的非铁蛋白多肽由两种不同的感染原编码,并且附接至用于组装成纳米颗粒的重链和轻链铁蛋白,所述不同的感染原例如不同的病原体(如流感、疏螺旋体属、RSV或EBV),病原体(如流感、疏螺旋体属、RSV或EBV)的不同株系或类型。
在一些实施方案中,抗原性铁蛋白多肽包含与轻链铁蛋白和非铁蛋白多肽一起组装的重链铁蛋白和非铁蛋白多肽以产生二价组合物。在一些实施方案中,铁蛋白是具有本文所述的一个或多个突变的幽门螺杆菌铁蛋白(对于示例性幽门螺杆菌铁蛋白序列参见SEQ ID NO:208或209)。在一些实施方案中,幽门螺杆菌铁蛋白(或其他细菌铁蛋白)与人铁蛋白之间较低的序列同源性在用作疫苗平台时可降低自身免疫的潜力(参见Kanekiyo等人,Cell 162,1090–1100(2015))。
在一些实施方案中,铁蛋白是具有本文所述的一个或多个突变的激烈火球菌铁蛋白(NCBI seq WP_011011871.1)。
在一些实施方案中,铁蛋白包含与野生型铁蛋白具有大于70%、大于75%、大于80%、大于85%、大于90%、大于95%、大于97%、大于98%、或大于99%同一性的序列。
在一些实施方案中,将能够形成纳米颗粒的不同蛋白质取代铁蛋白。在一些实施方案中,此蛋白质是2,4-二氧四氢喋啶合酶(参见Ra等人,Clin Exp Vaccine Res 3:227-234(2014))。在一些实施方案中,此蛋白质是2,4-二氧四氢喋啶合酶血清型1、2、3、4、5、6或7。示例性2,4-二氧四氢喋啶合酶序列提供为SEQ ID NO:216和219。在一些实施方案中,2,4-二氧四氢喋啶合酶包含与SEQ ID NO:216或219具有80%、85%、90%、95%、98%或99%同一性的序列。
A.铁蛋白突变
本文公开了包含一个或多个突变的铁蛋白。在一些实施方案中,一个或多个突变包括野生型铁蛋白的氨基酸序列的改变和/或例如在N或C末端的插入。在一些实施方案中,与野生型铁蛋白相比,(在一些实施方案中,除了任何N末端插入),铁蛋白中的一个、两个、三个、四个、五个或更多个不同的氨基酸被突变。一个或多个突变可以改变铁蛋白的功能特性,例如,如下文详细讨论的。通常,突变简单地是指相对于相应的野生型铁蛋白的序列差异(如取代、添加或缺失的一个或多个氨基酸残基)。
1.用于缀合的半胱氨酸
在一些实施方案中,铁蛋白被突变以提供用于缀合免疫刺激部分和/或非铁蛋白多肽的化学处理。这可以通过用半胱氨酸置换表面暴露的非半胱氨酸氨基酸的突变来实现。为了避免疑问,如“用半胱氨酸置换表面暴露的氨基酸”的语言必定意味着野生型或突变前序列中的表面暴露的氨基酸不是半胱氨酸。提供用于缀合免疫刺激部分或非铁蛋白多肽的化学处理的另一种方法是包括在铁蛋白的N或C末端的氨基酸区段(如接头),其中所述氨基酸区段包含半胱氨酸。在一些实施方案中,此半胱氨酸(无论是置换表面暴露的氨基酸还是在N或C末端接头中)是不成对的,这意指它没有合适的伴侣半胱氨酸来形成二硫键。在一些实施方案中,此半胱氨酸不改变铁蛋白的二级结构。在一些实施方案中,此半胱氨酸不改变铁蛋白的三级结构。
在一些实施方案中,此半胱氨酸可以用于将药剂(如免疫刺激部分)与铁蛋白缀合。在一些实施方案中,此半胱氨酸提供了反应性的游离硫醇基团。在一些实施方案中,与铁蛋白上的此半胱氨酸缀合的药剂暴露在组装的铁蛋白颗粒的表面上。在一些实施方案中,在组装铁蛋白颗粒的同时,此半胱氨酸可以在给予后与受试者的分子和细胞相互作用。
在一些实施方案中,此半胱氨酸的存在允许缀合一个或多个免疫刺激部分,例如佐剂。在一些实施方案中,在不存在此半胱氨酸的情况下不会发生免疫刺激部分的缀合。
在一些实施方案中,被半胱氨酸置换的非半胱氨酸氨基酸选自幽门螺杆菌铁蛋白的E12、S72、A75、K79、S100和S111。因此,在一些实施方案中,被置换为半胱氨酸的表面暴露的氨基酸是对应于幽门螺杆菌铁蛋白的E12、S26、S72、A75、K79、S100或S111的氨基酸残基。通过成对或结构比对可以在非幽门螺杆菌铁蛋白中找到类似的氨基酸。在一些实施方案中,被半胱氨酸置换的非半胱氨酸氨基酸可以选自对应于人轻链铁蛋白的S3、S19、S33、I82、A86、A102和A120的氨基酸。在一些实施方案中,基于以下理解来选择要被半胱氨酸置换的表面暴露的氨基酸:如果天然氨基酸被半胱氨酸置换,它将在组装的铁蛋白多聚体或颗粒中是反应性的和/或此半胱氨酸不会破坏铁蛋白多聚体或颗粒的稳定性和/或此半胱氨酸不会导致铁蛋白表达水平降低。
在一些实施方案中,铁蛋白包含E12C突变。在一些实施方案中,E12C残基可以用于将药剂(例如,免疫刺激部分和/或非铁蛋白多肽)与铁蛋白缀合。在一些实施方案中,E12C残基提供了反应性的游离硫醇基团。在一些实施方案中,与铁蛋白单体上的E12C残基缀合的药剂在组装的铁蛋白多聚体或颗粒的表面上表达。在一些实施方案中,铁蛋白多聚体或颗粒的表面上存在二十四个E12C残基(每个单体中一个)。
在一些实施方案中,铁蛋白包含S26C突变。在一些实施方案中,S26C残基可以用于将药剂(例如,免疫刺激部分和/或非铁蛋白多肽)与铁蛋白缀合。在一些实施方案中,S26C残基提供了反应性的游离硫醇基团。在一些实施方案中,与铁蛋白单体上的S26C残基缀合的药剂在组装的铁蛋白多聚体或颗粒的表面上表达。在一些实施方案中,铁蛋白多聚体或颗粒的表面上存在二十四个S26C残基(每个单体中一个)。
在一些实施方案中,铁蛋白包含S72C突变。在一些实施方案中,S72C残基可以用于将药剂(例如,免疫刺激部分和/或非铁蛋白多肽)与铁蛋白缀合。在一些实施方案中,S72C残基提供了反应性的游离硫醇基团。在一些实施方案中,与铁蛋白单体上的S72C残基缀合的药剂在组装的铁蛋白多聚体或颗粒的表面上表达。在一些实施方案中,铁蛋白多聚体或颗粒的表面上存在二十四个S72C残基(每个单体中一个)。
在一些实施方案中,铁蛋白包含A75C突变。在一些实施方案中,A75C残基可以用于将药剂(例如,免疫刺激部分和/或非铁蛋白多肽)与铁蛋白缀合。在一些实施方案中,A75C残基提供了反应性的游离硫醇基团。在一些实施方案中,与铁蛋白单体上的A75C残基缀合的药剂在组装的铁蛋白多聚体或颗粒的表面上表达。在一些实施方案中,铁蛋白多聚体或颗粒的表面上存在二十四个A75C残基(每个单体中一个)。
在一些实施方案中,铁蛋白包含K79C突变。在一些实施方案中,K79C残基可以用于将药剂(例如,免疫刺激部分和/或非铁蛋白多肽)与铁蛋白缀合。在一些实施方案中,K79C残基提供了反应性的游离硫醇基团。在一些实施方案中,与铁蛋白单体上的K79C残基缀合的药剂在组装的铁蛋白多聚体或颗粒的表面上表达。在一些实施方案中,铁蛋白多聚体或颗粒的表面上存在二十四个K79C残基(每个单体中一个)。
在一些实施方案中,铁蛋白包含S100C突变。在一些实施方案中,S100C残基可以用于将药剂(例如,免疫刺激部分和/或非铁蛋白多肽)与铁蛋白缀合。在一些实施方案中,S100C残基提供了反应性的游离硫醇基团。在一些实施方案中,与铁蛋白单体上的S100C残基缀合的药剂在组装的铁蛋白多聚体或颗粒的表面上表达。在一些实施方案中,铁蛋白多聚体或颗粒的表面上存在二十四个S100C残基(每个单体中一个)。
在一些实施方案中,铁蛋白包含S111C突变。在一些实施方案中,S111C残基可以用于将药剂(例如,免疫刺激部分和/或非铁蛋白多肽)与铁蛋白缀合。在一些实施方案中,S111C残基提供了反应性的游离硫醇基团。在一些实施方案中,与铁蛋白单体上的S111C残基缀合的药剂在组装的铁蛋白多聚体或颗粒的表面上表达。在一些实施方案中,铁蛋白多聚体或颗粒的表面上存在二十四个S111C残基(每个单体中一个)。
2.内部半胱氨酸的去除
在一些实施方案中,铁蛋白包含用非半胱氨酸氨基酸置换内部半胱氨酸的突变。去除天然内部半胱氨酸残基可以确保每个铁蛋白单体只有一个未配对的半胱氨酸,并且避免了不希望的反应(如二硫化物形成),并且可以导致更稳定且高效的结果(例如,佐剂呈递)。在一些实施方案中,幽门螺杆菌铁蛋白的C31被非半胱氨酸氨基酸置换。在一些实施方案中,用丝氨酸(C31S)置换幽门螺杆菌铁蛋白的C31,但是可以使用任何非半胱氨酸残基,例如丙氨酸、甘氨酸、苏氨酸或天冬酰胺。通过成对或结构比对可以在非幽门螺杆菌铁蛋白中找到类似的氨基酸。因此,在一些实施方案中,被置换为非半胱氨酸的内部半胱氨酸是与幽门螺杆菌铁蛋白的C31对齐的氨基酸残基。显示C31S突变的示例性铁蛋白序列在SEQ IDNO:201-207中示出。在一些实施方案中,当铁蛋白中存在多于一个内部半胱氨酸时,两个或更多个(例如,每个)内部半胱氨酸被非半胱氨酸氨基酸置换,所述非半胱氨酸氨基酸如丝氨酸或选自丝氨酸、丙氨酸、甘氨酸、苏氨酸或天冬酰胺的氨基酸。
3.糖基化
人相容性糖基化可有助于重组药物产品的安全性和功效。监管批准可能取决于证明适当的糖基化是关键的质量属性(参见Zhang等人,Drug Discovery Today 21(5):740-765(2016))。N-聚糖可以由天冬酰胺侧链的糖基化产生,并且在人与其他生物体(如细菌和酵母)之间的结构可能不同。因此,可能期望减少或消除根据本公开文本的铁蛋白中的非人糖基化和/或N-聚糖形成。在一些实施方案中,控制铁蛋白的糖基化改善了组合物的功效和/或安全性,尤其是当用于人疫苗接种时。
在一些实施方案中,铁蛋白被突变以抑制N-聚糖的形成。在一些实施方案中,与其相应的野生型铁蛋白相比,突变的铁蛋白具有降低的糖基化。
在一些实施方案中,铁蛋白包含用非天冬酰胺氨基酸置换表面暴露的天冬酰胺的突变。在一些实施方案中,表面暴露的天冬酰胺是幽门螺杆菌铁蛋白的N19或如通过成对或结构比对确定的对应于幽门螺杆菌铁蛋白的位置31的位置。在一些实施方案中,使这种天冬酰胺(例如幽门螺杆菌铁蛋白的N19)突变降低了铁蛋白的糖基化。在一些实施方案中,突变是用谷氨酰胺置换了天冬酰胺。在一些实施方案中,铁蛋白是包含N19Q突变的幽门螺杆菌铁蛋白。SEQ ID NO:201-207是包含N19Q突变的示例性铁蛋白序列。
暴露于细菌或酵母中产生的糖基化蛋白的哺乳动物可能会对糖基化蛋白产生免疫应答,因为细菌或酵母中给定蛋白的糖基化模式可能与哺乳动物中相同蛋白的糖基化模式不同。因此,一些糖基化的治疗性蛋白质可能不适合在细菌或酵母中生产。
在一些实施方案中,通过氨基酸突变进行的铁蛋白糖基化减少有利于蛋白质在细菌或酵母中的产生。在一些实施方案中,减少的铁蛋白糖基化降低了在给予在细菌或酵母中表达的突变铁蛋白后在哺乳动物中产生不利影响的可能性。在一些实施方案中,因为糖基化减少,所以在细菌或酵母中产生的突变铁蛋白在人受试者中的反应原性降低。在一些实施方案中,与野生型铁蛋白相比,用具有减少的糖基化的突变铁蛋白治疗后,人受试者中超敏反应的发生率较低。
在一些实施方案中,与包含野生型铁蛋白的组合物或包含具有野生型糖基化的相应铁蛋白的组合物相比,包含具有减少的糖基化的突变铁蛋白的组合物在受试者中的降解较慢。在一些实施方案中,与包含野生型铁蛋白的组合物或包含具有野生型糖基化的相应铁蛋白的组合物相比,包含具有减少的糖基化的突变铁蛋白的组合物在受试者中具有降低的清除率。在一些实施方案中,与野生型铁蛋白或包含具有野生型糖基化的相应铁蛋白的组合物相比,包含具有减少的糖基化的突变铁蛋白的组合物具有更长的血清半衰期。
4.突变的组合
在一些实施方案中,铁蛋白包含本文所述的多于一种类型的突变。在一些实施方案中,铁蛋白包含一种或多种独立地选自以下项的突变:减少糖基化的突变、去除内部半胱氨酸的突变和产生表面暴露的半胱氨酸的突变。在一些实施方案中,铁蛋白包含减少糖基化的突变、去除内部半胱氨酸的突变和产生表面暴露的半胱氨酸的突变。
在一些实施方案中,铁蛋白包含N19Q突变、C31S突变和产生表面暴露的半胱氨酸的突变。在一些实施方案中,铁蛋白包含N19Q突变、C31S突变和E12C突变。在一些实施方案中,铁蛋白包含N19Q突变、C31S突变和S72C突变。在一些实施方案中,铁蛋白包含N19Q突变、C31S突变和A75C突变。在一些实施方案中,铁蛋白包含N19Q突变、C31S突变和K79C突变。在一些实施方案中,铁蛋白包含N19Q突变、C31S突变和S100C突变。在一些实施方案中,铁蛋白包含N19Q突变、C31S突变和S111C突变。在一些实施方案中,铁蛋白包含对应于前述突变组中的任一种的突变,其中相应的突变在通过铁蛋白氨基酸序列与幽门螺杆菌铁蛋白氨基酸序列(SEQ ID NO:208或209)的成对比对确定的位置处将N改变为Q、将C改变为S,并且将非半胱氨酸表面暴露的氨基酸改变为半胱氨酸。
包含多于一种类型的突变的示例性铁蛋白提供于SEQ ID NO:201-207中。
5.结构比对
如上所讨论,可以通过成对或结构比对来鉴定对应于关于幽门螺杆菌铁蛋白描述的那些的突变位置。结构比对与大型蛋白质家族(如铁蛋白)有关,在大型蛋白质家族中,尽管有相当大的序列变异,但蛋白质共享相似的结构并且家族的许多成员已在结构上进行了表征;并且还可以用于鉴定本文所述的其他多肽(如流感(例如血凝素)、疏螺旋体属(例如OspA)、RSV(例如RSV F或G)和EBV(例如gL、gH、gp220或gp42))的不同形式中的相应位置。蛋白质数据库(PDB)包括许多铁蛋白的3D结构,包括下文用其登录号列出的那些。
2jd6、2jd7–PfFR-激烈火球菌。2jd8–PfFR+Zn。3a68–来自基因SferH4的soFR–大豆。3a9q-来自基因SferH4的soFR(突变体)。3egm、3bvf、3bvi、3bvk、3bvl–HpFR–幽门螺杆菌。5c6f–HpFR(突变体)+Fe。1z4a、1vlg–FR–海栖热袍菌(Thermotoga maritime)。1s3q、1sq3、3kx9–FR–闪烁古生球菌(Archaeoglubus fulgidus)。1krq–FR–空肠弯曲菌(Campylobacter jejuni)。1eum-EcFR–大肠杆菌。4reu–EcFR+Fe。4xgs–EcFR(突变体)+Fe2O2。4ztt–EcFR(突变体)+Fe2O+Fe2+Fe+O2。1qgh–LiFR-英诺克李斯特菌(Listeriainnocua)。3qz3-VcFR–霍乱弧菌(Vibrio cholerae)。3vnx–FR–孔石莼(Ulva pertusa)。4ism、4isp、4itt、4itw、4iwj、4iwk、4ixk、3e6s–PnmFR–多列拟菱形藻(Pseudo-nitschiamultiseries)。4zkh、4zkw、4zkx、4zl5、4zl6、4zlw、4zmc–PnmFR(突变体)+Fe。1z6o–FR–粉纹夜蛾。4cmy–FR+Fe–花柱绿杆菌(Chlorobaculum tepidum)。铁蛋白轻链(FTL)。1lb3、1h96–mFTL–小鼠。1rcc、1rcd、1rci–bFTL+酒石酸盐+Mg。1rce、1rcg-bFTL+酒石酸盐+Mn。3noz、3np0、3np2、3o7r–hoFTL(突变体)-马。3o7s、3u90-hoFTL。4v1w–hoFTL–低温EM。3rav、3rd0–hoFTL+巴比妥酸盐。铁蛋白轻+重链:5gn8–hFTH+Ca。
结构比对涉及通过以下方式来鉴定两个(或更多个)多肽序列中的相应残基:(i)使用第二序列的已知结构对第一序列的结构建模或(ii)比较两者均已知的第一序列和第二序列的结构,并且鉴定第一序列中与第二序列中的目的残基最相似定位的残基。在一些算法中,基于叠加结构中的α-碳距离最小化(例如,哪组成对α碳为比对提供最小的均方根偏差)鉴定出相应的残基。当鉴定非幽门螺杆菌铁蛋白中的对应于关于幽门螺杆菌铁蛋白描述的位置的位置时,幽门螺杆菌铁蛋白可以是“第二”序列。在目的幽门螺杆菌铁蛋白没有已知的可用结构,但相比于幽门螺杆菌铁蛋白与另一种具有已知结构的非幽门螺杆菌铁蛋白紧密相关的情况下,可能最有效的是使用紧密相关的非幽门螺杆菌铁蛋白的已知结构来对目的非幽门螺杆菌铁蛋白建模,然后将该模型与幽门螺杆菌铁蛋白结构进行比较,以鉴定目的铁蛋白中的期望的相应残基。关于结构建模和比对有大量文献,代表性的披露文本包括US 6859736;US 8738343;以及Aslam等人,Electronic Journal of Biotechnology20(2016)9–13中引用的内容。对于基于已知的一种或多种相关结构对结构建模的讨论,参见例如Bordoli等人,Nature Protocols 4(2009)1–13及其中引用的参考文献。
B.免疫刺激部分;佐剂;缀合的非铁蛋白多肽
在一些实施方案中,将非铁蛋白多肽和/或免疫刺激部分(如佐剂)附接至表面暴露的氨基酸。在一些实施方案中,表面暴露的氨基酸是半胱氨酸,例如,由上文讨论的突变产生的半胱氨酸。在一些实施方案中,表面暴露的氨基酸是赖氨酸、天冬氨酸或谷氨酸。使用戊二醛(用于将赖氨酸与带氨基的接头或部分缀合)或碳二亚胺(例如用于将天冬氨酸或谷氨酸与带氨基的接头或部分或将赖氨酸与带羧基的接头或部分缀合的1-环己基-3-(2-吗啉-4-基-乙基)碳二亚胺或1-乙基-3-(3-二甲基-氨基丙基)碳二亚胺(EDC;EDAC))的缀合程序例如描述于可从www.springer.com获得的Holtzhauer,M.,Basic Methods for theBiochemical Lab,Springer 2006,ISBN978-3-540-32785-1的第四章中。
在一些实施方案中,将免疫刺激部分(如佐剂)附接至铁蛋白的表面暴露的氨基酸。在一些实施方案中,将多于一个免疫刺激部分(如佐剂)附接至铁蛋白的表面暴露的氨基酸。在一些实施方案中,将二十四个免疫刺激部分附接至铁蛋白多聚体或颗粒(例如,幽门螺杆菌铁蛋白颗粒中每个单体有一个部分)。在具有多个附接至铁蛋白纳米颗粒的免疫刺激部分的实施方案中,所有的免疫刺激部分是相同的。在具有多个附接至铁蛋白纳米颗粒的免疫刺激部分的实施方案中,所有的免疫刺激部分是不相同的。
1.免疫刺激部分的类型;佐剂
可以附接至表面暴露的氨基酸(例如半胱氨酸)的任何免疫刺激部分都可以用于根据本公开文本的铁蛋白中。在一些实施方案中,免疫刺激部分是B细胞激动剂。
在一些实施方案中,免疫刺激部分不是疏水性的。在一些实施方案中,免疫刺激部分是亲水性的。在一些实施方案中,免疫刺激部分是极性的。在一些实施方案中,免疫刺激部分能够进行氢键结合或离子键结合,例如包含氢键供体、氢键受体、阳离子部分或阴离子部分。如果部分在生理上相关的pH(如pH 6、7、7.4或8)下在水性溶液中将被离子化,则可以认为所述部分是阳离子或阴离子的。
在一些实施方案中,免疫刺激部分是佐剂。在一些实施方案中,佐剂包括病原体相关分子模式(PAMP)。在一些实施方案中,佐剂是Toll样受体(TLR)激动剂,或干扰素基因刺激物(STING)激动剂。在一些实施方案中,佐剂激活B和/或T细胞中的TLR信号传导。在一些实施方案中,佐剂调节适应性免疫应答。
a)TLR2激动剂
在一些实施方案中,免疫刺激部分是TLR2激动剂。在一些实施方案中,免疫刺激部分刺激TLR2信号传导。在一些实施方案中,免疫刺激部分是TLR2的合成小分子配体。在一些实施方案中,免疫刺激部分是TLR2信号传导的合成小分子激动剂。
在一些实施方案中,TLR2激动剂是PAM2CSK4、FSL-1或PAM3CSK4。
b)TLR7/8激动剂
在一些实施方案中,免疫刺激部分是TLR7和/或TLR8激动剂(即,TLR7和TLR8中至少一者的激动剂)。在一些实施方案中,免疫刺激部分刺激TLR7和/或TLR8信号传导。在一些实施方案中,免疫刺激部分是TLR7和/或TLR8的合成小分子配体。在一些实施方案中,免疫刺激部分是TLR7和/或TLR8信号传导的合成小分子激动剂。
在一些实施方案中,TLR7和/或TLR8激动剂是单链的(ssRNA)。在一些实施方案中,TLR7和/或TLR8激动剂是咪唑并喹啉。在一些实施方案中,TLR7和/或TLR8激动剂是核苷类似物。
在一些实施方案中,TLR7和/或TLR8激动剂是咪唑并喹啉胺Toll样受体(TLR)激动剂,如3M-012(3M Pharmaceuticals)。游离3M-012的结构是:
应当理解的是,可以通过以下方式将免疫刺激部分(如3M-012)或本文所讨论的任何部分缀合至铁蛋白:用与本文所述的铁蛋白例如在表面暴露的半胱氨酸的硫处的键或与附接至这个硫的接头的键取代所述部分的适当的外围原子(例如氢)。因此,当缀合至铁蛋白时,免疫刺激部分的结构将与游离分子的结构略有不同。
在一些实施方案中,TLR7和/或TLR8激动剂是SM 7/8a。游离SM 7/8a的结构是:
参见,例如Nat Biotechnol.2015年11月;33(11):1201-10.doi:10.1038/nbt.3371。
c)TLR9激动剂
在一些实施方案中,免疫刺激部分是TLR9激动剂。在一些实施方案中,免疫刺激部分刺激TLR9信号传导。在一些实施方案中,免疫刺激部分是TLR9的合成小分子配体。在一些实施方案中,免疫刺激部分是TLR9信号传导的合成小分子激动剂。
在一些实施方案中,TLR9激动剂是CpG寡脱氧核苷酸(ODN)。在一些实施方案中,TLR9激动剂是未甲基化的CpG ODN。在一些实施方案中,CpG ODN包含部分或完整的硫代磷酸酯(PS)主链,而不是普通DNA中发现的天然磷酸二酯(PO)主链。
在一些实施方案中,CpG ODN是B类ODN,其包含一个或多个含有5'嘌呤(Pu)-嘧啶(Py)-C-G-Py-Pu 3'的6聚体CpG基序;具有完全硫代磷酸化(即PS改性)的主链;并且长度为18-28个核苷酸。在一些实施方案中,CpG ODN包含SEQ ID NO:210的序列,任选地包含在主链中的硫代磷酸酯连接。
在一些实施方案中,TLR9激动剂包含免疫刺激序列(ISS)。在一些实施方案中,TLR9激动剂是ISS-1018(Dynavax)(SEQ ID NO:210)。
d)STING激动剂
在一些实施方案中,免疫刺激部分是STING(干扰素基因蛋白的刺激物,也称为内质网IFN刺激物)激动剂。在一些实施方案中,免疫刺激部分刺激STING信号传导。在一些实施方案中,免疫刺激部分是STING的合成小分子配体。在一些实施方案中,免疫刺激部分是STING信号传导的合成小分子激动剂。
在一些实施方案中,STING激动剂是环状二核苷酸(CDN)。参见,例如Danilchanka等人,Cell 154:962-970(2013)。示例性CDN包括cdA、cdG、cAMP-cGMP和2'-5',3'-5'cGAMP(对于结构,参见Danilchanka等人)。STING激动剂还包括合成激动剂,如DMXAA
2.缀合的非铁蛋白多肽
在一些实施方案中,非铁蛋白多肽缀合至铁蛋白的表面暴露的氨基酸。在一些实施方案中,非铁蛋白多肽是来自病原体的多肽并使铁蛋白蛋白具有抗原性。在一些实施方案中,非铁蛋白多肽单独地具有抗原性,而在一些实施方案中,非铁蛋白多肽由于其与铁蛋白的缔合而具有抗原性。在一些实施方案中,非铁蛋白多肽是本文所述的任何非铁蛋白多肽。
3.缀合
在一些实施方案中,表面暴露的半胱氨酸(例如,由本文所述的突变产生)或附接至铁蛋白(例如,在铁蛋白的N末端)的肽接头中的半胱氨酸用于将免疫刺激部分(如佐剂)或非铁蛋白多肽缀合至铁蛋白。在一些实施方案中,接头与这种半胱氨酸缀合,可以随后将所述接头缀合至免疫刺激部分(如佐剂)或非铁蛋白多肽。在一些实施方案中,这种半胱氨酸产生用于缀合反应以附接佐剂、接头或非铁蛋白多肽的化学处理。在一些实施方案中,产生了生物缀合物,其中在还原这种半胱氨酸后将免疫刺激部分(如佐剂)或非铁蛋白多肽连接至铁蛋白。在一些实施方案中,半胱氨酸是不成对的表面暴露的半胱氨酸,即所述半胱氨酸缺乏适当位置的伴侣半胱氨酸来形成二硫键。在一些实施方案中,半胱氨酸是包含游离硫醇侧链的不成对半胱氨酸。
a)缀合化学的类型
可以使用任何类型的化学,例如经由表面暴露的氨基酸(如半胱氨酸)或另一种氨基酸(如Lys、Glu或Asp)的反应,来将免疫刺激部分(如佐剂)或非铁蛋白多肽与铁蛋白缀合。
在一些实施方案中,使用点击化学进行缀合。如本文所用,“点击化学”是指彼此快速且选择性地反应(即,“点击”)的一对官能团之间的反应。在一些实施方案中,点击化学可以在温和的水性条件下进行。在一些实施方案中,点击化学反应利用铁蛋白表面上的半胱氨酸(如由表面暴露的氨基酸突变产生的半胱氨酸)来使用可与所述半胱氨酸反应的官能团进行点击化学。
满足点击化学标准的多种反应在本领域中是已知的,并且本领域技术人员可以使用许多公布的方法中的任何一种(参见,例如Hein等人,Pharm Res 25(10):2216-2230(2008))。可以使用众多种可商购的点击化学试剂,如来自Sigma Aldrich、JenaBioscience或Lumiprobe的那些。在一些实施方案中,如以下实施例中所述那样使用点击化学进行缀合。
在一些实施方案中,点击化学反应在铁蛋白还原之后发生。
在一些实施方案中,点击化学可以是1步式点击反应。在一些实施方案中,点击化学可以是2步式点击反应。
在一些实施方案中,一个或多个反应包括无金属点击化学。在一些实施方案中,一个或多个反应包括硫醇-马来酰亚胺和/或二硫化物交换。
无金属点击化学
可以将无金属点击化学用于缀合反应以避免蛋白质的潜在氧化。无金属点击化学已被用于形成抗体缀合物(参见van Geel等人,Bioconjugate Chem.2015,26,2233-2242)。
在一些实施方案中,在反应中使用无金属点击化学以将佐剂附接至铁蛋白。在一些实施方案中,在反应中使用无铜缀合以将佐剂附接至铁蛋白。在一些实施方案中,无金属点击化学使用双环[6.1.0]壬炔(BCN)。在一些实施方案中,无金属点击化学使用二苯并氮杂环辛炔(DBCO)。在一些实施方案中,BCN或DBCO与叠氮化物基团反应。
DBCO在不存在催化剂的情况下经由应变促进的点击反应对叠氮化物基团具有高特异性,从而产生高产率的稳定三唑。在一些实施方案中,DBCO在不存在铜催化剂的情况下与叠氮化物反应。
在一些实施方案中,在1步式点击反应中使用无金属点击化学。在一些实施方案中,在2步式点击反应中使用无金属点击化学。
硫醇-马来酰亚胺和二硫化物交换
本文所述的铁蛋白可以包含含有硫醇(也称为巯基)的半胱氨酸,其可用于与巯基反应性化学基团反应(或其可通过还原而变为可用的)。因此,半胱氨酸允许化学选择性修饰以将免疫刺激部分(如佐剂)添加至铁蛋白。在碱性条件下,半胱氨酸将被去质子化以产生硫醇盐亲核体,所述硫醇盐亲核体可以与软亲电体(如马来酰亚胺和碘乙酰胺)反应。半胱氨酸与马来酰亚胺或碘乙酰胺的反应产生碳-硫键。
在一些实施方案中,巯基反应性化学基团与铁蛋白的表面暴露的半胱氨酸或铁蛋白接头中的半胱氨酸反应。在一些实施方案中,巯基反应性化学基团是卤代乙酰基、马来酰亚胺、氮丙啶、丙烯酰基、芳基化剂、乙烯基砜、吡啶基二硫化物或TNB-硫醇。
在一些实施方案中,巯基反应性化学基团通过烷基化(即形成硫醚键)与半胱氨酸的巯基缀合。在一些实施方案中,巯基反应性化学基团通过二硫化物交换(即形成二硫键)与半胱氨酸的巯基缀合。
在一些实施方案中,将免疫刺激部分(如佐剂)缀合至铁蛋白的反应是硫醇-马来酰亚胺反应。
在一些实施方案中,巯基反应性化学基团是马来酰亚胺。在一些实施方案中,马来酰亚胺与半胱氨酸的反应导致形成稳定的硫酯连接,例如不可逆的硫酯连接。在一些实施方案中,马来酰亚胺不与铁蛋白中的酪氨酸、组氨酸或甲硫氨酸反应。在一些实施方案中,未反应的马来酰亚胺在反应结束时通过添加例如过量的游离硫醇来淬灭。
在一些实施方案中,使免疫刺激部分(如佐剂)与铁蛋白缀合的反应是硫醇-二硫化物交换,也称为二硫化物互换。在一些实施方案中,反应涉及形成包含一部分原始二硫化物的混合二硫化物。在一些实施方案中,原始二硫化物是通过表面暴露的氨基酸的突变或N末端接头的添加而在铁蛋白中引入的半胱氨酸。
在一些实施方案中,巯基反应性化学基团是吡啶基二硫醇。在一些实施方案中,巯基反应性化学基团是TNB-硫醇基团。
b)用于缀合的接头
在一些实施方案中,免疫刺激部分(如佐剂)或非铁蛋白多肽经由与表面暴露的氨基酸(如半胱氨酸)共价结合的接头附接至铁蛋白。在一些实施方案中,接头包含聚乙二醇,例如PEG接头。在一些实施方案中,聚乙二醇(例如PEG)接头增加了与免疫刺激部分(如佐剂)连接的铁蛋白的水溶性和连接效率。PEG接头的长度在2至18个PEG之间,例如PEG4、PEG5、PEG6、PEG7、PEG8、PEG9、PEG10、PEG11、PEG12、PEG13、PEG14、PEG15、PEG16、PEG17和PEG18。
在一些实施方案中,接头包含马来酰亚胺。在一些实施方案中,接头包含免疫刺激部分(ISM)-接头-马来酰亚胺的组分。在一些实施方案中,通过马来酰亚胺与铁蛋白的半胱氨酸的反应,以1步式点击化学反应将ISM-接头-马来酰亚胺缀合至铁蛋白。在一些实施方案中,佐剂-接头-马来酰亚胺的ISM是SM7/8a。在一些实施方案中,ISM-接头-马来酰亚胺的接头是PEG4。在一些实施方案中,ISM-接头-马来酰亚胺是SM7/8a-PEG4-马来酰亚胺。
在一些实施方案中,用下述接头使用2步式点击化学方案,所述接头在一端包含巯基反应性化学基团,并且在另一端包含胺反应性基团。在这种2步式点击化学方案中,巯基反应性化学基团与铁蛋白的半胱氨酸反应,而胺反应性基团与附接至ISM的试剂反应。以这种方式,ISM经由一组2种点击化学试剂缀合至铁蛋白。
在2步式点击化学方案的一些实施方案中,巯基反应性化学基团是马来酰亚胺。在2步式点击化学方案的一些实施方案中,马来酰亚胺与通过表面暴露的氨基酸的突变或N末端接头的添加而引入铁蛋白中的半胱氨酸反应。
在2步式点击化学方案的一些实施方案中,胺反应性基团是DBCO。在2步式点击化学方案的一些实施方案中,DBCO与附接至ISM的叠氮化物基团反应。
在一些实施方案中,使用马来酰亚胺-接头-DBCO。在一些实施方案中,在铁蛋白还原后,将马来酰亚胺-接头-DBCO缀合至铁蛋白。在一些实施方案中,通过在第一步中马来酰亚胺与铁蛋白的半胱氨酸的反应,将马来酰亚胺-接头-试剂缀合至铁蛋白。在一些实施方案中,DBCO用于与附接至叠氮化物的ISM连接。在一些实施方案中,偶联至叠氮化物的ISM是ISS-1018。在一些实施方案中,偶联至叠氮化物的佐剂是3M-012或CpG。
在一些实施方案中,将具有反应性基团的接头添加至ISM。在一些实施方案中,接头是PEG4-叠氮化物接头或PEG4-马来酰亚胺接头。
在一些实施方案中,PEG4-叠氮化物接头缀合至3M-012。缀合至PEG4-叠氮化物接头的3M-012的示例性结构为:
在一些实施方案中,PEG4-叠氮化物接头缀合至SM7/8a。缀合至PEG4-叠氮化物接头的SM7/8a的示例性结构为:
在一些实施方案中,PEG4-马来酰亚胺接头缀合至SM7/8a。缀合至PEG4-马来酰亚胺接头的SM7/8a的示例性结构为:
在一些实施方案中,叠氮化物基团缀合至ISS-1018。缀合至NHS酯-叠氮化物接头的ISS-1018的示例性结构为:
C.抗原性铁蛋白多肽
在一些实施方案中,本文所述的铁蛋白是进一步包含非铁蛋白多肽的抗原性铁蛋白多肽的一部分。在一些实施方案中,抗原性铁蛋白多肽是包含与非铁蛋白多肽偶联的铁蛋白的融合蛋白。在一些实施方案中,非铁蛋白多肽融合至铁蛋白的N末端。在一些实施方案中,非铁蛋白多肽融合至铁蛋白的C末端。非铁蛋白多肽也可以如上所讨论,例如通过由表面暴露的氨基酸突变产生的或在N或C末端接头中引入的半胱氨酸而缀合至铁蛋白。
1.接头
在一些实施方案中,接头将非铁蛋白多肽的氨基酸序列与铁蛋白的氨基酸序列分开。可以使用任何接头。在一些实施方案中,接头是肽接头,其可以有利于抗原性铁蛋白多肽作为融合蛋白的表达(例如,从单一开放阅读框)。在一些实施方案中,接头是甘氨酸-丝氨酸接头。在一些实施方案中,甘氨酸-丝氨酸接头是GS、GGGS(SEQ ID NO:443)、2XGGGS(即,GGGSGGGS)(SEQ ID NO:444)或5XGGGS(SEQ ID NO:445)。接头可以在铁蛋白的N或C末端。
在一些实施方案中,接头的长度为2、3、4、5、6、7、8、9或10个氨基酸。在一些实施方案中,接头的长度为约2-4、2-6、2-8、2-10、2-12或2-14个氨基酸。在一些实施方案中,接头的长度为至少15个氨基酸。在一些实施方案中,接头的长度为至少25个氨基酸。在一些实施方案中,接头的长度为至少30个氨基酸。在一些实施方案中,接头的长度为至少35个氨基酸。在一些实施方案中,接头的长度为至少40个氨基酸。在一些实施方案中,接头的长度小于或等于60个氨基酸。在一些实施方案中,接头的长度小于或等于50个氨基酸。在一些实施方案中,接头的长度为约16、28、40、46或47个氨基酸。在一些实施方案中,接头是柔性的。在一些实施方案中,接头包含半胱氨酸,例如以用作用于缀合免疫刺激部分(例如,佐剂)的位点;包含半胱氨酸的示例性接头提供为SEQ ID NO:225。在一些实施方案中,接头包含与SEQID NO:225具有至少75%、80%、85%、90%或95%同一性的序列,并且进一步包含对应于SEQ ID NO:225中的半胱氨酸的半胱氨酸。在一些实施方案中,接头包含至少25个氨基酸(例如,25至60个氨基酸),其中半胱氨酸位于在自N末端的第8个氨基酸到自C末端的第8个氨基酸范围内的位置处,或位于接头的中心残基或键的10个氨基酸之内。
在一些实施方案中,接头包含甘氨酸(G)和/或丝氨酸(S)氨基酸。在一些实施方案中,接头包含以下项或由以下项组成:甘氨酸(G)、丝氨酸(S)、天冬酰胺(N)和/或丙氨酸(A)氨基酸以及任选的如上所讨论的半胱氨酸。在一些实施方案中,接头包含与SEQ ID NO:222具有至少80%、85%、90%、95%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,接头包含GGGGSGGGGSGGGGSG(SEQ ID NO:220)、GGSGSGSNSSASSGASSGGASGGSGGSG(SEQ ID NO:221)、GGSGSAS SGASASGSSNGSGSGSGSNSSASSGASSGGASGGSGGSG(SEQ ID NO:222)或GS。在一些实施方案中,接头包含FR1(SEQ ID NO:223)或FR2(SEQ ID NO:224)。在一些实施方案中,接头包含SEQ ID NO:233-238。
在一些实施方案中,铁蛋白包括具有牛蛙铁蛋白的氨基末端延伸区的幽门螺杆菌铁蛋白(其将被称为杂合铁蛋白)。在一些实施方案中,此杂合铁蛋白形成具有均匀分布在表面上的非铁蛋白多肽附接位点的多聚体(参见Kanekiyo 2015)。在一些实施方案中,具有杂合铁蛋白的N末端融合蛋白允许非铁蛋白多肽在铁蛋白纳米颗粒表面上的呈递。在一些实施方案中,非铁蛋白多肽是病毒或细菌多肽。在一些实施方案中,铁蛋白在对应于SEQ IDNO:208(杂合铁蛋白,其包含此谷氨酸)的位置13或在SEQ ID NO:209(野生型幽门螺杆菌铁蛋白,其中位置6是异亮氨酸)中的位置6的位置处包含谷氨酸。与牛蛙接头结合时,此谷氨酸被认为可以保留人和牛蛙铁蛋白中发现的保守盐桥(人轻链和牛蛙低级亚基铁蛋白中的6R和14E)。参见Kanekiyo等人,Cell 162,1090–1100(2015))。
在一些实施方案中,非铁蛋白多肽经由半胱氨酸-凝血酶-组氨酸接头连接至铁蛋白。在一些实施方案中,此接头用于经由点击化学将部分(例如,免疫刺激部分或非铁蛋白多肽)直接缀合至铁蛋白。包含半胱氨酸-凝血酶-组氨酸接头的示例性序列是SEQ ID NO:218。上文讨论了适合于涉及半胱氨酸-凝血酶-组氨酸接头的缀合反应的点击化学。
在一些实施方案中,将包含半胱氨酸作为免疫刺激部分(如佐剂)的缀合位点的接头用于包含缺乏不成对的表面暴露的半胱氨酸的铁蛋白分子的构建体中,或用于包含含有不成对的表面暴露的半胱氨酸的铁蛋白分子的构建体中。
在一些实施方案中,构建体不包含接头。在一些实施方案中,构建体包含一个接头。在一些实施方案中,构建体包含两个或多于两个的接头。
可用作掺入抗原性铁蛋白多肽中的非铁蛋白多肽来源的代表性病原体(病毒和细菌)包括爱泼斯坦-巴尔病毒(EBV)、流感、疏螺旋体属(例如,引起莱姆病的疏螺旋体属物种,如博氏疏螺旋体)和呼吸道合胞病毒(RSV)。在一些实施方案中,来自病原体的非铁蛋白多肽包含来自由病原体表达或编码的蛋白质的肽序列。在一些实施方案中,将非铁蛋白多肽的氨基酸连接至杂合铁蛋白的氨基酸序列,其中非铁蛋白多肽序列在牛蛙铁蛋白的N末端延伸区之前。
在一些实施方案中,将非铁蛋白多肽的氨基酸附接至杂合铁蛋白的氨基酸序列产生融合蛋白。在一些实施方案中,此融合蛋白以使得非铁蛋白多肽存在于铁蛋白的每个单体上的这种方式包含杂合铁蛋白和非铁蛋白多肽。在一些实施方案中,这些单体自组装成铁蛋白纳米颗粒。在一些实施方案中,包含杂合铁蛋白单体的铁蛋白纳米颗粒在纳米颗粒表面上包含多个拷贝的非铁蛋白多肽。在一些实施方案中,二十四个杂合铁蛋白单体的组装形成在纳米颗粒的表面上具有二十四个非铁蛋白多肽的铁蛋白纳米颗粒。
在一些实施方案中,抗原性铁蛋白多肽包含SEQ ID NO:1-76、301-343、401-403、410、413-414、417-427或501-523中的任一个的序列。在一些实施方案中,融合蛋白包含与任何前述序列具有至少80%、85%、90%、95%、98%或99%同一性的序列,其中铁蛋白序列包含用半胱氨酸置换表面暴露的氨基酸的突变。这种铁蛋白序列可以进一步包含在对应于游离幽门螺杆菌铁蛋白(SEQ ID NO:208)的位置19的位置处的Asn至Glu突变,和/或在对应于游离幽门螺杆菌铁蛋白(SEQ ID NO:208)的位置31的位置处的Cys至Ser突变。在一些实施方案中,由表面暴露的氨基酸突变产生的半胱氨酸对应于本文公开的半胱氨酸位置,例如幽门螺杆菌铁蛋白的位置12、26、72、75、79、100或111中的任一个。
2.作为非铁蛋白多肽的EBV多肽
在一些实施方案中,本文所述的铁蛋白多肽进一步包含EBV多肽。在一些实施方案中,本文所述的抗原性铁蛋白多肽的非铁蛋白多肽是EBV多肽。在一些实施方案中,本文所述的抗原性铁蛋白多肽也是抗原性EBV多肽。
a)包含gL和gH多肽的EBV多肽
EBV具有三种糖蛋白,即糖蛋白B(gB)、gH和gL,它们形成了核心膜融合机构以允许病毒穿透进入细胞。gL和gH先前已经在例如Matsuura等人,Proc Natl Acad Sci U SA.2010年12月28日;107(52):22641-6中进行了描述。用作疫苗的gL和gH的单体和三聚体已经例如在Cui等人,Vaccine.2016年7月25日;34(34):4050-5中进行了描述。gH和gL蛋白缔合形成异二聚体复合物,所述异二聚体复合物被认为是病毒进入所需的高效膜融合和与上皮细胞受体结合所必需的。
在一些实施方案中,EBV多肽包含EBV gL和EBV gH。在一些实施方案中,多肽以单链存在。在一些实施方案中,多肽例如通过铁蛋白或2,4-二氧四氢喋啶合酶的多聚化形成纳米颗粒(例如铁蛋白或2,4-二氧四氢喋啶合酶颗粒)。在一些实施方案中,根据本公开文本的抗原性EBV多肽包含EBV gL多肽和EBV gH多肽,以及将EBV gL多肽和EBV gH多肽分开、具有至少15个氨基酸的长度的接头。已经发现相对长的接头可以提供诸如改善的表达和/或免疫原性的益处。
在一些实施方案中,EBV gH和/或gL多肽包含全长gH和/或gL(对于示例性全长序列,分别参见GenBank登录号CEQ35765.1和YP_001129472.1)。在一些实施方案中,EBV gH和/或gL多肽是gH和/或gL的片段。在一些实施方案中,gL多肽是在gL C末端的末端具有7个氨基酸缺失的gL(D7)构建体。在一些实施方案中,gH多肽包含在C137处的突变,如C137A突变。在一些实施方案中,C137突变去除天然的不成对半胱氨酸以避免非特异性缀合。在一些实施方案中,gH多肽包含用以去除与SEQ ID NO:437的半胱氨酸137对应的半胱氨酸的突变,如C137A突变。在一些实施方案中,C137突变去除天然的不成对半胱氨酸以避免非特异性缀合。
在一些实施方案中,EBV gL多肽包含与SEQ ID NO:436具有至少80%、85%、90%、95%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,EBV gH多肽包含与SEQ ID NO:437具有至少80%、85%、90%、95%、97%、98%、99%或100%同一性的氨基酸序列。
在一些实施方案中,哺乳动物前导序列(也称为信号序列)附加至EBV多肽(如gH或gL多肽)的N末端,例如在所述多肽的N末端。在一些实施方案中,哺乳动物前导序列当在哺乳动物细胞中表达时导致蛋白质的分泌。
天然EBV gH和/或gL序列在GenBank登录号NC_009334.1(人疱疹病毒4,完整基因组,日期为2010年3月26日)中示出。全长或片段化的天然EBV gH和/或gL可以用作非铁蛋白多肽。对于本文公开的一些构建体,将NC_009334.1中gL氨基酸序列的氨基酸23-137用作gL多肽,并且将天然信号肽(NCBI序列的氨基酸1-22)替换为IgGκ前导序列。对于一些构建体,将NC_009334.1中gH氨基酸序列的氨基酸19-678用作gH多肽。在一些实施方案中,gL和gH经由如本文序列表中所示的接头连接。
在一些实施方案中,gL和gH多肽表达为单链单体。在一些实施方案中,单体组合物包含在序列表中示出并且在说明书中表示为“单体”的序列或由所述序列组成。包含gL和gH多肽的单链可以称为“gL/gH”,其可以与“gH_gL”、“gL_gH”或“gL/gH”互换使用。
gL/gH多肽可以与本文所讨论的铁蛋白或2,4-二氧四氢喋啶合酶中的任一种组合。例如,在一些实施方案中,抗原性EBV多肽包含单体或三聚体gL/gH多肽(+/-gp42和/或gp220),以及i)重链或轻链铁蛋白(例如粉纹夜蛾重链或轻链铁蛋白);或ii)铁蛋白,所述铁蛋白任选地包含表面暴露的半胱氨酸。
另外,在一些实施方案中,包含EBV gL/gH多肽和铁蛋白的任何抗原性EBV多肽可以存在于包含本文公开的另一种多肽的组合物中,所述另一种多肽如含有铁蛋白和除gL/gH以外的EBV多肽(例如gp220和/或gp42)的另一种抗原性EBV多肽。
b)包含gp220多肽的EBV多肽
在一些实施方案中,EBV多肽包含gp220多肽。gp220-杂合牛蛙/幽门螺杆菌铁蛋白纳米颗粒先前已经在Kanekiyo Cell.2015年8月27日;162(5):1090-100中进行了描述。除了与本文所述的某些铁蛋白的其他差异之外,此纳米颗粒不包含提供表面暴露的半胱氨酸的突变或包含半胱氨酸的接头。
在一些实施方案中,gp220多肽包含与SEQ ID NO:438具有至少80%、85%、90%、95%、97%、98%、99%或100%同一性的氨基酸序列。
在一些实施方案中,哺乳动物前导序列(也称为信号序列)附加至gp220多肽的N末端。在一些实施方案中,哺乳动物前导序列当在哺乳动物细胞中表达时导致蛋白质的分泌。
gp220多肽可以与本文所讨论的铁蛋白或2,4-二氧四氢喋啶合酶中的任一种组合。例如,在一些实施方案中,抗原性EBV多肽包含gp220多肽(+/-gL/gH和/或gp42),以及i)重链或轻链铁蛋白(例如粉纹夜蛾重链或轻链铁蛋白);或ii)铁蛋白,所述铁蛋白任选地包含如本文所述的表面暴露的半胱氨酸。
另外,在一些实施方案中,包含gp220多肽和铁蛋白的任何抗原性EBV多肽可以存在于包含本文公开的另一种多肽的组合物中,所述另一种多肽如含有铁蛋白和除gp220以外的EBV多肽(例如gL/gH和/或gp42)的另一种抗原性EBV多肽。
c)包含gp42多肽的EBV多肽
在一些实施方案中,EBV多肽包含gp42多肽。示例性gp42序列提供为SEQ ID NO:434。适合于包含在例如具有gL和gH多肽的融合体中的另外的示例性gp42序列提供为SEQID NO:239。适合于包含在例如具有gL和gH多肽的融合体中的另一种示例性gp42序列提供为SEQ ID NO:240。
在一些实施方案中,gp42多肽包含与SEQ ID NO:434具有至少80%、85%、90%、95%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,gp42多肽包含与SEQ ID NO:239具有至少80%、85%、90%、95%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,gp42多肽包含与SEQ ID NO:240具有至少80%、85%、90%、95%、97%、98%、99%或100%同一性的氨基酸序列。
在一些实施方案中,哺乳动物前导序列(也称为信号序列)附加至gp42多肽的N末端。在一些实施方案中,哺乳动物前导序列当在哺乳动物细胞中表达时导致蛋白质的分泌。示例性前导序列是SEQ ID NO:226的氨基酸1-22。
在一些实施方案中,包含gH和/或gL多肽的抗原性EBV多肽进一步包含gp42多肽。上述的包含gH和/或gL多肽的任何EBV多肽可以进一步包含gp42多肽。在一些实施方案中,gp42多肽位于gH和/或gL多肽的C末端,如SEQ ID NO:421和226-231中例示的。在一些实施方案中,gp42多肽位于铁蛋白的N末端,也如SEQ ID NO:421和227-231中例示的。因此,例如,抗原性EBV多肽可以在N末端至C末端取向上包含gL多肽、gH多肽、gp42多肽和任选的铁蛋白。如本文所述的那些的接头可以将gp42多肽与位于其N末端和/或C末端的EBV多肽和/或铁蛋白分开。在一些实施方案中,接头将抗原性铁蛋白多肽中的每个EBV多肽(例如,gL多肽、gH多肽和gp42多肽)分开,并且在存在时的铁蛋白和与其接近的EBV多肽(例如,gp42多肽)之间可以存在另外的接头。
在一些实施方案中,具有至少15个氨基酸的长度的接头将EBV gH多肽与EBV gp42多肽分开。这种接头可以具有15至60个氨基酸、20至60个氨基酸、30至60个氨基酸、40至60个氨基酸、30至50个氨基酸或40至50个氨基酸的长度。在一些实施方案中,接头包含与SEQID NO:234具有至少80%、85%、90%、95%、97%、98%、99%或100%同一性的氨基酸序列。
在一些实施方案中,在gp42和铁蛋白存在于多肽中的情况下,接头将EBV gp42多肽和铁蛋白分开。这种接头可以具有至少15个氨基酸的长度或具有15至60个氨基酸、20至60个氨基酸、30至60个氨基酸、40至60个氨基酸、30至50个氨基酸或40至50个氨基酸的长度。在一些实施方案中,这种接头包含与SEQ ID NO:233、234、235、236、237或238中的任一个具有至少80%、85%、90%、95%、97%、98%、99%或100%同一性的氨基酸序列。
gp42多肽可以与本文所讨论的铁蛋白或2,4-二氧四氢喋啶合酶中的任一种组合。例如,在一些实施方案中,多肽包含gp42多肽(+/-gL/gH和/或gp220),以及重链或轻链铁蛋白(例如粉纹夜蛾重链或轻链铁蛋白);或ii)铁蛋白,所述铁蛋白任选地包含如本文所述的表面暴露的半胱氨酸。
在一些实施方案中,抗原性EBV多肽包含与SEQ ID NO:226的氨基酸23-1078具有至少80%、85%、90%、95%、98%或99%同一性的序列。在一些实施方案中,抗原性EBV多肽包含与SEQ ID NO:226的氨基酸1-1078具有80%、85%、90%、95%、98%或99%同一性的序列。在一些实施方案中,抗原性EBV多肽包含与SEQ ID NO:226、227、228、229、230或231中的任一个具有80%、85%、90%、95%、98%或99%同一性的序列,任选地缺乏前导序列(例如,缺乏这些序列中的氨基酸1-22的任一个或全部)。
另外,在一些实施方案中,包含gp42多肽和铁蛋白的任何抗原性EBV多肽可以存在于包含本文公开的另一种多肽的组合物中,所述另一种多肽如含有铁蛋白和除gp42以外的EBV多肽(例如gL/gH和/或gp220)的另一种抗原性EBV多肽。
d)gL、gH、gp42、接头和/或铁蛋白序列中的突变以消除潜在的氧化、脱酰胺或异天冬氨酸形成位点
在一些实施方案中,抗原性EBV多肽包含一个或多个突变以消除潜在的氧化、脱酰胺或异天冬氨酸形成位点,如下表1中所示的示例性突变。
例如,在一些实施方案中,gL序列包含一个或多个突变以消除潜在的琥珀酰亚胺/异天冬氨酸或脱酰胺位点。例如,gL序列可以包含在对应于SEQ ID NO:227的位置36的位置处的G至A突变;在对应于SEQ ID NO:227的位置47的位置处的N至Q突变;或在对应于SEQ IDNO:227的位置105的位置处的N至Q突变。如果根据标准序列比对算法(如使用默认参数的Smith-Waterman算法),氨基酸序列中的位置与SEQ ID NO:227中的给定位置对齐,则所述氨基酸序列中的位置“对应于”SEQ ID NO:227中的所述给定位置。
在一些实施方案中,接头包含一个或多个突变以消除潜在的脱酰胺位点。例如,接头序列可以包含在对应于SEQ ID NO:227的位置132或141的位置处的N至G突变。
在一些实施方案中,gH序列包含一个或多个突变以消除潜在的琥珀酰亚胺/异天冬氨酸或氧化位点。例如,gH序列可以包含在对应于SEQ ID NO:227的位置189、401或729的位置处的M至L突变;在对应于SEQ ID NO:227的位置368的位置处的D至E突变;在对应于SEQID NO:227的位置499或639的位置处的M至I突变;或在对应于SEQ ID NO:227的位置653的位置处的N至Q突变。
在一些实施方案中,gp42序列包含一个或多个突变以消除潜在的脱酰胺位点。例如,gp42序列可以包含在对应于SEQ ID NO:227的位置959或990的位置处的N至Q突变;或在对应于SEQ ID NO:227的位置988的位置处的N至S突变。
在一些实施方案中,铁蛋白序列包含一个或多个突变以消除潜在的脱酰胺、氧化或异天冬氨酸形成位点。例如,铁蛋白序列可以包含在对应于SEQ ID NO:227的位置1150的位置处的Q至S突变;在对应于SEQ ID NO:227的位置1168的位置处的M至I突变;在对应于SEQ ID NO:227的位置1177的位置处的M至L突变;在对应于SEQ ID NO:227的位置1188的位置处的G至A突变;或在对应于SEQ ID NO:227的位置1253或1296的位置处的N至Q突变。
示例性突变在下表6中示出。位置编号对应于SEQ ID NO:227。
3.作为非铁蛋白多肽的流感多肽
在一些实施方案中,本文所述的铁蛋白多肽进一步包含流感多肽。在一些实施方案中,本文所述的抗原性铁蛋白多肽的非铁蛋白多肽是流感多肽。在一些实施方案中,本文所述的抗原性铁蛋白多肽是抗原性流感-铁蛋白多肽。
a)HA和NA多肽
在一些实施方案中,流感多肽是包含全长或部分长度的HA或NA的HA或NA多肽。可以使用任何HA或NA多肽。HA或NA多肽可以是天然存在的或从天然改变的。在一些实施方案中,HA来自H1-H18中的任一种。在一些实施方案中,NA来自N1-N11中的任一种。
在一些实施方案中,HA多肽包含HA胞外结构域。HA胞外结构域可能来自任何流感亚型,包括H1-H18。
在一些实施方案中,HA多肽包含HA的茎区。HA的茎区可以来自任何流感亚型,包括H1-H18。
在一些实施方案中,HA多肽来自甲型流感病毒。甲型流感病毒可以是A/波多黎各/1934、A/Weiss/1/1943、A/蒙茅斯堡/1/1947(FM47)、A/马来西亚/302/54(MAL54)、A/丹佛/1/1957(DV57)、A/新泽西州/8/1976、A/USSR/90/1977、A/香港/117/1977(HK77)、A/巴西/11/1978、A/智利/1/1983、A/台湾/1/1986、A/德克萨斯州/36/1991、A/北京/262/1995、A/新喀里多尼亚/20/1999(NC99)、A/所罗门群岛/6/2006、A/布里斯班/59/2007、A/加利福尼亚/07/2009(CA09)、A/孟加拉国/2021/2012或A/越南/3050/2013。
在一些实施方案中,HA多肽来自H1流感病毒。在一些实施方案中,H1病毒是A/南卡罗来纳州/1/18。
在一些实施方案中,HA多肽来自H2流感病毒。在一些实施方案中,H2病毒是1957大流行性H2N2甲型流感病毒。
在一些实施方案中,HA多肽来自H3流感病毒。在一些实施方案中,H3流感病毒是H3N8病毒。在一些实施方案中,H3N8病毒是马俄亥俄州2003。在一些实施方案中,H3N8病毒是马巴里2005。在一些实施方案中,H3N8病毒是马阿博因2003。在一些实施方案中,H3流感病毒是H3N2病毒。在一些实施方案中,H3N2病毒是伯斯2009。在一些实施方案中,H3N2病毒是维多利亚2011。
在一些实施方案中,HA多肽来自H5流感病毒。在一些实施方案中,H5流感病毒是H5/N1病毒。在一些实施方案中,H5/N1病毒是印度尼西亚2005。在一些实施方案中,H5/N1病毒是斑头雁2005。在一些实施方案中,H5/N1病毒是大天鹅2005。在一些实施方案中,H5/N1病毒是野鸭/华东2003。
在一些实施方案中,HA多肽来自乙型流感病毒。在一些实施方案中,乙型病毒是威斯康星州2010。在一些实施方案中,乙型病毒是马萨诸塞州2012。在一些实施方案中,乙型病毒是普吉岛2013。在一些实施方案中,乙型病毒是布里斯班2008。在一些实施方案中,布里斯班2008序列包含D197N突变。发现此突变改善了此纳米颗粒的表达,并且在其他株系(如B/布里斯班/2009和B/普吉岛/2013)中是天然存在的突变。此氨基酸可参与接触唾液酸受体。
在一些实施方案中,HA多肽包含根据Giles BM和Ross TM,Vaccine 29(16):3043-54(2011)或Carter DM等人,J Virol 90:4720-4734(2016)的实施例产生的计算优化的广泛反应性抗原(COBRA)。
在一些实施方案中,从人H1N1流感序列产生COBRA序列。在一些实施方案中,从跨越1999-2012的人H1N1流感序列产生COBRA序列。从跨越1999-2012的人H1N1流感序列产生的示例性COBRA序列是包含在SEQ ID NO:329中的COBRA X6。在一些实施方案中,从跨越1933-1957年和2009-2011年的人H1N1株系加上来自1931-1998年的猪H1N1流感株系产生COBRA序列。从跨越1933-1957年和2009-2011年的人H1N1株系加上来自1931-1998年的猪H1N1流感株系产生的示例性COBRA序列是包含在SEQ ID NO:327中的COBRA P1。
在一些实施方案中,COBRA序列是X3。在一些实施方案中,COBRA序列是从H5N1产生的hCOBRA-2。
消除HA受体结合位点的突变(Y98F)在Whittle等人,Journal of Virology 11(8):4047-4057(2014)中进行了描述。在一些实施方案中,HA多肽包含Y98F突变。上文提出的任何HA可以被修饰为包含Y98F突变。在一些实施方案中,HA来自H1/新喀里多尼亚/1999(NC99)病毒,并且包含Y98F突变。
4.作为非铁蛋白多肽的疏螺旋体属和OspA多肽
在一些实施方案中,本文所述的铁蛋白多肽进一步包含疏螺旋体属多肽。在一些实施方案中,本文所述的抗原性铁蛋白多肽的非铁蛋白多肽是疏螺旋体属多肽。在一些实施方案中,疏螺旋体属多肽来自博氏疏螺旋体。在一些实施方案中,疏螺旋体属多肽来自对应于血清型1、2、3、4、5、6或7的疏螺旋体属物种。在一些实施方案中,疏螺旋体属可以由硬蜱属(Ixodes)的蜱虫携带。
在一些实施例中,疏螺旋体属多肽是OspA多肽。在一些实施方案中,本文所述的抗原性铁蛋白多肽也是抗原性OspA多肽。
在一些实施方案中,OspA多肽包含疏螺旋体属的修饰的外表面蛋白A(OspA)。OspA以多种血清型存在,所述多种血清型如通过其与针对OspA的不同表位的单克隆抗体的反应性所定义(参见Wilske等人,J Clin Microbio 31(2):340-350(1993))。这些血清型与疏螺旋体属细菌的不同基因种相关联。在一些实施方案中,OspA是血清型1-7中的任一种。在一些实施方案中,OspA来自博氏疏螺旋体、梅奥疏螺旋体(Borrelia mayonii)、阿氏疏螺旋体(Borrelia afzelii)、伽氏疏螺旋体(Borrelia garinii)或巴伐利亚疏螺旋体(Borreliabavariensis)。在一些实施方案中,OspA是博氏疏螺旋体OspA。在一些实施方案中,疏螺旋体属可以由硬蜱属(Ixodes)的蜱虫携带。在一些实施方案中,疏螺旋体属是博氏疏螺旋体、梅奥疏螺旋体、阿氏疏螺旋体、伽氏疏螺旋体或巴伐利亚疏螺旋体。
在一些实施方案中,OspA多肽是OspA血清型1多肽,如OspA血清型1胞外结构域。文献报道,OspA血清型1的在SEQ ID NO:83的氨基酸165-173处的表位与人白细胞功能相关抗原1(hLFA-1)的序列片段(即SEQ ID NO:78)具有同源性(参见Gross,D.M.等人,Science281(5377):第703-6页(1998))。SEQ ID NO:83的氨基酸165-173在SEQ ID NO:77中示出为分离的九肽,并且称为hLFA-1同源位点。SEQ ID NO:83是示例性野生型血清型1OspA序列,所述序列在本文中用作讨论OspA中的氨基酸位置的参考序列。此同源位点可能在莱姆关节炎(包括抗生素抗性莱姆关节炎)的发生中起作用。在一些实施方案中,OspA多肽包含疏螺旋体属的修饰的OspA血清型1多肽,其中修饰的OspA不包含SEQ ID NO:77的序列。当用于引发抗体时,此类多肽可以具有改善的安全性,例如降低的触发自身免疫应答的风险。在一些实施方案中,OspA血清型1多肽具有降低与hLFA-1的同一性的一种或多种修饰。涵盖了降低与SEQ ID NO:78的同源性、降低与SEQ ID NO:78的同一性或相对于SEQ ID NO:78引入一个或多个非保守取代的任何修饰。
在一些实施方案中,OspA多肽包含疏螺旋体属的OspA血清型1多肽,其中OspA多肽不包含SEQ ID NO:77的序列。在一些实施方案中,OspA多肽包含OspA血清型1的胞外结构域,其中胞外结构域不包含SEQ ID NO:77的序列。在一些实施方案中,OspA血清型1多肽包含与SEQ ID NO:94-102中任一个的序列具有至少85%、90%、95%、97%、98%、99%、99.5%或100%同一性的序列。
“降低同源性”涵盖降低序列同一性和/或降低序列相似性,其中认为在下表4中列为保守取代的一组氨基酸中的每个成员与所列的原始残基以及与该组的其他成员相似;例如,表格的第一行指示丙氨酸、缬氨酸、亮氨酸和异亮氨酸彼此相似,并且第八行指示丙氨酸和甘氨酸彼此相似。相似性不具有传递性,因此例如,异亮氨酸和甘氨酸不被认为相似。在一些实施方案中,OspA多肽包括与野生型OspA血清型1相比具有降低的与hLFA-1的同源性的OspA血清型1蛋白。在一些实施方案中,修饰的OspA包括含有对SEQ ID NO:77的任何一个或多个氨基酸的修饰的OspA血清型1。在一些实施方案中,对SEQ ID NO:77的修饰是非保守氨基酸取代。非保守取代是与下表中所示的保守取代不同的取代。
表4:保守氨基酸取代
在一些实施方案中,OspA多肽包括OspA血清型1蛋白,其中SEQ ID NO:77的一个或多个氨基酸被非血清型1OspA(如血清型2、3、4、5、6或7OspA)的一个或多个相应氨基酸置换。在一些实施方案中,SEQ ID NO:77的每个氨基酸被血清型2、3、4、5、6或7OspA的一个或多个相应氨基酸置换。在一些实施方案中,SEQ ID NO:77的氨基酸被血清型2(S2,SEQ IDNO:79)或血清型3(S3,SEQ ID NO:80)的相应氨基酸置换。
在一些实施方案中,OspA多肽包含SEQ ID NO:81。在一些实施方案中,OspA多肽包含SEQ ID NO:82。SEQ ID NO:81和82旨在置换SEQ ID NO:77并由此降低了与SEQ ID NO:78的同源性。
在一些实施方案中,OspA多肽是全长OspA(例如,包括跨膜结构域和胞外结构域,其可以包含或可以不包含如本文所述的用以降低与hLFA-1的同源性的修饰)。
在一些实施方案中,OspA多肽缺乏跨膜结构域。在一些实施方案中,多肽缺乏跨膜结构域的一部分,例如野生型OspA序列的N末端2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23或24个氨基酸。在一些实施方案中,OspA多肽缺乏下述区段,所述区段包含OspA血清型1的氨基酸17或如通过成对或结构比对鉴定的其同源物的相应位置。在一些实施方案中,OspA多肽至少缺乏OspA(如OspA血清型1)的氨基酸1-17,或如通过成对或结构比对鉴定的其同源物中的对应氨基酸。在一些实施方案中,OspA多肽至少缺乏OspA(如OspA血清型1)的N末端18、19、20、21、22、23或24个氨基酸,或如通过成对或结构比对鉴定的其同源物中的对应氨基酸。在一些实施方案中,OspA多肽缺乏OspA(如OspA血清型1)的氨基酸1-25,或如通过成对或结构比对鉴定的其同源物中的对应氨基酸。在一些实施方案中,OspA多肽缺乏OspA血清型1的氨基酸1-26,或如通过成对或结构比对鉴定的其同源物中的对应氨基酸。为了避免疑问,缺乏跨膜结构域并不要求多肽缺乏N端甲硫氨酸;例如,认为其中第一残基是甲硫氨酸并且第二残基对应于野生型OspA的残基26,之后是对应于第27、第28等野生型OspA残基的残基的多肽缺乏跨膜结构域。在一些实施方案中,包含OspA多肽的多肽缺乏脂化位点,如野生型OspA血清型1的跨膜结构域内所包含的脂化位点。在一些实施方案中,OspA多肽缺乏OspA血清型1的半胱氨酸17。在一些实施方案中,OspA多肽不包含对应于野生型OspA(例如,SEQ ID NO:83-89中的任一种)的位置1-25中的任一个的半胱氨酸。在一些实施方案中,多肽缺乏或具有在OspA血清型1的半胱氨酸17处的取代。在一些实施方案中,OspA多肽缺乏野生型OspA跨膜结构域的至少一部分,由此使得其缺乏脂化位点。在一些实施方案中,OspA多肽缺乏与OspA血清型1的氨基酸1-17对齐的氨基酸。
在一些实施方案中,OspA多肽不包含棕榈酰基基团。在一些实施方案中,OspA多肽不包含二酰基甘油基团。在一些实施方案中,OspA多肽是非脂化的。在一些实施方案中,OspA多肽缺乏脂化位点。在一些实施方案中,此脂化位点包含在跨膜结构域内。在一些实施方案中,去除的脂化位点是OspA血清型1的半胱氨酸17。在一些实施方案中,OspA多肽缺乏或具有在OspA血清型1的半胱氨酸17处的取代。
在一些实施方案中,OspA脂化位点和/或跨膜结构域或其部分的去除,和/或棕榈酰基和/或二酰基甘油基团的缺乏使得蛋白质纯化更容易,例如,通过改善蛋白质的溶解性和/或使得蛋白质更适于通过如离子交换和其他形式的色谱的技术进行纯化。
在一些实施方案中,OspA多肽包含哺乳动物前导序列(也称为信号序列)。在一些实施方案中,哺乳动物前导序列当在哺乳动物细胞中表达时导致多肽的分泌。
在一些实施方案中,OspA多肽缺乏糖基化位点。本文详细描述了去除糖基化位点的修饰。根据本公开文本的OspA多肽可以包含任何这种修饰,这种修饰可以与本文所述的任何其他修饰(包括对hLFA-1同源位点的修饰和/或部分或全部跨膜结构域的缺失)组合。在一些实施方案中,多肽不包含SEQ ID NO:77(例如,具有降低的与hLFA-1a的同源性),并且具有修饰以减少糖基化和/或缺乏跨膜结构域。
a)糖基化的修饰
N-连接的糖基化是聚糖与蛋白质的天冬酰胺(Asn;N)残基的酰胺氮的附接。附接过程产生糖基化的蛋白质。糖基化可以发生在蛋白质翻译后可被糖基化酶接近并识别的蛋白质中的任何天冬酰胺残基处,并且最常见于为NXS/TX位点(其中在天冬酰胺之后的第二个氨基酸残基是丝氨酸或苏氨酸)的一部分的可接近天冬酰胺处。非人糖基化模式(例如,由在某些非人细胞类型中包含糖基化位点的多肽的表达而产生)可能在用于引发抗体时使多肽产生不期望的反应原性。另外,正常未被糖基化的多肽的糖基化可改变其免疫原性。例如,糖基化可以掩盖蛋白质内重要的免疫原性表位。因此,为了减少或消除糖基化,可以对天冬酰胺残基或丝氨酸/苏氨酸残基进行修饰,例如通过取代为另一个氨基酸。
在一些实施方案中,对包含OspA多肽的多肽进行修饰以减少或消除糖基化。在一些实施方案中,去除OspA中的一个或多个N-糖基化位点。在一些实施方案中,N-糖基化位点的去除降低了OspA的糖基化。在一些实施方案中,相对于野生型OspA(如野生型血清型1OspA),多肽具有降低的糖基化。在一些实施方案中,N-糖基化位点的去除消除了OspA的糖基化。
在一些实施方案中,将OspA中的一个或多个天冬酰胺置换为非天冬酰胺氨基酸。在一些实施方案中,将OspA中的每个天冬酰胺置换为非天冬酰胺氨基酸。蛋白质中发现的任何天然或非天然氨基酸(例如谷氨酰胺)都可以用于置换天冬酰胺。在一些实施方案中,用以减少或消除糖基化的修饰修饰了NXS/TX糖基化位点(其中在N之后的第二个残基是S或T)。在一些实施方案中,NXS/TX位点中的第一个X不是脯氨酸和/或NXS/TX位点中的第二个X不是脯氨酸。在一些实施方案中,用以减少或消除糖基化的修饰是N至Q取代。在一些实施方案中,用以减少或消除糖基化的修饰是S/T至A取代。
下面详细讨论了可以修饰以减少或消除糖基化的位置。位置编号是指提供为SEQID NO:83-89的全长OspA序列中的位置。应理解的是,应当针对部分和修饰的OspA序列适当地调节位置编号(例如,如果N末端缺失导致净缩短了25个氨基酸残基,则位置编号应当减少25)。
在一些实施方案中,用以减少或消除糖基化的修饰包括对OspA血清型1(SEQ IDNO:83)的N20、N71、N190、N202和N251中的任何一个或多个的取代。在一些实施方案中,修饰包括在OspA血清型1的N71、N190、N202和N251中的每一个处的修饰。在一些实施方案中,用以减少或消除糖基化的修饰包括OspA血清型1的N20Q、N71Q、N190Q、N202Q或N251Q中的一个或多个。通过成对比对,可以在不同血清型的OspA中找到相应的氨基酸。因此,在一些实施方案中,在血清型2-7的OspA中被置换的天冬酰胺残基是与OspA血清型1的N20、N71、N190、N202和N251对齐的氨基酸残基。在一些实施方案中,用以减少或消除糖基化的修饰包括对在OspA血清型1的位置22、73、192、204和253处的Ser或Thr残基中的任何一个或多个的取代。在一些实施方案中,修饰包括用丙氨酸取代OspA血清型1的位置22、73、192、204和253处的Ser或Thr残基中的一个或多个。
在一些实施方案中,用以减少或消除糖基化的修饰包括对OspA血清型2(SEQ IDNO:84)的N20、N71、N141、N164、N202和N205中的任何一个或多个的取代。在一些实施方案中,修饰包括在OspA血清型2的N20、N71、N141、N164、N202和N205中的每一个处的修饰。在一些实施方案中,用以减少或消除糖基化的修饰包括OspA血清型2的N20Q、N71Q、N141Q、N164Q、N202Q或N205Q中的一个或多个。通过成对比对,可以在不同血清型的OspA中找到类似的氨基酸。因此,在一些实施方案中,在血清型1或3-7的OspA中被置换的天冬酰胺残基是与OspA血清型2的N20、N71、N141、N164、N202和N205对齐的氨基酸残基。在一些实施方案中,用以减少或消除糖基化的修饰包括对在OspA血清型2的位置22、73、143、166、204和207处的Ser或Thr残基中的任何一个或多个的取代。在一些实施方案中,修饰包括用丙氨酸取代OspA血清型2的位置22、73、143、166、204和207处的Ser或Thr残基中的一个或多个。
在一些实施方案中,用以减少或消除糖基化的修饰包括对OspA血清型3(SEQ IDNO:85)的N20、N71、N95、N141、N191和N203中的任何一个或多个的取代。在一些实施方案中,修饰包括在OspA血清型3的N20、N20、N71、N95、N141、N191和N203中的每一个处的修饰。在一些实施方案中,用以减少或消除糖基化的修饰包括OspA血清型3的N20Q、N71Q、N95Q、N141Q、N191Q或N203Q中的一个或多个。通过成对比对,可以在不同血清型的OspA中找到类似的氨基酸。因此,在一些实施方案中,在血清型1-2或4-7的OspA中被置换的天冬酰胺残基是与OspA血清型3的N20、N20、N71、N95、N141、N191和N203对齐的氨基酸残基。在一些实施方案中,用以减少或消除糖基化的修饰包括对在OspA血清型3的位置22、73、97、143、193和205处的Ser或Thr残基中的任何一个或多个的取代。在一些实施方案中,修饰包括用丙氨酸取代OspA血清型3的位置22、73、97、143、193和205处的Ser或Thr残基中的一个或多个。
在一些实施方案中,用以减少或消除糖基化的修饰包括对OspA血清型4(SEQ IDNO:86)的N20、N71、N141、N202、N205和N219中的任何一个或多个的取代。在一些实施方案中,修饰包括在OspA血清型4的N20、N71、N141、N202、N205和N219中的每一个处的修饰。在一些实施方案中,用以减少或消除糖基化的修饰包括OspA血清型4的N20Q、N71Q、N141Q、N202Q、N205Q或N219Q中的一个或多个。通过成对比对,可以在不同血清型的OspA中找到类似的氨基酸。因此,在一些实施方案中,在血清型1-3或5-7的OspA中被置换的天冬酰胺残基是与OspA血清型4的N20、N71、N141、N202、N205和N219对齐的氨基酸残基。在一些实施方案中,用以减少或消除糖基化的修饰包括对在OspA血清型4的位置22、73、143、204、207和221处的Ser或Thr残基中的任何一个或多个的取代。在一些实施方案中,修饰包括用丙氨酸取代OspA血清型4的位置22、73、143、204、207和221处的Ser或Thr残基中的一个或多个。
在一些实施方案中,用以减少或消除糖基化的修饰包括对OspA血清型5的N20、N71和N141中的任何一个或多个的取代。(某些血清型(包括血清型5-7)比某些其他OspA序列(如血清型1)含有更少的糖基化位点)。在一些实施方案中,修饰包括在OspA血清型5(SEQID NO:87)的N20、N71和N141中的每一个处的修饰。在一些实施方案中,用以减少或消除糖基化的修饰包括OspA血清型5的N20Q、N71Q或N141Q中的一个或多个。通过成对比对,可以在不同血清型的OspA中找到类似的氨基酸。因此,在一些实施方案中,在血清型1-4或6-7的OspA中被置换的天冬酰胺残基是与OspA血清型5的N20、N71和N141对齐的氨基酸残基。在一些实施方案中,用以减少或消除糖基化的修饰包括对在OspA血清型5的位置22、73和143处的Ser或Thr残基中的任何一个或多个的取代。在一些实施方案中,修饰包括用丙氨酸取代OspA血清型5的位置22、73和143处的Ser或Thr残基中的一个或多个。
在一些实施方案中,用以减少或消除糖基化的修饰包括对OspA血清型6(SEQ IDNO:88)的N20、N71和N141中的任何一个或多个的取代。在一些实施方案中,修饰包括在OspA血清型6的N20、N71和N141中的每一个处的修饰。在一些实施方案中,用以减少或消除糖基化的修饰包括OspA血清型6的N20Q、N71Q或N141Q中的一个或多个。通过成对比对,可以在不同血清型的OspA中找到类似的氨基酸。因此,在一些实施方案中,在血清型1-5或7的OspA中被置换的天冬酰胺残基是与OspA血清型6的N20、N71和N141对齐的氨基酸残基。在一些实施方案中,用以减少或消除糖基化的修饰包括对在OspA血清型6的位置22、73和143处的Ser或Thr残基中的任何一个或多个的取代。在一些实施方案中,修饰包括用丙氨酸取代OspA血清型6的位置22、73和143处的Ser或Thr残基中的一个或多个。
在一些实施方案中,用以减少或消除糖基化的修饰包括对OspA血清型7(SEQ IDNO:89)的N20、N71、N141和N191中的任何一个或多个的取代。在一些实施方案中,修饰包括在OspA血清型7的N20、N71、N141和N191中的每一个处的修饰。在一些实施方案中,用以减少或消除糖基化的修饰包括OspA血清型7的N20Q、N71Q、N141Q或N191Q中的一个或多个。通过成对比对,可以在不同血清型的OspA中找到类似的氨基酸。因此,在一些实施方案中,在血清型1-6的OspA中被置换的天冬酰胺残基是与OspA血清型7的N20、N71、N141和N191对齐的氨基酸残基。在一些实施方案中,用以减少或消除糖基化的修饰包括对在OspA血清型7的位置22、73、143和193处的Ser或Thr残基中的任何一个或多个的取代。在一些实施方案中,修饰包括用丙氨酸取代OspA血清型7的位置22、73、143和193处的Ser或Thr残基中的一个或多个。
5.作为非铁蛋白多肽的RSV多肽
在一些实施方案中,本文所述的铁蛋白多肽进一步包含RSV多肽。在一些实施方案中,本文所述的抗原性铁蛋白多肽的非铁蛋白多肽是RSV多肽。在一些实施方案中,本文所述的抗原性铁蛋白多肽是抗原性RSV多肽。RSV多肽可以是RSV F多肽,如本文所述的任何RSV F多肽。RSV F多肽可以包含RSV F的整个序列或RSV F的一部分。与野生型序列相比,RSV F多肽可以包含一个或多个修饰(例如氨基酸取代)。RSV多肽可以是RSV G多肽,如本文所述的任何RSV G多肽。
a)RSV F多肽
在一些实施方案中,RSV F多肽是全长或片段的野生型RSV F多肽。在一些实施方案中,融合前RSV F与融合后RSV F之间共享的RSV多肽的表位被阻断。当将抗原性RSV多肽给予至受试者时,阻断表位减少或消除了针对表位的抗体的产生。这可以增加靶向于F的特定构象(如融合前构象)所特有的表位的抗体的比例。因为F在尚未进入细胞的病毒中具有融合前构象,所以靶向于融合前F的抗体的比例增加可以提供更大的中和度(例如,如本文所述,表示为中和与结合比率)。可以通过在共享表位附近工程化大体积部分(如N-聚糖)来实现阻断。例如,可以例如通过将适当的残基突变为天冬酰胺来添加野生型F中不存在的N-糖基化位点。在一些实施方案中,阻断的表位是RSV F的抗原性位点1的表位。在一些实施方案中,融合前RSV F与融合后RSV F之间共享的两个或更多个表位被阻断。在一些实施方案中,RSV F的抗原性位点1的两个或更多个表位被阻断。在一些实施方案中,与被阻断的表位在拓扑上重叠的一个或多个、或全部表位也被阻断,任选地其中被阻断的表位是RSV F的抗原性位点1的表位。
在一些实施方案中,RSV F多肽包含对应于SEQ ID NO:526的位置328、348或507的天冬酰胺。在一些实施方案中,多肽包含对应于SEQ ID NO:526的位置328、348或507中的至少两个的天冬酰胺。在一些实施方案中,多肽包含对应于SEQ ID NO:526的位置328、348或507的天冬酰胺。如实施例中所述,已发现此类天冬酰胺可充当糖基化位点。此外,不希望受任何特定理论的束缚,当将多肽给予至受试者时,这些位点处的聚糖可以抑制针对附近表位的抗体的产生,所述附近表位包括融合前和融合后RSV F蛋白共有的表位。在一些实施方案中,对应于SEQ ID NO:26的位置328、348或507的天冬酰胺的糖基化阻断融合前RSV F与融合后RSV F之间共享的至少一个表位,如抗原性位点1的表位。抑制针对融合前和融合后RSV F蛋白共有的表位的抗体的产生可能是有益的,因为它可以引导针对融合前RSV F蛋白所特有的表位(如位点0表位)的抗体产生,所述抗体产生可能比针对其他RSV F表位的抗体具有更有效的中和活性。位点0表位涉及SEQ ID NO:526的氨基酸残基62-69和196-209。因此,在一些实施方案中,RSV F多肽包含SEQ ID NO:526的氨基酸残基62-69或196-209。
应当指出的是,本文所述的构建体可以具有相对于野生型RSV F不同长度的缺失或取代。例如,在SEQ ID NO:523等的构建体中,野生型序列(SEQ ID NO:526)的位置98-144被置换为GSGNVGL(SEQ ID NO:523的位置98-104;也为SEQ ID NO:531),导致净去除40个氨基酸,由此使得SEQ ID NO:526的328、348或507对应于SEQ ID NO:523的位置288、308和467。通常,本文所述的构建体中的位置可以通过成对比对,例如使用具有标准参数(EBLOSUM62矩阵,空位罚分10,空位延伸罚分0.5)的Needleman-Wunsch算法映射到SEQ IDNO:526的野生型序列上。还参见作为用于鉴定相应位置的替代性方法的如本文提供的结构比对的讨论。
在一些实施方案中,RSV F多肽包含突变,所述突变为添加聚糖以阻断融合前抗原上的在结构上与融合后RSV F表面上的那些表位相似的表位。在一些实施方案中,添加聚糖以特异性地阻断可能存在于RSV F的融合后构象中的表位。在一些实施方案中,添加聚糖,所述聚糖阻断可能存在于RSV F的融合后构象中的表位,但不影响存在于RSV F的融合前构象上的一个或多个表位(如位点0表位)。
在一些实施方案中,与其他构建体相比,在上文讨论的一个或多个糖基化位点处添加的聚糖增加了在表达系统(如哺乳动物细胞)中的分泌。
在一些实施方案中,RSV F多肽包含与SEQ ID NO:517的氨基酸1-478具有至少85%、90%、95%、97%、98%、99%或99.5%同一性的序列。在一些实施方案中,RSV F多肽包含与SEQ ID NO:517的序列具有至少85%、90%、95%、97%、98%、99%或99.5%同一性的序列。在一些实施方案中,RSV F多肽包含SEQ ID NO:517的氨基酸1-478。在一些实施方案中,RSV F多肽包含SEQ ID NO:517的序列。
在一些实施方案中,RSV F多肽包含与SEQ ID NO:523的氨基酸1-478具有至少85%、90%、95%、97%、98%、99%或99.5%同一性的序列。在一些实施方案中,RSV F多肽包含与SEQ ID NO:523的序列具有至少85%、90%、95%、97%、98%、99%或99.5%同一性的序列。在一些实施方案中,RSV F多肽包含SEQ ID NO:523的氨基酸1-478。在一些实施方案中,RSV F多肽包含SEQ ID NO:523的序列。
在一些实施方案中,RSV F多肽包含DS-CAV1序列(如例如在McLellan,J.S.等人,Science 342(6158):592-598(2013)中所述)(SEQ ID NO:525),其中进行了进一步的修饰,包括以上所述的至少一个、两个或三个天冬酰胺。
在一些实施方案中,多肽进一步包含铁蛋白蛋白。铁蛋白蛋白可以进一步包含下面在关于铁蛋白的章节中所述的任何特征,或其组合。
RSV F多肽可替代地或另外包含以下讨论中阐述的任何附加特征,或此类特征的任何可行组合。
单链构建体
在一些实施方案中,RSV F多肽是单链构建体,例如缺少弗林蛋白酶切割位点的RSV F多肽。在一些实施方案中,RSV F缺乏一个或多个弗林蛋白酶切割位点。缺乏弗林蛋白酶切割位点的构建体表达为不会切割成天然F蛋白的生物学F1/F2片段的单一多肽。
氨基酸取代
在一些实施方案中,RSV F包含相对于野生型序列的单一氨基酸取代。在一些实施方案中,RSV F包含相对于野生型序列的多于一个的单一氨基酸取代,例如2、3、4、5、6、7、8、9、10、11、12、13、14或15个取代。示例性野生型序列是SEQ ID NO:526。
在一些实施方案中,氨基酸取代或氨基酸取代对是一个或多个原体间稳定化取代。可以是原体间稳定化的示例性取代是V207L;N228F;I217V和E218F;I221L和E222M;或Q224A和Q225L(使用SEQ ID NO:526的位置编号)。
在一些实施方案中,氨基酸取代或氨基酸取代对是原体内稳定化的。可以是原体内稳定化的示例性取代是V220I;和A74L和Q81L(使用SEQ ID NO:526的位置编号)。
在一些实施方案中,氨基酸取代是螺旋稳定化的,即被预测为其稳定化RSV F的螺旋结构域。螺旋结构域的稳定化通常可以有助于位点0表位和RSV F的融合前构象的稳定性。可以是螺旋稳定化的示例性取代是N216P或I217P(使用SEQ ID NO:526的位置编号)。
在一些实施方案中,氨基酸取代是螺旋加帽。在一些实施方案中,氨基酸取代是螺旋PRO加帽。螺旋加帽是基于以下的生物物理观察结果:虽然α螺旋中的脯氨酸残基突变放置可能破坏螺旋的形成,但螺旋区N末端处的脯氨酸可以通过稳定化PHI/PSI键角来帮助诱导螺旋形成。可以是螺旋加帽的示例性取代是N216P或I217P(使用SEQ ID NO:526的位置编号)。
在一些实施方案中,氨基酸取代置换了DS-CAV1的二硫化物突变。在一些实施方案中,将DS-CAV1的工程化二硫化物回复为DS-CAV1的野生型(C69S和/或C212S突变)(使用SEQID NO:526的位置编号)。在一些实施方案中,DS-CAV1的一个或多个C残基被置换为S残基以消除二硫键。在一些实施方案中,使用SEQ ID NO:526的位置编号的C69S或C212S取代消除了二硫键。在一些实施方案中,RSV F多肽包含使用SEQ ID NO:526的位置编号的C69S和C212S二者。在一些实施方案中,置换此类半胱氨酸并由此消除二硫键阻止了RSV F多肽的还原(即,接受来自还原剂的电子)。在一些实施方案中,在抗原中包含使用SEQ ID NO:526的位置编号的I217P取代而不是在C69和/或C212处的取代。SEQ ID NO:526中的位置217对应于SEQ ID NO:523中的位置177。
在一些实施方案中,氨基酸取代防止胰蛋白酶或胰蛋白酶样蛋白酶的蛋白水解。在一些实施方案中,防止这种蛋白水解的氨基酸取代是在RSV F的七肽重复区B(HRB)区域中。与包含野生型HRB区域的RSV F-铁蛋白构建体的蛋白水解相一致的片段的出现表明此区域中的赖氨酸或精氨酸被靶向用于蛋白水解。用以去除K或R残基的氨基酸取代可称为敲除(KO)。在一些实施方案中,K或R被L或Q取代。在一些实施方案中,K被L或Q取代。在一些实施方案中,RSV F多肽包含使用SEQ ID NO:526的位置编号的K498L和/或K508Q。SEQ ID NO:523中的相应位置分别是458和468。在一些实施方案中,RSV F多肽包含K498L和K508Q二者。
在一些实施方案中,氨基酸取代添加了聚糖。在一些实施方案中,氨基酸取代通过向RSV F多肽添加聚糖来增加糖基化。与天然糖基化(没有附加的聚糖)相比,用以添加聚糖的取代也可以称为工程化糖基化。
在一些实施方案中,用以添加聚糖的氨基酸取代是被N取代。在一些实施方案中,被N取代氨基酸允许N-连接的糖基化。在一些实施方案中,被N取代伴随着被在N的C末端的第二个氨基酸位置处的T或S取代,从而形成NxT/S糖基化基序。在一些实施方案中,N是表面暴露的。如以下实施例中所示,增加了糖基化的突变可以提供包含RSV F多肽的多肽的增加表达。基于修饰对RSV F多肽的特性的改变
对RSV F的氨基序列的修饰可以改变RSV F多肽的特性。RSV F多肽的特性可以包括RSV F多肽的任何结构或功能特征。
在一些实施方案中,对氨基酸序列的单一修饰改变了RSV F多肽的多种特性。在一些实施方案中,RSV F多肽可以包含改变RSV F多肽的不同特性的多种修饰。在一些实施方案中,多种修饰产生了RSV F多肽的特性的更大变化。
在一些实施方案中,多种修饰可以对特定特性具有累加作用。例如,与任一单一氨基酸取代相比,用于添加聚糖的两个氨基酸取代可以产生RSV F多肽的糖基化的更大增加。
在一些实施方案中,多种修饰影响RSV F多肽的不同特性。例如,可以进行一个或多个氨基酸取代以增加糖基化,同时进行一个或多个氨基酸取代以阻止还原。
在一些实施方案中,对RSV F多肽的修饰使得融合前构象稳定化。
在一些实施方案中,修饰使得融合前RSV F的位点0表位(也称为抗原性位点0)稳定化,如例如在McLellan等人,Science340(6136):1113-1117(2013)中所述。在一些实施方案中,使得位点0表位稳定化的修饰是原体间稳定化的。在一些实施方案中,使得位点0表位稳定化的修饰使得融合前F稳定化,如通过位点0和位点V结合所测量的,所述位点0和位点V结合如分别通过与抗体D25或AM14的结合而测量。
在一些实施方案中,修饰增加了RSV F在表达系统中的表达。在一些实施方案中,修饰增加了RSV F在表达系统中的分泌。在一些实施方案中,修饰增加了重组RSV F在表达后的稳定性。这种变化可以存在于任何类型的表达系统,如细菌、真菌、昆虫或哺乳动物中。
在一些实施方案中,与其他构建体相比,引入脯氨酸的氨基酸取代增加了表达。在一些实施方案中,与其他构建体相比,添加聚糖的氨基酸取代增加了表达。在一些实施方案中,与其他构建体相比,将K或R取代为其他氨基酸的氨基酸取代增加了表达。表达的可观察到的增加可以由增加发酵运行或其他产生过程的产量的任何机制导致,包括相对抑制蛋白酶切割或降解和/或增加在宿主细胞或细胞外环境中的稳定性。在一些实施方案中,与其他构建体相比,将RSV F的HRB区域中的一个或多个K残基取代为其他氨基酸的氨基酸取代增加了表达。
在一些实施方案中,将K取代为其他氨基酸的氨基酸取代增加了RSV F多肽的稳定性。在一些实施方案中,将RSV F的HRB区域中的一个或多个K残基取代为其他氨基酸的氨基酸取代增加了RSV F多肽的稳定性。在一些实施方案中,这种增加的稳定性归因于蛋白酶切割的减少。
在一些实施方案中,RSV F包含去除二硫化物(例如以防止还原后的缀合)的一个或多个突变。在一些实施方案中,I217P取代阻止了RSV F多肽的减少。在一些实施方案中,将K取代为其他氨基酸的氨基酸取代阻止了在还原剂的存在下RSV F多肽的还原。
在一些实施方案中,与其他构建体相比,单链构建体增加了表达。
在一些实施方案中,RSV F多肽包含DS-CAV1序列(SEQ ID NO:525)(如例如在McLellan,J.S.等人,Science 342(6158):592-598(2013)中所述)。在一些实施方案中,RSVF多肽包含其中进行进一步修饰(例如,包括以上所述的至少一个、两个或三个天冬酰胺)的DS-CAV1的序列。
b)RSV G多肽
如本文所用,RSV G多肽可以包含RSV G的整个序列或RSV G的一部分。与野生型序列相比,RSV G多肽可以包含修饰。在一些实施方案中,RSV G多肽是与野生型RSV G(SEQ IDNO:527)相比经修饰的RSVG。在一些实施方案中,这些修饰是与野生型RSV G相比对RSV G多肽的氨基酸的改变。
在一些实施方案中,RSV G多肽包含RSV G的胞外结构域(SEQ ID NO:528或对应于其的位置)的全部或一部分。在一些实施方案中,RSV G多肽包含Gcc区域(RSV G(SEQ IDNO:527)的氨基酸151-193)的全部或一部分。在一些实施方案中,RSV G多肽包含CX3C基序。在一些实施方案中,RSV G多肽结合CX3CR1受体。Gcc区域既是保守的又是免疫原性的,因此可以用于引发对RSV株系具有广泛活性的抗体。在一些实施方案中,提供了RSV Gcc株系A,如SEQ ID NO:536中所示。在一些实施方案中,提供了RSV Gcc株系B,如SEQ ID NO:537中所示。
在一些实施方案中,RSV G多肽未被糖基化。例如,RSV G多肽可以由于N或S/T残基的截短或突变(例如分别变为Q或A)或其组合而缺乏NXS/TX糖基化位点。
在一些实施方案中,RSV G多肽可以缀合至如本文所述的铁蛋白,如经由铁蛋白上的表面暴露的半胱氨酸进行。在一些实施方案中,此铁蛋白纳米颗粒是还包含RSV F多肽的融合蛋白,如上文所述的包含RSV F多肽和铁蛋白蛋白的任何多肽。
D.示例性组合物、试剂盒、核酸、用途和方法
在一些实施方案中,本发明提供了针对病原体感染免疫受试者的方法。本发明进一步提供了在受试者中引发针对病原体的免疫应答的方法。在一些实施方案中,本方法包括向受试者给予有效量的本文所述的药物组合物。在一些实施方案中,本方法包括向受试者给予有效量的本文所述的抗原性铁蛋白多肽或纳米颗粒。
在一些实施方案中,将本文所述的组合物给予至受试者(包括人)以对他们进行免疫而免受病原体感染。在一些实施方案中,本文所述的组合物用于在对受试者(如人)进行免疫中使用。在一些实施方案中,所给予的组合物包含含有SEQ ID NO:1-76、301-343、401-403、410、413-414、417-427或501-523中的任一个的序列的多肽。在一些实施方案中,给予使得针对流感、EBV、RSV或疏螺旋体属免疫。
同样,可以给予组合物以产生对针对将来的感染的保护性免疫应答。在一些实施方案中,将来的感染是流感、EBV、RSV或疏螺旋体属感染。
在一些实施方案中,保护性免疫应答降低了住院的发生率。在一些实施方案中,在组合物包含流感多肽的情况下,保护性免疫应答降低了实验室确认的流感感染的发生率。在一些实施方案中,在组合物包含EBV多肽的情况下时,保护性免疫应答降低了EBV感染、单核细胞增多症、由单核细胞增多症引起的并发症(例如肝炎、脑炎、重度溶血性贫血或脾肿大)、鼻咽癌、胃癌或B淋巴瘤(包括伯基特淋巴瘤或霍奇金淋巴瘤)的发生率。在一些实施方案中,在组合物包含RSV多肽的情况下,保护性免疫应答降低了RSV、肺炎、细支气管炎或哮喘感染的发生率。在一些实施方案中,在组合物包含疏螺旋体属多肽的情况下,保护性免疫应答降低了急性或慢性莱姆病(包括关节发炎、神经系统症状、认知缺陷或心律不齐)的发生率。
1.受试者
在一些实施方案中,受试者是哺乳动物。在一些实施方案中,受试者是人。
在一些实施方案中,受试者是成人(大于或等于18岁)。在一些实施方案中,受试者是儿童或青少年(小于18岁)。在一些实施方案中,受试者是老年人(大于60岁)。在一些实施方案中,受试者是非老年人(大于或等于18岁且小于或等于60岁)。
在一些实施方案中,向受试者给予多于一次的组合物给予。在一些实施方案中,加强免疫给予改善了免疫应答。
在一些实施方案中,本文所述的抗原性多肽或组合物中的任何一种或多种用于在哺乳动物,如灵长类动物(例如,非人灵长类动物,如猴子(例如,猕猴,如恒河猴或食蟹猴)或猿)、啮齿动物(例如,小鼠或大鼠)或驯养的哺乳动物(例如,犬、兔、猫、马、绵羊、牛、山羊、骆驼或驴)中使用。在一些实施方案中,本文所述的抗原性多肽或组合物中的任何一种或多种用于在鸟类,如禽类(例如,鸡、火鸡、鸭、鹅、豚鼠或天鹅)中使用。
2.佐剂
如本文所述,佐剂可以经由表面暴露的氨基酸例如半胱氨酸缀合至铁蛋白。非缀合的佐剂也可以与本文所述的抗原性铁蛋白多肽一起给予至受试者。在一些实施方案中,与在不伴有佐剂的情况下给予单独的非铁蛋白多肽或单独的抗原性铁蛋白多肽相比,与抗原性铁蛋白多肽一起给予佐剂在受试者中产生更高效价的针对非铁蛋白多肽的抗体。佐剂可以促进对抗原性多肽的更早、更强效或更持久的免疫应答。
在一些实施方案中,组合物包含一种佐剂。在一些实施方案中,组合物包含多于一种佐剂。在一些实施方案中,组合物不包含佐剂。
在一些实施方案中,佐剂包含铝。在一些实施方案中,佐剂是磷酸铝。在一些实施方案中,佐剂是明矾(Alyhydrogel’85 2%;Brenntag–目录号21645-51-2)。
在一些实施方案中,佐剂是有机佐剂。在一些实施方案中,佐剂是油基佐剂。在一些实施方案中,佐剂是水包油纳米乳剂。
在一些实施方案中,佐剂包含角鲨烯。在一些实施方案中,包含角鲨烯的佐剂是Ribi(Sigma adjuvant system目录号S6322-1vl)、AddavaxTM MF59、AS03或AF03(参见US9703095)。在一些实施方案中,包含角鲨烯的佐剂是纳米乳剂。
在一些实施方案中,佐剂包含聚丙烯酸聚合物(PAA)。在一些实施方案中,包含PAA的佐剂是SPA09(参见WO 2017218819)。
在一些实施方案中,佐剂包含非可代谢油。在一些实施方案中,佐剂是不完全弗氏佐剂(IFA)。
在一些实施方案中,佐剂包含非可代谢油和杀死的结核分枝杆菌。在一些实施方案中,佐剂是完全弗氏佐剂(CFA)。
在一些实施方案中,佐剂是脂多糖。在一些实施方案中,佐剂是单磷酰A(MPL或MPLA)。
3.药物组合物
在各种实施方案中,提供了药物组合物,所述药物组合物包含本文所述的抗原性铁蛋白多肽和/或相关实体。在一些实施方案中,药物组合物是能够引发免疫应答(如针对病原体的保护性免疫应答)的免疫原性组合物(例如,疫苗)。
例如,在一些实施方案中,药物组合物可以包含以下项中的一种或多种:(1)抗原性铁蛋白蛋白,所述抗原性铁蛋白蛋白包含(i)用半胱氨酸置换表面暴露的氨基酸的突变和(ii)非铁蛋白多肽;(2)抗原性铁蛋白蛋白,所述抗原性铁蛋白蛋白包含(i)用半胱氨酸置换表面暴露的氨基酸的突变和连接至所述半胱氨酸的免疫刺激部分;和(ii)非铁蛋白多肽;(3)抗原性铁蛋白蛋白,所述抗原性铁蛋白蛋白包含(i)表面暴露的半胱氨酸,(ii)在铁蛋白蛋白的N末端的肽接头,和(iii)在肽接头的N末端的非铁蛋白多肽;(4)抗原性铁蛋白蛋白,所述抗原性铁蛋白蛋白包含:(i)用半胱氨酸置换表面暴露的氨基酸的突变和连接至所述半胱氨酸的免疫刺激部分,(ii)用非半胱氨酸氨基酸置换在幽门螺杆菌铁蛋白的位置31处的内部半胱氨酸的突变,或用非半胱氨酸氨基酸置换如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中与位置31类似的位置处的内部半胱氨酸的突变,(iii)用非天冬酰胺氨基酸置换表面暴露的天冬酰胺的突变,和(iv)非铁蛋白多肽;或(5)包含前述铁蛋白蛋白中的任一种的铁蛋白颗粒。
在一些实施方案中,本发明提供了药物组合物,所述药物组合物包含与本文所述的抗原性多肽相关的抗体或其他药剂。在一个实施方案中,药物组合物包含与本文所述的抗原性多肽结合和/或竞争的抗体。可替代地,抗体可以识别包含本文所述的抗原性多肽的非铁蛋白多肽组分的病毒颗粒或细菌。
在一些实施方案中,将如本文所述的药物组合物单独给予或与一种或多种增强免疫应答的药剂(例如,以上所述的佐剂)组合给予。在一些实施方案中,药物组合物进一步包含如上所述的佐剂。
在一些实施方案中,药物组合物进一步包含药学上可接受的载体或赋形剂。如本文所用,术语“载体”是指与药物组合物一起给予的稀释剂、佐剂、赋形剂或媒介物。在示例性实施方案中,载体可以包括无菌液体,例如像水和油,包括石油、动物、植物或合成起源的油,例如像花生油、大豆油、矿物油、芝麻油等。在一些实施方案中,载体是或包括一种或多种固体组分。药学上可接受的载体还可包括但不限于盐水、缓冲盐水、右旋糖、甘油、乙醇及其组合。如本文所用,赋形剂是可以包含在药物组合物中例如以提供或有助于所希望的稠度或稳定作用的任何非治疗剂。合适的药物赋形剂包括但不限于淀粉、葡萄糖、乳糖、蔗糖、明胶、麦芽、稻、面粉、白垩、硅胶、硬脂酸钠、单硬脂酸甘油酯、滑石、氯化钠、脱脂乳粉、甘油、丙烯、二醇、水、乙醇等。在各种实施方案中,药物组合物是无菌的。
在一些实施方案中,药物组合物含有少量的润湿剂或乳化剂、或pH缓冲剂。在一些实施方案中,药物组合物可以包含多种添加剂(如稳定剂、缓冲液或防腐剂)中的任何一种。此外,可以包含辅助剂、稳定剂、增稠剂、润滑剂和着色剂。
在各种实施方案中,可以将药物组合物配制成适合任何所期望的给予方式。例如,药物组合物可以采取以下形式:溶液、悬浮液、乳剂、滴剂、片剂、丸剂、球剂、胶囊、含有液体的胶囊、明胶胶囊、粉末、缓释配制品、栓剂、乳剂、气雾剂、喷雾剂、悬浮液、冻干粉、冷冻悬浮液、干燥粉或任何其他适合使用的形式。在药剂的配制和生产中的一般考虑可以见于例如Remington’s Pharmaceutical Sciences,第19版,Mack Publishing Co.,宾夕法尼亚州伊斯顿,1995(通过引用并入本文)中。
可以经由任何给予途径来给予药物组合物。给予途径包括例如口服、皮内、肌内、腹膜内、静脉内、皮下、鼻内、粘膜、硬膜外、舌下、鼻内、脑内、阴道内、透皮、经直肠、通过气管内滴注、支气管滴注、吸入、或局部方式。给予可为局部或全身的。在一些实施方案中,给予是口服进行的。在另一个实施方案中,给予是通过肠胃外注射。在一些情况下,给予导致本文所述的抗原性铁蛋白多肽释放到血流中。给予方式可以由从业者决定。
在一些实施方案中,药物组合物适合于肠胃外给予(例如静脉内、肌内、腹膜内和皮下)。可以将此类组合物配制成例如溶液、悬浮液、分散体、乳剂等。它们也可以以无菌固体组合物(例如冻干的组合物)的形式生产,所述无菌固体组合物可以在临使用前溶解或悬浮于无菌可注射介质中。例如,肠胃外给予可以通过注射来实现。在此类实施方案中,注射剂以常规形式制备,即作为液体溶液或悬浮液、适合于在注射前溶解或悬浮于液体中的固体形式、或作为乳剂。在一些实施方案中,注射溶液和悬浮液由无菌粉末、冻干粉末或颗粒制备。
在另一个实施方案中,将药物组合物配制成用于通过吸入递送(例如,用于直接递送至肺和呼吸系统)。例如,组合物可以采取鼻喷雾剂或任何其他已知的气雾剂配制品的形式。在一些实施方案中,用于吸入或气雾剂递送的制剂包含多个颗粒。在一些实施方案中,此类制剂可以具有约1、约2、约3、约4、约5、约6、约7、约8、约9、约10、约11、约12或约13微米的平均粒度。在一些实施方案中,用于吸入或气雾剂递送的制剂被配制为干粉。在一些实施方案中,用于吸入或气雾剂递送的制剂例如通过包含润湿剂而被配制为湿粉。在一些实施方案中,润湿剂选自水、盐水或其他处于生理pH的液体。
在一些实施方案中,将根据本发明的药物组合物以滴剂的形式给予至鼻腔或颊腔。在一些实施方案中,剂量可以包含多滴(例如1-100、1-50、1-20、1-10、1-5滴等)。
可以将本发明的药物组合物以适合于实现所期望结果的任何剂量给予。在一些实施方案中,所期望的结果是诱导针对病原体的持久的适应性免疫应答,所述病原体如存在于组合物中的抗原性铁蛋白多肽中的非铁蛋白多肽的来源。在一些实施方案中,所期望的结果是降低一种或多种感染症状的强度、严重程度、频率和/或延迟一种或多种感染症状的发作。在一些实施方案中,所期望的结果是抑制或预防感染。所需的剂量将根据以下而在受试者之间有所不同:受试者的物种、年龄、体重和一般状况,被预防或治疗的感染的严重程度,所使用的特定组合物及其给予方式。
在一些实施方案中,将根据本发明的药物组合物以单一剂量或多个剂量给予。在一些实施方案中,将药物组合物在不同日期以多个剂量给予(例如初免-加强免疫疫苗接种策略)。在一些实施方案中,将药物组合物作为加强免疫方案的一部分给予。
在各种实施方案中,将药物组合物与一种或多种另外的治疗剂共同给予。如果治疗剂的给予的时间安排使得另外的治疗剂和药物组合物中的一种或多种活性成分的药理活性在时间上重叠,从而发挥组合的治疗作用,则共同给予不需要同时给予治疗剂。通常,每种药剂将以针对所述药剂确定的剂量和时间表来给予。
4.核酸/mRNA
还提供了核酸,所述核酸编码本文所述的抗原性多肽。在一些实施方案中,核酸是mRNA。出于本公开文本的目的,任何能够经历翻译而产生多肽的核酸被认为是mRNA。
5.试剂盒
本文还提供了试剂盒,所述试剂盒包括本文所述的一种或多种抗原性多肽、核酸、抗原性铁蛋白颗粒、抗原性2,4-二氧四氢喋啶合酶颗粒、组合物或药物组合物。在一些实施方案中,试剂盒进一步包括溶剂、溶液、缓冲液、说明书或干燥剂中的一种或多种。
***
此描述和示例性实施方案不应被视为是限制性的。为了本说明书和所附权利要求的目的,除非另有指示,否则在说明书和权利要求中使用的所有表达数量、百分比或比例的数字和其他数值应被理解为在所有情况下被术语“约”修饰至已无法将其如此修饰的程度。“约”指示实质上不影响所述主题的特性的变化程度,例如在10%、5%、2%或1%之内。因此,除非有相反的指示,否则以下说明书和所附权利要求中阐述的数值参数是近似值,所述近似值可以根据试图获得的所需特性而变化。在最低限度并且不试图限制对权利要求范围的等价范围的原则的应用,每个数值参数均应当至少考虑报吿的有效数字的数量和通过应用普通四舍五入技术来解读。
注意,如本说明书和所附权利要求所用,单数形式“一个/种(a、an)”和“所述(the)”以及任何词语的任何单数使用包括复数个指示物,除非明确地并且清楚地限于一个/种指示物。如本文所用,术语“包括”及其语法变体旨在是非限制性的,使得列表中项目的详述不排除可以取代或添加到所列项目的其他类似项目。除非上下文另有指示,否则词语“或”以包括性含义使用,即等同于“和/或”。
实施例
提供以下实施例以说明某些公开的实施方案,并且不应解释为以任何方式限制本公开文本的范围。
实施例1.OspA-铁蛋白抗原性多肽的制备
产生了包含OspA和铁蛋白的抗原性多肽。
由Genescript从以下序列合成OspA:博氏疏螺旋体株系B31(血清型1)NBCI序列IDWP_010890378.1、阿氏疏螺旋体株系PKO(血清型2)NCBI序列:WP_011703777.1、伽氏疏螺旋体株系PBr(血清型3)GenBank:CAA56549.1、巴伐利亚疏螺旋体(血清型4)NCBI序列WP_011187157.1、伽氏疏螺旋体(血清型5)GenBank CAA59727.1、伽氏疏螺旋体(血清型6)GenBank:CAA45010.1和伽氏疏螺旋体(血清型7)GenBank CAA56547.1。由Genescript合成了具有插入的N末端牛蛙铁蛋白序列的幽门螺杆菌铁蛋白,其中牛蛙铁蛋白序列与先前研究的相似(参见Kanekiyo,M.等人,Cell162(5):1090-100(2015))。将pet21a载体用于在大肠杆菌中表达带有His标签的OspA和OspA-铁蛋白纳米颗粒。将类似于先前使用的哺乳动物表达载体用于在Expi293细胞中表达(参见Xu,L.等人,Science 358(6359):85-90(2017))。
OspA-铁蛋白纳米颗粒是通过将OspA的胞外结构域在基因上融合至铁蛋白的氨基末端以产生抗原性多肽而产生的(图1A)。OspA是具有延伸的β-折叠结构的31-kDa脂蛋白,所述β-折叠结构由仅具有一个羧基末端α-螺旋的21个连续的反平行β链组成(图1B)(参见Kitahara,R.等人,Biophys J102(4):916-26(2012))。OspA的羧基末端还具有异常大的空腔(约200A),所述空腔代表了对于使用甘氨酸-丝氨酸序列与铁蛋白的连接具有相容性的位点(图1B)。铁蛋白的24个亚基自发组装成空心球形纳米颗粒(图1C)。本研究中使用的铁蛋白含有融合至幽门螺杆菌铁蛋白以产生与人铁蛋白最小相关的嵌合体的牛蛙铁蛋白氨基末端序列(参见Kanekiyo 2015)。氨基末端牛蛙铁蛋白序列从纳米颗粒核心呈放射状突出(参见Trikha,J.等人J Mol Biol248(5):949-67(1995)),从而有利于OspA在纳米颗粒表面上均匀地呈递。
对铁蛋白结构进行了三个另外的改变以改善其功能性:N19Q、C31S和S111C。N19Q取代去除了潜在的氨基末端糖基化位点。S111C取代在铁蛋白上引入了表面暴露的半胱氨酸,所述表面暴露的半胱氨酸可用于例如通过点击化学来缀合佐剂。最后,将半胱氨酸31修饰为丝氨酸,使得仅一个半胱氨酸将通过缀合被修饰。OspA在纳米颗粒表面上的展示提供了一种24聚体抗原性纳米颗粒(图1D)。
对于从大肠杆菌中的纯化,我们使用了BL21 Star(DE3)(Invitrogen目录号C601003)。我们在16℃下用100μM IPTG诱导蛋白质过夜。在Tris缓冲液(pH 8)、50mM NaCl中使用超声处理来裂解细胞沉淀物。通过从流穿液中收集OspA-铁蛋白,在阴离子交换柱(HiTrap Q HP,GE)上纯化过滤器灭菌的上清液。然后通过重复6次的1%Triton X114提取去除内毒素。然后使用Amicon 100MW截止过滤器(Millipore目录号UFC910096)浓缩水相,然后将纳米颗粒在120ml Superose 6制备型SEC柱上在4℃下进一步纯化。对于从哺乳动物细胞培养物中的纯化,按照制造商的说明书,使用FectoPRO转染试剂(Polyplus,目录号116-100)用质粒DNA转染Expi293细胞。培养转染的细胞,并且在第5天收集并过滤上清液。使用无内毒素的试剂和玻璃器皿来遵循无内毒素的方案。将Q琼脂糖快速流动珠(GE,目录号17-0510-01)用50mM Tris(pH 7)、50mM NaCl制备,并且将其通过重力流施加至过滤器灭菌的上清液。收集流穿液并且使用Amicon 100MW截止过滤器将其浓缩至4ml。然后在室温下在120ml Superose 6制备型SEC柱上进一步纯化纳米颗粒。
对于带有His6标签(SEQ ID NO:442)的OspA的纯化,将血清型1、4、5和7OspA从大肠杆菌BL21(DE3)(Invitrogen目录号C600003)中纯化,并且将血清型2和3从Expi293细胞中纯化。这些构建体缺乏跨膜结构域,包含C末端His6-标签(SEQ ID NO:442),并且否则为野生型。对于大肠杆菌纯化,将蛋白质在500μM IPTG下诱导5小时,并且将细胞沉淀并在-20℃下冷冻。将沉淀物重悬于在具有完全蛋白酶抑制剂(Sigma-Aldrich,目录号11697498001)的TBS缓冲液中的1%Triton中,并且超声处理以裂解细胞。将上清液过滤灭菌。对于哺乳动物细胞培养,在转染后第5天收集上清液并将其过滤除菌。将上清液在附接到AKTA Pure FPLC的GE HiTrap HP 5ml柱(目录号17-5248-02)上运行。将柱洗涤并对其加载,并且再次用在TBS中的20mM咪唑洗涤。将最终蛋白质用在TBS中的250mM咪唑洗脱。
在转化的人肾上皮细胞系Expi293中由融合至铁蛋白的博氏疏螺旋体株系B31表达OspA血清型1(图2A至图2D;SEQ ID NO:52)。通过尺寸排阻柱色谱(SEC)和SDS-PAGE(分别为图2A和图2B)确认了纳米颗粒的形成和蛋白质的纯度。SEC分析揭示了预期保留时间的单一对称峰(图2A)。
还进行了动态光散射(DLS)分析。将纯化的纳米颗粒以约0.4μg/ml的浓度加载至具有透明底部的黑色384孔板(Corning,目录号3540)中。用DynaPro板读取器II(Wyatt)在25℃的控制温度下读取样品。DLS显示颗粒大小为13nm并具有纯且无聚集体的低多分散性(7.4%)(图2C)。消除含有脂化位点的OspA跨膜结构域(aa 1-25)提高了纯化的容易性。OspA序列含有四个潜在的氨基连接的糖基化位点,并且从哺乳动物细胞中纯化的OspA-铁蛋白迁移在更高的分子量处,这与聚糖的添加一致(图2B)。
对OspA-铁蛋白纳米颗粒进行了透射电子显微镜负染色成像和2D类别平均化分析(图2D)。将OspA-铁蛋白纳米颗粒样品在1xTBS中稀释300倍,并且在由400目铜网格上的硝化纤维素支撑的连续碳层上成像。通过以下方式来制备网格:将3μl样品悬浮液施加至清洁的网格上,用滤纸吸干掉,并立即用甲酸铀酰染色。使用配备有FEI Eagle 4k x 4K CCD相机的FEI Tecnai T12电子显微镜进行电子显微镜检查。以67,000(0.16nm/像素)的放大倍率获取高放大倍率图像。图像是在-1.9μm至-0.8μm的标称弱焦点和约的电子剂量下获取的。使用自动拾取方案选择67,000x高放大倍率图像中的单独颗粒(参见Lander,G.C.等人,J Struct Biol,166(1):95-102(2009))。基于XMIPP处理软件包使用了无参考比对策略(参见Sorzano,C.O.等人,J Struct Biol 148(2):p.194-204(2004))。此包中的算法将选择的颗粒进行比对,并将其分选为自相似的组或类。
铁蛋白纳米颗粒显现为在中间具有空心中心的强圆形密度(图2D)。每个纳米颗粒都被多个短而均匀的OspA刺突包围,所述刺突的形状显现为微椭圆形。颗粒的总直径在约的范围内,具有直径的铁蛋白核心。刺突从颗粒表面在大小、形状和取向上均匀地延伸,长度多达 OspA刺突的宽度为约并且在铁蛋白的甘氨酸-丝氨酸接头处渐缩至最小密度。
当LYMErixTM疫苗在2002年停用时,引起了人们的关注,即疫苗含有与来自人白细胞功能相关抗原-1(hLFA-1,参见Gross,D.M.等人,Science 281(5377):第703-6页(1998))的九肽区段(SEQ ID NO:78)具有同源性的表位(SEQ ID NO:83的氨基酸165-173)(图5A)。SEQ ID NO:83的氨基酸165-173称为hLFA-1同源位点。OspA血清型1是唯一含有此序列同源性的血清型(图5B)。为避免与此序列有关的任何潜在问题,将hLFA-1同源位点置换为相应的OspA血清型2(SEQ ID NO:79)或血清型3(SEQ ID NO:80)九肽序列,或引入降低与hLFA-1的相似性并旨在防止与hLFA-1结合的抗体的产生的点取代(RD2,SEQ ID NO:81)(图5C)。对于点取代,取代了表面暴露的氨基酸以降低与hLFA-1的相似性,同时避免或最小化β-折叠结构的去稳定化。
在小鼠中测试了具有修饰的hLFA-1同源位点的hLFA-1纳米颗粒的免疫原性,以相对于未经这种修饰的OspA-铁蛋白纳米颗粒比较免疫应答(图5D)。由具有修饰的hLFA-1同源性位点的纳米颗粒引发的抗体效价是稳健的,并且与具有未修饰的hLFA-1同源性位点的纳米颗粒没有显著差异。
实施例2.对OspA-铁蛋白纳米颗粒的免疫原性的表征
为了评估OspA-铁蛋白纳米颗粒的免疫原性,用在Ribi佐剂的存在下的血清型1OspA-铁蛋白纳米颗粒或莱姆(博氏疏螺旋体的纯化的外表面蛋白A(OspA)的液体悬浮液)(一种其中OspA是全长、脂化、重组且为血清型1的犬类疫苗)免疫C3H小鼠两次(图4)。在第0周和第4周对C3H/HeN小鼠进行肌内疫苗接种。对第2剂量后2周对血清进行ELISA。将Ribi(Sigma adjuvant system目录号#S6322-1vl)重悬于1ml PBS中并且涡旋1分钟,然后在免疫之前以等体积添加至抗原。
使用酶联免疫吸附测定(ELISA)确定对重组OspA的抗体应答。简而言之,将96孔板用在PBS中稀释的1μg/ml OspA-His包被,并且在4℃下孵育过夜。去除OspA-His并用溶解于PBST中的5%脱脂乳封闭板。去除封闭试剂后,将原始血清样品在PBST中连续稀释后进行添加。将原始样品以等体积添加至封闭溶液,以实现最终50%封闭溶液浓度。孵育1小时后,将板用PBST洗涤,并在室温下与山羊抗小鼠IgG,即HRP连接的二抗(在封闭溶液中的1:5,000稀释液)一起孵育1小时。抽吸并洗涤二抗,并将板与Sure Blue TMB过氧化物酶底物(KPL,马里兰州盖瑟斯堡)一起孵育,之后与等体积的终止溶液(0.5N硫酸)一起孵育。在450nm下测量吸光度。
实施例3.糖基化突变体;功效的评价
为了评价此OspA-铁蛋白的保护性功效,使用了攻击模型,其中将免疫或对照小鼠通过携带博氏疏螺旋体的蜱虫进行感染(参见Rosa,P.A.等人Nat Rev Microbiol 3(2):第129-43页(2005))。
用与AddaVaxTM 1:1混合的1μg OspA-铁蛋白纳米颗粒或1μg铁蛋白纳米颗粒对C3H/HeN小鼠进行肌内疫苗接种。在第0周和第4周对小鼠进行疫苗接种。使用具有对hLFA-1同源性位点的合理设计修饰和去除所有潜在N-糖基化位点的修饰的血清型1OspA-铁蛋白纳米颗粒(SEQ ID NO:53)对小鼠进行免疫,因为天然细菌表达的OspA在这些位置处没有糖基化。所述序列含有以下N>Q取代以防止糖基化:N71Q、N190Q、N202Q和N251Q。其免疫原性与糖基化纳米颗粒相似(图13)。
也测试了当将糖基化位点丝氨酸/苏氨酸突变为丙氨酸时的OspA-铁蛋白的糖基化突变体(SEQ ID NO:63)。与具有野生型糖基化位点的OspA-铁蛋白(SEQ ID NO:52)相比,此构建体和以上讨论的N>Q构建体二者均给出了强的免疫应答,并且优于莱姆对照(图14)。
在评价OspA-铁蛋白纳米颗粒在蜱虫攻击模型中的保护性功效的进一步实验中,肩突硬蜱(Ixodes scapularis)蜱幼虫从俄克拉荷马州立大学(Oklahoma StateUniversity)(俄克拉荷马州斯蒂尔沃特)的国家蜱虫研究和教育中心获得。通过将未感染的幼虫在博氏疏螺旋体株系N40感染的SCID小鼠上喂养至饱食,来产生博氏疏螺旋体感染的若虫。收集饱血的幼虫,并且使其在室温和高相对湿度下在4-6周内蜕变为若虫。通过培养每批中回收的蜱虫的一部分来确定所喂养幼虫中的博氏疏螺旋体感染的流行性。
在第0周和第4周,用1μg剂量的伴有AddaVaxTM佐剂的OspA-铁蛋白(SEQ ID NO:53)或对照铁蛋白对小鼠免疫两次,并用莱姆来平行免疫比较组。通过将5至6只博氏疏螺旋体感染的若虫蜱喂养至饱食,在第6周(即,第二次疫苗接种剂量后2周)对小鼠进行攻击。收集喂养的若虫,并通过在BSK培养基中培养来测定博氏疏螺旋体感染。攻击后两周,处死小鼠并通过耳部、踝部和心脏培养物测定博氏疏螺旋体感染。通过暗视野显微镜观察培养物来确定博氏疏螺旋体的存在。如果通过暗视野显微镜发现一种或多种器官培养物为阳性,则将小鼠定义为感染了博氏疏螺旋体。也通过特定于博氏疏螺旋体的PCR来测试阴性培养物。
两周后处死小鼠。将来自心脏、踝部和耳部的组织样品在BSK培养基中与针对博氏疏螺旋体的抗生素一起培养6周。通过PCR测试阴性样品中博氏疏螺旋体的存在。所有阴性培养物均为PCR阴性。以未感染小鼠的百分比计算保护。
与阴性对照铁蛋白(其中5只动物中有4只被感染)形成对比,包含OspA-铁蛋白和AddaVaxTM佐剂的组合物未显示出感染(0/4)(表5;p<0.01)。
表5:OspA-铁蛋白纳米颗粒的保护性功效
实施例4.对与免疫刺激部分缀合的OspA-铁蛋白的功效的评价
通过在铁蛋白纳米颗粒的表面上工程化半胱氨酸(S111C)来产生自佐剂化构建体,所述半胱氨酸允许通过点击化学直接缀合免疫刺激部分,如TLR激动剂(图6A)或CpG(SEQ ID NO:210;ISS-1018,图7A)。直接缀合的程序如下:用50mM Tris(pH 8.5)中的10mMTCEP(Amresco K831-10G)还原哺乳动物产生的物质1小时以去除半胱氨酰化(cysteinylation)。然后将蛋白质透析到100mM Tris(pH 8)、50mM NaCl中以去除TCEP。不需要对大肠杆菌产生的物质进行还原。将DBCO-PEG4-马来酰亚胺接头(Sigma-Aldrich目录号760676-5mg)以5mg/ml重悬于DMSO中。将2.5mg接头添加至10ml体积中的3mg蛋白(最终DMSO浓度为5%)。将接头与还原的蛋白质在室温下孵育30分钟。使用Ambicon 100MW截止过滤浓缩器通过缓冲液交换(Millipore目录号UFC910096)来去除过量的接头。将叠氮化物-PEG4-3M-012(自行合成)和叠氮化物-CPG(由IDT定制合成的ISS-1018)用于最终点击化学步骤。将0.5mg佐剂添加至0.5mg蛋白质中以进行最终的缀合步骤,并且在37℃下孵育6小时,然后在4℃下孵育过夜。使用Ambicon 100MW截止过滤浓缩器通过缓冲液交换来去除过量的佐剂。通过针对3M-012的质谱和针对CPG的SDS-PAGE分析确认了缀合效率。
使用了TLR 7/8激动剂3M-012,先前已经显示其在直接缀合至HIV Gag蛋白时增加抗体应答(参见Wille-Reece,U.等人,Proc Natl Acad Sci U S A 102(42):第15190-4页(2005))。使用两步式点击化学方法将3M-012附接至SEQ ID NO:53的纳米颗粒。首先,将DBCO-PEG4-马来酰亚胺接头连接至半胱氨酸,然后通过无铜的叠氮化物-炔烃环加成来添加具有PEG4-叠氮化物接头的修饰的3M-012(图6A)。通过质谱确认了>99%的缀合效率,其质量移位为587道尔顿(图12)。除了叠氮化物-3M-012,还成功添加了叠氮化物-CPG(图7A),可以通过凝胶移位来确认其缀合(图7B)。
观察到铁蛋白的几乎完全缀合,这表明大多数纳米颗粒携带24个激动剂分子。然后评估缀合的OspA铁蛋白纳米颗粒在小鼠中的免疫原性。在第0周和第4周对C3H/HeN小鼠进行肌内疫苗接种。对第2剂量后2周对血清进行ELISA。在免疫前,将明矾(Alyhydrogel’852%;Brenntag–目录号21645-51-2)以等体积添加至抗原。将Ribi(Sigma adjuvant system目录号#S6322-1vl)重悬于1ml PBS中并且涡旋1分钟,然后在免疫之前以等体积添加至抗原。
用3M-012缀合的颗粒免疫的小鼠产生了比未缀合材料高4.5倍的OspA抗体应答(图6B,p<0.05)。与摩尔当量量的3M-012(29ng)混合的颗粒相比并且相比于与高1,000倍的剂量(20μg)的3M-012或标准明矾(Alyhydrogel'85 2%;Brenntag–目录号21645-51-2)佐剂混合的颗粒,由3M-012缀合的颗粒引发的抗体应答更高。
对于CPG缀合的OspA-铁蛋白纳米颗粒(SEQ ID NO:53)观察到了类似的抗体产生增强,与未缀合的颗粒相比,免疫应答增加6.3倍,并且相对于与纳米颗粒混合的等量的未缀合CPG,增加了4.7倍(图7C)。
因此,缀合至OspA-铁蛋白纳米颗粒的佐剂的靶向递送使得佐剂的量大大减少,同时刺激了有效且特异性的抗体应答。
实施例5.对包含不同血清型的OspA-铁蛋白纳米颗粒的免疫原性的评价
虽然血清型1OspA株系博氏疏螺旋体在美国引起疾病,而阿氏疏螺旋体(血清型2)、伽氏疏螺旋体(血清型3、5、6、7)和巴伐利亚疏螺旋体(血清型4型)在欧洲、亚洲和其他地方引起疾病。为了产生广泛的交叉保护性组合物,设计针对血清型1、2、3、4、5和7的OspA-铁蛋白纳米颗粒。(SEQ ID NO:1、5、6、7、8和10)。使用阴离子交换和尺寸排阻色谱从大肠杆菌中表达并纯化这些颗粒(图3A)。所有OspA-铁蛋白抗原性多肽均具有47kDa的预期分子量,并且DLS分析和透射电子显微镜也确认了所有六种OspA纳米颗粒的形成(图3B)。
通过以等摩尔比例组合OspA-铁蛋白的血清型1-5和7中的每一种来产生六组分组合物。
将伴有明矾的六组分组合物(即六价)的免疫原性在小鼠中与伴有相同佐剂的单血清型颗粒(即单价)进行比较(图8A至图8F)。将单价组合物以1μg剂量给予,并且将六价组合物以每种血清型1μg(共6μg剂量)给予。在免疫前,将明矾(Alyhydrogel’85 2%;Brenntag–目录号21645-51-2)以等体积添加至抗原。六组分组合物诱导针对OspA血清型1-5和7的所有六种的稳健抗体应答。此外,对单一血清型对照的应答与混合物相似,这表明六种血清型组合之间没有干扰。相对于单组分组合物,在六价组合物的情况下看到改善的针对血清型4的免疫应答(参见图8D,血清型4)。
在确定六价组合物是免疫原性的,并且在一些情况下优于单价组合物后,制备六种OspA-铁蛋白纳米颗粒中的每一种的3M-012和CpG缀合物。通过将六种与3M-012缀合的OspA-铁蛋白纳米颗粒组合,以及单独地将与CpG缀合的六种OspA-铁蛋白纳米颗粒组合,产生两种六组分缀合组合物。对于全球范围内发现的所有七种OspA血清型,相比于未缀合的六价组合物,CpG缀合的和3M-012缀合的六价组合物在小鼠中显示出抗体应答的显著增加(图9A至图9G),这表明六价配制品也赋予针对血清型6的保护,即使组合物中没有OspA血清型6多肽。
当在非人灵长类动物(NHP[恒河猴])中进行测试时,伴有AF03佐剂的六价纳米颗粒组合物(未缀合的)产生的针对所有七种循环疏螺旋体属血清型的Ab效价为莱姆对照的11至200倍(图10A至图10G)。与小鼠相似,六价组合物在佐剂的存在下引发高效价Ab应答。在NHP中,3M-012和CpG缀合的组合物诱导与莱姆对照类似的应答(分别将图10A-G与图10H-N进行比较)。六价疫苗在NHP中的抗体效价是稳健的,直至加强免疫剂量后的19周,并且保留了相比于莱姆对照的优势(图25)。
还将缀合组合物在蜱虫攻击模型中进行测试。在第0周和第4周以1μg剂量的抗原对小鼠进行疫苗接种。单价组合物含有1μg与3M-012缀合的OspA-铁蛋白血清型1。六价组合物包含1μg的来自血清型1、2、3、4、5和7的OspA,每种OspA与3M-012缀合。在第二次免疫后两周,用感染博氏疏螺旋体N40菌株(血清型1)的5-6只蜱虫攻击小鼠5天,并且两周后将所述小鼠处死。将来自心脏、踝部和耳部的组织样品在BSK培养基中与针对博氏疏螺旋体的抗生素一起培养6周。通过PCR测试阴性样品中博氏疏螺旋体的存在。阳性样品是对于培养或PCR呈阳性的。(图11)。
另外,我们在小鼠中测试含有所有七种血清型的七价疫苗。在第0周和第4周用以下项肌内对小鼠进行免疫:用明矾或AF03佐剂化的含有1ug对应于OspA血清型1-7的每种OspA-铁蛋白纳米颗粒的七价OspA-铁蛋白纳米颗粒组合物(共7ug),或莱姆(1μg剂量)。免疫后2周经由通过ELISA测量的终点效价来分析抗体应答。与相比,展示出稳健的免疫应答(图24A-G)。
因此,OspA-铁蛋白纳米颗粒引发对七种主要血清型的高效价抗体应答。此外,七组分莱姆疫苗候选物提供了控制莱姆病的全球蔓延的潜力。
实施例6:对具有不同柔性接头的OspA-铁蛋白构建体的表征
测试了若干种不同的接头,以提供在OspA与铁蛋白之间的柔性。构建体在一至五个-GGGS-(SEQ ID NO:443)序列内变化。纯化各种接头构建体并形成均匀大小的纳米颗粒。
包含GS1(GGGS)(SEQ ID NO:443)、GS2(SEQ ID NO:91)或GS5(SEQ ID NO:92)接头的OspA-接头-铁蛋白构建体全部可以表达(图15A),并且显示出一致的DLS(图15B、图15C和图15E)和EM(图15D)概况。
此外,不同的-GGGS-接头构建体(“GGGS”公开为SEQ ID NO:443)(接头1x GGGS(“1x GGGS”公开为SEQ ID NO:443)[SEQ ID NO:60],接头2x GGGS(“2x GGGS”公开为SEQID NO:444)[SEQ ID NO:61],和接头5x GGGS(“5x GGGS”公开为SEQ ID NO:445)[SEQ IDNO:62])均在C3H小鼠中显示出强的免疫应答(图16)。
实施例7:对2,4-二氧四氢喋啶合酶OspA纳米颗粒的表征
研究了另一种纳米颗粒,来自风产液菌的2,4-二氧四氢喋啶合酶来用于OspA的抗原性展示。通过阴离子交换和尺寸排阻色谱容易地从大肠杆菌细胞中纯化出包含不同血清型的OspA-2,4-二氧四氢喋啶合酶颗粒。产生并表征了包含以下项的构建体:OspA血清型1(SEQ ID NO:12,图19A至图19C);OspA血清型2(SEQ ID NO:16,图20A至图20C);OspA血清型3(SEQ ID NO:17,图21A至图21B);OspA血清型4(SEQ ID NO:18,图17A至图17C);OspA血清型5(SEQ ID NO:19,图22A至图22C);和OspA血清型7(SEQ ID NO:21,图23A至图23C)。OspA-2,4-二氧四氢喋啶合酶颗粒根据EM,形成的是15.8nm颗粒,并且根据DLS,大小是均匀的。
在小鼠中测试了OspA血清型4 2,4-二氧四氢喋啶合酶颗粒(SEQ ID NO:18)的免疫原性(图18)。伴有和不伴有明矾的OspA 2,4-二氧四氢喋啶合酶颗粒产生了强的免疫应答,所述免疫应答显现至少与相似的OspA血清型4铁蛋白纳米颗粒(SEQ ID NO:7)的免疫应答一样稳健。
因此,包含2,4-二氧四氢喋啶合酶和OspA多肽的抗原性多肽也可以用于引发抗OspA抗体应答。
实施例8:对HA-铁蛋白纳米颗粒的设计、纯化和表征
通过以下方式来产生HA纳米颗粒(HA-Np):将HA胞外结构域序列(缺乏48个C端跨膜残基)融合至铁蛋白的N末端以产生在哺乳动物细胞中自组装的纳米颗粒。铁蛋白包含用半胱氨酸置换表面暴露的氨基酸的突变(由相对于SEQ ID NO:208的铁蛋白序列的S26C、A75C或S111C突变产生),以允许将佐剂缀合至HA-Np上。这种半胱氨酸的表示呈现于图27中。
由上文所述的突变产生的半胱氨酸可用于缀合免疫刺激部分。图28A说明了使用马来酰亚胺-PEG4-SM7/8a点击试剂将TLR激动剂缀合至铁蛋白的示例性1步式点击化学反应的结果。在此反应中,使马来酰亚胺与不成对半胱氨酸反应,以经由中间接头将TLR7/8激动剂分子在表面暴露的半胱氨酸处共价缀合至铁蛋白,从而产生共价的TLR7/8-激动剂-铁蛋白缀合物。在此例子中,指示了在一个单体的表面上的一个半胱氨酸。铁蛋白纳米颗粒是多聚体,例如由24个单体组成。因此,铁蛋白纳米颗粒可以包含等于单体数量的表面暴露的半胱氨酸数量,并且每个表面暴露的半胱氨酸可以被缀合。
图28B和图29A至图29B说明了可以用于将佐剂缀合至铁蛋白纳米颗粒的示例性2步式点击化学,并且说明了CpG和3M-012(有时也称为3M012)也可经由中间双官能接头通过2步式点击化学反应缀合至铁蛋白的方式。示例性接头是含有马来酰亚胺和DBCO反应性基团的Sigma PEG接头(目录号760676)。在此例子中,TLR激动剂被反应性叠氮化物基团官能化。
将质谱(MS)用于以下所述的实验中,以表征伴有和不伴有缀合的免疫刺激部分的流感-铁蛋白。在一些情况下,进行MS的分析物是流感-铁蛋白的胰蛋白酶消化物。胰蛋白酶通常会在赖氨酸和精氨酸残基之后切割,除非在之后是脯氨酸时不切割。然而,结构化的纳米颗粒(在所指示的胰蛋白酶位点的C末端)是抗蛋白水解的。在图30中指示了在天然条件下牛蛙-幽门螺杆菌铁蛋白构建体(如SEQ ID NO:314)中的可以被胰蛋白酶切割的最远(C末端)胰蛋白酶位点。因此,胰蛋白酶消化物释放出适于MS分析的抗蛋白水解的铁蛋白颗粒。
因此,在接头序列是胰蛋白酶可接近的情况下,可以使用胰蛋白酶消化之后进行简化的MS分析(而不管未切割多肽中存在的N末端抗原如何),以评价与纳米颗粒的缀合。设计此方法以克服糖蛋白抗原对MS分析造成的复杂性。例如,H1/茎-Np原本只有在PNGase处理后才可以通过MS分析(图33A)。
将来自以下流感株系的HA序列与幽门螺杆菌-牛蛙杂合铁蛋白的N末端在基因上融合,以构建HA-纳米颗粒:A/蒙茅斯堡/1-JY2/1947(GenBank CY147342,氨基酸1-518,Y108F);A/马来西亚/302/1954(GenBank CY009340.1,氨基酸1-518,Y108F);A/丹佛/1957(GenBank CY008988,氨基酸1-517,Y108F);A/香港/117/1977(GenBank CY009292,氨基酸1-518,Y108F);A/新喀里多尼亚/20/99(GenBank AHJ09883.1,氨基酸1-518);A/加利福尼亚/4/2009(GenBank AHJ09884.1,氨基酸1-518);COBRA P1(美国专利公开案US20150017196A1中的SEQ ID NO:302,氨基酸1-518,Y108F)和COBRA X6(美国专利公开案US20140127248A1,氨基酸1-517,Y108F)。COBRA P1和COBRA X6是通过分层序列平均化的计算方法产生的(Carter DM,等人,J Virol 90:4720-4734(2016))。COBRA X6是从跨越1999-2012年的人H1N1流感序列产生的,并且COBRA P1是从跨越1933-1957年和2009-2011的人H1N1株系加上来自1931-1998年的猪H1N1流感株系产生的(Carter 2016)。将HA-铁蛋白基因克隆到SIB002载体的XbaI/BamHI位点中以进行哺乳动物表达,在ATG起始密码子前面具有gccacc kozak序列。对所有序列进行密码子优化以在人细胞系中表达。
将HA-Np质粒用Powerprep试剂盒(Origene目录号NP100009)纯化,并用于转染Expi293细胞(ThermoFisher目录号A14635)。将FectoPRO DNA转染试剂(Polyplus#116-100)在标准条件(0.5μg DNA/mL,0.75μl FectoPRO试剂/mL和0.45μl增强剂/mL)下使用。转染后4-6天,通过在4度下以3,488g离心15min从Expi293上清液收获纳米颗粒,并且将其通过0.45μm真空驱动的过滤器单元(Thermo Scientific目录号167-0045)进行过滤。使HA-Np通过重力流通过Q-Sepharose快速流动柱(GE目录号17051001),并且收集流穿液并将其用水稀释3倍,并且通过添加终浓度为50mM的Tris缓冲液(pH 8.5)来调节pH;或将上清液用缓冲液A(50mM Tris pH 8.5,5mM NaCl)稀释5倍,而不使用初始Q-琼脂糖柱。然后将样品加载至Q-琼脂糖柱(HiTrap Q HP,GE目录号17115401),并在NaCl梯度上洗脱蛋白质,其中使用缓冲液A(50mM Tris pH 8.5,5mM NaCl)和缓冲液B(50mM Tris,pH 8.5,1M NaCl)的0%-60%混合,经30个柱体积。收集HA-纳米颗粒蛋白质级分,并用Amicon Ultra-15离心过滤器装置(Millipore目录号UFC910024)浓缩,并且通过尺寸排阻色谱用Superose 6柱PG XK16/70,60-65cm(目录号:90100042)在磷酸盐缓冲液中进一步纯化。将最终的级分浓缩并通过0.22μm过滤器(Millipore SLGV004SL)过滤灭菌。使用无内毒素的溶液,并且使用带有LAL盒的Charles Rivers Endosafe PTS仪器对最终蛋白质进行测试,检测极限为0.05EU/ml。
示出了H1/茎-Np(SEQ ID NO:343,图31A)和H5/COBRA-Np(SEQ ID NO:332,图31B)的胰蛋白酶消化。在两种情况下,在胰蛋白酶消化的情况下(以“+”表示)的分子量移位对应于SM7/8a的分子量(711道尔顿)。因此,这些数据表明SM7/8a与包含表面暴露的半胱氨酸的铁蛋白纳米颗粒成功缀合。
在使用PNGase去除H1/茎-Np的糖基化而未经胰蛋白酶处理的凝胶移位实验(图32A)中,与低分子量分子(如马来酰亚胺-PEG4-SM7/8a)缀合后铁蛋白纳米颗粒重量变化的分辨率是不清楚的。如图32B所示,胰蛋白酶处理允许通过凝胶移位测定确认小分子如SM7/8a与H1/Stem-Np的缀合。可以通过去糖基化H1/Stem-Np的凝胶移位测定(图32A),以及还通过在天然条件下通过胰蛋白酶消化从H1/茎-Np释放的铁蛋白纳米颗粒的凝胶移位测定观察到更高分子量的分子(例如CpG)的缀合。因此,在天然条件下使用胰蛋白酶消化铁蛋白纳米颗粒提供一种表征与TLR激动剂缀合的核心片段的方法作为平台技术,所述核心片段原本可能难以在对于具有可能干扰凝胶移位或质谱(MS)实验的特性的给定抗原上通过这些分析测定来分析。
将SM7/8a-PEG4-马来酰亚胺缀合至H1/茎-Np并仅出于分析目的进行PNGase处理之后,在MS上看到质量为42930Da的缀合产物,其比未缀合的H1/茎-Np重约715kDa(图33A)。胰蛋白酶消化后,减小的铁蛋白纳米颗粒的重量为19510Da(基于纳米颗粒的H1/茎部分的切割)(图33B)。缀合后,胰蛋白酶消化的缀合纳米颗粒的重量也更重约715kDa。因此,图33A和图33B二者均支持在将包含佐剂的接头与铁蛋白纳米颗粒缀合中约100%的缀合效率。
在2步式点击化学反应中,将马来酰亚胺-PEG4-DBCO接头缀合至H1/茎-Np,其中马来酰亚胺与铁蛋白纳米颗粒上的表面暴露的半胱氨酸反应,在胰蛋白酶消化后通过MS分析看到与接头添加的分子量(大约675Da)一致的重量增加(图34)。
接下来,将叠氮化物-CpG添加至H1/茎-Np-PEG4-DBCO中间体(在图35中标记为“Mal-PEG4-DBCO之后”),将其通过凝胶移位测定来确认。叠氮化物-CpG从IDT订购(SEQ IDNO:345)。在SDS-PAGE之前,将缀合物和对照用PNGase处理。与接头缀合相比,由于增加的质量(约7.5kDa),CpG缀合引起向上的凝胶移位。在图36中示出了通过对标记为“茎-Np-CpG”和“茎-Np”的两个条带的密度测定而定量的50%缀合效率的例子。茎-Np是H1/茎-Np(SEQID NO:343)。未处理是指还原前的H1/茎-Np。TCEP还原的是指在室温下用3mM TCEP处理1小时并在4℃下用PBS透析过夜的H1/茎-Np。
也将烟草蚀纹病毒(TEV)蛋白酶切割位点(SEQ ID NO:344)用于评价缀合。使用2步式点击化学方法,将3M-012缀合至各种NC99HA-TEV-Np构建体(SEQ ID NO:309-312)。用2或10mM TCEP还原HA-TEV-Np构建体。通过透析(具有10kDa MWCO的3mL透析盒,Thermo#87730)至TRIS缓冲液(100mM TRIS pH 8.0,50mM NaCl)中来去除TCEP。添加DBCO-PEG4-马来酰亚胺接头(Sigma#760676)。在也缓冲液交换至PBS 7.4中的同时,用超滤(100kDaMWCO,Millipore Amicon#UFC810024或#UFC910096)去除过量的接头。最后,将叠氮化物官能化的TLR激动剂(CpG或3M-012)点击到分子上。通过超滤(100kDa MWCO,MilliporeAmicon#UFC810024或#UFC910096)或凝胶过滤去除过量的药物。HA-TEV-Np中的TEV切割位点允许TEV选择性切割以便分析缀合。
在将3M-012(约500Da+约600Da接头)缀合至HA-TEV-Np构建体之后,用TEV处理构建体。TEV切割后,在凝胶移位SDS-PAGE上所得的HA-条带为约57kDa加上聚糖和Ferr约20kDa(图36,标记为“+TEV”的泳道)。约20和21kDa的双条带(分别标记为“S26C”、“S72C”、“A75C”和“S111C”(分别为SEQ ID NO:310、311、312和309)的泳道)指示成功的缀合。缀合效力对应于条带强度,其中较低的条带是未缀合的而上面的条带是缀合的铁蛋白。
发现包含S111C的H1/茎-Np在293Expi细胞中表达时具有109道尔顿的翻译后修饰(与半胱氨酰化一致)(图37A),所述翻译后修饰通过以下方式而去除:在室温下用3mM浓度下的TCEP(三(2-羧乙基)膦)还原1小时以释放出反应性硫醇(图37B)。因此,可以还原修饰以将表面暴露的半胱氨酸暴露为游离硫醇,所述游离硫醇对商业接头或定制的小分子上的马来酰亚胺基团具有高反应性。
MS数据也确认了3M-012与HA-Np的成功缀合。HA-TEV-Np-S26C(SEQ ID NO:310;图37C)、A75C(SEQ ID NO:312;图37D)或S111C(SEQ ID NO:309;图37E)。包含A75C和S111C铁蛋白修饰的纳米颗粒(分别为SEQ ID NO:312和309)显示出与3M-012的大于95%缀合率。因此,MS数据指示,佐剂可以与由铁蛋白中突变产生的各种表面暴露的半胱氨酸连接,从而成功产生与佐剂连接的抗原性铁蛋白多肽。
负染色电子显微镜(EM)确认缀合不会影响纳米颗粒完整性。示出了单独的H1/茎-Np(SEQ ID NO:343)(图38A)、与马来酰亚胺-PEG4-SM7/8a缀合的H1/茎-Np(图38B)、与CpG缀合的H1/茎-Np(图38C)、单独的NC99 HA-Np(SEQ ID NO:309)(图38D),经由DBCO-马来酰亚胺接头与3M-012缀合的NC99 HA-Np(图38E)和经由DBCO-马来酰亚胺接头与CpG缀合的NC99 HA-Np(图38F)。此外,与未缀合的H1/茎-Np相比(图39C),将TLR7 8激动剂(马来酰亚胺-PEG4-SM7/8a,图38A)或经由马来酰亚胺-PEG4-DBCO接头将TLR9激动剂(CpG,图38B)缀合至H1/茎-Np不影响纳米颗粒完整性,如通过动态光散射(DLS)测量的。
这些数据证明了包含铁蛋白和HA多肽的抗原性多肽的成功制备。此外,可以将包含佐剂的接头成功地缀合至这些铁蛋白纳米颗粒。
实施例9:对HA-铁蛋白纳米颗粒组合物的免疫原性的表征
评估了各种佐剂和将TLR激动剂与H1/茎-Np缀合对H1/茎-Np组合物的免疫原性的影响。图40A示出了通过用H1/茎-Np TLR7/8-激动剂缀合物免疫诱导的针对H1/新喀里多尼亚/1999(NC99)HA三聚体的IgG抗体效价。在第0周和第3周用10μg H1/茎-Np进行给药,将所述H1/茎-Np在不伴有佐剂的情况下、在伴有等摩尔掺合的游离SM7/8a佐剂(83.3ng)的情况下、在伴有掺合的高剂量游离SM7/8a佐剂(21.84μg)的情况下、或在伴有1:1体积比的PAA或AF03佐剂的情况下进行给予。在不存在任何其他佐剂的情况下给予H1/茎-Np-SM7/8a缀合物。在第二次剂量后2周测定血清。图40B出了通过用H1/茎-Np TLR9-激动剂缀合物免疫诱导的针对H1/茎三聚体的IgG抗体效价。在第0周和第3周用10μg H1/茎-Np进行给药,将所述H1/茎-Np在不伴有佐剂的情况下、在伴有等摩尔掺合的游离CpG佐剂(850ng)的情况下、在伴有掺合的高剂量游离CpG佐剂(20μg)的情况下、或在伴有1:1体积比的AF03佐剂的情况下进行给予。在不存在任何其他佐剂的情况下给予H1/茎-Np-CpG缀合物。在第二次剂量后2周测定血清。
图40A中的数据表明,SM7/8a-缀合的H1/茎-Np显示出与掺合有聚丙烯酸(PAA)或AF03佐剂的未缀合的纳米颗粒可比的免疫原性。直接缀合至铁蛋白纳米颗粒的SM7/8a比作为与铁蛋白纳米颗粒分开的化合物给予的等摩尔剂量的SM7/8a(“等摩尔混合”)更有效。此外,直接缀合至铁蛋白纳米颗粒的SM7/8比作为与铁蛋白纳米颗粒分开的化合物给予的更高剂量的SM7/8a(“高混合”)更有效。因此,SM7/8a与包含HA多肽和铁蛋白的抗原性多肽的缀合使得所述化合物具有免疫原性和自我佐剂化。给予自佐剂化组合物可以允许减少或消除单独的佐剂。类似地,图40B表明,与未缀合的和等摩尔掺合的对照相比,TLR9激动剂CpG与H1/茎-Np的缀合将其免疫原性改善至与给予23倍高剂量的掺合CpG分子可比的水平。
还在体外评估了血清中和H1/新喀里多尼亚/1999(NC99)HA/NA假型化慢病毒的能力。如先前所述进行假型化中和测定(Kanekiyo等人,Nature 499:102-106(2013))。简而言之,通过用Profection哺乳动物转染试剂盒(Promega目录号E1200)转染5种质粒,即400ngHA、100ng NA、50ng TMPRSS2、7μg CMVΔR8.2和7μg pHR'CMV-Luc,将慢病毒包装在HEK293T细胞中。转染后48和72小时收集病毒颗粒,并且将其通过0.45μm过滤器过滤。
以三周的间隔对小鼠(n=5/组)免疫两次。将与3M-012缀合的NC99 HA-Np(SEQ IDNO:309)(HA-Ferr-3M-012,0.22μg/剂量)与以下掺合对照平行给予:NC99 HA-Np(0.22μg/剂量)和10μg 3M-012(典型的治疗剂量)的混合物,以及单独地,NC99 HA-Np(0.22μg/剂量)和1.7ng3M-012(缀合物的等摩尔匹配物)的混合物。另外的对照是以匹配的HA含量(0.17μgHA/剂量)投配的未缀合NC99 HA-Np和灭活流感疫苗(IIV)。在第5周,测定来自这些小鼠的血清的连续稀释物对用来自所指示株系的HA和神经氨酸酶(NA)基因假型化的慢病毒的中和活性。将一系列稀释度下的抗血清与固定量的慢病毒一起预孵育,并用于感染靶293A细胞。72小时后用Promega萤光素酶测定系统(目录号E1500)定量感染。使用Graphpad Prism软件根据这些中和曲线计算IC50值,以确定达到50%PsV中和的血清稀释因子。还分别在第5周和第8周测定终点效价(ELISA)和血凝抑制(HAI)效价。关于示例性ELISA和HAI程序,参见以下实施例。一式三份地运行所有样品。
基于ELISA终点效价(图41A)和假病毒中和IC50效价(图41B),与匹配的掺合物、未缀合的颗粒或IIV相比,与3M-012缀合的NC99 HA-Np诱导更强的结合和中和抗体应答。HA-Np-3M-012缀合物还诱导了比等摩尔掺合物对照显著更强的HAI效价(图41C)。另外,HAI效价比未缀合的HA-Ferr和IIV高3.7和1.6倍,但是这些结果并不显著。
还在非人灵长类动物模型中评估了H1/茎-Np-TLR激动剂缀合物的免疫原性。将十二只食蟹猴(长尾猕猴)由Bioqual公司依照所有联邦法规(包括USDA法规和动物福利法)饲养和照管。对动物进行预筛选并且通过ELISA选择对2016-2017年Fluzone四价抗原(A/加利福尼亚/07/2009;A/香港/4801/2014X-263B;B/普吉岛/3073/2013;B/布里斯班/60/2008)缺乏反应性的动物。将5至13岁、体重3.5kg至7.8kg的NHP受试者(10只雌性,2只雄性)随机分配到每个免疫组(n=3只动物/组)。使每个组在第0、4和10周接受三次剂量:50μg伴有AF03的H1-SS-np或200μg H1-SS-np(无佐剂对照)、或200μg H1-SS-np-SM7/8缀合物、或200μg H1-SS-np-CpG。在第0、2、4、6、8、10和12周收集10mL血液样品用于血清分离。在第0、2、5、6和12周收集10-16mL的血液样品用于PBMC分离。按照标准操作程序分离并低温保存血清和PBMC。食蟹猴被分配为在第0、4和10周用以下项免疫:50μg与掺合的AF03佐剂一起配制的H1/茎-Np、或200μg H1/茎-Np(无佐剂对照)、或200μg H1/茎-Np-SM7/8a缀合物(图28A中所示的)或200μg H1/茎-Np-CpG缀合物(图28B中所示的)。测定在各个时间点分离的血清的根据ELISA得出的抗HA抗体效价(图50A),以及所述血清对用H1亚型HA和NA(图50B)或用H5亚型HA和NA亚型(图25C)假型化的慢病毒的中和作用。合在一起,图50A-C中所示的结果证明,TLR激动剂的缀合改善了H1/茎-Np在非人灵长类动物模型中的免疫原性。在此模型中,TLR7/8激动剂缀合物显现比CpG缀合物产生更高的效价,并且AF03掺合佐剂在测试条件下引发最高的效价。
与掺合对照(HA-Np(0.22μg/剂量)和20μg CpG(典型的治疗剂量)的混合物,以及HA-ferr(0.22μg/剂量)和21ng CpG(缀合物的等摩尔匹配物)的混合物)相比,还评估了与CpG缀合的NC99 HA-Np(SEQ ID NO:309)(HA-Ferr-CpG,0.22μg/剂量)的免疫原性。另外的对照是以匹配HA含量(0.17μg HA/剂量)投配的未缀合HA-Np和IIV。如上所述,在第0周和第3周给药。ELISA和PsV测定是对于加强免疫后2周的血清进行的,并且在加强免疫后5周对血清进行HAI。一式三份地运行所有样品。
基于ELISA终点效价(图42A)或假病毒中和IC50效价(图42B),与匹配的掺合物、未缀合的颗粒或IIV相比,缀合物诱导更强的结合和中和抗体应答。HA-Np-CpG缀合物诱导了比等摩尔掺合物对照显著更强的HAI效价(图42C)。另外,HAI效价比未缀合的HA-Ferr和IIV高2.6和3.0倍,但是这些结果并不显著。
接下来,确定当以较高剂量给予时3M012缀合物的免疫原性是否可以改善。为此,以0.1μg、0.5μg、2.5μg和12.5μg剂量的HA-NP测试缀合物、等摩尔掺合物、较高剂量掺合物和未缀合的纳米颗粒(图51A-B)。在0.1μg和0.5μg HA-NP剂量下,在中和和HAI测定中看到最小应答,除了高掺合物剂量。在2.5μg剂量下,未缀合的HA-NP以及HA-NP与3M012的等摩尔掺合物二者诱导了最小的抗体应答。与高剂量掺合物组相比,3M012缀合的HA-NP尽管含有少>5000倍的3M012,但诱导相似的抗体应答,这证明了直接缀合和TLR激动剂靶向递送的功效。
实施例10:通过EM和DLS对包含候选多肽的纳米颗粒的表征
使用上文概述的方法表达图26A中所呈现的包含流感多肽的HA-Np,并将其释放到培养基中(在图26A中示出HA部分的序列比对和在图26B中示出系统树图)。图26B中的箭头指示候选多肽。通过阴离子交换和尺寸排阻色谱从293Expi细胞培养上清液中纯化图43A中列出的HA-Np。在图43B中示出了确认纳米颗粒的成功产物的考马斯染色结果。
电子显微镜(EM)和动态光散射(DLS)分析如下进行。
动态光散射是在25℃下在Wyatt的DynaPro板读取器II上测量的。纯化的HA-Np显示出根据动态光散射在16与18纳米之间的预期大小(图43A,通过“大小”度量指示)。还通过负染色透射电子显微镜(TEM)确认了纳米颗粒的形成(图43C)。对于EM,将HA-铁蛋白纳米颗粒样品吸附至碳涂覆网格持续1分钟,所述碳涂覆网格已通过暴露于辉光放电30秒而变得亲水。用滤纸(Whatman#1)去除过量的液体,并用0.75%甲酸铀酰将样品染色30秒。用滤纸去除多余的甲酸铀酰后,在TecnaiG2 Spirit BioTWIN中检查网格,并使用AMT 2k CCD相机记录图像。
实施例11:单一株系HA-铁蛋白纳米颗粒针对一组代表性的相异H1N1流感病毒的免疫原性
为了研究来自特定病毒株系的HA-Np的免疫原性,用来自目的株系的纳米颗粒对小鼠免疫两次,并在第二次免疫后3周使用血凝素抑制测定(HAI)来测定血清。所有免疫均遵循用于动物处理的既定准则。在第0周和第3周,用220ng HA-铁蛋白纳米颗粒(HA含量为170ng HA)免疫Balb/C小鼠(5只/组),并且所述HA-铁蛋白纳米颗粒在适用时在临肌内注射(每只后肢50μL)之前与佐剂1:1混合。如图例中所指示,使用Ribi(Sigma AdjuvantSystem,目录号S6322-1vl)或AF03(Sanofi Pasteur)。对于二价、三价和四价组合,在注射前将220ng的每种纳米颗粒预先混合。在加强免疫注射后2周和3周收集血清。
HA抑制测定(HAI)使用的流感种子原液来自美国疾病控制与预防中心(Centersfor Disease Control and Prevention)(美国乔治亚州亚特兰大)。通过用三份酶稀释一份血清用受体破坏酶(RDE)对免疫血清进行预处理,并且在37℃水浴中孵育过夜。通过在56℃下孵育30分钟、之后添加六份PBS至1/10的最终稀释度来使酶失活。在V型底96孔微量滴定板中进行HAI测定,所述微量滴定板具有在0.5%火鸡红细胞中的4个病毒HA单位(HAU)。将HAI效价确定为导致血凝完全抑制的最高血清稀释度。
对于所有数据,误差棒表示通过测定来自给定治疗组中每只动物的样品获得的平均值的标准误差;对于小鼠,n=5,并且对于雪貂,n=12。学生T检验是使用MicrosoftExcel计算的。方差分析是使用VassarStats(可通过网站在vassarstats.net/anova1u.html获得)计算的。
使用了跨越78年的病毒进化的一组16种代表性流感株系。所述组中的病毒列于表2中。
表2:用于HAI的H1N1流感株系组
| H1N1 HAI流感组 |
| A/波多黎各/1934 |
| A/Weiss/1/1943 |
| A/FM/1/1947 |
| A/丹佛/1/1957 |
| A/新泽西州/8/1976 |
| A/USSR/90/1977 |
| A/巴西/11/1978 |
| A/智利/1/1983 |
| A/台湾/1/1986 |
| A/德克萨斯州/36/1991 |
| A/北京/262/1995 |
| A/新喀里多尼亚/20/1999 |
| A/所罗门群岛/6/2006 |
| A/布里斯班/59/2007 |
| A/加利福尼亚/07/2009 |
在所有情况(CA09、NC99、FM47和HK77,图44A至图44D)下均观察到匹配株系的强效中和。
也通过ELISA确认了针对匹配抗原的血清学应答(图45A至图45F)。给予至每个组的免疫原列于图45A中。将三聚体用于ELISA,如通过图45B至图45F所指示的。
对于ELISA测定,将Nunc MaxiSorp 96孔板(目录号44-2404-21)在4℃下用100ng/孔三聚体HA或稳定化的茎蛋白包被过夜,并用在PBST中的5%脱脂乳封闭。如所指示那样稀释抗血清并在室温下孵育1小时,并且用也在室温下孵育1小时的在5%乳-PBST中的抗小鼠HRP抗体(目录号NA931,在1:5,000下)或抗猴HRP抗体(Southern Biotech目录号4700-05,批号A3814-P907,在1:5,000下)检测结合的抗体。用PBST洗涤5次后,用SureBlueTMB底物(目录号52-00-02)对HRP进行显色,并用0.5N硫酸终止。在450nm(Spectramax M5)下读取吸光度。终点效价是使用Graphpad prism以0.2的阈值和0.05的典型背景水平计算的。
还如上所述那样评价HA/NA假型化慢病毒的中和作用,并将结果示于表3中。在所有测试的情况下,对于匹配株系均观察到强的中和活性,并将这些值用作阈值。具有互补中和活性的HA-Np的组合以加和方式导致扩大的交叉反应性。
表3:用作为单一组分或组合给予的HA-铁蛋白纳米颗粒进行两次免疫后,小鼠中针对HA/NA假型化慢病毒(PsV)的中和IC50
CA09 HA-Np引发了强的免疫应答,但这些限于当代(2009年后)株系和也源自猪并且与CA09具有紧密同源性的1976年分离物(图44A)(参见Gaydos等人2006.Emerg InfectDis 12:23-28(1976))。NC99 HA-Np引发了针对从1990年代末至2000年代初的流感病毒的强效中和作用(图44B)。对FM47 HA-Np的免疫应答主要扩展到匹配的株系,但是它还显示出与1977年株系的中度交叉反应性(图44C)。这种水平的交叉反应性与1977年暴发(其主要影响26岁以下的人群)具有临床相关性,这表明暴露于来自1940-50年暴发的流感病毒赋予了针对1977年株系的保护(Kilbourne 2006)。有趣的是,在HA序列中,HK77 HA-Np脱颖而出,因为其交叉反应性扩展到来自1947、1978和1983年的株系(图44D)。另一方面,对MAL54 HA-Np和DV57 HA-Np的免疫应答限于匹配的株系(图44E、图44F和表3)。
用COBRA P1和COBRA X6纳米颗粒观察到的交叉反应性与其病毒样颗粒(VLP)对应物一致(参见Carter DM等人,J Virol 90:4720-4734(2016))。由COBRA P1 HA-Np引发的免疫应答与CA09 HA-Np相似(图44A和图44G),并且COBRA X6 HA-Np显示出与NC99 HA-Np相似的免疫概况(图44B和图44H)。
实施例12:HA-铁蛋白纳米颗粒的单价、二价、三价和四价配制品
评价了由选择的HA-Np的组合引发的HAI交叉反应性。用通过组合单独的纳米颗粒制备的二价、三价或四价配制品如上所述那样免疫和测试小鼠。相对于任一种单价组合物,NC99和CA09 HA-Np的二价组合显示出扩大的交叉反应性(图46A)。然而,此二价组合并未引发针对来自1934-1957年和1977-1991年的较早相异株系的可检测抗体效价。COBRA X6和COBRA P1二价组合的免疫原性遵循相同趋势(图46B)。与NC99/CA09二价组合物相比,此组合显示出增加的广度,但针对若干种株系的HAI效价是中等的。对于三价组合,当第三组分是FM47 HA-Np(图46C)或HK77 HA-Np(图46E)时,将第三组分包含到NC99和CA09 HA-Np中会增加交叉反应性,但MAL54HA-Np(图46D)并未增强广度。与NC99、CA09和HK77 HA-Np的三价组合相比,在四价配制品中添加第四组分不会导致另外的可观察到的交叉反应性(图46F至图46H)。
当使用不同的佐剂(即,Ribi对比AF03,图47A至图47F)时观察到可比较结果。重要的是,没有证据表明由共同给予不同的HA-Np引起的抗原性竞争。这些数据表明,对于在其单独的HAI概况中存在高度互补性的情况,交叉反应性概况是加和性的。还测量了用作为使用归一化剂量的HA的由蛋产生的灭活流感疫苗(IIV)递送的NC99和CA09免疫原获得的HAI概况(图48A至图48C)。
实施例13:在雪貂中用纳米颗粒组合物进行的针对攻击的保护
在与人类疾病相关的动物模型雪貂中测试了某些HA-Np组合的功效。用磷酸盐缓冲液(图49A)、CA09灭活的流感疫苗(IIV,图49B)、野生型HA-Np的三价组合(NC99+CA09+HK77,图49C)或COBRA P1+COBRA X6+HK77 HA-Np的组合(图49D)对雪貂(n=12/组)进行免疫。肌内注射之前,将这些组合物与AF03佐剂1:1混合,实现1ml最终注射体积。
两次免疫后,观察到针对匹配的株系的显著HAI效价(图49B至图49D)。用纳米颗粒组合免疫的两组雪貂均显示出针对FM47、HK77和NC99的显著HAI效价。如在小鼠中观察到的,CA09 IIV未在雪貂中引发针对FM47和HK77株系的交叉中和效价(图49B)。
免疫后,将雪貂用不匹配的相异株系H1/蒙茅斯堡/1947病毒攻击。在第二次免疫后4周通过以下方式来进行流感攻击:用1ml的A/蒙茅斯堡/1/1947病毒以50%组织培养物感染剂量(TCID50)的104.65倍进行鼻腔接种。每日跟踪临床症状,持续2周,并且在攻击后7天内每日收集鼻洗液并且通过标准TCID50测定测试其病毒载量。攻击后,从鼻洗液中定量病毒效价。接受三价NC99+CA09+HK77或COBRA-P1+X6+HK77纳米颗粒组合的雪貂群组比对照组更快地清除病毒,从而在感染后第5天显示出显著降低的病毒效价(图49E,p≤0.001)。相比之下,CA09 IIV免疫组未比PBS免疫对照组显著更快地清除病毒。在所有组中,FM47株系成功复制,并在感染后不超出一周被清除。因此,在与人类疾病相关的感染动物模型中,三价组合刺激了也针对相异病毒攻击进行保护的有效HAI应答。
实施例14:引发针对EBV的抗体的抗原性EBV多肽
开发了引发针对EBV的抗体的抗原性多肽。开发了以单链展示EBV gL和gH多肽的自组装铁蛋白纳米颗粒,并评价了这些纳米颗粒在小鼠中的免疫原性。
表达和纯化单体和三聚体gL/gH构建体。图52A示出了通过考马斯和蛋白质印迹(抗His)分析得出的单链gL和gH单体(SEQ ID NO:406)+/-His标签切割。图52B示出了以吸光度迹线并通过考马斯得出的gL和gH三聚体(SEQ ID NO:411)在SEC柱上的分级分离,以及确认由凝血酶蛋白酶进行的His标签切割的蛋白质印迹。对于SEQ ID NO:406构建体,样品的最终浓度为1mg/mL,总体积为15mL,并且内毒素水平为1.48EU/mL。
表达和纯化了单链gL/gH铁蛋白纳米颗粒(SEQ ID NO:414)。图53A至53E示出了对其通过6SEC分级分离(53A)、SEC级分的考马斯(53B)、用抗铁蛋白一级Ab对SEC级分进行的蛋白质印迹(53C)、动态光散射(DLS,53D)和电子显微镜(53E)进行的纯化和表征。
融合至铁蛋白的单链EBV gL和gH的示例性构建体示出在图54中。用于免疫刺激部分(如toll样受体7/8激动剂(TLR7/8a))的缀合位点可以存在于铁蛋白上或接头中(对于示例性序列,参见例如SEQ ID NO:414、419、422、420、423和433)。
将具有不同接头的gL/gH三聚体或纳米颗粒注射至小鼠内,并评估免疫血清(图55)。在伴有佐剂AF03(一种基于角鲨烯乳剂的佐剂)的情况下,向小鼠给予两次2-μg注射液,在剂量之间间隔3周。在第6周通过ELISA测量抗gL/gH抗体终点效价。对于gH_16_gL,纳米颗粒(SEQ ID NO:410)优于三聚体构建体(SEQ ID NO:416)。gL_28_gH纳米颗粒(SEQ IDNO:413)的表现与三聚体构建体(SEQ ID NO:411)没有显著不同。gL_46_gH纳米颗粒(SEQID NO:414)优于gL_46_gH三聚体(SEQ ID NO:412)。
这些数据表明,单链gL/gH纳米颗粒可以引发针对EBV的稳健免疫应答。
实施例15:针对gL/gH和gp220的二价免疫
使用包含单链gL/gH纳米颗粒和gp220纳米颗粒的组合物进行二价免疫。如通过使用来自如上所述进行疫苗接种的小鼠的血清进行ELISA结合测定所测量的,包括gp220纳米颗粒(SEQ ID NO:401)对由单链gL/gH纳米颗粒(gL-gH_C5 NP[SEQ ID NO:419])引发的免疫应答无显著干扰作用。(图56A至56B,分别示出了在各个稀释度和结合效价下的测量值)。类似地,如通过ELISA所测量的,当与单链gL/gH纳米颗粒组合给予时,在对gp220纳米颗粒的免疫应答中没有观察到干扰(图57A至图57B,分别示出了在各个稀释度和结合效价下的测量值)。
因此,用单链gL/gH纳米颗粒和gp220纳米颗粒二者免疫均不会降低对任一多肽的免疫应答。
实施例16:佐剂与铁蛋白纳米颗粒的缀合
接下来,评估佐剂与铁蛋白纳米颗粒的缀合。图58A说明了构建体,其中铁蛋白包含用半胱氨酸置换表面暴露的氨基酸的突变,所述半胱氨酸可用于缀合。图58B示出了连接至PEG4接头和马来酰亚胺的示例性免疫刺激部分(SM7/8a,TLR-7/8激动剂)。此马来酰亚胺可用于将接头(自身附接至SM7/8a)共价缀合至铁蛋白的表面暴露的半胱氨酸。在图58C的电子显微照片中示出了包含融合至与SM7/8a缀合的铁蛋白的单链gL/gH多肽的多肽。
在图59A中的铁蛋白分子结构中说明了由表面暴露的氨基酸突变产生的半胱氨酸。在图59B中说明了通过并置铁蛋白、接头和CpG佐剂来将CpG佐剂(SEQ ID NO:535)缀合至铁蛋白,所述缀合被取向成显示每个部分的彼此邻近地附接的部分。
使用2mM TCEP还原gL/gH纳米颗粒(SEQ ID NO:419),然后经由添加1X PBS和使用100kD微旋柱去除TCEP来将其氧化。然后将SM7/8a与gL/gH纳米颗粒一起孵育以进行缀合。通过100kD微旋柱从反应中去除过量的SM7/8a。质谱(MS)数据表明,基于主MS峰相对于未缀合多肽的光谱的移位(图60A),约100%的包含单链gL/gH和铁蛋白的多肽(SEQ ID NO:419)与SM7/8a缀合(图60B)。缀合多肽与未缀合多肽的质量之差对应于SM7/8a-接头-马来酰亚胺加合物的分子量(711Da)。
使用2mM TCEP还原gp220纳米颗粒(SEQ ID NO:401),然后经由添加1X PBS和使用100kD微旋柱去除TCEP来将所述纳米颗粒氧化。然后将SM7/8a与gL/gH纳米颗粒一起孵育以进行缀合。通过100kD微旋柱从反应中去除过量的SM7/8a。MS数据表明,基于主MS峰相对于未缀合多肽的光谱的移位(图61A),约100%的包含gp220和铁蛋白的缀合多肽(SEQ ID NO:401)与SM7/8a缀合(图61B)。
电子显微镜(EM)数据还确认,SM7/8a与包含单链gL/gH和铁蛋白(图62B,与图62A中的未缀合样品相比)或包含gp220和铁蛋白(图62D,与图62C中的未缀合样品相比)的多肽的缀合未破坏纳米颗粒组装。
在用1μg包含单链gL/gH的纳米颗粒(gL_gH_C5 NP,图63A和图63B)或包含gp220的纳米颗粒(图64A和图64B)免疫后,通过ELISA测定抗体应答。将纳米颗粒与1μg裸铁蛋白组合并且不缀合至或缀合至SM7/8a。在伴有或不伴有掺合的AF03佐剂的情况下给予未缀合的纳米颗粒。使每只小鼠接受100μL的如上所述的纳米颗粒组合物。对于接受AF03佐剂的小鼠,将1:1体积的AF03与纳米颗粒混合。将BALB/c小鼠(n=5/组)免疫两次,在剂量之间间隔3周。在第5周进行取血以用于ELISA分析。对于在AF03佐剂中给予的纳米颗粒,看到最稳健的ELISA应答。与不伴有佐剂的未缀合的纳米颗粒相比,与SM7/8a缀合产生更稳健的ELISA应答。
与图65A至65B和图66A至66B中的伴有裸铁蛋白纳米颗粒的任一纳米颗粒的单一给予相比,还评估了各自1μg的与SM7/8a缀合的gL_gH_C5纳米颗粒和与SM7/8a缀合的gp220纳米颗粒的共同给予的作用。没有观察到对于对单链gL/gH(图65A至图65B,分别在不伴有和伴有AF03的情况下)或gp220(图66A至图66B,分别在不伴有和伴有AF03的情况下)的免疫应答的干扰。
实施例17:长期免疫原性研究
进行研究以评估在用包含单链gL/gH的纳米颗粒(gL/gH_C5,SEQ ID NO:419)给药后3个月时的免疫原性。将BALB/c小鼠(n=5/组)免疫两次,在剂量之间间隔3周。将裸铁蛋白(即未与任何多肽或佐剂缀合的铁蛋白)以1μg与1μg包含单链gL/gH的纳米颗粒一起给予,并在存在或不存在掺合的AF03佐剂的情况下配制纳米颗粒。在第13周进行取血以用于ELISA分析。对于接受AF03佐剂的小鼠,将1:1体积的AF03与纳米颗粒组合物混合。使每只小鼠接受100μL的上文所述的纳米颗粒组合物。使一些小鼠接受其中铁蛋白与SM7/8a(图67至图68中的“7/8a”)缀合的包含单链gL/gH的纳米颗粒。
如图67中所示,与SM7/8a缀合的包含单链gL/gH的纳米颗粒在AF03中配制时产生最大的免疫应答。对于不伴有AF03的这些纳米颗粒,也看到了稳健的免疫应答。
使用gp220纳米颗粒(SEQ ID NO:401)(伴有或不伴有与SM7/8a的缀合)代替包含单链gL/gH的纳米颗粒进行了平行实验。对于这些纳米颗粒观察到相似的结果,其中包含掺合的AF03的配制品产生最稳健的应答,并且对于不伴有AF03的这些纳米颗粒也看到稳健的免疫应答(图68)。
评估了由包含含有单链gL/gH的纳米颗粒(gL/gH_C5;SEQ ID NO:419)和包含gp220的纳米颗粒(SEQ ID NO:401)的二价组合物引发的免疫应答。对BALB/c小鼠(n=5/组)进行免疫,在剂量之间间隔3周。给予100μL的含有1μg的每种纳米颗粒的纳米颗粒组合物。对于接受AF03佐剂的小鼠,将1:1体积的AF03与疫苗混合。进行终末期第13周取血以用于ELISA分析。对于针对单链gL/gH(图69)和gp220(图70)二者的免疫应答,与任一纳米颗粒与裸铁蛋白的组合的给予相比,未看到由于纳米颗粒组合的给予而引起的干扰。
使用gL/gH_C5纳米颗粒(SEQ ID NO:419)进行的进一步实验确认,当将纳米颗粒与SM7/8a(7/8a)缀合时或在AF03中配制纳米颗粒时,可以看到长期免疫应答(图72)。对BALB/c小鼠(n=5/组)进行免疫,在剂量之间间隔3周。给予100μL的含有1μg纳米颗粒的纳米颗粒组合物。对于接受AF03佐剂的小鼠,将1:1体积的AF03与疫苗混合。进行第2周(初免)、第5周(加强免疫)和第13周(终末期)取血以用于ELISA分析。使用gp220纳米颗粒(SEQID NO:401)进行了平行实验,并且对于gp220纳米颗粒也看到了类似的长期应答(图73)。
还评估了包含单链gL/gH的不同纳米颗粒(gL_gH_C7:SEQ ID NO:420)。gL_gH_C7构建体包含在gH多肽与铁蛋白之间的柔性接头,所述柔性接头具有半胱氨酸以作为免疫刺激部分的缀合位点。接头可以与缺乏表面暴露的半胱氨酸的铁蛋白(如SEQ ID NO:420中所示)一起使用。通过以下方式将SM7/8a缀合至gL_gH_C7:使用2mM TCEP还原蛋白质,然后通过添加1X PBS并使用100kD微旋柱去除TCEP来进行氧化。然后将SM7/8a与gL/gH纳米颗粒一起孵育。缀合后,通过100kD微旋柱从反应中去除过量的SM7/8a。
使小鼠接受1μg的这些gL/gH纳米颗粒(缀合至7/8a或未缀合)加上1μg裸铁蛋白。给予100μL的含有1μg纳米颗粒的纳米颗粒组合物。对BALB/c小鼠(n=5/组)进行免疫,在剂量之间间隔3周。对于接受AF03佐剂的小鼠,将1:1体积的AF03与纳米颗粒组合物混合。进行第2周(初免)、第5周(加强免疫)和第13周(终末期)取血以用于ELISA分析。如在初免取血时通过ELISA终点效价所测量的,这些纳米颗粒在AF03中配制时或在与SM7/8a缀合时引发免疫应答(图71A)。关于加强免疫取血(图67C)或终末期取血(图71D)样品看到了相似的结果。还将这些纳米颗粒与CpG寡脱氧核苷酸缀合,并以相同方式给予。在第5周时,对于CpG缀合物的结果类似于未缀合的纳米颗粒(图71B)。
实施例18:对包含粉纹夜蛾铁蛋白的纳米颗粒的表征
还开发了包含粉纹夜蛾铁蛋白和gp220和/或gL/gH多肽的纳米颗粒。粉纹夜蛾铁蛋白纳米颗粒含有以1:1比率自组装的重链和轻链。发现将具有轻链的一种非铁蛋白多肽与在重链上的另一种非铁蛋白多肽组合允许在单独纳米颗粒的表面上呈递两种不同的多肽。因此,例如,自组装的粉纹夜蛾铁蛋白纳米颗粒可以呈递gp220和gL/gH二者。
产生并纯化了粉纹夜蛾铁蛋白纳米颗粒,所述纳米颗粒具有与gp220(SEQ ID NO:424)或单链gL/gH(SEQ ID NO:425)融合的重链和与gp220(SEQ ID NO:426)或单链gL/gH(SEQ ID NO:427)融合的轻链(构建体展示于图74B中,并且通过图74A中的考马斯凝胶染色可视化,示出了相对于单独的轻链和重链的预期分子量增加)。分别与gL/gH和gp220融合的轻链和重链或反之亦然的组合产生了可以呈递两种不同EBV多肽的单个多价纳米颗粒。
还产生了在重链和轻链二者中均仅具有gp220(如图75E中所示)或在重链中具有gp220并且在轻链中具有gH_gL(如图76E中所示)的两种粉纹夜蛾铁蛋白纳米颗粒。纯化遵循两个步骤:第一纯化步骤是离子交换色谱步骤(Q柱,参见图75A和在图75C中的考马斯结果以及图76A和示于图76C中的考马斯结果)。此步骤之后进行尺寸排阻色谱(参见图75B和在图75D中的考马斯结果以及图76B和在图76D中的考马斯结果)。
基于考马斯染色(图77A)、相对于裸粉纹夜蛾铁蛋白(图78C)的DLS半径增加(图77D)、和EM分析(图77C)(其中相对于裸纳米颗粒显现出在纳米颗粒核心周围的附加周边密度),包含与gp220融合的粉纹夜蛾轻链和重链的纳米颗粒(SEQ ID NO:424和426;展示于图77B中)显示出与包含异源gp220多肽的纳米颗粒的形成一致的概况(图77B)。对于SEQ IDNO:424和427(具有gL/gH多肽的粉纹夜蛾轻链和具有gp220多肽的重链;对于通过考马斯染色进行的可视化、构建体的展示、电子显微照片和通过DLS进行的表征,分别参见图77E至77H),观察到表明纳米颗粒中存在异源gL/gH和gp220多肽的相似结果。为了进行比较,图78A至图78C示出了裸粉纹夜蛾铁蛋白(即未与任何多肽缀合)的考马斯染色(图78A)、DLS半径(图78B)和EM分析(图78C)。
因此,粉纹夜蛾铁蛋白的使用允许在单个纳米颗粒上呈递2种多肽。
实施例19:gH/gL/gp42构建体
在图86A中示出了与铁蛋白融合的gH/gL/gp42的单链构建体(如在SEQ ID NO:227-231和241-242中的每一种中)的图片。每种蛋白质之间的融合是经由柔性氨基酸接头或刚性氨基酸接头进行的。单链gH/gL/gp42分子提供了在纳米颗粒上1:1:1比率的异三聚体形成。
已解析出gH/gL/gp42带有His标签的融合体(SEQ ID NO:226)的晶体结构显示单链gH/gL/gp42可采用类似于自然界中发现的野生型gH、gL和gp42蛋白的异三聚体构象(图85和图86B)。在图85和图86B中,Gp42(在图85中为深灰色并用箭头指示)与gH/gL异二聚体相互作用。图86C是显示与铁蛋白融合的此单链gH/gL/gp42异三聚体如何展示在纳米颗粒上的模型。存在将在单一纳米颗粒上展示的二十四个拷贝的单链gH/gL/gp42。
将gH/gL/gp42 NP构建体(SEQ ID NO:227)在293expi细胞中表达并纯化(图79A)。从CHO池中纯化的gH/gL/gp42 NP具有约26.2nm的动态光散射半径(图79B)。
评估了由单价(gH/gL/gp42 NP+裸铁蛋白纳米颗粒)或二价(gH/gL/gp42 NP+gp220 NP)组合物引发的免疫应答。gH/gL/gp42 NP具有序列SEQ ID NO:227,并且gp220 NP具有SEQ ID NO:1的序列。对BALB/c小鼠(n=5/组)进行免疫,在剂量之间间隔3周。在伴有AF03佐剂(1:1体积的AF03与疫苗混合)的情况下,给予100μL的含有1μg的每种纳米颗粒的纳米颗粒组合物。加强免疫指示在第二次免疫后第5周收集血清。使用在第5周从小鼠收集的血清进行B细胞(图80A)和上皮细胞(图80B)中的EBV病毒中和测定分析。与单价形式(gH/gL/gp42与裸铁蛋白)的给予相比,未看到由于以二价配制品给予纳米颗粒而引起的干扰。
使用包含在佐剂AF03的存在下的单链gL/gH纳米颗粒(gL_gH_C137A_bfpFerr纳米颗粒N19Q/C31S/S111C[SEQ ID NO:22])和gp220纳米颗粒(SEQ ID NO:1)(图81A至81B)或在佐剂AF03的存在下的gL/gH/gp42 NP(SEQ ID NO:227)和gp220纳米颗粒(SEQ ID NO:1)(图81C-81E)的组合物对雪貂进行二价免疫。Inj.1=注射1(在注射1后2周从6只雪貂收集血清)。Inj.2=注射2(在注射2后2周从6只雪貂收集血清)。ELISA结合测定测量了针对图81A至图81E中所指示的抗原的终点结合效价。图81F-G示出了来自接受在佐剂AF03的存在下的gL/gH/gp42 NP(SEQ ID NO:227)和gp220纳米颗粒(SEQ ID NO:1)的二价疫苗接种的雪貂的血清的EBV病毒中和测定(分别在B细胞和上皮细胞中)。初免=Inj.1并且加强免疫=Inj.2。
表达gH/gL/gp42_NP_C12(SEQ ID NO:228)并且使用Superose6尺寸排阻色谱将其纯化(图82A)。图82A中样品的动态光散射分析显示出20.6nm的颗粒大小半径(图82B)。
表达gH/gL/gp42_NP_C13(SEQ ID NO:229)并且使用Superose6尺寸排阻色谱将其纯化(图83A)。图83A中样品的动态光散射分析显示出17.1nm的颗粒大小半径(图83B)。
表达gH/gL/gp42_NP_C14(SEQ ID NO:230)并且使用Superose6尺寸排阻色谱将其纯化(图84A)。图84A中样品的动态光散射分析显示出16.9nm的颗粒大小半径(图84B)。
图86D示出了对在293Expi细胞中表达后的SEQ ID NO:227的纯化。变性SDS考马斯凝胶显示,与铁蛋白融合的gH/gL/gp42在糖基化的情况下高于150kD。纯化产物的负染色电子显微镜分析显示,与铁蛋白融合的单链gH/gL/gp42可以成功地形成在表面上展示gH/gL/gp42抗原的纳米颗粒(图86E)。通过在第0、3、7或14天的温度、氧化和/或脱酰胺应激测试,已经由序列分析或质谱鉴定了SEQ ID NO:227的单链gH/gL/gp42纳米颗粒的潜在不稳定序列。为了改善此疫苗构建体的疫苗稳定性、表达和/或免疫原性,将以不同组合,特别是在表1中所列位点对SEQ ID NO:227进行保守氨基酸取代突变。还将在SEQ ID NO:228-230中测试在特定基因中对应位置处的保守氨基酸突变,所述SEQ ID NO:228-230与SEQ ID NO.227的不同之处仅在于使gp42的C末端与铁蛋白序列的N末端融合的接头序列。
实施例20:对RSV F多肽的修饰的设计和表征
像其他副粘病毒F蛋白一样,RSV F被表达为前体蛋白,所述前体蛋白具有N末端信号肽和将蛋白质锚定在病毒表面的C末端跨膜区。RSV F经历通过蛋白酶弗林蛋白酶进行的细胞内切割以释放疏水性融合肽(图87A中的“FP”),其作用是在感染过程中附着于靶细胞。与融合肽相邻的是七肽重复区A(HRA),而七肽重复区B(HRB)与跨膜结构域相邻。
呈融合前和融合后构象的RSV F胞外结构域三聚体的晶体结构展示了HRA和HRB区如何进行重要的重排以驱动细胞融合事件(图87B)(参见Swanson,K.A.等人,Proc NatlAcad Sci U S A 108(23):第9619-24页(2011);McLellan,J.S.等人,Science 342(6158):592-598(2013);McLellan,J.S.等人,J Virol 85(15):7788-96(2011);和McLellan,J.S.等人,Science 342(6158):第592-8页(2013))。在融合前构象中,七肽重复序列A(HRA)区与球状头部缔合,并且融合肽的尖端大部分包埋在蛋白质的中心中。融合前构象含有多个螺旋,并且包括原体之间的某些接触以形成融合前三聚体。
一系列氨基酸取代被设计为原体间稳定化的。示例性取代包括V207L;N228F;I217V和E218F;I221L和E222M;或Q224A和Q225L。实施例中的所有RSV F氨基酸序列编号均使用SEQ ID NO:526的编号。
氨基酸取代被设计为螺旋稳定化的。这样,预计这些取代将稳定化RSV F的螺旋结构域。示例性取代包括N216P或I217P。
氨基酸取代被设计为原体内稳定化的。示例性取代包括V220I;或A74L和Q81L。
氨基酸取代被设计为螺旋加帽的。示例性取代包括N216P或I217P。
设计氨基酸取代以减少聚集。示例性取代包括V192E和L61Q。
将其他氨基酸取代设计为通过引入疏水性氨基酸(如N228F)进行的空腔填充。
设计氨基酸取代E328N、S348N和R507N以通过用天冬酰胺置换非天冬酰胺残基来添加糖基化位点。假设添加非天然聚糖可用于阻断融合前F蛋白表面上的在融合后RSV F(图87B)中暴露的表位。
将目的RSV F构建体产生为单链(scF)融合蛋白,所述单链融合蛋白具有包含N末端牛蛙铁蛋白接头和幽门螺杆菌铁蛋白(pFerr)的杂合铁蛋白(图87A)。铁蛋白包含由K79C或S111C突变产生的表面暴露的半胱氨酸(铁蛋白序列编号对应于SEQ ID NO:208)。
使用本领域已知的标准克隆实践来产生各种RSV Pre-F-NP和铁蛋白编码序列。一般而言,由Genscript合成具有所述取代的RSV F构建体的DNA并克隆到哺乳动物表达载体中。RSV F DS-CAV1和融合后F三聚体的产生类似于先前公布的方案(参见McLellan,J.S.等人,Science 342(6158):592-598(2013))。DS-CAV1构建体保留了RSV F的C末端三聚化结构域,并将其与填充空腔的疏水取代组合。RSV F DS-CAV1包含S155C-S290C二硫化物突变(DS)和S190F-V207L(CAV1)。
将编码RSV F-铁蛋白纳米颗粒、裸铁蛋白(即,未与RSV F偶联)和RSV F三聚体的载体转染到293EXPI细胞中,并在4天后从条件培养基中收获表达产物。通过以下方式纯化RSV F纳米颗粒:使用常规色谱方法,在pH 7.0和8.5下进行一系列阴离子Q柱纯化(GEHealthcare,目录号17-1154-01),之后在PBS中进行Superose 6SEC纯化(GE Healthcare目录号90-1000-42)。将DS-CAV1融合前三聚体和融合后三聚体储存在-80℃下,并且将RSV F纳米颗粒储存在4℃下。
为了确定RSV F纳米颗粒的构象,进行电子显微镜检查。将RSV F纳米颗粒制剂(30μg/mL,在25mM Tris、50mM NaCl中)吸收到400目碳涂覆网格(Electron MicroscopySciences)上,并用0.75%甲酸铀酯染色。使用在80kV下操作的JEOL 1200EX显微镜分析样品。通过EM公司Nanoimaging Services,INC(加利福尼亚州圣地亚哥)以65,000×放大倍率获取显微照片并且使用本领域的常规方法制备2D类别平均值(图87D)。
通过抗RSV F蛋白质印迹评价由瞬时转染的293EXPI细胞(Invitrogen)对包含这些RSV F多肽和铁蛋白的多肽(SEQ ID NO:501-508和511-515)的表达和分泌。所有抗RSV F蛋白质印迹均使用McLellan等人,Science 340(6136):1113-1117(2013)和美国专利8,562,996中描述的位点0特异性D25抗体。如图88中所示,许多构建体被成功表达和分泌。
RF8085多肽(SEQ ID NO:501)表示融合至铁蛋白纳米颗粒N末端的公布的DS-CAV1RSV F的单链突变体(参见参见McLellan,J.S.等人,Science 342(6158):592-598(2013))。此构建体包含保留抗原性位点0的RSV F的S155C-S290C双突变体(DS)。
RF8106多肽(SEQ ID NO:509)具有I217P取代,而不是取代到DS-CAV1中的2个半胱氨酸。如图89中所示,如通过抗RSV F蛋白质印迹从4天后的条件培养基中评估的,RF8106构建体在瞬时转染的293EXPI细胞中具有显著更好的表达。
RF8106的尺寸排阻色谱(SEC)显示主峰在与融合至RSV抗原的组装铁蛋白颗粒一致的保留时间处洗脱,这与融合蛋白纳米颗粒一致(Pre-F-NP,图90)。RF8106的动态光散射(DLS)分析是在还原状态(图91B)和非还原状态(图91A)下进行的。通过用2mM TCEP处理来还原。RF8106具有大约15nm的半径,这与在还原状态和非还原状态二者下掺入纳米颗粒(24聚体)中一致。融合蛋白对还原剂的稳定性有利于佐剂与融合蛋白的缀合以形成自佐剂化纳米颗粒,如下所述。
接下来,评估佐剂与RSV F多肽和铁蛋白的融合蛋白(Pre-F-NP)的缀合。发现铁蛋白上的游离表面半胱氨酸可用于将另外的部分附接至scF-pFerr融合蛋白。图92示出了具有序列T*G*A*C*T*G*T*G*A*A*C*G*T*T*C*G*A*G*A*T*G*A(SEQ ID NO:530;星号指示硫代磷酸酯连接)的CpG寡脱氧核苷酸(ODN)与RF8106的成功缀合,如通过如由考马斯染色的SDS-PAGE凝胶评估的分子量增加所证明。
将使用E328N、S348N和R507N取代添加糖基化位点(RF8117,SEQ ID NO:517)的作用在用作为具有铁蛋白的融合蛋白的此构建体(即Pre-F-NP构建体)瞬时转染的293EXPI细胞中进行评估。与在RF8113中一样,RF8117也包含I217P取代。如图93中所示,与RF8085对照构建体和RF8113构建体(SEQ ID NO:516,其包含I217P的脯氨酸取代但不包含E328N、S348N和R507N取代)二者相比,对于RF8117看到增加的表达。RF8113与先前描述的RF8106相似,不同之处在于工程化的铁蛋白半胱氨酸位于铁蛋白残基K79C上而不是S111C上。RF8117构建体还显示出RF8113和RF8117的分子量增加,这表明聚糖的成功添加。
图94汇总了增加Pre-F-NP的蛋白水解稳定性的对RSV F纳米颗粒的修饰。起始构建体是RF8117(上文)。当与RF8090一样将较早的构建体RF8085克隆到CHO载体中并转染到CHO细胞中时,观察到在F部分与铁蛋白部分之间的一些材料被剪切。怀疑HRB区域或F部分与铁蛋白部分之间的接头中的精氨酸或赖氨酸残基被胰蛋白酶样蛋白酶切割。就在293细胞中的表达而言测试了所述区域内赖氨酸和精氨酸残基的突变。图94将突变K498L和R508Q(在RF8122中,SEQ ID NO:518)鉴定为相对于RF8117不影响或不增加表达。将具有R523Q的这些突变与本文提及的RF8117的突变组合以形成构建体RF8140(SEQ ID NO:523)。
在293细胞表达中,关于单链和脯氨酸(I217P)修饰的组合(具有这些取代的示例性构建体包括RF8106(SEQ ID NO:509)和RF8113(SEQ ID NO:516))观察到表达的更大改善(大约5倍),并且由于RSV F的添加的糖基化位点修饰而导致表达和溶解性的进一步改善(示例性构建体RF8117(SEQ ID NO:517)和RF8140(SEQ ID NO:23))。这些构建体全部具有融合肽和被序列GSGNVGL(SEQ ID NO:531)置换的p27肽区(SEQ ID NO:526的氨基酸98-144)。然而,当将RF8090在CHO生产细胞系中表达时,在蛋白质印迹中观察到另外的RSV F条带,这表明所述构建体易受蛋白水解的影响,所述蛋白水解可能是在精氨酸或赖氨酸残基处的胰蛋白酶样切割。
还研究了蛋白酶易感性的潜在作用。进行对HRB区域中以及在F部分与铁蛋白部分之间的接头中的K残基的取代(敲除或KO),因为预测所述K残基是最初在CHO生产细胞系中观察到的K介导的切割的可能位点。如图95A和图95B中所示,在CHO生产细胞系中,RF8117和RF8140二者均表达至相对于RF8090较高的水平,如通过D25蛋白质印迹或D25和AM14 Octet分析所测量的。
这些数据表明,单链构建体和用于螺旋加帽、增加糖基化以及消除易受蛋白酶切割的赖氨酸或精氨酸的氨基酸修饰可以改善RSV F多肽(包括RSV Pre-F-NP抗原)的表达。
实施例21:对RSV F和铁蛋白纳米颗粒的融合蛋白的表征
在进行动物研究之前,使用Octet通过结合分析DS-CAV1和RSV F纳米颗粒的浓度。还使用FortéBio Octet仪器测量融合前抗原与融合前特异性抗体D25和AM14的结合。所有测定均在30℃下在PBS中进行。将抗体加载至蛋白A(ProA)传感器尖端(fortéBio#18-5013)上400秒,以允许捕获达到接近饱和。然后将生物传感器尖端在PBS中平衡90秒,之后以已知浓度在PBS中进行抗原缔合300秒,之后在PBS中解离抗原。使用已知浓度的纯化Pre-F-NP的结合的外标曲线,使用Octet数据分析HT10.0软件进行数据分析和曲线拟合(假定1:1相互作用)。确定CHO条件培养基中的Pre-F-NP浓度的示例性测定结果示于图95B中。
实施例22:对RSV F多肽的免疫应答的体内表征
为了在小鼠中评估对RSV抗原的体内应答,在第0周、第3周和第6周用指定剂量的RSV抗原肌内免疫雌性BALBc小鼠。除非另有说明,否则用床边混合策略将RSV抗原(例如,尤其在图96A-B和图12A-B的实验中)用AF03佐剂化。即,在临将50μl注射至每条后肢中之前,将50μl的相关蛋白质溶液与50μl的Sanofi佐剂AF03(基于角鲨烯的乳剂;参见Klucker等人,J Pharm Sci.2012年12月;101(12):4490-500)混合。对于未佐剂化组,如上那样混合抗原,但是将AF03置换为等体积的PBS。对于与SPA09或明矾混合的抗原,在分别用等体积的SPA09或明矾置换AF03的情况下进行以上程序。对于任何配制品,均未观察到来自免疫的不利影响。在首次免疫前1天和在每次注射后至少2周(即第2、5和8周)采集血液。除非另有说明,否则示出的数据是关于第三次注射后2周(第8周,也表示为2wp3)的。典型地,对来自免疫前动物(表示为幼稚态)、第二次注射后两周(第2次后或2wp2)或第三次注射后两周(第3次后或2wp3)的血清进行分析。
对于Vero细胞中和测定,将血清在56℃下热灭活30分钟。在补充有2%胎牛血清(FBS)、1%GlutaMAX和1%抗生素-抗有丝分裂剂的达尔伯克改良伊格尔培养基(DMEM)中制备灭活血清的四倍系列稀释系列。将RSV病毒原液与血清稀释液1:1合并,并在37℃下孵育1.5小时。然后将病毒-血清混合物以100μL/孔添加至含有汇合Vero细胞单层的24孔板中,并在37℃、5%CO2下孵育1.5小时。然后将接种物覆盖1mL/孔的在补充有2%FBS和2%GlutaMAX和2%抗生素-抗有丝分裂剂的DMEM中的0.75%甲基纤维素。在37℃、5%CO2下孵育5天后,去除覆盖层,并将单层用冰冷的甲醇固定20分钟。
然后将板在水中洗涤一次,并在室温下在轻轻搅拌下用在磷酸盐缓冲盐水(PBS)中的5%脱脂乳粉封闭30分钟。然后用200μL/孔的在PBS中的2%乳粉置换封闭溶液,所述PBS含有与辣根过氧化物酶(Abcam AB20686)缀合的抗RSV抗体的1:2000稀释物。在室温下孵育3小时后,将板用水洗涤2次,用TrueBlue HRP底物显色,再在水中洗涤两次并风干。
使用解剖显微镜对染色的空斑进行计数。使用以下公式在模拟的中和病毒对照的60%减少终点处确定中和抗体效价:60%空斑减少效价=(C/V x 0.4-低)/(高-低)x(HSD-LSD)+LSD,其中C/V=模拟的中和病毒对照孔中RSV空斑的平均值,低和高是血清样品的两种稀释物中RSV空斑的平均数目(将C/V x 0.4值括上),并且HSD和LSD是较高和较低的血清稀释度。
对于HAE中和测定,将血清在56℃下热灭活30分钟。在补充有PneumaCultTM-ALI10X补充剂(Stem Cell Technologies;05003)和1%抗生素/抗真菌剂的PneumaCultTM-ALI基础培养基(Stem Cell Technologies;05002)(从此称为培养基)中制备灭活血清的四倍系列稀释系列。将RSV病毒原液与血清稀释液1:1合并,并在37℃下孵育1.5小时。然后将病毒-血清混合物以50μL/孔添加至含有完全分化的HAE细胞的24孔板中,并在37℃、5%CO2下孵育1.5小时。孵育后,去除接种物,用培养基洗涤孔两次以去除未结合的病毒,并在37℃、5%CO2下再孵育20小时。用荧光显微镜计数用表达mKate(TagFP635)报告物的RSV感染的培养物中的感染事件。
为了检测用不表达mKate报告物的RSV进行的感染,用培养基充分洗涤假复层上皮以去除粘液,然后在室温下用4%多聚甲醛固定30分钟,用0.25%Triton X-100透化30分钟,并且用补充有2%FBS的DMEM在37℃下封闭1小时。用在补充有2%FBS的DMEM中1:200稀释的100μL/孔小鼠抗RSV单克隆Ab混合物(Millipore;MAB 858-4)置换封闭溶液,并将板在37℃下孵育2小时。然后将板用补充有0.05%Tween 20的PBS洗涤3次。每孔添加100μL的在补充有2%FBS的DMEM中1:200稀释的山羊抗小鼠IgG(H+L)(Invitrogen;A11001),并将板在4℃下孵育过夜。第二天早晨,将板用补充有0.05%Tween 20的PBS洗涤3次,用具有DAPI的ProLong Gold AntiFade(Thermo Fisher Scientific;P36935)稳定化荧光信号,并用荧光显微镜计数。如上在60%减少终点处确定中和抗体效价。
对于抗F结合,使融合前F(DS-CAV1)或融合后F与Octet上的抗-HIS抗体尖端结合。除非另有说明,否则所有抗F结合均是指抗融合前F三聚体(DS-CAV1)结合。将带有His6标签(SEQ ID NO:442)的RSV F三聚体(DS-CAV1或融合后F)预加载至抗Penta-HIS(HIS1K)传感器尖端(FortéBio#18-5122)上400秒以允许捕获达到接近饱和。然后将生物传感器尖端在Octet洗涤缓冲液中平衡90秒,之后使稀释血清缔合300秒。使用Octet数据分析HT10.0软件测量缔合曲线最终响应,并将所述响应乘以稀释倍数(100或300)以获得最终报告的响应。
对于抗Gcc结合,在类似于上述的Octet尖端上使用具有C末端HIS标签的Gcc肽的三聚化二聚体。将带有His6标签(SEQ ID NO:442)的Gcc(A2株系)预加载至抗Penta-HIS(HIS1K)传感器尖端(FortéBio#18-5122)上400秒以允许捕获达到接近饱和。然后将生物传感器尖端在Octet洗涤缓冲液中平衡90秒,之后使稀释血清缔合300秒。使用Octet数据分析HT10.0软件测量缔合曲线最终响应,并将所述响应乘以稀释倍数(100或300)以获得最终报告的响应。
对于非人灵长类动物(NHP)研究,针对RSV响应预筛选NHP(发现基线低于所有测定的检测极限)。在伴有所指示佐剂的情况下用50μg RF8140免疫NHP,与以上小鼠方案相似,但使用更大的佐剂体积(图97C-D和图104)。
对于非人灵长类动物研究,如上所述那样进行VERO中和测定。通过下面的ELISA测定评估Pre-F结合。
将NHP血清样品连续稀释2倍(初始稀释度为1:100),并在37℃下在封闭的RSV可溶性F(Sinobiological#11049-V08B)包被的板(1μg/mL,100μL/孔)上孵育1h。在37℃下使用辣根过氧化物酶缀合的抗猴IgG(BioRad AAI42P,1:10,000稀释度)检测RSV F特异性IgG90分钟。使用3,3',5,5'-四甲基联苯胺(TMB Tebu-Bio)对板进行显色,并用1N盐酸(Prolabo#30024290)终止。用微板读取器(SpectraMax)在450nm-650nm下测量光密度(OD)。从滴定曲线(每个板上放有标准的小鼠超免疫血清),使用SoftmaxPro软件针对0.2至3.0的OD值范围计算RSV sF特异性IgG效价。
此参考的IgG效价(以任意ELISA单位(EU)表示)对应于给出1.0OD值情况下的倒数稀释度的log10。抗体检测的阈值为20(1.3log10)EU。所有最终效价均以log10表示,以便绘图。对于每个<1.3log10的效价,分配1.0log10的任意效价。
为了在NHP研究中评估细胞介导的免疫,按照制造商的说明书使用IFNγ/IL-2FluoroSpot试剂盒(FS-2122-10,Mabtech)。简而言之,将IPFL板的膜用35%乙醇预湿,并且将捕获抗体(抗IFNγ和抗IL-2)在4℃下包被过夜。
然后将板在37℃下用200μL/孔的含有10%胎牛血清(FCS)的细胞孵育培养基封闭2小时。去除培养基,并在孔中添加刺激物:全长F抗原(抗原特异性刺激)、抗CD3(阳性对照)或细胞培养基(未刺激对照)。将猕猴外周血单核细胞(PBMC)解冻并计数。每孔添加400,000个细胞,并在37℃下在具有5%CO2的潮湿培养箱中孵育24h。
为了检测,去除细胞,并且添加检测抗体(缀合的抗-IFNγ和抗IL-2)并在室温下孵育2h。然后添加荧光团缀合的试剂并在室温下孵育1h。将板清空、干燥并在室温下黑暗中储存直至分析。将抗CD3 mAb用作阳性对照,并且在所有样品中发现>500个斑点形成计数(SFC)/百万个PBMC的响应,验证了可接受的样品质量。对于F抗原刺激的细胞,应减去在未刺激孔(细胞培养基)中检测到的斑点。
对于人细胞(或B细胞)分析,进行的实验与参考实验-Dauner等人Vaccine 2017年10月4日;35(41):5487-5494(图106)类似。细胞是未处理的(用PBS处理)或用100ng剂量的如指示的RSV F或RSV G多肽处理。使用文献中所述的luminex测定,分别用包被有pre-F-三聚体(DS-CAV1)或G胞外结构域的珠进行F-结合和G-结合应答。
RF8117(SEQ ID NO:517)包含在E328N、S348N和R507N处的工程化糖基化位点,如上所提及,所述工程化糖基化位点不防止D25或AM14结合。为了证明此融合前纳米颗粒对其他融合前抗原(DS-CAV1)引发类似的免疫应答,我们用1μg或0.1μg剂量的pre-F三聚体(DS-CAV1)、融合后F或RF8117(全部均用AF03佐剂化)免疫组中小鼠(每组5只)三次,在注射之间有3周。在第三次免疫后两周使用VERO细胞测定测试血清的中和效价。较高剂量下的RF8117引发的中和效价与融合前对照相似,且优于融合后对照。在较低剂量下,RF8117引发的中和效价高于融合前对照和融合后对照二者(图96A)。
RSV Pre-F-NP含有糖基化位点,所述糖基化位点经工程化以阻断融合前构象与融合后构象之间共享的表位。评价了这些聚糖是否抑制中和应答。将具有工程化聚糖(SEQ IDNO:517)的RF8117与RF8113(类似于RF8117,但缺乏工程化聚糖;SEQ ID NO:516)和融合前三聚体对照(DS-CAV1)进行比较。用1μg或0.1μg剂量(全部均用AF03佐剂化)免疫组中小鼠(每组5只)三次,在注射之间有三周。在第三次免疫后两周使用VERO细胞测定测试血清的中和效价。如通过中和效价判断的,在RF8113与RF8117构建体之间,在任一剂量下均无显著差异(图96B)。
为了证明本文提及的RF8140(SEQ ID NO:523)的赖氨酸和精氨酸敲除不会破坏抗原引发中和应答的能力,我们在小鼠中将RF8140(SEQ ID NO:525)的免疫原性与融合后F三聚体(SEQ ID NO:524)的免疫原性进行了比较(图97A和B)。在低剂量(0.1μg)下,RF8140(SEQ ID NO:525)引发优于融合后三聚体(SEQ ID NO:524)的中和效价。为了证明RF8140(SEQ ID NO:523)在NHP中引发免疫应答,我们在伴有或不伴有佐剂(AF03)的情况下用RF8140(SEQ ID NO:525)免疫NHP。图97C示出了RSV F结合应答(ELISA效价),同时图97D比较了通过用Pre-F-NP(RF8140,SEQ ID NO:523)免疫引发的RSV中和效价。未佐剂化的和佐剂化的RF8140(SEQ ID NO:525)二者均在NHP中引发免疫应答。
在显示RF8117(SEQ ID NO:517)和RF8140(SEQ ID NO:523)的工程糖基化位点不会防止这些抗原引发中和应答后,我们想证明它们确实阻断了融合前构象与融合后构象之间共享的非中和表位或弱中和表位(图98)。通过Octet测量由用高(1μg)和低(0.1μg)剂量下的不伴有工程化糖基化的Pre-F-NP(RF8113,SEQ ID NO:516)或伴有工程化糖基化的Pre-F-NP(工程化Gly颗粒,RF8117 SEQ ID NO:517)免疫引发的对融合前F(DS-CAV1,SEQID NO:525)的抗体应答(图98A)。由任一Pre-F-NP引发的应答是相似的。通过Octet测量由用高(1μg)和低(0.1μg)剂量下的不伴有工程化糖基化的Pre-F-NP(RF8113,SEQ ID NO:516)或伴有工程化糖基化的Pre-F-NP(RF8117,SEQ ID NO:517)免疫引发的对融合后三聚体的抗体应答(图98B)。由RF8117(SEQ ID NO:517)引发的融合后F结合应答显著低于由RF8113(SEQ ID NO:516)引发的那些。因此,虽然RF8113和RF8117均引发对融合前F的稳健抗体应答,但由RF8117引发的融合后F抗体应答被大大阻遏。这是由于映射到共享的融合前和融合后表位的工程化聚糖(图88B)。
为了进一步证明工程化糖基化位点阻断非中和性表位,但使中和抗体效价偏倚向非中和抗体效价,我们以不同的方式分析了以上数据(图99A-C)。测量了在小鼠研究中由用具有野生型糖基化位点的Pre-F NP(Wt聚糖颗粒;RF8113,SEQ ID NO:516)与具有另外的工程化糖基化位点的Pre-F NP(+聚糖颗粒;RF8117,SEQ ID NO:517)免疫引发的如通过VERO细胞测定测量的RSV中和效价的比较,并且未显示出显著差异(图99A)。在小鼠研究中,由用Wt聚糖颗粒(RF8113,SEQ ID NO:516)与+聚糖颗粒(RF8117,SEQ ID NO:517)免疫引发的RSV融合后F三聚体结合抗体应答的比较显示对于具有工程化聚糖的Pre-F-NP的融合后F结合应答受阻遏(图99B)。为了证明工程化聚糖不会降低功能性中和抗体应答,但减少针对共享的融合前/融合后表位所引发的非中和抗体,从而提高了由工程化聚糖构建体引发的中和抗体与总抗体比率,绘制了中和效价与F结合应答的比率(图99C)。因此,在小鼠研究中,具有工程化聚糖的Pre-F-NP引发优于结合抗体概况的中和抗体概况。
为了证明铁蛋白纳米颗粒可以用于改善RSV G中央结构域抗原的免疫原性,我们开发了一种将Gcc肽(SEQ ID NO:529)化学缀合至铁蛋白纳米颗粒的方法。可以将含有本文所述的S111C突变的铁蛋白与Gcc肽(SEQ ID NO:529)缀合,所述Gcc肽被合成为在PEG4接头上具有经由NHS基团附接至N末端的马来酰亚胺基团。合成具有N末端马来酰亚胺的Gcc肽,并通过Peptides International(美国肯塔基州路易斯维尔)进行HPLC纯化。当将马来酰亚胺-Gcc抗原添加至铁蛋白S111C颗粒时,马来酰亚胺缀合至游离半胱氨酸并形成Gcc-NP,其可通过考马斯染色的SDS-PAGE凝胶观察到(图100A)。虽然缀合典型地是50%至90%有效的,但在图100B中示出了Gcc肽铁蛋白纳米颗粒(100%缀合)的模型。
为了确定Gcc-NP是否引发优于Gcc肽(SEQ ID NO:529)的免疫应答,用Gcc肽或Gcc-NP(对于每种免疫1.3μg剂量,与RIBI 1:1混合)免疫每组的5只小鼠。将第二次免疫后两周和第三次免疫后两周的Gcc结合应答(Octet)与代表性组的幼稚态小鼠血清进行比较(图100C)。还在HAE中和测定中比较了在第三次注射后的小鼠研究中,由用Gcc肽(SEQ IDNO.529)与Gcc-NP免疫引发的中和应答(图100D)。如通过Gcc结合应答和中和应答所判断,Gcc-NP引发比单独Gcc肽优越的免疫应答。
为了证明RSV Pre-F-NP(RF8140)和Gcc-NP的共同给予不会干扰任一抗原引发免疫应答的能力,用单独的Pre-F-NP(RF8140,SEQ ID NO:523)、Gcc-NP(与Gcc肽(SEQ ID NO:529)缀合的铁蛋白)、或Pre-F-NP(RF8140,SEQ ID NO:523)与Gcc-NP的组合对小鼠进行免疫(图101A-C)。将所有免疫用AF03佐剂化。用单独的RF8140(Pre-F-NP)或RF8140和Gcc-NP(Pre-F-NP+Gcc-NP)免疫的小鼠产生了结合融合前F三聚体(DS-CAV1,SEQ ID NO:525)的抗体,而用Gcc-NP免疫的小鼠并没有。用单独的Gcc-NP(Gcc-NP)或RF8140和Gcc-NP免疫的小鼠产生了结合Gcc肽的抗体,而仅用RF8140免疫的小鼠并没有。用单独的Pre-F-NP、单独的Gcc-NP、或Pre-F-NP和Gcc-NP的共同给予免疫的动物全部在第二次免疫后和第三次免疫后产生了中和应答,如通过HAE中和测定所测量的。
为了确定RSV Pre-F-NP和Gcc-NP的共同给予是否干扰任一抗原引发中和抗体的能力,在耗尽测定中研究了针对F和G二者的中和抗体(图102A-B)。为了证明添加Gcc-NP不会干扰Pre-F-NP引发中和应答的能力,通过F敏感性VERO细胞测定测量上文提及组的中和效价(图102A)。还对来自幼稚态动物的血清进行了测试,以判断抗原耗尽的质量。在VERO测定中,来自用单独的RF8140(SEQ ID NO:523)或与Gcc-NP混合的RF8140免疫的小鼠的血清引发相似的中和应答,而Gcc-NP在F抗体敏感性VERO测定中显现未引发中和应答。当从来自用单独的RF8140(SEQ ID NO:523)免疫或用RF8140(SEQ ID NO:523)和Gcc-NP免疫的动物的合并血清中耗尽结合融合前三聚体(DS-CAV1,SEQ ID NO:525)的抗体时,在VERO测定中观察到可测量中和效价的降低。当在HAE细胞测定中测量以上组的中和效价时,在F和G敏感性测定中观察到所有免疫组均产生中和应答(图102B)。来自用单独的RF8140(SEQ ID NO:523)免疫的动物的合并血清在HAE测定中引发中和应答,所述中和应答可以用融合前F三聚体(DS-CAV1,SEQ ID NO:525)清除。来自用单独的Gcc-NP免疫的动物的合并血清在HAE测定中引发中和应答,所述中和应答可以用G胞外结构域(SEQ ID NO:528)清除。来自用Pre-F-NP(RF8140,SEQ ID NO:523)和Gcc-NP二者免疫的动物的合并血清在HAE测定中引发中和应答,所述中和应答并未被DS-CAV1(SEQ ID NO:525)完全清除,但通过用DS-CAV1然后用G胞外结构域(SEQ ID NO:528)进行的随后耗尽而被完全清除。总之,这些数据表明用Pre-F-NP和Gcc-NP的共同给予不会干扰任一抗原分别引发对融合前F或G的中和抗体的能力。
为了证明佐剂化RF8117(SEQ ID NO:517)或RF8140(SEQ ID NO:523)的作用,向小鼠给药这些与AF03、SPA09或明矾混合的构建体。在图103A中,用10μg与佐剂混合的抗原对小鼠进行免疫,而在图103B中,用1μg与佐剂混合的抗原对小鼠进行免疫。在图103A中,在第三次免疫后两周时间点通过VERO细胞测定测量中和效价。示出了来自用以下情况下的RF8117(SEQ ID NO:517)免疫的小鼠的血清:未佐剂化(无佐剂)、用明矾佐剂化或用AF03佐剂化。在图103B中,通过VERO细胞测定测量来自用以下项免疫的小鼠的血清的中和效价:用AF03佐剂化的RF8117(SEQ ID NO:517)、用SPA09佐剂化的RF8117(SEQ ID NO:517)或用AF03佐剂化的RF8140。在RF8117(SEQ ID NO:517)或RF8140(SEQ ID NO:523)的所有情况下,在幼稚态小鼠中,佐剂化组比未佐剂化组引发更高的中和效价。用与AF03混合的RF8117(SEQ ID NO:517)或RF8140(SEQ ID NO:523)免疫的小鼠引发相似的中和应答,这表明RF8140(SEQ ID NO:523)中添加的赖氨酸和精氨酸突变不会干扰Pre-F-NP引发中和应答的能力。
为了进一步探究AF03和SPA09的佐剂化作用,用以下情况下的RF8140免疫非人灵长类(NHP):未佐剂化、用AF03佐剂化或用两种剂量的SPA09佐剂化(图104A)。在第0天和第29天,用50μg的与所指示佐剂混合的抗原免疫NHP,并在所指示时间点通过ELISA或VERO中和应答测量免疫应答。在用以下情况下的RF8140免疫后,在NHP血清中测量融合前F三聚体ELISA应答:未佐剂化(无佐剂)、用AF03佐剂化或用SPA09佐剂化(使用500μg和2000μg剂量的SPA09)。在所有时间点,用AF03或SPA09佐剂化引发优越的中和应答。也通过VERO细胞测定来测量针对以上NHP组的血清的中和效价(图104B)。在所有情况下,用伴有佐剂的RF8140进行的免疫在所有时间点均比未佐剂化组引发更高的中和效价。
测试了RF8140(SEQ ID NO:523)与TLR7/8激动剂SM7/8或TLR9激动剂CpG直接缀合的作用。将抗原与小分子SM7/8或CpG缀合,并向小鼠给药10μg。RF8140在其铁蛋白序列中含有用半胱氨酸置换表面暴露的氨基酸的突变(K79C),所述半胱氨酸可以用于通过点击化学进行的缀合。为了进行比较,向小鼠给药未佐剂化(无佐剂)或通过与小分子以高剂量或低剂量混合(未缀合)而佐剂化的RF8140,如图105中所指示。测试了在第二次免疫和第三次免疫后来自动物的血清的融合前F三聚体结合。
在图105A中,在来自以下项的血清中测量融合前F三聚体结合应答:幼稚态小鼠,用未佐剂化RF8140(SEQ ID NO:523)免疫的小鼠,用与SM7/8佐剂缀合的RF8140(SEQ IDNO:523)、用130ng SM7/8佐剂化的RF8140(SEQ ID NO:523)或用20μg SM7/8佐剂化的RF8140(SEQ ID NO:523)免疫的小鼠。与未佐剂化或SM7/8佐剂化组相比,与SM7/8缀合的RF8140(SEQ ID NO:523)引发更高的融合前F三聚体结合效价。
在图105B中,还在来自以下项的血清中测量融合前F三聚体结合应答:幼稚态小鼠,用未佐剂化RF8140(SEQ ID NO:523)免疫的小鼠,用与CpG佐剂缀合的RF8140(SEQ IDNO:523)、用680ng CpG佐剂化的RF8140(SEQ ID NO:523)或用20μg CpG佐剂化的RF8140(SEQ ID NO:523)免疫的小鼠。与未佐剂化或SM7/8佐剂化组相比,与SM7/8缀合的RF8140(SEQ ID NO:523)引发更高的融合前F三聚体结合效价。
为了证明Pre-F-NP抗原和Gcc-NP抗原在人细胞中引发应答的能力,用MIMIC平台进行了实验(图106A-D)。MIMIC平台仅由自体人免疫细胞构成,所述自体人免疫细胞能够在激发时快速且可再现地产生抗原特异性先天性应答和适应性应答。先前的工作证明了MIMIC系统再现针对如HBV、破伤风类毒素、单克隆抗体、YF-VAX和流感B细胞应答的不同靶标的体内免疫概况的能力。在人B细胞中比较了由用Pre-F-NP RF8140(SEQ ID NO:523)与融合后F三聚体(SEQ ID NO:524)处理引发的RSV融合前F三聚体结合抗体应答,并且示出了代表性基线应答以进行比较(未处理)(图106A)。在图106C中示出了所测量的在人B细胞中由用Pre-F-NP(RF8140,SEQ ID NO:523)与融合后F(SEQ ID NO:524)处理引发的对融合前F三聚体(DS-CAV1,SEQ ID NO:525)与融合后F三聚体(SEQ ID NO:524)的结合应答的比率。使用VERO细胞测定测量由用不同的F抗原处理引发的来自MIMIC的抗体(图106C)。将在人B细胞中由用Pre-F NP(RF8140,SEQ ID NO:523)与融合后F三聚体(SEQ ID NO:524)处理引发的中和效价与未处理组进行比较,显示RF8140(SEQ ID NO:523)在人细胞中引发优越的中和应答。
基于在MIMIC研究中研究的人受试者的血清状态确定对RSV感染或对F亚单位疫苗候选物的Ab应答的大小,并通过线性回归分析对其进行评估。在RSV处理后(图106E,p=0.0041)和在F后初免后(图106F,p=0.0019),具有更高的抗pre-F IgG的预先存在的循环效价的供体产生显著更多的抗pre-F IgG。尽管相关性没有达到统计学显著性,但pre-F还显示出诱导的Ab水平与预先存在的Ab水平之间的关系。值得注意的是,与其他处理不同的是,pre-F-NP从具有低预先存在的抗pre-F-IgG的供体中诱导了与具有高预先存在的Ab的供体可比的高水平的抗pre-F-IgG(图106F)。这表明,pre-F-NP甚至从具有低预先存在的IgG水平的供体中也能够有效挽救(或增强)Ab应答。
为了证明Gcc-NP与单独的Gcc肽(SEQ ID NO:529)相比引发优越的G抗体应答,在人B细胞中用单独的Gcc肽(SEQ ID NO:529)或与纳米颗粒缀合的Gcc肽(Gcc-NP)处理人B细胞。Gcc-NP引发了优越的G结合抗体应答(图106G)。综合起来,这些数据表明Pre-F-NP和Gcc-NP将在人类免疫中引发免疫应答。
实施例23:对RSV Gcc-铁蛋白纳米颗粒的免疫应答的体内表征
如上所述制备RSV Gcc-NP。为了在小鼠中评估对RSV Gcc-NP的体内应答,在第0周、第3周和第6周用指定剂量的RSV抗原以高剂量(5μg)或低剂量(0.5μg)的抗原肌内免疫雌性BALBc小鼠。除非另有说明,否则用床边混合策略将RSV Gcc-NP用AF03佐剂化。即,在临将50μl注射至每条后肢中之前,将50μl的蛋白质溶液与50μl的Sanofi佐剂AF03(基于角鲨烯的乳剂;参见Klucker等人,J Pharm Sci.2012年12月;101(12):4490-500)混合。未观察到来自免疫的不利影响。在首次免疫前1天和在每次注射后至少2周(即第2、5和8周)采集血液。除非另有说明,否则示出的数据是关于第三次注射后2周(第8周,也表示为2wp3)的。典型地,对来自免疫前动物(表示为幼稚态)、第二次注射后两周(第2次后或2wp2)或第三次注射后两周(第3次后或2wp3)的血清进行分析。
对于HAE中和测定,将血清在56℃下热灭活30分钟。在补充有PneumaCultTM-ALI10X补充剂(Stem Cell Technologies;05003)和1%抗生素/抗真菌剂的PneumaCultTM-ALI基础培养基(Stem Cell Technologies;05002)(从此称为培养基)中制备灭活血清的四倍系列稀释系列。将RSV病毒原液与血清稀释液1:1合并,并在37℃下孵育1.5小时。然后将病毒-血清混合物以50μL/孔添加至含有完全分化的HAE细胞的24孔板中,并在37℃、5%CO2下孵育1小时。孵育后,去除接种物,用培养基洗涤孔两次以去除未结合的病毒,并在37℃、5%CO2下再孵育20小时。用荧光显微镜计数用表达mKate(TagFP635)报告物的RSV感染的培养物中的感染事件。
为了检测用不表达mKate报告物的RSV进行的感染(RSV B株系中和),用培养基充分洗涤假复层上皮以去除粘液,然后在室温下用4%多聚甲醛固定30分钟,用0.25%TritonX-100透化30分钟,并且用补充有2%FBS的DMEM在37℃下封闭1小时。用在补充有2%FBS的DMEM中1:200稀释的100μL/孔小鼠抗RSV单克隆Ab混合物(Millipore;MAB 858-4)置换封闭溶液,并将板在37℃下孵育2小时。然后将板用补充有0.05%Tween 20的PBS洗涤3次。每孔添加100μL的在补充有2%FBS的DMEM中1:200稀释的山羊抗小鼠IgG(H+L)(Invitrogen;A11001),并将板在4℃下孵育过夜。第二天早晨,将板用补充有0.05%Tween 20的PBS洗涤3次,用具有DAPI的ProLong Gold AntiFade(Thermo Fisher Scientific;P36935)稳定化荧光信号,并用荧光显微镜计数。在60%减少终点处确定中和抗体效价。
为了证明更高的多价性改善了RSV G抗原对中和应答的引发,用RSV F抗原对小鼠进行免疫。将所有免疫用AF03佐剂化。用与AF03一起配制的RSV Gcc-NP对小鼠进行免疫,在第二次注射后2周和第三次注射后2周测量和中和效价(图107A-C)。RSV Gcc-NP引发了相对于幼稚态小鼠血清的中和应答。在第二次免疫后2周(图107A)和第三次免疫后2周(图107B),用含有来自A2株系的Gcc的Gcc-NP免疫的小鼠显示出对RSV A株系的中和应答。在第三次注射后2周,Gcc-NP也引发了对RSV B1株系的中和应答(图107C)。
对于抗Gcc结合,在Octet尖端上使用具有C末端HIS标签的Gcc肽的三聚化二聚体。将带有His6标签的Gcc(A2株系)六聚体或带有His6标签的Gcc(B1株系)六聚体预加载至抗Penta-HIS(HIS1K)传感器尖端(FortéBio#18-5122)上400秒以允许捕获达到接近饱和。然后将生物传感器尖端在Octet洗涤缓冲液中平衡90秒,之后使稀释血清缔合300秒。使用Octet数据分析HT10.0软件测量缔合曲线最终响应,并将所述响应乘以稀释倍数(100或300)以获得最终报告的响应。
为了确定RSV Gcc-NP是否引发Gcc结合免疫应答,测试了来自上文所述的免疫的血清结合Gcc A2六聚体或Gcc B1六聚体的能力。在第二次免疫后2周和第三次免疫后2周测试高剂量(图108A和图109A)和低剂量(图108B和图109B)下的Gcc结合应答。对于A2株系(图108A-B)和B1株系(图109A-B),相对于幼稚态小鼠血清而言RSV Gcc-NP引发了结合应答。
实施例24:在人细胞中对Pre-F-NP和Gcc-NP的应答
为了证明Pre-F-NP和Gcc-NP在人细胞中引发应答的能力,用MIMIC平台进行了实验。MIMIC平台仅由自体人免疫细胞构成,所述自体人免疫细胞能够在激发时快速且可再现地产生抗原特异性先天性应答和适应性应答。先前的工作证明了MIMIC系统再现针对如HBV、破伤风类毒素、单克隆抗体、YF-VAX和流感B细胞应答的不同靶标的体内免疫概况的能力。在人B细胞中比较了由用Pre-F-NP RF8140(SEQ ID NO:23)与融合后F三聚体(SEQ IDNO:24)处理引发的RSV融合前F三聚体结合抗体应答,并且将其与代表性基线应答进行比较。确定了所测量的在人B细胞中由用Pre-F-NP(RF8140,SEQ ID NO:23)与融合后F(SEQ IDNO:24)处理引发的对融合前F三聚体(DS-CAV1,SEQ ID NO:25)与融合后F三聚体(SEQ IDNO:24)的结合应答的比率。使用VERO细胞测定测量由用不同的F抗原处理引发的来自MIMIC的抗体。将在人B细胞中由用Pre-F NP(RF8140,SEQ ID NO:23)与融合后F三聚体(SEQ IDNO:24)处理引发的中和效价与未处理组进行比较,显示RF8140(SEQ ID NO:23)在人细胞中引发优越的中和应答。为了证明Gcc-NP与单独的Gcc肽(SEQ ID NO:29)相比引发优越的G抗体应答,在人B细胞中用单独的Gcc肽(SEQ ID NO:29)或与纳米颗粒缀合的Gcc肽(Gcc-NP)处理人B细胞。Gcc-NP引发了优越的G结合抗体应答。因此,Pre-F-NP和Gcc-NP将在人类免疫中引发免疫应答。
Claims (27)
1.一种铁蛋白蛋白,所述铁蛋白蛋白包含用半胱氨酸置换表面暴露的氨基酸的突变。
2.一种铁蛋白蛋白,所述铁蛋白蛋白包含含有半胱氨酸的N或C末端接头。
3.一种铁蛋白蛋白,所述铁蛋白蛋白包含一个或多个经由表面暴露的氨基酸连接至所述铁蛋白蛋白的免疫刺激部分。
4.根据前述权利要求中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白是进一步包含非铁蛋白多肽的抗原性铁蛋白蛋白。
5.一种抗原性铁蛋白蛋白,所述抗原性铁蛋白蛋白包含(i)用半胱氨酸置换表面暴露的氨基酸的突变和连接至所述半胱氨酸的免疫刺激部分;和(ii)非铁蛋白多肽。
6.一种抗原性铁蛋白蛋白,所述抗原性铁蛋白蛋白包含(i)表面暴露的半胱氨酸,(ii)在所述铁蛋白蛋白N末端的肽接头,和(iii)在所述肽接头N末端的非铁蛋白多肽。
7.根据前述权利要求中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白进一步包含用非天冬酰胺氨基酸置换表面暴露的天冬酰胺的突变。
8.根据前述权利要求中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白进一步包含用非半胱氨酸氨基酸置换内部半胱氨酸的突变。
9.根据权利要求8所述的铁蛋白蛋白,其中所述内部半胱氨酸在幽门螺杆菌铁蛋白的位置31处,或如通过成对或结构比对确定的对应于幽门螺杆菌铁蛋白的位置31的位置处。
10.一种抗原性铁蛋白蛋白,所述抗原性铁蛋白蛋白包含:
a.用半胱氨酸置换表面暴露的氨基酸的突变和连接至所述半胱氨酸的免疫刺激部分;
b.用非半胱氨酸置换在幽门螺杆菌铁蛋白的位置31处的内部半胱氨酸的突变,或用非半胱氨酸置换如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中与位置31类似的位置处的内部半胱氨酸的突变;
c.用非天冬酰胺氨基酸置换表面暴露的天冬酰胺的突变;以及
d.非铁蛋白多肽。
11.根据权利要求8-10中任一项所述的铁蛋白蛋白,其中所述非半胱氨酸氨基酸是丝氨酸。
12.根据权利要求7-11所述的铁蛋白蛋白,其中所述天冬酰胺在幽门螺杆菌铁蛋白的位置19处,或如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中的类似位置处。
13.根据前述权利要求中任一项所述的铁蛋白蛋白,其中所述铁蛋白包含幽门螺杆菌铁蛋白的E12C、S26C、S72C、A75C、K79C、S100C和S111C突变中的一种或多种或如通过成对或结构比对确定的非幽门螺杆菌铁蛋白中的一种或多种相应突变。
14.根据权利要求4-13中任一项所述的铁蛋白蛋白,其中所述非铁蛋白多肽是来自流感、爱泼斯坦-巴尔病毒、呼吸道合胞病毒或疏螺旋体属的多肽。
15.根据权利要求14所述的铁蛋白蛋白,其中所述非铁蛋白多肽包括RSV G多肽,任选地其中所述RSV G多肽包含G多肽中心保守区。
16.根据权利要求4-5或7-15中任一项的铁蛋白蛋白,所述铁蛋白蛋白进一步包含在所述铁蛋白与所述非铁蛋白多肽之间的肽接头。
17.根据前述权利要求中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含免疫刺激部分,所述免疫刺激部分连接至所述半胱氨酸并且包含能够进行氢键结合或离子键结合的部分。
18.根据前述权利要求中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含作为TLR2、TLR7/8、TLR9或STING的激动剂的免疫刺激部分。
19.根据前述权利要求中任一项所述的铁蛋白蛋白,所述铁蛋白蛋白包含与SEQ IDNO:201-207或211-215中的任一个具有80%、85%、90%、95%、98%或99%同一性的氨基酸序列。
20.一种铁蛋白颗粒,所述铁蛋白颗粒包含根据前述权利要求中任一项所述的铁蛋白蛋白。
21.一种组合物,所述组合物包含根据前述权利要求中任一项所述的铁蛋白蛋白或铁蛋白颗粒和药学上可接受的载体。
22.一种组合物,所述组合物包含第一铁蛋白蛋白和第二铁蛋白蛋白,其中所述第一铁蛋白蛋白包含铁蛋白重链和第一非铁蛋白多肽,所述第二铁蛋白蛋白包含铁蛋白轻链和第二非铁蛋白多肽,并且所述第一非铁蛋白多肽和所述第二非铁蛋白多肽是不同的,任选地其中铁蛋白颗粒包含所述第一铁蛋白蛋白和所述第二铁蛋白蛋白。
23.根据权利要求21或22所述的组合物,所述组合物进一步包含佐剂。
24.根据权利要求4-23中任一项所述的铁蛋白蛋白、铁蛋白颗粒或组合物,用于在对受试者进行疫苗接种中使用。
25.一种对受试者进行疫苗接种的方法,所述方法包括向受试者给予根据权利要求4-23中任一项所述的铁蛋白蛋白、铁蛋白颗粒或组合物。
26.根据权利要求24所述的铁蛋白蛋白、铁蛋白颗粒或组合物或根据权利要求25所述的方法,其中所述受试者是人。
27.一种核酸,所述核酸编码根据权利要求1-19中任一项所述的铁蛋白蛋白,任选地其中所述核酸是mRNA。
Applications Claiming Priority (11)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862652199P | 2018-04-03 | 2018-04-03 | |
| US201862652201P | 2018-04-03 | 2018-04-03 | |
| US201862652204P | 2018-04-03 | 2018-04-03 | |
| US201862652217P | 2018-04-03 | 2018-04-03 | |
| US201862652210P | 2018-04-03 | 2018-04-03 | |
| US62/652,204 | 2018-04-03 | ||
| US62/652,201 | 2018-04-03 | ||
| US62/652,217 | 2018-04-03 | ||
| US62/652,210 | 2018-04-03 | ||
| US62/652,199 | 2018-04-03 | ||
| PCT/US2019/025422 WO2019195316A1 (en) | 2018-04-03 | 2019-04-02 | Ferritin proteins |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN112512564A true CN112512564A (zh) | 2021-03-16 |
Family
ID=66397427
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201980036305.9A Pending CN112512564A (zh) | 2018-04-03 | 2019-04-02 | 铁蛋白蛋白 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US11904009B2 (zh) |
| EP (1) | EP3773698A1 (zh) |
| JP (2) | JP2021519596A (zh) |
| CN (1) | CN112512564A (zh) |
| WO (1) | WO2019195316A1 (zh) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2019195316A1 (en) | 2018-04-03 | 2019-10-10 | Sanofi | Ferritin proteins |
| CN112512566A (zh) | 2018-04-03 | 2021-03-16 | 赛诺菲 | 抗原性爱泼斯坦-巴尔病毒多肽 |
| WO2020205986A1 (en) * | 2019-04-02 | 2020-10-08 | Sanofi | Antigenic multimeric respiratory syncytial virus polypeptides |
| WO2021205077A1 (en) | 2020-04-09 | 2021-10-14 | Finncure Oy | Mimetic nanoparticles for preventing the spreading and lowering the infection rate of novel coronaviruses |
| EP4139331A1 (en) * | 2020-04-22 | 2023-03-01 | Medicago Inc. | Suprastructure comprising modified influenza hemagglutinin with reduced interaction with sialic acid |
| CA3199937A1 (en) | 2020-10-28 | 2022-05-05 | Sanofi Pasteur | Liposomes containing tlr4 agonist, preparation and uses thereof |
| CN112094355B (zh) * | 2020-11-23 | 2021-05-11 | 南京佰抗生物科技有限公司 | 一种用于临床诊断的复合质控品及其制备方法 |
| AU2022251938A1 (en) | 2021-04-02 | 2023-11-16 | Bureau D’Études Biologiques Scientifiques Et Médicales | IMMUNOGENIC COMPOSITION CONTAINING AN ANTIGEN AND AN ADJUVANT COMPRISING AL-MOFs |
Family Cites Families (45)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5585250A (en) | 1993-08-20 | 1996-12-17 | The United States Of America As Represented By The Department Of Health & Human Services | Dampening of an immunodominant epitope of an antigen for use in plant, animal and human compositions and immunotherapies |
| US6429199B1 (en) | 1994-07-15 | 2002-08-06 | University Of Iowa Research Foundation | Immunostimulatory nucleic acid molecules for activating dendritic cells |
| US6207646B1 (en) | 1994-07-15 | 2001-03-27 | University Of Iowa Research Foundation | Immunostimulatory nucleic acid molecules |
| CA2194761C (en) | 1994-07-15 | 2006-12-19 | Arthur M. Krieg | Immunomodulatory oligonucleotides |
| US6239116B1 (en) | 1994-07-15 | 2001-05-29 | University Of Iowa Research Foundation | Immunostimulatory nucleic acid molecules |
| WO1998037919A1 (en) | 1997-02-28 | 1998-09-03 | University Of Iowa Research Foundation | USE OF NUCLEIC ACIDS CONTAINING UNMETHYLATED CpG DINUCLEOTIDE IN THE TREATMENT OF LPS-ASSOCIATED DISORDERS |
| US6406705B1 (en) | 1997-03-10 | 2002-06-18 | University Of Iowa Research Foundation | Use of nucleic acids containing unmethylated CpG dinucleotide as an adjuvant |
| EP1003531B1 (en) | 1997-05-20 | 2007-08-22 | Ottawa Health Research Institute | Processes for preparing nucleic acid constructs |
| ES2284247T3 (es) | 1998-04-03 | 2007-11-01 | University Of Iowa Research Foundation | Metodos y productos para estimular el sistema inmunitario usando oligonucleotidos y citoquinas inmunoterapeuticos. |
| WO2001075436A1 (en) | 2000-04-03 | 2001-10-11 | Board Of Trustees Of The Leland Stanford Junior University | A method for protein structure alignment |
| AU2001285049A1 (en) | 2000-08-18 | 2002-03-04 | Brookhaven Sciences Associates, Llc | Altered ospa of borrelia burgdorferi |
| US7097841B2 (en) | 2002-05-10 | 2006-08-29 | New Century Pharmaceuticals, Inc. | Ferritin fusion proteins for use in vaccines and other applications |
| US7774185B2 (en) | 2004-09-14 | 2010-08-10 | International Business Machines Corporation | Protein structure alignment using cellular automata |
| EP1997830A1 (en) | 2007-06-01 | 2008-12-03 | AIMM Therapeutics B.V. | RSV specific binding molecules and means for producing them |
| US20100285051A1 (en) | 2007-12-21 | 2010-11-11 | Dominique Ingrid Lemoine | Vaccine |
| US20110117131A1 (en) | 2008-04-09 | 2011-05-19 | Ning Huang | Production of OspA for Lyme Disease Control |
| CA2798331C (en) | 2010-05-14 | 2022-03-15 | Baxter International Inc. | Ospa chimeras and use thereof in vaccines |
| WO2012006180A1 (en) | 2010-06-29 | 2012-01-12 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Hiv immunogens |
| US20120258041A1 (en) | 2011-04-07 | 2012-10-11 | Basi Guriqbal S | Compositions and methods for treating diseases of protein aggregation involving ic3b deposition |
| EP2515112B1 (en) | 2011-04-22 | 2015-08-12 | Sysmex Corporation | Method for electrochemically detecting analyte |
| JP5795184B2 (ja) * | 2011-04-22 | 2015-10-14 | 国立大学法人 奈良先端科学技術大学院大学 | 被検物質の電気化学的検出方法 |
| CA2839995A1 (en) | 2011-06-20 | 2012-12-27 | University Of Pittsburgh-Of The Commonwealth System Of Higher Education | Computationally optimized broadly reactive antigens for h1n1 influenza |
| US20140348865A1 (en) | 2011-09-12 | 2014-11-27 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Ser. | Immunogens based on an hiv-1 v1v2 site-of-vulnerability |
| MX2014003308A (es) | 2011-09-20 | 2015-03-09 | Sinai School Medicine | Vacunas para el virus de la influenza y usos de las mismas. |
| EP2758038B1 (en) * | 2011-09-23 | 2018-05-30 | The United States of America, as represented by The Secretary, Department of Health & Human Services | Novel influenza hemagglutinin protein-based vaccines |
| CN104395336B (zh) | 2012-03-30 | 2018-01-23 | 高等教育联邦系统-匹兹堡大学 | 以计算方式优化的h5n1和h1n1流感病毒的广泛反应性抗原 |
| US9962436B2 (en) | 2012-07-26 | 2018-05-08 | The Henry M. Jackson Foundation For The Advancement Of Military Medicine, Inc. | Multimeric fusion protein vaccine and immunotherapeutic |
| US10017543B2 (en) * | 2013-03-13 | 2018-07-10 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Prefusion RSV F proteins and their use |
| WO2015054639A1 (en) | 2013-10-11 | 2015-04-16 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Epstein-barr virus vaccines |
| CZ2014320A3 (cs) | 2014-05-09 | 2015-11-18 | VÝZKUMNÝ ÚSTAV VETERINÁRNÍHO LÉKAŘSTVÍ, v.v.i. | Polyepitopový antigen, vakcinační konstrukt a vakcína pro prevenci lymeské boreliózy |
| PL3148578T3 (pl) | 2014-05-27 | 2022-10-17 | The U.S.A. As Represented By The Secretary, Department Of Health And Human Services | Stabilizowane trimery regionu łodygi hemaglutyniny grypy i ich zastosowania |
| US9703095B2 (en) | 2015-01-05 | 2017-07-11 | Edward Pakhchyan | Light modulator for MEMS display |
| US10301377B2 (en) * | 2015-02-24 | 2019-05-28 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Middle east respiratory syndrome coronavirus immunogens, antibodies, and their use |
| CR20230116A (es) * | 2015-12-04 | 2023-05-05 | Dana Farber Cancer Inst Inc | Composición de vacuna que comprende el dominio alfa 3 de mica/b (div. 2018-350) |
| CN115960263A (zh) | 2016-03-29 | 2023-04-14 | 美国政府(由卫生和人类服务部的部长所代表) | 取代修饰的融合前rsv f蛋白及其用途 |
| EP3463444A1 (en) * | 2016-06-07 | 2019-04-10 | Deutsches Krebsforschungszentrum | Improvement of hpv l2 peptide immunogenicity |
| CA3027877A1 (en) | 2016-06-17 | 2017-12-21 | Merial, Inc. | Novel immunogenic formulations comprising linear or branched polyacrylic acid polymer adjuvants |
| EP3474893A1 (en) | 2016-06-27 | 2019-05-01 | The U.S.A. as represented by the Secretary, Department of Health and Human Services | Self-assembling insect ferritin nanoparticles for display of co-assembled trimeric antigens |
| CA3058979A1 (en) | 2017-04-19 | 2018-10-25 | Institute For Research In Biomedicine | Novel malaria vaccines and antibodies binding to plasmodium sporozoites |
| CA3083102A1 (en) | 2017-11-21 | 2019-05-31 | Modernatx, Inc. | Epstein-barr virus vaccines |
| CN112512566A (zh) | 2018-04-03 | 2021-03-16 | 赛诺菲 | 抗原性爱泼斯坦-巴尔病毒多肽 |
| JP2021519599A (ja) | 2018-04-03 | 2021-08-12 | サノフイSanofi | 抗原性ospaポリペプチド |
| CN112512565A (zh) | 2018-04-03 | 2021-03-16 | 赛诺菲 | 抗原性流感-铁蛋白多肽 |
| MX2020010199A (es) | 2018-04-03 | 2021-01-08 | Sanofi Sa | Polipeptidos antigenicos del virus sincitial respiratorio. |
| WO2019195316A1 (en) | 2018-04-03 | 2019-10-10 | Sanofi | Ferritin proteins |
-
2019
- 2019-04-02 WO PCT/US2019/025422 patent/WO2019195316A1/en unknown
- 2019-04-02 EP EP19721896.9A patent/EP3773698A1/en active Pending
- 2019-04-02 JP JP2020554442A patent/JP2021519596A/ja active Pending
- 2019-04-02 CN CN201980036305.9A patent/CN112512564A/zh active Pending
-
2020
- 2020-10-01 US US17/061,136 patent/US11904009B2/en active Active
-
2024
- 2024-02-09 JP JP2024018289A patent/JP2024054277A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| WO2019195316A1 (en) | 2019-10-10 |
| EP3773698A1 (en) | 2021-02-17 |
| US20210113681A1 (en) | 2021-04-22 |
| US11904009B2 (en) | 2024-02-20 |
| JP2021519596A (ja) | 2021-08-12 |
| JP2024054277A (ja) | 2024-04-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11904009B2 (en) | Ferritin proteins | |
| US10137190B2 (en) | Nucleic acid molecules encoding ferritin-hemagglutinin fusion proteins | |
| EP3166963B1 (en) | Influenza virus vaccines and uses thereof | |
| EP3148578B1 (en) | Stabilized influenza hemagglutinin stem region trimers and uses thereof | |
| KR101983989B1 (ko) | 인플루엔자 바이러스 백신 및 이의 용도 | |
| US10517941B2 (en) | Influenza virus vaccines and uses thereof | |
| TW202144384A (zh) | 用於檢測、預防和治療新型冠狀病毒(covid-19)疾病的設計胜肽及蛋白質 | |
| US20210017237A1 (en) | Antigenic respiratory syncytial virus polypeptides | |
| US20210017238A1 (en) | Antigenic OspA Polypeptides | |
| JP2024041980A (ja) | 抗原性インフルエンザ-フェリチンポリペプチド | |
| RU2807992C2 (ru) | Антигенные полипептиды на основе последовательности респираторно-синцитиального вируса | |
| RU2816208C2 (ru) | АНТИГЕННЫЕ ПОЛИПЕПТИДЫ НА ОСНОВЕ ПОСЛЕДОВАТЕЛЬНОСТИ OspA | |
| WO2023064631A1 (en) | Engineering antigen binding to, and orientation on, adjuvants for enhanced humoral responses and immunofocusing | |
| TW202320845A (zh) | 用於預防及治療2019冠狀病毒病(COVID—19)之SARS—CoV—2多重表位肽/蛋白質疫苗 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |