CN109938878B - 用于人工心脏瓣膜装置的液压输送系统及相关方法 - Google Patents
用于人工心脏瓣膜装置的液压输送系统及相关方法 Download PDFInfo
- Publication number
- CN109938878B CN109938878B CN201910044090.7A CN201910044090A CN109938878B CN 109938878 B CN109938878 B CN 109938878B CN 201910044090 A CN201910044090 A CN 201910044090A CN 109938878 B CN109938878 B CN 109938878B
- Authority
- CN
- China
- Prior art keywords
- delivery capsule
- fluid
- delivery
- heart valve
- sheath
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/02—Prostheses implantable into the body
- A61F2/24—Heart valves ; Vascular valves, e.g. venous valves; Heart implants, e.g. passive devices for improving the function of the native valve or the heart muscle; Transmyocardial revascularisation [TMR] devices; Valves implantable in the body
- A61F2/2427—Devices for manipulating or deploying heart valves during implantation
- A61F2/2436—Deployment by retracting a sheath
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/95—Instruments specially adapted for placement or removal of stents or stent-grafts
- A61F2/9517—Instruments specially adapted for placement or removal of stents or stent-grafts handle assemblies therefor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/95—Instruments specially adapted for placement or removal of stents or stent-grafts
- A61F2/962—Instruments specially adapted for placement or removal of stents or stent-grafts having an outer sleeve
Abstract
用于治疗自然心脏瓣膜的系统、装置和方法被在此公开。一种用于输送人工装置到患者心脏的系统包括细长导管体和输送胶囊。输送胶囊可以被液压驱动以在人工心脏瓣膜装置的至少一部分上展开。输送胶囊可以在患者体内的所希望的治疗部位释放人工心脏瓣膜设备。
Description
本申请是申请日为2014年2月4日,申请号为201480019245.7,发明名称为“用于人工心脏瓣膜装置的液压输送系统及相关方法”的申请的分案申请。
对相关申请的交互引用
本申请根据35U.S.C.§119(e)要求2013年2月4日提交的美国临时专利申请号为61/760,399,名称为“HYDRAULIC DELIVERY SYSTEMS FOR PROSTHETIC HEART VALVEDEVICES AND ASSOCIATED METHODS”以及2013年2月28日提交的美国临时专利申请号为61/770,986,名称为“HYDRAULIC DELIVERY SYSTEMS FOR PROSTHETIC HEART VALVE DEVICESAND ASSOCIATED METHODS”的优先权,其以引用方式被全部合并于此。
技术领域
本技术一般涉及液压输送系统和使用相同系统的方法。特别地,一些实施例涉及用于输送人工心脏瓣膜装置的液压输送系统。
背景技术
在心脏收缩正常期间(心缩期),当左心室收缩时,二尖瓣用作单向阀以防止流动含氧血流回左心房。含氧血通过主动脉瓣可以被泵入主动脉。二尖瓣返流可以显著降低心脏的泵血效率,将患者置于严重的渐进心脏衰竭的风险。二尖瓣反流可以通过从心脏的左心室通过不适当的二尖瓣逆流入左心房来进行表征。二尖瓣反流可由一些机械上的缺陷导致。例如,二尖瓣的瓣叶、耦合到瓣叶的腱索或乳头肌可能被损坏或其他不正常。在至少一些情况下,支撑瓣叶的二尖瓣瓣环可能被损坏,膨胀或减弱,从而限制了二尖瓣充分关闭以抵住左心室高压的能力。
二尖瓣置换经常被执行以治疗二尖瓣。不幸的是,二尖瓣置换带来了独特的解剖障碍,使得二尖瓣置换术的风险且相比其他类型的瓣置换,如主动脉瓣置换,更具挑战性。这是因为,二尖瓣环通常具有非平面的几何形状的非圆形D形状或肾形形状。可能难以在自然二尖瓣内适当地安置人工二尖瓣。如果人工二尖瓣是在不适当的方向,血液可能流动通过人工二尖瓣和自然二尖瓣的瓣叶和/或瓣环之间的间隙。经皮导管可用于输送人工瓣膜。不幸的是,由于轴向跳跃或自喷射,自扩张的人工二尖瓣可以以不受控制的方式展开。人工二尖瓣不受控制展开可能导致人工二尖瓣的安置不当,造成渗漏、人工二尖瓣的迁移以及其它不想要的问题。
附图说明
本公开的许多方面可以参照下面的附图被更好地理解。附图中的构件不一定是按比例绘制。相反,重点是清楚地示出本发明的原理。此外,构件可以在若干视图中被显示为透明的,仅为了阐述的清楚起见而不是指示所示出的构件必须是透明的。
图1和图1A是根据本技术的实施例的哺乳动物心脏的示意图,该哺乳动物心脏具有适于用人工装置置换的自然瓣膜构造。
图1A-1是哺乳动物心脏的自然二尖瓣的示意性横截面侧视图。
图1B是心脏的左心室的示意图,该心脏具有在自然二尖瓣中的脱垂瓣叶,并且其适合于用根据本技术的实施例的系统治疗。
图1C是心脏的示意图,该心脏是心肌病患者的心脏并且其适合于用根据本技术的实施例的系统治疗。
图1C-1是示出自然二尖瓣瓣叶的正常关闭的心脏的自然二尖瓣的示意图。
图1C-2是心脏的示意图,该心脏显示在扩张型心脏中的自然二尖瓣瓣叶异常关闭,并且其适合于用根据本技术的实施例的系统治疗。
图1D示出了心脏的左心室中的二尖瓣反流,该心脏具有受损乳头肌,并且其适合于用根据本技术的实施例的系统治疗。
图1E示出了心脏的二尖瓣的示意性说明,该心脏显示瓣环的尺寸,并且其适合于用根据本技术的实施例的系统治疗。
图1F是心脏的示意性横截面图,该图显示了根据本技术的各种实施例的从静脉血管到自然二尖瓣的顺行法。
图1G是心脏的示意性横截面图,该图显示了根据本技术的各种实施例的通过将导管放置在导线之上所保持的心房间隔(IAS)的进入。
图1H和1I是心脏的示意性横截面图,该图显示了根据本技术的各种实施例的通过主动脉瓣和动脉脉管系统的自然二尖瓣的反流方法。
图1J是心脏的示意性横截面图,该图显示了根据本技术的各种实施例的使用跨心尖穿刺的自然二尖瓣方法。
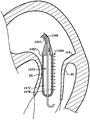
图2A是心脏和根据本技术的各种实施例的安置在心脏的自然二尖瓣中的输送胶囊的示意性横截面图。
图2B根据本技术的各种实施例示出了在展开结构中的图2A的输送胶囊和被展开的人工装置。
图3是根据本技术的各种实施例配置的用于所述人工装置的系统的等轴视图。
图4是图3的系统的远端部分的等轴视图。
图5是根据本技术的各种实施例的图4的远端部分的分解等轴视图。
图6是沿图4的6-6线截取的远端部分的横截面图。
图7是图3的系统的控制单元的横截面图。
图8是图7的控制部的内部结构的详细横截面图。
图9是沿图7的9-9线截取的控制单元的横截面图。
图10是根据本技术的各种实施例的旋转控制组件的横截面图。
图11-14是根据本技术的各种实施例从输送胶囊展开人工装置的方法一系列视图。
图15-17是根据本技术的各种实施例的从输送胶囊展开人工装置的方法一系列视图。
图18是根据本技术的各种实施例的用于输送人工装置的导管的等轴视图。
图19是根据本技术的各种实施例的图18的导管的控制单元的侧视图。
图20是沿图19的20-20线截取的控制单元的横截面图。
图21是图18的导管的远端部分的分解等轴视图。
图22是图18的导管的远端部分的横截面图。
图23-25是根据各种本技术的实施例的从图22的输送胶囊展开人工装置的方法一系列视图。
图26-29是根据本技术的各种实施例的在自然二尖瓣中展开人工装置的方法一系列视图。
图30是根据本技术的各种实施例的导管的远端部分的等轴视图。
图31和32是图30的远端部分的等轴剖视图。
图33-35是从图30中的导管展开人工装置的方法的一系列视图。
图36是根据本技术的各种实施例的导管的远端部分的横截面图。
图37是图36的保持人工装置处于部分地扩张的构造中的远端部分的横截面图。
图38是根据本技术的各种实施例的定位器的等轴视图。
图39是根据本技术的各种实施例的图36的远端部分的分解横截面图。
图40是根据本技术的各种实施例用于输送人工装置的导管的等轴视图。
图41是根据本技术的各种实施例的图40的导管的控制单元的等轴剖视图。
图42是图41的控制单元的致动机构的侧视图。
图43是图41的控制部的一部分的详细侧视图。
图44是心脏和根据本技术的各种实施例的导管的示意性横截面图,导管用于在自然二尖瓣中经心尖地(transapically)输送人工装置。
图45示出了与二尖瓣对齐的图44的导管的输送胶囊。
图46是根据本技术的各种实施例的导管的远端部分的等轴视图。
图47是根据本技术的各种实施例的定位组件的俯视图。
图48是沿图47的48-48线截取的定位组件的横截面图。
图49-53是根据本技术的各种实施例的对准输送胶囊与自然二尖瓣的方法一系列视图。
图54-56是根据本技术的另一实施例的对准输送胶囊与自然二尖瓣的方法一系列视图。
图57是根据本技术的另一实施例的心脏和安置在二尖瓣中的导管的远端部分的示意性横截面图。
图58是图57的远端部分的横截面侧视图。
图59是根据本技术的各种实施例的输送人工装置的系统的等轴视图。
图60是沿图59的60-60线截取的系统的远端部分的剖视图。
图61-65是根据本技术的各种实施例的安置图60的远端部分的方法的一系列视图。
图66是根据本技术的各种实施例的导管的远端部分的横截面侧视图。
图67是根据本技术的各种实施例的安置在自然二尖瓣中的导管的远端部分的俯视图。
图68是沿着图67的线68-68截取的远端部分的横截面侧视图。
图69根据本技术的各种实施例示出了在导引导管中的导管的远端部分。
图70示出了已被输送出图69的导引导管的输送胶囊。
图71是心脏和根据本技术的另一实施例的安置在二尖瓣中的导管的远端部分的示意性横截面图。
图72示出了图71的接触心脏的远端部分的展开的定位器。
图73和74是根据本技术的各种实施例的使用经心尖的方法安置导管的远端部分的方法的一系列视图。
图75是根据本技术的各种实施例的接合自然二尖瓣的瓣膜定位体的俯视图。
图76是沿图75的76-76线截取的心脏和瓣膜定位体的示意性横截面图。
图77是根据本技术的实施的用于输送人工装置的导管的视图。
图78-80是根据本技术的各种实施例的用于致动图77的导管的输送胶囊的方法的一系列视图。
图81-89是根据本技术的各种实施例的从输送胶囊展开人工装置的方法的一系列视图。
图90是根据本技术的各种实施例的用于输送装置进入患者的套件的的俯视图。
具体实施方式
本技术一般涉及治疗心脏瓣膜和其他解剖结构。本技术的一些实施例的具体细节将在下文中参照图1-90进行讨论。尽管关于使用人工装置的治疗自然心脏瓣膜的导管系统、人工装置和方法的许多实施例被讨论如下,但是除了在本文描述以外其他应用和其他实施例也在本技术的范围内。本领域的普通技术人员将相应地理解,本技术可以有具有额外的元件的其他的实施例,或者本技术可以有其它的不具有以下参照图1-90显示并描述的若干特征的实施例。
关于在本说明书中的术语“远的”和“近的”,除非另有规定,术语可以参照操作者和/或患者的位置在系统的部分、导管和/或相关输送装置的相对位置。例如,在提到适合于输送和定位在此描述的各种人工装置的导管中,“近的”可指更接近导管的操作者的位置或进入脉管系统的切口,而“远的”可以指更远离导管的操作者的位置或远离沿脉管的切口(例如,在导管端部的位置)。为便于参考,本公开中通篇相同的标记和/或字母被用于标识相似或类似的元件或特征,但相同的引用标记的使用并不意味着该部分应理解为是相同的。事实上,在本文中描述的许多实施例中,相同编号的部分在配置和/或功能中是不同的。本文所提供的标题只是为了方便起见。
概述
本技术一般涉及治疗在对象的身体内的一个或多个部位的系统、装置和方法。例如,本技术的至少一些实施例可被用于治疗心脏瓣膜(例如,二尖瓣,主动脉瓣,三尖瓣和/或肺动脉瓣)。该治疗可以包括,但不限于,瓣膜置换术,瓣膜修复,瓣膜交替,或影响瓣膜功能的其他手术。该装置和方法能够使用通过静脉或动脉插入心脏血管内输送导管的经皮途径。导管和方法也使用其他较少创伤的方法,包括但不限于经-心尖(trans-apical)方法,经-心房(trans-atrial)的方法,以及直接主动脉输送。在更具侵入性的方法中,该导管和方法能够使用侵入性的方法,包括开放式手术。
在一些实施方案中,导管包括配置成容纳人工装置(例如,人工心脏瓣膜装置,置换心脏瓣膜等)的输送装置。输送装置可以是被重新配置来展开人工装置的胶囊。在一些实施方案中,输送装置可以从用于保持人工装置的容纳结构移动到用于展开人工装置的展开结构。例如,所述胶囊的至少一部分可被致动(例如,液压致动,机械致动,等),以拔出或以其他方式释放人工装置的至少一部分。
胶囊可控制地展开人工装置以最小化、限制或基本上消除人工装置的不受控制的移动。在一些实施方案中,胶囊可以限制、最小化或基本上消除轴向跳跃,自喷射,和/或人工装置的移动,其可能会导致与自然瓣膜的不对准。在一些实施方案中,胶囊(例如,人工二尖瓣)保持人工装置相对于例如,自然瓣膜、自然瓣膜的相对侧上的心室或类似物的静止。
在输送结构中的人工装置可具有用于经心尖方法的约8毫米至约12毫米的外径。人工装置也可以具有适合于经由经-中隔(trans-septal)、反流,或在此描述的其他方式的通过安置在心脏中的小直径导引导管输送的低轮廓。例如,在输送结构中的人工装置可具有用于经-中隔方法的等于或小于约10毫米的外径。在一些实施方案中,经-中隔人工装置的外直径为约8mm到约10mm。在输送结构中的人工装置可具有用于反流方法的等于约8毫米到约10毫米的外径。其它尺寸也是可能的。
人工装置可以被配置为扩张到展开结构。如本文相对于人工装置所用的“展开结构”一般是指一旦在输送部位(例如,自体瓣膜部位)扩张的且受由自然解剖施加的约束和扭曲力限制的人工装置。如本文所用,“扩张的结构”一般指的当装置被允许自由扩张到无限制尺寸且不存在约束或扭曲力的时候的装置的结构。
如本文所用,术语“壳体”通常是指能够覆盖人工装置的结构。在一些实施方案中,壳体可以包括多个鞘(例如,一对鞘)。在其他实施方案中,壳体可以包括一个单一的鞘和一个盖。盖可用来关闭和打开所述鞘的开口端。在又进一步的实施方案中,壳体可以是蛤壳(clam shell)组件,其包括,但不限于,一对可移动分开来展开人工装置的蛤壳。壳体的该结构和部件可基于,例如,输送路径,治疗部位和/或人工装置的结构被选择。在仍然进一步的实施方案中,壳体是输送胶囊的一部分。
在一些实施方案中,用于输送人工装置到患者的心脏的导管包括在不同的结构(例如,用于保持所述人工装置的容纳结构,用于展开人工装置的展开结构等)之间可移动的输送胶囊和定位器(例如,经皮的细长的定位器)。该定位器从输送状态到组织-接触的状态可移动。在组织-接触的状态的定位器被配置为接触心脏的组织,以将包含在输送胶囊中的人工装置相对于自然瓣膜进行安置,同时输送胶囊被重新配置为在自然瓣膜内展开人工装置。
在一些实施方案中,系统可以包括具有控制装置的导管。控制装置可以被配置成通过液压释放人工装置的至少一部分来展开人工装置。例如,在一些实施例中,人工装置的一部分可以被机械地拔出且人工装置的另一部分可以被液压地拔出。然而,在其他实施方案中,整个人工装置可以被液压地拔出。输送胶囊可被偏压以抵消由人工装置产生的力。在一些实施方案中,例如,偏置力可以抵消由自扩张人工装置产生的力。
在一些实施方案中,例如,控制单元可被用来定位由导管承载的人工装置到治疗部位。控制单元可以包括,但不限于,螺钉致动机制来可控地移动壳体的至少一部分以拔出人工装置的第一部分。人工装置的另一部分可以在人工装置的第一部分被拔出之前、之间和/或之后被拔出。另外或替代地,控制单元可以包括用于轴向移动所述壳体的至少一部分以拔出人工装置的滑块机制。在仍然进一步的实施方案中,控制单元可以包括其它特征和/或不同的结构。
在进一步的实施方案中,用于人工心脏瓣膜植入装置的系统包括:细长的导管体和耦合到细长的导管体的输送胶囊。输送胶囊被配置为包含人工心脏瓣膜装置。输送胶囊被配置成被液压致动以展开人工装置(例如,人工心脏瓣膜装置)。在一些实施方案中,输送胶囊可包括壳体和液压机构(例如,活塞装置),其接触壳体以抑制输送胶囊从容纳结构到展开结构的移动。液压机构可以包括接触壳体的一个或多个活塞装置。另外或替代地,输送胶囊可以包括一个偏压装置,其当输送胶囊从容纳结构朝向展开结构移动时,促使输送胶囊的至少一部分朝向容纳结构。
在一些实施方案中,用于输送人工装置的系统包括:细长的导管体,一壳体,一柱塞或活塞,以及人工装置。该壳体可连接到所述细长的导管体且可包括远端鼻锥和近端胶囊。在一些实施方案中,壳体可以包括一个分离鞘。人工装置和柱塞可以被安置在壳体内以允许该壳体的液压致动。人工装置可以以受控的方式被展开,以最小化或限制人工装置的跳跃。
在进一步的实施方案中,输送人工装置的方法包括:优选地使用将人工装置保持在折叠结构中的液压致动输送装置将人工装置安置在位于自然心脏瓣膜的自然瓣环上游的第一心室中。人工装置的边缘被从输送装置展开,使得所述边缘至少部分地扩张到扩张形状,同时人工装置的主体的至少一部分保持在至少部分地折叠。在一些实施例中,当其扩张时,边缘的至少一部分位于该第一心脏腔室中。人工装置被移动以引起边缘通过与心脏组织的接合被偏转,如位于该自然心脏瓣膜的瓣叶的上游的心脏组织。例如,相对于该输送装置的纵向轴线和/或血液的流动方向的边缘的形状或边缘的角度可能随着人工装置相对于自然解剖被移动而改变。通过使用荧光,超声心电图,或其他合适的成像方式,边缘可以被可视化,以基于该边缘的偏转,确定人工装置相对于自然心脏瓣膜的瓣环的位置。人工装置的主体可以从输送装置被输送,使得它扩张成与自然然瓣环下游的心脏组织接合以固定人工装置到心脏瓣膜。
心脏生理学
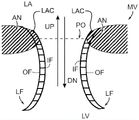
图1和1A示出了心脏H,其包括从身体接收血液并将血液从身体泵送到肺部的右心房RA和右心室RV。左心房从肺部经由肺静脉PV接收含氧血并将这样的含氧血通过二尖瓣MV泵送入左心室LV。左心室LV泵送血液通过主动脉瓣AV进入主动脉,血液从主动脉流动穿过身体。
在收缩中的正常心脏H的左心室LV被在图1A中阐述。在收缩中,左心室LV收缩且血液在箭头方向上通过主动脉瓣AV向外流动。通过二尖瓣MV的血液回流或“反流”被防止因为二尖瓣被配置为当左心室的压力比左心房LA中的压力更高时,防止逆流的“单向阀”。二尖瓣MV包括一对具有自由边缘FE的瓣叶,其符合均匀、或“接合”关闭,如图1A所示。瓣叶LF的相对端被经由称为瓣环AN的组织的瓣环区域附加到环绕心脏结构。瓣叶LF的自由边缘FE被通过腱索CT(以下称“腱”)固定到左心室LV的下部,腱包括多个被固定在每个瓣叶LF的下表面之上的分支腱。腱CT反过来被连接到乳头肌PM,其从左心室和心室间隔IVS的下壁向上延伸。
二尖瓣MV包括一对符合均匀地或“接合地”关闭的自由边缘FE的瓣叶,如图1A所示。瓣叶LF的相对端经由称作瓣环AN的组织的环形区域被附至围绕的心脏结构。
图1A-1是二尖瓣MV的组织的示意性横截面侧视图。二尖瓣MV包括瓣环AN和瓣叶LF。瓣叶LF的相对端经由瓣环AN的高密度连接组织的纤维环附至围绕的心脏结构,其与瓣叶组织LF以及心脏壁的邻接肌肉组织不同。瓣叶LF和瓣环AN是由具有变化的强度,韧性,纤维性,和灵活性的不同类型的心脏组织组成。瓣环AN的组织通常比瓣叶LF的组织更坚韧,更多的纤维,更强硬。另外,二尖瓣MV还可包含互连每个瓣叶LF至瓣环AN的独特的区域,在本文中称为瓣叶/瓣环连接组织LAC(通过图1A-1中重叠交叉阴影线表示)。二尖瓣MV的子环(subannulus)表面是位于平面PO的心室侧上的组织表面,并优选地一般面向下游,朝向左心室LV。该子环表面可以设置在瓣环AN本身之上或在自然瓣叶LF后面的心室壁之上,或者其可以包括自然瓣叶LF的表面,或者向内朝向IF或向外朝向OF,其位于平面PO下方。因而子环表面或子环组织可以包括瓣环AN本身、自然瓣叶LF、瓣叶/瓣环连接组织、心室壁或它们的组合。
图1B到1D示出在心脏中可导致二尖瓣反流的一些结构缺陷。破裂的腱RCT,如图1B所示,可引起瓣叶LF2脱垂因为不足张力被通过腱传送到瓣叶。而另一瓣叶LF1保持正常轮廓,这两个瓣叶不正确接触并从左心室LV到左心房LA的泄露将发生,如箭头所示。
反流也发生在心肌病的患者中,其中心脏扩张且增加的大小可以使瓣叶LF不能正常接触,如图1C所示。心脏的扩大导致二尖瓣扩大,使自由边缘FE不可能在收缩期接触。前、后瓣叶的自由边缘通常沿如图1C-1所示的接合C的线路接触,但显著间隙G可留在患有心肌病的患者中,如图1C-2所示。
图1D示出了受损的二尖瓣。二尖瓣反流也可发生在患有乳头肌PM的功能受损的缺血性心脏疾病的患者中。由于左心室LV在收缩期中收缩,乳头肌PM不充分收缩来实现正确的关闭。瓣叶LF1和LF2的一个和两个稍后脱垂,如图所示。泄漏从左心室LV到左心房LA再次发生,如箭头所示。
图1C1、1C2及1E说明二尖瓣的瓣叶L的形状和相对尺寸。可以看出整体瓣膜具有大致肾状,具有长轴MVA1和短轴MVA2。在健康人中的长轴MVA1通常是在从33.3毫米到42.5毫米的长度范围内(37.9+/-4.6毫米)和短轴MVA2是在约26.9至38.1毫米的长度范围内(32.5+/-9.1毫米)。然而,具有心功能降低的患者的这些值可以更大,例如MVA1可以是在从大约45毫米到55毫米的范围内,以及MVA2可以是在从约35毫米至约40毫米的范围内。接合线C的线路是弯曲的或C形,从而限定了一个比较大的前叶AL和小得多的后叶PL(图1C-1)。两个瓣叶从上级或心房侧通常可以是月牙形,在瓣膜中间的前叶AL实质上宽于在瓣膜中间的后叶。在接合线C的线路的相对端,瓣叶在角落处连接在一起被分别称为前外侧连合AC和后内侧连合PC。
图1E示出瓣环AN的形状和尺寸。瓣环AN是围绕瓣膜圆周的瓣环区域,且可以包括具有位于沿峰间轴IPD定位的第一峰部分PP1和第二峰部PP2,和沿谷间轴IVD定位的第一谷部VP1和第二谷部VP2的鞍形形状。第一和第二峰部分PP1和PP2在高度上相对含有谷部VP1,VP2的最低点的平面是较高的,在人类中典型地为约8-19毫米更高,从而给瓣膜整体鞍形形状。第一和第二峰部PP1、PP2之间的距离被称为峰间跨度IPD,其短于第一和第二谷部VP1、VP2之间的距离—谷间跨度IVD。患者的尺寸和生理可能会有所不同,并且虽然一些患者可包含不同的生理,如本文所描述的教导可被调整以适用于具有各种解剖结构条件、尺寸和形状的许多患者。例如,一些患者可能具有横跨瓣环的长尺寸和横跨二尖瓣的的瓣环的短尺寸,而不具有明确定义的峰和谷部,并且本文描述的方法和装置可被相应地配置。
进入输送部位
进入治疗部位可以通过各种技术和方法来提供。例如,微创外科手术技术,腹腔镜手术,和/或开放式外科手术可提供进入在心脏中的治疗部位。在以瓣膜为目标的手术中,微创外科手术技术可以是经皮手术,在其中进入可通过患者的脉管系统来实现。经皮手术是指在其中远离心脏的脉管系统的位置被通过皮肤进入,通常使用外科手术切割过程或微创手术,如使用针进入通过,例如,Seldinger技术。经皮进入远程脉管系统的能力是众所周知的并被在专利和医学文献中描述。例如,二尖瓣方法对可能是顺行,并且可能依赖于通过越过心房间隔进入左心房。可代替地,二尖瓣方法可是反流的,其中左心室被通过主动脉瓣进入。
使用经中隔方法,到二尖瓣的进入是经由下腔静脉LVC或上腔静脉SVC,通过右心房RA、穿过整个心房间隔IAS进入二尖瓣MV之上的左心房LA获得。如图1F所示,具有针12的导管10可以从下腔静脉LVC被推进到右心房RA。一旦导管10到达心房间隔IAS的前侧,针12可被推进,以使得它穿透隔膜,例如在卵圆窝FO或卵圆孔处进入左心房LA。在这一点上,导线可用于交换针12且导管10被撤回。
如图1G所示,通过心房间隔进入通常可通过导引导管14(例如,可操纵导管,导引鞘等)的放置,通常以被如上所述放置在导线16之上被保持。导引导管14能提供后续进入以允许导管的引入以治疗二尖瓣,如将在下文更详细地描述。
二尖瓣的顺行或经-中隔方法,如上所述,可以在许多方面是有利的。例如,顺行法的利用通常可能允许导引导管和/或人工装置(例如,人工心脏瓣膜)的更精确和更有效的居中和稳定。精确定位有助于安置人工瓣膜装置的准确度。顺行法也可减少导管和介入工具引入和操作过程中的损坏瓣下装置的风险。此外,顺行法可能会降低与在反流方法中跨越主动脉瓣相关的风险。这可以是特别相关于具有人工主动脉瓣膜的患者,其不能历经所有相当大的损坏风险或不具有相当大损坏风险。
二尖瓣的反流法的例子示于图1H-1I中。二尖瓣MV可通过从主动脉弓AA跨主动脉瓣AV的方法进行进入,并且进入二尖瓣MV下面的左心室。主动脉弓AA可通过常规的股动脉进入路径来进入,以及通过更直接的方法经由肱动脉、腋动脉或桡或颈动脉来进入。这种进入可以通过使用导线16来实现。一旦就位,引导导管14可以被在导线16之上跟踪(图1H)。导引导管14能提供后续进入,以允许人工装置的放置,如下面更详细地描述。在一些实例中,对二尖瓣的动脉反流方法因为它的优点是可优选的。反流法的使用可以消除跨中隔穿刺的需要。反流法也是心脏病学专家常用的,因而具有熟悉的优点。
至二尖瓣的额外方法是通过经心尖穿刺,如图1J所示。在这种方法中,心脏可以通过胸部切口被进入,其可以是传统的开胸或胸骨切开,或更小的肋间或子剑突的切口或穿刺。进入装置(例如,插管、导引导管,等)被稍后通过穿刺放置,通过荷包线缝合密封,在靠近心脏的心尖的左心室的壁中。本文所公开的导管和人工装置可通过此进入插管被引入到左心室。经心尖方法具有提供到二尖瓣或主动脉瓣的更短的、更直的和更直接的路径的优点。进一步的,因为它不涉及血管内进入,它可以外科医生来执行,该外科医生可能不具有介入心脏病学的必要训练以执行其他经皮方法的导管安置。
一旦进入瓣膜被实现,介入工具和导管可前进到心脏血管内并以各种方式被安置相邻于所述目标心脏瓣膜。在一些实施例中,进入输送部位可以通过患者的胸部,并且可以通过,例如,传统的经胸手术方式,开放和半开放心脏手术,腹腔镜技术,和端口进入技术被提供。这种外科进入和手术可以利用常规手术器械,包括例如,牵引器,肋牵开器,套管针,腹腔镜手术器械,镊子,拆线剪,剪刀,咬骨钳,固定装置(例如,施夹器,夹具等),缝合器,缝合线,针夹持器,烧灼器械,电外科笔,吸力装置,合拢器,和/或类似物。
在此公开的至少一些导管可以作为外科心脏手术(例如,冠状动脉旁路手术,置换和/或修复心脏部分等)的辅助来展开人工装置,以使得一个或多个人工装置可被输送,而无需执行用于进入治疗部位的附加复杂的手术。例如,在一个外科手术中,心脏瓣膜修复手术(例如,主动脉瓣修复,二尖瓣,肺动脉瓣修复等)可以在瓣膜上进行,以及瓣膜置换可以在另一个心脏瓣膜(例如,患病的主动脉瓣,二尖瓣,肺动脉瓣等)上进行。
在此公开的导管和/或人工装置可被配置为用于特定的方法或在方法中可互换。本领域技术人员能够确定用于单个患者的合适的方法并为识别的方法根据本文中所描述的实施例设计治疗装置。例如,血管内导管可以是灵活的,而经心尖导管通常可以是刚性的。导管的属性,尺寸(例如,宽度,长度等),和配置可以基于输送方法来选择。在一些实施方案中,导管可包括一个或多个腔,以用于从输送胶囊抽吸流体(例如,空气,血液等)。在一些手术中,腔可以用于在引入到患者的身体之前去除导管中的空气。
可以使用各种手术器械进入心脏,对心脏进行外科手术,并协助能够在心脏中输送人工装置的导管的操作。这样的手术器械包括,但不限于,尺寸控制环,气球,卡尺,量具,以及可基于,例如,期望的进入路径,输送装置的尺寸和配置,和心脏的解剖结构被选择的其他外科手术工具。治疗装置(例如,导管)的定向和转向可以与许多已知的导管、工具和装置组合。这样的定向可通过粗略转向治疗装置到所需的位置,然后精确转向治疗装置的部件以达到期望的结果来实现。
转向可以通过许多合适的方法来完成。例如,可转向导线可用于引入导引导管和导管用于输送人工装置到适当的位置。导引导管可以被引入,例如,使用手术切割或采用Seldinger进入患者腹股沟的股动脉。放置导线后,导引导管可以被在导线至上引入到所需的位置。可置换地,较短的和不同形状的导引导管可通过上述其它路径被引入。
导引导管可以是预先成形的,以提供相对于治疗部位的所需的取向。为了经由中隔方法进入,导引导管可在其尖端具有弯曲的形状、成角度的配置或其它合适的形状,以引导远端从该导引导管延伸通过的中隔穿刺的位置朝向二尖瓣。对于反流法,如图1H和1I,引导导管14可以具有预成形的J-端,其被配置成在它被放置在主动脉弓AA上和通过主动脉瓣AV之后使得它转向二尖瓣MV。如图1H,导引导管14可以被构造成向下延伸到左心室LV并外翻,从而介入工具或导管的定向被更紧密地与二尖瓣MV的轴线对齐。在任一情况下,预成形的导引导管可以被配置为通过穿过导向导管的内腔的管心针或硬导线的手段被校直为血管内输送。导引导管也可能有拉线或其他特征来调整其形状以用于更精确的转向调节。
治疗心脏瓣膜
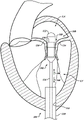
图2A是经由经心尖方法输送至二尖瓣的导管的输送胶囊和心脏的示意性横截面图示。图2B示出了在展开结构中的输送胶囊和展开的人工装置。首先参照图2A,系统100可以包括导引导管110,和通过导引导管110延伸的导管102。导引导管110被安置在经心尖开口114中,以提供进入到左心室LV。导管102可以包括液压致动输送胶囊122(“输送胶囊122”)和一个细长的导管体124(“导管体124”)。输送胶囊122可被安置在二尖瓣140的后叶130和前叶134之间。导管体124可方便地移动于向上的方向(如由箭头166所指示的)和向下的方向(如由箭头168所指示的),以将输送胶囊122安置在二尖瓣140的开口160内的期望的位置。
输送胶囊122可以从容纳结构(图2A)向展开结构(图2B)被液压地致动以展开人工装置150,如人工心脏瓣膜(人工装置150被示意性地在虚线中示出)。输送胶囊122有望减少、限制或基本上消除由与人工装置的扩张相关的力引起的人工装置150的不受控制的移动。这种不受控制的移动可以包括,例如,轴向跳跃,自喷射,或其他类型的不受控制的移动。例如,输送胶囊122被期望抑制或防止人工装置150的平移,同时人工装置150的至少一部分扩张以接触所述治疗部位。
偏压装置提供的偏置力可以限制或基本上防止由人工装置150产生的力引起的输送胶囊122的打开。例如,人工装置150的拔出部分可从部分地打开的输送胶囊122向外扩张,同时偏压装置禁止输送胶囊122的进一步打开。在一些实施方案中,例如,输送胶囊122可以以受控的方式被液压地致动朝向展开结构,以在治疗部位展开人工装置150。下面提供关于输送胶囊122的进一步的细节。
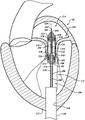
参照图2B,人工装置150处于展开结构。打开的输送胶囊122现在可以被移回到容纳结构且向近端地移到通过被展开的人工装置150。导管102可以向近端地被拉动穿过导引导管110并从患者移除。导管102可以被用来输送附加的人工装置,或者它可以被丢弃。
图3是包括导管102、导线208和流体系统206的系统100的等轴视图。流体系统206被配置为将流体输送到导管102,以液压地操作输送胶囊122。导管102可以包括手持式控制单元210(“控制单元210”),被配置来提供转向能力(例如,输送胶囊122的360度旋转,输送胶囊122的180度旋转,3轴转向,2轴转向等)。在一些实施方案中,例如,控制单元210可包括旋转控制组件214(“控制组件214”)和转向机构216。控制组件214的旋钮224可被旋转以使输送胶囊122绕其纵向轴线230转动。转向机构216的旋钮组件240可以被用于通过将其远端部分绕一横向轴线弯曲而将导管102转向。在其它实施例中,控制单元210可包括不同的特征和/或具有不同的布置。
流体系统206可以包括流体源250和线251,其连接流体源250到导管102。流体源250可包含可流动物质(例如,水,盐水等),并且可以包括,但不限于,一个或多个加压装置,流体连接器,配件,阀,或其它流体部件。加压设备,例如,可以包括泵(例如,正排量泵,柱塞泵等),注射泵(例如,手动操作的注射泵),或能加压可流动物质的其它设备。线251可包括,但不限于,一个或多个软管,管,或可流动物质通过的其它组件(例如,连接器,阀等)。
在一些实施方案中,流体源250可以包括控制器252,其包括但不限于一个或多个计算机,中央处理单元,处理装置,微处理器,数字信号处理器(DSP),和/或专用集成电路(ASIC)中。为了存储信息,例如,控制器252可以包括,但不限于,一个或多个存储元件,诸如易失性存储器,非易失性存储器,只读存储器(ROM),和/或随机存取存储器(RAM)。所存储的信息可以包括,泵送方案,病人信息,和/或可执行程序。控制器252还可以包括手动输入装置(例如,键盘,触摸屏等)或自动输入装置(例如,计算机,数据存储装置,服务器,网络等)。在其他实施方案中,控制器252可以包括不同的特征和/或具有不同的布置。
图3显示了在导线208上行进的导管102。导线208包括近端部分260,远端部分262和主体264。近端部分260从控制组件214向近端地延伸,以及远端部分262向远端地延伸超过输送胶囊122。下面参照图11更详细地讨论,导线208可以用来引导输送胶囊122进入自然心脏瓣膜。
图4是根据本技术的各种实施例配置的导管102的远端部分的等轴视图。输送胶囊122,例如,可包括配置成保持人工装置150(在虚线中示意性示出)的壳体268。壳体268可包括远端鞘270和近端鞘272。远端鞘270可包括封闭的远端274和远端容纳部分275。远端274可以具有导线-接收开口276,并且可以具有无创伤配置(例如,基本上部分球形形状,钝的配置,圆形配置等),以限制或防止伤害或创伤组织。远端容纳部分275可以包含人工装置150的远端部分。
近端鞘272可包括近端容纳部分284,锥形部分287和导引部分290。近端容纳部分284可以包含人工装置150的近端部分,并且可以与远端容纳部分275相配合。锥形部分287可具有截头圆锥形状,部分球形形状,或其他合适的结构以用于当输送胶囊122被向近端地拉动通过对象时,基本上防止或限制损伤或创伤组织。导引部分290可紧密地围绕导管体124。
在远端鞘270和/或近端鞘272可全部或部分地由金属,聚合物,塑料,复合材料,及其组合或能够保持人工装置150的其他材料制成。在一些实施方案中,远端容纳部分275可以是由金属或其它刚性材料制成的管形件(例如,具有大致圆形的横截面,大致椭圆形横截面等的管状部分)。在一些实施方案中,远端鞘270或近端鞘272可被配置为包含整个瓣膜人工装置150。
图5是导管102的远端部分的分解等轴距视图。参见图5可最好地看到,输送胶囊122可包括活塞装置292和偏压装置294。活塞装置292可包括远端头部组件300,近端头部组件304和连接器310。连接器310可包括分别连接到远端和近端头部组件300、304的端部330、350。
远端头部组件300可包括头部320和密封部件322。头部320可包括通孔331和用于接收密封部件322的通道332。近端头部组件304可以包括头部340和密封部件342。头部340可包括用于接收该密封件342的通道352和保持器360。
保持器360被配置为保持所述人工装置150,并可以包括轮毂362和以支柱364a,364b,364c(统称为“支柱364”)形式的维持特征。支柱364绕轮毂362周向间隔开。在示出的实施例中,三个支柱364径向向外延伸。然而,在其他实施方案中,支柱364的数量可以增加或减少,支柱364可被均匀地或不均匀地绕轮毂362布置。当人工装置150处于输送结构(例如,折叠状态,未展开状态等)中时,支柱364可穿过人工装置150的接收特征(例如,开口,孔,孔眼等),以抑制、防止或基本消除人工装置150沿输送胶囊122的纵轴230的移动。
当被展开时,人工装置150可沿支柱364径向扩张以移动朝向展开结构(例如,扩张结构)。例如,在一些实施例中,人工装置150可移动经过支柱364的端部以在其自身的弹簧负荷下脱离输送胶囊122。在其他实施方案中,这些支柱364可向内移动到轮毂362中,以释放人工装置150。保持器360还可以包括以钩、夹子或能够保持并释放人工装置的其他类型的特征的形式的一个或多个的维持特征。在其他实施方案中,支柱364可具有相对于人工装置150的不同的布置。
密封部件322和342被定位以分别接合远端鞘和近端鞘270和272,且可全部或部分地由硅,橡胶,聚合物,弹性体,及其组合,或其他适于形成密封的柔顺材料制成。在一些实施方案中,密封构件322,342中的一个或两个均是垫片或O形环,其全部或部分地由橡胶制成。在其它实施例中,密封部件322,342可以是囊状密封。其它类型的密封部件322,342可以被使用,如果需要或期望的话。
图5示出了由导管体124承载的偏压装置294。如本文所用,“偏压装置”通常是指一个或多个偏压构件,诸如线性弹簧,非线性弹簧,或能够提供偏置力的其它装置。在一些实施方案中,例如,偏压装置294可包括产生基本恒定的展开力的线性弹簧以用于展开人工装置150。在其他实施方案中,偏压装置294可包括产生不同的展开力的非线性弹簧以用于展开人工装置150。偏压装置294可以由金属、聚合物,或其组合制成。在金属实施例中,偏压装置294可全部或部分地由钢(例如,弹簧钢),镍钛(例如,镍钛诺),或其它合金制成。在一个具体的实施方案中,例如,偏压装置294是螺旋弹簧,其由镍钛诺制成。在又一个实施例中,偏压装置294是已被切割(例如,激光切割)的螺旋模式的金属海波管。偏压装置294可具有近端372,远端374,和主体376。近端372可邻近导管体124的肩部380。导管体124可包括延伸穿过偏压装置294的狭窄部分381和加宽部分383。加宽部分383限定肩部380。导管体124可以全部或部分地由塑料、热塑性弹性体(例如,树脂,如),或其他柔性材料制成。在一些实施方案中,导管体124可以是大致刚性,以用于使用例如,经心尖方法的输送。
图6是根据本技术的各种实施例配置的导管102的远端位置的部分示意性横截面图。远端鞘270,近端鞘272,和头部组件300,304配合以限定容纳和主室400。容纳室被配置为包含人工装置150。容纳室400的等份可设置在远端鞘270和近端鞘272之中,或容纳室400可以具有更大的部分或者甚至其全部被包含在远端或近端鞘之中。密封件322被定位成密封地接合所述远端鞘270,以形成流体室410(例如,流体密封的室或分离的流体室)。密封构件342被定位以密封地接合所述近端鞘272,以形成流体室412。流体室410、412可以被从容纳室400流体地密封。可流动物质可以被输送到流体室410以在远端方向(由箭头416指示的)上移动远端鞘270以拔出人工装置150的上游或心房部分424。流体可以被输送到流体室412以在近端方向(由箭头指示418的)移动近端鞘272以拔出人工装置150的下游或心室部分426。
所述远端鞘270的远端部274可包括壁440和通道444。杆450可被定位在通路444的至少一部分中。杆450可包括,例如,耦合到远端鞘270的远端部451,和定位在活塞装置294的腔454内的维持头部530。尽管未示出,杆450可以是中空的以接收导线。远端容纳部分275包括近端开口端432和圆柱形侧壁460。圆柱形侧壁460可包括内表面462和外表面464。密封构件322可以物理地接触内表面462以形成密封(例如,气密密封,流体密封等等)。
如参见图6可最好地看到,近端鞘272的近端容纳部分284可以包括远端开口端470和封闭的近端部472。远端开口端470由远端鞘270的近端开口端432接收。在一些实施方案中,密封件可以由远端开口端470和近端开口端432形成。近端鞘272的导引部分290具有限定了内腔490的侧壁488。近端鞘272可以进一步包括向内延伸入腔490的停止件496。当近端鞘272向近端地移动时(由箭头418所指示的),停止件496可以接触偏压装置294。
导管体124的狭窄部分381延伸通过偏压装置294,并且可以包括一个或多个端口500(端口500在图6中被识别)。流体可以沿流体腔388流动,通过端口500,并进入流体室412。端口500的数量,大小,和位置可被选择,以达到进入流体室412的流体的所需的流动。在停止件496和狭窄部381之间的密封件和/或导引部分290和加宽部分383之间的密封件509可以帮助实现在室412中的所需的流体压力。
尽管未示出,导管体124可包括多个腔。流体腔,例如,可提供与流体室410的流体连通,以及另一流体腔可以提供与流体室412的流体连通。流体可独立地被输送到各流体室410,412并从各流体室410,412除去。在一些实施例,在第一压力下的流体可以被输送到流体室410以移动所述远端鞘270。在相同或不同的时间,处于第二压力的流体可以输送到流体室412以移动近端鞘272。第二压力可以等于或不同于第一压力。
图7是图3的控制单元210的部分示意性横截面视图。控制单元210可进一步包括枢接机构218。枢接机构218包括一滑块组件519和耦合器520。滑块组件519可包括杆518和旋钮521。杆518可以具有螺纹接合螺纹保持器527的内螺纹的外螺纹。拉线523可以将耦合器520耦合到导管体124,使得关于旋转525的轴线的旋钮521的旋转引起杆518的轴移动。杆518可以向远端地或向近端地移动以分别减少或增加在拉线523上的张力以枢接导管102。在一些实施方案中,拉线523可被拉紧,例如,以向上或向下弯曲导管体124。可替代地,拉线523可以被拉紧以在其他方向弯曲或枢接导管体124。
管状部件531可耦合到导管体124和旋钮224(图3)。锁定特征529(例如,螺钉,紧固件,或类似物)被配置为可释放地接合所述管状部件531。例如,锁定特征529可以在锁定位置以安全地保持管状部件531,以防止导管体124的旋转。锁定特征529可以被移动到解锁位置,以允许管状部件531和导管体124的旋转。在其他实施例中,锁定特征529可以具有不同的布置和/或不同的特征。
图8是被配置为与图7的控制单元一起使用的连接器组件533的详细的横截面图。连接器组件533,例如,可以包括接合件534和旋转件538。接合件534被配置成流体地耦合线251到导管体124。线251耦合到接合件534的入口537。旋转构件538可以可旋转地将导管体124耦合到壳体517。
图9是沿图7的线9-9截取的具有旋钮组件240a,240b(统称为“旋钮组件240”)的控制单元210的横截面。旋钮组件240可被操作以移动输送胶囊122。例如,旋钮组件240a可被旋转以移动输送胶囊122到右侧,且旋钮组件240b可以被旋转以移动输送胶囊122到左侧。旋钮组件240可以被用来弯曲导管体124向左或向右,同时枢接机构218可以被用来移动弯曲导管体124向上或向下。旋钮组件240可以大致类似于彼此,因此,除非另有说明,一个旋钮组件的描述适用于另一个旋钮组件。在其他实施方案中,旋钮组件240可以包括不同的特征和/或具有不同的布置,例如,在相反的方向上可控制地移动导管体124。
旋钮组件240a,240b可以通过拉线542a,542b分别连接到导管体124。旋钮组件240A包括耦合到滑轮545a的旋钮543a。导线542a缠绕着滑轮545a,使得旋钮543a的转动可以增加或减少从滑轮545a伸出的拉线542a的长度。例如,旋钮543a可以被旋转以将线542a缠绕滑轮545a以增加线542a的张力。旋钮543a可被在相反的方向上被旋转以从滑轮545a解开线542a以降低线542a的张力。控制单元210还可以包括耦合到壳体517的应力释放特征516。应力释放特征516,例如,可被配置以围绕导管体124,并且可以由柔性材料制成。在其他实施方案中,然而,控制单元210可以不包括应力释放特征516或应力释放特征516可以包括不同的特征。
图10是图3的控制组件214的横截面视图。控制组件214可包括密封组件548和旋钮224。旋钮224可被固定地耦合到管状构件531。旋钮224,例如,可以绕旋转546的轴被转动,以引起管状构件531的相应的转动。在其他实施方案中,控制组件214可以包括不同的特征和/或具有不同的特性。
图11-14是展开人工装置150的方法的一系列视图。如下面更详细描述的,输送胶囊122被配置成在患者的二尖瓣140之内被安置。远端鞘270可以被液压地致动以拔出人工装置150的心房端424。拔出的心房端424可向外移动以接合二尖瓣140的组织,同时输送胶囊122保持人工装置150的心室端426。近端鞘272可被液压地致动以拔出人工装置150的心室端426。拔出的心室端426可向外移动以接合二尖瓣140的组织。
图11,例如,示出了在心脏H的顶点512形成的开口510以进入左心室LV。开口510可以是切口,其通过例如,针,切削工具,或导管(例如,针式导管)形成。导引导管110可以向远端地移动穿过开口510并进入左心室LV。导引导管110被定位在开口510中后,导线208可以通过导引导管110被移动并被定位在后叶和前叶130,134之间。导线208的远端部分262可以被移动进入左心房LA。在一些实施方案中,远端部分262可以是无创顶端(例如,挠性顶端,弯曲顶端,圆形顶端等),以预防、抑制或基本防止损伤心脏组织。
在图11所示的布置中,输送胶囊122准备好被在后叶和前叶130,134之间移动。当二尖瓣140打开和关闭时,输送胶囊122可以在导线208上前进。当二尖瓣140被关闭时(如图11所示),所述后叶和前叶130,134可以围绕导线208密封。此外,当二尖瓣140打开时,导线208可以方便地前进通过二尖瓣140。
图12示出了输送胶囊122,其被安置在后叶和前叶130,134之间。位置指示器之间(例如,以标记物501的形式)可被承载在近端鞘272之上。例如,输送胶囊122可以绕其纵向轴线230转动以将标记物501对准二尖瓣140。标记物可以位于所述远端鞘270的外表面上,位于近端鞘272的外表面上,位于输送胶囊122的内部部件之内,或位于其他合适的位置。在一些实施方案中,标记物可以是核磁共振成像-引导输送的谐振标记。在进一步的实施方案中,标记物可以是超声下可见的超声心电图标记。其他类型的标记都可以使用。在一些程序中,通过使用在输送胶囊122的后侧上的标记物,人工装置150的后侧可以与后叶130对准。另外或替代地,在输送胶囊122的前侧上的标记物可以被用于将输送胶囊122的前侧对准前叶134。
图12还示出了人工装置150准备好被展开。例如,流体系统206(图3)被配置成将流体输送到导管102,并且流体可向远端地沿着流体腔388,524流动并进入室410。流体填充室410并引起远端鞘270在远端方向上的移动。人工装置150和远端鞘270之间的摩擦,如果有的话,可能导致在人工装置150上的拉动。然而,输送胶囊122被配置为保持人工装置150,以防止,例如,人工装置150的无意中的远端移动。远端鞘270可以向远端推进,直到头部530接触停止件532。
图13示出了在远端鞘270已经移动到打开或展开位置的远端鞘270。人工装置150的拔出的心房端424已移动穿过开口540(如箭头所示),以允许心房端424径向扩张。心房端424的心房边缘427可以扩张到其完全展开结构(示出)以接合二尖瓣140圆周周围(例如,大部分或整个圆周)的自然心脏组织。在一些手术中,心房边缘427可以接触自然瓣环AN,靠近要么在心房要么在心室中的自然瓣环AN的组织,自然瓣叶,和/或适合于接触人工装置150的其他组织。例如,心房边缘427可以接触瓣叶/瓣环连接组织和靠近自然瓣环AN的瓣叶的组织。在自我扩张的实施方案中,径向不受约束的心房端424在拔出后扩张。在其他实施方案中,扩张器可以用来扩张未拔出的心房端424。例如,气球形式的扩张器可以被定位在人工装置150内,并且可以被充气来展开心房端424。
输送胶囊122可被期望以基本上防止人工装置150的轴向移动。例如,保持器360能防止当心房端424扩张时人工装置150的鞘套部分的平移。在一些实施例中,人工装置150的扩张的部分可在人工装置150的鞘套的部分上拉动。人工装置150将以不受控制的方式展开,但保持件360抑制人工装置150的轴向平移。在一些实施方案中,保持器360可以保持近端鞘272相对于二尖瓣140基本上静止。如图12和13所示,人工装置150的轴向位置可以在心房端424的整个扩张中被维持。
此外,由偏压装置294所施加的力可足以防止近端鞘272在近端方向上的不受控制的移动。例如,图13的部分扩张的人工装置150可接触并施加力分量(例如,轴向力分量,近端地定向的力分量等)到近端鞘272的远端470。被压缩的偏压装置294能促使近端鞘272在远端方向上抵消力分量。因此偏压装置294可以抑制、限制或基本上防止由人工装置150引起的近端鞘272在近端方向上的移动。偏压装置294的特征(例如,弹簧常数,施加的力与挠度曲线,等等)可以基于将由所述人工装置150产生的力来选择。线性弹簧例如,可以与人工装置一起使用,以产生基本恒定的展开力(例如,大致恒定的近端地定向力分量)。非线性弹簧可以与人工装置一起使用,例如,产生不同的展开力。
在一些实施例中,偏压装置294可提供可变力。当从人工装置150向输送胶囊122上推动的力是最高的且在输送胶囊和人工装置之间的阻力是最低的时候,可变力通常可以是最大值。随着人工装置150从输送胶囊122拔出时,人工装置的越来越大的部分被露出输送胶囊外部,且由人工装置的露出部分施加的促使输送胶囊到打开结构的力在增加。同时,保留在输送胶囊122中的人工装置150的表面区域在减少,从而减少了在人工装置150和输送胶囊122之间的摩擦阻力。因此,在一些实施方案中,由偏压装置294施加的力随着人工装置150被拔出而增加。在一些实施例中,偏压装置294可以是弹簧,其施加随着弹簧位移而增大的力。在一些实施例中,偏压装置294可包括多个弹簧。例如,弹簧可以具有低弹簧常数,以抵消由人工装置150施加到传递胶囊122的较小的力。另一个弹簧可以具有相对大的弹簧常数,以抵消由人工装置150施加到输送胶囊122较大的力。在一些实施例中,偏压装置294可偏置,使得远端鞘270和/或近端鞘272可以在偏压装置开始施加力之前移动一个预定距离。在第一弹簧(例如,具有低弹簧常数的弹簧)开始变形之前,远端鞘270和近端鞘272可以移动一个短距离(例如,1毫米-5毫米)。偏压装置294的第二弹簧(例如,具有高弹簧常数的弹簧)可在输送胶囊122接近展开结构时开始变形。弹簧的数量和特性可以被进行选择,以实现人工装置150的所需的展开。
图13示出了在闭合位置的近端鞘272。在操作过程中,流体可沿腔388流动,通过端口500,并进入室412中。室412的流体压力可以增加,直到流体压力引起近端鞘272的近端移动。在所述流体室412中的压力克服了偏压装置294的偏压力时,近端鞘272可向近端地移动,从而压缩偏压装置294。在一些实施方案中,近端鞘272的行进距离可以大致正比于室412中的流体压力,使得室412中的流体压力可以被增加以可控制地移动近端鞘272。
在一些实施例中,人工装置150(在扩张结构中)包括大体截头圆锥形,钟或其他喇叭状。特别是,心房端424可以具有大于在不受约束的展开结构中的下游或心室端426的直径的直径。例如,当心房端424离开开口540时,心房端424通常可以在近端方向上产生的第一力。当心室端426离开近端鞘272时,它通常可以在近端方向上产生第二力。在本实施例中,人工装置150与远端和近端鞘进行交互,使得第一力大于第二力。在其它实施例中,当在其输送结构和在其扩张结构时,人工装置150可沿其长度具有大致管状的形状和均匀的直径。在其他实施方案中,人工装置150可具有其它布置。
在近端鞘272的远端470向近端地移动经过人工装置150的心室端426后,心室端426可从支柱364径向向外移动,以接触后叶和前叶130,134。图14,例如,示出了在其整个轴向长度被拔出后的人工装置150。人工装置150可包括,但不限于,一个或多个锚固件,其接合自然瓣膜140以便于,例如,抵抗心缩力,防止人工装置150的上游迁移,等等。在一些实施例中,人工装置被配置为接合自然瓣膜140的子环组织。参照图1A-1和图14一起,如本文所用的“子环”是指位于自然孔口的平面PO之上或下游DN(图1A-1)的二尖瓣140的一部分。自然瓣孔的平面PO(图1A-1)是一个大致垂直于血液流动通过瓣膜的方向并含有长轴MVA1或短轴MVA2中的任一或两个(图1E)的平面。
人工装置150可包括被配置为接合自然瓣叶130,134的向内的表面的上游锚固件,其可以被向外推动并在自然瓣环之下被折叠。瓣叶130,134,例如,可以接合瓣环AN的心室侧,并且可以防止进一步在上游方向被推动,从而保持锚固件在自然瓣环的平面下方。组织接合元件可以穿透瓣叶130,134,瓣环AN的组织和/或其它组织,以稳定和牢固地固定人工装置150。在一些实施方案中,锚固件的一些部分可在瓣环AN上放延伸,且锚固件的至少一些部分在子环位置接合组织,以防止人工装置150朝着左心房LA的迁移。人工装置150被配置成符合二尖瓣环AN的不规则形状,有效地密封人工装置150抵靠自然瓣AN以固定人工装置150,并防止瓣膜周围渗漏。人工装置150,例如,可以是人工装置(例如,人工心脏瓣膜装置),如在以下被公开的人工装置中的一个或多个:(1)2012年6月21日提交的国际PCT专利申请号PCT/US2012/043636,题为“PROSTHETIC HEART VALVE DEVICES AND ASSOCIATEDSYSTEMS AND METHODS”;(2)2011年10月19日提交的美国临时专利申请号61/549,037,题为“SYSTEM FOR MITRAL VALVE REPLACEMENT”;(3)2012年3月1日提交的美国临时专利申请号61/605,699,题为“SYSTEM FOR MITRAL VALVE REPLACEMENT”;和(4)2012年10月19日提交的国际PCT专利申请号PCT/US2012/061215,题为“DEVICES,SYSTEMS AND METHODS FORHEART VALVE REPLACEMENT”。这些参考文献的每一个在此通过引用整体并入本文。例如,本文公开的输送导管可包括含有人工装置的鞘。鞘可以是一个分离鞘包括但不限于,远端鼻锥和近端胶囊,如在2012年3月1日提交的美国临时专利申请号61/605,699,题为“SYSTEMFOR MITRAL VALVE REPLACEMENT”中公开的。输送导管还可以包括于2012年3月1日提交的美国临时专利申请号为61/605,699,题为“SYSTEM FOR MITRAL VALVE REPLACEMENT”中公开的其它特征(例如,鞘,系绳,活塞,停止件,缆线等),将通过引用被全部合并的其他参考文献。然而,将应当理解的是,其它类型的人工装置也可以由输送胶囊进行展开。
在图示的实施例中,远端鞘270行进的距离DD可以大致上小于人工装置150的轴向长度L。例如,行进的距离DD可以小于人工装置150的轴向长度L的约70%,60%的或50%。在其他实施例中,但是,行进的距离DD可以具有相对于人工装置150的长度L的不同的值。在一些实施例中,每个鞘270,272可以包含大约人工装置150的一半。鞘270,272的行进距离DD、DP可以是大致相等,使得鞘270,272可以分别移动进入左心房LA和左心室LV,而不会接触心脏壁。在具体的实施方案中,远端鞘270可拔出人工装置150约8毫米到约16毫米,而近端鞘272可拔出人工装置150的约8毫米到约16毫米。长度L,例如,可以是约16毫米至约32毫米。在其他实施方案中,然而,该鞘270,272可被配置成拔出人工装置150的更多或更少和/或长度L是可以变化的。
继续参照图14,输送胶囊122可以返回到容纳结构。特别是,流体可流出室412和向近端地穿过腔388,且偏压装置294能促使近端鞘272返回到闭合位置。此外,流体可流出室410以移动远端鞘270返回到闭合位置。在一些实施例中,抽成真空以从一个或两个室410,412中抽取流体。另外或替代地,一个或多个偏压装置可以移动远端鞘270。
在输送胶囊122被移动到容纳构造之后,它可以被向近端地拉动穿过被展开的人工装置150并进入左心室LV。输送胶囊122可以被拉入导引导管110和从对象除去。其它技术可以用于从心脏取出导管102。
结合图11-14讨论的上述方法可以被修改以通过经中隔或反流方式输送人工装置150。例如,导管体124的长度,输送胶囊122的尺寸和导管102的转动性可以根据所选择的传送路径(例如,经由主动脉瓣,经由静脉脉管等)被选择。此外,各种类型的可视化技术可以与结合图11-14所讨论的方法一起使用。例如,可视化可用于帮助输送,定位,操作,和/或移除导管102。例如,荧光透视,计算机断层扫描(CT),磁共振成像(MRI),超声波或其它成像技术可以帮助在输送人工装置150之前、之间和/或之后评估进入路径,输送路径,治疗部位,和导管102和/或人工装置150的位置。
图15-17是根据本技术的各种实施例的从输送胶囊600展开人工装置的方法的一系列视图。输送胶囊600可包括大体类似于结合图2A-14所讨论的输送胶囊122的特征和功能的特征和功能,除了如下面详细描述。
图15,例如,是表示输送胶囊600的局部示意性横截面图,其包括机械致动的远端鞘604,液压致动的近端鞘606和活塞装置610。人工装置620(在虚线中示出)位于容纳室622中,其可以从流体室684中分离。
在远端鞘604可包括主鞘体640以及杆642(例如,实心轴,空心轴等)。主鞘体640包括管状部分643和一封闭的远端645。杆642可固定地耦合到封闭的远端645且延伸通过细长导主体648(“导管体648”)的腔646。杆642可向远端地移动,以从闭合位置(图15)到打开位置(图16)移动远端鞘604。在一些实施方案中,杆642可手动移动。在其他实施方案中,然而,驱动机构可以移动杆642。驱动机构可以包括,但不限于,螺杆驱动机构,气动驱动机构,或其它类型的能够提供线性运动的机构。
图16示出了被拔出的人工装置620的远端650。例如,远端650可向外扩张,如箭头670,672所指示的,而活塞装置610能够抑制人工装置620的近端698。在人工装置620的未被拔出的部后扩张后,流体可以沿着腔646被输送并进入腔室684以液压地移动近端鞘606从闭合位置(图16)到打开位置(图17)。在一些实施方案中,杆642的外径可以比腔646的直径略小,以允许流体向远端地沿细长导管体648流动。另外或替代地,杆642可以具有一个或多个流动特性,如通道,凹部,腔等。偏压装置690可以被在停止件692和导管体648之间被压缩。近端鞘606的开口端699向近端地移动经过近端人工装置620的近端698,近端698被允许向外移动到展开结构。
图18是根据本技术的另一实施例配置的用于输送人工装置的导管700的等轴视图。导管700可以包括,例如,控制单元710,输送胶囊712,以及细长的导管体714(“导管体714”)。控制单元710可包括致动机构716和枢接机构719。致动机构716可以用于操作输送胶囊712。枢接机构719可以被用来调节导管体714的接合区722的结构。
图19是控制单元710的侧视图,图20是沿着图19的线20-20截取的控制单元710的横截面图。一起参照图19和20,致动机构716可以包括滑块元件730a,730b(统称为“730”),其耦合到管状部件732(图20)。管状部件732可以延伸通过细长导管体714的外管状件734延伸,并可以耦合到输送胶囊712的鞘。滑块元件730可以向近端地(由图20的箭头739所指示的)沿着细长槽744a,744b移动以在近端方向上移动管状构件732。其他类型的致动机构可以被使用,并且能够包括,但不限于,一个或多个旋钮,槽,拉线,或类似物。
图21是图18的导管700的远端部分711的分解等轴视图。输送胶囊712,例如,可以包括远端鞘720,活塞装置722,和近端鞘731。导管体714可包括耦合到活塞装置722的内部组件741,耦合到所述近端鞘731的中间部件742(例如,空心轴),和外构件734。内部组件741可延伸通过中间部件742至少一部分。在其它实施例的,然而,输送胶囊712可以包括不同的特征和/或具有不同的布置。
图22是容纳结构中的图21的输送胶囊712的远端部分711的横截面图。如参见图22可最好地看到,远端鞘720和活塞装置722可协作以限定流体室743。流体室743可以从容纳室745被流体地密封。远端鞘720可以包括杆764,其限定了导线腔748。偏压装置746可耦合到杆764,以使得远端鞘720在远端方向的位移引起偏压装置746的压缩。
远端鞘720可包括远端部721,容纳部分723,和杆764。在多件式实施例中,杆764可以是经由一个或多个紧固件,粘合剂,焊接,或类似物固定地耦合到远端鞘720的管状构件。在单件式实施方案中,远端鞘720可以通过模制工艺(例如,注塑成型工艺,压缩成型法等),机械工艺,或另一种合适的制造技术来形成。
活塞装置722可包括头部750,密封件751,和管状体752。头部750包括凸缘760,其限定开口761。管状体752耦合头部750到内部组件741,其反过来被耦合到中间构件742。远端鞘720的杆764延伸通过开口761和在头部750中的接收槽754。偏压装置746(例如,弹簧)围绕杆764。偏压装置746的装配区749(图23)可以被固定地耦合至杆764。在其它实施方案中,偏压装置746可以具有不同的布置和/或包括不同的特征。
图23-25是展开人工装置770的方法的一系列视图。图23,例如,是输送胶囊712与近端鞘731在打开位置的横截面图。图24是输送胶囊712与远端鞘720在中间位置的横截面图,以及图25是输送胶囊712在展开结构的横截面图。通常,近端鞘731可以被机械地驱动以拔出人工装置770的近端772,且远端鞘720可以被液压驱动以拔出人工装置770的远端774。展开人工装置770的方法的各种细节将在下面讨论。
如上文参考图22,活塞装置722可保持人工装置770,且滑块元件730a(图20)可以被移动以机械地驱动近端鞘731从关闭位置(图22)到打开位置(图23)。更具体地,图23显示了人工装置770的未被拔出的近端772准备好向外扩张通过间隙781,由箭头782所指示。人工装置770的远端774可以通过沿着腔输送流体并经由端口790进入流体室743被拔出。在一些实施方案中,导线可被安置在腔748中。流体可在导线(未示出)和杆764之间的空间中沿着腔748向远端地流动。在其他实施方案中,在输送流体之前,导线可从腔748除去。
图24示出接触凸缘760的偏压装置746的端部796。被压缩的偏压装置746可在近端方向上施加力,以防止远端鞘720和/或人工装置770的不受控制的运动。在室743中的流体压力可以被增加以在远端方向上可控制地移动远端鞘720。在远端鞘720的开口端800向远端地移动经过人工装置770的远端774之后,远端774可以被允许向外扩张。参照图25,近端鞘731可以使用致动机构716(图18)从打开位置(图25)回到关闭位置(图22)。偏压装置746可以促使远端鞘720从打开位置(图25)回到关闭位置(图22)。
图26-29是使用经中隔方法展开心脏H中的人工装置770的方法的一系列视图。图26中,例如,示出了安置在二尖瓣MV中的导线800,以及图27示出了安置在二尖瓣MV中的输送胶囊712。图28示出了处于部分打开结构中的输送胶囊712,而图29示出了在展开结构中的输送胶囊712和展开的人工装置770。
首先参照图26,导线800被安置成延伸穿过二尖瓣MV和进入左心室LV。导引导管810可以被安置通过隔膜813中的穿刺或开口811,并且输送胶囊712可以被输送出导引导管810且被沿着导线800推进。
图27示出了安置在后叶和前叶812,814之间的输送胶囊712。人工装置770的上游或心房边缘815可相对于二尖瓣MV被安置。近端鞘731可向近端移动以拔出人工装置770的上游或心房端772,同时人工装置770的下游或心室端774被活塞装置722保持。
接下来参照图28,被拔出的心房端772向外扩张以接触二尖瓣MV。直至心房端772接合自然组织,人工装置770的心室端774由活塞装置722保持在远端鞘720之内,以防止人工装置770相对于导管体714的的轴向移动。在人工装置770的展开的部分是安装在二尖瓣MV之中后,流体被输送通过细长导管体714以液压地移动远端鞘720从关闭位置(图28)到打开位置(图29)。更具体地说,图29示出了处于完全展开构造的人工装置770。输送胶囊712然后可以返回到闭合配置,通过左心房拉出,并从心脏H除去。
图30是根据本技术的又一实施例配置的导管的远端部分的等轴视图。在本实施例中,导管的远端部分837可包括输送胶囊842和细长导管体844(“导管体844”)。输送胶囊842可包括液压地可致动的鞘850和盖组件852。在本实施例中,鞘850被配置成大体上包含人工装置880的整个长度,而盖组件852用于覆盖鞘850的开口近端871。
图31和32是图30的远端部分837的等轴横截面图。一起参照图31和32,导管体844可包括内轴845和外构件或轴846。内轴845例如,延伸通过盖组件852的腔849,并连接到活塞装置854。外构件846可以是围绕盖组件852的导引部分847的管状构件。控制单元可以耦合到导引部分847。
输送胶囊842可进一步包括鞘限制机构860(“限制机构860”),其具有被配置成提供相反于鞘850相对于活塞装置854的运动方向的阻力的系绳862。在一些实施方案中,例如,系绳862提供阻力以抵抗鞘850相对于活塞装置854的远端移动。阻力可以被克服以移动鞘850,并补偿人工装置所产生的力,如果有的话。在一些实施方案中,例如,系绳862可以最小化、限制或基本上消除由人工装置产生的力的作用,如果有的话,以防止或限制人工装置的不受控制的移动(例如,轴向跳动和自我喷射)和/或鞘850的不受控制的移动。
图32示出了系绳862,其具有近端部864至少部分地缠绕活塞装置854的头部866的轮毂869。系绳862的远端部分870(图31)可以固定地耦合到鞘850。例如,一个或多个紧固件(例如,紧定螺钉,销等)或其它特征(例如,夹具,焊接等)可以固定地耦合远端部分870到鞘850。在一个实施例中,系绳862通过一个或多个螺钉(例如,平底固定螺钉)被锁定就位。在其他实施方案中,然而,该系绳862也可以被使用其它合适的技术固定。扭矩(例如,约11盎司-英寸的扭矩)可以适用于螺钉,这反过来摩擦地保持系绳862。系绳862的远端部分870可接着被切割为所需的最小长度且被容纳在鞘850的帽879(例如,空心帽)中。另外或替代地,远端部分870可以绕鞘850的内部组件(例如,线轴,销等)缠绕。鞘850的内部组件可以被除去以调节连接活塞装置854到鞘850的系绳862的长度。在一些实施例中,系绳862可以是由镍钛诺、弹簧钢、塑料或它们的组合制成的丝。在一个具体的实施方案中,系绳862是直径为约0.012英寸(0.35毫米)的金属丝(例如,包括镍钛诺,弹簧钢等的丝)。其它直径可以基于展开人工装置所需的力来选择。图示的限制机构860具有单个系绳862。在其他实施例,然而,可以使用任何数量的系绳。此外,该限制机构860可包括,但不限于,一个或多个偏压装置,例如弹簧。偏压装置能促使输送胶囊842朝向容纳配置。
图33-35示出了展开人工装置880的方法。更具体地,图33示出了容纳结构中的输送胶囊842,图34示出处于部分打开结构中的输送胶囊842,以及图35示出了在展开结构中的输送胶囊842。参照图33,鞘850的开放的近端部871被在盖组件852的开放的远端部895中接收。流体可以沿着腔881流动并进入流体腔892。流体的足够体积可以被输送到流体室892以推动鞘850。当液压力(例如,在远端方向上的力分量)克服由限制机构860提供的阻力,鞘850在远端方向上相对于活塞装置854移动。在一些实施方案中,系绳862可以沿着螺杆(例如,紧固螺钉)滑动,以允许鞘850的远端移动。例如,系绳862可以相对转矩加载紧固螺钉滑动,其将压力施加到系绳862,以允许鞘850的远端移动和以受控的方式拔出人工装置。在一些实施方案中,系绳862可以变形(例如,塑性变形,弹性变形等)。在一些实施方案中,例如,系绳862最初经历弹性变形。在流体室892中的液压力可以被减少以允许系绳862返回到其初始状态,以拉动鞘850返回到闭合位置(图33)。在其他实施方案中,系绳862可以最初经历永久变形。图34示出了向外延伸通过开口890的人工装置880的被拔出的部分892。在流体室892中的流体体积可以被增加以移动鞘850从中间位置(图34)到打开位置(图35)。
图36是根据本技术的各种实施例配置的导管的远端部分的横截面图。远端部分904可包括输送胶囊910和细长导管体940(“导管体940”)。输送胶囊910,例如,包括鞘912,活塞装置914,以及棘轮元件924形式的定位器。鞘912包括中空内杆944,其延伸通过棘轮元件924,以使得棘轮元件924促进遍布整个活塞冲程的实质部分(例如,遍布大部分的活塞冲程)的人工装置的受控的输送。偏压装置930可以对抗人工装置962的自喷射负载(如果有的话),以用于遍布大部分的活塞冲程的人工装置962的受控的输送。
鞘912和盖916可以限定容纳室960。导管体940可包括耦合到活塞装置914的外构件942和耦接至鞘912的内杆944。偏压装置930的安装部分952可被固定地耦合到内杆944。活塞装置914包括一活塞头920和密封部件922。棘轮元件924可以固定地连接到活塞头920,并且可以包括接合结构926a,926b(统称为“926”)。
图36和37示出了展开人工装置962的方法。例如,盖916可以向近端地沿细长导管体940移动。流体可沿内杆944的腔972流动并通过端口980。流体可以填充流体室915,并导致鞘912的远端运动。图37示出偏压装置930的端部982接触接合结构926。偏压装置930,例如,可以施加偏置力,其可以通过液压力被克服,以进一步在远端方向上移动鞘912。人工装置962向外移动通过间隙970。棘轮元件924可在偏压装置930内被自落座,并确保偏压装置930被适当地安置。在一些实施方案中,接合构件926可以相对于弹簧端982居中。棘轮元件924可以抑制或防止活塞头920的旋转。
图38是配置了根据本技术的实施方式的棘轮元件924的等轴视图。棘轮元件924可以包括,例如,管状的主体1000和多个接合特征926。接合特征926可以是,但不限于,手指,缺口构件,悬臂部件,或能够与偏压装置930配合的其它特征。在一些实施方案中,接合特征926可以向内延伸,以紧密地围绕内杆944(图37)。在一些实施方案中,接合特征926可被偏压抵靠内部杆944,以使得接合特征926的端部可滑动地接触内连杆944。在其它实施例中,棘轮元件924可以包括不同的特征和/或具有不同的布置。
图39是准备好组装的输送胶囊910的局部示意性横截面侧视图。棘轮元件924可以便于输送胶囊910的组装。内杆944的一端1004可以被插入到棘轮元件924的开口1006。接合特征926可以帮助将端1004引导到外构件942中。活塞装置914可被移动到鞘912的内部区域1020,使得密封件922(图36和37)与鞘912的内表面1028形成密封。偏压装置930(图32和33)然后可被耦合到内杆944。
图40是根据本技术的各种实施例的被配置用于输送人工装置的导管1108的等轴视图。导管1108可包括细长的导管体1110(“导管体1110”),控制单元1123,和输送胶囊1100。输送胶囊1100,例如,包括液压致动的远端鞘1125和机械致动的近端鞘1127。该控制单元1123可以包括用于致动近端鞘1127的驱动机构1130,用于相对于控制单元1123旋转所述导管体1110的旋转控制组件1131,接合机构1132,和侧转向组件1134。控制单元1123,例如,具有和图3的控制单元210类似的的特性和功能,除了如下面详细描述的。
图41是控制单元1123的横截面等轴轴测图,以及图42是驱动机构1130的侧视图。参照图40-42一起,驱动机构1130可以包括回缩锁定机构1175(图40)和驱动机构1139。通常,回缩锁定机构1175(“锁定机构1175”)可用于锁定和解锁驱动机构1130。当驱动机构1130被解锁时,用户可以旋转的手柄1140以移动近端鞘1127。
如最好参见图41,驱动机构1130可以包括手柄1140,驱动构件1142,和连接组件1144。驱动构件1142可以包括连接到手柄1140的近端端部1160,连接到所述连接组件1144的远端部分1143(图42),以及螺主体1146。主体1146延伸穿过内螺纹轴环1151,它是由外部壳体1152保持。在一些实施方案中,驱动构件1142是致动螺杆。驱动构件1142的长度,螺距和其他特性可基于,例如,近端鞘1127的期望行程被选择。
参考图42,连接组件1144可包括轮毂组件1162和配件1164。轮毂组件1162可以包括主体1170和耦合器1172。主体1170可以包括螺纹特征,如螺母(例如,带螺纹的导螺杆螺母,低摩擦螺母等),或有螺纹的通道。在一些多件式实施例中,例如,主体1170可以包括一个或多个螺母。在单件式实施例中,主体1170可具有内螺纹通道。主体1170的接收特征1177(例如,开口,孔等)可接收锁定机构1175的柱塞1173(图40)。
该耦合器1172被配置为接合配件1164,使得耦合器1172平移引起配件1164沿着轴1180的平移。在一些实施例中,耦合器1172沿着配件1164的相对侧延伸。在其他实施例的中,耦合器1172可以是一个销,紧固件,或能够将轮毂组件1162耦合到配件1164的其它结构。配件1164可以是压缩接头,其固定地耦合到轴1180。
参考图42和43一起,停止件1184可以沿着轴1180被安置,并且可以被平移地固定至壳体1152(图43),以限制配件1164的行进距离。停止件1184的纵向长度可以被增加或减少,以减少或增加配件1164的行进长度。在操作中,用户可以手动旋转手柄1140(由图40中的箭头1141表示)以在近端方向上位移轮毂组件1162(由图42中的箭头1218表示)。随着轮毂组件1162沿致动部件1142移动,耦合器1172在近端方向上移动配件1164(图42中的箭头1219表示)。以这种方式,当手柄1140被旋转时,轮毂组件1162和配件1164可以一起移动。
如从图42可最好看到,配件1164可以包括接合耦合器1172的螺纹1176形式的接合特征。用户可以旋转手柄1194(图40和41),以旋转轴1180和配件1164以相对于轮毂组件1162移动配件1164。
图43是图41的控制部1123的一部分的详细侧视图。旋转的控制组件1131可包括安装装置1190,配件组件1192和手柄1194。配件组件1192,例如,可以包括一对配件1199A、1199B。配件1199A、1199B可以是,但不限于,鲁尔配件或其他类型的配件,可以建立与轴1180和其他组件的流体连接,例如流体管线或其他流体源。
再参考图40,用户可以旋转转向把手1210和手柄1212以转向输送胶囊1100朝着目标部位。旋转控制组件1131可用于绕细长导管主体1110的纵向轴线旋转地定位输送胶囊1100和人工装置。在一些实施例中,人工装置的后侧可以与后叶对齐,例如,使用位于人工装置后侧上的标记,位于人工装置后侧上的标记,和/或鞘1127,1125中的一个或两个上的标记。一旦输送胶囊1100的被定位在目标部位,手柄1140可以绕旋转轴1214(图42)旋转以受控制的方式回缩近端鞘1127。
固定工具(例如,夹具,止血件等)可以用于定位输送胶囊1100。导管主体1110包括螺母1204,其耦合到外引导鞘1123的远端1206。固定工具能握住螺母1204以手动定位输送胶囊1100。这样的实施方式可以采用开放式或半开放式的程序进行手动定位。螺母1204可以是六角螺母或其它类型的配置成由固定工具夹持的螺母。
人工装置可以具有优选的输送方向。例如,如果治疗部位是在二尖瓣中,人工装置的结构可被选择以匹配二尖瓣的解剖结构。人工装置可以被移动到期望的方位(例如,相对于输送部位的希望的旋转位置,相对于输送部位的希望的轴向位置,等等)。因为输送胶囊可以是大致对称(例如,绕其纵向轴线旋转对称),所以可能难以确定人工装置相对于输送部位的方位(例如,旋转位置)。系统、导管和用于相对于自然解剖结构定向人工装置的特征将结合图44-76被讨论。用于定向人工装置的特征可以结合到在此公开的导管(例如,结合图1F和图2A-43所讨论的导管)中。
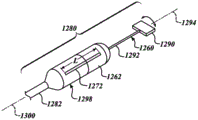
图44示出了经心尖导管1250,其被配置用于在二尖瓣MV内输送人工装置。导管1250可包括以旋转定位组件1260(“定位组件1260”)形式的定位组件,和输送胶囊1262。定位组件1260被定位在二尖瓣MV的开口1270中。定位组件1260的内部瓣膜定位器1290和输送胶囊1262上的标记1272可以用于在相对于二尖瓣MV的期望的旋转位置处定位输送胶囊1262。内部瓣膜定位器1290优选可透过射线,被由非透射性材料组成或含有标记或染料(例如,不透射线染料),或者其可以具有耦合或固定到它的不透射线标记。另外,也可以使用超声波或其它合适的技术来可视化。当二尖瓣MV关闭时,二尖瓣MV可以移动内部瓣膜定位器1290从未对准的位置(示于图44的虚线中),到在图45中所示的对准方位。随着医师使用,例如,荧光透视,可视化装置,输送胶囊1262可以绕其纵向轴1263旋转以将标记1272移动到相对于定位器1290的对准位置(图45)。
图45示出了与内部瓣膜定位器1290旋转地对准的输送胶囊1262。在这种布置中,标记1272和内部瓣膜定位器1290可以位于同一平面。对准的输送胶囊1262然后可以向远端地推进到二尖瓣MV中。
图46是根据本技术的各种实施例配置的导管的远端部分1280的等轴视图。远端部分1280可包括,例如,定位组件1260,输送胶囊1262,以及细长的导管主体1282。定位组件1260可包括内部瓣膜定位器1290和杆1292。内部瓣膜定位器1290被配置为围绕旋转1294的轴旋转。标记1272可以大致平行于输送胶囊1262的纵向轴1300延伸。标记1272的长度可被选择,以允许标记1272的取向的方便的判定。在一些实施方案中,长度L通常等于被包含在输送胶囊1262中的人工装置的长度。标记1272可以是横向相邻于人工装置并被用于轴向地对准人工装置。在图示的实施方式中,标记1272可以位于输送胶囊1262的外表面1298上。在其他实施方案中,然而,标记1272可以位于沿着输送胶囊1262的内表面,嵌入输送胶囊1262的侧壁,或在另一期望的位置。此外,标记1272可以具有较宽范围的不同配置(例如,一系列平行线,点,或其他形状,Z字形结构,蛇形配置,等等)并且可以在适合于评估输送胶囊1262的定向的不同方向处。当人工装置被装载到输送胶囊1262中,人工装置的方向可基于标记1272的位置被选择。例如,人工装置的一个特征(例如,锚固件,定位部件,或类似的)可从被成角度地从标记1272偏移或成角度地与标记1272对准。例如,用于接触瓣叶的锚固件可从标记1272偏移大约90度的角度(例如,大致垂直于纵向轴1300的平面内的角度)。
图47是定位组件1260的一部分的俯视图,和图48是图47的定位组件1260沿着线48-48截取的横截面图。参考图47和48一起,在内部瓣膜定位器1290可被旋转地耦合到杆1292。在其他实施方案中,内部瓣膜定位器1290固定地耦合到杆1292,其可旋转地耦合到输送胶囊1262。内部瓣膜定位器1290可具有大致平面的形状,并且可以具有被选择为允许二尖瓣MV的自然功能的长度L,宽度W,和厚度t(图48)。长度L可小于二尖瓣的开口的长度。宽度W可以被选择,以使得当输送胶囊1262转动时,二尖瓣的瓣可以牢固地保持内部瓣膜定位器1290。当二尖瓣关闭时(图50),自然叶密封内部瓣膜定位器的相对面,以密封并防止血液穿过二尖瓣MV的反流。
内部瓣膜定位器1290可以包含增强观察的材料。例如,定位器内部瓣膜1290可以全部或部分地由不透射线的材料制成,以提供在荧光透视下的观察。在一些实施方案中,定位器内部瓣膜1290可包括一个或多个标记(例如,不透射线标记,超声心动图标记,等等)。内部瓣膜定位器1290的标记物和标记1272可以同时观察(图46)。在一些实施方案中,定位器内部瓣膜1290是具有非平面配置的舵(例如,旋转舵)。非平面配置可以基于内部瓣膜定位器放置在在其中的解剖学特征的配置被选择。在其他实施方案中,然而,内部瓣膜定位器1290可包括其它特征和/或具有不同的布置。
参考图48,杆1292可以包括一个或多个旋转特征1306(例如,环形带,轴承等),其允许内部瓣膜定位器1290相对于杆1292的旋转。杆1292可以限定导线内腔1310,并且可以全部或部分地由塑料,热塑性弹性体(例如,树脂如),金属,或它们的组合制成。在非导线实施例中,杆1292可具有实心的横截面。
图49-53示出了在二尖瓣MV内定位输送胶囊1262的一种方法。通常,内部瓣膜定位器1290可以被定位在二尖瓣MV内。二尖瓣MV可以引起内部瓣膜定位器1290从不对准位置到对准位置的旋转。输送胶囊1262可与内部瓣膜定位器1290对准。在对准输送胶囊1262后,输送胶囊1262被插入二尖瓣MV,以及人工装置可以被展开。
图49示出了位于二尖瓣MV的前叶AL和二尖瓣MV的后叶PL之间的导线1314。导线1314的尖端1316可以被定位在左心室中。在本实施例中,内部瓣膜定位器1290可以在导线1314之上移动并插入打开的二尖瓣MV的开口1320。图49显示了在未对准方位中的内部瓣膜定位器1290。当二尖瓣MV在内部瓣膜定位1290上闭合时,前叶AL和后叶PL可引起内部瓣膜定位器旋转1290以使得内部瓣膜定位器1290与由接合区1328限定的弯曲接合线1330对准,接合区1328由前叶AL和后叶PL限定。图50示出了内部瓣膜定位器1290大致平行于接合线1330。随着二尖瓣MV的打开和关闭,它可以继续沿接合线1330重新定位内部瓣膜定位器1290。
参看图50,标记1272相对于导管的纵轴1300成角度地从内部瓣膜定位器1290偏移。导管主体1282可以围绕纵向轴线1300顺时针旋转,如箭头1342所指示的,以将标记1272与定位器1290对准。图51(和先前所述的图45)示出了与内部瓣膜定位1290相对于纵向轴线1300对准的标记1272。图45中,例如,示出了当从侧面观察时在上-下方向中与内部瓣膜定位1290对准的标记1272。
图52显示了准备输送到二尖瓣MV的输送胶囊1262。输送胶囊1262可以向远端地平移,由箭头1291指示的,无需可察觉量的旋转以维持输送胶囊1262的对准。标记1272可以被观察以确认对准一直被维持。图53示出了输送胶囊1262准备展开人工装置(未示出)。标记1272,例如,可以大致沿接合线1330被定位。输送胶囊1262定位可包括保持特征(例如,柱,销,或类似物),可以抑制人工装置的转动,从而保持人工装置的对准。当适当地定位时,输送胶囊1262可以被打开以释放人工装置。
图54-56是根据本技术的另一实施例定位导管的远端部分1345的方法的一系列视图。参看图54,例如,远端部分1345可包括输送胶囊1350和定位组件1352。输送胶囊1350可包括标记1356形式的对准特征。定位组件1352可以包括内部瓣膜定位器1360和杆组件1362。杆组件1362,例如,可以包括远端杆构件1370,近端杆构件1372,和对准特征1374。在此实施例中,远端杆构件1370固定地耦合到内部瓣膜定位器1360和对准特征1374。近端杆构件1372可旋转地耦合到远端杆件1370和固定地耦合到输送胶囊1350。对准特征1374可以包括,但不限于,一个或多个轴承,旋转,或允许在杆构件1370、1372之间的旋转的其他特征。
在操作中,当二尖瓣MV关闭时,前叶AL和后叶PL可以移动内部瓣膜定位1360到对准位置。图55和56,例如,示出了定位器内部瓣膜1360是对准位置。图55的输送胶囊1350可被关于其纵向轴线1357旋转(如由箭头1377所表示的)以对准标记1356和对准特征1363。例如,图55的输送胶囊1350可以关于纵向轴线1357以顺时针方向旋转大约90度,以对准标记1356和对准特征1363。图56示出了关于纵向轴线1377彼此对准的标记1356,1363。图56的对准的输送胶囊1350准备被推进到二尖瓣MV。
结合图44-56所讨论的输送胶囊可以在瓣膜中定位输送胶囊之前被与二尖瓣对准。然而,当输送胶囊被定位在二尖瓣中时,导管的输送胶囊也可以与二尖瓣对准,如以下结合图57-66所讨论的。
图57中,例如,示出了定位在二尖瓣MV的导管的远端部分1400。图58是远端部分1400的横截面图。通常,远端部分1400可以与组织交互,以指示所述远端部分1400相对于心脏的一个或多个自然解剖结构的位置。在一些实施方案中,例如,远端部分1400可以施加流体力至组织以改变组织的位置,从而指示远端部分1400的取向(例如,纵向位置,旋转位置等)例如,远端部分1400可输出流体以移动前叶,后叶,或二尖瓣MV的其它解剖结构。另外或替代地,远端部分1400可以输出流体以相对于二尖瓣MV的一个或多个解剖结构移动远端部分1400。
图57和58示出以端口1404的形式的位置指示器1403,其输出流体(由箭头表示)以移动前叶AL从初始位置1420到移动位置1422(示于虚线)。前叶AL的位置可被观察,例如,通过超声心动图。输送胶囊1402可关于旋转1426的轴进行旋转,以将输送装置1402与二尖瓣MV旋转地对准。由流体引起的前叶AL的位移的最大量通常将在当端口1404面向前叶AL时发生。一旦输送胶囊1402位于期望的方位,输送胶囊1402可以输送人工装置。
图59是根据本技术的各种实施例配置的用于输送人工装置的导管系统1430的等轴视图。该导管系统1430可以包括,例如,细长导管主体1432(“导管主体1432”),控制单元1434,和流体系统1442。流体系统1442被配置成独立地将流体输送给线路1444,1446。流过线路1444的流体可以向远端地沿导管主体1432输送并和流出端口1404。例如,流过线路1446的流体可以向远端地沿导管主体1432输送且被用于液压操作输送胶囊1402。流体系统1442可包括,但不限于,一个或多个加压装置,容器(如,内部罐或容器),阀,控制器,和/或功率源。控制单元1434可以包括致动器元件1450,其可沿着槽1460移动以移动输送胶囊1402的盖1462。在其它实施例中,控制器元件1450可被用于向远端地移动鞘1464。
图60是沿图59的线60-60截取的导管系统1430的远端部分1400的横截面图。输送胶囊1402可包括,例如,布置于鞘1464内的活塞装置1470(以虚线被示意性示出)。端口1404,例如,可包括多个通孔1474(只有一个端口被标识)。通孔1474可远离彼此间隔开并被定位在线性布置中,以向二尖瓣MV施加径向引导的流体力。在一些实施方案中,例如,通孔1474在基本上平行于输送胶囊1402的纵向轴线1480的方向上基本均匀地彼此隔开。在其他实施方案中,然而,通孔1474可以限定蜿蜒结构,大致Z字形结构,或其它合适的构造和样式。
图61-64示出了根据本技术的一个实施例的定位输送胶囊1402方法。人工装置1472可以具有优选展开位置以接合,例如,心脏的组织(例如,前叶AL,后叶PL,前环AA,后环PA等)。例如,相邻于端口1404的人工装置1472的一部分可被构造成接合前部组织(例如,前叶AL,前环AA等)。一旦输送胶囊1402是在所期望的位置,输送胶囊1402可释放人工装置1472。
首先参照图61,输送胶囊1402准备要插入二尖瓣MV。导线1482可在瓣叶PL,AL之间被插入。在定位导线1482之后,输送胶囊1402可以在导线1482之上被向远端地推进并进入二尖瓣MV。被直接定位在瓣叶PL,AL之间的输送胶囊1402的长度可以基于人工装置1472的尺寸(在图61的虚线中示意地示出),人工装置1472相对于输送胶囊1402的位置,和其它过程参数来选择。
图62示出了定位在二尖瓣MV中的输送胶囊1402。导线1482的尖端1484被定位在左心室LV中。端口1404被布置成面对前叶和后叶AL,PL之间的接合线1493(图61)。因此,如果流体被输送出端口1404,流体可沿接合线1493(图61)流动,并导致瓣叶PL,AL的最小位移。此外,后叶和前叶PL,AL的移动(如果有的话)在许多可视化技术下可能不被清楚地识别。因此,可能难以确定端口1404是面向二尖瓣的右侧还是左侧。
图63和64示出了朝向前叶AL的端口1404。参考图63,例如,前叶AL可以接触输送胶囊1402。流体可以被输送出端口1404,例如,以转移前叶AL。图64示出了流体(由箭头表示)输出朝向前叶AL。流体可被输出以维持前叶AL和输送胶囊1402之间的间隙。例如,前叶AL可以在完全打开位置和部分打开位置(以虚线示出)之间移动。在一些过程中,流体可以保持前叶AL处于完全打开的位置(例如与输送胶囊1402较远地隔开且邻近于心脏壁)。
参考图65,流体可以沿着腔1490流动,进入容纳室1435,并通过端口1404。其它结构可用于将流体输送到端口1404。流体可以是盐水或其它合适的生物相容性流体。在一些实施方案中,流体是可视流体(例如,无线电不透明流体,含有不透射线的材料或标记的流体,或类似的流体)。流体被可视以用于评估输送胶囊1402的方向。
图66是根据技术的各种实施例配置成的导管的远端部分1500的横截面图。远端部分1500可以包括,例如,输送胶囊1502,其被配置为输出流体而不破坏人工装置1510。流体F1,F2可以独立地输送通过胶囊1502以定位输送胶囊1402并在不同的时间致动输送胶囊1502。输送胶囊1502可包括远端鞘1520和近端鞘或盖1522。远端鞘1520可以包括位置指示器1528和通道1530。位置指示器1528可以包括与通道1530流体连通的多个间隔开的端口1534。通道1530向近端地延伸穿过远端鞘1520的杆1540。为了定位输送胶囊1502,流体F1可以向远端地沿着通道1530朝远端鞘1520的端1544流动。流体F1流动穿过通道1530的U形部分1550,并继续向近端地沿供给通道1552前进。流体F1被配置为沿着供给通道1552流动并流出端口1534。
流体F2可以向远端地沿腔1560流动,并且在一些实施方案中,可以操作活塞装置1562(以虚线示意性地示出)。流体F2可以被输送以从近端鞘1522松开远端鞘1520。流体F1然后可以被输出以定位输送胶囊1502。在定位输送胶囊1502后,流体F1的流量可被抑制或停止,以及流体F2可用于液压致动远端鞘1520。在其他实施方案中,输送胶囊1502可包括不同的布置和/或具有不同的特征。
图67和68示出了远端部分1600,其包括细长导管体1602(“导管体1602”),输送胶囊1604,和以机械定位器组件的形式的位置指示器1610,其在输送通过导向导管1660的输送状态和接合心脏组织的组织接触状态之间可移动。定位器组件1610,例如,可包括以可展开构件1620a-f(统称为“可展开构件1620”)的形式的定位器阵列,其被配置来帮助相对于二尖瓣MV定位输送胶囊1604。例如,可展开构件1620可以被展开以引导输送胶囊1604进入二尖瓣MV,以保持输送胶囊1604被位于二尖瓣MV内,和/或以其它方式(例如,轴向对准,旋转地对准,等)相对于心脏的解剖结构定位输送胶囊1604。可展开的构件1620可全部或部分地由不透射线的材料制成,或者可包含一个或多个不透射线标记。构件1620可以在荧光透视下进行查看,以帮助定位输送胶囊1604和/或定位心脏的解剖特征。在一些实施方案中,构件1620的尖端1621可以携带用于定位瓣环1634,心房壁AW的内表面1632,或其它感兴趣的解剖特征的不透射线标记。
图69示出了定位在导向导管1660中的输送胶囊1604,而图70示出了在输出导向导管1660之后的输送胶囊1604。首先参照图69中,导向导管1660可以保持构件1620在输送状态(例如,折叠结构,未扩张结构,等等)。输送胶囊1604可以在导引导管1660的端部1664被移出开口1666。随着构件1620退出端部1664,构件1620可以移动到组织接触状态(例如,展开结构,扩张结构等)。
接下来参考图70,构件1620c,1620f被示出在输送状态(以实线示出)和组织接触状态(以虚线示出)之间变化。构件1620,例如,可自展开或使用展开设备(例如,一个或多个气球,推杆等)可被展开。构件1620可经由一个以上的关节,枢轴,焊接,或类似物被耦合到近端鞘1654。构件1620的尺寸(例如,长度,横截面轮廓等)、组成和/或数量,可根据治疗部位和/或将被接触的组织的位置而选择。在图示的实施例中,以柔性细长臂或尖端形式的六个构件1620可全部或部分地由金属,聚合物,或其它适合接触心脏H的组织的材料制成。然而,在其它实施方案中,构件1620的数量可以改变。
由构件1620限定的横向尺寸可以选择,以避免构件1620通过二尖瓣MV。在一些实施方案中,例如,横向直径可以大于由瓣环1634(图68)的内部区域限定的内径(例如,最小直径,最大直径等)。构件1620可被配置为接触心房壁的相对侧。
展开人工装置1657的一个方法包括输送输送胶囊1604通过左心房LA并进入二尖瓣MV。具体地,输送胶囊1604的构件1620可以被移动到图68的组织接触状态。被定位成接触瓣环1634的组织的构件1620可能比瓣叶的组织的柔顺性更低。因此,当构件1620接触在瓣环1634的心房侧上的心脏组织,构件1620可以防止或限制输送胶囊1604在远端或下游方向的移动。构件1620f的尖端1621f可以变形,以防止心房壁AW的损坏或创伤。在一些过程中,导管体1602可以施加远端或下游指向的力到输送胶囊1604以保持构件1620落座在瓣环1634之上,同时输送胶囊1604展开人工装置1657。在一些实施例中,构件1620还可以配置分别接触前叶和后叶AL,PL的瓣叶基部1640,1644。远端鞘1656可以向远端地被推进到左心室LV,而构件1620基本上防止近端鞘1654的远端移动。在人工装置1657被展开后,导管可以被向近端地拉动和从对象除去。输送胶囊1604也可以在经心尖方法中使用。
图71显示了定位在二尖瓣MV中的输送胶囊1680,图72示出了以可展开构件1684a,1684b(统称“构件1684”)的形式的定位器。参见图71和72一起,输送胶囊1680可以包括盖1688和鞘1689。构件1684可以向远端地移动通过通道1686a,1686b并移出对应的开口1690a,1690b。在一些实施例中,构件1684可以被手动推动通过通道1686a,1686b。在其他实施方案中,然而,构件1684可以是使用,例如,推进器(例如,机动推杆组件,致动器等)被移动。构件1684可具有无创伤尖端1687a,1687b(图72),其带有预先形成的弯曲配置,钝端,或类似物。另外或替代地,尖端1687a,1687b可由高度柔顺的材料制成,其变形以防止或限制心脏的组织的损伤或创伤。
如图71最好地看出,输送胶囊1680可以在导线1692上传输并进入二尖瓣MV。鞘1689,例如,可定位在后叶PL与前叶AL之间。开口1690a,1690b被优选定位在瓣叶PL,AL和鞘1689的之间的接触界面。构件1684a,1684b可以被移动,直到尖端1687a,1687b接触瓣环1691的心脏壁和/或组织。远端力能够被施加以按压构件1684a,1684b抵住瓣环1691,从而落座构件1684。在一些实施例中,轻微的压力可以连续地施加以保持输送胶囊1680在落座的位置。人工装置1693可以在保持其相对于二尖瓣MV的纵向位置时进行展开。构件1684a,1684b可以保持抵住瓣环1691,以防止人工装置1693在上-下方向中的移动,同时人工装置1693被展开。
图67和68以及图71和72的定位器组件,也可以在经心尖方法中使用。以举例的方式,图67和68的输送胶囊1604可以通过左心室LV被输送到二尖瓣MV,以及构件1620可配置被落座在限定左心室LV的瓣环1634的心室侧。构件1620可被定位在输送胶囊1604的远端或心房端。构件1620的其它位置和结构也可以被使用。
图73和74示出了根据本技术的另外的实施方式的使用经心尖方法定位导管的远端部分的方法。参考图73,例如,输送胶囊1700准备被落座在二尖瓣MV中,并包括液压可致动鞘1702和定位器组件,其以可展开构件1704a,1704b(统称为“构件1704”)的形式可旋转地耦合到鞘1702。构件1704可以从未展开状态或输送状态1710被移动到展开状态1712(以虚线示出)。在本实施例中,在未展开状态或输送状态中的构件1704的外表面1724被配置成大体上与主体1718的外表面1730齐平。鞘1702可以包括主体1718和接收特征1720a,1720b(图74)。接收特征1720可以包括,但不限于,凹槽,槽,或其它能够至少部分地容纳各个构件1704的特征。
图73示出枢转地耦合构件1704到主体1718的销1732。偏置构件或推杆可以促使构件1704向外。耦合到构件1704的系绳可以被用来控制构件1704朝向展开位置1712的移动。在一些实施例中,系绳可以用来保持构件1704在未展开位置1710。当系绳被延长,偏压装置移动构件1704到展开位置1712。在其他实施方案,然而,柔性构件可以耦合构件1704到主体1711。
经心尖方法可用于输送胶囊1700。输送胶囊1700可通过左心室LV进入二尖瓣MV。在构件1704的近端已经清除了二尖瓣MV之后,构件1704可以移动到展开状态1712。
在展开构件1704后,输送胶囊1700可向近端地移动,由图73中的箭头1750所指示的。图74,例如,显示具有接触心脏组织的组织接触尖端1760a,1760b(统称为“尖端1760”)的构件1704。构件1704可全部或部分地由不透射线的材料制成,或者可包含一个或多个不透射线标记,并且可以在荧光透视下被观看。在一些实施方案中,尖端1760可以携带用于定位感兴趣的解剖特征的不透射线标记。在使用活塞装置1756展开人工装置1716之后,构件1704可以返回到未展开位置1710。输送胶囊1700然后可以从心脏除去。
本文所公开的导管还可以包括其他类型的定位特征。在一些实施方案中,例如,输送胶囊可具有非对称轮廓。当输送胶囊被旋转时,输送胶囊的轮廓可以被用于确定其方位。例如,不透射的鞘可具有非对称形状。在荧光透视下,鞘的可视轮廓可以用来确定输送胶囊的旋转位置。机械位置指示器可以包括,但不限于,一个或多个推杆,可展开的臂,或其它类型的定位器组件。在一些实施方案中,流体位置指示器和机械位置指示器都可以使用。
定位体可以用于定位解剖特征,定位输送胶囊,或以其他方式识别感兴趣的特征。图75和76,例如,显示了以瓣膜定位体1800的形式的定位器,其被配置为识别二尖瓣MV的瓣叶AL,PL的位置。在观察结构中的瓣膜定位体1800可以包括可视特征1804,其分别接触前叶和后叶AL,PL的下表面1810,1812(图76)。
瓣膜定位体1800可以包括轴1820和可视化特征1804。在一些实施例中,瓣膜定位器1800是由高度可变形材料制成,以当可视化特征1804被移动到图示位置时防止破坏组织。轴1820可全部或部分地由金属,聚合物,弹性体制成,并可以是柔性的以沿输送路径导航。该可视化特征1804可包括近端部1830,远端部1834,和主体1838。近端部1830被连接到轴1820。主体1838可被配置成缠绕前叶和后叶AL,PL。
该可视化特征1804可以全部或部分地由可视化的材料制成。在实施方案中,其中可视化包括荧光透视,例如,可视化特征1804可以全部或部分地由不透射的材料制成。其它类型的材料可用于其它类型的可视化技术。可视化特征1804也可以全部或部分地由形状记忆材料,如镍-钛(例如,镍钛诺),形状记忆塑料或聚合物,铜-镍-铝合金,或类似物制成,以便在不受约束的状态采取所希望的形状。在一些实施例中,形状记忆材料可具有一种或多种形状转变温度。当形状记忆材料的温度达到形状转变温度时,可视化特征1804可以采取预定的结构。在一些实施例中,可视化特征1804可以当温血温暖可视化特征1804时改变形状。另外或替代地,流体(例如,温或热的流体),加热器(例如,电阻加热器,珀耳帖装置等)或其它类型的有源加热元件可以被用于改变可视化特征1804的温度。在非形状记忆的实施方案中,可视化特征1804可以全部或部分地由金属(例如,钢,钛,铝等),聚合物(例如,导电聚合物),或其他弹性材料制成。例如,图76的输送鞘1850可以由硬质塑料制成。随着可视化特征1804被输出输送鞘1850的端1852,可视化特征1804可以采取输送结构。
在将可视化特征1804定位在二尖瓣MV的下侧之后,输送鞘1850可以向近端地拉动以露出可视化特征1804,并允许它采取其不受约束的形状。轴1820然后缩回以移动可视化特征1804抵住前叶和后叶AL,PL。主体1838可以从1830的近端部分向后部地延伸,并围绕后叶和前叶的交点,如图75所示。当然,各种其它的形状也可以被使用,这将相对于自然解剖结构落座在已知的位置中,以提供参考,以引导人工装置的定位。
凭借施加到瓣叶的轻微压力,医师可以查看瓣叶AL,PL的基部的位置。在一些实施例中,可视化特征1804被配置为接合前叶、后叶和瓣环的接合处。因而医师能够至少部分地基于位置特征1804的位置识别瓣环和二尖瓣的其它解剖学特征的位置。
瓣膜定位体1800可以与本申请中公开的导管结合使用。例如,瓣膜定位体1800可作为被输送到心脏的导线。在定位瓣膜定位体1800之后,输送胶囊可以移动超过瓣膜定位体1800。其它类型的可视化定位体还可以被使用。在经心尖方法中,可视化定位体可以通过左心室被输送,通过二尖瓣的开口,并进入左心房。可视化定位体可以被展开以接合瓣环,瓣叶和瓣环之间的接合处,或其他感兴趣特征。
图77是根据本技术的各种实施例的输送人工装置的导管2000。导管2000可包括,例如,控制单元2010,输送胶囊2012,以及细长的导管体2014(“导管体2014”)。输送胶囊2012可包括远端鞘2030和近端鞘2032。近端鞘2032可以包括回声特征2033(例如,螺纹,凹槽等),其可以使用超声波被可视化。密封件2015可以围绕导管体2014,并且可以在使用过程中用输送鞘(未示出)来进行密封。控制单元2010可以包括致动机构2016,冲洗组件2043,和液压致动组件2051。致动机构2016被配置为机械地移动远端鞘2030并包括杆2020和锁定机构2022。杆2020可以包括细长构件2031和接触锁定机构2022的停止件2033,以限制远端鞘2030的远端移动。杆2020可以被向远端地移动以将远端鞘2030移动远离近端鞘2032,直到停止件2033接触锁定机构2022。锁定机构2022可包括螺纹构件2032,其可被操作以保持和释放细长构件2031。冲洗组件2043具有冲洗端口2042,用于接收液体以冲洗输送胶囊2012。液压驱动组件2051具有端口2050,用于接收液体以液压地移动近端鞘2032。
图78-80是展开人工装置2060(以虚线示意性示出)的方法的一系列视图。图78是在关闭结构中的输送胶囊2012的横截面图。图79是远端鞘2030在打开位置的输送胶囊2012的横截面图。图80是近端鞘2032在打开位置的输送胶囊2012的横截面图。为了装载输送胶囊2012,杆2020可以被向远端地移动以分离远和近端鞘2030,2032。人工装置2060可滑过远端鞘2030,被压缩并插入到近端鞘2032。在将人工装置2060的近端2064插入近端鞘2032之后,人工装置2060的远端2062可以被折叠,并且杆2020可向近端地拉动以保护远端2062。液体(例如,盐水,水等)可被输送到冲洗端口2042(图77)以用液体淹没室2092(图78)以从室2092除去空气,或其它不想要的流体。在装载输送胶囊2012之后,远端鞘2030可以通过移动杆2022(图77)被机械地驱动,以拔出人工装置2060的远端2062,以及近端鞘2032可被液压驱动以拔出人工装置2060的近端2064。导管2000和展开人工装置2060的细节将在下面参照图78-80进行讨论。
现在参考图78,细长构件2031固定地耦合到远端鞘2030。构件2089包括一个或多个冲洗端口2090,流体经由冲洗端口2050(图77)被输送通过该冲洗端口2090,在加载人工装置2060到输送胶囊2012之前,期间,和/或之后可用流体淹没容纳室2092。细长构件2031延伸通过活塞装置2070,斜坡2072形式的凸轮特征由人工装置2060的远端2062包围。人工装置2060可以沿着表面2073滑动,其在近端方向向内地逐渐变细或倾斜(例如,相对光滑的圆锥形表面),且无需,例如,损坏人工装置2060或从自然心脏瓣膜移出人工装置2060以促进导管2000通过被展开的人工装置2060的回缩。
图79示出了在它已被移动到展开位置之后的远端鞘2030以允许扩张人工装置2060的远端2062。远端2062可以是边缘的形式,其能够通过远端鞘2030和近端鞘2032之间的窗口或间隙2079扩张。近端鞘2032在折叠结构中保持人工装置2060的主体2081。在一些实施方案中,近端2064被活塞装置2091保持,同时远端2062扩张。
图80示出了在近端鞘2032已被液压地从容纳位置移动到打开位置(例如,展开位置)之后的在展开结构中的输送胶囊2012。流体可被输送到室3009,以克服偏压装置3003以向近端地推动近端鞘2032。活塞装置2091可固定地耦合到所述导管体2014(图77)的细长构件2095以限定室3009。
各种输送技术可被用于输送人工装置2060,包括经股,经静脉,经中隔,经心房,经主动脉,以及经心尖方法。在一些实施方案中,通过将输送胶囊2012插入切口,穿刺,或在心脏顶点的端口,输送胶囊2012可以使用经心尖方法被定位在心脏内。在输送胶囊2012被定位在心脏内之后,用户可以手动地抓握并移动机械致动机构2016来展开人工装置2060的远端2062。人工装置2060与心脏组织的交互可用于确定人工装置2060的位置。在一些实施方案中,当其与自然心脏瓣膜间隔开时,远端2062至少部分地扩张到到扩张的形状。人工装置2060的其余部分在近端鞘2032内保持折叠,导管2000可相对心脏移动,以使被扩张的远端2062,或人工装置2060的另一部分,通过接合心脏室的壁或邻近于自然心脏瓣膜被偏转。这种偏转的程度或形状可以被用来确认人工装置2060的定位。在一些实施方案中,输送胶囊2012和/或人工装置2060可以由不透射线的和可透过射线的材料制成以有助于定位。例如,图77的输送胶囊2012包含不透射线的标记1362a,1362b,其可包括不透射线材料。在定位人工装置2060的远端2062之后,近端鞘2032可以液压驱动以释放人工装置2060,其扩张并锚固至心脏瓣膜。
图81-89是根据本技术的各种实施例从导管的输送胶囊3010展开人工装置3000的方法的一系列视图。图77-80的输送胶囊2012的描述也适用于图81-89的输送胶囊3010,除了图示的输送胶囊3010不包括斜坡(例如,图78的斜坡2072)。
图81处于部分展开结构的输送胶囊3010的侧视图。远端鞘3122与近端鞘3124间隔开,以暴露人工装置3000的远端3130。在一些实施例中,远端鞘3122被机械地移动远离近端鞘3124。例如,一推杆可用于移动远端鞘3122。在其他实施方案中,远端鞘3122可液压推进。
图82是人工装置3000的远端3130的部分地展开的边缘3125的侧视图。边缘3125包括,但不限于,一个或多个支撑构件(例如,线或支柱)和耦合到一个或多个支撑构件的覆盖(例如,织物,组织,网眼等)。在一些实施方案中,覆盖被缝合或以其它方式被耦合到全部或部分地由金属或其他可视化的材料(如,不透射线的材料,回声材料等)制成的支撑构件。部分或完全地扩张的边缘3125可以通过远端和近端鞘3122,3124之间的间隙向外张开。
图83是在近端鞘3124被向近端地移动以允许人工装置3000的主体3128的一部分的扩张之后的输送胶囊3010的侧视图,其中边缘3125处于完全展开结构。图84-86示出了近端鞘3124被移动朝向图87的展开位置的阶段。
为了输送人工装置3000,输送胶囊3010可以被移动通过心脏并进入位于自然心脏瓣膜上游的室。远端鞘3122可以向远端被推进以展开人工装置3000的远端3130,以使得边缘3125至少部分地扩张。导管可以相对于心脏瓣膜移动,以使边缘3125通过接合在心脏瓣膜上游的上游心脏腔室的壁或底而偏转。图88和89是示出被落座在自然心脏瓣膜3070中的人工装置3000的视图。图88显示了展开的边缘3125,其可在心脏的室中扩张,并从心房底3090被间隔开。最初边缘3125以相对于通过瓣膜的纵向或血流方向的大约90度+/-15度的角度径向向外延伸。该导管可向近端地被拉动,使边缘3125与心房底3090接合。随着导管向近端地被拉动,边缘3125相对于其初始方位偏转逐渐变陡的角度,或者相对于纵向方向偏转逐渐变窄的角度。边缘3125的角度和形状可以使用荧光或超声波来被可视化以确认人工装置3000相对于自然瓣膜3070的位置(例如,纵向位置)。图89示出了通过与心房底3090的接合被偏转的边缘3125。结合图88和89所讨论的方法可以被执行以输送在此公开的其他人工装置(例如,结合图78-80所讨论的人工装置3000)。例如,在图26-29中所示的人工装置770的近端772可以是边缘或其它特征的形式,其可被偏转以确定人工装置770的位置。
本文所公开的导管,导管组件,人工装置,以及相关方法的实施例可以基于,例如,将要执行的过程被混合和匹配。应当理解,例如,特定元件,子结构,优点,用途,和/或不同实施例的其它特征可以适当地互换,被取代的或以其他方式与另一个配置。例如,结合图44-56所讨论的机械位置指示器可以并入结合图2A-43所讨论的导管和/或输送胶囊。通过另一个示例的方式,结合图57-65所讨论的流体的位置指示器可以并入结合图2A-43所讨论的输送胶囊。取向评估过程可以涉及,但不限于,确定(1)在导管的一个或多个特性以及目标部位之间的相对位置,(2)在导管的一个或多个特性以及人工装置之间的相对位置,和(3)导管的一个或多个特性和/或人工装置的绝对位置。
目标输送部位可以在对象中的不同位置。本文所公开的实施例可用于输送设备到在血管系统、呼吸系统、消化系统,或患者的其它系统中的目标输送部位。在血管系统中,目标输送部位可以在心脏,动脉,或类似物中。在心脏内,任何自然瓣膜可以成为目标,包括二尖瓣,主动脉瓣或三尖瓣。在呼吸系统中,目标输送部位可以是气管,肺,或类似物。在消化系统,目标输送部位可位于沿着胃,结肠,肠等。人工装置可基于目标输送部位的位置进行选择。人工装置可以是,但不限于,自扩张装置,非自扩张设备(例如,设备通过球囊扩张),支架(例如,自扩张支架,球囊扩张支架,冠脉支架,输尿管支架,前列腺支架,动脉瘤的支架,末梢支架,气管支气管支架等),移植物(例如,自扩张移植物,管腔内移植物,等等),阻塞装置(例如,间隔装置阻塞装置,卵圆孔未闭闭塞装置等),阀(例如,单向阀,鸭嘴阀,止回阀,具有瓣叶和翼的阀,等),植入物(例如,微型泵,可植入电极,等),或类似物。
图90示出了套件1900,其可以包括导管1902,设备1904,和包装1905。导管1902,例如,可以是任何在此讨论的导管。设备1904可以是人工装置,其可装载到导管1902的输送胶囊1910。在一些实施方案中,套件1900可以包括人工装置的阵列。医师可以基于,例如,对象的解剖结构选择人工装置中的一个。包装1905可以是灭菌包装,其包括,例如,托盘,包,袋,和/或类似物。
套件1900可以进一步包括容器1918和使用说明1921。容器1918可以容纳填充物质(例如,凝胶,可流动的物质,流体等)。例如,填充物质可以是润滑剂,其减少或限制设备1904和输送胶囊1910之间的摩擦。注射器1919可以用于输送填充物质进入输送胶囊1910。在一些过程中,填充物质可以在装载设备1904到输送胶囊1910之前被输送到设备1904之上。在其它过程中,填充物质在装载设备1904之前、期间和/或之后,被输送到输送胶囊1910的表面上。在其他实施例中,套件1900可以具有不同的布置和/或包括不同的特征。使用说明可以包括导管1902和设备1904的使用说明。在优选实施方案,说明将包括根据在本文中的别处所描述的方法用于将人工装置植入心脏以修复或更换自然心脏瓣膜的说明。
结论
该技术的实施例的上述详细的描述并不旨在穷举或将本技术限制于以上公开的精确形式。虽然技术的具体实施例和示例出于说明目的被描述如上,在技术的范围之内的各种等同修改是可能的,正如那些相关领域技术人员将认识的一样。例如,虽然步骤是以一个给定的顺序被呈现,但替代实施例可以以不同的顺序步骤被执行。本文所描述的各种实施例也可以被组合以提供进一步的实施例。如上所述,本发明合并了以下申请中的主题:(1)2012年6月21日提交的国际PCT专利申请号为PCT/US2012/043636,名称为"PROSTHETICHEART VALVE DEVICES AND ASSOCIATED SYSTEMS AND METHODS";(2)2011年10月19日提交的美国临时专利申请号为61/549,037,名称为"SYSTEM FOR MITRAL VALVE REPLACEMENT";(3)2012年10月19日提交的国际PCT专利申请号为PCT/US2012/061215,名称为"DEVICES,SYSTEMS AND METHODS FOR HEART VALVE REPLACEMENT"以及(4)2012年3月1日提交的美国临时专利申请号为61/605,699,名称为"SYSTEM FOR MITRAL VALVE REPLACEMENT".这些申请的每一个都以引用的方式被全部合并于此。
由上可知,可以理解的是,技术的特定的实施例已经为了说明的目的被在本文中描述,但公知的结构和特征没有被详细示出或描述以避免不必要地模糊本技术的实施例的描述。如文义许可,单数或复数术语还可以分别包括复数或单数名词。
此外,除非词语“或”被明确地限定为仅指被从参考两个或多个项目的列表中的其他项目中排除的单个项目,则在这样的列表中的“或”的使用将被解释为包括(a)该列表中的任何一个项目,(b)该列表中的所有项目,或(c)该列表中的项目的任意组合。此外,被贯穿使用的术语“包括”意指包括至少所陈述的特征,以使得任何更多数量的相同的特征和/或其他类型的其他特征不排除使用。还应当理解的是,已在本文中描述的具体实施例是出于说明的目的,但各种修改可以在不脱离本技术范围内被作出。此外,虽然该技术的某些实施例相关联的优点已经在那些实施例的上下文中进行了描述,其他实施例也可能表现出这些优点,并且并非所有实施例都需要一定表现出这样的优点以落入本技术的范围。因此,本公开和相关联的技术可包括此处未明确示出或描述的其它实施例。
Claims (8)
1.一种用于在患者的自然心脏瓣膜输送用于植入的人工心脏瓣膜装置的系统,所述系统包括:
细长的导管体,所述细长的导管体具有延伸穿过其中的流体腔;
输送胶囊,其被耦合到所述细长的导管体且被配置为在容纳结构和展开结构之间被液压地驱动,所述容纳结构用于保持所述人工心脏瓣膜装置,以及所述展开结构用于展开所述人工心脏瓣膜装置,其中,所述输送胶囊包括:
壳体;
安置在所述壳体内的活塞装置,所述活塞装置具有头部,所述头部被配置为平移地限制所述人工心脏瓣膜装置;
容纳室,所述容纳室被配置为容纳所述人工心脏瓣膜装置的至少一部分;和
流体室,其中所述流体室与所述容纳室流体地密封且与所述细长的导管体的所述流体腔流体连通;和
偏压装置,所述偏压装置被配置为当所述输送胶囊从所述容纳结构朝向所述展开结构被液压地驱动时,推动所述输送胶囊的至少一部分朝向所述容纳结构,
其中,所述输送胶囊还包括安置在所述头部和所述壳体之间的密封件,以形成流体密封并限定所述流体室。
2.如权利要求1所述的系统,其中所述壳体包括封闭的远端的第一端和开放的近端的第一端,其中当流体通过所述流体腔被输送到所述流体室时,所述壳体被轴向驱动以将安置在所述容纳室中的所述人工心脏瓣膜装置的至少一部分拔出。
3.如权利要求1所述的系统,还包括人工心脏瓣膜装置,所述人工心脏瓣膜装置安置在所述输送胶囊内并被所述输送胶囊平移地限制,其中所述输送胶囊被配置为在所述人工心脏瓣膜装置的展开的一部分被设置在所述心脏的自然瓣膜中之后释放所述人工心脏瓣膜装置。
4.如权利要求1所述的系统,其中所述偏压装置包括弹簧,所述弹簧随着所述输送胶囊从所述容纳结构朝向所述展开结构移动而被压缩,以将整个轴向长度的人工心脏瓣膜装置拔出。
5.如权利要求1所述的系统,其中所述输送胶囊被配置为通过所述输送流体进入到所述流体室以克服由所述偏压装置提供的偏压力,而从所述容纳结构移动至所述展开结构。
6.一种用于在患者的自然心脏瓣膜输送用于植入的人工心脏瓣膜装置的系统,所述系统包括:
细长的导管体;
输送胶囊,所述输送胶囊耦合到所述细长的导管体且被配置为在容纳结构和展开结构之间被液压地驱动;
偏压装置,所述偏压装置被配置为当所述输送胶囊从所述容纳结构朝向所述展开结构被液压地驱动时,推动所述输送胶囊的至少一部分朝向所述容纳结构;和
安置在所述输送胶囊内的人工心脏瓣膜装置,所述人工心脏瓣膜装置包括边缘,所述边缘被配置为在所述输送胶囊释放所述人工心脏瓣膜装置之前从所述输送胶囊展开并通过与心脏组织的接合而偏转,以将所述人工心脏瓣膜装置固定至自然心脏瓣膜。
7.如权利要求6所述的系统,其中:
所述输送胶囊包括流体室,所述流体室与容纳室流体地密封,所述容纳室被安置为靠近所述流体室,并被配置为容纳所述人工心脏瓣膜装置的至少一部分;和
所述细长的导管体包括与所述流体室流体连通的流体腔,所述输送胶囊被配置为通过沿着所述流体腔输送流体并进入所述流体室以克服由所述偏压装置提供的偏压力,而从所述容纳结构移动至所述展开结构。
8.如权利要求6所述的系统,其中所述偏压装置包括具有近端和远端的弹簧,当所述输送胶囊从所述容纳结构朝向所述展开结构移动时,所述弹簧的所述远端沿近端方向移动。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361760399P | 2013-02-04 | 2013-02-04 | |
| US61/760,399 | 2013-02-04 | ||
| US201361770986P | 2013-02-28 | 2013-02-28 | |
| US61/770,986 | 2013-02-28 | ||
| CN201480019245.7A CN105263442B (zh) | 2013-02-04 | 2014-02-04 | 用于人工心脏瓣膜装置的液压输送系统及相关方法 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201480019245.7A Division CN105263442B (zh) | 2013-02-04 | 2014-02-04 | 用于人工心脏瓣膜装置的液压输送系统及相关方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN109938878A CN109938878A (zh) | 2019-06-28 |
| CN109938878B true CN109938878B (zh) | 2021-08-31 |
Family
ID=50138006
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201910044090.7A Active CN109938878B (zh) | 2013-02-04 | 2014-02-04 | 用于人工心脏瓣膜装置的液压输送系统及相关方法 |
| CN201910043755.2A Active CN109938877B (zh) | 2013-02-04 | 2014-02-04 | 用于人工心脏瓣膜装置的液压输送系统及相关方法 |
| CN201480019245.7A Active CN105263442B (zh) | 2013-02-04 | 2014-02-04 | 用于人工心脏瓣膜装置的液压输送系统及相关方法 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201910043755.2A Active CN109938877B (zh) | 2013-02-04 | 2014-02-04 | 用于人工心脏瓣膜装置的液压输送系统及相关方法 |
| CN201480019245.7A Active CN105263442B (zh) | 2013-02-04 | 2014-02-04 | 用于人工心脏瓣膜装置的液压输送系统及相关方法 |
Country Status (6)
| Country | Link |
|---|---|
| EP (1) | EP2950752B1 (zh) |
| JP (6) | JP6280932B2 (zh) |
| CN (3) | CN109938878B (zh) |
| AU (4) | AU2014211983B2 (zh) |
| CA (1) | CA2898991C (zh) |
| WO (1) | WO2014121280A2 (zh) |
Families Citing this family (132)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102007043830A1 (de) | 2007-09-13 | 2009-04-02 | Lozonschi, Lucian, Madison | Herzklappenstent |
| US8870950B2 (en) | 2009-12-08 | 2014-10-28 | Mitral Tech Ltd. | Rotation-based anchoring of an implant |
| EP3300695B1 (en) | 2009-12-08 | 2023-05-24 | Avalon Medical Ltd. | Device and system for transcatheter mitral valve replacement |
| US11653910B2 (en) | 2010-07-21 | 2023-05-23 | Cardiovalve Ltd. | Helical anchor implantation |
| EP2654624B1 (en) | 2010-12-23 | 2023-10-04 | Twelve, Inc. | System for mitral valve repair and replacement |
| US9554897B2 (en) | 2011-04-28 | 2017-01-31 | Neovasc Tiara Inc. | Methods and apparatus for engaging a valve prosthesis with tissue |
| US10500038B1 (en) | 2011-05-20 | 2019-12-10 | Tel Hashomer Medical Research Infrastructure And Services Ltd. | Prosthetic mitral valve, and methods and devices for deploying the prosthetic mitral valve |
| CA2840084C (en) | 2011-06-21 | 2019-11-05 | Foundry Newco Xii, Inc. | Prosthetic heart valve devices and associated systems and methods |
| US8852272B2 (en) | 2011-08-05 | 2014-10-07 | Mitraltech Ltd. | Techniques for percutaneous mitral valve replacement and sealing |
| WO2013021374A2 (en) | 2011-08-05 | 2013-02-14 | Mitraltech Ltd. | Techniques for percutaneous mitral valve replacement and sealing |
| WO2013021375A2 (en) | 2011-08-05 | 2013-02-14 | Mitraltech Ltd. | Percutaneous mitral valve replacement and sealing |
| EP2741711B1 (en) | 2011-08-11 | 2018-05-30 | Tendyne Holdings, Inc. | Improvements for prosthetic valves and related inventions |
| EA201400481A1 (ru) | 2011-10-19 | 2014-10-30 | Твелв, Инк. | Искусственные сердечно-клапанные устройства, искусственные митральные клапаны и соответствующие системы и способы |
| US9039757B2 (en) | 2011-10-19 | 2015-05-26 | Twelve, Inc. | Prosthetic heart valve devices, prosthetic mitral valves and associated systems and methods |
| US9763780B2 (en) | 2011-10-19 | 2017-09-19 | Twelve, Inc. | Devices, systems and methods for heart valve replacement |
| EA201400478A1 (ru) | 2011-10-19 | 2014-10-30 | Твелв, Инк. | Устройства, системы и способы протезирования сердечного клапана |
| US11202704B2 (en) | 2011-10-19 | 2021-12-21 | Twelve, Inc. | Prosthetic heart valve devices, prosthetic mitral valves and associated systems and methods |
| US9655722B2 (en) | 2011-10-19 | 2017-05-23 | Twelve, Inc. | Prosthetic heart valve devices, prosthetic mitral valves and associated systems and methods |
| US9827092B2 (en) | 2011-12-16 | 2017-11-28 | Tendyne Holdings, Inc. | Tethers for prosthetic mitral valve |
| US9579198B2 (en) | 2012-03-01 | 2017-02-28 | Twelve, Inc. | Hydraulic delivery systems for prosthetic heart valve devices and associated methods |
| WO2013175468A2 (en) | 2012-05-20 | 2013-11-28 | Tel Hashomer Medical Research Infrastructure And Services Ltd. | Prosthetic mitral valve |
| US9345573B2 (en) | 2012-05-30 | 2016-05-24 | Neovasc Tiara Inc. | Methods and apparatus for loading a prosthesis onto a delivery system |
| WO2014022124A1 (en) | 2012-07-28 | 2014-02-06 | Tendyne Holdings, Inc. | Improved multi-component designs for heart valve retrieval device, sealing structures and stent assembly |
| WO2014021905A1 (en) | 2012-07-30 | 2014-02-06 | Tendyne Holdings, Inc. | Improved delivery systems and methods for transcatheter prosthetic valves |
| US9681952B2 (en) | 2013-01-24 | 2017-06-20 | Mitraltech Ltd. | Anchoring of prosthetic valve supports |
| US10463489B2 (en) | 2013-04-02 | 2019-11-05 | Tendyne Holdings, Inc. | Prosthetic heart valve and systems and methods for delivering the same |
| US11224510B2 (en) | 2013-04-02 | 2022-01-18 | Tendyne Holdings, Inc. | Prosthetic heart valve and systems and methods for delivering the same |
| US9486306B2 (en) | 2013-04-02 | 2016-11-08 | Tendyne Holdings, Inc. | Inflatable annular sealing device for prosthetic mitral valve |
| US10478293B2 (en) | 2013-04-04 | 2019-11-19 | Tendyne Holdings, Inc. | Retrieval and repositioning system for prosthetic heart valve |
| US10111747B2 (en) | 2013-05-20 | 2018-10-30 | Twelve, Inc. | Implantable heart valve devices, mitral valve repair devices and associated systems and methods |
| US9610159B2 (en) | 2013-05-30 | 2017-04-04 | Tendyne Holdings, Inc. | Structural members for prosthetic mitral valves |
| CA2914856C (en) | 2013-06-25 | 2021-03-09 | Chad Perrin | Thrombus management and structural compliance features for prosthetic heart valves |
| US8870948B1 (en) | 2013-07-17 | 2014-10-28 | Cephea Valve Technologies, Inc. | System and method for cardiac valve repair and replacement |
| CA2919379C (en) | 2013-08-01 | 2021-03-30 | Tendyne Holdings, Inc. | Epicardial anchor devices and methods |
| WO2015058039A1 (en) | 2013-10-17 | 2015-04-23 | Robert Vidlund | Apparatus and methods for alignment and deployment of intracardiac devices |
| CN108403261B (zh) | 2013-10-28 | 2021-02-12 | 坦迪尼控股股份有限公司 | 假体心脏瓣膜以及用于输送假体心脏瓣膜的系统和方法 |
| US9526611B2 (en) | 2013-10-29 | 2016-12-27 | Tendyne Holdings, Inc. | Apparatus and methods for delivery of transcatheter prosthetic valves |
| WO2015120122A2 (en) | 2014-02-05 | 2015-08-13 | Robert Vidlund | Apparatus and methods for transfemoral delivery of prosthetic mitral valve |
| US9986993B2 (en) | 2014-02-11 | 2018-06-05 | Tendyne Holdings, Inc. | Adjustable tether and epicardial pad system for prosthetic heart valve |
| CN110338911B (zh) | 2014-03-10 | 2022-12-23 | 坦迪尼控股股份有限公司 | 用于定位和监测假体二尖瓣的系绳负荷的装置和方法 |
| EP2918249B1 (de) | 2014-03-14 | 2020-04-29 | Venus MedTech (HangZhou), Inc. | Supraclaviculäres kathetersystem für einen transseptalen zugang zum linken vorhof und linken ventrikel |
| US9572666B2 (en) | 2014-03-17 | 2017-02-21 | Evalve, Inc. | Mitral valve fixation device removal devices and methods |
| WO2016016899A1 (en) | 2014-07-30 | 2016-02-04 | Mitraltech Ltd. | Articulatable prosthetic valve |
| US9700445B2 (en) | 2014-11-04 | 2017-07-11 | Abbott Cardiovascular Systems, Inc. | One-way actuator knob |
| US10869755B2 (en) | 2014-12-09 | 2020-12-22 | Cephea Valve Technologies, Inc. | Replacement cardiac valves and methods of use and manufacture |
| CA2972966C (en) | 2015-01-07 | 2023-01-10 | Tendyne Holdings, Inc. | Prosthetic mitral valves and apparatus and methods for delivery of same |
| EP3253331B1 (en) | 2015-02-05 | 2021-04-07 | Tendyne Holdings, Inc. | Prosthetic heart valve with tether and expandable epicardial pad |
| CA3162308A1 (en) | 2015-02-05 | 2016-08-11 | Cardiovalve Ltd. | Prosthetic valve with axially-sliding frames |
| US9974651B2 (en) | 2015-02-05 | 2018-05-22 | Mitral Tech Ltd. | Prosthetic valve with axially-sliding frames |
| EP3695810B1 (en) | 2015-04-16 | 2022-05-18 | Tendyne Holdings, Inc. | Apparatus for retrieval of transcatheter prosthetic valves |
| EP3294221B1 (en) | 2015-05-14 | 2024-03-06 | Cephea Valve Technologies, Inc. | Replacement mitral valves |
| EP3294220B1 (en) | 2015-05-14 | 2023-12-06 | Cephea Valve Technologies, Inc. | Cardiac valve delivery devices and systems |
| US10376673B2 (en) | 2015-06-19 | 2019-08-13 | Evalve, Inc. | Catheter guiding system and methods |
| CN111658234B (zh) | 2015-08-21 | 2023-03-10 | 托尔福公司 | 可植入心脏瓣膜装置、二尖瓣修复装置以及相关系统和方法 |
| US10327894B2 (en) | 2015-09-18 | 2019-06-25 | Tendyne Holdings, Inc. | Methods for delivery of prosthetic mitral valves |
| CA3005908A1 (en) | 2015-12-03 | 2017-06-08 | Tendyne Holdings, Inc. | Frame features for prosthetic mitral valves |
| US10357351B2 (en) * | 2015-12-04 | 2019-07-23 | Edwards Lifesciences Corporation | Storage assembly for prosthetic valve |
| EP3397206B1 (en) | 2015-12-28 | 2022-06-08 | Tendyne Holdings, Inc. | Atrial pocket closures for prosthetic heart valves |
| US10531866B2 (en) | 2016-02-16 | 2020-01-14 | Cardiovalve Ltd. | Techniques for providing a replacement valve and transseptal communication |
| WO2017189276A1 (en) | 2016-04-29 | 2017-11-02 | Medtronic Vascular Inc. | Prosthetic heart valve devices with tethered anchors and associated systems and methods |
| US10470877B2 (en) | 2016-05-03 | 2019-11-12 | Tendyne Holdings, Inc. | Apparatus and methods for anterior valve leaflet management |
| WO2017218375A1 (en) | 2016-06-13 | 2017-12-21 | Tendyne Holdings, Inc. | Sequential delivery of two-part prosthetic mitral valve |
| EP3471665B1 (en) | 2016-06-17 | 2023-10-11 | Cephea Valve Technologies, Inc. | Cardiac valve delivery devices |
| JP6968113B2 (ja) | 2016-06-30 | 2021-11-17 | テンダイン ホールディングス,インコーポレイテッド | 人工心臓弁の経心尖送達装置 |
| US10736632B2 (en) | 2016-07-06 | 2020-08-11 | Evalve, Inc. | Methods and devices for valve clip excision |
| US11065116B2 (en) | 2016-07-12 | 2021-07-20 | Tendyne Holdings, Inc. | Apparatus and methods for trans-septal retrieval of prosthetic heart valves |
| US10661052B2 (en) | 2016-07-29 | 2020-05-26 | Cephea Valve Technologies, Inc. | Intravascular device delivery sheath |
| US10974027B2 (en) | 2016-07-29 | 2021-04-13 | Cephea Valve Technologies, Inc. | Combination steerable catheter and systems |
| US10639151B2 (en) | 2016-07-29 | 2020-05-05 | Cephea Valve Technologies, Inc. | Threaded coil |
| US11324495B2 (en) | 2016-07-29 | 2022-05-10 | Cephea Valve Technologies, Inc. | Systems and methods for delivering an intravascular device to the mitral annulus |
| US10646689B2 (en) * | 2016-07-29 | 2020-05-12 | Cephea Valve Technologies, Inc. | Mechanical interlock for catheters |
| US10856975B2 (en) | 2016-08-10 | 2020-12-08 | Cardiovalve Ltd. | Prosthetic valve with concentric frames |
| US10933216B2 (en) | 2016-08-29 | 2021-03-02 | Cephea Valve Technologies, Inc. | Multilumen catheter |
| US11045315B2 (en) | 2016-08-29 | 2021-06-29 | Cephea Valve Technologies, Inc. | Methods of steering and delivery of intravascular devices |
| US10751485B2 (en) | 2016-08-29 | 2020-08-25 | Cephea Valve Technologies, Inc. | Methods, systems, and devices for sealing and flushing a delivery system |
| US11109967B2 (en) | 2016-08-29 | 2021-09-07 | Cephea Valve Technologies, Inc. | Systems and methods for loading and deploying an intravascular device |
| US10632005B2 (en) * | 2016-09-19 | 2020-04-28 | Cti Vascular Ag | Catheter system for treating vascular and non-vascular diseases |
| US10874512B2 (en) | 2016-10-05 | 2020-12-29 | Cephea Valve Technologies, Inc. | System and methods for delivering and deploying an artificial heart valve within the mitral annulus |
| US11071564B2 (en) | 2016-10-05 | 2021-07-27 | Evalve, Inc. | Cardiac valve cutting device |
| US10363138B2 (en) | 2016-11-09 | 2019-07-30 | Evalve, Inc. | Devices for adjusting the curvature of cardiac valve structures |
| US10631981B2 (en) | 2016-11-15 | 2020-04-28 | Cephea Valve Technologies, Inc. | Delivery catheter distal cap |
| US10653523B2 (en) | 2017-01-19 | 2020-05-19 | 4C Medical Technologies, Inc. | Systems, methods and devices for delivery systems, methods and devices for implanting prosthetic heart valves |
| US10743991B2 (en) * | 2017-01-23 | 2020-08-18 | Edwards Lifesciences Corporation | Chordae tendineae adjustment |
| EP4209196A1 (en) | 2017-01-23 | 2023-07-12 | Cephea Valve Technologies, Inc. | Replacement mitral valves |
| CN110621260B (zh) | 2017-01-23 | 2022-11-25 | 科菲瓣膜技术有限公司 | 置换的二尖瓣 |
| US10561495B2 (en) | 2017-01-24 | 2020-02-18 | 4C Medical Technologies, Inc. | Systems, methods and devices for two-step delivery and implantation of prosthetic heart valve |
| CN106580531B (zh) * | 2017-01-24 | 2018-03-23 | 南华大学 | 用于可膨胀支架的递送系统 |
| EP3372199A1 (en) * | 2017-03-08 | 2018-09-12 | Epygon | Delivery system for transcatheter prosthetic heart valves |
| US10702378B2 (en) | 2017-04-18 | 2020-07-07 | Twelve, Inc. | Prosthetic heart valve device and associated systems and methods |
| US10575950B2 (en) * | 2017-04-18 | 2020-03-03 | Twelve, Inc. | Hydraulic systems for delivering prosthetic heart valve devices and associated methods |
| US10433961B2 (en) | 2017-04-18 | 2019-10-08 | Twelve, Inc. | Delivery systems with tethers for prosthetic heart valve devices and associated methods |
| US10792151B2 (en) | 2017-05-11 | 2020-10-06 | Twelve, Inc. | Delivery systems for delivering prosthetic heart valve devices and associated methods |
| US10646338B2 (en) * | 2017-06-02 | 2020-05-12 | Twelve, Inc. | Delivery systems with telescoping capsules for deploying prosthetic heart valve devices and associated methods |
| US10709591B2 (en) | 2017-06-06 | 2020-07-14 | Twelve, Inc. | Crimping device and method for loading stents and prosthetic heart valves |
| US10729541B2 (en) | 2017-07-06 | 2020-08-04 | Twelve, Inc. | Prosthetic heart valve devices and associated systems and methods |
| US10786352B2 (en) * | 2017-07-06 | 2020-09-29 | Twelve, Inc. | Prosthetic heart valve devices and associated systems and methods |
| JP7216066B2 (ja) | 2017-07-13 | 2023-01-31 | テンダイン ホールディングス,インコーポレイテッド | 人工心臓弁とその送達のための装置および方法 |
| US11793633B2 (en) | 2017-08-03 | 2023-10-24 | Cardiovalve Ltd. | Prosthetic heart valve |
| US10888421B2 (en) | 2017-09-19 | 2021-01-12 | Cardiovalve Ltd. | Prosthetic heart valve with pouch |
| EP3446731A1 (en) * | 2017-08-23 | 2019-02-27 | ECP Entwicklungsgesellschaft mbH | Device for compressing a compressible part of a catheter pump |
| WO2019040781A1 (en) * | 2017-08-24 | 2019-02-28 | Medtronic Vascular, Inc. | TRANS-SEPTAL DELIVERY SYSTEM HAVING A DEVIATION SEGMENT AND METHODS OF USE |
| WO2019036810A1 (en) | 2017-08-25 | 2019-02-28 | Neovasc Tiara Inc. | TRANSCATHETER MITRAL VALVULE PROSTHESIS WITH SEQUENTIAL DEPLOYMENT |
| JP7291124B2 (ja) | 2017-08-28 | 2023-06-14 | テンダイン ホールディングス,インコーポレイテッド | テザー連結部を有する人工心臓弁 |
| US11337803B2 (en) | 2017-09-19 | 2022-05-24 | Cardiovalve Ltd. | Prosthetic valve with inner and outer frames connected at a location of tissue anchor portion |
| US9895226B1 (en) | 2017-10-19 | 2018-02-20 | Mitral Tech Ltd. | Techniques for use with prosthetic valve leaflets |
| GB201720803D0 (en) | 2017-12-13 | 2018-01-24 | Mitraltech Ltd | Prosthetic Valve and delivery tool therefor |
| US11357626B2 (en) * | 2018-01-07 | 2022-06-14 | Jc Medical, Inc. | Heart valve prosthesis delivery system |
| GB201800399D0 (en) | 2018-01-10 | 2018-02-21 | Mitraltech Ltd | Temperature-control during crimping of an implant |
| WO2019224581A1 (en) * | 2018-05-23 | 2019-11-28 | Sorin Group Italia S.R.L. | A device for the in-situ delivery of heart valve prostheses |
| US11504231B2 (en) | 2018-05-23 | 2022-11-22 | Corcym S.R.L. | Cardiac valve prosthesis |
| CN110575285A (zh) * | 2018-06-08 | 2019-12-17 | 上海微创心通医疗科技有限公司 | 植入物输送管件和植入物输送系统 |
| JP7138928B2 (ja) * | 2018-08-22 | 2022-09-20 | 株式会社サンメディカル技術研究所 | 大動脈弁評価補助具 |
| US11857441B2 (en) | 2018-09-04 | 2024-01-02 | 4C Medical Technologies, Inc. | Stent loading device |
| CA3118599A1 (en) | 2018-11-08 | 2020-05-14 | Neovasc Tiara Inc. | Ventricular deployment of a transcatheter mitral valve prosthesis |
| US11724068B2 (en) | 2018-11-16 | 2023-08-15 | Cephea Valve Technologies, Inc. | Intravascular delivery system |
| CN111374797A (zh) * | 2018-12-27 | 2020-07-07 | 上海微创心通医疗科技有限公司 | 一种人工瓣膜的输送导管及输送装置 |
| CN109938879A (zh) * | 2019-03-19 | 2019-06-28 | 上海欣吉特生物科技有限公司 | 一种手术瓣膜及其植入装置 |
| EP3946163A4 (en) | 2019-04-01 | 2022-12-21 | Neovasc Tiara Inc. | ADJUSTABLE VALVE PROSTHESIS |
| EP3972673A4 (en) | 2019-05-20 | 2023-06-07 | Neovasc Tiara Inc. | INTRODUCER DEVICE WITH HEMOSTASIS MECHANISM |
| AU2020295566B2 (en) | 2019-06-20 | 2023-07-20 | Neovasc Tiara Inc. | Low profile prosthetic mitral valve |
| CN112741945B (zh) * | 2019-10-31 | 2022-07-05 | 杭州启明医疗器械股份有限公司 | 介入器械液压输送系统 |
| US11648110B2 (en) | 2019-12-05 | 2023-05-16 | Tendyne Holdings, Inc. | Braided anchor for mitral valve |
| US11648114B2 (en) | 2019-12-20 | 2023-05-16 | Tendyne Holdings, Inc. | Distally loaded sheath and loading funnel |
| US11931253B2 (en) | 2020-01-31 | 2024-03-19 | 4C Medical Technologies, Inc. | Prosthetic heart valve delivery system: ball-slide attachment |
| US11951002B2 (en) | 2020-03-30 | 2024-04-09 | Tendyne Holdings, Inc. | Apparatus and methods for valve and tether fixation |
| US11678980B2 (en) | 2020-08-19 | 2023-06-20 | Tendyne Holdings, Inc. | Fully-transseptal apical pad with pulley for tensioning |
| US11833046B2 (en) | 2020-08-26 | 2023-12-05 | Medtronic Vascular, Inc. | Delivery catheter system |
| CA3166824A1 (en) * | 2020-12-03 | 2022-06-09 | Michael ALBITOV | Transluminal delivery system |
| US20220346951A1 (en) * | 2021-05-03 | 2022-11-03 | Medtronic, Inc. | Telescoping capsule assembly for transcatheter valve repair and methods |
| WO2022234468A1 (en) * | 2021-05-05 | 2022-11-10 | Innovalve Bio Medical Ltd. | Delivery device |
| CN116098740A (zh) * | 2021-06-24 | 2023-05-12 | 杭州启明医疗器械股份有限公司 | 全回收人工心脏瓣膜系统 |
| WO2023242726A1 (en) * | 2022-06-16 | 2023-12-21 | Medtronic, Inc. | Delivery device having stability tube with compressible region |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3566963B2 (ja) * | 1993-10-22 | 2004-09-15 | シメッド ライフ システムズ インコーポレイテッド | 改良されたステント配送装置及び方法 |
| US5989280A (en) * | 1993-10-22 | 1999-11-23 | Scimed Lifesystems, Inc | Stent delivery apparatus and method |
| US5817101A (en) * | 1997-03-13 | 1998-10-06 | Schneider (Usa) Inc | Fluid actuated stent delivery system |
| US6113608A (en) * | 1998-11-20 | 2000-09-05 | Scimed Life Systems, Inc. | Stent delivery device |
| US6425916B1 (en) * | 1999-02-10 | 2002-07-30 | Michi E. Garrison | Methods and devices for implanting cardiac valves |
| US8518098B2 (en) * | 2006-02-21 | 2013-08-27 | Cook Medical Technologies Llc | Split sheath deployment system |
| US8652202B2 (en) * | 2008-08-22 | 2014-02-18 | Edwards Lifesciences Corporation | Prosthetic heart valve and delivery apparatus |
| US8986361B2 (en) * | 2008-10-17 | 2015-03-24 | Medtronic Corevalve, Inc. | Delivery system for deployment of medical devices |
| US8414644B2 (en) * | 2009-04-15 | 2013-04-09 | Cardiaq Valve Technologies, Inc. | Vascular implant and delivery system |
| US8998980B2 (en) * | 2010-04-09 | 2015-04-07 | Medtronic, Inc. | Transcatheter prosthetic heart valve delivery system with recapturing feature and method |
| CN102917668B (zh) * | 2010-04-27 | 2015-01-28 | 美敦力公司 | 具有偏置释放结构的经导管假体心脏瓣膜输送装置 |
| JP5926265B2 (ja) * | 2010-09-24 | 2016-05-25 | シメティス・ソシエテ・アノニムSymetis Sa | ステント弁、送達装置、および送達方法 |
| EP2474287A1 (en) * | 2011-01-11 | 2012-07-11 | Symetis Sa | Delivery catheter for stent-valve, and sub-assembly therefor |
| US9271855B2 (en) * | 2012-05-09 | 2016-03-01 | Abbott Cardiovascular Systems Inc. | Catheter having hydraulic actuator with tandem chambers |
-
2014
- 2014-02-04 JP JP2015556235A patent/JP6280932B2/ja active Active
- 2014-02-04 EP EP14705452.2A patent/EP2950752B1/en active Active
- 2014-02-04 WO PCT/US2014/014704 patent/WO2014121280A2/en active Application Filing
- 2014-02-04 CA CA2898991A patent/CA2898991C/en active Active
- 2014-02-04 CN CN201910044090.7A patent/CN109938878B/zh active Active
- 2014-02-04 CN CN201910043755.2A patent/CN109938877B/zh active Active
- 2014-02-04 AU AU2014211983A patent/AU2014211983B2/en active Active
- 2014-02-04 CN CN201480019245.7A patent/CN105263442B/zh active Active
-
2017
- 2017-02-16 JP JP2017026733A patent/JP6525476B2/ja active Active
-
2019
- 2019-05-03 JP JP2019087182A patent/JP2019115842A/ja active Pending
- 2019-07-17 AU AU2019206036A patent/AU2019206036B2/en active Active
-
2020
- 2020-12-01 AU AU2020281032A patent/AU2020281032B2/en active Active
-
2021
- 2021-03-10 JP JP2021038323A patent/JP7212706B2/ja active Active
-
2022
- 2022-11-22 AU AU2022275420A patent/AU2022275420A1/en active Pending
-
2023
- 2023-01-13 JP JP2023003903A patent/JP2023033419A/ja active Pending
- 2023-12-11 JP JP2023208414A patent/JP2024026335A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| JP2017080608A (ja) | 2017-05-18 |
| JP6280932B2 (ja) | 2018-02-14 |
| WO2014121280A3 (en) | 2014-10-30 |
| CN109938877A (zh) | 2019-06-28 |
| CA2898991A1 (en) | 2014-08-07 |
| AU2014211983B2 (en) | 2019-04-18 |
| AU2019206036A1 (en) | 2019-08-01 |
| AU2020281032A1 (en) | 2021-01-07 |
| CN105263442B (zh) | 2019-02-15 |
| JP2016506795A (ja) | 2016-03-07 |
| AU2020281032B2 (en) | 2022-09-15 |
| CA2898991C (en) | 2021-09-28 |
| CN109938878A (zh) | 2019-06-28 |
| CN109938877B (zh) | 2021-08-31 |
| EP2950752A2 (en) | 2015-12-09 |
| AU2022275420A1 (en) | 2023-01-05 |
| JP6525476B2 (ja) | 2019-06-05 |
| JP2024026335A (ja) | 2024-02-28 |
| JP2023033419A (ja) | 2023-03-10 |
| JP7212706B2 (ja) | 2023-01-25 |
| WO2014121280A2 (en) | 2014-08-07 |
| AU2014211983A1 (en) | 2015-08-13 |
| JP2019115842A (ja) | 2019-07-18 |
| AU2019206036B2 (en) | 2020-09-03 |
| CN105263442A (zh) | 2016-01-20 |
| EP2950752B1 (en) | 2022-07-27 |
| JP2021087876A (ja) | 2021-06-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2020281032B2 (en) | Hydraulic delivery systems for prosthetic heart valve devices and associated methods | |
| US11129714B2 (en) | Hydraulic delivery systems for prosthetic heart valve devices and associated methods | |
| US11654018B2 (en) | Heart and peripheral vascular valve replacement in conjunction with a support ring | |
| JP2016506795A5 (zh) | ||
| CN111787885A (zh) | 假体心脏瓣膜递送系统和方法 | |
| WO2009152297A1 (en) | System and method for implanting a heart implant | |
| US20210085456A1 (en) | Apparatus for use in replacing mitral valves and methods of use thereof | |
| US11793628B2 (en) | Transcatheter bio-prosthesis member and support structure |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |