CN103784413A - 阿替洛尔pH非依赖型缓释片及其制备方法 - Google Patents
阿替洛尔pH非依赖型缓释片及其制备方法 Download PDFInfo
- Publication number
- CN103784413A CN103784413A CN201410071567.8A CN201410071567A CN103784413A CN 103784413 A CN103784413 A CN 103784413A CN 201410071567 A CN201410071567 A CN 201410071567A CN 103784413 A CN103784413 A CN 103784413A
- Authority
- CN
- China
- Prior art keywords
- atenolol
- release tablets
- release
- independent sustained
- preparation
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Abstract
本发明涉及药物制剂领域,具体涉及一种阿替洛尔pH非依赖型缓释片及其制备方法,其特征是将处方量的阿替洛尔,HPMC K15M,尤特奇RSPO,高粘度PEO,单水乳糖按等量递加的方式混匀,再加入少量的硬脂酸镁和微粉硅胶作润滑剂,采用粉末直压工艺,制得阿替洛尔pH非依赖型缓释片。本发明有效的制备了pH非依赖型缓释片,证明了弱碱性药物阿替洛尔在模拟不同的胃肠道pH条件下具有相似的释放特性。本发明以缓释性能稳定的HPMC为缓释骨架,尤特奇RSPO为pH调节剂,高粘度PEO作为阻滞剂,制备工艺简单,并显著降低了药物的不良反应,提高了患者的顺应性,具有重要的经济价值和社会意义。
Description
技术领域
本发明涉及药物制剂领域,具体涉及一种阿替洛尔pH非依赖型缓释片,其特征是由20~40份缓释性能稳定的HPMC K15M为缓释骨架,15~35份尤特奇RSPO为pH调节剂,10~20份高粘度PEO(POLYOX)作为阻滞剂,经过粉末直压工艺制得阿替洛尔pH非依赖型缓释片。
背景技术
胃肠道的环境较其他给药途径复杂,相对较短的滞留时间也限制了胃肠道长效制剂的应用和研制。同时整个胃肠道多变的化学环境也使剂型的设计变得更为复杂。事实上药物在胃肠道吸收时要遭遇一系列pH值变化,正常人体口腔的pH为7,胃肠道的pH为1-7,胃液的pH为0.9-1.5,十二指肠的pH为7.6-8.2,小肠的pH为7.6,大肠的pH为8.3-8.4,且胃肠道环境的pH会因很多因素而改变,如食物(空腹时胃液的pH为0.9-1.5,饮水或进食后,pH可上升到3.0-5.0左右)、年龄、疾病、合用药物等。而胃肠道的不同pH环境决定弱酸性和弱碱性药物的解离状态,其pH的改变可影响口服药物的溶解度,进而对药物的吸收产生影响。此外,胃肠道中的pH可能对某些药物的稳定性产生影响。
口服缓释制剂由于在体内胃肠道中停留时间较长,因而胃肠道不同区段的不同pH环境可能对其释药速率产生影响。尤其是一些弱酸弱碱性药物,其溶解度呈明显的pH依赖性。从而一方面可能导致药物释放个体差异增大,另一方面也导致在恒定pH条件下进行的体外释放试验结果不能准确地反映制剂在体内的释放情况。因此,制备成pH非依赖型缓释制剂可以解决以上问题。
阿替洛尔是选择性β1肾上腺素受体阻滞剂,临床上主要用于治疗高血压,心绞痛等疾病,其普通片剂的口服生物利用度很低,个体差异性大,血药浓度相差4倍之多,导致患者的适应性差。原料药理化性质研究表明阿替洛尔为弱碱性药物,在不同的pH环境中溶解度有较大的差别,因此药物在体内的释放会受到胃肠道pH的影响很大,传统的口服给药因不能兼顾药物在不同肠道的吸收而引起血药浓度的波动,造成不良反应。将这类弱碱性药物制成非pH值依赖型缓释给药制剂能够很好的改善吸收。李凌冰等在缓释片中加入有机酸,制成阿替洛尔缓释片,通过在片剂中形成局部的微弱酸性环境,减少胃肠道pH对药物释放的影响,但是处方中琥珀酸用量的微小变化会对实验结果有较大的影响,不利于实验的重现。也有研究者将阿替洛尔制成单层渗透泵片,通过微孔渗透控制药物释放,药物受外界环境的影响较小,但是工艺较为复杂。研究证明,尤特奇系列的聚丙烯酸树脂单独或联合使用可以形成局部的酸性微环境来改善弱碱性药物的pH依赖性。因此本研究以缓释性能稳定的HPMC为缓释骨架,尤特奇RSPO为pH调节剂,高粘度PEO作为阻滞剂,利用直接压片法制备阿替洛尔非pH依赖型缓释骨架片。本发明的阿替洛尔pH非依赖型缓释片具有以下特点:
(1)药物的释放不依赖于胃肠道内的pH值,可避免口服给药后因不能兼顾阿替洛尔在不同肠道的吸收而引起血药浓度的波动,提高制剂的安全性。
(2)新型辅料尤特奇RSPO为pH调节剂,可以形成局部的微酸性环境来改善弱碱性药物阿替洛尔的pH依赖性。本发明还适用于其它pH依赖型药物,用以改善该类药物在胃肠道内的稳定性,实现pH非依赖性释放。
(3)本发明选用的辅料流动性及压缩成型性好,通过简单的粉末直压工艺制备,易于实现产品从实验室到企业的成果转化,具有重要的经济价值和社会意义。
发明内容
本发明涉及药物制剂领域,具体涉及一种阿替洛尔pH非依赖型缓释片,它含有下列组分及重量比:
阿替洛尔 10份
HPMC K15M 20~40份
尤特奇RSPO 15~35份
PEO(POLYOX) 10~20份
乳糖 17份
微粉硅胶和硬脂酸镁 1份
本发明的阿替洛尔pH非依赖型缓释片,各组分优选的重量比为:
阿替洛尔 10份
HPMC K15M 37份
尤特奇RSPO 22份
PEO(POLYOX) 13份
乳糖 17份
微粉硅胶和硬脂酸镁 1份
本发明是将处方量的阿替洛尔,HPMC K15M,尤特奇RSPO,高粘度PEO,单水乳糖按等量递加的方式混匀,再加入1%的硬脂酸镁和微粉硅胶作润滑剂,采用粉末直压工艺,制得阿替洛尔pH非依赖型缓释片。
本发明所涉及的比例均为重量比。在进行处方用量筛选时首先以释放度为主要指标,通过单因素实验确定了对本处方释放度影响较大的三个因素及其用量范围,结果见表1:
表1:单因素实验考察结果
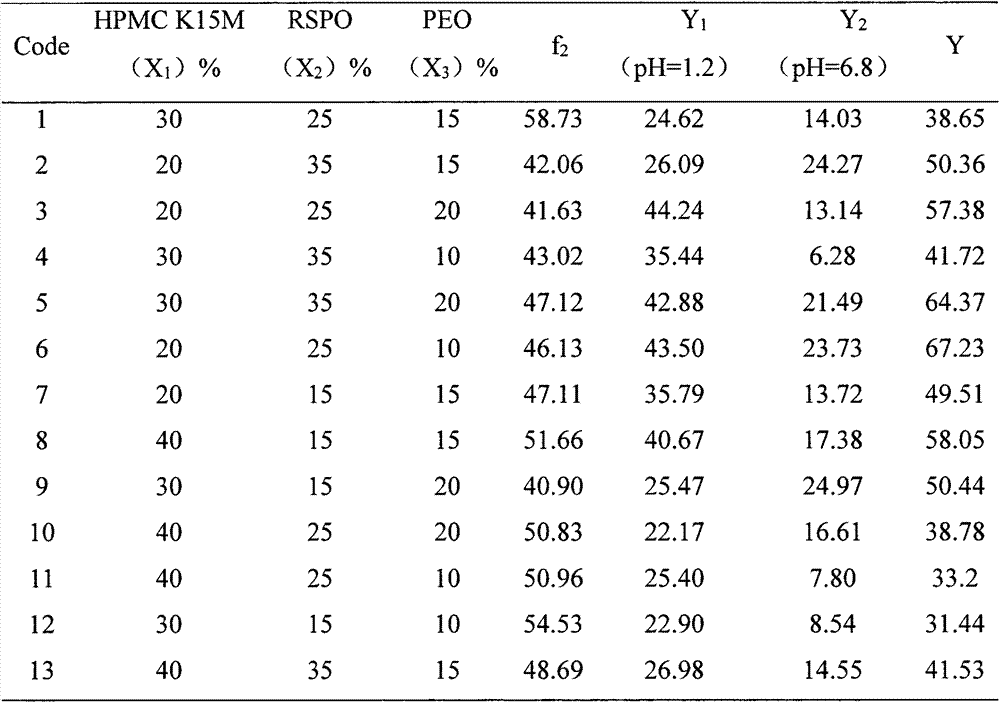
在单因素实验结果的基础上,采用BBD效应面法设计方案安排实验,制备阿替洛尔非pH依赖性骨架缓释片,测定其在两种不同pH介质中的释放曲线,测定累计释放度的综合评分Y,并计算释放曲线的相似因子f2。结果见表2。
表2:BBD效应面法的方案设计
注:Y1以及Y2分别为制剂在释放介质pH=1.2和pH=6.8中释药曲线的评分,Y=Y1-Y2。Y越小说明药物释放受pH的影响越小。
将上表中的实验数据采用Design-Expert7.0软件处理,以每一个处方在两种不同pH介质中释放度的相似度f2作为评价指标,分别对各个因素进行线性和二项式拟合:
线性方程为:Y=b+b1X1+b2X2+b3X3
二项式方程为:Y=b+b1X1+b2X2+b3X3+b4X12+b5X22+b6X32+b7X1X2+b8X1X3+b9X2X3
以R2最大和P值最小作为判定标准,得到的回归方程为:
f2=-38.83875+3.09388X1+1.59012X2+4.17225X3+0.02185X1X3+0.08865X2X3-0.051775X12-0.061725X22-0.2466X32(R2=0.9825,P<0.005)
Y=53.72442-0.6615X1+0.9345X3(R2=0.9543,P<0.005)
得到三维效应图,见图1。
对于释放度相似因子f2来说,值越大越好,对于Y值,值越小越好,通过设计软件得出的最优方案为:X1用量为:37%;X2的用量为:22%;X3的用量为:13%。
据此,根据单因素实验的结果,本发明首先确定HPMC K15M、尤特奇RSPO以及高粘度PEO为影响制剂释放性能的主要因素。进一步通过BBD效应面法得到三种主辅料的优选配比为:37份HPMC,22份尤特奇RSPO,13份高粘度PEO。
按最优处方制备缓释片,测定缓释片在pH1.2以及pH6.8中的释放度曲线,得到的相似因子f2为59.88,综合评分Y为11.92。释放曲线结果如图2所示。结果显示优化得到的阿替洛尔pH非依赖型缓释片在弱酸性(pH=1.2)和近中性(pH=6.8)释放条件下,释放曲线相似,说明药物释放受pH影响较小,可以很好的避免药物在胃肠道中的不稳定现象,提高药物的生物利用度,降低药物的不良反应。
附图说明
图1是本发明的阿替洛尔缓释骨架片的三维效应图
图2是本发明的阿替洛尔在pH1.2以及pH6.8中的释放曲线
具体实施方式
实施例1
阿替洛尔pH非依赖型缓释片单位处方(1000片,规格为25mg每片)。它含有下列组分及重量:
阿替洛尔 25g
HPMC K15M 92.5g
尤特奇RSPO 55g
PEO(POLYOX) 32.5g
乳糖 42.5g
微粉硅胶和硬脂酸镁 2.5g
上述阿替洛尔pH非依赖型缓释片的制备方法,是将处方量的阿替洛尔,HPMCK15M,尤特奇RSPO,高粘度PEO,单水乳糖按等量递加的方式混匀,再加入1%的硬脂酸镁和微粉硅胶作润滑剂,采用粉末直压工艺,即得阿替洛尔pH非依赖型缓释片。
实施例2
阿替洛尔pH非依赖型缓释片单位处方(1000片,规格为25mg每片)。它含有下列组分及重量:
阿替洛尔 25g
HPMC K15M 52.5g
尤特奇RSPO 87.5g
PEO(POLYOX) 40g
乳糖 42.5g
微粉硅胶和硬脂酸镁 2.5g
上述阿替洛尔pH非依赖型缓释片的制备方法,是将处方量的阿替洛尔,HPMCK15M,尤特奇RSPO,高粘度PEO,单水乳糖按等量递加的方式混匀,再加入1%的硬脂酸镁和微粉硅胶作润滑剂,采用粉末直压工艺,即得阿替洛尔pH非依赖型缓释片。
实施例3
阿替洛尔pH非依赖型缓释片单位处方(1000片,规格为25mg每片)。它含有下列组分及重量:
阿替洛尔 25g
HPMC K15M 80g
尤特奇RSPO 75g
PEO(POLYOX) 25g
乳糖 42.5g
微粉硅胶和硬脂酸镁 2.5g
上述阿替洛尔pH非依赖型缓释片的制备方法,是将处方量的阿替洛尔,HPMCK15M,尤特奇RSPO,高粘度PEO,单水乳糖按等量递加的方式混匀,再加入1%的硬脂酸镁和微粉硅胶作润滑剂,采用粉末直压工艺,即得阿替洛尔pH非依赖型缓释片。
Claims (3)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201410071567.8A CN103784413A (zh) | 2014-02-27 | 2014-02-27 | 阿替洛尔pH非依赖型缓释片及其制备方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201410071567.8A CN103784413A (zh) | 2014-02-27 | 2014-02-27 | 阿替洛尔pH非依赖型缓释片及其制备方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN103784413A true CN103784413A (zh) | 2014-05-14 |
Family
ID=50660755
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201410071567.8A Pending CN103784413A (zh) | 2014-02-27 | 2014-02-27 | 阿替洛尔pH非依赖型缓释片及其制备方法 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN103784413A (zh) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN108969502A (zh) * | 2018-10-11 | 2018-12-11 | 田国荣 | 一种阿替洛尔缓释片及其制备方法 |
| CN109700776A (zh) * | 2017-10-25 | 2019-05-03 | 郑州泰丰制药有限公司 | 一种新型阿替洛尔缓释滴丸及其制备方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2002058676A1 (en) * | 2000-12-20 | 2002-08-01 | Shire Laboratories, Inc. | Sustained release pharmaceutical dosage forms with minimized ph dependent dissolution profiles |
| CN101804033A (zh) * | 2010-04-20 | 2010-08-18 | 中国药科大学 | 一种阿替洛尔非pH依赖型缓释微丸及其制备方法 |
-
2014
- 2014-02-27 CN CN201410071567.8A patent/CN103784413A/zh active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2002058676A1 (en) * | 2000-12-20 | 2002-08-01 | Shire Laboratories, Inc. | Sustained release pharmaceutical dosage forms with minimized ph dependent dissolution profiles |
| CN101804033A (zh) * | 2010-04-20 | 2010-08-18 | 中国药科大学 | 一种阿替洛尔非pH依赖型缓释微丸及其制备方法 |
Non-Patent Citations (7)
| Title |
|---|
| A. CEBALLOS ET AL.: "Influence of formulation and process variables on in vitro release of theophylline from directly-compressed Eudragit matrix tablets", 《IL FARMACO》 * |
| 彼得厄特: "《尤特奇(聚甲基丙烯酸酯)应用技术指南》", 31 August 2009, 化学工业出版社 * |
| 李凌冰等: "人工神经网络多指标同步优化阿替洛尔非pH依赖型缓释片", 《山东大学学报(医学版)》 * |
| 李凌冰等: "阿替洛尔非pH依赖型缓释片的制备及处方优化", 《中国医药工业杂志》 * |
| 湖北中医学院等: "《全国高等医药院校试用教材 药剂学 中药专业用》", 31 August 1980, 上海科学技术出版社 * |
| 白靖等: "药用丙烯酸树脂在制剂中的应用进展", 《中国药房》 * |
| 赛那等: "阿替洛尔缓释微囊载药量的测定及体外释放行为研究", 《中南药学》 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN109700776A (zh) * | 2017-10-25 | 2019-05-03 | 郑州泰丰制药有限公司 | 一种新型阿替洛尔缓释滴丸及其制备方法 |
| CN108969502A (zh) * | 2018-10-11 | 2018-12-11 | 田国荣 | 一种阿替洛尔缓释片及其制备方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Goh et al. | 3D printing of four-in-one oral polypill with multiple release profiles for personalized delivery of caffeine and vitamin B analogues | |
| US20230293475A1 (en) | Methods of providing solriamfetol therapy to subjects with impaired renal function | |
| CN106074414B (zh) | 一种含有鲁拉西酮的口腔崩解片及其制备方法 | |
| CN104997743A (zh) | 包含多巴胺受体配体的药物制剂 | |
| Lin et al. | Preparation and characterization of a novel swellable and floating gastroretentive drug delivery system (sf GRDDS) for enhanced oral bioavailability of nilotinib | |
| CN103156819A (zh) | 苯甲酸阿格列汀组合物片剂及其制备方法 | |
| CN104873977A (zh) | 复合淀粉专用胶及其空心胶囊的制备方法 | |
| US10413514B2 (en) | Controlled-release solid preparation with partial coating | |
| CN103784413A (zh) | 阿替洛尔pH非依赖型缓释片及其制备方法 | |
| CN106309388A (zh) | 一种用于心衰治疗的药物组合物及其制备方法 | |
| CN101198869A (zh) | 胰腺炎的预防及治疗剂 | |
| CN102940864B (zh) | 一种蘘荷提取物的解酒新用途 | |
| KR101587140B1 (ko) | 위장관 질환 치료용 모사프리드 구연산염 미니정제 함유 서방성 캡슐 제제 및 이의 제조 방법 | |
| CN110960502A (zh) | 一种治疗代谢综合征的物质及其应用 | |
| Vijayanand et al. | Formulation, characterization and in vivo evaluation of novel edible dosage form containing nebivolol HCl | |
| CN104546793B (zh) | 一种降糖鸡腿蘑胶囊制剂及其制备方法 | |
| KR102512518B1 (ko) | 페마피브레이트를 함유하는 의약 | |
| CN103211830B (zh) | 一种用于治疗高血压病的中药配伍组分 | |
| CN101954090A (zh) | 双氢青蒿素β-环糊精包合物及其制备方法和含有该包合物的抗疟疾药物 | |
| CN102846731B (zh) | 用于治疗乳腺增生或乳腺炎的中药组合物及其制备方法 | |
| CN101695482B (zh) | 格列吡嗪口崩片及其制备工艺 | |
| CN103356478A (zh) | 一种布洛芬注射液组合物及其制备方法 | |
| CN201701513U (zh) | 装有头孢氨苄片和盐酸氨溴索片的片剂胶囊 | |
| CN202568930U (zh) | 装有瑞格列奈固体制剂和二甲双胍固体制剂的片剂胶囊 | |
| CN107389563B (zh) | 一种缓控释药用辅料缓释性能的质量检测方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20140514 |