WO2021106981A1 - 錯体化合物およびその製造方法 - Google Patents
錯体化合物およびその製造方法 Download PDFInfo
- Publication number
- WO2021106981A1 WO2021106981A1 PCT/JP2020/043947 JP2020043947W WO2021106981A1 WO 2021106981 A1 WO2021106981 A1 WO 2021106981A1 JP 2020043947 W JP2020043947 W JP 2020043947W WO 2021106981 A1 WO2021106981 A1 WO 2021106981A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- substituted
- complex compound
- fine particles
- resin fine
- Prior art date
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 67
- 238000004519 manufacturing process Methods 0.000 title claims abstract description 15
- 229920005989 resin Polymers 0.000 claims abstract description 78
- 239000011347 resin Substances 0.000 claims abstract description 78
- 238000006243 chemical reaction Methods 0.000 claims abstract description 75
- 239000010419 fine particle Substances 0.000 claims abstract description 69
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 32
- 125000003118 aryl group Chemical group 0.000 claims abstract description 29
- 239000003054 catalyst Substances 0.000 claims abstract description 19
- 229910052723 transition metal Inorganic materials 0.000 claims abstract description 16
- 150000003624 transition metals Chemical class 0.000 claims abstract description 16
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims abstract description 8
- 125000001183 hydrocarbyl group Chemical group 0.000 claims abstract 4
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 claims description 31
- 125000004432 carbon atom Chemical group C* 0.000 claims description 23
- 239000000126 substance Substances 0.000 claims description 13
- 150000003623 transition metal compounds Chemical class 0.000 claims description 10
- JRTIUDXYIUKIIE-KZUMESAESA-N (1z,5z)-cycloocta-1,5-diene;nickel Chemical compound [Ni].C\1C\C=C/CC\C=C/1.C\1C\C=C/CC\C=C/1 JRTIUDXYIUKIIE-KZUMESAESA-N 0.000 claims description 9
- 229910052759 nickel Inorganic materials 0.000 claims description 9
- 150000002816 nickel compounds Chemical class 0.000 claims description 8
- XYFCBTPGUUZFHI-UHFFFAOYSA-N phosphine group Chemical group P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 claims description 8
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 claims description 6
- 239000003960 organic solvent Substances 0.000 claims description 6
- KFBKRCXOTTUAFS-UHFFFAOYSA-N nickel;triphenylphosphane Chemical compound [Ni].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 KFBKRCXOTTUAFS-UHFFFAOYSA-N 0.000 claims description 3
- 229910052763 palladium Inorganic materials 0.000 claims description 3
- 229910052703 rhodium Inorganic materials 0.000 claims description 2
- 239000010948 rhodium Substances 0.000 claims description 2
- MHOVAHRLVXNVSD-UHFFFAOYSA-N rhodium atom Chemical compound [Rh] MHOVAHRLVXNVSD-UHFFFAOYSA-N 0.000 claims description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 44
- -1 heptylene group Chemical group 0.000 description 37
- 229910052698 phosphorus Inorganic materials 0.000 description 34
- 239000011574 phosphorus Substances 0.000 description 34
- 230000015572 biosynthetic process Effects 0.000 description 28
- 238000003786 synthesis reaction Methods 0.000 description 24
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 22
- 239000011734 sodium Substances 0.000 description 18
- 125000001424 substituent group Chemical group 0.000 description 16
- 229910052708 sodium Inorganic materials 0.000 description 15
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 14
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 14
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 12
- 229910052799 carbon Inorganic materials 0.000 description 12
- 238000002329 infrared spectrum Methods 0.000 description 12
- 239000000203 mixture Substances 0.000 description 12
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 10
- 239000002245 particle Substances 0.000 description 10
- 239000002994 raw material Substances 0.000 description 10
- MYRTYDVEIRVNKP-UHFFFAOYSA-N 1,2-Divinylbenzene Chemical compound C=CC1=CC=CC=C1C=C MYRTYDVEIRVNKP-UHFFFAOYSA-N 0.000 description 9
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 9
- 150000002430 hydrocarbons Chemical group 0.000 description 9
- 239000002244 precipitate Substances 0.000 description 9
- 125000003545 alkoxy group Chemical group 0.000 description 8
- 125000000753 cycloalkyl group Chemical group 0.000 description 8
- 239000000243 solution Substances 0.000 description 8
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 8
- 239000012299 nitrogen atmosphere Substances 0.000 description 7
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 6
- 125000003710 aryl alkyl group Chemical group 0.000 description 6
- 239000006227 byproduct Substances 0.000 description 6
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 6
- 239000006228 supernatant Substances 0.000 description 6
- HBAHZZVIEFRTEY-UHFFFAOYSA-N 2-heptylcyclohex-2-en-1-one Chemical compound CCCCCCCC1=CCCCC1=O HBAHZZVIEFRTEY-UHFFFAOYSA-N 0.000 description 5
- 229920001367 Merrifield resin Polymers 0.000 description 5
- 125000004104 aryloxy group Chemical group 0.000 description 5
- 239000003431 cross linking reagent Substances 0.000 description 5
- 238000000034 method Methods 0.000 description 5
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 5
- 150000002903 organophosphorus compounds Chemical class 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- 125000006414 CCl Chemical group ClC* 0.000 description 4
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 4
- BZRLFVYTFDNRJT-UHFFFAOYSA-N [P]C=C Chemical compound [P]C=C BZRLFVYTFDNRJT-UHFFFAOYSA-N 0.000 description 4
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Chemical compound C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 4
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 4
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 4
- 239000011261 inert gas Substances 0.000 description 4
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 4
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 4
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 4
- 125000001624 naphthyl group Chemical group 0.000 description 4
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 4
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 4
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 4
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 description 4
- 239000007858 starting material Substances 0.000 description 4
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 125000002252 acyl group Chemical group 0.000 description 3
- 125000004423 acyloxy group Chemical group 0.000 description 3
- 125000003342 alkenyl group Chemical group 0.000 description 3
- 125000001118 alkylidene group Chemical group 0.000 description 3
- 229910052786 argon Inorganic materials 0.000 description 3
- 125000002029 aromatic hydrocarbon group Chemical group 0.000 description 3
- 239000012298 atmosphere Substances 0.000 description 3
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 125000004093 cyano group Chemical group *C#N 0.000 description 3
- 125000000000 cycloalkoxy group Chemical group 0.000 description 3
- 239000006185 dispersion Substances 0.000 description 3
- 230000007613 environmental effect Effects 0.000 description 3
- 150000002170 ethers Chemical class 0.000 description 3
- 125000000623 heterocyclic group Chemical group 0.000 description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 229910052751 metal Inorganic materials 0.000 description 3
- 239000002184 metal Substances 0.000 description 3
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 3
- 125000004043 oxo group Chemical group O=* 0.000 description 3
- 229920005990 polystyrene resin Polymers 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 125000003396 thiol group Chemical group [H]S* 0.000 description 3
- 125000003944 tolyl group Chemical group 0.000 description 3
- 125000000094 2-phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 2
- UEXCJVNBTNXOEH-UHFFFAOYSA-N Ethynylbenzene Chemical group C#CC1=CC=CC=C1 UEXCJVNBTNXOEH-UHFFFAOYSA-N 0.000 description 2
- RSWGJHLUYNHPMX-ONCXSQPRSA-N abietic acid Chemical compound C([C@@H]12)CC(C(C)C)=CC1=CC[C@@H]1[C@]2(C)CCC[C@@]1(C)C(O)=O RSWGJHLUYNHPMX-ONCXSQPRSA-N 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 2
- AGEZXYOZHKGVCM-UHFFFAOYSA-N benzyl bromide Chemical compound BrCC1=CC=CC=C1 AGEZXYOZHKGVCM-UHFFFAOYSA-N 0.000 description 2
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 2
- 235000010290 biphenyl Nutrition 0.000 description 2
- 239000004305 biphenyl Substances 0.000 description 2
- 125000004106 butoxy group Chemical group [*]OC([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- JGUQDUKBUKFFRO-CIIODKQPSA-N dimethylglyoxime Chemical compound O/N=C(/C)\C(\C)=N\O JGUQDUKBUKFFRO-CIIODKQPSA-N 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 2
- 239000003063 flame retardant Substances 0.000 description 2
- 238000000769 gas chromatography-flame ionisation detection Methods 0.000 description 2
- 150000004820 halides Chemical class 0.000 description 2
- 125000001072 heteroaryl group Chemical group 0.000 description 2
- 229930195733 hydrocarbon Natural products 0.000 description 2
- 238000010813 internal standard method Methods 0.000 description 2
- 150000002576 ketones Chemical class 0.000 description 2
- 239000003446 ligand Substances 0.000 description 2
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- UMIPWJGWASORKV-UHFFFAOYSA-N oct-1-yne Chemical compound CCCCCCC#C UMIPWJGWASORKV-UHFFFAOYSA-N 0.000 description 2
- 239000000575 pesticide Substances 0.000 description 2
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 description 2
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N phenylbenzene Natural products C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 2
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 2
- 229910000073 phosphorus hydride Inorganic materials 0.000 description 2
- 230000035484 reaction time Effects 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 238000001179 sorption measurement Methods 0.000 description 2
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- DQWPFSLDHJDLRL-UHFFFAOYSA-N triethyl phosphate Chemical compound CCOP(=O)(OCC)OCC DQWPFSLDHJDLRL-UHFFFAOYSA-N 0.000 description 2
- YWWDBCBWQNCYNR-UHFFFAOYSA-N trimethylphosphine Chemical compound CP(C)C YWWDBCBWQNCYNR-UHFFFAOYSA-N 0.000 description 2
- VYXHVRARDIDEHS-UHFFFAOYSA-N 1,5-cyclooctadiene Chemical compound C1CC=CCCC=C1 VYXHVRARDIDEHS-UHFFFAOYSA-N 0.000 description 1
- 239000004912 1,5-cyclooctadiene Substances 0.000 description 1
- 125000004973 1-butenyl group Chemical group C(=CCC)* 0.000 description 1
- KWKAKUADMBZCLK-UHFFFAOYSA-N 1-octene Chemical group CCCCCCC=C KWKAKUADMBZCLK-UHFFFAOYSA-N 0.000 description 1
- RNFJDJUURJAICM-UHFFFAOYSA-N 2,2,4,4,6,6-hexaphenoxy-1,3,5-triaza-2$l^{5},4$l^{5},6$l^{5}-triphosphacyclohexa-1,3,5-triene Chemical compound N=1P(OC=2C=CC=CC=2)(OC=2C=CC=CC=2)=NP(OC=2C=CC=CC=2)(OC=2C=CC=CC=2)=NP=1(OC=1C=CC=CC=1)OC1=CC=CC=C1 RNFJDJUURJAICM-UHFFFAOYSA-N 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- CEBKHWWANWSNTI-UHFFFAOYSA-N 2-methylbut-3-yn-2-ol Chemical compound CC(C)(O)C#C CEBKHWWANWSNTI-UHFFFAOYSA-N 0.000 description 1
- IWTYTFSSTWXZFU-UHFFFAOYSA-N 3-chloroprop-1-enylbenzene Chemical compound ClCC=CC1=CC=CC=C1 IWTYTFSSTWXZFU-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 1
- ABLZXFCXXLZCGV-UHFFFAOYSA-N Phosphorous acid Chemical compound OP(O)=O ABLZXFCXXLZCGV-UHFFFAOYSA-N 0.000 description 1
- 238000007259 addition reaction Methods 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 150000001345 alkine derivatives Chemical class 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000002993 cycloalkylene group Chemical group 0.000 description 1
- 125000004956 cyclohexylene group Chemical group 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 239000012776 electronic material Substances 0.000 description 1
- 238000000921 elemental analysis Methods 0.000 description 1
- 125000005677 ethinylene group Chemical group [*:2]C#C[*:1] 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 125000004836 hexamethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- 125000006038 hexenyl group Chemical group 0.000 description 1
- 239000012280 lithium aluminium hydride Substances 0.000 description 1
- 239000008204 material by function Substances 0.000 description 1
- 238000000691 measurement method Methods 0.000 description 1
- UJNZOIKQAUQOCN-UHFFFAOYSA-N methyl(diphenyl)phosphane Chemical compound C=1C=CC=CC=1P(C)C1=CC=CC=C1 UJNZOIKQAUQOCN-UHFFFAOYSA-N 0.000 description 1
- 125000004957 naphthylene group Chemical group 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 150000002941 palladium compounds Chemical class 0.000 description 1
- 125000002255 pentenyl group Chemical group C(=CCCC)* 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 239000008213 purified water Substances 0.000 description 1
- 238000007086 side reaction Methods 0.000 description 1
- 238000007873 sieving Methods 0.000 description 1
- HSFQBFMEWSTNOW-UHFFFAOYSA-N sodium;carbanide Chemical group [CH3-].[Na+] HSFQBFMEWSTNOW-UHFFFAOYSA-N 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000012756 surface treatment agent Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 125000005023 xylyl group Chemical group 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/24—Phosphines, i.e. phosphorus bonded to only carbon atoms, or to both carbon and hydrogen atoms, including e.g. sp2-hybridised phosphorus compounds such as phosphabenzene, phosphole or anionic phospholide ligands
- B01J31/2404—Cyclic ligands, including e.g. non-condensed polycyclic ligands, the phosphine-P atom being a ring member or a substituent on the ring
- B01J31/2409—Cyclic ligands, including e.g. non-condensed polycyclic ligands, the phosphine-P atom being a ring member or a substituent on the ring with more than one complexing phosphine-P atom
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G83/00—Macromolecular compounds not provided for in groups C08G2/00 - C08G81/00
- C08G83/008—Supramolecular polymers
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/165—Polymer immobilised coordination complexes, e.g. organometallic complexes
- B01J31/1658—Polymer immobilised coordination complexes, e.g. organometallic complexes immobilised by covalent linkages, i.e. pendant complexes with optional linking groups, e.g. on Wang or Merrifield resins
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/24—Phosphines, i.e. phosphorus bonded to only carbon atoms, or to both carbon and hydrogen atoms, including e.g. sp2-hybridised phosphorus compounds such as phosphabenzene, phosphole or anionic phospholide ligands
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/24—Phosphines, i.e. phosphorus bonded to only carbon atoms, or to both carbon and hydrogen atoms, including e.g. sp2-hybridised phosphorus compounds such as phosphabenzene, phosphole or anionic phospholide ligands
- B01J31/2404—Cyclic ligands, including e.g. non-condensed polycyclic ligands, the phosphine-P atom being a ring member or a substituent on the ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/38—Phosphonic acids RP(=O)(OH)2; Thiophosphonic acids, i.e. RP(=X)(XH)2 (X = S, Se)
- C07F9/40—Esters thereof
- C07F9/4003—Esters thereof the acid moiety containing a substituent or a structure which is considered as characteristic
- C07F9/4015—Esters of acyclic unsaturated acids
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F8/00—Chemical modification by after-treatment
- C08F8/40—Introducing phosphorus atoms or phosphorus-containing groups
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2231/00—Catalytic reactions performed with catalysts classified in B01J31/00
- B01J2231/30—Addition reactions at carbon centres, i.e. to either C-C or C-X multiple bonds
- B01J2231/32—Addition reactions to C=C or C-C triple bonds
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2231/00—Catalytic reactions performed with catalysts classified in B01J31/00
- B01J2231/30—Addition reactions at carbon centres, i.e. to either C-C or C-X multiple bonds
- B01J2231/32—Addition reactions to C=C or C-C triple bonds
- B01J2231/323—Hydrometalation, e.g. bor-, alumin-, silyl-, zirconation or analoguous reactions like carbometalation, hydrocarbation
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/80—Complexes comprising metals of Group VIII as the central metal
- B01J2531/82—Metals of the platinum group
- B01J2531/822—Rhodium
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/80—Complexes comprising metals of Group VIII as the central metal
- B01J2531/82—Metals of the platinum group
- B01J2531/824—Palladium
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/80—Complexes comprising metals of Group VIII as the central metal
- B01J2531/84—Metals of the iron group
- B01J2531/847—Nickel
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/11—Compounds covalently bound to a solid support
Definitions
- the present invention relates to a complex compound. More specifically, the present invention relates to complex compounds useful as catalysts for hydrophosphorylation reactions. The present invention also relates to a method for producing the complex compound.
- Organophosphorus compounds are chemical substances widely used in various products such as flame retardants, plasticizers, pesticides, medical pesticides, and ligands for metal complexes.
- organic phosphorus compounds have attracted particular industrial attention in the fields of metal surface treatment agents as functional materials, constituent materials such as flame-retardant resins, and electronic materials.
- the alkenylphosphonic acid derivative is a useful precursor substance of the above-mentioned various chemical substances, and therefore various production methods have been studied conventionally.
- an alkenylphosphonic acid derivative has been produced by an addition reaction of a P (O) -H bond of a phosphonic acid to an alkyne (hereinafter referred to as a hydrophosphorylation reaction) using a catalyst.
- a hydrophosphorylation reaction a catalyst in which a transition metal is immobilized on a polystyrene resin to which triphenylphosphine is bound.
- Non-Patent Document 1 the catalyst in which the transition metal is immobilized on the polystyrene resin to which triphenylphosphine is bound as described in Non-Patent Document 1 does not have a sufficient phosphorus content on the resin surface, and it is very difficult to add the phosphorus amount required for the reaction. There are problems that a large amount of resin is required, the reaction efficiency is low, the metal component is leached from the resin surface a lot, and side reactions proceed a lot. Therefore, there is room for improvement in the reaction efficiency when used in the hydrophosphorylation reaction.
- an object of the present invention is to provide a complex compound useful as a catalyst for a hydrophosphorylation reaction.
- the present inventor has obtained a complex compound useful as a catalyst for a hydrophosphorylation reaction by reacting a resin having a phosphine substituent on the surface with a transition metal. It was found that this was possible, and the present invention was completed.
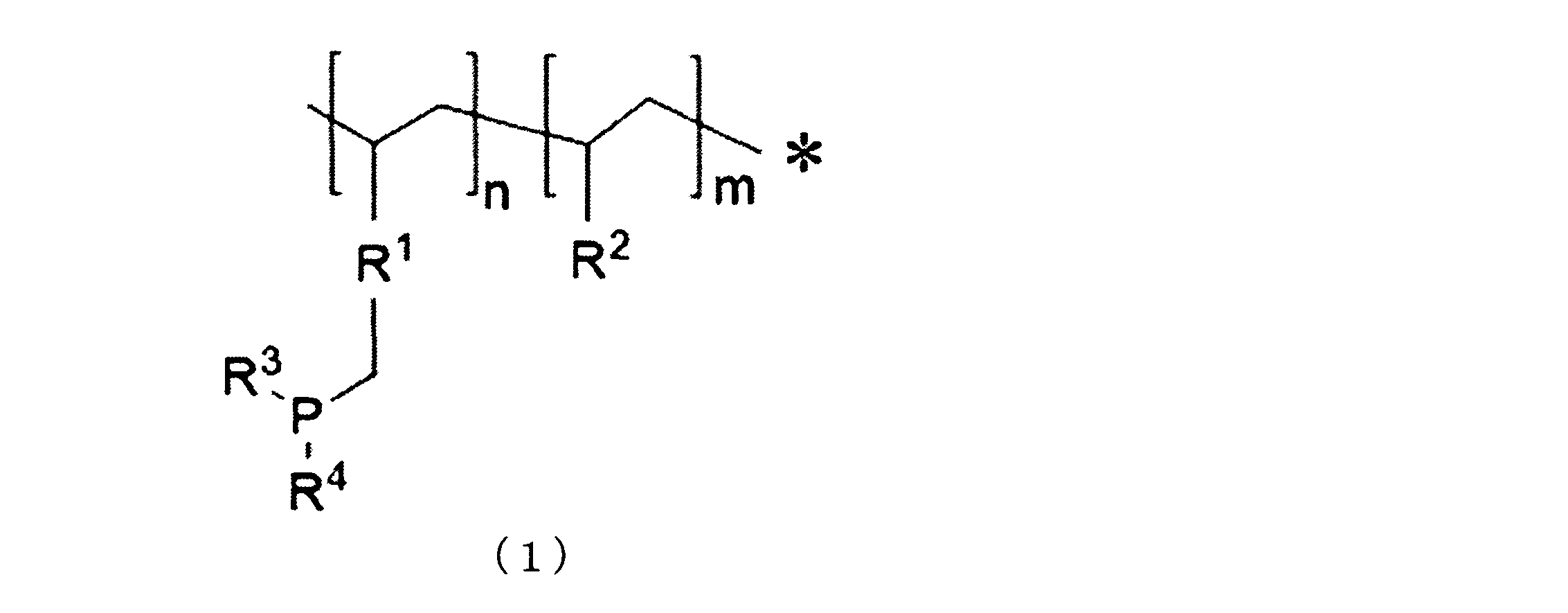
- R 1 represents a substituted or unsubstituted hydrocarbon group
- R 2 represents a substituted or unsubstituted alkyl group or a substituted or unsubstituted aryl group
- R 3 and R 4 Independently indicate a hydrogen atom, a substituted or unsubstituted alkyl group, or a substituted or unsubstituted aryl group
- the value of n is 20 to 100% with respect to the total of 100% of the values of n and m.
- a complex compound of resin fine particles represented by and a transition metal [2] The complex compound according to [1], wherein the substance amount ratio of the phosphine group and the transition metal in the resin fine particles is 10: 1 to 1: 2. [3] The complex compound according to [1] or [2] , wherein R 1 is a hydrocarbon group having 6 to 12 carbon atoms in the general formula (1). [4] In the general formula (1), R 2 is described in any one of [1] to [3], wherein R 2 is an alkyl group having 1 to 8 carbon atoms or an aryl group having 5 to 12 carbon atoms. Complex compound.
- R 3 and R 4 are any of [1] to [4], which are an alkyl group having 1 to 8 carbon atoms or an aryl group having 5 to 12 carbon atoms.
- the complex compound according to. [6] The complex compound according to any one of [1] to [5], wherein the transition metal is nickel or palladium.
- R 1 represents a substituted or unsubstituted hydrocarbon group
- R 2 represents a substituted or unsubstituted alkyl group or a substituted or unsubstituted aryl group
- R 3 and R 4 Independently indicate a hydrogen atom, a substituted or unsubstituted alkyl group, or a substituted or unsubstituted aryl group
- the value of n is 20 to 100% with respect to the total of 100% of the values of n and m.
- a method for producing a complex compound which comprises a step of reacting the resin fine particles represented by (1) and a transition metal compound in the presence of an organic solvent. [9] The method for producing a complex compound according to [8], wherein the transition metal compound is a zero-valent nickel compound. [10]
- the zero-valent nickel compound is at least one selected from the group consisting of bis (1,5-cyclooctadiene) nickel (0), tetrakis (triphenylphosphine) nickel (0), and nickel carbonyl.
- the present invention it is possible to provide a complex compound useful as a catalyst for a hydrophosphorylation reaction and a method for producing the same.
- the complex compound of the present invention can efficiently proceed with the hydrophosphorylation reaction under temperature conditions of room temperature or higher as a catalyst. Moreover, since an inexpensive commercially available material can be used as a raw material for the complex compound of the present invention, the production cost can be reduced.
- the complex compound of the present invention is a complex compound (resin-supported transition metal complex) of a resin fine particle described in detail below and a transition metal, and can be used as a catalyst for a hydrophosphorylation reaction.
- a complex compound resin-supported transition metal complex
- phosphine substituents on the surface of the resin fine particles, such a complex compound can efficiently proceed with the hydrophosphorylation reaction under temperature conditions of room temperature or higher.
- the resin fine particles forming the complex compound are represented by the following general formula (1).
- R 1 represents a substituted or unsubstituted hydrocarbon group
- R 2 represents a substituted or unsubstituted alkyl group or a substituted or unsubstituted aryl group
- R 3 and R 4 Independently indicate a hydrogen atom, a substituted or unsubstituted alkyl group, or a substituted or unsubstituted aryl group
- the value of n is 20 to 100% with respect to the total of 100% of the values of n and m.
- the value of m is in the range of 0 to 80%, and * is bonded to the surface of the resin fine particles.
- a hydrocarbon group having 6 to 12 carbon atoms is preferable as the substituted or unsubstituted hydrocarbon group of R 1 .
- the carbon number of the substituent does not include the carbon number of the substituent.
- the hydrocarbon group having 6 to 12 carbon atoms include an alkylene group such as a hexylene group, a heptylene group and an octylene group, a cycloalkylene group such as a cyclohexylene group, an aromatic hydrocarbon group such as a phenylene group and a naphthylene group.
- R 1 is preferably an aromatic hydrocarbon group, more preferably a phenylene group.
- examples of the substituted or unsubstituted alkyl group R 2 preferably an alkyl group having 1 to 8 carbon atoms
- examples of the substituted or unsubstituted aryl group, an aryl having a carbon number of 5 to 12 Groups are preferred.
- the carbon number of the substituent does not include the carbon number of the substituent.
- alkyl group having 1 to 8 carbon atoms examples include a methyl group, an ethyl group, a propyl group, an isopropyl group, an n-butyl group, an isobutyl group, a sec-butyl group, a tert-butyl group, a pentyl group, a hexyl group and the like. ..
- aryl group having 5 to 12 carbon atoms include a phenyl group, a tolyl group, a xsilyl group, and a naphthyl group.
- R 2 is preferably an aromatic hydrocarbon group, more preferably a phenyl group.
- the substituted or unsubstituted alkyl group of R 3 and R 4 is preferably an alkyl group having 1 to 8 carbon atoms, and the substituted or unsubstituted aryl group has 5 to 5 carbon atoms. Twelve aryl groups are preferred.
- the carbon number of the substituent does not include the carbon number of the substituent.
- alkyl group having 1 to 8 carbon atoms examples include a methyl group, an ethyl group, a propyl group, an isopropyl group, an n-butyl group, an isobutyl group, a sec-butyl group, a tert-butyl group, a pentyl group, a hexyl group and the like. ..
- aryl group having 5 to 12 carbon atoms include a phenyl group, a tolyl group, a xsilyl group, and a naphthyl group.
- R 3 and R 4 are each independently a hydrogen atom, a methyl group, or a phenyl group.
- examples of the substituents that R 1 , R 2 , R 3 and R 4 may have include an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group and a heterocyclic group.
- examples thereof include an alkylidene group, an amino group, a silyl group, an acyl group, an acyloxy group, a carboxy group, a cyano group, a nitro group, a hydroxy group, a mercapto group, and an oxo group.
- the number of carbon atoms contained in the substituent is preferably 1 to 6, more preferably 1 to 4, and even more preferably 1 to 3.
- R 1 , R 2 , R 3 and R 4 may have a fluorine atom.
- resin represented by the general formula (1) examples include a resin represented by the following formula.
- the value of n is 20 to 100%, preferably 50 to 100%, and more preferably 80 to 100% with respect to the total of 100% of the values of n and m.
- the value of m is 0 to 80%, preferably 0 to 50%, and more preferably 0 to 20%.
- the resin fine particles represented by the general formula (1) can be produced by the following method. For example, in a nitrogen atmosphere, a melifield resin and an alkali metal organophosphorus compound or a trivalent organophosphorus compound having an ester bond are added and reacted at ⁇ 20 to 150 ° C. for 1 to 48 hours. Resin fine particles can be produced.
- the Merrifield resin is a styrene / chloromethylstyrene crosslinked resin.
- the alkali metal organophosphorus compound include sodium diphenyl phosphide and sodium methyl phenyl phosphide.
- the trivalent organophosphorus compound having an ester bond include triethyl phosphate, methyl diphenyl subphosphine and the like.
- ethenylphenylmethylmagnesium chloride and phosphine halide are added to the reaction vessel and reacted at 0 to 100 ° C. for 1 to 48 hours to obtain phosphinylmethylstyrene, styrene, and a cross-linking agent.
- Resin fine particles can be produced by turbid polymerization.
- the phosphorus content on the surface is high, preferably 1.3 mmol / g or more, more preferably 2.0 mmol / g or more, and further preferably 2. It is 5.5 mmol / g or more.
- the phosphorus content on the surface of the resin fine particles can be measured by elemental analysis, the amount of adsorbed organic halide compound, and redox titration.
- the resin fine particles can be adjusted to a desired particle size by classifying them by a conventionally known method or adjusting the reaction conditions.
- the size of the resin fine particles is not particularly limited, but the average particle size is preferably 1 to 1000 ⁇ m, more preferably 10 to 100 ⁇ m, from the viewpoint of ease of forming a complex with the transition metal and reaction efficiency. Yes, more preferably 30-75 ⁇ m.
- the average particle size of the resin fine particles can be measured using a laser diffraction type particle size distribution measuring device or a sieving method (JIS K 0069: 1992).
- transition metal examples include nickel, palladium, and rhodium, with nickel being preferred.
- the hydrophosphorylation reaction can be efficiently promoted under temperature conditions of room temperature (20 ° C.) or higher and lower than 100 ° C.
- the substance amount ratio of the phosphine group and the transition metal in the resin fine particles is not particularly limited as long as a complex compound can be formed, but is preferably 10: 1 to 1: 2, and more preferably 8: 1 to 1: 1. More preferably, it is 5: 1 to 2: 1.
- the method for producing a complex compound of the present invention includes a step of reacting the resin fine particles represented by the above general formula (1) with a transition metal compound in the presence of an organic solvent.
- the resin fine particles represented by the general formula (1) are as described in detail above.
- the transition metal compound used in the method for producing a complex compound is preferably a nickel compound or a palladium compound, and more preferably a zero-valent nickel compound.
- the zero-valent nickel compound include bis (1,5-cyclooctadiene) nickel (0), tetrakis (triphenylphosphine) nickel (0), and nickel carbonyl.
- a complex compound can be formed by using a zero-valent nickel compound having a ligand having a coordination force weaker than that of phosphine existing on the surface of the resin fine particles.
- the reaction temperature of the resin fine particles and the transition metal compound is not particularly limited, but is preferably ⁇ 10 to 100 ° C., more preferably 0 to 60 ° C. in consideration of reaction efficiency, reaction rate, and by-products. More preferably, it is 10 to 30 ° C.
- the reaction time between the resin fine particles and the transition metal compound is not particularly limited, but is preferably 10 minutes to 24 hours, more preferably 1 hour to 18 hours in consideration of reaction efficiency, reaction rate, and by-products. , More preferably 6-18 hours.
- the organic solvent used for the reaction between the resin fine particles and the transition metal compound is not particularly limited, and examples thereof include ethers, hydrocarbons, ketones, esters, aromatic hydrocarbons, and the like, and ethers such as tetrahydrofuran are used. Is preferable.
- the reaction between the resin fine particles and the transition metal compound is preferably carried out in an inert gas atmosphere in consideration of the reaction efficiency, reaction rate and by-products.
- the inert gas it is preferable to use nitrogen, argon or the like.
- the above complex compound can be suitably used as a catalyst for the hydrophosphorylation reaction.
- an alkenyl phosphorus compound can be efficiently synthesized from a phosphorus compound and an alkynyl compound, which are raw materials, under a temperature condition of room temperature or higher.
- a phosphorus compound represented by the following general formula (2) can be used as the raw material for the hydrophosphorylation reaction.
- R 5 and R 6 are independently substituted or unsubstituted alkyl groups, substituted or unsubstituted alkoxy groups, substituted or unsubstituted cycloalkyl groups, substituted or unsubstituted, respectively. It represents an aralkyl group, a substituted or unsubstituted aryl group, or a substituted or unsubstituted aryloxy group. Further, R 5 and R 6 may be bonded to each other to form a cyclic structure.
- the alkyl group of R 5 and R 6, an alkoxy group, a cycloalkyl group, an aralkyl group, an aryl group, the number of carbon atoms of the aryloxy group is preferably 1-10.
- the carbon number of the substituent does not include the carbon number of the substituent.
- R 5 and R 6 include an alkyl group such as a methyl group, an ethyl group, a propyl group, an isopropyl group, an n-butyl group, an isobutyl group, a sec-butyl group, a pentyl group and a hexyl group, a methoxy group and an ethoxy group.
- Aalkyl groups such as butoxy groups, cycloalkyl groups such as cyclohexyl groups, aralkyl groups such as benzyl groups and phenethyl groups, aryl groups such as phenyl groups, trill groups, xsilyl groups and naphthyl groups, and aryloxy groups such as phenoxy groups.
- cycloalkyl groups such as cyclohexyl groups
- aralkyl groups such as benzyl groups and phenethyl groups
- aryl groups such as phenyl groups, trill groups, xsilyl groups and naphthyl groups
- aryloxy groups such as phenoxy groups.
- examples of the substituent that R 5 and R 6 may have include an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group, a heterocyclic group, an alkylidene group, a silyl group and an acyl group.
- examples thereof include a group, an acyloxy group, a carboxy group, a cyano group, a nitro group, a hydroxy group, a mercapto group, an oxo group and the like.
- the number of carbon atoms contained in the substituent is preferably 1 to 6, more preferably 1 to 4, and even more preferably 1 to 3.
- an alkynyl compound represented by the following general formula (3) can be used as a raw material for the hydrophosphorylation reaction.
- R 7 and R 8 are independently hydrogen atom, substituted or unsubstituted alkyl group, substituted or unsubstituted cycloalkyl group, substituted or unsubstituted aralkyl group, substituted or substituted.
- R 7 and R 8 include methyl group, ethyl group, propyl group, isopropyl group, n-butyl group, isobutyl group, sec-butyl group, pentyl group, hexyl group and other alkyl groups, cyclohexyl group and other cyclos.
- Aralkyl group such as alkyl group, benzyl group, phenethyl group, aryl group such as phenyl group, tolyl group, xylyl group, naphthyl group, 1-butenyl group, 2-butenyl group, 1,3-butadienyl group, pentenyl group, hexenyl
- alkenyl group such as a group, an alkoxy group such as a methoxy group, an ethoxy group and a butoxy group, and an aryloxy group such as a phenoxy group.
- examples of the substituent that R 7 and R 8 may have include an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group, a heterocyclic group, an alkylidene group, a silyl group and an acyl group.
- examples thereof include a group, an acyloxy group, a carboxy group, a cyano group, a nitro group, a hydroxy group, a mercapto group, an oxo group and the like.
- the number of carbon atoms contained in the substituent is preferably 1 to 6, more preferably 1 to 4, and even more preferably 1 to 3.
- the substance amount ratio of the phosphorus compound represented by the general formula (2) and the alkynyl compound represented by the general formula (3) of the raw material for the hydrophosphorylation reaction is preferably 10: 1 to 0.1: 1. , More preferably 3: 1 to 0.7: 1, and even more preferably 1.1: 1 to 0.9: 1.
- the amount of the complex compound (catalyst) used in the hydrophosphorylation reaction is not particularly limited as long as the reaction proceeds sufficiently, but is preferably 0.001 to 0.5 mol with respect to 1 mol of the phosphorus compound as a raw material. It is more preferably 0.01 to 0.1 mol, and even more preferably 0.025 to 0.05 mol.
- the reaction temperature of the hydrophosphorylation reaction is not particularly limited, but is preferably 50 to 120 ° C., more preferably 50 to 80 ° C., and even more preferably 50 to 80 ° C. in consideration of reaction efficiency, reaction rate, and by-products. It is 50 to 60 ° C.
- the reaction time of the hydrophosphorylation reaction is not particularly limited, but is preferably 30 minutes to 40 hours, more preferably 1 hour to 24 hours, and further, in consideration of reaction efficiency, reaction rate, and by-products. It is preferably 4 to 18 hours.
- the hydrophosphorylation reaction may be carried out under an organic solvent or without a solvent.
- the organic solvent used for the hydrophosphorylation reaction is not particularly limited, and examples thereof include alcohols, ethers, hydrocarbons, ketones, esters, aromatic hydrocarbons and the like.
- the hydrophosphorylation reaction is preferably carried out in an inert gas atmosphere in consideration of reaction efficiency, reaction rate and by-products.
- the inert gas it is preferable to use nitrogen, argon or the like.
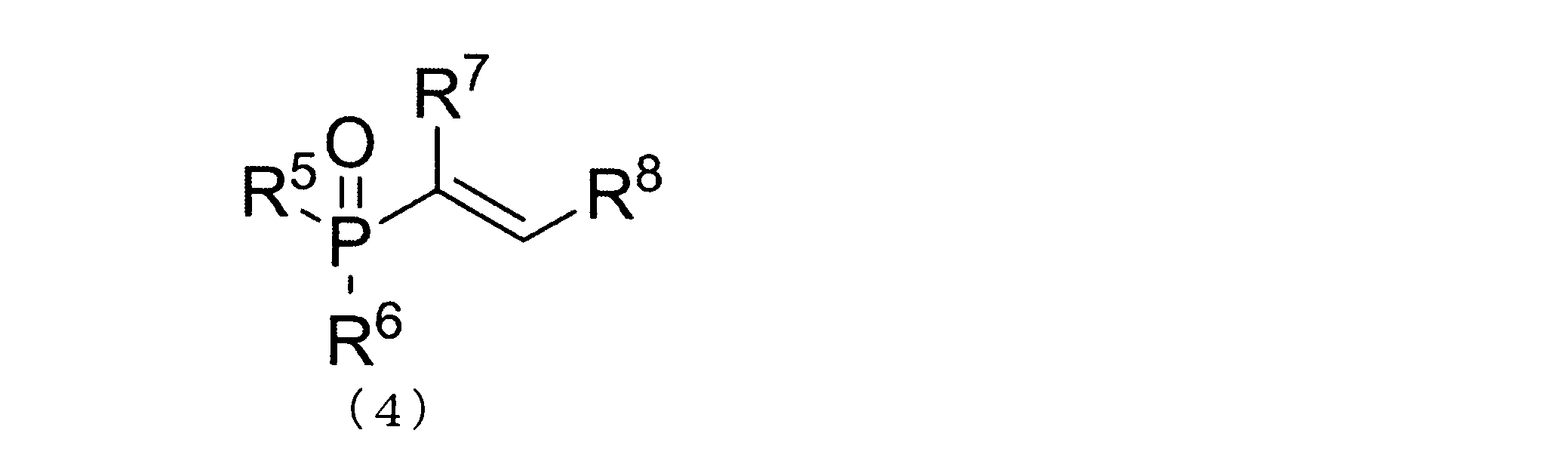
- alkenyl phosphorus compound represented by the following general formula (4)
- R 5 and R 6 has the general formula (2) have the same meanings as R 5 and R 6 of, R 7 and R 8 of the general formula in (2) R 7 and R It is synonymous with 8.
- the phosphorus content on the surface of the obtained resin fine particles (I) was measured by the following organic halide adsorption method and found to be 2.34 mmol / g.
- 100 mg of resin fine particles and 2.0 mL of a 5.5 mass% benzyl bromide THF solution were weighed into a vial, and the mixture was stirred at 60 ° C. for 18 hours.
- the supernatant was withdrawn, and the amount of substance of benzyl bromide adsorbed by the internal standard method (standard substance diphenyl ether) was calculated using GC-FID to determine the phosphorus content of the resin fine particles.
- the obtained resin fine particles (I) were sieved through a 300 mesh sieve, and the passed material was collected. As a result, 15.9 g of pale yellow resin fine particles were obtained.
- Nickel (0) is considered to have reacted with the resin fine particles (I) to form a complex.
- the obtained resin fine particles (I) were measured by IR.
- the obtained IR spectrum is shown in FIG.
- the formation of vinyl phosphorus was confirmed by coordinating with Ni above. From these results, it can be said that a chemical bond of phosphorus was formed on the surface of the resin fine particles.
- Example 2 Under a nitrogen atmosphere, 132 mL of THF and 20.17 g of triphenylphosphine were added to the reaction vessel and stirred well. Subsequently, 25.4 g of a metallic sodium dispersion (sodium content of about 25% by mass, average particle diameter of metallic sodium fine particles: 10 ⁇ m, manufactured by Shinko Environmental Solution Co., Ltd., SD) was added to the reaction vessel, and then the temperature was 25 ° C. The mixture was stirred for 18 hours to obtain sodium diphenylphosphide (Ph 2 P-Na).
- a metallic sodium dispersion sodium content of about 25% by mass, average particle diameter of metallic sodium fine particles: 10 ⁇ m, manufactured by Shinko Environmental Solution Co., Ltd., SD
- the phosphorus content on the surface of the obtained resin fine particles (II) was measured in the same manner as in Example 1 and found to be 2.96 mmol / g. (In the above formula, the value of n is 100% and the value of m is 0% with respect to the total of 100% of the values of n and m.)
- the obtained resin fine particles (II) were measured by IR.
- the obtained IR spectrum is shown in FIG.
- the formation of vinyl phosphorus was confirmed by coordinating with Ni above. From these results, it can be said that a chemical bond of phosphorus was formed on the surface of the resin fine particles.
- Example 3 Under an argon gas atmosphere, 30 mL of THF and 5.0 g of methyldiphenylphosphine were added to the reaction vessel. Next, 4.8 g of a metallic sodium dispersion (sodium content of about 25% by mass, average particle diameter of metallic sodium fine particles: 10 ⁇ m, SD manufactured by Shinko Environmental Solution Co., Ltd.) was added, and then the mixture was reacted at 0 ° C. for 18 hours. Sodium methylphenylphosphide (MePhP-Na) was obtained. 31 When confirmed by P-NMR, the yield was 70.0%.
- a metallic sodium dispersion sodium content of about 25% by mass, average particle diameter of metallic sodium fine particles: 10 ⁇ m, SD manufactured by Shinko Environmental Solution Co., Ltd.
- the phosphorus content on the surface of the obtained resin fine particles (III) was measured in the same manner as in Example 1 and found to be 3.85 mmol / g. (In the above formula, the value of n is 100% and the value of m is 0% with respect to the total of 100% of the values of n and m.)
- the obtained resin fine particles (III) were measured by IR.
- the obtained IR spectrum is shown in FIG.
- the formation of vinyl phosphorus was confirmed by coordinating with Ni above. From these results, it can be said that a chemical bond of phosphorus was formed on the surface of the resin fine particles.
- Example 4 Under a nitrogen atmosphere, 20 g of Merifield resin (manufactured by Sigma-Aldrich Japan LLC, 5.5 mmol Cl / g, cross-linking agent: divinylbenzene 5 mol%, particle size 16-50 mesh) and triethyl phosphate ((EtO)) were placed in the reaction vessel. ) 3 P) 50 mL was added, and heating and stirring were performed at 130 ° C. for 20 hours. The precipitate was collected from the reaction solution allowed to cool to room temperature and washed 5 times with 20 mL of acetone, 3 times with 20 mL of water, and 3 times with 20 mL of acetone to obtain 25.08 g of pale yellow resin fine particles.
- Merifield resin manufactured by Sigma-Aldrich Japan LLC, 5.5 mmol Cl / g, cross-linking agent: divinylbenzene 5 mol%, particle size 16-50 mesh
- (EtO) triethyl phosphate
- Table 1 shows a list of the results of the above synthesis examples 1 to 6.
- Table 2 shows a list of the results of the above synthesis examples 7 to 10.
Abstract
[課題]ヒドロホスホリル化反応の触媒として有用な錯体化合物およびその製造方法の提供。 [解決手段]本発明の錯体化合物は、下記一般式(1): (一般式(1)中、R1は、置換もしくは非置換の炭化水素基を表し、R2は、置換もしくは非置換のアルキル基または置換もしくは非置換のアリール基を示し、R3およびR4は、それぞれ独立して、水素原子、置換もしくは非置換のアルキル基、または置換もしくは非置換のアリール基を示し、nおよびmの値の合計100%に対して、nの値は20~100%の範囲内であり、mの値は0~80%の範囲内であり、*で樹脂微粒子表面と結合している。) で表される樹脂微粒子と、遷移金属との錯体化合物である。
Description
本発明は、錯体化合物に関する。より詳細には、本発明は、ヒドロホスホリル化反応の触媒として有用な錯体化合物に関する。また、本発明は、該錯体化合物の製造方法に関する。
有機リン化合物は、例えば、難燃剤、可塑剤、殺虫剤、医農薬、金属錯体の配位子等の様々な製品に幅広く使用されている化学物質である。近年、有機リン化合物は、機能性材料として金属表面処理剤、及び難燃性樹脂等の構成材料や電子材料分野においても、工業的に特に注目されている。
有機リン化合物の中でも、アルケニルホスホン酸誘導体は、上記の様々な化学物質の有用な前駆体物質であるため、従来から様々な製造方法が検討されてきた。例えば、触媒を用いて、ホスホン酸のP(O)-H結合のアルキン類への付加反応(以下、ヒドロホスホリル化反応)によって、アルケニルホスホン酸誘導体を製造することが行われてきた。例えば、非特許文献1では、トリフェニルホスフィンが結合したポリスチレン樹脂に遷移金属を固定化した触媒を用いて、ヒドロホスホリル化反応を行うことが提案されている。
Chem. Lett. 2013, 42, 1065-1067
しかしながら、非特許文献1に記載のトリフェニルホスフィンが結合したポリスチレン樹脂に遷移金属を固定化した触媒では、樹脂表面のリン含量が十分ではなく、反応に必要なリン量を添加するためには非常に多くの樹脂量が必要となったり、反応効率が低かったり、また、樹脂表面からの金属成分のリーチングが多く、副反応が多く進行するという問題があった。そのため、ヒドロホスホリル化反応に用いた際の反応効率に改善の余地があった。
したがって、本発明の目的は、ヒドロホスホリル化反応の触媒として有用な錯体化合物を提供することにある。
本発明者は、上記課題を解決するために鋭意検討を行った結果、表面にホスフィン置換基を有する樹脂と遷移金属とを反応させることで、ヒドロホスホリル化反応の触媒として有用な錯体化合物を得られることを見出し、本発明を完成するに至った。
すなわち、本発明によれば、以下の発明が提供される。
[1] 下記一般式(1):
(一般式(1)中、R1は、置換もしくは非置換の炭化水素基を表し、R2は、置換もしくは非置換のアルキル基または置換もしくは非置換のアリール基を示し、R3およびR4は、それぞれ独立して、水素原子、置換もしくは非置換のアルキル基、または置換もしくは非置換のアリール基を示し、nおよびmの値の合計100%に対して、nの値は20~100%の範囲内であり、mの値は0~80%の範囲内であり、*で樹脂微粒子表面と結合している。)
で表される樹脂微粒子と、遷移金属との錯体化合物。
[2] 前記樹脂微粒子中のホスフィン基と前記遷移金属の物質量比が10:1~1:2である、[1]に記載の錯体化合物。
[3] 一般式(1)中、R1は、炭素数が6~12の炭化水素基である、[1]または[2]に記載の錯体化合物。
[4] 一般式(1)中、R2は、炭素数が1~8のアルキル基、または炭素数が5~12のアリール基である、[1]~[3]のいずれかに記載の錯体化合物。
[5] 一般式(1)中、R3およびR4は、炭素数が1~8のアルキル基、または炭素数が5~12のアリール基である、[1]~[4]のいずれかに記載の錯体化合物。
[6] 前記遷移金属が、ニッケルまたはパラジウムである、[1]~[5]のいずれかに記載の錯体化合物。
[7] ヒドロホスホリル化反応の触媒として用いられる、[1]~[6]のいずれかに記載の錯体化合物。
[8] 下記一般式(1):
(一般式(1)中、R1は、置換もしくは非置換の炭化水素基を表し、R2は、置換もしくは非置換のアルキル基または置換もしくは非置換のアリール基を示し、R3およびR4は、それぞれ独立して、水素原子、置換もしくは非置換のアルキル基、または置換もしくは非置換のアリール基を示し、nおよびmの値の合計100%に対して、nの値は20~100%の範囲内であり、mの値は0~80%の範囲内であり、*で樹脂微粒子表面と結合している。)
で表される樹脂微粒子と、遷移金属化合物とを、有機溶媒の存在下で反応させる工程を含む、錯体化合物の製造方法。
[9] 前記遷移金属化合物がゼロ価ニッケル化合物である、[8]に記載の錯体化合物の製造方法。
[10] 前記ゼロ価ニッケル化合物が、ビス(1,5-シクロオクタジエン)ニッケル(0)、テトラキス(トリフェニルホスフィン)ニッケル(0)、およびニッケルカルボニルからなる群から選択される少なくとも1種である、[9]に記載の製造方法。
[1] 下記一般式(1):
で表される樹脂微粒子と、遷移金属との錯体化合物。
[2] 前記樹脂微粒子中のホスフィン基と前記遷移金属の物質量比が10:1~1:2である、[1]に記載の錯体化合物。
[3] 一般式(1)中、R1は、炭素数が6~12の炭化水素基である、[1]または[2]に記載の錯体化合物。
[4] 一般式(1)中、R2は、炭素数が1~8のアルキル基、または炭素数が5~12のアリール基である、[1]~[3]のいずれかに記載の錯体化合物。
[5] 一般式(1)中、R3およびR4は、炭素数が1~8のアルキル基、または炭素数が5~12のアリール基である、[1]~[4]のいずれかに記載の錯体化合物。
[6] 前記遷移金属が、ニッケルまたはパラジウムである、[1]~[5]のいずれかに記載の錯体化合物。
[7] ヒドロホスホリル化反応の触媒として用いられる、[1]~[6]のいずれかに記載の錯体化合物。
[8] 下記一般式(1):
で表される樹脂微粒子と、遷移金属化合物とを、有機溶媒の存在下で反応させる工程を含む、錯体化合物の製造方法。
[9] 前記遷移金属化合物がゼロ価ニッケル化合物である、[8]に記載の錯体化合物の製造方法。
[10] 前記ゼロ価ニッケル化合物が、ビス(1,5-シクロオクタジエン)ニッケル(0)、テトラキス(トリフェニルホスフィン)ニッケル(0)、およびニッケルカルボニルからなる群から選択される少なくとも1種である、[9]に記載の製造方法。
本発明によれば、ヒドロホスホリル化反応の触媒として有用な錯体化合物およびその製造方法を提供することができる。本発明の錯体化合物は、触媒として、室温以上の温度条件下においてヒドロホスホリル化反応を効率良く進行させることができる。また、本発明の錯体化合物は、原料に安価な市販の材料を用いることができるため、製造コストを低減することができる。
[錯体化合物]
本発明の錯体化合物は、下記で詳述する樹脂微粒子と、遷移金属との錯体化合物(樹脂担持遷移金属錯体)であり、ヒドロホスホリル化反応の触媒として用いることができる。このような錯体化合物は、樹脂微粒子の表面に高濃度にホスフィン置換基を有することで、室温以上の温度条件下においてヒドロホスホリル化反応を効率良く進行させることができる。
本発明の錯体化合物は、下記で詳述する樹脂微粒子と、遷移金属との錯体化合物(樹脂担持遷移金属錯体)であり、ヒドロホスホリル化反応の触媒として用いることができる。このような錯体化合物は、樹脂微粒子の表面に高濃度にホスフィン置換基を有することで、室温以上の温度条件下においてヒドロホスホリル化反応を効率良く進行させることができる。
(樹脂微粒子)
錯体化合物を形成する樹脂微粒子は、下記一般式(1)で表される。
(一般式(1)中、R1は、置換もしくは非置換の炭化水素基を表し、R2は、置換もしくは非置換のアルキル基または置換もしくは非置換のアリール基を示し、R3およびR4は、それぞれ独立して、水素原子、置換もしくは非置換のアルキル基、または置換もしくは非置換のアリール基を示し、nおよびmの値の合計100%に対して、nの値は20~100%の範囲内であり、mの値は0~80%の範囲内であり、*で樹脂微粒子表面と結合している。)
錯体化合物を形成する樹脂微粒子は、下記一般式(1)で表される。
一般式(1)中、R1の置換もしくは非置換の炭化水素基としては、炭素数6~12の炭化水素基が好ましい。なお、上記炭素数に置換基の炭素数は含まれない。炭素数6~12の炭化水素基としては、へキシレン基、へプチレン基、オクチレン基等のアルキレン基、シクロヘキシレン基等のシクロアルキレン基、フェニレン基、ナフチレン基等の芳香族炭化水素基等が挙げられる。これらの中でもR1は、芳香族炭化水素基であることが好ましく、フェニレン基であることがより好ましい。
一般式(1)中、R2の置換もしくは非置換のアルキル基としては、炭素数が1~8のアルキル基が好ましく、置換もしくは非置換のアリール基としては、炭素数が5~12のアリール基が好ましい。なお、上記炭素数に置換基の炭素数は含まれない。炭素数1~8のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基、ペンチル基、ヘキシル基等が挙げられる。炭素数が5~12のアリール基としては、フェニル基、トリル基、キシリル基、ナフチル基等が挙げられる。これらの中でも、R2は、芳香族炭化水素基であることが好ましく、フェニル基であることがより好ましい。
一般式(1)中、R3およびR4の置換もしくは非置換のアルキル基としては、炭素数が1~8のアルキル基が好ましく、置換もしくは非置換のアリール基としては、炭素数が5~12のアリール基が好ましい。なお、上記炭素数に置換基の炭素数は含まれない。炭素数1~8のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基、ペンチル基、ヘキシル基等が挙げられる。炭素数が5~12のアリール基としては、フェニル基、トリル基、キシリル基、ナフチル基等が挙げられる。これらの中でも、R3およびR4は、それぞれ独立して、水素原子、メチル基、フェニル基のいずれかであることが好ましい。
一般式(1)中、R1、R2、R3、およびR4が有してもよい置換基としては、例えば、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、複素環基、アルキリデン基、アミノ基、シリル基、アシル基、アシルオキシ基、カルボキシ基、シアノ基、ニトロ基、ヒドロキシ基、メルカプト基、およびオキソ基等が挙げられる。また、置換基に含まれる炭素数は好ましくは1~6であり、より好ましくは1~4であり、さらに好ましくは1~3である。また、R1、R2、R3、およびR4は、フッ素原子を有してもよい。
一般式(1)中、nおよびmの値の合計100%に対して、nの値は20~100%であり、好ましくは50~100%であり、より好ましくは80~100%であり、mの値は0~80%であり、好ましくは0~50%であり、より好ましくは0~20%である。
一般式(1)で表される樹脂微粒子は、以下の方法により製造することができる。例えば、窒素雰囲気下、反応容器中にメリフィールド樹脂とアルカリ金属の有機リン化合物やエステル結合を持つ三価の有機リン化合物とを加え、-20~150℃で1~48時間反応させることで、樹脂微粒子を製造することができる。なお、メリフィールド樹脂とは、スチレン・クロロメチルスチレン架橋樹脂のことである。アルカリ金属の有機リン化合物としては、例えば、ナトリウムジフェニルホスフィド、ナトリウムメチルフェニルホスフィド等が挙げられる。エステル結合を持つ三価の有機リン化合物としては、例えば、亜リン酸トリエチル、ジフェニル亜ホスフィン酸メチル等が挙げられる。
また、窒素雰囲気下、反応容器中にエテニルフェニルメチルマグネシウムクロリドとハロゲン化ホスフィンとを加え、0~100℃で1~48時間反応させて得られるホスフィニルメチルスチレンとスチレン、架橋剤を懸濁重合することで、樹脂微粒子を製造することができる。
樹脂微粒子は、*で樹脂微粒子表面と結合しているため、表面のリン含量が高く、好ましくは1.3mmol/g以上であり、より好ましくは2.0mmol/g以上であり、さらに好ましくは2.5mmol/g以上である。樹脂微粒子表面のリン含量は、元素分析、有機ハライド化合物の吸着量、および酸化還元滴定により測定することができる。
樹脂微粒子は、従来公知の方法により分級したり、反応条件を調節したりすることで、所望の粒子径に調整することができる。樹脂微粒子の大きさは特に限定されるものではないが、遷移金属との錯体の形成し易さと反応効率の観点から、平均粒子径が好ましくは1~1000μmであり、より好ましくは10~100μmであり、さらに好ましくは30~75μmである。樹脂微粒子の平均粒子径は、レーザー回折式の粒度分布測定装置やふるい分け法(JIS K 0069:1992)を使用して測定することができる。
(遷移金属)
錯体化合物を形成する遷移金属としては、ニッケル、パラジウム、およびロジウムが挙げられ、ニッケルが好ましい。特に樹脂微粒子とニッケルが形成した錯体化合物を触媒として用いることで、室温(20℃)以上100℃未満の温度条件下においてヒドロホスホリル化反応を効率良く進行させることができる。
錯体化合物を形成する遷移金属としては、ニッケル、パラジウム、およびロジウムが挙げられ、ニッケルが好ましい。特に樹脂微粒子とニッケルが形成した錯体化合物を触媒として用いることで、室温(20℃)以上100℃未満の温度条件下においてヒドロホスホリル化反応を効率良く進行させることができる。
樹脂微粒子中のホスフィン基と遷移金属の物質量比は、錯体化合物を形成できれば特に限定されないが、好ましくは10:1~1:2であり、より好ましくは8:1~1:1であり、さらに好ましくは5:1~2:1である。
[錯体化合物の製造方法]
本発明の錯体化合物の製造方法は、上記一般式(1)で表される樹脂微粒子と、遷移金属化合物とを、有機溶媒の存在下で反応させる工程を含むものである。一般式(1)で表される樹脂微粒子については、上記で詳述した通りである。
本発明の錯体化合物の製造方法は、上記一般式(1)で表される樹脂微粒子と、遷移金属化合物とを、有機溶媒の存在下で反応させる工程を含むものである。一般式(1)で表される樹脂微粒子については、上記で詳述した通りである。
錯体化合物の製造方法に用いる遷移金属化合物は、ニッケル化合物またはパラジウム化合物であることが好ましく、ゼロ価ニッケル化合物であることがより好ましい。ゼロ価ニッケル化合物としては、例えば、ビス(1,5-シクロオクタジエン)ニッケル(0)、テトラキス(トリフェニルホスフィン)ニッケル(0)、およびニッケルカルボニル等が挙げられる。ゼロ価ニッケル化合物は、樹脂微粒子の表面に存在するホスフィンよりも弱い配位力の配位子を有するものを用いることで、錯体化合物を形成することができる。
樹脂微粒子と遷移金属化合物の反応温度は、特に限定されないが、反応効率や反応速度、副生成物を考慮して、好ましくは-10~100℃であり、より好ましくは0~60℃であり、さらに好ましくは10~30℃である。
樹脂微粒子と遷移金属化合物の反応時間は、特に限定されないが、反応効率や反応速度、副生成物を考慮して、好ましくは10分~24時間であり、より好ましくは1時間~18時間であり、さらに好ましくは6~18時間である。
樹脂微粒子と遷移金属化合物の反応に用いる有機溶媒は、特に限定されないが、例えば、エーテル類、炭化水素、ケトン類、エステル類、芳香族炭化水素等が挙げられ、テトラヒドロフラン等のエーテル類を用いることが好ましい。
樹脂微粒子と遷移金属化合物の反応は、反応効率や反応速度、副生成物を考慮して、不活性ガス雰囲気下で実施することが好ましい。不活性ガスとしては、窒素、アルゴン等を用いることが好ましい。
[ヒドロホスホリル化反応]
上記の錯体化合物は、ヒドロホスホリル化反応の触媒として好適に用いることができる。特に、室温以上の温度条件下において、原料物質であるリン化合物とアルキニル化合物から、アルケニルリン化合物を効率良く合成することができる。
上記の錯体化合物は、ヒドロホスホリル化反応の触媒として好適に用いることができる。特に、室温以上の温度条件下において、原料物質であるリン化合物とアルキニル化合物から、アルケニルリン化合物を効率良く合成することができる。
ヒドロホスホリル化反応の原料物質としては、下記一般式(2)で表されるリン化合物を用いることができる。
(一般式(2)中、R5およびR6は、それぞれ独立して、置換もしくは非置換のアルキル基、置換もしくは非置換のアルコキシ基、置換もしくは非置換のシクロアルキル基、置換もしくは非置換のアラルキル基、置換もしくは非置換のアリール基、または置換もしくは非置換のアリールオキシ基を示す。また、R5およびR6は、互いに結合して環状構造を形成していてもよい。)
一般式(2)中、R5およびR6のアルキル基、アルコキシ基、シクロアルキル基、アラルキル基、アリール基、アリールオキシ基の炭素数は、1~10であることが好ましい。なお、上記炭素数に置換基の炭素数は含まれない。例えば、R5およびR6としては、メチル基、エチル基、プロピル基、イソプロピル基、n-ブチル基、イソブチル基、sec-ブチル基、ペンチル基、ヘキシル基等のアルキル基、メトキシ基、エトキシ基、ブトキシ基等のアルコキシ基、シクロヘキシル基等のシクロアルキル基、ベンジル基、フェネチル基等のアラルキル基、フェニル基、トリル基、キシリル基、ナフチル基等のアリール基、フェノキシ基等のアリールオキシ基が挙げられる。
一般式(2)中、R5およびR6が有してもよい置換基としては、例えば、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、複素環基、アルキリデン基、シリル基、アシル基、アシルオキシ基、カルボキシ基、シアノ基、ニトロ基、ヒドロキシ基、メルカプト基、およびオキソ基等が挙げられる。また、置換基に含まれる炭素数は好ましくは1~6であり、より好ましくは1~4であり、さらに好ましくは1~3である。
ヒドロホスホリル化反応の原料物質としては、下記一般式(3)で表されるアルキニル化合物を用いることができる。
(一般式(3)中、R7およびR8は、それぞれ独立して、水素原子、置換もしくは非置換のアルキル基、置換もしくは非置換のシクロアルキル基、置換もしくは非置換のアラルキル基、置換もしくは非置換のアリール基、置換もしくは非置換のヘテロアリール基、置換もしくは非置換のアルケニル基、置換もしくは非置換のアルコキシ基、置換もしくは非置換のアリールオキシ基、または置換もしくは非置換のシリル基を示す。)
一般式(3)中、R7およびR8のアルキル基、シクロアルキル基、アラルキル基、アリール基、ヘテロアリール基、アルケニル基、アルコキシ基、アリールオキシ基の炭素数は、1~10であることが好ましい。なお、上記炭素数に置換基の炭素数は含まれない。例えば、R7およびR8としては、メチル基、エチル基、プロピル基、イソプロピル基、n-ブチル基、イソブチル基、sec-ブチル基、ペンチル基、ヘキシル基等のアルキル基、シクロヘキシル基等のシクロアルキル基、ベンジル基、フェネチル基等のアラルキル基、フェニル基、トリル基、キシリル基、ナフチル基等のアリール基、1-ブテニル基、2-ブテニル基、1,3-ブタジエニル基、ペンテニル基、ヘキセニル基等のアルケニル基、メトキシ基、エトキシ基、ブトキシ基等のアルコキシ基、フェノキシ基等のアリールオキシ基が挙げられる。
一般式(3)中、R7およびR8が有してもよい置換基としては、例えば、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、複素環基、アルキリデン基、シリル基、アシル基、アシルオキシ基、カルボキシ基、シアノ基、ニトロ基、ヒドロキシ基、メルカプト基、およびオキソ基等が挙げられる。また、置換基に含まれる炭素数は好ましくは1~6であり、より好ましくは1~4であり、さらに好ましくは1~3である。
(反応条件)
ヒドロホスホリル化反応の原料物質の一般式(2)で表されるリン化合物と一般式(3)で表されるアルキニル化合物の物質量比は、好ましくは10:1~0.1:1であり、より好ましくは3:1~0.7:1であり、さらに好ましくは1.1:1~0.9:1である。
ヒドロホスホリル化反応の原料物質の一般式(2)で表されるリン化合物と一般式(3)で表されるアルキニル化合物の物質量比は、好ましくは10:1~0.1:1であり、より好ましくは3:1~0.7:1であり、さらに好ましくは1.1:1~0.9:1である。
ヒドロホスホリル化反応における錯体化合物(触媒)の使用量は、反応が十分に進行すれば特に限定されないが、原料物質であるリン化合物1molに対して、好ましくは0.001~0.5molであり、より好ましく0.01~0.1molであり、さらに好ましくは0.025~0.05molである。
ヒドロホスホリル化反応の反応温度は、特に限定されないが、反応効率や反応速度、副生成物を考慮して、好ましくは50~120℃であり、より好ましくは50~80℃であり、さらに好ましくは50~60℃である。
ヒドロホスホリル化反応の反応時間は、特に限定されないが、反応効率や反応速度、副生成物を考慮して、好ましくは30分~40時間であり、より好ましくは1時間~24時間であり、さらに好ましくは4~18時間である。
ヒドロホスホリル化反応は、有機溶媒下で行ってもよいし、無溶媒下で行ってもよい。ヒドロホスホリル化反応に用いる有機溶媒は、特に限定されないが、例えば、アルコール類、エーテル類、炭化水素、ケトン類、エステル類、芳香族炭化水素等が挙げられる。
ヒドロホスホリル化反応は、反応効率や反応速度、副生成物を考慮して、不活性ガス雰囲気下で実施することが好ましい。不活性ガスとしては、窒素、アルゴン等を用いることが好ましい。
(アルケニルリン化合物)
本発明においては、ヒドロホスホリル化反応により、下記一般式(4)で表されるアルケニルリン化合物を得ることができる。
(一般式(4)中、R5およびR6は、一般式(2)中のR5およびR6と同義であり、R7およびR8は、一般式(2)中のR7およびR8と同義である。)
本発明においては、ヒドロホスホリル化反応により、下記一般式(4)で表されるアルケニルリン化合物を得ることができる。
以下に実施例および比較例を挙げて本発明を具体的に説明するが、本発明はこれらの実施例に限定されるものではない。
<錯体化合物の合成>
[実施例1]
窒素雰囲気下、反応容器中にテトラヒドロフラン(THF)40mLとトリフェニルホスフィン10.5gを加えよく攪拌した。続いて、反応容器中に金属ナトリウム分散体(ナトリウム含有量約25質量%、金属ナトリウム微粒子の平均粒子径:10μm、(株)神鋼環境ソリューション製、SD)7.36gを加えた後、25℃で18時間攪拌を行い、ナトリウムジフェニルホスフィド(Ph2P-Na)を得た。
[実施例1]
窒素雰囲気下、反応容器中にテトラヒドロフラン(THF)40mLとトリフェニルホスフィン10.5gを加えよく攪拌した。続いて、反応容器中に金属ナトリウム分散体(ナトリウム含有量約25質量%、金属ナトリウム微粒子の平均粒子径:10μm、(株)神鋼環境ソリューション製、SD)7.36gを加えた後、25℃で18時間攪拌を行い、ナトリウムジフェニルホスフィド(Ph2P-Na)を得た。
窒素雰囲気下、上記のナトリウムジフェニルホスフィニドを調整した反応容器中にメリフィールド樹脂(シグマアルドリッチジャパン合同会社製、4.4mmoL Cl/g、架橋剤:ジビニルベンゼン1mol%)9.8gを加え、60℃で15時間反応させた。反応後、2-プロパノール20mLを反応液に1時間かけて滴下した。この懸濁液から沈殿物を空気中に取り出し、THF20mLで3回、精製水20mLで3回、アセトン20mLで1回洗浄した。60℃で18時間減圧乾燥し、下記式で表される樹脂微粒子(I)を得た。
(上記式中、nおよびmの値の合計100%に対して、nの値は50%であり、mの値は50%
である。)
である。)
得られた樹脂微粒子(I)の表面のリン含量を、下記の有機ハライド吸着法により測定したところ、2.34mmol/gであった。
(有機ハライド吸着法による表面リン含量測定法)
樹脂微粒子100mgと5.5質量%ベンジルブロミドTHF溶液2.0mLをバイアルに量り取り、60℃で18時間攪拌した。上澄み液を抜き取り、GC-FIDを使用して、内部標準法(標準物質ジフェニルエーテル)で吸着されたベンジルブロミドの物質量を算出し、樹脂微粒子のリン含量を求めた。
(有機ハライド吸着法による表面リン含量測定法)
樹脂微粒子100mgと5.5質量%ベンジルブロミドTHF溶液2.0mLをバイアルに量り取り、60℃で18時間攪拌した。上澄み液を抜き取り、GC-FIDを使用して、内部標準法(標準物質ジフェニルエーテル)で吸着されたベンジルブロミドの物質量を算出し、樹脂微粒子のリン含量を求めた。
得られた樹脂微粒子(I)を300メッシュのふるいに掛けて、通過したものを回収したところ、15.9gの淡黄色の樹脂微粒子を得た。
窒素雰囲気下、反応容器中で、得られた樹脂微粒子(I)0.21mmolと、ビス(1,5-シクロオクタジエン)ニッケル(0)0.05mmolとを、THF1.0mLの存在下で、25℃で6時間反応させた。沈殿物を回収しTHF1.0mLで3回洗浄し、錯体化合物(I)を得た。このとき、反応液の上澄み液に、ジメチルグリオキシムを100mg加えたところ、沈殿の生成はほとんど確認できなかった。一方、THFにビス(1,5-シクロオクタジエン)ニッケル(0)のみを溶解し、ジメチルグリオキシムを加えた場合には、大量の沈殿物が析出したため、ビス(1,5-シクロオクタジエン)ニッケル(0)は樹脂微粒子(I)と反応し、錯体を形成したと考えられる。
得られた樹脂微粒子(I)をIRにより測定した。得られたIRスペクトルを図1に示す。IRスペクトルを確認したところ、原料のメリフィールド樹脂に含まれるC-Cl由来のピーク(波数:1295cm-1)が消失し、P-C由来のピーク(波数:694cm-1)の生成が確認できた。また、上記でNiと配位させてビニルリンの生成が確認できた。これらの結果から樹脂微粒子の表面にはリンの化学的な結合が形成されたと言える。
[実施例2]
窒素雰囲気下、反応容器中にTHF132mLとトリフェニルホスフィン20.17gを加えよく攪拌した。続いて、反応容器中に金属ナトリウム分散体(ナトリウム含有量約25質量%、金属ナトリウム微粒子の平均粒子径:10μm、(株)神鋼環境ソリューション製、SD)25.4gを加えた後、25℃で18時間攪拌を行い、ナトリウムジフェニルホスフィド(Ph2P-Na)を得た。
窒素雰囲気下、反応容器中にTHF132mLとトリフェニルホスフィン20.17gを加えよく攪拌した。続いて、反応容器中に金属ナトリウム分散体(ナトリウム含有量約25質量%、金属ナトリウム微粒子の平均粒子径:10μm、(株)神鋼環境ソリューション製、SD)25.4gを加えた後、25℃で18時間攪拌を行い、ナトリウムジフェニルホスフィド(Ph2P-Na)を得た。
次に、反応容器中にメリフィールド樹脂(シグマアルドリッチジャパン合同会社製、5.5mmol Cl/g、架橋剤:ジビニルベンゼン5mol%、粒径16-50mesh)9.76gを加え、25℃で20時間反応させた後、2-プロパノール20mLを一時間かけて滴下し、沈殿物を空気中に取り出した。この沈殿物をTHF60mLで3回、水60mLで3回、アセトン30mLで1回洗浄した。これを60℃で18時間減圧乾燥し、下記式で表される樹脂微粒子(II)を得た。得られた樹脂微粒子(II)の表面のリン含量を、実施例1と同様にして測定したところ、2.96mmol/gであった。
(上記式中、nおよびmの値の合計100%に対して、nの値は100%であり、mの値は0%である。)
反応容器中で、得られた樹脂微粒子(II)0.21mmolと、ビス(1,5-シクロオクタジエン)ニッケル(0)0.05mmolとを、THF1.0mLの存在下で、25℃で6時間反応させた。沈殿物を回収し、THF1.0mLで3回洗浄し、錯体化合物(II)を得た。
得られた樹脂微粒子(II)をIRにより測定した。得られたIRスペクトルを図2に示す。IRスペクトルを確認したところ、原料のメリフィールド樹脂に含まれるC-Cl由来のピーク(波数:1285cm-1)が消失し、P-C由来のピーク(波数:694cm-1)の生成が確認できた。また、上記でNiと配位させてビニルリンの生成が確認できた。これらの結果から樹脂微粒子の表面にはリンの化学的な結合が形成されたと言える。
[実施例3]
アルゴンガス雰囲気下、反応容器中にTHF30mL、メチルジフェニルホスフィン5.0gを加えた。次いで、金属ナトリウム分散体(ナトリウム含有量約25質量%、金属ナトリウム微粒子の平均粒子径:10μm、(株)神鋼環境ソリューション製、SD)を4.8g加えた後、0℃で18時間反応させて、ナトリウムメチルフェニルホスフィド(MePhP-Na)を得た。31P-NMRで確認したところ収率70.0%であった。
アルゴンガス雰囲気下、反応容器中にTHF30mL、メチルジフェニルホスフィン5.0gを加えた。次いで、金属ナトリウム分散体(ナトリウム含有量約25質量%、金属ナトリウム微粒子の平均粒子径:10μm、(株)神鋼環境ソリューション製、SD)を4.8g加えた後、0℃で18時間反応させて、ナトリウムメチルフェニルホスフィド(MePhP-Na)を得た。31P-NMRで確認したところ収率70.0%であった。
調整したナトリウムメチルフェニルホスフィドにメリフィールド樹脂(シグマアルドリッチジャパン合同会社製、5.5mmol Cl/g、架橋剤:ジビニルベンゼン5mol%、粒径16-50mesh)3.81gを加え、60℃で23時間反応させた。上澄み液を抜き取り、2-プロパノール20mLを一時間かけて滴下した。上澄み液をデカントし、THF20mLで3回、イオン交換水20mLで3回、アセトン20mLで洗浄した後、60℃で18時間減圧乾燥し、下記式で表される樹脂微粒子(III)を得た。得られた樹脂微粒子(III)の表面のリン含量を、実施例1と同様にして測定したところ、3.85mmol/gであった。
(上記式中、nおよびmの値の合計100%に対して、nの値は100%であり、mの値は0%である。)
反応容器中で、得られた樹脂微粒子(III)0.21mmolと、ビス(1,5-シクロオクタジエン)ニッケル(0)0.05mmolとを、THFの存在下で、25℃で4時間反応させて、錯体化合物(III)を得た。
得られた樹脂微粒子(III)をIRにより測定した。得られたIRスペクトルを図3に示す。IRスペクトルを確認したところ、原料のメリフィールド樹脂に含まれるC-Cl由来のピーク(波数:1295cm-1)が消失し、P-C由来のピーク(波数:694cm-1)の生成が確認できた。また、上記でNiと配位させてビニルリンの生成が確認できた。これらの結果から樹脂微粒子の表面にはリンの化学的な結合が形成されたと言える。
[実施例4]
窒素雰囲気下、反応容器中にメリフィールド樹脂(シグマアルドリッチジャパン合同会社製、5.5mmol Cl/g、架橋剤:ジビニルベンゼン5mol%、粒径16-50mesh)20gと、亜リン酸トリエチル((EtO)3P)50mLとを加え、130℃で20時間加熱攪拌を行った。室温まで放冷した反応液から沈殿物を回収しアセトン20mLで5回、水20mLで3回、アセトン20mLで3回洗浄し、淡黄色の樹脂微粒子25.08gを得た。続いて、得られた樹脂1.0gと、水素化アルミニウムリチウム(1mol/LTHF溶液)8.46mLを25℃で二日間反応させた。反応液にメタノール2mLをゆっくり加えた後、上澄み液をデカントし、10質量%水酸化ナトリウム水溶液5mLで6回、水5mLで5回洗浄し、60℃で18時間減圧乾燥することで、下記式で表される樹脂微粒子(IV)を得た。得られた樹脂微粒子(IV)の表面のリン含量は、理論値で4.80mmol/gであった。
(上記式中、nおよびmの値の合計100%に対して、nの値は100%であり、mの値は0%である。)
窒素雰囲気下、反応容器中にメリフィールド樹脂(シグマアルドリッチジャパン合同会社製、5.5mmol Cl/g、架橋剤:ジビニルベンゼン5mol%、粒径16-50mesh)20gと、亜リン酸トリエチル((EtO)3P)50mLとを加え、130℃で20時間加熱攪拌を行った。室温まで放冷した反応液から沈殿物を回収しアセトン20mLで5回、水20mLで3回、アセトン20mLで3回洗浄し、淡黄色の樹脂微粒子25.08gを得た。続いて、得られた樹脂1.0gと、水素化アルミニウムリチウム(1mol/LTHF溶液)8.46mLを25℃で二日間反応させた。反応液にメタノール2mLをゆっくり加えた後、上澄み液をデカントし、10質量%水酸化ナトリウム水溶液5mLで6回、水5mLで5回洗浄し、60℃で18時間減圧乾燥することで、下記式で表される樹脂微粒子(IV)を得た。得られた樹脂微粒子(IV)の表面のリン含量は、理論値で4.80mmol/gであった。
反応容器中で、得られた樹脂微粒子(IV)2.8mmolと、ビス(1,5-シクロオクタジエン)ニッケル(0)0.7mmolとを、THF2mLの存在下で、25℃で18時間反応させ沈殿物を回収、THF1.0mLで三回洗浄し、錯体化合物(IV)を得た。
得られた樹脂微粒子(IV)100mgを5%過酸化水素水5.0mLで処理し、IRにより測定した。得られたIRスペクトルを図4に示す。IRスペクトルを確認したところ、原料のメリフィールド樹脂に含まれるC-Cl由来のピーク(波数:1295cm-1)が消失し、P-C由来のピーク(波数:703cm-1)およびP(O)-OH由来のピーク(波数:1025cm-1)の生成が確認できた。また、上記でNiと配位させてビニルリンの生成が確認できた。これらの結果から樹脂微粒子の表面にはリンとニッケルの配位が形成されたと言える。
[比較例1]
反応容器中で、トリメチルホスフィン(シグマアルドリッチジャパン合同会社製、1.0mol/L THF溶液)1mLと、ビス(1,5-シクロオクタジエン)ニッケル(0)68.75mgとを、0℃で1時間反応させた。このTHF溶液を減圧下で溶媒を留去することで錯体化合物(V)を得た。
反応容器中で、トリメチルホスフィン(シグマアルドリッチジャパン合同会社製、1.0mol/L THF溶液)1mLと、ビス(1,5-シクロオクタジエン)ニッケル(0)68.75mgとを、0℃で1時間反応させた。このTHF溶液を減圧下で溶媒を留去することで錯体化合物(V)を得た。
[比較例2]
反応容器に4-Diphenylphosphinomethyl Polystyrene Resin cross-linked with 2% DVB(200-400mesh) (0.5-1.0mmol/g)(カタログ番号D2766、東京化成(株)製)200mgとビス(1,5-シクロオクタジエン)ニッケル(0)13.8mgをはかりとりTHF1mLを加え25℃で18時間攪拌した。上澄み液をデカントし、沈殿物をTHF0.5mLで3回洗浄することで錯体化合物(VI)を得た。
反応容器に4-Diphenylphosphinomethyl Polystyrene Resin cross-linked with 2% DVB(200-400mesh) (0.5-1.0mmol/g)(カタログ番号D2766、東京化成(株)製)200mgとビス(1,5-シクロオクタジエン)ニッケル(0)13.8mgをはかりとりTHF1mLを加え25℃で18時間攪拌した。上澄み液をデカントし、沈殿物をTHF0.5mLで3回洗浄することで錯体化合物(VI)を得た。
<アルケニルリン化合物の合成>
[合成例1]
反応容器中に出発物質としてリン化合物((MeO)2P(O)H)300mmolを量り取り、錯体化合物(I)を1.5mmol添加した。反応装置にアセチレンバルーンを取り付け、60℃で4時間反応させて、アルケニルリン化合物((MeO)2P(O)CH=CH2)を得た。GC-FIDを用いて内部標準法(標準物質ジフェニルエーテル)によりアルケニルリン化合物の生成量を測定した結果、Ni1mmol当たりのアルケニルリン化合物の生成量は、1.46gであった。
[合成例1]
反応容器中に出発物質としてリン化合物((MeO)2P(O)H)300mmolを量り取り、錯体化合物(I)を1.5mmol添加した。反応装置にアセチレンバルーンを取り付け、60℃で4時間反応させて、アルケニルリン化合物((MeO)2P(O)CH=CH2)を得た。GC-FIDを用いて内部標準法(標準物質ジフェニルエーテル)によりアルケニルリン化合物の生成量を測定した結果、Ni1mmol当たりのアルケニルリン化合物の生成量は、1.46gであった。
[合成例2]
触媒として上記で合成した錯体化合物(II)1.5mmolを用いた以外は、合成例1と同様にして、アルケニルリン化合物((MeO)2P(O)CH=CH2)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、2.11gであった。
触媒として上記で合成した錯体化合物(II)1.5mmolを用いた以外は、合成例1と同様にして、アルケニルリン化合物((MeO)2P(O)CH=CH2)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、2.11gであった。
[合成例3]
反応温度を80℃に変更した以外は、合成例2と同様にして、アルケニルリン化合物((MeO)2P(O)CH=CH2)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、4.57gであった。
反応温度を80℃に変更した以外は、合成例2と同様にして、アルケニルリン化合物((MeO)2P(O)CH=CH2)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、4.57gであった。
[合成例4]
触媒として上記で合成した錯体化合物(III)1.5mmolを用いた以外は、合成例1と同様にして、アルケニルリン化合物((MeO)2P(O)CH=CH2)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、3.48gであった。
触媒として上記で合成した錯体化合物(III)1.5mmolを用いた以外は、合成例1と同様にして、アルケニルリン化合物((MeO)2P(O)CH=CH2)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、3.48gであった。
[合成例5]
触媒として上記で合成した錯体化合物(IV)1.5mmolを用いた以外は、合成例1と同様にして、アルケニルリン化合物((MeO)2P(O)CH=CH2)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、2.81gであった。
触媒として上記で合成した錯体化合物(IV)1.5mmolを用いた以外は、合成例1と同様にして、アルケニルリン化合物((MeO)2P(O)CH=CH2)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、2.81gであった。
[合成例6(比較)]
触媒として上記で合成した錯体化合物(V)1.5mmolを用いた以外は、合成例1と同様にして、アルケニルリン化合物((MeO)2P(O)CH=CH2)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、0.08gであった。
触媒として上記で合成した錯体化合物(V)1.5mmolを用いた以外は、合成例1と同様にして、アルケニルリン化合物((MeO)2P(O)CH=CH2)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、0.08gであった。
[合成例7]
リン化合物((MeO)2P(O)H)1mmol、アルキニル化合物(1-オクチン)1mmol、THF1mLをガラス製シュレンクに量り取り、錯体化合物(I)0.05mmolを加えた。60℃で3時間加熱攪拌を行い、アルケニルリン化合物(30%:(MeO)2P(O)CH=CC6H13、70%:(MeO)2P(O)C(C6H13)=CH2の混合物)を得た。Ni1mmolあたりのアルケニルリン化合物生成量は4.40gであった。
リン化合物((MeO)2P(O)H)1mmol、アルキニル化合物(1-オクチン)1mmol、THF1mLをガラス製シュレンクに量り取り、錯体化合物(I)0.05mmolを加えた。60℃で3時間加熱攪拌を行い、アルケニルリン化合物(30%:(MeO)2P(O)CH=CC6H13、70%:(MeO)2P(O)C(C6H13)=CH2の混合物)を得た。Ni1mmolあたりのアルケニルリン化合物生成量は4.40gであった。
[合成例8]
出発物質のアルキニル化合物としてフェニルアセチレンを用いた以外は、合成例7と同様にして、アルケニルリン化合物(64%:(MeO)2P(O)CH=CH-Ph、36%:(MeO)2P(O)CH(Ph)=CH2の混合物)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、1.27gであった。
出発物質のアルキニル化合物としてフェニルアセチレンを用いた以外は、合成例7と同様にして、アルケニルリン化合物(64%:(MeO)2P(O)CH=CH-Ph、36%:(MeO)2P(O)CH(Ph)=CH2の混合物)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、1.27gであった。
[合成例9]
出発物質のアルキニル化合物として2-メチル-3-ブチン-2-オールを用いた以外は、合成例7と同様にして、アルケニルリン化合物(37%:(MeO)2P(O)CH=CH-C(CH3)2OH、63%:(MeO)2P(O)C(C(CH3)2OH)=CH2の混合物)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、1.67gであった。
出発物質のアルキニル化合物として2-メチル-3-ブチン-2-オールを用いた以外は、合成例7と同様にして、アルケニルリン化合物(37%:(MeO)2P(O)CH=CH-C(CH3)2OH、63%:(MeO)2P(O)C(C(CH3)2OH)=CH2の混合物)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、1.67gであった。
[合成例10]
出発物質のリン化合物として(CF3CH2O)2P(O)Hを用いた以外は、合成例7と同様にして、アルケニルリン化合物(11%:(CF3CH2O)2P(O)CH=CH-C6H13、89%:(CF3CH2O)2P(O)C(C6H13)=CH2の混合物)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、4.06gであった。
出発物質のリン化合物として(CF3CH2O)2P(O)Hを用いた以外は、合成例7と同様にして、アルケニルリン化合物(11%:(CF3CH2O)2P(O)CH=CH-C6H13、89%:(CF3CH2O)2P(O)C(C6H13)=CH2の混合物)を得た。Ni1mmol当たりのアルケニルリン化合物の生成量は、4.06gであった。
[合成例11(比較)]
錯体化合物(I)の代わりに、錯体化合物(VI)を用いた以外は合成例7と同様の条件で反応を行ったが、生成物を得ることが出来ず、1-オクチンのオリゴマーのみが得られた。
錯体化合物(I)の代わりに、錯体化合物(VI)を用いた以外は合成例7と同様の条件で反応を行ったが、生成物を得ることが出来ず、1-オクチンのオリゴマーのみが得られた。
Claims (10)
- 前記樹脂微粒子中のホスフィン基と前記遷移金属の物質量比が10:1~1:2である、請求項1に記載の錯体化合物。
- 一般式(1)中、R1は、炭素数が6~12の炭化水素基である、請求項1または2に記載の錯体化合物。
- 一般式(1)中、R2は、炭素数が1~8のアルキル基、または炭素数が5~12のアリール基である、請求項1~3のいずれか一項に記載の錯体化合物。
- 一般式(1)中、R3およびR4は、炭素数が1~8のアルキル基、または炭素数が5~12のアリール基である、請求項1~4のいずれか一項に記載の錯体化合物。
- 前記遷移金属が、ニッケル、パラジウム、またはロジウムである、請求項1~5のいずれか一項に記載の錯体化合物。
- ヒドロホスホリル化反応の触媒として用いられる、請求項1~6のいずれか一項に記載の錯体化合物。
- 前記遷移金属化合物がゼロ価ニッケル化合物である、請求項8に記載の製造方法。
- 前記ゼロ価ニッケル化合物が、ビス(1,5-シクロオクタジエン)ニッケル(0)、テトラキス(トリフェニルホスフィン)ニッケル(0)、およびニッケルカルボニルからなる群から選択される少なくとも1種である、請求項9に記載の製造方法。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP20894359.7A EP3971222A4 (en) | 2019-11-27 | 2020-11-26 | COMPLEX CONNECTION AND PRODUCTION PROCESS THEREOF |
| US17/595,443 US20220212177A1 (en) | 2019-11-27 | 2020-11-26 | Complex compound and method for manufacturing the same |
| CN202080006756.0A CN113195597B (zh) | 2019-11-27 | 2020-11-26 | 配位化合物及其制造方法 |
| JP2021518804A JPWO2021106981A1 (ja) | 2019-11-27 | 2020-11-26 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019-214682 | 2019-11-27 | ||
| JP2019214682 | 2019-11-27 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2021106981A1 true WO2021106981A1 (ja) | 2021-06-03 |
Family
ID=76129406
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2020/043947 WO2021106981A1 (ja) | 2019-11-27 | 2020-11-26 | 錯体化合物およびその製造方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20220212177A1 (ja) |
| EP (1) | EP3971222A4 (ja) |
| JP (1) | JPWO2021106981A1 (ja) |
| CN (1) | CN113195597B (ja) |
| WO (1) | WO2021106981A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2021084875A (ja) * | 2019-11-27 | 2021-06-03 | 丸善石油化学株式会社 | アルケニルリン化合物の製造方法 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN117551225B (zh) * | 2024-01-11 | 2024-04-09 | 上海稀固科技有限公司 | 含磷树脂及其制备方法与应用 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS4621642B1 (ja) * | 1969-09-30 | 1971-06-19 | ||
| JPS4828273B1 (ja) * | 1969-10-20 | 1973-08-30 | ||
| US5369133A (en) * | 1992-09-26 | 1994-11-29 | Korea Advanced Institute Of Science And Technology | Method for preparing an improved porous polymer bead |
| JP2004026655A (ja) * | 2002-05-17 | 2004-01-29 | Japan Science & Technology Corp | アルケニルリン化合物の製造方法 |
| JP2007519628A (ja) * | 2003-12-23 | 2007-07-19 | サノフイ−アベンテイス | 1−ピペラジン−および1−ホモピペラジン−カルボキシレートの誘導体、その調製方法、およびfaah酵素の阻害剤としてのその使用 |
| JP2010524661A (ja) * | 2007-04-16 | 2010-07-22 | ユニヴェルシテ ドゥ オートゥ アルザス | 不均一系パラジウム触媒の合成方法、得られる触媒およびこの使用 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3836459B2 (ja) * | 2003-09-03 | 2006-10-25 | 独立行政法人科学技術振興機構 | アルケニルホスホン酸エステルの製造方法 |
| CN101835535B (zh) * | 2007-07-11 | 2012-11-07 | 东曹株式会社 | 催化剂组合物及使用该催化剂组合物的交叉偶联化合物的制造方法 |
| CN108368142B (zh) * | 2015-12-02 | 2021-02-19 | 住友化学株式会社 | 芳香族化合物的制造方法和钯配合物 |
-
2020
- 2020-11-26 CN CN202080006756.0A patent/CN113195597B/zh active Active
- 2020-11-26 WO PCT/JP2020/043947 patent/WO2021106981A1/ja unknown
- 2020-11-26 JP JP2021518804A patent/JPWO2021106981A1/ja active Pending
- 2020-11-26 EP EP20894359.7A patent/EP3971222A4/en active Pending
- 2020-11-26 US US17/595,443 patent/US20220212177A1/en active Pending
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS4621642B1 (ja) * | 1969-09-30 | 1971-06-19 | ||
| JPS4828273B1 (ja) * | 1969-10-20 | 1973-08-30 | ||
| US5369133A (en) * | 1992-09-26 | 1994-11-29 | Korea Advanced Institute Of Science And Technology | Method for preparing an improved porous polymer bead |
| JP2004026655A (ja) * | 2002-05-17 | 2004-01-29 | Japan Science & Technology Corp | アルケニルリン化合物の製造方法 |
| JP2007519628A (ja) * | 2003-12-23 | 2007-07-19 | サノフイ−アベンテイス | 1−ピペラジン−および1−ホモピペラジン−カルボキシレートの誘導体、その調製方法、およびfaah酵素の阻害剤としてのその使用 |
| JP2010524661A (ja) * | 2007-04-16 | 2010-07-22 | ユニヴェルシテ ドゥ オートゥ アルザス | 不均一系パラジウム触媒の合成方法、得られる触媒およびこの使用 |
Non-Patent Citations (3)
| Title |
|---|
| CHEM. LETT., vol. 42, 2013, pages 1065 - 1067 |
| CHEN TIEQIAO, ZHOU YONGBO, GUO CANCHENG, HAN LI-BIAO: "Selective Addition of P(O)–H Bonds to Alkynes Catalyzed by Transition Metals Immobilized on Polystyrene-bound Triphenylphosphine", CHEMISTRY LETTERS, vol. 42, no. 9, 30 November 2012 (2012-11-30), JP , pages 1065 - 1067, XP009532355, ISSN: 0366-7022, DOI: 10.1246/cl.130374 * |
| See also references of EP3971222A4 |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2021084875A (ja) * | 2019-11-27 | 2021-06-03 | 丸善石油化学株式会社 | アルケニルリン化合物の製造方法 |
| JP7282017B2 (ja) | 2019-11-27 | 2023-05-26 | 丸善石油化学株式会社 | アルケニルリン化合物の製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN113195597B (zh) | 2023-01-03 |
| CN113195597A (zh) | 2021-07-30 |
| EP3971222A1 (en) | 2022-03-23 |
| JPWO2021106981A1 (ja) | 2021-06-03 |
| EP3971222A4 (en) | 2024-02-21 |
| US20220212177A1 (en) | 2022-07-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2021106981A1 (ja) | 錯体化合物およびその製造方法 | |
| Khristolyubov et al. | Ln (II) and Ca (II) NC sp3 N pincer type diarylmethanido complexes–promising catalysts for C–C and C–E (E= Si, P, N, S) bond formation | |
| Đorđević et al. | E–H (E= B, Si, C) Bond Activation by Tuning Structural and Electronic Properties of Phosphenium Cations | |
| Kalden et al. | Surprisingly Different Reaction Behavior of Alkali and Alkaline Earth Metal Bis (trimethylsilyl) amides toward Bulky N‐(2‐Pyridylethyl)‐N′‐(2, 6‐diisopropylphenyl) pivalamidine | |
| Jia et al. | Scandium and gadolinium complexes with aryldiimine NCN pincer ligands: synthesis, characterization, and catalysis on isoprene and 1, 5-hexadiene polymerization | |
| Wu et al. | Reactivity of germylene toward phosphorus-containing compounds: Nucleophilic addition and tautomerism | |
| JP7349335B2 (ja) | 錯体化合物の製造方法 | |
| Knapp et al. | Platinum phosphinito catalysts for nitrile hydration | |
| WO2021106982A1 (ja) | アルケニルリン化合物の製造方法 | |
| JP2021084875A (ja) | アルケニルリン化合物の製造方法 | |
| WO2003066643A1 (fr) | Procede de production de phosphine tertiaire a groupe hydrocarbone volumineux lie | |
| JP2794089B2 (ja) | アルケニルホスフィンオキシド化合物の製造法 | |
| Baldovino-Pantaleón et al. | Reactivity of C6F5S-P (C6H5) 2 with [M3 (CO) 12](M= Fe, Ru, Os). The X-ray crystal structures of [Fe2 (μ-SC6F5)(μ-PPh2)(CO) 6],[Ru4 (μ3-SPPh2) 2 (μ-SC6F5) 2 (μ-PPh2) 2 (SC6F5) 2 (CO) 6] and [Os3 (η1-Ph2P-SC6F5)(CO) 11] | |
| EP0794190B1 (en) | Method of producing alkenylphosphine oxide or bis (alkenylphosphine oxide) | |
| JP2004075688A (ja) | アルケニルホスホン酸エステルの製造方法 | |
| JP4863258B2 (ja) | リン化合物およびその製造方法 | |
| JP2849712B2 (ja) | アルケニルホスフィンオキシド化合物の製造方法 | |
| CN103467524B (zh) | 一种双亚磷酸三(3,3’,5,5’-四叔丁基-2,2’-联苯酚)酯的微波合成方法 | |
| JP4572390B2 (ja) | リン化合物およびその製造方法 | |
| CN103328489B (zh) | 新的(三有机甲硅烷基)炔以及它们的衍生物和获得新的和常规的取代的(三有机甲硅烷基)炔以及它们的衍生物的新的催化方法 | |
| JP3007984B1 (ja) | 不飽和ホスホン酸エステルの製造方法 | |
| JP3987937B2 (ja) | 含リン有機ポリマーとその製造法 | |
| JP3951024B2 (ja) | 有機硫黄化合物の製造方法 | |
| JP3041396B1 (ja) | 不飽和ホスホン酸エステルを製造する方法 | |
| Rieb et al. | Rare Earth Metal Complexes with N-Heterocyclic Carbenes |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ENP | Entry into the national phase |
Ref document number: 2021518804 Country of ref document: JP Kind code of ref document: A |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 20894359 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2020894359 Country of ref document: EP Effective date: 20211214 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |