WO2016200220A1 - 분리된 비멘틴 유래 펩타이드에 특이적으로 결합하는 항체 또는 상기 펩타이드의 결합 단편 - Google Patents
분리된 비멘틴 유래 펩타이드에 특이적으로 결합하는 항체 또는 상기 펩타이드의 결합 단편 Download PDFInfo
- Publication number
- WO2016200220A1 WO2016200220A1 PCT/KR2016/006215 KR2016006215W WO2016200220A1 WO 2016200220 A1 WO2016200220 A1 WO 2016200220A1 KR 2016006215 W KR2016006215 W KR 2016006215W WO 2016200220 A1 WO2016200220 A1 WO 2016200220A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- seq
- heavy chain
- light chain
- hzvsf
- antibody
- Prior art date
Links
- 230000027455 binding Effects 0.000 title claims abstract description 87
- 108090000765 processed proteins & peptides Proteins 0.000 title claims abstract description 87
- 239000012634 fragment Substances 0.000 title claims abstract description 73
- 108010065472 Vimentin Proteins 0.000 title claims description 8
- 210000005048 vimentin Anatomy 0.000 title claims description 8
- 102000013127 Vimentin Human genes 0.000 title claims 2
- 230000000840 anti-viral effect Effects 0.000 claims abstract description 94
- 239000000203 mixture Substances 0.000 claims abstract description 65
- 230000009385 viral infection Effects 0.000 claims abstract description 51
- 208000036142 Viral infection Diseases 0.000 claims abstract description 35
- 238000000034 method Methods 0.000 claims abstract description 29
- 238000011282 treatment Methods 0.000 claims abstract description 29
- 239000013598 vector Substances 0.000 claims abstract description 27
- 208000027866 inflammatory disease Diseases 0.000 claims abstract description 22
- 108091033319 polynucleotide Proteins 0.000 claims abstract description 17
- 239000002157 polynucleotide Substances 0.000 claims abstract description 17
- 102000040430 polynucleotide Human genes 0.000 claims abstract description 17
- 238000004519 manufacturing process Methods 0.000 claims abstract description 12
- 210000004027 cell Anatomy 0.000 claims description 137
- 241000700605 Viruses Species 0.000 claims description 97
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 claims description 48
- 241000282414 Homo sapiens Species 0.000 claims description 34
- 241000712461 unidentified influenza virus Species 0.000 claims description 25
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 24
- 208000015181 infectious disease Diseases 0.000 claims description 24
- 210000002865 immune cell Anatomy 0.000 claims description 19
- 230000008595 infiltration Effects 0.000 claims description 18
- 238000001764 infiltration Methods 0.000 claims description 18
- 230000003612 virological effect Effects 0.000 claims description 17
- 239000000539 dimer Substances 0.000 claims description 9
- 241000725303 Human immunodeficiency virus Species 0.000 claims description 8
- 208000035473 Communicable disease Diseases 0.000 claims description 7
- 208000006454 hepatitis Diseases 0.000 claims description 7
- 239000002773 nucleotide Substances 0.000 claims description 7
- 125000003729 nucleotide group Chemical group 0.000 claims description 7
- 241000701024 Human betaherpesvirus 5 Species 0.000 claims description 6
- 108010021625 Immunoglobulin Fragments Proteins 0.000 claims description 6
- 102000008394 Immunoglobulin Fragments Human genes 0.000 claims description 6
- 230000006870 function Effects 0.000 claims description 6
- 231100000283 hepatitis Toxicity 0.000 claims description 6
- 241000710185 Mengo virus Species 0.000 claims description 5
- 241000712907 Retroviridae Species 0.000 claims description 5
- 241000711573 Coronaviridae Species 0.000 claims description 4
- 241000127282 Middle East respiratory syndrome-related coronavirus Species 0.000 claims description 4
- 241000712464 Orthomyxoviridae Species 0.000 claims description 4
- 241000702263 Reovirus sp. Species 0.000 claims description 4
- 241000711950 Filoviridae Species 0.000 claims description 3
- 241000710781 Flaviviridae Species 0.000 claims description 3
- 241000700739 Hepadnaviridae Species 0.000 claims description 3
- 208000009525 Myocarditis Diseases 0.000 claims description 3
- 241000150350 Peribunyaviridae Species 0.000 claims description 3
- 241000709664 Picornaviridae Species 0.000 claims description 3
- 125000000539 amino acid group Chemical group 0.000 claims description 3
- 210000004556 brain Anatomy 0.000 claims description 3
- 210000000170 cell membrane Anatomy 0.000 claims description 3
- 230000028709 inflammatory response Effects 0.000 claims description 3
- 230000002265 prevention Effects 0.000 claims description 3
- 241001115402 Ebolavirus Species 0.000 claims description 2
- 208000025370 Middle East respiratory syndrome Diseases 0.000 claims description 2
- 241000315672 SARS coronavirus Species 0.000 claims description 2
- 230000000241 respiratory effect Effects 0.000 claims 1
- 208000011580 syndromic disease Diseases 0.000 claims 1
- 241001529453 unidentified herpesvirus Species 0.000 claims 1
- 241000711549 Hepacivirus C Species 0.000 description 63
- 230000000694 effects Effects 0.000 description 48
- 238000010586 diagram Methods 0.000 description 40
- 239000003814 drug Substances 0.000 description 38
- 241000699666 Mus <mouse, genus> Species 0.000 description 37
- 108020003175 receptors Proteins 0.000 description 34
- 102000005962 receptors Human genes 0.000 description 34
- 241000700721 Hepatitis B virus Species 0.000 description 33
- 241000699670 Mus sp. Species 0.000 description 28
- 230000014509 gene expression Effects 0.000 description 27
- 229940027941 immunoglobulin g Drugs 0.000 description 26
- 108090000623 proteins and genes Proteins 0.000 description 25
- 150000001413 amino acids Chemical group 0.000 description 24
- 229940079593 drug Drugs 0.000 description 24
- 230000002401 inhibitory effect Effects 0.000 description 24
- 238000011529 RT qPCR Methods 0.000 description 23
- 230000002829 reductive effect Effects 0.000 description 21
- 102000014150 Interferons Human genes 0.000 description 19
- 108010050904 Interferons Proteins 0.000 description 19
- 230000003110 anti-inflammatory effect Effects 0.000 description 18
- 229940079322 interferon Drugs 0.000 description 18
- 102000004127 Cytokines Human genes 0.000 description 17
- 108090000695 Cytokines Proteins 0.000 description 17
- 230000005847 immunogenicity Effects 0.000 description 17
- 108020004414 DNA Proteins 0.000 description 16
- 235000001014 amino acid Nutrition 0.000 description 16
- 229940024606 amino acid Drugs 0.000 description 16
- 238000001727 in vivo Methods 0.000 description 16
- 230000002757 inflammatory effect Effects 0.000 description 16
- 210000004072 lung Anatomy 0.000 description 16
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Natural products NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 15
- 239000000872 buffer Substances 0.000 description 15
- 102000004169 proteins and genes Human genes 0.000 description 15
- 235000018102 proteins Nutrition 0.000 description 14
- 206010012601 diabetes mellitus Diseases 0.000 description 13
- 201000010099 disease Diseases 0.000 description 13
- 210000004369 blood Anatomy 0.000 description 12
- 239000008280 blood Substances 0.000 description 12
- 229940124597 therapeutic agent Drugs 0.000 description 12
- 210000001744 T-lymphocyte Anatomy 0.000 description 11
- 230000010076 replication Effects 0.000 description 11
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 10
- 102100021943 C-C motif chemokine 2 Human genes 0.000 description 10
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 10
- 108060003951 Immunoglobulin Proteins 0.000 description 10
- 206010061218 Inflammation Diseases 0.000 description 10
- 238000002474 experimental method Methods 0.000 description 10
- 102000018358 immunoglobulin Human genes 0.000 description 10
- 238000000338 in vitro Methods 0.000 description 10
- 230000004054 inflammatory process Effects 0.000 description 10
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 10
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 9
- 238000004458 analytical method Methods 0.000 description 9
- 239000000427 antigen Substances 0.000 description 9
- 108091007433 antigens Proteins 0.000 description 9
- 102000036639 antigens Human genes 0.000 description 9
- 239000011324 bead Substances 0.000 description 9
- 239000013604 expression vector Substances 0.000 description 9
- 239000008103 glucose Substances 0.000 description 9
- 230000005764 inhibitory process Effects 0.000 description 9
- 108010045069 keyhole-limpet hemocyanin Proteins 0.000 description 9
- 238000002360 preparation method Methods 0.000 description 9
- 108091036055 CccDNA Proteins 0.000 description 8
- 239000004471 Glycine Substances 0.000 description 8
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 8
- 230000000704 physical effect Effects 0.000 description 8
- 239000000523 sample Substances 0.000 description 8
- 102220624209 3-hydroxy-3-methylglutaryl-coenzyme A reductase_I76A_mutation Human genes 0.000 description 7
- 102100031181 Glyceraldehyde-3-phosphate dehydrogenase Human genes 0.000 description 7
- 241000282412 Homo Species 0.000 description 7
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 7
- 239000004473 Threonine Substances 0.000 description 7
- 239000003443 antiviral agent Substances 0.000 description 7
- 108020004445 glyceraldehyde-3-phosphate dehydrogenase Proteins 0.000 description 7
- 239000008194 pharmaceutical composition Substances 0.000 description 7
- 230000035755 proliferation Effects 0.000 description 7
- 102220053976 rs727503323 Human genes 0.000 description 7
- 239000000126 substance Substances 0.000 description 7
- 239000006228 supernatant Substances 0.000 description 7
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 6
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 6
- 101710155857 C-C motif chemokine 2 Proteins 0.000 description 6
- 102000004889 Interleukin-6 Human genes 0.000 description 6
- 108090001005 Interleukin-6 Proteins 0.000 description 6
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 6
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 6
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 6
- 102100035071 Vimentin Human genes 0.000 description 6
- 238000006243 chemical reaction Methods 0.000 description 6
- 238000004128 high performance liquid chromatography Methods 0.000 description 6
- 210000005228 liver tissue Anatomy 0.000 description 6
- 239000012139 lysis buffer Substances 0.000 description 6
- 238000004445 quantitative analysis Methods 0.000 description 6
- 239000011347 resin Substances 0.000 description 6
- 229920005989 resin Polymers 0.000 description 6
- 108091008146 restriction endonucleases Proteins 0.000 description 6
- 238000010186 staining Methods 0.000 description 6
- 239000000725 suspension Substances 0.000 description 6
- 238000001262 western blot Methods 0.000 description 6
- 238000002965 ELISA Methods 0.000 description 5
- 241000588724 Escherichia coli Species 0.000 description 5
- 208000005176 Hepatitis C Diseases 0.000 description 5
- 102100037850 Interferon gamma Human genes 0.000 description 5
- 108010074328 Interferon-gamma Proteins 0.000 description 5
- 101800001014 Non-structural protein 5A Proteins 0.000 description 5
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 5
- 230000006052 T cell proliferation Effects 0.000 description 5
- 230000009471 action Effects 0.000 description 5
- 238000003556 assay Methods 0.000 description 5
- 230000004071 biological effect Effects 0.000 description 5
- 239000002775 capsule Substances 0.000 description 5
- 238000012790 confirmation Methods 0.000 description 5
- 230000003013 cytotoxicity Effects 0.000 description 5
- 231100000135 cytotoxicity Toxicity 0.000 description 5
- 230000003247 decreasing effect Effects 0.000 description 5
- 230000001419 dependent effect Effects 0.000 description 5
- 239000003937 drug carrier Substances 0.000 description 5
- 239000000839 emulsion Substances 0.000 description 5
- 208000002672 hepatitis B Diseases 0.000 description 5
- 210000004969 inflammatory cell Anatomy 0.000 description 5
- 210000002540 macrophage Anatomy 0.000 description 5
- 238000006386 neutralization reaction Methods 0.000 description 5
- 230000002441 reversible effect Effects 0.000 description 5
- 230000028327 secretion Effects 0.000 description 5
- 210000002966 serum Anatomy 0.000 description 5
- JTZZSQYMACOLNN-VDWJNHBNSA-N simeprevir Chemical compound O=C([C@@]12C[C@H]1\C=C/CCCCN(C)C(=O)[C@H]1[C@H](C(N2)=O)C[C@H](C1)OC=1C2=CC=C(C(=C2N=C(C=1)C=1SC=C(N=1)C(C)C)C)OC)NS(=O)(=O)C1CC1 JTZZSQYMACOLNN-VDWJNHBNSA-N 0.000 description 5
- 229960002091 simeprevir Drugs 0.000 description 5
- TTZHDVOVKQGIBA-IQWMDFIBSA-N sofosbuvir Chemical compound N1([C@@H]2O[C@@H]([C@H]([C@]2(F)C)O)CO[P@@](=O)(N[C@@H](C)C(=O)OC(C)C)OC=2C=CC=CC=2)C=CC(=O)NC1=O TTZHDVOVKQGIBA-IQWMDFIBSA-N 0.000 description 5
- 229960002063 sofosbuvir Drugs 0.000 description 5
- 239000000243 solution Substances 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- 108700039887 Essential Genes Proteins 0.000 description 4
- 206010069767 H1N1 influenza Diseases 0.000 description 4
- XQFRJNBWHJMXHO-RRKCRQDMSA-N IDUR Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(I)=C1 XQFRJNBWHJMXHO-RRKCRQDMSA-N 0.000 description 4
- 241000711466 Murine hepatitis virus Species 0.000 description 4
- 206010035664 Pneumonia Diseases 0.000 description 4
- 229920002873 Polyethylenimine Polymers 0.000 description 4
- 235000003704 aspartic acid Nutrition 0.000 description 4
- CKLJMWTZIZZHCS-REOHCLBHSA-N aspartic acid group Chemical group N[C@@H](CC(=O)O)C(=O)O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 4
- 210000004081 cilia Anatomy 0.000 description 4
- 239000002299 complementary DNA Substances 0.000 description 4
- 150000001875 compounds Chemical class 0.000 description 4
- 239000003085 diluting agent Substances 0.000 description 4
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 4
- 210000002919 epithelial cell Anatomy 0.000 description 4
- 239000012091 fetal bovine serum Substances 0.000 description 4
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 4
- 238000009472 formulation Methods 0.000 description 4
- 239000000499 gel Substances 0.000 description 4
- 230000002163 immunogen Effects 0.000 description 4
- 238000011534 incubation Methods 0.000 description 4
- 230000003834 intracellular effect Effects 0.000 description 4
- 230000009545 invasion Effects 0.000 description 4
- 239000003446 ligand Substances 0.000 description 4
- 239000002609 medium Substances 0.000 description 4
- 231100000957 no side effect Toxicity 0.000 description 4
- 230000001717 pathogenic effect Effects 0.000 description 4
- 239000000546 pharmaceutical excipient Substances 0.000 description 4
- 239000002953 phosphate buffered saline Substances 0.000 description 4
- 102000004196 processed proteins & peptides Human genes 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- 238000010839 reverse transcription Methods 0.000 description 4
- 238000003998 size exclusion chromatography high performance liquid chromatography Methods 0.000 description 4
- 239000000829 suppository Substances 0.000 description 4
- 201000010740 swine influenza Diseases 0.000 description 4
- 208000024891 symptom Diseases 0.000 description 4
- 239000003826 tablet Substances 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- 238000001890 transfection Methods 0.000 description 4
- 210000002700 urine Anatomy 0.000 description 4
- 241000699800 Cricetinae Species 0.000 description 3
- 241000710188 Encephalomyocarditis virus Species 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- 108700039791 Hepatitis C virus nucleocapsid Proteins 0.000 description 3
- 101000600434 Homo sapiens Putative uncharacterized protein encoded by MIR7-3HG Proteins 0.000 description 3
- 102000006992 Interferon-alpha Human genes 0.000 description 3
- 108010047761 Interferon-alpha Proteins 0.000 description 3
- 102000003996 Interferon-beta Human genes 0.000 description 3
- 108090000467 Interferon-beta Proteins 0.000 description 3
- 206010028980 Neoplasm Diseases 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 102100037401 Putative uncharacterized protein encoded by MIR7-3HG Human genes 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 3
- 235000004279 alanine Nutrition 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- 230000001580 bacterial effect Effects 0.000 description 3
- 201000011510 cancer Diseases 0.000 description 3
- 238000004113 cell culture Methods 0.000 description 3
- 238000005119 centrifugation Methods 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 239000013078 crystal Substances 0.000 description 3
- 238000010494 dissociation reaction Methods 0.000 description 3
- 230000005593 dissociations Effects 0.000 description 3
- 239000008187 granular material Substances 0.000 description 3
- 229940048921 humira Drugs 0.000 description 3
- 229940072221 immunoglobulins Drugs 0.000 description 3
- 239000012535 impurity Substances 0.000 description 3
- 229960001388 interferon-beta Drugs 0.000 description 3
- 210000003292 kidney cell Anatomy 0.000 description 3
- 239000006193 liquid solution Substances 0.000 description 3
- 230000007774 longterm Effects 0.000 description 3
- 230000014759 maintenance of location Effects 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 238000010172 mouse model Methods 0.000 description 3
- OHDXDNUPVVYWOV-UHFFFAOYSA-N n-methyl-1-(2-naphthalen-1-ylsulfanylphenyl)methanamine Chemical compound CNCC1=CC=CC=C1SC1=CC=CC2=CC=CC=C12 OHDXDNUPVVYWOV-UHFFFAOYSA-N 0.000 description 3
- 108091027963 non-coding RNA Proteins 0.000 description 3
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 3
- 239000006187 pill Substances 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 239000002002 slurry Substances 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- 230000035899 viability Effects 0.000 description 3
- VZSRBBMJRBPUNF-UHFFFAOYSA-N 2-(2,3-dihydro-1H-inden-2-ylamino)-N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]pyrimidine-5-carboxamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C(=O)NCCC(N1CC2=C(CC1)NN=N2)=O VZSRBBMJRBPUNF-UHFFFAOYSA-N 0.000 description 2
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 2
- UMCMPZBLKLEWAF-BCTGSCMUSA-N 3-[(3-cholamidopropyl)dimethylammonio]propane-1-sulfonate Chemical compound C([C@H]1C[C@H]2O)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(=O)NCCC[N+](C)(C)CCCS([O-])(=O)=O)C)[C@@]2(C)[C@@H](O)C1 UMCMPZBLKLEWAF-BCTGSCMUSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- 108020004638 Circular DNA Proteins 0.000 description 2
- 241000701022 Cytomegalovirus Species 0.000 description 2
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- 241000196324 Embryophyta Species 0.000 description 2
- 108010067770 Endopeptidase K Proteins 0.000 description 2
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 2
- 241000238631 Hexapoda Species 0.000 description 2
- 101000897480 Homo sapiens C-C motif chemokine 2 Proteins 0.000 description 2
- 102000006496 Immunoglobulin Heavy Chains Human genes 0.000 description 2
- 108010019476 Immunoglobulin Heavy Chains Proteins 0.000 description 2
- 108020004684 Internal Ribosome Entry Sites Proteins 0.000 description 2
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 108091028043 Nucleic acid sequence Proteins 0.000 description 2
- 102000000447 Peptide-N4-(N-acetyl-beta-glucosaminyl) Asparagine Amidase Human genes 0.000 description 2
- 108010055817 Peptide-N4-(N-acetyl-beta-glucosaminyl) Asparagine Amidase Proteins 0.000 description 2
- 206010035226 Plasma cell myeloma Diseases 0.000 description 2
- 108010029485 Protein Isoforms Proteins 0.000 description 2
- 102000001708 Protein Isoforms Human genes 0.000 description 2
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 2
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 2
- 239000012722 SDS sample buffer Substances 0.000 description 2
- 229920002684 Sepharose Polymers 0.000 description 2
- 231100000480 WST assay Toxicity 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 230000009824 affinity maturation Effects 0.000 description 2
- 230000010056 antibody-dependent cellular cytotoxicity Effects 0.000 description 2
- 239000003125 aqueous solvent Substances 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 229940098773 bovine serum albumin Drugs 0.000 description 2
- 235000014121 butter Nutrition 0.000 description 2
- 239000006143 cell culture medium Substances 0.000 description 2
- 230000004709 cell invasion Effects 0.000 description 2
- 239000003638 chemical reducing agent Substances 0.000 description 2
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 2
- 238000010367 cloning Methods 0.000 description 2
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 2
- 230000016396 cytokine production Effects 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 238000007865 diluting Methods 0.000 description 2
- 238000010828 elution Methods 0.000 description 2
- 210000003527 eukaryotic cell Anatomy 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 210000002950 fibroblast Anatomy 0.000 description 2
- 230000004927 fusion Effects 0.000 description 2
- 230000012010 growth Effects 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 210000005260 human cell Anatomy 0.000 description 2
- 238000009396 hybridization Methods 0.000 description 2
- 210000000987 immune system Anatomy 0.000 description 2
- 238000011532 immunohistochemical staining Methods 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000001155 isoelectric focusing Methods 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- JTEGQNOMFQHVDC-NKWVEPMBSA-N lamivudine Chemical compound O=C1N=C(N)C=CN1[C@H]1O[C@@H](CO)SC1 JTEGQNOMFQHVDC-NKWVEPMBSA-N 0.000 description 2
- 229960001627 lamivudine Drugs 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 201000007270 liver cancer Diseases 0.000 description 2
- 208000014018 liver neoplasm Diseases 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 239000003550 marker Substances 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- 239000000178 monomer Substances 0.000 description 2
- 201000000050 myeloid neoplasm Diseases 0.000 description 2
- 210000000496 pancreas Anatomy 0.000 description 2
- 229920001184 polypeptide Polymers 0.000 description 2
- 239000013641 positive control Substances 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 230000004083 survival effect Effects 0.000 description 2
- 239000006188 syrup Substances 0.000 description 2
- 235000020357 syrup Nutrition 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- 230000032258 transport Effects 0.000 description 2
- 210000003462 vein Anatomy 0.000 description 2
- 239000000080 wetting agent Substances 0.000 description 2
- 210000005253 yeast cell Anatomy 0.000 description 2
- HNSDLXPSAYFUHK-UHFFFAOYSA-N 1,4-bis(2-ethylhexyl) sulfosuccinate Chemical compound CCCCC(CC)COC(=O)CC(S(O)(=O)=O)C(=O)OCC(CC)CCCC HNSDLXPSAYFUHK-UHFFFAOYSA-N 0.000 description 1
- KZEVSDGEBAJOTK-UHFFFAOYSA-N 1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-2-[5-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]-1,3,4-oxadiazol-2-yl]ethanone Chemical compound N1N=NC=2CN(CCC=21)C(CC=1OC(=NN=1)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)=O KZEVSDGEBAJOTK-UHFFFAOYSA-N 0.000 description 1
- JQMFQLVAJGZSQS-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-N-(2-oxo-3H-1,3-benzoxazol-6-yl)acetamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)CC(=O)NC1=CC2=C(NC(O2)=O)C=C1 JQMFQLVAJGZSQS-UHFFFAOYSA-N 0.000 description 1
- ZRPAUEVGEGEPFQ-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]pyrazol-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C=NN(C=1)CC(=O)N1CC2=C(CC1)NN=N2 ZRPAUEVGEGEPFQ-UHFFFAOYSA-N 0.000 description 1
- JVKRKMWZYMKVTQ-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]pyrazol-1-yl]-N-(2-oxo-3H-1,3-benzoxazol-6-yl)acetamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C=NN(C=1)CC(=O)NC1=CC2=C(NC(O2)=O)C=C1 JVKRKMWZYMKVTQ-UHFFFAOYSA-N 0.000 description 1
- YJLUBHOZZTYQIP-UHFFFAOYSA-N 2-[5-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-1,3,4-oxadiazol-2-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C1=NN=C(O1)CC(=O)N1CC2=C(CC1)NN=N2 YJLUBHOZZTYQIP-UHFFFAOYSA-N 0.000 description 1
- APRZHQXAAWPYHS-UHFFFAOYSA-N 4-[5-[3-(carboxymethoxy)phenyl]-3-(4,5-dimethyl-1,3-thiazol-2-yl)tetrazol-3-ium-2-yl]benzenesulfonate Chemical compound S1C(C)=C(C)N=C1[N+]1=NC(C=2C=C(OCC(O)=O)C=CC=2)=NN1C1=CC=C(S([O-])(=O)=O)C=C1 APRZHQXAAWPYHS-UHFFFAOYSA-N 0.000 description 1
- CONKBQPVFMXDOV-QHCPKHFHSA-N 6-[(5S)-5-[[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]methyl]-2-oxo-1,3-oxazolidin-3-yl]-3H-1,3-benzoxazol-2-one Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)C[C@H]1CN(C(O1)=O)C1=CC2=C(NC(O2)=O)C=C1 CONKBQPVFMXDOV-QHCPKHFHSA-N 0.000 description 1
- WTFUTSCZYYCBAY-SXBRIOAWSA-N 6-[(E)-C-[[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]methyl]-N-hydroxycarbonimidoyl]-3H-1,3-benzoxazol-2-one Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)C/C(=N/O)/C1=CC2=C(NC(O2)=O)C=C1 WTFUTSCZYYCBAY-SXBRIOAWSA-N 0.000 description 1
- DFGKGUXTPFWHIX-UHFFFAOYSA-N 6-[2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]acetyl]-3H-1,3-benzoxazol-2-one Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)CC(=O)C1=CC2=C(NC(O2)=O)C=C1 DFGKGUXTPFWHIX-UHFFFAOYSA-N 0.000 description 1
- 208000030507 AIDS Diseases 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 101001073212 Arabidopsis thaliana Peroxidase 33 Proteins 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 241000271566 Aves Species 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 102000014914 Carrier Proteins Human genes 0.000 description 1
- 108010078791 Carrier Proteins Proteins 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 208000000419 Chronic Hepatitis B Diseases 0.000 description 1
- 208000006154 Chronic hepatitis C Diseases 0.000 description 1
- 108010047041 Complementarity Determining Regions Proteins 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- BWGNESOTFCXPMA-UHFFFAOYSA-N Dihydrogen disulfide Chemical compound SS BWGNESOTFCXPMA-UHFFFAOYSA-N 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 1
- 108010046914 Exodeoxyribonuclease V Proteins 0.000 description 1
- 239000004606 Fillers/Extenders Substances 0.000 description 1
- 241000287828 Gallus gallus Species 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 241000150562 Hantaan orthohantavirus Species 0.000 description 1
- 241001091624 Hepatitis C virus JFH-1 Species 0.000 description 1
- 229920000209 Hexadimethrine bromide Polymers 0.000 description 1
- 101000935587 Homo sapiens Flavin reductase (NADPH) Proteins 0.000 description 1
- 101001123325 Homo sapiens Peroxisome proliferator-activated receptor gamma coactivator 1-beta Proteins 0.000 description 1
- 101001100327 Homo sapiens RNA-binding protein 45 Proteins 0.000 description 1
- 102100026120 IgG receptor FcRn large subunit p51 Human genes 0.000 description 1
- 101710177940 IgG receptor FcRn large subunit p51 Proteins 0.000 description 1
- 102000009786 Immunoglobulin Constant Regions Human genes 0.000 description 1
- 108010009817 Immunoglobulin Constant Regions Proteins 0.000 description 1
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 1
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 1
- 238000012404 In vitro experiment Methods 0.000 description 1
- 241000581650 Ivesia Species 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 1
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 1
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000005913 Maltodextrin Substances 0.000 description 1
- 229920002774 Maltodextrin Polymers 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 108010063312 Metalloproteins Proteins 0.000 description 1
- 102000010750 Metalloproteins Human genes 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- AFCARXCZXQIEQB-UHFFFAOYSA-N N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(CCNC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 AFCARXCZXQIEQB-UHFFFAOYSA-N 0.000 description 1
- 238000011887 Necropsy Methods 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 108090000526 Papain Proteins 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 102000057297 Pepsin A Human genes 0.000 description 1
- 108090000284 Pepsin A Proteins 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 102100028961 Peroxisome proliferator-activated receptor gamma coactivator 1-beta Human genes 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 102100038823 RNA-binding protein 45 Human genes 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 241000293869 Salmonella enterica subsp. enterica serovar Typhimurium Species 0.000 description 1
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 241000256248 Spodoptera Species 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 241000187747 Streptomyces Species 0.000 description 1
- 108091027544 Subgenomic mRNA Proteins 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 244000299461 Theobroma cacao Species 0.000 description 1
- 235000005764 Theobroma cacao ssp. cacao Nutrition 0.000 description 1
- 235000005767 Theobroma cacao ssp. sphaerocarpum Nutrition 0.000 description 1
- 101150018417 VIM gene Proteins 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 231100000354 acute hepatitis Toxicity 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 210000001552 airway epithelial cell Anatomy 0.000 description 1
- 150000001294 alanine derivatives Chemical group 0.000 description 1
- 210000004102 animal cell Anatomy 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000002022 anti-cellular effect Effects 0.000 description 1
- 239000002260 anti-inflammatory agent Substances 0.000 description 1
- 229940121363 anti-inflammatory agent Drugs 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 210000001130 astrocyte Anatomy 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 239000000022 bacteriostatic agent Substances 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 239000007975 buffered saline Substances 0.000 description 1
- 210000004899 c-terminal region Anatomy 0.000 description 1
- 235000001046 cacaotero Nutrition 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 230000005754 cellular signaling Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 235000013330 chicken meat Nutrition 0.000 description 1
- 238000000975 co-precipitation Methods 0.000 description 1
- 238000011284 combination treatment Methods 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 230000004540 complement-dependent cytotoxicity Effects 0.000 description 1
- 238000004590 computer program Methods 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000003235 crystal violet staining Methods 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 230000009615 deamination Effects 0.000 description 1
- 238000006481 deamination reaction Methods 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000006471 dimerization reaction Methods 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- 229940088598 enzyme Drugs 0.000 description 1
- YQGOJNYOYNNSMM-UHFFFAOYSA-N eosin Chemical compound [Na+].OC(=O)C1=CC=CC=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C(O)=C(Br)C=C21 YQGOJNYOYNNSMM-UHFFFAOYSA-N 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- -1 ethyl oleate Chemical class 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000000799 fluorescence microscopy Methods 0.000 description 1
- 238000012757 fluorescence staining Methods 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 239000003205 fragrance Substances 0.000 description 1
- 235000013376 functional food Nutrition 0.000 description 1
- 230000002538 fungal effect Effects 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- 125000003630 glycyl group Chemical group [H]N([H])C([H])([H])C(*)=O 0.000 description 1
- 230000009422 growth inhibiting effect Effects 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 235000013402 health food Nutrition 0.000 description 1
- 201000005787 hematologic cancer Diseases 0.000 description 1
- 230000002440 hepatic effect Effects 0.000 description 1
- 208000010710 hepatitis C virus infection Diseases 0.000 description 1
- 210000003494 hepatocyte Anatomy 0.000 description 1
- 229940022353 herceptin Drugs 0.000 description 1
- 229940098197 human immunoglobulin g Drugs 0.000 description 1
- 210000004408 hybridoma Anatomy 0.000 description 1
- 229960002751 imiquimod Drugs 0.000 description 1
- DOUYETYNHWVLEO-UHFFFAOYSA-N imiquimod Chemical compound C1=CC=CC2=C3N(CC(C)C)C=NC3=C(N)N=C21 DOUYETYNHWVLEO-UHFFFAOYSA-N 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 238000002649 immunization Methods 0.000 description 1
- 238000003119 immunoblot Methods 0.000 description 1
- 238000003125 immunofluorescent labeling Methods 0.000 description 1
- 230000016784 immunoglobulin production Effects 0.000 description 1
- 230000002134 immunopathologic effect Effects 0.000 description 1
- 238000001114 immunoprecipitation Methods 0.000 description 1
- 229960001438 immunostimulant agent Drugs 0.000 description 1
- 239000003022 immunostimulating agent Substances 0.000 description 1
- 230000003308 immunostimulating effect Effects 0.000 description 1
- 230000007688 immunotoxicity Effects 0.000 description 1
- 231100000386 immunotoxicity Toxicity 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 206010022000 influenza Diseases 0.000 description 1
- 208000037797 influenza A Diseases 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000007972 injectable composition Substances 0.000 description 1
- 239000002799 interferon inducing agent Substances 0.000 description 1
- 229940047124 interferons Drugs 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 210000004153 islets of langerhan Anatomy 0.000 description 1
- 229960000310 isoleucine Drugs 0.000 description 1
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 1
- BPHPUYQFMNQIOC-NXRLNHOXSA-N isopropyl beta-D-thiogalactopyranoside Chemical compound CC(C)S[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O BPHPUYQFMNQIOC-NXRLNHOXSA-N 0.000 description 1
- VMPHSYLJUKZBJJ-UHFFFAOYSA-N lauric acid triglyceride Natural products CCCCCCCCCCCC(=O)OCC(OC(=O)CCCCCCCCCCC)COC(=O)CCCCCCCCCCC VMPHSYLJUKZBJJ-UHFFFAOYSA-N 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- 229940057995 liquid paraffin Drugs 0.000 description 1
- 229960003511 macrogol Drugs 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 229940035034 maltodextrin Drugs 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- 230000037323 metabolic rate Effects 0.000 description 1
- 238000000520 microinjection Methods 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 201000006417 multiple sclerosis Diseases 0.000 description 1
- 239000002547 new drug Substances 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 210000003463 organelle Anatomy 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229940055729 papain Drugs 0.000 description 1
- 235000019834 papain Nutrition 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 229940111202 pepsin Drugs 0.000 description 1
- 230000008823 permeabilization Effects 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 102000013415 peroxidase activity proteins Human genes 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 239000013612 plasmid Substances 0.000 description 1
- 238000007747 plating Methods 0.000 description 1
- 238000002264 polyacrylamide gel electrophoresis Methods 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 210000001236 prokaryotic cell Anatomy 0.000 description 1
- 230000009696 proliferative response Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 229940024999 proteolytic enzymes for treatment of wounds and ulcers Drugs 0.000 description 1
- 210000001938 protoplast Anatomy 0.000 description 1
- 238000010379 pull-down assay Methods 0.000 description 1
- 230000002685 pulmonary effect Effects 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 229940116176 remicade Drugs 0.000 description 1
- 230000003362 replicative effect Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000002207 retinal effect Effects 0.000 description 1
- 230000001177 retroviral effect Effects 0.000 description 1
- 229960004641 rituximab Drugs 0.000 description 1
- 239000012723 sample buffer Substances 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 230000009870 specific binding Effects 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000008223 sterile water Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 230000002195 synergetic effect Effects 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 125000003831 tetrazolyl group Chemical group 0.000 description 1
- 125000000341 threoninyl group Chemical group [H]OC([H])(C([H])([H])[H])C([H])(N([H])[H])C(*)=O 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 238000010361 transduction Methods 0.000 description 1
- 230000026683 transduction Effects 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 230000001131 transforming effect Effects 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 230000029812 viral genome replication Effects 0.000 description 1
- 230000005727 virus proliferation Effects 0.000 description 1
- 239000011534 wash buffer Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
Definitions
- the present invention relates to an antibody that specifically binds to the peptide of SEQ ID NO: 1, specifically, to an antibody or a binding fragment of the peptide, the antibody or the peptide to specifically bind to the isolated peptide of SEQ ID NO:
- a composition for antiviral comprising a binding fragment of said antibody or said peptide
- a composition for preventing or treating an inflammatory disease comprising a binding fragment of said antibody or said peptide, and a viral infectious disease using said composition
- Method of treatment, or method of treatment of inflammatory diseases One will.
- Viral diseases unlike bacterial diseases, are difficult to treat due to poor listening to antibiotics, and viral diseases have always emerged as one of the main causes of disease and death in humans.
- Viral infectious diseases also cause inflammation, leading to various inflammatory diseases.
- Formulations developed for the treatment of such viral infectious diseases can be divided into chemicals and biologically-derived materials. Most chemicals have been developed to work only on specific viral diseases. There are many shortcomings such as the appearance.
- cytokines such as interferon (IFN) are well known as biologically-derived materials.
- interferon was first discovered among cytokines produced in virus-infected cells, and is known to have the best antiviral cytokines. It has been reported that interferon can be used to treat various diseases such as chronic hepatitis B, hepatitis C or hematologic cancer, and multiple sclerosis. Recently, the efficacy of HIV (Human immunodeficiency virus) patients have been demonstrated. In order to develop antiviral agents and immunostimulants for many years, genetic engineering or biotechnological studies have been conducted to mass-produce interferons, and recently, compounds that induce interferon activity from natural or synthetic compounds have been searched.
- HIV Human immunodeficiency virus
- interferon Although interferon is known as a powerful antiviral agent, it induces an inflammatory response such as invasion of immune cells, and almost all cells express receptors for interferon at all times and show various side effects such as anti-cell action, and require large amounts in clinical use. There is a disadvantage that can not be used for more than six months.
- the inventors of the present invention sought to develop a therapeutic agent having antiviral activity and anti-inflammatory action that specifically acts only on virus-infected cells and can inhibit inflammation by inhibiting infiltration of immune cells, resulting in a novel humanized antibody, hzVSF.
- the present invention was completed by confirming that it is a safe preparation that acts specifically on various viruses, suppresses immune cell infiltration and inhibits viruses, and has no side effects when administered to humans with a humanized antibody having low immunogenicity.
- One object of the present invention is to provide a novel antibody or binding fragment of the peptide that specifically binds to the peptide of SEQ ID NO: 1.
- Another object of the present invention is to produce a polynucleotide encoding the binding fragment of the antibody or the peptide, a vector comprising the polynucleotide, a cell into which the vector is introduced, an antibody or a binding fragment of the peptide using the cell. It is to provide a binding fragment of the method, the antibody produced by the production method or the peptide.
- Still another object of the present invention is to provide an antiviral composition comprising a binding fragment of the antibody or peptide.
- Still another object of the present invention is to provide a method for preventing or treating a viral infection disease using the antiviral composition.
- Still another object of the present invention is to provide a composition for preventing or treating an inflammatory disease including the binding fragment of the antibody or the peptide.
- Antibodies or binding fragments of the peptides that specifically bind to the peptide of SEQ ID NO: 1 of the present invention selectively act on virus-infected cells and require a small amount for treatment, have no side effects, and inhibit infiltration of immune cells. It can be provided as a humanized antibody new drug exhibiting excellent antiviral and anti-inflammatory action, which inhibits inflammation.
- FIG. 1 is a schematic diagram of a vector for the preparation of chimeric VSF.
- FIG. 2 is a schematic diagram of chimeric VSF.
- 3 is a diagram confirming the expression of chimeric VSF.
- Figure 4 shows the DNA sequence of the scFv of VSF.
- FIG. 5 is a schematic diagram of cloning a scFv of VSF into a vector.
- FIG. 6 is a diagram confirming the purification of the scFV of VSF.
- FIG. 7 is a diagram confirming the antiviral efficacy of VSF, scFv and anti-EMCD virus antibodies as the viability of cells in viral infection.
- FIG. 9 is a schematic diagram of a vector for the preparation of hzVSF, a humanized antibody.
- FIG. 10 is a schematic diagram of hzVSF, a humanized antibody of the present invention.
- FIG. 11 is a diagram confirming the expression of hzVSF, a humanized antibody.
- FIG. 12 is a diagram confirming the antiviral efficacy of the humanized antibody hzVSF.
- Figure 13 is a view showing the reduced and non-reduced SDS-PAGE results confirming the physical properties of the humanized antibody hzVSF_var13.
- FIG. 14 shows LC / MS results confirming the physical properties of hzVSF_var13, a humanized antibody.
- 15 is a diagram showing the results of SEC-HPLC confirming the physical properties of the humanized antibody hzVSF_var13.
- FIG. 16 is a diagram showing IF (Isoelectric focusing) confirming physical properties of hzVSF_var13, a humanized antibody.
- FIG. 16 is a diagram showing IF (Isoelectric focusing) confirming physical properties of hzVSF_var13, a humanized antibody.
- FIG. 17 shows the number of donors in which T cells proliferated in response to KLH, hzVSF_var12, and hzVSF_var13 among 51 blood donors.
- FIG. 18 is a diagram showing the extent of 51 T cell proliferative responses to hzVSF_var12 and hzVSF_var13, which are representative variants of the humanized antibody hzVSF.
- FIG. 21 is a diagram showing HPLC results confirming physical properties of hzVSF_var12 and hzVSF_var13, which are variants of hzVSF, which are representative humanized antibodies.
- hzVSF_var13 shows the pharmacokinetics of hzVSF_var13, a variant of hzVSF, a representative humanized antibody.
- Figure 23 is a diagram confirming the virus inhibitory ability of hzVSF_var12 and hzVSF_var13 representative variants of humanized antibody hzVSF and humanized antibody hzVSF.
- 24 is a diagram confirming the anti-cellular action of humanized antibodies hzVSF_var13 and hIFN- ⁇ in human cells.
- 25 is a diagram confirming the inhibition of inflammatory cell infiltration of the humanized antibody hzVSF in viral diabetes.
- 26 is a diagram confirming the anti-HBV effect of mVSF.
- Figure 27 is a diagram confirming the expression pattern of VSF receptor in HBV-infected liver tissue.
- FIG 30 shows the expression of VSF receptors in EMC-D virus infected cells.
- Fig. 31 shows the antiviral effect of hzVSF_var13 on the hepatitis B virus in cccDNA by real-time quantitative PCR.
- FIG. 32 shows the antiviral effect of hzVSF_var13 on hepatitis B virus in the amount of extracellular HBV DNA by real-time quantitative PCR.
- Figure 34 is a diagram confirming the antiviral effect of hzVSF against hepatitis C virus by FACS.
- 35 shows the antiviral effect of hzVSF against hepatitis C virus by real-time quantitative PCR.
- Figure 37 is a diagram confirming the long-term antiviral effect on hepatitis C virus gene type 1a of hzVSF_v13 by real-time quantitative PCR.
- Figure 40 is a diagram confirming the long-term antiviral effect on hepatitis C virus gene type 2a of hzVSF_v13 by real-time quantitative PCR.
- Fig. 41 shows the virus growth inhibitory effect against influenza virus (H1N1) of the humanized antibody hzVSF_v13.
- hzVSF_var13 a representative variant of hzVSF
- FIG. 43 is a diagram showing the protective effect of mouse mucosal epithelial cells and cilia by hzVSF_var13, a representative variant of hzVSF, in mice infected with influenza virus.
- 44 is a diagram showing the effect of inhibiting pneumonia by time and concentration of hzVSF_var13, a representative variant of hzVSF, in mice infected with influenza virus.
- hzVSF_var13 a representative variant of hzVSF
- 46 is a diagram showing the effect of inhibiting CD4 immune cell infiltration after administration of hzVSF_var13, a representative variant of hzVSF, to mice infected with influenza virus (10,000,000 pfu).
- 47 is a diagram showing the effect of inhibiting macrophage invasion after administration of hzVSF_var13, a representative variant of hzVSF, to mice infected with influenza virus (100,000 pfu).
- hzVSF_var13 a representative variant of hzVSF, to mice infected with influenza virus (10,000,000 pfu).
- 49 shows the inhibitory effect of hzVSF on inflammatory cytokine secretion after virus infection in mice.
- 50 is a diagram confirming the antiviral activity of hzVSF_v13 by MVIT assay after overexpressing wild-type VR and mutant-type VR in MCF-7 cells not expressing VSF receptor.
- 51 is a diagram confirming the antiviral activity of hzVSF_v13 by WST assay after overexpressing wild-type VR and mutant-type VR in MCF-7 cells not expressing VSF receptor.
- FIG. 52 shows the antiviral activity of hzVSF_v13 by MVIT assay after overexpressing wild-type VR and mutant-type VR in MCF-7 cells not expressing VSF receptor.
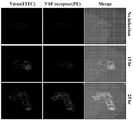
- FIG. 53 is a diagram showing the overexpression of wild-type VR and mutant-type VR in MCF-7 cells not expressing VSF receptor, followed by virus infection to confirm the association of VSF receptor and hzVSF_v13 by immunofluorescence staining.
- Figure 54 is a diagram confirming the binding of wild-type and mutant type VSF receptor (non-mentin) and hzVSF_v13 overexpressed in E. coli by a pull-down assay.
- FIG. 55 shows immunoprecipitation of the binding of VSF receptors (non-mentin) and hzVSF_v13 of wild-type and mutant typre overexpressed in HEK293T cells.
- 56 is a diagram simulating the binding site of vimentin and VSF.
- 57 is a diagram simulating the coupling of vimentin and VSF.
- 58 is a diagram simulating the binding site of vimentin and hzVSF_v13.
- the present invention provides an antibody or a binding fragment of the peptide, which specifically binds to the isolated peptide of SEQ ID NO: 1 as one embodiment.
- the antibody is not limited thereto, and may be, for example, a mouse antibody, chimeric antibody or humanized antibody.
- the humanized antibody or binding fragment of the peptide of the present invention implants the complementarity determining site of the variable region of a monoclonal or monoclonal antibody of a mouse that directly binds the antigen to the human antibody backbone, thereby providing the affinity and specificity of the original mouse antibody. It has superiority in inhibiting HAMA (human anti-mouse antibody) reaction in human body. Moreover, as a humanized antibody which lowered immunogenicity by using the de-immunization method, it can be used as a safe preparation by significantly lowering immunogenicity when administered to humans.
- mouse antibody that specifically binds to the isolated peptide of SEQ ID NO: 1 may be referred to as "mVSF (mouse Virus Suppressing Factor)", and the chimeric antibody may be referred to as “chVSF (chimeric Vrus Suppressing Factor)”.
- Humanized antibodies may be referred to collectively as "runningzed Virus Suppressing Factor”.
- humanized antibody hzVSF or a variant thereof may be mixed with each other, and hzVSF may be mixed with a hzVSF wild type (hzVSF_wt) and a variant of hzVSF (for example, hzVSF_var1, hzVSF_v1 or hzVSF_1, etc.).
- the isolated peptide of SEQ ID NO: 1 corresponds to the position of amino acids 142 to 294 of the vimentin, as long as the antibody or fragment thereof of the present invention can bind, the sequence as well as the sequence And at least 80%, preferably at least 90%, more preferably at least 95%, particularly preferably at least 97% homology.
- the isolated peptide of SEQ ID NO: 1 is an antigenic region comprising an epitope, 142 to 211 or 211 to 294 days of the non-mentin amino acid as long as it can be combined with an antibody or fragment thereof to exhibit a similar function as the present invention. Can be.
- Bimentin is a protein encoded by the VIM gene, which functions to support and fix organelles in cells, and is known to be mainly involved in the cellular skeleton, protein transport, and cell signaling. Although it is known to be used as a marker, it is not known that an antibody capable of binding to it may have an antiviral action.
- the antibody or binding fragment of the peptide which specifically binds to the isolated peptide of SEQ ID NO: 1 of the present invention, specifically reacts with a cell infected with a virus, and a receptor of a virus suppressing factor (VSF) in a virus-infected cell. Appear externally, to bind to it
- VSF virus suppressing factor
- Such a binding fragment of the antibody or the peptide of the present invention exhibits antiviral activity and anti-inflammatory activity by specific viral infection cell-specific binding as described above, preventing or treating antiviral compositions, viral infectious diseases, inflammatory diseases It can also be usefully used in the field.
- the binding fragment of the antibody or the peptide may specifically bind to the 9th, 45th, 54th, 76th, 94th or 129th amino acid residue of the peptide of SEQ ID NO: 1, more specifically although it may specifically bind to the 9th, 45th, 54th, 76th, 94th and 129th amino acid residues of the peptide of SEQ ID NO: 1, as long as it specifically binds to the isolated peptide of SEQ ID NO: This is not restrictive.
- antibody refers to a protein molecule that acts as a ligand that specifically recognizes an antigen, including an immunoglobulin molecule that is immunologically reactive with a specific antigen.
- Polyclonal antibodies monoclonal antibodies, It includes both whole antibodies and antibody fragments.
- the term also includes chimeric antibodies (eg, humanized murine antibodies) and bivalent or bispecific molecules (eg, bispecific antibodies), diabodies, triabodies, and tetrabodies.
- the term further encompasses single chain antibodies, caps, derivatives of antibody constant regions and artificial antibodies based on protein scaffolds that have a binding function to FcRn.
- the total antibody is a structure having two full length light chains and two full length heavy chains, each of which is linked by heavy and disulfide bonds.
- the total antibody includes IgA, IgD, IgE, IgM and IgG, and IgG is a subtype, including IgG1, IgG2, IgG3 and IgG4.
- fragment binding fragment of a peptide
- antibody fragment are used interchangeably to refer to any fragment of an antibody of the invention that retains the antigen-binding activity of the antibody.
- Exemplary antibody fragments include, but are not limited to, single chain antibodies, Fd, Fab, Fab ', F (ab') 2 , dsFv or scFv.
- Fd means the heavy chain portion included in the Fab fragment.
- the Fab has one antigen binding site in a structure having a variable region of the light and heavy chains, a constant region of the light chain and a first constant region of the heavy chain (CH1 domain).
- Fab 'd iffers from Fab in that it has a hinge region comprising at least one cysteine residue at the C terminus of the heavy chain CH1 domain.
- F (ab ') 2 antibodies are produced when the cysteine residues of the hinge region of Fab' form disulfide bonds.
- Fv (variable fragment) means a minimum antibody fragment having only the heavy chain variable region and light chain variable region.
- Double disulfide Fv is a heavy chain variable region and a light chain variable region are linked by disulfide bond
- single chain Fv (scFv) is generally covalently linked to the variable region of the heavy chain and the light chain through a peptide linker.
- Such antibody fragments can be obtained using proteolytic enzymes (e.g., the entire antibody can be restricted to papain and Fab can be obtained and pepsin can be used to obtain F (ab ') 2 fragment). Can be produced through genetic recombination techniques.
- the term “monoclonal antibody” refers to an antibody molecule of a single molecular composition obtained from substantially the same antibody population, which monoclonal antibody exhibits single binding specificity and affinity for a particular epitope.
- immunoglobulins have heavy and light chains and each heavy and light chain comprises a constant region and a variable region (the site is also known as a domain).
- the variable regions of the light and heavy chains comprise three variable regions and four structural regions (hereinafter referred to as "FR") called complementarity-determining regions ("CDRs").
- FR structural regions
- CDRs complementarity-determining regions
- the CDRs mainly serve to bind epitopes of antigens.
- the CDRs of each chain are typically called CDR1, CDR2, CDR3, starting sequentially from the N-terminus and also identified by the chain in which the particular CDR is located.
- the antibody of the present invention as described above comprises a constant region
- it may include a constant region derived from IgG, IgA, IgD, IgE, IgM, or a combination thereof or a hybrid thereof.
- dimers or multimers can be formed from two or more constant regions selected from the group consisting of constant regions of IgG, IgA, IgD, IgE and IgM.
- hybrid means that there is a sequence corresponding to two or more immunoglobulin heavy chain constant regions of different origin within a single chain immunoglobulin heavy chain constant region, for example IgG, IgA, IgD, IgE. And one to four domains selected from the group consisting of CH1, CH2, CH3 and CH4 of IgM.
- the humanized antibody of the present invention is not limited thereto, but may be humanized based on human immunoglobulin ⁇ 4, and may have an advantage of not causing CDC due to lack of complement binding.
- the binding fragment of the humanized antibody or peptide is a heavy chain CDR1 as set forth in SEQ ID NO: 2; A heavy chain CDR2 set forth in SEQ ID NO: 3 or SEQ ID NO: 14 (threonine, the ninth amino acid of SEQ ID NO: 3, replaced with aspartic acid); And a heavy chain variable region comprising a heavy chain CDR3 as set out in SEQ ID NO: 4 or SEQ ID NO: 15 (threonine as the fourth amino acid of SEQ ID NO: 4 replaced with arparagine), and a light chain CDR1 as set forth in SEQ ID NO: 5; SEQ ID NO: 6, SEQ ID NO: 16 (Threonine, the third amino acid of SEQ ID NO: 6, is replaced with aspartic acid); SEQ ID NO: 17 (Threonine, the third amino acid of SEQ ID NO: 6, is the aspartic acid; Alanine substituted with glycine or a light chain as set forth in SEQ ID NO: 18 (Threonine, the third amino acid
- the binding fragment of the humanized antibody or the peptide includes a human FR (framework region), but is not limited thereto, and may be human immunoglobulin gamma described by SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31, Or heavy chain FR1 (Framework region 1) set forth in SEQ ID NO: 20; Heavy chain FR2 set forth in SEQ ID NO: 21; A heavy chain FR3 as set forth in SEQ ID NO: 22 or SEQ ID NO: 28 (lysine, the eighth amino acid of SEQ ID NO: 22, is substituted for threonine, and isoleucine, the tenth amino acid, for alanine); And a heavy chain variable region comprising the heavy chain FR4 set forth in SEQ ID NO: 23, and a light chain FR1 set forth in SEQ ID NO: 24; Light chain FR2 set forth in SEQ ID NO: 25; Light chain FR3 as set forth in SEQ ID NO: 26; And a light chain variable region comprising
- the binding fragment of the humanized antibody or peptide is specifically (a) heavy chain CDR1, heavy chain CDR2, and heavy chain CDR3, and SEQ ID NO: 5, SEQ ID NO: 6, as set forth in SEQ ID NO: 2, SEQ ID NO: 3, and SEQ ID NO: 4, respectively; And light chain CDR1, light chain CDR2, light chain CDR3, each set forth in SEQ ID NO: 7; (b) heavy chain CDR1, heavy chain CDR2, and heavy chain CDR3, and the light chain CDR1, light chain CDR2, respectively set forth in SEQ ID NO: 2, SEQ ID NO: 3, and SEQ ID NO: 4, and SEQ ID NO: 5, SEQ ID NO: 16, and SEQ ID NO: 7, Light chain CDR3; (c) the heavy chain CDR1, heavy chain CDR2, and heavy chain CDR3, and the light chain CDR1, light chain CDR2, respectively set forth in SEQ ID NO: 2, SEQ ID NO: 3, and SEQ ID NO: 4, respectively; Light chain CDR3; (d) heavy chain CDR1, heavy chain CDR2,
- the antibody may include hzVSF_var10, (l) The antibody hzVSF_var11, (m) The antibody hzVSF_var12, (n) The antibody may include hzVSF_var13.
- the binding fragment of the humanized antibody and the peptide is not limited thereto, and SEQ ID NO: 10 and SEQ ID NO: 12, respectively; SEQ ID NO: 32 and SEQ ID NO: 34; SEQ ID NO: 36 and SEQ ID NO: 38; SEQ ID NO: 40 and SEQ ID NO: 42; SEQ ID NO: 44 and SEQ ID NO: 46; SEQ ID NO: 48 and SEQ ID NO: 50; SEQ ID NO: 52 and SEQ ID NO: 54; SEQ ID NO: 56 and SEQ ID NO: 58; SEQ ID NO: 60 and SEQ ID NO: 62; SEQ ID NO: 64 and SEQ ID NO: 66; SEQ ID NO: 68 and SEQ ID NO: 70; SEQ ID NO: 72 and SEQ ID NO: 74; SEQ ID NO: 76 and SEQ ID NO: 78; Or a binding fragment of the antibody or peptide comprising the heavy and light chain variable regions set forth in SEQ ID NO: 80 and SEQ ID NO: 82.
- the mouse antibody specifically, heavy chain CDR1 as set forth in SEQ ID NO: 137; A heavy chain CDR2 set forth in SEQ ID NO: 138; And a heavy chain variable region comprising the heavy chain CDR3 set forth in SEQ ID NO: 139, and a light chain CDR1 set forth in SEQ ID NO: 134;
- the chimeric antibody may specifically include a heavy chain variable region as set out in SEQ ID NO: 141 or SEQ ID NO: 142 and a light chain variable region as set out in SEQ ID NO: 140, and more specifically, the heavy chain and sequence as set forth in SEQ ID NO: 146 or SEQ ID NO: 148. It may include, but is not limited to, the light chain described in number 144.
- the scFv is not limited thereto, but scFv prepared for safety of mVSF may also be included.
- it may be an scFv prepared by the sequence described in FIG. 4.
- the heavy chain variable region set forth in SEQ ID NO: 131 and the light chain variable region set forth in SEQ ID NO: 133 may be linked to each other by a linker.
- the heavy chain variable region encoded by the nucleotide sequence of SEQ ID NO: 130 and the light chain variable region encoded by the nucleotide sequence of SEQ ID NO: 132 may be in the form of linkage.
- Such scFv can be cloned into the nucleotide sequence of SEQ ID NO: 150 in an E. coli expression vector.
- the inventors confirmed the antiviral efficacy after preparing hzVSF_wt, three alternatives and 13 variants thereof, humanized antibodies (Example 6).
- the immunogenicity similar to that of Humira which is the lowest immunogenic human antibody (Table 7) was caused when used as an antiviral or anti-inflammatory agent. It has been confirmed that it can be used as a safe antiviral or drug without any possible side effects.
- hzVSF_wt variant did not significantly affect the proliferation of T cells through T cell analysis (Table 8), and it was confirmed that it is unlikely to cause side effects by acting as an immunogen when used in clinical practice.
- the pharmacokinetic analysis confirmed that the half-life in vivo was high enough for clinical use (Example 8).
- the hzVSF (wild type and variant) of the present invention significantly inhibits the antiviral efficacy of EMC-D virus infection and the inhibition of immune cell invasion and thereby the destruction of Langerhans island in mice, and is excellent for treating diabetes due to viral infection. It was confirmed that it can (Example 12). Hepatitis virus was also confirmed that it can significantly inhibit (Examples 13 to 16). Influenza virus infection was also confirmed without the immune cell infiltration, antiviral effect and anti-inflammatory effect (Example 17), and confirmed that the antiviral effect against various viruses (Table 15), can be used as a general antiviral agent It was confirmed that there is. In addition, it was confirmed that the mouse model inhibits the secretion of inflammatory cytokines during virus infection (Example 19), and it can be used as a therapeutic agent for various inflammatory diseases.
- the present invention provides a polynucleotide encoding a binding fragment of the antibody or the peptide, a vector comprising the polynucleotide, a cell into which the vector is introduced, an antibody using the cell or a binding fragment of the peptide. It provides a production method and a binding fragment of the antibody or the peptide produced by the production method.
- Binding fragments of the antibody and the peptide are as described above.
- the vector comprising the polynucleotide encoding the antibody provided in the present invention is not particularly limited thereto, but may include mammalian cells (eg, human, monkey, rabbit, rat, hamster, mouse cells, etc.), plant cells, yeast cells. May be a vector capable of replicating and / or expressing the polynucleotide in eukaryotic or prokaryotic cells, including insect cells or bacterial cells (eg, E. coli, etc.), and preferably the nucleotide is expressed in a host cell. It may be a vector operably linked to an appropriate promoter, and comprising at least one selection marker.
- the polynucleotide may be introduced into a phage, plasmid, cosmid, mini-chromosome, virus or retroviral vector.
- the vector including the polynucleotide encoding the antibody may be an expression vector including polynucleotides encoding the heavy or light chains of the antibody, or an expression vector including both the polynucleotides encoding the heavy or light chains.
- Cells (transformers) into which the expression vector provided in the present invention is introduced are not particularly limited, but include bacterial cells such as E. coli, Streptomyces, Salmonella typhimurium, into which the expression vector is introduced and transformed; Yeast cells; Fungal cells such as Pchia pastoris; Insect cells such as Drozophila and Spodoptera Sf9 cells; Chinese hamster ovary cells (CHO), SP2 / 0 (mouse myeloma), human lymphoblastoid, COS, NSO (mouse myeloma), 293T, Bow melanoma cells, HT-1080, BHK ( Animal cells such as baby hamster kidney cells, baby hamster kidney cells, HEK (human embryonic kidney cells), and PERC.6 (human retinal cells); Or plant cells.
- bacterial cells such as E. coli, Streptomyces, Salmonella typhimurium, into which the expression vector is introduced and transformed
- Yeast cells Fun
- introduction refers to a method of delivering a vector comprising a polynucleotide encoding the antibody to a host cell.
- introductions include calcium phosphate-DNA coprecipitation, DEAE-dextran-mediated transfection, polybrene-mediated transfection, electroshock, microinjection, liposome fusion, lipofectamine and protoplast fusion. It can be carried out by various methods known in the art.
- transduction refers to the delivery of a target product into cells using viral particles by means of infection.
- the vector can be introduced into the host cell by gene bombardment or the like. Introduction in the present invention can be used interchangeably with transformation.
- the present invention provides a composition for antiviral, comprising a binding fragment of the antibody or the peptide.
- Binding fragments of the antibody and the peptide are as described above.
- antiviral means an effect of reducing, inhibiting or preventing a viral infection by inhibiting the proliferation or replication of a pathogenic virus.
- the "pathogenic virus” in which the proliferation or replication of the virus is inhibited by the antiviral activity is not limited thereto, but a part of the non-mentin of the host cell is exposed to the outside of the host cell membrane by the viral infection. Examples are viruses that cause disease in animals or humans.
- pathogenic viruses examples include Orthomyxoviridae virus, Picorna viridae virus, Retroviridae virus, and herpes (Herpes) Virus, Filoviridae Virus, Coronaviridae Virus, Hepadnaviridae Virus, Flaviviridae Virus, Bunyaviridae Genus viruses and the like.
- Pathogenic viruses include, for example, influenza viruses, hepatitis B and C viruses, brain myocarditis virus, mengovirus, Ebolavirus, Severe Acute Respiratory Syndrome Coronavirus (SARS), Middle East Respiratory Syndrome Coronavirus (Middle East Respiratory Syndrome Coronavirus (MERS), Leo virus (Reovirus), human immunodeficiency virus (HIV), human cytomegalovirus (HCMV), or hantan virus and the like, but is not limited thereto.
- the hzVSF according to the present invention is not only Mengo virus belonging to Picoraviridae, but also to Orthomyxoviridae, whose genome structure and lifespan are completely different from the EMC virus belonging to Picoraviridae. Influenza virus belonged to the antiviral effect, and also effectively inhibits the proliferation of HIV belonging to retroviridae (Retroviridae), such as the effect on the universal virus (Table 15).
- the composition may be in the form of a pharmaceutical composition, quasi-drug composition, a composition for health food.
- the pharmaceutical composition may further comprise a pharmaceutically acceptable carrier.
- the term "pharmaceutically acceptable carrier” refers to a carrier or diluent that does not irritate an organism and does not inhibit the biological activity and properties of the administered compound.
- Acceptable pharmaceutical carriers in compositions formulated as liquid solutions are sterile and physiologically compatible, including saline, sterile water, Ringer's solution, buffered saline, albumin injectable solutions, dextrose solution, maltodextrin solution, glycerol, ethanol and One or more of these components may be mixed and used, and other conventional additives such as antioxidants, buffers and bacteriostatic agents may be added as necessary.
- diluents may be additionally added to formulate injectable formulations, pills, capsules, granules or tablets such as aqueous solutions, suspensions, emulsions and the like.
- the pharmaceutical composition may be in various oral or parenteral formulations.
- diluents or excipients such as fillers, extenders, binders, wetting agents, disintegrating agents, and surfactants are usually used.
- Solid form preparations for oral administration include tablets, pills, powders, granules, capsules, and the like, which form at least one excipient such as starch, calcium carbonate, sucrose or lactose (at least one compound). lactose) and gelatin.
- lubricants such as magnesium stearate, talc and the like are also used.
- Liquid preparations for oral administration include suspensions, liquid solutions, emulsions, and syrups, and various excipients such as wetting agents, sweeteners, fragrances, and preservatives, in addition to commonly used simple diluents such as water and liquid paraffin, may be included.
- Formulations for parenteral administration include sterile aqueous solutions, non-aqueous solvents, suspensions, emulsions, lyophilized preparations, suppositories.
- non-aqueous solvent and the suspension solvent propylene glycol, polyethylene glycol, vegetable oil such as olive oil, injectable ester such as ethyl oleate, and the like can be used.
- As the base of the suppository witepsol, macrogol, tween 61, cacao butter, laurin butter, glycerogelatin and the like can be used.
- the pharmaceutical composition is any one selected from the group consisting of tablets, pills, powders, granules, capsules, suspensions, liquid solutions, emulsions, syrups, sterile aqueous solutions, non-aqueous solutions, suspensions, emulsions, lyophilized preparations and suppositories. It can have one formulation.
- composition of the present invention is administered in a pharmaceutically effective amount.
- the term “pharmaceutically effective amount” means an amount sufficient to treat a disease at a reasonable benefit / risk ratio applicable to medical treatment, and an effective dose level is determined by the type and severity, age, sex, disease of the individual. It may be determined according to the type, activity of the drug, sensitivity to the drug, time of administration, route of administration and rate of release, duration of treatment, factors including concurrently used drugs, and other factors well known in the medical field.
- the compositions of the present invention may be administered as individual therapeutic agents or in combination with other therapeutic agents and may be administered sequentially or simultaneously with conventional therapeutic agents. And single or multiple administrations. Taking all of the above factors into consideration, it is important to administer an amount that can obtain the maximum effect in a minimum amount without side effects, and can be easily determined by those skilled in the art.
- the other therapeutic agent may be interferon, but is not limited thereto.
- the composition may be a composition for performing the prevention or treatment of viral infectious diseases by antiviral action.
- the viral infectious disease is not limited thereto, and may include a disease in which a part of the non-mentin of the host cell is exposed to the outside of the host cell membrane by the viral infection, for example, hepatitis, AIDS, pneumonia, diabetes, , Orthomyxoviridae genus virus, Picorna viridae genus virus, Retroviridae genus virus, Filoviridae genus virus, Coronaviridae genus virus, Hepadnaviridae virus, Flaviviridae virus, Bunyaviridae virus Herpes (Herpes) can include all diseases that can be caused by infection.
- hepatitis AIDS, pneumonia, diabetes, , Orthomyxoviridae genus virus, Picorna viridae genus virus, Retroviridae genus virus, Filoviridae genus virus, Coronaviridae genus virus, Hepadnaviridae virus, Flaviviridae virus, Bunyaviridae
- prevention may refer to any action that inhibits or delays the onset of a disease by administration of the composition, and the “treatment” is improved or advantageously changed by the administration of the composition. It can mean any action that takes place.
- the composition may be a composition that functions specifically for virus infected cells.
- the composition may be to suppress immune cell infiltration, and may be to inhibit an inflammatory response (FIGS. 45 to 48).
- the composition of the present invention was confirmed to significantly inhibit the inflammation-induced cytokines IL-6, TNF- ⁇ , IFN- ⁇ , CCL2 (MCP-1) (Fig. 49).
- the present invention may be a method for treating a viral infection disease, comprising administering the antiviral composition to a subject in need thereof.
- the antiviral composition and viral infection disease are as described above.
- the method of treating a viral infection disease comprises administering a pharmaceutical composition comprising an antibody and a pharmaceutically acceptable carrier to a subject having or suspected of having a viral infection disease.
- the method for treating a viral infection disease may preferably be a method for treating a viral infection disease comprising administering a composition comprising an antibody to a subject having a viral infection disease.
- the subject includes mammals, birds, and the like, including cattle, pigs, sheep, chickens, dogs, humans, and the like, and includes, without limitation, individuals whose viral infection diseases are treated by administration of the composition of the present invention.
- the composition may be administered in a single or multiple doses in a pharmaceutically effective amount.
- the composition may be administered in the form of a liquid, powder, aerosol, capsule, enteric skin tablets or capsules or suppositories.
- Routes of administration include, but are not limited to, intraperitoneal, intravenous, intramuscular, subcutaneous, endothelial, oral, topical, nasal, pulmonary, rectal, and the like.
- the oral composition upon oral administration, since the peptide is digested, the oral composition must be formulated to coat the active agent or to protect it from degradation in the stomach.
- the pharmaceutical composition may be administered by any device in which the active agent may migrate to the target cell.
- the present invention provides a composition for preventing or treating an inflammatory disease comprising the binding fragment of the antibody or the peptide.
- composition for preventing or treating the inflammatory disease may be in the form of a pharmaceutical composition, quasi-drug composition, health functional food composition.
- the inflammatory disease may be due to viral infection.
- the present invention provides a method for treating an inflammatory disease, comprising administering the composition for preventing or treating the inflammatory disease to a subject in need thereof.
- the present invention provides an antiviral use of the binding fragment of the antibody or the peptide.
- Example 1-1 chVSF (chimeric VSF Manufacturing
- mouse VSF mouse VSF
- human immunoglobulins and chimerized human immunoglobulins were made to generate mouse / human hybridization antibodies (chAbs).
- chVSF produced an expression vector using the pCAGGS vector as a template (FIG. 1).
- the variable heavy chain (mVH) of mVSF (SEQ ID NO: 9) was amplified by PCR including the SacI and KpnI restriction enzyme sites.
- the variable light chain (mVL) (SEQ ID NO: 8) was amplified by PCR including the ClaI and XhoI restriction enzyme sites. Primers used in PCR were used in the primers described in Table 1, PCR conditions were performed for 35 cycles of 45 seconds at 94 °C, 45 seconds at 60 °C, 45 seconds at 72 °C, and proceeded for 10 minutes at 72 °C.
- the human heavy chain (SEQ ID NO: 11) used Kpn I and Sph I restriction enzyme sites, and the light chain (SEQ ID NO: 13) was cloned using Xho I and Bgl I restriction enzymes.
- an internal ribosome entry site (IRES) was cloned between the light and heavy chains using Sph I and Cla I restriction enzyme sites. Screening markers were inserted at Sal I restriction enzyme sites. In this manner, chVSFs as described in the schematic diagram of FIG. 2 were prepared.
- Example 1-2 using two vector expression systems chVSF Expression
- pCAGGS-GFP 15 ⁇ g of pCAGGS-GFP was transfected into HEK 293T cells using 1 mg / ml PEI (Polyethyleneimine) to confirm the degree of transfection and expression level.
- PEI Polyethyleneimine
- the medium was replaced with a medium containing 2% FBS after 6 hours.
- Cell cultures were collected every three days and impurities were removed using a 0.45 ⁇ m filter. ChVSF was purified using protein A sepharose beads.
- chVSF was eluted with 0.2 M glycine / hydrochloric acid buffer (Glycine / HCl) (pH 2.5) and 1 M Tris-Cl (Tris-Cl) buffer (pH 9.0) was used as neutralization buffer.
- the resin was homogenized using 1M Tris-Cl buffer (pH 8.0) at 10 times the resin volume, and then VSF culture was passed through the column.
- 0.1 M Tris-Cl buffer (pH 8.0) was washed with at least 5 times the column volume.
- chVSF was confirmed that the structure consisting of a heavy chain of 50 kDa and 25 kDa having the characteristics of immunoglobulin.
- ScFv was prepared using the variable region of VSF.
- scFv has a DNA sequence of SEQ ID NO: 150, and the scFv was prepared by cloning the DNA into pET-22b (+), an E. coli expression vector (FIGS. 4 and 5).
- scFv was prepared by connecting VH and VL of mVSF with a linker, inserted into a bacterial expression vector pET22b (+), and then induced by expression of IPTG, followed by purification using a Ni-NTA column ( 6).
- the antiviral activity was confirmed using the purified scFv. Specifically, L929 cells infected with EMC-D virus were incubated with scFv, VSF or anti-EMCD virus antibody at 37 ° C. for 30 hours. The supernatant was then removed and CellTiter96 AQueous One Solution was added, followed by OD 450 . As a result, it was confirmed that there was an antiviral effect in all groups treated with VSF (5 to 500 ng), scFv (5 to 10 ⁇ g) and anti-EMCD virus antigen (1:20 dilution) (FIG. 7).
- MVIT analysis was performed to confirm the antiviral activity of chVSF prepared in Example 1.
- chVSF of the present invention showed antiviral efficacy against EMC-D virus.
- PdCMV-dhfr-vector (FIG. 9) corresponding to two gene expression vectors, which is one of expression systems used to express two kinds of recombinant proteins using eukaryotic cells, was used.
- the vector expresses two kinds of genes into different transcription units in one vector and expresses them using its own promoter and polyA signal, and is a vector system using CMV (cytomegalovirus) promoter, a powerful mammalian expression promoter. .
- CMV cytomegalovirus
- amino acid sequence of the heavy chain variable region of hzVSF is shown in SEQ ID NO: 10, the heavy chain region of SEQ ID NO: 11, the amino acid sequence of the light chain variable region of SEQ ID NO: 12, and the light chain region of SEQ ID NO: 13.
- pCAGGS-GFP 15 ⁇ g of pCAGGS-GFP was transfected into HEK 293T cells using 1 mg / ml PEI (Polyethyleneimine) to confirm the degree of transfection and expression level.
- PEI Polyethyleneimine
- the medium was replaced with a medium containing 2% FBS.
- Cell cultures were collected every three days and impurities were removed using a 0.45 ⁇ m filter. ChVSF and hzVSF were purified using protein A sepharose beads.
- chVSF and hzVSF were eluted with 0.2 M glycine / hydrochloric acid buffer (Glycine / HCl) (pH 2.5) and 1 M Tris-Cl (Tris-Cl) buffer (pH 9.0) was used as neutralization buffer.
- the resin was homogenized using 1 M Tris-Cl buffer (pH 8.0) at 10 times the resin volume, and then VSF culture was passed through the column.
- 0.1 M Tris-Cl buffer (pH 8.0) was washed with at least 5 times the column volume.
- VSF used in the experiment is shown in Table 2 below.
- rmVSF recombinant of mouse VSF
- chVSF ⁇ 2 and chVSF ⁇ 4, hzVSF ⁇ 2 and hzVSF ⁇ 4 is composed of a 50 kDa heavy chain and 25 kDa light chain having the characteristics of immunoglobulin.
- Example 5-1 Basic molecular weight pattern and purity confirmation
- hzVSF_v13 was stained by Coomassie Staining according to the molecular weight by SDS-PAGE to confirm the molecular weight and purity of hzVSF_v13.
- lane 1 was a non-reducing gel, and a major band was observed at the expected position in the IgG antibody (150 kDa), and lane 2 was the reduced gel and the heavy chain (about 50 kDa) of the IgG antibody.
- a band was observed at the corresponding position in the light chain (about 25 kDa), and it was confirmed that hzVSF_v13 showed a general IgG antibody pattern.
- Example 5-2 Check molecular weight, sugar pattern and size variation
- Liquid Chromatography / Mass Spectrometry was performed to confirm molecular weight, sugar pattern, and size variation of hzVSF_v13. A small amount of hzVSF_v13 was injected into the HPLC to observe the peaks.
- hzVSF_v13 exhibits the characteristics of immunoglobulin G (IgG) (FIG. 14).
- IgG immunoglobulin G
- the total molecular weight about 140 kDa was observed, and the pattern of the corresponding peak was observed in the general glycosylated IgG such as G0 / G0, G0F / G1, G1 / G1.
- heavy chains about 49 kDa
- light chains about 23 kDa
- the glycan patterns of general IgG were confirmed (G0F, G1F, and G2F).
- HPLC system Dionex Ultimate 3000
- Example 5-4 pI And charge heterogeneity confirmation
- the pI of hzVS_v13F was analyzed to be 7.7, and acid and basic isoforms (acidic / basic isoforms) were also observed in addition to the main band. This corresponds to isomers commonly observed in IgG antibodies (eg, deamination of C-terminal regions).
- Example 6 virus suppression efficacy is maintained or Increasing Immunogenic Reduced Humanized antibodies hzVSF Variant Produce
- Example 6-1 hzVSF manufacture of alternative
- Example 4 Based on the hzVSF prepared in Example 4, three alternatives were prepared. The activity of each alternative was comparable to or less than that of the wild-type (0.5 ⁇ 1 U ⁇ 1 mg / ml) (Tables 3 and 4). The amino acid sequences of each of the alternative CDRs 1 to 3 are shown in Table 3, and the amino acid sequences of the FR1 to FR4 of each variant are listed in Table 4.
- Antibodies CDR1 CDR2 CDR3 hzVSF_WT Heavy chain GYNMN (SEQ ID NO: 2) NIDPYYGSTTY A QKF Q G (SEQ ID NO: 3) ETGTRAMDY (SEQ ID NO: 4) Light chain RASENIYSNLA (SEQ ID NO: 5) VATNLAD (SEQ ID NO: 6) QHFYGSPRT (SEQ ID NO: 7) hzVSF_a1 Heavy chain GYNMN (SEQ ID NO: 2) NIDPYYGSTTY A QKF Q G (SEQ ID NO: 3) ETGTRAMDY (SEQ ID NO: 4) Light chain RASENIYSNLA (SEQ ID NO: 5) VATNLAD (SEQ ID NO: 6) QHFYGSPRT (SEQ ID NO: 7) hzVSF_a2 Heavy chain GYNMN (SEQ ID NO: 2) NIDPYYGSTTY A QKF Q G (SEQ ID NO: 3) ETGTRAMDY (SEQ
- the hzVSF variant was prepared through affinity maturation and immunogenicity reduction for practical use in vivo. As a result, 13 variants were prepared (Table 5 and Table 6). The amino acid sequences of CDRs 1 to 3 of each variant are listed in Table 5 and the amino acid sequences of FR1 to FR4 of each variant are shown in Table 6.
- Antibodies CDR1 CDR2 CDR3 hzVSF_WT Heavy chain GYNMN (SEQ ID NO: 2) NIDPYYGSTTY A QKF Q G (SEQ ID NO: 3) ETGTRAMDY (SEQ ID NO: 4) Light chain RASENIYSNLA (SEQ ID NO: 5) VATNLAD (SEQ ID NO: 6) QHFYGSPRT (SEQ ID NO: 7) hzVSF_var1 Heavy chain GYNMN (SEQ ID NO: 2) NIDPYYGSTTYAQKFQG (SEQ ID NO: 3) ETGTRAMDY (SEQ ID NO: 4) Light chain RASENIYSNLA (SEQ ID NO: 5) VA D NLAD (SEQ ID NO: 16) QHFYGSPRT (SEQ ID NO: 7) hzVSF_var2 Heavy chain GYNMN (SEQ ID NO: 2) NIDPYYGSTTYAQKFQG (SEQ ID NO: 3) ETGTRAMDY (SEQ
- hzVSF_var12 which has the lowest immunogenicity, showed antiviral activity at 500 ng in 1 unit, similar to the hzVSF wild type, and in the case of hzVSF_var13 having high antiviral activity and relatively low immunogenicity, 250 ng / unit Virus activity was shown.
- Example 6-3 hzVSF Wild type and its Variant epitope count check
- each variant showed a wild-type-like activity (0.5 mg / U) from var1 to var12, var13 showed higher activity than the wild-type.
- Example 6-4 hzVSF Variant T cell analysis confirmed
- PBMCs Peripheral Blood Mononuclear Cells
- KLH Keyhole limpet hemocyanin
- the stimulation index (SI) of T cell proliferation induced by KLH, hzVSF_v12 or hzVSF_v13 was calculated using PBMC cultured for 7 days as a control. If the SI value is greater than 2, the immunogenicity is expected to be large when applied to humans. If the SI value is less than 0.5, it is expected to inhibit the proliferation of T cells. As a result, hzVSF_v12 and hzVSF_v13 are SI values of low values of 1.12 and 1.03, and it was confirmed that most individuals exhibit SI values of 0.6 or more and 2 or less. On the other hand KLH used as a positive control showed a high SI value of 3.91 (Fig. 18, 19, and Table 8).
- hzVSF_v12 and hzVSF_v13 are expected to have less immunogenicity when administered to patients with viral diseases, and side effects are expected to be low.
- Example 8 hzVSF Of variants Physical and pharmacokinetic confirmation
- Example 8-1 hzVSF Variant Check molecular weight pattern and purity
- SDS-PAGE was used to confirm the molecular weight patterns and purity of hzVSF_var12 and hzVSF_var13.
- the reduced sample was prepared by mixing NuPage 4X LDS sample buffer (Invitrogen, NP0007) and NuPage 10X sample reducing agent (Invitrogen, NP0009) with hzVSF_var12 and hzVSF_var13 and heating at 70 ° C for 10 minutes.
- Non-reducing samples were prepared by omitting the reducing agent and heating.
- hzVSF_var12 and hzVSF_var13 were electrophoresed at 4-12% SDS-PAGE, the gel was stained with InstantBlue (TripleRed, ISB01L) to confirm the purity of hzVSF_var12 and hzVSF_var13. .
- hzVSF_var12 and hzVSF_var13 were used on a Zorbax GF-250 ⁇ m 9.2 mm ID X 25 cm column (Agilent) to perform high-performance liquid chromatography (HPLC) of the Agilent 1200 series. It was analyzed by Size Exclusion (SE-HPLC). Samples at a concentration of 1 mg / ml were filtered through a 0.2 ⁇ m filter to remove impurities before injection into HPLC. HPLC was run at 1 mL / min for 15 min by injecting 100 ⁇ L of sample each. Analysis was performed using Chemstation software.
- the main peak was confirmed at the position corresponding to the monomer of the typical IgG antibody (retention time about 8.65 minutes), and the purity of hzVSF_var12 and hzVSF_var13 was confirmed to be 95% or more (FIG. 21).
- the peaks of about 3.72% and 4.43% were observed at the dimer position (establishment time of about 7.89-7.93 minutes), indicating that they showed the same shape as the IgG antibody as in the SDS-PAGE results.
- Example 8-2 hzVSF Variant Pharmacokinetics pharmacokineics ) analysis
- the ELISA was immobilized on a plate with human gamma specific immunoglobulin (anti-human IgG ( ⁇ specific)) for 2 hours at 37 ° C or overnight at 4 ° C and then coated with 3% BSA (Bovine Serum Albumin). Incubation was performed at 37 ° C. for 2 hours to block out the unpopulated portion. Serum collected from the mice was reacted at 37 ° C. for 1 hour and then reacted with human kappa specific immunoglobulin (anti-human IgG ( ⁇ specific)) attached to HRP (Hoseradish peroxidase) for 30 minutes at 37 ° C.
- HRP Hoseradish peroxidase
- PK parameters are shown in Table 9 and the graphs of FIG. 22 when a single dose is administered for each concentration of hzVSF_var13 administered to the mice.
- L929 cells which are mouse cells, were infected with EMC-D virus and treated with hzVSF_var12 and hzVSF_var13, which are representative variants of the hzVSF wild type and hzVSF variants, to confirm virus inhibition by the MVIT method of Example 2.
- the hzVSF wild type showed a 100% antiviral effect at a concentration of 0.5 ⁇ g / ml
- hzVSF_var12 is a 100% antiviral effect at a concentration of 0.2 ⁇ g / ml
- hzVSF_var13 0.1 ⁇ g / ml It confirmed that it represents.
- the minimum amount contained in ml of VSF showing 100% antiviral effect when the L929 cells were infected with EMC-D virus and treated with VSF at the same time was defined as 1 unit of biological activity.
- VSF Type Biological activity (1 unit) MW (kDa) mVSF 0.09 ⁇ g 163 hzVSF_wt 0.5 ⁇ g 147 hzVSF_var12 0.2 ⁇ g 147 hzVSF_var13 0.1 ⁇ g 147
- hzVSF variants prepared by human monoclonal antibody, immunogenicity reduction, and affinity maturation also have lower titers than mVSF, but have antiviral and anti-inflammatory effects with little side effects with better effects than hzVSF_wt. It suggests that there is.
- Affinity of the receptor for hzVSF was measured by the following method.
- VSF Type Affinity constant Ka
- Dissociation constant Kd
- hzVSF wt 8.2 x 10 9 L / mol 1.2 x 10 -10 M
- Example 11 In human cells hIFN - ⁇ and hzVSF _wt Anti-cell Check action
- EMC-D After infecting human fibroblasts with WI-38 cells, EMC-D was treated with different concentrations of human interferon and hzVSF_wt, and their antiviral activity and cell viability were measured by MTS method.
- the cells were placed in a 96-well plate and incubated at the bottom for 24 hours. After infection with 100 pfu of EMC-D virus, treatment with interferon or hzVSF. After 48 hours of incubation, MTS [3- (4,5-dimethylthiazol-2-yl) -5- (3-carboxymethoxyphenyl) -2- (4-sulfophenyl) -2H-tetrazolium] was treated. After incubation for another 2 to 3 hours, the absorbance at 490 nm was measured to confirm the viability of the cells.
- the cells treated with human interferon showed a 90% survival rate in a small amount compared to the hzVSF_wt treated cells, but it was confirmed that the cytotoxicity when treated with a high concentration of 4 nM or more.
- hzVSF_wt showed a 100% survival rate at about 4 nM and did not show cytotoxicity even at concentrations above 4 nM.
- Example 12 In Viral Diabetes hzVSF Inhibition of Inflammatory Cell Infiltration by _wt and Anti-inflammatory Confirm
- mice 100 pfu of EMC-D virus was intraperitoneally injected into 5 weeks old male DBA / 2N mice. Thereafter, 2, 4, and 16 units of hzVSF_wt were injected into the tail vein, and then the levels of blood glucose and urine glucose were examined from day 3. In addition, the mice were sacrificed at 3 and 7 days after infection, and the pancreas was extracted and histologically examined.
- diabetes mellitus did not develop in the group administered more than 4 units of hzVSF_wt, and the blood glucose level was less than 200 mg / dL, which corresponds to the range of normal mice.
- the blood glucose level was less than 200 mg / dL, which corresponds to the range of normal mice.
- no urine glucose was detected in the group administered more than 8 units (Table 12 to Table 14).
- the incidence of diabetes mellitus by hzVSF_wt drug concentration in viral diabetes is shown in Table 12, the blood glucose levels by hzVSF_wt drug concentration in Table 13, and the unrine glucose levels by hzVSF_wt drug concentration in Table 14.
- Group post-infection Diabetes prevalence 3 day 4 day 5 day 6 day 7 day virus control - 4/4 4/4 4/4 4/4 100% 2 unit / mouse - - - - 4/4 4/4 100% 4 unit / mouse - - - - 0 % 8 unit / mouse - - - - - 0 % 16 unit / mouse - - - - - 0 %
- diabetes is considered
- HepG2.2.15 cells which are human liver cancer cells expressing HBV, were used.
- HBsAg surface antigen
- liver tissues of patients with hepatitis B hepatitis B progression but no cancer
- liver tissues of patients with hepatitis C The part which progressed to liver cancer by hepatitis C but no cancer
- mVSF antibody hepatic tissue (part without cancer) not infected with the virus was used.
- VSF receptors were expressed in liver tissues obtained from patients infected with HBV and HCV, but not in control tissues, which means that VSF receptors are expressed specifically for viral infection. The same results were observed even when repeated experiments were performed on liver tissues derived from other patients (FIGS. 27 and 28).
- H1N1 influenza virus was infected with MDCK cell line, and then virus replication and VSF receptor expression were observed using fluorescence staining. As a result, the replication of the virus occurs over time after the influenza virus infection, it was confirmed that the expression of the VSF receptor increases accordingly (Fig. 29). These results indicate that the VSF receptor is induced by viral infection.
- FIG. 30 shows the expression of VSF receptor and antiviral efficacy of VSF.
- the left side of Figure 30 confirms the expression of VSF receptors following EMC-D infection
- the right side shows the anti-EMC-D effect and expression of VSF receptors according to hzVSF_wt treatment.
- virus-infected cells express VSF receptors with time difference, but the treatment of VSF did not affect the expression of the receptors, but showed antiviral effects.
- hzVSF_var13 a representative variant.
- Example 15-1 cccDNA (covalently closed circular DNA) analysis
- HepG2.2.15 cell line infected with HBV was treated with hzVSF_var13 and HBV drug (lamivudine; Lami) according to each dose, and the number of cells was counted every week to obtain the same amount of cells.
- HepG2.2.15 cells were recovered and then in lysis buffer (25 mM EDTA, 10 mM Tris-HCl; pH 7.5, 100 mM NaCl, 1% SDS, 0.1 mg / ml proteinase K). The cells were resuspended and reacted at 55 ° C. for 1 hour. After purifying total HBV DNA with MEGA quick-spin total fragment DNA purification kit (intron), the reaction was performed at 37 ° C. for 1 hour with plasmid-safe ATP-dependent DNase, and the enzyme was inactivated at 70 ° C. for 30 minutes.
- lysis buffer 25 mM EDTA, 10 mM Tris-HCl; pH 7.5, 100 mM NaCl, 1% SDS, 0.1 mg / ml proteinase K.
- the cells were resuspended and reacted at 55 ° C. for 1 hour.
- MEGA quick-spin total fragment DNA purification kit intron
- HBV rcDNA (relaxed circular DNA) was removed and only HBV cccDNA was obtained. Then, quantitative analysis of HBV cccDNA was performed by qPCR using Accupower 2x greenstar qPCR Master mix (Bioneer).
- hzVSF significantly reduced the amount of cccDNA in the cell, it can be seen that there is an excellent effect as an HBV therapeutic agent.
- hzVSF_var13 and HBV drug (lamivudine; Lami) were treated with HBV-infected HepG2.2.15 cell line according to each dose, and the cells were counted every week to obtain the same amount of cells.
- Intracellular HBV DNA was obtained as follows. The HepG2.2.15 cells obtained above were resuspended in lysis buffer (25 mM EDTA, 10 mM Tris-HCl; pH 7.5, 100 mM NaCl, 1% SDS, 0.1 mg / ml proteinase K). After reacting at 55 ° C for 1 hour. Then, intracellular HBV DNA was obtained using MEGA quick-spin total fragment DNA purification kit (intron). In the case of extracellular HBV DNA, a certain amount of cultured cultured cells were obtained and extracted by treating the culture with lysis buffer. Subsequently, quantitative analysis of HBV DNA was carried out using qPCR using Accupower 2x greenstar qPCR Master mix (bioneer).
- PCR primers were used as forward 5'-CCTCTTCATCCTGCTGCT-3 '(SEQ ID NO: 155) and reverse 5'-AACTGAAAGCCAAACAGTG-3' (SEQ ID NO: 156).
- the extracellular HBV DNA significantly reduced the amount of HBV DNA even when treated with very low concentration (0.1 ⁇ g / ml) of hzVSF_var13 compared to the control group Lami (Fig. 32).
- Intracellular HBV DNA was confirmed to inhibit the HBV DNA in a concentration-dependent manner of hzVSF_var13, it was confirmed to show a significantly superior effect compared to the control group Lami (Fig. 33).
- hzVSF significantly reduced the amount of intracellular and extracellular HBV DNA, it was found that it has an excellent effect as a therapeutic agent of HBV.
- Example 16-1 Hepatitis C Virus hzVSF Antiviral effect of _wt
- Hepatitis C virus JFH-1 strain was infected with human hepatocyte Huh7.5 cells with 0.1 MOI (multiplicity of infection), followed by 3 ng / ml of interferon ⁇ and 500, 1000, 2000 units. After treatment with hzVSF_wt, cell culture medium and cells were collected on day 4. Cells were measured for HCV NS5A using FACS using anti-HCV NS5A antibody staining, and cell culture medium was measured for HCV RNA titer using real-time quantitative PCR.
- hzVSF in vivo , interferon has side effects, whereas hzVSF not only has no side effects but also treats the symptoms caused by inflammation. Therefore, in the early stages of viral infection, the inhibition of virus growth in cells should be combined with chemicals and interferon, and after the mid-term or symptoms of viral infection, hzVSF and chemicals should be used in combination to suppress not only immunopathy but also virus growth. have.
- the above results suggest the possibility of the combination treatment of hzVSF_wt and various variants thereof of the present invention excellent in inhibiting the virus proliferation inhibitory chemicals (or interferon) and excellent immunopathologic effects.
- hzVSF_wt and its various variants alone suggests the application to the antiviral agent without side effects.
- Example 16-2 Hepatitis C virus ( HCV For 1a) hzVSF Variant Confirm antiviral effect
- hzVSF_var13 was treated in each dose of Huh7 cells infected with HCV TNcc (TN cell-culture derived; genotype 1a) and the cells were treated on days 3, 6, 9 and 12. Obtained. Then, the HCV infected cells were recovered and trizol was used to extract total RNA. After cDNA was obtained through reverse transcription, quantitative analysis of HCPD RNA and housekeeping gene (GAPDH) for calibration was performed by qPCR using Accupower 2x greenstar qPCR Master mix (bioneer).
- HCV TNcc TN cell-culture derived; genotype 1a
- HCV target PCR primers forward 5'-GGGCTATAAGGTGCTAGTGC-3 '(SEQ ID NO: 157) and reverse 5'-GGCTGCCAGTGGTAATTGTT-3' (SEQ ID NO: 158) were used.
- GAPDH PCR primers forward 5'-TCCCTGAGCTGAACGGGAAG-3 ' (SEQ ID NO: 159), reverse 5'-GGAGGAGTGGGTGTCGCTGT-3 '(SEQ ID NO: 160) was used.
- Huh7 cells infected with HCV TNcc (genotype 1a) were treated with hzVSF_var13 and HCV drugs (sofosbuvir, simeprevir) according to each dose, and recovered HCV infected cells every week, and total RNA was extracted using trizol. Thereafter, cDNA was obtained by reverse transcription. Subsequently, quantitative analysis of the HCV total RNA (using primers of SEQ ID NOs: 157 and 158) and GAPDH (housekeeping gene) for calibration was performed by qPCR using Accupower 2x greenstar qPCR Master mix (bioneer).
- HCV TNcc gene 1a
- Example 16-3 Hepatitis C virus ( HCV For 1b) hzVSF Variant Confirm antiviral effect
- hzVSF_var13 and HCV drugs were treated to Huh7 cells expressing subgenomic replicon of HCV genotype 1b according to each dose, and HCV infected cells every week. After recovery, total RNA was extracted using trizol. Thereafter, cDNA was obtained by reverse transcription. Quantitative analysis of total HCV RNA and housekeeping gene (GAPDH) for calibration using qPCR was performed using Accupower 2x greenstar qPCR Master mix (bioneer).
- HCV target PCR primers forward 5'-ATGCAGCCCAAGGGTATAAG-3 '(SEQ ID NO: 161) and reverse 5'-GGTTCTGATGTTAGGGTCGATAC-3' (SEQ ID NO: 162) were used.
- GAPDH PCR primers primers SEQ ID NOs: 159 and 160 were used. Used.
- hzVSF_var13 to HCV replicon (genotype 1b) expressing cells reduced the amount of HCV gene (RNA) and HCV NS5A protein, thus having an antiviral effect on HCV.
- Example 16-4 Hepatitis C virus ( HCV For 2a) hzVSF Variant Confirm antiviral effect
- hzVSF_var13 and HCV drugs were treated in each dose of JFH-1 cells infected with HCV genotype 2a according to each dose, and HCV infected cells were recovered every week. Trizol was then used to extract total RNA. Thereafter, cDNA was obtained by reverse transcription. Subsequently, quantitative analysis of total HCV RNA and housekeeping gene (GAPDH) for calibration was performed using qPCR using Accupower 2x greenstar qPCR Master mix (bioneer). The primers of SEQ ID NOs: 157 and 158 were used for HCV target PCR primers, and the primers of SEQ ID NOs: 159 and 160 were used for GAPDH PCR primers.
- HCV gene RNA
- HCV core protein A in FIG. 39
- Example 17 for influenza virus infection hzVSF Confirm treatment effect
- hzVSF_var13 a representative variant of hzVSF of the present invention, against influenza virus, the following experiment was performed in mice.
- mice Four-week-old female Balb / c mice were nasally infected with 1 ⁇ 10 5 pfu of H1N1 Influenza A / Puerto Rico / 8/34 virus, followed by 25, 100 or 400 units of hzVSF_var13 at 2, 4 or 6 days of infection. Intravenously. At 7 and 9 days after virus infection, mice were sacrificed for H & E staining, lung and body weight, mucosal epithelial cells and cilia, and immunohistochemical staining to infiltrate immune cells.
- influenza titers were reduced by 100 times or more in the group administered with 500 U hzVSF_var13 compared to the control group (FIG. 41).
- the group infected with H1N1 influenza virus developed immune cells and infiltrates in the alveoli
- the group treated with 100 U and 400 U were treated with influenza virus like normal lungs as the lung tissue of the non-infected control group regardless of the timing of administration. Symptoms were cured. Even when 25 U was administered, there was a difference depending on the timing of administration, but it was confirmed that there is a therapeutic effect because it suppresses infiltration of immune cells (FIG. 42).
- the virus-infected group increased the proportion of lungs by weight due to pneumonia-filled pneumonia, whereas the group receiving hzVSF_var13 was proportional to the concentration.
- the group receiving hzVSF_var13 was proportional to the concentration.
- hzVSF and various variants thereof of the present invention not only have excellent antiviral effect against influenza virus, but also inhibit inflammation with an anti-inflammatory effect that inhibits infiltration of immune cells. It suggests that it can be used.
- hzVSF_wt and variants thereof of the present invention exhibit antiviral effects against various viruses
- the effects of hzVSF_wt and representative variants hzVSF_var13 were confirmed in vitro and in vivo .
- In vitro experiments were for antiviral activity and in vivo experiments were for antiviral and anti-inflammatory.
- Encephalomyocarditis virus (EMCV) +++ +++ Mengovirus +++ NT Reovirus + NT Influenza virus + +++ HIV ++ NT HCMV + NT Mouse hepatitis virus (MHV) ++ +++ Hantaan Virus ++ NT HBV ++ NT HCV ++ NT
- hzVSF showed excellent antiviral activity and anti-inflammatory in both in vitro and in vivo for brain myocarditis (EMCV) virus.
- Mengovirus showed excellent antiviral activity in vitro .
- Reovirus has also been shown to be effective in vitro and in vivo .
- HIV has also shown antiviral efficacy in vitro . It also showed antiviral and anti-inflammatory effects against HCMV. It was shown to be effective in vitro against the Hantan virus and antiviral activity against hepatitis B and C viruses in vitro .
- MHV which causes hepatitis in mice with a mechanism similar to human hepatitis, has been shown to exhibit antiviral and anti-inflammatory properties, particularly in vivo .
- Influenza virus showed antiviral and anti-inflammatory effects in vitro and in vivo , and its efficacy was more excellent in vivo .
- Example 19 In the mouse model mVSF Inhibition of inflammatory cytokine secretion by administration
- mice were infected with EMC-D virus and 3 days after mVSF administration, the amount of inflammatory cytokines was measured by ELISA in serum. As shown in Table 16 below, inflammatory cytokines IL-6, TNF- ⁇ , IFN- ⁇ and MCP-1 were increased after viral infection, but administration of mVSF inhibited the expression of these inflammatory cytokines.
- mVSF also has an anti-inflammatory effect of inhibiting inflammation induced by viral infection.
- Cytokine (pg / ml) sample IL-12 TNF- ⁇ INF- ⁇ CCL2 (MCP-1) IL-10 IL-6 1 day after infection Normal ND 5.4 1.2 ND ND 1.2 Virus infection 14.2 40.0 166.2 1165.5 ND 205.6 virus + VSF ND 8.4 1.9 16.9 ND 5.0 virus + IFN- ⁇ 1 + VSF ND 9.1 1.6 13.0 ND 1.5 2 days after infection Normal ND 2.1 ND ND ND virus infection 8.7 38.0 724.3 344.5 ND 13.7 virus + VSF ND 32.4 74.5 129.9 ND 9.2 virus + IFN- ⁇ 1 + VSF ND 4.0 20.3 13.9 ND 1.4
- VSF also has anti-inflammatory effect of inhibiting inflammation induced by viral infection.
- Example 20 In the mouse model hzVSF Inhibition of inflammatory cytokine secretion by administration
- mice infected with 1 ⁇ 10 5 pfu of H1N1 (Influenza A / PR8) influenza virus and the lungs of mice administered 500 units of hzVSF_var13 were extracted one day after infection.
- GLB Greenberger Lysis Buffer
- PE detection reagent 1: 1: 1 1, and then blocked at room temperature Reaction was carried out for 2 hours. After the reaction, the bead was resuspended in the wash buffer, and data was measured by FACS cantoII.
- Example 21 Vimentin Effect of hzVSF after EMC-D Infection on Stable Cell Line
- Non-mentin (wt) or non-mentin (mt) overexpressing cell lines were prepared by transforming non-mentin-expressing MCF-7 cells with non-mentin (wt) or non-mentin (mt) mutated binding sites with hzVSF. Then, MVIT assay was performed using selected cells with similar expression levels.
- hzVSF_var13 was added by diluting 4 times serially from 256 U and incubated for 2 days. Then, the cells were fixed with methanol, stained with 0.5% crystal violet, and air dried.
- a WST assay was further performed to confirm cytotoxicity.
- the cells were treated with tetrazolium salt (WST-1) for an additional 4 hours and incubated at 450 nm wavelength. Absorbance was measured. After the measurement, the supernatant was removed, and the cells were fixed with methanol, followed by fixation staining using 0.5% crystal violet for 20 minutes, and air dried. Stained cells were dissolved in methanol and absorbance was measured at 540 nm.
- WST-1 tetrazolium salt
- VSF receptor (VR) VSF receptor
- each stable MCF-7 cells namely, non-mentin (wt) and non-mentin (mt) were infected with 5 MOI of EMC-D for 9 hours, and then cells were immunostained with hzVSF_var13. After fixing the cells, permeabilization and diluting 1: 250 hzVSF_var13 were reacted with the cells. The secondary antibody was reacted with FITC-goat human IgG and fluorescence microscopy confirmed receptor (VR) expression for hzVSF in cells (500 magnification).
- hzVSF_var13 was not bound to the non-mentin-expressing cells in which the binding sites of mock and hzVSF were mutated as shown in FIG. 55, but it was confirmed that VR was expressed by viral infection in the cells expressing the non-mentin of wt (Fig. 53).
- Example 22 E. in coli With refined VR WT and MT VSF Join check
- Example 23 HEK293T VR (mt) and overexpressed in cells With VSF Join check
- P60 WT or p60 MT was transformed into HEK293T cells and confirmed binding to hzVSF_v13.
- HEK293T cells were inoculated into a 100 mm culture dish, and then transformed with p60 wild-type and MT (mutant-type) DNA (vector: pcDNA3.1mycHisC) and incubated for 48 hours. . Then, after collecting the cells, 1 ml of 1% CHAPS lysis buffer was added, and the cells were lysed by standing on ice for 20 minutes. The lysed cells were centrifuged at 13,000 rpm for 15 minutes at 4 ° C to transfer the supernatant to a new tube. 50% slurry of protein A beads was added to 700 mg of protein, and then precleared at 4 ° C. for 1 hour.
- hzVSF_var13 was treated at 1: 100 and then incubated overnight at 4 ° C to combine VSF and VR. Then, 50% slurry of protein A was added, followed by reaction at 4 ° C. for 1 hour. Ptotein A-VSF-VR complex was obtained and centrifuged at 3,000 ⁇ g for 3 min at 4 ° C. to wash the beads and the supernatant was removed. The beads were then washed three times by adding 1% CHAPS lysis buffer to the precipitated complex. SX-PAGE and immunoblot were performed by adding 2X SDS-sample buffer and boiling.
- the antibody or binding fragment of the peptide specifically binding to the peptide of SEQ ID NO: 1 of the present invention exhibits antiviral and anti-inflammatory effects against a wide range of viral diseases, and is an existing antiviral agent interferon.
- chemotherapeutic agents it is possible to selectively apply only to virus-infected cells without side effects, and can be used in a small amount during treatment, to inhibit immune cell infiltration, to have anti-inflammatory action, and to be used as various virus therapeutic agents.
Abstract
Description
| 프라이머 | 서열 | 서열번호 |
| mVH F | cgagctcatgggatggagctggatc | 124 |
| mVH R | cggtacctgaggagacggtgactg | 125 |
| KpnI_delR | gggcccttggtggaagctgaggagacggtgactgagg | 126 |
| mVL F | catcgatatgagtgtgcccactcag | 127 |
| mVL R | cctcgagtttgatttccagcttgg | 128 |
| Xho_modR | agatggtgcagccaccgtgcgtttgatttccagcttggtgcc | 129 |
| VSF 종류 | 발현 세포 | mg/ℓ (harvested sup.) |
| mVSF | 마우스 하이브리도마 | 4.14 |
| *rmVSF | HEK293T | 5.71 |
| chVSFγ2 | HEK293T | 5.15 |
| chVSFγ4 | HEK293T | 7.32 |
| hzVSFγ2 | HEK293T | 5.01 |
| hzVSFγ4 | HEK293T | 9.38 |
| 항체 | CDR1 | CDR2 | CDR3 | |
| hzVSF_WT | 중쇄 | GYNMN(서열번호 2) | NIDPYYGSTTY A QKF Q G(서열번호 3) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VATNLAD(서열번호 6) | QHFYGSPRT(서열번호 7) | |
| hzVSF_a1 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGSTTY A QKF Q G(서열번호 3) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VATNLAD(서열번호 6) | QHFYGSPRT(서열번호 7) | |
| hzVSF_a2 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGSTTY A QKF Q G(서열번호 3) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VATNLAD(서열번호 6) | QHFYGSPRT(서열번호 7) | |
| hzVSF_a3 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGSTTY A QKF Q G(서열번호 3) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VATNLAD(서열번호 6) | QHFYGSPRT(서열번호 7) | |
| 항체 | FR1 | FR2 | FR3 | FR4 | |
| hzVSF_WT | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 22 | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_a1 | 중쇄 | 서열번호 151 | 서열번호 21 | 서열번호 22 | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_a2 | 중쇄 | 서열번호 20 | 서열번호 152 | 서열번호 22 | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_a3 | 중쇄 | 서열번호 151 | 서열번호 152 | 서열번호 22 | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| 항체 | CDR1 | CDR2 | CDR3 | |
| hzVSF_WT | 중쇄 | GYNMN(서열번호 2) | NIDPYYGSTTY A QKF Q G(서열번호 3) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VATNLAD(서열번호 6) | QHFYGSPRT(서열번호 7) | |
| hzVSF_var1 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGSTTYAQKFQG(서열번호 3) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VA D NLAD(서열번호 16) | QHFYGSPRT(서열번호 7) | |
| hzVSF_var2 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGSTTYAQKFQG(서열번호 3) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VA D NL G D(서열번호 17) | QHFYGSPRT(서열번호 7) | |
| hzVSF_var3 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGSTTYAQKFQG(서열번호 3) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VA D N RG D(서열번호 18) | QHFYGSPRT(서열번호 7) | |
| hzVSF_var4 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGSTTYAQKFQG(서열번호 3) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VA D N RG D(서열번호 18) | QHFYG T PRT(서열번호 19) | |
| hzVSF_var5 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGS D TYAQKFQG(서열번호 14) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VATNLAD(서열번호 6) | QHFYGSPRT(서열번호 7) | |
| hzVSF_var6 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGSTTYAQKFQG(서열번호 3) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VATNLAD(서열번호 6) | QHFYGSPRT(서열번호 7) | |
| hzVSF_var7 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGS D TYAQKFQG(서열번호 14) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VATNLAD(서열번호 6) | QHFYGSPRT(서열번호 7) | |
| hzVSF_var8 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGS D TYAQKFQG(서열번호 14) | ETG N RAMD(서열번호 15) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VATNLAD(서열번호 6) | QHFYGSPRT(서열번호 7) | |
| hzVSF_var9 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGS D TYAQKFQG(서열번호 14) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VA D N RG D(서열번호 18) | QHFYGSPRT(서열번호 7) | |
| hzVSF_var10 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGS D TYAQKFQG(서열번호 14) | ETG N RAMDY(서열번호 15) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VA D N RG D(서열번호 18) | QHFYGSPRT(서열번호 7) | |
| hzVSF_var11 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGS D TYAQKFQG(서열번호 14) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VA D N RG D(서열번호 18) | QHFYG T PRT(서열번호 19) | |
| hzVSF_var12 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGS D TYAQKFQG(서열번호 14) | ETG N RAMDY(서열번호 15) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VA D N RG D(서열번호 18) | QHFYG T PRT(서열번호 19) | |
| hzVSF_var13 | 중쇄 | GYNMN(서열번호 2) | NIDPYYGS D TYAQKFQG(서열번호 14) | ETGTRAMDY(서열번호 4) |
| 경쇄 | RASENIYSNLA(서열번호 5) | VA D NLAD(서열번호 16) | QHFYGSPRT(서열번호 7) | |
| 항체 | FR1 | FR2 | FR3 | FR4 | |
| hzVSF_WT | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 22 | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_var1 | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 22 | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_var2 | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 22 | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_var3 | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 22 | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_var4 | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 22 | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_var5 | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 22 | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_var6 | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 28(K74T, I76A) | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_var7 | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 28(K74T, I76A) | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_var8 | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 28(K74T, I76A) | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_var9 | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 28(K74T, I76A) | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_var10 | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 28(K74T, I76A) | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_var11 | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 28(K74T, I76A) | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_var12 | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 28(K74T, I76A) | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| hzVSF_var13 | 중쇄 | 서열번호 20 | 서열번호 21 | 서열번호 22 | 서열번호 23 |
| 경쇄 | 서열번호 24 | 서열번호 25 | 서열번호 26 | 서열번호 27 | |
| 단백질 종류 | DRB1 | DRB 3/4/5 | DQ | DP | Total |
| hzVSF w | 31 | 17 | 1 | 3 | 52 |
| hzVSF_var1 | 30 | 18 | 1 | 3 | 52 |
| hzVSF_var2 | 30 | 17 | 0 | 3 | 50 |
| hzVSF_var3 | 30 | 16 | 0 | 3 | 49 |
| hzVSF_var4 | 28 | 16 | 0 | 3 | 47 |
| hzVSF_var5 | 30 | 16 | 1 | 3 | 50 |
| hzVSF_var6 | 29 | 16 | 1 | 3 | 49 |
| hzVSF_var7 | 28 | 15 | 1 | 3 | 47 |
| hzVSF_var8 | 27 | 14 | 1 | 3 | 45 |
| hzVSF_var9 | 27 | 14 | 0 | 3 | 44 |
| hzVSF_var10 | 26 | 13 | 0 | 3 | 42 |
| hzVSF_var11 | 25 | 14 | 0 | 3 | 42 |
| hzVSF_var12 | 24 | 13 | 0 | 3 | 40 |
| hzVSF_var13 | 29 | 17 | 0 | 3 | 49 |
| Humira (human) | 25 | 12 | 4 | 1 | 42 |
| Remicade (chimeric) | 74 | 37 | 3 | 1 | 115 |
| Rituxan (chimeric) | 65 | 33 | 9 | 3 | 110 |
| Herceptin (humanized) | 40 | 20 | 3 | 1 | 64 |
| Product(Antigen) | Mean SI | p-value |
| hzVSF_var12 | 1.12 | 0.008 |
| hzVSF_var13 | 1.05 | 0.3229 |
| KLH | 3.91 | <0.0001 |
| Sham control(IgG 0.31 mg/kg) | hzVSF_var13(0.31 mg/kg) | hzVSF_var13(3.10 mg/kg) | hzVSF_var13(31.0 mg/kg) | |
| Female | ||||
| N | 6 | 6 | 6 | 6 |
| Cmax (㎍/㎖) | 5.5 ± 0.1 | 5.5 ±0.2 | 57.2 ± 1.0 | 607.2 ± 22.2 |
| AUC(㎍·day/㎖) | 178.1 ±53.9 | 113.0 ± 17.8 | 948.3 ± 296.7 | 8686.9 ± 2958.8 |
| t1/2(days) | 20.1 ± 2.9 | 13.4 ± 2.4 | 10.8 ± 3.8 | 10.2 ± 3.0 |
| CL(㎖/day/kg) | 1.8 ± 0.4 | 2.8 ± 0.4 | 3.5 ± 1.1 | 4.0 ± 1.5 |
| Male | ||||
| N | 5 | 5 | 5 | 5 |
| Cmax (㎍/㎖) | 5.5 ± 0.2 | 5.2 ± 0.3 | 54.6 ± 1.4 | 563.0 ± 8.2 |
| AUC(㎍·day/㎖) | 121.8 ± 15.3 | 78.8 ± 20.8 | 798.1 ± 274.5 | 6939.9 ± 2311.8 |
| t1/2(days) | 16.6 ± 2.4 | 10.1 ± 3.1 | 9.0 ± 4.0 | 8.9 ± 3.7 |
| CL(㎖/day/kg) | 2.6± 0.3 | 4.1 ± 0.8 | 4.2 ± 1.0 | 4.9 ± 1.2 |
| VSF 종류 | Biological activity (1 unit) | MW (kDa) |
| mVSF | 0.09 ㎍ | 163 |
| hzVSF_wt | 0.5 ㎍ | 147 |
| hzVSF_var12 | 0.2 ㎍ | 147 |
| hzVSF_var13 | 0.1 ㎍ | 147 |
| VSF 종류 | Affinity constant (Ka) | Dissociation constant (Kd) |
| mVSF | 2.1 x 1010 L/mol | 4.7 x 10-11 M |
| hzVSF wt | 8.2 x 109 L/mol | 1.2 x 10-10 M |
| hzVSF v13 | 1.7 x 1010 L/mol | 5.9 x 10-11 M |
| Group | post-infection | 당뇨병 발병률 | ||||
| 3 day | 4 day | 5 day | 6 day | 7 day | ||
| virus control | - | 4/4 | 4/4 | 4/4 | 4/4 | 100 % |
| 2 unit/mouse | - | - | - | 4/4 | 4/4 | 100 % |
| 4 unit/mouse | - | - | - | - | - | 0 % |
| 8 unit/mouse | - | - | - | - | - | 0 % |
| 16 unit/mouse | - | - | - | - | - | 0 % |
| Group | post-infection | ||||
| 3 day | 4 day | 5 day | 6 day | 7 day | |
| virus control | 157 ± 25 | 541 ± 84 | 540 ± 84 | 526 ± 91 | 529 ± 100 |
| 2 unit/mouse | 162 ± 24 | 157 ± 23 | 186 ± 53 | 484 ± 21 | 505 ± 26 |
| 4 unit/mouse | 149 ± 42 | 148 ± 6 | 135 ± 11 | 145 ± 8 | 122 ± 16 |
| 8 unit/mouse | 171 ± 42 | 148 ± 6 | 135 ± 11 | 145 ± 8 | 122 ± 16 |
| 16 unit/mouse | 163 ± 21 | 160 ± 4 | 144 ± 9 | 139 ± 8 | 157 ± 22 |
| Group | post-infection | ||||
| 3 day | 4 day | 5 day | 6 day | 7 day | |
| virus control | - | ++++ | ++++ | ++++ | ++++ |
| 2 unit/mouse | - | - | - | +++ | +++ |
| 4 unit/mouse | - | - | - | - | - |
| 8 unit/mouse | - | - | - | - | - |
| 16 unit/mouse | - | - | - | - | - |
| Virus | Antiviral effects | |
| in vitro | in vivo | |
| Encephalomyocarditis virus(EMCV) | +++ | +++ |
| Mengovirus | +++ | NT |
| Reovirus | + | NT |
| Influenza virus | + | +++ |
| HIV | ++ | NT |
| HCMV | + | NT |
| Mouse hepatitis virus (MHV) | ++ | +++ |
| Hantaan Virus | ++ | NT |
| HBV | ++ | NT |
| HCV | ++ | NT |
| Sample | Cytokine(pg/ml) : 바이러스감염 3일 후 측정 | ||||
| IL-12 | IL-6 | TNF-α | IFN-γ | CCL2 (MCP-1) | |
| Normal | ND | 2.9 | 4.6 | 1.3 | 13.8 |
| EMC-B | 1.1 | 190.3 | 44.3 | 91.4 | 1752.7 |
| EMC-D | 1.6 | 21.3 | 15.8 | 29.2 | 609.3 |
| EMC-D+VSF(1000unit) | 1.2 | 6.5 | 8.8 | 6.2 | 124.9 |
| Cytokine(pg/ml) | |||||||
| sample | IL-12 | TNF-α | INF-γ | CCL2(MCP-1) | IL-10 | IL-6 | |
| 감염후 1일 | Normal | ND | 5.4 | 1.2 | ND | ND | 1.2 |
| Virus infection | 14.2 | 40.0 | 166.2 | 1165.5 | ND | 205.6 | |
| virus+VSF | ND | 8.4 | 1.9 | 16.9 | ND | 5.0 | |
| virus+IFN-α 1회+VSF | ND | 9.1 | 1.6 | 13.0 | ND | 1.5 | |
| 감염 후 2일 | Normal | ND | 2.1 | ND | ND | ND | ND |
| virus infection | 8.7 | 38.0 | 724.3 | 344.5 | ND | 13.7 | |
| virus+VSF | ND | 32.4 | 74.5 | 129.9 | ND | 9.2 | |
| virus+IFN-α 1회+VSF | ND | 4.0 | 20.3 | 13.9 | ND | 1.4 | |
Claims (31)
- 서열번호 1의 펩타이드에 특이적으로 결합하는, 항체 또는 상기 펩타이드의 결합 단편.
- 제1항에 있어서, 상기 항체는 마우스 항체, 키메라 항체 또는 인간화 항체인 것인, 항체 또는 상기 펩타이드의 결합 단편.
- 제1항에 있어서, 상기 펩타이드의 결합 단편은 Fab, Fab', F(ab')2, scFv, dsFv, ds-scFv, 이들의 이량체, 미니바디(minibodies), 디아바디(diabodies) 및 다량체(multimer) 또는 이중 특이성 항체 단편인 것인, 항체 또는 상기 펩타이드의 결합 단편.
- 제2항에 있어서, 상기 인간화 항체 또는 상기 펩타이드의 결합 단편은서열번호 2로 기재된 중쇄 CDR1; 서열번호 3 또는 서열번호 14로 기재된 중쇄 CDR2; 및 서열번호 4 또는 서열번호 15로 기재된 중쇄 CDR3를 포함하는 중쇄 가변 영역, 및 서열번호 5로 기재된 경쇄 CDR1; 서열번호 6, 서열번호 16, 서열번호 17, 또는 서열번호 18로 기재된 경쇄 CDR2; 및 서열번호 7 또는 서열번호 19로 기재된 경쇄 CDR3를 포함하는 경쇄 가변 영역을 포함하는, 항체 또는 상기 펩타이드의 결합 단편.
- 제4항에 있어서, 상기 인간화 항체 또는 상기 펩타이드의 결합 단편은서열번호 20으로 기재된 중쇄 FR1 (Framework region 1); 서열번호 21로 기재된 중쇄 FR2; 서열번호 22 또는 서열번호 28로 기재된 중쇄 FR3; 및 서열번호 23으로 기재된 중쇄 FR4를 포함하는 중쇄 가변 영역, 및서열번호 24로 기재된 경쇄 FR1; 서열번호 25로 기재된 경쇄 FR2; 서열번호 26으로 기재된 경쇄 FR3; 및 서열번호 27로 기재된 경쇄 FR4를 포함하는, 경쇄 가변 영역을 추가로 포함하는, 항체 또는 상기 펩타이드의 결합 단편.
- 제2항에 있어서, 상기 인간화 항체 또는 상기 펩타이드의 결합 단편은,(a) 서열번호 2, 서열번호 3, 및 서열번호 4로 각각 기재된 중쇄 CDR1, 중쇄 CDR2, 및 중쇄 CDR3, 및 서열번호 5, 서열번호 6, 및 서열번호 7로 각각 기재된 경쇄 CDR1, 경쇄 CDR2, 경쇄 CDR3;(b) 서열번호 2, 서열번호 3, 및 서열번호 4로 각각 기재된 중쇄 CDR1, 중쇄 CDR2, 및 중쇄 CDR3, 및 서열번호 5, 서열번호 16, 및 서열번호 7로 각각 기재된 경쇄 CDR1, 경쇄 CDR2, 경쇄 CDR3;(c) 서열번호 2, 서열번호 3, 및 서열번호 4로 각각 기재된 중쇄 CDR1, 중쇄 CDR2, 및 중쇄 CDR3, 및 서열번호 5, 서열번호 17, 및 서열번호 7로 각각 기재된 경쇄 CDR1, 경쇄 CDR2, 경쇄 CDR3;(d) 서열번호 2, 서열번호 3, 및 서열번호 4로 각각 기재된 중쇄 CDR1, 중쇄 CDR2, 및 중쇄 CDR3, 및 서열번호 5, 서열번호 18, 및 서열번호 7로 각각 기재된 경쇄 CDR1, 경쇄 CDR2, 경쇄 CDR3;(e) 서열번호 2, 서열번호 3, 및 서열번호 4로 각각 기재된 중쇄 CDR1, 중쇄 CDR2, 및 중쇄 CDR3, 및 서열번호 5, 서열번호 18, 및 서열번호 19로 각각 기재된 경쇄 CDR1, 경쇄 CDR2, 경쇄 CDR3;(f) 서열번호 2, 서열번호 14, 및 서열번호 4로 각각 기재된 중쇄 CDR1, 중쇄 CDR2, 및 중쇄 CDR3, 및 서열번호 5, 서열번호 6, 및 서열번호 7로 각각 기재된 경쇄 CDR1, 경쇄 CDR2, 경쇄 CDR3;(g) 서열번호 2, 서열번호 3, 및 서열번호 4로 각각 기재된 중쇄 CDR1, 중쇄 CDR2, 및 중쇄 CDR3, 및 서열번호 20, 서열번호 21, 서열번호 28, 및 서열번호 23으로 각각 기재된 중쇄 FR1, FR2, FR3 및 FR4, 및 서열번호 5, 서열번호 6, 및 서열번호 7로 각각 기재된 경쇄 CDR1, 경쇄 CDR2, 경쇄 CDR3 및 서열번호 24, 서열번호 25, 서열번호 26, 및 서열번호 27로 각각 기재된 경쇄 FR1, FR2, FR3 및 FR4;(h) 서열번호 2, 서열번호 14, 및 서열번호 4로 각각 기재된 중쇄 CDR1, 중쇄 CDR2, 및 중쇄 CDR3, 및 서열번호 20, 서열번호 21, 서열번호 28, 및 서열번호 23으로 각각 기재된 중쇄 FR1, FR2, FR3 및 FR4, 및 서열번호 5, 서열번호 6, 및 서열번호 7로 각각 기재된 경쇄 CDR1, 경쇄 CDR2, 경쇄 CDR3 및 서열번호 24, 서열번호 25, 서열번호 26, 및 서열번호 27로 각각 기재된 경쇄 FR1, FR2, FR3 및 FR4;(i) 서열번호 2, 서열번호 14, 및 서열번호 15로 각각 기재된 중쇄 CDR1, 중쇄 CDR2, 및 중쇄 CDR3, 및 서열번호 20, 서열번호 21, 서열번호 28, 및 서열번호 23으로 각각 기재된 중쇄 FR1, FR2, FR3 및 FR4, 및 서열번호 5, 서열번호 6, 및 서열번호 7로 각각 기재된 경쇄 CDR1, 경쇄 CDR2, 경쇄 CDR3 및 서열번호 24, 서열번호 25, 서열번호 26, 및 서열번호 27로 각각 기재된 경쇄 FR1, FR2, FR3 및 FR4;(j) 서열번호 2, 서열번호 14, 및 서열번호 4로 각각 기재된 중쇄 CDR1, 중쇄 CDR2, 및 중쇄 CDR3, 및 서열번호 20, 서열번호 21, 서열번호 28, 및 서열번호 23으로 각각 기재된 중쇄 FR1, FR2, FR3 및 FR4, 및 서열번호 5, 서열번호 18, 및 서열번호 7로 각각 기재된 경쇄 CDR1, 경쇄 CDR2, 경쇄 CDR3 및 서열번호 24, 서열번호 25, 서열번호 26, 및 서열번호 27로 각각 기재된 경쇄 FR1, FR2, FR3 및 FR4;(k) 서열번호 2, 서열번호 14, 및 서열번호 15로 각각 기재된 중쇄 CDR1, 중쇄 CDR2, 및 중쇄 CDR3, 및 서열번호 20, 서열번호 21, 서열번호 28, 및 서열번호 23으로 각각 기재된 중쇄 FR1, FR2, FR3 및 FR4, 및 서열번호 5, 서열번호 18, 및 서열번호 7로 각각 기재된 경쇄 CDR1, 경쇄 CDR2, 경쇄 CDR3 및 서열번호 24, 서열번호 25, 서열번호 26, 및 서열번호 27로 각각 기재된 경쇄 FR1, FR2, FR3 및 FR4;(l) 서열번호 2, 서열번호 14, 및 서열번호 4로 각각 기재된 중쇄 CDR1, 중쇄 CDR2, 및 중쇄 CDR3, 및 서열번호 20, 서열번호 21, 서열번호 28, 및 서열번호 23으로 각각 기재된 중쇄 FR1, FR2, FR3 및 FR4, 및 서열번호 5, 서열번호 18, 및 서열번호 19로 각각 기재된 경쇄 CDR1, 경쇄 CDR2, 경쇄 CDR3 및 서열번호 24, 서열번호 25, 서열번호 26, 및 서열번호 27로 각각 기재된 경쇄 FR1, FR2, FR3 및 FR4;(m) 서열번호 2, 서열번호 14, 및 서열번호 15로 각각 기재된 중쇄 CDR1, 중쇄 CDR2, 및 중쇄 CDR3, 및 서열번호 20, 서열번호 21, 서열번호 28, 및 서열번호 23으로 각각 기재된 중쇄 FR1, FR2, FR3 및 FR4, 및 서열번호 5, 서열번호 18, 및 서열번호 19로 각각 기재된 경쇄 CDR1, 경쇄 CDR2, 경쇄 CDR3 및 서열번호 24, 서열번호 25, 서열번호 26, 및 서열번호 27로 각각 기재된 경쇄 FR1, FR2, FR3 및 FR4; 또는(n) 서열번호 2, 서열번호 14, 및 서열번호 4로 각각 기재된 중쇄 CDR1, 중쇄 CDR2, 및 중쇄 CDR3, 및 서열번호 5, 서열번호 16, 및 서열번호 7로 각각 기재된 경쇄 CDR1, 경쇄 CDR2, 경쇄 CDR3를 포함하는,항체 또는 상기 펩타이드의 결합 단편.
- 제2항에 있어서, 상기 인간화 항체는각각 서열번호 10 및 서열번호 12; 서열번호 32 및 서열번호 34; 서열번호 36 및 서열번호 38; 서열번호 40 및 서열번호 42; 서열번호 44 및 서열번호 46; 서열번호 48 및 서열번호 50; 서열번호 52 및 서열번호 54; 서열번호 56 및 서열번호 58; 서열번호 60 및 서열번호 62; 서열번호 64 및 서열번호 66; 서열번호 68 및 서열번호 70; 서열번호 72 및 서열번호 74; 서열번호 76 및 서열번호 78; 또는 서열번호 80 및 서열번호 82로 기재된 중쇄 및 경쇄 가변 영역을 포함하는, 항체 또는 상기 펩타이드의 결합 단편.
- 제2항에 있어서, 상기 마우스 항체는서열번호 137로 기재된 중쇄 CDR1; 서열번호 138로 기재된 중쇄 CDR2; 및 서열번호 139로 기재된 중쇄 CDR3를 포함하는 중쇄 가변 영역, 및서열번호 134로 기재된 경쇄 CDR1; 서열번호 135로 기재된 경쇄 CDR2; 및 서열번호 136으로 기재된 경쇄 CDR3를 포함하는 경쇄 가변 영역을 포함하는,항체 또는 상기 펩타이드의 결합 단편.
- 제2항에 있어서, 상기 마우스 항체는서열번호 9로 기재된 중쇄 가변 영역 및 서열번호 8로 기재된 경쇄 가변 영역을 포함하는, 항체 또는 상기 펩타이드의 결합 단편.
- 제2항에 있어서, 상기 키메라 항체는 서열번호 141 또는 서열번호 142로 기재된 중쇄 가변 영역 및 서열번호 140으로 기재된 경쇄 가변 영역을 포함하는, 항체 또는 상기 펩타이드의 결합 단편.
- 제2항에 있어서, 상기 키메라 항체는 서열번호 146 또는 서열번호 148로 기재된 중쇄 및 서열번호 144로 기재된 경쇄를 포함하는, 항체 또는 상기 펩타이드의 결합 단편.
- 제3항에 있어서, 상기 scFv는 서열번호 131로 기재된 중쇄 가변 영역 및 서열번호 133으로 기재된 경쇄 가변 영역이 링커로 연결된 것인, 항체 또는 상기 펩타이드의 결합 단편.
- 제3항에 있어서, 상기 scFv는 서열번호 130의 염기 서열로 코딩되는 중쇄 가변 영역 및 서열번호 132의 염기 서열로 코딩되는 경쇄 가변 영역이 링커로 연결된 것인, 항체 또는 상기 펩타이드의 결합 단편.
- 제1항에 있어서, 상기 항체 또는 상기 펩타이드의 결합 단편은 서열번호 1의 펩타이드의 9 번째, 45 번째, 54 번째, 76 번째, 94 번째 또는 129 번째 아미노산 잔기에 특이적으로 결합하는 것인, 항체 또는 상기 펩타이드의 결합 단편.
- 제1항 내지 제14항 중 어느 한 항의 항체 또는 상기 펩타이드의 결합 단편을 코딩하는 폴리뉴클레오티드.
- 제15항의 폴리뉴클레오티드를 포함하는 벡터.
- 제16항의 벡터가 도입된 세포.
- 제17항의 세포를 이용한 항체 또는 상기 펩타이드의 결합 단편의 생산방법.
- 제18항의 생산방법에 의해 생산된 항체 또는 상기 펩타이드의 결합 단편.
- 제1항 내지 제14항 중 어느 한 항의 항체 또는 상기 펩타이드의 결합 단편을 포함하는, 항바이러스용 조성물.
- 제20항에 있어서, 상기 조성물은 항바이러스 작용에 의한 바이러스 감염성 질환의 예방 또는 치료를 수행하는 것인 조성물.
- 제20항에 있어서, 상기 조성물은 바이러스 감염 세포 특이적으로 작용하는 것인 조성물.
- 제20항에 있어서, 상기 조성물은 면역세포 침윤을 억제하는 것인, 조성물.
- 제20항에 있어서, 상기 조성물은 염증반응을 억제하는 것인, 조성물.
- 제20항에 있어서, 상기 바이러스는 바이러스 감염에 의해 숙주 세포의 비멘틴 (vimentin)의 일부가 숙주 세포막 외부로 노출되는 것을 특징으로 하는 바이러스인, 조성물.
- 제20항에 있어서, 상기 바이러스는 오소믹소비리데(Orthomyxoviridae) 속 바이러스, 피코르나비리데(Picorna viridae) 속 바이러스, 레트로비리데(Retroviridae) 속 바이러스, 헤르페스(Herpes) 속 바이러스, 필로비리데(Filoviridae) 속 바이러스, 코로나비리데(Coronaviridae) 속 바이러스, 헤파드나비리데(Hepadnaviridae) 속 바이러스, 플라비비리데(Flaviviridae) 속 바이러스, 부냐비리데(Bunyaviridae) 속 바이러스로 구성된 군으로부터 선택된 것인, 조성물.
- 제20항에 있어서, 상기 바이러스는 인플루엔자 바이러스, 간염 바이러스, 뇌심근염 바이러스, 멩고 바이러스 (Mengovirus), 레오바이러스 (Reovirus), HIV (human immunodeficiency virus), 에볼라바이러스(Ebolavirus), 중증급성호흡기증후군 코로나바이러스(Severe Acute Respiratory Syndrome Coronavirus; SARS), 중동호흡기증후군 코로나바이러스(Middle East Respiratory Syndrome Coronavirus; MERS), HCMV (human cytomegalovirus), 및 한탄 바이러스로 이루어진 군에서 선택된 바이러스인 조성물.
- 제1항 내지 제14항 중 어느 한 항의 항체 또는 상기 펩타이드의 결합 단편을 포함하는, 염증성 질환의 예방 또는 치료용 조성물.
- 제28항에 있어서, 상기 염증성 질환은 바이러스 감염에 의한 것인 조성물.
- 제20항의 조성물을 바이러스에 감염된 인간을 제외한 개체에 투여하는 단계를 포함하는, 바이러스 감염 질환의 치료 방법.
- 제28항의 조성물을 염증성 질환에 걸린 인간을 제외한 개체에 투여하는 단계를 포함하는, 염증성 질환의 치료 방법.
Priority Applications (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP16807860.8A EP3309169A4 (en) | 2015-06-10 | 2016-06-10 | Antibody binding specifically to isolated vimentin-derived peptide, or binding fragment of the peptide |
| JP2018517109A JP6720298B2 (ja) | 2015-06-10 | 2016-06-10 | ビメンチン由来のペプチドに特異的に結合する抗体または断片 |
| AU2016277027A AU2016277027B2 (en) | 2015-06-10 | 2016-06-10 | Antibody binding specifically to isolated vimentin-derived peptide, or binding fragment of the peptide |
| CN202210259412.1A CN114605529A (zh) | 2015-06-10 | 2016-06-10 | 特异性结合衍生自波形蛋白的肽的抗体或片段 |
| CN201680034171.3A CN108026167B (zh) | 2015-06-10 | 2016-06-10 | 特异性结合分离的衍生自波形蛋白的肽的抗体或该肽的结合片段 |
| RU2017145521A RU2705899C2 (ru) | 2015-06-10 | 2016-06-10 | Антитело, специфично связывающееся с изолированным пептидом, образованным из виментина, или связывающийся с этим пептидом фрагмент |
| CA2988715A CA2988715C (en) | 2015-06-10 | 2016-06-10 | An antibody or a fragment specifically binding to peptide derived from vimentin |
| US15/570,734 US10961300B2 (en) | 2015-06-10 | 2016-06-10 | Antibody specifically binding to an isolated peptide derived from vimentin or a fragment binding to the peptide |
| AU2019204638A AU2019204638A1 (en) | 2015-06-10 | 2019-06-28 | Antibody Binding Specifically Isolated Vimentin-Derived Peptide, Or Binding Fragment Of The Peptide |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR20150082132 | 2015-06-10 | ||
| KR10-2015-0082132 | 2015-06-10 | ||
| KRPCT/KR2015/005917 | 2015-06-12 | ||
| PCT/KR2015/005917 WO2016199964A1 (ko) | 2015-06-10 | 2015-06-12 | 분리된 비멘틴 유래 펩타이드에 특이적으로 결합하는 항체 또는 상기 펩타이드의 결합 단편 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2016200220A1 true WO2016200220A1 (ko) | 2016-12-15 |
Family
ID=57503799
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/KR2016/006215 WO2016200220A1 (ko) | 2015-06-10 | 2016-06-10 | 분리된 비멘틴 유래 펩타이드에 특이적으로 결합하는 항체 또는 상기 펩타이드의 결합 단편 |
Country Status (1)
| Country | Link |
|---|---|
| WO (1) | WO2016200220A1 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2020532518A (ja) * | 2017-08-31 | 2020-11-12 | イミューンメッド インコーポレイテッドImmunemed Inc. | ビメンチン由来のペプチドに特異的に結合する物質を含む皮膚疾患の予防及び治療用組成物 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20030066419A (ko) * | 2002-02-01 | 2003-08-09 | 주식회사 이뮨메드 | 신규한 항바이러스 vsf 단백질 및 이를 분비하는하이브리도마 |
| KR20130027016A (ko) * | 2010-04-01 | 2013-03-14 | 센트로 데 인제니에리아 제네티카 와이 바이오테크놀로지아 | 포유류와 인간 세포에서 hiv 복제를 억제하는 방법 |
| WO2014138183A1 (en) * | 2013-03-05 | 2014-09-12 | Board Of Regents, The University Of Texas System | Specific detection tool for mesenchymal and epithelial-mesenchymal transformed circulating tumor cells |
| WO2015010791A2 (en) * | 2013-07-24 | 2015-01-29 | Klareskog, Lars | Novel antibodies for the diagnosis and treatment of rheumatoid arthritis |
-
2016
- 2016-06-10 WO PCT/KR2016/006215 patent/WO2016200220A1/ko active Application Filing
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20030066419A (ko) * | 2002-02-01 | 2003-08-09 | 주식회사 이뮨메드 | 신규한 항바이러스 vsf 단백질 및 이를 분비하는하이브리도마 |
| KR20130027016A (ko) * | 2010-04-01 | 2013-03-14 | 센트로 데 인제니에리아 제네티카 와이 바이오테크놀로지아 | 포유류와 인간 세포에서 hiv 복제를 억제하는 방법 |
| WO2014138183A1 (en) * | 2013-03-05 | 2014-09-12 | Board Of Regents, The University Of Texas System | Specific detection tool for mesenchymal and epithelial-mesenchymal transformed circulating tumor cells |
| WO2015010791A2 (en) * | 2013-07-24 | 2015-01-29 | Klareskog, Lars | Novel antibodies for the diagnosis and treatment of rheumatoid arthritis |
Non-Patent Citations (1)
| Title |
|---|
| LIANG ET AL.: "Vimentin Binding is Critical for Infection by the Virulent Sirain of Japanese Encephalitis Virus", CELLULAR MICROBIOLOGY, vol. 13, no. 9, 2011, pages 1358 - 1370, XP055333701 * |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2020532518A (ja) * | 2017-08-31 | 2020-11-12 | イミューンメッド インコーポレイテッドImmunemed Inc. | ビメンチン由来のペプチドに特異的に結合する物質を含む皮膚疾患の予防及び治療用組成物 |
| JP2022023216A (ja) * | 2017-08-31 | 2022-02-07 | イミューンメッド インコーポレイテッド | ビメンチン由来のペプチドに特異的に結合する物質を含む皮膚疾患の予防及び治療用組成物 |
| US11649277B2 (en) | 2017-08-31 | 2023-05-16 | Immunemed Inc. | Method for treating skin diseases using a humanized antibody that binds to vimentin |
| JP7323197B2 (ja) | 2017-08-31 | 2023-08-08 | イミューンメッド インコーポレイテッド | ビメンチン由来のペプチドに特異的に結合する物質を含む皮膚疾患の予防及び治療用組成物 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2018194381A1 (ko) | Lrig-1 단백질에 특이적인 결합 분자 및 이의 용도 | |
| WO2014158001A1 (ko) | 2 이상의 인플루엔자 a 바이러스 중화 결합 분자를 포함하는 조성물 | |
| WO2020050667A1 (ko) | 고형암을 위한 키메라 항원 수용체 및 키메라 항원 수용체가 발현된 t 세포 | |
| WO2016137108A1 (en) | Novel antibody binding to tfpi and composition comprising the same | |
| WO2015058573A1 (zh) | 拮抗抑制程序性死亡受体pd-1与其配体结合的单克隆抗体及其编码序列与用途 | |
| WO2018030806A1 (ko) | 항체 중쇄불변부위 이종이중체에 융합된 사이토카인 및 이를 포함하는 약제학적 조성물 | |
| WO2014077648A1 (ko) | 인간 및 마우스 l1cam 단백질에 특이적으로 결합하는 항체 및 이의 용도 | |
| WO2014090053A1 (zh) | 拮抗抑制血管内皮细胞生长因子与其受体结合的单克隆抗体及其编码序列与用途 | |
| WO2018026248A1 (ko) | 프로그램화된 세포 사멸 단백질(pd-1)에 대한 신규 항체 및 이의 용도 | |
| WO2016199964A1 (ko) | 분리된 비멘틴 유래 펩타이드에 특이적으로 결합하는 항체 또는 상기 펩타이드의 결합 단편 | |
| WO2021020846A1 (en) | Anti-her2/anti-4-1bb bispecific antibody and use thereof | |
| WO2020101365A1 (ko) | 안정성이 향상된 항 c-met 항체 또는 그의 항원 결합 단편 | |
| WO2020080854A1 (ko) | Lrig-1 단백질에 특이적인 결합 분자 및 이의 용도 | |
| WO2019045477A1 (ko) | 비멘틴 유래 펩타이드에 특이적으로 결합하는 물질을 포함하는 피부질환 예방 및 치료용 조성물 | |
| WO2012137993A1 (en) | Antibodies against angiopoietins 1 and 2, and their use | |
| WO2021020845A1 (en) | Anti-egfr/anti-4-1bb bispecific antibody and use thereof | |
| WO2016200220A1 (ko) | 분리된 비멘틴 유래 펩타이드에 특이적으로 결합하는 항체 또는 상기 펩타이드의 결합 단편 | |
| WO2016200189A1 (ko) | 광견병 바이러스 g 단백질의 에피토프 및 이에 특이적으로 결합하는 광견병 바이러스 중화 결합 분자 | |
| WO2022085905A1 (ko) | SARS-CoV-2 스파이크 단백질에 특이적으로 결합하는 항체 및 이의 용도 | |
| WO2022035201A1 (ko) | Il-12 및 항-fap 항체를 포함하는 융합단백질 및 이의 용도 | |
| WO2018026249A1 (ko) | 프로그램화된 세포 사멸 단백질 리간드-1 (pd-l1)에 대한 항체 및 이의 용도 | |
| WO2021071319A1 (ko) | 다중 특이적 융합 단백질 및 이의 용도 | |
| WO2015088256A1 (ko) | 광견병 바이러스를 중화시킬 수 있는 결합 분자 | |
| WO2020138868A1 (ko) | 타입 1 인터페론 중화 fc-융합 단백질 및 이의 용도 | |
| WO2023211229A1 (ko) | 항―wars1 항체 및 이의 용도 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 16807860 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2988715 Country of ref document: CA |
|
| ENP | Entry into the national phase |
Ref document number: 2018517109 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2016277027 Country of ref document: AU Date of ref document: 20160610 Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2017145521 Country of ref document: RU Ref document number: 2016807860 Country of ref document: EP |