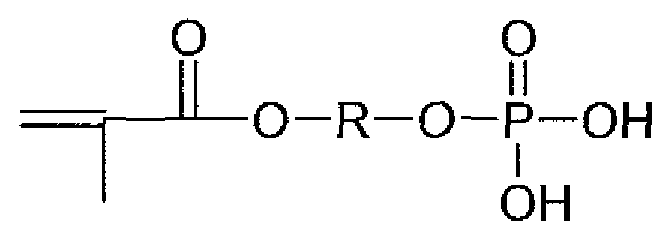WO2008107470A1 - Verwendung von protonenliefernden und/oder protonenakzeptierenden polymerteilchen - Google Patents
Verwendung von protonenliefernden und/oder protonenakzeptierenden polymerteilchen Download PDFInfo
- Publication number
- WO2008107470A1 WO2008107470A1 PCT/EP2008/052713 EP2008052713W WO2008107470A1 WO 2008107470 A1 WO2008107470 A1 WO 2008107470A1 EP 2008052713 W EP2008052713 W EP 2008052713W WO 2008107470 A1 WO2008107470 A1 WO 2008107470A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- polymer particles
- acid
- use according
- proton
- monomers
- Prior art date
Links
- WPYMKLBDIGXBTP-UHFFFAOYSA-N OC(c1ccccc1)=O Chemical compound OC(c1ccccc1)=O WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/02—Catalysts comprising hydrides, coordination complexes or organic compounds containing organic compounds or metal hydrides
- B01J31/06—Catalysts comprising hydrides, coordination complexes or organic compounds containing organic compounds or metal hydrides containing polymers
- B01J31/08—Ion-exchange resins
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/22—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof comprising organic material
- B01J20/26—Synthetic macromolecular compounds
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/281—Sorbents specially adapted for preparative, analytical or investigative chromatography
- B01J20/282—Porous sorbents
- B01J20/285—Porous sorbents based on polymers
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/02—Catalysts comprising hydrides, coordination complexes or organic compounds containing organic compounds or metal hydrides
- B01J31/06—Catalysts comprising hydrides, coordination complexes or organic compounds containing organic compounds or metal hydrides containing polymers
- B01J31/08—Ion-exchange resins
- B01J31/10—Ion-exchange resins sulfonated
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J39/00—Cation exchange; Use of material as cation exchangers; Treatment of material for improving the cation exchange properties
- B01J39/08—Use of material as cation exchangers; Treatment of material for improving the cation exchange properties
- B01J39/16—Organic material
- B01J39/18—Macromolecular compounds
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D5/00—Coating compositions, e.g. paints, varnishes or lacquers, characterised by their physical nature or the effects produced; Filling pastes
- C09D5/16—Antifouling paints; Underwater paints
- C09D5/1606—Antifouling paints; Underwater paints characterised by the anti-fouling agent
- C09D5/1637—Macromolecular compounds
Definitions
- the present invention relates to the use of polymer particles produced by emulsion polymerization having a mean particle diameter in the range of 5 to 500 nm, containing surface-standing and / or non-surface-standing ionic groups, as proton-providing and / or proton-accepting substance in heterogeneous chemical processes, particularly suitable polymer particles for the use in such processes as well as composite materials and moldings containing them.
- immobilized proton donors or proton donors or proton acceptors are required.
- immobilized proton donors or proton donors or proton acceptors are required.
- Proton acceptors offers fundamental advantages, such as facilitated separation.
- microgels for controlling the properties of elastomers or thermoplastics is known (WO2005 / 0331 85). In some cases, microgels have also been used which have functional groups on the surface or over the entire cross section.
- nanoparticle polymer particles modified with proton-providing or proton-accepting groups in heterogeneous chemical processes which require an immobilized proton donor or proton acceptor has hitherto not been known
- the present invention relates to the use of emulsion polymerized polymer particles having a mean particle diameter in the range of 5 to 500 nm, containing ionogenic groups as a proton-providing and / or proton-accepting substance, in heterogeneous chemical processes. Also included in the invention Applications in which the polymer particles are first at least partially neutralized.
- polymer particles offer numerous advantages over conventional proton donors or proton acceptors, since the chemical and physical properties of the polymer particles, such as particle size, particle morphology, quenching behavior, catalytic activity, hardness, dimensional stability, tackiness, aging resistance, impact resistance on the one hand by the manufacturing process, in particular by the polymerization process , as well as by selecting suitable base monomers and on the other hand by selecting suitable ionogenic groups whose concentration and Ansiedjungs Kunststoff in the polymer particles can be selectively adjusted or tailored within wide limits.
- Heterogeneous processes or processes are those in which phase boundaries, in particular solid / liquid and / or solid / gaseous, are involved, the polymer particles naturally being assigned to the solid phase.
- proton-delivering or proton-accepting means in particular, that the polymer particles can release or take up protons to a surrounding medium.
- the polymer particles are able to impart proton conductivity to the matrix.
- emulsion polymerization is understood in particular to be a process known per se, in which water is used as the reaction medium, in which the monomers used are polymerized in the presence of emulsifiers and free-radical-forming substances to form aqueous polymeriatices (see, for example, Römpp Lexikon der Chemie, Vol 2, 1 O. Edition 1 997; P, A. Loveil, MS El-Aasser, Emulsion Polymerization and Emulsion Polymers, John Wiley & Sons, ISBN: 0 471 96746 7, H. Gerrens, Fortschr. Hochpolym. Forsch. 234 (1 959)).
- the emulsion polymerization In contrast to suspension or dispersion polymerization, the emulsion polymerization generally gives finer particles which allow a lower particle absorbency in a matrix.
- the smaller particles are below with their small mean diameter the critical defect size, ie the matrices containing them are subject to only minor mechanical impairments, with a corresponding degree of dispersion.
- Particles of size less than 500 nm are generally not accessible by suspension or dispersion polymerization, as these particles are generally unsuitable for the purposes of this patent application.
- the choice of monomers sets the glass transition temperature and the glass transition width of the polymer particles.
- Glass transition (ATg) of the microgels is carried out by differential scanning calorimetry (DSC), preferably as described below.
- DSC differential scanning calorimetry
- two cooling / heating cycles are carried out for the determination of Tg and ATg.
- Tg and ATg are determined in the second heating cycle.
- approximately 10 -12 mg of the selected microgel is placed in a Perkin-Elmer DSC sample container (standard aluminum pan).
- the first DSC cycle is carried out by first cooling the sample with liquid nitrogen to -1 00 0 C and is then heated at a rate of 20K / min to + 1 50 0 C.
- the second DSC cycle is started by immediately cooling the sample as soon as a sample temperature of + 1 50 0 C is reached.
- the cooling takes place at a speed of about 320 K / min.
- the sample as in the first cycle is again heated to 50 + 1 0C.
- the heating rate in the second cycle is again 20K / min.
- Tg and ATg are determined graphically on the DSC curve of the second heating process.
- three straight lines are applied to the DSC curve.
- the 1 At the curve part of the DSC curve below Tg, the 2nd straight line at the curve branch with inflection point running through Tg and the 3rd straight line at the curve branch of the DSC curve above Tg are applied. In this way, three straight lines with two intersections are obtained. Both intersections are each characterized by a characteristic temperature.
- the glass transition temperature Tg is obtained as the average of these two temperatures and the width of the glass transition ATg is obtained from the difference between the two temperatures.
- Cumulative polymer particles have a gas temperature of generally ⁇ 23 ° C.
- Thermoplastic polymer teats have a glass transition temperature in general a glass transition temperature of> 23 ° C.,
- the width of the glass transition is preferably greater than 5 0 C, more preferably greater than 10 0 C. in the polymer used in the invention.
- Rubbery polymer particles are preferably those based on conjugated dienes such as butadiene, isoprene, 2-chlorobutadiene and 2,3-dichlorobutadiene, as well as ethene, esters of acrylic and
- Methacrylic acid vinyl acetate, styrene or derivatives thereof, acrylonitrile, acrylamides, methacrylamides, tetrafluoroethylene, vinylidene fluoride, hexafluoropropene, double bond-containing hydroxy compounds such. Hydroxyethyl methacrylate, hydroxyethyl acrylate, hydroxypropyl acrylate, hydroxybutyl methacrylate, acrolein or combinations thereof.
- Suitable base monomers are in particular the following compounds:
- Dimethylaminoethyl methacrylate vinylimidazole such as 1-vinylimidazole, vinylpyridine such as 2-vinylpyridine and 4-vinylpyridine, acrylamide, 2-acrylamidoglycolic acid, 2-acrylamido-2-methyl-1-propanesulfonic acid, acrylic acid [2 - (((butylamino) carbonyl ) -oxyl) ethyl ester], acrylic acid (2-diethylaminoethyl ester), acrylate (2- (dimethylamino) ethyl ester), acrylic acid (3- (dimethylamino) -propyl ester), acrylic acid-isopropylamide, acrylic acid phenylamide, acrylic acid (3 potassium salt, methacrylamide, methyl 2-aminoethyl methacrylate hydrochloride, methyl 2- (tert -butylamino) ethylacrylate, 2-dimethylaminoethyl methacryl
- Preferred monomers or monomer combinations include butadiene, isoprene, acrylonitrile, styrene, alpha-methylstyrene,
- Vinylidene fluoride and hexafluoropropene “On the basis” here means that the polymer particles preferably consist of more than 60% by weight, preferably more than 70% by weight, more preferably more than 90% by weight, of the stated monomers
- the polymer particles can be crosslinked or uncrosslinked be
- Traps of crosslinked polymer particles are also called microgels.
- the polymer particles may in particular be those based on
- Homopolymers and random copolymers are known to the person skilled in the art and are explained by Vollmert, Polymer Chemistry, for example.
- the polymer base of the rubbery, crosslinked or uncrosslinked polymer particles containing ionogenic groups may be used in particular:
- ABR butadiene / acrylic acid C 1-4 alkyl ester copolymers
- IR polyisoprene
- Styroig contents of 1-60, preferably 5-50 weight percent
- FKM fluororubber
- ACM acrylate rubber
- NBR polybutadiene-acrylonitrile copolymers
- thermoplastic polymer teats expediently have a gas transition temperature Tg of more than 23 ° C.
- the width of the glass transition is preferably greater than 5 0 C for the thermoplastic-like Poiymerteilchen (wherein it is determined the Tg and the width of the glass transition as described above).
- Non-rubbery, in particular thermoplastic, polymer particles are preferably those based on methacrylates, in particular methyl methacrylate, styrene or styroid derivatives, such as alpha-methylstyrene, para-methylstyrene, acrylonitrile, methacrylonitrile, vinylcarbazole or combinations thereof. "On the basis” here means that the polymer particles preferably consist of more than 60% by weight, preferably more than 70% by weight, more preferably more than 90% by weight, of the stated monomers. More preferred thermoplastic polymer particles are those
- methacrylates especially methyl methacrylate, styrene, alpha-methylstyrene and acrylonitrile.
- the polymer particles preferably have an approximately spherical geometry.
- the polymer particles used according to the invention have an average particle diameter in the range from 5 to 500 nm, preferably from 20 to 400, particularly preferably from 30 to 300 nm.
- the average particle diameter is determined by ultracentrifugation with the aqueous latex of the polymer particles from the emulsion polymerization. The method gives a mean value for the particle diameter taking into account any agglomerates. (G.G.Muller (1 99)) Colloid Polymer Science 267: 1131 3-116 and W. Scholtan, H. Lange (1972) Kolloid-Z and 2. Polymers 250: 782).
- Ultracentrifugation has the advantage of characterizing the total particle size distribution and calculating various mean values, such as means of drawing, weight average, from the distribution curve.
- the mean diameter data used according to the invention relate to the weight average.
- diameter data such as d ⁇ 0 , d 60 and d 80 are used. This information means that 10, 50 or 80 wt.% the particles have a diameter smaller than the corresponding numerical value in% by weight,
- the diameter determination by means of dynamic light scattering leads in first approximation to comparable average particle diameters. It is also done on the latex. Common are lasers operating at 633 nm (red) and 532 nm (green). In the case of dynamic light scattering, the entire particle size distribution is not characterized, as in the case of ultracentrifugation, but a mean value is obtained in which large particles are disproportionately weighted.
- the polymer particles used according to the invention preferably have a weight-average particle diameter in the range from 5 to 500 nm, preferably from 20 to 400, particularly preferably from 30 to 300 nm.
- the particles are prepared by emulsion polymerization, wherein the particle size is adjusted in a wide range of diameters by varying the starting materials, such as emulsifier concentration, initiator concentration, Fiottendream of organic to aqueous phase, ratio of hydrophilic to hydrophobic monomers, amount of crosslinking monomer, polymerization temperature, etc.
- the latices are treated by vacuum distillation or by treatment with superheated steam in order to separate off volatile components, in particular unreacted monomers,
- the processing of the polymer particles produced in this way can be carried out, for example, by evaporation, electrolytic coagulation, co-coagulation with another latex polymer, by freeze coagulation (cf., US-PS 21 87146) or by spray-drying.
- freeze coagulation cf., US-PS 21 87146
- spray-drying cf., US-PS 21 87146
- commercially available flow aids such as, for example, CaCO 3 or silica can also be added,
- the polymer particles produced by emulsion polymerization according to the invention are at least partially crosslinked in a preferred embodiment.
- Crosslinking of polymer backings may be achieved directly during emulsion polymerization, such as by copolymerization with crosslinking multifunctional compounds or by subsequent crosslinking as described below. Direct crosslinking during emulsion polymerization is preferred.
- polyhydric preferably 2- to 4-valent C 2 to C 10 alcohols
- ethylene glycol propanediol 1, 2, butanediol, hexanediol
- Polyethylengiykol having 2 to 20, preferably 2 to 8 oxyethylene units
- Neopentyl glycol bisphenol A, glycerol, trimethyl
- Crosslinking during emulsion polymerization can also be achieved by continuing the polymerization up to high conversions or in Mo ⁇ omerzul ⁇ ufverf ⁇ hren by polymerization with high internal conversions take place. Another possibility is to carry out the emulsion polymerization in the absence of regulators. For the crosslinking of the uncrosslinked or the weakly crosslinked polymer particles following the
- Emulsion polymerization is best used the latices obtained in the emulsion polymerization.
- Suitable crosslinking chemicals are organic peroxides, such as dicumyl peroxide, t-butylicyl peroxide, bis (t-butyl-peroxy-isopropyl) benzene, di-t-butyl peroxide, 2,5-ditmethylhexane-2,5-dihydroperoxide, 2, 5-dimethylhexine-3,2,5-dihydroper-oxide, dibenzoyl peroxide, bis (2,4-dichlorobenzoyl) peroxide, t-butyl perbenzoate and organic azo compounds such as azo-bis-isobutyronitrile and azo-bis-cyclohexanenitrile and di- and Polymercaptoverbi ⁇ ditch, such as dimercaptoethane, 1, 6-dimercaptohexane, 1, 3,5 Tri ⁇ mercaptotriazin and mercapto-terminated polysulfide such as mercapto-terminated reaction products of bis
- the optimal temperature for carrying out the post-crosslinking is naturally dependent on the reactivity of the crosslinking agent and can at temperatures from room temperature to ca, 1 80 0 C, optionally carried out at elevated pressure (see Houben-Weyl, Methoden der organischen Chemie, 4, pad, Volume 14/2, page 848).
- Particularly preferred crosslinking agents are peroxides.
- the crosslinked polymer particles used in accordance with the invention expediently have toluene at 23 ° C. insoluble fractions (gel content) of at least about 70% by weight, more preferably at least about 80% by weight, even more preferably at least about 90% by weight.
- the insoluble fraction in Toluoi is determined in toluene at 23 °.
- 250 mg of the polymer teats are swollen in 25 ml Toluoi 24 hours with shaking at 23 ° C. After centrifugation at 20,000 rpm, the insoluble fraction is separated and dried. The gel content results from the quotient of the dried residue and the weight and is given in percent by weight.
- the crosslinked polymer particles used erfi ⁇ dungswash further expediently have Toluoi at 23 0 C a swelling index of less than about 80, more preferably less than 60 more preferably less than 40.
- the swelling indexes of the polymer particles (Qi) can be more preferably between 1 - 1 5 and 1 - 1 0 are.
- the swelling index is calculated from the weight of the polymer particles polymerized in toluene at 23 ° for 24 hours (after centrifugation at 20,000 rpm) and the weight of the dry polymer particles:
- Qi wet weight of the polymer particles / dry weight of the polymer particles.
- the polymer particles used according to the invention contain ionogenic groups, according to the invention ionogenic groups are those which are ionic or capable of forming ionic groups; in this way they are capable of delivering protons and / or of accepting protons.
- the ionogenic groups are selected from one or more of the following functional groups: -COOH, -SO 3 H, -OSO 3 H,
- salts represent the conjugated bases to the acidic functional groups, ie -COO " , -SO 3 " , -OSO 3 -, -P (O) 2 (OH) - or -P (O) 3 3 " , -0 -P (O) 2 2 and -OP (O) 2 (OH) - or -OP (O) 3 2 " in the form of their metal, preferably alkali metal or ammonium salts.
- particularly preferred ionic groups in the context of the invention are selected from -SO 3 H, -PO (OH) 2 , -O-P (O) (OH) 2 and / or their salts and / or derivatives thereof, in particular partial esters thereof ,
- the ionogenic groups may be surface-active and / or non-surface-active.
- the ionogenic groups can be introduced into the polymer teats by copolymerization of appropriately functionalized monomers and / or by modification after polymerization.
- R is a divalent organic group, in particular C l to Cl O-Aikylen.
- R is a C 2 -C 4 alkylene group (i.e., a C 2 -C 4 alkanediyl group) such as methylene, ethylene or n-propylene.
- Saize of these compounds are also applicable, such as in particular alkali metal salts, preferably the sodium salt or ammonium salts.
- the corresponding acrylates can also be used.
- partial esters can be used with other saturated or unsaturated carboxylic acids of these compounds.
- partial ester includes both the case that a part of the acidic hydroxyl groups of the ionic group is partially esterified, as well as the case in which a part of the hydroxyl groups is esterified in the polymer, another part is not esterified.
- the proportion of the functionalized monomers having copolymerized ionogenic groups is preferably from 0.1 to 100% by weight, more preferably from 0.2 to 99.5% by weight, based on the total amount of the monomers. This means that homopolymers of these monomers carrying ionic groups can also be used. For example, at least 10 can be used.
- Wt .-% at least 20 wt .-% or at least 30 wt .-% of these monomers.
- the ionogenic groups -OSO 3 H and -OP (O) (OH) 2 can also be converted, for example, by reaction of hydroxyl-modified polymer particles (such as by polymerization of
- -P (O) (OH) 2 can also be introduced by sulfonation or phosphonation of aromatic vinyl polymers, ionogenic groups can also be prepared by reaction of hydroxyl-modified Polyme ⁇ teilchen with correspondingly functionalized epoxides.
- These reactive chemicals are in particular those compounds with whose help polar groups such. Aldehyde, hydroxyk, carboxyl, nitrile, etc. and sulfur containing groups, e.g. Mercapto, dithiocarbamate, polysulfide, xanthate and / or Dithiophosphorklare weakness and / or unsaturated
- Dicarboxylic acid groups can be chemically bonded to the polymer particles.
- the aim of the modification is, in particular, to improve the compatibility with a matrix polymer into which the polymer particles are optionally incorporated in order, for example, to achieve good distributability during production and good coupling.
- Particularly preferred methods of modification are the grafting of the polymer particles with functional monomers and the reaction with low molecular weight agents. In this way, if appropriate, the ionogenic, proton donating or proton accepting monomers can be introduced into the polymer particles.
- aqueous microgel dispersion which has been obtained with polar monomers such as vinylsulfonic acid, styrenesulfonic acid, acrylic acid, methacrylic acid, Itaconic acid, hydroxyethyl (meth) acrylate (The term "(meth) acrylate” in the present application includes both methacrylate and acrylate), hydroxypropyl (meth) acrylate, hydroxybutyl (meth) acrylate, acrylonitrile, acrylamide , Methacrylamide, acrolein, phosphonic acid or phosphoric acid group-containing
- polar monomers such as vinylsulfonic acid, styrenesulfonic acid, acrylic acid, methacrylic acid, Itaconic acid, hydroxyethyl (meth) acrylate (The term "(meth) acrylate” in the present application includes both methacrylate and acrylate), hydroxypropyl (meth) acrylate, hydroxybutyl (me
- polymerizable C C double bond-containing monomers or salts or derivatives, in particular partial esters thereof the conditions of a radical emulsion polymerization.
- the monomer used in the modification step grafted onto the unmodified polymer particle or microgel as quantitatively as possible.
- the functional monomers are added before complete crosslinking of the microgels.
- a modification of double bond-containing polymer particles e.g. by Ozonoiyse comes into question.
- the polymer particles, in particular the microgels are modified by hydroxyl groups, in particular also on the surface thereof.
- the hydroxyl group content of the polymer particles, in particular of the microgels is determined by reaction with acetic anhydride and titration of the acetic acid released herewith KOH according to DIN 53240 as hydroxyl Zahi with the dimension mg KOH / g polymer.
- the hydroxyl number of the polymer particles, in particular of the microgels is preferably between OJ - 100, more preferably between 0.5-50 mg KOH / g polymer.
- the amount of modifier used depends on its effectiveness and the particular requirements placed in the individual case and is in the range of 0.05 to 30 weight percent, based on the total amount of polymer used, in particular microgel, more preferably 0.5-10 Weight percent based on total amount of polymer particles, in particular microgel.
- the modification reactions can be carried out at temperatures from 0- 1 80 0 C, preferably 20-95 0 C, optionally under a pressure of 1 -30 bar, are carried out, the modifications can be made to rubber microgels in substance or in the form of their dispersion, inert organic solvents or water may be used as the reaction medium in the latter case. Particularly preferably, the modification is carried out in aqueous dispersion of the crosslinked rubber.
- polymer particles whose preparation can be carried out as described above are suitable, for example, as catalysts in acid-catalyzed reactions, such as the oligomerization of isobutene, the acid-catalyzed preparation of bisphenol A, esterification reactions, Friedel-Crafts reactions.
- Polymer matrices all in heterogeneous processes or processes in which phase boundaries, in particular solid / liquid, solid / gaseous involved.
- phase boundaries in particular solid / liquid, solid / gaseous involved.
- Membranes, films, etc. can be used according to the invention Polyrer particles in a proportion of milligram polymer to polymer particles of 1; 99 to 99: 1, preferably from 1 0: 90 to 90: 1 0, more preferably 20: 80 to 80: 20 be contained.
- the amount of polymer particles used in the invention depends on the desired properties of the molded articles, such as proton conductivity of the membranes.
- Suitable matrix polymers are, for example, thermoplastic polymers such as standard thermoplastics, so-called techno-thermoplastics and so-called high-performance thermoplastics (cf. H, G. Elias Makromoleküle Volume 2, 5 ed., Wegig & Wepf Verlag, 1 992, page 443 ff), such as for example, in polypropylene, polyethylene, such as HDPE, LDPE, LLDPE, polystyrene, etc.
- thermoplastic polymers such as standard thermoplastics, so-called techno-thermoplastics and so-called high-performance thermoplastics (cf. H, G. Elias Makromoleküle Volume 2, 5 ed., Hüthig & Wepf Verlag, 1 992, page 443 ff), such as for example, in polypropylene, polyethylene, such as HDPE, LDPE, LLDPE, polystyrene, etc.
- thermoplastic materials such as PU, PC, EVM, PVA, PVAC, polyvinyl butyral, PET, PBT, POM, PMMA, PVC, ABS, AES, SAN , PTFE, CTFE, PVF, PVDF, polyimides, PA, in particular PA- ⁇ (nylon), more preferably PA-4, PA-66 (perlon), PA-69, PA-61 0, PA-1, PA I 2, PA 61 2, PA-MXD6, etc.
- the weight ratio of these matrix polymers to the polymer particles may suitably be from 1:99 to 99; 1, preferably from 10:90 to 90: 1 0, more preferably 20: 80 to 80: 20.
- Preferred matrix polymer for use in polyelectrolyte membranes, in particular for fuel cells is polybenzimidazole (for example US Pat. No. 4,460,763).
- the invention further relates to novel polymer particles having an average particle diameter in the range of 5 to 500 nm (determined by ultracentrifugation as set forth above) obtained by emulsion polymerization containing ionogenic groups selected from the group consisting of: -SO 3 H, -OSO 3 H, -P (O) (OH) 2 , -O-P (OH) 2 and -O-P (O) (OH) 2 and / or their salts and / or derivatives thereof.
- ionogenic groups selected from the group consisting of: -SO 3 H, -OSO 3 H, -P (O) (OH) 2 , -O-P (OH) 2 and -O-P (O) (OH) 2 and / or their salts and / or derivatives thereof.
- the proportion of said ionic groups in the polymer particles is preferably in the range of 0.1 to 95% by weight, more preferably 1 to 90% by weight, based on the total amount of the polymer particles.
- Suitable salts of the polymer particles include metal or ammonium salts, especially alkali metal salts, alkaline earth metal salts, etc.
- Suitable derivatives of the polymer particles include, in particular, ester and partial esters of said ionic groups.
- the invention is not limited in the applications of these novel polymer particles, and they can be used in all applications already described above.
- the invention relates to novel composite materials of the aforementioned polymer particles wherein these are coated on at least one support material.
- support materials include inorganic and organic materials, for example: carbon black, silicon dioxide, calcium carbonate, calcium oxide, magnesium oxide, aluminum oxide, barium sulfate, zeolites, ion exchange resins, fibers, in particular polymer fibers, etc.
- novel polymer particles can also be used in pure form, for example in ion exchange or catalytic processes.
- the invention further relates to novel moldings, in particular films in which the above-mentioned polymer particles are contained in particular in a polymer matrix.
- the polymer particles used according to the invention in a proportion of matrix polymer to polymer particles can be from 1:99 to 99: 1, preferably from 10: 90 to
- microgels were prepared by emulsion polymerization.
- the Mo ⁇ omerkombinationen used for the production of microgels and essential dictionaryur Strukturteiie are summarized in Tables 1) and 2). All formulation ingredients are based on 1 00 parts by weight of the monomer mixture.
- Table 1 summarizes the experiments in which the emulsifier Mersolat® H 95 from Lanxess GmbH was used.
- Mersolat® H 95 is the sodium salt of a mixture of long chain (C l 6 -C 18) alkyl sulfonates.
- Table 2 summarizes the tests in which a mixture of disproportionated rosin acid (Dresinate® 731/70% by Abieta) and fatty acid (Edenor® HTICl N from Oleo Chemicals / 1 2% in water) was used as the emulsifier , In addition, 0.6 parts by weight of potassium hydroxide were added to these experiments (Table 2). Due to the amount of potassium hydroxide, the mixture of resin and fatty acid was formally neutralized to 1 50%.
- Trimethylolpropane trimethacrylate (90%) from Aldrich; Product number: 24684-0 (Abbreviation: TMPTMA) Hydroxyethyl methacrylate (96%) of Acros; Product number: 1 5633001 0 (abbreviation: HEMA)
- NaSS Na styrenesulfonate
- Na 2 VP was obtained from H 2 VP by in situ neutralization with 2 equiv, NaOH.
- the weight refers to the sodium salt of vinylphosphonic acid (Na 2 VP)
- the weight 2- (methacryloyloxy) ethyl phosphate refers to the free acid (H 2 MOOEP); before initiation of the polymerization, H 2 MOOEP was added by addition of 2 equiv. KOH neutralized, so that in the reaction mixture the corresponding dipotassium salt was present (K 2 MOOEP)
- the quantity refers to the total amount of Mersolat®H 95 in the reaction mixture
- the quantity refers to the total amount of water in Christsansafz
- an activator solution was prepared from 0.56 g of p-menthane hydroperoxide (Trigonox NT 50 from Akzo-Degussa) in 50 g of water and the remaining amount of MersoSat K30 / 95 (2.1 g),
- the latexes of Table 1) and 2) were filtered and treated with stabilizer as in Example 2 of US 6399706, coagulated and dried.
- the gels were measured both in the latex state by ultracentrifugation (UZ) and by dynamic light scattering (DLS) in terms of particle diameter and as a solid with respect to the solubility in toluene (Geigehalt, swelling index / Ql) and by DSC
- the latices have a characteristic particle size distribution which is described by the diameter data d 10 , d 50 and d 80 These diameter data mean that in each case 10 % by weight ( C 1, 0), 50% by weight (D 50 ) and 80% by weight (D ⁇ 0 ) of the particles have a diameter which is smaller than the stated numerical value ,
- S particle diameter determined on latex obtained by dynamic light scattering (DLS).
- DLS dynamic light scattering
- Tg and ⁇ Tg the DSC-2 instrument from Perkin-Elmer was used.
- the sample is cooled with liquid nitrogen at 320 K / min, to -130 0 C and at a heating rate of 20 K / min , heated to 1 50 0 C.
- the second measurement cycle is again - 1 30 0 C cooled and heated at 20 K / min.
- Tg and ⁇ Tg are determined in the 2nd measuring cycle.
- the insoluble fraction Galgeh ⁇ St
- Ql swelling index
- 250 mg of the microgel were swollen in 25 ml Toiuol 24 hours with shaking at 23 ° C. After centrifugation at 20,000 rpm, the insoluble fraction is separated and dried.
- the swelling index Q1 is calculated from the weight of the solvent-containing microgel swollen in toluene at 23 ° C for 24 hours (after centrifugation at 20,000 rpm) and the weight of the dry microgel according to the following formula:
- the two gels containing hydroxy groups OBR 1327 B and OBR 1330 I were first with sulfuric acid (50 g gel in 250 ml sulfuric acid / 1 0%) or, with phosphoric acid (50 g Gei in 250 ml of phosphoric acid / l 0% ig 24h at 96 ° treated C, isolated by filtration, redispersed in water and washed until neutral with deionized water and dried at 6O 0 C.
- each of 1 0 g of the acid-treated gel in a 0.32 molar aqueous solution of copper sulfate (CuSO 4 * 5H 2 0 from Aldrich, article number 20,920-1) was dispersed with stirring for 24 h, after which the gels were filtered off and dried to constant weight at 60 ° C.
- the contents of selected metals were measured both before (original samples) and after treatment with acid / Copper solution determined by AES-ICP (see following table).
- the experiment is carried out in an apparatus with a water separator and passing over nitrogen.
- the percentages are area percentages in the GC.
- the experiment is carried out in an apparatus with water separator and under
- microgel OBR 1297 is hexanol swollen prior to the start at room temperature for 4 days anhydrous in 97.0 g 2-Ethyl From Multiple stirring, under a stream of nitrogen is heated up within 50 minutes at 150 0 C for 6 hours stirred at 1 50 0 C and passing nitrogen. An hourly small sample is taken for GC measurement. These samples are blank. After the reaction, the microgel is filtered off, extracted and dried in a vacuum oven at 80 0 C and 100 mbar to constant weight. The microgel is returned virtually quantitatively. The evolution of sales is documented in Table 2.
- the percentages are area percentages in the GC.
- the experiment is carried out in an apparatus with a water separator and passing over nitrogen, batch
- the percentages are area percentages in the GC.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Analytical Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Wood Science & Technology (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Polymerisation Methods In General (AREA)
Abstract
Die vorliegende Erfindung betrifft die Verwendung von durch Emulsionspolymerisation hergestellten Polymerteilchen mit einem mittleren Teilchendurchmesser im Bereich von 5 bis 500 nm, enthaltend oberflächenständige und/oder nicht-oberflächenständige ionogene Gruppen, als protonenliefernde und/oder protonenakzeptierende Substanz in heterogenen chemischen Prozessen, besonders geeignete Polymerteilchen für die Anwendung in solchen Prozessen sowie sie enthaltende Verbundmaterialien und Formkörper.
Description
VERWENDUNG VON PROTONENLIEFERNDEN UND/ODER
PROTONENAKZEPTIERENDEN POLYMERTEILCHEN BESCHREIBUNG:
Die vorliegende Erfindung betrifft die Verwendung von durch Emulsionspolymerisαtion hergestellten Polymerteilchen mit einem mittleren Teilchendurchmesser im Bereich von 5 bis 500 nm, enthaltend oberflachenstandige und/oder nicht-oberflachenstandige ionogene Gruppen, als protonenliefernde und/oder protonenakzeptierende Substanz in heterogenen chemischen Prozessen, besonders geeignete Polymerteilchen für die Anwendung in solchen Prozessen sowie sie enthaltende Verbundmaterialien und Formkorper.
Für viele heterogene Verfahren, d. h solchen Verfahren in denen mindestens eine Phasengrenze vorliegt, werden immobilisierte, unlösliche Protonenlieferanten bzw. Protonendonatoren oder Protonenakzeptoren benotigt. Die Verwendung immobilisierter Protonenlieferanten bzw. Protonendonatoren oder
Protonenakzeptoren bietet grundsätzliche Vorteile, wie eine erleichterte Abtrennung.
Für derartige Verfahren besteht allgemein der Bedarf nach neuen Protonenlieferanten bzw. Protonenakzeptoren mit neuem bzw. verändertem Eigenschaftsprofil.
Der Einsatz von Mikrogelen zur Eigenschaftssteuerung von Elastomeren oder Thermoplasten ist bekannt (WO2005/0331 85). Dabei sind zum Teil auch Mikrogele verwendet worden, die oberflächlich oder über den gesamten Querschnitt funktionelle Gruppen aufweisen.
Nicht bekannt war bislang der Einsatz von mit protonenliefernden oder protonenakzeptierenden Gruppen modifizierten Polymerteilchen im Nanogroßenbereich in heterogenen chemischen Prozessen, die einen immobilisierten Protonenspender oder Protonenakzeptor erfordern
Die vorliegende Erfindung betrifft die Verwendung von durch Emulsionspolymerisation hergestellten Polymerteilchen mit einem mittleren Teilchendurchmesser im Bereich von 5 bis 500 nm, enthaltend ionogene Gruppen als protonenhefernde und/oder protonenakzeptierende Substanz, in heterogenen chemischen Prozessen. Erfindungsgemaß eingeschlossen sind auch
Anwendungen, in denen die Polymerteilchen zunächst zumindest teilweise neutralisiert werden.
Der Einsatz besagter Poiymerteilchen bietet gegenüber klassischen Protonenspendern bzw. Protonenakzeptoren zahlreiche Vorteile, da die chemischen und physikalischen Eigenschaften der Polymerteilchen, wie Teilchengröße, Teiichenmorphologie, Queliverhalten, Katalyseaktivität, Härte, Formstabilität, Klebrigkeit, Alterungsbeständigkeit, Schlagzähigkeit einerseits durch den Herstellungsprozess, insbesondere durch das Polymerisationsverfahren, sowie durch Auswahl geeigneter Basismonomere und andererseits durch Auswahl geeigneter ionogener Gruppen deren Konzentration und Ansiedjungsbereich im Polymerteilchen in weiten Grenzen gezielt eingestellt bzw. maßgeschneidert werden können. Heterogene Prozesse bzw. Verfahren sind solche, in denen Phasengrenzen, wie insbesondere fest/flüssig und/oder fest/gasförmig beteiligt sind, wobei die Polymerteilchen naturgemäß der festen Phase zuzuordnen sind. Protonenliefernd bzw. protonenakzeptierend bedeutet erfindungsgemäß insbesondere, dass die Polymerteilchen Protonen an ein sie umgebendes Medium abgeben können bzw. aufnehmen können. In einer Matrix, insbesondere in einer Polymermatrix, vermögen die Polymerteilchen der Matrix eine Protonenleitfähigkeit zu verleihen.
Unter Emulsionspolymerisation im Sinne der Erfindung wird insbesondere ein an sich bekanntes Verfahren verstanden, bei dem als Reaktionsmedium Wasser verwendet wird, worin die verwendeten Monomere in Anwesenheit von Emulgatoren und radikalbildenden Substanzen unter Bildung von wässrigen Polymeriatices polymerisiert werden (s. u.a, Römpp Lexikon der Chemie, Band 2, 1 0. Auflage 1 997; P, A. Loveil, M. S. El-Aasser, Emulsion Poiymerization and Emulsion Polymers, John Wiley & Sons, ISBN: 0 471 96746 7; H. Gerrens, Fortschr. Hochpolym. Forsch . 1 , 234 ( 1 959)). Die Emulsionspolymerisation liefert im Unterschied zur Suspensions- oder Dispersionspolymerisation in der Regel feinere Teilchen, welche einen niedrigeren Partikelabsfand in einer Matrix ermöglichen. Die kleineren Teilchen liegen mit ihrem geringen mittleren Durchmesser unterhalb
der kritischen Fehlsteilengröße, d.h. die sie enthaltenden Matrices unterliegen nur geringen mechanischen Beeinträchtigungen, bei entsprechendem Dispersionsgrad. Teilchen einer Größe von unterhalb 500 nm sind durch Suspensions- oder Dispersionspolymerisation im Allgemeinen nicht zugänglich, weshaib diese Teilchen in der Regel für die Zwecke dieser Patentanmeldung ungeeignet sind.
Durch die Wahl der Monomere stellt man die Glastemperatur und die Breite des Glasübergangs der Polymerteilchen ein. Die Bestimmung der Glastemperatur (Tg) und der Breite des
Glasübergangs (ATg) der Mikrogele erfolgt mittels Differential- Scanning-Kalorimetrie (DSC), bevorzugt wie im Folgenden beschrieben. Dazu werden für die Bestimmung von Tg und ATg zwei Abkühl/Aufheiz-Zykien durchgeführt. Tg und ATg werden im zweiten Aufheiz-Zyklus bestimmt. Für die Bestimmungen werden etwa 1 0- 1 2 mg des ausgewählten Mikrogels in einem DSC-Probenbehälter (Standard-Aluminium-Pfanne) von Perkin-Elmer eingesetzt. Der erste DSC-Zyklus wird durchgeführt, indem die Probe zuerst mit flüssigem Stickstoff auf -1 000C abgekühlt und dann mit einer Geschwindigkeit von 20K/min auf + 1 500C aufgeheizt wird. Der zweite DSC-Zyklus wird durch sofortige Abkühlung der Probe begonnen, sobald eine Probentemperatur von + 1 500C erreicht ist. Die Abkühlung erfolgt mit einer Geschwindigkeit von ungefähr 320 K/min. Im zweiten Aufheizzyklus wird die Probe wie im ersten Zyklus noch einmal auf + 1 500C aufgeheizt. Die Aufheizgeschwindigkeit im zweiten Zyklus ist erneut 20K/min. Tg und ATg werden graphisch an der DSC-Kurve des zweiten Aufheizvorgangs bestimmt, Für diesen Zweck werden an die DSC-Kurve drei Geraden angelegt. Die 1 . Gerade wird am Kurventeil der DSC-Kurve unterhalb Tg, die 2. Gerade an dem durch Tg verlaufenden Kurvenast mit Wendepunkt und die 3. Gerade an dem Kurvenast der DSC- Kurve oberhalb Tg angelegt. Auf diese Weise werden drei Geraden mit zwei Schnittpunkten erhalten. Beide Schnittpunkte sind jeweils durch eine charakteristische Temperatur gekennzeichnet. Die Glastemperatur Tg erhält man als Mittelwert dieser beiden Temperaturen und die Breite des Glasübergangs ATg erhält man aus der Differenz der beiden Temperaturen.
Kαutschukαrtige Polymerteilchen weisen eine Giαstemperαtur von im Allgemeinen < 23°C auf. Thermoplastische Polymerteüchen weisen eine Glastemperatur im Allgemeinen eine Glastemperatur von > 23°C auf, Die Breite des Glasübergangs ist bei den erfindungsgemäß verwendeten Polymerteüchen bevorzugt größer als 5 0C, bevorzugter größer als 100C.
Kautschukartige Polymerteilchen sind bevorzugt solche auf Basis von konjugierten Dienen wie Butadien, Isopren, 2-Chlorbutadien und 2,3-Dichlorbutadien, sowie Ethen, Ester der Acryl- und
Methacrylsäure, Vinylacetat, Styrol oder Derivate davon, Acrylnitril, Acrylamide, Methacrylamide, Tetrafluorethylen, Vinylidenfluorid, Hexafluorpropen, doppelbindungshaltige Hydroxyverbindungen wie z. B. Hydroxyethylmethacrylat, Hydroxyethylacrylat, Hydroxypropylacrylat, Hydroxybutylmethacrylat, Acrolein oder Kombinationen davon.
Beispiele für geeignete Basismonomere sind insbesondere folgende Verbindungen :
Vinylcarbazoi, Aminfunktionalisierte (Meth)acrylate, N-Vinyl-2- pyrrolidinon, N-Allyl-Harnstoff, N-Allyl-Thiohamstoff, sekundäre Arnino- (meth)-acrylsäureester, wie 2-tert.-Butylaminoethylmethacrylat, 2- terf.-Butylaminoethylmethacrylamid, Dimethylaminopropylmethacrylarnid, 2-
Dimethylaminoethylmethacrylat, Vinyllmidazol, wie 1 -Vinylimidazol, Vinylpyridin, wie 2-Vinylpyridin und 4-Viπylpyridin, Acrylamid, 2- Acrylamidoglykolsäure, 2-Acryiamido-2-methyl- l -Propansulfonsäure, Acrylsäure-[2-(((butylamino)-carbonyl)-oxyl)ethylester], Acrylsäure-(2- diethylaminoethylester), Acryfsäure-(2-(dimethylamino)-ethylester), Acrylsäure-(3-(dimethylamino)-propylester), Acrylsäure-isopropylamid, Acrylsäurephenylamid, Acrylsäure-(3-suifopropy!ester) Kaliumsalz, Methacrylsäureamid, Mθthacrylsäure-2-aminoethylester-hydrochlorid, Methacrylsäure- (2-(tert.-butylamino)-ethylester, Methacryisäure-2- dimethylaminoj-methylester, Methacrylsäure-(3- dimethylaminopropylamid), Methacrylsäureisopropylamid,
Methαcrylsäure-(3-suifopropylester) Kαliumsαlz, 3-Vinylαπilin, 4- Vinylαnilin, N-Vinylcαprolαctαm, N-Vinylformαrnid, l -Vinyl-2-pyrrolidon, 5-Viny!urαcÜ.
Bevorzugte Monomere bzw. Moπomerkombinαtionen schiießen ein: Butadien, Isopren, Acrylnitril, Styrol, alpha-Methylstyrol,
Chloropren, 2, 3-Dichlorbutadien, Butyiacrylat,
2-Ethylhexylacrylat, Hydroxyethyimethacrylat, Tetrafluorethylen,
Vinylidenfluorid und Hexafluorpropen . „Auf Basis" bedeutet hier, dass die Polymerteilchen bevorzugt zu mehr als 60 Gew.-%, bevorzugt mehr als 70 Gew.-%, bevorzugter zu mehr als 90 Gew.-% aus den genannten Monomeren bestehen. Die Polymerteilchen können vernetzt oder unvernetzt sein. Im
Falle vernetzter Polymerteilchen spricht man auch von Mikrogelen . Die Polymerteilchen können insbesondere solche auf Basis von
Homopolymeren oder statistischen Copolymeren sein. Die Begriffe
Homopolymere und statistische Copolymere sind dem Fachmann bekannt und beispielsweise erläutert bei Vollmert, Polymer Chemistry,
Springer 1 973. Als Polymerbasis der kautschukartigen, vernetzten oder unvernetzten Pojymerteilchen, enthaltend ionogene Gruppen, können insbesondere dienen :
BR: Polybutadien,
ABR : Butadien/Acrylsäure-Cl -4Alkylestercopolymere, IR : Polyisopren,
SBR : statistische Styrol-Butadien-Copolymerisate mit
Styroigehalten von 1 -60, vorzugsweise 5-50 Gewichtsprozent,
FKM: Fluorkautschuk, ACM: Acrylatkautschuk,
NBR: Polybutadien-Acrylnitril-Copolymerisate mit
Acrylnitrilgehalten von 5-60, vorzugsweise 1 0- 60 Gewichtsprozent,
CR : Polychloropren EAM: Ethylen/Acrylatcopolymere,
EVM : Ethylen/Vinylacetatcopolymere.
Erfindungsgemäße nicht-kautschukartige, insbesondere thermoplastische Polymerteüchen weisen zweckmäßig eine Giasübergangstemperatur Tg von mehr als 23°C auf. Die Breite des Glasübergangs ist bei den thermoplastartigen Poiymerteilchen bevorzugt größer als 5 0C (wobei die Tg bzw. die Breite des Glasübergangs wie oben beschrieben bestimmt wird). Nicht- kautschukartige, insbesondere thermoplastische Polymerteilchen sind bevorzugt solche auf Basis von Methacrylaten, insbesondere Methylmethacrylat, Styrol oder Styroiderivaten, wie alpha-Methylstyrol, para-Methylstyrol, Acrylnitrü, Methacrylnitril, Vinylcarbazol oder Kombinationen davon . „Auf Basis" bedeutet hier, dass die Polymerteilchen bevorzugt zu mehr als 60 Gew.-%, bevorzugt mehr als 70 Gew.-%, bevorzugter zu mehr als 90 Gew.-% aus den genannten Monomeren bestehen, Bevorzugtere thermoplastische Polymerteilchen sind solche auf
Basis von Methacrylaten, insbesondere Methylmethacrylat, Styrol, alpha-Methylstyrol und Acrylnitrü .
Die Polymerteilchen weisen bevorzugt eine annähernd kugelförmige Geometrie auf. Die erfindungsgemäß verwendeten Polymerteilchen weisen einen mittleren Teilchendurchmesser im Bereich von 5 bis 500 nm, bevorzugt von 20 bis 400, besonders bevorzugt von 30 bis 300 nm auf. Der mittlere Teilchendurchmesser wird mittels Ultrazentrifugation mit dem wässrigen Latex der Polymerteilchen aus der Emulsionspolymerisation bestimmt. Die Methode liefert einen Mittelwert für den Teilchendurchmesser unter Berücksichtigung etwaiger Agglomerate. (H . G. Müller ( 1 99ό) Colloid Polymer Science 267 : 1 1 1 3-1 1 16 sowie W. Scholtan, H. Lange (1972) Kolloid-Z u. 2. Polymere 250: 782). Die Ultrazentrifugation hat den Vorteil, dass die gesamte Teilchengrößenverteilung charakterisiert wird und verschiedene Mittelwerte wie Zahienmittel, Gewichtsmittel aus der Verteilungskurve berechnet werden können.
Die erfindungsgemäß verwendeten mittleren Durchmesserangaben beziehen sich auf das Gewichtsmittei. Nachfolgend werden Durchmesserangaben wie dπ 0, d60 und d80 verwendet. Diese Angaben bedeuten dass 10, 50 bzw. 80 Gew. %
der Teilchen einen Durchmesser besitzen, der kleiner als der entsprechende Zahlenwert in Gew. % ist,
Die Durchmesserbestimmung mittels dynamischer Lichtstreuung führt in erster Näherung zu vergleichbaren mittleren Teilchendurchmessern. Sie wird ebenfalls am Latex durchgeführt. Üblich sind Laser, die bei 633 nm (rot) und bei 532 nm (grün) arbeiten. Bei der dynamischen Lichtstreuung wird nicht wie bei der Ultrazentrifugation die gesamte Teilchengrößenverteilung charakterisiert, sondern man erhält einen Mittelwert, bei dem große Teilchen überproportional gewichtet werden.
Die erfindungsgemäß verwendeten Polymerteilchen weisen bevorzugt einen gewichtsmittleren Teilchendurchmesser im Bereich von 5 bis 500 nm, bevorzugt von 20 bis 400, besonders bevorzugt von 30 bis 300 nm auf. Die Teilchen werden durch Emulsionspoiymerisation hergestellt, wobei durch Variation der Einsatzstoffe wie Emuigatorkonzentration, Iπitiatorkonzentration, Fiottenverhältnis von organischer zu wässriger Phase, Verhältnis von hydrophilen zu hydrophoben Monomeren, Menge an vernetzendem Monomer, Polymerisationstemperatur etc. die Teilchengröße in einem weiten Durchmesserbereich eingestellt wird.
Nach der Polymerisation werden die Latices durch Vakuumdestillation oder durch Behandlung mit überhitztem Wasserdampf behandelt, um flüchtige Komponenten insbesondere nicht umgesetzte Monomeren abzutrennen,
Die Aufarbeitung der so hergestellten Polymerteilchen kann beispielsweise durch Eindampfen, Elektrolyt-Koagulation, durch Co- koagulation mit einem weiteren Latexpolymer, durch Gefrierkoagulation (vgl. US-PS 21 87146) oder durch Sprühtrocknung erfolgen. Bei der Aufarbeitung durch Sprühtrocknung können auch handelsübliche Fließhilfsmittel wie beispielsweise CaCO3 oder Kieselsäure zugesetzt werden ,
Die erfindungsgemäß verwendeten durch Emulsionspolymerisation hergestellten Polymerteilchen sind in einer bevorzugten Ausführungsform mindestens teilweise vernetzt.
Die Vernetzung der durch Emulsionspolymerisαtion hergestellten Poiymerteüchen erfolgt bevorzugt durch den Zusatz von poiyfunktionellen Monomeren bei der Polymerisation, wie z.B. durch den Zusatz von Verbindungen mit mindestens zwei, vorzugsweise 2 bis 4 copolymerisierbaren C = C-Doppelblndungen, wie
Diisopropenyibenzol, Divinylbenzol, Divinylether, Divinylsulfon, Diallylphthalat, Triallylcyanurat, Triallylisocyanurat, 1 ,2-Polybutadien, N,N'-m-Pheny!enmaleimid, 2,4-Toluyienbis(maleimid), Triallyltrimellitat, Acrylate und Methacrylate von mehrwertigen, vorzugsweise 2- bis 4- wertigen C2 bis C l O Alkoholen, wie Ethylenglykol, Propandiol- 1 ,2, Butandiol, Hexandiol, Polyethylengiykol mit 2 bis 20, vorzugsweise 2 bis 8 Oxyethyleneinheiten, Neopentylglykol, Bisphenol-A, Glycerin, Trimethylolpropan, Pentaerythrit, Sorbit sowie ungesättigten Polyestern aus aiiphatischen Di- und Polyolen und Maleinsäure, Fumarsäure, und/oder itaconsäure.
Die Vernetzung der Poiymerteüchen kann direkt während der Emulsionspoiymerisation, wie durch Copolymerisation mit vernetzend wirkenden multifunktionellen Verbindungen oder durch anschließende Vernetzung wie untenstehend beschrieben erreicht werden. Die direkte Vernetzung während der Emuisionspoiymerisation ist bevorzugt. Bevorzugte multifunktionelle Comonomere sind Verbindungen mit mindestens zwei, vorzugsweise 2 bis 4 copolymerisierbaren C = C-Doppelbindungen, wie Diisopropenyibenzol, Divinylbenzol, Divinyiether, Divinylsulfon, Diallylphthaiat, Triallylcyanurat, Triallylisocyanurat, 1 ,2-Polybutadien, N,N'-m-Phenylenmaleimid, 2,4-Toluylenbis(ma!eimid) und/oder Triallyltrimellitat. Darüber hinaus kommen in Betracht die Acrylate und Methacrylate von mehrwertigen, vorzugsweise 2- bis 4-wertigen C2 bis Cl O Alkoholen, wie Ethylenglykol, Propandiol- 1 ,2, Butandiol, Hexandiol, Polyethylengiykol mit 2 bis 20, vorzugsweise 2 bis 8 Oxyethyleneinheiten, Neopentylglykol, Bisphenol-A, Glycerin, Trimethylolpropan, Pentaerythrit, Sorbit mit ungesättigten Polyestern aus aiiphatischen Di- und Polyolen sowie Maleinsäure, Fumarsäure, und/oder Itaconsäure. Die Vernetzung während der Emulsionspolymerisation kann auch durch Fortführung der Polymerisation bis zu hohen Umsätzen
oder im Moπomerzulαufverfαhren durch Polymerisation mit hohen internen Umsätzen erfolgen. Eine andere Möglichkeit besteht auch in der Durchführung der Emulsionspolymerisation in Abwesenheit von Reglern. Für die Vernetzung der unvernetzten oder der schwach vernetzten Polymerteilchen im Anschluß an die
Emulsionspolymerisation setzt man am besten die Latices ein, die bei der Emulsionspolymerisation erhalten werden.
Geeignete, vernetzend wirkende Chemikalien sind beispielsweise organische Peroxide, wie Dicumylperoxid, t- Butyicumylperoxid, Bis-(t-butyl-peroxy-isopropyl)benzol, Di-t- butylperoxid, 2,5-Ditmethylhexan-2,5-dihydroperoxid, 2,5- Dimethylhexin-3,2,5-dihydroper-oxid, Dibenzoyi-peroxid, Bis- (2,4- dichlorobenzoyljperoxid, t-Butylperbenzoat sowie organische Azoverbindungen, wie Azo-bis-isobutyronitril und Azo-bis- cyclohexannitril sowie Di- und Polymercaptoverbiπdungen, wie Dimercaptoethan, 1 ,6-Dimercaptohexan, 1 ,3,5-Triιmercaptotriazin und Mercapto-terminierte Polysulfidkautschuke wie Mercapto- terminierte Umsetzungsprodukte von Bis-Chlorethyiformal mit Natriumpolysulfid.
Die optimale Temperatur zur Durchführung der Nachvernetzung ist naturgemäß von der Reaktivität des Vernetzers abhängig und kann bei Temperaturen von Raumtemperatur bis ca , 1 80 0C gegebenenfalls unter erhöhtem Druck durchgeführt werden (siehe hierzu Houben-Weyl, Methoden der organischen Chemie, 4, Auflage, Band 14/2, Seite 848) . Besonders bevorzugte Vernetzungsmittel sind Peroxide.
Die Vernetzung C = C-Doppelbindungen enthaltender Kautschuke zu Mikrogelen kann auch in Dispersion bzw. Emulsion bei gleichzeitiger, partieller, ggf. vollständiger, Hydrierung der C = C Doppelbindung durch Hydrazin wie in US 5,302,696 oder US 5,442,009 beschrieben oder ggf. andere Hydrierungsmitteln, beispielsweise Organometallhydridkomplexe erfolgen.
Vor, während oder nach der Nachvernetzung kann ggf. eine Teilchenvergrößerung durch Agglomeration durchgeführt werden.
Die erfindungsgemäß eingesetzten vernetzten Polymerteiichen weisen zweckmäßig in Toluoi bei 23°C unlösliche Anteile (Gelgehalt) von mindestens etwa 70 Gew.-%, bevorzugter mindestens etwa 80 Gew.-%, noch bevorzugter mindestens etwa 90 Gew.-% auf. Der in Toluoi unlösliche Anteil wird dabei in Toluoi bei 23° bestimmt. Hierbei werden 250 mg der Polymerteüchen in 25 ml Toluoi 24 Stunden unter Schütteln bei 23°C gequollen. Nach Zeπtrifugation mit 20.000 Upm wird der unlösliche Anteil abgetrennt und getrocknet. Der Gelgehalt ergibt sich aus dem Quotienten des getrockneten Rückstandes und der Einwaage und wird in Gewichtsprozent angegeben.
Die erfiπdungsgemäß eingesetzten vernetzten Polymerteilchen weisen weiterhin zweckmäßig in Toluoi bei 230C einen Quellungsindex von weniger als etwa 80, bevorzugter von weniger als 60 noch bevorzugter von weniger als 40 auf. So können die Quellungsindizes der Polymerteilchen (Qi) besonders bevorzugt zwischen 1 - 1 5 und 1 - 1 0 liegen. Der Quellungsindex wird aus dem Gewicht der in Toluoi bei 23° für 24 Stunden gequollenen iösungsmittelhaltigen Polymerteilchen (nach Zentrifugation mit 20.000 Upm) und dem Gewicht der trockenen Polymerteilchen berechnet:
Qi = Naßgewicht der Polymerteilchen / Trockengewicht der Polymerteiichen.
Zur Ermittlung des Quellungsindex läßt man 250 mg der Polymerteilchen in 25 ml Toluoi 24 h unter Schütteln quellen. Das Gel wird abzentrifugiert und gewogen und anschließend bei 70 0C bis zur Gewichtskonstanz getrocknet und nochmals gewogen.
Die erfindungsgemäß verwendeten Polymerteilchen enthalten ionogene Gruppen, lonogene Gruppen sind erfindungsgemäß solche Gruppe, die ionisch sind oder zur Bildung ionischer Gruppen befähigt sind, Sie vermögen auf diese Weise protonenliefernd und/oder protonenakzeptierend zu sein.
In einer bevorzugten Ausführuπgsform werden die ionogenen Gruppen ausgewählt aus einer oder mehreren der folgenden funktionellen Gruppen : -COOH, -SO3H, -OSO3H,
-P(O)(OH)2, -O-P(OH)2 und -Q-P(O)(OH)2 und/oder deren Salzen
und/oder deren Derivate, wie insbesondere Partialester davon. Die Salze stellen die konjugierten Basen zu den sauren funktionellen Gruppen dar, also -COO", -SO3 ", -OSO3-, -P(O)2(OH)- oder -P(O)3 3", -0-P(O)2 2 und -OP(O)2(OH)- oder -OP(O)3 2" in der Form ihrer Metall-, bevorzugt Alkalimetall- oder Ammoniumsalze.
Erfindungsgemäß besonders bevorzugte ionogene Gruppen im Sinne der Erfindung werden ausgewählt aus -SO3H, -PO(OH)2, -O- P(O)(OH)2 und/oder deren Salzen und/oder deren Derivate, wie insbesondere Partialester davon.
Die ionogenen Gruppen können je nach Herstellweise oberflächenständig und/oder nicht-oberflächenständig sein.
Die ionogenen Gruppen können durch Einpoiymerisation entsprechend funktionalisierter Monomere und/oder durch Modifikation nach der Polymerisation in die Polymerteüchen eingebracht werden.
Funktionalisierte Monomere werden beispielsweise aus der Gruppe ausgewählt, die besteht aus: Acrylsäure, Methacrylsäure, Vinylbenzoesäure, Itakonsäure, Maleinsäure, Fumarsäure, Crotonsäure, Vinylsulfonsäure, Styrolsulfonsäure, Phosponsäure- oder Phosphorsäuregruppen-enthaltenden Monomeren mit polymerisierbaren C = C-Doppelbindungen, wie Vinylphosphonsäure, 2-Phosphonomethyl-acrylsäure und 2-Phosphonomethyl- acrylsäureamid, Phosphonsäure- oder Phosphorsäureester von hydroxyfunktionellen, polymeπsierbare C = C-Doppelbindungen- aufweisenden Monomeren oder Salzen oder Derivaten davon .
Phosphorsäureester von hydroxyfunktionellen polymerisierbare C = C-Doppelbindungen-aufwetsenden Monomeren weisen bevorzugt die folgenden Formeln (I) oder (II) der folgenden Methacrylat- Verbindungen auf:
worin R eine zweiwertige organische Gruppe, wie insbesondere C l bis Cl O-Aikylen ist. Bevorzugt ist R eine C2-C4 Alkylengruppe (d. h., eine C2-C4-Alkandiylgruppe), wie Methylen, Ethylen oder n-Propylen. Auch Saize dieser Verbindungen sind anwendbar, wie insbesondere Alkalimetallsalze bevorzugt das Natriumsalz oder Ammoniumsalze. Auch die entsprechenden Acrylate sind einsetzbar. Weiterhin können Partialester mit anderen gesättigten oder ungesättigten Carbonsäuren dieser Verbindungen verwendet werden . Der Begriff der Partialester schließt erfindungsgemäß sowohl den Fall ein, dass ein Teil der sauren Hydroxylgruppen der ionogenen Gruppe teilweise verestert ist, als auch den Fall, worin in den Polymerteilchen ein Teil der Hydroxylgruppen verestert ist, ein anderer Teil nicht verestert ist. Der Anteil der einpolymerisierten ionogene Gruppen aufweisenden funktionellen Monomeren beträgt bevorzugt von 0, 1 bis 1 00 Gew. %, bevorzugter 0, 2 bis 99,5 Gew.-% bezogen auf die Gesamtmenge der Monomere. Dies bedeutet, dass auch Homopolymer dieser ionogene Gruppen tragenden Monomere eingesetzt werden können. Beispielsweise können mindestens 1 0
Gew.-%, mindestens 20 Gew.-% oder mindestens 30 Gew.-% dieser Monomere vorliegen.
Die ionogenen Gruppen -OSO3H und -OP(O)(OH)2 können beispielsweise auch durch Umsetzung von hydroxylmodifizierten Polymerteiichen (wie durch Eiπpolymerisation von
Hydroxya!kyl(meth)acrylaten erhaltene) oder durch Addition von Schwefel- bzw. Phosphorsäure an epxidhaltige (beispielsweise glycidylmethacrylathaltige) Polymerteilchen mit Schwefelsäure oder Phosphorsäure, durch Addition von Schwefelsäure oder
Phosphorsäure an doppelbindungshaltige Polymerteilchen, durch Zersetzung von Persulfaten oder Perphosphaten in Gegenwart von doppelbindungshaltigen Polymerteilchen, sowie durch Umesterung nach der Polymerisation in die Polymerteilchen eingebracht werden. Weiterhin können die Gruppen -SO3H und
-P(O)(OH)2 auch durch Sulfonierung bzw. Phosphonierung von aromatischen Vinylpolymeren eingebracht werden, lonogene Gruppen können weiterhin auch durch Umsetzung hydroxylmodifizierter Polymeτteilchen mit entsprechend funktionalisierten Epoxiden hergestellt werden.
Neben den genannten ionogenen Gruppen können weitere funktionelle Gruppen zur Steuerung der Eigenschaften insbesondere in die Oberfläche der Polymerteilchen eingebracht werden, wie durch chemische Umsetzung der bereits vernetzten Polymerteilchen mit gegenüber C = C-Doppelbindungen reaktiven Chemikalien. Diese reaktiven Chemikalien sind insbesondere solche Verbindungen, mit deren Hilfe polare Gruppen wie z. B. Aldehyd-, Hydroxyk Carboxyl-, Nitril- etc. sowie schwefelhaltige Gruppen, wie z.B. Mercapto-, Dithiocarbamat-, Polysulfid-, Xanthogenat- und/oder Dithiophosphorsäuregruppen und/oder ungesättigte
Dicarbonsäuregruppen an die Polymerteilchen chemisch gebunden werden können . Ziel der Modifizierung ist insbesondere die Verbesserung der Verträglichkeit mit einem Matrixpolymer, in das die Polymerteiichen gegebenenfalls eingearbeitet werden, um beispielsweise eine gute Verteilbarkeit bei der Herstellung sowie eine gute Ankopplung zu erreichen.
Besonders bevorzugte Methoden der Modifizierung sind die Pfropfung der Poiymerteilchen mit funktionellen Monomeren sowie die Umsetzung mit niedermolekularen Agentien. Auf diese Weise können gegebenenfalls auch die ionogenen, protonenspendenden oder protonenakzeptierenden Monomere in die Polymerteilchen eingebracht werden.
Für die Pfropfung der Polymerteilchen mit funktionellen Monomeren geht man zweckmäßigerweise von der wässrigen Mikrogeldispersion aus, die man mit polaren Monomeren wie Viπylsulfonsäure, Styrolsulfonsäure, Acrylsäure, Methacrylsäure,
Itαkonsäure, Hydroxyethyl-(meth)-acrylat (Der Ausdruck „(Meth)acrylat" schließt in vorliegender Anmeldung sowohl Methacrylat als auch Acrylat ein), Hydroxypropy!-(meth}-acrylat, Hydroxybutyl-(meth)- acrylat, Acryinitril, Acrylamid, Methacrylamid, Acrolein, Phosponsäure- oder Phosphorsäuregruppen-enthaltenden
Monomeren mit polymerisierbaren C = C-Doppelbindungen, wie Viπylphosphonsäure, 2-Phosphonomethyl-acrylsäure und 2- Phosphonomethyl-acrylsäureamid, Phosphonsäure- oder Phosphorsäureester von hydroxyfunktionellen, polymerisierbare C = C- Doppeibindungen-aufweisenden Monomeren oder Salzen oder Derivaten, wie insbesondere Partialester davon unter den Bedingungen einer radikalischen Emulsionspolymerisation umsetzt. Auf diese Weise werden Polymerteilchen mit einer Kern/Schale- Morphologie erhalten . Es ist wünschenswert, daß das im Modifi- kationsschritt verwendete Monomer möglichst quantitativ auf das unmodifizierte Polymerteilchen bzw. Mikrogel aufpfropft. Zweckmäßigerweise werden die funktionellen Monomere vor der vollständigen Vernetzung der Mikrogele hinzudosiert. Auch eine Modifikation doppelbindungshaltiger Polymerteilchen, wie z.B. durch Ozonoiyse kommt in Frage.
In einer bevorzugten Ausführungsform sind die Polymerteilchen, insbesondere die Mikrogele durch Hydroxyl-Gruppen insbesondere auch an der Oberfläche davon modifiziert. Der Hydroxylgruppengehalt der Polymerteilchen, insbesondere der Mikrogele wird durch Umsetzung mit Acetanhydrid und Titration der hierbei frei werdenden Essigsäure mit KOH nach DIN 53240 als Hydroxyl-Zahi mit der Dimension mg KOH/g Polymer bestimmt. Die Hydroxylzahl der Polymerteilchen, insbesondere der Mikrogele liegt bevorzugt zwischen OJ - 1 00, noch bevorzugter zwischen 0,5-50 mg KOH/g Polymer.
Die Menge des eingesetzten Modifizierungsmittels richtet sich nach dessen Wirksamkeit und den im Einzelfall gestellten Anforderungen und liegt im Bereich von 0,05 bis 30 Gewichtsprozent, bezogen auf die Gesamtmenge an eingesetzten Polymerteilchen, insbesondere Mikrogel, besonders bevorzugt sind 0,5- 10
Gewichtsprozent bezogen auf Gesamtmenge an Polymerteilchen, insbesondere Mikrogel .
Die Modifizierungsreaktionen können bei Temperaturen von 0- 1 80 0C, bevorzugt 20-95 0C, ggf. unter Druck von 1 -30 bar, durchgeführt werden, Die Modifizierungen können an Kautschuk- Mikrogelen in Substanz oder in Form ihrer Dispersion vorgenommen werden, wobei beim letzten Fall inerte organische Lösungsmittel oder auch Wasser als Reaktionsmedium verwendet werden können . Besonders bevorzugt wird die Modifizierung in wäßriger Dispersion des vernetzten Kautschuks durchgeführt.
Die Polymerteilchen, deren Herstellung wie vorstehend beschrieben erfolgen kann, eignen sich beispielsweise als Katalysator in säurekataiysierten Reaktionen, wie die Oligomerisierung von Isobuten, die säurekatalysierte Herstellung von Bisphenol A, Veresterungsreaktionen, Friedel-Crafts-
Acyiierungen und -Aikylierungen oder Dehydratisierungsreaktionen, als stationäre Phase in Säulen und Platten für Trennoperationen, insbesondere aufgrund ihrer potentielle Protoπenleitfähigkeit zum Einsatz in elektrochemischen Verfahren, zum Einsatz in lonenabsorptionsverfahren, insbesondere aufgrund ihrer protonenspendenden Brönstedtsäuren als Antifouling-Wirkstoffe in Formkörpern oder Beschichtungen, Beschichtungsmitteln, Anstrichmitteln, in Funktionsbekleidung bzw. in darin enthaltenen Fasern, als antimikrobielle Bestandteile in medizinischen Anwendungen, allgemein eingebettet in Polymermatrices, wie in der Form von Formkörpern, wie Folien oder Membranen, wie für Brennstoffzellen (s. DE-A- I 02004009396), - in deprotonierter Form als Hydrolyseschutzmittel in
Polymermatrices, sämtlich in heterogenen Prozessen bzw. Verfahren an denen Phasengrenzen, insbesondere fest/flüssig, fest/gasförmig beteiligt sind. In den Polymermatrices, wie in der Form von Formkörpern,
Membranen, Folien etc. können die erfindungsgemäß verwendeten
Polyrrserteilchen in einem Anteil von Mσtrixpolymer zu Polymerteilchen von 1 ; 99 bis 99 : 1 , bevorzugt von 1 0 : 90 bis 90 : 1 0, besonders bevorzugt 20 : 80 bis 80 : 20 enthalten sein. Die Menge der erfindungsgemäß verwendeten Polymerteilchen hängt von den gewünschten Eigenschaften der Formkόrper, wie beispielsweise Protonenleitfähigkeit der Membranen ab.
Geeignete Matrixpolymere sind beispielsweise thermoplastische Polymere wie Standard-Thermoplaste, sogenannte Techno- Thermoplaste und sogenannte Hochieistungs-Thermoplaste (Vgl. H, G. Elias Makromoleküle Band 2, 5 Aufl., Hüthig & Wepf Verlag , 1 992, Seite 443 ff), wie zum Beispiel bei Polypropylen, Polyethylen, wie HDPE, LDPE, LLDPE, Polystyrol etc. und polare thermoplastische Werkstoffe, wie PU, PC, EVM, PVA, PVAC, Polyvinylbutyral, PET, PBT, POM, PMMA, PVC, ABS, AES, SAN, PTFE, CTFE, PVF, PVDF, Polyimide, PA, wie insbesondere PA-ό (Nylon), bevorzugter PA- 4, PA-66 (Perlon), PA- 69, PA-61 0, PA- I 1 , PA- I 2, PA 61 2, PA-MXD6 etc. Das Gewichtsverhältnis dieser Matrixpolymere zu den Polymerteilchen kann zweckmäßig von 1 : 99 bis 99 ; 1 , bevorzugt von 10 : 90 bis 90 : 1 0, besonders bevorzugt 20 : 80 bis 80 : 20 betragen. Bevorzugtes Matrixpolymer für die Anwendung in Polyelektrolytmembranen, insbesondere für Brennstoffzellen ist Polybenzimidazol (z. B. US 4460763).
Die Erfindung betrifft weiterhin neue Polymerteilcheπ mit einem mittleren Teilchendurchmesser im Bereich von 5 bis 500 nm (bestimmt mittels Ultrazentrifugation wie zuvor dargelegt), erhalten durch Emulsionspolymerisation, enthaltend ionogene Gruppen, ausgewählt aus der Gruppe, die besteht aus: -SO3H, -OSO3H, -P(O)(OH)2, -0-P(OH)2 und -0-P(O)(OH)2 und/oder deren Salze und/oder Derivate davon. Bevorzugt sind -SO3H, -OSO3H, -P(O)(OH)2, -0-P(O)(OH)2 und/oder deren Salze und/oder deren Derivate, wie insbesondere Ester, wie Partialester.
Der Anteil der genannten ionogenen Gruppen in den Polymerteilchen liegt bevorzugt im Bereich von 0, 1 bis 95 Gew.-%, bevorzugter 1 bis 90 Gew.-% bezogen auf die Gesamtmenge der Polymerteilchen.
Geeignete Salze der Polymerteilchen schließen Metall- oder Ammoniumsaize, insbesondere Alkalimetailsalze, Erdalkalimetallsalze etc, ein.
Geeignete Derivate der Polymerteilchen schließen insbesondere Ester- und Partialester der genannten ionogenen Gruppen ein.
Die Erfindung ist hinsichtlich der Anwendungen dieser neuen Polymerteilchen nicht beschränkt, und sie können in sämtlichen vorstehend bereits beschriebenen Anwendungen verwendet werden. Die Erfindung betrifft insbesondere jedoch neue Verbundmaterialien der vorstehend genannten Polymerteilchen, worin diese auf mindestens ein TrägermateriaS aufgezogen bzw. darin inkorporiert sind. Derartige Trägermaterialien schließen anorganische und organische Materialien ein, beispielsweise: Ruß, Siiiciumdioxid, Calciumcarbonat, Calciumoxid, Magnesiumoxid, Aiuminiumoxid, Bariumsulfat, Zeolithe, lonenaustauschharze, Fasern, insbesondere Polymerfasern etc.
Die neuen Polymerteilchen können aber auch in reiner Form beispielsweise in lonenaustauschverfahren oder katalytischen Verfahren angewendet werden.
Die Erfindung betrifft weiterhin neue Formkörper, wie insbesondere Folien, in denen die vorstehend genannten Polymerteilchen insbesondere in einer Polymermatrix enthalten sind. In den Polymermatrices, wie in der Form von Formkörpern, Membranen, Folien etc, können die erfindungsgemäß verwendeten Polymerteilchen in einem Anteil von Matrixpolymer zu Polymerteilchen 1 : 99 bis 99 : 1 , bevorzugt von 1 0 : 90 bis
90 : 1 0, besonders bevorzugt 20 : 80 bis 80 : 20 enthalten sein. Zur Erreichung bestimmter Eigenschaften der Formkörper, wie Protonenleitfähigkeit kann ein bestimmter Anteil, wie beispielsweise mindestens 30 Gew.-% oder mindestens 40 Gew.-% auch überschritten werden, solange die mechanischen Eigenschaften des Formkörpers dies zulassen. Hinsichtlich der bevorzugten Matrixpolymere kann auf die vorstehenden Ausführungen verwiesen werden.
BEISPIELE:
Hersteilungsbeispiele für die Mikrogele
Nachfolgend wird die Herstellung der Mikrogele beschrieben, die in den weiteren Beispielen verwendet werden.
Sämtliche Mikrogele wurden durch Emulsionspolymerisation hergestellt. Die für die Herstellung der Mikrogele verwendeten Moπomerkombinationen sowie wesentliche Rezepturbestandteiie sind in den Tabellen 1 ) und 2) zusammengefasst. Sämtliche Rezepturbestandteile werden auf 1 00 Gew. -Teile der Monomermischung bezogen.
In Tabelle 1 ) sind die Versuche zusammengefasst, bei denen als Emulgator Mersolat® H 95 der Lanxess Deutschland GmbH verwendet wurde. Mersolat® H 95 ist das Natriumsalz einer Mischung langkettiger (C l 6-C l 8) Alkylsulfonate.
In Tabelle 2) sind die Versuche zusammengefasst, bei denen als Emulgator eine Mischung aus disproportionierter Harzsäure (Dresinate® 731 /70%ig von Abieta) und Fettsäure (Edenor® HTICl N der Firma Oleo Chemicals / 1 2%ig in Wasser) verwendet wurde. Bei diesen Versuchen wurde außerdem 0,6 Gew. -Teile Kaliumhydroxid zugesetzt (Tabelle 2). Durch die Kaliumhydroxidmenge wurde die Mischung an Harz- und Fettsäure formal zu 1 50 % neutralisiert.
Für die Herstellung der in den Tabellen 1 ) und 2) aufgeführten Mikrogele wurden folgende Monomeren verwendet:
Styrol (98%ig) von KMF Labor Chemie Handels GmbH
Butadien (99%ig, entstabilisiert) der Lanxess Deutschland GmbH
Trimethylolpropantrimethacrylat (90%ig) von Aldrich; Produktnummer: 24684-0 (Abkürzung: TMPTMA)
Hydroxyethylmethαcrylαt (96%) von Acros; Produktnummer: 1 5633001 0 (Abkürzung : HEMA)
Nα-Vinylsulfonαt; 30%ige wässrige Lösung von Fiuka; Produktnummer: 95061 (Abkürzung: NaVS)
Na-Styrolsulfonat (90%) von Fluka; Produktnummer: 94904 (Abkürzung : NaSS)
Vinylphosphonsäure (95%) von Fluka, Produktnummer: 95014 (Abkürzung: H2VP)
2-(Methacryloy!oxy)ethyl Phosphat von Aldrich, Produktnummer: 463337 (Abkürzung: H2MOOEP)
Tabelle 1 ) Mikrogelrezepturen auf Basis des Emulgators Mersoiat K30/95
K*
1 ) Na2VP wurde aus H2VP durch in-situ Neutralisation mit 2 equ, NaOH erhalten . Die Gewichtsangabe bezieht sich auf das Natriumsalz der Vinylphosphonsäure (Na2VP)
2) Die Gewichtsangabe 2-(Methacryloyioxy)ethyl Phosphat bezieht sich auf die freie Säure (H2MOOEP); vor der Initiierung der Polymerisation wurde H2MOOEP durch Zugabe von 2 equ . KOH neutralisiert, so dass im Reaktionsansatz das entsprechende Dikaliumsalz vorlag (K2MOOEP)
3) Die Mengenangabe bezieht sich auf die Gesamtmenge an Mersolat®H 95 im Reaktionsansatz
4) Die Mengenangabe bezieht sich auf die Gesamtmenge an Wasser im Reaktionsansafz
2) Mikrogelrezepturen auf Basis eines Emulgatorsysteims aus Harzsäure/Fettsäure
Mengenangabe fü r 1 00%iges Material
Die Produkte OBR 1290-2, OBR 1290-4, OBR 1293-1, OBR 1291-1, OBR 1297, OBR 1294-1 und OBR 1438-1 (Tabelle 1) wurden in einem 61- Glasreaktor mit Rührwerk hergestellt, während die Produkte OBR 1361- B, OBR 1435-4, OBR 1327 B und OBR 1330 I (Tabelle 1 und Tabelle 2) in einem 20-i-StaNautoklaven mit Rührwerk hergestellt wurden.
Bei der Durchführung der Emulsioπspolymerisationen im Glasreaktor wurden jeweils 3,93 kg Wasser vorgelegt und mit einem Stickstoffstrom gespült. In die Wasservorlage wurde ein Teil der gesamten Mersolatmenge zugegeben und gelöst. Bei Versuch OBR 1290-2 wurden 5,3 g Mersolat® H 95; bei OBR 1291-1 13,7 g Mersolat® H 95; bei OBR 1293-1, OBR 1297, OBR 1294-1, OBR 1361 -B und OBR 1438-1 wurden 24,2 g Mersolat® H 95 sowie bei OBR 1290-4 wurden 40,0 g Mersolat® H 95 in das Wasser gegeben und gelöst, Danach wurden 1000 g der in Tabelle 1) aufgeführten Monomermischungen zusammen mit 0,08 g 4-Methoxyphenol (Arcos Organics, Artikel-Nr. 126001000, 99 %) in das Reakiionsgefäß gegeben. Nach Aufheizung der Reaktioπsmischung auf 30-400C wurde eine frisch hergestellte 4%ige wässrige Prämixlösung zugegeben. Diese Prämixlόsung bestand aus:
0,169 g Ethylendiamintetraessigsäure (Fluka, Artikelnummer 03620), 0,135 g Eisen(ll)-sulfat*7H20 (Riedel de Haen, Artikelnummer. 12354), (ohne Kristallwasser berechnet) 0,347 g Rongalit C, Na-Formaldehydsulfoxylat-2-hydrat (Merck- Schuchardt, Artikelnummer 8,06455) (ohne Kristallwasser berechnet) sowie
0,524 g Trinatriumphosphat*! 2H2O (Acros, Artikelnummer 206520010) (ohne Kristallwasser berechnet) zudosiert.
Für die Aktivierung der Polymerisation wurde eine Aktivatorlösung aus 0,56 g p-Menthanhydroperoxid (Trigonox NT 50 der Akzo-Degussa) in 50 g Wasser und der Restmenge an MersoSat K30/95 (2,1 g) hergestellt,
Die Hälfte der wässrigen Aktivatorlösung wurde 5 Min. nach Zusatz der Prämixlösung in das Reaktionsgefäß gegeben. Hierdurch wurde die
Polymerisation gestartet. Nach 2,5 Stunden Reaktionszeit wurde die Reaktionstemperatur auf 40-50 0C erhöht, Nach einer weiteren Stunde wurde die zweite Hälfte der wässrigen Aktivatorlösung zugesetzt. Bei Erreichen eines Poiymerisationsumsatzes >90 % (üblicherweise: 95% - 100%) wurde die Polymerisation durch Zugabe einer wässrigen Lösung von 2,35 g Diethylhydroxylamin (DEHA, Aldrich, Artikelnummer 03620) abgestoppt.
Die Versuche OBR 1 361 -B. OBR 1 327 B und OBR 1 330 I wurden in analoger Weise in einem 20 Liter-Autoklaven mit Rührwerk durchgeführt. Bei den Autoklavenaπsätzen wurden jeweils 3,5 kg der
Monomermischung und eine Gesamtwassermenge von 1 4 kg verwendet. Die weitere Durchführung der Versuche erfolgte in analoger Weise wie bei den im Giasreaktor durchgeführten Versuchen beschrieben.
Nach dem Abstoppen der Polymerisationsreaktionen wurden nicht umgesetzte Monomere und flüchtige Bestandteile durch Strippen mit Wasserdampf aus dem Latex entfernt.
Die Latices der Tabelle 1 ) und 2) wurden filtriert und wie im Beispiel 2 der US 6399706 mit Stabilisator versetzt, koaguliert und getrocknet.
Die Gele wurden sowohl im Latexzustand mittels Ultrazentrifugation (UZ) und durch dynamische Lichtstreuung (DLS) bezüglich Teilchendurchmesser sowie als Feststoff bezüglich der Löslichkeit in Toluol (Geigehalt, Quellungsindex / Ql) und mittels DSC
(Glastemperatur/Tg und Breite der Tg-Stufe) charakterisiert.
Charakteristische Daten der in den Tabellen 1 ) und 2) beschriebenen Mikrogele sind in Tabelle 3) zusammengestellt.
Tabelle 3) Charakteristische Daten der Mikrogele (aus den Tabellen 1 und 2)
In Tabelle 3) bedeuten:
Cl1 0, d50 und d30 : Di© Teilchendurchmesser wurden am abgestoppten und mit Wasserdampf gestrippten Latex mittels Ultrazentrifugation bestimmt (W. Scholtan, H . Lange,
„Bestimmung der Teilchengrößenverteilung von Latices mit der Ultrazentrifuge", Kolloid-Zeitschrift und Zeitschrift für Polymere ( 1 972) Band 250, Heft, 8), Die Latices haben eine charakteristische Teüchengrößenverteiiung die durch die Durchmesserangaben d10, d50 und d80 beschrieben wird. Diese Durchmesserangaben bedeuten, dass jeweils 1 0 Gew. % (cl, o), 50 Gew.-% (d50) und 80 Gew.-% (dβ0) der Teilchen einen Durchmesser besitzen, der kleiner als der angegebene Zahlenwert ist, Die Teilchengröße der Mikrogele im Latex und in den aus dem Latex isolierten
Festprodukten wie sie in den erfindungsgemάßen Zusammensetzungen eingesetzt werden, sind praktisch identisch .
dd|S: am Latex bestimmter Teilchendurchmesser, der mittels dynamischer Lichtstreuung (DLS) erhalten wurde . Für die Bestimmung wurde ein Zetasizer® Nano Instrument (Modellnummer: Nano ZS) von Malvern Instruments Ltd. , Worcestershire, England verwendet. Mittels dynamischer Lichtstreuung wird ein mittlerer Teilchendurchmesser erhalten.
Tg: Glastemperatur
ΔTg : Breite der Tg-Stufe
Für die Bestimmung von Tg und ΔTg wurde das Gerät DSC-2 von Perkin-Elmer benutzt, Im ersten Messzyklus wird die Probe mit flüssigem Stickstoff mit 320 K/min , auf - 1 300C abgekühlt und mit einer Heizrate von 20 K/min, auf 1 500C aufgeheizt. Im zweiten Messzyklus wird wiederum auf - 1 300C gekühlt und mit 20 K/min , aufgeheizt. Tg und ΔTg werden im 2. Messzyklus bestimmt.
Zur Bestimmung des unlöslichen Anteils (GelgehαSt) und des Quellungsindex (Ql) wurden 250 mg des Mikrogels in 25 ml Toiuol 24 Stunden unter Schütteln bei 23°C gequollen. Nach Zentrifugation mit 20.000 Upm wird der unlösliche Anteil abgetrennt und getrocknet.
Der Geigehalt ergibt sich aus dem Quotienten des getrockneten Rückstandes und der Einwaage und wird in Gewichtsprozent angegeben.
Der Quellungsindex Ql wird aus dem Gewicht des in Toiuol bei 23°C für 24 Stunden gequollenen lösungsmittelhaltigen Mikrogels (nach Zentrifugation mit 20.000 Upm) und dem Gewicht des trockenen Mikrogels gemäß folgender Formel berechnet:
Ql = Naßgewicht des Mikrogels /Trockengewicht des
Mikrogels.
Anwendungsbeispieie für die Polvmerteilchen, hergestellt durch Emulsionspolvmerisαtion
Kupfer-Adsorption von vinylphosphonαt- und vinylsulfonαthαltiqen Gelen aus 0,32 molarer wässriger Kupfer-Sulfatlösuna
Zur Demonstration der Affinität vinylphosphonat- und vinylsulfonathaltiger GeSe für Kupfer wurden je 10 g der Gele OBR 1 297 und OBR 1 361 B in 75 mi einer 0,32 molaren wässrigen Lösung von Kupfersulfat (CuSO4*5H20 von Aldrich, Artikelnummer 20,920-1 ) unter Rühren 24 h dispergiert. Danach wurden die Gele abfiltriert und bis zur Gewichtskonstanz bei 6O0C getrocknet. Die in u, g , Tabelle angegebenen Metallgehalte der Gele wurden vor und nach der Behandlung mit Kupferlösung durch Atornemissionsspektroskopie mit induktiv gekoppeltem Hochfrequenzplasma (AES-ICP)
[http://www.schulchemie.de/atomems1 .htm] bestimmt.
Wie mit o. g. Versuchen gezeigt, werden bei der Kupferadsorption Alkali- und Erdalkalimetalle zugunsten des Kupfers verdrängt. Sowohl das vinylphosphonathaltige Gel (OBR 1 297) als auch das vinyisulfonathaltige Gel (OBR 1 361 B) weisen eine hohe Kapazität für die Adsorption von Kupferionen auf.
Kupfer-Adsorption aus 0,01 molarer Cu-Sulfatlösuna
Zur Demonstration der Kupferadsorption aus verdünnten wässrigen Lösungen, wurden wurden 20 g des vinylphosphonathaltigen Gels OBR 1297 in 225 ml einer 0,01 molarer wässrigen Lösung von
Kupfersulfαt (CuSO4*5H20 von ASdrich, Artikelnummer: 20,920-1 ) dispergiert, Nach 24 h wurde das Gel abgetrennt und bei 60°C getrocknet. Mittels AES-ICP wurde der Cu-Gehalt des Geis zu 7200 ppm bestimmt. Mit diesem Versuch wird gezeigt, dass das vinylphosphonathaltige Gel OBR 1 297 für eine nahezu quantitative Entfernung von Kupfer aus verdünnten Abwässern geeignet ist.
Silber-Adsorption aus 0, 1 molarer Silbernitratlösunq
Zur Demonstration der Fähigkeit zur Silberadsorption wurden 10 g des vinylphosphonathaltigen Gels OBR 1 297 in 75 ml einer 0, 1 molaren wässrigen Lösung von Sübernitrat (Merck, Artikelnummer: 1 512) unter Rühren 24 h dispergiert. Danach wurde das Gel abfiltriert und bis zur Gewichtskonstanz bei 6O0C getrocknet. Mitfels AES-ICP wurden die Silbergehalte vor und nach der Behandlung mit Silbernitratlösung bestimmt. Es wurde gefunden, dass das nicht exponierte Originalgel < 1 ppm Silber enthielt, Nach der Behandlung mit Silbernitratlösung betrug der Silbergehalt 78000 ppm. Hieraus resultiert, dass mit Hilfe des Gels ca. 96 % der zur Verfügung stehenden Silbermenge aus der wässrigen Lösung adsorbiert wurden. Mit dem Versuch wird gezeigt, dass das vinylphosphonathaltige Gel für die Entfernung von Silber aus Abwässern geeignet ist.
Zink-Adsorption aus 0,0094 molarer Zinksulfatlösuna
Zur Demonstration der Zinkadsorption aus einer verdünnten Lösung wurden 20 g des Gels OBR 1 297 in 200 ml einer 0,0094 molaren wässrigen Lösung aus Zinksulfat (Fluka, Artikelnummer: 96500) (enthält in Summe 61 4,5 mg Zink) unter Rühren 24 h dispergiert. Danach wurde das Gel abfiltriert und bis zur Gewichfskonstanz bei 600C getrocknet. Der Zinkgehalt des Gels wurde vor (< 1 ppm) und nach Behandlung (6900 ppm) mit Zinklösung mittels AES-ICP bestimmt.
Mit o.g. Beispiel wird die hohe Affinität des phosphonatmodifizierten Gele für Zinkionen demonstriert,
Kupfer-Adsorption von hvdroxyiαruppenhαltiqen Gelen nach Aktivierung mit Schwefelsäure bzw, Phosphorsäure
Die beiden hydroxyigruppenhaltigen Gele OBR 1327 B und OBR 1330 I wurden zunächst mit Schwefelsäure (50 g Gel in 250 ml Schwefelsäure/1 0%ig) bzw, mit Phosphorsäure (50 g Gei in 250 ml Phosphorsäure/l 0%ig 24h bei 96°C behandelt, durch Filtration isoliert, in Wasser redispergiert und bis zur Neutralität mit entionisiertem Wasser gewaschen und bei 6O0C getrocknet. Im Anschluss daran wurden jeweils 1 0 g des säurebehandelten Gels in einer 0,32 molaren wässrigen Lösung von Kupfersulfat (CuSO4*5H20 von Aldrich, Artikelnummer 20,920- 1 ) unter Rühren 24 h dispergiert. Danach wurden die Gele abfiltriert und bis zur Gewichtskonstanz bei 600C getrocknet. Die Gehalte ausgewählter Metalle wurden sowohl vor (Originalproben) als auch nach der Behandlung mit Säure / Kupferlösung mittels AES-ICP bestimmt (siehe folgende Tabelle).
Mit den Versuchen wird gezeigt, dass hydroxyigruppeπhaltige Gele sowohl nach Aktivierung mit Schwefelsäure als auch nach Aktivierung mit Phosphorsäure zur Adsorption von Kupfer befähigt sind.
Kondensation von 2-Ethylhexanol mit Benzoesäure auf Basis von säurearuppenhaltiaen Gelen
Zur Demonstration der Eignung der Polymerteilchen als regenerierbare Katalysatoren für saure Veresterungen werden mit vinyiphosphonat- und vinyisulfonathaltiger Gelen folgende Experimente durchgeführt. Die Kondensation erfolgt in Substanz bei 1 50 0C. Es wird kein Lösungsmittel eingesetzt. Di© Benzoesäure und 2- Ethylhexanol sind kommerziell von Aldrich bezogen worden, Die Menge des Katalysators beträgt 0,02 Säureäquivalente. Hierbei wird davon ausgegangen, dass die Säuregruppen aus der Mikrogelsynthese vollständig zugänglich sind. Der Fortschritt der Umsetzung wird mit Hilfe von Gaschromatographie verfolgt. In allen nachfolgend beschriebenen Ansätzen beträgt das Molverhältnis von Benzoesäure zu 2-Ethylhexanol eins zu drei, so dass auf eine wiederholte Angabe verzichten werden kann. Als Testreaktion dient die Kondensation von 2-Ethylhexanol mit Benzoesäure wie sie in Schema 1 dargestellt ist.
Schema 1 : Kondensation von 2-Ethylhexanol mit Benzoesäure
1 . Veresterung mit Mikrogel OBR 1 361 -B als Katalysator
Der Versuch wird in einer Apparatur mit Wasserabscheider und unter überleiten von Stickstoff durchgeführt.
Ansatz:
6,40 g Mikrogel OBR 1 361 B (mit H2SO4, 1 0-%ig aktiviert) 97,00 g 2-Ethylhexanol ( wasserfrei ) 3 eq
30,32 g Benzoesäure 1 eq
Durchführung :
6,40 g Mikrogel OBR 1 361 B vor Versuchsbegiπn bei Raumtemperatur 4 Tage iaπg in 97,0 g wasserfreiem 2-Ethy!hexanol unter mehrfachem Rühren gequollen. Die Benzoesäure wird portionsweise bei Raumtemperatur zugegeben. Unter Überleiten von Stickstoff wird innerhalb von 50 Minuten auf 1 50 °C aufgeheizt und 6 Stunden lang bei 1 50 0C und Überleiten von Stickstoff gerührt. Es wird stündlich eine kleine Probe zwecks GC-Messung entnommen. Diese Proben sind blank. Nach Reaktionsende wird das Mikrogel abfiltriert, extrahiert und im Vakuumtrockenschrank bei 80 0C und 1 00 mbar bis zur Gewichtskonstanz getrocknet. Man erhält das Mikrogel praktisch quantitativ zurück. Die Entwicklung des Umsatzes ist in Tabelle 1 dokumentiert. Tabelle l : Reaktion mit Hilfe von Mikrogel OBR 1361 B
2. Veresterung mit Mikrogel OBR 1 297 als Katalysator
Der Versuch wird in einer Apparatur mit Wasserabscheider und unter
Überleiten von Stickstoff durchgeführt.
Ansatz
7,38 g Mikrogel OBR 1 297 (mit H2SO4, 1 0-%ig aktiviert) 97,00 g 2-Ethylhexanol ( wasserfrei ) 3 eq 30,32 g Benzoesäure 1 eq
Durchführung
7,38 g Mikrogel OBR 1 297 wird vor Versuchsbeginn bei Raumtemperatur 4 Tage lang in 97,0 g wasserfreiem 2-Ethy!hexanol unter mehrfachem Rühren gequollen, Unter Überleiten von Stickstoff wird innerhalb von 50 Minuten auf 150 0C aufgeheizt und 6 Stunden lang bei 1 50 0C und Überleiten von Stickstoff gerührt. Es wird stündlich eine kleine Probe zwecks GC-Messung entnommen. Diese Proben sind blank. Nach Reaktionsende wird das Mikrogel abfiltriert, extrahiert und im Vakuumtrockenschrank bei 80 0C und 100 mbar bis zur Gewichtskonstanz getrocknet. Man erhält das Mikrogel praktisch quantitativ zurück. Die Entwicklung des Umsatzes ist in Tabelle 2 dokumentiert.
Tabelle 2: Reaktion mit Hilfe von Mikrogel OBR 1297:
Zeit [min] Menge Alkohol Menge Säure Menge Ester [%]
[%] L /o]
60 78 1 5 7
1 20 75 1 4 1 1
1 80 72,5 1 3 14,5
240 70,5 1 2 1 7,5
300 68,5 1 0,5 21
360 67,5 9, 5 23 Die Prozentangaben sind Flächenprozente im GC.
3. Veresterung ohne Mikrogel als Vergleichsversuch
Der Versuch wird in einer Apparatur mit Wasserabscheider und unter Überleiten von Stickstoff durchgeführt, Ansatz
97,00 g 2-Ethylhexanol (wasserfrei) 3 eq 30,32 g Benzoesäure 1 eq
Durchführung :
Das 2-Ethyihexanoi wird vorgelegt und unter kräftigem Rühren die Benzoesäure portionsweise bei Raumtemperatur zugegeben. Es entsteht nach kurzem Rühren eine blanke Lösung.
Unter Überleiten von Stickstoff wird innerhalb von 50 Minuten auf 150 0C aufgeheizt und 6 Stunden lang bei 150 0C und Überleiten von Stickstoff gerührt. Es wird stündlich eine kleine Probe zwecks GC- Messung entnommen. Diese Proben sind blank.
Tabelle 3: Reaktion ohne Hilfe von Mikrogel als Vergleichsversuch:
Zeit [min] Menge Alkohol Menge Säure Menge Ester [%] [%] [%]
60 80,2 16,2 3,6
120 78,4 15,3 6,3
180 76,7 14,5 8,8
240 75,4 13,3 11,3
300 73,8 12,7 13,6
360 72,7 11,9 15,4
Die Prozentangaben sind Flächenprozente im GC.
Claims
VERWENDUNG VON PROTONENLIEFERNDEN UND/ODER PROTONENAKZEPTIERENDEN POLYMERTEiLCHEN
Patentansprüche: 1 . Verwendung von durch Emuisionspolymerisation hergestellten
Polymerteilchen mit einem mittleren Teilchendurchmesser im Bereich von 5 bis 500 nm, enthaltend ionogene Gruppen, als protonenliefernde und/oder protonenakzeptierende Substanz in heterogenen chemischen Prozessen.
2, Verwendung nach einem der vorstehenden Ansprüche, worin die Polymerteilchen oberflächenständige und/oder nicht- oberflächenständige ionogene Gruppen enthalten,
3. Verwendung nach einem der vorstehenden Ansprüche, worin die durch Emulsionspolymerisation hergestellten Polymerteilchen kautschukartig oder nicht-kautschukartig sind.
4. Verwendung nach einem der vorstehenden Ansprüche, worin die kautschukartigen Polymerteilchen solche auf Basis von konjugierten Dienen wie Butadien, Isopren, 2-Chlorbutadien und 2,3-Dichlorbutadien, sowie Ethen, Ester der Acryl- und Methacrylsäure, Vinylacetat, Styrol oder Derivate davon, Acrylnitril, Acryiamide, Methacrylamide, Tetrafluorethylen, Vinylidenfluorid, Hexafluorpropen, doppelbindungshaltige
Hydroxyverbindungeπ wie z. B. Hydroxyethylmethacrylat, Hydroxyethylacrylat, Hydroxypropylacrylat, Hydroxybutylmethacrylat, Acrolein oder Kombinationen davon sind.
5, Verwendung nach einem der vorstehenden Ansprüche, worin die Polymerteilchen eine Glasübergangstemperatur, Tg, von - 1 00DC bis 1 500C aufweisen.
6. Verwendung nach einem der vorstehenden Ansprüche, worin die Polymerteilchen solche auf Basis von Methacrylaten, Insbesondere Methylmethαcrylαt, Styro! oder Styrolderivαten, wie αlphα-Methylstyrol, pαrα-Methylstyrol, Acrylnitril, Methαcrylnitril, Vinylcαrbαzol oder Kombinationen davon sind.
7, Verwendung nach einem der vorstehenden Ansprüche, worin die durch Emulsionspolymerisation hergestellten Polymerteilchen mindestens teilweise vernetzt sind.
8. Verwendung nach einem der vorstehenden Ansprüche, worin die durch Emulsionspolymerisation hergestellten
Polymerteilchen mindestens teilweise durch den Zusatz von polyfunktioπellen Monomeren bei der Polymerisation vernetzt sind.
9, Verwendung nach Anspruch 8, worin die polyfunktioneüen
Monomere aus der Gruppe ausgewählt werden, die besteht aus: Verbindungen mit mindestens zwei, vorzugsweise 2 bis 4 copolymerisierbaren C = C-Doppelbindungen, wie Diisopropenylbenzol, Divinylbenzol, Divinylether, Divinylsulfon, Diallylphthaiat, Triallylcyanurat, Triailylisocyanurat, 1 ,2-
Polybutadien, N,N'-m-Phenylenmaleimid, 2,4- Toluyienbis(maleimid), Triallyltrimellitat, Acrylate und Methacrylate von mehrwertigen, vorzugsweise 2- bis 4- wertigen C2 bis C l O Alkoholen, wie Ethylenglykol, Propandiol- 1 ,2, Butandiol, Hexandiol, Polyethyienglykol mit 2 bis 20, vorzugsweise 2 bis 8 Oxyethyleneinheiten, Neopentylglykol, Bisphenol-A, Glycerin, Trimethylolpropan, Pentaerythrit, Sorbit sowie ungesättigten Polyestern aus aliphatischen Di- und Polyoien und Maleinsäure, Fumarsaure, und/oder itaconsάure.
10. Verwendung nach einem der vorstehenden Ansprüche, worin die Polymerteilchen eine annähernd kugelförmige Geometrie aufweisen.
1 1 . Verwendung nach einem der vorstehenden Ansprüche, worin die Poiymerteüchen einen mittleren Teilchendurchmesser von weniger als 350 nm autweisen.
1 2, Verwendung nach einem der vorstehenden Ansprüche, worin die Polymerteilchen in Toluol bei 230C unlösliche Anteile von mindestens etwa 70 Gew.-% aufweisen.
1 3. Verwendung nach einem der vorstehenden Ansprüche, worin die Polymerteilchen in Toluol bei 23°C einen Quellungsindex von weniger als etwa 80 aufweisen.
1 4. Verwendung nach einem der vorstehenden Ansprüche, worin die Polymerteilchen eine Breite des Glasübergangsbereichs von größer als etwa 5 0C aufweisen.
1 5. Verwendung nach einem der vorstehenden Ansprüche, worin die ionogenen Gruppen ausgewählt werden aus einer oder mehreren der folgenden funktionellen Gruppen: -COOH, - SO3H, -OSO3H, -P(O)(OH)2, -0-P(OH)2 und -OP(O)(OH)2 und/oder deren Salzen und/oder deren Derivate.
16, Verwendung nach einem der vorstehenden Ansprüche, worin die ionogenen Gruppen durch Einpolymerisation entsprechend funktionalisierter Monomere und/oder durch
Modifikation nach der Polymerisation in die Polymerteilchen eingebracht werden ,
1 7. Verwendung nach Anspruch 1 6, worin die funktionalisierten Monomere aus der Gruppe ausgewählt sind, die besteht aus:
Acrylsäure, Methacrylsäure, Vinylbenzoesäure, Itakonsäure, Maleinsäure, Crotonsäure, Fumarsäure, Vinylsulfonsäure, Styroisulfonsäure, Phosponsäuregruppen-enthaltendert Monomeren mit polymerisierbaren C = C-Doppelbindungen, wie Vinylphosphonsäure, 2-Phosphonomethyl-acrylsäure und
2-Phosphonomethyl-acrylsäureamid, Phosphorsäure- oder Phosphonsöureester von hydroxyfunktionellen, polymerisierbαre C = C-Doppeibinduπgen-αufweisenden Monomeren oder Salzen oder Derivaten davon,
1 8. Verwendung nach Anspruch 1 7, worin die Phosphorsäureester von hydroxyfunktionellen polymerisierbare C = C- Doppelbindungen-autweisenden Monomeren die folgenden Formeln (I) bis (I!) aufweisen:
worin R eine zweiwertige organische Gruppe, wie insbesondere C l bis C 10-Alkylen ist.
19. Verwendung nach einem der vorstehenden Ansprüche, worin die ionogenen Gruppen -OSO3H oder -OP(O)(OH)2 sind, die durch Umsetzung von hydroxylmodifizierten Polymerteilchen mit Schwefelsäure oder Phosphorsäure, durch Addition von Schwefelsäure oder Phosphorsäure an doppelbindungshaltige
Polymerteilchen, durch Zersetzung von Persulfaten oder Perphosphaten in Gegenwart doppelbindungshaltiger Polymerteilchen, sowie durch Umesterung mittels Schwefeloder Phosphorsäure in die Polymerteilchen eingebracht werden.
20. Verwendung nach einem der vorstehenden Ansprüche, worin die ionogenen Gruppen -SO3H oder -P(O)(OH)2 sind und durch Sulfonierung bzw. Phosphonierung von aromatischen Vinylpolymeren eingebracht werden.
21 . Verwendung nach einem der vorstehend erwähnten Ansprüche, worin die Polymerteilchen als Katalysator in säurekatalysierten Reaktionen, wie die Oligomerisierung von Isobuten, die säurekatalysierte Herstellung von Bisphenol A, Veresterungsreaktionen,
Friedel-Crafts-Acylierungen und -Alkylierungen oder Dehydratisierungsreaktionen eingesetzt werden, als stationäre Phase in Säulen und Platten für Trennoperationen eingesetzt werden, - in elektrochemischen Verfahren eingesetzt werden, in lonenabsorptionsverfahren eingesetzt werden, als Antifouling-Wirkstoff eingesetzt werden, in Anstrichmitteln eingesetzt werden, in Funktionsbekleidung eingesetzt werden, - in medizinischen Artikeln eingesetzt werden, in Polymermatrices, wie in der Form von Formkörpern, wie Folien oder Membranen, wie für Brennstoffzellen, eingebettet eingesetzt werden, in deprotonierter Form als Hydrolyseschutzmittel eingebettet eingesetzt werden.
22. Polymerteilchen mit einem mittleren Teiichendurchmesser im Bereich von 5 bis 500 nm, erhalten durch Emulsionspolymerisation, enthaltend ionogene Gruppen ausgewählt aus der Gruppe, die besteht aus: -SO3H,
-OSO3H, -P(O)(OH)2, -0-P(OH)2 und -0-P(O)(OH)2 und/oder deren Salze und/oder Derivate davon.
23. Polymerteilchen nach Anspruch 22, worin die ionogenen Gruppen oberflächenständige und/oder nicht- oberflächenständige ionogene Gruppen sind.
24, Polymerteilchen nach Anspruch 23, worin die Derivate aus Estern ausgewählt werden.
25. Verwendung der Polymerteilchen nach einem der Ansprüche 22 bis 24, als Katalysator in säurekatalysierten Reaktionen, wie die Oligornerisierung von Isobuten, die säurekatalysierte Herstellung von Bispheno! A, Veresterungsreaktionen, Friedel-Crafts-Acylierungen und -Alkylierungen oder
Dehydratisierungsreaktionen eingesetzt werden, als stationäre Phase in Säulen und Platten für Trennoperafionen eingesetzt werden, in elektrochemischen Verfahren eingesetzt werden, - in lonenabsorptionsverfahren eingesetzt werden, ais Antifouiing-Wirkstoff eingesetzt werden, in Anstrichmitteln eingesetzt werden, in Funktionsbekleidung eingesetzt werden, in medizinischen Artikeln eingesetzt werden, - in Polymermatrices, wie in der Form von Formkörpern, wie Folien oder Membranen, wie für Brennstoffzellen, eingebettet eingesetzt werden, in deprotonierter Form als Hydrolyseschutzmittel eingebettet eingesetzt werden.
2ό. Verbundmateriai, enthaltend Polymerteilchen nach einem der Ansprüche 22 bis 24 und mindestens ein Trägermaterial.
27. Formkörper, aufweisend Polymerteilchen nach einem der Ansprüche 22 bis 24.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP08717460A EP2131956A1 (de) | 2007-03-08 | 2008-03-06 | Verwendung von protonenliefernden und/oder protonenakzeptierenden polymerteilchen |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102007011427.5 | 2007-03-08 | ||
| DE200710011427 DE102007011427A1 (de) | 2007-03-08 | 2007-03-08 | Verwendung von protonenliefernden und/oder protonenakzeptierenden Polymerteilchen |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2008107470A1 true WO2008107470A1 (de) | 2008-09-12 |
Family
ID=39494639
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2008/052713 WO2008107470A1 (de) | 2007-03-08 | 2008-03-06 | Verwendung von protonenliefernden und/oder protonenakzeptierenden polymerteilchen |
Country Status (3)
| Country | Link |
|---|---|
| EP (1) | EP2131956A1 (de) |
| DE (1) | DE102007011427A1 (de) |
| WO (1) | WO2008107470A1 (de) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105732371A (zh) * | 2016-03-22 | 2016-07-06 | 和夏化学(太仓)有限公司 | 一种无色透明的苯甲酸乙基己酯的制备方法 |
| CN115785513A (zh) * | 2021-09-09 | 2023-03-14 | 佛山市云米电器科技有限公司 | 一种具有高比表面积的弱酸基材及其应用 |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102008002457A1 (de) | 2008-06-16 | 2009-12-17 | Elcomax Membranes Gmbh | Verwendung eines protonenleitfähigkeitverleihenden Materials bei der Herstellung von Brennstoffzellen |
| DE102008056975A1 (de) * | 2008-11-13 | 2010-05-20 | Lanxess Deutschland Gmbh | Lagerstabile, hydroxylmodifizierte Mikrogellatices |
| DE102012103159A1 (de) * | 2012-04-12 | 2013-10-17 | Osram Opto Semiconductors Gmbh | Strahlung emittierendes Bauelement, transparentes Material und Füllstoffpartikel sowie deren Herstellungsverfahren |
Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2187146A (en) | 1936-10-24 | 1940-01-16 | Du Pont | Process of coagulation |
| US4460763A (en) | 1981-08-07 | 1984-07-17 | E. I. Dupont De Nemours And Company | Preparation of small particle polybenzimidazole |
| US5302696A (en) | 1989-05-16 | 1994-04-12 | Olin Corporation | Process for minimizing residual free hydrazine in polymer latices |
| US5442009A (en) | 1994-03-21 | 1995-08-15 | The Goodyear Tire & Rubber Company | Process for the preparation of hydrogenated rubber |
| EP0882747A2 (de) * | 1997-06-05 | 1998-12-09 | Kansai Paint Co., Ltd. | Phosphorsäure enthaltende nicht-wässrige Dispersion und Verfahren zu seiner Verwendung |
| US5922635A (en) * | 1997-05-07 | 1999-07-13 | Olah; George A. | Nanoscale solid superacid catalysts with pendant fluoroalkylsulfonic acid or fluoro, perfluoroalkylsulfonic acid groups |
| US6399706B1 (en) | 1999-06-26 | 2002-06-04 | Bayer Aktiengesellschaft | Microgel-containing rubber compounds which comprise sulfur-containing organosilicon compounds |
| EP1245276A2 (de) * | 2001-03-30 | 2002-10-02 | Rohm And Haas Company | Verbesserte Feststoffe |
| EP1245644A2 (de) * | 2001-03-30 | 2002-10-02 | Rohm And Haas Company | Farbstoffe, Dispersionen, Dispergiermittel und Tinten |
| DE69314136T3 (de) * | 1992-06-04 | 2004-05-06 | Société Prolabo | Nanopartikeln von funktionalisierten polymeren, deren verfahren zur herstellung und deren verwendung |
| WO2005033185A1 (de) | 2003-09-27 | 2005-04-14 | Rhein Chemie Rheinau Gmbh | Mikrogel-enthaltende thermoplastische elastomer- zusammensetzung |
| DE102004009396A1 (de) | 2004-02-24 | 2005-09-08 | Schuster, Robert H., Prof. Dr. | Membran, insbesondere für eine Verwendung in einer Brennstoffzelle und Verfahren zu ihrer Herstellung |
-
2007
- 2007-03-08 DE DE200710011427 patent/DE102007011427A1/de not_active Withdrawn
-
2008
- 2008-03-06 WO PCT/EP2008/052713 patent/WO2008107470A1/de active Application Filing
- 2008-03-06 EP EP08717460A patent/EP2131956A1/de not_active Withdrawn
Patent Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2187146A (en) | 1936-10-24 | 1940-01-16 | Du Pont | Process of coagulation |
| US4460763A (en) | 1981-08-07 | 1984-07-17 | E. I. Dupont De Nemours And Company | Preparation of small particle polybenzimidazole |
| US5302696A (en) | 1989-05-16 | 1994-04-12 | Olin Corporation | Process for minimizing residual free hydrazine in polymer latices |
| DE69314136T3 (de) * | 1992-06-04 | 2004-05-06 | Société Prolabo | Nanopartikeln von funktionalisierten polymeren, deren verfahren zur herstellung und deren verwendung |
| US5442009A (en) | 1994-03-21 | 1995-08-15 | The Goodyear Tire & Rubber Company | Process for the preparation of hydrogenated rubber |
| US5922635A (en) * | 1997-05-07 | 1999-07-13 | Olah; George A. | Nanoscale solid superacid catalysts with pendant fluoroalkylsulfonic acid or fluoro, perfluoroalkylsulfonic acid groups |
| EP0882747A2 (de) * | 1997-06-05 | 1998-12-09 | Kansai Paint Co., Ltd. | Phosphorsäure enthaltende nicht-wässrige Dispersion und Verfahren zu seiner Verwendung |
| US6399706B1 (en) | 1999-06-26 | 2002-06-04 | Bayer Aktiengesellschaft | Microgel-containing rubber compounds which comprise sulfur-containing organosilicon compounds |
| EP1245276A2 (de) * | 2001-03-30 | 2002-10-02 | Rohm And Haas Company | Verbesserte Feststoffe |
| EP1245644A2 (de) * | 2001-03-30 | 2002-10-02 | Rohm And Haas Company | Farbstoffe, Dispersionen, Dispergiermittel und Tinten |
| WO2005033185A1 (de) | 2003-09-27 | 2005-04-14 | Rhein Chemie Rheinau Gmbh | Mikrogel-enthaltende thermoplastische elastomer- zusammensetzung |
| DE102004009396A1 (de) | 2004-02-24 | 2005-09-08 | Schuster, Robert H., Prof. Dr. | Membran, insbesondere für eine Verwendung in einer Brennstoffzelle und Verfahren zu ihrer Herstellung |
Non-Patent Citations (9)
| Title |
|---|
| "Römpp Lexikon der Chemie", vol. 2, 1997 |
| H. G. MÜLLER, COLLOID POLYMER SCIENCE, vol. 267, 1996, pages 1113 - 1 1 16 |
| H. GERRENS, FORTSCHR. HOCHPOLYM. FORSCH., vol. 1, 1959, pages 234 |
| H.G. ELIAS: "Makromoleküle", vol. 2, 1992, HÜTHIG & WEPF VERLAG, pages: 443 |
| HOUBEN-WEYL: "Methoden der organischen Chemie", vol. 14/2, pages: 848 |
| P. A. LOVELL; M. S. EI-AASSER: "Emulsion Polymerization and Emulsion Polymers", JOHN WILEY & SONS |
| VOLLMERT: "Polymer Chemistry", 1973, SPRINGER |
| W. SCHOLTAN; H. LANGE, KOLLOID-Z U. Z. POLYMERE, vol. 250, 1972, pages 782 |
| W. SCHOLTAN; H. LANGE: "Bestimmung der Teilchengrößenverteilung von Latices mit der Ultrazentrifuge", KOLLOID-ZEITSCHRIFT UND ZEITSCHRIFT FÜR POLYMERE, vol. 250, 1972, XP000579440, DOI: doi:10.1007/BF01498571 |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105732371A (zh) * | 2016-03-22 | 2016-07-06 | 和夏化学(太仓)有限公司 | 一种无色透明的苯甲酸乙基己酯的制备方法 |
| CN105732371B (zh) * | 2016-03-22 | 2018-04-13 | 和夏化学(太仓)有限公司 | 一种无色透明的苯甲酸乙基己酯的制备方法 |
| CN115785513A (zh) * | 2021-09-09 | 2023-03-14 | 佛山市云米电器科技有限公司 | 一种具有高比表面积的弱酸基材及其应用 |
| CN115785513B (zh) * | 2021-09-09 | 2023-11-03 | 佛山市云米电器科技有限公司 | 一种具有高比表面积的弱酸基材及其应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2131956A1 (de) | 2009-12-16 |
| DE102007011427A1 (de) | 2008-09-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2137783B1 (de) | Polymerelektrolytmembran mit funktionalisierten nanopartikeln | |
| EP2186651B1 (de) | Lagerstabile, hydroxylmodifizierte Mikrogellatices | |
| WO2012107510A1 (de) | Nanofiltrationsmembran | |
| EP2286477B1 (de) | Gasdiffusionselektroden mit funktionalisierten nanopartikeln | |
| WO2008107470A1 (de) | Verwendung von protonenliefernden und/oder protonenakzeptierenden polymerteilchen | |
| WO2010084114A1 (de) | Silanhaltige kautschukmischungen mit gegebenenfalls funktionalisierten dienkautschuken und mikrogelen, ein verfahren zur herstellung und deren verwendung | |
| EP1724301B1 (de) | Mikrogel-enthaltende vulkanisierbare Zusammensetzung | |
| EP3253809B1 (de) | Zusammensetzungen, enthaltend nbr-basierte mikrogele | |
| DE10035493A1 (de) | Verfahren zur Herstellung vernetzter Kautschukpartikel | |
| WO2014016347A1 (de) | Nanofiltrationsmembran mit einer schicht aus polymer- und oxidpartikeln | |
| EP1757652B1 (de) | Schwachsaure Kationenaustauscher | |
| DE1620839A1 (de) | Verfahren zur Agglomerierung waessriger Latices | |
| DE19852667A1 (de) | Verfahren zur Herstellung von monodispersen gelförmigen Kationenaustauschern | |
| EP1130035A2 (de) | Polymerisationsinitiierende geträgerte Systeme zur radikalischen Polymerisation von konjugierten Dienen und zur Copolymerisation dieser mit weiteren Monomeren in Suspensions- oder Gasphasenverfahren | |
| WO2014016345A1 (de) | Nanofiltrationsmembran mit einer schicht aus durch emulsionspolymersiation hergestellten polymerteilchen | |
| DE10022871A1 (de) | Verfahren zur Herstellung von wässrigen Polymerdispersionen mit wasserlöslichen Polyolefinstabilisatoren | |
| DE1720668A1 (de) | Verfahren zur Herstellung von Ionenaustauschern auf Basis vernetzter Acrylsaeureester-Polymerisate |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 08717460 Country of ref document: EP Kind code of ref document: A1 |
|
| REEP | Request for entry into the european phase |
Ref document number: 2008717460 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2008717460 Country of ref document: EP |