RU2707103C1 - Кумарины с бициклическими монотерпеновыми заместителями - Google Patents
Кумарины с бициклическими монотерпеновыми заместителями Download PDFInfo
- Publication number
- RU2707103C1 RU2707103C1 RU2019118608A RU2019118608A RU2707103C1 RU 2707103 C1 RU2707103 C1 RU 2707103C1 RU 2019118608 A RU2019118608 A RU 2019118608A RU 2019118608 A RU2019118608 A RU 2019118608A RU 2707103 C1 RU2707103 C1 RU 2707103C1
- Authority
- RU
- Russia
- Prior art keywords
- trimethylbicyclo
- hept
- exo
- coumarins
- compounds
- Prior art date
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/35—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom
- A61K31/352—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom condensed with carbocyclic rings, e.g. methantheline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/18—Antioxidants, e.g. antiradicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/04—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring
- C07D311/06—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms directly attached in position 2
- C07D311/20—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms directly attached in position 2 hydrogenated in the hetero ring
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Biochemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Dermatology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
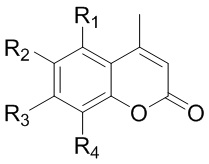
Изобретение относится к кумаринам общей формулы (I)
I
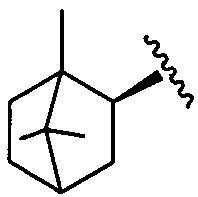
где R1=R4=H, R3=OH, R2= (1,7,7-триметилбицикло[2.2.1]гепт-экзо-2-ил) (1);
R1=R4=H, R2=OH, R3= (1,7,7-триметилбицикло[2.2.1]гепт-экзо-2-ил) (2);
R2=R4= (1,7,7-триметилбицикло[2.2.1]гепт-экзо-2-ил), R1=OH, R3= H (3).
R1=R4=H, R3=OH, R2= (2,2,3-триметилбицикло[2.2.1]гепт-экзо-5-ил) (4);
R1=R4=H, R2=OH, R3= (2,2,3-триметилбицикло[2.2.1]гепт-экзо-5-ил) (5).
Полученные кумарины могут быть использованы в качестве средства, обладающего антиоксидантной и мембранопротекторной активностью. 1 з.п. ф-лы, 2 табл. 6 пр.
Description
Изобретение относится к кумаринам, а именно к гидроксикумаринам с изоборнильным или изокамфильным заместителем в бензопирановом кольце.
Гидроксикумарины и их производные представляют интерес в качестве фармакологически активных соединений, поскольку проявляют противовирусные, противовоспалительные и противоопухолевые свойства [M.Z. Hassan, Н. Osman, М.А. Ali, M.J. Ahsan. Therapeutic potential of coumarins as antiviral agents // Eur. J. Med. Chem. 2016, 123, 236-255; M.A.I. Salem, M.I. Marzouk, A.M. Et-Kazak. Synthesis and characterization of some new coumarins with in vitro antitumor and antioxidant activity and high protective effects against DNA damage // Molecules. 2016, 21, 249; Vijaya Bhargavi, M.; Shashikala, P.; Sumakanth, M. Coumarins and chromones: a remarkable scaffolds for anti-inflammatory activity // J. Pharm. Sci. & Res. 2017, Vol. 9(9), 1483-1489; Carrico-Moniz, D. Coumarin derivatives for cancer therapy // Patent US 9388155 (2016); Ma, J.; Huang, K.; Ni, X.; Chen, R.; Yu, C.; Yan, Q.; Chen, S.; Hou, X. Coumarin derivative and its application in preparing drug for treating or preventing cancer and other proliferative disease // Patent CN 109232498. 18.06.2019]. Кроме того, гидроксикумарины могут выступать как промежуточные соединения в синтезе новых биологически активных производных, в том числе галогенсодержащих, аминов, амидов, сложных эфиров, бензоксазинов и так далее [Sun М., Hu J., Song X., Wu D., Kong L., Sun Y., Wang D., Wang Y., Chen N., Liu G. Coumarin derivatives protect against ischemic brain injury in rats // Eur. J. Med. Chem. 2013, 67, 39-53; Chen Y., Cheng M., Liu F.Q., Xia P., Qian K., Yu D., Xia Y., Yang Z.Y., Chen C.H., Morris-Natschke S.L., Lee K.H. Anti-AIDS agents 86. Synthesis and anti-HIV evaluation of 20,30-seco-30-nor DCP and DCK analogues // Eur. J. Med. Chem. 2011, 46, 4924-4936; Guo X.-Y., Liu G. Scaffold-hopping strategy toward calanolides with nitrogen-containing heterocycles // Chinese Chemical Letters. 2013, 24, 295-298; Zhang M.-Z., Zhang R.-R., Yin W.-Z., Yu X., Zhang Y.-L., Liu P., Gu Y.-C., Zhang W.-H. Microwave-assisted Synthesis and antifungal activity of coumarin[8,7-e][1,3]oxazine derivatives // Mol. Divers. 2016, 20:611-618].
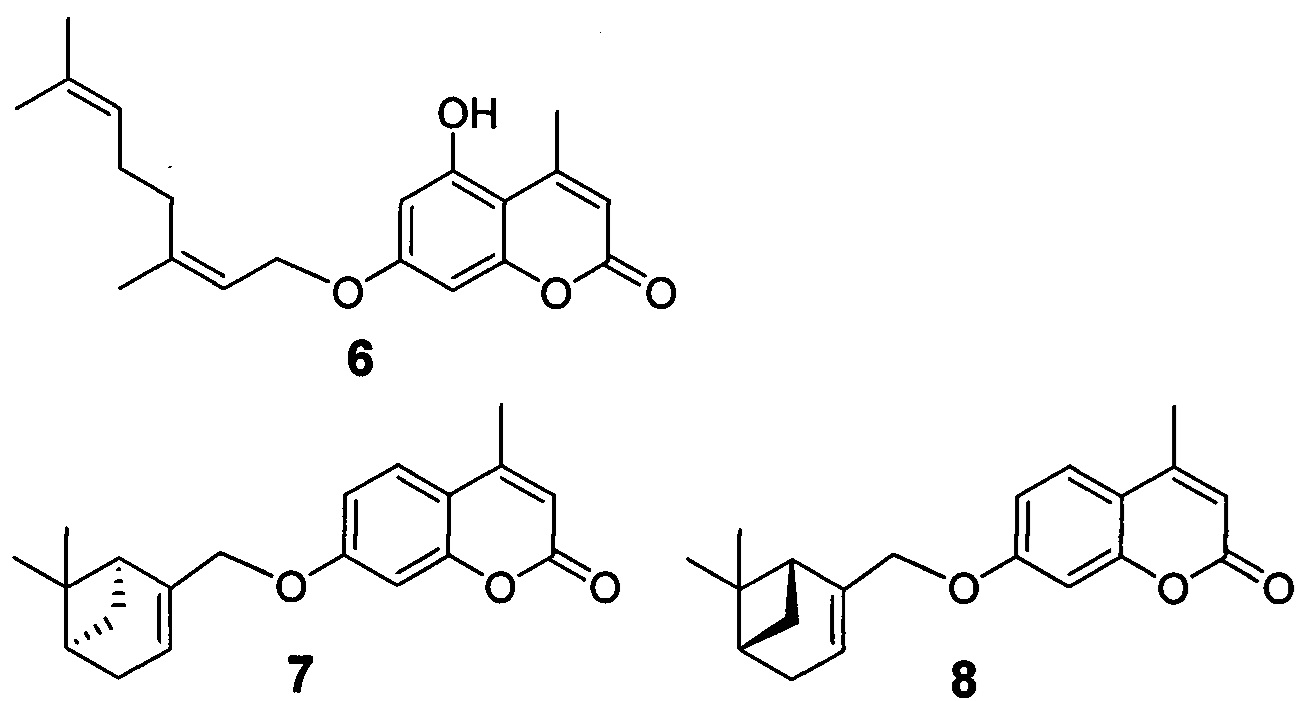
Ближайшими аналогами заявляемых соединений можно считать 4-метил-5-гидрокси-(Z)-аураптен (6) [Si, J.; Li, G.; Cao, L. Application of terpenoid coumarin compounds to treating gastric cancer // Patent CN 109223772. 18.06.2019], оказывающий хороший эффект против пролиферации раковых клеток желудка; 7-(((1R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ен-2-ил)метокси)-4-метил-2Н-хромен-2-он (7) и 7-(((1S,5R)-6,6-диметилбицикло[3.1.1]гепт-2-ен-2-ил)метокси)-4-метил-2Н-хромен-2-он (8), демонстрирующие ингибирующий эффект против вируса гриппа A/California/07/09 (H1N1)pdm09 [Т.М. Khomenko, V.V. Zarubaev, I.R. Orshanskaya, R.A. Kadyrova, V.A. Sannikova, D.V. Korchagina, K.P. Volcho, N.F. Salakhutdinov, Anti-influenza activity of monoterpene-containing substituted coumarins // Bioorg. Med. Chem. Lett. 2017, 27, 2920-2925].
Описания заявляемых соединений и их свойств в источниках информации не обнаружено.
Задачей изобретения является получение новых гидроксикумаринов с терпеновыми заместителями формулы I.
Технический результат состоит в расширении арсенала кумаринов, а именно гидроксикумаринов с изоборнильным или изокамфильным заместителем в бензопирановом кольце, которые могут найти применение в медицине, в частности для получения препаратов, обладающих антиоксидантной и мембранопротекторной активностью.
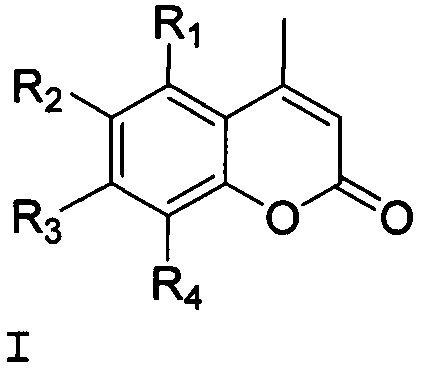
Технический результат достигается тем, что кумарины с бициклическими монотерпеновыми заместителями (изоборнильным или изокамфильным) имеют общую формулу структуры (I) Группа соединений, представлена общей формулой (I):
где R1=R4=H, R3=OH, R2=(1,7,7-триметилбицикло[2.2.1]гепт-экзо-2-ил) (1);
R1=R4=H, R2=OH, R3=(1,7,7-триметилбицикло[2.2.1]гепт-экзо-2-ил) (2);
R2=R4=(1,7,7-триметилбицикло[2.2.1]гепт-экзо-2-ил), R1=OH, R3=Н (3);
R1=R4=H, R3=OH, R2=(2,2,3-триметилбицикло[2.2.1]гепт-экзо-5-ил) (4);
R1=R4=H, R2=OH, R3=(2,2,3-триметилбицикло[2.2.1]гепт-экзо-5-ил) (5).
Полученные кумарины обладают антиоксидантной и мембранопротекторной активностью.
Синтез заявляемых соединений осуществлен методом конденсации Пехмана [P. Srivastava; V.K. Vyas; В. Variya; P. Patel; G. Qureshi; M. Ghate. Synthesis, anti-inflammatory, analgesic, 5-lipoxygenase (5-LOX) inhibition activities, and molecular docking study of 7-substituted coumarin derivatives. Bioorganic Chemistry, 2016, 67, 130-138] при взаимодействии соответствующих терпенофенолов с ацетоуксусным эфиром в среде концентрированной H2SO4.
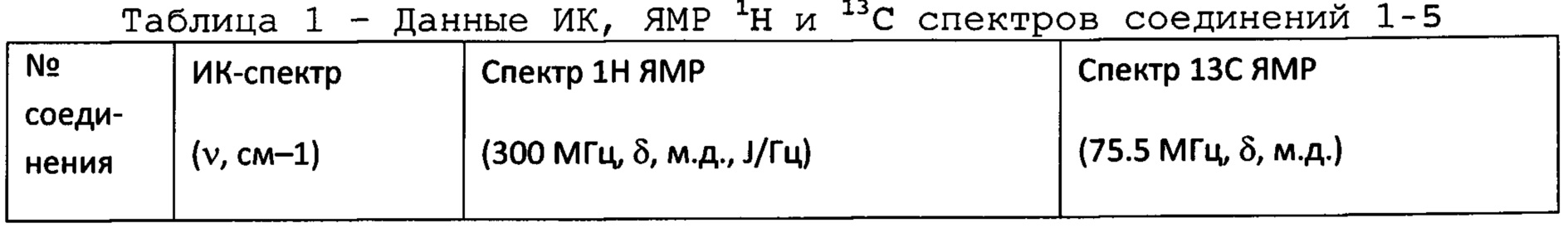
Соединения (1-5) представляют собой белые мелкокристаллические порошки, растворимые в хлороформе (умеренно), диметилсульфоксиде, бензоле, диэтиловом эфире, ацетоне, этаноле, нерастворимые в воде. Структуры соединений (1-5) подтверждены методами ИК и ЯМР спектроскопии, а так же масс-спектрометрии (ESI-MS). ИК-спектры регистрировали на ИК-Фурье-спектрометре Shimadzu IR Prestige 21 (Япония) в таблетках с KBr. Спектры ЯМР 1Н и 13С записывали на спектрометре Bruker Avance II 300 (Германия) при рабочей частоте прибора 300 и 75.5 МГц соответственно в DMSO или CDCl3. Масс-спектры записывали на масс-спектрометре Thermo Finnigan LCQ Fleet.
Сущность предлагаемого решения и возможность его осуществления подтверждается примером и результатами физико-химических исследований.
Пример 1. 7-Гидрокси-6-(1,7,7-триметилбицикло[2.2.1]гепт-экзо-2-ил)-4-метил-2Н-хромен-2-он (1) получен при взаимодействии смеси 4-(1,7,7-триметилбицикло[2.2.1]гепт-экзо-2-ил)бенз-1,3-диола (1 г, 4 ммоль) и ацетоуксусного эфира (0.8 г, 6 ммоль) при охлаждении (0-5°С), к которой по каплям добавили избыток концентрированной H2SO4 (2 мл) и перемешивали 4 ч при охлаждении, а затем еще ночь при комнатной температуре. Реакционную смесь вылили в лед. Образовавшийся осадок отфильтровали, промыли холодной водой и высушили. Полученный кумарин перекристаллизовали из этанола. Выход 1.1 г (93%), т. пл. 273°С с разложением. ESI-MS (70 eV) m/z: 313.19 [М+Н] Спектральные характеристики соединения (1) приведены в таблице 1.
Пример 2. 6-Гидрокси-7-(1,7,7-триметилбицикло[2.2.1]гепт-экзо-2-ил)-4-метил-2Н-хромен-2-он (2) получен аналогично примеру 1, исходя из 2-(1,7,7-триметилбицикло[2.2.1]гепт-экзо-2-ил)бенз-1,4-диола (1 г, 4 ммоль). Выход 1.0 г (86%), т. пл. 287°С с разложением. ESI-MS (70 eV) m/z: 313.21 [М+Н]. Спектральные характеристики соединения (2) приведены в таблице 1.
Пример 3. 5-Гидрокси-6,8-ди-(1,7,7-триметилбицикло[2.2.1]гепт-экзо-2-ил)-4-метил-2Н-хромен-2-он (3) получен аналогично примеру 1, исходя из 4,6-ди-(1,7,7-триметилбицикло[2.2.1]гепт-экзо-2-ил)бенз-1,3-диола (1.5 г, 4 ммоль). Продукт выделяли колоночной хроматографией на SiO2 (элюент - хлороформ). Выход 0.9 г (52%), т. пл. 284°С с разложением. ESI-MS (70 eV) m/z: 449.34 [М+Н]. Спектральные характеристики соединения (3) приведены в таблице 1.
Пример 4. 7-Гидрокси-6-(2,2,3-триметилбицикло[2.2.1]гепт-экзо-5-ил)-4-метил-2Н-хромен-2-он (4) получен аналогично примеру 1, исходя из 4-(2,2,3-триметилбицикло[2.2.1]гепт-экзо-5-ил)бенз-1,3-диола. Выход 91%, т. пл. 256°С с разложением. ESI-MS (70 eV) m/z: 313.47 [М+Н]. Спектральные характеристики соединения (4) приведены в таблице 1.
Пример 5. 6-Гидрокси-7-(2,2,3-триметилбицикло[2.2.1]гепт-экзо-5-ил)-4-метил-2Н-хромен-2-он (5) получен аналогично примеру 1, исходя из 2-(2,2,3-триметилбицикло[2.2.1]гепт-экзо-5-ил)бенз-1,4-диола. Выход 83%, т. пл. 256°С с разложением. ESI-MS (70 eV) m/z: 313.32 [М+Н]. Спектральные характеристики соединения (5) приведены в таблице 1.
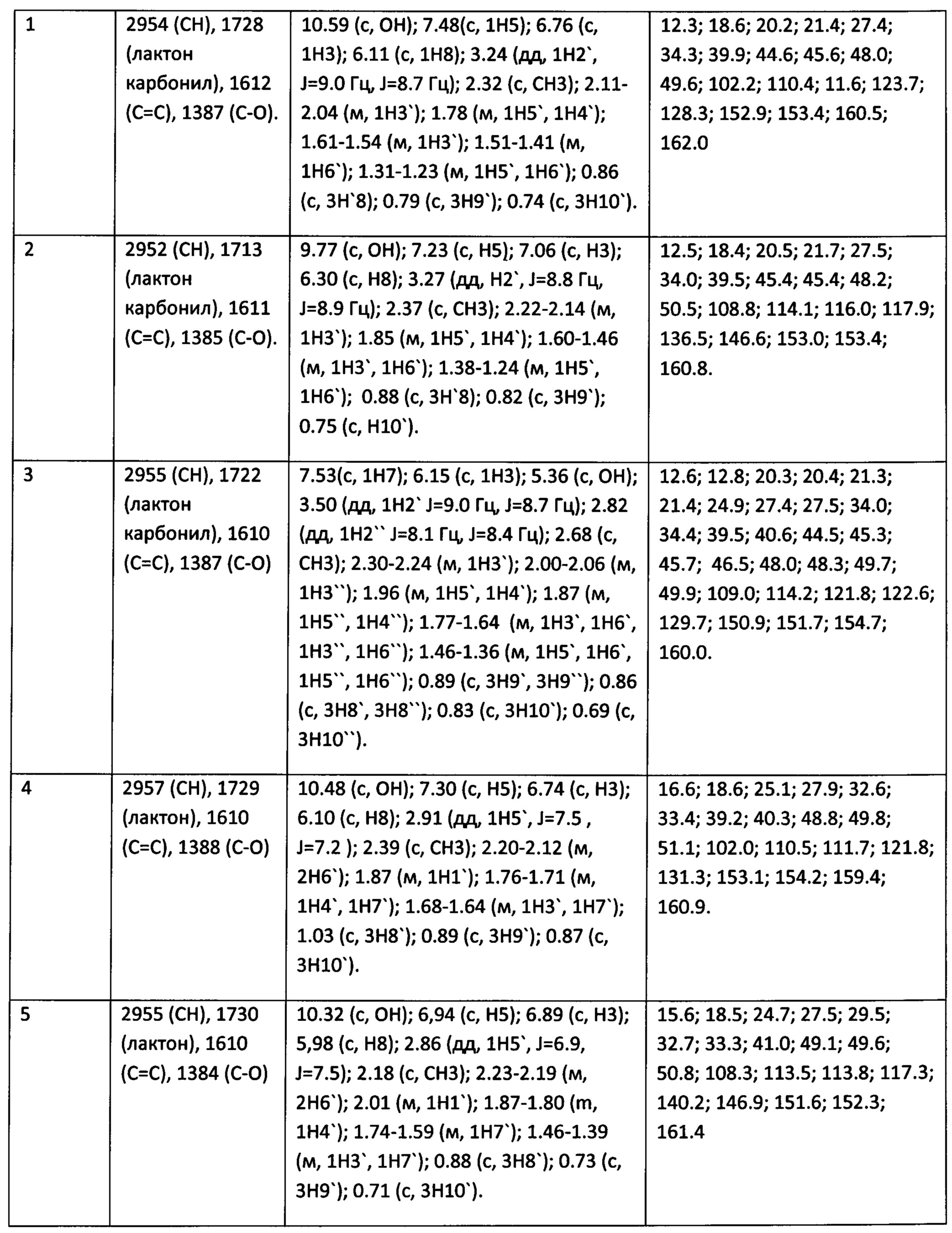
Поиск наиболее активных и относительно малотоксичных биологически активных веществ для использования их на практике обуславливает необходимость проведения их первичного отбора на модельных биологических системах. Для впервые синтезированных соединений нами будут проведены сравнительные исследования мембранопротекторной активности на модели H2O2-индуцированного гемолиза эритроцитов и антиоксидантные свойства по эффективности ингибирования накопления вторичных продуктов перекисного окисления липидов. Известно, что биологическая активность большинства соединений зависит от их способности влиять на регуляцию процессов окисления липидов, а также воздействовать на структурное состояние клеточных мембран [Burlakova Е.В. Chemical and Biological Kinetics: New Horizons. V. 2. Biological Kinetics. 2005]. Удобной клеточной моделью исследования механизмов развития окислительных повреждений являются эритроциты крови, чувствительные к оксидативным повреждениям вследствие значительного содержания полиненасыщенных жирных кислот в липидах мембран и наличия гемоглобина, являющегося потенциальным промотором окислительных процессов [О.Г. Шевченко, Л.Н. Шишкина. Успехи современной биологии. 2014. 134. 133-148].
Пример 6. Для оценки токсичности, антиоксидантной и мембранопротекторной активности соединений использовали 0.5% (v/v) суспензию эритроцитов лабораторных мышей в фосфатно-солевом буфере (PBS, рН 7.4). Исследуемые вещества предварительно растворяли в ацетоне. Токсичность (гемолитическую активность) оценивали по степени гемолиза эритроцитов через 1-5 ч после внесения растворов исследуемых соединений в концентрации 1 мкМ. Сравнительную оценку биологической активности кумаринов с бициклическими терпеновыми заместителями (изоборнильным или изокамфильным) проводили при концентрации 1 мкМ, поскольку для соединения (4) в концентрации 10 мкМ была выявлена цитотоксичность. Мембранопротекторную и антиоксидантную активность определяли по степени ингибирования H2O2-индуцированного гемолиза, торможения накопления вторичных продуктов ПОЛ и окисления оксигемоглобина в эритроцитах [Takebayashi J., Chen J., Tai A. // Advanced Protocols in Oxidative Stress II, Methods in Molecular Biology / Ed. Armstrong D. New York; Dordrecht; Heidelberg; London: Humana Press, 2010. V. 594. P. 287-296; Van den Berg J.J.M., Op den Kamp J.A.F., Lubin B.H., Roelofsen В., Kuypers F.A. // Free Radical Biol. Med. 1992. V. 12. P. 487-498]. 7-Гидрокси-4-метилкумарин в этой концентрации не изучали, поскольку в предварительных экспериментах было установлено отсутствие у них значимой мембранопротекторной активности даже при 10 мкМ.
Оценка антиоксидантной и мембранопротекторной активности заявляемых соединений показала высокий потенциал соединений как антиоксидантов.
По мембранопротекторной активности наиболее эффективным является кумарин 3, содержащий в составе два изоборнильных заместителя, действие которого существенно превышает незамещенный 7-гидрокси-4-метилкумарин.
Claims (8)
1 Кумарины с бициклическими монотерпеновыми заместителями (изоборнильным или изокамфильным) общей формулы (I)
где R1=R4=H, R3=OH, R2=(1,7,7-триметилбицикло[2.2.1]гепт-экзо-2-ил) (1);
R1=R4=H, R2=OH, R3=(1,7,7-триметилбицикло[2.2.1]гепт-зкзо-2-ил) (2);
R2=R4=(1,7,7-триметилбицикло[2.2.1]гепт-экзо-2-ил), R1=OH, R3=Н (3);
R1=R4=H, R3=OH, R2=(2,2,3-триметилбицикло[2.2.1]гепт-экзо-5-ил) (4);
R1=R4=H, R2=OH, R3=(2,2,3-триметилбицикло[2.2.1]гепт-экзо-5-ил) (5).
2 Кумарины по п. 1, обладающие антиоксидантной и мембранопротекторной активностью.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2019118608A RU2707103C1 (ru) | 2019-06-15 | 2019-06-15 | Кумарины с бициклическими монотерпеновыми заместителями |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2019118608A RU2707103C1 (ru) | 2019-06-15 | 2019-06-15 | Кумарины с бициклическими монотерпеновыми заместителями |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2707103C1 true RU2707103C1 (ru) | 2019-11-22 |
Family
ID=68653153
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2019118608A RU2707103C1 (ru) | 2019-06-15 | 2019-06-15 | Кумарины с бициклическими монотерпеновыми заместителями |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2707103C1 (ru) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112851618A (zh) * | 2021-03-04 | 2021-05-28 | 丽水学院 | 一种高釉质吸附型抑菌剂及其制备方法和应用 |
| RU2814111C1 (ru) * | 2023-06-16 | 2024-02-22 | Федеральное государственное бюджетное научное учреждение "НАУЧНЫЙ ЦЕНТР НЕВРОЛОГИИ" | Производные 5,8-диметокси-6,7-метилендиокси кумарина, обладающие антирадикальной активностью |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2125999C1 (ru) * | 1993-02-05 | 1999-02-10 | Дзе Апджон Компани | 4-гидроксибензопиран-2-он или 4-гидроксициклоалкил/в/-бензопиран-2-он и способ получения n-/3-/циклопропил(5,6,7,8,9,10-гексагидро-4-гидрокси-2-оксо-2h-циклоокта/в /- пиран-3-ил)метил/фенил/бензолсульфона |
| RU2016122428A (ru) * | 2016-06-06 | 2017-12-07 | Федеральное Государственное Бюджетное Учреждение Науки Институт Химии Коми Научного Центра Уральского Отделения Российской Академии Наук | Гибридные терпенофенолы с изоборнильным и 1-фенилэтильным или 1-фенилпропильным заместителями |
| CN109223772A (zh) * | 2017-07-11 | 2019-01-18 | 中国医学科学院药用植物研究所 | 萜类香豆素类化合物在治疗胃癌方面的应用 |
-
2019
- 2019-06-15 RU RU2019118608A patent/RU2707103C1/ru active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2125999C1 (ru) * | 1993-02-05 | 1999-02-10 | Дзе Апджон Компани | 4-гидроксибензопиран-2-он или 4-гидроксициклоалкил/в/-бензопиран-2-он и способ получения n-/3-/циклопропил(5,6,7,8,9,10-гексагидро-4-гидрокси-2-оксо-2h-циклоокта/в /- пиран-3-ил)метил/фенил/бензолсульфона |
| RU2016122428A (ru) * | 2016-06-06 | 2017-12-07 | Федеральное Государственное Бюджетное Учреждение Науки Институт Химии Коми Научного Центра Уральского Отделения Российской Академии Наук | Гибридные терпенофенолы с изоборнильным и 1-фенилэтильным или 1-фенилпропильным заместителями |
| CN109223772A (zh) * | 2017-07-11 | 2019-01-18 | 中国医学科学院药用植物研究所 | 萜类香豆素类化合物在治疗胃癌方面的应用 |
Non-Patent Citations (2)
| Title |
|---|
| Khomenko, T. M., Zarubaev, V. V., Orshanskaya, I. R., Kadyrova, R. A., Sannikova, V. A., Korchagina, D. V. Salakhutdinov, N. F. (2017). Anti-influenza activity of monoterpene-containing substituted coumarins. Bioorganic & Medicinal Chemistry Letters, 27(13), 2920-2925.doi:10.1016/j.bmcl.2017.04.091. * |
| Khomenko, T. M., Zarubaev, V. V., Orshanskaya, I. R., Kadyrova, R. A., Sannikova, V. A., Korchagina, D. V. Salakhutdinov, N. F. (2017). Anti-influenza activity of monoterpene-containing substituted coumarins. Bioorganic & Medicinal Chemistry Letters, 27(13), 2920-2925.doi:10.1016/j.bmcl.2017.04.091. RU 2125999 C1, * |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112851618A (zh) * | 2021-03-04 | 2021-05-28 | 丽水学院 | 一种高釉质吸附型抑菌剂及其制备方法和应用 |
| CN112851618B (zh) * | 2021-03-04 | 2022-05-31 | 丽水学院 | 一种高釉质吸附型抑菌剂及其制备方法和应用 |
| RU2814111C1 (ru) * | 2023-06-16 | 2024-02-22 | Федеральное государственное бюджетное научное учреждение "НАУЧНЫЙ ЦЕНТР НЕВРОЛОГИИ" | Производные 5,8-диметокси-6,7-метилендиокси кумарина, обладающие антирадикальной активностью |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Reddy et al. | PEG-SO3H catalyzed synthesis and cytotoxicity of α-aminophosphonates | |
| CN108864024B (zh) | 一类灯盏乙素苷元氮芥类衍生物及其制备方法和用途 | |
| Lozada et al. | Synthesis, cytotoxic and antioxidant evaluations of amino derivatives from perezone | |
| Khaligh et al. | Synthesis and in vitro antibacterial evaluation of novel 4-substituted 1-menthyl-1, 2, 3-triazoles | |
| Yang et al. | Design, synthesis and structure-activity relationship study of novel naphthoindolizine and indolizinoquinoline-5, 12-dione derivatives as IDO1 inhibitors | |
| JP2017513863A (ja) | 4,5−ジヒドロ−1h−ピロロ[2,3−f]キノリン−2,7,9−トリカルボン酸およびその二ナトリウム塩の多形形態、それらの調製方法ならびにそれらの使用 | |
| Venkatesh et al. | Design and synthesis of Quinazolinone, Benzothiazole derivatives bearing guanidinopropanoic acid moiety and their Schiff bases as cytotoxic and antimicrobial agents | |
| Al-Masoudi et al. | Synthesis and anti-HIV Activity of New Fused Chromene Derivatives Derived from 2-Amino-4-(1-naphthyl)-5-oxo-4H, 5H-pyrano [3, 2-c] chromene-3-carbonitrile | |
| RU2707103C1 (ru) | Кумарины с бициклическими монотерпеновыми заместителями | |
| CA2888015C (en) | 2',5'-dideoxy-5-fluorouridine derivatives having cytotoxic activity, a process for the manufacture thereof and application thereof | |
| CN106928293A (zh) | 一类具有抗肿瘤活性的呋咱no供体型灯盏乙素衍生物及其制备方法和用途 | |
| Lu et al. | Synthesis and bioactivity of quercetin aspirinates | |
| CN105968064A (zh) | 一种二间甲苯基四嗪二甲酰胺化合物及制备和应用 | |
| Elwarrakya et al. | An efficient and green one-pot synthesis of novel spirooxindole derivatives with potential anti-tumor activity in an aqueous solvent | |
| CN101985449B (zh) | 一种香豆素衍生物及其制备方法和作为抗癌药物的用途 | |
| Wróblewski et al. | Synthesis of four stereoisomers of protected 1, 2-epiimino-3-hydroxypropylphosphonates | |
| CN105111194A (zh) | 一种萘并吡喃酮类化合物及其制备方法和应用 | |
| RU2768824C1 (ru) | 2-(фенил(фенилимино)метил)изоиндолин-1,3-дион и способ его получения | |
| Paramita et al. | Synthesis and cytotoxic activities of hexyl esters derivatives of gallic acid against MCF-7 cell line | |
| CN110759961B (zh) | 一类熊果酸吲哚醌酰胺衍生物及其制备方法和应用 | |
| WO2016071382A1 (en) | Synthesis of pi3k inhibitor and salts thereof | |
| CN108101892B (zh) | 一种白杨素非天然氨基酸衍生物及其制备方法和应用 | |
| Hasan et al. | Microwave Synthesis, Characterization, and Antioxidant Activity of New Dihydrobenzimidazoquinazoline Compounds | |
| CN105801543B (zh) | 4-芳香胺-香豆素衍生物及其制备方法和医药用途 | |
| CN107236004B (zh) | 二氢杨梅素环磷酰胺衍生物及其制备方法和应用 |