RU2483715C2 - Твердая лекарственная форма препаратов мемантина и его солей - Google Patents
Твердая лекарственная форма препаратов мемантина и его солей Download PDFInfo
- Publication number
- RU2483715C2 RU2483715C2 RU2010154205/15A RU2010154205A RU2483715C2 RU 2483715 C2 RU2483715 C2 RU 2483715C2 RU 2010154205/15 A RU2010154205/15 A RU 2010154205/15A RU 2010154205 A RU2010154205 A RU 2010154205A RU 2483715 C2 RU2483715 C2 RU 2483715C2
- Authority
- RU
- Russia
- Prior art keywords
- memantine
- cellulose
- dosage form
- drug
- oral cavity
- Prior art date
Links
Images
Abstract
Изобретение относится к твердой быстро-дезинтегрируемой лекарственной форме средства противопаркинсонического действия, содержащей в качестве активного фармацевтического ингредиента мемантин и/или мемантин гидрохлорид и целлюлозу II при следующем соотношении ингредиентов, мас.%: мемантин и/или мемантин гидрохлорид - 5-10, целлюлоза II - 90-95. Лекарственная форма может представлять собой пеллету, созданную способом прямого пеллетирования. Техническим результатом изобретения является получение быстродезинтегрируемой в ротовой полости лекарственной формы, распределение ее по ротовой полости и замедление ее транспорта в желудок для обеспечения доставки лекарственного средства, минуя желудочно-кишечный тракт и исключая метаболизм лекарственного средства в печени. 1 з.п. ф-лы, 1 ил., 2 пр.
Description
Изобретение относится к области медицины, в частности к фармацевтической технологии производства готовых лекарственных средств, и касается твердой лекарственной формы средства противопаркинсонического действия, которое содержит в качестве активного фармацевтического ингредиента мемантин и/или мемантина гидрохлорид.
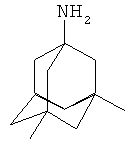
Мемантин (структурная формула показана ниже) является, с фармакологической точки зрения, низкоаффиным неконкурентным антагонистом глютаматергического НМДА-рецептора. Расстройство системы глютаматергической нейротрансмиссии, проявляющейся в виде нейрональной экцитоксичности, рассматривается как наиболее значимый компонент в этиологии паркинсонических расстройств и, в частности, болезни Альцгеймера.
Структурная формула мемантина
Мемантин имеет более высокую аффинность к белкам НМДА рецептора чем Mg2+, следовательно, обеспечивает пролонгацию инфлюкса ионов Са2+, которые ответственны за проявления нейрональной экцитоксичности. Посредством обладания низкой аффинностью мемантина к НМДА рецептору обеспечивается быстрое восстановление физиологической функции рецептора.
Мемантин и его соли представляют собой белые или белые с металлическими оттенками порошки, кристаллы игольчатой и других форм с экспериментальной растворимостью в воде порядка 26 мг/мл, плотностью порядка 1,365 г/см3 и горьким металлическим вкусом.
Лекарственные формы на основе мемантина на сегодняшний день представлены под торговыми марками Наменда, Акатинол, Абикса. Препараты представлены в дозе - 10 мг и имеют следующий состав (ИНСТРУКЦИЯ по медицинскому применению препарата Акатинол Мемантин (Akatinol Memantine), см. http://www.medkrug.ru/medicament/show/5229):
Мемантина гидрохлорид 10 мг
Вспомогательные вещества:
Лактоза 174,75 мг;
Целлюлоза микрокристаллическая 52,1 мг;
Кремния диоксид коллоидный 1,25 мг;
Тальк 11,15 мг;
Магния стеарат 0,75 мг.
Кроме этого известны запатентованные лекарственные формы противопаркинсонического действия, содержащие мемантин.
Так, из описания к патенту РФ №2326660 (МПК A61K 31/13 (2006.01), опубликован 20.06.2008) известен пероральный препарат в виде твердой лекарственной формы, содержащей мемантин в качестве активного вещества и вспомогательные компоненты, при следующих соотношениях компонентов, мас.%:
Мемантин 0,5-10,0
Дезинтегрант 2,0-40,0
антифрикционное вещество 0,2-10,0
физиологически нейтральный наполнитель - остальное.
При этом в качестве наполнителя может содержаться микроцеллюлоза.
Кроме этого из патента Евразии №011446 (опубликован 27.02.2009) известно лекарственное средство, представляющее собой твердую оральную лекарственную форму с модифицированным высвобождением, включающую мемантин или мемантина гидрохлорид, фармацевтически приемлемый полимерный носитель, оказывающий существенное воздействие на модификацию высвобождения активного ингредиента, и наполнитель, при этом полимерный носитель выбран из полимеров целлюлозы и их производных (гидроксиметилцеллюлозы, гидроксиэтилцеллюлозы, карбоксиметилцеллюлозы, полисахариды микрокристаллической целлюлозы и их производные), в качестве наполнителя содержит моногидрат лактозы, микрокристаллическую целлюлозу, двуокись кремния или их смесь, смазывающий агент. Активный ингредиент содержится в количестве до 35%мас., носитель - 20-70% мас., наполнитель - 5-80% мас., смазывающий агент - 0,8-1,2% мас.
Недостатком известной лекарственной формы является наличие большого количества ингредиентов, что приводит к удорожанию лекарственного препарата, усложнению технологии его производства и сокращению срока хранения. Наличие микрокристаллической целлюлозы в количестве более 20% мас. приведет к значительному замедлению высвобождения активного вещества, а отсутствие связующего не позволит достичь требуемой твердости таблетки.
Наиболее близким аналогом предлагаемого решения является лекарственная форма, содержащая мемантин в количестве 0,5-10% и микрокристаллическую целлюлозу в количестве 90-99,5% (патент РФ №2326660, опубликован 20.06.2008).
Недостатками известной лекарственной формы является использование в качестве лекарственной формы капсулы с содержащимся в ней гранулированным лекарственным средством, поскольку приводит к замедленному высвобождению активного вещества и интенсивному метаболизму активного вещества в печени.
Кроме этого использование таблеток и капсул мемантина в педиатрических целях не всегда возможно ввиду, например, неразвитой нервной системы у младенцев, а также из-за расстройств глотательного рефлекса. У лиц же пожилого возраста наблюдаются тремор, дисфагия, невозможность принимать жидкости и другие расстройства, ограничивающие возможность приема таблетированных препаратов.
В связи с этим актуальным является создание твердой быстродезинтегрируемой лекарственной формы средства противопаркинсонического действия на основе мемантина и/или его солей с использованием целлюлозы второй кристаллической модификации (гидратцеллюлоза, целлюлоза II) как единственного компонента, заменяющего наполнитель, дезинтегратор и связующее вещество.
Задачей изобретения является создание инновационной, устойчивой, твердой таблетированной быстродезинтегрируемой лекарственной формы мемантина или мемантина гидрохлорида с распадаемостью до 60 секунд, высвобождением более 80% в течение первых 60 минут после приема и твердостью свыше 80 Н с возможностью универсального буккального или энтерального введения в зависимости от выбираемой врачом терапии и возможностей пациента, а также упрощение получения данной лекарственной формы. Данная лекарственная форма должна удовлетворять всем требованиям на фармацевтическое средство в течение срока годности препарата, соответственно, прием быстродезинтегрируемых лекарственных форм должен обеспечивать терапевтическую концентрацию активного вещества в плазме крови в соответствии со значениями, полученными в результате клинических исследований.
Лекарственная форма должна быть покрыта полимерной оболочкой, легко высвобождать активное вещество, обеспечивать высокую биодоступность, быть безопасной для здоровья.
Техническим результатом предлагаемого изобретения является обеспечение доставки лекарственного средства, минуя желудочно-кишечный тракт, и исключение метаболизма лекарственного средства в печени.
Кроме этого техническим результатом является обеспечение возможности приема препарата без воды, обеспечение частичного всасывания препарата до попадания в желудок, что приведет к попаданию активного вещества напрямую в верхнюю полую вену, что позволяет избежать первичного метаболизма в печени.
Заявленный технический результат достигается за счет использования твердой быстродезинтегрируемой лекарственной формы средства противопаркинсонического действия, содержащей в качестве активного фармацевтического ингредиента мемантин и/или мемантин гидрохлорид и целевые добавки. Согласно настоящему изобретению в качестве целевой добавки лекарственная форма содержит целлюлозу II при следующем соотношении ингредиентов, мас.%:
мемантин и/или мемантин гидрохлорид - 5-10;
целлюлоза II - 90-95.
Как известно, целлюлоза существует в четырех видах кристаллической модификации: I, II, III, IV. Переход из одной кристаллической модификации (полиморфного состояния) в другую происходит в результате химического и/или термического влияния.
Ниже приведена фигура в виде блок-схемы, на которой схематично изображены формы модификаций микроцеллюлозы и способы конверсии полиморфов целлюлозы между собой.
Наиболее распространенными являются формы I и II. Природная целлюлоза состоит, в основном, из двух модификаций I-й формы: 1α и 1β. Данные алломорфы присутствуют в различных пропорциях в зависимости от происхождения (например, бактериального или растительного).
Модифицированная целлюлоза формы II (целлюлоза II) получается из формы I посредством регенерации или мерсерезации. Регенерация заключается в растворении кристаллической целлюлозы в растворителе с последующей рекристаллизацией в воде.
Процесс мерсерезации, впервые предложенный 150 лет назад Мерсером, представляет собой вымачивание целлюлозы I-й формы в концентрированном растворе гидроксида натрия с последующей рекристаллизацией в воде.
Как показали проведенные испытания, целлюлоза II имеет ярковыраженные свойства супердезинтегратора, в тоже время обладает высокой пластичностью, что позволит использовать ее в качестве наполнителя при создании новых эффективных лекарственных средств. Относительно высокое содержание целлюлозы-2 в качестве наполнителя позволит значительно уменьшить влияние таких факторов, как сегрегация при смешивании с активным веществом и/или таблетировании, что, в свою очередь, приводит к значительным флуктуациям активного вещества в единице продукции.
В настоящее время в качестве веществ-дезинтеграторов, то есть веществ, улучшающих проникновение водной среды в лекарственную форму и приводящих ее к быстрому набуханию и дезинтеграции, что приводит к ускорению высвобождения активного вещества, обычно используются прежелатинизированный крахмал, гидроксипропилметилцеллюлоза (ГПМЦ), кросскармелоза, кроссповидон, кислота альгиновая в виде ее соли или смеси ее солей. Инновационность предлагаемой лекарственной формы заключается во введении модифицированной целлюлозы II в качестве универсального ингредиента, заменяющего дезинтегратор и наполнитель, что, как показывают проведенные испытания, позволяет уменьшить время распадаемости, увеличить пластические свойства композиции для облегчения прессования и, соответственно, увеличить устойчивость данной лекарственной композиции к изменениям процесса, что приводит к снижению стоимости производства и значительному увеличению качества продукции по сравнению с существующими аналогами.
В тоже время свойства супердезинтегратора, проявляемые целлюлозой-2, позволяют создать таблетку или пелетту с высокой скоростью распадаемости.
За счет того что целлюлоза II обладает более низкой кристалличностью, чем микрокристаллическая целлюлоза, позволит использовать ее в качестве связующего.
Кроме этого плотность целлюлозы II ниже, чем у микрокристаллической целлюлозы, и составляет 1,5 г/см3, что близко к плотности активного вещества - мемантина (1,365 г/см3). Данное свойство позволит снизить проявление сегрегации и добиться точного соответствия дозы препарата в единице продукции без использования дополнительных вспомогательных ингредиентов. Более высокое значение удельной плотности целлюлозы-2 по сравнению с целлюлозой-1 в комбинации с мемантином приводит к более высокой твердости таблеток (более 80 Н).
Несмотря на то что свойства целлюлозы II заметно отличаются от свойств микрокристаллической целлюлозы (целлюлоза I), ее состав является идентичным составу целлюлозы I, что позволит произвести замену модификации I модификацией II без риска деградации активного вещества. В тоже время сокращение компонентов в составе твердой лекарственной формы приводит к увеличению стабильности активного компонента и, соответственно, к увеличению срока хранения препарата.
Использование целлюлозы II, как показали проведенные испытания, позволяет осуществить доставку лекарственного вещества (мемантина и/или мемантина гидрохлорид), минуя желудочно-кишечный тракт, т.е. посредством всасывания в ротовой полости и верней трети эзофагуса. Такой способ позволит миновать интенсивный метаболизм лекарственного вещества в печени, т.к. буккальный регион и регион верхней трети эзофагуса не обслуживаются портальной веной и растворенное вещество попадает в системную циркуляцию.
При органолептических тестах таблеток, изготовленных с применением целлюлозы II, было замечено, что частицы этого компонента быстро распределяются по ротовой полости, не вызывая дискомфорта, в тоже время обладая мукоадгезивными свойствами, замедляют транспорт растворенных частиц лекарственных веществ в ЖКТ, обеспечивая более полное всасывание через мембраны ротовой полости и эзофагуса.
Кумулятивный эффект повышения биодоступности не концентрируется на простом уменьшении времени дезинтегрирования (как было рассмотрено в указанных источниках), но состоит из трех основных фаз: быстрое диспергирование таблетки в ротовой полости (ни в желудке и последующих отделах кишечника, как рассмотрено в цитируемой диссертации), распределение по ротовой полости и замедление транспорта в желудок посредством мукоадгезивных свойств, что особенно важно при использовании лекарственного препарата в педиатрии, для лиц пожилого возраста, пациентов, страдающих тремором, дисфагией и другими расстройствами, ограничивающими прием таблетированных препаратов.
Таким образом, помимо перечисленных достоинств, предлагаемый состав является быстродезинтегрируемой универсальной лекарственной формой, позволяющей использовать ее и как обычную таблетку быстрого действия, и как орально-диспергирующуюся форму, а также упростить технологии производства готового лекарственного средства за счет оптимизации состава и технологических параметров, прочностных характеристик, стабильности во времени, удешевления готового продукта при обеспечении гарантированных для пациента значений показателей оценки биодоступности.
Лекарственная форма может быть выполнена в виде твердой пеллеты, созданной способом прямого пеллетирования.
Кроме этого лекарственная форма в качестве целевых добавок может дополнительно содержать лактозы моногидрат, гидроксипропилметилцеллюлозу (ГПМЦ), поливинилпирролидон (ПВП), лубриканты при следующем соотношении ингредиентов, мас.%:
| Компонент | Концентрация, масс. % | |
| Мемантин | или | 5-10 |
| Мемантина | ||
| Гидрохлорид | ||
| Целлюлозы-2 | 90-95% | |
| ГПМЦ и/или ПВП | 0-4% | |
| Лактозы моногидрат | 0-5% | |
| Лубрикант | 0-2% |
Инновационность патентуемой фармацевтической композиции заключается во введении целлюлозы-2 в качестве универсального ингредиента для замены вещества-дезинтегратора и вещества-наполнителя, что позволяет сократить количество ингредиентов в составе и значительно увеличить биодоступность активного вещества (мемантина), увеличить пластические свойства композиции для облегчения прессования и, соответственно, увеличения устойчивости данной лекарственной композиции к изменениям процесса производства, что, в свою очередь, ведет к понижению стоимости производства и значительному увеличению качества продукции по сравнению с аналогами.
Далее изобретение подтверждается примерами.
Пример №1
Лекарственная форма в виде таблетки была изготовлена методом прямого прессования и содержала, масс.%:
Мемантин - 5 и целлюлозу-2 - 95.
Смесь порошков мемантина и целлюлозы-2 смешивается в течение 15 минут в порошковом смесителе и таблетируется при давлениях, достаточных для достижения порозности не более 10 объемных процентов. Полученные таблетки обладают необходимой твердостью, устойчивостью к истиранию и высвобождением активного ингредиента.
Далее определяли характеристики полученной таблетки - распадаемость, высвобождение и твердость. Твердость полученных таблеток мемантина диаметром 9 мм была в пределах 80-100 Н. Распадаемость полученных таблеток варьировалась от 1 до 3 минут. Высвобождение активного вещества определялось в аппарате с мешалкой, скорость вращения которой составляла 50 об/мин. Скорость высвобождения составила более 80% активного ингредиента за 15 минут.
Также полученные таблетки были покрыты полимерной оболочкой, содержащей ГПМЦ, тальк и краситель. После определения профиля высвобождения было установлено, что нанесение косметического покрытия на полученные таблетки мемантина не оказывает влияния на профиль высвобождения.
Пример №2
Лекарственная форма в виде пеллетов была изготовлена методом прямого пеллетирования и содержала, масс.%:
Мемантин - 5 и целлюлозу-2 - 95.
Смесь порошков мемантина и целлюлозы-2 пеллетируется в пеллетизаторе с гладким вращающимся диском и распылением дистиллированной воды. Полученные пеллеты просеиваются с отделением фракции 250-800 мкм и высушиваются.
Далее определяли характеристики полученной пеллеты - распадаемость и высвобождение. Распадаемость пеллет была определена визуально после помещения пеллет в дистиллированную воду. Время распадаемости пеллет варьировалось в пределах 1 минуты. Определение профиля высвобождения производилось идентично способу, описанному в примере 1. Скорость высвобождения мемантина из пеллет составила более 80% активного вещества за 15 минут.
Claims (2)
1. Твердая быстродезинтегрируемая лекарственная форма средства противопаркинсонического действия, содержащая в качестве активного фармацевтического ингредиента мемантин и/или мемантин гидрохлорид и целевые добавки, отличающаяся тем, что в качестве целевых добавок содержит целлюлозу II при следующем соотношении ингредиентов, мас.%:
мемантин и/или мемантин гидрохлорид 5-10
целлюлоза II 90-95
2. Лекарственная форма по п.1, отличающаяся тем, что она представляет собой пеллету, созданную способом прямого пеллетирования.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2010154205/15A RU2483715C2 (ru) | 2010-12-30 | 2010-12-30 | Твердая лекарственная форма препаратов мемантина и его солей |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2010154205/15A RU2483715C2 (ru) | 2010-12-30 | 2010-12-30 | Твердая лекарственная форма препаратов мемантина и его солей |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2010154205A RU2010154205A (ru) | 2012-07-10 |
| RU2483715C2 true RU2483715C2 (ru) | 2013-06-10 |
Family
ID=46848176
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2010154205/15A RU2483715C2 (ru) | 2010-12-30 | 2010-12-30 | Твердая лекарственная форма препаратов мемантина и его солей |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2483715C2 (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2022025785A1 (ru) | 2020-07-29 | 2022-02-03 | ОБЩЕСТВО С ОГРАНИЧЕННОЙ ОТВЕТСТВЕННОСТЬЮ "НоваМедика" | Фармацевтическая композиция, включающая мемантин и цитиколин |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007114797A1 (en) * | 2006-04-06 | 2007-10-11 | Igc Center D.O.O. | Porous tablets for subsequent filling with active pharmaceutical ingredient |
| US20080008752A1 (en) * | 2006-07-05 | 2008-01-10 | Julia Hrakovsky | Pharmaceutical compositions of memantine |
| RU2326660C1 (ru) * | 2007-03-14 | 2008-06-20 | Закрытое акционерное общество "Биологические исследования и системы" | Пероральный лекарственный препарат мемантин (варианты) и способ его получения (варианты) |
| WO2009004440A2 (en) * | 2007-06-29 | 2009-01-08 | Orchid Chemicals & Pharmaceuticals Limited | Quick dissolve compositions of memantine hydrochloride |
| JP2010077304A (ja) * | 2008-09-26 | 2010-04-08 | Dai Ichi Kogyo Seiyaku Co Ltd | ペースト組成物および該ペースト組成物を含有してなるスプレー用組成物 |
-
2010
- 2010-12-30 RU RU2010154205/15A patent/RU2483715C2/ru not_active Application Discontinuation
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007114797A1 (en) * | 2006-04-06 | 2007-10-11 | Igc Center D.O.O. | Porous tablets for subsequent filling with active pharmaceutical ingredient |
| US20080008752A1 (en) * | 2006-07-05 | 2008-01-10 | Julia Hrakovsky | Pharmaceutical compositions of memantine |
| RU2326660C1 (ru) * | 2007-03-14 | 2008-06-20 | Закрытое акционерное общество "Биологические исследования и системы" | Пероральный лекарственный препарат мемантин (варианты) и способ его получения (варианты) |
| WO2009004440A2 (en) * | 2007-06-29 | 2009-01-08 | Orchid Chemicals & Pharmaceuticals Limited | Quick dissolve compositions of memantine hydrochloride |
| JP2010077304A (ja) * | 2008-09-26 | 2010-04-08 | Dai Ichi Kogyo Seiyaku Co Ltd | ペースト組成物および該ペースト組成物を含有してなるスプレー用組成物 |
Non-Patent Citations (1)
| Title |
|---|
| BALZANO, VINCENZO: «Soft tabletting of MCC 102 and UICEL-A/102 pellets into multiple unit pellet systems» / PhD Thesis, University of Basel, Faculty of Science, 2009. * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2022025785A1 (ru) | 2020-07-29 | 2022-02-03 | ОБЩЕСТВО С ОГРАНИЧЕННОЙ ОТВЕТСТВЕННОСТЬЮ "НоваМедика" | Фармацевтическая композиция, включающая мемантин и цитиколин |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2010154205A (ru) | 2012-07-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5775464B2 (ja) | 非晶質cddo−meを含有する遅延放出性経口投薬組成物 | |
| TWI330080B (en) | Solid pharmaceutical compositions containing pregabalin | |
| TWI702953B (zh) | 包含azd9291之醫藥組合物及錠劑以及其用途 | |
| ES2935800T3 (es) | Forma de dosificación oral de ketamina | |
| RU2720204C1 (ru) | Сублингвальная фармацевтическая композиция эдаравона и (+)-2-борнеола | |
| JP6170918B2 (ja) | 二相の放出制御システムによるプレガバリンを含む徐放錠 | |
| KR102241643B1 (ko) | 비정질 톨밥탄을 함유하는 경구 투여 현탁제 | |
| DK3294719T3 (en) | VORTIOXETIN-pyroglutamate | |
| WO2019098300A1 (ja) | 放出制御製剤 | |
| KR20190019044A (ko) | 마진돌 ir/sr 다층 정제 및 그의 주의력 결핍/과잉행동 장애 (adhd)의 치료를 위한 용도 | |
| DK2802311T3 (en) | SUBLINGUAL PHARMACEUTICAL COMPOSITION CONTAINING AN ANTIHISTAMIN MEDICINE AND PROCEDURE FOR PREPARING THEREOF | |
| RU2483715C2 (ru) | Твердая лекарственная форма препаратов мемантина и его солей | |
| JPWO2020090970A1 (ja) | 抗腫瘍剤を含む医薬組成物 | |
| KR101383430B1 (ko) | 새로운 조합의 구강내 속붕해 필름형성 조성물 및 pde5 저해제가 함유된 구강내 속붕해 필름제제 | |
| HUE032753T2 (en) | A pharmaceutical composition comprising a hydrogen carbonate salt and its use as a medicament for the treatment and / or prevention of urinary and related diseases | |
| WO2017192458A1 (en) | Compositions and methods of providing thyroid hormone or analogs thereof | |
| JP2019507101A (ja) | 含プレガバリン経口用徐放性三重錠剤 | |
| JP2010001242A (ja) | レバミピド固形製剤及びその製造方法 | |
| EP2793853A2 (en) | Pharmaceutical formulations of flurbiprofen and glucosamin | |
| WO2011153168A1 (en) | Pharmaceutical compositions of ibuprofen and an h2 receptor antagonist | |
| JP6150564B2 (ja) | 口腔内速崩壊性錠剤 | |
| TW202300138A (zh) | 拉考沙胺藥物組合物、其製備方法及應用 | |
| CN112449601A (zh) | 含纳呋拉啡口腔崩解片 | |
| US20130236538A1 (en) | Pharmaceutical compositions of ibuprofen and famotidine | |
| WO2017163268A2 (en) | A sustained release pharmaceutical dosage form of divalproex |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| FA92 | Acknowledgement of application withdrawn (lack of supplementary materials submitted) |
Effective date: 20120806 |
|
| FZ9A | Application not withdrawn (correction of the notice of withdrawal) |
Effective date: 20120817 |
|
| FA92 | Acknowledgement of application withdrawn (lack of supplementary materials submitted) |
Effective date: 20121018 |
|
| FZ9A | Application not withdrawn (correction of the notice of withdrawal) |
Effective date: 20121025 |
|
| PC41 | Official registration of the transfer of exclusive right |
Effective date: 20200228 |