RU2356503C1 - Способ укрепления гастродуоденоанастомоза - Google Patents
Способ укрепления гастродуоденоанастомоза Download PDFInfo
- Publication number
- RU2356503C1 RU2356503C1 RU2007149012/14A RU2007149012A RU2356503C1 RU 2356503 C1 RU2356503 C1 RU 2356503C1 RU 2007149012/14 A RU2007149012/14 A RU 2007149012/14A RU 2007149012 A RU2007149012 A RU 2007149012A RU 2356503 C1 RU2356503 C1 RU 2356503C1
- Authority
- RU
- Russia
- Prior art keywords
- anastomosis
- gastroduodenoanastomosis
- suturing
- stomach
- mesentery
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 45
- 230000003872 anastomosis Effects 0.000 claims abstract description 45
- 238000013110 gastrectomy Methods 0.000 claims abstract description 6
- 210000001519 tissue Anatomy 0.000 claims abstract description 6
- 210000000713 mesentery Anatomy 0.000 claims description 25
- 210000003384 transverse colon Anatomy 0.000 claims description 25
- 238000005728 strengthening Methods 0.000 claims description 7
- 210000000936 intestine Anatomy 0.000 claims 1
- 210000001198 duodenum Anatomy 0.000 abstract description 24
- 206010028980 Neoplasm Diseases 0.000 abstract description 22
- 201000011510 cancer Diseases 0.000 abstract description 12
- 210000004185 liver Anatomy 0.000 abstract description 10
- 210000001659 round ligament Anatomy 0.000 abstract description 10
- 238000001356 surgical procedure Methods 0.000 abstract description 8
- 210000004303 peritoneum Anatomy 0.000 abstract description 6
- 239000003814 drug Substances 0.000 abstract description 4
- 210000000056 organ Anatomy 0.000 abstract description 4
- 230000006378 damage Effects 0.000 abstract description 2
- 206010016717 Fistula Diseases 0.000 abstract 3
- 230000003890 fistula Effects 0.000 abstract 3
- 210000001537 mesocolon Anatomy 0.000 abstract 3
- 230000000694 effects Effects 0.000 abstract 1
- 239000012634 fragment Substances 0.000 abstract 1
- 238000002955 isolation Methods 0.000 abstract 1
- 239000000126 substance Substances 0.000 abstract 1
- 210000002784 stomach Anatomy 0.000 description 33
- 210000000683 abdominal cavity Anatomy 0.000 description 14
- 238000002271 resection Methods 0.000 description 13
- 230000002496 gastric effect Effects 0.000 description 11
- 238000002224 dissection Methods 0.000 description 7
- 206010027476 Metastases Diseases 0.000 description 6
- 210000001165 lymph node Anatomy 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 210000002151 serous membrane Anatomy 0.000 description 5
- 208000009956 adenocarcinoma Diseases 0.000 description 4
- 210000003041 ligament Anatomy 0.000 description 4
- 208000007502 anemia Diseases 0.000 description 3
- 238000009534 blood test Methods 0.000 description 3
- 210000004229 gastric stump Anatomy 0.000 description 3
- 210000001035 gastrointestinal tract Anatomy 0.000 description 3
- 208000014674 injury Diseases 0.000 description 3
- 230000002980 postoperative effect Effects 0.000 description 3
- 210000000813 small intestine Anatomy 0.000 description 3
- 230000008733 trauma Effects 0.000 description 3
- 206010002091 Anaesthesia Diseases 0.000 description 2
- 206010014418 Electrolyte imbalance Diseases 0.000 description 2
- 208000031481 Pathologic Constriction Diseases 0.000 description 2
- 208000005718 Stomach Neoplasms Diseases 0.000 description 2
- 208000025865 Ulcer Diseases 0.000 description 2
- 206010047700 Vomiting Diseases 0.000 description 2
- 206010052428 Wound Diseases 0.000 description 2
- 208000027418 Wounds and injury Diseases 0.000 description 2
- 230000037005 anaesthesia Effects 0.000 description 2
- 230000004888 barrier function Effects 0.000 description 2
- 238000001574 biopsy Methods 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 230000036772 blood pressure Effects 0.000 description 2
- 230000002183 duodenal effect Effects 0.000 description 2
- 206010017758 gastric cancer Diseases 0.000 description 2
- 238000009957 hemming Methods 0.000 description 2
- 230000000004 hemodynamic effect Effects 0.000 description 2
- 230000023597 hemostasis Effects 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000002350 laparotomy Methods 0.000 description 2
- 230000004807 localization Effects 0.000 description 2
- 210000004072 lung Anatomy 0.000 description 2
- 230000009401 metastasis Effects 0.000 description 2
- 230000000877 morphologic effect Effects 0.000 description 2
- 210000004400 mucous membrane Anatomy 0.000 description 2
- 230000000771 oncological effect Effects 0.000 description 2
- 230000036407 pain Effects 0.000 description 2
- 230000001020 rhythmical effect Effects 0.000 description 2
- 230000036262 stenosis Effects 0.000 description 2
- 208000037804 stenosis Diseases 0.000 description 2
- 201000011549 stomach cancer Diseases 0.000 description 2
- 238000011477 surgical intervention Methods 0.000 description 2
- 230000007704 transition Effects 0.000 description 2
- 238000002604 ultrasonography Methods 0.000 description 2
- 238000005353 urine analysis Methods 0.000 description 2
- 230000008673 vomiting Effects 0.000 description 2
- 230000004580 weight loss Effects 0.000 description 2
- 206010018852 Haematoma Diseases 0.000 description 1
- 208000034767 Hypoproteinaemia Diseases 0.000 description 1
- 208000002847 Surgical Wound Diseases 0.000 description 1
- 230000001464 adherent effect Effects 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 230000036770 blood supply Effects 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 210000002249 digestive system Anatomy 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 208000002173 dizziness Diseases 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 238000004299 exfoliation Methods 0.000 description 1
- 238000002594 fluoroscopy Methods 0.000 description 1
- 230000001483 mobilizing effect Effects 0.000 description 1
- 235000016709 nutrition Nutrition 0.000 description 1
- 230000035764 nutrition Effects 0.000 description 1
- 210000002747 omentum Anatomy 0.000 description 1
- 238000011275 oncology therapy Methods 0.000 description 1
- 235000016236 parenteral nutrition Nutrition 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 210000004203 pyloric antrum Anatomy 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- 231100000241 scar Toxicity 0.000 description 1
- 230000002966 stenotic effect Effects 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
Images
Landscapes
- Surgical Instruments (AREA)
Abstract
Изобретение относится к медицине, конкретно к онкохирургии, может быть использовано при субтотальной резекции желудка по поводу рака. После выполнения дистальной субтотальной резекции желудка с лимфодиссекцией D2 укрепляют гастродуоденоанастомоз. Для чего перитонизируют анастомоз наложением ткани на переднюю полуокружность гастродуоденоанастомоза и фиксацией ее швами вдоль линии анастомоза. При этом используют брыжейку поперечной ободочной кишки. Швы накладывают влево и вправо от соустья. Последовательно соединяют сначала нижний край анастомоза и участок основания брыжейки поперечной ободочной кишки. Затем накладывают швы, отступая вверх от предыдущих швов, до тех пор, пока верхний край гастродуоденального соустья не соединится с дистальной частью брыжейки поперечной ободочной кишки. Способ позволяет снизить частоту развития несостоятельности швов гастродуоденоанастомоза за счет создания дополнительной изоляции, укрытия области соустья, уменьшить травматичность оперативного вмешательства за счет отсутствия необходимости в отслоении брюшины от стенки двенадцатиперстной кишки либо пересечения и мобилизации круглой связки печени, а также сократить время операции и упростить методику укрепления швов гастродуоденального анастомоза, расширить возможности метода укрепления гастродуоденоанастомоза за счет отсутствия влияния анатомических особенностей органов пищеварения на методику перитонизации. 2 ил.
Description
Изобретение относится к медицине, точнее к онкохирургии, и может быть использовано при дистальной субтотальной резекции желудка по поводу рака.
Стандартным объемом оперативного вмешательства при раке нижней трети желудка является субтотальная дистальная резекция. Она подразумевает удаление 4\5 части желудка со всей малой кривизной, связочного аппарата и перигастральных лимфатических узлов. На сегодняшний день большинство хирургов придерживаются мнения о том, что данная операция должна заканчиваться соединением культи желудка с тонкой кишкой. В этом случае сначала наглухо ушивается двенадцатиперстная кишка, затем формируется соустье с петлей тонкой кишки либо по типу конец в бок (методика Бильрот-II), либо с тонкой кишкой по типу конец в конец (методика по РУ). Соединение культи желудка с двенадцатиперстной кишкой (гастродуоденоанастомоз) по методике Бильрот-1 после операций по поводу рака вызывает возражение, основанное на том, что данное соустье можно сформировать лишь в условиях натяжения сшиваемых органов, что, в свою очередь, несет огромный риск несостоятельности швов анастомоза.
Между тем в литературе встречаются данные об успешном использовании гастродуоденоанастомоза после резекции желудка по поводу рака. Настойчивость хирургов вопреки сложившемуся мнению заканчивать субтотальную дистальную резекцию желудка методом Бильрот-1 объясняется тем, что она имеет ряд преимуществ над методиками Бильрот-II и РУ.
1. Операция выполняется в верхнем этаже брюшной полости, что ограничивает возможное распространение опухолевых клеток по брюшной полости.
2. Сокращается время операции за счет отсутствия этапа ушивания культи желудка.
3. Дуоденальный пассаж пищи обеспечивает минимум постгастрорезекционных расстройств. Имеет наименьший риск развития рака культи желудка.
4. Отсутствуют осложнения, характерные для способа Бильрот-II: синдром приводящей петли, несостоятельность культи двенадцатиперстной кишки и т.п.
Недостаточность швов желудочно-кишечного анастомоза наиболее грозное и довольно частое осложнение субтотальной дистальной резекции желудка по поводу рака. Среди факторов, способствующих данному осложнению, основными являются нарушение кровоснабжения и натяжение сшиваемых органов. Сторонники операции Бильрот-I, чтобы уменьшить диастаз между культей желудка и двенадцатиперстной кишкой и избежать натяжения швов анастомоза, используют рассечение бессосудистых связок, фиксирующих культю желудка в брюшной полости, а также мобилизацию дуоденум по методике Кохера. Кроме того, существует ряд способов укрепления гастродуоденоанастомоза, обеспечивающих механическое и биологическое препятствие для выхода инфекции в свободную брюшную полость.
Известен способ дополнительной перитонизации гастродуоденоанастомоза с помощью листка брюшины, покрывающего верхнегоризонтальную часть двенадцатиперстной кишки (A.M.Ганичкин, С.Д.Резник. Методы восстановления желудочно-кишечной непрерывности при резекции желудка. - Л.: Медицина, 1973). Этот способ заключается в том, что рассекают и мобилизуют тонкий листок брюшины верхнегоризонтальной части двенадцатиперстной кишки, который натягивают и подшивают к культе желудка по всей передней полуокружности гастродуоденального соустья, формируя тем самым механическую защиту передней стенки анастомоза.
Однако при перитонизации гастродуоденального анастомоза имеют место частые разрывы тонкого листка брюшины при его мобилизации. Это приводит к травматизации и десерозированию стенки двенадцатиперстной кишки и вызывает образование субсерозных гематом, на месте которых в последующем формируется рубцовая ткань и возможно образование спаек. Кроме того, следует отметить сложность реализации способа из-за слабо выраженного у большинства больных листка брюшины, покрывающего верхнегоризонтальную часть двенадцатиперстной кишки, трудности при перемещении и подшивании, что не позволяет широко использовать предложенный способ.
Наиболее близким к предлагаемому способу является способ укрепления гастродуоденального анастомоза, в том числе и после дистальной субтотальной резекции желудка с лимфодиссекцией D2, с помощью круглой связки печени (п. РФ №2223051, опубл. 10,02.2004, А61В 17/00). Способ заключается в том, что рассекают круглую связку печени в средней трети и лигируют ее проксимальный отдел, на верхний край дистального отдела круглой связки печени накладывают Z-образные швы с захватом серозной оболочки культи желудка, отступив от линии анастомоза на 2,0-2,5 см, при этом вкол и выкол выполняют вдоль гастродуоденального соустья, затем на нижний край круглой связки накладывают Z-образные швы с захватом серозной оболочки двенадцатиперстной кишки, а вкол и выкол выполняют вдоль анастомоза.
Известный способ обеспечивает надежное укрытие гастродуоденоанастомоза фиброзным тяжем, что позволяет изолировать соустье от брюшной полости и предотвратить одно из основных и наиболее грозных осложнений дистальной резекции желудка - недостаточность швов анастомоза. Также способ исключает возможное метастазирование рака желудка в пупок (метастаз медсестры Джозефины) за счет рассечения и лигирования круглой связки печени.
Между тем метод имеет некоторые недостатки. Необходимость этапа мобилизации круглой связки печени увеличивает время операции, а возникающая при этом дополнительная травматизация тканей может провоцировать спаечный процесс. Поперечное пересечение круглой связки печени нарушает фиксационный (связочный) аппарат печени, что может привести к смещению ее в брюшной полости. Слабо выраженная круглая связка печени у некоторых больных создает трудности при перемещении и подшивании ее к области анастомоза, что не позволяет широко использовать предложенный способ.
Задача изобретения - снижение времени, затраченного на операцию, уменьшение травматичности, расширение возможности применения метода укрепления гастродуоденоанастомоза за счет отсутствия влияния анатомических особенностей органов пищеварения на методику перитонизации.
Поставленная задача решается тем, что после дистальной субтотальной резекции желудка с лимфодиссекцией D2, включающей перитонизацию анастомоза наложением ткани на переднюю полуокружность гастродуоденоанастомоза и ее фиксацию швами вдоль линии анастомоза, согласно изобретению перитонизацию выполняют с использованием брыжейки поперечной ободочной кишки, швы накладывают влево и вправо от соустья, последовательно соединяя сначала нижний край анастомоза и участок основания брыжейки поперечно-ободочной кишки, затем накладывают швы отступая вверх от предыдущих до тех пор, пока верхний край гастродуоденального соустья не соединится с дистальной частью брыжейки поперечно-ободочной кишки.
Поперечно-ободочная кишка начинается в правом подреберье, переходит в собственно надчревную и пупочную области и затем достигает левого подреберья. Она граничит с желудком своим верхним краем и фиксирована с ним желудочно-толстокишечной связкой. Стандартным этапом при выполнении резекции желудка по поводу рака является удаление макропрепарата в едином блоке с большим сальником, что приводит и к разрушению желудочно-толстокишечной связки. После удаления резецированного желудка с опухолью и наложения гастродуоденоанастомоза поперечно-ободочная кишка получает достаточно хорошую подвижность, так как остается фиксированной в брюшной полости только своей брыжейкой, которая берет свое начало как раз у нижнего края гастродуоденального соустья. Средняя длина брыжейки в этом месте составляет 10-15 см. Это позволяет без труда переместить поперечно-ободочную кишку в подпеченочное пространство, в результате чего ее брыжейка ложится на переднюю полуокружность гастродуоденоанастомоза. Соединив узловыми швами двенадцатиперстную кишку и культю желудка с брыжейкой поперечно-ободочной кишки, мы получаем дополнительное укрепление этой опасной зоны, что обеспечивает механическое и биологическое препятствие для выхода инфекции в свободную брюшную полость, а также профилактику натяжения швов соустья.
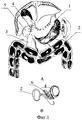
На фиг.1 представлена схема операционной картины анастомоза перед выполнением перитонизации, А - фронтальный вид; В - вид сбоку. 1 - культя желудка; 2 - поперечно-ободочная кишка; 3 - брыжейка поперечно-ободочной кишки; 4 - гастродуоденоанастомоз; 5 - двенадцатиперстная кишка; 6- лигатуры.
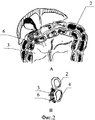
На фиг 2 - представлен окончательный вид операционной раны после выполнения перитонизации.
Сущность способа заключается в следующем. После восстановления непрерывности желудочно-кишечного тракта по методике Бильрот-1 вдоль анастомоза 4 на расстоянии, как правило, 1,5-2,0 см от соустья соединяют брыжейку 3 поперечно-ободочной кишки 2 с серозной оболочкой культи желудка 1 и двенадцатиперстной кишки 5 путем прошивания лигатурами 6. В результате этого гастродуоденальное соустье 4 оказывается надежно перитонизированно, а сшиваемые ткани хорошо прилегают друг к другу без натяжения (Фиг.2, А и В).
Соединение брыжейки 3 поперечно-ободочной кишки 2 с культей желудка 1 и двенадцатиперстной кишки 5 осуществляют узловыми швами путем прошивания лигатурами 6 через бессосудистый участок брыжейки 3 и серозный покров органов, формирующих анастомоз 1 и 5.
Швы накладывают влево и вправо от соустья 4, последовательно соединяя сначала нижний край анастомоза 4 и участок основания брыжейки 3 поперечно-ободочной кишки 2. Затем следующие 2 шва накладывают вверх от предыдущих до тех пор, пока верхний край гастродуоденального соустья 4 не соединится с дистальной частью брыжейки 3 поперечно-ободочной кишки 2.
Сущность способа поясняется примерами.
Пример 1.
Больной В., 1952 г.р., поступил в хирургическое отделение Приморского краевого онкологического диспансера 27 сентября 2007 г. с жалобами на общую слабость, тяжесть, боли умеренного характера в эпигастральной области, усиливающиеся после еды, похудание (за 4 мес. похудел на 8 кг).
Из анамнеза установлено, что вышеперечисленные жалобы появились около полугода назад, но к врачам не обращался. В начале сентября 2007 года боли в эпигастрии значительно усилились, в связи с чем больной обратился за медицинской помощью в поликлинику по месту жительства. При обследовании больному выполнена ФГДС. Эндоскопически в антральном отделе желудка по малой кривизне обнаружена блюдцеобразная опухоль до 3,5 см в диаметре, выполнена биопсия. Морфологическое заключение - высокодифференцированная аденокарцинома.
Для оперативного лечения в плановом порядке больной был направлен в хирургическое отделение Приморского краевого онкологического диспансера. При поступлении состояние больного удовлетворительное. Пациент правильного телосложения, пониженного питания. Кожа и видимые слизистые бледно-розового цвета. Гемодинамика стабильная, АД 130 и 90 мм рт.ст. Пульс 72 удара в мин, ритмичный, удовлетворительных качеств. В клиническом анализе крови и по данным биохимических анализов крови отклонений от нормы не отмечено. Анализ мочи без особенностей.
При инструментальных методах исследования (УЗИ брюшной полости, ФГДС, рентгенография легких) данных за отдаленные метастазы не выявлено. Выставлен диагноз: Рак антрального отдела желудка, блюдцеобразная форма, высокодифференцированная аденокарцинома. Учитывая локализацию опухоли в антральном отделе желудка (экзофитного роста), без отдаленных метастазов, больному была показана операция - субтотальная дистальная резекция желудка.
5 октября 2007 г. под эндотрахеальным наркозом произведена верхнесрединная лапаротомия. При ревизии брюшной полости признаков генерализации опухолевого процесса не выявлено. В антральном отделе желудка по малой кривизне определяется не прорастающая серозный покров опухоль до 3,5 см в диаметре. Произведена субтотальная дистальная резекция желудка со стандартной лимфодиссекцией D2. Учитывая достаточную мобильность культи желудка и достаточную длину двенадцатиперстной кишки, принято решение восстановить проходимость пищеварительного тракта по способу Бильрот-1 "конец в конец". При помощи двухрядного узлового шва сформирован гастродуоденоанастомоз. Затем, начиная с нижнего края соустья, отступя от него влево на 1,5 см, наложен узловой шов (путем прошивания лигатурой) на серозный покров двенадцатиперстной кишки и участок брыжейки поперечно-ободочной кишки. Далее, отступя от края соустья вправо на 1,5 см, наложен узловой шов на брыжейку поперечно-ободочной кишки и серозный покров культи желудка. Затем, отступая от предыдущих швов вверх на 1,0 см, накладывают в такой же последовательности два узловых шва, соединяющих брыжейку поперечно-ободочной кишки с серозной оболочкой двенадцатиперстной кишки и культи желудка и так далее. Последним моментом брыжейка поперечно-ободочной кишки фиксируется узловыми швами к двенадцатиперстной кишке и культе желудка на уровне верхнего края гастродуоденоанастомоза. В результате соустье надежно перитонизировано. Гемостаз, сухо. Контроль брюшной полости на инородные тела. Послойный шов раны.
Послеоперационный период протекал без каких-либо особенностей и осложнений. На 12-е сутки после операции больной в удовлетворительном состоянии был выписан. При контрольных осмотрах спустя 3 и 6 месяцев после операции:
состояние больного удовлетворительное, признаков прогрессирования ракового процесса нет.
Пример 2.
Больная Г., 1947 г.р., поступила в хирургическое отделение Приморского краевого онкологического диспансера 3 октября 2007 г. с жалобами на общую слабость, головокружение, тяжесть в эпигастрии после еды, рвоту накануне съеденной пищей, похудание (за 2 мес.похудела на 10 кг).
Из анамнеза установлено, что вышеперечисленные жалобы появились и стали нарастать около 3-х месяцев назад, но к врачам не обращалась. В конце сентября 2007 года рвота носила уже ежедневный характер, в связи с чем больная обратилась к врачу в поликлинику по месту жительства. При обследовании больной выполнена ФГДС и рентгеноскопия желудка. Эндоскопически желудок атоничен, увеличен в размерах, в антральном отделе желудка по задней стенке с переходом на малую кривизну обнаружена опухоль до 4,0 см в диаметре, экзофитно - язвенной форы, стенозирующая выходной отдел желудка. Выполнена биопсия. Морфологическое заключение - аденокарцинома средней степени дифференцировки. Рентгеноскопически опухоль пилоро-антрального отдела желудка, субкомпенсированный стеноз.
Для оперативного лечения в плановом порядке больная была направлена в хирургическое отделение Приморского краевого онкологического диспансера. При поступлении состояние больной средней степени тяжести. Пациентка правильного телосложения, пониженного питания. Кожа и видимые слизистые бледные. Гемодинамика стабильная, АД 100 и 70 мм рт.ст. Пульс 82 удара в мин, ритмичный, удовлетворительных качеств. В клиническом анализе крови анемия умеренной степени тяжести (Hb-84). В биохимическом анализе крови определяется гипопротеимэмия, водно-электролитные нарушения. Анализ мочи без особенностей.
При инструментальных методах исследования (УЗИ брюшной полости, ФГДС, рентгенография легких) данных за отдаленные метастазы не выявлено. Выставлен диагноз: Рак антрального отдела желудка, форма - умеренно-дифференцированная аденокарцинома. Субкомпенсированный стеноз. Анемия умеренной степени тяжести. Учитывая локализацию опухоли в антральном отделе желудка (экзофитно-язвенная роста), без отдаленных метастазов, больной показана операция - субтотальная дистальная резекция желудка.
В предоперационном периоде больной проводилась терапия, направленная на коррекцию анемии, водно-электролитных нарушений, парентеральное питание. 12 октября 2007 г. под эндотрахеальным наркозом произведена верхнесрединная лапаротомия. При ревизии брюшной полости признаков генерализации опухолевого процесса не выявлено. Желудок увеличен в размерах, в антральном отделе по задней стенке с переходом на малую кривизну определяется не прорастающая серозный покров опухоль до 4,0 см в диаметре. Произведена субтотальная дистальная резекция желудка со стандартной лимфодиссекцией D2. Диастаз между двенадцатиперстной кишкой и желудком в 3,0 см был устранен мобилизацией дуоденум по методике Кохера, мобильность культи желудка обеспечило рассечение селезеночно-диафрагмальной и желудочно-диафрагмальной связки. Принято решение восстановить проходимость пищеварительного тракта по способу Бильрот-1 "конец в конец". При помощи двухрядного узлового шва сформирован гастродуоденоанастомоз. Затем, начиная с нижнего края соустья, отступя от него влево на 2,0 см, наложен узловой шов (путем прошивания лигатурой) на серозный покров двенадцатиперстной кишки и участок брыжейки поперечно-ободочной кишки. Далее, отступя от края соустья вправо на 2,0 см, наложен узловой шов на брыжейку поперечно-ободочной кишки и серозный покров культи желудка. Затем, отступая от предыдущих швов вверх на 1,0 см, накладывают в такой же последовательности два узловых шва, соединяющих брыжейку поперечно-ободочной кишки с серозной оболочкой двенадцатиперстной кишки и культи желудка и так далее. Последним моментом брыжейка поперечно-ободочной кишки фиксируется узловыми швами к двенадцатиперстной кишке и культе желудка на уровне верхнего края гастродуоденоанастомоза. В результате соустье надежно перитонизировано. Гемостаз, сухо. Контроль брюшной полости на инородные тела. Послойный шов раны.
Послеоперационный период протекал без каких-либо особенностей и осложнений. На 15-е сутки после операции больная в удовлетворительном состоянии была выписана. При контрольных осмотрах спустя 3 и 6 месяцев после операции:
состояние больной удовлетворительное, проходимость гастродуоденоанастомоза сохранена, признаков прогрессирования ракового процесса нет.
Данный способ укрепления гастродуоденоанастомоза к настоящему времени использован у 12 больных. Всем пациентам выполнялась радикальная субтотальная дистальная резекция по методике Бильрот-1 с удовлетворительными результатами - ни у одного из них послеоперационный период не осложнился недостаточностью швов гастродуоденального соустья.
Таким образом, предлагаемый способ укрепления гастродуоденоанастомоза позволяет достичь заявляемого технического результата.
1. Снижается частота развития несостоятельности швов гастродуоденоанастомоза за счет создания дополнительного укрытия в области соустья с помощью брыжейки поперечно-ободочной кишки.
2. Уменьшается травматичность оперативного вмешательства за счет отсутствия необходимости в отслоении брюшины от стенки 12-перстной кишки либо пересечения и мобилизации круглой связки печени.
3. Сокращается время операции.
4. Упрощается методика укрепления швов гастродуоденального анастомоза. Способ разработан на кафедре онкологии и лучевой терапии с курсом лучевой диагностики Владивостокского государственного медицинского университета и прошел клиническую апробацию в хирургическом отделении Приморского краевого онкологического диспансера у 12 больных с удовлетворительными результатами.
Claims (1)
- Способ укрепления гастродуоденоанастомоза после дистальной субтотальной резекции желудка с лимфодиссекцией D2, включающий перитонизацию анастомоза наложением ткани на переднюю полуокружность гастродуоденоанастомоза и ее фиксацию швами вдоль линии анастомоза, отличающийся тем, что перитонизацию выполняют с использованием брыжейки поперечной ободочной кишки, при этом швы накладывают влево и вправо от соустья, последовательно соединяя сначала нижний край анастомоза и участок основания брыжейки поперечной ободочной кишки, затем накладывают швы, отступая вверх от предыдущих, до тех пор, пока верхний край гастродуоденального соустья не соединится с дистальной частью брыжейки поперечной ободочной кишки.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2007149012/14A RU2356503C1 (ru) | 2007-12-25 | 2007-12-25 | Способ укрепления гастродуоденоанастомоза |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2007149012/14A RU2356503C1 (ru) | 2007-12-25 | 2007-12-25 | Способ укрепления гастродуоденоанастомоза |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2356503C1 true RU2356503C1 (ru) | 2009-05-27 |
Family
ID=41023220
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2007149012/14A RU2356503C1 (ru) | 2007-12-25 | 2007-12-25 | Способ укрепления гастродуоденоанастомоза |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2356503C1 (ru) |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU1258387A1 (ru) * | 1984-05-25 | 1986-09-23 | Читинский государственный медицинский институт | Способ наложени межкишечного соусть |
| RU2045933C1 (ru) * | 1992-09-16 | 1995-10-20 | Иркутский медицинский институт | Способ укрепления анастомоза тонкой кишки |
| RU2223051C1 (ru) * | 2003-02-04 | 2004-02-10 | НИИ онкологии им. проф. Н.Н. Петрова | Способ укрепления гастродуоденального анастомоза |
| MD2577G2 (ru) * | 2004-05-14 | 2005-05-31 | Николай ГЛАДУН | Метод перитонизации абдоминального фланга после гемиколэктомии |
| RU2265404C2 (ru) * | 2000-10-20 | 2005-12-10 | Биличенко Вячеслав Борисович | Способ профилактики несостоятельности культи червеобразного отростка |
-
2007
- 2007-12-25 RU RU2007149012/14A patent/RU2356503C1/ru not_active IP Right Cessation
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU1258387A1 (ru) * | 1984-05-25 | 1986-09-23 | Читинский государственный медицинский институт | Способ наложени межкишечного соусть |
| RU2045933C1 (ru) * | 1992-09-16 | 1995-10-20 | Иркутский медицинский институт | Способ укрепления анастомоза тонкой кишки |
| RU2265404C2 (ru) * | 2000-10-20 | 2005-12-10 | Биличенко Вячеслав Борисович | Способ профилактики несостоятельности культи червеобразного отростка |
| RU2223051C1 (ru) * | 2003-02-04 | 2004-02-10 | НИИ онкологии им. проф. Н.Н. Петрова | Способ укрепления гастродуоденального анастомоза |
| MD2577G2 (ru) * | 2004-05-14 | 2005-05-31 | Николай ГЛАДУН | Метод перитонизации абдоминального фланга после гемиколэктомии |
Non-Patent Citations (1)
| Title |
|---|
| ЛИТТМАНН И. Брюшная хирургия. - Будапешт, 1970, 190. TAKEUCHI K. et al. A modidied stapling technique for performing Billroth I fnastomosis after distal gastrectomy, World. J. Surg., 2005, 29(1), 113-5. * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20040006351A1 (en) | Method and device for use in tissue approximation and fixation | |
| Mochiki et al. | The technique of laparoscopically assisted total gastrectomy with jejunal interposition for early gastric cancer | |
| Oshiro et al. | Successful management of refractory staple line leakage at the esophagogastric junction after a sleeve gastrectomy using the HANAROSTENT | |
| RU2727756C1 (ru) | Способ лапароскопического формирования культи желудка при гастроеюношунтировании по Ру | |
| RU2356503C1 (ru) | Способ укрепления гастродуоденоанастомоза | |
| RU2269948C2 (ru) | Способ хирургического лечения осложненных язв задней стенки желудка | |
| RU2336844C1 (ru) | Способ оперативного доступа в брюшную полость | |
| RU2156611C1 (ru) | Способ формирования коло-гастрального анастомоза при толстокишечной пластике пищевода | |
| RU2115373C1 (ru) | Способ формирования анастомоза после резекции толстой кишки | |
| RU2223051C1 (ru) | Способ укрепления гастродуоденального анастомоза | |
| RU2670694C1 (ru) | Способ обструктивной резекции тонкой кишки с наложением отсроченного анастомоза | |
| RU2826391C1 (ru) | Способ формирования пищеводно-желудочного анастомоза | |
| RU2846665C1 (ru) | Способ формирования ручного эзофагоэнтероанастомоза при лапароскопической гастрэктомии | |
| RU2813035C1 (ru) | Способ хирургического лечения морбидного ожирения у больных с сахарным диабетом 2 типа | |
| RU2742624C2 (ru) | Способ лапароскопического формирования пищеводно-кишечного анастомоза | |
| RU2822019C1 (ru) | Способ формирования надпапиллярного чресдивертикулярного холедоходуоденоанастомоза под контролем эндоскопической ультрасоногорафии при протяженной стриктуре дистального отдела холедоха и большого дуоденального сосочка | |
| RU2820732C1 (ru) | Способ хирургического лечения морбидного ожирения у больных с сахарным диабетом 2 типа | |
| RU2598796C1 (ru) | Способ проведения лапароскопической операции на кишечнике у детей с болезнью крона | |
| RU2741716C1 (ru) | Способ хирургического лечения ахалазии кардии | |
| RU2666516C1 (ru) | Способ дистальной резекции поджелудочной железы | |
| RU2768180C1 (ru) | Способ выполнения реконструктивно-восстановительной операции на внепеченочных желчных протоках | |
| RU2477081C2 (ru) | Способ двухэтапного лечения рака толстой кишки | |
| RU2437623C2 (ru) | Способ формирования арефлюксного пищеводно-тонкокишечного анастомоза | |
| RU2328992C1 (ru) | Способ хирургического формирования инвагинационного однорядного толстокишечного анастомоза | |
| RU2710215C1 (ru) | Способ асептической органосберегающей резекции полых органов пищеварительного тракта |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20101226 |
|
| NF4A | Reinstatement of patent |
Effective date: 20140610 |
|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20151226 |