RU2347750C2 - Method of complex processing natural and/or synthetic chalk, obtaining chemically pure chalk and ammonium nitrate lime - Google Patents
Method of complex processing natural and/or synthetic chalk, obtaining chemically pure chalk and ammonium nitrate lime Download PDFInfo
- Publication number
- RU2347750C2 RU2347750C2 RU2006145807/15A RU2006145807A RU2347750C2 RU 2347750 C2 RU2347750 C2 RU 2347750C2 RU 2006145807/15 A RU2006145807/15 A RU 2006145807/15A RU 2006145807 A RU2006145807 A RU 2006145807A RU 2347750 C2 RU2347750 C2 RU 2347750C2
- Authority
- RU
- Russia
- Prior art keywords
- chalk
- ammonium nitrate
- ammonium
- decomposition
- solution
- Prior art date
Links
Landscapes
- Removal Of Specific Substances (AREA)
- Fertilizers (AREA)
Abstract
Description
Изобретение относится к способу переработки природного или синтетического мела в первую очередь с целью получения химически чистого мела, который может быть использован в различных отраслях промышленности, таких как фармацевтическая, парфюмерная, пищевая, медицинская и др., а также к способу получения из отходов этого производства известково-аммиачной селитры, являющейся широко используемым в сельском хозяйстве удобрением. Основным продуктом способа является химически чистый мел (карбонат кальция).The invention relates to a method for processing natural or synthetic chalk in the first place with the aim of obtaining chemically pure chalk, which can be used in various industries, such as pharmaceutical, perfumery, food, medical, etc., as well as to a method for producing waste from this production. lime-ammonium nitrate, which is a widely used fertilizer in agriculture. The main product of the method is chemically pure chalk (calcium carbonate).
Известен способ получения очищенного карбоната кальция (мела), защищенный патентом РФ 2027672, С01F 11/18, 1995 г. Сущность этого способа заключается в разложении природного или синтетического карбоната кальция в азотной кислоте при ее расходе 1,13-1,28 кг/кг (стехиометрия 100-113%) при 50-55°С в течение 45-90 мин, обработке карбонатом кальция образовавшейся пульпы в течение 20-50 мин при расходе карбоната кальция 7,7-31% от массы исходного сырья. После отделения образовавшегося примесного осадка маточник обрабатывают карбонатом аммония в две ступени, на первую из которых подают 9,4-21,0% от общего расхода карбоната аммония, отделяют осадок - мел первой стадии конверсии. Этот мел возвращают в процесс на стадию обработки пульпы. Отделенный маточник на второй ступени обрабатывают оставшимся количеством карбоната аммония с последующим отделением целевого продукта. Целесообразно для обработки кислой пульпы использовать исходный природный или синтетический карбонат кальция или осадок - мел, полученный на первой ступени обработки карбонатом аммония.A known method of producing purified calcium carbonate (chalk), is protected by RF patent 2027672, С01F 11/18, 1995. The essence of this method is the decomposition of natural or synthetic calcium carbonate in nitric acid at a flow rate of 1.13-1.28 kg / kg (stoichiometry 100-113%) at 50-55 ° C for 45-90 minutes, treatment with calcium carbonate of the resulting pulp for 20-50 minutes at a flow of calcium carbonate of 7.7-31% by weight of the feedstock. After separation of the resulting impurity precipitate, the mother liquor is treated with ammonium carbonate in two stages, the first of which serves 9.4-21.0% of the total consumption of ammonium carbonate, and the precipitate is separated - chalk of the first conversion stage. This chalk is returned to the process to the pulp processing stage. The separated mother liquor in the second stage is treated with the remaining amount of ammonium carbonate, followed by separation of the target product. It is advisable for the treatment of acidic pulp to use the original natural or synthetic calcium carbonate or precipitate - chalk obtained in the first stage of treatment with ammonium carbonate.
В результате получают продукт, в котором содержится:The result is a product that contains:
СаСО3 - 98-99%;CaCO 3 - 98-99%;
MgCO3 - 0,30-0,37%;MgCO 3 - 0.30-0.37%;
Fe2O3 - 0,05-0,10%;Fe 2 O 3 - 0.05-0.10%;
Al2O3 - 0,05-0,10%.Al 2 O 3 - 0.05-0.10%.
Недостатком этого способа является, прежде всего, невозможность получения продукционного мела высокого качества, а также достаточно низкий выход готового продукта за счет использования полученного в процессе синтетического мела для подавления избыточной кислотности и выделения примесей. Способ предусматривает двухступенчатую очистку продукта, что технологически усложняет процесс.The disadvantage of this method is, first of all, the impossibility of obtaining a high quality production chalk, as well as a rather low yield of the finished product due to the use of synthetic chalk obtained in the process to suppress excess acidity and isolate impurities. The method involves a two-stage purification of the product, which technologically complicates the process.
Кроме того, данный способ позволяет в результате переработки получить только один продукт и иметь отход производства в виде нерастворимого остатка.In addition, this method allows as a result of processing to obtain only one product and have a waste product in the form of an insoluble residue.
Наиболее близким к описываемому по технической сущности и достигаемому результату является другой известный способ комплексной переработки природного мела с получением химически осажденного мела высокой чистоты и известково-аммиачной селитры (А.П. Филиппов, Г.К. Целищев. «Получение химически осажденного мела высокой чистоты». Химическая технология, №11, 2004, с.5-8).Closest to the described by the technical nature and the achieved result is another known method for the integrated processing of natural chalk to obtain chemically precipitated chalk of high purity and lime-ammonium nitrate (AP Filippov, GK Tselishchev. "Obtaining chemically deposited chalk of high purity ". Chemical technology, No. 11, 2004, p.5-8).
Предложенный способ включает разложение природного мела азотной кислотой, введение в полученную суспензию мела, отделение нерастворимого остатка фильтрацией, последующую конверсию раствора нитрата кальция карбонатом аммония, фильтрацию полученной суспензии с отделением мела и переработку отделенного от мела раствора нитрата аммония на известково-аммиачную селитру.The proposed method involves the decomposition of natural chalk with nitric acid, the introduction of chalk into the resulting suspension, separation of the insoluble residue by filtration, the subsequent conversion of the calcium nitrate solution with ammonium carbonate, the filtration of the resulting suspension with the separation of chalk, and the conversion of the ammonium nitrate solution separated from the chalk into lime-ammonium nitrate.
По этому способу разложение природного и/или синтетического мела, представляющего по существу карбонат кальция с некоторым количеством примесей (полуторные оксиды и силикаты), осуществляют азотной кислотой. По данному способу на разложение подают азотную кислоту в количестве 100-113,5% от стехиометрического, время разложения при этом не менее 90 минут, что было признано наиболее целесообразным, так как указано в статье, установлено, что при продолжительности контактирования реагентов менее 90 мин процесс разложения карбонатов протекает с сильным пенообразованием и выбросом пульпы. Соотношение твердой фазы к жидкой фазе (далее Т:Ж) на этой стадии составляет 1:(1,90-2,25). Температура разложения 50-55°С (в соответствии с таблицей 1 статьи). В полученную суспензию разложения вводят мел в количестве 7,7-13,5% от количества исходного сырья, значение рН маточника - 4,6-5,1 (таблица 2, там же). Температура процесса 60-70°С (первая ступень очистки). Далее по известному способу суспензию (после обработки мелом) фильтруют и маточный раствор подвергают второй ступени очистки при температуре 60-70°С раствором карбоната аммония, концентрацией 30-35%, взятого в количестве, необходимом для достижения рН 6,5-7,5.In this method, the decomposition of natural and / or synthetic chalk, which is essentially calcium carbonate with a certain amount of impurities (sesquioxides and silicates), is carried out with nitric acid. According to this method, nitric acid is supplied for decomposition in an amount of 100-113.5% of the stoichiometric, decomposition time of at least 90 minutes, which was recognized as the most appropriate, as indicated in the article, it was found that when the contact time of the reagents is less than 90 minutes the decomposition of carbonates proceeds with strong foaming and pulp discharge. The ratio of solid phase to liquid phase (hereinafter T: G) at this stage is 1: (1.90-2.25). The decomposition temperature is 50-55 ° C (in accordance with table 1 of the article). Chalk in the amount of 7.7–13.5% of the amount of the feedstock is introduced into the resulting decomposition suspension, the pH of the mother liquor is 4.6–5.1 (table 2, ibid.). The process temperature is 60-70 ° C (first stage of cleaning). Then, according to the known method, the suspension (after chalking) is filtered and the mother liquor is subjected to a second purification step at a temperature of 60-70 ° C with a solution of ammonium carbonate, concentration of 30-35%, taken in an amount necessary to achieve a pH of 6.5-7.5 .
В результате проведения этой операции получают осадок - мел, загрязненный примесями, которые возвращают на первую ступень очистки, и маточник, содержащий раствор нитрата кальция. Этот маточник обрабатывают оставшимся количеством (от второй ступени очистки) карбоната аммония. В результате получают готовый продукт (очищенный мел белизной 97-99,8%). Далее осадок примесей, отделенный ранее и содержащий 10-17% кальция, и раствор нитрата аммония смешивают в определенных пропорциях с исходным мелом, смесь сушат и гранулируют, т.е. получают известково-аммиачную селитру (ИАС).As a result of this operation, a precipitate is obtained - chalk contaminated with impurities that are returned to the first stage of purification, and a mother liquor containing a solution of calcium nitrate. This mother liquor is treated with the remaining amount (from the second stage of purification) of ammonium carbonate. The result is a finished product (purified chalk with a whiteness of 97-99.8%). Next, the precipitate of impurities, previously separated and containing 10-17% calcium, and a solution of ammonium nitrate are mixed in certain proportions with the original chalk, the mixture is dried and granulated, i.e. get calcium-ammonium nitrate (IAS).
Недостатком способа является получение недостаточно чистого конечного продукта (мела). Так, в конечном продукте содержание СаСО3+MgCO3 - 99,2%, Fe2O3 - 0,002%, Al2O3 - 0,02-0,07%, MnO - 0,001%, NO3 - 0,20-0,25%, H2O - 0,45%. Белизна продукта - 97-99,8%.The disadvantage of this method is to obtain not enough pure final product (chalk). So, in the final product, the content of CaCO 3 + MgCO 3 is 99.2%, Fe 2 O 3 is 0.002%, Al 2 O 3 is 0.02-0.07%, MnO is 0.001%, NO 3 is 0.20 -0.25%; H 2 O, 0.45%. The whiteness of the product is 97-99.8%.
Кроме того, за счет полного разложения сырья азотной кислотой практически все примеси переходят в раствор, что в дальнейшем потребует конверсию нитрата кальция карбонатом аммония осуществлять ступенчато (1-я ступень - доочистка раствора нитрата кальция, 2-я ступень - получение готового продукта - очищенного мела). Весь технологический процесс длителен по времени и требует большого числа технологических аппаратов и их объемов.In addition, due to the complete decomposition of the feedstock with nitric acid, almost all impurities pass into the solution, which in the future will require the conversion of calcium nitrate with ammonium carbonate in stages (the 1st stage - the post-treatment of the calcium nitrate solution, the 2nd stage - obtaining the finished product - purified chalk ) The whole technological process is time-consuming and requires a large number of technological devices and their volumes.
Что касается получения второго продукта - ИАС, то на его производство потребуются значительные энергетические затраты на стадии сушки вследствие получения разбавленного раствора.As for the production of the second product, IAS, its production will require significant energy costs at the drying stage due to the preparation of a diluted solution.
Задачей изобретения являлась разработка такого способа комплексной переработки природного и/или синтетического мела, который позволил бы получить готовый продукт - мел более высокого качества при одновременном технологическом упрощении процесса за счет снижения объемов технологического оборудования и числа операций, а на стадии получения ИАС позволил бы сократить энергозатраты.The objective of the invention was the development of such a method of complex processing of natural and / or synthetic chalk, which would make it possible to obtain a finished product - chalk of higher quality while simplifying the process technologically by reducing the volume of technological equipment and the number of operations, and at the stage of obtaining IAS would reduce energy costs .
Поставленная задача решается тем, что предложен способ комплексной переработки природного и/или синтетического мела, включающий разложение его азотной кислотой, введение в полученную суспензию мела, отделение нерастворимого остатка фильтрацией, последующую конверсию раствора нитрата кальция карбонатом аммония, фильтрацию полученной суспензии с отделением мела и переработку отделенного от мела раствора нитрата аммония на известково-аммиачную селитру путем его смешения с отделенным нерастворимым остатком и сырьевым мелом, гранулирование продукта. В предложенном способе разложение мела азотной кислотой осуществляют при норме ее 80-95% от стехиометрического в течение 30-50 минут при соотношении Т:Ж = 1: (2,5-3,5), мел вводят в суспензию разложения в количестве, необходимом до достижения рН 5,5-6,0, а полученный после конверсии мел выводят из процесса в качестве готового продукта, раствор нитрата аммония упаривают до концентрации 70-95% по нитрату аммония и направляют на получение ИАС. В этом способе целесообразно на конверсию нитрата кальция подавать 47-54%-ный раствор карбоната аммония в количестве, необходимом до достижения рН 7,5-8,5.The problem is solved in that a method is proposed for the complex processing of natural and / or synthetic chalk, including its decomposition with nitric acid, introduction of chalk into the resulting suspension, separation of the insoluble residue by filtration, subsequent conversion of the calcium nitrate solution with ammonium carbonate, filtration of the resulting suspension with separation of chalk and processing ammonium nitrate solution separated from the chalk on lime-ammonium nitrate by mixing it with the separated insoluble residue and raw chalk, granular product. In the proposed method, the decomposition of chalk with nitric acid is carried out at a rate of 80-95% of stoichiometric for 30-50 minutes at a ratio of T: W = 1: (2.5-3.5), chalk is introduced into the decomposition suspension in the amount necessary until a pH of 5.5-6.0 is reached, and the chalk obtained after the conversion is removed from the process as a finished product, a solution of ammonium nitrate is evaporated to a concentration of 70-95% by ammonium nitrate and sent to obtain IAS. In this method, it is advisable to apply a 47-54% solution of ammonium carbonate in the amount necessary to achieve a pH of 7.5-8.5 for the conversion of calcium nitrate.
Сущность способа заключается в том, что на стадию разложения природного и/или синтетического мела азотную кислоту подают в количестве 80-95% от стехиометрического. При этом процесс разложения идет без дополнительного подвода тепла - разогрев происходит только за счет тепла реакции. Это основано на том, что особенностью природного мела и его основного вещества - карбоната кальция - является способность растворяться в кислотах без нагревания. Мел состоит из кальцита (СаСО3), доломита (CaMg(CO3)2), магнезита (MgCO3), сидерита (FeCO3). При расходе азотной кислоты менее 100% от стехиометрического происходит взаимодействие только с кальцийсодержащими минералами, остальные минералы остаются практически не разложенными и уходят в нерастворимый остаток, а полученный после фильтрации раствор нитрата кальция получается достаточно чистым. Норма кислоты 80-95% от стехиометрического выбрана, исходя из следующего: при уменьшении ее ниже 80% кальцийсодержащие минералы растворяются не полностью, а при расходе более 95% начинают растворяться примеси, что, с одной стороны, для получения чистого мела потребует стадии дополнительной очистки, а с другой стороны, - не позволит использовать полученный осадок в производстве ИАС. Отсутствие дополнительного разогрева не вызывает бурного пенообразования, поэтому нет необходимости растягивать процесс по времени.The essence of the method lies in the fact that at the stage of decomposition of natural and / or synthetic chalk, nitric acid is fed in an amount of 80-95% of the stoichiometric. In this case, the decomposition process proceeds without additional heat supply - heating occurs only due to the reaction heat. This is based on the fact that a feature of natural chalk and its main substance - calcium carbonate - is the ability to dissolve in acids without heating. Chalk consists of calcite (CaCO 3 ), dolomite (CaMg (CO 3 ) 2 ), magnesite (MgCO 3 ), siderite (FeCO 3 ). At a nitric acid consumption of less than 100% of the stoichiometric interaction only with calcium-containing minerals occurs, the remaining minerals remain virtually undecomposed and go into an insoluble residue, and the calcium nitrate solution obtained after filtration is quite clean. The acid norm of 80-95% of the stoichiometric value is selected based on the following: when it decreases below 80%, calcium-containing minerals do not completely dissolve, and when more than 95% are consumed, impurities begin to dissolve, which, on the one hand, will require an additional purification step to obtain pure chalk and, on the other hand, it will not allow the use of the obtained precipitate in the production of IAS. The absence of additional heating does not cause violent foaming, so there is no need to stretch the process in time.
Установлено, что наиболее целесообразное время реакции составляет 30-50 мин. Снижение его до менее 30 мин не позволит полностью провести реакцию разложения, а при 50 мин полностью достигается необходимый эффект и увеличение его нецелесообразно. Большую роль играет и соотношение Т:Ж. Выбранное нами соотношение Т:Ж=1:2,5-3,5 обеспечивает получение суспензии, которая хорошо перемешивается, обеспечивая необходимый режим разложения мела, а также способствует дальнейшей хорошей фильтрации. Уменьшение в ней жидкой фазы приводит к очень плохой фильтрации, а увеличение - разбавляет раствор нитрата кальция и в итоге вызывает дополнительные затраты энергии.It was found that the most appropriate reaction time is 30-50 minutes. Reducing it to less than 30 minutes will not allow the decomposition reaction to be completely carried out, and at 50 minutes the desired effect is fully achieved and its increase is impractical. A large role is played by the ratio T: F. The ratio T: W = 1: 2.5-3.5 that we have chosen provides a suspension that mixes well, providing the necessary decomposition mode for chalk, and also contributes to further good filtration. Reducing the liquid phase in it leads to very poor filtration, and an increase dilutes the calcium nitrate solution and ultimately causes additional energy costs.
Далее на стадии получения ИАС было предложено раствор нитрата аммония предварительно упаривать до концентрации 70-95%, а затем смешивать с остальными компонентами. Это приводит к сбережению энергоресурсов, т.к. удаление влаги на стадии упаривания - менее энергоемкий процесс, чем на стадии сушки. Кроме того, этот прием позволит получать гранулированный ИАС, используя не только грануляторы типа БГС, но и башни приллирования, что дает более широкие возможности использования способа в зависимости от имеющегося на конкретном предприятии оборудования.Further, at the stage of obtaining IAS, it was proposed to pre-evaporate the ammonium nitrate solution to a concentration of 70-95%, and then mix with the rest of the components. This leads to energy conservation, as moisture removal at the evaporation stage is a less energy-intensive process than at the drying stage. In addition, this technique will make it possible to obtain granular IAS using not only granulators such as BGS, but also prilling towers, which gives wider possibilities of using the method depending on the equipment available at a particular enterprise.
Осуществление способа проиллюстрировано в примере.The implementation of the method is illustrated in the example.
Пример. Все опыты проводили на пробе следующего химического состава (мас.%): СаСО3 - 93,84; MgO - 0,17; Fe2O3 - 0,27; Al2O3 - 0,73; н.о. - 3,68; SiO2 - 1,50; Cu -0,0067; Mn - 0,040 (в пересчете на сухое вещество).Example. All experiments were carried out on a sample of the following chemical composition (wt.%): CaCO 3 - 93.84; MgO - 0.17; Fe 2 O 3 0.27; Al 2 O 3 - 0.73; but. - 3.68; SiO 2 - 1.50; Cu -0.0067; Mn - 0.040 (in terms of dry matter).
Навеску 1000 г исходного природного мела смешивали с промывной водой в количестве 774 г. В полученную пульпу дозировали концентрированную азотную кислоту (53%) в количестве 90% от стехиометрического количества на СаО исходного мела - 2226 г. Температура пульпы повышалась за счет выделения теплоты химической реакции до 40°С. Время подачи кислоты - 40 минут, Т:Ж=1:3. После окончания подачи кислоты пульпу нагревают до t=75-85°С. Суспензия содержит 134 г/л Са, в нее дозируют порцию исходного мела в количестве 100 г (10%), значение рН 5,9. Пульпу в количестве 3637,1 г фильтруют. При этом получают фильтрат, содержащий 140 г/л Са, и нерастворимый остаток в количестве 173,6 г, влажностью 50%, который без промывки используют для получения азотсодержащего удобрения, известково-аммиачной селитры. Очищенный раствор нитрата кальция в количестве 3463,5 г подвергают обработке раствором карбоната аммония в количестве 1613,1 г (концентрация 52%). Пульпу фильтруют, осадок (целевой мел) промывают трехкратной противоточной промывкой и сушат. При этом получают СаСО3 в количестве 868,4 г. Карбонат кальция состава, % на сухое вещество: СаСО3 - 99,8%, Fe2O3 - 2∙10-4, Al2O3 - 4∙10-4, Cu - 5∙10-4, NO3 - следы, MnO - 0,001%. Белизна - коэффициент отражения - 99%. Раствор нитрата аммония, основной фильтрат, в количестве 3339,8 г, и первую промывную воду направляют на упарку. Полученный раствор в количестве 1661,7 г с содержанием основного вещества (нитрата аммония) 74% смешивают с высушенным нерастворимым остатком в количестве 86,8 г и исходным карбонатным сырьем в количестве 301,5 г, полученную смесь подают в барабанный гранулятор-сушилку (БГС). Полученное удобрение содержит 26% азота общего, имеет прочность 2 кг на гранулу.A portion of 1000 g of the original natural chalk was mixed with wash water in an amount of 774 g. Concentrated nitric acid (53%) was dosed into the resulting pulp in an amount of 90% of the stoichiometric amount in CaO of the initial chalk - 2226 g. The pulp temperature was increased due to the heat of the chemical reaction up to 40 ° C. Acid supply time - 40 minutes, T: W = 1: 3. After completion of the acid supply, the pulp is heated to t = 75-85 ° C. The suspension contains 134 g / l of Ca, a portion of the initial chalk is dosed into it in an amount of 100 g (10%), pH 5.9. The pulp in the amount of 3637.1 g is filtered. In this case, a filtrate containing 140 g / l of Ca and an insoluble residue in an amount of 173.6 g, humidity 50%, which without washing are used to obtain nitrogen-containing fertilizer, lime-ammonium nitrate, are obtained. A purified solution of calcium nitrate in an amount of 3463.5 g is subjected to treatment with a solution of ammonium carbonate in an amount of 1613.1 g (concentration 52%). The pulp is filtered, the precipitate (target chalk) is washed three times with countercurrent washing and dried. In this case, CaCO 3 in the amount of 868.4 g is obtained. Calcium carbonate composition,% on dry matter: CaCO 3 - 99.8%, Fe 2 O 3 - 2 ∙ 10 -4 , Al 2 O 3 - 4 ∙ 10 -4 , Cu - 5 ∙ 10 -4 , NO 3 - traces, MnO - 0.001%. Whiteness - reflection coefficient - 99%. A solution of ammonium nitrate, the main filtrate, in the amount of 3339.8 g, and the first wash water is directed to the evaporation. The resulting solution in an amount of 1661.7 g with a basic substance (ammonium nitrate) content of 74% is mixed with a dried insoluble residue in an amount of 86.8 g and an initial carbonate feed in an amount of 301.5 g, the resulting mixture is fed to a drum granulator dryer ) The resulting fertilizer contains 26% of total nitrogen, has a strength of 2 kg per granule.
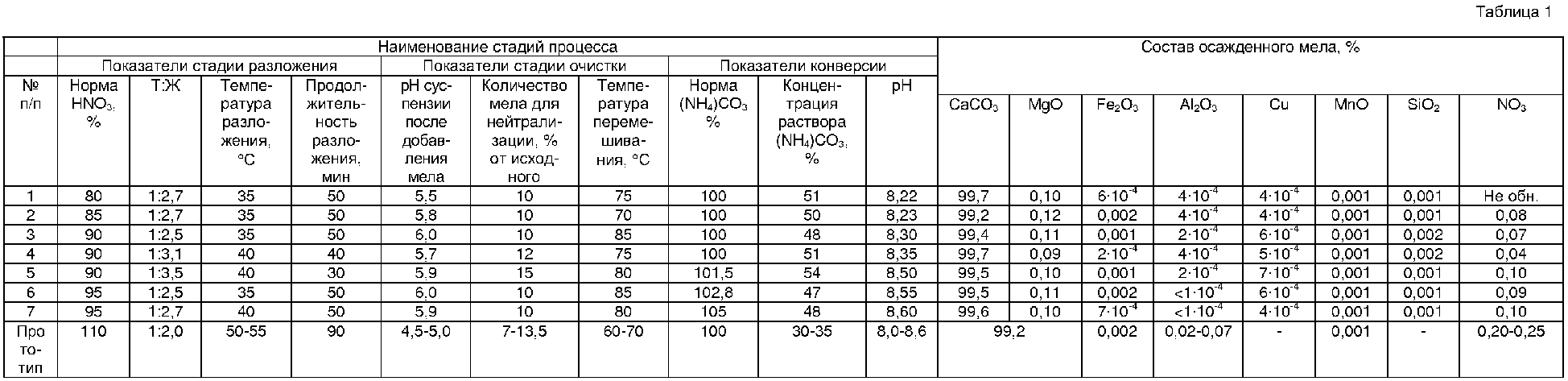
Результаты остальных опытов сведены в таблицу 1.The results of the remaining experiments are summarized in table 1.
Как следует из данных, представленных в таблице 1, предложенный способ получения химически чистого мела позволяет, прежде всего, повысить качество очистки исходного мела от сопутствующих примесей, а также сократить приблизительно в 2 раза продолжительность стадии разложения мела при снижении пеновыделения вследствие более низкой температуры (около 40°С против 50-55°С в прототипе); количество стадий очистки мела (до одной); снизить металлоемкость аппаратурного оформления процесса; повысить концентрацию продукционного раствора аммиачной селитры, исключить стадию доочистки раствора нитрата кальция методом конверсии.As follows from the data presented in table 1, the proposed method for producing chemically pure chalk allows, first of all, to improve the quality of purification of the initial chalk from associated impurities, as well as to reduce by about 2 times the duration of the stage of decomposition of chalk with a decrease in foam due to lower temperature (about 40 ° C against 50-55 ° C in the prototype); the number of stages of chalk cleaning (up to one); reduce the intensity of the hardware design process; increase the concentration of the production solution of ammonium nitrate, exclude the stage of post-treatment of the calcium nitrate solution by the conversion method.
Claims (2)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2006145807/15A RU2347750C2 (en) | 2006-12-21 | 2006-12-21 | Method of complex processing natural and/or synthetic chalk, obtaining chemically pure chalk and ammonium nitrate lime |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2006145807/15A RU2347750C2 (en) | 2006-12-21 | 2006-12-21 | Method of complex processing natural and/or synthetic chalk, obtaining chemically pure chalk and ammonium nitrate lime |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2006145807A RU2006145807A (en) | 2008-06-27 |
| RU2347750C2 true RU2347750C2 (en) | 2009-02-27 |
Family
ID=39679772
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2006145807/15A RU2347750C2 (en) | 2006-12-21 | 2006-12-21 | Method of complex processing natural and/or synthetic chalk, obtaining chemically pure chalk and ammonium nitrate lime |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2347750C2 (en) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2509724C1 (en) * | 2012-08-13 | 2014-03-20 | Общество с ограниченной ответственностью Инженерно-производственная компания "ИНТЕРФОС" | Method of producing highly pure calcium carbonate and nitrogen-sulphate fertiliser during complex processing of phosphogypsum |
-
2006
- 2006-12-21 RU RU2006145807/15A patent/RU2347750C2/en not_active IP Right Cessation
Non-Patent Citations (1)
| Title |
|---|
| ФИЛИППОВ А.П., ЦЕЛИЩЕВ Г.К. Получение химически осажденного мела высокой чистоты. Химическая технология, №11, 2004, с.5-8. * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2509724C1 (en) * | 2012-08-13 | 2014-03-20 | Общество с ограниченной ответственностью Инженерно-производственная компания "ИНТЕРФОС" | Method of producing highly pure calcium carbonate and nitrogen-sulphate fertiliser during complex processing of phosphogypsum |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2006145807A (en) | 2008-06-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN108529652B (en) | Resource utilization process of industrial sodium chloride | |
| CN210559433U (en) | System for utilize ardealite to prepare calcium carbonate | |
| US6419887B1 (en) | Process for the treatment of residual liquors from the ammoniation and carbonation of alkali metal salts | |
| RU2347750C2 (en) | Method of complex processing natural and/or synthetic chalk, obtaining chemically pure chalk and ammonium nitrate lime | |
| CA2766767A1 (en) | Process for production of commercial quality potassium nitrate from polyhalite | |
| CN106564926B (en) | A kind of method that hydrochloric acid decomposition phosphorus tailing prepares calcium sulfate and high magnesium compound fertilizer | |
| RU2412140C2 (en) | Method of producing compound fertilisers | |
| CN101555209A (en) | Clean producing method of aminoacetic acid with chloroactic acid ammonolysis method | |
| RU2687439C1 (en) | Method of producing soda ash and gypsum | |
| US4007030A (en) | Process for the simultaneous manufacture of phosphoric acid or the salts thereof and a complex multi-component mineral fertilizer | |
| RU2238906C2 (en) | Manufacture of alkali metal salts via combined ion-exchange/crystallization method | |
| RU2509724C1 (en) | Method of producing highly pure calcium carbonate and nitrogen-sulphate fertiliser during complex processing of phosphogypsum | |
| US1924041A (en) | Process of manufacturing alpha product containing ammonium nitrate and calcium carbonate | |
| RU2283283C1 (en) | Process of producing h-purity lithium carbonate from lithium-bearing chloride brines | |
| RU2314278C1 (en) | Method of manufacturing granulated complex fertilizer | |
| US2801155A (en) | Method of producing magnesium hydroxide from dolomite by means of nitric acid | |
| CN105621459B (en) | A kind of preparation method of sodium nitrate | |
| CN105565363B (en) | A kind of method that lignocellulosic ester catalysis processing waste sulfuric acid from alkylation prepares copper sulphate | |
| RU2404947C1 (en) | Method of obtaining complex fertilisers | |
| US1903684A (en) | Process for the simultaneous production of precipitated dicalcium phosphate and nitrates | |
| RU2181349C1 (en) | Method to obtain humous-mineral fertilizer | |
| RU2680269C1 (en) | Method of processing phosphogipsa for nitrogen-phosphorous fertilizer | |
| RU2145316C1 (en) | Method of preparing complex fertilizers | |
| RU2789134C1 (en) | Method for producing ammonium bromide | |
| RU2027672C1 (en) | Method of production of purified calcium carbonate |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20121222 |