RU196383U1 - Устройство для иммунохроматографической экспрессной лабораторной и внелабораторной одновременной детекции токсичных контаминантов - поверхностно активных веществ нонилфенола и бисфенола а в питьевых, бытовых, природных и сточных водах - Google Patents
Устройство для иммунохроматографической экспрессной лабораторной и внелабораторной одновременной детекции токсичных контаминантов - поверхностно активных веществ нонилфенола и бисфенола а в питьевых, бытовых, природных и сточных водах Download PDFInfo
- Publication number
- RU196383U1 RU196383U1 RU2019138779U RU2019138779U RU196383U1 RU 196383 U1 RU196383 U1 RU 196383U1 RU 2019138779 U RU2019138779 U RU 2019138779U RU 2019138779 U RU2019138779 U RU 2019138779U RU 196383 U1 RU196383 U1 RU 196383U1
- Authority
- RU
- Russia
- Prior art keywords
- membrane
- nonylphenol
- bisphenol
- test
- analysis
- Prior art date
Links
- IGFHQQFPSIBGKE-UHFFFAOYSA-N Nonylphenol Natural products CCCCCCCCCC1=CC=C(O)C=C1 IGFHQQFPSIBGKE-UHFFFAOYSA-N 0.000 title claims abstract description 51
- SNQQPOLDUKLAAF-UHFFFAOYSA-N nonylphenol Chemical compound CCCCCCCCCC1=CC=CC=C1O SNQQPOLDUKLAAF-UHFFFAOYSA-N 0.000 title claims abstract description 51
- 238000001514 detection method Methods 0.000 title claims abstract description 31
- 239000000356 contaminant Substances 0.000 title claims abstract description 16
- 231100000331 toxic Toxicity 0.000 title claims abstract description 15
- 230000002588 toxic effect Effects 0.000 title claims abstract description 15
- 239000013543 active substance Substances 0.000 title claims abstract description 7
- IISBACLAFKSPIT-UHFFFAOYSA-N bisphenol A Chemical compound C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 claims abstract description 118
- 238000012360 testing method Methods 0.000 claims abstract description 86
- 239000012528 membrane Substances 0.000 claims abstract description 74
- 241000283973 Oryctolagus cuniculus Species 0.000 claims abstract description 17
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 claims abstract description 15
- 239000000020 Nitrocellulose Substances 0.000 claims abstract description 12
- 238000010521 absorption reaction Methods 0.000 claims abstract description 12
- 229920001220 nitrocellulos Polymers 0.000 claims abstract description 12
- 108010078791 Carrier Proteins Proteins 0.000 claims abstract description 11
- 102000014914 Carrier Proteins Human genes 0.000 claims abstract description 11
- 238000006243 chemical reaction Methods 0.000 claims abstract description 8
- 241000283707 Capra Species 0.000 claims abstract description 7
- 108060003951 Immunoglobulin Proteins 0.000 claims abstract description 7
- 239000004793 Polystyrene Substances 0.000 claims abstract description 7
- 102000018358 immunoglobulin Human genes 0.000 claims abstract description 7
- 229940072221 immunoglobulins Drugs 0.000 claims abstract description 7
- 229920002223 polystyrene Polymers 0.000 claims abstract description 7
- 238000000926 separation method Methods 0.000 claims abstract description 7
- 239000011152 fibreglass Substances 0.000 claims abstract description 6
- 239000000203 mixture Substances 0.000 claims abstract description 5
- 108091003079 Bovine Serum Albumin Proteins 0.000 claims abstract 2
- 235000010469 Glycine max Nutrition 0.000 claims abstract 2
- 244000068988 Glycine max Species 0.000 claims abstract 2
- 101710162629 Trypsin inhibitor Proteins 0.000 claims abstract 2
- 229940122618 Trypsin inhibitor Drugs 0.000 claims abstract 2
- 229940098773 bovine serum albumin Drugs 0.000 claims abstract 2
- 239000002753 trypsin inhibitor Substances 0.000 claims abstract 2
- 239000002250 absorbent Substances 0.000 claims description 4
- 230000002745 absorbent Effects 0.000 claims description 4
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 claims description 2
- 239000000758 substrate Substances 0.000 claims 1
- 238000004458 analytical method Methods 0.000 abstract description 77
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 abstract description 14
- 239000004094 surface-active agent Substances 0.000 abstract description 9
- 239000007787 solid Substances 0.000 abstract description 7
- 239000002131 composite material Substances 0.000 abstract description 6
- 230000035622 drinking Effects 0.000 abstract description 5
- 239000003365 glass fiber Substances 0.000 abstract description 5
- 239000002351 wastewater Substances 0.000 abstract description 5
- 238000000034 method Methods 0.000 abstract description 4
- 239000008239 natural water Substances 0.000 abstract description 4
- 239000003153 chemical reaction reagent Substances 0.000 abstract description 3
- 238000002360 preparation method Methods 0.000 abstract description 2
- MYSWGUAQZAJSOK-UHFFFAOYSA-N Ciprofloxacin Natural products C12=CC(N3CCNCC3)=C(F)C=C2C(=O)C(C(=O)O)=CN1C1CC1 MYSWGUAQZAJSOK-UHFFFAOYSA-N 0.000 description 17
- 238000010186 staining Methods 0.000 description 14
- WIIZWVCIJKGZOK-RKDXNWHRSA-N chloramphenicol Chemical compound ClC(Cl)C(=O)N[C@H](CO)[C@H](O)C1=CC=C([N+]([O-])=O)C=C1 WIIZWVCIJKGZOK-RKDXNWHRSA-N 0.000 description 12
- 238000002965 ELISA Methods 0.000 description 10
- 229960005091 chloramphenicol Drugs 0.000 description 10
- 229960003405 ciprofloxacin Drugs 0.000 description 9
- 239000007788 liquid Substances 0.000 description 7
- 238000011161 development Methods 0.000 description 6
- 239000000427 antigen Substances 0.000 description 5
- 108091007433 antigens Proteins 0.000 description 5
- 102000036639 antigens Human genes 0.000 description 5
- 230000015572 biosynthetic process Effects 0.000 description 4
- 235000013365 dairy product Nutrition 0.000 description 4
- 239000003651 drinking water Substances 0.000 description 4
- 235000020188 drinking water Nutrition 0.000 description 4
- 239000012530 fluid Substances 0.000 description 4
- 238000012544 monitoring process Methods 0.000 description 4
- 239000003242 anti bacterial agent Substances 0.000 description 3
- 229940088710 antibiotic agent Drugs 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 2
- 230000007613 environmental effect Effects 0.000 description 2
- 229940124307 fluoroquinolone Drugs 0.000 description 2
- 235000013305 food Nutrition 0.000 description 2
- 238000003018 immunoassay Methods 0.000 description 2
- 230000000984 immunochemical effect Effects 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 239000002105 nanoparticle Substances 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 239000002689 soil Substances 0.000 description 2
- 108091023037 Aptamer Proteins 0.000 description 1
- 231100000678 Mycotoxin Toxicity 0.000 description 1
- 239000003945 anionic surfactant Substances 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000012965 benzophenone Substances 0.000 description 1
- 150000008366 benzophenones Chemical class 0.000 description 1
- QRUDEWIWKLJBPS-UHFFFAOYSA-N benzotriazole Chemical compound C1=CC=C2N[N][N]C2=C1 QRUDEWIWKLJBPS-UHFFFAOYSA-N 0.000 description 1
- 239000012964 benzotriazole Substances 0.000 description 1
- 210000000133 brain stem Anatomy 0.000 description 1
- 238000005251 capillar electrophoresis Methods 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 238000004737 colorimetric analysis Methods 0.000 description 1
- 239000002537 cosmetic Substances 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- RGLYKWWBQGJZGM-ISLYRVAYSA-N diethylstilbestrol Chemical compound C=1C=C(O)C=CC=1C(/CC)=C(\CC)C1=CC=C(O)C=C1 RGLYKWWBQGJZGM-ISLYRVAYSA-N 0.000 description 1
- 229960000452 diethylstilbestrol Drugs 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 239000011363 dried mixture Substances 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 210000000750 endocrine system Anatomy 0.000 description 1
- 239000003344 environmental pollutant Substances 0.000 description 1
- 229960005309 estradiol Drugs 0.000 description 1
- 229930182833 estradiol Natural products 0.000 description 1
- 229940011871 estrogen Drugs 0.000 description 1
- 239000000262 estrogen Substances 0.000 description 1
- 102000015694 estrogen receptors Human genes 0.000 description 1
- 108010038795 estrogen receptors Proteins 0.000 description 1
- 230000003203 everyday effect Effects 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 229910001385 heavy metal Inorganic materials 0.000 description 1
- 239000003845 household chemical Substances 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000002636 mycotoxin Substances 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 229920000847 nonoxynol Polymers 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000000575 pesticide Substances 0.000 description 1
- 239000002953 phosphate buffered saline Substances 0.000 description 1
- 230000010287 polarization Effects 0.000 description 1
- 231100000719 pollutant Toxicity 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 238000002198 surface plasmon resonance spectroscopy Methods 0.000 description 1
- 210000001685 thyroid gland Anatomy 0.000 description 1
- 239000000273 veterinary drug Substances 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/558—Immunoassay; Biospecific binding assay; Materials therefor using diffusion or migration of antigen or antibody
Landscapes
- Health & Medical Sciences (AREA)
- Immunology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Chemical & Material Sciences (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Investigating Or Analyzing Non-Biological Materials By The Use Of Chemical Means (AREA)
Abstract
Заявленное устройство предназначено для иммунохроматографической экспрессной лабораторной и внелабораторной одновременной детекции токсичных контаминантов - поверхностно активных веществ (ПАВ) нонилфенола и бисфенола А в питьевых, бытовых, природных и сточных водах. Устройство представляет собой мультимембранный композит с нанесенными иммунореагентами (тест-полоску). Мультимембранный композит состоит из рабочей нитроцеллюлозной мембраны на твердой полистироловой основе с нанесенными иммунореагентами, стекловолоконной мембраны с нанесенными иммунореагентами, мембраны для впитывания и сепарации исследуемого образца и конечной адсорбирующей мембраны для впитывания компонентов образца после прохождения реакции. Отличительной особенностью заявленного устройства является то, что в контрольную зону (К.З.) нанесены поликлональные козьи антитела, специфичные к иммуноглобулинам кролика. В первую тестовую зону (Т.З.1) нанесен конъюгат нонилфенола с белком-носителем бычьим сывороточным альбумином (БСА). Во вторую тестовую зону (Т.З.2) нанесен конъюгат бисфенола А с белком-носителем соевым ингибитором трипсина (СИТ). На стекловолоконную мембрану нанесена смесь конъюгатов поликлональных кроличьих антител, специфичных к нонилфенолу, с коллоидным золотом и поликлональных кроличьих антител, специфичных к бисфенолу А, с коллоидным золотом. Для проведения анализа не требуется никаких дополнительных приспособлений. Продолжительность анализа составляет 10 мин без учета пробоподготовки. Технической задачей заявленной полезной модели является одновременная детекция двух токсичных контаминантов - нонилфенола и бисфенола А в пробах воды. Технический результат заявленной полезной модели заключается в одновременной детекции на одной тест-полоске двух токсичных контаминантов - поверхностно активных веществ нонилфенола и бисфенола А с использованием простой одностадийной процедуры проведения анализа, обеспечиваемой за счет нанесения на тест-полоску всех необходимых реагентов.
Description
Полезная модель относится к определению токсичных контаминантов - поверхностно активных веществ нонилфенола и бисфенола А и может быть использована как экспрессное средство лабораторного и внелабораторного контроля для обеспечения безопасности разных видов потребительской продукции (питьевой и бытовой воды) и мониторинга окружающей среды (природных и сточных вод).
Устройство предназначено для иммунохроматографической экспрессной лабораторной и внелабораторной одновременной детекции токсичных контаминантов - поверхностно активных веществ нонилфенола и бисфенола А в питьевых, бытовых, природных и сточных водах.
Поверхностно активные вещества, используемые человеком в повседневной жизни, распространяются в составе сточных вод и, в связи с возрастающими объемами потребления, являются загрязнителями мирового масштаба. Широко применяются в промышленности представители анионных ПАВ - линейные алкилбензолсульфонаты и неионные ПАВ - нонилфенолполиэтоксилаты, которые в процессе деградации образуют стабильные продукты - октилфенол и нонилфенол.
Наиболее опасными ПАВ являются бисфенол А, нонилфенол, бензофеноны и бензотриазол. Структура бисфенола А сходна со структурой эстрогенов - эстрадиола и диэтилстильбэстрола, в связи с чем данное соединение и его аналоги отнесены к факторам разрушения эндокринной системы. Связываясь с рецепторами эстрогенов, данные соединения нарушают нормальное функционирование щитовидной и поджелудочной желез, мозга, иммунной системы. В связи с вышеперечисленными свойствами в странах Евросоюза установлена предельно допустимая концентрация бисфенола А в воде и почве - 0,6 мг/кг. В РФ нормативы содержания бисфенола А в почве и пище не установлены, в воде установлен ПДК, равный 0,01 мг/дм. С января 2005 г. оксиэтилированные нонилфенолы (неонолы) запрещены Еврокомиссией к использованию на территории ЕС в концентрации более 0,1% в промышленных средствах очистки, товарах бытовой химии, косметике и других областях применения. В РФ установлен ПДК нонилфенолов в воде объектов рыбохозяйственного значения в пределах от 0,001 до 0,3 мг/дм3.
Для определения ПАВ используется жидкостная хроматография, газовая хроматография с масс-спектрометрической детекцией, капиллярный электрофорез. Колориметрические методы определения контаминант с использованием наночастиц перспективны благодаря сочетанию эффекта поверхностного плазмонного резонанса и селективной адсорбции рецепторных молекул на поверхность частиц за счет различных типов взаимодействий. Несмотря на такие преимущества, как высокая точность и низкий предел обнаружения, для применения вышеперечисленных инструментальных методов необходимо дорогостоящее оборудование, высокоочищенные растворители, квалифицированный персонал, а стоимость характеристики одной пробы довольно высока.
В последнее десятилетие для определения ПАВ активно развиваются альтернативные методы - иммуноферментный анализ (ИФА), поляризационный флуороиммуноанализ (ПФИА), рассматривается применение аптамеров в качестве рецепторных молекул и различных наночастиц в качестве маркеров. Возможности иммуноанализа связаны с его методической простотой, а также производительностью, обеспечивающей одновременное тестирование до 80 проб в течение 1-2 часов, а в кинетических форматах - в течение 10-20 мин. Так, Huang и соавторы использовали моноклональные антитела к бисфенолу А для разработки гомогенного ПФИА с пределом обнаружения 5,6 нг/мл. Мартьяновым и соавторами был разработан ИФА нонилфенола и его структурных аналогов в загрязненных образцах воды с пределом обнаружения 10 нг/мл. Аналогичные результаты были представлены в последующей публикации Бураковского и Лухверчик. Представленные в литературе разработки иммунохимических тест-систем для определения ПАВ в основном сфокусированы на создании и апробации различных вариантов иммуносенсорных систем, предполагающих использование дополнительного приборного обеспечения и в связи с этим непригодных для быстрого внелабораторного тестирования.
Простой формой иммунохимического анализа является иммунохроматографический анализ (ИХА), который обнаруживает присутствие антигена (токсичного контаминанта) в жидкой пробе за 10-15 минут. ИХА основан на движении жидкой пробы вдоль мембраны, которое приводит к образованию на разных участках мембраны специфических иммунных комплексов. Конъюгированный со специфическими антителами окрашенный маркер (коллоидное золота) распределяется по мембране, и его наличие или отсутствие в определенных участках мембраны по окончании анализа является основанием для вывода о полученных результатах. Использование ИХА для детекции токсичных контаминантов обеспечивает достижение ряда преимуществ - проведение эффективного контроля во внелабораторных условиях, экспрессность проведения анализа при минимальной пробоподготовке, проведение анализа в одну стадию без необходимости в дополнительных реагентах и манипуляциях и простоту детектирования и интерпретации результатов анализа.
Несмотря на то, что ИХА активно разрабатывается и применяется для диагностики токсичных контаминантов (пестицидов, микотоксинов, ветеринарных препаратов, поверхностно активных веществ, тяжелых металлов), в научной и коммерческой литературе нет описания разработки иммунохроматографических тест-систем для одновременного определения нонилфенола и бисфенола А.
Наиболее близкими аналогами заявляемой полезной модели являются основанные на реакции антиген-антитело иммунохроматографические тест-системы для детекции одного и двух токсичных контаминантов:
тест-система для определения бисфенола А в талой воде, описанная в публикации Дзантиева и соавторов «Lateral flow immunoassay for bisphenol A: Development of test strips and their application for ecological monitoring» (Иммунохроматографический анализ бисфенола А: разработка тестов и их применение для экологического мониторинга), International Conference on Applied Physics, Power and Material Science, IOP Conf. Series: Journal of Physics: Conf. Series, 2019, v. 1172, 012088. DOI: 10.1088/1742-6596/1172/1/012088;
тест-система для одновременного определения двух антибиотиков - ципрофлоксацина и хлорамфеникола, в молочных продуктах, описанная в публикации Гендриксон и соавторов ((Development of a multicomponent immunochromatographic test system for the determination of fluoroquinolone and amphenicol antibiotics in dairy products)) (Разработка многокомпонентной иммунохроматографической тест-системы для определения фторхинолоновых и амфениколовых антибиотиков в молочных продуктах), Journal of the Science of Food and Agriculture, 2019, v. 99, N 8, p. 3834-3842. DOI: 10.1002/jsfa.9605.
Представленная в публикации Дзантиева и соавторов тест-система представляет собой мультимембранный композит размерами 78×3,5×1,5 мм, который состоит из:
нитроцеллюлозной рабочей мембраны на твердой полистироловой основе с нанесенными в контрольную зону поликлональными козьими антителами к иммуноглобулинам кролика и нанесенным в тестовую зону конъюгатом бисфенола А с белком-носителем СИТ;
стекловолоконной мембраны с нанесенным конъюгатом поликлональных кроличьих антител, специфичных к бисфенолу А, с коллоидным золотом;
мембраны для впитывания и сепарации исследуемого образца;
конечной адсорбирующей мембраны для впитывания компонентов образца после прохождения реакции.
Анализ проводят следующим образом:
1. Образцы снега расплавляют при комнатной температуре, твердые примеси отфильтровывают и полученную талую воду используют для ИХА.
2. 100 мкл фильтрованной талой воды переносят в пластиковую пробирку вместимостью 1,5 мл.
3. Тест-полоску погружают вертикально нижним концом мембраны для впитывания образца в жидкость на 10 мин.
4. Через 10 мин тест-полоску вынимают. Результат анализа фиксируют визуально или с использованием детектора с видеоцифровой регистрацией.
Результат анализа интерпретируют следующим образом:
1. Если через 10 мин на рабочей мембране тест-полоски появляются две линии (контрольная и тестовая), окрашенные в темно-красный цвет, то результат анализа считается отрицательным, т.е. в образце не содержится бисфенол А или его концентрация ниже предела обнаружения.
2. Если через 10 мин на рабочей мембране тест-полоски появляется одна темно-красная линия (контрольная), то результат анализа считается положительным, т.е. в образце содержится бисфенол А в концентрации равной или выше предела обнаружения.
3. Если через 10 мин на рабочей мембране тест-полоски не образуется ни одной окрашенной линии или образуется только одна тестовая окрашенная линия, то результат анализа считается недействительным.
Представленная в публикации Гендриксон и соавторов тест-система представляет собой мультимембранный композит размерами 80×3,5×2,0 мм, который состоит из:
нитроцеллюлозной рабочей мембраны на твердой полистироловой основе с нанесенной в контрольную зону смесью поликлональных козьих антител к иммуноглобулинам мыши и кролика, нанесенным в первую тестовую зону конъюгатом хлорамфеникола с белком-носителем СИТ и нанесенным во вторую тестовую зону конъюгатом ципрофлоксацина с белком-носителем яичным альбумином;
стекловолоконной мембраны с нанесенной смесью конъюгатов моноклональных мышиных антител, специфичных к хлорамфениколу, с коллоидным золотом и поликлональных кроличьих антител, специфичных к ципрофлоксацину, с коллоидным золотом;
мембраны для впитывания и сепарации исследуемого образца;
конечной адсорбирующей мембраны для впитывания компонентов образца после прохождения реакции.
Анализ проводят следующим образом:
1. Образцы молочных продуктов разбавляют в два раза 0,15 М фосфатно-солевым буфером с рН 7,4.
2. По 100 мкл пробы вносят в лунку иммунологического микропланшета.
3. Тест-полоску погружают вертикально нижним концом мембраны для впитывания образца в жидкость на 15 мин.
4. Через 15 мин после начала анализа тест-полоску вынимают и результат фиксируют визуально или с использованием детектора с видеоцифровой регистрацией.
Результат анализа интерпретируют следующим образом.
1. Если через 15 мин на рабочей мембране тест-полоски появляются три линии (контрольная и две тестовые), окрашенные в темно-красный цвет, то результат анализа считается отрицательным, т.е. в образце не содержатся хлорамфеникол и ципрофлоксацин или их концентрации ниже пределов обнаружения.
2. Если через 15 мин на рабочей мембране тест-полоски появляются две темно-красные линии (контрольная и первая по ходу движения жидкости тестовая), то результат анализа считается положительным по ципрофлоксацину и отрицательным по хлорамфениколу, т.е. в образце содержится ципрофлоксацин в концентрации равной или выше предела обнаружения и не содержится хлорамфеникол (или его концентрация ниже предела обнаружения).
3. Если через 15 мин на рабочей мембране тест-полоски появляются две темно-красные линии (контрольная и вторая по ходу движения жидкости тестовая), то результат анализа считается положительным по хлорамфениколу и отрицательным по ципрофлоксацину, т.е. в образце содержится хлорамфеникол в концентрации равной или выше предела обнаружения и не содержится ципрофлоксацин (или его концентрация ниже предела обнаружения).
4. Если через 15 мин на рабочей мембране тест-полоски появляется одна темно-красная линия (контрольная), то результат анализа считается положительным по ципрофлоксацину и хлорамфениколу, т.е. в образце содержатся ципрофлоксацин и хлорамфеникол в концентрациях равных или выше пределов обнаружения.
5. Если через 15 мин на рабочей мембране тест-полоски не образуется ни одной окрашенной линии или образуются только тестовые линии (одна или две), то результат анализа считается недействительным.
Технической задачей заявленной полезной модели является одновременная детекция двух токсичных контаминантов - нонилфенола и бисфенола А в пробах воды.
Технический результат заявленной полезной модели заключается в одновременной детекции на одной тест-полоске двух токсичных контаминантов - поверхностно активных веществ нонилфенола и бисфенола А с использованием простой одностадийной процедуры проведения анализа, обеспечиваемой за счет нанесения на тест-полоску всех необходимых реагентов.
Предлагается устройство для иммунохроматографической экспрессной лабораторной и внелабораторной одновременной детекции токсичных контаминантов - поверхностно активных веществ нонилфенола и бисфенола А, в питьевых, бытовых, природных и сточных водах. Устройство представляет собой мультимембранный композит с нанесенными иммунореагентами (тест-полоску). Мультимембранный композит состоит из рабочей нитроцеллюлозной мембраны на твердой полистироловой основе с нанесенными иммунореагентами, стекловолоконной мембраны с нанесенными иммунореагентами, мембраны для впитывания и сепарации исследуемого образца и конечной адсорбирующей мембраны для впитывания компонентов образца после прохождения реакции.
Указанный технический результат достигается тем, что:
в контрольную зону (К.З.) нанесены поликлональные козьи антитела, специфичные к иммуноглобулинам кролика;
в первую тестовую зону (Т.З.1) нанесен конъюгат нонилфенола с белком-носителем БСА;
во вторую тестовую зону (Т.З.2) нанесен конъюгат бисфенола А с белком-носителем СИТ;
на стекловолоконную мембрану нанесена смесь конъюгатов поликлональных кроличьих антител, специфичных к нонилфенолу, с коллоидным золотом и поликлональных кроличьих антител, специфичных к бисфенолу А, с коллоидным золотом.
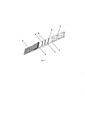
На прилагаемом чертеже (рис. 1) представлено заявляемое устройство, где 1 - твердая основа рабочей нитроцеллюлозной мембраны из полистирола, 2 - рабочая нитроцеллюлозная мембрана с нанесенными и высушенными иммунореагентами, 3 - конечная адсорбирующая мембрана для впитывания компонентов образца после прохождения реакции, 4 -стекловолоконная мембрана с нанесенными и высушенными иммунореагентами, 5 - мембрана для впитывания и сепарации исследуемого образца, А - К.З. с нанесенными поликлональными козьими антителами, специфичными к иммуноглобулинам кролика, Б - Т.З.2 с нанесенным конъюгатом бисфенола А с белком-носителем СИТ, В - Т.З.1 с нанесенным конъюгатом нонилфенола с белком-носителем БСА.
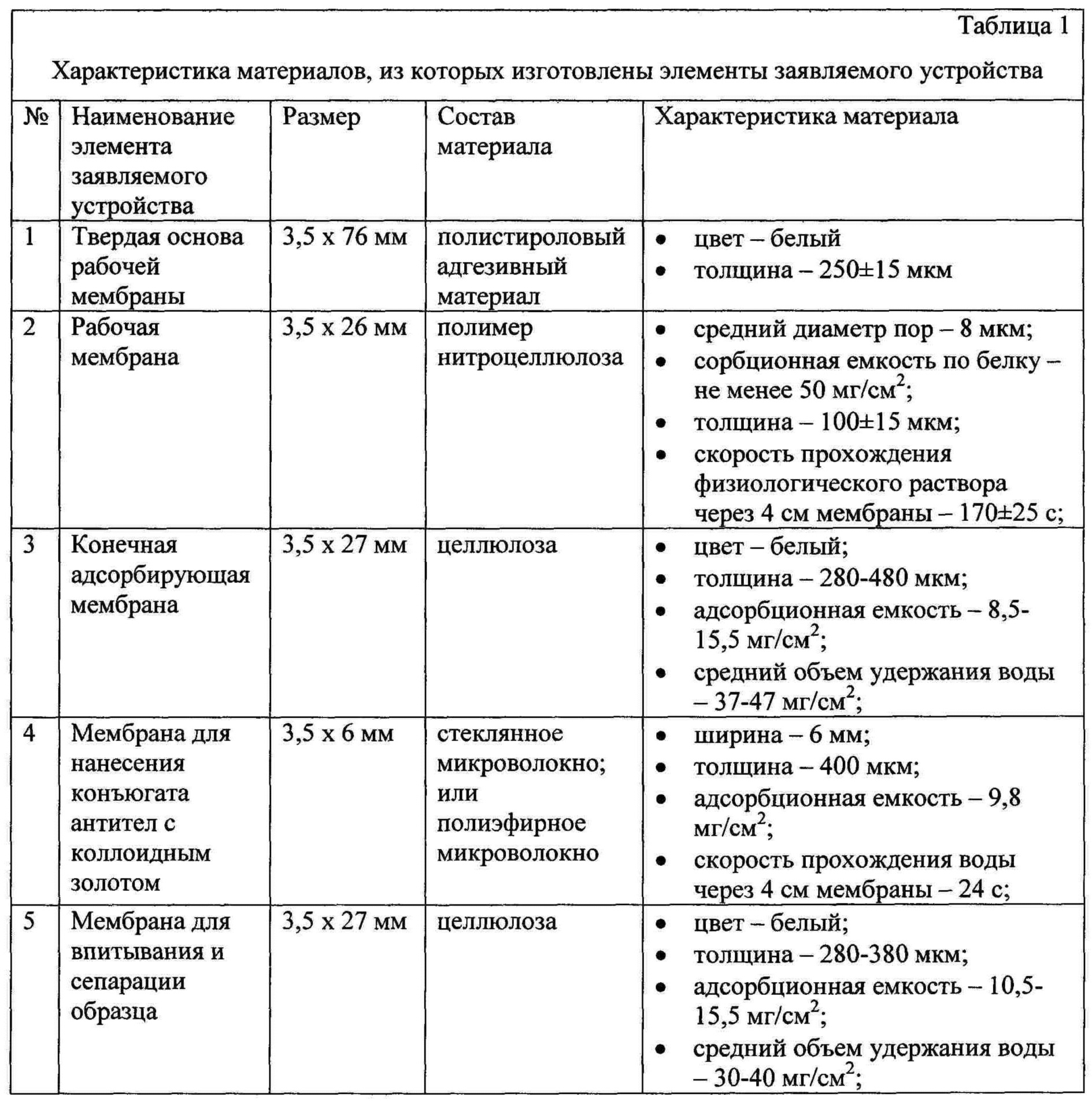
В таблице 1 приведена характеристика материалов, из которых изготовлены элементы заявляемого устройства.
Анализ проводят следующим образом.
1. 100-120 мкл анализируемой воды (питьевой, бытовой, природной, сточной) вносят в пластиковую пробирку вместимостью 1,5 мл.
2. Тест-полоску погружают вертикально нижним концом мембраны для впитывания образца на глубину 0,5 см в жидкость и инкубируют при комнатной температуре в течение 1 мин.
3. Вынимают тест-полоску и помещают ее на сухую горизонтальную поверхность на 9 мин.
4. Через 10 мин после начала движения жидкости по тест-полоске результат анализа фиксируют визуально или с использованием детектора с видеоцифровой регистрацией. Заявляемое устройство функционирует следующим образом (см. рис. 1): Если в образце присутствуют нонилфенол и бисфенол А, то они с потоком жидкости перемещаются по впитывающей мембране (5), доходят до стекловолоконной мембраны (4) и реагируют с конъюгатами коллоидного золота со специфическими антителами с образованием двойных окрашенных комплексов (растворенный антиген - антитела, меченные коллоидным золотом). Образовавшиеся двойные окрашенные комплексы под действием капиллярных сил движутся вдоль рабочей нитроцеллюлозной мембраны (2) и взаимодействуют с иммобилизованными в Т.З.1 (В) и Т.З.2 (Б) конъюгатами антигенов нонилфенола с белком-носителем БСА (Т.З.1, В) и бисфенола А с белком-носителем СИТ (Т.З.2, Б) с образованием тройных комплексов (иммобилизованный на мембране через белок-носитель антиген - меченные коллоидным золотом антитела - антиген из раствора). Избыток не связавшихся двойных окрашенных комплексов продолжает двигаться вдоль рабочей нитроцеллюлозной мембраны (2) и взаимодействует с антивидовыми антителами, иммобилизованными в К.З. (А), с образованием двойных комплексов (иммобилизованные на мембране антивидовые антитела - антитела, меченные коллоидным золотом).
Интерпретация результатов анализа производится в соответствие со схемой, представленной на рис. 2:
1. Если через 10 мин на рабочей мембране тест-полоски появляются три красные линии (К.З., Т.З.1 и Т.З.2), то результат анализа считается отрицательным, т.е. в образце не содержатся нонилфенол и бисфенол А или их концентрации ниже пределов обнаружения (рис. 2а).
2. Если через 10 мин на рабочей мембране тест-полоски появляются две красные линии (К.З. и первая по ходу движения жидкости Т.З.1), то результат анализа считается положительным по бисфенолу А и отрицательным по нонилфенолу, т.е. в образце содержится бисфенол А в концентрации равной или выше предела обнаружения и не содержится нонилфенол (или его концентрация ниже предела обнаружения), как показано на рис. 2б.
3. Если через 10 мин на рабочей мембране тест-полоски появляются две красные линии (К.З. и вторая по ходу движения жидкости Т.З.2), то результат анализа считается положительным по нонилфенолу и отрицательным по бисфенолу А, т.е. в образце содержится нонилфенол в концентрации равной или выше предела обнаружения и не содержится бисфенол А (или его концентрация ниже предела обнаружения), как показано на рис. 2в.
4. Если через 10 мин на рабочей мембране тест-полоски появляется одна красная линия (К.З.), то результат анализа считается положительным по нонилфенолу и бисфенолу А, т.е. в образце содержатся нонилфенол и бисфенол А в концентрациях равных или выше пределов обнаружения (рис. 2г).
5. Если через 10 мин на рабочей мембране тест-полоски не образуется ни одной окрашенной линии или образуются только тестовые линии (одна или две), то результат анализа считается недействительным (рис. 2д).
Эффективность данного подхода подтверждается следующими представленными ниже примерами:
Пример 1 (исследование времени получения отрицательных по нонилфенолу и бисфенолу А результатов анализа с использованием заявляемого устройства).
С использованием заявляемого устройства проводят анализ питьевой воды, не содержащей нонилфенол и бисфенол А по данным ИФА. 120 мкл образца вносят в пробирку. Заявляемое устройство (тест-полоску) погружают вертикально нижним концом мембраны для впитывания образца на глубину 0,5 см в образец и инкубируют при комнатной температуре в течение 1 мин. Вынимают тест-полоску и помещают ее в паз выдвижной каретки детектирующего устройства для видеоцифровой регистрации. Результат анализа оценивают через 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 и 15 мин с помощью программного обеспечения видеоцифрового детектора. Время анализа контролируют с помощью секундомера. Анализ проводят в пяти повторностях, используя тест-полоски пяти разных серий (полоски №№1-5).
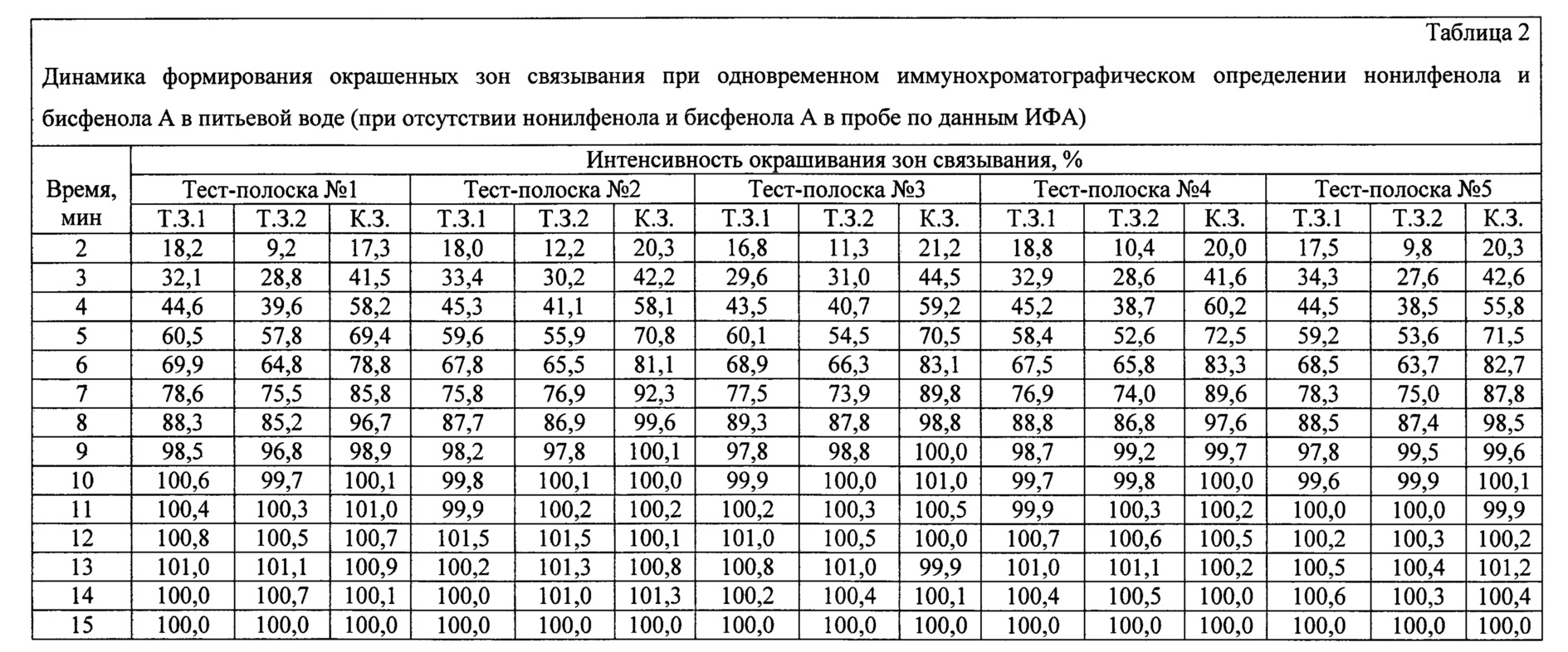
Результаты анализа приведены в таблице 2. Интенсивности окрашивания каждой из зон связывания нормированы на ее среднее значение, полученное через 15 мин после начала анализа.
Из приведенных экспериментальных данных видно, что через 10 мин после начала анализа интенсивности окрашивания К.З. достигают 100-101,0%, зон связывания нонилфенола (Т.З.1) - 99,6-100,6% и зон связывания бисфенола А (Т.З.2) - 99,7-100,1% и практически не изменяются в течение следующих пяти минут, т.е. время анализа с использованием заявленного устройства при отсутствии в пробе нонилфенола и бисфенола А составляет 10 мин.
Пример 2 (исследование времени получения положительного по бисфенолу А результата анализа с использованием заявляемого устройства).
С использованием заявляемого устройства проводят анализ питьевой воды, содержащей бисфенол А в концентрации 0,1 мкг/мл и не содержащей нонилфенол по данным ИФА. 120 мкл образца вносят в пробирку. Заявляемое устройство (тест-полоску) погружают вертикально нижним концом мембраны для впитывания образца на глубину 0,5 см в образец и инкубируют при комнатной температуре в течение 1 мин. Вынимают тест-полоску и помещают ее в паз выдвижной каретки детектирующего устройства для видеоцифровой регистрации. Результат анализа оценивают через 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 и 15 мин с помощью программного обеспечения видеоцифрового детектора. Время анализа контролируют с помощью секундомера. Анализ проводят в пяти повторностях, используя тест-полоски пяти разных серий (полоски №№1-5).
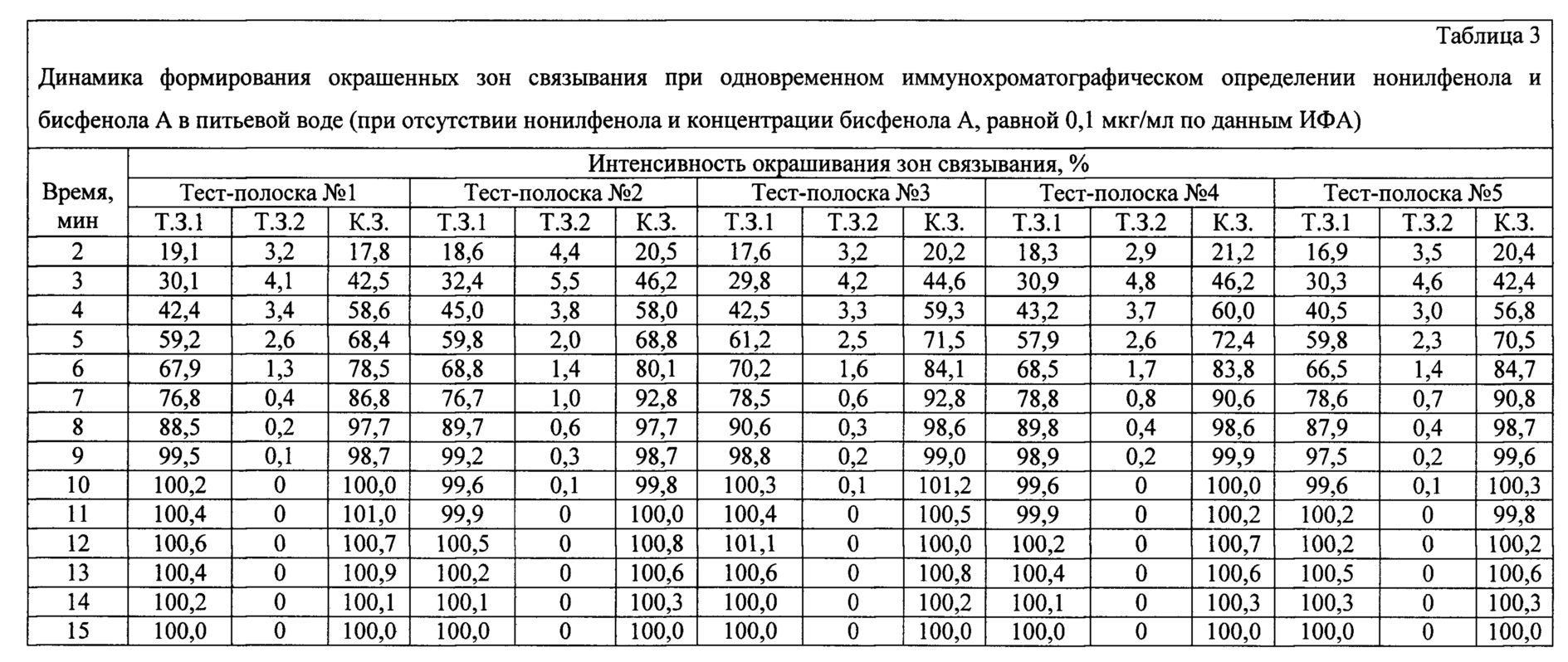
Результаты анализа приведены в таблице 3. Интенсивности окрашивания К.З. и Т.З.1 нормированы на их средние значения, полученные через 15 мин после начала анализа. Интенсивности окрашивания Т.З.2 нормированы на ее среднее значение, полученное при отсутствии бисфенола А в пробе (см. Пример 1).
Из приведенных экспериментальных данных видно, что через 10 мин после начала анализа интенсивности окрашивания достигают 99,8-101,2% для контрольных зон (К.З.) и 99,6-100,3% - для тестовых зон связывания нонилфенола (Т.З.1) и практически не изменяются в течение следующих пяти минут. Интенсивности окрашивания тестовых зон связывания бисфенола А (Т.З.2) через 10 мин после начала анализа составляют от 0 до 0,1% и не изменяются в течение следующих пяти минут. Таким образом, время анализа воды, содержащей бисфенол А в концентрации 0,1 мкг/мл и не содержащей нонилфенол по данным ИФА, с использованием заявленного устройства составляет 10 мин.
Пример 3 (исследование времени получения положительного по нонилфенолу результата анализа с использованием заявляемого устройства).
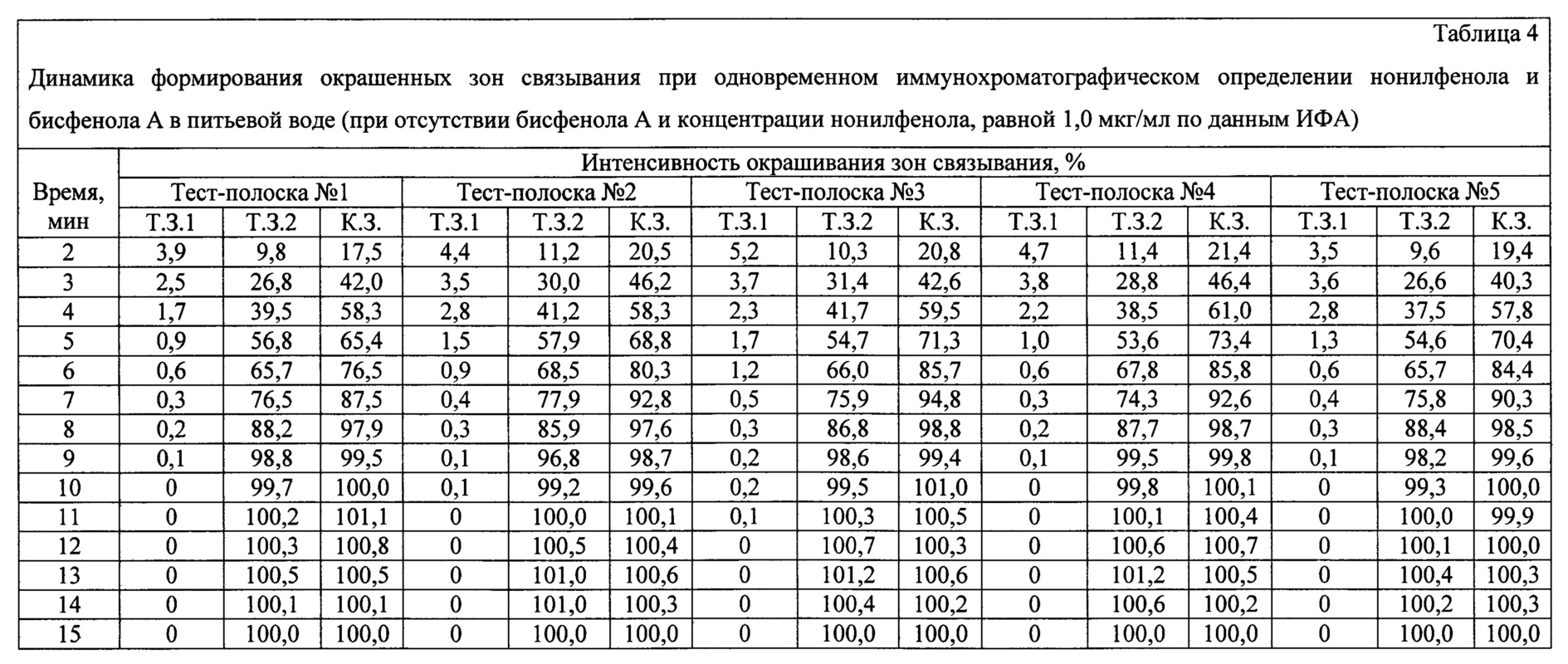
С использованием заявляемого устройства проводят анализ питьевой воды, содержащей нонилфенол в концентрации 1,0 мкг/мл и не содержащей бисфенол А по данным ИФА. 120 мкл образца вносят в пробирку. Заявляемое устройство (тест-полоску) погружают вертикально нижним концом мембраны для впитывания образца на глубину 0,5 см в образец и инкубируют при комнатной температуре в течение 1 мин. Вынимают тест-полоску и помещают ее в паз выдвижной каретки детектирующего устройства для видеоцифровой регистрации. Результат анализа оценивают через 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 и 15 мин с помощью программного обеспечения видеоцифрового детектора. Время анализа контролируют с помощью секундомера. Анализ проводят в пяти повторностях, используя тест-полоски пяти разных серий (полоски №№1-5).
Результаты анализа приведены в таблице 4. Интенсивности окрашивания К.З. и Т.З.2 нормированы на их средние значения, полученные через 15 мин после начала анализа. Интенсивности окрашивания Т.З.1 нормированы на ее среднее значение, полученное при отсутствии нонилфенола в пробе (см. Пример 1).
Из приведенных экспериментальных данных видно, что через 10 мин после начала анализа интенсивности окрашивания достигают 99,6-101,0% для контрольных зон (К.З.) и 99,2-99,8% - для тестовых зон связывания бисфенола А (Т.З.2) и практически не изменяются в течение следующих пяти минут. Интенсивности окрашивания тестовых зон связывания нонилфенола (Т.З.1) через 10 мин после начала анализа составляют от 0 до 0,2% и не изменяются в течение следующих пяти минут. Таким образом, время анализа воды, содержащей нонилфенол в концентрации 1,0 мкг/мл и не содержащей бисфенол А по данным ИФА, с использованием заявленного устройства составляет 10 мин.
Пример 4 (исследование времени получения положительных по нонилфенолу и бисфенолу А результатов анализа с использованием заявляемого устройства).
С использованием заявляемого устройства проводят анализ питьевой воды, содержащей по данным ИФА нонилфенол в концентрации 1,0 мкг/мл и бисфенол А в концентрации 0,1 мкг/мл. 120 мкл образца вносят в пробирку. Заявляемое устройство (тест-полоску) погружают вертикально нижним концом мембраны для впитывания образца на глубину 0,5 см в образец и инкубируют при комнатной температуре в течение 1 мин. Вынимают тест-полоску и помещают ее в паз выдвижной каретки детектирующего устройства для видеоцифровой регистрации. Результат анализа оценивают через 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 и 15 мин с помощью программного обеспечения видеоцифрового детектора. Время анализа контролируют с помощью секундомера. Анализ проводят в пяти повторностях, используя тест-полоски пяти разных серий (полоски №№1-5).
Результаты анализа приведены в таблице 5. Интенсивности окрашивания К.З. нормированы на их среднее значение, полученное через 15 мин после начала анализа. Интенсивности окрашивания Т.З.1 и Т.З.2 нормированы на их средние значения, полученные при отсутствии нонилфенола и бисфенола А в пробе (см. Пример 1).
Из приведенных экспериментальных данных видно, что через 10 мин после начала анализа интенсивности окрашивания контрольных зон (К.З.) достигают 99,5-101,3% и практически не изменяются в течение следующих пяти минут. Интенсивности окрашивания тестовых зон связывания нонилфенола (Т.З.1) и бисфенола А (Т.З.2) через 10 мин после начала анализа составляют от 0 до 0,2% и не изменяются в течение следующих пяти минут. Таким образом, время анализа воды, содержащей нонилфенол в концентрации 1,0 мкг/мл и бисфенол А в концентрации 0,1 мкг/мл по данным ИФА, с использованием заявленного устройства составляет 10 мин.
Краткое описание чертежей
На рис. 1 изображена схема заявляемого устройства для иммунохроматографической экспрессной лабораторной и внелабораторной одновременной детекции токсичных контаминантов - поверхностно активных веществ нонилфенола и бисфенола А. 1 - твердая полистирольная основа рабочей нитроцеллюлозной мембраны; 2 - рабочая нитроцеллюлозная мембрана; 3 - конечная адсорбирующая мембрана для впитывания компонентов образца после прохождения реакции; 4 - стекловолоконная мембрана с нанесенной и высушенной смесью конъюгатов коллоидного золота с поликлональными кроличьими антителами, специфичными к нонилфенолу и поликлональными кроличьими антителами, специфичными к бисфенолу А; 5 - мембрана для впитывания и сепарации исследуемого образца; А - К.З. с нанесенными поликлональными козьими антителами, специфичными к иммуноглобулинам кролика; Б - Т.З.2 с нанесенным конъюгатом бисфенола А с белком-носителем СИТ; В - Т.З.1 с нанесенным конъюгатом нонилфенола с белком-носителем БСА.
На рис. 2 изображен алгоритм интерпретации результатов анализа. В том случае, когда на рабочей мембране тест-полоски появляются три красные линии (в К.З., Т.З.1 и Т.З.2), результат анализа считается отрицательным (рис. 2а). В том случае, когда на рабочей мембране тест-полоски появляются две красные линии (в К.З. и Т.З.1), результат анализа считается положительным по бисфенолу А и отрицательным по нонилфенолу (рис. 2б). В том случае, когда на рабочей мембране тест-полоски появляются две красные линии (в К.З. и Т.З.2), результат анализа считается положительным по нонилфенолу и отрицательным по бисфенолу А (рис. 2в). В том случае, когда на рабочей мембране тест-полоски появляется одна красная линия (в К.З.), результат анализа считается положительным по нонилфенолу и бисфенолу А (рис. 2г). В том случае, когда на рабочей мембране тест-полоски не образуется ни одной окрашенной линии или образуются только тестовые линии (одна или две), результат анализа считается недействительным (рис. 2д).
Claims (1)
- Устройство для иммунохроматографической экспрессной лабораторной и внелабораторной одновременной детекции токсичных контаминантов - поверхностно активных веществ нонилфенола и бисфенола А, содержащее тест-полоску, состоящую из полистироловой подложки, на которую наклеены нитроцеллюлозная мембрана с нанесенными и высушенными иммунореагентами, стекловолоконная мембрана с нанесенными и высушенными иммунореагентами, мембрана для впитывания и сепарации исследуемого образца и конечная адсорбирующая мембрана для впитывания компонентов образца после прохождения реакции, на нитроцеллюлозную мембрану нанесены контрольная и две тестовые зоны, отличающееся тем, что в контрольную зону нанесены поликлональные козьих антитела, специфичные к иммуноглобулинам кролика, в первую тестовую зону нанесен конъюгат нонилфенола с белком-носителем бычьим сывороточным альбумином и во вторую тестовую зону нанесен конъюгат бисфенола А с белком-носителем соевым ингибитором трипсина, на стекловолоконную мембрану нанесена смесь конъюгатов поликлональных кроличьих антител, специфичных к нонилфенолу, с коллоидным золотом и поликлональных кроличьих антител, специфичных к бисфенолу А, с коллоидным золотом.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2019138779U RU196383U1 (ru) | 2019-11-29 | 2019-11-29 | Устройство для иммунохроматографической экспрессной лабораторной и внелабораторной одновременной детекции токсичных контаминантов - поверхностно активных веществ нонилфенола и бисфенола а в питьевых, бытовых, природных и сточных водах |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2019138779U RU196383U1 (ru) | 2019-11-29 | 2019-11-29 | Устройство для иммунохроматографической экспрессной лабораторной и внелабораторной одновременной детекции токсичных контаминантов - поверхностно активных веществ нонилфенола и бисфенола а в питьевых, бытовых, природных и сточных водах |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU196383U1 true RU196383U1 (ru) | 2020-02-27 |
Family
ID=69630776
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2019138779U RU196383U1 (ru) | 2019-11-29 | 2019-11-29 | Устройство для иммунохроматографической экспрессной лабораторной и внелабораторной одновременной детекции токсичных контаминантов - поверхностно активных веществ нонилфенола и бисфенола а в питьевых, бытовых, природных и сточных водах |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU196383U1 (ru) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU202181U1 (ru) * | 2020-09-14 | 2021-02-05 | Федеральное государственное учреждение "Федеральный исследовательский центр "Фундаментальные основы биотехнологии" Российской академии наук (ФИЦ Биотехнологии РАН) | Устройство для иммунохроматографической экспрессной лабораторной и внелабораторной одновременной индивидуальной детекции токсичных контаминантов в воде |
| RU208858U1 (ru) * | 2020-09-16 | 2022-01-18 | Шэньчжэнь Биоизи Биотекнолоджи Ко., Лтд | Тест-кассета с множеством соединений для двухэтапной иммунохроматографической диагностики |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050148097A1 (en) * | 2002-03-07 | 2005-07-07 | Enbiotec Laboratories C., Ltd. | Instruments for detecting low-molecular weight substance |
| US20050208593A1 (en) * | 2004-03-19 | 2005-09-22 | Arizona Board Of Regents, Acting For And On Behalf Of Northern Arizona University | Lateral flow diagnostic assay reader with radial cassette |
-
2019
- 2019-11-29 RU RU2019138779U patent/RU196383U1/ru active
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050148097A1 (en) * | 2002-03-07 | 2005-07-07 | Enbiotec Laboratories C., Ltd. | Instruments for detecting low-molecular weight substance |
| US20050208593A1 (en) * | 2004-03-19 | 2005-09-22 | Arizona Board Of Regents, Acting For And On Behalf Of Northern Arizona University | Lateral flow diagnostic assay reader with radial cassette |
Non-Patent Citations (3)
| Title |
|---|
| PENG X. et al. A signal-enhanced lateral flow strip biosensor for ultrasensitive and on-site detection of bisphenol // FOOD AND AGRICULTURAL IMMUNOLOGY, 2017, V.29, pp.1-12. * |
| РУДАКОВ О.Б. и др. Определение бисфенола А, триклозана и нонилфенола в материалах и экстрактах методом ТСХ, совмещенным с цифровой цветометрией // Сорбционные и хроматографические процессы, 2016 Т.16, N.5, стр.686-694. * |
| РУДАКОВ О.Б. и др. Определение бисфенола А, триклозана и нонилфенола в материалах и экстрактах методом ТСХ, совмещенным с цифровой цветометрией // Сорбционные и хроматографические процессы, 2016, Т.16, N.5, стр.686-694. PENG X. et al. A signal-enhanced lateral flow strip biosensor for ultrasensitive and on-site detection of bisphenol // FOOD AND AGRICULTURAL IMMUNOLOGY, 2017, V.29, pp.1-12. * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU202181U1 (ru) * | 2020-09-14 | 2021-02-05 | Федеральное государственное учреждение "Федеральный исследовательский центр "Фундаментальные основы биотехнологии" Российской академии наук (ФИЦ Биотехнологии РАН) | Устройство для иммунохроматографической экспрессной лабораторной и внелабораторной одновременной индивидуальной детекции токсичных контаминантов в воде |
| RU208858U1 (ru) * | 2020-09-16 | 2022-01-18 | Шэньчжэнь Биоизи Биотекнолоджи Ко., Лтд | Тест-кассета с множеством соединений для двухэтапной иммунохроматографической диагностики |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2063269B1 (en) | Chromatography apparatus for detecting Staphylococcus aureus | |
| Brecht et al. | Optical immunoprobe development for multiresidue monitoring in water | |
| CN107430120B (zh) | 免疫检测方法和用于其的测试条 | |
| RU196383U1 (ru) | Устройство для иммунохроматографической экспрессной лабораторной и внелабораторной одновременной детекции токсичных контаминантов - поверхностно активных веществ нонилфенола и бисфенола а в питьевых, бытовых, природных и сточных водах | |
| Yazynina et al. | Immunoassay techniques for detection of the herbicide simazine based on use of oppositely charged water-soluble polyelectrolytes | |
| KR102481751B1 (ko) | 면역크로마토그래피 시험편 및 그것을 사용한 면역크로마토그래피법 | |
| Garcinuno et al. | Development of a fluoroimmunosensor for theophylline using immobilised antibody | |
| Zhang et al. | SERS based immunochromatographic assay for rapid and quantitative determination of bisphenol A | |
| KR102593963B1 (ko) | 면역학적 측정용 시약 조성물 및 이의 용도 | |
| Glad et al. | Immunocapillarymigration—a new method for immunochemical quantitation | |
| Yeow et al. | Indirect antiglobulin paper test for red blood cell antigen typing by flow-through method | |
| Paek et al. | Performance control strategies of one-step immuno-chromatographic assay system for Salmonella typhimurium | |
| RU202181U1 (ru) | Устройство для иммунохроматографической экспрессной лабораторной и внелабораторной одновременной индивидуальной детекции токсичных контаминантов в воде | |
| JPWO2016052690A1 (ja) | 免疫測定用ブロッキング方法及び免疫測定用器具 | |
| CN107209179A (zh) | 用于检测含红细胞的样品中的对象物的免疫色谱用测试条、及使用该测试条的免疫色谱 | |
| Dietrich et al. | Continuous immunochemical determination of pesticides via flow injection immunoanalysis using monoclonal antibodies against terbutryne immobilized to solid upports | |
| Boltovets et al. | Surface capturing of virion‐antibody complexes: Kinetic study | |
| Lu et al. | Development of an amperometric immunosensor based on flow injection analysis for the detection of red blood cells | |
| CN102680621A (zh) | 一种化学发光检测技术及其用途 | |
| KR102844310B1 (ko) | 위양성의 억제에 의해 특이성을 개선한 검사 키트 | |
| US8039268B2 (en) | Immunochromatoassay method and immunochromatoassay kit | |
| JP6703354B2 (ja) | 非特異反応抑制剤および前処理方法 | |
| KR102866597B1 (ko) | 위음성의 억제에 의해 특이성을 개선한 검사 시약 | |
| RU2523393C1 (ru) | Тест-полоска для высокочувствительного иммунохроматографического анализа | |
| EP0893690A1 (en) | Detection of mycotoxins by flow-through membrane-based enzyme immunoassay |