KR20210143848A - 리소좀 축적 장애를 위한 비강 유전자 전달 및 경구 신남산, 올레아미드 또는 젬피브로질의 병용 - Google Patents
리소좀 축적 장애를 위한 비강 유전자 전달 및 경구 신남산, 올레아미드 또는 젬피브로질의 병용 Download PDFInfo
- Publication number
- KR20210143848A KR20210143848A KR1020217034175A KR20217034175A KR20210143848A KR 20210143848 A KR20210143848 A KR 20210143848A KR 1020217034175 A KR1020217034175 A KR 1020217034175A KR 20217034175 A KR20217034175 A KR 20217034175A KR 20210143848 A KR20210143848 A KR 20210143848A
- Authority
- KR
- South Korea
- Prior art keywords
- composition
- disease
- gene
- administered
- lysosomal storage
- Prior art date
Links
- 208000015439 Lysosomal storage disease Diseases 0.000 title claims abstract description 30
- HEMJJKBWTPKOJG-UHFFFAOYSA-N Gemfibrozil Chemical compound CC1=CC=C(C)C(OCCCC(C)(C)C(O)=O)=C1 HEMJJKBWTPKOJG-UHFFFAOYSA-N 0.000 title claims description 27
- 229960003627 gemfibrozil Drugs 0.000 title claims description 25
- 235000013985 cinnamic acid Nutrition 0.000 title claims description 15
- FATBGEAMYMYZAF-KTKRTIGZSA-N oleamide Chemical compound CCCCCCCC\C=C/CCCCCCCC(N)=O FATBGEAMYMYZAF-KTKRTIGZSA-N 0.000 title claims description 15
- WBYWAXJHAXSJNI-SREVYHEPSA-N Cinnamic acid Chemical compound OC(=O)\C=C/C1=CC=CC=C1 WBYWAXJHAXSJNI-SREVYHEPSA-N 0.000 title claims description 14
- FATBGEAMYMYZAF-UHFFFAOYSA-N oleicacidamide-heptaglycolether Natural products CCCCCCCCC=CCCCCCCCC(N)=O FATBGEAMYMYZAF-UHFFFAOYSA-N 0.000 title claims description 14
- WBYWAXJHAXSJNI-UHFFFAOYSA-N methyl p-hydroxycinnamate Natural products OC(=O)C=CC1=CC=CC=C1 WBYWAXJHAXSJNI-UHFFFAOYSA-N 0.000 title claims description 13
- WBYWAXJHAXSJNI-VOTSOKGWSA-M .beta-Phenylacrylic acid Natural products [O-]C(=O)\C=C\C1=CC=CC=C1 WBYWAXJHAXSJNI-VOTSOKGWSA-M 0.000 title claims description 12
- 229930016911 cinnamic acid Natural products 0.000 title claims description 12
- 238000001476 gene delivery Methods 0.000 title description 6
- 239000000203 mixture Substances 0.000 claims abstract description 80
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 58
- 238000000034 method Methods 0.000 claims abstract description 45
- 102000004190 Enzymes Human genes 0.000 claims abstract description 28
- 108090000790 Enzymes Proteins 0.000 claims abstract description 28
- 230000002132 lysosomal effect Effects 0.000 claims abstract description 26
- 239000003814 drug Substances 0.000 claims abstract description 19
- 208000002537 Neuronal Ceroid-Lipofuscinoses Diseases 0.000 claims description 52
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 31
- 201000010099 disease Diseases 0.000 claims description 28
- 239000003795 chemical substances by application Substances 0.000 claims description 24
- 230000001225 therapeutic effect Effects 0.000 claims description 22
- 239000013603 viral vector Substances 0.000 claims description 21
- 208000031277 Amaurotic familial idiocy Diseases 0.000 claims description 20
- 208000025014 late infantile neuronal ceroid lipofuscinosis Diseases 0.000 claims description 18
- -1 cln2 Proteins 0.000 claims description 13
- 208000017482 infantile neuronal ceroid lipofuscinosis Diseases 0.000 claims description 13
- 201000007642 neuronal ceroid lipofuscinosis 1 Diseases 0.000 claims description 13
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 claims description 12
- 229930002330 retinoic acid Natural products 0.000 claims description 12
- 102100022548 Beta-hexosaminidase subunit alpha Human genes 0.000 claims description 11
- 101150016456 Hexa gene Proteins 0.000 claims description 11
- 208000022292 Tay-Sachs disease Diseases 0.000 claims description 11
- 108010039203 Tripeptidyl-Peptidase 1 Proteins 0.000 claims description 11
- 201000007607 neuronal ceroid lipofuscinosis 3 Diseases 0.000 claims description 11
- 102100022440 Battenin Human genes 0.000 claims description 10
- 101150038645 CLN3 gene Proteins 0.000 claims description 10
- 102100034197 Tripeptidyl-peptidase 1 Human genes 0.000 claims description 10
- 208000017476 juvenile neuronal ceroid lipofuscinosis Diseases 0.000 claims description 10
- 108020002591 Palmitoyl protein thioesterase Proteins 0.000 claims description 9
- 229940125753 fibrate Drugs 0.000 claims description 8
- 230000008499 blood brain barrier function Effects 0.000 claims description 7
- 210000001218 blood-brain barrier Anatomy 0.000 claims description 7
- YMTINGFKWWXKFG-UHFFFAOYSA-N fenofibrate Chemical compound C1=CC(OC(C)(C)C(=O)OC(C)C)=CC=C1C(=O)C1=CC=C(Cl)C=C1 YMTINGFKWWXKFG-UHFFFAOYSA-N 0.000 claims description 6
- 229960002297 fenofibrate Drugs 0.000 claims description 5
- 101150002054 galE gene Proteins 0.000 claims description 5
- 241000701161 unidentified adenovirus Species 0.000 claims description 5
- 101100054624 Corynebacterium glutamicum (strain ATCC 13032 / DSM 20300 / BCRC 11384 / JCM 1318 / LMG 3730 / NCIMB 10025) acpS gene Proteins 0.000 claims description 4
- 208000024720 Fabry Disease Diseases 0.000 claims description 4
- 208000015872 Gaucher disease Diseases 0.000 claims description 4
- 102000016871 Hexosaminidase A Human genes 0.000 claims description 4
- 108010053317 Hexosaminidase A Proteins 0.000 claims description 4
- 208000014060 Niemann-Pick disease Diseases 0.000 claims description 4
- 101150087584 PPT1 gene Proteins 0.000 claims description 4
- CRQQGFGUEAVUIL-UHFFFAOYSA-N chlorothalonil Chemical compound ClC1=C(Cl)C(C#N)=C(Cl)C(C#N)=C1Cl CRQQGFGUEAVUIL-UHFFFAOYSA-N 0.000 claims description 4
- DDOVBCWVTOHGCU-QMXMISKISA-N n-[(e,2s,3r)-3-hydroxy-1-[(2r,3r,4s,5r,6r)-3,4,5-trihydroxy-6-(hydroxymethyl)oxan-2-yl]oxynonadec-4-en-2-yl]octadecanamide Chemical compound CCCCCCCCCCCCCCCCCC(=O)N[C@H]([C@H](O)\C=C\CCCCCCCCCCCCCC)CO[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O DDOVBCWVTOHGCU-QMXMISKISA-N 0.000 claims description 4
- 102100025824 Palmitoyl-protein thioesterase 1 Human genes 0.000 claims 1
- 238000011282 treatment Methods 0.000 abstract description 24
- 239000008194 pharmaceutical composition Substances 0.000 abstract description 23
- 238000001415 gene therapy Methods 0.000 abstract description 14
- 230000007246 mechanism Effects 0.000 abstract description 6
- 238000013459 approach Methods 0.000 abstract description 4
- 238000011260 co-administration Methods 0.000 abstract description 4
- 238000002560 therapeutic procedure Methods 0.000 abstract description 3
- 241000699670 Mus sp. Species 0.000 description 25
- 229940088598 enzyme Drugs 0.000 description 24
- 230000037396 body weight Effects 0.000 description 15
- 101150092324 TPP1 gene Proteins 0.000 description 14
- 210000004556 brain Anatomy 0.000 description 13
- 230000035508 accumulation Effects 0.000 description 11
- 238000009825 accumulation Methods 0.000 description 11
- 208000015122 neurodegenerative disease Diseases 0.000 description 10
- 230000035772 mutation Effects 0.000 description 9
- 201000008051 neuronal ceroid lipofuscinosis Diseases 0.000 description 9
- 241000699666 Mus <mouse, genus> Species 0.000 description 8
- 102000005327 Palmitoyl protein thioesterase Human genes 0.000 description 8
- 230000002068 genetic effect Effects 0.000 description 8
- 230000004770 neurodegeneration Effects 0.000 description 7
- 102000004169 proteins and genes Human genes 0.000 description 7
- 229940079593 drug Drugs 0.000 description 6
- 238000009472 formulation Methods 0.000 description 6
- 238000012546 transfer Methods 0.000 description 6
- 239000000463 material Substances 0.000 description 5
- 230000001537 neural effect Effects 0.000 description 5
- 230000003442 weekly effect Effects 0.000 description 5
- 241000700605 Viruses Species 0.000 description 4
- 230000007812 deficiency Effects 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- 101150022753 galc gene Proteins 0.000 description 4
- 210000003712 lysosome Anatomy 0.000 description 4
- 230000001868 lysosomic effect Effects 0.000 description 4
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 4
- 239000007787 solid Substances 0.000 description 4
- 239000007921 spray Substances 0.000 description 4
- 208000024891 symptom Diseases 0.000 description 4
- 208000024827 Alzheimer disease Diseases 0.000 description 3
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 3
- 206010010904 Convulsion Diseases 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 108010061312 Sphingomyelin Phosphodiesterase Proteins 0.000 description 3
- 102000010126 acid sphingomyelin phosphodiesterase activity proteins Human genes 0.000 description 3
- 239000002671 adjuvant Substances 0.000 description 3
- 238000010171 animal model Methods 0.000 description 3
- IIBYAHWJQTYFKB-UHFFFAOYSA-N bezafibrate Chemical compound C1=CC(OC(C)(C)C(O)=O)=CC=C1CCNC(=O)C1=CC=C(Cl)C=C1 IIBYAHWJQTYFKB-UHFFFAOYSA-N 0.000 description 3
- 230000015556 catabolic process Effects 0.000 description 3
- 210000003169 central nervous system Anatomy 0.000 description 3
- APEJMQOBVMLION-UHFFFAOYSA-N cinnamic acid amide Natural products NC(=O)C=CC1=CC=CC=C1 APEJMQOBVMLION-UHFFFAOYSA-N 0.000 description 3
- 235000014113 dietary fatty acids Nutrition 0.000 description 3
- 208000035475 disorder Diseases 0.000 description 3
- 239000003937 drug carrier Substances 0.000 description 3
- 239000000839 emulsion Substances 0.000 description 3
- 239000000194 fatty acid Substances 0.000 description 3
- 229930195729 fatty acid Natural products 0.000 description 3
- 150000004665 fatty acids Chemical class 0.000 description 3
- 230000001965 increasing effect Effects 0.000 description 3
- 230000000366 juvenile effect Effects 0.000 description 3
- 150000002632 lipids Chemical class 0.000 description 3
- 238000002663 nebulization Methods 0.000 description 3
- 239000006199 nebulizer Substances 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- 230000004044 response Effects 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- 102000006772 Acid Ceramidase Human genes 0.000 description 2
- 108020005296 Acid Ceramidase Proteins 0.000 description 2
- 102100022146 Arylsulfatase A Human genes 0.000 description 2
- 102100031491 Arylsulfatase B Human genes 0.000 description 2
- 108010023546 Aspartylglucosylaminase Proteins 0.000 description 2
- 102000016614 Autophagy-Related Protein 5 Human genes 0.000 description 2
- 108010092776 Autophagy-Related Protein 5 Proteins 0.000 description 2
- 102100032487 Beta-mannosidase Human genes 0.000 description 2
- 201000004569 Blindness Diseases 0.000 description 2
- 102000004171 Cathepsin K Human genes 0.000 description 2
- 108090000625 Cathepsin K Proteins 0.000 description 2
- 108010036867 Cerebroside-Sulfatase Proteins 0.000 description 2
- KPSRODZRAIWAKH-JTQLQIEISA-N Ciprofibrate Natural products C1=CC(OC(C)(C)C(O)=O)=CC=C1[C@H]1C(Cl)(Cl)C1 KPSRODZRAIWAKH-JTQLQIEISA-N 0.000 description 2
- BMOVQUBVGICXQN-UHFFFAOYSA-N Clinofibrate Chemical compound C1=CC(OC(C)(CC)C(O)=O)=CC=C1C1(C=2C=CC(OC(C)(CC)C(O)=O)=CC=2)CCCCC1 BMOVQUBVGICXQN-UHFFFAOYSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 2
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 2
- 102100028875 Formylglycine-generating enzyme Human genes 0.000 description 2
- 101710192607 Formylglycine-generating enzyme Proteins 0.000 description 2
- 102100023364 Ganglioside GM2 activator Human genes 0.000 description 2
- 108010010803 Gelatin Proteins 0.000 description 2
- 102000004547 Glucosylceramidase Human genes 0.000 description 2
- 108010017544 Glucosylceramidase Proteins 0.000 description 2
- 101000685969 Homo sapiens Ganglioside GM2 activator Proteins 0.000 description 2
- 102100039283 Hyaluronidase-1 Human genes 0.000 description 2
- 101710199679 Hyaluronidase-1 Proteins 0.000 description 2
- 102100029199 Iduronate 2-sulfatase Human genes 0.000 description 2
- 101710096421 Iduronate 2-sulfatase Proteins 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- 206010061218 Inflammation Diseases 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 201000002832 Lewy body dementia Diseases 0.000 description 2
- 102100033448 Lysosomal alpha-glucosidase Human genes 0.000 description 2
- 102000009565 Lysosomal-Associated Membrane Protein 2 Human genes 0.000 description 2
- 108010009491 Lysosomal-Associated Membrane Protein 2 Proteins 0.000 description 2
- 102000008135 Mechanistic Target of Rapamycin Complex 1 Human genes 0.000 description 2
- 108010035196 Mechanistic Target of Rapamycin Complex 1 Proteins 0.000 description 2
- 102100026502 Mucolipin-1 Human genes 0.000 description 2
- 208000001089 Multiple system atrophy Diseases 0.000 description 2
- 102100021003 N(4)-(beta-N-acetylglucosaminyl)-L-asparaginase Human genes 0.000 description 2
- 108010027520 N-Acetylgalactosamine-4-Sulfatase Proteins 0.000 description 2
- 208000018737 Parkinson disease Diseases 0.000 description 2
- 102000017852 Saposin Human genes 0.000 description 2
- 108050007079 Saposin Proteins 0.000 description 2
- 102100023105 Sialin Human genes 0.000 description 2
- 101710105284 Sialin Proteins 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- 102000000019 Sterol Esterase Human genes 0.000 description 2
- 108010055297 Sterol Esterase Proteins 0.000 description 2
- 239000000443 aerosol Substances 0.000 description 2
- 108010028144 alpha-Glucosidases Proteins 0.000 description 2
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 description 2
- 239000003963 antioxidant agent Substances 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- SESFRYSPDFLNCH-UHFFFAOYSA-N benzyl benzoate Chemical compound C=1C=CC=CC=1C(=O)OCC1=CC=CC=C1 SESFRYSPDFLNCH-UHFFFAOYSA-N 0.000 description 2
- 108010055059 beta-Mannosidase Proteins 0.000 description 2
- 229960000516 bezafibrate Drugs 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 210000001715 carotid artery Anatomy 0.000 description 2
- 210000004027 cell Anatomy 0.000 description 2
- KPSRODZRAIWAKH-UHFFFAOYSA-N ciprofibrate Chemical compound C1=CC(OC(C)(C)C(O)=O)=CC=C1C1C(Cl)(Cl)C1 KPSRODZRAIWAKH-UHFFFAOYSA-N 0.000 description 2
- KNHUKKLJHYUCFP-UHFFFAOYSA-N clofibrate Chemical compound CCOC(=O)C(C)(C)OC1=CC=C(Cl)C=C1 KNHUKKLJHYUCFP-UHFFFAOYSA-N 0.000 description 2
- 229960001214 clofibrate Drugs 0.000 description 2
- 208000010877 cognitive disease Diseases 0.000 description 2
- GHVNFZFCNZKVNT-UHFFFAOYSA-N decanoic acid Chemical compound CCCCCCCCCC(O)=O GHVNFZFCNZKVNT-UHFFFAOYSA-N 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 230000007547 defect Effects 0.000 description 2
- 238000006731 degradation reaction Methods 0.000 description 2
- 230000002939 deleterious effect Effects 0.000 description 2
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- MMXKVMNBHPAILY-UHFFFAOYSA-N ethyl laurate Chemical compound CCCCCCCCCCCC(=O)OCC MMXKVMNBHPAILY-UHFFFAOYSA-N 0.000 description 2
- 230000029142 excretion Effects 0.000 description 2
- 239000000796 flavoring agent Substances 0.000 description 2
- 239000008273 gelatin Substances 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- 235000011852 gelatine desserts Nutrition 0.000 description 2
- IPCSVZSSVZVIGE-UHFFFAOYSA-N hexadecanoic acid Chemical compound CCCCCCCCCCCCCCCC(O)=O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 2
- 230000001771 impaired effect Effects 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 230000004054 inflammatory process Effects 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- 239000003446 ligand Substances 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- 235000019359 magnesium stearate Nutrition 0.000 description 2
- 201000006417 multiple sclerosis Diseases 0.000 description 2
- 210000002850 nasal mucosa Anatomy 0.000 description 2
- 210000002569 neuron Anatomy 0.000 description 2
- 231100000252 nontoxic Toxicity 0.000 description 2
- 230000003000 nontoxic effect Effects 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 235000019198 oils Nutrition 0.000 description 2
- 230000036542 oxidative stress Effects 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 230000002028 premature Effects 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 230000000750 progressive effect Effects 0.000 description 2
- 201000002212 progressive supranuclear palsy Diseases 0.000 description 2
- 230000000069 prophylactic effect Effects 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 239000011232 storage material Substances 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 150000008163 sugars Chemical class 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- 231100000331 toxic Toxicity 0.000 description 2
- 230000002588 toxic effect Effects 0.000 description 2
- 239000013598 vector Substances 0.000 description 2
- WDVIDPRACNGFPP-QWRGUYRKSA-N (2s)-2-[[(2s)-6-amino-2-[[2-[(2-aminoacetyl)amino]acetyl]amino]hexanoyl]amino]-5-(diaminomethylideneamino)pentanoic acid Chemical compound NCC(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCN=C(N)N)C(O)=O WDVIDPRACNGFPP-QWRGUYRKSA-N 0.000 description 1
- OYHQOLUKZRVURQ-NTGFUMLPSA-N (9Z,12Z)-9,10,12,13-tetratritiooctadeca-9,12-dienoic acid Chemical compound C(CCCCCCC\C(=C(/C\C(=C(/CCCCC)\[3H])\[3H])\[3H])\[3H])(=O)O OYHQOLUKZRVURQ-NTGFUMLPSA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- WCHRPSHIMRQFRS-UHFFFAOYSA-N 2-bromo-5,6-dihydro-4h-thieno[2,3-c]pyridin-7-one Chemical compound C1CNC(=O)C2=C1C=C(Br)S2 WCHRPSHIMRQFRS-UHFFFAOYSA-N 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- 102100027824 3'(2'),5'-bisphosphate nucleotidase 1 Human genes 0.000 description 1
- 101710097446 3'(2'),5'-bisphosphate nucleotidase 1 Proteins 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- 101150102163 ATG7 gene Proteins 0.000 description 1
- 244000215068 Acacia senegal Species 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 101710164561 Alpha-L-fucosidase 1 Proteins 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 102100034561 Alpha-N-acetylglucosaminidase Human genes 0.000 description 1
- 241000710929 Alphavirus Species 0.000 description 1
- 206010068220 Aspartylglucosaminuria Diseases 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 108010092778 Autophagy-Related Protein 7 Proteins 0.000 description 1
- 102000016613 Autophagy-Related Protein 7 Human genes 0.000 description 1
- 101710195294 Beta-galactosidase 1 Proteins 0.000 description 1
- 101710124976 Beta-hexosaminidase A Proteins 0.000 description 1
- 101710124978 Beta-hexosaminidase B Proteins 0.000 description 1
- 208000024806 Brain atrophy Diseases 0.000 description 1
- 208000036632 Brain mass Diseases 0.000 description 1
- 101150011252 CTSK gene Proteins 0.000 description 1
- 239000005632 Capric acid (CAS 334-48-5) Substances 0.000 description 1
- 108010059081 Cathepsin A Proteins 0.000 description 1
- 102000005572 Cathepsin A Human genes 0.000 description 1
- 208000027647 Cerebral Cortical Thinning Diseases 0.000 description 1
- 208000028698 Cognitive impairment Diseases 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 206010011777 Cystinosis Diseases 0.000 description 1
- 101100283465 Danio rerio gnptab gene Proteins 0.000 description 1
- 208000016192 Demyelinating disease Diseases 0.000 description 1
- 206010012305 Demyelination Diseases 0.000 description 1
- 241000702421 Dependoparvovirus Species 0.000 description 1
- 206010061818 Disease progression Diseases 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 239000001856 Ethyl cellulose Substances 0.000 description 1
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 1
- 108700024394 Exon Proteins 0.000 description 1
- 102100028496 Galactocerebrosidase Human genes 0.000 description 1
- 208000017462 Galactosialidosis Diseases 0.000 description 1
- 108010042681 Galactosylceramidase Proteins 0.000 description 1
- 101150050387 Galns gene Proteins 0.000 description 1
- 206010064571 Gene mutation Diseases 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 102000053187 Glucuronidase Human genes 0.000 description 1
- 108010060309 Glucuronidase Proteins 0.000 description 1
- 229920000084 Gum arabic Polymers 0.000 description 1
- 102100039991 Heparan-alpha-glucosaminide N-acetyltransferase Human genes 0.000 description 1
- 108030000639 Heparan-alpha-glucosaminide N-acetyltransferases Proteins 0.000 description 1
- 101150071246 Hexb gene Proteins 0.000 description 1
- 102000016870 Hexosaminidase B Human genes 0.000 description 1
- 108010053345 Hexosaminidase B Proteins 0.000 description 1
- 102000002268 Hexosaminidases Human genes 0.000 description 1
- 108010000540 Hexosaminidases Proteins 0.000 description 1
- 101001066305 Homo sapiens N-acetylgalactosamine-6-sulfatase Proteins 0.000 description 1
- 101001123859 Homo sapiens Sialidase-1 Proteins 0.000 description 1
- 208000023105 Huntington disease Diseases 0.000 description 1
- 108010003272 Hyaluronate lyase Proteins 0.000 description 1
- 102000001974 Hyaluronidases Human genes 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 208000031226 Hyperlipidaemia Diseases 0.000 description 1
- 102000004627 Iduronidase Human genes 0.000 description 1
- 108010003381 Iduronidase Proteins 0.000 description 1
- 108091092195 Intron Proteins 0.000 description 1
- 241001580017 Jana Species 0.000 description 1
- 101150117895 LAMP2 gene Proteins 0.000 description 1
- 239000005639 Lauric acid Substances 0.000 description 1
- 241000713666 Lentivirus Species 0.000 description 1
- 208000009829 Lewy Body Disease Diseases 0.000 description 1
- 102000004882 Lipase Human genes 0.000 description 1
- 108090001060 Lipase Proteins 0.000 description 1
- 239000004367 Lipase Substances 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 101100283467 Mus musculus Gnptab gene Proteins 0.000 description 1
- 101100506743 Mus musculus Hgsnat gene Proteins 0.000 description 1
- GXCLVBGFBYZDAG-UHFFFAOYSA-N N-[2-(1H-indol-3-yl)ethyl]-N-methylprop-2-en-1-amine Chemical compound CN(CCC1=CNC2=C1C=CC=C2)CC=C GXCLVBGFBYZDAG-UHFFFAOYSA-N 0.000 description 1
- 102100031688 N-acetylgalactosamine-6-sulfatase Human genes 0.000 description 1
- 102100023282 N-acetylglucosamine-6-sulfatase Human genes 0.000 description 1
- 108010023320 N-acetylglucosamine-6-sulfatase Proteins 0.000 description 1
- 108010006140 N-sulfoglucosamine sulfohydrolase Proteins 0.000 description 1
- 102100027661 N-sulphoglucosamine sulphohydrolase Human genes 0.000 description 1
- 101150098207 NAAA gene Proteins 0.000 description 1
- 208000028389 Nerve injury Diseases 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 108010006232 Neuraminidase Proteins 0.000 description 1
- 102000005348 Neuraminidase Human genes 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- 101100164201 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) apg-4 gene Proteins 0.000 description 1
- 101100380569 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) apg-5 gene Proteins 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 101710090026 Omega-hydroxyceramide transacylase Proteins 0.000 description 1
- 102100031247 Omega-hydroxyceramide transacylase Human genes 0.000 description 1
- 235000021314 Palmitic acid Nutrition 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- 108010068563 PepT tripeptidase Proteins 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 102000003728 Peroxisome Proliferator-Activated Receptors Human genes 0.000 description 1
- 108090000029 Peroxisome Proliferator-Activated Receptors Proteins 0.000 description 1
- 102000013353 Phosphoinositide Phosphatases Human genes 0.000 description 1
- 108010090786 Phosphoinositide Phosphatases Proteins 0.000 description 1
- 101710122111 Probable proline iminopeptidase Proteins 0.000 description 1
- 101710170844 Proline iminopeptidase Proteins 0.000 description 1
- 102100036197 Prosaposin Human genes 0.000 description 1
- 101710152403 Prosaposin Proteins 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 101150002602 Psap gene Proteins 0.000 description 1
- 101710122579 Putative proline iminopeptidase Proteins 0.000 description 1
- 208000032561 Rare neurodegenerative disease Diseases 0.000 description 1
- 102000010155 SLC38A9 Human genes 0.000 description 1
- 108060000385 SLC38A9 Proteins 0.000 description 1
- 108091006657 SLC9A6 Proteins 0.000 description 1
- 101000718529 Saccharolobus solfataricus (strain ATCC 35092 / DSM 1617 / JCM 11322 / P2) Alpha-galactosidase Proteins 0.000 description 1
- 235000019485 Safflower oil Nutrition 0.000 description 1
- 101710192761 Serine-type anaerobic sulfatase-maturating enzyme Proteins 0.000 description 1
- 102100028760 Sialidase-1 Human genes 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 1
- 102100029972 Sodium/hydrogen exchanger 6 Human genes 0.000 description 1
- 208000010346 Sphingolipidoses Diseases 0.000 description 1
- 201000001307 Sphingolipidosis Diseases 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 102000005262 Sulfatase Human genes 0.000 description 1
- 101710141373 Tissue alpha-L-fucosidase Proteins 0.000 description 1
- 102100040526 Tissue alpha-L-fucosidase Human genes 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 108010070926 Tripeptide aminopeptidase Proteins 0.000 description 1
- 241000287433 Turdus Species 0.000 description 1
- 108010044965 UDP-N-acetylglucosamine-lysosomal-enzyme N-acetylglucosaminephosphotransferase Proteins 0.000 description 1
- HGWPFSBHDACWNL-GFBLOWMDSA-N [(1r,5s)-8-methyl-8-oxido-8-azoniabicyclo[3.2.1]octan-3-yl] 3-hydroxy-2-phenylpropanoate Chemical compound C([C@H]1CC[C@@H](C2)[N+]1([O-])C)C2OC(=O)C(CO)C1=CC=CC=C1 HGWPFSBHDACWNL-GFBLOWMDSA-N 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 239000000205 acacia gum Substances 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 210000000577 adipose tissue Anatomy 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- NNISLDGFPWIBDF-MPRBLYSKSA-N alpha-D-Gal-(1->3)-beta-D-Gal-(1->4)-D-GlcNAc Chemical compound O[C@@H]1[C@@H](NC(=O)C)C(O)O[C@H](CO)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO)O2)O)[C@@H](O)[C@@H](CO)O1 NNISLDGFPWIBDF-MPRBLYSKSA-N 0.000 description 1
- 108010012864 alpha-Mannosidase Proteins 0.000 description 1
- 102000019199 alpha-Mannosidase Human genes 0.000 description 1
- 102000002014 alpha-N-Acetylgalactosaminidase Human genes 0.000 description 1
- 108010015684 alpha-N-Acetylgalactosaminidase Proteins 0.000 description 1
- 108010009380 alpha-N-acetyl-D-glucosaminidase Proteins 0.000 description 1
- DTOSIQBPPRVQHS-PDBXOOCHSA-N alpha-linolenic acid Chemical compound CC\C=C/C\C=C/C\C=C/CCCCCCCC(O)=O DTOSIQBPPRVQHS-PDBXOOCHSA-N 0.000 description 1
- 235000020661 alpha-linolenic acid Nutrition 0.000 description 1
- 201000008333 alpha-mannosidosis Diseases 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- 239000003524 antilipemic agent Substances 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 230000005775 apoptotic pathway Effects 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- 101150111036 arsB gene Proteins 0.000 description 1
- 101150096483 atg5 gene Proteins 0.000 description 1
- 230000004900 autophagic degradation Effects 0.000 description 1
- 210000004227 basal ganglia Anatomy 0.000 description 1
- 235000019445 benzyl alcohol Nutrition 0.000 description 1
- 229960002903 benzyl benzoate Drugs 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 102000006995 beta-Glucosidase Human genes 0.000 description 1
- 108010047754 beta-Glucosidase Proteins 0.000 description 1
- 108010085377 beta-N-Acetylhexosaminidases Proteins 0.000 description 1
- 102000007478 beta-N-Acetylhexosaminidases Human genes 0.000 description 1
- 230000008436 biogenesis Effects 0.000 description 1
- 230000017531 blood circulation Effects 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 230000003822 cell turnover Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 1
- 208000024042 cholesterol ester storage disease Diseases 0.000 description 1
- 208000013760 cholesteryl ester storage disease Diseases 0.000 description 1
- 210000000349 chromosome Anatomy 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 150000001851 cinnamic acid derivatives Chemical class 0.000 description 1
- 229960002174 ciprofibrate Drugs 0.000 description 1
- 229950003072 clinofibrate Drugs 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 230000007278 cognition impairment Effects 0.000 description 1
- 230000006999 cognitive decline Effects 0.000 description 1
- 230000001149 cognitive effect Effects 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 238000011970 concomitant therapy Methods 0.000 description 1
- 235000005687 corn oil Nutrition 0.000 description 1
- 239000002285 corn oil Substances 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 230000001054 cortical effect Effects 0.000 description 1
- 235000012343 cottonseed oil Nutrition 0.000 description 1
- 239000002385 cottonseed oil Substances 0.000 description 1
- 239000003431 cross linking reagent Substances 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 230000007850 degeneration Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 230000005750 disease progression Effects 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 210000005064 dopaminergic neuron Anatomy 0.000 description 1
- 239000012154 double-distilled water Substances 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 229940000406 drug candidate Drugs 0.000 description 1
- 238000002651 drug therapy Methods 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 210000002472 endoplasmic reticulum Anatomy 0.000 description 1
- 230000009088 enzymatic function Effects 0.000 description 1
- 201000010063 epididymitis Diseases 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 235000019441 ethanol Nutrition 0.000 description 1
- 235000019325 ethyl cellulose Nutrition 0.000 description 1
- 229920001249 ethyl cellulose Polymers 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 235000019197 fats Nutrition 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 201000008049 fucosidosis Diseases 0.000 description 1
- 150000002270 gangliosides Chemical class 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 230000004077 genetic alteration Effects 0.000 description 1
- 231100000118 genetic alteration Toxicity 0.000 description 1
- 101150091511 glb-1 gene Proteins 0.000 description 1
- 230000002518 glial effect Effects 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 208000035474 group of disease Diseases 0.000 description 1
- 210000002443 helper t lymphocyte Anatomy 0.000 description 1
- 108010089932 heparan sulfate sulfatase Proteins 0.000 description 1
- 210000001320 hippocampus Anatomy 0.000 description 1
- 229960002773 hyaluronidase Drugs 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 230000005847 immunogenicity Effects 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 230000028709 inflammatory response Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 229960004488 linolenic acid Drugs 0.000 description 1
- KQQKGWQCNNTQJW-UHFFFAOYSA-N linolenic acid Natural products CC=CCCC=CCC=CCCCCCCCC(O)=O KQQKGWQCNNTQJW-UHFFFAOYSA-N 0.000 description 1
- 235000019421 lipase Nutrition 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 238000007443 liposuction Methods 0.000 description 1
- 239000012669 liquid formulation Substances 0.000 description 1
- 229940063720 lopid Drugs 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 230000001926 lymphatic effect Effects 0.000 description 1
- VTHJTEIRLNZDEV-UHFFFAOYSA-L magnesium dihydroxide Chemical compound [OH-].[OH-].[Mg+2] VTHJTEIRLNZDEV-UHFFFAOYSA-L 0.000 description 1
- 239000000347 magnesium hydroxide Substances 0.000 description 1
- 229910001862 magnesium hydroxide Inorganic materials 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 210000005060 membrane bound organelle Anatomy 0.000 description 1
- 230000003340 mental effect Effects 0.000 description 1
- 230000037353 metabolic pathway Effects 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 239000011859 microparticle Substances 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 239000006082 mold release agent Substances 0.000 description 1
- 230000007659 motor function Effects 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 201000002273 mucopolysaccharidosis II Diseases 0.000 description 1
- 208000022018 mucopolysaccharidosis type 2 Diseases 0.000 description 1
- 210000003007 myelin sheath Anatomy 0.000 description 1
- WQEPLUUGTLDZJY-UHFFFAOYSA-N n-Pentadecanoic acid Natural products CCCCCCCCCCCCCCC(O)=O WQEPLUUGTLDZJY-UHFFFAOYSA-N 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- 239000007923 nasal drop Substances 0.000 description 1
- 229940100662 nasal drops Drugs 0.000 description 1
- 230000008764 nerve damage Effects 0.000 description 1
- 230000002314 neuroinflammatory effect Effects 0.000 description 1
- 230000001962 neuropharmacologic effect Effects 0.000 description 1
- 230000000324 neuroprotective effect Effects 0.000 description 1
- 210000001331 nose Anatomy 0.000 description 1
- 108020004707 nucleic acids Proteins 0.000 description 1
- 150000007523 nucleic acids Chemical class 0.000 description 1
- 102000039446 nucleic acids Human genes 0.000 description 1
- 210000004940 nucleus Anatomy 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 229940126701 oral medication Drugs 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 230000007918 pathogenicity Effects 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 239000003380 propellant Substances 0.000 description 1
- 235000019419 proteases Nutrition 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- WBHHMMIMDMUBKC-XLNAKTSKSA-N ricinelaidic acid Chemical compound CCCCCC[C@@H](O)C\C=C\CCCCCCCC(O)=O WBHHMMIMDMUBKC-XLNAKTSKSA-N 0.000 description 1
- 229960003656 ricinoleic acid Drugs 0.000 description 1
- FEUQNCSVHBHROZ-UHFFFAOYSA-N ricinoleic acid Natural products CCCCCCC(O[Si](C)(C)C)CC=CCCCCCCCC(=O)OC FEUQNCSVHBHROZ-UHFFFAOYSA-N 0.000 description 1
- 235000005713 safflower oil Nutrition 0.000 description 1
- 239000003813 safflower oil Substances 0.000 description 1
- 235000003441 saturated fatty acids Nutrition 0.000 description 1
- 150000004671 saturated fatty acids Chemical class 0.000 description 1
- 239000008159 sesame oil Substances 0.000 description 1
- 235000011803 sesame oil Nutrition 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 238000009097 single-agent therapy Methods 0.000 description 1
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 description 1
- 229960002930 sirolimus Drugs 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 1
- 239000003549 soybean oil Substances 0.000 description 1
- 235000012424 soybean oil Nutrition 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 108060007951 sulfatase Proteins 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 230000003977 synaptic function Effects 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 239000000196 tragacanth Substances 0.000 description 1
- 229940116362 tragacanth Drugs 0.000 description 1
- 108091005703 transmembrane proteins Proteins 0.000 description 1
- 102000035160 transmembrane proteins Human genes 0.000 description 1
- 150000003626 triacylglycerols Chemical class 0.000 description 1
- 229940055755 tricor Drugs 0.000 description 1
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 1
- 210000003901 trigeminal nerve Anatomy 0.000 description 1
- 241001529453 unidentified herpesvirus Species 0.000 description 1
- 241001430294 unidentified retrovirus Species 0.000 description 1
- 235000021122 unsaturated fatty acids Nutrition 0.000 description 1
- 150000004670 unsaturated fatty acids Chemical class 0.000 description 1
- 238000009834 vaporization Methods 0.000 description 1
- 230000008016 vaporization Effects 0.000 description 1
- 230000004393 visual impairment Effects 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/005—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'active' part of the composition delivered, i.e. the nucleic acid delivered
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/192—Carboxylic acids, e.g. valproic acid having aromatic groups, e.g. sulindac, 2-aryl-propionic acids, ethacrynic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/20—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids
- A61K31/203—Retinoic acids ; Salts thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/216—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acids having aromatic rings, e.g. benactizyne, clofibrate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/1703—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- A61K38/1709—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/46—Hydrolases (3)
- A61K38/465—Hydrolases (3) acting on ester bonds (3.1), e.g. lipases, ribonucleases
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/46—Hydrolases (3)
- A61K38/47—Hydrolases (3) acting on glycosyl compounds (3.2), e.g. cellulases, lactases
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/46—Hydrolases (3)
- A61K38/48—Hydrolases (3) acting on peptide bonds (3.4)
- A61K38/4813—Exopeptidases (3.4.11. to 3.4.19)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/24—Hydrolases (3) acting on glycosyl compounds (3.2)
- C12N9/2402—Hydrolases (3) acting on glycosyl compounds (3.2) hydrolysing O- and S- glycosyl compounds (3.2.1)
- C12N9/2465—Hydrolases (3) acting on glycosyl compounds (3.2) hydrolysing O- and S- glycosyl compounds (3.2.1) acting on alpha-galactose-glycoside bonds, e.g. alpha-galactosidase (3.2.1.22)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/48—Hydrolases (3) acting on peptide bonds (3.4)
- C12N9/485—Exopeptidases (3.4.11-3.4.19)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y302/00—Hydrolases acting on glycosyl compounds, i.e. glycosylases (3.2)
- C12Y302/01—Glycosidases, i.e. enzymes hydrolysing O- and S-glycosyl compounds (3.2.1)
- C12Y302/01022—Alpha-galactosidase (3.2.1.22)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y302/00—Hydrolases acting on glycosyl compounds, i.e. glycosylases (3.2)
- C12Y302/01—Glycosidases, i.e. enzymes hydrolysing O- and S-glycosyl compounds (3.2.1)
- C12Y302/01046—Galactosylceramidase (3.2.1.46)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y302/00—Hydrolases acting on glycosyl compounds, i.e. glycosylases (3.2)
- C12Y302/01—Glycosidases, i.e. enzymes hydrolysing O- and S-glycosyl compounds (3.2.1)
- C12Y302/01052—Beta-N-acetylhexosaminidase (3.2.1.52)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y304/00—Hydrolases acting on peptide bonds, i.e. peptidases (3.4)
- C12Y304/14—Dipeptidyl-peptidases and tripeptidyl-peptidases (3.4.14)
- C12Y304/14009—Tripeptidyl-peptidase I (3.4.14.9)
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2217/00—Genetically modified animals
- A01K2217/07—Animals genetically altered by homologous recombination
- A01K2217/075—Animals genetically altered by homologous recombination inducing loss of function, i.e. knock out
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2227/00—Animals characterised by species
- A01K2227/10—Mammal
- A01K2227/105—Murine
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/0306—Animal model for genetic diseases
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/10011—Adenoviridae
- C12N2710/10311—Mastadenovirus, e.g. human or simian adenoviruses
- C12N2710/10341—Use of virus, viral particle or viral elements as a vector
- C12N2710/10343—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14141—Use of virus, viral particle or viral elements as a vector
- C12N2750/14143—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Genetics & Genomics (AREA)
- Medicinal Chemistry (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Epidemiology (AREA)
- Biotechnology (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Immunology (AREA)
- Gastroenterology & Hepatology (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Microbiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biophysics (AREA)
- Psychiatry (AREA)
- Hospice & Palliative Care (AREA)
- Plant Pathology (AREA)
- Physics & Mathematics (AREA)
- Virology (AREA)
- Cell Biology (AREA)
- Toxicology (AREA)
- Diabetes (AREA)
- Emergency Medicine (AREA)
Abstract
본원에는 리소좀 효소를 암호화하는 유전자 및 약제의 투여를 포함하는 리소좀 축적 질환의 치료 방법이 제공된다. 공동투여에 의한 유전자 요법과 약제학적 조성물의 병용은 각 개별 요법의 효과를 더욱 향상시킬 뿐만 아니라 각 개별 조성물의 다양한 작용 메커니즘으로 인해 치료에 대한 다면적 접근을 제공한다.
Description
관련 출원에 대한 상호 참조
본 출원은 2019년 3월 22일에 출원된 미국 가특허출원 제62/822,310호에 대한 우선권을 주장하며, 이는 그 전체가 본원에 참조로 포함된다.
기술 분야
본 발명은 리소좀 효소를 암호화하는 유전자를 후기 영아 바텐병 및 크라베병과 같은 리소좀 축적 장애의 치료를 위한 약제와 병용하여 투여하는 방법에 관한 것이다.
리소좀은 지질, 단백질, 탄수화물 및 핵산의 분해를 담당하는 몇몇 효소를 함유하는 막 결합된 소기관이다(De Duve and Wattiaux, 1966). 이들 성분 중 거의 모든 것의 결함 및 결핍은 리소좀 내의 분해되지 않고/거나 부분적으로 분해된 물질의 축적을 초래하여, 바텐병(영아, 후기-영아 및 소아(juvenile) 신경세포 세로이드 리포푸신증), 크라베병 및 테이-삭스병을 포함하는 수많은 리소좀 축적 장애(LSD)의 기초를 형성한다(De Duve and Wattiaux, 1966, Perez-Sala et al., 2009).
신경세포 세로이드 리포푸신증(neuronal ceroid lipofuscinosis: NCL)은 주로 전형적인 상염색체 열성 리소좀 축적 장애로 구성된 신경퇴행성 질환의 한 그룹이다. NCL은 뉴런 또는 다른 세포 유형 내의 자가형광 저장 물질의 축적과 같은 조직학적 소견을 동반하는 진행성 정신 저하, 인지 장애, 시각 기능상실, 발작 및 운동 기능 약화와 같은 임상 징후를 특징으로 할 수 있다(Hachiya et al., 2006). NCL은 발병 연령, 축적된 저장 물질의 초미세구조적 변이 및 각각의 특정 질환 유형 고유의 유전적 변경에 기반하여 여러 그룹(1형 내지 10형)으로 세분화되었다(Lane et al., 1996 and Mole el al., 2005).
영아 신경세포 세로이드 리포푸신증(INCL)은 그 자체로 실명, 인지 결함, 발작 및 조기 사망을 포함하는 증상으로 약 18개월령의 아동에서 나타난다(Hawkins-Salsbury et al., 2013). 리소좀 효소 팔미토일 단백질 티오에스테라제-1(PPT1)을 암호화하는 clnl 유전자의 결함은 중추 신경계와 조직 둘 다에서 리포푸신과 같은 다양한 자가형광 물질 기질의 축적을 유발한다(Id.). 뒤이어 발생하는 신경 변성, 피질 박막화 및 뇌 위축은 이환되지 않은 아동에 비해 뇌 질량의 약 50% 감소를 초래한다(Id.). 현재 이용 가능한 치료법은 없다.
후기 영아 신경세포 세로이드 리포푸신증(얀스키-빌쇼스키병(Jansky-Bielschowsky disease), LINCL, 2형)는 전형적으로 2세 내지 4세에 증상을 야기하고, 빠르고 진행되고, 뉴런 및 다른 세포의 수가 급격히 감소한 결과로서 8세 내지 15세에 사망으로 종결된다(Lane et al, 1996 and Sleat et al., 1997). LINCL은 염색체 11pl5.5에 매핑된 총 길이 6.65kb의 13개 엑손과 12개 인트론의 cln2 유전자의 돌연변이와 연관된다. cln2 유전자는 리소좀 구획의 산성 환경에서 단백질의 아미노 말단으로부터 트리펩타이드를 제거하는 기능을 하는 46 KD 단백질인 리소좀 트리펩티딜 트리펩티다제 I(TPP-I 또는 펩스틴 비민감성 프로테아제)을 암호화한다(Goebel 1995 and Vines et al., 1999). 이러한 cln2 유전자의 돌연변이는 TPP1 단백질의 결핍 및/또는 기능 상실을 초래하여, 세로이드-리포푸신으로서 공지된 자가형광 지방색소가 리소좀 내부에 축적되도록 야기한다(Goebel, 1995). 현재 상기 질환용으로 이용 가능한 확립된 치료법 또는 약물은 없으며 모든 접근법은 단지 보조적이거나 대증적이며, 이는 신규한 치료적 방식이 필요함을 나타낸다(Chang et al., 2008). 그러나, cln2 돌연변이의 상이한 변이체들이 있으며 LINCL 환자에서 잔류 TPP-1 활성이 발견될 수 있다는 보고가 있으며, 이는 LINCL에 걸린 환자에서 정상 cln2 유전자의 수개의 카피가 남아있어야 함을 나타낸다 [Viglio et al, 2001 and Walus et al, 2010].
또 다른 NCL은 소아 바텐병(소아 영아 신경세포 세로이드 리포푸신증(JINCL))이다. cln3 유전자는 시냅스 기능 또는 분해에 관여할 수 있는 리소좀 막관통 단백질을 암호화한다(Dolisca et al, 2013). JINCL과 연관된 cln3의 돌연변이는 1.01 kb 결실을 특징으로 한다. 다른 NCL과 마찬가지로, JINCL의 발병은 점진적인 실명, 운동 및 인지 저하, 발작 및 조기 사망을 포함하는 증상으로 4세 내지 7세의 아동에서 발생한다.
크라베병은 희귀한 리소좀 축적 질환으로, 미엘린초(myelin sheath)의 스핑고리피도스 기반 저하의 결과이다. 상기 질환은 β-갈락토세레브로시다제 리소좀 저장 효소의 돌연변이, 그로 인한 세포독성 대사산물 축적 및 탈수초화를 초래하는 붕괴된 다양한 대사 경로에 의해 유발된다. 크라베병은 영아형, 후기 영아형, 소아형 및 심지어 성인형일 수 있다(Pavuluri et al., 2017).
테이-삭스병은 GM2 강글리오시드를 GM3 강글리오시드로 프로세싱하는 역할을 하는 효소인 β-헥소스아미니다제를 암호화하는 hexa 유전자가 돌연변이된 결과이다(Dersh et al., 2016). 상기 효소는 2개의 서브유닛으로 구성되며 돌연변이는 상기 효소의 상실 또는 비활성화를 초래하여 GM2의 축적을 초래한다. 테이-삭스병과 연관된 hexa 유전자에서 식별된 100가지가 넘는 돌연변이가 있다(Id.).
다양한 유전자 돌연변이가 다수의 효소와 연관되어 리소좀 축적 장애를 초래하기 때문에, 유전자 요법은 잠재적인 치료 옵션이다. 그러나, 특히 신경퇴행성 질환의 치료를 위한 유전자 전달은 치료 유전자를 뇌에 전달하는 문제를 나타낸다. 바이러스 기반 유전자 전달 메커니즘은 익히 공지되어 있으며, 유전자 전달은 바이러스의 불량한 면역원성 때문에 아데노-연관 바이러스 벡터의 사용을 통해 명확하게 달성될 수 있다(Shaw et al., 2013). 또한, 치료 유전자를 포함하는 이들 바이러스 벡터의 비강 투여는 뇌로의 전달을 허용한다. 비강 전달은 뇌로 직접 전달하기 위해 혈뇌 장벽을 우회할 수 있는 몇 가지 가능성이 있는 "코-뇌"(N2B) 수송 시스템(Djupesland, 2013)을 이용하는 것으로 믿어진다. 여기에는 비점막에서 흡수된 약물의 부비동으로 및 결국에는 경동맥으로의 배출이 포함되며, 여기서 정맥혈로부터 뇌로의 "역류 전달"이 발생할 수 있다. 중추신경계(CNS) 사이의 후각 삼차 신경부터 혈관주위 공간으로의 림프로(lymphatic drainage) 또한 N2B 수송의 메커니즘으로서 가정되었다.
더욱이, 유전자 요법과 경구 약제 치료의 병용은 단일 요법의 효과를 향상시키는 또 다른 강력한 치료학적 접근법을 제공한다. 유전자 요법과의 병용을 위한 2가지 약제 후보는 신남산과 올레아미드를 포함한다. 신남산은 신경보호 효과를 갖는 식물에서 발견되는 천연 발생 지방산이다(Prorok et al., 2019). 이는 파킨슨병에서 도파민성 뉴런의 보호를 위한 퍼옥시좀 증식인자-활성화 수용체a(PPARa)의 활성화에 관여하는 것으로 밝혀졌다(Id). 신남산의 다양한 유도체는 이의 항산화 프로파일 및 혈뇌 장벽을 가로지르는 능력에 대해서도 알려져 있고, 이로 인해서 이들 제제는 신경퇴행성 장애 치료에 이상적이 된다(Roleira et al., 2010). 올레아미드는 광범위한 신경약리학적 작용을 갖는 또 다른 지방산이다. 공지된 내인성 지방산인 올레아미드는 뇌척수액에서 처음 발견되었다(Nam et al., 2017). 이는 해마에 항시(constitutively) 존재하고, 여기서 PPARa 리간드로 작용하고 수면 유도에 관여한다(Pahan, 2017). 따라서, 유전자 요법과 병용된 천연 약제로서의 신남산과 내인성 뇌 리간드로서의 올레아미드의 잠재적인 사용은 가치가 있다.
또한, 여러 연구는 신경-염증 및 세포자멸사(apoptotic) 경로의 유도가 LINCL을 포함하는 대부분의 형태의 NCL에서 신경 손상에 기인할 수 있다고 결론을 내렸다(Geraets et al. 2016, Dhar et al. 2002, Puranam et al. 1997, Kohan et al. 2011). 염증이 LINCL에서 개시 인자는 아니지만, 신경교-매개 지속 염증 반응은 질환 진행에 기여하는 것으로 믿어진다(Cooper et al. 2015, Macauley et al. 2014). FDA 승인된 지질-저하 약물인 젬피브로질은 혈액 순환에서 트리글리세라이드의 수준을 감소시키고 고지혈증의 위험을 감소시키는 것으로 공지되어 있다(Robins et al. 2001, Rubins & Robins 1992, Rubins et al. 1999). 그러나, 최근의 수많은 연구는 젬피브로질이 이의 지질 저하 효과 외에도, 염증, T-헬퍼 세포의 전환, 세포-대-세포 접촉, 이동, 산화 스트레스 및 리소좀 생물발생을 담당하는 다른 많은 신호전달 경로를 또한 조절할 수 있음을 밝히고 있다(Ghosh & Pahan 2012a, Corbett et al. 2012, Ghosh et al. 2012, Jana et al. 2007, Jana & Pahan 2012, Dasgupta et al. 2007, Pahan et al. 2002, Roy & Pahan 2009, Ghosh et al. 2015). 따라서, 젬피브로질과 병용된 유전자 요법도 큰 잠재력을 가지고 있다.
본원에 기재된 일 실시형태는 리소좀 효소를 암호화하는 유전자의 치료학적 유효량을 포함하는 제1 조성물 및 약제의 치료학적 유효량을 포함하는 제2 조성물을 이를 필요로 하는 대상체에게 투여하는 것을 포함하는, 리소좀 축적 질환의 치료 방법이다.
한 측면에서, 제1 조성물은 비강내 투여된다.
또 다른 측면에서, 유전자는 혈뇌 장벽을 가로질러 전달된다.
또 다른 측면에서, 제1 조성물은 약 7일 내지 30일마다 1회 투여된다.
또 다른 측면에서, 제1 조성물은 리소좀 효소를 암호화하는 유전자를 포함하는 바이러스 벡터를 포함한다.
한 측면에서, 바이러스 벡터는 아데노바이러스-연관 바이러스 벡터이다.
또 다른 측면에서, 유전자는 ppt1, cln2, cln3, gale 또는 hexa를 포함한다.
또 다른 측면에서, 리소좀 효소는 팔미토일-단백질 티오에스테라제-1, 트리펩티딜 펩티다제 1, 갈락토실세라마이드, 바테닌 또는 헥소스아미니다제 A를 포함한다.
또 다른 측면에서, 방법은 영아 신경세포 세로이드 리포푸신증을 포함하는 리소좀 축적 질환을 치료하기 위한 pptl 유전자를 포함하는 제1 조성물을 투여하는 것을 포함한다.
한 측면에서, 방법은 후기 영아 신경세포 세로이드 리포푸신증을 포함하는 리소좀 축적 질환을 치료하기 위한 cln2 유전자를 포함하는 제1 조성물을 투여하는 것을 포함한다.
또 다른 측면에서, 방법은 소아 신경세포 세로이드 리포푸신증을 포함하는 리소좀 축적 질환을 치료하기 위한 cln3 유전자를 포함하는 제1 조성물을 투여하는 것을 포함한다.
또 다른 측면에서, 방법은 크라베병을 포함하는 리소좀 축적 질환을 치료하기 위한 gale 유전자를 포함하는 제1 조성물을 투여하는 것을 포함한다.
또 다른 측면에서, 상기 방법은 테이-삭스병을 포함하는 리소좀 축적 질환을 치료하기 위한 hexa 유전자를 포함하는 제1 조성물을 투여하는 것을 포함한다.
한 측면에서, 약제는 신남산, 올레아미드 또는 피브레이트를 포함한다.
또 다른 측면에서, 피브레이트는 젬피브로질 또는 페노피브레이트이다.
또 다른 측면에서, 제2 조성물은 치료학적 유효량의 올-트랜스 레티노산( all-trans retinoic acid)을 추가로 포함한다.
또 다른 측면에서, 약제의 치료학적 유효량은 약제가 올-트랜스 레티노산 없이 전달될 때보다 약제가 올-트랜스 레티노산과 병용되어 투여될 때 더 낮다.
한 측면에서, 제2 조성물은 경구 투여된다.
또 다른 측면에서, 제2 조성물은 1일 1회 투여된다.
또 다른 측면에서, 제1 조성물과 제2 조성물을 투여하는 것은 제1 조성물 또는 제2 조성물을 단독으로 투여하는 것보다 대상체에서 더 큰 치료 효과를 제공한다.
또 다른 측면에서, 리소좀 축적 장애는 후기 영아 바텐병, 소아 바텐병, 크라베병, 테이-삭스병, 니만-픽병, 파브리병, 파버병 및 고셔병(Gaucher disease)으로 이루어진 그룹으로부터 선택된다.
한 측면에서, 제1 조성물은 비강내 투여되고 제2 조성물은 경구 투여된다.
또 다른 측면에서, 제1 조성물은 적어도 7일마다 1회 투여되고, 제2 조성물은 1일 1회 투여된다.
또 다른 측면에서, 바이러스 벡터는 아데노바이러스-연관 바이러스 벡터이다.
또 다른 측면에서, 유전자는 cln2를 포함한다.
또 다른 측면에서, 제2 조성물은 젬피브로질을 포함한다.
또 다른 측면에서, 제1 조성물의 투여는 수명을 약 100일 증가시켰다.
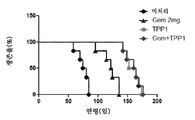
도 1: 아데노바이러스 인간 Cln2 유전자(Ad-Cln2)의 비강내 전달은 후기 영아 바텐병의 동물 모델인 Cln2(-/-) 마우스의 수명을 연장시킨다. 비강내 유전자 전달을 위해, Cln2(-/-) 마우스에게 2주령부터 시작하여 4주 동안 주 2회 5 ㎕의 용적 중의 Ad-Cln2의 5 x 106 게놈 카피를 비강내(2.5 ㎕/콧구멍)로 투여하였다. 젬피브로질(gem) 처리를 위해, 마우스에게 6주령부터 시작하여 7.5 mg/체중 kg/일의 용량으로 gem(0.1% MeC에 용해됨)을 경구 투여하였다. 도 1은 카플란-마이어 플롯으로 도시되는 생존율(%)을 설명한다.
도 2: 아데노바이러스 인간 Cln2 유전자(Ad-Cln2)의 비강내 전달은 후기 영아 바텐병의 동물 모델인 Cln2(-/-) 마우스의 수명을 연장시킨다. 비강내 유전자 전달을 위해, Cln2(-/-) 마우스에게 2주령부터 시작하여 4주 동안 주 2회 5 ㎕의 용적 중의 Ad-Cln2의 5 x 106 게놈 카피를 비강내(2.5 ㎕/콧구멍)로 투여하였다. 젬피브로질(gem) 처리를 위해, 마우스에게 6주령부터 시작하여 7.5 mg/체중 kg/일의 용량으로 gem(0.1% MeC에 용해됨)을 경구 투여하였다. 도 2는 평균 생존 일수를 설명한다. 3마리의 수컷과 3마리의 암컷을 포함하는 6마리의 마우스(n=6)가 각 그룹에서 사용되었다. ***p< 0.001; NS, 유의하지 않음.
도 2: 아데노바이러스 인간 Cln2 유전자(Ad-Cln2)의 비강내 전달은 후기 영아 바텐병의 동물 모델인 Cln2(-/-) 마우스의 수명을 연장시킨다. 비강내 유전자 전달을 위해, Cln2(-/-) 마우스에게 2주령부터 시작하여 4주 동안 주 2회 5 ㎕의 용적 중의 Ad-Cln2의 5 x 106 게놈 카피를 비강내(2.5 ㎕/콧구멍)로 투여하였다. 젬피브로질(gem) 처리를 위해, 마우스에게 6주령부터 시작하여 7.5 mg/체중 kg/일의 용량으로 gem(0.1% MeC에 용해됨)을 경구 투여하였다. 도 2는 평균 생존 일수를 설명한다. 3마리의 수컷과 3마리의 암컷을 포함하는 6마리의 마우스(n=6)가 각 그룹에서 사용되었다. ***p< 0.001; NS, 유의하지 않음.
본원에 개시된 실시형태는 총망라한 것이거나 다음의 설명에서 본 개시내용의 범위를 정확한 형태로 한정하려는 것은 아니다. 오히려, 실시형태의 교시를 당업자가 이용할 수 있도록 실시형태가 선택되고 설명된다.
본 개시내용은 리소좀 효소를 암호화하는 유전자를 후기 영아 바텐병 및 크라베병과 같은 리소좀 축적 장애의 치료를 위한 약제와 병용하여 공동투여하는 방법에 관한 것이다.
정의
달리 정의되지 않는 한, 본원에서 사용되는 모든 기술 용어 및 과학 용어는 당업자가 통상적으로 이해하는 것과 동일한 의미를 갖는다. 상충되는 경우, 정의를 포함하는 본 문서가 우선할 것이다. 본원에 기재된 것과 유사하거나 동등한 방법 및 재료가 본 발명의 실시 또는 시험에서 사용될 수 있지만, 바람직한 방법 및 재료가 하기에 기재된다. 본원에 언급된 모든 간행물, 특허출원, 특허 및 기타 참고 문헌은 그 전체가 참고로 포함된다. 본원에 개시된 재료, 방법 및 예는 단지 예시적이며 제한하려는 의도가 아니다.
본원에서 사용되는 용어 "포함한다(comprise(s))", "포함된다(include(s))", "갖는(having)", "갖다(has)", "할 수 있다(can)", "함유한다(contain(s))" 및 이들의 변형어는 추가 행위 또는 구조의 가능성을 배제하지 않는 개방형 전환 구, 용어 또는 단어인 것으로 의도된다. 단수형("a", "and" 및 "the")은 문맥상 명확히 달리 나타내지 않는 한, 복수의 지시대상을 포함한다. 본 개시내용은 또한 명시적으로 나타내건 아니건, 본원에 제시된 실시형태 또는 요소를 "포함하는", "이로 구성되는" 및 "이로 본질적으로 구성되는" 다른 실시형태를 고려한다.
본원에서 사용되는 용어 "비강내"는 비점막 표면과의 접촉 또는 폐의 기관지 통로에서의 흡수를 위한 흡입을 포함하는 투여 방식을 지칭한다.
본원에서 사용되는 용어 "경구"는 경구(oral), 장관, 구강(buccal), 구순하 및 설하 위(gastric) 투여를 포함하는 투여 방식을 지칭한다.
본원에서 사용되는 "치료하는", "치료하다" 또는 "치료"는 장애 또는 질환과 연관된 증상의 완화, 또는 이러한 증상의 추가 진행 또는 악화의 중단, 또는 질환 또는 장애의 방지 또는 예방을 의미한다. 예를 들어, 본 개시내용의 맥락 내에서, 성공적인 치료는 신경퇴행성 질환의 예방, 신경퇴행성 질환과 관련된 증상의 완화 또는 신경퇴행성 질환과 같은 질환의 진행의 정지를 포함할 수 있다. 본원에서 사용되는 바와 같이, 대조군은 그것과 비교하여 치료를 측정하기 위한 것으로, 대조군은 치료제를 투여받지 않은 대상체이다.
본원에서 수치 범위의 언급을 위해, 동일한 정도의 정확성을 가진 그 사이의 각각의 개재 숫자가 명시적으로 고려된다. 예를 들어, 6 내지 9의 범위의 경우, 6 및 9 이외에도 숫자 7 및 8이 추가로 고려되고, 범위 6.0 내지 7.0의 경우, 숫자 6.0, 6.1, 6.2, 6.3, 6.4, 6.5, 6.6, 6.7, 6.8, 6.9 및 7.0이 명시적으로 고려된다.
리소좀 효소를 암호화하는 유전자와 약제학적 조성물을 대상체에게 공동투여하는 방법으로서, 상기 유전자의 치료학적 유효량와 리소좀 축적 장애의 치료를 위한 약제를 투여하는 것을 포함하는 방법이 본원에 제공된다.
유전자 조성물
일 실시형태에서, 관심대상의 치료 유전자의 "치료학적 유효량"을 포함할 수 있는 유전자 조성물이 본원에 기재된다. "치료학적 유효량"은 원하는 치료 결과를 달성하기 위해 필요한 투여량에서 및 기간 동안 유효한 양을 지칭한다. 치료 유전자의 치료학적 유효량은 당업자에 의해 결정될 수 있고, 개체의 질환 상태, 연령, 성별 및 체중과 같은 인자 및 개체에서 원하는 반응을 유발하는 조성물의 능력에 따라 달라질 수 있다. 치료학적 유효량은 또한 유전자의 임의의 독성 또는 유해한 효과보다 치료학적으로 유익한 효과가 더 큰 양이다.
본원에 기재된 한 측면에서, 치료 유전자를 포함하는 조성물을 전달하는 방법은 비강내 투여를 통한 것이다. 치료 유전자를 포함하는 조성물을 전달하는 방법은 수동적 또는 능동적 전달 메커니즘을 통한 비강 투여를 위한 조성물의 액체 또는 분말 제형의 전달을 포함하는 임의의 수의 코로의 투여 방식을 포함한다. 일 실시형태에서, 액체 제형은 비강 흡입, 수동 작동 비강 장치 및 기계적 분무 펌프를 통한 기화를 포함하는 다양한 메커니즘을 통해 전달될 수 있다. 또 다른 실시형태에서, 이러한 전달 메커니즘을 위한 제형은 에어로졸을 함유하는 추진제 또는 추진제-비함유 흡입가능한 용액의 형태일 수 있다. 다른 실시형태에서, 기계적 분무 펌프는 수동 작동 또는 가스 구동될 수 있거나, 전기로 작동하는 네블라이저 및 아토마이저의 경우와 같이 전기적일 수 있다. 추가 실시형태에서, 분말 제형은 기계적 동력 분무기, 비강 흡입기 및 네블라이저/아토마이저를 통해 전달될 수 있다.
비강내 투여의 목표는 궁극적으로 치료 유전자를 혈뇌 장벽을 가로질러 뇌로 전달하는 것이다. 어떠한 이론에도 얽매임 없이, 유전자 요법의 비강 투여는 뇌로 직접 전달하기 위해 혈뇌 장벽을 우회할 수 있는 몇 가지 가능성이 있는 "코-뇌"(N2B) 수송 시스템(Djupesland, 2013)을 이용할 수 있다. 여기에는 비점막에서 흡수된 약물의 부비동으로 및 결국에는 경동맥으로의 배출이 포함되며, 여기서 정맥혈로부터 뇌로의 "역류 전달"이 발생할 수 있다. 따라서, 본원에 기재된 한 측면에서, 유전자는 혈뇌 장벽을 가로질러 전달된다.
본원에 기재된 한 실시형태에서, 치료학적 유효량의 유전자를 포함하는 유전자 조성물은 약 1일 내지 약 100일마다 1회, 약 2일 내지 약 90일마다 1회, 약 3일 내지 약 80일마다 1회, 약 4일 내지 약 70일마다 1회, 약 5일 내지 약 60일마다 1회, 약 6일 내지 약 50일마다 1회, 7일 내지 약 40일마다 1회, 약 8일 내지 약 30일마다 1회 또는 약 9일 내지 20일마다 1회 투여된다. 한 측면에서, 유전자 조성물은 약 7일 내지 약 30일마다 1회 투여된다. 다른 측면에서, 유전자 조성물은 약 7일마다 1회 투여된다.
본원에 기재된 일 실시형태에서, 치료 유전자는 바이러스 벡터의 사용을 통해 전달된다. 유전자 요법에 이상적인 바이러스 벡터는 독성을 유발하지 않으면서 표적 세포를 성공적으로 감염시키고 핵으로 전달되며 발현 수준을 유지할 수 있다. 바이러스 벡터는 레트로바이러스 또는 아데노바이러스를 포함하는 유전자 요법에 적합한 임의의 바이러스로 구성될 수 있다. 바이러스 벡터에 적합한 다른 바이러스는 아데노-연관 바이러스, 렌티바이러스, 폭스 바이러스, 알파바이러스 및 헤르페스 바이러스를 포함한다. 아데노-연관 바이러스 벡터는 이의 상대적으로 낮은 병원성과 지속적인 발현으로 인해 이상적인 벡터이다. 따라서, 본원에 기재된 한 측면에서, 바이러스 벡터는 아데노-연관 바이러스 벡터를 포함한다.
본원에 기재된 다른 실시형태에서, 바이러스 벡터는 리소좀 효소를 암호화하는 치료 유전자를 포함한다. 리소좀 효소 및 연관 단백질을 암호화하는 유전자는 아스파르틸글루코스아미니다제(ago), 아릴설파타제 A(arsa), 아릴설파타제 B(arsb), 산 세라미다제(asahl), 자가포식 단백질 5(atg5), 자가포식 단백질 7(atg7), 팔미토일 단백질 티오에스테라제 1 또는 PPT1(cln1), 트리펩티딜 펩티다제 1(cln2), 바테닌(cln3), 막관통 소포체 단백질(cln6), 소포체 탑재물 수용체(cln8), 시스티노신(ctns), 카텝신 A(ctsa), 카텝신 K(ctsk), 포스포이노시티드 포스파타제(fig4), 알파-L-푸코시다제 1(fuca1), 산 알파-글루코시다제(gaa), 갈락토실세라미다제(galc), 갈락토사민(N-아세틸)-6-설파타제(galns), 베타-글루코세레브로시다제(gba), 알파-갈락토시다제 A(gld), 베타-갈락토시다제 1(glb1), GM2 강글리오시드 활성화제(gm2a), glcNAc-1-포스포트랜스퍼라제(gnptab), N-아세틸글루코사민-1-포스포트랜스퍼라제(gnptg), N-아세틸글루코사민-6-설파타제(gns), 베타-글루쿠로니다제(gush), 베타-헥소스아미니다제 A(hexa), 베타-헥소스아미니다제 B(hexb), 헤파란-알파-글루코사미니드 N-아세틸트랜스퍼라제(hgsnat), 히알루로니다제-1(hyal1), 이두로네이트 2-설파타제(ids), 알파-L-이두로니다제(idua), 리소좀 연관 막 단백질 2(lamp2), 리소좀 산 리파제(lipa), 알파-만노시다제(man2bl), 베타-만노시다제(manba), 무코리핀-1(mcolnl), 라파마이신 복합체 1의 포유동물 표적 또는 라파마이신 복합체 1의 기계론적 표적(mtorcl), 알파-N-아세틸갈락토스아미니다제(naga), 알파-N-아세틸글루코스아미니다제(naglu), 뉴라미니다제 1(neul), 니만-픽 Cl(npcl), 니만-픽 Cl(npc2), 파타틴-유사 포스포리파제 도메인-함유 단백질 1(pnpla2), 팔미토일-단백질 티오에스테라제 1(pptl), 프로사포신(psap), N-설포글루코사민 설포하이드롤라제(sgsh), 시알린 단백질(slc17a5), TOR 조절 단백질(slc389), 나트륨/수소 교환체 6(slc9A6), 산 스핑고미엘리나제(smpdl), 포르밀글리신-생성 효소(sumfl) 또는 트리펩티딜 펩티다제 1 (tppT)을 포함한다. 본원에 기재된 한 측면에서, 치료 유전자는 ppt1, cln2, cln3, galc 또는 hexa를 포함한다.
리소좀 축적 질환을 일으키는 리소좀 효소는 광범위하다. 리소좀 축적 질환에 관여하는 리소좀 효소의 예로는 N-아세틸갈락토스아미니다제, 산 세라미다제, 산 말타제, 산 스핑고미엘리나제, 산 스핑고미엘리나제, 산 β-글루코시다제, 지방조직 트리글리세라이드 리파제, 아릴설파타제 A, 아릴설파타제 B, ATG5, ATG7, 바테닌, 카텝신 K, 시스티노신, 부고환 분비 단백질 HE1, 갈락토사민-6-설페이트 설파타제, 갈락토실세라마이드, N-아세틸글루코사민-1-포스포트랜스퍼라제의 감마 서브유닛, 글리코실아스파라기나제, GM2-활성화제 단백질, 헤파란 N-설파타제, 헥소스아미니다제 A 및 B, 히알루로니다제, 이두로네이트 2-설파타제, 리소좀 산 리파제, 리소좀 β-만노시다제, 리소좀-연관 막 단백질-2, 일가 나트륨-선택적 나트륨/수소 교환체(NHE), mTORCl, 무콜리핀-1, Na-a-아세틸글루코스아미니다제, 뉴라미니다제, 팔미토일-단백질 티오에스테라제-1, PIP(2) 5-포스파타제, 보호성 단백질/카테스핀 A. 사포신 B, 사포신 C, 시알린, SLC38A9, 설파타제-변형 인자-1, 트리펩티딜 펩티다제 1, a-갈락토시다제, a-L-푸코시다제, a-L-이두로니다제, a-만노시다제 또는 β-글루코시다제가 포함된다. 본원에 기재된 한 측면에서, 리소좀 효소는 팔미토일-단백질 티오에스테라제-1, 트리펩티딜 펩티다제 1, 갈락토실세라마이드, 바테닌 또는 헥소스아미니다제 A를 포함한다.
뇌를 표적화하기 위한 치료 유전자의 비강내 전달은 신경퇴행성 장애 및 리소좀 축적 장애의 치료에 이상적이다. 신경퇴행성 장애로는 알츠하이머병(AD), 헌팅턴병, 근위축성 측삭 경화증(ALS), 다계통 위축증(MSA)와 같은 파킨슨 플러스병을 포함하는 파킨슨병, 다발성 경화증(MS), 진행성 핵상 마비(PSP), 피질기저핵 변성(CBD) 또는 루이소체 치매(DLB)가 포함될 수 있다. 신경퇴행성 질환은 리소좀 축적 장애로 인해 유발될 수 있다. 바텐병은 영아 신경세포 세로이드 리포푸신증(INCL), 후기 영아 신경세포 세로이드 리포푸신증(LINCL) 및 소아 신경세포 세로이드 리포푸신증(JINCL)을 포함하는 신경세포 세로이드 리포푸신증(NCL)이라 칭해지는 장애의 그룹 중 가장 흔한 형태이다. 리소좀 축적 장애는 또한 예를 들어 테이-삭스병, 파브리병, 니만-픽병, 크라베병, 고셔병, 헌터 증후군, 알파-만노시드증, 아스파르틸글루코사민뇨증, 콜레스테롤 에스테르 축적 질환, 만성 헥소스아미니다제 A 결핍증, 시스틴증, 다논병, 파버병, 푸코시드축적증(Fucosidosis) 또는 갈락토시알리도시스일 수 있다. 한 측면에서, 리소좀 축적 장애는 영아 신경세포 세로이드 리포푸신증(INCL), 후기 영아 신경세포 세로이드 리포푸신증(LINCL) 및 소아 신경세포 리포푸신증 또는 크라베병을 포함한다. 본원에 기재된 한 측면에서, 리소좀 축적 장애는 후기 영아 바텐병, 소아 바텐병, 크라베병, 테이-삭스병, 니만-픽병, 파브리병, 파버병 및 고셔병을 포함한다.
본 명세서에 기재된 또 다른 측면에서, pptl 유전자는 영아 신경세포 세로이드 리포푸신증에 관여하는 효소를 암호화한다. 또 다른 측면에서, cln2 유전자는 후기 영아 신경세포 세로이드 리포푸신증에 관여하는 효소를 암호화한다. 또 다른 측면에서, cln3 유전자는 소아 신경세포 세로이드 리포푸신증에 관여하는 효소를 암호화한다. 또 다른 측면에서, gale 유전자는 크라베병에 관여하는 효소를 암호화한다. 또 다른 측면에서, hexa 유전자는 테이-삭스병에 관여하는 효소를 암호화한다.
약제학적 조성물
약제학적 조성물은 약제의 "치료학적 유효량" 또는 "예방학적 유효량"을 포함할 수 있다. "치료학적 유효량"은 원하는 치료 결과를 달성하기 위해 필요한 투여량에서 및 기간 동안 유효한 양을 지칭한다. 조성물의 치료학적 유효량은 당업자에 의해 결정될 수 있고, 개체의 질환 상태, 연령, 성별 및 체중과 같은 인자 및 개체에서 원하는 반응을 유발하는 조성물의 능력에 따라 달라질 수 있다. 치료학적 유효량은 또한 제제의 임의의 독성 또는 유해한 효과보다 치료학적으로 유익한 효과가 더 큰 양이다. "예방학적 유효량"은 원하는 예방학적 결과를 달성하기 위해 필요한 투여량에서 및 기간 동안 유효한 양을 지칭한다. 전형적으로, 예방학적 용량은 질환의 전 또는 초기 단계에서 대상체에서 사용되기 때문에, 예방학적 유효량은 치료학적 유효량보다 적을 것이다.
약제는 리소좀 축적 장애의 치료를 위한 치료 효과를 유도하는 임의의 활성 성분일 수 있다. 제제는 천연 발생 또는 합성일 수 있다. 천연 발생 제제의 예로는 천연 포화 지방산 및 이들의 유도체, 예를 들어 스테아르산, 팔미트산, 신남산, 라우르산, 카프르산 등이 포함된다. 천연 발생 불포화 지방산 및 이들의 유도체의 예로는 올레산, 올레아미드, 리놀레산, 리놀렌산 및 리시놀레산이 포함된다. 본원에 기재된 한 측면에서, 약제는 신남산 또는 올레아드마이드이다.
약제로서 합성 제제의 예로는, 예를 들어 피브레이트와 같은 지질 저하 약물이 포함된다. 피브레이트의 비제한적인 예로는 젬피브로질, 페노피브레이트, 클로피브레이트, 베자피브레이트, 시프로피브레이트 및 클리노피브레이트가 포함된다. 젬피브로질 (5-(2,5-디메틸페녹시)-2,2-디메틸펜탄산)은 화이자(Pfizer)에 의해 상표명 Lopid® 하에 시판되고 있다. 페노피브레이트 (2-(4-(4-클로로벤조일)페녹시)-2-메틸-프로판산 1-메틸 에틸 에스테르)는 애브비(Abbvie)에 의해 Tricor®로서 시판되고 있다. 추가의 피브레이트로는 클로피브레이트 (2-(4-클로로페녹시)-2-메틸-프로판산 에틸 에스테르), 베자피브레이트 (2-(4-(2-(4-클로로-벤조일아미노)-에틸)페녹시)-2-메틸-프로판산), 시프로피브레이트 (2-(4-(2,2-디클로로사이클로프로필)페녹시)-2-메틸 프로판산) 및 클리노비브레이트 (2-[4-[1-[4-(2-카복시부탄-2-일옥시)페닐]사이클로헥실]페녹시]-2-메틸부탄산)이 포함된다. 본원에 기재된 한 측면에서, 약제는 피브레이트이다. 본원에 기재된 다른 측면에서, 약제는 젬피브로질 또는 페노피브레이트이다.
제제는 대상체(인간 또는 비-인간일 수 있는 환자와 같은)에 대한 투여에 적합한 약제학적 조성물 내로 혼입될 수 있다.
약제학적 조성물은 다른 치료학적으로 유효한 제제를 추가로 포함할 수 있다. 본원에 기재된 한 측면에서, 약제학적 조성물은 치료학적 유효량의 올-트랜스 레티노산을 추가로 포함한다. 올-트랜스 레티노산은 인지 활동과 관련되었으며 알츠하이머병과 연관된 산화 스트레스를 감소시키는 것으로 제안되었다(Lee et al., 2009). 따라서, 올-트랜스 레티노산과 약제 및 치료 유전자를 함께 투여하는 것은 올-트랜스 레티노산, 약제 또는 치료 유전자를 단독으로 투여하는 것보다 대상체에서 더욱 향상된 치료 효과를 제공할 수 있다. 본원에 기재된 다른 측면에서, 약제의 치료학적 유효량은 약제가 올-트랜스 레티노산 없이 전달될 때보다 약제가 올-트랜스 레티노산과 병용되어 투여될 때 더욱 낮다.
약제학적 조성물은 약제학적으로 허용되는 담체를 포함할 수 있다. 본원에 사용된 용어 "약제학적으로 허용되는 담체"는 비독성, 불활성 고체, 반고체 또는 액체 충전제, 희석제, 캡슐화 물질 또는 임의 유형의 제형 보조제를 의미한다. 약제학적으로 허용되는 담체로서 작용할 수 있는 물질의 일부 예는 락토오스, 글루코오스 및 수크로오스와 같지만 이에 한정되지 않는 당; 옥수수 전분 및 감자 전분과 같지만 이에 한정되지 않는 전분; 나트륨 카복시메틸 셀룰로오스, 에틸 셀룰로오스 및 셀룰로오스 아세테이트와 같지만 이에 한정되지 않는 셀룰로오스 및 이의 유도체; 분말 트라가칸트; 맥아; 젤라틴; 활석; 코코아 버터 및 좌제 왁스와 같지만 이에 한정되지 않는 부형제; 땅콩유, 면실유, 홍화유, 참기름, 올리브유, 옥수수유 및 대두유와 같지만 이에 한정되지 않는 오일; 글리콜; 프로필렌 글리콜과 같은; 에틸 올레이트 및 에틸 라우레이트와 같지만 이에 한정되지 않는 에스테르; 한천; 수산화마그네슘 및 수산화알루미늄과 같지만 이에 한정되지 않는 완충제; 알긴산; 무-발열원 물; 등장 식염수; 링거액; 에틸 알코올 및 포스페이트 완충액뿐만 아니라 나트륨 라우릴 설페이트 및 마그네슘 스테아레이트와 같지만 이에 한정되지 않는 기타 비독성 상용성 윤활제이며, 뿐만 아니라 착색제, 이형제, 코팅제, 감미료, 향미제 및 방향제, 보존제제 및 항산화제가 조제자의 판단에 따라 조성물에 또한 존재할 수 있다.
후기 영아 신경세포 세로이드 리포푸신증과 같은 신경계 질환을 치료하는 방법은 약제 또는 약제의 약제학적 조성물을 투여하는 임의의 수의 방식을 포함할 수 있다. 본원에 기재된 한 측면에서, 약제학적 조성물은 유전자 조성물과 함께 투여된다.
본원에 기재된 또 다른 측면에서, 약제학적 조성물은 경구 투여된다. 경구 투여는 정제, 환제, 당의정, 경질 및 연질 겔 캡슐, 과립, 펠렛, 수성, 지질, 유성 또는 기타 용액, 수중유 에멀젼과 같은 에멀젼, 리포좀, 수성 또는 유성 현탁액, 시럽, 엘릭시르, 고체 에멀젼, 고체 분산액 또는 분산성 분말을 포함할 수 있다. 경구 투여용 약제학적 조성물의 제조를 위해, 제제는 예를 들어 아라비아 검, 활석, 전분, 당(예를 들어, 만니토오스, 메틸 셀룰로오스, 락토오스와 같은), 젤라틴, 계면활성제, 마그네슘 스테아레이트, 수성 또는 비수성 용매, 파라핀 유도체, 가교결합제, 분산제, 유화제, 윤활제, 보존제, 향미제(예를 들어, 에테르 오일), 용해도 향상제(예를 들어, 벤질 벤조에이트 또는 벤질 알코올) 또는 생체이용률 향상제(예를 들어, Gelucire.TM)와 같은 통상적으로 공지되고 사용되는 보조제 및 부형제과 함께 혼화될 수 있다. 약제학적 조성물에서, 제제는 또한 마이크로입자, 예를 들어 나노입자, 조성물에 분산될 수 있다.
일 실시형태에서, 치료학적 유효량의 약제학적 조성물은 약 1일 내지 약 100일마다 1일 1회, 약 2일 내지 약 90일마다 1일 1회, 약 3일 내지 약 80일마다 1일 1회, 약 4일 내지 약 70일마다 1일 1회, 약 5일 내지 약 60일마다 1일 1회, 약 6일 내지 약 50일마다 1일 1회, 7일 내지 약 40일마다 1일 1회, 약 8일 내지 약 30일마다 1일 1회 또는 약 9일 내지 약 20일마다 1일 1회 투여된다. 본원에 기재된 다른 실시형태에서, 약제학적 조성물은 약 1일 내지 약 100일마다 2회, 약 2일 내지 약 90일마다 2회, 약 3일 내지 약 80일마다 1회, 약 4일 내지 약 70일마다 1회, 약 5일 내지 약 60일마다 1회, 약 6일 내지 약 50일마다 1회, 7일 내지 약 40일마다 1회, 약 8일 내지 약 30일마다 1회, 또는 약 9일 내지 약 20일마다 1회 투여된다. 본원에 기재된 한 측면에서, 약제학적 조성물은 매일 투여된다.
병용 요법
공동투여에 의해 유전자 요법과 약제학적 조성물을 병용하면 각 개별 요법의 효과가 더욱 향상될 뿐만 아니라, 각 개별 조성물의 다양한 작용 메커니즘으로 인해 치료에 대한 다면적 접근을 제공한다. 이러한 방식으로, 효소 기능이 회복될 뿐만 아니라 기능적 효소의 집단이 향상된다. 따라서, 본원에 기재된 한 측면에서, 유전자 전달은 리소좀 기능을 회복시키고, 약제는 리소좀의 양을 증가시킨다. 본원에 기재된 또 다른 측면에서, 제1 조성물과 제2 조성물의 공동투여는 제1 조성물 또는 제2 조성물 단독의 투여보다 대상체에서 더 큰 치료 효과를 제공한다. 일부 측면에서, 유전자 조성물은 하나의 간격으로 전달될 수 있고 약제학적 조성물은 제2의 상이한 간격으로 전달될 수 있다. 일부 측면에서, 유전자 조성물은 약제학적 조성물보다 덜 빈번하게 전달될 수 있다. 비제한적인 예로서, 유전자 조성물은 매주 전달될 수 있고 약제학적 조성물은 매일 전달될 수 있다. 다른 병용 투약 용법도 병요 요법을 전달하는 데 사용될 수 있다.
본 개시내용은 하기의 비제한적 실시예에 의해 예시되는 다수의 측면을 갖는다.
실시예
신경퇴행성 장애의 동물 모델에서 약제학적 조성물과 병용된 비강내 유전자 요법의 효과를 평가하기 위한 연구가 수행될 것이다.
유전자 조성물 및 약제학적 조성물. 유전자 조성물은 ppt1, cln2, cln3, galc 또는 hexa 유전자를 포함하는 아데노-연관 바이러스 벡터를 사용하여 제조될 것이다. 경구 젬피브로질, 신남산 또는 올레아미드 조성물이 사용될 것이다.
분무. 일부 측면에서, 비강내 전달을 위해 분무가 사용될 것이지만, 점비액, 연고, 분무 펌프 및 가압 에어로졸과 같지만 이에 한정되지 않는 다른 비강내 방법도 사용될 수도 있다. DSI™에 의한 북스코 흡입 타워 올인원 컨트롤러(Buxco Inhalation Tower All-In-One Controller)가 분무용 공기 공급을 위해 사용될 것이다(도 1A). 전신 챔버에는 북스코 바이어스 유동 펌프로부터 공기가 공급되는 Aeroneb® Ultrasonic Nebulizer(도 1B)가 장착될 것이다. 마우스에게 3분 동안 적절한 용량으로 유전자 조성물(100pi 이중 증류수/마우스의 용적으로 가용화됨)이 분무될 것이다. 마우스의 대조군은 또한 분무에 의해 100 ㎕ 물을 투여받을 것이다.
실시예 1: 영아 신경세포 세로이드 리포푸신증
INCL을 갖는 마우스에서 비강내 유전자 요법 및 경구 젬피브로질, 신남산 또는 올레아미드로의 pptl (-/-) 마우스 처리: 동일한 배경 유래의 연령- 및 성별-일치된 pptl(+/+) 마우스가 야생형(WT) 대조군으로서 사용될 것이고, pptl(-/-) 동물은 다른 처리군에서 사용될 것이다. 마우스는 유전자 요법 조성물, 및 젬피브로질, 신남산 및 올레아미드로 이루어진 그룹으로부터 선택된 약제학적 조성물로 처리될 것이고, 대조군은 담체로만 처리될 것이다.
pptl(-/-) 마우스 및 대조군은 매주 비강 AAV1-PPT1(마우스당 2 x 106개 게놈 카피를 함유하는 2㎕) + 매일 경구 신남산(25 mg/체중 kg/일), 올레아미드(5 mg/체중 kg/일) 또는 젬피브로질(8 mg/체중 kg/일)을 처리한 후, 수명을 기록하고 뇌 내의 축적 물질을 모니터링할 것이다.
실시예 2: 소아 바텐병
Cln3(-/-) 마우스는 매주 비강 AAV1-CLN3(마우스당 2 x 106개 게놈 카피를 함유하는 2㎕) + 매일 경구 신남산(25 mg/체중 kg/일), 올레아미드(5 mg/체중 kg/일) 또는 젬피브로질(8 mg/체중 kg/일)로 처리한 후, 수명을 기록하고 뇌 내의 축적 물질을 모니터링할 것이다.
실시예 3: 크라베병
Galc(-/-) 마우스는 매주 비강 AAV1-GALC(마우스당 2 x 106개 게놈 카피를 함유하는 2㎕) + 매일 경구 신남산(25 mg/체중 kg/일), 올레아미드(5 mg/체중 kg) 또는 젬피브로질(8 mg/체중 kg/일)로 처리한 후, 수명을 기록하고 뇌 내의 축적 물질을 모니터링할 것이다.
실시예 4: 테이-삭스병
Hexa(-/-) 마우스는 매주 비강 AAV1-HEXA(마우스당 2 x 106개 게놈 카피를 함유하는 2㎕) + 매일 경구 신남산(25 mg/체중 kg/일), 올레아미드(5 mg/체중 kg/일) 또는 젬피브로질(8 mg/체중 kg/일)로 처리한 후, 수명을 기록하고 뇌 내의 축적 물질을 모니터링할 것이다.
실시예 5: 후기 영아 신경세포 세로이드 리포푸신증(LINCL)
비강내 유전자 전달은 치명적인 리소좀 축적 장애에 대한 유효한 옵션으로서 조사하였다. 트리펩티딜 펩티다제 1(TPP1) 효소의 결핍 또는 기능 상실을 초래하는 Cln2 유전자의 돌연변이로 인해 유발되는 희귀 신경퇴행성 질환인 후기 영아 신경세포 세로이드 리포푸신증(LINCL)의 마우스 모델을 사용하였다.
아데노바이러스 벡터는 인간 Cln2 유전자(Ad-Cln2)를 비강내 경로를 통해 2주령 Cln2-/- 마우스에 전달하였다(주 2회 5 ㎕ 용적 중의 Ad-Cln2의 5x106개 게놈 카피; 2.5 ㎕/콧구멍). 4주의 비강내 유전자 요법 후, 한 마우스 그룹(n=6)은 처리하지 않고 남겨두고 다른 마우스 그룹(n=6)은 7.5mg/체중 kg/일의 용량에서 젬피브로질로 경구 처리하였다. 따라서, Ad-Cln2를 투여받지 않은 한 그룹의 Cln2-/- 마우스도 젬피브로질로 경구 처리하였다.
젬피브로질 처리는 Cln2-/- 마우스의 수명을 유의하게 증가시키는 것으로 밝혀졌다(도 1 내지 도 2). 그러나, 4주간의 격주 비강내 유전자 전달 단독은 Cln2-/- 마우스의 수명을 증가시키는 데 있어 젬피브로질보다 유의하게 더 효과적이었다(도 1 내지 도 2). 그러나, 4주간의 격주 비강내 유전자 전달 단독은 Cln2-/- 마우스의 수명을 증가시키는데 있어 젬피브로질보다 유의하게 더 효과적이었다(도 1 내지 도 2). 대조적으로, 경구 젬피브로질 처리는 비강내 Ad-Cln2를 투여받은 Cln2-/- 마우스의 수명을 더 증가시키지 않았다(도 1 내지 도 2).
본 명세서에 인용된 모든 간행물, 특허 및 특허출원은 이러한 인용이 사용되는 교시를 위해 본원에 참고로 포함된다.
관찰된 특정 반응은 사용되는 제형의 특정 유형 및 투여 방식에 따라 그리고 이에 의존하여 달라질 수 있고, 이러한 결과의 예상된 변화 또는 차이는 본 발명의 실시에 따라 고려된다.
본원에서 본 발명의 구체적인 실시형태가 상세히 예시되고 설명되지만, 본 발명은 이에 한정되지 않는다. 상기 상세한 설명은 본 발명의 예시로서 제공되며, 본 발명의 어떠한 제한으로도 해석되지 않아야 한다. 변형은 당업자에게 명백할 것이며, 본 발명의 취지를 벗어나지 않는 모든 변형은 첨부된 청구범위에 포함되는 것으로 의도된다.
참고문헌
Claims (27)
- 리소좀 축적 질환의 치료 방법으로서, 리소좀 효소를 암호화하는 유전자의 치료학적 유효량을 포함하는 제1 조성물 및 약제의 치료학적 유효량을 포함하는 제2 조성물을 이를 필요로 하는 대상체에게 투여하는 것을 포함하는, 방법.
- 제1항에 있어서, 상기 제1 조성물이 비강내 투여되는, 방법.
- 제1항에 있어서, 상기 유전자가 혈뇌 장벽을 가로질러 전달되는, 방법.
- 제1항에 있어서, 상기 제1 조성물이 약 7일 내지 30일마다 1회 투여되는, 방법.
- 제1항에 있어서, 상기 제1 조성물이 리소좀 효소를 암호화하는 유전자를 포함하는 바이러스 벡터를 포함하는, 방법.
- 제6항에 있어서, 상기 바이러스 벡터가 아데노바이러스-연관 바이러스 벡터인, 방법.
- 제1항에 있어서, 상기 유전자가 ppt1, cln2, cln3, gale 또는 hexa를 포함하는, 방법.
- 제1항에 있어서, 상기 리소좀 효소가 팔미토일-단백질 티오에스테라제-1, 트리펩티딜 펩티다제 1, 갈락토실세라마이드, 바테닌 또는 헥소스아미니다제 A를 포함하는, 방법.
- 제7항에 있어서, 영아 신경세포 세로이드 리포푸신증을 포함하는 리소좀 축적 질환을 치료하기 위한 pptl 유전자를 포함하는 제1 조성물을 투여하는 것을 포함하는, 방법.
- 제7항에 있어서, 후기 영아 신경세포 세로이드 리포푸신증을 포함하는 리소좀 축적 질환을 치료하기 위한 cln2 유전자를 포함하는 제1 조성물을 투여하는 것을 포함하는, 방법.
- 제7항에 있어서, 소아 신경세포 세로이드 리포푸신증을 포함하는 리소좀 축적 질환을 치료하기 위한 cln3 유전자를 포함하는 제1 조성물을 투여하는 것을 포함하는, 방법.
- 제7항에 있어서, 크라베병을 포함하는 리소좀 축적 질환을 치료하기 위한 gale 유전자를 포함하는 제1 조성물을 투여하는 것을 포함하는, 방법.
- 제7항에 있어서, 테이-삭스병을 포함하는 리소좀 축적 질환을 치료하기 위한 hexa 유전자를 포함하는 제1 조성물을 투여하는 것을 포함하는, 방법.
- 제1항에 있어서, 상기 약제가 신남산, 올레아미드 또는 피브레이트를 포함하는, 방법.
- 제14항에 있어서, 상기 피브레이트가 젬피브로질 또는 페노피브레이트인, 방법.
- 제1항에 있어서, 상기 제2 조성물이 치료학적 유효량의 올-트랜스 레티노산(all-trans retinoic acid)을 추가로 포함하는, 방법.
- 제1항에 있어서, 상기 약제의 치료학적 유효량이, 해당 약제가 올-트랜스 레티노산 없이 전달될 때보다 올-트랜스 레티노산과 병용되어 투여될 때 더 낮은, 방법.
- 제1항에 있어서, 상기 제2 조성물이 경구 투여되는, 방법.
- 제1항에 있어서, 상기 제2 조성물이 1일 1회 투여되는, 방법.
- 제1항에 있어서, 상기 제1 조성물과 상기 제2 조성물의 투여가, 제1 조성물 또는 제2 조성물의 단독 투여보다 대상체에서 더 큰 치료 효과를 제공하는, 방법.
- 제1항에 있어서, 리소좀 축적 장애가 후기 영아 바텐병, 소아 바텐병, 크라베병, 테이-삭스병, 니만-픽병, 파브리병, 파버병 및 고셔병으로 이루어진 그룹으로부터 선택되는, 방법.
- 제1항에 있어서, 상기 제1 조성물이 비강내 투여되고 상기 제2 조성물이 경구 투여되는, 방법.
- 제1항 또는 제22항에 있어서, 상기 제1 조성물이 적어도 7일마다 1회 투여되고 상기 제2 조성물이 1일 1회 투여되는 방법.
- 제23항에 있어서, 상기 바이러스 벡터가 아데노바이러스-연관 바이러스 벡터인, 방법.
- 제23항에 있어서, 상기 유전자가 cln2를 포함하는, 방법.
- 제23항에 있어서, 상기 제2 조성물이 젬피브로질을 포함하는, 방법.
- 제25항에 있어서, 제1 조성물의 투여가 수명을 약 100일 증가시키는, 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962822310P | 2019-03-22 | 2019-03-22 | |
| US62/822,310 | 2019-03-22 | ||
| PCT/US2020/023768 WO2020197967A1 (en) | 2019-03-22 | 2020-03-20 | Combination of nasal gene delivery and oral cinnamic acid, oleamide or gemfibrozil for lysosomal stoarge disorders |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20210143848A true KR20210143848A (ko) | 2021-11-29 |
Family
ID=72609912
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020217034175A KR20210143848A (ko) | 2019-03-22 | 2020-03-20 | 리소좀 축적 장애를 위한 비강 유전자 전달 및 경구 신남산, 올레아미드 또는 젬피브로질의 병용 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US20220152165A1 (ko) |
| EP (1) | EP3941584A4 (ko) |
| JP (1) | JP2022525888A (ko) |
| KR (1) | KR20210143848A (ko) |
| CN (1) | CN113811359A (ko) |
| AU (1) | AU2020245415A1 (ko) |
| CA (1) | CA3132379A1 (ko) |
| EA (1) | EA202192328A1 (ko) |
| WO (1) | WO2020197967A1 (ko) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA3207205A1 (en) * | 2021-01-20 | 2022-07-28 | Rush University Medical Center | Improved treatment for globoid cell leukodsytrophy or krabbe disease |
| WO2024155759A1 (en) * | 2023-01-18 | 2024-07-25 | Rush University Medical Center | Oral gemfibrozil for the treatment of cln3-related juvenile neuronal ceroid lipofuscinosis |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20050012771A (ko) * | 2002-06-03 | 2005-02-02 | 노파르티스 아게 | 치환된 시아노피롤리딘의 용도 및 이들을 함유하는고지혈증 및 관련 질환의 치료를 위한 조합 제제 |
| US9750712B2 (en) * | 2012-12-07 | 2017-09-05 | Rush University Medical Center | Composition and method for treating neuronal ceroid lipofuscinosis |
| CA2967468A1 (en) * | 2014-12-16 | 2016-06-23 | Board Of Regents Of The University Of Nebraska | Gene therapy for juvenile batten disease |
| US11045557B2 (en) * | 2016-06-09 | 2021-06-29 | Queen's University At Kingston | Methods and gene therapy constructs for treating GM2 gangliosidoses |
| RU2764919C2 (ru) * | 2016-06-13 | 2022-01-24 | Дзе Юниверсити Оф Норт Каролина Эт Чепел Хилл | Оптимизированные гены и экспрессионные кассеты cln1, и их применение |
| EP3468594A4 (en) * | 2016-06-13 | 2020-01-22 | Bluebird Bio, Inc. | GENE THERAPY OF NEURONAL CEROID LIPOFUSCINOSIS |
| CN118078860A (zh) * | 2017-01-20 | 2024-05-28 | 联邦高等教育系统匹兹堡大学 | 用脐带血移植(ucbt)和增加的半乳糖脑苷酯酶(galc)表达治疗克拉伯病 |
-
2020
- 2020-03-20 EA EA202192328A patent/EA202192328A1/ru unknown
- 2020-03-20 JP JP2021555592A patent/JP2022525888A/ja active Pending
- 2020-03-20 EP EP20777092.6A patent/EP3941584A4/en not_active Withdrawn
- 2020-03-20 WO PCT/US2020/023768 patent/WO2020197967A1/en active Application Filing
- 2020-03-20 CN CN202080022852.4A patent/CN113811359A/zh active Pending
- 2020-03-20 US US17/441,029 patent/US20220152165A1/en active Pending
- 2020-03-20 KR KR1020217034175A patent/KR20210143848A/ko unknown
- 2020-03-20 AU AU2020245415A patent/AU2020245415A1/en active Pending
- 2020-03-20 CA CA3132379A patent/CA3132379A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| EP3941584A4 (en) | 2022-11-30 |
| US20220152165A1 (en) | 2022-05-19 |
| AU2020245415A1 (en) | 2021-09-16 |
| CA3132379A1 (en) | 2020-10-01 |
| EP3941584A1 (en) | 2022-01-26 |
| JP2022525888A (ja) | 2022-05-20 |
| CN113811359A (zh) | 2021-12-17 |
| WO2020197967A1 (en) | 2020-10-01 |
| EA202192328A1 (ru) | 2022-02-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20210228692A1 (en) | Intraventricular enzyme delivery for lysosomal storage diseases | |
| RU2692251C2 (ru) | Опосредованный аденоассоциированным вирусом перенос генов в центральную нервную систему | |
| EP1673104B1 (en) | Delivery of therapeutic compounds to the brain and other tissues | |
| EP2646044B1 (en) | Methods for increasing intracellular activity of hsp70 | |
| KR20210143848A (ko) | 리소좀 축적 장애를 위한 비강 유전자 전달 및 경구 신남산, 올레아미드 또는 젬피브로질의 병용 | |
| EP2977057B1 (en) | Isolated recombinant human n-glycosylated lysosomal acid lipase | |
| US12023332B2 (en) | Compositions and methods for activating signaling through the CB1 cannabinoid receptor for treating and preventing diseases and disorders characterized by abnormal cellular accumulation of sphingolipids such as sphingomyelin | |
| EP3119384B1 (en) | Treatment of intrahepatic cholestatic diseases | |
| WO2016044947A1 (en) | Exosomes useful to treat lysosomal storage disease | |
| JP2015526481A (ja) | 片頭痛の治療用組成物 | |
| JP2015518872A (ja) | アロステリックシャペロンおよびその使用 | |
| Salegio et al. | Safety study of adeno-associated virus serotype 2-mediated human acid sphingomyelinase expression in the nonhuman primate brain | |
| US20180015054A1 (en) | Method of Maintaining the Anti-Depressant Effect of Ketamine With Lithium | |
| WO2020261230A1 (en) | Combination therapy with acetyl-leucine and miglustat | |
| WO2017040647A1 (en) | Methods and compositions for the treatment of cytopplasmic glycogen storage disorders | |
| KR20190101424A (ko) | 젬피브로질에 의하여 후기 영유아 뉴런 세로이드 지방갈색소증 환자의 장수에서 증가 및 보행 활동의 개선 | |
| JP2022543695A (ja) | Otc及び医薬品のバイオアベイラビリティを増加する方法 | |
| EP3518962B1 (en) | Sebelipase alfa for use in liver fibrosis and treating lysosomal acid lipase deficiency in patients based on ishak fibrosis stage | |
| US9474763B2 (en) | Compositions and methods for amelioration and prevention of drug-induced toxicity | |
| WO2021236890A1 (en) | Compositions and methods for activating signaling through the cb2 cannabinoid receptor for treating and preventing lysosomal storage diseases and disorders | |
| Sestito et al. | Pathobiological insights into the newly targeted therapies of lysosomal storage disorders | |
| US20230404972A1 (en) | Inhibition of caspase pathway as a treatment for lysosomal storage disorders | |
| US20200069585A1 (en) | Compositions for upregulating defensin expression | |
| US20200338088A1 (en) | Methods for Treating Neutrophilic Dermatoses with SYK Inhibitors | |
| EP4138916A1 (en) | Novel therapy for acute damage to lung tissue |