KR20210114932A - 음이온 펜던트 및 보조기를 함유하는 철 (iii) mri 조영제로 사용하기 위한 화합물 - Google Patents
음이온 펜던트 및 보조기를 함유하는 철 (iii) mri 조영제로 사용하기 위한 화합물 Download PDFInfo
- Publication number
- KR20210114932A KR20210114932A KR1020217017914A KR20217017914A KR20210114932A KR 20210114932 A KR20210114932 A KR 20210114932A KR 1020217017914 A KR1020217017914 A KR 1020217017914A KR 20217017914 A KR20217017914 A KR 20217017914A KR 20210114932 A KR20210114932 A KR 20210114932A
- Authority
- KR
- South Korea
- Prior art keywords
- substituted
- group
- alkyl
- unsubstituted
- pendant
- Prior art date
Links
- 125000000129 anionic group Chemical group 0.000 title claims description 56
- 150000001875 compounds Chemical class 0.000 title claims description 46
- VTLYFUHAOXGGBS-UHFFFAOYSA-N Fe3+ Chemical compound [Fe+3] VTLYFUHAOXGGBS-UHFFFAOYSA-N 0.000 title abstract description 88
- 239000002616 MRI contrast agent Substances 0.000 title description 20
- 150000002678 macrocyclic compounds Chemical class 0.000 claims abstract description 103
- ITWBWJFEJCHKSN-UHFFFAOYSA-N 1,4,7-triazonane Chemical group C1CNCCNCCN1 ITWBWJFEJCHKSN-UHFFFAOYSA-N 0.000 claims abstract description 62
- 238000003384 imaging method Methods 0.000 claims abstract description 16
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 88
- 238000000034 method Methods 0.000 claims description 81
- 229910001868 water Inorganic materials 0.000 claims description 81
- 125000000217 alkyl group Chemical group 0.000 claims description 79
- 125000003118 aryl group Chemical group 0.000 claims description 61
- -1 Fe(III) cation Chemical class 0.000 claims description 43
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 claims description 29
- 239000000203 mixture Substances 0.000 claims description 26
- 208000035896 Twin-reversed arterial perfusion sequence Diseases 0.000 claims description 22
- 210000000056 organ Anatomy 0.000 claims description 22
- 210000001519 tissue Anatomy 0.000 claims description 20
- 210000004027 cell Anatomy 0.000 claims description 19
- 210000005166 vasculature Anatomy 0.000 claims description 19
- 102000008100 Human Serum Albumin Human genes 0.000 claims description 18
- 108091006905 Human Serum Albumin Proteins 0.000 claims description 18
- 230000005291 magnetic effect Effects 0.000 claims description 17
- 125000001424 substituent group Chemical group 0.000 claims description 17
- 125000000547 substituted alkyl group Chemical group 0.000 claims description 17
- 238000002595 magnetic resonance imaging Methods 0.000 claims description 16
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 14
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 13
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 12
- 150000003839 salts Chemical class 0.000 claims description 12
- 229910052757 nitrogen Inorganic materials 0.000 claims description 10
- 229920000642 polymer Polymers 0.000 claims description 9
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 8
- 239000003795 chemical substances by application Substances 0.000 claims description 7
- 102000004169 proteins and genes Human genes 0.000 claims description 7
- 108090000623 proteins and genes Proteins 0.000 claims description 7
- 239000000412 dendrimer Substances 0.000 claims description 6
- 229920000736 dendritic polymer Polymers 0.000 claims description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 claims description 6
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 6
- 125000006539 C12 alkyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 5
- WSNMPAVSZJSIMT-UHFFFAOYSA-N COc1c(C)c2COC(=O)c2c(O)c1CC(O)C1(C)CCC(=O)O1 Chemical compound COc1c(C)c2COC(=O)c2c(O)c1CC(O)C1(C)CCC(=O)O1 WSNMPAVSZJSIMT-UHFFFAOYSA-N 0.000 claims description 5
- 239000003937 drug carrier Substances 0.000 claims description 5
- 150000002170 ethers Chemical class 0.000 claims description 5
- 125000001072 heteroaryl group Chemical group 0.000 claims description 5
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical compound CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 claims description 3
- 150000001768 cations Chemical class 0.000 claims description 3
- 229960003194 meglumine Drugs 0.000 claims description 3
- 125000005647 linker group Chemical group 0.000 claims description 2
- 125000003277 amino group Chemical group 0.000 abstract 1
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 91
- 239000000243 solution Substances 0.000 description 82
- 239000003446 ligand Substances 0.000 description 54
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 52
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 51
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 36
- 238000005481 NMR spectroscopy Methods 0.000 description 27
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 27
- 230000007935 neutral effect Effects 0.000 description 27
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 26
- 150000007942 carboxylates Chemical class 0.000 description 23
- 239000000047 product Substances 0.000 description 23
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 21
- 230000015572 biosynthetic process Effects 0.000 description 20
- 229930040373 Paraformaldehyde Natural products 0.000 description 19
- 229920002866 paraformaldehyde Polymers 0.000 description 19
- 238000010992 reflux Methods 0.000 description 19
- 239000002904 solvent Substances 0.000 description 19
- 238000003786 synthesis reaction Methods 0.000 description 18
- 241000699670 Mus sp. Species 0.000 description 16
- 239000002872 contrast media Substances 0.000 description 16
- ABLZXFCXXLZCGV-UHFFFAOYSA-N Phosphorous acid Chemical compound OP(O)=O ABLZXFCXXLZCGV-UHFFFAOYSA-N 0.000 description 15
- 125000005842 heteroatom Chemical group 0.000 description 15
- UEZVMMHDMIWARA-UHFFFAOYSA-M phosphonate Chemical compound [O-]P(=O)=O UEZVMMHDMIWARA-UHFFFAOYSA-M 0.000 description 15
- 150000004703 alkoxides Chemical class 0.000 description 13
- 239000007864 aqueous solution Substances 0.000 description 13
- 229910052760 oxygen Inorganic materials 0.000 description 13
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 13
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 12
- 229910019142 PO4 Inorganic materials 0.000 description 12
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 12
- 239000010452 phosphate Substances 0.000 description 12
- ACVYVLVWPXVTIT-UHFFFAOYSA-M phosphinate Chemical compound [O-][PH2]=O ACVYVLVWPXVTIT-UHFFFAOYSA-M 0.000 description 12
- 229910052742 iron Inorganic materials 0.000 description 11
- 239000007787 solid Substances 0.000 description 11
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 10
- 238000006243 chemical reaction Methods 0.000 description 10
- 229910052739 hydrogen Inorganic materials 0.000 description 10
- 239000011734 sodium Substances 0.000 description 10
- 238000003756 stirring Methods 0.000 description 10
- 239000001257 hydrogen Substances 0.000 description 9
- 150000003014 phosphoric acid esters Chemical class 0.000 description 9
- 239000003642 reactive oxygen metabolite Substances 0.000 description 9
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 8
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 8
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 8
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 8
- 150000001298 alcohols Chemical class 0.000 description 8
- 238000002347 injection Methods 0.000 description 8
- 239000007924 injection Substances 0.000 description 8
- 230000005298 paramagnetic effect Effects 0.000 description 8
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 7
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 7
- 239000007995 HEPES buffer Substances 0.000 description 7
- QPCDCPDFJACHGM-UHFFFAOYSA-N N,N-bis{2-[bis(carboxymethyl)amino]ethyl}glycine Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(=O)O)CCN(CC(O)=O)CC(O)=O QPCDCPDFJACHGM-UHFFFAOYSA-N 0.000 description 7
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 7
- 125000000623 heterocyclic group Chemical group 0.000 description 7
- 229910052751 metal Inorganic materials 0.000 description 7
- 239000002244 precipitate Substances 0.000 description 7
- 230000009467 reduction Effects 0.000 description 7
- 150000003871 sulfonates Chemical class 0.000 description 7
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 6
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 6
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 6
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 6
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 6
- 238000010494 dissociation reaction Methods 0.000 description 6
- 230000005593 dissociations Effects 0.000 description 6
- 230000003993 interaction Effects 0.000 description 6
- 210000003734 kidney Anatomy 0.000 description 6
- 230000007246 mechanism Effects 0.000 description 6
- 239000002184 metal Substances 0.000 description 6
- 125000004430 oxygen atom Chemical group O* 0.000 description 6
- ISIJQEHRDSCQIU-UHFFFAOYSA-N tert-butyl 2,7-diazaspiro[4.5]decane-7-carboxylate Chemical compound C1N(C(=O)OC(C)(C)C)CCCC11CNCC1 ISIJQEHRDSCQIU-UHFFFAOYSA-N 0.000 description 6
- 150000003852 triazoles Chemical class 0.000 description 6
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 5
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical group CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 5
- 239000002253 acid Substances 0.000 description 5
- 150000007513 acids Chemical class 0.000 description 5
- 125000004429 atom Chemical group 0.000 description 5
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 5
- 229910052799 carbon Inorganic materials 0.000 description 5
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical class C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 5
- 239000007789 gas Substances 0.000 description 5
- 230000006872 improvement Effects 0.000 description 5
- 238000001095 inductively coupled plasma mass spectrometry Methods 0.000 description 5
- 239000010410 layer Substances 0.000 description 5
- 210000004185 liver Anatomy 0.000 description 5
- 229910021645 metal ion Inorganic materials 0.000 description 5
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 5
- 230000003647 oxidation Effects 0.000 description 5
- 238000007254 oxidation reaction Methods 0.000 description 5
- 239000001301 oxygen Substances 0.000 description 5
- ACVYVLVWPXVTIT-UHFFFAOYSA-N phosphinic acid Chemical compound O[PH2]=O ACVYVLVWPXVTIT-UHFFFAOYSA-N 0.000 description 5
- 150000003009 phosphonic acids Chemical class 0.000 description 5
- 235000018102 proteins Nutrition 0.000 description 5
- 239000011780 sodium chloride Substances 0.000 description 5
- 150000003460 sulfonic acids Chemical class 0.000 description 5
- 125000004434 sulfur atom Chemical group 0.000 description 5
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 4
- FCKYPQBAHLOOJQ-UHFFFAOYSA-N Cyclohexane-1,2-diaminetetraacetic acid Chemical compound OC(=O)CN(CC(O)=O)C1CCCCC1N(CC(O)=O)CC(O)=O FCKYPQBAHLOOJQ-UHFFFAOYSA-N 0.000 description 4
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 4
- CWYNVVGOOAEACU-UHFFFAOYSA-N Fe2+ Chemical compound [Fe+2] CWYNVVGOOAEACU-UHFFFAOYSA-N 0.000 description 4
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 4
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 4
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 4
- HCBDSERWVIIISK-UHFFFAOYSA-N [4,7-bis[[ethoxy(hydroxy)phosphoryl]methyl]-1,4,7-triazonan-1-yl]methyl-ethoxyphosphinic acid Chemical compound CCOP(O)(=O)CN1CCN(CP(O)(=O)OCC)CCN(CP(O)(=O)OCC)CC1 HCBDSERWVIIISK-UHFFFAOYSA-N 0.000 description 4
- 238000000862 absorption spectrum Methods 0.000 description 4
- 239000012298 atmosphere Substances 0.000 description 4
- 239000012043 crude product Substances 0.000 description 4
- 239000013078 crystal Substances 0.000 description 4
- LMZLQYYLELWCCW-UHFFFAOYSA-N dimethoxy(phenyl)phosphane Chemical compound COP(OC)C1=CC=CC=C1 LMZLQYYLELWCCW-UHFFFAOYSA-N 0.000 description 4
- 235000019439 ethyl acetate Nutrition 0.000 description 4
- 238000010438 heat treatment Methods 0.000 description 4
- 238000000338 in vitro Methods 0.000 description 4
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical class CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 4
- ISWSIDIOOBJBQZ-UHFFFAOYSA-M phenolate Chemical compound [O-]C1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-M 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- 239000011541 reaction mixture Substances 0.000 description 4
- 229910052717 sulfur Inorganic materials 0.000 description 4
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 4
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 3
- LSUCINGZOPDXQJ-UHFFFAOYSA-N 1-[4-(2-hydroxypropyl)-1,4,7-triazonan-1-yl]propan-2-ol Chemical compound CC(O)CN1CCNCCN(CC(C)O)CC1 LSUCINGZOPDXQJ-UHFFFAOYSA-N 0.000 description 3
- YLKRUSPZOTYMAT-YFKPBYRVSA-N 6-hydroxy-L-dopa Chemical compound OC(=O)[C@@H](N)CC1=CC(O)=C(O)C=C1O YLKRUSPZOTYMAT-YFKPBYRVSA-N 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- 239000004471 Glycine Substances 0.000 description 3
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 3
- WAEMQWOKJMHJLA-UHFFFAOYSA-N Manganese(2+) Chemical compound [Mn+2] WAEMQWOKJMHJLA-UHFFFAOYSA-N 0.000 description 3
- BVMWIXWOIGJRGE-UHFFFAOYSA-N NP(O)=O Chemical compound NP(O)=O BVMWIXWOIGJRGE-UHFFFAOYSA-N 0.000 description 3
- 101000694110 Nicotiana tabacum Lignin-forming anionic peroxidase Proteins 0.000 description 3
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 3
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 3
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 3
- 235000001014 amino acid Nutrition 0.000 description 3
- 150000001413 amino acids Chemical class 0.000 description 3
- 229940072107 ascorbate Drugs 0.000 description 3
- 235000010323 ascorbic acid Nutrition 0.000 description 3
- 239000011668 ascorbic acid Substances 0.000 description 3
- 235000003704 aspartic acid Nutrition 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 3
- 235000010290 biphenyl Nutrition 0.000 description 3
- 239000004305 biphenyl Substances 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 125000001246 bromo group Chemical group Br* 0.000 description 3
- 239000003054 catalyst Substances 0.000 description 3
- 125000001309 chloro group Chemical group Cl* 0.000 description 3
- 238000002484 cyclic voltammetry Methods 0.000 description 3
- 238000010511 deprotection reaction Methods 0.000 description 3
- 239000012153 distilled water Substances 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- NMCUIPGRVMDVDB-UHFFFAOYSA-L iron dichloride Chemical compound Cl[Fe]Cl NMCUIPGRVMDVDB-UHFFFAOYSA-L 0.000 description 3
- 150000002576 ketones Chemical class 0.000 description 3
- 210000003205 muscle Anatomy 0.000 description 3
- 239000012044 organic layer Substances 0.000 description 3
- 239000008188 pellet Substances 0.000 description 3
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 3
- 238000001953 recrystallisation Methods 0.000 description 3
- 239000000523 sample Substances 0.000 description 3
- 150000003384 small molecules Chemical class 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 229910001428 transition metal ion Inorganic materials 0.000 description 3
- CFERECYCUQQHGK-UHFFFAOYSA-N 1,4,7-triazatricyclo[5.2.1.04,10 ]decane Chemical compound C1CN2CCN3C2N1CC3 CFERECYCUQQHGK-UHFFFAOYSA-N 0.000 description 2
- KBPLFHHGFOOTCA-UHFFFAOYSA-N 1-Octanol Chemical compound CCCCCCCCO KBPLFHHGFOOTCA-UHFFFAOYSA-N 0.000 description 2
- FNJKRVYABOAQHB-UHFFFAOYSA-N 1-benzyl-1,4,7-triazonane Chemical compound C=1C=CC=CC=1CN1CCNCCNCC1 FNJKRVYABOAQHB-UHFFFAOYSA-N 0.000 description 2
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 2
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 2
- ZSXGLVDWWRXATF-UHFFFAOYSA-N N,N-dimethylformamide dimethyl acetal Chemical compound COC(OC)N(C)C ZSXGLVDWWRXATF-UHFFFAOYSA-N 0.000 description 2
- UBQYURCVBFRUQT-UHFFFAOYSA-N N-benzoyl-Ferrioxamine B Chemical compound CC(=O)N(O)CCCCCNC(=O)CCC(=O)N(O)CCCCCNC(=O)CCC(=O)N(O)CCCCCN UBQYURCVBFRUQT-UHFFFAOYSA-N 0.000 description 2
- 206010028980 Neoplasm Diseases 0.000 description 2
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 description 2
- WDLRUFUQRNWCPK-UHFFFAOYSA-N Tetraxetan Chemical compound OC(=O)CN1CCN(CC(O)=O)CCN(CC(O)=O)CCN(CC(O)=O)CC1 WDLRUFUQRNWCPK-UHFFFAOYSA-N 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- 229910052786 argon Inorganic materials 0.000 description 2
- 239000012300 argon atmosphere Substances 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 125000005841 biaryl group Chemical group 0.000 description 2
- 150000001721 carbon Chemical group 0.000 description 2
- 125000004432 carbon atom Chemical group C* 0.000 description 2
- 150000001735 carboxylic acids Chemical class 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 239000013626 chemical specie Substances 0.000 description 2
- 230000000536 complexating effect Effects 0.000 description 2
- 238000010668 complexation reaction Methods 0.000 description 2
- 229960000958 deferoxamine Drugs 0.000 description 2
- 239000008367 deionised water Substances 0.000 description 2
- 229910021641 deionized water Inorganic materials 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 125000001033 ether group Chemical group 0.000 description 2
- 238000001704 evaporation Methods 0.000 description 2
- 230000008020 evaporation Effects 0.000 description 2
- LGMLJQFQKXPRGA-VPVMAENOSA-K gadopentetate dimeglumine Chemical compound [Gd+3].CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO.CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO.OC(=O)CN(CC([O-])=O)CCN(CC([O-])=O)CCN(CC(O)=O)CC([O-])=O LGMLJQFQKXPRGA-VPVMAENOSA-K 0.000 description 2
- 210000000232 gallbladder Anatomy 0.000 description 2
- RWSXRVCMGQZWBV-WDSKDSINSA-N glutathione Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O RWSXRVCMGQZWBV-WDSKDSINSA-N 0.000 description 2
- 229910052736 halogen Inorganic materials 0.000 description 2
- 150000002367 halogens Chemical class 0.000 description 2
- 239000012216 imaging agent Substances 0.000 description 2
- 229940030980 inova Drugs 0.000 description 2
- 238000005342 ion exchange Methods 0.000 description 2
- 150000002505 iron Chemical class 0.000 description 2
- VCJMYUPGQJHHFU-UHFFFAOYSA-N iron(3+);trinitrate Chemical compound [Fe+3].[O-][N+]([O-])=O.[O-][N+]([O-])=O.[O-][N+]([O-])=O VCJMYUPGQJHHFU-UHFFFAOYSA-N 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- 238000012417 linear regression Methods 0.000 description 2
- LGAILEFNHXWAJP-BMEPFDOTSA-N macrocycle Chemical group N([C@H]1[C@@H](C)CC)C(=O)C(N=2)=CSC=2CNC(=O)C(=C(O2)C)N=C2[C@H]([C@@H](C)CC)NC(=O)C2=CSC1=N2 LGAILEFNHXWAJP-BMEPFDOTSA-N 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 239000002105 nanoparticle Substances 0.000 description 2
- 125000001624 naphthyl group Chemical group 0.000 description 2
- 229910017604 nitric acid Inorganic materials 0.000 description 2
- 150000002978 peroxides Chemical class 0.000 description 2
- 150000002989 phenols Chemical class 0.000 description 2
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 2
- 229920001467 poly(styrenesulfonates) Polymers 0.000 description 2
- 229920001223 polyethylene glycol Chemical class 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 239000001103 potassium chloride Substances 0.000 description 2
- 235000011164 potassium chloride Nutrition 0.000 description 2
- 238000001556 precipitation Methods 0.000 description 2
- 239000000741 silica gel Substances 0.000 description 2
- 229910002027 silica gel Inorganic materials 0.000 description 2
- 238000000967 suction filtration Methods 0.000 description 2
- 239000003115 supporting electrolyte Substances 0.000 description 2
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- MHCVCKDNQYMGEX-UHFFFAOYSA-N 1,1'-biphenyl;phenoxybenzene Chemical group C1=CC=CC=C1C1=CC=CC=C1.C=1C=CC=CC=1OC1=CC=CC=C1 MHCVCKDNQYMGEX-UHFFFAOYSA-N 0.000 description 1
- FSSPGSAQUIYDCN-UHFFFAOYSA-N 1,3-Propane sultone Chemical compound O=S1(=O)CCCO1 FSSPGSAQUIYDCN-UHFFFAOYSA-N 0.000 description 1
- OXHOPZLBSSTTBU-UHFFFAOYSA-N 1,3-bis(bromomethyl)benzene Chemical group BrCC1=CC=CC(CBr)=C1 OXHOPZLBSSTTBU-UHFFFAOYSA-N 0.000 description 1
- GWBXLDZPGACFKR-UHFFFAOYSA-N 1,4,7-triazabicyclo[5.2.1]decane Chemical compound C1N2CCN1CCNCC2 GWBXLDZPGACFKR-UHFFFAOYSA-N 0.000 description 1
- HNFSOULQCAPHLE-UHFFFAOYSA-N 1,4,7-tris(diethoxyphosphorylmethyl)-1,4,7-triazonane Chemical compound CCOP(=O)(OCC)CN1CCN(CP(=O)(OCC)OCC)CCN(CP(=O)(OCC)OCC)CC1 HNFSOULQCAPHLE-UHFFFAOYSA-N 0.000 description 1
- HOLOCXLMBBUKHI-UHFFFAOYSA-N 1-[1-(2-hydroxypropyl)-1,4,7-triazonan-2-yl]propan-2-ol Chemical compound CC(CC1CNCCNCCN1CC(C)O)O HOLOCXLMBBUKHI-UHFFFAOYSA-N 0.000 description 1
- YEZOLEPJWZHLMN-UHFFFAOYSA-N 1-[[3-(1,4,7-triazonan-1-ylmethyl)phenyl]methyl]-1,4,7-triazonane Chemical compound C=1C=CC(CN2CCNCCNCC2)=CC=1CN1CCNCCNCC1 YEZOLEPJWZHLMN-UHFFFAOYSA-N 0.000 description 1
- GLQKLMDNPYNLKE-UHFFFAOYSA-N 1-benzyl-1,4,7-triazonane dihydrobromide Chemical compound C1CNCCN(CCN1)CC2=CC=CC=C2.Br.Br GLQKLMDNPYNLKE-UHFFFAOYSA-N 0.000 description 1
- AIGUAFXOIPWWBG-UHFFFAOYSA-N 1-phenyl-1,4,7-triazonane Chemical compound C1CNCCNCCN1C1=CC=CC=C1 AIGUAFXOIPWWBG-UHFFFAOYSA-N 0.000 description 1
- 238000005165 17O NMR spectroscopy Methods 0.000 description 1
- FZQZIWPHRQKFPS-UHFFFAOYSA-N 2-[(2-hydroxyphenyl)methylamino]acetic acid Chemical compound OC(=O)CNCC1=CC=CC=C1O FZQZIWPHRQKFPS-UHFFFAOYSA-N 0.000 description 1
- CDAWCLOXVUBKRW-UHFFFAOYSA-N 2-aminophenol Chemical compound NC1=CC=CC=C1O CDAWCLOXVUBKRW-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- ODJAOEVGCRPXOQ-UHFFFAOYSA-N 4-[[methoxy(phenyl)phosphoryl]methyl]-1,4,7-triazabicyclo[5.2.1]decane Chemical compound N12CCN(CCN(CC1)C2)CP(OC)(=O)C1=CC=CC=C1 ODJAOEVGCRPXOQ-UHFFFAOYSA-N 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- 238000004252 FT/ICR mass spectrometry Methods 0.000 description 1
- 229910000608 Fe(NO3)3.9H2O Inorganic materials 0.000 description 1
- 229910052688 Gadolinium Inorganic materials 0.000 description 1
- 108010024636 Glutathione Proteins 0.000 description 1
- 229910021575 Iron(II) bromide Inorganic materials 0.000 description 1
- 229910021577 Iron(II) chloride Inorganic materials 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 229910021260 NaFe Inorganic materials 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- GOOHAUXETOMSMM-VKHMYHEASA-N S-propylene oxide Chemical compound C[C@H]1CO1 GOOHAUXETOMSMM-VKHMYHEASA-N 0.000 description 1
- 102000007562 Serum Albumin Human genes 0.000 description 1
- 108010071390 Serum Albumin Proteins 0.000 description 1
- 239000000589 Siderophore Substances 0.000 description 1
- OUUQCZGPVNCOIJ-UHFFFAOYSA-M Superoxide Chemical compound [O-][O] OUUQCZGPVNCOIJ-UHFFFAOYSA-M 0.000 description 1
- 241001377894 Trias Species 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 125000003158 alcohol group Chemical group 0.000 description 1
- 150000001336 alkenes Chemical class 0.000 description 1
- 125000003342 alkenyl group Chemical group 0.000 description 1
- 150000001345 alkine derivatives Chemical class 0.000 description 1
- 150000003973 alkyl amines Chemical class 0.000 description 1
- 125000000304 alkynyl group Chemical group 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 150000003927 aminopyridines Chemical class 0.000 description 1
- 239000000908 ammonium hydroxide Substances 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 125000002178 anthracenyl group Chemical class C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- AGEZXYOZHKGVCM-UHFFFAOYSA-N benzyl bromide Chemical compound BrCC1=CC=CC=C1 AGEZXYOZHKGVCM-UHFFFAOYSA-N 0.000 description 1
- 210000003445 biliary tract Anatomy 0.000 description 1
- 125000006267 biphenyl group Chemical group 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 238000011088 calibration curve Methods 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 239000007894 caplet Substances 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 125000002837 carbocyclic group Chemical group 0.000 description 1
- 238000001460 carbon-13 nuclear magnetic resonance spectrum Methods 0.000 description 1
- 238000009903 catalytic hydrogenation reaction Methods 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 210000003793 centrosome Anatomy 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000013522 chelant Substances 0.000 description 1
- 229920001429 chelating resin Polymers 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 210000000038 chest Anatomy 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 150000004696 coordination complex Chemical class 0.000 description 1
- KDBQRAGSEVVHSN-UHFFFAOYSA-L copper(II) sulfate hexahydrate Chemical compound O.O.O.O.O.O.[Cu+2].[O-]S([O-])(=O)=O KDBQRAGSEVVHSN-UHFFFAOYSA-L 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000004856 decahydroquinolinyl group Chemical group N1(CCCC2CCCCC12)* 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000000151 deposition Methods 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 230000005292 diamagnetic effect Effects 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 125000000532 dioxanyl group Chemical group 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 239000003480 eluent Substances 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- TWQLMAJROCNXEA-UHFFFAOYSA-N ethyl 4-(bromomethyl)benzoate Chemical compound CCOC(=O)C1=CC=C(CBr)C=C1 TWQLMAJROCNXEA-UHFFFAOYSA-N 0.000 description 1
- 125000003916 ethylene diamine group Chemical group 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 229960002089 ferrous chloride Drugs 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- UIWYJDYFSGRHKR-UHFFFAOYSA-N gadolinium atom Chemical compound [Gd] UIWYJDYFSGRHKR-UHFFFAOYSA-N 0.000 description 1
- 229940044350 gadopentetate dimeglumine Drugs 0.000 description 1
- RYHQMKVRYNEBNJ-BMWGJIJESA-K gadoterate meglumine Chemical compound [Gd+3].CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO.OC(=O)CN1CCN(CC([O-])=O)CCN(CC([O-])=O)CCN(CC([O-])=O)CC1 RYHQMKVRYNEBNJ-BMWGJIJESA-K 0.000 description 1
- 229960003180 glutathione Drugs 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 150000002430 hydrocarbons Chemical group 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 230000005364 hyperfine coupling Effects 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 238000011503 in vivo imaging Methods 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 238000007917 intracranial administration Methods 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 238000002075 inversion recovery Methods 0.000 description 1
- 238000005040 ion trap Methods 0.000 description 1
- 150000004698 iron complex Chemical class 0.000 description 1
- GYCHYNMREWYSKH-UHFFFAOYSA-L iron(ii) bromide Chemical compound [Fe+2].[Br-].[Br-] GYCHYNMREWYSKH-UHFFFAOYSA-L 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 238000013507 mapping Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- 238000001465 metallisation Methods 0.000 description 1
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 1
- DYGOPFFOGFHOIB-UHFFFAOYSA-N methylperoxyethane Chemical class CCOOC DYGOPFFOGFHOIB-UHFFFAOYSA-N 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000010606 normalization Methods 0.000 description 1
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 238000001139 pH measurement Methods 0.000 description 1
- 238000005192 partition Methods 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 125000004193 piperazinyl group Chemical group 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 230000001376 precipitating effect Effects 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- TVDSBUOJIPERQY-UHFFFAOYSA-N prop-2-yn-1-ol Chemical compound OCC#C TVDSBUOJIPERQY-UHFFFAOYSA-N 0.000 description 1
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 125000004076 pyridyl group Chemical class 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 125000005493 quinolyl group Chemical class 0.000 description 1
- 125000004621 quinuclidinyl group Chemical group N12C(CC(CC1)CC2)* 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 238000004064 recycling Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 238000002390 rotary evaporation Methods 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 150000003335 secondary amines Chemical class 0.000 description 1
- 238000004904 shortening Methods 0.000 description 1
- 238000004088 simulation Methods 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- 235000010378 sodium ascorbate Nutrition 0.000 description 1
- PPASLZSBLFJQEF-RKJRWTFHSA-M sodium ascorbate Substances [Na+].OC[C@@H](O)[C@H]1OC(=O)C(O)=C1[O-] PPASLZSBLFJQEF-RKJRWTFHSA-M 0.000 description 1
- 229960005055 sodium ascorbate Drugs 0.000 description 1
- PPASLZSBLFJQEF-RXSVEWSESA-M sodium-L-ascorbate Chemical compound [Na+].OC[C@H](O)[C@H]1OC(=O)C(O)=C1[O-] PPASLZSBLFJQEF-RXSVEWSESA-M 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 239000011550 stock solution Substances 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 208000023516 stroke disease Diseases 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 1
- 125000001412 tetrahydropyranyl group Chemical group 0.000 description 1
- 125000003507 tetrahydrothiofenyl group Chemical group 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- BDZBKCUKTQZUTL-UHFFFAOYSA-N triethyl phosphite Chemical compound CCOP(OCC)OCC BDZBKCUKTQZUTL-UHFFFAOYSA-N 0.000 description 1
- 238000003828 vacuum filtration Methods 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 210000003462 vein Anatomy 0.000 description 1
- 210000001631 vena cava inferior Anatomy 0.000 description 1
- 239000003643 water by type Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F19/00—Metal compounds according to more than one of main groups C07F1/00 - C07F17/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/06—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations
- A61K49/08—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations characterised by the carrier
- A61K49/10—Organic compounds
- A61K49/101—Organic compounds the carrier being a complex-forming compound able to form MRI-active complexes with paramagnetic metals
- A61K49/106—Organic compounds the carrier being a complex-forming compound able to form MRI-active complexes with paramagnetic metals the complex-forming compound being cyclic, e.g. DOTA
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D255/00—Heterocyclic compounds containing rings having three nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D249/00 - C07D253/00
- C07D255/02—Heterocyclic compounds containing rings having three nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D249/00 - C07D253/00 not condensed with other rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/02—Iron compounds
- C07F15/025—Iron compounds without a metal-carbon linkage
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6515—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having three nitrogen atoms as the only ring hetero atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6558—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing at least two different or differently substituted hetero rings neither condensed among themselves nor condensed with a common carbocyclic ring or ring system
- C07F9/65583—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing at least two different or differently substituted hetero rings neither condensed among themselves nor condensed with a common carbocyclic ring or ring system each of the hetero rings containing nitrogen as ring hetero atom
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Medicinal Chemistry (AREA)
- Radiology & Medical Imaging (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
매크로사이클릭 복합체(macrocyclic complex) 및 매크로사이클릭 화합물. 매크로사이클릭 복합체 또는 매크로사이클릭 화합물은 하나 이상의 아민기(들)을 갖는 TACN 모이어티 또는 O- 또는 S-치환된 TACN 모이어티를 갖는다. 매크로사이클릭 복합체는 TACN 모이어티에 배위된 고스핀(high-spin) Fe(III) 원자를 갖는다. 매크로사이클릭 복합체는 영상화(imaging) 방법에 사용될 수 있다.
Description
(관련 출원의 상호 참조)
본 출원은 2018년 11월 16일에 출원된 미국 가출원 제62/768,823호의 우선권을 주장하며, 이의 개시 내용은 본 명세서에 참조로 포함된다.
(연방 지원 연구에 관한 진술)
본 발명은 국립과학재단이 수여한 계약 번호 1710224 및 국립보건원이 수여한 계약 번호 EB025369 하에서 정부 지원으로 이루어졌다. 정부는 본 발명에 대한 특정 권리를 갖는다.
본 개시 내용은 일반적으로 매크로사이클릭 화합물(macrocyclic compound)에 관한 것이다. 철(III)과 복합체화될 때, 이러한 화합물은 MRI 조영제(contrast agent)로 사용될 수 있다.
3가 철로서 Fe(III)를 함유하는 조영제는 Gd(III) 조영제에 대한 대안을 제공할 것이다. 현재까지, 임상적으로 사용되는 거의 모든 조영제는, 미국 인구(약 10%)의 환자 중 상당 부분이 Gd(III) 조영제가 제공될 위험이 있는 것으로 간주된다는 사실에도 불구하고, 가돌리늄(3가 Gd(III)으로서의 Gd)을 함유한다. Gd(III) 기반 MRI 조영제가 모든 환자의 뇌, 뼈 및 피부에 Gd(III) 침착을 초래한다는 새로운 우려가 있다. 고스핀(high spin) Fe(III) 복합체와 같은 생물학적으로 관련된 전이 금속 이온을 포함하는 Gd(III) 조영제에 대한 대안은 가치 있을 것이다. 생물학적으로 관련된 전이 금속 이온을 포함하는 Gd(III) 조영제의 대안은 고스핀 Mn(II) 및 고스핀 Fe(III) 복합체를 포함한다. Fe(III) 사용의 잠재적인 이점은 전이 금속 이온 중 가장 풍부한 철의 재활용 및 저장을 위한 인체의 광범위한 메커니즘을 포함한다. 또한, Fe(III) 복합체는 Mn(II)보다 해리의 경향이 적다. 특히, Mn(II) 및 Fe(III) 복합체의 산화 환원 전위는 활성 산소 종(ROS) 생성을 방지하도록 조정될 수 있다. 예를 들면, 특정 리간드는 가혹한 조건에서도 하이드록실 라디칼을 생성하지 않는 산화 환원 비활성 Fe(III) 복합체를 형성한다. 본 명세서에 기재된 철 기반 MRI 조영제(3가 Fe(III)로서)는 Gd(III) 제제와 동일한 상자성 메커니즘에 의해 조영(contrast)을 생성하고, 배위 복합체와 같은 소분자 형태이며, 즉 나노 입자가 아니다.
현재까지 보고된 대부분의 Fe(III) MRI 조영제는 EHBG (NN'-에틸렌비스[(2-하이드록시벤질)글리신)과 같은 페놀과 카르복실레이트 펜던트의 조합을 갖는 에틸렌 디아민 백본을 포함하는 단순한 선형 킬레이트를 함유한다. 다른 유형은 EDTA의 Fe(III) 복합체와 같은 폴리아미노카르복실레이트 리간드를 함유한다. 세번째 유형은 세균성 사이드로포어(siderophore)인 데스페리옥사민(desferrioxamine, DFO)을 함유한다. 이러한 모든 복합체는 교환 가능한 물 리간드의 부족, ROS 생성에 적합한 환원 전위 및/또는 합성 변형의 어려움을 포함하는 단점이 있다. 또한, Fe(III) 복합체의 수용액 화학물질은 수산화물 및 가교 산화물 리간드와의 불용성 복합체의 형성에 의해 지배된다. 산화 환원 전위를 조정하여 Fe(III)를 안정화하고, 바람직한 T1 이완제(relaxivity agent)인 ROS 생성에 효과적인 촉매가 아닌 Fe(III) 복합체를 얻기 위해 개선이 필요하다. 추가 고려 사항은 복합체의 전체 전하이다. Fe(III)에 펜던트로서 결합하거나, 보조기로서 더 멀리 떨어져 있는 음이온기는 조영제의 약동학 및 이의 체내 제거를 조절하는데 중요하다.
적어도 상술한 바에 기초하여, 개선된 특성을 갖는 Fe(III) MRI 조영제에 대한 당업계에서 계속되고 충족되지 않은 요구가 존재한다.
본 발명의 목적은 Fe(III)와 복합체화될 수 있는 매크로사이클릭 화합물을 제공하는 것이다. 또한, 본 발명의 목적은 조성물, 및 화합물과 복합체를 제조 및 사용하는 방법을 제공하는 것이다.
T1 MRI 조영제로서 사용하기 위한 Fe(III) 배위 결합 복합체(coordination complex)가 개시된다. 개시된 Fe(III) T1 MRI 조영제는 매크로사이클릭 리간드를 함유한다. 또한, Fe(III) 복합체는 T2 MRI 조영제로 사용될 수 있다.
본 개시 내용은, i) 리간드 공여체(ligand donor)로서 적어도 2개의 헤테로원자를 포함하는 매크로사이클릭 코어(macrocyclic core); 및 ii) 상기 매크로사이클릭 코어의 치환체로서 음이온성 펜던트라고 할 수 있는 적어도 하나의 펜던트 공여체;를 갖는 매크로사이클릭 화합물 또는 매크로사이클을 제공한다. 상기 매크로사이클릭 코어는 탄소원자 및 적어도 하나의 헤테로원자(예를 들면, N 원자, O 원자, 또는 S 원자)를 포함하는 고리 구조를 갖는다. 상기 매크로사이클릭 코어는 TACN 모이어티일 수 있다. 상기 마이크로사이클릭 코어는 N 원자(들) 중 하나 이상이 O 원자 또는 S 원자로 치환되는 TACN 모이어티일 수 있다.
예를 들면, 펜던트 공여체(pendent donor)는 산소-함유기(예를 들면, 알콜, 산화물(예를 들면, 알콕사이드 또는 페녹사이드), 설포네이트, 포스피네이트, 포스포네이트 등)일 수 있다. 일부 펜던트 공여체, 예를 들면 알콜, 포스핀산, 포스폰산 또는 설폰산은 Fe(III)와 또는 특정 pH에서 복합체화될 때 탈양성자화될 수 있다.
매크로사이클릭 화합물은 하나 이상의 보조 펜던트기를 포함할 수 있다. 보조 펜던트기(들)은 하나 이상의 배위 보조 펜던트기 및/또는 하나 이상의 비-배위 보조 펜던트기(non-coordinating ancillary pendent group)일 수 있다.
하나의 양태에서, 본 개시 내용의 화합물은 방향족(예를 들면, 아릴)기, 매크로사이클, 폴리머, 덴드리머, 단백질, 또는 펩티드를 통해 함께 묶이는 하나 이상의 매크로사이클릭 코어를 갖는다.
본 개시 내용의 방법에 사용하기 위해, 본 명세서에 기재된 화합물 또는 복합체는 약제학적 제제로서 투여될 수 있다. 따라서, 이들은 다양한 조성물로 제공될 수 있고, 하나 이상의 약제학적으로 허용되는 담체와 혼합될 수 있다.
하나의 측면에서, 본 개시 내용은 본 명세서에 기재된 매크로사이클릭 화합물을 사용하여 영상화 방법을 제공한다. 영상화 방법은 자기 공명 영상법(magnetic resonance imaging method)을 사용한다. 이러한 방법의 예는, 자기 공명 영상(MRI)을 포함하지만, 이에 제한되지 않는다. 구체적으로, 본 개시 내용의 매크로사이클릭 화합물은, Fe(III)와 복합체화될 때, T1 MRI 조영제로 사용될 수 있다. 본 개시 내용의 영상화 방법은 세포, 조직, 기관, 혈관계 또는 이들의 일부를 영상화하는데 사용될 수 있다. 세포, 조직, 기관, 혈관계는 개체의 일부일 수 있다.
도 1은 TASO 리간드의 합성 도식을 도시한다.
도 2는 TRAP-Ph 매크로사이클과 포스피닉 펜던트의 합성 도식 및 및 대응하는 Fe(III) 복합체를 도시한다.
도 3은 포스핀산 펜던트와 매크로사이클 화합물의 합성을 도시한다.
도 4는 매크로사이클 화합물과 포스핀산 펜던트 또는 포스폰산 펜던트의 합성 및 대응하는 Fe(III) 복합체를 도시한다.
도 5는 Fe(III) 복합체의 형성 및 매크로사이클에 이들의 부착을 포함하는 음이온성기와 트리아졸 펜던트의 합성 도식을 도시한다.
도 6은 Fe(TASO)의 1H NMR이 고스핀 Fe(III)과 일치하여 기준선으로 확장된 것을 보여준다. t-부탄올 양성자 공명의 이동이 관측되었다.
도 7은 Fe(TASO)와 같은 Fe(III) 조영제가 EDTA 또는 CDTA의 Fe(III) 복합체와는 달리 퍼옥사이드 및 아스코르베이트의 존재 하에 벤조에이트를 산화하지 못하는 것을 보여준다. pH 7.2에서 50 μM 복합체, 50 μM H2O2 및 50 μM 아스코르베이트를 사용한 벤조에이트 산화. [Fe(EDTA)]- 산화는 100%로 설정된다.
도 8은 다양한 온도 17O NMR 연구의 데이터의 플롯을 보여준다. 온도의 함수로서 17O NMR 공명의 가로 이완성(transverse relaxivity)의 역의 자연 로그(natural log)가 pH 4.5에서 20 mM Fe(TASO)를 함유하는 실험에 대해 도시된다.
도 9는 Gd(DTPA) 및 Fe(TOB)와 비교하여 간, 신장을 포함한 다양한 조직에 Fe-TASO를 주입한 후 시간에 따른 마우스의 T1 이완성 변화의 플롯을 보여준다.
도 10은 Gd(DTPA) 및 Fe(TOB)와 비교하여 혈액에 Fe(TASO) 주입 후 시간에 따른 마우스의 T1 이완성 변화의 플롯을 보여준다.
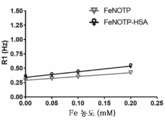
도 11은 본 개시 내용의 매크로사이클릭 복합체의 예에 대해 4.7 Tesla 및 37 ℃에서 얻어진 이완성 데이터를 보여준다. Fe-NOTP는 0.66 ± 0.01 mM-1s-1 r1을 나타냈고, HSA가 있는 Fe-NOTP는 1.04 ± 0.06 mM-1s-1의 r1을 나타냈다.
도 12는 지지 전해질 및 HEPES 완충액으로서 포타슘 클로라이드 (100 mM)를 사용하여 수중에서 다양한 pH에서 Fe(TASO)의 1.0 mM 용액의 순환 전압전류도를 보여준다. 전체 스위프(sweep) 폭은 -1.5 V와 1.5 V 사이에서 취했으며, 100 mV/s의 스캔 속도에서, pH 7에서 Fe(TASO) E1/2는 -204 mV로, pH 3에서 NHE 에 대해 보정되어 513 mV로 확인되었다.
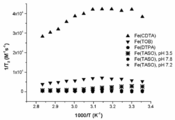
도 13은 는 pH 값 범위에 걸쳐 측정된 Fe(DTPA), Fe(TOB) 및 Fe(CDTA)와 비교하여 Fe(TASO)에 대한 온도 함수로서의 가로 17O NMR 이완성, ln(1/T2r)을 보여준다. Fe(CDTA)는 교환 가능한 물 리간드가 있지만, Fe(DTPA)는 교환 가능한 내권 물 리간드(exchangeable innersphere water ligand)가 없다.
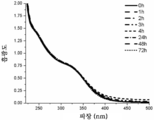
도 14는 37 ℃에서 72시간에 걸쳐 얻어진 Fe(TASO)의 UV-vis 흡광도 스펙트럼을 보여준다. 수용액은 0.1M HCl에 용해된 0.2 mM Fe(TASO)를 함유했다. ε(250nm) = 6097 M-1 cm-1, ε(325nm) = 3557 M-1 cm-1. 24시간 후 해리는 18.1%였다. 72시간 후 해리는 53.6%였다.
도 15는 7.1 pH에서 25 mM NaHCO3, 0.50 mM Na2HPO4, 10 mM HEPES 완충액에 용해된 0.2 mM Fe(TASO)를 함유하는 수용액을 사용하여 37 ℃에서 72시간에 걸쳐 얻어진 Fe(TASO)의 UV-vis 흡광도 스펙트럼을 보여준다. ε(245nm) = 6960 M-1 cm-1, ε(325nm) = 3571 M-1 cm-1.
도 16은 Fe(TASO)의 UV-vis 흡광도 스펙트럼을 37 ℃에서 72시간에 걸쳐 얻었다. 수용액은 7.1 pH에서 10 mM HEPES 완충액에 용해된 0.2 mM Fe(TASO)를 함유했다. ε(245nm) = 6762 M-1 cm-1, ε(325nm) = 3687 M-1 cm-1.
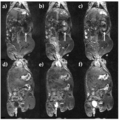
도 17은 0.2 mmol/kg의 Fe(TASO)의 용량에서 4.7 T의 건강한 Balb/C 마우스의 T1-강조 MRI(T1-weighted MRI)를 보여준다. 상단줄: 신장의 향상(화살표)을 보여주는 주사 전(a), 5분 후(b) 및 40분(c) 주사 후 영상. 하단줄: 방광 영상 (화살표) 주사 전(d), 5분 및 40분 후(f).
도 18은 0.05 mmol/kg Fe(TASO)의 용량에서 4.7 T에서 건강한 Balb/C 마우스의 T1-강조 MRI를 보여준다. 상단줄: 신장의 향상(화살표)을 보여주는 주사 전(a), 30분 후(b) 및 4시간 후(c) 및 24시간(d) 주사 후 영상. 위는 S로 표시했다. 하단줄: 간(L) 및 담낭 영상(화살표) 주사 전(e), 30분 후(f), 4시간 후(g) 및 24시간(h) 주사 후 영상.
도 19는 Fe(TASO)에 대한 마우스의 약동학적 데이터를 보여준다.
도 20은 임상적으로 사용되는 Gd 복합체와 비교하여 Fe(TASO)에 대한 마우스의 약동학적 데이터를 보여준다.
도 21은 3분, 7분, 12분에 0.05 mmol/kg의 용량에서 4.7T의 Fe(L4)에서 건강한 Balb/C 마우스의 T1-강조 MR 영상을 보여준다. 방광에 향상을 보여준다.
도 2는 TRAP-Ph 매크로사이클과 포스피닉 펜던트의 합성 도식 및 및 대응하는 Fe(III) 복합체를 도시한다.
도 3은 포스핀산 펜던트와 매크로사이클 화합물의 합성을 도시한다.
도 4는 매크로사이클 화합물과 포스핀산 펜던트 또는 포스폰산 펜던트의 합성 및 대응하는 Fe(III) 복합체를 도시한다.
도 5는 Fe(III) 복합체의 형성 및 매크로사이클에 이들의 부착을 포함하는 음이온성기와 트리아졸 펜던트의 합성 도식을 도시한다.
도 6은 Fe(TASO)의 1H NMR이 고스핀 Fe(III)과 일치하여 기준선으로 확장된 것을 보여준다. t-부탄올 양성자 공명의 이동이 관측되었다.
도 7은 Fe(TASO)와 같은 Fe(III) 조영제가 EDTA 또는 CDTA의 Fe(III) 복합체와는 달리 퍼옥사이드 및 아스코르베이트의 존재 하에 벤조에이트를 산화하지 못하는 것을 보여준다. pH 7.2에서 50 μM 복합체, 50 μM H2O2 및 50 μM 아스코르베이트를 사용한 벤조에이트 산화. [Fe(EDTA)]- 산화는 100%로 설정된다.
도 8은 다양한 온도 17O NMR 연구의 데이터의 플롯을 보여준다. 온도의 함수로서 17O NMR 공명의 가로 이완성(transverse relaxivity)의 역의 자연 로그(natural log)가 pH 4.5에서 20 mM Fe(TASO)를 함유하는 실험에 대해 도시된다.
도 9는 Gd(DTPA) 및 Fe(TOB)와 비교하여 간, 신장을 포함한 다양한 조직에 Fe-TASO를 주입한 후 시간에 따른 마우스의 T1 이완성 변화의 플롯을 보여준다.
도 10은 Gd(DTPA) 및 Fe(TOB)와 비교하여 혈액에 Fe(TASO) 주입 후 시간에 따른 마우스의 T1 이완성 변화의 플롯을 보여준다.
도 11은 본 개시 내용의 매크로사이클릭 복합체의 예에 대해 4.7 Tesla 및 37 ℃에서 얻어진 이완성 데이터를 보여준다. Fe-NOTP는 0.66 ± 0.01 mM-1s-1 r1을 나타냈고, HSA가 있는 Fe-NOTP는 1.04 ± 0.06 mM-1s-1의 r1을 나타냈다.
도 12는 지지 전해질 및 HEPES 완충액으로서 포타슘 클로라이드 (100 mM)를 사용하여 수중에서 다양한 pH에서 Fe(TASO)의 1.0 mM 용액의 순환 전압전류도를 보여준다. 전체 스위프(sweep) 폭은 -1.5 V와 1.5 V 사이에서 취했으며, 100 mV/s의 스캔 속도에서, pH 7에서 Fe(TASO) E1/2는 -204 mV로, pH 3에서 NHE 에 대해 보정되어 513 mV로 확인되었다.
도 13은 는 pH 값 범위에 걸쳐 측정된 Fe(DTPA), Fe(TOB) 및 Fe(CDTA)와 비교하여 Fe(TASO)에 대한 온도 함수로서의 가로 17O NMR 이완성, ln(1/T2r)을 보여준다. Fe(CDTA)는 교환 가능한 물 리간드가 있지만, Fe(DTPA)는 교환 가능한 내권 물 리간드(exchangeable innersphere water ligand)가 없다.
도 14는 37 ℃에서 72시간에 걸쳐 얻어진 Fe(TASO)의 UV-vis 흡광도 스펙트럼을 보여준다. 수용액은 0.1M HCl에 용해된 0.2 mM Fe(TASO)를 함유했다. ε(250nm) = 6097 M-1 cm-1, ε(325nm) = 3557 M-1 cm-1. 24시간 후 해리는 18.1%였다. 72시간 후 해리는 53.6%였다.
도 15는 7.1 pH에서 25 mM NaHCO3, 0.50 mM Na2HPO4, 10 mM HEPES 완충액에 용해된 0.2 mM Fe(TASO)를 함유하는 수용액을 사용하여 37 ℃에서 72시간에 걸쳐 얻어진 Fe(TASO)의 UV-vis 흡광도 스펙트럼을 보여준다. ε(245nm) = 6960 M-1 cm-1, ε(325nm) = 3571 M-1 cm-1.
도 16은 Fe(TASO)의 UV-vis 흡광도 스펙트럼을 37 ℃에서 72시간에 걸쳐 얻었다. 수용액은 7.1 pH에서 10 mM HEPES 완충액에 용해된 0.2 mM Fe(TASO)를 함유했다. ε(245nm) = 6762 M-1 cm-1, ε(325nm) = 3687 M-1 cm-1.
도 17은 0.2 mmol/kg의 Fe(TASO)의 용량에서 4.7 T의 건강한 Balb/C 마우스의 T1-강조 MRI(T1-weighted MRI)를 보여준다. 상단줄: 신장의 향상(화살표)을 보여주는 주사 전(a), 5분 후(b) 및 40분(c) 주사 후 영상. 하단줄: 방광 영상 (화살표) 주사 전(d), 5분 및 40분 후(f).
도 18은 0.05 mmol/kg Fe(TASO)의 용량에서 4.7 T에서 건강한 Balb/C 마우스의 T1-강조 MRI를 보여준다. 상단줄: 신장의 향상(화살표)을 보여주는 주사 전(a), 30분 후(b) 및 4시간 후(c) 및 24시간(d) 주사 후 영상. 위는 S로 표시했다. 하단줄: 간(L) 및 담낭 영상(화살표) 주사 전(e), 30분 후(f), 4시간 후(g) 및 24시간(h) 주사 후 영상.
도 19는 Fe(TASO)에 대한 마우스의 약동학적 데이터를 보여준다.
도 20은 임상적으로 사용되는 Gd 복합체와 비교하여 Fe(TASO)에 대한 마우스의 약동학적 데이터를 보여준다.
도 21은 3분, 7분, 12분에 0.05 mmol/kg의 용량에서 4.7T의 Fe(L4)에서 건강한 Balb/C 마우스의 T1-강조 MR 영상을 보여준다. 방광에 향상을 보여준다.
본 개시 내용의 목적은 Fe(III)와 복합체화될 수 있는 매크로사이클릭 화합물을 제공하는 것이다. 또한, 본 개시 내용의 목적은 화합물 및 복합체를 제조 및 사용하여 조성물 및 방법을 제공하는 것이다.
매크로사이클릭 리간드와의 고스핀 Fe(III) 복합체는 T1 MRI 조영제로서 개발될 수 있다. 특히, 고스핀 Fe(III)은 물 분자와의 내권(innersphere) 및 외권(outersphere) 모두의 상호 작용을 통해 MRI 조영(contrast)에 대한 물의 양성자의 T1 이완 시간을 줄이는 유리한 상자성 특성을 가지고 있다.
T1 MRI 조영제로 사용하기 위한 Fe(III) 배위 결합 복합체가 개시된다. 개시된 Fe(III) T1 MRI 조영제는 매크로사이클릭 리간드를 함유한다. 임의의 특정 이론에 얽매이지 않고, 매크로사이클릭 리간드는 스핀과 산화 상태를 조절하고, 음이온기는 복합체의 전체 전하를 조절한다고 생각된다. 또한, Fe(III) 복합체는 T2 MRI 조영제로 사용될 수 있다.
Fe(III)와 복합체화되는 경우, 본 개시내용의 매크로사이클릭 화합물(리간드로서)은 스핀 및 산화 상태에 대한 제어 및 또한 내권 및 외권 물과의 상호작용을 달성하는 이점을 갖는다. 이러한 매크로사이클릭거 리간드의 구멍은 고스핀 형태의 Fe(III) 안정화에 적합하다. 또한, 이러한 매크로사이클릭 화합물을 사용하여 수용액 화학물질의 제어가 달성될 수 있다. 여기에 기재되는 매크로사이클릭 복합체는 거의 Fe(III)를 캡슐화하지만, 일부 경우에는, T1 MRI 조영제로서의 효능을 향상시키는 물 리간드에 대한 배위 부위가 있다. 일부 경우에, 내권 물 리간드는 두 번째 구 상호작용을 통해 벌크 물 양성자의 T1 이완성을 생성할 수 있다. 본 명세서에 기재된 철 기반 MRI 조영제(고스핀, 3가 Fe(III)와 복합체화된 매크로사이클)는 Gd(III) 제제와 동일한 상자성 메커니즘에 의해 조영(contrast)을 생성하고, 배위 복합체와 같은 작은 분자 형태이며, 즉 이들은 나노 입자가 아니다.
본 명세서에서 사용되는, 달리 언급하지 않으면, 용어 "기(group)" 또는 "모이어티(moiety)"는 1가(즉, 다른 화학적 종에 공유 결합될 수 있는 하나의 말단을 갖는), 2가, 또는 다가(즉, 다른 화학적 종에 공유 결합될 수 있는 둘 이상의 말단을 갖는)인 화학적 개체를 말한다. 기들의 예는 하기를 포함하지만, 이에 제한되지 않는다:
본 명세서에서 사용되는, 달리 언급하지 않으면, 용어 "알킬(alkyl)" 또는 "알킬기(alkyl group)"는 분지형 또는 비-분지형 포화 탄화수소기를 말한다. 알킬기의 예는, 메틸기, 에틸기, n- 및 이소프로필기, n-, iso-, sec-, 및 tert-부틸기 등을 포함하지만, 이에 제한되지 않는다. 예를 들면, 알킬기는 이들 사이의 탄소의 모든 정수의 수 및 탄소의 수의 범위를 포함하여 C1 내지 C12일 수 있다. 알킬기는 하나 이상의 치환체로 비치환되거나 치환될 수 있다. 치환체의 예는, 예를 들면 할로겐(-F, -Cl, -Br, 및 -I), 지방족기(예를 들면, 알킬기, 알케닐기, 및 알키닐기), 아릴기, 알콕사이드기, 티오알콕사이드기, 카르복실레이트기, 카르복실산, 에테르기, 등, 및 이들의 조합과 같은 다양한 치환체를 포함하지만, 이에 제한되지 않는다.
본 명세서에 사용되는, 달리 언급되지 않으면, 용어 "아릴(aryl)" 또는 "아릴기(aryl group)"는 이들 사이의 탄소의 모든 정수의 수 및 탄소의 수의 범위를 포함하여 C5 내지 C12, 방향족 또는 부분 방향족 카르보사이클릭기를 말한다. 또한, 아릴기는 방향족기라고도 할 수 있다. 아릴기는, 예를 들면 융합된 고리(fused ring) 또는 비아릴기(biaryl group)와 같은 폴리아릴기를 포함할 수 있다. 아릴기는 하나 이상의 치환체로 비치환되거나 치환될 수 있다. 치환체의 예는, 예를 들면 할로겐(-F, -Cl, -Br, 및 -I), 지방족기(예를 들면, 알켄, 알킨, 등), 아릴기, 알콕사이드, 티오알콕사이드, 카르복실레이트, 카르복실산, 에테르기, 등, 및 이들의 조합과 같은 치환체를 포함하지만, 이에 제한되지 않는다. 아릴기의 예는, 페닐기, 비아릴기(예를 들면, 비페닐기 등), 및 융합된 고리기(예를 들면, 나프틸기 등)를 포함하지만, 이에 제한되지 않는다.
본 명세서에서 사용되는, 달리 언급되지 않으면, 용어 "아랄킬(aralkyl)"은 알킬기 상의 하나 이상의 수소원자를 하나 이상의 아릴기로 대체함으로써 알킬기로부터 유래되는 임의의 기를 말한다.
본 명세서에서 사용되는, 달리 언급되지 않으면, 용어 "헤테로사이클릭기(heterocyclic group)"는 고리 구조의 일부로서 하나 이상의 헤테로원자(예를 들면, N, O, S, 등)를 함유하는 C3-C20 (예를 들면, C3, C4, C5, C6, C7, C8, C9, C10, C11, C12, C13, C14, C15, C16, C17, C18, C19, C20) 사이클릭기를 말한다. 헤테로사이클릭기는 치환되거나 비치환될 수 있고/있거나, 추가적인 불포화도를 가질 수 있다. 헤테로사이클릭기는 융합된 고리(예를 들면, 피롤리지디닐기(pyrrolizidinyl group) 등)일 수 있다. 헤테로사이클릭기의 비제한적인예는 푸라닐기, 옥사졸릴기, 이소티아졸릴기, 티아졸릴기, 테트라하이드로피라닐기(tetrahydropyranyl group), 피페라지닐기(piperazinyl group), 디옥사닐기, 피롤리디닐기, 테트라하이드로티오페닐기(tetrahydrothiophenyl group), 테트라하이드로푸라닐기(tetrahydrofuranyl group), 퀴누클리디닐기(quinuclidinyl group), 아자아다만타닐기(azaadamantanyl group), 데카하이드로퀴놀리닐기(decahydroquinolinyl group) 등을 포함한다.
본 개시 내용은, i) 리간드 공여체(ligand donor)로서 적어도 2개의 헤테로원자를 포함하는 매크로사이클릭 코어(macrocyclic core); 및 ii) 상기 매크로사이클릭 코어의 치환체로서 적어도 하나의 펜던트 공여체;를 갖는 매크로사이클릭 화합물 또는 매크로사이클을 제공한다. 상기 매크로사이클릭 코어는 탄소원자 및 적어도 하나의 헤테로원자(예를 들면, N 원자, O 원자, 또는 S 원자)를 포함하는 고리 구조를 갖는다. 본 명세서에서 사용되는, "매크로사이클 공여체(macrocycle donor)"는 화합물의 매크로사이클릭 코어에 존재할 때 Fe(III) 중심에 공여하는 이용 가능한 고립 전자 쌍이 있는 헤테로원자를 말한다. 예를 들면, 매크로사이클 공여체는 질소원자(예를 들면, 3차 아민, 2차 아민), 또는 산소원자(예를 들면, 에테르)일 수 있다. 본 명세서에서 사용되는, 음이온성 펜던트 및 보조 펜던트(ancillary pendent)를 포함하는 "펜던트 공여체(pendent donor)"는 화합물의 매크로사이클릭 코어 상의 치환체에 존재할 때 Fe(III) 중심에 공여하는 이용 가능한 고립 전자 쌍이 있는 헤테로원자를 말한다. 예를 들면, 펜던트 공여체는 산소-함유기(예를 들면, 알콜, 산화물(예를 들면, 알콕사이드 또는 페녹사이드), 설포네이트, 포스피네이트, 포스포네이트 등)일 수 있다. 예를 들면, 알콜, 포스핀산, 포스폰산 또는 설폰산과 같은 일부 펜던트 공여체는 특정 pH에서 또는 Fe(III)와 복합체화될 때 탈양성자화될 수 있다. 이러한 양성자화된 및 탈양성자화된 형태는 본 개시 내용의 범위 내이다. 일부 양태에서, 매크로사이클릭 화합물은 Fe(III)과 복합체화 되어, 안정화된 3가 상태이다(Eo < 0 mV 대 NHE). 도식 I 및 II의 특정 양태에서, R1은 Fe(III)에 결합되지 않는 보조기일 수 있다. 음이온성기는 설포네이트, 포스피네이트, 포스페이트, 포스포네이트 또는 카르복실레이트기를 포함하는, Fe(III)에 결합되지 않는 보조기에 첨가될 수 있다.
매크로사이클릭 코어는 TACN 모이어티일 수 있다. 매크로사이클릭 코어는, 하나 이상의 N 원자(들)이 O 원자 또는 S 원자로 치환되는 TACN 모이어티일 수 있다.
특정 양태에서, 매크로사이클은 하기 구조를 갖는다:
도식 I
여기서 X1, X2, X3은 N이고; W1은 O 또는 S이고; Y1, Y2, Y3은 각각 독립적으로 i) O를 포함하는 펜던트 공여체, 여기서 O는 적어도 하나의 고립 전자쌍, 바람직하게는 2개 또는 3개의 고립 전자쌍(예를 들면, 케톤, 알코올, 알콕사이드, 페놀 또는 페녹사이드, 설폰산, 포스핀산 또는 포스폰산 또는 이들의 탈양성자화된 형태, 예를 들면 알콕사이드 또는 페녹사이드를 포함하는 산화물)을 가지며; 또는 ii) N을 포함하는 펜던트 공여체, 여기서 N은, 예를 들면 트리아졸과 같은 적어도 하나의 고립 전자쌍을 가지며; m1, m2 및 m3은 각각 독립적으로 1, 2 또는 3이고; n1, n2, 및 n3은 각각 독립적으로 1 또는 2 또는 3이고; R1은 치환 또는 비치환된 아릴, 치환 또는 비치환된 헤테로사이클릭기 또는 치환 또는 비치환된 알킬이고, 여기서 알킬-Y 사슬의 알킬 세그먼트(알킬-Y1, 알킬-Y2 및/또는 알킬-Y3)는 각각 독립적으로 치환 또는 비치환될 수 있다. 다른 양태에서, 알킬-Y1, 알킬-Y2, 알킬-Y3 중 어느 하나 또는 전부는 독립적으로 도식 III에 정의된 바와 같은 구조 1-9 중 하나일 수 있다.
특정 양태에서, R1은 펜던트 공여체로 치환되지 않는다.
일부 양태에서, 매크로사이클은 하기 구조를 가질 수 있다(도식 II):
도식 II
여기서, R1은 치환 또는 비치환된 아릴, 치환 또는 비치환된 헤테로아릴 또는 치환 또는 비치환된 알킬이고, 상기 매크로사이클이 구조 I을 가지면, Z1은 H 또는 도식 III의 펜던트기 중 하나이고, Z2 및 Z3은 각각 독립적으로 도식 III의 펜던트기 중 하나이며; 상기 매크로사이클이 구조 II 또는 III을 가지면, Z1 및 Z2는 각각 독립적으로 도식 III의 펜던트기 중 하나이며; 전체 구조 I-III에서, 각각의 Z1, Z2, 및 Z3은 적용 가능하게 서로 독립적으로 선택된다. 이 단락은 추후 "도식 II"라고 한다.
일부 양태에서, 도식 II의 매크로사이클이 Fe(III)와 복합체화되면, R1은 Fe(III)로 배위되지 않는다.
하나의 양태에서, 단락 [0045]에서 의미론적으로 정의되거나 도식 I 또는 II에 따른 매크로사이클은 매크로사이클 코어 상에 적어도 하나의 펜던트 공여체를 갖는다. 예를 들면, 상기 펜던트 공여체는 하기 구조를 가질 수 있다(도식 III):
도식 III
여기서 R2는 치환 또는 비치환된 알킬기, 치환 또는 비치환된 방향족기이고, 이는 아릴기, 또는 치환된 에테르일 수 있고; R3은 치환 또는 비치환된 알킬 또는 치환 또는 비치환된 아릴기이고; R4는 치환된 알킬(예를 들면, 하이드록실 또는 카르복실레이트기 등으로 치환된) 또는 비치환된 알킬 또는 치환되거나 비치환된 아릴기이다. 예를 들면, 알콜, 포스핀산, 포스폰산 또는 설폰산과 같은 일부 펜던트 공여체는 특정 pH 값에서 또는 Fe(III)와 복합체화될 때 탈양성자화될 수 있다. 이러한 양성자화된 및 탈양성자화된 형태는 본 개시 내용의 범위 내이다. 예를 들면, 펜던트 공여체는 도식 IV에 나타낸 바와 같은 알콕사이드, 포스피네이트, 포스포네이트 또는 설포네이트일 수 있다.
도식 IV - 이온화기
특정 양태에서, 도식 I 및 II에서 상기 매크로사이클의 R1 기(배위 보조기 또는 비-배위 보조기일 수 있음)는 도식 V에 따른 구조일 수 있고,
도식 V
여기서, A 및 A'는 각각 독립적으로 선형 또는 분지형 구조의 치환 또는 비치환된 C1 내지 C12 알킬기 또는 양성자이고, Q1은 음이온성기로 치환된 아릴(예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스피네이트), 음이온성기로 치환된 알킬기(예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스피네이트) 또는 음이온성기로 치환된 아랄킬기 (예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스피네이트)이고; 여기서, A 또는 A' 중 적어도 하나는 음이온성기로 치환된 알킬기이다(예를 들면, 아미노산, 특히 글리신, 세린 또는 아스파르트산). 아미노 포스핀산 및 포스페이트 에스테르가 바람직하다.
하나의 양태에서, Q1은 아랄킬이고, 상기 아랄킬기의 알킬 부분은 메틸(C1)이다.
일부 양태에서, 도식 V의 펜던트 공여체(예를 들면, 도식 I 및 II에서 R1)는 Fe(III) 중심을 배위하지 않는다. 임의의 특정 이론에 얽매이지 않고, 이들 펜던트는 복합체 상의 전하를 조절하여, 혈청 알부민에 결합을 증진하는 작용을 하는 것으로 간주된다. 다른 양태에서, 도식 V의 펜던트 공여체(예를 들면, 도식 I 및 II에서 R1)는 중심을 배위한다.
앞서 언급한 바와 같이, 예를 들면 알코올, 설폰산, 포스핀산 또는 포스폰산과 같은 일부 펜던트 공여체는 Fe(III)와 복합체화되거나 pH가 더 염기성으로 만들어짐에 따라 용액에서 탈양성자화될 수 있다. 이의 상응하는 알콕사이드, 설포네이트, 포스피네이트, 포스포네이트는 본 개시 내용의 범위 내이다.
특정 펜던트는 하나 이상의 N 또는 O 공여체 원자(예: 트리아졸 또는 포스포네이트 또는 포스피네이트)를 가질 수 있지만, 일반적으로 오직 하나가 금속 이온에 배위된다.
하나 이상의 펜던트 공여체가 존재할 때, 이들은 동일하거나 상이할 수 있다. 다양한 예에서, 하나 이상의 펜던트 공여체가 존재할 때, 개별 펜던트는 동일하거나 상이할 수 있다.
매크로 화합물은 하나 이상의 보조 펜던트기를 포함할 수 있다. 보조 펜던트 기(들)은 하나 이상의 배위 보조 펜던트기 및/또는 하나 이상의 비-배위 보조 펜던트 기일 수 있다.
비-배위 보조 펜던트기는, Fe(III) 금속 이온에 결합하여 5원 또는 6원 킬레이트를 형성할 수 있는 헤테로원자를 가지지 않는다. 비-배위 보조 펜던트기의 비제한적인 예는 벤질기, 페닐기, 및 다른 방향족(예를 들면, 아릴)기 (방향족기에 부착되는 하나 이상의 메틸렌기를 가지거나 메틸렌기 없는 기), 알킬기(분지형 및 선형 기) 등을 포함한다. 비-배위 보조 펜던트기의 다른 비제한적인 예는 비페닐, 나프틸, 안트라세닐, 피리딜, 퀴놀릴, 메틸, 에틸, 이소프로필, n-프로필, 에틸 메톡시에테르, PEG 유도체(폴리에틸렌글리콜) 등을 포함한다.
배위 보조 펜던트기(예를 들면, 2개가 하이드록실 프로필, 포스피네이트 또는 포스포네이트일 때 세번째 펜던트기)의 비제한적인 예는, 예를 들면 아미드, 카르복실레이트, 알콜 또는 페놀, 또는 트리아졸의 유도체, 이미다졸, 피라졸, 피콜릴, 피리딘, 알킬아민, 아미노피리딘, 아미노페놀, 아닐린 등과 같은 5원 또는 6원 킬레이트를 형성하는 산소 또는 질소 공여체를 포함한다. 이들 기들의 일부는 Fe(III)와 결합될 때 탈양성화될 수 있다.
하나 이상의 비-배위 보조 펜던트기를 포함하는 매크로사이클릭 복합체는 내권 물 분자(들), 하이드록사이드(들), 또는 이의 조합일 수 있는 하나 이상의 개방 배위 부위(들)(개방 배위 결합을 가짐)를 가질 수 있다. 하나 이상의 배위 보조 펜던트기를 포함하는 매크로사이클릭 복합체는 개방 배위 부위(폐쇄된 배위 결합(closed coordination)을 가짐)를 갖지 않을 수 있다. 폐쇄된 배위 결합 또는 개방 배위 결합의 경우, 매크로사이클 복합체는 두번째 구체 물 분자(들)(second sphere water molecule(s))을 가질 수 있다.
다양한 예에서, 매크로사이클 코어는 2개 또는 3개의 질소원자, 0개 또는 1개의 산소원자, 및/또는 0개 또는 1개의 황원자를 가질 수 있다. 예를 들면, 매크로사이클릭 코어는 6개, 7개, 8개 또는 9개의 탄소를 가질 수 있다. 예를 들면, 매크로사이클릭 코어는 이들 사이의 모든 범위 및 정수를 포함하여 9 내지 12개의 원자를 가질 수 있고, 매크로사이클릭 코어 내의 원자들 중 적어도 하나는, 예를 들면 N과 같은 헤테로원자이다. 다른 양태에서, 매크로사이클릭 코어 내의 원자들 중 적어도 2개는, 예를 들면 N과 같은 헤테로원자이다. 다양한 예에서, 매크로사이클릭 코어 내의 헤테로원자를 분리하는 2개 또는 3개의 탄소원자가 존재한다. 매크로사이클릭 코어의 하나 이상의 탄소는 비치환되거나(예를 들면, -CH2-) 치환되고(예를 들면, -CHR- 또는 -CHRR-), 단 매크로사이클릭 코어의 적어도 하나의 탄소는 펜던트 공여체로 치환된다. 예를 들면, 이들은 본 명세서에 개시된 치환체로 치환될 수 있다. 다른 양태에서, 매크로사이클릭 코어는 각각 독립적으로 N 또는 O이고 적어도 2개의 탄소 원자에 의해 서로 분리된 적어도 2개의 헤테로원자를 포함한다.
일부 양태에서, 펜던트기는 매크로사이클릭 코어에(예를 들면, 질소에) 공유 부착된다: 특히 TACN (I)의 경우.
매크로사이클릭 화합물의 비제한적인 예는 하기 도식 VI 및 VII에 도시된다:
일부 양태에서, 상기 매크로사이클 화합물이 도식 II의 구조(I)을 가지고, Z1 및 Z2는 도식 III의 구조 6 - 이때 R3은 비치환된 에틸임- 인 경우, Z3은 도식 III의 구조 6 - 이때 Z3은 비치환된 에틸기임- 이 아니다. 추가 양태에서, 상기 매크로사이클 화합물이 도식 II의 구조(I)을 가지고, Z1 및 Z2는 도식 III의 구조 6 - 이때 R3은 비치환되거나 치환된 에틸임- 인 경우, Z3은 도식 III의 구조 6 - 이때 R3은 비치환되거나 치환된 에틸기임- 이 아니다. 추가된 양태에서, 상기 매크로사이클 화합물이 도식 II의 구조(I)을 가지고, Z1 및 Z2는 도식 III의 구조 6 - 이때 R3은 비치환된 알킬임- 인 경우, Z3은 도식 III의 구조 6 - 이때 R3은 비치환된 알킬임- 이 아니다. 또 다른 양태에서, 상기 매크로사이클 화합물이 도식 II의 구조(I)을 가지고, Z1 및 Z2는 도식 III의 구조 6 - 이때 R3은 비치환되거나 치환된 알킬임- 인 경우, Z3은 도식 III의 구조 6 - 이때 R3은 비치환되거나 치환된 알킬임- 이 아니다.
특정 양태에서, 상기 매크로사이클이 도식 II의 구조(I)을 가지고, Z1 및 Z2는 도식 III의 구조 7인 경우, Z3은 도식 III의 구조 7이 아니다.
특정 양태에서, 상기 매크로사이클이 도식 II의 구조(I)을 가지고, Z1 및 Z2는 도식 III의 구조 8 - 이때 R3은 말단 하이드록실 치환체를 갖는 알킬임- 인 경우, Z3은 도식 III의 구조 8 - 이때 R3은 말단 하이드록실 치환체를 갖는 알킬이 아님- 이 아니다. 추가 양태에서, 상기 매크로사이클이 도식 II의 구조(I)을 가지고, Z1 및 Z2는 도식 III의 구조 8 - 이때 R3은 치환된 알킬임- 인 경우, Z3은 도식 III의 구조 8 - 이때 R3은 치환된 알킬임- 이 아니다.
일부 양태에서, 상기 매크로사이클이 도식 II의 구조(II)을 가지고, Z1 및 Z2는 도식 III의 구조 8 - 이때 R4는 말단 하이드록실 치환체를 갖는 알킬임- 인 경우, R1은 말단 아릴기를 갖는 알킬이 아니다. 추가 양태에서, 상기 매크로사이클이 도식 II의 구조(II)을 가지고, Z1 및 Z2는 도식 III의 구조 8 - 이때 R4는 말단 하이드록실 치환체를 갖는 알킬임- 인 경우, R1은 치환된 알킬이 아니다.
특정 양태에서, Fe(III)은 매크로사이클에 복합체화된다. 다른 양태에서, Fe(III)은 매크로사이클에 복합체화되지 않는다. Fe(III)는 본 명세서에서 나타내는 매크로사이클에 복합체화될 수 있다.
임의의 특정 이론에 얽매이지 않고, Fe(III)에 결합될 때, 본 명세서에 기재된 매크로사이클이 3가 철(Fe(III)) 상태를 안정화시킬 수 있는 것으로 간주된다. 배위 기하학은, 예를 들면 생물학적으로 관련된 조건 하에서 Fe(III) 산화 상태를 유지하기 위해 Fe(II)와 비교하여 Fe(III)의 바람직한 결합을 위해 고안되었다. 또한, Fe(III) 상태의 안정화(Eo < 0 mV vs. NHE)는 복합체의 Fe(II) 상태로의 환원을 통해 발생하는 활성 산소 종의 생성을 억제하는 역할을 한다.
Fe(III) 중심은 Fe(III)에 비해 안정화되어, 생물학적 환원제와 반응하여 반응성 산소 종(ROS)을 생성하지 않는 것이 바람직하다. 이러한 산화 환원-비활성 Fe(III) 중심은 NHE에 대해 음의 산화 환원 전위를 갖는다. 안정화된 Fe(III)를 생성하는 매크로사이클릭 코어 및 펜던트 기를 갖는 본 발명의 매크로사이클릭 복합체의 예는 Fe(III)의 결합 시 탈양성자화되는 1,4,7-트리아자사이클로노난 매크로사이클릭 코어 및 알코올 펜던트 기를 포함하지만 이에 제한되지 않는다.
다양한 예에서, 본 개시 내용의 매크로사이클릭 화합물 또는 화합물은 생물학적으로 적절한 pH(예를 들면, pH 6.5-7.5 또는 7.2-7.4)의 수용액에서 일반 수소 전극(NHE)에 대한 0 mV 미만의 환원 전위(Eo)를 나타낸다. 다양한 다른 예에서, 본 개시 내용의 매크로사이클릭 화합물 또는 화합물은 생물학적으로 적절한 pH(예를 들면, pH 6.5-7.5 또는 7.2-7.4)의 수용액에서 일반 수소 전극(NHE)에 대한 적어도 -100, 적어도 -150, 적어도 -200, 적어도 -300, 적어도 -400, 적어도 - 500, 또는 적어도 -600 mV의 환원 전위(Eo)를 나타낸다. 다양한 다른 예에서, 본 개시 내용의 매크로사이클릭 화합물 또는 화합물은 생물학적으로 적절한 pH(예를 들면, pH 6.5-7.5 또는 7.2-7.4)의 수용액에서 일반 수소 전극(NHE)에 대한 0 미만, -100보다 더 음(negative)인, -150보다 더 음인, -200보다 더 음인, -300보다 더 음인, -400보다 더 음인, -500보다 더 음인, 또는 -600 mV보다 더 음인 환원 전위(Eo)를 나타낸다.
다양한 다른 예에서, 본 개시 내용의 매크로사이클릭 화합물 또는 화합물은 생물학적으로 적절한 pH(예를 들면, pH 6.5-7.5 또는 7.2-7.4)의 수용액에서 일반 수소 전극(NHE)에 대한 0 미만 내지 -600 mV의 환원 전위(Eo)를 나타낸다. 다양한 다른 예에서, 본 개시 내용의 매크로사이클릭 화합물 또는 화합물은 생물학적으로 적절한 pH(예를 들면, pH 6.5-7.5 또는 7.2-7.4)의 수용액에서 일반 수소 전극(NHE)에 대한 0 내지 -600 mV의 환원 전위(Eo)를 나타낸다.
물 양성자의 T1 이완 시간의 단축, T1 이완성(relaxivity)은 내권 물과 외권 물 모두에 의해 촉진된다. 따라서, 다양한 예에서, 본 개시 내용의 매크로사이클릭 복합체 및 화합물은, 예를 들면 산소 또는 질소와 같은 헤테로원자를 통해 물에 수소 결합할 수 있는 하나 이상의 펜던트 공여체 기를 포함한다. 이러한 펜던트 도너 기의 비제한적인 예는 알콕시드 기로 탈양성자화하는 펜던트 알코올 기, 포스피네이트, 및 두번째 구체 물에 수소 결합을 형성하는 포스포네이트이다. 또한, 다양한 예에서, 본 개시 내용의 매크로사이클릭 화합물 및 화합물은 물에 결합하기 위해 개방 배위 부위를 포함한다. 이러한 물 리간드는, 예를 들면 pH-전위차 적정법에 의해 나타내는 바와 같이 중성 pH에서 이온화하여 하이드록사이드 리간드를 형성할 수 있다. 물 리간드가 빠르게 교환되는 것이 바람직할 수 있다. 물 리간드를 빠르게 교환한다는 증거는 다양한 온도 17O NMR 분광학 연구에 의해 보여진다. 감소된 가로 이완 시간(T2r)은 17O 공명의 선폭 측정에 의해 근사화된다.
Fe(III)의 배위 화학물질은 배위 수에 따라 달라진다. 본 개시 내용의 화합물은 매크로사이클 공여체라고도 하는 매크로사이클릭 코어의 일부일 수 있는 공여체기를 가지며, 펜던트(또는 펜던트) 공여체라고도 하는 매크로사이클릭 코어 상의 치환체의 일부일 수 있다. 하나의 양태에서, Fe(III)가 본 개시 내용의 화합물과 복합체화되는 경우, 4 내지 7개의 공여체는 금속 이온 중심에 복합체화될 수 있다. 하나의 양태에서, 매크로사이클릭 코어는 이들의 모든 조합을 포함하여 2 내지 4개의 공여체 및 1 내지 4개(예를 들면, 2 내지 4개)의 펜던트 공여체를 가질 수 있다. 다양한 양태에서, 2개의 매크로사이클 공여체 및 3개의 펜던트 공여체, 2개의 매크로사이클 공여체 및 4개의 펜던트 공여체, 3개의 매크로사이클 공여체 및 1개의 펜던트 공여체, 3개의 매크로사이클 공여체 및 2개의 펜던트 공여체, 3개의 매크로사이클 공여체 및 3개의 펜던트 공여체가 존재한다.
도식 VIII은 본 개시 내용의 범위 내인 일부 매크로사이클릭 복합체(Fe(III)를 갖는)를 제공한다.
도식 VIII
본 명세서에서 사용되는, 매크로사이클릭 복합체는 Fe(III)와 복합체화되는 매크로사이클릭 화합물을 말한다. 매크로사이클릭 복합체의 일부 양태에서, 매크로사이클이 도식 II의 구조(I)를 가지고, Z1 및 Z2는 도식 III의 구조 5인 경우, Z3은 도식 III의 구조 5가 아니다.
매크로사이클릭 복합체의 일부 양태에서, 매크로사이클이 도식 II의 구조(I)를 가지고, Z1 및 Z2는 도식 III의 구조 8 - 이때 R4는 비치환된 아릴임- 인 경우, Z3은 도식 III의 구조 8 - 이때 R4는 비치환된 아릴임- 이 아니다.
하나의 양태에서, 본 개시 내용의 화합물은 방향족(예를 들면, 아릴)기, 매크로사이클, 폴리머, 덴드리머, 단백질, 또는 펩티드를 통해 함께 묶이는 하나 이상의 매크로사이클릭 코어를 가질 수 있다.
도식 IX
종양 흡수 및 유지를 위해서, 조영제를 함유하는 분자의 크기가 중요하다. 또한, T1 이완성의 크기는 철 복합체의 수에 비례하여 증가하고, 분자의 크기, 보다 정확하게는 회전 상관 시간(τc)에 따라 증가한다는 점을 감안할 때, 다중 테더링된 매크로사이클릭 복합체의 사용은 조영(contrast)을 증가시켜야 한다. 또한, τc의 증가는 혈액 단백질, 특히 인간 혈청 알부민(HSA)에 결합함으로써 달성될 수 있다. 특정 리간드 작용기는 인간 혈청 알부민(HSA)에 대한 결합을 촉진시킨다. 일반적으로, 이들은 음이온성 기 및 방향족 기(예를 들면, 아릴기)를 함유한다.
다양한 양태에서, 본 개시 내용의 화합물은 염, 부분염, 수화물, 다형체, 또는 본 개시 내용의 입체 이성질체 또는 화합물, 또는 이들의 혼합물이다. 예를 들면, 화합물은 라세미 혼합물, 단일 거울상 이성질체, 단일 부분 입체 이성질체, 또는 부분 입체 이성질체의 혼합물로서 존재할 수 있다. 특정 양태에서, 금속의 복합체화 후, 화합물은 NMR에 의해 결정될 수 있는, 부분 입체 이성질체 및/또는 형태 이성질체로서 존재한다. 부분 입체 이성질체는 매크로사이클릭 코어의 형태와 매크로사이클릭 코어 상의 치환체의 방향성으로부터 발생한다.
본 개시 내용의 화합물은 내권 물 또는 대안적으로, 하이드록사이드 리간드를 가질 수 있다. 하나의 양태에서, 화합물은 방정식 1에서와 같은 이완성에 기여하는 하나의 내권 리간드(q)를 갖는다.
r1 = r1 SS + r1 IS 방정식 1
방정식 1은, 이완성이 결합된 물(내권, IS) 및 두번째-구체(SS) 및 (외권) 물로부터의 기여를 갖는 것을 보여준다. 방정식 2는, 더 많은 수의 결합된 물 분자 및 빠른 리간드 교환 속도 상수(결합된 물(τm)에 대한 짧은 수명)가 유리할 것을 예측한다. 특히 이완성을 특성화하는데 사용되는 파라미터인 r1은 mM-1s-1의 단위를 가지며, T1obs (s-1) 대 조영제 농도의 플롯으로부터 얻어진다. 수와 체류 시간이 잘 정의되어 있지는 않지만, 두번째-구체 물에 대해서도 유사한 관계가 존재한다. r1 및 r2 이완성(37 ℃에서 4.7 T의 T1 및 T2 이완 속도 상수로부터)는 표 1에 요약했다.
[표 1] 4.7 Tesla MRI 스캐너 상에서 중성 pH, HEPES 완충액, 37 ℃에서 Fe(III) 복합체의 이완성
표 1에서 특정 복합체의 구조는 하기에 제시된다.
특히, 본 개시 내용의 매크로사이클릭 복합체 또는 화합물의 T1 대 T2 이완성의 비(r1/r2)가 가능한 한 1(통일)에 가까운 것이 바람직하다. 가로 이완성 r2는 정의상 항상 세로 이완성 r1보다 크다. 다양한 바람직한 예에서, 본 개시내용의 Fe(III) 조영제는, 예를 들면 표 1에 나타낸 바와 같이, 1에 가까운 r1/r2 비율을 제공하기 위해 작은 r2를 갖는다. 다양한 예에서, 본 개시 내용의 매크로사이클릭 복합체 또는 화합물은 r1/r2 비가 0.3 내지 1.0이다. 이들 데이터는, 예를 들면 Fe(TOP)와 같은 단핵 복합체에 대한 개방 배위 부위가 없는 복합체와 비교하여, Fe(TASO)에서 TACN 리간드, 알코올 펜던트 및 개방 배위 부위의 바람직함을 보여준다(예를 들면, 표 1 참조). 그러나, 포스포네이트 및 포스피네이트와 같은 펜던트 기는 표 1에서 Fe(TRAP-Ph)로 표시된 것과 같이 r1을 증가시키는 강력한 두번째 구체 상호작용을 가질 것으로 예상된다.
표 1은, Fe(III) 복합체와 물 분자의 상호 작용이 물의 양성자의 이완성을 향상시킬 수 있는 것을 보여준다. 임의의 특정 이론에 얽매이지 않고, 내권 물과 벌크 물의 교환은 양성자 이완성을 위해 중요한 메커니즘인 것으로 간주된다. 그러나, Fe(III)는 Gd(III)보다 훨씬 더 작은 금속 이온이다(각각 0.78 Å vs. 1.25 Å). Gd(III)에 비해 Fe(III)의 결합된 물에서 더 짧은 M-H 거리는, 2개의 금속 이온 복합체에 대해 두번째-구형 대 내권 기여의 상대적인 효능이 상이할 수 있음을 시사한다.
관련 물 (1/T1m)의 상자성 이완에 기여하는 3가지 메커니즘: 스칼라(scalar) (컨택트) 기여, 쌍극자-쌍극자 기여 및 퀴리 스핀 이완(Curie spin relaxation)이 존재한다. 여기서 고려되는 세로 이완에 대해 이들 중 가장 중요한 것은 쌍극자-쌍극자 기여(1/T1DD)이다. 1.5 T 이상의 전계 강도에서, 1/T1DD는 방정식 3과 같이 정의되고, 여기서 S는 스핀 양자수, ωH는 양성자의 라모 주파수(Larmor frequency), rMH은 금속 이온-양성자 거리, γH는 양성자 자기 회전 비율(proton gyromagnetic ratio), ge는 전자 g 인자, μB는 보어 마그네톤(Bohr magneton), μo는 진공의 유전율이다. 특히, 1/T1DD 항은 Fe(III)보다 Gd(III)를 선호하는 더 큰 총 스핀(S)으로 증가한다(더 높은 이완성). 그러나, 상자성 Fe(III) 중심에서 물 양성자(rMH)까지의 더 짧은 거리는 특히 1/r6 의존성을 고려할 때 Fe(III) 양성자 이완을 선호한다.
쌍극자 이완 메커니즘에 대한 상관 시간(τc)은 결합된 물의 수명(1/τm), 조영제의 회전 운동(1/τR) 및 홀 전자(upaired electron)의 세로 이완(1/T1e)을 포함하여 상이한 과정에 의해 영향을 받는다. 이들 3개의 과정 중 하나가 기여할 수 있지만, 이들의 중요성은 자기장의 강도에 따라 달라진다. 대부분의 문헌은 낮은 전계 강도(<1 T)에서 이러한 과정의 중요성에 초점을 맞추고 있다. 이러한 조건 하에서, 회전 과정 또는 전자 이완 시간이 제한될 수 있으며, τm은 10 ns (kex = 108 s-1)에 가까운 좁은 범위 내여야 한다. 그러나, 높은 전계 강도(≥ 1.5 T)에서, 시뮬레이션은, 최적의 τm이 더 큰 범위(1-100 ns)를 가지고, 회전 운동이 소분자와 단백질 사이의 중간 값을 가져야 함을 보여준다. 중요한 파라미터는 전자 이완 시간인 T1e이다. Fe(III)에 대한 긴 T1e는 대칭도가 높은 복합체에서 기인할 수 있으며, 제로 자기장 분할(zero field splitting)이 거의 없고 전자 상태의 느린 이완이 발생할 수 있다. 또한, 배위 구체는 낮은 스핀 S = ½ Fe(III)가 아닌 높은 스핀(S=5/2)을 선호할 필요가 있다. 또한, Fe(TASO)에 대해 정의된 1H NMR 스펙트럼이 없다는 것은 물 양성자를 효율적으로 이완시키는 고스핀 Fe(III)와도 일치한다(도 6). 또한, 5.8의 용액 유효 자기 모멘트(solution effective magnetic moment) μeff는 S = 5/2 상태와 일치한다.
금속 복합체가 결합된 물이 있는지를 결정하기 위한 연구는 다양한 온도의 17O NMR 데이터 수집을 포함할 수 있다. 도 8의 데이터는 광대역 프로브가 있는 Varian 400MHz NMR 분광기를 사용하여 얻어졌다. 17O 동위원소는 자연 존재비(natural abundance)가 낮기 때문에, 각 복합체는 H2 17O가 풍부한 물 용액에 용해되어, NMR에 의해 측정되는 피크가 더 커서, 시각적으로 더 쉽게 감지할 수 있다. NMR 연구는 다양한 온도에서 수행되었다. Fe(TASO)에 대한 온도 범위는 298 K 내지 340 K였다. 온도 의존 가로 이완성 데이터는, Windows 버전 3.0을 위한 과학자를 사용하여 최소 자승 분석(least squares fit)을 통해 다양한 방정식에 적합했다. 첫째, 개방 배위 부위가 있는 복합체는 방정식 5a에 나타낸 바와 같이 Swift-Connick 방정식을 따르는 것으로 알려져 있다:
상기 방정식 5a에서, 는 감소된 가로 이완 속도이고, Pm은 결합된 물의 몰 분율이며, (Δυobserved - Δυsolvent)는 복합체가 존재하거나 존재하지 않는 H2 17O 사이의 선폭의 차이이다. 관측된 선폭은 NMR 분광법을 사용하여 측정될 수 있고, PM을 미리 계산할 수 있으므로, 이들은 방정식에서 측정 가능한 양이다. 또한, 은 결합된 물 분자의 체류 시간, 는 결합된 물의 가로 이완 속도, 는 결합된 물과 벌크 물 사이의 화학적 이동 차이이다. T2OS는 리간드 원자와 벌크 물의 수소 결합을 고려한 용어이다.
데이터가 기록 및 분석된 온도 범위에서 연구된 복합체에서, 및 는 무시될 수 있으며, 스위프트-코닉(Swift-Connick) 방정식은 방정식 5b로 축소된다. 이와 함께, 감소된 가로 이완 속도는 종종 상당히 크기 때문에, 방정식의 양변에 자연 로그를 취하면, 방정식 5c에 나타낸 바와 같이 데이터의 우수한 스케일링과 더 간단한 표현을 허용한다:
역 결합된 물의 체류 시간 및 결합된 물과 벌크 물 사이의 화학적 이동 차이를 각각 방정식 6a 및 6b로 나타냈다:
방정식 6a에서, kex는 배위 부위에서 물 교환 속도 상수(water exchange rate constant)이고, 결합된 물 체류 시간의 역수이다. kb는 볼츠만 상수(Boltzmann's constant), h는 플랑크 상수(Planck's constant), T는 절대 온도, 및 은 각각 활성화 엔트로피와 엔탈피를 나타낸다. 방정식 6b에서, gL은 등엔트로피(isentropic) 란데 인자(Lande factor)이고, mb는 자기 모멘트이고, S는 총 스핀 상태를 나타내고, B는 인가된 자기장을 나타내고, 는 초미세 결합 상수(hyperfine coupling constant)를 나타낸다. 방정식 6b에서, 등엔트로피 란데 인자, 자기 모멘트, 스핀 상태, 자기장, 및 초미세 결합 상수 용어는 데이터 처리에서 해결되는 단일 파라미터로 통합된다. 이 통합은 방정식 6a를 단순한 역 온도 의존성으로 줄이고, 단순화된 상수는 상수 C로 표시된다. 이 접근 방식은 도 8에 도시되는 바와 같이 Fe(TASO)의 결합된 물에 대한 교환 속도 상수를 연구하는데 사용되었다. 다양한 pH 값에 대한 추가 연구는, 중성 pH에서 내부-구체 리간드(inner-sphere ligand)의 부족을 뒷받침했다(도 13). 이 데이터는 결합된 물이 있는 복합체인 Fe(CDTA)와, 내부-구체 물(inner-sphere wate)이 결여된 복합체인 Fe(DTPA)를 비교했고, Fe(TASO)는 직접적으로 결합된 내부-구체 물이 결여되어 있음을 발견했다. 따라서, T1 이완성은 두번째 구체 및 외권 물 분자에 의해 생성된다.
본 개시 내용의 화합물은 열역학적으로 안정하고/하거나, 해리에 대해 동역학적으로 불활성이다. 하나의 양태에서, 화합물은 열역학적으로 안정하고, 해리에 대해 동역학적으로 불활성이다. 하나의 양태에서, 본 개시 내용의 화합물의 동역학적 불활성은 해리에 대한 속도 상수를 사용하여 기재될 수 있다. 하나의 양태에서, 매크로사이클릭 공여체 및 펜던트 공여체는, 1) 25 mM 카보네이트, 0.40 mM 포스페이트, 100 mM NaCl, pH 7.2의 존재 하에 중성 pH에서 최대 24시간 동안 금속 중심으로부터 상당히 해리되지 않는다.
하나의 양태에서, Fe(III)는 고스핀 S = 5/2이다. 효과적인 T1(세로) 이완을 위해서, 상자성 스핀 상태가 필요하다. Fe(III)를 높은 스핀 상태로 유지하기 위해, 리간드(또는 결정) 자기장 분할이 너무 크지 않아야 한다. 결정 자기장 분할이 짝 에너지(pairing energy)보다 크면, 낮은 스핀(S = ½) 상태가 발생한다. Fe(III)은 특히 음이온성 산소 또는 질소 공여체를 함유하는 다양한 리간드 공여체 기와 함께 고스핀 상자성 상태로 쉽게 유지된다.
Fe(III) 복합체는 3가 산화 상태로 유지되고, 예를 들면 포유동물 세포(예를들면, 인간 세포)와 같은 세포의 세포외 매질에 존재하는 농도에서 퍼옥사이드, 수퍼옥사이드, 아스코르베이트 또는 글루타티온에 의해 환원되지 않는 것이 바람직하다. 일반적으로, NHE에 대해 0 mV보다 더 음인(<0 mV) 산화 환원 전위가 충분하다. 복합체가 Fe(II) 및 Fe(II) 복합체로 환원되고, 복합체가 NHE에 대해 양인 산화 환원 전위를 가지면, 활성 산소 종이 생성될 수 있다. 예를 들면, [Fe(EDTA)]-는 약 300 mV의 산화 환원 전위를 가지며, 도 7의 분석에서 볼 수 있는 바와 같이 ROS를 생성한다.
본 개시 내용의 방법에 사용하기 위해, 본 명세서에 기재된 화합물 또는 복합체는 약제학적 제제로 투여될 수 있다. 따라서, 이들은 다양한 조성물에 제공될 수 있고, 하나 이상의 약제학적으로 허용되는 담체와 혼합될 수 있다. 약제학적으로 허용되는 담체의 일부 예는, Remington: The Science and Practice of Pharmacy (2005) 21st Edition, Philadelphia, PA. Lippincott Williams & Wilkins에서 확인할 수 있다. 이 조성물은 액체, 용액, 또는 고체로 제공될 수 있으며, 캐플릿(caplet), 캡슐, 정제, 흡입제 또는 에어로졸 등을 포함하지만 이에 제한되지 않는 임의의 적합한 전달 형태 또는 운반체와 조합하여 제공될 수 있다.
당업자에게 알려진 다양한 방법이 본 개시 내용의 조성물을 개체에 도입하는데 사용될 수 있다. 이러한 방법은 정맥 내, 근육 내, 두개 내, 척추강 내, 피 내, 피하 및 경구 경로가 포함하지만, 이로 제한되지 않는다. 하나의 양태에서, 조성물은 정맥 내 투여된다.
특정 양태에서, 본 개시 내용의 방법에 사용되는 복합체는 하기 구조를 가질 수 있다:
도식 X
도식 XI
복합체의 필요한 용해도는 생성하는 조영(contrast)에서 이들의 효율에 따라 달라진다. 우수한 이완성이 있는 Fe(III) T1 조영제의 경우에, 복합체는 100 μM-2 mM의 용해도가 필요하다. 그러나, 예를 들면 인간 혈청 알부민(HSA) 또는 메글루민과 같은 다른 첨가제는 용해도를 증가시키거나 이완성을 증가시키는데 사용될 수 있다. 비제한적인 예에서, 시험관 내(in vitro)에서 인간 혈청 알부민에 결합할 때 4.7 Tesla에서 이완성이 적어도 1.5 mM-1 s-1인 조영제는 우수한 이완성을 갖는 것으로 간주될 수 있다. 일부 Fe(III) 복합체에 HSA (35 mg/mL)를 추가하면, 표 1에 표시된 바와 같이 더 큰 T1 이완성을 생성할 수 있다. 그러나, 시험관에서 적당한 이완성을 가진 조영제(0.6 내지 1.4 mM-1s-1)는, 조영제가, 예를 들면 신장 또는 간과 같은 장기와 상호 작용하는 경우, 생체 내(in vivo)에서 우수한 조영(contrast)을 생성할 수 있다. 용해도는 일반적으로 37 ℃에서 25 mM 카보네이트 및 0.4 mM 포스페이트가 있는 100 mM NaCl 중 거의 중성 pH (6.5 내지 7.5)의 수용액에서 측정된다. 사용되는 조성물의 용량은 필수적으로 본 개시 내용의 조성물이 투여될 개체의 필요성에 따라 달라질 것이다. 이러한 요인들은 개체의 체중, 연령, 성별, 및 의학적 히스토리를 포함하지만, 이것으로 필수적으로 제한되지 않는다. 마우스에 행해진 생체 내 MRI 연구로부터의 데이터는 도 9 및 10에 도시된다. 조영제, Fe(TASO)를 0.20 mL의 6.3 mM Fe(TASO)(10.5 mg의 HSA 또는 2당량의 메글루아민)에 주입했다.
하나의 측면에서, 본 개시 내용은 본 명세서에 기재되는 매크로사이클릭 화합물을 사용하여 영상화 방법을 제공한다. 영상화 방법은 자기 공명 영상화 방법을 사용한다. 이러한 방법의 예는 자기 공명 영상(MRI)을 포함하지만, 이에 제한되지 않는다.
구체적으로, 본 개시 내용의 매크로사이클릭 화합물은, Fe(III)와 복합체화될 때, T1 MRI 조영제로서 사용될 수 있다. 이러한 복합체는 pH의 변경과 함께 변화하는 특성을 갖는다. 이러한 특성은, 예를 들면 암, 뇌졸중 및 심장병과 같은 질병의 우수한 치료를 가능하게 하기 위해 이러한 복합체를 pH 매핑에 유용하게 만든다 Fe(III)와 복합체화될 때, 매크로사이클은 T2 MRI 조영제로서 사용될 수도 있다.
본 개시 내용의 영상화 방법은 세포, 조직, 기관, 혈관계, 또는 이들의 일부를 영상화하는데 사용될 수 있다. 세포, 조직, 기관, 혈관계는 개체의 일부일 수 있다. "개체(individual)"는, 인간 또는 동물을 의미한다. 하나의 양태에서, 본 개시 내용은 세포, 조직, 기관, 또는 혈관계 중 적어도 일부의 영상을 수득하는 방법을 제공하고, 상기 방법은, 세포, 조직, 기관, 또는 혈관계를 본 개시 내용의 화합물과 접촉시키는 단계, 및 세포, 조직, 기관, 또는 혈관계의 적어도 일부분을 영상화하여, 세포, 조직, 기관, 또는 혈관계의 일부분의 영상을 수득하는 단계;를 포함한다. 세포, 조직, 기관, 또는 혈관계의 적어도 일부분은 살아 있거나 죽었을 수 있다. 마찬가지로, 개체는 또한 살아있거나 죽었을 수 있다.
하나의 양태에서, 매크로사이클릭 화합물은 Fe(III)와 복합체화되고, T1 MRI 조영제로서 사용될 수 있다. 이러한 조영(contrast)은, 철 복합체가 축적되는 영역에 포지티브한 조영을 제공하기 위해 T1 강조 영상에 의해 생성된다. 복합체는, 벌크 물 양성자의 T1 이완 시간을 감소시키는, 내권 또는 외권 물의 상호 작용에서 생물학적으로 환원되는 조건 하에서의 고스핀 Fe(III)이다.
하기 서술(Statement)은 본 개시 내용의 매크로사이클릭 복합체, 매크로사이클 화합물, 및 영상화 방법의 비제한적인 예를 기술한다:
서술 1: 매크로사이클릭 복합체(macrocyclic complex), 또는 이의 염, 부분염(partial salt), 수화물, 다형체, 또는 입체 이성질체로서,
상기 매크로사이클릭 복합체는,
1,4,7-트리아자사이클로노난(triazacyclononane) (TACN) 모이어티 또는 치환된 TACN 모이어티(예를 들면, O-치환된 TACN 모이어티 또는 S-치환된 TACN 모이어티);
하기:
, 이의 치환된 유사체, 이의 탈양성자화된 유사체(deprotonated analog), 이의 입체 이성질체, 및 이들의 조합으로부터 독립적으로 선택된, 상기 TACN 모이어티 상의 치환체인 하나 이상의 음이온성 펜던트기로, 여기서 R2는 치환 또는 비치환된 알킬기, 치환 또는 비치환된 방향족기이고, 이는 아릴기, 또는 치환된 에테르일 수 있고; R3은 치환 또는 비치환된 알킬 또는 치환 또는 비치환된 아릴기이고; R4는 치환된 알킬(예를 들면, 하이드록실 또는 카르복실레이트기 등으로 치환된) 또는 비치환된 알킬 또는 치환되거나 비치환된 아릴기이고; Q1은 음이온성기로 치환된 아릴(예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스피네이트), 음이온성기로 치환된 알킬기(예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스파이트) 또는 음이온성기로 치환된 아랄킬기(예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스피네이트)인 것인, 하나 이상의 음이온성 펜던트기; 및
i) TACN 모이어티 또는 치환된 TACN 모이어티 및 ii) 매크로사이클릭 화합물의 적어도 하나의 음이온성 펜던트기 치환체(예를 들면, TACN 모이어티 또는 치환된 TACN 모이어티)와 복합체화된 고스핀(high-spin) Fe(III) 양이온;을 포함하는 것인, 매크로사이클릭 복합체.
서술 2: 서술 1에 있어서,
상기 매크로사이클이 도식 II의 구조(I)를 가지고, Z1 및 Z2는 도식 III의 구조 5인 경우, Z3은 도식 III의 구조 5가 아니고; 및/또는
상기 매크로사이클이 도식 II의 구조(I)를 가지고, Z1 및 Z2는 도식 III의 구조 8 - 이때 R4는 비치환된 아릴임 - 인 경우, Z3은 도식 III의 구조 8 - 이때 R4는 비치환된 아릴임 - 이 아닌 것인, 매크로사이클릭 복합체.
서술 3: 서술 1 또는 2에 있어서,
상기 하나 이상의 펜던트기의 적어도 하나 또는 전부는 TACN 모이어티 상의 질소원자에 공유 결합되는 것인, 매크로사이클릭 복합체.
서술 4: 서술 1 내지 3 중 어느 하나에 있어서,
상기 매크로사이클릭 복합체는 적어도 하나의 개방 배위 결합 부위(open coordination site)를 갖는 것인, 매크로사이클릭 복합체.
서술 5: 서술 1 내지 4 중 어느 하나에 있어서,
상기 매크로사이클릭 복합체는 고스핀 Fe(III) 양이온에 복합체화된 적어도 하나의 물 및/또는 적어도 하나의 하이드록사이드를 갖는 것인, 매크로사이클릭 복합체.
서술 6: 서술 1 내지 5 중 어느 하나에 있어서,
적어도 하나의 펜던트기는 벤질 위치 또는 펜던트기의 헤테로원자를 유도하는 알킬기의 임의의 탄소에서 치환되는 것인, 매크로사이클릭 복합체.
서술 7: 서술 1 내지 6 중 어느 하나에 있어서,
상기 매크로사이클릭 복합체는 하나 이상의 보조기(들)(예를 들면, 하나 이상의 배위 펜던트기(들), 하나 이상의 비-배위 펜던트기(들)(non-coordinating pendent group(s)), 또는 이들의 조합)를 포함하는 것인, 매크로사이클릭 복합체.
서술 8: 서술에 있어서,
상기 배위 펜던트기(들) 또는 비-배위 펜던트기(들)는 하기 구조:
를 가지며,
여기서, A 및 A'는 각각 독립적으로 선형 또는 분지형 구조의 치환 또는 비치환된 C1 내지 C12 알킬기 또는 양성자이고, Q1은 음이온성기로 치환된 아릴(예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스피네이트), 음이온성기로 치환된 알킬기(예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스피네이트) 또는 음이온성기로 치환된 아랄킬기 (예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스피네이트)이고; 여기서, A 또는 A' 중 적어도 하나는 음이온성기로 치환된 알킬기이다(예를 들면, 아미노산, 특히 글리신, 세린 또는 아스파르트산). 아미노 포스핀산 및 포스페이트 에스테르가 바람직하다. 일례로서, Q1은 아랄킬이고, 상기 아랄킬기의 알킬 부분은 메틸(C1)인 것인, 매크로사이클릭 복합체.
서술 9: 서술 1 내지 8 중 어느 하나에 있어서,
상기 매크로사이클릭 복합체는,
를 포함하는 것인, 매크로사이클릭 복합체.
서술 10: 서술 1에 있어서,
상기 TACN 모이어티는 하기 구조:
중 하나를 가지며, 여기서 X1, X2, X3은 N이고; W1은 O 또는 S이고; Y1, Y2, Y3은 각각 독립적으로 i) O를 포함하는 펜던트 공여체, 여기서 O는 적어도 하나의 고립 전자쌍, 바람직하게는 2개 또는 3개의 고립 전자쌍(예를 들면, 케톤, 알코올, 알콕사이드, 페놀 또는 페녹사이드, 설폰산, 포스핀산 또는 포스폰산 또는 이들의 탈양성자화된 형태, 예를 들면 알콕사이드 또는 페녹사이드를 포함하는 산화물)을 가지며; 또는 ii) N을 포함하는 펜던트 공여체, 여기서 N은 트리아졸과 같은 적어도 하나의 고립 전자쌍을 가지며; m1, m2 및 m3은 각각 독립적으로 1, 2 또는 3이고; n1, n2, 및 n3은 각각 독립적으로 1 또는 2 또는 3이고; R1은 치환 또는 비치환된 아릴, 치환 또는 비치환된 헤테로사이클릭기 또는 치환 또는 비치환된 알킬이고, 여기서 알킬-Y 사슬의 알킬 세그먼트(알킬-Y1, 알킬-Y2 및/또는 알킬-Y3)는 각각 독립적으로 치환 또는 비치환되는 것인, 매크로사이클릭 복합체.
서술 11: 서술 1 내지 10 중 어느 하나에 있어서,
상기 TACN 모이어티 또는 O-치환된 TACN 모이어티는 하기 구조:
를 가지며,
여기서, R1은 치환 또는 비치환된 아릴, 치환 또는 비치환된 헤테로아릴 또는 치환 또는 비치환된 알킬이고, Z1, Z2, 및 Z3은 독립적으로 음이온성 펜던트기인 것인, 매크로사이클릭 복합체.
서술 12: 서술 11에 있어서,
상기 매크로사이클이 구조 I을 갖는 경우, Z1은 H 또는 도식 III의 펜던트기 중 하나이고, Z2 및 Z3은 각각 독립적으로 도식 III의 펜던트기 중 하나이며; 및/또는
상기 매크로사이클이 구조 II 또는 III을 갖는 경우, Z1 및 Z2는 각각 독립적으로 도식 III의 펜던트기 중 하나이며; 및/또는
전체 구조 I-III에서, 각각의 Z1, Z2, 및 Z3은 적용 가능한 경우 독립적으로 선택되는 것인, 매크로사이클릭 복합체.
서술 13: 서술 1 내지 12 중 어느 하나에 있어서,
상기 TACN 모이어티는 하기 구조 중 하나를 갖는 것인, 매크로사이클릭 복합체:
서술 14: 서술 1 내지 13 중 어느 하나에 있어서, 상기 매크로사이클릭 복합체는 하기 구조들 중 하나를 갖는 것인, 매크로사이클릭 복합체:
서술 15: 연결기(linker group)에 공유 결합된 하나 이상의 펜던트 매크로사이클릭 복합체 기; 또는 폴리머, 덴드리머, 단백질, 또는 펩티드에 공유 결합된 하나 이상의 펜던트 매크로사이클릭 복합체 기를 포함하는 폴리머, 덴드리머, 단백질, 또는 펩티드;를 포함하는 화합물 또는 폴리머로서,
각각의 개별적인 매크로사이클릭 복합체 기는 서술 1 내지 14 중 어느 하나의 매크로사이클릭 복합체로부터 유도되는 것인, 화합물 또는 폴리머.
서술 16: 서술 15에 있어서,
상기 화합물은 하기 구조를 포함하는 것인, 화합물 또는 폴리머:
서술 17: 서술 15에 있어서,
상기 화합물은 하기 구조를 포함하는 것인, 화합물 또는 폴리머:
서술 18: 서술 1-14 중 어느 하나에 기재된 하나 이상의 매크로사이클릭 화합물 및/또는 서술 15-17 중 어느 하나에 기재된 하나 이상의 화합물 또는 폴리머, 및 약제학적으로 허용되는 담체를 포함하는, 조성물.
서술 19: 서술 18에 있어서,
상기 조성물은 인간 혈청 알부민 및/또는 메글루민(meglumine)을 더 포함하는 것인, 조성물.
서술 20: 세포, 기관, 혈관계 또는 조직 중 적어도 일부의 영상을 수득하는 방법으로서, 상기 방법은,
세포, 기관, 혈관계 또는 조직(또는 이의 일부)을 서술 1-14 중 어느 하나에 기재된 하나 이상의 매크로사이클릭 화합물 및/또는 서술 15-17 중 어느 하나에 기재된 하나 이상의 화합물 및/또는 서술 18-19 중 어느 하나에 기재된 하나 이상의 조성물 및/또는 Fe(NOTP) 및/또는 Fe(TRAP-Ph)과 접촉시키는 단계; 및
세포, 기관, 혈관계 또는 조직의 적어도 일부분을 영상화하여, 세포, 기관, 혈관계 또는 조직의 일부분의 영상을 수득하는 단계;를 포함하는데,
상기 영상은 자기 공명을 사용함으로써 수득되는 것인, 방법.
서술 21: 서술 20에 있어서,
상기 세포, 기관, 혈관계 또는 조직은 개체의 일부인 것인, 방법.
서술 22: 서술 20 또는 20에 있어서,
상기 영상은 자기 공명 영상(MRI)을 사용하여 수득되는 것인, 방법.
서술 23: 서술 20 내지 22 중 어느 하나에 있어서,
상기 매크로사이클릭 화합물(들) 및/또는 화합물(들)은 T1 제제 또는 T1 제제들인 것인, 방법.
서술 24: 매크로사이클릭 화합물, 또는 이의 염, 부분염, 수화물, 다형체, 또는 입체 이성질체로서,
상기 매크로사이클릭 화합물은,
1,4,7-트리아자사이클로노난 (TACN) 모이어티 또는 O-치환된 TACN 모이어티; 및
하기:
이의 치환된 유사체, 이의 탈양성자화된 유사체, 이의 입체 이성질체, 및 이들의 조합으로부터 독립적으로 선택된, 상기 TACN 모이어티 상의 치환체인 하나 이상의 음이온성 펜던트기로, 여기서 R2는 치환 또는 비치환된 알킬기, 치환 또는 비치환된 방향족기이고, 이는 아릴기, 또는 치환된 에테르일 수 있고; R3은 치환 또는 비치환된 알킬 또는 치환 또는 비치환된 아릴기이고; R4는 치환된 알킬(예를 들면, 하이드록실 또는 카르복실레이트기 등으로 치환된) 또는 비치환된 알킬 또는 치환되거나 비치환된 아릴기이고; Q1은 음이온성기로 치환된 아릴(예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스피네이트), 음이온성기로 치환된 알킬기(예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스파이트) 또는 음이온성기로 치환된 아랄킬기(예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스피네이트)인 것인, 하나 이상의 음이온성 펜던트기;를 포함하는 것인, 매크로사이클릭 화합물.
서술 25: 서술 24에 있어서,
상기 매크로사이클 화합물이 도식 II의 구조(I)을 가지고, Z1 및 Z2는 도식 III의 구조 6 - 이때 R3은 비치환된 에틸임- 인 경우, Z3은 도식 III의 구조 6 - 이때 Z3은 비치환된 에틸기임- 이 아니고; 및/또는
상기 매크로사이클 화합물이 도식 II의 구조(I)을 가지고, Z1 및 Z2는 도식 III의 구조 6 - 이때 R3은 비치환되거나 치환된 에틸임 - 인 경우, Z3은 도식 III의 구조 6 - 이때 R3은 비치환되거나 치환된 에틸기임 - 이 아니고; 및/또는
상기 매크로사이클 화합물이 도식 II의 구조(I)을 가지고, Z1 및 Z2는 도식 III의 구조 6 - 이때 R3은 비치환된 알킬임- 인 경우, Z3은 도식 III의 구조 6 - 이때 R3은 비치환된 알킬임- 이 아니고; 및/또는
상기 매크로사이클 화합물이 도식 II의 구조(I)을 가지고, Z1 및 Z2는 도식 III의 구조 6 - 이때 R3은 비치환되거나 치환된 알킬임- 인 경우, Z3은 도식 III의 구조 6 - 이때 R3은 비치환되거나 치환된 알킬임- 이 아니고; 및/또는
상기 매크로사이클이 도식 II의 구조(I)을 가지고, Z1 및 Z2는 도식 III의 구조 7인 경우, Z3은 도식 III의 구조 7이 아니고; 및/또는
상기 매크로사이클이 도식 II의 구조(I)을 가지고, Z1 및 Z2는 도식 III의 구조 8 - 이때 R3은 말단 하이드록실 치환체를 갖는 알킬임- 인 경우, Z3은 도식 III의 구조 8 - 이때 R3은 말단 하이드록실 치환체를 갖는 알킬이 아님- 이 아니고; 및/또는
상기 매크로사이클이 도식 II의 구조(I)을 가지고, Z1 및 Z2는 도식 III의 구조 8 - 이때 R3은 치환된 알킬임- 인 경우, Z3은 도식 III의 구조 8 - 이때 R3은 치환된 알킬임- 이 아니고; 및/또는
상기 매크로사이클이 도식 II의 구조(II)을 가지고, Z1 및 Z2는 도식 III의 구조 8 - 이때 R4는 말단 하이드록실 치환체를 갖는 알킬임- 인 경우, R1은 말단 아릴기를 갖는 알킬이 아니고; 및/또는
상기 매크로사이클이 도식 II의 구조(II)을 가지고, Z1 및 Z2는 도식 III의 구조 8 - 이때 R4는 말단 하이드록실 치환체를 갖는 알킬임- 인 경우, R1은 치환된 알킬이 아닌 것인, 매크로사이클릭 화합물.
서술 26: 서술 24 또는 25에 있어서,
상기 하나 이상의 펜던트기의 적어도 하나 또는 전부는 TACN 모이어티 상의 N에 공유 결합되는 것인, 매크로사이클 화합물.
서술 27: 서술 24 내지 26 중 어느 하나에 있어서,
상기 펜던트기의 적어도 하나는 벤질 위치 또는 펜던트기의 헤테로원자를 유도하는 알킬기의 임의의 탄소에서 치환되는 것인, 매크로사이클 화합물.
서술 28: 서술 24 내지 27 중 어느 하나에 있어서,
상기 매크로사이클은 하나 이상의 보조기(들)(예를 들면, 하나 이상의 배위 펜던트기(들), 하나 이상의 비-배위 펜던트기(들), 또는 이들의 조합)을 더 포함하는 것인, 매크로사이클 화합물.
서술 29: 서술 28에 있어서,
여기서, A 및 A'는 각각 독립적으로 선형 또는 분지형 구조의 치환 또는 비치환된 C1 내지 C12 알킬기 또는 양성자이고, Q1은 음이온성기로 치환된 아릴(예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스피네이트), 음이온성기로 치환된 알킬기(예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스피네이트) 또는 음이온성기로 치환된 아랄킬기 (예를 들면, 카르복실레이트, 설포네이트, 포스포네이트, 포스페이트 에스테르 또는 포스피네이트)이고; 여기서, A 또는 A' 중 적어도 하나는 음이온성기로 치환된 알킬기이다(예를 들면, 아미노산, 특히 글리신, 세린 또는 아스파르트산). 아미노 포스핀산 및 포스페이트 에스테르가 바람직하다. 일례로서, Q1은 아랄킬이고, 상기 아랄킬기의 알킬 부분은 메틸(C1)인 것인, 매크로사이클릭 화합물.
서술 30: 서술 24 내지 29 중 어느 하나에 있어서,
상기 매크로사이클이 하기 구조:
중 하나를 가지며, 여기서 X1, X2, X3은 N이고; W1은 O 또는 S이고; Y1, Y2, Y3은 각각 독립적으로
i) O를 포함하는 펜던트 공여체, 여기서 O는 적어도 하나의 고립 전자쌍, 바람직하게는 2개 또는 3개의 고립 전자쌍(예를 들면, 케톤, 알코올, 알콕사이드, 페놀 또는 페녹사이드, 설폰산, 포스핀산 또는 포스폰산 또는 이들의 탈양성자화된 형태, 예를 들면 알콕사이드 또는 페녹사이드를 포함하는 산화물)을 가지며; 또는
ii) N을 포함하는 펜던트 공여체, 여기서 N은 트리아졸과 같은 적어도 하나의 고립 전자쌍을 가지며; m1, m2 및 m3은 각각 독립적으로 1, 2 또는 3이고; n1, n2, 및 n3은 각각 독립적으로 1 또는 2 또는 3이고; R1은 치환 또는 비치환된 아릴, 치환 또는 비치환된 헤테로사이클릭기 또는 치환 또는 비치환된 알킬이고, 여기서 알킬-Y 사슬의 알킬 세그먼트(알킬-Y1, 알킬-Y2 및/또는 알킬-Y3)는 각각 독립적으로 치환 또는 비치환되는 것인, 매크로사이클릭 화합물.
서술 31: 서술 24 내지 30 중 어느 하나에 있어서,
상기 매크로사이클이 하기 구조:
를 가지며,
여기서, R1은 치환 또는 비치환된 아릴, 치환 또는 비치환된 헤테로아릴 또는 치환 또는 비치환된 알킬이고, Z1, Z2, 및 Z3은 독립적으로 음이온성 펜던트기이고,
상기 매크로사이클은 구조 I을 가지며, Z1은 H 또는 도식 III의 펜던트기 중 하나이고, Z2 및 Z3은 각각 독립적으로 도식 III의 펜던트기 중 하나이며; 또는
상기 매크로사이클은 구조 II 또는 III을 가지며, Z1 및 Z2는 각각 독립적으로 도식 III의 펜던트기 중 하나이며; 및/또는
전체 구조 I-III에서, 각각의 Z1, Z2 및 Z3은 적용 가능한 경우 독립적으로 선택되는 것인, 매크로사이클릭 화합물.
서술 32: 서술 24 내지 31 중 어느 하나에 있어서,
상기 매크로사이클은 하기 구조를 갖는 것인, 매크로사이클 화합물:
본 출원에서, 단수 형태는 복수를 포함하고, 그 반대도 마찬가지이다.
본 개시 내용의 매크로사이클릭 화합물은, 예를 들면 실험 세부 사항에 기재된 바와 같이 제조될 수 있다. 하기 실시예는 본 개시내용을 예시하기 위해 제시된다. 이들은 어떤 식으로든 제한하기 위한 것이 아니다. 당업자는 본 개시내용의 범위 내에 있도록 의도된 이러한 양태에 대한 일상적인 변형이 이루어질 수 있음을 인식할 것이다.
본 명세서에 개시된 다양한 양태 및 실시예에 기재된 방법의 단계는 본 개시내용의 방법을 수행하기에 충분하다. 따라서, 하나의 양태에서, 방법은 필수적으로 본 명세서에 개시된 방법의 단계의 조합으로 구성된다. 다른 양태에서, 방법은 이러한 단계들로 구성된다.
실험 세부 사항
기기. FTS 시스템 TC-84 키네틱 에어 젯 온도 조절기가 장착된 Varian Inova 500 MHz NMR 분광기를 사용하여 1H NMR 데이터를 수집했다. 75 MHz에서 작동하는 Varian Mercury 300 MHz NMR 분광계를 사용하여 13C NMR 스펙트럼을 획득했다. 54.24 MHz의 공명 주파수에서 작동하는 5mm 광대역 프로브가 장착된 Varian Inova 400MHz 분광계에서 17O NMR 스펙트럼을 기록했다. 모든 pH 측정은 702 SM Titrino pH에 연결된 Orion 8115BNUWP Ross Ultra Semi Micro pH 전극을 사용하여 얻었다. Surveyor HPLC 시스템이 장착된 ThermoFinnigan LCQ Advantage IonTrap LC/MS를 사용하여 질량 스펙트럼 데이터를 수집했다. Peltier 온도 조절기가 장착된 Beckman-Coulter DU 800 UV-vis 분광 광도계를 사용하여 흡광도(absorbance) 스펙트럼을 수집했다. 1% H2 17O가 포함된 물에서 샘플을 준비했다. 대칭 물 피크(symmetric water peak)의 절반 높이에서의 선폭과 화학적 이동은 다양한 온도 및 pH 6에서 금속 복합체의 부재 및 존재 하에 결정되었다. 가변 온도에서 금속 복합체의 부재 및 존재 시 신호의 절반 높이에서의 선폭을 사용하여 Swift-Connick 방정식(방정식 5-6)을 사용하여 가로 이완 시간을 계산했다. 모든 피팅은 측정된 데이터의 동시 최소 제곱 t에서부터이다.
TASO. 가스 주입구 및 교반 막대(stir bar)가 있는 25 mL 둥근 바닥 플라스크에 4 mL 톨루엔 1 mL 클로로포름 용액 중 0.100 g TACN (1,4,7-트리아자사이클로노난) (0.774 mmol)를 첨가했다. 0.0920 g N,N-디메틸포름아미드 디메틸아세탈 (0.774 mmol)을 플라스크에 첨가했다. 용액을 실온에서 24시간 동안 교반했다. 1,4,7-트리아자트리사이클로[5.2.1.04,10]데칸 (TACN-오르토아미드)의 ESI-MS (m/z), 계산치: 140.1 [M + H+] (100%). 용액을 회전 증발기 상의 플라스크에 놓아 건조시켰다. 건조된 TACN-오르토아미드 및 15 mL 건조 테트라하이드로푸란(THF)을 자기 교반 막대, 리플럭스 응축기, 가스 유입관 및 첨가 깔때기가 장착된 50 mL 3구 둥근 바닥 플라스크에 첨가했다. 92.2 μL 벤질 브로마이드 (0.774 mmol)를 플라스크에 첨가하고, 용액을 실온에서 밤새 교반했다. 백색-베이지색 침전물을 흡인 여과법으로 수집하고, 건조 THF(10 mL) 및 디에틸 에테르(10 mL)로 세척했다. 7 mL 메탄올 및 7 mL 12 M HCl을 첨가하여 탈보호 과정에서 플라스크 내에 침전시켰다. 용액을 가열하여, 4시간 동안 리플럭스했다. 용액을 실온으로 냉각한 후, NaOH 펠릿을 첨가하여 용액의 pH를 8로 제공했다. 그 후, 용액을 여과하여 NaCl 염 침전물을 제거하고, 클로로포름(3 x 60 mL)으로 추출했다. ESI-MS (m/z), 계산치: 220.3 [M + H+] (100 %). 용액을 회전 증발시키고, 0.225 g S-프로필렌 옥사이드(3.870 mmol)가 포함된 25 mL 둥근 바닥 플라스크에서 15 mL 에탄올에 용해시키고, 실온에서 24시간 동안 교반했다. 용액을 회전 증발시키고, 진공 하에서 Schlenk 라인에서 건조시키고, 10 mL 메탄올에 용해시켰다. % ESI-MS(m/z), 계산치: 336.3 [M + H+](100%). 벤질 탈보호는 Pd/C(10%) 촉매에 의해 수행했다. 5 mL 메탄올 및 1 mL 물 중 30 mg Pd/C(10%)를 리간드 용액에 첨가했다. 아르곤 가스 하에서 30분 동안 용액으로부터 공기를 제거했다. 촉매 수소화 반응은 수소 분위기 하에 실온에서 격렬하게 교반하면서 3일 동안 수행했다. 혼합물을 셀라이트 상에서 여과하여, 반응 용액으로부터 촉매를 제거하여, (1,4,7-트리아조난-1,4-디일)비스(프로판-2-올)(DACO 리간드)를 얻었다. ESI-MS(m/z), 계산치: 246.3 [M + H+](100%). 용액을 회전 증발기 상에서 플라스크를 놓아 건조시켰다. DACO 리간드를 25 mL 둥근 바닥 플라스크에서 15 mL 아세토니트릴에 용해시켰다. 3 mL 아세토니트릴 중 1당량의 1,3 프로판설톤 및 N,N-디이소프로필에틸아민(DIEA)을 플라스크에 첨가했다. 용액을 리플럭스 하에서 3일 동안 교반했다. 용액을 회전 증발시키고, 진공 하에서 Schlenk 라인에서 건조시켰다. 정제 공정은 MeOH/DCM 용매가 있는 염기성 알루미나 컬럼에 의해 적용했다. 수율은 37%로 계산되었다. ESI-MS(m/z)(0.1% 포름산 방법), 계산치: 368.3 [M + H+](100%) 및 390.3 [M + Na+](27%).
Fe(TASO) (예를 들면, 도 1 참조). 교반 막대기를 포함하는 25 mL 둥근 바닥 플라스크에, TASO 리간드 (0.0589 g, 0.160 mmol) 및 8 mL 에탄올을 첨가했다. 그 후, FeCl2·4H2O (0.0318 g, 0.160 mmol)를 2 mL 에탄올에 용해하고, 플라스크에 첨가했다. 용액을 실온에서 2일 동안 교반했다. 황색 침전물을 수득했다. 침전물을 원심분리로 얻고, 디에틸 에테르로 3시간 동안 세척했다. 황색 분말을 회전 증발을 통해 용매를 제거함으로써 얻었다. ESI-MS (m/z), 계산치: 421.1 [M+H+] (100 %) and 443.2 [M+Na+] (55%). 여기서, M은 중성 형태의 Fe(TASO)이다. Fe(TASO)의 자화율(Magnetic susceptibility)은 에반법(Evans' method)을 사용하여 측정한 수용액에서 5.67 μeff이다.
NOTPMe. (예를 들면, 도 4 참조). 1,4,7-트리아자사이클로노난 (3.1 mmol)을 2구 플라스크에 첨가했다. 파라포름알데히드 (15.4mmol, 5 당량) 및 트리에틸 포스파이트 ((31mmol, 10 당량)을 아르곤 분위기 하에서 첨가했다. 반응물을 12시간 동안 60 ℃에서 교반시켰다. 과량의 반응물은 감압 하에서 제거했다. 0.50g의 생성된 물질(헥사에틸((1,4,7-트리아조난-1,4,7-트리일)트리스(메틸렌))트리스(포스포네이트))을 2.5mL의 H2O를 함유하는 플라스크에 칭량했다. 1.25g의 소듐 하이드록사이드 펠릿을 첨가하고, 소듐 하이드록사이드가 모두 용해될 때까지 혼합물을 교반했다. 일단 용해되면, 혼합물을 15분 동안 리플럭스한 후, 플라스크를 장치에서 제거하고, 제거 즉시 3mL의 H2O를 첨가한 후, 실온으로 냉각시켰다. 실온에 도달된 후, 플라스크를 15분 동안 얼음에서 냉각시켰고, 이 시간 동안 결정이 형성되기 시작했다. 용매를 제거한 후, 결정을 물, 에탄올과 에틸에테르의 1:1 혼합물로 세척했다. ESI-MS: 494 [M-H+], 516 [M+Na+]. 여기서, M은 중성 리간드(NOTPMe)이다.
Trap-H 합성(예를 들면, 도 3 참조). 트리아자사이클로노난(500 mg, 3.87 mmol) 및 파라포름알데히드(527 mg, 17.5 mmol)를 수(18.75 mL) 중 차아인산(2.5 mL의 50% 중량 수용액, 23.2 mmol)에 용해하고, 실온에서 48시간 동안 교반했다. 반응 혼합물을 40 ℃ 미만으로 온화하게 가열하면서 진공 하에 증발시켰다. 생성된 오일을 강력한 양이온 교환기, DOWEX 50 H+ 형태에서 물 용리와 함께 정제했다. 순수한 리간드를 함유하는 분획(LCQ에 대한 ESI 질량 분석으로 확인됨)을 혼합하고, 40 ℃ 미만에서 부드럽게 가열하면서 용매를 제거하여, 투명한 오일(492 mg, 35%)을 얻었다. MS(ESI, 양성): m/z 364[(TRAP-H)+H+].
TRAP-Ph 합성 (예를 들면, 도 2 참조). 1,4,7-트리아자사이클로노난 (0.30mmol)을 아르곤 분위기 하에서 리플럭스 장치에 부착된 2구 플라스크에 첨가했다. 그 후, 디메틸 페닐포스포나이트 (1.35mmol, 4.5 당량) 및 파라포름알데히드 (1.8mmol, 6 당량)를 15mL의 건조 테트라하이드로푸란과 함께 플라스크에 첨가했다. 용액을 16시간 동안 리플럭스했다. 그 후, 과량의 용매를 감압 하에서 제거했다. ESI-MS: 634[M+H+].
그 후, 생성된 TRAP-Ph-메톡시를 4mL의 50% w/v 카보네이트 프리 소듐 하이드록사이드와 함께 이중 다음 플라스크로 옮겼다. 플라스크를 리플럭스 장치에 부착하여, 30분 동안 리플럭스시켰다. 4mL의 증류수를 첨가하고, 용액을 추가 30분 동안 리플러스시켰다. 두번째 리플럭스 후에, 리플럭스 장치를 제거하고, 용매를 2개 층 시스템이 재형성될 때까지 증발시켰다. 그 후, 플라스크의 열을 제거하고, 실온으로 냉각시켰다. 상청액 오일을 제거하고, 에탄올에 용해시켰다. 에탄올을 증발시켜 TRAP-Ph를 남겼다. 생성된 생성물을 메탄올, 이어서 아세톤, 그 후 디클로로메탄에서의 재결정화를 통해 정제했다. ESI-MS: 590 [M+H+]. 여기서, M은 중성 형태의 TRAP-pH이다.
Fe(TRAP-Ph) (예를 들면, 도 2 참조). TRAP-Ph를 메탄올 중 0.01M 철 (III) 나이트레이트의 1 당량과 혼합함으로써 TRAP-P를 철과 복합체화했다. 용액을 4일 동안 실온에서 교반했다. 그 후, 메탄올을 증발시켜, 생성된 생성물을 수득했다. ESI-MS: 645, 667 [M+Na+].
1,4,7-트리아자사이클로노난 (0.15 mmol)을 2구 플라스크로 측정하고, 리플럭스 장치에 설치했다. 플라스크에 0.35mL 염산, 1.0mL의 증류수와 함께 아인산(0.9 mmol, 6 당량)을 추가로 첨가했다. 일단, 이 용액이 리플럭스에 제공되면, 파라포름알데히드(0.675 mmol, 4.5 당량)를 1시간에 걸쳐 용액에 첨가했다. 파라포름알데히드의 첨가가 완료된 후, 용액을 추가 시간 동안 리플럭스시켰다. 용액을 실온으로 냉각한 후, 얼음 욕 내의 에탄올에 천천히 적가했다. 전체 용액을 첨가한 후, 혼합물을 추가 시간 동안 교반한 후, 고체를 수집하고 에테르 및 에탄올로 세척했다. 이 고체를 소량의 고온수에서 재결정화하여, 백색 고체로서 순수한 NOTP를 수득했다. 네거티브 모드에서 ESI-MS: 410.2 [M-H+]. 여기서, M은 중성 NOTP이다.
NOTP는 NOTP와 0.01M 수성 철(II) 브로마이드의 1 당량과 혼합함으로써 철과 복합체화했다. 용액을 실온에서 4일 동안 교반시키고, 그 후 물을 증발시켰다. ESI-MS (네거티브 모드): 465 [M-H+]. 여기서, M은 중성 형태의 Fe(NOTP)이다.
DRAP-H의 합성(예를 들면, 도 3 참조). 1-벤질-1,4,7-트리아자사이클로노난 디하이드로브로마이드 (1.0 g, 2.64 mmol) 및 파라포름알데히드 (0.24 g,7.92 mmol)를 50% aq H3PO2 (1.3 mL, 11.9 mmol) 및 물 (5 mL)의 혼합물에서 용해했다. 반응 혼합물을 실온에서 24시간 동안 교반한 후, 물로 3번 함께 증발시키고, 강한 양이온 교환기 (DOWEX50, H+-형태) 상에서 크로마토그래피했다. 컬럼을 탈이온수로 세척한 후, NaCl 구배(5 중량% 내지 10 중량%)를 증가시켜, 벤질 TRAP-H (MS로 모니터링된 바와 같이)를 갖는 분획을 수집했다. 용리액을 증발시켜, 밝은 갈색 오일을 수득했다. 1H NMR (300 MHz, D2O): δ = 3.023.52 (m, 고리-CH2,12H 및 N-CH2-P, 4H), 4.35 (s, N-CH2-C6H5, 2H), 7.30-7.50 (m, -C6H5, 5H). MS (ESI, 포지티브): m/z =376 [M + H+]. 여기서, M은 중성 리간드이다.
DRAP-OH의 합성(도 3). DRAP-H를 6 M HCl (20 mL)에 용해했다. 파라포름알데히드(0.24 g, 7.92 mmol)를 첨가하고, 용액을 5시간 동안 리플럭스한 후(MS로 모니터링되는 바와 같이), 증발시켜 크루드한(crude) 벤질 DRAP-OH를 수득했다. MS (ESI, 포지티브): m/z] =436 [M + H+]. M은 중성 리간드이다. 1:1 비율로 Fe(NO3)3.9H2O 및 벤질 DRAP-OH를 10 mL 탈이온수로 용해하고, 4일 동안 교반했다(MS를 사용함으로써 모니터링됨). MS (ESI, 포지티브): m/z =489 [M+]. 여기서, M은 중성 Fe(III) 복합체이다.
"클릭된(clicked)" 트리아졸 펜던트 및 매크로사이클에 대한 이들의 추가에 대한 일반 절차(예를 들면, 도 5 참조). 적절한 크기의 둥근 바닥 플라스크를 사용하여, 메탄올 중 브로모/클로로 시약의 용액에 소듐 아지드의 2당량을 첨가했다. 용액을 60 ℃로 가열하고, 4시간 동안 교반했다. 다음 반응 단계는 이전 생성물의 분리 또는 정제 없이 수행했다. 1.1 당량의 프로파길 알코올을 이전 반응의 교반 용액에 첨가했다. 분리 플라스크에서, 2 mL의 물에 0.1 당량의 구리 설페이트 헥사하이드레이트 및 0.2 당량의 소듐 아스코르베이트를 혼합했다. 혼합물을 1분 동안 교반한 후(min=분(들)), 이전 반응 플라스크에 첨가했다. 반응 혼합물을 60 ℃에서 8-12시간 동안 또는 완료될 때까지(TLC에 의해 모니터링됨) 교반했다. 반응 혼합물을 건조될 때까지 증발시키고, 물을 첨가하고, 생성물을 EtOAc(3x)로 추출했다. 유기층을 합하고, 무수 소듐 설페이트로 건조시켰다. EtOAc를 진공 하에서 제거하여 조 생성물(crude product)을 수득했다. 정제를 0 ℃에서 EtOAc/DCM 용액 또는 실리카 겔(헥산 중 25-50% EtOAc)에서 재결정화하여 수행했다. ESI-MS(m/z): 262.3(생성물 1), 186.2(생성물 2). 3당량의 PBr3를 Ar(g) 하에서 DCM 중 이전 생성물의 용액에 첨가하였다. 12시간 후, 반응을 물로 급냉시키고, 생성물을 DCM으로 추출했다. 유기층을 혼합하고, 무수 소듐 설페이트로 건조시켰다. DCM을 진공 하에 제거하여, 조 생성물을 수득했다. 정제를 0 ℃의 EtOAC/DCM 용액 또는 실리카겔(헥산 중 25-50% EtOAC)에서 재결정화하여 수행했다. ESI-MS(m/z): 323.1/325.1(생성물 1), 247.1/249.1(생성물 2).
출발 시약을 아세토니트릴에 용해시키고, 1.5 당량의 DIPEA를 첨가했다. 8시간 동안 또는 완료될 때까지 교반했다(ESI-MS에 의해 모니터링됨). 용매를 진공 하에 제거하고, 조 생성물을 염기성 알루미나(DCM 중 1-10% MeOH) 상에서 정제했다. ESI-MS(m/z): 489.6(생성물 1), 413.5(생성물 2)
에탄올에 이전 반응으로부터의 리간드를 용해시키고, 물에 용해된 2 당량의 KOH를 추가했다. 약 4시간 동안 또는 완료될 때까지 교반했다(ESI-MS에 의해 모니터링됨). 진공 하에서 용매를 제거했다. 등가의 1M HCl 및 DCM을 첨가했다. DCM(3x)에서 생성물을 추출하고, 층을 혼합하고, 무수 소듐 설페이트로 건조시켰다.
리간드를 에탄올에 용해시키고, 60 ℃에서 교반하면서 FeCl2 1 당량을 첨가했다. 금속화 완료 후(ESI-MS로 모니터링), 생성물이 침전될 때까지 디에틸 에테르를 첨가했다. 생성물을 여과하고, 디에틸 에테르로 세척하고, 진공 하에서 건조시켰다.
ICP-MS. Thermo X-Series 2 ICP-MS를 사용하여 철 농도를 결정했다. 모든 샘플을 10 mL 총 수용액에 2% 질산으로 희석하고(1μM), 24시간 동안 가열(90 ℃)하여 분해했다. 정량화를 위해 0.1 ppb 내지 250 ppb의 범위인 철 금속에 대한 선형 칼리브레이션 곡선을 매일 생성했다. 샘플을 4일의 기간에 걸쳐 질산에서 분해하고, 철 농도를 측정했다.
자기 모멘트(Magnetic moment). 에반법을 사용하여 자기 모멘트 연구를 위한 샘플을 D2O에 5% t-부탄올의 반자성 표준을 포함하는 동축 NMR 삽입물을 사용하여 제조했다. 외측 5 mm NMR 튜브는 고정된 농도의 5 mM 상자성 복합체를 함유했다; 5 % t-부탄올의 존재 하에 4 mM, 8 mM, 40 mM, 및 70 mM. 298 K(T)에서 소분자에 대해 수정된 에반법을 사용하여 유효 자기 모멘트(effective magnetic moment)(μeff, BM)를 계산했다.
팬텀 MR 영상화를 위한 샘플 제조: 팬텀 영상화 실험을 위한 샘플은 50-500 μM 복합체, 20 mM HEPES 및 100 mM NaCl을 함유했다. 인간 혈청 알부민(HSA)을 함유하는 샘플의 경우, 35 mg의 HSA가 이러한 용액에 첨가되었다. 모든 용액의 pH를 7.0으로 조정했다.
4.7 T에서 팬텀(시험관 내) 영상화. AVANCE 디지털 전자 장치(ParaVision v 3.0.2 획득 소프트웨어가 있는 Bruker BioSpec 플랫폼, Bruker Medical, 빌레리카, 매사추세츠)를 통합한 General Electric 4.7T/33 cm 수평 보어 자석(GE NMR instrument, 프리몬트, 캘리포니아)을 사용하여 MRI 획득을 수행했다. 각 복합체를 100 mM NaCl(pH 7.4)에서 HEPES로 0.0.5 mM 내지 400 mM의 범위의 농도로 희석하고, 25 ℃에서 영상화했다. 포화 회복(saturation recovery), 고정 에코 시간(fixed echo time, TE), 10 ms 및 75 내지 8000 ms 범위의 반복 시간(TR)이 있는 스핀 에코(spin-echo, SE) 서열을 사용하여 T1 이완 속도(r1)를 획득했다. 각 반복 시간의 신호 강도는 상업적으로 이용 가능한 영상 처리 소프트웨어(Analyze 7.0, AnalyzeDirect, 오버랜드, 캔자스)를 사용하여 관심 영역(ROI's) 내의 평균 강도를 취하여 샘플링했으며, r1 및 SMAX는 매트랩 곡선 피팅 툴박스(Matlab's Curve Fitting Toolbox)(Matlab 7.0, MathWorks Inc., 네이틱, 매사추세츠)를 사용하여 방정식의 비선형 피팅에 의해 계산했다. 그 후, 데이터의 선형 회귀 피팅을 통해 화합물의 몰 농도 대 r1의 기울기를 얻음으로써, 각각의 복합체의 T1 이완성을 결정했다. 마찬가지로, 고정 TR이 2500 ms이고 TE 시간이 15 내지 300 ms 범위인 다중 에코(multiecho), CPMG(Carr-Purcell-Meiboom Gill) SE 서열을 사용하여 T2 이완 속도(R2)를 획득했다. R2 및 SMAX를 이전과 같이 방정식을 사용하여 상기 기재된 바와 같이 계산하고, 데이터로부터 선형 회귀 피팅을 통해 농도 대 r2의 기울기를 얻음으로써, T2 이완성을 결정했다.
마우스에서 생체 내 영상화. 생체 내 조영 향상을 위한 Fe(III) 복합체의 효능을 4.7 T Bruker 전임상 MRI에서 마우스 모델(BABC/cJ, Jackson Laboratory)에서 연구했다. 신호 정규화(signal normalization)를 위한 영상화 세션에 봉인된 팬텀이 포함되었다. 조영제를 투여하기 전에, 향상의 기준 값으로 사용하기 위해 스캔을 획득했다. 두 가지 스캔 프로토콜: (1) 신호 향상을 결정하기 위해 흉부에서 꼬리까지 마우스를 덮는 T1-강조, 3D, 스포일드 구배 에코 스캔(spoiled-gradient echo scan) 및 (2) 반전 회복(inversion-recovery), 일정 상태 자유 세차 스캔(steady state free precession scan)(IR-SSFP)을 사용하여, 혈액(하대정맥), 신장, 간, 담낭 및 등 근육의 T1 속도를 측정했다. 화합물을 50-200 μmol [Fe]/kg의 용량으로 꼬리 정맥을 통해 정맥내 주사하고, 주사 후 최대 1시간 동안 MR 데이터를 지속적으로 획득하여, 분포 및 제거 동역학을 연구했다. 따라서, 0.2 mL의 6 mM 스톡 용액을 0.05 mmol/kg, 0.100 mmol/kg, 또는 0.200 mmol/kg으로 마우스에 주입했다. 주사 후 3시간 및 6시간에 추가 스캔을 획득하여, 담도계에 의한 더 느린 제거율을 특징화했다. FDA 승인 MRI 조영제 가도펜테테이트 디메글루민 (gadopentetate dimeglumine)(Gd-DTPA, Magnevist®) 또는 도타렘(Dotarem)(Gd(DOTA))을 비교를 위해 50 μmol[Gd]/kg의 별도 마우스 코호트에 주사했다. 데이터를 도 17 및 18에 나타냈다. SPGR 데이터 세트의 경우, 신호 강도를 팬텀으로 정규화하고, 각 기관에 대한 신호 증가 및 등 근육과 비교하여 조영 대 노이즈 비의 증가를 측정했다. T1 비율의 증가를 계산하고, 시험관 내에서 결정된 화합물의 이완성 값으로 나눔으로써, Fe(III) 농도를 추정했다.
NOTP 합성 도식
NOTP 철 복합체화
도 11은 본 개시내용의 매크로사이클릭 복합체의 예에 대한 이완성 데이터를 보여준다. Fe-NOTP는 0.66 ± 0.01 mM-1s-1의 r1을 나타냈고, HSA가 있는 Fe-NOTP는 1.04 ± 0.06 mM-1s-1의 r1을 나타냈다.
문헌에서 발견된 것과 유사한 절차를 사용하여 NOTP를 합성했다. 회백색 침전물을 진공 여과를 통해 수집한 후, 순수한 흰색 고체가 형성될 때까지 50:50 고온수:에탄올 혼합물로부터 여러 번 재결정화했다. MS (ESI 네거티브 모드) m/z: 410.2 (M-H+). 1H NMR (D2O) 3.19 (6H, 이중선(doublet), J 11.30) 3.42 (12H, 단일선(singlet)). 31P NMR (D2O) 11.95. 13C NMR (D2O) 51.02 (6C, 단일선) 53.03 (3C, 이중선, J 141.61).
정제된 NOTP 리간드(0.33 mmol)를 소듐 하이드록사이드(1.01 mmol, 3 당량)과 함께 물(20 mL)에 용해했다. 이 용액을 5분 동안 55 ℃로 가열했다. 5분 후, 수(10mL) 중 FeBr2(0.33mmol, 1 당량)의 용액을 고온 용액에 첨가했다. 혼합된 용액을 추가 1시간 동안 가열했다. 실온으로 냉각 시, 용매를 감압 하에서 증발시켜, 황색 오일을 생성했다. 황색 오일을 물(2 mL)에 용해하고, 에탄올(20 mL)을 첨가하여 황색 고체의 침전을 유도했다. 고체를 수집 및 건조시켰다. MS (ESI 네거티브 모드) m/z: 463.2 (M-H+). 여기서, M은 중성 Fe(NOTP) 복합체이다. μeff 5.85 ± 0.14. ICP-MS 순도: 95%. Fe-NOTP의 로그 P 옥탄올 수: -2.02 ± 0.30.
DAPO의 합성. DAPO를 하기와 같이 합성했다:
1,4,7-트리아조난-1,4-디일-비스(프로판-2-올)을 이전에 공개된 바와 같이 합성했다. 1,4,7-트리아조난-1,4-디일-비스(프로판-2-올)(0.301 mmol)을 500μL의 3.3M HCl 용액에 용해했다. 이 용액에, 아인산(1.80 mmol, 6 당량)을 첨가하고, 혼합물을 리플럭스하도록 설정했다. 리플럭스에 도달 시에, 파라포름알데히드 (1.35 mmol, 4.5 당량)를 1시간의 과정에 걸쳐 첨가하고, 그 후 용액을 추가적인 24시간 동안 리플럭스시켰다.
TRAP-POP의 합성. TRAP-POP를 하기와 같이 합성했다:
디-tert-부틸 1,4,7-트리아자사이클로난-1,4-디카르복실레이트를 문헌에 공개된 바와 같이 합성했다. 0.566 mmol을 아인산(1.98 mmol, 3.5 당량)과 함께 1.1 mL의 3.3 M HCl에 용해시켰다. 이 용액을 리플럭스하도록 설정하고, 리플럭스에 도달 시에, 파라포름알데히드(1.13 mmol, 3 당량)를 1시간의 과정에 걸쳐 첨가했다. 일단, 모든 파라포름알데히드가 첨가되면, 용액을 추가로 1시간 동안 리플럭스시켰다. MS-ESI: 224.1 [M + H+]. 단계 1의 생성물(1.52 mmol)을 30 mL MeOH에 용해시키고, 아르곤을 사용하여 불활성 분위기를 생성했다. 디메틸 페닐포스포나이트(3.04 mmol, 2 당량) 및 파라포름알데히드(1.52 mmol, 1 당량)를 첨가하고, 용액을 실온에서 16시간 동안 교반했다. 용매를 감압 하에 제거했다. MS-ESI(네거티브 모드): 557.7 [M - H+]. 여기서, M은 중성 리간드이다.
NOTPMe의 합성. NOTPMe를 하기와 같이 합성했다:
합성을 문헌에 보고된 바와 같이 수행했다. ESI-MS: 494 [M+H+], 516 [M+Na+]. 여기서, M은 중성 리간드이다.
PhOTO의 합성/ PhOTO를 하기와 같이 합성했다:
30 mL 메탄올 중에 TACN-벤질(0.74mmol)을 용해시킴으로써, PhOTO-메톡시를 합성했다. 디메틸 페닐포스포나이트(3.68 mmol, 5 당량)를 파라포름알데히드(2.94 mmol, 4 당량)와 함께 용액에 첨가했다. 이 용액을 불활성 분위기 하에서 16시간 동안 리플럭스시킨 후, 용매를 감압 하에 제거했다. MS(ESI) m/z: 556.2(M + H+). 여기서, M은 중성 리간드이다. 건조된 PhOTO-메톡시를 4 mL의 30% w/v 카보네이트 프리 소듐 하이드록사이드에 용해시켰다. 이 용액을 격렬하게 교반하면서 30분 동안 리플럭스하고, 이때 4 mL의 카보네이트 프리 물을 첨가했다. 물을 첨가한 후, 용액을 추가 30분 동안 리플럭스했다. 두번째 리플럭스의 종료 시에, 용액을 가열하여 2상 시스템이 나타날 때까지 용매 부피를 줄였다. 플라스크를 실온으로 냉각시켰다. 상층(오일)을 수집하고, 에탄올에 용해시킨 후, 증발 건조시켰다. MS(ESI) m/z: 526.4(M-H+). 여기서, M은 중성 리간드이다.
TOPA의 합성. TOPA를 하기와 같이 합성했다:
1-벤질-1,4,7-트리아자사이클로노난을 이전에 공개된 절차에 따라 합성했다. 1-벤질-1,4,7-트리아자사이클로노난 (0.576 mmol)을 2구 플라스크로 칭량하고, 리플럭스 장치에 설치했다. 플라스크에 아인산(6.91 mmol, 12 당량)을 0.200 mL 브롬화 수소산 및 0.538 mL의 증류수와 함께 추가로 첨가했다. 일단, 이 용액이 리플럭스 되면, 파라포름알데히드(1.15 mmol, 2 당량)를 1시간의 과정에 걸쳐 용액에 첨가했다. 파라포름알데히드의 첨가가 완료된 후, 용액을 24시간 동안 리플럭스시켰다. 그 후, 용액을 최소 부피로 줄이고, Dowex H+ 이온 교환 컬럼 상에 로딩했다. 먼저, 컬럼을 물로 용리하여, 불순물을 제거한 후, 5% 암모늄 하이드록사이드 용액으로 용리하여 생성물을 용리시켰다. 리간드를 함유하는 분획을 감압 하에서 건조하고, 물에 용해시켰다. Amberlite CG-50-타입 1 이온 교환 컬럼을 사용하여, 물로 용출하여 백색 고체를 수득한 생성물을 수득했다. MS (ESI) m/z: 406.18 (M - H+). 여기서, M은 중성 리간드이다. δH (D2O) 3.05 (4H, 이중선, J 10.96) 3.32 (12H, 다중선(multiplet)) 4.34 (2H, 단일선) 7.38 (5H, 다중선). δP (D2O) 14.93.
비스(포스포네이트)비페닐 TACN (TOBP). 비페닐 TACN 유도체로부터 시작하여, TOPA 리간드에 대해 유사한 절차를 사용했다. δH (D2O) (500 MHz): 이중선 (2H, 7.704-7.687) 이중선 (2H, 7.644-7.628) 이중선 (2H, 7.601-7.585), 삼중선(triplet) (2H, 7.452-7.421), 삼중선 (1H, 중앙의(centered) 7.354), 단일선 (4.369, 2H), 3.365-2.973 사이에 넓은 공명, 약 21 H로 나타냄. MS (ESI) m/z: 484.2 (M-H+). Fe(NO3)3의 첨가 및 밤새 리플럭스에 의해 Fe(III) 복합체를 제조했다. MS (ESI) m/z: 535.17 (M-). 여기서, M은 중성 Fe(TOBP) 복합체이다.
TRAP-OPO의 합성. TRAP-OPO를 하기와 같이 합성했다:
1,4,7-트리아자비사이클로[5.2.1]데칸(0.475 mmol)을 10 mL의 메탄올에 용해시켰다. 불활성 분위기를 생성하고, 디메틸 페닐포스포나이트(0.095 mmol, 0.2 당량)를 파라포름알데히드(0.118 mmol, 0.25 당량)와 함께 첨가했다. 용액을 실온에서 밤새 교반시키고, 용매를 감압 하에서 제거했다. MS-ESI: 310.2 [M+H+]. 여기서, M은 중성 리간드이다. 건조된 다운 메틸((1,4,7-트리아자비사이클로[5.2.1]데칸-4-일)메틸)(페닐)포스피네이트(0.221 mmol)를 400 μL의 3.3 M HCl 및 아인산(1.11 mmol, 5 당량)에 용해시켰다. 이 용액을 리플럭스하도록 설정하고, 리플럭스에 도달 시, 파라포름알데히드(0.442 mmol, 2 당량)를 1시간의 과정에 걸쳐 첨가했다. 파라포름알데히드의 첨가가 완료된 후, 용액을 추가 1시간 동안 리플럭스했다. MS-ESI(네거티브 모드): 470.5 [M-H+]. 여기서, M은 중성 리간드이다.
TRAP-Ph의 합성. TRAP-Ph를 하기와 같이 합성했다:
TRAP-Ph-메톡시를 이전에 보고된 바와 같이 합성했다. 건조된 TRAP-Ph-메톡시를 4 mL의 50% w/v 카보네이트 프리 소듐 하이드록사이드에 용해시켰다. 이 용액을 30분 동안 격렬하게 교반하면서 리플럭스시키고, 이때 4 mL 카보네이트 프리 물을 첨가했다. 물의 첨가 후에, 용액을 추가 30분 동안 리플럭스했다. 두번째 리플럭스의 종료 시에, 용액을 가열하여 2상이 나타날 때까지 용매 부피를 줄였다. 용액을 실온으로 냉각시키고, 상층(오일)을 제거하고, 에탄올에 용해시킨 후, 증발 건조시켰다. 그 후, TRAP-Ph를 침전법에 의해 정제했다. 메탄올을 사용하여 염을 침전시킴으로서, 과량의 염을 제거했다. 메탄올을 감압 하에 제거하고, 아세톤의 첨가 시, 디클로로메탄으로 재결정화되는 다른 고체가 형성되었다. MS (ESI) m/z: 590.7 (M-H+). 1H NMR (D2O, pD~0.9) 3.02 (12H, 다중선), 3.09 (6H, 이중선, J 7.12), 7.31 (9H, 다중선), 7.48(6H, 다중선) 31P NMR (D2O, pD~0.9) 29.27. 철 복합체는 이전에 공개된 절차를 따라 합성했다. MS (ESI) m/z: 645.1 (M+H+), 667.1 (M+Na+). 여기서, M은 중성 리간드이다.
1,3-비스((1,4,7-트리아조난-1-일)메틸)벤젠의 합성. 가스 주입구 및 교반 막대가 있는 25 mL 둥근 바닥 플라스크에, 4 mL 톨루엔 1 mL 클로로포름 용액 중 0.100 g TACN (0.774 mmol)을 첨가했다. 0.0920 g N,N-디메틸포름아미드 디메틸아세탈(0.774 mmol)을 플라스크에 첨가했다. 용액을 실온에서 24시간 동안 교반했다. 1,4,7-트리아자트리사이클로[5.2.1.04,10]데칸(TACN 오르토아미드)의 ESI-MS(m/z), 계산치: 140.1 [M + H+](100%). 용액을 회전 증발기 상의 플라스크에 놓아 건조시켰다. 건조된 TACN 오르토아미드 및 15 mL 건조 아세토니트릴을 자석 교반 막대, 리플럭스 응축기, 가스 유입관 및 첨가 깔때기가 장착된 50 mL 3구 둥근 바닥 플라스크에 첨가했다. 10 ml 건조 아세토니트릴 용액 중 0.100 g α,α'-디브로모-m-자일렌(0.384 mmol)을 첨가 깔때기를 사용하여 30분 동안 적가함으로써 플라스크에 첨가했다. 용액을 2시간 동안 가열하여 리플럭스하고, 실온에서 밤새 교반했다. 흡인 여과법에 의해 백색-베이지색 침전물을 수집하고, 건조 아세토니트릴(5 mL) 및 디에틸 에테르(5 mL)로 세척했다. 6 mL 메탄올 및 6 mL 12 M HCl을 첨가하여 탈보호 과정에서 플라스크 내에 침전시켰다. 용액을 가열하여, 4시간 동안 리플럭스했다. 용액을 실온으로 냉각한 후, NaOH 펠릿을 첨가하여 용액의 pH를 8로 제공했다. 그 후, 용액을 여과하여 NaCl 염 침전물을 제거하고, 클로로포름(3 x 60 mL)으로 추출했다. ESI-MS (m/z), 계산치: 361.4 [M + H+] (100 %). 여기서, M은 중성 리간드이다.
m-diTOPA의 합성. 1,3-비스((1,4,7-트리아조난-1-일)벤젠 (0.155 mmol)을 500μL의 3.3 M HCl에 용해시키고, 아인산 (1.86 mmol, 12 당량)을 첨가했다. 용액을 리플럭스 장치에 부착하고, 리플러스 조건에 도달 시, 파라포름알데히드 (0.930 mmol, 6 당량)을 1시간의 과정에 걸쳐 첨가했다. 일단, 모든 파라포름알데히드가 첨가되면, 용액을 추가 1시간 동안 리플럭스시켰다. MS-ESI-: 735.3 [M-H+]. 여기서, M은 중성 리간드이다.
철(II) 클로라이드 테트라하이드레이트를 사용하여 Fe(TASO) 복합체를 합성했다. 에탄올 용매에서 디에틸 에테르 세척에 의해 생성물이 황색 고체로 분리되었다. Fe 함량은 ICP-MS를 통해 NaFe(L1)Cl에 대해 11.29%로 계산되고, 실측치는 11.13% ± 0.17%였다. LCQ-MS: 실측치 m/z 421.2 (M+H+, 70%), m/z 443.2 (M+Na+, 30%), m/z 841.0 (2M+H+, 100%) 및 m/z 863.0 (2M+Na+, 18%). 여기서, M은 중성 Fe(TASO) 복합체이다. 유효 자기 모멘트는 5.68이다.
Fe(TASO)는 도 12에 도시된 바와 같이 순환 전압전류법(cyclic voltammetry)으로 특성화했다. Fe(TASO)의 1.0mM 용액의 순환 전압전류법을 지지 전해질(supporting electrolyte) 및 HEPES 완충액으로 포타슘 클로라이드(100 mM)를 사용하여 수중에서 다양한 pH에서 얻었다.
Fe(TASO)를 UV-vis 흡광도로 특성화했다. 데이터를 도 14-16에 나타냈다.
TBzC 에스테르. 비스(2-하이드록시프로필)-1,4,7-트리아자사이클로노난(0.245 g, 1.0 mmol)을 아세토니트릴(5.0 mL)에 용해시키고, 60 ℃로 가열했다. 그 후, 무수 포타슘 카보네이트(0.207 g, 1.5 mmol)을 용액에 첨가한 후, 에틸 4-(브로모메틸)벤조에이트)(0.304 g, 1.2 mmol)를 첨가했다. 반응이 완료될 때까지 8-12시간 동안 반응물을 교반했다(ESI-MS를 통해 모니터링됨). 그 후, 용매를 진공 하에서 제거하고, 조 생성물을 0/100 내지 5/95 메탄올/디클로로메탄을 사용하여 알루미나 상에서 정제하고, 생성물을 약 1/99 메탄올/디클로로메탄에서 엷은 황색 오일(0.288 g, 71%)로 용리했다. 1H NMR (500 MHz, DCM-d2) δ 7.98 (d, J = 10 Hz, 2H), 7.49 (d, J = 10 Hz, 2H), 4.35 (dd, J = 15 Hz, 2H), 3.89 (s, 2H), 3.72-3.68 (m, 2H), 2.88-2.76 (m, 6H), 2.67-2.45 (m, 10H), 2.25 (dd, J = 10 Hz, 2H), 1.39 (t, J = 5 Hz, 3H), 1.05 (d, J = 10 Hz, 6H). 13C NMR (75 MHz, CHCl3-d) δ 167.0, 144.8, 129.5, 129.4, 128.9, 66.5, 63.9, 62.5, 60.8, 55.7, 55.4, 54.6, 19.8, 14.3. ESI-MS: m/z 408.3 (M+, 100%), 430.3 (M+Na+, 10%).
TBZC 합성. TBZC 에스테르 (0.408 g, 1.0 mmol)를 에탄올에 용해하고, 90 ℃로 가열했다. 그 후, NaOH (0.120 g, 3.0 mmol)을 용액에 첨가하고, ESI-MS에 의해 모니터링되는 바와 같이 완료될 때까지 반응물을 12-24시간 동안 교반했다. 용액을 디클로로메탄으로 세척하고(3 x 25 mL), 수성층을 수집했다. 용매를 감압 하에서 제거했다. 용액의 pH가 3이 될 때까지 12M HCl을 첨가하여 리간드를 수득하고, 생성물(7)을 디클로로메탄으로 추출했다(3 x 25mL). 그 후, 유기층을 혼합하고, 무수 소듐 설페이트 상에서 건조시키고, 용매를 진공 하에서 제거했다. 생성물을 담황색 오일(0.278 g, 73%)로 단리했다. 1H NMR (500 MHz, D2O) δ 7.77 (d, J = 5 Hz, 2H), 7.40 (d, J = 5 Hz, 2H), 3.82 (q, J = 15 Hz, 2H), 3.00 (d, J = 10 Hz, 2H), 2.87-2.58 (m, 16H), 1.04 (d, J = 5 Hz, 6H). 13C NMR (75 MHz, D2O) δ 171.0, 140.4, 135.8, 129.7, 129.0, 63.6, 63.0, 60.2, 51.0, 49.7, 48.8, 19.7. ESI-MS: m/z 380.3 (M+, 100%).
Fe(TBZC). 염화제일철 4 수화물을 사용하여 복합체를 합성하고, 생성물을 황색 고체로서 단리시켰다 (45.7mg, 52%). Fe 함량을 ICP-MS를 통해 [Fe(H2-L4)Cl]Cl에 대해 9.56%로 계산했고, 실측치는 9.52% ± 0.10 %였다. FT-ICR-MS: 계산치 m/z 514.198541, 실측치 m/z 514.198394 (M +, 100%). 여기서, M은 중성 Fe(TZBC) 복합체이다.
pH 3.5에서 측정된 Fe(L2)에 대한 온도의 함수로서의 가로 17O NMR 이완성, ln(1/T2r)을 본 개시 내용의 매크로사이클릭 화합물의 다양한 예에 대해 측정했다. 데이터를 도 13에 나타냈다.
Gd(DTPA)와 비교하여 4.7T 및 9.4T, pH 7.2 및 37 ℃에서 측정된 HSA가 있거나 없는 Fe(TASO)에 대한 이완성 값. 데이터를 표 2 및 3에 나타냈다.
[표 2] Gd(DTPA)와 비교하여 4.7T 및 9.4T, pH 7.2 및 37 ℃에서 측정된 HSA가 있거나 없는 Fe(TASO)에 대한 이완성 값
[표 3] Fe(TASO) 및 Fe(TZBC)에 대한 Log P 옥탄올/물 분배 계수.
Fe(TASO)를 T1 영상화제(imaging agent)로 사용했다. 0.2 mmol/kg의 Fe(TASO) 용량에서 4.7 T에서 건강한 Balb/C 마우스의 T1-강조 MRI를 도 17에 나타냈다. 0.05 mmol/kg Fe(TASO)의 용량에서 4.7 T에서 건강한 Balb/C 마우스의 T1-강조 MRI를 도 18에 나타냈다. Fe(TBZC)를 영상화제로 사용했으며, T1-강조 MRI를 도 19에 나타냈다.
Fe(TASO)의 약동학적 연구를 수행했다. Fe(TASO)에 대한 마우스에서의 약동학적 데이터를 도 19 및 20에 나타냈다. 0.05 mmol/kg의 Fe(L3) 용량에서 4.7T에서 건강한 Balb/C 마우스의 T1-강조 MR 이미지를 얻었다. 0.05mmol/kg에서 4.7T에서 건강한 Balb/C 마우스의 신장, 간 및 혈액에서 시간에 걸쳐 Fe(TASO), Gd(DOTA) 및 Gd-DTPA에 대한 T1 속도 상수를 변경했다. 신호 강도를 팬텀으로 정규화하고, 각 기관의 신호 증가를 측정하고, 조영 대 노이즈 비율의 증가를 근육과 비교했다.
본 개시 내용이 하나 이상의 특정 양태 및/또는 실시예에 대해 기재되었지만, 본 개시 내용의 범위를 벗어나지 않고, 본 개시 내용의 다른 양태 및/또는 실시예가 이루어질 수 있음이 이해될 것이다.
Claims (28)
- 매크로사이클릭 복합체(macrocyclic complex), 또는 이의 염, 부분염(partial salt, 수화물, 다형체, 또는 입체 이성질체로서,
상기 매크로사이클릭 복합체는,
1,4,7-트리아자사이클로노난(triazacyclononane) (TACN) 모이어티 또는 O-치환된 TACN 모이어티;
하기:
, 및 , 이의 치환된 유사체, 이의 탈양성자화된 유사체(deprotonated analog), 이의 입체 이성질체, 및 이들의 조합으로부터 독립적으로 선택된, 상기 TACN 모이어티 또는 O-치환된 TACN 모이어티 상의 치환체인 하나 이상의 음이온성 펜던트기로, 여기서 R2는 치환 또는 비치환된 알킬기, 치환 또는 비치환된 방향족기 또는 치환된 에테르이고; R3은 치환 또는 비치환된 알킬 또는 치환 또는 비치환된 아릴기이고; R4는 치환된 알킬 또는 비치환된 알킬 또는 치환되거나 비치환된 아릴기이고; Q1은 음이온성기로 치환된 아릴, 음이온성기로 치환된 알킬기 또는 음이온성기로 치환된 아랄킬기인 것인, 하나 이상의 음이온성 펜던트기; 및
상기 TACN 모이어티 및 1,4,7-트리아자사이클로노난 (TACN) 모이어티 또는 O-치환된 TACN 모이어티의 적어도 하나의 음이온성 펜던트기 치환체와 복합체화된 고스핀(high-spin) Fe(III) 양이온;을 포함하고,
상기 매크로사이클릭 복합체가 하기 구조:
를 갖는 경우,
Z1 및 Z2는 이고, Z3은 이 아니고; 및/또는
Z1 및 Z2는 - 이때 R4는 비치환 아릴임- 이고, Z3은 -이때 R4 는 비치환 아릴임- 이 아닌 것인, 매크로사이클릭 복합체.
- 제1항에 있어서,
상기 하나 이상의 음이온성 펜던트기의 적어도 하나 또는 전부는 TACN 모이어티 상의 질소원자에 공유 결합되는 것인, 매크로사이클릭 복합체.
- 제1항에 있어서,
상기 매크로사이클릭 복합체는 적어도 하나의 개방 배위 결합 부위(open coordination site)를 갖는 것인, 매크로사이클릭 복합체.
- 제1항에 있어서,
상기 매크로사이클릭 복합체는 고스핀 Fe(III) 양이온에 복합체화된 적어도 하나의 물 및/또는 적어도 하나의 하이드록사이드를 갖는 것인, 매크로사이클릭 복합체.
- 제1항에 있어서,
상기 매크로사이클릭 복합체는 하나 이상의 보조기(들)(ancillary group(s))를 더 포함하는 것인, 매크로사이클릭 복합체.
- 제5항에 있어서,
상기 하나 이상의 보조기(들)는 하나 이상의 배위 펜던트기(들), 하나 이상의 비-배위 펜던트기(들)(non-coordinating pendent group(s)), 또는 이들의 조합인 것인, 매크로사이클릭 복합체.
- 제9항에 있어서,
상기 매크로사이클이 구조 I을 가지면, Z1은 H 또는 음이온성 펜던트기이고, Z2 및 Z3은 각각 독립적으로 음이온성 펜던트기이며; 및/또는
상기 매크로사이클이 구조 II 또는 III을 가지면, Z1 및 Z2는 각각 독립적으로 음이온성 펜던트기이며; 및/또는
전체 구조 I-III에서, 각각의 Z1, Z2 및 Z3은 적용 가능한 경우 독립적으로 선택되는 것인, 매크로사이클릭 복합체.
- 연결기(linker group)에 공유 결합된 하나 이상의 펜던트 매크로사이클릭 복합체 기; 또는 폴리머, 덴드리머, 단백질, 또는 펩티드에 공유 결합된 하나 이상의 펜던트 매크로사이클릭 복합체 기를 포함하는 폴리머, 덴드리머, 단백질, 또는 펩티드;를 포함하는 화합물 또는 폴리머로서,
각각의 개별적인 매크로사이클릭 복합체 기는 제1항 내지 제12항 중 어느 한 항에 기재된 매크로사이클릭 복합체로부터 유도되는 것인, 화합물 또는 폴리머.
- 제1항 내지 제12항 중 어느 한 항에 기재된 하나 이상의 매크로사이클릭 화합물 및/또는 제13항 내지 제15항 중 어느 한 항에 기재된 하나 이상의 화합물 또는 폴리머, 및 약제학적으로 허용되는 담체를 포함하는, 조성물.
- 제16항에 있어서,
상기 조성물은 인간 혈청 알부민 및/또는 메글루민(meglumine)을 더 포함하는 것인, 조성물.
- 세포, 기관, 혈관계 또는 조직 중 적어도 일부의 영상을 수득하는 방법으로서, 상기 방법은,
세포, 기관, 혈관계 또는 조직을 제1항의 하나 이상의 매크로사이클릭 화합물 및/또는 제13항의 하나 이상의 화합물, 또는 Fe(NOTP) 또는 Fe(TRAP-Ph)과 접촉시키는 단계; 및
세포, 기관, 혈관계 또는 조직의 적어도 일부분을 영상화하여, 세포, 기관, 혈관계 또는 조직의 일부분의 영상을 수득하는 단계;를 포함하는데,
상기 영상은 자기 공명을 사용함으로써 수득되는 것인, 방법.
- 제18항에 있어서,
상기 세포, 기관, 혈관계 또는 조직은 개체의 일부인 것인, 방법.
- 제18항에 있어서,
상기 영상은 자기 공명 영상(MRI)을 사용하여 수득되는 것인, 방법.
- 제18항에 있어서,
상기 매크로사이클릭 화합물(들) 및/또는 화합물(들)은 T1 제제 또는 T1 제제들인 것인, 방법.
- 매크로사이클릭 화합물, 또는 이의 염, 부분염, 수화물, 다형체, 또는 입체 이성질체로서,
상기 매크로사이클릭 화합물은,
1,4,7-트리아자사이클로노난 (TACN) 모이어티 또는 O-치환된 TACN 모이어티; 및
하기:
, 및 , 이의 치환된 유사체, 이의 탈양성자화된 유사체, 이의 입체 이성질체, 및 이들의 조합으로부터 독립적으로 선택된, 상기 TACN 모이어티 또는 O-치환된 TACN 모이어티 상의 치환체인 하나 이상의 음이온성 펜던트기로, 여기서 R2는 치환 또는 비치환된 알킬기, 치환 또는 비치환된 방향족기 또는 치환된 에테르이고; R3은 치환 또는 비치환된 알킬 또는 치환 또는 비치환된 아릴기이고; R4는 치환된 알킬 또는 비치환된 알킬 또는 치환되거나 비치환된 아릴기이고; Q1은 음이온성기로 치환된 아릴, 음이온성기로 치환된 알킬기 또는 음이온성기로 치환된 아랄킬기인 것인, 하나 이상의 음이온성 펜던트기;를 포함하고,
상기 매크로사이클릭 화합물이 하기 구조:
를 가지고, Z1은 및 Z2는 - 이때 R3은 비치환된 에틸임- 인 경우, Z3은 - 이때 R3은 비치환된 에틸기임- 이 아니고; 및/또는
상기 매크로사이클 화합물이 하기 구조:
를 가지고, Z1 및 Z2는 - 이때 R3은 비치환 또는 치환된 에틸임- 인 경우, Z3은 - 이때 R3은 비치환 또는 치환된 에틸기임- 이 아니고; 및/또는
상기 매크로사이클 화합물이 하기 구조:
를 가지고, Z1 및 Z2는 - 이때 R3은 비치환된 알킬임- 인 경우, Z3은 - 이때 R3은 비치환된 알킬임- 이 아니고; 및/또는
상기 매크로사이클 화합물이 하기 구조:
를 가지고, Z1 및 Z2는 - 이때 R3은 비치환 또는 치환된 알킬임- 인 경우, Z3은 - 이때 R3은 비치환 또는 치환된 알킬임- 이 아니고; 및/또는
상기 매크로사이클 화합물이 하기 구조:
를 가지고, Z1 및 Z2는 인 경우, Z3은 이 아니고; 및/또는
상기 매크로사이클 화합물이 하기 구조:
를 가지고, Z1 및 Z2는 - 이때 R4는 말단 하이드록실 치환체(terminal hydroxyl substitution)를 갖는 알킬임- 인 경우, Z3은 - 이때 R4는 말단 하이드록실 치환체를 갖는 알킬이 아님- 이 아니고; 및/또는
상기 매크로사이클 화합물이 하기 구조:
를 가지고, Z1 및 Z2는 - 이때 R4는 치환된 알킬임- 인 경우, Z3은 - 이때 R4는 치환된 알킬임- 이 아니고; 및/또는
상기 매크로사이클 화합물이 하기 구조:
를 가지고, Z1 및 Z2는 - 이때 R4는 말단 하이드록실 치환체를 갖는 알킬임- 인 경우, R1은 말단 아릴기를 갖는 알킬이 아니고; 및/또는
상기 매크로사이클 화합물이 하기 구조:
를 가지고, Z1 및 Z2는 - 이때 R4는 말단 하이드록실 치환체를 갖는 알킬임- 인 경우, R1은 치환된 알킬이 아닌 것인, 매크로사이클 화합물.
- 제22항에 있어서,
상기 하나 이상의 음이온성 펜던트기의 적어도 하나 또는 전부는 TACN 모이어티 상의 N에 공유 결합되는 것인, 매크로사이클 화합물.
- 제22항에 있어서,
상기 매크로사이클은 하나 이상의 보조기(들)을 더 포함하는 것인, 매크로사이클 화합물.
- 제24항에 있어서,
상기 하나 이상의 보조기(들)은 하나 이상의 배위 펜던트기(들), 하나 이상의 비-배위 펜던트기(들), 또는 이들의 조합인 것인, 매크로사이클 화합물.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862768823P | 2018-11-16 | 2018-11-16 | |
| US62/768,823 | 2018-11-16 | ||
| PCT/US2019/062077 WO2020102820A1 (en) | 2018-11-16 | 2019-11-18 | Compounds for use as iron (iii) mri contrast agents containing anionic pendents and ancillary groups |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20210114932A true KR20210114932A (ko) | 2021-09-24 |
Family
ID=70730921
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020217017914A KR20210114932A (ko) | 2018-11-16 | 2019-11-18 | 음이온 펜던트 및 보조기를 함유하는 철 (iii) mri 조영제로 사용하기 위한 화합물 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US11344635B2 (ko) |
| EP (1) | EP3880257A4 (ko) |
| JP (1) | JP2022507519A (ko) |
| KR (1) | KR20210114932A (ko) |
| CN (1) | CN113646009A (ko) |
| AU (1) | AU2019381793A1 (ko) |
| WO (1) | WO2020102820A1 (ko) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20240037178A (ko) * | 2021-03-20 | 2024-03-21 | 더 리서치 파운데이션 포 더 스테이트 유니버시티 오브 뉴욕 | Mri 조영제로서 혼합 하이드록실 펜던트를 갖는 철(iii) 매크로사이클릭 복합체 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5236695A (en) | 1989-11-27 | 1993-08-17 | Concat, Ltd. | MRI image enhancement of bone and related tissue using complexes of paramagnetic cations and polyphosphonate ligands |
| US5409689A (en) | 1993-08-13 | 1995-04-25 | Concat, Ltd. | MRI image enhancement using complexes of paramagnetic cations and amine ligands containing a mixture of phosphonate and non-phosphonate pendant arms |
| JP3356289B2 (ja) * | 1995-06-26 | 2002-12-16 | コンキャット リミティド | 第一遷移系列元素に対してキレート化親和性および選択性のある化合物とその医療および診断への使用 |
| US6264966B1 (en) | 2000-02-22 | 2001-07-24 | Concat, Ltd. | Compounds with chelation affinity and selectivity for first transition elements and their use in cosmetics and personal care products, inhibition of metalloenzymes, and inhibition of reperfusion injury |
| US20050112066A1 (en) | 2003-11-26 | 2005-05-26 | Concat Lp, A California Limited Partnership | Complexes of cyclic polyaza chelators with cations of alkaline earth metals for enhanced biological activity |
| JP6124078B2 (ja) | 2010-08-26 | 2017-05-10 | ツイ,クンユァン | 巨大環状脂肪族化合物及びその応用 |
| WO2013060793A1 (en) | 2011-10-25 | 2013-05-02 | Technische Universität München | Bifunctional ligands for radiometals |
| WO2015038943A1 (en) * | 2013-09-12 | 2015-03-19 | The Research Foundation For The State University Of New York University At Buffalo | Macrocycles, cobalt and iron complexes of same, and methods of making and using same |
| CN104119402B (zh) | 2014-08-01 | 2016-08-24 | 南京大学 | 具有单分子磁行为和荧光精细结构的有机膦酸镝配合物 |
| KR20200010385A (ko) | 2017-05-19 | 2020-01-30 | 더 리서치 파운데이션 포 더 스테이트 유니버시티 오브 뉴욕 | 철 (iii) mri 조영제로서 사용을 위한 화합물 |
-
2019
- 2019-11-18 KR KR1020217017914A patent/KR20210114932A/ko not_active Application Discontinuation
- 2019-11-18 AU AU2019381793A patent/AU2019381793A1/en active Pending
- 2019-11-18 WO PCT/US2019/062077 patent/WO2020102820A1/en unknown
- 2019-11-18 EP EP19884487.0A patent/EP3880257A4/en active Pending
- 2019-11-18 CN CN201980089289.XA patent/CN113646009A/zh active Pending
- 2019-11-18 JP JP2021526521A patent/JP2022507519A/ja active Pending
- 2019-11-18 US US16/973,349 patent/US11344635B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US20210260222A1 (en) | 2021-08-26 |
| EP3880257A1 (en) | 2021-09-22 |
| US11344635B2 (en) | 2022-05-31 |
| CN113646009A (zh) | 2021-11-12 |
| EP3880257A4 (en) | 2022-07-27 |
| JP2022507519A (ja) | 2022-01-18 |
| WO2020102820A1 (en) | 2020-05-22 |
| AU2019381793A1 (en) | 2021-06-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Aime et al. | Synthesis and NMR studies of three pyridine-containing triaza macrocyclic triacetate ligands and their complexes with lanthanide ions | |
| KR101469900B1 (ko) | Do3a-디아미노바이페닐 화합물 및 이를 리간드로 포함하는 가돌리늄 착물 | |
| US20220259244A1 (en) | Compounds for use as iron(iii) mri contrast agents | |
| Phukan et al. | A new bis (aquated) high relaxivity Mn (II) complex as an alternative to Gd (III)-based MRI contrast agent | |
| US10960088B2 (en) | Macrocycles, cobalt and iron complexes of same, and methods of making and using same | |
| US11097017B2 (en) | Gadolinium-based contrast agents for sensitive detection of Zn2+with MRI | |
| Kras et al. | Comparison of phosphonate, hydroxypropyl and carboxylate pendants in Fe (III) macrocyclic complexes as MRI contrast agents | |
| US9302019B2 (en) | Fe(II) sequestering agents and uses thereof | |
| KR20210114932A (ko) | 음이온 펜던트 및 보조기를 함유하는 철 (iii) mri 조영제로 사용하기 위한 화합물 | |
| KR101836461B1 (ko) | 페로센을 기반으로 한 새로운 형태의 mr 조영제의 개발 | |
| KR20240037178A (ko) | Mri 조영제로서 혼합 하이드록실 펜던트를 갖는 철(iii) 매크로사이클릭 복합체 | |
| CN117729943A (zh) | 具有混合羟基侧基的铁(iii)大环配合物作为mri造影剂 | |
| Kras | A Comparison of Oxygen-Donor Pendant Groups for Iron (III) Macrocyclic T 1 MRI Probes | |
| Pradhan et al. | A mono-aquated di-pyridine-based Gd (III) complex as T1-weighted MRI probe with high relaxivity and stability | |
| Zhang et al. | Synthesis neutral rare earth complexes of diethylenetriamine-N, N ″-bis (acetyl-isoniazid)-N, N′, N ″-triacetic acid as potential contrast enhancement agents for magnetic resonance imaging | |
| WO2023126336A1 (en) | Novel bispidine-based metal chelating ligands displaying good relaxivity | |
| Garcia | Studies on the physicochemical properties of europium cryptates: Implications to contrast agents for magnetic resonance imaging | |
| AL-YASSIRY et al. | Development of Optimized MRI Contrast Agents for Copper (I) Click Reactions | |
| Ali | Design, synthesis and applications of multi-functional MRI contrast agents for bio-imaging | |
| WO2020263761A1 (en) | Iron(iii) and gallium(iii) metal organic polyhedra, methods of making same, and uses thereof | |
| JP2024520899A (ja) | アルデヒドのin vivo検出のための分子プローブ | |
| Allen | Developing New Ligand Platforms for MRI Contrast Agents |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal |