KR20200143436A - Nk 세포 결합 항체 융합 구조체 - Google Patents
Nk 세포 결합 항체 융합 구조체 Download PDFInfo
- Publication number
- KR20200143436A KR20200143436A KR1020207032435A KR20207032435A KR20200143436A KR 20200143436 A KR20200143436 A KR 20200143436A KR 1020207032435 A KR1020207032435 A KR 1020207032435A KR 20207032435 A KR20207032435 A KR 20207032435A KR 20200143436 A KR20200143436 A KR 20200143436A
- Authority
- KR
- South Korea
- Prior art keywords
- seq
- amino acid
- acid sequence
- antigen
- set forth
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/283—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against Fc-receptors, e.g. CD16, CD32, CD64
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2878—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the NGF-receptor/TNF-receptor superfamily, e.g. CD27, CD30, CD40, CD95
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
- A61K2039/507—Comprising a combination of two or more separate antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/33—Crossreactivity, e.g. for species or epitope, or lack of said crossreactivity
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/35—Valency
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/526—CH3 domain
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/53—Hinge
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
- C07K2317/732—Antibody-dependent cellular cytotoxicity [ADCC]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Hematology (AREA)
- Oncology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
본 발명은 NK 세포에서 발현되는 CD16A (FcgRIIIA)와 결합하여 NK 세포 세포독성을 유발하기 위한, 자연 살해 (NK) 세포와 결합하기 위한 다중특이적 항원-결합 단백질에 관한 것으로, 이러한 항원-결합 단백질은 적어도 2개의 CD16A 항원-결합 모이어티 및 적어도 하나의 추가 표적 항원-결합 모이어티를 포함한다. 상기 CD16A 항원-결합 모이어티는 폴리펩티드 사슬에서 차례로 연결된 경쇄 및 중쇄 가변 영역들을 포함하고 CD16A 항원-결합 모이어티를 포함하는 폴리펩티드 사슬의 N-말단의 가변 영역은 경쇄 가변 영역이다.
Description
관련 출원에 대한 상호 참고
본 출원은 2018 년 4 월 13 일에 출원된 유럽 가특허 출원 제 EP18167384.9, 2018 년 4 월 13 일에 출원된 유럽 가특허 출원 제 EP18167385.6, 2018 년 8 월 24 일에 출원된 유럽 가특허 출원 제 EP18190661.1, , 2018 년 8 월 24 일에 출원 된 유럽가 특허 출원 번호 EP18190662.9에 대하여 우선권을 주장하며, 이들 문헌 각각의 내용은 그 전문이 참고문헌으로 포함된다.
서열 목록
본원은 ASCII 형식으로 전자적으로 제출된 서열 목록을 포함하며, 이러한 서열 목록은 본원에 그 전문이 참고로 포함된다. 2019년 4월 10일자에 생성된 상기 ASCII 사본의 파일명은 087353_0101_SL.txt이고 137,653 바이트 크기이다.
발명의 분야
본 발명은 NK 세포에서 발현되는 CD16A (FcgRIIIA)와 결합하여 NK 세포 세포독성을 유발하기 위한, 자연 살해 (NK) 세포와 결합하기 위한 다중특이적 항원-결합 단백질에 관한 것으로, 이러한 항원-결합 단백질은 적어도 2개의 CD16A 항원-결합 모이어티 및 적어도 하나의 추가 표적 항원-결합 모이어티를 포함한다.
배경기술
WO 2006/125668 및 Reusch 외, MABS, 2014, 6:3:728-739는 CD16A와 결합하기 위한 이중특이적 탠덤 디아바디 및 NK 세포 면역요법에 있어서 이의 용도를 설명한다.
자연 살해 (NK) 세포는 바이러스에 감염된 세포 및 암 세포에 대한 첫 번째 방어선을 구성하는 것으로 간주되는 세포독성 IFN-γ-생성 선천성 림프구이다 (Cerwenka and Lanier, Nat Rev Immunol. 2001;1(1):41-9). NK 세포의 세포독성 잠재력은 NK 세포 용해를 종양 세포로 재지시하고 NK 세포의 세포 표면에서 발현되는 활성화 수용체 CD16A (FcγRIIIA로도 알려져 있음)를 자극함으로써 암 면역요법에 활용 될 수 있다.
다중 특이적 항체를 사용하여 NK 세포를 종양 세포 용해를 위해 지시하는 것은 독성이 낮고 허용가능한 안전성 프로필을 가지는 강력한 면역치료법으로 간주된다.
CD16A는 NK 세포의 세포독성 활성을 유발하는 활성화 수용체이다. CD16A에 대한 항체의 친화성은 NK 세포 활성화를 유발하는 능력과 직접적으로 관련되어 활성화에 필요한 항체 용량을 줄인다.
NK 세포의 세포독성 활성은 CD16A에 대한 다가 결합, 예를 들어, CD16A에 대한 2가 결합을 통해 결합력을 증가시킴으로써 증가 될 수 있다.
그러나, CD16A에 대한 2가 및 다가는 NK 세포, gd T 세포 및 단핵구, 대식세포 및 수지상 세포의 서브세트를 비롯한 CD16A 발현 세포의 항체 매개 가교 결합을 초래할 수 있다. 이러한 상호작용은 CD16A를 통한 원치않는 세포 자극을 가져올 것으로 예상된다. 예를 들어, NK 세포와 CD16A-발현 면역 세포의 가교 결합은 NK 세포 활성화, 사이토카인 방출 및 세포-지시된 세포독성의 유도를 초래하여 NK 세포 활성을 감소시키고 원하는 항 종양 효과와 무관하게 NK 세포 고갈을 가속화한다. 따라서, CD16A-발현 면역 세포와 NK 세포의 교차 결합은 NK 세포-결합(engagement)의 치료 효능을 감소시킬 것으로 예상된다. 가장 중요한 것은, 히말라야 원숭이 및 타마린에서 CD16에 2가인 CD16-지시된 쥐과 IgG 항체 (3G8)을 사용하여 기존에 설명된 바와 같이 (Choi 외, Immunology 2008;124:215-222; Yoshida 외, Frontier in Microbiology (2010);1:128), CD16A와의 2가 또는 다가 상호작용을 통한 2개 이상의 NK 세포의 가교는 NK 세포 활성화 및 동족살해 (fratricide) (NK-NK 세포 용해)의 유도를 유발하여 궁극적으로 생체내에서 효율적인 NK 세포 고갈을 초래할 수 있다는 것이다. 따라서 NK 용해의 유도는 ADCC를 매개하는데 사용할 수 있는 이펙터 세포의 수를 감소시키고 치료 항체 효능을 손상시킨다.
따라서, 동족살해 (NK-NK 세포 용해)에 의해 감소되지 않는, NK 세포 결합을 향상시킬 수 있는 항체가 필요하다.
발명의 요약
본 발명은 NK 세포상에서 CD16A와 적어도 2가 상호작용을 할 수 있고, 그리하여 증가된 결합 친화성 및 세포독성 효능을 가질 수 있지만, 바람직하게는 NK-NK 세포 용해를 유도 할 수 없는 CD16A-결합 항체를 제공한다.
본 발명은 다음을 의미한다:
적어도 하나의 표적 항원-결합 모이어티 및 적어도 2개의 CD16A 항원-결합 모이어티를 포함하는 다가 및 다중특이적 항원-결합 단백질, 이 때 상기 2개의 CD16A 항원-결합 모이어티는 불변 도메인, 예를 들어, Fab 단편 또는 Fc 부분에 융합된다. 바람직하게는, 상기 표적 항원-결합 모이어티 또한 상기 Fab 단편 또는 Fc 부분에 융합된다.
예를 들어, 각각의 항원-결합 모이어티는 단쇄 디아바디 (scDb), 디아바디 (Db), 단쇄 Fv (scFv) 또는 Fab 단편으로 구성된 그룹에서 선택 될 수 있다.
일부 구체예에서, CD16A 항원-결합 모이어티의 경쇄 및 중쇄 가변 영역은 폴리펩티드에서 차례로 연결되어 폴리펩티드 사슬의 N-말단의 가변 영역이 경쇄 가변 영역이 되고, 이로써 동족살해 (NK-NK 세포 용해) 유도가 방지된다.
불변 도메인, 가령, F(ab)', F(ab)2', CH2-CH3, 힌지-CH2-CH3, Fc, CH1-힌지-CH2-CH3 또는 IgG를 포함하는 다양한 단위들에 N-말단 또는 C-말단으로 항원-결합 모이어티를 융합함으로써 다양한 단백질 구조들을 사용할 수 있다.
일부 구체예에서 항원-결합 단백질은 Fc-감마R에 결합하지 않지만, FcRn에 대한 결합 그리고, 선택적으로, 적어도 하나의 추가 Fc-기능성을 보유하는 침묵된 Fc 부분을 포함한다.
일부 구체예에서 항원-결합 단백질은 한 쪽에서는 Fc-γR에 결합하지 않도록 침묵되고 다른 한 쪽에서는 FcRn에 결합하는 능력을 증가 또는 감소시키는 또 다른 돌연변이를 포함할 수 있는 Fc 부분을 포함하는데, 이는 다양한 트랜스사이토시스 및 재활용 능력을 기반으로 하는 다양한 생체내 약동학과 상관관계가 있다.
특정 구체예에서, 상기 항원-결합 단백질은 적어도 하나의 HSA 항원-결합 모이어티를 포함한다. 예를 들어, 항원-결합 단백질은 2, 3 또는 4 개의 HSA 항원-결합 모이어티를 포함 할 수 있다.
특정 구체예에서, 항원-결합 단백질은 적어도 2개의 상이한 표적 항원-결합 모이어티, 즉, 제 1 및 제 2 표적 항원-결합 모이어티를 포함한다.
특정 구체예에서, CD16A에 대한 친화성이 증가 또는 감소된 CD16A 항원-결합 모이어티가 적용된다.
무엇보다도 본 발명의 특징은 다음과 같다:
1. 다음에 의한, 강화된 NK 세포 결합 기능
·
Fab 단편 또는 Fc 부분에 융합된 2개의 CD16A 항원-결합 모이어티, 이로써 CD16A에 대한 2가 결합으로 인해 세포독성 효능이 증가.
·
CD16A에 대한 높은 친화성 결합을 갖는 항-CD16A 항원-결합 모이어티를 사용.
·
동족살해를 유도하지 않는 특정 순서로 CD16A 항원-결합을 배열하여 동족살해 (NK-NK 세포 용해) 유도를 방지하여 표적 세포에 대한 NK 세포의 세포독성 활성 약화를 방지.
·
동족살해를 방지하는 것은 CD16A 항원-결합 모이어티의 결합 친화성과 무관하다.
·
Fc-감마R-양성 단핵구 또는 Fc-감마R을 발현하는 다른 세포에 대한 추가 결합을 방지함과 동시에 FcRn에 대한 결합을 유지하기 위하여 침묵된 Fc 부분을 사용함으로써, 혈청 반감기를 연장.
2. 이러한 강화된 NK 세포 결합 기능은 조정가능한 세포독성, 표적 친화성, CD16A 기능성, 표적 생물학, 조직 침투 및 분포, 반감기 및 노출을 구현하는 다수의 단백질 구조들로의 항원-결합 모이어티의 조절가능성으로 인한 것일 수 있다.
본원에 구체적으로 기재된 다양한 항체 형태들의 사용 그리고 다양한 반감기 및 상이한 노출들을 비롯한 기능성은 새로운 치료제들을 의학적 수요가 높은 다양한 적응증들에 맞게 맞춤화하여, 각각의 설정을 목표로하는 제품 개발을 제공할 수 있다.
또한, NK 세포 동족살해 부재는, 보다 긴 세포 체류 시간으로 특징되고 내인성 NK 세포들의 결합을 위해 사용되거나 NK 세포 치료 접근법과 조합될, 높은 친화성의 적어도 2가의 면역 세포 관여항체 (관여항체) 형태들에 있어 중요한 특징이다. 이들에는 다양한 출처로부터, 가령, 예를 들면, 건강한 기증자의 말초 혈액,자가 치료를 위한 환자 또는 줄기 세포로부터 유래한 NK 세포들이 포함된다. 이들 관여항체들은 이러한 NK 세포들과 공동-주입 또는 사전-혼합될 수 있다.
표적에 대한 적어도 2가 결합에 의한 표적 결합 친화성의 증가 및/또는 2개의 상이한 제 1 및 제 2 표적 항원-결합 모이어티에 의한 표적의 이중-표적화에 의한 표적 선택성의 증가를 추가로 가능하게 하는 단백질 형태들이 본원에 제시된다.
또 다른 기능, 가령, 예를 들면, 인간 혈청 알부민 (HSA) 결합 모이어티가 이러한 항원-결합 단백질에 포함될 수 있다.
도면의 간단한 설명
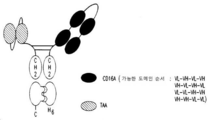
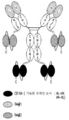
도 1-2는 단량체이고 그리고 단량체 Fc 부분에 융합된 scDb 형태의 2가 CD16A 항원-결합 모이어티를 포함하는 scDb-mFc 항원-결합 단백질을 도시하며, 이 때 도 1에서 2개의 CD16A 항원-결합 모이어티로 구성된 scDb는 변이체 CH2-CH3 폴리펩티드 및 Fc 부분의 C-말단에 융합된 단일 표적 항원-결합 모이어티를 포함하는 scFv로 구성된 Fc 부분의 N-말단에 융합되고, 그리고 도 2에서 2개의 CD16A 항원-결합 모이어티로 구성된 scDb는 변이체 CH2-CH3 폴리펩티드 및 Fc 부분의 N-말단에 융합된 단일 표적 항원-결합 모이어티를 포함하는 scFv로 구성된 Fc 부분의 C-말단에 융합된다. 상기 표적은 종양 관련 표적이다.
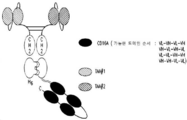
도 3-6은 이종이량체이고, 그리고 이종이량체 (KiH) Fc 부분에 융합된 scDb 형태의 2가 CD16A 항원-결합 모이어티를 포함하는 KiH-scDb-Fc 항원-결합 단백질을 보여 주며, 이 때 도 3에서 2개의 CD16A 항원-결합 모이어티로 구성된 scDb는 CH2-CH3 이종이량체로 구성된 Fc 부분의 N-말단에서 힌지 또는 중간 힌지에 융합되고 및 단일 표적 항원-결합 모이어티를 포함하는 scFv는 Fc 부분의 C-말단에 융합되고; 도 4에서 2개의 CD16A 항원-결합 모이어티로 구성된 scDb는 CH2-CH3 이종이 량체로 구성된 Fc 부분의 2 개 폴리 펩타이드 중 하나의 N-말단에서 힌지 또는 중간 힌지에 융합되고 단일 표적 항원-결합 모이어티를 포함하는 scFv는 CH2-CH3 이종이량체 (KiH) Fc 부분의 다른 하나의 폴리펩티드의 N-말단에서 힌지에 융합되고; 도 5에서 CD16A 항원-결합 모이어티로 구성된 scDb는 CH2-CH3 이종이량체로 구성된 Fc 부분의 C-말단에 융합되고 단일 표적 항원-결합 모이어티를 포함하는 scFv는 힌지 또는 중간 힌지 CH2-CH3 이종이량체 (KiH) Fc 부분의 다른 하나의 폴리펩티드의 N-말단에서 힌지 또는 중간 힌지에 융합되고; 그리고 도 6에서 2개의 CD16A 항원-결합 모이어티로 구성된 scDb는 CH2-CH3 이종이량체로 구성된 Fc 부분의 C-말단에 융합되고 제 1 표적 항원-결합 모이어티를 포함하는 제 1 scFv는 Fc 부분의 N-말단에서 힌지 또는 중간 힌지에 융합되고 제 2 (그리고 제 1 과 상이한) 표적 항원-결합 모이어티를 포함하는 제 2 scFv는 CH2-CH3 이종이량체 (KiH) Fc 부분의 다른 하나의 폴리펩티드의 N-말단에서 힌지 또는 중간 힌지에 융합된다. 제 1 및 제 2 표적은 두 개의 다른 종양 관련 표적이다.
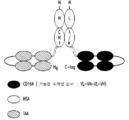
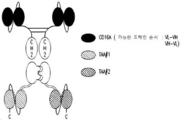
도 7-8은 CD16A, 표적 및 HSA 항원-결합 모이어티를 포함하는 이종이량체 Fab 단편-scDb 융합물인 삼중특이적 scDb-TriB 항원-결합 단백질을 보여주며, 이 때 도 7에서 2개의 CD16A 항원-결합 모이어티로 구성된 2가 scDb는 Fab 단편의 두 폴리펩티드 중 하나의 C-말단에 융합되고 2개의 표적 항원-결합 모이어티로 구성된 2가 scDb는 Fab 단편의 다른 폴리펩티드의 C-말단에 융합되고 Fab 단편의 N-말단은 HSA 항원-결합 모이어티를 제공하고; 그리고 도 8에서 2개의 CD16A 항원-결합 모이어티로 구성된 2가 scDb는 Fab 단편의 두 폴리펩티드 중 하나의 C-말단에 융합되고 단일 표적 항원-결합 모이어티로 구성된 scFv는 Fab 단편의 다른 하나의 폴리펩티드의 C-말단에 융합되고 Fab 단편의 N-말단의 Fv는 HSA 항원-결합 모이어티를 제공한다. 상기 표적은 종양 관련 표적이다.
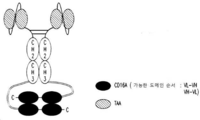
도 9-10은 동종이량체이고 동종이량체 Fc 부분의 N-말단에서 중간 힌지에 또는 C-말단에 융합된 Db 형태의 2가 CD16A 항원-결합 모이어티 및 scFv 형태의 2개의 표적 항원-결합 모이어티를 포함하는 Db-Fc 항원-결합 단백질을 보여주며, 이 때 도 9에서 scFv는 동종이량체화 CH2-CH3 폴리펩티드의 C-말단에 융합되고 Db를 포함하는 폴리펩티드는 CH2-CH3 폴리펩티드의 N-말단에서 중간 힌지에 융합되며, 이 때 2개의 Db 폴리펩티드는 2개의 CD16A 항원-결합 모이어티를 포함하는 Db에 비-공유적으로 결합한다. 표적은 종양 관련 표적이고, 도 10에서 scFv 표적 항원-결합 모이어티는 동종이량체화 CH2-CH3 폴리펩티드의 N-말단에서 중간 힌지에 융합되고 2개의 CD16A 항원-결합 모이어티를 포함하는 Db를 포함하는 폴리펩티드는 Fc 동종이량체의 C-말단에 융합된다. 상기 표적은 종양 관련 표적이다.
도 11-12는 2개의 CD16A 항원-결합 모이어티 및 2개의 표적 항원-결합 모이어티를 포함하며 각각 scFv 형태로 Fc 동종이량체에 융합된 동종이량체 및 4가인 Bi-scFv-Fc 항원-결합 단백질을 보여주며, 이 때 도 11에서 2개의 CD16A 항원-결합 scFv는 CH2-CH3 폴리펩티드 중 하나의 N-말단에서 힌지에 융합되고 2개의 표적 항원-결합 scFv는 CH2-CH3 폴리펩티드의 C-말단에 융합되며; 그리고 도 12에서 CD16A 항원-결합 모이어티 scFv는 Fc 동종이량체에 C-말단 융합되며, 반면 표적 항원-결합 scFv는 Fc 동종이량체의 N-말단에서 힌지에 융합된다. 상기 표적은 종양 관련 표적이다.
도 13은 IgG 항체-융합물을 포함하는 scFv-IgAb 항원-결합 단백질을 보여주며, scFv 형태의 2개의 CD16A 항원-결합 모이어티는 H 사슬의 C-말단에 융합되는 반면, 2개의 표적 항원-결합 모이어티는 IgG의 Fab 아암에서 각 Fv에 의해 제공된다. 상기 표적은 종양 관련 표적이다.
도 14는 4개의 scFv 항원-결합 모이어티가 융합된 IgG 항체-융합물을 포함하는 Bi-scFv-IgAb 항원-결합 단백질을 보여주며, 여기서 scFv 형태의 2개의 CD16A 항원-결합 모이어티 각각은 H 사슬의 C-말단에 융합되는 반면, 제 1 표적에 결합하는 2개의 항원-결합 모이어티는 IgG의 Fab 아암에서 각 Fv에 의해 제공되고 제 2 표적에 결합하는 2개의 항원-결합 모이어티 각각은 2개의 CL 사슬의 C-말단에 융합된다.
도 15A 및 15B는 KiH-scFv-Fc 항원-결합 단백질을 보여주며, 여기서 4개의 항원-결합 scFv는 이종이량체 (KiH) Fc 부분에 융합되고 , 2개의 CD16A 항원-결합 모이어티는 Fc 부분의 N-또는 C-말단에서 융합된다. 도 15A는 각각 CH2-CH3 폴리펩티드 중 하나의 N-말단에서 힌지에 융합된 2개의 CD16A 항원-결합 모이어티를 가지는 KiH-scFv-Fc를 보여주며, 제 1 표적 항원-결합 모이어티를 포함하는 scFv는 CH2-CH3 폴리펩티드 중 하나의 C-말단에 융합되고 제 2 표적 항원-결합 모이어티를 포함하는 또 다른 scFv는 다른 하나의 CH2-CH3 폴리펩티드의 C-말단에 융합된다. 도 15B는 각각 CH2-CH3 폴리펩티드 중 하나의 C-말단에 융합된 2개의 CD16A 항원-결합 모이어티를 가지는 KiH-scFv-Fc를 보여주며, 제 1 표적 항원-결합 모이어티를 포함하는 scFv는 CH2-CH3 폴리펩티드 중 하나의 N-말단에서 힌지에 융합되고 제 2 표적 항원-결합 모이어티를 포함하는 또 다른 scFv는 다른 하나의 CH2-CH3 폴리펩티드의 N-말단에서 힌지에 융합된다.
도 16은 IgG 항체-융합물을 포함하는 scFv-IgAb 항원-결합 단백질을 보여주며, scFv 형태의 2개의 표적 항원-결합 모이어티는 H 사슬의 C-말단에 융합되는 반면, 2개의 CD16A 항원-결합 모이어티는 IgG의 Fab 아암에서 각 Fv에 의해 제공된다. 상기 표적은 종양 관련 표적이다.
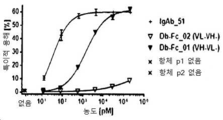
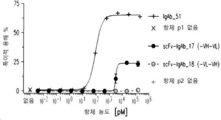
도 17A-17N은 실시예 6에서 항체-매개 NK-NK 세포 용해 결과를 보여준다. 도 17A는 도 1에서 보는 바와 같이 N-말단에서 단량체 Fc에 융합된 디아바디 형태 (scDb)의 2개의 항-CD16A 모이어티 (및 C-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17B는 도 2에서 보는 바와 같이 C-말단에서 단량체 Fc에 융합된 디아바디 형태 (scDb)의 2개의 항-CD16A 모이어티 (및 N-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17C는 도 3에서 보는 바와 같이 N-말단에서 비대칭 Fc에 융합된 디아바디 형태 (scDb)의 2개의 항-CD16A 모이어티 (및 C-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17D는 도 4에서 보는 바와 같이 N-말단에서 비대칭 Fc에 융합된 디아바디 형태 (scDb)의 2개의 항-CD16A 모이어티 (및 N-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17E는 도 5에서 보는 바와 같이 C-말단에서 비대칭 Fc에 융합된 디아바디 형태 (scDb)의 2개의 항-CD16A 모이어티 (및 N-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17F는 도 7에서 보는 바와 같이 CL의 C-말단에서 Fab에 융합된 디아바디 형태 (scDb)의 2개의 항-CD16A 모이어티 (및 CH1의 C-말단에 TAA를 표적하는 scDb)를 보여준다. 도 17G는 도 8에서 보는 바와 같이 CH1의 C-말단에서 Fab에 융합된 디아바디 형태 (scDb)의 2개의 항-CD16A 모이어티 (및 CL의 C-말단에 TAA를 표적하는 scDb)를 보여준다. 도 17H는 도 9에서 보는 바와 같이 N-말단에서 Fc에 융합된 디아바디 (Db) 형태의 2개의 항-CD16A 모이어티 (및 C-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17I는 도 10에서 보는 바와 같이 C-말단에서 Fc에 융합된 디아바디 (Db) 형태의 2개의 항-CD16A 모이어티 (및 N-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17J는 도 11에서 보는 바와 같이 N-말단에서 Fc에 융합된 scFv 형태의 2개의 항-CD16A 모이어티 (및 C-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17K는 도 12에서 보는 바와 같이 C-말단에서 Fc에 융합된 scFv 형태의 2개의 항-CD16A 모이어티 (및 N-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17L는 도 13에서 보는 바와 같이 C-말단에서 Fc에 융합된 scFv 형태의 2개의 항-CD16A 모이어티 (및 N-말단에 TAA를 표적하는 Fab 아암)를 보여준다. 도 17M은 도 15a 및 15b에서 보는 바와 같이 N-말단에서 비대칭 Fc에 융합된 scFv 형태의 2개의 항-CD16A 모이어티 (및 C-말단에서 2개의 TAA를 표적하는 2개 scFv) 및 C-말단에서 비대칭 Fc에 융합된 scFv 형태의 2개의 항-CD16A 모이어티 (및 N-말단에서 2개의 TAA를 표적하는 2개 scFv)를 보여준다. 도 17N은 C-말단에서 Fc에 융합된 TAA를 표적하는 2개의 scFv가 있는 IgG의 Fab 아암에서의 2개의 항-CD16A 모이어티 (도 16에 도시됨)를, 도 13에 도시된 바와 같이 C-말단에서 Fc에 융합된 scFv 형태의 2개의 항-CD16A 모이어티 (및 N-말단에서 TAA를 표적하는 Fab 아암)와 비교하여 보여준다.
도 18A 및 18B 상이한 항-CD16 scFv의 SPR 분석. 야생형 IgG1 및 조작된 인간 IgG1 Fc (S239D/I332E)와 비교한, 항-CD16 결합 scFv 항체 (Ab16고, Ab16중, 3G8, Ab16저)에 관한 정규화된 상대 결합 신호의 SPR 센소그램. 도 18A는 인간 CD16A-158V에 대한 강화된 결합을 보여준다. 도 18B는 인간 CD16A-158F에 대한 결합을 보여준다. 분석물은 312.5 nM의 단일 농도에서 측정되었다.
도 19A-19C는 위치 140의 티로신 (Y)이 scFv 항체의 입체형태 에피토프의 형성 및 CD16A-특이적 반응성에 중요함을 보여준다. 단량체 Fc 또는 막 앵커가 있는 ECD 서열들의 융합 단백질로서 발현된 상이한 재조합 CD16 변이체들을 분석하였다. 도 19A는 제시된 CD16 결합 scFv와의 반응성에 대해 테스트되었던, 니트로셀룰로스 막 상에서 정의된 CD16 항원 변이체들을 함유하는 단백질 스팟들을 보여준다. 도 19B는 항체 염색 및 유세포 분석에 의해 분석한, EGFR 막경유 도메인 또는 GPI에 대한 융합을 통해 고정된, CHO 세포상에서 발현된 상이한 항-CD16 scFv, 대조 scFv, 또는 mAbs와 CD16 항원 변이체 또는 EGFR 항원의 반응성을 보여준다. 도 19C는 SDS-PAGE 및 웨스턴 블롯으로 분리한 이후 CD16 항원 변이체들에 대한 상이한 항-CD16 항체들의 결합을 보여준다.
도 20은 항-CD16 결합 도메인 (Ab16저, Ab16중, Ab16고, 3G8)의 인간 CD16A-158V 및 인간 CD16A-158F에 대한 결합에 관한 SPR 센서그램을, 인간 IgG1 Fc-야생형, 인간 IgG1 Fc 강화 (S239D/I332E), 인간 IgG1 Fc-침묵 (L234F/L235E /D265A)과 비교하여 보여준다. KD 값은 1:1 결합 모델을 사용하여 계산되었으며 표 5에 나타낸다. 가로축: 반응 (RU), 세로축: 시간 [초].
도 21은 본원에 기재된 특정 실험에서 재조합 항원으로 사용된 인간 및 시노몰구스 CD16A 및 인간 CD16B 변이체의 ECD 서열들의 서열 정렬을 보여준다. 인간 CD16A 또는 CD16B에서 다형성이 있는 위치는 각각 얇은 그리고 두꺼운 화살표로 표시된다. 기호 '#'은 인간 CD16B를 GPI 막 앵커에 연결하는 위치를 표시하고, 'd'로 표시된 위치는 성숙한 CD16B 항원 서열에서 절단된다. 시노몰구스 CD16A ECD 서열에서의 변이는 볼드체로 표시한다. 인간 CD16A와 인간 CD16B 간 서열 변이가 있는 위치는 괄호로 표시한다 (테스트 항-CD16 항체의 CD16A-특이적 결합에 중요). CLUSTAL O (1.2.4) 다중 서열 정렬 도구가 정렬에 사용되었다.
도 22는 CD16A에 대한 mAb 3G8과 상이한 항-CD16 scFv 항체들의 결합 경쟁을 ELISA로 보여준다. CD16A-158V ECD-Fc 융합 항원으로 코팅된 플레이트들을 1 nM의 mAb 3G8과 지시된 농도 범위의 상이한 항-CD16 scFv들의 연속 희석액의 혼합물과 함께 배양하였다. CD16A-결합된 mAb 3G8은 퍼옥시다제 접합된 염소 항-마우스 IgG(H+L)로 탐지되었다. TMB 기질 반응을 450nm에서 측정하고 (Ext (450nm)), 플롯하고 분석하였다.
도 23은 ROCK® 플랫폼 개요를 보여준다.
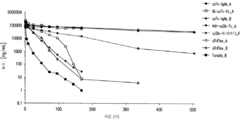
도 24A-24C 는 다양한 CD16A 2가 결합 ROCK® 관여항체들의 정규화된 상대 결합 해리 상들의 SPR 센소그램을 보여준다. scFv-IgAb_C, Db-Fc_A, scFv-IgAb_D, KiH-scDb-Fc_A, TandAb_C를 내포하는 2가 항-CD16A 도메인들을 IgAb_E (Fc-강화; S239D/I332E) 및 1가 항-CD16A 단편 scFv Ab16고 on 고정화된 인간 CD16A-158V 및 시노몰구스 CD16에서 IgAb_E (Fc-강화; S239D/I332E) 및 1가 항-CD16A 단편 scFv Ab16고와 비교하였다. 도 24A는 고정된 인간 CD16A-158V에 대한 SPR 센소그램을 보여준다. 도 24B는 시노몰구스 CD16에 대한 SPR 센소그램을 보여준다. 도 24C는 3시간의 해리 후 수용체에 남아있는 항체의 범례 및 백분율을 보여준다. 분석물은 50 nM의 단일 농도에서 측정되었다.
도 25는 NK 세포상의 IgG와 비교하여 ROCK® 항체의 세포 표면 잔류를 보여준다. 농축된 일차 인간 NK 세포들에 100 μg/mL TandAb 또는 400 μg/mL IgG를 45분 동안 얼음위에서 사전부하하고, 세척하고 37°C에서 지시된 시간 동안 배양하여 해리시켰다. 세척 후, 나머지 항체들을 His-태그된 가용성 BCMA, 그리고 이어서 10 μg/mL mAb 항-His 및 15 μg/mL FITC-접합 염소 항-마우스 IgG로 탐지하였다. 시점 0에서 평균 형광 강도를 100%로 설정하고 나머지 항체의 백분율을 비선형 회귀를 사용하여 플롯했다.
도 26A-26C은 ROCK® 형태에 있어서 CD16A 겉보기 친화성이 가변 도메인, 위치 및 연결기 길이에 의해 조정가능함을 보여준다. 상이한 위치에서 상이한 CD16 결합 Fv (Ab16중, Ab16고) (N: Fc의 항-CD16 Fvs N-말단, C: Fc의 항-CD16 Fvs C-말단), 항체 형태들, 및 상이한 도메인 순서를 내포하는 ROCK® 항체들에 대한 가용성 CD16 항원의 결합을 ELISA로 분석하였다. 점선 기호로 표시된 CD16 결합 Fv가 있는 대표적인 픽토그램은 각 그룹 아래에 표시된다. 도 26A는 Fab 또는 scFv-기반 CD16 관여에 의한 CD16A 겉보기 친화성의 요약을 보여준다. 도 26A는 디아바디 (Db)-기반 CD16 관여에 의한 CD16A 겉보기 친화성의 요약을 보여준다. 도 26C는 상이한 연결기 길이 (10aa 또는 30aa) 및 도메인 순서의 항-CD16 Fv (HL: scFv 도메인 순서 VH-VL, LH: scFv 도메인 순서 VL-VH)를 포함하는 C-말단 scFv-기반 CD16 관여에 의한 CD16A 겉보기 친화성의 요약을 보여준다. 분석된 모든 항체는 침묵된 Fc를 내포하거나 Fab의 C-말단에 융합된 경우 Fc가 없다. 검은색 또는 음영으로 도시된 결합 특이성은 BCMA, CD19, CD20, EGFR, HSA 또는 RSV를 표적하는 항체 도메인들을 포함하였다.
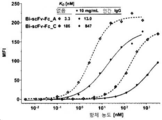
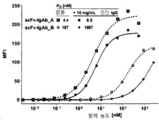
도 27A-27C는 인간 IgG의 존재 또는 부재시 일차 인간 NK 세포에 대한 ROCK® 항체의 결합을 보여준다. 도 27A는 일차 인간 NK 세포들이 37°C에서 10 mg/mL 다클론 인간 IgG의 존재 또는 부재시 제시된 증가된 농도의 무-Fc ROCK®로 염색되었음을 보여준다. 도 27B는 일차 인간 NK 세포들이 37°C에서 10 mg/mL 다클론 인간 IgG의 존재 또는 부재시 제시된 증가된 농도의 Fc 융합 ROCK®로 염색되었음을 보여준다. 도 27C는 일차 인간 NK 세포들이 37°C에서 10 mg/mL 다클론 인간 IgG의 존재 또는 부재시 제시된 증가된 농도의 IgG-유사 ROCK® 구조체들로 염색되었음을 보여준다. 세포 결합 항체들은 유세포 분석으로 탐지하였으며, 비-선형 회귀에 의한 겉보기 친화성 (K D ) 계산에 중앙 형광 광도 (MFI)를 사용하였다.
도 28은 시험관내 NK 동족살해에 관한 다양한 ROCK® 항체 형태들의 비교 분석을 보여준다. 1:1의 E:T로 4시간 공-배양 후 상이한 ROCK® 항체 형태들의 존재시 자가 NK 세포들에 대한 농축된 일차 인간 NK 세포들의 시험관내 칼세인-방출 세포독성. 여러 독립 실험들의 평균 EC50 값을 요약하고 개별 점들로 플롯한다. ROCK® 항체 형태들을 항-CD16 도메인의 위치 및 형태/도메인 순서에 기초하여 분류한다. 고 친화성 항-CD16 도메인 및 침묵된 Fc를 내포하는 구조체들만이 그래프에 포함되었다. HL: scFv 도메인 순서 VH-VL, LH: scFv 도메인 순서 VL-VH. N-term. = N-말단, C-term. = C-말단.
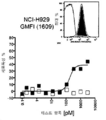
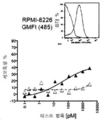
도 29A-29E는 상응하는 종양 표적을 발현하는 세포주에 대한 여러 ROCK® 항체의 존재시 농축된 일차 인간 NK 세포의 시험관내 세포 독성을 보여준다. 도 29A는 5:1의 E:T 비율에서 SABC 값들 (≥3회 분석의 평균)로 나타내었을 때 상이한 수준의 BCMA를 발현하는 표적 세포주 NCI-H929 및 NK 세포들을 사용하여 4시간 칼세인-방출 세포독성 분석에서 제시된 BCMA-표적화 ROCK® 항체들의 대표적인 S형 용량-반응 곡선을 나타낸다. 도 29B는 5:1의 E:T 비율에서 SABC 값들 (≥3회 분석의 평균)로 나타내었을 때 상이한 수준의 BCMA를 발현하는 표적 세포주 MM.1S 및 NK 세포들을 사용하여 4시간 칼세인-방출 세포독성 분석에서 제시된 BCMA-표적화 ROCK® 항체들의 대표적인 S형 용량-반응 곡선을 나타낸다. 도 29C는 5:1의 E:T 비율에서 SABC 값들 (≥3회 분석의 평균)로 나타내었을 때 상이한 수준의 BCMA를 발현하는 표적 세포주 MC/CAR 및 NK 세포들을 사용하여 4시간 칼세인-방출 세포독성 분석에서 제시된 BCMA-표적화 ROCK® 항체들의 대표적인 S형 용량-반응 곡선을 나타낸다. 도 29D는 5:1의 E:T 비율에서 NK 세포 및 SW-982 표적 세포를 사용한 4시간 칼세인-방출 세포독성 분석에서 제시된 EGFR-표적화 ROCK® 항체, 비교인자, 또는 1가 결합 대조의 대표적인 S형 용량-반응 곡선들을 보여준다. 도 29E는 시험관내 종양 표적 세포에 대한 NK 세포 결합 친화성 및 세포독성 역가에 관한 ROCK® 항체의 상관관계를 보여준다. 일차 인간 NK 세포에서 ROCK® 항체 형태들의 겉보기 친화성 (KD)을 나타낸다. 동일한 ROCK® 항체들의 EC50 값들은 2:1의 E:T 비율에서 NK 세포 및 BCMA-발현 RPMI-8226 표적 세포들을 이용한 3시간 칼세인-방출 세포독성 측정에서 (왼쪽) 또는 5:1의 E:T 비율에서 NK 세포 및 BCMA-발현 NCI-H929 표적 세포를 사용한 4시간 칼세인-방출 세포독성에서 (오른쪽) 결정되었다. SABC, 특이적 항체-결합능.
도 30은 다양한 ROCK® 관여항체 형태들의 약동학 비교를 보여준다: 300 μg 테스트 항목의 단회 i.v. 투여 후 시간에 따른 (1 또는 3주 관찰 기간) 항체 농도.
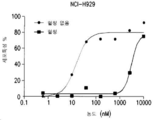
도 31A-31B는 CD16A-158V/V 건강한 공여체 (실선) 및 CD16A-158F/F (점선)에 대한 CD16A/BCMA 항체의 세포독성을 보여준다. 도 31A는 NCI-H929 세포주의 결과를 보여준다. 도 31B는 MM.1S 세포주에 대한 결과를 보여준다.
도 32A-32E는 다발성 골수종 세포주에서 CD16A/BCMA 항체 I의 시험관내 세포독성을 보여준다. 165K의 PBMC 당 CD56+CD3e-NK 세포의 대략적인 수는 약 ~8000개 세포였으므로, NK:종양 비율은 ~0.4였다 (MM 환자 NK 대 종양 세포 비율을 추정하는 임상 데이터와 유사; 데이터 도시하지 않음). 도 32A는 건강한 인간 혈액 공여체로부터 분리되어 차후 실험을 위해 냉동시킨 인간 PBMC를 보여준다. 해동시 PBMC는 트리판 블루 염색에 의해 ~85% 생존가능하였으며 추후 7AAD를 사용하는 FACS에 의해 확인되었다. PBMC (~165K)를 BCMA+ 다발성 골수종 종양 세포주 (~20K)와 공배양하였고, 5% CO2와 함께 37°C에서 약 20시간 동안 0.1 - 3000pM의 3-배 연속 희석 테스트 항목들에 노출시켰다. 165K의 PBMC 당 CD56+CD3e-NK 세포의 대략적인 수는 약 ~8000개 세포였으므로, NK:종양 비율은 ~0.4였다 (MM 환자 NK 대 종양 세포 비율을 추정하는 임상 데이터와 유사; 데이터 도시하지 않음). 도 32B-32E에서 보는 바와 같이, 항체 염색 및 FACS를 사용하여 MM 종양 세포에서 BCMA 발현을 결정하고 다발성 골수종 표적 세포의 세포독성을 모니터하였다. 데이터는 소프트웨어 프로그램 FlowJo 및 GraphPad Prism 6으로 분석되었다. 도 32B는 NCI-H929 세포주를 나타내고, 도 32C는 RPMI-8226 세포주를 나타내고, 도 32D는 MM.1S 세포주를 나타내고, 도 32E는 MOLP-2 세포주를 나타낸다. 비-BCMA 표적화/CD16a 음성 대조는 열린 기호로 표시한다. CD16A/BCMA 항체 I은 채워진 기호로 표시한다.
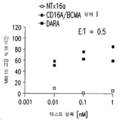
도 33A-33C는 다발성 골수종 세포주에서 CD16A/BCMA 항체 I의 시험관내 세포독성을 보여준다. 도 33A는 NCI-H929 세포주를 나타내고, 도 33B는 RPMI-8226 세포주를 나타내고, 도 33C는 MM.15 세포주를 나타낸다. 비-BCMA 표적화/CD16a 음성 대조는 채워지지 않은 사각형으로 표시한다. CD16A/BCMA 항체 I은 솔리드 원으로 표시한다. 다라투무맙 ("Dara")은 채워진 사각형으로 표시한다.
도 34A-34C는 다발성 골수종 세포주에서 CD16A/BCMA 항체 I의 시험관내 세포독성을 보여준다. NK 세포는 BCMA+ 다발성 골수종 종양 세포주와 E:T ~4-5로 공배양되었다. 공여체 A - NK 및 종양 세포를 NK 세포 및 테스트 항목을 첨가하기 전 적어도 30분 동안 0.5 mg/ml 저 내독소 hIgG와 함께 사전배양하였다. 공여체 B-사전배양 단계 없음. 도 34A는 공여체 A에 대한 BCMA+ 표적 세포의 고갈을 보여준다.도 34B는 공여체 B에 대한 SK-MM-2의 고갈을 보여준다.도 34C는 공여체 B에 대한 MOLP-2의 고갈을 나타낸다. 도 34B 및 34C에서, 비 -BCMA 표적화/CD16a 음성 대조는 열린 기호로 표시되고 CD16A/BCMA 항체 I는 채워진 기호로 표시된다.
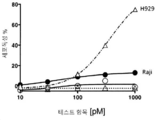
도 35A-35D는 낮은 BCMA 발현 Raji 종양 세포주에 대한 CD16A/BCMA 항체 I, CD16A/BCMA 항체 II 및 CD16A/BCMA 항체 III의 시험관내 세포독성을 보여준다. 거의 탐지불가능한 BCMA 표면 발현에도 불구하고 BCMA+ 표적 세포의 시험관내 용해가 관찰된다. 이러한 시험관내 세포독성 분석은 농축된 일차 인간 NK 세포들, E:T 5:1의 4시간 칼세인-방출 분석을 사용하여 수행되었다. 도 35A는 Raji 세포주의 용해를 보여준다. 도 35B는 Raji 세포주의 세포독성을 보여준다. 도 35C는 시판되는 항-BCMA 항체 및 아이소형에 의해 탐지된 BCMA 발현을 보여준다. 도 35D는 CD16A/BCMA 항체 I, CD16A/BCMA 항체 II, CD16A/BCMA 항체 III, BCMA (Fc 침묵) 및 아이소형에 의해 탐지된 BCMA 발현을 보여준다.
도 36A-36C는 낮은 BCMA 발현 Raji 종양 세포주에 대한 CD16A/BCMA 항체 I의 시험관내 세포독성을 보여준다. 도 36A는 Raji 세포에서의 BCMA 발현을 보여준다. 도 36B는 NCI-H929 (MM 양성 대조) 세포에서의 BCMA 발현을 보여준다. (A) 및 (B)의 경우, APC에 접합된 시판 항-BCMA를 Raji 및 NCI-H929 (MM 양성 대조) 세포에서 BCMA 발현의 정량화에 사용했다. (C) Raji 세포 및 H929 세포의 세포독성. CD16A/BCMA 항체 I은 채워진 기호로 표시되고 비-BCMA 표적화/CD16a 음성 대조는 열린 기호로 표시된다.
도 37A 및 37B는 자가 BCMA+ 정상 인간 형질 세포에 대한 CD16A/BCMA 항체 I의 시험관내 활성을 보여준다. 도 37A는 양성 대조로서 동종이계 세포를 보여준다. 도 37B는 자가 BCMA+ 정상 인간 형질 세포를 보여준다. CD16A/BCMA 항체 I은 채워진 기호로 표시되고 비-BCMA 표적화/CD16a 음성 대조는 열린 기호로 표시된다.
도 38A-38C는 BCMA+ 표적 세포의 존재시 CD16A/BCMA 항체 I에 의한 NK 세포상의 CD16 활성화를 보여준다. 도 38A는 NK-CD16+ 세포의 수를 보여준다. 도 38B는 NKCD69+CD25+ 세포의 수를 보여준다. 도 38C는 표적 세포의 수를 보여준다.
도 39A 및 39B는 BCMA+ 표적 세포의 부재시 CD16A/BCMA 항체 I에 의한 NK 세포상의 CD16 활성화를 보여준다. 도 39A는 NK-CD16+ 세포의 수를 보여준다. 도 39B는 NKCD69+CD25+ 세포의 수를 보여준다.
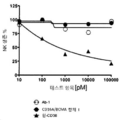
도 40A-40E는 혈청의 존재시 CD16A/BCMA 항체 I의 NK 세포에 대한 결합 및 CD16A/BCMA 항체 I의 세포독성을 보여준다. 도 40A는 외인성 인간 Ig의 존재시 항-BCMA/CD16a의 결합을 보여준다. 새로이 준비된 인간 NK 세포들을 10 mg/mL의 SCIG (Hizentra)와 함께 및 없이 37C에서 1-시간 동안 사전-배양한 다음, 제시된 농도의 DyLight650 표지된 항-AFM26/CD16a로 염색하였다. 도 40B는 100% 자가 인간 혈청의 존재시 항-BCMA/CD16 유도된 표적 세포 용해를 보여준다. 다발성 골수종 세포주 NCI-H929를, 이펙터 세포로서 새로이 준비된 인간 NK 세포를 사용하여 제시된 농도의 CD16A/BCMA 항체 I로 처리했다. CD16A/BCMA 항체 I을 첨가하기 전에, 세포를 37°C에서 30분 동안 동일한 건강한 공여체로부터의 열-불활성화된 자가 인간 혈청과 함께 사전 배양하였다. 도 40C 및 40D는 항-BCMA/CD16a가 NK 세포의 손실없이 50% 자가 인간 혈청의 존재시 BCMA+ 표적 세포를 고갈시킨다는 것을 보여준다. 도 40C 및 40D에서 CD16A/BCMA 항체 I이 예로서 사용된다. 도 40C 및 40D에서 건강한 인간 혈액 공여체로부터 인간 NK 세포를 분리했다. NK (도 40D) 및 MM.1S 세포들 (도 40C)을 분석 셋업 전에 2시간 동안 50% 인간 자가 혈청에서 별도로 사전배양하였다. NK 세포를 MM.1S 종양 세포주와 대략 5의 E:T 비율로 공배양하고, 5% CO2와 함께 37°C에서 약 20시간 동안 0.1 - 100pM의 10-배 연속 희석 테스트 항목들에 노출하였다. CD138 및 CD56를 이용한 항체 염색 후 FACS를 사용하여 MM.1S 표적 세포의 세포독성 및 NK 생존을 모니터하였다. 데이터는 소프트웨어 프로그램 FlowJo 및 GraphPad Prism 6으로 분석되었다. Ab-1, 비-BCMA 표적화/CD16a 음성 대조는 열린 기호로 표시한다. BCMA/CD16a 항체 I은 채워진 기호로 표시한다. 도 40E는 2차 R/R MM이 항-BCMA/CD16A 항체로 치료하기 위한 표적 적응증임을 보여준다. 본 예에서, BCMA/CD16A 항체 I이 예로서 사용된다. 구체적으로, 이 도면의 데이터는 항-BCMA/CD16A 항체 (예시 목적으로 사용된 BCMA/CD16A 항체 I)가 항-CD38 항체 (다라투무맙)와 구별됨을 보여준다. 다라투무맙은 MM에서 보체 의존성 세포 독성 활성 (de Weers, M. 외 2011. J. Immun. 186(3):1840-1848) 및 CD38의 교차 결합을 통한 신호전달에 의해 세포자멸사를 유도하는 능력 (Overdijk, M.B., 외, 2016 J. Immun. 197(3):807-813)을 가지는 반면, BCMA/CD16A 항체 I는 이러한 활성을 가지지 않는다. 더욱이, 다라투무맙과 달리 BCMA/CD16A 항체 I의 활성은 도 41A 및 41B에서 보는 바와 같이 Fc 매개 약물의 활성을 감소시키는 CD16A 다형성에 의해 영향을 받지 않는다. 전체적으로, 도 40E는 BCMA/CD16A 항체 I이 NK 세포 (CD38 양성)를 고갈시키지 않지만 다라투무맙은 고갈시킨다는 것을 보여준다.
도 41A 및 41B는 BCMA+ 표적 세포의 부재하에 CD16A 발현 및 NK 세포의 활성화에 대한 혈청의 영향을 보여준다. 또한, 혈청의 존재시 낮은 CD16 발현은 NK 세포의 비-CD16A 매개 활성화를 시사한다. 도 41A는 혈청에 의한 보다 낮은 CD16A 탐지를 보여준다. 도 41B는 혈청에 의한 더 높은 비-표적 매개 활성화를 보여준다.
도 42A-42C는 IL-15 처리가 MM 세포에 대한 항-CD16A/BCMA 항체의 활성을 증가 시켰음을 보여준다. 도 42A는 a) 항체 없음, b) 음성 대조 1, c) 음성 대조 2, d) BCMA/CD16A 항체 I, e) 항-BCMA/CD19 항체, 및 f) 다라투무맙으로 처리된 종양 세포들의 용해 퍼센트를 보여준다. 도 42B는 a) 항체 없음 + IL-15, b) 음성 대조 1 + IL-15, c) 음성 대조 2 + IL-15, d) BCMA/CD16A 항체 I + IL-15, e) 항-BCMA/CD19 항체 + IL-15, 및 f) 다라투무맙 + IL-15으로 처리된 종양 세포들의 용해 퍼센트를 보여준다. 도 42c는 도 42A 및 42B에 도시된 음성 대조 # 1, 음성 대조 # 2 및 BCMA/CD19의 구조를 도시한다.
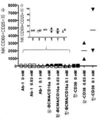
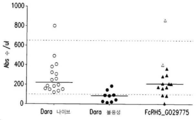
도 43은 다라투무맙 나이브 환자, 다라투무맙 불응성 환자들의 말초 혈액 내 NK 세포들의 수를 보여준다. 도 43은 아테졸리주맙 시험에 대한 기준선에서의 말초 혈액에서의 NK 유동 데이터 (절대 수/uL)를 보여준다. NK 세포는 CD56/CD16+림프구: CD45xSSC 낮은 집단 (표준 게이팅)으로 게이팅된 다음, CD56/CD16 + 집단으로 서브게이팅되었다. 아테졸리주맙에서 Dara 불응성 환자의 NK 수준은 Dara 나이브보다 낮았고 건강한 공여체 범위 (점선들 사이의 영역)보다 낮았다.
도 44는 R/R MM 환자 골수에서 NK/종양 비율을 보여준다.
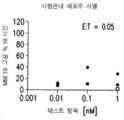
도 45A 및 45B는 CD16A/BCMA 항체 I를 사용한 세포주의 시험관내 사멸을 보여준다. CD16A/BCMA 항체 I은 채워진 원으로 표시되고, 다라투무맙 ("Dara")은 채워진 사각형으로 표시되고, NTx16a, 비-표적화 항-CD16A 이중특이적 항체는 채워지지 않은 사각형으로 표시된다. 도 45A에서, E:T는 0.05였다. 도 45B에서, E:T는 0.5였다.
도 46A-46D는 CD16A/BCMA 항체 I 및 CD16A/BCMA 항체 II의 세포독성에 대한 새로운 NK 세포들의 영향을 보여준다. "새로이 준비된 NK 세포"는 같은 날 새로 분리된 PBMC에서 정제된 NK 세포를 나타낸다. "2일차 NK 세포"는 1일차에 분리된 PBMC에서 정제되고 RPMI 배지에서 밤새 배양된 NK 세포를 나타낸다. 도 46A는 NCI-H929 세포에서 새로이 준비된 NK 세포의 세포독성을 보여준다. 도 46B는 MM.1S 세포에서 새로이 준비된 NK 세포의 세포독성을 보여준다. 도 46C는 NCI-H929 세포에서 2일차 NK 세포의 세포독성을 보여준다. 도 46D는 MM.1S 세포에서 2일차 NK 세포의 세포독성을 보여준다.
도 47은 냉동된 일차 골수종 골수 단핵 세포 (BMMC)에서 FcRH5, BCMA 및 CD38의 발현을 보여준다. 20명의 공여체 및 대조 (골수종 세포주 MOLP-2)로부터 얻은 냉동된 일차 골수종 골수 단핵구 세포 (BMMC)를 FcRH5, BCMA (Biolegend 19F2), CD38 세포 표면 발현에 대해 평가하였다. 요약하면, BMMC를 해동하고 멸균 PBS로 세척한 다음, 1x10^6 세포/mL의 최종 농도로 재현탁시켰다. BMMC는 생존력 및 골수종 마커 (CD45, CD319, CD138, CD38, BCMA, FcRH5)로 염색되었다. 세포를 고정하고 세척한 후, 세포들을 Canto II에서 판독하였다. 생존/단일항/CD45-/CD319+ 세포들 (골수종 세포들)을 선택하여 FlowJo에서 FcRH5, BCMA, 및 CD38의 분석을 실시하였다. FcRH5, BCMA 및 CD38에 대한 MESF (Log10) 값을 통계 플롯팅 소프트웨어 Prism에서 플롯하였다.
도 48A 및 48B는 정상 인간 형질 세포 및 일차 MM 세포에 대한 BCMA 발현을 보여준다. 도 48A는 정상 인간 형질 세포에 대한 BCMA의 발현을 보여준다. 도 48B는 냉동 일차 골수종 BMMC에서 BCMA 발현의 한 예를 보여준다. 도 48A 및 48B 모두에서, BCMA를 사용하여 도 47에서 상기 설명한 프로토콜에 따라 세포를 염색하고 게이팅한 다음, 최대%를 FlowJo에서 플롯하였다. 회색 음영 피크는 형광 마이너스 1 (FMO) 대조이고 적색 피크는 BCMA 발현이다.
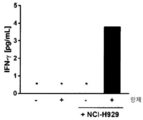
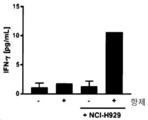
도 49A-49F는 ROCK 관여항체에 의한 NK 세포 활성화 및 IFN-γ 방출의 유도가 표적 세포의 존재에 엄격하게 의존함을 보여준다. 도 49A-49C는 BCMA+ RPMI-8226 표적 세포의 존재 및 부재시 증가하는 농도의 BCMA/CD16A ROCK 관여항체 TandAb_A, scFv-IgAb_D 및 KiH-scDb-Fc_A에서 PBMC 배양물에서 CD69+ NK 세포의 백분율을 보여준다. 도 49A는 TandAb_A, 도 49B는 scFv-IgAb_D, 도 49C는 KiH-scDb-Fc_A에 관한 것이다. 인간 PBMC를 증가하는 농도의 항체 존재시 (사각형) 또는 항체 없이 (삼각형) RPMI-8226 표적 세포와 함께 (채워진 기호) 또는 없이 (열린 기호) (E:T 비율: 50:1) 배양하였다. 22시간 배양 후, CD56+ NK 세포에서의 CD69 표면 발현을 유세포 분석으로 분석하였다. 도 49D-49F는 새로이 분리된 인간 PBMC가 10 μg/mL TandAb_A, scFv-IgAb_D 또는 KiH-scDb-Fc_A와 함께 또는 없이 50:1의 E:T 비율로 BCMA + NCI-H929 세포의 존재 또는 부재하에 배양되었음을 보여준다. 도 49D는 TandAb_A, 도 49E는 scFv-IgAb_D, 도 49F는 KiH-scDb-Fc_A에 관한 것이다. 24시간 배양 후, 상청액에서 IFN-γ 농도를 정량하였다. *: 하한 탐지 한계 미만.
도 50은 BCMA-지시된 T 세포 관여항체 및 ROCK 관여항체에 의해 유도된 인간 PBMC 배양물에서 염증성 사이토카인 방출의 비교를 보여준다. 새로이 분리된 인간 PBMC를 증가하는 농도의 BCMA/CD3 BiTE, 또는 NK-세포 관여 ROCK 관여항체 scFv-IgAb_D 또는 KiH-scDb-Fc_A의 존재 또는 부재시 BCMA+ 세포주 NCI-H929 (E:T 비율 50:1)와 공배양하였다. 24시간 배양 후, 상청액에서의 사이토카인 농도를 정량하였다. 대조: 첨가된 항체 없음.
도 51은 여러 ROCK® 항체 형태의 존재시 A-431 세포에 대한 농축된 일차 인간 NK 세포의 시험관내 세포독성을 보여준다. 5:1의 E:T 비율에서의 4시간 칼세인-방출 세포독성 분석에서 제시된 EGFR-표적화 ROCK 항체의 대표적인 S형 용량-반응 곡선들. SABC, 특이적 항체-결합능 (≥3회 분석의 평균값).
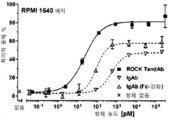
도 52A-52D는 경쟁 다클론, 단클론, 또는 Fc-강화된 IgG의 존재 또는 부재시 시험관내 세포독성 분석에서 ROCK® 및 IgG 항체의 비교를 보여준다. CD30/CD16A TandAb, 항-CD30 IgG1 (IgAb), 또는 Fc-매개 이펙터 기능 강화 돌연변이 S239D/I332E가 있는 항-CD30 IgG1 (IgAb (Fc-강화))의 연속 희석물의 존재하에서 이펙터 세포로서 일차 인간 NK 세포들과 칼세인-표지된 CD30+ KARPAS-299 표적 세포들을 5:1의 E:T 비율로 이용한 4시간 칼세인-방출 세포독성 분석. 분석은 RPMI 1640 배지, 또는 10 mg/mL 다클론 인간 IgG, 10 mg/mL 단클론 인간 항-EGFR IgG1 (IgAb), 또는 10 mg/mL Fc-강화된 단클론 인간 항-EGFR IgG1 (IgAb (Fc-강화))로 보충한 배지에서 수행되었다. 도 52A는 RPMI 1640 배지를 보여준다. 도 52B는 10mg/mL 다클론 인간 IgG가 보충된 배지를 보여준다. 도 52C는 10mg/mL 단클론 인간 항-EGFR IgG1을 보여준다. 도 52D는 10mg/mL Fc-강화 단클론 인간 항-EGFR IgG1을 보여준다.
도 53A-53D는 CD16A/BCMA 항체 I의 BCMA-표적화 모이어티 및 CD16A 항원-결합 모이어티의 서열을 보여준다. 도 53A는 CD16A/BCMA 항체 I의 BCMA-표적화 모이어티의 CDR 서열을 보여준다. 도 53B는 CD16A/BCMA 항체 I의 BCMA-표적화 모이어티의 중쇄 및 경쇄 가변 영역 서열을 보여준다. 도 53C는 CD16A/BCMA 항체 I의 CD16A 항원-결합 모이어티의 CDR 서열을 보여준다. 도 53D는 CD16A/BCMA 항체 I의 CD16A 항원-결합 모이어티의 중쇄 및 경쇄 가변 영역 서열을 보여준다.
도 1-2는 단량체이고 그리고 단량체 Fc 부분에 융합된 scDb 형태의 2가 CD16A 항원-결합 모이어티를 포함하는 scDb-mFc 항원-결합 단백질을 도시하며, 이 때 도 1에서 2개의 CD16A 항원-결합 모이어티로 구성된 scDb는 변이체 CH2-CH3 폴리펩티드 및 Fc 부분의 C-말단에 융합된 단일 표적 항원-결합 모이어티를 포함하는 scFv로 구성된 Fc 부분의 N-말단에 융합되고, 그리고 도 2에서 2개의 CD16A 항원-결합 모이어티로 구성된 scDb는 변이체 CH2-CH3 폴리펩티드 및 Fc 부분의 N-말단에 융합된 단일 표적 항원-결합 모이어티를 포함하는 scFv로 구성된 Fc 부분의 C-말단에 융합된다. 상기 표적은 종양 관련 표적이다.
도 3-6은 이종이량체이고, 그리고 이종이량체 (KiH) Fc 부분에 융합된 scDb 형태의 2가 CD16A 항원-결합 모이어티를 포함하는 KiH-scDb-Fc 항원-결합 단백질을 보여 주며, 이 때 도 3에서 2개의 CD16A 항원-결합 모이어티로 구성된 scDb는 CH2-CH3 이종이량체로 구성된 Fc 부분의 N-말단에서 힌지 또는 중간 힌지에 융합되고 및 단일 표적 항원-결합 모이어티를 포함하는 scFv는 Fc 부분의 C-말단에 융합되고; 도 4에서 2개의 CD16A 항원-결합 모이어티로 구성된 scDb는 CH2-CH3 이종이 량체로 구성된 Fc 부분의 2 개 폴리 펩타이드 중 하나의 N-말단에서 힌지 또는 중간 힌지에 융합되고 단일 표적 항원-결합 모이어티를 포함하는 scFv는 CH2-CH3 이종이량체 (KiH) Fc 부분의 다른 하나의 폴리펩티드의 N-말단에서 힌지에 융합되고; 도 5에서 CD16A 항원-결합 모이어티로 구성된 scDb는 CH2-CH3 이종이량체로 구성된 Fc 부분의 C-말단에 융합되고 단일 표적 항원-결합 모이어티를 포함하는 scFv는 힌지 또는 중간 힌지 CH2-CH3 이종이량체 (KiH) Fc 부분의 다른 하나의 폴리펩티드의 N-말단에서 힌지 또는 중간 힌지에 융합되고; 그리고 도 6에서 2개의 CD16A 항원-결합 모이어티로 구성된 scDb는 CH2-CH3 이종이량체로 구성된 Fc 부분의 C-말단에 융합되고 제 1 표적 항원-결합 모이어티를 포함하는 제 1 scFv는 Fc 부분의 N-말단에서 힌지 또는 중간 힌지에 융합되고 제 2 (그리고 제 1 과 상이한) 표적 항원-결합 모이어티를 포함하는 제 2 scFv는 CH2-CH3 이종이량체 (KiH) Fc 부분의 다른 하나의 폴리펩티드의 N-말단에서 힌지 또는 중간 힌지에 융합된다. 제 1 및 제 2 표적은 두 개의 다른 종양 관련 표적이다.
도 7-8은 CD16A, 표적 및 HSA 항원-결합 모이어티를 포함하는 이종이량체 Fab 단편-scDb 융합물인 삼중특이적 scDb-TriB 항원-결합 단백질을 보여주며, 이 때 도 7에서 2개의 CD16A 항원-결합 모이어티로 구성된 2가 scDb는 Fab 단편의 두 폴리펩티드 중 하나의 C-말단에 융합되고 2개의 표적 항원-결합 모이어티로 구성된 2가 scDb는 Fab 단편의 다른 폴리펩티드의 C-말단에 융합되고 Fab 단편의 N-말단은 HSA 항원-결합 모이어티를 제공하고; 그리고 도 8에서 2개의 CD16A 항원-결합 모이어티로 구성된 2가 scDb는 Fab 단편의 두 폴리펩티드 중 하나의 C-말단에 융합되고 단일 표적 항원-결합 모이어티로 구성된 scFv는 Fab 단편의 다른 하나의 폴리펩티드의 C-말단에 융합되고 Fab 단편의 N-말단의 Fv는 HSA 항원-결합 모이어티를 제공한다. 상기 표적은 종양 관련 표적이다.
도 9-10은 동종이량체이고 동종이량체 Fc 부분의 N-말단에서 중간 힌지에 또는 C-말단에 융합된 Db 형태의 2가 CD16A 항원-결합 모이어티 및 scFv 형태의 2개의 표적 항원-결합 모이어티를 포함하는 Db-Fc 항원-결합 단백질을 보여주며, 이 때 도 9에서 scFv는 동종이량체화 CH2-CH3 폴리펩티드의 C-말단에 융합되고 Db를 포함하는 폴리펩티드는 CH2-CH3 폴리펩티드의 N-말단에서 중간 힌지에 융합되며, 이 때 2개의 Db 폴리펩티드는 2개의 CD16A 항원-결합 모이어티를 포함하는 Db에 비-공유적으로 결합한다. 표적은 종양 관련 표적이고, 도 10에서 scFv 표적 항원-결합 모이어티는 동종이량체화 CH2-CH3 폴리펩티드의 N-말단에서 중간 힌지에 융합되고 2개의 CD16A 항원-결합 모이어티를 포함하는 Db를 포함하는 폴리펩티드는 Fc 동종이량체의 C-말단에 융합된다. 상기 표적은 종양 관련 표적이다.
도 11-12는 2개의 CD16A 항원-결합 모이어티 및 2개의 표적 항원-결합 모이어티를 포함하며 각각 scFv 형태로 Fc 동종이량체에 융합된 동종이량체 및 4가인 Bi-scFv-Fc 항원-결합 단백질을 보여주며, 이 때 도 11에서 2개의 CD16A 항원-결합 scFv는 CH2-CH3 폴리펩티드 중 하나의 N-말단에서 힌지에 융합되고 2개의 표적 항원-결합 scFv는 CH2-CH3 폴리펩티드의 C-말단에 융합되며; 그리고 도 12에서 CD16A 항원-결합 모이어티 scFv는 Fc 동종이량체에 C-말단 융합되며, 반면 표적 항원-결합 scFv는 Fc 동종이량체의 N-말단에서 힌지에 융합된다. 상기 표적은 종양 관련 표적이다.
도 13은 IgG 항체-융합물을 포함하는 scFv-IgAb 항원-결합 단백질을 보여주며, scFv 형태의 2개의 CD16A 항원-결합 모이어티는 H 사슬의 C-말단에 융합되는 반면, 2개의 표적 항원-결합 모이어티는 IgG의 Fab 아암에서 각 Fv에 의해 제공된다. 상기 표적은 종양 관련 표적이다.
도 14는 4개의 scFv 항원-결합 모이어티가 융합된 IgG 항체-융합물을 포함하는 Bi-scFv-IgAb 항원-결합 단백질을 보여주며, 여기서 scFv 형태의 2개의 CD16A 항원-결합 모이어티 각각은 H 사슬의 C-말단에 융합되는 반면, 제 1 표적에 결합하는 2개의 항원-결합 모이어티는 IgG의 Fab 아암에서 각 Fv에 의해 제공되고 제 2 표적에 결합하는 2개의 항원-결합 모이어티 각각은 2개의 CL 사슬의 C-말단에 융합된다.
도 15A 및 15B는 KiH-scFv-Fc 항원-결합 단백질을 보여주며, 여기서 4개의 항원-결합 scFv는 이종이량체 (KiH) Fc 부분에 융합되고 , 2개의 CD16A 항원-결합 모이어티는 Fc 부분의 N-또는 C-말단에서 융합된다. 도 15A는 각각 CH2-CH3 폴리펩티드 중 하나의 N-말단에서 힌지에 융합된 2개의 CD16A 항원-결합 모이어티를 가지는 KiH-scFv-Fc를 보여주며, 제 1 표적 항원-결합 모이어티를 포함하는 scFv는 CH2-CH3 폴리펩티드 중 하나의 C-말단에 융합되고 제 2 표적 항원-결합 모이어티를 포함하는 또 다른 scFv는 다른 하나의 CH2-CH3 폴리펩티드의 C-말단에 융합된다. 도 15B는 각각 CH2-CH3 폴리펩티드 중 하나의 C-말단에 융합된 2개의 CD16A 항원-결합 모이어티를 가지는 KiH-scFv-Fc를 보여주며, 제 1 표적 항원-결합 모이어티를 포함하는 scFv는 CH2-CH3 폴리펩티드 중 하나의 N-말단에서 힌지에 융합되고 제 2 표적 항원-결합 모이어티를 포함하는 또 다른 scFv는 다른 하나의 CH2-CH3 폴리펩티드의 N-말단에서 힌지에 융합된다.
도 16은 IgG 항체-융합물을 포함하는 scFv-IgAb 항원-결합 단백질을 보여주며, scFv 형태의 2개의 표적 항원-결합 모이어티는 H 사슬의 C-말단에 융합되는 반면, 2개의 CD16A 항원-결합 모이어티는 IgG의 Fab 아암에서 각 Fv에 의해 제공된다. 상기 표적은 종양 관련 표적이다.
도 17A-17N은 실시예 6에서 항체-매개 NK-NK 세포 용해 결과를 보여준다. 도 17A는 도 1에서 보는 바와 같이 N-말단에서 단량체 Fc에 융합된 디아바디 형태 (scDb)의 2개의 항-CD16A 모이어티 (및 C-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17B는 도 2에서 보는 바와 같이 C-말단에서 단량체 Fc에 융합된 디아바디 형태 (scDb)의 2개의 항-CD16A 모이어티 (및 N-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17C는 도 3에서 보는 바와 같이 N-말단에서 비대칭 Fc에 융합된 디아바디 형태 (scDb)의 2개의 항-CD16A 모이어티 (및 C-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17D는 도 4에서 보는 바와 같이 N-말단에서 비대칭 Fc에 융합된 디아바디 형태 (scDb)의 2개의 항-CD16A 모이어티 (및 N-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17E는 도 5에서 보는 바와 같이 C-말단에서 비대칭 Fc에 융합된 디아바디 형태 (scDb)의 2개의 항-CD16A 모이어티 (및 N-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17F는 도 7에서 보는 바와 같이 CL의 C-말단에서 Fab에 융합된 디아바디 형태 (scDb)의 2개의 항-CD16A 모이어티 (및 CH1의 C-말단에 TAA를 표적하는 scDb)를 보여준다. 도 17G는 도 8에서 보는 바와 같이 CH1의 C-말단에서 Fab에 융합된 디아바디 형태 (scDb)의 2개의 항-CD16A 모이어티 (및 CL의 C-말단에 TAA를 표적하는 scDb)를 보여준다. 도 17H는 도 9에서 보는 바와 같이 N-말단에서 Fc에 융합된 디아바디 (Db) 형태의 2개의 항-CD16A 모이어티 (및 C-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17I는 도 10에서 보는 바와 같이 C-말단에서 Fc에 융합된 디아바디 (Db) 형태의 2개의 항-CD16A 모이어티 (및 N-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17J는 도 11에서 보는 바와 같이 N-말단에서 Fc에 융합된 scFv 형태의 2개의 항-CD16A 모이어티 (및 C-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17K는 도 12에서 보는 바와 같이 C-말단에서 Fc에 융합된 scFv 형태의 2개의 항-CD16A 모이어티 (및 N-말단에 TAA를 표적하는 scFv)를 보여준다. 도 17L는 도 13에서 보는 바와 같이 C-말단에서 Fc에 융합된 scFv 형태의 2개의 항-CD16A 모이어티 (및 N-말단에 TAA를 표적하는 Fab 아암)를 보여준다. 도 17M은 도 15a 및 15b에서 보는 바와 같이 N-말단에서 비대칭 Fc에 융합된 scFv 형태의 2개의 항-CD16A 모이어티 (및 C-말단에서 2개의 TAA를 표적하는 2개 scFv) 및 C-말단에서 비대칭 Fc에 융합된 scFv 형태의 2개의 항-CD16A 모이어티 (및 N-말단에서 2개의 TAA를 표적하는 2개 scFv)를 보여준다. 도 17N은 C-말단에서 Fc에 융합된 TAA를 표적하는 2개의 scFv가 있는 IgG의 Fab 아암에서의 2개의 항-CD16A 모이어티 (도 16에 도시됨)를, 도 13에 도시된 바와 같이 C-말단에서 Fc에 융합된 scFv 형태의 2개의 항-CD16A 모이어티 (및 N-말단에서 TAA를 표적하는 Fab 아암)와 비교하여 보여준다.
도 18A 및 18B 상이한 항-CD16 scFv의 SPR 분석. 야생형 IgG1 및 조작된 인간 IgG1 Fc (S239D/I332E)와 비교한, 항-CD16 결합 scFv 항체 (Ab16고, Ab16중, 3G8, Ab16저)에 관한 정규화된 상대 결합 신호의 SPR 센소그램. 도 18A는 인간 CD16A-158V에 대한 강화된 결합을 보여준다. 도 18B는 인간 CD16A-158F에 대한 결합을 보여준다. 분석물은 312.5 nM의 단일 농도에서 측정되었다.
도 19A-19C는 위치 140의 티로신 (Y)이 scFv 항체의 입체형태 에피토프의 형성 및 CD16A-특이적 반응성에 중요함을 보여준다. 단량체 Fc 또는 막 앵커가 있는 ECD 서열들의 융합 단백질로서 발현된 상이한 재조합 CD16 변이체들을 분석하였다. 도 19A는 제시된 CD16 결합 scFv와의 반응성에 대해 테스트되었던, 니트로셀룰로스 막 상에서 정의된 CD16 항원 변이체들을 함유하는 단백질 스팟들을 보여준다. 도 19B는 항체 염색 및 유세포 분석에 의해 분석한, EGFR 막경유 도메인 또는 GPI에 대한 융합을 통해 고정된, CHO 세포상에서 발현된 상이한 항-CD16 scFv, 대조 scFv, 또는 mAbs와 CD16 항원 변이체 또는 EGFR 항원의 반응성을 보여준다. 도 19C는 SDS-PAGE 및 웨스턴 블롯으로 분리한 이후 CD16 항원 변이체들에 대한 상이한 항-CD16 항체들의 결합을 보여준다.
도 20은 항-CD16 결합 도메인 (Ab16저, Ab16중, Ab16고, 3G8)의 인간 CD16A-158V 및 인간 CD16A-158F에 대한 결합에 관한 SPR 센서그램을, 인간 IgG1 Fc-야생형, 인간 IgG1 Fc 강화 (S239D/I332E), 인간 IgG1 Fc-침묵 (L234F/L235E /D265A)과 비교하여 보여준다. KD 값은 1:1 결합 모델을 사용하여 계산되었으며 표 5에 나타낸다. 가로축: 반응 (RU), 세로축: 시간 [초].
도 21은 본원에 기재된 특정 실험에서 재조합 항원으로 사용된 인간 및 시노몰구스 CD16A 및 인간 CD16B 변이체의 ECD 서열들의 서열 정렬을 보여준다. 인간 CD16A 또는 CD16B에서 다형성이 있는 위치는 각각 얇은 그리고 두꺼운 화살표로 표시된다. 기호 '#'은 인간 CD16B를 GPI 막 앵커에 연결하는 위치를 표시하고, 'd'로 표시된 위치는 성숙한 CD16B 항원 서열에서 절단된다. 시노몰구스 CD16A ECD 서열에서의 변이는 볼드체로 표시한다. 인간 CD16A와 인간 CD16B 간 서열 변이가 있는 위치는 괄호로 표시한다 (테스트 항-CD16 항체의 CD16A-특이적 결합에 중요). CLUSTAL O (1.2.4) 다중 서열 정렬 도구가 정렬에 사용되었다.
도 22는 CD16A에 대한 mAb 3G8과 상이한 항-CD16 scFv 항체들의 결합 경쟁을 ELISA로 보여준다. CD16A-158V ECD-Fc 융합 항원으로 코팅된 플레이트들을 1 nM의 mAb 3G8과 지시된 농도 범위의 상이한 항-CD16 scFv들의 연속 희석액의 혼합물과 함께 배양하였다. CD16A-결합된 mAb 3G8은 퍼옥시다제 접합된 염소 항-마우스 IgG(H+L)로 탐지되었다. TMB 기질 반응을 450nm에서 측정하고 (Ext (450nm)), 플롯하고 분석하였다.
도 23은 ROCK® 플랫폼 개요를 보여준다.
도 24A-24C 는 다양한 CD16A 2가 결합 ROCK® 관여항체들의 정규화된 상대 결합 해리 상들의 SPR 센소그램을 보여준다. scFv-IgAb_C, Db-Fc_A, scFv-IgAb_D, KiH-scDb-Fc_A, TandAb_C를 내포하는 2가 항-CD16A 도메인들을 IgAb_E (Fc-강화; S239D/I332E) 및 1가 항-CD16A 단편 scFv Ab16고 on 고정화된 인간 CD16A-158V 및 시노몰구스 CD16에서 IgAb_E (Fc-강화; S239D/I332E) 및 1가 항-CD16A 단편 scFv Ab16고와 비교하였다. 도 24A는 고정된 인간 CD16A-158V에 대한 SPR 센소그램을 보여준다. 도 24B는 시노몰구스 CD16에 대한 SPR 센소그램을 보여준다. 도 24C는 3시간의 해리 후 수용체에 남아있는 항체의 범례 및 백분율을 보여준다. 분석물은 50 nM의 단일 농도에서 측정되었다.
도 25는 NK 세포상의 IgG와 비교하여 ROCK® 항체의 세포 표면 잔류를 보여준다. 농축된 일차 인간 NK 세포들에 100 μg/mL TandAb 또는 400 μg/mL IgG를 45분 동안 얼음위에서 사전부하하고, 세척하고 37°C에서 지시된 시간 동안 배양하여 해리시켰다. 세척 후, 나머지 항체들을 His-태그된 가용성 BCMA, 그리고 이어서 10 μg/mL mAb 항-His 및 15 μg/mL FITC-접합 염소 항-마우스 IgG로 탐지하였다. 시점 0에서 평균 형광 강도를 100%로 설정하고 나머지 항체의 백분율을 비선형 회귀를 사용하여 플롯했다.
도 26A-26C은 ROCK® 형태에 있어서 CD16A 겉보기 친화성이 가변 도메인, 위치 및 연결기 길이에 의해 조정가능함을 보여준다. 상이한 위치에서 상이한 CD16 결합 Fv (Ab16중, Ab16고) (N: Fc의 항-CD16 Fvs N-말단, C: Fc의 항-CD16 Fvs C-말단), 항체 형태들, 및 상이한 도메인 순서를 내포하는 ROCK® 항체들에 대한 가용성 CD16 항원의 결합을 ELISA로 분석하였다. 점선 기호로 표시된 CD16 결합 Fv가 있는 대표적인 픽토그램은 각 그룹 아래에 표시된다. 도 26A는 Fab 또는 scFv-기반 CD16 관여에 의한 CD16A 겉보기 친화성의 요약을 보여준다. 도 26A는 디아바디 (Db)-기반 CD16 관여에 의한 CD16A 겉보기 친화성의 요약을 보여준다. 도 26C는 상이한 연결기 길이 (10aa 또는 30aa) 및 도메인 순서의 항-CD16 Fv (HL: scFv 도메인 순서 VH-VL, LH: scFv 도메인 순서 VL-VH)를 포함하는 C-말단 scFv-기반 CD16 관여에 의한 CD16A 겉보기 친화성의 요약을 보여준다. 분석된 모든 항체는 침묵된 Fc를 내포하거나 Fab의 C-말단에 융합된 경우 Fc가 없다. 검은색 또는 음영으로 도시된 결합 특이성은 BCMA, CD19, CD20, EGFR, HSA 또는 RSV를 표적하는 항체 도메인들을 포함하였다.
도 27A-27C는 인간 IgG의 존재 또는 부재시 일차 인간 NK 세포에 대한 ROCK® 항체의 결합을 보여준다. 도 27A는 일차 인간 NK 세포들이 37°C에서 10 mg/mL 다클론 인간 IgG의 존재 또는 부재시 제시된 증가된 농도의 무-Fc ROCK®로 염색되었음을 보여준다. 도 27B는 일차 인간 NK 세포들이 37°C에서 10 mg/mL 다클론 인간 IgG의 존재 또는 부재시 제시된 증가된 농도의 Fc 융합 ROCK®로 염색되었음을 보여준다. 도 27C는 일차 인간 NK 세포들이 37°C에서 10 mg/mL 다클론 인간 IgG의 존재 또는 부재시 제시된 증가된 농도의 IgG-유사 ROCK® 구조체들로 염색되었음을 보여준다. 세포 결합 항체들은 유세포 분석으로 탐지하였으며, 비-선형 회귀에 의한 겉보기 친화성 (K D ) 계산에 중앙 형광 광도 (MFI)를 사용하였다.
도 28은 시험관내 NK 동족살해에 관한 다양한 ROCK® 항체 형태들의 비교 분석을 보여준다. 1:1의 E:T로 4시간 공-배양 후 상이한 ROCK® 항체 형태들의 존재시 자가 NK 세포들에 대한 농축된 일차 인간 NK 세포들의 시험관내 칼세인-방출 세포독성. 여러 독립 실험들의 평균 EC50 값을 요약하고 개별 점들로 플롯한다. ROCK® 항체 형태들을 항-CD16 도메인의 위치 및 형태/도메인 순서에 기초하여 분류한다. 고 친화성 항-CD16 도메인 및 침묵된 Fc를 내포하는 구조체들만이 그래프에 포함되었다. HL: scFv 도메인 순서 VH-VL, LH: scFv 도메인 순서 VL-VH. N-term. = N-말단, C-term. = C-말단.
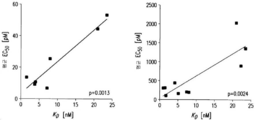
도 29A-29E는 상응하는 종양 표적을 발현하는 세포주에 대한 여러 ROCK® 항체의 존재시 농축된 일차 인간 NK 세포의 시험관내 세포 독성을 보여준다. 도 29A는 5:1의 E:T 비율에서 SABC 값들 (≥3회 분석의 평균)로 나타내었을 때 상이한 수준의 BCMA를 발현하는 표적 세포주 NCI-H929 및 NK 세포들을 사용하여 4시간 칼세인-방출 세포독성 분석에서 제시된 BCMA-표적화 ROCK® 항체들의 대표적인 S형 용량-반응 곡선을 나타낸다. 도 29B는 5:1의 E:T 비율에서 SABC 값들 (≥3회 분석의 평균)로 나타내었을 때 상이한 수준의 BCMA를 발현하는 표적 세포주 MM.1S 및 NK 세포들을 사용하여 4시간 칼세인-방출 세포독성 분석에서 제시된 BCMA-표적화 ROCK® 항체들의 대표적인 S형 용량-반응 곡선을 나타낸다. 도 29C는 5:1의 E:T 비율에서 SABC 값들 (≥3회 분석의 평균)로 나타내었을 때 상이한 수준의 BCMA를 발현하는 표적 세포주 MC/CAR 및 NK 세포들을 사용하여 4시간 칼세인-방출 세포독성 분석에서 제시된 BCMA-표적화 ROCK® 항체들의 대표적인 S형 용량-반응 곡선을 나타낸다. 도 29D는 5:1의 E:T 비율에서 NK 세포 및 SW-982 표적 세포를 사용한 4시간 칼세인-방출 세포독성 분석에서 제시된 EGFR-표적화 ROCK® 항체, 비교인자, 또는 1가 결합 대조의 대표적인 S형 용량-반응 곡선들을 보여준다. 도 29E는 시험관내 종양 표적 세포에 대한 NK 세포 결합 친화성 및 세포독성 역가에 관한 ROCK® 항체의 상관관계를 보여준다. 일차 인간 NK 세포에서 ROCK® 항체 형태들의 겉보기 친화성 (KD)을 나타낸다. 동일한 ROCK® 항체들의 EC50 값들은 2:1의 E:T 비율에서 NK 세포 및 BCMA-발현 RPMI-8226 표적 세포들을 이용한 3시간 칼세인-방출 세포독성 측정에서 (왼쪽) 또는 5:1의 E:T 비율에서 NK 세포 및 BCMA-발현 NCI-H929 표적 세포를 사용한 4시간 칼세인-방출 세포독성에서 (오른쪽) 결정되었다. SABC, 특이적 항체-결합능.
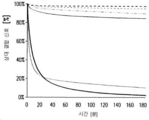
도 30은 다양한 ROCK® 관여항체 형태들의 약동학 비교를 보여준다: 300 μg 테스트 항목의 단회 i.v. 투여 후 시간에 따른 (1 또는 3주 관찰 기간) 항체 농도.
도 31A-31B는 CD16A-158V/V 건강한 공여체 (실선) 및 CD16A-158F/F (점선)에 대한 CD16A/BCMA 항체의 세포독성을 보여준다. 도 31A는 NCI-H929 세포주의 결과를 보여준다. 도 31B는 MM.1S 세포주에 대한 결과를 보여준다.
도 32A-32E는 다발성 골수종 세포주에서 CD16A/BCMA 항체 I의 시험관내 세포독성을 보여준다. 165K의 PBMC 당 CD56+CD3e-NK 세포의 대략적인 수는 약 ~8000개 세포였으므로, NK:종양 비율은 ~0.4였다 (MM 환자 NK 대 종양 세포 비율을 추정하는 임상 데이터와 유사; 데이터 도시하지 않음). 도 32A는 건강한 인간 혈액 공여체로부터 분리되어 차후 실험을 위해 냉동시킨 인간 PBMC를 보여준다. 해동시 PBMC는 트리판 블루 염색에 의해 ~85% 생존가능하였으며 추후 7AAD를 사용하는 FACS에 의해 확인되었다. PBMC (~165K)를 BCMA+ 다발성 골수종 종양 세포주 (~20K)와 공배양하였고, 5% CO2와 함께 37°C에서 약 20시간 동안 0.1 - 3000pM의 3-배 연속 희석 테스트 항목들에 노출시켰다. 165K의 PBMC 당 CD56+CD3e-NK 세포의 대략적인 수는 약 ~8000개 세포였으므로, NK:종양 비율은 ~0.4였다 (MM 환자 NK 대 종양 세포 비율을 추정하는 임상 데이터와 유사; 데이터 도시하지 않음). 도 32B-32E에서 보는 바와 같이, 항체 염색 및 FACS를 사용하여 MM 종양 세포에서 BCMA 발현을 결정하고 다발성 골수종 표적 세포의 세포독성을 모니터하였다. 데이터는 소프트웨어 프로그램 FlowJo 및 GraphPad Prism 6으로 분석되었다. 도 32B는 NCI-H929 세포주를 나타내고, 도 32C는 RPMI-8226 세포주를 나타내고, 도 32D는 MM.1S 세포주를 나타내고, 도 32E는 MOLP-2 세포주를 나타낸다. 비-BCMA 표적화/CD16a 음성 대조는 열린 기호로 표시한다. CD16A/BCMA 항체 I은 채워진 기호로 표시한다.
도 33A-33C는 다발성 골수종 세포주에서 CD16A/BCMA 항체 I의 시험관내 세포독성을 보여준다. 도 33A는 NCI-H929 세포주를 나타내고, 도 33B는 RPMI-8226 세포주를 나타내고, 도 33C는 MM.15 세포주를 나타낸다. 비-BCMA 표적화/CD16a 음성 대조는 채워지지 않은 사각형으로 표시한다. CD16A/BCMA 항체 I은 솔리드 원으로 표시한다. 다라투무맙 ("Dara")은 채워진 사각형으로 표시한다.
도 34A-34C는 다발성 골수종 세포주에서 CD16A/BCMA 항체 I의 시험관내 세포독성을 보여준다. NK 세포는 BCMA+ 다발성 골수종 종양 세포주와 E:T ~4-5로 공배양되었다. 공여체 A - NK 및 종양 세포를 NK 세포 및 테스트 항목을 첨가하기 전 적어도 30분 동안 0.5 mg/ml 저 내독소 hIgG와 함께 사전배양하였다. 공여체 B-사전배양 단계 없음. 도 34A는 공여체 A에 대한 BCMA+ 표적 세포의 고갈을 보여준다.도 34B는 공여체 B에 대한 SK-MM-2의 고갈을 보여준다.도 34C는 공여체 B에 대한 MOLP-2의 고갈을 나타낸다. 도 34B 및 34C에서, 비 -BCMA 표적화/CD16a 음성 대조는 열린 기호로 표시되고 CD16A/BCMA 항체 I는 채워진 기호로 표시된다.
도 35A-35D는 낮은 BCMA 발현 Raji 종양 세포주에 대한 CD16A/BCMA 항체 I, CD16A/BCMA 항체 II 및 CD16A/BCMA 항체 III의 시험관내 세포독성을 보여준다. 거의 탐지불가능한 BCMA 표면 발현에도 불구하고 BCMA+ 표적 세포의 시험관내 용해가 관찰된다. 이러한 시험관내 세포독성 분석은 농축된 일차 인간 NK 세포들, E:T 5:1의 4시간 칼세인-방출 분석을 사용하여 수행되었다. 도 35A는 Raji 세포주의 용해를 보여준다. 도 35B는 Raji 세포주의 세포독성을 보여준다. 도 35C는 시판되는 항-BCMA 항체 및 아이소형에 의해 탐지된 BCMA 발현을 보여준다. 도 35D는 CD16A/BCMA 항체 I, CD16A/BCMA 항체 II, CD16A/BCMA 항체 III, BCMA (Fc 침묵) 및 아이소형에 의해 탐지된 BCMA 발현을 보여준다.
도 36A-36C는 낮은 BCMA 발현 Raji 종양 세포주에 대한 CD16A/BCMA 항체 I의 시험관내 세포독성을 보여준다. 도 36A는 Raji 세포에서의 BCMA 발현을 보여준다. 도 36B는 NCI-H929 (MM 양성 대조) 세포에서의 BCMA 발현을 보여준다. (A) 및 (B)의 경우, APC에 접합된 시판 항-BCMA를 Raji 및 NCI-H929 (MM 양성 대조) 세포에서 BCMA 발현의 정량화에 사용했다. (C) Raji 세포 및 H929 세포의 세포독성. CD16A/BCMA 항체 I은 채워진 기호로 표시되고 비-BCMA 표적화/CD16a 음성 대조는 열린 기호로 표시된다.
도 37A 및 37B는 자가 BCMA+ 정상 인간 형질 세포에 대한 CD16A/BCMA 항체 I의 시험관내 활성을 보여준다. 도 37A는 양성 대조로서 동종이계 세포를 보여준다. 도 37B는 자가 BCMA+ 정상 인간 형질 세포를 보여준다. CD16A/BCMA 항체 I은 채워진 기호로 표시되고 비-BCMA 표적화/CD16a 음성 대조는 열린 기호로 표시된다.
도 38A-38C는 BCMA+ 표적 세포의 존재시 CD16A/BCMA 항체 I에 의한 NK 세포상의 CD16 활성화를 보여준다. 도 38A는 NK-CD16+ 세포의 수를 보여준다. 도 38B는 NKCD69+CD25+ 세포의 수를 보여준다. 도 38C는 표적 세포의 수를 보여준다.
도 39A 및 39B는 BCMA+ 표적 세포의 부재시 CD16A/BCMA 항체 I에 의한 NK 세포상의 CD16 활성화를 보여준다. 도 39A는 NK-CD16+ 세포의 수를 보여준다. 도 39B는 NKCD69+CD25+ 세포의 수를 보여준다.
도 40A-40E는 혈청의 존재시 CD16A/BCMA 항체 I의 NK 세포에 대한 결합 및 CD16A/BCMA 항체 I의 세포독성을 보여준다. 도 40A는 외인성 인간 Ig의 존재시 항-BCMA/CD16a의 결합을 보여준다. 새로이 준비된 인간 NK 세포들을 10 mg/mL의 SCIG (Hizentra)와 함께 및 없이 37C에서 1-시간 동안 사전-배양한 다음, 제시된 농도의 DyLight650 표지된 항-AFM26/CD16a로 염색하였다. 도 40B는 100% 자가 인간 혈청의 존재시 항-BCMA/CD16 유도된 표적 세포 용해를 보여준다. 다발성 골수종 세포주 NCI-H929를, 이펙터 세포로서 새로이 준비된 인간 NK 세포를 사용하여 제시된 농도의 CD16A/BCMA 항체 I로 처리했다. CD16A/BCMA 항체 I을 첨가하기 전에, 세포를 37°C에서 30분 동안 동일한 건강한 공여체로부터의 열-불활성화된 자가 인간 혈청과 함께 사전 배양하였다. 도 40C 및 40D는 항-BCMA/CD16a가 NK 세포의 손실없이 50% 자가 인간 혈청의 존재시 BCMA+ 표적 세포를 고갈시킨다는 것을 보여준다. 도 40C 및 40D에서 CD16A/BCMA 항체 I이 예로서 사용된다. 도 40C 및 40D에서 건강한 인간 혈액 공여체로부터 인간 NK 세포를 분리했다. NK (도 40D) 및 MM.1S 세포들 (도 40C)을 분석 셋업 전에 2시간 동안 50% 인간 자가 혈청에서 별도로 사전배양하였다. NK 세포를 MM.1S 종양 세포주와 대략 5의 E:T 비율로 공배양하고, 5% CO2와 함께 37°C에서 약 20시간 동안 0.1 - 100pM의 10-배 연속 희석 테스트 항목들에 노출하였다. CD138 및 CD56를 이용한 항체 염색 후 FACS를 사용하여 MM.1S 표적 세포의 세포독성 및 NK 생존을 모니터하였다. 데이터는 소프트웨어 프로그램 FlowJo 및 GraphPad Prism 6으로 분석되었다. Ab-1, 비-BCMA 표적화/CD16a 음성 대조는 열린 기호로 표시한다. BCMA/CD16a 항체 I은 채워진 기호로 표시한다. 도 40E는 2차 R/R MM이 항-BCMA/CD16A 항체로 치료하기 위한 표적 적응증임을 보여준다. 본 예에서, BCMA/CD16A 항체 I이 예로서 사용된다. 구체적으로, 이 도면의 데이터는 항-BCMA/CD16A 항체 (예시 목적으로 사용된 BCMA/CD16A 항체 I)가 항-CD38 항체 (다라투무맙)와 구별됨을 보여준다. 다라투무맙은 MM에서 보체 의존성 세포 독성 활성 (de Weers, M. 외 2011. J. Immun. 186(3):1840-1848) 및 CD38의 교차 결합을 통한 신호전달에 의해 세포자멸사를 유도하는 능력 (Overdijk, M.B., 외, 2016 J. Immun. 197(3):807-813)을 가지는 반면, BCMA/CD16A 항체 I는 이러한 활성을 가지지 않는다. 더욱이, 다라투무맙과 달리 BCMA/CD16A 항체 I의 활성은 도 41A 및 41B에서 보는 바와 같이 Fc 매개 약물의 활성을 감소시키는 CD16A 다형성에 의해 영향을 받지 않는다. 전체적으로, 도 40E는 BCMA/CD16A 항체 I이 NK 세포 (CD38 양성)를 고갈시키지 않지만 다라투무맙은 고갈시킨다는 것을 보여준다.
도 41A 및 41B는 BCMA+ 표적 세포의 부재하에 CD16A 발현 및 NK 세포의 활성화에 대한 혈청의 영향을 보여준다. 또한, 혈청의 존재시 낮은 CD16 발현은 NK 세포의 비-CD16A 매개 활성화를 시사한다. 도 41A는 혈청에 의한 보다 낮은 CD16A 탐지를 보여준다. 도 41B는 혈청에 의한 더 높은 비-표적 매개 활성화를 보여준다.
도 42A-42C는 IL-15 처리가 MM 세포에 대한 항-CD16A/BCMA 항체의 활성을 증가 시켰음을 보여준다. 도 42A는 a) 항체 없음, b) 음성 대조 1, c) 음성 대조 2, d) BCMA/CD16A 항체 I, e) 항-BCMA/CD19 항체, 및 f) 다라투무맙으로 처리된 종양 세포들의 용해 퍼센트를 보여준다. 도 42B는 a) 항체 없음 + IL-15, b) 음성 대조 1 + IL-15, c) 음성 대조 2 + IL-15, d) BCMA/CD16A 항체 I + IL-15, e) 항-BCMA/CD19 항체 + IL-15, 및 f) 다라투무맙 + IL-15으로 처리된 종양 세포들의 용해 퍼센트를 보여준다. 도 42c는 도 42A 및 42B에 도시된 음성 대조 # 1, 음성 대조 # 2 및 BCMA/CD19의 구조를 도시한다.
도 43은 다라투무맙 나이브 환자, 다라투무맙 불응성 환자들의 말초 혈액 내 NK 세포들의 수를 보여준다. 도 43은 아테졸리주맙 시험에 대한 기준선에서의 말초 혈액에서의 NK 유동 데이터 (절대 수/uL)를 보여준다. NK 세포는 CD56/CD16+림프구: CD45xSSC 낮은 집단 (표준 게이팅)으로 게이팅된 다음, CD56/CD16 + 집단으로 서브게이팅되었다. 아테졸리주맙에서 Dara 불응성 환자의 NK 수준은 Dara 나이브보다 낮았고 건강한 공여체 범위 (점선들 사이의 영역)보다 낮았다.
도 44는 R/R MM 환자 골수에서 NK/종양 비율을 보여준다.
도 45A 및 45B는 CD16A/BCMA 항체 I를 사용한 세포주의 시험관내 사멸을 보여준다. CD16A/BCMA 항체 I은 채워진 원으로 표시되고, 다라투무맙 ("Dara")은 채워진 사각형으로 표시되고, NTx16a, 비-표적화 항-CD16A 이중특이적 항체는 채워지지 않은 사각형으로 표시된다. 도 45A에서, E:T는 0.05였다. 도 45B에서, E:T는 0.5였다.
도 46A-46D는 CD16A/BCMA 항체 I 및 CD16A/BCMA 항체 II의 세포독성에 대한 새로운 NK 세포들의 영향을 보여준다. "새로이 준비된 NK 세포"는 같은 날 새로 분리된 PBMC에서 정제된 NK 세포를 나타낸다. "2일차 NK 세포"는 1일차에 분리된 PBMC에서 정제되고 RPMI 배지에서 밤새 배양된 NK 세포를 나타낸다. 도 46A는 NCI-H929 세포에서 새로이 준비된 NK 세포의 세포독성을 보여준다. 도 46B는 MM.1S 세포에서 새로이 준비된 NK 세포의 세포독성을 보여준다. 도 46C는 NCI-H929 세포에서 2일차 NK 세포의 세포독성을 보여준다. 도 46D는 MM.1S 세포에서 2일차 NK 세포의 세포독성을 보여준다.
도 47은 냉동된 일차 골수종 골수 단핵 세포 (BMMC)에서 FcRH5, BCMA 및 CD38의 발현을 보여준다. 20명의 공여체 및 대조 (골수종 세포주 MOLP-2)로부터 얻은 냉동된 일차 골수종 골수 단핵구 세포 (BMMC)를 FcRH5, BCMA (Biolegend 19F2), CD38 세포 표면 발현에 대해 평가하였다. 요약하면, BMMC를 해동하고 멸균 PBS로 세척한 다음, 1x10^6 세포/mL의 최종 농도로 재현탁시켰다. BMMC는 생존력 및 골수종 마커 (CD45, CD319, CD138, CD38, BCMA, FcRH5)로 염색되었다. 세포를 고정하고 세척한 후, 세포들을 Canto II에서 판독하였다. 생존/단일항/CD45-/CD319+ 세포들 (골수종 세포들)을 선택하여 FlowJo에서 FcRH5, BCMA, 및 CD38의 분석을 실시하였다. FcRH5, BCMA 및 CD38에 대한 MESF (Log10) 값을 통계 플롯팅 소프트웨어 Prism에서 플롯하였다.
도 48A 및 48B는 정상 인간 형질 세포 및 일차 MM 세포에 대한 BCMA 발현을 보여준다. 도 48A는 정상 인간 형질 세포에 대한 BCMA의 발현을 보여준다. 도 48B는 냉동 일차 골수종 BMMC에서 BCMA 발현의 한 예를 보여준다. 도 48A 및 48B 모두에서, BCMA를 사용하여 도 47에서 상기 설명한 프로토콜에 따라 세포를 염색하고 게이팅한 다음, 최대%를 FlowJo에서 플롯하였다. 회색 음영 피크는 형광 마이너스 1 (FMO) 대조이고 적색 피크는 BCMA 발현이다.
도 49A-49F는 ROCK 관여항체에 의한 NK 세포 활성화 및 IFN-γ 방출의 유도가 표적 세포의 존재에 엄격하게 의존함을 보여준다. 도 49A-49C는 BCMA+ RPMI-8226 표적 세포의 존재 및 부재시 증가하는 농도의 BCMA/CD16A ROCK 관여항체 TandAb_A, scFv-IgAb_D 및 KiH-scDb-Fc_A에서 PBMC 배양물에서 CD69+ NK 세포의 백분율을 보여준다. 도 49A는 TandAb_A, 도 49B는 scFv-IgAb_D, 도 49C는 KiH-scDb-Fc_A에 관한 것이다. 인간 PBMC를 증가하는 농도의 항체 존재시 (사각형) 또는 항체 없이 (삼각형) RPMI-8226 표적 세포와 함께 (채워진 기호) 또는 없이 (열린 기호) (E:T 비율: 50:1) 배양하였다. 22시간 배양 후, CD56+ NK 세포에서의 CD69 표면 발현을 유세포 분석으로 분석하였다. 도 49D-49F는 새로이 분리된 인간 PBMC가 10 μg/mL TandAb_A, scFv-IgAb_D 또는 KiH-scDb-Fc_A와 함께 또는 없이 50:1의 E:T 비율로 BCMA + NCI-H929 세포의 존재 또는 부재하에 배양되었음을 보여준다. 도 49D는 TandAb_A, 도 49E는 scFv-IgAb_D, 도 49F는 KiH-scDb-Fc_A에 관한 것이다. 24시간 배양 후, 상청액에서 IFN-γ 농도를 정량하였다. *: 하한 탐지 한계 미만.
도 50은 BCMA-지시된 T 세포 관여항체 및 ROCK 관여항체에 의해 유도된 인간 PBMC 배양물에서 염증성 사이토카인 방출의 비교를 보여준다. 새로이 분리된 인간 PBMC를 증가하는 농도의 BCMA/CD3 BiTE, 또는 NK-세포 관여 ROCK 관여항체 scFv-IgAb_D 또는 KiH-scDb-Fc_A의 존재 또는 부재시 BCMA+ 세포주 NCI-H929 (E:T 비율 50:1)와 공배양하였다. 24시간 배양 후, 상청액에서의 사이토카인 농도를 정량하였다. 대조: 첨가된 항체 없음.
도 51은 여러 ROCK® 항체 형태의 존재시 A-431 세포에 대한 농축된 일차 인간 NK 세포의 시험관내 세포독성을 보여준다. 5:1의 E:T 비율에서의 4시간 칼세인-방출 세포독성 분석에서 제시된 EGFR-표적화 ROCK 항체의 대표적인 S형 용량-반응 곡선들. SABC, 특이적 항체-결합능 (≥3회 분석의 평균값).
도 52A-52D는 경쟁 다클론, 단클론, 또는 Fc-강화된 IgG의 존재 또는 부재시 시험관내 세포독성 분석에서 ROCK® 및 IgG 항체의 비교를 보여준다. CD30/CD16A TandAb, 항-CD30 IgG1 (IgAb), 또는 Fc-매개 이펙터 기능 강화 돌연변이 S239D/I332E가 있는 항-CD30 IgG1 (IgAb (Fc-강화))의 연속 희석물의 존재하에서 이펙터 세포로서 일차 인간 NK 세포들과 칼세인-표지된 CD30+ KARPAS-299 표적 세포들을 5:1의 E:T 비율로 이용한 4시간 칼세인-방출 세포독성 분석. 분석은 RPMI 1640 배지, 또는 10 mg/mL 다클론 인간 IgG, 10 mg/mL 단클론 인간 항-EGFR IgG1 (IgAb), 또는 10 mg/mL Fc-강화된 단클론 인간 항-EGFR IgG1 (IgAb (Fc-강화))로 보충한 배지에서 수행되었다. 도 52A는 RPMI 1640 배지를 보여준다. 도 52B는 10mg/mL 다클론 인간 IgG가 보충된 배지를 보여준다. 도 52C는 10mg/mL 단클론 인간 항-EGFR IgG1을 보여준다. 도 52D는 10mg/mL Fc-강화 단클론 인간 항-EGFR IgG1을 보여준다.
도 53A-53D는 CD16A/BCMA 항체 I의 BCMA-표적화 모이어티 및 CD16A 항원-결합 모이어티의 서열을 보여준다. 도 53A는 CD16A/BCMA 항체 I의 BCMA-표적화 모이어티의 CDR 서열을 보여준다. 도 53B는 CD16A/BCMA 항체 I의 BCMA-표적화 모이어티의 중쇄 및 경쇄 가변 영역 서열을 보여준다. 도 53C는 CD16A/BCMA 항체 I의 CD16A 항원-결합 모이어티의 CDR 서열을 보여준다. 도 53D는 CD16A/BCMA 항체 I의 CD16A 항원-결합 모이어티의 중쇄 및 경쇄 가변 영역 서열을 보여준다.
발명의 상세한 설명
I.
정의
용어 "다중특이적"은 적어도 2개의 상이한 에피토프, 특히, 상이한 항원의 에피토프에 결합하는 항원-결합 부위를 포함하는 항원-결합 분자를 지칭한다. "다중특이적"은 이중 특이 적, 삼중 특이 적 및 사중 특이 적을 포함하지만 이에 제한되지 않는다.
용어 "-가"는 항원-결합 단백질에서 결정된 수의 항원-결합 모이어티의 존재를 나타낸다. 천연 IgG는 2개의 항원-결합 모이어티를 가지며 2 가이다. 본 발명에 따른 항원-결합 단백질은 적어도 3가이다. 4가, 5가 및 6가 항원-결합 단백질의 예가 본원에 기재되어있다.
용어 "폴리펩티드"는 아미드 결합에 의해 연속적으로 연결된 아미노산 잔기의 중합체를 지칭한다. 특정 구체예에서, 용어 "폴리펩티드"는 일반적으로 30개 이상의 아미노산으로 구성된 분자들의 그룹을 지칭한다. 폴리펩티드는 이량체, 삼량체 및 고등 올리고머, 즉, 하나 이상의 폴리펩티드 분자로 구성된 다량체를 또한 형성 할 수 있다. 이러한 이량체, 삼량체 등을 형성하는 폴리펩티드 분자는 동일하거나 동일하지 않을 수 있다. 이에 해당하는 이러한 다량체의 고차 구조는 결과적으로 동종 또는 이종이량체, 동종 또는 이종삼량체 등으로 명명된다. 이종 다량체의 예는, 자연 발생 형태에서, 두 개의 동일한 경쇄 폴리펩티드 사슬과 두 개의 동일한 중쇄 폴리펩티드 사슬로 구성된 항체 분자이다. 용어 "펩티드", "폴리펩티드"및 "단백질"은 또한, 예를 들어, 당화, 아세틸화, 인산화 등과 같은 번역 후 변형에 의해 변형이 이루어진 자연적으로 변형된 펩티드/폴리펩티드/단백질을 지칭한다. 본원에서 언급되는 "펩티드", "폴리펩티드" 또는 "단백질"은 또한 페길화와 같이 화학적으로 변형 될 수도 있다. 이러한 변형은 당업계에 잘 공지되어 있으며 아래에서 설명된다.
"Fv 폴리펩티드"는 항체 가변 (Fv) 도메인들이 차례로 연결된 융합 폴리펩티드를 의미한다. 상기 폴리펩티드는 N-말단 및/또는 C-말단 서열 연장부 이외에도 연속적인 아미노산 잔기를 가질 수있다. 예를 들어, 상기 폴리펩티드는 폴리펩티드의 정제 뿐만 아니라 탐지에 유용 할 수 있는 태그 서열을, 바람직하게는 C-말단에 포함 할 수있다. 태그 서열의 예는 히스티딘-태그, 예를 들어, 6 개의 His-잔기로 구성된 His-태그 (서열 번호:58), 또는 C-태그, 예컨대, EPEA 테트라펩티드 (서열 번호:59)이다. 다량체 항원-결합 분자의 경우, 상이한 태그 서열들이 상이한 폴리펩티드들에, 예컨대, 이종이량체 분자의 제 1 폴리펩티드에 His-태그 그리고 제 2 폴리펩티드에 C-태그가 사용될 수 있다. 특정 구체예에서 상기 폴리펩티드는 항원-결합 부위 및 불변 항체 도메인을 제공하는 가변 도메인, 예를 들어, CL, CH1CH 및/또는 폴리펩티드에 연결된 Fc 부분 (CH2-CH3)을 포함한다. 예를 들어, 이러한 구체예는 적어도 하나의 불변 항체 도메인, 예를 들어, Fc 부분에 융합된 Fv 폴리펩티드를 포함한다. 추가 구체예에서, 상기 폴리펩티드는 또 다른 물질, 예를 들어, 독소, 면역-조절제 또는 신호 생성제에 연결될 수 있다.
용어 "Fc 부분"은 면역글로불린 H 사슬의 C-말단 부분을 포함하고 IgG 영역의 Fc-영역의 적어도 하나의 기능성, 특히, FcRn에 대한 결합 기능을 보유하는 폴리펩티드를 지칭한다. 항체 이펙터 기능은 Fc 영역의 서열들에 의해 결정된다. Fc 부분은 CH2 도메인, CH3 도메인 또는 CH2-CH3 폴리펩티드 사슬을 포함 할 수 있다. CH2-CH3 폴리펩티드 사슬은 또 다른 CH2-CH3 폴리펩티드 사슬과 함께 서로 결합된 2개의 CH2-CH3 폴리펩티드들의 이량체로 조립되며, 이 때 이량체화는 CH2 도메인에 대한 힌지 영역 NC-말단에서 공유 결합에 의해 촉진된다. 따라서, 일부 구체예에서 Fc 부분은 2개의 CH2-CH3 폴리펩티드 사슬들의 이량체 및 힌지 영역을 포함한다. 바람직하게는, Fc 부분은 Ig 클래스의 불변 도메인, 예를 들어, IgA, IgD, IgE, IgM, 바람직하게는 IgG1, IgG2, IgG2, IgG4, 특히, IgG1 불변 도메인을 포함한다. 경쇄 불변 영역 (CL)은 카파 (κ), 람다 (λ) 및 시그마 (σ)로부터 선택 될 수 있으며, 여기서 인간 람다 클래스는 서브클래스 람다 1-4를 갖는다.
"힌지"도메인은 Fc 부분과 동일하거나 상이한 IgG 클래스이거나 자연적으로 발생하지 않는 조작된 힌지 도메인 일 수 있다. IgG 힌지 영역의 예는 서열 번호:23에 제시된 아미노산 서열을 가진다. 또한 야생형 힌지 영역의 변이체, 가령, 단축된 힌지 영역들, 예를 들어, 서열 번호:24의 아미노산 서열을 가지는 중간.힌지로 표시된 힌지가 포함된다.
용어 "항원-결합 단백질" 및 "항원-결합 분자" (하이픈이 있거나 없음)는 항원-결합 특성을 갖는 면역글로불린 유도체를 지칭하기 위해 본원에서 호환적으로 사용된다; 즉, 이러한 결합 단백질은 항원-결합 분자이다. 이러한 결합 단백질은 표적 항원에 결합 할 수 있는 면역학적 기능성 면역글로불린 부분을 포함한다. 면역학적 기능성 면역글로불린 부분은 면역글로불린 또는 이의 부분, 면역글로불린 부분으로부터 유래한 융합 펩티드 또는 항원-결합 부위를 형성하는 면역글로불린 부분들을 조합한 접합체를 포함 할 수 있다. 각각의 항원-결합 모이어티는 적어도 항원-결합 모이어티가 유래된 면역글로불린 중쇄 또는 경쇄의 CDR들을 포함한다. 용어 "항원-결합 단백질"및 "항원-결합 분자"(하이픈이 있거나 없는)는 본원에서 예를 들어, 추가적인 불변 도메인을 가진 Fv 도메인에 기반한 IgG-유사 융합 폴리펩티드를 비롯한 이들의 항원에 대한 특이성 및 친화성을 보유하는 항체 단편, 항체 유도체 또는 항체-유사 결합 단백질을 지칭하기 위해 호환적으로 사용된다. 결합가, 다중특이성, 약동학 및 약력학적 특성과 같은 원하는 특징에 따라 Fv 및 불변 도메인 및/또는 또 다른 기능적 도메인은, 예를 들어, Brinkmann and Kontermann, mAbs, 2017, 9(2):182-192 또는 Spiess 외, Molecular Immunology 2015;67:95-106에 설명된 것과 같은 상이한 분자 형태 또는 단백질 스캐폴드로 모듈식으로 조립된다.
일부 구체예에서, 항원-결합 단백질은 단일 폴리펩티드 사슬로 구성된다. 이러한 항원-결합 단백질은 단량체이다. 다른 구체예에서 항원-결합 단백질은 적어도 2개의 폴리펩티드 사슬들을 포함한다. 이러한 항원-결합 단백질은 다량체, 예를 들어, 이량체, 삼량체 또는 사량체이다.
바람직하게는, 항원-결합 단백질은 인간, 가장 바람직하게는 완전 인간이다.
용어 "항원-결합 모이어티"는 특히 항원의 항원 결정기 (에피토프)에 특이적으로 결합하는 항원-결합 단백질의 항체-항원-결합 부위 또는 파라토프를 지칭한다. 항원-결합 부위는 항원을 인식 할 수 있고 항원에 특이적으로 결합하는 항원-결합 단백질의 결합 부분이다.
본원에 기재된 "Fv"는 항원을 인식하는, 즉, 항원의 에피토프에 결합하는 항체의 경쇄 (VL) 및 중쇄 (VH) 둘 모두의 가변 도메인을 포함하는 항원-결합 모이어티를 나타낸다. 특정 구체예에서 항원-결합 부위는 단일 도메인 (sdAb), 예를 들어 낙타 류의 VHH 단편 또는 연골 어류의 VNAR 단편 일 수 있다.
각 항원-결합 부분은 동일한 에피토프에 결합하는 항체, 즉, 면역글로불린, 가변 중쇄 도메인 (VH) 및 항체 가변 경쇄 도메인 (VL)에 의해 형성되는 반면 가변 중쇄 도메인 (VH)은 3개의 중쇄 상보성 결정 영역 (CDR): HCDR1, HCDR2 및 HCDR3을 포함하고; 가변 경쇄 도메인 (VL)은 3개의 경쇄 상보적 결정 영역 (CDR): LCDR1, LCDR2 및 LCDR3을 포함한다. 항원-결합 부위의 가변 중쇄 및 경쇄 도메인은, 예를 들어, 펩티드 링커에 의해 서로 공유적으로 연결되거나, 서로 비공유적으로 결합되어 항원-결합 부위를 형성할 수 있다.
"링커"는 다른 병치 도메인의 N-말단에 연결된 하나의 도메인의 C-말단과 또는 그 역으로 항원-결합 모이어티를 형성하는 2개의 병치된 가변 도메인을 연결하는 링커 펩티드를 포함하는 아미노산 서열을 지칭한다. 아미노산 조성과 관련하여, Fv, 즉, VH/VL, 항원-결합-및 인식 부위의 형성을 방해하지 않을 뿐만 아니라 다량체화, 예컨대, 다중특이적 항원-결합 단백질의 폴리펩티드들의 이량체화를 방해하지 않는 펩티드 링커 서열이 선택된다. 예를 들어, 글리신 및 세린 잔기를 포함하는 링커는 일반적으로 프로테아제 내성을 제공한다. 일부 구체예에서 (G2S)x 펩티드 링커가 사용되고, 이 때, 예를 들면, x = 1-20이며, 예를 들면, (G2S), (G2S)2, (G2S)3, (G2S)4, (G2S)5, (G2S)6, (G2S)7 또는 (G2S)8 , 또는 (G3S)x 펩티드 링커가 사용되고, 이 때, 예를 들어, x = 1-15이며 또는 (G4S)x 펩티드 링커가 사용되며, 이 때, 예를 들어 x = 1-10, 바람직하게는 1-6이다. 링커의 아미노산 서열은, 예를 들어, 파지-디스플레이 방법에 의해 최적화되어, 항원-결합 부위의 형성 및 폴리펩티드의 생성 수율을 개선할 수 있다.
"연결기"는 항원-결합 모이어티를 Fab 단편에, 힌지 또는 Fc 부분에 연결하는 펩티드를 지칭한다. 정의에 따라 연결기는 두 개의 가변 도메인을 연결하는 펩티드가 아니다.
링커 및 연결기의 길이는 항원-결합 모이어티의 Fv 폴리펩티드의 폴딩 및 가요성에 영향을 미칠 수 있다. 원하는 Fv 폴리펩티드의 가요성은 표적 항원 밀도 및 표적 항원, 즉, 표적 항원의 에피토프의 접근성에 따라 달라진다. 보다 긴 링커 또는 연결기는 보다 재빠른 항원-결합 부위를 가진 보다 가요성인 Fv 폴리펩티드를 제공 할 수 있다. 이량체성 항원-결합 폴리펩티드의 형성에 대한 링커 길이의 효과는, 예를 들어, Todorovska 외, Journal of Immunological Methods 2001;248:47-66; Perisic 외, Structure 1994;2:1217-1226; Le Gall 외, Protein Engineering 2004;17:357-366 및 WO 94/13804에 기재되어 있다.
"단쇄 가변 항체 단편" 또는 "scFv"는 중쇄 가변 도메인 (VH)으로 구성된 항원-결합 부위를 포함하는데, 이는 펩티드 링커를 통해 경쇄 가변 도메인 (VL)에 선택적으로 융합된다. scFv는 다음과 같은 폴리펩티드 사슬 일 수 있다: 폴리펩티드 사슬의 N-으로부터 C-말단으로 VL-링커-VH 또는 VH-링커-VL (Huston 외, Proc. Natl. Acad.Sci. USA, 1988, 85:5879-83). VH와 VL 도메인 사이의 링커는 항원-결합 할 수 있는 원하는 구조의 형성을 가능하게 한다.
"항원-결합 (Fab) 단편" 또는 "Fab"는 중쇄 (H) 유래 및 경쇄 (L) 유래 서열들 각각의 이량체화에 의해 형성된 하나의 불변 (CH1, CL) 및 하나의 가변 도메인 (VH, VL)을 포함하며, 이 때 가변 도메인 VH 및 VL는 항원-결합 부위를 구성한다. 2개의 Fab' 단편들은 F(ab')2 단편으로서 힌지-영역을 통해 Fc 부분에 N-말단으로 연결된다.
"디아바디" (Db)는 두 VL/VH 항원-결합 부위에 결합하는 두 쌍의 가변 중쇄 (VH) 및 가변 경쇄 (VL) 사슬 도메인, 제 1 쌍 및 제 2 쌍으로 구성된 2가 Fv-분자를 나타낸다. 각 가변 도메인들 쌍은 폴리펩티드에서 차례로 연결된다. 특정 구체예에서 2가 Fv-분자는 2개의 병치된 가변 도메인의 제 1 및 제 2 쌍으로 구성되며, 이 때 각 쌍에서 2개의 가변 도메인은 짧은 링커에 의해 연결된 가변 도메인들 사이의 분자내 결합을 배제하는 짧은 펩티드 링커에 의해 융합된다. 제 1 가변 도메인 쌍은 제 2 가변 도메인 쌍과 교차 결합하여 2개의 Fv 항원-결합 부위를 형성한다. 따라서, 2개의 항원-결합 모이어티 각각은 제 1 가변 도메인 쌍의 하나의 가변 도메인 및 제 2 가변 도메인 쌍의 하나의 가변 도메인에 의해 형성된다. 따라서, 이러한 디아바디는 짧은 링커에 의해 직접 연결되지 않은 2개의 가변 도메인들로 구성된 적어도 하나의 항원-결합 부위를 포함한다. 디아바디에서 제 1 항원-결합 모이어티의 가변 도메인은 링커에 의해 제 2 항원-결합 모이어티의 가변 도메인과 연결된다. 예를 들어, 제 1 항원-결합 모이어티의 VH는 제 1 링커에 의해 제 1 폴리펩티드에 있는 제 2 항원-결합 모이어티의 VL에 연결되고 제 1 항원-결합 모이어티의 VL은 제 2 링커에 의해 제 2 폴리펩티드에 있는 제 2 항원-결합 모이어티의 VH에 연결된다. 각각의 병치된 가변 도메인 쌍에서 짧은 제 1 또는 제 2 링커는 한 가변 도메인의 C-말단을 다른 가변 도메인의 N-말단과 연결하거나 그 반대이다. 각 쌍에서 가변 도메인은 VL-VH, VH-VL, VH-VH 및 VL-VL로서 N-으로부터 C-말단으로 배향 될 수 있으며, 이 때 해당 쌍의 두 가변 도메인은 상이한 항원 에피토프 특이성 또는 동일한 항원 에피토프 특이성을 가질 수 있다. 특정 예들에서 2개의 가변 도메인은 해당 쌍의 한 가변 도메인의 C-말단과 다른 가변 도메인의 N-말단 사이의 펩티드 결합에 의해 직접 연결된다. 디아바디의 제 1 및 제 2 가변 도메인 쌍 각각에서 2개의 가변 도메인을 연결하는 짧은 펩티드 링커의 길이는 링커에 의해 연결된 가변 도메인들 사이의 분자내 결합을 배제시킨다. 이러한 링커는 "짧다", 즉, 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 또는 약 12의 아미노산 잔기로 구성된다. 0개 아미노산 잔기의 경우 링커는 펩티드 결합이다. 이러한 짧은 링커는 두 쌍의 가변 도메인들 사이의 정확한 이량체화 및 2개 Fv 항원-결합 부위의 형성을 선호한다. 링커를 약 12개 이하의 아미노산 잔기로 단축시키면 일반적으로 동일한 폴리펩티드 사슬의 인접 도메인이 서로 상호작용하는 것을 방지한다. 본 발명의 한 구체예에서, 이들 링커는 약 3 내지 약 12개, 예를 들어, 5 내지 10개, 특히, 7 내지 9개의 인접 아미노산 잔기들로 구성된다. 링커 길이는 디아바디의 폴리펩티드 내에서 특정 도메인 배향에 대해 조정될 수 있다. 게다가, 원칙적으로 해당 쌍의 가변 항체 도메인들 사이에 12개 이상의 아미노산 잔기를 갖는 링커를 갖는 2개의 폴리펩티드는 서로 올바르게 이량체화 될 수 있다 (예를 들어, Le Gall 외, Protein Engineering 2004;17:357-366 참고).
"단쇄 디아바디 (scDb)"는 제 1 및 제 2 폴리펩티드를 융합하는 추가 링커를 추가함으로써 단일 폴리펩티드 사슬로 전환된 디아바디 유도체를 의미한다 (Kontermann 외, Immunol. Methods, 1999;226: 179-188). 따라서, 추가 링커는 제 1 링커에 의해 연결된 제 1 및 제 2 항원-결합 모이어티의 가변 도메인을 포함하는 제 1 폴리펩티드의 C-말단을, 제 2 링커에 의해 연결된 제 1 및 제 2 항원-결합 모이어티의 동족 가변 도메인을 포함하는 제 2 폴리펩티드의 N-말단과 연결한다. 따라서, scDb는 단일 폴리펩티드 사슬, 즉, Fv 폴리펩티드로 구성되며, 이 때 2개의 항원-결합 모이어티의 4개의 가변 도메인은 N-으로부터 C-말단으로 다음과 같이 배열된다:
-
VL-링커1-VH-링커3-VL-링커2-VH, 또는
-
VL-링커1-VL-링커3-VH-링커2-VH, 또는
-
VH-링커1-VL-링커3-VH-링커2-VL, 또는
-
VH-링커1-VH-링커3-VL-링커2-VL.
링커1및 링커2는 디아바디로 사용되는 "짧은" 링커들이다, 예컨대, 이들은, 13개 미만, 예를 들어, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 또는 12개 아미노산 잔기들로 구성된다.
링커3은 분자내 접힘 (folding back) 및 2개의 N-말단 가변 도메인과 2개의 C-말단 가변 도메인의 2개의 항원-결합 모이어티로의 결합을 촉진시키는 scFv를 위해 사용되는 더 큰 가요성의 링커이다. 링커3은 13개 이상의 아미노산 잔기, 예를 들어, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 또는 30개 아미노산 잔기들로 구성된다. 일부 구체예에서 링커3은 15 내지 25개, 바람직하게는 15 내지 20개 또는 13 내지 18개 아미노산이다.
용어 "탠덤 디아바디"는 단일 유전자 구조체에서 적어도 4개의 가변 도메인 (2개의 중쇄 가변 도메인 (VH) 및 2개의 경쇄 가변 도메인 (VL))을 연결하여 제작된 항원-결합 분자를 지칭하며, 번역된 폴리펩티드 사슬들 중 2개의 동종-이량체화를 가능하게 한다. 이러한 탠덤 디아바디에서 링커 길이는 가변 도메인의 분자내 페어링을 방지하므로 해당 분자는 자체적으로 단량체 단쇄 분자를 형성하기 위해 접힐 수 없고 오히려 다른 사슬의 상보적 도메인과 페어링하게 된다. 가변 도메인들은 또한 이러한 이량체화 동안 상응하는 가변 도메인들이 페어링되도록 배열된다 (Weichel 외, European Pharmaceutical Review 2015;20(1):27-32; Reusch 외, mAbs 2014;6:3, 728-739).
"이중-친화성 재표적화 분자 (DARTs)"는, 배열 VL(A)-VH(B) + VL(B)-VH(A)에서 제 1 항원-결합 모이어티의 VH가 제 2 폴리펩티드 상의 제 2 항원-결합 모이어티의 VL에 연결되고, 제 2 항원-결합 모이어티의 VH가 제 1 폴리펩티드 상의 VL에 연결되는 단백질 스캐폴드를 지칭하며, 이 때 사슬내 이황화결합이 분자를 안정화시키기 위해 도입된다.
용어 "표적"또는 "표적 항원"은 NK 세포가 NK 세포 세포 독성을 유도 또는 촉발하도록 지시되어야 하는 세포 유형, 즉, 표적 세포 또는 바이러스 감염 세포에 의해 발현되거나 이와 연관된 항원을 지칭한다. 표적 항원의 예들은 종양 항원 또는 종양-관련 항원 (Tumor-Associated 항원, TAA) 일 수 있다. 종양 항원 또는 TAA는 표적 세포의 표면에 발현되거나 MHC 제한 펩티드로서 MHC 복합체에 의해 표시 될 수 있다. 종양 항원의 예에는, CD5, CD19, CD20, CD22, CD30, CD33, CD38, CD123, CD138, CCR4, CS-1, GD2, 기질 금속단백분해효소 1 (MMP1), 라미난 수용체 전구체 단백질, BCMA, EGFR, EGFRvIII, Ep-CAM, gpA33, AMHRII, PDGFRα, SLAMF7, PLAP, 톰슨-프라이덴라이히 (TF) 항원, MUC-1 (뮤신), IGFR, IL4-R alpha, IL13-R, HER2/neu, HER3, PSMA, CEA, TAG-72, HPV E6, HPV E7, BING-4, 사이클린-B1, 9D7, EphA2, EphA3, 텔로머라제, 메소텔린, SAP-1, 서비빈, 암 정소 항원 (BAGE 패밀리, CAGE 패밀리, GAGE 패밀리, MAGE 패밀리, SAGE 패밀리, XAGE 패밀리), NY-ESO-1/LAGE-1, PRAME, SSX-2, Melan-A/MART-1, Gp100/pmel17, 티로시나제, TRP-1/-2, MC1R, ß-카테닌, BRCA1/2, CDK4, CML66, MART-2, p53, Ras, TGF-ßRII 및 TCR (Categories of Tumor 항원s로부터, Holland-Frei Cancer Medicine. 6th edition. Kufe DW, Pollock RE, Weichselbaum RR. 외, editors Hamilton (ON):Becker; 2003)가 포함되나 이에 제한되는 것은 아니다. "표적" 및 "표적 항원"은 또한 혈청 알부민, 특히, 인간 혈청 알부민 (HSA)을 포함한다. 특정 구체예에서, 표적 항원은 BCMA이다.
다른 구체예에서 표적 항원은 바이러스 또는 박테리아 병원체, 예를 들어 뎅기 바이러스, 단순 포진, 거대 세포 바이러스, 간염 바이러스, 인간 T-세포 림프구 바이러스, 인플루엔자 바이러스, RSV, 유두종 바이러스 (위에서 언급 한 E6 및 E7 이외의 항원 포함), 인플루엔자 바이러스 또는 HIV와 같은 감염성 물질 일 수 있다. MHC-제한 펩티드로서 MHC 복합체에 의해 제시된 펩티드 표적도 포함된다.
"CD16A"는 FcγRIIIA로도 공지되어 있는, NK 세포의 세포 표면에서 발현되는 활성화 수용체 CD16A를 지칭한다. CD16A는 NK 세포의 세포독성 활성을 유발하는 활성화 수용체이다. CD16A에 대한 항체의 친화성은 NK 세포 활성화를 유발하는 능력과 직접적으로 관련되어, CD16A에 대한 보다 높은 친화성은 활성화에 필요한 항체 용량을 줄인다. 항원-결합 단백질의 항원-결합 부위는 CD16A에는 결합하지만 CD16B에는 결합하지 않는다. 예를 들어, CD16A에 결합하지만 CD16B에 결합하지 않는 중쇄 (VH) 및 경쇄 (VL) 가변 도메인을 포함하는 항원-결합 부위는 CD16A의 C-말단 서열 SFFPPGYQ (서열 번호:57)의 아미노산 잔기 및/또는 CD16B에 존재하지 않는 CD16A (서열 번호:48)의 잔기 G130 및/또는 Y141을 포함하는 CD16A의 에피토프에 특이적으로 결합하는 항원-결합 부위에 의해 제공될 수 있다.
"골수종 세포"는 신생물 형질 전환에 의해 골수에 있는 형질 세포에서 발생하는 악성 (암성) 형질 세포이다. 골수종에서 악성 형질 세포는 감염과 싸우는 능력이 부족한 다량의 비정상 항체를 생성한다. 이러한 비정상 항체는 골수종에 대한 종양 마커 역할을 하는 소위, 단일클론 단백질, 또는 M-단백질이다. 골수종 세포는 표현형 CD19-/CD38+/CD138+/BCMA+를 가진다. 따라서 CD38, CD138 및 BCMA는 골수종 세포에서 발현되는 항원을 나타낸다. 또한 CD19/CD20/CD22/BCMA 및 기타 항원에 대해 양성인 B 세포 계통의 악성 표현형도 포함된다 (여기에는 고전적으로 형질 세포로 이해되지 않는 표현형이 포함되어야 하지만 기억 B 세포 또는 전-형질 세포 계통으로부터 진화된 것일 수 있다).
"EGFR"은 활성화, 돌연변이를 가지는 것으로 기재되고 병태생리학적 과정에 관여하는 모든 아이소형 또는 변이체들을 포함하는 인간의 표피 성장 인자 수용체 (EGFR; ErbB-1; HER1)를 지칭한다. EGFR 항원-결합 부위는 EGFR의 세포외 도메인에서 에피토프를 인식한다. 특정 구체예에서 항원-결합 부위는 인간 및 시노몰구스 EGFR에 특이적으로 결합한다.
표피 성장 인자 수용체 (EGFR)는 수용체 티로신 키나아제의 HER 패밀리의 구성원이며 다음 4가지 구성원으로 구성된다: EGFR (ErbB1/HER1), HER2/neu (ErbB2), HER3 (ErbB3) 및 HER4 (ErbB4). 리간드 결합 (예를 들어, EGF, TGFa, HB-EGF, 뉴레굴린, 베타셀룰린, 암피레귤린)을 통한 수용체의 자극은 티로신 인산화를 통해 세포내 도메인에서 고유 수용체 티로신 키나제를 활성화하고 HER 패밀리 구성원과의 수용체 동종 또는 이종이량체화를 촉진한다. 이러한 세포내 포스포-티로신은 MAPK 및 PI(3)K/Akt를 포함한 다양한 어댑터 단백질 또는 효소에 대한 도킹 부위 역할을 하며, 동시에 세포 증식, 혈관신생, 세포자멸사 내성, 침습 및 전이에 영향을 미치는 많은 신호전달 연쇄반응을 시작한다.
"EGFRvIII"은 EGFR 코딩 서열의 엑손 2-7에 걸친 염기 쌍의 인-프레임 결실로부터 생성된 EGFR의 세포외 도메인 돌연변이체를 지칭한다 (Gan HK 외, FEBS 2013, 280:5350-5370).
용어 "결합 도메인"은 본 발명과 관련하여 표적 분자 (항원)상의 주어진 표적 에피토프 또는 주어진 표적 측면, 예를 들어, 각각, CD16 및 표적 세포 표면 항원에 (특이적으로) 결합/이와 상호작용/이를 인식하는 도메인을 특징으로 한다. 제 1 결합 도메인의 구조 및 기능 (예를 들어, CD16 인식), 그리고 바람직하게는 또한 제 2 결합 도메인의 구조 및/또는 기능 (표적 세포 표면 항원 인식)은, 예를 들어, 전장 또는 전체 면역글로불린 분자의 항체의 구조 및/또는 기능에 기초하며 및/또는 항체 또는 이의 단편의 가변 중쇄 (VH) 및/또는 가변 경쇄 (VL) 도메인으로부터 유도된다. 바람직하게는 제 1 결합 도메인은 3개의 경쇄 CDR (즉, VL 영역의 CDR1, CDR2 및 CDR3) 및/또는 3개의 중쇄 CDR (즉, VH 영역의 CDR1, CDR2 및 CDR3)의 존재를 특징으로 한다. 제 2 결합 도메인은 또한 바람직하게는 표적 결합을 허용하는 항체의 최소 구조적 요건을 포함한다. 보다 바람직하게는, 제 2 결합 도메인은 적어도 3개의 경쇄 CDR (즉, VL 영역의 CDR1, CDR2 및 CDR3) 및/또는 3개의 중쇄 CDR (즉, VH 영역의 CDR1, CDR2 및 CDR3)을 포함한다. 제 1 및/또는 제 2 결합 도메인은 기존 (단클론) 항체로부터의 CDR 서열을 스캐 폴드에 접목시키는 것보다 파지 디스플레이 또는 라이브러리 스크리닝 방법에 의해 생성되거나 얻을 수 있는 것으로 예상된다.
용어 "(특이적으로) 결합한다", "(특이적으로) 인식한다", "(특이적으로) 지시된다" 또는 "(특이적으로) 반응한다"라는 용어는 본 발명에 따르면 결합 도메인이 표적 분자 (항원), 예를 들어 CD16a 및 표적 세포 표면 항원, 예를 들어, BCMA 상에서 각각 주어진 에피토프 또는 주어진 표적 측면과 상호작용함을 의미한다.
용어 "본질적으로/실질적으로 결합하지 않는다"또는 "결합 할 수 없다"는 본 발명의 결합 도메인이 CD16a 이외의 항원 또는 단백질, 및 표적 세포 표면 항원에 결합하지 않음을, 즉, CD16a 이외의 항원 또는 단백질, 및 표적 세포 표면 항원과 약 30% 초과의 반응성을 보이지 않음을, 바람직하게는 약 20% 이하, 더 바람직하게는 약 10% 이하, 특히 바람직하게는 약 9%, 약 8%, 약 7%, 약 6% 또는 약 5% 이하이고, 이에 의해 CD16a, 및 표적 세포 표면 항원 각각에 대한 결합은 약 100%로 설정됨을 의미한다.
특이 적 결합은 결합 도메인 및 항원의 아미노산 서열에서 특이적 모티프에 의해 영향을 받는 것으로 여겨진다. 따라서, 결합은 이들의 1차, 2차 및/또는 3차 구조의 결과, 뿐만 아니라 상기 구조들의 2차 변형의 결과로 달성된다. 항원-상호작용 측면과 그의 특이적 항원의 특이적 상호작용은 상기 측면이 항원에 간단히 결합하게 할 수 있다. 더욱이, 항원-상호 작용 측면과 이의 특이적 항원의 특이적 상호작용은 대안적으로 또는 추가적으로, 예를 들어, 항원의 입체구조 변화 유도, 항원의 올리고머화 등으로 인한 신호의 개시를 가져올 수 있다.
용어 "가변"은 그 서열에서 가변성을 나타내고 특정 항체의 특이성 및 결합 친화성을 결정하는데 관여하는 항체 또는 면역글로불린 도메인의 일부분을 지칭한다 (즉, "가변 도메인 (들)"). 가변 중쇄 (VH)와 가변 경쇄 (VL)의 페어링은 함께 단일 항원-결합 측면을 형성한다.
변이성은 항체의 가변 도메인들 전체에 걸쳐 고르게 분포되는 것은 아니며; 중쇄 및 경쇄 가변 영역들 각각의 하위-도메인들에 집중되어 있다. 이러한 하위-도메인들을 "초가변 영역" 또는 "상보성 결정 영역" (CDRs)이라 부른다. 가변 도메인들 중 더욱 보존되는 (즉, 비-초가변) 부분들을 "프레임워크" 영역 (FRM 또는 FR)이라 부르며 삼차원 공간에서 여섯 개의 CDR들에 대한 스캐폴드를 제공하여 항원-결합 표면을 형성한다. 자연 발생 중쇄 및 경쇄의 가변 도메인들은 각각네 개의 FRM 영역들 (FR1, FR2, FR3, 및d FR4)을 포함하는데, 이들은 대부분 -쉬트 입체구조를 채택하고, 세 개의 초가변 영역들에 의해 연결되어 있으며, -쉬트 구조를 연결하는, 그리고 일부 경우 -쉬트 구조의 일부를 형성하는 루프를 형성한다. 각 사슬의 초가변 영역들은 FRM에 의해 다른 사슬의 초가변 영역들과 근접하게 함께 지지되며, 항원-결합 측면의 형성에 기여한다 (Kabat 외, loc. cit. 참고).
용어 "CDR", 및 이의 복수형 "CDRs"은, 상보성 결정 영역을 지칭하는데, 세 개의 상보성 결정 영역은 경쇄 가변 영역의 결합 특성을 구성하고 (CDR-L1, CDR-L2 및 CDR-L3) 세 개는 중쇄 가변 영역의 결합 특성을 구성한다 (CDR-H1, CDR-H2 및 CDR-H3). CDRs은 항원과 항체의 특이적 상호작용을 담당하는 대부분의 잔기들을 내포하므로, 항체 분자의 기능적 활성에 기여하며: 항원 특이성의 주요 결정인자이다.
정확한 정의상의 CDR 경계 및 길이는 상이한 분류 및 넘버링 체계에 따라 달라질 수 있다. 그러므로 CDRs은 Kabat, Chothia, 접촉 또는 본 출원에 기재된 넘버링 체계를 비롯한 임의의 다른 경계 정의에 의해 지칭될 수 있다. 상이한 경계에도 불구하고, 이들 체계 각각은 무엇이 가변 서열들 내부의 소위 "초가변 영역들"을 구성하는지에 있어서 어느 정도의 중복을 가진다. 그러므로 이러한 체계들에 따른 CDR 정의들은 인접한 프레임워크 영역들에 대한 경계 영역 및 길이가 상이할 수 있다. 예를 들어 Kabat (종간 서열 변이성에 근거한 접근 방법), Chothia (항원-항체 복합체의 결정학 연구에 근거한 접근 방법), MacCallum, Honegger, 및 IMGT (Wu 및 Kabat, J. Exp. Med. 1970;132:211-250; Chothia 외, J. Mol. Biol, 1987, 196: 901 -917; MacCallum 외, J. Mol. Biol, 1996, 262: 732; Lefranc 외, Dev. Comp. Immunol. 2003;27:55-77; Honegger 외, J. Mol. Bol. (2001);309:657-670)를 참고하라. 또 다른 항원-결합 측면 특성화 기준은 Oxford Molecular사 AbM 항체 모델링 소프트웨어가 사용하는 AbM 정의이다. 예컨대, 항체 가변 도메인들의 단백질 서열 및 구조 분석을 참고하라. In: 항체 Engineering Lab Manual (Ed.: Duebel, S. and Kontermann, R., Springer-Verlag, Heidelberg). 두 개의 잔기 식별 기법들이 동일한 영역들은 아니지만 중복되는 영역들을 정의하는 한, 이들을 조합하여 하이브리드 CDR을 정의할 수 있다. 그러나, 소위 Kabat 체계에 따른 넘버링이 선호된다. 특정 구체예에서, 본원에 개시된 CDR은 Kabat 넘버링 체계에 따라 식별된다. 특정 구체예에서, 본원에 개시된 CDR은 IMGT 접근법에 따라 식별된다. 특정 구체예에서, 본원에 개시된 CDR은 Honegger 접근법에 따라 식별된다.
경쇄의 CDR3 그리고, 특히, 중쇄의 CDR3는 경쇄 및 중쇄 가변 영역들 내부에서 항원-결합에 있어서 가장 중요한 결정인자들을 구성할 수 있다. 일부 항체 구조체들에서, 중쇄 CDR3는 항원과 항체 사이의 주요 접촉 영역을 구성하는 것으로 보인다. 항체의 결합 성질을 변화시키기 위해 또는 어떤 잔기들이 항원의 결합에 기여하는지를 결정하기 위해 CDR3만이 변화하는 시험관 내 선발 체계가 사용될 수 있다. 그러므로, CDR3는 통상적으로 항체-결합 측면 내 분자 다양성의 가장 큰 원인이다. 예를 들면, H3는, 두 개의 아미노산 잔기만큼 짧거나 또는 26개 이상의 아미노산일 수 있다.
전형적인 전장 항체 또는 면역글로불린에서, 각 경 (L)쇄는 하나의 공유 이황화 결합에 의해 중(H)쇄에 연결되지만, 두 개의 H 쇄는 H 쇄 아이소형에 따라 하나 이상의 이황화 결합에 의해 서로에 연결된다. VH에 가장 가까운 CH 도메인은 일반적으로 CH1로 지정된다. 불변 ("C") 도메인은 항원-결합에 직접 관여하지 않지만 항체 의존성, 세포 매개 세포독성 및 보체 활성화와 같은 다양한 이펙터 기능을 나타낸다. 항체의 Fc 영역은 중쇄 불변 도메인 내에 포함되며 예를 들어 세포 표면에 위치한 Fc 수용체와 상호작용할 수 있다.
본원에 기재된 항체 결합 분자의 아미노산 서열 변형이 또한 고려된다. 예를 들면, 항체 구조체의 상기 결합 친화성 및/또는 다른 생물학적 성질들을 개선하는 것이 바람직할 수 있다. 이러한 항체 구조체들의 아미노산 서열 변이체들은 적절한 뉴클레오티드 변화를 항체 구조체 핵산에 도입하거나 펩티드 합성에 의해 제조된다. 하기 기재된 모든 아미노산 서열 변형은 비 변형 모체 분자의 원하는 생물학적 활성 (CD16a 및 표적 세포 표면 항원에 대한 결합)을 여전히 보유하는 항체 구조체를 생성해야 한다.
아미노산 변형은 예를 들면, 상기 항체 결합 분자들의 아미노산 서열로부터의 잔기 결실, 및/또는 이들 아미노산 서열 내부로의 잔기 삽입 및/또는 치환을 포함한다. 최종 분자가 원하는 특징을 갖는 한, 최종 분자에 도달하기 위해 결실, 삽입, 및 치환의 임의의 조합이 이루어진다. 아미노산 변화는 또한 글리코실화 부위의 수 또는 위치를 변화시키는 것과 같은, 항체 결합 분자의 해독 후 과정을 변화시킬 수 있다.
예를 들어, 1, 2, 3, 4, 5 또는 6개의 아미노산이 각각의 CDR에 삽입, 치환 또는 결실 될 수 있으며 (물론 길이에 따라 다름), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 또는 25개의 아미노산이 각각의 FR에 삽입, 치환 또는 결실 될 수 있다. 바람직하게는, 아미노산 서열의 항체 구조체로의 삽입은 1, 2, 3, 4, 5, 6, 7, 8, 9 또는 10개 잔기에서 수백 또는 그 이상의 잔기가 함유된 폴리펩티드 범위, 뿐만 아니라 단일 또는 다수의 아미노산 잔기의 서열내 삽입이 포함된 아미노-및/또는 카르복실-말단 융합을 포함한다. 상응하는 변형은 본 발명의 내용에서 정의된 항체 구조체의 제 3 도메인 내에서도 수행 될 수 있다. 본 발명의 내용에서 정의된 항체 구조체의 삽입 변이체는 효소의 항체 결합 분자의 N-말단 또는 C-말단에 대한 융합 또는 폴리펩티드에 대한 융합을 포함한다.
치환 돌연변이유발에 있어서 가장 큰 관심 부위는 중쇄 및/또는 경쇄의 CDR, 특히 초가변 영역을 포함하지만 (그러나 이에 제한되는 것은 아님), 중쇄 및/또는 경쇄의 FR 변경 또한 고려된다. 치환은 바람직하게는 본원에 기재된 보존적 치환이다. 바람직하게는, CDR 또는 FR의 길이에 따라 CDR에서 1, 2, 3, 4, 5, 6, 7, 8, 9 또는 10 개의 아미노산이 치환 될 수 있으며, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 또는 25개의 아미노산이 프레임 워크 영역 (FR)에서 치환 될 수 있다. 예를 들어, CDR 서열이 6개의 아미노산을 포함하는 경우, 이러한 아미노산 중 1개, 2개 또는 3개가 치환되는 것으로 예상된다. 유사하게, CDR 서열이 15개의 아미노산을 포함하는 경우, 이러한 아미노산 중 1, 2, 3, 4, 5 또는 6개가 치환되는 것으로 예상된다.
일반적으로, 아미노산이 중쇄 및/또는 경쇄의 CDR 중 하나 이상 또는 모두에서 치환되는 경우, 그 때 수득된 "치환된"서열은 "원래" CDR 서열과 적어도 약 60% 또는 약 65%, 더 바람직하게는 약 70% 또는 약 75%, 훨씬 더 바람직하게는 약 80% 또는 약 85%, 특히 바람직하게는 약 90% 또는 약 95% 동일하다. 이는 "치환된" 서열과 동일한 정도가 CDR의 길이에 의존적임을 의미한다. 예를 들어, 5개의 아미노산을 갖는 CDR은 적어도 하나의 아미노산이 치환되도록 하기 위해 그 치환된 서열과 약 80% 동일한 것이 바람직하다. 따라서, 항체 구조체의 CDR은 그 치환된 서열에 대해 상이한 정도의 동일성을 가질 수 있다, 예를 들어 CDRL1은 약 80%를 가질 수 있는 반면, CDRL3은 약 90%를 가질 수 있다.
선호되는 치환 (또는 대체)는 보존적 치환이다. 그러나, 항체 구조체가 제 1 도메인을 통한 CD16a에 그리고 제 2 도메인을 통해 표적 세포 표면 항원에 결합하는 능력을 보유하는 한 및/또는 이의 CDR들이 이렇게 치환된 서열들에 동일성을 가지는 한 ("본래" CDR 서열에 적어도 약 60% 또는 약 65%, 더욱 바람직하게는 약 70% 또는 약 75%, 더 더욱 바람직하게는 약 80% 또는 약 85%, 및 특히 바람직하게는 약 90% 또는 약 95% 동일) 임의의 치환 (비-보존적 치환 또는 표 A에 열거된 "예시적 치환" 중 하나 이상을 포함)이 예상된다.
보존적 치환을 "바람직한 치환"이라는 제목으로 표 A에서 나타낸다. 그러한 치환이 생물학적 활성의 변화를 초래하는 경우, 표 A에서 "예시적 치환"으로 표시된 또는 아미노산 부류와 관련하여 아래에서 추가로 설명되는 보다 실질적인 변화가 도입 될 수 있으며 생성물을 원하는 특성에 대해 스크리닝 할 수 있다.
표 A: 아미노산 치환
본 발명의 항체 구조체의 생물학적 성질들에 있어서 실질적 변형은 (a) 치환 부위에서 폴리펩티드 골격의 구조를, 예를 들면, 쉬트 또는 이중나선 입체구조로서, (b) 표적 부위에서 분자의 전하 또는 소수성, 또는 (c) 측쇄의 벌크를 유지시키는 것에 대한 효과가 유의하게 상이한 치환들을 선택함으로써 이루어진다. 자연 발생 잔기들은 공통 측쇄 성질을 기준으로 다음과 같은 그룹들로 나누어진다: (1) 소수성: 노르류신, met, ala, val, leu, ile; (2) 중성 친수성: cys, ser, thr, asn, gin; (3) 산성: asp, glu; (4) 염기성: his, lys, arg; (5) 사슬 배향에 영향을 미치는 잔기: gly, pro; 및 (6) 방향족: trp, tyr, phe.
비-보존성 치환들은 이들 클래스 중 하나의 구성원을 또 다른 클래스로 교환하게 할 것이다. 항체 구조체의 적절한 형태를 유지하는 데 관여하지 않는 모든 시스테인 잔기는 일반적으로 세린으로 치환되어 분자의 산화 안정성을 개선하고 비정상적인 가교를 방지 할 수 있다. 역으로, 시스테인 결합(들)은 그 안정성 (특히, 항체가 항체 단편, 가령, Fv 단편인 경우)을 개선하기 위해 상기 항체에 추가될 수 있다.
아미노산 서열들에 있어서, 서열 동일성 및/또는 유사성은 Smith 및 Waterman, 1981, Adv. Appl. Math. 2:482의 국소 서열 동일성 알고리즘, Needleman 및 Wunsch, 1970, J. Mol. Biol. 48:443의 서열 동일성 정렬 알고리즘 , Pearson 및 Lipman, 1988, Proc. Nat. Acad. Sci. U.S.A. 85:2444의 유사성 방법의 조사, 이들 알고리즘의 컴퓨터 실행 (Wisconsin Genetics Software Package, Genetics Computer Group, 575 Science Drive, Madison, Wis.의 Wisconsin Genetics Software Package의 GAP, BESTFIT, FASTA, 및 TFASTA), Devereux 외, 1984, Nucl. Acid Res. 12:387-395에 기재된 최우수 적합 서열 프로그램을 비롯한 (그러나 이에 제한되는 것은 아님) 해당 분야에 공지된 표준 기법들 또는 조사를 사용하여 바람직하게는 기본 설정을 사용하여 결정된다. 바람직하게는 동일성 퍼센트는 다음 매개 변수에 기초하여 FastDB에 의해 계산된다: 불일치 패널티 1; 갭 패널티 1; 갭 크기 패널티 0.33; 및 결합 패널티 30, "Current Methods in Sequence Comparison and Analysis," Macromolecule Sequencing and Synthesis, Selected Methods and Applications, pp 127-149 (1988), Alan R. Liss, Inc.
유용한 알고리즘의 예는 PILEUP이다. PILEUP은 점진적인 페어링 정렬을 사용하여 관련 서열들 그룹에서 다수의 서열 정렬을 만든다. 이는 또한 이들 정렬을 생성하는데 사용된 클러스터링 관계를 보여주는 트리를 플롯할 수도 있다. PILEUP은 Feng & Doolittle, 1987, J. Mol. Evol. 35 : 351-360의 점진적 정렬 방법의 단순화를 사용한다; 이 방법은 Higgins and Sharp, 1989, CABIOS 5: 151 -153에서 설명한 것과 유사하다. 유용한 PILEUP 매개 변수에는 기본 갭 가중치 3.00, 기본 갭 길이 가중치 0.10, 및 가중치가 적용된 말단 갭이 포함된다.
유용한 알고리즘의 또 다른 예는 다음에 설명된 BLAST 알고리즘이다: Altschul 외, 1990, J. Mol. Biol. 215 : 403-410; Altschul 외, 1997, Nucleic Acids Res. 25 : 3389-3402; 및 Karin 외, 1993, Proc. Natl. Acad. Sci. U.S.A. 90 : 5873-5787. 특히 유용한 BLAST 프로그램은 Altschul 외, 1996, Methods in Enzymology 266 : 460-480에서 얻은 WU-BLAST-2 프로그램이다. WU-BLAST-2는 여러 검색 매개 변수를 사용하는데 이들 대부분은 기본값으로 설정된다. 조정가능한 매개 변수는 다음 값들로 설정된다: 중복 스팬 = 1, 중복 분율 = 0.125, 워드 임계값 (T) = 11. HSP S 및 HSP S2 매개 변수는 동적 값이며 특정 서열의 구성 및 관심 서열이 검색되는 특정 데이터베이스의 구성에 따라 프로그램 자체에 의해 설정된다; 그러나 감도를 높이기 위해 값을 조정할 수 있다.
또 다른 유용한 알고리즘은 Altschul 외, 1993, Nucl. Acids Res. 25 : 3389-3402에 의해 보고된 갭화 (gapped) BLAST이다. Gapped BLAST는 다음과 같은 BLOSUM-62 치환 점수를 사용한다; 9로 설정된 임계값 T 매개변수; 2번의 히트 방법은 비갭화 연장을 유발하고, 갭 길이 k에 10+k 비용을 부과하며; Xu는 16으로 설정되고, 그리고 Xg는 데이터베이스 검색 단계에서는 40으로 그리고 알고리즘 출력 단계에서는 67로 설정된다. 갭화된 정렬은 약 22 비트에 해당하는 점수에 의해 촉발된다.
일반적으로, 개별 변이체 CDR 또는 VH/VL 서열 간의 아미노산 상동성, 유사성 또는 동일성은 본원에 묘사된 서열에 대해 적어도 약 60%이고, 보다 일반적으로 바람직하게는, 적어도 약 65% 또는 약 70%, 더 바람직하게는 적어도 약 75% 또는 약 80%, 훨씬 더 바람직하게는 적어도 약 85%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99% 및 거의 약 100%의 상동성 또는 동일성을 증가시킨다. 유사한 방식으로, 본원에서 확인된 결합 단백질의 핵산 서열에 대한 "퍼센트 (%) 핵산 서열 동일성"은 항체 구조체의 코딩 서열에 있는 뉴클레오티드 잔기와 동일한 후보 서열의 뉴클레오티드 잔기들의 백분율로 정의된다. 특정 방법은 기본 매개변수로 설정된 WU-BLAST-2의 BLASTN 모듈을 활용하며, 중첩 범위와 중첩 분율은 각각 1과 0.125로 설정된다.
일반적으로, 개별 변이체 CDR 또는 VH/VL 서열을 인코딩하는 뉴클레오티드 서열과 본원에 제시된 뉴클레오티드 서열 사이의 핵산 서열 상동성, 유사성 또는 동일성은 적어도 약 60%이고, 보다 일반적으로 바람직하게는 상동성 또는 동일성은 약 65%, 약 70%, 약 75%, 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98% 또는 약 99% 및 거의 100%로 증가한다. 따라서, "변이체 CDR"또는 "변이체 VH/VL 영역"은 본 발명의 내용에서 정의된 모체 CDR/VH/VL에 대해 명시된 상동성, 유사성 또는 동일성을 갖는 것이며, 모체 CDR 또는 VH/VL의 특이성 및/또는 활성의 적어도 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86% , 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 또는 약 99%를 비롯한 (그러나 이에 제한되는 것은 아님) 생물학적 기능을 공유한다.
한 구체예에서, 본 발명에 따른 항체 구조체의 인간 생식선에 대한 동일성 백분율은 ≥ 약 70% 또는 ≥ 약 75%, 더욱 바람직하게는 ≥ 약 80% 또는 ≥ 약 85%, 더 더욱 바람직하게는 ≥ 약 90%, 및 가장 바람직하게는 ≥ 약 91%, ≥ 약 92%, ≥ 약 93%, ≥ 약 94%, ≥ 약 95% 또는 심지어 ≥ 약 96%이다. 인간 항체 생식선 유전자 생성물에 대한 동일성은 치료 중인 환자의 약물에 대한 면역 반응을 유도하는 치료 단백질의 위험을 줄이는 중요한 특징으로 생각된다. Hwang & Foote ("Immunogenicity of engineered antibodies"; Methods 36 (2005) 3-10)은 약물 항체 구조체의 비-인간 부분의 감소가 치료 중인 환자에서 항-약물 항체를 유도 할 위험을 감소시킨다는 것을 보여준다. 임상적으로 평가된 수많은 항체 약물과 각각의 면역원성 데이터를 비교한 결과, 항체의 V-영역의 인간화는 변경되지 않은 비인간 V 영역들을 운반하는 항체 (환자의 평균 약 23.59%) 보다 단백질의 면역원성을 더 작게 만드는 경향 (환자의 평균 약 5.1%)이 나타난다. 따라서 인간 서열에 대한 더 높은 수준의 동일성은 항체 구조체 형태의 V-영역 기반 단백질 치료제에 바람직하다. 이러한 생식선 동일성을 결정하기 위해, VL 의 V-영역은 벡터 NTI 소프트웨어를 사용하여 인간 생식선 V 세그먼트 및 J 세그먼트들의 아미노산 서열들과 함께 정렬될 수 있으며 (http://vbase.mrc-cpe.cam.ac.uk/) 해당 아미노산 서열은 동일한 아미노산 잔기들을 VL의 총 아미노산 잔기들의 수로 나누어 퍼센트로 계산할 수 있다. VH CDR3는 높은 다양성 및 기존 인간 생식선 VH CDR3 정렬 파트너들의 부족으로 인해 제외 될 수 있다는 점을 제외하고는 VH 세그먼트에 대해서도 동일하다(http://vbase.mrc-cpe.cam.ac.uk/). 그런 다음 재조합 기술을 사용하여 인간 항체 생식선 유전자에 대한 서열 동일성을 높일 수 있다.
본 명세서에서 용어 "항체"는 가장 넓은 의미로 사용되고, 이들이 원하는 항원-결합 활성을 나타내는 한, 비제한적으로 단클론 항체, 다클론 항체, 다중특이적 항체 (예를 들면, 이중특이적 항체), 및 항체 단편을 포함하는, 다양한 항체 구조를 포괄한다.
본원에서 사용되는 용어 "약" 또는 "대략"은 해당 기술 분야의 통상의 지식을 가진 자에 의해 결정된 특정 수치에 대해 허용가능한 오차 범위 내에 있음을 의미하며, 이는 부분적으로 그 수치가 어떻게 측정 또는 결정되는지, 즉, 측정 시스템의 한계에 따라 달라질 것이다. 예를 들면, "약"은 해당 기술 분야의 실제에 따르면 3 또는 3 초과의 표준 편차 이내임을 의미할 수 있다. 대안적으로, "약"은 주어진 수치의 최대 20%, 바람직하게는 최대 10%, 더욱 바람직하게는 최대 5%, 그리고 더욱 바람직하게는 또한 최대 1% 범위를 의미할 수 있다. 대안적으로, 특히 생물학적 시스템 또는 과정들과 관련하여, 이 용어는 하나의 값의 바람직하게는 5-배 이내, 그리고 더욱 바람직하게는 2-배 이내의 자리수에 속함을 의미할 수 있다.
본 출원에서 사용되는 단수형태 "하나" 및 "그것"은 내용상 명확히 달리 언급이 없는 한 복수의 언급을 포함한다. 그러므로, 예를 들어, "하나의 시약"에 대한 언급은 하나 이상의 상이한 시약들을 포함하며 "그 방법"에 대한 언급은 본 출원에 기재된 방법들에 대해 변형 또는 치환될 수 있는, 해당 기술분야의 통상의 지식을 가진자들에게 공지된 균등한 단계들 및 방법들에 대한 언급을 포함한다.
달리 언급이 없는 한, 일련의 요소들 앞에 오는 용어 "~이상"은 그 일련의 요소들에 있는 각 요소를 의미하는 것으로 이해하여야 한다. 해당 기술 분야의 숙련된 기술자들은 통상적인 실험을 통해 본 출원에 기재된 본 발명의 특정 구체예들에 대한 많은 균등예들을 인식 또는 알 수 있을 것이다. 이러한 균등예들은 본 발명에 포함되는 것으로 한다.
본원에서 사용되는 용어 "및/또는" 은 "및," "또는," 및 " 모두 또는 상기 용어에 의해 연결되는 요소들의 임의의 다른 조합"의 의미를 포함한다.
"보다 작다"또는 "보다 큼"이라는 용어에는 구체적인 숫자가 포함된다. 예를 들어, 20 미만은 이와 작거나 같음을 의미한다. 유사하게, 초과 또는 보다 큼은 각각 이보다 초과하거나 이와 같음 또는 이보다 크거나 이와 같음을 의미한다.
본 명세서 및 하기 청구범위를 통해, 내용상 달리 요구되지 않는 한, 용어 "포함하다", 및 이의 변형들, 가령 "포함하다" 및 "포함하는"은, 언급된 정수 또는 단계 또는 정수들 또는 단계들의 군을 포함함을 의미하지만 임의의 그 외 정수 또는 단계 또는 정수 또는 단계의 군을 제외시키지 않음이 이해될 것이다. 본 출원에서 용어 "포함하는"이 사용될 경우, 이는 용어 "함유하는" 또는 "비롯한"으로 치환될 수 있거나 때때로 용어 "가지는"과 함께 사용될 경우도 있다.
"~로 구성된"이 본 출원에서 사용될 경우 이는 청구범위 요소에 특정되어 있지 않은 임의의 요소, 단계, 또는 성분을 제외시킨다. "실질적으로 ~로 구성된"이 본 출원에서 사용될 경우 이는 청구범위의 기본적이고 신규한 특성들에 물질적으로 영향을 주지 않는 물질들 또는 단계들을 제외시키지 않는다.
본 명세서의 각각의 경우에서, "포함하는", "본질적으로 구성되는"및 "구성되는"의 임의의 용어는 다른 두 용어 중 하나로 대체 될 수있다.
II.
CD16A 항원-결합 단백질
첫 번째 측면에서 본 발명은 자연 살해 (NK) 세포 기반 표적화 접근법을 위한 CD16A 항원-결합 단백질을 제공한다, 즉:
다음을 포함하는 다중특이적 항원-결합 단백질
-적어도 하나의 제 1 표적 항원-결합 모이어티;
-적어도 2개의 CD16A 항원-결합 모이어티; 및
-적어도 하나의 항체 불변 도메인.
일부 구체예에서 상기 불변 도메인은 Fab 단편의 일부 또는 Fc 부분이다.
일부 구체예에서 CD16A 항원-결합 모이어티는 불변 도메인에 융합되고, 여기서 불변 도메인은 Fab 단편의 일부 (CH1 또는 CL) 또는 Fc 부분 일 수 있다.
따라서, 또 다른 구체예에서 다중특이적 항원-결합 단백질은 다음을 포함한다:
-적어도 하나의 제 1 표적 항원-결합 모이어티;
-예를 들어, Fab 단편 또는 Fc 부분의 불변 도메인에 융합된 적어도 2개의 CD16A 항원-결합 모이어티.
이 항원-결합 단백질은 NK 세포에 결합하여 표적, 예를 들어, 종양 항원 양성 세포, 바이러스 감염 세포 또는 병원체에 대한 NK 세포 매개 세포독성을 재지시한다.
2개의 CD16A 결합 모이어티에 의한 2가 결합으로 인해 CD16A를 통한 NK 세포 결합 강도의 결합력이 증가하고 NK 세포 이펙터 기능, 가령, 예를 들어, 항체 의존성 세포 매개 세포독성 (ADCC)이 단일클론 항체 또는 항체 단편에 비해 향상 될 수 있다.
NK 세포는 그 CD16A 수용체를 통해 다중특이적 항원-결합 단백질에 의해 결합되고, 이에 의해, 표적, 예를 들어 종양 관련 항원 (TAA) 발현 표적 세포를 향해 재지시된다. 따라서, 이러한 다중특이적 항원-결합 단백질은 NK 세포를 선택적으로 재지시하고 종양 세포, 바이러스 감염 세포 또는 병원균에 대한 용해를 매개 할 수 있다. 대조적으로, IgG 아이소형의 전장 항체는 그들의 Fc 영역을 통해 CD16A, CD16B (FcgRIIIB), CD32A (FcgRIIA), CD32B (FcgRIIB) and CD64 (FcgRI)를 포함하는 활성화 및 억제 Fcγ 수용체에 결합한다. 그러나, CD16A에 대한 특이성을 갖는 항원-결합 단백질은, NK 세포 및 대 식세포에서 발견되지만 호중구에서는 발견되지 않는 활성화 아형 CD16A를 선택적으로 표적화한다. 또한, NK 세포 결합 항원-결합 단백질은 CD16A와 2가 상호작용하여 일반 항체에 비해 약 1,000배 더 높은 친화성을 가져온다.
CD16A는 NK 세포의 세포독성 활성을 유발하는 활성화 수용체이다. CD16A에 대한 항체의 친화성은 NK 세포 활성화를 유발하는 능력과 직접적으로 관련이 있다. 항원-결합 단백질은 CD16A에 2가 결합, 즉, 2개의 항원-결합 모이어티와 결합하여 제공되어, CD16A에 대한 높은 결합력으로 인해 친화성을 증가시킨다.
또한, 항원-결합 모이어티를 Fc 부분 또는 FcRn 결합이 가능한 IgG 기반 항체에 융합시킴으로써 scFv-기반 항원-결합 스캐폴드에 비해 혈청 반감기가 연장 될 수 있으며, 이는 생체내 치료 적용을 보다 편리하게 만든다. 이에 의해, 이러한 Fc 부분은 FcRn에 대한 결합 증가 또는 감소를 위해 변형 될 수 있으며, 이는 혈청 반감기 및/또는 세포들 간 결합된 IgG의 수송을 추가로 조절한다. 후자는 또한 트랜스사이토시스로 설명되고 있다 (Dickinson 외, 1999).
또한, 항원-결합 단백질과 인간 혈청 알부민 (HSA) 또는 HSA 결합-모이어티의 융합에 의해 혈청 반감기가 연장 될 수 있다. 예를 들어, Fab 단편의 혈청 반감기는 Fab 단편의 Fv 영역에서 HSA 결합-모이어티에 의해 연장 될 수 있는 반면, CD16A-및 표적 항원-결합 모이어티는 Fab 단편의 C-말단에 융합된다. 대안 적으로, HSA 결합 모이어티는 Fab 단편의 C-말단에 융합 될 수 있고 Fab 단편의 Fv 영역은 표적 항원 또는 CD16A 결합 모이어티를 제공 할 수 있다.
항원-결합 모이어티는 다양한 방식으로 Fab 단편 또는 Fc 부분에 융합 될 수 있으며, 본원에 기재된 항원-결합 단백질의 모듈형 구조는 원하는 적용에 따라 쉽게 설계되고 선택 될 수 있는 수많은 스캐폴드를 이용가능하게 만든다.
바람직하게는, VH 및 VL 가변 영역은 가변 영역이 항원-결합에 필요한 형태로 결합 할 수 있게 하는 펩티드 링커에 의해 연결된다. 여분의 가변 도메인 영역을 포함하는 폴리펩티드는 연결기에 의해 Fab 단편의 불변 도메인 또는 Fc 부분에 융합된다.
항원-결합 모이어티는 하나 이상의 Fv 폴리펩티드를 포함하는 항원-결합 분자 형태에 의해, 예를 들면, 단쇄 Fv (scFv), 단일 폴리펩티드로 연결된 2개의 scFv들로 구성된 탠덤 단쇄 Fv ((scFv)2), 디아바디 (Db), 단쇄 디아바디 (scDb), 탠덤 디아바디 (TandAb®), Fab, F(ab')2 또는 이중 친화성 재표적화 항체 (DARTTM)에 의해 제공된다. CD16A 항원-결합 단백질에 특히 바람직한 것은 scFv, Db 또는 scDb이다. 각 scFv는 단일 항원-결합 모이어티를 제공하지만, 2가 Db, scDb 및 (scFv)2는 항원-결합 단백질에 2개의 항원-결합 모이어티를 제공한다. 바람직하게는, 2가 Db, scDb 또는 (scFv)2 또는 2개의 scFv들은 단일특이적이며 동일한 항원 특이성의 2개의 항원-결합 모이어티, 즉, CD16A 또는 표적 항원을 제공한다.
각각의 항원-결합 모이어티는 "연결기"또는 펩티드 결합에 의해 Fab의 불변 도메인 또는 Fc 부분에 연결된다. 바람직하게는 연결기는 펩티드이다. 특히, 연결기는 1 내지 30개 아미노산 잔기, 예를 들어, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30개의 아미노산 잔기의 연속 사슬로 구성된 펩티드이다. 보다 구체적으로, 연결기는 3 내지 30 개, 6 내지 20 개, 6 내지 18 개 또는 6 내지 15 개의 아미노산 잔기로 구성된다. 일부 구체예에서 연결기는 G 및 S 아미노산 잔기로 구성되는데, 예를 들어, 연결기는 (G2S)x 펩티드이고, 이 때 x = 1-10 이거나, (G4S)y,이고 이 때 y = 1-6이며, 예컨대, 서열 번호: 19, 20, 21 또는 22에 제시된 아미노산 서열을 가지는 연결기이다.
특정 구체예에서 항원-결합 모이어티는 힌지 영역을 통해 Fc 부분의 CH2 도메인의 N-말단에 융합된다. 힌지 영역은 Fc 부분과 동일하거나 상이한 IgG 클래스이거나 자연적으로 발생하지 않는 조작된 힌지 도메인 일 수 있다. IgG 야생형 힌지 영역의 한 예는 서열 번호:23에 제시된 아미노산 서열을 가진다. 변형된 (단축된) 힌지 영역 (중간.힌지)의 한 예는 서열 번호: 24에 제시된 아미노산 서열을 가진다.
일부 구체예에서 2개의 CD16A 항원-결합 모이어티는 Fc 부분의 N-말단에 융합되는 반면, 1 또는 2개의 표적 항원-결합 모이어티는 Fc 부분의 C-말단에 융합되고; 또는 2개의 CD16A 항원-결합 모이어티는 Fc 부분의 C-말단에 융합되고 1 또는 2개의 표적 항원-결합 모이어티는 Fc 부분의 N-말단에 융합된다 (예컨대, KiH-scDb-Fc; 도 3-6; Db-Fc, 도 9-10; Bi-scFv-Fc, 도 11-12 및 KiH-scFv-Fc, 도 15A 및 15B).
추가 구체예에서, 항원-결합 모이어티는 Ig 항체, 예를 들어, IgG에 통합되거나 융합된다. 각각의 CD16A 항원-결합 모이어티는 Fc 부분의 C-말단에 scFv로서 융합 될 수 있고, 표적 항원-결합 모이어티는 2개의 Fab 아암들 각각에 통합될 수 있다 (scFv-IgAb, 도 13). 대안적으로, 각각의 CD16A 항원-결합 모이어티는 각각의 Fab 아암에서 Fv 도메인으로 통합 될 수 있는 반면, 1 또는 2개의 표적 항원-결합 모이어티는 Fc 부분의 C-말단에 융합될 수 있다 (scFv-IgAb, 도 16). 특정 구체예에서 추가의 표적 항원-결합 모이어티는 각각의 CL 도메인들의 C-말단에 융합 될 수 있다 (Bi-scFv-IgAb, 도 14).
추가 구체예에서 2개의 CD16A 항원-결합 모이어티 및 표적 항원 모이어티는 Fab의 C-말단에 융합되는 반면, Fab의 Fv 도메인은 제 2 또는 제 3 표적 항원-결합 모이어티를 제공한다 (scDb-TriBs (-scFv), 도 7 및 8). 대안적으로, 2개의 CD16A 항원-결합 모이어티는 Fab의 C-말단에 융합 될 수 있고 표적 항원-결합 모이어티는 Fab의 Fv 도메인에 통합된다.
항원-결합 단백질은 CD16A에 대해 적어도 2가이다, 즉, 적어도 2개의 CD16A 항원-결합 모이어티를 포함한다.
일부 구체예에서 항원-결합 단백질은 동일한 항원에 대한 적어도 2개의 표적 항원-결합 모이어티 및 2개의 CD16A 항원-결합 모이어티를 포함하는 4가 및 이중 특이 적이다.
추가 구체예에서 항원-결합 모이어티는 제 1 및 제 2 표적 항원-결합 모이어티 및 2개의 CD16A 항원-결합 모이어티를 포함하는 4가 및 삼중 특이 적이다. 이러한 항원-결합 단백질은 공동 또는 이중 표적화에 사용될 수 있다. 예를 들어, 이러한 항원-결합 단백질은 제 1 종양 항원-결합 모이어티 (TAA1) 및 제 2 종양 항원-결합 모이어티 (TAA2) 및 NK 세포 세포독성을 제 1 (TAA1) 및 제 2 (TAA2) 종양 항원들을 나타내는 세포들에 대해 재지시하는 2개의 CD16A 항원-결합 모이어티를 포함한다. 대안적으로, 제 1 (TAA1) 종양 항원-결합 모이어티 및 제 2 (TAA2) 종양 항원-결합 모이어티 및 2개의 CD16A 항원-결합 모이어티를 포함하는 이러한 삼중 특이 적 항원-결합 단백질을 사용하여 NK 세포 세포독성을 제 1 (TAA1) 또는 제 2 (TAA2) 종양 항원을 발현하는 표현형에서 구별되는 세포 유형으로 재지시 할 수 있다.
특정 구체예에서 항원-결합 단백질은 3가 및 이중특이적 , 3가 및 삼중특이적, 4가 및 이중특이적 , 4가 및 삼중특이적, 4가 및 사중특이적, 6가 및 삼중특이적 또는 6가 및 이중특이적 일 수 있다.
두 번째 측면에서 본 발명은 적어도 2개의 CD16A 항원-결합 모이어티 및, NK 세포 동족살해를 방지하고 효율적인 NK 세포 결합 및 강화된 면역 이펙터 기능들, 가령, 예를 들면, 강화된 ADCC를 위한 동원을 가능하게 하는 CD16A 항원-결합 모이어티의 폴리펩티드 내부에 결정된 항-CD16A 도메인 배열을 가지는 특정 항원-결합 단백질 형태들을 제공한다.
CD16A 항원-결합 단백질은 다라투무맙이 50% 이상의 NK 용해를 유도한 분석에서 최대 30 μg/mL의 항체 농도에서 측정가능한 용해가 없거나 10% 미만의 최소 일 때 NK-NK 용해 유도에 대해 음성으로 간주된다.
NK 세포 동족살해를 방지하면서 NK 세포 결합 및 이펙터 기능에 대한 동원은 향상되는 효과는, 본원에 기술된 항원-결합 단백질의 특정 3D 구조의 고유한 특성과 관련되어야 한다.
본원에 개시된 항원-결합 단백질 (예를 들어, 실시예 7에 기재된 것들)의 N-말단에서의 CD16A 결합은 일반적으로 C-말단에서의 CD16A 결합보다 적은 NK 세포 동족살해를 초래하였다. 그러나, 본 발명은 N-또는 C-말단에서 CD16A에 결합하는 항원-결합 단백질을 포함한다 (예를 들어, 양쪽 말단 중 하나에서의 결합의 예는 실시예 7, 8 및 9 참고). N-말단 CD16 결합과 상세히 관련하여, Fab 기반 CD16A 결합을 사용하여 실시예 8에 개시된 바와 같이 보다 뚜렷한 NK 세포 고갈이 관찰되었다. 더욱이, CD16 Fv의 도메인 순서를 분석함으로써 VH-VL 순서를 포함하는 것과 비교하여 VL-VH 도메인 순서를 포함하는 항체 형태에 의해 NK 세포 동족살해 발생의 명확한 감소가 유도된다.
특정 구체예에서, NK 세포 동족살해 유도 항체의 비율 및 NK 세포 사멸의 효능은 Fab-기반 CD16A 결합을 피하고 CD16 결합 Fv 도메인의 유익한 VL-VH 순서에 초점을 맞춤으로써 개선된다.
특정 구체예에서, CD16A 항원-결합 모이어티의 폴리펩티드 내의 가변 영역은 폴리펩티드의 N-말단, 즉, Fv 폴리펩티드에 경쇄 가변 영역 (VL)이 위치하도록 차례로 연결되어야한다. N-말단에 위치하는 VL 옆의 가변 영역은 VL 또는 VH 일 수 있다. 주의 할 점은, CD16A 항원-결합 모이어티의 가변 영역이 VL이 CD16A 항원-결합 모이어티의 N-말단에 위치하도록 배치되는 경우, CD16A 항원-결합 모이어티의 결합 친화성과는 독립적으로 동족살해를 피할 수 있다.
특히, CD16A 항원-결합 모이어티가 scFv 인 경우 가변 영역은 폴리펩티드의 N-로부터 C-말단으로 다음과 같이 위치한다:VL-VH.
특히, CD16A 항원-결합 모이어티가 Db 인 경우 가변 영역은 Db를 형성하는 2개의 폴리펩티드 각각에서 N-로부터 C-말단으로 다음과 같이 위치한다:VL-VH.
특히, CD16A 항원-결합 모이어티가 scDb 인 경우 가변 영역은 폴리펩티드의 N-로부터 C-말단으로 (i) VL-VH-VL-VH 또는 (ii) VL-VL-VH-VH. 또는 (iii) VH-VH-VL-VL로 위치한다.
특히, CD16A 항원-결합 모이어티가 (scFv)2 인 경우 가변 영역은 폴리펩티드의 N-로부터 C-말단으로 다음과 같이 위치한다: VL-VH-VL-VH.
CD16A 항원-결합 모이어티, 예를 들어, scFv, Db 또는 scDb의 이러한 폴리펩티드는 연결기를 통해 (i) C-말단에 의해 Fc 부분의 CH2 도메인의 N-말단에 또는 힌지/중간 힌지 영역에, 또는 (ii) N-말단에 의해 Fc 부분의 CH3 도메인의 C-말단에 또는 CL 또는 CH1 도메인의 C-말단에 융합된다.
바람직하게는, CD16A 항원-결합 모이어티는 모두 항원-결합 단백질에서 N-말단 또는 C-말단에 위치한다.
일부 구체예에서 CD16A 항원-결합 모이어티는 Fc 부분에 융합된다. 바람직하게는, 두 CD16A 결합 모이어티들은 Fc 부분에 N-말단 또는 C-말단으로 융합된다. Fc 부분은 IgG Fc 영역의 적어도 하나의 기능을 보유하는 불변 영역의 일부를 포함한다. "Fc 부분"은 고유 서열 Fc 영역 및 변이체 Fc 영역을 포함한다.
바람직하게는, Fc 부분은 "침묵"된다. "침묵된 Fc 부분"은 CD16A (FcγRIIIA)를 포함하는 Fc-감마 수용체 (Fcγ) 수용체 (FcγR)에 그 자체로 결합하지 않지만 신생아 Fc 수용체 (FcRn)에 대한 결합을 유지하는 변형된 Fc 부분을 지칭한다. FcRn 결합은 상피 장벽을 통과하여 트랜스사이토시스를 가능하게 하고 FcRn 결합 Fc 부분들을 포함하는 IgG 또는 융합 단백질들을 리소좀 분해로부터 보호하기 위해 재순환시켜 혈청 반감기가 연장되고 순환에서 더 오래 지속되도록 한다. 항원-결합 단백질은 CD16A 항원-결합 모이어티를 통해 특이적으로 NK 세포에서 CD16A와 결합하도록 설계되었으므로, 바람직한 구체예에서 다른 Fc-감마 수용체에 대한 Fc 결합은 방지되어야 한다. 따라서, FcRn 결합을 유지 또는 증강시키는 Fc-융합 항원-결합 단백질의 Fc 부분에서의 변형이 바람직하다.
Fc-감마 수용체에 대한 결합이 감소되거나 없는 IgG1 Fc 부분을 생성하기 위한 여러 세트의 돌연변이 또는 변화들( "침묵 돌연변이"또는 "무-이펙터 돌연변이"라고 함)은 C220S, C229S, E233P, L234A, L234V, L234F, L235A, L235E, P238S, D265A, N297A, N297Q, P331S으로 구성된 그룹의 돌연변이들로부터 선택되고; 또는 Fc-감마 수용체에 대한 결합이 감소된 IgG2 Fc 부분을 생성하기 위한 돌연변이들은 H268Q, V309L, A330S, A331S로 구성된 그룹에서 선택될 수 있고; 또는 Fc-감마 수용체에 대한 결합이 감소된 IgG4 Fc 부분을 생성하기 위한 돌연변이들은 L235A, G237A, E318A로 구성된 그룹에서 선택될 수 있는 것으로 기재된 바 있다 (Strohl W., Current Opinion in Biotechnology (2009);20:1-7; Kaneko E and Niwa R, Biodrugs (2011);25(1):1-11; Baudino L., J. Immunology (2008);181:6664-6669).
추가로, Fc 부분은 혈청 반감기를, 예를 들어, 증가 또는 감소와 같이 조절하도록 조작 될 수 있다. 항원-결합 단백질의 혈청 반감기를 증가시키는 다음과 같은 IgG1 Fc 부분의 돌연변이가 기재된 바 있다: T250Q, M252Y, S254T, T256E, T307A, E380A, M428L, H433K, N434A, N434Y (Srohl W., Current Opinion in Biotechnology (2009); 20 : 1-7; Borrok MJ, 외, J. Pharmaceutical Sciences 2017; 106 (4) : 1008-1017).
일부 구체예에서 IgG, 특히 IgG1, Fc 부분은 Kabat EU 넘버링에 따라 위치 234, 235 및 265에서 돌연변이 세트를 포함하고, 특히, 돌연변이 세트는 L234F/V/A, L235A/E 및 D265A에서 선택된다. 돌연변이 L234F, L235E 및 D265A 세트를 포함하는 IgG1 Fc 부분이 특히 바람직하다. 따라서, 일부 구체예에서 항원-결합 단백질은 돌연변이 세트 L234F, L235E 및 D265A를 갖는 침묵된 IgG1 Fc 부분을 포함한다. 언급 된 모든 돌연변이는 Kabat EU 넘버링 체계에 상응한다 (Kabat, E.A. 외, Sequences of proteins of immunological interest. 5th Edition -US Department of Health and Human Services, NIH publication n° 91-3242, pp 662,680,689 (1991). 특정 구체예에서 항원-결합 단백질은 돌연변이 세트 L234F 및 L235E를 갖는 침묵된 IgG1 Fc 부분을 포함한다.
일부 구체예에서 CD16A 항원-결합 모이어티는 서로 조립된 2개의 동일한 CH2-CH3 폴리펩티드를 포함하는 동종이량체 Fc 부분에 융합되고, 여기서 공유 이량체화는 CH2 도메인에 대하여 N-말단으로 힌지 영역에 의해 촉진된다.
항원-결합 모이어티는 힌지 영역을 통해 Fc 부분에 N-말단으로 또는 CH3 도메인에 C-말단으로 융합 될 수 있다. CD16A 항원-결합 모이어티가 N-말단으로 융합된 경우, 제 1 표적 항원-결합 모이어티는 바람직하게는 Fc 영역에 C-말단으로 융합된다.
특정 구체예에서, 2개의 CD16A 항원-결합 모이어티는 융합되어 Db가 이량체화에 의해 Fc 부분의 N-말단 또는 C-말단에서 (Db-Fc) 형성되고, 여기서 CD16A 항원-결합 VL-VH-폴리펩티드는 연결기 및 힌지 영역을 통해 CH3의 N-말단 또는 C-말단에서 CH2-CH3 폴리펩티드에 융합되고 표적 항원-결합 모이어티는 각각의 반대쪽 말단에 scFv로서 융합된다 (도 9, 10). 바람직하게는, 힌지는 중간.힌지이다 (서열 번호: 24). 예를 들어, 이러한 항원-결합 단백질은 Fc 영역에서 이량체화된 2개의 폴리펩티드 사슬을 포함하고, 여기서 각 폴리펩티드 사슬은 N-으로부터 C-말단으로 다음을 포함한다:
(i) VL(CD16A)-VH(CD16A)-힌지-CH2-CH3-VH(표적)-VL(표적) (도 9);
(ii)VL(CD16A)-VH(CD16A)-힌지-CH2-CH3-VL(표적)-VH(표적) (도 9);
(iii) VL(표적)-VH(표적)-힌지-CH2-CH3-VL(CD16A)-VH(CD16A) (도 10); 또는
(iv) VH(표적)-VL(표적)-힌지-CH2-CH3-VL(CD16A)-VH(CD16A) (도 10).
또 다른 구체예에서 2개의 CD16A 항원-결합 모이어티는 scFv로서 Fc 부분에 융합되고 (Bi-scFv-Fc), 여기서 제 1 특이성 (표적-또는 CD16A-결합)의 scFv들은 CH2-CH3 폴리펩티드의 한 말단에 융합되고, 제 2 특이성 (CD16A-또는 표적-결합)의 scFv들은 이량체 Fc 부분을 형성하는 CH2-CH3 폴리펩티드의 다른 말단에 융합된다. 이에 의해, 2개의 표적 항원-결합 모이어티 각각은 2개의 CH2-CH3 폴리펩티드 각각의 각 반대편 말단에 scFv로서 융합된다 (도 11, 12). 예를 들어, 이러한 항원-결합 단백질은 힌지 및 Fc 영역에서 동종이량체화하는 2개의 폴리펩티드 사슬을 포함하며, 여기서 각 폴리펩티드 사슬은 N-말단 및 C-말단에서 scFv를 포함하고 각각의 CH2-CH3 폴리펩티드 및 도메인들은 N-으로부터 C-말단으로 다음과 같이 배치된다:
(i) VL(CD16A)-VH(CD16A)-힌지-CH2-CH3-VH(표적)-VL(표적) (도 11);
(ii)VL(CD16A)-VH(CD16A)-힌지-CH2-CH3-VL(표적)-VH(표적) (도 11);
(iii) VL(표적)-VH(표적)-힌지-CH2-CH3-VL(CD16A)-VH(CD16A) (도 12); 또는
(iv) VH(표적)-VL(표적)-힌지-CH2-CH3-VL(CD16A)-VH(CD16A) (도 12).
일부 구체예에서 CD16A 항원-결합 모이어티는 이종이량체 (비대칭) Fc 부분에 융합된다. 이러한 이종이량체 Fc 부분은 2개의 폴리펩티드의 (이종) 이량체화를 촉진하는 Fc 영역의 2개의 CH2-CH3 폴리펩티드 각각의 변형을 포함한다. 이들은 2개의 CH2-CH3 폴리펩티드의 조립을 촉진하기 위해 서로 상보적인 폴리펩티드들 각각에서 개별적인 변형들을 포함한다. 상기 변형들은 아미노산 치환으로 번역되는 핵산 돌연변이 일 수 있다. 이러한 변형은 "놉-인투-홀"(KiH)로 알려져 있으며 다양한 변이체들의 구조는 예를 들어 Ridgway 외 (Protein Engineering, vol.9, no.7, pp.617-621, 1996)에 기재된 바 있다. 예를 들어, EU 넘버링 체계에 따르면 하나의 CH2-CH3 폴리펩티드에서 T366Y 치환 및 다른 폴리펩티드에서 Y407T 치환이 있다 (Kabat 외, Sequences of Proteins of Immunological Interest, 5th edn. NIH, 1991). 제 1 IgG1 CH2-CH3 폴리펩티드에서 놉-인투-홀 치환 T366Y 및 제 2 IgG1 CH2-CH3 폴리펩티드에서 Y407T 치환을 포함하는 Fc 부분의 한 예는 서열 번호: 31, 32에 제시된 아미노산 서열을 갖는다. 또한 이종이량체화를 촉진하는 상보적 경계면을 생성하기 위한 또 다른 전략이 개발되었다 (Brinkmann 및 Kontermann, MABS 2017;9(2):182-212에서 검토됨). 추가 구체예에서, 이황화 가교를 혼입하여 이종이량체를 추가로 안정화시키고 수율을 증가시킬 수 있다 (Merchant 외, Nature Biotech. 1998;16: 677-681; Atwell 외; J. Mol. Biol. 270 (1997) 26-35).
특정 구체예에서 2개의 CD16A 항원-결합 모이어티는 이종이량체 Fc 부분에 scDb로서 융합되고 (KiH-scDb-Fc), 여기서 scDb의 단일 폴리펩티드는 제 1 CH2-CH3 폴리펩티드에 융합되고, 단일 표적 항원-결합 모이어티는 동일한 또는 제 2 CH2-CH3 폴리펩티드의 각각의 반대쪽 말단에 scFv로서 융합된다 (도 3, 5). 예를 들어, 이러한 항원-결합 단백질은 중앙에 이종이량체화된 2개의 폴리펩티드 사슬을 포함한다. 힌지 또는 힌지 및 Fc 영역, 여기서 제 1 폴리펩티드 사슬은 N-으로부터 C-말단으로 다음을 포함하고: VL(CD16A)-VH(CD16A)-VL(CD16A)-VH(CD16A)-힌지-CH2-CH3 또는 VL(CD16A)-VL(CD16A)-VH(CD16A)-VH(CD16A)-힌지-CH2-CH3 그리고 제 2 폴리펩티드는 N-으로부터 C-말단으로 다음을 포함하고: 힌지-CH2-CH3-VH(표적)-VL(표적) 또는 힌지-CH2-CH3-VL(표적)-VH(표적) (도 3); 또는 제 1 폴리펩티드 사슬은 N-으로부터 C-말단으로 다음을 포함하고: 힌지-CH2-CH3-VL(CD16A)-VH(CD16A)-VL(CD16A)-VH(CD16A) 또는 힌지-CH2-CH3-VL(CD16A)-VL(CD16A)-VH(CD16A)-VH(CD16A) 및 제 2 폴리펩티드는 N-으로부터 C-말단으로 다음을 포함하고: VH(표적)-VL(표적)-힌지-CH2-CH3 또는 VL(표적)-VH(표적)-힌지-CH2-CH3 (도 5); 또는 scDb의 단일 폴리펩티드는 제 1 CH2-CH3 폴리펩티드에 융합되고 단일 표적 항원-결합 모이어티는 제 2 CH2-CH3 폴리펩티드의 동일한 말단에 scFv로서 융합된다 (도 4). 예를 들어, 이러한 항원-결합 단백질은 2개의 폴리펩티드 사슬을 포함하고, 여기서 제 1 폴리펩티드 사슬은 N-으로부터 C-말단으로: VL(CD16A)-VH(CD16A)-VL(CD16A)-VH(CD16A)-힌지-CH2-CH3 또는 VL(CD16A)-VL(CD16A)-VH(CD16A)-VH(CD16A)-힌지-CH2-CH3을 포함하고 제 2 폴리펩티드는 N-으로부터 C-말단으로: VH(표적)-VL(표적)-힌지-CH2-CH3 또는 VL(표적)-VH(표적)-힌지-CH2-CH3를 포함한다 (도 4).
또 다른 구체예에서 2개의 CD16A 항원-결합 모이어티는 scDb로서 이종이량체 Fc 부분에 융합되고 scDb의 단일 폴리펩티드는 제 1 CH2-CH3 폴리펩티드에 융합되고 단일 제 1 표적 항원-결합 모이어티 (TAA1)는 이러한 제 1 CH2-CH3 폴리펩티드의 각각의 반대쪽 말단에 scFv로서 융합되고 제 2 표적 항원-결합 모이어티 (TAA2)는 제 1 표적 항원-결합 모이어티와 동일한 말단에서 제 2 CH2-CH3 폴리펩티드에 scFv로서 융합된다 (도 6). 예를 들어, 이러한 항원-결합 단백질은 힌지 또는 중간 힌지 및 Fc 영역에서 이종이량체화하는 2개의 폴리펩티드 사슬을 포함하고, 여기서 제 1 폴리펩티드 사슬은 N-으로부터 C-말단으로: VH(표적1)-VL(표적1)-힌지-CH2-CH3-VL(CD16A)-VH(CD16A)-VL(CD16A)-VH(CD16A) ) 또는 VH(표적1)-VL(표적1)-힌지-CH2-CH3-VL(CD16A)-VL(CD16A)-VH(CD16A)-VH(CD16A) 또는 VL(표적1)-VH(표적1)-힌지-CH2-CH3-VL(CD16A)-VH(CD16A)-VL(CD16A)-VH(CD16A) 또는 VL(표적1)-VH(표적1)-힌지-CH2-CH3-VL(CD16A)-VL(CD16A)-VH(CD16A)-VH(CD16A)를 포함하고 그리고 제 2 폴리펩티드는 N-으로부터 C-말단으로: VH(표적2)-VL(표적2)-힌지-CH2-CH3 또는 VL(표적2)-VH(표적2)-힌지-CH2-CH3를 포함한다 (도 6).
추가 구체예에서 2개의 CD16A 항원-결합 모이어티는 각각 이종이량체 Fc 부분에 scFv로서 융합되고 (KiH-scFv-Fc), 2개의 scFv 각각은 제 1 및 제 2 CH2-CH3 폴리펩티드 중 하나에 융합되고 단일 제 1 표적 항원-결합 모이어티 (TAA1)는 제 1 CH2-CH3 폴리펩티드의 각각의 반대편 말단에 scFv로 융합되고 제 2 표적 항원-결합 모이어티 (TAA2)는 제 1 표적 항원-결합 모이어티와 동일한 말단에서 제 2 CH2-CH3 폴리펩티드에 scFv로 융합된다 (도 15). 예를 들면, 이러한 항원-결합 단백질은에서 이종이량체화하는 2개의 폴리펩티드 사슬들을 포함하고, 여기서 제 1 폴리펩티드 사슬은 N-으로부터 C-말단으로: VH(표적1)-VL(표적1)-힌지-CH2-CH3-VL(CD16A)-VH(CD16A) 또는 VL(표적1)-VH(표적1)-힌지-CH2-CH3-VL(CD16A)-VH(CD16A)를 포함하고 그리고 제 2 폴리펩티드는 N-으로부터 C-말단으로: VH(표적2)-VL(표적2)-힌지-CH2-CH3-VL(CD16A)-VH(CD16A) 또는 VL(표적2)-VH(표적2)-힌지-CH2-CH3-VL(CD16A)-VH(CD16A)를 포함하고 (도 15b); 대안적으로, 이러한 항원-결합 단백질은 Fc 영역에서 이종이량체화하는 2개의 폴리펩티드 사슬들을 포함하고, 여기서 제 1 폴리펩티드 사슬은 N-으로부터 C-말단으로: VL(CD16A)-VH(CD16A)-힌지-CH2-CH3-VH(표적1)-VL(표적1) 또는 VL(CD16A)-VH(CD16A)-힌지-CH2-CH3-VL(표적1)-VH(표적1)을 포함하고 그리고 제 2 폴리펩티드는 N-으로부터 C-말단으로: VL(CD16A)-VH(CD16A)-힌지-CH2-CH3-VH(표적2)-VL(표적2) 또는 VL(CD16A)-VH(CD16A)-힌지-CH2-CH3-VL(표적2)-VH(표적2)를 포함한다 (도 15a).
추가 구체예에서, 2개의 CD16A 항원-결합 모이어티는 scDb로서 단량체 Fc 부분에 융합된다 (scDb-mFc, 도 1, 2). 이러한 단량체 Fc 부분 (mFc)은 다른 CH2-CH3 폴리펩티드와의 이량체화를 방지하고 힌지 영역이 없는 CH3 도메인의 돌연변이를 포함하지만, FcRn 수용체에 대한 결합을 유지하고 다른 Fc-감마R에 결합하지 않는다. 이러한 돌연변이들은 Ying 외 (MABS, 2014;6(5):1201-1210; 또는 WO 2013/138643)에 기재되어 있다. 이러한 단량체 Fc 부분의 예는 서열 번호:30에 제시된 아미노산 서열을 가진다. 이러한 항원-결합 단백질은 단일 폴리펩티드 사슬로 구성되며, 여기서 2개의 CD16A 항원-결합 모이어티를 포함하는 scDb는 단량체 Fc 부분의 한 말단에 융합되고 표적 항원-결합 모이어티는 단량체 Fc 부분의 다른 말단에 융합된다. 이러한 항원-결합 단백질은 N-으로부터 C-말단으로 다음을 포함하는 단일 폴리펩티드 사슬로 구성된다: VL(CD16A)-VH(CD16A)-VL(CD16A)-VH(CD16A)-CH2-CH3-VH(표적)-VL(표적) 또는 VL(CD16A)-VH(CD16A)-VL(CD16A)-VH(CD16A)-CH2-CH3-VL(표적)-VH(표적), 또는 VL(CD16A)-VL(CD16A)-VH(CD16A)-VH(CD16A)-CH2-CH3-VH(표적)-VL(표적), 또는 VL(CD16A)-VL(CD16A)-VH(CD16A)-VH(CD16A)-CH2-CH3-VL(표적)-VH(표적) (도1), 또는 VH(표적)-VL(표적)-CH2-CH3-VL(CD16A)-VH(CD16A)-VL(CD16A)-VH(CD16A), 또는 VL(표적)-VH(표적)-CH2-CH3-VL(CD16A)-VH(CD16A)-VL(CD16A)-VH(CD16A), 또는 VH(표적)-VL(표적)-CH2-CH3-VL(CD16A)-VL(CD16A)-VH(CD16A)-VH(CD16A), 또는 VL(표적)-VH(표적)-CH2-CH3-VL(CD16A)-VL(CD16A)-VH(CD16A)-VH(CD16A) (도 2).
다른 구체예에서, 항원-결합 모이어티의 폴리펩티드의 N-말단은 Fab 단편의 C-말단에 융합된다. 예를 들어, 2개의 CD16A 항원-결합 모이어티를 포함하는 Db, scDb 또는 2개의 scFv는 Fab 단편의 C-말단에 융합되고 Fab 단편의 Fv는 표적 항원-결합 모이어티를 포함한다.
다른 구체예에서 항원-결합 단백질은 삼중 특이 적 (scDb-TriBs (-scFv)이고, 여기서 2개의 CD16A 항원-결합 모이어티를 포함하는 scDb는 Fab 단편의 2개의 폴리펩티드 중 제 1에 C-말단으로 융합되고 제 1 표적 항원-결합 모이어티 (TAA1)는 scFv 또는 2가 scDb로서 Fab 단편의 제 2 폴리펩티드에 C-말단으로 융합되고 Fab 단편의 Fv는 제 2 표적 항원-결합 모이어티 (TAA2)를 제공한다. 특정 구체예에서 Fv의 제 2 표적 항원-결합 모이어티는 인간 혈청 알부민 (HSA) 항원-결합 모이어티이다. 이러한 항원-결합 단백질은 C-말단에서 Fab에 융합된 2개의 scDb를 가지는 Fab 단편-융합에 이량체화된 2개의 폴리펩티드 사슬들을 포함하고, 여기서 제 1 폴리펩티드 사슬은 N-으로부터 C-말단으로: VL(HSA)-CL-VL(CD16A)-VH(CD16A)-VL(CD16A)-VH(CD16A)를 포함하고 제 2 폴리펩티드는 N-으로부터 C-말단으로: VH(HSA)-CH1-VH(표적1)-VL(표적1)-VH(표적1)-VL(표적1)을 포함한다 (도 7). 또 다른 구체예에서 2개의 CD16A 항원-결합 모이어티를 포함하는 scDb 및 제 1 표적 항원-결합 모이어티를 포함하는 scFv는 C-말단에서 Fab 단편에 융합되고, 여기서 제 1 폴리펩티드 사슬은 N-으로부터 C-말단으로: VL(HSA)-CL-VH(표적1)-VL(표적1) 및 제 2 폴리펩티드는 N-으로부터 C-말단으로: VH(HSA)-CH1-VL(CD16A)-VH(CD16A)-VL(CD16A)-VH(CD16A)를 포함한다 (도 8).
추가 구체예에서, 2개의 CD16A 항원-결합 모이어티는 IgG에 C-말단으로 융합되고, 여기서 IgG의 2개의 Fab 아암은 2개의 추가 항원-결합 모이어티를 제공한다 (scFv-IgAb, 도 13). 이러한 항원-결합 단백질에서 CD16A 항원-결합 모이어티를 포함하는 제 1 scFv는 제 1 H 사슬의 CH3에 C-말단으로 융합되고 CD16A 항원-결합 모이어티를 포함하는 제 2 scFv는 제 2 H 사슬의 CH3에 융합되며, 2개의 Fab 아암은 각각의 Fv에 표적 항원-결합 모이어티를 제공한다. 두 Fv들은 동일한 표적 항원-결합 모이어티를 가질 수 있거나 두 Fv들은 제 1 및 제 2 표적 항원-결합 모이어티를 제공 할 수 있다. 예를 들어, 이러한 항원-결합 단백질은 2개의 동일한 H 및 2개의 동일한 L 사슬을 포함하며, 여기서 H 사슬은 N-으로부터 C-말단으로: VH(표적)-CH1-힌지-CH2-CH3-VL(CD16A)-VH(CD16A)를 포함하고, L 사슬은 N-으로부터 C-말단으로: VL(표적)-CL을 포함한다 (도 13).
대안 적으로, scFv-IgAb 2개의 CD16A 항원-결합 모이어티는 IgG의 Fab 아암의 2개의 Fv에 의해 제공되고 1 또는 2개의 추가 항원-결합 모이어티는 IgG에 C-말단으로 융합된다. 이러한 항원-결합 단백질에서 2개의 Fab 아암 각각은 각각의 Fv를 갖는 CD16A 항원-결합 모이어티를 제공하고 표적 항원-결합 모이어티를 포함하는 제 1 scFv는 제 1 H 사슬의 CH3에 C-말단으로 융합되고, 선택적으로, 추가의 제 1 또는 제 2 표적 항원-결합 모이어티를 포함하는 제 2 scFv는 제 2 H 사슬의 CH3에 융합된다. 예를 들어, 이러한 항원-결합 단백질은 2개의 동일한 H 및 2개의 동일한 L 사슬을 포함하며, 여기서 H 사슬은 N-으로부터 C-말단으로: VH(CD16A)-CH1-힌지-CH2-CH3-VL(표적)-VH(표적)를 포함하고 L 사슬은 N-으로부터 C-말단으로: VL(CD16A)-CL을 포함하고 (도 16) 또는 H 사슬은 N-으로부터 C-말단으로: VH(CD16A)-CH1-힌지-CH2-CH3-VH(표적)-VL(표적)을 포함하고 L 사슬은 N-으로부터 C-말단으로: VL(CD16A)-CL을 포함한다.
추가 구체예에서, 2개의 CD16A 항원-결합 모이어티는 IgG에 C-말단으로 융합되고, IgG의 2개의 Fab 아암은 2개의 제 1 표적 항원-결합 모이어티 (TAA1)를 제공하고 추가 scFv 제 2 표적 항원-결합 모이어티 (TAA2)는 2개의 CL 도메인 각각에 C-말단으로 융합된다 (Bi-scFv-IgAb, 도 14). 이러한 항원-결합 단백질에서 CD16A 항원-결합 모이어티를 포함하는 제 1 scFv는 제 1 H 사슬의 CH3에 C-말단으로 융합되고 CD16A 항원-결합 모이어티를 포함하는 제 2 scFv는 제 2 H 사슬의 CH3에 융합되며, 상기 2개의 Fab 아암은 각 Fv에 제 1 표적 항원-결합 모이어티 (TAA1)를 제공하고 2개의 추가 제 2 표적 항원-결합 모이어티 (TAA2)는 CL 도메인들 각각에 융합된 각각의 scFv 제 2 표적 항원-결합 모이어티에 의해 제공된다. 예를 들어, 이러한 항원-결합 단백질은 2개의 동일한 H 및 2개의 동일한 L 사슬을 포함하며, 여기서 H 사슬은 N-으로부터 C-말단으로: VH(표적1)-CH1-힌지-CH2-CH3-VL(CD16A)-VH(CD16A)를 포함하고 L 사슬은 N-으로부터 C-말단으로: VL(표적1)-CL-VL(표적2)-VH(표적2) 또는 VL(표적1)-CL-VH(표적2)-VL(표적2)을 포함한다(도 14).
본 발명에 따르면, 다중특이적 항원-결합 단백질은 CD16A에 특이적으로 결합하는 CD16A 항원-결합 모이어티 및 CD16A와 상이한 적어도 하나의 표적 항원 (TA)을 포함한다.
일부 구체예에서, CD16A 결합 모이어티는 인간 및 시노몰구스 CD16A에 결합한다.
일부 구체예에서, CD16A 항원-결합 모이어티는 CD16A에 특이적인 중쇄 및 경쇄 가변 도메인을 포함하고, 여기서 (i) CD16A에 특이적인 중쇄 가변 도메인 (VH)은 서열 번호:50에 제시된 아미노산 서열을 가지는 중쇄 CDR1; 서열 번호:51 또는 서열 번호:56에 제시된 아미노산 서열을 가지는 중쇄 CDR2; 서열 번호:52에 제시된 아미노산 서열을 가지는 중쇄 CDR3를 포함하고 CD16A에 특이적인 경쇄 가변 도메인 (VL)은 서열 번호:53에 제시된 아미노산 서열을 가지는 경쇄 CDR1; 서열 번호:54에 제시된 아미노산 서열을 가지는 경쇄 CDR2; 및 서열 번호:55에 제시된 아미노산 서열을 가지는 경쇄 CDR3를 포함하고; 또는
(ii) CD16A에 특이적인 중쇄 가변 도메인 (VH)은 서열 번호:1 또는 서열 번호:3에 제시된 아미노산 서열을 가지고; 및/또는
(iii) CD16A에 특이적인 경쇄 가변 도메인 (VL)은 서열 번호:2에 제시된 아미노산 서열을 가진다.
일부 구체에들에서, CD16A 항원-결합 모이어티는 중쇄 가변 도메인 (VH) 및 경쇄 가변 도메인 (VL)을 포함하고, 여기서 (a) VH는 서열 번호:73에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:74에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:75에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함하고; 그리고 (b) VL은 서열 번호:76에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:77에 제시된 아미노산 서열을 포함하거나 가지는 경쇄 CDR2, 및 서열 번호:78에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함한다.
특정 구체예에서, CD16A 항원-결합 모이어티의 VH는 서열 번호: 3에 제시된 아미노산 서열을 포함하거나 가진다. 특정 구체예에서, CD16A 항원-결합 모이어티의 VL는 서열 번호: 2에 제시된 아미노산 서열을 포함하거나 가진다.
일부 구체에들에서, CD16A 항원-결합 모이어티는 VH 및 VL을 포함하고, 여기서 (a) VH는 서열 번호:82에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:83에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:52에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함하고; 그리고 (b) VL은 서열 번호:84에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:85에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:86에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함한다.
특정 구체예에서, CD16A 항원-결합 모이어티의 VH는 서열 번호: 4에 제시된 아미노산 서열을 포함하거나 가진다. 특정 구체예에서, CD16A 항원-결합 모이어티의 VL는 서열 번호: 5에 제시된 아미노산 서열을 포함하거나 가진다.
일부 구체에들에서, CD16A 항원-결합 모이어티는 VH 및 VL을 포함하고, 여기서 (a) VH는 서열 번호:87에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:88에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:52에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함하고; 그리고 (b) VL은 서열 번호:89에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:95에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:90에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함한다.
특정 구체예에서, CD16A 항원-결합 모이어티의 VH는 서열 번호: 6에 제시된 아미노산 서열을 포함하거나 가진다. 특정 구체예에서, CD16A 항원-결합 모이어티의 VL는 서열 번호: 7에 제시된 아미노산 서열을 포함하거나 가진다.
일부 구체에들에서, CD16A 항원-결합 모이어티는 VH 및 VL을 포함하고, 여기서 (a) VH는 서열 번호:91에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:92에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:52에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함하고; 그리고 (b) VL은 서열 번호:93에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:85에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:94에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함한다.
특정 구체예에서, CD16A 항원-결합 모이어티의 VH는 서열 번호: 8에 제시된 아미노산 서열을 포함하거나 가진다. 특정 구체예에서, CD16A 항원-결합 모이어티의 VL는 서열 번호: 9에 제시된 아미노산 서열을 포함하거나 가진다.
일부 구체에들에서, CD16A 항원-결합 모이어티는 VH 및 VL을 포함하고, 여기서 (a) VH는 서열 번호:82에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:95에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:52에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함하고; 그리고 (b) VL은 서열 번호:96에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:97에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:99에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함한다.
특정 구체예에서, CD16A 항원-결합 모이어티의 VH는 서열 번호: 10에 제시된 아미노산 서열을 포함하거나 가진다. 특정 구체예에서, CD16A 항원-결합 모이어티의 VL는 서열 번호: 11에 제시된 아미노산 서열을 포함하거나 가진다.
일부 구체에들에서, CD16A 항원-결합 모이어티는 VH 및 VL을 포함하고, 여기서 (a) VH는 서열 번호:82에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:99에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:52에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함하고; 그리고 (b) VL은 서열 번호:100에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:101에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:102에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함한다.
특정 구체예에서, CD16A 항원-결합 모이어티의 VH는 서열 번호: 12에 제시된 아미노산 서열을 포함하거나 가진다. 특정 구체예에서, CD16A 항원-결합 모이어티의 VL는 서열 번호: 13에 제시된 아미노산 서열을 포함하거나 가진다.
일부 구체에들에서, CD16A 항원-결합 모이어티는 VH 및 VL을 포함하고, 여기서 (a) VH는 서열 번호:50에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:103에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:52에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함하고; 그리고 (b) VL은 서열 번호:53에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:54에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:104에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함한다.
일부 구체에들에서, CD16A 항원-결합 모이어티는 VH 및 VL을 포함하고, 여기서 (a) VH는 서열 번호:50에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:103에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:52에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함하고; 그리고 (b) VL은 서열 번호:53에 제시된 아미노산 서열을 포함하거나 가지는 CDR1, 서열 번호:54에 제시된 아미노산 서열을 포함하거나 가지는 CDR2, 및 서열 번호:105에 제시된 아미노산 서열을 포함하거나 가지는 CDR3를 포함한다.
CD16A에 대한 이러한 CD16A 항원-결합 모이어티는 CD16B에 결합하지 않으며 유사한 친화성을 가지는 것으로 알려진 CD16A 동종이형 F158 및 V158에 결합한다. IgG의 힌지 영역과의 상호작용에 중요한 위치 158의 아미노산을 변경하는, 2개의 대립유전자 단일 뉴클레오티드 다형성이 인간 CD16A에서 확인되었다. 동형접합 158 F/F 및 이형접합 158 V/F 대립유전자의 대립유전자 빈도는 백인 집단내에서 유사한데 각각 35 내지 52% 또는 38 내지 50% 범위인 반면, 동종접합 158V/V 대립유전자는 10-15%에서만 발견된다 (Lopez-Escamez JA 외; BMC Med Genet 2011;12:2). 따라서 유사한 친화성으로 인해 모든 환자 집단에서 이러한 항-CD16A 도메인에 의한 NK 세포의 결합 및 활성화가 유리하다. 이 CD16A 항원-결합 모이어티는 인간과 시노몰구스 CD16A에 결합한다. 추가로, CD16A에는 결합하지만 CD16B에는 결합하지 않는 중쇄 및 경쇄 가변 사슬 도메인을 포함하는 CD16A 항원-결합 모이어티가 WO 2006/125668에 기재되어 있다.
일부 구체예에서 다중특이적 항원-결합 분자는, 서열 번호: 1 및 2를 가지는 항-CD16A와 비교하여, CD16A에 대한 결합이 개선된 그리고 CD16B에 결합하지 않으며 유사한 친화성을 가지는 것으로 공지된 CD16A 동종이형 F158 및 V158을 인식하는 항-CD16A Fv 도메인을 포함한다. 특정 구체예에서, 친화성이 개선된 항-CD16A Fv 도메인은 서열 번호: 53, 54, 55에 나타낸 서열을 갖는 VCDR을 포함하거나 서열 번호: 2에 나타낸 서열을 갖는 VL 및 서열 번호: 1에 제시된 서열에 적어도 1개의 변이를 갖는 VH로 구성된다.
이러한 개선된 결합제는 친화성 성숙된 CD16A Fv 항원-결합 모이어티 일 수 있다.
따라서, 일부 구체예에서 CD16A 항원-결합 모이어티는, Biacore T200 시스템에서 정제된 scFv 분자로 측정하여 0.16 μg/ml 인간 CD16A (서열 번호: 48)로 코팅된 웰상의 ELISA에서 테스트하였을 때, 서열 번호: 1 및 2의 항-CD16A Fv보다 인간 CD16A에 대한 더 높은 친화성 (예를 들어, 친화성 성숙에 의한 개선) 및/또는 선택성을 나타내는 Fv 도메인을 포함한다. 예를 들어, 인간 CD16A에 대한 이러한 더 높은 친화성은 2, 3, 4, 5, 6, 7, 8, 9, 10, 50, 100, 150 배 이상 일 수 있다. 예를 들어, Biacore T200 시스템에서 측정 된 1가 결합 친화성은 KD= 0.27 nM 내지 1.91 nM 일 수 있으며, 이는 인간 CD16A에 대한 서열 번호: 1 및 2의 결합에 대해 측정한 40.5 nM 보다 21-내지 150-배 더 높은 친화성이다.
바람직하게는, 이러한 친화성 성숙된 Fv 도메인은 Biacore T200 시스템에서 정제 된 scFv 분자로 측정된 0.16 μg/ml 시노몰구스 CD16A (서열 번호: 49)로 코팅된 웰상에서 ELISA에서 테스트하는 경우 시노몰구스 CD16A에 대해 유사하게 개선된 친화성을 추가로 나타낸다. 예를 들어, 시노몰구스 CD16A에 대한 이러한 더 높은 친화성은 2, 3, 4, 5, 6, 7, 8, 9, 10, 50, 100, 150, 200, 250, 300, 400, 500, 541-배 이상 일 수 있다. 예를 들어, Biacore T200 시스템에서 측정된 1가 결합 친화성은 KD= 0.24 nM 내지 3.63 nM 일 수 있으며, 이는 시노몰구스 CD16A에 대한 서열 번호: 1, 2의 결합에 대해 측정한 132 nM 보다 36-내지 541-배 더 높은 친화성이다.
서열 번호: 1,2의 항-CD16 Fv에서 특정 서열 위치 (X37, X44, X46)가 확인되었으며, 여기서 아미노산 치환은 VL 도메인에서 특정 CD16A 결합에 유익하다 (서열 번호 2). 표 1을 참고하라.
표 1: 아미노산 치환의 가장 강력한 효과 요약. 생식선 서열 및 서열 번호: 1-2의 참고 서열에서 인코드된 잔기들을 비교를 위해 제공한다.
표 1에 제시된 모든 아미노산 치환이 CD16A에 대한 결합에 동등하게 중요한 것은 아니다. 위치 X44 및 X46에서의 치환은 더 중요 할 수 있으며, 바람직하게는 친화성 성숙된 클론은 서열 번호: 2의 아미노산을 보존한다.
특정 구체예에서 CD16A 결합의 또 다른 원인은 LCDR3의 서열 및 또한 LCDR1의 N-말단 잔기 NI 또는 LCDR2의 QDX 서열 모티프이다.
특정 구체예에서, CD16A 항원-결합 모이어티의 VL은 서열 번호: 53, 54 및 55에 제시된 서열과 비교하여 1, 2, 3, 4 또는 5 개의 아미노산 치환을 포함하는 경쇄 CDR1, 경쇄 CDR2 및 경쇄 CDR3을 포함하고, VL은 CD16A에 대한 결합 특이성을 유지한다. 특정 구체예에서, 서열 번호: 53의 서열에서의 하나 이상의 치환은 위치 3 내지 6에 존재한다. 특정 구체예에서, 서열 번호: 54의 서열에서의 치환은 위치 3에 존재한다. 특정 구체예에서, 서열 번호: 55의 서열의 위치 6에 있는 잔기 Y 및 위치 8에 있는 V는 치환되지 않는다. 바람직하게는, LCDR3은 서열 번호:55에 제시된 서열을 가진다.
추가 구체예에서 CD16A 항원-결합 모이어티의 VL은 서열 번호: 2의 서열과 비교하여 적어도 99%, 98%, 97%, 96%, 95%, 94%, 93%, 92%, 91%, 90%, 89%, 88%, 87%, 86%, 85%, 84%, 83%, 82%, 81% 또는 80%의 서열 동일성을 가지며, 여기서 서열 번호:2의 위치 23 내지 27의 잔기 GGHNI, 서열 번호:2의 위치 49 내지 52의 서열 모티프 QDXK는 돌연변이되지 않으며 VL은 CD16A에 대한 결합 특이성을 유지한다.
CD16A 항원-결합 모이어티의 VH에서 서열 번호: 1의 서열과 비교하여 HCDR1의 위치 9 및/또는 HCDR2의 위치 11에서의 치환은 CD16A에 대한 결합을 개선하는데 유리하다. 특히 HCDR1의 위치 9에 있는 잔기는 Q이고 및/또는 HCDR2의 위치 11에 있는 잔기는 V이다.
따라서, 추가 구체예에서 CD16A 항원-결합 모이어티의 VH는 서열 번호 1의 서열과 비교하여 적어도 99%, 98%, 97%, 96%, 95%, 94%, 93%, 92%, 91%, 90%, 89%, 88%, 87%, 86%, 85%, 84%, 83%, 82%, 81% 또는 80% 서열 동일성을 가지며, HCDR1에서 위치 9의 잔기는 Q이고 및/또는 HCDR2에서 위치 11의 잔기는 V이다.
따라서, 특정 구체예에서 CD16A 항원-결합 모이어티는 VL 및 VH를 포함하고, 여기서 CD16A의 VL은 서열 번호: 2의 서열과 비교하여 적어도 99%, 98%, 97%, 96%, 95%, 94%, 93%, 92%, 91%, 90%, 89%, 88%, 87%, 86%, 85%, 84%, 83%, 82%, 81% 또는 80%의 서열 동일성을 가지며, 여기서 서열 번호: 2의 위치 23 내지 27의 잔기 GGHNI, 서열 번호: 2의 위치 49 내지 52의 서열 모티프 QDXK는 돌연변이되지 않고 VL 은 CD16A에 대한 결합 특이성을 유지하고 CD16A 항원-결합 모이어티의 VH는 서열 번호: 1의 서열과 비교하여 적어도 99%, 98%, 97%, 96%, 95%, 94%, 93%, 92%, 91%, 90%, 89%, 88%, 87%, 86%, 85%, 84%, 83%, 82%, 81% 또는 80%의 서열 동일성을 가지며, HCDR1에서 위치 9의 잔기는 Q이고 및/또는 HCDR2에서 위치 11의 잔기는 V이다.
추가 구체예에서 CD16A 항원-결합 모이어티의 VL은 서열 번호: 2의 서열과 비교하여 적어도 약 99%, 약 98%, 약 97%, 약 96%, 약 95%, 약 94%, 약 93%, 약 92%, 약 91%, 약 90%, 약 89%, 약 88%, 약 87%, 약 86%, 약 85%, 약 84%, 약 83%, 약 82%, 약 81% 또는 약 80%의 서열 동일성을 가지며, 여기서 서열 번호:2의 위치 23 내지 27의 잔기 GGHNI, 서열 번호:2의 위치 49 내지 52의 서열 모티프 QDXK는 돌연변이되지 않으며 VL은 CD16A에 대한 결합 특이성을 유지한다.
CD16A 항원-결합 모이어티의 VH에서 서열 번호: 1의 서열과 비교하여 HCDR1의 위치 9 및/또는 HCDR2의 위치 11에서의 치환은 CD16A에 대한 결합을 개선하는데 유리하다. 특히 HCDR1의 위치 9에 있는 잔기는 Q이고 및/또는 HCDR2의 위치 11에 있는 잔기는 V이다.
그러므로, 추가 구체예에서 CD16A 항원-결합 모이어티의 VH는 서열 번호: 1의 서열과 비교하여 적어도 약 99%, 약 98%, 약 97%, 약 96%, 약 95%, 약 94%, 약 93%, 약 92%, 약 91%, 약 90%, 약 89%, 약 88%, 약 87%, 약 86%, 약 85%, 약 84%, 약 83%, 약 82%, 약 81% 또는 약 80%의 서열 동일성을 가지며, HCDR1에서 위치 9의 잔기는 Q이고 및/또는 HCDR2에서 위치 11의 잔기는 V이다.
따라서, 특정 구체예에서 CD16A 항원-결합 모이어티는 VL 및 VH를 포함하고, 여기서 CD16A 항원-결합 모이어티의 VL은 서열 번호: 2의 서열과 비교하여 적어도 약 99%, 약 98%, 약 97%, 약 96%, 약 95%, 약 94%, 약 93%, 약 92%, 약 91%, 약 90%, 약 89%, 약 88%, 약 87%, 약 86%, 약 85%, 약 84%, 약 83%, 약 82%, 약 81% 또는 약 80%의 서열 동일성을 가지며, 여기서 서열 번호: 2의 위치 23 내지 27의 잔기 GGHNI, 서열 번호: 2의 위치 49 내지 52의 서열 모티프 QDXK는 돌연변이되지 않고 VL 은 CD16A에 대한 결합 특이성을 유지하고 CD16A 항원-결합 모이어티의 VH는 서열 번호: 1의 서열과 비교하여 적어도 약 99%, 약 98%,약 97%, 약 96%, 약 95%, 약 94%, 약 93%, 약 92%, 약 91%, 약 90%, 약 89%, 약 88%, 약 87%, 약 86%, 약 85%, 약 84%, 약 83%, 약 82%, 약 81% 또는 약 80%의 서열 동일성을 가지며, HCDR1에서 위치 9의 잔기는 Q이고 및/또는 HCDR2에서 위치 11의 잔기는 V이다.
특정 구체예에서, CD16A 항원-결합 모이어티의 VH는 서열 번호: 3에 제시된 서열과 비교하여 적어도 약 99%, 약 98%, 약 97%, 약 96%, 약 95%, 약 94%, 약 93%, 약 92%, 약 91%, 약 90%, 약 89%, 약 88%, 약 87%, 약 86%, 약 85%, 약 84%, 약 83%, 약 82%, 약 81% 또는 약 80%의 서열 동일성을 가진다.
특정 구체예에서, CD16A 항원-결합 모이어티는 서열 번호: 2에 제시된 아미노산 서열과 적어도 약 99%, 약 98%, 약 97%, 약 96%, 약 95%, 약 94%, 약 93%, 약 92%, 약 91%, 약 90%, 약 89%, 약 88%, 약 87%, 약 86%, 약 85%, 약 84%, 약 83%, 약 82%, 약 81% 또는 약 80% 동일하거나 상동성인 아미노산 서열을 포함하는 VH 및 서열 번호: 2에 제시된 아미노산 서열과 적어도 약 99%, 약 98%, 약 97%, 약 96%, 약 95%, 약 94%, 약 93%, 약 92%, 약 91%, 약 90%, 약 89%, 약 88%, 약 87%, 약 86%, 약 85%, 약 84%, 약 83%, 약 82%, 약 81% 또는 약 80% 인 동일하거나 상동성인 아미노산 서열을 포함하는 VL을 포함한다.
특정 구체예에서, CD16A 항원-결합 모이어티는 VL 및 VH를 포함하고, 여기서 VL은 서열 번호: 2, 5, 7, 9, 11 및 13을 갖는 영역들로 구성된 그룹에서 선택되고, VH는 서열 번호: 1, 3, 4, 6, 8, 10 및 12로 구성된 그룹에서 선택된다.
III.
표적 항원-결합 모이어티
특정 구체예에서, 표적 항원-결합 모이어티의 표적 항원은 골수종 세포 또는 형질 세포에 제시된 항원이다. 골수종 세포는 골수의 형질 세포에서 발생하는 악성 (암성) 형질 세포이다. 골수종에서 악성 형질 세포는 감염과 싸우는 능력이 부족한 다량의 비정상 항체를 생성한다. 이러한 비정상 항체는 골수종에 대한 종양 마커 역할을 하는 단일클론 단백질, 또는 M-단백질이다. 골수종 세포는 표현형 CD19-/CD38+/CD138+/BCMA+를 가진다. 따라서 CD38, CD138 및 BCMA는 골수종 세포에서 발현되는 항원을 나타낸다.
A.
BCMA
B 세포 성숙 항원 (BCMA, CD269 또는 TNFRSF17)은 B 세포 활성화 (BAFF)와 A 증식 유도 리간드 (APRIL)의 결합을 통해 형질 세포의 장기 생존에 중요한 TNF 수용체 수퍼패밀리의 단백질이다 (O'Connor, B.P. 외 BCMA is essential for the survival of long-lived bone marrow 형질 세포. J. Exp. Med. 2004, 199, 91-96). 인간 BCMA는 54 aa 세포외 도메인, 23 aa 막경유 도메인 및 107 aa 세포내 도메인으로 구성된 184개 아미노산 (aa) 단백질이다 (Entrez 유전자 ID: 608 (인간) 102145399 (시노몰구스 원숭이); UniProt Q02223 (인간)).
BCMA는 형질 세포의 장기 세포 생존에 중요한 역할을 한다 (O'Connor, JEM 2004;199(1):91-98). BCMA는 정상 형질 세포에서 발현되며 다발성 골수종에서 상향 조절되고 높은 유병률을 보인다.
특정 구체예에서 표적 항원-결합 모이어티는 BCMA에, 예를 들어, BCMA의 세포외 도메인에 특이적으로 결합한다.
바람직하게는, 본 발명의 항원-결합 단백질에 사용되는 이러한 항-BCMA Fv는 10-7 M 미만, 바람직하게는 10-8 M 미만, 10-9 M 미만, 가장 바람직하게는 10-10 M 미만의 평형 해리 상수 (KD) (Biacore로 측정)로 BCMA와 상호작용한다. 표적 항원-결합 모이어티에 통합된 이러한 항-BCMA Fv 도메인은 BCMA+ MM (다발성 골수종) 세포의 존재하에 CD16A 결합된 NK 세포를 재지시하고 ADCC를 유도 할 수 있다. 시험관내 및 생체내에서 BCMA+ 골수종 세포에 대해 CD3를 통해 T 세포와 결합하는 이중특이적 항체에 대한 개념 증명이 보고된 바 있다 (예컨대, Hipp S. 외, Leukemia. 2017 Aug;31(8):1743-1751. Epub 2016 Dec 27). 특정 구체예에서, 표적 항원-결합 모이어티는 약 1 x 10-9 M 내지 약 5 x 10-9 M의 KD로 BCMA에 결합한다. 특정 구체예에서, 표적 항원-결합 모이어티는 약 2 x 10-9 M의 KD로 BCMA에 결합한다.
이러한 BCMA 항원-결합 모이어티는, 예를 들어, 파지 또는 리보솜 라이브러리 스크리닝 방법 또는, 예를 들면, Ryan M.C, 외, Antibody targeting of B-cell maturation antigen on malignant plasma cells. Mol Cancer Ther. (2007);6:3009-3018에 기재된 BCMA의 세포외 도메인을 이용한 비-인간 동물의 면역화에 의해 수득가능하다.
Ryan 외는 IgG 또는 항체 약물 접합체와 같은 세포독성 활성을 갖는 항-BCMA 항체의 생산을 설명한다. 참고로 포함된 Ryan M.C, 외는, 종양 세포 표적화를 위한 인간 BCMA-선택적 항체의 생성을 설명한다. 항체는 인간 BCMA 세포외 도메인 (ECD, 아미노산 5-51; NP_001183)에 대해 생성되었다. 항체는 CD16A 결합을 향상시키는 Fc 돌연변이로 증가된 시험관내 MM 세포에 대해 강력한 ADCC를 유도하였다. H929 세포에 대한 SG1의 결합 친화성 KD는 포화 결합에 의해 51 nmol/L이었다. 이들 항체는 MM 세포주에 대한 시험관내 항종양 활성을 나타내었으며, 따라서 이들의 Fv-도메인은 본 발명에 따른 항원-결합 단백질에서 BCMA 항원-결합 모이어티로서 사용될 수 있다.
또한, WO 02/066516은 TACI와 교차 반응하는 BCMA 항체를 설명한다. 항-BCMA/TACI 이중특이적 항체는 BCMA의 잔기 1-48 및 TACI의 잔기 30-67 및 68-154에 결합하는 것으로 설명된다. 이의 가변 중쇄 및 경쇄 도메인은 본 발명의 항원-결합 단백질에서 BCMA 항원-결합 모이어티로서 사용될 수 있으며, 이들은 참고로 포함된다.
참고로 포함된, Ramadoss 외, J. Am.Chem.Soc. 2015;137:5288-5291은, 악성 MM 세포들를 용해하도록 T 세포들을 재지시하는 이중특이적 (BiFab-BCMA) 항체를 기재한다. 이중특이적 항체는 MM의 치료에 유용 할 수 있는데, 왜냐하면 종양 관련 항원의 수가 적을 뿐만 아니라 정지 상태의 암 줄기 세포를 표적으로 하기 때문이다.
WO 2014/122144는 이중특이적 형태로 인간 BCMA 및 CD3에 특이적으로 결합하는 이중특이적 항체를 설명한다. 개시된 항-BCMA 가변 도메인은 본 발명에 따른 BCMA 항원-결합 모이어티에 적합하다.
WO 2013/072406은 T 세포와 결합하기 위해 CD3에 대한 제 2 특이성을 갖는 이중특이적 단쇄 항체에서 BCMA-1 내지 BCMA-108로 지정된 항-BCMA Fv 도메인을 개시한다. 인간 종양 이종이식 모델에서 이들 BCMA/CD3 이중특이적 단쇄 항체의 항-종양 효능이 기재되어 있으므로, 이들 항-BCMA Fv 도메인은 본 발명의 BCMA 항원-결합 모이어티에 사용될 수 있다.
T-또는 NK 세포와 같은 면역 이펙터 세포와 결합하는 이중특이적 항체에 사용될 수 있는 추가 항-BCMA 항체는 WO 2010/104949, WO 2012/163805, WO 2013/072415, WO 2014/140248 및 WO 2014/068079에 개시되어 있다.또한 이들 참고문헌은 강력하고 효과적인 골수종 세포 용해를 유도하는 이러한 항-BCMA Fv-도메인을 사용하는 고 친화성 및 이중특이적 항체로 BCMA를 특이적으로 표적화하는 항-BCMA Fv-도메인을 설명한다. 그러므로, MM 세포들을 용해시키도록 T 세포들을 재지시하기 위한 이중특이적 항체들에서 항-BCMA Fv-도메인들에 대한 개념 증명을 제시하였다.
골수종 세포, 특히 BCMA에서 발현되는 항원에 결합하는 추가 항원-결합 모이어티는 다른 공지된 또는 상업적으로 입수가능한 항체로부터 유도되거나 당업계에 공지된 방법에 의해 새로이 생성 될 수 있다. 예를 들어, BCMA에 특이적인 가변 도메인은 BCMA에 특이적인 가변 단편 (Fvs)을 선택하여 얻을 수 있다. 이는, 예를 들어, 단쇄 Fv (scFv) 파지 디스플레이 라이브러리를 스크리닝하거나 하이브리도마 기술을 통해 이루어질 수 있다. 예를 들어, 인간 scFv 서열의 IgM-기반 파지 디스플레이 라이브러리는 BCMA에 특이적인 결합제를 농축하게 하기 위해 여러 주기의 시험관내 선택을 거칠 수 있다 (실시예 1). 선택된 scFv의 친화성은 친화성 성숙에 의해 더 증가 될 수 있다.
특정 구체예들에서, 상기 BCMA-표적화 모이어티는 서열 번호:67에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:68에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:69에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:70에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:71에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:72에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함한다.
특정 구체예에서, BCMA-표적화 모이어티의 VH는 서열 번호: 65에 제시된 아미노산 서열과 적어도 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 약 100% 상동성이거나 동일한 아미노산 서열을 포함한다.
특정 구체예에서, BCMA-표적화 모이어티의 VL은 서열 번호: 66에 제시된 아미노산 서열과 적어도 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 약 100% 상동성이거나 동일한 아미노산 서열을 포함한다.
특정 구체예에서, BCMA-표적화 모이어티의 VH는 서열 번호: 65에 제시된 아미노산 서열을 포함하거나 가진다. 특정 구체예에서, BCMA-표적화 모이어티의 VL은 서열 번호: 66에 제시된 아미노산 서열을 포함하거나 가진다.
특정 구체예에서, BCMA-표적화 모이어티의 VH는 서열 번호: 37에 제시된 아미노산 서열과 적어도 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 약 100% 상동성이거나 동일한 아미노산 서열을 포함한다.
특정 구체예에서, BCMA-표적화 모이어티의 VL은 서열 번호: 38에 제시된 아미노산 서열과 적어도 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 약 100% 상동성이거나 동일한 아미노산 서열을 포함한다.
특정 구체예에서, BCMA-표적화 모이어티의 VH는 서열 번호: 65에 제시된 아미노산 서열을 포함하거나 가진다. 특정 구체예에서, BCMA-표적화 모이어티의 VL은 서열 번호: 66에 제시된 아미노산 서열을 포함하거나 가진다.
특정 구체예에서, CD16A/BCMA 결합 항체는 도 13에 도시된 구조를 갖는 scFv-IgAb 항원-결합 단백질이며, 이는 (a) 동종이량체 인간 IgG CH2-CH3 Fc 부분의 C-말단에 VL-VH 순서로 융합된 scFv 형태의 2개의 CD16A 항원-결합 모이어티, 및 (b) IgG의 Fab 아암에서 각 Fv에 의해 제공되는 2개의 표적 항원-결합 모이어티를 포함하고, 여기서 표적 항원-결합 모이어티는 BCMA에 결합한다.
특정 구체예들에서, 각각의 상기 CD16A 항원-결합 모이어티는 서열 번호:73에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:74에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:75에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:76에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:77에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:78에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함한다. 특정 구체예에서, CDR은 Kabat 넘버링 체계에 따라 식별된다. 각각의 CD16A 항원-결합 모이어티는 서열 번호: 3에 제시된 아미노산 서열을 갖는 VH 및 서열 번호: 2에 제시된 아미노산 서열을 갖는 VL을 포함한다.
특정 구체예에서, CD16A 항원-결합 모이어티는 서열 번호 22에 제시된 아미노산 서열을 갖는 연결기를 통해 Fc 부분의 C-말단에 다음 순서로 융합된다: VL (CD16A)-링커 L3-VL (CD16A), 여기서 링커 L3는 서열 번호: 18에 제시된 아미노산 서열을 가진다.
특정 구체예들에서, 각각의 상기 BCMA-표적화 모이어티는 서열 번호:67에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:68에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:69에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:70에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:71에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:72에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함한다. 특정 구체예에서, CDR은 Kabat 넘버링 체계에 따라 식별된다. 각각의 BCMA-표적화 모이어티는 서열 번호: 65에 제시된 아미노산 서열을 갖는 VH 및 서열 번호: 66에 제시된 아미노산 서열을 갖는 VL을 포함한다.
특정 구체예에서, CD16A/BCMA 항체의 Fc 부분은 인간 IgG1 CH2 및 CH3 중쇄 불변 도메인을 포함하는 침묵된 Fc 부분이며, 이는 서열 번호: 29에 제시된 아미노산 서열을 포함한다. CH2 중쇄 불변 도메인은 2개의 침묵 돌연변이 ("무-이펙터 돌연변이"라고도 함): L234F 및 L235E를 가진다. CH2 중쇄 불변 도메인은 서열 번호: 79에 제시된 아미노산 서열을 포함한다. CH3 중쇄 불변 도메인은 서열 번호: 109에 제시된 아미노산 서열을 포함한다. BCMA 표적화 모이어티에 연결되는 CH1 중쇄 불변 도메인은 서열 번호: 33에 제시된 아미노산 서열을 포함한다.
특정 구체예들에서, CD16A/BCMA 항체 I은 서열 번호: 61에 제시된 아미노산 서열을 가지는 폴리펩티드 사슬 1, 및 서열 번호: 62에 제시된 아미노산 서열을 가지는 폴리펩티드 사슬 2를 포함한다.
특정 구체예들에서, CD16A/BCMA 항체는 도 5에 도시된 구조를 가지는 KiH-scDb-Fc이며, 이는 (a) IgG CH2-CH3 Fc 부분의 C-말단에 VL-VH-VL-VH의 순서로 융합된 scDb 형태의 2개의 CD16A 항원-결합 모이어티, 및 (b) Fc 부분의 N-말단에 융합된 scFv 형태의 단일 표적 항원-결합 모이어티를 포함하고, 여기서 상기 표적 항원-결합 모이어티는 BCMA에 결합한다.
특정 구체예들에서, 각각의 상기 CD16A 항원-결합 모이어티는 서열 번호:73에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:74에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:75에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:76에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:77에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:78에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함한다. 특정 구체예에서, CDR은 Kabat 넘버링 체계에 따라 식별된다. 각각의 CD16A 항원-결합 모이어티는 서열 번호: 3에 제시된 아미노산 서열을 갖는 VH 및 서열 번호: 2에 제시된 아미노산 서열을 갖는 VL을 포함한다.
특정 구체예에서, CD16A 항원-결합 모이어티는 이종이량체 Fc 부분에 융합되고 서열 번호: 20에 제시된 아미노산 서열을 갖는 연결기를 통해 다음 순서로 연결되며: VL (CD16A)-링커 L1-VH (CD16A)-링커 L2-VL (CD16A)-링커 L1-VH (CD16A), 여기서 링커 L1은 서열 번호: 16에 제시된 아미노산 서열을 가지고, 링커 L2는 서열 번호: 17에 제시된 아미노산 서열을 가진다.
특정 구체예들에서, 각각의 상기 BCMA-표적화 모이어티는 서열 번호:67에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:68에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:69에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:70에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:71에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:72에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함한다. 특정 구체예에서, CDR은 Kabat 넘버링 체계에 따라 식별된다. 각각의 BCMA-표적화 모이어티는 서열 번호: 65에 제시된 아미노산 서열을 갖는 VH 및 서열 번호: 66에 제시된 아미노산 서열을 갖는 VL을 포함한다.
특정 구체예에서, CD16A/BCMA 항체 III의 Fc 부분은 서열 번호: 31에 제시된 아미노산 서열을 가지는 인간 IgG1 CH2 및 CH3 중쇄 불변 도메인을 포함하는 침묵된 Fc 부분이다. CH2 중쇄 불변 도메인은 2개의 침묵 돌연변이 또는 무-이펙터 돌연변이: L234F 및 L235E를 가진다. CH2 중쇄 불변 도메인은 서열 번호: 79에 제시된 아미노산 서열을 포함한다. CH3 중쇄 불변 도메인은 1개의 침묵 돌연변이 또는 무-이펙터 돌연변이 D265A를 가진다. CH3 중쇄 불변 도메인은 서열 번호: 81에 제시된 아미노산 서열을 포함한다.
특정 구체예들에서, CD16A/BCMA 항체 I은 서열 번호: 63에 제시된 아미노산 서열을 가지는 폴리펩티드 사슬 1, 및 서열 번호: 64에 제시된 아미노산 서열을 가지는 폴리펩티드 사슬 2를 포함한다.
본 발명의 다중특이적 항원-결합 단백질의 한 구체예에서 상기 단백질은 서열 번호: 61 및 62 또는 서열 번호: 63 및 64에 나타낸 아미노산 서열을 갖는 폴리펩티드를 포함하는 사량체이다.
B.
EGFR
또한 자연 살해 (NK) 세포 기반 EGFR 표적화 접근을 위한 EGFR/CD16A 항원-결합 단백질도 제공된다.
일부 구체예에서 본원에 기재된 EGFR에 대한 항원-결합 모이어티는 또한 EGFRvIII에 결합한다. 따라서, EGFR/CD16A 항원-결합 단백질은 EGFR 발현 및 EGFRvIII 발현 암 모두의 치료에 사용될 수 있다. EGFR과 달리 EGFRvIII는 암세포에서만 발현되지만 건강한 조직에서는 발현되지 않는다. 따라서, 보다 광범위한 EGFR-및/또는 EGFRvIII-양성 종양, 그리고 이에 따라 보다 광범위한 환자 집단이 본원에 기재된 EGFR/CD16A 항원-결합 단백질로 표적화 될 수 있다. 본원에 기재된 항원-결합 단백질에 적합한 EGFR 결합 도메인의 예는 서열 번호: 40에 제시된 아미노산 서열을 VH로서 포함하고 서열 번호: 41에 제시된 아미노산 서열을 VL로서 포함한다.
IV.
폴리뉴클레오티드
본원에 기재된 구체예 중 어느 하나에 따른 항원-결합 단백질은 항원-결합 분자를 형성하는 개별 폴리펩티드 사슬을 인코딩하는 폴리뉴클레오티드를 발현함으로써 생성 될 수 있다. 따라서, 본 발명의 추가 구체예는 상기 본원에 기재된 항체 분자의 폴리펩티드를 인코딩하는 폴리뉴클레오티드, 예를 들어, DNA 또는 RNA이다.
폴리뉴클레오티드는, 당업자에게 알려진 방법에 의해, 예를 들어, 펩티드 링커에 의해 분리되거나 폴리펩티드 사슬의 펩티드 결합에 의해 직접 연결된 가변 도메인들을 인코딩하는 유전자를, 적합한 프로모터 그리고 선택적으로 적합한 전사 종결인자에 작동가능하게 연결된 유전자 구조체에 조합하고, 및 박테리아 또는 다른 적절한 발현 시스템, 예를 들어 CHO 세포에서 이를 발현시킴으로써 제작될 수 있다. 사용되는 벡터 시스템 및 숙주에 따라, 항시성 및 유도성 프로모터를 비롯하여 임의의 수의 적합한 전사 및 번역 요소들이 사용될 수 있다. 프로모터는 각각의 숙주 세포에서 폴리뉴클레오티드의 발현을 유도하도록 선택된다.
폴리뉴클레오티드는 벡터, 바람직하게는 발현 벡터에 삽입 될 수 있으며, 이는 본 발명의 추가 구체예를 나타낸다.
본 발명의 폴리펩티드 사슬을 인코딩하는 폴리뉴클레오티드를 함유하고 발현하기 위해 다양한 발현 벡터/숙주 시스템이 이용 될 수 있다. 대장균에서의 발현을 위한 발현 벡터의 예는 포유 동물 세포에서의 발현을 위한 pSKK (LeGall 외, J Immunol Methods. (2004);285(1):111-27) 또는 pcDNA5 (Invitrogen)이다.
V.
치료 방법
본 발명은 추가로 다중특이적 항원-결합 단백질, 특히, 상기 본원에 기재된 다중특이적 항원-결합 단백질 및 적어도 하나의 추가 성분을 포함하는 조성물을 제공한다.
본 발명은 추가로 다중특이적 항원-결합 단백질, 또는, 상기 본원에 기재된 다중특이적 항원-결합 단백질을 포함하는, NK 세포 기반 면역요법에 사용하기 위한 조성물을 제공한다. NK 세포 기반 면역요법은 내인성 또는 입양 전달된 NK 세포가 본 발명의 항원-결합 분자에 의한 결합을 통해 활성화되는 활성 NK 세포 기반 요법을 포함한다. 특히 암세포와 같은 비정상 세포를 공격하고 사멸시키는 NK 세포의 능력이 강화된다.
또한 현재의 면-종양학 (IO) 환경에는 항-CTLA4 및 항-PD-1 항체와 같은 시판 체크포인트 조절제가 포함된다. 이러한 물질들은 임상적 효능 (일반적으로 다양한 적응증에 걸쳐 20-30% ORR)을 입증하였지만, 의학적 필요성과 기회는 여전히 남아 있다. 따라서 최근의 치료 발전에도 불구하고 더 많은 수의 환자에서 증가된 환자 반응률과 장기적인 관해를 달성하기 위해서는 새로운 치료법이 필요하다. 예를 들어, NK 세포는 MM에 대한 면역 반응에서 핵심적인 역할을 하며, IMiD, 프로테아좀 억제제, 최근 승인된 면역 요법 및 자가 줄기 세포 이식 (ASCT)을 비롯한 현재 표준이 되는 치료적 개입들의 임상 효능과 관련되어 있다. MM에서 빈번하게 조절에 장애가 있는 골수종 세포에 대한 자연 NK 세포 세포독성을 향상시키기 위해 수많은 전략이 개발되고 있다. 접근법에는 사이토카인 자극 또는 면역 체크포인트 표적화를 통한 활성 조절, ASCT-적격 MM에서 배양 확장된 NK 세포의 입양 전달이 포함된다. 이러한 접근법은 매우 매력적이지만, NK 세포의 자연 세포독성에 의존하기 때문에 표적화되지 않으며, 항원 특이 적 재표적화 및 이펙터 활성화로부터 이점을 얻을 수 있다.
또한 IO의 합리적인 조합은 안전성을 제어하면서 최대한의 면역 효능을 발휘할 수 있는 물질에 기반해야 한다. 유망한 접근법은 적응 면역 (대부분의 체크포인트 항체는 T 세포에서만 활성임)을 넘어 선천 면역의 활성화를 포함하므로, 통합 면역 반응을 생성한다. 연장된 혈청 반감기를 기준으로, 본원에 기재된 항체 형태는 이러한 목적에 이상적으로 적합하며 현재 시판되는 단일클론 항체와 유사하게 편리하게 투여될 수 있고 항-LAG3 또는 항-PD1 항체와 같은 체크포인트 조절제와 이상적으로 조합 될 수 있다.
특정 구체예에서, 본 발명은 다중 특이적 항원-결합 단백질을 투여하는 것을 포함하는 다발성 골수종의 치료에 사용하기 위해, 상기 기재된 바와 같은, CD16A에 특이적으로 결합하는 다중특이적 항원-결합 단백질 및 BCMA, CS-1, CD19, CD20, CD22, CD38 및 CD138로 구성된 그룹에서 선택된 골수종 세포 또는 형질 세포에서 발현되는 항원을 제공한다. 특정 구체예에서, 본 발명은 표적 세포 항원, 예를 들어, 종양 항원, 및 CD16A에 특이적으로 결합하는, NK 세포 면역요법에서 사용하기 위한 다중특이적 항원-결합 분자를 제공하며, 여기서 다중특이적 항원-결합 단백질은 NK 세포와 세포외에서 혼합되고 NK 세포 및 다중특이적 항원-결합 분자의 조성물이 환자에게 투여된다.
특정 구체예에서, 종양 항원은 BCMA이고 조성물은 형질 세포 장애 또는자가 면역 질환, 특히 다발성 골수종의 치료에 사용된다.
형질 세포 장애에는 다발성 골수종, 형질 세포종, 형질 세포 백혈병, 거대글로불린혈증, 아밀로이드증, 발덴스트롬 거대글로불린혈증, 고독한 골 형질세포종, 골수외 형질세포종, 골경화성 골수종, 중쇄 질환, 의미불명 단일클론 감마병증 (MGUS) 및 무증상 골수종이 포함된다.
자가 면역 질환은, 예를 들어, 전신성 홍반성 루푸스 (SLE) 또는 류마티스성 관절염 (RA)이다.
따라서, 본 발명은, 특정 구체예들에서, 상기 기재된 바와 같은 BCMA 및 CD16A에 특이적인 항원-결합 단백질, 예를 들어, scDb-mFc, KiH-scDb-Fc, scDb-Trib(-scFv), scFv-IgAb, Bi-scFv-IgAb, KiH-scFv-Fc, Db-Fc, 또는 Bi-scFv-Fc가 BCMA+ 암 또는 자가면역 질환, 예를 들면, 다발성 골수종의 치료를 위해 대상체에게 유효량으로 투여되는 의학적 용도 및 방법을 제공한다.
투여는 상이한 방식, 예를 들어, 정맥내, 복강내, 피하, 근육내, 외용 또는 피내 투여에 의해 이루어진다. 투여량은 주치의 및 기타 임상 요인에 의해 결정될 것이다. 임의의 한 대상체에 대한 투여량들은 환자의 체중, 체 표면적, 연령, 성별, 투여 할 특정 화합물, 투여 시간 및 경로, 요법의 종류, 일반적인 건강 및 동시에 투여되는 다른 약물들을 비롯한 여러 요인들에 따라 달라진다. "유효량"은 질환의 진행 및 중증도에 영향을 주어 해당 병리의 감소 또는 완화를 가져오기에 충분한 활성 성분의 양을 지칭한다. BCMA+ 질환의 치료 및/또는 예방에 유용한 "유효량"은 공지된 방법을 사용하여 결정될 수 있다.
더욱이, 본 발명은 질환의 치료 또는 개선 방법을 제공하며, 이 방법은 본 발명의 다중특이적 항원-결합 단백질을 필요로 하는 대상체에게 투여하는 단계를 포함한다.
질환의 치료 또는 개선 방법의 바람직한 구체예에서, 상기 질환은 다발성 골수종이다.
본 발명은 암, 예를 들어, 다발성 골수종을 치료 및/또는 예방하는, 본원에 개시된 항원-결합 분자, 예를 들어, CD16A/BCMA 항원-결합 분자의 용도를 제공한다. 특정 구체예에서, 상기 방법은 본원에 개시된 항원-결합 분자, 예를 들어, CD16A/BCMA 항원-결합 분자, 또는 이를 포함하는 제약 조성물을 다발성 골수종 ("MM")을 앓고 있는 대상체에게 투여하는 단계를 포함한다.
특정 구체예에서, 항원-결합 분자, 예를 들어, CD16A/BCMA 항원-결합 분자, 또는 이를 포함하는 제약학적 조성물로 치료를 받는 대상체는 재발성/불응성 ("R/R") 다발성 골수종 환자이다. 특정 구체예에서, 대상체는 다라투무맙을 제공받았다. 특정 구체예에서, 대상체는 다라투무맙 나이브이다. 특정 구체예에서, 대상체는 다라투무맙 내성이다. 특정 구체예에서, 대상체는 다라투무맙 불응성이다. 특정 구체예에서, 대상체는 다라투무맙 재발성이다.
특정 구체예에서, 항원-결합 분자, 예를 들어, CD16A/BCMA 항원-결합 분자, 또는 이를 포함하는 제약학적 조성물로 치료를 받는 대상체는 CD16A 다형성을 발현한다. 예를 들어, 제한없이, CD16A 다형성은 CD16A-158V/F 다형성이다. 실시예 8 (예컨대, 도 31A 및 31B)를 참고하라.
특정 구체예에서, 본원에 기재된 치료 방법은 제 2 요법, 예를 들어, T-세포-기반 요법 또는 체크-포인트 억제제-기반 요법을 투여하는 단계를 추가로 포함한다. 이러한 제 2 요법에는, 항-TIGIT 항체의 투여를 포함하는 요법, 항-PD-1 항체 (예컨대, 니볼루맙, 펨브롤리주맙)의 투여를 포함하는 요법, 항-PD-L1 항체 (예컨대, 아테졸리주맙)의 투여를 포함하는 요법, 항-VEGF 항체 (예컨대, 베바시주맙)의 투여를 포함하는 요법, 및 CD3 이중특이적 항체 (예컨대, 항-FcRH5/CD3 항체 (PCT/US2016/037879에 개시된 항체들을 포함하나 이에 제한되지 않음, 이 문헌은 그 전문이 참고로 포함됨))의 투여를 포함하는 요법이 포함되지만 이에 제한되지 않는다.
특정 구체예에서, 본원에 기재된 치료 방법은 사이토카인 요법의 투여를 추가로 포함한다. 본원에서 사용되는 "사이토카인 요법"은 페길화된 사이토카인 및 Fc 융합 사이토카인을 비롯한 (그러나 이에 제한되지 않음) 임의의 사이토카인 유도체 또는 이의 변형을 지칭한다. 이러한 구체예와 관련하여 사용될 수 있는 사이토카인의 비 제한적인 예는 IL-15, IL-2, IL-12, IL-21, IL-17, IL-18, IL-23, IL-27 및 IL-6을 포함한다. 특정 구체예에서, 상기 방법은 IL-15를 투여하는 단계를 추가로 포함한다. 특정 구체예에서, 상기 방법은 IL-2를 투여하는 단계를 추가로 포함한다. 실시예 8에서 보는 바와 같이, IL-15 및 IL-2는 본원에 개시된 CD16A/BCMA 항원-결합 분자의 활성을 증가시킬 수 있다.
특정 구체예에서, 본원에 개시된 항원-결합 분자, 예를 들어, CD16A/BCMA 항원-결합 분자, 또는 이를 포함하는 제약학적 조성물의 투여는 1차 (1L) 치료가 될 것이다. 예를 들어, 제한없이, 이러한 1차 투여는, Fc-기반 MOA, 예를 들어, 다라투무맙 요법을 통한 치료 기능의 효과 감소를 나타내는 CD16A 다형성을 나타내는 대상체에서 발생할 것이다. 특정 구체예에서, 본 발명의 항원-결합 분자의 1차 투여는 NK 세포 동족살해가 금지되어 있는 대상체에서 발생할 것이다. 실시예 8 (예컨대, 도 40A-40E)을 참고하라. 특정 구체예에서, 본 발명의 항원-결합 분자의 1차 투여는 CRS를 피할 필요가 있는 대상체에서 발생할 것이다.
특정 구체예에서, 본원에 개시된 항원-결합 분자, 예를 들어, CD16A/BCMA 항원-결합 분자, 또는 이를 포함하는 제약학적 조성물의 투여는 2차 (2L) 또는 3차 (3L) 치료가 될 것이다. 예를 들어, 제한없이, 이러한 2차 또는 3차 투여는 Fc-기반 MOA, 예를 들어, 다라투무맙 치료를 통해 이미 치료 작용을 제공받은 대상체에서 발생할 것이다. 특정 구체예에서, 이러한 2차 또는 3차 치료는 다라투무맙 치료에 불응성이거나 내성이 있는 대상체에서 발생할 것이다.
특정 구체예에서, 다음 기준 중 하나 이상을 사용하여, 다발성 골수종 치료에 사용하기 위한 NK 세포 관여항체를 선택한다:
·
NK 세포 관여항체는 2개의 표적들: NK 세포 상의 CD16A, 및 다발성 골수종 세포 상의 BCMA에 결합할 수 있다,
·
NK 세포 관여항체는 CD16A에 대해 적어도 2가이다, 예컨대, 적어도 2개의 CD16A 항원-결합 모이어티를 포함한다,
·
NK 세포 관여항체는 CD16B와 교차 반응하지 않고 바람직하게는 비인간 영장류와 교차 반응하는 NK 세포 이중특이적 항체이다,
·
NK 세포 관여항체는 강력하고 우세하며, BCMA+ 종양 세포들 (예컨대, EC50 ≤ 5nM로 사멸된 ≥ 약 60% 세포) 및 일차 골수종의 표적-의존성 시험관내 사멸을 보유한다,
·
NK 세포 관여항체는 NK 세포를 유의하게 사멸시키지 않는다, 예컨대, NK 세포 동족살해를 감소시키거나 회피한다,
·
NK 세포 관여항체는 허용가능한 안전성 프로파일을 가지고 있으며, 예를 들어, 다른 T-세포 관여항체보다 우수한 시험관내 사이토카인 방출 프로파일을 가지고 (예를 들어, NK 세포 관여항체는 CRS가 없음), 이상 반응은 모니터링 가능하고, 관리가능하며, 가역적이다,
·
NK 세포 관여항체는 다발성 골수종 대상체에게 정맥내 투여 될 수 있다, 그리고
·
NK 세포 관여항체는 주 1 회 (QW) 이하의 투여 빈도를 필요로 한다.
특정 구체예에서, 본 발명의 항원-결합 단백질의 투여와 관련하여 다음과 같은 약력학 (PD) 바이오마커가 사용될 수 있다: 혈청 M 단백질 및 유리 경쇄 (FLC)의 농도, 단일클론 형질 세포의 감소, 치료 후 골수 샘플에서 NK 세포 활성화 및 동원 및 말초 NK 세포 활성화. 특정 구체예에서, 치료 방법은 BMCA 의존성 진단을 포함 할 수 있지만, 이러한 진단은 다발성 골수종에서 BMCA의 높은 유병률을 고려할 때 반드시 필요한 것은 아니다.
VI.
예시적 구체예들
특정 구체예에서, 본 발명은 (a) 적어도 제 1 표적 항원-결합 모이어티 및 (b) 적어도 2개의 CD16A 항원-결합 모이어티를 포함하는 다중특이적 항원-결합 단백질에 관한 것이며, 여기서 적어도 2개의 CD16A 항원-결합 모이어티는 적어도 하나의 불변 도메인을 포함하는 Fab 단편 또는 Fc 부분에 융합된다. 특정 구체예들에서, 상기 2개의 CD16A 항원-결합 모이어티 중 적어도 하나는 단쇄 Fv (scFv), 단쇄 디아바디 (scDb) 및 디아바디 Db로 구성된 그룹에서 선택된 항원-결합 분자이다. 특정 구체예들에서, 적어도 2개의 CD16A 항원-결합 모이어티 각각은 scFv이다. 특정 구체예들에서, 적어도 2개의 CD16A 항원-결합 모이어티는 scDb 형태이다. 특정 구체예들에서, 상기 적어도 2개의 CD16A 항원-결합 모이어티 각각은 폴리펩티드 사슬에서 차례로 연결된 경쇄 가변 영역 (VL) 및 중쇄 가변 영역 (VH)을 포함하고, 폴리펩티드 사슬의 N-말단의 가변 영역은 VL이다. 특정 구체예들에서, 상기 폴리펩티드 사슬에서 적어도 2개의 CD16A 항원-결합 모이어티의 가변 영역은 N-말단으로부터 C-말단으로 VL-VH, VL-VL-VH-VH 또는 VL-VH-VL-VH의 순서로 배치된다. 특정 구체예들에서, 상기 폴리펩티드 사슬에서 적어도 2개의 CD16A 항원-결합 모이어티의 가변 영역은 N-말단으로부터 C-말단으로 VL-VH의 순서로 배치된다. 특정 구체예들에서, 상기 폴리펩티드 사슬에서 적어도 2개의 CD16A 항원-결합 모이어티의 가변 영역은 N-말단으로부터 C-말단으로 VL-VH-VL-VH의 순서로 배치된다. 특정 구체예에서, (i) 폴리펩티드 사슬의 C-말단은 Fc 부분의 CH2 도메인의 N-말단에 융합되고; 또는 (ii) 폴리펩티드 사슬의 C-말단은 Fc 부분의 힌지의 N-말단에 융합되고; (iii) 폴리펩티드 사슬의 N-말단은 Fc 부분의 CH3 도메인의 C-말단에 융합되고, 또는 (iv) 폴리펩티드 사슬의 N-말단은 Fab 단편의 C-말단에 융합된다. 특정 구체예들에서, 폴리펩티드 사슬의 N-말단은 Fc 부분의 CH3 도메인의 C-말단에 융합된다. 특정 구체예들에서, Fc 부분은 단량체 CH2-CH3 단편, 이종이량체 Fc 영역, 및 동종이량체 Fc 영역으로 구성된 그룹에서 선택된다. 특정 구체예들에서, 상기 Fc 부분은 Fc-감마 수용체에 결합하지 않지만 신생아 Fc 수용체에 대한 결합을 보유한다. 특정 구체예들에서, 상기 2개의 CD16 항원-결합 모이어티를 포함하는 scDb 또는 Db는 Fab 단편 중 하나의 사슬의 C-말단에 융합되고 제 1 표적 항원-결합 모이어티는 Fab 단편의 다른 사슬의 C-말단에 융합된다. 특정 구체예들에서, Fab 단편은 N-말단에 HSA 항원-결합 Fv를 포함한다.
특정 구체예들에서, 본원에 기재된 항원-결합 단백질은 4가이다.
특정 구체예에서, 본원에 기재된 다중특이적 항원-결합 단백질은 적어도 2개의 표적 항원-결합 모이어티를 포함한다.
특정 구체예들에서, 본원에 기재된 다중특이적 항원-결합 단백질은 이량체 Fc 부분에 융합된, 적어도 2개의 CD16A 항원-결합 모이어티, 제 1 표적 항원-결합 모이어티, 및 제 2 표적 항원-결합 모이어티를 포함한다.
특정 구체예들에서, 본원에 기재된 다중특이적 항원-결합 단백질은 IgG의 각 중쇄의 C-말단에 융합된 CD16A 항원-결합 모이어티를 포함하고, 여기서 상기 IgG는 2개의 Fab 각각에서 N-말단에서 제 1 표적 항원-결합 Fv 모이어티를 포함하고 제 2 표적 항원-결합 모이어티는 C-말단에서 CL 도메인들 각각에 융합된다.
특정 구체예들에서, 본원에 기재된 CD16A 항원-결합 모이어티는 다음을 포함한다: (i) 서열 번호: 50에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 51에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 52에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 53에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 54에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 55에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역.
특정 구체예들에서, 본원에 기재된 다중특이적 항원-결합 단백질은 다음을 포함하는 CD16A 항원-결합 모이어티를 포함한다: (i) 서열 번호: 73에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 74에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 75에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 76에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 77에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 78에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역.
특정 구체예들에서, 본원에 기재된 다중특이적 항원-결합 단백질은 CD16A 항원-결합 모이어티를 포함하며, 이는 (i) 서열 번호: 3에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 이와 동일한 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 2에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 이와 동일한 아미노산 서열을 포함하는 경쇄 가변 영역을 포함한다.
특정 구체예들에서, 본원에 기재된 다중특이적 항원-결합 단백질은, (i) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하는, CD16A 항원-결합 모이어티를 포함한다.
특정 구체예에서, 본원에 기재된 다중특이적 항원-결합 단백질은 BCMA 및 EGFR로부터 선택되는 제 1 표적 항원에 결합한다. 특정 구체예에서, 본원에 기재된 다중특이적 항원-결합 단백질은 BCMA인 제 1 표적 항원에 결합한다.
특정 구체예들에서, 본원에 기재된 다중특이적 항원-결합 단백질은 서열 번호: 61 또는 63에 제시된 아미노산 서열을 갖는 제 1 폴리펩티드 사슬, 및 서열 번호: 62 또는 64에 제시된 아미노산 서열을 갖는 제 2 폴리펩티드 사슬을 포함하는 사량체를 포함한다. 특정 구체예에서, 본원에 기재된 다중특이적 항원-결합 단백질은 다음으로부터 선택된 제 1 및 제 2 폴리펩티드를 포함하는 사량체를 포함한다: (i) 서열 번호: 61에 제시된 아미노산 서열을 갖는 제 1 폴리펩티드 및 서열 번호: 62에 제시된 아미노산 서열을 갖는 제 2 폴리펩티드; (ii) 서열 번호: 61에 제시된 아미노산 서열을 갖는 제 1 폴리펩티드 및 서열 번호: 64에 제시된 아미노산 서열을 갖는 제 2 폴리펩티드; (iii) 서열 번호: 63에 제시된 아미노산 서열을 갖는 제 1 폴리펩티드 및 서열 번호: 62에 제시된 아미노산 서열을 갖는 제 2 폴리펩티드; 및 (iv) 서열 번호: 63에 제시된 아미노산 서열을 갖는 제 1 폴리펩티드 및 서열 번호: 64에 제시된 아미노산 서열을 갖는 제 2 폴리펩티드.
특정 구체예들에서, 본원에 기재된 다중특이적 항원-결합 단백질은 다음을 포함하는 BCMA 항원-결합 모이어티를 포함한다: (i) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역.
특정 구체예들에서, 본원에 기재된 다중특이적 항원-결합 단백질은 다음을 포함하는 BCMA 항원-결합 모이어티를 포함한다: (i) 서열 번호: 65에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 이와 동일한 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 66에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 이와 동일한 아미노산 서열을 포함하는 경쇄 가변 영역.
특정 구체예들에서, 본원에 기재된 다중특이적 항원-결합 단백질은 다음을 포함하는 BCMA 항원-결합 모이어티를 포함한다: (i) 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역.
특정 구체예들에서, 본원에 기재된 다중특이적 항원-결합 단백질은 다음을 포함하는 항원-결합 단백질을 포함한다: (i) 다음을 포함하는 CD16A 항원-결합 모이어티: (a) 서열 번호:73에 제시된 아미노산 서열을 가지는 CDR1; 서열 번호:74에 제시된 아미노산 서열을 가지는 CDR2; 및 서열 번호:75에 제시된 아미노산 서열을 가지는 CDR3을 포함하는 중쇄 가변 영역, 및 (b) 서열 번호:76에 제시된 아미노산 서열을 가지는 CDR1; 서열 번호:77에 제시된 아미노산 서열을 가지는 CDR2; 및 서열 번호:78에 제시된 아미노산 서열을 가지는 CDR3를 포함하는 경쇄 가변 영역; 및 (ii) 다음을 포함하는 BCMA 항원-결합 모이어티: (a) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및 (b) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역.
특정 구체예에서, 본 발명은 본원에 기재된 다중특이적 항원-결합 단백질 및 제약학적으로 허용되는 담체를 포함하는 제약학적 조성물에 관한 것이다.
특정 구체예에서, 본원에 기재된 다중특이적 항원-결합 단백질은 약제로서 사용하기 위해 기재되어 있다.
특정 구체예들에서, 본 발명은 본원에 기재된 다중특이적 항원-결합 단백질 또는 본원에 기재된 제약학적 조성물을 필요로 하는 대상체에게 투여하는 단계를 포함하는, 질환의 치료 또는 개선 방법에 관한 것이다. 특정 구체예들에서, 상기 질환은 암이다. 특정 구체예들에서, 상기 질환은 혈액암이다. 특정 구체예에서, 상기 질환은 다발성 골수종이다.
특정 구체예들에서, 본 발명은 본원에 기재된 이중특이적 항원-결합 단백질 또는 본원에 기재된 제약학적 조성물을 필요로 하는 대상체에게 투여하는 단계를 포함하는, 대상체에서 질환의 치료 및/또는 예방 방법에 관한 것이다. 특정 구체예들에서, 다중특이적 항원-결합 단백질은 정맥내 투여된다. 특정 구체예들에서, 다중특이적 항원-결합 단백질은 피하 투여된다. 특정 구체예에서, 본원에 개시된 방법은 제 2 요법을 투여하는 것을 포함한다. 특정 구체예들에서, 상기 제 2 요법은 항-PD-1 항체를 포함하는 요법, 항-PD-L1 항체를 포함하는 요법, CD3 이중특이적 항체를 포함하는 요법, 항-TIGIT 항체를 포함하는 요법, 항-VEGF 항체를 포함하는 요법, 및 항-FcRH5 항체를 포함하는 요법으로 구성된 그룹에서 선택된다. 특정 구체예에서, 제 2 요법은 사이토카인 요법이다. 특정 구체예에서, 상기 사이토카인 요법은 IL-15, IL-2, IL-12, IL-21 및 IL6으로 구성된 그룹에서 선택된 사이토카인의 투여를 포함한다. 특정 구체예에서, 사이토카인 요법은 IL-2의 투여를 포함한다. 특정 구체예에서, 사이토카인 요법은 IL-15의 투여를 포함한다.
특정 구체예에서, 본원에 기재된 치료되는 대상체는 암 환자이다. 특정 구체예에서, 대상체는 혈액암 환자이다. 특정 구체예들에서, 대상체는 다발성 골수종 환자이다. 특정 구체예에서, 대상체는 재발성/불응성 다발성 골수종 환자이다. 특정 구체예에서, 대상체는 항-CD38 요법을 제공받았다. 특정 구체예에서, 대상체는 다라투무맙을 제공받았다. 특정 구체예에서, 대상체는 다라투무맙 나이브, 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성이다. 특정 구체예에서, 대상체는 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성이다. 특정 구체예에서, 대상체는 CD16A 다형성을 발현한다. 특정 구체예에서, 상기 CD16A 다형성은 CD16A-158V/F 다형성이다.
특정 구체예에서, 본 발명은 (a) 적어도 하나의 BCMA-결합 모이어티 및 (b) 적어도 2개의 CD16A 항원-결합 모이어티를 포함하는 이중특이적 항원-결합 단백질에 관한 것이며, 여기서 적어도 2개의 CD16A 항원-결합 모이어티는 적어도 하나의 불변 도메인을 포함하는 Fab 단편 또는 Fc 부분에 융합된다. 특정 구체예들에서, 상기 2개의 CD16A 항원-결합 모이어티 중 적어도 하나는 단쇄 Fv (scFv), 단쇄 디아바디 (scDb) 및 디아바디 Db로 구성된 그룹에서 선택된 항원-결합 분자이다. 특정 구체예들에서, 적어도 2개의 CD16A 항원-결합 모이어티 각각은 scFv이다. 특정 구체예들에서, 적어도 2개의 CD16A 항원-결합 모이어티는 scDb 형태이다. 특정 구체예들에서, 상기 적어도 2개의 CD16A 항원-결합 모이어티 각각은 폴리펩티드 사슬에서 차례로 연결된 경쇄 가변 영역 (VL) 및 중쇄 가변 영역 (VH)을 포함하고, 폴리펩티드 사슬의 N-말단의 가변 영역은 VL이다. 특정 구체예들에서, 상기 폴리펩티드 사슬에서 적어도 2개의 CD16A 항원-결합 모이어티의 가변 영역은 N-말단으로부터 C-말단으로 VL-VH, VL-VL-VH-VH 또는 VL-VH-VL-VH의 순서로 배치된다.
특정 구체예들에서, 상기 폴리펩티드 사슬에서 적어도 2개의 CD16A 항원-결합 모이어티의 가변 영역은 N-말단으로부터 C-말단으로 VL-VH의 순서로 배치된다. 특정 구체예들에서, 상기 폴리펩티드 사슬에서 적어도 2개의 CD16A 항원-결합 모이어티의 가변 영역은 N-말단으로부터 C-말단으로 VL-VH-VL-VH의 순서로 배치된다.
특정 구체예에서, 본 발명은 이중특이적 항원-결합 단백질에 관한 것이며, 이 때: (i) 폴리펩티드 사슬의 C-말단은 Fc 부분의 CH2 도메인의 N-말단에 융합되고; 또는 (ii) 폴리펩티드 사슬의 C-말단은 Fc 부분의 힌지의 N-말단에 융합되고; (iii) 폴리펩티드 사슬의 N-말단은 Fc 부분의 CH3 도메인의 C-말단에 융합되고, 또는 (iv) 폴리펩티드 사슬의 N-말단은 Fab 단편의 C-말단에 융합된다. 특정 구체예들에서, 폴리펩티드 사슬의 N-말단은 Fc 부분의 CH3 도메인의 C-말단에 융합된다. 특정 구체예들에서, Fc 부분은 단량체 CH2-CH3 단편, 이종이량체 Fc 영역, 및 동종이량체 Fc 영역으로 구성된 그룹에서 선택된다. 특정 구체예들에서, 상기 Fc 부분은 Fc-감마 수용체에 결합하지 않지만 신생아 Fc 수용체에 대한 결합을 보유한다. 특정 구체예에서, Fc 부분은 적어도 하나의 무-이펙터 돌연변이를 포함한다. 특정 구체예들에서, 상기 적어도 하나의 무-이펙터 돌연변이는 C220S, C229S, E233P, L234A, L234V, L234F, L235A, L235E, P238S, D265A, N297A, N297Q, 및 P331S로 구성된 그룹에서 선택된다. 특정 구체예에서, 적어도 하나의 무-이펙터 돌연변이는 L234A, L234V, L234F, L235A, L235E, P238S 및 D265A로 구성된 그룹에서 선택된다. 특정 구체예에서, 적어도 하나의 무-이펙터 돌연변이는 L234F, L235E 및 D265A로 구성된 그룹에서 선택된다. 특정 구체예에서, Fc 부분은 2개의 무-이펙터 돌연변이를 갖는다. 특정 구체예들에서, 상기 2개의 무-이펙터 돌연변이는 L234F 및 L235E이다. 특정 구체예에서, Fc 부분은 3개의 무-이펙터 돌연변이를 갖는다. 특정 구체예에서, 상기 3개의 무-이펙터 돌연변이는 L234F, L235E 및 D265A이다.
특정 구체예들에서, 본 발명의 이중특이적 항원-결합 단백질은 Fc 부분에 융합된 적어도 2개의 CD16A 항원-결합 모이어티를 포함한다. 특정 구체예에서, 본 발명의 이중특이적 항원-결합 단백질은 2개의 BCMA-표적화 모이어티를 포함한다. 특정 구체예에서, 본 발명의 이중특이적 항원-결합 단백질은 2개의 CD16A 항원-결합 모이어티 및 2개의 BCMA-표적화 모이어티를 포함한다. 특정 구체예들에서, 2개의 CD16A 항원-결합 모이어티 각각은 IgG의 각 중쇄의 C-말단에 융합되고, 2개의 BCMA-표적화 모이어티 각각은 IgG의 N-말단에 융합된다.
특정 구체예에서, 본 발명의 이중특이적 항원-결합 단백질은 도 13에 도시된 구조를 갖는 이중특이적 항원-결합 단백질을 포함한다. 이러한 특정 구체예에서, 이중특이적 항원-결합 단백질은 하나의 BCMA-표적화 모이어티를 포함한다. 특정 구체예들에서, 상기 BCMA-표적화 모이어티는 적어도 2개의 CD16A 항원-결합 모이어티가 융합되는 Fc 부분의 N-말단에 융합된다.
특정 구체예에서, 이중특이적 항원-결합은 도 5에 도시된 구조를 갖는다.
특정 구체예들에서, 본 발명의 이중특이적 항원-결합 단백질은 다음을 포함하는 CD16A 항원-결합 모이어티를 포함한다: (i) 서열 번호: 50에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 51 또는 56에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 52에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 53에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 54에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 55에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역. 특정 구체예들에서, 중쇄 가변 영역 CDR2는 서열 번호: 51에 제시된 아미노산 서열을 갖는 이중특이적 항원-결합 단백질. 특정 구체예들에서, 중쇄 가변 영역 CDR2는 서열 번호: 56에 제시된 아미노산 서열을 갖는 이중특이적 항원-결합 단백질.
특정 구체예들에서, 본 발명의 이중특이적 항원-결합 단백질은 다음을 포함하는 CD16A 항원-결합 모이어티를 포함한다: (i) 서열 번호: 73에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 74에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 75에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 76에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 77에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 78에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역. 특정 구체예들에서, 상기 CD16A 항원-결합 모이어티는 (i) 서열 번호: 3에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 이와 동일한 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 2에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 이와 동일한 아미노산 서열을 포함하는 경쇄 가변 영역을 포함한다. 특정 구체예들에서, 상기 CD16A 항원-결합 모이어티는, (i) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함한다.
특정 구체예들에서, 본 발명의 이중특이적 항원-결합 단백질은 다음을 포함하는 BCMA 항원-결합 모이어티를 포함한다: (i) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역. 특정 구체예들에서, 상기 BCMA 항원-결합 모이어티는 (i) 서열 번호: 65에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 이와 동일한 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 66에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 이와 동일한 아미노산 서열을 포함하는 경쇄 가변 영역을 포함한다. 특정 구체예들에서, 상기 BCMA 항원-결합 모이어티는, (i) 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함한다.
특정 구체예에서, 본 개시 내용의 이중특이적 항원-결합 단백질은 2개의 CD16A 항원-결합 모이어티 및 2개의 BCMA-표적화 모이어티를 포함하고, 여기서: (a) 상기 각각의 CD16A 항원-결합 모이어티는 서열 번호:73에 제시된 아미노산 서열을 갖는 VH CDR1, 서열 번호:74에 제시된 아미노산 서열을 갖는 VH CDR2, 서열 번호:75에 제시된 아미노산 서열을 갖는 VH CDR3, 서열 번호:76에 제시된 아미노산 서열을 갖는 VL CDR1, 서열 번호:77에 제시된 아미노산 서열을 갖는 VL CDR2, 및 서열 번호:78에 제시된 아미노산 서열을 갖는 VL CDR3를 포함하고; 및 (b) 상기 각각의 BCMA 항원-결합 모이어티는 서열 번호:67에 제시된 아미노산 서열을 갖는 VH CDR1, 서열 번호:68에 제시된 아미노산 서열을 갖는 VH CDR2, 서열 번호:69에 제시된 아미노산 서열을 갖는 VH CDR3, 서열 번호:70에 제시된 아미노산 서열을 갖는 VL CDR1, 서열 번호:71에 제시된 아미노산 서열을 갖는 VL CDR2, 및 서열 번호:72에 제시된 아미노산 서열을 갖는 VL CDR3를 포함한다. 특정 구체예에서, (a) 각각의 CD16A 항원-결합 모이어티는 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역, 및 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하고; 및 (b) 각각의 BCMA-표적화 모이어티는 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역, 및 (ii) 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함한다.
특정 구체예에서, 본 발명의 이중특이적 항원-결합 단백질은 서열 번호: 61에 제시된 아미노산 서열을 갖는 제 1 폴리펩티드, 및 서열 번호: 62에 제시된 아미노산 서열을 갖는 제 2 폴리펩티드를 포함하는 사량체이다. 특정 구체예에서, 본 발명의 이중특이적 항원-결합 단백질은 서열 번호: 63에 제시된 아미노산 서열을 갖는 제 1 폴리펩티드, 및 서열 번호: 64에 제시된 아미노산 서열을 갖는 제 2 폴리펩티드를 포함하는 사량체이다.
특정 구체예들에서, 본 발명의 이중특이적 항원-결합 단백질은 2개의 CD16A 항원-결합 모이어티 및 2개의 BCMA 항원-결합 모이어티를 포함하며, 여기서: (i) CD16A 항원-결합 모이어티는 각각 다음을 포함하고: (a) 서열 번호:73에 제시된 아미노산 서열을 가지는 CDR1; 서열 번호:74에 제시된 아미노산 서열을 가지는 CDR2; 및 서열 번호:75에 제시된 아미노산 서열을 가지는 CDR3을 포함하는 중쇄 가변 영역, 및 (b) 서열 번호:76에 제시된 아미노산 서열을 가지는 CDR1; 서열 번호:77에 제시된 아미노산 서열을 가지는 CDR2; 및 서열 번호:78에 제시된 아미노산 서열을 가지는 CDR3를 포함하는 경쇄 가변 영역; 및 (ii) BCMA 항원-결합 모이어티는 각각 다음을 포함한다: (a) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및 (b) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역.
특정 구체예들에서, 본 발명은 본원에 기재된 이중특이적 항원-결합 단백질 및 제약학적으로 허용되는 담체를 포함하는 제약학적 조성물에 관한 것이다. 특정 구체예들에서, 제약학적 조성물은 약제로 사용된다.
특정 구체예들에서, 본 발명은 질환의 치료 및/또는 예방 방법에 관한 것이며, 이 방법은 본원에 기재된 이중특이적 항원-결합 단백질 또는 제약학적 조성물을 필요로 하는 대상체에게 투여하는 것을 포함한다. 특정 구체예들에서, 상기 질환은 암이다. 특정 구체예들에서, 상기 질환은 혈액암이다. 특정 구체예에서, 상기 질환은 다발성 골수종이다. 특정 구체예들에서, 이중특이적 항원-결합 단백질은 정맥내 투여된다. 특정 구체예들에서, 이중특이적 항원-결합 단백질은 피하 투여된다. 특정 구체예들에서, 이중특이적 항원-결합 단백질은 제 2 요법과 함께 투여된다. 특정 구체예들에서, 상기 제 2 요법은 항-PD-1 항체를 포함하는 요법, 항-PD-L1 항체를 포함하는 요법, CD3 이중특이적 항체를 포함하는 요법, 항-TIGIT 항체를 포함하는 요법, 항-VEGF 항체를 포함하는 요법, 및 항-FcRH5 항체를 포함하는 요법으로 구성된 그룹에서 선택된다. 특정 구체예에서, 제 2 요법은 사이토카인 요법이다. 특정 구체예들에서, 상기 사이토카인 요법은 IL-15, IL-2, IL-12, IL-21, IL-17, IL-18, IL-23, IL-27, 및 IL-6으로 구성된 그룹에서 선택된 사이토카인의 투여이다. 특정 구체예에서, 사이토카인은 IL-15이다. 특정 구체예에서, 사이토카인은 IL-2이다. 특정 구체예에서, 대상체는 암 환자이다. 특정 구체예에서, 대상체는 혈액암 환자이다. 특정 구체예들에서, 대상체는 다발성 골수종 환자이다. 특정 구체예에서, 대상체는 재발성/불응성 다발성 골수종 환자이다. 특정 구체예에서, 대상체는 항-CD38 요법을 제공받았다. 특정 구체예에서, 대상체는 다라투무맙을 제공받았다. 특정 구체예에서, 대상체는 다라투무맙 나이브, 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성이다. 특정구체예에서, 대상체는 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성이다. 특정구체예에서, 대상체는 CD16A 다형성을 발현한다. 특정구체예에서, 상기 CD16A 다형성은 CD16A-158V/F 다형성이다.
특정 구체예에서, 본 발명은 본원에 기재된 다중특이적 항원-결합 단백질 또는 본원에 기재된 이중특이적 항원-결합 단백질에 관한 것이며, 여기서 상기 다중특이적 항원-결합 단백질 또는 이중특이적 항원-결합 단백질은 대상체에게 투여될 때 상기 대상체의 자연 살해 (NK) 세포 집단을 실질적으로 고갈시키거나 감소시키지 않는다.
특정 구체예에서, 본 발명은 본원에 기재된 다중특이적 항원-결합 단백질 또는 본원에 기재된 이중특이적 항원-결합 단백질을 투여하는 것을 포함하는, 고갈되거나 감소된 NK 세포 집단을 갖는 대상체의 치료 방법에 관한 것이다. 특정 구체예에서, 상기 대상체는 항-CD38 요법으로 이전에 치료받았다. 특정 구체예에서, 상기 항-CD38 요법은 다라투무맙 요법이다.
특정 구체예에서, 본 발명은 2개의 CD16A 항원-결합 모이어티 및 2개의 BCMA-표적화 모이어티를 포함하는 이중특이적 항원-결합 단백질에 관한 것이며, 여기서 상기 2개의 CD16A 항원-결합 모이어티 각각은 IgG의 각 중쇄의 C-말단에 융합되고, 상기 2개의 BCMA-표적화 모이어티 각각은 IgG의 중쇄 각각의 N-말단에 융합되며, 여기서: (i) CD16A 항원-결합 모이어티 각각은 다음을 포함하고: (a) 서열 번호:73에 제시된 아미노산 서열을 가지는 CDR1; 서열 번호:74에 제시된 아미노산 서열을 가지는 CDR2; 및 서열 번호:75에 제시된 아미노산 서열을 가지는 CDR3을 포함하는 중쇄 가변 영역, 및 (b) 서열 번호:76에 제시된 아미노산 서열을 가지는 CDR1; 서열 번호:77에 제시된 아미노산 서열을 가지는 CDR2; 및 서열 번호:78에 제시된 아미노산 서열을 가지는 CDR3를 포함하는 경쇄 가변 영역; 및 (ii) BCMA 항원-결합 모이어티 각각은 다음을 포함한다: (a) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및 (b) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역.
특정 구체예에서, 본 발명은 2개의 CD16A 항원-결합 모이어티 및 2개의 BCMA-표적화 모이어티를 포함하는 이중특이적 항원-결합 단백질을 대상체에 투여하는 단계를 포함하는, 대상체의 암 치료 방법에 관한 것이며, 여기서 상기 2개의 CD16A 항원-결합 모이어티 각각은 IgG의 각 중쇄의 C-말단에 융합되고, 상기 2개의 BCMA-표적화 모이어티 각각은 IgG의 중쇄 각각의 N-말단에 융합되며, 여기서: (i) CD16A 항원-결합 모이어티 각각은 다음을 포함하고: (a) 서열 번호:73에 제시된 아미노산 서열을 가지는 CDR1; 서열 번호:74에 제시된 아미노산 서열을 가지는 CDR2; 및 서열 번호:75에 제시된 아미노산 서열을 가지는 CDR3을 포함하는 중쇄 가변 영역, 및 (b) 서열 번호:76에 제시된 아미노산 서열을 가지는 CDR1; 서열 번호:77에 제시된 아미노산 서열을 가지는 CDR2; 및 서열 번호:78에 제시된 아미노산 서열을 가지는 CDR3를 포함하는 경쇄 가변 영역; 및 (ii) BCMA 항원-결합 모이어티 각각은 다음을 포함한다: (a) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및 (b) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역. 특정 구체예에서, 상기 암은 다발성 골수종이다.
특정 구체예에서, 본 발명은 다음을 포함하는, CD16A 및 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질에 관한 것이다: (i) 서열 번호:73에 제시된 아미노산 서열을 가지는 CDR1; 서열 번호:74에 제시된 아미노산 서열을 가지는 CDR2; 및 서열 번호:75에 제시된 아미노산 서열을 가지는 CDR3을 포함하는 제 1 중쇄 가변 영역, 및 (ii) 서열 번호:76에 제시된 아미노산 서열을 가지는 CDR1; 서열 번호:77에 제시된 아미노산 서열을 가지는 CDR2; 및 서열 번호:78에 제시된 아미노산 서열을 가지는 CDR3를 포함하는 제 1 경쇄 가변 영역; (iii) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 제 2 중쇄 가변 영역, 및 (iv) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 제 2 경쇄 가변 영역. 예를 들어, 특정 구체예에서, CD16A 및 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질은 다음을 포함한다: (i) 서열 번호:3에 제시된 아미노산 서열을 포함하는 제 1 중쇄 가변 영역; (ii) 서열 번호: 2에 제시된 아미노산 서열을 포함하는 제 1 경쇄 가변 영역; (iii) 서열 번호: 65에 제시된 아미노산 서열을 포함하는 제 2 중쇄 가변 영역; (iv) 서열 번호: 66에 제시된 아미노산 서열을 포함하는 제 2 경쇄 가변 영역; (v) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 제 1 중쇄 가변 영역 및 서열 번호: 2에 제시된 아미노산 서열을 포함하는 제 1 경쇄 가변 영역; (vi) 서열 번호: 65에 제시된 아미노산 서열을 포함하는 제 2 중쇄 가변 영역 및 서열 번호: 66에 제시된 아미노산 서열을 포함하는 제 2 경쇄 가변 영역; 또는 (vii) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 제 1 중쇄 가변 영역; 및 서열 번호: 2에 제시된 아미노산 서열을 포함하는 제 1 경쇄 가변 영역; 및 서열 번호: 65에 제시된 아미노산 서열을 포함하는 제 2 중쇄 가변 영역 및 서열 번호: 66에 제시된 아미노산 서열을 포함하는 제 2 경쇄 가변 영역. 특정 구체예에서, 본원에 기재된 CD16A 및 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질은 CD16B에 결합하지 않는다. 특정 구체예에서, 본원에 기재된 CD16A 및 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질은 대상체에게 투여될 때 대상체의 자연 살해 (NK) 세포 집단을 실질적으로 고갈시키거나 감소시키지 않는다. 특정 구체예에서, 본원에 기재된 CD16A 및 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질은 인간 CD16A에 결합한다. 특정 구체예에서, 본원에 기재된 CD16A 및 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질은 인간 BCMA에 결합한다.
특정 구체예에서, 본 발명은 본원에 기재된 CD16A 및 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질 및 제약학적으로 허용되는 담체를 포함하는 제약학적 조성물에 관한 것이다.
특정 구체예에서, 본원에 기재된 CD16A 및 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질은 약제로 사용된다.
143.
특정 구체예에서, 본 발명은 질환의 치료 및/또는 예방 방법에 관한 것이며, 여기서 이 방법은 본원에 기재된 CD16A 및 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질 또는 본원에 기재된 CD16A 및 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질을 포함하는 제약학적 조성물을 필요로하는 투여하는 단계를 포함한다. 특정 구체예들에서, 상기 질환은 암이다. 특정 구체예들에서, 상기 질환은 혈액암이다. 특정 구체예에서, 상기 질환은 다발성 골수종이다. 특정 구체예에서, 항체 또는 항원-결합 단백질은 정맥내 투여된다. 특정 구체예에서, 항체 또는 항원-결합 단백질은 피하 투여된다. 특정 구체예에서, 본원에 기재된 CD16A 및 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질 또는 본원에 기재된 CD16A 및 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질을 포함하는 제약학적 조성물을 필요로하는 투여하는 단계를 포함하는 질환의 치료 및/또는 예방 방법은 제 2 요법을 투여하는 것을 포함한다. 특정 구체예들에서, 상기 제 2 요법은 항-PD-1 항체를 포함하는 요법, 항-PD-L1 항체를 포함하는 요법, CD3 이중특이적 항체를 포함하는 요법, 항-TIGIT 항체를 포함하는 요법, 항-VEGF 항체를 포함하는 요법, 및 항-FcRH5 항체를 포함하는 요법으로 구성된 그룹에서 선택된다. 특정 구체예에서, 제 2 요법은 사이토카인 요법이다. 특정 구체예들에서, 상기 사이토카인 요법은 IL-15, IL-2, IL-12, IL-21, IL-17, IL-18, IL-23, IL-27, 및 IL-6으로 구성된 그룹에서 선택된 사이토카인의 투여이다. 특정 구체예에서, 사이토카인은 IL-15이다. 특정 구체예에서, 사이토카인은 IL-2이다. 특정 구체예에서, 대상체는 암 환자이다. 특정 구체예에서, 대상체는 혈액암 환자이다. 특정 구체예들에서, 대상체는 다발성 골수종 환자이다. 특정 구체예에서, 대상체는 재발성/불응성 다발성 골수종 환자이다. 특정 구체예에서, 대상체는 항-CD38 요법을 제공받았다. 특정 구체예에서, 대상체는 다라투무맙을 제공받았다. 특정 구체예에서, 대상체는 다라투무맙 나이브, 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성이다. 특정 구체예에서, 대상체는 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성이다. 특정 구체예에서, 대상체는 CD16A 다형성을 발현한다. 특정 구체예에서, 상기 CD16A 다형성은 CD16A-158V/F 다형성이다.
특정 구체예에서, 본 발명은 본원에 기재된 CD16A 및 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질 또는 본원에 기재된 CD16A 및 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질을 포함하는 제약학적 조성물을 투여하는 단계를 포함하는, 고갈되거나 감소된 NK 세포 집단을 갖는 대상체의 치료 방법에 관한 것이다. 특정 구체예에서, 상기 대상체는 항-CD38 요법으로 이전에 치료받았다. 특정 구체예에서, 상기 항-CD38 요법은 다라투무맙 요법이다.
특정 구체예에서, 본 발명은 CD16A에 결합하거나 결합 할 수 있는 적어도 하나의 아암, 및 BCMA에 결합하거나 결합 할 수 있는 적어도 하나의 아암을 포함하는 항체 또는 항원-결합 단백질에 관한 것이며, 여기서: (i) CD16A에 결합하거나 결합 할 수 있는 적어도 하나의 아암은 다음을 포함하고: (a) 서열 번호:73에 제시된 아미노산 서열을 가지는 CDR1; 서열 번호:74에 제시된 아미노산 서열을 가지는 CDR2; 및 서열 번호:75에 제시된 아미노산 서열을 가지는 CDR3을 포함하는 중쇄 가변 영역, 및 (b) 서열 번호:76에 제시된 아미노산 서열을 가지는 CDR1; 서열 번호:77에 제시된 아미노산 서열을 가지는 CDR2; 및 서열 번호:78에 제시된 아미노산 서열을 가지는 CDR3를 포함하는 경쇄 가변 영역; 및 (ii) BCMA에 결합하거나 결합 할 수 있는 적어도 하나의 아암은 다음을 포함한다: (a) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및 (b) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역. 특정 구체예에서, CD16A에 결합하거나 결합 할 수 있는 적어도 하나의 아암은 BCMA에 결합하거나 결합 할 수 있는 적어도 하나의 아암과 구별된다. 이러한 특정 구체예에서: (i) CD16A에 결합하거나 이에 결합 할 수 있는 적어도 하나의 아암은 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역을 포함하고; (ii) CD16A에 결합하거나 결합 할 수 있는 적어도 하나의 아암은 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하고; (iii) BCMA에 결합하거나 결합 할 수 있는 적어도 하나의 아암은 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역을 포함하고; (iv) BCMA에 결합하거나 결합 할 수 있는 적어도 하나의 아암은 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하고; (v) CD16A에 결합하거나 결합 할 수 있는 적어도 하나의 아암은 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역 및 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하고; (vi) BCMA에 결합하거나 결합 할 수 있는 적어도 하나의 아암은 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역 및 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하고; 또는 (vii) CD16A에 결합하거나 결합 할 수 있는 적어도 하나의 아암은 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역 및 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하고; 및 BCMA에 결합하거나 결합 할 수 있는 적어도 하나의 아암은 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역 및 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함한다. 특정 구체예에서, 상기 항체 또는 항원-결합 단백질은 CD16B에 결합하지 않는다. 특정 구체예에서, 상기 항체 또는 항원-결합 단백질은 대상체에게 투여될 때 상기 대상체의 자연 살해 (NK) 세포 집단을 실질적으로 고갈시키거나 감소시키지 않는다. 이러한 특정 구체예에서, 항체 또는 항원-결합 단백질은 인간 CD16A에 결합한다. 이러한 특정 구체예에서, 항체 또는 항원-결합 단백질은 인간 BCMA에 결합한다.
특정 구체예에서, 본 발명은 CD16A에 결합하거나 결합 할 수 있는 적어도 하나의 아암, 및 본원에 개시된 BCMA에 결합하거나 결합 할 수 있는 적어도 하나의 아암 및 제약학적으로 허용되는 담체를 포함하는 항체 또는 항원-결합 단백질을 포함하는 제약학적 조성물에 관한 것이다.
특정 구체예에서, 본 발명은 CD16A에 결합하거나 결합 할 수 있는 적어도 하나의 아암, 및 BCMA에 결합하거나 결합 할 수 있는 적어도 하나의 아암을 포함하는, 약제로 사용되는 항체 또는 항원-결합 단백질에 관한 것이다.
특정 구체예에서, 본 발명은 다음을 포함하는 질환의 치료 및/또는 예방 방법에 관한 것이다: CD16A에 결합하거나 결합 할 수 있는 적어도 하나의 아암, 및 본원에 기재된 BCMA에 결합하거나 결합 할 수 있는 적어도 하나의 아암 또는 이러한 항체 또는 항원-결합 단백질을 포함하는 제약학적 조성물을 필요로 하는 대상체에게 투여하는 단계. 특정 구체예들에서, 상기 질환은 암이다. 특정 구체예들에서, 상기 질환은 혈액암이다. 특정 구체예에서, 상기 질환은 다발성 골수종이다. 특정 구체예에서, 항체 또는 항원-결합 단백질은 정맥내 투여된다. 특정 구체예에서, 항체 또는 항원-결합 단백질은 피하 투여된다. 특정 구체예에서, CD16A에 결합하거나 결합 할 수 있는 적어도 하나의 아암, 및 본원에 기재된 BCMA에 결합하거나 결합 할 수 있는 적어도 하나의 아암 또는 이러한 항체 또는 항원-결합 단백질을 포함하는 제약학적 조성물을 필요로 하는 대상체에게 투여하는 단계를 포함하는 질환의 치료 및/또는 예방 방법은 제 2 요법을 투여하는 것을 포함한다. 특정 구체예들에서, 상기 제 2 요법은 항-PD-1 항체를 포함하는 요법, 항-PD-L1 항체를 포함하는 요법, CD3 이중특이적 항체를 포함하는 요법, 항-TIGIT 항체를 포함하는 요법, 항-VEGF 항체를 포함하는 요법, 및 항-FcRH5 항체를 포함하는 요법으로 구성된 그룹에서 선택된다. 특정 구체예에서, 제 2 요법은 사이토카인 요법이다. 특정 구체예들에서, 상기 사이토카인 요법은 IL-15, IL-2, IL-12, IL-21, IL-17, IL-18, IL-23, IL-27, 및 IL-6으로 구성된 그룹에서 선택된 사이토카인의 투여이다. 특정 구체예에서, 사이토카인은 IL-15이다. 특정 구체예에서, 사이토카인은 IL-2이다. 특정 구체예에서, 대상체는 암 환자이다. 특정 구체예에서, 대상체는 혈액암 환자이다. 특정 구체예들에서, 대상체는 다발성 골수종 환자이다. 특정 구체예에서, 대상체는 재발성/불응성 다발성 골수종 환자이다. 특정 구체예에서, 대상체는 항-CD38 요법을 제공받았다. I특정 구체예에서, 대상체는 다라투무맙을 제공받았다. 특정 구체예에서, 대상체는 다라투무맙 나이브, 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성이다. 특정 구체예에서, 대상체는 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성이다. 특정 구체예에서, 대상체는 CD16A 다형성을 발현한다. 특정 구체예에서, 상기 CD16A 다형성은 CD16A-158V/F 다형성이다. 특정 구체예에서, 상기 방법은 고갈되거나 감소된 NK 세포 집단을 갖는 대상체를 치료하는 것을 포함한다. 특정 구체예에서, 상기 대상체는 항-CD38 요법으로 이전에 치료받았다. 특정 구체예에서, 상기 항-CD38 요법은 다라투무맙 요법이다.
특정 구체예들에서, 본 발명은 다음을 포함하는, BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질에 관한 것이다: (i) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및 (ii) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역. 특정 구체예에서, BCMA는 인간 BCMA이다. 특정 구체예에서, 항체 또는 항원-결합 단백질은 CD16A에 결합하거나 결합 할 수 있는 적어도 하나의 아암을 포함한다. 특정 구체예에서, CD16A는 인간 CD16A이다. 특정 구체예에서, CD16A에 결합하거나 결합 할 수 있는 적어도 하나의 아암은 다음을 포함한다: (i) 서열 번호: 73에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 74에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 75에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및 (ii) 서열 번호: 76에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 77에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 78에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역. 이러한 특정 구체예에서, BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질은 다음을 포함한다: (i) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역; (ii) 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역; (iii) 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역; (iv) 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역; (v) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역 및 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역; 또는 (vi) 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역 및 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역; 또는 (vii) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 제 1 중쇄 가변 영역, 서열 번호: 2에 제시된 아미노산 서열을 포함하는 제 1 경쇄 가변 영역; 및 서열 번호: 65에 제시된 아미노산 서열을 포함하는 제 2 중쇄 가변 영역 및 서열 번호: 66에 제시된 아미노산 서열을 포함하는 제 2 중쇄 가변 영역.
특정 구체예에서, 본 발명은 본원에 개시된 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질 및 제약학적으로 허용되는 담체를 포함하는 제약학적 조성물에 관한 것이다.
특정 구체예에서, 본 발명은 약제로 사용되는, 본원에 개시된 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질에 관한 것이다.
특정 구체예에서, 본 발명은 질환의 치료 및/또는 예방 방법에 관한 것으로, 이 방법은 BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질 또는 이를 포함하는 제약학적 조성물을 필요로 하는 대상체에게 투여하는 단계를 포함한다. 특정 구체예들에서, 상기 질환은 암이다. 특정 구체예들에서, 상기 질환은 혈액암이다. 특정 구체예에서, 상기 질환은 다발성 골수종이다. 특정 구체예에서, 항체 또는 항원-결합 단백질은 정맥내 투여된다. 특정 구체예에서, 항체 또는 항원-결합 단백질은 피하 투여된다. 특정 구체예에서, BCMA에 결합하거나 결합 할 수 있는 항체 또는 항원-결합 단백질 또는 이를 포함하는 제약학적 조성물을 필요로 하는 대상체에게 투여하는 단계를 포함하는 질환의 치료 및/또는 예방 방법은 제 2 요법을 투여하는 것을 포함한다. 특정 구체예들에서, 상기 제 2 요법은 항-PD-1 항체를 포함하는 요법, 항-PD-L1 항체를 포함하는 요법, CD3 이중특이적 항체를 포함하는 요법, 항-TIGIT 항체를 포함하는 요법, 항-VEGF 항체를 포함하는 요법, 및 항-FcRH5 항체를 포함하는 요법으로 구성된 그룹에서 선택된다. 특정 구체예에서, 제 2 요법은 사이토카인 요법이다. 특정 구체예들에서, 상기 사이토카인 요법은 IL-15, IL-2, IL-12, IL-21, IL-17, IL-18, IL-23, IL-27, 및 IL-6으로 구성된 그룹에서 선택된 사이토카인의 투여이다. 특정 구체예에서, 사이토카인은 IL-15이다. 특정 구체예에서, 사이토카인은 IL-2이다. 특정 구체예에서, 대상체는 암 환자이다. 특정 구체예에서, 대상체는 혈액암 환자이다. 특정 구체예들에서, 대상체는 다발성 골수종 환자이다. 특정 구체예에서, 대상체는 재발성/불응성 다발성 골수종 환자이다. 특정 구체예에서, 대상체는 항-CD38 요법을 제공받았다. 특정 구체예에서, 대상체는 다라투무맙을 제공받았다. 특정 구체예에서, 대상체는 다라투무맙 나이브, 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성이다. 특정구체예에서, 대상체는 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성이다. 특정구체예에서, 대상체는 CD16A 다형성을 발현한다. 특정구체예에서, 상기 CD16A 다형성은 CD16A-158V/F 다형성이다. 특정 구체예에서, 상기 항체 또는 항원-결합 단백질은 고갈되거나 감소된 NK 세포 집단을 갖는 대상체에게 투여된다. 특정 구체예에서, 상기 대상체는 항-CD38 요법으로 이전에 치료받았다. 특정 구체예에서, 상기 항-CD38 요법은 다라투무맙 요법이다.
실시예
실시예 1: BCMA 항원-결합 모이어티의 제작
항원-결합 모이어티를 제작하기 위해, 선택된 표적 항원에 대한 선택적 결합을 갖는 항체 단편들은, 예를 들면, Smith GP (Science, 1985, 228: 1315-7) 및 Clackson 외 (Nature, 1991, 352: 624-8)에 기재된 바와 같이, 사상 융합 파지에서 단쇄 Fv 도메인들 (scFv)의 발현과 제시 및 재조합 표적 항원\항원 또는 표적 항원-양성 세포에서의 패닝(panning)에 의한 표적 결합을 나타내는 scFv를 인코딩하는 파지 입자들의 농축에 의해 인간 항체 라이브러리로부터 분리될 수 있다. BCMA-결합 항체 단편을 분리하기 위해, 인간 CD3제타의 세포질 도메인 및 막경유 영역에 융합된, 세포 표면 고정된 인간 BCMA(1-54) 또는 시노몰구스 BCMA(1-53)를 안정하게 발현하는 재조합 인간 BCMA(1-54)-Fc, 시노몰구스 BCMA(1-53)-Fc 및 CHO 세포들을 후속 패닝 주기들에서 사용하여 결합 파지 입자들을 농축하게 할 수 있다. 이를 위해, 파지 입자를 용액에서 재조합 Fc-융합 항원과 함께, 예를 들어, 실온에서 2시간 동안 배양한 다음, 단백질 G-코팅된 비드로 포획하고 PBS-Tween 및 PBS에서 세척하여 결합되지 않은 파지를 제거한다. 결합된 파지는 글리신으로 용리된다. 표적 항원-발현 세포에서 결합 파지의 농축을 위해, 파지를 안정하게 형질감염된 CHO 세포와 함께, 예를 들어, 실온에서 1시간 동안 배양한 다음, 세포 배양 배지로 세척하고 결합된 파지를 글리신으로 용리시킨다. Fc 또는 형질감염되지 않은 CHO 세포들에 선택적으로 결합하는 항체 단편들을 인코딩하는 파지 입자들의 농축을 감소시키기 위하여, 파지 풀들을 관련없는 Fc-융합 항원 또는 표적 항원-음성 CHO 세포들과 함께 배양한다. 결합된 파지의 패닝 및 용리 각 라운드에 후속하여, 용리된 파지 입자를 사용하여 대장균 (XL1 Blue)을 감염시키고 파지 및 scFv-인코딩 DNA를 번식시킨다. 파지 패닝 및 농축해진 파지 클론들의 번식 반복 후, DNA는 대장균으로부터 분리되고, 후속하여 대장균에서 His-태그된 (서열 번호:59) scFv 항체 단편들을 생성하고 박테리아 주변세포질 추출물들을 준비하기 위한 표준 분자 생물학 기술들을 사용하여 박테리아 발현 벡터, 예컨대, pSKK2에 재클로닝된다. scFv 항체 단편을 포함하는 주변세포질 추출물은 표적 항원-결합을 평가하기 위해 ELISA 또는 유세포 분석과 같은 스크리닝 방법을 거치게 된다. 예를 들어, 재조합 인간 BCMA(1-54)-Fc 또는 시노몰구스 BCMA(1-53)-Fc는 표준 ELISA 마이크로 웰 플레이트에 코팅된 항-인간 Fc 항체에 의해 결합된 다음 박테리아 주변세포질 추출물과 함께 배양되고 광범위하게 세척된다. scFv 결합은 항-His-HRP 접합체를 사용하여 탐지된다. 세포-발현 BCMA에 대한 scFv 결합을 평가하기 위해, 박테리아 주변세포질 추출물을 세포 표면 고정된 인간 또는 시노몰구스 BCMA를 발현하는 재조합 CHO 세포와 함께 배양 한 다음, 유세포 분석에 의해 항-His-R-PE를 사용하여 결합된 scFv를 세척 및 탐지한다. 인간 및/또는 시노몰구스 BCMA 항원에 선택적으로 결합하는 scFv 항체 단편을 인코딩하는 플라스미드는 각각의 박테리아 클론으로부터 분리되고 DNA 시퀀싱에 의해 분석되어 scFv 인코딩 DNA 서열들이 수득된다. 예를 들면, 서열 번호:39에 제시된 아미노산 서열을 가지는 BCMA 항원-결합 모이어티가 수득되었는데, 여기서 VH는 서열 번호:37에 제시되고 VL은 서열 번호:38에 제시된다.
실시예 2: 다양한 항원-결합 단백질 스캐폴드 생성
2.1
scDb-mFc (도1 및 도2):
scDb-mFc는, 단량체이고 단량체 Fc 부분에 융합된 scDb 형태의 2가 CD16A 항원-결합 모이어티를 포함하는 항원-결합 단백질을 지칭한다. 2개의 CD16A 항원-결합 모이어티로 구성된 scDb는, 변이체 CH2-CH3 폴리펩티드 및 Fc 부분의 C-말단에 융합된 단일 표적 항원-결합 모이어티로 구성된 scFv로 구성된 Fc 부분의 N-말단에 융합되거나 (도 1) 또는 2개의 CD16A 항원-결합 모이어티로 구성된 scDb는 변이체 CH2-CH3 폴리펩티드 및 Fc 부분의 N-말단에 융합된 단일 표적 항원-결합 모이어티로 구성된 scFv로 구성된 Fc 부분의 C-말단에 융합된다 (도 2).
CHO 세포에서 scDb-mFc 항원-결합 단백질의 발현을 위해 분자의 코딩 서열을 포유류 발현 벡터 시스템에 클로닝하였다. 간단히 말해서, scFv에서 짧은 펩티드 링커를 인코딩하는 유전자 서열들 (서열 번호:16-18)에 의해 연결된 scFv 형태의 항-TAA (Tumor associated Antigen, 종양 관련 항원) Fv 도메인 및 항-CD16A Fv 도메인을 인코딩하는 유전자 서열들 (서열 번호: 1-13)을 Thermo Fisher Scientific/Invitrogen GeneArt (Regensburg, 독일)에 의해 합성하였다. 상이한 가변 도메인 및 침묵 점 돌연변이들을 내포하는 단량체 Fc 부분 (서열 번호 30)의 PCR-앰플리콘들을 상응하는 프라이머를 사용하여 생성하였다. 그 후 서로 다른 중복 DNA 단편들 및 선형화된 골격 벡터가 하나의 등온 반응에서 함께 결합된다. scDb-mFc 발현 구조체는 항체 분비를 촉진하기 위한 N-말단 신호 펩티드 및 항체 분비와 정제를 촉진하기 위한 Fc 부분 각각에 대한 코딩 서열을 포함하도록 설계되었다. 모든 구조체들의 서열들은 맞춤 제작된 프라이머를 사용하여 GATC (Kφln, 독일)에서 DNA 시퀀싱으로 확인되었다. scDb-mFc에 대한 발현 카세트는 항-CD16A 도메인이 다음과 같은 가능한 순서로 단량체 Fc 부분의 N-또는 C-말단에 배치되고 연결기 서열 (서열 번호: 19-22)을 통해 연결되도록 클로닝된다:
1.)
VL(CD16A)-L1-VH(CD16A)-L2-VL(CD16A)-L1-VH(CD16A)
2.)
VH(CD16A)-L1-VL(CD16A)-L3-VH(CD16A)-L1-VL(CD16A)
3.)
VL(CD16A)-L4-VL(CD16A)-L3-VH(CD16A)-L4-VH(CD16A)
4.)
VH(CD16A)-L4-VH(CD16A)-L2-VL(CD16A)-L4-VL(CD16A)
항원-결합 단백질 scDb-mFc_01, scDb-mFc_02, scDb-mFc_05 및 scDb-mFc_06의 구조에서 링커 L1에 서열 번호:16이 사용되며, 링커 L2에 서열 번호:17이 사용되고 L3에 서열 번호:18이 사용된다. 항원-결합 단백질 scDb-mFc_01, scDb-mFc_02, scDb-mFc_05 및 scDb-mFc_06의 구조에서 링커 L4에 서열 번호:60이 사용되며, 링커 L2에 서열 번호:17이 사용되고 L3에 서열 번호:18이 사용된다.
2.2
KiH-scDb-Fc (도3-6):
KiH-scDb-Fc 항원-결합 단백질은 이종이량체이고 이종이량체 (KiH) Fc 부분에 융합된 scDb 형태의 2가 CD16A 항원-결합 모이어티를 포함한다. 단일 표적 항원-결합 모이어티는 scFv에 의해 제공된다.
KiH-scDb-Fc를 인코딩하는 DNA 발현 구조는, 동일한 벡터들로부터 2개의 유전자 카세트들을 공동-발현하기 위하여 항-CD16A Fv 도메인들의 인코딩 서열들 (서열 번호: 1-13)을 Fc 침묵화 및 "놉-인투-홀" 점 돌연변이들이 있는 IgG1 불변 도메인 CH2 및 CH3 (서열 번호:31,32)를 포함하는 CMV-제어된 발현 카세트들을 내포하는 변형된 포유동물 발현 벡터에 클로닝함으로써 생성된다. "놉-인투-홀" 돌연변이는 이종이량체 3가 이중특이적 (도 3-5) 또는 4가 삼중 특이 적 (도 6) Fc 융합 구조체들의 생성을 가능하게 한다. 그 후, PCR 앰플리콘들은 상응하는 프라이머를 가지는 항-TAA (Tumor associated Antigen, 종양 관련 항원) Fv 도메인들을 인코딩하는 유전자 서열들로부터 생성된다. 생성된 중복 DNA-단편들은 관련 위치에서 공동-발현 벡터에 삽입된다. 가변 도메인 및 Fc 침묵 및 "놉-인투-홀" 점 돌연변이를 포함하는 불변 도메인을 인코딩하는 모든 필요한 유전자 서열들은 Thermo Fisher Scientific/Invitrogen GeneArt (Regensburg, 독일)에 의해 합성되었다.KiH-scDb-Fc 발현 구조체는 각각 항체 분비 및 정제를 촉진하기 위해 N-말단 신호 펩티드, C-태그 및/또는 His-태그 (6xHis)에 대한 코딩 서열들을 포함하도록 설계되었다. 모든 구조체들의 서열들은 맞춤 제작된 프라이머를 사용하여 GATC (Kφln, 독일)에서 DNA 시퀀싱으로 확인되었다. KiH-scDb-Fc 구조체들에 대한 발현 카세트들은 다음과 같은 가능한 순서로 CD16A 항원-결합 모이어티가 이종이량체 Fc 부분의 N-말단에 배치되고 연결기 (서열 번호:19-22) 및 힌지 (서열 번호:23) 또는 중간.힌지 (서열 번호:24)에 의해 연결되도록, 또는 이종이량체 Fc 부분의 C-말단에 배치되고 연결기 (서열 번호:19-22) 단독에 의해 연결되도록 클로닝된다:
1.)
VL(CD16A)-L1-VH(CD16A)-L2-VL(CD16A)-L1-VH(CD16A)
2.)
VH(CD16A)-L1-VL(CD16A)-L3-VH(CD16A)-L1-VL(CD16A)
3.)
VL(CD16A)-L4-VL(CD16A)-L3-VH(CD16A)-L4-VH(CD16A)
4.)
VH(CD16A)-L4-VH(CD16A)-L2-VL(CD16A)-L4-VL(CD16A)
링커 L1에 서열 번호: 16이 사용되고, 링커 L2에 서열 번호:17이 사용되고, 링커 L3에 서열 번호:18이 사용되고 그리고 링커 L4에 서열 번호:60이 사용된다.
이러한 항원-결합 단백질의 예는 N-으로부터 C-말단으로 다음 구조를 포함하는 KiH-scDb-Fc_08 및 KiH-scDb-Fc_12이다:
제 1 폴리펩티드 사슬 VL(CD16A)-VH(CD16A)-VL(CD16A)-VH(CD16A)-중간.힌지-CH2-CH3 및 제 2 폴리펩티드 사슬 힌지-CH2-CH3-VH(표적)-VL(표적) (도 3); 또는 제 1 폴리펩티드 사슬 중간.힌지-CH2-CH3-VL(CD16A)-VH(CD16A)-VL(CD16A)-VH(CD16A) 및 제 2 폴리펩티드 VH(표적)-VL(표적)-힌지-CH2-CH3 (도 5).
2.3
scDb-TriBs 또는 scDb-TriBs-scFv
scDb-TriB는 CD16A-, 표적 및 HSA 항원-결합 모이어티를 포함하는 이종이량체 Fab 단편인 삼중특이적 항원-결합 단백질이며, 여기서 항원-결합 모이어티는 Fab 단편의 C-말단에 융합된 2개의 scDb (도 7) 또는 2개의 CD16A 항원-결합 단백질들을 포함하는 scDb에 의해 제공되며 표적 항원-결합 모이어티를 포함하는 scFv는 Fab 단편의 C-말단에 융합된다 (도8).
상기 scDb-TriBs(-scFv)를 인코딩하는 DNA 발현 구조체는, 동일한 벡터로부터의 2개 유전자 카세트들이 융합된 그리고 이들을 공동-발현하기 위한, Fab 부분 단독 중쇄 및 경쇄 불변 도메인들 (서열 번호:33-35)을 포함하는 CMV-제어된 발현 카세트들을 내포하는 변형된 포유동물 발현 벡터에 항-HSA Fv 도메인들의 인코딩 서열들 (서열 번호:14,15)을 클로닝하여 생성된다. 그 후 상응하는 프라이머들을 가지는 항-TAA (Tumor associated Antigen, 종양 관련 항원) Fv 도메인들 및 항 CD16A Fv 도메인들 (서열 번호:1-13)을 인코딩하는 유전자 서열들로부터 PCR 앰플리콘들이 생성된다. 생성된 중복 DNA-단편들은 관련 위치에서 공동-발현 벡터에 삽입된다. 가변 도메인들 및 Fab 부분 단독 불변 도메인들을 인코딩하는 필요한 모든 유전자 서열들은 Thermo Fisher Scientific/Invitrogen GeneArt (Regensburg, 독일)에 의해 합성되었다.scDb-TriBs(-scFv) 발현 구조체는 각각 항체 분비 및 정제를 촉진하기 위해 N-말단 신호 펩티드, C-태그 및/또는 His-태그 (6xHis)에 대한 코딩 서열들을 포함하도록 설계되었다. 모든 구조체들의 서열들은 맞춤 제작된 프라이머를 사용하여 GATC (Kφln, 독일)에서 DNA 시퀀싱으로 확인되었다. scDb-TriBs (-scFv) 구조체들을 위한 발현 카세트는 항-CD16A 도메인이 다음과 같은 가능한 순서로 연결기 (서열 번호: 19-22)를 통해 Fab의 중쇄 또는 경쇄에 연결된 Fab의 CL 또는 CH1의 C-말단에 배치되도록 클로닝된다:
1.)
VL(CD16A)-L1-VH(CD16A)-L2-VL(CD16A)-L1-VH(CD16A)
2.)
VL(CD16A)-L1-VL(CD16A)-L2-VH(CD16A)-L1-VH(CD16A)
이러한 항원-결합 단백질의 예는 scDb-TriB-scFv_01이며 이는 N-으로부터 C-말단으로 다음 구조를 포함한다: 제 1 폴리펩티드 사슬 VH(HSA)-CH1-VL(CD16A)-VH(CD16A)-VL(CD16A)-VH(CD16A) 및 제 2 폴리펩티드 사슬 VL(HSA)-CL-VH(표적)-VL(표적) (도 8). 링커 L1에는 서열 번호: 16이 사용되고 링커 L2에는 서열 번호: 17 또는 서열 번호: 18이 사용된다.
2.4
Db-Fc (도9-10):
Db-Fc는, 동종이량체이고 동종이량체 Fc 부분 (CH2-CH3)의 N-말단에서 힌지에 융합된 Db 형태의 2가 CD16A 항원-결합 모이어티 및 상기 Fc 부분의 다른쪽 말단에 융합된 scFv 형태의 2개의 표적 항원-결합 모이어티를 포함하는, 항원-결합 단백질이다. CHO 세포에서 Db-Fc 항원-결합 단백질의 발현을 위해 분자의 코딩 서열을 포유류 발현 벡터 시스템에 클로닝하였다. 간단히 말해서, 짧은 펩티드 링커(서열 번호:16)에 의해 연결된 항-TAA (Tumor associated Antigen, 종양 관련 항원) Fv 도메인 및 항-CD16A Fv 도메인을 인코딩하는 유전자 서열들 (서열 번호 1-13)을 Thermo Fisher Scientific/Invitrogen GeneArt (Regensburg, 독일)에 의해 합성하였다. 상이한 가변 도메인 및 침묵 점 돌연변이들을 내포하는 Fc 부분 (서열 번호 29)의 PCR-앰플리콘들을 상응하는 프라이머를 사용하여 생성하였다. 그 후 서로 다른 중복 DNA 단편들 및 선형화된 골격 벡터가 하나의 등온 반응에서 결합된다. Db-Fc 발현 구조체는 항체 분비를 촉진하기 위해 N-말단 신호 펩티드에 대한 서열을 포함하도록 설계되었다. 모든 구조체들의 서열들은 맞춤 제작된 프라이머를 사용하여 GATC (Kφln, 독일)에서 DNA 시퀀싱으로 확인되었다. Db-Fc에 대한 발현 카세트는, 항-CD16A 도메인들이 연결기 (서열 번호: 19-22)에 의해 중간.힌지 (서열 번호:24)에 또는 연결기 (서열 번호: 19-22) 단독에 의해 CH3의 C-말단에 연결된 동종이량체 Fc 부분 (CH2-CH3)의 N-말단 또는 C-말단에 다음과 같은 순서로 배치되도록 클로닝된다:
1.)
VL(CD16A)-L1-VH(CD16A)
2.)
VH(CD16A)-L1-VL(CD16A)
이러한 항원-결합 단백질의 예는 N-으로부터 C-말단으로 다음 구조를 포함하는 Db-Fc_02 및 Db-Fc_04이며: VL (CD16A) -VH (CD16A)-중간.힌지-CH2-CH3-VH (표적 ) -VL (표적) (도 9); 또는 VH (표적) -VL (표적) -중간.힌지-CH2-CH3-VL (CD16A) -VH (CD16A) (도 10), 링커 L1에 서열 번호: 16이 사용된다.
2.5
Bi-scFv-Fc (도11-12):
Bi-scFv-Fc는 2개의 CD16A 항원-결합 모이어티 및 2개의 표적 항원-결합 모이어티를 포함하는 동종이량체 및 4가 항원-결합 단백질이며, 각각은 scFv 형태로 Fc 동종이량체에 융합된다.
CHO 세포에서 Bi-scFv-Fc 항원-결합 단백질의 발현을 위해 분자의 코딩 서열을 포유류 발현 벡터 시스템에 클로닝하였다. 간단히 말해서, 짧은 펩티드 링커 (서열 번호:17-18)에 의해 연결된 항-TAA (Tumor associated Antigen, 종양 관련 항원) Fv 도메인 및 항-CD16A Fv 도메인을 인코딩하는 유전자 서열들 (서열 번호 1-13)을 Thermo Fisher Scientific GeneArt (Regensburg, 독일)에 의해 합성하였다. 상이한 가변 도메인 및 침묵 점 돌연변이들을 내포하는 Fc 부분 (서열 번호 29) 또는 야생형 Fc 부분 (서열 번호:36)의 PCR-앰플리콘들을 상응하는 프라이머를 사용하여 생성하였다. 그 후 서로 다른 중복 DNA 단편들 및 선형화된 골격 벡터가 하나의 등온 반응에서 함께 결합된다. Bi-scFv-Fc 발현 구조체는 N-말단 신호 펩티드 및 항체 분비와 정제를 촉진하기 위한 Fc 부분 각각에 대한 코딩 서열을 포함하도록 설계되었다. 모든 구조체들의 서열들은 맞춤 제작된 프라이머를 사용하여 GATC (Kφln, 독일)에서 DNA 시퀀싱으로 확인되었다. Bi-scFv-Fc에 대한 발현 카세트는 항-CD16A 도메인이 다음과 같은 가능한 순서로 연결기 (서열 번호 19-22) 또는 힌지 (서열 번호 23)에 의해 연결된 Fc 부분의 N-말단에 또는 연결기 (서열 번호:19-22) 단독에 의해 CH3에 연결된 Fc 부분의 C-말단에 배치되도록 클로닝된다:
1.)
VL(CD16A)-L3-VH(CD16A)
2.)
VH(CD16A)-L2-VL(CD16A)
이러한 항원-결합 단백질의 예는 N-으로부터 C-말단으로 다음 구조를 포함하는 Bi-scFv-Fc_27 및 Bi-scFv-Fc_26이다: VL(CD16A)-VH(CD16A)-힌지-CH2-CH3-VH(표적)-VL(표적) (도 11); 또는 VH(표적)-VL(표적)-힌지-CH2-CH3-VL(CD16A)-VH(CD16A)(도12). 링커 L2에는 서열 번호: 17이 사용되고 링커 L3에는 서열 번호: 18이 사용된다.
2.6
scFv-IgAb (도 13):
scFv-IgAb 항원-결합 단백질은 scFv 형태의 2개의 CD16A 항원-결합 모이어티 및 IgG 항체를 포함하며, 여기서 scFv CD16A 항원-결합 모이어티 각각은 H 사슬 중 하나의 C-말단에 융합되고, 2개의 표적 항원-결합 모이어티는 IgG의 Fab 아암에서 각 Fv에 의해 제공된다.
상기 scFv-IgAb를 인코딩하는 DNA 발현 구조체는, 동일한 벡터로부터의 2개 유전자 카세트들 모두를 공동-발현하기 위해, 침묵 점-돌연변이 (서열 번호: 25,27-28) 또는 야생형 Fc 부분 (서열 번호:26-28)을 가지는 중쇄 및 경쇄 불변 도메인들을 포함하는 CMV-제어된 발현 카세트들을 내포하는 변형된 포유동물 발현 벡터에 항-TAA Fv 도메인들의 인코딩 서열들을 클로닝함으로써 생성된다. 그 후 짧은 펩티드 링커들 (서열 번호:17-18)에 의해 분리된 항-CD16A Fv 도메인들 (서열 번호:1-13)을 인코딩하는 유전자 서열들로부터 PCR 앰플리콘들이 상응하는 프라이머들과 함께 생성된다. 생성된 중복 DNA-단편은 관련 위치에서 공동-발현 벡터에 삽입된다. 가변 도메인 및 Fc 침묵 및 점 돌연변이를 포함하는 불변 도메인을 인코딩하는 모든 필요한 유전자 서열들은 Thermo Fisher Scientific/Invitrogen GeneArt (Regensburg, 독일)에 의해 합성되었다. scFv-IgAb 발현 구조체는 N-말단 신호 펩티드 및 항체 분비와 정제를 촉진하기 위한 Fc 부분 각각에 대한 코딩 서열을 포함하도록 설계되었다. 모든 구조체들의 서열들은 맞춤 제작된 프라이머를 사용하여 GATC (Kφln, 독일)에서 DNA 시퀀싱으로 확인되었다. scFv-IgAb에 대한 발현 카세트는 항-CD16A 도메인이 다음과 같은 가능한 순서로 Fc 부분의 C-말단에 배치되고 연결기 서열 (서열 번호: 19-22)을 통해 연결되도록 클로닝된다:
1.)
VL(CD16A)-L3-VH(CD16A)
2.)
VH(CD16A)-L2-VL(CD16A)
이러한 항원-결합 단백질의 예는 scFv-IgAb_30이며 이는 N-으로부터 C-말단으로 다음 구조를 포함한다:
제 1 폴리펩티드 사슬 VH(표적)-CH1-힌지-CH2-CH3-VL(CD16A)-VH(CD16A) 및 제 2 폴리펩티드 사슬 VL(표적)-CL (도 13). 링커 L2에는 서열 번호: 17이 사용되고 링커 L3에는 서열 번호: 18이 사용된다.
2.7
Bi-scFv-IgAb (도 14):
Bi-scFv-IgAb 항원-결합 단백질은 IgG 항체 및 이에 융합된 4개의 scFv 항원-결합 모이어티를 포함하며, 여기서 scFv 형태의 2개의 CD16A 항원-결합 모이어티 각각은 2개의 H 사슬 중 하나의 C-말단에 융합되고 2개의 표적 항원-결합 모이어티 각각은 2개의 CL 영역 중 하나의 C-말단에 융합된다.
상기 Bi-scFv-IgAb를 인코딩하는 DNA 발현 구조체는, 동일한 벡터로부터의 2개 유전자 카세트들 모두를 공동-발현하기 위해 침묵 점-돌연변이를 가지는 중쇄 및 경쇄 불변 도메인들 (서열 번호: 25,27-28)을 포함하는 CMV-제어된 발현 카세트들을 내포하는 변형된 포유동물 발현 벡터에 항-TAA Fv 도메인들의 인코딩 서열들을 클로닝함으로써 생성된다. 그 후 짧은 펩티드 링커들에 의해 분리된 항-CD16A 또는 표적 항원-결합 Fv 도메인들 (서열 번호:1-13)을 인코딩하는 유전자 서열들로부터 PCR 앰플리콘들이 상응하는 프라이머들과 함께 생성된다. 생성된 중복 DNA-단편들은 관련 위치에서 공동-발현 벡터에 삽입된다. 가변 도메인 및 Fc 침묵 및 점 돌연변이를 포함하는 불변 도메인을 인코딩하는 모든 필요한 유전자 서열들은 Thermo Fisher Scientific/Invitrogen GeneArt (Regensburg, 독일)에 의해 합성되었다. Bi-scFv-IgAb 발현 구조체는 N-말단 신호 펩티드 및 항체 분비와 정제를 촉진하기 위한 Fc 부분 각각에 대한 코딩 서열을 포함하도록 설계되었다. 모든 구조체들의 서열들은 맞춤 제작된 프라이머를 사용하여 GATC (Kφln, 독일)에서 DNA 시퀀싱으로 확인되었다. Bi-scFv-IgAb에 대한 발현 카세트는 항-CD16A 도메인이 다음과 같은 가능한 순서로 Fc 부분의 C-말단에 배치되고 연결기 서열 (서열 번호: 19-22)을 통해 연결되도록 클로닝된다:
1.)
VL(CD16A)-L3-VH(CD16A)
2.)
VH(CD16A)-L2-VL(CD16A)
이러한 항원-결합 단백질의 예는 Bi-scFv-IgAb_03이며 N-으로부터 C-말단으로 다음 구조를 포함한다:
제 1 폴리펩티드 사슬 VH(표적1)-CH1-힌지-CH2-CH3-VL(CD16A)-VH(CD16A) 및 제 2 폴리펩티드 사슬 VL(표적1)-CL-VL(표적2)-VH(표적2) (도 14). 링커 L2에는 서열 번호: 17이 사용되고 링커 L3에는 서열 번호: 18이 사용된다.
2.8
KiH-scFv-Fc (도15a 및 15b):
KiH-scFv-Fc 항원-결합 단백질은 이종이량체 (KiH) Fc 부분에 융합된 4 개의 scFv 항원-결합 모이어티를 포함하고, 여기서 2개의 CD16A 항원-결합 모이어티는 Fc 부분에 N-또는 C-말단으로 융합된다.
KiH-scFv-Fc를 인코딩하는 DNA 발현 구조는, 동일한 벡터들로부터의 2개 유전자 카세트들을 공동-발현하기 위해, Fc 침묵화 및 "놉-인투-홀" 점 돌연변이들을 가지는 gG1 불변 도메인 CH2 및 CH3 (서열 번호:31,32)를 포함하는 CMV-제어된 발현 카세트들을 내포하는 변형된 포유동물 발현 벡터에 항-CD16A Fv 도메인들의 인코딩 서열들 (서열 번호: 1-13)을 클로닝함으로써 생성된다. "놉-인투-홀" 돌연변이는 이중특이적 Fc 융합 구조체의 생성을 가능하게 한다. 그 후, PCR 앰플리콘들은 상응하는 프라이머를 가지는 항-TAA (Tumor associated Antigen, 종양 관련 항원) Fv 도메인들을 인코딩하는 유전자 서열들로부터 생성된다. 생성된 중복 DNA-단편들은 관련 위치에서 공동-발현 벡터에 삽입된다. 가변 도메인 및 Fc 침묵 및 "놉-인투-홀" 점 돌연변이를 포함하는 불변 도메인을 인코딩하는 모든 필요한 유전자 서열들은 Thermo Fisher Scientific/Invitrogen GeneArt (Regensburg, 독일)에 의해 합성되었다.KiH-scFv-Fc 발현 구조체는 각각 항체 분비 및 정제를 촉진하기 위해 N-말단 신호 펩티드, Fc 부분, C-태그 및 His-태그 (6xHis)에 대한 코딩 서열들을 포함하도록 설계되었다. 모든 구조체들의 서열들은 맞춤 제작된 프라이머를 사용하여 GATC (Kφln, 독일)에서 DNA 시퀀싱으로 확인되었다. KiH-scFv-Fc 구조체들에 대한 발현 카세트는 항-CD16A 도메인이 다음과 같은 가능한 순서로 연결기 (서열 번호 19-22) 또는 힌지 (서열 번호 23)에 의해 연결된 이종이량체 Fc 부분의 N-말단에 또는 연결기 (서열 번호:19-22) 단독에 의해 Fc 부분의 C-말단에 배치되도록 클로닝된다:
1.)
VL(CD16A)-L3-VH(CD16A)
2.)
VH(CD16A)-L2-VL(CD16A)
이러한 항원-결합 단백질의 예는 N-으로부터 C-말단으로 다음 구조를 포함하는 KiH-scFv-Fc_09 및 KiH-scFv-Fc_11이다:
제 1 폴리펩티드 사슬 VL(CD16A)-VH(CD16A)-힌지-CH2-CH3-VH(표적1)-VL(표적1) 및 제 2 폴리펩티드 사슬 VL(CD16A)-VH(CD16A)-힌지-CH2-CH3-VH(표적2)-VL(표적2) (도 15a); or first 폴리펩티드 사슬 VH(표적1)-VL(표적1)-힌지-CH2-CH3-VL(CD16A)-VH(CD16A) 및 제 2 폴리펩티드 사슬 VH(표적2)-VL(표적2)-힌지-CH2-CH3-VL(CD16A)-VH(CD16A) (도 15b). 링커 L2에는 서열 번호: 17이 사용되고 링커 L3에는 서열 번호: 18이 사용된다.
실시예 3: 안정한 CHO 세포 풀을 사용한 NK 세포 관여 항체 형태의 생성
숙주 세포 배양
CHO-K1 중국 햄스터 난소 세포들 (ATCC, CCL-61) (Kao and Puck, 1968)의 유도체인 Flp-In CHO 세포들 (Life Technologies)을, L-글루타민, 10% FCS 및 100 μg/ml 제오신이 보충된 Ham의 F-12 영양소 믹스에서 배양했다. 부착 세포를 0.25% 트립신-EDTA로 분리하고 Life Technologies에서 제공하는 표준 세포 배양 프로토콜에 따라 계대배양했다.
현탁액에서의 성장에 적응시키기 위해, 세포를 조직 배양 플라스크에서 분리하고 37°C, 5% CO2 및 120rpm의 진탕 플라스크에서 후속 배양하기 위해 무-혈청 HyClone CDM4 CHO 배지에 두었다. 현탁액-적응된 Flp-In CHO 숙주 세포들의 배양을 위한 표준 배지는 L-글루타민, HT 보충제, 페니실린/스트렙토마이신 및 100 μg/ml 제오신이 보충된 HyClone CDM4 CHO였다. 현탁액-적응된 세포를 10% DMSO가 포함된 배지에서 냉동보존하고 MycoAlert 마이코플라스마 탐지 키트 (Lonza)를 사용하여 마이코플라스마에 대해 음성으로 테스트했다.
안정적으로 형질감염된 세포 풀들의 생성
분비된 재조합 항체, Fc 융합 구조체 또는 비교 항체들을 안정적으로 발현하는 재조합 Flp-In CHO 세포주들이 현탁액-적응된 숙주 세포의 형질감염에 의해 생성되었다. 이를 위해, 관심 단백질 (pcDNA5-FRT) 및 Flp 재조합효소 (pOG44, Life Technologies)를 인코딩하는 발현 플라스미드 (2.5μg)와 폴리에틸렌이민 (PEI)을 사용하여 공동 형질감염하기 하루 전에 제오신이 없는 표준 배지에 세포들을 넣었다. 간단히 말해서, 벡터 DNA와 형질감염 시약은 총 100μL의 OptiMEM I 배지에서 1:3 (μg/μg)의 DNA:PEI 비율로 혼합하고 1 ml의 CHO-S-SFMII 배지 (Life Technologies)에 현탁된 2E+6 Flp-In CHO 세포에 첨가하기 전에 10 분 동안 배양했다. 24-48 시간 배양 후, CHO-S-SFMII 배지에서 0.2E+6 생존 세포/mL의 밀도로 배양물을 희석한 후 6-7 μg/mL 퓨로마이신 디하이드로클로라이드를 첨가하여 안정적하게 형질감염된 세포들에 대한 선택을 시작했다. Flp 재조합효소는 부위 특이적 DNA 재조합을 통해 통합된 FRT 부위의 게놈에 Flp-In 발현 구조체의 삽입을 매개한다 (O 'Gorman et al 1991). 선택하는 동안 생존 세포 밀도를 일주일에 두 번 측정하고, 세포를 원심분리하고 0.2E+6 생존 세포/mL의 최대 밀도로 신선한 선택 배지에 재현탁하였다. 재조합 단백질 생성물을 안정적으로 발현하는 세포 풀들은 세포가 진탕 플라스크의 표준 배양 배지로 옮겨졌던 시점인 선택 2-3주 후 회수되었다. 재조합 분비 단백질들의 발현은 Criterion Stain-Free (Bio-Rad) 기술을 사용하여 세포 배양 상청액들을 단백질 겔 전기영동하여 확인되었다 (아래 참고). 안정한 세포 풀들은 7.5% DMSO 함유 배지에서 냉동보존되었다.
유가식 CHO 세포 현탁액 배양에서 재조합 단백질의 생성
재조합 단백질은 세포 배양 상청액으로의 분비에 의해 안정적으로 형질감염된 CHO 세포의 10-또는 11-일 유가식 배양에서 생성되었다. 이를 위해 재조합 항체, Fc 융합 항원 또는 비교 항체를 안정적으로 발현하는 세포를 기체 투과성 캡 (Corning)이 있는 폴리카보네이트 삼각플라스크의 표준 배양 배지에 6E+5개 세포/mL의 시작 밀도로 씨딩(seed) 하고 140rpm에서 교반하면서 37°C 및 5% CO2에서 배양했다. 유가식 배양 동안 배지는 0일차 (시작일)에 40mL/L ActiCHO 공급물 A (GE Healthcare) 및 4mL/L ActiCHO 공급물 B (GE Healthcare)로 보충되었고 3일, 5일, 및 7일차에는 두 배의 양으로 보충되었다. 세포 배양 상청액들은 전형적으로 >75%의 배양 생존력에서 10 또는 11일 후에 수확되었다. 공급 전 격일로 생성 배양물들로부터 샘플을 수집하고 세포 밀도 및 생존력을 평가했다. 수확 당일, 세포 배양 상청액들은 추가 사용 전에 원심 분리 및 Millipore Express PLUS 막 필터 (Millipore)를 사용한 진공 여과 (0.22 μm)에 의해 정제되었다.
발현 역가 정량:
세포 배양 상청액 (CSS)의 단백질 발현 역가 및 생성물 무결성은 생성 배양 5, 7 및 10 또는 11일차에 SDS-PAGE로 분석된다. 샘플들은 4-20% Criterion TGX Precast SDS Page Gel (Biorad)에 부하하기 전에 SDS PAGE 샘플 완충액과 혼합된다. 총 단백질은 Criterion Stain-free 분자 이미징 시스템 (Biorad)을 사용하여 겔에서 시각화된다. 생성물 역가는 알려진 농도의 참고 항체와 비교하여 반-정량적으로 결정된다.
항원-결합 단백질의 정제
1. Fc 부분을 포함하는 항원-결합 단백질 (실시예 2에 기재된 scDb-mFc, Db-Fc, Bi-scFv-Fc, Bi-scFv-IgAb, scFv-Fc, scFv-IgAb)
단백질 A 및 분취 SEC를 포함하는 2 단계 절차로 정제된 CHO 세포 배양 상청액으로부터 표적 단백질을 정제하였다. 단백질 A의 경우 정제된 상청액을 HiTrap MabSelectSuRe 컬럼 (GE-Healthcare)에 부하하였다. 인산염 완충 식염수 pH 7.4 및 10mM 인산 나트륨 pH 7.0으로 세척 한 후, 50mM 아세트산 나트륨 pH 3.5 및 10mM 글리신/HCL pH 2.0을 사용하여 2 단계 구배로 단백질을 용리시켰다. 분획들의 순도는 SE-HPLC 및 SDS-PAGE를 사용하여 분석되었다. 허용가능한 순도를 나타내는 분획들을 모으고 Superdex 200 프렙용 컬럼 (GE-Healthcare)을 사용하여 분취 겔 여과 처리하였다. 정제된 표적 분자를 포함하는 용리액 분획들을 모으고 10mM 아세트산 나트륨, 4.5% 소르비톨 pH 5.0을 포함하는 Sephadex G-25 컬럼을 사용하여 완충액 교환을 실시하고, 한외여과로 약. 1mg/ml의 일반적인 농도로 농축시켰다. 이러한 구조체들의 전형적인 순도 (SE-HPLC로 측정)는 87,6% 내지 99,8% 범위였으며 균질성 (비-환원 SDS-PAGE에서)은 58,4% 내지 100%였다.
단백질 L, IMAC 및 분취 SEC를 포함하는 3 단계 절차로 정제된 CHO 세포 배양 상청액으로부터 표적 단백질을 정제하였다. 단백질 L의 경우 정제된 상청액을 HiTrap 단백질 L 컬럼 (GE-Healthcare)에 부하하였다. 인산염 완충 식염수 pH 7.4 및 10mM 인산 나트륨 pH 7.0으로 세척 한 후, 10mM 글리신/HCL pH 3.0 및 10mM 글리신/HCL pH 2.0을 사용하여 2 단계 구배로 단백질을 용리시켰다. 분획들의 순도는 SE-HPLC 및 SDS-PAGE를 사용하여 분석되었다. 허용가능한 순도를 나타내는 분획들을 모으고 추가 IMAC 정제를 실시했다. 따라서 샘플을 평형화 완충액 (50mM Tris/HCL, 150mM 염화 나트륨 pH 7.5)로 희석 (1:4)하고 HisTrap FF 컬럼 (GE Healthcare)에 부하하였다. 평형화 완충액 (50mM Tris/HCL, 150mM 염화나트륨 pH 7.5)으로 세척 한 후 단백질을 7%/30%/100% 용리 완충액 (50mM Tris/HCL, 0.4M 아르기닌, 500mM 이미다졸 pH7.5)으로 3-단계 구배로 용리하였다. 분획들의 순도는 SE-HPLC 및 SDS-PAGE를 사용하여 분석되었다. 허용가능한 순도를 나타내는 분획들을 모으고 Superdex 200 프렙용 컬럼 (GE-Healthcare)을 사용하여 분취 겔 여과 처리하였다. 정제된 표적 분자를 포함하는 용리액 분획들을 모으고 10mM 아세트산 나트륨, 4.5% 소르비톨 pH 5.0을 포함하는 Sephadex G-25 컬럼을 사용하여 완충액 교환을 실시하고, 한외여과로 약. 1mg/ml의 일반적인 농도로 농축시켰다. 이러한 구조체들의 전형적인 순도 (SE-HPLC로 측정)는 95,9% 내지 99,8% 범위였으며 균질성 (비-환원 SDS-PAGE에서)은 72,2% 내지 99,0%였다.
3) 제 1 폴리펩티드에 C-태그를 그리고 제 2 폴리펩티드에 His-태그를 내포하는 항원-결합 단백질 분자 KiH-scFv-Fc 및 KiH-scDb-Fc
C-태그 친화성 크로마토그래피, IMAC 및 분취 SEC를 포함하는 3 단계 절차로 정제된 CHO 세포 배양 상청액으로부터 표적 단백질을 정제하였다. C-태그 친화성 크로마토그래피의 경우, 정제된 상청액을 CaptureSelect C-태그 XL 컬럼 (Thermo Scientific)에 부하하였다. 인산염 완충 식염수 pH 7.4로 세척 한 후 단백질을 20mM 구연산 나트륨 pH 3.0으로 용리시켰다. 분획들의 순도는 SE-HPLC 및 SDS-PAGE를 사용하여 분석되었다. 허용가능한 순도를 나타내는 분획들을 모으고 추가 IMAC 정제를 실시했다. 따라서 샘플을 평형화 완충액 (50mM Tris/HCL, 150mM 염화 나트륨 pH 7.5)로 희석 (1:4)하고 HisTrap FF 컬럼 (GE Healthcare)에 부하하였다. 평형화 완충액 (50mM Tris/HCL, 150mM 염화나트륨 pH 7.5)으로 세척 한 후 단백질을 7%/30%/100% 용리 완충액 (50mM Tris/HCL, 0.4M 아르기닌, 500mM 이미다졸 pH7.5)으로 3-단계 구배로 용리하였다. 분획들의 순도는 SE-HPLC 및 SDS-PAGE를 사용하여 분석되었다. 허용가능한 순도를 나타내는 분획들을 모으고 Superdex 200 프렙용 컬럼 (GE-Healthcare)을 사용하여 분취 겔 여과 처리하였다. 정제된 표적 분자를 포함하는 용리액 분획들을 모으고 10mM 아세트산 나트륨, 4.5% 소르비톨 pH 5.0을 포함하는 Sephadex G-25 컬럼을 사용하여 완충액 교환을 실시하고, 한외여과로 약. 1mg/ml의 일반적인 농도로 농축시켰다. 이러한 구조체들의 전형적인 순도 (SE-HPLC로 측정)는 94,8% 내지 99,0% 범위였으며 균질성 (비-환원 SDS-PAGE에서)은 86,8% 내지 100%였다.
4) scDb-트리바디
IMAC 및 분취 SEC를 포함하는 2 단계 절차로 정제된 CHO 세포 배양 상청액으로부터 단백질을 정제하였다. IMAC의 경우 정화된 상청액과 5mM 이미다졸 pH7.0을 HisTrap FF 컬럼 (GE Healthcare)에 부하하였다. 평형화 완충액 (50mM Tris/HCL, 150mM 염화나트륨 pH 7.5)으로 세척 한 후 단백질을 7%/30%/100% 용리 완충액 (50mM Tris/HCL, 0.4M 아르기닌, 500mM 이미다졸 pH7.5)으로 3-단계 구배로 용리하였다. 분획들의 순도는 SE-HPLC 및 SDS-PAGE를 사용하여 분석되었다. 허용가능한 순도를 나타내는 분획들을 모으고 Superdex 200 프렙용 컬럼 (GE-Healthcare)을 사용하여 분취 겔 여과 처리하였다. 정제된 표적 분자를 포함하는 용리액 분획들을 모으고 10mM 아세트산 나트륨, 4.5% 소르비톨 pH 5.0을 포함하는 Sephadex G-25 컬럼을 사용하여 완충액 교환을 실시하고, 한외여과로 약. 1mg/ml의 일반적인 농도로 농축시켰다. 이러한 구조체들의 전형적인 순도 (SE-HPLC로 측정)는 95,1% 내지 100% 범위였으며 균질성 (비-환원 SDS-PAGE에서)은 85,8% 보다 높았다.
a)
scDb-트리바디_09-10
Fab/람다 친화성 크로마토그래피 및 분취 SEC를 포함하는 2 단계 절차로 정제된 CHO 세포 배양 상청액으로부터 단백질을 정제하였다. Fab/람다 친화성 크로마토그래피의 경우 정제된 상청액을 Fab 선택 람다 컬럼 (GE Healthcare)에 부하하였다. 인산염 완충 식염수 pH 7.4로 세척 한 후 단백질을 100mM 아세트산 나트륨 pH 3.5로 용리시켰다. 분획들의 순도는 SE-HPLC 및 SDS-PAGE를 사용하여 분석되었다. 허용가능한 순도를 나타내는 분획들을 모으고 Superdex 200 프렙용 컬럼 (Ge-Healthcare)을 사용하여 분취 겔 여과 처리하였다. 정제된 표적 분자를 포함하는 용리액 분획들을 모으고 10mM 아세트산 나트륨, 4.5% 소르비톨 pH 5.0을 포함하는 Sephadex G-25 컬럼을 사용하여 완충액 교환을 실시하고, 한외여과로 약. 1mg/ml의 일반적인 농도로 농축시켰다. 이러한 구조체들의 전형적인 순도 (SE-HPLC로 측정)는 94,8% 보다 높았으며 균질성 (비-환원 SDS-PAGE에서)은 92,7% 보다 높았다.
단백질 분석
최종 샘플의 균질성은 환원 및 비-환원 조건 하에서 SDS-PAGE에 의해 평가되었다. 샘플을 비-환원 2x SDS PAGE 샘플 완충액 또는 환원제로서 디티오트레이톨 (DTT)을 함유하는 환원 2x SDS-Page 샘플 완충액과 혼합하였다. 모든 샘플은 4-20% Criterion TGX Precast SDS Page Gel에 부하하기 전에 95°C에서 5분 동안 가열되었다. 2 μg의 정제된 단백질 샘플들을 부하하였다. 겔에서 단백질을 분리하기 위해 SDS-PAGE를 1x Tris/글리신/SDS 완충액에서 300V에서 약 22분 동안 실시하였다. 총 단백질은 Criterion Stain-free 분자 이미징 시스템 (Biorad)을 사용하여 겔에서 시각화되었다. 분자량 마커로서 Page 룰러 비염색 단백질 사다리를 사용하였다. 비-환원 SDS-PAGE에서 생성물 밴드의 상대적 신호 강도를 가능한 고 또는 저 분자량 종들과 비교하였다.
단백질 제제의 순도는 Superdex 200 Increase 10/300GL 컬럼 (GE-Healthcare)을 사용하여 분석 SE-HPLC로 평가되었다.
정제된 단백질은 추가 사용 전까지 -80°C에서 분취량으로 보관되었다.
실시예 4: 37°C에서 일차 인간 NK 세포 또는 ELISA에서 재조합 인간 CD16A 가용성 항원에 대한 CD16A 항원-결합 단백질의 결합
방법
버피 코트에서 PBMC 분리 및 인간 NK 세포 농축
PBMC는 밀도 구배 원심 분리에 의해 버피 코트 (German Red Cross, Mannheim, 독일)로부터 분리되었다. 버피 코트 샘플을 2-3 배 부피의 PBS (Invitrogen, 카탈로그번호: 14190-169)로 희석하고, Lymphoprep (Stem Cell Technologies, 카탈로그번호: 07861)의 쿠션 위에 적층하고 25분 동안 800 xg에서 브레이크없이 실온에서 원심분리했다. 경계면에 위치한 PBMC를 수집하고 PBS로 3회 세척 한 후 10% FCS가 보충된 완전 RPMI 1640 배지에서 밤새 자극없이 배양했다. NK 세포들의 농축을 위해, 제조업체의 지침에 따라 PBMC들을 하룻밤 배양물들로부터 수집하고 감작되지 않은 인간 NK 세포들의 면역자성 분리를 위한 EasySep™ 인간 NK 세포 농축 키트 (Stem Cell Technologies, 카탈로그번호: 19955) 및 Big Easy EasySep™ Magnet (Stem Cell Technologies, 카탈로그번호: 18001)를 사용한 1 주기의 음성 선택에 사용하였다.
세포 결합 분석 및 유세포 분석
농축된 인간 NK 세포의 분취량을 2% 열 불활성화 FCS (Invitrogen, 카탈로그번호: 10270-106), 0.1% 아지드화 나트륨 (Roth, Karlsruhe, 독일, 카탈로그번호: A1430.0100)를 함유하는 FACS 완충액 (PBS, Invitrogen, 카탈로그번호: 14190-169)에서 지시된 CD16A AAF 구조체들의 100μL 연속 희석액과 함께 37°C에서 45분 동안 배양하였다. FACS 완충액으로 반복 세척 한 후, 15 μg/mL FITC-접합 염소 항-인간 IgG (Dianova, 카탈로그번호: 109-095-098)로 세포-결합 항체를 탐지하였다. 마지막 염색 단계 후, 세포를 다시 세척하고 죽은 세포를 배제하기 위해 2 μg/mL 프로피듐 아이오다이드 (PI) (Sigma, 카탈로그번호: P4170)를 포함하는 0.2 mL의 FACS 완충액에 재현탁시켰다. 2-5 x 103개의 살아있는 세포들의 형광을 Millipore Guava EasyCyte 유세포 분석기 (Merck Millipore, Schwalbach, 독일)를 사용하여 측정하였다. 세포 샘플들의 평균 형광 강도는 Incyte 소프트웨어 (Merck Millipore, Schwalbach, 독일)를 사용하여 계산되었다. 2 차 및 3 차 시약으로만 염색된 세포들의 형광 강도 값을 뺀 후,이 값을 GraphPad Prism 소프트웨어 (Windows용 GraphPad Prism 버전 6.00, GraphPad Software, 미국 캘리포니아 La Jolla)를 사용하는 비선형 회귀 분석에 사용했다. KD 계산을 위해 단일-부위 결합 (쌍곡선) 방정식을 사용했다.
ELISA에서 CD16A 가용성 항원-결합 분석
96-웰 ELISA 플레이트 (Immuno MaxiSorp; Nunc)를 100mM 탄산염-중탄산염 완충액에서 재조합 NK 세포 관여 항체 형태 또는 대조군 항체로 4°C에서 밤새 코팅하였다. 분자량에 따라 항체는 약 20 nM의 몰 농도에 해당하는 2,0 - 5,0 μg/mL의 농도로 코팅되었다. PBS에 용해된 3% (w/v) 탈지 분유 (Merck)를 이용한 차단 단계 후, 0.3% (w/v) 탈지 분유 분말을 포함하는 PBS에서 인간 IgG1 Fc 부분에 융합된 비오티닐화 재조합 인간 CD16A (48R-158V)의 연속 희석액을 실온에서 1.5 시간 동안 플레이트에서 배양하였다. 웰당 0.1% (v/v) Tween 20을 함유하는 PBS 300 μL로 3회 세척 한 후, 플레이트를 1:10000 희석으로 탐지 접합체 스트렙타비딘-HRP (Roche)와 실온에서 1 시간 동안 배양했다. 웰당 0.1% (v/v) Tween 20을 함유하는 PBS 300 μL로 3회 세척 한 후, 플레이트를 발색이 명확하게 보일 때까지 테트라메틸벤지딘 (TMB) 기질 (Seramun)과 함께 배양했다. 웰당 100 μL의 0.5 M H2SO4를 첨가하여 반응을 중단시켰다. 다중라벨 플레이트 판독기 (Victor, Perkin Elmer)를 사용하여 450 nm에서 흡광도를 측정하였다. 흡광도 값들은 비선형 회귀, S형형 용량-반응 (가변 기울기), 최소 제곱 (일반) 핏을 사용하여 GraphPad Prism 버전 6.07 (GraphPad Software, 미국 캘리포니아 La Jolla)로 플롯 및 분석되었다.
결과
제시된 CD16A 항원-결합 단백질의 명백한 결합 친화성은 적어도 2회의 독립 실험에서 37°C에서 일차 인간 NK 세포에서 결정되었다. 또한, 가용성 CD16A에 결합하는 CD16A 항원-결합 단백질의 능력은 ELISA에서 분석되었다. 두 방법 모두 CD16A 항원-결합 단백질이 CD16A에 특이적 결합을 나타냄을 입증한다. 2가 CD16 결합으로 인해 높은 친화성이 수득된다. NK 세포 결합에서 측정된 KD 값과 ELISA에서 측정된 EC50 값의 절대 값들의 차이는 다른 방법론, 시약 및 분석 설정에 의한 것이다. 결과를 표 2에 나타낸다.
표 2 -37°C에서 일차 인간 NK 세포들에 대한 CD16A 항체 구조체들의 겉보기 친화성 (독립 실험들의 평균 KD가 제시된다) 또는 ELISA로 분석된 코팅된 항체 구조체들에 대한 CD16A 항원의 겉보기 결합 (EC50 값들이 제시됨).
표 3: 제시된 종양 세포주들의 항체-매개 용해는 제시된 항체 구조체들의 연속 희석물들의 존재하에서 그리고 3시간 또는 4시간 분석 배양하에서 이펙서 세포들로서 제시된 E:T 비율 (5:1 또는 2:1)의 농축된 인간 NK 세포들을 사용하여 칼세인-방출 분석에서 평가되었다.
실시예 6:
CD16A 항원-결합 단백질에 의한 NK-NK 용해의 평가
방법:
버피 코트에서 PBMC 분리 및 인간 NK 세포 농축
PBMC는 밀도 구배 원심 분리에 의해 버피 코트 (German Red Cross, Mannheim, 독일)로부터 분리되었다. 버피 코트 샘플을 2-3 배 부피의 PBS (Invitrogen, 카탈로그번호: 14190-169)로 희석하고, Lymphoprep (Stem Cell Technologies, 카탈로그번호: 07861)의 쿠션 위에 적층하고 25분 동안 800 xg에서 브레이크없이 실온에서 원심분리했다. 경계면에 위치한 PBMC를 수집하고 PBS로 3회 세척 한 후 10% FCS가 보충된 완전 RPMI 1640 배지에서 밤새 자극없이 배양했다. NK 세포들의 농축을 위해, 제조업체의 지침에 따라 PBMC들을 하룻밤 배양물들로부터 수집하고 감작되지 않은 인간 NK 세포들의 면역자성 분리를 위한 EasySep™ 인간 NK 세포 농축 키트 (Stem Cell Technologies, 카탈로그번호: 19055) 및 Big Easy EasySep™ Magnet (Stem Cell Technologies, 카탈로그번호: 18001)를 사용한 1 주기의 음성 선택에 사용하였다.
4시간 칼세인-방출 세포독성 분석
NK-NK 세포 용해를 평가하기 위한 칼세인-방출 세포독성 분석을 위해, 농축된 비-활성화 NK 세포들의 절반을 FCS가없는 RPMI 1640 배지로 세척하고 10μM 칼세인 AM (Invitrogen/Molecular Probes, 카탈로그번호: C3100MP)으로 30분 동안 FCS없는 RPMI 배지에서 37°C에서 표지하였다. 부드럽게 세척한 후 표지된 세포들을 완전 RPMI 배지 (10% 열-불활성화 FCS, 4mM L-글루타민, 100U/mL 페니실린 G 소듐, 100μg/mL 스트렙토마이신 설페이트로 보충된 RPMI 1640 배지)에 재현탁시켰다. 이후 5x104개의 표적 세포들을 둥근 바닥 96-웰 마이크로플레이트의 개개 웰들에 1:1 E:T 비율의 동일한 공여체의 NK 세포 및 제시된 항체와 함께 전체 200 μL/웰 부피로 2회 반복하여 씨딩하였다. 항체의 부재하에 이펙터에 의한 자발적 방출, 최대 방출 및 표적의 사멸은 각 플레이트에서 4회 반복하여 결정되었다.
200 x g에서 2분 동안 원심분리 후 분석은 5% CO2로 가습 된 대기에서 37°C에서 4시간 동안 배양되었다. 배양 종료 15분 전에 RPMI 배지에서 20 μL의 10% Triton X-100을 표적 세포들을 포함하는 웰들에 첨가하였다. 20 μL RPMI 배지를 다른 모든 웰들에 첨가하였다. 500g에서 5분간 추가 원심분리 후 100μL 세포 배양 상청액을 각 웰로부터 수확하고 방출된 칼세인의 형광을 형광 플레이트 판독기 (Victor 3, Perkin Elmer)를 사용하여 520 nm에서 측정했다. 측정된 계수를 기반으로 비 세포 용해는 다음 공식에 따라 계산되었다: [형광 (샘플) - 형광 (자발)]/[형광 (최대) - 형광 (자발)] x 100%. 형광 (자발)은 이펙터 세포와 항체의 부재하에서 표적 세포의 형광 계수를 나타내고 형광 (최대)은 Triton X-100을 추가하여 유도된 총 세포 용해를 나타낸다. S형 용량 반응 곡선 및 EC50 값은 GraphPad Prism 소프트웨어 (Windows 용 GraphPad Prism 버전 6.00, GraphPad Software, 미국 캘리포니아 La Jolla)를 사용하여 비선형 회귀/4-매개변수 로지스틱 적합에 의해 계산되었으며, EC50 [pM] 및 E최대 [%] 값을 결정하기 위해 사용되었다.
CD16A 항원-결합 단백질은 다라투무맙이 50% 이상의 NK 용해를 유도한 분석에서 최대 30 μg/mL의 항체 농도에서 측정가능한 용해가 없거나 10% 미만의 최소 일 때 NK-NK 용해 유도에 대해 음성으로 간주된다.
결과:
각각의 항원-결합 단백질은 NK 세포-매개 NK 용해에 대해 적어도 2개의 독립적인 4시간 칼세인-방출 세포독성 분석에서 테스트되었다.
결과는 표 4에 요약하였으며 도 17A-17N은 CD16A 항원-결합 단백질에 의해 유도된 NK-NK 용해에 대한 역가 (EC50) 및 효능 (E최대)이 NK 세포에서 재조합 CD16A 항원 또는 CD16A에 대한 이러한 단백질의 명백한 결합 친화성과 상관관계가 없음을 명확하게 보여준다 (표 2에 요약됨). 또한, 항원-양성 종양 표적 세포의 용해를 위한 CD16A 항원-결합 단백질의 역가 (EC50)는 NK-NK 용해 매개에서의 역가와 관련이 없다. 이러한 발견으로부터 NK-NK 용해를 매개하는 성향은 항-CD16A Fv 도메인 그 자체의 특성이 아니며 이들의 겉보기 친화성의 기능이 아니라 형태의 특징적인 특성, 특히, 주어진 CD16A 항원-결합 단백질의 가변 중쇄 및 경쇄 세그먼트의 도메인 순서인 것으로 결론지을 수 있다.
표 4: 항체-매개 NK-NK 세포 용해는 제시된 항체 구조체들의 연속 희석물의 존재하에서 1:1의 E:T 비율로 칼세인-표지된 NK 세포들을 표적 세포들로 그리고 동일한 공여체의 비-표지된 NK 세포들을 이펙터 세포들로 사용하는 4 h 칼세인-방출 분석에서 평가되었다.
표 4는, Fc 부분 또는 Fab 영역에 융합된 scDb, Db 또는 scFv 형태의 2개의 CD16A 항원-결합 모이어티를 포함하는 항원-결합 단백질들은, 가변 영역들이 N-으로부터 C-말단으로 scDb VL-VH-VL-VH 또는 scDb VL-VL-VH-VH로, Db VL-VH 또는 scFv VL-VH로 배열되는 경우, NK-NK 용해를 유도하지 않음을 보여준다. 따라서, 상기 결과는 NK-NK 용해가 EC50 및 E최대에 의해 정의된 바와 같이 NK 세포상의 재조합 CD16A 또는 CD16A에 대한 이들 항원-결합 모이어티의 겉보기 결합 친화성과 무관함을 입증한다. 또한, NK-NK 용해는 표적 항원-결합 도메인과도 무관하다.
실시예 7 - 재지시된 최적화 세포 사멸 (ROCK
®
): 매우 다목적의 다중특이적인 선천 면역 관여 목적에 부합하는 항체 플랫폼
요약
ROCK® (재지시된 최적화 세포 사멸) 플랫폼을 기반으로 고유한 특성을 가진 면역 세포 관여항체 포트폴리오가 개발되었다. 이러한 새로운 모듈식 플랫폼은 고전적인 단일클론 항체 및 기타 관여항체 개념에 비해 NK 세포 관여의 이점을 제공한다. 분자 설계, 결합 친화성, 면역 이펙터 세포의 활성화 및 PK 특성이 고려되었다. ROCK® 플랫폼은 선천 및 적응 면역의 활성화를 목표로 하는 새로운 항체를 생성하는데 사용될 수 있다.
본 실시예에서, 선천 및 적응 면역의 활성화를 목적으로 하는 새로운 클래스의 NK 세포 동원 항체들을 생성하기 위한 고유한 항-CD16A 결합 도메인이 구비된 광범위한 다양한 형태들을 포함하는 "재지시된 최적화 세포 사멸" (ROCK®) 플랫폼이라 불리는 새롭고 완전한 모듈식 플랫폼이 제공된다.
재료 & 방법
ROCK® 재조합 항체, 대조 및 항원 변이체 생성
다양한 재조합 단백질 (항원, 항체, 대조)에 대한 유전자 서열들은 Thermo Fisher Scientific/Invitrogen GeneArt (Regensburg, 독일)에 의해 합성되거나 PCR에 의해 유도되었다. 이들 재조합 단백질을 인코딩하는 발현 벡터는 표준 분자 생물학 기술을 사용하여 포유류 발현 벡터 pcDNA5/FRT (Life Technologies) 또는 이의 변형된 형태에 각각의 서열 요소들을 클로닝함으로써 생성되었다. 가용성 재조합 항원 변이체는 단량체 Fc에 대한 ECD 서열의 융합 단백질로서 제작되었다 (Ying 외, J Biol Chem 2012; 287:19399-408). 세포 표면 고정된 항원 변이체의 발현을 위해, ECD 서열들은 인간 EGFR의 막경유 도메인에 융합되거나 (Wang 외, Blood 2011; 118:1255-63) GPI-고정부에 대한 번역후 가공 및 지질화를 위한 전장 프로펩티드 서열과 함께 인간 CD16B 내인성 서열을 사용하여 GPI를 통해 고정되었다. 일부 발현 구조체들에서, 본래 벡터는 2개의 항체 사슬의 공동 발현을 위한 2개의 CMV-프로모터 제어된 발현 카세트들을 포함하도록 변형되었다. 포유류 발현 벡터의 추가 변형은 하이그로마이신 내성을 퓨로마이신 내성 유전자로 대체하는 것이었다. 발현 구조체들은 또한 분비를 촉진하는 N-말단 신호 펩티드들에 대한 코딩 서열을 포함하도록 설계되었다. 재조합 융합 작제물 (예를 들어, IgG1 Fc 부분을 갖는 항원)의 경우 융합 파트너를 인코딩하는 서열들을 연장된 프라이머를 사용하여 PCR 증폭하여, 유전자 융합 또는 제한 효소 분해를 위한 상응하는 링커 또는 연결기 서열을 제작하였다. 생성된 중복 DNA 단편을 Gibson 어셈블리 방법을 사용하여 관련 위치에서 공동-발현 벡터에 삽입하여 최종 구조체를 생성했다 (Gibson 외, Nat Methods 2010; 7:901-3; Gibson 외, Nat Methods 2009; 6:343-5). 모든 구조체들의 서열들은 맞춤 제작된 프라이머를 사용하여 GATC (Kφln, 독일)에서 실시된 Sanger 시퀀싱으로 확인되었다.
가용성 항체 또는 항원 또는 세포 표면 고정된 항원은 이전에 설명한 바와 같이 CHO에서 발현되었다 (Reusch 외, Clin Cancer Res 2016; 22:5829-38). 표적 단백질들은 -경쇄 또는 Fc 부분의 존재하에서 단량체 또는 다량체 (동종이량체-, 이종이량체 또는 -사량체) 생성물 형태 그리고 융합된 친화성 태그에 따라 1 또는 2개의 표준 친화성 크로마토그래피 방법들 (단백질 A, 단백질 L, Capture Select C-태그 또는 IMAC)을 사용하여 세포 배양 상청액으로부터 정제되었다. 모든 단백질 제재들은 크기 배제 크로마토그래피를 통해 추가로 연마되고 SEC-MALS, SDS-PAGE 및 UV-Vis 분광법을 사용하여 분석되었다.
닷블롯, SDS-PAGE 및 웨스턴 블롯
정제된 재조합 CD16 항원 변이체들을 니트로셀룰로스 막에 스팟팅하거나 샘플 버퍼와 혼합하고 4-20% Criterion TGX Precast Gels (Bio-Rad)에서 분리하였다. 총 단백질은 Bio-Rad Molecular Imager Gel Documentation 시스템을 사용하여 이미지화되었다. 단백질은 Trans-Blot Turbo 시스템 (Bio-Rad)을 사용하여 웨스턴 블롯팅에 의해 PVDF Midi 막으로 전달되었다. TBS에 용해된 3% (w/v) 탈지 분유 (Merck)로 30분 동안 막을 차단하고 실온에서 1시간 동안 2-4μg/mL의 항-CD16 scFv 항체와 함께 배양한 다음 TBST (TBS 함유 0,1% (v/v) Tween 20)로 그리고 두 번은 TBS로 세척하였다. 실온에서 1시간 동안 2차 탐지 접합체로서 희석된 항-Penta-His-HRP (QIAGEN) 1:3000과 함께 막들을 배양하였다. 세척 후, 새로이 준비된 TBS에서의 0,66mg/mL DAB, 0,02% CoCl2, 0,015% H2O2 의 혼합물을 첨가하여 비색 현상을 시작하였으며 막을 물에 세척함으로써 중단되었다. 막을 건조시키고 촬영하였다.
ELISA에서 CD16A 항원-결합 분석
96-웰 ELISA 플레이트 (Immuno MaxiSorp; Nunc)를 100mM 탄산염-중탄산염 완충액에서 재조합 항원 또는 상이한 NK 세포 관여 항체 형태로 4°C에서 밤새 코팅하였다. 분자 질량에 따라, 0,5-3μg/mL의 항원 또는 2-5μg/mL의 항체 형태들이 코팅되었으며, 이는 코팅된 항원의 경우 약 30nM 또는 코팅된 항체의 경우 10-20nM과 등몰 농도이다. PBS에 용해된 3% (w/v) 탈지 분유 (Merck)로 차단한 후, 0,3% (w/v) 탈지분유를 함유하는 PBS에서의, His-태그된 scFv 항체 또는 비오티닐화된 CD16A-158V ECD-단량체 Fc-융합 항원의 연속 희석액들을 각각 항원 또는 항체로 코팅된 플레이트에서 실온에서 1,5 시간 동안 배양하였다. 결합 경쟁을 평가하기 위해, scFv를 적정하고 1nM 또는 10nM의 3G8 mAb와 함께 플레이트에서 공배양하였다. 웰당 0,1% (v/v) Tween 20을 함유하는 PBS 300μL로 3회 세척 후, 탐지 접합체, 1:3000 희석된 Penta-His-HRP (Qiagen), 스트렙타비딘-HRP (Roche) 또는 경쟁제 3G8의 탐지의 경우, 1:10000 희석된 Peroxidase AffiniPure 염소 항-마우스 IgG (H+L) (Dianova)와 함께 실온에서 1 시간 동안 플레이트들을 배양하였다. 세척 후, 플레이트를 테트라메틸벤지딘 (TMB) 기질 (Seramun)과 함께 1-2분 동안 또는 발색이 명확하게 보일 때까지 배양하였다. 0.5M H2SO4 (100μL/웰)을 첨가하여 반응을 중단시켰다. 멀티웰 플레이트 판독기 (Victor, Perkin Elmer)를 사용하여 450nm (1s)에서 흡광도를 측정하였다. 흡광도 값을 플롯하고 GraphPad Prism 버전 6.07 (GraphPad Software, 미국 캘리포니아 La Jolla)을 사용하여 S형 용량-반응 곡선 (4개의 매개변수 로지스틱 적합)에 비선형 회귀 모델을 적합시켜 EC50 값을 결정하였다.
세포주 및 세포 배양
NCI-H929 (DSMZ, cat.: ACC-163), MC/CAR (ATCC, cat.: CRL-8083), MM.1S (ATCC, cat.: CRL-2974), RPMI-8226 (DSMZ, cat.: ACC 402), KARPAS-299 (DSMZ, cat.: ACC 31), 및 SW-982 (ATCC, cat.: HTB-93)를 구입하였으며, A-431은 G. Moldenhauer 박사 (DKFZ Heidelberg)에 의해 제공되었다. 모든 세포들을 다음이 보충된 DMEM (cat.: 41965-039), IMDM (cat.: 12440-053), 또는 RPMI 1640 (cat.: 21875-034) 배지에서 표준 조건하에 37°C의 가습된 5% CO2 대기에서 배양하였다: 10% 열-불활성화 소 태아 혈청 (FCS) (cat.: 10270-106), 100 U/mL 페니실린 G/100 mg/mL 스트렙토마이신 (cat.: 1540-122), 및 2 mM L-글루타민 (cat.: 25030-024; 모두 Life Technologies).
인간 NK 세포의 분리
말초 혈액 단핵구 세포 (PBMC)는, 기존에 설명한 바와 같이 (Fuss 외, Curr Protoc Immunol 2009; Chapter 7:Unit7 1), Lymphoprep (StemCell Technologies, cat.: 07861)을 사용한 밀도 구배 원심분리에 의해 건강한 지원자의 버피 코트 (German Red Cross, Mannheim, 독일)로부터 분리되었다. PBMC들을 10% 열-불활성화 FCS, 2mM L-글루타민, 및 100U/mL 페니실린 G 소듐/100μg/mL 스트렙토마이신 설페이트가 보충된 RPMI 1640 배지에서 37°C 및 가습된 5% CO2 대기에서 O/N 배양한 후, NK 세포들을 제조업체의 지침에 따라 EasySEP™ Negative NK 세포 농축 키트 (StemCell Technologies, cat.: 17955)를 사용하여 음성 비드 선택에 의해 농축시켰다. NK 세포 분리의 순도는 유세포 분석에 의해 결정되었으며 일반적으로 >80% CD56+ 세포임이 입증되었다 (데이터는 표시되지 않음).
세포 결합 분석 및 유세포 분석
농축된 인간 NK 세포의 분취량을 2% 열 불활성화 FCS (Invitrogen, 카탈로그번호: 10270-106), 0.1% 아지드화 나트륨 (Roth, Karlsruhe, 독일, 카탈로그번호: A1430.0100)를 함유하는 FACS 완충액 (PBS, Invitrogen, 카탈로그번호: 14190-169)에서 지시된 구조체들의 100μL 연속 희석액과 함께 다클론 인간 IgG (Gammanorm, Octapharma)의 부재하에 37°C에서 45분 동안, 또는 이의 존재가 제시된 경우 37°C에서 45분 동안 배양하였다. FACS 완충액으로 반복 세척한 후, 세포-결합된 His-태그된 scFv, TandAb, 또는 TriFlex 항체들을 10 μg/mL 항-His mAb 13/45/31-2 (Dianova, Hamburg, 독일, cat.: DIA910-1MG)로, 이어서 15 μg/mL FITC-접합된 염소 항-마우스 IgG (Dianova, cat.: 115-095-062)로 탐지하였다. 이중특이적 BCMA/CD16A 항체 구조체들을 가용성 His-태그된 BCMA, 이어서 10 μg/mL 항-His mAb 13/45/31-2, 이어서 15 μg/mL FITC-접합된 염소 항-마우스 IgG로 탐지하고, 그리고 이중특이적 Fc-함유 EGFR/CD16A 구조체들을 15 μg/mL FITC-접합된 염소 항-인간 IgG (Dianova, cat.: 109-095-098)로 탐지하였다. 마지막 염색 단계 후, 세포를 다시 세척하고 죽은 세포를 배제하기 위해 2 μg/mL 프로피듐 아이오다이드 (PI) (Sigma, 카탈로그번호: P4170)를 포함하는 0.2 mL의 FACS 완충액에 재현탁시켰다. 2-5 x 103개의 살아있는 세포의 형광을 Millipore Guava EasyCyte 유세포 분석기 (Merck Millipore, Schwalbach, 독일) 또는 CytoFlex 세포계 (Beckman Coulter, Krefeld, 독일)를 사용하여 측정하고 세포 샘플의 형광 강도 중앙값을 측정했다. 2 차 및 3 차 시약으로만 염색된 세포들의 형광 강도 값을 뺀 후,이 값을 비선형 회귀 분석에 사용했다. 평형 해리 상수 (K D )는 단일-부위-결합 (쌍곡선) 적합 및 GraphPad Prism 소프트웨어 V6 또는 V7 (GraphPad Software, 미국 캘리포니아 La Jolla)을 사용하여 계산되었다.
세포독성 분석
칼세인 방출 분석을 위해, 표적 세포들을 37°C의 RPMI 배지에서 30분 동안 10mM 칼세인 AM (Life Technologies, 카탈로그번호: C3100MP)으로 표지하고, 세척하고, 항체 농도를 증가시키면서 1 x 104 개의 종양 표적 세포들을 200 μL 총 부피의 이펙터 세포와 함께 제시된 이펙터:표적 (E:T) 비율로 96웰 마이크로플레이트의 개별 웰에 씨딩하였다. NK 동족살해의 평가를 위해, 5x104 개의 칼세인 표지된 일차 인간 NK 세포를 항체 농도를 증가시키면서 1:1의 E:T 비율로 자가 NK 세포와 공배양하였다. 달리 지시가 없는 한, 5% CO2 가습 대기에서 37°C에서 4 h 동안 배양 후, 상청액으로 방출된 칼세인의 형광 (F)을 520nm에서 플레이트 판독기 (Victor 3 또는 EnSight, Perkin Elmer, Turku, 핀란드)로 측정하였다. 특이적 세포 용해는 다음과 같이 계산되었다: [F(샘플) -F(자발)]/[F(최대) -F(자발)] x 100%. F (자발)은 이펙터 세포와 항체의 부재시 표적 세포에서 방출된 형광을 나타내고 F (최대)는 Triton X-100 (Roth, 카탈로그번호: 3051.2)을 최종 1%의 농도까지 첨가하여 유도된 전체 세포 용해 후 방출되는 형광을 나타낸다. 특이적 표적 세포 용해의 평균 값 (%) 및 표준 편차 (SD)를 플롯하고 GraphPad Prism (v6 및 v7; GraphPad Software, 미국 캘리포니아 La Jolla)을 사용하여 S형 용량-반응 곡선 (가변 기울기)에 비선형 회귀 모델을 적합시켜 시험관내 역가 (EC50)를 결정하였다.
표면 플라스몬 공명
CD16A에 대한 1가 상호작용의 동역학적 결합 분석 및 1가 및 2가 항-CD16A 결합 분석물의 정성적 해리 단계 비교는 25°C에서 러닝 완충액으로 그리고 희석에 HBS-P+ (10 mM HEPES, 150 mM NaCl, 0.05% (w/v) 폴리소르베이트 20, pH 7.4)를 사용하는 Biacore T200 Instrument (GE Healthcare)에서 수행되었다. CAP 센서 칩 (비오틴 캡쳐 키트, GE Healthcare)은 HBS-P+ 버퍼를 사용하여 밤새 사전-전처리되었다. 사전-캡쳐 단계에서, 칩 표면을 유세포 1-4에서 100s 동안 5 μL/분으로 Biotin CAPture 시약 (GE Healthcare)으로 처리하였다.
다양한 항-CD16A scFv의 동역학적 결합 분석을 위해, 비오티닐화된 모노-Fc(침묵) -Avi-태그된 수용체들을 HBS-P+에서 제조하고 유세포 Fc 2 및 Fc 4에서 캡쳐하였다 (인간 CD16A-158V, 인간 CD16A-158F scFvs와의 상호작용 측정시 약 40 RU 및 IgG와의 상호작용 측정시 약 10 RU). IgG 및 scFv는 제시된 일련의 농도로 HBS-P+ 완충액에서 준비되었으며 40 μL/분의 유속으로 기준 표면 (Fc 1, Fc 3) 및 수용체 포획 표면 (Fc 2, Fc 4)에 주입된다 (결합 시간 180초, 해리 시간 300초). 10mL/분으로 120초 동안 6 M 구아니딘-HCl/250 mM NaOH과 재생 주기 이후 상호작용들을 Multi Cycle Kinetic 모드를 사용하여 측정하였다 (모든 항체들을 4-배 연속 희석하여 제조하였다: scFv-Ab16중 150 nM - 0.586 nM; scFv-Ab16고 50 nM - 0.195 nM, scFv-AB16저 500 nM - 1.953 nM, scFv-3G8 및 인간 IgG1 Fc-강화 200 nM - 0.781 nM, 인간 IgG1 및 인간 IgG1 Fc-침묵 2000 nM - 7.813 nM) 데이터를 참고 표면 (Fc 2-1, Fc 4-3) 및 제로 농도 (버퍼 대조) 신호에서 신호들을 뺀 것으로 언급하였다. Biacore T200 평가 소프트웨어 (v3.1)를 사용하여 데이터를 1:1 결합 모델 (R최대 및 RI 국부 적합됨)에 적합시켜 동역학적 평가를 실시하였다. 센소그램의 정성적 비교를 위해, 단일 농도 (312.5 nM)의 scFv 및 IgG를 증가된 포획 수준 (인간 CD16A-158V 180 RU 및 인간 CD16A-158F 90 RU)의 수용체 포획 표면 및 참고 표면에 주사하였다. 언급된 곡선들을 각 곡선 최대값으로 정규화하고 중첩시켰다. 1가 및 2가 CD16A-결합 항체 또는 리간드의 정성적 해리 단계 비교를 통한 수용체 잔류를 조사하기 위해, 비오티닐화된 모노-Fc (침묵) -Avi-태그된 수용체를 HBS-P+에서 제조하고 유세포 Fc 2 및 Fc 3에서 캡쳐하였다 (인간 CD16A-158V 약 160RU, 시노몰구스 CD16 약 320RU). Ab16고 결합 도메인 및 비교인자들, 강화된 인간 IgG1 Fc (S239D/I332E) 및 1가 결합 scFv-Ab16고 를 통합한 관심 항체들 (scFv-IgAb, Db-Fc, KiH-scDb-Fc, TandAb)을 HBS-P+ 완충액에서 50nM 농도로 희석하여 참고 표면 (Fc 1) 및 수용체 포획 표면 (Fc 2, Fc 3)에 30 μL/분의 유속으로 주사한다 (결합 시간 180초, 해리 시간 3시간). 표면은 10mL/분의 6M 구아니딘-HCl/250mM NaOH를 사용하여 120초 동안 재생되었다. 데이터를 참고 표면 (Fc 2-1, Fc 4-3) 및 제로 농도 (버퍼 대조) 신호에서 신호들을 뺀 것으로 언급하였다. 언급된 곡선들을 각 곡선 최대값으로 정규화되고 중첩시켰다.
ROCK 관여항체의 약동학적 연구
다양한 ROCK® 플랫폼 형태들의 기본 약동학 매개변수를 CD-1 SWISS 마우스에서 평가하였다. Heidelberg Pharma GmbH사에 의해 생애 상 연구가 수행되었다. CD-1 SWISS 암컷 마우스 (예를 들어, n=24)는 0.3 mg (~ 10 mg/kg 체중)의 테스트 항목을 정맥내 단일 투여 받았다. 상이한 시점들에서 혈액을 1 내지 3주 기간 동안 수집하였다. 혈액에서 혈청을 채취하여 ELISA 또는 MSD 기술에 기반한 확립된 분석법으로 분석하였다. 대표적인 혈액 채취 일정은 13개 시점들, 예컨대, 투여 7일전, 5 분, 30 분, 30 분, 1 시간, 4 시간, 8 시간 및 1, 2, 3, 4, 7, 14 및 21일차를 포함하였다. 혈청 농도는 강화된 화학발광 (ECL) 탐지를 사용하여 Tristar LB941 (Berthold instruments)에서 ELISA로 결정되었다. 분석 설정을 위해, 포획 및/또는 탐지자로서 혈청 항원 및/또는 단일클론 항체의 다양한 조합들을 테스트하였다. 분석은 분석간/분석내 분석 정밀도 및 정확도, 희석 선형성 및 선택성, 후크 효과 및 매트릭스 효과와 같은 추가적인 중요한 매개변수들과 관련하여 특성화되었다.
NK 세포 활성화 분석
5 x 105 개 인간 PBMC를 제시된 항체 농도가 존재하에서 완전 RPMI 1640 배지에서 1 x 104 개 RPMI-8226 세포의 존재 또는 부재하에서 편평 바닥 96-웰 마이크로플레이트의 개개 웰들에 씨딩하였다. 5% CO2 가습 대기에서 37°C에서 22시간 배양 후, 세포를 수확하고 세척하고 FACS/hIgG 완충액 (1mg/mL 다클론 인간 IgG로 보충된 FACS 완충액)에 재현탁하였다. 그 다음 세포를 15분 동안 암실의 얼음위에서 FACS/hIgG 완충액에서의 CD56-PC7 및 CD69-PC5로 염색하였다. FACS 완충액으로 반복 세척한 후, 1 x 103 - 1 x 104 개 세포들을 유세포 분석으로 분석하고 CD56+ NK 세포 중 CD69+ 세포 백분율로 정량화하였다.
사이토카인 방출 분석
편평 바닥 96-웰 마이크로적정 플레이트들을 RPMI-1640/5% FCS로 2-4 시간 동안 RT에서 차단한 후, 10 μg/mL의 제시된 항체들의 존재 또는 부재시 1 x 104 NCI-H929 종양 세포들이 있거나 없는 5 x 105 PBMC를 200 μL/웰의 총 부피로 씨딩하였다. 37°C 및 5% CO2 가습 배양기에서 24시간 동안 플레이트들을 배양하였다. BD™ 사이토메트릭 비드 어레이 (Cytometric Bead Array, CBA) 인간 Th1/Th2 사이토카인 키트 II (BD Bioscience)를 사용하여 Bioassay GmbH사 (Heidelberg, 독일)에서 사이토카인을 정량할 때까지 세포 배양 상청액을 수확하고 -80°C에서 보관하였다.
결과
항-CD16A 항체 도메인 생성에 대한 이론적 근거
Fc 부분을 포함하는 대부분의 고전적인 치료용 항체는 낮은 고유 CD16A 결합 친화성 (FcγRIIIA 결합 친화성)를 나타내며, 또한 CD16A상의 인식 부위를 사용하는 면역-관여항체는 IgG 항체의 Fc 부분에 의해 결합되고 (de Palazzo 외, Cancer Res. 1990;50:7123-8; de Palazzo 외, Cancer Res. 1992;52:5713-9) CD16A 결합을 위해 혈청 IgG와 경쟁해야하므로, 이는 CD16A 점유를 제한하고 효능있게 하는데 필요한 치료 항체 용량을 증가시킨다. 혈장 IgG와의 경쟁은 다발성 골수종과 같은 높은 수준의 혈장 IgG를 특징으로 하는 질환 상태에서 더욱 두드러 질 수 있다 (Michallet 외, Leukemia 2017). 또한, 인간의 CD16A 다형성 (Mahaweni 외, Sci. Rep 2018;8:15983), (가장 두드러진 변이체 CD16A-158V 및 CD16A-158F는 IgG에 대한 결합 친화성, 그리하여 ADCC와 같은 FcR 기능에 있어서 상이함)은, 환자 개개의 CD16A 유전자형에 따라 고전적 mAb 요법의 효능 수준을 다르게 한다 (Bowles 외, Blood 2006;108:2648-54; Burchard 외, Cancer Genetics 2013;206:130-4). ROCK® 플랫폼을 활용하여 본 발명자들은 CD16A2 상의 고유한 에피토프를 인식하고 혈장 IgG 경쟁 및 CD16A 다형성에 의해 거의 영향을 받지 않는 항-CD16A 도메인을 생성하였다. 또한 이것은 매우 강력한 ADCC를 매개하는 CD16A에 대한 높은 친화성 결합을 위해 설계되어 효과적인 면역-감시를 제공한다.
상기 기재된 바와 같은 CD16A에 대한 높은 친화성 및 선택성을 갖는 이러한 항체 모이어티의 기준을 충족시키기 위해, 인간 PBMC로부터 유래한 scFv 라이브러리를 스크리닝하였다. 음성 선택을 위해 인간 CD16B 변이체를 사용하면 초기에 CD16A에 대한 낮은 친화성 그러나 높은 선택성을 가지는 항체를 식별할 수 있다. 친화성 성숙을 위한 상이한 접근법 (예를 들어, 경쇄 셔플링, 중쇄의 CDR에서의 이론적 돌연변이들)을 사용하여 CD16A에 대한 친화성을 최대 2 nM의 Kd까지 적어도 인자 100만큼 증가시킬 수 있다 (AB16hi, 표 5). 낮은 친화성 (Ab16저), 중간 친화성 (Ab16중), 및 높은 친화성 결합 scFv (Ab16고) 항체들의 CD16A 결합 성질들을 SPR에서 특성화하였으며 기존에 설명되고 잘 특성화된 CD16 범-특이적 항체 3G8 (Tamm 외, J Immunol 1996; 157:1576-81), 뿐만 아니라 IgG1 Fc 또는 CD16A-결합-및 Fc-매개된 이펙터 기능 강화 돌연변이들 S239D/I332E (Lazar 외, Proc Natl Acad Sci U S A 2006; 103:4005-10) 또는 침묵 돌연변이들 L234F/L235E/D265A (Vidarsson 외, Front Immunol 2014; 5:520; Baudino 외, J Immunol 2008; 181:6664-9; Hezareh 외, Journal of virology 2001; 75:12161-8)을 가지는 유전자 변형된 Fc 변이체와 비교하였다. Ab16중과 Ab16고 모두 CD16A에 대한 우수한 결합 특성이 확인되었다 (도 18A 및 18B). 야생형 IgG1 Fc, 강화된 IgG1 Fc 및 CD16 범-특이적 항체 3G8의 CD16A 결합 동역학은 CD16A 다형성에 의존하는 반면, Ab16고 뿐만 아니라 Ab16중 및 Ab16저는 대립 유전자 형태, CD16A-158V 및 CD16A-158F과 관계없이 비등한 동적 결합 성질들을 보여주었다 (표 5, 도 18A, 18B 및 20). 또한 두 항체 모두 시노몰구스 CD16A와 우수한 교차 반응성을 보여주었다 (도 19A, 표 6). 또한, 다른 친화성 성숙 전략들로부터 확인된 항-CD16A 결합제의 특성화는 또 다른 독특한 특성을 확인시켜주었다: CD16A 유전자형 변이와 관계없이 균일하게 CD16A에 관여 (표 5, 도 18A, 18B 및 20).
표 5: 상이한 CD16A 결합 scFv 또는 Fc 부분의 SPR 결합 동역학.
표 6: 1.5μg/mL (32nM)의 농도로 코팅되고 ELISA에서 분석된 CD16 항원 변이체에 대한 다양한 항-CD16 scFv 항체의 결합 요약.
혈청 IgG의 존재하에서 상이한 에피토프에 대한 CD16A 특이적 결합
높은 수준의 다형성을 나타내는 CD16A 외에도 인간 CD16B (FcγRIIIB)의 동종 변이체는 세포외 도메인 (ECD)의 5개 아미노산이 다르며 (도 21), 일부는 추가 당화를 가능하게 하여, NA1, NA2 및 SH로 명명된, GPI-고정된 CD16B 과립구 항원의 3가지 다른 변이체를 생성한다. 특히 CD16A와 B의 성숙한 ECD에서 2개 아미노산 위치만이 일관되게 다르다 (도 21). 또 다른 변이는 CD16A 및 CD16B의 다양한 막 고정 방식에 있다. 성숙한 GPI-고정 형태로 절단된 CD16B의 카복시말단 프로펩티드 서열은 CD16A ECD를 막경유 도메인에 연결하는 서열과 높은 상동성을 가진다 (도 21). CD16A/CD16B 서열 변이들 중 어느 것이 우리의 엄격한 CD16A-선택적 항체에 대한 결합 부위를 결정하는지 조사하기 위해, 일련의 재조합 CD16 항원 변이체들을 생성하고 특성화하였다. CD16B (NA1) ECD는 성숙된 형태 (프로펩티드 결핍) (CD16Bmat) 또는 프로펩티드 서열을 포함하는 전구체 (CD16Bpr)로 표현되었다. 또한 CD16B-특이적 아미노산이 CD16A의 상동성 잔기로 대체된 CD16Bpr ECD 돌연변이체를 생성하고 결합 분석에서 테스트했다: CD16Bpr,D129G, CD16Bpr,H140Y, CD16Bpr,S185F.
모든 테스트 CD16A 및 CD16B 항원 변이체들은 CD16 범-특이적 항체 3G8에 의해 이들의 분자 무결성을 확인하여 인식되었다 (도 19A, 19B, 19C 및 표 6). ScFv 항체 Ab16중 또는 친화성-개선된 Ab16고는 recognized the CD16A 항원을 인식하였으나, CD16B의 성숙 또는 프로펩티드-함유 ECD 융합 항원들은 인식하지 못했다. 그러나 140 위치의 CD16B ECD 히스티딘 (H)이 티로신 (Y)-CD16A의 상응하는 위치에 존재하는 아미노산-으로 돌연변이 된 경우 이러한 돌연변이체 형태의 CD16B (CD16Bpr,H140Y)는 친화성 최적화된 scFv 항체 Ab16mid and Ab16hi에 의해 잘 인식되었다 (도 19A-19C, 표 6). 도 19A, 19B 및 19C에서 보는 바와 같이, 위치 140의 티로신 (Y)은 scFv 항체의 입체형태 에피토프의 형성 및 CD16A-특이적 반응성에 중요하다.
시노몰구스 CD16 ECD 서열이 인간 CD16A와 총 16 개 아미노산이 다르다는 사실에도 불구하고 (도 21의 정렬 참고), 두 항-CD16 scFv 모두 시노몰구스 CD16 과 양호한 교차 반응을 유지하였다(도 19A, 19B, 19C 및 표 6). 테스트 항체 Ab16중 및 Ab16고에 의한 CD16A-특이적 인식에 있어서 CD16 ECD의 위치 140에서의 티로신 (Y)의 결합 선택성 및 중요성은 상이한 CD16 항원 변이체의 유전자삽입 발현을 갖는 재조합 CHO 세포를 사용하여 확인되었다 (도 19B). CD16Bpr 또는 CD16Bmat 항원 변이체와 대조적으로 CD16A 또는 CD16Bpr,H140Y는 이들 scFv 항체를 사용한 웨스턴 블롯에서 SDS-PAGE 후에 인식되었다 (도 19C, 데이터는 나타내지 않음). 환원된 샘플의 웨스턴 블롯에서는 신호가 수득되지 않았는데 (데이터는 표시되지 않음), 이는 Ab16중 및 Ab16고에 의한 인식의 경우 CD16의 위치 140에서 티로신에 의해 결정될 수 있는 입체형태 에피토프를 암시하는 것이다.
CD16A의 IgG 결합 부위는 수용체의 막 근위 ECD 상의 불연속 결합 부위이다. IgG의 Fc 부분과 CD16A의 낮은 친화성 상호작용에 중요한 아미노산은 이전에 확인되고 설명된 바 있다 (Ahmed 외, J Struct Biol 2016; 194:78-89). 항체 3G8은 CD16A 및 CD16B에 결합하여 IgG 결합을 차단하는 것으로 보고되었다 (Tamm 외, J Immunol 1996; 157:1576-81). CD16A에 대한 테스트 항체 결합의 IgG에 의한 차단은 관찰되지 않았다. CD16A에 대한 3G8 mAb의 결합은 3G8의 상응하는 가변 도메인을 포함하는 scFv 항체의 농도가 증가함에 따라 보다 우월하였던 반면, 항-CD16 scFv 항체 Ab16중 및 Ab16고는 CD16A 상의 3G8 mAb를 차단하거나 대체하지 않고 독립적으로 결합하며 (도 22), 경쟁 3G8 mAb의 부재 또는 존재하에서 유사한 친화성을 가진다 (표 8). 표 8에서 보는 바와 같이, 3G8은 CD16 상의 Fc 결합 부위를 차단하였다. CD16A 상의 3G8 결합 부위의 점유는 IgG 결합을 차단하는 것으로 알려져 있기 때문에, CD16A 상의 테스트 항-CD16 항체들의 결합 부위는 IgG 결합 부위와 구별된다는 결론에 도달하였다. 따라서 scFv 항체 Ab16고 및 Ab16중의 NK 세포 결합 K D 값은 10mg/mL 인간 IgG의 첨가에 의해 단지 약간만 영향을 받았지만, 항체 3G8의 CD16 결합 모이어티의 결합 친화성은 생리학적 IgG 농도의 존재하에서 20배 이상 감소되었다 (표 7). 따라서, 이러한 결과는 테스트 CD16A-결합 항체 Ab16고 및 Ab16중이 경쟁 IgG 수준 (예컨대, 인간 혈액)에 의해 손상되지 않거나 단지 최소한으로만 손상되는, CD16A-특이적 에피토프에 대한 높은 친화성 결합의 이점을 제공하며, 나아가 이들의 힘이 다가 항-종양 NK 세포-관여 ROCK® 항체에서 이용되었음을 시사한다.
표 7: 일차 인간 NK 세포들에 대한 항-CD16 scFv의 겉보기 친화성.
표 8: 0.5μg/mL (10nM) 농도로 코팅되고 경쟁제로서 등몰 농도의 CD16-범 특이적 항체 3G8 (10nM)의 부재 또는 존재하에서 ELISA에서 분석된, CD16 항원에 대한 상이한 항-CD16 scFv 항체의 결합 및 경쟁 요약.
ROCK
®
플랫폼
ROCK
®
형태
항-CD16A 도메인의 다양성을 입증하고 그 잠재력을 최대한 활용하기 위해 알려진 항체 형태 (Spiess 외, Mol Immunol 2015; 67:95-106)를 기반으로 한 광범위한 ROCK® 구조 및 새로 설계된 이의 변이체들을 생성하였다.
ROCK® 플랫폼 항체들은 적어도 하나의 표적-결합 부위 및 2가 결합을 가능하게 하는 2개의 CD16A 항원-결합 모이어티가 있는 다가 다중특이적이다. 원자가, 다중특이성, 약동학 및 약력학적 특성과 같은 원하는 기능에 따라, 구조체들은 불변 영역과 함께 또는 불변 영역 없이 결합 도메인으로부터 모듈식으로 조립된다. ROCK® 항체 형태들은 i) 무-Fc ROCK®, ii) Fc 융합 ROCK® , iii) IgG-유사 ROCK® 및 iv) 단편 항체 결합 도메인 (Fab) 융합 ROCK®을 포함하는 4개의 상이한 패밀리들로 그룹화 될 수 있다. 패밀리 구성원들 ii), iii) 및 iv)의 표적 및 이펙터 세포 결합 모이어티는 단쇄 Fv (scFv), 단쇄 디아바디 (scDb), 디아바디 (Db) 또는 as 다양한 기능을 가능하게 하는 Fab 형태일 수 있다. 결합 도메인은 가요성 링커를 통해 CH2/CH3 불변 도메인의 N-및 C-말단에 융합되거나, 대안적으로 힌지 또는 더 짧은 중간 힌지를 통해 N-말단에 융합된다 (Merchant 외, Proc. Natl. Acad. Sci. U.S.A. 2013;110:E2987-96). 패밀리 i)의 경우, 결합 도메인은 펩타이드 링커에 의해 연결되고 TandAb (McAleese 외, Future Oncol 2012; 8:687-95) 또는 aTriFlex 분자 (Gantke 외, Protein Eng Des Sel 2017; 30:673-84)로 조립된다. NK 세포의 강력한 결합 및 활성화를 확보하기 위해 항-CD16A 모이어티는 모든 패밀리에서 2가 결합을 위해 설계되었다. ROCK® 관여항체들에서 종양 표적 결합 도메인은 원하는 결합 강도 및/또는 표적 생물학에 따라 1가 또는 2 가일 수 있다. 또한 플랫폼의 모듈화는 하나 이상의 종양 항원의 공동-표적화를 위한 다가 및 다중특이적 관여항체들의 제작을 용이하게 한다. 도 23은 4가지 ROCK® 패밀리들 모두 (i-iv)를 관련된 형태들로 보여준다. ROCK® 형태들의 다양성을 보여주기 위하여, 상이한 표적 결합 모이어티, 가령, BCMA, CD19, CD20, EGFR, HSA 또는 RSV가 선택되었다.
본원에 기재된 기능적 분석에서 더욱 상세하게 특성화되는 ROCK® 구조체들의 대표적인 예는 다발성 골수종에서의 표적인 고형 종양 표적 EGFR 또는 B 세포 성숙 항원 (BCMA)을 표적으로 한다 (표 9A, 9B 및 9C). 표 9A, 9B 및 9C의 구조들에서 표시된 기호는 그림 23에 표시된 기호와 일치한다. 모든 ROCK® 구조는 완전 인간 항체 도메인으로 구성되었으며 대략 102 - 250 kDa의 분자량을 가진다. 여러 사례들에서, 태그 (C-태그 및/또는 6xHis 태그)를 C-말단에 추가하는 것은 친화성 크로마토 그래피를 통한 이종이량체 항체의 선택적 정제, 비대칭 생성물에서 두 가지 다른 폴리펩티드 사슬의 분석, 마지막으로 고순도 (> 90%)의 원하는 생성물 종을 가능하게 한다.
무-Fc ROCK ® 패밀리 (i): 무-Fc 구조체들의 이 그룹은 여러 생성물들이 이미 임상 개발 중인 잘-알려져 있는 TandAb (Reusch 외, MAbs 2014; 6:728-39; Reusch 외, MAbs 2015; 7:584-604; Ellwanger 외, Frontiers in Oncology 2017; 7; Reusch 외, Clin. Cancer Res. 2016;22:5829-38) 및 aTriFlex (Gantke 외, 단백질 Eng Des Sel 2017; 30:673-84) 분자들을 조합한다. 후자는 2개의 상이한 종양-관련 항원 또는 표적 에피토프를 어드레스 (address)하기 위해 2개의 상이한 scFv 특이성을 사용하는 삼중 특이 적 형태로 조작되거나 PK-확장에 사용될 수있다. 이러한 목적을 위해, 항-인간 혈청 알부민 (HSA) 결합 도메인을 사용하여 그 외 짧은 수명의 무-Fc 항체 형태의 혈청 반감기를 연장하였다. 이 패밀리에 속하는 두 형태들 모두 2개의 개별 폴리펩티드 사슬들에서 상응하는 중쇄 및 경쇄 가변 도메인의 상호작용에 의해 헤드-투-테일 동종이량체 (TandAb 형태) 또는 헤드-투-테일 또는 헤드-투-헤드 형태의 이종이량체 (aTriFlex)로서 이량체로 조립된다. 이 그룹의 구성원들은 약 105 kDa 질량의 기능적 이량체를 가지는 크기가 최소인 ROCK® 이중특이적 구조체들로서 Fc-부분과 당화 모두 없다.
Fc 융합 ROCK ® 패밀리 (ii): 본 Fc-함유 항체 형태들의 패밀리는 Fcγ 수용체 결합을 피하지만 반감기 연장을 위한 FcγRn 결합을 여전히 유지하기 위해 여러 Fc 변이체들을 포함한다 (Vidarsson 외, Front Immunol 2014; 5:520; Baudino 외, J Immunol 2008; 181:6664-9; Hezareh 외, Journal of virology 2001; 75:12161-8). 따라서, Fcγ 수용체 결합은 NK 세포 결합 도메인에 의해 독점적으로 매개되고 CD16A로 제한된다. 또한이 패밀리의 Fc 부분은 IgG1-기반 동종이량체 (Bi-scFv-Fc, Db-Fc), 이종이량체 (KiH-scFv-Fc, KiH-scDb-Fc) 또는 단량체 Fc (scDb-mFc) 일 수 있다. 이종이량체 화를 촉진하기 위해 고전적인 Y407T ( "홀") 및 T366Y ( "놉") 돌연변이를 사용하는 "놉-인투-홀" (KiH) 기술이 사용되었다 (Ridgway 외, Protein Eng 1996; 9:617-21). 단량체 Fc (mFc) 부분은 표적 및 NK 세포 결합 모이어티와의 융합을 위해 가용성 연결기를 사용하여 이전에 공개된 바와 같이 조작되었다 (Ying 외, J. Biol. Chem. 2012;287:19399-408). 항-CD16A는 N-또는 C-말단에서 항-표적 결합 도메인의 반대편에 위치하거나 KiH-scDb-Fc 구조체들 중 하나에서 나타났던 바와 같이 N-말단에서 이에 병치된다. CD16A 결합 도메인에 대한 scDb 형태는 KiH-scDb-Fc 및 scDb-mFc 구조체들에 적용되었다. Db-Fc 형태는 C-또는 N-말단에 디아바디 분자를 나타내는 동종이량체이다. 이 Db-Fc 형식은 C-에서 가요성 링커를 통해 또는 N-말단에서 확장된 힌지 영역을 통해 불변 영역에 융합된 2개의 VL/VH 도메인으로부터 조립된다.
IgG-유사 ROCK ® 패밀리 (iii): 이 이중특이적 항체 그룹은 원칙적으로 두 Fab 아암들 내부에서 가변 단편들 (Fv)로서 C-말단에 융합되거나 N-말단에 위치하는 2개의 CD16A 항원-결합 모이어티를 가지는 "확장된 인간 IgG1"분자인 scFv-IgAbs 및 Bi-scFv-IgAbs를 포함한다 (Coloma 외, Nat Biotechnol 1997; 15:159-63). 상응하는 반대쪽 단부에 위치한 종양 표적-결합 도메인에 대해서도 이는 마찬가지이다. Bi-scFv-IgAb 분자는 가요성 링커를 통해 CH3 및 카파 또는 람다 불변 영역의 C-말단에 융합된 2개의 추가적인 항원-결합 scFv 쌍들을 가지는 6가 삼중 특이 적 IgG-유사 구조를 나타낸다.
Fab 융합 ROCK® 패밀리 (iv): 이 그룹의 구성원은 "확장된 Fab"분자이며, scDb-TriB 및 scDb-TriB-scFv 형태로 세분화 될 수 있다. 둘 모두 scDb-TriB-scFv에서 카파 또는 람다 불변 영역의 C-말단에, 또는 scDb-TriB의 경우, CH 1의 C-말단 단부에 융합된 2가 scDb로서 항-CD16A 결합 모이어티를 포함한다. PK-확장의 경우 Fab 단편의 N-말단에있는 가변 도메인은 HSA 결합을 제공한다. 종양 표적화는 각각의 유리 C-말단에 융합된 1가 (scDb-TriB-scFv) 또는 2가 (scDb-TriB) 결합 모이어티 (scFv 대 scDb)에 의해 구현된다.
ROCK® 관여항체들은 CD16A를 통해 NK 세포 관여를 최대화하기 위하여 결합력을 이용한다
다양한 ROCK® 관여항체 형태들의 CD16A 결합 유지를 SPR에서 조사하고, 인간 CD16A-158V 또는 시노몰구스 CD16로부터의 해리를 비교함으로써 scFv Ab16고 및 인간 CD16A에 대한 결합을 강화시키는 조작된 인간 IgG1 Fc (S239D/I332E)의 1가 결합과 비교하였다. 3 시간 해리 동안 테스트 항체들의 상대 결합 신호들은, 훨씬 더 신속하게 해리하는 IgG Fc (S239D/I332E) (10%) 또는 1가 결합 scFv Ab16고 (0% -2.4%)에 비해, 두 가지 인간 CD16A-158V (76.6% -92.5%) 및 시노몰구스 CD16 (84.9% -97.9%) 모두에서 모든 테스트 ROCK® 관여항체들의 수용체 잔류에 있어 명백한 우수성을 보여주었다. SPR에 의한 해리 측정 결과와 일관되게, ROCK® 관여항체들, 가령, Ab16고 Fv 도메인들이 있는 TandAb는, 야생형 Fc 도메인이 있는 고전적인 IgG 또는 Fc에 S239D/I332E 돌연변이들이 있는 강화된 IgG 보다 NK 세포 표면에서 실질적으로 보다 장기 잔류를 나타내었다 (도 25).
모두 CD16A에 대한 2개의 결합 부위들을 내포하는, 상이한 ROCK® NK 세포 관여항체들의 겉보기 CD16-결합 강도는 또한, 다중특이적 (이중-또는 삼중특이적 포함, 그러나 이에 제한되는 것은 아님) 및 다가 (4가 또는 6가) ROCK® NK 세포 관여항체들에서 항-CD16 가변 도메인 동일성 (고 친화성 Ab16고, 또는 중 친화성 Ab16중), 항체 형태 및 항-CD16 모이어티의 위치에 따라 달라진다. 1가 결합 특성과 유사하게, ROCK® 항체를 포함하는 Ab16고에 의한 2가 CD16A 결합은 Ab16중 도메인을 포함하는 상응하는 ROCK® 관여항체보다 ELISA에서 더 높은 겉보기 친화성을 가졌다. 또한 ROCK® 관여항체에서 항-CD16A 도메인의 상이한 배치는 점진적인 친화성 조정을 가능하게 하였다. Fc 도메인들의 N-말단에서 CD16 결합 모이어티를 포함하는 ROCK® 구조는 Fc의 C-말단에 대한 항-CD16 도메인의 융합을 포함하는 항체들 보다 CD16A에 대해 보다 높은 겉보기 결합 친화성을 매개하였다 (도 26A 및 26B). 결합 친화성의 미세 조정은 2개의 CD16 결합 scFv의 융합에 비해 결합 강도를 강화한 Fc의 N-말단에서 Fab 또는 디아바디-기반 결합 모듈을 사용하여 구현될 수 있다 (도 26A 및 26B). Fc의 C-말단에 scFv를 포함하는 ROCK® 관여항체들에서 CD16 결합 강도의 추가 조정은 연결기의 길이를 변경함으로써 구현 될 수 있으며, 이에 따라 보다 긴 연결기가 보다 짧은 연결기보다 높은 겉보기 친화성 CD16 결합을 촉진 할 수 있다 (도 26C). 아마도, 결합력 뿐만 아니라 입체적 양상들 또한 이러한 설정에서 겉보기 결합 친화성에 영향을 미치는 반면, 조작된 상이한 표적 결합 특이성들의 CD16A 결합에 대한 영향은 무시할 만 하였다.
ELISA에 의해 측정된 CD16A 결합 특성이 NK 세포에 대한 결합과 상관 관계가 있는지 평가하기 위해, Ab16중 Fv 도메인들을 내포하는 선택된 ROCK® 관여항체들의 세트를 인간 혈청의 생리학적 환경을 모사하는 다클론 인간 IgG가 부재 또는 존재하는 일차 인간 NK 세포들에서 적정하였으며, 겉보기 친화성을 비-선형 회귀로 결정하였다 (도 27A, 27B, 및 27C). 다시, N-말단 Fab 또는 scFv (scFv-IgAb_A 및 Bi-scFv-Fc_A)에 항-CD16A 도메인들이 있는 구조체들은 C-말단 scFv (scFv-IgAb_B 및 Bi-scFv-Fc_C)에 항-CD16A 도메인들이 있는 상응하는 구조체들에 비해 NK 세포에 대해 실질적으로 더 높은 친화성을 나타냈다. 흥미롭게도, 중앙 항-CD16A 디아바디를 갖는 TandAb (표 9B)는 NK 세포에 대해 N-말단 Fab 또는 scFv를 갖는 구조체와 유사한 높은 친화성을 보인 반면, aTriFlex는 구조체의 코어에서 유사한 항-CD16A 디아바디 모티프 및 비대칭 가변 도메인 순서에도 불구하고 NK 세포에 대해 가장 낮은 친화성을 나타냈다. 높은 IgG 농도는 N-말단 Fab에서 항-CD16A 도메인을 갖는 TandAb 및 scFv-IgAb 구조체의 겉보기 친화성에 실질적인 영향을 미치지 않았으며, 해당 구조체에 N-또는 C-말단으로 융합되는지 여부와 무관하게 항-CD16A scFv를 포함하는 구조체들의 결합에 대하여 보통의 영향 (계수 4-9)을 주었고, aTriflex의 친화성에 대해 가장 강력한 억제 효과가 관찰되었다.
NK 세포 동족살해 및 ROCK
®
형태들의 설계
CD16에 대한 항체의 다가 고친화성 결합은 여러 NK 세포에서 수용체를 교차 결합시키고 교차 결합된 세포의 CD16A 매개 사멸을 초래하여 NK 세포 집단을 고갈시킬 위험이 있다 (Choi 외, Immunology 2008;124:215-22). 이러한 NK 세포 동족살해는 NK 세포의 형질 막 상의 CD38을 표적하는 다라투무맙과 같은 다른 단클론 항체들에 대해 이미 나타난 바 있다 (Casneuf 외, Blood Adv. 2017 Oct 24;1(23):2105-2114). 주 이펙터 세포 집단의 감소는 아마도 항체-매개 항 종양 반응의 효능을 방해 할 것이다. 이러한 이유로 ROCK® 형태에 의해 유도된 NK 세포 동족살해 정도를 모니터하는 다양한 시험관내 분석이 확립되었다. 여기서는 동일한 공여체의 일차 인간 NK 세포를 이펙터 및 표적 세포로 사용하여 전술한 바와 같이 NK 세포 용해의 효능을 결정할 수 있었다. 양성 대조로서 다라투무맙이 분석 설정에 포함되었다. 본 발명자들은 CD16A에 대한 단일 결합 부위만을 함유하는 항체에 의한 NK-NK 동족살해를 관찰 한 적이 없으며, 이는 2가 CD16A가 NK 세포 가교 및 후속 동족살해의 전제 조건임을 시사한다. 흥미롭게도 ROCK® 항체 형식이나 도메인 순서에 따라 NK 세포 동족살해의 발생 뿐만 아니라 NK 세포 사멸의 효능도 조절할 수 있다 (도 28).
일반적으로, 분석된 모든 ROCK® 항체 형태는 다라투무맙에 비해 개선된 NK 세포 동족살해 프로파일을 보였으며, 이는 158pM의 평균 역가로 NK 세포 지시 사멸을 유도하였다. 모든 테스트 ROCK® 항체 형태들은 덜 두드러지거나 NK 세포 사멸을 전혀 유발하지 않았다.
ROCK® 항체의 N-말단 융합된 항-CD16A 모이어티를 통한 CD16A 관여는 C-말단에서의 CD16A 관여에 비해 NK 세포 동족살해를 더 강력하게 피하는 것으로 나타났다. 그러나 N-말단 CD16 관여를 보다 상세히 살펴보면, 1439 내지 2389pM의 평균 역가 값을 갖는 Fab 기반 CD16A 관여를 사용할 때 NK 세포 고갈 보다 두드러졌던 것으로 나타났다.
흥미롭게도, CD16 Fv의 도메인 순서를 분석하였을 때, 도메인 순서가 VL-VH 인 경우 실질적으로 보다 적은 수의 구조체들이 NK 세포 동족살해를 유도하였으며, 반면에 VH-VL 도메인 순서를 포함하는 구조체들은 모두 NK 세포 용해를 유도하였던 것으로 나타났다. C 또는 N-말단에서 CD16 Fv VL-VH 도메인을 포함하는 ROCK® 항체 중에서 NK 세포 동족살해를 유도한 구조체는 거의 없었다.
요약하면, NK 세포 동족살해 유도 항체의 비율 및 NK 세포 사멸의 역가는 Fab-기반 CD16A 관여를 피하고 CD16 결합 Fv 도메인의 유익한 VL-VH 순서에 초점을 둠으로써 개선된다.
ROCK 관여항체들의 보다 우수한 시험관내 세포독성
EGFR 또는 BCMA를 표적으로하는 다양한 ROCK® 관여항체의 시험관내 세포 독성을 칼세인 방출 분석에서 평가했다 (도 29A, 29B, 29C, 29D 및 29E). Ab16고 Fv 도메인을 가지는 BCMA-표적화 관여항체들 (TandAb_A, scFv-IgAb_D, Bi-scFv-Fc_B, 및 KiH-scDb-Fc_A)을 세포 표면에서 고 (NCI-H929), 중 (MM.1S), 또는 저 (MC/CAR) BCMA 수준을 발현하는 표적 세포들 상의 Ab16중 Fv-함유 관여항체 scFv-IgAb_E 및 Fc에 S239D/I332E 돌연변이들이 있는 Fc-강화된 항-BCMA IgG1 (IgAb_C)와 비교하였다 (도 29A-29C). 예시적인 세포 독성 결과는 BCMA고 NCI-H929 표적 세포들에서 서로 다른 ROCK® 관여항체 형태들 간에 약간의 역가 및 효능 차이를 (EC50 범위: 9.5 pM - 52.7 pM), BCMA중 MM.1S 표적 세포들에서는 유사한 효능이지만 보다 강력한 역가 차이 (EC50 범위: 1.8 pM - 29.1 pM)를, BCMA저 MAC/CAR 표적 세포들에서는 효능 및 역가에 있어서 강력한 차이 (EC50 범위: 59 pM - 859 pM)를 보여주었다. BCMA-표적화 TandAb_A, KiH-scDb-Fc_A 및 scFv-IgAb_D에 대해 보다 낮은 EC50 값이 생성되었다. 이러한 결과는 보다 적은 수의 세포 표면 표적 항원들을 발현하는 취약성이 더 적은 표적 세포들 및/또는 표적 세포들의 NK 세포-매개 용해를 유발함에 CD16A에 대한 2가 및 NK 세포에 대한 겉보기 친화성이 유리함을 시사한다. 참고로, CD16A 단독에 대한 2가는 NK 세포 활성화를 매개하기에 충분하지 않았는데, 이는 NK 세포 활성화 마커 CD69의 항체 유도 발현 및 인간 PBMC 배양에서 사이토카인 방출이 표적 세포의 존재에 엄격하게 의존하였기 때문이다 (도 49A-49F). 더욱이, NK 세포 관여 ROCK® 항체에 의해 인간 PBMC 배양물에서 방출된 염증성 사이토 카인 수준은 BCMA-지시된 T 세포 관여항체에 의해 방출된 것보다 수 배 더 낮았다 (도 50).
BCMA-표적화 ROCK 관여항체에서 수득된 결과와 유사하게, EGFR-표적화 ROCK® 관여항체, EGFR-표적화 ROCK® 관여항체는, 동일한 이펙터-및 표적-결합 도메인들을 포함하는 Fc에 S239D/I332E 돌연변이를 가진 Fc-강화된 항-EGFR IgG1 (IgAb_D), 전형적인 EGFR-표적화 IgG1 (IgAb_B) 또는 1가 결합 이중특이적 관여항체 (BiKE)와 비교하였을 때, SW-982 및 A-431 표적 세포에 대한 사멸 분석에서 한 자릿수 pM EC50 값에 도달하여 우수한 역가를 보였다 (도 29D, 및 도 51). EGFR/CD16A aTriFlex_A는 다른 ROCK® 관여항체 (도 27A-27C)보다 인간 NK 세포에 대한 겉보기 친화성이 실질적으로 낮음에도 불구하고 Fc-강화 항 EGFR IgG1 (IgAb_D)과 유사한 역가를 보여주었다 (도 51). BCMA-표적화 scFv-IgAb_E는 EGFR 양성, BCMA 음성 표적 세포주 A-431에 대한 살해 활성을 나타내지 않았기 때문에 비특이적 살해를 배제 할 수 있다 (도 51).
다양한 BCMA/CD16A 관여항체의 겉보기 친화성 및 도 29E에 나타낸 시험관내 세포독성 분석에서 각각의 역가에 대한 분석은 NK 세포에서 CD16A에 대한 겉보기 친화성과 역가의 상관관계를 시사한다. 이러한 상관관계는 2:1의 E:T에서 RPMI-8226 표적 세포에 대한 3시간 세포독성 분석에서 관찰되었을 뿐만 아니라 5:1의 E:T 비율에서 NCI-H929 표적 세포에 대한 4시간 분석에서도 관찰되었는데, 이는 NK 세포에서 CD16A에 대한 높은 친화성 결합이 우수한 세포독성 역가에 기여함을 시사한다.
기존의 그리고 Fc-조작된 항-CD30 항체들과 비해 ROCK® CD30/CD16A 표적화 TandAb의 우수성은 생리학적 수준의 경쟁 IgG 존재하에서 시험관내 세포독성 분석을 실시하였을 때 더욱 두드러졌다. 10mg/mL 다클론 IgG의 보충으로 모든 배양물에서 배경 용해가 명확하게 증가했으며 (도 52B), NK 세포에 의한 혈청 IgG-유도된 탈과립화로 인한 것일 가능성이 가장 높다 (Jacobi 외, Clin. Immunol. 2009;133:393-401). 그러나, 단일클론 IgG (도 52C) 또는 Fc-조작된 IgG (도 52D)와의 경쟁은 기존 항체의 활성을 완전히 차단하거나 역가 및 효능을 명백히 손상시킨다. ROCK CD30/CD16A TandAb 항체는 생리학적 농도의 경쟁 IgG의 존재하에서 조차도 모든 테스트 조건들하에서 최대의 세포독성 역가 및 효능을 보여주었다 (도 52A-52D, 표 10).
CD30/CD16A TandAb, 항-CD30 IgG1 (IgAb), 또는 Fc-강화된 항-CD30 IgG1 (IgAb (Fc-강화))의 연속 희석물의 존재하에서 이펙터 세포로서 일차 인간 NK 세포들과 칼세인-표지된 CD30+ KARPAS-299 표적 세포들을 5:1의 E:T 비율로 이용한 4시간 칼세인-방출 세포독성 분석. 분석은 RPMI 1640 배지 단독에서, 또는 10 mg/mL 다클론 인간 IgG, 10 mg/mL 단클론 항-EGFR IgG1 (IgAb_B), 또는 10 mg/mL Fc-강화된 항-EGFR IgG1 (IgAb_D (Fc-강화))로 보충한 배지에서 수행되었다.
PK의 조절
치료용 항체의 또 다른 중요한 매개변수는 혈청 반감기이다. 세포독성이 높은 항체의 경우, 빠른 제거를 가능하게 하는 짧은 반감기가 선호 될 수 있다. 대조적으로, 좋은 안전성 프로파일을 가진 항체의 경우, 잦은 투여 또는 지속적인 주입의 필요성을 피함으로써 환자의 편의를 높이기 위해 더 긴 반감기가 선호 될 가능성이 있다.
선택된 일련의 ROCK® 플랫폼 형태들의 기본 약동학 매개변수를 CD-1 SWISS 마우스에서 평가하였다. ROCK® 관여항체의 IgG-유사 패밀리의 경우, N-말단 Fab에 항-CD16 모이어티를 포함하거나 CH3의 C-말단에 융합된 scFvs와 같은 2개의 대표적인 scFv-IgAb 항체들 (scFv-IgAb_A 및 scFv-IgAb_D)이 선택되었다. ROCK® 관여항체의 Fc 융합 패밀리의 경우, 대칭 Bi-scFv-Fc_A 및 비대칭 scDb 함유 KiH-scDb-Fc_A 항체가 분석되었다. 마지막으로 Fab 융합 및 무-Fc 패밀리의 경우, PK 분석을 위해 TandAb_B, aTriFlex_A, aTriFlex_B 및 scDb-Trib_A 항체가 선택되었다. 후자 2개는 PK-확장을 위해 aTriFlex_A에서의 고 친화성 HSA 결합 도메인에 비해 낮은 친화성을 갖는 HSA-결합 모이어티를 사용한다. 선택된 ROCK® 관여항체에서 종양 표적화 도메인은 인간 EGFR 또는 BCMA에 특이적이었다. 표적-및 CD16A-결합 모이어티 모두 해당 마우스 유사체에 교차 반응하지 않기 때문에 (데이터는 표시되지 않음), 표적-관련 약력학적 효과를 가정 할 수 없다. 0.3 mg (~10 mg/kg 체중)의 다양한 테스트 항목을 단회 정맥 투여받은 동물들의 혈청 샘플들을 1주 또는 3주 동안 서로 다른 시점에서 수집하고 ELISA 또는 MSD 기술을 기반으로 한 확립된 분석법으로 분석했다. 기본 약동학 매개변수는 비-구획 약동학 분석에 의해 결정되었다 (표 11). 표 11의 구조들에서 표시된 기호는 도 23에 표시된 기호와 일치한다. 상이한 ROCK® 형태들을 정맥내 투여 후, 혈청 농도는 이중지수 방식으로 감소했다 (도 30). 두 IgG-유사 형태들 모두의 반감기는 각각 329.2 및 364.3 시간으로 동일한 범위내에 있는 것으로 나타났으며 이는 표준 IgG 분자들과 비등한 것이다63. Fc 융합 형태들 Bi-scFv-Fc_A 및 KiH-scDb-Fc_A에 대해 각각 95.8 또는 74.3 시간의 보다 짧은 반감기가 측정되었다. 이들의 혈청 반감기는 IgG-유사 및 무-Fc 및 Fab 융합 ROCK® 형태들 사이에 존재하였다. 그러나 Bi-scFv-Fc_A의 관찰 기간은, 두 가지 scFv-IgAb 형태들 모두의 경우 3주였던 것에 비해 단 1주였다. 그러므로, 이 값은 과소평가될 수 있다. 가장 짧은 반감기는 무-Fc 및 Fab 융합 ROCK® 형태들에서 측정되었다. 평균 겉보기 최종 반감기는 고 친화성 항-HSA 결합 모이어티를 포함하는 aTriFlex_A의 경우 37.4 시간, TandAb의 경우 18.0 시간이었다. scDb-Trib_A의 저 친화성 항-HSA 도메인은 이 구조체의 반감기 (14.0 시간)를 연장 할 수 없다. 순환계에서 변화되지 않은 약물을 정의하는 평균 체류 시간 (MRT)을 기반으로 유사한 순위결정이 수행 될 수 있다. 가장 높은 MRT는 IgG-유사 및 Fc 융합 테스트 항목에 대해 528.5 내지 110.6 시간으로 나타났으며, 뒤이어 각각 TandAb, aTriFlex 및 scDb-Trib로 표시되는 무-Fc 및 Fab 융합 형태의 경우 61.6 내지 28.5 시간의 비교적 짧은 MRT 값을 보였다. 이러한 순위는 0.006 내지 1.228 mL/h 범위의 클리어런스 (C)에 대해서도 적용되며, 가장 높은 값은 Fc도 항-HSA 도메인도 포함하지 않는 TandAb 구조체에서 수득되었다. 중요한 매개변수는 또한 시간 경과에 따른 유기체 내 분자의 최대 양 또는 노출을 정의하는 곡선 아래 면적 (AUC)에 의해 결정된다. 예상대로 가장 높은 AUC 값들은 Fc-함유 형태들에서 도달되었다. 더 작은 무-Fc 형태에 대해 거의 10-배 더 낮은 값이 측정되었다. 또 한번, TandAb는 긴 반감기의 테스트 항목들에 비해 AUC에 있어 100-배 차이인 가장 낮은 노출을 나타내었다. 약물이 신체 전체에 고르게 분포되어있는 경우 신체의 총 약물 양을 설명하는 데 필요한 겉보기 부피를 정의하는 정상 상태 분포 부피 (Vss)는 TandAb에서 가장 높았고 (4.8 mL), 이에 이어 두 가지 IgG-유사 (각각 3.3 mL 및 3.1 mL), Fc 융합 (2.2 mL), aTriFlex (2.2 mL) 및 scDb 트리바디 (1.5 mL)였다. scDb 트리바디의 Vss 값이 낮다는 것은 분자의 대부분이 혈액 구획 (혈액)에 잔류함을 의미한다. 결론적으로, 서로 다른 ROCK® 형식은 반감기가 14 내지 364 시간인 CD-1 마우스에서 뚜렷한 PK 프로파일을 보여주었다.
표 11: 마우스 PK 연구에서 분석된 ROCK® 형태들
실시예 8-CD16A/BCMA 결합 항체의 활성
8.1.
CD16A/BCMA 결합 항체
본 실시예에서, CD16A/BCMA 결합 항체: CD16A/BCMA 항체 I, CD16A/BCMA 항체 II 및 CD16A/BCMA 항체 III에 대한 연구가 제시된다.
본 실시예에 제시된 데이터에 의해 입증된 바와 같이, CD16A/BCMA 항체 I은 ADCC와 유사한 메커니즘으로 다발성 골수종을 치료하는데 사용하기 위한 NK 세포 관여항체이며 유리한 안전성 프로파일로 상당한 활성을 달성할 가능성을 가지고 있다. 또한, CD16A/BCMA 항체 I은 다라투무맙 (항-CD38 항체) 내성 및 불응성 다발성 골수종 환자를 치료할 가능성이 있는 것으로 나타났다. 또한, CD16A/BCMA 항체 I은 다발성 골수종에 대한 다른 치료제, 예를 들어, 항체를 포함하는 치료제 (항-TIGIT 항체, 항-PD1 항체, 항-PD-L1 항체 및 항-VEGF 항체를 포함 하나 이에 제한되지 않음) 및 사이토카인 (예컨대, IL-12, IL-2 등)을 포함하는 치료제와 조합 될 수 있다.
8.1.1. CD16A/BCMA 항체 I
CD16A/BCMA 항체 I은 도 13에 도시된 구조를 갖는 scFv-IgAb 항원-결합 단백질이며, 이는 (a) 동종이량체 인간 IgG CH2-CH3 Fc 부분의 C-말단에 VL-VH 순서로 융합된 scFv 형태의 2개의 CD16A 항원-결합 모이어티, 및 (b) IgG의 Fab 아암에서 각 Fv에 의해 제공되는 2개의 표적 항원-결합 모이어티를 포함하고, 여기서 표적 항원-결합 모이어티는 BCMA에 결합한다.
각각의 상기 CD16A 항원-결합 모이어티는 서열 번호:73에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:74에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:75에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:76에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:77에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:78에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함한다. CDR은 Kabat 넘버링 체계에 따라 식별된다. 각각의 CD16A 항원-결합 모이어티는 서열 번호: 3에 제시된 아미노산 서열을 갖는 VH 및 서열 번호: 2에 제시된 아미노산 서열을 갖는 VL을 포함한다.
CD16A/BCMA 항체 I의 CD16A 항원-결합 모이어티는 해당 분자의 Fc 부분의 C-말단에 융합되며 (서열 번호 22에 제시된 아미노산 서열을 갖는) 연결기를 통해 다음 순서로 연결된다: VL (CD16A)-링커 L3-VL (CD16A), 여기서 링커 L3는 서열 번호: 18에 제시된 아미노산 서열을 가진다.
각각의 상기 BCMA-표적화 모이어티는 서열 번호:67에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:68에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:69에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:70에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:71에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:72에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함한다. CDR은 Kabat 넘버링 체계에 따라 식별된다. 각각의 BCMA-표적화 모이어티는 서열 번호: 65에 제시된 아미노산 서열을 갖는 VH 및 서열 번호: 66에 제시된 아미노산 서열을 갖는 VL을 포함한다.
CD16A/BCMA 항체 I은 2개의 CD16A 항원-결합 모이어티 및 2개의 BCMA-표적화 모이어티를 포함하며, 여기서 (a) 각각 2개의 상기 CD16A 항원-결합 모이어티는 서열 번호:73에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:74에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:75에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:76에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:77에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:78에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함하고; 그리고 (b) 각각 2개의 상기 BCMA-표적화 모이어티는 서열 번호:67에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:68에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:69에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:70에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:71에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:72에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함한다.
CD16A/BCMA 항체 I에 대한 CD16A 항원-결합 모이어티 및 BCMA-표적화 모이어티의 CDR 서열들의 요약이 도 53A 및 53C에 도시되어 있다.
CD16A/BCMA 항체 I은 2개의 CD16A 항원-결합 모이어티 및 2개의 BCMA-표적화 모이어티를 포함하고, 여기서 (a) 2개 CD16A 항원-결합 모이어티 각각은 서열 번호: 3에 제시된 아미노산 서열을 포함하는 VH, 및 서열 번호: 2에 제시된 아미노산 서열을 포함하는 VL을 포함하고; 및 (b) 2개 BCMA-표적화 모이어티 각각은 서열 번호: 65에 제시된 아미노산 서열을 포함하는 VH, 및 (ii) 서열 번호: 66에 제시된 아미노산 서열을 포함하는 VL을 포함한다.
CD16A/BCMA 항체 I에 대한 CD16A 항원-결합 모이어티 및 BCMA-표적화 모이어티의 VH 및 VL 서열의 요약이 도 53B 및 53D에 도시되어 있다.CD16A/BCMA 항체의 Fc 부분은 인간 IgG1 CH2 및 CH3 중쇄 불변 도메인을 포함하는 침묵된 Fc 부분이며, 이는 서열 번호: 29에 제시된 아미노산 서열을 포함한다. CH2 중쇄 불변 도메인은 2개의 침묵 돌연변이 ("무-이펙터 돌연변이"라고도 함): L234F 및 L235E를 가진다. CH2 중쇄 불변 도메인은 서열 번호: 79에 제시된 아미노산 서열을 포함한다. CH3 중쇄 불변 도메인은 서열 번호: 109에 제시된 아미노산 서열을 포함한다. BCMA 표적화 모이어티에 연결되는 CH1 중쇄 불변 도메인은 서열 번호: 33에 제시된 아미노산 서열을 포함한다.
CD16A/BCMA 항체 I은 BCMA-표적화 모이어티의 VH, 동종이량체 인간 IgG CH2-CH3 Fc 부분, 하나의 CD16A 항원-결합 모이어티를 포함하는 폴리펩티드 사슬 1을 포함하며, 여기서 폴리펩티드 사슬 1은 서열 번호: 61에 제시된 아미노산 서열을 가진다. CD16A/BCMA 항체 I은 BCMA-표적화 모이어티의 VL를 포함하는 폴리펩티드 사슬 2를 포함하고, 여기서 폴리펩티드 사슬 2는 서열 번호: 62에 제시된 아미노산 서열을 가진다.
8.1.2. CD16A/BCMA 항체 II
CD16A/BCMA 항체 II는 도 23에 도시된 구조를 가지는 무-Fc TandAb로서 ("TandAb"의 구조 참고), 2개의 CD16A 항원-결합 모이어티 및 2개의 표적 항원-결합 모이어티를 포함하고, 여기서 CD16A 항원-결합 모이어티는 scFv의 형태로 제공되고 표적 항원-결합 모이어티의 VH와 VL 사이에 위치한다.
CD16A 항원-결합 모이어티는 다음 순서로 표적 항원-결합 모이어티에 융합된다 :
VH BCMA-링커 L5-VL CD16A-링커 L6-VH CD16A-링커 L5-VL BCMA
링커 L5는 서열 번호: 129에 제시된 아미노산 서열을 가진다. 링커 L5는 서열 번호: 130에 제시된 아미노산 서열을 가진다.
각각의 상기 CD16A 항원-결합 모이어티는 서열 번호:73에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:74에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:75에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:76에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:77에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:78에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함한다. CDR은 Kabat 넘버링 체계에 따라 식별된다. 각각의 CD16A 항원-결합 모이어티는 서열 번호: 3에 제시된 아미노산 서열을 갖는 VH 및 서열 번호: 2에 제시된 아미노산 서열을 갖는 VL을 포함한다.
각각의 상기 BCMA-표적화 모이어티는 서열 번호:67에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:68에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:69에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:70에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:71에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:72에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함한다. CDR은 Kabat 넘버링 체계에 따라 식별된다. 각각의 BCMA-표적화 모이어티는 서열 번호: 65에 제시된 아미노산 서열을 갖는 VH 및 서열 번호: 66에 제시된 아미노산 서열을 갖는 VL을 포함한다.
CD16A/BCMA 항체 II는 2개의 폴리펩티드를 포함하고, 이들 각각은 서열 번호: 126에 제시된 아미노산 서열을 가진다.
8.1.3. CD16A/BCMA 항체 III
CD16A/BCMA 항체 III은 도 5에 도시된 구조를 가지는 KiH-scDb-Fc이며, 이는 (a) IgG CH2-CH3 Fc 부분의 C-말단에 VL-VH-VL-VH의 순서로 융합된 scDb 형태의 2개의 CD16A 항원-결합 모이어티, 및 (b) Fc 부분의 N-말단에 융합된 scFv 형태의 단일 표적 항원-결합 모이어티를 포함하고, 여기서 상기 표적 항원-결합 모이어티는 BCMA에 결합한다.
각각의 상기 CD16A 항원-결합 모이어티는 서열 번호:73에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:74에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:75에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:76에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:77에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:78에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함한다. CDR은 Kabat 넘버링 체계에 따라 식별된다. 각각의 CD16A 항원-결합 모이어티는 서열 번호: 3에 제시된 아미노산 서열을 갖는 VH 및 서열 번호: 2에 제시된 아미노산 서열을 갖는 VL을 포함한다.
CD16A 항원-결합 모이어티는 이종이량체 Fc 부분에 융합되고 서열 번호: 20에 제시된 아미노산 서열을 갖는 연결기를 통해 다음 순서로 연결된다: VL (CD16A)-링커 L1-VH (CD16A)-링커 L2-VL (CD16A)-링커 L1-VH (CD16A). 링커 L1은 서열 번호: 16에 제시된 아미노산 서열을 갖고, 링커 L2는 서열 번호: 17에 제시된 아미노산 서열을 갖는다.
상기 BCMA-표적화 모이어티는 서열 번호:67에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:68에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:69에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:70에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:71에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:72에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함한다. CDR은 Kabat 넘버링 체계에 따라 식별된다. 각각의 BCMA-표적화 모이어티는 서열 번호: 65에 제시된 아미노산 서열을 갖는 VH 및 서열 번호: 66에 제시된 아미노산 서열을 갖는 VL을 포함한다.
CD16A/BCMA 항체 III은 2개의 CD16A 항원-결합 모이어티 및 하나의 BCMA-표적화 모이어티를 포함하며, 여기서 (a) 각각 2개의 상기 CD16A 항원-결합 모이어티는 서열 번호:73에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:74에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:75에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:76에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:77에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:78에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함하고; 그리고 (b) 상기 BCMA-표적화 모이어티는 서열 번호:67에 제시된 아미노산 서열을 포함하는 VH CDR1, 서열 번호:68에 제시된 아미노산 서열을 포함하는 VH CDR2, 서열 번호:69에 제시된 아미노산 서열을 포함하는 VH CDR3, 서열 번호:70에 제시된 아미노산 서열을 포함하는 VL CDR1, 서열 번호:71에 제시된 아미노산 서열을 포함하는 VL CDR2, 및 서열 번호:72에 제시된 아미노산 서열을 포함하는 VL CDR3를 포함한다.
CD16A/BCMA 항체 III의 Fc 부분은 서열 번호: 31에 제시된 아미노산 서열을 가지는 인간 IgG1 CH2 및 CH3 중쇄 불변 도메인을 포함하는 침묵된 Fc 부분이다. CH2 중쇄 불변 도메인은 2개의 침묵 돌연변이 ("무-이펙터 돌연변이"): L234F 및 L235E를 가진다. CH2 중쇄 불변 도메인은 서열 번호: 79에 제시된 아미노산 서열을 포함한다. CH3 중쇄 불변 도메인은 1개의 침묵 돌연변이 (무-이펙터 돌연변이) D265A를 가진다. CH3 중쇄 불변 도메인은 서열 번호: 81에 제시된 아미노산 서열을 포함한다.
CD16A/BCMA 항체 III은 IgG CH2-CH3 Fc 부분 및 2개의 CD16A 항원-결합 모이어티를 포함하는 폴리펩티드 사슬 1을 포함하며, 여기서 폴리펩티드 사슬 1은 서열 번호: 63에 제시된 아미노산 서열을 가진다. CD16A/BCMA 항체 III은 하나의 BCMA-표적화 모이어티를 포함하는 폴리펩티드 사슬 2를 포함하고, 여기서 폴리펩티드 사슬 2는 서열 번호: 64에 제시된 아미노산 서열을 가진다.
8.2. 결합 특성
CD16A/BCMA 항체 I 및 CD16A/BCMA 항체 III는 둘 다 CD16A에 특이적으로 결합하지만 CD16B에는 결합하지 않는다. CD16A/BCMA 항체 I는 CD16A 및 BCMA에 대한 높은 결합 친화성을 가진다, 예를 들어, 이 항체는 약 16 nM의 KD로 CD16A에 결합하고, 약 2 nM의 KD로 BCMA에 결합한다.
CD16A/BCMA 항체 I에는 ELISA로 확인시 FcγR 결합이 없다. CD16A/BCMA 항체 I는 Fc 영역을 통해 CD16A에 결합하지 않기 때문에 CD16A 다형성과 무관하게 CD16A에 결합한다. 예를 들어, 다발성 골수종 세포주에 대한 CD16A/BCMA 항체 I의 세포 독성은 같은 날 CD16A-158V/V 건강한 공여체와 CD16A-158F/F 건강한 공여체에 대해 평가되었다. 결과를 도 31A 및 31B에 나타낸다. CD16A/BCMA 항체 I은 CD16A-158V/V와 비교하여 CD16A-158F/F에서 변화가 없거나 심지어 증가된 활성을 나타냈다. 대조적으로, Fc 영역에 의해 CD16a에 결합하는 다라투무맙은 CD16A-158V/V에 비해 CD16A-158F/F 에서 감소된 활성을 보여주었다. 다발성 골수종 세포주에 대한 CD16A/BCMA 항체 I의 세포독성 또한 CD16A-158V/F 건강한 공여자에서 평가되었으며, 이는 CD16A-158F/F 및 CD16A-158V/V에서 관찰된 세포독성 사이에 존재하였다 (데이터는 표시되지 않음).
8.3 다발성 골수종 표적 세포의 시험관내 세포독성
8.3.1. 칼세인 AM 세포독성 분석을 사용한 세포독성 평가
칼세인 AM 세포독성 분석은 이펙터 세포로서 인간 NK 세포를 사용하고 표적 세포로서 다발성 골수종 세포주를 사용하여 수행되었다. 간단히 말해서, 표적 세포를 무-혈청 배지를 사용하여 37°C에서 30분 동안 10 uM 칼세인 AM (Thermo Fisher Scientific; Waltham, MA)으로 새로이 표지하였다. 원심분리하여 2회 세척한 후, 세포를 분석 배지 (10% 열-불활성화 소 태아 혈청으로 보충된 RPMI 1640)에 재현탁시키고 1 X 104 세포/웰의 밀도로 96-웰, U-바닥 조직 배양 플레이트에 분배하였다. 이어서 새로 준비된 이펙터 세포를 5 X 104 세포/웰의 밀도로 각 웰에 첨가하였다. 30분 배양 후, 테스트 샘플 (0.64, 3.2, 16, 80, 400 및 2000 pm)의 연속 희석액을 플레이트에 첨가하고 5% CO2가 있는 가습 배양기에서 37°C에서 추가로 4시간 동안 배양하였다. 배양 후, 플레이트를 300 x g에서 10분 동안 원심분리하였다. 상청액을 검은색 불투명 96-웰 마이크로플레이트 (OptiPlate-96; PerkinElmer; Waltham, MA)로 옮기고 Infinite M1000 PRO 플레이트 판독기 (Tecan Trading AG; Mδnnedorf)를 사용하여 495/515 nm에서의 여기/방출로 상대 형광 단위 (RFU)로 형광 신호를 측정하였다. 표적 세포만을 포함하는 웰의 신호는 표지된 세포로부터 칼세인의 자발적 방출을 나타내는 반면 10% Triton X-100 (Sigma-Aldrich; St. Louis, MO)으로 용해된 표적 세포를 포함하는 웰은 최대 방출을 나타낸다. 비특이적 이펙터 세포 매개된 세포독성은 테스트 샘플을 첨가하지 않은 표적 및 이펙터 세포를 포함하는 웰에서 측정되었다. 특이적 세포독성의 정도는 다음과 같이 계산되었다:
%세포독성 = 100 * (실험상의 방출 - 비특이적 방출)/(최대 방출 - 자발적 방출)
GraphPad Prism 6 소프트웨어 (GraphPad 소프트웨어; San Diego, CA)를 사용하여 4 -매개변수 비선형 회귀 모델에 적합시켜 데이터를 분석하고 플롯하였다.
결과를 표 12에 나타낸다.
8.3.2. FACS를 사용한 세포독성 평가
건강한 인간 혈액 공여체 A로부터 인간 PBMC 및 분리된 NK 세포를 분리하고 추후 실험을 위해 냉동시켰다. 해동시 PBMC는 트리판 블루 염색에 의해 ~85% 생존가능하였으며 추후 7AAD를 사용하는 FACS에 의해 확인되었다. PBMC를 E:T 비율이 약 0.4 또는 약 4-5 인 BCMA+ 다발성 골수종 종양 세포주와 공배양하였고, 5% CO2와 함께 37°C에서 약 20시간 동안 0.1 - 3000pM의 3-배 연속 희석 테스트 항목들에 노출시켰다. 항체 염색 및 FACS를 사용하여 MM 종양 세포에서 BCMA 발현을 결정하고 다발성 골수종 표적 세포의 세포독성을 모니터하였다. 데이터는 소프트웨어 프로그램 FlowJo 및 GraphPad Prism 6으로 분석되었다. 결과를 도 32A-32E, 33A-33C, 및 34A-34C에 나타낸다. 도 32A-32E는 CD16A/BCMA 항체 I이 약 0.4의 E:T 비율에서 효능이 있었음을 보여준다 (다발성 골수종 환자의 코호트로부터 결정됨). 도 33A-33C 및 34A-34C는 CD16A/BCMA 항체 I에 노출된 인간 NK 세포가 BCMA+ 표적 세포를 특이적으로 표적화하여 고갈시켰음을 보여준다.
두 방법에 의한 평가는 CD16A/BCMA 항체 I가 광범위한 표적 발현 수준에 걸쳐 시험관내에서 효능이 있음을 입증한다. 관찰된 효능은 E:T 비율과 상관관계가 없었고 BCMA 발현과도 상관관계가 없었다. 또한, CD16A/BCMA 항체 I는 다발성 골수종 세포주에서 다라투무맙과 유사한 효능을 나타냈다. 도 33A-33C를 참고하라.
8.4. 낮은 BCMA 발현 종양 세포에 대한 시험관내 세포독성
CD16A/BCMA 항체 I의 낮은 BCMA 발현 Raji 종양 세포주에 대한 시험관내 세포 독성을 칼세인 방출 분석 및 FACS로 평가하였다. 위에서 설명한, 다발성 골수종 표적 세포의 시험관내 세포 독성을 평가하기 위해 사용된 칼세인 방출 분석이 본 연구에서 사용되었다. 새로 준비한 NK 세포와 Raji Burkitt 림프종 종양 세포주의 E:T 비율은 약 5였다. 결과를 도 35A-35D에 나타낸다. 거의 탐지불가능한 BCMA 표면 발현에도 불구하고 CD16A/BCMA 항체 I, CD16A/BCMA 항체 II 및 CD16A/BCMA 항체 III에서 BCMA+ 표적 세포의 시험관내 용해가 관찰되었다.
FACS 분석을 위해 건강한 인간 혈액 공여체로부터 인간 NK 세포를 분리했다. NK 및 Raji 세포는 0.5 mg/ml 저 내독소 hIgG와 별도로 분석 셋업 전 적어도 1시간 동안 사전배양되었다. NK 세포를 Raji Burkitt 림프종 종양 세포주와 대략 5의 E:T 비율로 공배양하고, 5% CO2와 함께 37°C에서 약 20시간 동안 10 - 1000pM의 3-배 연속 희석 테스트 항목들에 노출하였다. 항체 염색과 FACS를 사용하여 RAJI 표적 세포의 세포독성을 모니터하였다. 데이터는 소프트웨어 프로그램 FlowJo 및 GraphPad Prism 6으로 분석되었다. 결과를 도 36A-36C에 나타낸다. 도 36C에서 보는 바와 같이, CD16A/BCMA 항체 I은 낮은 BCMA 발현 Raji 종양 세포주에 대해 시험관내 세포독성을 나타냈다.
8.5. 자가 BCMA
+
정상 인간 형질 세포에 대한 시험관내 활성
CD16A/BCMA 항체 I의 자가 BCMA+ 정상 인간 형질 세포에 대한 시험관내 활성을 FACS로 평가하였다. 건강한 인간 혈액 공여체의 말초 혈액으로부터 인간 NK를 분리하였다. 동일한 인간 공여체의 골수를 사용하여 인간 형질 세포를 분리하였다. NK, 형질 세포 및 NCI-H929 세포는 0.5 mg/ml 저 내독소 hIgG와 별도로 분석 셋업 전 적어도 1시간 동안 사전배양되었다. 동종이계: NK 세포는 대략 3의 E:T 비율로 NCI-H929 종양 세포주와 공배양되었으며, 동시에 5% CO2와 함께 37°C에서 약 20 시간 동안 3 - 3000pM 범위의 3-배 연속 희석 테스트 항목들에 노출되었다. 자가: NK 세포를 대략 23의 E:T 비율로 인간 형질 세포와 공배양하고 상기 기재된 바와 같이 테스트 항목들과 함께 배양하였다. 항-CD56 E-450 및 CD138-APC로 항체 염색 후 FACS를 사용하여 H929 및 형질 세포의 세포독성을 모니터하였다. 데이터는 소프트웨어 프로그램 FlowJo 및 GraphPad Prism 6으로 분석되었다.
결과를 도 37A 및 37B에 나타낸다. CD16A/BCMA 항체 I은 자가 BCMA+ 정상 인간 형질 세포에 대한 시험관내 활성을 나타내었다.
8.6. BCMA
+
표적 세포의 부재시 CD16A의 활성화 결여
본 발명자들은 또한 CD16A/BCMA 항체 I이 BCMA+ 표적 세포 부재시 NK 세포를 활성화 할 수 있는지 여부를 조사했다. 먼저, BCMA+ 표적 세포의 존재시 NK 세포에서 CD16의 활성화 및 CD16 수준 유지를 연구하였다. NK 세포는 두 명의 독립적인 건강한 인간 혈액 공여체로부터 유래된 것이었다. NK 세포를 MM.1S BCMA+ 표적 세포와 공배양하고 0, 0.03 또는 0.1 nM의 항-BCMA/CD16A 항체 I 또는 Ab-1 (음성 대조/ CD16a) 또는 항-CD38 (DARA 양성 대조)에 37°C에서 20시간 동안 노출시켰다. 항체 염색 및 FACS를 사용하여 각각 도 34A 및 34B에 도시된 바와 같이 살아있는 CD56dim/CD16+ 세포 및 CD56dim/CD16+/CD69+/CD25+의 수를 결정하였다. BCMA+ 표적 세포의 고갈은 도 34C에 제시되어 있다. 데이터는 소프트웨어 프로그램 FlowJo 및 GraphPad Prism 6으로 분석되었다. 결과를 도 38A-38C에 나타낸다. CD16A/BCMA 항체 I은 BCMA+ 표적 세포의 존재시 NK 세포에서 CD16 수준을 활성화하고 유지하였다.
다음으로, BCMA+ 표적 세포의 부재시 NK 세포에서 CD16의 활성화 및 CD16 수준 유지를 연구하였다. NK 세포는 두 명의 독립적인 건강한 인간 혈액 공여체로부터 유래된 것이었다. NK 세포를 단독 배양하고 0, 0.03 또는 0.1 nM의 항-BCMA/CD16a 항체 I 또는 Ab-1 (음성 대조/ CD16a) 또는 항-CD38 (DARA 양성 대조)에 37°C에서 20시간 동안 노출시켰다. CD 마커 (CD56, CD16, CD69 및 CD25)에 대한 항체 염색 및 FACS를 사용하여 각각 도 32A 및 32B에 도시된 바와 같이 살아있는 CD56dim/CD16+ 세포 및 CD56dim/CD16+/CD69+/CD25+의 수를 결정하였다. 데이터는 소프트웨어 프로그램 FlowJo 및 GraphPad Prism 6으로 분석되었다. 결과를 도 39A-39C에 나타낸다. 도 39A-39C에서 보는 바와 같이, CD16A/BCMA 항체 I은 BCMA+ 표적 세포의 부재시 NK 세포에서 CD16 수준을 활성화하거나 감소시키지 않았다. 다라투무맙과 비교하여, BCMA+ 표적 세포의 부재시 CD16A/BCMA 항체 I은 NK 세포에서 CD16+ 의 수 및 발현에 있어서 최소한의 감소를 나타내었고 유의하게 보다 적은 CD69+25+ NK 세포수를 나타냈다 (예컨대, ~100-배 (n = 2의 공여체; 단회 실험)). BCMA+ 표적 세포 존재시, CD16A/BCMA 항체 I은 다라투무맙과 유사한 활성을 보여주었다. 도 38C를 참고하라.
8.7. 혈청 Ig의 존재시 활성
혈청 또는 Ig 존재시 CD16A/BCMA 항체 I의 NK 세포에 대한 결합 및 CD16A/BCMA 항체 I의 세포독성 및 NK 생존을 연구하였다.
건강한 인간 혈액 공여체로부터 인간 NK 세포를 분리했다. NK 세포 및 NCI-H929 세포 또는 MM.1S 세포를 분석 셋업 전 2시간 동안 10mg/mL 혈청 Ig, 50% 인간 자가 혈청 또는 100% 인간 혈청에서 별도로 사전배양하였다. NK 세포를 NCI-H929 또는 MM.1S 세포와 대략 5의 E:T 비율로 공배양하고, 5% CO2와 함께 37°C에서 약 20시간 동안 0.1 - 100pM의 10-배 연속 희석 테스트 항목들에 노출하였다. CD138 및 CD56를 이용한 항체 염색 후 FACS를 사용하여 MM.1S 또는 NCI-H929 표적 세포의 세포독성 및 NK 생존을 모니터하였다. 데이터는 소프트웨어 프로그램 FlowJo 및 GraphPad Prism 6으로 분석되었다.
도 40A에서 보는 바와 같이, CD16A/BCMA 항체 I은 Ig 또는 혈청 부재시에 비해 10 mg/mL Ig 또는 혈청 존재시 감소된 친화성으로 NK 세포에 결합 할 수 있었다. 도 40B에서 보는 바와 같이, CD16A/BCMA 항체 I은 Ig 또는 혈청 부재시에 비해 혈청 존재시 감소된 역가로 BCMA+ 표적 세포들을 사멸시킬 수 있었다. 도 40C 및 40D에서 보는 바와 같이, CD16A/BCMA 항체 I은 NK 세포 손실 없이 50% 자가 인간 혈청 존재시 BCMA+ 표적 세포를 고갈시켰다. 도 40D 및 40E에서 보는 바와 같이, CD16A/BCMA 항체 I은 NK 세포를 고갈시키지 않았으나 다라투무맙은 고갈시켰다. 따라서 인간 Ig는 CD16A/BCMA 항체 I의 NK 활성을 방해하지 않을 것이다.
BCMA+ 표적 세포의 부재시, 혈청은 CD16A 발현 및 NK 세포의 활성화에 영향을 주었다. 도 41A 및 41B를 참고하라. 도 41A에서 보는 바와 같이, 혈청은 CD16A 발현을 감소시켰다. 도 41B에서 보는 바와 같이, 혈청은 NK 세포의 비-표적화 매개 활성화를 증가시켰다. 따라서, 혈청의 존재시 낮은 CD16 발현은 NK 세포의 비-CD16A 매개 활성화를 시사한다.
8.8. 사이토카인과의 조합 요법
다라투무맙 및 엘로투주맙은 면역조절 약물 (IMiDs) 및 프로테아좀 억제제와 조합시 효과적이다. 조합 활성의 메커니즘이 NK 세포 관여항체에 적용될 것으로 예상된다. 예를 들어, IMiD는 TNF-α, IL-12, 및 IL-6 생성에 영향을 미치고 T 세포가 IL-2 및 IFN-γ를 분비하도록 자극하여 NK 세포 수와 기능을 간접적으로 향상시킨다 (Liu 외, Jour. Of Leukocyte. (2018);103(5):821-828). 프로테아제 억제제는 MH 클래스 I의 발현을 감소시킨다. CD16A/BCMA 항체 I을 iMiD와 조합하는 이론적 근거에는 다음이 포함된다: IL-15는 증식을 통해 NK 세포수를 증가시키고, 항-TIGIT 항체는 CD8+ T 세포 및 NK 세포에 대한 체크포인트 억제제이며, 항-FcRH5/CD3 항체는 이들의 세포독성 가능성을 위해 NK 세포를 사용하여 또 다른 T 세포 침윤을 종양으로 유도한다.
사이토카인 처리가 CD16A/BCMA 항체의 활성에 영향을 미칠 수 있는지 조사하기 위해 IL-15를 CD16A/BCMA 항체 I의 처리에 추가하였다. 도 42A 및 42B에서 보는 바와 같이, IL-15는 MM 세포에서 CD16A/BCMA 항체 I의 활성을 증가시켰다. IL-15를 첨가한 CD16A/BCMA 항체 I에서 MM 고갈의 증가가 관찰되었지만 다라투무맙에서는 그렇지 않았다.
8.9. CD16A/BCMA 항체 I의 다라투무맙 R/R 다발성 골수종 환자 치료 용도
CD16A/BCMA 항체는 다라투무맙 ( "Dara"라고도 함)과 다르다. 예를 들어, 다라투무맙은 다발성 골수종 ( "MM"이라고도 함)에서 보체 의존성 세포독성 활성 (de Weers, M. 외, J. immun. 2011, 186(3):1840-1848) 및 CD38의 교차 결합을 통한 신호전달에 의한 세포자멸사 유도 능력 (Overdijk, M.B. 외, Journal of immunology 2016;197(3):807-813)을 가진다. 그러나, CD16A/BCMA 항체 I은 이러한 활성을 가지지 않는다.
다라투무맙과 달리 CD16A/BCMA 항체 I의 활성은 Fc-매개 약물의 활성을 감소시키는 CD16A 다형성에 의해 영향 받지 않는다. 도 31A 및 31B를 참고하라. 또한, CD38 요법 (예컨대, 다라투무맙)과 달리 CD16A/BCMA 항체 I은 NK 세포를 고갈시키지 않는다. 도 40A, 40B, 40C, 40D, 및 40E를 참고하라. 또한 IL-15 치료는 CD16A/BCMA 항체 I의 활성을 증가시키지만 다라투무맙은 그렇지 않다. 도 42A 및 42B를 참고하라.
다라투무맙과 구별되는, 본원에 개시된 항-BCMA/CD16A 항체, 예컨대, CD16A/BCMA 항체 I의 특징을 고려할 때, 이들 항-BCMA/CD16A 항체들, 예컨대, CD16A/BCMA 항체 I은, 재발성/불응성 ("R/R") MM 환자들 (예컨대, 다라투무맙 R/R 다발성 골수종 환자)의 치료를 위한 후보가 된다. 다라투무맙-불응성 표현형은 보체 억제 단백질의 CD38 하향조절 및 상향조절에 의해 매개되는 것으로 보인다 (Nijhof 외, Leukemia (2015);29(10);2039-2049 Nijhof 외, Blood (2016);128(7):959-970). 이러한 CD38 발현과 NK-세포 동족살해의 소실은 다라투무맙 내성에 원인이 된다. 본원에 개시된 항-BCMA/CD16A 항체의 작용 메커니즘은 이러한 항-BCMA/CD16A 항체가 다라투무맙 R/R 다발성 골수종 환자를 치료하는데 사용될 수 있음을 나타낸다.
다라투무맙 불응성 환자는 말초 혈액에서 보다 낮은 NK 수준을 가진다 (Casneuf 외, Blood Adv. (2017); 24;1(23):2105-2114). Steward 외, Blood Cancer J. (2019);9(2):17은 R/R MM을 치료하기 위해 모노메틸 아우리스타틴 E (MMAE)에 접합된 항-FcRH5 항체-약물인 DFRF4539A의 1상 연구를 개시한다. DFRF4539A의 1상 연구에서 Dara 나이브 MM 환자, Dara 불응성 MM 환자 및 R/R MM 환자의 말초 혈액 내 NK 세포 수를 비교하고 그 결과를 도 43에 나타낸다.
DFRF4539A의 I 상 연구에서 R/R MM 환자의 골수에서의 NK/종양 E:T 비율을 도 44에 나타낸다. 도 45A 및 45B에 나타낸 CD16A/BCMA 항체 I의 시험관내 세포주 사멸 데이터는 CD16A/BCMA 항체 I이 DFRF4539A 1상 집단에서 발견되는 E : T 비율에서 효과적임을 나타낸다.
8.10. 새로운 NK 세포들은 세포독성에 영향을 준다
새로운 NK 세포에서 CD16A/BCMA 항체 I 및 CD16A/BCMA 항체 II의 세포독성을 2일차 NK 세포와 비교하였다. 새로운 NK 세포는 같은 날 새로 분리된 PBMC에서 정제된 NK 세포였다. 2 (2nd)일차 NK 세포들은 1일차에 분리된 PBMC에서 정제되고 RPMI 배지에서 밤새 배양된 NK 세포였다. 결과를 도 46A, 46B, 46C, 및 46D에 나타낸다. 도 46A,46B, 46C, 및 46D에서 보는 바와 같이, 새로운 NK 세포들은 2일차 NK 세포들 보다 높은 세포독성을 보여주었다.
실시예 9-CD16A/BCMA 결합 항체의 다발성 골수종 치료 용도
다발성 골수종 ( "MM")은 형질 세포의 악성 종양이다. 미국과 유럽에서 매년 약 56,000 명의 새로운 MM 사례가 진단된다. 전체 생존이 개선되고 있지만, 다음을 비롯하여 충족되지 않은 높은 수요의 영역들이 남아있다: those 이용가능한 치료법에 재발성/불응성인 환자들, 및 고 위험 1차 ("1L") 질환을 나타내는 환자들. 세 가지 치료 클래스는 MM 요법을 변형시켰으며 특정 사례에서 여러 치료 라인들에서 사용되는 클래스를 포함하는 현재의 표준 치료 ("SOC")의 골격을 형성한다. (1) 면역조절제 ( "IMiD", 예컨대, 레날리도마이드) - 항 증식 효과, 적응 및 선천 면역 시스템의 증강을 포함하는 다수의 잠재적 MOA; (2) 프로테아좀 억제제 (예컨대, 보르테조밉); 및 (3) 다라투무맙 (항-CD38 항체, 이의 ADCC, CDC 및 세포자멸사가 CD38의 가교에 의해 유발됨).
NK 세포는 면역요법에 널리 사용되어 왔다. 활성화 및 억제 수용체 신호의 균형은 NK 세포 활성화 및 세포 독성을 조절한다, 예컨대, 정상적인 건강한 조직에서 억제 신호가 우세하다. NK 세포는 다발성 골수종에서 Fc-매개 암 치료, 예컨대, 다라투무맙 및 엘로투주맙 (항-SLAMF7 항체)의 중요한 이펙터였다. NK 세포 활성화 및 종양 사멸은 다음과 같은 작용 메커니즘 ("MOA")을 통해 발생할 수 있다: (a) 종양 세포에서 MHC 클래스 I의 손실 (예를 들어, T-세포 반응을 피하기 위해); (b) 활성화 NK 세포 수용체들 (NKG2D, NKp30, NKp44, NKp46 및 DNAM-1)를 결찰시키는 손상된 세포에 의한 스트레스 리간드의 과발현, 및 (c) 그 Fc 영역을 통한 활성화 수용체 CD16A (FcγRIIIa)에 대한 종양-관련 항원 (TAA)-특이적 치료 항체 결합에 의한 NK 세포의 활성화. NK 세포 관여항체들은 MOA (c)를 모사하지만, 본원에서 논의된 바와 같이, 다라투무맙과 구별되는 MOA를 이용한다. 통상적인 Fc-CD16A 상호작용을 통해 NK 세포를 동원하지 않는 본 발명의 NK 관여항체는 SOC와 조합하여 MM 환자, 특히, 2차 ("2L") 환자를 치료할 가능성을 가진다. 더욱이, 많은 2L 및 3차 ("3L") 환자 집단은 재발시 다라투무맙 불응성일 것으로 예상되지만, NK 세포 관여항체, 예컨대, 본원에 개시된 CD16A/BCMA 항체 I 및 III에 대해 (MOA의 차이로 인해) 반응성일 것으로 예상된다.
본원에 개시된 CD16A 항원-결합 단백질 (예를 들어, CD16A/BCMA 항체 I 및 III)은 CD16A에 결합하는 NK 세포 관여항체이다. CD16A는 약 95%의 NK 세포 및 대식세포에서 항시적으로 발현되며 NK 세포 활성화 수용체이다.
CD16A/BCMA 항체 I, II 및 III는 B-세포 성숙 항원 (BCMA)에 결합한다. 본원에서 논의된 바와 같이, BCMA는 TNF-수용체 수퍼패밀리의 구성원이며 형질 세포의 장기 세포 생존에 일정한 역할을 한다 (O'Connor, JEM 2004;199(1):91-98). BCMA는 정상 형질 세포에서 발현되며 다발성 골수종에서 상향 조절되고 높은 유병률을 보인다. BCMA는 BCMA-표적화 키메라 항원 수용체 (CAR) T 세포 요법 및 BCMA 항체-약물 접합체 (ADC) 요법을 비롯하여 R/R 다발성 골수종 면역요법에 대해 잘 검증된 표적이다.
냉동된 일차 골수종 골수 단핵구 세포 (BMMC)에서 BCMA, CD38 및 FcRH5의 발현 수준을 측정하고 그 결과를 도 47에 나타낸다. 도 47에서 보는 바와 같이, 20명의 공여체 및 대조 (골수종 세포주 MOLP-2)로부터 얻은 냉동된 일차 골수종 골수 단핵구 세포 (BMMC)를 FcRH5, BCMA (Biolegend 19F2), CD38 세포 표면 발현에 대해 평가하였다 요약하면, BMMC를 해동하고 멸균 PBS로 세척한 다음, 1x10^6 세포/mL의 최종 농도로 재현탁시켰다. BMMC는 생존력 및 골수종 마커 (CD45, CD319, CD138, CD38, BCMA, FcRH5)로 염색되었다. 세포를 고정하고 세척한 후, 세포들을 Canto II에서 판독하였다. 생존/단일항/CD45-/CD319+ 세포들 (골수종 세포들)을 선택하여 FlowJo에서 FcRH5, BCMA, 및 CD38의 분석을 실시하였다. FcRH5, BCMA 및 CD38에 대한 MESF (Log10) 값을 통계 플롯팅 소프트웨어 Prism에서 플롯하였다.
도 48A 및 48B에서 보는 바와 같이, BCMA는 인간 형질 세포에서 발현되고 (도 48A) 상향조절되며 MM에서 높은 유병률로 발견된다 (도 48B). 도 48B에 도시한 실험들에서 사용된 일차 MM 세포들은 냉동된 일차 골수종 BMMC로서, 이들을 도 47에 대해 상기 기재한 프로토콜에 따라 염색하고 게이팅한 다음 FlowJo에서 최대%를 플롯하였다. 도 48B의 회색 음영 피크는 형광 마이너스 1 (FMO) 대조이고 다른 피크는 BCMA 발현이다. CD16A/BCMA 항체 I은 테스트 항-BCMA 항체와 유사한 결과를 나타냈다.
BCMA 표적화 CAR-T 세포 요법 및 CD3/BCMA 이중특이적 항체가 인상적인 항-MM 활성을 보였으나, 이들은 또한 심각한 사이토카인 방출 증후군 ("CRS") 사례와 관련되어 있었다. NK 관여항체인, 본원에 개시된 CD16A 항원-결합 단백질 (예컨대, CD16A/BCMA 항체 I)의 MOA는 이러한 CRS-관련 치료법들과의 구별을 가능하게 한다. 예를 들어, 유리한 안전성 프로파일 및 CRS의 부재는 본원에 개시된 CD16A 항원-결합 단백질 (예를 들어, CD16A/BCMA 항체 I)을 MM에서의 SOC 또는 다른 면역요법들 (예컨대, 사이토카인 (예컨대, 본원에 개시된 IL-15 및 IL-12)과 조합할 수 있게 한다 (예컨대, 도 42A 및 42B 참고). 본원에 개시된 NK-세포 기반 접근법은 또한 T-세포 요법 및 체크포인트 억제제 요법 (예를 들어, CD3 이중특이적 항체, 항-PD-1 항체 (예컨대, 니볼루맙, 펨브롤리주맙), 항-TIGIT 항체, 항-PD-L1 항체 (예컨대, 아테졸리주맙), 항-VEGF 항체 (예컨대, 베바시주맙), FcRH5/CD3 이중특이적 항체 등)과 상승작용을 가져올 수 있다.
전술한 내용을 고려할 때, 다발성 골수종 치료에 사용하기 위한 NK 세포 관여항체를 선택하기 위해 다음 기준 중 하나 이상이 사용된다:
·
NK 세포 관여항체는 2개의 표적들: NK 세포 상의 CD16A, 및 다발성 골수종 세포 상의 BCMA에 결합할 수 있다,
·
NK 세포 관여항체는 CD16A에 대해 적어도 2가이다, 예컨대, 적어도 2개의 CD16A 항원-결합 모이어티를 포함한다,
·
NK 세포 관여항체는 CD16B와 교차 반응하지 않고, 비인간 영장류의 CD16A와 교차 반응하는 NK 세포 이중특이적 항체이다,
·
NK 세포 관여항체는 강력하고 우세하며, BCMA+ 종양 세포들 및 일차 골수종의 표적-의존성 시험관내 사멸을 보유한다 (예컨대, EC50 ≤ 5nM로 사멸된 ≥ 약 60% 세포),
·
NK 세포 관여항체는 NK 세포를 유의하게 사멸시키지 않는다, 예컨대, NK 세포 동족살해를 감소시키거나 회피한다,
·
NK 세포 관여항체는 허용가능한 안전성 프로파일을 가지고 있으며, 예를 들어, 다른 T-세포 관여항체보다 우수한 시험관내 사이토카인 방출 프로파일을 가지고 (예를 들어, NK 세포 관여항체는 CRS가 없음), 이상 반응은 모니터링 가능하고, 관리가능하며, 가역적이다,
·
NK 세포 관여항체는 다발성 골수종 대상체에게 정맥내 투여 될 수 있다, 그리고
·
NK 세포 관여항체는 주 1 회 (QW) 이하의 투여 빈도를 필요로 한다.
본원에 기재된 선택 전략과 관련하여, 다음과 같은 약력학 (PD) 바이오마커가 사용될 수 있다: 혈청 M 단백질 및 유리 경쇄 (FLC)의 농도, 단일클론 형질 세포의 감소, 치료 후 골수 샘플에서 NK 세포 활성화 및 동원 및 말초 NK 세포 활성화. 본원에 기재된 선택 전략은 진단을 포함 할 수 있지만 다발성 골수종에서 BMCA의 높은 유병률을 고려할 때 반드시 진단이 필요한 것은 아니다.
특정 CD16A/BCMA 항원-결합 단백질 (예컨대, CD16A/BCMA 항체 I 및 CD16A/BCMA 항체 III)은 상기 기준을 충족시킨다.
요약하면, 본원에 개시된 CD16A/BCMA 항원-결합 단백질 (예컨대, CD16A/BCMA 항체 I 및 CD16A/BCMA 항체 III)을 다발성 골수종 치료에 사용하여,유리한 안전성 프로파일과 함께 내성 완화를 구현할 수 있다.
본원에 개시된 전술한 발명들은 명확한 이해를 목적으로 예시 및 실시예로서 보다 상세히 설명하였으나, 이러한 설명 및 실시예들은 본원에 개시된 발명의 범위를 제한시키는 것으로 간주되어서는 안된다. 본원에 인용 된 모든 특허 및 과학 문헌의 내용은 그 전체가 참고문헌으로 포함된다.
SEQUENCE LISTING
<110> AFFIMED GMBH
<120> NK CELL ENGAGING ANTIBODY FUSION CONSTRUCTS
<130> 087353.0101
<140>
<141>
<150> EP 18190661.1
<151> 2018-08-24
<150> EP 18190662.9
<151> 2018-08-24
<150> EP 18167384.9
<151> 2018-04-13
<150> EP 18167385.6
<151> 2018-04-13
<160> 136
<170> PatentIn version 3.5
<210> 1
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 1
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ser Ala Tyr Tyr Tyr Asp Phe Ala Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 2
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 2
Ser Tyr Val Leu Thr Gln Pro Ser Ser Val Ser Val Ala Pro Gly Gln
1 5 10 15
Thr Ala Thr Ile Ser Cys Gly Gly His Asn Ile Gly Ser Lys Asn Val
20 25 30
His Trp Tyr Gln Gln Arg Pro Gly Gln Ser Pro Val Leu Val Ile Tyr
35 40 45
Gln Asp Asn Lys Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Asn Tyr Ser Val Leu
85 90 95
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 3
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 3
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Glu Pro Met Tyr Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ser Ala Tyr Tyr Tyr Asp Phe Ala Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 4
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 4
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Tyr Met Gln Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Val Ile Asn Pro Gly Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ser Ala Tyr Tyr Tyr Asp Phe Ala Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 5
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 5
Ser Tyr Val Leu Thr Gln Pro Ser Ser Val Ser Val Ala Pro Gly Gln
1 5 10 15
Thr Ala Arg Ile Thr Cys Gly Gly His Asn Ile Gly Ser Gln Ser Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Gln Asp Ser Lys Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Asn Tyr Ser Val Val
85 90 95
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 6
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 6
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Ser Asp Phe
20 25 30
Tyr Ile Gln Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Gly Gly Ala Ser Thr Thr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ser Ala Tyr Tyr Tyr Asp Phe Ala Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 7
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 7
Ser Tyr Val Leu Thr Gln Pro Ser Ser Val Ser Val Ala Pro Gly Gln
1 5 10 15
Thr Ala Arg Ile Thr Cys Gly Gly Tyr Asn Ile Gly Arg Gln Ser Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Gln Asp Ser Lys Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Asn Tyr Thr Val Val
85 90 95
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 8
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 8
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Glu Pro Arg Gly Val Arg Ile Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ser Ala Tyr Tyr Tyr Asp Phe Ala Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 9
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 9
Ser Tyr Val Leu Thr Gln Pro Ser Ser Val Ser Val Ala Pro Gly Gln
1 5 10 15
Thr Ala Arg Ile Thr Cys Gly Gly His Asn Ile Gly Ser Thr Asn Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Gln Asp Ser Lys Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Asn Tyr Ser Val Gln
85 90 95
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 10
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 10
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Tyr Met Gln Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Val Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ser Ala Tyr Tyr Tyr Asp Phe Ala Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 11
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 11
Ser Tyr Val Leu Thr Gln Pro Ser Ser Val Ser Val Ala Pro Gly Gln
1 5 10 15
Thr Ala Arg Ile Thr Cys Gly Gly Asn Asn Ile Gly Ser Lys Ser Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Gln Asp Lys Lys Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Asp Tyr Ile Val Leu
85 90 95
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 12
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 12
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Val Ile Glu Pro Asp Gly Gly Arg Arg Thr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ser Ala Tyr Tyr Tyr Asp Phe Ala Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 13
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 13
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Gly His Gln Gly Val Ser Gly Asp
20 25 30
Val His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gln Ala Asn Lys Arg Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Trp Asp Asn Tyr Ser Val
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 14
<211> 121
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 14
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Ile Asp Leu Ser Asn Tyr
20 25 30
Ala Ile Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Ile Ile Trp Ala Ser Gly Thr Thr Phe Tyr Ala Thr Trp Ala Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Thr Val Pro Gly Tyr Ser Thr Ala Pro Tyr Phe Asp Leu Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 15
<211> 110
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 15
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ser Ser Pro Ser Val Trp Ser Asn
20 25 30
Phe Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Glu Ala Ser Lys Leu Thr Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gly Gly Gly Tyr Ser Ser Ile
85 90 95
Ser Asp Thr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 16
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 16
Gly Gly Ser Gly Gly Ser
1 5
<210> 17
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 17
Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly
1 5 10 15
Gly Ser
<210> 18
<211> 21
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 18
Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly
1 5 10 15
Gly Ser Gly Gly Ser
20
<210> 19
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 19
Gly Gly Gly Gly Ser
1 5
<210> 20
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 20
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 21
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 21
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 22
<211> 30
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 22
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25 30
<210> 23
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 23
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
<210> 24
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 24
Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10
<210> 25
<211> 329
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 25
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Ala Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu
225 230 235 240
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly
325
<210> 26
<211> 329
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 26
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu
225 230 235 240
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly
325
<210> 27
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 27
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 28
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 28
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 29
<211> 216
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 29
Ala Pro Glu Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Ala Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
115 120 125
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly
210 215
<210> 30
<211> 215
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 30
Ala Pro Glu Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Ala Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Lys Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Ser Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
145 150 155 160
Tyr Lys Thr Thr Val Pro Val Leu Asp Ser Asp Gly Ser Phe Arg Leu
165 170 175
Ala Ser Tyr Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro
210 215
<210> 31
<211> 216
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 31
Ala Pro Glu Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Ala Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
115 120 125
Thr Lys Asn Gln Val Ser Leu Tyr Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly
210 215
<210> 32
<211> 216
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 32
Ala Pro Glu Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Ala Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
115 120 125
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Thr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly
210 215
<210> 33
<211> 98
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 33
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val
<210> 34
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 34
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Ser Ser
100 105
<210> 35
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 35
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Ser
100 105
<210> 36
<211> 216
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 36
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
115 120 125
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly
210 215
<210> 37
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 37
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Thr Pro Gly Glu
1 5 10 15
Pro Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Asp Ser
20 25 30
Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Tyr Ala Gly Asp Ser Asp Ala Arg Tyr Ser Pro Ser Phe
50 55 60
Gln Gly Gln Val Thr Ile Ser Ala Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Asn Phe Gly Asp His Trp Gly Gln Gly Thr Leu Val Thr Val
100 105 110
Ser Ser
<210> 38
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 38
Ser Tyr Glu Leu Thr Gln Ser Pro Ser Val Ser Val Ala Pro Gly Gln
1 5 10 15
Thr Ala Arg Ile Phe Cys Gly Gly Asp Asn Ile Gly Ser Lys Asn Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Arg Asp Ser Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ala
50 55 60
Asn Ser Glu Asn Thr Ala Thr Leu Thr Ile Ser Arg Ala Gln Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Ser Arg Thr Tyr Val
85 90 95
Phe Gly Thr Gly Thr Lys Leu Thr Val Leu
100 105
<210> 39
<211> 249
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 39
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Thr Pro Gly Glu
1 5 10 15
Pro Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Asp Ser
20 25 30
Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Tyr Ala Gly Asp Ser Asp Ala Arg Tyr Ser Pro Ser Phe
50 55 60
Gln Gly Gln Val Thr Ile Ser Ala Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Asn Phe Gly Asp His Trp Gly Gln Gly Thr Leu Val Thr Val
100 105 110
Ser Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly
115 120 125
Ser Gly Gly Ser Ser Tyr Glu Leu Thr Gln Ser Pro Ser Val Ser Val
130 135 140
Ala Pro Gly Gln Thr Ala Arg Ile Phe Cys Gly Gly Asp Asn Ile Gly
145 150 155 160
Ser Lys Asn Val His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val
165 170 175
Leu Val Ile Tyr Arg Asp Ser Asn Arg Pro Ser Gly Ile Pro Glu Arg
180 185 190
Phe Ser Gly Ala Asn Ser Glu Asn Thr Ala Thr Leu Thr Ile Ser Arg
195 200 205
Ala Gln Ala Gly Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Ser
210 215 220
Arg Thr Tyr Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu Ala Ala
225 230 235 240
Ala Gly Ser His His His His His His
245
<210> 40
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 40
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Val Ser Ser Gly
20 25 30
Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Asn Pro Ile Ser Ile Pro Ala Phe Asp Ile Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 41
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 41
Gln Pro Val Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Gly Lys
1 5 10 15
Thr Ala Arg Ile Thr Cys Gly Gly Asn Asn Ile Gly Ser Lys Ser Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Tyr Asp Ser Asp Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Thr Ser Ser Asp His
85 90 95
Val Leu Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 42
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 42
Gly Gly Ser Val Ser Ser Gly Ser Tyr Tyr
1 5 10
<210> 43
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 43
Ile Tyr Tyr Ser Gly Ser Thr
1 5
<210> 44
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 44
Ala Arg Asn Pro Ile Ser Ile Pro Ala Phe Asp Ile
1 5 10
<210> 45
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 45
Asn Ile Gly Ser Lys Ser
1 5
<210> 46
<211> 3
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 46
Tyr Asp Ser
1
<210> 47
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 47
Gln Val Trp Asp Thr Ser Ser Asp His Val Leu
1 5 10
<210> 48
<211> 192
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 48
Gly Met Arg Thr Glu Asp Leu Pro Lys Ala Val Val Phe Leu Glu Pro
1 5 10 15
Gln Trp Tyr Arg Val Leu Glu Lys Asp Ser Val Thr Leu Lys Cys Gln
20 25 30
Gly Ala Tyr Ser Pro Glu Asp Asn Ser Thr Gln Trp Phe His Asn Glu
35 40 45
Ser Leu Ile Ser Ser Gln Ala Ser Ser Tyr Phe Ile Asp Ala Ala Thr
50 55 60
Val Asp Asp Ser Gly Glu Tyr Arg Cys Gln Thr Asn Leu Ser Thr Leu
65 70 75 80
Ser Asp Pro Val Gln Leu Glu Val His Ile Gly Trp Leu Leu Leu Gln
85 90 95
Ala Pro Arg Trp Val Phe Lys Glu Glu Asp Pro Ile His Leu Arg Cys
100 105 110
His Ser Trp Lys Asn Thr Ala Leu His Lys Val Thr Tyr Leu Gln Asn
115 120 125
Gly Lys Gly Arg Lys Tyr Phe His His Asn Ser Asp Phe Tyr Ile Pro
130 135 140
Lys Ala Thr Leu Lys Asp Ser Gly Ser Tyr Phe Cys Arg Gly Leu Phe
145 150 155 160
Gly Ser Lys Asn Val Ser Ser Glu Thr Val Asn Ile Thr Ile Thr Gln
165 170 175
Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Phe Pro Pro Gly Tyr Gln
180 185 190
<210> 49
<211> 192
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 49
Gly Met Arg Ala Glu Asp Leu Pro Lys Ala Val Val Phe Leu Glu Pro
1 5 10 15
Gln Trp Tyr Arg Val Leu Glu Lys Asp Arg Val Thr Leu Lys Cys Gln
20 25 30
Gly Ala Tyr Ser Pro Glu Asp Asn Ser Thr Arg Trp Phe His Asn Glu
35 40 45
Ser Leu Ile Ser Ser Gln Thr Ser Ser Tyr Phe Ile Ala Ala Ala Arg
50 55 60
Val Asn Asn Ser Gly Glu Tyr Arg Cys Gln Thr Ser Leu Ser Thr Leu
65 70 75 80
Ser Asp Pro Val Gln Leu Glu Val His Ile Gly Trp Leu Leu Leu Gln
85 90 95
Ala Pro Arg Trp Val Phe Lys Glu Glu Glu Ser Ile His Leu Arg Cys
100 105 110
His Ser Trp Lys Asn Thr Leu Leu His Lys Val Thr Tyr Leu Gln Asn
115 120 125
Gly Lys Gly Arg Lys Tyr Phe His Gln Asn Ser Asp Phe Tyr Ile Pro
130 135 140
Lys Ala Thr Leu Lys Asp Ser Gly Ser Tyr Phe Cys Arg Gly Leu Ile
145 150 155 160
Gly Ser Lys Asn Val Ser Ser Glu Thr Val Asn Ile Thr Ile Thr Gln
165 170 175
Asp Leu Ala Val Ser Ser Ile Ser Ser Phe Phe Pro Pro Gly Tyr Gln
180 185 190
<210> 50
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 50
Gly Tyr Thr Phe Thr Ser Tyr Tyr
1 5
<210> 51
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 51
Ile Glu Pro Met Tyr Gly Ser Thr
1 5
<210> 52
<211> 13
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 52
Ala Arg Gly Ser Ala Tyr Tyr Tyr Asp Phe Ala Asp Tyr
1 5 10
<210> 53
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 53
Asn Ile Gly Ser Lys Asn
1 5
<210> 54
<211> 3
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 54
Gln Asp Asn
1
<210> 55
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 55
Gln Val Trp Asp Asn Tyr Ser Val Leu
1 5
<210> 56
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 56
Ile Asn Pro Ser Gly Gly Ser Thr
1 5
<210> 57
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 57
Ser Phe Phe Pro Pro Gly Tyr Gln
1 5
<210> 58
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
6xHis tag"
<400> 58
His His His His His His
1 5
<210> 59
<211> 4
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 59
Glu Pro Glu Ala
1
<210> 60
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 60
Gly Gly Ser Gly Gly Ser Gly Gly Ser
1 5
<210> 61
<211> 727
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 61
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Asp Met Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Thr Arg Gly Asp Ile Thr Ser Tyr Arg Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Asp Tyr Tyr Thr Asp Tyr Met Gly Phe Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Phe Glu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
450 455 460
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
465 470 475 480
Ser Tyr Val Leu Thr Gln Pro Ser Ser Val Ser Val Ala Pro Gly Gln
485 490 495
Thr Ala Thr Ile Ser Cys Gly Gly His Asn Ile Gly Ser Lys Asn Val
500 505 510
His Trp Tyr Gln Gln Arg Pro Gly Gln Ser Pro Val Leu Val Ile Tyr
515 520 525
Gln Asp Asn Lys Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
530 535 540
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met
545 550 555 560
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Asn Tyr Ser Val Leu
565 570 575
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gly Ser Gly Gly Ser
580 585 590
Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gln
595 600 605
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu Ser
610 615 620
Leu Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Tyr
625 630 635 640
Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
645 650 655
Ala Ile Glu Pro Met Tyr Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln
660 665 670
Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr Met
675 680 685
Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala
690 695 700
Arg Gly Ser Ala Tyr Tyr Tyr Asp Phe Ala Asp Tyr Trp Gly Gln Gly
705 710 715 720
Thr Leu Val Thr Val Ser Ser
725
<210> 62
<211> 214
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 62
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Glu Asp Ile Tyr Asn Gly
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Ser Leu Gln Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Glu Ala Thr Tyr Tyr Cys Ala Gly Pro His Lys Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 63
<211> 729
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 63
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Phe Glu Gly
1 5 10 15
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
20 25 30
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Val Ser His
35 40 45
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
50 55 60
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
65 70 75 80
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
85 90 95
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
100 105 110
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
115 120 125
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
130 135 140
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
145 150 155 160
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
165 170 175
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Thr Ser Lys Leu Thr Val
180 185 190
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
195 200 205
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
210 215 220
Pro Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Tyr Val Leu
225 230 235 240
Thr Gln Pro Ser Ser Val Ser Val Ala Pro Gly Gln Thr Ala Thr Ile
245 250 255
Ser Cys Gly Gly His Asn Ile Gly Ser Lys Asn Val His Trp Tyr Gln
260 265 270
Gln Arg Pro Gly Gln Ser Pro Val Leu Val Ile Tyr Gln Asp Asn Lys
275 280 285
Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser Asn Ser Gly Asn
290 295 300
Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met Asp Glu Ala Asp
305 310 315 320
Tyr Tyr Cys Gln Val Trp Asp Asn Tyr Ser Val Leu Phe Gly Gly Gly
325 330 335
Thr Lys Leu Thr Val Leu Gly Gly Ser Gly Gly Ser Gln Val Gln Leu
340 345 350
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu Ser Leu Lys Val
355 360 365
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Tyr Met His Trp
370 375 380
Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Ala Ile Glu
385 390 395 400
Pro Met Tyr Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln Gly Arg Val
405 410 415
Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
420 425 430
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly Ser
435 440 445
Ala Tyr Tyr Tyr Asp Phe Ala Asp Tyr Trp Gly Gln Gly Thr Leu Val
450 455 460
Thr Val Ser Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser
465 470 475 480
Gly Gly Ser Gly Gly Ser Ser Tyr Val Leu Thr Gln Pro Ser Ser Val
485 490 495
Ser Val Ala Pro Gly Gln Thr Ala Thr Ile Ser Cys Gly Gly His Asn
500 505 510
Ile Gly Ser Lys Asn Val His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
515 520 525
Pro Val Leu Val Ile Tyr Gln Asp Asn Lys Arg Pro Ser Gly Ile Pro
530 535 540
Glu Arg Phe Ser Gly Ser Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile
545 550 555 560
Ser Gly Thr Gln Ala Met Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp
565 570 575
Asp Asn Tyr Ser Val Leu Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
580 585 590
Gly Gly Ser Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu
595 600 605
Val Lys Lys Pro Gly Glu Ser Leu Lys Val Ser Cys Lys Ala Ser Gly
610 615 620
Tyr Thr Phe Thr Ser Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly
625 630 635 640
Gln Gly Leu Glu Trp Met Gly Ala Ile Glu Pro Met Tyr Gly Ser Thr
645 650 655
Ser Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr
660 665 670
Ser Thr Ser Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp
675 680 685
Thr Ala Val Tyr Tyr Cys Ala Arg Gly Ser Ala Tyr Tyr Tyr Asp Phe
690 695 700
Ala Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ala
705 710 715 720
Ala Gly Ser His His His His His His
725
<210> 64
<211> 469
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 64
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Asp Met Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Thr Arg Gly Asp Ile Thr Ser Tyr Arg Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Asp Tyr Tyr Thr Asp Tyr Met Gly Phe Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Ala Ile Gln Met Thr Gln Ser Pro
130 135 140
Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
145 150 155 160
Ala Ser Glu Asp Ile Tyr Asn Gly Leu Ala Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Gly Ala Ser Ser Leu Gln Asp
180 185 190
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr
195 200 205
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Glu Ala Thr Tyr Tyr Cys
210 215 220
Ala Gly Pro His Lys Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val
225 230 235 240
Glu Ile Lys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
245 250 255
Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
260 265 270
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Ala
275 280 285
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
290 295 300
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
305 310 315 320
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
325 330 335
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
340 345 350
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
355 360 365
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
370 375 380
Gln Val Ser Leu Tyr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
385 390 395 400
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
405 410 415
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
420 425 430
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
435 440 445
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
450 455 460
Ser Leu Ser Pro Gly
465
<210> 65
<211> 121
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 65
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Asp Met Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Thr Arg Gly Asp Ile Thr Ser Tyr Arg Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Asp Tyr Tyr Thr Asp Tyr Met Gly Phe Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 66
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 66
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Glu Asp Ile Tyr Asn Gly
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Ser Leu Gln Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Glu Ala Thr Tyr Tyr Cys Ala Gly Pro His Lys Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 67
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 67
Asn Tyr Asp Met Ala
1 5
<210> 68
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 68
Ser Ile Ser Thr Arg Gly Asp Ile Thr Ser Tyr Arg Asp Ser Val Lys
1 5 10 15
Gly
<210> 69
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 69
Gln Asp Tyr Tyr Thr Asp Tyr Met Gly Phe Ala Tyr
1 5 10
<210> 70
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 70
Arg Ala Ser Glu Asp Ile Tyr Asn Gly Leu Ala
1 5 10
<210> 71
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 71
Gly Ala Ser Ser Leu Gln Asp
1 5
<210> 72
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 72
Ala Gly Pro His Lys Tyr Pro Leu Thr
1 5
<210> 73
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 73
Ser Tyr Tyr Met His
1 5
<210> 74
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 74
Ala Ile Glu Pro Met Tyr Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 75
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 75
Gly Ser Ala Tyr Tyr Tyr Asp Phe Ala Asp Tyr
1 5 10
<210> 76
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 76
Gly Gly His Asn Ile Gly Ser Lys Asn Val His
1 5 10
<210> 77
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 77
Gln Asp Asn Lys Arg Pro Ser
1 5
<210> 78
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 78
Gln Val Trp Asp Asn Tyr Ser Val Leu
1 5
<210> 79
<211> 110
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 79
Ala Pro Glu Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Ala Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
100 105 110
<210> 80
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 80
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
1 5 10 15
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
20 25 30
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
35 40 45
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
50 55 60
Phe Leu Thr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
65 70 75 80
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
85 90 95
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
100 105
<210> 81
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 81
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
1 5 10 15
Glu Met Thr Lys Asn Gln Val Ser Leu Tyr Cys Leu Val Lys Gly Phe
20 25 30
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
35 40 45
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
50 55 60
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
65 70 75 80
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
85 90 95
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
100 105
<210> 82
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 82
Gly Tyr Thr Phe Thr Asn Tyr Tyr
1 5
<210> 83
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 83
Ile Asn Pro Gly Gly Gly Ser Thr
1 5
<210> 84
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 84
Asn Ile Gly Ser Gln Ser
1 5
<210> 85
<211> 3
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 85
Gln Asp Ser
1
<210> 86
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 86
Gln Val Trp Asp Asn Tyr Ser Val Val
1 5
<210> 87
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 87
Gly Tyr Ser Phe Ser Asp Phe Tyr
1 5
<210> 88
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 88
Ile Asn Pro Gly Gly Ala Ser Thr
1 5
<210> 89
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 89
Asn Ile Gly Arg Gln Ser
1 5
<210> 90
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 90
Gln Val Trp Asp Asn Tyr Thr Val Val
1 5
<210> 91
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 91
Gly Tyr Thr Phe Ser Ser Tyr Tyr
1 5
<210> 92
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 92
Ile Glu Pro Arg Gly Val Arg Ile
1 5
<210> 93
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 93
Asn Ile Gly Ser Thr Asn
1 5
<210> 94
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 94
Gln Val Trp Asp Asn Tyr Ser Val Gln
1 5
<210> 95
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 95
Ile Asn Pro Ser Gly Gly Val Thr
1 5
<210> 96
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 96
Asn Ile Gly Ser Lys Ser
1 5
<210> 97
<211> 3
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 97
Gln Asp Lys
1
<210> 98
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 98
Gln Val Trp Asp Asp Tyr Ile Val Leu
1 5
<210> 99
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 99
Ile Glu Pro Asp Gly Gly Arg Arg
1 5
<210> 100
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 100
Gln Gly Val Ser Gly Asp
1 5
<210> 101
<211> 3
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 101
Gln Ala Asn
1
<210> 102
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 102
Gln Gln Trp Asp Asn Tyr Ser Val Thr
1 5
<210> 103
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 103
Ile Glu Pro Ser Gly Gly Ser Thr
1 5
<210> 104
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 104
Gln Val Trp Asp Ser Tyr Ser Val Leu
1 5
<210> 105
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 105
Gln Val Trp Asp Asn Tyr Asn Val Leu
1 5
<210> 106
<211> 329
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 106
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Gly Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu
225 230 235 240
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly
325
<210> 107
<211> 216
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 107
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Gly Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
115 120 125
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly
210 215
<210> 108
<211> 110
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 108
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Gly Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
100 105 110
<210> 109
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 109
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
1 5 10 15
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
20 25 30
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
35 40 45
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
50 55 60
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
65 70 75 80
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
85 90 95
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
100 105
<210> 110
<211> 329
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 110
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu
225 230 235 240
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly
325
<210> 111
<211> 216
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 111
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
115 120 125
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly
210 215
<210> 112
<211> 110
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 112
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
100 105 110
<210> 113
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 113
Gly Phe Thr Phe Ser Asn Tyr Asp
1 5
<210> 114
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 114
Ile Ser Thr Arg Gly Asp Ile Thr
1 5
<210> 115
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 115
Ala Arg Gln Asp Tyr Tyr Thr Asp Tyr Met Gly Phe Ala Tyr
1 5 10
<210> 116
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 116
Glu Asp Ile Tyr Asn Gly
1 5
<210> 117
<211> 3
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 117
Gly Ala Ser
1
<210> 118
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 118
Gly Phe Thr Phe Ser Asn Phe Asp
1 5
<210> 119
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 119
Ile Thr Thr Gly Gly Gly Asp Thr
1 5
<210> 120
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 120
Val Arg His Gly Tyr Tyr Asp Gly Tyr His Leu Phe Asp Tyr Trp Gly
1 5 10 15
<210> 121
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 121
Gln Gly Ile Ser Asn Asn
1 5
<210> 122
<211> 3
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 122
Tyr Thr Ser
1
<210> 123
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 123
Gln Gln Phe Thr Ser Leu Pro Tyr Thr
1 5
<210> 124
<211> 121
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 124
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Phe
20 25 30
Asp Met Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Val Trp Val
35 40 45
Ser Ser Ile Thr Thr Gly Gly Gly Asp Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Ser Thr Leu Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Arg His Gly Tyr Tyr Asp Gly Tyr His Leu Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 125
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 125
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Asn Gln Gly Ile Ser Asn Asn
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile
35 40 45
Tyr Tyr Thr Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Thr Ser Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 126
<211> 481
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 126
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Asp Met Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Thr Arg Gly Asp Ile Thr Ser Tyr Arg Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Asp Tyr Tyr Thr Asp Tyr Met Gly Phe Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Ser Gly Gly Ser Gly
115 120 125
Gly Ser Gly Gly Ser Ser Tyr Val Leu Thr Gln Pro Ser Ser Val Ser
130 135 140
Val Ala Pro Gly Gln Thr Ala Thr Ile Ser Cys Gly Gly His Asn Ile
145 150 155 160
Gly Ser Lys Asn Val His Trp Tyr Gln Gln Arg Pro Gly Gln Ser Pro
165 170 175
Val Leu Val Ile Tyr Gln Asp Asn Lys Arg Pro Ser Gly Ile Pro Glu
180 185 190
Arg Phe Ser Gly Ser Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser
195 200 205
Gly Thr Gln Ala Met Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp
210 215 220
Asn Tyr Ser Val Leu Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
225 230 235 240
Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro
245 250 255
Gly Glu Ser Leu Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr
260 265 270
Ser Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu
275 280 285
Trp Met Gly Ala Ile Glu Pro Met Tyr Gly Ser Thr Ser Tyr Ala Gln
290 295 300
Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr
305 310 315 320
Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr
325 330 335
Tyr Cys Ala Arg Gly Ser Ala Tyr Tyr Tyr Asp Phe Ala Asp Tyr Trp
340 345 350
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Ser Gly Gly Ser
355 360 365
Gly Gly Ser Gly Gly Ser Ala Ile Gln Met Thr Gln Ser Pro Ser Ser
370 375 380
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
385 390 395 400
Glu Asp Ile Tyr Asn Gly Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys
405 410 415
Ala Pro Lys Leu Leu Ile Tyr Gly Ala Ser Ser Leu Gln Asp Gly Val
420 425 430
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr
435 440 445
Ile Ser Ser Leu Gln Pro Glu Asp Glu Ala Thr Tyr Tyr Cys Ala Gly
450 455 460
Pro His Lys Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
465 470 475 480
Lys
<210> 127
<211> 721
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 127
Ser Tyr Val Leu Thr Gln Pro Ser Ser Val Ser Val Ala Pro Gly Gln
1 5 10 15
Thr Ala Thr Ile Ser Cys Gly Gly His Asn Ile Gly Ser Lys Asn Val
20 25 30
His Trp Tyr Gln Gln Arg Pro Gly Gln Ser Pro Val Leu Val Ile Tyr
35 40 45
Gln Asp Asn Lys Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Asn Tyr Ser Val Leu
85 90 95
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gly Ser Gly Gly Ser
100 105 110
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
115 120 125
Ser Leu Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
130 135 140
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
145 150 155 160
Gly Ala Ile Glu Pro Met Tyr Gly Ser Thr Ser Tyr Ala Gln Lys Phe
165 170 175
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
180 185 190
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
195 200 205
Ala Arg Gly Ser Ala Tyr Tyr Tyr Asp Phe Ala Asp Tyr Trp Gly Gln
210 215 220
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
225 230 235 240
Gly Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Phe
245 250 255
Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
260 265 270
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Val
275 280 285
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
290 295 300
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
305 310 315 320
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
325 330 335
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
340 345 350
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
355 360 365
Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln
370 375 380
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
385 390 395 400
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
405 410 415
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
420 425 430
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
435 440 445
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
450 455 460
Leu Ser Pro Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val
465 470 475 480
Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu
485 490 495
Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr Asp Met
500 505 510
Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser
515 520 525
Ile Ser Thr Arg Gly Asp Ile Thr Ser Tyr Arg Asp Ser Val Lys Gly
530 535 540
Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln
545 550 555 560
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
565 570 575
Gln Asp Tyr Tyr Thr Asp Tyr Met Gly Phe Ala Tyr Trp Gly Gln Gly
580 585 590
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
595 600 605
Ser Gly Gly Gly Gly Ser Ala Ile Gln Met Thr Gln Ser Pro Ser Ser
610 615 620
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
625 630 635 640
Glu Asp Ile Tyr Asn Gly Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys
645 650 655
Ala Pro Lys Leu Leu Ile Tyr Gly Ala Ser Ser Leu Gln Asp Gly Val
660 665 670
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr
675 680 685
Ile Ser Ser Leu Gln Pro Glu Asp Glu Ala Thr Tyr Tyr Cys Ala Gly
690 695 700
Pro His Lys Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
705 710 715 720
Lys
<210> 128
<211> 960
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 128
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Asp Met Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Thr Arg Gly Asp Ile Thr Ser Tyr Arg Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Asp Tyr Tyr Thr Asp Tyr Met Gly Phe Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Ala Ile Gln Met Thr Gln Ser Pro
130 135 140
Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
145 150 155 160
Ala Ser Glu Asp Ile Tyr Asn Gly Leu Ala Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Gly Ala Ser Ser Leu Gln Asp
180 185 190
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr
195 200 205
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Glu Ala Thr Tyr Tyr Cys
210 215 220
Ala Gly Pro His Lys Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val
225 230 235 240
Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Pro Glu
245 250 255
Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
260 265 270
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Ala
275 280 285
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
290 295 300
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
305 310 315 320
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
325 330 335
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
340 345 350
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
355 360 365
Pro Gln Val Tyr Thr Lys Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
370 375 380
Gln Val Ser Leu Ser Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
385 390 395 400
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
405 410 415
Thr Val Pro Val Leu Asp Ser Asp Gly Ser Phe Arg Leu Ala Ser Tyr
420 425 430
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
435 440 445
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
450 455 460
Ser Leu Ser Pro Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Tyr
465 470 475 480
Val Leu Thr Gln Pro Ser Ser Val Ser Val Ala Pro Gly Gln Thr Ala
485 490 495
Thr Ile Ser Cys Gly Gly His Asn Ile Gly Ser Lys Asn Val His Trp
500 505 510
Tyr Gln Gln Arg Pro Gly Gln Ser Pro Val Leu Val Ile Tyr Gln Asp
515 520 525
Asn Lys Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser Asn Ser
530 535 540
Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met Asp Glu
545 550 555 560
Ala Asp Tyr Tyr Cys Gln Val Trp Asp Asn Tyr Ser Val Leu Phe Gly
565 570 575
Gly Gly Thr Lys Leu Thr Val Leu Gly Gly Ser Gly Gly Ser Gln Val
580 585 590
Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu Ser Leu
595 600 605
Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Tyr Met
610 615 620
His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Ala
625 630 635 640
Ile Glu Pro Met Tyr Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln Gly
645 650 655
Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr Met Glu
660 665 670
Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
675 680 685
Gly Ser Ala Tyr Tyr Tyr Asp Phe Ala Asp Tyr Trp Gly Gln Gly Thr
690 695 700
Leu Val Thr Val Ser Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly
705 710 715 720
Gly Ser Gly Gly Ser Gly Gly Ser Ser Tyr Val Leu Thr Gln Pro Ser
725 730 735
Ser Val Ser Val Ala Pro Gly Gln Thr Ala Thr Ile Ser Cys Gly Gly
740 745 750
His Asn Ile Gly Ser Lys Asn Val His Trp Tyr Gln Gln Arg Pro Gly
755 760 765
Gln Ser Pro Val Leu Val Ile Tyr Gln Asp Asn Lys Arg Pro Ser Gly
770 775 780
Ile Pro Glu Arg Phe Ser Gly Ser Asn Ser Gly Asn Thr Ala Thr Leu
785 790 795 800
Thr Ile Ser Gly Thr Gln Ala Met Asp Glu Ala Asp Tyr Tyr Cys Gln
805 810 815
Val Trp Asp Asn Tyr Ser Val Leu Phe Gly Gly Gly Thr Lys Leu Thr
820 825 830
Val Leu Gly Gly Ser Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly
835 840 845
Ala Glu Val Lys Lys Pro Gly Glu Ser Leu Lys Val Ser Cys Lys Ala
850 855 860
Ser Gly Tyr Thr Phe Thr Ser Tyr Tyr Met His Trp Val Arg Gln Ala
865 870 875 880
Pro Gly Gln Gly Leu Glu Trp Met Gly Ala Ile Glu Pro Met Tyr Gly
885 890 895
Ser Thr Ser Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg
900 905 910
Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser
915 920 925
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly Ser Ala Tyr Tyr Tyr
930 935 940
Asp Phe Ala Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
945 950 955 960
<210> 129
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 129
Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser
1 5 10
<210> 130
<211> 3
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<400> 130
Gly Gly Ser
1
<210> 131
<211> 190
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 131
Gly Met Arg Thr Glu Asp Leu Pro Lys Ala Val Val Phe Leu Glu Pro
1 5 10 15
Gln Trp Tyr Arg Val Leu Glu Lys Asp Ser Val Thr Leu Lys Cys Gln
20 25 30
Gly Ala Tyr Ser Pro Glu Asp Asn Ser Thr Gln Trp Phe His Asn Glu
35 40 45
Ser Arg Ile Ser Ser Gln Ala Ser Ser Tyr Phe Ile Asp Ala Ala Thr
50 55 60
Val Asp Asp Ser Gly Glu Tyr Arg Cys Gln Thr Asn Leu Ser Thr Leu
65 70 75 80
Ser Asp Pro Val Gln Leu Glu Val His Ile Gly Trp Leu Leu Leu Gln
85 90 95
Ala Pro Arg Trp Val Phe Lys Glu Glu Asp Pro Ile His Leu Arg Cys
100 105 110
His Ser Trp Lys Asn Thr Ala Leu His Lys Val Thr Tyr Leu Gln Asn
115 120 125
Gly Lys Gly Arg Lys Tyr Phe His His Asn Ser Asp Phe Tyr Ile Pro
130 135 140
Lys Ala Thr Leu Lys Asp Ser Gly Ser Tyr Phe Cys Arg Gly Leu Val
145 150 155 160
Gly Ser Lys Asn Val Ser Ser Glu Thr Val Asn Ile Thr Ile Thr Gln
165 170 175
Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Phe Pro Pro Gly
180 185 190
<210> 132
<211> 190
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 132
Gly Met Arg Thr Glu Asp Leu Pro Lys Ala Val Val Phe Leu Glu Pro
1 5 10 15
Gln Trp Tyr Arg Val Leu Glu Lys Asp Ser Val Thr Leu Lys Cys Gln
20 25 30
Gly Ala Tyr Ser Pro Glu Asp Asn Ser Thr Gln Trp Phe His Asn Glu
35 40 45
Ser Arg Ile Ser Ser Gln Ala Ser Ser Tyr Phe Ile Asp Ala Ala Thr
50 55 60
Val Asp Asp Ser Gly Glu Tyr Arg Cys Gln Thr Asn Leu Ser Thr Leu
65 70 75 80
Ser Asp Pro Val Gln Leu Glu Val His Ile Gly Trp Leu Leu Leu Gln
85 90 95
Ala Pro Arg Trp Val Phe Lys Glu Glu Asp Pro Ile His Leu Arg Cys
100 105 110
His Ser Trp Lys Asn Thr Ala Leu His Lys Val Thr Tyr Leu Gln Asn
115 120 125
Gly Lys Gly Arg Lys Tyr Phe His His Asn Ser Asp Phe Tyr Ile Pro
130 135 140
Lys Ala Thr Leu Lys Asp Ser Gly Ser Tyr Phe Cys Arg Gly Leu Phe
145 150 155 160
Gly Ser Lys Asn Val Ser Ser Glu Thr Val Asn Ile Thr Ile Thr Gln
165 170 175
Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Phe Pro Pro Gly
180 185 190
<210> 133
<211> 190
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 133
Gly Met Arg Ala Glu Asp Leu Pro Lys Ala Val Val Phe Leu Glu Pro
1 5 10 15
Gln Trp Tyr Arg Val Leu Glu Lys Asp Arg Val Thr Leu Lys Cys Gln
20 25 30
Gly Ala Tyr Ser Pro Glu Asp Asn Ser Thr Arg Trp Phe His Asn Glu
35 40 45
Ser Leu Ile Ser Ser Gln Thr Ser Ser Tyr Phe Ile Ala Ala Ala Arg
50 55 60
Val Asn Asn Ser Gly Glu Tyr Arg Cys Gln Thr Ser Leu Ser Thr Leu
65 70 75 80
Ser Asp Pro Val Gln Leu Glu Val His Ile Gly Trp Leu Leu Leu Gln
85 90 95
Ala Pro Arg Trp Val Phe Lys Glu Glu Glu Ser Ile His Leu Arg Cys
100 105 110
His Ser Trp Lys Asn Thr Leu Leu His Lys Val Thr Tyr Leu Gln Asn
115 120 125
Gly Lys Gly Arg Lys Tyr Phe His Gln Asn Ser Asp Phe Tyr Ile Pro
130 135 140
Lys Ala Thr Leu Lys Asp Ser Gly Ser Tyr Phe Cys Arg Gly Leu Ile
145 150 155 160
Gly Ser Lys Asn Val Ser Ser Glu Thr Val Asn Ile Thr Ile Thr Gln
165 170 175
Asp Leu Ala Val Ser Ser Ile Ser Ser Phe Phe Pro Pro Gly
180 185 190
<210> 134
<211> 190
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 134
Gly Met Arg Thr Glu Asp Leu Pro Lys Ala Val Val Phe Leu Glu Pro
1 5 10 15
Gln Trp Tyr Arg Val Leu Glu Lys Asp Ser Val Thr Leu Lys Cys Gln
20 25 30
Gly Ala Tyr Ser Pro Glu Asp Asn Ser Thr Gln Trp Phe His Asn Glu
35 40 45
Asn Leu Ile Ser Ser Gln Ala Ser Ser Tyr Phe Ile Asp Ala Ala Thr
50 55 60
Val Asp Asp Ser Gly Glu Tyr Arg Cys Gln Thr Asn Leu Ser Thr Leu
65 70 75 80
Ser Asp Pro Val Gln Leu Glu Val His Val Gly Trp Leu Leu Leu Gln
85 90 95
Ala Pro Arg Trp Val Phe Lys Glu Glu Asp Pro Ile His Leu Arg Cys
100 105 110
His Ser Trp Lys Asn Thr Ala Leu His Lys Val Thr Tyr Leu Gln Asn
115 120 125
Gly Lys Asp Arg Lys Tyr Phe His His Asn Ser Asp Phe His Ile Pro
130 135 140
Lys Ala Thr Leu Lys Asp Ser Gly Ser Tyr Phe Cys Arg Gly Leu Val
145 150 155 160
Gly Ser Lys Asn Val Ser Ser Glu Thr Val Asn Ile Thr Ile Thr Gln
165 170 175
Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Ser Pro Pro Gly
180 185 190
<210> 135
<211> 190
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 135
Gly Met Arg Thr Glu Asp Leu Pro Lys Ala Val Val Phe Leu Glu Pro
1 5 10 15
Gln Trp Tyr Ser Val Leu Glu Lys Asp Ser Val Thr Leu Lys Cys Gln
20 25 30
Gly Ala Tyr Ser Pro Glu Asp Asn Ser Thr Gln Trp Phe His Asn Glu
35 40 45
Ser Leu Ile Ser Ser Gln Ala Ser Ser Tyr Phe Ile Asp Ala Ala Thr
50 55 60
Val Asn Asp Ser Gly Glu Tyr Arg Cys Gln Thr Asn Leu Ser Thr Leu
65 70 75 80
Ser Asp Pro Val Gln Leu Glu Val His Val Gly Trp Leu Leu Leu Gln
85 90 95
Ala Pro Arg Trp Val Phe Lys Glu Glu Asp Pro Ile His Leu Arg Cys
100 105 110
His Ser Trp Lys Asn Thr Ala Leu His Lys Val Thr Tyr Leu Gln Asn
115 120 125
Gly Lys Asp Arg Lys Tyr Phe His His Asn Ser Asp Phe His Ile Pro
130 135 140
Lys Ala Thr Leu Lys Asp Ser Gly Ser Tyr Phe Cys Arg Gly Leu Val
145 150 155 160
Gly Ser Lys Asn Val Ser Ser Glu Thr Val Asn Ile Thr Ile Thr Gln
165 170 175
Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Ser Pro Pro Gly
180 185 190
<210> 136
<211> 190
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<400> 136
Gly Met Arg Thr Glu Asp Leu Pro Lys Ala Val Val Phe Leu Glu Pro
1 5 10 15
Gln Trp Tyr Ser Val Leu Glu Lys Asp Ser Val Thr Leu Lys Cys Gln
20 25 30
Gly Ala Tyr Ser Pro Glu Asp Asn Ser Thr Gln Trp Phe His Asn Glu
35 40 45
Ser Leu Ile Ser Ser Gln Ala Ser Ser Tyr Phe Ile Asp Asp Ala Thr
50 55 60
Val Asn Asp Ser Gly Glu Tyr Arg Cys Gln Thr Asn Leu Ser Thr Leu
65 70 75 80
Ser Asp Pro Val Gln Leu Glu Val His Val Gly Trp Leu Leu Leu Gln
85 90 95
Ala Pro Arg Trp Val Phe Lys Glu Glu Asp Pro Ile His Leu Arg Cys
100 105 110
His Ser Trp Lys Asn Thr Ala Leu His Lys Val Thr Tyr Leu Gln Asn
115 120 125
Gly Lys Asp Arg Lys Tyr Phe His His Asn Ser Asp Phe His Ile Pro
130 135 140
Lys Ala Thr Leu Lys Asp Ser Gly Ser Tyr Phe Cys Arg Gly Leu Val
145 150 155 160
Gly Ser Lys Asn Val Ser Ser Glu Thr Val Asn Ile Thr Ile Thr Gln
165 170 175
Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Ser Pro Pro Gly
180 185 190
Claims (230)
- 다음을 포함하는 다중특이적 항원-결합 단백질
(a) 적어도 하나의 제 1 표적 항원-결합 모이어티, 및
(b) 적어도 2개의 CD16A 항원-결합 모이어티, 여기서 적어도 2개의 CD16A 항원-결합 모이어티는 적어도 하나의 불변 도메인을 포함하는 Fab 단편 또는 Fc 부분에 융합됨. - 청구항 1에 있어서, 상기 2개의 CD16A 항원-결합 모이어티 중 적어도 하나는 단쇄 Fv (scFv), 단쇄 디아바디 (scDb) 및 디아바디 Db로 구성된 그룹에서 선택된 항원-결합 분자인 다중특이적 항원-결합 단백질.
- 청구항 1 또는 2에 있어서, 적어도 2개의 CD16A 항원-결합 모이어티 각각은 scFv인 다중특이적 항원-결합 단백질.
- 청구항 1 또는 2에 있어서, 적어도 2개의 CD16A 항원-결합 모이어티는 scDb 형태인 다중특이적 항원-결합 단백질.
- 청구항 1 내지 4 중 어느 한 항에 있어서, 상기 적어도 2개의 CD16A 항원-결합 모이어티 각각은 폴리펩티드 사슬에서 차례로 연결된 경쇄 가변 영역 (VL) 및 중쇄 가변 영역 (VH)을 포함하고, 폴리펩티드 사슬의 N-말단의 가변 영역은 VL인 다중특이적 항원-결합 단백질.
- 청구항 5에 있어서, 상기 폴리펩티드 사슬에서 적어도 2개의 CD16A 항원-결합 모이어티의 가변 영역은 N-말단으로부터 C-말단으로 VL-VH, VL-VL-VH-VH 또는 VL-VH-VL-VH의 순서로 배치되는 것인 다중특이적 항원-결합 단백질.
- 청구항 5 또는 6에 있어서, 상기 폴리펩티드 사슬에서 적어도 2개의 CD16A 항원-결합 모이어티의 가변 영역은 N-말단으로부터 C-말단으로 VL-VH의 순서로 배치되는 것인 다중특이적 항원-결합 단백질.
- 청구항 5 또는 6에 있어서, 상기 폴리펩티드 사슬에서 적어도 2개의 CD16A 항원-결합 모이어티의 가변 영역은 N-말단으로부터 C-말단으로 VL-VH-VL-VH의 순서로 배치되는 것인 다중특이적 항원-결합 단백질.
- 청구항 5 내지 8 중 어느 한 항에 있어서,
(i) 폴리펩티드 사슬의 C-말단은 Fc 부분의 CH2 도메인의 N-말단에 융합되거나; 또는
(ii) 폴리펩티드 사슬의 C-말단은 Fc 부분의 힌지의 N-말단에 융합되고;
(iii) 폴리펩티드 사슬의 N-말단은 Fc 부분의 CH3 도메인의 C-말단에 융합되거나; 또는
(iv) 폴리펩티드 사슬의 N-말단은 Fab 단편의 C-말단에 융합된 것인
다중특이적 항원-결합 단백질. - 청구항 5 내지 9 중 어느 한 항에 있어서, 폴리펩티드 사슬의 N-말단이 Fc 부분의 CH3 도메인의 C-말단에 융합된 것인 다중특이적 항원-결합 단백질.
- 청구항 1 내지 10 중 어느 한 항에 있어서, Fc 부분이 단량체 CH2-CH3 단편, 이종이량체 Fc 영역, 및 동종이량체 Fc 영역으로 구성된 그룹에서 선택되는 것인 다중특이적 항원-결합 단백질.
- 청구항 1 내지 11 중 어느 한 항에 있어서, 상기 Fc 부분은 Fc-감마 수용체에 결합하지 않지만 신생아 Fc 수용체에 대한 결합을 유지하는 것인 다중특이적 항원-결합 단백질.
- 청구항 12에 있어서, 상기 2개의 CD16 항원-결합 모이어티를 포함하는 scDb 또는 Db는 Fab 단편 중 하나의 사슬의 C-말단에 융합되고 제 1 표적 항원-결합 모이어티는 Fab 단편의 다른 사슬의 C-말단에 융합된 것인 다중특이적 항원-결합 단백질.
- 청구항 13에 있어서, Fab 단편은 N-말단에 HSA 항원-결합 Fv를 포함하는 것인 다중특이적 항원-결합 단백질.
- 청구항 1 내지 14 중 어느 한 항에 있어서, 4가인 다중특이적 항원-결합 단백질.
- 청구항 15에 있어서, 적어도 2개의 표적 항원-결합 모이어티를 포함하는 다중특이적 항원-결합 단백질.
- 청구항 16에 있어서, 이량체 Fc 부분에 융합된, 적어도 2개의 CD16A 항원-결합 모이어티, 제 1 표적 항원-결합 모이어티, 및 제 2 표적 항원-결합 모이어티를 포함하는 다중특이적 항원-결합 단백질.
- 청구항 1에 있어서, CD16A 항원-결합 모이어티는 IgG의 각 중쇄의 C-말단에 융합되고, IgG는 2개의 Fab 각각에서 N-말단에서 제 1 표적 항원-결합 Fv 모이어티를 포함하고 제 2 표적 항원-결합 모이어티는 C-말단에서 CL 도메인들 각각에 융합된 것인 다중특이적 항원-결합 단백질.
- 청구항 1 내지 18 중 어느 한 항에 있어서, CD16A 항원-결합 모이어티는 다음을 포함하는 것인 다중특이적 항원-결합 단백질:
(i) 서열 번호: 50에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 51에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 52에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및/또는
(ii) 서열 번호: 53에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 54에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 55에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역. - 청구항 1 내지 18 중 어느 한 항에 있어서, CD16A 항원-결합 모이어티는 다음을 포함하는 것인 다중특이적 항원-결합 단백질:
(i) 서열 번호: 73에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 74에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 75에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및/또는
(ii) 서열 번호: 76에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 77에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 78에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역. - 청구항 1 내지 20 중 어느 한 항에 있어서, CD16A 항원-결합 모이어티는 (i) 서열 번호: 3에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 이와 동일한 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 2에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 이와 동일한 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하는 것인 다중특이적 항원-결합 단백질.
- 청구항 1 내지 21 중 어느 한 항에 있어서, CD16A 항원-결합 모이어티는 (i) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하는 것인 다중특이적 항원-결합 단백질.
- 청구항 1 내지 15 중 어느 한 항에 있어서, 제 1 표적 항원은 BCMA 및 EGFR로부터 선택되는 것인 다중특이적 항원-결합 단백질.
- 청구항 23에 있어서, 제 1 표적 항원은 BCMA인 다중특이적 항원-결합 단백질.
- 청구항 24에 있어서, 서열 번호: 61 또는 63에 제시된 아미노산 서열을 갖는 제 1 폴리펩티드 사슬, 및 서열 번호: 62 또는 64에 제시된 아미노산 서열을 갖는 제 2 폴리펩티드 사슬을 포함하는 사량체인 다중특이적 항원-결합 단백질.
- 청구항 25에 있어서, 다음으로부터 선택된 제 1 및 제 2 폴리펩티드를 포함하는 사량체인 다중특이적 항원-결합 단백질:
(i) 서열 번호: 61에 제시된 아미노산 서열을 갖는 제 1 폴리펩티드 및 서열 번호: 62에 제시된 아미노산 서열을 갖는 제 2 폴리펩티드;
(ii) 서열 번호: 61에 제시된 아미노산 서열을 갖는 제 1 폴리펩티드 및 서열 번호: 64에 제시된 아미노산 서열을 갖는 제 2 폴리펩티드;
(iii) 서열 번호: 63에 제시된 아미노산 서열을 갖는 제 1 폴리펩티드 및 서열 번호: 62에 제시된 아미노산 서열을 갖는 제 2 폴리펩티드; 및
(iv) 서열 번호: 63에 제시된 아미노산 서열을 갖는 제 1 폴리펩티드 및 서열 번호: 64에 제시된 아미노산 서열을 갖는 제 2 폴리펩티드. - 청구항 24에 있어서, BCMA 항원-결합 모이어티는 다음을 포함하는 것인 다중특이적 항원-결합 단백질:
(i) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및/또는
(ii) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역. - 청구항 24에 있어서, BCMA 항원-결합 모이어티는 다음을 포함하는 것인 다중특이적 항원-결합 단백질:
(i) 서열 번호: 65에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 동일한 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는
(ii) 서열 번호: 66에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 동일한 아미노산 서열을 포함하는 경쇄 가변 영역. - 청구항 24에 있어서, BCMA 항원-결합 모이어티는 다음을 포함하는 것인 다중특이적 항원-결합 단백질:
(i) 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는
(ii) 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역. - 청구항 24에 있어서, 다음을 포함하는 다중특이적 항원-결합 단백질:
(i) 다음을 포함하는 CD16A 항원-결합 모이어티:
(a) 서열 번호: 73에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 74에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 75에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및
(b) 서열 번호: 76에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 77에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 78에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역; 및
(ii) 다음을 포함하는 BCMA 항원-결합 모이어티:
(a) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및
(ii) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역. - 청구항 1 내지 30 중 어느 한 항의 다중특이적 항원-결합 단백질 및 제약학적으로 허용되는 담체를 포함하는 제약학적 조성물.
- 청구항 1 내지 30 중 어느 한 항에 있어서, 약제로 사용하기 위한 다중특이적 항원-결합 단백질.
- 청구항 31에 있어서, 약제로 사용하기 위한 제약학적 조성물.
- 청구항 1 내지 30 중 어느 한 항의 다중특이적 항원-결합 단백질 또는 청구항 31의 제약학적 조성물을 필요로 하는 대상체에게 투여하는 것을 포함하는, 질환의 치료 또는 개선 방법.
- 청구항 34에 있어서, 상기 질환은 암인 방법.
- 청구항 34 또는 35에 있어서, 상기 질환은 혈액암인 방법.
- 청구항 34 내지 36 중 어느 한 항에 있어서, 상기 질환은 다발성 골수종인 방법.
- 청구항 1 내지 30 중 어느 한 항의 이중특이적 항원-결합 단백질 또는 청구항 31의 제약학적 조성물을 필요로 하는 대상체에게 투여하는 것을 포함하는, 대상체에서 질환의 치료 및/또는 예방 방법.
- 청구항 38에 있어서, 상기 이중특이적 항원-결합 단백질을 정맥내로 투여하는 것을 포함하는 방법.
- 청구항 38에 있어서, 상기 이중특이적 항원-결합 단백질을 피하 투여하는 것을 포함하는 방법.
- 청구항 38 내지 40 중 어느 한 항에 있어서, 제 2 요법을 투여하는 것을 포함하는 방법.
- 청구항 41에 있어서, 상기 제 2 요법은 항-PD-1 항체를 포함하는 요법, 항-PD-L1 항체를 포함하는 요법, CD3 이중특이적 항체를 포함하는 요법, 항-TIGIT 항체를 포함하는 요법, 항-VEGF 항체를 포함하는 요법, 및 항-FcRH5 항체를 포함하는 요법으로 구성된 그룹에서 선택되는 것인 방법.
- 청구항 41에 있어서, 제 2 요법은 사이토카인 요법인 방법.
- 청구항 43에 있어서, 상기 사이토카인 요법은 IL-15, IL-2, IL-12, IL-21 및 IL-6으로 구성된 그룹에서 선택된 사이토카인의 투여를 포함하는 것인 방법.
- 청구항 44에 있어서, 상기 사이토카인 요법은 IL-2의 투여를 포함하는 것인 방법.
- 청구항 44에 있어서, 상기 사이토카인 요법은 IL-15의 투여를 포함하는 것인 방법.
- 청구항 34 내지 46 중 어느 한 항에 있어서, 대상체는 암 환자인 방법.
- 청구항 34 내지 46 중 어느 한 항에 있어서, 대상체는 혈액암 환자인 방법.
- 청구항 34 내지 48 중 어느 한 항에 있어서, 대상체는 다발성 골수종 환자인 방법.
- 청구항 34 내지 49 중 어느 한 항에 있어서, 대상체는 재발성/불응성 다발성 골수종 환자인 방법.
- 청구항 34 내지 50 중 어느 한 항에 있어서, 대상체는 항-CD38 요법을 받은 적이 있는 것인 방법.
- 청구항 34 내지 51 중 어느 한 항에 있어서, 대상체는 다라투무맙을 받은 적이 있는 것인 방법.
- 청구항 34 내지 52 중 어느 한 항에 있어서, 대상체는 다라투무맙 나이브, 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성인 방법.
- 청구항 53에 있어서, 대상체는 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성인 방법.
- 청구항 34 내지 54 중 어느 한 항에 있어서, 대상체는 CD16A 다형성을 발현하는 것인 방법.
- 청구항 55에 있어서, 상기 CD16A 다형성은 CD16A-158V/F 다형성인 방법.
- 다음을 포함하는 이중특이적 항원-결합 단백질:
(a) 적어도 하나의 BCMA-결합 모이어티, 및
(b) 적어도 2개의 CD16A 항원-결합 모이어티, 여기서 적어도 2개의 CD16A 항원-결합 모이어티는 적어도 하나의 불변 도메인을 포함하는 Fab 단편 또는 Fc 부분에 융합됨. - 청구항 57에 있어서, 상기 2개의 CD16A 항원-결합 모이어티 중 적어도 하나는 단쇄 Fv (scFv), 단쇄 디아바디 (scDb) 및 디아바디 Db로 구성된 그룹에서 선택된 항원-결합 분자인 이중특이적 항원-결합 단백질.
- 청구항 57 또는 58에 있어서, 적어도 2개의 CD16A 항원-결합 모이어티 각각은 scFv인 이중특이적 항원-결합 단백질.
- 청구항 57 내지 59 중 어느 한 항에 있어서, 적어도 2개의 CD16A 항원-결합 모이어티는 scDb 형태인 이중특이적 항원-결합 단백질.
- 청구항 57 내지 59 중 어느 한 항에 있어서, 상기 적어도 2개의 CD16A 항원-결합 모이어티 각각은 폴리펩티드 사슬에서 차례로 연결된 경쇄 가변 영역 (VL) 및 중쇄 가변 영역 (VH)을 포함하고, 폴리펩티드 사슬의 N-말단의 가변 영역은 VL인 이중특이적 항원-결합 단백질.
- 청구항 61에 있어서, 상기 폴리펩티드 사슬에서 적어도 2개의 CD16A 항원-결합 모이어티의 가변 영역은 N-말단으로부터 C-말단으로 VL-VH, VL-VL-VH-VH 또는 VL-VH-VL-VH의 순서로 배치되는 것인 이중특이적 항원-결합 단백질.
- 청구항 61 또는 62에 있어서, 상기 폴리펩티드 사슬에서 적어도 2개의 CD16A 항원-결합 모이어티의 가변 영역은 N-말단으로부터 C-말단으로 VL-VH의 순서로 배치되는 것인 이중특이적 항원-결합 단백질.
- 청구항 61 또는 62에 있어서, 상기 폴리펩티드 사슬에서 적어도 2개의 CD16A 항원-결합 모이어티의 가변 영역은 N-말단으로부터 C-말단으로 VL-VH-VL-VH의 순서로 배치되는 것인 이중특이적 항원-결합 단백질.
- 청구항 61 내지 64 중 어느 한 항에 있어서,
(i) 폴리펩티드 사슬의 C-말단은 Fc 부분의 CH2 도메인의 N-말단에 융합되거나; 또는
(ii) 폴리펩티드 사슬의 C-말단은 Fc 부분의 힌지의 N-말단에 융합되고;
(iii) 폴리펩티드 사슬의 N-말단은 Fc 부분의 CH3 도메인의 C-말단에 융합되거나; 또는
(iv) 폴리펩티드 사슬의 N-말단은 Fab 단편의 C-말단에 융합된 것인
이중특이적 항원-결합 단백질. - 청구항 61 내지 64 중 어느 한 항에 있어서, 폴리펩티드 사슬의 N-말단은 Fc 부분의 CH3 도메인의 C-말단에 융합된 것인 이중특이적 항원-결합 단백질.
- 청구항 57 내지 66 중 어느 한 항에 있어서, Fc 부분은 단량체 CH2-CH3 단편, 이종이량체 Fc 영역, 및 동종이량체 Fc 영역으로 구성된 그룹에서 선택되는 것인 이중특이적 항원-결합 단백질.
- 청구항 57 내지 67 중 어느 한 항에 있어서, 상기 Fc 부분은 Fc-감마 수용체에 결합하지 않지만 신생아 Fc 수용체에 대한 결합을 유지하는 것인 이중특이적 항원-결합 단백질.
- 청구항 57 내지 67 중 어느 한 항에 있어서, Fc 부분은 적어도 하나의 무-이펙터 돌연변이를 포함하는 것인 이중특이적 항원-결합 단백질.
- 청구항 69에 있어서, 상기 적어도 하나의 무-이펙터 돌연변이는 C220S, C229S, E233P, L234A, L234V, L234F, L235A, L235E, P238S, D265A, N297A, N297Q, 및 P331S로 구성된 그룹에서 선택되는 것인 이중특이적 항원-결합 단백질.
- 청구항 69 또는 70에 있어서, 상기 적어도 하나의 무-이펙터 돌연변이는 L234A, L234V, L234F, L235A, L235E, P238S, 및 D265A로 구성된 그룹에서 선택되는 것인 이중특이적 항원-결합 단백질.
- 청구항 69 내지 71 중 어느 한 항에 있어서, 상기 적어도 하나의 무-이펙터 돌연변이는 L234F, L235E, 및 D265A로 구성된 그룹에서 선택되는 것인 이중특이적 항원-결합 단백질.
- 청구항 69 내지 72 중 어느 한 항에 있어서, 상기 Fc 부분은 2개의 무-이펙터 돌연변이를 포함하는 것인 이중특이적 항원-결합 단백질.
- 청구항 73에 있어서, 상기 2개의 무-이펙터 돌연변이는 L234F 및 L235E인 이중특이적 항원-결합 단백질.
- 청구항 69 내지 72 중 어느 한 항에 있어서, 상기 Fc 부분은 3개의 무-이펙터 돌연변이를 포함하는 것인 이중특이적 항원-결합 단백질.
- 청구항 75에 있어서, 상기 3개의 무-이펙터 돌연변이는 L234F, L235E 및 D265A인 이중특이적 항원-결합 단백질.
- 청구항 57 내지 77 중 어느 한 항에 있어서, 적어도 2개의 CD16A 항원-결합 모이어티는 Fc 부분에 융합된 것인 이중특이적 항원-결합 단백질.
- 청구항 57 내지 77 중 어느 한 항에 있어서, 2개의 BCMA-표적화 모이어티를 포함하는 이중특이적 항원-결합 단백질.
- 청구항 57 내지 78 중 어느 한 항에 있어서, 2개의 CD16A 항원-결합 모이어티 및 2개의 BCMA-표적화 모이어티를 포함하는 이중특이적 항원-결합 단백질.
- 청구항 79에 있어서, 2개의 CD16A 항원-결합 모이어티 각각은 IgG의 각 중쇄의 C-말단에 융합되고, 2개의 BCMA-표적화 모이어티 각각은 IgG의 N-말단에 융합된 것인 이중특이적 항원-결합 단백질.
- 청구항 77 내지 80 중 어느 한 항에 있어서, 도 13에 도시된 구조를 가지는 이중특이적 항원-결합 단백질.
- 청구항 57 내지 77 중 어느 한 항에 있어서, 하나의 BCMA-표적화 모이어티를 포함하는 이중특이적 항원-결합 단백질.
- 청구항 82에 있어서, 상기 BCMA-표적화 모이어티는 적어도 2개의 CD16A 항원-결합 모이어티가 융합된 Fc 부분의 N-말단에 융합된 것인 이중특이적 항원-결합 단백질.
- 청구항 82 또는 83에 있어서, 도 5에 도시된 구조를 가지는 이중특이적 항원-결합 단백질.
- 청구항 57 내지 84 중 어느 한 항에 있어서, CD16A 항원-결합 모이어티는 다음을 포함하는 것인 이중특이적 항원-결합 단백질:
(i) 서열 번호: 50에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 51 또는 56에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 52에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및/또는
(ii) 서열 번호: 53에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 54에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 55에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역. - 청구항 84에 있어서, 중쇄 가변 영역 CDR2는 서열 번호: 51에 제시된 아미노산 서열을 갖는 것인 이중특이적 항원-결합 단백질.
- 청구항 85에 있어서, 중쇄 가변 영역 CDR2는 서열 번호: 56에 제시된 아미노산 서열을 갖는 것인 이중특이적 항원-결합 단백질.
- 청구항 57 내지 85 중 어느 한 항에 있어서, CD16A 항원-결합 모이어티는 다음을 포함하는 것인 이중특이적 항원-결합 단백질:
(i) 서열 번호: 73에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 74에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 75에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및/또는
(ii) 서열 번호: 76에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 77에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 78에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역. - 청구항 57 내지 88 중 어느 한 항에 있어서, CD16A 항원-결합 모이어티는 (i) 서열 번호: 3에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 이와 동일한 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 2에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 이와 동일한 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하는 것인 이중특이적 항원-결합 단백질.
- 청구항 57 내지 89 중 어느 한 항에 있어서, CD16A 항원-결합 모이어티는 (i) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하는 것인 이중특이적 항원-결합 단백질.
- 청구항 57 내지 90 중 어느 한 항에 있어서, BCMA 항원-결합 모이어티는 다음을 포함하는 것인 이중특이적 항원-결합 단백질:
(i) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및/또는
(ii) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역. - 청구항 57 내지 91 중 어느 한 항에 있어서, BCMA 항원-결합 모이어티는 (i) 서열 번호: 65에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 이와 동일한 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 66에 제시된 아미노산 서열과 적어도 약 80% 상동성이거나 이와 동일한 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하는 것인 이중특이적 항원-결합 단백질.
- 청구항 57 내지 92 중 어느 한 항에 있어서, BCMA 항원-결합 모이어티는 (i) 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역, 및/또는 (ii) 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하는 것인 이중특이적 항원-결합 단백질.
- 청구항 57 내지 74, 77 내지 81, 및 85 내지 93 중 어느 한 항에 있어서, 2개의 CD16A 항원-결합 모이어티 및 2개의 BCMA-표적화 모이어티를 포함하며,
(a) 상기 각각의 CD16A 항원-결합 모이어티는 서열 번호:73에 제시된 아미노산 서열을 갖는 VH CDR1, 서열 번호:74에 제시된 아미노산 서열을 갖는 VH CDR2, 서열 번호:75에 제시된 아미노산 서열을 갖는 VH CDR3, 서열 번호:76에 제시된 아미노산 서열을 갖는 VL CDR1, 서열 번호:77에 제시된 아미노산 서열을 갖는 VL CDR2, 및 서열 번호:78에 제시된 아미노산 서열을 갖는 VL CDR3을 포함하고;
(b) 상기 각각의 BCMA-표적화 모이어티는 서열 번호:67에 제시된 아미노산 서열을 갖는 VH CDR1, 서열 번호:68에 제시된 아미노산 서열을 갖는 VH CDR2, 서열 번호:69에 제시된 아미노산 서열을 갖는 VH CDR3, 서열 번호:70에 제시된 아미노산 서열을 갖는 VL CDR1, 서열 번호:71에 제시된 아미노산 서열을 갖는 VL CDR2, 및 서열 번호:72에 제시된 아미노산 서열을 갖는 VL CDR3을 포함하는 것인
이중특이적 항원-결합 단백질. - 청구항 57 내지 74, 77 내지 81, 및 85 내지 94 중 어느 한 항에 있어서, 2개의 CD16A 항원-결합 모이어티 및 2개의 BCMA-표적화 모이어티를 포함하며,
(a) 각각의 CD16A 항원-결합 모이어티는 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역, 및 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하고;
(b) 각각의 BCMA-표적화 모이어티는 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역, 및 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하는 것인
이중특이적 항원-결합 단백질. - 청구항 57 내지 74, 77 내지 81, 및 85 내지 95 중 어느 한 항에 있어서, 서열 번호: 61에 제시된 아미노산 서열을 갖는 제 1 폴리펩티드, 및 서열 번호: 62에 제시된 아미노산 서열을 갖는 제 2 폴리펩티드를 포함하는 사량체인 이중특이적 항원-결합 단백질.
- 청구항 57 내지 93 중 어느 한 항에 있어서, 서열 번호: 63에 제시된 아미노산 서열을 갖는 제 1 폴리펩티드, 및 서열 번호: 64에 제시된 아미노산 서열을 갖는 제 2 폴리펩티드를 포함하는 사량체인 이중특이적 항원-결합 단백질.
- 청구항 81에 있어서,
(i) CD16A 항원-결합 모이어티는 각각
(a) 서열 번호: 73에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 74에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 75에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및
(b) 서열 번호: 76에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 77에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 78에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역
을 포함하고;
(ii) 상기 BCMA 항원-결합 모이어티는 각각
(a) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및
(ii) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역
을 포함하는 것인
이중특이적 항원-결합 단백질. - 청구항 57 내지 98 중 어느 한 항의 이중특이적 항원-결합 단백질 및 제약학적으로 허용되는 담체를 포함하는 제약학적 조성물.
- 청구항 57 내지 98 중 어느 한 항에 있어서, 약제로 사용하기 위한 이중특이적 항원-결합 단백질.
- 청구항 99에 있어서, 약제로 사용하기 위한 제약학적 조성물.
- 청구항 57 내지 98 중 어느 한 항의 이중특이적 항원-결합 단백질 또는 청구항 99의 제약학적 조성물을 필요로 하는 대상체에게 투여하는 것을 포함하는, 질환의 치료 및/또는 예방 방법.
- 청구항 102에 있어서, 상기 질환은 암인 방법.
- 청구항 102 또는 103에 있어서, 상기 질환은 혈액암인 방법.
- 청구항 102 내지 104 중 어느 한 항에 있어서, 상기 질환은 다발성 골수종인 방법.
- 청구항 102 내지 105 중 어느 한 항에 있어서, 이중특이적 항원-결합 단백질을 정맥내 투여하는 것을 포함하는 방법.
- 청구항 102 내지 105 중 어느 한 항에 있어서, 이중특이적 항원-결합 단백질을 피하 투여하는 것을 포함하는 방법.
- 청구항 102 내지 107 중 어느 한 항에 있어서, 제 2 요법을 투여하는 것을 포함하는 방법.
- 청구항 108에 있어서, 상기 제 2 요법은 항-PD-1 항체를 포함하는 요법, 항-PD-L1 항체를 포함하는 요법, CD3 이중특이적 항체를 포함하는 요법, 항-TIGIT 항체를 포함하는 요법, 항-VEGF 항체를 포함하는 요법, 및 항-FcRH5 항체를 포함하는 요법으로 구성된 그룹에서 선택되는 것인 방법.
- 청구항 108에 있어서, 제 2 요법은 사이토카인 요법인 방법.
- 청구항 110에 있어서, 상기 사이토카인 요법은 IL-15, IL-2, IL-12, IL-21, IL-17, IL-18, IL-23, IL-27, 및 IL-6으로 구성된 그룹에서 선택된 사이토카인의 투여인 방법.
- 청구항 111에 있어서, 사이토카인은 IL-15인 방법.
- 청구항 111에 있어서, 사이토카인은 IL-2인 방법.
- 청구항 102 내지 113 중 어느 한 항에 있어서, 대상체는 암 환자인 방법.
- 청구항 102 내지 114 중 어느 한 항에 있어서, 대상체는 혈액암 환자인 방법.
- 청구항 102 내지 115 중 어느 한 항에 있어서, 대상체는 다발성 골수종 환자인 방법.
- 청구항 102 내지 116 중 어느 한 항에 있어서, 대상체는 재발성/불응성 다발성 골수종 환자인 방법.
- 청구항 102 내지 117 중 어느 한 항에 있어서, 대상체는 항-CD38 요법을 받은 적이 있는 것인 방법.
- 청구항 102 내지 118 중 어느 한 항에 있어서, 대상체는 다라투무맙을 받은 적이 있는 것인 방법.
- 청구항 102 내지 119 중 어느 한 항에 있어서, 대상체는 다라투무맙 나이브, 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성인 방법.
- 청구항 120에 있어서, 대상체는 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성인 방법.
- 청구항 102 내지 121 중 어느 한 항에 있어서, 대상체는 CD16A 다형성을 발현하는 것인 방법.
- 청구항 122에 있어서, 상기 CD16A 다형성은 CD16A-158V/F 다형성인 방법.
- 청구항 1 내지 30 중 어느 한 항의 다중특이적 항원-결합 단백질 또는 청구항 57 내지 98 중 어느 한 항의 이중특이적 항원-결합 단백질에 있어서, 다중특이적 항원-결합 단백질 또는 이중특이적 항원-결합 단백질은 대상체에게 투여될 때 상기 대상체의 자연 살해 (NK) 세포 집단을 실질적으로 고갈시키거나 감소시키지 않는, 다중특이적 항원-결합 단백질 또는 이중특이적 항원-결합 단백질.
- 청구항 1 내지 30 중 어느 한 항의 다중특이적 항원-결합 단백질 또는 청구항 57 내지 98 중 어느 한 항의 이중특이적 항원-결합 단백질을 투여하는 것을 포함하는, 고갈되거나 감소된 NK 세포 집단을 갖는 대상체의 치료 방법.
- 청구항 125에 있어서, 상기 대상체는 항-CD38 요법으로 이전에 치료받은 적이 있는 것인 방법.
- 청구항 126에 있어서, 상기 항-CD38 요법은 다라투무맙 요법인 방법.
- 2개의 CD16A 항원-결합 모이어티 및 2개의 BCMA-표적화 모이어티를 포함하는 이중특이적 항원-결합 단백질이며, 상기 2개의 CD16A 항원-결합 모이어티 각각은 IgG의 각 중쇄의 C-말단에 융합되고, 2개의 BCMA-표적화 모이어티 각각은 IgG의 각 중쇄의 N-말단에 융합되며,
(i) CD16A 항원-결합 모이어티는 각각
(a) 서열 번호: 73에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 74에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 75에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및
(b) 서열 번호: 76에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 77에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 78에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역
을 포함하고;
(ii) BCMA 항원-결합 모이어티는 각각
(a) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및
(ii) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역
을 포함하는 것인
이중특이적 항원-결합 단백질. - 2개의 CD16A 항원-결합 모이어티 및 2개의 BCMA-표적화 모이어티를 포함하는 이중특이적 항원-결합 단백질을 대상체에게 투여하는 것을 포함하는 대상체의 암 치료 방법이며, 상기 2개의 CD16A 항원-결합 모이어티 각각은 IgG의 각 중쇄의 C-말단에 융합되고, 2개의 BCMA-표적화 모이어티 각각은 IgG의 각 중쇄의 N-말단에 융합되며,
(i) CD16A 항원-결합 모이어티는 각각
(a) 서열 번호: 73에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 74에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 75에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및
(b) 서열 번호: 76에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 77에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 78에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역
을 포함하고;
(ii) BCMA 항원-결합 모이어티는 각각
(a) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및
(ii) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역
을 포함하는 것인
암 치료 방법. - 청구항 129에 있어서, 상기 암은 다발성 골수종인 방법.
- 다음을 포함하는, CD16A 및 BCMA에 결합하거나 결합할 수 있는 항체 또는 항원-결합 단백질:
(i) 서열 번호: 73에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 74에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 75에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 제 1 중쇄 가변 영역,
(ii) 서열 번호: 76에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 77에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 78에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 제 1 경쇄 가변 영역;
(iii) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 제 2 중쇄 가변 영역, 및
(iv) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 제 2 경쇄 가변 영역. - 청구항 131에 있어서, 다음과 같은 항체 또는 항원-결합 단백질:
(i) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 제 1 중쇄 가변 영역;
(ii) 서열 번호: 2에 제시된 아미노산 서열을 포함하는 제 1 경쇄 가변 영역;
(iii) 서열 번호: 65에 제시된 아미노산 서열을 포함하는 제 2 중쇄 가변 영역;
(iv) 서열 번호: 66에 제시된 아미노산 서열을 포함하는 제 2 경쇄 가변 영역;
(v) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 제 1 중쇄 가변 영역, 및 서열 번호: 2에 제시된 아미노산 서열을 포함하는 제 1 경쇄 가변 영역;
(vi) 서열 번호: 65에 제시된 아미노산 서열을 포함하는 제 2 중쇄 가변 영역, 및 서열 번호: 66에 제시된 아미노산 서열을 포함하는 제 2 경쇄 가변 영역; 또는
(vii) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 제 1 중쇄 가변 영역 및 서열 번호: 2에 제시된 아미노산 서열을 포함하는 제 1 경쇄 가변 영역; 및 서열 번호: 65에 제시된 아미노산 서열을 포함하는 제 2 중쇄 가변 영역 및 서열 번호: 66에 제시된 아미노산 서열을 포함하는 제 2 경쇄 가변 영역. - 청구항 131 또는 132에 있어서, CD16B에 결합하지 않는 항체 또는 항원-결합 단백질.
- 청구항 131 내지 133 중 어느 한 항에 있어서, 대상체에게 투여될 때 상기 대상체의 자연 살해 (NK) 세포 집단을 실질적으로 고갈시키거나 감소시키지 않는 항체 또는 항원-결합 단백질.
- 청구항 131 내지 134 중 어느 한 항에 있어서, CD16A는 인간 CD16A인 항체 또는 항원-결합 단백질.
- 청구항 131 내지 135 중 어느 한 항에 있어서, BCMA는 인간 BCMA인 항체 또는 항원-결합 단백질.
- 청구항 131 내지 136 중 어느 한 항의 항체 또는 항원-결합 단백질 및 제약학적으로 허용되는 담체를 포함하는 제약학적 조성물.
- 청구항 131 내지 136 중 어느 한 항에 있어서, 약제로 사용하기 위한 항체 또는 항원-결합 단백질.
- 청구항 137에 있어서, 약제로 사용하기 위한 제약학적 조성물.
- 청구항 131 내지 136 중 어느 한 항의 이중특이적 항원-결합 단백질 또는 청구항 137의 제약학적 조성물을 필요로 하는 대상체에게 투여하는 것을 포함하는, 질환의 치료 및/또는 예방 방법.
- 청구항 140에 있어서, 상기 질환은 암인 방법.
- 청구항 140 또는 141에 있어서, 상기 질환은 혈액암인 방법.
- 청구항 140 내지 142 중 어느 한 항에 있어서, 상기 질환은 다발성 골수종인 방법.
- 청구항 140 내지 143 중 어느 한 항에 있어서, 상기 항체 또는 항원-결합 단백질을 정맥내 또는 피하 투여하는 것을 포함하는 방법.
- 청구항 140 내지 144 중 어느 한 항에 있어서, 제 2 요법을 투여하는 것을 포함하는 방법.
- 청구항 145에 있어서, 상기 제 2 요법은 항-PD-1 항체를 포함하는 요법, 항-PD-L1 항체를 포함하는 요법, CD3 이중특이적 항체를 포함하는 요법, 항-TIGIT 항체를 포함하는 요법, 항-VEGF 항체를 포함하는 요법, 및 항-FcRH5 항체를 포함하는 요법으로 구성된 그룹에서 선택되는 것인 방법.
- 청구항 145에 있어서, 제 2 요법은 사이토카인 요법인 방법.
- 청구항 147에 있어서, 상기 사이토카인 요법은 IL-15, IL-2, IL-12, IL-21, IL-17, IL-18, IL-23, IL-27, 및 IL-6으로 구성된 그룹에서 선택된 사이토카인의 투여인 방법.
- 청구항 148에 있어서, 사이토카인은 IL-15인 방법.
- 청구항 148에 있어서, 사이토카인은 IL-2인 방법.
- 청구항 140 내지 150 중 어느 한 항에 있어서, 대상체는 암 환자인 방법.
- 청구항 140 내지 151 중 어느 한 항에 있어서, 대상체는 혈액암 환자인 방법.
- 청구항 140 내지 152 중 어느 한 항에 있어서, 대상체는 다발성 골수종 환자인 방법.
- 청구항 140 내지 153 중 어느 한 항에 있어서, 대상체는 재발성/불응성 다발성 골수종 환자인 방법.
- 청구항 140 내지 154 중 어느 한 항에 있어서, 대상체는 항-CD38 요법을 받은 적이 있는 것인 방법.
- 청구항 140 내지 155 중 어느 한 항에 있어서, 대상체는 다라투무맙을 받은 적이 있는 것인 방법.
- 청구항 140 내지 156 중 어느 한 항에 있어서, 대상체는 다라투무맙 나이브, 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성인 방법.
- 청구항 157에 있어서, 대상체는 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성인 방법.
- 청구항 140 내지 158 중 어느 한 항에 있어서, 대상체는 CD16A 다형성을 발현하는 것인 방법.
- 청구항 159에 있어서, 상기 CD16A 다형성은 CD16A-158V/F 다형성인 방법.
- 청구항 131 내지 136 중 어느 한 항의 항체 또는 항원-결합 단백질 또는 청구항 137의 제약학적 조성물을 투여하는 것을 포함하는, 고갈되거나 감소된 NK 세포 집단을 갖는 대상체의 치료 방법.
- 청구항 161에 있어서, 상기 대상체는 항-CD38 요법으로 이전에 치료받은 적이 있는 것인 방법.
- 청구항 162에 있어서, 상기 항-CD38 요법은 다라투무맙 요법인 방법.
- CD16A에 결합하거나 결합할 수 있는 적어도 하나의 아암, 및 BCMA에 결합하거나 결합할 수 있는 적어도 하나의 아암을 포함하는, 항체 또는 항원-결합 단백질이며,
(i) CD16A에 결합하거나 결합할 수 있는 적어도 하나의 아암은
(a) 서열 번호: 73에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 74에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 75에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및
(b) 서열 번호: 76에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 77에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 78에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역
을 포함하고;
(ii) BCMA에 결합하거나 결합할 수 있는 적어도 하나의 아암은
(a) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및
(ii) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역
을 포함하는 것인
항체 또는 항원-결합 단백질. - 청구항 164에 있어서, CD16A에 결합하거나 결합할 수 있는 적어도 하나의 아암은 BCMA에 결합하거나 결합할 수 있는 적어도 하나의 아암과 구별되는 것인 항체 또는 항원-결합 단백질.
- 청구항 164 또는 165에 있어서,
(i) CD16A에 결합하거나 결합할 수 있는 적어도 하나의 아암은 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역을 포함하거나;
(ii) CD16A에 결합하거나 결합할 수 있는 적어도 하나의 아암은 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하거나;
(iii) BCMA에 결합하거나 결합할 수 있는 적어도 하나의 아암은 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역을 포함하거나;
(iv) BCMA에 결합하거나 결합할 수 있는 적어도 하나의 아암은 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하거나;
(v) CD16A에 결합하거나 결합할 수 있는 적어도 하나의 아암은 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역 및 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하거나;
(vi) BCMA에 결합하거나 결합할 수 있는 적어도 하나의 아암은 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역 및 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하거나; 또는
(vii) CD16A에 결합하거나 결합할 수 있는 적어도 하나의 아암은 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역 및 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하고; BCMA에 결합하거나 결합할 수 있는 적어도 하나의 아암은 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역 및 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역을 포함하는 것인
항체 또는 항원-결합 단백질: - 청구항 164 내지 166 중 어느 한 항에 있어서, CD16B에 결합하지 않는 항체 또는 항원-결합 단백질.
- 청구항 164 내지 167 중 어느 한 항에 있어서, 대상체에게 투여될 때 상기 대상체의 자연 살해 (NK) 세포 집단을 실질적으로 고갈시키거나 감소시키지 않는 항체 또는 항원-결합 단백질.
- 청구항 164 내지 168 중 어느 한 항에 있어서, CD16A는 인간 CD16A인 항체 또는 항원-결합 단백질.
- 청구항 164 내지 169 중 어느 한 항에 있어서, BCMA는 인간 BCMA인 항체 또는 항원-결합 단백질.
- 청구항 164 내지 170 중 어느 한 항의 항체 또는 항원-결합 단백질 및 제약학적으로 허용되는 담체를 포함하는 제약학적 조성물.
- 청구항 164 내지 170 중 어느 한 항에 있어서, 약제로 사용하기 위한 항체 또는 항원-결합 단백질.
- 청구항 172에 있어서, 약제로 사용하기 위한 제약학적 조성물.
- 청구항 164 내지 170 중 어느 한 항의 항체 또는 항원-결합 단백질 또는 청구항 171의 제약학적 조성물을 필요로 하는 대상체에게 투여하는 것을 포함하는, 질환의 치료 및/또는 예방 방법.
- 청구항 174에 있어서, 상기 질환은 암인 방법.
- 청구항 174 또는 175에 있어서, 상기 질환은 혈액암인 방법.
- 청구항 174 내지 176 중 어느 한 항에 있어서, 상기 질환은 다발성 골수종인 방법.
- 청구항 174 내지 177 중 어느 한 항에 있어서, 상기 항체 또는 항원-결합 단백질을 정맥내 또는 피하 투여하는 것을 포함하는 방법.
- 청구항 174 내지 178 중 어느 한 항에 있어서, 제 2 요법을 투여하는 것을 포함하는 방법.
- 청구항 179에 있어서, 상기 제 2 요법은 항-PD-1 항체를 포함하는 요법, 항-PD-L1 항체를 포함하는 요법, CD3 이중특이적 항체를 포함하는 요법, 항-TIGIT 항체를 포함하는 요법, 항-VEGF 항체를 포함하는 요법, 및 항-FcRH5 항체를 포함하는 요법으로 구성된 그룹에서 선택되는 것인 방법.
- 청구항 179에 있어서, 제 2 요법은 사이토카인 요법인 방법.
- 청구항 181에 있어서, 상기 사이토카인 요법은 IL-15, IL-2, IL-12, IL-21, IL-17, IL-18, IL-23, IL-27, 및 IL-6으로 구성된 그룹에서 선택된 사이토카인의 투여인 방법.
- 청구항 182에 있어서, 사이토카인은 IL-15인 방법.
- 청구항 182에 있어서, 사이토카인은 IL-2인 방법.
- 청구항 174 내지 184 중 어느 한 항에 있어서, 대상체는 암 환자인 방법.
- 청구항 174 내지 185 중 어느 한 항에 있어서, 대상체는 혈액암 환자인 방법.
- 청구항 174 내지 186 중 어느 한 항에 있어서, 대상체는 다발성 골수종 환자인 방법.
- 청구항 174 내지 187 중 어느 한 항에 있어서, 대상체는 재발성/불응성 다발성 골수종 환자인 방법.
- 청구항 174 내지 188 중 어느 한 항에 있어서, 대상체는 항-CD38 요법을 받은 적이 있는 것인 방법.
- 청구항 174 내지 189 중 어느 한 항에 있어서, 대상체는 다라투무맙을 받은 적이 있는 것인 방법.
- 청구항 174 내지 190 중 어느 한 항에 있어서, 대상체는 다라투무맙 나이브, 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성인 방법.
- 청구항 191에 있어서, 대상체는 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성인 방법.
- 청구항 174 내지 192 중 어느 한 항에 있어서, 대상체는 CD16A 다형성을 발현하는 것인 방법.
- 청구항 193에 있어서, 상기 CD16A 다형성은 CD16A-158V/F 다형성인 방법.
- 청구항 164 내지 170 중 어느 한 항의 항체 또는 항원-결합 단백질 또는 청구항 171의 조성물을 투여하는 것을 포함하는, 고갈되거나 감소된 NK 세포 집단을 갖는 대상체의 치료 방법.
- 청구항 195에 있어서, 상기 대상체는 항-CD38 요법으로 이전에 치료받은 적이 있는 것인 방법.
- 청구항 196에 있어서, 상기 항-CD38 요법은 다라투무맙 요법인 방법.
- (i) 서열 번호: 67에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 68에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 69에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및 (ii) 서열 번호: 70에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 71에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 72에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역을 포함하는, BCMA에 결합하거나 결합할 수 있는 항체 또는 항원-결합 단백질.
- 청구항 198에 있어서, BCMA는 인간 BCMA인 항체 또는 항원-결합 단백질.
- 청구항 198 또는 199에 있어서, CD16A에 결합하거나 결합할 수 있는 적어도 하나의 아암을 추가로 포함하는 항체 또는 항원-결합 단백질.
- 청구항 200에 있어서, CD16A는 인간 CD16A인 항체 또는 항원-결합 단백질.
- 청구항 200 또는 201에 있어서, CD16A에 결합하거나 결합할 수 있는 적어도 하나의 아암은 (i) 서열 번호: 73에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 74에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 75에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 중쇄 가변 영역, 및 (ii) 서열 번호: 76에 제시된 아미노산 서열을 갖는 CDR1; 서열 번호: 77에 제시된 아미노산 서열을 갖는 CDR2; 및 서열 번호: 78에 제시된 아미노산 서열을 갖는 CDR3을 포함하는 경쇄 가변 영역을 포함하는 것인 항체 또는 항원-결합 단백질.
- 청구항 198 내지 202 중 어느 한 항에 있어서, 다음을 포함하는 항체 또는 항원-결합 단백질:
(i) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역;
(ii) 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역;
(iii) 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역;
(iv) 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역;
(v) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역 및 서열 번호: 2에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역;
(vi) 서열 번호: 65에 제시된 아미노산 서열을 포함하는 중쇄 가변 영역 및 서열 번호: 66에 제시된 아미노산 서열을 포함하는 경쇄 가변 영역; 또는
(vii) 서열 번호: 3에 제시된 아미노산 서열을 포함하는 제 1 중쇄 가변 영역 및 서열 번호: 2에 제시된 아미노산 서열을 포함하는 제 1 경쇄 가변 영역; 및 서열 번호: 65에 제시된 아미노산 서열을 포함하는 제 2 중쇄 가변 영역 및 서열 번호: 66에 제시된 아미노산 서열을 포함하는 제 2 경쇄 가변 영역. - 청구항 198 내지 203 중 어느 한 항의 항체 또는 항원-결합 단백질 및 제약학적으로 허용되는 담체를 포함하는 제약학적 조성물.
- 청구항 198 내지 203 중 어느 한 항에 있어서, 약제로 사용하기 위한 항체 또는 항원-결합 단백질.
- 청구항 207에 있어서, 약제로 사용하기 위한 제약학적 조성물.
- 청구항 198 내지 203 중 어느 한 항의 이중특이적 항원-결합 단백질 또는 청구항 204의 제약학적 조성물을 필요로 하는 대상체에게 투여하는 것을 포함하는, 질환의 치료 및/또는 예방 방법.
- 청구항 207에 있어서, 상기 질환은 암인 방법.
- 청구항 207 또는 208에 있어서, 상기 질환은 혈액암인 방법.
- 청구항 207 내지 209 중 어느 한 항에 있어서, 상기 질환은 다발성 골수종인 방법.
- 청구항 207 내지 210 중 어느 한 항에 있어서, 상기 항체 또는 항원-결합 단백질을 정맥내 또는 피하 투여하는 것을 포함하는 방법.
- 청구항 207 내지 211 중 어느 한 항에 있어서, 제 2 요법을 투여하는 것을 포함하는 방법.
- 청구항 212에 있어서, 상기 제 2 요법은 항-PD-1 항체를 포함하는 요법, 항-PD-L1 항체를 포함하는 요법, CD3 이중특이적 항체를 포함하는 요법, 항-TIGIT 항체를 포함하는 요법, 항-VEGF 항체를 포함하는 요법, 및 항-FcRH5 항체를 포함하는 요법으로 구성된 그룹에서 선택되는 것인 방법.
- 청구항 212에 있어서, 제 2 요법은 사이토카인 요법인 방법.
- 청구항 214에 있어서, 상기 사이토카인 요법은 IL-15, IL-2, IL-12, IL-21, IL-17, IL-18, IL-23, IL-27, 및 IL-6으로 구성된 그룹에서 선택된 사이토카인의 투여인 방법.
- 청구항 215에 있어서, 사이토카인은 IL-15인 방법.
- 청구항 215에 있어서, 사이토카인은 IL-2인 방법.
- 청구항 207 내지 217 중 어느 한 항에 있어서, 대상체는 암 환자인 방법.
- 청구항 207 내지 218 중 어느 한 항에 있어서, 대상체는 혈액암 환자인 방법.
- 청구항 207 내지 219 중 어느 한 항에 있어서, 대상체는 다발성 골수종 환자인 방법.
- 청구항 207 내지 220 중 어느 한 항에 있어서, 대상체는 재발성/불응성 다발성 골수종 환자인 방법.
- 청구항 207 내지 221 중 어느 한 항에 있어서, 대상체는 항-CD38 요법을 받은 적이 있는 것인 방법.
- 청구항 207 내지 222 중 어느 한 항에 있어서, 대상체는 다라투무맙을 받은 적이 있는 것인 방법.
- 청구항 207 내지 223 중 어느 한 항에 있어서, 대상체는 다라투무맙 나이브, 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성인 방법.
- 청구항 224에 있어서, 대상체는 다라투무맙 내성, 다라투무맙 불응성, 또는 다라투무맙 재발성인 방법.
- 청구항 207 내지 225 중 어느 한 항에 있어서, 대상체는 CD16A 다형성을 발현하는 것인 방법.
- 청구항 226에 있어서, 상기 CD16A 다형성은 CD16A-158V/F 다형성인 방법.
- 청구항 198 내지 203 중 어느 한 항의 항체 또는 항원-결합 단백질 또는 청구항 204의 조성물을 투여하는 것을 포함하는, 고갈되거나 감소된 NK 세포 집단을 갖는 대상체의 치료 방법.
- 청구항 228에 있어서, 상기 대상체는 항-CD38 요법으로 이전에 치료받은 적이 있는 것인 방법.
- 청구항 229에 있어서, 상기 항-CD38 요법은 다라투무맙 요법인 방법.
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP18167384 | 2018-04-13 | ||
| EP18167385.6 | 2018-04-13 | ||
| EP18167385 | 2018-04-13 | ||
| EP18167384.9 | 2018-04-13 | ||
| EP18190662 | 2018-08-24 | ||
| EP18190662.9 | 2018-08-24 | ||
| EP18190661 | 2018-08-24 | ||
| EP18190661.1 | 2018-08-24 | ||
| PCT/IB2019/053040 WO2019198051A2 (en) | 2018-04-13 | 2019-04-12 | Nk cell engaging antibody fusion constructs |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20200143436A true KR20200143436A (ko) | 2020-12-23 |
Family
ID=66625219
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020207032435A KR20200143436A (ko) | 2018-04-13 | 2019-04-12 | Nk 세포 결합 항체 융합 구조체 |
Country Status (20)
| Country | Link |
|---|---|
| US (3) | US11001633B2 (ko) |
| EP (1) | EP3774914A2 (ko) |
| JP (1) | JP2021521275A (ko) |
| KR (1) | KR20200143436A (ko) |
| CN (3) | CN113880952A (ko) |
| AU (1) | AU2019252970A1 (ko) |
| BR (1) | BR112020020828A2 (ko) |
| CA (1) | CA3095373A1 (ko) |
| CL (2) | CL2020002625A1 (ko) |
| CO (1) | CO2020014167A2 (ko) |
| CR (1) | CR20200549A (ko) |
| IL (1) | IL277925A (ko) |
| MA (1) | MA52227A (ko) |
| MX (1) | MX2020010728A (ko) |
| PE (1) | PE20201346A1 (ko) |
| PH (1) | PH12020551664A1 (ko) |
| RU (1) | RU2022105827A (ko) |
| SG (1) | SG11202010064QA (ko) |
| TW (1) | TW202012441A (ko) |
| WO (1) | WO2019198051A2 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024186092A1 (ko) * | 2023-03-06 | 2024-09-12 | 주식회사 드노보 바이오테라퓨틱스 | 신규한 항-cd16 항체 및 이의 용도 |
Families Citing this family (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20220396635A1 (en) * | 2019-09-25 | 2022-12-15 | Universität Stuttgart | Trivalent binding molecules |
| WO2021116277A1 (en) * | 2019-12-10 | 2021-06-17 | Institut Pasteur | New antibody blocking human fcgriiia and fcgriiib |
| WO2021130383A1 (en) | 2019-12-27 | 2021-07-01 | Affimed Gmbh | Method for the production of bispecific fcyriii x cd30 antibody construct |
| EP4225792A1 (en) | 2020-10-08 | 2023-08-16 | Affimed GmbH | Trispecific binders |
| KR20230104659A (ko) * | 2020-11-08 | 2023-07-10 | 씨젠 인크. | 면역 세포 억제제를 이용한 조합-요법 항체 약물 접합체 |
| WO2022120033A1 (en) * | 2020-12-03 | 2022-06-09 | Amgen Inc. | Immunoglobuline constructs with multiple binding domains |
| JP2024516230A (ja) | 2021-04-30 | 2024-04-12 | ジェネンテック, インコーポレイテッド | がんのための治療及び診断方法並びに組成物 |
| CN116574190A (zh) * | 2021-07-30 | 2023-08-11 | 启愈生物技术(上海)有限公司 | 抗原靶向、抗cd16a和免疫效应细胞激活三功能融合蛋白及其应用 |
| WO2023007023A1 (en) | 2021-07-30 | 2023-02-02 | Affimed Gmbh | Duplexbodies |
| CN113929785B (zh) * | 2021-09-10 | 2023-05-23 | 钦元再生医学(珠海)有限公司 | 一种可自分泌pd1-trem2双特异性抗体的嵌合抗原受体免疫细胞及其应用 |
| CA3233085A1 (en) * | 2021-09-24 | 2023-03-30 | Synergy Imt, Inc. | Composition of recombinant antigen binding molecules and method of making and using thereof |
| EP4426433A1 (en) | 2021-11-03 | 2024-09-11 | Affimed GmbH | Bispecific cd16a binders |
| KR20240099382A (ko) | 2021-11-03 | 2024-06-28 | 아피메트 게엠베하 | 이중특이적 cd16a 결합제 |
| CN116284385A (zh) * | 2021-12-07 | 2023-06-23 | 信达细胞制药(苏州)有限公司 | 靶向bcma的p329g抗体及其与嵌合抗原受体细胞的组合和应用 |
| CN114349869B (zh) * | 2021-12-20 | 2023-09-26 | 上海恩凯细胞技术有限公司 | 一种双特异性的nk细胞激动剂及制备方法和应用 |
| WO2024027828A1 (en) * | 2022-08-05 | 2024-02-08 | Chimagen Biosciences, Ltd | Multi-specific antibodies targeting a dimerizable tumor antigen and an immunostimulatory antigen |
| WO2024059677A2 (en) * | 2022-09-14 | 2024-03-21 | Ibio, Inc. | Pd-1 agonist antibodies |
| WO2024165028A1 (en) * | 2023-02-06 | 2024-08-15 | Concept To Medicine Biotech Co., Ltd. | Anti-cd16a antibodies and uses thereof |
Family Cites Families (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1994013804A1 (en) | 1992-12-04 | 1994-06-23 | Medical Research Council | Multivalent and multispecific binding proteins, their manufacture and use |
| US6737056B1 (en) * | 1999-01-15 | 2004-05-18 | Genentech, Inc. | Polypeptide variants with altered effector function |
| CA2438682A1 (en) | 2001-02-20 | 2002-08-29 | Zymogenetics, Inc. | Antibodies that bind both bcma and taci |
| GB0510790D0 (en) * | 2005-05-26 | 2005-06-29 | Syngenta Crop Protection Ag | Anti-CD16 binding molecules |
| US8268314B2 (en) * | 2008-10-08 | 2012-09-18 | Hoffmann-La Roche Inc. | Bispecific anti-VEGF/anti-ANG-2 antibodies |
| NZ594985A (en) | 2009-03-10 | 2013-07-26 | Biogen Idec Inc | Anti-bcma (b-cell maturation antigen, cd269, tnfrsf17) antibodies |
| PT2361936T (pt) * | 2010-02-25 | 2016-07-15 | Affimed Gmbh | Molécula que se liga a antigénio e utilizações desta |
| US20140105915A1 (en) | 2011-05-27 | 2014-04-17 | Glaxo Group Limited | Bcma (cd269/tnfrsf17) - binding proteins |
| TWI679212B (zh) | 2011-11-15 | 2019-12-11 | 美商安進股份有限公司 | 針對bcma之e3以及cd3的結合分子 |
| EP2825557B1 (en) | 2012-03-16 | 2017-06-28 | The U.S.A. as represented by the Secretary, Department of Health and Human Services | Soluble engineered monomeric fc |
| SG11201408646VA (en) * | 2012-07-06 | 2015-01-29 | Genmab Bv | Dimeric protein with triple mutations |
| EP2914628A1 (en) | 2012-11-01 | 2015-09-09 | Max-Delbrück-Centrum für Molekulare Medizin | An antibody that binds cd269 (bcma) suitable for use in the treatment of plasma cell diseases such as multiple myeloma and autoimmune diseases |
| WO2014122143A1 (en) | 2013-02-05 | 2014-08-14 | Engmab Ag | Method for the selection of antibodies against bcma |
| AR095374A1 (es) | 2013-03-15 | 2015-10-14 | Amgen Res (Munich) Gmbh | Moléculas de unión para bcma y cd3 |
| CA2903056A1 (en) * | 2013-03-15 | 2014-09-18 | Merck Patent Gmbh | Tetravalent bispecific antibodies |
| CA2936785A1 (en) * | 2014-01-15 | 2015-07-23 | Zymeworks Inc. | Bi-specific cd3 and cd19 antigen-binding constructs |
| WO2016106158A1 (en) * | 2014-12-22 | 2016-06-30 | Systimmune, Inc. | Bispecific tetravalent antibodies and methods of making and using thereof |
| BR112017015136A2 (pt) * | 2015-01-14 | 2018-01-30 | Compass Therapeutics Llc | polipeptídeo de construto de ligação ao antígeno imunomodulador multiespecífico, construto de ligação ao antígeno imunomodulador multiespecífico, conjugado, composição farmacêutica, método para tratar um indivíduo com câncer, método para inibir ou reduzir o crescimento de câncer, composição, célula, método de fazer um polipeptídeo de construto de ligação ao antígeno imunomodulador multiespecífico, vetor ou conjunto de vetores e kit |
| EP3091031A1 (en) * | 2015-05-04 | 2016-11-09 | Affimed GmbH | Combination of a bispecific antibody with an immune modulating molecule for the treatment of a tumor |
| DK3292153T3 (da) * | 2015-05-04 | 2019-10-21 | Affimed Gmbh | Kombination af en cd30xcd16a-antistof med en anti-pd-1 antagonistisk antistof til behandling |
| JP6971153B2 (ja) * | 2015-06-23 | 2021-11-24 | イナート・ファルマ・ソシエテ・アノニムInnate Pharma Pharma S.A. | 多重特異的nkエンゲイジャータンパク質 |
| MA53750A (fr) * | 2015-08-17 | 2021-09-15 | Janssen Pharmaceutica Nv | Anticorps anti-bcma, molécules de liaison d'antigène bispécifiques qui se lient au bcma et cd3 et leurs utilisations |
| EP3156417A1 (en) * | 2015-10-13 | 2017-04-19 | Affimed GmbH | Multivalent fv antibodies |
| CN105367660B (zh) * | 2015-12-22 | 2018-12-21 | 深圳市北科生物科技有限公司 | 一种抗cd16a抗原和抗muc1抗原的双特异性抗体 |
| CN106632681B (zh) * | 2016-10-11 | 2017-11-14 | 北京东方百泰生物科技有限公司 | 抗egfr和抗cd3双特异抗体及其应用 |
| JP7115758B2 (ja) * | 2017-02-28 | 2022-08-09 | アッフィメッド・ゲー・エム・ベー・ハー | Cd16a指向性nk細胞エンゲージメント用タンデムダイアボディ |
-
2019
- 2019-04-12 CN CN202111125559.3A patent/CN113880952A/zh active Pending
- 2019-04-12 MA MA052227A patent/MA52227A/fr unknown
- 2019-04-12 KR KR1020207032435A patent/KR20200143436A/ko unknown
- 2019-04-12 RU RU2022105827A patent/RU2022105827A/ru unknown
- 2019-04-12 JP JP2021504593A patent/JP2021521275A/ja active Pending
- 2019-04-12 CR CR20200549A patent/CR20200549A/es unknown
- 2019-04-12 CN CN201980033176.8A patent/CN112119097B/zh active Active
- 2019-04-12 EP EP19725409.7A patent/EP3774914A2/en active Pending
- 2019-04-12 SG SG11202010064QA patent/SG11202010064QA/en unknown
- 2019-04-12 AU AU2019252970A patent/AU2019252970A1/en active Pending
- 2019-04-12 MX MX2020010728A patent/MX2020010728A/es unknown
- 2019-04-12 CN CN202111125475.XA patent/CN113817066A/zh active Pending
- 2019-04-12 PE PE2020001584A patent/PE20201346A1/es unknown
- 2019-04-12 WO PCT/IB2019/053040 patent/WO2019198051A2/en active Application Filing
- 2019-04-12 BR BR112020020828-0A patent/BR112020020828A2/pt unknown
- 2019-04-12 CA CA3095373A patent/CA3095373A1/en active Pending
- 2019-04-15 TW TW108113068A patent/TW202012441A/zh unknown
- 2019-12-13 US US16/714,396 patent/US11001633B2/en active Active
-
2020
- 2020-10-08 PH PH12020551664A patent/PH12020551664A1/en unknown
- 2020-10-09 CL CL2020002625A patent/CL2020002625A1/es unknown
- 2020-10-11 IL IL277925A patent/IL277925A/en unknown
- 2020-11-12 CO CONC2020/0014167A patent/CO2020014167A2/es unknown
-
2021
- 2021-04-20 US US17/235,854 patent/US20210253698A1/en not_active Abandoned
-
2023
- 2023-04-14 CL CL2023001085A patent/CL2023001085A1/es unknown
-
2024
- 2024-04-17 US US18/637,556 patent/US20240294647A1/en active Pending
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024186092A1 (ko) * | 2023-03-06 | 2024-09-12 | 주식회사 드노보 바이오테라퓨틱스 | 신규한 항-cd16 항체 및 이의 용도 |
Also Published As
| Publication number | Publication date |
|---|---|
| PE20201346A1 (es) | 2020-11-25 |
| CN113880952A (zh) | 2022-01-04 |
| MX2020010728A (es) | 2020-11-06 |
| WO2019198051A2 (en) | 2019-10-17 |
| US11001633B2 (en) | 2021-05-11 |
| IL277925A (en) | 2020-11-30 |
| CA3095373A1 (en) | 2019-10-17 |
| SG11202010064QA (en) | 2020-11-27 |
| JP2021521275A (ja) | 2021-08-26 |
| CR20200549A (es) | 2021-03-18 |
| RU2022105827A (ru) | 2022-04-05 |
| AU2019252970A1 (en) | 2020-11-26 |
| TW202012441A (zh) | 2020-04-01 |
| CN113817066A (zh) | 2021-12-21 |
| CL2020002625A1 (es) | 2021-02-19 |
| CN112119097B (zh) | 2021-10-15 |
| EP3774914A2 (en) | 2021-02-17 |
| BR112020020828A2 (pt) | 2021-01-19 |
| CN112119097A (zh) | 2020-12-22 |
| MA52227A (fr) | 2021-04-21 |
| CO2020014167A2 (es) | 2021-04-08 |
| US20240294647A1 (en) | 2024-09-05 |
| CL2023001085A1 (es) | 2023-10-06 |
| US20210253698A1 (en) | 2021-08-19 |
| PH12020551664A1 (en) | 2021-12-13 |
| WO2019198051A3 (en) | 2019-11-14 |
| US20200109202A1 (en) | 2020-04-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11001633B2 (en) | NK cell engaging antibody fusion constructs | |
| US11584794B2 (en) | Bispecific heterodimeric fusion proteins containing IL-15-IL-15Ralpha Fc-fusion proteins and immune checkpoint antibody fragments | |
| US11524991B2 (en) | PD-1 targeted heterodimeric fusion proteins containing IL-15/IL-15Ra Fc-fusion proteins and PD-1 antigen binding domains and uses thereof | |
| US11377477B2 (en) | PD-1 targeted IL-15/IL-15RALPHA fc fusion proteins and uses in combination therapies thereof | |
| US20220073588A1 (en) | TARGETED HETERODIMERIC Fc FUSION PROTEINS CONTAINING IL-15 IL-15alpha AND ANTIGEN BINDING DOMAINS | |
| JP7010854B2 (ja) | 二重特異性チェックポイント阻害剤抗体 | |
| JP7115758B2 (ja) | Cd16a指向性nk細胞エンゲージメント用タンデムダイアボディ | |
| TW202235104A (zh) | 雙功能分子 | |
| CN114127112A (zh) | 与t细胞结合的多功能分子及其治疗自身免疫性病症的用途 | |
| JP2024521701A (ja) | 抗cd137抗体及びその使用方法 | |
| RU2774711C2 (ru) | Слитые конструкции антител для вовлечения nk-клеток | |
| US20240209113A1 (en) | Anti-gpc3 and anti-cd137 multispecific antibodies and methods of use |