KR20200121817A - T 세포 계통의 세포를 생성하기 위한 방법 - Google Patents
T 세포 계통의 세포를 생성하기 위한 방법 Download PDFInfo
- Publication number
- KR20200121817A KR20200121817A KR1020207024814A KR20207024814A KR20200121817A KR 20200121817 A KR20200121817 A KR 20200121817A KR 1020207024814 A KR1020207024814 A KR 1020207024814A KR 20207024814 A KR20207024814 A KR 20207024814A KR 20200121817 A KR20200121817 A KR 20200121817A
- Authority
- KR
- South Korea
- Prior art keywords
- cells
- cell
- progenitor
- notch ligand
- lineage
- Prior art date
Links
- 210000004027 cell Anatomy 0.000 title claims abstract description 337
- 210000001744 T-lymphocyte Anatomy 0.000 title claims abstract description 203
- 238000000034 method Methods 0.000 title claims description 55
- 210000000130 stem cell Anatomy 0.000 claims abstract description 125
- 239000003446 ligand Substances 0.000 claims abstract description 108
- 239000000725 suspension Substances 0.000 claims abstract description 78
- 210000001978 pro-t lymphocyte Anatomy 0.000 claims abstract description 31
- 238000012258 culturing Methods 0.000 claims abstract description 14
- 102100031573 Hematopoietic progenitor cell antigen CD34 Human genes 0.000 claims description 53
- 101000777663 Homo sapiens Hematopoietic progenitor cell antigen CD34 Proteins 0.000 claims description 53
- 239000011325 microbead Substances 0.000 claims description 34
- 210000004263 induced pluripotent stem cell Anatomy 0.000 claims description 26
- 102100023543 Vascular cell adhesion protein 1 Human genes 0.000 claims description 25
- 210000003958 hematopoietic stem cell Anatomy 0.000 claims description 22
- 101001057504 Homo sapiens Interferon-stimulated gene 20 kDa protein Proteins 0.000 claims description 15
- 101001055144 Homo sapiens Interleukin-2 receptor subunit alpha Proteins 0.000 claims description 15
- 239000002609 medium Substances 0.000 claims description 13
- 239000001963 growth medium Substances 0.000 claims description 12
- 210000001671 embryonic stem cell Anatomy 0.000 claims description 11
- 230000001965 increasing effect Effects 0.000 claims description 10
- 239000002245 particle Substances 0.000 claims description 10
- 101000800116 Homo sapiens Thy-1 membrane glycoprotein Proteins 0.000 claims description 6
- 102100033523 Thy-1 membrane glycoprotein Human genes 0.000 claims description 6
- 102100031585 ADP-ribosyl cyclase/cyclic ADP-ribose hydrolase 1 Human genes 0.000 claims description 4
- 101000777636 Homo sapiens ADP-ribosyl cyclase/cyclic ADP-ribose hydrolase 1 Proteins 0.000 claims description 4
- 101000622304 Homo sapiens Vascular cell adhesion protein 1 Proteins 0.000 claims description 3
- 210000005260 human cell Anatomy 0.000 claims description 3
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 claims description 2
- 229910052698 phosphorus Inorganic materials 0.000 claims description 2
- 239000011574 phosphorus Substances 0.000 claims description 2
- 102100026878 Interleukin-2 receptor subunit alpha Human genes 0.000 claims 2
- 239000000203 mixture Substances 0.000 abstract description 20
- 108010070047 Notch Receptors Proteins 0.000 description 140
- 102000005650 Notch Receptors Human genes 0.000 description 140
- 239000011324 bead Substances 0.000 description 67
- 241000282414 Homo sapiens Species 0.000 description 55
- 101000716102 Homo sapiens T-cell surface glycoprotein CD4 Proteins 0.000 description 41
- 102100036011 T-cell surface glycoprotein CD4 Human genes 0.000 description 41
- 102100034922 T-cell surface glycoprotein CD8 alpha chain Human genes 0.000 description 35
- 230000011712 cell development Effects 0.000 description 33
- 102000017420 CD3 protein, epsilon/gamma/delta subunit Human genes 0.000 description 29
- 241000699666 Mus <mouse, genus> Species 0.000 description 27
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 25
- 108090000623 proteins and genes Proteins 0.000 description 25
- 102000004169 proteins and genes Human genes 0.000 description 24
- 102100027208 T-cell antigen CD7 Human genes 0.000 description 23
- 108091008874 T cell receptors Proteins 0.000 description 22
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 21
- 108010000134 Vascular Cell Adhesion Molecule-1 Proteins 0.000 description 21
- 210000004700 fetal blood Anatomy 0.000 description 20
- 230000011664 signaling Effects 0.000 description 19
- 102000004127 Cytokines Human genes 0.000 description 18
- 108090000695 Cytokines Proteins 0.000 description 18
- 210000001541 thymus gland Anatomy 0.000 description 18
- 230000000694 effects Effects 0.000 description 16
- 108010090804 Streptavidin Proteins 0.000 description 15
- 230000014509 gene expression Effects 0.000 description 15
- 206010028980 Neoplasm Diseases 0.000 description 14
- 230000004913 activation Effects 0.000 description 14
- 230000004069 differentiation Effects 0.000 description 14
- 238000000684 flow cytometry Methods 0.000 description 14
- 102100027268 Interferon-stimulated gene 20 kDa protein Human genes 0.000 description 13
- 102100025244 T-cell surface glycoprotein CD5 Human genes 0.000 description 13
- 108010002586 Interleukin-7 Proteins 0.000 description 12
- 102100021592 Interleukin-7 Human genes 0.000 description 12
- 229960002685 biotin Drugs 0.000 description 12
- 235000020958 biotin Nutrition 0.000 description 12
- 239000011616 biotin Substances 0.000 description 12
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 12
- 229940100994 interleukin-7 Drugs 0.000 description 12
- 239000000523 sample Substances 0.000 description 12
- 210000001185 bone marrow Anatomy 0.000 description 11
- 238000011161 development Methods 0.000 description 11
- 230000018109 developmental process Effects 0.000 description 11
- 108010019670 Chimeric Antigen Receptors Proteins 0.000 description 10
- 201000011510 cancer Diseases 0.000 description 10
- 108060001084 Luciferase Proteins 0.000 description 9
- 241000699670 Mus sp. Species 0.000 description 9
- 238000004458 analytical method Methods 0.000 description 9
- 201000010099 disease Diseases 0.000 description 9
- 210000001519 tissue Anatomy 0.000 description 9
- 102100024222 B-lymphocyte antigen CD19 Human genes 0.000 description 8
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 8
- 101000980825 Homo sapiens B-lymphocyte antigen CD19 Proteins 0.000 description 8
- 101000738771 Homo sapiens Receptor-type tyrosine-protein phosphatase C Proteins 0.000 description 8
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 8
- 102100037422 Receptor-type tyrosine-protein phosphatase C Human genes 0.000 description 8
- 239000000427 antigen Substances 0.000 description 8
- 108091007433 antigens Proteins 0.000 description 8
- 102000036639 antigens Human genes 0.000 description 8
- 238000013459 approach Methods 0.000 description 8
- 238000005516 engineering process Methods 0.000 description 8
- 238000004519 manufacturing process Methods 0.000 description 8
- 210000001577 neostriatum Anatomy 0.000 description 8
- 210000002966 serum Anatomy 0.000 description 8
- 238000011282 treatment Methods 0.000 description 8
- 239000005089 Luciferase Substances 0.000 description 7
- 210000003719 b-lymphocyte Anatomy 0.000 description 7
- 238000007413 biotinylation Methods 0.000 description 7
- 230000006287 biotinylation Effects 0.000 description 7
- 210000003995 blood forming stem cell Anatomy 0.000 description 7
- 239000003636 conditioned culture medium Substances 0.000 description 7
- 230000006698 induction Effects 0.000 description 7
- 210000004698 lymphocyte Anatomy 0.000 description 7
- 239000000463 material Substances 0.000 description 7
- 239000000243 solution Substances 0.000 description 7
- 101000872077 Homo sapiens Delta-like protein 4 Proteins 0.000 description 6
- 239000004793 Polystyrene Substances 0.000 description 6
- 230000010261 cell growth Effects 0.000 description 6
- 238000003501 co-culture Methods 0.000 description 6
- 239000012091 fetal bovine serum Substances 0.000 description 6
- 108020001507 fusion proteins Proteins 0.000 description 6
- 102000037865 fusion proteins Human genes 0.000 description 6
- 239000013612 plasmid Substances 0.000 description 6
- 229920002223 polystyrene Polymers 0.000 description 6
- 101001046686 Homo sapiens Integrin alpha-M Proteins 0.000 description 5
- 102100022338 Integrin alpha-M Human genes 0.000 description 5
- 238000007792 addition Methods 0.000 description 5
- 230000024245 cell differentiation Effects 0.000 description 5
- 230000001413 cellular effect Effects 0.000 description 5
- 230000021615 conjugation Effects 0.000 description 5
- 210000002950 fibroblast Anatomy 0.000 description 5
- 230000003394 haemopoietic effect Effects 0.000 description 5
- 239000008194 pharmaceutical composition Substances 0.000 description 5
- 108010049955 Bone Morphogenetic Protein 4 Proteins 0.000 description 4
- 102100024505 Bone morphogenetic protein 4 Human genes 0.000 description 4
- 239000007760 Iscove's Modified Dulbecco's Medium Substances 0.000 description 4
- 108700018351 Major Histocompatibility Complex Proteins 0.000 description 4
- 101710120037 Toxin CcdB Proteins 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 230000001605 fetal effect Effects 0.000 description 4
- 108700014844 flt3 ligand Proteins 0.000 description 4
- 102000044457 human DLL4 Human genes 0.000 description 4
- 210000004185 liver Anatomy 0.000 description 4
- 239000002105 nanoparticle Substances 0.000 description 4
- 239000013642 negative control Substances 0.000 description 4
- 210000000056 organ Anatomy 0.000 description 4
- 210000005259 peripheral blood Anatomy 0.000 description 4
- 239000011886 peripheral blood Substances 0.000 description 4
- 108090000765 processed proteins & peptides Proteins 0.000 description 4
- 230000004044 response Effects 0.000 description 4
- 238000000926 separation method Methods 0.000 description 4
- 241000894007 species Species 0.000 description 4
- 210000000952 spleen Anatomy 0.000 description 4
- 239000013589 supplement Substances 0.000 description 4
- 230000020382 suppression by virus of host antigen processing and presentation of peptide antigen via MHC class I Effects 0.000 description 4
- 230000001225 therapeutic effect Effects 0.000 description 4
- 230000002992 thymic effect Effects 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 description 3
- 102100039619 Granulocyte colony-stimulating factor Human genes 0.000 description 3
- 206010061598 Immunodeficiency Diseases 0.000 description 3
- 208000029462 Immunodeficiency disease Diseases 0.000 description 3
- 241000699660 Mus musculus Species 0.000 description 3
- 108020004511 Recombinant DNA Proteins 0.000 description 3
- 101150052863 THY1 gene Proteins 0.000 description 3
- 230000003213 activating effect Effects 0.000 description 3
- 150000001413 amino acids Chemical class 0.000 description 3
- 230000001745 anti-biotin effect Effects 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 238000013461 design Methods 0.000 description 3
- 239000003085 diluting agent Substances 0.000 description 3
- 208000035475 disorder Diseases 0.000 description 3
- 239000003814 drug Substances 0.000 description 3
- 229940088598 enzyme Drugs 0.000 description 3
- 235000011187 glycerol Nutrition 0.000 description 3
- 230000007813 immunodeficiency Effects 0.000 description 3
- 238000000338 in vitro Methods 0.000 description 3
- 230000001939 inductive effect Effects 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 238000011081 inoculation Methods 0.000 description 3
- 238000002826 magnetic-activated cell sorting Methods 0.000 description 3
- 239000003550 marker Substances 0.000 description 3
- 238000013508 migration Methods 0.000 description 3
- 230000005012 migration Effects 0.000 description 3
- 230000035772 mutation Effects 0.000 description 3
- 210000001778 pluripotent stem cell Anatomy 0.000 description 3
- 229920001184 polypeptide Polymers 0.000 description 3
- 239000002243 precursor Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 102000004196 processed proteins & peptides Human genes 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 230000001172 regenerating effect Effects 0.000 description 3
- 238000012546 transfer Methods 0.000 description 3
- 238000002054 transplantation Methods 0.000 description 3
- 238000001262 western blot Methods 0.000 description 3
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 2
- 208000030507 AIDS Diseases 0.000 description 2
- HJCMDXDYPOUFDY-WHFBIAKZSA-N Ala-Gln Chemical compound C[C@H](N)C(=O)N[C@H](C(O)=O)CCC(N)=O HJCMDXDYPOUFDY-WHFBIAKZSA-N 0.000 description 2
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 2
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- 102100033553 Delta-like protein 4 Human genes 0.000 description 2
- 108091006020 Fc-tagged proteins Proteins 0.000 description 2
- 102100024785 Fibroblast growth factor 2 Human genes 0.000 description 2
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 description 2
- 102100020715 Fms-related tyrosine kinase 3 ligand protein Human genes 0.000 description 2
- 101710162577 Fms-related tyrosine kinase 3 ligand protein Proteins 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- 229920002683 Glycosaminoglycan Polymers 0.000 description 2
- 208000009329 Graft vs Host Disease Diseases 0.000 description 2
- 229920002971 Heparan sulfate Polymers 0.000 description 2
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 101100220044 Homo sapiens CD34 gene Proteins 0.000 description 2
- 101000934338 Homo sapiens Myeloid cell surface antigen CD33 Proteins 0.000 description 2
- 101710177504 Kit ligand Proteins 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 102100025243 Myeloid cell surface antigen CD33 Human genes 0.000 description 2
- 229930193140 Neomycin Natural products 0.000 description 2
- 208000001388 Opportunistic Infections Diseases 0.000 description 2
- 108010076504 Protein Sorting Signals Proteins 0.000 description 2
- 241000700157 Rattus norvegicus Species 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- 208000029052 T-cell acute lymphoblastic leukemia Diseases 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 238000002306 biochemical method Methods 0.000 description 2
- 239000012620 biological material Substances 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 239000012888 bovine serum Substances 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 239000007853 buffer solution Substances 0.000 description 2
- 210000004899 c-terminal region Anatomy 0.000 description 2
- 244000309466 calf Species 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 239000002458 cell surface marker Substances 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 230000008021 deposition Effects 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 230000004927 fusion Effects 0.000 description 2
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 2
- 239000010931 gold Substances 0.000 description 2
- 229910052737 gold Inorganic materials 0.000 description 2
- 208000024908 graft versus host disease Diseases 0.000 description 2
- 238000011134 hematopoietic stem cell transplantation Methods 0.000 description 2
- 238000003119 immunoblot Methods 0.000 description 2
- 238000010348 incorporation Methods 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 238000007914 intraventricular administration Methods 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 238000003670 luciferase enzyme activity assay Methods 0.000 description 2
- 239000008176 lyophilized powder Substances 0.000 description 2
- 230000003211 malignant effect Effects 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- 229960004927 neomycin Drugs 0.000 description 2
- 150000007523 nucleic acids Chemical class 0.000 description 2
- 238000005457 optimization Methods 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 2
- 208000028529 primary immunodeficiency disease Diseases 0.000 description 2
- 230000002035 prolonged effect Effects 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- RXWNCPJZOCPEPQ-NVWDDTSBSA-N puromycin Chemical compound C1=CC(OC)=CC=C1C[C@H](N)C(=O)N[C@H]1[C@@H](O)[C@H](N2C3=NC=NC(=C3N=C2)N(C)C)O[C@@H]1CO RXWNCPJZOCPEPQ-NVWDDTSBSA-N 0.000 description 2
- 210000003370 receptor cell Anatomy 0.000 description 2
- 238000011084 recovery Methods 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 238000013341 scale-up Methods 0.000 description 2
- 210000005212 secondary lymphoid organ Anatomy 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 210000002536 stromal cell Anatomy 0.000 description 2
- 239000006228 supernatant Substances 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 230000004083 survival effect Effects 0.000 description 2
- 238000004114 suspension culture Methods 0.000 description 2
- 230000002459 sustained effect Effects 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 2
- YMXHPSHLTSZXKH-RVBZMBCESA-N (2,5-dioxopyrrolidin-1-yl) 5-[(3as,4s,6ar)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoate Chemical compound C([C@H]1[C@H]2NC(=O)N[C@H]2CS1)CCCC(=O)ON1C(=O)CCC1=O YMXHPSHLTSZXKH-RVBZMBCESA-N 0.000 description 1
- LDGWQMRUWMSZIU-LQDDAWAPSA-M 2,3-bis[(z)-octadec-9-enoxy]propyl-trimethylazanium;chloride Chemical compound [Cl-].CCCCCCCC\C=C/CCCCCCCCOCC(C[N+](C)(C)C)OCCCCCCCC\C=C/CCCCCCCC LDGWQMRUWMSZIU-LQDDAWAPSA-M 0.000 description 1
- GHCZTIFQWKKGSB-UHFFFAOYSA-N 2-hydroxypropane-1,2,3-tricarboxylic acid;phosphoric acid Chemical compound OP(O)(O)=O.OC(=O)CC(O)(C(O)=O)CC(O)=O GHCZTIFQWKKGSB-UHFFFAOYSA-N 0.000 description 1
- 108091023037 Aptamer Proteins 0.000 description 1
- 206010003694 Atrophy Diseases 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 108700031361 Brachyury Proteins 0.000 description 1
- 102100021933 C-C motif chemokine 25 Human genes 0.000 description 1
- 102100031650 C-X-C chemokine receptor type 4 Human genes 0.000 description 1
- 238000011740 C57BL/6 mouse Methods 0.000 description 1
- -1 CD1a Proteins 0.000 description 1
- 102100032912 CD44 antigen Human genes 0.000 description 1
- 108010032795 CD8 receptor Proteins 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 102000055007 Cartilage Oligomeric Matrix Human genes 0.000 description 1
- 108700005376 Cartilage Oligomeric Matrix Proteins 0.000 description 1
- 102000019034 Chemokines Human genes 0.000 description 1
- 108010012236 Chemokines Proteins 0.000 description 1
- 108091026890 Coding region Proteins 0.000 description 1
- 102000029816 Collagenase Human genes 0.000 description 1
- 108060005980 Collagenase Proteins 0.000 description 1
- 208000035473 Communicable disease Diseases 0.000 description 1
- IGXWBGJHJZYPQS-SSDOTTSWSA-N D-Luciferin Chemical compound OC(=O)[C@H]1CSC(C=2SC3=CC=C(O)C=C3N=2)=N1 IGXWBGJHJZYPQS-SSDOTTSWSA-N 0.000 description 1
- 108091008102 DNA aptamers Proteins 0.000 description 1
- 102100030074 Dickkopf-related protein 1 Human genes 0.000 description 1
- 206010061819 Disease recurrence Diseases 0.000 description 1
- 241000255581 Drosophila <fruit fly, genus> Species 0.000 description 1
- 108010092408 Eosinophil Peroxidase Proteins 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 102000008857 Ferritin Human genes 0.000 description 1
- 108050000784 Ferritin Proteins 0.000 description 1
- 238000008416 Ferritin Methods 0.000 description 1
- 229920001917 Ficoll Polymers 0.000 description 1
- 239000012739 FreeStyle 293 Expression medium Substances 0.000 description 1
- 208000031886 HIV Infections Diseases 0.000 description 1
- 208000037357 HIV infectious disease Diseases 0.000 description 1
- 101100118545 Holotrichia diomphalia EGF-like gene Proteins 0.000 description 1
- 101000897486 Homo sapiens C-C motif chemokine 25 Proteins 0.000 description 1
- 101000922348 Homo sapiens C-X-C chemokine receptor type 4 Proteins 0.000 description 1
- 101000868273 Homo sapiens CD44 antigen Proteins 0.000 description 1
- 101000864646 Homo sapiens Dickkopf-related protein 1 Proteins 0.000 description 1
- 101000584743 Homo sapiens Recombining binding protein suppressor of hairless Proteins 0.000 description 1
- 101000701405 Homo sapiens Serine/threonine-protein kinase 36 Proteins 0.000 description 1
- 101000914484 Homo sapiens T-lymphocyte activation antigen CD80 Proteins 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- 206010021143 Hypoxia Diseases 0.000 description 1
- 208000026350 Inborn Genetic disease Diseases 0.000 description 1
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 description 1
- 102000004218 Insulin-Like Growth Factor I Human genes 0.000 description 1
- 108090000177 Interleukin-11 Proteins 0.000 description 1
- 108010002386 Interleukin-3 Proteins 0.000 description 1
- 108090001005 Interleukin-6 Proteins 0.000 description 1
- 102100020880 Kit ligand Human genes 0.000 description 1
- 101100335081 Mus musculus Flt3 gene Proteins 0.000 description 1
- 102100023181 Neurogenic locus notch homolog protein 1 Human genes 0.000 description 1
- 108700037638 Neurogenic locus notch homolog protein 1 Proteins 0.000 description 1
- 102100025246 Neurogenic locus notch homolog protein 2 Human genes 0.000 description 1
- 108700037064 Neurogenic locus notch homolog protein 2 Proteins 0.000 description 1
- 102100025247 Neurogenic locus notch homolog protein 3 Human genes 0.000 description 1
- 102100025254 Neurogenic locus notch homolog protein 4 Human genes 0.000 description 1
- 230000005913 Notch signaling pathway Effects 0.000 description 1
- 102000001759 Notch1 Receptor Human genes 0.000 description 1
- 108010029755 Notch1 Receptor Proteins 0.000 description 1
- 108010029756 Notch3 Receptor Proteins 0.000 description 1
- 108010029741 Notch4 Receptor Proteins 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 102100030000 Recombining binding protein suppressor of hairless Human genes 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 241000376353 Stips Species 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 102100027222 T-lymphocyte activation antigen CD80 Human genes 0.000 description 1
- 101710113649 Thyroid peroxidase Proteins 0.000 description 1
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 1
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 1
- 101710160666 Vascular cell adhesion protein 1 Proteins 0.000 description 1
- 101150097457 Vcam1 gene Proteins 0.000 description 1
- 210000005006 adaptive immune system Anatomy 0.000 description 1
- 230000004721 adaptive immunity Effects 0.000 description 1
- 238000004115 adherent culture Methods 0.000 description 1
- 102000019997 adhesion receptor Human genes 0.000 description 1
- 108010013985 adhesion receptor Proteins 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 230000032683 aging Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 230000000735 allogeneic effect Effects 0.000 description 1
- 230000006229 amino acid addition Effects 0.000 description 1
- 125000000539 amino acid group Chemical group 0.000 description 1
- 239000003146 anticoagulant agent Substances 0.000 description 1
- 229940127219 anticoagulant drug Drugs 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 210000000709 aorta Anatomy 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 230000037444 atrophy Effects 0.000 description 1
- 230000005784 autoimmunity Effects 0.000 description 1
- 244000052616 bacterial pathogen Species 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 150000001615 biotins Chemical class 0.000 description 1
- 108091006004 biotinylated proteins Proteins 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 238000002619 cancer immunotherapy Methods 0.000 description 1
- 229910002091 carbon monoxide Inorganic materials 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 239000002771 cell marker Substances 0.000 description 1
- 230000011748 cell maturation Effects 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 239000000919 ceramic Substances 0.000 description 1
- DWQOTEPNRWVUDA-UHFFFAOYSA-N chembl1442125 Chemical compound OC(=O)C1=CC=CC=C1N=NC1=CC=C(O)C=C1 DWQOTEPNRWVUDA-UHFFFAOYSA-N 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 238000010224 classification analysis Methods 0.000 description 1
- 230000004186 co-expression Effects 0.000 description 1
- 229960002424 collagenase Drugs 0.000 description 1
- 230000002508 compound effect Effects 0.000 description 1
- 230000001143 conditioned effect Effects 0.000 description 1
- 230000001268 conjugating effect Effects 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 230000001054 cortical effect Effects 0.000 description 1
- 230000002338 cryopreservative effect Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 108700041286 delta Proteins 0.000 description 1
- 238000011033 desalting Methods 0.000 description 1
- 238000000502 dialysis Methods 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 210000003317 double-positive, alpha-beta immature T lymphocyte Anatomy 0.000 description 1
- 230000004064 dysfunction Effects 0.000 description 1
- 239000012636 effector Substances 0.000 description 1
- 210000002257 embryonic structure Anatomy 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- 210000003386 epithelial cell of thymus gland Anatomy 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 210000002304 esc Anatomy 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000013613 expression plasmid Substances 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 210000003754 fetus Anatomy 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 238000007667 floating Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 208000016361 genetic disease Diseases 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 150000002343 gold Chemical class 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 201000005787 hematologic cancer Diseases 0.000 description 1
- 208000024200 hematopoietic and lymphoid system neoplasm Diseases 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 239000012510 hollow fiber Substances 0.000 description 1
- 102000053342 human STK36 Human genes 0.000 description 1
- 208000033519 human immunodeficiency virus infectious disease Diseases 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 208000013403 hyperactivity Diseases 0.000 description 1
- 230000001146 hypoxic effect Effects 0.000 description 1
- 210000002861 immature t-cell Anatomy 0.000 description 1
- 210000002865 immune cell Anatomy 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 230000036737 immune function Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 230000037451 immune surveillance Effects 0.000 description 1
- 208000026278 immune system disease Diseases 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 238000007917 intracranial administration Methods 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 238000011031 large-scale manufacturing process Methods 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 230000001926 lymphatic effect Effects 0.000 description 1
- 239000006166 lysate Substances 0.000 description 1
- 239000012139 lysis buffer Substances 0.000 description 1
- 238000007885 magnetic separation Methods 0.000 description 1
- 230000005415 magnetization Effects 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 210000001161 mammalian embryo Anatomy 0.000 description 1
- 108010082117 matrigel Proteins 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 210000003716 mesoderm Anatomy 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 230000000394 mitotic effect Effects 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 210000005087 mononuclear cell Anatomy 0.000 description 1
- 230000000877 morphologic effect Effects 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 210000000066 myeloid cell Anatomy 0.000 description 1
- 229920005615 natural polymer Polymers 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 102000039446 nucleic acids Human genes 0.000 description 1
- 108020004707 nucleic acids Proteins 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 235000019198 oils Nutrition 0.000 description 1
- 238000006384 oligomerization reaction Methods 0.000 description 1
- 230000005868 ontogenesis Effects 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- YIQPUIGJQJDJOS-UHFFFAOYSA-N plerixafor Chemical compound C=1C=C(CN2CCNCCCNCCNCCC2)C=CC=1CN1CCCNCCNCCCNCC1 YIQPUIGJQJDJOS-UHFFFAOYSA-N 0.000 description 1
- 229960002169 plerixafor Drugs 0.000 description 1
- 229920001606 poly(lactic acid-co-glycolic acid) Polymers 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 235000020004 porter Nutrition 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000004094 preconcentration Methods 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000000159 protein binding assay Methods 0.000 description 1
- 229950010131 puromycin Drugs 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 230000008707 rearrangement Effects 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 210000004994 reproductive system Anatomy 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 238000007790 scraping Methods 0.000 description 1
- 238000010187 selection method Methods 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 210000004927 skin cell Anatomy 0.000 description 1
- 210000001082 somatic cell Anatomy 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000008223 sterile water Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- ACTRVOBWPAIOHC-XIXRPRMCSA-N succimer Chemical compound OC(=O)[C@@H](S)[C@@H](S)C(O)=O ACTRVOBWPAIOHC-XIXRPRMCSA-N 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 229920001059 synthetic polymer Polymers 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 238000003151 transfection method Methods 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 230000008733 trauma Effects 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 244000052613 viral pathogen Species 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 238000003260 vortexing Methods 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 210000001325 yolk sac Anatomy 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/0068—General culture methods using substrates
- C12N5/0075—General culture methods using substrates using microcarriers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K39/46
- A61K2239/31—Indexing codes associated with cellular immunotherapy of group A61K39/46 characterized by the route of administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K39/46
- A61K2239/38—Indexing codes associated with cellular immunotherapy of group A61K39/46 characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
- A61K35/17—Lymphocytes; B-cells; T-cells; Natural killer cells; Interferon-activated or cytokine-activated lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/461—Cellular immunotherapy characterised by the cell type used
- A61K39/4611—T-cells, e.g. tumor infiltrating lymphocytes [TIL], lymphokine-activated killer cells [LAK] or regulatory T cells [Treg]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/464—Cellular immunotherapy characterised by the antigen targeted or presented
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0636—T lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2121/00—Preparations for use in therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/40—Regulators of development
- C12N2501/42—Notch; Delta; Jagged; Serrate
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/50—Cell markers; Cell surface determinants
- C12N2501/599—Cell markers; Cell surface determinants with CD designations not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2506/00—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells
- C12N2506/11—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from blood or immune system cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2506/00—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells
- C12N2506/45—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from artificially induced pluripotent stem cells
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Biomedical Technology (AREA)
- Cell Biology (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Microbiology (AREA)
- Wood Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Epidemiology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Biochemistry (AREA)
- Mycology (AREA)
- General Engineering & Computer Science (AREA)
- Hematology (AREA)
- Molecular Biology (AREA)
- Gastroenterology & Hepatology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Toxicology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Peptides Or Proteins (AREA)
- Developmental Biology & Embryology (AREA)
- Virology (AREA)
Abstract
(a) 줄기 세포 또는 선조 세포를 포함하는 샘플을 현탁 지지체에 접합된 Notch 리간드와 함께 배양하는 단계, 및 (b) T 세포 계통의 세포를 단리하는 단계를 포함하는, T 세포 계통의 세포를 생성하는 방법이 제공된다. 일 구현예에서, T-세포 계통의 세포는 선조 T 세포 또는 성숙 T 세포이다. 이의 조성물, 키트 및 용도가 또한 제공된다.
Description
관련 출원에 대한 교차 참조
본 출원은 그의 내용 전체가 참조로서 본원에 포함되는, 2018년 2월 14일자로 출원된 미국 가특허 출원 제62/630,497호에 대한 우선권의 이익을 청구한다.
분야
본 출원은 T 세포 계통의 세포를 생성하기 위한 방법, 조성물 및 키트와, 이의 용도에 관한 것이다. 구체적으로, 본 출원은 선조 (progenitor) 및 성숙 T 세포를 생성하기 위한 방법, 조성물 및 키트와, 이의 용도에 관한 것이다.
T 세포는 적응성 면역의 중요한 매개체이며 병원균에 대한 치료제로서, 그리고 암 면역요법에 사용될 수 있다. 조혈 줄기 세포 이식 (HSCT)은 광범위한 스펙트럼의 악성 및 비-악성 장애에 효과적인 치료를 제공하지만, 치료 전에 필요한 전처리 요법 (preconditioning regimen)으로 인해 T 세포 회복의 지연이 연장된다 (Krenger et al., 2011). 골수 (BM)에서 발생하는, 대부분의 다른 조혈 계통과는 달리, T 세포 발생은 BM-유래 선조체의 흉선으로의 이동을 요구하고, 이때 유입되는 림프구 선조체는 이들의 T-계통 세포로의 분화를 유도하는 중요한 신호를 수용한다 (Shah and Zuniga-Pflucker, 2014).
흉선 기질 세포에 의해 유입되는 림프구 선조체로 전달되는 중요한 신호는, 피질 흉선 상피 세포에 의해 발현되는, Notch 리간드 델타-유사-4에 의해 매개된다 (Thompson and Zuniga-Pflucker, 2011). 림프구 선조체에 의해 발현된 Notch 수용체는 Notch 수용체 활성화를 효과적으로 유도하기 위해 델타-유사-4 운반 세포 (bearing cell)에 의해 유도되는 기계적 견인력 (pulling force)을 요구한다 (D'Souza et al., 2010; Gordon et al., 2015; Meloty-Kapella et al., 2012). 또한, T 세포 발생은 일정하고 높은 수준의 Notch 수용체 활성화를 요구하는 것으로 나타났다 (Schmitt et al., 2004). Notch1 수용체 신호 또는 델타-유사-4 유도 신호의 부재시에, T 세포 발생은 흉선에서 일어나지 않고, 그보다는 B 세포와 같은, 대체 림프구 계통이 대신 발생한다. 따라서, 흉선내 (intrathymic) T 세포 발생은 Notch 신호전달 경로에 바탕을 둔다 (Zuniga-Pflucker, 2004).
HSCT의 맥락에서, 각각 림프구를 생성하는 이식된 HSCs의 제한된 용량과 결합된, 조절 및 노화의 결과로서, 흉선 기능장애 또는 위축은 흉선에서 T 세포 발생의 범위를 제한한다 (Porter and June, 2005). 이는 환자가 감염 및/또는 암의 재발에 걸리기 쉬운, 충분하지 않은 면역 감시를 초래하고, 심각한 임상 문제로 남는다.
인간 또는 마우스 proT 세포가 이들의 이종 또는 동종 기원에도 불구하고 면역결핍 마우스의 흉선을 생착시키는 것으로 나타남에 따라 선조 T (proT) 세포의 입양 전달 (adoptive transfer)이 T 세포 재구성을 증강시키는데 유망한 전략으로 대두되었다 (Awong et al., 2009; Awong et al., 2013; Zakrzewski et al., 2006; Zakrzewski et al., 2008). ProT 세포는 발생적으로 미성숙하고 숙주 흉선에서 양성 및 음성 선택을 경험한다. 따라서, 이들은 이식편대숙주병 (graft-versus-host disease, GVHD)과 연관된 임상적 문제를 우회할 수 있는 숙주 내성 T 세포를 생성하는 수용자의 주요 조직적합성 복합체 (MHC)로 제한된다. 중요하게는, proT 세포를 이용한 생착은 흉선 구조를 복원하고 HSC-유래 선조체에 의한 후속 흉선 접종을 개선한다. 본질적인 재생 의학 특성 외에도, proT 세포는 또한 암 치료를 위한 종양-관련 항원 (TAA)에 특이성을 부여하기 위해 T 세포 수용체 (TCRs) 및 키메라 항원 수용체 (CARs)로 조작될 수 있고, 또한 맞춤형 반응 프로그램을 조작하기 위해 합성 유전자 회로로 조작될 수 있다.
이 분야에서 충족되지 않은 과제는 인간 조혈 줄기/선조 세포 (HSPC)의 다양한 공급원으로부터 대량의 proT 세포를 생성하기 위해 쉽게 확장될 수 있는 임상적으로 관련된 시스템의 개발이다. 이전 방법은 Notch 리간드 델타-유사-1 (DL1) 또는 델타-유사-4 (DL4)를 발현하는 마우스-유래 OP9 세포에 의존했지만, 이 접근법은 임상적 번역에 대한 몇 가지 과제를 제시한다 (Awong et al., 2009; Awong et al., 2013). 무-기질 세포 접근법에 대한 대부분의 전략은 2차원 (2D) 조직 배양 플랫폼에 의존해왔고, 그에 의해 Notch 리간드, DL1 또는 DL4는 조직-배양 플레이트 위에 고정된다 (Gehre et al., 2015; Reimann et al., 2012; Simons et al., 2017). 혈관 세포 부착 분자-1 (VCAM-1)과 같은, 추가의 접착 수용체 리간드가 또한 이 형식에 포함되어 있다 (Shukla et al., 2017). 이러한 전략을 사용하여 생산된 인간 proT 세포는 면역결핍 마우스의 흉선을 성공적으로 재구성하는 것으로 나타났다. 고무적인 진전이지만, 치료용으로 proT 세포를 생성하기 위한 이들 접근법의 유용성은 임상적 제조를 위한 대규모 가공 (scale-up processing)의 필요성으로 인해 제한적이고, 임상적으로 적용될 수 있는 대규모 세포 수의 통상적인 생성에 효과적인 방법이 아니다. 이상적으로, 실제로 확장가능한 플랫폼은 폐쇄형 자동화 생물반응기 시스템에서 proT 세포가 성장되게 할 것이다 (Lipsitz et al., 2016).
요약
본 발명자들은 마우스 또는 인간 조혈 줄기/선조 세포 (HSPCs) 및 유도 만능 줄기 세포 (iPSCs)로부터 T 세포 계통의 세포를 생성하기 위한 무-세포, 비드-기반 시스템을 개발하였다. Notch 리간드의 비-플레이트-결합된 현탁액 (예를 들어, DL4-μ비드)은 선조 T 세포 및 성숙 T 세포를 포함하는 T-계통 세포의 효과적인 생성을 허용한다.
따라서, 본 개시내용은 (a) 줄기 세포 또는 선조 세포를 포함하는 샘플을 현탁 지지체에 접합된 Notch 리간드와 함께 배양하는 단계, 및 (b) T 세포 계통의 세포를 단리하는 단계를 포함하는, T 세포 계통의 세포를 생성하는 방법을 제공한다.
일 구현예에서, 현탁 지지체는 입자이다.
다른 구현예에서, 현탁 지지체는 마이크로비드이다.
일 구현예에서, 줄기 세포 또는 선조 세포는 Notch 리간드와 함께 현탁 상태로 배양된다.
다른 구현예에서, 줄기 세포는 조혈 줄기/선조 세포 (HSPCs), 배아 줄기 세포 또는 유도 만능 줄기 세포 (iPSCs)로부터 선택된다.
다른 구현예에서, 줄기 세포는 인간 줄기 세포, 선택적으로 CD34+ 또는 CD34+CD38-/lo HSPCs이다.
다른 구현예에서, 줄기 세포는 CD34+ 조혈 전구 세포 (precursor cell), 선택적으로 iPSCs로부터 분화된 CD34+ 조혈 전구 세포이다.
다른 구현예에서, Notch 리간드는 DL1 또는 DL4이다.
다른 구현예에서, T 세포 계통의 세포는 선조 T (proT) 세포이다.
다른 구현예에서, 줄기 세포 또는 선조 세포는 인간 세포이고 proT 세포는 표현형 CD34+CD7+ 또는 CD7+CD5+CD1a-를 갖는다.
다른 구현예에서, 줄기 세포 또는 선조 세포는 마우스 세포, 선택적으로 계통-CD117+Sca-1+ 마우스 세포이고, proT 세포는 표현형 CD25+ 또는 CD25+CD90+을 갖는다.
다른 구현예에서, T-세포 계통의 세포는 CD4+CD8+ 이중 양성 세포, CD4+CD8+CD3+ 이중 양성 세포, CD8+CD3+ 단일 양성 세포 또는 CD4+CD3+ 단일 양성 세포이다.
다른 구현예에서, 줄기 세포 또는 선조 세포는 무-기질 세포 배지에서 배양된다.
다른 구현예에서, 줄기 세포 또는 선조 세포는 현탁 지지체에 부착된 적어도 하나의 T 세포 공동-자극 분자와 함께 배양되고, 선택적으로 적어도 하나의 T 세포 공동-자극 분자는 VCAM1이다.
본 개시내용은 또한 다음을 포함하는 방법에 의해 생성된 T 세포 계통의 세포를 제공한다: (a) 줄기 세포 또는 선조 세포를 포함하는 샘플을 현탁 지지체에 접합된 Notch 리간드와 함께 배양하는 단계, 및 (b) T 세포 계통의 세포를 단리하는 단계.
일 구현예에서, 세포는 선조 T 세포, CD4+CD8+ 이중 양성 세포, CD4+CD8+CD3+ 이중 양성 세포 또는 CD8+CD3+ 단일 양성 세포, CD4+CD3+ 단일 양성 세포이다.
본 개시내용은 또한 (a) Notch 리간드 및 (b) 현탁 지지체, 선택적으로 마이크로비드를 포함하고, Notch 리간드가 현탁 지지체에 접합되는, 현탁 Notch 리간드를 제공한다.
일 구현예에서, 현탁 지지체는 마이크로비드이고 (i) 마이크로비드는 6.5 내지 100 μm, 선택적으로 20 내지 30 μm의 직경을 갖고/갖거나, (ii) Notch 리간드의 C-말단 영역은 마이크로비드에 접합된다.
본 개시내용은 또한 T 세포 계통의 세포를 생성하기 위한 현탁 Notch 리간드의 용도를 제공한다.
본 개시내용은 또한 (i) (a) Notch 리간드, 및 (b) 현탁 지지체를 포함하고, Notch 리간드가 현탁 지지체드에 접합되는, 현탁 Notch 리간드 및 (ii) T 세포 계통의 세포를 생성하기 위한 현탁 Notch 리간드의 사용을 위한 지침서를 포함하는 키트를 제공한다.
본 개시내용은 또한 (i) (a) Notch 리간드 및 (b) 현탁 지지체를 포함하고, Notch 리간드가 현탁 지지체드에 접합되는, 현탁 Notch 리간드 및 (ii) 배양 배지를 포함하는 키트를 제공한다.
키트의 일 구현예에서, 현탁 Notch 리간드는 마이크로비드에 접합된 DL4를 포함한다.
다른 구현예에서, 키트는 (iii) 현탁 지지체에 부착된 적어도 하나의 T 세포 공동-자극 분자를 추가로 포함하고, 여기서 선택적으로 적어도 하나의 T 세포 공동-자극 분자는 VCAM1이다.
본 개시내용은 다음을 포함하는, T 세포의 수적 증가를 요구하는 상태를 갖는 대상체를 치료하는 방법을 제공한다:
(i) (a) 줄기 세포 또는 선조 세포를 포함하는 샘플을 현탁 지지체에 접합된 Notch 리간드와 함께 배양하고, (b) T 세포 계통의 세포를 단리하는 것을 포함하는, T 세포 계통의 세포를 생성하는 단계, 및
(ii) T 세포 계통의 세포의 유효량을 대상체에 투여하는 단계.
일 구현예에서, T 세포 계통의 세포는 선조 T 세포이다.
다른 구현예에서, T 세포 계통의 세포는 성숙 T 세포이다.
다른 구현예에서, T 세포 계통의 세포는 CD4+CD8+ 이중 양성 세포, CD4+CD8+CD3+ 이중 양성 세포, CD8+CD3+ 단일 양성 세포 또는 CD4+CD3+ 단일 양성 세포이다.
본 출원의 다른 특징 및 이점은 다음의 상세한 설명으로부터 명백할 것이다. 그러나 출원의 요지 및 범위 내에서 다양한 변경 및 변형이 상세한 설명으로부터 통상의 기술자에게 명백할 것이기 때문에, 상세한 설명 및 특정 실시예는 본 출원의 바람직한 구현예를 나타내면서 단지 예시로서 제공된다는 점을 이해해야 한다.
상세한 설명
상기에 기술된 바와 같이, 본 발명자들은 마우스 또는 인간 조혈 줄기/선조 세포 (HSPCs) 또는 유도 만능 줄기 세포 (iPSCs)와 같은 줄기 또는 선조 세포로부터 T-세포 계통의 세포를 생성하는 무-세포, 비드-기반 시스템을 개발하였다. Notch 리간드의 비-플레이트-결합된 현탁액 (예를 들어, DL4-μ비드)은 선조 T 세포 및 성숙 T 세포를 포함하는 T-계통 세포의 효과적인 생성을 가능케 한다.
I. 세포 생성 방법
따라서, 본 개시내용은 (a) 줄기 세포 또는 선조 세포를 포함하는 샘플을 현탁 지지체에 접합된 Notch 리간드와 함께 배양하는 단계, 및 (b) T 세포 계통의 세포를 단리하는 단계를 포함하는 T-세포 계통의 세포를 생성하는 방법을 제공한다.
용어 "T 세포 계통의 세포"는 세포를 다른 림프구 세포와 구분하는 T 세포 또는 이의 전구체 또는 선조체의 적어도 하나의 표현형적 특징을 나타내는 세포, 및 적혈구 또는 골수 계통의 세포를 지칭한다. 이러한 표현형적 특징은 세포 또는 이의 전구체 또는 선조체 상의 T-계통에 특이적인 하나 이상의 단백질의 발현, 또는 T 세포에 특이적인 생리학적, 형태학적, 기능적, 또는 면역학적 특성을 포함할 수 있다.
T 세포 계통의 세포는 (a) T 세포 계통에 수임된 (committed) 선조 또는 전구 세포 (본원에 기술된 바와 같이, "선조 T 세포" 또는 "proT 세포"); (b) CD25+ 미성숙 T 세포; (c) CD4 또는 CD8 계통 수임 (lineage commitment)을 겪은 세포 (예컨대, CD4+CD8 lo TCR inT 세포); (d) TCR 유전자 재배열을 특징으로 하는 세포; (e) CD4+CD8+ 이중 양성 (DP)인 전구체 흉선세포; (f) CD4-CD8+ 또는 CD4+CD8- 및 선택적으로 TCR hi ; (g) CD3+CD90+; (h) CD4-CD8+ 또는 CD4+CD8- 및 TCR hi 인 단일 양성 (SP) 세포; (i) TCR-αβ+ 및/또는 TCR-γδ+; (j) 임의의 다중 Vβ 쇄 (예컨대, Vβ-3, -6, 및 17a)의 발현을 특징으로 하는 세포; 또는 (k) TCR/CD3 hi , CD4-CD8+ 또는 CD4+CD8-를 특징으로 하는 성숙 및 기능적 또는 활성화 T 세포일 수 있다.
일 구현예에서, T 세포 계통의 세포는 "선조 T 세포" 또는 "proT 세포"이다. 용어 "선조 T 세포" 또는 "proT 세포"는 본원에 사용된 바와 같이 성숙 T 세포 또는 림프구로 성숙할 수 있는 T 세포를 의미한다.
일 구현예에서, 선조 T 세포는 인간 선조 T 세포이다. 인간 선조 T 세포의 표현형은 CD34+CD7+ 및 CD7+CD5+CD1a-를 포함한다. 다른 구현예에서, 선조 T 세포는 마우스 선조 T 세포이다. 마우스 선조 T 세포의 표현형은 CD25+를 포함한다.
다른 구현예에서, T 세포 계통의 세포는 CD4+CD8+ 또는 CD4+CD8+CD3+ 표현형을 특징으로 하는 CD4 및 CD8 이중 양성 (DP) 세포이다. 다른 구현예에서, T 세포 계통의 세포는 CD4-CD8+, CD4+CD8- 또는 CD4-CD8+CD3+, CD4+CD8-CD3+을 특징으로 하는 CD4 또는 CD8 단일 양성 (SP) 세포이다.
본원에 사용된 바와 같이 용어 "현탁 지지체"는 Notch 리간드 또는 다른 T 세포 공동-자극 분자에 접합되는 경우, Notch 리간드 (또는 공동-자극 분자)가 배양 배지 중에 현탁되게 하는 임의의 재료를 지칭한다. 현탁 지지체는 매우 다양한 재료로 만들어질 수 있고 다양한 형식일 수 있다. 현탁 지지체로 사용될 수 있는 지지체의 예시에는 입자, 비드 (마이크로비드 포함), 단백질, 지질, 핵산 분자, 필터, 섬유, 스크린, 메쉬, 튜브, 중공 섬유, 생물학적 조직 및 이들의 임의의 조합이 포함되지만, 이들로 제한되지 않는다.
일 구현예에서, 현탁 지지체는 입자이다. 각각은 구형, 타원형, 막대 또는 직사각형을 포함하지만 이로 제한되지 않는 임의의 모양일 수 있다. 입자는 천연 또는 합성 중합체, 천연 또는 합성 왁스, 세라믹, 금속, 생물학적 재료 또는 이들의 조합을 포함하지만 이로 제한되지 않는 다양한 재료일 수 있다.
일 구현예에서, 현탁 지지체는 마이크로비드이다. 본원에 사용된 바와 같이, 용어 "마이크로비드" 또는 "μ비드 (μbead)"는 0.01 μm (10 nm) 내지 500 μm, 선택적으로 1 내지 200 μm의 직경을 갖는 구형 또는 대략 구형의 비드를 지칭한다. 다른 구현예에서, 마이크로비드는 6.5 내지 100 μm, 선택적으로 20 내지 30 μm, 24 내지 26 μm 또는 25 μm의 직경을 갖는다.
다양한 형태의 마이크로비드가 본원에서 고려된다. 일 구현예에서, 마이크로비드는 중합체, 실리카 또는 자성 마이크로비드이다. 다른 구현예에서, 마이크로비드는 폴리스티렌 마이크로비드, 금 나노입자 또는 Dynanead이다. 다른 구현예에서, 마이크로비드는 젖산과 글리콜산의 공-중합체 (PLGA)이다.
단백질을 지지체에 접합시키는 다양한 수단이 당해 분야에 공지되어 있다. 단백질은 현탁 지지체, 예를 들어 마이크로비드에 직접 또는 간접적으로 접합될 수 있다.
일 구현예에서, 본원에 기술된 Notch 리간드는 비오틴/스트렙타비딘 시스템을 사용하여 현탁 지지체에 접합된다. 여기서, Notch 리간드는 비오틴화된 후 스트렙타비딘-코팅된 현탁 지지체 (예를 들어, 스트렙타비딘-코팅된 마이크로비드)에 접합된다. 다른 구현예에서, 본원에 기술된 Notch 리간드는 단백질-G 또는 단백질 A를 통해 현탁 지지체에 접합된다.
본원에 사용된 바와 같이, 용어 "Notch 리간드"는 조혈 줄기/선조 세포를 포함하는 다수의 상이한 포유류 세포의 막에 존재하는 Notch 수용체 폴리펩티드에 결합할 수 있는 리간드를 지칭한다. 인간 세포에서 확인된 Notch 수용체에는 Notch-1, Notch-2, Notch-3 및 Notch-4가 포함된다. Notch 리간드는 전형적으로 아미노 말단에 20-22개 아미노산 및 세포외 표면 위에 3 내지 8개 사이의 EGF 반복을 포함하는 진단적 DSL 도메인 (D-델타, S-Serrate, 및 L-Lag2)을 갖는다.
용어 Notch 리간드는 Notch 신호전달에 결합하고 이에 관여할 수 있는 항-Notch 항체 및 압타머 (예를 들어, DNA 압타머)를 포함한다.
T 세포 계통의 세포의 분화 및 증식을 촉진하고 유지하는 Notch 리간드가 선택된다. Notch 리간드는 선택적으로 인간 기원이거나, 또는 설치류, 개, 고양이, 돼지, 양, 소, 염소 및 영장류와 같은 포유류 종을 포함하는, 다른 종으로부터 유래할 수 있다.
Notch 리간드의 특정 예시에는 델타 패밀리가 포함된다. 델타 패밀리에는 델타-1 (Genbank 등재 번호 AF003522, Homo sapiens), 델타-3 (Genbank 등재 번호 AF084576, Rattus norvegicus), 델타-유사 1 (DL1; Genbank 등재 번호 NM_005618 and NP_005609, Homo sapiens; Genbank 등재 번호 X80903, 148324, M. musculus), 델타-유사 3 (Genbank 등재 번호 NM_053666, N_446118, Rattus norvegicus), 델타-4 (Genbank 등재 번호 AF273454, BAB18580, Mus musculus; Genbank 등재 번호 AF279305, AAF81912, Homo sapiens), 및 델타-유사 4 (DL4; Genbank Accession. No. Q9NR61, AAF76427, AF253468, NM_019074, Homo sapiens; Genbank 등재 번호 NM 019454, mus musculus)가 포함된다. Notch 리간드는 상업적으로 이용가능하거나 재조합 DNA 기법에 의해 생산되고 다양한 수준으로 정제될 수 있다.
용어 "Notch 리간드"는 표준 기법에 의해 확인될 수 있는 공지의 Notch 리간드의 동족체를 포함한다. "동족체"는 공지의 Notch 리간드 중 어느 하나에 대해서, 아미노산 또는 핵산 서열 상동성인, 서열 상동성을 나타내는 유전자 산물을 지칭한다. Notch 리간드는 상응하는 Notch 리간드에 대해 아미노산 수준에서 적어도 20%, 30%, 40%, 50%, 60%, 70%, 80%, 바람직하게는 90%, 더욱 바람직하게는 95%, 가장 바람직하게는 98-99% 동일할 수 있다.
일 구현예에서, Notch 리간드의 동족체는 N-말단에 DSL 도메인을 포함하고 세포외 표면 위에 3 내지 8개 사이의 EGF-유사 반복을 갖는다. 적합한 동족체는 또한 Notch 수용체에 결합할 수 있을 것이다. Notch 수용체에 대한 결합은 시험관 내 결합 분석을 비롯한 당해 분야에 공지된 다양한 방법에 의해 결정될 수 있다.
용어 "Notch 리간드"는 또한 공지의 Notch 리간드의 변이체 또는 변형체를 포함한다. 용어 "변이체"는 하나 이상의 아미노산 부가, 치환 또는 결실에 의해 야생형 폴리펩티드와 다른 일차 아미노산 서열을 갖는 폴리펩티드를 지칭한다. 바람직하게는, 변이체는 야생형 서열과 적어도 90% 서열 동일성을 갖는다. 바람직하게는, 변이체는 전체 야생형 서열에 걸쳐 20개 이하의 돌연변이를 갖는다. 더욱 바람직하게는, 변이체는 전체 야생형 서열에 걸쳐 10개 이하의 돌연변이, 가장 바람직하게는 5개 이하의 돌연변이를 갖는다.
선택적으로, Notch 리간드는 적어도 하나의 단백질 태그 (tag)를 포함한다. 단백질 태그는 Notch 리간드와 같은 관심 단백질에 부가된 (appended) 펩티드 서열이다. 단백질 태그는 관심 단백질에 직접 또는 간접적으로 연결될 수 있다. 다양한 단백질 태그가 당해 분야에 공지되어 있으며 다양한 목적을 위해 사용될 수 있다. 일 구현예에서, Notch 리간드는 Fc 태그 (Fc-융합 단백질로도 알려짐)를 포함한다. 본원에 사용된 바와 같이, 용어 "Fc"는 IgG의 Fc 도메인을 지칭한다. 하나의 특정 구현예에서, Notch 리간드 DL4가 Fc에 융합된다 (DL4-Fc). 다른 구현예에서, 태그는 His 태그이다. 추가 구현예에서, 태그는 Notch 리간드의 올리고머화를 촉진하는 분자이다. 예를 들어, COMP (연골 올리고머 기질 단백질)의 작은 도메인이 Notch 리간드 (예를 들어, DL4)에 융합되어 DL4 오량체를 형성할 수 있다. 페리틴 (ferritin)이 유사한 방식으로 사용되어 DL4 다량체를 형성할 수 있다.
본원에 기술된 방법에 따라, T 세포 계통의 세포는 줄기 세포 또는 선조 세포를 포함하는 샘플을 배양함으로써 생성된다. 줄기 또는 선조 세포는, 제한 없이, 제대혈, 배아, 배아 조직, 태아 조직, 골수 및 혈액을 포함하는 임의의 적합한 공급원으로부터 수득될 수 있다. 일 구현예에서, 줄기 또는 선조 세포는 조혈 줄기 또는 선조 세포 (HSPC)이다. 다른 구현예에서, 줄기 세포는 배아 줄기 세포 (ESC)이다. 추가 구현예에서, 줄기 또는 선조 세포는 유도 만능 줄기 세포이다. 다른 구현예에서, 줄기 또는 선조 세포는 CD34+ 조혈 전구 세포, 선택적으로 ESC 또는 iPSC로부터 분화된 CD34+ 조혈 (hemogenic) 내피 전구 세포, 또는 ESC 또는 다능성 줄기 세포 (PSC)로부터 분화된 CD34+ 전-조혈 세포이다. CD34+ 세포를 수득하기 위한 다양한 분화 프로토콜이 당해 분야에 알려져 있다. 치료적 응용을 위해, T 세포 계통의 세포를 생성하기 위해 사용되는 줄기 세포 또는 선조 세포는 치료될 환자로부터 수득될 수 있다.
본원에 사용된 바와 같이, 용어 "조혈 줄기/선조 세포", "조혈 줄기 또는 선조 세포" 또는 "HSPC"는 T 세포 계통의 세포을 포함하는 다른 세포 유형으로 분화할 수 있는 미분화된 조혈 세포를 지칭한다. HSPCs는 골수, 제대혈 및 동원된 말초 혈액 (mobilized peripheral blood, mPB)을 포함하지만, 이로 제한되지 않는 다수의 공급원으로부터 수득될 수 있다. HSPCs는 또한 여러 태아 및 배아 부위, 예컨대, 간, 난황낭 (yolk sac) 또는 등쪽 대동맥 (dorsal aorta)으로부터 수득될 수 있다. HSPCs는 또한 배양 중에 ESCs 또는 iPSCs의 분화를 유도함으로써 수득될 수 있다.
본원에 사용된 바와 같이, 용어 "배아 줄기 세포" 또는 "ESC"는 발생 중인 배아의 생식계 내로 통합되고 그의 일부가 되는 능력을 갖는 미분화된 배아 줄기 세포를 지칭한다.
본원에 사용된 바와 같이, 용어 "유도 만능 줄기 세포" 또는 "iPSC"는 배아-유사 다능성 상태로 다시 재프로그래밍된 피부 또는 혈액 세포와 같이, 체세포로부터 유래한 세포를 지칭한다. 일 구현예에서, iPSCs는 공지 또는 비공지의 TCR 특이성을 갖는 T 세포 (예를 들어, 암에 대한 특이성을 갖는 TCRs을 보유하는 T 세포)로부터 유래한다.
전형적으로, 줄기 또는 선조 세포를 함유하는 샘플은 먼저 비-줄기 세포 또는 성숙 세포가 고갈된다. 당해 분야에 공지된 음성 및 양성 선택 방법이 줄기 또는 선조 세포의 농축 (enrichment)을 위해 사용될 수 있다. 예를 들어, 세포는 형광 활성화 세포 분류기, 또는 특정 세포 표면 항원에 결합하는 자성 비드를 사용하여 세포 표면 항원을 기준으로 분류될 수 있다. 음성 선택 칼럼이 계통 특이적 표면 항원을 발현하는 세포를 제거하는데 사용될 수 있다.
구현예에서, 줄기 또는 선조 세포를 함유하는 샘플은 계통-음성 (Lin-) 및 계통 양성 (Lin+) 분획으로 분리된다. Lin- 분획이 CD34+ 세포에 대해 분류될 수 있다.
선조 세포 또는 줄기 세포는 T 세포 계통의 세포를 생성하기 위해 본원에 기술된 바와 같은 적합한 조건에서 배양된다. 바람직하게는, 상기 세포를 T 세포 계통의 세포를 형성하기에 충분한 시간 동안 현탁 지지체에 접합된 하나 이상의 Notch 리간드의 존재하에 배양한다.
본원에 기술된 방법의 하나의 이점은 T 세포 계통의 세포가 현탁 중에 배양되게 할 수 있다는 것이다. 구현예에서, 선조 세포 또는 줄기 세포는 마이크로비드와 같은 현탁 지지체에 접합된 Notch 리간드와 함께 현탁 중에 배양된다. 현탁 배양에서, 세포는 배양 배지 중에서 자유롭게 부유하면서 성장한다. 반대로, 부착 배양에서는, 세포가 인공 기질 위에서 단층으로 성장한다.
다른 구현예에서, 선조 세포 또는 줄기 세포는 현탁 지지체에 접합된 Notch 리간드와 함께 생물반응기, 선택적으로 폐쇄된 또는 폐쇄된 자동화 생물반응기 중에서 현탁 배양된다. 일 구현예에서, 현탁 지지체는 생물반응기와 호환되는 직경을 갖는 마이크로비드이다. 다양한 생물반응기가 당해 분야에 공지되어 있고 회분식, 유가식 또는 연속식 생물반응기를 포함할 수 있다. 연속식 생물반응기의 예시는 연속식 교반-탱크 반응기 모델이다.
배양 중의 선조 세포 또는 줄기 세포의 다양한 농도가 고려된다. 예를 들어, 배양 중의 선조 세포 또는 줄기 세포의 농도는 배지 ml당 1 내지 수 백만 개의 세포일 수 있다.
일 구현예에서, 마이크로비드-접합 Notch 리간드 대 선조 세포 또는 줄기 세포의 비율은 1:1과 27:1 사이, 선택적으로 5:1 내지 15:1, 8:1 내지 10:1 또는 9:1이다. 이 비율은 또한 본원에서 "마이크로비드 대 세포 비율"로 지칭된다.
본 발명자들은 또한 Notch 리간드의 현탁 지지체에 대한 배향 지향이 Notch 신호전달을 증강시킬 수 있음을 보여주었다. 따라서, 일 구현예에서, Notch 리간드의 C-말단은 현탁 지지체에 접합된다. 이는, 예를 들어 비오틴 분자에 효소적으로 접합될 수 있는 Notch 리간드의 C-말단에 서열을 추가함으로써 조작될 수 있다. 다른 구현예에서, C-말단 영역에 존재하는, 융합 단백질의 Fc 분절인, Notch 리간드-Fc는 현탁 지지체에 접합되는 단백질 A 또는 단백질 G에 직접 결합할 수 있다.
T 세포 계통의 세포의 수임 및 분화를 촉진하는 하나 이상의 양성 사이토카인이 또한 배양물에 첨가될 수 있다. 사이토카인은 인간 기원일 수 있거나, 또는 다른 종으로부터 유래할 수 있다. 배양물 중 사이토카인의 농도는 전형적으로 약 1-10 ng/ml이다. 다음은 본 출원에서 사용될 수 있는 사이토카인의 대표적인 예시이다: Flt-3-리간드의 모든 구성원, 및 인터루킨-7 (IL-7) 및 줄기 세포 인자. 일 구현예에서, 본원에서 사용된 사이토카인은 Flt-3-리간드 및 IL-7 및 줄기 세포 인자이다. 사이토카인은 헤파린 설페이트와 같은 글리코사미노글리칸의 동일한 몰 또는 그 이상의 양과 조합하여 사용될 수 있다. 사이토카인은 상업적으로 이용가능하거나 또는 재조합 DNA 기법에 의해 생산되고 다양한 정도로 정제될 수 있다. 일부 사이토카인은 표준 생화학적 기법에 의헤 세포주의 배양 배지로부터 정제될 수 있다.
각각 현탁 지지체에 접합되는, 하나 이상의 추가 분자가 또한 배양물에 첨가될 수 있다. 일 구현예에서, 추가 분자는 "T 세포 공동-자극 분자"로도 지칭되는, T 세포 발생을 촉진하는 (예를 들어, T 세포 계통의 세포의 수임 및 분화를 촉진하는) 분자이다. 일례로서, 본 발명자들은 HSPCs와 함께 배양된 마이크로비드-접합된 DL4 및 VCAM1이 T 세포 계통으로의 분화를 가속화시켰음을 보여주었다. 따라서, 일 구현예에서, T 세포 공동-자극 분자는 VCAM1이다. 본원에 사용된 바와 같이, 용어 "VCAM1"은 혈관 세포 부착 분자 1 (VCAM1) 또는 분화 클러스터 106 (CD106)으로도 알려진 혈관 세포 부착 단백질 1을 지칭하는데, 이는 인간에서 VCAM1 유전자에 의해 인코딩되는 단백질이다. 용어 "VCAM1"은 또한 VCAM1의 변이체 또는 변형체를 포함한다. 다른 구현예에서, T 세포 공동-자극 분자는 사이토카인 또는 케모카인 (줄기 세포 인자, IL-7, CCL25, 또는 CXCR4), 주요 조직적합성 복합체 (MHC) 클래스 I 또는 클래스 II, 또는 공동-자극 (CD80, CD86) 분자이다. 선택적으로, T 세포 공동-자극 분자는 적어도 하나의 단백질 태그 (tag)를 포함한다. 다양한 단백질 태그가 당해 분야에 알려져 있으며 다수의 목적을 위해 사용될 수 있다. 일 구현예에서, T 세포 공동-자극 분자는 Fc 태그 (Fc-융합 단백질로도 알려짐)를 포함한다.
선조 세포 및 줄기 세포는 조건화 배지, 비-조건화 배지, 또는 배아 줄기 세포 배지를 포함하는 배양 배지에서 배양될 수 있다. 적합한 조건화 배지의 예시에는 배아 섬유아 세포 (예컨대, 인간 배아 섬유아 세포 또는 마우스 배아 섬유아 세포)로 조건화된, IMDM, DMEM, 또는 αMEM, 또는 등가 배지가 포함된다. 적합한 비-조건화 배지의 예시에는 IMDM (Iscove's Modified Dulbecco's Medium), DMEM, 또는 αMEM, 또는 등가 배지가 포함된다. 배양 배지는 혈청 (예컨대, 소 혈청, 소 태아 혈청, 송아지 소 혈청, 말 혈청, 인간 혈청, 또는 인공 혈청 대체물)을 포함할 수 있거나, 또는 무혈청일 수 있다. 본 발명의 방법에 유용한 배지의 다른 예시에는 StemCell Technologies 배지 (StemSpanTMSFEM II) 또는 임의의 다른 상업적으로 이용가능한 등가 배지가 포함된다.
일 구현예에서, 배양 조건은 준비 중인 세포가 proT 세포를 형성하도록 충분한 시간 동안 선조 세포 또는 줄기 세포를 배양하는 것을 수반한다. 다른 구현예에서, 배양 조건은 세포가 성숙 T 세포, 예를 들어, 성숙 SP T 세포를 형성하도록 충분한 시간 동안 선조 세포 또는 줄기 세포를 배양하는 것을 수반한다. 원하는 세포 조성을 달성하는데 필요한 적절한 시간 동안 세포가 유지될 수 있음을 이해할 것이다. 선택적으로, 선조 세포 또는 줄기 세포는 적어도 6, 8, 10, 12, 14, 21, 28, 35 또는 42일간 배양된다. 일례에서, 선조 세포 또는 줄기 세포는 proT 세포를 생성하기 위해 본원에 기술된 Notch 리간드와 4 내지 21일, 6 내지 18일 또는 7 내지 14일간 배양된다. 또 다른 예에서, 선조 세포 또는 줄기 세포는 성숙 T 세포를 생성하기 위해 본원에 기술된 Notch 리간드와 적어도 21, 28, 35 또는 42일간 배양된다.
본 출원의 방법은 대량으로 T 세포 계통의 세포의 생성을 가능케 한다. 특히, 일 구현예에서, 14일 이상의 배양 후, 줄기 세포 또는 선조 세포의 초기 출발 수에 비해 50-배, 75-배, 100-배, 125-배, 150-배, 175-배 또는 200-배 초과의 세포 확장이 달성된다.
본원에 사용된 바와 같이 용어 "단리된"은 선조 세포가 그들의 천연 환경에서 세포와 함께 발견되는 세포 또는 생물학적 물질로부터 분리 또는 정제되었음을 의미한다. 따라서 이는 세포가 자연에 존재하는 방식과 구별된다.
용어 "세포" 또는"그 세포"는 복수의 세포를 포함한다.
II. 현탁 Notch 리간드
본 발명자들은 또한 신규한 현탁 Notch 리간드를 개발하였다. 본원에 사용된 바와 같이, 용어 "현탁 Notch 리간드"는 현탁 세포 배양에 사용하기 위한 Notch 리간드를 지칭한다.
따라서, 본 개시내용은 또한 본원에 기술된 바와 같은 현탁 Notch 리간드를 제공한다. 현탁 Notch 리간드는 (a) Notch 리간드 및 (b) 현탁 지지체를 포함하고, 여기서 Notch 리간드는 현탁 지지체에 접합된다.
구체적으로, 본 발명자들은 25 μm 직경의 마이크로비드에 직접적으로 접합되는 경우, DL4가 강력하고 지속적인 신호를 전달하여 HSPCs가 T 세포 계통의 세포로 발생하도록 유도함을 보여주었다. 따라서, 일 구현예에서, 현탁 지지체는 10 내지 100 μm, 선택적으로 20 내지 30 μm, 24 내지 26 μm 또는 25 μm의 직경을 갖는 마이크로비드이다.
본 발명자들은 또한 Notch 리간드의 현탁 지지체에 대한 배향 지향이 Notch 신호전달을 증강시킬 수 있음을 보여주었다. 따라서, 다른 구현예에서, Notch 리간드의 C-말단은 현탁 지지체에 접합된다. 상기에 기술된 바와 같이, 이는, 예를 들어, 비오틴 분자에 효소적으로 접합될 수 있는 Notch 리간드의 C-말단에 서열을 추가함으로써 조작될 수 있다.
Notch 리간드는 선택적으로 DL4이고 태그, 예를 들어, Fc 태그에 융합될 수 있다.
현탁 T 세포 공동-자극 분자가 또한 본원에 제공된다. 본원에 사용된 바와 같이, 용어 "현탁 T 세포 공동-자극 분자"는 현탁 세포 배양에 사용하기 위한 T 세포 공동-자극 분자를 지칭한다. 현탁 T 세포 공동-자극 분자는 (a) T 세포 공동-자극 분자 및 (b) 현탁 지지체를 포함하고, 여기서 T 세포 공동-자극 분자는 현탁 지지체에 접합된다.
T 세포 공동-자극 분자는 선택적으로 VCAM1이고 태그, 예를 들어, Fc 태그에 융합될 수 있다.
III. 키트
현탁 Notch 리간드는 T 세포 계통의 세포를 생성하는데 사용하기 위한 키트로 제조 및 패키징될 수 있다.
따라서, 현탁 Notch 리간드를 포함하는 T 세포 계통의 세포를 생산하기 위한 키트가 또한 본원에 제공되며, 여기서 현탁 Notch 리간드는 (a) Notch 리간드 및 (b) 현탁 지지체를 포함하고, 상기 Notch 리간드는 현탁 지지체에 접합된다. 선택적으로, 현탁 Notch 리간드는 보존제 및/또는 완충제 용액 중에 함유되고 키트는 바이알 또는 주사기와 같이 현탁 Notch 리간드를 분배하기 위한 장치를 추가로 포함한다.
일 구현예에서, 키트는 줄기 세포 또는 선조 세포를 포함하는 샘플을 현탁 Notch 리간드와 함께 배양하기 위한 배양 배지를 추가로 포함한다. 배양 배지의 예시에는 조건화 배지, 비-조건화 배지, 또는 배아 줄기 세포 배지가 포함된다. 배양 배지는 혈청 (예컨대, 소 혈청, 소 태아 혈청, 송아지 소 혈청, 말 혈청, 인간 혈청, 또는 인공 혈청 대체물)을 포함할 수 있거나 또는 무혈청일 수 있다. 유용한 배양 배지의 다른 예시에는 StemCell 배지 또는 임의의 다른 상업적으로 이용가능한 등가 배지가 포함된다.
다른 구현예에서, 키트는 각각이 현탁 지지체에 접합된, 하나 이상의 추가 분자를 더 포함한다. 일 구현예에서, 추가 분자는 본원에서 "T 세포 공동-자극 분자"로도 지칭되는, T 세포 발생을 촉진하는 (예를 들어, T 세포 계통의 세포의 수임 및 분화를 촉진하는) 분자이다. 다른 구현예에서, T 세포 공동-자극 분자는 VCAM1이다.
배지는 선택적으로 T 세포 계통의 세포의 수임 및 분화를 촉진하는 하나 이상의 사이토카인을 포함한다. 사이토카인은 인간 기원일 수 있거나, 또는 다른 종으로부터 유래할 수 있다. 배양물 내 사이토카인의 농도는 전형적으로 약 1-10 ng/ml이다. 다음이 본 출원에 사용될 수 있는 사이토카인의 대표적인 예시이다: Flt-3-리간드의 모든 구성원, 및 인터루킨-7 (IL-7) 및 줄기 세포 인자. 일 구현예에서, 본원에 사용되는 사이토카인은 Flt-3-리간드 및 IL-7 및 줄기 세포 인자이다. 사이토카인은 헤파린 설페이트와 같은 글리코사미노글리칸의 동일한 몰 또는 그 이상의 양과 조합하여 사용될 수 있다. 사이토카인은 상업적으로 이용가능하거나 또는 재조합 DNA 기법에 의해 생산되고 다양한 정도로 정제될 수 있다. 일부 사이토카인은 표준 생화학적 기법에 의해 세포주의 배양 배지로부터 정제될 수 있다.
일 구현예에서, 키트는 본원에 기술된 시약을 위한 하나 이상의 용기를 포함한다.
시약(들)의 사용에 대한 지침을 제공하는 인쇄된 설명서가 또한 다양한 구현예에서 키트에 포함될 수 있다. 용어 "지침" 또는 "사용 설명서"는 전형적으로 시약 농도 또는 현탁 Notch 리간드의 양 및/또는 적어도 하나의 분석 방법 매개변수, 예컨대 현탁 Notch 리간드 및 혼합되는 세포의 상대적 양, 배양 기간, 온도, 배지 조건 등을 설명하는 명시적인 표현을 포함한다. 예를 들어, 일 구현예에서, 지침은 (a) 줄기 세포 또는 선조 세포를 포함하는 샘플을 현탁 지지체에 접합된 Notch 리간드와 배양하는 단계, 및 (b) T 세포 계통의 세포를 단리하는 단계를 포함하는, 방법을 설명한다.
IV. T 세포 계통의 세포
본 개시내용은 본원에 기술된 방법, 시스템 및 키트에 의해 생성된 T 세포 계통의 세포, 또는 상기 세포의 자손인 유사분열된 또는 분화된 세포를 추가로 제공한다.
일 구현예에서, 본 개시내용은 본원에 기술된 방법에 의해 생성된 "선조 T 세포 (progenitor T cell)" 또는 "proT 세포"를 제공한다. 다른 구현예에서, 선조 T 세포는 인간 선조 T 세포, 예를 들어, CD34+CD7+ 또는 CD7+CD5+CD1a-를 특징으로 하는 인간 선조 T 세포이다.
다른 구현예에서, 선조 T 세포는 마우스 선조 T 세포, 예를 들어, CD25+를 특징으로 하는 마우스 선조 T 세포이다.
본 개시내용은 또한 CD4+CD8+ 또는 CD4+CD8+CD3+를 특징으로 하는 이중 양성 (DP) T-세포를 제공한다. 본 개시내용은 CD4-CD8+, CD4+CD8- 또는 CD8+CD3+, CD4+CD3+를 특징으로 하는 단일 양성 (SP) 세포인 T-세포 계통의 세포를 추가로 제공한다.
일 구현예에서, 본원에 기술된 방법에 의해 생성된 T 세포 계통의 세포 (예를 들어, 선조 T 세포 또는 성숙 T 세포)는 T 세포 수용체 (TCR) 또는 키메라 항원 수용체 (CAR)로 조작되어 종양 관련 항원 (TAA)에 대한 특이성을 부여한다. 이렇게 조작된 세포는 암과 같은 상태를 치료하는데 유용할 수 있다.
다른 양태에서, 본 개시내용은 본원에 기술된 방법에 의해 생성된 단리된 T 세포 계통의 세포 및 약제학적으로 허용가능한 희석제 또는 담체를 포함하는 약제학적 조성물을 제공한다.
적합한 희석제 및 담체는, 예를 들어, Remington's Pharmaceutical Sciences에 기술되어 있다. 이에 기초하여, 조성물은, 비록 독점적으로는 아니지만, 하나 이상의 약제학적으로 허용가능한 부형제 또는 희석제와 결합된 proT 세포의 용액을 포함하고, 적합한 pH를 가지며 생리학적 유체와 등장성인 완충 용액에 함유된다.
약제학적 조성물은, 제한 없이, 동결건조된 분말 또는 수성 또는 비수성 멸균 주사 용액 또는 현탁액을 포함하고, 이는 항산화제, 완충제, 정균제 (bacteriostats), 및 조성물이 의도된 수용자의 조직 또는 혈액과 실질적으로 호환되게 하는 용질을 추가로 포함할 수 있다. 이러한 조성물 내에 존재할 수 있는 다른 성분에는, 예를 들어, 물, 계면활성제 (예컨대, Tween™), 알코올, 폴리올, 글리세린 및 식물성유가 포함된다. 즉석 주사 용액 및 현탁액이 멸균 분말, 과립, 정제, 또는 농축 용액 또는 현탁액으로부터 제조될 수 있다. 조성물은, 예를 들어, 제한 없이, 환자에게 투여하기 전에 멸균수로 재구성되는, 동결건조된 분말로서 공급될 수 있다.
약제학적 조성물은 또한 동결보존제 (cyropreservative) 용액을 포함할 수 있다. 일 구현예에서, 본원에 기술된 방법에 의해 생성된 T 세포 계통의 세포는 적절한 배지, 예를 들어, 약제학적으로 허용가능하거나 또는 GMP-등급 배지 중에 동결보존되고 선택적으로 이를 필요로 하는 대상체로의 투여를 위해 제제화된다.
적합한 약제학적으로 허용가능한 담체는 본질적으로 약제학적 조성물의 생물학적 활성의 효능을 방해하지 않는 화학적으로 불활성 및 비독성 조성물을 포함한다. 적합한 약제학적 담체의 예시에는 물, 식염수 용액, 글리세롤 용액, 에탄올, N-(1(2,3-디올레일옥시)프로필)N,N,N-트리메틸암모늄 클로라이드 (DOTMA), 디올레일포스파티딜-에탄올아민 (diolesyl-phosphotidyl-ethanolamine) (DOPE), 및 리포좀이 포함되지만, 이들로 제한되지 않는다. 이러한 조성물은 환자에게 직접 투여하기 위한 형태를 제공하기 위해, 적합한 양의 담체와 함께, 치료학적 유효량의 화합물을 함유해야만 한다.
조성물은, 예를 들어, 비경구, 정맥내, 피하, 근육내, 두개내 (intracranial), 안와내 (intraorbital), 안과적 (ophthalimic), 심실내 (intraventricular), 관절낭내 (intracapsular), 척추내, 수조내 (intracisternal), 복강내, 비강내, 에어로졸 또는 경구 투여로 투여될 수 있다. 비경구 투여를 위해, 본원에 기술된 pro-T 세포의 용액이 히드록시프로필셀룰로스와 같은 계면활성제와 적절히 혼합된 물 중에 제조될 수 있다. 분산액이 또한 글리세롤, 액체 폴리에틸렌 글리콜, DMSA 및 알코올 존재 또는 부재의 이들의 혼합물 중, 및 오일 중에 제조될 수 있다. 일반적인 보관 및 사용 조건에서, 이러한 제제는 미생물의 성장을 방지하기 위한 방부제를 함유한다. 당업자는 적합한 제제를 제조하는 방법을 인지할 것이다.
바람직하게는, T 세포 계통의 세포는 이를 필요로 하는 대상체에서 질환 상태를 치료하는데 효과적인 양으로 존재한다. 일 구현예에서, T 세포 계통의 세포는 이를 필요로 하는 대상체에서 조혈 선조 세포 생착을 증강시키는데 효과적인 양으로 존재한다. 선택적으로, 조성물은 T 세포 계통의 세포, 또는 이식용 조직을 추가로 포함한다. 일 구현예에서, 조직은 흉선을 포함한다. 다른 구현예에서, 조직은 기관을 포함한다.
V. 치료적 응용
시험관 내-유래 인간 선조 T 세포를 생성하고 인간/마우스 면역 생착 모델에서 이의 안정성을 시험하는 능력은 T 계통의 면역-관련 장애를 치료하기 위한 세포 기반 접근법의 길을 열어준다 (Legrand et al., 2006; van den Brink et al., 2004). T 세포는 바이러스 및 박테리아 병원체를 인식하고 제거하는 적응 면역계의 주요 이펙터 아암 (effector arm)이다. T 세포 급성 림프모구성 백혈병 (acute lymphoblastic leukemia) (T-ALL)과 같은 특정 희귀 혈액암에서, T 세포는 증식하여, 건강한 면역 세포를 밀어내고 정상적인 면역 기능을 교란시킨다 (Ferrando et al., 2002; Weng et al., 2004). 화학요법이 종종 암 환자에게 치료적 이점을 제공할 수 있지만, 이는 자주 면역-결핍 및 기회 감염에 대한 감수성을 유발할 수 있다. 기회 감염은 HIV 감염 후 CD4+ T 세포가 고갈된 AIDS 환자에서 심각한 우려를 제기한다. 면역결핍은 HIV/AIDS 및 암에서 심각한 문제로 남아있지만, 면역-과다활동 (immune-hyperactivity)은 적절한 조절 제어가 없는 T 세포가 자가-조직에 대한 면역 반응을 생성하는 자가면역 질환에서 똑같이 문제가 된다.
따라서, 본 출원은 다음을 포함하는, T 세포의 수적 증가가 필요한 상태를 갖는 대상체를 치료하는 방법을 포함한다:
(i) (a) 줄기 세포 또는 선조 세포를 포함하는 샘플을, 선택적으로 입자 또는 마이크로비드인, 현탁 지지체에 접합된 Notch 리간드와 함께 배양하고, (b) T 세포 계통의 세포를 단리하는 것을 포함하는, T 세포 계통의 세포를 생성하는 단계, 및
(ii) T 세포 계통의 세포의 유효량을 이를 필요로 하는 대상체에 투여하는 단계.
일 구현예에서, T 세포 계통의 세포는 선조 T 세포이다.
다른 구현예에서, T 세포 계통의 세포는 성숙 T 세포이다.
본 개시내용은 또한 T 세포의 수적 증가를 필요로 하는 상태를 갖는 대상체를 치료하기 위한, 본원에 기술된 방법에 의해 생성된 T 세포 계통의 세포, 선택적으로 선조 T 세포 또는 성숙 T 세포의 용도를 제공한다.
본 개시내용은 또한 재생 의학을 위한, 예를 들어, 질병 또는 외상에 의해 영향을 받은 조직을 대체 및/또는 재생하기 위한, 본원에 기술된 방법에 의해 생성된 T 세포 계통의 세포, 선택적으로 선조 T 세포 또는 성숙 T 세포의 용도를 제공한다.
본원에 사용된 바와 같이, "유효량" 또는 "치료학적 유효량"이라는 문구는 원하는 결과를 달성하는데 필요한 투여량 및 기간 동안에 효과적인 양을 의미한다. 유효량은 대상체의 질환 상태, 연령, 성별, 체중과 같은 요인에 따라 달라질 수 있다. 그러한 양에 해당하는 소정의 세포 제제의 양은 다양한 인자에 따라, 예컨대 약제학적 제형, 투여 경로, 질환 또는 장애의 유형, 치료될 대상체 또는 숙주의 정체 등에 따라 달라질 것이지만, 그럼에도 불구하고 당업자에 의해 통상적으로 결정될 수 있다. "유효량"은 바람직하게는 T 세포 계통의 세포를 치료될 대상체에 생착시키는데 효과적인 양일 것이다.
본원에서 사용되고 당업계에서 잘 이해되는 바와 같이, 용어 "치료하는" 또는 "치료"는 임상 결과를 비롯한 유익하거나 또는 원하는 결과를 달성하기 위한 접근법을 의미한다. 유익하거나 또는 원하는 결과에는, 검출 가능 여부와 무관하게, 하나 이상의 증상 또는 상태의 완화 또는 개선, 질병 정도의 감소, 질병 상태의 안정화 (즉, 악화되지 않음), 질병의 확산 방지, 질병 진행의 지연 또는 둔화, 질병 상태의 개선 또는 완화, 질병 재발의 감소, 및 회복 (부분적이든 전체적이든)을 포함하지만, 이들로 제한되지 않는다. "치료하는" 및 "치료"는 또한 치료를 받지 않은 경우 예상되는 생존과 비교하여 연장된 생존을 의미할 수 있다. 본원에 사용된 바와 같이 "치료하는" 및 "치료"는 또한 예방적 치료를 포함한다.
본원에 사용된 바와 같이 용어 "대상체"는 동물계의 모든 구성원을 의미하고 바람직하게는 인간이다.
"T 세포의 수적 증가를 필요로 하는 상태"는 T 세포 수준이 건강한 동물에 비해 감소된 임의의 상태로, 제한 없이, 면역결핍, 암, 유전 질환 (예를 들어, 원발성 면역결핍 질환 (PIDs)), 감염 질환, 면역 장애 및 자가면역을 포함하는, 상태를 포함한다.
전술한 바와 같이, 본원에 기술된 T-세포 계통의 세포는 종양 관련 항원을 특이적으로 인식하는 T 세포 수용체 (TCRs) 또는 키메라 항원 수용체 (CARs)를 발현하도록 조작될 수 있다.
따라서, 본 출원은 또한 다음을 포함하는, 대상체에서 암을 치료하는 방법을 포함한다:
(i) (a) 줄기 세포 또는 선조 세포를 포함하는 샘플을 현탁 지지체, 선택적으로 입자 또는 마이크로비드에 접합된 Notch 리간드와 배양하고, (b) T 세포 계통의 세포를 단리하는 것을 포함하는, T 세포 계통의 세포를 생성하는 단계, 및
(ii) 이를 필요로 하는 대상체에 유효량의 T 세포 계통의 세포를 투여하는 단계,
여기서, T 세포 계통의 세포는 T 세포 수용체 (TCR) 또는 키메라 항원 수용체 (CAR)로 조작되어 종양-관련 항원에 대한 특이성을 부여한다.
본 개시내용은 또한 암을 갖는 대상체를 치료하기 위한, 본원에 기술된 방법에 의해 생성된 T 세포 계통의 세포, 선택적으로 선조 T 세포 또는 성숙 T 세포의 용도를 제공하고, 여기서 T 세포 계통의 세포는 T 세포 수용체 (TCR) 또는 키메라 항원 수용체 (CAR)로 조작되어 종양-관련 항원에 대한 특이성을 부여한다. 선택적으로, iPSCs는 공지 또는 미지의 TCR 특이성을 갖는 T 세포 (예를 들어, 암에 대한 특이성을 갖는 TCR을 보유하는 T 세포)로부터 유래할 수 있고, 그 후에 이들 T-iPSCs는 본원에 기술된 방법에 의해 T 세포를 생성하는데 사용될 수 있다.
이하에서는 본 발명의 구현예가 도면과 관련하여 설명될 것이다:
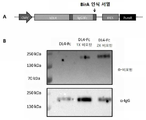
도 1은 DL4-Fc 컨스트럭트의 설계 및 비오틴화를 나타낸다. A) DL4-Fc 융합 컨스트럭트를 그의 인간 DL4의 세포외 도메인의 성분, 정제 목적 및 인간 IgG3의 Fc 영역 (IgG3Fc)으로 도시한다. B) 비-환원 조건에서 항-비오틴 (상부) 및 항-인간 IgG (하부)를 사용하는 화학적으로 비오틴화된 DL4-Fc의 웨스턴 블롯 분석.
도 2는 1 세대 DL4-μ비드에 의한 Notch 수용체 세포의 활성화를 나타낸다. A) 화학적으로 비오틴화된 DL4-Fc 단백질을 SA-코팅된 비드에 접합시켜, 50 nm 금 나노입자 (GNP) 내지 100 μm μ비드 범위의 무작위-배향된 (randomly-oriented) 1 세대 DL4-μ비드를 형성하였다. B) 3×104 3T3-N1Cluc 세포를 음성 대조군으로서 hIgG 또는 지시된 바와 같은 상이한 농도의 DL4-Fc로 전처리된 플레이트 상에서 인큐베이션하였다. 대안적으로, 세포를 비처리 플레이트 상에서 상이한 수의 DL4-μ비드와 함께 인큐베이션하였다. 각 조건에서의 비드 수는 전체적으로 동일한 표면적, 및 따라서 동일한 총 수의 DL4-Fc 분자를 표시하였다. 도말 24시간 후, 세포를 용해시키고 루시퍼라제 활성에 대해 분석하였다.
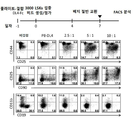
도 3은 1 세대 DL4-μ비드를 사용한 마우스 HSCs로부터 T 세포 발생의 유도를 보여준다. 마우스 태아 간 유래 HSPCs를 7일간 FBS, SCF, IL-7 및 Flt3-L을 함유하는 배지 중에서 비접합 μ비드 또는 DL4-μ비드와 함께 인큐베이션하였다. 공동-배양물을 수확하고 유세포 분석을 사용하여 T-계통 (CD25+), B-계통 (CD19+), 또는 골수성 (CD11b+) 세포의 존재에 대해 분석하였다. 플롯 내 숫자는 각 사분면 내의 세포 비율을 나타낸다.
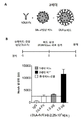
도 4는 DL4-Fc의 부위-특이적 비오틴화를 나타낸다. A) DL4-Fc 융합 컨스트럭트를 그의 C-말단에 BirA 인식 서열 (AviTagTM)을 포함하도록 재설계하였고 여기에 비오틴 모이어티가 효소 BirA에 의해 접합될 수 있다. B) 환원 조건에서 항-인간 IgG (상부) 및 항-비오틴 (하부)을 사용하는 화학적으로 비오틴화된 DL4-Fc의 웨스턴 블롯 분석.
도 5는 Notch를 활성화하기 위한 1 및 2 세대 DL4-μ비드의 차등적 능력을 보여준다. A) BirA-비오틴화된 DL4-Fc 단백질을 SA-코팅된 비드에 접합시켜 방향 지향성 (directionally oriented) 2 세대 DL4-μ비드를 형성하였다. B) 3×104 3T3-N1Cluc 세포를 IgG- 또는 DL4-Fc 플레이트-결합된 대조군 상에서 또는 1 또는 2 세대 DL4-μ비드 (25 μm)와 함께 인큐베이션하였다. 도말 24시간 후, 세포를 용해시키고 루시퍼라제 활성에 대해 분석하였다.
도 6은 Notch 활성화에 미치는 μ비드 크기의 영향에 대한 평가를 보여준다. 6.5 μm 내지 100 μm 크기 범위의 DL4-μ비드를 3×104 3T3-N1Cluc 세포와 함께 밤새 인큐베이션하였다. 플레이트-결합된 (PB) IgG 및 DL4-Fc를 각각 음성 및 양성 대조군으로 포함시켰다. 각 조건에서 비드의 수는 전체적으로 동일한 표면적, 및 따라서 DL4-Fc 분자의 동일한 총 수를 나타내었다. 도말 24시간 후, 세포를 용해시키고 루시퍼라제 활성에 대해 분석하였다.
도 7은 μ비드의 다양한 농도 및 상이한 조성에서 DL4-Fc에 의해 유도된 Notch 활성화를 나타낸다. A) 증가하는 양의 DL4-Fc를 일정한 수의 25 μm 직경의 SA-코팅된 μ비드에 접합시켜 DL4-μ비드를 제조하였다. 25 μm 직경의 자성 μ비드를 포함시켜 μ비드의 코어 조성을 변경하는 효과가 Notch를 활성화하는 이들의 능력에 미치는 영향을 평가하였다. B) 비오틴화된 DL4-Fc를 동일한 크기의 SA-μ비드 또는 단백질-G-μ비드에 결합시켜 Fc 영역에의 결합이 Notch를 활성화하는데 동일하게 효과적인지 여부를 결정하였다. DL4-μ비드를 3×104 3T3-N1Cluc 세포와 함께 밤새 인큐베이션하였다. 플레이트-결합된 IgG를 음성 대조군으로 포함시켰다. 도말 24시간 후, 세포를 용해시키고 루시퍼라제 활성에 대해 분석하였다.
도 8은 2 세대 DL4-μ비드를 사용한 마우스 HSPCs로부터의 T 세포 발생의 유도를 보여준다. 1×103, 3×103 또는 8×103 마우스 태아 간 유래 HSPCs를 FBS, SCF, IL-7 및 Flt3-L을 함유하는 배지 중에서 10:1 (비드:세포)의 비율로 비접합 μ비드 또는 DL4-μ비드와 함께 7일간 인큐베이션하였다. 공동-배양물을 수확하고 유세포 분석을 사용하여 T-계통 (CD25+), B-계통 (CD19+), 또는 골수성 (CD11b+) 세포의 존재에 대해 분석하였다. 플롯 내 숫자는 각 사분면 내의 세포 비율을 나타낸다.
도 9는 HSPC 대 DL4-μ비드 비율의 최적화를 나타낸다. 마우스 태아 간 유래 HSPCs를 다음 조건에서 7일간 배양하였다: 비접합 μ비드, 플레이트-결합된 DL4-Fc (PB-DL4), 또는 DL4-μ비드의 3배 적정. 배양물을 유세포 분석을 사용하여 CD11b+ 골수성 및 CD19+ B-계통 세포의 억제 및 proT (CD90+ CD25+) 세포의 출현에 대해 분석하였다.
도 10은 DL4-μ비드와 함께 공동-배양된 HSPCs로부터 인간 T-계통 세포의 발생 진행을 보여준다. A) 인간 제대혈-유래 CD34+ 세포를 StemSpanTM T 세포 선조체 확장 보충제가 보충된 StemSpanTMSFEM II 중에서 비접합 μ비드, 플레이트-결합된 DL4-Fc 또는 DL4-μ비드와 함께 14일간 배양하였다. 2일마다 (화살촉) 세포를 수확하고 유세포 분석을 사용하여 CD34, CD5, CD1a 및 CD7의 표면 발현에 대해 분석하였다. B) 세포를 또한 계수하여 총 세포 확장을 평가하였다. 지정된 날짜의 총 계수를 0일째 배양 시작 시 초기 접종 양으로 나누어 배수 확장을 계산하였다.
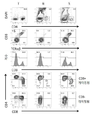
도 11은 DL4-μ비드로 생성된 성숙 인간 T 세포의 존재에 대한 분석을 보여준다. 인간 제대혈-유래 CD34+ 세포를 StemSpanTM T 세포 선조체 확장 보충제가 보충된 StemSpanTMSFEM II 중에서 DL4-μ비드와 함께 배양하였다. 28일 및 47일째에, 세포를 수확하고 CD34, CD5, CD1a, CD4, CD8 및 CD3의 표면 발현에 대해 분석하였다. 화살표로 표시된 바와 같이, CD3의 공동-발현이 SP-게이팅된 (SP-gated) 세포, DP-게이팅된 세포 또는 DN-게이팅된 세포 중 하나에서 나타난다.
도 12는 DL4-μ비드가 G-CSF 및 플레릭사포르 (PLX) 동원된 (mobilized) 말초 혈액 (mPB) 유래의 CD34 + 세포로부터 T 세포의 발생을 유도함을 보여준다. G-CSF 및 PLX로 5일간 처리된, 제대혈 및 성인 인간 (n=3)으로부터 유래하는, 3×103 CD34+ 세포를 9,000 DL4-μ비드와 함께 인큐베이션하였다. A) T 세포 발생으로의 진행을 14일째에 유세포 분석을 사용하여 세포 표면 마커 CD5, CD7 및 CD34의 발현에 대해 분석하였다. B) 세포 계수를 혈구계를 사용하여 14일째에 수행하였고 배수 확장을 출발 세포 수를 기준으로 계산하였다. 제대혈 (CB)을 사용한 확장률을 비교군 (comparator)으로 사용하였다.
도 13은 DL4-μ비드를 사용한 유도 만능 줄기 세포 (iPSCs)로부터 T 세포 생성의 초기 및 후기 유도를 보여준다. 인간 iPSCs를 먼저 유도하여 중배엽 운명으로 분화시킨 후 CD34+ 조혈-전 (pre-hematopoietic) 운명으로 분화시켰다. (A) 3×103 MACS-풍부 CD34+ 세포를 27×103 DL4-μ비드와 함께 인큐베이션하고 T 세포 발생으로의 이들의 진행을 유세포 분석을 사용하여 CD5, CD7 및 CD34의 표면 세포 발현에 대해 6, 8, 10, 및 12일째에 분석하였다. B) D14, D28 및 D35로부터의 배양물을 CD3뿐만 아니라 T 세포 공동-수용체 CD4 및 CD8에 대한 세포 표면 마커를 사용하여 성숙 T 세포의 존재에 대해 분석하였다. 역 삼각형은 분석 일자를 나타낸다. RCN; 상대적 세포 수.
도 14는 T 세포-유래 iPSCs (T-iPSC)로부터 T 세포 생성의 초기 및 후기 유도를 보여준다. T-iPSCs를 중배엽으로 유도한 후 조혈-전 운명으로 유도하였다. 3×103 MACS-풍부 CD34+ 세포를 27×103 DL4-μ비드와 함께 인큐베이션하고 T 세포 발생으로의 이들의 진행을 유세포 분석으로 12일 (D12) 및 24일째 (D24)에 CD5, CD7 (초기 T 세포 발생) 및 CD4, CD8, CD3 및 TCRαβ (후기 T 세포 발생)의 세포 표면 발현에 대해 분석하였다.
도 15는 재조합 VCAM1-Fc의 비오틴화를 나타낸다. VCAM-1 세포외 도메인, IgG3 Fc 도메인 및 Avi-태그 비오틴화 부위로 구성되는 재조합 VCAM1-Fc를 DL4-Fc와 유사하게 유전적으로 조작하였다. VCAM1-Fc가 HEK293T 세포에서 발현되었고, 배지 내로 분비된 후 단백질 G 접합 비드를 사용하여 정제되고 BirA 효소를 사용하여 시험관 내에서 비오틴화되었다. R&D Systems (R&D)에서 시판중인 상업적으로 이용가능한 VCAM1-Fc, 실험실-정제된 VCAM1-Fc (-Fc) 및 시험관 내-비오틴화된 VCAM1-Fc (비오틴)로부터의 샘플을 폴리아크릴아미드 겔에서 전기영동하였다. 웨스턴 면역블롯 분석을 사용하여, A) VCAM-Fc 샘플의 크기 및 농도를 항-VCAM-1 항체와 서로 비교하고 B) 비오틴화된 단백질의 존재를 항-비오틴 항체를 사용해 검출하였다.
도 16은 인간 T 세포 발생에 대한 VCAM-1 및 DL4의 화합물 효과를 보여준다. 비오틴화된 VCAM1-Fc (VCAM)를 지시된 바와 같이, DL4-Fc (DL4)와 함께 상이한 비율로 μ비드에 결합시키고, 비접합 μ비드 (UN) 및 DL4-μ비드와 비교하였다. DL4-Fc 양을 1 μg/ 2×105 SA-μ비드로 일정하게 유지하면서, VCAM-Fc를 0.01 μg (100:1의 경우), 0.1 μg (10:1의 경우), 1 μg (1:1의 경우) 및 10 μg (1:10의 경우)으로 첨가하였다. 그 후에 DL4:VCAM1-μ비드를 3×103 CB-유래 CD34+ 세포와 함께 인큐베이션하고 CD34, CD7 및 CD5 세포 표면 마커를 사용한 T 세포 발생의 진행에 대해 D7에서 분석하였다.
도 17은 면역결핍 NOD - SCID IL2rγ null (NSG) 마우스의 흉선 내로 선조 T (proT) 세포의 생착을 보여준다. 인간 CB로부터 유래한 CD34+ 세포를 7일간 DL4-μ비드와 함께 인큐베이션하였다. CD34+ CD7+ 선조 T (proT) 세포를 유세포 분석을 사용하여 분류하고 3×105개를 면역결핍 NSG 마우스 내로 정맥 내 주사하였다. 지시된 바와 같이, IL-7 주사 부스터 (injection boosts)를 3-4일 간격으로 제공하였다. 3주 후, 흉선을 수확하고 가공하였다. 유세포 분석 후, 살아있는 (DAPI-) 인간 조혈 세포 (CD45+)를 확인하였다. 또한, 세포 표면 마커 CD19 (B 세포), CD33 (골수성 세포), CD3, CD4 및 CD8 (T 세포)를 사용하여 전자적으로-게이팅된 (electronically-gated) 살아있는 CD45+ 세포에 대해 계통 분석을 수행하였다.
도 18은 proT 세포의 흉선 내로의 생착 및 골수 및 2차 림프 기관인 비장으로의 이들의 후속 이동을 보여준다. D7에 CB-HSPC/DL4-μ비드 배양물로부터 분류된, ProT 세포를 NSG 마우스 내로 주사하였다. 주사 12주 후, 흉선 (T), 골수 (BM) 및 비장 (S)을 수확하고 유세포 분석을 사용하여 CD45+ 인간 조혈 세포의 생착을 평가하기 위해 가공하였다 (상부 패널). 인간 CD45+ 세포를 전자적으로 게이팅시켜, 성숙 T 세포의 존재를 지시된 바와 같이 각 기관에 대해 세포 표면 마커 CD3, CD4, CD8 및 TCRαβ를 사용하여 결정하였다.
도 19는 세포 성분으로부터 자성 DL4-μ비드의 분리를 보여준다. 2×105 CD34+ CB-유래 HSPCs를 T25 플라스크 내에서 1.8×106 산화철-코팅된 DL4-μ비드와 함께 배양하였다. A) 배양 5일째에, CD34+ CD7+ proT 세포의 비율을 결정하였다. B) 그 후에 배양물을 자화된 (magnetized) 입자가 비-결합 세포 성분으로부터 분리되는 AutoMACS-매개 분리에 적용하였다. 음성 분획은 기기의 자화된 프로브에 결합하지 않은 성분을 나타낸다. 양성은 결합된 분획이다. 각 분획에 대해, 그의 비드 및 세포 함량을 계수하고 혈구계를 사용하여 원래 혼합물 (Pre-sort)과 비교하였다. 세포는 각 분획에 대해 좌측 막대에 표시되고 비드는 우측 막대 상에 표시된다.
도 1은 DL4-Fc 컨스트럭트의 설계 및 비오틴화를 나타낸다. A) DL4-Fc 융합 컨스트럭트를 그의 인간 DL4의 세포외 도메인의 성분, 정제 목적 및 인간 IgG3의 Fc 영역 (IgG3Fc)으로 도시한다. B) 비-환원 조건에서 항-비오틴 (상부) 및 항-인간 IgG (하부)를 사용하는 화학적으로 비오틴화된 DL4-Fc의 웨스턴 블롯 분석.
도 2는 1 세대 DL4-μ비드에 의한 Notch 수용체 세포의 활성화를 나타낸다. A) 화학적으로 비오틴화된 DL4-Fc 단백질을 SA-코팅된 비드에 접합시켜, 50 nm 금 나노입자 (GNP) 내지 100 μm μ비드 범위의 무작위-배향된 (randomly-oriented) 1 세대 DL4-μ비드를 형성하였다. B) 3×104 3T3-N1Cluc 세포를 음성 대조군으로서 hIgG 또는 지시된 바와 같은 상이한 농도의 DL4-Fc로 전처리된 플레이트 상에서 인큐베이션하였다. 대안적으로, 세포를 비처리 플레이트 상에서 상이한 수의 DL4-μ비드와 함께 인큐베이션하였다. 각 조건에서의 비드 수는 전체적으로 동일한 표면적, 및 따라서 동일한 총 수의 DL4-Fc 분자를 표시하였다. 도말 24시간 후, 세포를 용해시키고 루시퍼라제 활성에 대해 분석하였다.
도 3은 1 세대 DL4-μ비드를 사용한 마우스 HSCs로부터 T 세포 발생의 유도를 보여준다. 마우스 태아 간 유래 HSPCs를 7일간 FBS, SCF, IL-7 및 Flt3-L을 함유하는 배지 중에서 비접합 μ비드 또는 DL4-μ비드와 함께 인큐베이션하였다. 공동-배양물을 수확하고 유세포 분석을 사용하여 T-계통 (CD25+), B-계통 (CD19+), 또는 골수성 (CD11b+) 세포의 존재에 대해 분석하였다. 플롯 내 숫자는 각 사분면 내의 세포 비율을 나타낸다.
도 4는 DL4-Fc의 부위-특이적 비오틴화를 나타낸다. A) DL4-Fc 융합 컨스트럭트를 그의 C-말단에 BirA 인식 서열 (AviTagTM)을 포함하도록 재설계하였고 여기에 비오틴 모이어티가 효소 BirA에 의해 접합될 수 있다. B) 환원 조건에서 항-인간 IgG (상부) 및 항-비오틴 (하부)을 사용하는 화학적으로 비오틴화된 DL4-Fc의 웨스턴 블롯 분석.
도 5는 Notch를 활성화하기 위한 1 및 2 세대 DL4-μ비드의 차등적 능력을 보여준다. A) BirA-비오틴화된 DL4-Fc 단백질을 SA-코팅된 비드에 접합시켜 방향 지향성 (directionally oriented) 2 세대 DL4-μ비드를 형성하였다. B) 3×104 3T3-N1Cluc 세포를 IgG- 또는 DL4-Fc 플레이트-결합된 대조군 상에서 또는 1 또는 2 세대 DL4-μ비드 (25 μm)와 함께 인큐베이션하였다. 도말 24시간 후, 세포를 용해시키고 루시퍼라제 활성에 대해 분석하였다.
도 6은 Notch 활성화에 미치는 μ비드 크기의 영향에 대한 평가를 보여준다. 6.5 μm 내지 100 μm 크기 범위의 DL4-μ비드를 3×104 3T3-N1Cluc 세포와 함께 밤새 인큐베이션하였다. 플레이트-결합된 (PB) IgG 및 DL4-Fc를 각각 음성 및 양성 대조군으로 포함시켰다. 각 조건에서 비드의 수는 전체적으로 동일한 표면적, 및 따라서 DL4-Fc 분자의 동일한 총 수를 나타내었다. 도말 24시간 후, 세포를 용해시키고 루시퍼라제 활성에 대해 분석하였다.
도 7은 μ비드의 다양한 농도 및 상이한 조성에서 DL4-Fc에 의해 유도된 Notch 활성화를 나타낸다. A) 증가하는 양의 DL4-Fc를 일정한 수의 25 μm 직경의 SA-코팅된 μ비드에 접합시켜 DL4-μ비드를 제조하였다. 25 μm 직경의 자성 μ비드를 포함시켜 μ비드의 코어 조성을 변경하는 효과가 Notch를 활성화하는 이들의 능력에 미치는 영향을 평가하였다. B) 비오틴화된 DL4-Fc를 동일한 크기의 SA-μ비드 또는 단백질-G-μ비드에 결합시켜 Fc 영역에의 결합이 Notch를 활성화하는데 동일하게 효과적인지 여부를 결정하였다. DL4-μ비드를 3×104 3T3-N1Cluc 세포와 함께 밤새 인큐베이션하였다. 플레이트-결합된 IgG를 음성 대조군으로 포함시켰다. 도말 24시간 후, 세포를 용해시키고 루시퍼라제 활성에 대해 분석하였다.
도 8은 2 세대 DL4-μ비드를 사용한 마우스 HSPCs로부터의 T 세포 발생의 유도를 보여준다. 1×103, 3×103 또는 8×103 마우스 태아 간 유래 HSPCs를 FBS, SCF, IL-7 및 Flt3-L을 함유하는 배지 중에서 10:1 (비드:세포)의 비율로 비접합 μ비드 또는 DL4-μ비드와 함께 7일간 인큐베이션하였다. 공동-배양물을 수확하고 유세포 분석을 사용하여 T-계통 (CD25+), B-계통 (CD19+), 또는 골수성 (CD11b+) 세포의 존재에 대해 분석하였다. 플롯 내 숫자는 각 사분면 내의 세포 비율을 나타낸다.
도 9는 HSPC 대 DL4-μ비드 비율의 최적화를 나타낸다. 마우스 태아 간 유래 HSPCs를 다음 조건에서 7일간 배양하였다: 비접합 μ비드, 플레이트-결합된 DL4-Fc (PB-DL4), 또는 DL4-μ비드의 3배 적정. 배양물을 유세포 분석을 사용하여 CD11b+ 골수성 및 CD19+ B-계통 세포의 억제 및 proT (CD90+ CD25+) 세포의 출현에 대해 분석하였다.
도 10은 DL4-μ비드와 함께 공동-배양된 HSPCs로부터 인간 T-계통 세포의 발생 진행을 보여준다. A) 인간 제대혈-유래 CD34+ 세포를 StemSpanTM T 세포 선조체 확장 보충제가 보충된 StemSpanTMSFEM II 중에서 비접합 μ비드, 플레이트-결합된 DL4-Fc 또는 DL4-μ비드와 함께 14일간 배양하였다. 2일마다 (화살촉) 세포를 수확하고 유세포 분석을 사용하여 CD34, CD5, CD1a 및 CD7의 표면 발현에 대해 분석하였다. B) 세포를 또한 계수하여 총 세포 확장을 평가하였다. 지정된 날짜의 총 계수를 0일째 배양 시작 시 초기 접종 양으로 나누어 배수 확장을 계산하였다.
도 11은 DL4-μ비드로 생성된 성숙 인간 T 세포의 존재에 대한 분석을 보여준다. 인간 제대혈-유래 CD34+ 세포를 StemSpanTM T 세포 선조체 확장 보충제가 보충된 StemSpanTMSFEM II 중에서 DL4-μ비드와 함께 배양하였다. 28일 및 47일째에, 세포를 수확하고 CD34, CD5, CD1a, CD4, CD8 및 CD3의 표면 발현에 대해 분석하였다. 화살표로 표시된 바와 같이, CD3의 공동-발현이 SP-게이팅된 (SP-gated) 세포, DP-게이팅된 세포 또는 DN-게이팅된 세포 중 하나에서 나타난다.
도 12는 DL4-μ비드가 G-CSF 및 플레릭사포르 (PLX) 동원된 (mobilized) 말초 혈액 (mPB) 유래의 CD34 + 세포로부터 T 세포의 발생을 유도함을 보여준다. G-CSF 및 PLX로 5일간 처리된, 제대혈 및 성인 인간 (n=3)으로부터 유래하는, 3×103 CD34+ 세포를 9,000 DL4-μ비드와 함께 인큐베이션하였다. A) T 세포 발생으로의 진행을 14일째에 유세포 분석을 사용하여 세포 표면 마커 CD5, CD7 및 CD34의 발현에 대해 분석하였다. B) 세포 계수를 혈구계를 사용하여 14일째에 수행하였고 배수 확장을 출발 세포 수를 기준으로 계산하였다. 제대혈 (CB)을 사용한 확장률을 비교군 (comparator)으로 사용하였다.
도 13은 DL4-μ비드를 사용한 유도 만능 줄기 세포 (iPSCs)로부터 T 세포 생성의 초기 및 후기 유도를 보여준다. 인간 iPSCs를 먼저 유도하여 중배엽 운명으로 분화시킨 후 CD34+ 조혈-전 (pre-hematopoietic) 운명으로 분화시켰다. (A) 3×103 MACS-풍부 CD34+ 세포를 27×103 DL4-μ비드와 함께 인큐베이션하고 T 세포 발생으로의 이들의 진행을 유세포 분석을 사용하여 CD5, CD7 및 CD34의 표면 세포 발현에 대해 6, 8, 10, 및 12일째에 분석하였다. B) D14, D28 및 D35로부터의 배양물을 CD3뿐만 아니라 T 세포 공동-수용체 CD4 및 CD8에 대한 세포 표면 마커를 사용하여 성숙 T 세포의 존재에 대해 분석하였다. 역 삼각형은 분석 일자를 나타낸다. RCN; 상대적 세포 수.
도 14는 T 세포-유래 iPSCs (T-iPSC)로부터 T 세포 생성의 초기 및 후기 유도를 보여준다. T-iPSCs를 중배엽으로 유도한 후 조혈-전 운명으로 유도하였다. 3×103 MACS-풍부 CD34+ 세포를 27×103 DL4-μ비드와 함께 인큐베이션하고 T 세포 발생으로의 이들의 진행을 유세포 분석으로 12일 (D12) 및 24일째 (D24)에 CD5, CD7 (초기 T 세포 발생) 및 CD4, CD8, CD3 및 TCRαβ (후기 T 세포 발생)의 세포 표면 발현에 대해 분석하였다.
도 15는 재조합 VCAM1-Fc의 비오틴화를 나타낸다. VCAM-1 세포외 도메인, IgG3 Fc 도메인 및 Avi-태그 비오틴화 부위로 구성되는 재조합 VCAM1-Fc를 DL4-Fc와 유사하게 유전적으로 조작하였다. VCAM1-Fc가 HEK293T 세포에서 발현되었고, 배지 내로 분비된 후 단백질 G 접합 비드를 사용하여 정제되고 BirA 효소를 사용하여 시험관 내에서 비오틴화되었다. R&D Systems (R&D)에서 시판중인 상업적으로 이용가능한 VCAM1-Fc, 실험실-정제된 VCAM1-Fc (-Fc) 및 시험관 내-비오틴화된 VCAM1-Fc (비오틴)로부터의 샘플을 폴리아크릴아미드 겔에서 전기영동하였다. 웨스턴 면역블롯 분석을 사용하여, A) VCAM-Fc 샘플의 크기 및 농도를 항-VCAM-1 항체와 서로 비교하고 B) 비오틴화된 단백질의 존재를 항-비오틴 항체를 사용해 검출하였다.
도 16은 인간 T 세포 발생에 대한 VCAM-1 및 DL4의 화합물 효과를 보여준다. 비오틴화된 VCAM1-Fc (VCAM)를 지시된 바와 같이, DL4-Fc (DL4)와 함께 상이한 비율로 μ비드에 결합시키고, 비접합 μ비드 (UN) 및 DL4-μ비드와 비교하였다. DL4-Fc 양을 1 μg/ 2×105 SA-μ비드로 일정하게 유지하면서, VCAM-Fc를 0.01 μg (100:1의 경우), 0.1 μg (10:1의 경우), 1 μg (1:1의 경우) 및 10 μg (1:10의 경우)으로 첨가하였다. 그 후에 DL4:VCAM1-μ비드를 3×103 CB-유래 CD34+ 세포와 함께 인큐베이션하고 CD34, CD7 및 CD5 세포 표면 마커를 사용한 T 세포 발생의 진행에 대해 D7에서 분석하였다.
도 17은 면역결핍 NOD - SCID IL2rγ null (NSG) 마우스의 흉선 내로 선조 T (proT) 세포의 생착을 보여준다. 인간 CB로부터 유래한 CD34+ 세포를 7일간 DL4-μ비드와 함께 인큐베이션하였다. CD34+ CD7+ 선조 T (proT) 세포를 유세포 분석을 사용하여 분류하고 3×105개를 면역결핍 NSG 마우스 내로 정맥 내 주사하였다. 지시된 바와 같이, IL-7 주사 부스터 (injection boosts)를 3-4일 간격으로 제공하였다. 3주 후, 흉선을 수확하고 가공하였다. 유세포 분석 후, 살아있는 (DAPI-) 인간 조혈 세포 (CD45+)를 확인하였다. 또한, 세포 표면 마커 CD19 (B 세포), CD33 (골수성 세포), CD3, CD4 및 CD8 (T 세포)를 사용하여 전자적으로-게이팅된 (electronically-gated) 살아있는 CD45+ 세포에 대해 계통 분석을 수행하였다.
도 18은 proT 세포의 흉선 내로의 생착 및 골수 및 2차 림프 기관인 비장으로의 이들의 후속 이동을 보여준다. D7에 CB-HSPC/DL4-μ비드 배양물로부터 분류된, ProT 세포를 NSG 마우스 내로 주사하였다. 주사 12주 후, 흉선 (T), 골수 (BM) 및 비장 (S)을 수확하고 유세포 분석을 사용하여 CD45+ 인간 조혈 세포의 생착을 평가하기 위해 가공하였다 (상부 패널). 인간 CD45+ 세포를 전자적으로 게이팅시켜, 성숙 T 세포의 존재를 지시된 바와 같이 각 기관에 대해 세포 표면 마커 CD3, CD4, CD8 및 TCRαβ를 사용하여 결정하였다.
도 19는 세포 성분으로부터 자성 DL4-μ비드의 분리를 보여준다. 2×105 CD34+ CB-유래 HSPCs를 T25 플라스크 내에서 1.8×106 산화철-코팅된 DL4-μ비드와 함께 배양하였다. A) 배양 5일째에, CD34+ CD7+ proT 세포의 비율을 결정하였다. B) 그 후에 배양물을 자화된 (magnetized) 입자가 비-결합 세포 성분으로부터 분리되는 AutoMACS-매개 분리에 적용하였다. 음성 분획은 기기의 자화된 프로브에 결합하지 않은 성분을 나타낸다. 양성은 결합된 분획이다. 각 분획에 대해, 그의 비드 및 세포 함량을 계수하고 혈구계를 사용하여 원래 혼합물 (Pre-sort)과 비교하였다. 세포는 각 분획에 대해 좌측 막대에 표시되고 비드는 우측 막대 상에 표시된다.
다음의 비-제한적인 예시는 본 출원을 설명한다:
실시예
실시예 1
재료 및 방법:
조혈 줄기 세포 공급원
인간 제대혈 (UCB) 샘플을 Research Ethics Board of Sunnybrook Health Sciences Centre에서 확립한 승인된 지침에 따라 분만 후 동의한 산모로부터 주사기 추출로 채취하고 시트레이트 포스페이트 항-응고제 (Baxter Healthcare, Deerfield, Illinois)를 함유하는 혈액-팩 유닛에 수집하였다. 수집 24시간 이내에, Ficoll 밀도 원심분리를 사용하여 UCB 단핵 세포를 단리하고, 제조사의 지침에 따라서 EasySep 인간 CD34 양성 선별 키트 (Stemcell Technologies, Vancouver, B.C.)를 사용하여 계통 음성 (Lin-) CD34+ 세포에 대해 사전-농축하였다. 인간 HSPCs를 단리하기 위해, Lin- 세포를 항-인간 CD38-APC 및 항-인간 CD34-PE mAbs로 염색하고 BD Biosciences FACSAria 분류기 (BD, San Jose, CA)를 사용하여 CD34+CD38-/lo 세포에 대해 분류하였다. 분류된 인간 HSPCs는 분류-후 분석에 의해 결정되는 바와 같이 99% 초과의 순도를 나타내었다. 제대혈로부터 유래한 일부 CD34+ 세포 및 동원된 말초 혈액 (mPB)으로부터 유래한 모든 CD34+ 세포는 Stemcell Technologies로부터 구입하였다. mPB의 경우, 지원자는 G-CSF (수집 전 3-5일간 최대 10 μg/kg/일의 G-CSF) 및 플레릭사포르 (Plerixafor) (수집 1일 전 최대 0.24 mg/kg)의 조합으로 처리되었다.
DL4-Fc 설계 및 생산
히스티딘 (His) 태그에 인간 DLL4 (아미노산 잔기 [aa] 1-529)의 세포외 도메인의 코딩 서열을 융합시키고 이어서 링커 서열에 의해 간격을 둔 C-말단에 Bir1A 인식 서열 (AvitagTM)과 함께 인간 IgG3의 Fc 부분 (힌지 영역 포함)을 융합시켜 델타-유사-4를 pDL4-Fc-His-B 플라스미드 컨스트럭트 내로 유전적으로 조작하였다. 이들 방법에 사용될 수 있는 다른 컨스트럭트는 i) IgG1의 Fc 부분에 융합된 인간 DLL4 (aa 1-524), ii) 알칼라인 포스파타제에 대한 신호 서열 (aa 1-17) IgG1의 Fc 부분에 융합된 인간 DLL4 (aa 27-524); iii) C-말단에서 StreptagII 및 6xHis에 융합된 인간 DLL4 (aa 1-524); iv) 알칼라인 포스파타제에 대한 신호 서열 (aa 1-17) C-말단에서 10× His에 융합된 인간 DLL4 (aa 27-524) 및 이들의 임의의 조합을 포함한다. 본 발명의 컨스트럭트를 pIRESpuro2 포유류 발현 플라스미드 (Clontech, Mountainview, CA) 내로 삽입하였다. 결과 플라스미드를 표준 CaPO4 형질감염 방법을 사용하여 HEK-293T 세포 내로 형질감염시키고 안정적으로 통합된 플라스미드를 갖는 세포를 표준 DMEM [10%(v/v) FBS, 2 mM 글루타맥스 (Glutamax), 페니실린 (100 U/ml)/스트렙토마이신 (100 mg/ml) (모두 Rockford, IL 소재 Thermo Fisher Scientific의 제품), 2 mM 2-머캅토에탄올 (Sigma-Aldrich, St. Louis, MI)가 보충됨]에 첨가된 2 mg/ml의 퓨로마이신에 대한 이들의 내성을 기준으로 선별하였다. 세포를 확장시키고 Freestyle 293 발현 배지 (Thermo Fisher Scientific)로 이동하여 성장시켰다. 배지 내로 분비된 DL4-Fc 융합 단백질을 AKTAprime 플러스 (GE Healthcare) 자동화 크로마토그래피 시스템에 부착된 HiTrap 단백질 G 친화 칼럼 (GE Healthcare Life Sciences, Marlborough, MA)을 사용하여 정제하였다.
VCAM1-Fc 설계 및 생산
재조합 VCAM1-Fc를 DL4-Fc와 유사하게 VCAM-1 세포외 도메인, IgG3 Fc 도메인 및 AvitagTM 비오틴화 부위를 포함하도록 유전적으로 조작하였다. VCAM1-Fc 융합 단백질의 제작 및 정제에 사용되는 재료 및 방법은 상기에 기술된 DL4-Fc 융합 단백질과 동일하였다.
DL4-Fc 및 VCAM1-Fc의 비오틴화
NHS-활성화 비오틴을 DL4-Fc 분자당 2개 비오틴 분자를 달성하도록 최적화된 몰비로 정제된 DL4-Fc에 첨가하였다. 비-반응 NHS-비오틴을 PBS 중의 투석 또는 완충제 교환에 의해 혼합물로부터 제거하고 비오틴 혼입을 HABA (4'-히드록시아조벤젠-2-카르복실산) 방법 (Pierce Biotin Quantitation Kit, Product No. 28005)을 사용하여 평가하였다. 그 후에 비오틴화된 DL4-Fc를 4℃에서 보관하였다.
스트렙타비딘 (SA)-코팅된 표면 위에 DL4-Fc의 방향을 유도하기 위해, 단일 비오틴 분자를 제조사의 지침에 따라서 BirA-500 키트 (Avidity)를 사용하여 DL4-Fc의 Fc 영역에 있는 AviTagTM 서열에 효소적으로 접합하였다. 간략히는, 2.5 μg의 BirA를 500 mL의 PBS의 반응 부피 중에서 500 μg의 DL4-Fc에 첨가하고 RT에서 1시간 동안 인큐베이션하였다. 임의의 잔존하는 비오틴을 제거하기 위해, 350 μL의 정제된 DL4-Fc 단백질을 제조사의 지침에 따라서 40K MWCO Zeba™ 스핀 탈염 칼럼 (Thermo-Fisher)을 사용하여 탈염하였다. 그 후에 비오틴화된 DL4-Fc를 4℃에서 보관하였다. AvitagTM을 함유하는 VCAM1-Fc 단백질을 상기에 기술된 것과 동일한 방법 및 재료를 사용하여 C-말단에서 비오틴화시켰다.
스트렙타비딘-코팅된-마이크로비드에 대한 비오틴화된 DL4-Fc 접합
1 μg의 비오틴화된 DL4-Fc를 직경이 1 μm 내지 100 μm 범위인 다양한 크기의 스트렙타비딘 (SA)-코팅된 폴리스티렌 μ비드 (Spherotech, Lake Forest, IL)와 함께 인큐베이션하였다. D4-Fc를 또한 SA-코팅된 Dynaneads (Thermo-Fisher) 및 50 nm 나노골드 (nanogold) 입자에 접합시키고 각각을 2 ml의 PBS 중 RT에서 30분간 인큐베이션하고, 10분마다 볼텍싱으로 혼합하였다. 모든 경우에, 입자의 표면적은 25 μm SA-μ비드의 2×105에 해당하였다. DL4-Fc 접합된 비드를 4 ml의 PBS로 세척하고 10분간 3000×g로 회전시켰다. 상청액을 조심스럽게 수집하여 혼합물로부터 임의의 비결합 리간드를 제거하고 DL4-Fc 함량을 분석하여 μ비드에의 결합을 평가하였다. 두 번째 세척 후, DL4-μ비드를 다양한 부피의 PBS에 재-현탁하여 본문에 언급된 바와 같은 지시된 농도를 달성하였다. 음성 대조군으로 사용하기 위해, 비접합 μ비드를 병렬로 제조하였다.
SA-μ비드에 대한 DL4-Fc 및 VCAM1-Fc의 화합물 접합을 위해, DL4-Fc 양은 2×105 SA-μ비드당 1 μg으로 일정하게 유지하는 반면, VCAM1-Fc는 0.01 μg (100:1), 0.1 μg (10:1), 1 μg (1:1) 및 10 μg (1:10)으로 첨가하였다.
NOTCH-활성화 수용체 세포주, 3T3-N1Cluc의 개발
Notch-반응성 요소 (8× RBPJ 보존적 반응 부위)를 프로모터가 없는 (promoterless) pGL4.17[luc2/Neo] 플라스미드 (Promega) 내로 삽입하였다. 그로써, 네오마이신에 대한 내성을 부여하면서 루시퍼라제 효소를 발현함으로써 Notch 활성화를 보고하는 단일 플라스미드 (pGL4.17-N1Rep로 명명됨)를 생성하였다. 그 후에 NIH3T3 세포를 pMIGR-NOTCH1 (Dr. Warren Pear, UPenn으로부터 기증받음) 및 pGL4.17N1Rep 플라스미드로 형질감염시켰다. 네오마이신 처리 (1 μg/mL)에 대해 내성인 세포를 먼저 선별하고 유세포 분석에 의해 GFP를 발현하는 세포를 분류하였다. 다음으로, NIH3T3 세포의 클론을 96-웰 플레이트 내로의 단일 세포 침착 (single cell deposition)에 의해 단리하였다. 그 후에 플레이트-결합된 DL4-Fc에의 활성화에 대한 각 클론의 반응 (20 μg/mL로 밤새 침착)을 측정하였다. 배경의 양이 가장 적고 Notch 활성화 반응이 가장 높은, 3T3N1CLuc로 명명된 클론을 확장시키고 Notch 수용체 활성화를 측정하기 위한 실험을 수행하는데 사용하였다.
Notch 활성화를 측정하기 위한 3T3-N1CLuc 루시퍼라제 분석
DL4-μ비드를 표준 조직 배양 (TC)-처리된 평평-바닥 96-웰 플레이트에서 3×104 3T3-N1CLuc 세포에 첨가하고 5% FBS가 보충된 MEM 중에서 밤새 인큐베이션하였다. 세포를 용해시키고 제조사의 지침에 따라서 초파리 루시퍼라제 분석 키트 2.0 (Biotium, Fremont, CA)을 사용하여 루시퍼라제 활성에 대해 분석하였다. 간략히는, 성장 배지를 제거하고 세포를 용해 완충제 첨가 전에 PBS로 세척하였다. 세포를 -80℃에서 10분간 동결시키고 해동시켜 용해시킨 후 96-웰 평평-바닥 불투명 폴리스티렌 플레이트 (Corning)로 용해물을 옮겼다. D-루시페린을 제조하고 자동 디스펜서로 각 웰에 첨가하고 Synergy H1 플레이트 판독기 (BioTek Instruments Inc., Winooski, VT)를 사용하여 분석하였다. 인간 IgG 및 DL4-Fc 플레이트-결합된 대조군을 다음날 3T3-N1CLuc 세포의 세척 및 접종 전에 4℃에서 밤새 평평-바닥 96-웰 플레이트에 50 μL/웰의 단백질 (5-20 μg/mL)을 흡착시킴으로써 전날 제조하였다.
HSPCs와 함께 코팅된 DL4-Fc 플레이트 및 DL4-μ비드 배양물
상이한 수의 DL4-μ비드를 3×103 마우스 Lin- Sca-1+ cKit+ HSCs (유세포 분석에 의해 C57BL6 마우스의 골수로부터 분류됨)에 첨가하여 1:1, 1:3, 1:9 및 1:27의 세포 대 비드 비율을 달성하였다. 각 조건의 경우, 세포-비드 조합을 200 μL의 IMDM [20% BIT (STEMCELL Technologies), 1% 글루타맥스 (Thermo), 50 ng/mL SCF, 10 ng/mL Flt3L 및 10 ng/mL IL-7 (R&D Systems, Minneapolis, MN)이 보충됨] 중의 둥근-바닥 96-웰 플레이트의 각 웰에서 인큐베이션하였다. 인간 IgG 및 DL4-Fc 플레이트-결합된 대조군을 다음날 세포의 세척 및 도말 전에 4℃에서 밤새 평평-바닥 96-웰 플레이트에 50 μL/웰의 단백질 (20 μg/mL)을 흡착시킴으로써 전날 제조하였다. 공동-배양 7일째, 세포를 수확하고 마우스 CD45, CD25, CD44, CD90, CD11b, 및 CD19에 대한 항체로 염색한 후, 이어서 LSR II 세포분석기 (cytometer) (BD Biosciences)로 분석하였다.
인간 HSPCs의 경우, Lin- CD34+ CD38-/lo 세포를 유세포 분석에 의해 UCB로부터 분류하고 4×103 세포를 StemSpanTM T 세포 선조체 확장 보충제 (Stemcell Technologies)가 보충된 200 μL의 StemSpanTMSFEM II (Stemcell Technologies) 중에서 둥근-바닥 96-웰 플레이트의 웰당 36,000 DL4-μ비드와 함께 14일간 배양하면서 7일째에 배지의 50%를 교환하였다. 14일을 초과하는 배양의 경우, 세포를 수확하고, 계수하고, 신선한 DL4-μ비드를 접종하였다. 공동-배양 14일째, 세포를 계수하여 세포 확장을 결정하고 CD34, CD5, CD1a 및 CD7에 대한 항체로 염색하여 계통 진행을 분석하였다. proT 세포 단계를 벗어나는 발생을 분석하기 위해, 세포를 또한 이후 시점에 CD4, CD8 및 CD3에 대한 항체로 염색하였다.
인간 유도 만능 줄기 세포 (iPSCs)의 CD34
+
조혈-전 또는 조혈 내피세포의 T 세포로의 분화
재프로그래밍된 hiPSC 세포주는 섬유아세포 (AlStemBio Cat #iPSC11) 및 T 세포 (Harvard Stem Cell Science Cat # STiPS A3)로부터 유래하였다. 이들을 마트리겔 (Matrigel) 상의 mTeSR 배지 (StemCellTech)에서 배양하였다. 자가-응집된 EBs를 생성하기 위해, iPSCs를 콜라게나제 B로 20분간 처리하고 단기로 트립신-EDTA 단계를 처리하였다. 세포 스크래퍼 (scraper)로 세포를 부드럽게 긁어 작은 응집체를 형성하였다. EBs가 BMP-4의 존재하에 StemPro-34 (Invitrogen)에서 배양 초기 24시간 동안 생성되었고, 그 후에 이를 BMP-4 및 bFGF의 존재하에 이후 24시간 동안 배양한 후, BMP-4, bFGF, 및 SB의 존재하에 다음 48시간 (2-4일) 동안 배양하였다. 4일째, BMP-4 및 SB를 제거하고 VEGF, IL-6, IL-11, IGF-1, SCF, EPO, TPO, Flt-3, IL-3, 및 DKK1 (모든 사이토카인은 Miltenyi Biotec, Auburn, CA 또는 R&D Systems로부터 입수)로 대체하였다. 배양물을 5% CO2/5% O2/90% N2에서 8일간 저산소 환경에서 유지하였다. 8일째, 세포를 기술된 바와 같이, CD34+ 세포에 대해 MACS-농축시키고 (Kennedy et al., 2012), 상기에 기술된 바와 같이, T 세포를 생성하기 위해, StemSpanTM T 세포 선조체 확장 보충제 (Stemcell Technologies)가 보충된 DL4-μ비드 플러스 StemSpanTMSFEM II (Stemcell Technologies)와 인큐베이션하였다.
면역결핍 마우스 내로 선조 T 세포의 입양 전달 (Adoptive Transfer)
면역결핍 마우스로의 입양 전달을 준비하기 위해, 대규모 인간 HPSC/DL4-μ비드 배양물을 설정하였다. 2×105 CD34+ HSPCs를 T25 플라스크 (Thermo Scientific)에서 7-10일간 1.8×106 DL4-μ비드와 인큐베이션하고, 이 시점에, CD34+CD7+ 세포로 확인된 선조 T (proT) 세포를 FACSAria 세포 분류기 (BD Biosciences, San Jose, CA)를 사용하여 분류하였다. 별법으로, HSPCs를 산화철-코팅된 DL4-μ비드와 함께 배양하는 경우, 세포 성분으로부터 DL4-μ비드의 자기 분리를 autoMACS-pro 세포 분류기 (Miltenyi Biotec)를 사용하여 수행하였다. proT 세포를 3-6일째 면역결핍 NOD-Scid/IL2rγnull (NSG) 신생아의 간질내로 (intrahepatically) 주입하였다. 각각의 마우스는 총 50 μl 부피의 α-MEM 중에서 hIL-7 (0.5 μg/마우스) 및 항-IL-7 단일클론 항체 (mAb), 클론 M25 (2.5 μg/마우스)와 함께 3-5×105 proT 세포를 투여 받았다. 마우스를 3-4일마다 IL-7/M25 칵테일로 부스팅하였다. 림프 기관 흉선, 비장 및 골수를 이식 후 3주 또는 12주 후에 채취하였다. 단일 세포 현탁액을 각 기관으로부터 제조하고, 염색한 후 LSR-II 세포측정기 (BD Biosciences)를 사용하여 분석하였다. 세포 사멸 마커 4'-6-디아미디노-2-페닐인돌 (DAPI)을 배제한 살아있는 세포 및 인간 CD45를 발현하는 세포에 대한 전자적 게이팅에 의해 생착을 평가하였다.
결과:
DL4-μ비드는 강력한 Notch 신호전달을 포함함
본 발명자들의 실험실의 이전 연구에 따르면 DL4 융합 단백질인, DL4-Fc가, 표준 TC-처리된 웰/플레이트의 표면에 고정되는 경우, T-계통 세포로의 발생을 유도하기에 충분한 마우스 및 인간 HSPCs에서 Notch 신호전달을 유도할 수 있음을 보여주었다 (Shukla et al., 2017). 그러나 이 2D 형식은 T 세포 발생을 촉진하기 위해 강력하고 지속적인 Notch 신호를 전달하는 확장성 (scalability) 및 용량에 재한이 있다.
Taqvi 등의 그룹 (2006)은 DL4로 2.8 μm 자성 비드를 기능화하고 이들을 마우스 HSCs와 공동-배양하려고 시도하였다. 혼합물을 이들 사이의 투과성 삽입물과 함께 OP9 세포의 위에 놓았다. 이는 줄기 세포와 기질 세포 사이의 물리적 접촉을 방지하지만, 분화를 촉진하기 위해 필요한 용해성 인자가 통과할 수 있게 하였다. 일부 CD90+ (Thy1) 세포가 DL4 기능화된 μ비드와의 배양물로부터 나타났지만, Thy1 발현은 확실한 T-계통 마커가 아니다. 중요하게도, CD19+ B 세포가 또한 나타났다. T 세포 발생을 촉진하고 B 세포 발생을 억제하는데 필요한 지속적인 Notch 활성화의 역치가 존재한다. B 세포가 여전히 존재했다는 사실은 이 시스템이 Notch 신호전달을 활성화하고 유지하는 능력이 없음을 입증한다. 실제로, 1:1에서 5:1로의 비드 대 세포 비의 증가는 B 세포 분화를 촉진하고 Thy1 발현을 차단하였다. 강력한 Notch 신호전달을 유도하기 위한 세포-기반 또는 플레이트-결합된 Notch 리간드에 대해 알려진 요구조건과 함께, μ비드 형식으로 제시된 가용성 Notch 리간드가 Notch 신호의 요구된 수준을 유도하지 못했다는 개념은 이 접근법이 HSPCs로부터 T 세포의 생성에 적용할 수 없을 것임을 시사한다. 또한, 이러한 유형의 연구는 아직 인간 CD34+ 세포를 사용하여 수행되지 않았다. 따라서, DL4로 기능화된 μ비드가 HSPCs로부터 T 세포 발생을 유도하는데 필요한 높고 일정한 수준의 Notch 신호전달을 제공할 수 있는지, 그 후에 임상용으로 쉽게 확장 및 번역할 수 있는지 여부는 여전히 확립되지 않았다.
이에 본 발명자들은 μ비드에 대한 DL4-Fc의 접합이 Notch 수용체에 효과적으로 관여시키고 현탁 상태로 HSPCs와 기능할 수 있으며, 따라서 스케일-업이 가능한 고차 (high-order) D4 다량체 플랫폼을 생성하는지 여부를 조사하였다.
μ비드에 대한 DL4-Fc의 연결을 촉진하기 위해, DL4-Fc를 SA-코팅된 폴리스티렌 비드에 대한 결합을 준비하는 과정에서 화학적으로 비오틴화하였다 (도 1A). DL4-Fc에의 비오틴 혼입을 웨스턴 블롯을 통해 확인하고 (도 1B) μ비드에의 후속 접합을 접합-전 및 -후에 수확된 상청액의 단백질 정량을 통해 분석하였다. Notch 신호전달에 대한 비드 크기의 영향을 평가하기 위해, 비-비오틴화된 DL4-Fc를 50 nm NHS-활성화 금 나노입자에, 비오틴화된 DL4-Fc를 1 μm SA-코팅된 DynaneadsTM 및 25 μm 및 100 μm 폴리스티렌 비드에 공유적으로 접합시켰다 (도 2). 기능화된 비드를 리포터로서 루시퍼라제 유전자를 사용하여 Notch 활성화를 보고하는 3T3-N1Cluc와 인큐베이션하였다. 각 조건에서 비드의 수는 전체적으로 동일한 총 표면적을 나타내고, 따라서 동일한 총수의 DL4-Fc 분자를 나타낸다. 루시퍼라제 활성 수준에 의해 나타난 바와 같이 (도 2B), 비드의 크기가 Notch 신호전달을 활성화시키는 DL4-Fc 비드의 능력에 영향을 미치는 것으로 나타났다. 참고로, 25 μm 직경의 DL4-μ비드는 동일한 재료의 다른 크기 비드 또는 1 μm Dynaneads 및 50 nm 나노입자와 비교할 때 Notch 수용체의 활성화를 최적으로 증강시켰다.
25 μm DL4-μ비드로 달성된 Notch 신호전달의 수준은 T-계통 분화 유도에 필요한 것으로 알려진 수준보다 더 높았으며, 이는 20 μg/mL의 플레이트-결합된 (PB) DL4-Fc에 해당한다. 이어서 IL-7, Flt3L, 및 SCF의 첨가와 함께, DL4-μ비드를 마우스 HSCs와 7일간 인큐베이션함으로써 이들이 T 세포 발생을 유도하는 능력을 갖는지 여부를 결정하였다. 결과에 따르면, DL4-μ비드와 인큐베이션하는 경우, 마우스 HSCs가 41%의 세포에서 CD25의 발현으로 표시되는 바와 같이, 쉽게 proT 세포를 발생시켰음을 보여주었다 (도 3). 반대로, PB-DL4-Fc는 단지 4%의 세포에서만 CD25의 발현을 유도하였다. DL4-μ비드는 또한 Notch 신호전달에 의해 예방되는 것으로 알려진 대체 B 세포 (CD19+) 및 골수성 (CD11b+) 계통 결과를 억제하였다.
μ비드에 대한 DL4-Fc의 방향성 접합은 Notch 신호전달의 유도를 증강시킴
무작위-배향된 1-세대 DL4-μ비드를 개선하기 위해, 본 발명자들은 비드 표면에 대한 DL4-Fc의 배향 지향이 Notch 신호전달을 증강시킬 것인지 여부를 조사하였다. 이를 위해, 단일 비오틴 분자가 효소적으로 접합될 수 있는, 그의 C-말단에 BirA 인식 서열 (AviTagTM)을 갖는 DL4-Fc를 설계하였다 (도 4). 이들 2 세대 DL4-μ비드의 인큐베이션은, 3T3N1CLuc 세포 루시퍼라제 활성에 의해 평가되는 바와 같이, Notch 신호전달의 수준을 상당히 증가시켰다 (도 5). 방향성 접합 방법을 사용하여, Notch 전달에 대한 비드 크기의 영향을 재평가하였다. 결과는 100 μm, 25 μm, 10 μm 및 6.5 μm 직경의 비드 모두가 Notch를 활성화시키는 능력을 갖지만, 25 μm 직경의 비드가 가장 효과적이었음을 보여주었다 (도 6). 비드 대 세포의 최적 비를 또한 평가하였고 비드 대 세포의 비가 3:1인 경우 플레이트-결합된 대조군에 비해 Notch 활성화가 10-배 증가한 것으로 확인되었다 (도 6).
다음으로 Notch 신호전달을 최적으로 활성화시키는 비드당 DL4-Fc의 양을 결정하기 위해 SA μ비드가 비오틴화된 DL4-Fc로 포화되었는지 여부를 조사하였다. 상이한 양의 DL4-Fc (0.01, 0.1, 1 및 10 μg)를 동일한 수의 25 μm SA-비드와 인큐베이션하였다. 그 후에 비드를 3T3-N1Cluc 세포와 밤새 인큐베이션하였다. 결과에 따르면, 2.25×105 SA-μ비드당 1 μg DL4-Fc가 최대 반응을 제공하는 것으로 나타났으며, 이는 DL4-μ비드의 활성이 포화되었음을 시사한다 (도 7A). 자화된 (magnetized) 25 μm 폴리스티렌 비드 (산화철로 코팅됨)가 이들의 비-자화된 대응물과 마찬가지로 Notch를 활성화하는데 동일하게 효과적임을 입증하였다 (도 7A). 또한, 동일한 직경의 SA-μ비드의 단백질 G-μ비드로의 대체는 Notch를 활성화하는 DL4-Fc의 능력에 유의미한 차이를 만들지 않았다 (도 7B).
따라서, 결과는 다음의 매개변수를 확립하였다: ii) DL4 분자의 배향, 및 iii) 비드 대 세포의 비율. 이들 매개변수의 최적화는 Notch 활성의 자극 및 T 세포 발생을 위한 최적의 조건을 결정하는데 영향을 미쳤다. 또한, 비드에 대한 DL4-Fc 로우딩에 대해 최대 활성을 얻기 위한 DL4-Fc 대 비드의 비율을 결정하였고 비드의 자화는 Notch 활성에 영향을 미치지 않았다. 나아가, DL4-Fc의 Fc 영역에 결합하는 단백질 G-μ비드는 SA-μ비드와 유사하게 DL4-Fc를 지향하는 것으로 보인다.
HSPCs로부터 T 세포 발생을 극대화하기 위한 DL4-μ비드 조건
상기 결과를 근거로, 본 발명자들은 이어서 동일한 인자가 T 세포 발생에 영향을 미치는지 여부를 결정하도록 설정하였다. 최초로 마우스 HSPCs를 사용하여 시험하였다. 도 8에 나타난 바와 같이, DL4-μ비드는 마우스 T 세포 발생을 유도하는데 PB-DL4보다 더 효과적이다.
proT 세포의 생성을 극대화하기 위한 HSPCs 대 DL4-μ비드의 최적 비율을 결정하기 위해, DL4-μ비드의 수를 3배로 증가시키면서 각 조건에 대해 3×103 HSPCs를 인큐베이션하였다 (도 9). 7일간의 인큐베이션 후, HSPCs의 proT 세포 (CD25+)로의 분화를 상이한 HSPC:DL4-μ비드 비율로 분석하였다. 최적의 HSPC:DL4-μ비드 비율은 약 1:9로 나타났는데, 이 비율이 CD25+ 세포의 가장 높은 비율을 생성하였기 때문이다. HSPC:비드 수의 비율을 1:27로 증가시켜도 T-계통 분화가 개선되지 않았다.
DL4-μ비드를 이용한 인간 T 세포 발생의 동역학 및 확장
다음으로 CD34+ UCB-유래 HSPCs로부터 인간 T 세포 발생을 유도하기 위한 DL4-μ비드의 사용을 검증하였다. 이를 위해, 상기에서 확립된 1:9의 최적 HSPC:DL4-μ비드 비율을 사용하였다. 2일마다, 세포를 계수하고 유세포 분석을 수행하였다. 결과는 배양 4일째까지 CD34, CD7 및 CD5를 공동-발현하는 인간 proT 세포의 출현을 보여주었다 (도 10A). 이러한 결과는 강력한 proT 세포 표현형 (CD34+CD7+ 또는 CD7+CD5+CD1a-)이 비접합 μ비드 또는 PB-DL4-Fc가 아닌, DL4-μ비드와 인큐베이션된 인간 HSPCs에 의해 달성됨을 입증하는 것으로, 플레이트-결합된 DL4-Fc에 비해 Notch를 활성화시키는 DL4-μ비드의 더 높은 능력을 확인한다.
임상적으로 관련된 proT 세포를 달성하기 위한 하나의 과제는 충분한 세포 수를 수득하는데 어려움이 있다는 것이다. 이를 해결하기 위해, 발생 도중 세포 확장을 또한 평가하였고, 14일까지 초기 시작 수에 비해 150배 이상의 세포 확장이 달성될 수 있음이 확인되었다 (도 10B).
DL4-μ비드는 성숙 인간 T 세포 발생을 촉진함
다음으로, Notch를 활성화시키는 DL4-μ비드의 증가된 능력이 발생 중인 세포를 T 세포 발생의 후기 단계로 분화하도록 유도하고, 그로써 후기 배양 시점에서 더욱 성숙한 표현형을 발현할 수 있는지 여부를 조사하였다 (도 11). 2일 및 47일째 배양물 둘 다의 분석은 CD4+ CD8+ 이중 양성 (DP) 세포가 세포의 약 25%를 구성하였음을 보여주었다. 흥미롭게도, 47일째 배양물은 CD4+CD8+CD3+ DP 세포 및 CD8+CD3+ 단일 양성 (SP) 세포의 출현을 나타내었다. 이러한 결과는 DL4-μ비드에 의해 유도된 강력한 Notch 신호전달이 PB-DL4-Fc를 사용하는 이전 시도에서 나타난 T 세포 성숙의 발생 장애를 극복할 수 있음을 보여준다.
동원된 말초 혈액 (mPB)-유래 HSPCs는 DL4-μ비드와 배양 시 T 계통 세포로 분화함
개인으로부터 수득된 HSPCs의 수가 UCB의 것보다 약 100×이기 때문에, 성인 mPB는 잠재적으로 UCB보다 더 쉽게 입수가능한 공급원이다. T 계통 발생의 개체 발생 (ontogeny)을 비교하기 위해, 3명의 상이한 개인으로부터의 mPB-유래 CD34+ HSPCs를 DL4-μ비드와 배양하고 UBC-유래 HSPC 배양물과 비교하였다 (도 12A). D14에, T 세포 발생의 진행은 유사한 비율의 proT 세포 집단 (CD34+CD7+)을 갖는 CB-유래 HSPCs의 진행과 매우 유사한 것으로 관찰되었다. 그러나 14일 후의 확장 속도는 mPB-유래 HSPCs의 경우 110×였지만, CB-유래 세포의 경우에는 190×에 가까웠다 (도 12B).
DL4-μ비드를 사용한 iPSCs에서 T 세포 발생의 유도
섬유아세포로부터 유래한 인간 iPSCs를 본원에 기술된 방법에 따라 CD34+ 조혈-전 전구 세포로 분화하도록 유도하였다. CD34+ 세포를 DL4-μ비드와 인큐베이션하여 발생의 초기 (도 13A) 및 후기 단계 (도 13B) 동안 다능성 세포를 T-계통으로 다능성 세포를 유도하는 이들의 능력을 결정하였다. 발생의 초기 단계는 CD7 세포 표면 마커에 이은, CD5의 정상적인 획득을 보여준다. T 세포 발생의 후기 단계는 20일째 CD4+ 미성숙 단일 양성 (iSP) 마커 및 D35에 단일 양성 마커 CD8 세포의 획득으로 표시된다. 주목할 점은 T 세포 수용체 (TCR) 성분, CD3, 세포 표면 마커의 존재로, 이는 이 배양에서 성숙 T 세포의 존재를 나타낸다.
iPSCs가 T 세포 (T-iPSC)로부터 유래하는 경우, 이는 TCRα 및 TCRβ 유전자좌가 이미 유전적으로 재배열되었음을 의미하고, T 계통 운명으로 재-분화된 경우, 세포는 이미 재배열된 TCRαβ를 발현할 것이다. 발생 중인 TCR의 어느 단계에서 T-iPSC-유래 세포에 의해 발현되는지를 결정하기 위해, CD34+ 조혈-전 전구 세포를 DL4-μ비드와 인큐베이션하였다. D12에 검사된 배양물은 성숙 T 세포 마커 CD4 및 CD8이 아직 발현되지 않은 시점에, 세포의 40%에서 TCRαβ 및 CD3의 세포 표면 발현을 나타내지만, 세포의 80%는 초기 T 세포 마커 CD7을 발현하였다 (도 14, 좌측 패널). CD7+ 세포에 대해 게이팅되는 경우, 이들은 70% 이상의 TCRαβ 및 CD3 발현을 나타내었다. D24에서 80% 이상의 세포가 TCRαβ 및 CD3을 발현하였고, 이들 세포의 다수가 CD4 및 CD8의 발현을 획득하였다 (도 14, 우측 패널).
VCAM-1은 HSPCs의 T 세포로의 분화를 가속화함
SA-μ비드가 다른 비오틴화된 분자의 추가를 위한 모듈형 기초 (modular base)로 기능할 수 있는지 여부를 결정하기 위해, VCAM-1의 기능적 효과를 조사하였다. 이전에 플레이트-결합된 DLL4에의 VCAM-1 추가는 HSPCs의 T 세포로의 분화를 가속화하는 것으로 나타났다 (Shukla et al., 2017). 본원에서, 새로운 융합 단백질, VCAM1-Fc를 유전적으로 설계하고, 발현시키고 비오틴화시켰다. 면역블롯 분석을 사용하여, 생성된 VCAM1-Fc의 크기가 상업적으로 이용가능한 VCAM1 제품의 크기와 유사한 것으로 결정되었다 (도 15, 좌측 패널). 또한, BirA 효소 비오틴화를 위한 표적 서열을 함유하는 VCAM1-Fc는 비오틴화되는 것으로 입증되었다 (도 15, 우측 패널). 그 후에 비오틴화된 VCAM1-Fc를 사용하여 SA-μ비드의 표면을 불변량의 DL4-Fc와 함께, 코팅하고 UBC-유래 HSPCs와 배양하였다. D7 배양물 분석에 따르면 일반적으로 VCAM1-Fc/DL4-Fc 비율이 높을수록 분화 속도의 가속화가 초래되는 것으로 나타났다 (도 16). 이는 VCAM-1의 활성뿐만 아니라, T 세포 발생에 관여하는 공동-자국 분자의 제어된 추가를 위한 플랫폼으로서 μ비드의 유연성을 입증하였다.
면역결핍 마우스 내로 선조 T 세포 생착 및 그 후 주변으로의 이동
HSPC/DL4-μ비드 배양물로부터 유래한 CD34+ CD7+ 선조 T (proT) 세포가 흉선을 생착시키는 능력을 평가하기 위해, 면역결핍 NSG 마우스 모델을 선택하였다. proT 세포의 생산은 선형적으로 확장되어, 96-웰 플레이트를 T25 플라스크로 전환시켰다. ProT 세포를 D7 배양물로부터 분류하고 NSG 신생아에게 간질내로 주입하였다. 3주차에 초기 생착을 조사하여, 인간 CD45+ 세포의 존재가 나타났고, 이들 대부분은 흉선 내에서 이중 양성 CD4+ CD8+ (DP) 성숙 T 세포 단계에 있다 (도 17). B (CD19) 및 골수성 (CD33) 세포의 발생은 흉선에서 부재하였다.
이식 후 12주차 분석은 proT 세포의 재생이 일어나지 않은 흉선에서, 인간 CD45+ 세포가 거의 모두 CD4 및 CD8 SP로 분화되고 성숙된 것으로 나타났다 (도 18). 성숙 CD4 및 CD8 SPs가 흉선에서 비장은 물론 골수로 이동한 것으로 보였다. 이는 proT 세포가 흉선 내에서 성숙하고 일반적으로 이차 림프 기관으로 이동하는 능력을 가지고 있음을 입증한다.
배양물 중에서 세포 성분으로부터 μ비드의 분리
임상 목적을 위해 HSPC/DL4-μ비드 공동-배양으로부터 proT 세포의 대규모 생산을 준비하기 위해, 공동-배양된 세포로부터 산화철 코팅된 DL4-μ비드를 분리하는 AutoMACS (Miltenyi)의 능력을 평가하였다 (도 19A). 임상적으로 승인된 CliniMACS (Miltenyi)와 유사하게 기능하는, AutoMACS는 이들이 세포 분획에서 검출될 수 없었기 때문에 세포 성분으로부터 μ비드를 완전히 분리하였다 (도 19B). 반대로, 일부 세포는 비드 분획에서 단리된 μ비드에 포획되거나 부착되어 있다.
요약
본원에서, 마우스 및 인간 HSPCs 둘 다는 물론 iPSCs로부터 T 세포의 생성을 위한 무세포 기반 시스템의 개발이 기술된다. 비-플레이트-결합된 또는 현탁 Notch 리간드, 예컨대 DL4-μ비드는 T-계통 세포의 효과적인 생성을 허용하는 독특한 전략을 나타내고, 이는 대규모 생물반응기-기반 현탁 배양에서 쉽게 달성될 수 있으며, 잠재적으로 플레이트-결합된 접근법과 관련된, 비효율성 및 확장성 단점과, 발생 장애를 극복할 수 있다.
이전 연구는 무세포 지지체 시스템에서 미성숙 proT 세포 단계를 벗어나는 인간 T-계통 세포의 생성을 입증하지 못했다. 또한, 본원의 결과는 무세포 지지체 배양 시스템을 사용하여 iPSCs로부터 proT 및 성숙 SP CD4 및 CD8 세포를 비롯한 T-계통 세포의 생성을 최초로 보여주었다. 여기서, 본원에 기술된 현탁 Notch 리간드 배양 시스템이 성숙 SP T 세포의 출현을 허용하는 것으로 나타났고, 이는 본원에 기술된 DL4-μ비드로 달성된 Notch 신호전달이 플레이트-결합된 접근법에서 나타나는 T 세포 성숙에 대한 발생 장애를 극복할 수 있음을 보여준다.
참고문헌
Claims (27)
- (a) 줄기 세포 또는 선조 세포 (progenitor cell)를 포함하는 샘플을 현탁 지지체에 접합된 Notch 리간드와 함께 배양하는 단계, 및 (b) T 세포 계통의 세포를 단리하는 단계를 포함하는, T 세포 계통의 세포를 생성하는 방법.
- 제1항에 있어서, 현탁 지지체가 입자인, 방법.
- 제1항 또는 제2항에 있어서, 현탁 지지체가 마이크로비드인, 방법.
- 제1항 내지 제3항 중 어느 한 항에 있어서, 줄기 세포 또는 선조 세포가 Notch 리간드와 함께 현탁 상태로 배양되는, 방법.
- 제1항 내지 제4항 중 어느 한 항에 있어서, 줄기 세포가 조혈 줄기/선조 세포 (HSPCs), 배아 줄기 세포 또는 유도 만능 줄기 세포 (iPSCs)로부터 선택되는, 방법.
- 제1항 내지 제5항 중 어느 한 항에 있어서, 줄기 세포가 CD34+ 또는 CD34+CD38-/lo HSPCs인, 방법.
- 제1항 내지 제4항 중 어느 한 항에 있어서, 줄기 세포가 CD34+ 조혈 전구 세포 (precursor cell), 선택적으로 iPSCs로부터 분화된 CD34+ 조혈 전구 세포인, 방법.
- 제1항 내지 제7항 중 어느 한 항에 있어서, Notch 리간드가 DL4인, 방법.
- 제1항 내지 제8항 중 어느 한 항에 있어서, T 세포 계통의 세포가 선조 T (proT) 세포인, 방법.
- 제9항에 있어서, 줄기 세포 또는 선조 세포가 인간 세포이고, proT 세포가 표현형 CD34+CD7+ 또는 CD7+CD5+CD1a-를 갖는, 방법.
- 제10항에 있어서, 줄기 세포 또는 선조 세포가 마우스 세포, 선택적으로 계통-CD117+ Sca-1+ 마우스 세포이고, proT 세포가 표현형 CD25+ 또는 CD25+CD90+를 갖는, 방법.
- 제1항 내지 제8항 중 어느 한 항에 있어서, T-세포 계통의 세포가 CD4+CD8+ 이중 양성 세포, CD4+CD8+CD3+ 이중 양성 세포, CD8+CD3+ 단일 양성 세포 또는 CD4+CD3+ 단일 양성 세포인, 방법.
- 제1항 내지 제12항 중 어느 한 항에 있어서, 줄기 세포 또는 선조 세포가 무-기질 세포 (stromal cell-free) 배지에서 배양되는, 방법.
- 제1항 내지 제13항 중 어느 한 항에 있어서, 줄기 세포 또는 선조 세포가 현탁 지지체에 부착된 적어도 하나의 T 세포 공동-자극 분자와 함께 배양되고, 선택적으로 적어도 하나의 T 세포 공동-자극 분자가 VCAM1인, 방법.
- 제1항 내지 제14항 중 어느 한 항의 방법에 의해 생성된, T 세포 계통의 세포.
- 제15항에 있어서, 세포가 선조 T 세포, CD4+CD8+ 이중 양성 세포, CD4+CD8+CD3+ 이중 양성 세포, CD8+CD3+ 단일 양성 세포 또는 CD4+CD3+ 단일 양성 세포인, 세포.
- (a) Notch 리간드 및 (b) 마이크로비드를 포함하고, Notch 리간드가 마이크로비드에 접합되는, 현탁 Notch 리간드 (suspension Notch ligand).
- 제17항에 있어서, (i) 마이크로비드가 6.5 내지 100 μm의 직경을 갖고/갖거나 (ii) Notch 리간드의 C-말단이 마이크로비드에 접합되는, 현탁 Notch 리간드.
- T 세포 계통의 세포를 생성하기 위한 제17항 또는 제18항의 현탁 Notch 리간드의 용도.
- (i) (a) Notch 리간드 및 (b) 현탁 지지체를 포함하고, Notch 리간드가 현탁 지지체에 접합되는, 현탁 Notch 리간드, 및 (ii) T 세포 계통의 세포를 생성하기 위한 상기 현탁 Notch 리간드의 사용을 위한 지침서를 포함하는 키트.
- (i) (a) Notch 리간드 및 (b) 현탁 지지체를 포함하고, Notch 리간드가 현탁 지지체에 접합되는, 현탁 Notch 리간드, 및 (ii) 배양 배지를 포함하는 키트.
- 제20항 또는 제21항에 있어서, 현탁 Notch 리간드가 마이크로비드에 접합된 DL4를 포함하는, 키트.
- 제20항 내지 제22항 중 어느 한 항에 있어서, (iii) 현탁 지지체에 부착된 적어도 하나의 T 세포 공동-자극 분자를 추가로 포함하고, 선택적으로 적어도 하나의 T 세포 공동-자극 분자가 VCAM1인, 키트.
- 하기 단계를 포함하는, T 세포의 수적 증가를 필요로 하는 상태를 갖는 대상체를 치료하는 방법:
(i) (a) 줄기 세포 또는 선조 세포를 포함하는 샘플을 현탁 지지체에 접합된 Notch 리간드와 함께 배양하고, (b) T 세포 계통의 세포를 단리하는 것을 포함하는, T 세포 계통의 세포를 생성하는 단계, 및
(ii) T 세포 계통의 세포의 유효량을 대상체에 투여하는 단계. - 제24항에 있어서, T 세포 계통의 세포가 선조 T 세포인. 방법.
- 제23항에 있어서, T 세포 계통의 세포가 CD4+CD8+ 이중 양성 세포, CD4+CD8+CD3+ 이중 양성 세포, CD8+CD3+ 단일 양성 세포 또는 CD4+CD3+ 단일 양성 세포인, 방법.
- 제23항에 있어서, T 세포 계통의 세포가 성숙 T 세포인, 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862630497P | 2018-02-14 | 2018-02-14 | |
| US62/630,497 | 2018-02-14 | ||
| PCT/CA2019/050181 WO2019157597A1 (en) | 2018-02-14 | 2019-02-14 | Method for generating cells of the t cell lineage |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20200121817A true KR20200121817A (ko) | 2020-10-26 |
Family
ID=67619677
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020207024814A KR20200121817A (ko) | 2018-02-14 | 2019-02-14 | T 세포 계통의 세포를 생성하기 위한 방법 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20200399599A1 (ko) |
| EP (1) | EP3752602A4 (ko) |
| JP (2) | JP2021514185A (ko) |
| KR (1) | KR20200121817A (ko) |
| CN (1) | CN112041431A (ko) |
| AU (1) | AU2019220935A1 (ko) |
| CA (1) | CA3091158A1 (ko) |
| WO (1) | WO2019157597A1 (ko) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA3195223A1 (en) * | 2020-10-28 | 2022-05-05 | Sangamo Therapeutics, Inc. | Generation of cd4+ effector and regulatory t cells from human pluripotent stem cells |
| CA3172507A1 (en) | 2020-11-24 | 2022-06-02 | Raul E. VIZCARDO SAKODA | Methods for making, compositions comprising, and methods of using rejuvenated t cells |
| CA3201621A1 (en) | 2020-12-03 | 2022-06-09 | Century Therapeutics, Inc. | Genetically engineered cells and uses thereof |
| US11661459B2 (en) | 2020-12-03 | 2023-05-30 | Century Therapeutics, Inc. | Artificial cell death polypeptide for chimeric antigen receptor and uses thereof |
| JPWO2022168959A1 (ko) * | 2021-02-05 | 2022-08-11 | ||
| WO2022216524A1 (en) | 2021-04-07 | 2022-10-13 | Century Therapeutics, Inc. | Combined artificial cell death/reporter system polypeptide for chimeric antigen receptor cell and uses thereof |
| JP2024514522A (ja) | 2021-04-07 | 2024-04-02 | センチュリー セラピューティクス,インコーポレイテッド | 遺伝子導入ベクターおよび細胞を操作する方法 |
| WO2023129937A1 (en) | 2021-12-29 | 2023-07-06 | Century Therapeutics, Inc. | Genetically engineered cells having anti-cd19 / anti-cd22 chimeric antigen receptors, and uses thereof |
| WO2023164440A1 (en) | 2022-02-22 | 2023-08-31 | Juno Therapeutics, Inc. | Proteinase 3 (pr3) chimeric autoantibody receptor t cells and related methods and uses |
| WO2023215826A1 (en) | 2022-05-04 | 2023-11-09 | Century Therapeutics, Inc. | Cells engineered with an hla-e and hla-g transgene |
| WO2023240147A1 (en) | 2022-06-08 | 2023-12-14 | Century Therapeutics, Inc. | Genetically engineered cells expressing cd16 variants and nkg2d and uses thereof |
| WO2023240212A2 (en) | 2022-06-08 | 2023-12-14 | Century Therapeutics, Inc. | Genetically engineered cells having anti-cd133 / anti-egfr chimeric antigen receptors, and uses thereof |
| WO2023240169A1 (en) | 2022-06-08 | 2023-12-14 | Century Therapeutics, Inc. | Immunoeffector cells derived from induced pluripotent stem cells genetically engineered with membrane bound il12 and uses thereof |
| WO2024102838A1 (en) | 2022-11-09 | 2024-05-16 | Century Therapeutics, Inc. | Engineered interleukin-7 receptors and uses thereof |
| WO2024103017A2 (en) | 2022-11-10 | 2024-05-16 | Century Therapeutics, Inc. | Genetically engineered cells having anti-nectin4 chimeric antigen receptors, and uses thereof |
| WO2024156066A1 (en) * | 2023-01-27 | 2024-08-02 | Notch Therapeutics (Canada), Inc. | Method for generating t cell lineage populations from stem/progenitor cells |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2003226537A1 (en) * | 2002-04-05 | 2003-10-27 | Lorantis Limited | Modulators of the notch signalling pathway and uses thereof in medical treatment |
| US7575925B2 (en) * | 2002-12-10 | 2009-08-18 | Sunnybrook Health Sciences Centre | Cell preparations comprising cells of the T cell lineage and methods of making and using them |
| WO2004064863A1 (en) * | 2003-01-23 | 2004-08-05 | Lorantis Limited | Treatment of autoimmune diseases using an activator for the notch signaling pathway |
| WO2007027226A2 (en) * | 2005-04-28 | 2007-03-08 | Board Of Regents, The University Of Texas System | Systems and methods for the production of differentiated cells |
| US8772028B2 (en) * | 2008-11-07 | 2014-07-08 | Sunnybrook Health Sciences Centre | CD34+CD7+CD5+CD1a-human progenitor T-cells produced in vitro and methods of using |
| WO2013075222A1 (en) * | 2011-11-21 | 2013-05-30 | University Health Network | Populations of hematopoietic progenitors and methods of enriching stem cells therefor |
| US10180254B2 (en) * | 2014-09-16 | 2019-01-15 | Hitachi Zosen Inova Ag | Method and device for processing slag occurring in a combustion chamber of a refuse incineration plant |
| FR3026744B1 (fr) * | 2014-10-06 | 2024-04-19 | Hopitaux Paris Assist Publique | Methode de generation de progeniteurs de cellules t |
| US10626372B1 (en) * | 2015-01-26 | 2020-04-21 | Fate Therapeutics, Inc. | Methods and compositions for inducing hematopoietic cell differentiation |
| WO2017173551A1 (en) * | 2016-04-08 | 2017-10-12 | The Governing Council Of The University Of Toronto | Method for generating progenitor t cells from stem and/or progenitor cells and use of same |
| EP4326856A1 (en) * | 2021-04-23 | 2024-02-28 | Sunnybrook Research Institute | Stem cells comprising an unrearranged t cell receptor (tcr) gene locus and methods of use thereof |
| CA3219496A1 (en) * | 2021-05-18 | 2022-11-24 | Peter William ZANDSTRA | A method for producing blood progenitor and progenitor t cells, resulting cells and methods and uses thereof |
-
2019
- 2019-02-14 EP EP19754265.7A patent/EP3752602A4/en active Pending
- 2019-02-14 CA CA3091158A patent/CA3091158A1/en active Pending
- 2019-02-14 JP JP2020543276A patent/JP2021514185A/ja active Pending
- 2019-02-14 US US16/969,854 patent/US20200399599A1/en active Pending
- 2019-02-14 AU AU2019220935A patent/AU2019220935A1/en active Pending
- 2019-02-14 WO PCT/CA2019/050181 patent/WO2019157597A1/en unknown
- 2019-02-14 CN CN201980025370.1A patent/CN112041431A/zh active Pending
- 2019-02-14 KR KR1020207024814A patent/KR20200121817A/ko unknown
-
2023
- 2023-11-10 JP JP2023191915A patent/JP2024016217A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| AU2019220935A1 (en) | 2020-10-01 |
| EP3752602A4 (en) | 2021-11-24 |
| CN112041431A (zh) | 2020-12-04 |
| EP3752602A1 (en) | 2020-12-23 |
| CA3091158A1 (en) | 2019-08-22 |
| JP2024016217A (ja) | 2024-02-06 |
| US20200399599A1 (en) | 2020-12-24 |
| JP2021514185A (ja) | 2021-06-10 |
| WO2019157597A1 (en) | 2019-08-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20200121817A (ko) | T 세포 계통의 세포를 생성하기 위한 방법 | |
| AU784928B2 (en) | Hematopoietic differentiation of human embryonic stem cells | |
| KR102651433B1 (ko) | 혈관 콜로니 형성 세포 | |
| US20190330593A1 (en) | Lilrb2 and notch-mediated expansion of hematopoietic precursor cells | |
| MXPA06006706A (es) | Celulas madre. | |
| KR20170041204A (ko) | 치료 용도를 위한 푸코실화된 세포의 제조 및 동결보존 | |
| KR20120112511A (ko) | 인간 배아줄기세포 유래된 혈액모세포로부터 자연 살해 세포 및 수지상 세포를 생성하는 방법 | |
| WO2012133948A1 (ja) | 生体組織から単離できるssea-3陽性の多能性幹細胞を含む他家移植用細胞治療用組成物 | |
| Wang et al. | Mouse mesenchymal stem cells can support human hematopoiesis both in vitro and in vivo: the crucial role of neural cell adhesion molecule | |
| EP1735429A2 (en) | Methods and compositions for obtaining hematopoietic stem cells derived from embryonic stem cells and uses thereof | |
| US7776586B2 (en) | Method for isolating cells from mammary secretion | |
| WO2000070022A9 (en) | Ex vivo expansion of mammalian hematopoietic stem cells | |
| US20030100107A1 (en) | Compositions and methods for generating differentiated human cells | |
| WO2017038958A1 (ja) | 造血系細胞の作製方法 | |
| US20120177618A1 (en) | Hematopoietic stromal progenitor cells and uses thereof | |
| JPWO2005054459A1 (ja) | 造血幹細胞あるいは血管内皮前駆細胞の製造方法 | |
| KR100818215B1 (ko) | Cd34양성 줄기세포로부터 t 임파구 전구체를 제조하는 방법 | |
| US12054743B2 (en) | Method for obtaining T cells from pluripotent stem cells, and uses thereof | |
| Mizokami et al. | Preferential expansion of human umbilical cord blood-derived CD34-positive cells on major histocompatibility complex-matched amnion-derived mesenchymal stem cells | |
| WO2002033043A2 (en) | Method and marker for the isolation of human multipotent hematopoietic stem cells | |
| RU2797260C2 (ru) | Способ получения предшественников т-клеток | |
| JP2024525910A (ja) | 多能性幹細胞から免疫細胞の集団を作製する方法 | |
| Shukla | Controlled generation of progenitor T-Cells from hematopoietic stem cells and pluripotent stem cells | |
| Wang et al. | ĐFerrata Storti Foundation | |
| EP1424388A1 (en) | Method of enriching and/or propagating non-embryonic stem cells while preventing differentiation |