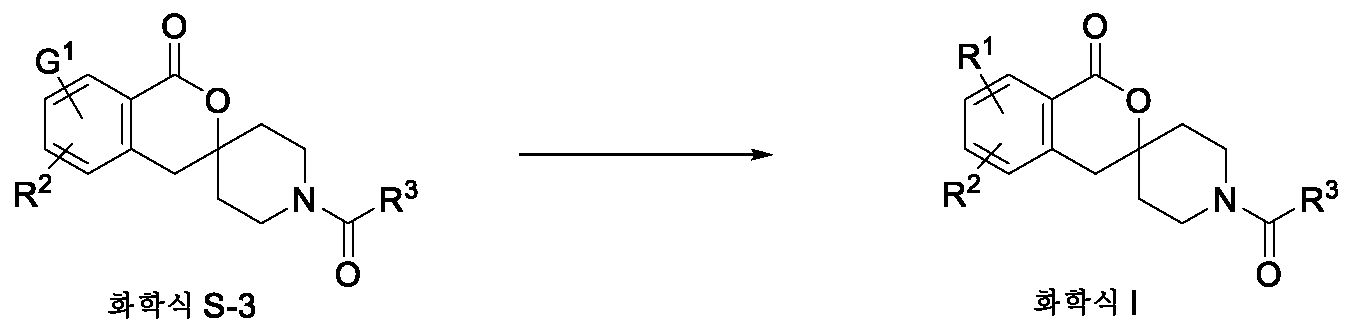
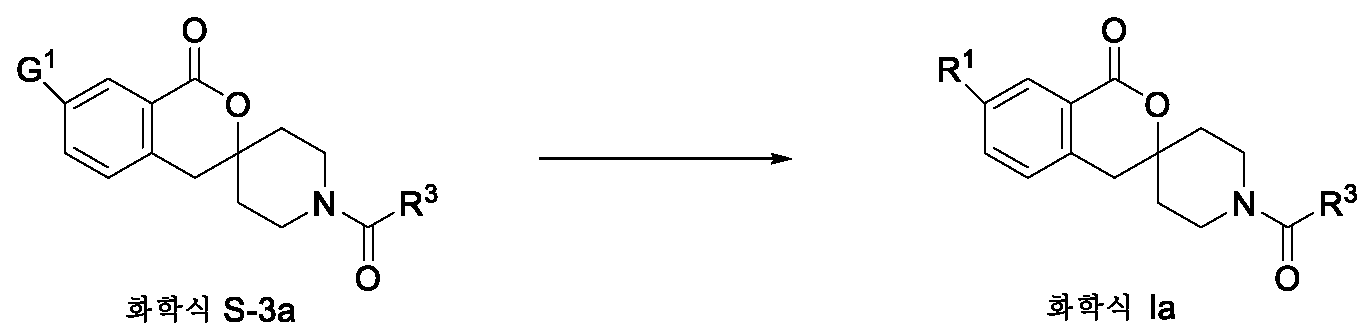
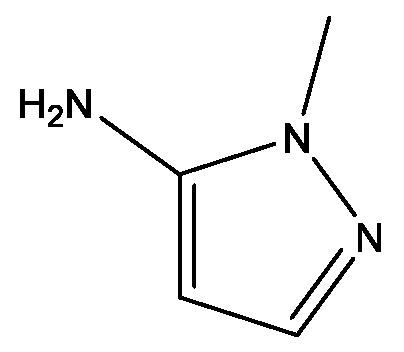
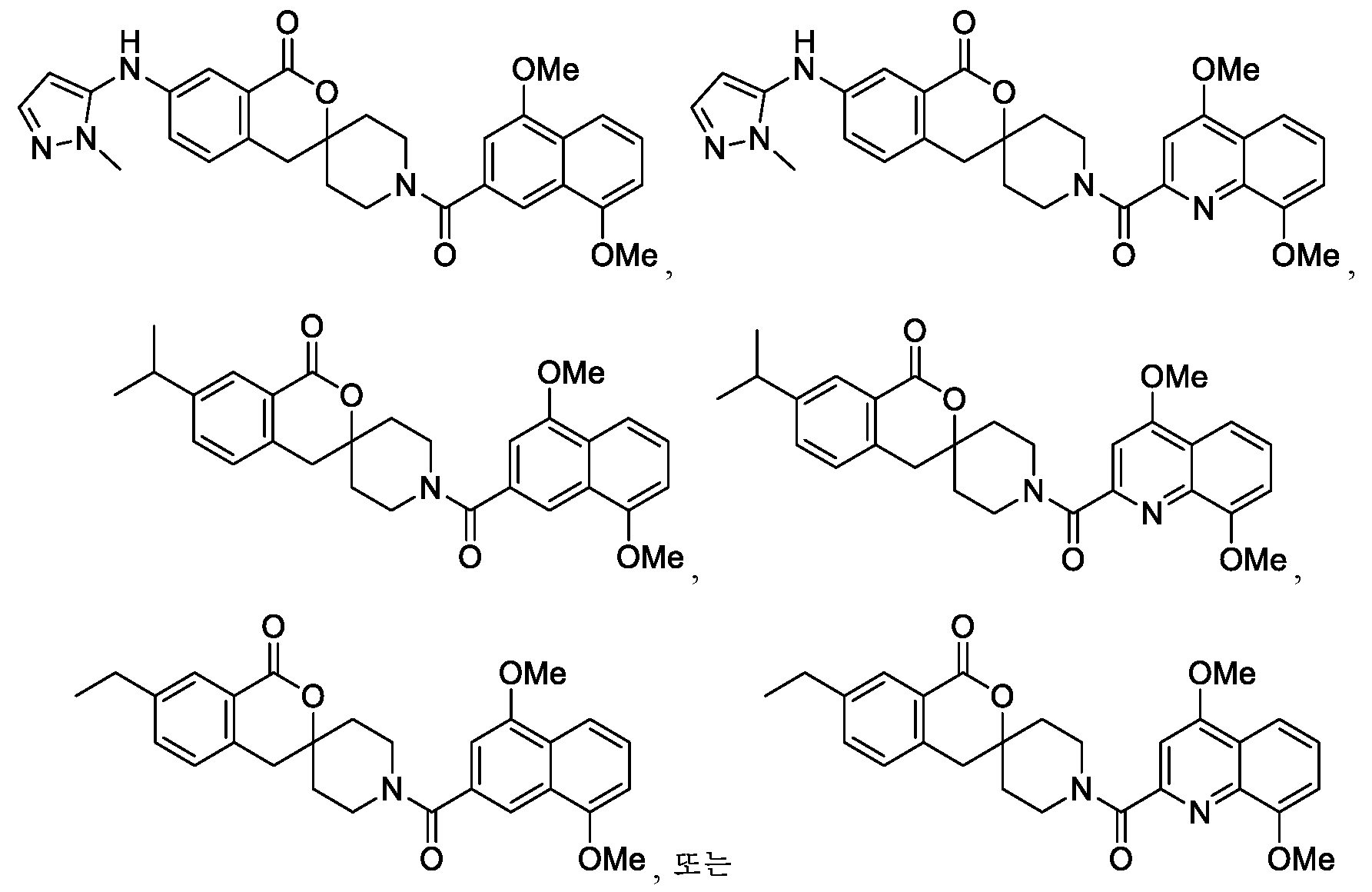
KR20200034723A - 신규 스피로락톤 화합물 - Google Patents
신규 스피로락톤 화합물 Download PDFInfo
- Publication number
- KR20200034723A KR20200034723A KR1020207002707A KR20207002707A KR20200034723A KR 20200034723 A KR20200034723 A KR 20200034723A KR 1020207002707 A KR1020207002707 A KR 1020207002707A KR 20207002707 A KR20207002707 A KR 20207002707A KR 20200034723 A KR20200034723 A KR 20200034723A
- Authority
- KR
- South Korea
- Prior art keywords
- optionally substituted
- alkyl
- compound
- pharmaceutically acceptable
- isochroman
- Prior art date
Links
- LXMSZDCAJNLERA-ZHYRCANASA-N spironolactone Chemical class C([C@@H]1[C@]2(C)CC[C@@H]3[C@@]4(C)CCC(=O)C=C4C[C@H]([C@@H]13)SC(=O)C)C[C@@]21CCC(=O)O1 LXMSZDCAJNLERA-ZHYRCANASA-N 0.000 title abstract description 30
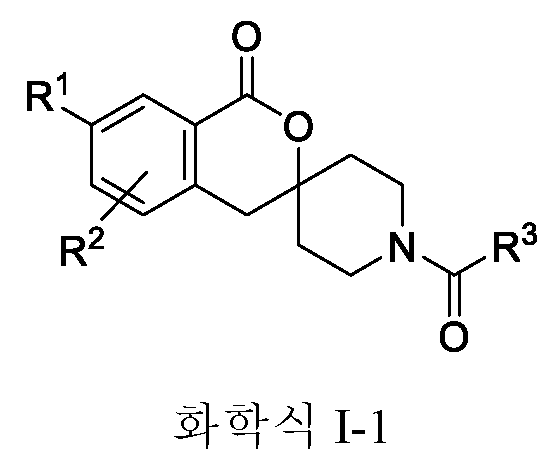
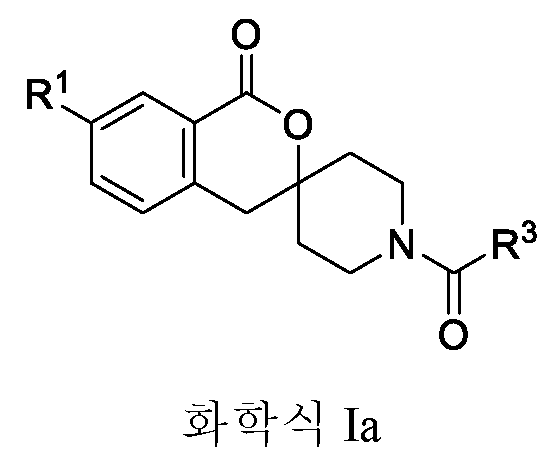
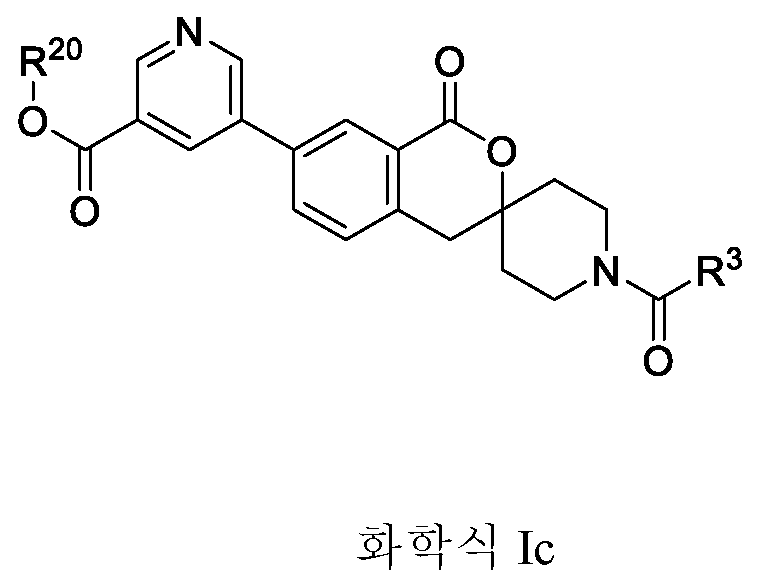
- -1 spirolactone compound Chemical class 0.000 claims abstract description 153
- 150000003839 salts Chemical class 0.000 claims abstract description 111
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 99
- 239000003112 inhibitor Substances 0.000 claims abstract description 91
- 230000000694 effects Effects 0.000 claims abstract description 63
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 63
- 238000011282 treatment Methods 0.000 claims abstract description 56
- 201000010099 disease Diseases 0.000 claims abstract description 50
- 208000035475 disorder Diseases 0.000 claims abstract description 49
- 208000008338 non-alcoholic fatty liver disease Diseases 0.000 claims abstract description 39
- 206010000496 acne Diseases 0.000 claims abstract description 36
- 208000002874 Acne Vulgaris Diseases 0.000 claims abstract description 35
- 101000677540 Homo sapiens Acetyl-CoA carboxylase 2 Proteins 0.000 claims abstract description 34
- 101000894929 Homo sapiens Bcl-2-related protein A1 Proteins 0.000 claims abstract description 33
- 101710190443 Acetyl-CoA carboxylase 1 Proteins 0.000 claims abstract description 30
- 206010053219 non-alcoholic steatohepatitis Diseases 0.000 claims abstract description 21
- 208000008589 Obesity Diseases 0.000 claims abstract description 20
- 230000002159 abnormal effect Effects 0.000 claims abstract description 20
- 235000020824 obesity Nutrition 0.000 claims abstract description 20
- 206010012601 diabetes mellitus Diseases 0.000 claims abstract description 18
- 150000001875 compounds Chemical class 0.000 claims description 186
- 125000000217 alkyl group Chemical group 0.000 claims description 177
- 238000000034 method Methods 0.000 claims description 114
- 229910052736 halogen Inorganic materials 0.000 claims description 103
- 150000002367 halogens Chemical class 0.000 claims description 101
- 125000001424 substituent group Chemical group 0.000 claims description 86
- 210000004027 cell Anatomy 0.000 claims description 79
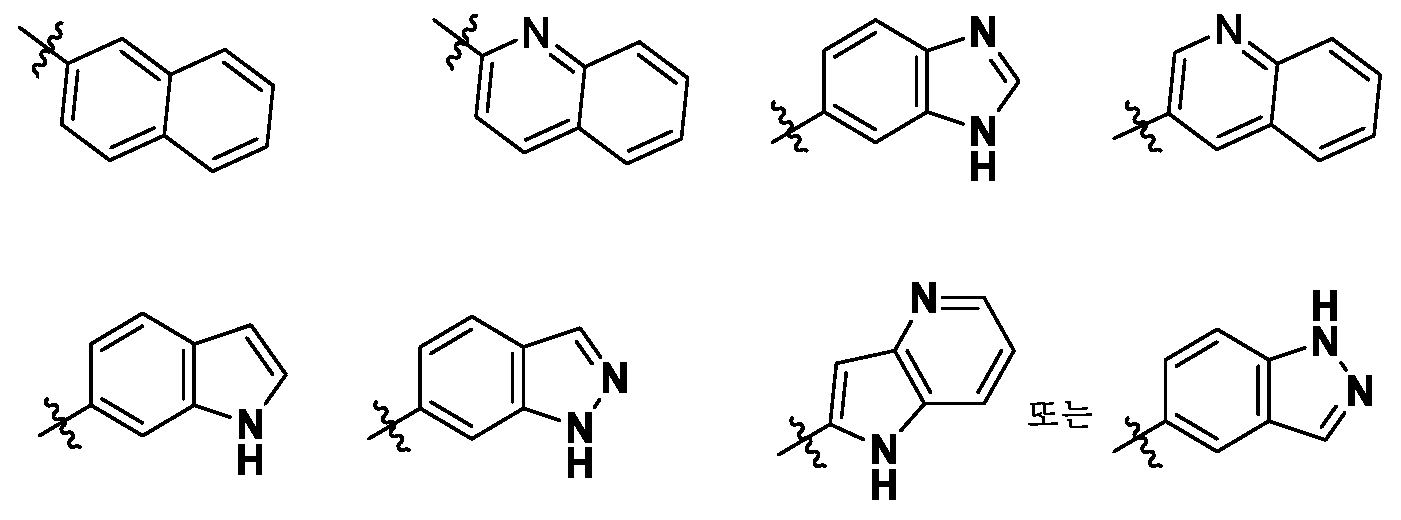
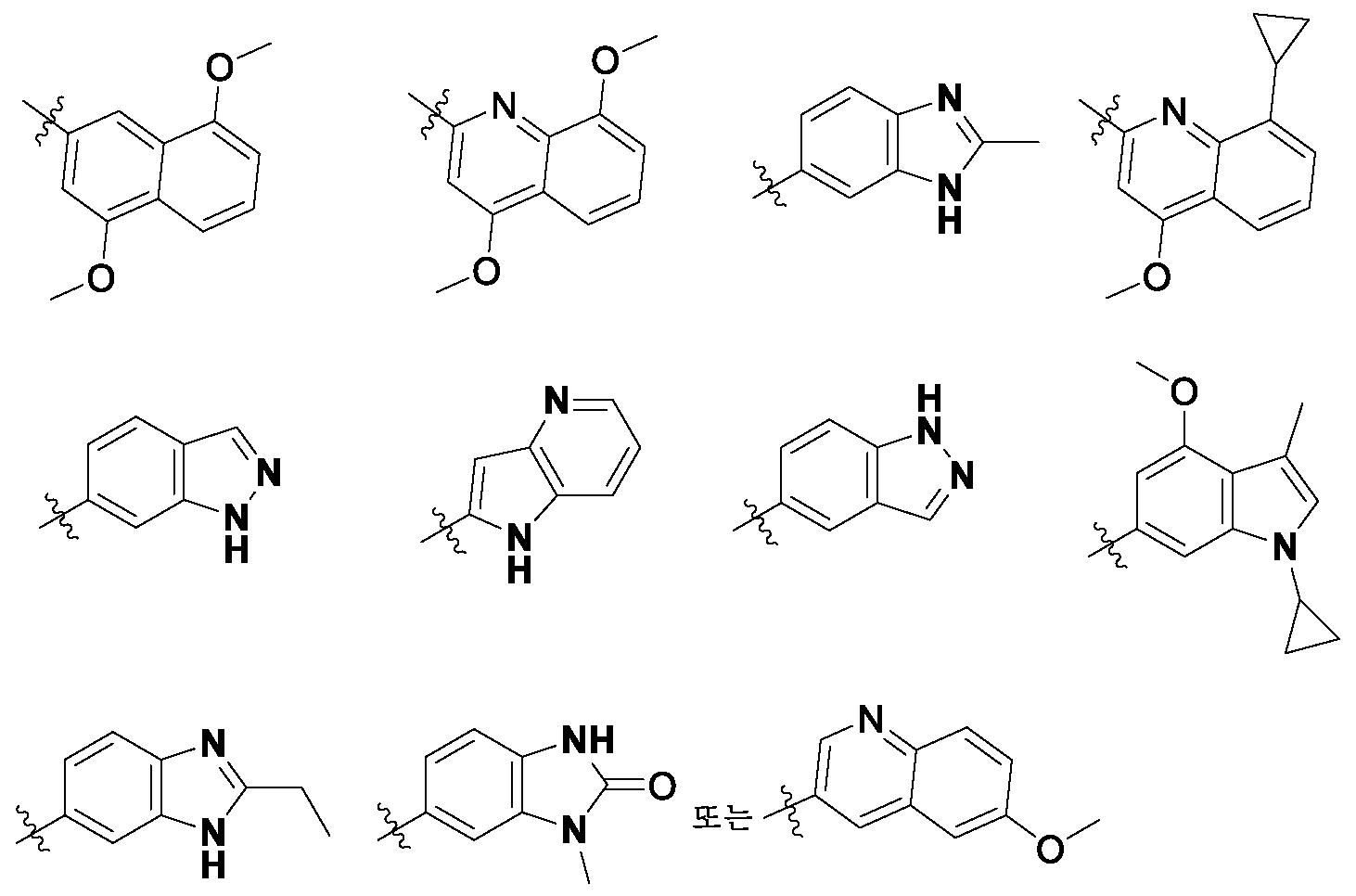
- 125000001072 heteroaryl group Chemical group 0.000 claims description 65
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims description 62
- 102100021334 Bcl-2-related protein A1 Human genes 0.000 claims description 62
- 125000003118 aryl group Chemical group 0.000 claims description 61
- 125000000623 heterocyclic group Chemical group 0.000 claims description 61
- 229910052739 hydrogen Inorganic materials 0.000 claims description 58
- 239000001257 hydrogen Substances 0.000 claims description 57
- PVNIIMVLHYAWGP-UHFFFAOYSA-N Niacin Chemical compound OC(=O)C1=CC=CN=C1 PVNIIMVLHYAWGP-UHFFFAOYSA-N 0.000 claims description 53
- 125000003545 alkoxy group Chemical group 0.000 claims description 52
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 50
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 45
- 125000000000 cycloalkoxy group Chemical group 0.000 claims description 43
- 210000002510 keratinocyte Anatomy 0.000 claims description 38
- 238000004519 manufacturing process Methods 0.000 claims description 38
- 235000001968 nicotinic acid Nutrition 0.000 claims description 38
- 239000011664 nicotinic acid Substances 0.000 claims description 38
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 37
- 210000003491 skin Anatomy 0.000 claims description 36
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 30
- 239000005557 antagonist Substances 0.000 claims description 30
- 150000002632 lipids Chemical class 0.000 claims description 28
- 150000002431 hydrogen Chemical class 0.000 claims description 27
- 108010018763 Biotin carboxylase Proteins 0.000 claims description 26
- 239000003795 chemical substances by application Substances 0.000 claims description 26
- 102000000452 Acetyl-CoA carboxylase Human genes 0.000 claims description 25
- 108010016219 Acetyl-CoA carboxylase Proteins 0.000 claims description 25
- 210000001789 adipocyte Anatomy 0.000 claims description 25
- 239000000556 agonist Substances 0.000 claims description 23
- 230000035755 proliferation Effects 0.000 claims description 23
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 22
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 claims description 21
- 230000002401 inhibitory effect Effects 0.000 claims description 21
- 125000000547 substituted alkyl group Chemical group 0.000 claims description 21
- 125000001153 fluoro group Chemical group F* 0.000 claims description 20
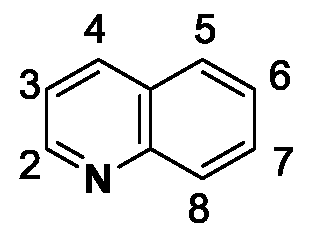
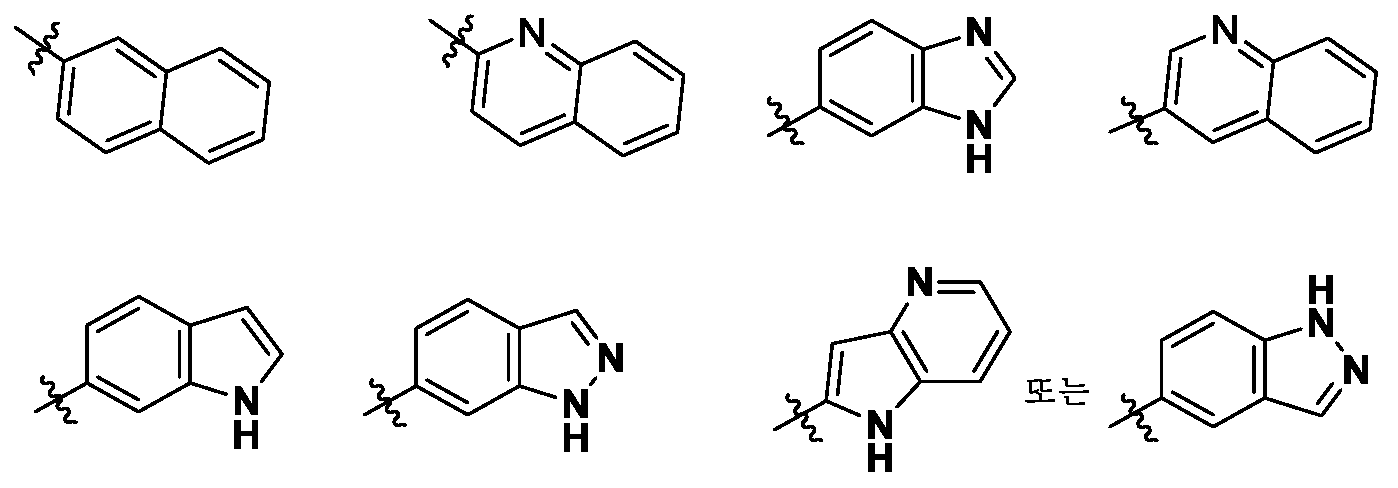
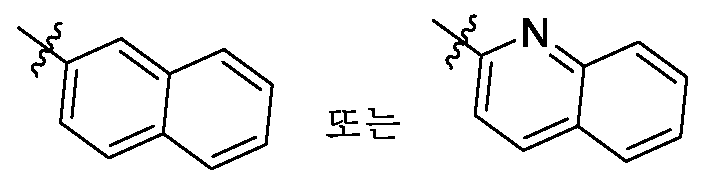
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 claims description 20
- 125000001624 naphthyl group Chemical group 0.000 claims description 19
- 239000002904 solvent Substances 0.000 claims description 19
- 125000005346 substituted cycloalkyl group Chemical group 0.000 claims description 19
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 17
- LTYOQGRJFJAKNA-KKIMTKSISA-N Malonyl CoA Natural products S(C(=O)CC(=O)O)CCNC(=O)CCNC(=O)[C@@H](O)C(CO[P@](=O)(O[P@](=O)(OC[C@H]1[C@@H](OP(=O)(O)O)[C@@H](O)[C@@H](n2c3ncnc(N)c3nc2)O1)O)O)(C)C LTYOQGRJFJAKNA-KKIMTKSISA-N 0.000 claims description 16
- LTYOQGRJFJAKNA-DVVLENMVSA-N malonyl-CoA Chemical compound O[C@@H]1[C@H](OP(O)(O)=O)[C@@H](COP(O)(=O)OP(O)(=O)OCC(C)(C)[C@@H](O)C(=O)NCCC(=O)NCCSC(=O)CC(O)=O)O[C@H]1N1C2=NC=NC(N)=C2N=C1 LTYOQGRJFJAKNA-DVVLENMVSA-N 0.000 claims description 16
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 16
- 229960003512 nicotinic acid Drugs 0.000 claims description 15
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 15
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 claims description 14
- 239000002253 acid Substances 0.000 claims description 13
- 210000002950 fibroblast Anatomy 0.000 claims description 13
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 13
- UUUHXMGGBIUAPW-UHFFFAOYSA-N 1-[1-[2-[[5-amino-2-[[1-[5-(diaminomethylideneamino)-2-[[1-[3-(1h-indol-3-yl)-2-[(5-oxopyrrolidine-2-carbonyl)amino]propanoyl]pyrrolidine-2-carbonyl]amino]pentanoyl]pyrrolidine-2-carbonyl]amino]-5-oxopentanoyl]amino]-3-methylpentanoyl]pyrrolidine-2-carbon Chemical compound C1CCC(C(=O)N2C(CCC2)C(O)=O)N1C(=O)C(C(C)CC)NC(=O)C(CCC(N)=O)NC(=O)C1CCCN1C(=O)C(CCCN=C(N)N)NC(=O)C1CCCN1C(=O)C(CC=1C2=CC=CC=C2NC=1)NC(=O)C1CCC(=O)N1 UUUHXMGGBIUAPW-UHFFFAOYSA-N 0.000 claims description 12
- 102000019034 Chemokines Human genes 0.000 claims description 12
- 108010012236 Chemokines Proteins 0.000 claims description 12
- 108010001348 Diacylglycerol O-acyltransferase Proteins 0.000 claims description 12
- 102000015868 Diacylglycerol O-acyltransferase 1 Human genes 0.000 claims description 12
- 102000016622 Dipeptidyl Peptidase 4 Human genes 0.000 claims description 12
- 101000930822 Giardia intestinalis Dipeptidyl-peptidase 4 Proteins 0.000 claims description 12
- 102100021948 Lysyl oxidase homolog 2 Human genes 0.000 claims description 12
- 101710183215 Lysyl oxidase homolog 2 Proteins 0.000 claims description 12
- 102000004270 Peptidyl-Dipeptidase A Human genes 0.000 claims description 12
- 108090000882 Peptidyl-Dipeptidase A Proteins 0.000 claims description 12
- 102100039314 Rho-associated protein kinase 2 Human genes 0.000 claims description 12
- 101710088493 Rho-associated protein kinase 2 Proteins 0.000 claims description 12
- 108091006269 SLC5A2 Proteins 0.000 claims description 12
- 102000058081 Sodium-Glucose Transporter 2 Human genes 0.000 claims description 12
- 108060008682 Tumor Necrosis Factor Proteins 0.000 claims description 12
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 claims description 12
- 102000014384 Type C Phospholipases Human genes 0.000 claims description 12
- 108010079194 Type C Phospholipases Proteins 0.000 claims description 12
- 238000011374 additional therapy Methods 0.000 claims description 12
- 125000001589 carboacyl group Chemical group 0.000 claims description 12
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 claims description 12
- RWSXRVCMGQZWBV-WDSKDSINSA-N glutathione Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O RWSXRVCMGQZWBV-WDSKDSINSA-N 0.000 claims description 12
- 230000005764 inhibitory process Effects 0.000 claims description 12
- HYAFETHFCAUJAY-UHFFFAOYSA-N pioglitazone Chemical compound N1=CC(CC)=CC=C1CCOC(C=C1)=CC=C1CC1C(=O)NC(=O)S1 HYAFETHFCAUJAY-UHFFFAOYSA-N 0.000 claims description 12
- 239000002243 precursor Substances 0.000 claims description 12
- 125000004076 pyridyl group Chemical group 0.000 claims description 12
- SSQPWTVBQMWLSZ-AAQCHOMXSA-N ethyl (5Z,8Z,11Z,14Z,17Z)-icosapentaenoate Chemical compound CCOC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/C\C=C/CC SSQPWTVBQMWLSZ-AAQCHOMXSA-N 0.000 claims description 11
- 238000001727 in vivo Methods 0.000 claims description 11
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 claims description 11
- 125000001041 indolyl group Chemical group 0.000 claims description 11
- 125000006570 (C5-C6) heteroaryl group Chemical group 0.000 claims description 10
- ULGZDMOVFRHVEP-RWJQBGPGSA-N Erythromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 ULGZDMOVFRHVEP-RWJQBGPGSA-N 0.000 claims description 10
- 230000004069 differentiation Effects 0.000 claims description 10
- 206010041823 squamous cell carcinoma Diseases 0.000 claims description 10
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 10
- 125000001313 C5-C10 heteroaryl group Chemical group 0.000 claims description 9
- 206010061218 Inflammation Diseases 0.000 claims description 9
- SHGAZHPCJJPHSC-NUEINMDLSA-N Isotretinoin Chemical compound OC(=O)C=C(C)/C=C/C=C(C)C=CC1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-NUEINMDLSA-N 0.000 claims description 9
- 206010039796 Seborrhoeic keratosis Diseases 0.000 claims description 9
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 claims description 9
- 210000004207 dermis Anatomy 0.000 claims description 9
- 210000002615 epidermis Anatomy 0.000 claims description 9
- 230000004054 inflammatory process Effects 0.000 claims description 9
- 210000001821 langerhans cell Anatomy 0.000 claims description 9
- 210000002752 melanocyte Anatomy 0.000 claims description 9
- 210000000716 merkel cell Anatomy 0.000 claims description 9
- 206010033675 panniculitis Diseases 0.000 claims description 9
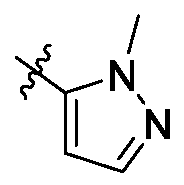
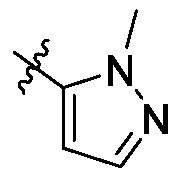
- 125000003226 pyrazolyl group Chemical group 0.000 claims description 9
- 201000003385 seborrheic keratosis Diseases 0.000 claims description 9
- 210000000130 stem cell Anatomy 0.000 claims description 9
- 210000004304 subcutaneous tissue Anatomy 0.000 claims description 9
- 206010012426 Dermal cyst Diseases 0.000 claims description 8
- 208000010305 Epidermal Cyst Diseases 0.000 claims description 8
- 206010048810 Sebaceous hyperplasia Diseases 0.000 claims description 8
- 229940098113 Transglutaminase inhibitor Drugs 0.000 claims description 8
- 208000009621 actinic keratosis Diseases 0.000 claims description 8
- FPIPGXGPPPQFEQ-OVSJKPMPSA-N all-trans-retinol Chemical compound OC\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-OVSJKPMPSA-N 0.000 claims description 8
- 239000003242 anti bacterial agent Substances 0.000 claims description 8
- 229960005280 isotretinoin Drugs 0.000 claims description 8
- 201000001441 melanoma Diseases 0.000 claims description 8
- 201000008407 sebaceous adenocarcinoma Diseases 0.000 claims description 8
- 201000005218 sebaceous adenoma Diseases 0.000 claims description 8
- 201000007321 sebaceous carcinoma Diseases 0.000 claims description 8
- 229910052717 sulfur Inorganic materials 0.000 claims description 8
- 208000011580 syndromic disease Diseases 0.000 claims description 8
- 125000003831 tetrazolyl group Chemical group 0.000 claims description 8
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 claims description 7
- 229940124158 Protease/peptidase inhibitor Drugs 0.000 claims description 7
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical group [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 7
- 235000012000 cholesterol Nutrition 0.000 claims description 7
- 239000000137 peptide hydrolase inhibitor Substances 0.000 claims description 7
- 238000007920 subcutaneous administration Methods 0.000 claims description 7
- IXXFZUPTQVDPPK-ZAWHAJPISA-N (1r,2r,4r,6r,7r,8r,10s,13r,14s)-17-[4-[4-(3-aminophenyl)triazol-1-yl]butyl]-7-[(2s,3r,4s,6r)-4-(dimethylamino)-3-hydroxy-6-methyloxan-2-yl]oxy-13-ethyl-10-fluoro-6-methoxy-2,4,6,8,10,14-hexamethyl-12,15-dioxa-17-azabicyclo[12.3.0]heptadecane-3,9,11,16-tet Chemical compound O([C@@H]1[C@@H](C)C(=O)[C@](C)(F)C(=O)O[C@@H]([C@]2(OC(=O)N(CCCCN3N=NC(=C3)C=3C=C(N)C=CC=3)[C@@H]2[C@@H](C)C(=O)[C@H](C)C[C@@]1(C)OC)C)CC)[C@@H]1O[C@H](C)C[C@H](N(C)C)[C@H]1O IXXFZUPTQVDPPK-ZAWHAJPISA-N 0.000 claims description 6
- SHKXZIQNFMOPBS-OOMQYRRCSA-N (4r)-4-[(3s,5s,7r,8r,9s,10s,12s,13r,14s,17r)-7,12-dihydroxy-3-(icosanoylamino)-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-17-yl]pentanoic acid Chemical compound O[C@H]1C[C@@H]2[C@@]3(C)CC[C@H](NC(=O)CCCCCCCCCCCCCCCCCCC)C[C@H]3C[C@@H](O)[C@H]2[C@@H]2CC[C@H]([C@H](C)CCC(O)=O)[C@]21C SHKXZIQNFMOPBS-OOMQYRRCSA-N 0.000 claims description 6
- 102000004277 11-beta-hydroxysteroid dehydrogenases Human genes 0.000 claims description 6
- 108090000874 11-beta-hydroxysteroid dehydrogenases Proteins 0.000 claims description 6
- GKHIVNAUVKXIIY-UHFFFAOYSA-N 2-[3-[4-(1h-indazol-5-ylamino)quinazolin-2-yl]phenoxy]-n-propan-2-ylacetamide Chemical compound CC(C)NC(=O)COC1=CC=CC(C=2N=C3C=CC=CC3=C(NC=3C=C4C=NNC4=CC=3)N=2)=C1 GKHIVNAUVKXIIY-UHFFFAOYSA-N 0.000 claims description 6
- XBUXXJUEBFDQHD-UHFFFAOYSA-N 4-[2-[2-chloro-4-[[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]methoxy]phenyl]cyclopropyl]benzoic acid Chemical compound C1=CC(C(=O)O)=CC=C1C1C(C=2C(=CC(OCC=3C(=NOC=3C3CC3)C=3C(=CC=CC=3Cl)Cl)=CC=2)Cl)C1 XBUXXJUEBFDQHD-UHFFFAOYSA-N 0.000 claims description 6
- BSYNRYMUTXBXSQ-FOQJRBATSA-N 59096-14-9 Chemical compound CC(=O)OC1=CC=CC=C1[14C](O)=O BSYNRYMUTXBXSQ-FOQJRBATSA-N 0.000 claims description 6
- SDDSJMXGJNWMJY-BRHAQHMBSA-N 7-[(2r,4ar,5r,7ar)-2-[(3s)-1,1-difluoro-3-methylpentyl]-2-hydroxy-6-oxo-3,4,4a,5,7,7a-hexahydrocyclopenta[b]pyran-5-yl]heptanoic acid Chemical compound O1[C@](C(F)(F)C[C@@H](C)CC)(O)CC[C@@H]2[C@@H](CCCCCCC(O)=O)C(=O)C[C@H]21 SDDSJMXGJNWMJY-BRHAQHMBSA-N 0.000 claims description 6
- 101710159293 Acyl-CoA desaturase 1 Proteins 0.000 claims description 6
- XUKUURHRXDUEBC-KAYWLYCHSA-N Atorvastatin Chemical compound C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CC[C@@H](O)C[C@@H](O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-KAYWLYCHSA-N 0.000 claims description 6
- XUKUURHRXDUEBC-UHFFFAOYSA-N Atorvastatin Natural products C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CCC(O)CC(O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-UHFFFAOYSA-N 0.000 claims description 6
- 102100031151 C-C chemokine receptor type 2 Human genes 0.000 claims description 6
- 101710149815 C-C chemokine receptor type 2 Proteins 0.000 claims description 6
- 102100035875 C-C chemokine receptor type 5 Human genes 0.000 claims description 6
- 101710149870 C-C chemokine receptor type 5 Proteins 0.000 claims description 6
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 claims description 6
- 102000011727 Caspases Human genes 0.000 claims description 6
- 108010076667 Caspases Proteins 0.000 claims description 6
- 102000004225 Cathepsin B Human genes 0.000 claims description 6
- 108090000712 Cathepsin B Proteins 0.000 claims description 6
- 108010062745 Chloride Channels Proteins 0.000 claims description 6
- 102000011045 Chloride Channels Human genes 0.000 claims description 6
- JZUFKLXOESDKRF-UHFFFAOYSA-N Chlorothiazide Chemical compound C1=C(Cl)C(S(=O)(=O)N)=CC2=C1NCNS2(=O)=O JZUFKLXOESDKRF-UHFFFAOYSA-N 0.000 claims description 6
- 229920000064 Ethyl eicosapentaenoic acid Polymers 0.000 claims description 6
- 101800000224 Glucagon-like peptide 1 Proteins 0.000 claims description 6
- DTHNMHAUYICORS-KTKZVXAJSA-N Glucagon-like peptide 1 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1N=CNC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 DTHNMHAUYICORS-KTKZVXAJSA-N 0.000 claims description 6
- 102400000322 Glucagon-like peptide 1 Human genes 0.000 claims description 6
- 108010024636 Glutathione Proteins 0.000 claims description 6
- 229940121710 HMGCoA reductase inhibitor Drugs 0.000 claims description 6
- 108090000174 Interleukin-10 Proteins 0.000 claims description 6
- 108090001005 Interleukin-6 Proteins 0.000 claims description 6
- LTXREWYXXSTFRX-QGZVFWFLSA-N Linagliptin Chemical compound N=1C=2N(C)C(=O)N(CC=3N=C4C=CC=CC4=C(C)N=3)C(=O)C=2N(CC#CC)C=1N1CCC[C@@H](N)C1 LTXREWYXXSTFRX-QGZVFWFLSA-N 0.000 claims description 6
- YSDQQAXHVYUZIW-QCIJIYAXSA-N Liraglutide Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCNC(=O)CC[C@H](NC(=O)CCCCCCCCCCCCCCC)C(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=C(O)C=C1 YSDQQAXHVYUZIW-QCIJIYAXSA-N 0.000 claims description 6
- 108010019598 Liraglutide Proteins 0.000 claims description 6
- 102100038831 Peroxisome proliferator-activated receptor alpha Human genes 0.000 claims description 6
- 239000002333 angiotensin II receptor antagonist Substances 0.000 claims description 6
- 229960005370 atorvastatin Drugs 0.000 claims description 6
- 125000002843 carboxylic acid group Chemical group 0.000 claims description 6
- PNDKCRDVVKJPKG-WHERJAGFSA-N cenicriviroc Chemical compound C1=CC(OCCOCCCC)=CC=C1C1=CC=C(N(CC(C)C)CCC\C(=C/2)C(=O)NC=3C=CC(=CC=3)[S@@](=O)CC=3N(C=NC=3)CCC)C\2=C1 PNDKCRDVVKJPKG-WHERJAGFSA-N 0.000 claims description 6
- 229950011033 cenicriviroc Drugs 0.000 claims description 6
- 229950005980 cobiprostone Drugs 0.000 claims description 6
- UFULAYFCSOUIOV-UHFFFAOYSA-N cysteamine Chemical compound NCCS UFULAYFCSOUIOV-UHFFFAOYSA-N 0.000 claims description 6
- 229940121360 farnesoid X receptor (fxr) agonists Drugs 0.000 claims description 6
- AFLFKFHDSCQHOL-IZZDOVSWSA-N gft505 Chemical compound C1=CC(SC)=CC=C1C(=O)\C=C\C1=CC(C)=C(OC(C)(C)C(O)=O)C(C)=C1 AFLFKFHDSCQHOL-IZZDOVSWSA-N 0.000 claims description 6
- 229960003180 glutathione Drugs 0.000 claims description 6
- 108700012707 hepatitis C virus NS3 Proteins 0.000 claims description 6
- 229960002003 hydrochlorothiazide Drugs 0.000 claims description 6
- 239000002471 hydroxymethylglutaryl coenzyme A reductase inhibitor Substances 0.000 claims description 6
- 229960002600 icosapent ethyl Drugs 0.000 claims description 6
- 210000003405 ileum Anatomy 0.000 claims description 6
- NRYBAZVQPHGZNS-ZSOCWYAHSA-N leptin Chemical class O=C([C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](N)CC(C)C)CCSC)N1CCC[C@H]1C(=O)NCC(=O)N[C@@H](CS)C(O)=O NRYBAZVQPHGZNS-ZSOCWYAHSA-N 0.000 claims description 6
- 239000003446 ligand Substances 0.000 claims description 6
- 229960002397 linagliptin Drugs 0.000 claims description 6
- 229960002701 liraglutide Drugs 0.000 claims description 6
- 101150062900 lpl gene Proteins 0.000 claims description 6
- 229960003151 mercaptamine Drugs 0.000 claims description 6
- ZXERDUOLZKYMJM-ZWECCWDJSA-N obeticholic acid Chemical compound C([C@@]12C)C[C@@H](O)C[C@H]1[C@@H](CC)[C@@H](O)[C@@H]1[C@@H]2CC[C@]2(C)[C@@H]([C@H](C)CCC(O)=O)CC[C@H]21 ZXERDUOLZKYMJM-ZWECCWDJSA-N 0.000 claims description 6
- 229960001601 obeticholic acid Drugs 0.000 claims description 6
- 108091012330 pegilodecakin Proteins 0.000 claims description 6
- 229950007092 pegilodecakin Drugs 0.000 claims description 6
- 108091008725 peroxisome proliferator-activated receptors alpha Proteins 0.000 claims description 6
- 229960005095 pioglitazone Drugs 0.000 claims description 6
- CJMKTEIIPMBTJB-DXFHJFHKSA-M potassium;[(2r,3r,4s,5r,6r)-6-[[3-[(3s,4r,5r)-3-butyl-7-(dimethylamino)-3-ethyl-4-hydroxy-1,1-dioxo-4,5-dihydro-2h-1$l^{6}-benzothiepin-5-yl]phenyl]carbamoylamino]-3,5-dihydroxy-4-phenylmethoxyoxan-2-yl]methyl sulfate Chemical compound [K+].O([C@H]1[C@H](O)[C@@H](COS([O-])(=O)=O)O[C@H]([C@@H]1O)NC(=O)NC=1C=CC=C(C=1)[C@@H]1C2=CC(=CC=C2S(=O)(=O)C[C@@]([C@@H]1O)(CC)CCCC)N(C)C)CC1=CC=CC=C1 CJMKTEIIPMBTJB-DXFHJFHKSA-M 0.000 claims description 6
- FDBYIYFVSAHJLY-UHFFFAOYSA-N resmetirom Chemical compound N1C(=O)C(C(C)C)=CC(OC=2C(=CC(=CC=2Cl)N2C(NC(=O)C(C#N)=N2)=O)Cl)=N1 FDBYIYFVSAHJLY-UHFFFAOYSA-N 0.000 claims description 6
- 108010003524 sodium-bile acid cotransporter Proteins 0.000 claims description 6
- 229950008588 solithromycin Drugs 0.000 claims description 6
- 239000000021 stimulant Substances 0.000 claims description 6
- 125000001425 triazolyl group Chemical group 0.000 claims description 6
- SGKRLCUYIXIAHR-AKNGSSGZSA-N (4s,4ar,5s,5ar,6r,12ar)-4-(dimethylamino)-1,5,10,11,12a-pentahydroxy-6-methyl-3,12-dioxo-4a,5,5a,6-tetrahydro-4h-tetracene-2-carboxamide Chemical compound C1=CC=C2[C@H](C)[C@@H]([C@H](O)[C@@H]3[C@](C(O)=C(C(N)=O)C(=O)[C@H]3N(C)C)(O)C3=O)C3=C(O)C2=C1O SGKRLCUYIXIAHR-AKNGSSGZSA-N 0.000 claims description 5
- FFTVPQUHLQBXQZ-KVUCHLLUSA-N (4s,4as,5ar,12ar)-4,7-bis(dimethylamino)-1,10,11,12a-tetrahydroxy-3,12-dioxo-4a,5,5a,6-tetrahydro-4h-tetracene-2-carboxamide Chemical compound C1C2=C(N(C)C)C=CC(O)=C2C(O)=C2[C@@H]1C[C@H]1[C@H](N(C)C)C(=O)C(C(N)=O)=C(O)[C@@]1(O)C2=O FFTVPQUHLQBXQZ-KVUCHLLUSA-N 0.000 claims description 5
- 229940123263 Phosphodiesterase 3 inhibitor Drugs 0.000 claims description 5
- 239000004098 Tetracycline Substances 0.000 claims description 5
- KPWYNAGOBXLMSE-UHFFFAOYSA-N Tipelukast Chemical compound CCCC1=C(O)C(C(C)=O)=CC=C1SCCCOC1=CC=C(C(C)=O)C(OCCCC(O)=O)=C1CCC KPWYNAGOBXLMSE-UHFFFAOYSA-N 0.000 claims description 5
- 229960002916 adapalene Drugs 0.000 claims description 5
- LZCDAPDGXCYOEH-UHFFFAOYSA-N adapalene Chemical compound C1=C(C(O)=O)C=CC2=CC(C3=CC=C(C(=C3)C34CC5CC(CC(C5)C3)C4)OC)=CC=C21 LZCDAPDGXCYOEH-UHFFFAOYSA-N 0.000 claims description 5
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 claims description 5
- 229960002227 clindamycin Drugs 0.000 claims description 5
- KDLRVYVGXIQJDK-AWPVFWJPSA-N clindamycin Chemical compound CN1C[C@H](CCC)C[C@H]1C(=O)N[C@H]([C@H](C)Cl)[C@@H]1[C@H](O)[C@H](O)[C@@H](O)[C@@H](SC)O1 KDLRVYVGXIQJDK-AWPVFWJPSA-N 0.000 claims description 5
- 229960003722 doxycycline Drugs 0.000 claims description 5
- 229960003276 erythromycin Drugs 0.000 claims description 5
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 claims description 5
- 229960004023 minocycline Drugs 0.000 claims description 5
- 239000002570 phosphodiesterase III inhibitor Substances 0.000 claims description 5
- 230000000306 recurrent effect Effects 0.000 claims description 5
- 229960002180 tetracycline Drugs 0.000 claims description 5
- 229930101283 tetracycline Natural products 0.000 claims description 5
- 235000019364 tetracycline Nutrition 0.000 claims description 5
- 150000003522 tetracyclines Chemical class 0.000 claims description 5
- 229950004996 tipelukast Drugs 0.000 claims description 5
- 229960001727 tretinoin Drugs 0.000 claims description 5
- FPIPGXGPPPQFEQ-UHFFFAOYSA-N 13-cis retinol Natural products OCC=C(C)C=CC=C(C)C=CC1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-UHFFFAOYSA-N 0.000 claims description 4
- 229940123932 Phosphodiesterase 4 inhibitor Drugs 0.000 claims description 4
- 102100033451 Thyroid hormone receptor beta Human genes 0.000 claims description 4
- 108060008539 Transglutaminase Proteins 0.000 claims description 4
- OGQICQVSFDPSEI-UHFFFAOYSA-N Zorac Chemical compound N1=CC(C(=O)OCC)=CC=C1C#CC1=CC=C(SCCC2(C)C)C2=C1 OGQICQVSFDPSEI-UHFFFAOYSA-N 0.000 claims description 4
- 229940125388 beta agonist Drugs 0.000 claims description 4
- 230000003115 biocidal effect Effects 0.000 claims description 4
- VAOCPAMSLUNLGC-UHFFFAOYSA-N metronidazole Chemical compound CC1=NC=C([N+]([O-])=O)N1CCO VAOCPAMSLUNLGC-UHFFFAOYSA-N 0.000 claims description 4
- 229960000282 metronidazole Drugs 0.000 claims description 4
- 239000002587 phosphodiesterase IV inhibitor Substances 0.000 claims description 4
- 229960003471 retinol Drugs 0.000 claims description 4
- 235000020944 retinol Nutrition 0.000 claims description 4
- 239000011607 retinol Substances 0.000 claims description 4
- SKIVFJLNDNKQPD-UHFFFAOYSA-N sulfacetamide Chemical compound CC(=O)NS(=O)(=O)C1=CC=C(N)C=C1 SKIVFJLNDNKQPD-UHFFFAOYSA-N 0.000 claims description 4
- 229960002673 sulfacetamide Drugs 0.000 claims description 4
- 229960000565 tazarotene Drugs 0.000 claims description 4
- 108091008762 thyroid hormone receptors ß Proteins 0.000 claims description 4
- 102000003601 transglutaminase Human genes 0.000 claims description 4
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims description 3
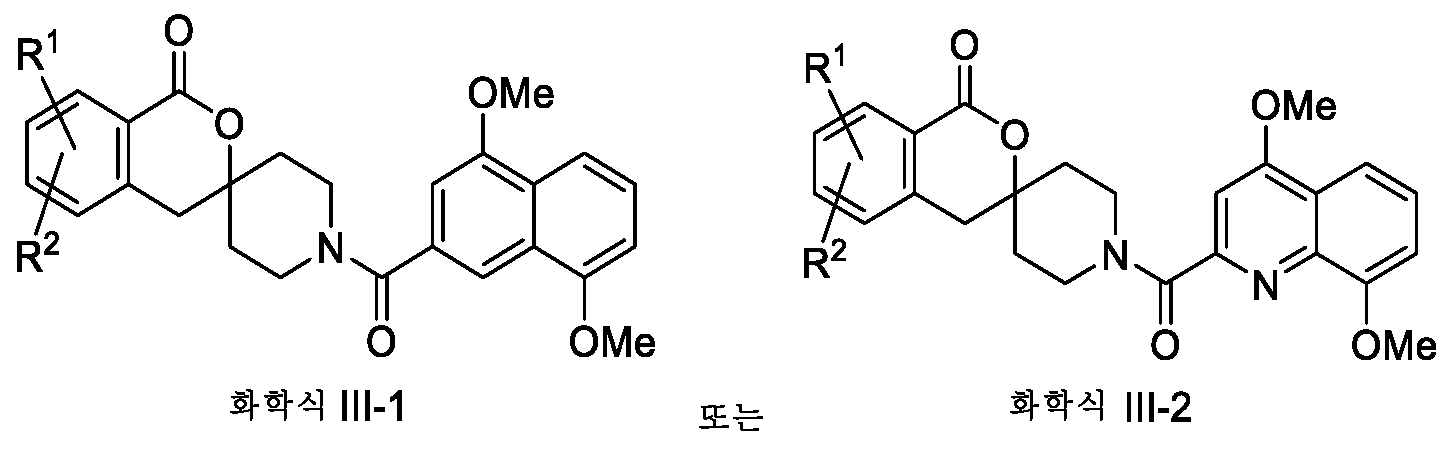
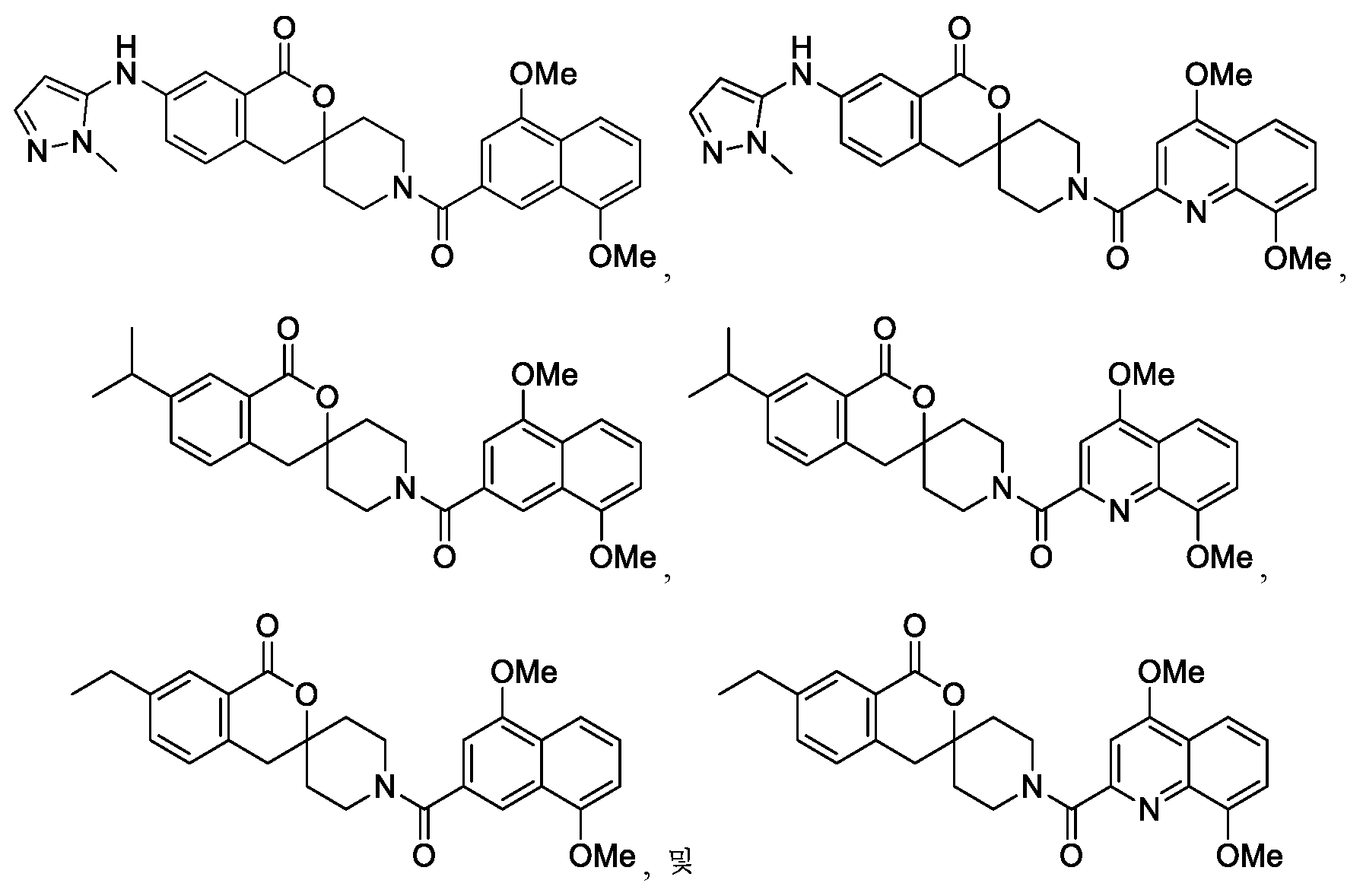
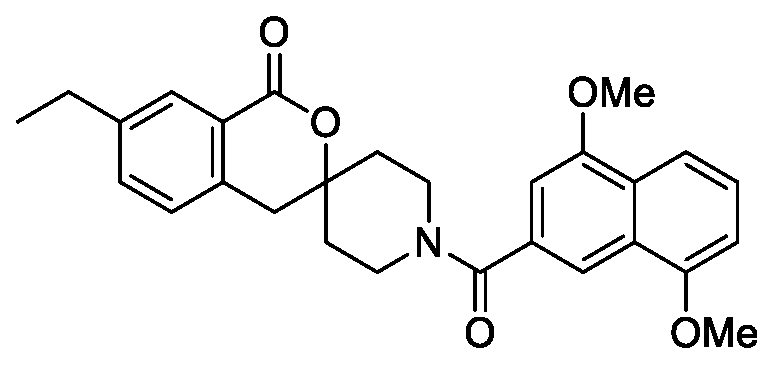
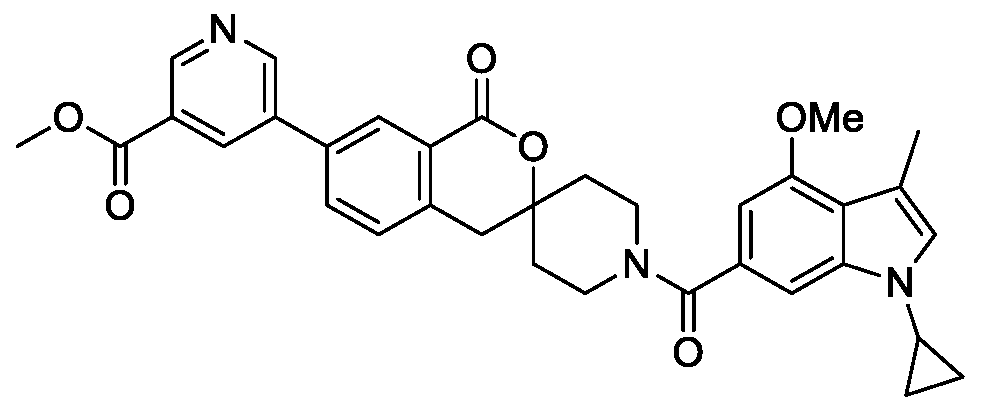
- JXCOMKILRUYASG-UHFFFAOYSA-N CCc1ccc2CC3(CCN(CC3)C(=O)c3cc(OC)c4cccc(OC)c4c3)OC(=O)c2c1 Chemical compound CCc1ccc2CC3(CCN(CC3)C(=O)c3cc(OC)c4cccc(OC)c4c3)OC(=O)c2c1 JXCOMKILRUYASG-UHFFFAOYSA-N 0.000 claims description 3
- JQNOSUAHJFMMBW-UHFFFAOYSA-N CCc1ccc2CC3(CCN(CC3)C(=O)c3cc(OC)c4cccc(OC)c4n3)OC(=O)c2c1 Chemical compound CCc1ccc2CC3(CCN(CC3)C(=O)c3cc(OC)c4cccc(OC)c4n3)OC(=O)c2c1 JQNOSUAHJFMMBW-UHFFFAOYSA-N 0.000 claims description 3
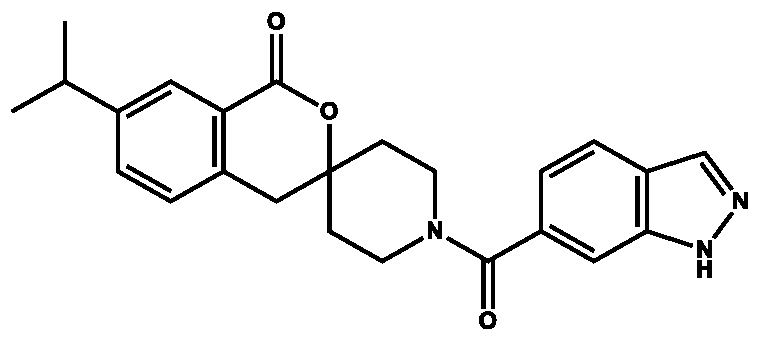
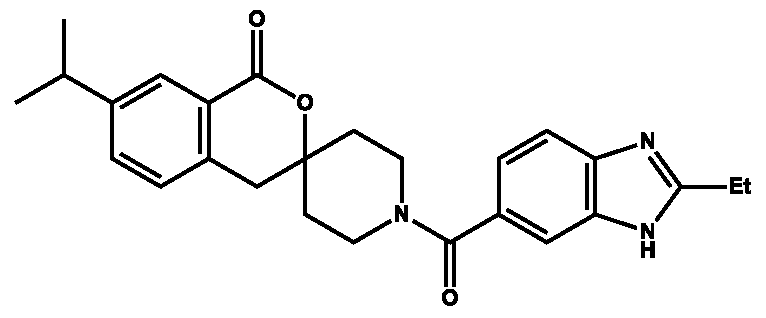
- KAFIAZORSPHRPW-UHFFFAOYSA-N CCc1nc2ccc(cc2[nH]1)C(=O)N1CCC2(CC1)Cc1ccc(cc1C(=O)O2)C(C)C Chemical compound CCc1nc2ccc(cc2[nH]1)C(=O)N1CCC2(CC1)Cc1ccc(cc1C(=O)O2)C(C)C KAFIAZORSPHRPW-UHFFFAOYSA-N 0.000 claims description 3
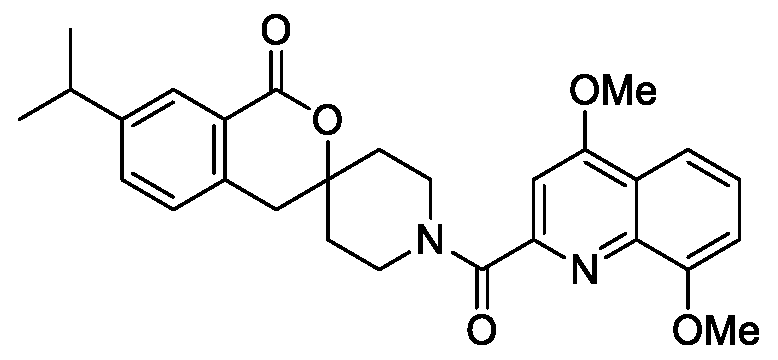
- XAVOIUXGIQDQAX-UHFFFAOYSA-N COc1ccc2ncc(cc2c1)C(=O)N1CCC2(CC1)Cc1ccc(cc1C(=O)O2)C(C)C Chemical compound COc1ccc2ncc(cc2c1)C(=O)N1CCC2(CC1)Cc1ccc(cc1C(=O)O2)C(C)C XAVOIUXGIQDQAX-UHFFFAOYSA-N 0.000 claims description 3
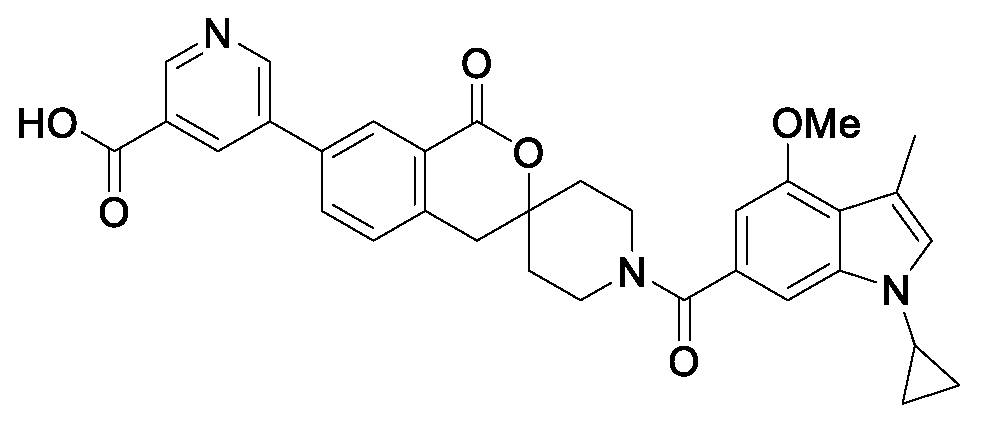
- WOSGFGVMQGSUFU-UHFFFAOYSA-N COc1cccc2c(OC)cc(cc12)C(=O)N1CCC2(CC1)Cc1ccc(cc1C(=O)O2)C(C)C Chemical compound COc1cccc2c(OC)cc(cc12)C(=O)N1CCC2(CC1)Cc1ccc(cc1C(=O)O2)C(C)C WOSGFGVMQGSUFU-UHFFFAOYSA-N 0.000 claims description 3
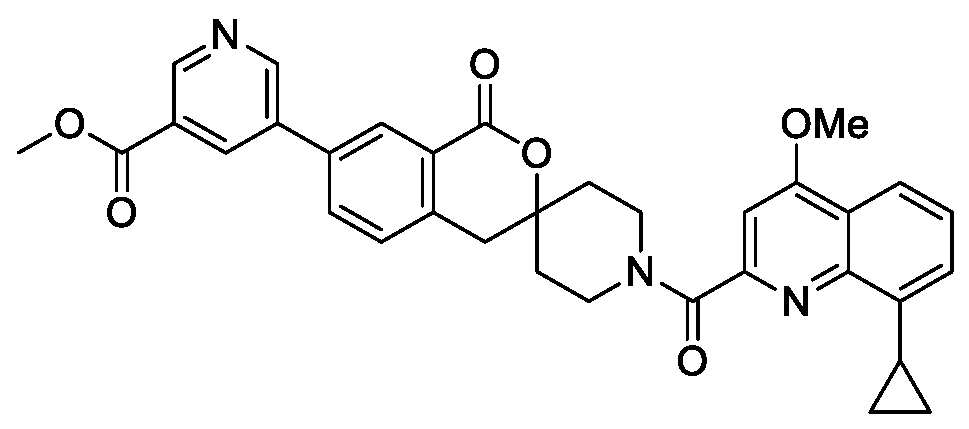
- GPXBFHUOVYXQKP-UHFFFAOYSA-N COc1cccc2c(OC)cc(nc12)C(=O)N1CCC2(CC1)Cc1ccc(cc1C(=O)O2)C(C)C Chemical compound COc1cccc2c(OC)cc(nc12)C(=O)N1CCC2(CC1)Cc1ccc(cc1C(=O)O2)C(C)C GPXBFHUOVYXQKP-UHFFFAOYSA-N 0.000 claims description 3
- 108010016731 PPAR gamma Proteins 0.000 claims description 3
- 102100038824 Peroxisome proliferator-activated receptor delta Human genes 0.000 claims description 3
- 102100038825 Peroxisome proliferator-activated receptor gamma Human genes 0.000 claims description 3
- 108091008765 peroxisome proliferator-activated receptors β/δ Proteins 0.000 claims description 3
- 150000004492 retinoid derivatives Chemical class 0.000 claims description 3
- AWUAOFONWXKBBD-UHFFFAOYSA-N CC(C)c1ccc2CC3(CCN(CC3)C(=O)c3ccc4[nH]c(=O)n(C)c4c3)OC(=O)c2c1 Chemical compound CC(C)c1ccc2CC3(CCN(CC3)C(=O)c3ccc4[nH]c(=O)n(C)c4c3)OC(=O)c2c1 AWUAOFONWXKBBD-UHFFFAOYSA-N 0.000 claims description 2
- MMHFATNHZCVGRP-UHFFFAOYSA-N CC(C)c1ccc2CC3(CCN(CC3)C(=O)c3ccc4nc(C)[nH]c4c3)OC(=O)c2c1 Chemical compound CC(C)c1ccc2CC3(CCN(CC3)C(=O)c3ccc4nc(C)[nH]c4c3)OC(=O)c2c1 MMHFATNHZCVGRP-UHFFFAOYSA-N 0.000 claims description 2
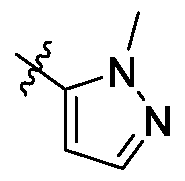
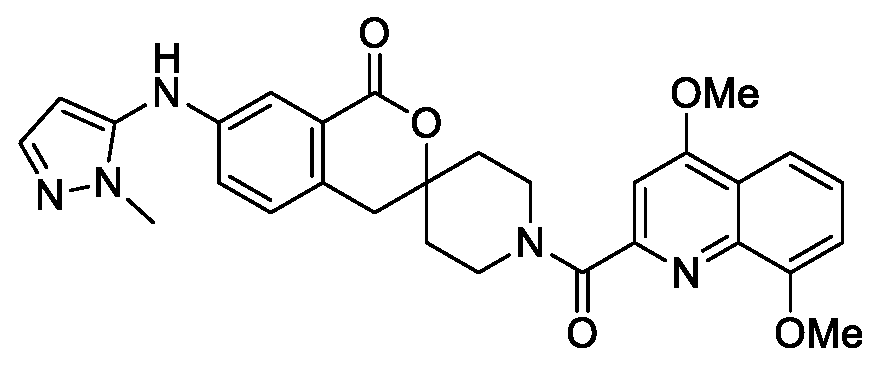
- OISOGTAQARTQNT-UHFFFAOYSA-N COc1cccc2c(OC)cc(cc12)C(=O)N1CCC2(CC1)Cc1ccc(Nc3ccnn3C)cc1C(=O)O2 Chemical compound COc1cccc2c(OC)cc(cc12)C(=O)N1CCC2(CC1)Cc1ccc(Nc3ccnn3C)cc1C(=O)O2 OISOGTAQARTQNT-UHFFFAOYSA-N 0.000 claims description 2
- HEBMCVBCEDMUOF-UHFFFAOYSA-N isochromane Chemical compound C1=CC=C2COCCC2=C1 HEBMCVBCEDMUOF-UHFFFAOYSA-N 0.000 claims description 2
- 108010001517 Galectin 3 Proteins 0.000 claims 2
- 102100039558 Galectin-3 Human genes 0.000 claims 2
- UAOCLDQAQNNEAX-ABMICEGHSA-N remogliflozin etabonate Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](COC(=O)OCC)O[C@H]1OC1=NN(C(C)C)C(C)=C1CC1=CC=C(OC(C)C)C=C1 UAOCLDQAQNNEAX-ABMICEGHSA-N 0.000 claims 2
- 229950011516 remogliflozin etabonate Drugs 0.000 claims 2
- MWTVNTKQRZEJFI-UHFFFAOYSA-N COc1cccc2c(OC)cc(nc12)C(=O)N1CCC2(CC1)Cc1ccc(Nc3ccnn3C)cc1C(=O)O2 Chemical compound COc1cccc2c(OC)cc(nc12)C(=O)N1CCC2(CC1)Cc1ccc(Nc3ccnn3C)cc1C(=O)O2 MWTVNTKQRZEJFI-UHFFFAOYSA-N 0.000 claims 1
- 241000220317 Rosa Species 0.000 claims 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 claims 1
- SNJCRKAPYZZDKF-UHFFFAOYSA-N spiro[4h-isochromene-3,4'-piperidine]-1-one Chemical compound C1C2=CC=CC=C2C(=O)OC21CCNCC2 SNJCRKAPYZZDKF-UHFFFAOYSA-N 0.000 claims 1
- 229960002256 spironolactone Drugs 0.000 abstract description 28
- 206010028980 Neoplasm Diseases 0.000 abstract description 11
- 201000011510 cancer Diseases 0.000 abstract description 11
- 102100039164 Acetyl-CoA carboxylase 1 Human genes 0.000 abstract 2
- 102100021641 Acetyl-CoA carboxylase 2 Human genes 0.000 abstract 2
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 45
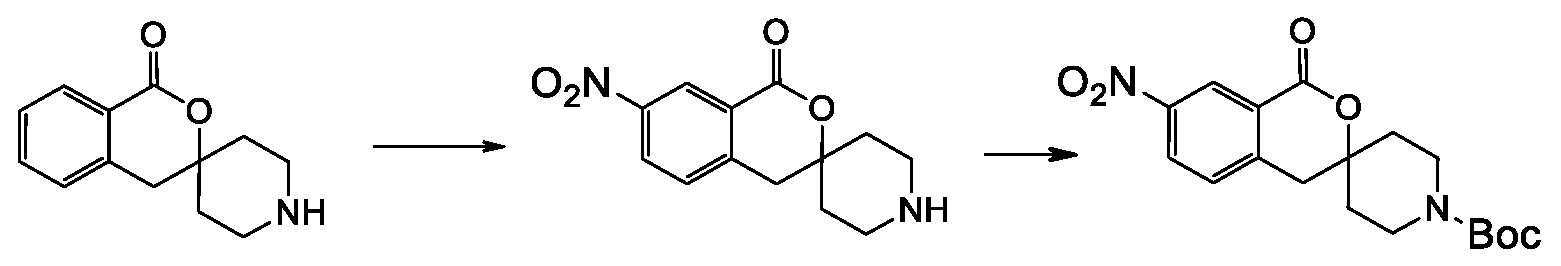
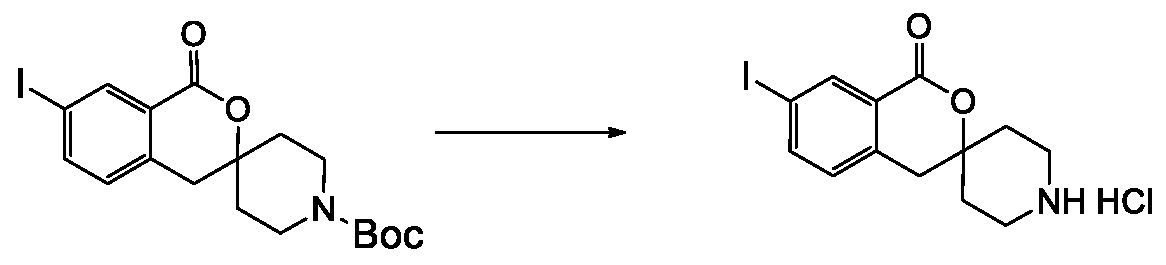
- 238000003786 synthesis reaction Methods 0.000 description 34
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 33
- 230000015572 biosynthetic process Effects 0.000 description 30
- 125000000304 alkynyl group Chemical group 0.000 description 29
- 239000000203 mixture Substances 0.000 description 29
- 125000003342 alkenyl group Chemical group 0.000 description 27
- 238000005481 NMR spectroscopy Methods 0.000 description 26
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 24
- 239000013543 active substance Substances 0.000 description 19
- 210000002374 sebum Anatomy 0.000 description 18
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 17
- 239000012049 topical pharmaceutical composition Substances 0.000 description 17
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 16
- 238000006243 chemical reaction Methods 0.000 description 16
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 15
- 229940121373 acetyl-coa carboxylase inhibitor Drugs 0.000 description 15
- 239000007787 solid Substances 0.000 description 15
- 239000000243 solution Substances 0.000 description 15
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 14
- 239000001963 growth medium Substances 0.000 description 14
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 13
- 241000699670 Mus sp. Species 0.000 description 13
- 125000005843 halogen group Chemical group 0.000 description 13
- 208000030159 metabolic disease Diseases 0.000 description 13
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 12
- 238000009472 formulation Methods 0.000 description 12
- 125000001188 haloalkyl group Chemical group 0.000 description 12
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 12
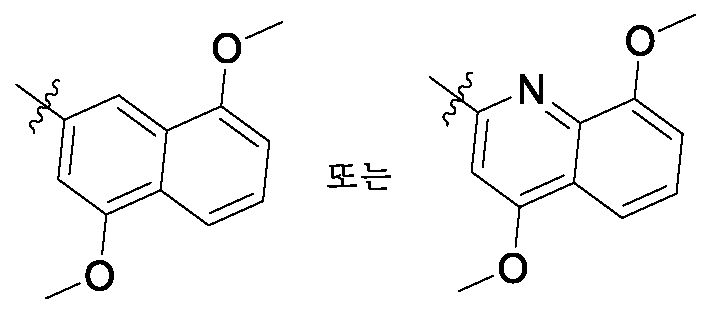
- VLSHUNALBMISTE-UHFFFAOYSA-N 4,8-dimethoxynaphthalene-2-carboxylic acid Chemical compound C1=C(C(O)=O)C=C2C(OC)=CC=CC2=C1OC VLSHUNALBMISTE-UHFFFAOYSA-N 0.000 description 11
- 239000003153 chemical reaction reagent Substances 0.000 description 11
- 210000004185 liver Anatomy 0.000 description 11
- 238000002360 preparation method Methods 0.000 description 11
- 210000001732 sebaceous gland Anatomy 0.000 description 11
- 239000003981 vehicle Substances 0.000 description 11
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 10
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 10
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 10
- 239000000843 powder Substances 0.000 description 10
- 125000003107 substituted aryl group Chemical group 0.000 description 10
- 230000000699 topical effect Effects 0.000 description 10
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 9
- 235000019000 fluorine Nutrition 0.000 description 9
- 229910052757 nitrogen Inorganic materials 0.000 description 9
- 238000002560 therapeutic procedure Methods 0.000 description 9
- 210000001519 tissue Anatomy 0.000 description 9
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 8
- ZSLZBFCDCINBPY-ZSJPKINUSA-N acetyl-CoA Chemical compound O[C@@H]1[C@H](OP(O)(O)=O)[C@@H](COP(O)(=O)OP(O)(=O)OCC(C)(C)[C@@H](O)C(=O)NCCC(=O)NCCSC(=O)C)O[C@H]1N1C2=NC=NC(N)=C2N=C1 ZSLZBFCDCINBPY-ZSJPKINUSA-N 0.000 description 8
- 238000002648 combination therapy Methods 0.000 description 8
- 125000005842 heteroatom Chemical group 0.000 description 8
- 230000000670 limiting effect Effects 0.000 description 8
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 8
- 125000003003 spiro group Chemical group 0.000 description 8
- 150000003626 triacylglycerols Chemical class 0.000 description 8
- 241001303601 Rosacea Species 0.000 description 7
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 7
- 229910052794 bromium Inorganic materials 0.000 description 7
- 230000036470 plasma concentration Effects 0.000 description 7
- 125000006239 protecting group Chemical group 0.000 description 7
- 201000004700 rosacea Diseases 0.000 description 7
- 239000006228 supernatant Substances 0.000 description 7
- 0 *C(*(CC1)CCC1(Cc1ccccc11)OC1=O)=O Chemical compound *C(*(CC1)CCC1(Cc1ccccc11)OC1=O)=O 0.000 description 6
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 6
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 6
- NTYJJOPFIAHURM-UHFFFAOYSA-N Histamine Chemical compound NCCC1=CN=CN1 NTYJJOPFIAHURM-UHFFFAOYSA-N 0.000 description 6
- 229940088710 antibiotic agent Drugs 0.000 description 6
- 125000004452 carbocyclyl group Chemical group 0.000 description 6
- 239000000460 chlorine Substances 0.000 description 6
- 229910052801 chlorine Inorganic materials 0.000 description 6
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 6
- 239000012043 crude product Substances 0.000 description 6
- 125000004122 cyclic group Chemical group 0.000 description 6
- 238000011161 development Methods 0.000 description 6
- 235000014113 dietary fatty acids Nutrition 0.000 description 6
- 238000010790 dilution Methods 0.000 description 6
- 239000012895 dilution Substances 0.000 description 6
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 6
- 238000001704 evaporation Methods 0.000 description 6
- 230000008020 evaporation Effects 0.000 description 6
- 239000000194 fatty acid Substances 0.000 description 6
- 229930195729 fatty acid Natural products 0.000 description 6
- 229910052731 fluorine Inorganic materials 0.000 description 6
- 238000011534 incubation Methods 0.000 description 6
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 6
- 239000006210 lotion Substances 0.000 description 6
- 239000002609 medium Substances 0.000 description 6
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 6
- 125000004043 oxo group Chemical group O=* 0.000 description 6
- 229910052760 oxygen Inorganic materials 0.000 description 6
- 239000002953 phosphate buffered saline Substances 0.000 description 6
- 238000011002 quantification Methods 0.000 description 6
- 150000003254 radicals Chemical class 0.000 description 6
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 6
- 238000013207 serial dilution Methods 0.000 description 6
- 238000011200 topical administration Methods 0.000 description 6
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical group N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 5
- 125000006376 (C3-C10) cycloalkyl group Chemical group 0.000 description 5
- 229940124125 5 Lipoxygenase inhibitor Drugs 0.000 description 5
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical class Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 5
- 239000000867 Lipoxygenase Inhibitor Substances 0.000 description 5
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 5
- 238000005859 coupling reaction Methods 0.000 description 5
- 150000004665 fatty acids Chemical class 0.000 description 5
- 235000011187 glycerol Nutrition 0.000 description 5
- 210000005260 human cell Anatomy 0.000 description 5
- IBTWUVRCFHJPKN-UHFFFAOYSA-N hydron;pyridine-3-carboxylic acid;chloride Chemical compound Cl.OC(=O)C1=CC=CN=C1 IBTWUVRCFHJPKN-UHFFFAOYSA-N 0.000 description 5
- 238000011532 immunohistochemical staining Methods 0.000 description 5
- 238000002347 injection Methods 0.000 description 5
- 239000007924 injection Substances 0.000 description 5
- 239000003921 oil Substances 0.000 description 5
- 239000001301 oxygen Substances 0.000 description 5
- 239000012071 phase Substances 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 239000011541 reaction mixture Substances 0.000 description 5
- 208000017520 skin disease Diseases 0.000 description 5
- 239000011734 sodium Substances 0.000 description 5
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 description 4
- RUDATBOHQWOJDD-UHFFFAOYSA-N (3beta,5beta,7alpha)-3,7-Dihydroxycholan-24-oic acid Natural products OC1CC2CC(O)CCC2(C)C2C1C1CCC(C(CCC(O)=O)C)C1(C)CC2 RUDATBOHQWOJDD-UHFFFAOYSA-N 0.000 description 4
- 125000000171 (C1-C6) haloalkyl group Chemical group 0.000 description 4
- 125000006708 (C5-C14) heteroaryl group Chemical group 0.000 description 4
- VTAKZNRDSPNOAU-UHFFFAOYSA-M 2-(chloromethyl)oxirane;hydron;prop-2-en-1-amine;n-prop-2-enyldecan-1-amine;trimethyl-[6-(prop-2-enylamino)hexyl]azanium;dichloride Chemical compound Cl.[Cl-].NCC=C.ClCC1CO1.CCCCCCCCCCNCC=C.C[N+](C)(C)CCCCCCNCC=C VTAKZNRDSPNOAU-UHFFFAOYSA-M 0.000 description 4
- LTYOQGRJFJAKNA-PLHOLKBESA-N 3-[2-[3-[[(2R)-4-[[[(2R,3S,4R,5R)-5-(6-aminopurin-9-yl)-4-hydroxy-3-phosphonooxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-hydroxyphosphoryl]oxy-2-hydroxy-3,3-dimethylbutanoyl]amino]propanoylamino]ethylsulfanyl]-3-oxo(313C)propanoic acid Chemical compound [13C](CC(=O)O)(=O)SCCNC(CCNC([C@@H](C(COP(OP(OC[C@@H]1[C@H]([C@H]([C@@H](O1)N1C=NC=2C(N)=NC=NC1=2)O)OP(=O)(O)O)(=O)O)(=O)O)(C)C)O)=O)=O LTYOQGRJFJAKNA-PLHOLKBESA-N 0.000 description 4
- YPFZNQWLNDDXEJ-UHFFFAOYSA-N 4,8-dimethoxyquinoline-2-carboxylic acid Chemical compound C1=C(C(O)=O)N=C2C(OC)=CC=CC2=C1OC YPFZNQWLNDDXEJ-UHFFFAOYSA-N 0.000 description 4
- 125000006163 5-membered heteroaryl group Chemical group 0.000 description 4
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 4
- 239000004342 Benzoyl peroxide Substances 0.000 description 4
- OMPJBNCRMGITSC-UHFFFAOYSA-N Benzoylperoxide Chemical compound C=1C=CC=CC=1C(=O)OOC(=O)C1=CC=CC=C1 OMPJBNCRMGITSC-UHFFFAOYSA-N 0.000 description 4
- 125000006374 C2-C10 alkenyl group Chemical group 0.000 description 4
- 229920002905 Colesevelam Polymers 0.000 description 4
- 229940126043 Galectin-3 inhibitor Drugs 0.000 description 4
- WZUVPPKBWHMQCE-UHFFFAOYSA-N Haematoxylin Chemical compound C12=CC(O)=C(O)C=C2CC2(O)C1C1=CC=C(O)C(O)=C1OC2 WZUVPPKBWHMQCE-UHFFFAOYSA-N 0.000 description 4
- 241001465754 Metazoa Species 0.000 description 4
- 206010033307 Overweight Diseases 0.000 description 4
- 235000019483 Peanut oil Nutrition 0.000 description 4
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 4
- YASAKCUCGLMORW-UHFFFAOYSA-N Rosiglitazone Chemical compound C=1C=CC=NC=1N(C)CCOC(C=C1)=CC=C1CC1SC(=O)NC1=O YASAKCUCGLMORW-UHFFFAOYSA-N 0.000 description 4
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 4
- 235000019400 benzoyl peroxide Nutrition 0.000 description 4
- 239000008280 blood Substances 0.000 description 4
- 210000004369 blood Anatomy 0.000 description 4
- 230000037396 body weight Effects 0.000 description 4
- 239000000872 buffer Substances 0.000 description 4
- 125000004432 carbon atom Chemical group C* 0.000 description 4
- 229960001152 colesevelam Drugs 0.000 description 4
- 239000006071 cream Substances 0.000 description 4
- 208000016097 disease of metabolism Diseases 0.000 description 4
- 238000005516 engineering process Methods 0.000 description 4
- 238000001952 enzyme assay Methods 0.000 description 4
- 150000002148 esters Chemical class 0.000 description 4
- 229950009769 etabonate Drugs 0.000 description 4
- 230000004136 fatty acid synthesis Effects 0.000 description 4
- 239000000945 filler Substances 0.000 description 4
- 238000003304 gavage Methods 0.000 description 4
- 239000000499 gel Substances 0.000 description 4
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 4
- 208000019423 liver disease Diseases 0.000 description 4
- BDJRBEYXGGNYIS-UHFFFAOYSA-N nonanedioic acid Chemical compound OC(=O)CCCCCCCC(O)=O BDJRBEYXGGNYIS-UHFFFAOYSA-N 0.000 description 4
- 235000019198 oils Nutrition 0.000 description 4
- 239000002674 ointment Substances 0.000 description 4
- 238000007254 oxidation reaction Methods 0.000 description 4
- 239000006072 paste Substances 0.000 description 4
- 239000000312 peanut oil Substances 0.000 description 4
- 238000012746 preparative thin layer chromatography Methods 0.000 description 4
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- 125000006413 ring segment Chemical group 0.000 description 4
- 239000012723 sample buffer Substances 0.000 description 4
- 239000001509 sodium citrate Substances 0.000 description 4
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 4
- 239000000725 suspension Substances 0.000 description 4
- 125000001544 thienyl group Chemical group 0.000 description 4
- RUDATBOHQWOJDD-UZVSRGJWSA-N ursodeoxycholic acid Chemical compound C([C@H]1C[C@@H]2O)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(O)=O)C)[C@@]2(C)CC1 RUDATBOHQWOJDD-UZVSRGJWSA-N 0.000 description 4
- 229960001661 ursodiol Drugs 0.000 description 4
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- 102000004276 BCL2-related protein A1 Human genes 0.000 description 3
- 238000011746 C57BL/6J (JAX™ mouse strain) Methods 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 3
- 241000699800 Cricetinae Species 0.000 description 3
- 108010061435 Enalapril Proteins 0.000 description 3
- 208000009774 Follicular Cyst Diseases 0.000 description 3
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 3
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 3
- 239000007995 HEPES buffer Substances 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 101000963424 Homo sapiens Acetyl-CoA carboxylase 1 Proteins 0.000 description 3
- 241000283973 Oryctolagus cuniculus Species 0.000 description 3
- 229940122054 Peroxisome proliferator-activated receptor delta agonist Drugs 0.000 description 3
- 229940080774 Peroxisome proliferator-activated receptor gamma agonist Drugs 0.000 description 3
- 102000001708 Protein Isoforms Human genes 0.000 description 3
- 108010029485 Protein Isoforms Proteins 0.000 description 3
- 206010039792 Seborrhoea Diseases 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 210000000577 adipose tissue Anatomy 0.000 description 3
- 125000005907 alkyl ester group Chemical group 0.000 description 3
- BFNBIHQBYMNNAN-UHFFFAOYSA-N ammonium sulfate Chemical class N.N.OS(O)(=O)=O BFNBIHQBYMNNAN-UHFFFAOYSA-N 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 3
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 3
- 229960002685 biotin Drugs 0.000 description 3
- 235000020958 biotin Nutrition 0.000 description 3
- 239000011616 biotin Substances 0.000 description 3
- 229910052799 carbon Inorganic materials 0.000 description 3
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 3
- 238000004113 cell culture Methods 0.000 description 3
- 235000010980 cellulose Nutrition 0.000 description 3
- 229920002678 cellulose Polymers 0.000 description 3
- 239000001913 cellulose Substances 0.000 description 3
- ZAIPMKNFIOOWCQ-UEKVPHQBSA-N cephalexin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@@H]3N(C2=O)C(=C(CS3)C)C(O)=O)=CC=CC=C1 ZAIPMKNFIOOWCQ-UEKVPHQBSA-N 0.000 description 3
- 238000004587 chromatography analysis Methods 0.000 description 3
- 230000001684 chronic effect Effects 0.000 description 3
- 229910052802 copper Inorganic materials 0.000 description 3
- 239000010949 copper Substances 0.000 description 3
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 3
- 230000001086 cytosolic effect Effects 0.000 description 3
- 238000000502 dialysis Methods 0.000 description 3
- UAOMVDZJSHZZME-UHFFFAOYSA-N diisopropylamine Chemical compound CC(C)NC(C)C UAOMVDZJSHZZME-UHFFFAOYSA-N 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 239000003814 drug Substances 0.000 description 3
- GBXSMTUPTTWBMN-XIRDDKMYSA-N enalapril Chemical compound C([C@@H](C(=O)OCC)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(O)=O)CC1=CC=CC=C1 GBXSMTUPTTWBMN-XIRDDKMYSA-N 0.000 description 3
- 229960000873 enalapril Drugs 0.000 description 3
- 239000003925 fat Substances 0.000 description 3
- 239000000835 fiber Substances 0.000 description 3
- 239000010408 film Substances 0.000 description 3
- 239000006260 foam Substances 0.000 description 3
- 125000000524 functional group Chemical group 0.000 description 3
- 239000003349 gelling agent Substances 0.000 description 3
- 230000012010 growth Effects 0.000 description 3
- 210000003494 hepatocyte Anatomy 0.000 description 3
- 229960001340 histamine Drugs 0.000 description 3
- 238000001802 infusion Methods 0.000 description 3
- 238000010253 intravenous injection Methods 0.000 description 3
- 229910052740 iodine Inorganic materials 0.000 description 3
- 150000002500 ions Chemical class 0.000 description 3
- 239000006166 lysate Substances 0.000 description 3
- 238000012423 maintenance Methods 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 230000004048 modification Effects 0.000 description 3
- 238000012986 modification Methods 0.000 description 3
- 239000012074 organic phase Substances 0.000 description 3
- 229910052763 palladium Inorganic materials 0.000 description 3
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 125000000714 pyrimidinyl group Chemical group 0.000 description 3
- 239000011535 reaction buffer Substances 0.000 description 3
- 229960004889 salicylic acid Drugs 0.000 description 3
- 239000000523 sample Substances 0.000 description 3
- 208000008742 seborrheic dermatitis Diseases 0.000 description 3
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 3
- 239000002453 shampoo Substances 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- 210000000434 stratum corneum Anatomy 0.000 description 3
- 238000005556 structure-activity relationship Methods 0.000 description 3
- 125000005415 substituted alkoxy group Chemical group 0.000 description 3
- 238000006467 substitution reaction Methods 0.000 description 3
- 239000011593 sulfur Substances 0.000 description 3
- 230000009885 systemic effect Effects 0.000 description 3
- 239000003826 tablet Substances 0.000 description 3
- 239000000454 talc Substances 0.000 description 3
- 229910052623 talc Inorganic materials 0.000 description 3
- 239000007930 transdermal spray Substances 0.000 description 3
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 3
- 229910052725 zinc Inorganic materials 0.000 description 3
- 239000011701 zinc Substances 0.000 description 3
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 description 2
- GVJHHUAWPYXKBD-UHFFFAOYSA-N (±)-α-Tocopherol Chemical compound OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 2
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 2
- 125000001622 2-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C(*)C([H])=C([H])C2=C1[H] 0.000 description 2
- XMTQQYYKAHVGBJ-UHFFFAOYSA-N 3-(3,4-DICHLOROPHENYL)-1,1-DIMETHYLUREA Chemical compound CN(C)C(=O)NC1=CC=C(Cl)C(Cl)=C1 XMTQQYYKAHVGBJ-UHFFFAOYSA-N 0.000 description 2
- CZRCFAOMWRAFIC-UHFFFAOYSA-N 5-(tetradecyloxy)-2-furoic acid Chemical compound CCCCCCCCCCCCCCOC1=CC=C(C(O)=O)O1 CZRCFAOMWRAFIC-UHFFFAOYSA-N 0.000 description 2
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 2
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 2
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 2
- 239000005695 Ammonium acetate Substances 0.000 description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 2
- VGTVJQAVZUQNNB-UHFFFAOYSA-N CC(C)c1ccc2CC3(CCN(CC3)C(=O)c3ccc4[nH]ncc4c3)OC(=O)c2c1 Chemical compound CC(C)c1ccc2CC3(CCN(CC3)C(=O)c3ccc4[nH]ncc4c3)OC(=O)c2c1 VGTVJQAVZUQNNB-UHFFFAOYSA-N 0.000 description 2
- YNHIYYNDYFIDSX-UHFFFAOYSA-N CC(C)c1ccc2CC3(CCN(CC3)C(=O)c3ccc4cn[nH]c4c3)OC(=O)c2c1 Chemical compound CC(C)c1ccc2CC3(CCN(CC3)C(=O)c3ccc4cn[nH]c4c3)OC(=O)c2c1 YNHIYYNDYFIDSX-UHFFFAOYSA-N 0.000 description 2
- SXCXZPAHYIENCQ-UHFFFAOYSA-N COc1cccc2c(OC)cc(cc12)C(=O)N1CCC2(CC1)Cc1ccc(I)cc1C(=O)O2 Chemical compound COc1cccc2c(OC)cc(cc12)C(=O)N1CCC2(CC1)Cc1ccc(I)cc1C(=O)O2 SXCXZPAHYIENCQ-UHFFFAOYSA-N 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical group [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- RGHNJXZEOKUKBD-SQOUGZDYSA-N D-gluconic acid Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O RGHNJXZEOKUKBD-SQOUGZDYSA-N 0.000 description 2
- 108020004414 DNA Proteins 0.000 description 2
- MQJKPEGWNLWLTK-UHFFFAOYSA-N Dapsone Chemical compound C1=CC(N)=CC=C1S(=O)(=O)C1=CC=C(N)C=C1 MQJKPEGWNLWLTK-UHFFFAOYSA-N 0.000 description 2
- 101100296720 Dictyostelium discoideum Pde4 gene Proteins 0.000 description 2
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 2
- DHCLVCXQIBBOPH-UHFFFAOYSA-N Glycerol 2-phosphate Chemical compound OCC(CO)OP(O)(O)=O DHCLVCXQIBBOPH-UHFFFAOYSA-N 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- 239000007821 HATU Substances 0.000 description 2
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 2
- 102000004877 Insulin Human genes 0.000 description 2
- 108090001061 Insulin Proteins 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 2
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 2
- 241000699666 Mus <mouse, genus> Species 0.000 description 2
- NPGIHFRTRXVWOY-UHFFFAOYSA-N Oil red O Chemical compound Cc1ccc(C)c(c1)N=Nc1cc(C)c(cc1C)N=Nc1c(O)ccc2ccccc12 NPGIHFRTRXVWOY-UHFFFAOYSA-N 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- 101100082610 Plasmodium falciparum (isolate 3D7) PDEdelta gene Proteins 0.000 description 2
- 229920002565 Polyethylene Glycol 400 Polymers 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N Propane Chemical compound CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 description 2
- 241000283984 Rodentia Species 0.000 description 2
- 235000019485 Safflower oil Nutrition 0.000 description 2
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 2
- 229920002125 Sokalan® Polymers 0.000 description 2
- 229940123876 Thyroid hormone receptor beta agonist Drugs 0.000 description 2
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 2
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 150000001263 acyl chlorides Chemical class 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 2
- 150000001408 amides Chemical class 0.000 description 2
- 235000019257 ammonium acetate Nutrition 0.000 description 2
- 229940043376 ammonium acetate Drugs 0.000 description 2
- 229910052921 ammonium sulfate Inorganic materials 0.000 description 2
- 235000011130 ammonium sulphate Nutrition 0.000 description 2
- 150000008064 anhydrides Chemical class 0.000 description 2
- 239000003963 antioxidant agent Substances 0.000 description 2
- 235000006708 antioxidants Nutrition 0.000 description 2
- YZXBAPSDXZZRGB-DOFZRALJSA-N arachidonic acid Chemical compound CCCCC\C=C/C\C=C/C\C=C/C\C=C/CCCC(O)=O YZXBAPSDXZZRGB-DOFZRALJSA-N 0.000 description 2
- 229960002255 azelaic acid Drugs 0.000 description 2
- 230000004888 barrier function Effects 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- SESFRYSPDFLNCH-UHFFFAOYSA-N benzyl benzoate Chemical compound C=1C=CC=CC=1C(=O)OCC1=CC=CC=C1 SESFRYSPDFLNCH-UHFFFAOYSA-N 0.000 description 2
- 125000002619 bicyclic group Chemical group 0.000 description 2
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 description 2
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Chemical group BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 2
- 235000019437 butane-1,3-diol Nutrition 0.000 description 2
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 229940075509 carbomer 1342 Drugs 0.000 description 2
- 229940085237 carbomer-980 Drugs 0.000 description 2
- 235000011089 carbon dioxide Nutrition 0.000 description 2
- VDTNNGKXZGSZIP-UHFFFAOYSA-N carbutamide Chemical compound CCCCNC(=O)NS(=O)(=O)C1=CC=C(N)C=C1 VDTNNGKXZGSZIP-UHFFFAOYSA-N 0.000 description 2
- 229960003362 carbutamide Drugs 0.000 description 2
- 239000004359 castor oil Substances 0.000 description 2
- 235000019438 castor oil Nutrition 0.000 description 2
- 230000005754 cellular signaling Effects 0.000 description 2
- 229960004106 citric acid Drugs 0.000 description 2
- 235000015165 citric acid Nutrition 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 235000005687 corn oil Nutrition 0.000 description 2
- 239000002285 corn oil Substances 0.000 description 2
- 235000012343 cottonseed oil Nutrition 0.000 description 2
- 239000002385 cottonseed oil Substances 0.000 description 2
- 125000001352 cyclobutyloxy group Chemical group C1(CCC1)O* 0.000 description 2
- 125000000131 cyclopropyloxy group Chemical group C1(CC1)O* 0.000 description 2
- 229960000860 dapsone Drugs 0.000 description 2
- NNBZCPXTIHJBJL-UHFFFAOYSA-N decalin Chemical compound C1CCCC2CCCCC21 NNBZCPXTIHJBJL-UHFFFAOYSA-N 0.000 description 2
- 238000010511 deprotection reaction Methods 0.000 description 2
- XXJWXESWEXIICW-UHFFFAOYSA-N diethylene glycol monoethyl ether Chemical compound CCOCCOCCO XXJWXESWEXIICW-UHFFFAOYSA-N 0.000 description 2
- METQSPRSQINEEU-UHFFFAOYSA-N dihydrospirorenone Natural products CC12CCC(C3(CCC(=O)C=C3C3CC33)C)C3C1C1CC1C21CCC(=O)O1 METQSPRSQINEEU-UHFFFAOYSA-N 0.000 description 2
- 229960004845 drospirenone Drugs 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- MMXKVMNBHPAILY-UHFFFAOYSA-N ethyl laurate Chemical compound CCCCCCCCCCCC(=O)OCC MMXKVMNBHPAILY-UHFFFAOYSA-N 0.000 description 2
- 238000000605 extraction Methods 0.000 description 2
- 235000019197 fats Nutrition 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 239000011737 fluorine Substances 0.000 description 2
- 238000004108 freeze drying Methods 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 125000002541 furyl group Chemical group 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- ZEMPKEQAKRGZGQ-XOQCFJPHSA-N glycerol triricinoleate Natural products CCCCCC[C@@H](O)CC=CCCCCCCCC(=O)OC[C@@H](COC(=O)CCCCCCCC=CC[C@@H](O)CCCCCC)OC(=O)CCCCCCCC=CC[C@H](O)CCCCCC ZEMPKEQAKRGZGQ-XOQCFJPHSA-N 0.000 description 2
- 210000002216 heart Anatomy 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 239000003906 humectant Substances 0.000 description 2
- 238000005984 hydrogenation reaction Methods 0.000 description 2
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 2
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 2
- 239000005457 ice water Substances 0.000 description 2
- 125000002883 imidazolyl group Chemical group 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 229940125396 insulin Drugs 0.000 description 2
- 239000000543 intermediate Substances 0.000 description 2
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 2
- 125000003253 isopropoxy group Chemical group [H]C([H])([H])C([H])(O*)C([H])([H])[H] 0.000 description 2
- 125000001786 isothiazolyl group Chemical group 0.000 description 2
- 125000000842 isoxazolyl group Chemical group 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- 230000037356 lipid metabolism Effects 0.000 description 2
- 230000004807 localization Effects 0.000 description 2
- 150000004668 long chain fatty acids Chemical class 0.000 description 2
- 239000012139 lysis buffer Substances 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 238000013227 male C57BL/6J mice Methods 0.000 description 2
- 210000001161 mammalian embryo Anatomy 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- 229920000609 methyl cellulose Polymers 0.000 description 2
- 239000001923 methylcellulose Substances 0.000 description 2
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 2
- 210000003470 mitochondria Anatomy 0.000 description 2
- 210000001700 mitochondrial membrane Anatomy 0.000 description 2
- 125000002950 monocyclic group Chemical group 0.000 description 2
- 239000004006 olive oil Substances 0.000 description 2
- 235000008390 olive oil Nutrition 0.000 description 2
- 238000003305 oral gavage Methods 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 238000012261 overproduction Methods 0.000 description 2
- CTSLXHKWHWQRSH-UHFFFAOYSA-N oxalyl chloride Chemical compound ClC(=O)C(Cl)=O CTSLXHKWHWQRSH-UHFFFAOYSA-N 0.000 description 2
- 125000004430 oxygen atom Chemical group O* 0.000 description 2
- JLFNLZLINWHATN-UHFFFAOYSA-N pentaethylene glycol Chemical compound OCCOCCOCCOCCOCCO JLFNLZLINWHATN-UHFFFAOYSA-N 0.000 description 2
- 239000006187 pill Substances 0.000 description 2
- 229920001983 poloxamer Polymers 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 2
- 229940069328 povidone Drugs 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 239000000651 prodrug Substances 0.000 description 2
- 229940002612 prodrug Drugs 0.000 description 2
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 2
- 239000003380 propellant Substances 0.000 description 2
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 2
- 125000000168 pyrrolyl group Chemical group 0.000 description 2
- 238000010791 quenching Methods 0.000 description 2
- 230000000171 quenching effect Effects 0.000 description 2
- 125000005493 quinolyl group Chemical group 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- GHMLBKRAJCXXBS-UHFFFAOYSA-N resorcinol Chemical compound OC1=CC=CC(O)=C1 GHMLBKRAJCXXBS-UHFFFAOYSA-N 0.000 description 2
- 229960004586 rosiglitazone Drugs 0.000 description 2
- 239000003813 safflower oil Substances 0.000 description 2
- 235000005713 safflower oil Nutrition 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 239000008159 sesame oil Substances 0.000 description 2
- 235000011803 sesame oil Nutrition 0.000 description 2
- RMAQACBXLXPBSY-UHFFFAOYSA-N silicic acid Chemical compound O[Si](O)(O)O RMAQACBXLXPBSY-UHFFFAOYSA-N 0.000 description 2
- 239000000377 silicon dioxide Substances 0.000 description 2
- 235000012239 silicon dioxide Nutrition 0.000 description 2
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 2
- 239000003549 soybean oil Substances 0.000 description 2
- 235000012424 soybean oil Nutrition 0.000 description 2
- 238000010186 staining Methods 0.000 description 2
- 238000010561 standard procedure Methods 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 125000005017 substituted alkenyl group Chemical group 0.000 description 2
- 125000004426 substituted alkynyl group Chemical group 0.000 description 2
- 125000005338 substituted cycloalkoxy group Chemical group 0.000 description 2
- 150000003457 sulfones Chemical class 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- UEUXEKPTXMALOB-UHFFFAOYSA-J tetrasodium;2-[2-[bis(carboxylatomethyl)amino]ethyl-(carboxylatomethyl)amino]acetate Chemical compound [Na+].[Na+].[Na+].[Na+].[O-]C(=O)CN(CC([O-])=O)CCN(CC([O-])=O)CC([O-])=O UEUXEKPTXMALOB-UHFFFAOYSA-J 0.000 description 2
- 125000000335 thiazolyl group Chemical group 0.000 description 2
- 229940098465 tincture Drugs 0.000 description 2
- 229940100613 topical solution Drugs 0.000 description 2
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 2
- IEDVJHCEMCRBQM-UHFFFAOYSA-N trimethoprim Chemical compound COC1=C(OC)C(OC)=CC(CC=2C(=NC(N)=NC=2)N)=C1 IEDVJHCEMCRBQM-UHFFFAOYSA-N 0.000 description 2
- 229960001082 trimethoprim Drugs 0.000 description 2
- 230000004584 weight gain Effects 0.000 description 2
- 235000019786 weight gain Nutrition 0.000 description 2
- MWLSOWXNZPKENC-SSDOTTSWSA-N zileuton Chemical compound C1=CC=C2SC([C@H](N(O)C(N)=O)C)=CC2=C1 MWLSOWXNZPKENC-SSDOTTSWSA-N 0.000 description 2
- 229960005332 zileuton Drugs 0.000 description 2
- ZNOVTXRBGFNYRX-STQMWFEESA-N (6S)-5-methyltetrahydrofolic acid Chemical compound C([C@@H]1N(C=2C(=O)N=C(N)NC=2NC1)C)NC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 ZNOVTXRBGFNYRX-STQMWFEESA-N 0.000 description 1
- 125000004765 (C1-C4) haloalkyl group Chemical group 0.000 description 1
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 1
- 125000006650 (C2-C4) alkynyl group Chemical group 0.000 description 1
- 125000006714 (C3-C10) heterocyclyl group Chemical group 0.000 description 1
- 125000006652 (C3-C12) cycloalkyl group Chemical group 0.000 description 1
- 125000006552 (C3-C8) cycloalkyl group Chemical group 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- PHIQHXFUZVPYII-ZCFIWIBFSA-O (R)-carnitinium Chemical compound C[N+](C)(C)C[C@H](O)CC(O)=O PHIQHXFUZVPYII-ZCFIWIBFSA-O 0.000 description 1
- MHCVCKDNQYMGEX-UHFFFAOYSA-N 1,1'-biphenyl;phenoxybenzene Chemical compound C1=CC=CC=C1C1=CC=CC=C1.C=1C=CC=CC=1OC1=CC=CC=C1 MHCVCKDNQYMGEX-UHFFFAOYSA-N 0.000 description 1
- 229940058015 1,3-butylene glycol Drugs 0.000 description 1
- LDVVTQMJQSCDMK-UHFFFAOYSA-N 1,3-dihydroxypropan-2-yl formate Chemical compound OCC(CO)OC=O LDVVTQMJQSCDMK-UHFFFAOYSA-N 0.000 description 1
- WORJRXHJTUTINR-UHFFFAOYSA-N 1,4-dioxane;hydron;chloride Chemical compound Cl.C1COCCO1 WORJRXHJTUTINR-UHFFFAOYSA-N 0.000 description 1
- HUXJXNSHCKHFIL-UHFFFAOYSA-N 1-(2-bromoethoxy)-2-methoxyethane Chemical compound COCCOCCBr HUXJXNSHCKHFIL-UHFFFAOYSA-N 0.000 description 1
- DLGFZOSPWIUMKY-UHFFFAOYSA-N 1-[2-(2-iodoethoxy)ethoxy]-2-methoxyethane Chemical compound COCCOCCOCCI DLGFZOSPWIUMKY-UHFFFAOYSA-N 0.000 description 1
- YVRGKFXJZCTTRB-UHFFFAOYSA-N 1-chloroethyl ethyl carbonate Chemical compound CCOC(=O)OC(C)Cl YVRGKFXJZCTTRB-UHFFFAOYSA-N 0.000 description 1
- FGYADSCZTQOAFK-UHFFFAOYSA-N 1-methylbenzimidazole Chemical class C1=CC=C2N(C)C=NC2=C1 FGYADSCZTQOAFK-UHFFFAOYSA-N 0.000 description 1
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 1
- MAVGBUDLHOOROM-UHFFFAOYSA-N 1h-indazole-5-carboxylic acid Chemical compound OC(=O)C1=CC=C2NN=CC2=C1 MAVGBUDLHOOROM-UHFFFAOYSA-N 0.000 description 1
- DNCVTVVLMRHJCJ-UHFFFAOYSA-N 1h-indazole-6-carboxylic acid Chemical compound OC(=O)C1=CC=C2C=NNC2=C1 DNCVTVVLMRHJCJ-UHFFFAOYSA-N 0.000 description 1
- KBHQUFPZXCNYKN-UHFFFAOYSA-N 1h-pyrrolo[3,2-b]pyridine-2-carboxylic acid Chemical compound C1=CC=C2NC(C(=O)O)=CC2=N1 KBHQUFPZXCNYKN-UHFFFAOYSA-N 0.000 description 1
- JVKUCNQGESRUCL-UHFFFAOYSA-N 2-Hydroxyethyl 12-hydroxyoctadecanoate Chemical compound CCCCCCC(O)CCCCCCCCCCC(=O)OCCO JVKUCNQGESRUCL-UHFFFAOYSA-N 0.000 description 1
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 description 1
- UOXJNGFFPMOZDM-UHFFFAOYSA-N 2-[di(propan-2-yl)amino]ethylsulfanyl-methylphosphinic acid Chemical compound CC(C)N(C(C)C)CCSP(C)(O)=O UOXJNGFFPMOZDM-UHFFFAOYSA-N 0.000 description 1
- 125000000069 2-butynyl group Chemical group [H]C([H])([H])C#CC([H])([H])* 0.000 description 1
- GECPBJINOLYRJI-UHFFFAOYSA-N 2-ethyl-3h-benzimidazole-5-carboxylic acid Chemical compound C1=C(C(O)=O)C=C2NC(CC)=NC2=C1 GECPBJINOLYRJI-UHFFFAOYSA-N 0.000 description 1
- 125000002941 2-furyl group Chemical group O1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- GZHWABCBKGMLIE-UHFFFAOYSA-N 2-methyl-3h-benzimidazole-5-carboxylic acid Chemical compound C1=C(C(O)=O)C=C2NC(C)=NC2=C1 GZHWABCBKGMLIE-UHFFFAOYSA-N 0.000 description 1
- JESRNIJXVIFVOV-UHFFFAOYSA-N 2-methylpyrazol-3-amine Chemical compound CN1N=CC=C1N JESRNIJXVIFVOV-UHFFFAOYSA-N 0.000 description 1
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 125000000175 2-thienyl group Chemical group S1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- APIXJSLKIYYUKG-UHFFFAOYSA-N 3 Isobutyl 1 methylxanthine Chemical compound O=C1N(C)C(=O)N(CC(C)C)C2=C1N=CN2 APIXJSLKIYYUKG-UHFFFAOYSA-N 0.000 description 1
- 125000003682 3-furyl group Chemical group O1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- QNGRDARNLFTZBH-UHFFFAOYSA-N 3-methyl-2-oxo-1h-benzimidazole-5-carboxylic acid Chemical group OC(=O)C1=CC=C2NC(=O)N(C)C2=C1 QNGRDARNLFTZBH-UHFFFAOYSA-N 0.000 description 1
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 125000001541 3-thienyl group Chemical group S1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- FFDVZARSBRNLFY-UHFFFAOYSA-N 4,5-dihydro-3h-pyrazol-3-ylurea Chemical compound NC(=O)NC1CCN=N1 FFDVZARSBRNLFY-UHFFFAOYSA-N 0.000 description 1
- WZRJTRPJURQBRM-UHFFFAOYSA-N 4-amino-n-(5-methyl-1,2-oxazol-3-yl)benzenesulfonamide;5-[(3,4,5-trimethoxyphenyl)methyl]pyrimidine-2,4-diamine Chemical compound O1C(C)=CC(NS(=O)(=O)C=2C=CC(N)=CC=2)=N1.COC1=C(OC)C(OC)=CC(CC=2C(=NC(N)=NC=2)N)=C1 WZRJTRPJURQBRM-UHFFFAOYSA-N 0.000 description 1
- UNBMPKNTYKDYCG-UHFFFAOYSA-N 4-methylpentan-2-amine Chemical compound CC(C)CC(C)N UNBMPKNTYKDYCG-UHFFFAOYSA-N 0.000 description 1
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 1
- SUBDBMMJDZJVOS-UHFFFAOYSA-N 5-methoxy-2-{[(4-methoxy-3,5-dimethylpyridin-2-yl)methyl]sulfinyl}-1H-benzimidazole Chemical compound N=1C2=CC(OC)=CC=C2NC=1S(=O)CC1=NC=C(C)C(OC)=C1C SUBDBMMJDZJVOS-UHFFFAOYSA-N 0.000 description 1
- QSFFBQNKTUMKNW-UHFFFAOYSA-N 6-methoxyquinoline-3-carboxylic acid Chemical compound N1=CC(C(O)=O)=CC2=CC(OC)=CC=C21 QSFFBQNKTUMKNW-UHFFFAOYSA-N 0.000 description 1
- ARSRBNBHOADGJU-UHFFFAOYSA-N 7,12-dimethyltetraphene Chemical compound C1=CC2=CC=CC=C2C2=C1C(C)=C(C=CC=C1)C1=C2C ARSRBNBHOADGJU-UHFFFAOYSA-N 0.000 description 1
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 1
- NZWANRYNROPQMV-UHFFFAOYSA-N 8-cyclopropyl-4-methoxyquinoline-2-carboxylic acid Chemical compound C1=CC=C2C(OC)=CC(C(O)=O)=NC2=C1C1CC1 NZWANRYNROPQMV-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N Acrylic acid Chemical compound OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 238000009020 BCA Protein Assay Kit Methods 0.000 description 1
- 101710201279 Biotin carboxyl carrier protein Proteins 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 239000004255 Butylated hydroxyanisole Substances 0.000 description 1
- 239000004322 Butylated hydroxytoluene Substances 0.000 description 1
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 1
- JKLOBUPRLOHBCV-UHFFFAOYSA-N C(C)(C)C1=CC=C2CC3(CCN(CC3)C(=O)C3=CC4=NC=CC=C4N3)OC(C2=C1)=O Chemical compound C(C)(C)C1=CC=C2CC3(CCN(CC3)C(=O)C3=CC4=NC=CC=C4N3)OC(C2=C1)=O JKLOBUPRLOHBCV-UHFFFAOYSA-N 0.000 description 1
- YDNKGFDKKRUKPY-JHOUSYSJSA-N C16 ceramide Natural products CCCCCCCCCCCCCCCC(=O)N[C@@H](CO)[C@H](O)C=CCCCCCCCCCCCCC YDNKGFDKKRUKPY-JHOUSYSJSA-N 0.000 description 1
- WQVFYORWANLQLC-UHFFFAOYSA-N CC(C)(C)OC(=O)N1CCC2(CC1)Cc1ccc(I)cc1C(=O)O2 Chemical compound CC(C)(C)OC(=O)N1CCC2(CC1)Cc1ccc(I)cc1C(=O)O2 WQVFYORWANLQLC-UHFFFAOYSA-N 0.000 description 1
- STKKRFILWFOZST-UHFFFAOYSA-N COc1cc(C(N(CC2)CCC2(Cc(c2c3)ccc3-c3cc(C(O)=O)cnc3)OC2=O)=O)nc2c(C3CC3)cccc12 Chemical compound COc1cc(C(N(CC2)CCC2(Cc(c2c3)ccc3-c3cc(C(O)=O)cnc3)OC2=O)=O)nc2c(C3CC3)cccc12 STKKRFILWFOZST-UHFFFAOYSA-N 0.000 description 1
- 102000007132 Carboxyl and Carbamoyl Transferases Human genes 0.000 description 1
- 108010072957 Carboxyl and Carbamoyl Transferases Proteins 0.000 description 1
- 108010078791 Carrier Proteins Proteins 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- 229910021589 Copper(I) bromide Inorganic materials 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 241000186427 Cutibacterium acnes Species 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- ZAKOWWREFLAJOT-CEFNRUSXSA-N D-alpha-tocopherylacetate Chemical compound CC(=O)OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C ZAKOWWREFLAJOT-CEFNRUSXSA-N 0.000 description 1
- RGHNJXZEOKUKBD-UHFFFAOYSA-N D-gluconic acid Natural products OCC(O)C(O)C(O)C(O)C(O)=O RGHNJXZEOKUKBD-UHFFFAOYSA-N 0.000 description 1
- VFZRZRDOXPRTSC-UHFFFAOYSA-N DMBA Natural products COC1=CC(OC)=CC(C=O)=C1 VFZRZRDOXPRTSC-UHFFFAOYSA-N 0.000 description 1
- XMSXQFUHVRWGNA-UHFFFAOYSA-N Decamethylcyclopentasiloxane Chemical compound C[Si]1(C)O[Si](C)(C)O[Si](C)(C)O[Si](C)(C)O[Si](C)(C)O1 XMSXQFUHVRWGNA-UHFFFAOYSA-N 0.000 description 1
- 201000004624 Dermatitis Diseases 0.000 description 1
- 101100135868 Dictyostelium discoideum pde3 gene Proteins 0.000 description 1
- QZKRHPLGUJDVAR-UHFFFAOYSA-K EDTA trisodium salt Chemical compound [Na+].[Na+].[Na+].OC(=O)CN(CC([O-])=O)CCN(CC([O-])=O)CC([O-])=O QZKRHPLGUJDVAR-UHFFFAOYSA-K 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 244000148064 Enicostema verticillatum Species 0.000 description 1
- BFPYWIDHMRZLRN-SLHNCBLASA-N Ethinyl estradiol Chemical compound OC1=CC=C2[C@H]3CC[C@](C)([C@](CC4)(O)C#C)[C@@H]4[C@@H]3CCC2=C1 BFPYWIDHMRZLRN-SLHNCBLASA-N 0.000 description 1
- 239000001856 Ethyl cellulose Substances 0.000 description 1
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 1
- 206010015548 Euthanasia Diseases 0.000 description 1
- 239000004606 Fillers/Extenders Substances 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 206010020649 Hyperkeratosis Diseases 0.000 description 1
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 1
- 206010022489 Insulin Resistance Diseases 0.000 description 1
- 208000001126 Keratosis Diseases 0.000 description 1
- QAQJMLQRFWZOBN-LAUBAEHRSA-N L-ascorbyl-6-palmitate Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](O)[C@H]1OC(=O)C(O)=C1O QAQJMLQRFWZOBN-LAUBAEHRSA-N 0.000 description 1
- 239000011786 L-ascorbyl-6-palmitate Substances 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- 229930182816 L-glutamine Natural products 0.000 description 1
- GDBQQVLCIARPGH-UHFFFAOYSA-N Leupeptin Natural products CC(C)CC(NC(C)=O)C(=O)NC(CC(C)C)C(=O)NC(C=O)CCCN=C(N)N GDBQQVLCIARPGH-UHFFFAOYSA-N 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 206010027626 Milia Diseases 0.000 description 1
- 239000004909 Moisturizer Substances 0.000 description 1
- 101100288142 Mus musculus Klkb1 gene Proteins 0.000 description 1
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 1
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 1
- GXCLVBGFBYZDAG-UHFFFAOYSA-N N-[2-(1H-indol-3-yl)ethyl]-N-methylprop-2-en-1-amine Chemical compound CN(CCC1=CNC2=C1C=CC=C2)CC=C GXCLVBGFBYZDAG-UHFFFAOYSA-N 0.000 description 1
- CRJGESKKUOMBCT-VQTJNVASSA-N N-acetylsphinganine Chemical compound CCCCCCCCCCCCCCC[C@@H](O)[C@H](CO)NC(C)=O CRJGESKKUOMBCT-VQTJNVASSA-N 0.000 description 1
- 150000001204 N-oxides Chemical class 0.000 description 1
- 101000755720 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) Palmitoyltransferase akr1 Proteins 0.000 description 1
- 206010054107 Nodule Diseases 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- MHQJUHSHQGQVTM-HNENSFHCSA-N Octadecyl fumarate Chemical compound CCCCCCCCCCCCCCCCCCOC(=O)\C=C/C(O)=O MHQJUHSHQGQVTM-HNENSFHCSA-N 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 208000012868 Overgrowth Diseases 0.000 description 1
- 206010033733 Papule Diseases 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- HLCFGWHYROZGBI-JJKGCWMISA-M Potassium gluconate Chemical compound [K+].OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C([O-])=O HLCFGWHYROZGBI-JJKGCWMISA-M 0.000 description 1
- 241000186429 Propionibacterium Species 0.000 description 1
- 206010037888 Rash pustular Diseases 0.000 description 1
- 208000025747 Rheumatic disease Diseases 0.000 description 1
- 206010040880 Skin irritation Diseases 0.000 description 1
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical class [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 1
- 229920001304 Solutol HS 15 Polymers 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- AOBORMOPSGHCAX-UHFFFAOYSA-N Tocophersolan Chemical compound OCCOC(=O)CCC(=O)OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C AOBORMOPSGHCAX-UHFFFAOYSA-N 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 229930003427 Vitamin E Natural products 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- 239000001089 [(2R)-oxolan-2-yl]methanol Substances 0.000 description 1
- KPCZJLGGXRGYIE-UHFFFAOYSA-N [C]1=CC=CN=C1 Chemical group [C]1=CC=CN=C1 KPCZJLGGXRGYIE-UHFFFAOYSA-N 0.000 description 1
- AYECZRVHKOLPIP-UHFFFAOYSA-N [P]C1CC1 Chemical compound [P]C1CC1 AYECZRVHKOLPIP-UHFFFAOYSA-N 0.000 description 1
- 239000003655 absorption accelerator Substances 0.000 description 1
- 231100000230 acceptable toxicity Toxicity 0.000 description 1
- 230000035508 accumulation Effects 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 150000001241 acetals Chemical group 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 238000010306 acid treatment Methods 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 125000000641 acridinyl group Chemical group C1(=CC=CC2=NC3=CC=CC=C3C=C12)* 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 1
- 230000006978 adaptation Effects 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 229940023476 agar Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 125000002877 alkyl aryl group Chemical group 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 229940024545 aluminum hydroxide Drugs 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 238000012870 ammonium sulfate precipitation Methods 0.000 description 1
- LSQZJLSUYDQPKJ-NJBDSQKTSA-N amoxicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=C(O)C=C1 LSQZJLSUYDQPKJ-NJBDSQKTSA-N 0.000 description 1
- 229960003022 amoxicillin Drugs 0.000 description 1
- 238000000540 analysis of variance Methods 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 230000000843 anti-fungal effect Effects 0.000 description 1
- 230000000845 anti-microbial effect Effects 0.000 description 1
- 239000000427 antigen Substances 0.000 description 1
- 102000036639 antigens Human genes 0.000 description 1
- 108091007433 antigens Proteins 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000007900 aqueous suspension Substances 0.000 description 1
- 229940114079 arachidonic acid Drugs 0.000 description 1
- 235000021342 arachidonic acid Nutrition 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 235000010385 ascorbyl palmitate Nutrition 0.000 description 1
- IUKQLMGVFMDQDP-UHFFFAOYSA-N azane;piperidine Chemical compound N.C1CCNCC1 IUKQLMGVFMDQDP-UHFFFAOYSA-N 0.000 description 1
- 150000001540 azides Chemical class 0.000 description 1
- MQTOSJVFKKJCRP-BICOPXKESA-N azithromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)N(C)C[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 MQTOSJVFKKJCRP-BICOPXKESA-N 0.000 description 1
- 229960004099 azithromycin Drugs 0.000 description 1
- 239000000440 bentonite Substances 0.000 description 1
- 229910000278 bentonite Inorganic materials 0.000 description 1
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 1
- 125000005605 benzo group Chemical group 0.000 description 1
- 125000004618 benzofuryl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 229960002903 benzyl benzoate Drugs 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000031018 biological processes and functions Effects 0.000 description 1
- 238000007413 biotinylation Methods 0.000 description 1
- 230000006287 biotinylation Effects 0.000 description 1
- 239000012267 brine Substances 0.000 description 1
- 239000001273 butane Substances 0.000 description 1
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 1
- 235000019282 butylated hydroxyanisole Nutrition 0.000 description 1
- 229940043253 butylated hydroxyanisole Drugs 0.000 description 1
- CZBZUDVBLSSABA-UHFFFAOYSA-N butylated hydroxyanisole Chemical compound COC1=CC=C(O)C(C(C)(C)C)=C1.COC1=CC=C(O)C=C1C(C)(C)C CZBZUDVBLSSABA-UHFFFAOYSA-N 0.000 description 1
- 235000010354 butylated hydroxytoluene Nutrition 0.000 description 1
- 229940095259 butylated hydroxytoluene Drugs 0.000 description 1
- 125000000480 butynyl group Chemical group [*]C#CC([H])([H])C([H])([H])[H] 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 239000000378 calcium silicate Substances 0.000 description 1
- 229910052918 calcium silicate Inorganic materials 0.000 description 1
- OYACROKNLOSFPA-UHFFFAOYSA-N calcium;dioxido(oxo)silane Chemical compound [Ca+2].[O-][Si]([O-])=O OYACROKNLOSFPA-UHFFFAOYSA-N 0.000 description 1
- 125000001951 carbamoylamino group Chemical group C(N)(=O)N* 0.000 description 1
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 1
- 229960001631 carbomer Drugs 0.000 description 1
- 150000001722 carbon compounds Chemical class 0.000 description 1
- 229910002091 carbon monoxide Inorganic materials 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 230000021523 carboxylation Effects 0.000 description 1
- 238000006473 carboxylation reaction Methods 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical group 0.000 description 1
- 229960004203 carnitine Drugs 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 229960001777 castor oil Drugs 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 239000013592 cell lysate Substances 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 238000002737 cell proliferation kit Methods 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 229940106164 cephalexin Drugs 0.000 description 1
- 229940106189 ceramide Drugs 0.000 description 1
- ZVEQCJWYRWKARO-UHFFFAOYSA-N ceramide Natural products CCCCCCCCCCCCCCC(O)C(=O)NC(CO)C(O)C=CCCC=C(C)CCCCCCCCC ZVEQCJWYRWKARO-UHFFFAOYSA-N 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 150000005827 chlorofluoro hydrocarbons Chemical class 0.000 description 1
- 125000004230 chromenyl group Chemical group O1C(C=CC2=CC=CC=C12)* 0.000 description 1
- 229940047766 co-trimoxazole Drugs 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- DOBRDRYODQBAMW-UHFFFAOYSA-N copper(i) cyanide Chemical compound [Cu+].N#[C-] DOBRDRYODQBAMW-UHFFFAOYSA-N 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 239000003246 corticosteroid Substances 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 150000003950 cyclic amides Chemical group 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 229940086555 cyclomethicone Drugs 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 208000031513 cyst Diseases 0.000 description 1
- 210000000172 cytosol Anatomy 0.000 description 1
- ZAKOWWREFLAJOT-UHFFFAOYSA-N d-alpha-Tocopheryl acetate Natural products CC(=O)OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C ZAKOWWREFLAJOT-UHFFFAOYSA-N 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- XUWHAWMETYGRKB-UHFFFAOYSA-N delta-valerolactam Chemical group O=C1CCCCN1 XUWHAWMETYGRKB-UHFFFAOYSA-N 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical group OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 1
- 229940075557 diethylene glycol monoethyl ether Drugs 0.000 description 1
- 229940043279 diisopropylamine Drugs 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- KCIDZIIHRGYJAE-YGFYJFDDSA-L dipotassium;[(2r,3r,4s,5r,6r)-3,4,5-trihydroxy-6-(hydroxymethyl)oxan-2-yl] phosphate Chemical compound [K+].[K+].OC[C@H]1O[C@H](OP([O-])([O-])=O)[C@H](O)[C@@H](O)[C@H]1O KCIDZIIHRGYJAE-YGFYJFDDSA-L 0.000 description 1
- 230000008034 disappearance Effects 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- METQSPRSQINEEU-HXCATZOESA-N drospirenone Chemical compound C([C@]12[C@H]3C[C@H]3[C@H]3[C@H]4[C@@H]([C@]5(CCC(=O)C=C5[C@@H]5C[C@@H]54)C)CC[C@@]31C)CC(=O)O2 METQSPRSQINEEU-HXCATZOESA-N 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 210000005069 ears Anatomy 0.000 description 1
- 229940009662 edetate Drugs 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 231100001129 embryonic lethality Toxicity 0.000 description 1
- 210000002514 epidermal stem cell Anatomy 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- 229940011871 estrogen Drugs 0.000 description 1
- 239000000262 estrogen Substances 0.000 description 1
- 229960002568 ethinylestradiol Drugs 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- 235000019325 ethyl cellulose Nutrition 0.000 description 1
- 229920001249 ethyl cellulose Polymers 0.000 description 1
- 125000004494 ethyl ester group Chemical group 0.000 description 1
- 229960001617 ethyl hydroxybenzoate Drugs 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 235000010228 ethyl p-hydroxybenzoate Nutrition 0.000 description 1
- 239000004403 ethyl p-hydroxybenzoate Substances 0.000 description 1
- DEFVIWRASFVYLL-UHFFFAOYSA-N ethylene glycol bis(2-aminoethyl)tetraacetic acid Chemical compound OC(=O)CN(CC(O)=O)CCOCCOCCN(CC(O)=O)CC(O)=O DEFVIWRASFVYLL-UHFFFAOYSA-N 0.000 description 1
- NUVBSKCKDOMJSU-UHFFFAOYSA-N ethylparaben Chemical compound CCOC(=O)C1=CC=C(O)C=C1 NUVBSKCKDOMJSU-UHFFFAOYSA-N 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 230000004129 fatty acid metabolism Effects 0.000 description 1
- 150000002185 fatty acyl-CoAs Chemical class 0.000 description 1
- 239000012091 fetal bovine serum Substances 0.000 description 1
- 239000013020 final formulation Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 125000004785 fluoromethoxy group Chemical group [H]C([H])(F)O* 0.000 description 1
- MKXKFYHWDHIYRV-UHFFFAOYSA-N flutamide Chemical compound CC(C)C(=O)NC1=CC=C([N+]([O-])=O)C(C(F)(F)F)=C1 MKXKFYHWDHIYRV-UHFFFAOYSA-N 0.000 description 1
- 229960002074 flutamide Drugs 0.000 description 1
- 230000003325 follicular Effects 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 235000021588 free fatty acids Nutrition 0.000 description 1
- 125000003838 furazanyl group Chemical group 0.000 description 1
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 239000000174 gluconic acid Substances 0.000 description 1
- 235000012208 gluconic acid Nutrition 0.000 description 1
- 229950006191 gluconic acid Drugs 0.000 description 1
- 235000001727 glucose Nutrition 0.000 description 1
- 125000003827 glycol group Chemical group 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 238000005658 halogenation reaction Methods 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000006038 hexenyl group Chemical group 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000005980 hexynyl group Chemical group 0.000 description 1
- 238000000265 homogenisation Methods 0.000 description 1
- 229940125697 hormonal agent Drugs 0.000 description 1
- 102000047784 human ACACB Human genes 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 230000036571 hydration Effects 0.000 description 1
- 238000006703 hydration reaction Methods 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 229920003063 hydroxymethyl cellulose Polymers 0.000 description 1
- 229940031574 hydroxymethyl cellulose Drugs 0.000 description 1
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 1
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 1
- 208000013403 hyperactivity Diseases 0.000 description 1
- 238000010191 image analysis Methods 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 230000037456 inflammatory mechanism Effects 0.000 description 1
- 125000001977 isobenzofuranyl group Chemical group C=1(OC=C2C=CC=CC12)* 0.000 description 1
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 125000000555 isopropenyl group Chemical group [H]\C([H])=C(\*)C([H])([H])[H] 0.000 description 1
- 125000005956 isoquinolyl group Chemical group 0.000 description 1
- 125000001793 isothiazol-3-yl group Chemical group [H]C1=C([H])C(*)=NS1 0.000 description 1
- 125000004500 isothiazol-4-yl group Chemical group S1N=CC(=C1)* 0.000 description 1
- 230000000155 isotopic effect Effects 0.000 description 1
- 125000004284 isoxazol-3-yl group Chemical group [H]C1=C([H])C(*)=NO1 0.000 description 1
- 125000004499 isoxazol-5-yl group Chemical group O1N=CC=C1* 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- GDBQQVLCIARPGH-ULQDDVLXSA-N leupeptin Chemical compound CC(C)C[C@H](NC(C)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](C=O)CCCN=C(N)N GDBQQVLCIARPGH-ULQDDVLXSA-N 0.000 description 1
- 108010052968 leupeptin Proteins 0.000 description 1
- 229940017804 levomefolate Drugs 0.000 description 1
- 230000006372 lipid accumulation Effects 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- DLEDOFVPSDKWEF-UHFFFAOYSA-N lithium butane Chemical compound [Li+].CCC[CH2-] DLEDOFVPSDKWEF-UHFFFAOYSA-N 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- VTHJTEIRLNZDEV-UHFFFAOYSA-L magnesium dihydroxide Chemical compound [OH-].[OH-].[Mg+2] VTHJTEIRLNZDEV-UHFFFAOYSA-L 0.000 description 1
- 239000000347 magnesium hydroxide Substances 0.000 description 1
- 229910001862 magnesium hydroxide Inorganic materials 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 1
- 235000019341 magnesium sulphate Nutrition 0.000 description 1
- 210000005075 mammary gland Anatomy 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000001819 mass spectrum Methods 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- 125000004184 methoxymethyl group Chemical group [H]C([H])([H])OC([H])([H])* 0.000 description 1
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 1
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 description 1
- 229960002216 methylparaben Drugs 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 230000001333 moisturizer Effects 0.000 description 1
- 239000003068 molecular probe Substances 0.000 description 1
- 239000012452 mother liquor Substances 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- MZRVEZGGRBJDDB-UHFFFAOYSA-N n-Butyllithium Substances [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 1
- IJDNQMDRQITEOD-UHFFFAOYSA-N n-butane Chemical compound CCCC IJDNQMDRQITEOD-UHFFFAOYSA-N 0.000 description 1
- OFBQJSOFQDEBGM-UHFFFAOYSA-N n-pentane Natural products CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 1
- 125000004593 naphthyridinyl group Chemical group N1=C(C=CC2=CC=CN=C12)* 0.000 description 1
- 239000007922 nasal spray Substances 0.000 description 1
- VVGIYYKRAMHVLU-UHFFFAOYSA-N newbouldiamide Natural products CCCCCCCCCCCCCCCCCCCC(O)C(O)C(O)C(CO)NC(=O)CCCCCCCCCCCCCCCCC VVGIYYKRAMHVLU-UHFFFAOYSA-N 0.000 description 1
- VOFUROIFQGPCGE-UHFFFAOYSA-N nile red Chemical compound C1=CC=C2C3=NC4=CC=C(N(CC)CC)C=C4OC3=CC(=O)C2=C1 VOFUROIFQGPCGE-UHFFFAOYSA-N 0.000 description 1
- 231100000956 nontoxicity Toxicity 0.000 description 1
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- 230000037311 normal skin Effects 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 235000021313 oleic acid Nutrition 0.000 description 1
- 239000003217 oral combined contraceptive Substances 0.000 description 1
- 238000006053 organic reaction Methods 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 125000002524 organometallic group Chemical group 0.000 description 1
- 125000004287 oxazol-2-yl group Chemical group [H]C1=C([H])N=C(*)O1 0.000 description 1
- 125000003145 oxazol-4-yl group Chemical group O1C=NC(=C1)* 0.000 description 1
- 125000004304 oxazol-5-yl group Chemical group O1C=NC=C1* 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- LSQZJLSUYDQPKJ-UHFFFAOYSA-N p-Hydroxyampicillin Natural products O=C1N2C(C(O)=O)C(C)(C)SC2C1NC(=O)C(N)C1=CC=C(O)C=C1 LSQZJLSUYDQPKJ-UHFFFAOYSA-N 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 125000003538 pentan-3-yl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000002255 pentenyl group Chemical group C(=CCCC)* 0.000 description 1
- 125000005981 pentynyl group Chemical group 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- 230000003285 pharmacodynamic effect Effects 0.000 description 1
- 125000004934 phenanthridinyl group Chemical group C1(=CC=CC2=NC=C3C=CC=CC3=C12)* 0.000 description 1
- 125000004625 phenanthrolinyl group Chemical group N1=C(C=CC2=CC=C3C=CC=NC3=C12)* 0.000 description 1
- 125000001791 phenazinyl group Chemical group C1(=CC=CC2=NC3=CC=CC=C3N=C12)* 0.000 description 1
- 125000001644 phenoxazinyl group Chemical group C1(=CC=CC=2OC3=CC=CC=C3NC12)* 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 125000004592 phthalazinyl group Chemical group C1(=NN=CC2=CC=CC=C12)* 0.000 description 1
- SIOXPEMLGUPBBT-UHFFFAOYSA-N picolinic acid Chemical compound OC(=O)C1=CC=CC=N1 SIOXPEMLGUPBBT-UHFFFAOYSA-N 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920002647 polyamide Polymers 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 230000004481 post-translational protein modification Effects 0.000 description 1
- 239000004224 potassium gluconate Substances 0.000 description 1
- 235000013926 potassium gluconate Nutrition 0.000 description 1
- 229960003189 potassium gluconate Drugs 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 239000000583 progesterone congener Substances 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 239000001294 propane Substances 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 229940055019 propionibacterium acne Drugs 0.000 description 1
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 1
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 description 1
- 235000013772 propylene glycol Nutrition 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- 230000004800 psychological effect Effects 0.000 description 1
- 125000001042 pteridinyl group Chemical group N1=C(N=CC2=NC=CN=C12)* 0.000 description 1
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 1
- 208000029561 pustule Diseases 0.000 description 1
- 125000004309 pyranyl group Chemical group O1C(C=CC=C1)* 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000000246 pyrimidin-2-yl group Chemical group [H]C1=NC(*)=NC([H])=C1[H] 0.000 description 1
- 125000004527 pyrimidin-4-yl group Chemical group N1=CN=C(C=C1)* 0.000 description 1
- 125000004528 pyrimidin-5-yl group Chemical group N1=CN=CC(=C1)* 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- 239000002516 radical scavenger Substances 0.000 description 1
- 238000009790 rate-determining step (RDS) Methods 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000000552 rheumatic effect Effects 0.000 description 1
- 238000002390 rotary evaporation Methods 0.000 description 1
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 230000001932 seasonal effect Effects 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 229920002545 silicone oil Polymers 0.000 description 1
- 230000036556 skin irritation Effects 0.000 description 1
- 231100000475 skin irritation Toxicity 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- 229960001790 sodium citrate Drugs 0.000 description 1
- 235000011083 sodium citrates Nutrition 0.000 description 1
- FQENQNTWSFEDLI-UHFFFAOYSA-J sodium diphosphate Chemical compound [Na+].[Na+].[Na+].[Na+].[O-]P([O-])(=O)OP([O-])([O-])=O FQENQNTWSFEDLI-UHFFFAOYSA-J 0.000 description 1
- 229940048086 sodium pyrophosphate Drugs 0.000 description 1
- RPACBEVZENYWOL-XFULWGLBSA-M sodium;(2r)-2-[6-(4-chlorophenoxy)hexyl]oxirane-2-carboxylate Chemical compound [Na+].C=1C=C(Cl)C=CC=1OCCCCCC[C@]1(C(=O)[O-])CO1 RPACBEVZENYWOL-XFULWGLBSA-M 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- 239000012453 solvate Substances 0.000 description 1
- 239000011877 solvent mixture Substances 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- BENYHUNHQCUDFZ-UHFFFAOYSA-N spiro[4h-isochromene-3,4'-piperidine]-1-one;hydrochloride Chemical compound Cl.C1C2=CC=CC=C2C(=O)OC21CCNCC2 BENYHUNHQCUDFZ-UHFFFAOYSA-N 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 229940071138 stearyl fumarate Drugs 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 150000005846 sugar alcohols Polymers 0.000 description 1
- 229960005404 sulfamethoxazole Drugs 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- JLKIGFTWXXRPMT-UHFFFAOYSA-N sulphamethoxazole Chemical compound O1C(C)=CC(NS(=O)(=O)C=2C=CC(N)=CC=2)=N1 JLKIGFTWXXRPMT-UHFFFAOYSA-N 0.000 description 1
- 230000000153 supplemental effect Effects 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 238000010189 synthetic method Methods 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- BSYVTEYKTMYBMK-UHFFFAOYSA-N tetrahydrofurfuryl alcohol Chemical compound OCC1CCCO1 BSYVTEYKTMYBMK-UHFFFAOYSA-N 0.000 description 1
- 235000019818 tetrasodium diphosphate Nutrition 0.000 description 1
- 239000001577 tetrasodium phosphonato phosphate Substances 0.000 description 1
- 150000003536 tetrazoles Chemical class 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 125000004495 thiazol-4-yl group Chemical group S1C=NC(=C1)* 0.000 description 1
- 125000004496 thiazol-5-yl group Chemical group S1C=NC=C1* 0.000 description 1
- 238000004809 thin layer chromatography Methods 0.000 description 1
- 229960000984 tocofersolan Drugs 0.000 description 1
- AOBORMOPSGHCAX-DGHZZKTQSA-N tocofersolan Chemical compound OCCOC(=O)CCC(=O)OC1=C(C)C(C)=C2O[C@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C AOBORMOPSGHCAX-DGHZZKTQSA-N 0.000 description 1
- 229940042585 tocopherol acetate Drugs 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 238000000844 transformation Methods 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 229960002117 triamcinolone acetonide Drugs 0.000 description 1
- YNDXUCZADRHECN-JNQJZLCISA-N triamcinolone acetonide Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H]3OC(C)(C)O[C@@]3(C(=O)CO)[C@@]1(C)C[C@@H]2O YNDXUCZADRHECN-JNQJZLCISA-N 0.000 description 1
- YNJBWRMUSHSURL-UHFFFAOYSA-N trichloroacetic acid Chemical compound OC(=O)C(Cl)(Cl)Cl YNJBWRMUSHSURL-UHFFFAOYSA-N 0.000 description 1
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 1
- 229960005066 trisodium edetate Drugs 0.000 description 1
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 1
- GPRLSGONYQIRFK-MNYXATJNSA-N triton Chemical compound [3H+] GPRLSGONYQIRFK-MNYXATJNSA-N 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 208000035408 type 1 diabetes mellitus 1 Diseases 0.000 description 1
- 230000002861 ventricular Effects 0.000 description 1
- PXXNTAGJWPJAGM-UHFFFAOYSA-N vertaline Natural products C1C2C=3C=C(OC)C(OC)=CC=3OC(C=C3)=CC=C3CCC(=O)OC1CC1N2CCCC1 PXXNTAGJWPJAGM-UHFFFAOYSA-N 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 239000011709 vitamin E Substances 0.000 description 1
- 229940046009 vitamin E Drugs 0.000 description 1
- 235000019165 vitamin E Nutrition 0.000 description 1
- 239000011534 wash buffer Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
- 238000009736 wetting Methods 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 125000001834 xanthenyl group Chemical group C1=CC=CC=2OC3=CC=CC=C3C(C12)* 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
- 239000011787 zinc oxide Substances 0.000 description 1
- 125000004933 β-carbolinyl group Chemical group C1(=NC=CC=2C3=CC=CC=C3NC12)* 0.000 description 1
- 150000003952 β-lactams Chemical group 0.000 description 1
- 150000003953 γ-lactams Chemical group 0.000 description 1
- 150000003954 δ-lactams Chemical group 0.000 description 1
- 150000003955 ε-lactams Chemical group 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/10—Spiro-condensed systems
- C07D491/107—Spiro-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4709—Non-condensed quinolines and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/145—Amines having sulfur, e.g. thiurams (>N—C(S)—S—C(S)—N< and >N—C(S)—S—S—C(S)—N<), Sulfinylamines (—N=SO), Sulfonylamines (—N=SO2)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/18—Sulfonamides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/192—Carboxylic acids, e.g. valproic acid having aromatic groups, e.g. sulindac, 2-aryl-propionic acids, ethacrynic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/197—Carboxylic acids, e.g. valproic acid having an amino group the amino and the carboxyl groups being attached to the same acyclic carbon chain, e.g. gamma-aminobutyric acid [GABA], beta-alanine, epsilon-aminocaproic acid, pantothenic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/20—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids
- A61K31/203—Retinoic acids ; Salts thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/401—Proline; Derivatives thereof, e.g. captopril
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/438—The ring being spiro-condensed with carbocyclic or heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/444—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a six-membered ring with nitrogen as a ring heteroatom, e.g. amrinone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/575—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of three or more carbon atoms, e.g. cholane, cholestane, ergosterol, sitosterol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/60—Salicylic acid; Derivatives thereof
- A61K31/612—Salicylic acid; Derivatives thereof having the hydroxy group in position 2 esterified, e.g. salicylsulfuric acid
- A61K31/616—Salicylic acid; Derivatives thereof having the hydroxy group in position 2 esterified, e.g. salicylsulfuric acid by carboxylic acids, e.g. acetylsalicylic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/65—Tetracyclines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7048—Compounds having saccharide radicals and heterocyclic rings having oxygen as a ring hetero atom, e.g. leucoglucosan, hesperidin, erythromycin, nystatin, digitoxin or digoxin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/7056—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing five-membered rings with nitrogen as a ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/26—Glucagons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/32—Macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. carbomers, poly(meth)acrylates, or polyvinyl pyrrolidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/005—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'active' part of the composition delivered, i.e. the nucleic acid delivered
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0014—Skin, i.e. galenical aspects of topical compositions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/10—Anti-acne agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Abstract
Description
관련 출원의 상호 참조
본 출원은 2017년 6월 30일 출원된 미국 가출원 번호 62/527,829의 이익을 청구하며, 이 가출원의 내용은 그 전문이 본원에 참조로 포함된다.
발명의 분야
다양한 실시양태에서, 본 발명은 일반적으로, 신규 부류의 스피로락톤 화합물, 그의 염, 그를 포함하는 제약 조성물, 그의 합성 방법, 및 그의 용도에 관한 것이다.
지방산은 멤브레인 생합성, 신호전달 지질의 생성, 번역후 변형, 에너지 생성 및 저장 등을 포함한 살아있는 세포의 정상적 기능을 위한 필수 구성요소이다. 아세틸-CoA 카르복실라제 (ACC)는, 세포에서의 지방산 대사에 있어 속도-제한 단계인 아세틸-CoA에서 말로닐-CoA로의 전환을 촉매하는 세포질 효소이다. 세포질 말로닐-CoA는 지질 대사의 두가지 하류 경로, 드 노보 지방산 합성 및 지방산 β-산화를 제어한다. 말로닐-CoA는 장쇄 지방산 합성 및 신장에 있어 구성 요소이다. 말로닐-CoA는 또한 미토콘드리아 멤브레인 상의 지방산 수송체, 카르니틴 팔미토일트랜스퍼라제-1을 알로스테릭 억제하고, 미토콘드리아 내로의 지방 아실-CoA의 도입을 차단한다. ACC를 억제함으로써, 미토콘드리아에서 세포 장쇄 지방산 합성이 차단될 수 있고 β-산화가 자극될 수 있다. 그 결과, 세포 지질 함량이 감소된다.
ACC는 각각 시토졸 및 미토콘드리아 멤브레인에서 국소화되는 2종의 이소형, ACC1 및 ACC2를 갖는다. ACC 단백질은 3개의 도메인으로 구성되며, 여기서 비오틴 카르복실라제 도메인은 비오틴 카르복실 담체 단백질 도메인에 공유 연결된 비오틴의 카르복실화를 촉매하고, 카르복실트랜스퍼라제 도메인은 카르복실 비오틴으로부터 아세틸-CoA로의 카르복실 기의 전달을 촉매한다 (Zhang et al., Science 299:2064-2067 (2003)). ACC1 및 ACC2의 분자 질량은 각각 약 265 및 약 280 kDa이다. 두 이소형 모두 상이한 조직에서 나타나지만, ACC1은 주로 지방형성 조직, 예컨대 간, 아디포즈, 및 수유 유선에서 발현되고, ACC2는 대부분 근육 조직 및 심장에서 발현된다. 설치류에서, ACC1은 주로 드 노보 지방산 합성의 원인이고, ACC2는 지방산 베타-산화의 원인이다 (Abu-Elheiga et al., The Journal of biological chemistry 272:10669-10677 (1997); Abu-Elheiga et al., Proceedings of the National Academy of Sciences of the United States of America 92:4011-4015(1995)). 인간에서, ACC2 이소형은 또한 아디포즈 조직 및 간에서 풍부하게 발현되고 이들 조직에서 드 노보 지질생성이 가능하다 (Castle et al., PloS one 4:e4369(2009)). 유전학 연구는, ACC1이 발달에 있어 필수적이고, ACC1 결핍이 배아 치사를 야기함을 제시한다 (Abu-Elheiga et al., Proceedings of the National Academy of Sciences of the United States of America 97:1444-1449(2000)). 반면, ACC2 돌연변이 마우스는 증가된 지방산 산화로 인해 보다 제지방인 상태이지만 정상적으로 생존 및 번식하고, 체중 증가 및 인슐린 내성과 관련하여 고-지방 고-탄수화물 식이에 대해 저항성이다 (Abu-Elheiga et al., Science 291:2613-2616(2001); Abu-Elheiga et al., Proceedings of the National Academy of Sciences of the United States of America 102:12011-12016(2005); Abu-Elheiga et al., Proceedings of the National Academy of Sciences of the United States of America 100:10207-10212(2003)).
다양한 질환 또는 장애가 비정상적 ACC1 및/또는 ACC2 활성과 연관된다. 따라서, ACC1 및/또는 ACC2 활성을 조절할 수 있는 신규 화합물에 대한 필요성이 존재한다.
다양한 실시양태에서, 본 개시내용은 ACC1 및/또는 ACC2의 억제제일 수 있는 스피로락톤 화합물, 또는 그의 제약상 허용되는 염을 제공한다. 일부 실시양태에서, 본 개시내용은 또한 스피로락톤 화합물 또는 그의 제약상 허용되는 염을 포함하는 제약 조성물을 제공한다. 일부 실시양태에서, 본 개시내용은 또한, 비정상적 ACC1 및/또는 ACC2 활성과 연관된 질환 또는 장애, 예를 들어, 비-알콜성 지방간염 (NASH), 여드름, 비만, 당뇨병, 및 암의 치료를 위한 스피로락톤 화합물 또는 그의 제약상 허용되는 염의 사용 방법을 제공한다.
본 개시내용의 특정 실시양태는 화학식 I의 화합물 또는 그의 제약상 허용되는 염에 관한 것이다:
여기서 R1, R2 및 R3은 본원에서 정의된다. 일부 실시양태에서, 화학식 I의 화합물은 본원에서 정의된 바와 같은 화학식 I-1, 화학식 Ia, 화학식 Ib, 화학식 Ic, 화학식 II-1 내지 II-3, 또는 화학식 III-1 내지 III-6의 화합물이다. 본원에 기재된 실시양태 중 임의의 것에서, 스피로락톤 화합물은 1'-(4,8-디메톡시-2-나프토일)-7-이소프로필스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 1), 1'-(4,8-디메톡시퀴놀린-2-카르보닐)-7-이소프로필스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 2), 1'-(4,8-디메톡시-2-나프토일)-7-에틸스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 3), 1'-(4,8-디메톡시퀴놀린-2-카르보닐)-7-에틸스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 4), 1'-(4,8-디메톡시-2-나프토일)-7-((1-메틸-1H-피라졸-5-일)아미노)스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 5), 1'-(4,8-디메톡시퀴놀린-2-카르보닐)-7-((1-메틸-1H-피라졸-5-일)아미노)스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 6), 7-이소프로필-1'-(2-메틸-1H-벤조[d]이미다졸-6-카르보닐)스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 7), 1'-(1H-인다졸-5-카르보닐)-7-이소프로필스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 8), 7-이소프로필-1'-(1H-피롤로[3,2-b]피리딘-2-카르보닐)-스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 9), 1'-(1H-인다졸-6-카르보닐)-7-이소프로필스피로-[이소크로만-3,4'-피페리딘]-1-온 (실시예 10), 7-이소프로필-1'-(6-메톡시퀴놀린-3-카르보닐)스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 11), 1'-(2-에틸-1H-벤조[d]이미다졸-6-카르보닐)-7-이소프로필스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 12), 7-이소프로필-1'-(3-메틸-2-옥소-2,3-디히드로-1H-벤조[d]이미다졸-5-카르보닐)스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 13), 메틸 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 (실시예 14), 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산 (실시예 15), 1-((에톡시카르보닐)옥시)에틸 5-(1'-(4,8-디메톡시-퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 (실시예 16), 2-(2-(2-메톡시에톡시)에톡시)에틸 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 (실시예 17), 2-(2-메톡시에톡시)에틸 5-(1'-(4,8-디메톡시-퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 (실시예 18), 메틸 5-(1'-(8-시클로프로필-4-메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 (실시예 19), 5-(1'-(8-시클로프로필-4-메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산 (실시예 20), 메틸 5-(1'-(1-시클로프로필-4-메톡시-3-메틸-1H-인돌-6-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 (실시예 21), 또는 5-(1'-(1-시클로프로필-4-메톡시-3-메틸-1H-인돌-6-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산 (실시예 22), 또는 그의 제약상 허용되는 염일 수 있다.
본 개시내용의 특정 실시양태는 본원에서 정의된 바와 같은 화학식 I의 스피로락톤 화합물 (예를 들어, 화학식 I-1, 화학식 Ia, 화학식 Ib, 화학식 Ic, 화학식 II-1 내지 II-3, 또는 화학식 III-1 내지 III-6의 화합물, 또는 실시예 1-22 중 임의의 것), 또는 그의 제약상 허용되는 염을 포함하는 제약 조성물에 관한 것이다. 일부 실시양태에서, 제약 조성물은 하나 이상의 추가의 활성제를 추가로 포함한다.
본원에 기재된 제약 조성물은 상이한 투여 경로를 위해 제제화될 수 있다. 일부 실시양태에서, 제약 조성물은 정맥내 주사 또는 주입, 경구 투여, 흡입, 또는 국소 투여를 위해 제제화될 수 있다. 일부 실시양태에서, 제약 조성물은 국소 용액, 로션, 샴푸, 경피 스프레이, 국소 필름, 포움, 분말, 페이스트, 스폰지, 경피 패치, 팅크제, 테이프, 크림, 겔, 또는 연고의 형태로 제제화될 수 있다.
본 개시내용의 특정 실시양태는 세포에서 ACC1 및/또는 ACC2 활성을 억제하는 방법에 관한 것이다. 일부 실시양태에서, 방법은, 세포를 본원에 기재된 스피로락톤 화합물 또는 그의 제약상 허용되는 염, 또는 본원에 기재된 제약 조성물과 접촉시키는 것을 포함한다.
일부 실시양태에서, 본 개시내용은 또한, 말로닐-CoA 생성, 세포 (예를 들어, 피지세포, 지방세포, 또는 간세포)에서의 지질 생성, 세포 (예를 들어, 피지세포, 각질세포, 지방세포, 멜라닌세포, 편평 세포, 메르켈 세포, 랑게르한스 세포, 또는 피부 줄기 세포, 예를 들어, 표피, 진피, 및/또는 피하조직에서의 것)의 증식, 섬유모세포의 지방세포로의 분화, 피지 생성, 또는 이들의 조합의 억제를 필요로 하는 대상체에서 이들을 억제하는 방법을 제공한다. 일부 실시양태에서, 대상체는 여드름, 지루, 피지 증식증, 지루성 각화증, 피지 선종, 피지 낭종, 광선 각화증, 피지 암종, 편평 세포 암종, 흑색종, 비류성 장미증, 버트-호그-두베 증후군에서의 섬유모낭종, 및 이들의 조합으로부터 선택된 질환 또는 장애를 갖는 것을 특징으로 한다. 일부 실시양태에서, 대상체는 비-알콜성 지방간염 (NASH)을 갖는 것을 특징으로 한다. 일부 실시양태에서, 방법은, 대상체에게 유효량의 본원에 기재된 스피로락톤 화합물 또는 그의 제약상 허용되는 염, 또는 본원에 기재된 제약 조성물을 투여하는 것을 포함한다.
본 개시내용의 특정 실시양태는 ACC1 및/또는 ACC2와 연관된 질환 또는 장애의 치료를 필요로 하는 대상체에서 상기 질환 또는 장애를 치료하는 방법에 관한 것이다. 일부 실시양태에서, 방법은, 치료 유효량의 본원에 기재된 스피로락톤 화합물 (예를 들어, 화학식 I, 화학식 I-1, 화학식 Ia, 화학식 Ib, 화학식 Ic, 화학식 II-1 내지 II-3, 또는 화학식 III-1 내지 III-6의 화합물, 또는 실시예 1-22 중 임의의 것), 또는 그의 제약상 허용되는 염, 또는 본원에 기재된 제약 조성물을, 그를 필요로 하는 대상체에게 투여하는 것을 포함한다. 일부 실시양태에서, 방법은, 각각의 질환 또는 장애 (예를 들어, 본원에 기재된 바와 같은 것)에 대한 하나 이상의 추가의 요법으로 그를 필요로 하는 대상체를 치료하는 것을 추가로 포함한다. 본원에 기재된 방법으로 치료하기에 적합한 비제한적 질환 또는 장애는 피부 질환, 예컨대 비정상적 피지세포 및/또는 각질세포 활성과 연관된 질환 또는 장애 (예를 들어, 여드름), 비-알콜성 지방간 질환 (예컨대 비-알콜성 지방간염 (NASH)), 대사 질환 또는 장애 (예를 들어, 비만 또는 당뇨병), 및 암을 포함한다.
본 개시내용의 추가의 실시양태 및 이점은, 부분적으로, 하기 설명에 기재될 것이며, 설명으로부터 유출되거나, 본 개시내용의 실행에 의해 습득될 수 있다. 본 개시내용의 실시양태 및 이점은 첨부된 청구범위에 특별히 기재된 요소 및 조합에 의해 실현되고 달성될 것이다.
상기 개요 및 하기 상세한 설명 모두 단지 예시적 및 설명적인 것이며, 청구된 발명을 제한하지 않음을 이해하여야 한다.
본 발명의 일부 실시양태는, 단지 예로서의 첨부된 도면을 참조로 하여 본원에 기재된다. 이제 상세히 도면을 구체적으로 참조함에 있어, 제시된 세부사항들은 예시적이며 본 발명의 실시양태의 예시적 논의를 위한 것임이 강조된다.
도 1은 C57BL/6J 마우스에서 ACC 억제제 (예를 들어, 실시예 14 또는 20)로의 만성 치료가 간 트리글리세리드 (TG)를 감소시켰음을 보여주는 막대 그래프를 제시한다. 데이터는 평균 ± SEM으로서 나타내었다. 통계적 유의성은 아노바(ANOVA) 분석을 사용하여 결정되었으며, 비히클에 대하여 ** p < 0.01이다.
도 1은 C57BL/6J 마우스에서 ACC 억제제 (예를 들어, 실시예 14 또는 20)로의 만성 치료가 간 트리글리세리드 (TG)를 감소시켰음을 보여주는 막대 그래프를 제시한다. 데이터는 평균 ± SEM으로서 나타내었다. 통계적 유의성은 아노바(ANOVA) 분석을 사용하여 결정되었으며, 비히클에 대하여 ** p < 0.01이다.
본 개시내용은 일반적으로, ACC 억제제 (ACC1 및/또는 ACC2 억제제)로서 사용될 수 있는 신규 부류의 스피로락톤 화합물에 관한 것이다. 다양한 실시양태에서, 본 개시내용은 본원에 기재된 신규 스피로락톤 화합물과 관련된 화합물, 제약 조성물, 방법, 및 용도를 제공한다.
스피로락톤 화합물
본 개시내용의 특정 실시양태는 신규 스피로락톤 화합물에 관한 것이다. 일부 실시양태에서, 본 개시내용은 화학식 I의 화합물, 또는 그의 제약상 허용되는 염을 제공하고:
여기서
R1 및 R2는 각각 독립적으로 수소, 할로겐, 시아노, 임의로 치환된 알킬 (예를 들어, 임의로 치환된 C1-6 알킬), 임의로 치환된 시클로알킬 (예를 들어, 임의로 치환된 C3-6 시클로알킬), 임의로 치환된 알케닐 (예를 들어, 임의로 치환된 C2-6 알케닐), 임의로 치환된 알키닐 (예를 들어, 임의로 치환된 C2-6 알키닐), 임의로 치환된 아릴 (예를 들어, 임의로 치환된 C6-10 아릴), 임의로 치환된 헤테로아릴 (예를 들어, 임의로 치환된 5-10원 헤테로아릴), 임의로 치환된 헤테로시클릴 (예를 들어, 임의로 치환된 4-6원 헤테로시클릴), NR10R11, COOR12, CONR13R14, CN, S(O)nR15, 또는 OR16이고;
여기서
R10 및 R11은 각각 독립적으로 수소, 임의로 치환된 알킬 (예를 들어, 임의로 치환된 C1-6 알킬), 임의로 치환된 시클로알킬 (예를 들어, 임의로 치환된 C3-6 시클로알킬), 임의로 치환된 알카노일 (예를 들어, 임의로 치환된 C1-6 알카노일), 임의로 치환된 시클로알카노일 (예를 들어, 임의로 치환된 C3-6 시클로알카노일), 임의로 치환된 아릴 (예를 들어, 임의로 치환된 C6-10 아릴), 임의로 치환된 헤테로아릴 (예를 들어, 임의로 치환된 5-10원 헤테로아릴), 임의로 치환된 헤테로시클릴 (예를 들어, 임의로 치환된 4-6원 헤테로시클릴), COOR12, 또는 CONR13R14이고;
R12, R13 및 R14는 각각 독립적으로 수소 또는 임의로 치환된 알킬 (예를 들어, 임의로 치환된 C1-6 알킬)이고;
n은 0, 1, 또는 2이고;
R15는 임의로 치환된 알킬 (예를 들어, 임의로 치환된 C1-6 알킬), 임의로 치환된 시클로알킬 (예를 들어, 임의로 치환된 C3-6 시클로알킬), 또는 NR10R11이고;
R16은 수소, 임의로 치환된 알킬 (예를 들어, 임의로 치환된 C1-6 알킬), 임의로 치환된 시클로알킬 (예를 들어, 임의로 치환된 C3-6 시클로알킬), 임의로 치환된 알카노일 (예를 들어, 임의로 치환된 C1-6 알카노일), 임의로 치환된 시클로알카노일 (예를 들어, 임의로 치환된 C3-6 시클로알카노일), 임의로 치환된 아릴 (예를 들어, 임의로 치환된 C6-10 아릴), 임의로 치환된 헤테로아릴 (예를 들어, 임의로 치환된 5-10원 헤테로아릴), 임의로 치환된 헤테로시클릴 (예를 들어, 임의로 치환된 4-6원 헤테로시클릴) 또는 CONR13R14이고;
R3은 임의로 치환된 아릴 (예를 들어, 임의로 치환된 C6-10 아릴) 또는 임의로 치환된 헤테로아릴 (예를 들어, 임의로 치환된 5-10원 헤테로아릴)이며,
단, R1 및 R2가 둘 다 수소인 경우, R3은 임의로 치환된 페닐이 아니다.
일부 실시양태에서, R1 및 R2는 둘 다 수소이며, 단, R3은 임의로 치환된 페닐이 아니다. 일부 실시양태에서는, R1 및 R2 중 단지 하나가 수소이고, 즉, 화학식 I에서 페닐 고리는 단일치환된다. 일부 실시양태에서는, R1 및 R2 둘 다 수소가 아니고, 즉, 화학식 I에서 페닐 고리는 이치환된다.
일부 바람직한 실시양태에서, 화학식 I의 화합물은 화학식 I-1의 화합물이다:
여기서 R1, R2 및 R3은 본원에서 정의된 바와 같다. 일부 실시양태에서, R1은 수소가 아니다. 일부 실시양태에서, R1은 수소이다.
본원에 기재된 실시양태 중 임의의 것에서, R2는 수소일 수 있다. 예를 들어, 일부 실시양태에서, 화학식 I의 화합물은 화학식 Ia의 화합물이다.
여기서 R1 및 R3은 본원에서 정의된 바와 같다. 일부 실시양태에서, R1은 수소가 아니다. 일부 실시양태에서, R1은 수소이다.
일부 실시양태에서, R1은 할로겐, 예컨대 F, Cl, Br, 또는 I이다. 일부 실시양태에서, R1은 CN이다. R1이 할로겐인 경우, 화학식 I의 화합물 (예를 들어, 화학식 Ia의 화합물)은 또한, 커플링 반응 (예를 들어, 팔라듐 매개된 또는 구리 매개된 커플링 반응)을 통한, 다른 화합물, 예컨대 R1이 임의로 치환된 알킬, 임의로 치환된 시클로알킬, 임의로 치환된 아릴, 임의로 치환된 헤테로아릴, 임의로 치환된 헤테로시클릴, NR10R11, COOR12, CONR13R14, CN, S(O)nR15, 또는 OR16인 화학식 I의 화합물의 합성을 위한 합성 중간체의 역할을 할 수 있다.
일부 실시양태에서, R1은 임의로 치환된 알킬이다. 일부 실시양태에서, R1은 임의로 치환된 C1-6 알킬이다. 일부 바람직한 실시양태에서, R1은 임의로 치환된 C1-4 알킬이다. 예를 들어, 일부 실시양태에서, R1은 C1-4 알킬 (예를 들어, 메틸, 에틸, 이소프로필, sec-부틸, tert-부틸)일 수 있다. 일부 실시양태에서, R1은 할로겐 (예를 들어, F) 및 C1-4 알킬로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 임의로 치환된 C1-4 알킬일 수 있다. 예를 들어, R1은 1-3개의 플루오린 등으로 임의로 치환된 C1-4 알킬, 예컨대 CF3, CF3CH2일 수 있다.
일부 실시양태에서, R1은 임의로 치환된 알콕시이다. 일부 실시양태에서, R1은 임의로 치환된 C1-6 알콕시이다. 일부 바람직한 실시양태에서, R1은 임의로 치환된 C1-4 알콕시이다. 예를 들어, R1은 C1-4 알콕시 (예를 들어, 메톡시, 에톡시, 이소프로폭시, sec-부톡시, tert-부톡시)일 수 있다. 일부 실시양태에서, R1은 할로겐 (예를 들어, F) 및 C1-4 알킬로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 임의로 치환된 C1-4 알콕시일 수 있다. 예를 들어, R1은 1-3개의 플루오린으로 임의로 치환된 C1-4 알콕시, 예컨대 CF3O, CF3CH2O 등일 수 있다.
일부 실시양태에서, R1은 임의로 치환된 시클로알킬이다. 일부 실시양태에서, R1은 임의로 치환된 C3-6 시클로알킬이다. 일부 실시양태에서, R1은 C3-6 시클로알킬이다. 일부 실시양태에서, R1은 할로겐 (예를 들어, F) 및 C1-4 알킬로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 임의로 치환된 C3-6 시클로알킬이다. 예를 들어, 일부 실시양태에서, R1은 시클로프로필 또는 시클로부틸이다. 일부 실시양태에서, R1은 1-3개의 플루오린으로 임의로 치환된 시클로프로필 또는 시클로부틸이다.
일부 실시양태에서, R1은 임의로 치환된 시클로알콕시이다. 일부 실시양태에서, R1은 임의로 치환된 C3-6 시클로알콕시이다. 일부 실시양태에서, R1은 C3-6 시클로알콕시이다. 일부 실시양태에서, R1은 할로겐 (예를 들어, F) 및 C1-4 알킬로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 임의로 치환된 C3-6 시클로알콕시이다. 예를 들어, 일부 실시양태에서, R1은 시클로프로폭시 또는 시클로부톡시이다. 일부 실시양태에서, R1은 1-3개의 플루오린으로 임의로 치환된 시클로프로폭시 또는 시클로부톡시이다.
일부 바람직한 실시양태에서, R1은 할로겐, 임의로 치환된 C1-6 알킬, 임의로 치환된 C1-6 알콕시, 임의로 치환된 C3-6 시클로알킬, 또는 임의로 치환된 C3-6 시클로알콕시이다. 일부 바람직한 실시양태에서, R1은 할로겐 및 C1-4 알킬로부터 독립적으로 선택된 1 내지 3개의 치환기로 각각 임의로 치환된 C1-4 알킬, C1-4 알콕시, C3-6 시클로알킬, 또는 C3-6 시클로알콕시이다. 일부 바람직한 실시양태에서, R1은, 각각 1-3개의 플루오린으로 임의로 치환된 C1-4 알킬 또는 C1-4 알콕시이다.
일부 실시양태에서, R1은 임의로 치환된 아릴, 예컨대 임의로 치환된 C6-12 아릴 (예를 들어, 페닐)이다. 일부 실시양태에서, R1은 할로겐, 히드록실, 시아노, 임의로 치환된 C1-4 알킬, 임의로 치환된 C1-4 알콕시, 임의로 치환된 C3-6 시클로알킬, 및 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1 또는 2개의) 치환기로 임의로 치환된 C6-12 아릴 (예를 들어, 페닐)이다. 일부 실시양태에서, R1은 할로겐 (예를 들어, F, Cl), 시아노, C1-4 알킬, C1-4 알콕시, C3-6 시클로알킬, 및 C3-6 시클로알콕시로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1 또는 2개의) 치환기로 임의로 치환된 C6-12 아릴 (예를 들어, 페닐)이고, 여기서 알킬, 알콕시, 시클로알킬, 및 시클로알콕시는 각각 할로겐 (예를 들어, F) 및 C1-4 알킬로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된다.
일부 실시양태에서, R1은 임의로 치환된 헤테로아릴이다. 예를 들어, 일부 실시양태에서, R1은 할로겐, 시아노, 임의로 치환된 C1-4 알킬, 임의로 치환된 C1-4 알콕시, 임의로 치환된 C3-6 시클로알킬, 및 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1 또는 2개의) 치환기로 임의로 치환된 5-10원 헤테로아릴 (예를 들어, 본원에 기재된 바와 같은 5 또는 6원 헤테로아릴)이다. 일부 실시양태에서, R1은 할로겐 (예를 들어, F, Cl), 시아노, C1-4 알킬, C1-4 알콕시, C3-6 시클로알킬, 및 C3-6 시클로알콕시로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1 또는 2개의) 치환기로 임의로 치환된 5-10원 헤테로아릴 (예를 들어, 본원에 기재된 바와 같은 5 또는 6원 헤테로아릴)이고, 여기서 알킬, 알콕시, 시클로알킬, 및 시클로알콕시는 각각 할로겐 (예를 들어, F) 및 C1-4 알킬로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된다.
일부 실시양태에서, R1은 할로겐, 히드록실, 시아노, COOR12 (여기서 R12는 수소 또는 임의로 치환된 C1-6 알킬, 임의로 치환된 C1-4 알킬, 임의로 치환된 C1-4 알콕시, 임의로 치환된 C3-6 시클로알킬, 및 임의로 치환된 C3-6 시클로알콕시임)로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1 또는 2개의) 치환기로 임의로 치환된 5-10원 헤테로아릴 (예를 들어, 본원에 기재된 바와 같은 5 또는 6원 헤테로아릴, 예컨대 테트라졸릴, 피리디닐 등)일 수 있다. 일부 실시양태에서, R1은 임의로 치환된 피리디닐 (예를 들어, 2-, 3-, 또는 4-피리디닐)일 수 있다. 일부 실시양태에서, 피리디닐은 할로겐, 히드록실, 시아노, COOR12, 여기서 R12는 수소 또는 임의로 치환된 C1-6 알킬, 임의로 치환된 C1-4 알킬, 임의로 치환된 C1-4 알콕시, 임의로 치환된 C3-6 시클로알킬, 및 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1 또는 2개의) 치환기로 임의로 치환될 수 있다. 일부 실시양태에서, 피리디닐은 COOR12 (예를 들어, COOH)로 치환될 수 있다. 일부 실시양태에서, 피리디닐은 COOH 또는 생체내에서 카르복실산 기 (또는 그의 염)로 전환될 수 있는 기로 치환될 수 있다. 생체내에서 카르복실산 기 (또는 그의 염)로 전환될 수 있는 적합한 기는 관련 기술분야에 공지된 것들, 예를 들어, 에스테르, 아미드 등을 포함한다. 이론에 의해 국한되길 바라지는 않지만, 카르복실산 관능기, 예컨대 피리디닐 카르복실산은, 간으로의 화합물의 표적화된 전달을 도울 수 있고, 따라서, 예를 들어, 전신 노출의 요구를 감소시키면서, 간 질환 (예를 들어, NASH)의 치료를 위해 특히 유용할 수 있다고 여겨진다.
일부 실시양태에서, R1은 임의로 치환된 3-피리디닐일 수 있다. 예를 들어, 일부 실시양태에서, 화학식 I의 화합물은 화학식 Ic의 화합물일 수 있다:
여기서 R3 및 R20은 본원에서 정의된 바와 같다. 화학식 Ic의 화합물에 적합한 R20은, COOR20 기가 COOH (또는 그의 염)이거나 생체내에서 COOH (또는 그의 염)으로 전환될 수 있는 것인 임의의 기를 포함한다. 일부 실시양태에서, R20은 수소, 임의로 치환된 알킬, 또는 임의로 치환된 시클로알킬 (예를 들어, 임의로 치환된 C3-6 시클로알킬)일 수 있다. 일부 실시양태에서, R20은 임의로 치환된 C1-6 알킬 (예를 들어, 임의로 치환된 C1-4 알킬)일 수 있다. 일부 실시양태에서, R20은 수소 또는 임의로 치환된 C1-4 알킬 (예를 들어, 메틸, 에틸 등)일 수 있다. 알킬 또는 시클로알킬에 대한 다양한 치환기(들)가 사용될 수 있고, 이는 생체내에서 에스테르 기에서 카르복실산 기 (또는 그의 염)로의 전환을 막지 않는 임의의 것들을 포함한다. 그러나, 바람직하게는, R20 기 (임의의 치환기(들) 포함)는, 화학식 Ic의 화합물 또는 그의 생성된 분열 부산물 (즉, 생성된 스피로락톤 생성물이 아님)이 치료 유효 용량에서 대상체 사용자에 대한 독성을 갖지 않거나 허용가능한 독성을 갖도록 선택된다. 일부 실시양태에서, COOR20 기는 단순 알킬 에스테르 (예를 들어, 메틸, 에틸, 또는 다른 C1-4 알킬 에스테르)일 수 있다.
일부 실시양태에서, R20은 올리고- 또는 폴리에틸렌 글리콜 사슬을 포함할 수 있다. 예를 들어, 일부 실시양태에서, R20은 일 수 있고, 여기서 p는 1-500 (예를 들어, 1-10, 1-50, 1-100 등, 예를 들어, 1, 2, 또는 3)의 정수이고, R21은 수소, C1-4 알킬 (예를 들어, 메틸), 또는 산소 보호 기이다. 적합한 산소 보호 기는 관련 기술분야에 공지된 것들, 예를 들어, 메틸, 메톡시메틸 등, 예를 들어, 문헌 ["Protective Groups in Organic Synthesis", 4th ed. P. G. M. Wuts; T. W. Greene, John Wiley, 2007], 및 그에 인용된 참조문헌에 기재된 것을 포함한다. 일부 실시양태에서, R20은 산소 치환된 알킬일 수 있고, 이는 "아세탈" 구조를 형성한다. 이론에 의해 국한되길 바라지는 않지만, 이러한 기는 보다 반응성인(labile) 에스테르를 형성할 수 있고, 생체내에서 보다 빠르게 분열될 수 있다. 예를 들어, 일부 실시양태에서, R20은 일 수 있고, 여기서 R22는 C1-4 알킬이고, R23은 수소 또는 C1-4 알킬이다.
상기에서 논의된 접근은 본원에 기재된 스피로락톤 코어로 제한되지 않는다. 예를 들어, 본 개시내용을 고려하여 관련 기술분야의 통상의 기술자에게 용이하게 명백한 바와 같이, 임의의 ACC 억제제를 간 표적화 모이어티, 예컨대 COOH 또는 생체내에서 카르복실산 기로 전환될 수 있는 기, 예를 들어, 에스테르, 아미드 등으로 치환된 피리디닐을 포함하도록 엔지니어링할 수 있고, 이는 간 질환 (예를 들어, NASH)의 치료를 위해 특히 유용할 수 있다. 일부 실시양태에서, 이러한 ACC 억제제는, 단순 알킬 에스테르일 수 있는, 본원에 기재된 바와 같은 COOR20으로 치환된 피리디닐을 포함하도록 엔지니어링될 수 있다.
일부 실시양태에서, R1은 또한 임의로 치환된 헤테로시클릴일 수 있다. 예를 들어, 일부 실시양태에서, R1은 할로겐, 옥소, 임의로 치환된 C1-4 알킬, 임의로 치환된 C1-4 알콕시, 임의로 치환된 C3-6 시클로알킬, 및 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1 또는 2개의) 치환기로 임의로 치환된 4-6원 헤테로시클릴이다. 일부 실시양태에서, R1은 할로겐 (예를 들어, F, Cl), C1-4 알킬, C1-4 알콕시, C3-6 시클로알킬, 및 C3-6 시클로알콕시로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1 또는 2개의) 치환기로 임의로 치환된 4-6원 헤테로시클릴이고, 여기서 알킬, 알콕시, 시클로알킬, 및 시클로알콕시는 각각 할로겐 (예를 들어, F) 및 C1-4 알킬로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된다.
일부 바람직한 실시양태에서, R1은 NR10R11이다. 예를 들어, 일부 실시양태에서, 화학식 Ia의 화합물은 화학식 Ib의 화합물이다:
여기서 R10, R11 및 R3은 본원에서 정의된 바와 같다. 일부 실시양태에서, R10 및 R11 중 하나는 임의로 치환된 페닐 또는 임의로 치환된 5 또는 6원 헤테로아릴 (예를 들어, 본원에 기재된 바와 같은 것)이다. 일부 실시양태에서, R10 및 R11 중 하나는 할로겐, 시아노 및 C1-4 알킬로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1 또는 2개의) 치환기로 임의로 치환된 5원 헤테로아릴 (예를 들어, 본원에 기재된 바와 같은 2-4개의 질소 원자를 갖는 것들)이다. 예를 들어, 일부 실시양태에서, R10 및 R11 중 하나는 피라졸릴, 트리아졸릴 또는 테트라졸릴이다. 일부 실시양태에서, R10 및 R11 중 하나는 1 또는 2개의 독립적으로 선택된 C1-4 알킬 (예를 들어, 메틸 또는 에틸)로 각각 임의로 치환된 피라졸릴, 트리아졸릴 또는 테트라졸릴이다. 이들 실시양태 중 임의의 것에서, R10 및 R11 중 다른 하나는 수소 또는 임의로 치환된 알킬 (예를 들어, C1-4 알킬, 예컨대 메틸 또는 에틸)일 수 있다. 다른 적합한 R10 및 R11은 본원에 기재된다.
일부 실시양태에서, R1은 COOR12 또는 CONR13R14일 수 있고, 여기서 R12, R13 및 R14는 본원에서 정의된다. 예를 들어, 일부 실시양태에서, R1은 COOR12이고, R12는 수소 또는 임의로 치환된 알킬일 수 있다. 일부 실시양태에서, R12는 수소 또는 임의로 치환된 C1-6 알킬, 예컨대 할로겐 및 C1-4 알킬로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 임의로 치환된 C1-4 알킬일 수 있다. 일부 실시양태에서, R1은 CONR13R14이고, R13 및 R14는 각각 독립적으로 수소 또는 임의로 치환된 알킬이다. 일부 실시양태에서, R13 및 R14는 각각 독립적으로 수소 또는 임의로 치환된 C1-6 알킬, 예컨대 할로겐 및 C1-4 알킬로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 임의로 치환된 C1-4 알킬이다.
일부 실시양태에서, R1은 S(O)nR15일 수 있고, 여기서 n 및 R15는 본원에서 정의된다. 일부 실시양태에서, n은 0이다. 일부 실시양태에서, n은 1이다. 일부 실시양태에서, n은 2이다. 일부 실시양태에서, R15는 임의로 치환된 알킬이다. 일부 실시양태에서, R15는 임의로 치환된 C1-6 알킬, 예컨대 할로겐 및 C1-4 알킬로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 임의로 치환된 C1-4 알킬이다. 일부 실시양태에서, R15는 임의로 치환된 시클로알킬이다. 일부 실시양태에서, R15는 임의로 치환된 C3-6 시클로알킬, 예컨대 할로겐 및 C1-4 알킬로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 임의로 치환된 C3-6 시클로알킬이다. 일부 실시양태에서, R15는 NR10R11이고, R10 및 R11에 적합한 기는 본원에 기재된다.
일부 실시양태에서, R1은 OR16일 수 있고, 여기서 R16은 본원에서 정의된다. 일부 실시양태에서, R16은 H이다. 일부 바람직한 실시양태에서, R16은 임의로 치환된 알킬 (예를 들어, 임의로 치환된 C1-6 알킬) 또는 임의로 치환된 시클로알킬 (예를 들어, 임의로 치환된 C3-6 시클로알킬)이고, 따라서 R1은 본원에 기재된 바와 같은 임의로 치환된 알콕시 또는 시클로알콕시이다. 다른 적합한 R16은 본원에 기재된다.
화학식 I의 화합물 (예를 들어, 화학식 I-1, 화학식 Ia, 화학식 Ib, 또는 화학식 Ic의 화합물)에 적합한 R3은 본원에 기재된다. 일부 실시양태에서, R3은 임의로 치환된 아릴, 예를 들어, 임의로 치환된 C6-10아릴이다. 일부 실시양태에서, R3은 할로겐, 히드록실, 시아노, 임의로 치환된 C1-4 알킬, 임의로 치환된 C1-4 알콕시, 임의로 치환된 C3-6 시클로알킬, 및 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 임의로 치환된 C6-10아릴이다. 일부 실시양태에서, R3은 임의로 치환된 페닐일 수 있다. 일부 실시양태에서, R3은 임의로 치환된 비시클릭 아릴일 수 있다. 예를 들어, 일부 바람직한 실시양태에서, R3은 임의로 치환된 나프틸이다. 일부 실시양태에서, R3은 할로겐, 히드록실, 시아노, C1-4 알킬, C1-4 알콕시, C3-6 시클로알킬, 및 C3-6 시클로알콕시로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된 나프틸이고, 여기서 알킬, 알콕시, 시클로알킬, 및 시클로알콕시는 각각 할로겐 (예를 들어, F) 및 C1-4 알킬로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된다. 일부 실시양태에서, R3은 할로겐, 히드록실, 시아노, 1-3개의 할로겐으로 임의로 치환된 C1-4 알킬, 1-3개의 할로겐으로 임의로 치환된 C1-4 알콕시, 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알킬, 및 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된 나프틸이다. 일부 실시양태에서, R3은 플루오로, 클로로, 히드록실, 메틸, 에틸, 트리플루오로메틸, 트리플루오로메톡시, 메톡시, 에톡시, 및 시클로프로필로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된 나프틸이다.
일부 실시양태에서, R3은 또한 임의로 치환된 헤테로아릴일 수 있다. 예를 들어, 일부 실시양태에서, R3은 임의로 치환된 8-10원 비시클릭 헤테로아릴이다. 일부 실시양태에서, R3은 할로겐, 시아노, 임의로 치환된 C1-4 알킬, 임의로 치환된 C1-4 알콕시, 임의로 치환된 C3-6 시클로알킬, 및 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 임의로 치환된 8-10원 비시클릭 헤테로아릴이다. 일부 실시양태에서, R3은 임의로 치환된 벤즈이미다졸릴, 피롤로피리디닐, 피라졸로피리디닐, 인다졸릴, 인돌릴, 퀴놀리닐 또는 이소퀴놀리닐이다. 일부 실시양태에서, R3은 할로겐, 히드록실, 시아노, C1-4 알킬, C1-4 알콕시, C3-6 시클로알킬, 및 C3-6 시클로알콕시로부터 독립적으로 선택된 1 내지 3개의 치환기로 각각 임의로 치환된 벤즈이미다졸릴, 피롤로피리디닐, 피라졸로피리디닐, 인다졸릴, 인돌릴, 퀴놀리닐 또는 이소퀴놀리닐이고, 여기서 알킬, 알콕시, 시클로알킬, 및 시클로알콕시는 각각 할로겐 (예를 들어, F) 및 C1-4 알킬로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된다. 일부 실시양태에서, R3은 할로겐, 히드록실, 시아노, 1-3개의 할로겐으로 임의로 치환된 C1-4 알킬, 1-3개의 할로겐으로 임의로 치환된 C1-4 알콕시, 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알킬, 및 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1 내지 3개의 치환기로 각각 임의로 치환된 벤즈이미다졸릴, 피롤로피리디닐, 피라졸로피리디닐, 인다졸릴, 인돌릴, 퀴놀리닐 또는 이소퀴놀리닐이다. 일부 실시양태에서, R3은 플루오로, 클로로, 히드록실, 메틸, 에틸, 트리플루오로메틸, 트리플루오로메톡시, 메톡시, 에톡시, 및 시클로프로필로부터 독립적으로 선택된 1 내지 3개의 치환기로 각각 임의로 치환된 벤즈이미다졸릴, 피롤로피리디닐, 피라졸로피리디닐, 인다졸릴, 인돌릴, 퀴놀리닐 또는 이소퀴놀리닐이다. 바람직하게는, 본원에서 헤테로아릴의 치환은, 할로겐, 시아노, 또는 산소 원자 (예를 들어, 히드록실, 알콕시 또는 시클로알콕시 기로부터의 것)가 헤테로아릴의 고리 헤테로원자, 예컨대 고리 질소 원자에 직접 부착되게 하지 않는다. 또한, 관련 기술분야의 통상의 기술자는, 화합물이 질소 고리 원자 바로 옆의 탄소에 부착된 히드록실 기를 갖는 경우, 화합물은 대부분 하나 이상의 호변이성질체 형태로 존재할 수 있음을 이해한다. 예를 들어, 2-히드록실 치환된 1-메틸-벤즈이미다졸은 대부분 하기에 제시된 바와 같이 형태 B로 존재할 수 있다:
. 따라서, 본원에서 사용되는 바와 같이, 히드록실 기로 치환된 헤테로아릴은 가능한 경우 모든 호변이성질체 형태, 예를 들어 상기 형태 A 및 B를 포함하는 것으로 이해되어야 한다.
R3에 적합한 비시클릭 아릴 또는 헤테로아릴의 다양한 위치, 예를 들어 원위 고리에 바로 인접하지 않은 위치가 스피로락톤 코어에 대한 부착에 사용될 수 있다. 예를 들어, 1- 및 2-나프틸 둘 다 적합한 R3 기이다. 일부 실시양태에서, R3은 바람직하게는 2-나프틸이다. 유사하게, 퀴놀리닐은 위치 2-8: 중 하나에 7개의 상이한 부착점을 가질 수 있다. 일부 실시양태에서, R3은 바람직하게는 2-, 3-, 6-, 또는 7-퀴놀리닐 (원위 고리에 바로 인접하지 않은 위치)이다. 일부 실시양태에서, R3은 4-, 5-, 또는 8-퀴놀리닐이다.
본원에 기재된 실시양태 중 임의의 것에서, R3은 임의로 치환된 나프틸, 퀴놀리닐, 벤즈이미다졸릴, 피롤로피리디닐, 인돌릴, 또는 인다졸릴일 수 있다:
일부 실시양태에서, 나프틸, 퀴놀리닐, 벤즈이미다졸릴, 피롤로피리디닐, 인돌릴, 또는 인다졸릴은 할로겐, 시아노, 히드록실, C1-4 알킬, C1-4 알콕시, C3-6 시클로알킬, 및 C3-6 시클로알콕시로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 임의로 치환되고, 여기서 알킬, 알콕시, 시클로알킬, 및 시클로알콕시는 각각 할로겐 (예를 들어, F) 및 C1-4 알킬로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 임의로 치환된다. 일부 실시양태에서, 나프틸, 퀴놀리닐, 벤즈이미다졸릴, 피롤로피리디닐, 인돌릴, 또는 인다졸릴은 할로겐, 시아노, 히드록실, 1-3개의 할로겐으로 임의로 치환된 C1-4 알킬, 1-3개의 할로겐으로 임의로 치환된 C1-4 알콕시, 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알킬, 및 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 임의로 치환된다. 일부 실시양태에서, 나프틸, 퀴놀리닐, 벤즈이미다졸릴, 피롤로피리디닐, 인돌릴, 또는 인다졸릴은 플루오로, 클로로, 히드록실, 메틸, 트리플루오로메틸, 에틸, 메톡시, 트리플루오로메톡시, 에톡시, 및 시클로프로필로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 임의로 치환된다. 바람직하게는, 본원에서 벤즈이미다졸릴, 피롤로피리디닐, 인돌릴, 또는 인다졸릴의 치환은, 할로겐, 시아노, 또는 산소 원자 (예를 들어, 히드록실, 알콕시 또는 시클로알콕시 기로부터의 것)가 고리 질소 원자에 직접 부착되게 하지 않는다.
본원에 기재된 실시양태 중 임의의 것에서, R3은 임의로 치환된 나프틸 또는 퀴놀리닐일 수 있다:
일부 실시양태에서, 나프틸 또는 퀴놀리닐은 할로겐, 시아노, C1-4 알킬, C1-4 알콕시, C3-6 시클로알킬, 및 C3-6 시클로알콕시로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환되고, 여기서 알킬, 알콕시, 시클로알킬, 및 시클로알콕시는 각각 할로겐 (예를 들어, F) 및 C1-4 알킬로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된다. 일부 실시양태에서, 나프틸 또는 퀴놀리닐은 할로겐, 시아노, 1-3개의 할로겐으로 임의로 치환된 C1-4 알킬, 1-3개의 할로겐으로 임의로 치환된 C1-4 알콕시, 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알킬, 및 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된다. 일부 실시양태에서, 나프틸 또는 퀴놀리닐은 플루오로, 클로로, 히드록실, 메틸, 트리플루오로메틸, 에틸, 메톡시, 트리플루오로메톡시, 에톡시, 및 시클로프로필로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된다.
일부 실시양태에서, R3은 하기와 같을 수 있다:
본원에 기재된 실시양태 중 임의의 것에서, R3은 하기와 같을 수 있다:
예시적 스피로락톤 화합물
본 개시내용의 특정 실시양태는 일부 예시적 스피로락톤 화합물에 관한 것이다.
일부 실시양태에서, 본 개시내용은 화학식 II-1 내지 화학식 II-3의 화합물, 또는 그의 제약상 허용되는 염을 제공한다:
여기서 R3은 본원에서 정의된 것들 중 임의의 것일 수 있다. 예를 들어, 일부 바람직한 실시양태에서, R3은 임의로 치환된 나프틸이다. 일부 실시양태에서, R3은 할로겐, 시아노, 1-3개의 할로겐으로 임의로 치환된 C1-4 알킬, 1-3개의 할로겐으로 임의로 치환된 C1-4 알콕시, 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알킬, 및 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된 나프틸이다. 일부 실시양태에서, R3은 플루오로, 클로로, 히드록실, 메틸, 에틸, 트리플루오로메틸, 트리플루오로메톡시, 메톡시, 에톡시, 및 시클로프로필로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된 나프틸이다. 일부 바람직한 실시양태에서, R3은 임의로 치환된 퀴놀리닐이다. 일부 실시양태에서, R3은 할로겐, 시아노, 1-3개의 할로겐으로 임의로 치환된 C1-4 알킬, 1-3개의 할로겐으로 임의로 치환된 C1-4 알콕시, 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알킬, 및 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된 퀴놀리닐이다. 일부 실시양태에서, R3은 플루오로, 클로로, 히드록실, 메틸, 에틸, 트리플루오로메틸, 트리플루오로메톡시, 메톡시, 에톡시, 및 시클로프로필로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된 퀴놀리닐이다.
일부 실시양태에서, 화학식 II-1 내지 화학식 II-3에서 R3은, 하기와 같을 수 있고:
이는 각각 플루오로, 클로로, 히드록실, 메틸, 트리플루오로메틸, 에틸, 메톡시, 트리플루오로메톡시, 에톡시, 및 시클로프로필로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된다.
일부 실시양태에서, 본 개시내용은 화학식 III-1 또는 화학식 III-2의 화합물, 또는 그의 제약상 허용되는 염을 제공하고:
여기서 R1 및 R2는 본원에서 정의된 것들 중 임의의 것일 수 있다. 일부 실시양태에서, 화학식 III-1 또는 화학식 III-2에서 R2는 수소이다.
일부 실시양태에서, 본 개시내용은 화학식 III-3 내지 화학식 III-6의 화합물, 또는 그의 제약상 허용되는 염을 제공하고:
여기서 R1 및 R2는 적합한 것으로 본원에서 정의된 것들 중 임의의 것일 수 있다.
일부 실시양태에서, 화학식 III-1 내지 화학식 III-6 중 임의의 것에서 R1은 임의로 치환된 C1-4 알킬, 예를 들어, 메틸, 에틸, 이소프로필, 또는 tert-부틸일 수 있다. 일부 실시양태에서, 화학식 III-1 내지 화학식 III-6 중 임의의 것에서 R1은 임의로 치환된 C1-4 알콕시, 예를 들어, 메톡시, 트리플루오로메톡시, 에톡시 또는 이소프로폭시일 수 있다. 일부 실시양태에서, 화학식 III-1 내지 화학식 III-6 중 임의의 것에서 R1은 NR10R11일 수 있다. 일부 실시양태에서, R10 및 R11 중 하나는 임의로 치환된 5 또는 6원 헤테로아릴이다. 일부 실시양태에서, R10 및 R11 중 하나는, 할로겐, 시아노 및 C1-4 알킬로부터 독립적으로 선택된 1 또는 2개의 치환기로 임의로 치환된, 2-4개의 고리 질소 원자를 갖는 5원 헤테로아릴이다. 일부 실시양태에서, R10 및 R11 중 하나는 C1-4 알킬로 각각 임의로 치환된 피라졸릴, 트리아졸릴 또는 테트라졸릴이다. 이들 실시양태 중 임의의 것에서, R10 및 R11 중 다른 하나는 수소 또는 C1-4 알킬 (예를 들어, 메틸)일 수 있다. 예를 들어, 일부 실시양태에서, R10 및 R11 중 하나는 이고, R10 및 R11 중 다른 하나는 수소 또는 메틸이다. 일부 실시양태에서, 화학식 III-1, 화학식 III-2, 화학식 III-4 및 화학식 III-6 중 임의의 것에서 R2는 수소일 수 있다. 다른 적합한 R1 및 R2는 본원에 기재된다.
일부 실시양태에서, 본 개시내용은 또한, 실시예 1-22의 화합물 중 임의의 것, 또는 그의 염 (예를 들어, 제약상 허용되는 염)을 제공한다. 예를 들어, 일부 실시양태에서, 본 개시내용은 또한, 하기 화합물, 또는 그의 제약상 허용되는 염을 제공한다:
합성 방법
본 개시내용의 특정 실시양태는 본원에 기재된 스피로락톤 화합물의 합성 방법에 관한 것이다.
일부 실시양태에서, 본 개시내용은 화학식 I의 화합물의 합성 방법을 제공하고:
여기서 R1, R2, 및 R3은 본원에서 정의된 바와 같다. 일부 실시양태에서, 방법은, 화학식 S-1의 화합물, 또는 그의 염을, 화학식 S-2의 산, 또는 그의 활성화 형태 (예를 들어, 아실 클로라이드, 무수물)와 반응시켜 화학식 I의 화합물을 형성하는 것을 포함하고:
여기서 R1, R2, 및 R3은 본원에서 정의된 바와 같다. 적합한 시약 및 이러한 전환의 조건은 관련 기술분야에 공지되어 있고, 실시예 섹션에 예시되어 있으며, 예를 들어, HATU ((1-[비스(디메틸아미노)메틸렌]-1H-1,2,3-트리아졸로[4,5-b]피리디늄 3-옥시드 헥사플루오로포스페이트)) 및 디이소프로필 아민을 사용한다.
일부 실시양태에서, 방법은 화학식 S-3의 화합물을 R1G2 또는 또 다른 작용제와 반응시켜 화학식 I의 화합물을 형성하는 것을 포함하고:
여기서 G1은 할로 (바람직하게는 Br 또는 I), CN, 또는 NH2이고, R1, R2, 및 R3은 본원에서 정의된 바와 같고, 여기서 R1G2는 적합한 조건 하에 화학식 S-3의 화합물과 반응하여 화학식 I을 형성할 수 있다. 예를 들어, 일부 실시양태에서, G1은 할로이고, R1G2는, 예를 들어, 팔라듐 또는 구리 촉매화된 커플링 반응 조건 하에, 화학식 S-3의 화합물과 반응하여 화학식 I의 화합물을 형성할 수 있는 유기아연 시약, 유기붕소 시약, 유기주석 시약일 수 있다. 일부 실시양태에서, R1G2는 아미노 화합물이고 여기서 G2는 H이고, G1은 할로이고, R1G2는, 예를 들어, 팔라듐 또는 구리 촉매화된 커플링 반응 조건 하에, 화학식 S-3의 화합물과 반응하여 화학식 I의 화합물을 형성할 수 있다. 일부 실시양태에서, R2는 H이다. 일부 실시양태에서, 화학식 S-3의 화합물은 화학식 S-3a이고, 여기서 G1 및 R3은 본원에서 정의되고, 예를 들어, 화학식 S-3a의 일부 실시양태에서, G1은 할로 (예를 들어, Br 또는 I)이고, 하기이다:
. 일부 실시양태에서, R1G2는 이다. 일부 실시양태에서, R1G2는 유기붕소 작용제, 유기주석 작용제, 또는 유기금속 작용제, 예컨대 유기아연 작용제이고, 여기서 G2는 보론산 또는 에스테르, 삼치환된 Sn, 또는 금속 이온, 예컨대 Zn이고, 일부 실시양태에서, R1은 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴 (예를 들어, 5- 또는 6원 헤테로아릴, 예컨대 2-, 3-, 또는 4-피리디닐)이다. 적합한 커플링 반응 조건은 관련 기술분야에 공지되어 있고, 실시예 섹션에 예시되어 있다. G1이 CN인 일부 실시양태에서, 화학식 S-3 또는 S-3a의 화합물은 또 다른 작용제, 예컨대 아지드와 반응하여 화학식 I 또는 Ia에서의 R1 기와 같은 테트라졸을 형성할 수 있다.
화학식 S-1의 화합물은 본 개시내용을 고려하여 관련 기술분야의 통상의 기술자에 의해 용이하게 접근가능할 수 있다. 예를 들어, 화학식 S-1의 특정 화합물은 하기 반응식 1에 의해 제조될 수 있고:
여기서 Pg1은 질소 보호 기, 예컨대 벤질이고, R100 및 R101은 독립적으로 수소 또는 C1-4 알킬 (예를 들어, 메틸)이고, R1 및 R2는 본원에서 정의된다. 일부 실시양태에서, R100 및 R101은 둘 다 수소이다. 일부 실시양태에서, R100 및 R101 중 하나는 수소이고, R100 및 R101 중 다른 하나는 C1-4 알킬 (예를 들어, 메틸)이다. 따라서, 화학식 S-4의 화합물을, 예를 들어, 강염기, 예컨대 n-BuLi로 처리할 수 있고, 이어서 화학식 S-5의 화합물과 반응시킬 수 있다. 적합한 조건, 예를 들어, 수시간 동안의 환류 하에, 산 처리 (예를 들어, 50% 아세트산 및 농축 H2SO4) 후, 화학식 S-6의 스피로시클릭 화합물을 얻을 수 있다. 예를 들어, 문헌 [Yamato M. et al. "Synthesis and Structure-Activity Relationship of Spiro[isochromanpiperidine] Analogues for Inhibition of Histamine Release," J. Med. Chem. 24:194-198 (1981)]을 참조하며, 이것의 내용은 그 전체가 본원에 참조로 포함된다. 화학식 S-6의 화합물의 탈보호에 의해 화학식 S-1의 화합물을 얻을 수 있다. 예를 들어, Pg1이 벤질인 경우, 수소화 반응은 화학식 S-6의 화합물을 화학식 S-1의 화합물로 전환시킬 수 있다. 다른 적합한 질소 보호 기는 관련 기술분야에 공지되어 있고, 예를 들어, 문헌 ["Protective Groups in Organic Synthesis", 4th ed. P. G. M. Wuts; T. W. Greene, John Wiley, 2007], 및 그에 인용된 참조문헌에 기재되어 있다.
일부 실시양태에서, 본 개시내용은, 예를 들어, 하기 반응식 2에 의한, 화합물 B3 및 화학식 S-1a의 화합물, 또는 그의 염의 제조 방법을 제공하고:
여기서 G1은 할로겐, 예를 들어, Br 또는 I, 또는 시아노이다. 일부 실시양태에서, B1, B2, B3, 및 화학식 S-1a의 화합물에서 피페리딘 질소는 질소 보호 기, 예컨대 벤질, Boc 등으로 보호될 수 있다. 다른 적합한 질소 보호 기는, 예를 들어, 문헌 ["Protective Groups in Organic Synthesis", 4th ed. P. G. M. Wuts; T. W. Greene, John Wiley, 2007], 및 그에 인용된 참조문헌에 기재된 바와 같은, 관련 기술분야에 공지된 것들을 포함한다. 예를 들어, 반응식 1에 기재된 방법에 의해 얻어질 수 있는 화합물 B1, 또는 그의 염을, 질화 반응 (예를 들어, HNO3 사용)시켜 화합물 B2, 또는 그의 염을 형성할 수 있고, 이어서 이것 (또는 그의 N-보호된 유도체)을 환원 (예를 들어, Pd/C로의 수소화)시켜 화합물 B3, 또는 그의 염, 또는 그의 N-보호된 유도체를 형성할 수 있다. 이어서, 화합물 B3, 또는 그의 염, 또는 그의 N-보호된 유도체를, 예를 들어, 전형적인 샌드마이어(Sandmeyer) 조건 (예를 들어, 디아조화 후 CuBr, CuCN 또는 CuI와의 반응) 하에, 할로겐화 반응시켜 아민 기를 할로겐 (예를 들어, Br, 또는 I)으로 전환시킬 수 있다. 화합물 B3 또는 화학식 S-1a의 화합물을 화학식 S-2의 산, 또는 그의 활성화 형태 (예를 들어, 아실 클로라이드, 무수물)와 반응시켜 화학식 S-3a의 특정 화합물을 형성할 수 있다.
관련 기술분야의 통상의 기술자에게 명백한 바와 같이, 특정 관능기가 원치않는 반응에 놓이는 것을 막기 위해 종래의 보호 기가 필수적일 수 있다. 다양한 관능기에 적합한 보호 기 뿐만 아니라 특정 관능기의 보호 및 탈보호에 적합한 조건은 관련 기술분야에 널리 공지되어 있다. 예를 들어, 많은 보호 기가 문헌 ["Protective Groups in Organic Synthesis", 4th ed. P. G. M. Wuts; T. W. Greene, John Wiley, 2007], 및 그에 인용된 참조문헌에 기재되어 있다. 본원에 기재된 반응의 시약은 일반적으로 공지된 화합물이거나 공지된 절차 또는 그의 분명한 변형에 의해 제조될 수 있다. 예를 들어, 많은 시약이 상업적 공급원, 예컨대 알드리치 케미칼 컴파니(Aldrich Chemical Co., 미국 위스콘신주 밀와우키), 시그마(Sigma, 미국 미주리주 세인트 루이스)로부터 입수가능하다. 다른 것들은 표준 참조 문헌, 예컨대 문헌 [Fieser and Fieser's Reagents for Organic Synthesis, Volumes 1-15 (John Wiley and Sons, 1991)], [Rodd's Chemistry of Carbon Compounds, Volumes 1-5 and Supplemental (Elsevier Science Publishers, 1989)], [Organic Reactions, Volumes 1-40 (John Wiley and Sons, 1991)], [March's Advanced Organic Chemistry, (Wiley, 7th Edition)], 및 [Larock's Comprehensive Organic Transformations (Wiley-VCH, 1999)]에 기재된 절차, 또는 그의 분명한 변형에 의해 제조될 수 있다.
제약 조성물
특정 실시양태는 본 개시내용의 스피로락톤 화합물 중 하나 이상을 포함하는 제약 조성물에 관한 것이다.
제약 조성물은 임의로 제약상 허용되는 부형제를 함유할 수 있다. 일부 실시양태에서, 제약 조성물은 본 개시내용의 스피로락톤 화합물 및 제약상 허용되는 부형제를 포함한다. 제약상 허용되는 부형제는 관련 기술분야에 공지되어 있다. 비제한적인 적합한 부형제는, 예를 들어, 캡슐화 물질 또는 첨가제, 예컨대 흡수 가속화제, 산화방지제, 결합제, 완충제, 코팅제, 착색제, 희석제, 붕해제, 유화제, 증량제, 충전제, 착향제, 함습제, 윤활제, 향수, 보존제, 추진제, 이형제, 멸균제, 감미제, 가용화제, 습윤제 및 이들의 혼합물을 포함한다. 또한, 제약 조성물의 제제화에 사용되는 다양한 부형제 및 그의 제조를 위한 공지된 기술을 개시하는 문헌 [Remington's The Science and Practice of Pharmacy, 21st Edition, A. R. Gennaro (Lippincott, Williams & Wilkins, Baltimore, Md., 2005); (본원에 참조로 포함됨)]을 참조한다.
제약 조성물은 본 개시내용의 스피로락톤 화합물 중 임의의 하나 이상을 포함할 수 있다. 예를 들어, 일부 실시양태에서, 제약 조성물은 화학식 I, 화학식 I-1, 화학식 Ia, 화학식 Ib, 화학식 Ic, 화학식 II-1 내지 II-3, 및 화학식 III-1 내지 III-6 중 임의의 것의 화합물, 또는 실시예 1-22 중 임의의 것, 또는 그의 제약상 허용되는 염을 포함한다. 본원에 기재된 실시양태 중 임의의 것에서, 제약 조성물은 실시예 1-22의 화합물 중 임의의 것, 또는 그의 제약상 허용되는 염을 포함한다. 예를 들어, 일부 실시양태에서, 제약 조성물은 하기 화합물 또는 그의 제약상 허용되는 염을 포함할 수 있다:
제약 조성물은 또한 경구, 비경구, 흡입, 국소 등과 같은 상이한 경로를 통한 전달을 위해 제제화될 수 있다.
일부 실시양태에서, 제약 조성물은 경구 투여를 위해 제제화된다. 경구 제제는, 각각 미리 정해진 양의 활성 화합물을 함유하는 별개의 단위, 예컨대 캡슐, 환제, 카세제, 로젠지, 또는 정제 중에; 분말 또는 과립으로서; 수성 또는 비수성 액체 중의 용액 또는 현탁액으로서; 또는 수중유 또는 유중수 에멀젼으로서 존재할 수 있다. 경구 투여를 위한 조성물의 제조를 위한 부형제는 관련 기술분야에 공지되어 있다. 비제한적인 적합한 부형제는, 예를 들어, 아가, 알긴산, 수산화알루미늄, 벤질 알콜, 벤질 벤조에이트, 1,3-부틸렌 글리콜, 카르보머, 피마자 오일, 셀룰로스, 셀룰로스 아세테이트, 코코아 버터, 옥수수 전분, 옥수수 오일, 목화씨 오일, 크로스-포비돈, 디글리세리드, 에탄올, 에틸 셀룰로스, 에틸 라우레에이트, 에틸 올레에이트, 지방산 에스테르, 젤라틴, 배아 오일, 글루코스, 글리세롤, 땅콩유, 히드록시프로필메틸 셀룰로스, 이소프로판올, 등장 식염수, 락토스, 수산화마그네슘, 스테아르산마그네슘, 맥아, 만니톨, 모노글리세리드, 올리브 오일, 낙화생 오일, 인산칼륨 염, 감자 전분, 포비돈, 프로필렌 글리콜, 링거액, 홍화 오일, 참깨 오일, 나트륨 카르복시메틸 셀룰로스, 인산나트륨 염, 나트륨 라우릴 술페이트, 나트륨 소르비톨, 대두 오일, 스테아르산, 스테아릴 푸마레이트, 수크로스, 계면활성제, 활석, 트라가칸트, 테트라히드로푸르푸릴 알콜, 트리글리세리드, 물, 및 이들의 혼합물을 포함한다.
일부 실시양태에서, 제약 조성물은 비경구 투여 (예컨대 정맥내 주사 또는 주입)를 위해 제제화된다. 비경구 제제는, 예를 들어, 수용액, 현탁액, 또는 에멀젼일 수 있다. 비경구 제제의 제조를 위한 부형제는 관련 기술분야에 공지되어 있다. 비제한적인 적합한 부형제는, 예를 들어, 1,3-부탄디올, 피마자 오일, 옥수수 오일, 목화씨 오일, 덱스트로스, 배아 오일, 땅콩유, 리포솜, 올레산, 올리브 오일, 낙화생 오일, 링거액, 홍화 오일, 참깨 오일, 대두 오일, U.S.P. 또는 등장 염화나트륨 용액, 물 및 이들의 혼합물을 포함한다.
일부 실시양태에서, 제약 조성물은 흡입을 위해 제제화된다. 흡입성 제제는, 예를 들어, 계량-용량 흡입기를 통해 투여가능한 제제화된 비강 스프레이, 건조 분말, 또는 에어로졸로서 제제화될 수 있다. 흡입을 위한 제제의 제조를 위한 부형제는 관련 기술분야에 공지되어 있다. 비제한적인 적합한 부형제는, 예를 들어, 락토스, 활석, 규산, 수산화알루미늄, 규산칼슘 및 폴리아미드 분말, 및 이들 물질의 혼합물을 포함한다. 스프레이는 추가로 추진제, 예컨대 클로로플루오로히드로카본 및 휘발성 비치환된 탄화수소, 예컨대 부탄 및 프로판을 함유할 수 있다.
일부 실시양태에서, 제약 조성물은 국소 투여를 위해 제제화된다. 국소 제제는, 예를 들어, 국소 용액, 로션, 샴푸, 경피 스프레이, 국소 필름, 포움, 분말, 페이스트, 스폰지, 경피 패치, 팅크제, 테이프, 크림, 겔, 또는 연고의 형태일 수 있다. 국소 제제의 제조를 위한 부형제는 관련 기술분야에 공지되어 있다. 비제한적인 적합한 부형제는, 예를 들어, 동물 및 식물 지방, 오일, 왁스, 파라핀, 전분, 트라가칸트, 셀룰로스 유도체, 폴리에틸렌 글리콜, 실리콘, 벤토나이트, 규산, 활석 및 산화아연, 및 이들의 혼합물을 포함한다.
예를 들어, 본원에 기재된 국소 제제는 털피지선 단위로의 담체로서 작용하는 하나 이상의 "친지성 용매(들)"를 가질 수 있다. 본 발명에서 유용한 친지성 용매는 물 및/또는 저급 사슬 (예를 들어, C1-6) 알콜과 혼화성일 수 있다. 일부 실시양태에서, 친지성 용매는 글리콜, 예를 들어, 프로필렌 글리콜일 수 있다. 일부 실시양태에서, 친지성 용매는, 예를 들어, 200 내지 20000 달톤 범위의 평균 분자량 (예를 들어, Mn 또는 Mw)을 갖는 폴리에틸렌 글리콜일 수 있다. 일부 실시양태에서, 친지성 용매는 글리콜 에테르, 예를 들어, 디에틸렌 글리콜 모노에틸 에테르 (트랜스큐톨)이다.
본원에 기재된 국소 제제는 또한 하나 이상의 "충전제(들)"를 가질 수 있다. 비제한적인 유용한 충전제는 물 및 저급 (예를 들어, C1-6) 알콜, 예컨대 에탄올, 2-프로판올 및 n-프로판올을 포함한다. 일부 실시양태에서, 충전제는 물, 에탄올 및/또는 2-프로판올이다.
본원에 기재된 국소 제제는 또한, 습윤 효과를 제공하기 위해 사용되는 하나 이상의 "함습제(들)"를 가질 수 있다. 비제한적인 유용한 함습제는 글리세린, 다가 알콜 및 실리콘 오일을 포함한다. 일부 실시양태에서, 국소 제제는 글리세린, 프로필렌 글리콜 및 시클로메티콘로부터 선택된 하나 이상의 함습제를 포함한다.
본원에 기재된 국소 제제는 또한, 최종 제제의 점도를 증가시키는 겔화제를 가질 수 있다. 일부 실시양태에서, 겔화제는 또한 유화제로서 작용할 수 있다. 비제한적인 유용한 겔화제는 셀룰로스, 아크릴레이트 중합체 및 아크릴레이트 공중합체, 예를 들어, 히드록시프로필 셀룰로스, 히드록시메틸 셀룰로스, 플루로닉(Pluronic) PF127 중합체, 카르보머 980, 카르보머 1342 및 카르보머 940의 부류를 포함한다. 일부 실시양태에서, 국소 제제는 히드록시프로필 셀룰로스 (클루셀(Klucel)® EF, GF 및/또는 HF), 플루로닉 PF127, 카르보머 980 및 카르보머 1342 (페물렌(Pemulen)® TR-1, TR-2 및/또는 카르보폴(Carbopol)® ETD 2020)로부터 선택된 하나 이상의 겔화제를 포함한다.
본원에 기재된 국소 제제는 또한 하나 이상의 산화방지제, 라디칼 스캐빈저, 및/또는 안정화제를 가질 수 있다. 비제한적인 유용한 예는 부틸화된 히드록시톨루엔, 부틸화된 히드록시아니솔, 아스코르빌 팔미테이트, 시트르산, 비타민 E, 비타민 E 아세테이트, 비타민 E-TPGS, 아스코르브산, 토코페르솔란 및 프로필 갈레이트를 포함한다.
본원에 기재된 국소 제제는 또한 항-박테리아 및/또는 항-진균 특성을 나타내는 하나 이상의 보존제를 가질 수 있다. 비제한적인 유용한 예는 디아졸리닐 우레아, 메틸파라벤, 프로필파라벤, 사나트륨 EDTA, 및 에틸파라벤을 포함한다.
본원에 기재된 국소 제제는 또한 하나 이상의 킬레이팅제를 가질 수 있다. 본원에서의 사용을 위한 비제한적 예는 EDTA, 이나트륨 에데테이트, 이칼륨 에데테이트, 시클로덱스트린, 삼나트륨 에데테이트, 사나트륨 에데테이트, 시트르산, 시트르산나트륨, 글루콘산 및 글루콘산칼륨을 포함한다.
활성 성분 및 부형제의 다양한 양이 본원에 기재된 국소 제제에 적합하다. 예를 들어, 일부 실시양태에서, 국소 제제는 본 개시내용의 스피로락톤을 제제의 총 중량의 약 0.001 내지 약 5 중량% (예를 들어, 약 0.01 내지 약 1 중량%, 약 0.01 중량% 내지 약 0.5 중량%)의 양으로 포함할 수 있다. 일부 실시양태에서, 국소 제제는 하기 성분을 (제제의 총 중량에 대한 중량 백분율로) 포함할 수 있다:
제약 조성물은 다양한 인자, 예컨대 화합물의 의도된 용도 및 효능에 따라, 다양한 양의 본 개시내용의 스피로락톤 화합물을 포함할 수 있다. 예를 들어, 일부 실시양태에서, 제약 조성물은, 본 개시내용의 스피로락톤 화합물을, 시험관내에서, 생체내에서, 또는 생체외에서, 세포에서의 ACC1 및/또는 ACC2 활성을 억제하기에 효과적인 양으로 포함할 수 있다. 일부 실시양태에서, 양은, 대조군에 비해, ACC1 및/또는 ACC2 활성의 약 10%, 약 20%, 약 50%, 약 70%, 약 90%, 약 99% 억제, 또는 언급된 값들 사이의 임의의 범위를 달성하기에 효과적인 양이다.
일부 실시양태에서, 제약 조성물은, 본 개시내용의 스피로락톤 화합물을, 그를 필요로 하는 대상체 (예를 들어, 인간)에게 투여시, 대상체에서의 하나 이상의 활성을 억제하기에 효과적인 양으로 포함할 수 있다. 일부 실시양태에서, 하나 이상의 활성은 아세틸-CoA 카르복실라제 ACC1 및/또는 ACC2 활성, 지질생성, 표피, 진피, 및/또는 피하조직에서의 세포 (예를 들어, 지방세포, 멜라닌세포, 각질세포, 편평 세포, 메르켈 세포, 랑게르한스 세포, 또는 피부 줄기 세포)의 증식, 인간 피지세포의 증식, 인간 각질세포의 증식, 피부 및/또는 피하 층에서의 섬유모세포의 지방세포로의 분화, 피지 생성, 염증, 및 이들의 조합으로부터 선택된다. 일부 실시양태에서, 제약 조성물은, 본 개시내용의 스피로락톤 화합물을, 이들 필요로 하는 대상체 (예를 들어, 인간)에게 투여시, (a) 대상체의 세포 (예를 들어, 피지세포, 지방세포)에서의 아세틸-CoA 카르복실라제 ACC1 및/또는 ACC2 활성을 억제하기에 효과적인; (b) 대상체에서 지질생성 (예를 들어, 피지세포의 지질생성, 지방세포의 지질생성 등)을 억제하기에 효과적인; (c) 대상체에서 표피, 진피, 및/또는 피하조직에서의 세포, 예컨대 지방세포, 멜라닌세포, 각질세포, 편평 세포, 메르켈 세포, 랑게르한스 세포, 또는 피부 줄기 세포의 증식을 억제하기에 효과적인; (d) 대상체에서 인간 피지세포의 증식을 억제하기에 효과적인; (e) 대상체에서 인간 각질세포의 증식을 억제하기에 효과적인; (f) 대상체에서 피부 및/또는 피하 층에서의 섬유모세포의 지방세포로의 분화를 억제하기에 효과적인; (g) 대상체에서 피지 생성을 억제하기에 효과적인; (h) 대상체에서 염증을 억제하기에 효과적인, 또는 임의의 이들의 조합의 양으로 포함할 수 있다. 일부 실시양태에서, 대상체는 여드름, 지루, 피지 증식증, 지루성 각화증, 피지 선종, 피지 낭종, 광선 각화증, 피지 암종, 편평 세포 암종, 흑색종, 비류성 장미증, 버트-호그-두베 증후군에서의 섬유모낭종, 및 이들의 조합으로부터 선택된 질환 또는 장애를 갖는 것을 특징으로 한다. 일부 실시양태에서, 대상체는 NASH를 갖는 것을 특징으로 한다.
일부 실시양태에서, 제약 조성물은 치료 유효량의 본 개시내용의 스피로락톤 화합물을 포함한다. 일부 실시양태에서, 제약 조성물은 치료 유효량의 본 개시내용의 스피로락톤 화합물 및 제약상 허용되는 부형제를 포함한다. 본원에서 사용되는 바와 같이, 치료 유효량의 본 개시내용의 스피로락톤 화합물은 본원에 기재된 바와 같은 질환 또는 장애를 치료하기에 효과적인 양이며, 이는 치료 수용자, 치료되는 질환 또는 장애 및 그의 중증도, 화합물을 함유하는 조성물, 투여 시간, 투여 경로, 치료의 지속기간, 화합물 효능, 그의 클리어런스 속도, 및 또 다른 약물이 공동-투여되는지의 여부에 따라 달라질 수 있다.
제약 조성물은 다양한 질환 또는 장애의 치료를 위해 사용될 수 있다. 이러한 치료에 적합한 비제한적 질환 또는 장애는 피부 질환 (예컨대 비정상적 피지세포 및/또는 각질세포 활성과 연관된 질환 또는 장애), 비-알콜성 지방간 질환 또는 장애, 대사 질환 또는 장애, 및 증식성 질환, 예컨대 암을 포함한다. 비정상적 피지세포 및/또는 각질세포 활성과 연관된 비제한적인 적합한 질환 또는 장애는, 예를 들어, 여드름, 지루, 피지 증식증, 지루성 각화증, 피지 선종, 피지 낭종, 광선 각화증, 피지 암종, 편평 세포 암종, 흑색종, 비류성 장미증, 버트-호그-두베 증후군에서의 섬유모낭종, 및 이들의 조합을 포함한다. 비제한적인 적합한 비-알콜성 지방간 질환 또는 장애는, 예를 들어, 비-알콜성 지방간염 (NASH)을 포함한다. 비제한적인 적합한 대사 질환 또는 장애는, 예를 들어, 비만 및/또는 당뇨병을 포함한다.
제약 조성물은 또한 본 개시내용의 스피로락톤 화합물에 추가로 하나 이상의 활성제를 포함할 수 있다. 본 개시내용의 스피로락톤 화합물 및 하나 이상의 활성제는 단일 투여 형태 (예를 들어, 단일 환제, 정제, 캡슐, 국소 연고, 겔, 페이스트, 크림 등)로 또는 별도의 투여 형태로 존재할 수 있다. 예를 들어, 본 개시내용의 스피로락톤 화합물은 경구 또는 국소 제제로 존재할 수 있으며, 하나 이상의 활성제는 동일한 제제 또는 상이한 경구 또는 국소 제제로 존재할 수 있다. 상이한 투여 형태의 경우, 본 개시내용의 스피로락톤 화합물 및 하나 이상의 활성제는 키트 내에 포함될 수 있다.
다양한 활성제가 제약 조성물 중에서 본 개시내용의 스피로락톤 화합물과 조합될 수 있다. 예를 들어, 일부 실시양태에서, 하나 이상의 활성제는 비정상적 피지세포 및/또는 각질세포 활성, 예컨대 여드름과 연관된 질환 또는 장애의 치료에 적합하다. 비제한적인 유용한 예는 항생제 (예를 들어, 클린다마이신, 에리트로마이신, 메트로니다졸, 술프아세트아미드, 또는 테트라시클린, 예컨대 독시시클린 및 미노시클린), 레티노이드 (예를 들어, 아다팔렌, 이소트레티노인, 레티놀, 타자로텐, 또는 트레티노인), 및 이들의 조합을 포함한다. 일부 실시양태에서, 하나 이상의 활성제는 비정상적 피지세포 및/또는 각질세포 활성과 연관된 질환 또는 장애, 예컨대 여드름의 치료에 효과적인 양으로 존재한다.
일부 실시양태에서, 하나 이상의 활성제는 대사 질환 또는 비-알콜성 지방간 질환의 치료에 적합하다. 이러한 작용제의 비제한적인 유용한 예는 안지오텐신 II 수용체 길항제, 안지오텐신 전환 효소 (ACE) 억제제, 카스파제 억제제, 카텝신 B 억제제, CCR2 케모카인 길항제, CCR5 케모카인 길항제, 클로라이드 채널 자극제, 콜레스테롤 가용화제, 디아실 글리세롤 O-아실트랜스퍼라제 1 (DGAT1) 억제제, 디펩티딜 펩티다제 IV (DPPIV) 억제제, 파르네소이드 X 수용체 (FXR) 효능제, 갈렉틴-3 억제제, 글루카곤-유사 펩티드 1 (GLPl) 효능제, 글루타티온 전구체, C형 간염 바이러스 NS3 프로테아제 억제제, HMG CoA 리덕타제 억제제, 11β-히드록시스테로이드 데히드로게나제 (11β-HSDl) 억제제, IL-Iβ 길항제, IL-6 길항제, IL-10 효능제, IL-17 길항제, 회장 나트륨 담즙산 공동수송체 억제제, 렙틴 유사체, 5-리폭시나제 억제제, LPL 유전자 자극제, 리실 옥시다제 동족체 2 (LOXL2) 억제제, PDE3 억제제, PDE4 억제제, 포스포리파제 C (PLC) 억제제, PPAR-알파 효능제, PPAR-감마 효능제, PPAR-델타 효능제, Rho 연관 단백질 키나제 2 (ROCK2) 억제제, 나트륨 글루코스 수송체-2 (SGLT2) 억제제, 스테아로일 CoA 데새투라제-1 억제제, 갑상선 호르몬 수용체 β 효능제, 종양 괴사 인자 알파 (TNF-알파) 리간드 억제제, 트랜스글루타미나제 억제제, 트랜스글루타미나제 억제제 전구체, 및 이들의 조합을 포함한다. 일부 구체적 실시양태에서, 하나 이상의 활성제는 아세틸살리실산, 알리포젠 티파보벡, 아람콜, 아토르바스타틴, BLX-1002, 세니크리비록, 코비프로스톤, 콜레세벨람, 엠리카산, 에날라프릴, GFT-505, GR-MD-02, 히드로클로로티아지드, 이코사펜트 에틸 에스테르 (에틸 에이코사펜타엔산), IMM-124E, KD-025, 리나글립틴, 리라글루티드, 메르캅타민, MGL-3196, 오베티콜산, 올레속심, 페그-일로데카킨, 피오글리타존, PX-102, 레모글리플로진 에타보네이트, SHP-626, 솔리트로마이신, 티펠루카스트, TRX-318, 우르소데옥시콜산, VBY-376, 및 이들의 조합으로부터 선택될 수 있다. 일부 실시양태에서, 하나 이상의 활성제는 비-알콜성 지방간 질환 (예를 들어, NASH)의 치료를 위한 치료 유효량으로 존재한다. 일부 실시양태에서, 하나 이상의 활성제는 대사 질환 (예를 들어, 비만 및/또는 당뇨병)의 치료를 위한 치료 유효량으로 존재한다.
치료 방법
본 개시내용의 스피로락톤 화합물은, 세포에서 ACC1 및/또는 ACC2 활성을 억제하기에, 또한 ACC1 및/또는 ACC2 활성과 연관된 질환 또는 장애 (예를 들어, 대사 질환, 비정상적 피지 생성과 연관된 질환, 또는 비-알콜성 지방간 질환)를 치료하기에 유용하다.
일부 실시양태에서, 본 개시내용은 세포에서 ACC1 및/또는 ACC2 활성을 억제하는 방법을 제공한다. 일부 실시양태에서, 방법은 세포를 유효량의 본 개시내용의 스피로락톤 화합물 또는 본원에 기재된 제약 조성물과 접촉시키는 것을 포함한다. 일부 실시양태에서, 세포는 시험관내에서 (예를 들어, 인간 세포주), 생체내에서 (예를 들어, 인간 대상체의 인간 세포), 또는 생체외에서 (인간 대상체로부터의 인간 세포) 존재할 수 있다. 생체내에서 ACC1 및/또는 ACC2 활성의 억제는 전신 투여되는 경우에 검출되거나 추정될 수 있고, 각각의 화합물의 혈액 농도 (또는 국소 투여된, 또한 국소화된 농도)는 대략 그의 각각의 IC50 값 (단백질 결합의 고려 후) 또는 그 초과이다.
일부 실시양태에서, ACC1 및/또는 ACC2 활성의 억제는 또한, 질환 또는 장애, 예컨대 비정상적 피지세포 및/또는 각질세포 활성과 연관된 질환 또는 장애 (예를 들어, 여드름, 및 본원에 기재된 바와 같은 다른 것들), 대사 질환 (예를 들어, 비만, 당뇨병, 및 본원에 기재된 바와 같은 다른 것들), 비-알콜성 지방간 질환 (예를 들어, NASH), 및 암에 관여되는, 세포에서의 말로닐-CoA 생성, 지질생성, 세포의 증식, 섬유모세포의 지방세포로의 분화, 피지 생성, 및/또는 염증의 억제를 제공할 수 있다.
따라서, 일부 실시양태에서, 본 개시내용은 세포에서 지질생성을 억제하는 방법을 제공한다. 일부 실시양태에서, 방법은 세포 (예를 들어, 인간 세포)를 유효량의 본 개시내용의 스피로락톤 화합물 또는 본원에 기재된 제약 조성물과 접촉시키는 것을 포함한다. 일부 실시양태에서, 세포는 피지세포, 지방세포, 또는 간세포이다.
일부 실시양태에서, 본 개시내용은 세포에서 증식을 억제하는 방법을 제공한다. 일부 실시양태에서, 방법은 세포 (예를 들어, 인간 세포)를 유효량의 본 개시내용의 스피로락톤 화합물 또는 본원에 기재된 제약 조성물과 접촉시키는 것을 포함한다. 일부 실시양태에서, 세포는 지방세포, 멜라닌세포, 각질세포, 편평 세포, 메르켈 세포, 랑게르한스 세포, 및/또는 피부 줄기 세포이다. 일부 실시양태에서, 세포는 표피, 진피, 및/또는 피하조직에서의 지방세포, 멜라닌세포, 각질세포, 편평 세포, 메르켈 세포, 랑게르한스 세포, 및/또는 피부 줄기 세포이다. 일부 실시양태에서, 세포는 인간 피지세포이다. 일부 실시양태에서, 세포는 인간 각질세포이다.
일부 실시양태에서, 본 개시내용은 섬유모세포 (예를 들어, 인간 섬유모세포)의 지방세포로의 분화를 억제하는 방법을 제공한다. 일부 실시양태에서, 방법은 섬유모세포를 유효량의 본 개시내용의 스피로락톤 화합물 또는 본원에 기재된 제약 조성물과 접촉시키는 것을 포함한다. 일부 실시양태에서, 방법은 피부 및/또는 피하 층에서의 섬유모세포의 지방세포로의 분화를 억제한다.
일부 실시양태에서, 본 개시내용은 피지 생성을 억제하는 방법을 제공한다. 일부 실시양태에서, 방법은 피지세포 (예를 들어, 인간 피지세포)를 유효량의 본 개시내용의 스피로락톤 화합물 또는 본원에 기재된 제약 조성물과 접촉시키는 것을 포함한다.
일부 실시양태에서, 본 개시내용은 또한, ACC1 및/또는 ACC2 활성 및 하기의 하나 이상의 (예를 들어, 1, 2, 3, 4, 5, 6종의, 또는 모든) 활성의 억제를 필요로 하는 대상체 (예를 들어, 인간 대상체)에서 상기 활성을 억제하는 방법을 제공하며, 여기서 하나 이상의 활성은 (a) 대상체에서의 지질생성 (예를 들어, 피지세포의 지질생성, 지방세포의 지질생성, 간세포의 지질생성 등); (b) 대상체에서의 세포, 예컨대 표피, 진피, 및/또는 피하조직에서의 지방세포, 멜라닌세포, 각질세포, 편평 세포, 메르켈 세포, 랑게르한스 세포, 또는 피부 줄기 세포의 증식; (c) 대상체에서의 인간 피지세포의 증식; (d) 대상체에서의 인간 각질세포; (e) 대상체에서의 피부 및/또는 피하 층에서의 섬유모세포의 지방세포로의 분화; (f) 대상체에서의 피지 생성; (g) 대상체에서의 염증, 및 이들의 조합으로부터 선택되는 것이며, 상기 방법은 상기 대상체에게 유효량의 본 개시내용의 스피로락톤 화합물 또는 본원에 기재된 제약 조성물을 투여하는 것을 포함한다. 일부 실시양태에서, 대상체는 여드름, 지루, 피지 증식증, 지루성 각화증, 피지 선종, 피지 낭종, 광선 각화증, 피지 암종, 편평 세포 암종, 흑색종, 비류성 장미증, 버트-호그-두베 증후군에서의 섬유모낭종, 및 이들의 조합으로부터 선택된 질환 또는 장애를 갖는 것을 특징으로 한다.
일부 실시양태에서, 본 개시내용은 또한, ACC1 및/또는 ACC2와 연관된 질환 또는 장애의 치료를 필요로 하는 대상체에서 상기 질환 또는 장애를 치료하는 방법을 제공한다. 일부 실시양태에서, 방법은 대상체에게 치료 유효량의 본 개시내용의 스피로락톤 화합물 또는 본원에 기재된 제약 조성물을 투여하는 것을 포함한다. 다양한 질환 또는 장애가 원치않는 또는 비정상적 (예를 들어, 과다활성) ACC1 및/또는 ACC2 활성과 연관되며 본원에 기재된 방법에 의해 치료될 수 있다.
피부 질환의 치료 방법
피부는 외부 환경과 숙주 사이의 계면을 제공하는 인간 신체의 가장 큰 기관이다. 지질은 피부의 투과성 및 항미생물 장벽 둘 다의 형성 및 유지에 있어 필수적인 역할을 한다. 피부의 정상적 기능은, 체내의 물 및 전해질의 손실을 막는, 주로 세라미드, 콜레스테롤, 및 유리 지방산으로 구성된 각질층 내의 소수성 세포외 지질 매트릭스에 의해 유지된다. 피지선은 피지를 생성하고 소낭관으로 분비하는 기관이며, 이는 장벽으로서 피부의 정상적 기능을 유지하도록 피부의 표면에 도달한다.
심상성 여드름 (여드름)은 많은 사람들에게 발병하는 통상적 피부과 병태이다. 여드름은, 구진, 농포, 또는 결절 (또한 낭포로서 공지됨)을 포함한, 개방 또는 폐쇄 면포 (블랙헤드 및 화이트헤드)에 있어 두드러진 만성 염증성 피부병이다. Zaenglein, A. et al., J. Am. Acad. Dermatol, 74:945-73 (2016). 여드름의 발생에 있어 중요한 역할을 하는 주요 병원성 인자는 소낭 각화항진, 프로피오니박테리움 아크네스(Propionibacterium acnes)로의 미생물 군집화, 피지 생성, 및 선천적 및 후천적 면역 둘 다를 포함하는 복합적 염증성 메커니즘이다. 여드름은 상이한 중증도, 예컨대 경증, 중등도, 및 경증을 가질 수 있다. 병태의 중증도는, 계절적 및 심리적 영향을 포함한 다양한 인자에 의해 영향받는다.
여드름, 예컨대 중등도 내지 중증 여드름의 치료를 위한 폭넓게 다양한 요법이 이용가능하다. 예를 들어, 문헌 [Zaenglein, A. et al., J. Am. Acad. Dermatol, 74:945-73 (2016)] 참조. 이들 요법은, 예를 들어, (1) 항생제 (경구 또는 국소), 예컨대 테트라시클린, 독시시클린, 미노시클린, 트리메토프림/술파메톡사졸 (TMP/SMX), 트리메토프림, 에리트로마이신, 클린다마이신, 아젤라산, 댑손, 아지트로마이신, 아목시실린, 및 세팔렉신; (2) 호르몬제, 예컨대 조합된 경구 피임약과 에스트로겐 및 프로게스틴, 예를 들어, 에티닐 에스트라디올/노게스티메이트, 에티닐 에스트라디올/노레틴드론 아세테이트/제1철 푸마레이트, 에티닐 에스트라디올/드로스피레논, 및 에티닐 에스트라디올/드로스피레논/레보메폴레이트; (3) 경구 레티노이드, 예컨대 경구 이소트레티노인, (아큐탄(Accutane)®, 13-시스-레티노산); (4) 국소 치료제, 예컨대 벤조일 퍼옥시드 (BP), 살리실산, 항생제, 조합된 항생제와 BP, 레티노이드 (예를 들어, 트레티노인, 아다팔렌, 타자로텐), 레티노이드와 BP, 레티노이드와 항생제, 아젤라산, 및 술폰 작용제 (예를 들어, 댑손) 등; 및 (5) 기타의 것, 예컨대 스피로놀락톤, 플루타미드, 병변내 코르티코스테로이드 (트리암시놀론 아세토니드), 글리콜산 필(peel), 살리실산 필, 및 레조르시놀 및 살리실산을 포함한다. 그러나, 여드름을 위해 현재 이용가능한 요법은 현저히 부족하다. 피부과 요법은 여드름, 예컨대 경증 내지 중등도 여드름에 대하여 완전히 효과적이지 않고, 이들 요법에 사용되는 많은 작용제가 피부 자극을 생성하거나 다른 부작용을 갖는다. 예를 들어, 문헌 [Zaenglein, A. et al., J. Am. Acad. Dermatol, 74:945-73 (2016)] 참조. 예를 들어, 아큐탄은 잠재적인 염증성 장 질환 부작용에 대한 소송 중에 2009년 미국 시장에서 제외되었다.
여드름 치료 수단으로서 피지 생성 감소가 또한 기재되었으며, 그 결과는 여드름이 피지 생성을 억제하는 비-레티노이드에 의해 현저히 개선될 수 있음을 나타내었다. 예를 들어, 문헌 [Zouboulis, C. C. et al., "Zileuton, an oral 5-lipoxygenase inhibitor, directly reduces sebum production", Dermatology (2005), Vol. 210, pp. 36-38]; 및 [Zouboulis, C. C. et al., "A new concept for acne therapy: a pilot study with zileuton, an oral 5-lipoxygenase inhibitor", Arch. Dermatol. (2003), Vol. 139, pp. 668-670]을 인용하는, 미국 특허 번호 8,884,034 (Daynard, T. et al. (2014)) 참조.
피지선은 성숙 피지세포로 충전되어 있고, 이는 주로 시토졸 내의 지질 액적에 의해 점유되고 완전 분비가 일어난다. 피지선의 정상적 기능을 유지하기 위해, 성숙 피지세포는 표피 줄기 세포로부터 지속적으로 재생된다. 피지의 증식, 분화, 및 생성을 포함한 피지세포의 과다활성은 여드름, 지루, 피지 증식증, 지루성 각화증, 피지 선종, 피지 낭종, 광선 각화증, 피지 암종, 편평 세포 암종, 흑색종, 비류성 장미증, 및 버트-호그-두베 증후군에서의 섬유모낭종 등을 포함한 상이한 피부 질환을 야기할 수 있다.
지질 대사는 피부에서 활성이지만, 피부, 특히 피지선에서의 ACC의 발현 수준 및 효소 활성은 완전히 설명되지 않았다. ACC1 및/또는 ACC2의 억제가 상기에 언급된 피부 질환의 발생 및 진행을 방해하는지의 여부는 공지되지 않았다. US 2016/0220557에는 여드름 치료를 위한 ACC 억제제가 개시되어 있다. 최근, PF-06423264로의 제1기 여드름 시험이 의미있는 약력학 반응을 제시하지 않는 것으로 종결되었다. 또한, 올루마코스타트 글라사레틸은, 긍정적인 제II기 데이터를 제시하였지만, 제III기 연구에서는 그의 1차 종점을 충족하지 않았다. 올루마코스타트 글라사레틸은 알려진 ACC 억제제, (5-(테트라데실옥시)-2-푸란카르복실산의 전구약물로서 작용한다고 제안되었지만, 올루마코스타트 글라사레틸의 관찰된 효과는 ACC 억제에 기인하지 않을 수 있다.
그럼에도 불구하고, 본 발명자들은, ACC 단백질이 인간 피부에서의 피지선에서 풍부하게 특이적으로 발현됨을 발견하였다. 이 결과는 우선, 인간 피부 구조에서의 ACC 단백질의 국소화를 제시하고, 예를 들어, ACC 억제제의 국소 투여를 통한, 피지선으로의 ACC 억제제의 투여가 피지선에서 ACC를 억제함으로써 피지세포의 과다생성과 관련된 질환의 진행 및 지질 축적을 억제할 수 있음을 시사하는 증거를 제공한다. 따라서, 일부 실시양태에서, 본 개시내용의 스피로락톤 화합물은 또한, 예를 들어, 국소 투여를 통해, 비정상적 피지세포 및/또는 각질세포 활성과 연관된 질환 또는 장애의 치료에 사용될 수 있다. 실시예 섹션에 제시된 바와 같이, 본 개시내용의 예시적 대표적 스피로락톤 화합물은 ACC1 및/또는 ACC2의 억제제이다. 또한, 본 개시내용의 예시적 대표적 스피로락톤 화합물은 피지세포 활성, 예컨대 피지세포의 지질생성을 억제하는 것으로 제시하였다.
따라서, 일부 실시양태에서, 본 개시내용은 비정상적 피지세포 및/또는 각질세포 활성과 연관된 질환 또는 장애의 치료를 필요로 하는 대상체에서 상기 질환 또는 장애를 치료하는 방법을 제공한다. 일부 실시양태에서, 방법은 치료 유효량의 본 개시내용의 스피로락톤 화합물 또는 본원에 기재된 제약 조성물을 그를 필요로 하는 대상체에게 투여하는 것을 포함한다. 비정상적 피지세포 및/또는 각질세포 활성과 연관된 비제한적인 적합한 질환 또는 장애는, 예를 들어, 여드름, 지루, 피지 증식증, 지루성 각화증, 피지 선종, 피지 낭종, 광선 각화증, 피지 암종, 편평 세포 암종, 흑색종, 비류성 장미증, 버트-호그-두베 증후군에서의 섬유모낭종, 및 이들의 조합을 포함한다. 다양한 투여 경로가 적합하고, 예를 들어, 경구 또는 국소 경로이다. 방법은 본 개시내용의 스피로락톤 화합물을 활성제로서 사용하거나 그를 또 다른 요법과 조합하여 사용할 수 있다. 일부 실시양태에서, 본 개시내용의 스피로락톤 화합물은 비정상적 피지세포 및/또는 각질세포 활성과 연관된 질환 또는 장애의 치료를 위해 대상체에게 투여되는 유일한 활성제이다. 일부 실시양태에서, 방법은 조합 요법이고, 대상체를 비정상적 피지세포 및/또는 각질세포 활성과 연관된 질환 또는 장애의 치료에 효과적인 하나 이상의 추가의 요법으로 치료하는 것을 추가로 포함한다. 조합 요법에서 사용시, 본 개시내용의 스피로락톤 화합물은 대상체에게 하나 이상의 추가의 요법과 동시에, 그 이전에, 또는 그 이후에 투여될 수 있다. 본 개시내용의 스피로락톤 화합물 및 하나 이상의 추가의 요법은 동일한 또는 상이한 경로를 통해 대상체에게 투여될 수 있다. 예를 들어, 일부 실시양태에서, 본 개시내용의 스피로락톤 화합물은 국소 투여될 수 있으며, 하나 이상의 추가의 요법 (예를 들어, 추가의 활성제)는 경구 투여될 수 있다.
일부 구체적 실시양태에서, 본 개시내용은 여드름의 치료를 필요로 하는 대상체에서 여드름을 치료하는 방법을 제공한다. 일부 실시양태에서, 방법은 치료 유효량의 본 개시내용의 스피로락톤 화합물 또는 본원에 기재된 제약 조성물을 그를 필요로 하는 대상체에게 투여 (예를 들어, 국소)하는 것을 포함한다. 일부 실시양태에서, 방법은 조합 요법이고, 대상체를 여드름을 위한 추가의 요법으로 치료하는 것을 추가로 포함한다. 여드름 치료를 위한 공지된 요법 중 임의의 것이 조합 요법의 일부가 될 수 있고, 이들 중 일부는 본원에서 예시된다. 예를 들어, 일부 실시양태에서, 방법은, 대상체에게, 항생제 (국소 또는 전신), 레티노이드 (국소 또는 전신), 또는 이들의 조합을 투여하는 것을 추가로 포함한다. 일부 실시양태에서, 항생제는 클린다마이신, 에리트로마이신, 메트로니다졸, 술프아세트아미드, 테트라시클린, 예컨대 독시시클린 및 미노시클린, 또는 이들의 조합이다. 일부 실시양태에서, 레티노이드는 아다팔렌, 이소트레티노인, 레티놀, 타자로텐, 트레티노인, 또는 이들의 조합이다. 다른 적합한 항생제 및 레티노이드는 관련 기술분야에 공지되어 있고, 본원에서 예시된다.
다른 질환의 치료 방법
ACC1 및/또는 ACC2 활성의 억제는 또한, 다양한 대사 질환, 비-알콜성 지방간 질환, 및/또는 암과 연관되고/거나 그의 치료에 유용한 것으로 나타났다. 예를 들어, 미국 특허 번호 8,288,405 및 문헌 [Griffith et al., Journal of medicinal chemistry 57:10512-10526(2014)] (비만, 당뇨병); [Harriman et al., Proceedings of the National Academy of Sciences of the United States of America 113:E1796-1805(2016)] (비-알콜성 지방간염 (NASH)), 및 [Svensson et al., Nature medicine 22, 1108-1119(2016)] (암) 참조.
따라서, 본 개시내용의 특정 실시양태는, 대사 질환, 비-알콜성 지방간 질환, 및/또는 암의 치료를 위한, 본 개시내용의 스피로락톤 화합물 또는 본원에 기재된 제약 조성물의 용도에 관한 것이다. 다양한 투여 경로가 적합하고, 예를 들어, 경구 또는 국소 경로이다. 방법은 본 개시내용의 스피로락톤 화합물을 활성제로서 사용하거나 그를 또 다른 요법과 조합하여 사용할 수 있다. 일부 실시양태에서, 본 개시내용의 스피로락톤 화합물은 대사 질환, 비-알콜성 지방간 질환, 및/또는 암의 치료를 위해 대상체에게 투여되는 유일한 활성제이다. 일부 실시양태에서, 방법은 조합 요법이고, 대상체를 대사 질환, 비-알콜성 지방간 질환, 및/또는 암의 치료에 효과적인 하나 이상의 추가의 요법으로 치료하는 것을 추가로 포함한다. 조합 요법에서 사용시, 본 개시내용의 스피로락톤 화합물은 대상체에게 하나 이상의 추가의 요법과 동시에, 그 이전에, 또는 그 이후에 투여될 수 있다. 본 개시내용의 스피로락톤 화합물 및 하나 이상의 추가의 요법은 동일한 또는 상이한 경로를 통해 대상체에게 투여될 수 있다. 예를 들어, 일부 실시양태에서, 본 개시내용의 스피로락톤 화합물은 국소 투여될 수 있으며, 하나 이상의 추가의 요법 (예를 들어, 활성제)는 경구 투여될 수 있다.
일부 구체적 실시양태에서, 본 개시내용은 비만 및/또는 비만-관련 장애 (예를 들어, 과체중, 체중 증가, 또는 체중 유지)의 치료를 필요로 하는 대상체 (예를 들어, 인간 대상체)에서 상기 장애를 치료하는 방법을 제공한다. 비만 및 과체중은 일반적으로 체질량 지수 (BMI)에 의해 정의되며, 이는 총 체지방과 상관되며 질환의 상대적 위험성을 추정하는 것이다. BMI는 킬로그램 단위의 체중을 미터 단위의 신장의 제곱으로 나누어 계산한다 (kg/m2). 과체중은 전형적으로 25-29.9 kg/m2의 BMI로서 정의되고, 비만은 전형적으로 30 kg/m2의 BMI로서 정의된다. 예를 들어, 하기 참조: National Heart, Lung, and Blood Institute, Clinical Guidelines on the Identification, Evaluation, and Treatment of Overweight and Obesity in Adults, The Evidence Report, Washington, D.C.: U.S. Department of Health and Human Services, NIH 공개 번호 98-4083 (1998). 일부 실시양태에서, 방법은 치료 유효량의 본 개시내용의 스피로락톤 화합물 또는 본원에 기재된 제약 조성물을 그를 필요로 하는 대상체에게 투여 (예를 들어, 경구)하는 것을 포함한다.
일부 실시양태에서, 본 개시내용은 또한, 당뇨병 및/또는 당뇨병-관련 장애, 예컨대 타입 1 (인슐린-의존적 진성 당뇨병, 또한 "IDDM"으로서 언급됨) 및 타입 2 (비-인슐린-의존적 진성 당뇨병, 또한 "NIDDM"으로서 언급됨) 당뇨병 등의 치료를 필요로 하는 대상체 (예를 들어, 인간 대상체)에서 상기 장애를 치료하는 방법을 제공한다. 일부 실시양태에서, 방법은 치료 유효량의 본 개시내용의 스피로락톤 화합물 또는 본원에 기재된 제약 조성물을 그를 필요로 하는 대상체에게 투여 (예를 들어, 경구)하는 것을 포함한다.
일부 실시양태에서, 본 개시내용은 또한, 비-알콜성 지방간 질환, 예를 들어 NASH의 치료를 필요로 하는 대상체 (예를 들어, 인간 대상체)에서 상기 질환을 치료하는 방법을 제공한다. 일부 실시양태에서, 방법은 치료 유효량의 본 개시내용의 스피로락톤 화합물 (예를 들어, 화학식 Ic의 화합물, 또는 실시예 14-22) 또는 본원에 기재된 제약 조성물을 그를 필요로 하는 대상체에게 투여 (예를 들어, 경구)하는 것을 포함한다.
일부 실시양태에서, 비만, 비만-관련 장애, 당뇨병, 당뇨병-관련 장애, 및/또는 비-알콜성 지방간 질환을 치료하는 방법은 조합 요법일 수 있다. 예를 들어, 방법은 대상체에게 하나 이상의 추가의 활성제를 각각의 질환 또는 장애의 치료를 위한 치료 유효량으로 투여하는 것을 포함할 수 있다. 조합 요법을 위한 비제한적인 유용한 작용제는 안지오텐신 II 수용체 길항제, 안지오텐신 전환 효소 (ACE) 억제제, 카스파제 억제제, 카텝신 B 억제제, CCR2 케모카인 길항제, CCR5 케모카인 길항제, 클로라이드 채널 자극제, 콜레스테롤 가용화제, 디아실 글리세롤 O-아실트랜스퍼라제 1 (DGAT1) 억제제, 디펩티딜 펩티다제 IV (DPPIV) 억제제, 파르네소이드 X 수용체 (FXR) 효능제, 갈렉틴-3 억제제, 글루카곤-유사 펩티드 1 (GLPl) 효능제, 글루타티온 전구체, C형 간염 바이러스 NS3 프로테아제 억제제, HMG CoA 리덕타제 억제제, 11β-히드록시스테로이드 데히드로게나제 (11β-HSDl) 억제제, IL-Iβ 길항제, IL-6 길항제, IL-10 효능제, IL-17 길항제, 회장 나트륨 담즙산 공동수송체 억제제, 렙틴 유사체, 5-리폭시나제 억제제, LPL 유전자 자극제, 리실 옥시다제 동족체 2 (LOXL2) 억제제, PDE3 억제제, PDE4 억제제, 포스포리파제 C (PLC) 억제제, PPAR-알파 효능제, PPAR-감마 효능제, PPAR-델타 효능제, Rho 연관 단백질 키나제 2 (ROCK2) 억제제, 나트륨 글루코스 수송체-2 (SGLT2) 억제제, 스테아로일 CoA 데새투라제-1 억제제, 갑상선 호르몬 수용체 β 효능제, 종양 괴사 인자 알파 (TNF-알파) 리간드 억제제, 트랜스글루타미나제 억제제, 트랜스글루타미나제 억제제 전구체, 및 이들의 조합을 포함한다. 예를 들어, 일부 실시양태에서, 하나 이상의 추가의 작용제는 아세틸살리실산, 알리포젠 티파보벡, 아람콜, 아토르바스타틴, BLX-1002, 세니크리비록, 코비프로스톤, 콜레세벨람, 엠리카산, 에날라프릴, GFT-505, GR-MD-02, 히드로클로로티아지드, 이코사펜트 에틸 에스테르 (에틸 에이코사펜타엔산), IMM-124E, KD-025, 리나글립틴, 리라글루티드, 메르캅타민, MGL-3196, 오베티콜산, 올레속심, 페그-일로데카킨, 피오글리타존, PX-102, 레모글리플로진 에타보네이트, SHP-626, 솔리트로마이신, 티펠루카스트, TRX-318, 우르소데옥시콜산, VBY-376, 및 이들의 조합으로부터 선택될 수 있다.
일부 실시양태에서, 본 개시내용은 또한 암을 치료하는 방법을 제공한다.
예시적 실시양태
본 개시내용은 또한 하기 예시적 실시양태 E1-E52를 제공한다.
1. 화학식 I의 화합물, 또는 그의 제약상 허용되는 염:
여기서
R1 및 R2는 각각 독립적으로 수소, 할로겐, 시아노, 임의로 치환된 C1-6 알킬, 임의로 치환된 C3-6 시클로알킬, 임의로 치환된 C2-6 알케닐, 임의로 치환된 C2-6 알키닐, 임의로 치환된 C6-10 아릴, 임의로 치환된 5-10원 헤테로아릴, 임의로 치환된 4-6원 헤테로시클릴, NR10R11, COOR12, CONR13R14, CN, S(O)nR15, 또는 OR16이고;
여기서
R10 및 R11은 각각 독립적으로 수소, 임의로 치환된 C1-6 알킬, 임의로 치환된 C3-6 시클로알킬, 임의로 치환된 C1-6 알카노일, 임의로 치환된 C3-6 시클로알카노일, 임의로 치환된 C6-10 아릴, 임의로 치환된 5-10원 헤테로아릴, 임의로 치환된 4-6원 헤테로시클릴, COOR12, 또는 CONR13R14이고;
R12, R13 및 R14는 각각 독립적으로 수소 또는 임의로 치환된 C1-6 알킬이고;
n은 0, 1, 또는 2이고;
R15는 임의로 치환된 C1-6 알킬, 임의로 치환된 C3-6 시클로알킬, 또는 NR10R11이고;
R16은 수소, 임의로 치환된 C1-6 알킬, 임의로 치환된 C3-6 시클로알킬, 임의로 치환된 C1-6 알카노일, 임의로 치환된 C3-6 시클로알카노일, 임의로 치환된 C6-10 아릴, 임의로 치환된 5-10원 헤테로아릴, 임의로 치환된 4-6원 헤테로시클릴 또는 CONR13R14이고;
R3은 임의로 치환된 C6-10아릴 또는 임의로 치환된 5-10원 헤테로아릴이며,
단, R1 및 R2가 둘 다 수소인 경우, R3은 임의로 치환된 페닐이 아니다.
2. R1이 할로겐, 임의로 치환된 C1-6 알킬, 임의로 치환된 C1-6 알콕시, 임의로 치환된 C3-6 시클로알킬, 또는 임의로 치환된 C3-6 시클로알콕시인, E1의 화합물, 또는 그의 제약상 허용되는 염.
3. R1이 할로겐 및 C1-4 알킬로부터 독립적으로 선택된 1 내지 3개의 치환기로 각각 임의로 치환된 C1-4 알킬, C1-4 알콕시, C3-6 시클로알킬, 또는 C3-6 시클로알콕시인, E1 또는 2의 화합물, 또는 그의 제약상 허용되는 염.
4. R1이 1-3개의 플루오린으로 각각 임의로 치환된 C1-4 알킬 또는 C1-4 알콕시인, E1-3 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염.
5. R1이 할로겐, 시아노, 임의로 치환된 C1-4 알킬, 임의로 치환된 C1-4 알콕시, 임의로 치환된 C3-6 시클로알킬, 및 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1 또는 2개의 치환기로 임의로 치환된 5-10원 헤테로아릴인, E1의 화합물, 또는 그의 제약상 허용되는 염.
6. R1이 할로겐, 옥소, 임의로 치환된 C1-4 알킬, 임의로 치환된 C1-4 알콕시, 임의로 치환된 C3-6 시클로알킬, 및 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1 또는 2개의 치환기로 임의로 치환된 4-6원 헤테로시클릴인, E1의 화합물, 또는 그의 제약상 허용되는 염.
7. R1이 NR10R11인, E1의 화합물, 또는 그의 제약상 허용되는 염.
8. R10 및 R11 중 하나가 임의로 치환된 페닐 또는 임의로 치환된 5 또는 6원 헤테로아릴인, E7의 화합물, 또는 그의 제약상 허용되는 염.
9. R10 및 R11 중 하나가, 할로겐, 시아노 및 C1-4 알킬로부터 독립적으로 선택된 1 또는 2개의 치환기로 임의로 치환된 5원 헤테로아릴인, E7의 화합물, 또는 그의 제약상 허용되는 염.
10. R10 및 R11 중 하나가, 할로겐, 시아노 및 C1-4 알킬로부터 독립적으로 선택된 1 또는 2개의 치환기로 임의로 치환된, 2-4개의 고리 질소 원자를 갖는 5원 헤테로아릴인, E7의 화합물, 또는 그의 제약상 허용되는 염.
11. R10 및 R11 중 하나가 1 또는 2개의 독립적으로 선택된 C1-4 알킬로 각각 임의로 치환된 피라졸릴, 트리아졸릴 또는 테트라졸릴인, E7의 화합물, 또는 그의 제약상 허용되는 염.
12. R2가 H인, E1-11 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염.
13. R3이 할로겐, 임의로 치환된 C1-4 알킬, 임의로 치환된 C1-4 알콕시, 임의로 치환된 C3-6 시클로알킬, 및 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된 C6-10아릴인, E1-12 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염.
14. R3이 임의로 치환된 8-10원 비시클릭 헤테로아릴인, E1-12 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염.
15. R3이 할로겐, 시아노, 1-3개의 할로겐으로 임의로 치환된 C1-4 알킬, 1-3개의 할로겐으로 임의로 치환된 C1-4 알콕시, 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알킬, 및 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1 내지 3개의 치환기로 각각 임의로 치환된 나프틸 또는 퀴놀리닐인, E1-12 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염.
16. R3이 플루오로, 클로로, 히드록실, 메틸, 에틸, 트리플루오로메틸, 트리플루오로메톡시, 메톡시, 에톡시, 및 시클로프로필로부터 독립적으로 선택된 1 내지 3개의 치환기로 각각 임의로 치환된 나프틸 또는 퀴놀리닐인, E1-12 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염.
17. 화학식 Ia의 화합물, 또는 그의 제약상 허용되는 염:
여기서
R1은 수소, 할로겐, 시아노, 임의로 치환된 C1-6 알킬, 임의로 치환된 C3-6 시클로알킬, 임의로 치환된 C2-6 알케닐, 임의로 치환된 C2-6 알키닐, 임의로 치환된 C6-10 아릴, 임의로 치환된 5-10원 헤테로아릴, 임의로 치환된 4-6원 헤테로시클릴, NR10R11, COOR12, CONR13R14, CN, S(O)nR15, 또는 OR16이고;
여기서
R10 및 R11은 각각 독립적으로 수소, 임의로 치환된 C1-6 알킬, 임의로 치환된 C3-6 시클로알킬, 임의로 치환된 C1-6 알카노일, 임의로 치환된 C3-6 시클로알카노일, 임의로 치환된 C6-10 아릴, 임의로 치환된 5-10원 헤테로아릴, 임의로 치환된 4-6원 헤테로시클릴, COOR12, 또는 CONR13R14이고;
R12, R13 및 R14는 각각 독립적으로 수소 또는 임의로 치환된 C1-6 알킬이고;
n은 0, 1, 또는 2이고;
R15는 임의로 치환된 C1-6 알킬, 임의로 치환된 C3-6 시클로알킬, 또는 NR10R11이고;
R16은 수소, 임의로 치환된 C1-6 알킬, 임의로 치환된 C3-6 시클로알킬, 임의로 치환된 C1-6 알카노일, 임의로 치환된 C3-6 시클로알카노일, 임의로 치환된 C6-10 아릴, 임의로 치환된 5-10원 헤테로아릴, 임의로 치환된 4-6원 헤테로시클릴 또는 CONR13R14이고;
R3은 임의로 치환된 C6-10아릴 또는 임의로 치환된 5 내지 10원 헤테로아릴이며,
단, R1이 수소인 경우, R3은 임의로 치환된 페닐이 아니다.
18. R1이 임의로 치환된 C1-4 알킬인, E17의 화합물, 또는 그의 제약상 허용되는 염.
19. R1이 메틸, 에틸, 이소프로필, 또는 tert-부틸인, E17 또는 18의 화합물, 또는 그의 제약상 허용되는 염.
20. R1이 임의로 치환된 C1-4 알콕시인, E17의 화합물, 또는 그의 제약상 허용되는 염.
21. R1이 메톡시, 트리플루오로메톡시, 에톡시 또는 이소프로폭시인, E20의 화합물, 또는 그의 제약상 허용되는 염.
22. 화학식 Ib를 갖는 E17의 화합물, 또는 그의 제약상 허용되는 염:
여기서 R10 및 R11 중 하나는 임의로 치환된 페닐 또는 임의로 치환된 5 또는 6원 헤테로아릴이다.
23. R10 및 R11 중 하나가 임의로 치환된 5 또는 6원 헤테로아릴인, E22의 화합물, 또는 그의 제약상 허용되는 염.
24. R10 및 R11 중 하나가, 할로겐, 시아노 및 C1-4 알킬로부터 선택된 1 또는 2개의 치환기로 임의로 치환된, 2-4개의 고리 질소 원자를 갖는 5원 헤테로아릴인, E22의 화합물, 또는 그의 제약상 허용되는 염.
25. R10 및 R11 중 하나가 C1-4 알킬로 각각 임의로 치환된 피라졸릴, 트리아졸릴 또는 테트라졸릴인, E22의 화합물, 또는 그의 제약상 허용되는 염.
27. R3이 할로겐, 시아노, 임의로 치환된 C1-4 알킬, 임의로 치환된 C1-4 알콕시, 임의로 치환된 C3-6 시클로알킬, 및 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된 C6-10아릴인, E17-26 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염.
28. R3이 임의로 치환된 8-10원 비시클릭 헤테로아릴인, E17-26 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염.
29. R3이 할로겐, 시아노, 1-3개의 할로겐으로 임의로 치환된 C1-4 알킬, 1-3개의 할로겐으로 임의로 치환된 C1-4 알콕시, 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알킬, 및 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된 나프틸 또는 퀴놀리닐인, E17-26 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염.
30. R3이 플루오로, 클로로, 히드록실, 메틸, 트리플루오로메틸, 에틸, 메톡시, 트리플루오로메톡시, 에톡시, 및 시클로프로필로부터 독립적으로 선택된 1 내지 3개의 치환기로 각각 임의로 치환된 인, E17-26 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염.
32. 하기 화합물로부터 선택된 E17-26 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염.
33. E1-32 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염, 및 제약상 허용되는 부형제를 포함하는 제약 조성물.
34. 정맥내 주사 또는 주입, 경구 투여, 흡입, 또는 국소 투여를 위해 제제화된 E33의 제약 조성물.
35. 국소 용액, 로션, 샴푸, 경피 스프레이, 국소 필름, 포움, 분말, 페이스트, 스폰지, 경피 패치, 팅크제, 테이프, 크림, 겔, 또는 연고 형태로 제제화된 E33 또는 34의 제약 조성물.
36. 아세틸-CoA 카르복실라제 ACC1 및/또는 ACC2 활성, 지질생성, 표피, 진피, 및/또는 피하조직에서의 세포 (예를 들어, 지방세포, 멜라닌세포, 각질세포, 편평 세포, 메르켈 세포, 랑게르한스 세포, 또는 피부 줄기 세포)의 증식, 인간 피지세포의 증식, 인간 각질세포의 증식, 피부 및/또는 피하 층에서의 섬유모세포의 지방세포로의 분화, 피지 생성, 염증, 및 이들의 조합으로부터 선택된 하나 이상의 활성의 억제를 필요로 하는 인간에서 상기 하나 이상의 활성을 억제하기에 효과적인 양의 E1-32 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염을 포함하는 E33-35 중 어느 하나의 제약 조성물.
37. 아세틸-CoA 카르복실라제 (ACC1 및/또는 ACC2) 활성, 말로닐-CoA 생성, 지질생성, 피지세포의 증식, 각질세포의 증식, 표피, 진피, 및/또는 피하조직에서의 세포 (예를 들어, 지방세포, 멜라닌세포, 각질세포, 편평 세포, 메르켈 세포, 랑게르한스 세포, 및 피부 줄기 세포)의 증식, 피부 및/또는 피하 층에서의 섬유모세포의 지방세포로의 분화, 염증, 및 이들의 조합으로부터 선택된 하나 이상의 활성의 억제를 필요로 하는 대상체에게 치료 유효량의 E1-32 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염, 또는 E33-36 중 어느 하나의 제약 조성물을 투여하는 것을 포함하는, 상기 대상체에서 상기 하나 이상의 활성을 억제하는 방법.
38. E1-32 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염, 또는 E33-36 중 어느 하나의 제약 조성물을 대상체에게 국소 투여하는 것인 E37의 방법.
39. 비정상적 피지세포 및/또는 각질세포 활성과 연관된 질환 또는 장애의 치료를 필요로 하는 대상체에게 치료 유효량의 E1-32 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염, 또는 E33-36 중 어느 하나의 제약 조성물을 투여하는 것을 포함하는, 상기 대상체에서 상기 질환 또는 장애를 치료하는 방법.
40. 질환 또는 장애가 여드름, 지루, 피지 증식증, 지루성 각화증, 광선 각화증, 피지 선종, 피지 낭종, 피지 암종, 편평 세포 암종, 흑색종, 비류성 장미증, 버트-호그-두베 증후군에서의 섬유모낭종, 또는 이들의 조합인, E39의 방법.
41. 질환 또는 장애가 여드름인, E39 또는 40의 방법.
42. E1-32 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염, 또는 E33-36 중 어느 하나의 제약 조성물을 대상체에게 국소 투여하는 것인, E39-41 중 어느 하나의 방법.
43. 대상체를 비정상적 피지세포 및/또는 각질세포 활성과 연관된 질환 또는 장애의 치료에 효과적인 하나 이상의 추가의 요법으로 치료하는 것을 추가로 포함하는 E39-42 중 어느 하나의 방법.
44. 대상체에게 항생제 (예를 들어, 클린다마이신, 에리트로마이신, 메트로니다졸, 술프아세트아미드, 또는 테트라시클린, 예컨대 독시시클린 및 미노시클린) 또는 레티노이드 (예를 들어, 아다팔렌, 이소트레티노인, 레티놀, 타자로텐, 또는 트레티노인)를 여드름 및/또는 염증의 치료를 위한 치료 유효량으로 투여하는 것을 추가로 포함하는 E39-42 중 어느 하나의 방법.
45. 비-알콜성 지방간 질환 (예를 들어, 비-알콜성 지방간염 (NASH))의 치료를 필요로 하는 대상체에게 치료 유효량의 E1-32 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염, 또는 E33-36 중 어느 하나의 제약 조성물을 투여하는 것을 포함하는, 상기 대상체에서 상기 질환을 치료하는 방법.
46. 대상체에게 하나 이상의 추가의 작용제를 비-알콜성 지방간 질환의 치료를 위한 치료 유효량으로 투여하는 것을 추가로 포함하는 E45의 방법.
47. 하나 이상의 추가의 작용제가 안지오텐신 II 수용체 길항제, 안지오텐신 전환 효소 (ACE) 억제제, 카스파제 억제제, 카텝신 B 억제제, CCR2 케모카인 길항제, CCR5 케모카인 길항제, 클로라이드 채널 자극제, 콜레스테롤 가용화제, 디아실 글리세롤 O-아실트랜스퍼라제 1 (DGAT1) 억제제, 디펩티딜 펩티다제 IV (DPPIV) 억제제, 파르네소이드 X 수용체 (FXR) 효능제, 갈렉틴-3 억제제, 글루카곤-유사 펩티드 1 (GLPl) 효능제, 글루타티온 전구체, C형 간염 바이러스 NS3 프로테아제 억제제, HMG CoA 리덕타제 억제제, 11β-히드록시스테로이드 데히드로게나제 (11β-HSDl) 억제제, IL-Iβ 길항제, IL-6 길항제, IL-10 효능제, IL-17 길항제, 회장 나트륨 담즙산 공동수송체 억제제, 렙틴 유사체, 5-리폭시나제 억제제, LPL 유전자 자극제, 리실 옥시다제 동족체 2 (LOXL2) 억제제, PDE3 억제제, PDE4 억제제, 포스포리파제 C (PLC) 억제제, PPAR-알파 효능제, PPAR-감마 효능제, PPAR-델타 효능제, Rho 연관 단백질 키나제 2 (ROCK2) 억제제, 나트륨 글루코스 수송체-2 (SGLT2) 억제제, 스테아로일 CoA 데새투라제-1 억제제, 갑상선 호르몬 수용체 β 효능제, 종양 괴사 인자 알파 (TNF-알파) 리간드 억제제, 트랜스글루타미나제 억제제, 트랜스글루타미나제 억제제 전구체, 및 이들의 조합으로부터 선택되는 것인, E46의 방법.
48. 하나 이상의 추가의 작용제가 아세틸살리실산, 알리포젠 티파보벡, 아람콜, 아토르바스타틴, BLX-1002, 세니크리비록, 코비프로스톤, 콜레세벨람, 엠리카산, 에날라프릴, GFT-505, GR-MD-02, 히드로클로로티아지드, 이코사펜트 에틸 에스테르 (에틸 에이코사펜타엔산), IMM-124E, KD-025, 리나글립틴, 리라글루티드, 메르캅타민, MGL-3196, 오베티콜산, 올레속심, 페그-일로데카킨, 피오글리타존, PX-102, 레모글리플로진 에타보네이트, SHP-626, 솔리트로마이신, 티펠루카스트, TRX-318, 우르소데옥시콜산, VBY-376, 및 이들의 조합으로부터 선택되는 것인, E46-47 중 어느 하나의 방법.
49. 비만 및/또는 당뇨병의 치료를 필요로 하는 대상체에게 치료 유효량의 E1-32 중 어느 하나의 화합물, 또는 그의 제약상 허용되는 염, 또는 E33-36 중 어느 하나의 제약 조성물을 투여하는 것을 포함하는, 상기 대상체에서의 비만 및/또는 당뇨병을 치료하는 방법.
50. 대상체에게 하나 이상의 추가의 작용제를 비만 및/또는 당뇨병의 치료를 위한 치료 유효량으로 투여하는 것을 추가로 포함하는 E49의 방법.
51. 하나 이상의 추가의 작용제가 안지오텐신 II 수용체 길항제, 안지오텐신 전환 효소 (ACE) 억제제, 카스파제 억제제, 카텝신 B 억제제, CCR2 케모카인 길항제, CCR5 케모카인 길항제, 클로라이드 채널 자극제, 콜레스테롤 가용화제, 디아실 글리세롤 O-아실트랜스퍼라제 1 (DGAT1) 억제제, 디펩티딜 펩티다제 IV (DPPIV) 억제제, 파르네소이드 X 수용체 (FXR) 효능제, 갈렉틴-3 억제제, 글루카곤-유사 펩티드 1 (GLPl) 효능제, 글루타티온 전구체, C형 간염 바이러스 NS3 프로테아제 억제제, HMG CoA 리덕타제 억제제, 11β-히드록시스테로이드 데히드로게나제 (11β-HSDl) 억제제, IL-Iβ 길항제, IL-6 길항제, IL-10 효능제, IL-17 길항제, 회장 나트륨 담즙산 공동수송체 억제제, 렙틴 유사체, 5-리폭시나제 억제제, LPL 유전자 자극제, 리실 옥시다제 동족체 2 (LOXL2) 억제제, PDE3 억제제, PDE4 억제제, 포스포리파제 C (PLC) 억제제, PPAR-알파 효능제, PPAR-감마 효능제, PPAR-델타 효능제, Rho 연관 단백질 키나제 2 (ROCK2) 억제제, 나트륨 글루코스 수송체-2 (SGLT2) 억제제, 스테아로일 CoA 데새투라제-1 억제제, 갑상선 호르몬 수용체 β 효능제, 종양 괴사 인자 알파 (TNF-알파) 리간드 억제제, 트랜스글루타미나제 억제제, 트랜스글루타미나제 억제제 전구체, 및 이들의 조합으로부터 선택되는 것인, E50의 방법.
52. 하나 이상의 추가의 작용제가 아세틸살리실산, 알리포젠 티파보벡, 아람콜, 아토르바스타틴, BLX-1002, 세니크리비록, 코비프로스톤, 콜레세벨람, 엠리카산, 에날라프릴, GFT-505, GR-MD-02, 히드로클로로티아지드, 이코사펜트 에틸 에스테르 (에틸 에이코사펜타엔산), IMM-124E, KD-025, 리나글립틴, 리라글루티드, 메르캅타민, MGL-3196, 오베티콜산, 올레속심, 페그-일로데카킨, 피오글리타존, PX-102, 레모글리플로진 에타보네이트, SHP-626, 솔리트로마이신, 티펠루카스트, TRX-318, 우르소데옥시콜산, VBY-376, 및 이들의 조합으로부터 선택되는 것인, E50-51 중 어느 하나의 방법.
정의
모든 모이어티 및 이들의 조합에 대하여 적절한 원자가가 유지됨을 이해하여야 한다.
또한, 본원에서 가변적 모이어티의 구체적 실시양태는 동일한 식별자를 갖는 또 다른 구체적 실시양태와 동일하거나 상이할 수 있음을 이해하여야 한다.
화학식 I (예를 들어, 화학식 I-1, 화학식 Ia, 화학식 Ib, 화학식 Ic, 화학식 II-1 내지 화학식 II-3, 또는 화학식 III-1 내지 화학식 III-6)의 화합물에서 R1, R2, 및 R3에 적합한 기는 독립적으로 선택된다. 기재된 본 발명의 실시양태는 조합될 수 있다. 이러한 조합은 본 발명의 범위 내에 있는 것으로 고려된다. 예를 들어, R1, R2, 및 R3 중 임의의 것의 실시양태는 R1, R2, 및 R3 중 임의의 다른 것에 대해 정의된 실시양태와 조합될 수 있음이 고려된다.
본원에서 사용되는 바와 같이, 용어 "본 개시내용의 스피로락톤 화합물(들)"은 화학식 I (예를 들어, 화학식 I-1, 화학식 Ia, 화학식 Ib, 화학식 Ic, 화학식 II-1 내지 화학식 II-3, 또는 화학식 III-1 내지 화학식 III-6, 또는 실시예 1-22 중 임의의 것)에 따른 본원에 기재된 화합물, 이들의 동위원소 표지된 화합물(들), 이들의 가능한 입체이성질체 (부분입체이성질체, 거울상이성질체, 및 라세미 혼합물 포함), 이들의 호변이성질체, 이들의 형태 이성질체, 및/또는 이들의 제약상 허용되는 염 (예를 들어, 산 부가 염, 예컨대 HCl 염 또는 염기 부가 염, 예컨대 Na 염) 중 임의의 것을 지칭한다. 각각 화합물(들)이 물 또는 용매와 회합되어 있는 것인, 본 개시내용의 스피로락톤 화합물의 수화물 및 용매화물도 본 개시내용의 조성물로 고려된다.
본원에서 사용되는 바와 같이, 화합물의 "투여", 화합물을 "투여하는"의 어구, 또는 이들의 다른 변형어는 치료를 필요로 하는 개체에게 화합물 또는 화합물의 전구약물을 제공하는 것을 의미한다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "알킬"은 1 내지 12개의 탄소 원자 (즉, C1-12 알킬) 또는 지정된 수의 탄소 원자 (즉, C1 알킬, 예컨대 메틸, C2 알킬, 예컨대 에틸, C3 알킬, 예컨대 프로필 또는 이소프로필 등)를 함유하는 직쇄 또는 분지쇄 지방족 탄화수소를 지칭한다. 하나의 실시양태에서, 알킬 기는 직쇄 C1-10 알킬 기이다. 또 다른 실시양태에서, 알킬 기는 분지쇄 C3-10 알킬 기이다. 또 다른 실시양태에서, 알킬 기는 직쇄 C1-6 알킬 기이다. 또 다른 실시양태에서, 알킬 기는 분지쇄 C3-6 알킬 기이다. 또 다른 실시양태에서, 알킬 기는 직쇄 C1-4 알킬 기이다. 또 다른 실시양태에서, 알킬 기는 분지쇄 C3-4 알킬 기이다. 또 다른 실시양태에서, 알킬 기는 직쇄 또는 분지쇄 C3-4 알킬 기이다. 비제한적 예시적 C1-10 알킬 기는 메틸, 에틸, 프로필, 이소프로필, 부틸, sec-부틸, tert-부틸, 이소-부틸, 3-펜틸, 헥실, 헵틸, 옥틸, 노닐, 데실 등을 포함한다. 비제한적 예시적 C1-4 알킬 기는 메틸, 에틸, 프로필, 이소프로필, 부틸, sec-부틸, tert-부틸, 및 이소-부틸을 포함한다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "임의로 치환된 알킬"은, 상기에서 정의된 바와 같은 알킬이, 예를 들어, 할로 (예를 들어, F), 옥소, 니트로, 시아노, ORa, CO2Ra, OCO2Ra, OSO2NRbRc, SO3Ra, OSO3Ra, OS(O)nRe, NRbRc, C(=O)NRbRc, OC(=O)NRbRc, SO2NRbRc, OC(=O)Rd, C(=O)Rd, S(O)nRe, C(=NRf)NRbRc, 알킬, 시클로알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 및 헤테로시클릴 (여기서 각각의 알킬, 시클로알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 및 헤테로시클릴은 추가로 1-5개의 Rg로 임의로 치환되고, 여기서 n은 0, 1, 또는 2이고, Ra, Rb, Rc, Rd, Re, Rf 및 Rg는 본원에서 정의됨)로부터 각각 독립적으로 선택된 1개 이상의 (예를 들어, 1, 2, 또는 3개의) 치환기로 치환되거나 비치환됨을 의미한다. 하나의 실시양태에서, 임의로 치환된 알킬은 3개의 치환기, 예를 들어, 3개의 플루오린으로 치환된다. 하나의 실시양태에서, 임의로 치환된 알킬은 1개의 치환기로 치환된다. 하나의 실시양태에서, 임의로 치환된 알킬은 2개의 치환기로 치환된다.
본원에서 사용되는 바와 같이, 각각의 Ra, Rd 및 Re는 각 경우에 독립적으로 수소, C1-10 알킬, C1-10 할로알킬, C2-10 알케닐, C2-10 알키닐, C3-10 시클로알킬, 3-14원 헤테로시클릴, C6-14 아릴, 및 5-14원 헤테로아릴로부터 선택되고, 여기서 각각의 알킬, 알케닐, 알키닐, 카르보시클릴, 헤테로시클릴, 아릴, 및 헤테로아릴은 독립적으로 0, 1, 2, 3, 4, 또는 5개의 Rg 기로 치환된다.
본원에서 사용되는 바와 같이, 각각의 Rb, Rc 및 Rf는 각 경우에 수소, 니트로, 시아노, ORaa, CO2Raa, SO3Raa, NRbbRcc, C(=O)NRbbRcc, SO2NRbbRcc, OC(=O)Rdd, C(=O)Rdd, S(O)nRee, C(=NRff)NRbbRcc, C1-10 알킬, C1-10 할로알킬, C2-10 알케닐, C2-10 알키닐, C3-10 시클로알킬, 3-14원 헤테로시클릴, C6-14 아릴, 및 5-14원 헤테로아릴로부터 선택되거나, 또는 Rb 및 Rc, 또는 Rf 및 Rb 및 Rc 중 하나가 연합되어 3-14원 헤테로시클릴 또는 5-14원 헤테로아릴 고리를 형성하고, 여기서 각각의 알킬, 알케닐, 알키닐, 카르보시클릴, 헤테로시클릴, 아릴, 및 헤테로아릴은 독립적으로 0, 1, 2, 3, 4, 또는 5개의 Rg 기로 치환되고, 여기서 n은 0, 1, 또는 2이고, Raa, Rbb, Rcc, Rdd, Ree 및 Rff는 본원에서 정의된다. 일부 실시양태에서, Rb 및 Rc 중 적어도 하나는 수소, C1-10 알킬, C1-10 할로알킬, C2-10 알케닐, C2-10 알키닐, C3-10 시클로알킬, 3-14원 헤테로시클릴, C6-14 아릴, 및 5-14원 헤테로아릴로부터 선택되고, 여기서 각각의 알킬, 알케닐, 알키닐, 카르보시클릴, 헤테로시클릴, 아릴, 및 헤테로아릴은 독립적으로 치환된 0, 1, 2, 3, 4, 또는 5개의 Rg 기로 치환된다. 일부 실시양태에서, Rb 및 Rc 둘 다 수소, C1-10 알킬, C1-10 할로알킬, C2-10 알케닐, C2-10 알키닐, C3-10 시클로알킬, 3-14원 헤테로시클릴, C6-14 아릴, 및 5-14원 헤테로아릴로부터 독립적으로 선택되고, 여기서 각각의 알킬, 알케닐, 알키닐, 카르보시클릴, 헤테로시클릴, 아릴, 및 헤테로아릴은 독립적으로 0, 1, 2, 3, 4, 또는 5개의 Rg 기로 치환된다.
본원에서 사용되는 바와 같이, Rg는 각 경우에 독립적으로 할로 (예를 들어, F), 니트로, 시아노, ORaa, CO2Raa, NRbbRcc, C(=O)NRbbRcc, SO2NRbbRcc, NRbb(SO2NRbbRcc), OSO2NRbbRcc, NRbb(SO3Raa), SO3Raa, OSO3Raa, NRbb(S(O)nRee), O(S(O)nRee), OC(=O)Rdd, OCO2Raa, NRbbCO2Raa, OC(=O)NRbbRcc, NRbb(C(=O)Rdd), C(=O)Rdd, S(O)nRee, C(=NRff)NRbbRcc, -NRhh-C(=O)NRbbRcc, -NRhh-C(=NRff)NRbbRcc, C1-6 알킬, C1-6 할로알킬, C2-6 알케닐, C2-6 알키닐, C3-10 시클로알킬, C6-10 아릴, 3-10원 헤테로시클릴, 5-10원 헤테로아릴로부터 선택되고, 여기서 각각의 알킬, 알케닐, 알키닐, 카르보시클릴, 헤테로시클릴, 아릴, 및 헤테로아릴은 독립적으로 0, 1, 2, 3, 4, 또는 5개의 Rgg 기로 치환되거나, 또는 2개의 같은자리 Rgg 치환기가 연합되어 =O 또는 =S를 형성할 수 있고, 여기서 n은 0, 1, 또는 2이고, Raa, Rbb, Rcc, Rdd, Ree, Rff, Rgg 및 Rhh는 본원에서 정의된다.
본원에서 사용되는 바와 같이, 각각의 Raa, Rbb, Rcc, Rdd, Ree, Rff 및 Rhh는 각 경우에 수소, C1-6 알킬, C1-6 할로알킬, C2-6 알케닐, C2-6 알키닐, C3-6 시클로알킬, 4-6원 헤테로시클릴, C6-10 아릴, 및 5-10원 헤테로아릴로부터 독립적으로 선택되거나, 또는 Rbb 및 Rcc, Rff 및 Rhh, Rff 및 Rbb 및 Rcc 중 하나, 또는 Rhh 및 Rbb 및 Rcc 중 하나가 연합되어 4-6원 헤테로시클릴 또는 5-10원 헤테로아릴 고리를 형성하고, 여기서 각각의 알킬, 알케닐, 알키닐, 카르보시클릴, 헤테로시클릴, 아릴, 및 헤테로아릴은 독립적으로 0, 1, 2, 3, 4, 또는 5개의 Rgg 기로 치환된다.
본원에서 사용되는 바와 같이, Rgg는 각 경우에 할로 (예를 들어, F), 니트로, 시아노, 히드록시, NH2, N(H)(C1-6 알킬), N(C1-6 알킬)(C1-6 알킬), N(H)(C3-6 시클로알킬), N(C1-6 알킬)(C3-6 시클로알킬), N(C3-6 시클로알킬)(C3-6 시클로알킬), O-C1-6 알킬, C1-6 알킬, C1-6 할로알킬, O-C1-6 할로알킬, 할로겐, C1-4 알킬, 및 C3-6 시클로알킬로부터 독립적으로 선택된 1-5개의 치환기로 임의로 치환된 C3-6 시클로알킬, 할로겐, C1-4 알킬, 및 C3-6 시클로알킬로부터 독립적으로 선택된 1-5개의 치환기로 임의로 치환된 O-C3-6 시클로알킬, 할로겐, 옥소, C1-4 알킬, 및 C3-6 시클로알킬로부터 독립적으로 선택된 1-3개의 치환기로 임의로 치환된 4-6원 헤테로시클릴, 할로겐, 시아노, C1-4 알킬, 및 C3-6 시클로알킬로부터 독립적으로 선택된 1-5개의 치환기로 임의로 치환된 C6-10 아릴, 및 할로겐, 시아노, C1-4 알킬, 및 C3-6 시클로알킬로부터 독립적으로 선택된 1-5개의 치환기로 임의로 치환된 5-10원 헤테로아릴로부터 독립적으로 선택되거나, 또는 2개의 같은자리 Rgg 치환기가 연합되어 =O 또는 =S를 형성할 수 있다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "시클로알킬"은 3 내지 12개의 탄소 원자 (즉, C3-12 시클로알킬) 또는 지정된 수의 탄소를 갖는 1 내지 3개의 고리를 함유하는 포화 및 부분 불포화 (1 또는 2개의 이중 결합을 함유함) 시클릭 지방족 탄화수소를 지칭한다. 하나의 실시양태에서, 시클로알킬 기는 2개의 고리를 갖는다. 하나의 실시양태에서, 시클로알킬 기는 1개의 고리를 갖는다. 또 다른 실시양태에서, 시클로알킬 기는 C3-8 시클로알킬 기이다. 또 다른 실시양태에서, 시클로알킬 기는 C3-6 시클로알킬 기이다. 비제한적 예시적 시클로알킬 기는 시클로프로필, 시클로부틸, 시클로펜틸, 시클로헥실, 시클로헵틸, 시클로옥틸, 노르보르닐, 데칼린, 아다만틸, 시클로펜테닐, 및 시클로헥세닐을 포함한다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "임의로 치환된 시클로알킬"은, 상기에서 정의된 바와 같은 시클로알킬이, 예를 들어, 할로 (예를 들어, F), 옥소, 니트로, 시아노, ORa, CO2Ra, OCO2Ra, OSO2NRbRc, SO3Ra, OSO3Ra, OS(O)nRe, NRbRc, C(=O)NRbRc, OC(=O)NRbRc, SO2NRbRc, OC(=O)Rd, C(=O)Rd, S(O)nRe, C(=NRf)NRbRc, 알킬, 시클로알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 및 헤테로시클릴 (여기서 각각의 알킬, 시클로알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 및 헤테로시클릴은 추가로 1-5개의 Rg로 임의로 치환되고, 여기서 n은 0, 1, 또는 2이고, Ra, Rb, Rc, Rd, Re, Rf 및 Rg는 본원에서 정의됨)로부터 각각 독립적으로 선택된 1개 이상의 (예를 들어, 1, 2, 또는 3개의) 치환기로 치환되거나 비치환됨을 의미한다. 하나의 실시양태에서, 임의로 치환된 시클로알킬은 3개의 치환기로 치환된다. 하나의 실시양태에서, 임의로 치환된 시클로알킬은 2개의 치환기로 치환된다. 또 다른 실시양태에서, 임의로 치환된 시클로알킬은 1개의 치환기로 치환된다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "알케닐"은 1, 2 또는 3개의 탄소-탄소 이중 결합을 함유하는 상기에서 정의된 바와 같은 알킬 기를 지칭한다. 하나의 실시양태에서, 알케닐 기는 C2-6 알케닐 기이다. 또 다른 실시양태에서, 알케닐 기는 C2-4 알케닐 기이다. 비제한적 예시적 알케닐 기는 에테닐, 프로페닐, 이소프로페닐, 부테닐, sec-부테닐, 펜테닐, 및 헥세닐을 포함한다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 본원에서 사용되는 용어 "임의로 치환된 알케닐"은, 상기에서 정의된 바와 같은 알케닐이, 예를 들어, 할로 (예를 들어, F), 옥소, 니트로, 시아노, ORa, CO2Ra, OCO2Ra, OSO2NRbRc, SO3Ra, OSO3Ra, OS(O)nRe, NRbRc, C(=O)NRbRc, OC(=O)NRbRc, SO2NRbRc, OC(=O)Rd, C(=O)Rd, S(O)nRe, C(=NRf)NRbRc, 알킬, 시클로알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 및 헤테로시클릴 (여기서 각각의 알킬, 시클로알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 및 헤테로시클릴은 추가로 1-5개의 Rg로 임의로 치환되고, 여기서 n은 0, 1, 또는 2이고, Ra, Rb, Rc, Rd, Re, Rf 및 Rg는 본원에서 정의됨)로부터 각각 독립적으로 선택된 1개 이상의 (예를 들어, 1, 2, 또는 3개의) 치환기로 치환되거나 비치환됨을 의미한다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "알키닐"은 1 내지 3개의 탄소-탄소 삼중 결합을 함유하는 상기에서 정의된 바와 같은 알킬 기를 지칭한다. 하나의 실시양태에서, 알키닐은 1개의 탄소-탄소 삼중 결합을 갖는다. 하나의 실시양태에서, 알키닐 기는 C2-6 알키닐 기이다. 또 다른 실시양태에서, 알키닐 기는 C2-4 알키닐 기이다. 비제한적 예시적 알키닐 기는 에티닐, 프로피닐, 부티닐, 2-부티닐, 펜티닐, 및 헥시닐 기를 포함한다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 본원에서 사용되는 용어 "임의로 치환된 알키닐"은, 상기에서 정의된 바와 같은 알키닐이, 예를 들어, 할로 (예를 들어, F), 옥소, 니트로, 시아노, ORa, CO2Ra, OCO2Ra, OSO2NRbRc, SO3Ra, OSO3Ra, OS(O)nRe, NRbRc, C(=O)NRbRc, OC(=O)NRbRc, SO2NRbRc, OC(=O)Rd, C(=O)Rd, S(O)nRe, C(=NRf)NRbRc, 알킬, 시클로알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 및 헤테로시클릴 (여기서 각각의 알킬, 시클로알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 및 헤테로시클릴은 추가로 1-5개의 Rg로 임의로 치환되고, 여기서 n은 0, 1, 또는 2이고, Ra, Rb, Rc, Rd, Re, Rf 및 Rg는 본원에서 정의됨)로부터 각각 독립적으로 선택된 1개 이상의 (예를 들어, 1, 2, 또는 3개의) 치환기로 치환되거나 비치환됨을 의미한다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "할로알킬"은 1개 이상의 플루오린, 염소, 브로민 및/또는 아이오딘 원자로 치환된 알킬을 지칭한다. 바람직한 실시양태에서, 할로알킬은 1, 2, 또는 3개의 플루오린 원자로 치환된 알킬 기이다. 하나의 실시양태에서, 할로알킬 기는 C1-10 할로알킬 기이다. 하나의 실시양태에서, 할로알킬 기는 C1-6 할로알킬 기이다. 하나의 실시양태에서, 할로알킬 기는 C1-4 할로알킬 기이다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "임의로 치환된 할로알킬"은 1개 이상의 플루오린, 염소, 브로민 및/또는 아이오딘 원자로 치환된 임의로 치환된 알킬을 지칭한다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "알콕시"는 Ra1이 알킬인 화학식 ORa1의 라디칼을 지칭한다. 본원에서 사용되는 바와 같이, 용어 "임의로 치환된 알콕시"는 Ra1이 임의로 치환된 알킬인 화학식 ORa1의 라디칼을 지칭하다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "시클로알콕시"는 Ra1이 시클로알킬인 화학식 ORa1의 라디칼을 지칭한다. 본원에서 사용되는 바와 같이, 용어 "임의로 치환된 시클로알콕시"는 Ra1이 임의로 치환된 시클로알킬인 화학식 ORa1의 라디칼을 지칭한다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "아릴"은 6 내지 14개의 탄소 원자 (즉, C6-14 아릴)를 갖는 모노시클릭, 비시클릭 또는 트리시클릭 방향족 고리 시스템을 지칭한다. 하나의 실시양태에서, 아릴 기는 C6-12 아릴이다. 하나의 실시양태에서, 아릴 기는 페닐 및 나프틸로부터 선택된다. 하나의 실시양태에서, 아릴 기는 나프틸이다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "임의로 치환된 아릴"은, 상기에서 정의된 바와 같은 아릴이, 예를 들어, 할로 (예를 들어, F), 니트로, 시아노, ORa, CO2Ra, OCO2Ra, OSO2NRbRc, SO3Ra, OSO3Ra, OS(O)nRe, NRbRc, C(=O)NRbRc, OC(=O)NRbRc, SO2NRbRc, OC(=O)Rd, C(=O)Rd, S(O)nRe, C(=NRf)NRbRc, 알킬, 시클로알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 및 헤테로시클릴 (여기서 각각의 알킬, 시클로알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 및 헤테로시클릴은 추가로 1-5개의 Rg로 임의로 치환되고, 여기서 n은 0, 1, 또는 2이고, Ra, Rb, Rc, Rd, Re, Rf 및 Rg는 본원에서 정의됨)로부터 각각 독립적으로 선택된 1 내지 5개의 치환기로 치환되거나 비치환되거나; 또는 치환기 중 2개가 연합되어 아릴에 융합된 임의로 치환된 시클로알킬 또는 임의로 치환된 헤테로시클릴 고리를 형성함을 의미한다.
본원에서 사용되는 바와 같이, 용어 "헤테로아릴" 또는 "헤테로방향족"은 5 내지 14개의 고리 원자 (즉, 5- 내지 14원 헤테로아릴) 및 산소, 질소 및 황으로부터 독립적으로 선택된 1, 2, 3, 또는 4개의 헤테로원자를 갖는 모노시클릭, 비시클릭 또는 트리시클릭 방향족 고리 시스템을 지칭한다. 하나의 실시양태에서, 헤테로아릴은 3개의 헤테로원자, 예를 들어, 3개의 질소 원자를 갖는다. 또 다른 실시양태에서, 헤테로아릴은 2개의 헤테로원자, 예를 들어, 2개의 질소 원자, 1개의 질소 및 1개의 산소, 또는 1개의 질소 및 1개의 황을 갖는다. 또 다른 실시양태에서, 헤테로아릴은 1개의 헤테로원자, 예를 들어, 1개의 질소를 갖는다. 하나의 실시양태에서, 헤테로아릴은 5개의 고리 원자를 갖고, 예를 들어 피라졸릴이다. 또 다른 실시양태에서, 헤테로아릴은 6개의 고리 원자를 갖고, 예를 들어 피리딜이다. 비제한적 예시적 헤테로아릴 기는 티에닐, 벤조[b]티에닐, 나프토[2,3-b]티에닐, 티안트레닐, 푸릴, 벤조푸릴, 피라닐, 이소벤조푸라닐, 벤조옥사조닐, 크로메닐, 크산테닐, 2H-피롤릴, 피롤릴, 이미다졸릴, 피라졸릴, 피리딜, 피라지닐, 피리미디닐, 피리다지닐, 이소인돌릴, 3H-인돌릴, 인돌릴, 인다졸릴, 퓨리닐, 이소퀴놀릴, 퀴놀릴, 프탈라지닐, 나프티리디닐, 신놀리닐, 퀴나졸리닐, 프테리디닐, 4aH-카르바졸릴, 카르바졸릴, β-카르볼리닐, 페난트리디닐, 아크리디닐, 피리미디닐, 페난트롤리닐, 페나지닐, 티아졸릴, 이소티아졸릴, 페노티아졸릴, 이속사졸릴, 푸라자닐, 및 페녹사지닐을 포함한다. 하나의 실시양태에서, 헤테로아릴은 티에닐 (예를 들어, 티엔-2-일 및 티엔-3-일), 푸릴 (예를 들어, 2-푸릴 및 3-푸릴), 피롤릴 (예를 들어, 1H-피롤-2-일 및 1H-피롤-3-일), 이미다졸릴 (예를 들어, 2H-이미다졸-2-일 및 2H-이미다졸-4-일), 피라졸릴 (예를 들어, 1H-피라졸-3-일, 1H-피라졸-4-일, 및 1H-피라졸-5-일), 피리딜 (예를 들어, 피리딘-2-일, 피리딘-3-일, 및 피리딘-4-일), 피리미디닐 (예를 들어, 피리미딘-2-일, 피리미딘-4-일, 및 피리미딘-5-일), 티아졸릴 (예를 들어, 티아졸-2-일, 티아졸-4-일, 및 티아졸-5-일), 이소티아졸릴 (예를 들어, 이소티아졸-3-일, 이소티아졸-4-일, 및 이소티아졸-5-일), 옥사졸릴 (예를 들어, 옥사졸-2-일, 옥사졸-4-일, 및 옥사졸-5-일) 및 이속사졸릴 (예를 들어, 이속사졸-3-일, 이속사졸-4-일, 및 이속사졸-5-일)로부터 선택된다. 하나의 실시양태에서, 헤테로아릴은 8 내지 10개의 고리 원자를 갖는 비시클릭 헤테로아릴, 예를 들어, 1, 2, 또는 3개의 질소 고리 원자를 갖는 비시클릭 헤테로아릴, 예컨대 퀴놀릴이다. 본원에서 사용되는 바와 같이, 용어 "헤테로아릴"은 또한 가능한 N-옥시드를 포함하도록 의도된다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "임의로 치환된 헤테로아릴"은, 상기에서 정의된 바와 같은 헤테로아릴이, 예를 들어, 할로 (예를 들어, F), 니트로, 시아노, ORa, CO2Ra, OCO2Ra, OSO2NRbRc, SO3Ra, OSO3Ra, OS(O)nRe, NRbRc, C(=O)NRbRc, OC(=O)NRbRc, SO2NRbRc, OC(=O)Rd, C(=O)Rd, S(O)nRe, C(=NRf)NRbRc, 알킬, 시클로알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 및 헤테로시클릴 (여기서 각각의 알킬, 시클로알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 및 헤테로시클릴은 추가로 1-5개의 Rg로 임의로 치환되고, 여기서 n은 0, 1, 또는 2이고, Ra, Rb, Rc, Rd, Re, Rf 및 Rg는 본원에서 정의됨)로부터 각각 독립적으로 선택된 1개 이상의 (예를 들어, 1, 2, 3, 4, 또는 5개의) 치환기로 치환되거나 비치환되거나; 또는 치환기 중 2개가 연합되어 헤테로아릴에 융합된 임의로 치환된 시클로알킬 또는 임의로 치환된 헤테로시클릴 고리를 형성함을 의미한다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "헤테로사이클" 또는 "헤테로시클릴"은 3 내지 14개의 고리 구성원 (즉, 3- 내지 14원 헤테로사이클) 및 적어도 1개의 헤테로원자를 갖는 1, 2, 또는 3개의 고리를 함유하는 포화 및 부분 불포화 (예를 들어, 1 또는 2개의 이중 결합을 함유함) 시클릭 기를 지칭한다. 각각의 헤테로원자는 산소, 황 (술폭시드 및 술폰 포함), 및/또는 질소 원자 (이는 사급화될 수 있음)로 이루어진 군으로부터 독립적으로 선택된다. 용어 "헤테로시클릴"은 시클릭 우레이도 기, 예컨대 이미다졸리디닐-2-온, 시클릭 아미드 기, 예컨대 β-락탐, γ-락탐, δ-락탐 및 ε-락탐, 및 시클릭 카르바메이트 기, 예컨대 옥사졸리디닐-2-온을 포함하도록 의도된다. 하나의 실시양태에서, 헤테로시클릴 기는 1개의 고리 및 1 또는 2개의 산소 및/또는 질소 원자를 함유하는 4-, 5-, 6-, 7- 또는 8원 시클릭 기이다. 하나의 실시양태에서, 헤테로시클릴 기는 1개의 고리 및 1 또는 2개의 질소 원자를 함유하는 5- 또는 6원 시클릭 기이다. 하나의 실시양태에서, 헤테로시클릴 기는 2개의 고리 및 1 또는 2개의 질소 원자를 함유하는 8-, 9-, 10-, 11-, 또는 12원 시클릭 기이다. 헤테로시클릴은 임의로, 탄소 또는 질소 원자를 통해 분자의 나머지 부분에 연결될 수 있다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 본원에서 사용되는 용어 "임의로 치환된 헤테로시클릴"은, 상기에서 정의된 바와 같은 헤테로시클릴이, 예를 들어, 할로 (예를 들어, F), 옥소, 니트로, 시아노, ORa, CO2Ra, OCO2Ra, OSO2NRbRc, SO3Ra, OSO3Ra, OS(O)nRe, NRbRc, C(=O)NRbRc, OC(=O)NRbRc, SO2NRbRc, OC(=O)Rd, C(=O)Rd, S(O)nRe, C(=NRf)NRbRc, 알킬, 시클로알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 및 헤테로시클릴 (여기서 각각의 알킬, 시클로알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 및 헤테로시클릴은 추가로 1-5개의 Rg로 임의로 치환되고, 여기서 n은 0, 1, 또는 2이고, Ra, Rb, Rc, Rd, Re, Rf 및 Rg는 본원에서 정의됨)로부터 각각 독립적으로 선택된 1개 이상의 (예를 들어, 1, 2, 3, 4, 또는 5개의) 치환기로 치환되거나 비치환되거나; 또는 치환기 중 2개가 연합되어 헤테로시클릴에 융합된 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴 고리를 형성함을 의미한다. 치환은 임의의 이용가능한 탄소 또는 질소 원자 상에서 일어날 수 있고, 스피로사이클을 형성할 수 있다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "알카노일"은 Rd1이 알킬 기인 화학식 C(=O)-Rd1의 라디칼을 지칭한다. 본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "임의로 치환된 알카노일"은 Rd1이 임의로 치환된 알킬 기인 C(=O)-Rd1을 지칭한다.
본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "시클로알카노일"은 Rd1이 시클로알킬 기인 화학식 C(=O)Rd1의 라디칼을 지칭한다. 본원에서 사용되는 바와 같이, 그 자체로 또는 또 다른 기의 부분으로서 사용되는 용어 "임의로 치환된 시클로알카노일"은 Rd1이 임의로 치환된 시클로알킬 기인 C(=O)Rd1을 지칭한다.
본원에서 사용되는 바와 같이, 용어 "염"은 내부 염 및 외부 염 둘 다를 포함한다. 일부 실시양태에서, 염은 내부 염, 즉, 쯔비터이온 구조를 함유하는 염이다. 일부 실시양태에서, 염은 외부 염이다. 일부 실시양태에서, 외부 염은 적합한 반대 이온을 갖는 제약상 허용되는 염이다. 제약 용도에 적합한 반대 이온은 관련 기술분야에 공지되어 있다.
본원에서 사용되는 바와 같이, 용어 "치료하다", "치료하는", "치료" 등은 질환 또는 병태, 및/또는 이들과 연관된 증상을 제거하거나 감소시키거나 개선시킴을 지칭한다. 배제적인 것은 아니지만, 질환 또는 병태의 치료는, 질환, 병태, 또는 이들과 연관된 증상이 완전히 제거되는 것을 요구하지는 않는다. 본원에서 사용되는 바와 같이, 용어 "치료하다", "치료하는", "치료" 등은, 질환 또는 병태의 재발달 또는 질환 또는 병태의 재발을 갖지 않지만 이들의 위험이 있는 또는 이들에 취약한 대상체에서의, 질환 또는 병태의 재발달, 또는 이전에 제어된 질환 또는 병태의 재발의 가능성을 감소시킴을 지칭하는 "예방적 치료"를 포함할 수 있다. 용어 "치료" 및 동의어는 치료 유효량의 본원에 기재된 화합물을 이러한 치료를 필요로 하는 대상체에게 투여하는 것을 고려한다.
용어 "억제", "억제하는", "억제하다", 또는 "억제제"는 화합물이 특정 생물학적 과정의 활성 (예를 들어, 비히클에 대한 세포에서의 ACC 효소의 활성)을 감소시키거나 둔화시키거나 중단시키거나 막는 능력을 지칭한다.
본원에서 사용되는 바와 같이, 용어 "대상체" (다르게는 본원에서 "환자"로서 언급됨)는 치료, 관찰 또는 실험의 대상이 된 동물, 바람직하게는 포유류, 가장 바람직하게는 인간을 지칭한다.
실시예
바람직한 실시양태의 다양한 출발 물질, 중간체, 및 화합물은 적절한 경우 종래 기술, 예컨대 침전, 여과, 결정화, 증발, 증류, 및 크로마토그래피를 사용하여 단리 및 정제될 수 있다. 이들 화합물의 특성화는 종래 방법을 사용하여, 예컨대 융점, 질량 스펙트럼, 핵 자기 공명, 및 다양한 다른 분광 분석에 의해 수행될 수 있다. NMR 분광법에서, 일부 신호는 미세 분열이 완전히 분석되지 않는 경우 단일선으로서 특성화될 수 있다. 본원에 기재된 생성물의 합성을 수행하기 위한 단계의 예시적 실시양태가 하기에 보다 상세히 기재된다.
실시예 1. 1'-(4,8-디메톡시-2-나프토일)-7-이소프로필스피로[이소크로만-3,4'-피페리딘]-1-온의 합성.
문헌 (예를 들어, [Yamato M. et al. "Synthesis and Structure-Activity Relationship of Spiro[isochromanpiperidine] Analogues for Inhibition of Histamine Release," J. Med. Chem. 24:194-198 (1981)] 참조)에 보고된 것들과 유사한 절차에 따라 화합물 A1 및 A2로부터 제조된 화합물 A4, 7-이소프로필-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-윰 클로라이드 (31 mg, 0.106 mmole), 4,8-디메톡시-2-나프토산 (26 mg, 0.107 mmole), DIEA (45 uL, 0.265 mmole), 및 HATU (47 mg, 0.125 mmole)를 DMF (0.75 mL) 중에서 혼합하고, 실온에서 4 hr 동안 방치시켰다. 반응물을 에틸 아세테이트 (5 mL)로 희석하고, 0.1 N HCl (2X), 포화 NaHCO3 (2X), 및 염수로 세척하였다. 유기 용매의 증발 후 조 생성물을 에틸 아세테이트/디클로로메탄 (1:10)으로 용리하며 TLC 상에서 크로마토그래피하였다. 생성물 밴드를 수집하고, 에틸 아세테이트로 세척하여, 진공에서 건조 후 백색 분말로서 실시예 1을 수득하였다 (45 mg). NMR (CDCl3) δ: 7.99 (d, 1H); 7.89 (s, 1H); 7.84 (d, 1H); 7.45 (m, 2H); 7.19 (d, 1H); 6.91 (s, 1H); 6.90 (d, 1H); 4.4-4.6 (br, 1H); 4.04 (s, 3H); 4.00 (s, 3H); 3.45-3.9 (br, 3H); 3.06 (S, 2H); 2.98 (pent, 1H); 1.55-2.15 (br, 4H); 1.29 (d, 6H).
실시예 2. 1'-(4,8-디메톡시퀴놀린-2-카르보닐)-7-이소프로필스피로[이소크로만-3,4'-피페리딘]-1-온의 합성
7-이소프로필-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-윰 클로라이드 및 4,8-디메톡시퀴놀린-2-카르복실산을 사용하여 실시예 1과 유사한 절차로 실시예 2를 제조하였다. 제조용 TLC를 MeOH/에틸 아세테이트 (1:10)로 용리하였다. NMR (CDCl3) δ: 7.99 (d, 1H); 7.80 (d, 1H); 7.50 (t, 1H); 7.45 (dd, 1H); 7.20 (d, 1H); 7.19 (s, 1H); 7.11 (d, 1H); 4.56 (br d, 1H); 4.15 (br, 1H); 4.12 (s, 3H); 4.06 (s, 3H); 3.69 (br t, 1H); 3.48 (br t, 1H); 3.08 (s, 2H); 2.98 (pent, 1H); 2.11-2.14 (m, 2H); 1.97-2.00 (m, 2H); 1.29 (d, 6H).
실시예 3. 1'-(4,8-디메톡시-2-나프토일)-7-에틸스피로[이소크로만-3,4'-피페리딘]-1-온의 합성
7-에틸-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-윰 클로라이드 및 4,8-디메톡시-2-나프토산을 사용하여 실시예 1과 유사한 절차로 실시예 3을 제조하였다. 제조용 TLC를 에틸 아세테이트/디클로로메탄 (1:1)로 용리하였다. NMR (CDCl3) δ: 7.96 (br s, 1H); 7.89 (br s, 1H); 7.84 (d, 1H); 7.46 (d, 1H); 7.42 (t, 1H);7.18 (d, 1H); 6.91 (s, 1H); 6.905 (d, 1H); 4.4-4.7 (br, 1H); 4.04 (s, 3H); 4.01 (s, 3H); 3.45-3.95 (br, 3H); 3.06 (s, 2H); 2.71 (q, 2H); 1.5-2.2 (br, 4H); 1.28 (t, 3H).
실시예 4. 1'-(4,8-디메톡시퀴놀린-2-카르보닐)-7-에틸스피로[이소크로만-3,4'-피페리딘]-1-온의 합성
7-에틸-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-윰 클로라이드 및 4,8-디메톡시퀴놀린-2-카르복실산을 사용하여 실시예 1과 유사한 절차로 실시예 4를 제조하였다. 제조용 TLC를 MeOH/ 에틸 아세테이트/ (1:10)로 용리하였다. NMR (CDCl3) δ: 7.96 (br s, 1H); 7.80 (d, 1H); 7.51 (t, 1H); 7.42 (dd, 1H); 7.20 (d, 1H); 7.19 (s, 1H); 7.11 (d, 1H); 4.55-4.58 (m, 1H); 4.05-4.15 (m, 1H); 4.12 (s, 3H); 4.06 (s, 3H); 3.68 (m, 1H); 3.48 (m, 1H); 3.08 (s, 2H); 2.72 (q, 2H); 2.1-2.2 (m, 2H); 1.9-2.0 (m, 2H); 1.28 (t, 3H).
실시예 5. 1'-(4,8-디메톡시-2-나프토일)-7-((1-메틸-1H-피라졸-5-일)아미노)스피로[이소크로만-3,4'-피페리딘]-1-온의 합성
단계 1. tert-부틸 7-니트로-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-카르복실레이트
문헌 보고 방법 (예를 들어, [Yamato M. et al. "Synthesis and Structure-Activity Relationship of Spiro[isochromanpiperidine] Analogues for Inhibition of Histamine Release," J. Med. Chem. 24:194-198 (1981)] 참조)을 사용하여 이용가능한 스피로[이소크로만-3,4'-피페리딘]-1-온 히드로클로라이드 (25.3 g)를 0℃에서 H2SO4 (60 mL) 및 그 후 0℃ 미만에서 H2SO4 (50 mL) 중의 KNO3 (12 g)의 용액과 혼합하였다. 반응물을 1시간 후 빙수에 붓고, Na2CO3 첨가에 의해 pH를 10으로 조정하였다. 혼합물을 Boc2O로 처리하고, EA (200 mL)로 추출하고, EA 상을 분리하고, 증발시켜, tert-부틸 7-니트로-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-카르복실레이트 (20 g)를 밝은 황색 고체로서 수득하였다.
단계 2. tert-부틸 7-아미노-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-카르복실레이트
MeOH (150 mL) 중의 tert-부틸 7-니트로-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-카르복실레이트 (20.3 g) 및 Pd/C (1 g)의 혼합물을 3h 동안 H2 (50 psi)로 처리하였다. 반응 혼합물을 여과하고, 여액을 증발시켜, tert-부틸 7-아미노-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-카르복실레이트 (15 g)를 밝은 황색 고체로서 수득하였다.
단계 3. tert-부틸 7-아이오도-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-카르복실레이트)
아세토니트릴 (20 mL) 중의 tert-부틸 7-아미노-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-카르복실레이트 (2.6 g), NaI (2.6 g), I2 (1.3 g) 및 CuI (0.5 g)의 혼합물에 t-부틸니트릴 (2.4 g)을 50℃에서 적가하였다. 1시간 후, 반응 혼합물을 Na2S2O3 용액 중에 붓고, MTBE (30 mL)로 추출하고, 유기 상을 건조시키고, 실리카 패드로 통과시키고, 증발시켜, tert-부틸 7-아이오도-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-카르복실레이트를 밝은 황색 오일로서 수득하였다 (2.2 g). NMR (CDCl3) δ: 8.44 (s, 1H); 7.89 (d, 1H); 7.01 (d, 1H); 3.9 (br, 2H); 3.3 (br, 2H); 2.98 (s, 2H); 1.94 (br, 2H); 1.65 (br, 2H); 1.49 (s, 9H).
단계 4. 화합물 B5 (7-아이오도-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-윰 클로라이드)의 제조.
tert-부틸 7-아이오도-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-카르복실레이트 (500 mg)를 수분 동안 4 N HCl/디옥산 (5 mL)으로 처리하였다. 과량의 시약 및 용매를 회전증발에 의해 제거하고, 잔류물을 진공에서 건조시켜, B5를 백색 고체로서 수득하였다. 분석용 HPLC는 1개의 지배적인 생성물 피크를 가지며 출발 물질의 완전한 소실을 나타내었다. 이 물질을 추가의 정제 없이 사용하였다.
단계 5. 화합물 B7 (1'-(4,8-디메톡시-2-나프토일)-7-아이오도스피로[이소크로만-3,4'-피페리딘]-1-온)의 제조.
7-아이오도-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-윰 클로라이드 (48 mg, 0.126 mmole), 4,8-디메톡시-2-나프토산 (31 mg, 1.07 eq.)을 실시예 1과 동일한 절차로 커플링하였다. 조 생성물을 다음 단계에서 추가의 정제 없이 사용하였다.
단계 6. 실시예 5의 제조.
화합물 B7, 1'-(4,8-디메톡시-2-나프토일)-7-아이오도스피로[이소크로만-3,4'-피페리딘]-1-온 (~ 78 mg, 0.13 mmol)을 DMF (1.5 mL) 중의 1-메틸-1H-피라졸-5-아민 (15 mg, 1.07 eq.), Cs2CO3 (60 mg, 1.3 eq.), 브레트포스(BrettPhose) Pd G1 메틸 t-부틸 에테르 부가생성물 (알드리치, 8 mg, 0.07 eq.)과 혼합하고, 4 hr 동안 90-100℃까지 가열하였다. 반응 혼합물을 여과하고, 증발 후 조 생성물을 제조용 TLC 플레이트 (2 플레이트) 상에 로딩하고, MeOH/에틸 아세테이트 (1:10)로 용리하여, 실시예 5를 건조 후 백색 분말로서 수득하였다. NMR (CDCl3) δ: 7.90 (s, 1H); 7.84 (d, 1H); 7.57 (m, 2H); 7.47 (t, 1H); 7.17 (d, 1H); 7.07 (d, 1H); 6.86 (d, 1H); 6.85 (s, 1H); 6.20 (br s, 1H): 6.1 (br s, 1H); 4.51 (m, 1H); 4.0-4.1 (br, 1H); 4.07 (s, 3H); 4.05 (s, 3H); 3.6-3.9 (br, 2H); 3.85 (s, 3H); 3.02 (s, 2H); 2.2 (br, 1H); 1.7-2.16 (br, 3H).
실시예 6. 1'-(4,8-디메톡시퀴놀린-2-카르보닐)-7-((1-메틸-1H-피라졸-5-일)아미노)스피로[이소크로만-3,4'-피페리딘]-1-온의 합성
4,8-디메톡시-2-나프토산을 4,8-디메톡시퀴놀린-2-카르복실산으로 대체하여, 실시예 5와 동일한 절차를 사용하여 실시예 6을 제조하였다. NMR (CDCl3) δ: 7.80 (d, 1H); 7.5 (m, 3H); 7.19 (s, 1H); 7.12 (s, 1H); 7.12 (t, 1H); 6.95 (dd, 1H);6.11 (d, 1H); 5.74 (br, 1H); 4.52-4.59 (m, 1H); 4.05-4.15 (m, 1H); 4.12 (s, 3H); 4.04 (s, 3H); 3.77 (s, 3H); 3.60-3.72 (m, 1H); 3.39-3.50 (m, 1H); 3.04 (s, 2H); 1.9-2.15 (m, 4H).
실시예 7. 7-이소프로필-1'-(2-메틸-1H-벤조[d]이미다졸-6-카르보닐)스피로[이소크로만-3,4'-피페리딘]-1-온의 합성
4,8-디메톡시-2-나프토산을 2-메틸-1H-벤조[d]이미다졸-6-카르복실산으로 대체하여, 실시예 1과 동일한 절차를 사용하여 실시예 7을 제조하였다. NMR (CDCl3) δ: 8.00 (s, 1H); 7.52 (s, 1H);7.46 (d, 1H); 7.44 (d, 1H); 7.24 (d, 1H); 7.20 (d, 1H); 4.52 (br, 1H); 3.7 (br, 1H); 3.5 (br, 2H);3.05 (s, 2H); 2.99 (hep, 1H); 2.54 (s, 3H);1.6-2.2 (br, 4H);1.28 (d, 6H).
실시예 8. 1'-(1H-인다졸-5-카르보닐)-7-이소프로필스피로[이소크로만-3,4'-피페리딘]-1-온의 합성
4,8-디메톡시-2-나프토산을 1H-인다졸-5-카르복실산으로 대체하여, 실시예 1과 동일한 절차를 사용하여 실시예 8을 제조하였다. NMR (CDCl3) δ: 8.13(s, 1H); 7.99 (s, 1H); 7.88 (s, 1H); 7.5 (d, 1H); 7.48 (d, 1H); 7.45 (d, 1H); 7.19 (d, 1H); 4.55(br, 1H); 3.4-3.7 (br, 3H); 3.04 (s, 2H); 2.99 (hept, 1H); 1.9-2.1 (br, 2H); 1.7-1.8 (br, 2H); 1.29 (d, 6H).
실시예 9. 7-이소프로필-1'-(1H-피롤로[3,2-b]피리딘-2-카르보닐)-스피로[이소크로만-3,4'-피페리딘]-1-온의 합성
4,8-디메톡시-2-나프토산을 1H-피롤로[3,2-b]피리딘-2-카르복실산으로 대체하여, 실시예 1과 동일한 절차를 사용하여 실시예 9를 제조하였다. NMR (CDCl3) δ: 9.89 (s, 1H); 8.54 (d, 1H); 8.02 (s, 1H); 7.76 (d, 1H); 7.47 (d, 1H); 7.21 (d, 1H); 7.20 (dd, 1H); 6.99 (s, 1H); 4.59 (br, 2H); 3.4-4.0 (br, 2H); 3.08 (s, 2H); 3.00 (hept, 1H); 2.16 (br, 2H); 1.83 (br, 2H); 1.30 (d, 6H).
실시예 10. 1'-(1H-인다졸-6-카르보닐)-7-이소프로필스피로-[이소크로만-3,4'-피페리딘]-1-온의 합성
4,8-디메톡시-2-나프토산을 1H-인다졸-6-카르복실산으로 대체하여, 실시예 1과 동일한 절차를 사용하여 실시예 10을 제조하였다. NMR (CDCl3) δ: 10.76 (s, 1H); 8.13 (s, 1H); 7.99 (s, 1H); 7.80 (d, 1H); 7.62 (s, 1H); 7.45 (d, 1H); 7.20 (d, 1H); 7.19 (d, 1H); 4.6 (br, 1H); 3.64 (br, 2H); 3.46 (br, 1H); 3.03 (s, 2H); 3.0 (hept, 1H); 1.6-2.2 (m, 4H); 1.29 (d, 6H).
실시예 11. 7-이소프로필-1'-(6-메톡시퀴놀린-3-카르보닐)스피로[이소크로만-3,4'-피페리딘]-1-온의 합성
4,8-디메톡시-2-나프토산을 6-메톡시퀴놀린-3-카르복실산으로 대체하여, 실시예 1과 동일한 절차를 사용하여 실시예 11을 제조하였다. NMR (CDCl3) δ: 8.81 (s, 1H); 8.15 (s, 1H); 8.03 (d, 1H); 7.99 (s, 1H); 7.46 (d, 1H); 7.45 (d, 1H); 7.20 (d, 1H); 7.10 (s, 1H); 4.6 (br, 1H); 3.98 (s, 3H); 3.7 (br, 2H); 3.5 (br, 1H); 3.05 (s, 2H); 2.99 (hept, 1H); 1.6-2.2 (br, 4H); 1.30 (d, 6H).
실시예 12. 1'-(2-에틸-1H-벤조[d]이미다졸-6-카르보닐)-7-이소프로필스피로[이소크로만-3,4'-피페리딘]-1-온의 합성
4,8-디메톡시-2-나프토산을 2-에틸-1H-벤조[d]이미다졸-6-카르복실산으로 대체하여, 실시예 1과 동일한 절차를 사용하여 실시예 12를 제조하였다. NMR (CDCl3) δ: 7.99 (s, 1H); 7.55(br, 1H); 7.48 (br, 1H); 7.46 (d, 1H); 7.24 (d, 1H); 7.19 (d, 1H); 4.55(br, 1H); 3.7 (br, 1H); 3.5 (br, 2H); 3.04 (s, 2H); 2.99 (hept, 1H); 2.90 (q, 2H); 1.6-2.18 (br, 4H); 1.42 (t, 3H); 1.27 (d, 6H).
실시예 13. 7-이소프로필-1'-(3-메틸-2-옥소-2,3-디히드로-1H-벤조[d]이미다졸-5-카르보닐)스피로[이소크로만-3,4'-피페리딘]-1-온의 합성
4,8-디메톡시-2-나프토산을 3-메틸-2-옥소-2,3-디히드로-1H-벤조[d]이미다졸-5-카르복실산으로 대체하여, 실시예 1과 동일한 절차를 사용하여 실시예 13을 제조하였다. NMR (CDCl3) δ: 9.19 (s, 1H); 8.0 (s, 1H); 7.45 (d, 1H); 7.05-7.2 (m, 4 H); 4.53 (br, 1H); 3.58 (br, 3H); 3.46 (s, 3H); 3.06 (s, 2H); 2.99 (hept, 1H); 2.02(br, 2H); 1.72 (br, 2H); 1.3 (d, 6H).
실시예 14. 메틸 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트의 합성
단계 1. tert-부틸 7-(5-(메톡시카르보닐)피리딘-3-일)-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-카르복실레이트의 제조.
밀봉 튜브에 용매 혼합물 (톨루엔/물/메탄올: 10 ml/1 ml/3 ml) 중의 tert-부틸 7-아이오도-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-카르복실레이트 ( 2.2 g, 4.96 mmol), 5-(메톡시카르보닐)피리딘-3-일)보론산 (2.0 g, 11 mmol), NaHCO3 (2.2 g, 26 mmol), Pd(PPh3)4 (50 mg)를 첨가하였다. 이를 2 hr 동안 90℃에서 가열하였다. 용매 증발 후, 잔류물을 실리카 컬럼에 의해 정제하여 tert-부틸 7-(5-(메톡시카르보닐)피리딘-3-일)-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-카르복실레이트를 백색 고체로서 수득하였다. NMR (CDCl3) δ: 9.26 (s, 1H); 9.07 (s, 1H); 8.55 (d, 1H); 8.42 (s, 1H); 7.86 (d, 1H); 7.42 (d, 1H); 4.03 (s, 3H); 3.85-3.98 (br, 2H); 3.3-3.44 (br, 2H); 3.11 (s, 2H); 1.95-2.04 (br, 2H); 1.65-1.76 (br, 2H); 1.44 (s, 9H).
단계 2. 메틸 5-(1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 히드로클로라이드.
tert-부틸 7-(5-(메톡시카르보닐)피리딘-3-일)-1-옥소스피로[이소크로만-3,4'-피페리딘]-1'-카르복실레이트 (1.7 g)를 에틸 아세테이트 (15 mL) 중에 용해시키고, rt에서 수분 동안 EA (10 mL) 중 4 N HCl로 처리하였다. 반응물을 용매 증발시켜 메틸 5-(1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 히드로클로라이드를 황색 고체로서 수득하였다 (1.6 g).
단계 3. 메틸 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트.
DCM (10 mL) 중의 4,8-디메톡시퀴놀린-2-카르복실산 (0.233 g)의 용액에 옥살릴 클로라이드 (1 mL, 과량)를 실온에서 첨가하고, 생성된 용액을 2 hr 동안 교반하였다. 용매 및 과량의 시약을 증발시켜 상응하는 산 클로라이드를 고체로서 수득하였다.
상기 고체를 0℃에서 냉각시킨 DCM (10 mL) 중의 메틸 5-(1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 히드로클로라이드 (0.4 g), 트리에틸아민 (2 mL)의 혼합물로 전달하였다. 혼합물을 실온에서 30 min 동안 교반한 후, 빙수를 첨가하였다. 수성 층을 DCM (15 mL)으로 추출하고, 합한 유기 상을 MgSO4로 건조시켰다. 용매의 증발 후 조 생성물을 컬럼 정제에 의해 정제하여 메틸 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트를 회백색 고체로서 수득하였다. NMR (CDCl3) δ: 9.23 (s, 1H); 9.03 (s, 1H); 8.52 (s, 1H); 8.38 (s, 1H); 7.85 (d, 1H); 7.75 (d, 1H); 7.4-7.5 (m, 2H); 7.16 (s, 1H); 7.06 (d, 1H); 4.58 (br, 1H); 4.18 (br, 1H); 4.1 (s, 3H); 4.05 (s, 3H); 4.02 (s, 3H); 3.66 (br, 1H); 3.45 (br, 1H); 3.16 (s, 2H); 1.9-2.2 (br, 4H).
실시예 15. 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산의 합성
NaOH의 용액 (2M, 0.5 mL)을 MeOH (5 mL) 중의 메틸 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 (91 mg)의 현탁액에 첨가하였다. 혼합물을 30 min 동안 50℃까지 가열하고, 이 때 모든 고체가 용해되었다. HPLC로부터 출발 물질의 완전한 전환이 확인되었다. 반응 혼합물을 농축 HCl (35%, 0.15 mL)로 중화시키고, 건조물로 증발시켰다. 잔류물을 5 min 동안 4 N HCl/EA 용액 (2 mL)으로 다시 처리하였다. 이 혼합물을 감압 하에 건조물로 증발시켰다. 잔류물을 MeOH/EA (1:1)로 수거하였다. 백색 고체를 여과에 의해 제거하였다. 용매를 증발시키고 아세토니트릴/물로부터 동결건조시켜, 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산을 백색 플러피 고체로서 수득하였다. NMR (DMSO-d6) δ: 9.21 (d, 1H); 9.12 (d, 1H); 8.56 (t, 1H); 8.28 (d, 1H); 8.14 (dd, 1H); 7.76 (d, 1H); 7.63 (t, 1H); 7.62 (d, 1H); 7.41 (s, 1H); 7.40 (d, 1H); 4.28 (br, 1H); 4.17 (s, 3H); 4.02 (s, 3H); 3.3-3.6(br, 3H); 3.30 (s, 2H); 1.8-2.1 (br, 4H).
실시예 16. 1-((에톡시카르보닐)옥시)에틸 5-(1'-(4,8-디메톡시-퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트의 합성
아세톤 (0.8 mL) 중의 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산 (22 mg), 1-클로로에틸 에틸 카르보네이트 (30 uL), Cs2CO3 (126 mg), 및 KI (50 mg)의 현탁액을 40 hr 동안 55℃까지 가열하였다. 조 생성물을 PrepTLC (1:20 MeOH:EA) 정제하여 1-((에톡시카르보닐)옥시)에틸 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트를 동결건조 후 플러피 고체로서 수득하였다. NMR (CDCl3) δ: 9.27 (s, 1H); 9.07 (s, 1H); 8.53 (s, 1H); 8.40 (s, 1H); 7.86 (dd, 1H); 7.81 (d, 1H); 7.50 (t, 1H); 7.47 (d, 1H); 7.21 (s, 1H); 7.11 (d, 1H); 7.10 (q, 1H); 4.6(br, 1H); 4.29 (q, 2H); 4.2 (br, 1H); 4.12 (s, 3H); 4.05 (s, 3H); 3.7 (br, 1H); 3.5 (br, 1H); 3.21 (s, 2H); 1.9-2.2 (m, 4H); 1.74 (d, 3H); 1.36 (t, 3H).
실시예 17. 2-(2-(2-메톡시에톡시)에톡시)에틸 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트의 합성
아세톤 (1.0 mL) 중의 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산 (31 mg), 1-아이오도-2-(2-(2-메톡시에톡시)에톡시)에탄 (75 uL), Cs2CO3 (136 mg)의 현탁액을 18 hr 동안 55℃까지 가열하였다. 조 생성물을 PrepTLC (1:10 MeOH:EA) 정제하여 2-(2-(2-메톡시에톡시)에톡시)에틸 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트를 동결건조 후 플러피 고체로서 수득하였다. NMR (CDCl3) δ: 9.28 (d, 1H); 9.06 (d, 1H); 8.56 (t, 1H); 8.41 (d, 1H); 7.87 (dd, 1H); 7.80 (d, 1H); 7.49 (t, 1H); 7.46 (d, 1H); 7.21 (s, 1H); 7.10 (d, 1H); 4.6 (br, 1H); 4.60(t, 2H); 4.2 (br, 1H); 4.12 (s, 3H); 4.06 (s, 3H); 3.91 (t, 2H); 3.7 (m, 7H); 3.54 (t, 2H); 3.48 (br, 1H); 3.39 (s, 3H); 3.21 (s, 2H); 1.9-2.2 (m, 4H).
실시예 18. 2-(2-메톡시에톡시)에틸 5-(1'-(4,8-디메톡시-퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트의 합성
5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산 (28 mg, 0.05 mmol), 1-브로모-2-(2-메톡시에톡시)에탄 (68 mg, 0.37 mmol), Cs2CO3 (140 mg, 0.43 mmol); KI (40 mg)의 현탁액을 아세톤 (0.8 mL) 중에서 55℃에서 24 hr 동안 가열하였다. 고체를 여과하고, 여액을 증발시켰다. 잔류물을 DCM (~1 mL) 중에 용해시키고, MeOH:EA (3:20)로 용리하며 prepTLC 플레이트 상에 로딩하여, 2-(2-메톡시에톡시)에틸 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트를 백색 고체로서 수득하였다. NMR (CDCl3) δ: 9.28 (d, 1H); 9.06 (d, 1H); 8.56 (t, 1H); 8.41 (d, 1H); 7.87 (dd, 1H); 7.80 (d, 1H); 7.49 (t, 1H); 7.46 (d, 1H); 7.21 (s, 1H); 7.10 (d, 1H); 4.6 (br, 1H); 4.60(t, 2H); 4.2 (br, 1H); 4.12 (s, 3H); 4.06 (s, 3H); 3.91 (t, 2H); 3.74 (t, 2H); 3.5 (br, 1H); 3.61 (t, 2H); 3.48 (br, 1H); 3.41 (s, 3H); 3.20 (s, 2H); 1.9-2.2 (m, 4H).
실시예 19. 메틸 5-(1'-(8-시클로프로필-4-메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트의 합성
메틸 5-(1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 히드로클로라이드 및 8-시클로프로필-4-메톡시퀴놀린-2-카르복실산으로부터 실시예 14와 동일한 방식으로 실시예 19, 메틸 5-(1'-(8-시클로프로필-4-메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트를 제조하였다. NMR (CDCl3) δ: 9.26 (d, 1H); 9.08 (d, 1H); 8.56 (t, 1H); 8.42 (d, 1H); 8.04 (dd, 1H); 7.88 (dd, 1H);7.48 (t, 1H); 7.46 (d, 1H); 7.22 (s, 1H); 7.20 (dd, 1H); 4.67 (br, 1H); 4.5 (br, 1H); 4.12 (s, 3H); 4.03 (s, 3H); 3.79 (m, 1H); 3.5 (m, 1H); 3.2 (s, 2H); 3.09 (m, 1H); 1.9-2.2 (m, 4H); 1.12 (br, 2H); 0.83 (br, 2H).
실시예 20. 5-(1'-(8-시클로프로필-4-메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산의 합성
메틸 5-(1'-(8-시클로프로필-4-메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트로부터 실시예 15와 동일한 방식으로 실시예 20, 5-(1'-(8-시클로프로필-4-메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산을 제조하였다. NMR (DMSO-d6) δ: 9.19 (s, 1H); 9.09 (s, 1H); 8.53 (s, 1H); 8.27 (s, 1H); 8.12 (d, 1H); 7.97 (d, 1H); 7.58 (d, 1H); 7.51 (t, 1H); 7.26 (d, 1H); 7.23 (s, 1H); 4.3 (br, 2H); 4.12 (s, 3H); 3.85 (br, 1H); 3.55 (br, 1H); 3.33 (s, 2H); 3.09 (m, 1H); 1.9 (m, 4H); 1.09 (m, 2H); 0.82 (m, 2H).
실시예 21. 메틸 5-(1'-(1-시클로프로필-4-메톡시-3-메틸-1H-인돌-6-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트의 합성
메틸 5-(1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 히드로클로라이드 및 1-시클로프로필-4-메톡시-3-메틸-1H-인돌-6-카르복실산으로부터 실시예 14와 동일한 방식으로 실시예 21, 메틸 5-(1'-(1-시클로프로필-4-메톡시-3-메틸-1H-인돌-6-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트를 제조하였다. NMR (CDCl3) δ: 9.24 (s, 1H); 9.04 (s, 1H); 8.54 (s, 1H); 8.40 (s, 1H); 7.85 (d, 1H); 7.42 (d, 1H); 7.22 (s, 1H); 6.82 (s, 1H); 6.50 (s, 1H); 4.02 (s, 3H); 3.90 (s, 3H); 3.6 (br, 4H); 3.23 (br, 1H); 3.14 (s, 2H); 2.42 (s, 3H); 1.6-2.1 (br, 4H); 1.0 (m, 4H).
실시예 22. 5-(1'-(1-시클로프로필-4-메톡시-3-메틸-1H-인돌-6-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산의 합성
메틸 5-(1'-(1-시클로프로필-4-메톡시-3-메틸-1H-인돌-6-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트로부터 실시예 15와 동일한 방식으로 실시예 22, 5-(1'-(1-시클로프로필-4-메톡시-3-메틸-1H-인돌-6-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산을 제조하였다. NMR (DMSO-d6) δ: 9.15 (s, 1H); 9.07 (s, 1H); 8.50 (s, 1H); 8.23 (s, 1H); 8.07 (d, 1H); 7.52 (d, 1H); 7.12 (s, 1H); 6.98 (s, 1H); 6.49 (s, 1H); 3.9 (br, 1H); 3.81 (s, 3H); 3.68 (br, 1H); 3.6 (br, 1H); 3.4 (br, 1H); 3.3 (br, 1H); 3.25 (s, 2H); 2.3 (s, 3H); 1.8 (br, 4H), 0.8-1.0 (m, 4H).
제제 실시예 1.
본 개시내용의 화합물을 국소 제제, 예컨대 로션으로 제제화할 수 있다. 예시적 제제를 하기에 제시하였다:
제제 #1: (w/w%)
제제 #2: (w/w%)
생물학적 실시예 1. 마우스 ACC 효소 활성 검정
카르복실라제 도메인에서의 비오티닐화를 이용하여 ACC 단백질을 정제하였다. CO2 흡입 방법을 사용하여 8-12주령의 수컷 C57BL/6J 마우스 (잭슨 래보러토리(Jackson Laboratory))를 안락사시키고, 간을 드라이 아이스 상에서 즉시 동결시켰다. 100 mg 간에 1 mL 빙냉 조직 용해 완충제 (20 mM 트리스(Tris)-HCl pH 7.5, 150 mM NaCl, 1 mM Na2EDTA, 1 mM EGTA, 1% 트리톤(Triton), 2.5 mM 나트륨 피로포스페이트, 1 mM β-글리세로포스페이트, 1 mM Na3VO4, 1 μg/mL 류펩틴, 1 정제의 프로테아제 억제제 칵테일 (로슈(Roche))/10 mL 용해 완충제)를 첨가한 후 파워 겐(Power Gen) 125 균질화기 (피셔 사이언티픽(Fisher Scientific))로 아이스 상에서 균질화시켰다. 아이스 상에서 30 min 인큐베이션 후, 조직 용해물을 18 ½ G 니들로 10 mL 시린지를 통해 10회 통과시켜 DNA 전단을 수행하였다. 이어서, 880 mg 황산암모늄 분말 (시그마)을 아이스 상에서 교반하며 10 min 내에 10 mL 간 용해물에 첨가함으로써 용해물을 17.5% - 35% 포화 황산암모늄 침전에 적용하였다. 샘플을 4℃에서 10 min 동안 14,000 rpm으로 원심분리하고 (에펜도르프(Eppendorf)), 880 mg 황산암모늄 분말을 아이스 상에서 교반하며 10 min 내에 10 ml 상청액에 첨가함으로써 추가 정제를 위해 상청액을 저장하였다. 샘플을 4℃에서 10 min 동안 14,000 rpm으로 원심분리하였다. 상청액을 폐기하고, 펠릿을 10 mL 샘플 완충제 (100 mM 트리스-HCl, pH 7.5, 1 mM EDTA, 0.1 mM DTT, 0.5 M NaCl, 및 5% 글리세롤) 중에 용해시켰다. 이어서, 샘플을 1 mL의 스트렙 맥(Strep Mag) 비드 슬러리 (젠스크립트(Genscript))와 함께 첨가하고, 4℃에서 1시간 동안 회전시켰다. 상청액을 폐기하고, 비드를 샘플 완충제로 3회 세척하였다. 이어서, 샘플 완충제 중에서 제조된 10 mL의 2 mM 비오틴 (프로메가(Promega))을 첨가함으로써 단백질을 용리하였다. 이어서, 200 mL 투석 완충제 (50 mM HEPES, pH 7.5, 0.1 mM DTT, 1.0 mM EDTA, 및 10% 글리세롤)의 3회 변화에 대하여 슬라이드-에이-라이저(Slide-A-Lyzer)™ 투석 카세트 10K MWCO (써모 피셔 사이언티픽(Thermo Fisher Scientific))를 사용함으로써 용리액을 4℃에서 1시간 동안 투석하였다. 이어서, BCA 단백질 검정 키트 (피어스(Pierce))를 사용하여 총 단백질 농도를 정량화하였다.
ACC 효소 활성 검정을 위해, 이중으로 DMSO 중에서 제조된 1 μL 연속 희석 화합물을 37℃에서 10 min 동안 8 μL 투석 샘플과 혼합하였다. 91 μL의 반응 완충제 (50 mM HEPES pH 7.5, 10 mM MgCl2, 2.0 mM DTT, 0.5 mM 아세틸-CoA, 4.0 mM ATP, 15 mM 13C-NaHCO3, 0.75 mg/mL BSA, 0.5 mM 시트르산나트륨)를 튜브에 첨가하고, 철저히 혼합하였다. 37℃에서 1시간 동안 인큐베이션 후, 300 μL 빙냉 켄칭 완충제 (아세토니트릴:메탄올 = 1:1, 내부 표준물로서의 20 μM 카르부타미드)를 각각의 튜브에 첨가하고, 잘 혼합하여 반응을 종결시켰다. 샘플을 10 min 동안 14,000 rpm으로 원심분리하고 (에펜도르프), 말로닐-13C-CoA의 정량화를 위해 상청액을 LC-MS/MS 상으로 로딩하였다 (Gao et al., Journal of chromatography B, Analytical technologies in the biomedical and life sciences 853, 303-313 (2007)).
생물학적 실시예 2. 인간 ACC 효소 활성 검정
정제된 인간 ACC1 및 ACC2 단백질 (비피에스 바이오사이언시스(BPS Bioscience))을 사용하여 인간 ACC 효소 활성 검정을 수행하였다. ACC1 및 ACC2 단백질을 24.5 μL 반응 완충제 (50 mM HEPES pH 7.5, 10 mM MgCl2, 2.0 mM DTT, 4.0 mM ATP, 15 mM 13C-NaHCO3, 0.75 mg/mL BSA, 0.5 mM 시트르산나트륨) 중에 희석하였고, ACC1 및 ACC2의 최종 농도는 0.4 μg/mL 및 0.48 μg/mL였다. 각각의 반응에 대하여, 0.5 μL의 연속 희석 화합물을 이중 또는 삼중으로 DMSO 중에서 제조하였고, 37℃에서 10 min 동안 ACC 단백질을 갖는 상기 24.5 μL 반응 혼합물과 혼합하였다. 한편, 25 μL의 반응 완충제 플러스 아세틸-CoA (최종 농도: 5 μM)를 신선하게 제조하고, 상기 25 μL 혼합물에 첨가하여 반응을 개시하였다. 37℃에서 1-2시간 동안 인큐베이션 후, 말로닐-13C3- CoA (최종 농도: 40 nM, 시그마-알드리치)를 갖는 100 μL 빙냉 10% TCA를 첨가하여 반응을 종결시켰다. LC-MS/MS 분석을 위해, 300 μL 켄칭 완충제 (아세토니트릴:메탄올 = 1:1, 내부 표준물로서 20 μM 카르부타미드)를 각각의 튜브에 첨가하고, 잘 혼합하였다. 이어서, 샘플을 10 min 동안 14,000 rpm으로 원심분리하고 (에펜도르프), 말로닐-13C-CoA의 정량화를 위해 상청액을 LC-MS/MS 상으로 로딩하였다 (Gao et al., Journal of chromatography B, Analytical technologies in the biomedical and life sciences 853, 303-313 (2007)).
생물학적 실시예 3. LC-MS/MS에 의한 말로닐-CoA의 정량화
시마쯔(Shimadzu) LC 시스템을 샘플 분석에 사용하였고, 이는 시스템 컨트롤러 (시마쯔 CBM-20A), 오토샘플러 (시마쯔 SIL-20A), 펌프 A 및 B (시마쯔 LC-20AD), 컬럼 오븐 (시마쯔 CTO-20A), 및 분석 컬럼 (페노메넥스 제미니(Phenomenex Gemini) 5u C18 11A, 100 × 2 mm)으로 이루어졌다. LC를 이동 상 A (5 mM 아세트산암모늄 및 5 mM DMBA (물 중) (1,3-디메틸부틸아민)) 및 B (메탄올)로 2원 구배 모드로 200 μL/min으로 진행시켰다. 샘플을 AB 시엑스(Sciex) QTrap4000 LC-MS/MS 삼중 사중극자 질량 분광계 (어플라이드 바이오시스템즈(Applied Biosystems)) 상에서 분석하였다. 말로닐-CoA 및 말로닐-13C-CoA를 각각 854.2/347.1 및 855.1/246.1에서의 MRM 전이에 따라 양이온 모드로 모니터링하였다. 생성물 및 내부 표준물을 50% H2O, 25% MeCN, 25% 아세톤, 및 5 mM 아세트산암모늄으로 3 s 내에 질량 분광계에 대하여 공동용리시켰다. 이온 크로마토그램을 아날리스트(Analyst) 1.5.2 소프트웨어를 사용하여 적분하였다. 피크 면적 비율을 표준 곡선에 대하여 비교하고, 말로닐-CoA의 최종 세포 농도 또는 말로닐-13C-CoA의 생성 속도를 pmoles/mg 단백질/분으로서 계산하였다.
생물학적 실시예 4. 인간 피지세포에서의 말로닐-CoA의 세포 수준에 대한 ACC 억제제의 효과
인간 피지세포 (셀프로겐(Celprogen))를, 100% 전면생장률까지 5% CO2로 보충된 가습 물 재킷화된 인큐베이터 (포르마 사이언티픽(Forma Scientific)) 내에서 37℃에서 성장 배지 (4.5 g/L 글루코스, 0.584 g/L L-글루타민 (시그마), 100 단위/mL의 페니실린 및 100 μg/mL의 스트렙토마이신 (깁코(Gibco)), 10% 소 태아 혈청 (깁코)을 갖는 DMEM)에서 성장시켰다. 152 cm2 세포 배양 디쉬 (코닝(Corning)) 내에서 성장된 세포를 0.25% 트립신-EDTA (깁코)로 트립신처리하고, 10 min 동안 800 rpm으로 원심분리하고 (에펜도르프), 4 mL 성장 배지 중에 재현탁시켰다. DMSO 중의 1 μL 연속 희석 화합물에, 99 μL 세포 (성장 배지 중에 현탁된 약 0.5백만 세포)를 첨가하고, 잘 혼합한 후, 30 min 동안 세포 배양 인큐베이터 내에서 인큐베이션하였다. 이어서, 세포를 10 min 동안 800 rpm으로 원심분리하고, 70 μL 10% 트리클로로아세트산을 각각의 웰에 첨가하여 세포를 용해시키고 단백질을 침전시켰다. 말로닐-CoA의 세포 수준을 LC-MS/MS에 의해 정량화하였다.
생물학적 실시예 5. 인간 피지세포의 지질생성에 대한 ACC 억제제의 효과
인간 피지세포 (셀프로겐)를, 100% 전면생장률까지 성장 배지를 갖는 콜라겐-코팅된 96-웰 배양 마이크로플레이트 (화이트/클리어 저부, 코닝 바이오코트(Corning BioCoat)) 내에서 성장시켰다. 배양 배지를 성장 배지 플러스 DMSO 중에서 제조된 화합물을 갖는 100 μM 아라키돈산 (시그마) 및 10 μM 로시글리타존 (토크리스(Tocris)) (성장 배지 중 1:1000 희석)으로 교체하였다. 세포를 48시간 후 교체된 화합물을 함유하는 배지로 96시간 동안 화합물로 처리하였다. 처리 완료시, 세포를 200 μL 인산염 완충 식염수 (PBS)로 세척하고, 이어서 100 μL 4% 포름알데히드 (시그마)를 첨가함으로써 고정시키고, 실온에서 1시간 동안 인큐베이션하였다. 이어서, 세포를 PBS로 3회 세척하였다. 마이크로플레이트를, 37℃에서 1시간 동안 인큐베이션함으로써 PBS 중에서 제조된 100 μL 나일 레드 용액 (2 mg/mL, 1:400 희석)으로 염색하고, 이어서 PBS로 3회 세척하였다. 형광을 Ex 492 nm 및 Em 595 nm에서 판독하였다 (테칸 스펙트로플루오르플러스(TECAN SpectrofluorPlus)). 피지세포에서의 지질생성에 대한 화합물의 효과를 DMSO 비히클 대조군에 대한 %로 계산하였다.
생물학적 실시예 6. 인간 피지세포 및 각질세포의 증식에 대한 ACC 억제제의 효과
인간 피지세포 (셀프로겐) 및 각질세포 (ATCC)를 약 50% 전면생장률까지 성장 배지를 갖는 96-웰 배양 마이크로플레이트 (코닝) 내에서 성장시켰다. 배지를 DMSO 중의 연속 희석 화합물 (1:1000 희석)과 혼합된 성장 배지로 교체하였다. 24시간 동안 처리 후, 배지를 100 μL 페놀 레드 무함유 DMEM으로 교체하고, 비브란트(Vybrant)® MTT 세포 증식 검정 키트 (몰레큘라 프로브스(Molecular Probes))를 사용하여 세포 수를 정량화하였다. 10 μL의 12 mM MTT 모액을 각각의 웰에 첨가하고, 마이크로플레이트를 37℃에서 4시간 동안 인큐베이션하였다. 이어서, 100 μL의 SDS-HCl 용액을 각각의 웰에 첨가하고, 피펫을 사용하여 철저히 혼합하였다. 마이크로플레이트를 세포 배양 인큐베이터 내에서 37℃에서 4시간 동안 인큐베이션하였다. 마이크로플레이트를 피펫을 사용하여 다시 혼합하고, 흡광도를 570 nm에서 판독하였다 (다이넥스(Dynex) MRXe 마젤란 바이오사이언시스(Magellan Biosciences)). 인간 각질세포의 증식에 대한 화합물의 효과를 DMSO 비히클 대조군에 대한 %로 계산하였다.
생물학적 실시예 7. 3T3-L1 지방세포의 지질생성에 대한 ACC 억제제의 효과
3T3-L1 섬유모세포 세포 (젠-바이오(Zen-Bio))를 약 90-100% 전면생장률까지 성장 배지를 갖는 96-웰 배양 마이크로플레이트 (코닝) 내에서 성장시켰다. 배양 배지를 분화 배지 (3-이소부틸-1-메틸크산틴 500 μM, 덱사메타손 1 μM, 인슐린 10 μg/mL, 및 로시글리타존 2 μM 보충된 성장 배지) 플러스 DMSO 중에서 제조된 연속 희석 화합물 (1:1000 희석)로 교체하였다. 2일 동안 인큐베이션 후, 배지를 유지 배지 (인슐린 10 μg/mL 보충된 성장 배지) 플러스 DMSO 중에서 제조된 연속 희석 화합물 (1:1000 희석)로 2일마다 배지를 교체하며 약 1주 동안 교체하였다. 처리 완료시, 배양 배지를 폐기하고, 200 μL 0.01% SDS를 각각의 웰에 첨가하고, 1시간 동안 진탕시켜 세포를 용해시켰다. 이어서, 세포 용해물을 400 μL 폴츠 용액 (클로로포름:메탄올 = 2:1)으로 전달하고 잘 혼합하였다. 20 min 동안 2,000 rpm으로 원심분리 후, 200 μL의 저부 유기 상을 10 μL 샘플 완충제 (클로로포름:트리톤-100 = 3:1)를 갖는 플레이트로 전달하였다. 샘플을 질소 하에 블로잉 건조시키고, 200 μL 트리글리세리드 (TG) 정량화 시약 (써모 피셔 사이언티픽)을 첨가하고, 혼합하고, 37℃에서 30 min 동안 인큐베이션하였다. TG 농도를 535 nm에서의 흡광도를 판독함으로써 측정하고 (다이넥스 MRXe 마젤란 바이오사이언시스) 표준 곡선으로부터 계산하였다.
생물학적 실시예 8. 인간 피부 조직에 대한 IHC 염색
인간으로부터의 피부 조직의 포르말린-고정, 파라핀-임베딩된 슬라이드 (암스바이오(Amsbio) 및 프로사이(ProSci))를 65℃에서 30 min 동안 베이킹하고, 각각 5 min 동안 크실렌으로의 3회 세척, 각각 10 min 동안 100% 에탄올로의 2회 세척, 각각 10 min 동안 95% 에탄올로의 2회 세척, 및 마지막으로 각각 5 min 동안 dH2O 중에서의 2회 세척으로 인큐베이션함으로써 파라핀제거/수화시켰다. 이어서, 슬라이드를 1× 항원 언마스킹 용액 (벡터 래보러토리즈(Vector Laboratories)) 중에서 10 min 동안 비등시켰다. dH2O 중에서 세척 후, 슬라이드를 실온에서 1시간 동안 또는 4℃에서 밤새 토끼 IgG 이소타입 대조군 항체 또는 토끼 모노클로날 항-ACC (18 μg/mL, 1:50 희석, 셀 시그널링 테크놀로지(Cell Signaling Technology))로 염색하였다. 이어서, 섹션을 각각 5 min 동안 세척 완충제로 3회 세척하고, 래빗 온 로덴트 에이치알피-폴리머(Rabbit on Rodent HRP-Polymer) (바이오케어 메디칼((BioCare Medical)) 및 디에이비 퀀토 크로마겐 앤 서브스트레이트(DAB Quanto Chromagen and Substrate) (써모 피셔 사이언티픽)를 사용하여 암갈색을 발색시켜 ACC 단백질의 발현을 드러내었다. 슬라이드를 헤마톡실린 (리카 케미칼(RICCA Chemical))로 대비염색하고, 탈수시키고, 벡타마운트(VectaMount) (벡터 래보러토리즈)를 사용하여 커버슬립으로 밀봉하였다. 자이스 프리모 스타(Zeiss Primo Star) 및 니콘(Nikon) D800을 사용하여 사진을 얻었다.
인간 피부의 상기 연구에서 표피, 진피, 및 피하조직의 층을 포함한 인간 정상 피부 구조의 IHC 염색의 이미지 분석은, ACC 단백질이 피지선에서 풍부하게 특이적으로 발현됨을 제시한다. 이는 인간 피부 구조에서의 ACC 단백질의 국소화에 대한 최초 보고를 나타내고, 이는, ACC 억제제의 국소 투여 등에 의한 피지세포로의 ACC 억제제의 전달이, 피지선에서의 ACC를 특이적으로 억제하고, 그에 따라 지질 축적 및 피지세포에서의 지질의 과다생성과 관련된 질환의 진행을 억제하는 강력한 방법을 제공함을 시사한다.
반면, 인간 정상 피부의 IHC 염색의 이미지는, ACC 단백질이 인간 정상 피부의 각질세포에서는 풍부하게 발현되지 않음을 제시한다.
피지선을 포함한 인접 피부 조직과의 인간 계내 편평 세포 암종의 IHC 염색의 이미지는, 편평 세포 암종의 종양 세포, 피지선 및 표피 편평 세포가 유사한 밀도의 어두운 색으로 염색됨을 제시하며, 이는 ACC 단백질의 풍부한 발현을 나타낸다.
마지막으로, 인간 지루성 각화증의 IHC 염색의 이미지에서는, 각질 층이 이 질환에서 명백하며, 각질 층 바로 옆의 각질세포는 어두운 색으로 염색되고, 이는 각화증의 피부 질환에서 각질세포에서의 ACC 단백질의 풍부한 발현을 나타낸다.
생물학적 실시예 9. 햄스터의 피부 조직의 오일 레드 O 염색
8-12주령의 수컷 햄스터를, 좌측 귀에는 비히클로, 또한 우측 귀에는 화합물로, QD로 14일 동안 귀에 로션을 적용함으로써, 비히클 또는 화합물 (비히클 중 0.01, 0.05, 및 0.1%)로 처리한다 (n = 4). CO2 흡입 사용에 의한 안락사 후, 귀를 O.C.T. 화합물 상에 마운팅하고, 5 μm로 동결 절단한다 (레이카(Leica) CM1900). 제공업체 (아브캠(Abcam))로부터의 지시에 따라 오일 레드 O 키트를 사용하여 슬라이드를 염색한다. 슬라이드를 변형된 마이어스 헤마톡실린(Modified Mayer's Hematoxylin) (아메리칸 마스터테크 사이언티픽(American MasterTech Scientific))으로 대비염색하고, 아쿠아-마운트(Aqua-Mount) (러너 래보러토리즈(Lerner Laboratories))로 밀봉한다. 이미지제이(ImageJ) (NIH)를 사용하여 지질 액적 염색 면적을 정량화한다.
생물학적 실시예 10. 마우스 및 햄스터에서의 생체내 PK/PD 연구
조직 PK/PD. 8-12주령의 수컷 C57BL/6 마우스를, 등 피부에 로션을 적용함으로써, 비히클 또는 화합물 (비히클 중 0.01, 0.05, 및 0.1%)로 처리하였다 (n = 5). 처리 후 10, 30, 60, 180, 360, 및 1440 min에 CO2 흡입을 사용하여 동물을 안락사시키고, 화합물 및 말로닐-CoA의 수준을 측정하기 위해 피부를 채취하였다. 약 100 mg 중량의 피부를 200 μL 10% TCA 중에서 균질화시키고, 10 min 동안 14,000 rpm으로 원심분리하였다. 화합물 및 말로닐-CoA의 정량화를 위해 상청액 (10 μL)을 LC/MS에 로딩하였다.
표준 PK. 수컷 카테터삽입 CD-1 마우스를, IV에 대해 1 mg/kg (5 mL/kg) 또는 PO에 대해 5 mg/kg (10 mL/kg)의 용량으로 비히클 (5% DMSO + 10% 솔루톨(Solutol) + 85% PBS, PH = 7.4) 중에서 제조된 화합물 6으로 처리하였다. 혈액 샘플 (20 μL)을 투여 후 0.083, 0.25, 0.5, 1, 2, 4, 8, 및 24 hr에 수집하고, 60 μL 0.1 M 시트르산나트륨과 혼합하였다. 아세토니트릴 사용에 의한 추출에 따라, 화합물 6의 혈액 농도를 LC-MS/MS에 의해 정량화하였다. 윈놀린(WinNonlin)® 6.4를 사용하여 PK 파라미터를 계산하였다.
생물학적 실시예 11. 화합물 실시예 14 및 15에 대한 마우스에서의 PK 연구
수컷 C57 마우스로 약동학 연구를 수행하였다. 화합물 (실시예 14 및 실시예 15)을 각각 5% DMSO + 10% 솔루톨 HS 15 + 85% 식염수 중에서 제제화하고, IV 주사에 대해 1 mpk (5 mL/kg) 및 경구 위관영양에 대해 10 mpk (10 mL/kg)로 투여하였다. 다양한 시점의 혈장 샘플을 LC-MS로 정량화하였다. 기록된 데이터는 3마리 마우스의 평균이었다.
하기 표 1 및 2는, 각각, 1 mpk IV 주사 및 10 mpk PO 위관영양 후 수컷 C57 마우스에서의 실시예 14의 혈장 농도 (ng/mL) 및 PK 파라미터를 제시한다. 산 화합물, 실시예 15의 혈장 농도 (ng/mL)를 또한 측정하고 하기에 기록하였다.
표 1. 1 mpk IV 주사 후 수컷 C57 마우스에서의 실시예 14의 혈장 농도 (ng/mL) 및 PK 파라미터
표 2. 10 mpk PO 위관영양 후 수컷 C57 마우스에서의 실시예 14의 혈장 농도 (ng/mL) 및 PK 파라미터
하기 표 3 및 4는, 각각, 1 mpk IV 주사 및 10 mpk PO 위관영양 후 수컷 C57 마우스에서의 실시예 15의 혈장 농도 (ng/mL) 및 PK 파라미터를 제시한다.
표 3. 1 mpk IV 주사 후 수컷 C57 마우스에서의 실시예 15의 혈장 농도 (ng/mL) 및 PK 파라미터
표 4. 10 mpk PO 위관영양 후 수컷 C57 마우스에서의 실시예 15의 혈장 농도 (ng/mL) 및 PK 파라미터
생물학적 실시예 12. C57BL/6J 마우스에서의 간 트리글리세리드의 감소를 위한 ACC 억제제로의 만성 치료
약 9주령의 수컷 C57BL/6J 마우스 (잭슨 래보러토리)를 비히클 (0.5% 메틸셀룰로스 또는 PEG400) 또는 실시예 14 (30 mg/킬로그램 체중, PEG400 중에서 제조된 투여 용액) 및 실시예 20 (20 mg/킬로그램 체중, 0.5% 메틸셀룰로스 중에서 제조된 투여 용액)으로 경구 위관영양에 의해 2주 동안 1일 1회 ~9:00 am에 처리하였다. 실시예 14 및 실시예 20의 농도는 각각 15 mg/ml 및 2 mg/ml였다. 실시예 14 및 실시예 20의 투여 부피는 각각 2 ml/킬로그램 체중 및 10 ml/킬로그램 체중이었다. 14일 처리 후, 동물을 투여 후 2시간에 CO2로 안락사시키고, 간을 동결시키고 드라이 아이스 상에서 유지하였다. 클로로포름:메탄올 2:1 (v/v)로의 지질 추출 후 인피니티(Infinity)™ 트리글리세리드 시약 (써모 사이언티픽)으로의 정량화에 의해 에 간 TG를 측정하였다.
도 1에 제시된 결과는, 실시예 14 및 20 둘 다 C57BL/6J 마우스에서 간 TG를 감소시켰음을 나타낸다.
표 5. 일부 실시예에 대한 데이터
표 5의 데이터는 본 출원에 개시된 방법 및/또는 관련 기술분야에 공지된 표준 기술에 따라 얻었다. ACC 효소 활성은 생물학적 실시예 1 및 2에 따라 측정하였고; 피지세포에서의 말로닐-CoA는 생물학적 실시예 4에 따라 측정하였고; 3T3-L1 지방세포에 대한 지질생성의 효과는 생물학적 실시예 7에 따라 측정하였고; 피지세포의 지질생성에 대한 효과는 생물학적 실시예 5에 따라 측정하였고; 피지세포의 증식에 대한 효과는 생물학적 실시예 6에 따라 측정하였고; 마우스 PK는 생물학적 실시예 10에 따라 측정하였고; 혈장 단백질 결합 (인간 또는 마우스)은 표준 기술에 의해 측정하였다.
개요 및 요약 섹션이 아닌, 상세한 설명 섹션은 청구범위를 해석하기 위해 사용되는 것으로 의도됨을 인지하여야 한다. 개요 및 요약 섹션은 본 발명자(들)에 의해 고려되는 본 발명의 하나 이상의 (그러나 모두는 아님) 예시적 실시양태를 기재할 수 있고, 따라서, 본 발명 및 첨부된 청구범위를 어떠한 방식으로든 제한하도록 의도되지 않는다.
본 발명은 특정된 기능 및 그의 관계의 실행을 나타내는 기능적 구성 요소의 도움으로 기재되었다. 이들 기능적 구성 요소의 경계는 설명의 편의를 위해 본원에서 임의로 정의되었다. 특정된 기능 및 그의 관계가 적절히 수행되는 한 대안적 경계가 정의될 수 있다.
속으로 기재된 본 발명의 측면에 대하여, 모든 개개의 종이 개별적으로 본 발명의 별도의 측면으로 고려된다. 본 발명의 측면이 특징을 "포함하는" 것으로 기재되는 경우, 실시양태는 또한 그 특징으로 "이루어진" 또는 "본질적으로 이루어진" 것으로 고려된다.
구체적 실시양태의 상기 설명은, 다른 자들이, 관련 기술분야의 기술 내의 지식을 적용함으로써, 본 발명의 일반적 개념으로부터 벗어나지 않으면서, 과도한 실험 없이, 이러한 구체적 실시양태를 다양한 응용을 위해 쉽게 변형 및/또는 적합화할 수 있도록 본 발명의 일반적 성질을 충분히 드러낼 것이다. 따라서, 이러한 적합화 및 변형은, 본원에 제시된 교시 및 지침에 기초하여, 개시된 실시양태의 의미 및 등가물의 범위 내에 포함되도록 의도된다. 본원에서의 어구 또는 용어는 설명을 위한 것이며 제한을 위한 것은 아니고, 따라서 본 명세서의 용어 또는 어구는 교시 및 지침에 비추어 관련 기술분야의 통상의 기술자에 의해 해석되어야 함을 이해하여야 한다.
본 발명의 범주 및 범위는 상기에 기재된 예시적 실시양태 중 임의의 것에 의해 제한되지 않아야 하며, 단지 하기 청구범위 및 그의 등가물에 따라 정의되어야 한다.
본원에 기재된 모든 다양한 측면, 실시양태, 및 옵션은 임의의 및 모든 변경으로 조합될 수 있다.
본 명세서에서 언급된 모든 공개, 특허, 및 특허 출원은, 각각의 개별적 공개, 특허, 또는 특허 출원이 참조로 포함된다고 구체적 및 개별적으로 지시되는 것과 동일한 정도로 본원에 참조로 포함된다. 본원에서 용어의 임의의 의미 또는 정의가 참조로 포함된 문헌에서의 동일한 용어의 임의의 의미 또는 정의와 상충되는 경우, 본원에서 그 용어에 주어진 의미 또는 정의가 지배적일 것이다.
Claims (36)
- 화학식 Ia의 화합물, 또는 그의 제약상 허용되는 염:
여기서
R1은 수소, 할로겐, 시아노, 임의로 치환된 C1-6 알킬, 임의로 치환된 C3-6 시클로알킬, 임의로 치환된 C2-6 알케닐, 임의로 치환된 C2-6 알키닐, 임의로 치환된 C6-10 아릴, 임의로 치환된 5-10원 헤테로아릴, 임의로 치환된 4-6원 헤테로시클릴, NR10R11, COOR12, CONR13R14, CN, S(O)nR15, 또는 OR16이고;
여기서
R10 및 R11은 각각 독립적으로 수소, 임의로 치환된 C1-6 알킬, 임의로 치환된 C3-6 시클로알킬, 임의로 치환된 C1-6 알카노일, 임의로 치환된 C3-6 시클로알카노일, 임의로 치환된 C6-10 아릴, 임의로 치환된 5-10원 헤테로아릴, 임의로 치환된 4-6원 헤테로시클릴, COOR12, 또는 CONR13R14이고;
R12, R13 및 R14는 각각 독립적으로 수소 또는 임의로 치환된 C1-6 알킬이고;
n은 0, 1, 또는 2이고;
R15는 임의로 치환된 C1-6 알킬, 임의로 치환된 C3-6 시클로알킬, 또는 NR10R11이고;
R16은 수소, 임의로 치환된 C1-6 알킬, 임의로 치환된 C3-6 시클로알킬, 임의로 치환된 C1-6 알카노일, 임의로 치환된 C3-6 시클로알카노일, 임의로 치환된 C6-10 아릴, 임의로 치환된 5-10원 헤테로아릴, 임의로 치환된 4-6원 헤테로시클릴 또는 CONR13R14이고;
R3은 임의로 치환된 C6-10아릴 또는 임의로 치환된 5 내지 10원 헤테로아릴이며,
단, R1이 수소인 경우, R3은 임의로 치환된 페닐이 아니다. - 제2항에 있어서, R10 및 R11 중 하나가 임의로 치환된 5 또는 6원 헤테로아릴인 화합물, 또는 그의 제약상 허용되는 염.
- 제2항에 있어서, R10 및 R11 중 하나가, 할로겐, 시아노 및 C1-4 알킬로부터 독립적으로 선택된 1 또는 2개의 치환기로 임의로 치환된, 2-4개의 고리 질소 원자를 갖는 5원 헤테로아릴인 화합물, 또는 그의 제약상 허용되는 염.
- 제2항에 있어서, R10 및 R11 중 하나가 C1-4 알킬로 각각 임의로 치환된 피라졸릴, 트리아졸릴 또는 테트라졸릴인 화합물, 또는 그의 제약상 허용되는 염.
- 제1항에 있어서, R1이 임의로 치환된 5 또는 6원 헤테로아릴인 화합물, 또는 그의 제약상 허용되는 염.
- 제7항에 있어서, R1이 임의로 치환된 테트라졸릴 또는 피리디닐인 화합물, 또는 그의 제약상 허용되는 염.
- 제7항에 있어서, R1이 카르복실산 기 또는 생체내에서 카르복실산 기 또는 그의 염으로 전환될 수 있는 기로 임의로 치환된 피리디닐인 화합물, 또는 그의 제약상 허용되는 염.
- 제10항에 있어서, R20이 임의로 치환된 C1-6 알킬 (예를 들어, 임의로 치환된 C1-4 알킬)인 화합물, 또는 그의 제약상 허용되는 염.
- 제10항에 있어서, R20이 수소 또는 C1-4 알킬인 화합물, 또는 그의 제약상 허용되는 염.
- 제1항 내지 제14항 중 어느 한 항에 있어서, R3이 할로겐, 히드록실, 시아노, 임의로 치환된 C1-4 알킬, 임의로 치환된 C1-4 알콕시, 임의로 치환된 C3-6 시클로알킬, 및 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1 내지 3개의 치환기로 임의로 치환된 C6-10아릴인 화합물, 또는 그의 제약상 허용되는 염.
- 제1항 내지 제14항 중 어느 한 항에 있어서, R3이 임의로 치환된 8-10원 비시클릭 헤테로아릴인 화합물, 또는 그의 제약상 허용되는 염.
- 제1항 내지 제14항 중 어느 한 항에 있어서, R3이 할로겐, 시아노, 히드록실, 1-3개의 할로겐으로 임의로 치환된 C1-4 알킬, 1-3개의 할로겐으로 임의로 치환된 C1-4 알콕시, 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알킬, 및 1-3개의 할로겐으로 임의로 치환된 C3-6 시클로알콕시로부터 독립적으로 선택된 1개 이상의 (예를 들어, 1-3개의) 치환기로 각각 임의로 치환된 나프틸, 벤즈이미다졸릴, 피롤로피리디닐, 피라졸로피리디닐, 인다졸릴, 인돌릴, 퀴놀리닐 또는 이소퀴놀리닐인 화합물, 또는 그의 제약상 허용되는 염.
- 제1항에 있어서, 화합물이 1'-(4,8-디메톡시-2-나프토일)-7-이소프로필스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 1), 1'-(4,8-디메톡시퀴놀린-2-카르보닐)-7-이소프로필스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 2), 1'-(4,8-디메톡시-2-나프토일)-7-에틸스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 3), 1'-(4,8-디메톡시퀴놀린-2-카르보닐)-7-에틸스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 4), 1'-(4,8-디메톡시-2-나프토일)-7-((1-메틸-1H-피라졸-5-일)아미노)스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 5), 1'-(4,8-디메톡시퀴놀린-2-카르보닐)-7-((1-메틸-1H-피라졸-5-일)아미노)스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 6), 7-이소프로필-1'-(2-메틸-1H-벤조[d]이미다졸-6-카르보닐)스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 7), 1'-(1H-인다졸-5-카르보닐)-7-이소프로필스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 8), 7-이소프로필-1'-(1H-피롤로[3,2-b]피리딘-2-카르보닐)-스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 9), 1'-(1H-인다졸-6-카르보닐)-7-이소프로필스피로-[이소크로만-3,4'-피페리딘]-1-온 (실시예 10), 7-이소프로필-1'-(6-메톡시퀴놀린-3-카르보닐)스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 11), 1'-(2-에틸-1H-벤조[d]이미다졸-6-카르보닐)-7-이소프로필스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 12), 7-이소프로필-1'-(3-메틸-2-옥소-2,3-디히드로-1H-벤조[d]이미다졸-5-카르보닐)스피로[이소크로만-3,4'-피페리딘]-1-온 (실시예 13), 메틸 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 (실시예 14), 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산 (실시예 15), 1-((에톡시카르보닐)옥시)에틸 5-(1'-(4,8-디메톡시-퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 (실시예 16), 2-(2-(2-메톡시에톡시)에톡시)에틸 5-(1'-(4,8-디메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 (실시예 17), 2-(2-메톡시에톡시)에틸 5-(1'-(4,8-디메톡시-퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 (실시예 18), 메틸 5-(1'-(8-시클로프로필-4-메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 (실시예 19), 5-(1'-(8-시클로프로필-4-메톡시퀴놀린-2-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산 (실시예 20), 메틸 5-(1'-(1-시클로프로필-4-메톡시-3-메틸-1H-인돌-6-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코티네이트 (실시예 21), 또는 5-(1'-(1-시클로프로필-4-메톡시-3-메틸-1H-인돌-6-카르보닐)-1-옥소스피로[이소크로만-3,4'-피페리딘]-7-일)니코틴산 (실시예 22)인 화합물, 또는 그의 제약상 허용되는 염.
- 제1항 내지 제20항 중 어느 한 항의 화합물, 또는 그의 제약상 허용되는 염, 및 제약상 허용되는 부형제를 포함하는 제약 조성물.
- 아세틸-CoA 카르복실라제 (ACC1 및/또는 ACC2) 활성, 말로닐-CoA 생성, 지질생성, 피지세포의 증식, 각질세포의 증식, 표피, 진피, 및/또는 피하조직에서의 세포 (예를 들어, 지방세포, 멜라닌세포, 각질세포, 편평 세포, 메르켈 세포, 랑게르한스 세포, 및 피부 줄기 세포)의 증식, 피부 및/또는 피하 층에서의 섬유모세포의 지방세포로의 분화, 염증, 및 이들의 조합으로부터 선택된 하나 이상의 활성의 억제를 필요로 하는 대상체에게 치료 유효량의 제1항 내지 제20항 중 어느 한 항의 화합물, 또는 그의 제약상 허용되는 염, 또는 제21항의 제약 조성물을 투여하는 것을 포함하는, 상기 대상체에서 상기 하나 이상의 활성을 억제하는 방법.
- 비정상적 피지세포 및/또는 각질세포 활성과 연관된 질환 또는 장애의 치료를 필요로 하는 대상체에게 치료 유효량의 제1항 내지 제20항 중 어느 한 항의 화합물, 또는 그의 제약상 허용되는 염, 또는 제21항의 제약 조성물을 투여하는 것을 포함하는, 상기 대상체에서 상기 질환 또는 장애를 치료하는 방법.
- 제23항에 있어서, 질환 또는 장애가 여드름, 지루, 피지 증식증, 지루성 각화증, 광선 각화증, 피지 선종, 피지 낭종, 피지 암종, 편평 세포 암종, 흑색종, 비류성 장미증, 버트-호그-두베 증후군에서의 섬유모낭종, 또는 이들의 조합인 방법.
- 제23항 또는 제24항에 있어서, 제1항 내지 제20항 중 어느 한 항의 화합물, 또는 그의 제약상 허용되는 염, 또는 제21항의 제약 조성물이 대상체에게 국소 투여되는 것인 방법.
- 제23항 내지 제25항 중 어느 한 항에 있어서, 대상체를 비정상적 피지세포 및/또는 각질세포 활성과 연관된 질환 또는 장애의 치료에 효과적인 하나 이상의 추가의 요법으로 치료하는 것을 추가로 포함하는 방법.
- 제23항 내지 제25항 중 어느 한 항에 있어서, 대상체에게 항생제 (예를 들어, 클린다마이신, 에리트로마이신, 메트로니다졸, 술프아세트아미드, 또는 테트라시클린, 예컨대 독시시클린 및 미노시클린) 또는 레티노이드 (예를 들어, 아다팔렌, 이소트레티노인, 레티놀, 타자로텐, 또는 트레티노인)를 여드름 및/또는 염증의 치료를 위한 치료 유효량으로 투여하는 것을 추가로 포함하는 방법.
- 비-알콜성 지방간 질환의 치료를 필요로 하는 대상체에게 치료 유효량의 제1항 내지 제20항 중 어느 한 항의 화합물, 또는 그의 제약상 허용되는 염, 또는 제21항의 제약 조성물을 투여하는 것을 포함하는, 상기 대상체에서 상기 질환을 치료하는 방법.
- 제28항에 있어서, 비-알콜성 지방간 질환이 비-알콜성 지방간염 (NASH)인 방법.
- 제28항 또는 제29항에 있어서, 대상체에게 하나 이상의 추가의 작용제를 비-알콜성 지방간 질환의 치료를 위한 치료 유효량으로 투여하는 것을 추가로 포함하는 방법.
- 제30항에 있어서, 하나 이상의 추가의 작용제가 안지오텐신 II 수용체 길항제, 안지오텐신 전환 효소 (ACE) 억제제, 카스파제 억제제, 카텝신 B 억제제, CCR2 케모카인 길항제, CCR5 케모카인 길항제, 클로라이드 채널 자극제, 콜레스테롤 가용화제, 디아실 글리세롤 O-아실트랜스퍼라제 1 (DGAT1) 억제제, 디펩티딜 펩티다제 IV (DPPIV) 억제제, 파르네소이드 X 수용체 (FXR) 효능제, 갈렉틴-3 억제제, 글루카곤-유사 펩티드 1 (GLPl) 효능제, 글루타티온 전구체, C형 간염 바이러스 NS3 프로테아제 억제제, HMG CoA 리덕타제 억제제, 11β-히드록시스테로이드 데히드로게나제 (11β-HSDl) 억제제, IL-Iβ 길항제, IL-6 길항제, IL-10 효능제, IL-17 길항제, 회장 나트륨 담즙산 공동수송체 억제제, 렙틴 유사체, 5-리폭시나제 억제제, LPL 유전자 자극제, 리실 옥시다제 동족체 2 (LOXL2) 억제제, PDE3 억제제, PDE4 억제제, 포스포리파제 C (PLC) 억제제, PPAR-알파 효능제, PPAR-감마 효능제, PPAR-델타 효능제, Rho 연관 단백질 키나제 2 (ROCK2) 억제제, 나트륨 글루코스 수송체-2 (SGLT2) 억제제, 스테아로일 CoA 데새투라제-1 억제제, 갑상선 호르몬 수용체 β 효능제, 종양 괴사 인자 알파 (TNF-알파) 리간드 억제제, 트랜스글루타미나제 억제제, 트랜스글루타미나제 억제제 전구체, 및 이들의 조합으로부터 선택되는 것인 방법.
- 제30항 또는 제31항에 있어서, 하나 이상의 추가의 작용제가 아세틸살리실산, 알리포젠 티파보벡, 아람콜, 아토르바스타틴, BLX-1002, 세니크리비록, 코비프로스톤, 콜레세벨람, 엠리카산, 에날라프릴, GFT-505, GR-MD-02, 히드로클로로티아지드, 이코사펜트 에틸 에스테르 (에틸 에이코사펜타엔산), IMM-124E, KD-025, 리나글립틴, 리라글루티드, 메르캅타민, MGL-3196, 오베티콜산, 올레속심, 페그-일로데카킨, 피오글리타존, PX-102, 레모글리플로진 에타보네이트, SHP-626, 솔리트로마이신, 티펠루카스트, TRX-318, 우르소데옥시콜산, VBY-376, 및 이들의 조합으로부터 선택되는 것인 방법.
- 비만 및/또는 당뇨병의 치료를 필요로 하는 대상체에게 치료 유효량의 제1항 내지 제20항 중 어느 한 항의 화합물, 또는 그의 제약상 허용되는 염, 또는 제21항의 제약 조성물을 투여하는 것을 포함하는, 상기 대상체에서의 비만 및/또는 당뇨병을 치료하는 방법.
- 제33항에 있어서, 대상체에게 하나 이상의 추가의 작용제를 비만 및/또는 당뇨병의 치료를 위한 치료 유효량으로 투여하는 것을 추가로 포함하는 방법.
- 제34항에 있어서, 하나 이상의 추가의 작용제가 안지오텐신 II 수용체 길항제, 안지오텐신 전환 효소 (ACE) 억제제, 카스파제 억제제, 카텝신 B 억제제, CCR2 케모카인 길항제, CCR5 케모카인 길항제, 클로라이드 채널 자극제, 콜레스테롤 가용화제, 디아실 글리세롤 O-아실트랜스퍼라제 1 (DGAT1) 억제제, 디펩티딜 펩티다제 IV (DPPIV) 억제제, 파르네소이드 X 수용체 (FXR) 효능제, 갈렉틴-3 억제제, 글루카곤-유사 펩티드 1 (GLPl) 효능제, 글루타티온 전구체, C형 간염 바이러스 NS3 프로테아제 억제제, HMG CoA 리덕타제 억제제, 11β-히드록시스테로이드 데히드로게나제 (11β-HSDl) 억제제, IL-Iβ 길항제, IL-6 길항제, IL-10 효능제, IL-17 길항제, 회장 나트륨 담즙산 공동수송체 억제제, 렙틴 유사체, 5-리폭시나제 억제제, LPL 유전자 자극제, 리실 옥시다제 동족체 2 (LOXL2) 억제제, PDE3 억제제, PDE4 억제제, 포스포리파제 C (PLC) 억제제, PPAR-알파 효능제, PPAR-감마 효능제, PPAR-델타 효능제, Rho 연관 단백질 키나제 2 (ROCK2) 억제제, 나트륨 글루코스 수송체-2 (SGLT2) 억제제, 스테아로일 CoA 데새투라제-1 억제제, 갑상선 호르몬 수용체 β 효능제, 종양 괴사 인자 알파 (TNF-알파) 리간드 억제제, 트랜스글루타미나제 억제제, 트랜스글루타미나제 억제제 전구체, 및 이들의 조합으로부터 선택되는 것인 방법.
- 제34항 또는 제35항에 있어서, 하나 이상의 추가의 작용제가 아세틸살리실산, 알리포젠 티파보벡, 아람콜, 아토르바스타틴, BLX-1002, 세니크리비록, 코비프로스톤, 콜레세벨람, 엠리카산, 에날라프릴, GFT-505, GR-MD-02, 히드로클로로티아지드, 이코사펜트 에틸 에스테르 (에틸 에이코사펜타엔산), IMM-124E, KD-025, 리나글립틴, 리라글루티드, 메르캅타민, MGL-3196, 오베티콜산, 올레속심, 페그-일로데카킨, 피오글리타존, PX-102, 레모글리플로진 에타보네이트, SHP-626, 솔리트로마이신, 티펠루카스트, TRX-318, 우르소데옥시콜산, VBY-376, 및 이들의 조합으로부터 선택되는 것인 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762527829P | 2017-06-30 | 2017-06-30 | |
| US62/527,829 | 2017-06-30 | ||
| PCT/US2018/040328 WO2019006324A1 (en) | 2017-06-30 | 2018-06-29 | NEW SPIROLACTONE COMPOUNDS |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20200034723A true KR20200034723A (ko) | 2020-03-31 |
Family
ID=64742735
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020207002707A KR20200034723A (ko) | 2017-06-30 | 2018-06-29 | 신규 스피로락톤 화합물 |
Country Status (12)
| Country | Link |
|---|---|
| US (2) | US11541046B2 (ko) |
| EP (1) | EP3644998B1 (ko) |
| JP (1) | JP7142375B2 (ko) |
| KR (1) | KR20200034723A (ko) |
| CN (1) | CN110799187B (ko) |
| AU (1) | AU2018291163A1 (ko) |
| BR (1) | BR112019028027A2 (ko) |
| CA (1) | CA3068623A1 (ko) |
| IL (1) | IL271687A (ko) |
| MX (1) | MX2019015849A (ko) |
| RU (1) | RU2020103730A (ko) |
| WO (1) | WO2019006324A1 (ko) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2020532551A (ja) | 2017-09-03 | 2020-11-12 | アンジオン バイオメディカ コーポレーション | Rho関連コイルドコイルキナーゼ(ROCK)阻害剤としてのビニルヘテロ環 |
| EP4154880A1 (en) * | 2020-05-21 | 2023-03-29 | Shionogi & Co., Ltd | Pharmaceutical for treating fatty liver diseases |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3686186A (en) | 1970-10-05 | 1972-08-22 | William J Houlihan | Substituted isochroman or phthalan piperidenes |
| US5578593A (en) | 1992-12-11 | 1996-11-26 | Merck & Co., Inc. | Spiro piperidines and homologs promote release of growth hormone |
| AU2006270145B2 (en) * | 2005-07-19 | 2011-04-14 | Msd K.K. | Spirochromanone derivatives as acetyl coenzyme a carboxylase (ACC) inhibitors |
| PE20081559A1 (es) | 2007-01-12 | 2008-11-20 | Merck & Co Inc | DERIVADOS DE ESPIROCROMANONA SUSTITUIDOS COMO INHIBIDORES DE ACETIL CoA CARBOXILASA |
| EP2123652A1 (en) | 2007-02-20 | 2009-11-25 | Takeda Pharmaceutical Company Limited | Heterocyclic compound |
| AU2010215035B2 (en) | 2009-02-17 | 2014-06-12 | Merck Canada Inc. | Novel spiro compounds useful as inhibitors of stearoyl-coenzyme A delta-9 desaturase |
| CN102482249B (zh) | 2009-07-08 | 2016-06-08 | 德米拉(加拿大)公司 | 用于治疗皮肤病症或疾病状态的tofa类似物 |
| EP2470021B1 (en) | 2009-08-27 | 2014-10-22 | Merck Sharp & Dohme Corp. | Novel pyrrolidine derived beta 3 adrenergic receptor agonists |
| KR101478517B1 (ko) | 2009-11-10 | 2015-01-02 | 화이자 인코포레이티드 | N1-피라졸로스피로케톤 아세틸-coa 카복실라아제 억제제 |
| ES2635030T3 (es) * | 2010-12-23 | 2017-10-02 | Merck Sharp & Dohme Corp. | Quinoxalinas y aza-quinoxalinas como moduladores del receptor CRTH2 |
| AU2014319990A1 (en) | 2013-09-12 | 2016-02-25 | Pfizer Inc. | Use of acetyl-CoA carboxylase inhibitors for treating acne vulgaris |
-
2018
- 2018-06-29 MX MX2019015849A patent/MX2019015849A/es unknown
- 2018-06-29 JP JP2020521484A patent/JP7142375B2/ja active Active
- 2018-06-29 US US16/627,627 patent/US11541046B2/en active Active
- 2018-06-29 AU AU2018291163A patent/AU2018291163A1/en active Pending
- 2018-06-29 CN CN201880043420.4A patent/CN110799187B/zh active Active
- 2018-06-29 CA CA3068623A patent/CA3068623A1/en active Pending
- 2018-06-29 KR KR1020207002707A patent/KR20200034723A/ko not_active Application Discontinuation
- 2018-06-29 WO PCT/US2018/040328 patent/WO2019006324A1/en active Application Filing
- 2018-06-29 RU RU2020103730A patent/RU2020103730A/ru unknown
- 2018-06-29 BR BR112019028027-8A patent/BR112019028027A2/pt active Search and Examination
- 2018-06-29 EP EP18824003.0A patent/EP3644998B1/en active Active
-
2019
- 2019-12-24 IL IL271687A patent/IL271687A/en unknown
-
2023
- 2023-01-03 US US18/092,723 patent/US20230355609A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| CN110799187A (zh) | 2020-02-14 |
| JP2020526580A (ja) | 2020-08-31 |
| US20210145822A1 (en) | 2021-05-20 |
| WO2019006324A1 (en) | 2019-01-03 |
| EP3644998A4 (en) | 2020-12-02 |
| US20230355609A1 (en) | 2023-11-09 |
| RU2020103730A3 (ko) | 2021-10-29 |
| JP7142375B2 (ja) | 2022-09-27 |
| IL271687A (en) | 2020-02-27 |
| US11541046B2 (en) | 2023-01-03 |
| CN110799187B (zh) | 2023-10-03 |
| MX2019015849A (es) | 2020-08-03 |
| AU2018291163A1 (en) | 2020-01-23 |
| CA3068623A1 (en) | 2019-01-03 |
| BR112019028027A2 (pt) | 2020-07-07 |
| EP3644998B1 (en) | 2024-04-10 |
| EP3644998A1 (en) | 2020-05-06 |
| RU2020103730A (ru) | 2021-07-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6923683B2 (ja) | オピオイド受容体リガンド並びにそれらの使用方法及び製造方法 | |
| US20230355609A1 (en) | Spirolactone Compounds | |
| KR101663436B1 (ko) | N-치환된 벤즈아미드 및 이의 사용 방법 | |
| EP2542254B1 (en) | Nmda receptor agonists and uses thereof | |
| EP3730491B1 (en) | Isoxazole derivative, preparation method therefor, and use thereof | |
| KR101456994B1 (ko) | 안드로겐 수용체 길항제 및 그의 용도 | |
| JP6991993B2 (ja) | 痛覚過敏を治療する方法 | |
| KR102243637B1 (ko) | 바이사이클릭 진통 화합물 | |
| JP7120549B2 (ja) | Trek(twik関連kチャネル)チャネルのアクチベータ | |
| CA2986930A1 (en) | Chemical modulators of signaling pathways and therapeutic use | |
| KR20180094938A (ko) | 오피오이드 수용체 리간드와 시토크롬 p450 억제제의 결합 | |
| JP2021519308A (ja) | 転写活性化タンパク質のイミダゾピペラジン阻害剤 | |
| TW201016671A (en) | Novel imidazolidine compounds as androgen receptor modulators | |
| US20190070154A1 (en) | New methods of use for an anti-diarrhea agent | |
| TW201632514A (zh) | 作為丙型肝炎抑制劑的化合物及其在藥物中的應用 | |
| US11071738B2 (en) | Therapeutic agent for fatty liver diseases and therapeutic agent for adiposity | |
| WO2019099457A1 (en) | Benzodioxinone compounds | |
| EP3747881B1 (en) | Nitrogen-containing benzoheterocycle compound comprising carboxylic acid group, preparation method and use thereof | |
| TW201331202A (zh) | [1,2,4]三唑并吡啶及其作為磷酸二酯酶抑制劑之用途 | |
| WO2022197690A1 (en) | Non-hydroxamate hdac6 inhibitors and related methods of use | |
| TW201829387A (zh) | 嗎啡喃衍生物和其用於治療自體免疫、發炎或感染相關的障礙的組合物 | |
| CN109734712A (zh) | 芳基或杂芳基取代的吡咯烷酰胺衍生物及其用途 | |
| WO2020135765A1 (zh) | Cxcr4抑制剂及其应用 | |
| CN109776374A (zh) | 酰基取代的吡咯烷酰胺衍生物及其用途 | |
| CN109776373A (zh) | 酰胺取代的吡咯烷酰胺衍生物及其用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| E902 | Notification of reason for refusal | ||
| E601 | Decision to refuse application |