KR20200029559A - 사용된 강황 - 이의 방법 및 조성물 - Google Patents
사용된 강황 - 이의 방법 및 조성물 Download PDFInfo
- Publication number
- KR20200029559A KR20200029559A KR1020207004552A KR20207004552A KR20200029559A KR 20200029559 A KR20200029559 A KR 20200029559A KR 1020207004552 A KR1020207004552 A KR 1020207004552A KR 20207004552 A KR20207004552 A KR 20207004552A KR 20200029559 A KR20200029559 A KR 20200029559A
- Authority
- KR
- South Korea
- Prior art keywords
- turmeric
- protein
- water
- hours
- concentrate
- Prior art date
Links
- 235000003373 curcuma longa Nutrition 0.000 title claims abstract description 235
- 235000003392 Curcuma domestica Nutrition 0.000 title claims abstract description 234
- 235000013976 turmeric Nutrition 0.000 title claims abstract description 234
- 238000000034 method Methods 0.000 title claims abstract description 50
- 239000000203 mixture Substances 0.000 title claims abstract description 37
- 244000163122 Curcuma domestica Species 0.000 title description 151
- 206010039073 rheumatoid arthritis Diseases 0.000 claims abstract description 17
- 244000008991 Curcuma longa Species 0.000 claims abstract 84
- 235000018102 proteins Nutrition 0.000 claims description 148
- 102000004169 proteins and genes Human genes 0.000 claims description 148
- 108090000623 proteins and genes Proteins 0.000 claims description 148
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 claims description 144
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 100
- 150000004676 glycans Chemical class 0.000 claims description 65
- 229920001282 polysaccharide Polymers 0.000 claims description 65
- 239000005017 polysaccharide Substances 0.000 claims description 65
- 239000002244 precipitate Substances 0.000 claims description 54
- 229920002472 Starch Polymers 0.000 claims description 50
- 239000012141 concentrate Substances 0.000 claims description 50
- 235000019698 starch Nutrition 0.000 claims description 50
- 239000008107 starch Substances 0.000 claims description 50
- 239000000284 extract Substances 0.000 claims description 48
- 239000000706 filtrate Substances 0.000 claims description 43
- 102000003886 Glycoproteins Human genes 0.000 claims description 42
- 108090000288 Glycoproteins Proteins 0.000 claims description 42
- 238000003756 stirring Methods 0.000 claims description 34
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 claims description 27
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 claims description 27
- 230000002209 hydrophobic effect Effects 0.000 claims description 27
- 238000001035 drying Methods 0.000 claims description 26
- 239000000843 powder Substances 0.000 claims description 26
- 239000000428 dust Substances 0.000 claims description 22
- 239000002245 particle Substances 0.000 claims description 22
- 239000004576 sand Substances 0.000 claims description 22
- 239000006228 supernatant Substances 0.000 claims description 22
- 241000124008 Mammalia Species 0.000 claims description 20
- 235000001014 amino acid Nutrition 0.000 claims description 20
- 150000001413 amino acids Chemical class 0.000 claims description 20
- 238000001914 filtration Methods 0.000 claims description 20
- 206010061218 Inflammation Diseases 0.000 claims description 17
- 230000004054 inflammatory process Effects 0.000 claims description 17
- 238000007873 sieving Methods 0.000 claims description 16
- 230000008569 process Effects 0.000 claims description 14
- 239000007787 solid Substances 0.000 claims description 14
- 239000003960 organic solvent Substances 0.000 claims description 13
- 238000010298 pulverizing process Methods 0.000 claims description 13
- 230000001603 reducing effect Effects 0.000 claims description 12
- 238000005406 washing Methods 0.000 claims description 12
- 229930153442 Curcuminoid Natural products 0.000 claims description 11
- 238000001816 cooling Methods 0.000 claims description 11
- 230000000694 effects Effects 0.000 claims description 11
- 238000001694 spray drying Methods 0.000 claims description 11
- 108060008682 Tumor Necrosis Factor Proteins 0.000 claims description 10
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 claims description 10
- 210000002966 serum Anatomy 0.000 claims description 10
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 claims description 9
- 235000006408 oxalic acid Nutrition 0.000 claims description 9
- 239000013557 residual solvent Substances 0.000 claims description 9
- GNFTZDOKVXKIBK-UHFFFAOYSA-N 3-(2-methoxyethoxy)benzohydrazide Chemical compound COCCOC1=CC=CC(C(=O)NN)=C1 GNFTZDOKVXKIBK-UHFFFAOYSA-N 0.000 claims description 8
- FGUUSXIOTUKUDN-IBGZPJMESA-N C1(=CC=CC=C1)N1C2=C(NC([C@H](C1)NC=1OC(=NN=1)C1=CC=CC=C1)=O)C=CC=C2 Chemical compound C1(=CC=CC=C1)N1C2=C(NC([C@H](C1)NC=1OC(=NN=1)C1=CC=CC=C1)=O)C=CC=C2 FGUUSXIOTUKUDN-IBGZPJMESA-N 0.000 claims description 8
- 230000009467 reduction Effects 0.000 claims description 8
- 238000003809 water extraction Methods 0.000 claims description 8
- 108090001005 Interleukin-6 Proteins 0.000 claims description 7
- 235000018417 cysteine Nutrition 0.000 claims description 7
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 claims description 6
- 206010030113 Oedema Diseases 0.000 claims description 6
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 claims description 6
- 229930182817 methionine Natural products 0.000 claims description 6
- 235000006109 methionine Nutrition 0.000 claims description 6
- 108010064851 Plant Proteins Proteins 0.000 claims description 5
- 239000000463 material Substances 0.000 claims description 5
- 235000021118 plant-derived protein Nutrition 0.000 claims description 5
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 claims description 4
- 230000008961 swelling Effects 0.000 claims description 4
- 208000024891 symptom Diseases 0.000 claims description 4
- 241000196324 Embryophyta Species 0.000 claims description 3
- 125000002791 glucosyl group Chemical group C1([C@H](O)[C@@H](O)[C@H](O)[C@H](O1)CO)* 0.000 claims description 3
- 238000000227 grinding Methods 0.000 claims description 3
- 238000002791 soaking Methods 0.000 claims description 3
- 229920000856 Amylose Polymers 0.000 claims description 2
- 229920000294 Resistant starch Polymers 0.000 claims description 2
- 235000021254 resistant starch Nutrition 0.000 claims description 2
- 229920000945 Amylopectin Polymers 0.000 claims 1
- 230000000975 bioactive effect Effects 0.000 abstract description 8
- 230000003110 anti-inflammatory effect Effects 0.000 abstract description 6
- 230000001225 therapeutic effect Effects 0.000 abstract description 6
- 230000037396 body weight Effects 0.000 description 18
- 239000002671 adjuvant Substances 0.000 description 14
- 238000004458 analytical method Methods 0.000 description 13
- 241000699670 Mus sp. Species 0.000 description 6
- 241000187479 Mycobacterium tuberculosis Species 0.000 description 6
- 241000700159 Rattus Species 0.000 description 6
- 230000000052 comparative effect Effects 0.000 description 6
- 238000000605 extraction Methods 0.000 description 6
- 241001465754 Metazoa Species 0.000 description 5
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 4
- 206010003246 arthritis Diseases 0.000 description 4
- 125000003147 glycosyl group Chemical group 0.000 description 4
- 235000015097 nutrients Nutrition 0.000 description 4
- 239000002904 solvent Substances 0.000 description 4
- 239000006286 aqueous extract Substances 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 238000006243 chemical reaction Methods 0.000 description 3
- 206010012601 diabetes mellitus Diseases 0.000 description 3
- RWSXRVCMGQZWBV-WDSKDSINSA-N glutathione Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O RWSXRVCMGQZWBV-WDSKDSINSA-N 0.000 description 3
- HMJSBVCDPKODEX-NXZHAISVSA-N (1e,6e)-1,7-bis(3,4-dimethoxyphenyl)hepta-1,6-diene-3,5-dione Chemical compound C1=C(OC)C(OC)=CC=C1\C=C\C(=O)CC(=O)\C=C\C1=CC=C(OC)C(OC)=C1 HMJSBVCDPKODEX-NXZHAISVSA-N 0.000 description 2
- GZCWLCBFPRFLKL-UHFFFAOYSA-N 1-prop-2-ynoxypropan-2-ol Chemical compound CC(O)COCC#C GZCWLCBFPRFLKL-UHFFFAOYSA-N 0.000 description 2
- 102000013563 Acid Phosphatase Human genes 0.000 description 2
- 108010051457 Acid Phosphatase Proteins 0.000 description 2
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 2
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 238000009010 Bradford assay Methods 0.000 description 2
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 2
- 108010024636 Glutathione Proteins 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 2
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 2
- 229920002774 Maltodextrin Polymers 0.000 description 2
- 206010030124 Oedema peripheral Diseases 0.000 description 2
- 102000019197 Superoxide Dismutase Human genes 0.000 description 2
- 108010012715 Superoxide dismutase Proteins 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 102000004139 alpha-Amylases Human genes 0.000 description 2
- 108090000637 alpha-Amylases Proteins 0.000 description 2
- 229940024171 alpha-amylase Drugs 0.000 description 2
- 235000003704 aspartic acid Nutrition 0.000 description 2
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 210000004027 cell Anatomy 0.000 description 2
- VFLDPWHFBUODDF-FCXRPNKRSA-N curcumin Chemical compound C1=C(O)C(OC)=CC(\C=C\C(=O)CC(=O)\C=C\C=2C=C(OC)C(O)=CC=2)=C1 VFLDPWHFBUODDF-FCXRPNKRSA-N 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 239000002158 endotoxin Substances 0.000 description 2
- 235000020776 essential amino acid Nutrition 0.000 description 2
- 239000003797 essential amino acid Substances 0.000 description 2
- 238000002290 gas chromatography-mass spectrometry Methods 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 235000013922 glutamic acid Nutrition 0.000 description 2
- 239000004220 glutamic acid Substances 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 230000003859 lipid peroxidation Effects 0.000 description 2
- 229920006008 lipopolysaccharide Polymers 0.000 description 2
- 239000003550 marker Substances 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- -1 monosaccharide methyl glycosides Chemical class 0.000 description 2
- FEMOMIGRRWSMCU-UHFFFAOYSA-N ninhydrin Chemical compound C1=CC=C2C(=O)C(O)(O)C(=O)C2=C1 FEMOMIGRRWSMCU-UHFFFAOYSA-N 0.000 description 2
- 230000003389 potentiating effect Effects 0.000 description 2
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- RGHNJXZEOKUKBD-SQOUGZDYSA-M D-gluconate Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C([O-])=O RGHNJXZEOKUKBD-SQOUGZDYSA-M 0.000 description 1
- 108010073178 Glucan 1,4-alpha-Glucosidase Proteins 0.000 description 1
- 229920002971 Heparan sulfate Polymers 0.000 description 1
- UCUNFLYVYCGDHP-BYPYZUCNSA-N L-methionine sulfone Chemical compound CS(=O)(=O)CC[C@H](N)C(O)=O UCUNFLYVYCGDHP-BYPYZUCNSA-N 0.000 description 1
- 239000005913 Maltodextrin Substances 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- 102000003992 Peroxidases Human genes 0.000 description 1
- 102000004160 Phosphoric Monoester Hydrolases Human genes 0.000 description 1
- 108090000608 Phosphoric Monoester Hydrolases Proteins 0.000 description 1
- 241000700157 Rattus norvegicus Species 0.000 description 1
- ZSJLQEPLLKMAKR-UHFFFAOYSA-N Streptozotocin Natural products O=NN(C)C(=O)NC1C(O)OC(CO)C(O)C1O ZSJLQEPLLKMAKR-UHFFFAOYSA-N 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 238000005903 acid hydrolysis reaction Methods 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 235000012754 curcumin Nutrition 0.000 description 1
- 229940109262 curcumin Drugs 0.000 description 1
- 239000004148 curcumin Substances 0.000 description 1
- 150000001945 cysteines Chemical class 0.000 description 1
- 230000016396 cytokine production Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- VFLDPWHFBUODDF-UHFFFAOYSA-N diferuloylmethane Natural products C1=C(O)C(OC)=CC(C=CC(=O)CC(=O)C=CC=2C=C(OC)C(O)=CC=2)=C1 VFLDPWHFBUODDF-UHFFFAOYSA-N 0.000 description 1
- 239000013024 dilution buffer Substances 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 229960003180 glutathione Drugs 0.000 description 1
- 229930182470 glycoside Natural products 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 235000009200 high fat diet Nutrition 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 125000004435 hydrogen atom Chemical class [H]* 0.000 description 1
- 230000003301 hydrolyzing effect Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 239000002440 industrial waste Substances 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 238000004255 ion exchange chromatography Methods 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 229940035034 maltodextrin Drugs 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 238000006140 methanolysis reaction Methods 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000012452 mother liquor Substances 0.000 description 1
- 230000003472 neutralizing effect Effects 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 230000001766 physiological effect Effects 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 238000002731 protein assay Methods 0.000 description 1
- 238000001243 protein synthesis Methods 0.000 description 1
- 239000001008 quinone-imine dye Substances 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000007974 sodium acetate buffer Substances 0.000 description 1
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 1
- 239000001509 sodium citrate Substances 0.000 description 1
- 239000008279 sol Substances 0.000 description 1
- 238000000638 solvent extraction Methods 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- ZSJLQEPLLKMAKR-GKHCUFPYSA-N streptozocin Chemical compound O=NN(C)C(=O)N[C@H]1[C@@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O ZSJLQEPLLKMAKR-GKHCUFPYSA-N 0.000 description 1
- 229960001052 streptozocin Drugs 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 230000014616 translation Effects 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/88—Liliopsida (monocotyledons)
- A61K36/906—Zingiberaceae (Ginger family)
- A61K36/9066—Curcuma, e.g. common turmeric, East Indian arrowroot or mango ginger
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/197—Carboxylic acids, e.g. valproic acid having an amino group the amino and the carboxyl groups being attached to the same acyclic carbon chain, e.g. gamma-aminobutyric acid [GABA], beta-alanine, epsilon-aminocaproic acid or pantothenic acid
- A61K31/198—Alpha-amino acids, e.g. alanine or edetic acid [EDTA]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
- A61K31/716—Glucans
- A61K31/718—Starch or degraded starch, e.g. amylose, amylopectin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/415—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from plants
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08B—POLYSACCHARIDES; DERIVATIVES THEREOF
- C08B30/00—Preparation of starch, degraded or non-chemically modified starch, amylose, or amylopectin
- C08B30/20—Amylose or amylopectin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2236/00—Isolation or extraction methods of medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2236/00—Isolation or extraction methods of medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicine
- A61K2236/30—Extraction of the material
- A61K2236/33—Extraction of the material involving extraction with hydrophilic solvents, e.g. lower alcohols, esters or ketones
- A61K2236/331—Extraction of the material involving extraction with hydrophilic solvents, e.g. lower alcohols, esters or ketones using water, e.g. cold water, infusion, tea, steam distillation, decoction
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2236/00—Isolation or extraction methods of medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicine
- A61K2236/30—Extraction of the material
- A61K2236/39—Complex extraction schemes, e.g. fractionation or repeated extraction steps
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2236/00—Isolation or extraction methods of medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicine
- A61K2236/50—Methods involving additional extraction steps
- A61K2236/51—Concentration or drying of the extract, e.g. Lyophilisation, freeze-drying or spray-drying
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2236/00—Isolation or extraction methods of medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicine
- A61K2236/50—Methods involving additional extraction steps
- A61K2236/53—Liquid-solid separation, e.g. centrifugation, sedimentation or crystallization
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Natural Medicines & Medicinal Plants (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Rheumatology (AREA)
- Botany (AREA)
- Molecular Biology (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Medical Informatics (AREA)
- Biotechnology (AREA)
- Alternative & Traditional Medicine (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pain & Pain Management (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Biochemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Polymers & Plastics (AREA)
- Gastroenterology & Hepatology (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Materials Engineering (AREA)
- Medicines Containing Plant Substances (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
본 발명은 사용된 강황(spent turmeric)으로부터 생리 활성 성분 및 상기 생리 활성 성분을 포함하는 조성물의 분리 방법에 관한 것이다. 또한, 본 발명은 상기 생리 활성 조성물의 강력한 항염증 활성 및 류마티스 관절염에 이의 치료적 적용을 설명한다.
Description
(관련 출원의 상호 참조)
본 발명은 2017년 7월 24일에 출원된 인도 출원 제201741026215의 우선권을 주장하는 PCT 출원이다.
본 발명은 일반적으로 울금(Curcuma longa)(강황)에 관한 것이다. 더욱 구체적으로, 본 발명은 사용된 강황(spent turmeric)으로부터 소수성 단백질과 함께 발생하는 다당류 및 생리 활성 당단백질의 분리 및 이의 강력한 항염증 활성 및 류마티스 관절염의 치료적 관리를 위한 적용에 관한 것이다.
사용된 강황은 강황 분말 (울금의 분말 건조 뿌리 줄기(rhizome))의 용매 추출 후 남아있는 불용성 고형분을 구성한다. 이는 산업 폐기물로 간주된다. 그럼에도 불구하고, 사용된 강황의 치료적 가능성은 당 업계에 보고되어 있다.
Gurusiddiah Suresh Kumar et al, "Effect of spent turmeric on kidney glycoconjugates in streptozotocin-induced diabetic rats", J Diabetes Metab Disord. 2014; 13: 78은 당뇨병 동안 당단백질 및 헤파란 설페이트(heparan sulfate) 관련 신장 합병증과 같은 당 접합체(glycoconjugate)를 제어하는데 사용된 강황의 유리한 효과를 개시한다.
Han KH et al, "Spent turmeric reduces fat mass in rats fed a high-fat diet", Food Funct. 2016 Apr; 7(4):1814-24.
사용된 강황의 생리 활성 성분을 특성화하기 위해 예비 조사를 통해 유용한 기술적 통찰력을 얻었다. Smitha S 등은 Biochemie. 2009 Sep; 91 (9): 1156-1162에서 강황 폐기물 그릿(grit)으로부터 34 kDa 당단백질(베타-터메린(turmerin))을 보고했다.
따라서, 사용된 강황 및 이의 치료적 가능성의 본질에서 생리 활성 성분의 전체 스펙트럼을 탐색할 기술적인 필요성이 존재한다.
본 발명의 주요 목적은 신규한 생리 활성을 찾아 사용된 강황 물질의 치료 및 이들의 치료적 가능성의 설명을 위한 신규하고, 진보성 있고, 산업상 적용 가능한 공정 스킴을 개시하는 것이다.
본 발명의 다른 목적은 사용된 강황의 치료를 위해 신규하고, 진보성 있고, 산업상 적용 가능한 공정 스킴에 의해 수득된 사용된 강황의 면역 자극/항염증성 당단백질 및 전분 성분을 개시하는 것이다.
본 발명은 상술한 목적을 달성하고 추가로 관련된 이점을 제공한다.
사용된 강황(울금)으로부터 생리 활성 성분을 분리하는 방법 및 상기 생리 활성 성분을 포함하는 조성물이 기술된다. 또한, 본 발명은 류마티스 관절염에서 상기 생리 활성 조성물의 강력한 항염증 활성 및 이의 치료적 적용을 설명한다. 본 발명의 우수한 이점은 본 발명의 방법이 식물 단백질 공급원에서 거의 발견되지 않는 상당한 양의 속도 제한 아미노산, 시스테인 및 메티오닌을 포함하는 당단백질을 생성하는 기술적 효과이다. 따라서, 본 발명의 방법을 사용하여 분리된 당단백질은 사용된 강황 뿌리 줄기로부터 "전체 단백질(whole protein)"로 간주될 수 있다.
하기 용어는 본 명세서에 기재된 본 발명의 과학적 맥락을 이해하기 위해 포함되었다.
A. 속도 제한 아미노산(Rate limiting amino acid): 식이가 임의의 필수 아미노산이 부족한 경우, 단백질 합성은 해당 아미노산을 사용할 수 있는 속도 이상으로 진행될 수 없다. 이러한 필수 아미노산을 "속도 제한 아미노산" 또는 간단히 "제한 아미노산(limiting amino acid)"이라고 한다.
B. 총 용존 고형물(Total dissolved solid, TDS): 총 용존 고형물(TDS)은 액체에 포함된 모든 무기 및 유기 물질의 총 함량을 측정한 것이다. 이는 분자, 이온화 또는 미세 과립(Micro-granular) (콜로이드 졸(colloidal sol))과 같은 형태로 현탁될 수 있다.
C. 커큐미노이드(Curcuminoid): 커큐미노이드는 커큐민(curcumin), 디메톡시커큐민(demethoxycurcumin) 및 비스디메톡시커큐민(bisdemethoxycurcumin)을 포함하지만 이에 제한되지 않는 강황에서 발견되는 천연 화학 화합물이다.
본 발명의 다른 특징 및 이점은, 예를 들어 본 발명의 원리를 예시하는 첨부 된 도면과 관련하여 다음의 보다 상세한 설명으로부터 명백해질 것이다.
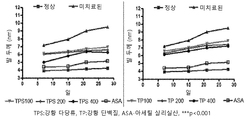
도 1은 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제(adjuvant) 유도된 류마티스 관절염)을 함유하는 완전 보강제(Complete adjuvant)를 투여함으로써 유도된 (발 두께의 감소에 의해 측정된) 쥐의 발의 염증을 감소시키는 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
도 2는 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여함으로써 유도된 (발 두께의 감소에 의해 측정된) 쥐의 발의 염증을 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
도 3은 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여함으로써 유도된 (발 부종의 감소에 의해 측정된) 쥐의 발의 염증을 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
도 4는 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여함으로써 유도된 (발 두께 및 부종의 감소에 의해 측정된) 쥐의 발의 염증을 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
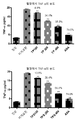
도 5는 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여한 후 혈청 염증 마커 IL-6을 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
도 6은 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여한 후 혈청 염증 마커 TNF-α를 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
도 2는 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여함으로써 유도된 (발 두께의 감소에 의해 측정된) 쥐의 발의 염증을 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
도 3은 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여함으로써 유도된 (발 부종의 감소에 의해 측정된) 쥐의 발의 염증을 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
도 4는 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여함으로써 유도된 (발 두께 및 부종의 감소에 의해 측정된) 쥐의 발의 염증을 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
도 5는 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여한 후 혈청 염증 마커 IL-6을 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
도 6은 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여한 후 혈청 염증 마커 TNF-α를 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
가장 바람직한 양태에서, 본 발명은 사용된 강황의 물 추출 방법에 관한 것이고, 상기 방법은 하기 단계를 포함한다:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 20%의 총 용존 고형물(total dissolved solid, TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계; 및
d) 단계 c)의 단백질이 없는 단계 a)의 사용된 강황 재료-2를 24시간 동안 120 ℃에서 건조시킨 후, 분말화(powdering) 및 체질(sieving)하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질(hydrophobic protein)과 함께 발생하는 것인, 단계.
바람직한 양태에서, 상기 단계 a)에서 사용된 강황과 물의 비율은 1:10 내지 1:50의 범위 내이다.
다른 가장 바람직한 양태에서, 본 발명은 사용된 강황의 물 추출 방법에 관한 것이고, 상기 방법은 하기 단계를 포함한다:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린(decanting) 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계;
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계;
g) 단계 f)의 단백질이 없는 단계 a)의 사용된 강황 재료-2에 각각 46 ℃ 및 30 ℃에서 4시간 동안 담금 체적(soaking volume)의 아세톤 및 메탄올로 세척하여, 미량의 커큐미노이드(curcuminoid) 및 옥살산 함량을 제거하여 세척된 사용된 강황 재료-2를 형성하는 단계; 및
h) 24시간 동안 단계 g)의 세척된 사용된 강황 재료-2를 건조시켜 잔여 용매를 제거한 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
바람직한 양태에서, 상기 단계 a)에서 사용된 강황과 물의 비율은 1:10 내지 1:50의 범위 내이다.
또 다른 가장 바람직한 양태에서, 본 발명은 포유류의 염증을 치료하여 염증 감소 효과를 발생시키는 방법에 관한 것이고, 상기 방법은 사용된 강황 단백질 또는 사용된 강황 전분의 유효량을 상기 포유류에 투여하는 단계를 포함하고, 상기 단백질 및 전분은 하기 단계를 포함하는 공정에 의해 수득된다:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 20%의 총 용존 고형물(TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계; 및
d) 단계 c)의 단백질이 없는 단계 a)의 사용된 강황 재료-2를 24시간 동안 120 ℃에서 건조시킨 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
바람직한 양태에서, 상기 단계 a)에서 사용된 강황과 물의 비율은 1:10 내지 1:50의 범위 내이다.
또 다른 가장 바람직한 양태에서, 본 발명은 포유류의 염증을 치료하여 염증 감소 효과를 발생시키는 방법에 관한 것이고, 상기 방법은 사용된 강황 단백질 또는 사용된 강황 전분의 유효량을 상기 포유류에 투여하는 단계를 포함하고, 상기 단백질 및 전분은 하기 단계를 포함하는 공정에 의해 수득된다:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계;
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계;
g) 단계 f)의 단백질이 없는 단계 a)의 사용된 강황 재료-2에 각각 46 ℃ 및 30 ℃에서 4시간 동안 담금 체적의 아세톤 및 메탄올로 세척하여, 미량의 커큐미노이드 및 옥살산 함량을 제거하여 세척된 사용된 강황 재료-2를 형성하는 단계; 및
h) 24시간 동안 단계 g)의 세척된 사용된 강황 재료-2를 건조시켜 잔여 용매를 제거한 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
또 다른 가장 바람직한 양태에서, 본 발명은 포유류의 류마티스 관절염을 치료하여, 통증, 종창, 부종을 포함하는 포유류의 류마티스 관절염 증상을 감소시키고, IL-6 및 TNF-α의 혈청 마커를 감소시키는 효과를 발생시키는 방법에 관한 것이고, 상기 방법은 사용된 강황 단백질 또는 사용된 강황 전분의 유효량을 상기 포유류에 투여하는 단계를 포함하고, 상기 단백질 및 전분은 하기 단계를 포함하는 공정에 의해 수득된다:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 20%의 총 용존 고형물(TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계; 및
d) 단계 c)의 단백질이 없는 단계 a)의 사용된 강황 재료-2를 24시간 동안 120 ℃에서 건조시킨 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
바람직한 양태에서, 상기 단계 a)에서 사용된 강황과 물의 비율은 1:10 내지 1:50의 범위 내이다.
또 다른 가장 바람직한 양태에서, 본 발명은 포유류의 류마티스 관절염을 치료하여, 통증, 종창, 부종을 포함하는 포유류의 류마티스 관절염 증상을 감소시키고, IL-6 및 TNF-α의 혈청 마커를 감소시키는 효과를 발생시키는 방법에 관한 것이고, 상기 방법은 사용된 강황 단백질 또는 사용된 강황 전분의 유효량을 상기 포유류에 투여하는 단계를 포함하고, 상기 단백질 및 전분은 하기 단계를 포함하는 공정에 의해 수득된다:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계;
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계;
g) 단계 f)의 단백질이 없는 단계 a)의 사용된 강황 재료-2에 각각 46 ℃ 및 30 ℃에서 4시간 동안 담금 체적의 아세톤 및 메탄올로 세척하여, 미량의 커큐미노이드 및 옥살산 함량을 제거하여 세척된 사용된 강황 재료-2를 형성하는 단계; 및
h) 24시간 동안 단계 g)의 세척된 사용된 강황 재료-2를 건조시켜 잔여 용매를 제거한 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
바람직한 양태에서, 상기 단계 a)에서 사용된 강황과 물의 비율은 1:10 내지 1:50의 범위 내이다.
또 다른 가장 바람직한 양태에서, 본 발명은 사용된 강황 재료로부터 수득된 단백질 조성물에 관한 것이고, 상기 단백질 조성물은 하기 단계를 포함하는 사용된 강황의 물 추출에 의해 수득된다:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계; 및
c) 고진공 하에서 20%의 총 용존 고형물(TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계.
또 다른 가장 바람직한 양태에서, 본 발명은 사용된 강황 재료로부터 수득된 단백질 조성물에 관한 것이고, 상기 단백질 조성물은 하기 단계를 포함하는 사용된 강황의 물 추출에 의해 수득된다:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계; 및
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계.
또 다른 가장 바람직한 양태에서, 본 발명은 소수성 단백질을 갖는 다당류를 포함하는 다당류 조성물에 관한 것이고, 상기 조성물은 하기 단계를 포함하는 공정을 통해 사용된 강황으로부터 수득된다:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계; 및
c) 고진공 하에서 20%의 총 용존 고형물(TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계; 및
d) 단계 c)의 단백질이 없는 단계 a)의 사용된 강황 재료-2를 24시간 동안 120 ℃에서 건조시킨 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
바람직한 양태에서, 상기 단계 a)에서 사용된 강황과 물의 비율은 1:10 내지 1:50의 범위 내이다.
또 다른 가장 바람직한 양태에서, 본 발명은 소수성 단백질을 갖는 다당류를 포함하는 다당류 조성물에 관한 것이고, 상기 조성물은 하기 단계를 포함하는 공정을 통해 사용된 강황으로부터 수득된다:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계;
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계;
g) 단계 f)의 단백질이 없는 단계 a)의 사용된 강황 재료-2에 각각 46 ℃ 및 30 ℃에서 4시간 동안 담금 체적의 아세톤 및 메탄올로 세척하여, 미량의 커큐미노이드 및 옥살산 함량을 제거하여 세척된 사용된 강황 재료-2를 형성하는 단계; 및
h) 24시간 동안 단계 g)의 세척된 사용된 강황 재료-2를 건조시켜 잔여 용매를 제거한 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
또 다른 가장 바람직한 양태에서, 본 발명은 식물 단백질 조성물에 관한 것이고, 상기 단백질 조성물은 사용된 강황으로부터 수득되고, 상기 단백질 조성물은 속도 제한 아미노산(rate limiting aminoacid) 시스테인 및 메티오닌을 포함하는 것을 특징으로 한다.
또 다른 가장 바람직한 양태에서, 본 발명은 식물 다당류 조성물(전분)에 관한 것이고, 상기 다당류 조성물은 사용된 강황으로부터 수득되고, α, 1-4 결합(아밀로오스) 및 α, 1-6 결합(아밀로펙틴)에 의해 연결된 90%의 글루코오스 잔기를 갖는 저항성 전분(resistant starch)으로서 소수성 당단백질과 함께 발생하는 것을 특징으로 한다.
본 발명의 기술적 특징 및 기술적 효과를 포함하는 상기 가장 바람직한 양태는 본 명세서에 하기에 나타내는 실시예를 통해 설명된다.
실시예
1
1kg의 사용된 강황을 65 ℃에서 6시간 동안 가끔 교반하면서 물 (1:10 비율)로 추출하여 사용된 강황 및 사용된 부분-2의 물 추출물을 수득했다. 6시간 추출 후, 즉시 물 추출물을 하이플로 베드 원심 분리기(Hyflo bedded centrifuge)를 통해 여과하여, 임의의 모래 또는 먼지 입자를 포획했다. 수득된 7L의 여과액을 고진공 하에서 20%의 총 총 용존 고형물 (TDS)로 농축시켰다. 또한, 물 추출물을 100L/hr의 유속으로 120 ℃에서 분무 건조시켰다. 연갈색의 분말을 4% 수율로 수득했다. 크루드(crude)한 물 추출물 샘플을 CHNS (탄소, 수소, 질소, 및 황) 분석 및 브래드포드법(Bradford method)에 의해 분석하여, 단백질의 총 퍼센트를 추정했다. 총 단백질 퍼센트는 CHNS 방법에 의해 6.73% 및 브래드포드법 (단백질 검정)에 의해 3%인 것으로 밝혀졌다. 또한, 아미노산 분석은, 사용된 강황 단백질이 높은 퍼센트의 아스파르트산 및 글루탐산 (각각 1030mg/100gm 및 985mg/100gm)을 갖는 18개의 중요한 아미노산으로 구성되었으며, 단백질의 총 퍼센트는 4.91gm/100gm의 분무 건조된 물 추출물로 밝혀지는 것을 나타냈다. 시스테인과 메티오닌은 식물의 단백질 공급원에서 거의 발견되지 않는 두 가지 속도 제한 아미노산이다. 사용된 강황으로부터의 당단백질은 50mg의 시스테인 및 110 mg의 메티오닌/100gm의 당단백질로 구성된다. 사용된 당단백질에서 이러한 아미노산의 존재로 인해 이는 "전체 단백질(whole Protein)"이 된다. 사용된 부분-2를 24시간 동안 120 ℃의 고온의 공기 오븐에서 추가 건조시키고, 미세한 분말로 만들어 눈이 80개인 메쉬 스크린(80 number mesh screen)을 통해 체질하여, 사용된 강황으로부터 전분을 수득했다. 강황 전분을 80% 수율로 생산되었으며, 전분의 총 퍼센트는 49%로 밝혀졌다. 사용된 강황 전분(다당류)은 소수성 단백질과 함께 발생된다.
실시예
2
유기 용매(
실시예로서
아세톤)를 사용하여 침전을 통한 단백질 농축(enrichment)
1kg의 사용된 강황을 65 ℃에서 6시간 동안 가끔 교반하면서 물 (1:10 비율)로 추출하여 사용된 강황 및 사용된 부분-2의 물 추출물을 수득했다. 6시간 추출 후, 즉시 물 추출물을 하이플로 베드 원심 분리기를 통해 여과하여, 임의의 모래 또는 먼지 입자를 포획했다. 수득된 7L의 여과액을 고진공 하에서 60 ℃에서 1리터로 농축시켰다. 냉각 후, 1:2 비율의 아세톤을 가끔 교반하면서 물 추출물에 첨가하고, 4시간 동안 실온에서 배양을 유지하여, 침전물을 완전히 침강시켰다. 침전물을 파괴하지 않으면서 상청액을 조심스럽게 따라 버리고, 와트만(Whatmann) 필터지를 통해 여과했다. 아세톤으로 세척함으로써 침전물에서 수분을 제거한 후 와트만 필터지를 통해 여과시켰다. 수득된 단백질 침전물이 미세한 크림색 단백질 분말이 될 때까지 즉시 고진공 하에서 60 ℃에서 건조시켰다. 분말을 4% 수율로 수득했고, 샘플을 CHNS 분석에 의해 분석하여, 단백질의 총 퍼센트를 추정했다. 총 단백질 퍼센트는 3gm/100gm으로 밝혀졌다. CHNS 분석은 9% w/w의 단백질을 나타냈지만, 아미노산 분석은 8.595 % w/w의 단백질을 나타냈다. 아미노산 분석은 24시간 동안 110 ℃에서 6N HCl을 사용하여 산 가수분해를 수행한 후, 과산화포름산(performic acid)(시스테인산 및 메티오닌 설폰과 같은 시스테인 및 메티오닌의 결정을 위한)에 의한 HCl 샘플의 산화에 의해 수행되었다. NorLeu 희석 완충액을 가수 분해된 샘플에 첨가하고, 볼텍싱하고(vortexed), 회전 속도를 늦췄다. 소듐 시트레이트(sodium citrate) 완충 시스템을 사용하여 아미노산을 분리하기 위해 이온 교환 크로마토그래피 컬럼으로 구성된 L-8800 히타치 분석기(Hitachi analyzer)에 50 ㎕의 가수 분해물을 적재한 후, 포스트 컬럼 닌하이드린 반응 검출 시스템(post column Ninhydrin reaction detection system) (아미노산의 분리, 검출 및 분석)을 수행했다. 아미노산 분석은, 사용된 강황으로부터의 단백질이 많은 양(% w/w)의 아스파르트산 및 글루탐산 (각각 1170 mg/100gm 및 1044 mg/100 g)을 갖는 18개의 중요한 아미노산으로 구성되었으며, 단백질의 총 퍼센트는 8.595 gm/100gm의 건조된 단백질 분말로 밝혀지는 것을 나타냈다. 사용된 부분-2를 4시간 동안 각각 46 ℃ 및 30 ℃에서 담금 체적(soaking volume)의 아세톤 및 메탄올로 세척하여, 커큐미노이드(curcuminoid) 및 옥살산 함량을 제거했다. 사용된 강황 전분 아세톤 모액(여과액)은 총 커큐미노이드 w/w의 16% 검정으로 0.2% 수율을 함유했다(커큐민-11.99%,, 디메톡시커큐민(demethoxycurcumin) 2-.68% 및 비스디메톡시커큐민(bisdemethoxycurcumin) - 1.50%). 그 후, 전분이 풍부한 사용된 강황을 24시간 동안 고온의 공기 오븐에서 건조시키고, 잔여 용매를 제거하고, 미세한 분말로 만들고 눈이 80개인 메쉬 스크린을 통해 체질했다. 강황 전분을 75% 수율로 생산되었으며, 전분의 총 퍼센트는 60%로 밝혀졌다. 사용된 강황으로부터의 다당류(전분)은 소수성 단백질과 함께 발생된다.
총 전분 분석:
사용된 강황으로부터의 전분을 4 ℃에서 2M KOH와 샘플을 교반한 후, 소듐 아세테이트 완충액으로 중화시키고 α-아밀라아제로 가수 분해함으로써 미리 용해시켰다. 열 안정성 α-아밀라아제 전분을 가용성 분지형 및 미분지형 말토덱스트린으로 가수분해했다. 아밀로글루코시다아제는 말토덱스트린을 D-글루코오스로 정량적으로 가수분해했다. 과산화수소의 방출로 D-글루코오스를 D-글루코네이트로 산화시키고, 이를 과산화효소를 사용하는 비색 반응 및 퀴논이민(quinoneimine) 염료의 생성에서 정량적으로 측정했다.
글루코오스 퍼센트 & 결합 패턴:
기체 크로마토그래피 및 질량 분석법을 혼합함으로써 글리코실 조성 분석 및 글리코실 결합 분석을 수행했다. 글리코실 조성 분석을 위해, 80 ℃에서 17시간 동안 샘플에 메탄올성 HCl을 사용하는 산성 메탄분해(acidic methanolysis)를 수행하여 단당류 메틸 글리코사이드(monosaccharide methyl glycoside)를 생성했고, GC-MS에 의해 분석했다. 글리코실 결합 분석을 위해, 샘플을 퍼메틸화(permethylate), 해중합(depolymerize), 환원 및 아세틸화하고, 생성된 부분적으로 메틸화된 알디톨 아세테이트를 GC-MS에 의해 분석했다. 사용된 강황으로부터의 전분은 글루코오스의 약 90%를 구성하고, 총 피크 면적의 90%를 갖는 4개의 연결된 글루코오스 잔기를 보여 주었고, 이는 샘플이 전분이 풍부하다는 것을 나타낸다.
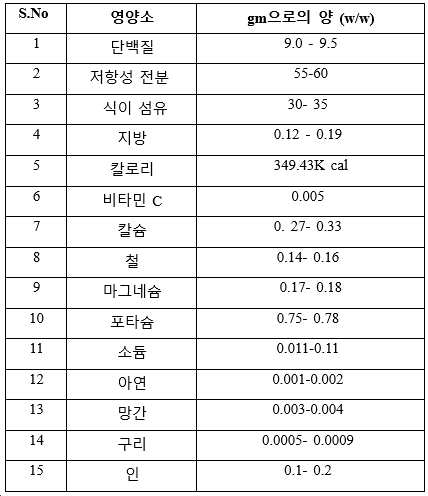
본 발명의 방법(용매 기반 추출, 예시적으로 아세톤)에 의해 수득되는 100gm의 사용된 강황 다당류의 영양소 프로파일을 표 A에 나타냈다.
[표 A]
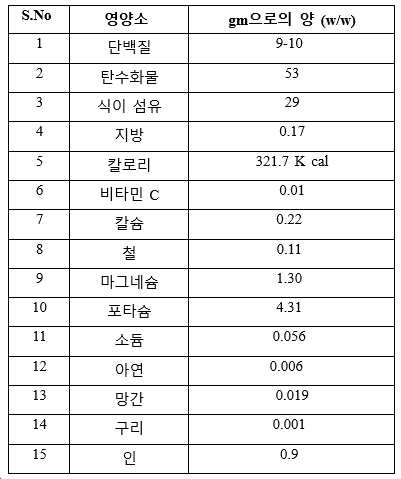
본 발명의 방법(용매를 사용하지 않는 물만으로의 추출)에 의해 수득되는 100gm의 사용된 강황 다당류의 영양소 프로파일을 표 B에 나타냈다.
[표 B]
본 발명의 방법(용매 기반 추출, 예시적으로 아세톤)에 의해 수득되는 100gms의 사용된 강황 당단백질의 영양소 프로파일을 표 C에 나타냈다.
[표 C]
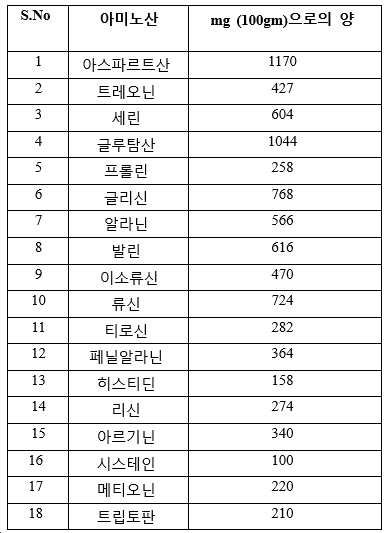
본 발명의 방법(용매 기반 추출, 예시적으로 아세톤)에 의해 수득되는 100gms의 사용된 강황 당단백질의 아미노산 프로파일을 표 D에 나타냈다.
[표 D]
100gms의 사용된 강황 당단백질(임의의 용매 없는 수성 추출물)의 영양소 프로파일을 표 E에 나타냈다.
[표 E]
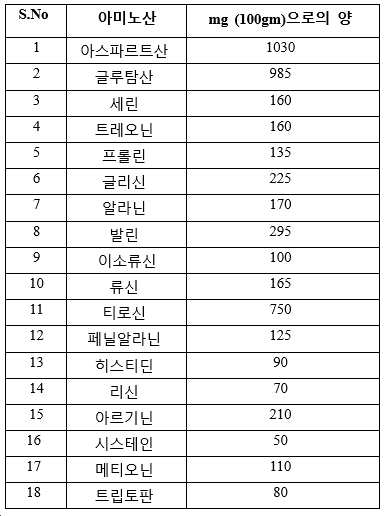
사용된 강황(임의의 용매 없는 수성 추출물)의 수성 추출물의 아미노산 프로파일을 표 F에 나타냈다.
[표 F]
실시예
III
생체 외(In vitro) 항염증 활성
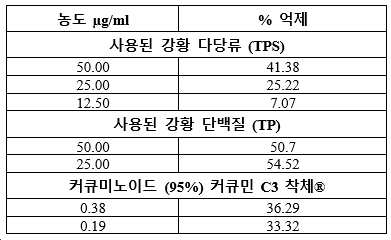
지질다당류(lipopolysaccharide) 자극된(24시간 동안 LPS=100 ng/ml) 인간 단핵구성 세포주(Human Monocytic cell line) THP-1 또는 뮤린 대식 세포주(Murine macrophage cell line) J774에 의해 사이토킨 생산에 대한 사용된 강황 단백질(TP) 및 사용된 강황 다당류(전분)(TPS)의 항염증 활성을 표 1에 나타냈다. 사이토킨 TNF-α을 세포 상청액에서 측정했다.
[표 1]
결과: 사용된 강황 다당류는 TNF-α 방출의 41.3%의 억제를 보였지만, 사용된 강황 당단백질은 TNF-α를 50.7% 억제했다.
실시예
IV
생체 내(In
vivo
) 생물학적(
항관절염
) 활성
150-180 kg 무게의 수컷 위스타(Wistar) 쥐에 1일-28일부터 100, 200 및 400 mg/kg의 사용된 강황 다당류를 경구 투여했다. 관절염을 유발시키기 위해 연구 7, 15, 21 및 28일에 0.1 ml의 투여 수준으로 이 동물의 발에 프로인드 완전 보강제(Freund's complete adjuvant)를 피내 주사했다. 7, 15, 21 및 28일에 발 체적의 증가로서 보강제에 의해 유도된 부종을 측정했다. 연구 종료 시에, 동물을 희생시키고, 염증 파라미터를 분석하기 위해 혈액 및 조직을 수집했다. 연구된 염증 파라미터는 하기를 포함한다:
a. 발의 염증
b. 혈액 생화학
c. 지질 과산화
d. 혈청에서 감소된 글루타티온
e. 혈청에서 수퍼옥사이드 디스뮤타아제(superoxide dismutase) 활성
f. 산 및 알칼리 포스파타아제(phosphatase)의 수준
g. TNF-α의 수준
h. IL6 수준
결과:
a. 염증의 혈청 마커인 IL-6, TNF-α의 동시 감소와 함께 사용된 강황 당단백질 및 다당류로의 치료 시에 발 부종(염증)의 현저한 감소가 관측되었다(도 1, 2, 3, 4, 5 및 6).
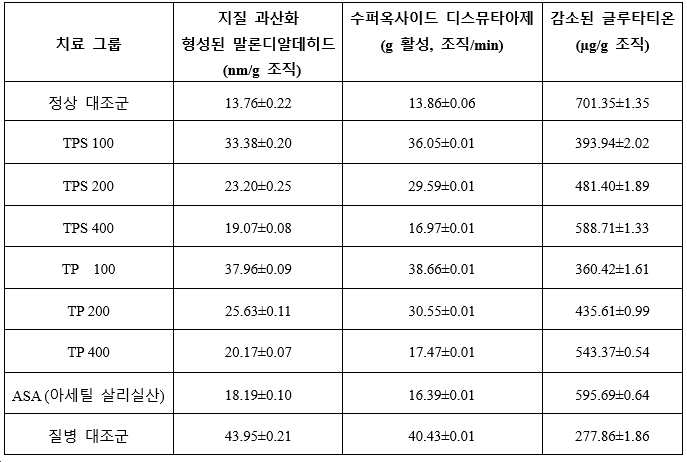
b. 또한, 사용된 강황 단백질 및 다당류로의 치료는 지질과산화, 수퍼옥사이드 디스뮤타아제 활성을 감소시키고, 관절염 동물의 혈청에서 감소된 글루타티온의 농도를 증가시켰다(표 2).
[표 2]
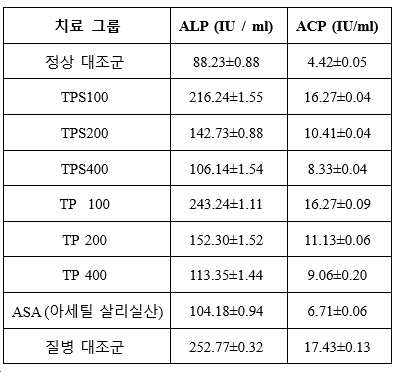
c. 사용된 강황 단백질 및 다당류는 관절염 동물에서 높은 수준의 산 포스파타아제(ACP) 및 알칼리 포스파타아제(ALP)를 감소시켰다(표 3).
[표 3]
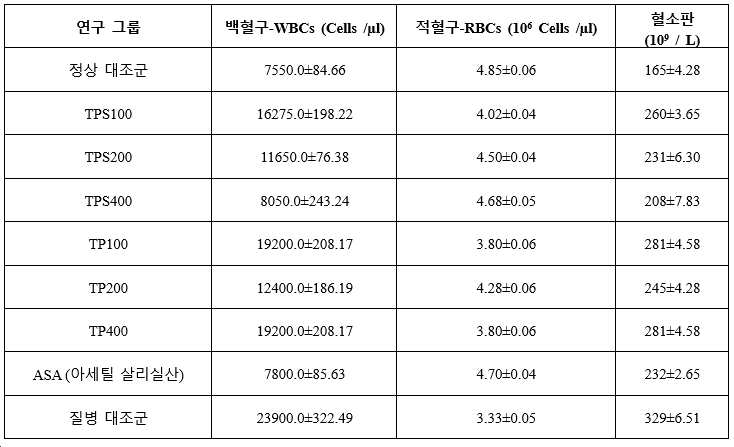
d. 사용된 강황 단백질 및 다당류는 관절염 동물에서 증가된 수의 혈액 세포 (RBC, WBC 및 혈소판)을 정상으로 회복시켰다(표 4).
[표 4]
본 발명의 다른 변경 및 변형은 상술한 개시 및 교시로부터 당업자에게 명백 할 것이다. 따라서, 본 발명의 특정 양태들만 본 명세서에 구체적으로 기재되었지만, 본 발명의 사상 및 범위를 벗어나지 않고 다수의 변경이 이루어질 수 있음이 명백할 것이다.
Claims (12)
- 사용된 강황(spent turmeric)의 물 추출(water extraction) 방법으로서,
상기 방법은,
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 20%의 총 용존 고형물(total dissolved solid, TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계; 및
d) 단계 c)의 단백질이 없는 단계 a)의 사용된 강황 재료-2를 24시간 동안 120 ℃에서 건조시킨 후, 분말화(powdering) 및 체질(sieving)하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질(hydrophobic protein)과 함께 발생하는 것인, 단계;
를 포함하는 것인, 사용된 강황의 물 추출 방법.
- 사용된 강황의 물 추출 방법으로서,
상기 방법은,
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린(decanting) 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계;
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계;
g) 단계 f)의 단백질이 없는 단계 a)의 사용된 강황 재료-2에 각각 46 ℃ 및 30 ℃에서 4시간 동안 담금 체적(soaking volume)의 아세톤 및 메탄올로 세척하여, 미량의 커큐미노이드(curcuminoid) 및 옥살산 함량을 제거하여 세척된 사용된 강황 재료-2를 형성하는 단계; 및
h) 24시간 동안 단계 g)의 세척된 사용된 강황 재료-2를 건조시켜 잔여 용매를 제거한 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계;
를 포함하는 것인, 사용된 강황의 물 추출 방법.
- 포유류의 염증을 치료하여 염증 감소 효과를 발생시키는 방법으로서,
상기 방법은 사용된 강황 단백질 또는 사용된 강황 전분의 유효량을 상기 포유류에 투여하는 단계를 포함하고, 상기 단백질 및 전분은 하기 단계를 포함하는 공정에 의해 수득되는 것인, 포유류의 염증을 치료하여 염증 감소 효과를 발생시키는 방법:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 20%의 총 용존 고형물(TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계; 및
d) 단계 c)의 단백질이 없는 단계 a)의 사용된 강황 재료-2를 24시간 동안 120 ℃에서 건조시킨 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
- 포유류의 염증을 치료하여 염증 감소 효과를 발생시키는 방법으로서,
상기 방법은 사용된 강황 단백질 또는 사용된 강황 전분의 유효량을 상기 포유류에 투여하는 단계를 포함하고, 상기 단백질 및 전분은 하기 단계를 포함하는 공정에 의해 수득되는 것인, 포유류의 염증을 치료하여 염증 감소 효과를 발생시키는 방법:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계;
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계;
g) 단계 f)의 단백질이 없는 단계 a)의 사용된 강황 재료-2에 각각 46 ℃ 및 30 ℃에서 4시간 동안 담금 체적의 아세톤 및 메탄올로 세척하여, 미량의 커큐미노이드 및 옥살산 함량을 제거하여 세척된 사용된 강황 재료-2를 형성하는 단계; 및
h) 24시간 동안 단계 g)의 세척된 사용된 강황 재료-2를 건조시켜 잔여 용매를 제거한 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
- 포유류의 류마티스 관절염을 치료하여, 통증, 종창, 부종을 포함하는 포유류의 류마티스 관절염 증상을 감소시키고, IL-6 및 TNF-α의 혈청 마커를 감소시키는 효과를 발생시키는 방법으로서,
상기 방법은 사용된 강황 단백질 또는 사용된 강황 전분의 유효량을 상기 포유류에 투여하는 단계를 포함하고, 상기 단백질 및 전분은 하기 단계를 포함하는 공정에 의해 수득되는 것인, 방법:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 20%의 총 용존 고형물(TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계; 및
d) 단계 c)의 단백질이 없는 단계 a)의 사용된 강황 재료-2를 24시간 동안 120 ℃에서 건조시킨 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
- 포유류의 류마티스 관절염을 치료하여, 통증, 종창, 부종을 포함하는 포유류의 류마티스 관절염 증상을 감소시키고, IL-6 및 TNF-α의 혈청 마커를 감소시키는 효과를 발생시키는 방법으로서,
상기 방법은 사용된 강황 단백질 또는 사용된 강황 전분의 유효량을 상기 포유류에 투여하는 단계를 포함하고, 상기 단백질 및 전분은 하기 단계를 포함하는 공정에 의해 수득되는 것인, 방법:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계;
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계;
g) 단계 f)의 단백질이 없는 단계 a)의 사용된 강황 재료-2에 각각 46 ℃ 및 30 ℃에서 4시간 동안 담금 체적의 아세톤 및 메탄올로 세척하여, 미량의 커큐미노이드 및 옥살산 함량을 제거하여 세척된 사용된 강황 재료-2를 형성하는 단계; 및
h) 24시간 동안 단계 g)의 세척된 사용된 강황 재료-2를 건조시켜 잔여 용매를 제거한 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
- 사용된 강황 재료로부터 수득된 단백질 조성물로서,
상기 단백질 조성물은 하기 단계를 포함하는 사용된 강황의 물 추출에 의해 수득되는 것인, 단백질 조성물:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계; 및
c) 고진공 하에서 20%의 총 용존 고형물(TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계.
- 사용된 강황 재료로부터 수득된 단백질 조성물로서,
상기 단백질 조성물은 하기 단계를 포함하는 사용된 강황의 물 추출에 의해 수득되는 것인, 단백질 조성물:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계; 및
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계.
- 소수성 단백질을 갖는 다당류를 포함하는 다당류 조성물로서,
상기 조성물은 하기 단계를 포함하는 공정을 통해 사용된 강황으로부터 수득되는 것인, 다당류 조성물:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계; 및
c) 고진공 하에서 20%의 총 용존 고형물(TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계; 및
d) 단계 c)의 단백질이 없는 단계 a)의 사용된 강황 재료-2를 24시간 동안 120 ℃에서 건조시킨 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
- 소수성 단백질을 갖는 다당류를 포함하는 다당류 조성물로서,
상기 조성물은 하기 단계를 포함하는 공정을 통해 사용된 강황으로부터 수득되는 것인, 다당류 조성물:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계;
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계;
g) 단계 f)의 단백질이 없는 단계 a)의 사용된 강황 재료-2에 각각 46 ℃ 및 30 ℃에서 4시간 동안 담금 체적의 아세톤 및 메탄올로 세척하여, 미량의 커큐미노이드 및 옥살산 함량을 제거하여 세척된 사용된 강황 재료-2를 형성하는 단계; 및
h) 24시간 동안 단계 g)의 세척된 사용된 강황 재료-2를 건조시켜 잔여 용매를 제거한 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
- 식물 단백질 조성물로서,
상기 단백질 조성물은 사용된 강황으로부터 수득되고,
상기 단백질 조성물은 속도 제한 아미노산(rate limiting aminoacid) 시스테인 및 메티오닌을 포함하는 것을 특징으로 하는 것인, 식물 단백질 조성물.
- 식물 다당류 조성물(전분)으로서,
상기 다당류 조성물은 사용된 강황으로부터 수득되고,
α, 1-4 결합(아밀로오스) 및 α, 1-6 결합(아밀로펙틴)에 의해 연결된 90%의 글루코오스 잔기를 갖는 저항성 전분(resistant starch)으로서 소수성 당단백질과 함께 발생하는 것을 특징으로 하는 것인, 식물 다당류 조성물.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020227009200A KR20220041945A (ko) | 2017-07-24 | 2018-07-17 | 사용된 강황 - 이의 방법 및 조성물 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IN201741026215 | 2017-07-24 | ||
| IN201741026215 | 2017-07-24 | ||
| PCT/US2018/042390 WO2019022991A1 (en) | 2017-07-24 | 2018-07-17 | CURCUMA RESIDUES - METHODS AND COMPOSITIONS THEREOF |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227009200A Division KR20220041945A (ko) | 2017-07-24 | 2018-07-17 | 사용된 강황 - 이의 방법 및 조성물 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20200029559A true KR20200029559A (ko) | 2020-03-18 |
Family
ID=65039792
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020207004552A KR20200029559A (ko) | 2017-07-24 | 2018-07-17 | 사용된 강황 - 이의 방법 및 조성물 |
| KR1020227009200A KR20220041945A (ko) | 2017-07-24 | 2018-07-17 | 사용된 강황 - 이의 방법 및 조성물 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227009200A KR20220041945A (ko) | 2017-07-24 | 2018-07-17 | 사용된 강황 - 이의 방법 및 조성물 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US11298395B2 (ko) |
| EP (1) | EP3658161A4 (ko) |
| JP (1) | JP7209691B2 (ko) |
| KR (2) | KR20200029559A (ko) |
| AU (1) | AU2018307222B2 (ko) |
| CA (1) | CA3071190C (ko) |
| WO (1) | WO2019022991A1 (ko) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102237450B1 (ko) * | 2019-08-30 | 2021-04-06 | 한국식품연구원 | 강황잎 추출물을 유효성분으로 포함하는 장기능 개선용 조성물 |
| CN116606385B (zh) * | 2023-04-28 | 2024-04-16 | 广州工程技术职业学院 | 莪术多糖及其制备方法和应用 |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6067428A (ja) * | 1983-09-22 | 1985-04-17 | Takuo Kosuge | 蛋白結合多糖体,その製造法,及び該蛋白結合多糖体を有効成分とする抗腫瘍剤 |
| EP0726074B1 (en) * | 1994-08-03 | 2003-06-25 | A.S.A.C. Pharmaceutical International, A.I.E. | Method for obtaining apolar and polar extracts of curcuma and applications thereof |
| US20020018787A1 (en) | 1999-05-21 | 2002-02-14 | Roger V. Kendall | Methods and compositions for modulating immune response and for the treatment of inflammatory disease |
| ES2154615B1 (es) | 1999-09-23 | 2001-11-16 | Asac Compania De Biotecnologia | Nuevas actividades farmacologicas de los extractos del curcuma longa. |
| WO2004104036A1 (ja) | 2003-05-21 | 2004-12-02 | Fuji Oil Company, Limited | 大豆ホエー蛋白及び大豆ホエー蛋白分解物の製造法 |
| US7205011B2 (en) * | 2003-11-14 | 2007-04-17 | Board Of Regents, Acting For And On Behalf Of, University Of Arizona | Anti-inflammatory activity of a specific turmeric extract |
| US7070816B2 (en) * | 2003-12-05 | 2006-07-04 | New Chapter, Inc. | Methods for treating prostatic intraepithelial neoplasia with herbal compositions |
| US20170042833A1 (en) * | 2014-03-12 | 2017-02-16 | Benny Antony | Formulation of Curcuminoids with Enhanced Bioavailability of Curcumin, Demethoxycurcumin, Bisdemethoxycurcumin and method of preparation and uses thereof |
| AU2007227397A1 (en) * | 2006-03-17 | 2007-09-27 | Herbalscience Singapore Pte. Ltd. | Extracts and methods comprising curcuma species |
| TWI320714B (en) | 2006-09-15 | 2010-02-21 | Dev Center Biotechnology | Plant extracts for the treatment of rheumatoid arthritis |
| TWI504394B (zh) | 2011-04-29 | 2015-10-21 | Ind Tech Res Inst | 安托芬之製備方法 |
| US9345258B2 (en) | 2011-08-25 | 2016-05-24 | Natural Remedies Pvt Ltd. | Synergistic phytochemical composition and a process for preparation thereof |
| US20140010903A1 (en) * | 2012-07-04 | 2014-01-09 | Akay Flavours & Aromatics Pvt Ltd. | Curcuminoid composition with enhanced bioavailability and a process for its preparation |
| KR101495991B1 (ko) * | 2013-03-22 | 2015-02-26 | 한규호 | 울금의 커큐민을 제거한 울금 잔사를 포함하는 식욕억제 및 비만의 예방 또는 치료용 조성물 |
| US20160151440A1 (en) * | 2013-08-19 | 2016-06-02 | Aurea Biolabs Private Limited | A Novel Composition of Curcumin with Enhanced Bioavailability |
| US10323227B2 (en) * | 2014-08-29 | 2019-06-18 | Sami Labs Limited | Process for enhancing the viable counts of lactic acid bacteria and useful compositions thereof |
| US20160256513A1 (en) * | 2015-03-04 | 2016-09-08 | The Synergy Company of Utah, LLC d/b/a Synergy Production Laboratories | Synergized turmeric |
| WO2017195220A1 (en) * | 2016-05-11 | 2017-11-16 | Deshpande Rajendra Sham | Process for extraction of curcuminoids |
-
2018
- 2018-07-17 AU AU2018307222A patent/AU2018307222B2/en active Active
- 2018-07-17 US US16/632,953 patent/US11298395B2/en active Active
- 2018-07-17 WO PCT/US2018/042390 patent/WO2019022991A1/en unknown
- 2018-07-17 CA CA3071190A patent/CA3071190C/en active Active
- 2018-07-17 EP EP18838837.5A patent/EP3658161A4/en active Pending
- 2018-07-17 JP JP2020503985A patent/JP7209691B2/ja active Active
- 2018-07-17 KR KR1020207004552A patent/KR20200029559A/ko not_active IP Right Cessation
- 2018-07-17 KR KR1020227009200A patent/KR20220041945A/ko not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| US11298395B2 (en) | 2022-04-12 |
| JP7209691B2 (ja) | 2023-01-20 |
| EP3658161A4 (en) | 2021-04-21 |
| KR20220041945A (ko) | 2022-04-01 |
| WO2019022991A1 (en) | 2019-01-31 |
| CA3071190C (en) | 2023-02-14 |
| AU2018307222B2 (en) | 2022-02-24 |
| US20200164019A1 (en) | 2020-05-28 |
| EP3658161A1 (en) | 2020-06-03 |
| CA3071190A1 (en) | 2019-01-31 |
| AU2018307222A1 (en) | 2020-03-05 |
| JP2021509660A (ja) | 2021-04-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Pari et al. | Effect of tetrahydrocurcumin on blood glucose, plasma insulin and hepatic key enzymes in streptozotocin induced diabetic rats | |
| Pari et al. | Effect of Cassia auriculata flowers on blood sugar levels, serum and tissue lipids in streptozotocin diabetic rats | |
| Yang et al. | Anti-hyperuricemic and anti-gouty arthritis activities of polysaccharide purified from Lonicera japonica in model rats | |
| Bais et al. | Antiobesity and hypolipidemic activity of Moringa oleifera leaves against high fat diet-induced obesity in rats | |
| Pari et al. | Antidiabetic activity of Boerhaavia diffusa L.: effect on hepatic key enzymes in experimental diabetes | |
| Ravikumar et al. | Hepatoprotective and antioxidant activity of a mangrove plant Lumnitzera racemosa | |
| Chen et al. | Preparation, characterization and anti-diabetic activity of polysaccharides from adlay seed | |
| Lu et al. | Preparation of the controlled acid hydrolysates from pumpkin polysaccharides and their antioxidant and antidiabetic evaluation | |
| Savych et al. | Antioxidant activity in vitro of antidiabetic herbal mixtures | |
| Kumar et al. | Effect of Helicteres isora bark extract on blood glucose and hepatic enzymes in experimental diabetes | |
| KR20200029559A (ko) | 사용된 강황 - 이의 방법 및 조성물 | |
| JP6117333B2 (ja) | 免疫関連疾患及び酸化的ストレス関連疾患の予防または治療用組成物 | |
| Chowdhury et al. | The potential role of mushrooms in the prevention and treatment of diabetes: a review | |
| Arken et al. | Biochemical characterization, and anti-inflammatory and antitumor activities of glycoprotein from lamb abomasum | |
| JP4233029B2 (ja) | マイタケ由来の抽出物およびグリコプロテイン並びにその製造方法 | |
| Huang et al. | Antidiabetic effect of a new peptide from Squalus mitsukurii liver (S‐8300) in streptozocin‐induced diabetic mice | |
| Kavishankar et al. | Hepatoprotective and antioxidant activity of N-Trisaccharide in different experimental rats | |
| CN109106930A (zh) | 抗老化黑姜提取物及其制备方法 | |
| CN113880962A (zh) | 一种无花果多糖及其提取方法和应用 | |
| El-Batal et al. | Ameliorating effect of yeast Glucan with zinc Bisglycinate in Histological and Biochemical changes in γ-irradiated rats | |
| JP2009126856A (ja) | 血中中性脂肪上昇抑制剤 | |
| JP2021512998A (ja) | 分離された白茅根多糖及びその用途 | |
| Gara et al. | Inhibition of key digestive enzymes related to diabetes and protection of β-cell and liver-kidney functions by Hypnea spinella sulfated polysaccharide in diabetic rats | |
| RU2516886C1 (ru) | Средство, обладающее адаптогенной и иммуномодулирующей активностью | |
| JPH10306032A (ja) | 精力増強剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AMND | Amendment | ||
| E902 | Notification of reason for refusal | ||
| AMND | Amendment | ||
| E601 | Decision to refuse application | ||
| X091 | Application refused [patent] | ||
| AMND | Amendment | ||
| X601 | Decision of rejection after re-examination |