KR20180123687A - 맞춤형 시설 - Google Patents
맞춤형 시설 Download PDFInfo
- Publication number
- KR20180123687A KR20180123687A KR1020187028608A KR20187028608A KR20180123687A KR 20180123687 A KR20180123687 A KR 20180123687A KR 1020187028608 A KR1020187028608 A KR 1020187028608A KR 20187028608 A KR20187028608 A KR 20187028608A KR 20180123687 A KR20180123687 A KR 20180123687A
- Authority
- KR
- South Korea
- Prior art keywords
- unit
- module
- shell
- facility
- central
- Prior art date
Links
- 238000004519 manufacturing process Methods 0.000 claims abstract description 85
- 238000000855 fermentation Methods 0.000 claims abstract description 61
- 230000004151 fermentation Effects 0.000 claims abstract description 61
- 238000000034 method Methods 0.000 claims abstract description 33
- 241000700605 Viruses Species 0.000 claims abstract description 19
- 238000004891 communication Methods 0.000 claims abstract description 4
- 239000000825 pharmaceutical preparation Substances 0.000 claims description 8
- 229940127557 pharmaceutical product Drugs 0.000 claims description 8
- 238000004806 packaging method and process Methods 0.000 claims description 7
- 229960000106 biosimilars Drugs 0.000 claims description 5
- 238000002659 cell therapy Methods 0.000 claims description 5
- 238000009472 formulation Methods 0.000 claims description 3
- 239000000203 mixture Substances 0.000 claims description 3
- 210000004027 cell Anatomy 0.000 description 63
- 239000000047 product Substances 0.000 description 50
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 24
- 238000000746 purification Methods 0.000 description 19
- 210000003494 hepatocyte Anatomy 0.000 description 18
- 229960005486 vaccine Drugs 0.000 description 14
- 102000004877 Insulin Human genes 0.000 description 12
- 108090001061 Insulin Proteins 0.000 description 12
- 210000003527 eukaryotic cell Anatomy 0.000 description 12
- 229940125396 insulin Drugs 0.000 description 12
- 108090000765 processed proteins & peptides Proteins 0.000 description 12
- 208000001132 Osteoporosis Diseases 0.000 description 11
- 238000010276 construction Methods 0.000 description 11
- -1 F. oxysporum) Chemical compound 0.000 description 10
- 210000004962 mammalian cell Anatomy 0.000 description 10
- 235000014469 Bacillus subtilis Nutrition 0.000 description 9
- 244000063299 Bacillus subtilis Species 0.000 description 7
- 108010050904 Interferons Proteins 0.000 description 7
- 102000014150 Interferons Human genes 0.000 description 7
- 206010028980 Neoplasm Diseases 0.000 description 7
- 206010057190 Respiratory tract infections Diseases 0.000 description 7
- 238000004113 cell culture Methods 0.000 description 7
- 229940079322 interferon Drugs 0.000 description 7
- 238000002955 isolation Methods 0.000 description 7
- 210000001236 prokaryotic cell Anatomy 0.000 description 7
- 238000003860 storage Methods 0.000 description 7
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 6
- 238000011143 downstream manufacturing Methods 0.000 description 6
- RWSXRVCMGQZWBV-WDSKDSINSA-N glutathione Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O RWSXRVCMGQZWBV-WDSKDSINSA-N 0.000 description 6
- 102000004196 processed proteins & peptides Human genes 0.000 description 6
- 235000018102 proteins Nutrition 0.000 description 6
- 108090000623 proteins and genes Proteins 0.000 description 6
- 102000004169 proteins and genes Human genes 0.000 description 6
- 241000193830 Bacillus <bacterium> Species 0.000 description 5
- 241000196324 Embryophyta Species 0.000 description 5
- 201000011510 cancer Diseases 0.000 description 5
- 238000011049 filling Methods 0.000 description 5
- 239000011521 glass Substances 0.000 description 5
- 238000002347 injection Methods 0.000 description 5
- 239000007924 injection Substances 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- 210000000130 stem cell Anatomy 0.000 description 5
- 238000002560 therapeutic procedure Methods 0.000 description 5
- 238000011282 treatment Methods 0.000 description 5
- 230000003612 virological effect Effects 0.000 description 5
- 241000222122 Candida albicans Species 0.000 description 4
- 108020004414 DNA Proteins 0.000 description 4
- 241000711549 Hepacivirus C Species 0.000 description 4
- 229940095731 candida albicans Drugs 0.000 description 4
- 238000004140 cleaning Methods 0.000 description 4
- 238000009295 crossflow filtration Methods 0.000 description 4
- 239000003814 drug Substances 0.000 description 4
- 239000013586 microbial product Substances 0.000 description 4
- 230000004048 modification Effects 0.000 description 4
- 238000012986 modification Methods 0.000 description 4
- 239000002245 particle Substances 0.000 description 4
- 229920001184 polypeptide Polymers 0.000 description 4
- 206010039073 rheumatoid arthritis Diseases 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- OGBMKVWORPGQRR-UMXFMPSGSA-N teriparatide Chemical compound C([C@H](NC(=O)[C@H](CCSC)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@@H](N)CO)C(C)C)[C@@H](C)CC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC=1N=CNC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1N=CNC=1)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(O)=O)C1=CNC=N1 OGBMKVWORPGQRR-UMXFMPSGSA-N 0.000 description 4
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 3
- 241000222120 Candida <Saccharomycetales> Species 0.000 description 3
- 102000004127 Cytokines Human genes 0.000 description 3
- 108090000695 Cytokines Proteins 0.000 description 3
- 241000588724 Escherichia coli Species 0.000 description 3
- 108010054218 Factor VIII Proteins 0.000 description 3
- 102000001690 Factor VIII Human genes 0.000 description 3
- 108010024636 Glutathione Proteins 0.000 description 3
- 108010047761 Interferon-alpha Proteins 0.000 description 3
- 102000006992 Interferon-alpha Human genes 0.000 description 3
- 241000235058 Komagataella pastoris Species 0.000 description 3
- 108010000817 Leuprolide Proteins 0.000 description 3
- 108090000445 Parathyroid hormone Proteins 0.000 description 3
- 108010049264 Teriparatide Proteins 0.000 description 3
- 230000001464 adherent effect Effects 0.000 description 3
- 229940024606 amino acid Drugs 0.000 description 3
- 150000001413 amino acids Chemical class 0.000 description 3
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 3
- 229960000074 biopharmaceutical Drugs 0.000 description 3
- 238000004587 chromatography analysis Methods 0.000 description 3
- 238000012258 culturing Methods 0.000 description 3
- 238000011018 current good manufacturing practice Methods 0.000 description 3
- 206010012601 diabetes mellitus Diseases 0.000 description 3
- 229960000301 factor viii Drugs 0.000 description 3
- 108020001507 fusion proteins Proteins 0.000 description 3
- 102000037865 fusion proteins Human genes 0.000 description 3
- 239000007789 gas Substances 0.000 description 3
- 229960003180 glutathione Drugs 0.000 description 3
- 238000003306 harvesting Methods 0.000 description 3
- 229940088597 hormone Drugs 0.000 description 3
- 239000005556 hormone Substances 0.000 description 3
- GFIJNRVAKGFPGQ-LIJARHBVSA-N leuprolide Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CC=C(O)C=C1 GFIJNRVAKGFPGQ-LIJARHBVSA-N 0.000 description 3
- 229960004338 leuprorelin Drugs 0.000 description 3
- 229940126601 medicinal product Drugs 0.000 description 3
- 229940115256 melanoma vaccine Drugs 0.000 description 3
- 239000012514 monoclonal antibody product Substances 0.000 description 3
- 229910052760 oxygen Inorganic materials 0.000 description 3
- 239000001301 oxygen Substances 0.000 description 3
- 238000012545 processing Methods 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 230000000699 topical effect Effects 0.000 description 3
- 210000005253 yeast cell Anatomy 0.000 description 3
- HBOMLICNUCNMMY-XLPZGREQSA-N zidovudine Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](N=[N+]=[N-])C1 HBOMLICNUCNMMY-XLPZGREQSA-N 0.000 description 3
- 229960002555 zidovudine Drugs 0.000 description 3
- GHOKWGTUZJEAQD-ZETCQYMHSA-N (D)-(+)-Pantothenic acid Chemical compound OCC(C)(C)[C@@H](O)C(=O)NCCC(O)=O GHOKWGTUZJEAQD-ZETCQYMHSA-N 0.000 description 2
- XBBVURRQGJPTHH-UHFFFAOYSA-N 2-hydroxyacetic acid;2-hydroxypropanoic acid Chemical compound OCC(O)=O.CC(O)C(O)=O XBBVURRQGJPTHH-UHFFFAOYSA-N 0.000 description 2
- 102100021266 Alpha-(1,6)-fucosyltransferase Human genes 0.000 description 2
- 241000271566 Aves Species 0.000 description 2
- 241000894006 Bacteria Species 0.000 description 2
- YNXLOPYTAAFMTN-SBUIBGKBSA-N C([C@H](N)C(=O)N1CCC[C@H]1C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CO)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(N)=O)C1=CC=C(O)C=C1 Chemical compound C([C@H](N)C(=O)N1CCC[C@H]1C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CO)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(N)=O)C1=CC=C(O)C=C1 YNXLOPYTAAFMTN-SBUIBGKBSA-N 0.000 description 2
- 102000055006 Calcitonin Human genes 0.000 description 2
- 108060001064 Calcitonin Proteins 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 108010008165 Etanercept Proteins 0.000 description 2
- 108091006020 Fc-tagged proteins Proteins 0.000 description 2
- 229920002430 Fibre-reinforced plastic Polymers 0.000 description 2
- 241000233866 Fungi Species 0.000 description 2
- CATMPQFFVNKDEY-YPMHNXCESA-N Golotimod Chemical compound C1=CC=C2C(C[C@H](NC(=O)CC[C@@H](N)C(O)=O)C(O)=O)=CNC2=C1 CATMPQFFVNKDEY-YPMHNXCESA-N 0.000 description 2
- 229940033330 HIV vaccine Drugs 0.000 description 2
- 241000238631 Hexapoda Species 0.000 description 2
- 101000819490 Homo sapiens Alpha-(1,6)-fucosyltransferase Proteins 0.000 description 2
- 101000976075 Homo sapiens Insulin Proteins 0.000 description 2
- 206010020751 Hypersensitivity Diseases 0.000 description 2
- 208000019693 Lung disease Diseases 0.000 description 2
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 2
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 2
- 241000191940 Staphylococcus Species 0.000 description 2
- 229910000831 Steel Inorganic materials 0.000 description 2
- 229940124840 Streptococcal vaccine Drugs 0.000 description 2
- 241000223259 Trichoderma Species 0.000 description 2
- 241000499912 Trichoderma reesei Species 0.000 description 2
- 239000000427 antigen Substances 0.000 description 2
- 108091007433 antigens Proteins 0.000 description 2
- 102000036639 antigens Human genes 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 208000010668 atopic eczema Diseases 0.000 description 2
- 230000001580 bacterial effect Effects 0.000 description 2
- 239000010796 biological waste Substances 0.000 description 2
- 239000003114 blood coagulation factor Substances 0.000 description 2
- 238000009435 building construction Methods 0.000 description 2
- 229960004015 calcitonin Drugs 0.000 description 2
- BBBFJLBPOGFECG-VJVYQDLKSA-N calcitonin Chemical compound N([C@H](C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(N)=O)C(C)C)C(=O)[C@@H]1CSSC[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1 BBBFJLBPOGFECG-VJVYQDLKSA-N 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 239000006143 cell culture medium Substances 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 238000013270 controlled release Methods 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 210000004748 cultured cell Anatomy 0.000 description 2
- 238000006298 dechlorination reaction Methods 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 238000011118 depth filtration Methods 0.000 description 2
- 239000012502 diagnostic product Substances 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 238000004821 distillation Methods 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 239000000428 dust Substances 0.000 description 2
- 210000001671 embryonic stem cell Anatomy 0.000 description 2
- 229940088598 enzyme Drugs 0.000 description 2
- 210000001808 exosome Anatomy 0.000 description 2
- 239000011151 fibre-reinforced plastic Substances 0.000 description 2
- 239000011152 fibreglass Substances 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 230000002538 fungal effect Effects 0.000 description 2
- 108010049353 golotimod Proteins 0.000 description 2
- 230000012010 growth Effects 0.000 description 2
- 210000004408 hybridoma Anatomy 0.000 description 2
- 210000004263 induced pluripotent stem cell Anatomy 0.000 description 2
- PBGKTOXHQIOBKM-FHFVDXKLSA-N insulin (human) Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@H]1CSSC[C@H]2C(=O)N[C@H](C(=O)N[C@@H](CO)C(=O)N[C@H](C(=O)N[C@H](C(N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=3C=CC(O)=CC=3)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=3C=CC(O)=CC=3)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=3C=CC(O)=CC=3)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=3NC=NC=3)NC(=O)[C@H](CO)NC(=O)CNC1=O)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(=O)N[C@@H](CC(N)=O)C(O)=O)=O)CSSC[C@@H](C(N2)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@@H](NC(=O)CN)[C@@H](C)CC)[C@@H](C)CC)[C@@H](C)O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@@H](NC(=O)[C@@H](N)CC=1C=CC=CC=1)C(C)C)C1=CN=CN1 PBGKTOXHQIOBKM-FHFVDXKLSA-N 0.000 description 2
- 229940078795 lactoferrin Drugs 0.000 description 2
- 239000002502 liposome Substances 0.000 description 2
- 210000002901 mesenchymal stem cell Anatomy 0.000 description 2
- 244000005700 microbiome Species 0.000 description 2
- 108020004707 nucleic acids Proteins 0.000 description 2
- 150000007523 nucleic acids Chemical class 0.000 description 2
- 102000039446 nucleic acids Human genes 0.000 description 2
- 235000015097 nutrients Nutrition 0.000 description 2
- 108010044644 pegfilgrastim Proteins 0.000 description 2
- 230000010412 perfusion Effects 0.000 description 2
- 239000010817 post-consumer waste Substances 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 238000011027 product recovery Methods 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 239000010935 stainless steel Substances 0.000 description 2
- 229910001220 stainless steel Inorganic materials 0.000 description 2
- 239000010959 steel Substances 0.000 description 2
- 230000001954 sterilising effect Effects 0.000 description 2
- 238000004659 sterilization and disinfection Methods 0.000 description 2
- 229960005460 teriparatide Drugs 0.000 description 2
- 238000012549 training Methods 0.000 description 2
- 238000004065 wastewater treatment Methods 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- SFGFYNXPJMOUHK-PKAFTLKUSA-N (2r)-2-[[(2r)-2-amino-5-(diaminomethylideneamino)pentanoyl]amino]-n-[(2r)-1-[[(2r)-1-[[(2r)-1-[[(2r)-1-[[(2r)-1-[[(2r)-1-[[2-[[(2r)-1-amino-3-(4-hydroxyphenyl)-1-oxopropan-2-yl]amino]-2-oxoethyl]amino]-1-oxohexan-2-yl]amino]-1-oxohexan-2-yl]amino]-1-oxohe Chemical compound NC(N)=NCCC[C@@H](N)C(=O)N[C@H](CCCC)C(=O)N[C@H](CCCC)C(=O)N[C@H](CCCC)C(=O)N[C@H](CCCN=C(N)N)C(=O)N[C@H](CCCC)C(=O)N[C@H](CCCC)C(=O)N[C@H](CCCC)C(=O)NCC(=O)N[C@@H](C(N)=O)CC1=CC=C(O)C=C1 SFGFYNXPJMOUHK-PKAFTLKUSA-N 0.000 description 1
- KATZUZNTRINHDT-HALMFYTRSA-N (2s)-1-[(2s)-2-[[(2s)-2-[[(2r)-2-[[(2s)-2-[[(2s)-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-acetamido-3-naphthalen-2-ylpropanoyl]amino]-3-(4-chlorophenyl)propanoyl]amino]-3-pyridin-3-ylpropanoyl]amino]-3-hydroxypropanoyl]-methylamino]-3-(4-hydroxyphenyl)propanoyl]amino Chemical compound C([C@@H](C(=O)N[C@H](CCCCNC(N)=O)C(=O)N[C@@H](CCCC)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N1[C@@H](CCC1)C(=O)N[C@H](C)C(N)=O)N(C)C(=O)[C@H](CO)NC(=O)[C@@H](CC=1C=NC=CC=1)NC(=O)[C@@H](CC=1C=CC(Cl)=CC=1)NC(=O)[C@@H](CC=1C=C2C=CC=CC2=CC=1)NC(C)=O)C1=CC=C(O)C=C1 KATZUZNTRINHDT-HALMFYTRSA-N 0.000 description 1
- RIWLPSIAFBLILR-WVNGMBSFSA-N (2s)-1-[(2s)-2-[[(2s,3s)-2-[[(2s)-2-[[(2s,3r)-2-[[(2r,3s)-2-[[(2s)-2-[[2-[[2-[acetyl(methyl)amino]acetyl]amino]acetyl]amino]-3-methylbutanoyl]amino]-3-methylpentanoyl]amino]-3-hydroxybutanoyl]amino]pentanoyl]amino]-3-methylpentanoyl]amino]-5-(diaminomethy Chemical compound CC(=O)N(C)CC(=O)NCC(=O)N[C@@H](C(C)C)C(=O)N[C@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N1CCC[C@H]1C(=O)NCC RIWLPSIAFBLILR-WVNGMBSFSA-N 0.000 description 1
- CUCSSYAUKKIDJV-FAXBSAIASA-N (2s)-2-[[(2r)-2-[[(2s)-2-[[(2r)-2-[[(2s)-2-amino-5-(diaminomethylideneamino)pentanoyl]amino]-3-(1h-indol-3-yl)propanoyl]-methylamino]-3-phenylpropanoyl]amino]-3-(1h-indol-3-yl)propanoyl]amino]-n-[(2s)-1-amino-4-methylsulfanyl-1-oxobutan-2-yl]-4-methylpent Chemical compound C([C@@H](C(=O)N[C@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(N)=O)N(C)C(=O)[C@@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@@H](N)CCCN=C(N)N)C1=CC=CC=C1 CUCSSYAUKKIDJV-FAXBSAIASA-N 0.000 description 1
- JDKLPDJLXHXHNV-MFVUMRCOSA-N (3s,6s,9r,12s,15s,23s)-15-[[(2s)-2-acetamidohexanoyl]amino]-9-benzyl-6-[3-(diaminomethylideneamino)propyl]-12-(1h-imidazol-5-ylmethyl)-3-(1h-indol-3-ylmethyl)-2,5,8,11,14,17-hexaoxo-1,4,7,10,13,18-hexazacyclotricosane-23-carboxamide Chemical compound C([C@@H]1C(=O)N[C@@H](CCCN=C(N)N)C(=O)N[C@@H](CC=2C3=CC=CC=C3NC=2)C(=O)N[C@@H](CCCCNC(=O)C[C@@H](C(N[C@@H](CC=2NC=NC=2)C(=O)N1)=O)NC(=O)[C@@H](NC(C)=O)CCCC)C(N)=O)C1=CC=CC=C1 JDKLPDJLXHXHNV-MFVUMRCOSA-N 0.000 description 1
- SNAJPQVDGYDQSW-DYCFWDQMSA-N (4r,7s,10r,13s,16r)-7-(4-aminobutyl)-n-[(2s,3r)-1-amino-3-hydroxy-1-oxobutan-2-yl]-16-[[(2r)-2-amino-3-phenylpropanoyl]amino]-13-[(4-hydroxyphenyl)methyl]-10-(1h-indol-3-ylmethyl)-6,9,12,15-tetraoxo-1,2-dithia-5,8,11,14-tetrazacycloheptadecane-4-carboxami Chemical compound C([C@@H](N)C(=O)N[C@H]1CSSC[C@H](NC(=O)[C@H](CCCCN)NC(=O)[C@@H](CC=2C3=CC=CC=C3NC=2)NC(=O)[C@H](CC=2C=CC(O)=CC=2)NC1=O)C(=O)N[C@@H]([C@H](O)C)C(N)=O)C1=CC=CC=C1 SNAJPQVDGYDQSW-DYCFWDQMSA-N 0.000 description 1
- DEQANNDTNATYII-OULOTJBUSA-N (4r,7s,10s,13r,16s,19r)-10-(4-aminobutyl)-19-[[(2r)-2-amino-3-phenylpropanoyl]amino]-16-benzyl-n-[(2r,3r)-1,3-dihydroxybutan-2-yl]-7-[(1r)-1-hydroxyethyl]-13-(1h-indol-3-ylmethyl)-6,9,12,15,18-pentaoxo-1,2-dithia-5,8,11,14,17-pentazacycloicosane-4-carboxa Chemical compound C([C@@H](N)C(=O)N[C@H]1CSSC[C@H](NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCCCN)NC(=O)[C@@H](CC=2C3=CC=CC=C3NC=2)NC(=O)[C@H](CC=2C=CC=CC=2)NC1=O)C(=O)N[C@H](CO)[C@H](O)C)C1=CC=CC=C1 DEQANNDTNATYII-OULOTJBUSA-N 0.000 description 1
- PUDHBTGHUJUUFI-SCTWWAJVSA-N (4r,7s,10s,13r,16s,19r)-10-(4-aminobutyl)-n-[(2s,3r)-1-amino-3-hydroxy-1-oxobutan-2-yl]-19-[[(2r)-2-amino-3-naphthalen-2-ylpropanoyl]amino]-16-[(4-hydroxyphenyl)methyl]-13-(1h-indol-3-ylmethyl)-6,9,12,15,18-pentaoxo-7-propan-2-yl-1,2-dithia-5,8,11,14,17-p Chemical compound C([C@H]1C(=O)N[C@H](CC=2C3=CC=CC=C3NC=2)C(=O)N[C@@H](CCCCN)C(=O)N[C@H](C(N[C@@H](CSSC[C@@H](C(=O)N1)NC(=O)[C@H](N)CC=1C=C2C=CC=CC2=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(N)=O)=O)C(C)C)C1=CC=C(O)C=C1 PUDHBTGHUJUUFI-SCTWWAJVSA-N 0.000 description 1
- PHEWVCZHSBTZFX-DBCSJUPNSA-N (4s)-4-[[2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-amino-3-hydroxypropanoyl]amino]-3-(1h-imidazol-5-yl)propanoyl]amino]-4-methylpentanoyl]amino]-3-methylbutanoyl]amino]-4-carboxybutanoyl]amino]pro Chemical compound NC(N)=NCCC[C@@H](C(=O)NCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@@H](N)CO)CC1=CN=CN1 PHEWVCZHSBTZFX-DBCSJUPNSA-N 0.000 description 1
- 101710149439 20 kDa chaperonin, chloroplastic Proteins 0.000 description 1
- UHPMCKVQTMMPCG-UHFFFAOYSA-N 5,8-dihydroxy-2-methoxy-6-methyl-7-(2-oxopropyl)naphthalene-1,4-dione Chemical compound CC1=C(CC(C)=O)C(O)=C2C(=O)C(OC)=CC(=O)C2=C1O UHPMCKVQTMMPCG-UHFFFAOYSA-N 0.000 description 1
- 108010077593 ACE-011 Proteins 0.000 description 1
- 229940023859 AIDSVAX Drugs 0.000 description 1
- 108010093583 ART123 Proteins 0.000 description 1
- 241001019659 Acremonium <Plectosphaerellaceae> Species 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 102400000068 Angiostatin Human genes 0.000 description 1
- 108010079709 Angiostatins Proteins 0.000 description 1
- 102000004411 Antithrombin III Human genes 0.000 description 1
- 108090000935 Antithrombin III Proteins 0.000 description 1
- 241000219194 Arabidopsis Species 0.000 description 1
- 240000002900 Arthrospira platensis Species 0.000 description 1
- 235000016425 Arthrospira platensis Nutrition 0.000 description 1
- 241000228212 Aspergillus Species 0.000 description 1
- 241001225321 Aspergillus fumigatus Species 0.000 description 1
- 241000228245 Aspergillus niger Species 0.000 description 1
- 240000006439 Aspergillus oryzae Species 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- 108700001281 BIM 51077 Proteins 0.000 description 1
- 241000193744 Bacillus amyloliquefaciens Species 0.000 description 1
- 241000194107 Bacillus megaterium Species 0.000 description 1
- 241000276408 Bacillus subtilis subsp. subtilis str. 168 Species 0.000 description 1
- 241000193388 Bacillus thuringiensis Species 0.000 description 1
- 108010039209 Blood Coagulation Factors Proteins 0.000 description 1
- 102000015081 Blood Coagulation Factors Human genes 0.000 description 1
- 108030001720 Bontoxilysin Proteins 0.000 description 1
- 101710117542 Botulinum neurotoxin type A Proteins 0.000 description 1
- 108010048913 CTCE-0214 Proteins 0.000 description 1
- 108010053045 CTCE-9908 Proteins 0.000 description 1
- 102100038518 Calcitonin Human genes 0.000 description 1
- 108090000932 Calcitonin Gene-Related Peptide Proteins 0.000 description 1
- 101100348617 Candida albicans (strain SC5314 / ATCC MYA-2876) NIK1 gene Proteins 0.000 description 1
- 244000025254 Cannabis sativa Species 0.000 description 1
- 241001214176 Capros Species 0.000 description 1
- 101710132601 Capsid protein Proteins 0.000 description 1
- 108010078791 Carrier Proteins Proteins 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- GHOKWGTUZJEAQD-UHFFFAOYSA-N Chick antidermatitis factor Natural products OCC(C)(C)C(O)C(=O)NCCC(O)=O GHOKWGTUZJEAQD-UHFFFAOYSA-N 0.000 description 1
- 241000195649 Chlorella <Chlorellales> Species 0.000 description 1
- 108010089448 Cholecystokinin B Receptor Proteins 0.000 description 1
- 241000123346 Chrysosporium Species 0.000 description 1
- 101710177832 Co-chaperonin GroES Proteins 0.000 description 1
- 102000029816 Collagenase Human genes 0.000 description 1
- 108060005980 Collagenase Proteins 0.000 description 1
- 101000944206 Conus geographus Conantokin-G Proteins 0.000 description 1
- 241000287781 Crassicarpon thermophilum Species 0.000 description 1
- 241000699802 Cricetulus griseus Species 0.000 description 1
- 241000195493 Cryptophyta Species 0.000 description 1
- 240000008067 Cucumis sativus Species 0.000 description 1
- 235000009849 Cucumis sativus Nutrition 0.000 description 1
- 241001464430 Cyanobacterium Species 0.000 description 1
- 201000003883 Cystic fibrosis Diseases 0.000 description 1
- 108010068294 CytoFab Proteins 0.000 description 1
- 108010049954 DRF 7295 Proteins 0.000 description 1
- 108010000437 Deamino Arginine Vasopressin Proteins 0.000 description 1
- 201000004624 Dermatitis Diseases 0.000 description 1
- 208000008960 Diabetic foot Diseases 0.000 description 1
- 208000003556 Dry Eye Syndromes Diseases 0.000 description 1
- 206010013774 Dry eye Diseases 0.000 description 1
- 241001415140 Dunalia Species 0.000 description 1
- 108010003953 EP-2104R Proteins 0.000 description 1
- 108010040545 ETC 642 Proteins 0.000 description 1
- 102400001047 Endostatin Human genes 0.000 description 1
- 108010079505 Endostatins Proteins 0.000 description 1
- 108090000394 Erythropoietin Proteins 0.000 description 1
- 102000003951 Erythropoietin Human genes 0.000 description 1
- 108010011459 Exenatide Proteins 0.000 description 1
- HTQBXNHDCUEHJF-XWLPCZSASA-N Exenatide Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)NCC(=O)NCC(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 HTQBXNHDCUEHJF-XWLPCZSASA-N 0.000 description 1
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 description 1
- 102100024785 Fibroblast growth factor 2 Human genes 0.000 description 1
- 108090000385 Fibroblast growth factor 7 Proteins 0.000 description 1
- 102000003972 Fibroblast growth factor 7 Human genes 0.000 description 1
- 241000223218 Fusarium Species 0.000 description 1
- 241000223221 Fusarium oxysporum Species 0.000 description 1
- 108010027258 GEM 21S Proteins 0.000 description 1
- 108010003795 GW002 peptide Proteins 0.000 description 1
- 102000052874 Gastrin receptors Human genes 0.000 description 1
- 108010072051 Glatiramer Acetate Proteins 0.000 description 1
- 102400000321 Glucagon Human genes 0.000 description 1
- 108060003199 Glucagon Proteins 0.000 description 1
- 244000068988 Glycine max Species 0.000 description 1
- 235000010469 Glycine max Nutrition 0.000 description 1
- 108010069236 Goserelin Proteins 0.000 description 1
- BLCLNMBMMGCOAS-URPVMXJPSA-N Goserelin Chemical compound C([C@@H](C(=O)N[C@H](COC(C)(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N1[C@@H](CCC1)C(=O)NNC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 BLCLNMBMMGCOAS-URPVMXJPSA-N 0.000 description 1
- 108010051696 Growth Hormone Proteins 0.000 description 1
- 102000001554 Hemoglobins Human genes 0.000 description 1
- 108010054147 Hemoglobins Proteins 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000977692 Homo sapiens Iroquois-class homeodomain protein IRX-6 Proteins 0.000 description 1
- 101001063991 Homo sapiens Leptin Proteins 0.000 description 1
- 101000578784 Homo sapiens Melanoma antigen recognized by T-cells 1 Proteins 0.000 description 1
- 101000767631 Human papillomavirus type 16 Protein E7 Proteins 0.000 description 1
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 1
- 108010043766 IRX 2 Proteins 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 108010065920 Insulin Lispro Proteins 0.000 description 1
- 108010078049 Interferon alpha-2 Proteins 0.000 description 1
- 102100039350 Interferon alpha-7 Human genes 0.000 description 1
- 108010005716 Interferon beta-1a Proteins 0.000 description 1
- 108010005714 Interferon beta-1b Proteins 0.000 description 1
- 102000003996 Interferon-beta Human genes 0.000 description 1
- 108090000467 Interferon-beta Proteins 0.000 description 1
- 108010002386 Interleukin-3 Proteins 0.000 description 1
- 102100039064 Interleukin-3 Human genes 0.000 description 1
- 102000004388 Interleukin-4 Human genes 0.000 description 1
- 108090000978 Interleukin-4 Proteins 0.000 description 1
- 102100023527 Iroquois-class homeodomain protein IRX-6 Human genes 0.000 description 1
- 241000235649 Kluyveromyces Species 0.000 description 1
- 241001138401 Kluyveromyces lactis Species 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- 241000186660 Lactobacillus Species 0.000 description 1
- 108010063045 Lactoferrin Proteins 0.000 description 1
- 102000010445 Lactoferrin Human genes 0.000 description 1
- 102000004882 Lipase Human genes 0.000 description 1
- 108090001060 Lipase Proteins 0.000 description 1
- 239000004367 Lipase Substances 0.000 description 1
- 108010028921 Lipopeptides Proteins 0.000 description 1
- YSDQQAXHVYUZIW-QCIJIYAXSA-N Liraglutide Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCNC(=O)CC[C@H](NC(=O)CCCCCCCCCCCCCCC)C(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=C(O)C=C1 YSDQQAXHVYUZIW-QCIJIYAXSA-N 0.000 description 1
- 108010019598 Liraglutide Proteins 0.000 description 1
- XVVOERDUTLJJHN-UHFFFAOYSA-N Lixisenatide Chemical compound C=1NC2=CC=CC=C2C=1CC(C(=O)NC(CC(C)C)C(=O)NC(CCCCN)C(=O)NC(CC(N)=O)C(=O)NCC(=O)NCC(=O)N1C(CCC1)C(=O)NC(CO)C(=O)NC(CO)C(=O)NCC(=O)NC(C)C(=O)N1C(CCC1)C(=O)N1C(CCC1)C(=O)NC(CO)C(=O)NC(CCCCN)C(=O)NC(CCCCN)C(=O)NC(CCCCN)C(=O)NC(CCCCN)C(=O)NC(CCCCN)C(=O)NC(CCCCN)C(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)CC)NC(=O)C(NC(=O)C(CC(C)C)NC(=O)C(CCCNC(N)=N)NC(=O)C(NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(CCC(O)=O)NC(=O)C(CCC(O)=O)NC(=O)C(CCSC)NC(=O)C(CCC(N)=O)NC(=O)C(CCCCN)NC(=O)C(CO)NC(=O)C(CC(C)C)NC(=O)C(CC(O)=O)NC(=O)C(CO)NC(=O)C(NC(=O)C(CC=1C=CC=CC=1)NC(=O)C(NC(=O)CNC(=O)C(CCC(O)=O)NC(=O)CNC(=O)C(N)CC=1NC=NC=1)C(C)O)C(C)O)C(C)C)CC1=CC=CC=C1 XVVOERDUTLJJHN-UHFFFAOYSA-N 0.000 description 1
- 108060001084 Luciferase Proteins 0.000 description 1
- 239000005089 Luciferase Substances 0.000 description 1
- 241000219745 Lupinus Species 0.000 description 1
- 102000009151 Luteinizing Hormone Human genes 0.000 description 1
- 108010073521 Luteinizing Hormone Proteins 0.000 description 1
- 235000007688 Lycopersicon esculentum Nutrition 0.000 description 1
- 108010016230 MBP-8298 Proteins 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 240000004658 Medicago sativa Species 0.000 description 1
- 235000017587 Medicago sativa ssp. sativa Nutrition 0.000 description 1
- 102100022430 Melanocyte protein PMEL Human genes 0.000 description 1
- 102100028389 Melanoma antigen recognized by T-cells 1 Human genes 0.000 description 1
- 201000009906 Meningitis Diseases 0.000 description 1
- YFGBQHOOROIVKG-FKBYEOEOSA-N Met-enkephalin Chemical compound C([C@@H](C(=O)N[C@@H](CCSC)C(O)=O)NC(=O)CNC(=O)CNC(=O)[C@@H](N)CC=1C=CC(O)=CC=1)C1=CC=CC=C1 YFGBQHOOROIVKG-FKBYEOEOSA-N 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 1
- 229920001410 Microfiber Polymers 0.000 description 1
- 102000029749 Microtubule Human genes 0.000 description 1
- 108091022875 Microtubule Proteins 0.000 description 1
- 108010072915 NAc-Sar-Gly-Val-(d-allo-Ile)-Thr-Nva-Ile-Arg-ProNEt Proteins 0.000 description 1
- 108010083255 NBI6024 Proteins 0.000 description 1
- 229940038430 NY-ESO-1 vaccine Drugs 0.000 description 1
- 101100287577 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) gpe-1 gene Proteins 0.000 description 1
- 244000061176 Nicotiana tabacum Species 0.000 description 1
- 235000002637 Nicotiana tabacum Nutrition 0.000 description 1
- 241000199478 Ochromonas Species 0.000 description 1
- 108010016076 Octreotide Proteins 0.000 description 1
- 241000320412 Ogataea angusta Species 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 102000003982 Parathyroid hormone Human genes 0.000 description 1
- 235000002233 Penicillium roqueforti Nutrition 0.000 description 1
- 108010088847 Peptide YY Proteins 0.000 description 1
- 102100029909 Peptide YY Human genes 0.000 description 1
- 108091007643 Phosphate carriers Proteins 0.000 description 1
- 241000235648 Pichia Species 0.000 description 1
- 206010035226 Plasma cell myeloma Diseases 0.000 description 1
- 241000224016 Plasmodium Species 0.000 description 1
- 229920005372 Plexiglas® Polymers 0.000 description 1
- 206010035664 Pneumonia Diseases 0.000 description 1
- 108700019404 Pro-Gly-Pro- ACTH (4-7) Proteins 0.000 description 1
- 101100528525 Prochlorococcus marinus (strain SARG / CCMP1375 / SS120) rnc gene Proteins 0.000 description 1
- 241000589517 Pseudomonas aeruginosa Species 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- 229940123452 Rapid-acting insulin Drugs 0.000 description 1
- 102000018120 Recombinases Human genes 0.000 description 1
- 108010091086 Recombinases Proteins 0.000 description 1
- 206010038743 Restlessness Diseases 0.000 description 1
- 206010039085 Rhinitis allergic Diseases 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 241000235070 Saccharomyces Species 0.000 description 1
- 101100007329 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) COS1 gene Proteins 0.000 description 1
- 101100221606 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) COS7 gene Proteins 0.000 description 1
- 241000607142 Salmonella Species 0.000 description 1
- 108010026951 Short-Acting Insulin Proteins 0.000 description 1
- 108020004459 Small interfering RNA Proteins 0.000 description 1
- 240000003768 Solanum lycopersicum Species 0.000 description 1
- 244000061456 Solanum tuberosum Species 0.000 description 1
- 235000002595 Solanum tuberosum Nutrition 0.000 description 1
- 102100038803 Somatotropin Human genes 0.000 description 1
- 101710145796 Staphylokinase Proteins 0.000 description 1
- 241000194017 Streptococcus Species 0.000 description 1
- 241000187747 Streptomyces Species 0.000 description 1
- 101800001271 Surface protein Proteins 0.000 description 1
- 108010028908 TP 9201 Proteins 0.000 description 1
- 108010039185 Tenecteplase Proteins 0.000 description 1
- 244000299461 Theobroma cacao Species 0.000 description 1
- 235000005764 Theobroma cacao ssp. cacao Nutrition 0.000 description 1
- 235000005767 Theobroma cacao ssp. sphaerocarpum Nutrition 0.000 description 1
- 241000011102 Thera Species 0.000 description 1
- 108090000190 Thrombin Proteins 0.000 description 1
- 102000005763 Thrombopoietin Receptors Human genes 0.000 description 1
- 108010070774 Thrombopoietin Receptors Proteins 0.000 description 1
- 108090000373 Tissue Plasminogen Activator Proteins 0.000 description 1
- 102000003978 Tissue Plasminogen Activator Human genes 0.000 description 1
- 108700019146 Transgenes Proteins 0.000 description 1
- 101100472152 Trypanosoma brucei brucei (strain 927/4 GUTat10.1) REL1 gene Proteins 0.000 description 1
- 102100039094 Tyrosinase Human genes 0.000 description 1
- 108060008724 Tyrosinase Proteins 0.000 description 1
- 241001123668 Verticillium dahliae Species 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- 108010045610 ZT-031 Proteins 0.000 description 1
- FHEAIOHRHQGZPC-KIWGSFCNSA-N acetic acid;(2s)-2-amino-3-(4-hydroxyphenyl)propanoic acid;(2s)-2-aminopentanedioic acid;(2s)-2-aminopropanoic acid;(2s)-2,6-diaminohexanoic acid Chemical compound CC(O)=O.C[C@H](N)C(O)=O.NCCCC[C@H](N)C(O)=O.OC(=O)[C@@H](N)CCC(O)=O.OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 FHEAIOHRHQGZPC-KIWGSFCNSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- YAJCHEVQCOHZDC-QMMNLEPNSA-N actrapid Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@H]1CSSC[C@H]2C(=O)N[C@H](C(=O)N[C@@H](CO)C(=O)N[C@H](C(=O)N[C@@H](C(N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=3C=CC(O)=CC=3)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=3C=CC(O)=CC=3)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=3C=CC(O)=CC=3)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=3N=CNC=3)NC(=O)[C@H](CO)NC(=O)CNC1=O)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H]([C@H](C)O)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@H](C)O)C(O)=O)C(=O)N[C@@H](CC(N)=O)C(O)=O)=O)CSSC[C@@H](C(N2)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@@H](NC(=O)CN)[C@H](C)CC)[C@H](C)CC)[C@H](C)O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@@H](NC(=O)[C@@H](N)CC=1C=CC=CC=1)C(C)C)C(N)=O)C1=CNC=N1 YAJCHEVQCOHZDC-QMMNLEPNSA-N 0.000 description 1
- 230000003044 adaptive effect Effects 0.000 description 1
- 208000009956 adenocarcinoma Diseases 0.000 description 1
- 210000004504 adult stem cell Anatomy 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 238000004378 air conditioning Methods 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 230000000172 allergic effect Effects 0.000 description 1
- 201000010105 allergic rhinitis Diseases 0.000 description 1
- 102000005840 alpha-Galactosidase Human genes 0.000 description 1
- 108010030291 alpha-Galactosidase Proteins 0.000 description 1
- 229960003318 alteplase Drugs 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000001093 anti-cancer Effects 0.000 description 1
- 230000036436 anti-hiv Effects 0.000 description 1
- 230000003579 anti-obesity Effects 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 229960005348 antithrombin iii Drugs 0.000 description 1
- 108010055530 arginyl-tryptophyl-N-methylphenylalanyl-tryptophyl-leucyl-methioninamide Proteins 0.000 description 1
- 229940009098 aspartate Drugs 0.000 description 1
- FZCSTZYAHCUGEM-UHFFFAOYSA-N aspergillomarasmine B Natural products OC(=O)CNC(C(O)=O)CNC(C(O)=O)CC(O)=O FZCSTZYAHCUGEM-UHFFFAOYSA-N 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 229940120638 avastin Drugs 0.000 description 1
- 229940003504 avonex Drugs 0.000 description 1
- 229940097012 bacillus thuringiensis Drugs 0.000 description 1
- 238000011021 bench scale process Methods 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 229940021459 betaseron Drugs 0.000 description 1
- 239000003833 bile salt Substances 0.000 description 1
- 239000007844 bleaching agent Substances 0.000 description 1
- 230000023555 blood coagulation Effects 0.000 description 1
- 230000010478 bone regeneration Effects 0.000 description 1
- 229940089093 botox Drugs 0.000 description 1
- 231100001103 botulinum neurotoxin Toxicity 0.000 description 1
- 235000008429 bread Nutrition 0.000 description 1
- 239000012512 bulk drug substance Substances 0.000 description 1
- 235000001046 cacaotero Nutrition 0.000 description 1
- 239000003518 caustics Substances 0.000 description 1
- 239000000919 ceramic Substances 0.000 description 1
- RCTCWZRPYFBGLQ-KVBIMOIYSA-N chembl2105639 Chemical compound C([C@@H](C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@H]([C@@H](C)CC)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@@H](NC(=O)[C@@H](NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](N)CC(O)=O)C(C)C)C(C)C)C1=CC=CC=C1 RCTCWZRPYFBGLQ-KVBIMOIYSA-N 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229960002424 collagenase Drugs 0.000 description 1
- HTBKFGWATIYCSF-QGXIKSNHSA-N conantokin g Chemical compound NC(=O)C[C@@H](C(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CC(C(O)=O)C(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C(O)=O)C(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C(O)=O)C(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C(O)=O)C(O)=O)NC(=O)[C@H](CC(C(O)=O)C(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)CN HTBKFGWATIYCSF-QGXIKSNHSA-N 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- KJQOYUHYAZGPIZ-PIJHVLQJSA-N conotoxin vc1.1 Chemical compound C([C@H]1C(=O)N2CCC[C@H]2C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@H](C(N[C@@H](CSSC[C@@H]2NC(=O)[C@@H](NC(=O)CN)CSSC[C@H](NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@@H]3CCCN3C(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC2=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N[C@@H](CC(O)=O)C(=O)N1)C(N)=O)=O)[C@@H](C)CC)C1=CN=CN1 KJQOYUHYAZGPIZ-PIJHVLQJSA-N 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 238000012864 cross contamination Methods 0.000 description 1
- VUYRSKROGTWHDC-HZGLMRDYSA-N ctce 9908 Chemical compound C([C@H](NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)CNC(=O)[C@@H](N)CCCCN)C(C)C)CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCCCC[C@H](NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)CNC(=O)[C@@H](N)CCCCN)C(C)C)C(N)=O)C1=CC=C(O)C=C1 VUYRSKROGTWHDC-HZGLMRDYSA-N 0.000 description 1
- 230000009849 deactivation Effects 0.000 description 1
- 230000023753 dehiscence Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 229960004281 desmopressin Drugs 0.000 description 1
- NFLWUMRGJYTJIN-NXBWRCJVSA-N desmopressin Chemical compound C([C@H]1C(=O)N[C@H](C(N[C@@H](CC(N)=O)C(=O)N[C@@H](CSSCCC(=O)N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(N)=O)=O)CCC(=O)N)C1=CC=CC=C1 NFLWUMRGJYTJIN-NXBWRCJVSA-N 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- VGGRNGOEDNBLPH-YJHCMWSWSA-N diapep277 Chemical compound CC(C)[C@H](N)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)NCC(=O)NCC(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N1CCC[C@H]1C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@H](C(=O)N[C@@H](C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(O)=O)CCC1 VGGRNGOEDNBLPH-YJHCMWSWSA-N 0.000 description 1
- DCOPUUMXTXDBNB-UHFFFAOYSA-N diclofenac Chemical compound OC(=O)CC1=CC=CC=C1NC1=C(Cl)C=CC=C1Cl DCOPUUMXTXDBNB-UHFFFAOYSA-N 0.000 description 1
- 229960001259 diclofenac Drugs 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 229940073621 enbrel Drugs 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 108010067416 epoetin delta Proteins 0.000 description 1
- 229950002109 epoetin delta Drugs 0.000 description 1
- 229940105423 erythropoietin Drugs 0.000 description 1
- 229960000403 etanercept Drugs 0.000 description 1
- XAVJHWWXMYRTDC-UHFFFAOYSA-N europine Natural products COC(C)C(O)(C(=O)OCC1CCN2CCC(O)C12)C(C)(C)O XAVJHWWXMYRTDC-UHFFFAOYSA-N 0.000 description 1
- 229960001519 exenatide Drugs 0.000 description 1
- 238000013265 extended release Methods 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 230000008014 freezing Effects 0.000 description 1
- 238000001415 gene therapy Methods 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 229960003776 glatiramer acetate Drugs 0.000 description 1
- MASNOZXLGMXCHN-ZLPAWPGGSA-N glucagon Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 MASNOZXLGMXCHN-ZLPAWPGGSA-N 0.000 description 1
- 229960004666 glucagon Drugs 0.000 description 1
- 108091005608 glycosylated proteins Proteins 0.000 description 1
- 102000035122 glycosylated proteins Human genes 0.000 description 1
- 230000013595 glycosylation Effects 0.000 description 1
- 238000006206 glycosylation reaction Methods 0.000 description 1
- 238000011194 good manufacturing practice Methods 0.000 description 1
- 229960002913 goserelin Drugs 0.000 description 1
- 210000005256 gram-negative cell Anatomy 0.000 description 1
- 210000005255 gram-positive cell Anatomy 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 239000000122 growth hormone Substances 0.000 description 1
- 230000035876 healing Effects 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 1
- 230000002440 hepatic effect Effects 0.000 description 1
- 229940022353 herceptin Drugs 0.000 description 1
- 239000012510 hollow fiber Substances 0.000 description 1
- WNRQPCUGRUFHED-DETKDSODSA-N humalog Chemical compound C([C@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CS)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@H](CO)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CS)NC(=O)[C@H](CS)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@@H](NC(=O)CN)[C@@H](C)CC)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(O)=O)C1=CC=C(O)C=C1.C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CS)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(C)C)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CS)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@@H](NC(=O)[C@@H](N)CC=1C=CC=CC=1)C(C)C)C1=CN=CN1 WNRQPCUGRUFHED-DETKDSODSA-N 0.000 description 1
- 102000049953 human LEP Human genes 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 229940048921 humira Drugs 0.000 description 1
- 210000004754 hybrid cell Anatomy 0.000 description 1
- 230000009610 hypersensitivity Effects 0.000 description 1
- 239000012729 immediate-release (IR) formulation Substances 0.000 description 1
- 238000009169 immunotherapy Methods 0.000 description 1
- 229940032219 immunotherapy vaccine Drugs 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 229910001026 inconel Inorganic materials 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 229960002068 insulin lispro Drugs 0.000 description 1
- 229960001388 interferon-beta Drugs 0.000 description 1
- 229940028885 interleukin-4 Drugs 0.000 description 1
- 239000000543 intermediate Substances 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 210000004153 islets of langerhan Anatomy 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- CSSYQJWUGATIHM-IKGCZBKSSA-N l-phenylalanyl-l-lysyl-l-cysteinyl-l-arginyl-l-arginyl-l-tryptophyl-l-glutaminyl-l-tryptophyl-l-arginyl-l-methionyl-l-lysyl-l-lysyl-l-leucylglycyl-l-alanyl-l-prolyl-l-seryl-l-isoleucyl-l-threonyl-l-cysteinyl-l-valyl-l-arginyl-l-arginyl-l-alanyl-l-phenylal Chemical compound C([C@H](N)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](C)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CS)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(O)=O)C1=CC=CC=C1 CSSYQJWUGATIHM-IKGCZBKSSA-N 0.000 description 1
- 229940039696 lactobacillus Drugs 0.000 description 1
- 235000021242 lactoferrin Nutrition 0.000 description 1
- 108010021336 lanreotide Proteins 0.000 description 1
- 229960002437 lanreotide Drugs 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 108010024409 linaclotide Proteins 0.000 description 1
- KXGCNMMJRFDFNR-WDRJZQOASA-N linaclotide Chemical compound C([C@H](NC(=O)[C@@H]1CSSC[C@H]2C(=O)N[C@H]3CSSC[C@H](N)C(=O)N[C@H](C(N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N2)=O)CSSC[C@H](NC(=O)[C@H](C)NC(=O)[C@@H]2CCCN2C(=O)[C@H](CC(N)=O)NC3=O)C(=O)N[C@H](C(NCC(=O)N1)=O)[C@H](O)C)C(O)=O)C1=CC=C(O)C=C1 KXGCNMMJRFDFNR-WDRJZQOASA-N 0.000 description 1
- 229960000812 linaclotide Drugs 0.000 description 1
- 235000019421 lipase Nutrition 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- 229960002701 liraglutide Drugs 0.000 description 1
- 108010004367 lixisenatide Proteins 0.000 description 1
- 229960001093 lixisenatide Drugs 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 229940040129 luteinizing hormone Drugs 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 229940124735 malaria vaccine Drugs 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 108010080780 melanotan-II Proteins 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 229910001092 metal group alloy Inorganic materials 0.000 description 1
- 125000001360 methionine group Chemical group N[C@@H](CCSC)C(=O)* 0.000 description 1
- 238000001471 micro-filtration Methods 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 239000003658 microfiber Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 201000000050 myeloid neoplasm Diseases 0.000 description 1
- 108010083475 myelopeptides Proteins 0.000 description 1
- 229940112646 myobloc Drugs 0.000 description 1
- 230000009826 neoplastic cell growth Effects 0.000 description 1
- 229940071846 neulasta Drugs 0.000 description 1
- 229960002700 octreotide Drugs 0.000 description 1
- 230000000174 oncolytic effect Effects 0.000 description 1
- 244000309459 oncolytic virus Species 0.000 description 1
- 229950010444 onercept Drugs 0.000 description 1
- 229940100629 oral lozenge Drugs 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 108010011957 ozarelix Proteins 0.000 description 1
- 229950008505 ozarelix Drugs 0.000 description 1
- 229960002404 palifermin Drugs 0.000 description 1
- 229940055726 pantothenic acid Drugs 0.000 description 1
- 235000019161 pantothenic acid Nutrition 0.000 description 1
- 239000011713 pantothenic acid Substances 0.000 description 1
- 229960002566 papillomavirus vaccine Drugs 0.000 description 1
- 239000000199 parathyroid hormone Substances 0.000 description 1
- HQQSBEDKMRHYME-UHFFFAOYSA-N pefloxacin mesylate Chemical compound [H+].CS([O-])(=O)=O.C1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCN(C)CC1 HQQSBEDKMRHYME-UHFFFAOYSA-N 0.000 description 1
- 229960001373 pegfilgrastim Drugs 0.000 description 1
- 108010092851 peginterferon alfa-2b Proteins 0.000 description 1
- 229940106366 pegintron Drugs 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- 238000011020 pilot scale process Methods 0.000 description 1
- 239000013612 plasmid Substances 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 210000001778 pluripotent stem cell Anatomy 0.000 description 1
- 230000004481 post-translational protein modification Effects 0.000 description 1
- OXCMYAYHXIHQOA-UHFFFAOYSA-N potassium;[2-butyl-5-chloro-3-[[4-[2-(1,2,4-triaza-3-azanidacyclopenta-1,4-dien-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol Chemical compound [K+].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C2=N[N-]N=N2)C=C1 OXCMYAYHXIHQOA-UHFFFAOYSA-N 0.000 description 1
- 235000012015 potatoes Nutrition 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 238000011165 process development Methods 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 229940030749 prostate cancer vaccine Drugs 0.000 description 1
- 238000001742 protein purification Methods 0.000 description 1
- 229940023143 protein vaccine Drugs 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 229960003876 ranibizumab Drugs 0.000 description 1
- 108010003189 recombinant human tumor necrosis factor-binding protein-1 Proteins 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 238000007670 refining Methods 0.000 description 1
- 229940116176 remicade Drugs 0.000 description 1
- 208000023504 respiratory system disease Diseases 0.000 description 1
- 108010074523 rimabotulinumtoxinB Proteins 0.000 description 1
- 229960005560 rindopepimut Drugs 0.000 description 1
- 229960004641 rituximab Drugs 0.000 description 1
- AFEHBIGDWIGTEH-AQRCPPRCSA-N semax Chemical compound C([C@H](NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](N)CCSC)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N1[C@@H](CCC1)C(=O)NCC(=O)N1[C@@H](CCC1)C(O)=O)C1=CNC=N1 AFEHBIGDWIGTEH-AQRCPPRCSA-N 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 230000009919 sequestration Effects 0.000 description 1
- 229940082787 spirulina Drugs 0.000 description 1
- 238000012453 sprague-dawley rat model Methods 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- IHBMMJGTJFPEQY-UHFFFAOYSA-N sulfanylidene(sulfanylidenestibanylsulfanyl)stibane Chemical compound S=[Sb]S[Sb]=S IHBMMJGTJFPEQY-UHFFFAOYSA-N 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- WRGVLTAWMNZWGT-VQSPYGJZSA-N taspoglutide Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)NC(C)(C)C(=O)N[C@@H](CCCNC(N)=N)C(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)C(C)(C)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 WRGVLTAWMNZWGT-VQSPYGJZSA-N 0.000 description 1
- 229950007151 taspoglutide Drugs 0.000 description 1
- 229960000216 tenecteplase Drugs 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 229960004072 thrombin Drugs 0.000 description 1
- 229960003766 thrombin (human) Drugs 0.000 description 1
- ZRXXHPDJLAQCPC-SFJRRRFZSA-N tigapotide Chemical compound C([C@@H](C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H]([C@H](O)C)C(O)=O)NC(=O)[C@H](CSCNC(C)=O)NC(=O)[C@@H](NC(=O)[C@H](CSCNC(C)=O)NC(=O)[C@@H](NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CSCNC(C)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@@H](N)CCC(O)=O)[C@@H](C)O)[C@@H](C)O)[C@@H](C)O)C1=CC=C(O)C=C1 ZRXXHPDJLAQCPC-SFJRRRFZSA-N 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 229940042129 topical gel Drugs 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 229960000575 trastuzumab Drugs 0.000 description 1
- 108010075758 trebananib Proteins 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 238000000108 ultra-filtration Methods 0.000 description 1
- 238000010977 unit operation Methods 0.000 description 1
- 108010084171 vanutide cridificar Proteins 0.000 description 1
- 208000019553 vascular disease Diseases 0.000 description 1
- 238000009423 ventilation Methods 0.000 description 1
- 239000013603 viral vector Substances 0.000 description 1
- BICRTLVBTLFLRD-PTWUADNWSA-N voclosporin Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C=C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O BICRTLVBTLFLRD-PTWUADNWSA-N 0.000 description 1
- ZKKBZMXTFBAQLP-INNXVHPBSA-N z44m8u8y9a Chemical compound C([C@H](C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CCCCN)C(=O)N[C@H](C(C)C)C(=O)N[C@H](C)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H](CCCCN)C(=O)N[C@H](CC=1C=CC=CC=1)C(=O)N[C@H](CCCCN)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H](C)C(=O)N[C@H](CC=1C=CC=CC=1)C(N)=O)NC(=O)[C@@H](CC=1C=CC=CC=1)NC(=O)[C@@H](C)NC(=O)[C@@H](CCCCN)NC(=O)[C@@H](CC=1C=CC=CC=1)NC(=O)[C@@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@@H](CC(O)=O)NC(C)=O)C1=CC=C(O)C=C1 ZKKBZMXTFBAQLP-INNXVHPBSA-N 0.000 description 1
- WHNFPRLDDSXQCL-UAZQEYIDSA-N α-msh Chemical compound C([C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](C(C)C)C(N)=O)NC(=O)[C@H](CO)NC(C)=O)C1=CC=C(O)C=C1 WHNFPRLDDSXQCL-UAZQEYIDSA-N 0.000 description 1
Images
Classifications
-
- E—FIXED CONSTRUCTIONS
- E04—BUILDING
- E04H—BUILDINGS OR LIKE STRUCTURES FOR PARTICULAR PURPOSES; SWIMMING OR SPLASH BATHS OR POOLS; MASTS; FENCING; TENTS OR CANOPIES, IN GENERAL
- E04H5/00—Buildings or groups of buildings for industrial or agricultural purposes
- E04H5/02—Buildings or groups of buildings for industrial purposes, e.g. for power-plants or factories
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M37/00—Means for sterilizing, maintaining sterile conditions or avoiding chemical or biological contamination
-
- E—FIXED CONSTRUCTIONS
- E04—BUILDING
- E04H—BUILDINGS OR LIKE STRUCTURES FOR PARTICULAR PURPOSES; SWIMMING OR SPLASH BATHS OR POOLS; MASTS; FENCING; TENTS OR CANOPIES, IN GENERAL
- E04H1/00—Buildings or groups of buildings for dwelling or office purposes; General layout, e.g. modular co-ordination or staggered storeys
- E04H1/005—Modulation co-ordination
-
- E—FIXED CONSTRUCTIONS
- E04—BUILDING
- E04H—BUILDINGS OR LIKE STRUCTURES FOR PARTICULAR PURPOSES; SWIMMING OR SPLASH BATHS OR POOLS; MASTS; FENCING; TENTS OR CANOPIES, IN GENERAL
- E04H5/00—Buildings or groups of buildings for industrial or agricultural purposes
-
- F24F3/161—
-
- F—MECHANICAL ENGINEERING; LIGHTING; HEATING; WEAPONS; BLASTING
- F24—HEATING; RANGES; VENTILATING
- F24F—AIR-CONDITIONING; AIR-HUMIDIFICATION; VENTILATION; USE OF AIR CURRENTS FOR SCREENING
- F24F3/00—Air-conditioning systems in which conditioned primary air is supplied from one or more central stations to distributing units in the rooms or spaces where it may receive secondary treatment; Apparatus specially designed for such systems
- F24F3/12—Air-conditioning systems in which conditioned primary air is supplied from one or more central stations to distributing units in the rooms or spaces where it may receive secondary treatment; Apparatus specially designed for such systems characterised by the treatment of the air otherwise than by heating and cooling
- F24F3/16—Air-conditioning systems in which conditioned primary air is supplied from one or more central stations to distributing units in the rooms or spaces where it may receive secondary treatment; Apparatus specially designed for such systems characterised by the treatment of the air otherwise than by heating and cooling by purification, e.g. by filtering; by sterilisation; by ozonisation
- F24F3/167—Clean rooms, i.e. enclosed spaces in which a uniform flow of filtered air is distributed
-
- E—FIXED CONSTRUCTIONS
- E04—BUILDING
- E04B—GENERAL BUILDING CONSTRUCTIONS; WALLS, e.g. PARTITIONS; ROOFS; FLOORS; CEILINGS; INSULATION OR OTHER PROTECTION OF BUILDINGS
- E04B1/00—Constructions in general; Structures which are not restricted either to walls, e.g. partitions, or floors or ceilings or roofs
- E04B2001/0053—Buildings characterised by their shape or layout grid
Abstract
적어도 하나의 제품을 제조하기 위한 맞춤형 시설은 적어도 하나의 모듈 유닛에 유틸리티를 제공하도록 구성된 적어도 하나의 중앙 유닛과 연통하는 적어도 하나의 모듈 유닛을 갖는다. 일부 실시예에서, 중앙 유닛(들) 및 모듈 유닛(들)은 적어도 부분적으로 쉘 내에 위치된다. 각 모듈 유닛은 발효 유닛, 프리-바이러스 유닛, 포스트-바이러스 유닛, 유틸리티 공간, 창고, 배지 버퍼 시설, 사무실, 개인 유닛 또는 다른 유닛일 수 있다. 모듈 유닛은 쉘의 풋프린트를 최소화하면서 쉘 내에서 모듈 유닛의 수를 최대화하도록 배열될 수 있다. 적어도 하나의 제품을 제조하기 위한 시설을 조립하는 방법은 적어도 하나의 중앙 유닛을 제공하는 단계 및 유틸리티가 중앙 유닛(들)에 의해 모듈 유닛(들)에 제공되도록 중앙 유닛과 연통하는 적어도 하나의 모듈 유닛을 제공하는 단계를 포함한다.
Description
관련 출원에 대한 상호 참조
본 출원은 2016년 3월 10일자로 출원된 미국 특허 가출원 제62/306,556호의 우선권의 이익을 주장하며, 이 출원은 모든 목적을 위해 본 명세서에 그 전문이 본원에 포함된다.
발명의 분야
본 개시내용은 사용자가 시설 내에서 다수의 제품을 제조할 수 있게 하는 맞춤형 시설에 관한 것이다. 특히, 본 개시내용은 클린 룸 환경에서 제품을 제조하기 위한 맞춤형 시설에 관한 것이다.
단일 클론 항체 및 미생물 제품과 같은 제품을 제조하기 위한 전통적인 구조는 구조의 공간을 효율적으로 사용할 수 없다. 전통적인 구조의 레이아웃은 종종 새로운 제품 라인을 제조하기 위해 쉽게 구성되거나 확장되는 것을 제한한다. 따라서, 사용자가 제품 라인 사이에서 공통적인 자원을 효율적으로 사용할 수 있게 하고 시설 정지 시간을 감소시켜 새로운 제조 프로세스 또는 새로운 제조 라인을 수용하기 위해 시설을 용이하게 수정할 수 있게 하는 제조 시설이 필요하다.
본 개시내용은 적어도 하나의 생산 프로세스(예를 들어, 발효 유닛 및 정제 유닛을 사용하는 생산 프로세스)를 이용하여 적어도 하나의 제품을 제조하기 위한 맞춤형 시설을 제공한다. 본 개시내용의 일 양태에 따르면, 맞춤형 시설은 쉘, 쉘 내에 위치되는 적어도 하나의 중앙 유닛, 및 적어도 하나의 모듈 유닛을 포함하며, 각 모듈 유닛은 쉘 내에 위치된다. 쉘, 중앙 유닛(들) 및 모듈 유닛(들)은 다양한 범위의 제조 능력 변경의 속도 및 용이성을 최대화하도록 구성 및 배열된다.
본 개시내용의 다른 양태에 따르면, 적어도 하나의 제약 제품을 제조하기 위한 맞춤형 시설은 적어도 하나의 중앙 유닛을 포함한다. 적어도 하나의 모듈 유닛은 적어도 하나의 중앙 유닛과 연통하여, 적어도 하나의 중앙 유닛이 하나 이상의 모듈 유닛에 유틸리티를 제공한다.
일부 실시예에서, 맞춤형 시설은 쉘을 포함하고, 적어도 하나의 중앙 유닛은 적어도 부분적으로 쉘 내에 위치되고 적어도 하나의 모듈 유닛은 적어도 부분적으로 쉘 내에 위치된다.
일부 실시예에서, 적어도 하나의 모듈 유닛은 발효 유닛, 프리-바이러스 유닛, 포스트-바이러스 유닛, 유틸리티 공간, 창고, 배지(media) 버퍼 시설, 사무실, 개인 유닛, 생산 유닛, 충전 완료 유닛, 투여량 제형화 유닛 및 포장 유닛 중 적어도 하나를 포함한다.
일부 실시예에서, 적어도 하나의 모듈 유닛 중 적어도 하나는 적어도 하나의 중앙 유닛에 직접 인접한다.
일부 실시예에서, 적어도 하나의 모듈 유닛은 쉘의 풋프린트를 최소화하면서 쉘 내의 모듈 유닛의 개수를 최대화하도록 배열된 복수의 모듈 유닛을 포함한다.
일부 실시예에서, 복수의 모듈 유닛의 각각의 모듈 유닛은 적어도 하나의 중앙 유닛 중 적어도 하나와 복수의 모듈 유닛 중 다른 하나에 직접 인접한다.
일부 실시예에서, 적어도 하나의 중앙 유닛 및 복수의 모듈 유닛은 허브 및 스포크 형태를 형성한다.
일부 실시예에서, 적어도 하나의 중앙 유닛 및 복수의 모듈 유닛은 H 형상 레이아웃으로 배열된다.
일부 실시예에서, 맞춤형 시설은 쉘 내의 지면 상에 지지된 생물반응기를 포함한다.
일부 실시예에서, 맞춤형 시설은 적어도 하나의 모듈 유닛 중 하나 내에 지지되는 생물반응기를 포함한다.
일부 실시예에서, 맞춤형 시설의 외부 벽은 다음 구성 중 하나이다: 쉘에 의해 형성되고, 쉘은 적어도 하나의 중앙 유닛 및 적어도 하나의 모듈 유닛을 전체적으로 둘러싸는 구성; 및 쉘, 및 적어도 하나의 중앙 유닛의 외부 벽과 적어도 하나의 모듈 유닛의 외부 벽 중 적어도 하나에 의해 형성되는 구성.
일부 실시예에서, 쉘은 적어도 하나의 측부 벽 및 지붕을 포함하고, 적어도 하나의 측부 벽은 적어도 하나의 중앙 유닛 및 적어도 하나의 모듈 유닛을 둘러싸고, 지붕은 적어도 하나의 측부 벽의 상부 에지에 고정되고, 지붕은 적어도 하나의 중앙 유닛 및 적어도 하나의 모듈 유닛 위로 연장된다.
일부 실시예에서, 적어도 하나의 모듈 유닛 중 적어도 하나는 클린 룸이다.
일부 실시예에서, 적어도 하나의 모듈 유닛은 세포 치료 작업을 위해 구성된다.
본 개시내용의 다른 양태에 따르면, 적어도 하나의 제약 제품을 제조하기 위한 시설을 조립하는 방법은 적어도 하나의 중앙 유닛을 제공하는 단계; 및 적어도 하나의 중앙 유닛이 적어도 하나의 모듈 유닛에 유틸리티를 제공하도록 적어도 하나의 중앙 유닛과 연통하는 적어도 하나의 모듈 유닛을 제공하는 단계를 포함한다.
일부 실시예에서, 이 방법은 쉘을 제공하는 단계; 적어도 하나의 중앙 유닛을 적어도 부분적으로 쉘 내에 위치시키는 단계; 및 적어도 하나의 모듈 유닛을 적어도 부분적으로 쉘 내에 위치시키는 단계를 포함한다.
일부 실시예에서, 적어도 하나의 모듈 유닛은 발효 유닛, 프리-바이러스 유닛, 포스트-바이러스 유닛, 유틸리티 공간, 창고, 배지 버퍼 시설, 사무실, 개인 유닛, 생산 유닛, 충전 완료 유닛, 투여량 제형화 유닛 및 포장 유닛 중 적어도 하나를 포함한다.
일부 실시예에서, 적어도 하나의 모듈 유닛은 쉘의 풋프린트를 최소화하면서 쉘 내의 모듈 유닛의 개수를 최대화하도록 배열된 복수의 모듈 유닛을 포함한다.
일부 실시예에서, 복수의 모듈 유닛의 각각의 모듈 유닛은 적어도 하나의 중앙 유닛 중 적어도 하나와 적어도 하나의 모듈 유닛 중 다른 하나에 직접 인접한다.
일부 실시예에서, 적어도 하나의 중앙 유닛 및 복수의 모듈 유닛은 허브 및 스포크 형태를 형성한다.
일부 실시예에서, 적어도 하나의 중앙 유닛 및 복수의 모듈 유닛은 H 형상 레이아웃으로 배열된다.
일부 실시예에서, 방법은 쉘 내의 지면 상에 생물반응기를 지지하는 단계 및 적어도 하나의 모듈 유닛 중 하나 내에 생물반응기를 지지하는 단계 중 하나를 포함한다.
일부 실시예에서, 맞춤형 시설의 외부 벽은 다음 구성 중 하나이다: 쉘에 의해 형성되고, 쉘은 적어도 하나의 중앙 유닛 및 적어도 하나의 모듈 유닛을 전체적으로 둘러싸는 구성; 및 쉘, 및 적어도 하나의 중앙 유닛의 외부 벽과 적어도 하나의 모듈 유닛의 외부 벽 중 적어도 하나에 의해 형성되는 구성.
일부 실시예에서, 쉘은 적어도 하나의 측부 벽 및 지붕을 포함하고, 적어도 하나의 측부 벽은 적어도 하나의 중앙 유닛 및 적어도 하나의 모듈 유닛을 둘러싸고, 지붕은 적어도 하나의 측부 벽의 상부 에지에 고정되고, 지붕은 적어도 하나의 중앙 유닛 및 적어도 하나의 모듈 유닛 위로 연장된다.
일부 실시예에서, 적어도 하나의 제약 제품은 바이오시밀러 제품이다.
첨부 도면은 일정한 비율로 그려지도록 의도된 것은 아니다. 명확성을 위해 모든 구성요소가 모든 도면에 표시되지는 않는다.
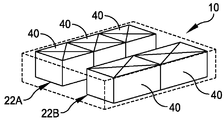
도 1은 본 개시내용에 따른 맞춤형 시설의 실시예의 평면도이다.
도 2a는 도 1의 실시예의 사시도이다.
도 2b는 도 1의 실시예의 사시도이며, 맞춤형 시설 내의 구성요소의 위치를 보여준다.
도 2c는 도 1의 실시예의 사시도이며 맞춤형 시설 내의 다른 구성요소의 위치를 보여준다.
도 2d는 도 1의 실시예의 사시도이며 맞춤형 시설 내의 다른 구성요소의 위치를 보여준다.
도 2e는 도 1의 실시예의 사시도이며, 맞춤형 시설 내의 다른 구성요소의 위치를 보여준다.
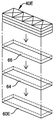
도 3a는 본 개시내용에 따른 모듈 유닛의 실시예의 분해도이다.
도 3b는 본 개시내용에 따른 모듈 유닛의 다른 실시예의 분해도이다.
도 3c는 본 개시내용에 따른 모듈 유닛의 다른 실시예의 분해도이다.
도 3d는 본 개시내용에 따른 모듈 유닛의 다른 실시예의 분해도이다.
도 3e는 본 개시내용에 따른 모듈 유닛의 다른 실시예의 분해도이다.
도 4는 본 개시내용에 따른 맞춤형 시설의 실시예의 전방 사시 절결도를 도시한다.
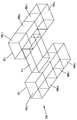
도 5는 H 형상 레이아웃으로 배열된 모듈 유닛 및 중앙 유닛의 세트의 사시도이다.
도 6은 H 형상 레이아웃으로 배열된 모듈 유닛 세트 및 중앙 유닛의 평면도이다.
도 7은 그 사시도이다.
도 8은 쉘 내의 다른 배열로 배열된 모듈 유닛 및 중앙 유닛의 평면도이다.
도 9는 쉘 내에 배열된 모듈 유닛 및 중앙 유닛의 다른 배열의 평면도이다.
도 10은 모듈 유닛 및 중앙 유닛의 다른 배열의 평면도이다.
도 11은 중추에 배열된 한 세트의 모듈 유닛 및 중앙 유닛의 개략도이다.
도 1은 본 개시내용에 따른 맞춤형 시설의 실시예의 평면도이다.
도 2a는 도 1의 실시예의 사시도이다.
도 2b는 도 1의 실시예의 사시도이며, 맞춤형 시설 내의 구성요소의 위치를 보여준다.
도 2c는 도 1의 실시예의 사시도이며 맞춤형 시설 내의 다른 구성요소의 위치를 보여준다.
도 2d는 도 1의 실시예의 사시도이며 맞춤형 시설 내의 다른 구성요소의 위치를 보여준다.
도 2e는 도 1의 실시예의 사시도이며, 맞춤형 시설 내의 다른 구성요소의 위치를 보여준다.
도 3a는 본 개시내용에 따른 모듈 유닛의 실시예의 분해도이다.
도 3b는 본 개시내용에 따른 모듈 유닛의 다른 실시예의 분해도이다.
도 3c는 본 개시내용에 따른 모듈 유닛의 다른 실시예의 분해도이다.
도 3d는 본 개시내용에 따른 모듈 유닛의 다른 실시예의 분해도이다.
도 3e는 본 개시내용에 따른 모듈 유닛의 다른 실시예의 분해도이다.
도 4는 본 개시내용에 따른 맞춤형 시설의 실시예의 전방 사시 절결도를 도시한다.
도 5는 H 형상 레이아웃으로 배열된 모듈 유닛 및 중앙 유닛의 세트의 사시도이다.
도 6은 H 형상 레이아웃으로 배열된 모듈 유닛 세트 및 중앙 유닛의 평면도이다.
도 7은 그 사시도이다.
도 8은 쉘 내의 다른 배열로 배열된 모듈 유닛 및 중앙 유닛의 평면도이다.
도 9는 쉘 내에 배열된 모듈 유닛 및 중앙 유닛의 다른 배열의 평면도이다.
도 10은 모듈 유닛 및 중앙 유닛의 다른 배열의 평면도이다.
도 11은 중추에 배열된 한 세트의 모듈 유닛 및 중앙 유닛의 개략도이다.
맞춤형 시설에 대한 본 명세서에 개시된 구조는 주어진 시간에 적어도 하나의 제품을 제조하는 데 유용하다. 본 명세서에 개시된 구조는 공통 자원을 이용하는 다양한 제품을 제조하는 데 특히 유용하다.
본 개시내용은 하나 이상의 스케일링 가능한 제품 라인이 맞춤형 시설의 쉘 내에 적어도 부분적으로 둘러싸이는 것을 허용하는 시스템 및 방법을 제공한다. 구조가 적응성이기 때문에 사용자가 긴 시간 동안 단일 제품 라인에 구조를 적용할 필요가 없다. 구조는 제품 라인의 치수 요건을 충족하도록 재구성될 수 있다.
본 개시내용의 맞춤형 시설은 사용자가 건설 일정을 감소시키고, 자본 지출을 감소시키며, 글로벌 설계 표준화를 증가시키고, 전세계의 다양한 표준을 준수할 수 있게 한다.
맞춤형 구조는 개념에서 건설에 이르는 소요 시간을 단축하고 건설 현장의 혼잡을 줄이며 새로운 제품 라인을 구현할 때 고정 자산을 덜 필요로 한다.
일반적으로, 맞춤형 시설은 쉘, 쉘 내에 위치되는 적어도 하나의 중앙 유닛, 및 적어도 하나의 모듈 유닛을 포함하며, 각각의 모듈 유닛은 쉘 내에 위치된다.
도 1은 일반적으로 10으로 표시된 맞춤형 시설의 예시적인 실시예의 평면도이다. 도 1의 맞춤형 시설은 제1 단계(12), 제2 단계(14) 및 후속 단계와 같은 일련의 단계로 구성될 수 있다.
도 1의 맞춤형 시설(10)의 구성의 제1 단계(12)에 설치된 피처(feature)는 공기 제어 입구 통로(16), 탈의 영역(18), 유틸리티 영역(20), 제1 제조 윙(22A), 제1 사무실 공간(24A) 및 맞춤형 시설(10)의 점유자가 맞춤형 시설(10) 내에서 하나의 영역으로부터 다른 영역으로 이동할 수 있게 하는 적어도 하나의 복도(28)를 포함한다.
맞춤형 시설(10)의 외측에는 장비 및 재료를 취급하기 위한 취급 영역(32)을 포함하는 야적지(30)가 있다. 야적지 영역(30)은 도로(34)에 인접하여 도시되어 있다. 일반적으로, 맞춤형 시설(10)은 임의의 방향으로 확장될 수 있다. 또한, 맞춤형 시설(10)은 야적지 영역(30) 및 도로(34)와 같은 주변 피처의 물리적 제약 내에서 일련의 건설 단계 및/또는 하위 단계로 확장될 수 있도록 구성된다.
도 1은 제2 제조 윙(22B) 및 제2 사무실 공간(24B)과 같은 건설의 제2 단계(14) 동안 추가될 수 있는 추가적인 피처를 도시한다.
맞춤형 시설(10)의 레이아웃은 클린 룸 환경에서의 제조를 위해 구성될 수 있다. 맞춤형 시설(10)은 하이브리드 스틱 또는 프레임 건축 건물 및 유틸리티 유닛(또는 유틸리티 허브)을 갖춘 모듈 건물을 이용한다.
이제 도 2a 내지 도 2e를 참조하면, 맞춤형 시설의 다양한 구성요소의 상대적인 위치가 도시되어 있다.
도 2a는 맞춤형 시설(10)의 외부 쉘(36)의 외부 벽의 사시도를 도시한다. 외부 쉘(또는 쉘)(36)은 중앙 유닛(중앙 유틸리티 유닛일 수 있음)(38)을 적어도 부분적으로 둘러싸고, 이하에 더 상세히 설명되는 바와 같이 복수의 모듈 유닛(40)을 적어도 부분적으로 둘러싼다. 일부 실시예에서, 외부 쉘(36)은 유틸리티 유닛(중앙 유틸리티 유닛일 수 있음)(38)을 전체적으로 둘러싸고, 복수의 모듈 유닛(40)을 전체적으로 둘러싼다.
외부 쉘(36)은 종래의 스틱 건물에 따라 건설될 수 있거나, 조립식 모듈과 같은, 그러나 이에 한정되지 않는, 다른 방법으로 건설될 수 있다. 예를 들어, 외부 쉘(36)은 전통적인 건축 방법을 사용하여 강철 구조로 제조될 수 있다. 외부 쉘(36)은 지면에 고정된 기초부에 지지될 수 있다. 외부 쉘(36)은 내후성이다.
외부 쉘(36)은 상부구조를 형성한다. 일부 실시예에서, 외부 쉘(36)은 건물 건설 분야에서 공지된 "버틀러(Butler)" 스타일 건물일 수 있다.
외부 쉘(36)은 맞춤형 시설(10)에 포함되고 이하에서보다 상세히 설명되는 하나 이상의 중앙 유닛(38) 및 하나 이상의 모듈 유닛(40)을 둘러싸도록 치수설정 및 구성되는 측부 벽(42)을 포함한다.
지붕(44)은 측부 벽(42)의 상부 에지에 고정되고, 지붕(44)은 중앙 유닛(들)(38) 및 모듈 유닛(들)(40) 위로 연장된다. 따라서, 측부 벽(42)과 지붕(44)은 중앙 유닛(들)(38) 및 모듈 유닛(들)(40)을 둘러싸고 있으며, 이들은 쉘(36) 내에 위치된다. 중앙 유닛(들)(38) 및 모듈 유닛(들)(40)은 쉘(36)의 바닥 상에 또는 쉘이 고정되는 다른 지지 표면 상에 지지될 수 있다. 맞춤형 시설(10)은 모듈 유형의 요소로 채워지는 기본 상부구조를 포함하는 부분 모듈(모듈 스틱 빌드라고도 함) 방법을 제공한다.
일 실시예에서, 도 2a의 맞춤형 시설(10)의 외부 높이는 30 미터이다. 일 실시예에서, 각각의 제조 윙은 100 미터의 길이 및 30 미터의 폭을 갖는다.
도 2b는 맞춤형 시설(10)의 외부를 점선으로 도시하고, 유틸리티 영역은 실선으로 나타낸다. 유틸리티 영역(20)은 맞춤형 시설(10)의 중앙을 향하여 위치되는 중앙 유닛(중앙 유틸리티 베이(CUB) 또는 유틸리티 건물 또는 중앙 유틸리티 모듈이라고도 함)(38)을 포함할 수 있다.
도 1의 쉘(36)은 또한 도 1의 미래 유틸리티 모듈에 의해 완전히 점유되는 미래 유틸리티 영역(46)을 포함한다. 미래 유틸리티 영역(46)은 유틸리티 모듈(38)에 인접하며, 도 1에 도시된다. 미래 유틸리티 영역(46)은 유틸리티 모듈(38)에 인접한 창고 영역으로서 사용될 수 있다. 이 맞춤형 시설(10) 내의 미래 유틸리티 영역(46)은 자동화된 조사 및 검색 시스템(ASARS)을 갖는 40 피트 높이의 창고와 같은 스위트 하이 베이 애플리케이션일 수도 있다.
일부 실시예에서, 유틸리티 모듈(38) 및 미래 유틸리티 영역(46)은 유틸리티 섹션 및 미래 유틸리티 섹션으로 분할되는 단일 유틸리티 모듈이다.
중앙 유틸리티 모듈(38)은 맞춤형 시설(10)의 중심에 있을 필요는 없다. 중앙 유틸리티 모듈(38)은 일부 실시예에서 맞춤형 시설(10)의 외부 에지를 따라 위치될 수 있다.
도 2c는 맞춤형 시설(10)의 외부를 점선으로 도시하고, 제조 윙(22A, 22B)을 실선으로 도시한다.
제조 윙(22A, 22B)은 발효 모듈 또는 정제 모듈과 같은 제품 라인을 위한 모듈 유닛(40)을 수용하도록 구성된다. 맞춤형 시설(10)은 쉽게 확장 가능하고 스케일링 가능하며, 제조 윙(22A, 22B) 내의 상이한 모듈 유닛(40)은 동일한 맞춤형 시설(10)에서 완전히 다른 제품을 생산하는 데 사용될 수 있다.
예를 들어, 제1 발효 모듈로 구성된 모듈 유닛(40)에서, 사용자는 포유 동물 세포계에서 유래된 단일 클론 항체 제품과 같은 한 유형의 제품을 제조할 수 있다. 제2 모듈 유닛(40)에서, 사용자는 미생물 제품과 같은 완전히 다른 제품을 제조할 수 있다. 본 개시내용의 맞춤형 시설(10)은 단일의 팽창 가능한 상부구조로부터 다수의 제품 라인을 동시에 그리고 다수의 고객을 지원할 수 있다. 본 개시내용의 맞춤형 시설(10)은 추가적인 제품 라인을 추가하도록 확장될 수 있다.
반응기는 맞춤형 시설(10)의 제조 윙(22A, 22B)의 모듈 유닛(40) 내에 지지될 수 있다. 맞춤형 시설(10)은 임의의 바람직한 적합한 용기 체적을 지지할 수 있다. 예를 들어, 도 1에 도시된 것과 같은 일부 양태에서, 맞춤형 시설(10)은 20,000 리터 이하의 생산 용기 및 20,000 리터를 초과하는(예를 들어, 23,000 내지 24,000 리터) 저장 용기(예를 들어, 수확)를 수용하도록 구성될 수 있다. 예를 들어, 맞춤형 시설(10)은 약 20,000 리터, 15,000 리터, 10,000 리터, 5,000 리터, 2,000 리터 및/또는 1,000 리터의 용적을 갖는 용기를 지지하도록 치수 및 구성될 수 있다. 다른 용적을 갖는 용기도 지지될 수 있다.
임의의 전형적인 제조 및 클린 룸 장비가 맞춤형 시설(10)에 포함될 수 있고, 맞춤형 시설(10)은 cGMP(현재 양호한 제조 관례) 프로세스에 완전히 적합할 수 있다.
맞춤형 시설(10)에 적합할 수 있는 일부 장비의 예로는 다음을 포함하지만, 이에 한정되지는 않는다: 생물반응기, 디스크 스택 원심 분리기, 접선 유동 여과(TFF) 스키드, 깊이 여과 스키드, 인라인 희석 스키드, 관련 제어 장비를 갖는 크로마토그래피 컬럼, 배지 탱크, 수확 탱크, 정제 용기, 깊이 필터 홀더, 연수 및 탈염소화 시스템, 청정 증기 발생기, 주입수(WFI) 저장 탱크, WFI 중단 탱크, WFI 증류기, 냉각 타워, 배전반, 비상 발전기, 냉각기, 순환수식 펌프, 오토클레이브, 공기 취급 유닛, 프로세스 폐기물 중화(예컨대, 유리섬유 보강 플라스틱(FRP)), 생물폐기물 수집 및 불활성화 시스템, 현장 청정 시스템, 유리 와셔 및/또는 기타 장비.
본 개시내용의 맞춤형 시설(10)에서의 생물반응기는 지상 기반 반응기일 수 있다. 대안적으로, 생물반응기는 구조 자체로부터 현수될 수 있다. 예를 들어, 생물반응기는 하나 이상의 모듈 유닛(40)으로부터 현수될 수 있다.
맞춤형 시설(10)은 하나 이상의 중앙 유닛(38) 및 하나 이상의 모듈 유닛(40)을 포함할 수 있다. 일부 실시예에서, 각 모듈 유닛(40)은 발효 또는 세포 배양 유닛, 프리-바이러스 유닛, 포스트-바이러스 유닛, 유틸리티 야적지, 창고, 배지 버퍼 시설, 사무실, 개인 유닛, 생산 유닛, 충전 완료 유닛, 투여량 제형화 유닛 및 포장 유닛의 그룹으로부터 선택된다. 생산 유닛은 제품을 제조하는 데 유용하다. 충전 완료 유닛은 유리병과 같은 컨테이너를 채우는 데 유용하다. 투여량 제형화 유닛은 설정된 투여량의 제품을 분배한다. 포장 유닛은 유통 또는 판매용으로 제품을 포장한다.
각 모듈 유닛에 할당된 공간은 특정 처리 요구 사항에 맞게 필요에 따라 추가로 나눌 수 있다. 각각의 제조 윙(22A, 22B)은 하나보다 많은 모듈 유닛(40)이 각각의 제조 윙(22A, 22B) 내에 위치되도록 구성될 수 있다.
도 1 및 도 2c에서, 제1 제조 윙(22A)은 3개의 모듈 유닛(40)을 포함한다. 제2 제조 윙(22B)은 2개의 모듈 유닛(40)을 포함한다. 중앙 유틸리티 영역(20)은 길이가 50 미터이고 폭이 20 미터이며, 3개의 내부 레벨을 갖는다. 중앙 유틸리티 블록은 확장 가능하다.
일부 실시예에서, 모듈 유닛(40) 중 적어도 하나는 클린 룸이다. 일부 실시예에서, 모듈 유닛(40) 중 적어도 하나는 각각의 모듈 유닛(40) 내에 클린 룸 섹션을 포함한다.
건물 쉘(36)은 상이한 생산 모듈을 수용하도록 설계된다. 일부 실시예에서, 쉘은 포유 동물 세포계에 대해 4개의 20,000 리터 용기를 수용할 수 있다. 일부 실시예에서, 쉘은 일회용 기술 작업을 위해 4개의 2,000 리터 용기를 수용할 수 있다.
일부 실시예에서, 제조 윙은 4개의 20,000 리터 용기 및 하류 처리 장비를 포함하고 포유 동물 세포계 유래의 단일 클론 항체 제품을 제조하도록 구성된 모듈 유닛, 4개의 20,000 리터 용기를 갖는 포유 동물 세포계로부터 유래된 단일 클론 항체 제품을 제조하기 위한 일회용 장비를 수용하는 모듈 유닛, 미생물 제품을 제조하기 위해 구성된 모듈 유닛, 및/또는 미생물 제품을 제조하기 위한 일회용 장비를 수용하는 모듈 유닛을 포함할 수 있다.
일 실시예에서, 모듈 유닛은 포유류 제조를 위해 구성되며 4개의 20,000 리터 용기 및 하류 처리 장비를 포함한다. 다른 실시예에서, 모듈 유닛은 상업적 및 임상적 생산을 위해 4개의 20,000 리터 용기를 포함한다. 다른 실시예에서, 모듈 유닛은 임상 생산을 위해 하나의 1,000 리터 용기를 포함한다. 다른 실시예에서, 모듈 유닛은 미생물 제품을 제조하도록 구성되며, 하나의 15,000 리터 용기를 포함한다. 다른 실시예에서, 모듈 유닛은 3개의 5,000 리터 용기를 포함한다. 다른 실시예에서, 모듈 유닛은 하나 이상의 프로세스 개발 랩을 포함한다. 다른 실시예에서, 모듈 유닛은 충전 및 완료 임상 개발 유리병 충전 장비, 하나 이상의 동결건조 장비 세트, 미리 충전된 주사기를 제조하기 위한 장비 및/또는 상업적 응용을 위한 고효능 제품을 제조하기 위한 장비를 포함한다. 일부 실시예에서, 모듈 유닛은 세포 치료 장비를 포함한다. 일부 실시예에서, 모듈 유닛은 바이러스 치료 장비를 포함한다.
도 2d는 맞춤형 시설(10)의 외부를 점선으로 나타내고, 제1 사무실 공간(24A) 및 제2 사무실 공간(24B)을 실선으로 나타낸다. 제1 사무실 공간(24A)은 사무실, 개인 보관용 사물함 및 지원 영역을 포함한다. 제2 사무실 공간(24B)은 사무실, 개인 보관용 사물함 및 지원 영역을 포함한다. 제1 사무실 공간(24A)의 전방 벽(48A)은 도 2a에 도시된 바와 같이 맞춤형 시설(10)의 전방 외부 표면의 일부를 형성한다. 제1 사무실 공간(24B)의 전방 벽(48B)은 맞춤형 시설(10)의 전방 외부 표면의 일부를 형성한다. 따라서, 각각의 사무실 공간(24A, 24B)은 맞춤형 시설(10)의 쉘(36)에 의해서 단지 부분적으로 둘러싸여있다.
유사하게, 일부 실시예에서, 중앙 유닛의 외부 벽 및/또는 적어도 하나의 모듈 유닛 중 하나의 외부 벽은 맞춤형 시설의 외부 벽의 적어도 일부를 형성한다. 일부 실시예에서, 중앙 유틸리티 모듈의 상부 표면 및/또는 모듈 유닛의 상부 표면은 맞춤형 시설의 상부 표면의 일부를 형성한다.
도 2e는 맞춤형 시설(10)의 외부를 점선으로 도시하고, 탈의 영역(18)은 실선으로 나타낸다. 탈의 영역(18)은 사용자가 맞춤형 시설(10)에 들어가고 외출복을 작업복으로 변경하도록 허용한다. 도 2e의 탈의 영역(18)은 남성 탈의 영역(18A)과 여성 탈의 영역(18B)으로 추가로 세분된다. 일부 실시예에서, 탈의 영역(18)은 2개 이상의 탈의 영역으로 세분된다. 일부 실시예에서, 탈의 영역(18)은 세분되지 않는다.
다른 실시예에서, 제1 제조 윙(22A)과 제2 제조 윙(22B), 제1 사무실 공간(24A), 제2 사무실 공간(24B), 탈의 영역(18) 및 유틸리티 영역(20)의 상대 위치는 맞춤형 시설(10)에서 상이하게 위치될 수 있고 및/또는 맞춤형 시설(10)에 대해 상이하게 배향될 수 있다.
발판 및 복도(28)는 맞춤형 시설(10)의 사용자가 유틸리티 영역(20)의 유틸리티 유닛(38) 및 모듈 유닛(발효 등의 모듈)(40)에 접근할 수 있게 한다.
맞춤형 시설(10)에 건설의 제2 단계(14)를 추가한 후, 사용자는 맞춤형 시설(10)을 추가로 확장하고자 할 수 있다. 예를 들어 사용자가 제조하는 제품에 대해 세계 경제의 소비자의 수요가 증가하거나, 사용자가 생산할 수 있는 제품에 대해 세계 경제의 소비자의 수요가 증가할 수 있다. 제품에 대한 이러한 수요 증가에 대응하기 위해, 사용자는 도 1의 맞춤형 시설에 추가 피처를 추가하는 후속 건설 단계에서 맞춤형 시설(10)을 확장할 수 있다. 일부 실시예에서, 이런 추가 피처(예컨대, 추가적인 모듈 유닛, 추가적인 제조 윙 또는 맞춤형 시설의 다른 구성요소)는 제1 제조 윙(22A) 또는 제2 제조 윙(22B)에 수평으로 인접하여 위치된다. 일부 실시예에서, 이러한 추가 피처는 제1 제조 윙(22A) 및/또는 제2 제조 윙(22B)에 수직방향으로 인접하여 위치된다.
이제 도 3a 내지 도 3e를 참조하면, 사용자는 도 1의 제1 제조 윙(22A) 또는 제2 제조 윙(22B)과 같은 제조 윙을 다른 하위 단계에서 확장할 수 있다. 사용자는 도 3a 내지 도 3e에 도시된 구성 중 하나로부터 도 3a 내지 도 3e에 도시된 다른 구성으로 제조 윙 레이아웃을 변환할 수 있다. 대안적으로, 사용자는 제조 윙 레이아웃을 다른 구성으로 변환할 수 있다.
도 3a는 충전 완료 모듈로서 구성된 모듈 유닛(40A)의 실시예의 부분 분해도를 도시한다. 도 3a의 충전 완료 모듈은 1,500 평방 미터의 풋프린트를 갖는 단일 바닥(60A)을 갖는다. 충전 완료 모듈에는 HVAC 플랜트 룸 및 일부 국소 유틸리티를 위한 메자닌(mezzanine)이 포함된다. 프리 필드(50A)는 충전 완료 모듈에 인접한 점선으로 도시되어 있으며 1,500 평방 미터의 풋프린트를 갖는다. 프리 필드(50A)는 제품 저장과 같은 다양한 목적으로 사용될 수 있다. 충전 완료 모듈(40A) 및 프리 필드(50A)는 함께 제2 제조 윙(22B)의 3,000 평방 미터의 풋프린트에 걸쳐 연장된다.
도 3b는 "2k 모듈"로서 구성된 모듈 유닛(40B)의 실시예의 부분 분해도를 도시한다. 도 3b의 2k 모듈은 1,500 평방 미터의 풋프린트를 갖는 단일 바닥(60B)을 갖는다. 2k 모듈은 2,000 리터 용기를 둘러쌀 수 있다. 2k 모듈에는 HVAC 플랜트 룸 및 일부 국소 유틸리티용 메자닌이 포함된다. 프리 필드(50B)는 2k 모듈에 인접한 점선으로 도시되고, 1,500 평방 미터의 풋프린트를 갖는다. 프리 필드(50B)는 제품 저장과 같은 다양한 목적으로 사용될 수 있다. 2k 모듈(40B) 및 프리 필드(50B)는 함께 제2 제조 윙(22B)의 3,000 평방 미터의 풋프린트에 걸쳐 연장된다.
도 3c는 "5k 모듈"로서 구성된 모듈 유닛(40C)의 실시예의 부분 분해도를 도시한다. 도 3c의 5k 모듈은 3,000 평방 미터의 풋프린트를 갖는 단일 바닥(60C)을 갖는다. 5k 모듈은 5,000 리터 용기를 둘러쌀 수 있다. 5k 모듈에는 HVAC 플랜트 룸 및 일부 국소 유틸리티용 메자닌이 포함된다. 5k 모듈은 제조 윙의 3,000 평방 미터 풋프린트에 걸쳐 연장한다.
도 3d는 "15k 모듈"로서 구성된 모듈 유닛(40D)의 일 실시예의 부분 분해도를 도시한다. 도 3d의 15k 모듈은 제1 바닥(60D)과 제2 바닥(62)을 갖는다. 도 3d의 15k 모듈은 3,000 평방 미터의 풋프린트를 가지고 있다. 15k 모듈은 15,000 리터 용기를 둘러쌀 수 있다. 15k 모듈은 로컬 HVAC 유닛, 현장 세정(CIP) 유닛 및 온도 제어 유닛(TCU)을 포함한다. 일부 실시예에서 온도 제어 유닛은 제품 라인에 사용되는 탱크의 온도를 제어하기 위해 탱크 상에 열교환기를 갖는 워터 재킷을 포함한다. CIP 유닛은 일반적으로 모듈식 스키드이며 세정 용액(예컨대, 가성 용액 및 표백제)을 보유하는 다수의 탱크, 펌프 및 적절한 세정 대상 탱크에 세정 용액을 보내기 위한 센서를 갖는다.
15k 모듈의 제1 바닥(60D)은 제조 윙의 3,000 평방 미터의 풋프린트에 걸쳐 연장한다. 15k 모듈의 제2 바닥(62)은 15k 모듈의 제1 바닥 수직방향 위쪽에서 연장하며 제조 윙의 3,000 평방 미터 풋프린트에 걸쳐 연장한다. 15k 모듈의 제1 바닥(60D)과 15k 모듈의 제2 바닥(62)은 함께 6,000 평방 미터의 조합된 영역을 갖는다.
도 3e는 "20k 모듈"로 구성된 모듈 유닛(40E)의 실시예의 부분 분해도를 도시한다. 도 3e의 20k 모듈은 3,000 평방 미터의 풋프린트를 가지고 있다. 20k 모듈은 20,000 리터 용기를 둘러쌀 수 있다. 20k 모듈에는 로컬 HVAC 유닛, CIP 유닛 및 TCU가 포함된다. 20k 모듈은 제1 바닥, 제2 바닥 및 제3 바닥을 포함한다. 20k 모듈의 제1 바닥(60E)은 제조 윙의 3,000 평방 미터의 풋프린트에 걸쳐 연장한다. 20k 모듈의 제2 바닥(64)은 20k 모듈의 제1 바닥(60E) 수직방향 위쪽에서 연장되고 제조 윙의 3,000 평방 미터 풋프린트에 걸쳐 연장된다. 20k 모듈의 제3 바닥(66)은 20k 모듈의 제1 바닥(60E) 및 20k 모듈의 제2 바닥(64) 수직방향 위쪽에서 연장되고 제조 윙의 3,000 평방 미터 풋프린트에 걸쳐 연장된다. 20k 모듈의 제1 바닥(60E), 20k 모듈의 제2 바닥(64) 및 20k 모듈의 제3 바닥(66)은 함께 9,000 평방 미터의 조합된 영역을 갖는다.
도 4는 본 개시내용에 따라 일반적으로 110으로 표시된 맞춤형 시설의 예시적인 실시예의 전방 사시 절결도이다. 맞춤형 시설(110) 레이아웃은 클린 룸 환경에서의 제조를 위해 구성될 수 있다. 맞춤형 시설(110)은 중앙에 위치된 유틸리티 허브(또는 중앙 유닛)(114)를 갖는 하이브리드 스틱 또는 프레임 축조 건물 및 모듈 건물을 이용한다.
외부 쉘(또는 쉘)(112)은 중앙 유닛(114) 및 중앙 유닛(114)에 인접한 복수의 모듈 유닛(116)을 둘러싸고 있다. 외부 쉘(112)은 종래의 스틱 건물 또는 조립식 모듈과 같은, 그러나 이에 한정되지 않는, 다른 방법으로 구성될 수 있다. 예를 들어, 외부 쉘(112)은 전통적인 건축 방법을 사용하여 강철 구조로부터 제조될 수 있다. 외부 쉘(112)은 지면에 고정된 기초부에 지지될 수 있다. 외부 쉘(112)은 내후성이다.
외부 쉘(112)은 상부구조를 형성한다. 일부 실시예에서, 외부 쉘(112)은 건물 건설 분야에서 공지된 "버틀러" 스타일 건물일 수 있다.
쉘(112)은 맞춤형 시설(110)에 포함되고 이하에서보다 상세하게 설명되는 하나 이상의 중앙 유닛(114) 및 하나 이상의 모듈 유닛(116)을 둘러싸도록 치수설정 및 구성되는 측부 벽(118)을 포함한다. 지붕(120)은 측부 벽(118)의 상부 에지에 고정되고, 지붕(120)은 중앙 유닛(들)(114) 및 모듈 유닛(들)(116) 위로 연장된다. 따라서, 측부 벽(118)과 지붕(120)은 쉘(112) 내에 위치된 중앙 유닛(들)(114) 및 모듈 유닛(들)(116)을 둘러싸고 있다. 중앙 유닛(들)(114) 및 모듈 유닛(들)(116)은 쉘(112)의 바닥(122) 또는 쉘(112)이 고정되는 다른 지지 표면 상에 지지될 수 있다. 맞춤형 시설(110)은 모듈 유형 요소로 채워지는 기본 상부구조를 포함하는 부분 모듈(모듈 스틱 빌드라고도 함) 방법을 제공한다.
쉘(112) 내에서, 도 4의 맞춤형 시설(110)은 적어도 하나의 중앙 유닛(114)을 포함하며, 이들 각각은 중앙 유틸리티 베이(CUB)로 지칭될 수 있다. 중앙 유닛(114)은 도 4에 중앙 유틸리티를 제공한다. 도시된 바와 같이, CUB(114)는 CUB(114)(또는 복수의 CUB)로부터 유래하는 제조 포드라 불리는 모듈 유닛(116)을 갖는 구조의 중간에 있다. 도 4에서, 모듈 유닛(116)은 발효 모듈이다. 맞춤형 시설(110)은 쉽게 확장 가능하고 스케일링 가능하며, 포드/모듈 접근법(즉, 허브 및 스포크 유형 접근법)은 상이한 모듈이 동일한 맞춤형 시설(110)에서 완전히 다른 제품을 생산할 수 있게 한다.
예를 들어, 도 4의 좌측 발효 모듈과 같은 제1 발효 모듈에서, 사용자는 포유 동물 세포계에서 유래된 단일 클론 항체 제품과 같은 한 유형의 제품을 제조할 수 있다. 도 4의 우측에 있는 발효 모듈과 같은 제2 모듈에서, 사용자는 미생물 제품과 같은 완전히 다른 제품을 제조할 수 있다. 본 개시내용의 맞춤형 시설(110)은 단일의 확장 가능한 상부구조로부터 다수의 제품 라인을 동시에 그리고 다수의 고객을 지원할 수 있다.
도 4는 맞춤형 시설(110) 내에 지지되는 반응기(124)를 도시한다. 맞춤형 시설(110)은 임의의 바람직한 및 적합한 용기 용적을 지지할 수 있다. 예를 들어, 도 4에 도시된 것과 같은 일부 양태에서, 시설(110)은 20,000 리터 이하의 생산 용기 및 20,000 리터를 초과하는(예를 들어, 23,000 내지 24,000 리터) 저장 용기(예를 들어, 수확)를 수용하도록 구성될 수 있다. 예를 들어, 맞춤형 시설(110)은 약 20,000 리터, 15,000 리터, 10,000 리터, 5,000 리터, 2,000 리터 및/또는 1,000 리터의 용적을 갖는 용기(124)를 지지하도록 치수설정 및 구성될 수 있다. 다른 용적을 갖는 용기(124)가 또한 지지될 수 있다.
발판(126) 및 복도(128)는 시설(110)의 사용자가 중앙 유닛(중앙 유틸리티)(114) 및 모듈 유닛(발효 등의 모듈)(116)에 접근할 수 있게 한다. 도 4에 도시된 바와 같이, 발판(126)은 쉘(112) 내에 위치된다.
일부 실시예에서, 하나 이상의 중앙 유닛(CUB)(114) 및 하나 이상의 모듈 유닛(116)은 허브 및 스포크 배열로 배열된다.
임의의 전형적인 제조 및 클린 룸 장비가 맞춤형 시설(110)에 포함될 수 있으며, 맞춤형 시설(110)은 cGMP 프로세스에 완전히 적합할 수 있다.
시설(110)에 적합할 수 있는 일부 장비의 예로는 다음을 포함하지만, 이에 한정되지는 않는다: 생물반응기, 디스크 스택 원심 분리기, 접선 유동 여과(TFF) 스키드, 깊이 여과 스키드, 인라인 희석 스키드, 관련 제어 장비를 갖는 크로마토그래피 컬럼, 배지 탱크, 수확 탱크, 정제 용기, 깊이 필터 홀더, 연수 및 탈염소화 시스템, 청정 증기 발생기, 주입수(WFI) 저장 탱크, WFI 중단 탱크, WFI 증류기, 냉각 타워, 배전반, 비상 발전기, 냉각기, 순환수식 펌프, 오토클레이브, 공기 취급 유닛, 프로세스 폐기물 중화(예컨대, 유리섬유 보강 플라스틱(FRP)), 생물폐기물 수집 및 불활성화 시스템, 현장 청정 시스템, 유리 와셔 및/또는 기타 장비.
본 개시내용의 맞춤형 시설(110) 내의 생물반응기는 도 4에 도시된 바와 같이 지상 기반 반응기(124)를 가질 수 있다. 대안적으로, 생물반응기(124)는 구조 자체로부터 현수될 수 있다. 예를 들어, 생물반응기(124)는 하나 이상의 모듈 유닛(116)으로부터 현수될 수 있다.
도 4의 쉘(112)은 시설(110)의 후방 우측을 향해 창고 영역(130)을 둘러싼다. 이 시설(110) 내의 창고 영역(130)은 또한 자동화된 조사 및 검색 시스템(ASARS)을 갖는 40 피트 높이의 창고와 같은 스위트 하이 베이 애플리케이션일 수 있다.
맞춤형 시설(110)은 하나 이상의 중앙 유닛(114) 및 하나 이상의 모듈 유닛(116)을 포함할 수 있다. 일부 실시예에서, 각 모듈 유닛(116)은 발효 또는 세포 배양 유닛, 프리-바이러스 유닛, 포스트-바이러스 유닛, 유틸리티 야적지, 창고, 배지 버퍼 시설, 사무실, 개인 유닛, 생산 유닛, 충전 완료 유닛, 투여량 제형화 유닛 및 포장 유닛의 그룹으로부터 선택된다. 각 모듈 유닛에 할당된 공간은 특정 처리 요구 사항에 맞게 필요에 따라 추가로 나눌 수 있다.
일부 실시예에서, 모듈 유닛(들)(116) 중 적어도 하나는 클린 룸이다.
도 5는 H 형상 레이아웃(132)으로 배열된 중앙 유닛(114) 및 모듈 유닛(116)의 세트의 사시도를 도시한다. 각각의 모듈 유닛(116)의 위치는 처리 요구 사항에 가장 잘 맞도록 조정될 수 있다.
도 6 및 도 7은 중앙 유닛(114) 및 정제 유닛(116A)과 발효 유닛(116B)으로 구성된 8개의 모듈 유닛 세트가 위에서 볼 때 H 형상 레이아웃(133)으로 배열되는 맞춤형 시설의 실시예를 도시한다. 쉘(112)은 이 도면에 도시되지 않는다. 도 6의 평면도는 중앙 유닛(114)의 제1 측면(136)에 인접한 선형 어레이(134)에 배열된 정제 유닛(116A) 및 발효 유닛(116B)으로 구성된 모듈 유닛의 제1 행 및 중앙 유닛(114)의 제2 측면(140)에 인접한 선형 어레이(138)에 배열된 정제 유닛(116A) 및 발효 유닛(116B)으로 구성된 모듈 유닛의 제2 행을 갖는 중앙 유닛(중앙 유틸리티 건물로 표시됨)(114)을 도시한다. 모듈 유닛의 어레이(134)는 어레이(134)의 제1 단부에 제1 정제 유닛(116A), 어레이(134)의 중간에 2개의 발효 유닛(116B), 어레이(134)의 제2 단부에 제2 정제 유닛(116A)을 갖는 4개의 모듈 유닛을 포함한다. 유사하게, 모듈 유닛의 어레이(138)는 어레이(138)의 제1 단부에 제1 정제 유닛(116A), 어레이(138)의 중간에 2개의 발효 유닛(116B), 어레이(138)의 제2 단부에 제2 정제 유닛(116A)을 갖는 4개의 모듈 유닛을 포함한다.
모듈 유닛의 제1 어레이(134)의 2개의 발효 유닛(116B) 각각은 중앙 유닛(114)의 제1 측부 벽(136)과 직접 대면 결합하는 측부 벽을 포함한다. 유사하게, 모듈 유닛의 제2 어레이(138)의 2개의 발효 유닛(116B) 각각은 중앙 유닛(114)의 제2 측부 벽(140)과 직접 대면 결합하는 측부 벽을 포함한다. 정제 유닛(116A)은 그 각각의 인접한 발효 유닛(116B)과 직접 대면하는 관계에 있다. 중앙 유닛(114)과 발효 유닛(116B)의 직접 대면 결합 때문에, 주어진 크기의 쉘(112) 내에 설치될 수 있는 중앙 유닛(114) 및 모듈 유닛의 수가 증가된다. 마찬가지로, 주어진 세트의 중앙 유닛(114) 및 모듈 유닛을 둘러싸기 위해 필요한 쉘(112)의 풋프린트가 감소된다. 선택적으로, 일부 양태에서, 발효 유닛(116B)(또는 다른 모듈 유닛)의 측부 벽은 직접 대면 결합 상태일 필요는 없으며, 임의의 원하는 풋프린트를 제공하도록 이격될 수 있다.
모듈 유닛(들)(116) 및 중앙 유닛(들)(114)은 동시적인 복수의 제품의 제조를 용이하게 하도록 배열될 수 있다. 모듈 유닛(들)(116) 및 중앙 유닛(들)(114)은 각각의 제품의 제조 라인 사이에서 자원을 효율적으로 공유하도록 배열된다. 예를 들어, 일부 실시예에서, 중앙 유닛(114)은 발전기, 배관 라인, 전력 라인 및 모듈 유닛(116)에 의해 공유될 수 있는 다른 자원 중 적어도 하나를 포함한다. 또한, 모듈 유닛(들)(116) 및 중앙 유닛(들)(114)은 제조 용량의 장래의 확장을 용이하게 하도록 배열될 수 있다. 예를 들어, 단일 모듈 유닛(116)은 기존의 동작에 대한 영향을 최소화하면서 추후에 추가적인 모듈 유닛(116)을 추가할 수 있는 능력을 구비한 상태로, 최초에 이용될 수 있다.
일부 실시예에서, 모듈 유닛(116) 각각은 작동 및 분리를 위해 요구되는 바에 따라 그 자신의 각각의 가열, 환기 및 공조(HVAC) 시스템을 포함한다.
일부 실시예에서, 허브 및 스포크 배열은 도 6의 평면도에서와 같이 문자 H와 유사할 수 있다. 다른 실시예에서, 허브 및 스포크 배열은 문자 H와 유사하지 않다. 중앙 유닛(중앙 유틸리티 베이)을 가지고 적어도 하나의 모듈 유닛이 그로부터 연장한다면, 정사각형, 직사각형, 오각형 및 기타 기하학적 형상을 포함하지만 이에 한정되지 않는 다른 모양이 가능하다. 예를 들어, 도 10에 도시된 바와 같이, 추가적인 형상이 가능하다. 일부 실시예에서, 예를 들어, 선형 "중추" 형상이 사용될 수 있거나 허브 및 스포크 배열이 문자 "E"와 유사하도록 "E" 형상이 사용될 수 있다.
일부 실시예에서, 중앙 유닛(114)은 중앙 유닛(114) 및 모듈 유닛(116)의 배열의 중심에 있지 않다. 모듈 유닛(116) 및 중앙 유닛(114)의 배열은 주어진 세트의 제조 라인에 요구되는 모듈 유닛(116)의 수를 감소시키도록 구성되는 것이 바람직하다.
모듈 유닛(116)은 제품 또는 스위트의 교차 오염을 감소시키기 위해 서로 분획될 수 있다.
도 8은 본 개시내용의 맞춤형 시설(1000)의 다른 바람직한 실시예의 평면도를 도시한다. 2개의 중앙 유닛(114)은 도 8에 도시된 구조의 평면도의 저부 중앙을 향하여 위치되며, 중앙 유닛(114)의 벽을 따라 연장되는 공유 복도(128) 사이에 위치된다. 중앙 유닛(114)의 좌측에는 6개의 모듈 유닛의 그룹이 있다. 이 그룹은 두 개의 프리-바이러스 유닛(116C), 두 개의 포스트-바이러스 유닛(116D) 및 두 개의 발효 유닛(116B)을 포함한다. 도 8에 도시된 중앙 유닛(114)의 우측에는 2개의 프리-바이러스 유닛(116C), 2개의 포스트-바이러스 유닛(116D) 및 2개의 발효 유닛(116B)을 포함하는 6개의 모듈 유닛의 그룹이 있다. 이 구성은 필요에 따라 추가 능력을 확장하도록 설계된다(예를 들어 확장 옵션을 보여주는 실시예의 예로서 도 10 참조). 도 8에 도시된 바와 같이 시설(1000)의 상부를 따라, 유틸리티 야적지 유닛(116E), 2개의 창고 유닛(116F), 2개의 배지/버퍼 시설 유닛(116G), 및 사무실 유닛(116H) 및 2개의 개인 액세스 유닛(116J)을 포함하는 다른 모듈 유닛이 있다. 이 도면에는 각 정제 유닛 바로 위에 독립 버퍼 보유 모듈 유닛을 추가할 수 있는 기능이 도시되어 있지 않다. 공유 복도(128)는 유닛의 벽을 따라 연장되어, 사용자는 공통 복도(128)로부터 도 8의 모듈 유닛 각각 및 중앙 유닛(114)에 접근할 수 있다.
서로 다른 유닛은 등급 표준에 기초하여 서로 다른 분류 레벨을 가질 수 있다. 예를 들어, 상이한 유닛은 미국 식품 의약국(United States Food and Drug Administration)에 의해 설정된 등급 표준 또는, 유럽 연합의 Sterile Medicinal Products의 Annex 1 Manufacture에 의해 보충된, EudraLex, The Rules Governing Medicinal Products in the European Union Volume 4 EU Guidelines to Good Manufacturing Practice Medicinal Products for Human and Veterinary Use, 에 의해 설정된 등급 표준에 기초하여 상이한 분류 레벨을 가질 수 있다. 예를 들어, 도 8의 프리-바이러스 유닛(116C), 포스트-바이러스 유닛(116D) 및 배지/버퍼 시설 유닛(116G)은 "등급 C"로 분류되고, 발효 유닛(116B)은 유럽 연합 표준에 따라 "등급 D"로 분류되며, 나머지 유닛은 분류되지 않는다. 유닛에 대한 다른 분류도 가능하며 사용자 요구에 따라 선택할 수 있다.
도 9는 본 개시내용의 맞춤형 시설(1200)의 다른 실시예를 도시한다. 도 9의 실시예는 중앙 유닛(114)의 양측에 깨끗한 재료 및 인력을 위한 복도(128)를 갖는 중앙 유닛(중앙 유틸리티 건물)(114)을 포함한다. 복도(128)는 도 9에 도시된 시설(1200)의 상단부의 창고(116F)로부터 시설의 저부의 중앙 유닛(114)을 넘어 연장된다. 각 복도(128)의 외측에는 라커 룸 유닛(116K), 프리-바이러스 유닛(116C), 포스트-바이러스 유닛(116D) 및 발효 유닛(116B)이 있다.
도 9에 도시된 것과 같은 일 실시예에서, 발효 유닛(116B)은 각각 63 피트 Х 65 피트의 치수를 가지며 높이가 35 피트이다. 도 9에 도시된 것과 같은 일 실시예에서, 프리-바이러스 유닛(116C)은 62 피트 Х 50 피트의 치수를 가질 수 있고, 높이는 17 피트이다. 도 9에 도시된 것과 같은 일 실시예에서, 포스트-바이러스 유닛(116D)은 각각 62 피트 Х 65 피트의 치수를 가지며 높이가 35 피트이다. 다른 실시예에서, 유닛은 다른 치수를 가질 수 있다.
도 10은 쉘(112)이 도시되지 않은 본 개시내용의 맞춤형 시설(1300)의 다른 실시예를 도시한다. 도 10은 구역들의 5개의 행을 포함한다. 도 10의 평면도의 제1 행(상부 행)(142)은 정제 구역(117A)을 포함한다. 제2 행(144)은 발효 구역(117B)을 포함한다. 제3 행(150)은 중앙 유틸리티 구역(114)을 포함한다. 제4 행(146)은 발효 구역(117B)을 포함한다. 제5 행(148)은 정제 구역(117A)을 포함한다.
일부 양태에서, 적어도 하나의 제약 제품을 제조하기 위한 맞춤형 시설은 적어도 하나의 중앙 유닛 및 적어도 하나의 모듈 유닛을 포함할 수 있지만, 맞춤형 시설은 쉘을 포함하지 않는다. 각각의 모듈 유닛은 적어도 하나의 중앙 유닛과 연통하여 적어도 하나의 중앙 유닛이 각 모듈 유닛에 유틸리티를 제공한다.
실선으로 표시된 구역은 초기 구성에서 제공될 수 있는 구역 세트를 나타낸다. 이 초기 구성(160)에는 제1 행(142)에 3개의 정제 구역(PURE1, PURE3, PURE5)(117A), 제2 행(144)에 3개의 발효 구역(FERM1, FERM3, FERM5)(117B), 제3 행(150)에 중앙 유틸리티 구역(CENTRAL UTILITIES 1)(115), 제4 행(146)에 3개의 발효 구역(FERM 2, FERM 4, FERM 6)(117B) 및 제5 행(148)에 3개의 정제 구역(PURE 2, PURE 4, PURE 6)(117A)이 있다.
한 세트의 구역(162)이 구역의 어레이를 오른쪽으로 확장함으로써 추가될 수 있다. 예를 들어, 2개의 추가적인 정제 구역(PURE 7, PURE 9)(117A)이 제1 행(142)에 추가될 수 있고, 2개의 추가적인 발효 구역(FERM 7, FERM 9)(117B)이 제2 행(144)에 추가될 수 있으며; 추가적인 중앙 유틸리티 구역(114)이 제3 행(150)에 추가될 수 있고, 2개의 추가 발효 구역(FERM 8, FERM 10)(117B)이 제4 행(146)에 추가될 수 있고, 2개의 추가 정제 구역(PURE 8, PURE 10)(117A)이 제5 행(148)에 추가될 수 있다. FERM 9 및 FERM N+1로 표시된 발효 구역(117B) 사이의 화살표 A와 같은 우향 화살표는 구역 배열의 잠재적 확장 방향을 나타낸다. 필요에 따라 추가적인 구역을 각 행에 추가할 수 있으며, 도 10은 제1 행(142)의 단부에 정제 유닛(PURE N+1)(117A), 제2 행(144)의 단부에 발효 구역(FERM N+1)(117B), 제4 행(146)의 단부에서 화살표 B의 방향을 따라 발효 구역(FERM N)(117B) 및 제5 행(148)의 단부에 정제 구역(PURE N)(117A)을 도시한다. N의 값은 필요에 따라 사용자에 의해 선택된 정수 값일 수 있고 모듈 유닛(116) 및 중앙 유닛(들)(114)이 위치되는 쉘(112)의 내부 치수에 의해서만 제한된다.
제3 행은 화살표 C를 따라 중앙 유틸리티 구역(114)을 제3 행(150)에 추가함으로써 확장될 수 있다.
도 10의 구역은 각각이 중앙 유닛 또는 모듈 유닛(예를 들어, 발효 유닛, 정제 유닛 등) 또는 유닛을 위한 장비를 지원할 수 있는 영역일 수 있는 영역들이다. 도 10은 구역(예를 들어, 구역 FERM 1)을 도시하는 경우, 이 구역은 발효 유닛(FERM 1) 및 구역 내의 하나 이상의 통로로 세분될 수 있다. 적어도 일부 구역에서는 유닛이 전체 구역을 점유할 수 있다.
여기에 개시된 모듈 유닛(116)은 하위 유닛으로 더 세분될 수 있다. 예를 들어, 유닛은 프리-바이러스 하위 유닛과 포스트-바이러스 하위 유닛을 가질 수 있다. 포스트-바이러스 하위 유닛은 바이러스가 없다.
도 4 내지 도 9와 관련하여, 도면은 유닛으로 설명된 영역으로 분할된 모습들을 도시하고 있지만, 이 모습들의 영역들은 각각이 유닛 및 유닛을 연결하는 하나 이상의 통로를 포함하는 구역(즉, 정제 영역, 발효 구역 등)을 나타낼 수 있다.
도 11은 중앙 유닛(114)이 중추로부터 나오는 복수의 모듈(116)을 갖는 선형 "중추"의 형상인 시설(1400)의 다른 예시적 실시예를 도시한다. 이 실시예에서, 모듈(116)은 시설이 시간이 지남에 따라 확장되도록 다수의 건설 단계에서 후속적으로 추가될 수 있다.
본 개시내용의 일 양태에 따르면, 적어도 하나의 제약 제품을 제조하기 위한 시설을 조립하는 방법은 쉘을 제공하는 단계, 적어도 하나의 중앙 유닛을 쉘 내에 적어도 부분적으로 위치시키는 단계 및 적어도 하나의 모듈 유닛을 적어도 부분적으로 쉘 내에 위치시키는 단계를 포함할 수 있다.
발효 유닛의 예
발효 유닛(116B)은 세포 배양 및/또는 발효에 적합한 장비를 수용한다. 예를 들어, 세포 배양 및 발효를 위한 장비는 생물반응기(예를 들어, 세포 배양 또는 발효에 적합), 탱크(예를 들어, 세포, 배지 또는 세포에 의해 생산된 제품을 수용하기에 적합), 경사 분리 장치, 원심 분리기, 펌프 및 제품 회수에 유용한 기타 장비를 포함하지만 이에 한정되지는 않는다. 리폴드 탱크 및 마이크로여과 유닛이 미생물 발효 프로세스에 포함될 것이다.
일 실시예에서, 발효 유닛(116B)은 세포 배양에 적합한 하나 이상의 생물반응기 유닛을 포함한다. 생물반응기 유닛은 영양소 및/또는 탄소원의 공급, 적절한 가스(예를 들어, 산소)의 주입, 발효 또는 세포 배양 배지의 흐름, 기체와 액체 상의 분리, 성장 온도의 유지, pH 수준의 유지, 교반(예를 들어, 휘젓기) 및/또는 세정/살균 중 하나 이상이나 전부를 수행할 수 있다. 발효 유닛은 하나, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 60, 70, 80, 90 또는 100이나 그 이상의 생물반응기를 포함할 수 있다. 다양한 실시예에서, 생물반응기는 회분식, 반 유가식, 유가식, 관류 및/또는 연속 발효 프로세스에 적합하다. 일 실시예에서, 생물반응기는 교반 탱크 반응기이다. 일 실시예에서, 생물반응기는 에어리프트(airlift) 반응기이다. 일 실시예에서, 생물반응기는 약 100 밀리리터 내지 약 50,000 리터의 용적을 가질 수 있다. 비제한적 예는 100 밀리리터, 250 밀리리터, 500 밀리리터, 750 밀리리터, 1 리터, 2 리터, 3 리터, 4 리터, 5 리터, 6 리터, 7 리터, 8 리터, 9 리터, 10 리터, 15 리터, 20 리터, 25 리터, 30 리터, 40 리터, 50 리터, 60 리터, 70 리터, 80 리터, 90 리터, 100 리터, 150 리터, 200 리터, 250 리터, 300 리터, 350 리터, 400 리터, 450 리터, 500 리터, 550 리터, 600 리터, 650 리터, 700 리터, 750 리터, 800 리터, 850 리터, 900 리터, 950 리터, 1000 리터, 1500 리터, 2000 리터, 2500 리터, 3000 리터, 3500 리터, 4000 리터, 4500 리터, 5000 리터, 6000 리터, 7000 리터, 8000 리터, 9000 리터, 10,000 리터, 15,000 리터, 20,000 리터, 또는 50,000 리터의 용적을 포함한다.
일 실시예에서, 생물반응기는 현탁 세포 또는 부착-의존성(부착성) 세포의 배양에 적합하다. 일 실시예에서, 발효 스위트는 세포 치료 및/또는 바이러스 치료 작업에 적합하다. 일 실시예에서, 생물반응기는 원핵 세포 또는 진핵 세포를 배양하는 데 적합하다. 세포의 예로는 박테리아 세포(예를 들면, E. 콜라이 P. 파스토리스), 효모 세포(예를 들어, S. 세레비지에, T. 레에세이), 식물 세포, 곤충 세포(예를 들어, Sf9), 중국 햄스터 난소 세포(CHO 및 임의의 유전적으로 변형되거나 유도된 CHO 세포계), 쥐 세포(예를 들어, 쥐 배아 섬유모세포, 쥐 암 모델 유래 세포), 인간 세포(예를 들어, 임의의 조직 또는 기관의 세포, 암 또는 다른 질병 세포계의 세포, 줄기 세포), 하이브리도마 세포 또는 기타 유전적으로 변형된 또는 하이브리드 세포를 포함하지만, 이에 한정되지는 않는다. 일 실시예에서, 세포는 재조합균주 치료 또는 진단 제품과 같은 제품을 발현 또는 생성한다. 세포에 의해 생산된 제품의 예는 항체 분자(예를 들어, 단일 클론 항체, 이중특이적 항체), 융합 단백질(예를 들어, Fc 융합 단백질, 키메라 시토카인), 기타 재조합 단백질(예를 들어, 글리코실화 단백질, 효소, 호르몬), 또는 지질-캡슐화된 입자(예를 들어, 엑소솜, 바이러스 유사 입자)를 포함하지만 이에 한정되는 것은 아니다. 실시예에서, 발효 유닛은 또한 세포로부터의 이런 제품의 분리, 정제 및 격리를 위한 장비를 포함한다. 일 실시예에서, 시설 및/또는 생물반응기는 바이오시밀러 제품의 제조를 위해 사용될 수 있다.
실시예에서, 발효 유닛은 양호한 제조 프로세스 및 생물학적 안전 표준을 따른다. 일 실시예에서, 발효 유닛은 생물안전성 레벨 1(BSL1), 생물안전성 레벨 2(BSL2), 생물안전성 레벨 3(BSL3) 또는 생물안전성 레벨 4(BSL4)를 따른다.
발효 유닛은 각각의 하위 구획이 세포 배양, 발효 및 생산 프로세스를 지원하는 상이한 기능 또는 양태를 수행하는 데 사용될 수 있는 하위 구획을 포함할 수 있다. 예로서, 발효 유닛은 하나 이상의 생물반응기를 수용하는 하위 구획, 제품 회수를 위한 장비를 수용하는 하위 구획, 접종물을 위한 하위 구획 및 장비와 이런 장비를 취급하는 조작자의 세정 및 오염제거를 위한 하위 구획을 포함한다.
하류 처리 유닛의 예
전술한 정제 유닛(116A)은 하류 처리 유닛의 예이다.
일 예로서, 표준 하류 처리(DSP) 유닛은 프리-바이러스 분리 및 포스트-바이러스 분리 하위 유닛을 포함한다. 바이러스 감소가 전형적인 포유 동물 세포 유도 단백질 정제를 통해 일어나지만 중요한 바이러스 감소 단계는 공간 분리를 위한 적절한 지점으로 간주되며, 포스트-바이러스 분리 하위 유닛은 본질적으로 바이러스가 없는 것으로 간주된다. 포스트-바이러스 분리 하위 유닛은 초미세여과(접선 여과), 정상 여과, 크로마토그래피, 제형화, 적정, 혼합, 농축, 버퍼 교환, 벌크 약품 물질 컨테이너 충전 및 동결 중 임의의 하나에 적합한 장비 및 유틸리티를 수용한다.
본 개시내용의 다양한 실시예 및/또는 예의 설명은 예시의 목적으로 제공된 것이며, 모두를 설명하는 것을 의도하거나 개시된 실시예에 한정되는 것을 의도하지 않는다. 설명된 실시예의 범위 및 사상을 벗어나지 않고 통상의 숙련자에게 많은 변형 및 변화가 명백할 것이다. 여기에 사용된 용어는 실시예의 원리, 시장에서 발견된 기술에 대한 실제 적용 또는 기술적 개선을 가장 잘 설명하거나 통상의 숙련자가 여기에 개시된 실시예를 이해할 수 있게 하기 위해 선택되었다.
본 개시내용의 다양한 실시예에 대한 설명은 제약 및 생물제약 제품의 생산에 활용될 수 있다. 여기에 설명된 디바이스, 시설 및 방법은 원핵 및/또는 진핵 세포계를 포함한 임의의 원하는 세포계 배양에 적합하다. 또한, 실시예에서, 디바이스, 시설 및 방법은 현탁 세포 또는 부착-의존성(부착성) 세포의 배양에 적합하며, 제약 및 생물제약 제품- 세포 및/또는 바이러스 치료에 사용되는 것들 같은 예컨대 폴리펩티드 제품, 핵산 제품(예, DNA 또는 RNA), 또는 세포 및/또는 바이러스 -의 생산을 위해 구성된 생산 작업에 적합하다.
실시예에서, 세포는 재조합균주 치료 또는 진단 제품과 같은 제품을 발현 또는 생성한다. 하기에 보다 상세히 설명되는 바와 같이, 세포에 의해 생성된 제품의 예로는 항체 분자(예를 들어, 단일 클론 항체, 이중특이적 항체), 항체 모방체(예를 들어, 항원에 구체적으로 결합하지만 DARPin, 아피바디, 아드넥틴, 또는 IgNAR 같은 항체에 구조적으로 관련되지 않는 폴리펩티드 분자), 융합 단백질(예를 들어, Fc 융합 단백질, 키메라 시토카인), 다른 재조합균주 단백질(예를 들어, 글리코실화 단백질, 효소, 호르몬), 바이러스 치료제(예를 들어, 항-암 온콜리틱 바이러스, 유전자 요법 및 바이러스 면역 요법을 위한 바이러스 벡터), 세포 치료제(예를 들어, 만능 줄기 세포, 중간엽 줄기 세포 및 성인 줄기 세포), 백신 또는 지질-캡슐화된 입자(예를 들어, 엑소솜, 바이러스 유사 입자), RNA(예를 들어 siRNA 같은) 또는 DNA(예를 들어 플라스미드 DNA), 항생제 또는 아미노산을 포함하지만 이에 한정되지는 않는다. 실시예에서, 디바이스, 시설 및 방법은 바이오시밀러를 생산하는 데 사용될 수 있다.
언급된 바와 같이, 실시예에서, 디바이스, 시설 및 방법은 진핵 세포, 예를 들어 포유 동물 세포 또는 예를 들어 효모 세포 또는 사상 균류 세포 같은 하등 진핵 세포, 또는 원핵 세포, 예컨대, 그람-양성 또는 그람-음성 세포 및/또는 예를 들어 진핵 세포에 의해 합성되는 단백질, 펩티드, 항생제, 아미노산, 핵산(예컨대, DNA 또는 RNA)과 같은 진핵 세포 또는 원핵 세포의 제품의 생산을 대규모 방식으로 가능하게 한다. 여기에 달리 명시되지 않은 한, 디바이스, 시설 및 방법은 벤치 규모, 파일럿 규모 및 전체 생산 규모 능력을 포함하되 이에 제한되지 않는 임의의 원하는 용적 또는 생산 능력이 포함될 수 있다.
또한, 디바이스, 시설 및 방법은 교반 탱크, 에어리프트, 섬유, 마이크로 파이버, 중공 섬유, 세라믹 매트릭스, 유동층, 고정층 및/또는 분출층 생물반응기를 포함하지만 이에 한정되지 않는 임의의 적절한 반응기(들)를 포함할 수 있다. 본 명세서에서 사용되는 "반응기"는 발효기 또는 발효 유닛, 또는 임의의 다른 반응 용기를 포함할 수 있으며, 용어 "반응기"는 "발효기"와 교환 가능하게 사용된다. 예를 들어, 일부 양태에서, 생물반응기 유닛은 영양소 및/또는 탄소원의 공급, 적절한 가스(예를 들어, 산소)의 주입, 발효 또는 세포 배양 배지의 유입 및 유출 흐름, 기체와 액체 상의 분리, 온도의 유지, 산소 및 CO2 수준의 유지, pH 수준의 유지, 교반(예를 들어, 휘젓기) 및/또는 세정/살균 중 하나 이상이나 전부를 수행할 수 있다. 발효 유닛과 같은 예시적인 반응기 유닛은 유닛 내에 다수의 반응기를 포함할 수 있으며, 예를 들어 유닛은 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 60, 70, 80, 90 또는 100이나 그 이상의 생물반응기를 각 유닛 내에 가질 수 있고 및/또는 시설은 시설 내에 단일 또는 다중 반응기를 갖는 다수의 유닛을 포함할 수 있다. 다양한 실시예에서, 생물반응기는 회분식, 반 유가식, 유가식, 관류 및/또는 연속 발효 프로세스에 적합할 수 있다. 임의의 적합한 반응기 직경이 사용될 수 있다. 실시예에서, 생물반응기는 약 100 mL 내지 약 50,000 L의 용적을 가질 수 있다. 비제한적 예는 100 밀리리터, 250 밀리리터, 500 밀리리터, 750 밀리리터, 1 리터, 2 리터, 3 리터, 4 리터, 5 리터, 6 리터, 7 리터, 8 리터, 9 리터, 10 리터, 15 리터, 20 리터, 25 리터, 30 리터, 40 리터, 50 리터, 60 리터, 70 리터, 80 리터, 90 리터, 100 리터, 150 리터, 200 리터, 250 리터, 300 리터, 350 리터, 400 리터, 450 리터, 500 리터, 550 리터, 600 리터, 650 리터, 700 리터, 750 리터, 800 리터, 850 리터, 900 리터, 950 리터, 1000 리터, 1500 리터, 2000 리터, 2500 리터, 3000 리터, 3500 리터, 4000 리터, 4500 리터, 5000 리터, 6000 리터, 7000 리터, 8000 리터, 9000 리터, 10,000 리터, 15,000 리터, 20,000 리터, 및/또는 50,000 리터의 용적을 포함한다. 또한, 적합한 반응기는 다회용, 일회용, 사용후폐기형 또는 비-사용후폐기형일 수 있으며, 스테인레스 스틸(예를 들어, 316L 또는 임의의 다른 적합한 스테인레스 강) 및 인코넬 같은 금속 합금, 플라스틱 및/또는 유리를 포함하는 임의의 적합한 재료로 형성될 수 있다.
실시예에서 그리고 여기서 달리 언급하지 않는 한, 본원에 설명된 디바이스, 시설 및 방법은 또한 이러한 제품의 분리, 정제, 그리고 격리를 위한 조작 및/또는 장비와 같이 달리 언급되지 않는 임의의 적절한 유닛 동작 및/또는 장비를 포함할 수 있다. 기존의 스틱 건설 시설, 모듈식, 이동식 및 임시 시설 또는 기타 적합한 구조, 시설 및/또는 레이아웃과 같은 임의의 적합한 시설 및 환경이 사용될 수 있다. 예를 들어, 일부 실시예에서는 모듈식 클린 룸이 사용될 수 있다. 추가적으로, 그리고, 달리 언급되지 않는 한, 여기에 설명된 디바이스, 시스템 및 방법은 단일 위치 또는 시설에서 수용 및/또는 수행될 수 있거나, 또는 대안적으로 개별 또는 다수의 위치 및/또는 시설에서 수용 및/또는 수행될 수 있다.
제한적이지 않은 비제한적인 예로서, 미국 특허 공보 2013/0280797; 2012/0077429; 2011/0280797; 2009/0305626; 및 미국 특허 8,298,054; 7,629,167; 및 5,656,491은 그 전체가 본원에 참고로 인용되며, 적합할 수 있는 예시적인 시설, 장비 및/또는 시스템을 개시한다.
실시예에서, 세포는 진핵 세포, 예컨대 포유 동물 세포이다. 포유 동물 세포는 예를 들어 인간 또는 설치류 또는 소 세포계 또는 세포주일 수 있다. 그러한 세포, 세포계 또는 세포주의 예는 예를 들어, 쥐 골수종(NSO)-세포계, 중국 햄스터 난소(CHO)-세포계, HT1080, H9, HepG2, MCF7, MDBK Jurkat, NIH3T3, PC12, BHK(아기 햄스터 신장 세포), VERO, SP2/0, YB2/0, Y0, C127, L 세포, COS, 예를 들어, COS1 및 COS7, QC1-3, HEK-293, VERO, PER.C6, HeLA, EB1, EB2, EB3, 온콜리틱 또는 하이브리도마 세포계이다. 바람직하게 포유 동물 세포는 CHO-세포계이다. 일 실시예에서, 세포는 CHO 세포이다. 일 실시예에서, 세포는 CHO-K1 세포, CHO-K1 SV 세포, DG44 CHO 세포, DUXB11 CHO 세포, CHOS, CHO GS 녹아웃 세포, CHO FUT8 GS 녹아웃 세포, CHOZN 또는 CHO 유래 세포일 수 있다. CHO GS 녹아웃 세포(예컨대, GSKO 세포)는 예를 들어 CHO-K1 SV GS 녹아웃 세포이다. CHO FUT8 녹아웃 세포는 예를 들어 Potelligent® CHOK1 SV(Lonza Biologics, Inc.)이다. 진핵 세포는 또한 조류 세포, 세포계 또는 세포주, 예를 들어 EBx® 세포, EB14, EB24, EB26, EB66 또는 EBv13일 수 있다.
일 실시예에서, 진핵 세포는 줄기 세포이다. 줄기 세포는 예를 들어 배아 줄기 세포(ESC), 성체 줄기 세포, 유도된 만능 줄기 세포(iPSC), 조직 특이적 줄기 세포(예를 들어, 조혈 모세포) 및 중간엽 줄기 세포(MSC)를 포함하는 만능 줄기 세포일 수 있다.
일 실시예에서, 세포는 본원에 설명된 임의의 세포의 분화된 형태이다. 일 실시예에서, 세포는 배양 중 임의의 1차 세포로부터 유래된 세포이다.
실시예에서, 세포는 인간 간세포, 동물 간세포 또는 비-실질 세포와 같은 간세포이다. 예를 들어, 세포는 부착 대사 적격 인간 간세포, 부착 유도 적격 인간 간세포, 부착 Qualyst Transporter CertifiedTM 인간 간세포, 현탁 적격 인간 간세포(10-도너 및 20-도너 혼합 간세포 포함), 인간 간 쿠퍼 세포, 인간 간 성상 세포, 개 간세포(단일 및 혼합 비글 간세포 포함), 쥐 간세포(CD-1 및 C57BI/6 간세포 포함), 래트 간세포(Sprague-Dawley, Wistar Han 및 Wistar 간세포 포함), 원숭이 간세포(시노몰구스 또는 레서스 원숭이 간세포 포함), 고양이 간세포(Domestic Shorthair 간세포 포함) 및 토끼 간세포(New Zealand White 간세포 포함)일 수 있다. 예시적 간세포는 Triangle Research Labs, LLC(6 Davis Drive Research Triangle Park, North Carolina, USA 27709)로부터 상업적으로 입수 가능하다.
일 실시예에서, 진핵 세포는 예를 들어 효모 세포(예를 들어, 피키아 속(예를 들어 피키아 파스토리스, 피키아 메타놀리카, 피키아 클루이베리 및 피키아 안귀스타), 코마가타엘라 속(예를 들어 코마가타엘라 파스토리스, 코마가타엘라 수도파스토리스 또는 코마가타엘라 파프피이), 사카로미세스 속(예를 들어 사카로미세스 세레비지에, 세레비지아에, 사카로미세스 클루이베리, 사카로미세스 우바륨), 클루이베로미세스 속(예를 들어 클루이베로미세스 락티스, 클루이베로미세스 마르시아누스), 칸디다 속(예를 들어 칸디다 유틸리스, 칸디다 카카오이, 칸디다 보이디니이), 지오트리쿰 속(예를 들어 지오트리쿰 페르멘탄스), 한세눌라 폴리모르파, 야로위아 리폴리티카, 또는 쉬조사카로미세스 폼베 같은 하등 진핵 세포이다. 피키아 파스토리스 종이 선호된다. 피키아 파스토리스 균주의 예는 X33, GS115, KM71, KM71H; 및 CBS7435이다.
일 실시예에서, 진핵 세포는 진균 세포(예를 들어 아스페르길루스(예컨대 A. 니제르, A. 푸미가투스, A. 오르지아에, A. 니둘라), 아크레모늄(예컨대 A. 더모필륨), 카에토미움(예컨대 C. 더모필륨), 크리소스포리움(예컨대 C. 내열성 세균), 코르디셉스(예컨대 C. 밀리타리스), 코리나스쿠스, 크테노미세스, 푸사리움(예컨대 F. 옥시스포룸), 글로메렐라(예컨대 G. 그라미니콜라), 하이포크레아(예컨대 H. 제코리나), 마그나포르테(예컨대 M. 오르지아에), 미셀리오프토라(예컨대 M. 내열성 세균), 넥트리아(예컨대 N. 헤아마토콕카), 붉은빵곰팡이(예컨대 N. 크라사), 푸른곰팡이속의 곰팡이, 스포로트릭스(예컨대 S. 내열성 세균), 티엘라비아(예컨대 T. 테레스트리스, T. 헤테로탈리카), 트리코더마(예컨대 T. 레에세이), 또는 베르티실리움(예컨대 V. 달리아))이다.
일 실시예에서, 진핵 세포는 곤충 세포(예를 들어, Sf9, MimicTM Sf9, Sf21, High FiveTM(BT1-TN-5B1-4) 또는 BT1-Ea88 세포), 조류 세포(예를 들어, 암포라, 규조류, 두날리엘라, 클로렐라, 클라미도모나스, 남조식물(시아노박테리아), 난노클로롭시스, 스피룰리나 또는 오크로모나스 속의 조류 세포) 또는 식물 세포(예를 들어, 단자엽 식물(예를 들어, 옥수수, 벼, 밀, 또는 세타리아) 또는 쌍자엽 식물(예를 들어, 카사바, 감자, 콩, 토마토, 담배, 알팔파, 피스코미트렐라 파텐스 또는 애기장대)로부터의 세포)이다.
일 실시예에서, 세포는 박테리아 또는 원핵 세포이다.
실시예에서, 원핵 세포는 바실러스, 스트렙토미세스, 스트렙토코쿠스, 스타필로코쿠스 또는 락토바실러스와 같은 그람-양성 세포이다. 사용될 수 있는 바실러스는 예를 들어, B.수브틸리스, B.아밀로리퀴파시언스, B.리케니포르미스, B.나토 또는 B.메가테리움이다. 실시예에서, 세포는 B.수브틸리스, 예컨대 B.수브틸리스 3NA 및 B.수브틸리스 168이다. 바실러스는 예를 들어, Bacillus Genetic Stock Center(Biological Sciences 556, 484 West 12th Avenue, Columbus OH 43210-1214)로부터 얻을 수 있다.
일 실시예에서, 원핵 세포는 그람-음성 세포, 예컨대 살모넬라 종 또는 에스케리키아 콜라이, 예를 들어, TG1, TG2, W3110, DH1, DHB4, DH5a, HMS 174, HMS174(DE3), NM533, C600, HB101, JM109, MC4100, XL1-Blue 및 오리가미, 그리고, 예를 들어 BL-21 또는 BL21(DE3) 같은 E. 콜라이 B-균주로부터 유래된 것들이며, 이들 모두는 상업적으로 입수할 수 있다.
적절한 숙주 세포는 예를 들어 DSMZ(Deutsche Sammlung von Mikroorganismen and Zellkulturen GmbH, Braunschweig, Germany) 또는 ATCC(American Type Culture Collection)와 같은 배양물 은행으로부터 상업적으로 입수 가능하다.
실시예에서, 배양된 세포는 치료용으로 단백질, 예컨대 단일 클론 항체 및/또는 재조합 단백질과 같은 항체를 생산하는 데 사용된다. 실시예에서, 배양된 세포는 펩티드, 아미노산, 지방산 또는 다른 유용한 생화학적 중간체 또는 대사 산물을 생산한다. 예를 들어, 실시예에서, 약 4000 달톤 내지 약 140,000 달톤 초과의 분자량을 갖는 분자를 생산할 수 있다. 실시예에서, 이 분자는 일정 범위의 복잡성을 가질 수 있으며, 글리코실화를 포함하는 번역 후 변형을 포함할 수 있다.
실시예에서, 단백질은 예를 들어, BOTOX, 미요블록, 뉴로블록, 디스포트(또는 보툴리늄 신경독소의 다른 혈청형), 알글루코시다아제 알파, 답토마이신, YH-16, 코리오고나도트로핀 알파, 필그라스팀, 세트로렐릭스, 인터루킨-2, 알데슬로이킨, 테셀레울린, 데니류킨 디프티톡스, 인테페론 알파-n3(주사), 인테페론 알파-nl, DL-8234, 인테페론, 산토리(감마-1a), 인테페론 감마, 티모신 알파 1, 타소네르민, DigiFab, ViperaTAb, EchiTAb, CroFab, 네시리티드, 아바타셉트, 알레파셉트, 레비프, 엡토테르미민알파, 테리파라티드(골다공증), 칼시토닌 주사가능(뼈 질환), 칼시토닌(코, 골다공증), 에타네르셉트, 헤모글로빈 글루타머 250(소), 드로트레코긴 알파, 콜라게나제, 카르페리타이드, 재조합균주 인간 표피 성장 인자(국소 겔, 상처 치유), DWP401, 다르베포에틴 알파, 에포에틴 오메가, 에포에틴 베타, 에포에틴 알파, 데시루딘, 레피루딘, 비발리루딘, 노나코그 알파, 모노닌, 엡타코그 알파(활성화), 재조합균주 인자 VIII+VWF, 리콤비네이트, 재조합균주 인자 VIII, 인자 VIII(재조합균주), 알픈메이트, 옥토코그 알파, 인자 VIII, 팔리페르민, 인디키나제, 테넥테플라제, 알테플라제, 파미테플라제, 레테플라제, 나테플라제, 몬테플라제, 폴리트로핀 알파, rFSH, hpFSH, 미카펀진, 페그필그라스팀, 레노그라스팀, 나르토그라스팀, 세르모렐린, 글루카곤, 엑세나티드, 프람린티드, 이니글루세라제, 갈술파제, 류코트로핀, 몰그라모스팀, 트립토렐린 아세테이트, 히스트렐린(피하 임플란트, 하이드론), 데슬로렐린, 히스트렐린, 나파렐린, 류프롤리드 지속 방출 데포(ATRIGEL), 류프롤리드 임플란트(DUROS), 고세렐린, 유트로핀, KP-102 프로그램, 소마트로핀, 메카세르민(발육 부전), 에늘파비르티드, Org-33408, 인슐린 글라진, 인슐린 글루리신, 인슐린(흡입), 인슐린 리스프로, 인슐린 디터미어, 인슐린(구강, RapidMist), 메카세르민 린파베이트, 애나킨라, 셀모류킨, 99 mTc-압시티드 주사, 미엘로피드, 베타세론, 글라티라머 아세테이트, 게폰, 사르그라모스팀, 오프렐베킨, 인간 백혈구 유래 알파 인테페론, 빌라이브, 인슐린(재조합균주), 재조합균주 인간 인슐린, 인슐린 아스파르트, 메카세닌, 로페론-A, 인터페론 알파 2, 알파페론, 인테페론 알파콘-1, 인터페론알파, 아보넥스 재조합균주 인간 황체 형성 호르몬, 도르나제 알파, 트라페르민, 지코노티드, 탈티렐린, 디보테르민알파, 아토시반, 베카플레르민, 엡티피바티드, 제마이라, CTC-111, 산백-B, HPV 백신(4가), 옥트레오티드, 란레오티드, 안세스티른, 아갈시다제 베타, 아갈시다제 알파, 라로니다제, 프레자티드 구리 아세테이트(국소 겔), 라스부리카제, 라니비주맙, 액티뮨, PEG-인트론, 트리코민, 재조합균주 집 먼지 진드기 과민반응 감도 억압 주사, 재조합균주 인간 부갑상선 호르몬(PTH) 1-84(sc, 골다공증), 에포에틴 델타, 이식 유전자 항트롬빈 III, 그랜디트로핀, 비트라제, 재조합균주 인슐린, 인터페론 알파(경구 마름모꼴), GEM-21S, 바프레오티드, 이두르술파제, 옴나파트릴라트, 재조합균주 장액 알부민, 세르톨리주맙 페골, 글루카르피다제, 인간 재조합균주 C1 에스테르분해효소 억제자(맥관부종), 라노테플라제, 재조합균주 인간 성장 호르몬, 엔푸비르티드(무바늘 주사, 바이오젝터 2000), VGV-1, 인테페론(알파), 루시나크탄트, 아비프타딜(흡입, 폐 질환), 이카티반트, 에칼란티드, 오미가난, 아우로그랍, 펙시가난아세테이트, ADI-PEG-20, LDI-200, 데가렐릭스, 신트레델리베수도톡스, Favld, MDX-1379, ISAtx-247, 리라글루티드, 테리파라티드(골다공증), 티파코긴, AA4500, T4N5 리포솜 로션, 카투막소맙, DWP413, ART-123, 크리살린, 데스모테플라제, 아메디플라제, 코리폴리트로핀알파, TH-9507, 테두글루티드, 디아미드, DWP-412, 성장 호르몬(지속 방출 주사), 재조합균주 G-CSF, 인슐린(흡입, AIR), 인슐린(흡입, 인류의 과학 기술적 행동), 인슐린(흡입, AERx), RGN-303, DiaPep277, 인테페론 베타(간염 C 바이러스 감염(HCV)), 인테페론 알파-n3(경구), 벨라타셉트 경피 인슐린 패치, AMG-531, MBP-8298, 크세레셉트, 오페바칸, AIDSVAX, GV-1001, LymphoScan, 란피르나제, 리폭시산, 루수풀티드, MP52(베타-트리칼슘포스페이트 캐리어, 뼈 재생), 흑색종 백신, 시퓰레우셀-T, CTP-37, 인세지아, 비테스펜, 인간 트롬빈(동결, 외과 블리딩), 트롬빈, TransMID, 알피메프라제, 퓨리카제, 테를리프레신(정맥용, 간신장증후군), EUR-1008M, 재조합균주 FGF-I(주사가능, 혈관 질환), BDM-E, 로티갑티드, ETC-216, P-113, MBI-594AN, 듀라마이신(흡입, 낭성 섬유증), SCV-07, OPI-45, 엔도스타틴, 안지오스타틴, ABT-510, 바우만 버크 억제자 농축물, XMP-629, 99 mTc-히닉-안넥신 V, 카할랄리드 F, CTCE-9908, 테베렐릭스(확장 방출), 오자렐릭스, 로르니뎁신, BAY-504798, 인터루킨4, PRX-321, 펩스캔, 이보크타데킨, rh락토페린, TRU-015, IL-21, ATN-161, 실렌지타이드, 알부페론, 비파식스, IRX-2, 오메가 인테페론, PCK-3145, CAP-232, 파시레오티드, huN901-DMI, 난소 암 면역요법 백신, SB-249553, 온코박스-CL, 온코박스-P, BLP-25, CerVax-16, 멀티-에피토프 펩티드 흑색종 백신(MART-1, gp100, 티로시나아제), 네미피티드, rAAT(흡입), rAAT(피부과), CGRP(흡입, 천식), 페그수네르셉트, 티모신베타4, 플리티뎁신, GTP-200, 라모플라닌, GRASPA, OBI-1, AC-100, 연어 칼시토닌(경구, 엘리겐), 칼시토닌(경구, 골다공증), 엑사모렐린, 카프로모렐린, 카르데바, 벨라페르민, 131I-TM-601, KK-220, T-10, 울라리티드, 데펠레스타트, 헤마티드, 크리살린(국소), rNAPc2, 재조합균주 인자 V111(페길화 리포솜), bFGF, 페길화 재조합균주 스타필로키나제 변형, V-10153, 소노리시스 프롤리세, 뉴로박스, CZEN-002, 섬 세포 신생 요법, rGLP-1, BIM-51077, LY-548806, 엑세나티드(제어된 방출, 메디소르브), AVE-0010, GA-GCB, 아보렐린, ACM-9604, 리나클로타이드 아세테이트, CETi-1, 헤모스판, VAL(주사가능한), 급속작용인슐린(주사가능한, 비아델), 비강내 인슐린, 인슐린(흡입), 인슐린(경구, 엘리겐), 재조합균주 메티오닐 인간 렙틴, 피트라킨라 피하 주사, 습진), 피트라킨라(흡입 건조 분말, 천식), 멀티카인, RG-1068, MM-093, NBI-6024, AT-001, PI-0824, Org-39141, Cpn10(자가면역 질환/염증), 탈락토페린(국소), rEV-131(안과), rEV-131(호흡기질환), 경구 재조합균주 인간 인슐린(당뇨병), RPI-78M, 오프렐베킨(경구), CYT-99007 CTLA4-Ig, DTY-001, 발라테그라스트, 인테페론 알파-n3(국소), IRX-3, RDP-58, 타우페론, 담즙 염 자극 리파아제, 메리스파제, 알라인 인산분해효소, EP-2104R, 멜라노탄-II, 브레멜라노티드, ATL-104, 재조합균주 인간 마이크로플라스민, AX-200, SEMAX, ACV-1, Xen-2174, CJC-1008, 디놀핀 A, SI-6603, LAB GHRH, AER-002, BGC-728, 말라리아 백신(비로솜, PeviPRO), ALTU-135, 파르보바이러스 B19 백신, 인플루엔자 백신(재조합균주 뉴라미니다아제), 말라리아/HBV 백신, 안트락스 백신, Vacc-5q, Vacc-4x, HIV 백신(경구), HPV 백신, 타트 톡소이드, YSPSL, CHS-13340, PTH(1-34) 리포솜 크림(노바솜), 오스타볼린-C, PTH 아날로그(국소, 건선), MBRI-93.02, MTB72F 백신(결핵), MVA-Ag85A 백신(결핵), FARA04, BA-210, 재조합균주 전염병 FIV 백신, AG-702, OxSODrol, rBetV1, Der-p1/Der-p2/Der-p7 알레르겐-표적 백신(먼지 진드기 과민반응), PR1 펩티드 항원(백혈병), 돌연변이 라스 백신, HPV-16 E7 리포펩티드 백신, 라비리틴 백신(선암종), CML 백신, WT1-펩티드 백신(암), IDD-5, CDX-110, 펜트리스, 노렐린, CytoFab, P-9808, VT-111, 이크로캅티드, 텔베르민(피부과, 당뇨성 족부궤양), 루핀트리비르, 레티쿨로스, rGRF, HA, 알파-갈락토시다아제 A, ACE-011, ALTU-140, CGX-1160, 안지오텐신 치료 백신, D-4F, ETC-642, APP-018, rhMBL, SCV-07(경구, 결핵), DRF-7295, ABT-828, ErbB2-특정 항체 독소(항암제), DT3SSIL-3, TST-10088, PRO-1762, 콤보톡스, 콜레시스토키닌-B/가스트린-수용체 결합 펩티드, 111In-hEGF, AE-37, 트랜스니주맙-DM1, 대항제 G, IL-12(재조합균주), PM-02734, IMP-321, rhIGF-BP3, BLX-883, CUV-1647(국소), L-19 기초 방사선면역치료제(암), Re-188-P-2045, AMG-386, DC/1540/KLH 백신(암), VX-001, AVE-9633, AC-9301, NY-ESO-1 백신(펩티드), NA17.A2 펩티드, 흑색종 백신(펄스 항원 치료), 전립선암 백신, CBP-501, 재조합균주 인간 락토페린(건조 눈), FX-06, AP-214, WAP-8294A(주사가능), ACP-HIP, SUN-11031, 펩티드 YY [3-36](비만, 비강내), FGLL, 아타시셉트, BR3-Fc, BN-003, BA-058, 인간 부갑상선 호르몬 1-34(코, 골다공증), F-18-CCR1, AT-1100(배 질환/당뇨병), JPD-003, PTH(7-34) 리포솜 크림(노바솜), 듀라마이신(안과, 건조 눈), CAB-2, CTCE-0214, 글리코페길화 적혈구형성인자, EPO-Fc, CNTO-528, AMG-114, JR-013, 인자 XIII, 아미노칸딘, PN-951, 716155, SUN-E7001, TH-0318, BAY-73-7977, 테베렐릭스(즉시 방출), EP-51216, hGH(제어된 방출, 생물권), OGP-I, 시푸비르티드, TV4710, ALG-889, Org-41259, rhCC10, F-991, 티모펜틴(폐 질환), r(m)CRP, 헤파토실렉티브 인슐린, 수발린, L19-IL-2 융합 단백질, 엘라핀, NMK-150, ALTU-139, EN-122004, rhTPO, 트롬보포이에틴 수용체 작용제(혈소판감소성 장애), AL-108, AL-208, 신경 성장 인자 대항제(통증), SLV-317, CGX-1007, INNO-105, 경구 테리파라티드(엘리겐), GEM-OS1, AC-162352, PRX-302, LFn-p24 융합 백신(테라포어), EP-1043, S 뉴모니아에 소아 백신, 말라리아 백신, 네이세리아 메닌기티디스 그룹 B 백신, 네오나탈 그룹 B 연쇄상 구균 백신, 안트락스 백신, HCV 백신(gpE1+gpE2+MF-59), 이염 매체 요법, HCV 백신(코어 항원+ISCOMATRIX), hPTH(1-34)(경피, ViaDerm), 768974, SYN-101, PGN-0052, 아비스쿰닌, BIM-23190, 결핵 백신, 멀티-에피토프 티로시나아제 펩티드, 암 백신, 엔카스팀, APC-8024, GI-5005, ACC-001, TTS-CD3, 혈관-표적 TNF(고형 종양), 데스모프레신(구강 제어-방출), 오네르셉트, 및 TP-9201이다.
일부 실시예에서, 폴리펩티드는 아달리무맙(HUMIRA), 인플릭시맙(REMICADETM), 리툭시맙(RITUXANTM/MAB THERATM), 에타네르셉트(ENBRELTM), 베바시주맙(AVASTINTM), 트라스투주맙(HERCEPTINTM), 페그릴그라스팀(NEULASTATM), 또는 바이오시밀러와 바이오베터를 포함하는 임의의 다른 적합한 폴리펩티드이다.
다른 적합한 폴리펩티드는 아래 및 US2016/0097074의 표 1에 나열된 것들이다:
실시예에서, 폴리펩티드는 표 2에 나타난 바와 같은 호르몬, 혈액 클로팅/응고 인자, 시토카인/성장 인자, 항체 분자, 융합 단백질, 단백질 백신, 또는 펩티드이다.
실시예에서, 단백질은 표 3에 제시된 바와 같은 다중특이적 단백질, 예를 들어, 이중특이적 항체이다.
다르게 정의되지 않는 한, 본원에서 사용된 모든 기술 및 과학 용어는 본 개시내용과 관련된 분야의 통상의 숙련자에 의해 일반적으로 이해되는 것과 동일한 의미를 갖는다. 본원에 설명된 것과 유사한 또는 동등한 임의의 방법 및 물질이 본 개시내용의 실시 및/또는 테스트를 위해 사용될 수 있지만, 바람직한 물질 및 방법이 본원에 기재되어 있다. 본 개시내용의 설명 및 청구에 있어서, 정의가 제공되는 경우에 정의된 방식에 따라 다음의 용어가 사용된다.
또한, 본 명세서에서 사용된 용어는 특정 실시예만을 설명하기 위한 것이며, 제한하려는 의도는 아니라는 것을 이해해야 한다.
단수형 표현은 단수 표현의 문법적 대상의 하나 또는 하나 초과(즉, 적어도 하나)를 나타내기 위해 본 명세서에서 사용된다. 예로서, "모듈 유닛"은 하나의 모듈 유닛 또는 하나보다 많은 모듈 유닛을 의미할 수 있다.
추가 설명없이도, 통상의 숙련자는 전술한 설명 및 예시적인 예를 사용하여 본 개시내용의 맞춤형 시설을 만들고 활용할 수 있다고 믿어진다.
본 개시내용은 특정 양태를 참조하여 개시되었지만, 본 개시내용의 진정한 사상 및 범위를 벗어나지 않고 본 개시내용의 다른 양태 및 변형이 통상의 숙련자에 의해 안출될 수 있음이 명백하다. 첨부된 청구범위는 모든 이런 양태 및 동등한 변형을 포함하는 것으로 해석되도록 의도된다.
Claims (25)
- 적어도 하나의 제약 제품을 제조하기 위한 맞춤형 시설이며,
적어도 하나의 중앙 유닛; 및
적어도 하나의 모듈 유닛으로서, 적어도 하나의 중앙 유닛이 적어도 하나의 모듈 유닛에 유틸리티를 제공하도록 적어도 하나의 중앙 유닛과 연통하는 적어도 하나의 모듈 유닛을 포함하는, 맞춤형 시설. - 제1항에 있어서, 쉘을 더 포함하고, 적어도 하나의 중앙 유닛은 적어도 부분적으로 쉘 내에 위치되며, 적어도 하나의 모듈 유닛은 적어도 부분적으로 쉘 내에 위치되는, 맞춤형 시설.
- 제1항 또는 제2항에 있어서, 적어도 하나의 모듈 유닛은 발효 유닛, 프리-바이러스 유닛, 포스트-바이러스 유닛, 유틸리티 공간, 창고, 배지 버퍼 시설, 사무실, 개인 유닛, 생산 유닛, 충전 완료 유닛, 투여량 제형화 유닛 및 포장 유닛 중 적어도 하나를 포함하는, 맞춤형 시설.
- 제1항 내지 제3항 중 어느 한 항에 있어서, 적어도 하나의 모듈 유닛 중 적어도 하나는 적어도 하나의 중앙 유닛에 직접 인접하는, 맞춤형 시설.
- 제2항 내지 제4항 중 어느 한 항에 있어서, 적어도 하나의 모듈 유닛은 쉘의 풋프린트를 최소화하면서 쉘 내의 모듈 유닛의 개수를 최대화하도록 배열된 복수의 모듈 유닛을 포함하는, 맞춤형 시설.
- 제5항에 있어서, 복수의 모듈 유닛의 각각의 모듈 유닛은 적어도 하나의 중앙 유닛 중 적어도 하나와 복수의 모듈 유닛 중 다른 하나에 직접 인접하는, 맞춤형 시설.
- 제5항 또는 제6항에 있어서, 적어도 하나의 중앙 유닛 및 복수의 모듈 유닛은 허브 및 스포크 형태를 형성하는, 맞춤형 시설.
- 제5항 내지 제7항 중 어느 한 항에 있어서, 적어도 하나의 중앙 유닛 및 복수의 모듈 유닛은 H 형상 레이아웃으로 배열되는, 맞춤형 시설.
- 제2항 내지 제8항 중 어느 한 항에 있어서, 쉘 내의 지면 상에 지지된 생물반응기를 추가로 포함하는, 맞춤형 시설.
- 제1항 내지 제9항 중 어느 한 항에 있어서, 적어도 하나의 모듈 유닛 중 하나 내에 지지된 생물반응기를 추가로 포함하는, 맞춤형 시설.
- 제2항 내지 제10항 중 어느 한 항에 있어서, 맞춤형 시설의 외부 벽은,
쉘에 의해 형성되고, 쉘은 적어도 하나의 중앙 유닛 및 적어도 하나의 모듈 유닛을 전체적으로 둘러싸는 구성; 및
쉘, 및 적어도 하나의 중앙 유닛의 외부 벽과 적어도 하나의 모듈 유닛의 외부 벽 중 적어도 하나에 의해 형성되는 구성
중 하나인, 맞춤형 시설. - 제2항 내지 제10항 중 어느 한 항에 있어서, 쉘은 적어도 하나의 측부 벽 및 지붕을 포함하고, 적어도 하나의 측부 벽은 적어도 하나의 중앙 유닛 및 적어도 하나의 모듈 유닛을 둘러싸고, 지붕은 적어도 하나의 측부 벽의 상부 에지에 고정되며, 지붕은 적어도 하나의 중앙 유닛 및 적어도 하나의 모듈 유닛 위로 연장되는, 맞춤형 시설.
- 제1항 내지 제12항 중 어느 한 항에 있어서, 적어도 하나의 모듈 유닛 중 적어도 하나는 클린 룸인, 맞춤형 시설.
- 제1항 내지 제13항 중 어느 한 항에 있어서, 적어도 하나의 모듈 유닛은 세포 치료 작업을 위해 구성되는, 맞춤형 시설.
- 적어도 하나의 제약 제품을 제조하기 위한 시설을 조립하는 방법이며,
적어도 하나의 중앙 유닛을 제공하는 단계; 및
적어도 하나의 모듈 유닛을 제공하는 단계로서, 적어도 하나의 모듈 유닛은 적어도 하나의 중앙 유닛이 적어도 하나의 모듈 유닛에 유틸리티를 제공하도록 적어도 하나의 중앙 유닛과 연통하는, 단계
를 포함하는, 방법. - 제15항에 있어서,
쉘을 제공하는 단계,
적어도 하나의 중앙 유닛을 적어도 부분적으로 쉘 내에 위치시키는 단계, 및
적어도 하나의 모듈 유닛을 적어도 부분적으로 쉘 내에 위치시키는 단계를 더 포함하는, 방법. - 제15항 또는 제16항에 있어서, 적어도 하나의 모듈 유닛은 발효 유닛, 프리-바이러스 유닛, 포스트-바이러스 유닛, 유틸리티 공간, 창고, 배지 버퍼 시설, 사무실, 개인 유닛, 생산 유닛, 충전 완료 유닛, 투여량 제형화 유닛 및 포장 유닛 중 적어도 하나를 포함하는, 방법.
- 제16항 또는 제17항에 있어서, 적어도 하나의 모듈 유닛은 쉘의 풋프린트를 최소화하면서 쉘 내의 모듈 유닛의 개수를 최대화하도록 배열된 복수의 모듈 유닛을 포함하는, 방법.
- 제18항에 있어서, 복수의 모듈 유닛의 각각의 모듈 유닛은 적어도 하나의 중앙 유닛 중 적어도 하나와 적어도 하나의 모듈 유닛의 다른 하나에 직접 인접하는, 방법.
- 제18항 또는 제19항에 있어서, 적어도 하나의 중앙 유닛 및 복수의 모듈 유닛은 허브 및 스포크 형태를 형성하는, 방법.
- 제18항 내지 제20항 중 어느 한 항에 있어서, 적어도 하나의 중앙 유닛 및 복수의 모듈 유닛은 H 형상 레이아웃으로 배열되는, 방법.
- 제16항 내지 제21항 중 어느 한 항에 있어서, 쉘 내의 지면 상에 생물반응기를 지지하는 단계 및 적어도 하나의 모듈 유닛 중 하나 내에 생물반응기를 지지하는 단계 중 하나를 추가로 포함하는, 방법.
- 제16항 내지 제22항 중 어느 한 항에 있어서, 맞춤형 시설의 외부 벽은,
쉘에 의해 형성되고, 쉘은 적어도 하나의 중앙 유닛 및 적어도 하나의 모듈 유닛을 전체적으로 둘러싸는 구성; 및
쉘, 및 적어도 하나의 중앙 유닛의 외부 벽과 적어도 하나의 모듈 유닛의 외부 벽 중 적어도 하나에 의해 형성되는 구성
중 하나인, 방법. - 제16항 내지 제22항 중 어느 한 항에 있어서, 쉘은 적어도 하나의 측부 벽 및 지붕을 포함하고, 적어도 하나의 측부 벽은 적어도 하나의 중앙 유닛 및 적어도 하나의 모듈 유닛을 둘러싸고, 지붕은 적어도 하나의 측부 벽의 상부 에지에 고정되며, 지붕은 적어도 하나의 중앙 유닛 및 적어도 하나의 모듈 유닛 위로 연장되는, 방법.
- 제15항 내지 제24항 중 어느 한 항에 있어서, 적어도 하나의 제약 제품은 바이오시밀러 제품인, 방법.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020227014066A KR20220062128A (ko) | 2016-03-10 | 2017-03-10 | 맞춤형 시설 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662306556P | 2016-03-10 | 2016-03-10 | |
| US62/306,556 | 2016-03-10 | ||
| PCT/US2017/021838 WO2017156420A1 (en) | 2016-03-10 | 2017-03-10 | Customizable facility |
Related Child Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020247013334A Division KR20240058963A (ko) | 2016-03-10 | 2017-03-10 | 맞춤형 시설 |
| KR1020227014066A Division KR20220062128A (ko) | 2016-03-10 | 2017-03-10 | 맞춤형 시설 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20180123687A true KR20180123687A (ko) | 2018-11-19 |
Family
ID=58398282
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020187028608A KR20180123687A (ko) | 2016-03-10 | 2017-03-10 | 맞춤형 시설 |
| KR1020227014066A KR20220062128A (ko) | 2016-03-10 | 2017-03-10 | 맞춤형 시설 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227014066A KR20220062128A (ko) | 2016-03-10 | 2017-03-10 | 맞춤형 시설 |
Country Status (12)
| Country | Link |
|---|---|
| US (2) | US11236520B2 (ko) |
| EP (1) | EP3426217A1 (ko) |
| JP (1) | JP7009378B2 (ko) |
| KR (2) | KR20180123687A (ko) |
| CN (1) | CN109414365A (ko) |
| AU (1) | AU2017230823A1 (ko) |
| BR (1) | BR112018068281A2 (ko) |
| CA (1) | CA3017165A1 (ko) |
| EA (1) | EA201892029A1 (ko) |
| IL (1) | IL261709B (ko) |
| SG (1) | SG11201807780XA (ko) |
| WO (1) | WO2017156420A1 (ko) |
Families Citing this family (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9795957B2 (en) | 2009-08-16 | 2017-10-24 | G-Con Manufacturing, Inc. | Modular, self-contained, mobile clean room |
| JP6783143B2 (ja) | 2014-03-25 | 2020-11-11 | テルモ ビーシーティー、インコーポレーテッド | 培地の受動的補充 |
| WO2017004592A1 (en) | 2015-07-02 | 2017-01-05 | Terumo Bct, Inc. | Cell growth with mechanical stimuli |
| EP3464565A4 (en) | 2016-05-25 | 2020-01-01 | Terumo BCT, Inc. | CELL EXPANSION |
| US11104874B2 (en) | 2016-06-07 | 2021-08-31 | Terumo Bct, Inc. | Coating a bioreactor |
| US11685883B2 (en) | 2016-06-07 | 2023-06-27 | Terumo Bct, Inc. | Methods and systems for coating a cell growth surface |
| JP7393945B2 (ja) | 2017-03-31 | 2023-12-07 | テルモ ビーシーティー、インコーポレーテッド | 細胞増殖 |
| GB201718917D0 (en) * | 2017-11-16 | 2018-01-03 | Ge Healthcare Bioprocess R&D Ab | Method and system for manufacturing of biopharmaceutical products |
| CN107965167B (zh) * | 2017-12-20 | 2019-05-10 | 北京臻惠康生物科技有限公司 | 一种细胞制备实验室设计方案 |
| US20190367858A1 (en) | 2018-06-01 | 2019-12-05 | Lonza Ltd. | Midscale Model For Organic Growth and Phasing |
| WO2021030568A1 (en) | 2019-08-15 | 2021-02-18 | G-Con Manufacturing, Inc. | Removable panel roof for modular, self-contained, mobile clean room |
| US11773613B2 (en) * | 2020-05-05 | 2023-10-03 | The Boldt Group, Inc. | Modular configurable hospital system and method |
| EP3926031A1 (en) * | 2020-06-15 | 2021-12-22 | ESTR Biosystems GmbH | Assembly system for a smart tank for a bio-pharma process |
| US11725411B2 (en) * | 2020-08-17 | 2023-08-15 | Terrapower, Llc | Nuclear fuel assembly with multi-pitch wire wrap |
| US11492795B2 (en) | 2020-08-31 | 2022-11-08 | G-Con Manufacturing, Inc. | Ballroom-style cleanroom assembled from modular buildings |
Family Cites Families (51)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4667580A (en) | 1984-07-19 | 1987-05-26 | Wetzel Lawrence E | Clean room module |
| GB8515629D0 (en) * | 1985-06-20 | 1985-07-24 | Celltech Ltd | Fermenter |
| DE9014558U1 (ko) * | 1989-11-24 | 1991-01-03 | Bourdichon, Alain, Tacoronte, Teneriffa, Es | |
| US5272071A (en) | 1989-12-22 | 1993-12-21 | Applied Research Systems Ars Holding N.V. | Method for the modification of the expression characteristics of an endogenous gene of a given cell line |
| GB9022545D0 (en) | 1990-10-17 | 1990-11-28 | Wellcome Found | Culture medium |
| JPH0733717B2 (ja) * | 1991-06-17 | 1995-04-12 | 戸田建設株式会社 | 多用途生産システムの構築方法と建物 |
| DE4218615C1 (ko) | 1992-06-05 | 1993-07-15 | Nukem Gmbh, 8755 Alzenau, De | |
| IT1258959B (it) | 1992-06-09 | 1996-03-11 | Impianto a moduli mobili per lo sviluppo e la produzione di prodotti biotecnologici su scala pilota | |
| US6673901B2 (en) | 1997-06-12 | 2004-01-06 | Research Corporation Technologies, Inc. | Artificial antibody polypeptides |
| US6688048B2 (en) * | 1998-04-24 | 2004-02-10 | Udo I. Staschik | Utilities container |
| CA2269967C (en) * | 1998-04-24 | 2005-09-13 | Udo Ingmar Staschik | Utilities container |
| US6176046B1 (en) | 1998-11-24 | 2001-01-23 | Northstar Industries, Inc. | Portable, pre-manufactured, modular natural gas delivery stations |
| WO2001029058A1 (en) | 1999-10-15 | 2001-04-26 | University Of Massachusetts | Rna interference pathway genes as tools for targeted genetic interference |
| US6326193B1 (en) | 1999-11-05 | 2001-12-04 | Cambria Biosciences, Llc | Insect control agent |
| US20010047628A1 (en) * | 1999-12-21 | 2001-12-06 | Roy Mouton | Relocatable fire, storm and contaminant resistant modular building structures |
| WO2001096584A2 (en) | 2000-06-12 | 2001-12-20 | Akkadix Corporation | Materials and methods for the control of nematodes |
| US20050193643A1 (en) * | 2002-05-08 | 2005-09-08 | Pettus Daryl O. | Modular containment unit |
| GB0224760D0 (en) * | 2002-10-25 | 2002-12-04 | Jowett E C | Waste water treatment station in shipping container |
| US7182858B2 (en) | 2003-03-04 | 2007-02-27 | Kinetico Incorporated | Multiple barrier filter apparatus |
| EP1719025B1 (en) | 2004-02-03 | 2019-10-23 | GE Healthcare Bio-Sciences Corp. | System and method for manufacturing |
| US20050235581A1 (en) * | 2004-04-26 | 2005-10-27 | Intellectual Property, Llc | System for production of standard size dwellings using a satellite manufacturing facility |
| DK1773976T4 (da) | 2004-06-04 | 2020-02-10 | Global Life Sciences Solutions Usa Llc | Engangsbioreaktorsystemer og -fremgangsmåder |
| DE102005036763B4 (de) | 2005-08-04 | 2007-07-26 | Inheco Industrial Heating And Cooling Gmbh | System aus mehreren Inkubatoren |
| CA2632520A1 (en) | 2005-12-05 | 2007-06-14 | Ernest G. Hope | Prevalidated, modular good manufacturing practice-compliant facility |
| CA2682738A1 (en) | 2007-04-16 | 2008-10-23 | Momenta Pharmaceuticals, Inc. | Defined glycoprotein products and related methods |
| EP2103548B1 (en) | 2008-03-22 | 2014-10-01 | Pall Corporation | System comprising a tote and a flexible container |
| CA2668216A1 (en) * | 2008-06-03 | 2009-12-03 | Atlantic Bioventure Centre | Modular portable micro-factory system |
| KR101660852B1 (ko) * | 2008-12-23 | 2016-09-28 | 조마 (유에스) 엘엘씨 | 유연성 제조 시스템 |
| US9713575B2 (en) | 2009-05-07 | 2017-07-25 | Gea Process Engineering Limited | Tablet production module and method for continuous production of tablets |
| US9398717B2 (en) * | 2009-05-29 | 2016-07-19 | Rosendin Electric, Inc. | Modular power skid assembled with different electrical cabinets and components mounted on the skid |
| US9192069B2 (en) * | 2013-08-05 | 2015-11-17 | Rosendin Electric, Inc. | Modular power skid assembled with different electrical cabinets and components mounted on the skid |
| ES2665972T3 (es) | 2009-08-16 | 2018-04-30 | G-Con Manufacturing Inc. | Sala blanca móvil autónoma modular |
| US9795957B2 (en) * | 2009-08-16 | 2017-10-24 | G-Con Manufacturing, Inc. | Modular, self-contained, mobile clean room |
| EP2585656A4 (en) | 2010-01-07 | 2014-05-14 | Comau Inc | MODULAR MANUFACTURING SYSTEM AND METHOD THEREFOR |
| US9670689B2 (en) * | 2010-04-06 | 2017-06-06 | Schneider Electric It Corporation | Container based data center solutions |
| US8771635B2 (en) | 2010-04-26 | 2014-07-08 | Toyota Motor Engineering & Manufacturing North America, Inc. | Hydrogen release from complex metal hydrides by solvation in ionic liquids |
| WO2012032112A1 (en) * | 2010-09-10 | 2012-03-15 | Cellerix, S.A. | Stem cell culture media and methods |
| US10371394B2 (en) | 2010-09-20 | 2019-08-06 | Biologics Modular Llc | Mobile, modular cleanroom facility |
| WO2012122413A1 (en) | 2011-03-08 | 2012-09-13 | University Of Maryland Baltimore County | Microscale bioprocessing system and method for protein manufacturing |
| LT2773326T (lt) | 2011-11-04 | 2019-04-25 | Nitto Denko Corporation | Lipidų-nukleorūgščių dalelių sterilios gamybos būdas |
| US9091496B2 (en) * | 2012-03-08 | 2015-07-28 | Google Inc. | Controlling data center cooling |
| US9158345B1 (en) * | 2012-10-15 | 2015-10-13 | Google Inc. | Managing computer performance |
| DE102013201171A1 (de) * | 2013-01-24 | 2014-07-24 | Infracor Gmbh | Verfahren und System zur Nutzung eines Industriegrundstücks |
| KR101920129B1 (ko) * | 2013-10-14 | 2018-11-19 | 지-콘 메뉴팩츄어링 인코포레이티드 | 모듈형 모바일 룸을 연결하기 위한 유닛 |
| DK3102935T3 (da) | 2014-02-07 | 2021-04-06 | Cmc Biologics As | Bioreaktoranordning og fremgangsmåde til fremstilling af en biopolymer |
| KR20170040255A (ko) * | 2014-07-11 | 2017-04-12 | 지-콘 메뉴팩츄어링 인코포레이티드 | 유틸리티를 청정실, 격리 또는 봉쇄 큐비클, 포드 또는 모듈에 공급하는 모듈형 부품 |
| US20160376784A1 (en) * | 2015-06-25 | 2016-12-29 | Erden Timur | Method and system for urban room structures |
| US20160208209A1 (en) * | 2015-01-19 | 2016-07-21 | Dakota Systems, Inc. | Bioreactor Docking Station Systems, and Methods of Use Thereof |
| US9617748B2 (en) * | 2015-04-21 | 2017-04-11 | Kasita, LLC | Modular housing units, reusable support structure, and utility connector |
| ITUB20152618A1 (it) * | 2015-07-30 | 2017-01-30 | Sinteco Impianti Srl | Struttura di camera bianca prefabbricata |
| US10689873B2 (en) * | 2016-03-10 | 2020-06-23 | Lonza Ltd | Customizable facility |
-
2017
- 2017-03-10 WO PCT/US2017/021838 patent/WO2017156420A1/en active Application Filing
- 2017-03-10 CA CA3017165A patent/CA3017165A1/en not_active Abandoned
- 2017-03-10 AU AU2017230823A patent/AU2017230823A1/en not_active Abandoned
- 2017-03-10 EA EA201892029A patent/EA201892029A1/ru unknown
- 2017-03-10 KR KR1020187028608A patent/KR20180123687A/ko not_active IP Right Cessation
- 2017-03-10 SG SG11201807780XA patent/SG11201807780XA/en unknown
- 2017-03-10 BR BR112018068281A patent/BR112018068281A2/pt not_active Application Discontinuation
- 2017-03-10 JP JP2018547273A patent/JP7009378B2/ja active Active
- 2017-03-10 US US15/455,836 patent/US11236520B2/en active Active
- 2017-03-10 CN CN201780026484.9A patent/CN109414365A/zh active Pending
- 2017-03-10 KR KR1020227014066A patent/KR20220062128A/ko not_active Application Discontinuation
- 2017-03-10 EP EP17712910.3A patent/EP3426217A1/en active Pending
-
2018
- 2018-09-12 IL IL261709A patent/IL261709B/en unknown
-
2021
- 2021-12-16 US US17/553,283 patent/US11613900B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CN109414365A (zh) | 2019-03-01 |
| JP7009378B2 (ja) | 2022-02-10 |
| IL261709A (en) | 2018-10-31 |
| SG11201807780XA (en) | 2018-10-30 |
| IL261709B (en) | 2021-09-30 |
| US11613900B2 (en) | 2023-03-28 |
| US20170260763A1 (en) | 2017-09-14 |
| US20220106800A1 (en) | 2022-04-07 |
| WO2017156420A1 (en) | 2017-09-14 |
| WO2017156420A8 (en) | 2018-10-11 |
| CA3017165A1 (en) | 2017-09-14 |
| JP2019516029A (ja) | 2019-06-13 |
| EA201892029A1 (ru) | 2019-03-29 |
| BR112018068281A2 (pt) | 2019-04-02 |
| US11236520B2 (en) | 2022-02-01 |
| KR20220062128A (ko) | 2022-05-13 |
| AU2017230823A1 (en) | 2018-09-27 |
| EP3426217A1 (en) | 2019-01-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20180123687A (ko) | 맞춤형 시설 | |
| KR102423233B1 (ko) | 맞춤형 시설 | |
| CN109312291A (zh) | 可变直径生物反应器 | |
| US11377865B2 (en) | Customizable facility | |
| CN108348817A (zh) | 一种用于生产生物药品的生产设施 | |
| KR20210018872A (ko) | 유기적 성장 및 단계화를 위한 중간 스케일 모델 | |
| EP3942014A1 (en) | Continuous blade impeller | |
| CN110225790A (zh) | 减少药物中病毒滴度的方法 | |
| KR20230122078A (ko) | 바이오프로세스 시스템을 위한 멸균 단절기 및 이의사용 방법 | |
| CN110072602A (zh) | 具有过滤器锁定设计的过滤器组件 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| E902 | Notification of reason for refusal | ||
| E601 | Decision to refuse application | ||
| J201 | Request for trial against refusal decision | ||
| J301 | Trial decision |
Free format text: TRIAL NUMBER: 2022101000965; TRIAL DECISION FOR APPEAL AGAINST DECISION TO DECLINE REFUSAL REQUESTED 20220426 Effective date: 20230313 |
|
| E902 | Notification of reason for refusal | ||
| S601 | Decision to reject again after remand of revocation | ||
| E801 | Decision on dismissal of amendment | ||
| S601 | Decision to reject again after remand of revocation |