KR20170054459A - 친수성 약물의 표적 전달 방법 - Google Patents
친수성 약물의 표적 전달 방법 Download PDFInfo
- Publication number
- KR20170054459A KR20170054459A KR1020177009510A KR20177009510A KR20170054459A KR 20170054459 A KR20170054459 A KR 20170054459A KR 1020177009510 A KR1020177009510 A KR 1020177009510A KR 20177009510 A KR20177009510 A KR 20177009510A KR 20170054459 A KR20170054459 A KR 20170054459A
- Authority
- KR
- South Korea
- Prior art keywords
- straight chain
- sulfonate
- chain alkyl
- amphipathic
- sulfate
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5107—Excipients; Inactive ingredients
- A61K9/5123—Organic compounds, e.g. fats, sugars
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
- A61K31/136—Amines having aromatic rings, e.g. ketamine, nortriptyline having the amino group directly attached to the aromatic ring, e.g. benzeneamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4738—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4745—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems condensed with ring systems having nitrogen as a ring hetero atom, e.g. phenantrolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7028—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages
- A61K31/7034—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin
- A61K31/704—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin attached to a condensed carbocyclic ring system, e.g. sennosides, thiocolchicosides, escin, daunorubicin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Nanotechnology (AREA)
- Dermatology (AREA)
- Physics & Mathematics (AREA)
- Biomedical Technology (AREA)
- Optics & Photonics (AREA)
- Molecular Biology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
100 ㎛ 이하 크기의 입자들로 된 수계 콜로이드 또는 수성 현탁물 형태의 약학적 조성물은 물 또는 수성 체액에서 0.1 중량% 미만의 용해도를 가진 친수성 항암제의 양친매성 설포네이트 또는 설페이트를 포함하거나 또는 이들로 구성된다. 또한, 본 발명은 분말성 형태의 입자, 그 제조 방법, 콜로이드 및 콜로이드성 현탁물 (courser suspension)의 제조 방법, 약학적 조성물 투여에 의한 간암, 특히 고형 간 종양 치료 방법, 및 본 발명에 따른 조성물의 설계 방법을 개시한다.
Description
본 발명은 친수성 약물을 인간 또는 동물의 간 및 고형 간 종양에 투여하는 방법에 관한 것이다. 보다 상세하게는, 본 발명은 친수성 약물, 특히 항암제의 투여 방법에 관한 것이다.
치료 범위 (therapeutic window)는 질환을 효과적이고 안전하게 치료할 수 있는 약물의 투여량 범위를 나타낸다. 그 범위는 인지가능한 치료학적 효과가 나타나는 용량에서부터 치료학적 이점이 부작용에 의해 상쇄되는 용량까지이다.
항암제의 대부분은 좁은 치료 범위를 가지고 있다. 또한, 대게는 투여된 용량 중 소량만 치료할 부위에 도달한다. 경구 섭취나 혈관내 주입에 의한 전신 투여시, 약물은 순환계를 통해 신체 전역으로 퍼지게 되어, 전신에 영향을 미치게 된다. 이상적으로는, 약물은 치료가 필요한 장기나 조직과 같이 원하는 신체 부위로만 안내되어야 한다. 이런 표적 투여는 나머지 신체 부위에서의 유해성을 회피할 수 있을 것이다. 이런 유형의 투여는 치료가 필요없는 조직으로는 상당량의 약물이 도달하지 않도록 하면서 원하는 조직으로 약물을 안내하기 위한 것이다.
신체의 특정 부위로 안내되어야 하는 약물의 예로는 항암제인 독소루비신이 있다. 독소루비신의 치료학적 효능은 표적화된 약물 전달에 의해 현저하게 개선될 수 있다는 것이 일반적인 인식인데, 그 이유는 이의 위협적인 부작용을 회피하거나 또는 적어도 실질적으로 낮출 수 있기 때문이다. 독소루비신의 가장 위협적인 부작용은 심장 손상이다. 독소루비신의 누적 용량이 550 mg/m2에 도달하게 되면, 심장 부작용 위험성이 급격하게 증가한다. 독소루비신의 심장 독성은 미토콘드리아의 산화적 인산화가 용량-의존적으로 저하되는 것을 특징으로 한다. 독소루비신과 철의 상호작용에 의해 생성되는 반응성 산소 종이 근세포를 손상시켜, 근원섬유 감소 및 세포질 액포화를 야기할 수 있다. 이러한 유형의 과잉 손상이 환자의 사망을 일으킬 수도 있다. 따라서, 독소루비신의 심장내 농도는 가능한 낮게 유지시키는 것이 좋다.
간암은 독소루비신의 투여가 처방되는 여러가지 악성 암들 중 하나이다. 특히, 간암은 경동맥성 화학색전술로 알려진 시술을 통한 표적화된 (또는 국소) 투여에 의해 치료할 수 있다. 이 시술에서, 독소루비신은 카테터를 통해 간의 병변 부위로 공급되는 동맥(들)으로 직접 투여되지만, 질병에 걸리지 않은 간 부위로 공급되는 동맥들은 예를 들어 젤라틴 스폰지로 차단한다.
고립형 간 관류 (isolated liver perfusion)는 간으로 약물을 표적 전달하기 위한 한가지 방법이다. 이 방법은 간으로의 혈액의 순환을 전체 순환계로부터 분리시켜 별도로 혈액을 관류시키는 동안에 이루어지는 외과적 시술을 포함한다. 분리시킨 후, 약물을 간으로 관류하는 혈액에 주입함으로써, 화학치료제(들)를 전신 투여시 보다 더 고 농도로 사용할 수 있다. 하지만 이러한 침습적인 시술은 기술적으로 복잡하며, 안전하지 않다.
전술한 항암제와 같은 다수의 약학적 활성 물질들은, 하나 이상의 아미노 기를 포함하고 있어, 약 염기이다. 이로 인해, 이들 물질은 강 산 및 약 산과 염을 형성하며, 통상적으로 염 형태로 투여된다. 약제학적으로 허용가능한 통상적인 염, 특히 하이드로클로라이드, 하이드로브로마이드, 포스페이트, 설페이트, 락테이트, 타르트레이트 등은 수성 체액에 대한 용해도가 유리 염기의 용해도 보다 통상적으로 높다. 그래서, 이들 염의 수용액은 대응 염기의 수용액을 대신하여 정맥내 주입 용도로 사용된다.
이런 유형의 인간 또는 동물의 항암제를 간에 투여하기 위해서는 양이온성 양친매성 형태 (약제학적으로 허용가능한 산과의 염 형태)로 제공된다. 이런 투여 방식은, 비제한적인 예로, 예를 들어 안트라사이클린 (독소루비신, 에피루비신 (epirubicin), 다우노루비신 (daunorubicin), 이다루비신 (idarubicin), 미토산트론 (mitoxantrone)), 빈카 알카로이드 (빈블라스틴 (vinblastine), 빈크리스틴 (vincristine), 비노렐빈 (vinorelbine)), 암사크린 (amsacrine), 토포테칸 (topotecan) 및 이리노테칸 (Irinotecan) 등의 항암제에 해당된다. 약학적 활성 물질이 아미노 기를 하나 보다 많이 포함한다면, 이의 아미노 기 2개 이상이 양성자화되어, 산과 염을 형성할 수도 있다.
전술한 유형의 양이온성 양친매성 약물 (CAD)들은 양친매성 음이온성 계면활성제, 예를 들어 알킬 설페이트 또는 알칸 설포네이트와 반응하여, 수불용성 착체를 형성한다.
수불용성 착체가 유기산 또는 무기산과의 유기 염기의 염에 대한 정의를 여전히 만족시키면서, 수불용성 착체는 비-공유결합력에 의해 부가적으로 어느 정도 연결된다.
본 발명의 제1 과제는, 공지된 약물 조성물의 한가지 이상의 문제점이 해소되거나 또는 적어도 완화된, 하나 이상의 아미노 관능기를 포함하는 항암제를 간에 표적 투여하기 위한 약학적 조성물을 제공하는 것이다.
본 발명의 다른 과제는, 공지된 약물 조성물의 한가지 이상의 문제점이 해소되거나 또는 적어도 완화된, 하나 이상의 아미노 관능기를 포함하는 항암제를 고형 간 종양에 표적 투여하기 위한 약학적 조성물을 제공하는 것이다.
본 발명의 또 다른 과제는, 정맥내 투여 후, 간 또는 고형 간 종양에서 약물의 바람직한 타겟 농도를 제공하는 상기한 유형의 약학적 조성물을 설계하는 방법을 제공하는 것이다.
본 발명의 부가적인 과제들은 후술하는 본 발명에 대한 간단한 설명, 바람직한 구현예 및 첨부된 청구항에 대한 학습을 통해 명확해질 것이다.
본 발명은, 양친매성 화합물, 특히 아미노 관능기(들)를 포함하는 친수성 항암제의 직쇄 알킬 설포네이트 및 직쇄 알칸 설페이트 입자들의 수성 현탁물이, 간 또는 고형 간 종양에 대한 치료학적 효과를 집중시키는, 즉, 간 또는 고형 종양을 표적으로 하는 방식으로 이들 약물을 투여할 수 있는 유용한 형태라는 인식을 토대로 한다. 따라서, 표적화는 다른 조직에 비해 간암 조직 등의 간 조직내에서 높은 약물 농도 (w/w)를 달성하기 위해 간으로 우선적으로 전달하는 것으로 이해된다. 친수성 항암제의 직쇄 알킬 설포네이트 및 직쇄 알칸 설페이트의 주 특징은 25℃에서 물 및 수성 체액에 대한 용해도가 0.1 mg/mL 미만으로 낮다는 것이다.
그러나, 결코 결합은 아닌 본 발명의 토대가 되는 생물 기전에 대한 가능성있는 해명은, 상기한 유형의 항암제의 미립자 수성 현탁물을 전신 순환계 또는 간 또는 고형 간 종양에 투여하면, 약물 입자가 소정의 기간 이내에 체내 평형 분포에 도달할 것이라는 것이다. 약물이 수성 매질에서의 용해도는 매우 낮지만, 전혀 용해되지 않는 것은 아니다. 따라서, 이의 용해도에 의해 결정되는 평형에 도달할 때까지 체액에 느리게 용해될 것이다. 용해된 물질이 비가역적으로 분해 산물로 화학적으로 변환되기 때문에, 평형을 유지하기 위해 더 많은 물질들이 시간 경과에 따라 용해되게 된다. 평형이 물질 용해에 의해 뒷받침되는 한, 약물의 정상 상태 농도는 국소적으로 유지된다.
또한, 본 발명은, 아미노 관능기(들)를 포함하는 친수성 항암제의 양친매성 직쇄 알킬 설포네이트와 아미노 관능기(들)를 포함하는 친수성 항암제의 양친매성 직쇄 알칸 설페이트의 수계 콜로이드 (aqueous colloid)가, 이들 약물을 바람직한 장기, 특히 간 또는 바람직한 고형 종양으로 그 치료학적 효과를 집중시키는 방식으로, 즉, 장기 또는 고형 종양을 표적화하는 방식으로 투여할 수 있는, 특히 유용한 형태라는, 인식을 토대로 한다. 수계 콜로이드는 약 10000 nm 이하 크기의 입자들로 구성되거나 또는 이들 입자들을 포함한다.
본 발명에 따른 수계 콜로이드의 중요한 특성은 이의 낮은 침강 속도이다. 일반적으로, 소정의 입자 타입의 침강 속도는 입자 크기에 따라 증가한다. 그러나, 수상의 점성을 높이거나 및/또는 입자의 표면 특성, 예를 들어 표면 거칠기 (surface roughness)에 변화를 줌으로써 증가를 방지할 수 있으며, 심지어 낮출 수도 있다.
본 발명은, 하나 이상의 아미노 기를 포함하는 친수성 항암제와, 수용성 알킬 설페이트 또는 알칸 설포네이트 또는 상기한 설페이트 또는 설포네이트로 된 2 이상의 혼합물로 된, 염의 고체 입자를 제공한다. 상기 염의 주요 특징은 수 용해성이 낮다는 것이다. 다시 말해, 본 발명의 염은 실질적으로 불용성이다. "실질적으로 불용성"이라는 것은 물 또는 수성 체액에서의 용해도가 0.1 중량% 미만, 특히 0.05 또는 0.02 중량% 미만인 것으로 이해된다.
본 발명은, 친수성 항암제와, 수용성 알킬 설페이트 또는 알칸 설포네이트 또는 상기한 설페이트 또는 설포네이트로 된 2 이상의 혼합물로 된, 수불용성 염의 고체 입자의 제조 방법을 제공한다.
또한, 본 발명은, 본 발명의 하나 이상의 양친매성 설포네이트 및/또는 설페이트; 및 액체 캐리어를 포함하는 약학적 조성물을 제공한다. 약학적 조성물은 동맥내, 복막내, 근육내, 경피 또는 정맥내 투여와 같은 임의의 적절한 경로를 통해 투여될 수 있다. 본 발명에 따른 양친매성 설포네이트 및 설페이트의 수계 콜로이드를 포함하는 볼루스 (bolus) 투여가 바람직하다.
또한, 본 발명은, 친수성 항암제; 및 수용성 알킬 설페이트 또는 알칼 설포네이트 또는 상기한 설페이트 또는 설포네이트 2 이상의 혼합물로 된, 수불용성 염을 고체 입자 형태로 포함하는 약학적 조성물의 제조 방법을 제공한다.
본 발명의 조성물은 완충제와, 삼투질 농도 조절제 (osmolality controlling agent) 및 점성 조절제와 같은 약제학적으로 허용가능한 부형제를 더 포함할 수 있다. 사용되는 제조 방법으로 인해, 조성물은 수용성 알킬 설페이트 또는 알칸 설포네이트의 양이온과 항암제의 음이온으로 구성되는 염 또는 대응되는 이온을 부가적으로 포함한다. 알칼리 알킬 설페이트 및 알칼리 알칸 설포네이트, 특히 소듐 및 포타슘 알킬 설페이트 및 알칸 설포네이트를 사용하는 것이 바람직하다.
본 발명의 양친매성 미립자 설포네이트 및 설페이트는 아미노 기 1-4개를 포함하하며 그 중 하나 이상의 양성자화된 항암 활성을 가진 약리학적 물질 D와, 하나 이상의 설페이트 또는 설포네이트 음이온으로 구성된다. 이는 식 (1) 및 (2)로 표시된다:
Dn +(R1SO3)- n
(1)
Dn +(R2OSO3)- n
(2)
상기 식에서, R1은 C6-C30의 직쇄 알킬이고; R2는 C6-C30의 직쇄 알킬이고; n은 1 - 4의 정수이다.
바람직하게는, R1과 R2는 C10-C20의 직쇄 알킬이며, 더 바람직하게는 C12-C18의 직쇄 알킬, 보다 더 바람직하게는 약 C16의 직쇄 알킬이다. 따라서, R1은 C12, C13, C14, C15, C16, C17, C18의 직쇄 알킬 중 어느 것일 수 있으며; R2는 C12, C13, C14, C15, C16, C17, C18의 직쇄 알킬 중 어느 것일 수 있다.
콜로이드 입자들 중 90%는 입자 크기가 바람직하게는 10000 nm 이하이고, 더 바람직하게는 5000 nm 이하이다.
본 발명의 바람직한 측면에서, 최대 10 ㎛ 또는 50 ㎛, 심지어 최대 100 ㎛ 크기의 입자 및 이의 현탁물 등과 같이, 콜로이드 입자 보다 크기가 더 큰 입자 및 이의 수성 현탁물도 본 발명을 구성한다.
본 발명의 입자는, 예를 들어, 원심분리 또는 저온침전 (cryoprecipitation)에 의해 수상으로부터 분리시킬 수 있다. 원심분리에 의해 분리하는 경우, 수용성 알킬 설페이트 또는 알칸 설포네이트의 양이온과 항암제의 음이온으로 구성되는 수반된 염 또는 해당 이온들이 수상과 함께 제거된다. 수득되는 분말 (필요에 따라서는 부가적으로 건조시킴)은 적어도 50%까지, 더 바람직하게는 적어도 80%까지는 콜로이드성 입자 크기를 유지한다. 수성 매질에서의 재-현탁을 촉진하기 위해, 이 분말은 글루코스, 락토스 또는 알부민과 같은 재현탁 촉진제 (re-suspension facilitating agent)를 포함할 수 있다. 다른 구현예로, 본 발명의 입자는 저온침전 등의 수성 매질의 증발에 의해 제조될 수 있으며; 이 경우, 수용성 알킬 설페이트 또는 알칸 설포네이트의 양이온과 항암제의 음이온을 포함하는 수반되는 염이 섞일 것이며; 필요에 따라서는 이를 재현탁 촉진제와 혼합시킬 수 있다.
본 발명의 또 다른 측면에서, 본 발명의 콜로이드성 입자는 치료할 종양의 표면 항원에 대해 적절한 항체 구조를 가지는 것 등의 친화성을 가진 마이크로 캐리어 입자에 의해 구성될 수 있다.
본 발명의 양친매성 설포네이트 및 설페이트에서 바람직한 약학적 활성 물질 D로는 독소루비신, 에피루비신 (epirubicin), 다우노루비신 (daunorubicin), 이다루비신 (idarubicin), 미토산트론 (mitoxantrone), 빈블라스틴 (vinblastine), 빈크리스틴 (vincristine), 비노렐빈 (vinorelbine), 암사크린 (amsacrine), 토포테칸 (topotecan), 이리노테칸 (irinotecan) 등이 있으나, 이들로 한정되는 것은 아니다.
본 발명의 또 다른 바람직한 측면에서, 전술한 약제 이외에 본 발명의 양친매성 설포네이트 및 설페이트의 제조에 적합한 항암제는, 독소루비신, 에피루비신, 다우노루비신, 이다루비신, 이톡산트론, 빈블라스틴, 빈크리스틴, 비노렐빈, 암사크린, 토포테칸, 이리노테칸과 유사한 친수성을 가진 것이다.
또한, 본 발명은 본 발명의 약학적 조성물 또는 본 발명의 양친매성 미립자 설포네이트 또는 설페이트 분말을 포함하는 약학적 조성물을 치료학적인 유효량으로 개체에게 투여하는 단계를 포함하는 개체의 간암 치료 방법을 개시한다. 바람직한 투여 방법은 정맥 또는 동맥, 특히 간문맥 또는 간 동맥으로의 주입 또는 주사에 의한 것이다. 또 다른 바람직한 투여 방법은 말초 순환계로의 주입 또는 주사를 통해 고형 간 종양에 투여하는 것이다. 바람직한 세번째 투여 방법은 고형 간 종양에 직접 주입 또는 주사하는 것이다. 본 발명의 바람직한 측면에서, 투여는 볼루스 (bolus) 또는 다중 볼루스 (several boli)에 의한 것이 바람직하다. 간 또는 간 종양에의 투여에 대한 일 측면은 정맥 또는 동맥, 특히 간문맥 또는 간 동맥으로의 주입 또는 주사에 의한 것이다.
본 발명은 1시간 이상 또는 6시간 이상 또는 심지어 1일 이상과 같이 장기간에 걸쳐 약물을 원하는 농도로 제공할 수 있는, 편리하고 비-침습적인 정맥내 투여용 약물 전달 시스템을 제공한다. 상기한 농도는 간 또는 고형 간 종양 또는 기타 조직에 제공 및 유지된다. 본 발명의 바람직한 측면에서, 본 발명은 간과 다른 장기 및 조직 간의 약물 배분 비율을 조절하는 방법을 제공한다.
본 명세서에서, 달리 언급되지 않은 한, 용어 "간 질환" (liver disease, hepatic disease)은 원발성 간암 (예, 간세포암 및/또는 담관암, 혈관육종 간의 혈관육종), 이차성 악성 (즉, 위장관과, 신장, 폐, 유방 또는 전립선과 같은 다른 장기의 원발성 암으로부터 전이된 이차성 병변); 바이러스에 의해 유발된 간 염증 (바이러스성 간염), 간 독소 (예, 알코올성 간염), 자가면역 (자가면역성 간염) 또는 유전 질환; 알코올 과다 섭취로 인해 유발되는 간경변을 포함한다.
본 발명은, 또한, 미리 정해진 기간 동안 간 및 고형 간 종양으로부터 선택되는 인간 또는 동물의 치료 표적에, 식 (1) 또는 식 (2)로 표시되는, 아미노 기 1-4개를 포함하는 약학적 활성 물질 D의 설페이트 또는 설포네이트, 또는 이들의 혼합물을 미리 정해진 농도로 제공하도록 약학적 조성물을 설계하는 방법을 개시하며:
Dn+(R1SO3)- n
(1)
Dn+(R2OSO3)- n
(2)
상기 식에서, R1은 C6-C30의 직쇄 알킬이고; R2는 C6-C30의 직쇄 알킬이고; n은 1 - 4의 정수이며;
이 방법은,
i)
용매 수용액에서, Dn+(R1SO3)- n 및/또는 Dn+(R2OSO3)- n의 다양한 탄소 쇄 길이 X, Y에 따른 용해도를 측정하는 단계;
ii)
약학적 활성 물질의 설페이트 또는 설포네이트의 용해도와, 개체 또는 동물에 약학적 활성 물질 D의 투여시 치료 표적에서 약학적 활성 물질 D의 예상되는 농도 간의 상관관계를 결정하는 단계;
iii)
치료 표적에서 약학적 활성 물질 D의 필요한 농도에 기초하여, 약학적 활성 물질의 설페이트 또는 설포네이트의 용매에서의 표적 용해도를 구하는 단계;
iv)
표적 용해도에 부합되는 상기 탄소 쇄 길이(들) X, Y를 결정하는 단계;
v)
결정된 탄소 쇄 길이(들) X, Y를 포함하는 약학적 활성 물질의 설페이트 또는 설포네이트를 제공하는 단계;
vi)
유체 캐리어를 제공하는 단계;
vii)
결정된 탄소 쇄 길이(들) X, Y를 포함하는 약학적 활성 물질의 설페이트 또는 설포네이트를, 유체 캐리어와, 표적에서 미리 정해진 기간 동안 미리 정해진 농도를 유지할 수 있는 양으로 조합하는 단계를 포함한다.
본 발명의 바람직한 측면에서, 용해도는, 5 % 내지 50 %, 바람직하게는 10 % 내지 30 % (v/v) 농도의, 알코올 수용액, 특히 에탄올 수용액과 같은 유기 용매 수용액에서 측정한다. 그외 수 혼화성 용매, 예를 들어 저분자량의 케톤, 아미드, 에스테르, 아미드 및 설폭사이드도 사용될 수 있다.
본 발명의 바람직한 측면에서, 약학적 조성물은 식 (1) 또는 식 (2)로 표시되는 본 발명의 여러가지 설페이트 또는 설포네이트 중 2 이상으로 된 혼합물 또는 하나는 식 (1)로 표시되고 다른 하나는 식 (2)로 표시되는 서로 다른 2 이상의 설페이트 또는 설포네이트로 된 혼합물을 포함한다.
바람직한 약학적 활성 물질 D는 독소루비신, 에피루비신, 다우노루비신, 이다루비신, 미토산트론, 빈블라스틴, 빈크리스틴, 비노렐빈, 암사크린, 토포테칸, 이리노테칸으로 이루어진 군으로부터 선택된다. 조성물은 또한 콜로이드를 포함하는 것이 바람직하다.
바람직한 유체 캐리어는, 약학적 활성 물질 D의 설페이트 또는 설포네이트가 불용성이거나 또는 실질적으로 불용성인, 물 또는 수성 매질이다. "실질적으로 불용성"이라는 것은 용해도가 0.1 중량% 미만, 특히 0.05 또는 0.02 중량% 미만인 것으로 이해된다. 본 조성물은 동맥내, 복막내, 근육내, 경피 또는 정맥내 투여용으로 설계될 수 있다. 상기 단계들은 임의의 적절한 순서로 수행될 수 있다.
약학적 활성 물질 D의 설페이트 또는 설포네이트의 바람직한 형태는, 평균 입자 크기 (N)가 100 ㎛ 이하, 바람직하게는 50 ㎛ 이하, 또는 10 ㎛ 이하, 또는 5 ㎛ 이하인 분말이다. 본 발명의 약학적 조성물의 바람직한 형태는 수성 현탁물, 특히 수계 콜로이드 (aqueous colloid)이다.
또한, 본 발명은, 양친매성이 아닌 무기산 또는 유기산과의 상기한 항암제의 염의 제1 수용액을 제공하는 단계; 식 (Na 또는 K)+(R1SO3)-로 표시되는 알킬 설포네이트의 소듐 또는 포타슘 염 또는 식 (Na 또는 K)+(R2OSO3)-로 표시되는 알칸 설페이트의 소듐 또는 포타슘 염을 상기 염의 양에 해당되는 함량으로 포함하는 제2 수용액을 제공하는 단계; 상기 제1 수용액과 상기 제2 수용액을 혼합하는 단계를 포함하는, 본 발명의 약학적 조성물을 제조 방법을 개시한다. 소듐 및 포타슘 염 이외의 염도 본 발명에 사용될 수 있지만, 바람직한 것은 아니다. 바람직하게는, R1은 C6-C30의 직쇄 알킬이고; R2는 C6-C30의 직쇄 알킬이고; n은 1 - 4의 정수이다. 바람직하게는, R1과 R2는 C10-C20의 직쇄 알킬이고, 더 바람직하게는 C12-C18의 직쇄 알킬이며, 가장 바람직하게는 약 C16의 직쇄 알킬이다.
본 발명은, 또한, 인간 또는 동물의 간에 표적 전달하기 위한, 독소루비신, 에피루비신, 다우노루비신, 이다루비신, 미토산트론, 빈블라스틴, 빈크리스틴, 비노렐빈, 암사크린, 토포테칸 및 이리노테칸으로 이루어진 군으로부터 선택되는 항암제를 포함하는 본 발명의 조성물의 용도를 개시한다.
또한, 본 발명은, 인간 또는 동물의 간에 표적 전달할 수 있는 약학적 조성물을 포함하는 약제의 제조에 있어서의, 독소루비신, 에피루비신, 다우노루비신, 이다루비신, 미토산트론, 빈블라스틴, 빈크리스틴, 비노렐빈, 암사크린, 토포테칸 및 이리노테칸으로 이루어진 군으로부터 선택되는 항암제를 포함하는 본 발명의 양친매성 미립자 설포네이트 분말의 용도를 개시한다.
이제 본 발명은 비-제한적인 다수의 실시예들을 들어 보다 상세하게 설명될 것이다.
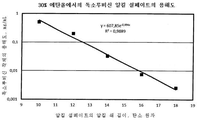
도 1은 30% 에탄올 수용액에서의 독소루비신 알킬 설페이트의 알킬 쇄 길이에 따른 용해도를 나타낸 그래프이다.
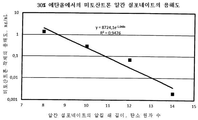
도 2는 30% 에탄올 수용액에서의 독소루비신 알칸 설포네이트의 알킬 쇄 길이에 따른 용해도를 나타낸 그래프이다.
도 3은 30% 에탄올 수용액에서의 미토산트론 알킬 설페이트의 알킬 쇄 길이에 따른 용해도를 나타낸 그래프이다.
도 4는 30% 에탄올 수용액에서의 미토산트론 알칸 설포네이트의 알킬 쇄 길이에 따른 용해도를 나타낸 그래프이다.
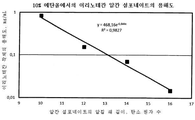
도 5는 10% 에탄올 수용액에서의 이리노테칸 알칸 설포네이트의 알킬 쇄 길이에 따른 용해도를 나타낸 그래프이다.
도 6은 20% 에탄올 수용액에서의 비노렐빈 알칸 설포네이트의 알킬 쇄 길이에 따른 용해도를 나타낸 그래프이다.
도 7은 30% 에탄올 수용액에서의 독소루비신 알칸 설페이트 및 설포네이트의 용해도에 대한, 2시간 볼루스 주사 후 Wistar 랫 간내 독소루비신의 농도 의존성을 나타낸 그래프이다.
도 8은 30% 에탄올 수용액에서의 독소루비신의 비-공유결합성 착체의 용해도와 정맥내 주사한지 0.5시간 후 캘리포니아 토끼의 간에서의 독소루비신 농도 증가 간의 상관관계를 나타낸 그래프이다.
도 9는 독소루비신 하이드로클로라이드 수용액 5 mg/kg 및 실시예 1에 따른 본 발명의 조성물 1.25 mg/kg을 정맥내 주사한 경우의 간 및 심장내 독소루비신 농도를 나타낸 그래프이다.
지수 추세선 (도 1-6)과 로그 추세선 (도 7 및 8) 및 이들의 등식은 마이크로소프트 엑셀 소프트웨어를 사용해 구하였다.
도 2는 30% 에탄올 수용액에서의 독소루비신 알칸 설포네이트의 알킬 쇄 길이에 따른 용해도를 나타낸 그래프이다.
도 3은 30% 에탄올 수용액에서의 미토산트론 알킬 설페이트의 알킬 쇄 길이에 따른 용해도를 나타낸 그래프이다.
도 4는 30% 에탄올 수용액에서의 미토산트론 알칸 설포네이트의 알킬 쇄 길이에 따른 용해도를 나타낸 그래프이다.
도 5는 10% 에탄올 수용액에서의 이리노테칸 알칸 설포네이트의 알킬 쇄 길이에 따른 용해도를 나타낸 그래프이다.
도 6은 20% 에탄올 수용액에서의 비노렐빈 알칸 설포네이트의 알킬 쇄 길이에 따른 용해도를 나타낸 그래프이다.
도 7은 30% 에탄올 수용액에서의 독소루비신 알칸 설페이트 및 설포네이트의 용해도에 대한, 2시간 볼루스 주사 후 Wistar 랫 간내 독소루비신의 농도 의존성을 나타낸 그래프이다.
도 8은 30% 에탄올 수용액에서의 독소루비신의 비-공유결합성 착체의 용해도와 정맥내 주사한지 0.5시간 후 캘리포니아 토끼의 간에서의 독소루비신 농도 증가 간의 상관관계를 나타낸 그래프이다.
도 9는 독소루비신 하이드로클로라이드 수용액 5 mg/kg 및 실시예 1에 따른 본 발명의 조성물 1.25 mg/kg을 정맥내 주사한 경우의 간 및 심장내 독소루비신 농도를 나타낸 그래프이다.
지수 추세선 (도 1-6)과 로그 추세선 (도 7 및 8) 및 이들의 등식은 마이크로소프트 엑셀 소프트웨어를 사용해 구하였다.
일반적인 방법.
재료 및 방법.
에탄올 수용액에서의 용해도는, 갓 제조한 콜로이드를 적당량 3000 rpm에서 30-90분 동안 원심분리하고, 상층액은 버리고, 물 10 mL을 첨가하여 혼합물을 교반한 후, 다시 원심분리, 교반 및 세척을 3회 실시함으로써, 측정하였다. 마지막 원심분리에서 수득된 원심분리물들을 실온에서 72시간 동안 공기 건조한 다음 24시간 동안 진공 건조하였다. 건조된 원심분리물 중 일부 (20 mg)를 에탄올 수용액 6 mL에 넣고 실온에서 24시간 동안 교반하여 재현탁하였다. 혼합물을 3000 rpm에서 10분간 원심분리한 다음, 상층액을 0.2 ㎛ 필터로 여과하여 용해되지 않은 고형 응집물을 제거하였다. 화합물의 용해도는 UV 방법으로 측정하였다.
생체내 실험에 사용되는 조성물은 직후에 제조하거나 또는 농축물을 희석하여 준비하였다. 생체내 실험을 위해, 체중이 300 g ± 30 g인 60 - 75일령의 Wistar 암컷 랫을 선택하였다. 조성물 한 종에 대한 검사시 동물 4마리를 사용하였다. 독소루비신 조성물은 꼬리를 통해 독소루비신을 5 mg/kg 용량으로 1회 볼루스 주사로 투여하였다. 랫은 안락사 직후 액체 질소에서 급속 냉동시켰다.
간 조직에서 독소루비신의 생체-분포 측정. 총 무게 약 1 g의 간 조직 절편 5개 또는 6개를 간의 여러 부위에서 취하였다. 이들 샘플을 HCl이 첨가된 에탄올 수용액으로 20초간 7000 rpm으로, 그리고 10초간 11000 rpm으로 균질화하였다. 균질물을 30분간 볼텍싱하고, 3000 rpm에서 30분간 원심분리하였다. 상층액에, 모노클로로아세트산 용액을 처리하여 1시간 인큐베이션하였다. 혼합물을 15000 rpm에서 15분간 원심분리하였다. 최종 상층액의 독소루비신 농도를 형광측정 분석으로 측정하였다.
실시예 1. 콜로이드형 독소루비신 알킬 설페이트 및 알칸 설포네이트의 제조
에를렌마이어 플라스크에서, 5% 덱스트로스 수용액 중의 독소루비신 하이드로클로라이드 (50 mL, 1 mg/mL) 용액에, 실온에서, 독소루비신 하이드로클로라이드에 사용된 동일한 용매 중의 5-10 % 몰 과잉의 Na+(R1SO3)- 또는 Na+(R2OSO3)- 용액을 첨가하였다. 본 실시예와 그외 실시예들에서, 5% 덱스트로스 수용액 대신에, 링거액 또는 0.9% 생리식염수 또는 포스페이트-완충화된 염수 또는 삼투질농도 (osmolality)가 270 - 300 mOsm/L인 다른 수용액을 사용할 수 있다. 콜로이드 형성 과정은 육안으로 모니터링하였다. 첨가 완료 후, 혼합물을 30분 - 7일 동안 볼텍싱하거나 또는 교반하였다. 그런 다음, 콜로이드를 바로 사용하거나 또는 냉장고에 보관하였다. 이 조성물의 독소루비신 농도는 495 또는 233 nm에서 UV 방법으로 측정하였다. 샘플링을 위해, 콜로이드 일부를 취해 메탄올로 희석하였다 (메탄올이 과량으로 사용됨, >20:1).
실시예 2. 콜로이드형 미토산트론 알킬 설페이트 및 알칸 설포네이트의 제조
에를렌마이어 플라스크에서, 5% 덱스트로스 수용액 중에 왕성하게 교반한 미토산트론 다이하이드로클로라이드 (40 mL, 0.2 mg/mL) 용액에, 실온에서, 미토산트론 다이하이드로클로라이드에 대한 용매와 동일한 용매 중에 Na+(R1SO3)- 또는 Na+(R2OSO3)-를 0.03 mmol로 포함하는 용액을 첨가하였다. 블랙 콜로이드의 형성을 육안으로 모니터링하였다. 콜로이드는 서서히 블랙 침전물과 옅은 상층액으로 분리되었다. 첨가 완료 후, 수득된 혼합물을 좀더 (1 - 7일) 교반하였다. 콜로이드 조성물은 바로 사용하거나 또는 향후 사용을 위해 냉장고에 보관하였다. 이 콜로이드 조성물의 미토산트론 농도는 662, 611 또는 242 nm에서 UV 방법으로 측정하였다. 샘플링을 위해, 콜로이드 일부를 취해 메탄올에 >20:1로 희석하였다.
실시예 3. 콜로이드성 이리노테칸 알킬 설페이트 및 알칸 설포네이트의 제조
탈이온수 중에 이리노테칸 하이드로클로라이드 삼수화물 (5 mL, 4 mg/mL)을 왕성하게 교반한 용액에, 실온에서, 탈이온수 중에 Na+(R1SO3)- 또는 Na+(R2OSO3)-를 포함하는 용액을 첨가하였다. 콜로이드의 형성을 육안으로 모니터링하였다. 첨가 완료 후, 수득된 혼합물을 2일간 교반하고, 혼합물을 3000 rpm에서 10분간 원심분리하였다. 이를 세워두면, 백색 콜로이드가 서서히 백색 침전물과 거의 무색의 상층액으로 분리되었다. 상층액을 5% 덱스트로스 수용액으로 교체하였다. 침전물은 물을 첨가하고 10분간 볼텍싱하여 재현탁하였다. 수득한 조성물은 바로 사용하거나 또는 향후 사용을 위해 냉장고에 보관하였다. 이 콜로이드 또는 변형된 콜로이드에서 이리노테칸의 농도를 360, 255 또는 220 nm에서 UV 방법으로 측정하였다. 샘플링을 위해, 생성물의 일부를 취해 메탄올에 희석하였다 (메탄올이 과량으로 사용됨, >20:1).
실시예 4. 콜로이드성 비노렐빈 알킬 설페이트 및 알칸 설포네이트의 제조
에를렌마이어 플라스크에서, 5% 덱스트로스 수용액 중에 왕성하게 교반한 비노렐빈 타르트레이트 (2 mL, 5 mg/mL) 용액에, 실온에서, 비노렐빈 타르트레이트와 동일한 용매 중에 Na+(R1SO3)- 또는 Na+(R2OSO3)-를 1당량 포함하는 용액을 첨가하였다. 콜로이드의 형성을 육안으로 모니터링하였다. 첨가 완료 후, 수득된 혼합물을 7일간 볼텍싱하거나 또는 교반하였다. 이를 세워두면, 콜로이드가 서서히 침전물과 맑은 상층액으로 분리되었다. 콜로이드는 바로 사용하거나 또는 향후 사용을 위해 냉장고에 보관하였다. 콜로이드에서 비노렐빈의 농도를 268 또는 212 nm에서 UV 방법으로 측정하였다. 샘플링을 위해, 콜로이드에서 일부를 취해 메탄올에 희석하였다 (메탄올이 과량으로 사용됨, >20:1).
실시예 5. 콜로이드성 독소루비신 알킬 설페이트 및 알칸 설포네이트의 30% 에탄올 수용액에서의 용해도
용해도는 재료 및 방법 바로 아래에 기술된 일반적인 방법에 따라 측정하였다. 그 결과를 표 1에 요약 개시하며, 도 1 및 2로 나타낸다.
표 1. 콜로이드성 독소루비신 알킬 설페이트 및 알칸 설포네이트의 30 %(v/v) 에탄올 수용액에서의 용해도
| 음이온의 일반식 | 알킬 쇄 길이, n | 용해도, mg/mL |
| CnH2n+1OSO3 - | 10 | 0.50769 |
| 12 | 0.20560 | |
| 14 | 0.03281 | |
| 16 | 0.00729 | |
| 18 | 0.00260 | |
| CnH2n+1SO3 - | 10 | 1.06429 |
| 12 | 0.23953 | |
| 14 | 0.04596 | |
| 16 | 0.01194 | |
| 18 | 0.00279 |
실시예 6. 콜로이드성 미토산트론 알킬 설페이트 및 알칸 설포네이트의 30% 에탄올 수용액에서의 용해도
용해도는 재료 및 방법 바로 아래에 기술된 일반적인 방법에 따라 측정하였다. 그 결과를 표 2에 요약 개시하며, 도 3 및 4로 나타낸다.
표 2. 콜로이드성 미토산트론 알킬 설페이트 및 알칸 설포네이트의 30 %(v/v) 에탄올 수용액에서의 용해도
| 음이온의 일반식 | 알킬 쇄 길이, n | 용해도, mg/mL |
| CnH2n+1OSO3 - | 8 | 1.34798 |
| 10 | 0.29487 | |
| 12 | 0.06813 | |
| 14 | 0.00203 | |
| CnH2n+1SO3 - | 8 | 0.78058 |
| 10 | 0.17582 | |
| 12 | 0.06484 | |
| 14 | 0.00720 |
실시예 7. 이리노테칸 알칸 설포네이트의 10% 에탄올 수용액에서의 용해도
용해도는 재료 및 방법 바로 아래에 기술된 일반적인 방법에 따라 측정하였다. 그 결과를 표 3 및 도 5에 요약 개시한다.
표 3. 콜로이드성 이리노테칸 알칸 설포네이트의 10 %(v/v) 에탄올 수용액에서의 용해도
| 알킬 쇄 길이, n | 용해도, mg/mL |
| 10 | 0.83483 |
| 12 | 0.15453 |
| 14 | 0.07064 |
| 16 | 0.01476 |
실시예 8. 콜로이드성 비노렐빈 알칸 설포네이트의 20% 에탄올 수용액에서의 용해도
용해도는 재료 및 방법 바로 아래에 기술된 일반적인 방법에 따라 측정하였다. 그 결과를 표 4 및 도 6에 요약 개시한다.
표 4. 콜로이드성 비노렐빈 알칸 설포네이트의 20 %(v/v) 에탄올 수용액에서의 용해도
| 알킬 쇄 길이, n | 용해도, mg/mL |
| 10 | 1.11868 |
| 12 | 0.25692 |
| 14 | 0.06731 |
| 16 | 0.01977 |
실시예 9. Wistar 랫에서의 간내 독소루비신 분포에 대한 생체내 분석
독소루비신 하이드로클로라이드의 수용액, 독소루비신 알칸 설페이트의 수계 콜로이드 및 독소루비신 알칸 설포네이트의 수계 콜로이드를 꼬리를 통한 1회 볼루스 주사로 투여하였다. 꼬리를 통한 1회 볼루스 주사 투여 후 2시간 후 동물을 안락사시켰다; 총 독소루비신 용량 5 mg/kg. 간에서 독소루비신의 농도를 상기 방법에 따라 측정하였다.
그 결과는 표 5 및 도 7에 요약 개시한다.
표 5. Wistar 랫에서의 간내 독소루비신 분포에 대한 생체내 분석
| 독소루비신 염의 음이온 | 독소루비신 농도, ㎍/kg (SDI) | 30% 에탄올에서의 용해도, mg/mL | 간 조직내 독소루비신 농도 증가율, 배수 |
| Cl- | 11.47 ± 2.98 | (1) | (1) |
| (C12H25OSO3)- | 7.15 ± 2.07 | 0.20560 | 0.64 |
| (C14H29OSO3)- | 21.45 ± 4.33 | 0.03281 | 1.87 |
| (C16H33OSO3)- | 31.77 ± 2.82 | 0.00729 | 2.77 |
| (C12H25SO3)- | 9.52 ± 1.03 | 0.23953 | 0.83 |
| (C16H33SO3)- | 29.75 ± 3.51 | 0.01194 | 2.60 |
실시예 10. 캘리포니아 토끼에서의 간내 독소루비신 분포에 대한 생체내 분석
독소루비신 및 독소루비신 하이드로클로라이드의 콜로이드성 비-공유결합 착체를 캘리포니아 토끼의 변연 귀 정맥 (marginal ear vein)에 1 ml/분의 속도로 천천히 투여하였으며, 독소루비신의 총 용량은 5 mg/kg이다. 투여한 지 0.5시간 후에 안락사시켰다. 간내 독소루비신의 농도를 전술한 방법에 따라 측정하였다. 그 결과는 표 6 및 도 8을 참조한다.
표 6. 캘리포니아 토끼의 간내 독소루비신 분포
| 독소루비신 염의 음이온 | 독소루비신의 농도, ㎍/kg (SDI) | 30% 에탄올에서의 용해도, mg/mL | 간 조직내 독소루비신 농도 증가율, 배수 |
| Cl- (독소루비신) | 0.392 ± 0.128 | (1) | (1) |
| C12H25OSO3 | 0.496 ± 0.201 | 0.20560 | 1.27 |
| C14H27OSO3 | 0.776 ± 0.301 | 0.03281 | 1.98 |
| C16H33OSO3 | 1.141 ± 0.203 | 0.00729 | 2.91 |
| C12H25SO3 | 0.423 ± 0.078 | 0.23953 | 1.08 |
| C12H25SO3 | 1.128 ± 0.148 | 0.01194 | 2.88 |
실시예 11. 30% 수성 에탄올에서 원하는 용해도를 가진 독소루비신 설포네이트를 포함하는 콜로이드의 제조
본 실시예는 특정 용매에 대해 원하는 용해도를 가진 본 발명의 콜로이드의 제조 방법을 예시한다. 아래 파라미터들을 설정하였다: 활성 물질: 독소루비신; 음이온: 짝수 개의 탄소 원자를 가진 알칸 설포네이트; 용매: 30% 수성 에탄올; 원하는 용해도: 0.1 mg/mL.
계산은 중간 길이의 쇄를 가진 알칸 설포네이트 라디칼의 탄소 원자의 수를 더하는 것을 전제로 이루어졌다. 또한, 계산은 30% 에탄올 수용액에서의 용해도에 대한 연속 함수를 전제로 하였다.
실시예 5 (비교. 도 2)에서 수득된 함수 (f1)은, 탄소 원자의 수 x와 용해도 y 간의 관계를 나타낸다:
y = f1(x) = 1754.71710 exp(-0.74429 x) (eq. 1)
함수 (f2)는 역산할 수 있으며, 즉 주어진 용해도 Y로부터 탄소 원자의 수 X를 구할 수 있다:
x = f2(y) = -1/0.7442855697 ln(y/1754.71709855) (eq. 2)
용해도 y = 0.1 mg/mL이면, 함수 f2에서 x는 13.20628이다.
라디칼의 탄소 원자의 수를 더하는 전제에 따라, 제시된 C13.20628 라디칼을 제공하기 위한 C12 및 C14 설포네이트의 비율 거동 (원하는 용해도에 가장 가까운 용해도를 가진 설포네이트 쌍):
C13.20628 1 당량은 C12 0.397 당량과 C14 0.603 당량을 더한 것이다.
C12 및 C14를 계산된 비율로 포함하는 독소루비신 설포네이트 혼합물을 실시에 1에 언급된 전형적인 방법에 따라 제조하였다. 그 용해도를 전술한 일반 방법에 따라 측정하였으며, 0.098713 mg/mL로 확인되었다.
실시예 12. 본 발명의 조성물을 캘리포니아 토끼의 간으로 표적 투여하기 위한 정맥내 전달
실시예 1에 따른 본 발명의 독소루비신 조성물 (R = C16 설포네이트)을, 귀 정맥에 체중 당 독소루비신 1.25 mg/kg 농도로 주사하여, 캘리포니아 토끼에 투여하였다. 비교를 위해, 독소루비신 하이드로클로라이드 수용액을 체중 당 독소루비신 5.0 mg/kg의 농도로 동일한 방식으로 투여하였다. 도 9에 나타낸 바와 같이, 본 발명의 조성물은, 선행 기술에 따른 독소루비신 하이드로클로라이드 수용액과 비교해, 독소루비신을 간으로 전달하는데 약 4배 효과적이며, 심장 전달에는 차이가 없다.
Claims (35)
- 약학적 조성물로서,
상기 약학적 조성물은, 친수성 항암제의 양친매성 미립자 설포네이트 또는 양친매성 미립자 설페이트인 고체 입자를 포함하거나 또는 상기 고체 입자로 구성되는 수계 콜로이드 (aqueous colloid) 형태이며,
상기 입자는 물 또는 수성 체액에서 0.1 중량% 미만, 특히 0.05 중량% 미만 또는 0.02 중량% 미만의 용해도를 가지며,
상기 입자의 90% 이상이 10000 nm 이하, 특히 5000 nm 이하의 크기를 가지는, 약학적 조성물. - 제1항에 있어서,
상기 고체 입자가 양친매성 설포네이트 입자인, 약학적 조성물. - 제1항에 있어서,
상기 고체 입자가 양친매성 설페이트 입자인, 약학적 조성물. - 제2항 또는 제3항에 있어서,
완충제; 및/또는 삼투질 농도 조절제 및 점성 조절제와 같은 약제학적으로 허용가능한 부형제를 더 포함하는, 약학적 조성물. - 제2항에 있어서,
양친매성 미립자 설포네이트가, 아미노 기 1-4개를 포함하며 그 중 하나 이상이 양성자화된 (protonated), 약리학적으로 활성인 항암제 D; 및 대응되는 갯수의 설페이트 또는 설포네이트 음이온으로 구성되는, 약학적 조성물. - 제3항에 있어서,
양친매성 미립자 설페이트가, 아미노 기 1-4개를 포함하며 그 중 하나 이상이 양성자화된 약리학적으로 활성인 항암제 D; 및 대응되는 갯수의 설페이트 또는 설포네이트 음이온으로 구성되는, 약학적 조성물. - 제2항에 있어서,
상기 양친매성 미립자 설포네이트가 식 (1): Dn +(R1SO3)- n (1)으로 표시되며,
상기 식에서, R1이 C6-C30의 직쇄 알킬이고; R2가 C6-C30의 직쇄 알킬이고; n이 1 - 4의 정수인, 약학적 조성물. - 제3항에 있어서,
상기 양친매성 미립자 설페이트가 식 (2): Dn +(R2OSO3)- n (2)으로 표시되며,
상기 식에서, R1이 C6-C30의 직쇄 알킬이고; R2가 C6-C30의 직쇄 알킬이고; n이 1 - 4의 정수인, 약학적 조성물. - 제7항 또는 제8항에 있어서,
R1과 R2가 C10-C20의 직쇄 알킬이고, 더 바람직하게는 C12-C18의 직쇄 알킬이고, 가장 바람직하게는 약 C16 알킬인, 약학적 조성물. - 제5항 내지 제9항 중 어느 한항에 있어서,
상기 D가 독소루비신 (doxorubicin), 에피루비신 (epirubicin), 다우노루비신 (daunorubicin), 이다루비신 (idarubicin), 미토산트론 (mitoxantrone), 빈블라스틴 (vinblastine), 빈크리스틴 (vincristine), 비노렐빈 (vinorelbine), 암사크린 (amsacrine), 토포테칸 (topotecan) 및 이리노테칸 (irinotecan)으로 이루어진 군으로부터 선택되는, 약학적 조성물. - 제2항, 제4항, 제5항, 제7항, 제9항 또는 제10항 중 어느 한항에 따른 약학적 조성물의 제조 방법으로서,
양친매성이 아닌 무기산 또는 유기산과의 친수성 항암제의 염의 제1 수용액을 제공하는 단계;
상기 염의 양과 동일한 함량으로, 식 (Na 또는 K)+(R1SO3)-로 표시되는 알킬 설포네이트의 소듐 또는 포타슘 염을 포함하는 제2 수용액을 제공하는 단계;
상기 제1 수용액과 상기 제2 수용액을 혼합하는 단계를 포함하는, 제조 방법. - 제3항, 제4항, 제6항, 제8항 또는 제10항 중 어느 한항에 따른 약학적 조성물의 제조 방법으로서,
양친매성이 아닌 무기산 또는 유기산과의 친수성 항암제의 염의 제1 수용액을 제공하는 단계;
상기 염의 양과 동일한 함량으로, 식 (Na 또는 K)+(R2OSO3)-로 표시되는 알칸 설페이트의 소듐 또는 포타슘 염을 포함하는 제2 수용액을 제공하는 단계;
상기 제1 수용액과 상기 제2 수용액을 혼합하는 단계를 포함하는, 제조 방법. - 제11항에 있어서,
R1이 C6-C30의 직쇄 알킬이고, n이 1 - 4의 정수인, 제조 방법. - 제11항에 있어서,
R2가 C6-C30의 직쇄 알킬이고, n이 1 - 4의 정수인, 제조 방법. - 제13항에 있어서,
R1이 C10-C20의 직쇄 알킬, 더 바람직하게는 C12-C18의 직쇄 알킬, 가장 바람직하게는 약 C16 알킬인, 제조 방법. - 제14항에 있어서,
R1 및 R2가 C10-C20의 직쇄 알킬, 더 바람직하게는 C12-C18의 직쇄 알킬, 가장 바람직하게는 약 C16 알킬인, 제조 방법. - 양친매성 미립자 설포네이트 분말로서,
아미노 기 1-4개를 포함하고 그 중 하나 이상이 양성자화된 약학적 활성 물질 D, 및 상기 양성자화된 아미노 기의 갯수에 대응되는 갯수의 식 (1): Dn+(R1SO3)- n (1)로 표시되는 설페이트 또는 설포네이트 음이온을 포함하거나, 또는 이들로 구성되며,
상기 식에서, R1이 C6-C30의 직쇄 알킬이고, n이 1 - 4의 정수인, 양친매성 미립자 설포네이트 분말. - 제17항에 있어서,
R1이 C10-C20의 직쇄 알킬, 더 바람직하게는 C12-C18의 직쇄 알킬, 가장 바람직하게는 약 C16의 직쇄 알킬인, 양친매성 미립자 설포네이트 분말. - 제18항에 있어서,
입자의 크기가 100 ㎛ 이하, 또는 50 ㎛ 이하, 또는 10 ㎛ 이하인, 양친매성 미립자 설포네이트 분말. - 제17항 내지 제19항 중 어느 한항에 있어서,
재현탁 촉진제 (re-suspension facilitating agent) 및/또는 염화수소산 또는 브롬화수소산의 소듐 또는 포타슘 염을 포함하는, 양친매성 미립자 설포네이트 분말. - 양친매성 미립자 설페이트 분말로서,
아미노 기 1-4개를 포함하고 그 중 하나 이상이 양성자화된 약학적 활성 물질 D, 및 상기 양성자화된 아미노 기의 갯수에 대응되는 갯수의 식 (2): Dn+(R2OSO3)- n (2)로 표시되는 설페이트 또는 설포네이트 음이온을 포함하거나, 또는 이들로 구성되며,
상기 식에서, R2가 C6-C30의 직쇄 알킬이고, n이 1 - 4의 정수인, 양친매성 미립자 설페이트 분말. - 제20항에 있어서,
R1이 C10-C20의 직쇄 알킬, 더 바람직하게는 C12-C18의 직쇄 알킬, 가장 바람직하게는 C16의 직쇄 알킬인, 양친매성 미립자 설페이트 분말. - 제21항에 있어서,
R2가 C10-C20의 직쇄 알킬, 더 바람직하게는 C12-C18의 직쇄 알킬, 가장 바람직하게는 C16의 직쇄 알킬인, 양친매성 미립자 설페이트 분말. - 제21항 내지 제23항 중 어느 한항에 있어서,
입자의 크기가 100 ㎛ 이하, 또는 50 ㎛ 이하, 또는 10 ㎛ 이하인, 양친매성 미립자 설페이트 분말. - 제17항 내지 제24항 중 어느 한항에 있어서,
재현탁 촉진제 (re-suspension facilitating agent) 및/또는 염화수소산 또는 브롬화수소산의 소듐 또는 포타슘 염을 포함하는, 양친매성 미립자 설포네이트 분말 또는 양친매성 미립자 설페이트 분말. - 약학적 조성물의 설계 방법으로서,
상기 방법은, 미리 정해진 기간 동안 치료 표적으로서 인간 또는 동물의 간에, 식 (1) 또는 식 (2)로 표시되는, 아미노 기 1-4개를 포함하는 약학적 활성 물질 D의 설페이트 또는 설포네이트, 또는 이들의 혼합물을 미리 정해진 농도로 제공하도록 약학적 조성물을 설계하는 방법이며:
Dn +(R1SO3)- n (1)
Dn +(R2OSO3)- n (2)
상기 식에서, R1은 C6-C30의 직쇄 알킬이고; R2는 C6-C30의 직쇄 알킬이고; n은 1 - 4의 정수이며;
상기 방법이,
i) 용매 수용액에서, Dn+(R1SO3)- n 및/또는 Dn+(R2OSO3)- n의 다양한 탄소 쇄 길이 X, Y에 따른 용해도를 측정하는 단계;
ii) 상기 약학적 활성 물질의 설페이트 또는 설포네이트의 용해도와, 개체 또는 동물에 상기 약학적 활성 물질 D의 투여시 상기 치료 표적에서 상기 약학적 활성 물질 D의 예상되는 농도 간의 상관관계를 결정하는 단계;
iii) 상기 치료 표적에서 상기 약학적 활성 물질 D의 필요한 농도에 기초하여, 상기 약학적 활성 물질의 설페이트 또는 설포네이트의 상기 용매에서의 표적 용해도를 구하는 단계;
iv) 상기 표적 용해도에 부합되는 상기 탄소 쇄 길이(들) X, Y를 결정하는 단계;
v) 결정된 탄소 쇄 길이(들) X, Y를 포함하는 상기 약학적 활성 물질의 설페이트 또는 설포네이트를 제공하는 단계;
vi) 유체 캐리어를 제공하는 단계;
vii) 상기에서 결정된 탄소 쇄 길이(들) X, Y를 포함하는 상기 약학적 활성 물질의 설페이트 또는 설포네이트를, 상기 유체 캐리어와, 상기 표적에서 상기 미리 정해진 기간 동안 상기 미리 정해진 농도를 유지할 수 있는 양으로 조합하는 단계를 포함하는, 약학적 조성물의 설계 방법. - 제26항에 있어서,
상기 용해도는, 5 % 내지 50 %, 바람직하게는 10 % 내지 30 % (v/v) 농도의, 알코올 수용액, 특히 에탄올 수용액과 같은 유기 용매 수용액에서 측정되는, 약학적 조성물의 설계 방법. - 제26항 또는 제27항에 있어서,
상기 D가 독소루비신, 에피루비신, 다우노루비신, 이다루비신, 미토산트론, 빈블라스틴, 빈크리스틴, 비노렐빈, 암사크린, 토포테칸 및 이리노테칸으로 이루어진 군으로부터 선택되는, 약학적 조성물의 설계 방법. - 암 치료 방법으로서,
제1항, 제2항, 제4항, 제5항, 제7항, 제9항 또는 제10항 중 어느 한항에 따른 약학적 조성물, 제1항, 제3항, 제4항, 제6항 또는 제8항 내지 제10항 중 어느 한항에 따른 약학적 조성물, 또는 제17항 내지 제20항 또는 제25항 중 어느 한항에 따른 양친매성 미립자 설포네이트 분말 또는 제21항 내지 제25항 중 어느 한항에 따른 양친매성 미립자 설페이트 분말을 포함하는 약학적 조성물을, 치료학적인 유효량으로 개체에게 투여하는 단계를 포함하는, 암 치료 방법. - 제29항에 있어서,
상기 투여가 정맥 또는 동맥, 특히 간문맥 (portal vein) 또는 간 동맥으로의 주입 또는 주사인, 암 치료 방법. - 제29항에 있어서,
상기 투여가 말초 순환계로의 주입 또는 주사를 통한 고형 간 종양에의 투여인, 암 치료 방법. - 제29항에 있어서,
상기 투여가 고형 간 종양으로의 직접 주입 또는 주사에 의한 것인, 암 치료 방법. - 제29항 내지 제32항 중 어느 한항에 있어서,
상기 투여가 볼루스 (bolus) 또는 다중 볼루스 (several boli)에 의한 것인, 암 치료 방법. - 독소루비신, 에피루비신, 다우노루비신, 이다루비신, 미토산트론, 빈블라스틴, 빈크리스틴, 비노렐빈, 암사크린, 토포테칸 및 이리노테칸으로 이루어진 군으로부터 선택되는 항암제를, 인간 또는 동물의 간으로 정맥내 표적 전달하기 위한, 제1항 내지 제10항 중 어느 한항에 따른 조성물의 용도.
- 인간 또는 동물의 간으로 정맥내 표적 전달할 수 있는 약학적 조성물을 포함하는 약제의 제조에 있어서의, 독소루비신, 에피루비신, 다우노루비신, 이다루비신, 미토산트론, 빈블라스틴, 빈크리스틴, 비노렐빈, 암사크린, 토포테칸 및 이리노테칸으로 이루어진 군으로부터 선택되는 항암제를 포함하는 제17항 내지 제25항 중 어느 한항에 따른 양친매성 미립자 설포네이트 분말의 용도.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| SE1400427-9 | 2014-09-10 | ||
| SE1400427 | 2014-09-10 | ||
| PCT/SE2015/000055 WO2016039678A1 (en) | 2014-09-10 | 2015-09-09 | Targeted delivery of hydrophilic drugs |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170054459A true KR20170054459A (ko) | 2017-05-17 |
Family
ID=55459328
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177009510A KR20170054459A (ko) | 2014-09-10 | 2015-09-09 | 친수성 약물의 표적 전달 방법 |
Country Status (11)
| Country | Link |
|---|---|
| US (2) | US10034838B2 (ko) |
| EP (1) | EP3191138B1 (ko) |
| JP (1) | JP6951971B2 (ko) |
| KR (1) | KR20170054459A (ko) |
| CN (1) | CN107073129B (ko) |
| AU (1) | AU2015316252A1 (ko) |
| CA (1) | CA2958820A1 (ko) |
| EA (1) | EA033526B1 (ko) |
| IL (1) | IL250637A0 (ko) |
| MX (1) | MX2017003049A (ko) |
| WO (1) | WO2016039678A1 (ko) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3426228A1 (en) * | 2016-03-07 | 2019-01-16 | Double Bond Pharmaceutical AB | Targeted delivery of hydrophilic drugs to lung |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1994008599A1 (en) * | 1992-10-14 | 1994-04-28 | The Regents Of The University Of Colorado | Ion-pairing of drugs for improved efficacy and delivery |
| EP1073419A4 (en) * | 1998-03-18 | 2009-03-25 | Univ Technology Corp | COMPOSITION, CONTAINING AMORPHOUS POLYMER, FOR DELAYED RELEASE. |
| US6613358B2 (en) * | 1998-03-18 | 2003-09-02 | Theodore W. Randolph | Sustained-release composition including amorphous polymer |
| US6384081B2 (en) * | 1998-10-09 | 2002-05-07 | Charles L. Berman | Treatment of diseases of the eye characterized by the formation of metalloproteinase |
| US8313760B2 (en) | 2002-05-24 | 2012-11-20 | Angiotech International Ag | Compositions and methods for coating medical implants |
| ES2330326T3 (es) * | 2002-05-24 | 2009-12-09 | Angiotech International Ag | Composiciones y metodos para recubrir implantes medicos. |
| US20040161466A1 (en) * | 2003-02-14 | 2004-08-19 | Biocompatibles Uk Limited | Chemoembolisation |
| GB2415904B (en) * | 2005-02-07 | 2006-10-25 | Chiron Corp | Preparing aldesleukin for pharmaceutical use |
| WO2009078756A1 (en) * | 2007-12-19 | 2009-06-25 | Ardenia Investments, Ltd. | Drug delivery system for administration of a water soluble, cationic and amphiphilic pharmaceutically active substance |
| CA2714514C (en) * | 2008-02-08 | 2016-08-16 | Qps Llc | Non-polymeric compositions for controlled drug delivery |
| CN101327190B (zh) * | 2008-07-29 | 2011-04-27 | 北京大学 | 一种供注射用的抗肿瘤长循环靶向脂质体 |
| NZ606195A (en) * | 2010-07-26 | 2015-02-27 | Servier Lab | Methods and compositions for liver cancer therapy |
| KR101728011B1 (ko) * | 2013-01-23 | 2017-04-20 | 재단법인 유타 인하 디디에스 및 신의료기술개발 공동연구소 | 덱스트란 메타크릴레이트 및 생체적합성 음이온성 고분자를 포함하는 생분해성 마이크로 비드 및 이의 제조방법 |
-
2015
- 2015-09-09 MX MX2017003049A patent/MX2017003049A/es unknown
- 2015-09-09 US US15/509,875 patent/US10034838B2/en active Active
- 2015-09-09 KR KR1020177009510A patent/KR20170054459A/ko unknown
- 2015-09-09 CN CN201580048892.5A patent/CN107073129B/zh active Active
- 2015-09-09 WO PCT/SE2015/000055 patent/WO2016039678A1/en active Application Filing
- 2015-09-09 EP EP15840525.8A patent/EP3191138B1/en active Active
- 2015-09-09 CA CA2958820A patent/CA2958820A1/en not_active Abandoned
- 2015-09-09 JP JP2017514562A patent/JP6951971B2/ja active Active
- 2015-09-09 EA EA201790272A patent/EA033526B1/ru not_active IP Right Cessation
- 2015-09-09 AU AU2015316252A patent/AU2015316252A1/en not_active Abandoned
-
2017
- 2017-02-16 IL IL250637A patent/IL250637A0/en unknown
-
2018
- 2018-07-17 US US16/037,429 patent/US10973772B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2017527593A (ja) | 2017-09-21 |
| EA033526B1 (ru) | 2019-10-31 |
| WO2016039678A1 (en) | 2016-03-17 |
| EP3191138A4 (en) | 2018-06-20 |
| AU2015316252A1 (en) | 2017-03-09 |
| CA2958820A1 (en) | 2016-03-17 |
| US10973772B2 (en) | 2021-04-13 |
| US20190046462A1 (en) | 2019-02-14 |
| US20170239192A1 (en) | 2017-08-24 |
| IL250637A0 (en) | 2017-04-30 |
| US10034838B2 (en) | 2018-07-31 |
| CN107073129B (zh) | 2021-10-15 |
| JP6951971B2 (ja) | 2021-10-20 |
| CN107073129A (zh) | 2017-08-18 |
| EA201790272A1 (ru) | 2017-07-31 |
| EP3191138C0 (en) | 2024-05-29 |
| EP3191138A1 (en) | 2017-07-19 |
| EP3191138B1 (en) | 2024-05-29 |
| MX2017003049A (es) | 2017-05-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Shen et al. | Versatile hyaluronic acid modified AQ4N-Cu (II)-gossypol infinite coordination polymer nanoparticles: multiple tumor targeting, highly efficient synergistic chemotherapy, and real-time self-monitoring | |
| US10398663B2 (en) | Mitochondrial delivery of 3-bromopyruvate | |
| KR20130114240A (ko) | 화학요법적 항종양 약물을 함유하는 나노입자 | |
| Chen et al. | Cooperative coordination-mediated multi-component self-assembly of “all-in-one” nanospike theranostic nano-platform for MRI-guided synergistic therapy against breast cancer | |
| CN112933046B (zh) | 一种阿霉素前药主动载药脂质体及其制备方法和应用 | |
| CN110665003A (zh) | 一种双载药无载体纳米粒及其制备方法 | |
| Xu et al. | Selective self-induced stimulus amplification prodrug platform for inhibiting multidrug resistance and lung metastasis | |
| Zeng et al. | Highly efficient Chemo/Photothermal therapy alleviating tumor hypoxia against cancer and attenuate liver metastasis in vivo | |
| Zheng et al. | Self-assembled thioether-bridged paclitaxel-dihydroartemisinin prodrug for amplified antitumor efficacy-based cancer ferroptotic-chemotherapy | |
| Fu et al. | Synergistic chemotherapy/PTT/oxygen enrichment by multifunctional liposomal polydopamine nanoparticles for rheumatoid arthritis treatment | |
| US10973772B2 (en) | Targeted delivery of hydrophilic drugs | |
| WO2020151733A1 (en) | Albumin nanoparticles, the making method, and uses thereof | |
| WO2022228230A1 (zh) | 一种双亲性材料及其在制备脂质体中的应用 | |
| CN115317462A (zh) | 一种铜/砷剂矿化蛋白质纳米粒及其制备方法与协同治疗的应用 | |
| Sun et al. | Facile preparation of cabazitaxel-loaded nanoparticles directly lyophilized from dioxane | |
| Yang et al. | Maximizing Arsenic Trioxide's Anticancer Potential: Targeted Nanocarriers for Solid Tumor Therapy | |
| CN115990136B (zh) | 一种抗肿瘤组合物、纳米制剂、制备方法和用途 | |
| Han et al. | Self-assembled nanoparticles covalently consisting of doxorubicin and EDB fibronectin specific peptide for solid tumour treatment | |
| Gaber et al. | In vivo pharmacodynamics of lactoferrin-coupled lipid nanocarriers for lung carcinoma: intravenous versus powder for inhalation | |
| Huang et al. | Hyaluronic Acid Stabilized Doxorubicin Nano-Precipitations for Osteosarcoma Treatment | |
| KR20240111723A (ko) | 헤파린이 결합된 표적 항암 치료용 화합물 및 이의 나노입자 | |
| US20210186879A1 (en) | Targeted delivery of hydrophilic drugs to lung | |
| KR20240105108A (ko) | 표적 항암 치료용 지방산 및 펩타이드 결합형 약물전구체 기반 나노입자 및 이의 제조방법 | |
| Bai et al. | Bone-targeted PAMAM micelle to treat bone metastases of lung cancer | |
| Komorowicz et al. | Can arsenic do anything good? Arsenic nanodrugs in the fight against cancer–last decade review |