KR20150060662A - 활성제가 제어되어 방출되는 드레싱 - Google Patents
활성제가 제어되어 방출되는 드레싱 Download PDFInfo
- Publication number
- KR20150060662A KR20150060662A KR1020157000796A KR20157000796A KR20150060662A KR 20150060662 A KR20150060662 A KR 20150060662A KR 1020157000796 A KR1020157000796 A KR 1020157000796A KR 20157000796 A KR20157000796 A KR 20157000796A KR 20150060662 A KR20150060662 A KR 20150060662A
- Authority
- KR
- South Korea
- Prior art keywords
- dressing
- hours
- weight
- dressings
- polysulfated
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L15/00—Chemical aspects of, or use of materials for, bandages, dressings or absorbent pads
- A61L15/16—Bandages, dressings or absorbent pads for physiological fluids such as urine or blood, e.g. sanitary towels, tampons
- A61L15/42—Use of materials characterised by their function or physical properties
- A61L15/44—Medicaments
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/02—Cosmetics or similar toiletry preparations characterised by special physical form
- A61K8/0204—Specific forms not provided for by any of groups A61K8/0208 - A61K8/14
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/02—Cosmetics or similar toiletry preparations characterised by special physical form
- A61K8/0208—Tissues; Wipes; Patches
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/60—Sugars; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L15/00—Chemical aspects of, or use of materials for, bandages, dressings or absorbent pads
- A61L15/16—Bandages, dressings or absorbent pads for physiological fluids such as urine or blood, e.g. sanitary towels, tampons
- A61L15/20—Bandages, dressings or absorbent pads for physiological fluids such as urine or blood, e.g. sanitary towels, tampons containing organic materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L15/00—Chemical aspects of, or use of materials for, bandages, dressings or absorbent pads
- A61L15/16—Bandages, dressings or absorbent pads for physiological fluids such as urine or blood, e.g. sanitary towels, tampons
- A61L15/22—Bandages, dressings or absorbent pads for physiological fluids such as urine or blood, e.g. sanitary towels, tampons containing macromolecular materials
- A61L15/28—Polysaccharides or their derivatives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L15/00—Chemical aspects of, or use of materials for, bandages, dressings or absorbent pads
- A61L15/16—Bandages, dressings or absorbent pads for physiological fluids such as urine or blood, e.g. sanitary towels, tampons
- A61L15/42—Use of materials characterised by their function or physical properties
- A61L15/425—Porous materials, e.g. foams or sponges
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L15/00—Chemical aspects of, or use of materials for, bandages, dressings or absorbent pads
- A61L15/16—Bandages, dressings or absorbent pads for physiological fluids such as urine or blood, e.g. sanitary towels, tampons
- A61L15/42—Use of materials characterised by their function or physical properties
- A61L15/58—Adhesives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
- A61Q19/06—Preparations for care of the skin for countering cellulitis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/40—Chemical, physico-chemical or functional or structural properties of particular ingredients
- A61K2800/56—Compounds, absorbed onto or entrapped into a solid carrier, e.g. encapsulated perfumes, inclusion compounds, sustained release forms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/20—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices containing or releasing organic materials
- A61L2300/23—Carbohydrates
- A61L2300/232—Monosaccharides, disaccharides, polysaccharides, lipopolysaccharides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/40—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a specific therapeutic activity or mode of action
- A61L2300/412—Tissue-regenerating or healing or proliferative agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/60—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a special physical form
- A61L2300/602—Type of release, e.g. controlled, sustained, slow
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2420/00—Materials or methods for coatings medical devices
- A61L2420/02—Methods for coating medical devices
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Hematology (AREA)
- Materials Engineering (AREA)
- Birds (AREA)
- Dermatology (AREA)
- Biomedical Technology (AREA)
- Dispersion Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicinal Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Materials For Medical Uses (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Cosmetics (AREA)
- Adhesives Or Adhesive Processes (AREA)
Abstract
본 발명은 활성 성분들이 지속적으로 방출되는 폴리설페이트화 올리고당들을 함유하는 신규한 드레싱들에 관한 것이다. 본 발명은 또한 그의 제조를 위한 방법에 관한 것으로, 이 방법은 에틸렌 옥사이드에 의한 처리 단계를 포함한다. 본 발명은 또한 상처 보호 및 흉터들 및 스트레치 마크들의 치료 및/또는 방지를 위한 그의 사용에 관한 것이다.
Description
본 발명은 활성 성분(active ingrdient)들이 지속적으로 방출하는 폴리설페이트화 올리고당(polysulfated oligosaccharide)들을 함유하는 신규한 드레싱들에 관한 것이다. 또한, 본 발명은 그의 제조 방법에 관한 것으로, 이 방법은 에틸렌 옥사이드에 의한 처리 단계를 포함한다. 또한, 본 발명은 상처 보호 및 흉터들 및 스트레치 마크(stretch mark)들의 치료 및/또는 방지를 위한 그의 사용에 관한 것이다.
올리고당들은 오로지 오스(ose)들을 제공하는 가수분해 탄수화물들이다. 이들은 단당(simple sugar)들(또는 오스들)의 적어도 2개의 분자의 결합에 의해 형성되는 당들이다. 올리고당들은 사카로오스(saccharose)라고도 불리는 자당, 2 오스, 즉 글루코오스(glucose)의 하나의 분자 및 과당의 하나의 분자의 응축에 의해 형성된 이당(double sugar)을 포함한다.
다양한 설페이트화 올리고당 화합물들이 문헌에 공지되어 있고, 다수의 생물학적, 코스메틱 및/또는 치료적 활동을 갖는다. 이들 화합물은 특히 수크로오스 옥타설페이트(sucrose octasulfate)의 칼륨염, 수크로오스 옥타설페이트의 나트륨염, 수크로오스 옥타설페이트의 하이드록시알루미늄 복합체(hydroxyaluminium complex) 또는 수크로오스 옥타설페이트의 아미노산염들과 같은 수크로오스 옥타설페이트의 상이한 염들을 포함한다.
이러한 후자의 화합물들은 특히 위의 염증 문제뿐만 아니라 치유에 대한 그들의 유익한 작용이 알려져 있다.
상처의 치유는 자연적 생물학적인 현상이고, 인간 및 동물 조직들은 특정한 복구 및 재생 처리들을 통하여 국부적인 병변(lesion)들을 복구할 수 있다.
상처의 자연 치유는 주로 자신의 세포 및 분자 활동을 각각 갖는 3개의 연속하는 단계로 생긴다. 이들은 연속적이다:
염증 단계는, 특히 상이한 세포 및 분자 인자들에 의해 중재되는 섬유소(fibrin)로 구성되는 혈전의 형성 및 "섬유소(fibrinous)" 조직 또는 "옐로우" 조직이라 불리는 임시 매트릭스의 형성과 같은 동작 중에 염증 및 도관(vascular) 현상의 구현에 의해 외상에 연속적으로 시작된다.
새살(granulation) 단계는, 손상된 조직의 신혈관형성(neovascularisation)에 필요한 새로운 내피 세포들 및 섬유아세포들의 상처 부위에서의 발현에 의해 특징지어진다. 활성화되면, 섬유아세포들은 근섬유아세포들로 변형되고 이에 따라 새살 조직의 성숙에 가담한다.
상피화(epithelialisation) 단계는, 세포외 매트릭스(extra-cellular matrix)의 재조직화에 의해 특징지어진다. 예를 들면, 타입-3 콜라겐이 타입-1 콜라겐으로 대체된다. 대부분의 세포들의 증식이 관찰된다. 이들은 처음의 근섬유아세포, 섬유아세포 및 내피 세포 타입에서는 침습성 행동을 보이고, 그 후 그들의 활동에서 실질적인 감소를 나타낸다. 이 단계는 장기간에 걸쳐서 상처 치유 과정이 정상적인 코스를 수반할 때에 부드러워지고 더이상 아프지 않은 리모델링된 흉터로 이어진다. 그러나, 이 단계에서 병리적인 흉터들이 종단의 치유 단계들의 빈약한 실현에 의해 생길 수 있다.
치유 과정 또는 흉터들에 관한 수개의 일반적인 이슈들이 특히 본 출원인에 의해 이미 연구 주제로 되어 있다.
접하게 되는 제1 문제점들 중 하나는 염증 단계 중에 괴사 및/또는 섬유소 조직의 제거이었다. 실제로, 자연적인 괴사 조직 제거(natural debridement)의 과정이 불충분한 경우, 이에 따라 이 조직이 제거되고, 이는 치유 과정을 해치게 된다. 수많은 해결책들은 기계적, 외과적, 효소적, 자가분해적(autolytic) 또는 생물학적 타입의 보조 괴사 조직 제거 등으로 과거에 제시되어 있다. 그들은 모두 그들의 구성 섬유소 및 괴사 조직의 상처들을 제거하는 목적을 갖는다.
그러나 이러한 상이한 기술들은 수많은 단점들을 갖는다. 이들은 환자에게 매우 고통을 주거나 매우 비효율적임을 입증한다.
이러한 문제점들은 Laboratoires URGO에 의한 출원 FR 2 956 322에 설명된 화합물들의 작용을 통해 해결되었다. 이 문헌은, 상처 괴사 조직 제거제로서, 1 내지 4 오스 유닛들을 갖는 폴리설파이트화 올리고당들, 그들의 염들 또는 복합체들 중에서 선택된 화합물의 사용을 설명하고 있다.
이들 화합물 중에서, 수크로오스 옥타설페이트의 칼륨염은 섬유아세포들에 대한 그의 작용을 통한 발아(budding) 단계 중에 상처들의 치료를 위해 이미 공지되어 있다. 이러한 작용은 예를 들어 특허출원 EP 230 023, WO 89/05645 또는 WO 98/22114에 설명되어 있다. 이러한 화합물은 상처의 보조 괴사 조직 제거를 수행한 후에 그리고 괴사 및/또는 섬유소 조직을 제거한 후에 사용되었다. 따라서, 이는 세정되고 괴사 조직이 제거된 상처에 사용되었다.
폴리설파이트화 올리고당들의 페밀리 내의 일부 화합물의 치유에 대한 유익한 작용이 또한 설명되어 있다. 예를 들면, 출원 FR 2 824 474 및 FR 2 953 522는 치유, 재생에서 그들의 사용을 위해 또는 피부 염증 문제점들을 해결하기 위해 단독으로 또는 전이 금속들의 염들과 연관된 수크랄페이트(sucralfate)를 함유하는 조성물들을 설명하고 있다.
또 다른 문제점인 고려되는 병리적인 흉터들 및 팽창선(striae distensae)(스트레치 마크)을 해결하고자 했다.
병리적인 흉터들은 위축성(atrophic), 신축성(retractile) 또는 비후성(hypertrophic) 흉터들을 의미한다.
스트레치 마크는 피부의 빠르고 갑작스런 스트레칭 다음에 생긴다. 상기 스트레칭은 체중 증가 및/또는 호르몬 변화로부터 초래될 수 있다. 각 스트레치 마크는 피부 눈물(skin tear)처럼 보인다. 이는 실제로 섬유아세포들의 근섬유아세포로의 변형 현상에 의해 피부 조직이 악화된 것이다. 팽창선은 수 센티미터의 길이 및 1 센티미터까지의 폭의 평행하고, 긴 피부 줄무늬를 형성한다. 스트레치 마크들은 얇고 거의 보이지 않을 수 있지만, 피부에 비정규적인 양상를 주는 작은 오목부를 가질 수 있다. 제1 단계에서, 이들은 처음에 연분홍색으로부터 자주색으로 변한다(미숙 또는 염증 스트레치 마크들). 시간 경과에 따라, 이들은 색상을 바꾸고 진주처럼 흰색의 모습을 취하는 경향이 있다(성숙된 스트레치 마크들). 그러면 스트레치 마크는 적게 보여질 수 있지만, 흉터는 남는다. 체중 증가와 연관된 호르몬 변화는 임신 중인 수많은 여성들에게서 스트레치 마크들의 발현으로 이어진다. 유전적 요인들이 또한 그들의 발현에 영향을 미친다. 그들은 또한 일부 생리적 또는 병리적 조건들과 병행해서 나타날 수 있고, 유전병을 나타내는 증상을 형성할 수 있다. 주요 유발 요인들은 염증, 기계적 스트레스 및 호르몬 환경이다. 이러한 모든 요인들은 지원 조직의 파열없이 콜라겐과 엘라스틴 섬유들의 스트레칭, 방향 감각 상실(disorientation) 및 해체(disorganisation)를 야기한다. 스트레치 마크들은 (그들이 피부 외상 후에 수반되는 것과 동일한 형성 단계들을 격게 되기 때문에) 상처에 비유될 수 있다. 그의 치유는 현재 불가능하지만, 병변들의 약화 및 개선은 가능하다. 치료법들은, 레티노산 (retinoic acid) 또는 과일산(fruit acid)들의 유도체들, 필링 또는 레이저 사용에 의한 국소적인 치료와 같이 근본적으로 국소적이다. 그러나, 현재까지 알려진 치료법들은 항상 잘 견디지 못하고 그들의 효능이 완전히 만족스럽지 않기 때문에 완전히 만족스럽지 않다. 수용 가능한 피부 내성을 가지고서, 스트레치 마크들의 효율적인 방지 및/또는 치료를 할 수 있는 제품 개발에 대한 요구가 있다.
드레싱들은 특히 출원 FR 2 956 322로부터 공지되어 있고, 1 내지 4 오스를 갖는 폴리설파이트화 올리고당, 그들의 염들 또는 유도체들로 형성된 그룹으로부터 선택된 화합물을 포함하며, 바람직하게는 환자의 흉터 부위에 활성 성분의 효율적인 생체 이용율(bioavailability)을 보장하기 위해서, 드레싱의 코팅 또는 함침 매스 내에 포함된다.
이러한 드레싱들은 괴사 조직 제거, 치유, 스트레치 마크들 또는 병리적 흉터들의 문제점들을 방지하거나 치료하기 위해서 활성 성분의 지속적인 생체 이용율을 보장한다. 그러나, 수시간의 적용 시간 후에 활성 성분의 방출이 불충분하게 되는 것을 발견하였다. 또한, 드레싱 내에 함유되는 활성 성분의 일부만이 치료될 피부 상에 방출된다. 그리고 수시간의 적용 시간 후에 예상되는 효능에 도달하도록 활성 성분의 충분한 레벨을 피부 상에 유지하고자 하는 경우에는 새로운 드레싱이 도포된다. 초래되는 비용 이외에도, 드레싱의 정기적인 변경은 사용자들/환자들의 활동과 항상 양립될 수 없다. 보다 양호한 치료 효능을 얻기 위해서, 활성 성분의 매우 높은 지속적인 생체 이용율을 갖는 드레싱들을 개발하고자 하였다. 즉, 드레싱들은 상처 부위에서 활성 성분의 효율적인 고 농도를 갖는 것이 개발되어 있고, 이 효능은 제때에 지속된다. 이러한 결과는 드레싱 내에 함유된 활성 성분의 높고 지속적인 방출의 결과이다. 따라서, 이러한 새로운 드레싱들은 보다 신속하고 보다 효율적인 환자 치료를 할 수 있다.
또한, 에틸렌 옥사이드에 의한 처리를 통해 드레싱들의 멸균을 위한 방법이 종래 기술에 공지되어 있다. 그러나, 이러한 타입의 처리는 폴리설페이트화 올리고당들을 함유하는 드레싱들에는 지금까지 적용되지 않고 있다. 또한, 상기 처리가 매우 대조적으로 활성 성분의 방출 시간을 길게 할 수 있고 방출된 활성 성분의 총량을 증가시킬 수 있다는 것이 종래 기술에서는 언급되지도 제안되지도 않았다. 종래 기술에서는, 이론 상으로 모든 멸균 방법(예들 들어 방사선 멸균, 오토클레이브(autoclave) 멸균 또는 에틸렌 옥사이드를 사용한 다른 멸균)은, 멸균 타입이 활성 성분 그 자체를 저하시키기 때문에 또는 활성 성분(들)이 합체되는 마이크로 부착 엘라스토머 매스( micro-adhering elastomeric mass)의 유전적 및/또는 구조적 특성들을 바꾸기 때문에, 이러한 처리의 드레싱 주체에 함유된 활성 성분의 방출에 대하여 불리한 영향을 미치는 것이 개시되어 있다(Radiation effects on polypropylene/polybutylene blends, Richard J. Rolando, June 1993 Tappi Journal, Vol. 76, N°6 and Influence of processing conditions on medical material degradation/failure, Michael T. K. Ling et al., Antec 200 pages 2724 to 2730).
발명의 개요
하나의 바람직한 실시예에 따르면, 본 발명은 적어도 하나의 마이크로 부착 계면을 포함하는 드레싱에 관한 것으로, 상기 마이크로 부착 계면은 1 내지 4 오스들을 포함하는 폴리설페이트화 올리고당들, 그들의 염들 및 복합체들 중에서 선택된 적어도 하나의 화합물을 포함하며, 상기 드레싱은 에틸렌 옥사이드로 처리되어 있다.
하나의 바람직한 실시예에 따르면, 폴리설페이트화 올리고당 화합물은,
- 수크로오스 옥타설페이트의 칼륨염
- 수크로오스 옥타설페이트의 은염(silver salt)
- 수크로오스 옥타설페이트의 하이드록시알루미늄 복합체
중에서 선택된다.
하나의 바람직한 실시예에 따르면, 드레싱은 1 내지 4 오스들을 갖는 폴리설파이트 올리고당들, 그들의 염들 및 복합체들 중에서 선택된 화합물을 0.5 내지 2㎎/㎠, 바람직하게는 0.7 내지 1.9㎎/㎠, 유리하게는 0.9 내지 1.7㎎/㎠ 포함한다.
하나의 바람직한 실시예에 따르면, 마이크로 부착 계면 구성은 접착성 엘라스토머 조성물이다.
하나의 바람직한 실시예에 따르면, 마이크로 부착 계면은,
- 10 내지 60 중량%의 적어도 하나의 점착성 수지(tackyfying resin);
- 2 내지 20 중량%, 바람직하게는 12 내지 16 중량%의 적어도 하나의 하이드로콜로이드 화합물;
- 10 내지 65 중량%의 적어도 하나의 가소성 광유(plasticizing mineral oil);
- 3 내지 25 중량%의 적어도 하나의 엘라스토 폴리머
를 포함한다.
바람직하게는, 접착성 엘라스토머 매스의 층은,
- 0.05 내지 1 중량%의 적어도 하나의 항산화제;
- 10 내지 60 중량%의 적어도 하나의 점착성 수지;
- 2 내지 20 중량%, 바람직하게는 12 내지 16 중량%의 적어도 하나의 하이드로콜로이드 화합물;
- 10 내지 65 중량%의 적어도 하나의 가소성 광유;
- 3 내지 25 중량%의 적어도 하나의 엘라스토머 폴리머;
- 1 내지 15 중량%의 적어도 하나의 안정화제(stabilising agent)
를 포함한다.
하나의 바람직한 실시예에 따르면, 드레싱은, 1 내지 4 오스들을 갖는 폴리설페이트화 올리고당들, 그들의 염들 및 복합체들 중에서 선택된 적어도 하나의 화합물을 마이크로 부착 계면의 총 중량에 대하여 1 내지 15 중량%, 바람직하게는 5 내지 10 중량% 포함한다.
본 발명은 또한 1 내지 4 오스들을 갖는 폴리설페이트화 올리고당들, 그들의 염들 및 복합체들 중에서 선택된 적어도 하나의 화합물에 합체되거나 피착되는 마이크로 부착 계면을 포함하며, 상기 화합물이 지속적으로 방출되는 드레싱에 관한 것으로서, 상기 드레싱은 40㎖의 생리 식염수로 형성된 용해 매질(dissolution medium)에서, 봉지 방법(sachet method)에 따라 측정한 바, 5시간에 4% 이상, 10시간에 5% 이상, 15시간에 5.5% 이상, 20시간에 6% 이상 용해되는 것을 특징으로 한다.
하나의 바람직한 실시예에 따르면, 드레싱은 상기 올리고당이 지속적으로 방출되며, 40㎖의 생리 식염수로 형성된 용해 매질에서, 봉지 방법에 따라 측정한 바, 5시간에 5%, 10시간에 5.5%, 15시간에 6%, 20시간에 7% 용해되는 것을 특징으로 한다.
본 발명의 하나의 바람직한 실시예에 따르면, 상기 마이크로 부착 계면은 0.5와 100cN/㎝ 사이, 바람직하게는 5와 40cN/㎝ 사이로 포함되는 스틸 플레이트(steel plate) 상에서 측정된 부착력을 드레싱에 부여한다.
다른 실시예에 따르면, 본 발명은, 괴사 조직 제거 또는 상처 치유에서의 사용을 위한, 스트레치 마크들의 방지 및 치료에서의 사용을 위한 그리고 흉터들, 특히 병리적 흉터들의 방지 및 치료를 위한 드레싱에 관한 것이다.
최종 실시예에 따르면, 본 발명은 드레싱을 제조하기 위한 방법에 관한 것으로서, 상기 방법은,
(a) 1 내지 4 오스들을 갖는 폴리설페이트화 올리고당들, 그들의 염들 및 복합체들 중에서 선택된 적어도 하나의 화합물을 드레싱의 마이크로 부착 계면 상에 또는 내에 각각 피착 또는 합체하는 단계;
(b) 에틸렌 옥사이드로 상기 드레싱을 처리하는 단계
를 포함한다.
하나의 바람직한 실시예에 따르면, 에틸렌으로 상기 드레싱을 처리하는 단계 (b)는 적어도 다음의 단계들,
(i) 프리컨디셔닝(pre-conditioning) 단계
(ⅱ) 에틸렌 옥사이드로의 노출 단계
(ⅲ) 린싱(rinsing) 단계
를 포함한다.
하나의 바람직한 실시예에 따르면,
- 프리컨디셔닝 단계 (i)에서 드레싱 또는 활성층은 5 내지 15시간 동안 25 내지 60℃ 범위의 온도 및 50 내지 95% 범위의 상대 습도로 처리되고;
단계 (ⅱ)는 30℃ 이상의 온도에서, 그리고 적어도 2시간의 시간 동안 50% 이상의 상대 습도를 갖는 챔버 내에 920mBar 이상의 압력으로 가스 에틸렌 옥사이드에 의한 처리를 포함하고;
단계 (ⅲ)은 팽창에 의해 수반되는 질소 주입의 적어도 2개의 연속 시퀀스를 포함한다.
최종 실시예에 따르면, 본 발명은 스트레치 마크들 또는 흉터들 또는 스트레치 마크들에 기인한 피부 병변들의 방지 및/또는 코스메틱 치료를 위한 방법에 관한 것으로서, 이 방법은 고려되는 피부 영역(들)에 대한 드레싱의 도포를 포함한다. 동일 방법은 흉터들 또는 피부 병변들의 방지 및/또는 코스메틱 치료에 적용될 수 있다.
상세한 설명
본 발명의 다른 특징들 및 이점들은 예로서 주어진 본 발명의 하나의 바람직한 실시예의 다음의 설명을 첨부된 도면들을 참조하여 읽음으로써 보다 용이하게 명백해질 것이다.
가장 놀랍게도 본 출원인은 활성 성분이 높고 지속적으로 방출되는 폴리설페이트화 올리고당들을 함유하는 마이크로 부착 계면을 포함하는 신규한 드레싱들을 개발하였다.
이들 드레싱은 1 내지 4 오스 유닛들을 갖는 폴리설페이트화 올리고당들로부터 선택된 적어도 하나의 화합물을, 피부 또는 상처와 접촉하게 하려는 드레싱 계면 상에 또는 내에 각각 피착 또는 합체하는 것을 포함하는 방법을 이용하여 얻어지고, 이 방법은 에틸렌 옥사이드에 의한 처리를 또한 포함한다.
이들 드레싱은, 1 내지 4 오스들을 갖는 폴리설페이트화 올리고당들 중에서 선택된 적어도 하나의 화합물을 포함하고, 에틸렌 옥사이드로 처리되지 않은 드레싱들과 비교하여 이들의 활성 성분들이 보다 높고 지속적으로 방출된다.
본 발명의 드레싱들은 1 내지 4 오스 유닛들을 갖는 폴리설페이트화 올리고당들, 그들의 염들 및 복합체들 중에서 선택된 적어도 하나의 화합물을 포함하거나 이로부터 제조된다.
본 발명에서 사용될 수 있는 올리고당들은, 일반적으로 알파 또는 베타 글리코시드 본딩( glycosidic bonding)을 통해 함께 링크된, 1 내지 4 단당류 유닛들, 바람직하게는 1 또는 2 단당류 유닛들로 형성된 올리고머(oligomer)들이다. 즉, 이들은 단당류, 이당류, 삼당류 또는 사당류들, 바람직하게는 단당류 또는 이당류들이다. 이들 다당류의 오스 유닛들의 성질에 대해서는 특별히 한정되지 않는다. 바람직하게는 이들이 펜토오스(pentose)들 또는 헥소오스(hexose)들이다.
단당류들의 예들로서, 글루코오스(glucose), 갈락토오스(galactose) 또는 마노오스(mannose)로 이루어지는 것을 들 수 있다. 이당류들의 예들로서, 말토오스(maltose), 락토오스(lactose), 수크로오스(sucrose) 또는 트레할로오스(trehalose)를 들 수 있다. 삼당류의 예로서, 멜레지토오스(melezitose)를 들 수 있다. 사당류의 예로서, 스타키오스(stachyose)를 들 수 있다. 바람직하게는, 올리고당이 이당류이고, 더욱 바람직하게는 수크로오스이다.
"폴리설페이트화 올리고당"은 각 단당류의 적어도 2개 그리고 바람직하게는 모든 하이드록실 그룹이 설페이트 그룹으로 치환되어 있는 올리고당을 의미한다. 바람직하게는, 폴리설페이트화 올리고당은 수크로오스 옥타설페이트이다.
본 발명에서 사용되는 폴리설페이트화 올리고당들은 염들 또는 복합체들의 형태의 것일 수 있다.
일반적으로, 본 출원 명세서에서, 표현 "폴리설페이트화 올리고당들"은 이들 화합물들의 염들 및 복합체들을 포함한다.
염들의 예들로서, 나트륨, 칼슘 또는 칼륨염들 등의 알카리 금속염들; 은염들, 아연염들과 같은 전이 금속염들 및 아미노산염들로 이루지는 것을 들 수 있다.
복합체들의 예로서, 하이드록시알루미늄을 갖는 복합체들로 이루어진 것을 들 수 있다.
본 발명을 구현하기 위한 특히 바람직한 화합물들은 다음과 같다:
- 수크로오스 옥타설페이트의 칼륨염,
- 수크로오스 옥타설페이트의 은염
- 수크랄페이트(수크로오스 알루미늄 설파이트용)로서 공통으로 알려진 수크로오스 옥타설페이트의 하이드록시알루미늄 복합체
바람직하게는, 1 내지 4 오스들을 갖는 폴리설페이트화 올리고당, 그들의 염들 및 복합체들 중에서 선택된 화합물이 미소화된(micronized) 형태의 드레싱 제조에 사용된다.
상술한 화합물들은 단독으로 또는 혼합으로, 또는 하나(또는 그 이상)의 다른 활성 성분(들)과 조합으로 사용될 수 있고, 이러한 활성 성분(들)은 치유를 유도하거나 촉진할 수 있게 하거나, 또는 상처 치료에 바람직한 역할을 할 수 있거나, 또는 병리적이거나 그렇지 않은 스트레치 마크들 또는 흉터들을 치료 및/또는 방지할 수 있다.
이들 활성 성분들 중에서, 예들로서, 특히
- 은염들 또는 복합체들(황산은들, 질산은들, 실버 설파미드들 또는 은함유 제올라이트들 등), 아연 또는 구리염들, 메트로니다졸(metronidazole),네오마이신(neomycin), 페니실린들, 클라불란산(clavulanic acid), 테트라사이클린(tetracycline)들, 미노사이클린(mynocycline), 클로로테트라사이클린(chlorotetracycline), 아미노글리코사이드(aminoglycoside)들, 아미카신(amikacin), 젠타마이신(gentamicin), 프로바이오틱스(probiotics)와 같은 항균제들;
- 클로헥시딘(chlorhexidine), 트리클로산(trichlosan), 비구아나이드(biguanide), 헥사미딘(hexamidine), 티몰(thymol), 루골(lugol), 포비돈 요오드(povidone-iodine), 벤잘코늄(benzalkonium) 및 벤제토늄 클로라이드(benzethonium chloride)와 같은 방부제들;
- 파라세타몰(paracetamol), 코데인(codeine), 덱스트로프로폭시펜(dextropropoxyphene), 트라마돌(tramadol), 모르핀(morphine) 및 그의 유도체들, 코르티코이드(corticoid)들 및 그의 유도체들과 같은 진통제들;
- 리도카인(lidocaine), 벤조카인(benzocaine), 디부카인(dibucaine), 프라목신 하이드로클로라이드(pramoxine hydrochloride), 부피바카인(bupivacaine), 메피바카인(mepivacaine), 프릴로카인(prilocaine), 에티도카인(etidocaine)과 같은 국소 마취제들;
- 비스테로이드성 소염제들(NSAIDs), 아스피린 또는 아세틸살리실산(acetylsalicylic acid), 이부프로펜(ibuprofen), 케토프로펜(ketoprofen), 플루르비프로펜(flurbiprofen), 디클로페낙(diclofenac), 아세클로페낙(aceclofenac), 케토톨락(ketorolac), 멜록시캄(meloxicam), 피록시캄(piroxicam), 테녹시캄(tenoxicam), 나프록센(naproxen), 인도메타신(indomethacin), 나프록시노드(naproxcinod), 니메술리드(nimesulid), 셀레콕시브(celecoxib), 에토리콕시브(etoricoxib), 파레콕시브(parecoxib), 로페콕시브(rofecoxib), 발데콕시브(valdecoxib), 페닐부타존(phenylbutazone), 니플룸산(niflumic acid), 메페남산(mefenamic acid)과 같은 소염제들
을 들 수 있다.
분명히, 본 발명의 드레싱들에서 사용되는 화합물들은 또한 괴사 조직 제거 단계에서 그들의 작용을 위해서 공지된 하나 이상의 다른 화합물, 예를 들면
- 효소들;
- 요소(urea)
와 연관해서 사용될 수 있다.
본 발명의 드레싱들에서 사용되는 폴리설페이트화 올리고당 화합물들은 또한
- 레티노산의 유도체들;
- 과일산들
과 같은, 스트레치 마크들의 치료를 위해서 공지된 하나 이상의 다른 화합물들과 연관해서 사용될 수 있다.
본 발명의 드레싱들에서 사용되는 폴리설페이트화 올리고당 화합물들은 또한
레티놀, 비타민 A, 비타민 E, N-아세틸-히드록시프롤린, 병풀(centella asiatica), 파파인(papain)의 추출물들, 백리향, 니아오우리(niaouli), 로즈마리, 세이지의 에센셜 오일들, 히알루론산(hyaluronic acid), 알란토인(allantoin), 요소, 스트렙토키나아제(streptokinase), 트립신(trypsin) 또는 콜라게나아제(collagenase) 등의 단백질 분해 효소들, 프로테아제 억제제들
과 같은, 그들의 치유 작용을 위해 공지된 하나 이상의 다른 화합물들과 연관해서 사용될 수 있다.
본 발명에서는, 폴리설페이트화 올리고당 화합물들이 마이크로 부착 계면의 구성 성분인 코팅 또는 함침 매스를 통해 드레싱 내에 통합된다.
본 발명에서의 드레싱은 적어도 하나의 마이크로 부착 계면을 포함하는 임의의 의료 디바이스의 드레싱 타입을 의미한다.
특히, 본 발명은 상처들의 치료를 위해 사용되는 드레싱들, 및 흉터들의 치료 사용되는 드레싱들, 코스메틱 패치들에 적용된다.
드레싱의 선택은 치료할 병변의 타입에 의존한다. 예를 들면, 흡수성 드레싱들은, 괴사 조직 제거 단계 중에 종종 높게 삼출되므로 상처들의 치료를 위해 바람직하다.
바람직하게는, 신속한 작용을 돕기 위해서, 이러한 폴리설페이트화 올리고당 화합물(또는 이를 함유하는 코팅 또는 함침 매스)가 피부와 접촉하게 되는 드레싱의 층에 합체되거나, 피부와 접촉하게 되는 드레싱의 표면 상에 피착된다.
이러한 피착 기술들은 당업자에게 잘 알려져 있고, 예를 들면 특허출원 WO 2006/007844에 설명되어 있다.
유리하게는, 폴리설페이트화 올리고당 화합물은, 코팅 또는 함침 매스를 포함하지 않는 경우에 피부와 접촉하게 하려는 층의 표면 상에 피착되고, 이 층에는,
- 예를 들면 폴리설페이트화 올리고당 화합물을 함유하는 용액 또는 현탄액을 기화시킴으로써 액체 형태로,
- 또는 예를 들면 폴리설페이트화 올리고당 화합물을 함유하는 파우더를 체질(sieving) 및/또는 분사함으로써 고체 형태로,
폴리설페이트화 올리고당 화합물이 없는 코팅 또는 함침 매스에 의한 선행의 코팅 또는 함침 단계가 처리될 것이다.
한편, 폴리설페이트화 올리고당 화합물이 코팅 또는 함침 매스 내에 미리 포함되어 있는 구성에서는, 이 매스가 연속적으로(균일한 코팅, 매스 또는 웨프트(weft) 코팅을 통해) 또는 불연속적으로(병렬 코팅 밴드들을 통해) 피부와 접촉하게 하려는 층의 표면 상에 피착된다.
또한, 그의 제조 중에 드레싱의 특정층의 조성물에 직접 폴리설페이트화 올리고당 화합물을 제형화(formulate)하는 것도 가능하다.
드레싱에서 사용되는 폴리설페이트화 올리고당 화합물의 양은 원하는 방출 운동에 관련하여 조정된다. 유리하게는, 0.5 내지 2㎎/㎠, 바람직하게는 0.7 내지 1.9㎎/㎠, 유리하게는 0.9 내지 1.7㎎/㎠의 폴리설페이트화 올리고당 활성 성분을 포함하는 드레싱이 제공된다. 이 값은 드레싱의 활성 표면 영역, 즉 활성 성분을 방출하려고 하는 표면에 관련되고, "경계(border)"라고도 불리는 드레싱의 비활성 부분들은 일반적으로 처리될 영역 부근에서 그의 고정을 허용하는 것이다.
드레싱의 일부로 사용될 때에, 폴리설페이트화 올리고당 화합물은, 이 화합물의 방출량이 24시간 후에 70과 140㎍/㎠ 사이, 바람직하게는 80과 130㎍/㎠ 사이로 포함되도록 하는 양으로 합체된다. 이 값은 드레싱의 활성 표면에 관련된다.
본 발명의 드레싱들은 폴리설페이트화 올리고당이 피착 또는 합체되는 엘라스토머층과 같은 적어도 하나의 마이크로 부착 계면 구성을 포함한다.
본 발명에서 사용될 수 있는 공지된 드레싱들 중에서 다음과 같은 예들을 들 수 있다:
상표명 Opsite®로 Smith & Nephew에 의해, 또는 상표명 Tegaderm®으로 3M에 의해 또는 상표명 Optiskin®으로 Laboratoires URGO에 의해 판매되는 제품 등의 폴리우레탄 필름들. 이들 드레싱들은 접착 표면을 갖는 폴리우레탄의 얇은 투명 필름(20 내지 50㎛ 정도)으로 형성된다. 그들의 투명성은 처리할 영역에 걸쳐서 시각적인 제어를 허용한다. 이들 폴리우레탄 필름들은 반투과성이고; 가스 교환에 대해서는 투과성이고 액체들 및 박테리아에 대해서는 비투과성이다. 이들 폴리우레탄 필름들은 마찰, 러빙 및 전단 현상에 대하여 기계적 보호를 부여한다.
상표명 Mepilex®로 Molnlycke에 의해 또는 상표명 Allevyn®으로 Smith & Nephew에 의해, 또는 상표명 Cellosorb®로 Laboratoires URGO에 의해 판매되는 제품 등의 하이드로셀룰러 드레싱들. 이들 드레싱들은 일반적으로 폴리우레탄 발포체일 수 있는 흡수층의, 폴리우레탄 필름 또는 부직포일 수 있는 백킹(backing)으로 형성된다. 상처와 접촉하게 하려는 이 흡수층의 측면은 마이크로 부착되거나 되지 않을 수 있는 코팅 매스로 코팅될 수 있다. 이들 드레싱들은 하이드로셀룰러 구조 내의 모세관 현상 및/또는 유지력를 통해 높은 흡수 용량을 갖는다.
예를 들어 상표명 Aquacel®로 Convatec에 의해 판매되는 하이드로피브레(hydrofibre) 드레싱들. 이들 드레싱들은 순수 하이드로콜로이드들(카르복시메틸셀룰로오스 나트륨(sodium carboxymethylcellulose))의 부직 섬유들이다. 이들 드레싱들은 친수성이 높고, 삼출물과 접촉할 때에 응집력 있는 겔로 변형된다. 이들 드레싱들은 매우 높은 흡수 용량을 가지며, 또한 박테리아를 "트래핑(trappng)"할 수 있어 박테리아 오염을 제어한다.
상표명 Algisite®로 Smith & Nephew에 의해 또는 상표명 Seasorb® Soft로 Coloplast에 의해 또는 상표명 Urgosorb®로 Laboratoires URGO에 의해 판매되는 제품들과 같은 알긴산염(alginate)들. 이들 드레싱들은 일반적으로 압축 또는 패킹 형태의 것이다. 이들 드레싱들은 천연 다당류들로 형성되고, 삼출물과 접촉할 때에 겔화된다. 이들 드레싱들은 매우 높은 흡수 용량을 가지며, 또한 박테리아를 "트랩(trap)"할 수 있어 박테리아 오염을 제어한다.
예를 들어 상표명 Duoderm®으로 ConvaTec에 의해 또는 상표명 Comfeel®로 Coloplast에 의해 또는 상표명 Algoplaque®로 Laboratoires URGO에 의해 판매되는 것, 또는 일반 대중을 위해서, 상표명 Compeed®로 Johnson & Johnson에 의해 또는 상표명 URGO® Ampoules로 Laboratoires URGO에 의해 판매되는 것 등의 하이드로콜로이드 드레싱들. 이들 제품들은 일반적으로 폴리우레탄 필름인 백킹 및 하이드로콜로이드들을 함유하는 접착성 엘라스토머 매스로 형성된다. 이들 드레싱들은 친수성이며, 하이드로콜로이드들을 함유하는 접착성 엘라스토머 매스가 삼출물과 접촉하여 겔로 된다. 그들은 상처가 아닌 건강한 피부에 부착된다.
이전에 설명한 바와 같은 본 발명의 드레싱들은 폴리설페이트화 올리고당이 피착되거나 합체되는 적어도 하나의 마이크로 부착 계면 구성 예를 들어 엘라스토머층을 포함한다. 이러한 마이크로 부착 계면은 피부와 또는 상처와 접촉하게 하려는 것이다.
건강한 조직 또는 상처의 에지들에 대한 손상 발생을 회피하기 위해서, 특히 드레싱을 제거할 때에, 상처에 부착하지 않고 피부에 부착하는 특성을 갖는 접착제에 대하여 우선순위가 부여된다. 상기 접착제의 예로서, 실리콘 또는 폴리우레탄 겔들과 같은 실리콘 또는 폴리우레탄 엘라스토머들을 함유하는 접착제들 및 하이드로콜로이드 접착제들로 이루어지는 것을 들 수 있다.
바람직하게는, 본 발명의 드레싱들은 폴리설페이트화 올리고당 화합물(들)이 합체되는, 접착성 엘라스토머 매스의 층들 또는 조성물 중에서 선택된 마이크로 부착 계면을 포함한다.
상기 접착성 엘라스토머 조성물들은, 가소성 오일들 예를 들어 광유들 중에서 선택된 하나 이상의 화합물과 연관하거나, 또한 점착성 수지들 또는 카르복시메틸셀룰로오스 나트륨과 같은 바람직하게는 소량의 하이드로콜로이드(3 내지 20 중량%) 및 필요한 경우 항산화제들과 연관해서 폴리(스티렌-올레핀-스티렌) 블럭 폴리머들 중에서 선택된 하나 이상의 엘라스토머를 함유하는 엘라스토머 매트릭스로 형성된다.
상기 접착성 엘라스토머 매스들의 제형화(fomulation)들은 잘 알려져 있고 예를 들어 특허출원 FR 2 916 356에 설명되어 있다.
폴리설페이트화 올리고당 화합물은 바람직하게는 접착성 조성물의 총 중량에 대하여 바람직하게는 1과 15 중량% 사이, 더욱 바람직하게는 5와 10 중량% 사이로 포함된 양으로 사용된다.
유리하게는, 본 발명의 드레싱에서, 접착성 엘라스토머 매스의 층은 특히 다음의 엘리먼트들, 엘라스토머 화합물, 하이드로콜로이드, 적어도 하나의 점착성 수지 및 적어도 하나의 가소성 오일을 포함한다. 또한, 상기 층은 1 내지 4 오스들을 갖는 폴리설페이트화 올리고당들, 그들의 염들 및 복합체들 중에서 선택된 적어도 하나의 화합물을 포함한다.
접착성 엘라스토머 매스는 드레싱의 도포 뿐만 아니라 드레싱의 비외상성 포지셔닝(atraumatic positioning) 및 제거를 용이하게 할 수 있는 지질 콜로이드(lipid-colloid) 매트릭스로 형성된 마이크로 부착 계면층을 제형화하도록 할 수 있다. 이러한 임시 포지셔닝은 또한 간병인 또는 사용자가 다른 부착 수단을 사용하여 드레싱을 부착하는데, 예를 들어 억제 수단 또는 접착성 테이프로 드레싱을 덮는데 도움을 줄 수 있다. 이 경우, 계면층은 드레싱이 스틸 플레이트 방법에 의해 측정한 바 0.5와 100cN/㎝ 사이, 바람직하게는 5와 40cN/㎝ 사이로 포함된 접착력을 갖도록 선택될 수 있다. 이 접착력은 표준 EN 1939에 의해 규정된 바와 같이 측정되며, 여기서 폭 20mm 및 길이 150mm의 드레싱 샘플이 스틸 플레이트 상에 놓이고 10분 후에 동력계를 이용하여 100mm/min의 탈거 속도 및 90°의 각도로 접착력이 측정된다. 엘라스토머 화합물은 선택적으로 디블럭 코폴리머와 연관된, 모든 폴리(스티렌-올레핀-스티렌) 트리블럭 폴리머들을 의미한다. 트리블럭 코폴리머들은 상표명 Kraton G1651®, Kraton G1654® 또는 Kraton G1652®로 판매되는 SEBS로 알려진 폴리(스티렌-에틸렌-부틸렌-스티렌) 블럭 코폴리머들일 수 있다. 디블럭 코폴리머들은 SEPS로도 알려진 폴리(스티렌-에틸렌-프로필렌-스티렌) 블럭 코폴리머들일 수 있다. 엘라스토머 화합물은 또한 폴리(스티렌-이소프렌-스티렌)(폴리(SIS)라 약칭함) 트리블럭 코폴리머들의 패밀리 및 폴리(SIS) 트리블럭 코폴리머들과 폴리(스티렌-이소프렌) 디블럭 코폴리머들의 혼합물들에 속하는 엘라스토머들 중에서 선택될 수도 있다.
하이드로콜로이드들은, 임의의 적절한 하이드로콜로이드 화합물 예를 들어 펙틴(pectin), 알긴산염들, 천연 식물 검들(카라야 검(Karaya gum)), 카르복시메틸셀룰로오스들 및 그들의 알카리 금속염들(리퍼런스 CMC Blanose 7H4XF®로 알려진 카르복시메틸셀룰로오스 나트륨 또는 칼슘염들) 등의 셀룰로오스 유도체들, 및 특히 상표명 Luquasorb 1003®로 BASF®에 의해, 또는 상표명 Salcare SC91®로 CIBA Speciality Chemicals®에 의해 판매되는 제품들 등의 초흡수성 아크릴산의 염들을 함유하는 합성 폴리머들, 및 이들 화합물들의 혼합물들을 의미한다. 이들 하이드로콜로이드는 유리하게는 접착성 조성물을 제조하도록 파티클 형태로 사용된다.
접착성 하이드로콜로이드 매스들의 조성물 내에 포함되는 점착성 수지들은 특히 저분자 중량의 폴리이소부틸렌들 중에서 선택된다. 일반적으로, Escorez® 시리즈 5000 수지들, 및 보다 바람직하게는 수지 Escorez 5380® 등의 수소첨가 수지(hydrogenated resin)들을 사용하는 것이 바람직하다.
본 발명을 구현하는데 사용될 수 있는 가소성 오일들 중에서는, 광유들, 폴리부텐들 또는 프탈산 유도체들을 들 수 있다. 바람직하게는 가소성 광유가 상표명 Ondina 917®, Ondina 919® 또는 Ondina 933®로 Shell®에 의해 판매되는 제품들 중에서 선택된 것이 사용된다. 하나의 특정 실시예에 따르면, Ondina® 오일의 선택량은 Aiglon®에 의해 판매되는 Codex A® Vaseline의 등가량으로 치환될 수 있다.
접착성 하이드로콜로이드 매스의 층은 항산화제, 안정화제 및 가소성 화합물 등의 추가 화합물들을 포함할 수 있다.
"항산화제"는 다른 화학 성분들의 산화를 감소 또는 방지하는 임의의 분자를 의미한다. 항산화제는 예를 들어 상표명 Irganox 1010®, Irganox 565® 및 Irganox 1076®으로 CIBA-GEIGY®에 의해 판매되는 제품들 등의 페놀 항산화제들 및 예를 들어 상표명 PERKACIT ZDBC®로 AKZO®에 의해 판매되는 아연 디부틸디티오카바메이트 등의 황함유 항산화제 중에서 선택될 수 있다. 바람직하게는 사용되는 항산화제는 Irganox 1010®이다.
안정화제는 2-메틸-2-[(1-옥소-2-프로 페닐)아미노]-1-프로판설폰산의 염 및 프로펜산의 2-히드록시에틸 에스테르의 코폴리머로도 알려진, SEPPIC에 의해 판매되는 폴리머 SEPINOV® EMT 10 등의, 조성물 내에 함유될 수 있는 활성 성분들의 겔화 속도, 습윤성, 및 심지어 방출을 최적화할 수 있는 임의의 화합물을 의미한다.
바람직하게는, 폴리설페이트화 올리고당(들) 이외에, 접착성 엘라스토머 매스의 층은,
10 내지 60 중량%의 적어도 하나의 점착성 수지;
2 내지 20 중량%, 바람직하게는 12 내지 16 중량%의 적어도 하나의 하이드로콜로이드 화합물;
10 내지 65 중량%의 적어도 하나의 가소성 광유;
3 내지 25 중량%의 적어도 하나의 엘라스토머 폴리머
를 필수적으로 포함한다.
바람직하게는, 폴리설페이트화 올리고당 화합물이 접착성 엘라스토머 매스의 층 내에 포함되는 경우, 이 매스는,
10 내지 60 중량%의 적어도 하나의 점착성 수지;
2 내지 20 중량%, 바람직하게는 12 내지 16 중량%의 적어도 하나의 하이드로콜로이드 화합물;
10 내지 65 중량%의 적어도 하나의 가소성 광유;
3 내지 25 중량%의 적어도 하나의 엘라스토머 폴리머;
1 내지 15 중량%의 폴리설페이트화 올리고당
을 필수적으로 포함한다.
바람직하게는, 폴리설페이트화 올리고당(들) 이외에, 접착성 엘라스토머 매스의 층은,
0.05 내지 1 중량%의 적어도 하나의 항산화제;
10 내지 60 중량%의 적어도 하나의 점착성 수지;
2 내지 20 중량%, 바람직하게는 12 내지 16 중량%의 적어도 하나의 하이드로콜로이드 화합물;
10 내지 65 중량%의 적어도 하나의 가소성 광유;
3 내지 25 중량%의 적어도 하나의 엘라스토머 폴리머;
1 내지 15 중량%의 적어도 하나의 안정화제
를 필수적으로 포함한다.
바람직하게는, 폴리설페이트화 올리고당 화합물이 접착성 엘라스토머 매스의 층 내에 포함되는 경우, 이 매스는,
0.05 내지 1 중량%의 적어도 하나의 항산화제;
10 내지 60 중량%의 적어도 하나의 점착성 수지;
2 내지 20 중량%, 바람직하게는 12 내지 16 중량%의 적어도 하나의 하이드로콜로이드 화합물;
10 내지 65 중량%의 적어도 하나의 가소성 광유;
3 내지 25 중량%의 적어도 하나의 엘라스토머 폴리머;
1 내지 15 중량%의 적어도 하나의 안정화제;
1 내지 15 중량%의 폴리설페이트화 올리고당
을 필수적으로 포함한다.
본 발명에서는, 때때로 마이크로 부착 매스라고도 불리는 마이크로 부착 계면층이, 선택적으로 백킹층, 흡수층 및 비흡수성 웹으로 형성된 그룹 중에서 선택된 적어도 하나의 화합물과 연관될 수 있다. 바람직하게는, 마이크로 부착 계면층은 단독의 흡수층과, 또는 백킹층, 비흡수성 웹 및 흡수층과, 또는 단독의 백킹층과 또는 백킹층 및 흡수층과 연관된다.
"백킹층"은, 본 발명에서, 가변성의 폴리머 재료들, 예를 들어 폴리아미드, 폴리우레탄, 폴리에스테르, 폴리에테르, 폴리비닐 클로라이드, 폴리비닐리덴 클로라이드, 폴리비닐 알코올, 폴리비닐 아세테이트, 폴리스티렌, 폴리비닐 플루오라이드, 폴리올레핀 예를 들어 폴리에틸렌 또는 폴리프로필렌, 폴리에스테르 폴리에테르 코폴리머, 폴리에스테르 또는 폴리에테르 폴리우레탄 코폴리머, 폴리에테르 폴리아미드 코폴리머를 포함하는 재료로 형성될 수 있는 층을 의미한다.
백킹층은 유연하고, 주로 겨우 신장 가능한 비탄성 재료의 직물로 형성될 수 있다. 이 백킹은 대형의 오픈워크 메쉬(openwork mesh)를 갖는 직물의 형태이고, 오픈워크 메쉬를 보통 사각형 또는 다각형 형상으로 얻을 수 있는 편직 또는 직조 기법을 사용하여 얻어질 수 있다. 직조의 경우에는 메쉬가 양호한 치수 안정성을 얻기 위해 실을 둘러싸서 고착될 수 있다. 메쉬 크기는 개구들의 단위 표면적이 0.2 내지 10㎟, 바람직하게는 0.5 내지 10㎟ 및 더욱 바람직하게는 0.5 내지 3㎟ 정도가 되도록 하고, 직물의 오픈워크 비율이(총 표면적에 대한 개방 표면적의 비율)이 50 내지 90% 정도이다. 직물을 제조하는데 사용되는 얀(yarn)은 바람직하게는 겨우 신장 가능한 비탄성 스트랜드(strand)들을 갖는 연속 스트랜드 얀이며, 신장 또는 파단 강도가 35 % 미만이다. 연속 스트랜드 얀은 하나 이상의 긴 꼬인 스트랜드들로 형성된 얀을 의미하고; 긴 스트랜드들의 선택은 백킹으로부터 탈거될 수 있고, 상처와의 접촉 표면에 가깝게 분산될 수 있는 짧은 섬유의 사용을 피한다. 같은 이유로 얀의 구성 재료는 바람직하게는 인공 또는 합성 성질의 소수성 타입이고; 폴리에스테르들, 폴리아미드들, 셀룰로오스 아세테이트들 등의 이들 구성 성분들은 예를 들어 짧은 섬유들로부터 얻어진 얀보다 많이 적은 피브릴(fibril)들을 갖는 긴 스트랜드들 및 얀들을 얻을 수 있게 한다. 폴리에스테르와 같은 일부 합성 재료들의 선택은 또한 백킹의 오픈워크 메쉬 구조를 열 접합(thermo-bonding)할 가능성을 제공한다. 오픈워크 메쉬 직물은 바람직하게는 동일한 성질의 얀들을 사용하여 생성되지만, 예를 들어 다른 성질의 날실(warp yarn)과 씨실(weft yarn)로 이루어진 직물들을 사용하는 것도 가능하다. 얀의 성질은 예를 들어 폴리에틸테레프탈레이트 타입의 폴리에스테르, 폴리아미드 또는 셀룰로오스 아세테이트일 수 있고; 바람직하게는 오픈워크 메쉬직물은 폴리에스테르의 연속 열접합 얀(테르갈(Tergal) 또는 폴리에틸테레프탈레이트), 예를 들면 약 20 내지 80g/㎡ 및 바람직하게는 30 내지 80g/㎡의 그램 중량을 갖는 상표명 marquisette로 판매되는 직물들로 사용된다. 실질적으로 날실과 씨실 방향으로 비신장성인 이들 직물은 탄성 직물들보다 작업하기가 보다 용이한 이점을 가지며, 얀의 보다 규칙적인 코팅이 얻어진다.
백킹층은 피부 또는 상처와 접촉하게 하려는 측면 상에 접착제로 코팅될 수도 안될 수도 있다.
백킹층은 단일층 또는 피부 또는 상처와 접촉하게 하려는 표면의 반대 표면을 형성하는 제2 층과 같은 이중층필름(bilayer film)과 같은 멀티층일 수 있다. 이 제2 층은 이전에 언급한 바와 같은 동일한 성질의 폴리머 재료 또는 실리콘 페이퍼일 수도 아닐 수도 있는 페이퍼로 형성될 수 있다.
바람직하게는 백킹층은 Zodiac®에 의해 상표명 Novesil®로 판매되는, 폴리디메틸실록산타입의 접착성 실리콘 겔로 코팅된 오픈워크 보강재 및 연속 필름으로 혈성될 수 있다.
이 경우, 백킹층은 필름 또는 필름을 통합하는 임의의 복합체로 형성될 수 있다. 사용될 수 있는 필름들 중에서, 예로서 폴리우레탄, 폴리에테르우레탄, 폴리에테르아미드, 또는 폴리에테르에스테르의 필름들을 들 수 있다.
보강재는 피부에 대한 드레싱을 최상으로 유지하기 위해서 천공된 필름, 열가소성 네트, 직포, 니트, 또는 부직포 바람직하게는 엘라스틱과 같은 임의의 오픈 워크 재료(openwork material)로 형성될 수 있다. 천공된 필름은 예를 들어 폴리에틸렌 또는 폴리프로필렌의 것일 수 있다. 직포는 예를 들어 폴리에틸렌테레프탈레이트 또는 폴리아미드의 것일 수 있다.
본 발명에서의 흡수층은, 드레싱들 또는 기저귀들 등의 위생 제품들 분야에서 흡수층을 생성하는데 사용되는 임의의 재료 또는 재료들의 관계를 의미한다.
이들 재료 중에서, 친수성 흡수성 발포체, 예를 들어 폴리우레탄 발포체들, 텍스타일 재료들 특히 흡수성 섬유들 또는 겔화 섬유들을 함유하는 직포들 및 부직포들, 예를 들어 특히 파티클들 또는 섬유들 형태의 아크릴 폴리머들을 함유하는 초흡수성 재료들, 바람직하게는 하이드로콜로이드 파티클들 및 하이드로겔들을 함유하는 접착성 조성물들을 들 수 있다.
흡수층의 예로서, 발포체들은 각각 리퍼런스 MCF03 및 L 00562-B로 CORPURA 및 RYNEL사에 의해 판매되는 것을 들 수 있다.
부직포의 하나의 카테고리는 셀룰로오스 섬유들을 함유하는 부직포들로 표현된다.
이들 부직포들은 또한 그들의 흡수 용량을 증가시키기 위해서 압축의 총 중량에 대하여 10과 60 중량% 사이로 포함되는 비율로 아크릴 폴리머들(나트륨 폴리아크릴레이트들)을 갖는 SAPs로 공통으로 알려진 초흡수성 폴리머들의 파티클들을 합체할 수도 있다. 마찬가지로, 흡수 중에 부직포들의 통합성을 돕기 위해서, 흡수성 섬유들이 열 접합 섬유들 또는 라텍스 예를 들어 EVA 라텍스와 함께 접합된 섬유들 등의 비흡수성 섬유들과 연관될 수 있다. 이러한 모든 흡수성 부직포는 당업자에게 잘 알려져 있고 용어 "하이브리브 접합(hybrid bonded)", "멀티접합(multibonded)" 또는 "에어레이드(airlaid)"로 표기되어 있다(예를 들면 WO 95/30394 또는 WO 94/10954 참조).
보조적으로, 흡수층으로서는, 앞서 인용한 부직포들의 조합을 사용할 수 있다.
겔화 섬유들을 함유하는 부직포들의 사용은 당업자에게도 잘 알려져 있다. 겔화 섬유들의 예들로서, 히알루론산, 키토산, 펙틴, 알긴산염들, 나트륨 카르복시메틸셀룰로오스, 알긴산염들과 연관된 나트륨 카르복시메틸셀룰로오스, 화학적으로 개질된 특히 카르복시메틸화 셀룰로오스 섬유들, 또는 초흡수성 폴리머들을 함유하는 섬유들을 들 수 있다.
예들로서 섬유들은 Lanseal F 상표명들로 판매되는 것을 들 수 있다.
앞에서와 같이, 이들 겔화 섬유들은 예를 들어 열 접합 섬유들을 갖는 부직포의 특성들을 개선하기 위해서 다른 타입의 섬유들과 연관될 수 있다.
상기 부직포들 및 그들의 가능한 다른 구성 성분 섬유들은 예를 들어 다음의 특허출원들, WO 2007/025546, WO 2007/08531, WO 93/12275, WO 00/01425, WO 94/16746, WO 95/19795, EP 878 204, EP 1 435 247 또는 WO 86/01400에 설명되어 있다.
초흡수성은 본 명세서에서 파우더, 섬유 형태 또는 생물학적 액체들과 접촉하여 겔화되는 임의의 다른 형태의 폴리머들을 의미한다.
초흡수 특성을 갖는 파티클 형태의 친수성 폴리머들은 예를 들어 출원 US 4,102,340에 설명되어 있다. 특히, 가교 폴리아크릴아미드들 등의 흡수성 재료들이 이러한 목적을 위해 사용된다. 바람직한 초흡수성 파티클들은 부분적으로 중화된 가교 폴리아크릴산으로 구성된다. 예들로서, 상표명 LUQUASORB로 BASF에 의해 판매되는 제품들 또는 상표명 SALCARE로 Ciba Speciality Chemicals에 의해 판매되는 제품들을 들 수 있다.
일반적으로, 이러한 초흡수성은 상기에서 설명한 바와 같이 셀룰로오스 섬유들과 연관하여 사용되거나, 조성물들, 바람직하게는 하이드로콜로이드 드레싱들에서 사용되는 접착성 조성물들에 합체된다.
흡수층은 또한 단독으로 또는 2 분배 층 사이에 합체되거나, 예를 들어 셀룰로오스 또는 비스코오스 섬유들 등의 흡수성 섬유 부직포와 합체되는, 이들 초흡수제들로 구성될 수 있다 (EP 358,412 또는 US 6,096,942 참조).
비흡수성 웹은 흡수성 발포체와 백킹을 함께 결합하려고 흡수성 발포체와 백킹 사이에 삽입되는 웹을 의미한다. 이러한 결합은 접착성 실리콘 겔로 코팅된 백킹의 표면이 특히 습한 환경에서 흡수성 발포체에 충분히 부착되지 않기 때문에 필요하다.
흡수성 발포체와 백킹 사이에 삽입되는 웹은 부직포이고, 비흡수성이며 낮은 그램 중량의 것이다. 부직포는 드레싱들 및 위생 분야에서 일상적으로 사용되는 임의의 타입의 부직포, 특히 스펀 레이드(spun laid), 카드형 또는 스펀 레이스(spun lace) 부직포로부터 선택될 수 있다.
이는 폴리아미드, 폴리에스테르, 폴리우레탄 및/또는 폴리올레핀 섬유들로 형성될 수 있다. 일 실시예에 따르면, 웹은 폴리에틸렌 섬유들를 포함한다. 섬유들은 단일 성분 또는 시스(sheath)/피부 또는 사이드-바이-사이드 타입의 2 성분일 수 있다. 예를 들어 스펀 레이드 부직포는 바람직하게는 스펀본드(spunbond) 타입으로 선택된다.
비흡수성 웹은 바람직하게는 소수성 섬유들로 형성되지만, 또한 친수성 섬유들로 형성될 수도 있으며 소수성이 되도록 처리된다. 웹은 충분한 다공성을 갖는 것이 제공된 수개의 층들로 형성될 수 있고, 접착성 실리콘 겔과 접촉하는 층은 비흡수성이고 바람직하게는 소수성이다.
웹은 열, 초음파, 고주파 또는 접착제들 등의 종래의 접합 기술들을 이용하여 그의 전체 표면에 걸쳐서, 또는 바람직하게는 그의 주변만 흡수성 발포체에 부착된다.
본 발명에 따르면, 1 내지 4 오스 유닛들을 갖는 폴리설페이트화 올리고당들, 그들의 염들 및 복합체들 중에서 선택된 적어도 하나의 화합물을 포함하는 드레싱은 에틸렌 옥사이드에 의한 적어도 하나의 처리를 포함하는 방법을 사용하여 제조된다. 이러한 에틸렌 옥사이드 처리는 전체 드레싱에 유리하게 적용된다.
바람직하게는, 이 프로세서는 적어도 3개의 단계들,
(i) 프리컨디셔닝 단계;
(ⅱ) 에틸렌 옥사이드로의 노출 단계
(ⅲ) 린싱 단계
를 포함한다.
프리컨디셔닝 단계 (i)는 드레싱이 25 내지 60℃ 범위의 온도 및 50 내지 95% 범위의 상대 습도로 처리되는 것을 수반한다.
바람직하게는 이 단계 중에 온도가 30 내지 55℃이고, 유리하게는 35 내지 50℃이며, 바람직하게는 40 내지 45℃이다. 바람직하게는, 이 단계에서 상대 습도가 55 내지 90%이고, 보다 바람직하게는 60 내지 80%이며, 더욱 바람직하게는 65 내지 75%이다. 처리 시간은 5와 15시간 사이, 바람직하게는 9와 12시간 사이로 유리하게 포함된다. 그 자체로 알려져 있는 바와 같이 컨디셔닝 단계는 에어컨디션 챔버 예를 들어 오븐 내에서 수행될 수 있다.
그러면 드레싱들은 우선 가스 질소가 주입되고 나서 에틸렌 옥사이드가 주입되거나, 또는 이들 가스들 양쪽이 동시 주입되는 다른 챔버로 이송되어, 920과 960mBar 사이로 포함된 최종 압력을 얻고; 에틸렌 옥사이드의 분압은 300과 550mBar 사이로 포함되고, 이 압력은 가능하면 챔버 내에 주입되는 에틸렌 옥사이드의 질량에 의해 제어된다.
바람직하게는, 단계 (ⅱ)에서의 처리 챔버 내의 상대 습도는 50% 이상이다.
유리하게는, 챔버 내에 주입되는 N2 및 에틸렌 옥사이드(EO)의 상대 %[N2]/[EO](몰)는
0.85≤[N2]/[EO]≤2.15
를 검증한다.
에틸렌 옥사이드의 질량은 간접적으로 즉 질량 또는 체적 유량계를 이용하거나 단순히 칭량해서 제어될 수 있다.
유리하게는, 단계 (ⅱ)는 적어도 2시간, 바람직하게는 적어도 4시간, 유리하게는 적어도 6시간의 시간 동안 30℃ 이상, 바람직하게는 35℃ 이상, 유리하게는 40℃ 이상의 온도 상승을 포함한다. 이러한 온도 상승은 에틸렌 옥사이드 압력하에 드레싱을 유지함과 동시에 적용된다. 최종 단계 (ⅲ)에서 하나 이상의 린싱 동작들이 팽창에 의해 수반되는 챔버 내에 질소를 주입함으로써 수행된다. 바람직하게는, 적어도 2개의 연속 린싱 동작이 수행된다. 바람직하게는 질소의 주입이 920mBar 이상의 압력으로 실시된다.
본 발명의 하나의 바람직한 실시예에 따르면, 드레싱은, 1 내지 4 오스들을 갖는 적어도 하나의 폴리설페이트화 올리고당을 함유하는 적어도 하나의 층을 포함하며, 에틸렌 옥사이드로 처리되고, 상기 올리고당이 지속적으로 방출되는 드레싱이며, 40㎖의 생리 식염수로 형성된 용해 매질에서, 봉지 테스트 방법에 따라 측정한 바, 5시간에서 4% 이상, 10시간에서 5% 이상, 15시간에서 5.5% 이상, 20시간에서 6% 이상 용해되는 것을 특징으로 한다.
유리하게는, 본 발명의 드레싱은, 상기 올리고당이 지속적으로 방출되며, 40㎖의 생리 식염수로 형성된 용해 매질에서, 봉지 테스트 방법에 따라 측정한 바, 5시간에 5% 이상, 10시간에 5.5% 이상, 15시간에 6% 이상, 20시간에 7% 이상 용해되는 것을 특징으로 한다.
유리하게는 상기 마이크로 부착 계면은 0.5와 100cN/㎝ 사이, 바람직하게는 5와 40cN/㎝ 사이로 포함된, 스틸 플레이트 상에서의 접착력을 드레싱에 부여한다. 이러한 접착력은 EN 1939로 명시된 방법을 사용하여 측정된다.
봉지 테스트 방법은 다음의 단계들, 드레싱의 샘플들을 커팅하고 이들을 투과성 봉지 내에 합체하는 단계, 생리 식염수와 접촉하는 봉지들을 리셉터클 내에 배치하는 단계; 결정된 시간 후에 액체를 수집하는 단계; 액체 내의 활성 성분의 양을 측정하는 단계를 포함한다.
본 발명은 또한 상술한 바와 같은 드레싱을 의료 디바이스로서 사용하기 위한 것에 관한 것이다. 일 실시예에 따르면, 본 발명의 드레싱은 상처를 제거하는데 사용된다. 일 실시예에 따르면, 본 발명의 드레싱은 상처 치유를 돕는데 사용된다. 본 발명은 상술한 바와 같은 드레싱의 사용을 포함하는 상처들을 치료하는 방법에 관한 것이다. 이 방법에서, 이러한 드레싱이 상처에 도포된다. 본 발명은 특히 화상 및 급성 또는 만성 상처들의 괴사 조직 제거 및/또는 치유에 관한 것이다. 본 발명은, 특히 화상, 방사선 피부염, 다양한 기원의 염증, 피부염, 벗겨진 상처(graze), 스크래치, 찰과상, 베인 상처, 다리 궤양, 욕창, 당뇨병으로 인한 상처, 흉터 형성 여드름, 물집, 구순염(cheilitis), 습진, 기저귀 발진, 진피 다공 현상(dermatoporosis)의 괴사 조직 제거 및/또는 치유에 관한 것이다.
괴사 조직 제거제로서 본 발명의 드레싱들에서 사용되는 화합물들의 활성은 특히 문헌 FR 2 956 322에서 입증되었다. 치유 및/또는 소염제로서 본 발명의 드레싱들에서 사용되는 화합물들의 활성은 특히 문헌 FR 2 824 474에서 입증되었다.
본 발명의 상처 치료 방법은 자가용해성 괴사 조직 제거에 대해 특히 유리하고, 이러한 기술에서 일상적으로 사용되는 흡수성 드레싱은 섬유소 조직의 저하 및 파편의 흡수를 조합하여 최적의 제품이 얻어질 수 있게 한다.
다른 실시예에 따르면, 본 발명의 드레싱은 스트레치 마크들의 방지 또는 치료에 사용된다. 폴리설페이트화 올리고당 타입의 화합물들은 FR 11 56431호로 출원된 출원서에 설명되어 있는 바와 같이 스트레치 마크들의 방지 및 치료에 상당한 효능을 나타낸다. 본 발명의 드레싱들은 스트레치 마크들 형성 단계 전, 중 또는 후에 사용될 수 있어, 스트레치 마크들에 기인한 피부 상의 흉터들 또는 병변들의 발현을 방지, 지연 및/또는 감소시킨다. 이러한 흉터들 또는 병변들은 병리적 성질은 아니지만 보기 안 좋은 모습을 갖는다. 특히, 본 발명의 드레싱들은 스트레치 마크들을 발달시킬 높은 위험(특히 임신)을 가진 사람들에게 예방적으로 사용될 수 있다. 드레싱들은 또한 흉터들 또는 그로부터 초래된 피부 병변들을 감소, 약화 및/또는 그들의 소멸을 유도하도록 스트레치 마크들의 형성 후에 사용될 수도 있다. 본 발명의 또 다른 주제는 스트레치 마크들, 또는 흉터들 또는 스트레치 마크들에 기인한 피부 병변들의 방지 및/또는 코스메틱 치료를 위한 방법이고, 이 방법은 드레싱이 고려되는 피부 영역(들)에 대한 드레싱의 도포를 포함한다. 본 발명에 따르면, 이러한 도포는 스트레치 마크들 형성 전, 중 또는 후에 이루어질 수 있다.
다른 실시예에 따르면, 본 발명의 드레싱은 흉터들, 특히 여드름 흉터, 수술 다음의 흉터들, 냉동요법 흉터들, 코스메틱 더마톨로지 후에 수반되는 흉터들, 특히 신축성 비후성 흉터들과 같은 병리적인 흉터들을 방지 및 치료하는데 사용된다. 실제로, 폴리설페이트화 올리고당 타입의 화합물들은 FR 11 56 436호로 출원된 출원서에서 설명되어 있는 바와 같이 흉터들의 방지 및 치료에 상당한 효능을 나타낸다. 본 발명의 드레싱들은 피부 상의 흉터들의 출현을 방지, 회피, 지연 및/또는 감소시키도록 흉터들의 형성 단계 전, 중 또는 후에 사용될 수 있다. 본 발명은 특히 병리적인 성질을 갖지 않지만 보기 흉한 모습을 갖는 흉터들 또는 병변들을 고려하고 있다. 특히, 본 발명의 드레싱들은 흉터들(특히 여드름 흉터)을 발달시킬 높은 위험을 가진 사람들에게 예방적으로 사용될 수 있다. 드레싱들은 또한 흉터들 또는 피부 병변들을 감소, 약화 및/또는 그들의 소멸을 초래하도록 스트레치 마크들의 형성 후에 사용될 수도 있다. 본 발명의 또 다른 주제는 흉터들 또는 피부 병변들의 방지 및/또는 코스메틱 치료를 위한 방법이고, 이 방법은 드레싱이 고려되는 피부 영역(들)에 대한 드레싱의 도포를 포함한다. 본 발명에 따르면, 이러한 도포는 흉터들 또는 피부 병변들의 형성 전, 중 또는 후에 이루어질 수 있다.
지속적인 방출을 가능하게 하는 드레싱들 내의 폴리설페이트화 화합물들의 사용은 종래 기술에서 공지된 다른 실시예들과 비교하여 이들 활성 성분들의 효능을 증가시킨다.
마지막으로, 본 발명의 최종 실시예는, 상기 드레싱 내에 함유되는 폴리설페이트화 올리고당들의 방출을 증가시키도록, 상술한 바와 같은 드레싱의 에틸렌 옥사이드에 의한 처리 방법에 관한 것이다.
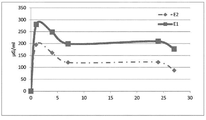
도 1은 예 1 및 예 2에서 설명되는 드레싱들로부터 방출된 활성 성분을 %로 평가한 비축적형(non-accumulated) 용해 프로파일들을 도시하는 그래프.
도 2는 예 1 및 제2에서 설명되는 드레싱들로부터 방출되는 활성 성분을 ㎍/㎖로 평가한 비축적형 용해 프로파일들을 도시하는 그래프.
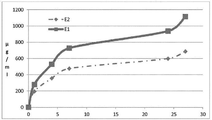
도 3은 예 1 및 예 2에서 설명되는 드레싱들로부터 방출되는 활성 성분을 %로 평가한 축적형 용해 프로파일들을 도시하는 그래프.
도 4는 예 1 및 예 2에서 설명되는 드레싱들로부터 방출되는 활성 성분을 ㎍/㎖로 평가한 축적형 용해 프로파일들을 도시하는 그래프.
모든 도면에서, E1은 예 n°1(본 발명에 따른)에서의 드레싱을 언급하며, E2는 예 n°2(비교예)에서의 드레싱을 언급한다.
도 2는 예 1 및 제2에서 설명되는 드레싱들로부터 방출되는 활성 성분을 ㎍/㎖로 평가한 비축적형 용해 프로파일들을 도시하는 그래프.
도 3은 예 1 및 예 2에서 설명되는 드레싱들로부터 방출되는 활성 성분을 %로 평가한 축적형 용해 프로파일들을 도시하는 그래프.
도 4는 예 1 및 예 2에서 설명되는 드레싱들로부터 방출되는 활성 성분을 ㎍/㎖로 평가한 축적형 용해 프로파일들을 도시하는 그래프.
모든 도면에서, E1은 예 n°1(본 발명에 따른)에서의 드레싱을 언급하며, E2는 예 n°2(비교예)에서의 드레싱을 언급한다.
실험 부분
Ⅰ- 실험 프로토콜들:
프로토콜 A : 하이드로콜로이드 조성물의 층 내의 수크로오스 옥타설페이트의 칼륨염을 포함하는 드레싱의 제조 및 조성물
드레싱은 하이드로콜로이드 마이크로 부착 계면층, 흡수성 발포체, 에어레이드 부직포, 비흡수성 폴리에틸렌 웹 및 접착성 실리콘 겔로 코팅된 백킹을 포함한다.
다음의 재료들이 사용된다:
- 백킹은 30㎛ 두께의 폴리우레탄 필름 상에 적층되는 실리콘 매스(200g/㎡)로 코팅되고 10000g/㎡/24시간보다 높은 수증기 투과율(MVTR)을 갖는 40g/㎡ 폴리에스테르 니트이다. 이 백킹은 300㎛ 정도의 두께 및 5000g/㎡/24시간 정도의 MVTR값을 갖는다.
- 비흡수성 웹은 Freudenberg에 의해 리퍼런스 Vilmed® LSO 1040 WEISS로 판매되는 40g/㎡ 폴리에틸렌 부직포이다.
- 흡수성 발포체는 리퍼런스 MCF 03으로 CORPURA에 의해 판매되는 3mm 친수성 폴리우레탄 발포체이다.
- 흡수성 부직포는 웹과 발포체 사이에 삽입되고; 상표명 Novathin®으로 EMA사에 의해 판매되는 초흡수성 폴리머를 함유하는 에어레이드 부직포(200g/㎡)이다.
- 박리 보호 플루오로-실리콘 코팅 PET는 50마이크론 두께이며 환자의 상처 상에 위치하는 계면의 중앙부 상에 겹치는 2개의 파트 또는 윙(wing)으로 형성되고; SILICONATURE에 의해 공급되어 리퍼런스 SILFLU® M1R88001로 판매되고 있다.
드레싱은 다음의 방법에 따라 제조된다:
- 흡수성 발포체 상에 계면층 및 코팅 제조:
총 중량에 대하여 중량%로 표현되는 다음의 조성물이 제조된다.
- 상표명 Ondina®917로 Shell에 의해 판매되는 광유 : 32.7%
- 상표명 CMC Blanose®7H4XF로 AQUALON에 의해 판매되는 카르복시메틸셀룰로오스 나트륨염 : 14%
- 상표명 KRATON®G 1654로 KRATON에 의해 판매되는 폴리(스티렌-에틸렌-부틸렌) 블럭 코폴리머 : 6%
- 상표명 IRGANOX® 1010으로 CIBA SPECIALTY CHEMICALS에 의해 판매되는 항산화제 : 0.1%
- 상표명 SEPINOV® EMT 10으로 SEPPIC에 의해 판매되는 2-메틸-2-[(1-옥소-2-프로페닐)아미노]-1-프로판설폰산의 염 및 프로펜산(방출제)의 2-히드록시에틸 에스테르의 코폴리머 : 5%
- 상표명 ESCOREZ® 5380으로 EXXON CHEMICALS에 의해 판매되는 점착성 수지 : 35%
- 미소화 형태의 수크로오스 옥타설페이트의 칼륨염 : 7.5%
100과 110℃ 사이로 포함되는 온도로 된 광유, 하이드로콜로이드, 엘라스토머, KSOS 그리고 항산화제와 방출제 및 최종적으로 점착성 수지가 균질의 혼합물을 얻도록 MEL-40 믹서기 내에 놓인다.
상기 혼합물은 친수성 폴리우레탄 발포체 상에서 170g/㎡의 양으로 연속적으로 코팅된다.
- 층 어셈블링:
- 폴리에틸렌 웹의 시트(sheet)가 다음의 조건들 하에서 코로나(Corona) 처리된다:
· 생성기 전력 : 570 와트
· 전극 수/폭 : 3/0.25m
· 에어 갭 설정 : 2mm
· 주행 속도 : 2m/분
- 코로나에 의한 처리 효과가 부분적으로 사라지기 전에, 2mm 폭의 용접이 AMIS 매뉴얼 용접기를 사용하여 웹 및 폴리우레탄 발포체의 일측면 상에서 이루어지고; 그 후에 흡수성 부직포가 발포체와 웹 사이에 삽입된다.
- 최종의 3번의 용접이 8cm×8cm 사각형을 형성하도록 앞에서와 같이 동일한 조건 하에서 수행되고, 그 후에 어셈블링된 복합체들의 에지들이 커팅된다.
- 백킹이 15cm×15cm 사각형으로 커팅되고, 10kg 롤러를 사용하여 2개의 수직 방향으로 롤링함으로써 상기 복합체 상에 어셈블링된다.
- 그 후 최종의 드레싱이 13cm×13cm로 커팅되고, 코너들을 라운딩한다.
프로토콜 B : 에틸렌 옥사이드로 드레싱을 처리하기 위한 방법
프로토콜 A에 따라 생성된 드레싱들은 12시간의 시간 동안, 36과 50℃ 사이, 바람직하게는 43℃에서 발진하는 온도 및 62와 80% 사이, 바람직하게는 70%로 포함되는 상대 습도에서 에어컨디션 챔버 내에 배치된다. 이 프리컨디셔닝 단계는 활성 단계에서의 체류 시간, 즉 드레싱이 차후에 에틸렌 옥사이드로 압력받는 동안의 시간을 최적화할 수 있게 한다. 제2 단계에서 드레싱들은 다른 에어컨디션 챔버로 이송된다. 제2 챔버는 50% 정도의 상대 습도를 얻기 위해서, 수증기의 임의의 사전 주입 전에, 70mbar의 초기 진공 하에 있는다. 그 후, 질소(N2)의 제1 주입이 360mbar의 분압 하에서 이루어진다. 동시에 가스 에틸렌 옥사이드가 920mbar의 분압으로 수행되고, 최종적으로 질소의 제2 주입이 930mbar 값의 분압으로 수행된다. 그 후 에틸렌 옥사이드의 질량이 제어되고 적어도 6시간의 시간 동안 온도가 45℃로 된다. 최종 단계에서, 2개의 연속하는 린싱 동작이 압력을 약 150 내지 170mbar로 팽창시키기 전에, 970mbar의 압력 하에서 질소를 주입하여 수행된다.
프로토콜 C : 봉지 방법을 사용한 활성 성분의 용해 프로파일의 측정
용해 또는 방출 프로파일은 소위 "봉지 방법"을 사용하여 측정된다. 이는 유사한 드레싱 중 3개의 샘플에 대한 분석을 수행하는 것을 수반한다. 이들 샘플은 25㎠의 표면적, 즉 5cm×5cm의 컷아웃(cut-out)을 갖는다. 각 샘플은 얇은 투과성 소수성 부직포로 형성된 봉지 내에 사전에 배치되며, 이러한 어셈블리들은 밀봉 병 안의 평탄면에 도입되고, 부착 계면은 밀봉 병의 바닥과 대면한다. 40㎖의 생리 식염수(H2O+0.9% 염화나트륨)가 각각의 테스트 병에 첨가된다. 그 후 각각의 병이 닫히고 1시간, 4시간, 7시간 및 24시간 동안 32℃(온도 프로브가 서모쉐이크(thermoshake) 내에 사전에 배치됨)에서 120 쉐이크/분으로 접선 교반(tangential agitation) 하에서 유지된다. 모든 상청액(supernatan)이 각각의 이들 4개의 시간 기간 후에 수집된다. 각 시간 기간 후에, 제거된 액체는 10㎖의 생리 식염수로 대체되고, 각각의 병은 다음 설정 시간까지 접선 교반 하에 남는다. 상청액에 함유된 활성 성분의 양이 HPLC 크로마토그래피에 의해(굴절 계측 검출로) 각각의 시간 기간 후에 측정된다.
Ⅱ - 실시의 예들
- 예 n°1 : 본 발명에 따른 드레싱
드레싱이 다음의 프로토콜 A 및 B로 제조되었다.
- 예 n°2 : 종래 기술에 따른 드레싱
드레싱이 다음의 프로토콜 A만으로 제조되었다.
-결과들 :
평가 프로토콜 C가 2개의 타입의 드레싱에 적용되었다. 용해 프로파일이 얻어졌고 예 n°1의 드레싱과 예 n°2의 드레싱 간을 비교할 수 있도록 하나의 동일한 그래프 상에 나타내었다.
예 n°1 및 예 n°2의 드레싱들은 전체적으로 다른 용해 프로파일을 나타냈다.
도 1 및 도 2는 각 드레싱으로부터 활성 성분의 방출을 도시하는 그래프(이전 값들과 비누적으로 측정된 곡선 상의 각 포인트의 값들)이다. 방출값들은 시간의 함수로서 방출된 활성 성분의 %로(도 1), 또는 시간의 함수로서 방출된 활성 성분의 ㎍/㎖로(도 2) 정의된다. 이는 관심있는 선택된 그래프 표현이 무엇이든, 활성 성분의 방출이 비처리된 드레싱들보다도 본 발명의 처리된 드레싱들 주체에서 거의 2배 높다는 것을 매우 명백하게 나타낸다. 이러한 특징의 직접적인 결과는 병변 부위 상에 다시 발견된 활성 성분의 효과적인 농도가 에틸렌 옥사이드로 처리된 드레싱에서 보다 양호하다는 것이다.
따라서, 고려 중인 부위에서 다시 발견된 활성 성분의 보다 높은 효과적인 농도를 통해 치유, 괴사 조직 제거, 병리적 흉터들 또는 스트레치 마크들의 문제점과 같은 병변 부위에서 접하는 상이한 문제점들을 해결하는 것 - 즉 활성 성분의 지속적이고 보다 큰 방출을 통해 달성되는 것 -이 더욱 양호하다.
도 3 및 도 4는 각각 도 1 및 도 2의 데이터를 재생하지만 방출값들은 축적된 값들을 표현한다(곡선의 1 포인트에서 기록된 각각의 값이 이전의 값들에 가산됨). 이러한 축적은 제품의 필수적인 특성, 제때에 상이한 포인트들에서 방출된 총량을 도시한다.
분명하게, 본 발명은 설명되고 도시되어 있는 예들 및 실시예들에 한정되는 것이 아니라, 당업자에게 접근 가능한 다양한 변형들을 포함한다.
Claims (15)
- 적어도 하나의 마이크로 부착 계면(micro-adherent interface)을 포함하는 드레싱으로서,
상기 마이크로 부착 계면은 1 내지 4 오스(ose)들을 포함하는 폴리설페이트화 올리고당(polysulfated oligosaccharide)들, 그들의 염들 및 복합체들 중에서 선택된 적어도 하나의 화합물을 포함하고, 상기 드레싱은 에틸렌 옥사이드로 처리되는 드레싱. - 제1항에 있어서,
상기 폴리설페이트화 올리고당 화합물은,
- 수크로오스 옥타설페이트(sucrose octasulfate)의 칼륨염
- 수크로오스 옥타설페이트의 은염(silver salt) 및
- 수크로오스 옥타설페이트의 하이드록시알루미늄 복합체(hydroxyaluminium complex)
중에서 선택되는 드레싱. - 제1항 또는 제2항에 있어서,
1 내지 4 오스들을 갖는 폴리설페이트화 올리고당들, 그들의 염들 및 복합체들 중에서 선택된 화합물을 0.5 내지 2㎎/㎠, 바람직하게는 0.7 내지 1.9㎎/㎠, 유리하게는 0.9 내지 1.7㎎/㎠를 포함하는 드레싱. - 제1항 내지 제3항 중 어느 한 항에 있어서,
상기 마이크로 부착 계면 구성은 접착성 엘라스토머 조성물인 드레싱. - 제1항 내지 제4항 중 어느 한 항에 있어서,
상기 마이크로 부착 계면은,
- 10 내지 60 중량%의 적어도 하나의 점착성 수지(tackyfying resin);
- 2 내지 20 중량%, 바람직하게는 12 내지 16 중량%의 적어도 하나의 하이드로콜로이드 화합물;
- 10 내지 65 중량%의 적어도 하나의 가소성 광유(plasticizing mineral oil); 및
- 3 내지 25 중량%의 적어도 하나의 엘라스토머 폴리머
를 포함하는 드레싱. - 제1항 내지 제5항 중 어느 한 항에 있어서,
1 내지 4 오스들을 갖는 폴리설페이트화 올리고당들, 그들의 염들 및 복합체들 중에서 선택된 적어도 하나의 화합물을, 마이크로 부착 계면의 총 중량에 대하여 1 내지 15 중량%, 바람직하게는 5 내지 10 중량%을 포함하는 드레싱. - 1 내지 4 오스들을 갖는 폴리설페이트화 올리고당들, 그들의 염들 및 복합체들 중에서 선택된 적어도 하나의 화합물에 합체되거나 피착되는 적어도 하나의 마이크로 부착 계면을 포함하는 드레싱으로서,
40㎖의 생리 식염수로 형성된 용해 매질(dissolution medium)에서, 봉지 방법(sachet method)에 따라 측정한 바, 5시간에 4% 이상, 10시간에 5% 이상, 15시간에 5.5% 이상, 20시간에 6% 이상 용해되는 것을 특징으로 하는 상기 화합물이 지속적으로 방출되는 드레싱. - 제7항에 있어서,
40㎖의 생리 식염수로 형성된 용해 매질에서, 봉지 방법에 따라 측정한 바, 5시간에 5% 이상, 10시간에 5.5% 이상, 15시간에 6% 이상, 20시간에 7% 이상 용해되는 것을 특징으로 하는 상기 폴리설페이트화 올리고당이 지속적으로 방출되는 드레싱. - 제1항 내지 제8항 중 어느 한 항에 있어서,
상기 마이크로 부착 계면은 0.5와 100cN/㎝ 사이, 바람직하게는 5와 40cN/㎝ 사이로 포함되는 스틸 플레이트(steel plate) 상에서 측정된 접착력을 상기 드레싱에 부여하는 드레싱. - 제1항 내지 제9항 중 어느 한 항에 있어서,
스트레치 마크들의 방지 및 치료에서 그리고 흉터들의 방지 및 치료에서, 괴사 조직 제거(debridement) 또는 상처의 치유를 위해 사용하는 드레싱. - 제1항 내지 제9항 중 어느 한 항에 따른 드레싱을 제조하기 위한 방법으로서,
(a) 1 내지 4 오스들을 갖는 폴리설페이트화 올리고당들, 그들의 염들 및 복합체들 중에서 선택된 적어도 하나의 화합물을 드레싱의 마이크로 부착 계면 상에 또는 내에 각각 피착 또는 합체하는 단계; 및
(b) 에틸렌 옥사이드로 상기 드레싱을 처리하는 단계
를 포함하는 드레싱을 제조하기 위한 방법. - 제11항에 있어서,
에틸렌 옥사이드로 상기 드레싱을 처리하는 단계 (b)는 적어도 다음의 단계들,
(i) 프리컨디셔닝(pre-conditioning) 단계
(ⅱ) 에틸렌 옥사이드로의 노출 단계 및
(ⅲ) 린싱(rinsing) 단계
를 포함하는 드레싱을 제조하기 위한 방법. - 제12항에 있어서,
- 상기 프리컨디셔닝 단계 (i)에서 상기 드레싱 또는 활성층은 5 내지 15시간 동안 25 내지 60℃ 범위의 온도 및 50 내지 95% 범위의 상대 습도로 처리되고;
- 단계 (ⅱ)는 적어도 2시간의 시간 동안 30℃ 이상의 온도에서 50% 이상의 상대 습도를 갖는 챔버 내에서 920mBar 이상의 압력으로 가스 에틸렌 옥사이드로 처리하는 것을 포함하며;
- 단계 (ⅲ)은 팽창에 의해 수반되는 질소 주입의 적어도 2개의 연속 시퀀스를 포함하는 드레싱을 제조하기 위한 방법. - 스트레치 마크들, 또는 스트레치 마크들에 기인한 흉터들 또는 피부 병변의 방지 및/또는 코스메틱 치료를 위한 방법으로서,
제1항 내지 제9항 중 어느 한 항에 따른 드레싱을 고려되는 피부 영역(들) 상에 도포하는 것을 포함하는 방법. - 흉터들 또는 피부 병변들의 방지 및/또는 코스메틱 치료를 위한 방법으로서,
제1항 내지 제9항 중 어느 한 항에 따른 드레싱을 고려되는 피부 영역(들) 상에 도포하는 것을 포함하는 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR1256829 | 2012-07-13 | ||
| FR1256829A FR2993182B1 (fr) | 2012-07-13 | 2012-07-13 | Pansement a liberation prolongee d'actifs |
| PCT/EP2013/064718 WO2014009488A2 (fr) | 2012-07-13 | 2013-07-11 | Pansement a liberation prolongee d'actifs |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20150060662A true KR20150060662A (ko) | 2015-06-03 |
Family
ID=46852260
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020157000796A KR20150060662A (ko) | 2012-07-13 | 2013-07-11 | 활성제가 제어되어 방출되는 드레싱 |
Country Status (28)
| Country | Link |
|---|---|
| US (1) | US10172972B2 (ko) |
| EP (1) | EP2872187B1 (ko) |
| JP (1) | JP6212552B2 (ko) |
| KR (1) | KR20150060662A (ko) |
| CN (1) | CN104507506B (ko) |
| AU (1) | AU2013288664B2 (ko) |
| BR (1) | BR112015005673B1 (ko) |
| CA (1) | CA2878869C (ko) |
| CL (1) | CL2015000091A1 (ko) |
| CO (1) | CO7240418A2 (ko) |
| DK (1) | DK2872187T3 (ko) |
| ES (1) | ES2717276T3 (ko) |
| FR (1) | FR2993182B1 (ko) |
| HK (1) | HK1207830A1 (ko) |
| HU (1) | HUE042014T2 (ko) |
| MA (1) | MA37709B1 (ko) |
| MX (1) | MX354272B (ko) |
| MY (1) | MY171069A (ko) |
| PH (1) | PH12015500013A1 (ko) |
| PL (1) | PL2872187T3 (ko) |
| PT (1) | PT2872187T (ko) |
| RU (1) | RU2641031C2 (ko) |
| SG (1) | SG11201408829RA (ko) |
| TN (1) | TN2014000542A1 (ko) |
| TR (1) | TR201903940T4 (ko) |
| UA (1) | UA117658C2 (ko) |
| WO (1) | WO2014009488A2 (ko) |
| ZA (1) | ZA201500137B (ko) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104926889A (zh) * | 2015-05-24 | 2015-09-23 | 广西师范学院 | 蔗糖硫酸酯铜银类化合物及其制作方法和用途 |
| FR3064488B1 (fr) | 2017-03-31 | 2021-01-01 | Urgo Rech Innovation Et Developpement | Composition contenant un derive de cellulose, un plastifiant, un solvant volatil et un actif, ses utilisations comme pansement |
| FR3066390B1 (fr) | 2017-05-17 | 2019-07-12 | Urgo Recherche Innovation Et Developpement | Utilisation de composes oligosaccharidiques pour traiter les plaies des patients diabetiques arteriopatiques |
| FR3068975B1 (fr) * | 2017-07-12 | 2020-07-17 | Urgo Recherche Innovation Et Developpement | Composition pour pansement interface |
| CN109208335B (zh) * | 2018-09-05 | 2021-05-11 | 杭州鸿江纺织印染有限公司 | 一种面料的后整理工艺 |
| FR3113583A1 (fr) | 2020-08-26 | 2022-03-04 | Urgo Recherche Innovation Et Developpement | Utilisation de composes oligosaccharidiques pour augmenter l’oxygenation de la peau lors du traitement des plaies ischemiques |
| CN113730642B (zh) * | 2021-08-20 | 2022-05-31 | 东华大学 | 一种梯度弹性变形的差别化释药复合敷料及其制备方法 |
| CN113952497B (zh) * | 2021-09-28 | 2022-07-29 | 振德医疗用品股份有限公司 | 细菌黏附性抗感染创面敷料 |
Family Cites Families (56)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR1156431A (fr) | 1956-07-18 | 1958-05-16 | Jeu de société dit : les langues vivantes | |
| FR1156436A (fr) | 1956-07-19 | 1958-05-16 | Perfectionnements aux dispositifs de vidange de lavabos et analogues | |
| US4102340A (en) | 1974-12-09 | 1978-07-25 | Johnson & Johnson | Disposable article with particulate hydrophilic polymer in an absorbent bed |
| US4650479A (en) | 1984-09-04 | 1987-03-17 | Minnesota Mining And Manufacturing Company | Sorbent sheet product |
| AU607690B2 (en) | 1985-12-24 | 1991-03-14 | Marion Laboratories, Inc. | Use of synthetic sulfated saccharides to enhance wound healing |
| DK505488D0 (da) | 1987-12-21 | 1988-09-09 | Bar Shalom Daniel | Middel og anvendelse af samme |
| US4901714A (en) | 1988-09-09 | 1990-02-20 | E. R. Squibb & Sons, Inc. | Bandage |
| GB9126193D0 (en) | 1991-12-10 | 1992-02-12 | Courtaulds Plc | Cellulosic fibres |
| SE508961C2 (sv) | 1992-11-17 | 1998-11-23 | Sca Hygiene Prod Ab | Absorberande struktur och absorberande alster innehållande strukturen ifråga |
| JP3220700B2 (ja) * | 1992-12-01 | 2001-10-22 | 日東電工株式会社 | 医療用吸水性ポリマー及びこれを用いた創傷用被覆材並びに医療用外用材更にこれらの製造方法 |
| WO1994016746A1 (en) | 1993-01-22 | 1994-08-04 | Courtaulds Plc | Wound dressings |
| GB9400994D0 (en) | 1994-01-20 | 1994-03-16 | Bristol Myers Squibb Co | Wound dressing |
| SE510466C2 (sv) | 1994-05-04 | 1999-05-25 | Sca Hygiene Prod Ab | Ett förfarande för framställning av en absorberande struktur och ett absorberande sårförband innehållande en absorberande struktur framställd enligt förfarandet |
| US5702669A (en) * | 1995-12-21 | 1997-12-30 | Green; Edward Francis | Apparatus method for sterilization using ethylene oxide |
| WO1998022114A1 (en) | 1996-11-15 | 1998-05-28 | Dumex-Alpharma A/S | A method for promoting tissue repair |
| NL1005812C1 (nl) | 1997-04-15 | 1997-06-04 | Claus Jurgen Timmermans | Superabsorberend wondverband. |
| FR2759379A1 (fr) | 1997-10-06 | 1998-08-14 | Urgo Laboratoires | Nouvelle masse adhesive hydrophile |
| US6096942A (en) | 1998-04-24 | 2000-08-01 | Pabban Development Inc. | Surgical dressing, and process for manufacturing same |
| SE9801899L (sv) * | 1998-05-28 | 1999-07-05 | Moelnlycke Health Care Ab | Sårförband eller fixeringstejp för hud innefattande ett laminat av en plastfilm och ett material med oregelbunden ytstruktur och som är belagt med en klibbig elastomer |
| JP2002519153A (ja) | 1998-07-01 | 2002-07-02 | アコーディス スペシャリティー ファイバーズ リミティド | 傷手当用品及びその製造並びにその使用に適切な材料の製造 |
| FR2783412B1 (fr) | 1998-09-18 | 2000-12-15 | Lhd Lab Hygiene Dietetique | Compresse non adherente sterile |
| AU2000238098A1 (en) * | 2000-03-09 | 2001-09-17 | Syntacoll Ag | Novel natural polymer-based material with improved properties for use in human and veterinary medicine and the method of manufacturing such |
| JP2001325554A (ja) | 2000-05-15 | 2001-11-22 | Nec Corp | リユースシステム |
| JP2001326151A (ja) | 2000-05-16 | 2001-11-22 | Nec Corp | 半導体集積回路製作システム |
| FR2824474B1 (fr) | 2001-05-11 | 2004-01-02 | Fabre Pierre Dermo Cosmetique | Composition cosmetique a base de sucralfate et de sulfates de cuivre et de zinc |
| FR2830747B1 (fr) | 2001-10-17 | 2004-08-13 | Urgo Laboratoires | Pansement adhesif |
| FR2838748B1 (fr) * | 2002-04-17 | 2004-07-09 | Urgo Laboratoires | Nouvelles compositions adhesives thermofusibles hydrophiles |
| EP1435247B1 (en) | 2003-01-06 | 2006-11-02 | Speciality Fibres and Materials Limited | Wound dressings comprising an alginate fabric and a superabsorbent |
| CN1569902A (zh) * | 2003-07-23 | 2005-01-26 | 中国科学院生态环境研究中心 | 一种活性寡糖衍生物及其制备方法 |
| US20080064999A1 (en) | 2004-07-16 | 2008-03-13 | Kristian Larsen | Wound Care Device |
| US7520406B2 (en) | 2005-07-08 | 2009-04-21 | S. C. Johnson & Son, Inc. | Device for dispensing a controlled dose of a flowable material |
| US20090156974A1 (en) | 2005-08-31 | 2009-06-18 | Jens Hog Truelsen | Absorbent wound care device |
| JP4986273B2 (ja) * | 2005-09-15 | 2012-07-25 | 持田製薬株式会社 | アルギン酸を含む創傷被覆材 |
| FR2893249B1 (fr) | 2005-11-17 | 2008-09-12 | Urgo Sa Lab | Pansement comprenant un applicateur de film mince |
| GB0606661D0 (en) * | 2006-04-03 | 2006-05-10 | Brightwake Ltd | Improvements relating to dressings |
| DK2010220T3 (da) * | 2006-04-03 | 2022-05-23 | Ceva Animal Health Pty Ltd | Stabiliserede pentosanpolysulfat-(pps)-formuleringer |
| FR2914847B1 (fr) | 2007-04-13 | 2009-07-10 | Urgo Soc Par Actions Simplifie | Nouveau protecteur pour pansements |
| FR2916355B1 (fr) * | 2007-05-25 | 2009-08-28 | Urgo Soc Par Actions Simplifie | Nouveau principe actif dans la cicatrisation et son utilisation |
| FR2916356B1 (fr) | 2007-05-25 | 2009-08-28 | Urgo Soc Par Actions Simplifie | Nouvel agent permettant le relargage d'actifs dans des pansements contenant au moins un corps gras |
| JP5271263B2 (ja) * | 2007-05-30 | 2013-08-21 | ピアック株式会社 | X線検知材料含有布帛、x線検知用絆創膏およびx線検知用絆創膏の製造方法 |
| US8828952B2 (en) * | 2007-10-16 | 2014-09-09 | Progen Pharmaceuticals Limited | Sulfated oligosaccharide derivatives |
| FR2929511B1 (fr) * | 2008-04-02 | 2010-12-31 | Basf Beauty Care Solutions France Sas | Nouveau principe actif stimulant la proliferation et/ou l'activite des fibroblastes. |
| BRPI0915684A2 (pt) * | 2008-07-07 | 2017-06-20 | Laboratoire Medidom S A | curativo redutor de temperatura para ferimentos |
| FR2933618B1 (fr) | 2008-07-10 | 2011-01-07 | Urgo Lab | Procede de fabrication de pansements contenant au moins un actif |
| FR2953522B1 (fr) | 2009-12-07 | 2012-03-09 | Fabre Pierre Dermo Cosmetique | Sucrose octasulfates de zinc, leur preparation et leurs applications pharmaceutiques et cosmetiques |
| FR2955033B1 (fr) | 2010-01-14 | 2012-03-02 | Urgo Lab | Nouveau pansement comprenant un voile de microfibres ou de nanofibres capable de gelifier ou se solubiliser |
| FR2956322A1 (fr) * | 2010-02-17 | 2011-08-19 | Urgo Lab | Utilisation d'oligosaccharides polysulfates synthetiques comme agents de detersion d'une plaie. |
| FR2959417B1 (fr) | 2010-04-28 | 2012-07-13 | Urgo Lab | Pansement ampoule comprenant au moins deux resines tackifiantes |
| FR2972928B1 (fr) | 2011-03-25 | 2013-11-29 | Urgo Lab | Composition contenant une cellulose, une huile vegetale et un solvant volatil, ses utilisations comme pansement |
| FR2973223B1 (fr) | 2011-03-31 | 2013-04-19 | Urgo Lab | Pansement absorbant cicatrisant, ses utilisations pour les plaies chroniques |
| FR2974004B1 (fr) | 2011-04-15 | 2014-05-02 | Urgo Lab | Pansement absorbant hydrocellulaire, ses utilisations pour le traitement des plaies chroniques et aigues |
| FR2974005B1 (fr) | 2011-04-15 | 2014-05-02 | Urgo Lab | Pansement adhesif mince tres absorbant, ses utilisations pour le traitement des plaies chroniques |
| FR2977149B1 (fr) | 2011-06-28 | 2013-07-19 | Urgo Lab | Pansement pour recouvrir une partie saillante |
| WO2013093213A1 (fr) | 2011-12-19 | 2013-06-27 | Laboratoires Urgo | Pansement interface adherent |
| FR2993464B1 (fr) | 2012-07-17 | 2014-08-22 | Urgo Lab | Pansement interface autoporte |
| FR3003463B1 (fr) | 2013-03-20 | 2015-04-10 | Urgo Lab | Pansement ayant un bord peripherique adhesif avec un pourtour ondule |
-
2012
- 2012-07-13 FR FR1256829A patent/FR2993182B1/fr active Active
-
2013
- 2013-07-11 US US14/414,562 patent/US10172972B2/en active Active
- 2013-07-11 MX MX2015000568A patent/MX354272B/es active IP Right Grant
- 2013-07-11 JP JP2015520996A patent/JP6212552B2/ja active Active
- 2013-07-11 RU RU2015104803A patent/RU2641031C2/ru not_active IP Right Cessation
- 2013-07-11 CA CA2878869A patent/CA2878869C/fr active Active
- 2013-07-11 BR BR112015005673A patent/BR112015005673B1/pt not_active IP Right Cessation
- 2013-07-11 HU HUE13735301A patent/HUE042014T2/hu unknown
- 2013-07-11 SG SG11201408829RA patent/SG11201408829RA/en unknown
- 2013-07-11 AU AU2013288664A patent/AU2013288664B2/en active Active
- 2013-07-11 ES ES13735301T patent/ES2717276T3/es active Active
- 2013-07-11 WO PCT/EP2013/064718 patent/WO2014009488A2/fr active Application Filing
- 2013-07-11 MY MYPI2015000049A patent/MY171069A/en unknown
- 2013-07-11 CN CN201380037157.5A patent/CN104507506B/zh active Active
- 2013-07-11 TR TR2019/03940T patent/TR201903940T4/tr unknown
- 2013-07-11 EP EP13735301.7A patent/EP2872187B1/fr active Active
- 2013-07-11 KR KR1020157000796A patent/KR20150060662A/ko not_active Application Discontinuation
- 2013-07-11 PT PT13735301T patent/PT2872187T/pt unknown
- 2013-07-11 DK DK13735301.7T patent/DK2872187T3/en active
- 2013-07-11 PL PL13735301T patent/PL2872187T3/pl unknown
- 2013-11-07 UA UAA201500240A patent/UA117658C2/uk unknown
-
2014
- 2014-12-29 MA MA37709A patent/MA37709B1/fr unknown
- 2014-12-30 TN TN2014000542A patent/TN2014000542A1/fr unknown
-
2015
- 2015-01-05 PH PH12015500013A patent/PH12015500013A1/en unknown
- 2015-01-08 ZA ZA2015/00137A patent/ZA201500137B/en unknown
- 2015-01-13 CL CL2015000091A patent/CL2015000091A1/es unknown
- 2015-01-20 CO CO15010431A patent/CO7240418A2/es unknown
- 2015-09-01 HK HK15108526.9A patent/HK1207830A1/xx unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10172972B2 (en) | Dressing having sustained release of active agents | |
| US8940325B2 (en) | Use of synthetic polysulphated oligosaccharides as cleaning agents for a wound | |
| CA2848351A1 (en) | Composition and dressing for wound treatment | |
| US20190151496A1 (en) | Novel active ingredient in cicatrization and use thereof | |
| JP2020519578A (ja) | 動脈疾患の糖尿病患者の創傷を処置するためのオリゴ糖化合物の使用 | |
| Kumar et al. | New frontiers in wound-dressings: An interdisciplinary perspective | |
| OA18477A (en) | Dressing having sustained release of active substances. |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E90F | Notification of reason for final refusal | ||
| E601 | Decision to refuse application |